Штамм ganoderma lucidum - продуцент протеогликанаgоо9, обладающий противоопухолевой и иммуностимулирующей активностью - RU2082755C1
Код документа: RU2082755C1
Чертежи






Описание
Изобретение касается штамма, продуцирующего протеогликан, эффективный в повышении противоопухолевого иммунитета.
Чтобы найти новый протеогликан, усиливающий противоопухолевый иммунитет, заявители настоящего изобретения собрали большое количество базидиальных грибов и пытались выделить продуцируемый ими протеогликан. Впоследствии было обнаружено, что штаммы рода Ganoderma, принадлежащего к базидиальным грибам, добываемые в области Dooryoon Mauntains, расположенных в провинции South Cholla, продуцируют протеогликан, обладающий способностью усиливать противоопухолевый иммунитет при культивировании в подходящей культуральной среде. После выделения протеогликана и проверки его физико-химических и биофизических свойств его обозначили как G009, обладающий способностью усиливать противоопухолевый иммунитет, а продуцирующий его штамм обозначили как Ganoderma IV 009 (внесен в Korean Species Association под номером КРСС-107090, 5 октября 1990).
Настоящее изобретение касается штамма IV 009, продуцирующего G009. Хотя исследования проводили в таких медицинских компонентах, как антибактириальные, снижающие галлюцинации, токсичность и холестерин компоненты из базидиальных грибов, принадлежащих к высшим грибам, здесь приведено серьезное исследование противоопухолевого компонента и его свойства повышения иммунитета, таким образом повышают важность базидиальных грибов. Поэтому эти штаммы, секрет (особое вещество) которых содержит противоопухолевый компонент и повышает иммунную функцию, выделяют и культивируют в жидкости для изучения их фармакологического действия.
При изучении мутантный штамм, обладающий большим противоопухолевым эффектом и способностью повышать иммунитет, чем образцы, принадлежащие к виду Ganoderma, идентифицированные до того, выделяют, культивируют мицелий в жидкости и затем подтверждают противоопухолевый эффект и функцию повышения иммунитета этих компонентов, экстрагированных из культивированного мицелия.
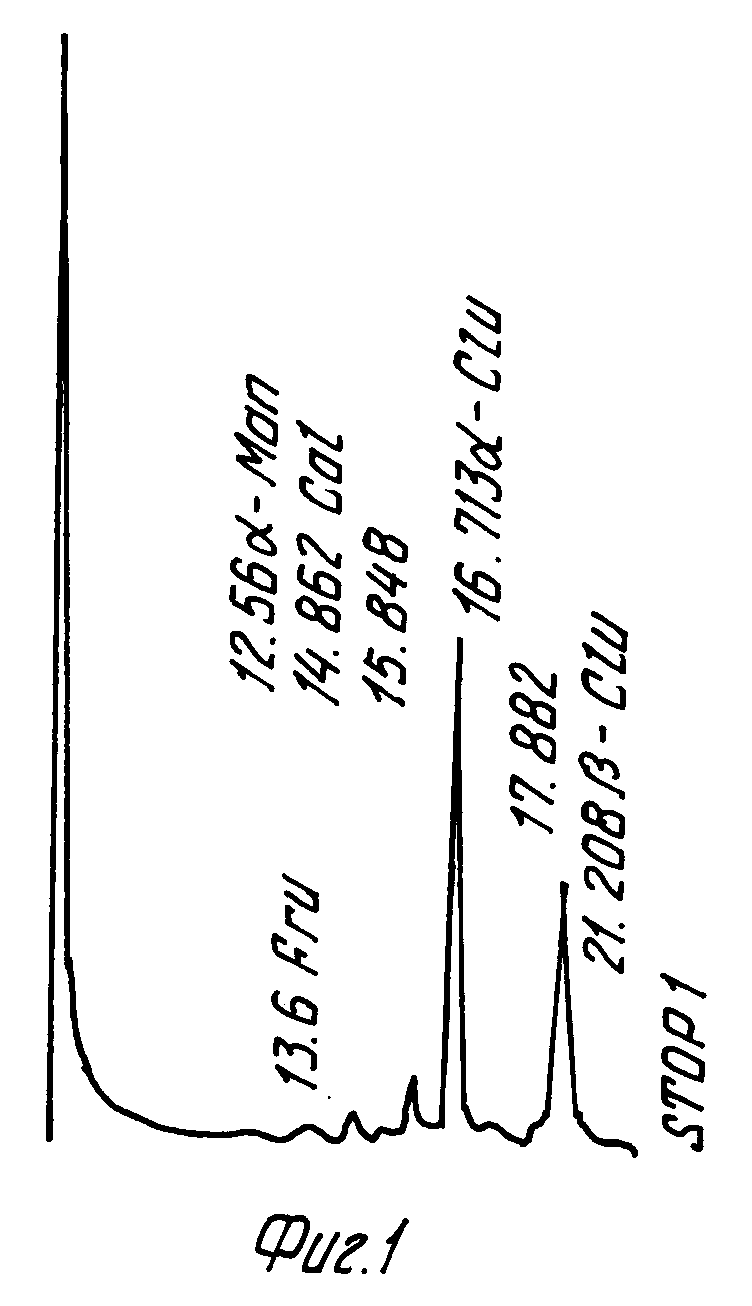
На фиг. 1 дана хроматограмма анализа сахаридов протеогликана G009; на фиг.2 хроматограмма аминокислот протеогликана G009; на фиг.3 ИК-спектр протеогликана G009.
Пример. Выделение протеогликанов.
1) Штамм. Штаммы ganoderma lucidum собирают в области Dooryoon Mountains, расположенных в провинции South cholla, выделяют и идентифицируют.
2) Консервирующая культуральная среда. Культуральная среда для картофельного агара с декстрозой (PDA); 39 г культуральной среды картофельной декстрозы (Difico США) доводят до объема 1 л, растворяя в дистиллированной воде, и помещают ее в скошенную культуральную среду после стерилизации при высоком давлении в течение 20 мин при 121oC.
Культуральная среда для культивирования в жидкости: смесь 50 г глюкозы, 20 г пептона, 0,87 г KH2PO4, 0,5 г MgSO4 •7H2O, 10 мг FeCl2•6H2O, 7 мг MnCl2•4H2O, 10 мг ZnSO2•5H2O и 4 мг ZnCl2 доводят до объема 1 л, добавляя дистиллированную воду. Стерилизуют в течение 20 мин при 121oC, доводя pH до 5,5.
3) Культура. Штамм, который хранился закрытым, трансплантируют в наклонную культуральную среду для PDA и выращивают в течение 7 дней при 25±1oC. Затем выращенный мицелий отделяют, соблюдая условия стерильности, и помещают в 100 мл культуральной среды для ведения культуры в жидкости, растирают при помощи микросмесителя в течение 15 мин. Затем переносят в трехгорлую колбу на 500 мл и культивируют, перемешивая при 180 об/мин и 25±1oC в течение 10 дней до тех пор, пока не образуется зрелая грибница с диаметром около 5 мм. После того как грибницу растирают при помощи микросмесителя в течение 10 с, ее вносят (5 об.) на 5% в 500-миллилитровую колбу, содержащую 100 мл культуральной среды для ведения культуры в жидкости и выращивают при перемешивании в течение 10 дней при тех же условиях, что описаны выше.
Из культивированных мицелиев готовят образцы, растирая их снова в течение 10 с, 100 мл культуральной среды для ведения культуры в жидкости помещают в 500 мл трехорлую колбу, туда вносят образец 5% на 5% Затем их культивируют при вращении 170 об/мин, в течение 7 дней на орбительном вибраторе (радиус вращения 2,54 см, Vision Science Co.) при 25±1oC.
4) Экстракция и выделение протеогликанов. После того, как весь полученный раствор культуры разделяют центрифугированием в течение 15 мин при 6000 об/мин, отбирают мицелий и помещают для переваривания в двукратное количество 2,5 N раствора NaOH. Оставляют раствор на 24 ч при комнатной температуре и разделяют на центрифуге в течение 15 мин при 6000 об/мин. Затем супернатант нейтрализуют до pH 7,4 ледяной уксусной кислотой и проводят диализ в течение 3 дней с visking tube (Sigma, США). После диализа раствор концентрируют и добавляют к нему двукратное количество этанола. Затем оставляют его стоять в течение 24 ч при 4oC и разделяют на центрифуге при 6000 об/мин в течение 15 мин, получая осадок. Осадок растворяют в деионизированной воде, а супернатант концентрируют при центрифугировании в течение 1 мин при 6000 об/мин и отделяют оттуда протеогликан, лиофилизируя концентрированный раствор.
5) Очистка протеогликана. После растворения образца в воде, как указано выше, и добавки избытка этанола берут 12,5 г осадка и снова растворяют его в воде. Раствор образца пропускают через колонку (3•6 см) с DEAE-целлюлозой (Cl-форма), а затем разделяют на центрифуге, добавив 200 мл метанола к такому же количеству элюата, полученному при элюировании водой; промыв осадок этанолом и высушив его при пониженном давлении, получают G1 (2,1 г), G2 (0,42 г) получают, высушив при пониженном давлении осадок, полученный после того, как супернатант (400 мл) делят на центрифуге, добавив туда 400 мл этанола. G1 (1,1 г) получают, высушив при пониженном давлении осадок, полученный после того, как супернатант (400 мл) делят на центрифуге, добавив к супернатантному раствору (800 мл), оставшемуся после удаления G2, 800 мл этанола.
G1 элюируют, растворяя его в воде, на Sephatex G-100. G4 (1,5 г) получают, лиофилизируя фракцию из колонок N 25-33, и выделяют, высушивая G5 (0,3 г), включая фракцию из колонок N 34-44, при пониженном давлении. После того, как G4 растворяют в воде и к 0,15 M cetavelon (cethy - триметиламмонийборат) и 0,1 M боратного буфера (pH 8,0) добавляют при перемешивании такое же количество раствора, доводят pH до 9,0 0,5 M раствором NaOH и получают осадок (G7) и супернатант (G6). Затем G7 растворяют в воде, добавив 2M ледяной уксусной кислоты, и получают осадок, добавив двукратное количество метанола. Осадок промывают в метаноле и ацетоне, а затем сушат при пониженном давлении (G8). Затем G8 растворяют в небольшом количестве воды и наносят на Sephararose C1-4B и элюируют водой, получая из колонок N 25-30 G9. G10 получают из колонок N 31-46.
Эксперимент 1. Противораковый тест. Проверку активности полученных выше фракций относительно саркомы-180 проводят следующим образом: фракцию трансплантируют с интервалом в одну неделю в брюшную полость самцов мыши ICR (20-25 г) и используют в качестве экспериментальных опухолевых клеток удачно пересаженные клетки саркомы-180.
Клетки саркомы-180 культивируют в течение 7 дней в брюшной полости этих мышей, добавляют туда охлажденный льдом стерильный солевой раствор и берут их вместе с отеком, делят на центрифуге в течение 5 мин при 4000 об/мин, осажденные клетки отделяют.
Отделенные клетки промывают физиологическим солевым раствором три раза и разбавляют до концентрации 1•107 клеток/мг. 0,1 мл этой клеточной суспензии трансплантируют hyperdanically в левую паховую область мышам группы из 10 животных.
Через 72 ч после трансплантации опухолевых клеток этим мышам вводят протеогликаны (которые представляют собой очищенные фракции) в течение 10 последующих дней. Контрольной группе вводят физиологический солевой раствор, проверяемой группе вводят протеогликан, растворенный в физиологическом солевом растворе, 0,1 мл на 0,1 мл, при концентрировании его до 20 мг/кг.
На 30 день после трансплантации опухолевых клеток этих мышей
умерщвляют и извлекают образовавшуюся твердую раковую опухоль. Затем взвешивают и определяют средний вес опухоли и процентное соотношение ингибирования роста опухоли, рассчитываемое по данной ниже
формуле:
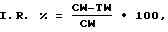
I.R. коэффициент ингибирования (в процентах);
CW средний вес опухоли контрольной группы;
TW средний вес опухоли тестовой группы.
В результате экспериментов по проверке противоопухолевой активности, проведенных с саркомой-180, было найдено, что G9 обладает наибольшей активностью в проверенной группе, как показано в табл.1, его выбрали и обозначили G009. Анализ G009 выполнен в следующих экспериментах. Для химического анализа G009 определяют общее количество сахаридов методов Anthrone по окрашиванию (Anthroneis color developing method) и определяют содержание белков методом Lowry и др. Затем анализируют аминокислоты и сахариды. Результаты приведены в табл.2, 3 и 4. Хроматограмма сахаридов приведена на фиг.1. Хроматограмма аминокислот на фиг.2, а ИК-спектр на фиг.3.
Для анализа сахаридов используют газожидкостной хроматограф G.L.C. (Shimadgu GC 9A, Япония): колонка 3% 0-17 (80-100) (пористый шималит) 3 мм D x 1 колонка из борсиликатного стекла, температурный градиент колонки 150-180o C, детектор 190oC, скорость истечения N2 50 мл/мин, H2 60 мл/мин (0,6 кг/см2), воздуха 60 мл/мин (0,6 кг/см2), чувствительность 102 •21 (ампер полной шкалы).
Необходимые требования для использования аминокислотного автоанализатора (Beckman Sys. 6300, США):
Колонка 2,6•200 мм
Ионообменная смола 338076 (Beckman)
Скорость истечения Буферного раствора 0,33 мл/мин Нингидрина 0,17 мл/мин
Время аналитического цикла 60 мин
Давление в колонке 2100
фунт/дюйм2 (147 кг/см2)
Давление нингидрина 100 фунт/дюйм2 (7 кг/см2)
Температура колонки Градиент 50-70oC
Давление
газообразного N2 40 фунт/дюйм2 (2,8 кг/см2)
Температура реакционной бани 130oC
Длина волны 570 нм, 440 нм
Эксперимент 2.
Различное противоопухолевое действие G009 в зависимости от способа приема.
G009 трансплантируют в брюшную полость 20-25 г самцов мыши ICP с интервалом в 1 неделю, в качестве экспериментальных клеток используют клетки саркомы-180. Клетки саркомы-180 культивируют в течение 7 дней в брюшной полости мышей и берут их вместе с отеком. Делят их центрифугированием при 3000 об/мин в течение 5 мин после того, как добавили стерильный солевой раствор, охлажденный льдом, осадок клеток отделяют.
Отделенные клетки промывают трижды физиологическим солевым раствором и разбавляют до концентрации 1•107 клеток/мл. Через 24 ч суспензию клеток с концентрацией 1•107 клеток/мл трансплантируют мышам группы из 10 животных, вводя по 20 мг/кг в мышцу, в подкожный слой, под кожу и в брюшину в течение 10 дней и по 10 мг/кг вводят в вену в течение 5 дней. Контрольной группе вводят физиологический раствор аналогичным образом 0,1 мл на 0, 1 мл. Через 30 дней определяют и сравнивают вес твердой раковой опухоли. Как показано в табл. 5, ингибирование роста раковой опухоли происходит независимо от способа введения.
Эксперимент 3. Влияние введения G009 на продолжительность жизни
Для измерения противоопухолевой активности G009 по отношению к продолжительности жизни мыши используют клетки
асцитной опухоли
Эрлиха (EAT). В брюшную полость вводят 1•106 и 5•107 клеток/мл EAT. Через 24 ч G009 растворяют в фосфатном буфере и вводят этот раствор в брюшную
полость и в рот
(100 мг/кг) в течение 12 последовательных дней. Затем отмечают среднюю продолжительность жизни 20, 25, 30, 40 и 50 дней. В то же время контрольной группе животных вводят такое же
количество
физиологического раствора. Как показано в табл.6, введение G009 в брюшную полость и в вену оказывают одинаковый противоопухолевый эффект.
Эксперимент 4. Противораковый
эффект G009 в
мышах, которым ввели trypan blue
G009 трансплантируют в брюшную полость 20-25 г самцов ICR с интервалом в одну неделю, а в качестве экспериментальных опухолевых клеток
используют клетки
саркомы-180, которые можно успешно переносить. Клетки саркомы-180 культивируют в течение 7 дней в брюшной полости и берут вместе с отеком. Отделяют их центрифугированием при 4000
об/мин в течение 5
мин после того, как туда добавили стерильный солевой раствор, охлажденный льдом; отделяют осадок клеток. Отделенные клетки трижды промывают физиологическим солевым раствором и
разбавляют до
концентрации 1•107 клеток/мл, вводят подкожно в левую паховую область 0,1 мл на 0,1 мл.
Через день в брюшную полость вводят 4 мг/кг (0,4 мл) trypan blue. Еще через один день вводят подкожно 1 мг/мышь (0,1 мл) trypan blue и так продолжают вводить до общего количества 13 мг/мышь с интервалом в 3 дня. Сразу после введения trypan blue вводят внутривенно 10 мг G009. В контрольной группе вместо G009 вводят физиологический раствор. Обе сравниваемые группы, контрольная и тестовая, включают по 10 животных. Через 10 дней после трансплантации опухолей мышей умерщвляют и определяют вес опухолей. Результаты эксперимента по определению противоопухолевого эффекта G009 в мышах, на которые действовали trypan blue, показаны в табл.7. Эти результаты показывают, что G009 компонент, экстрагированный согласно настоящему изобретению, активирует макрофаги, связанные с противоопухолевым действием, при введении мышам trypan blue фактора, дезактивирующего макрофаги, и что G009 проявляет противоопухолевый эффект путем активации функции макрофага вместе с противоопухолевой активностью Т-лимфоцита.
Эксперимент 5. Эффект G009, производимый при введении новорожденным мышам, когда после тимэктомии им вводили антитимусный глобулин. 2-Дневным мышам ICR проводят тимэктомию в соответствии со способом Sjodin, через 6 недель после тимэктомии в паховую область трансплантируют суспензию клеток саркомы-180 0,1 мл на 0,1 мл, концентрируя их до 1•107 клеток/мл.
Через 24 ч после трансплантации вводят внутримышечно по 20 мг/кг G009 в течение 10 дней. Для предотвращения инфицирования мышам, которым сделали тимэктомию, дают воду, содержащую тетрациклин-HCl. В соответствии с методом Tadakuma отделяют противотимусную сыворотку. Клетки тимуса выделяют, вырезая тимус у 1-, 2- или 3-недельных мышей и готовя клеточную суспензию при разбавлении раствором фосфатного буфера.
Затем 1•106 клеток/мл тимуса вводят в вену кролику три раза с интервалом в три недели для иммунизации. Через неделю после третьей инъекции берут антитимусную сыворотку и дезактивируют в течение 30 мин при 55oC.
Затем фракцию Ig C (иммуноглобулин C) выделяют из дезактивированной противотимусной сыворотки, осаждая ее сульфатом аммония, 0,1 мл этой фракции вводят в течение 10 дней в брюшную полость мышей (через один день после заражения клетками саркомы-180 1•107 клеток/мл). G009 начинают вводить также через один день после трансплантации саркомы и вводят 20 мг/кг внутримышечно в течение 5 дней. Как показано в табл.8, приведенной ниже, противоопухолевый эффект, производимый G009 на мышей, у которых удалили тимус, в связи с функцией T-клеток значительно ниже, чем у контрольной группы; и противоопухолевый эффект, производимый G009 на животных с введенным противотимусным глобулином снижен более, чем у контрольной группы, на которую псевдо-воздействуют нормальным глобулином кролика.
Таким образом, результаты этих рассмотренных экспериментов показывают, что G009 оказывает противоопухолевое воздействие путем активации функции T-клеток.
Таблица 8. Сравнение противоопухолевых эффектов, производимых при введении G009 после трансплантации саркомы-180 новорожденным мышам с удаленным тимусом (Эксперимент 1) и мышам с введенным противотимусным глобулином (Эксперимент 2).
N.M. обычная мышь; T.M. мышь с удаленным тимусом;
A.T.M. мышь с введенным противотимусным глобулином;
N.P.G.M. мышь с введенным обычным глобулином кролика.
Эксперимент 6. Влияние G009 на комплементную систему.
В начале комплемента используют сыворотку морской свинки и свежуют сыворотку человека. В качестве красных кровяных клеток используют красные кровяные клетки овцы. В качестве антител используют гемолизин. Эксперимент по активированию комплемента проводят следующим образом: в тестовую пробирку помещают 150 мл желатин-веронал-буферного раствора (GVB2+) и 50 μл образца, туда добавляют 50 μл комплемента (100 единиц/мл). Через 30 мин протекания реакции при 37oC концентрацию комплемента доводят до 1 ед/мл, добавляя туда GVB2+. После того, как к этой смеси добавляют 2 мл сенсибилизированных в гемолизине красных кровяных клеток овцы (2MHU/мл) и 1,0, 1,2 и 1,6 единиц соответственно добавляют к смеси комплемента, разбавленной раствором GVB2+, общее количество доводят до 5 мл, добавляя GVB2+.
После реакции в течение 60 мин при 37oC определяют поглощение света при 541 нм раствора супернатанта, полученного разделением центрифигурованием в течение 5 мин при 2500 об/мин. Степень активности определяют количеством (5) комплемента, расходованного в контрольной группе и G009.
Как показано в табл.9, количество расходованного комплемента пропорционально увеличивается с ростом концентарции G009. Можно считать, что такое увеличение показывает, что G009 повышает иммунитет, активируя функцию комплемента, которая является одной из важных защитных функций иммунной системы.
Эксперимент 7. Эффект, производимый G009 на вес органов, связанных с иммунитетом. Через 5 дней после внутривенного введения G009 мышам в количестве 10 мг/кг выделяют и определяют вес легких, печени и селезенки. Лизоцим активируют streptococcus lysodeicus растворенным в растворе фосфатного буфера (pH 6,2) в качестве субстрата, и определяют поглощение света при 660 нм.
Как показано в табл.10, причиной увеличения веса селезенки и регистрируемой степени активности лизоцима в группе мышей с введенным G009 является активация протеогликаном G009 макрофагов, вследствие этого увеличивается активность лизоцима.
Эксперимент 8. Влияние G009 на количество клеток, образующих гемолитические бляшки.
1) В качестве лабораторных животных используют группу из 5 самцов мыши ICR весом по 20-25 г, в брюшные полости животных в течение 5 последовательных дней вводят образец, концентрированный до 20 мг/кг. Через 7 дней после пятого введения их иммунизируют, вводя в брюшную полость красные кровяные клетки овцы в количестве 1•106 клеток/мл. Через 4 дня после введения красных кровяных клеток овцы извлекают селезенку.
Клетки селезенки выделяют, растирая селезенку мешалкой с равновесным солевым раствором, охлажденным льдом. Выделенные клетки селезенки суспендируют в 0, 83%-ном растворе хлористого аммония и оставляют на 3 мин при температуре 37oC, удаляют супернатант, отделяя его центрифугированием в течение 5 мин при 2000 об/мин. Эти клетки снова суспендируют в равновесном солевом растворе, охлажденном льдом, отделяют центрифугированием и определяют количество клеток селезенки при помощи гемометра.
2) Красные кровяные клетки
овцы суспендируют в растворе Cllser (20,5 г глюкозы, 4,2 г хлорида натрия и 8,0 г цитрата натрия растворяют в 1 л
дистиллированной воды и используют при фильтрации через миллипористый фильтр (0,45
μм), промывают четыре раза равновесным солевым раствором в течение 5 мин при 2000 об/мин и суспендируют в
таком же растворе таким образом, чтобы окончательная концентрация составляла 10%
3) Пластину основания готовят, наливая 10 мл 1,5% агара (noble agar, Difco) в чашку Петри. Затем 100 μл
(1) и 100 μл красных кровяных клеток овцы из (2) смешивают с 2 мл 0,7% агара
и наливают в чашку Петри, добиваясь однородности покрытия. После сенсибилизации в течение 60 мин при 37o
C добавляют туда 2,5 мл на 2,5 мл поглощающей влагу сыворотки морской свинки,
десятикратно разбавленной равновесным солевым раствором, в качестве комплемента; культивируют в течение 30 мин при 37oC. Затем считают полученное количество клеток, образующих
гемолитические бляшки, и отношение количества клеток, образующих гемолитические бляшки, ко всем клеткам селезенки (PFC/селезенка).
Как показано в табл.11, G009 способствует значительному увеличению количества клеток селезенки и количества клеток, образующих гемолитические бляшки. Таким образом, рассмотренный G009 связан с иммуностимулирующим действием.
Эксперимент 9. Иммуностимулирующее действие. Каждая группа включает 10 6-недельных мышей, 20-25 г, самцы ICR мыши, G009 растворяют в физиологическом селевом растворе и вводят в брюшные полости животных 0,2 мл раствора определенной концентрации. Через 24 ч в хвостовую вену вводят 0,2 мл угольной суспензии, полученной смешиванием 1 мл черных чернил (perikan drawing ink 17 black) и физиологического солевого раствора. Затем через 1, 5, 10 и 15 мин берут 0,02 мл крови из глазницы при помощи гематокритного капилляра, покрытого гепарином, и сразу разбавляют ее и гемолизируют в 1,6 мл водного раствора карбоната натрия. Этот раствор калориметрируют при 675 нм и определяют показатель фагоцитоза (величина K) по уравнению Helpern и др. В контрольной группе мышам вводят 0,2 мл физиологического солевого раствора.

В приведенном уравнении Co содержание угольного порошка в крови во время to; C содержание угольного порошка в крови во время t.
Результаты этих экспериментов приведены в табл.12. Показатель (K) иммунофагоцитоза увеличивается пропорционально концентрации G009. В соответствии с этими результатами кажется наиболее вероятным, что G009 производят иммуностимулирующий эффект, принимая участие в иммунной реакции.
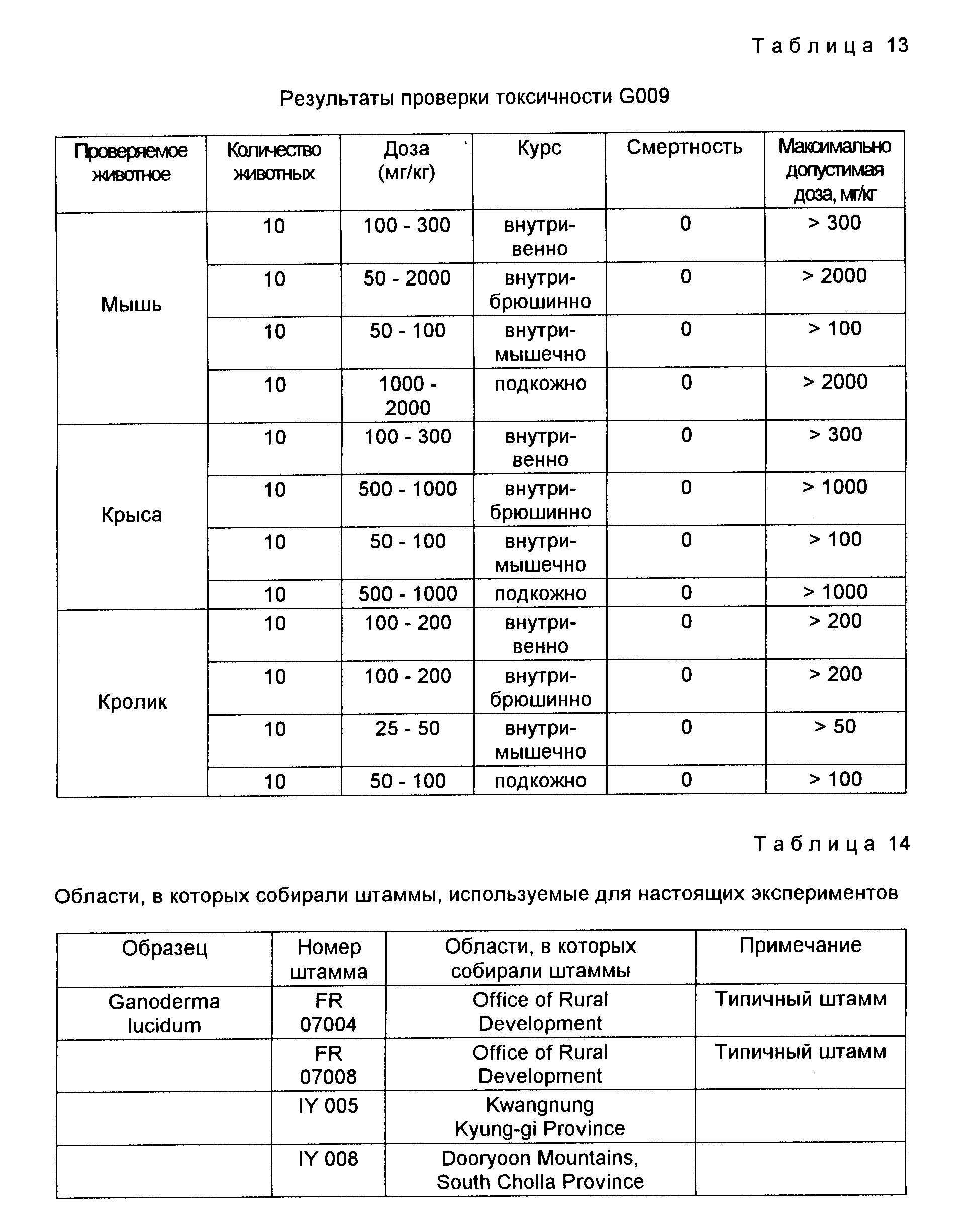
Эксперимент 10. Проверка токсичности G009. Проверку G009 на высокую токсичность проводят на мышах, крысах и кроликах и результаты получают через 14 дней после введения G009. Как показано в табл.13, для разных курсов и видов не обнаружено смертельных случаев. Следовательно, G009 является безопасным материалом с низкой токсичностью.
Эксперимент 11. Сравнение характеристик для разных видов.
Для выяснения филогенетической классификации и физиологических генетических различий четырех видов или типов штаммов (хранятся в секции Bacteria 2 Сельскохозяйственного Технологического Института Agracultural Technolgy Institute, office of Rural Development), проявивших, как было найдено, превосходные свойства при исследовании противораковых эффектов, производимых этими ganoderma lucodum штаммами, собранными в различных областях страны, проводили следующие эксперименты. Экспериментальные материалы и способы.
Использованные штаммы, культуральная среда и культура. Для настоящих экспериментов использовали четыре штамма, для которых обнаружен превосходный противораковый эффект среди тех ganoderma lucidum, которые растут в природе страны, места сбора приведены в табл.14.
Экстракция образцов. Мицелий, получаемый делением центрифугированием после культивирования в жидкости, промывают три раза солевым раствором фосфатного буфера (pH 7,5) и подвергают воздействию сверхзвуковых волн в течение 30 с при охлаждении льдом. После деления центрифугированием при 12000 g супернатант используют в качестве образца для электрофореза.
Определение количества протеинов. Количество протеинов в образцах определяли при помощи бычьего сывороточного альбумина (BSA), который использовали в качестве типичного вещества, применяя реагент для анализа протеинов (Pierce Co.).
Электрофорез. Для электрофореза используют прерывную буферную систему. Разделяющий гель готовят концентрированием до 10% C, 10% T в 240 нМ Трис-Cl-буферном растворе (pH 8,48), стекинг-гель (Stacking-gel) готовят концентрированием до 3,125% T и 20% C в Трис-буферном растворе (39,5 мМ Трис, 0,06 N H3PO4, pH 6,9).
Для того, чтобы сделать эти гели твердыми, используют TEMED и персульфат аммония. В качестве жидких буферов используют на аноде 40 мМ Трис-глицин-буферного раствора (pH 8,8), а на катоде 60 мМ Трис-Cl-буферного раствора (pH 7,47). Образец обрабатывают в течение 2 ч при 100 V, 4oC, нагружая его на гели, 70 μг на 70 μг.
Окрашивание геля.
(1) Эстераза (E.C. 3, 1, 1, 1,). Обработанные гели переваривают в 0,2 М фосфатном буферном растворе (pH 6,5) в течение 30 мин.
Пока эти гели перевариваются, указанный раствор заменяют три раза новым. По достижении требуемой активности переваренного геля к нему добавляют окрашивающий раствор ( α-нафтилацетат 20 мг, этиленгликольмоноэтиловый эфир 2 мл, fast blue RR соль 20 мг, 0,2 М фосфатный буфер 120 мл) и встряхивают при 35oC в темном месте до появления цвета.
(2) Кислая фосфатаза (Е.С. 3, 1, 3, 2). По достижении требуемой активности геля при переваривания его в 0,1 М растворе ацетатного буфера (pH 5,2) к нему добавляют окрашивающий раствор (10%-ного раствора MgCl2 6 мл, fast garnet GBC 70 мг, a-нафтилфосфат 80 мг, b-нафтилфосфат 40 мг, 0,1 М ацетатный буфер 100 мл) для появлении цвета в течение 30 мин при 37oC.
(3) Лейцин-аминопептидаза (E. C. 3, 4, 11, 1). Окрашивающий раствор (a-лейцил-b-нафтиламид HCl 20 мг, fast blue K соль 20 мг, дистиллированная вода 50 мл, 0,2 М Трис-малат-буфер (pH 5,4) 120 мл) добавляют к гелю для появления цвета в течение 30 мин в темном месте.
(4) Пероксидаза (E. C. 1, 11, 1, 7). Гели промывают водой, после чего туда добавляют окрашивающий раствор (бензидин 1% уксусная кислота 9 мл, смешанный раствор: 1 часть раствора бензидина, смешанного с 40 мл дистиллированной воды, 1 часть 0, 03% H2O2 и 4 части дистиллированной воды) до появления цвета в темном месте.
Далее приведены результаты этих экспериментов. Строение изоферментов эстеразы. Что касается полос эстеразы ganoderma lucidum, всего появляются 17 полос, показанных на фиг. 1. Пятая и пятнадцатая полосы общие для всех штаммов. Образцы эстеразы типичных штаммов Fr 07004, Fr 07008 и IV 005 очень похожи друг на друга, а образцы эстеразы IV 009 и IV 010 сильно отличаются друг от друга.
Строение изоферментов кислой фосфатазы.
Образцы кислой фосфатазы типичных штаммов Fr 07004, Fr 07008 и IV 005 очень похожи друг на друга, а IV 009 и IV 010 дают отличающиеся полосы.
Строение изоферментов лейцинаминопептидазы. Для ganaderma lucidum получают всего три полосы лейцинаминопептидазы. Штаммы типов Fr 07004, Fr 07008 и IV 005 дают одинаковые полосы для большинства частей, тогда как IV 009 полностью отличаются от них.
Строение изоферментов пероксидазы. Штамм ganoderma lucidum дает 2 полосы пероксидазы, типичные штаммы Fr 07004, Fr 07008 и IV 005 очень похожи.
Сходство образцов. Как показано в табл.15, схожесть штаммов типа Fr 07008 и IV 005 составляет 93,8% схожесть штаммов типа Fr 07004 и типа IV 005 составляет 82,4% а схожесть Fr 07004 и IV 010, между Fr 07004 и IV 009 составляет 30,4 и 31,8% В соответствии с приведенными выше результатами различие изоферментного строения в некоторых образцах происходит вследствие биохимического изменения, вызванного генетической мутацией, являющейся результатом различия географического окружения, по-видимому, такие различия являются наиболее вероятной причиной, обусловливающей тот факт, что каждый штамм создает протеогликан, отличающийся своей противораковой активностью.
Реферат
Использование: медицина, в качестве вещества, усиливающего противоопухолевый иммунитет. Сущность изобретения: касается штамма Ganoderma Lucidum IV 009, который продуцирует протеогликан C 009, обладающий противоопухолевой и иммуностимулирующей активностью. Культуральная среда для культивирования содержит β-глюкозу, a-глюкозу, галактозу, a-маннозу и фруктозу в качестве сахаридов; глицин, аланин, гистидин, аргинин, аспаргиновую кислоту, треонин, изолейцин, серин, лейцин, глутаминовую кислоту, тирозин, пролин, фенилаланин и метионин в качестве протеиновых компонентов. 3 ил., 15 табл.

Комментарии