Рекомбинантные белки и их применения в терапевтических целях - RU2766595C2
Код документа: RU2766595C2
Чертежи
























Описание
ОБЛАСТЬ ТЕХНИКИ
[0001] Настоящее раскрытие относится к области рекомбинантных белков для применения при лечении заболеваний.
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0002] Согласно настоящей заявке испрашивается приоритет по заявке на патент США с серийным номером 61/563128, поданной 23 ноября 2011 года, под названием "ИММУНОГЕННЫЕ ИСКУССТВЕННЫЕ РЕКОМБИНАНТНЫЕ БЕЛКИ" (IMMUNOGENIC SYNTHETIC RECOMBINANT PROTEINS) и заявке на патент США с серийным номером 61/654401, поданной 1 июня 2012 года, под названием "ИММУНОГЕННЫЕ ИСКУССТВЕННЫЕ РЕКОМБИНАНТНЫЕ БЕЛКИ" (IMMUNOGENIC SYNTHETIC RECOMBINANT PROTEINS), каждая из которых включена в данный документ посредством ссылки в полном объеме.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
[0003] Иммунология рака представляет собой область науки, занимающуюся изучением взаимодействий между иммунной системой и раковыми клетками, такими как опухоли или новообразования. Особый интерес представляет запуск иммунного ответа, такой как узнавание специфических для раковых клеток антигенов, которые экспрессируются опухолями у человека и не экспрессируются в нормальных тканях. В целом, способы контроля деления и пролиферации злокачественных клеток заключались в выделении этих антигенов и презентирование их так, чтобы они распознавались иммунной системой как "чужие" антигены и вызывали специфический иммунный ответ.
[0004] В настоящее время идентифицировано значительное количество факторов роста, и было показано, что большинство, если не все, являются важными медиаторами пролиферации клеток в различных видах рака в дополнение к тому, что они вовлечены в другие болезненные состояния. Как правило, факторы роста являются растворимыми сывороточными белками, которые распознаются и связываются группой рецепторов факторов роста, расположенных на поверхностях клеток. Определенные факторы роста могут быть специфическими в отношении отдельного рецептора или могут связываться с несколькими близкородственными рецепторами с различными аффинностями. Сходным образом, некоторые рецепторы связывают только один лиганд, представляющий собой фактора роста, в то время как другие могут связывать множество родственных факторов роста, опять же, как правило, с отличающимися аффиностями. При связывании со своим природным рецептором цитоплазматический домен рецептора фосфорилируется, и это инициирует внутриклеточный сигнальный каскад, который приводит в результате к изменению транскрипции одного или нескольких генов и, в конечном счете, к прохождению по клеточному циклу и к пролиферации клеток.
[0005] Факторы роста и их рецепторы являются важными компонентами нормальных процессов роста, развития и восстановления, а их профили распределения в тканях и уровни экспрессии непосредственно регулируют клеточный рост. Как было показано с помощью множества исследований, факторы роста могут стимулировать пролиферацию множества клеточных типов как in vitro, так и in vivo (Cohen S., Carpenter G., PNAS USA 72, 1317, 1975, Witsch E et al: Physiology: 25(2):85-101, (2010)). Более того, было показано, что определенные факторы роста стимулируют пролиферацию в некоторых линиях раковых клеток, например, эпидермальный фактор роста (EGF) может стимулировать клетки некоторых видов немелкоклеточного рака легких (Osborne C. K. et al. Can Res. 40, 2. 361 (1980)). Другие факторы роста, такие как фактор роста эндотелия сосудов (VEGF), фактор роста фибробластов (FGF) и тромбоцитарный фактор роста (PDGF), важны при некоторых онкологических заболеваниях, таких как немелкоклеточный рак легкого (NSCLC) (Ballas MS, Chachoua A., Onco Targets and Therapy: 4, 43-58 (201 1)), рак предстательной железы (Cox ME et al; Prostate 69 (l):33-40 (2009)) и рак молочной железы (Law J et al, Cancer Res; 68,24: 10238-10346 (2008)).
[0006] В злокачественных тканях были обнаружены высокие уровни различных рецепторов факторов роста. Например, рецептор эпидермального фактора роста (EGFR) был обнаружен в необычайно больших количествах в злокачественных опухолях эпителиального происхождения, таких как рак легких, рак молочной железы, рак мочевого пузыря, рак яичников, рак наружных женских половых органов, рак толстой кишки, рак легкого, рак головного мозга и рак пищевода. Роль, которую играют факторы роста и их рецепторы в регуляции развития опухоли, неизвестна, но существуют предположения, что экспрессия рецептора фактора роста в опухолевых клетках обеспечивает механизм аутокринной стимуляция роста, что приводит к неконтролируемой пролиферации (Schlessinger J., Schreiber A. B., Levi A., Liberman T., Yarden Y. Crit. Rev. Biochem. 1983, 14 (2) 93-1 11). Кроме того, в работах Liao Y et al; Hum Pathol 36(1 1): 1186-1 196 (2005) и Cox ME et al; Prostate: 69(1) 33-40 (2009) описано значение повышенного количества рецепторов и фактора роста островковых клеток при метастатическом раке предстательной железы.
[0007] Одна стратегия лечения с целенаправленным воздействием на передачу сигнала с участием фактора роста при противораковой терапии предусматривала применение пассивной иммунотерапии, например, с помощью моноклональных антител к определенному задействованному рецептору/рецепторам. Такие исследования показали, что специфическое узнавание антителом рецептора, что может ингибировать связывание лиганда, может обладать ингибирующим действием на митогенную стимуляцию злокачественных клеток (SATO J. D., et al. Methods in Enzymology, vol. 146 pp 63-81, 1987). Тем не менее, антитела мышиного происхождения будут, как правило, вызывать ответ с участием человеческих антител к антителу мыши (HAMA), что, таким образом, ограничивает их до однократного введения.
[0008] Другие стратегии лечения предусматривали применение активной иммунотерапии с помощью вакцин, которые содержали представляющий интерес фактор роста, для индукции иммунного ответа против молекулы с целью ингибирования пролиферативного действия фактора роста на опухоли. В патенте США № 5984018, Davila et al, под названием "Вакцинная композиция, содержащая аутогенный эпидермальный фактор роста или его фрагмент или его производное, обладающая противоопухолевой активностью, и ее применение в терапии злокачественных заболеваний" (Vaccine Composition Comprising Autologous Epidermal Growth Factor or a Fragment or a Derivative Thereof having Anti-tumor Activity and use Thereof in the Therapy of Malignant Diseases) раскрыто, например, применение вакцины, которая содержит смесь фактора роста и иммуногенный (т. е. не являющийся человеческим) белок-носитель, химически конъюгированные вместе с помощью глутарового альдегида. Тем не менее, не желая привязываться к какой-либо определенной теории, полагают, что химическая конъюгация препятствует иммунным ответам против вакцины.
[0009] Это технически затруднительный подход, поскольку он требует, чтобы хозяин вырабатывал иммунный ответ к "собственному антигену", а иммунные системы позвоночных развивались так, чтобы предупреждать возникновение таких ответов. В тех случаях, когда сильный иммунный ответ вырабатывается против "собственного антигена", например, такой, который включает активацию Т-хелперных клеток, обычно это приводит к развитию аутоиммунного болезненного состояния. В течение многих лет предполагали, что некоторые аутоиммунные нарушения, например, волчанка, рассеянный склероз (MS), диабет и т.д., могут вызываться ранним воздействием фактора окружающей среды, который включает иммуногенные эпитопы (T-клеточные эпитопы), которые полностью имитируют собственные эпитопы хозяина. Это может приводить к стимуляции T-хелперных клеток, характеризующихся перекрестной реактивностью с эпитопами хозяина. Последующее воздействие фактора окружающей среды может впоследствии приводить к аутоиммунному ответу (Albert, L.J., and Inman, R.D New England Journal of Medicine, Dec. 30th pp 2068-2074, 1999). С тех пор было показано, что вирусный антиген может в действительности вызывать аутоиммунный ответ против белка нервных клеток (Levin, M.C. et. al, Nature Medicine vol 8 (5) pp 509-513, 2002).
[0010] В публикации патента США № 2006/0251654, Casimiro et al, под названием "Способы лечения злокачественных и инфекционных хронических заболеваний" (Method for Treatment of Malignant and Infectious Chronic Diseases) (публикация '654) раскрыт способ лечения субъекта, страдающего злокачественным или инфекционным хроническим заболеванием, включающий способ иммунизации субъекта вакциной, содержащей "собственный антиген", ассоциированный со злокачественным или инфекционным хроническим заболеванием, который связан с белком-носителем; лечение субъекта иммуномодулирующим средством; и вторичную иммунизацию субъекта вакциной этапа 1 и соответствующим адъювантом, выбранным из гидроксида алюминия и Montanide ISA 51 (Seppic, Париж, Франция). К сожалению, получение вакцины химической конъюгацией, как полагают, тормозит иммунный ответ.
[0011] Большинство описанных выше вакцин характеризуются рядом ограничений, главным образом, обусловленных способом получения и возможным отсутствием однородности и гомологии белкового продукта. Описанные выше вакцины, как правило, содержат смесь рекомбинантного белка-носителя и полипептидов человеческого происхождения, которые химически связаны с помощью глутарового альдегида. К сожалению, этот реакционно-способный реагент может образовывать нежелательные ковалентные поперечные связи между различными химическими группами и, как правило, приводит к получению весьма неоднородного продукта. Таким образом, полученные вакцины могут включать не только молекулы белков-носителей с различными количествами прикрепленных к ним целевых полипептидов человека (например, 0, 1, 2, 3 и т. д.), но и каждый из полипептидов человека может быть прикреплен к носителю посредством различных атомов, а также в различных положениях и в различных ориентациях. Кроме того, как целевой полипептид, так и молекулы белков-носителей могут связываться сами с собой, что приводит к образованию разнообразных гомомультимеров, которые могут не обладать клинической эффективностью и могут не способствовать выработке противоопухолевого иммунного ответа у пациента.
КРАТКОЕ ОПИСАНИЕ
[0012] Настоящее раскрытие относится к рекомбинантным белкам и соответствующим способам их получения, описанию рекомбинантных белков и терапевтических способов применения рекомбинантных белков для лечения хронических заболеваний, таких как, например, рак легких, рак молочной железы, рак мочевого пузыря, рак предстательной железы, рак яичников, рак наружных женских половых органов, рак толстой кишки, рак ободочной и прямой кишки, рак кишечника, рак легкого, рак головного мозга, рак пищевода, другие виды рака и другие заболевания.
[0013] В иллюстративном варианте осуществления рекомбинантный белок представляет собой иммуногенную белковую молекулу, включающую одну или несколько последовательностей, которые сворачиваются в физическую структуру, например, включающую одну или несколько последовательностей белкового холерного токсина B (CT-B) из Vibrio cholera или его искусственного эквивалента, и включающую одну или несколько последовательностей одного или нескольких эпитопов факторов роста человека. Включения факторов роста или их частей могут присутствовать в нескольких участках, в виде отдельного антигена, в паре и/или в виде более длинных цепей антигенной молекулы(молекул) на участок.
[0014] В другом иллюстративном варианте осуществления рекомбинантный белок представляет собой иммуногенную белковую молекулу, включающую одну или несколько последовательностей, которые сворачиваются в физическую структуру, например, включающую одну или несколько последовательностей белкового холерного токсина B (CT-B) из Vibrio cholera или его искусственного эквивалента, и включающую одну или несколько последовательностей одного или нескольких опухолевых антигенов или их частей. Рекомбинантный белок может также включать одну или несколько последовательностей одного или нескольких факторов роста или их частей и/или одну или несколько последовательностей одного или нескольких рецепторов или их частей.
[0015] В другом иллюстративном варианте осуществления рекомбинантный белок представляет собой иммуногенную белковую молекулу, включающую одну или несколько последовательностей, которые сворачиваются в физическую структуру, например, включающую одну или несколько последовательностей белкового холерного токсина B (CT-B) из Vibrio cholera или его искусственного эквивалента, и включающую одну или несколько последовательностей одного или нескольких рецепторов или их частей. Рекомбинантный белок может также включать одну или несколько последовательностей одного или нескольких факторов роста или их частей и/или одну или несколько последовательностей одного или нескольких опухолевых антигенов или их частей.
[0016] В данных иллюстративных вариантах осуществления включения опухолевого антигена(ов) или их частей, рецептора(ов) или их частей и/или фактора(ов) роста или их частей могут присутствовать в нескольких участках в виде отдельного антигена или рецептора, в паре и/или в виде более длинных цепей антигенной или рецепторной молекулы(молекул) на участок.
[0017] В иллюстративном варианте осуществления последовательность опухолевого антигена может включать в себя последовательность простатического специфического антигена (PSA) или его части. В иллюстративном варианте осуществления последовательность рецептора может включать в себя последовательность рецептора эпидермального фактора роста человека 2 (Her2) или его части и/или рецептора эпидермального фактора роста человека 3 (Her3) или его части.
[0018] В иллюстративном варианте осуществления последовательность фактора роста может включать в себя последовательность эпидермального фактора роста (EGF) или значительную часть соответствующей кодирующей области(ей) EGF, включающей нейтрализующий домен EGF, в одном или нескольких положениях в рекомбинантном белке. В других иллюстративных вариантах осуществления последовательность фактора роста может включать в себя цепь полной длины, или ее часть, одного или нескольких из приведенных далее факторов роста и/или альтернативных "собственных антигенов", таких как, без ограничения, другие факторы роста, включая, без ограничения, EGF, IGF-1, IGF-2, FGF, TGF-β, TGF-α, VEGF-A, VEGF-B, VEGF-C, VEGF-D, PDGF, NGF, EGF, HGF, BMP и IL 1-6. В пределах объема настоящего раскрытия подразумевают, что факторы роста могут быть выбраны из факторов роста, которые имеют человеческое и нечеловеческое происхождение. В пределах объема настоящего раскрытия также подразумевают, что указанная последовательность факторов роста может быть практически подобной факторам роста либо человеческого, либо нечеловеческого происхождения, или указанная последовательность может содержать их функциональные части. Кроме того, рекомбинантный белок может включать один или несколько включений других последовательностей, которые можно применять для функционального моделирования части или всех факторов роста в пределах последовательности рекомбинантного иммуногенного белка. В одном варианте осуществления можно включить или добавить дополнительные фланкирующие остатки к минимальной последовательности, что обеспечивает присутствие целостного нейтрализующего домена молекулы в естественной конформации и обеспечивает его доступность для клеток иммунной системы.
[0019] В контексте настоящего раскрытия "нейтрализующий домен" означает область или области одного или двух членов пары специфического связывания, например, фактора роста и его родственного рецептора, при этом связывание третьей молекулы, которая не является членом пары специфического связывания, с вышеупомянутой областью(ями) будет препятствовать последующему связыванию двух членов пары специфического связывания. Третья молекула может быть другой белковой молекулой, в том числе, без ограничения, антителом, или может быть малой небелковой молекулой и по происхождению может быть либо природной, либо искусственной. Нейтрализующий домен будет, как правило, включать те области членов пары специфического связывания, которые вступают в непосредственный контакт при связывании, и будет также включать области за пределами указанных областей, при этом при связывании с третьей молекулой, привносится достаточное стерическое несоответствие для препятствования непосредственному связыванию членов пары специфического связывания.
[0020] Из уровня техники хорошо известно, что специфическое узнавание лиганда его родственным рецептором определяется взаимодействием между участком связывания рецептора и конкретным "молекулярным портретом" (эпитопом) лиганда. Таким образом, антитело, которое либо связывает, либо другим образом блокирует участок связывания рецептора или связывает или другим образом блокирует эпитоп узнавания у лиганда, будет препятствовать лиганд-рецепторным взаимодействиям. Такие антитела описаны как "нейтрализующие". В контексте настоящего раскрытия желательно, чтобы нейтрализующие антитела вырабатывались хозяином при введении рекомбинантного белка, и, таким образом, последовательность белка может содержать или включать одно или несколько из любого из фактора роста или опухолевого антигена, или соответствующей полученной из них последовательности, такие, чтобы эпитопы, необходимые для связывания с рецептором, присутствовали в функциональной (нативной) конформации.
[0021] Помимо включения множественных копий отдельного опухолевого антигена, рецептора и/или фактора роста, представленных в виде отдельного опухолевого антигена, рецептора и/или фактора роста или его части на физический участок, и/или в виде цепей повторяющихся последовательностей опухолевого антигена, рецептора и/или фактора роста (например, n=1 или несколько), белок в соответствии с настоящим раскрытием может также включать в себя включения одного или нескольких эпитопов или участков связывания из двух или более различных опухолевых антигенов, рецепторов и/или факторов роста, которые представлены в виде отдельных таковых или в виде цепей в различных положениях в пределах последовательности рекомбинантного белка.
[0022] Полученный белок может быть отдельным полипептидом, включающим опухолевый антиген, рецептор и/или фактор роста или один или несколько их эпитопов или участков связывания в пределах последовательности рекомбинантного белка. В иллюстративном варианте осуществления последовательность рекомбинантного белка включает одну или нескольких частей последовательности CT-B и представляет собой включение(ия) последовательности(ей) опухолевого антигена, рецептора и/или фактора роста или одно или несколько включений их эпитопов или участков связывания на поверхности рекомбинантного белка в естественной конформации.
[0023] В другом иллюстративном варианте осуществления раскрыт способ получения состава с белком. В данном иллюстративном варианте осуществления способ включает сборку одного или нескольких отдельных моновалентных или поливалентных мономеров вместе с получением поливалентной вакцины, включающей рекомбинантный белок, включающий один или несколько опухолевых антигенов, рецепторов и/или факторов роста или их части.
[0024] В еще одном иллюстративном варианте осуществления раскрыт способ лечения пациента. В данном иллюстративном варианте осуществления способ включает введение пациенту отдельно одного или нескольких моновалентных или поливалентных искусственных белков на основе одного опухолевого антигена, рецептора и/или фактора роста в один день или в чередующиеся дни или разы на протяжении периода вакцинации.
[0025] В следующем иллюстративном варианте осуществления раскрыт способ лечения пациента. В данном иллюстративном варианте осуществления способ включает введение пациенту отдельно одного или нескольких моновалентных или поливалентных вакцинных искусственных белков на основе одного опухолевого антигена, рецептора и/или фактора роста в фармацевтически приемлемом носителе, включающем адъювант для повышения иммунного ответа.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
[0026] Варианты осуществления, описанные в настоящем раскрытии, проиллюстрированы на фигурах сопроводительных графических материалов, которые предназначены для иллюстрации, а не ограничения, на которых одинаковые позиции подразумевают как относящиеся к одинаковым или соответствующим частям, и в которых:
[0027] на фигуре 1 показана таблица последовательностей и структур молекул EGF ряда организмов;
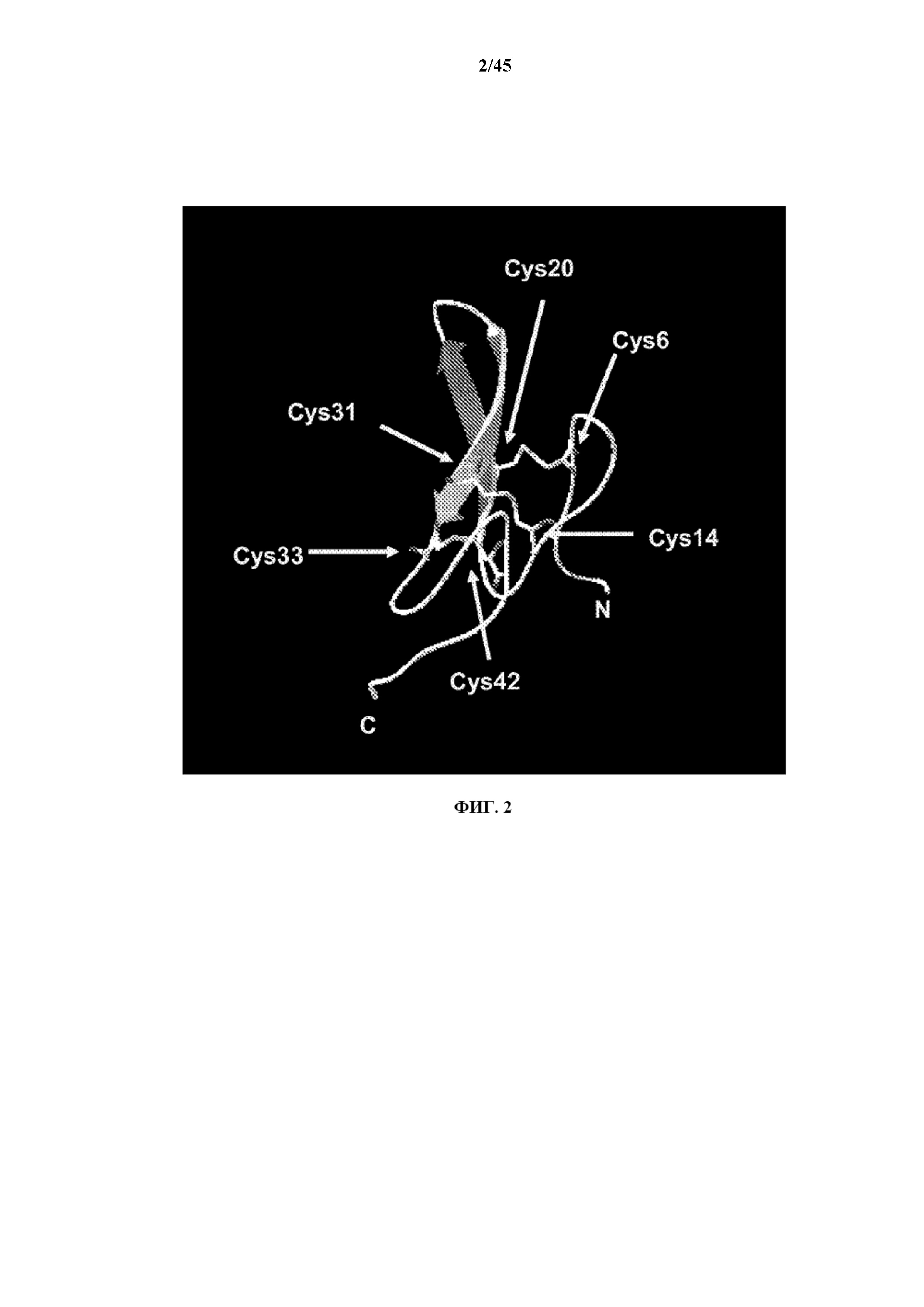
[0028] на фигуре 2 показан вариант осуществления структуры молекулы EGF человека, включающий нейтрализующий домен EGF;
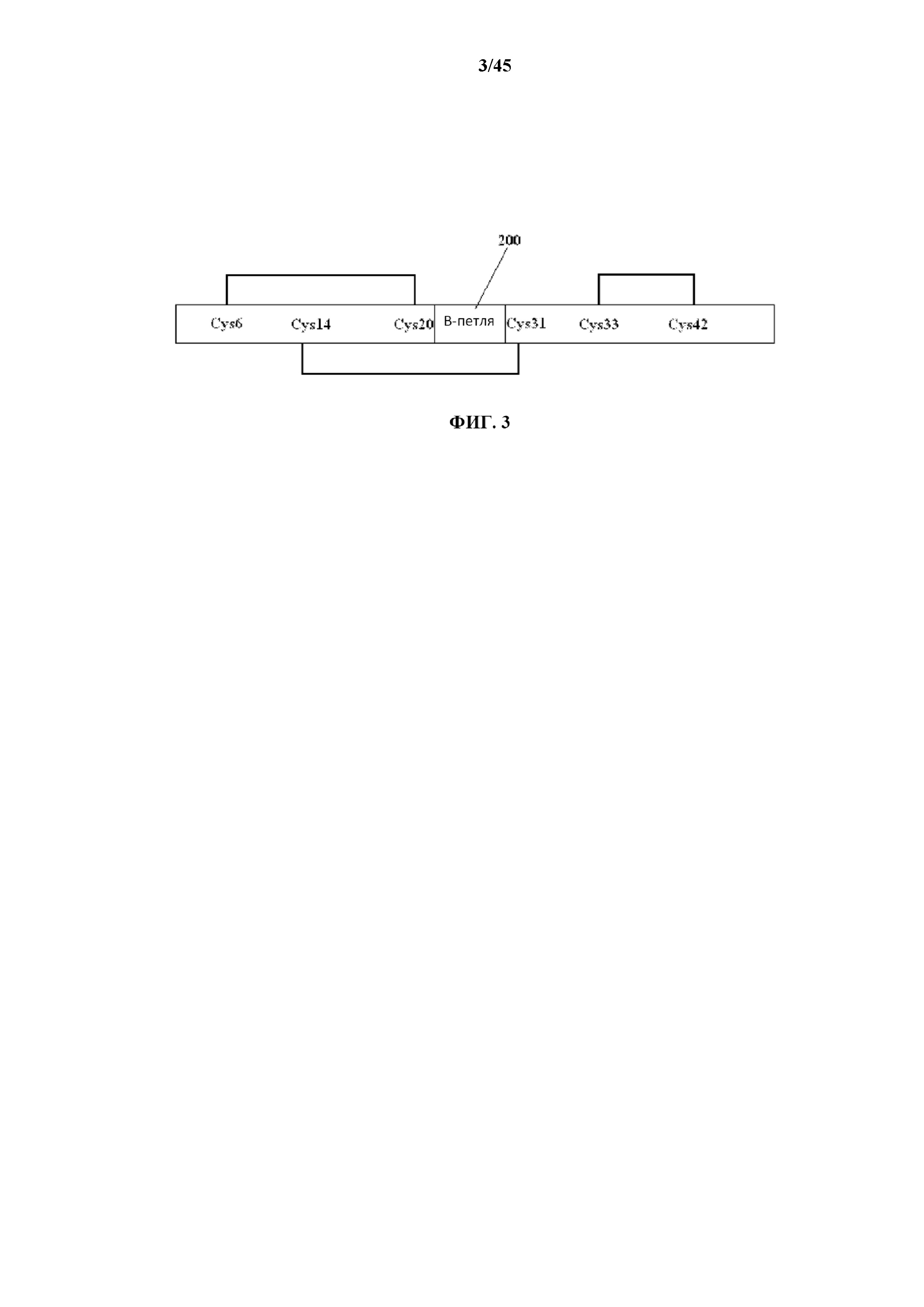
[0029] на фигуре 3 показан вариант осуществления упрощенной линейной структуры цистеиновых пар молекулы EGF, включающей нейтрализующий домен EGF;
[0030] на фигуре 4 показан вариант осуществления минимальной последовательности молекулы EGF, которая представляет собой нейтрализующий домен EGF в правильной конформации;
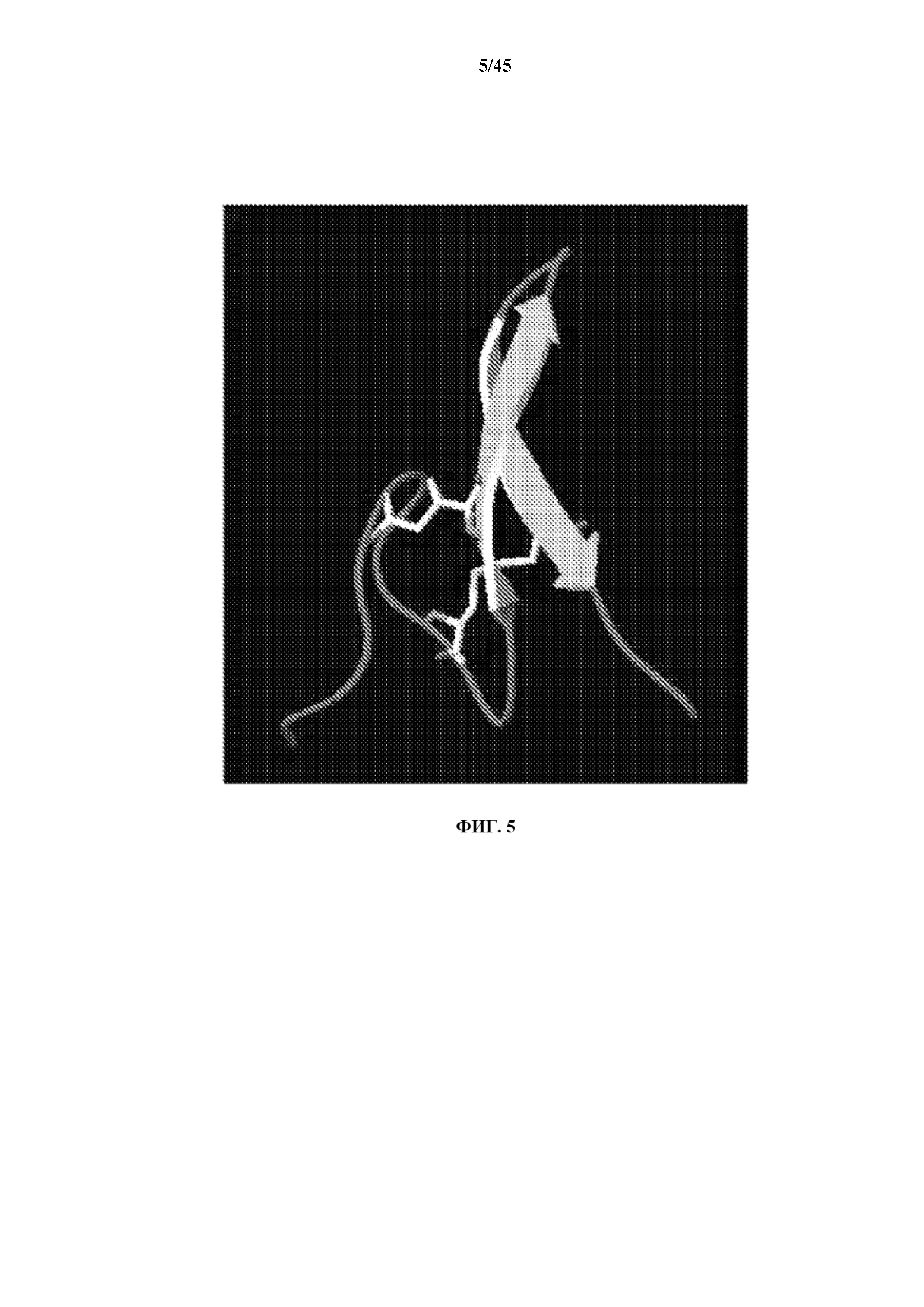
[0031] на фигуре 5 показан вариант осуществления структуры модифицированной искусственной молекулы, включающей нейтрализующий домен EGF;
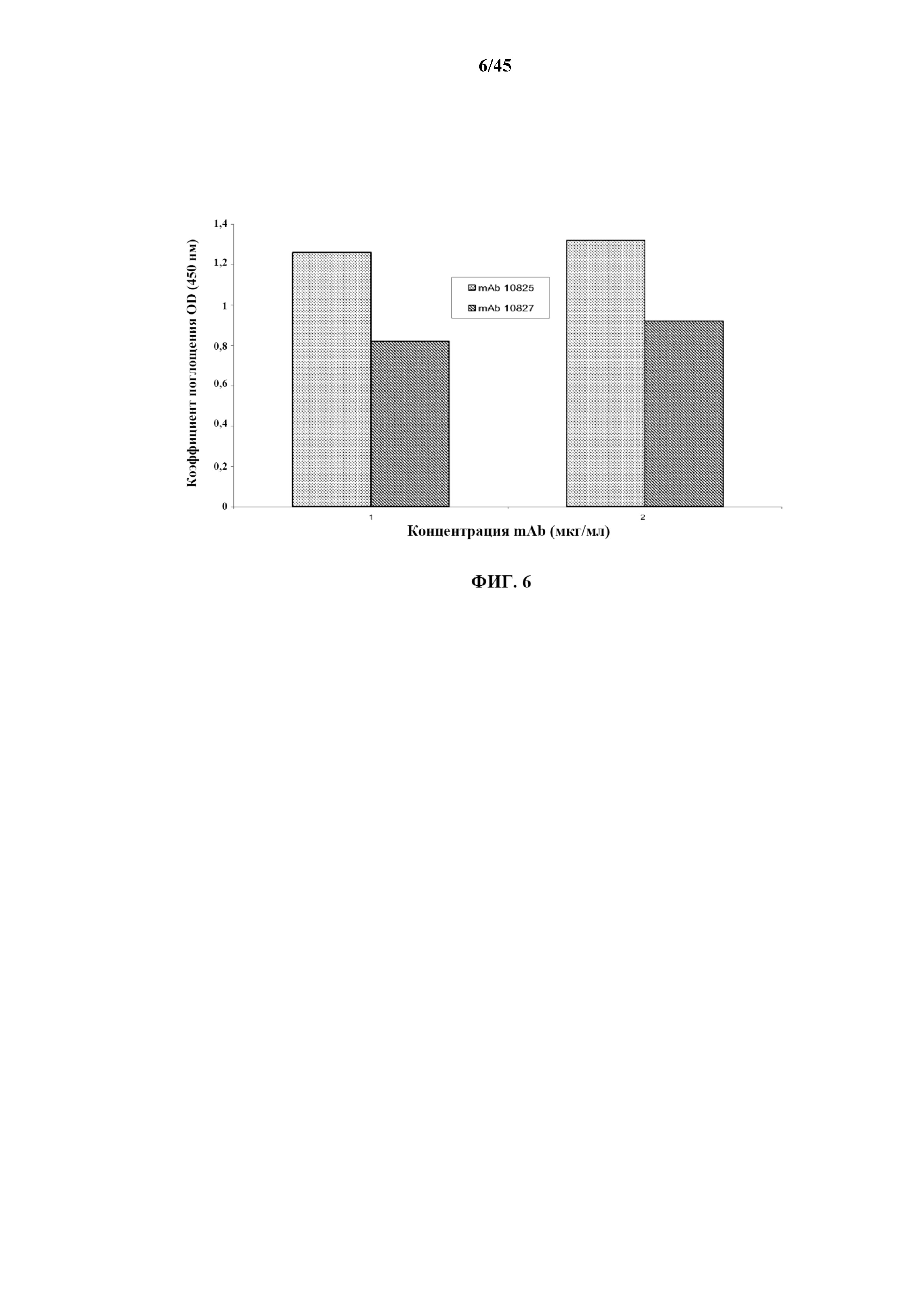
[0032] на фигуре 6 показана гистограмма связывания mAb 10825 и mAb 10827 с rHuEGF с оптической плотностью (OD), измеряемой при 450 нм;
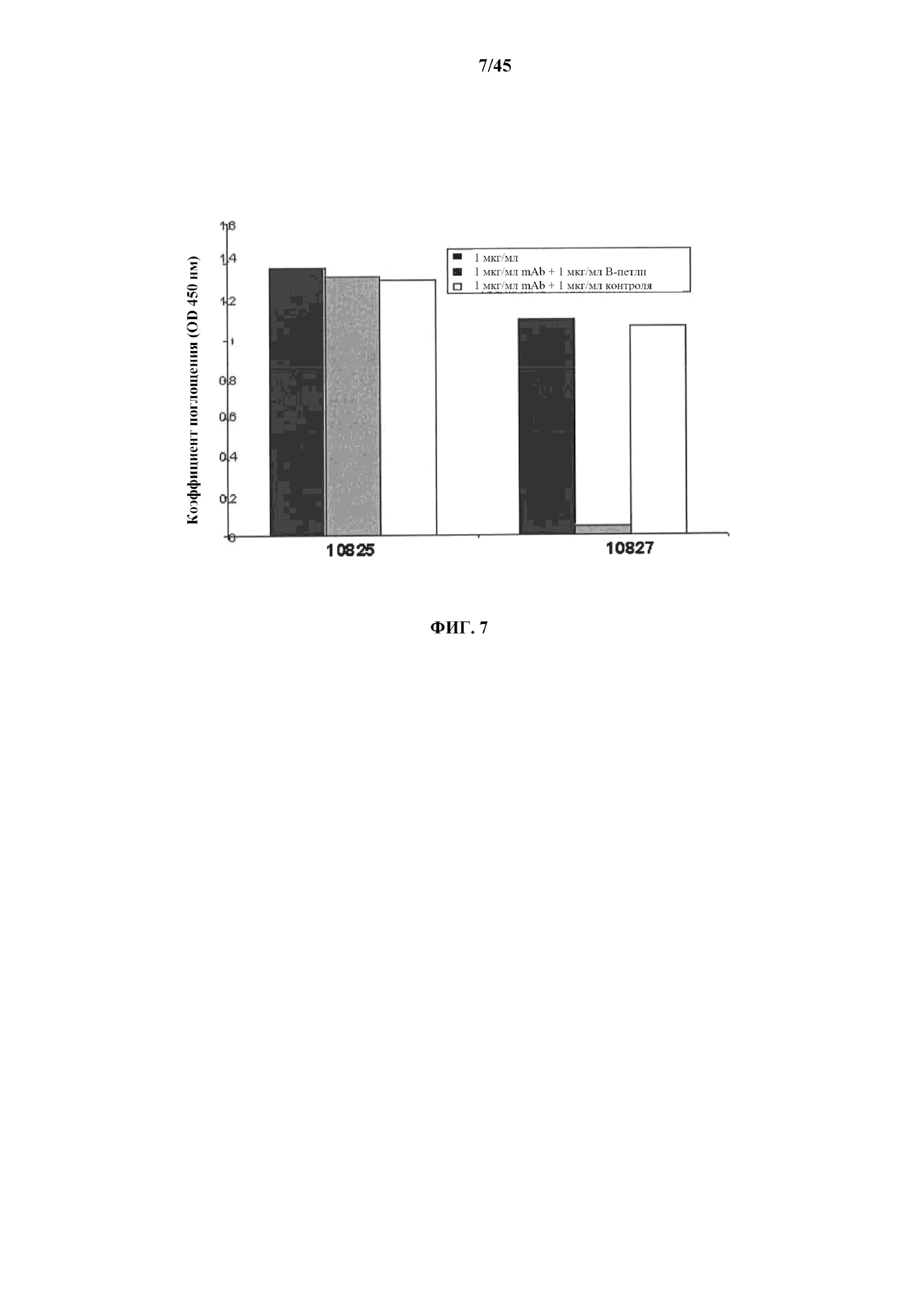
[0033] на фигуре 7 показана гистограмма связывания mAb 10825 и mAb 10827 с rHuEGF в конкуренции со свободным растворимым пептидом, полученным из нейтрализующего домена;
[0034] на фигуре 8 показана линейная диаграмма связывания mAb 10827 к нейтрализующему домену EGF с 6 искусственными белками EGF-CT-B, адсорбированными непосредственно на планшетах для ELISA;
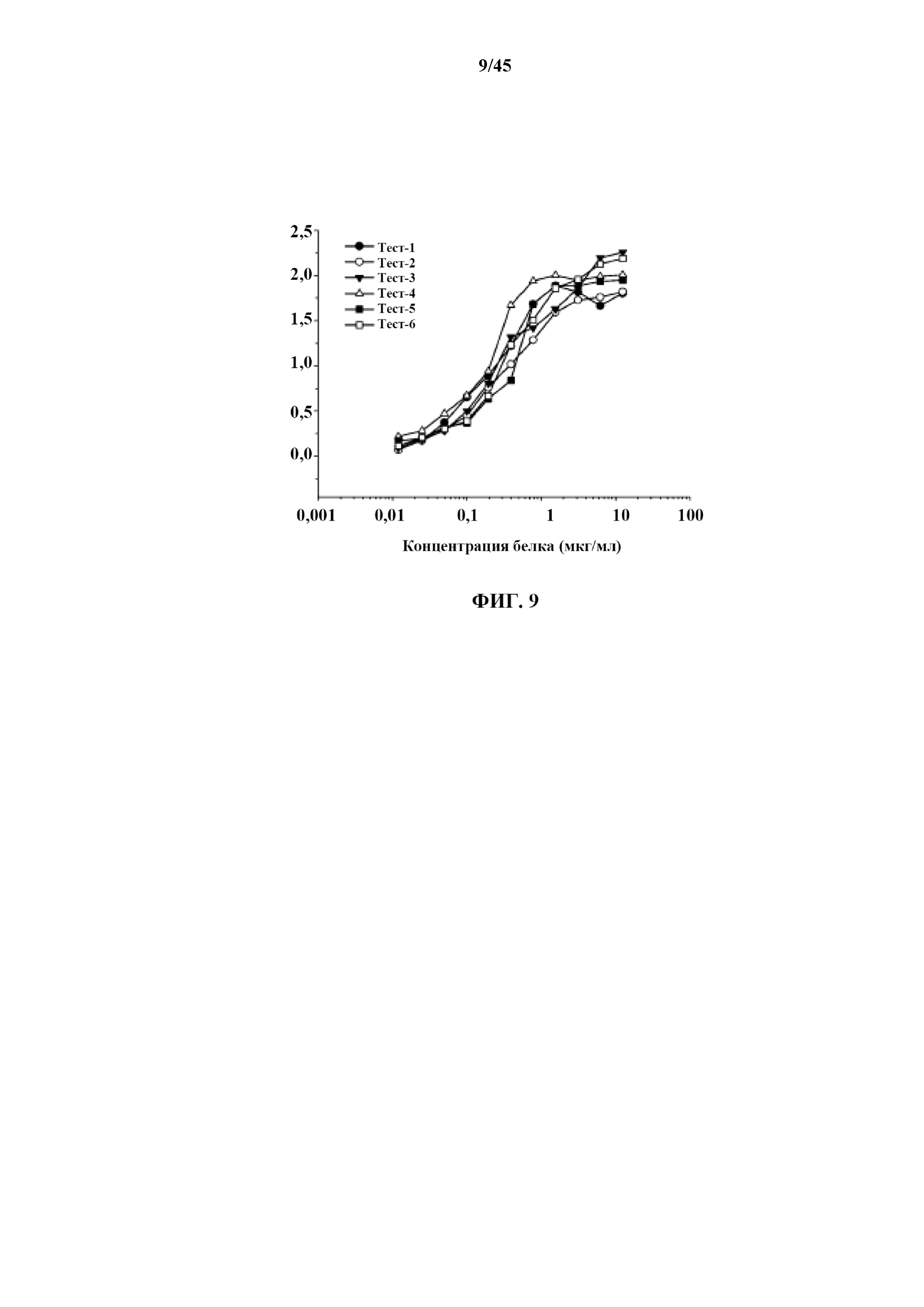
[0035] на фигуре 9 показана линейная диаграмма связывания mAb 10827 к нейтрализующему домену EGF с 6 искусственными белками EGF-CT-B, захваченными антителом кролика к CT-B;
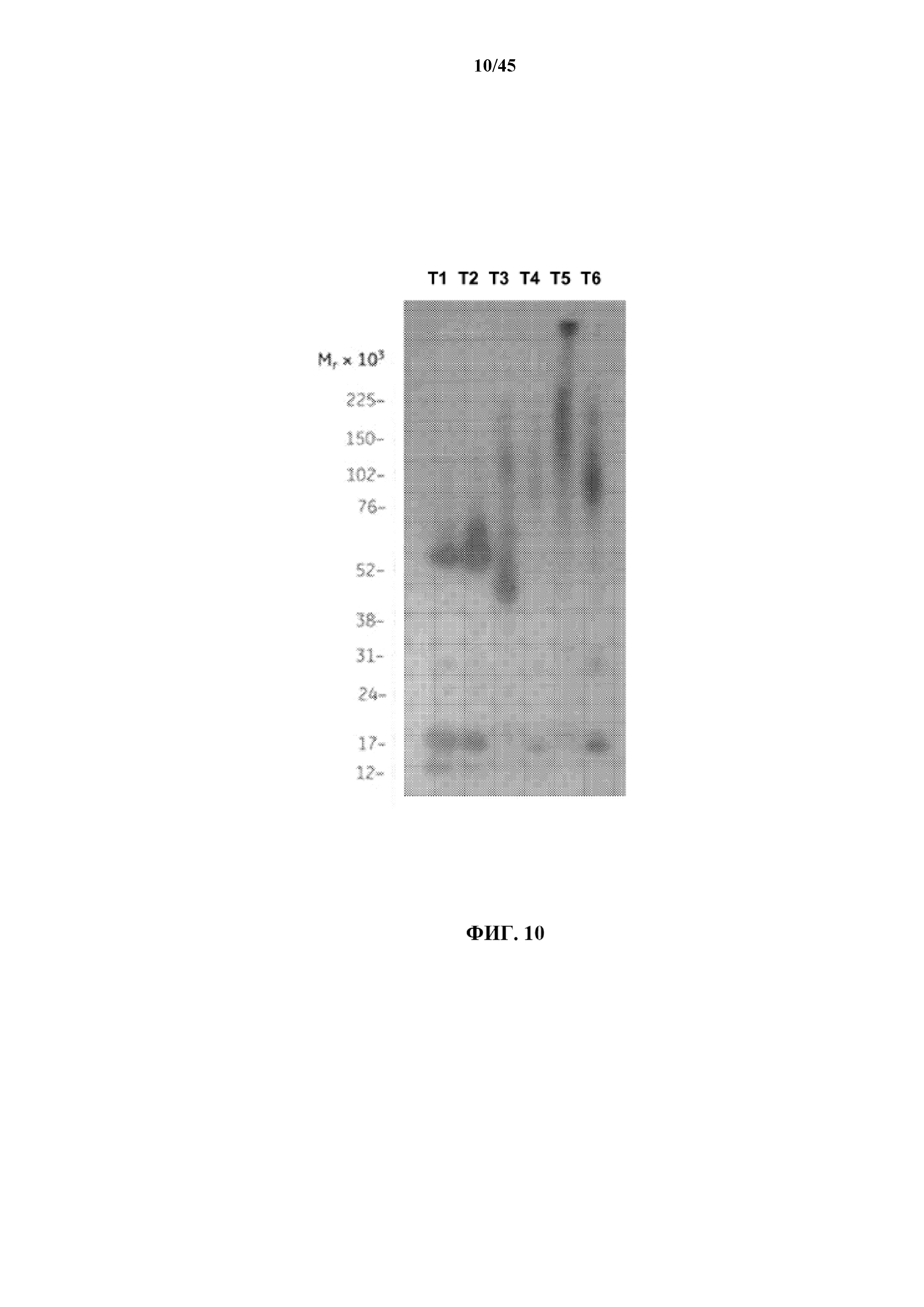
[0036] на фигуре 10 показаны результаты вестерн-блоттинга 6 моновалентных искусственных белков EGF-CT-B, прогнанных на SDS-геле при нативных (без кипячения) условиях и детектированных с помощью антитела к CT-B;
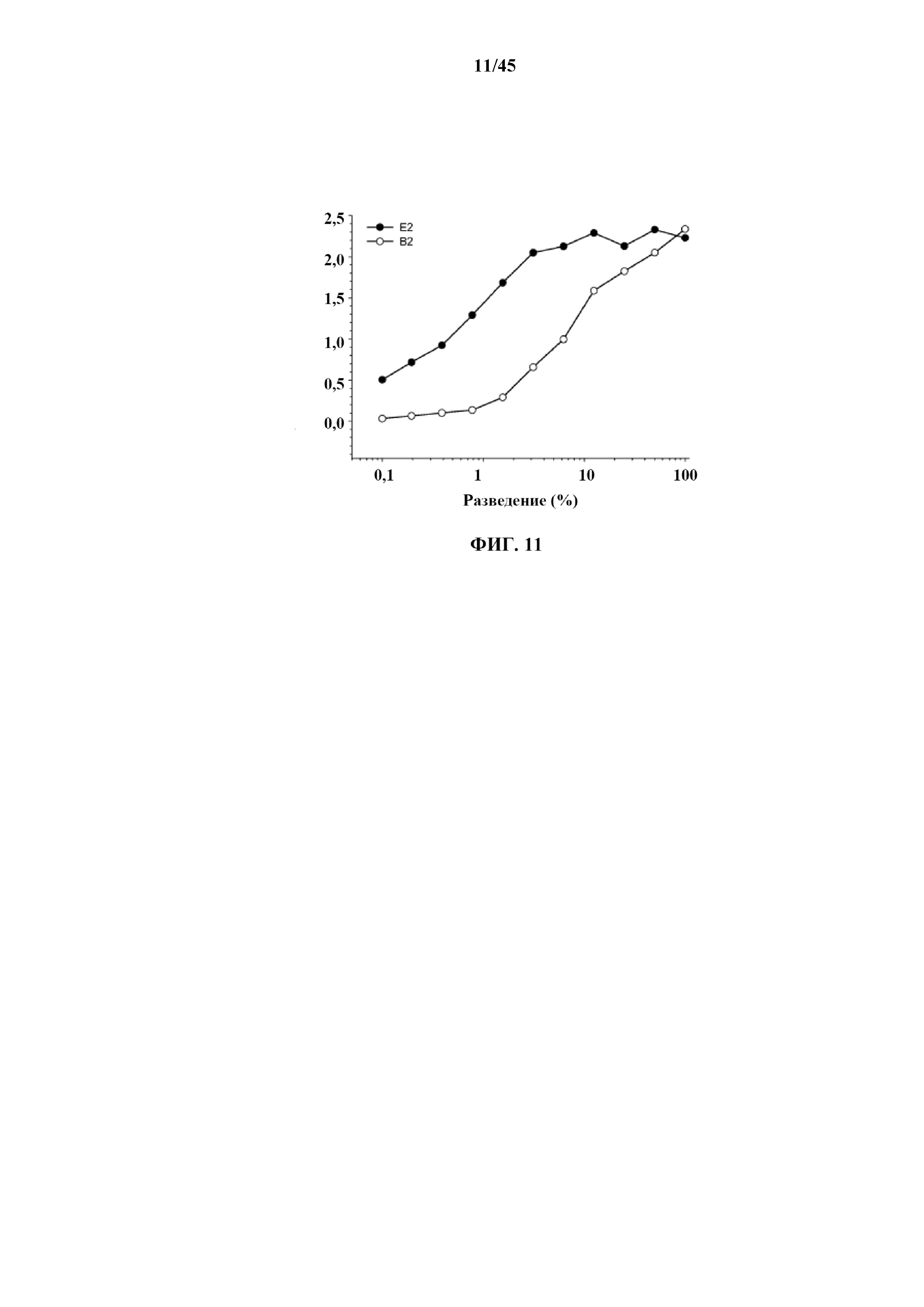
[0037] на фигуре 11 показана линейная диаграмма связывания mAb 10827 к нейтрализующему домену EGF с искусственными белками EGF-CT-B, включающими либо 2 полноразмерные последовательности EGF (E2), либо две частичные последовательности EGF (B2);
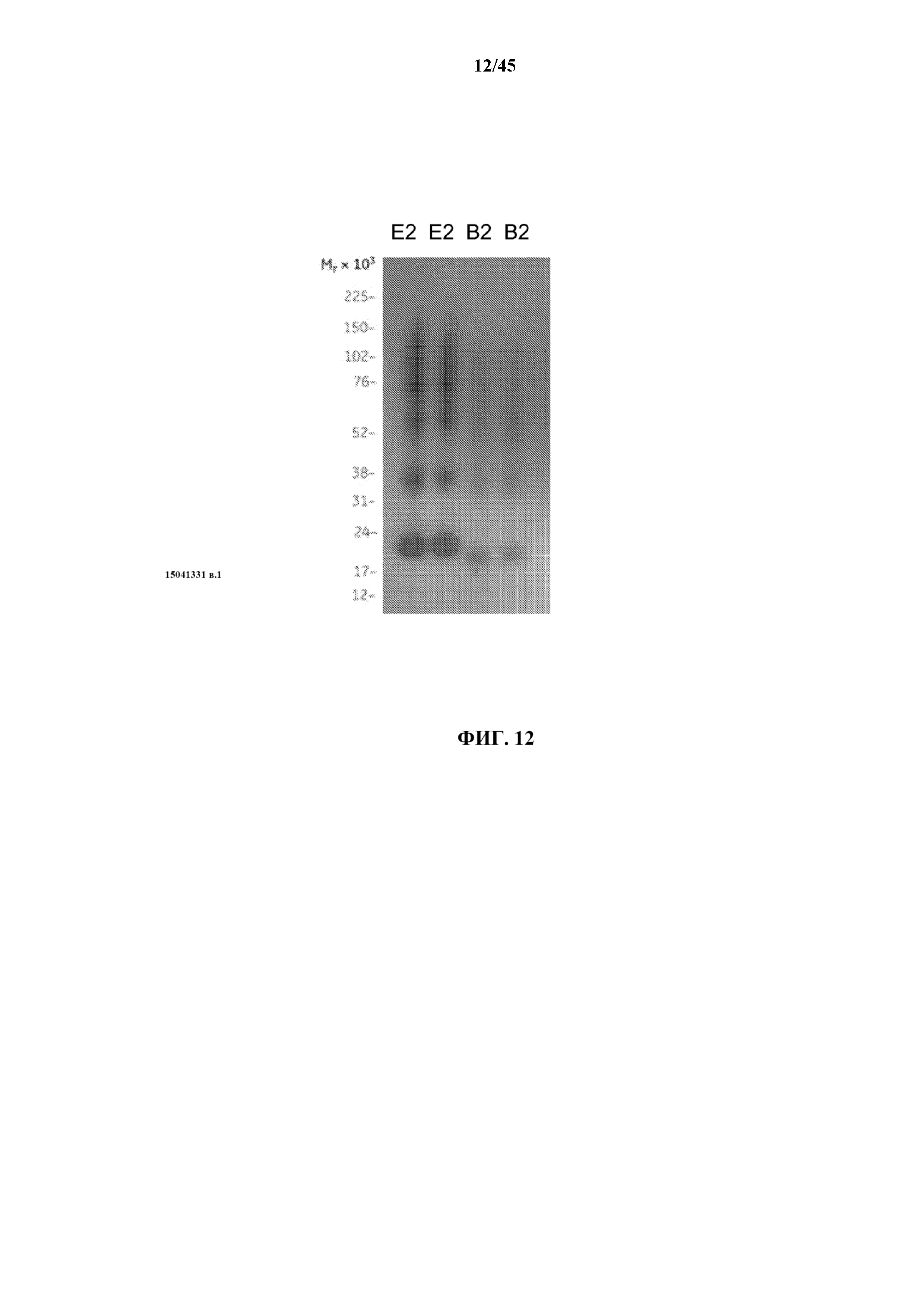
[0038] на фигуре 12 показаны результаты вестерн-блоттинга бивалентных искусственных белков EGF-CT-B, прогнанных на гелях для неденатурирующего SDS-PAGE;
[0039] на фигуре 13 показана последовательность искусственного белка, включающая две полноразмерные последовательности EGF (подчеркнутые) и последовательность CT-B (курсив);
[0040] на фигуре 14 показана последовательность искусственного белка, включающая две последовательности нейтрализующего домена EGF (подчеркнутые) и последовательность CT-B (курсив);
[0041] на фигуре 15 показана последовательность искусственного белка, включающая две частичные последовательности молекулы EGF, включающей нейтрализующий домен EGF, Cys6 - Cys31, (подчеркнутый) и последовательность CT-B (курсив);
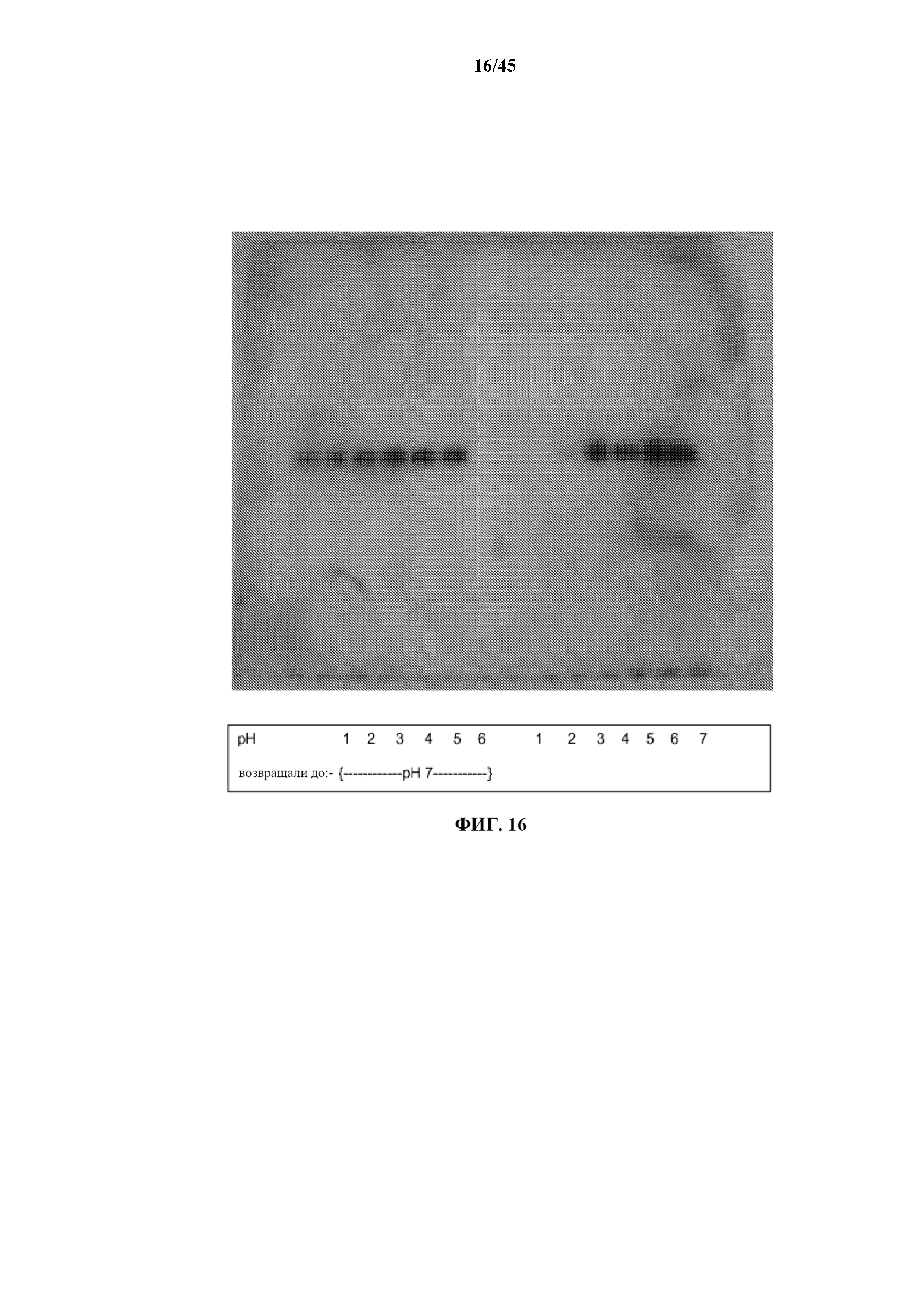
[0042] на фигуре 16 показаны результаты вестерн-блоттинга, демонстрирующие влияние сдвига pH на мультимеризацию нативного белка CT-B; образцы в правой части геля инкубировали в течение 5 мин. при pH, указанном дальше, перед анализом в геле; образцы в левой части инкубировали при pH, указанном дальше, в течение 5 мин., затем нейтрализовали до pH 7,0 в течение 1 часа перед анализом в геле;
[0043] на фигуре 17 показана таблица конструктов T1-T6, E2 и B2, включающих последовательности, содержащие EGF и CT-B;
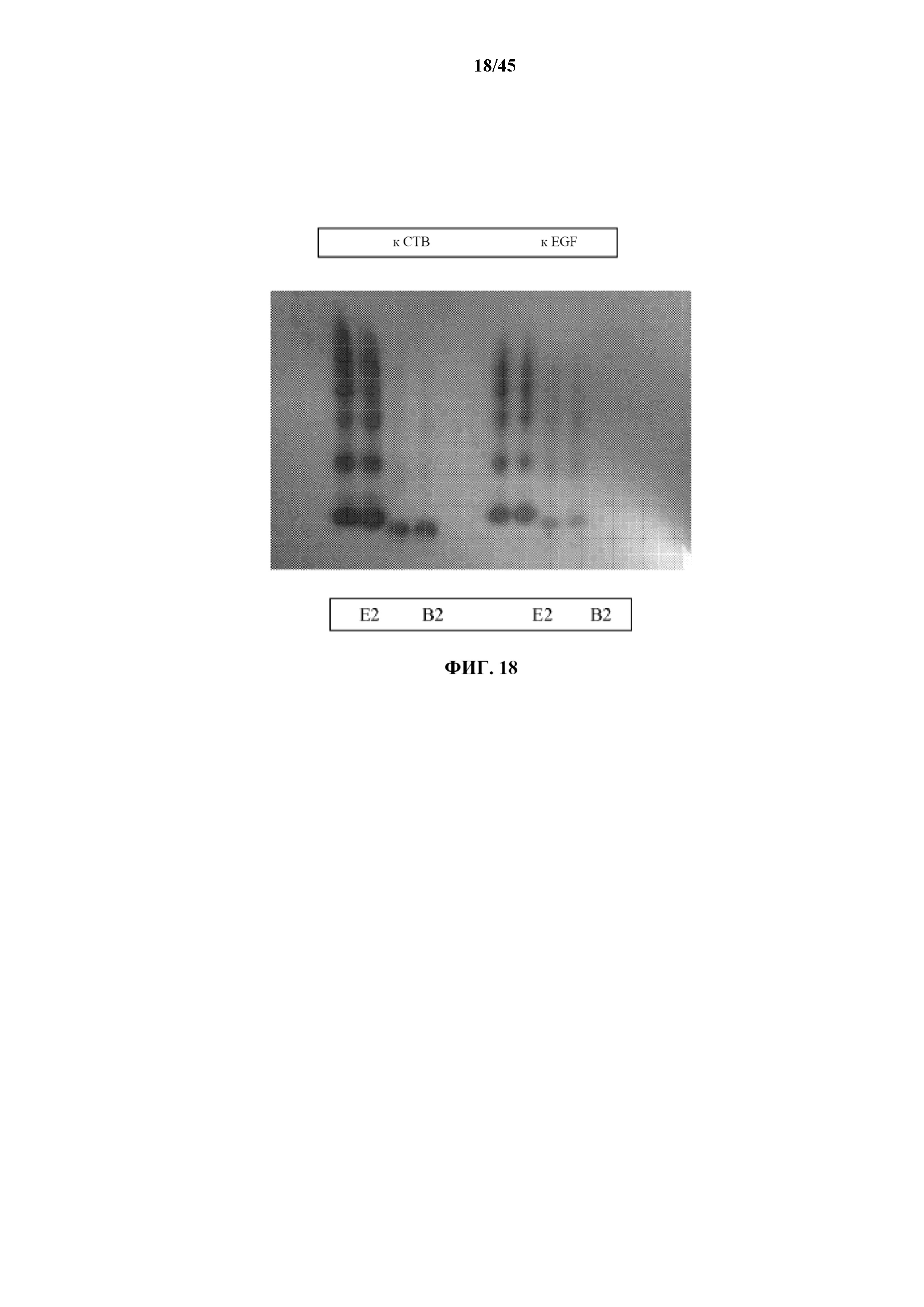
[0044] на фигуре 18 показаны результаты вестерн-блоттинга конструктов E2 и B2;
[0045] на фигуре 19 показаны конструкты E2, E2N и E2C, включающие последовательности, содержащие EGF и CT-B;
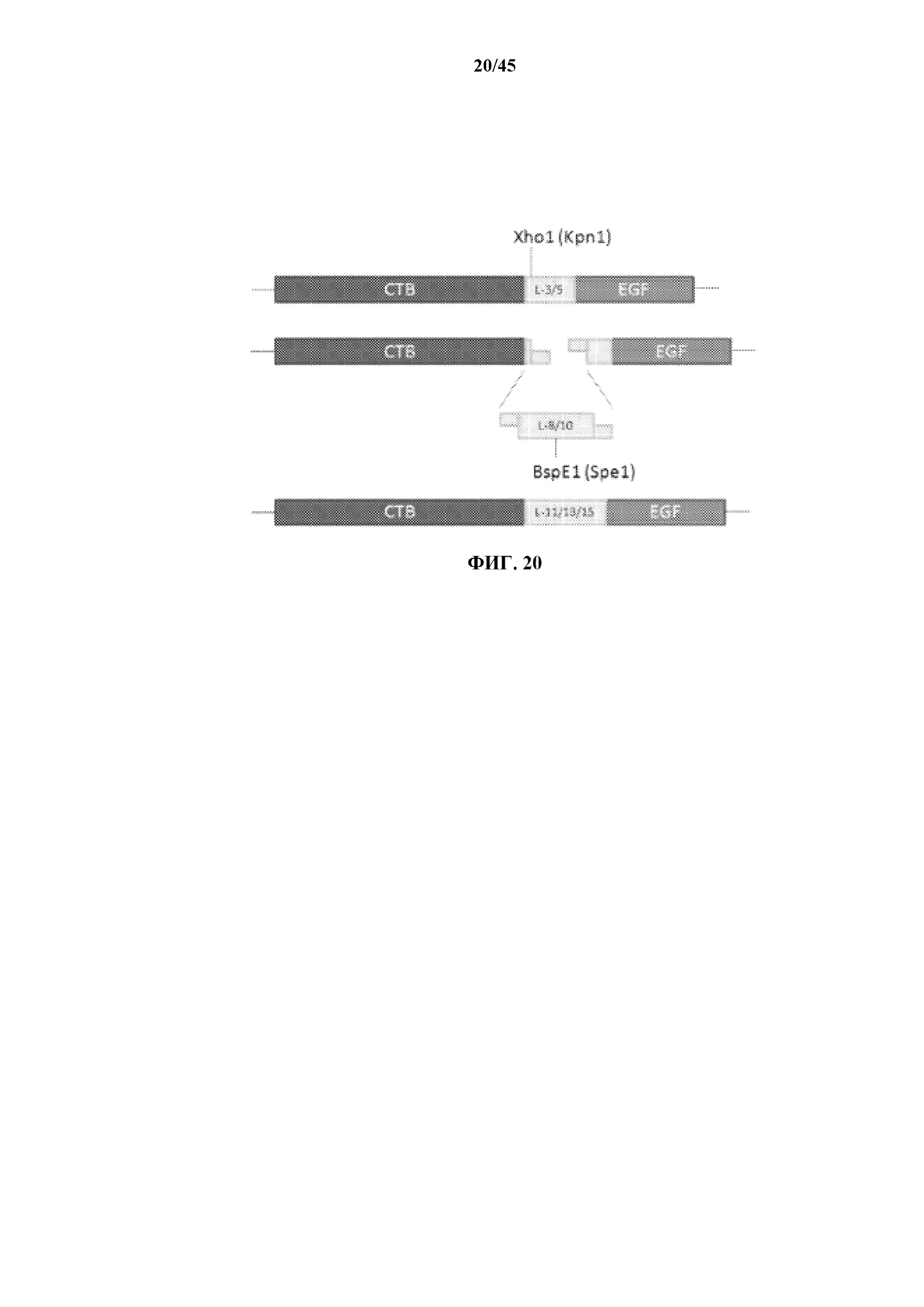
[0046] на фигуре 20 показаны конструкты, включающие последовательности, содержащие EGF и CT-B и содержащие удлиненные аминокислотные линкеры;
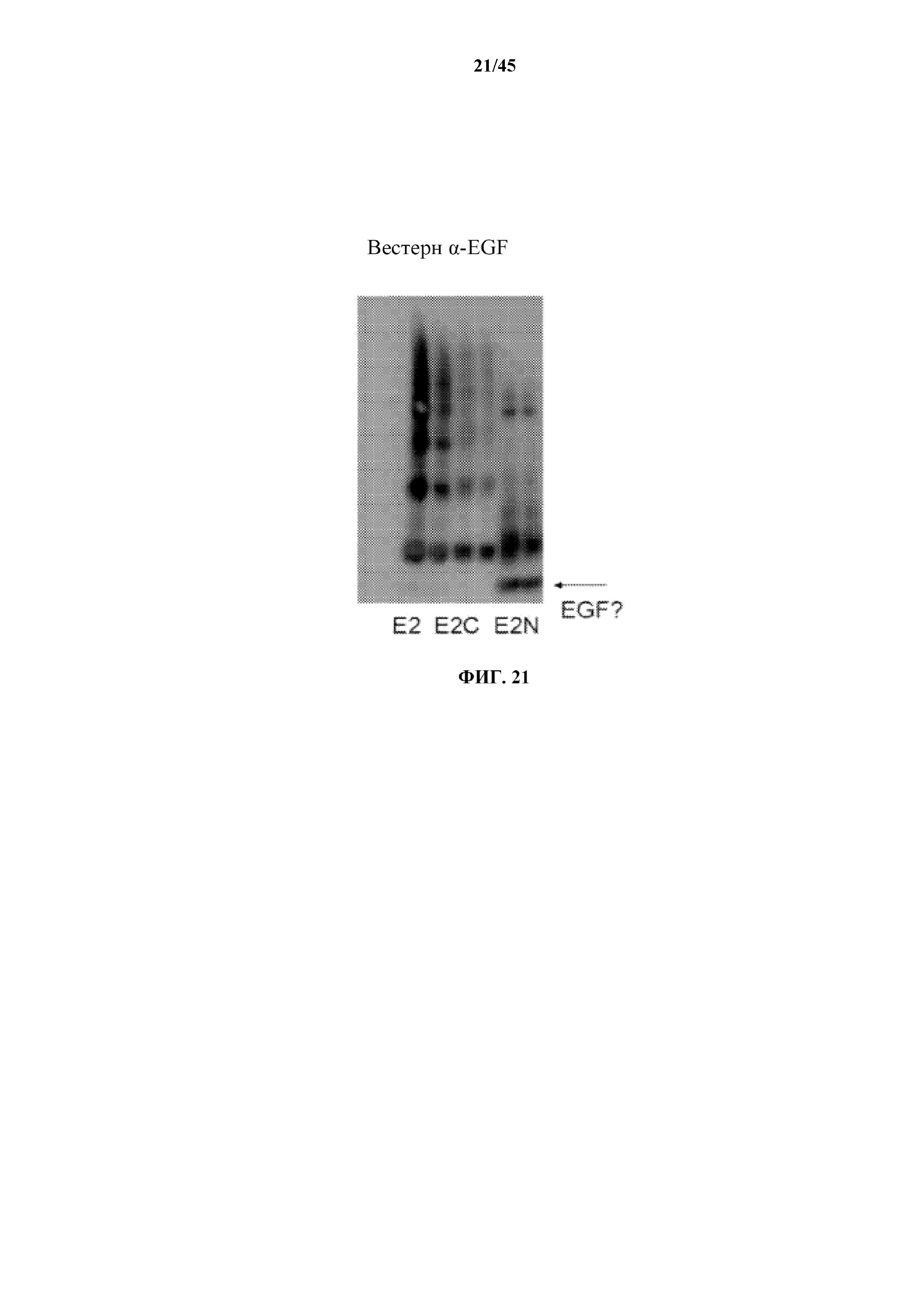
[0047] на фигуре 21 показаны результаты вестерн-блоттинга конструктов E2, E2N и E2C;
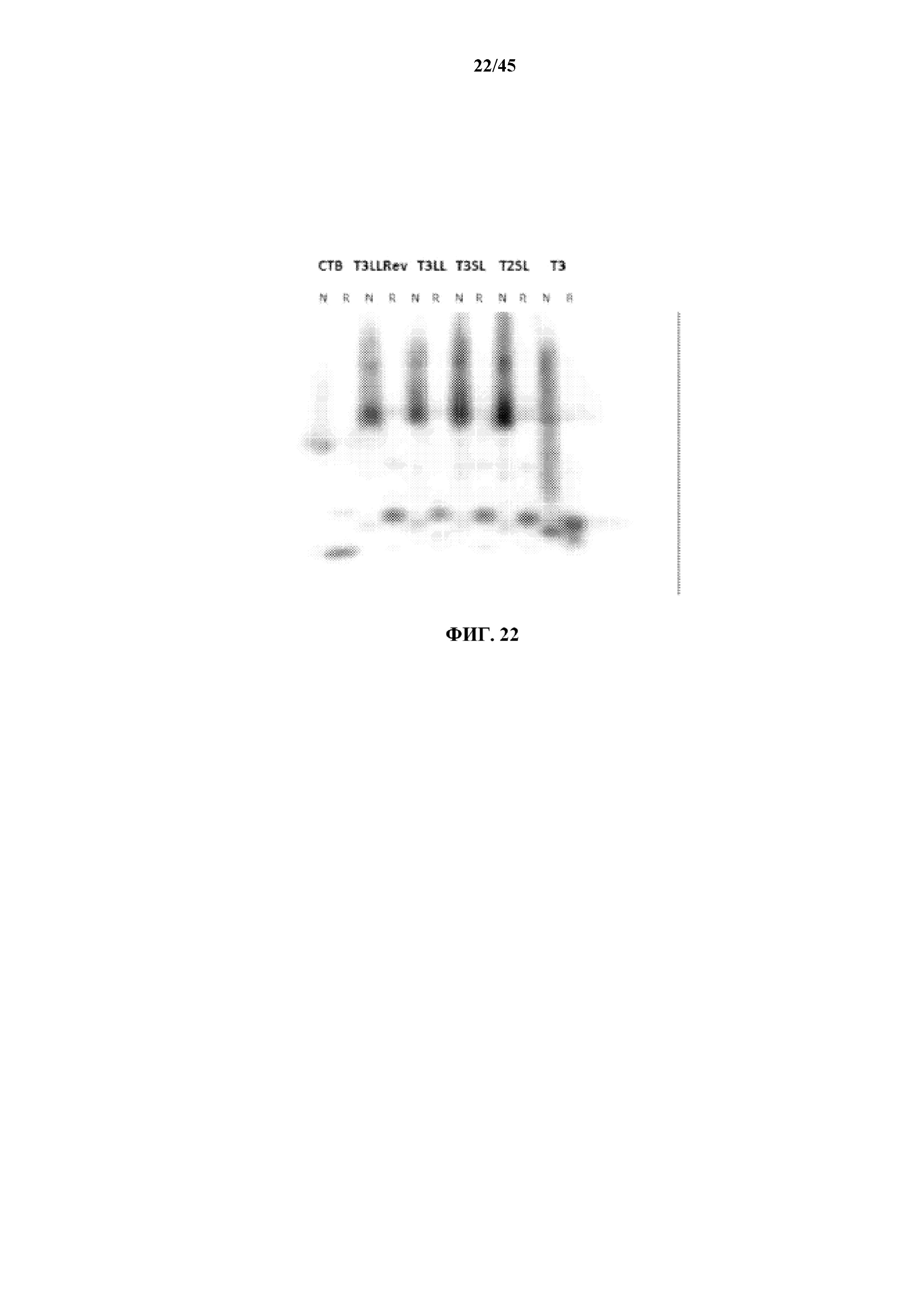
[0048] на фигуре 22 показаны результаты вестерн-блоттинга ряда N-концевых конструктов, включающих удлиненные аминокислотные линкеры; и
[0049] на фигуре 23 показаны результаты вестерн-блоттинга ряда C-коневых конструктов, включающих удлиненные аминокислотные линкеры;
[0050] на фигуре 24 показана последовательность искусственного белка, включающая последовательности IGF1 (подчеркнутая), EGF (подчеркнутая и курсив) и CT-B (курсив);
[0051] на фигуре 25 показана гистограмма результатов ELISA с захватом, демонстрирующих одновременное присутствие последовательностей IGF, EGF и CTB на отдельном рекомбинантном белке; в виде столбцов A и B представлены результаты захвата антителом к EGF, а в виде столбца C представлены результаты антителом к IGF; белки выявляли следующим образом: в случае A антителом к CTB, в случае B антителом к IGF и в случае C антителом к CTB;
[0052] на фигуре 26 показана последовательность искусственного белка, включающая последовательность Hu-IGFl (подчеркнутая) и последовательность CT-B (курсив);
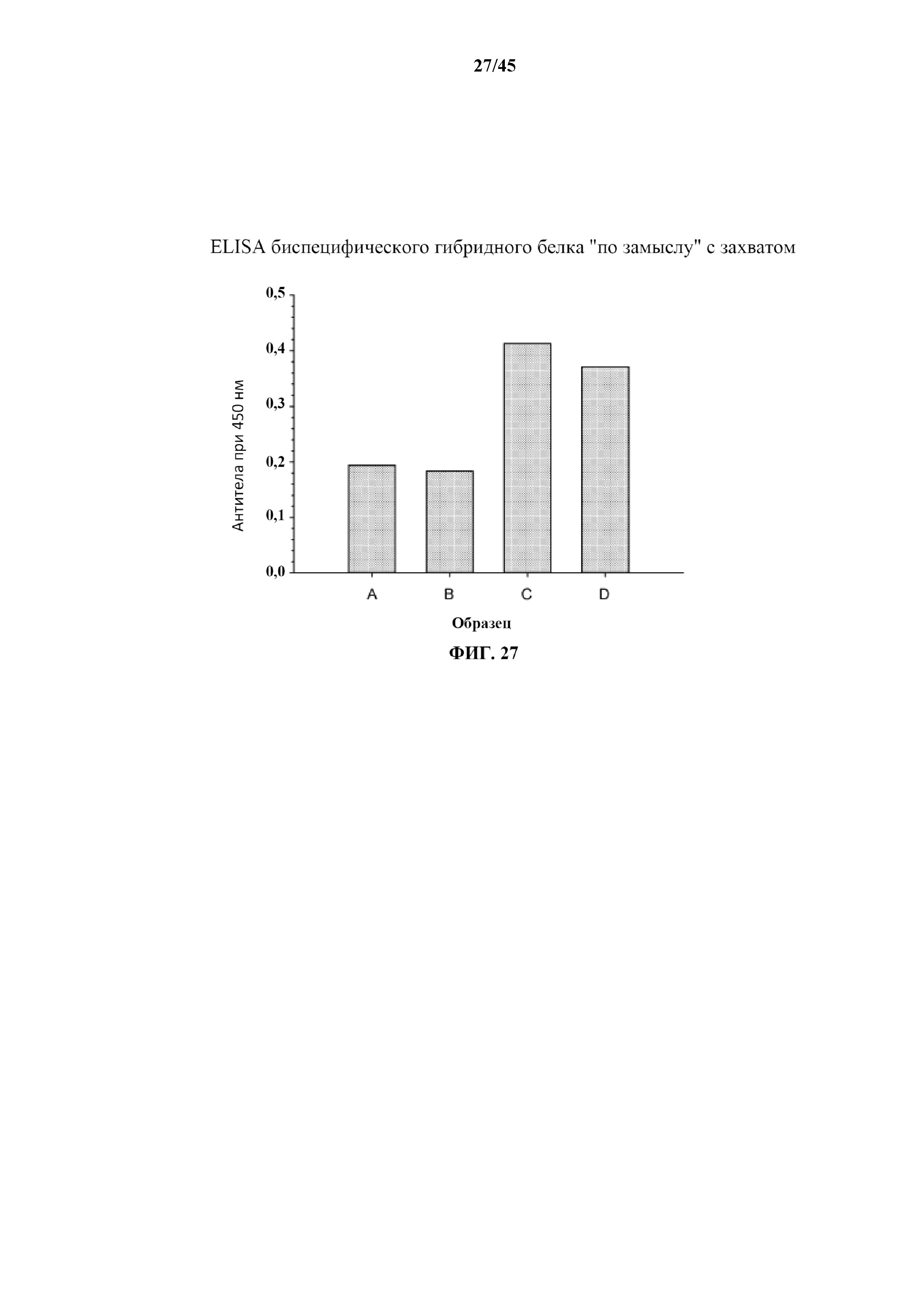
[0053] на фигуре 27 показана гистограмма результатом ELISA с захватом, при котором выявлены гетероолигомеры IGF-CTB и EGF-CTB; все образцы включают IGF, находящийся на С-конце по отношению к CTB. образцы A и B включают EGF, находящийся на С-конце по отношению к CTB, а образцы B и D включают от EGF, находящийся на N-конце по отношению к CTB; образцы A и B захватывались антителом к EGF и выявляли IGF, в то время как образцы C и D захватывались антителом к IGF и выявляли EGF;
[0054] на фигуре 28 (a-e) показаны последовательности искусственного белка, включающие последовательность CT-B (курсив) и последовательности факторов роста (подчеркнуты) a) TGF-бета 1, b) FGF2, c) HGF (NKl), d) IGF 1/2 и e) VEGF-A/C (последовательность VEGF-C подчеркнута и выделена курсивом);
[0055] на фигуре 29 показана гистограмма результатов ELISA с захватом различного спектра гибридных рекомбинантных белков, включающих последовательности, полученные из одного или нескольких факторов роста, совместно с последовательностями CTB; в каждом случае рекомбинантный белок захватывали антителом, специфическим по отношению к одной из последовательностей, а затем выявляли антителом, специфичным для отличной последовательности, как указано далее:
[0056] HGF и TGF-B1 захватывали антителами к α-HGF и α-TGF-B1 и выявляли CTB;
[0057] FGF2 захватывали антителом к α-CTB и выявляли FGF2;
[0058] VEGF A/C захватывали (i) антителом к α-VEGF-A и (ii) антителом к α-VEGF-C и в обоих случаях выявляли CTB;
[0059] IGF 1/2 захватывали антителом к α-IGF1, в обоих случаях, и выявляли (i) антителом к α-CTB и (ii) антителом к α-IGF2;
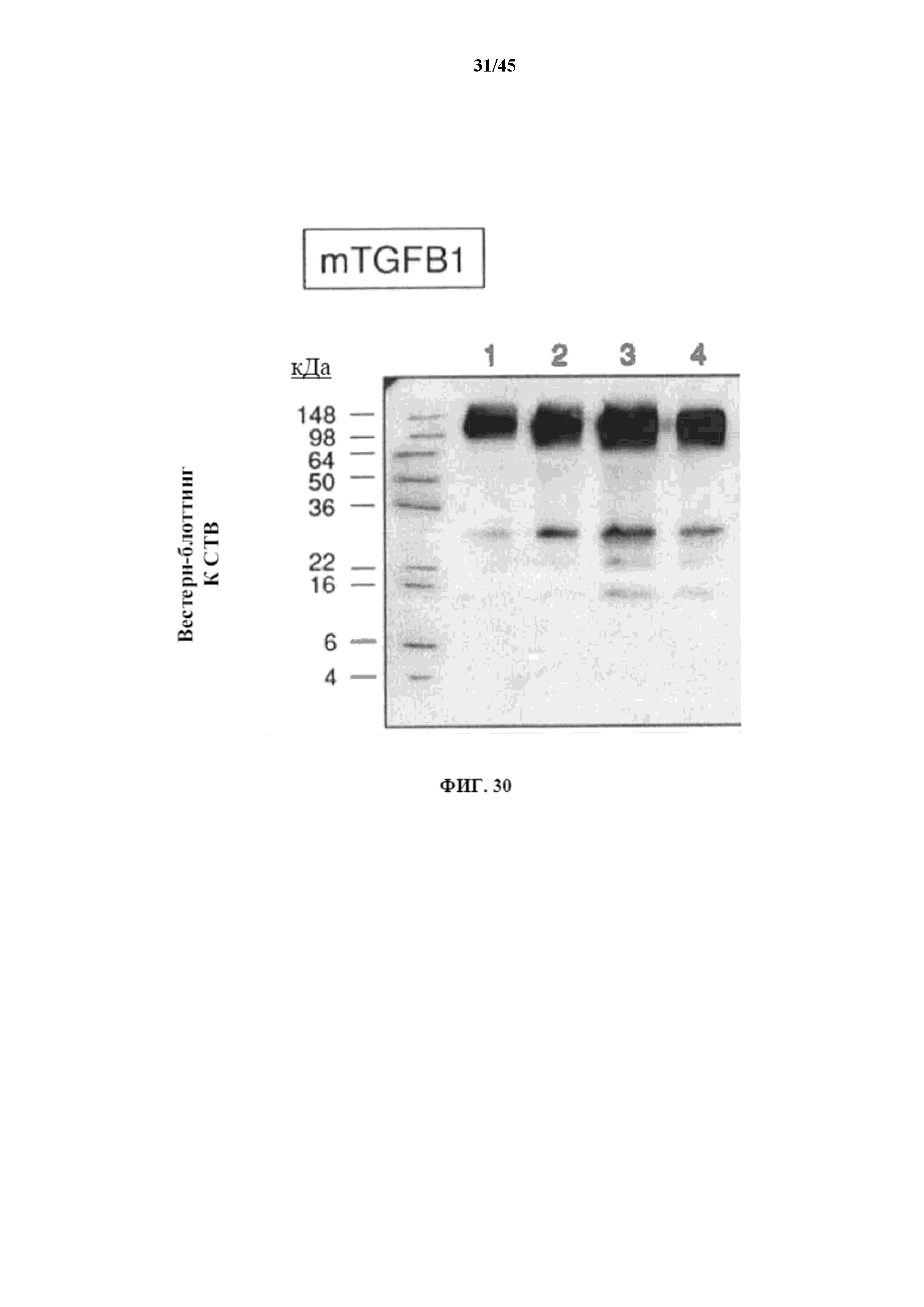
[0060] на фигуре 30 показаны результаты вестерн-блоттинга SDS-PAGE геля нативного рекомбинантного белка TGF-B1-CTB согласно фигуре 28a, из которых видно присутствие в основном пентамерного рекомбинантного белка;
[0061] на фигуре 31 показана последовательность искусственного белка, включающая a) последовательность искусственного белка, включающую последовательность TGF-B1 (подчеркнутая) и последовательность CT-B (курсив), и b) последовательность лигандсвязывающего домена рецептора TGF-бета 2 (подчеркнутая) и последовательность CT-B (курсив);
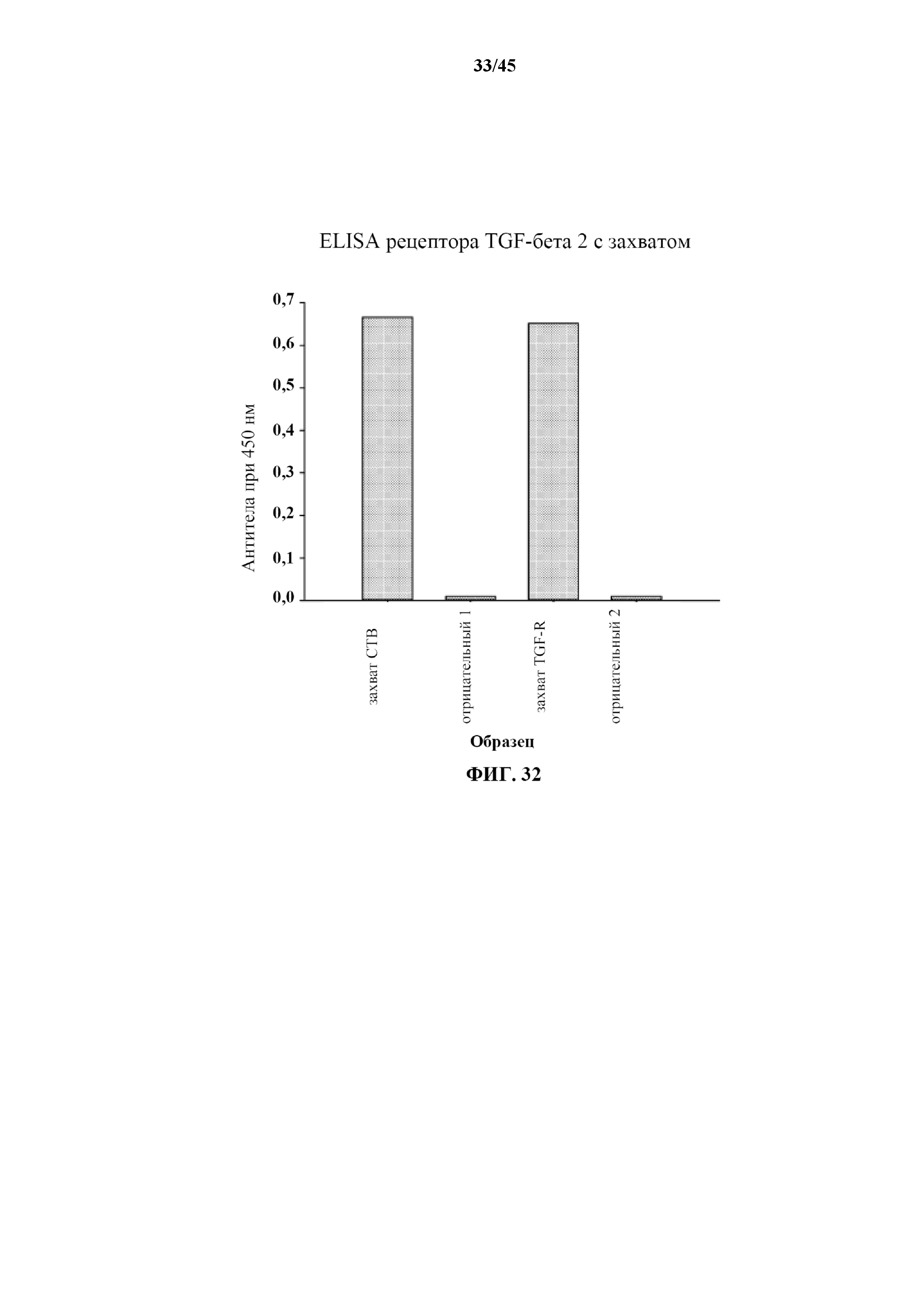
[0062] на фигуре 32 показана гистограмма результатов ELISA с захватом рекомбинантного белка, содержащего последовательности как TGF-бета R2, так и CTB; из диаграммы видно, что обе последовательности могут быть одновременно связаны в обеих ориентациях без асимметрии;
[0063] на фигуре 33 показано, что рекомбинантный белок, содержащий последовательности, полученные из TGF-бета и CTB, способен связываться с рекомбинантным белком, содержащим последовательности, полученные из лигандсвязывающего домена рецептора TGF-бета 2 и CTB;
[0064] на фигуре 34 показаны гуморальные иммунные ответы с участием IgG в сыворотках мышей группы 1 при разведении 1/100 по отношению к r-IGF после иммунизации;
[0065] на фигуре 35 показаны гуморальные иммунные ответы с участием IgG сывороток мышей группы 2 при разведении 1/100 по отношению к r-EGF после иммунизации;
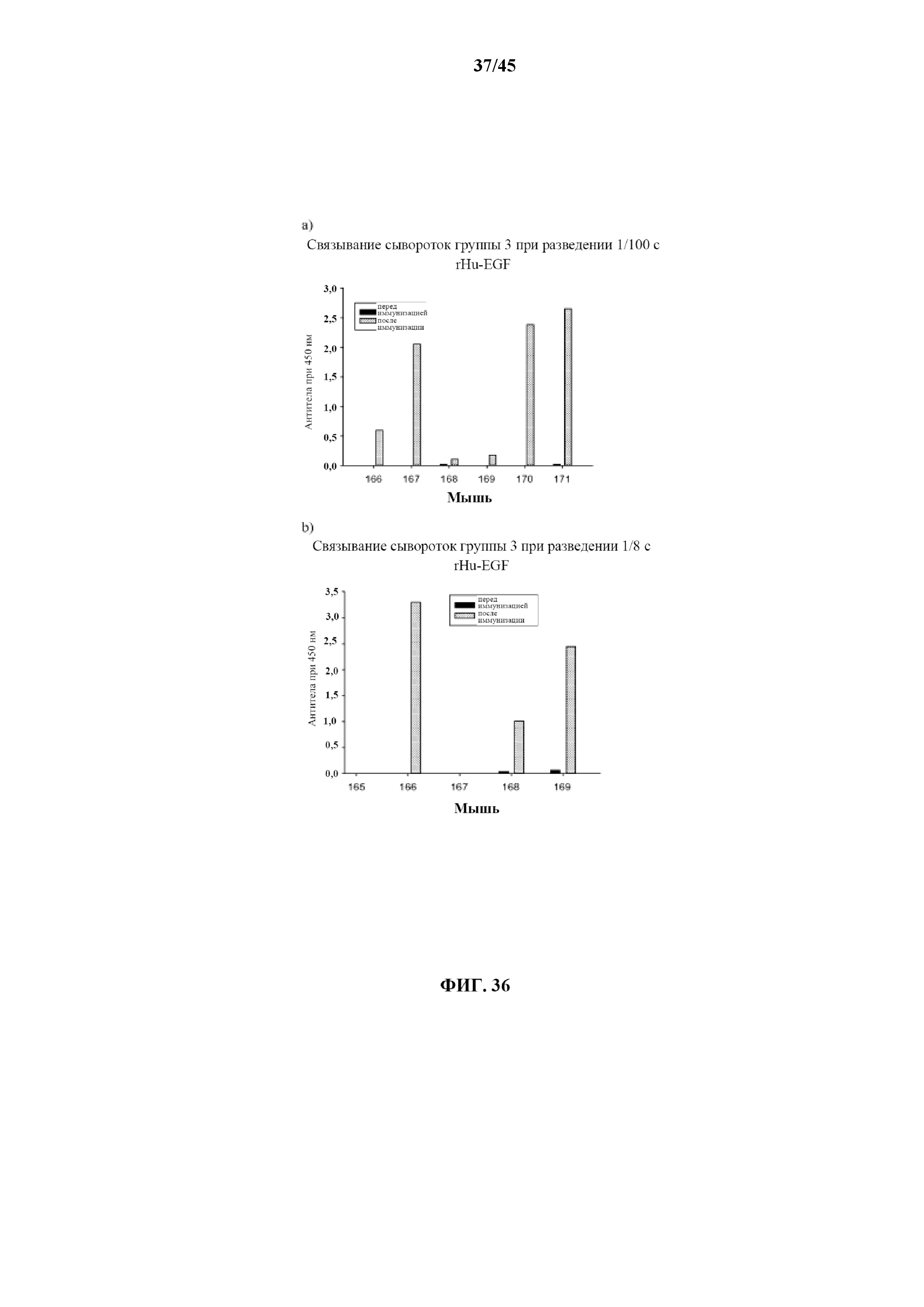
[0066] на фигуре 36 показаны гуморальные иммунные ответы с участием IgG сывороток мышей группы 3 при разведении (a) 1/100 и (b) 1/8 по отношению к r-EGF после иммунизации;
[0067] на фигуре 37 показаны гуморальные иммунные ответы с участием IgG сывороток мышей группы 3 при разведении (a) 1/100 и (b) 1/8 по отношению к r-IGF после иммунизации;
[0068] на фигуре 38 показаны гуморальные иммунные ответы с участием IgG сывороток мышей группы 4 при разведении (a) 1/100 и (b) 1/8 по отношению к r-EGF после иммунизации;
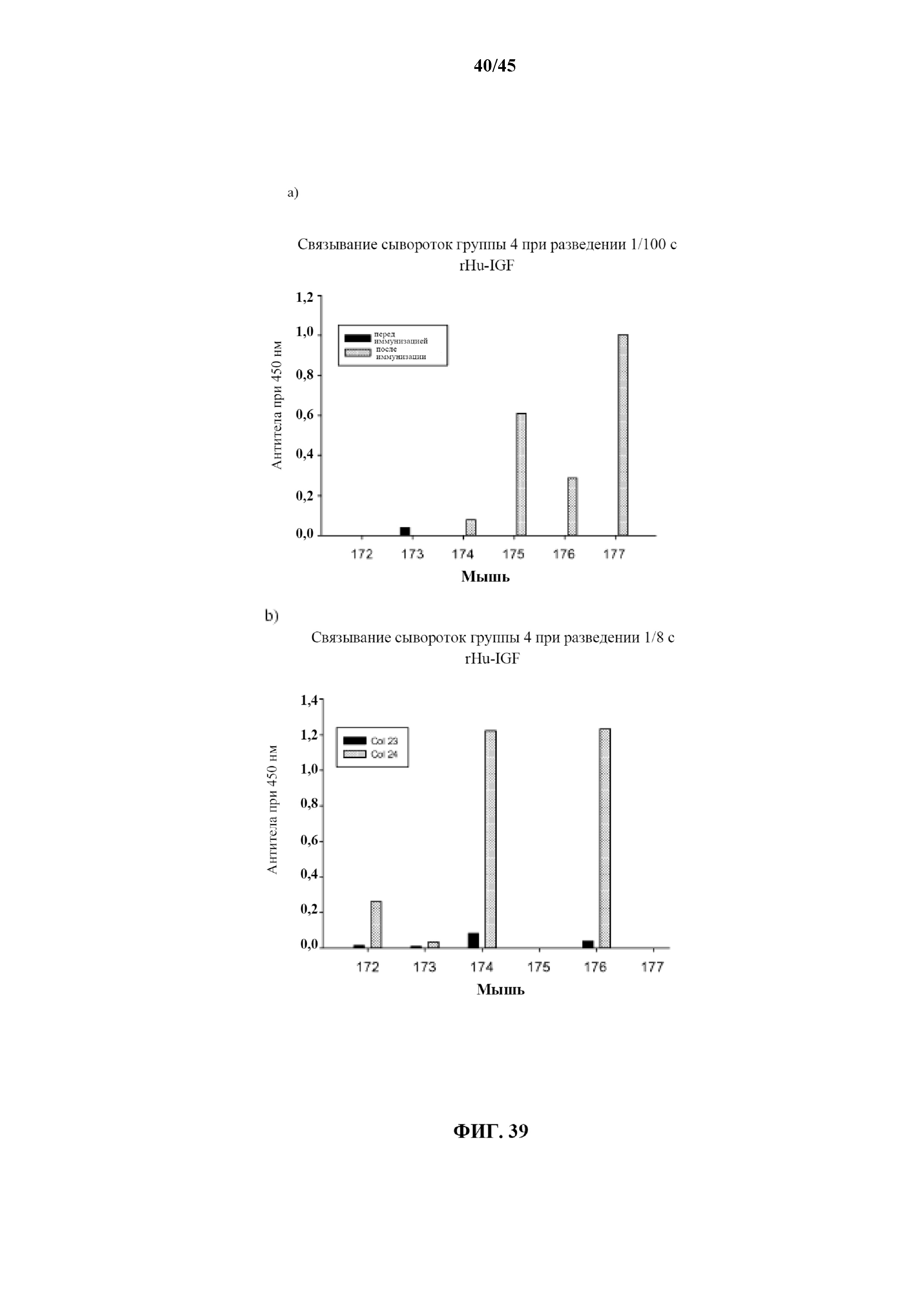
[0069] на фигуре 39 показаны гуморальные иммунные ответы с участием IgG сывороток мышей группы 4 при разведении (a) 1/100 и (b) 1/8 по отношению к r-IGF после иммунизации;
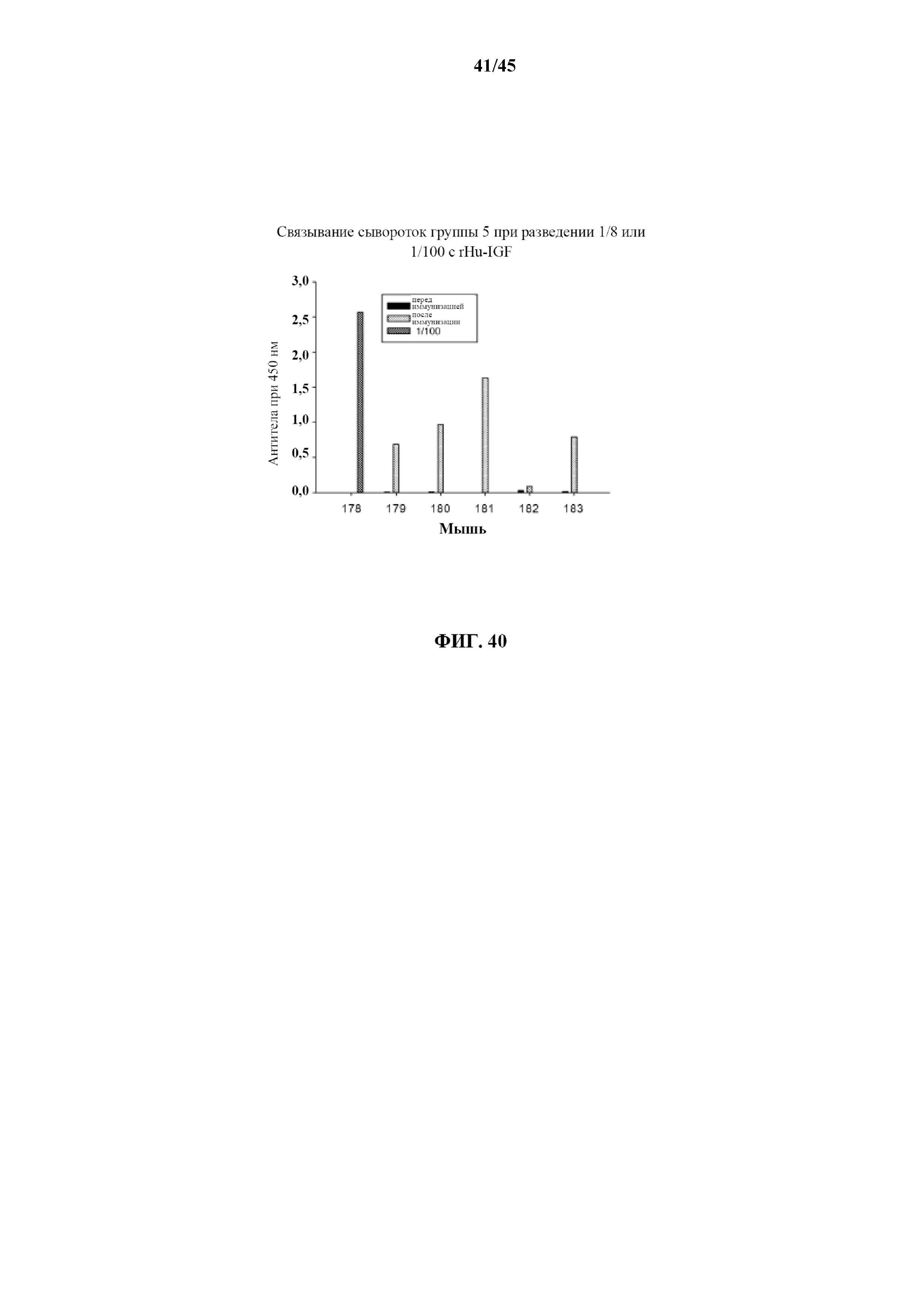
[0070] на фигуре 40 показаны гуморальные иммунные ответы с участием IgG сывороток мышей группы 5 при разведении 1/8 (кроме образца 178, при разведении 1/100) по отношению к r-IGF после иммунизации;
[0071] на фигуре 41 показаны гуморальные иммунные ответы с участием IgG сывороток мышей группы 6 при разведении 1/100 по отношению к a) r-IGF и b) rHu-EGF после иммунизации;
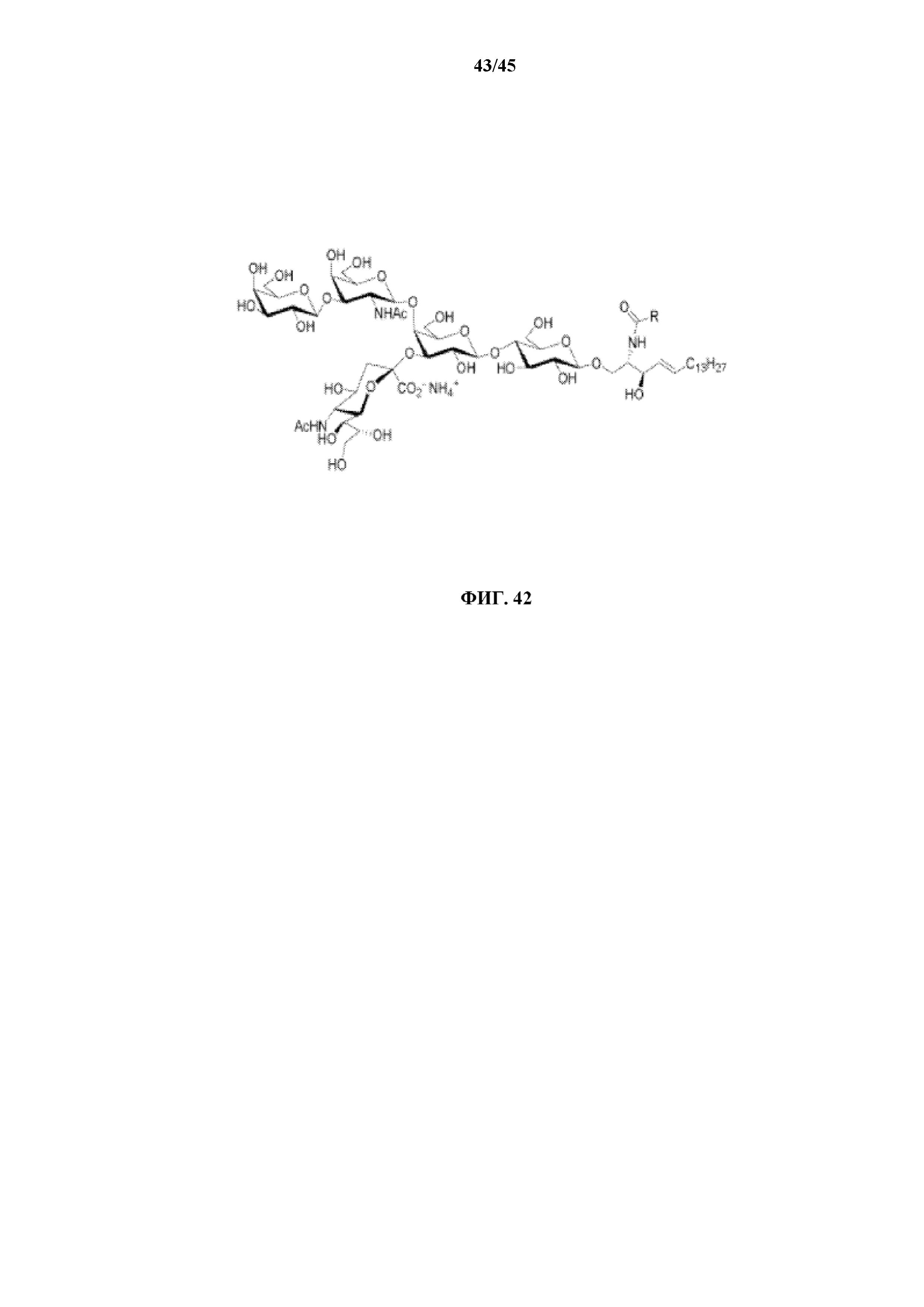
[0072] на фигуре 42 показана структура моноганглиозида GM1, природного партнера связывания субъединицы B холерного токсина;
[0073] на фигуре 43 показана структура коммерчески доступной D-галактозы, связанной с твердой подложкой (Pierce); и
[0074] на фигуре 44 показан SDS-PAGE гель очистки rCTB из надосадочной жидкости культуры (среды) трех штаммов клеток E. coli, трансформированных вектором экспрессии CTB, как указано далее: дорожка 1 показывает маркерную лестницу; дорожки 2, 5 и 8 показывают неочищенную надосадочную жидкость культуры; дорожки 3, 6 и 9 показывают неочищенные периплазматические фракции; дорожки 4, 7 и 10 показывают элюированный очищенный CTB; дорожка 11 показывает His-меченный CTB, очищенный с помощью IMAC.
ПОДРОБНОЕ ОПИСАНИЕ
[0075] В настоящем документе раскрыты подробные варианты осуществления настоящих рекомбинантных белков или вакцин, тем не менее, следует понимать, что раскрытые варианты осуществления являются только иллюстративными и могут быть осуществлены в различных видах. Следовательно, конкретные функциональные детали, раскрытые в настоящем документе, не следует интерпретировать как ограничивающие, а лишь в качестве основы для формулы изобретения и в качестве показательной основы для того, чтобы показать специалисту в данной области различные применения рекомбинантного белка, раскрытого в настоящем документе.
[0076] Настоящее раскрытие предлагает гомогенный рекомбинантный белок для улучшения презентирования максимального количества эпитопов факторов роста, эпитопов опухолевых антигенов и/или участков связывания рецептора в качестве элементов иммуногенного рекомбинантного белка. В одном иллюстративном варианте осуществления описан рекомбинантный белок, включающий полностью или части холерного токсина B (CT-B) и эпидермального фактора роста (EGF) человека, опухолевого антигена и/или рецептора. В альтернативных иллюстративных вариантах осуществления белок может включать другие иммуногенные рекомбинантные белки, которые смоделированы на основе известных иммуногенных белков. В пределах объема настоящего раскрытия подразумевают, что такие рекомбинантные белки будут включать полипептиды, которые обладают высокой иммуногенностью по отношению к иммунной системе человека. Предпочтительно рекомбинантные белки придают дополнительные свойства гибридному белку, например, высокий выход при экспрессии и технологичность, стабильность при пероральном применении и способность поступать из желудочно-кишечного тракта в кровеносную систему и/или предварительное безопасное применение в клинической практике.
[0077] В иллюстративном варианте осуществления рекомбинантные белки, раскрытые в настоящем документе, могут содержать или включать высокую долю белковой последовательности, полученной из целевых "собственных" антигенов, относительно общего молекулярного веса. Этого можно достигнуть, например, путем применения крупной белковой модели, содержащей многочисленные эпитопы факторов роста. Данные эпитопы факторов роста могут являться множественными копиями целого или части отдельного фактора роста или копиями целого или части нескольких различных факторов роста.
[0078] Согласно настоящему раскрытию включения эпитопов факторов роста должны быть свернуты так, чтобы их естественная конформация в значительной степени сохранялась и презентировалась компонентам иммунной системы хозяина с тем, чтобы вызывать сильный иммунный ответ хозяина к указанным эпитопам. Примеры подходящих природных белковых моделей для моделирования домена рекомбинантного белка, несущего эпитоп, включают, без ограничения, субъединицу B холерного токсина, субъединицы B термолабильных энтеротоксинов LT и LT-II E. coli, вератоксин, коклюшный токсин, энтеротоксин C. jejuni, токсин Шига, токсин Listeria, столбнячный анатоксин, дифтерийный анатоксин, наружный белок мембраны N. meningitidis, белок оболочки бактериофага, белок оболочки аденовируса и другие белки вирусной оболочки. Альтернативно, "чужой" компонент белка может иметь небольшой размер. Как минимум, "чужая" последовательность(последовательности) должна быть длиною приблизительно 9, 10, 11 или более аминокислот и включать либо целый, либо частично по меньшей мере один T-клеточный эпитоп человека. Альтернативно, можно применять неприродные "искусственные" полипептиды, которые удовлетворяют требованиям придания иммуногенности всему белку и обеспечения соответствующего презентирования фактора(ов) роста, рецепторов, опухолевых антигенов или их эпитопов по отношению к иммунной системе хозяина.
[0079] В иллюстративном варианте осуществления домен рекомбинантного белка, несущий эпитоп, вне зависимости от того, получен ли он из природной или из искусственной последовательности полипептида, должен обладать способностью к самоорганизации в олигомерные мультимеры при соответствующих химических/внешних условиях или к уменьшению до мономеров при альтернативных условиях. Оптимально, участвующие в мультимеризации домены будут собираться в стабильные мультимеры с небольшим числом субъединиц, например, димеры, тримеры, тетрамеры, пентамеры и т.д., так, чтобы образовывался продукт с частицами с равномерным размером. Примеры природных полипептидов включают, без ограничения, лейциновые застежки, белок lac-репрессор, стрептавидин/авидин, субъединицу B холерного токсина, субъединицы B других токсинов AB5, участвующий в тримеризации домен Pseudomonas и вирусные капсидные белки.
[0080] Согласно настоящему раскрытию рекомбинантные белки, независимо от того содержат ли факторы роста или их части, клеточные рецепторы или их части, опухолевые антигены или их части, относятся в широком диапазоне либо клеточных путей, задействованных при хроническом заболевании, либо видов рака к факторам роста и рецепторам и, в наиболее широком диапазоне солидных опухолей, к применению опухолевых антигенов в указанных искусственных белках. Белки представлены в форме рекомбинантного белка и могут быть пригодны при лечении хронических заболеваний, например, рака молочной железы, рака легких, рака мочевого пузыря, рака яичников, рака наружных женских половых органов, рака толстой кишки, рака легкого, рака головного мозга, рака ободочной и прямой кишки, рака кишечника, рака головы и шеи и рака пищевода. Поскольку при указанных заболеваниях могут экспрессироваться опухолевые антигены и сверхэкспрессироваться множество клеточных рецепторов и факторов роста, белки, описанные в настоящем документе, могут содержать один или несколько различных опухолевых антигенов, один или несколько различных рецепторов или факторов роста из одного или множества ассоциированных с заболеванием клеточных путей. Такие белки называют "поливалентными".
[0081] В иллюстративном варианте осуществления раскрыт белок, состоящий из гомогенного рекомбинантного белка, включающего один или нескольких нейтрализующих доменов эпидермальных факторов роста (EGF). Белок представлен в форме рекомбинантного белка и может быть пригодным при лечении хронических заболеваний, например, рака молочной железы, рака легких, рака мочевого пузыря, рака яичников, рака наружных женских половых органов, рака толстой кишки, рака легкого, рака головного мозга, рака ободочной и прямой кишки, рака головы и шеи и рака пищевода. В иллюстративном варианте осуществления белок является рекомбинантным белком, содержащим или включающим последовательности EGF и последовательности CT-B.
[0082] В другом иллюстративном варианте осуществления раскрыт белок, состоящий из гомогенного рекомбинантного белка, включающего один фактор роста фибробластов (FGF). В иллюстративном варианте осуществления белок является рекомбинантным белком, содержащим или включающим последовательности FGF и последовательности CT-B.
[0083] В дополнительном иллюстративном варианте осуществления раскрыт белок, состоящий из гомогенного рекомбинантного белка, включающего один трансформирующий фактор роста бета 1 (TGF-β1). В иллюстративном варианте осуществления белок является рекомбинантным белком, содержащим или включающим последовательности TGF-β1 и последовательности CT-B.
[0084] В еще одном иллюстративном варианте осуществления раскрыт белок, состоящий из гомогенного рекомбинантного белка, включающего один трансформирующий фактор роста бета 1 (TGF-β1). В иллюстративном варианте осуществления белок является рекомбинантным белком, содержащим или включающим последовательности TGF-β1 и последовательности CT-B.
[0085] В одном иллюстративном варианте осуществления раскрыт белок, состоящий из гомогенного рекомбинантного белка, включающего один инсулиноподобный фактор роста 1 (IGF-1). В иллюстративном варианте осуществления белок является рекомбинантным белком, содержащим или включающим последовательности IGF-1 и последовательности CT-B.
[0086] В другом иллюстративном варианте осуществления раскрыт белок, состоящий из гомогенного рекомбинантного белка, включающего один фактор роста гепатоцитов (HGF). В иллюстративном варианте осуществления белок является рекомбинантным белком, содержащим или включающим последовательности HGF и последовательности CT-B.
[0087] В дополнительном иллюстративном варианте осуществления раскрыт белок, состоящий из гомогенного рекомбинантного белка, включающего один инсулиноподобный фактор роста 1 (IGF-1) и один инсулиноподобный фактор роста 2. В иллюстративном варианте осуществления белок является рекомбинантным белком, содержащим или включающим последовательности IGF-1, последовательности IGF-2 и последовательности CT-B.
[0088] В еще одном иллюстративном варианте осуществления раскрыт белок, состоящий из гомогенного рекомбинантного белка, включающего один фактор роста эндотелия сосудов-A (VEGF-A) и один фактор роста эндотелия сосудов-C (VEGF-C). В иллюстративном варианте осуществления белок является рекомбинантным белком, содержащим или включающим последовательности нейтрализующего домена VEGF-A, последовательности VEGF-C и последовательности CT-B.
[0089] Для определения соответствующей кодирующей области(ей) HuEGF, подлежащей включению или введению в состав, проанализировали последовательности и структуры молекул EGF ряда организмов. Таблица, иллюстрирующая последовательности и структуры молекул EGF ряда организмов, описана на фиг. 1. Как показано на фиг. 1, рамка 100 охватывает часть последовательности молекул EGF ряда организмов, которая представляет собой эпитоп нейтрализующего домена молекул EGF. Несмотря на то, что существует значительная часть консервативных участков в эпитопах нейтрализующих доменов молекул EGF различных видов, тем не менее, также существует большая доля изменчивости между видами. Для исследований in vivo примечательно, что один нейтрализующий домен (последовательность в рамке 100) полностью консервативна среди приматов, но отличается у грызунов и других видов. Аналогично, различные последовательности молекул EGF сравнимы с различиями в третичной структуре.
[0090] Структура молекулы EGF человека, включающей нейтрализующий домен EGF, согласно иллюстративному варианту осуществления описана на фиг. 2. Молекула EGF содержит шесть цистеиновых остатков, включающие Cys6, Cys14, Cys20, Cys31, Cys33 и Cys42. Шесть цистеиновых остатков важны при определении сворачивания молекулы EGF. Нейтрализующий домен EGF 200 (показанный как встречно-параллельный β-лист) ограничен двумя обособленными связанными дисульфидной связью цистеиновыми парами, Cys6-Cys20 и Cys14-Cys31. Две связанные дисульфидной связью цистеиновые пары, Cys6-Cys20 и Cys14-Cys31, важны, поскольку данные две пары определяют минимальную последовательность или минимальный пептид молекулы EGF, которая(ый) представляет собой нейтрализующий домен EGF 200 в правильной конформации.
[0100] Упрощенная линейная структура цистеиновых пар молекулы EGF, включающая B-петлю EGF 200, согласно иллюстративному варианту осуществления описана на фиг. 3. Как показано на фиг. 3, Cys6 связан с Cys20, Cys14 связан с Cys31, и Cys33 связан с Cys42. B-петля EGF 200 расположена между Cys20 и Cys31. Таким образом, минимальная последовательность или минимальный пептид 400 молекулы EGF, которая(ый) представляет собой нейтрализующий домен EGF 200 в правильной конформации, является последовательностью от Cys6 до Cys31, которая показана на фиг. 4.
[0101] Структура молекулы модифицированного рекомбинантного белка в соответствии с настоящим раскрытием включающего по меньшей мере часть молекулы EGF, содержащей нейтрализующий домен EGF, согласно иллюстративному варианту осуществления, описана на 5. Отдельную мутацию или изменение вносят в Cys33 молекулы EGF для получения модифицированной искусственной молекулы, что приводит к изменению Cys33 на Ala33 с удалением Cys33 для предотвращения любых возможных проблем, связанных с неправильным сворачиванием.
[0102] Аланин применяют потому, что аланин довольно "нейтральный" в отношении функциональных характеристик и имеет наиболее малую боковую цепь, за исключением глицина. Следовательно, аланин считают наименее подходящим остатком для придания "ненативных" характерных свойств модифицированному рекомбинантному белку. В пределах объема настоящего раскрытия подразумевают, что потенциально можно применять любой другой остаток или даже совсем не вносить изменений.
[0103] В иллюстративном варианте осуществления можно использовать любую часть молекулы EGF из области, определенной остатками Met21-Ala30, вплоть до целостной последовательности EGF. Последовательности, выбранные для экспрессии в рекомбинантные белки EGF-CT-B в примерах, включают все последовательности EGF и отдельно область, которая, как считают, необходима для правильного презентирования нейтрализующего домена, определенного как нейтрализующий домен в используемом контексте, и не включают любую другую часть EGF, которая не считается необходимой для осуществления этого.
[0104] В другом иллюстративном варианте осуществления раскрыт белок, состоящий из гомогенного рекомбинантного белка, включающего нейтрализующий домен фактора роста эндотелия сосудов-A (VEGF-A). В иллюстративном варианте осуществления белок является рекомбинантным белком, содержащим или включающим последовательности VEGF-A и последовательности CT-B. В иллюстративном варианте осуществления последовательность VEGF-A будет включать нейтрализующий домен, содержащий последовательность от Cys57 до Cys104 зрелого белка. В другом иллюстративном варианте осуществления последовательность VEGF-A будет включать один или несколько фланкирующих остатков, продолжающихся до Val14 и Lys108.
[0105] В другом иллюстративном варианте осуществления раскрыт белок, состоящий из гомогенного рекомбинантного белка, включающего лигандсвязывающий домен рецептора TGF-бета II. В иллюстративном варианте осуществления белок является рекомбинантным белком, содержащим или включающим последовательности TGFB-RII и последовательности CT-B. Последовательность TGFB-RII будет включать любую последовательность внеклеточного домена от Thr23 до Gln166.
[0106] В другом иллюстративном варианте осуществления раскрыт белок, состоящий из гомогенного рекомбинантного белка, включающего лигандсвязывающий домен рецептора HGF (c-Met). В иллюстративном варианте осуществления белок является рекомбинантным белком, содержащим или включающим последовательности рецептора HGF и последовательности CT-B. Предпочтительно последовательность рецептора HGF будет включать любую последовательность внеклеточного домена SEMA от Lys27 до Leu515.
[0107] Пример I: протоколы ELISA
[0108] С целью определения того, могут ли рекомбинантные белки, такие как искусственные белки EGF-CT-B согласно настоящему раскрытию, нести B-петлю EGF в правильной конформации, получали два коммерческих моноклональных антитела (антитела Santa Cruz, номера по каталогу 10825 и 10827), которые, как известно, блокируют связывание EGF с рецептором EGF. Вне связи с какой-либо определенной теорией, из некоторых источников приняли то, что связывание с рецептором EGF осуществляется частично посредством области, определенной остатками Met21-Ala30.
[0109] В иллюстративном варианте осуществления для связывания рекомбинантного белка EGF (rEGF) в ELISA использовали mAb 10825 и mAb 10827 в концентрациях 1 мкг/мл и 2 мкг/мл, и оптическую плотность (OD) измеряли при 450 нм. Результаты показаны на гистограмме, которая изображена на фиг. 6. Как показано на фиг. 6, rEGF сохраняет свою естественную конформацию при абсорбции на планшете для ELISA, и для получения хорошего сигнала достаточно 1 мкг/мл mAb 10825 либо mAb 10827.
[0110] Для оценки узнавания остатков Met21-Ala30 планшет покрывали приблизительно 100 мкл/лунка белка (rEGF) в количестве приблизительно 1 мкг/мл и инкубировали при приблизительно 37°C в течение приблизительно 1 ч. Планшет промывали дважды с помощью приблизительно 200 мкл/лунка PBS-0,5% Tween (PBST), затем дважды с помощью приблизительно 200 мкл PBS. Планшет блокировали с помощью приблизительно 200 мкл/лунка 2% сухого молока в PBS (MPBS) и инкубировали в течение приблизительно 1 часа при приблизительно 37°C. Планшет затем промывали дважды с помощью PBST и дважды с помощью PBS, как указано выше. Добавляли приблизительно 100 мкл тестовых антител в количестве приблизительно 1 мкг/мл либо приблизительно 2 мкг/мл и инкубировали в течение приблизительно 1 часа при температуре, приблизительно равной комнатной (RT). Планшет промывали еще раз, как описано выше. Затем добавляли антитело (HRP-меченное Fc-специфическое антитело к антителу мыши, код изделия, присвоенный Sigma, A0168) при разведении приблизительно 1/1000 в количестве приблизительно 100 мкл/лунка и инкубировали в течение приблизительно 1 ч при температуре, приблизительно равной RT. Планшет промывали еще раз, как указано выше, и проявляли с помощью приблизительно 100 мкл/лунка субстрата Sureblue TMB до тех пор, пока не проявлялся цвет (обычно приблизительно 5-10 мин.). Реакцию останавливали с помощью приблизительно 50 мкл/лунка 1M H2SО4, и с планшета считывали данные при приблизительно 450 нм.
[0111] Дополнительно проводили ELISA с конкурентным связыванием. Во втором ELISA связывание каждого из антител mAb 10825 и mAb 10827 с rEGF оценивали в присутствии либо свободного растворимого пептида, соответствующего эпитопу, представляющему интерес (пептидная последовательность MYIEALDKYA), либо контрольного несоответствующего пептида (пептидная последовательность SLAGSSGALSK). Проводили ELISA с приблизительно 100 мкл/лунка при приблизительно 1 мкг/мл mAb 10825, а также приблизительно 1 мкг/мл свободного растворимого пептида, соответствующего целевому эпитопу, приблизительно 1 мкг/мл mAb 10827, а также приблизительно 1 мкг/мл свободного растворимого пептида Met21-Ala30, приблизительно 1 мкг/мл mAb 10825, а также приблизительно 1 мкг/мл контрольного несоответствующего пептида, и приблизительно 1 мкг/мл mAb 10827, а также приблизительно 1 мкг/мл контрольного несоответствующего пептида.
[0112] Оптическую плотность (OD) измеряли при 450 нм. Результаты показаны на гистограмме, которая изображена на фиг. 7. Как показано на фиг. 7, на которой изображены два антитела, mAb 10825 и mAb 10827, ясно, что антитело mAb 10827 связывается с нейтрализующим эпитопом Met21-Ala30, а антитело mAb 10825 этого не делает. Антитело mAb 10825, вероятно, нейтрализует посредством внесения стерического несоответствия в процесс связывания с рецептором путем блокирования области EGF, конформационно проксимальной по отношению к области, определенной остатками Met21-Ala30. Таким образом, антитело mAb 10827 связывается с нейтрализующим эпитопом rEGF Met21-Ala30 в его нативном состоянии, и его применяют в следующем анализе искусственных предшественников EGF-CT-B для вакцины.
[0113] Пример II: презентирование нейтрализующего эпитопа EGF
[0114] Для того, чтобы определить, может или нет вакцина с рекомбинантным белком EGF-CT-B, содержащим EGF на концах последовательности CT-B, препятствовать проявлению любой из необходимых индивидуальных характеристик домена(ов) EGF, а именно правильного конформационного презентирования эпитопа Met21-Ala30 EGF и способности мономеров CT-B собираться в мультимеры (пентамерные кольца) при соответствующих физико-химических условиях, или иным образом влиять на них, создали шесть рекомбинантных белков, содержащие целостную кодирующую область EGF в последовательности CT-B на N-конце (тест 1 - тест 3) либо C-конце (тест 4 - тест 6).
[0115] Тест 1 и тест 4 включают вакцину с рекомбинантным белком EGF-CT-B, включающим последовательности EGF полной длины непосредственно на домене CT-B. Тест 2 и тест 5 включают вакцину с искусственным EGF-CT-B, включающим последовательности EGF полной длины, отделенные от домена CT-B короткой пептидной последовательностью длиной в 3 аминокислоты. Рекомбинантный белок EGF-CT-B из вакцины, содержащий последовательность EGF на N-конце, включает SerGlyGly в качестве пептидной последовательности длиной в 3 аминокислоты и включает сайт рестрикции KpnI. Рекомбинантный белок EGF-CT-B из вакцины, содержащий последовательность EGF на C-конце, включает SerSerGly в качестве пептидной последовательности длиной в 3 аминокислоты и включает сайт рестрикции XhoI.
[0116] Тест 3 и тест 6 включают рекомбинантный белок EGF-CT-B, содержащий последовательность EGF полной длины, отделенную от домена CT-B короткой пептидной последовательностью длиной в 5 аминокислот. Рекомбинантный белок EGF-CT-B, содержащий последовательность EGF на N-конце, включает GlyGlySerGlyGly в качестве пептидной последовательности длиной в 5 аминокислот и включает сайт рестрикции KpnI. Искусственный EGF-CT-B, содержащий последовательность EGF на C-конце, включает SerSerGlyGlyGly в качестве пептидной последовательности длиной в 5 аминокислот и включает сайт рестрикции XhoI. Короткие пептидные последовательности длиной в 3 и 5 аминокислот служат как для отделения домена фактора роста от последовательности CT-B, так и, к тому же, для обеспечения степени свободы подвижности одного домена, связанного с другим, таким образом, уменьшая любое возможное стерическое несоответствие.
[0117] Каждый из шести рекомбинантных белков EGF-CT-B клонировали в вектор экспрессии в бактериях (pIMS147) так, чтобы искусственные рекомбинантные белки EGF-CT-B могли экспрессироваться в периплазме E. coli, и очищали путем введения C-концевой метки 6xHis. Каждую рекомбинантную последовательность EGF-CT-B экспрессировали, очищали и количественно определяли с помощью геля для белков в способе Бредфорда.
[0118] Презентирование нейтрализующего эпитопа EGF Met21-Ala30 в каждом из шести рекомбинантных белков EGF-CT-B определяли с помощью ELISA. Рекомбинантные белки EGF-CT-B, включающие один концевой домен EGF, иммобилизировали на планшете для ELISA. Эпитопы Met21-Ala30 EGF определяли с помощью антитела mAb 10827 (Santa Cruz).
[0119] Планшет для ELISA покрывали серийными 2-кратными разведениями искусственных белков EGF-CT-B, очищенных с помощью 6-His, и инкубировали при приблизительно 37°C в течение приблизительно 1 часа. Планшеты промывали и блокировали с помощью приблизительно 2% MPBS, как указано выше. Промывание включало внесение пипеткой приблизительно 200 мкл PBS или PBST в каждую лунку, переворачивание планшета и простукивание лунок до полного удаления жидкости, а также повторения. Затем во все лунки добавляли антитело mAb 10827 в количестве приблизительно 1 мкг/мл и инкубировали при температуре, приблизительно равной комнатной, в течение приблизительно 1 часа. Планшеты повторно промывали, и в лунки добавляли антитело к антителу мыши, меченное пероксидазой хрена (HRP), и инкубировали в течение приблизительно 1 дополнительного часа. Планшеты повторно промывали и проявляли с применением SureBlue TMB.
[0120] При добавлении субстрата SureBlue TMB HRP-меченное антитело к антителу мыши, конъюгированное со вторичным антителом, перерабатывало субстрат ферментативным путем с получением голубого продукта. Реакцию наблюдали и контролировали до тех пор, пока не было решено, что интенсивность окраски достигла достаточного уровня. (Если окраска начинала появляться в контрольных лунках, которые не содержали первичное антитело, тогда реакцию останавливали на данном этапе.) Реакцию останавливали путем добавления приблизительно 50 мкл H2SO4, которая подавляет активность HRP-меченного антитела. Это также изменяет окраску продукта реакции с голубого на желтый. Это может затем быть измерено в планшет-ридере с поглощением при приблизительно 450 нм.
[0121] Результаты ELISA со связыванием показаны на линейной диаграмме, которая изображена на фиг. 8. Как показано на фиг. 8, антитело mAb 10827 было способно связываться со всеми шестью рекомбинантными белками EGF-CT-B, очищенными с помощью 6-His, демонстрируя то, что в каждом составе эпитоп EGF-Met21-Ala30 присутствует в своей нативной конформации и является доступным для компонентов иммунной системы.
[0122] Для того, чтобы подтвердить то, что искусственный рекомбинантный белок EGF-CT-B включал в себя включения домена EGF и последовательность CT-B, проводили второй ELISA, в котором не адсорбировали рекомбинантный белок непосредственно на планшетах, а захватывали вместо этого рекомбинантный белок с применением антитела кролика к CT-B (Antibodies On-Line), как показано на фиг. 9. Поскольку данное антитело 'захвата' специфично к нативному CT-B, анализ показал, что обнаруженные нейтрализующие домены EGF являются компонентами большего рекомбинантного белка, который включает правильно свернутый домен CT-B.
[0123] Пример III: сборка мультимеров белка EGF-CT-B
[0124] Для того, чтобы исследовать влияние экспрессии структурного домена, содержащего фактор роста на концах рекомбинантного белка, полученного из CT-B, на сборку мультимеров из мономерных субъединиц, искусственные белки из теста 1 - теста 6 прогоняли на геле для SDS-PAGE при нативных условиях (без уменьшения, без кипячения). Искусственные рекомбинантные белки EGF-CT-B затем переносили на нитроцеллюлозную мембрану посредством электроблоттинга и исследовали с применением антитела кролика к CT-B (как указано выше в примере II). Связывание вторичного HRP-меченного антитела к антителу кролика определяли по испусканию света с использованием ECL-субстрата на авторадиографической пленке. Как показано на фиг. 10, вестерн-блоттинг подтверждает присутствие высокомолекулярного CT-B, что указывает на то, что искусственные мономерные белки EGF-CT-B способны собираться в мультимеры посредством домена CT-B.
[0125] В отдельном эксперименте дублирующие образцы нативного (без кипячения или уменьшения) белка CT-B инкубировали в течение 5 мин. при диапазоне различных значений pH от pH 1,0 до pH 7,0. После инкубирования один из дублирующих образцов в каждом случае нейтрализовали до pH 7,0 в течение одного часа. Все образцы затем прогоняли на геле для SDS-PAGE, подвергали вестерн-блоттингу, и белок выявляли с помощью антитела к CTB (фиг. 16). Это показывает, что i) пентамеры CTB могут быть уменьшены до мономеров при pH 3,0 или ниже за 5 мин., и ii) что возвращение к нейтральному pH возобновляет образование пентамеров. Ранее было показано, что гибридный белок, содержащий белок CT-B, слитый с участком связывания антитела верблюда и метками посредством соответствующего линкера (молекулярный вес ~ 16 кДа), может быть получен с образованием функционально активных пентамеров (Li et. al, 2009 Molecular Immunology 46; 1718-1726).
[0126] Пример IV: бивалентные искусственные белки EGF-CT-B
[0127] В иллюстративном варианте осуществления создавали два дополнительных искусственных рекомбинантных белка EGF-CT-B, в которых i) полноразмерный ген EGF экспрессируется как на N-конце, так и на C-конце, отделен от гена CT-B последовательностью длиной в три аминокислоты, как указано выше для теста 2 и теста 5, и обозначается 'E2', или ii) усеченный EGF, включающий нейтрализующий эпитоп Met21-Ala30, экспрессируется на обоих концах гена CT-B, как указано выше, и обозначается 'B2'. Оба рекомбинантных белка клонировали в вектор экспрессии pIMS147 в E. coli, как указано выше. Оба рекомбинантных белка EGF-CT-B экспрессировали, и очищали, как описано ранее, и оценивали в отношении присутствия правильно свернутого домена CT-B и презентирования нейтрализующего эпитопа Met21-Ala30 EGF в правильной конформации. Результаты показаны на линейной диаграмме, которая изображена на фиг. 11. Как показано на фиг. 11, рекомбинантные белки EGF-CT-B как с E2, так и с B2 содержат как домен CT-B, так и по меньшей мере один функционально правильный эпитоп Met21-Ala30 EGF, представленный для того, чтобы быть доступным для антитела.
[0128] Дополнительный анализ включал прогон образцов очищенных рекомбинантных белков EGF-CT-B с E2 и B2 на гелях для неденатурирующего SDS-PAGE при pH 7,0 без первоначального кипячения образцов и перенос на нитроцеллюлозную мембрану посредством электропереноса. Перенесенные белки выявляли с использованием поликлонального антитела кролика к CT-B AbOL (Antibodies On-Line) и HRP-меченного антитела к антителу кролика. Как показано на фиг. 12, вестерн-блоттинг показывает, что рекомбинантные белки, содержащие домен CT-B, как существуют в качестве мономеров, так и, к тому же, образуют серии олигомерных мультимеров, в том числе димеры, тримеры, тетрамеры и пентамеры.
[0129] Пример V: последовательность белка EGF-CT-B
[0130] Один пример последовательности искусственного рекомбинантного белка EGF-CT-B показан на фиг. 13. Как показано на фиг. 13, последовательность образца показывает последовательность искусственного белка, включающую две полноразмерные последовательности EGF, которые подчеркнуты, и последовательность CT-B, которая выделена курсивом.
[0131] Пример VI: последовательность белка EGF-CT-B
[0132] Другой пример последовательности искусственного рекомбинантного белка EGF-CT-B показан на фиг. 14. Как показано на фиг. 14, последовательность образца показывает последовательность белка, включающую две последовательности нейтрализующего домена EGF, которые подчеркнуты, и последовательность CT-B, которая выделена курсивом.
[0133] Пример VII: последовательность белка EGF-CT-B
[0134] Еще один пример последовательности рекомбинантного белка EGF-CT-B показан на фиг. 15. Как показано на фиг. 15, последовательность образца показывает последовательность белка, включающую частичные последовательности молекулы EGF, содержащие нейтрализующий домен (Cys6 - Cys31) EGF, которые подчеркнуты, и последовательность CT-B, которая выделена курсивом.
[0135] Пример VIII: последовательности белка EGF-CT-B, включающие линкеры
[0136] Согласно настоящему документу в других иллюстративных вариантах осуществления раскрыты дополнительные рекомбинантные белки EGF-CT-B, включающие один или несколько линкеров или спейсеров. Один или несколько из вариантов осуществления, раскрытых выше, включают EGF, слитые с CT-B на одном или обоих концах CT-B так, чтобы один ген переходил непосредственно в следующий. Данные полученные рекомбинантные или гибридные белки главным образом включали EGF, слитый непосредственно с CT-B. В других иллюстративных вариантах осуществления компоненты EGF и CT-B гибридного белка фактически отделены 3 или 5 аминокислотами, которые образуют подвижный спейсер или линкер между двумя доменами. Следующие аминокислоты, которые можно применять в качестве линкеров, включали, без ограничения, следующие: SSG, SSGGG, SGG, GGSGG и GGGGS.
[0137] Добавление линкеров может уменьшать препятствия, возникающие, например, в результате стерического несоответствия, и способствовать образованию пентамеров с помощью домена CT-B. Линкеры также делают возможным включение уникальных сайтов рестрикции в линкеры, что дает возможность осуществления последующей манипуляции с генетическими конструктами. В данном примере описаны восемь конструктов (T1-T6, E2 и B2) с последовательностями, перечисленными в таблице, показанной на фиг. 17. В одном иллюстративном варианте осуществления сайты рестрикции включают, без ограничения, следующие: Xhol, Kpnl, BspEl и Spel.
[0138] Осуществляли вестерн-блот-анализ конструктов T1-T6, E2 и B2, и он описан ниже с использованием фиг. 18. Как показано на фиг. 18, в вестерн-блоттинге конструктов E2 и B2, по-видимому, присутствует некоторое препятствие, например, стерическое несоответствие и/или другое препятствие, что давало продуцируемые белки, состоящие из ряда олигомеров, например, мономеров, димеров, тримеров и т.д. Альтернативно, концентрация белка, присутствующего в образцах, может оказывать влияние на олигомеризацию, поскольку она является зависимым фактором для пентамеризации нативного CTB.
[0139] Самые нижние полосы соответствуют мономерам, следующие по направлению вверх соответствуют димерам и т.д. Поскольку B2 включает усеченные EGF, он, по-видимому, меньше, чем E2, что показано тем, что B2 находится ниже на вестерн-блоте.
[0140] Похожий результат обнаруживается для конструктов T1-T6, несмотря на то, что число и доля олигомеров изменяются от конструкта к конструкту. Изначально представлялось, что белки с EGF на N-конце, включающие аминокислотные линкеры, могут давать более высокую долю пентамеров. Однако, впоследствии было обнаружено, что доля пентамеров изменялась от партии к партии.
[0141] Поскольку изначально было предположено, что слияние на одном или другом конце способствовало пентамеризации, были сконструированы две молекулы тандемного слияния в дополнение к конструкту E2, и они показаны на фиг. 19. Первая молекула тандемного слияния, обозначенная E2N, содержит два последовательных EGF на N-конце CT-B. В ней L-3 представляет собой SGG, L-4 представляет собой GSSG. Вторая молекула слияния, обозначенная E2C, содержит два последовательных EGF на C-конце CT-B. В ней L-3 представляет собой SSG, L-5 представляет собой GGSGG.
[0142] В иллюстративном варианте осуществления длину аминокислотных линкеров на N-конце и C-конце увеличивали для определения того, будет или нет длина аминокислотного линкера на каждом конце обуславливать образование только пентамеров, или же, вполне возможно, один конец, N-конец или C-конец, будет обуславливать образование более высокой доли пентамеров. Как видно из фиг. 20, N-концевые и C-концевые аминокислотные линкеры удлиняли с помощью конструктов T2/3 и T4/5, соответственно. Графический материал (фиг. 20) относится к молекуле C-концевого слияния, E2C. В данном иллюстративном примере L3 представляет собой SSG, L5 представляет собой SSGGG, L8 представляет собой SSGGGSGG, а L10 представляет собой SSGGGGSGGG. В варианте с N-концевыми линкерами длина вставленных линкеров-спейсеров составляла приблизительно 7 и 9 остатков. В данном примере 4 линкера будут следующими: L3 SGG, L5 GGSGG, L7 TSGGGSG и L9 TSGGGGSGG. Каждый из линкеров-спейсеров может быть вставлен в каждый из более коротких линкеров L3 и L5. В связи с этим вставка как L7 в L5, так и L9 в L3 дает линкеры длиной 12 остатков, однако они будут иметь различные последовательности, названные ниже 'a' и 'b'. N-концевые линкеры также удлиняли до 10, 12 и 14 аминокислот, и C-концевые линкеры удлиняли до 11, 13 и 15 аминокислот, как показано на фиг. 20. В данном иллюстративном примере L10 представляет собой SSGGGSGGSSG, L12a представляет собой GGSGGTSGGGSG, L12b представляет собой SGGTSGGGGSGG, и L14 представляет собой GGSGGTSGGGGSGG. Аналогично, L11 представляет собой SSGGGSGGSSG, L13a представляет собой SSGGGGSGGGSSG, L13b представляет собой SSGGGSGGSSGGG, а L15 представляет собой SSGGGGSGGGSSGGG.
[0143] Как видно из фиг. 21, вестерн-блот-анализ молекул тандемного слияния EGF, E2N и E2C в сравнении с таковым для бивалентных конструктов с исходным E2 демонстрирует, что как E2, так и E2C продуцируют много олигомеров. E2N также продуцирует олигомеры, однако, существует явный признак того, что первый домен EGF либо экспрессировался в виде усеченного белка, либо расщеплялся на какой-то стадии в ходе экспрессии/очистки.
[0144] Также проводили сравнительный вестерн-блот-анализ в отношении моновалентных конструктов 'Т' с удлиненными линкерами, и он показан на фиг. 22. В тех случаях, когда вышеуказанные удлиненные линкеры вводили в конструкты, ранее названные T2 и T3 (N-концевые линкеры длиной в 3 и 5 аминокислот, соответственно), получали T2SL (с коротким удлиненным линкером, т.е. L10), T2LL (с длинным линкером, L12a), T3SL (с коротким линкером L12b) и T3LL (с длинным линкером L14). Аналогично, конструкты T5 и T6 с N-концевыми линкерами становились T5SL (с L11), T5LL (с L13a), T6SL (с L13b) и T6LL (с L15).
[0145] В тех случаях, когда вставляли линкеры-спейсеры, они фактически могли быть клонированы в одном из двух направлений, давая совершенно разные последовательности. По мере возможности секвенировали соответствующие клоны для обнаружения такового со вставкой в необходимом направлении. В случае T3LL-Rev изначально имели только клон с необходимой длиной линкера (т.е. 14 аминокислот), но со вставкой в 'ошибочной' ориентации. Это действительно служит иллюстрацией того, что определенные последовательности данных линкеров не обязательно являются критически важными, по меньшей мере в отношении действия в качестве физического спейсера. Фактическая линкерная последовательность T3LL-Rev будет представлять собой GGSGGTRPSTAATS (подчеркнутые = инвертированный участок).
[0146] Как показано на вестерн-блоте, показанном на фиг.22, N и R относятся к нативному и уменьшенному/денатурированному белку, соответственно. Первые две дорожки показывают CT-B дикого типа в виде пентамера (нативный) и мономера (уменьшенный). Как показано на других дорожках, видно, что T3 (включающий линкер длиной в 5 аминокислот) продуцировал некоторые олигомеры различных размеров, однако все конструкты с N-концевыми более длинными линкерами продуцируют преимущественно пентамеры при прогоне в природных условиях.
[0147] В отличие от этого, как показано на фиг. 23, вестерн-блоттинг конструктов с C-концевыми линкерами давал множество полос в природных условиях даже с удлиненными линкерами.
[0148] С учетом этих данных молекула тандемного N-концевого слияния EGF с CT-B, по-видимому, представляет существенный интерес. Кроме того, первый линкер (между двумя доменами EGF) может быть удлинен в попытке предотвратить усечение/протеолиз, упомянутые выше, с помощью конструкта E2N, и обеспечить подвижность при введении альтернативных факторов роста. Последовательность молекулы N-концевого слияния EGF с CT-B с помощью удлиненного первого линкера выглядит следующим образом:
[0149] HHHHHHIEGRNSDSECPLSHDGYCLHDGVCMYI EALDKYACNCVVGYIGERCQYRDLKWWELRGGSGGTSGGGGSGGTPQNITDLCAEYHNTQIHTLNDKIFSYTESLAGKREMAIITFKNGATFQVEVPGSQHIDSQKKAIERMKDTLRIAYLTEAKVEKLCVWNNKTPHAIAAISMAN
[0150] Несмотря на то, что применительно к некоторым вариантам осуществления были описаны и показаны гомогенные рекомбинантные белки, содержащие или включающие эпитопы B-петли EGF, многие варианты и модификации будут очевидны для специалистов в данной области и могут быть произведены без отклонения от сущности и объема настоящего раскрытия.
[0151] Пример IX: биспецифический белок IGF1-EGF-CTB (a)
[0152] Для того, чтобы установить возможность нацеливания нескольких факторов роста с помощью одного искусственного рекомбинантного белка, синтезировали ген, кодирующий инсулиноподобный фактор роста 1 (IGF1) человека, включающий короткие фланкирующие области для обеспечения возможности клонирования в конструкт E2N, описанный в примере VIII. Вкратце, N-концевой ген EGF удаляли из вектора путем расщепления ДНК рестрикционными эндонуклеазами NcoI и XhoI. Затем его заменяли геном IGF1 человека, расщепленным подобным образом, с использованием способов, известных специалистам в данной области. Полученный ДНК-вектор секвенировали для подтверждения того, что он кодирует необходимый рекомбинантный ген так, чтобы обеспечить экспрессию рекомбинантного белка согласно замыслу. Последовательность нового рекомбинантного белка показана на фиг. 24.
[0153] Впоследствии белок, полученный в результате экспрессии вышеупомянутого вектора, анализировали с помощью ELISA, чтобы показать, что оба фактора роста могут быть одновременно представлены компонентам (т.е. антителам) иммунной системы млекопитающего. Кратко, лунки планшета для ELISA покрывали соответствующим разведением антитела к CTB и затем блокировали с помощью PBS, содержащего 2% сухого молока, как описано ранее. Образцы рекомбинантного белка наносили на планшет и инкубировали в течение 1 часа при комнатной температуре. После промывания различные лунки готовили, как описано, затем инкубировали с 1/1000 (или согласно рекомендациям поставщика) i) антитела мыши к EGF AbOL 10827 либо ii) антитела кролика к IGF1 человека 2o. После промывания лунки инкубировали с соответствующим разведением i) HRP-меченного антитела к антителу мыши или ii) HRP-меченного антитела к антителу кролика и затем проявляли, как описано ранее. Как показано на фиг. 25, образованные сигналы подтверждали, что как IGF, так и EGF представлены в своей нативной конфигурации. Сигнал, образованный антителом к IGF, также подтверждает, что последовательности IGF, EGF и CTB присутствуют в той же молекуле за счет взаимного расположения кодирующих последовательностей ДНК в векторе экспрессии.
[0154] Пример X: биспецифический белок IGF1-EGF-CTB (b)
[0155] Для того, чтобы продемонстрировать, что биспецифические рекомбинантные белки могут быть получены с использованием естественного характерного свойства CTB, заключающегося в образовании олигомеров, ген IGF, описанный в примере IX, модифицировали с помощью ПЦР с использованием методик, знакомых специалистам в данной области, для способствования его клонированию в конструкт T5 c заменой гена EGF. Полученный рекомбинантный белок включал последовательности IGF от C-конца до последовательности CTB и отделялся линкером длиной в 3 аминокислоты (фиг. 26).
[0156] Образцы вышеупомянутого рекомбинантного белка объединяли отдельно с равными (молярными) количествами i) белка T2 и ii) белка T5. При необходимости каждую из смесей доводили до pH 3,0 путем добавления забуференной 10 мМ Трис-HCl и инкубировали при 4°C в течение 15 мин. для диссоциации любых присутствующих олигомеров. Белковые смеси затем нейтрализовали, и продолжали инкубацию в течение 60 мин. для того, чтобы способствовать олигомеризации. Для определения наличия гетероолигомеров лунки планшета для ELISA покрывали антителом мыши к EGF либо антителом кролика к IGF и блокировали. После промывания смесь IGF-CTB/T2 и смесь IGF-CTB/T5 по отдельности наносили на лунки, покрытые антителом к EGF либо антителом к IGF, и инкубировали в течение 60 мин. при комнатной температуре.
[0157] После промывания добавляли антитело, специфичное к фактору роста, на который не нацеливается покрывающее антитело, и инкубировали в течение 60 мин. Таким образом, антитело кролика к IGF наносили на лунки, покрытые антителом мыши к EGF, и наоборот. После промывания для удаления несвязанного антитела 2o при необходимости наносили HRP-меченное антитело к антителу мыши или HRP-меченное антитело к антителу кролика для нацеливания на антитело 2o. Результаты показаны на фиг. 27, и они демонстрируют то, что покрывающее антитело к EGF может захватывать и иммобилизировать белок, содержащий последовательности IGF. Подобным образом, антитело к IGF может захватывать и иммобилизировать белок, который включает последовательности EGF. В обоих случаях это вызвано олигомеризацией мономеров, содержащих IGF и EGF, с присутствием их обоих. Кроме того, гетероолигомеры способны образовываться в тех случаях, когда оба фактора роста расположены на противоположных концах компонента CTB (т.е. IGF-CTB и T2), и в тех случаях, когда оба фактора роста находятся на том же (C) конце (т.е. IGF-CTB и T5). Анализ также работает в любой из двух ориентаций.
[0158] Пример XI: презентирование различных факторов роста
[0159] Для дополнительной демонстрации вариативности настоящего изобретения создавали панель рекомбинантных белков, которые включали последовательность, полученную из CTB, наряду с дополнительной последовательностью, полученной из одного или нескольких из ряда факторов роста, и представляли ряд доменов различных размеров согласно фигуре 28 с использованием стандартных методик, известных специалистам в данной области. Образцы каждого из белков получали путем экспрессии генного конструкта в E. coli и очищали с помощью IMAC посредством гексагистидиновой метки на N-конце каждого белка. Очищенные рекомбинантные белки анализировали с помощью ELISA, чтобы продемонстрировать то, что каждая из различных последовательностей присутствовала и была представлена правильно, с помощью антител, специфичных для каждой последовательности (фигура 29). Нативный белок прогоняли с образцами рекомбинантного белка, включающего последовательности, полученные из mTGF B1 и CTB, и получали вестерн-блот (фигура 30). Белок выявляли с помощью антитела к α-CTB, и показывали, что в применяемых условиях рекомбинантный гибридный белок был способен формировать стабильные пентамеры, сохраняющие данное характерное свойство CTB.
[0160] Пример XII: презентирование рецептора фактора роста
[0161] Для того, чтобы продемонстрировать, что технология, описанная в настоящем раскрытии, применима к функциональному анализу белков, отличных от факторов роста, получали рекомбинантные белки, включающие последовательности, полученные из рецепторов факторов роста и CTB, и было показано присутствие таких последовательностей в естественной конформации вместе с последовательностями CTB. ДНК, кодирующую последовательность белка TGF-бета 1 человека, клонировали выше гена CTB путем замещения ДНК, кодирующей EGF, из клона T3LL с использованием стандартных методик, известных специалистам в данной области. Данный конструкт применяли для получения рекомбинантного белка, включающего последовательности как TGF-бета 1 человека, так и CTB (фигура 31a). Аналогично, получали второй рекомбинантный белок, который включал последовательности внеклеточного лигандсвязывающего домена рецептора TGF-бета 2 человека и CTB (фигура 31b).
[0162] Одновременное присутствие последовательностей как TGF-бета R2, так и CTB в отдельном рекомбинантном белке определяли с помощью ELISA с захватом. Вкратце, лунки планшета для ELISA покрывали i) антителом мыши к CTB или ii) антителом козы к TGF-бета R2 и блокировали с помощью PBS, содержащего сухое молоко. Образцы рекомбинантного белка, который показан на фигуре 31b, затем приводили в контакт с лунками и инкубировали в течение приблизительно 1 часа. После промывания лунки приводили в контакт с i) антителом козы к TGF-бета R2 или ii) антителом мыши к CTB, соответственно, и инкубировали в течение 1 часа. Вслед за промыванием лунки приводили в контакт с i) HRP-меченным антителом к антителу овцы (козы) и ii) HRP-меченным антителом к антителу мыши, соответственно, и инкубировали в течение приблизительно 1 часа. Планшет проявляли с помощью субстрата TMB, и интенсивность окраски измеряли при 450 нм. Анализ продемонстрировал, что последовательности как TGF-бета R2, так и CTB присутствовали в одном и том же гибридном рекомбинантном белке (фигура 32).
[0163] Для того, чтобы продемонстрировать, что как TGF-бета 1, так и TGF-бета R2 представлены в отдельности с последовательностями CTB в нативной конфигурации, определяли взаимодействие между TGF-бета 1 и его природным рецептором с помощью ELISA. Вкратце, лунки планшета для ELISA покрывали антителом мыши к CTB в качестве блокированного. Лунки затем приводили в контакт с рекомбинантным белком, содержащим последовательности TGF-бета 1 человека и CTB, согласно фигуре 31a и инкубировали в течение приблизительно 1 часа. После промывания лунки приводили в контакт с рекомбинантным белком, содержащим последовательности TGF-бета R2 человека и CTB, согласно фигуре 31b и инкубировали в течение приблизительно 1 часа. Лунки промывали и затем приводили в контакт с антителом козы к TGF-бета R2 в течение 1 часа. В конечном счете лунки промывали и приводили в контакт с HRP-меченным антителом к антителу овцы (козы) в течение приблизительно 1 часа. Планшет проявляли с помощью субстрата TMB, и данные с него считывали при 450 нм. На фигуре 33 показано, что два рекомбинантных белка способны воспроизводить естественное связывающее взаимодействие рецептора и лиганда и что оно не нарушается антителом к рецептору, применяемому в анализе.
[0164] Пример XIII: иммунные ответы мышей на составы с рекомбинантными белками
[0165] В других экспериментальных группах мышей их иммунизировали рекомбинантными белками, включающими последовательности из CTB и одного или нескольких факторов роста согласно настоящему раскрытию, для того, чтобы оценить эффекты различных составов на иммунные ответы указанных мышей. Иммунизировали шесть групп мышей, в каждой из которых содержалось шесть мышей, составами с различными рекомбинантными белками по схеме, описанной ниже.
[0166] Если не указано иное, мышей иммунизировали с помощью 25 мкг рекомбинантного белка в 75 мкл буфера, эмульгированного в 75 мкл адъюванта Montanide. Иммуногены вводили посредством внутримышечной инъекции в день 0 и день 14. Образцы сыворотки забирали в день 0 (предварительная иммунизация) и в день 28 и анализировали на присутствие антител IgG к последовательностям факторов роста, содержащимся в рекомбинантном белке для иммунизации. Группы мышей иммунизировали следующими антигенами.
[0167] Группа 1: SB1, 75 мкл (25 мкг) рекомбинантного белка, включающего последовательности IGF человека и CTB в соответствии с фигурой 26, эмульгированного с 75 мкл Montanide;
[0168] группа 2: SB2, 75 мкл (25 мкг) рекомбинантного белка, включающего последовательности EGF человека и CTB согласно примеру VIII и называемого T3LL, эмульгированного с 75 мкл Montanide;
[0169] группа 3: SB3, 75 мкл (25 мкг) рекомбинантного белка, включающего последовательности IGF человека, EGF человека и CTB в соответствии с фигурой 24 и согласно примеру IX, эмульгированного с 75 мкл Montanide;
[0170] группа 4: SB4, 37,5 мкл (12,5 мкг) SB1 и 37,5 мкл (12,5 мкг) SB2, объединенные по способу согласно примеру X и включающие олигомеры, содержащие как IGF-CTB, так и EGF-CTB, эмульгированные с 75 мкл Montanide;
[0171] группа 5: SB5, 75 мкл (25 мкг) SB1, как в группе 1, за исключением того, что его эмульгировали с 20 мкл адъюванта Matrix-M; и
[0172] группа 6: SB6, 37,5 мкл (12,5 мкг) SB1, эмульгированного с 37,5 мкл Montanide, с последующими через 5 мин. 37,5 мкл (12,5 мкг) SB2, эмульгированного в 37,5 мкл Montanide и вводимого через другой участок.
[0173] Непосредственно перед иммунизацией и через 14 дней после нее забирали образцы крови, и сыворотку анализировали с помощью ELISA на присутствие и относительные титры антител IgG к компоненту-фактору роста антигенов-рекомбинантных белков для иммунизации. Планшеты для ELISA покрывали коммерчески доступными рекомбинантными IGF или EGF человека в концентрации 1 мкг/мл. После блокирования и промывания, сыворотку от субъектов-мышей в различных разведениях наносили на лунки и инкубировали в течение 1 часа при комнатной температуре. Несвязанное антитело и другие белки удаляли путем промывания, а связанные IgG мышей выявляли с помощью HRP-меченного антитела к антителу мыши.
[0174] Все шесть групп включали животных, которые вырабатывали специфический иммунный ответ на компонент-фактор роста иммуногенных рекомбинантных гибридных белков. Очевидно, что для всех групп более сильные ответы наблюдали в отношении EGF, нежели в отношении IGF, включая группы, где были включены последовательности только из одного фактора роста (группы 1 и 2, фиг. 34 и 35). Вне связи с какой-либо определенной теорией, наблюдаемое, возможно, является отображением степени гомологии между белками мыши и человека, при которой EGF отличаются на 15/53 остатков, а IGF отличаются только на 4 из 70 остатков. Также интересно отметить, что различия между ответами отдельных животных в группе зачастую превышают различия между группами для одного и того же антигена.
[0175] Применение Matrix-M вместо Montanide в качестве адъюванта (группа 5 в сравнении с группой 1, фиг. 40 и 34) приводило к более слабому иммунному ответу, при этом одна из мышей вообще не вырабатывала иммунный ответ, а четыре других образца необходимо было подвергнуть скринингу при значительно больших концентрациях, чем с Montanide.
[0176] Группы 3, 4 и 6 получали белки, которые включали последовательности как из EGF, так и из IGF, при этом различие состояло в составе или пути введения. В группе 3 все мыши, получавшие рекомбинантный белок, который включал последовательности как EGF, так и IGF в каждой молекуле белка, вырабатывали иммунный ответ на EGF, хотя две из шести не проявляли иммунный ответ на α-IGF (фиг. 36 и 37). В группах 4 и 6 также все мыши вырабатывали антитела к EGF (фиг. 38, 39 и 41). В группе 4 одно животное не вырабатывало иммунный ответ к IGF, а другое вырабатывало только очень слабый иммунный ответ. Только в группе 6, где EGF- и IGF-содержащие белки вводили по отдельности и в различные участки, все 6 животных сформировали иммунный ответ к IGF.
[0177] Пример XIV: общая одноэтапная очистка
[0178] Желателен простой первостепенный способ очистки, который можно применять ко всем без исключения иммуногенным рекомбинантным белкам, подробно описанным в настоящем раскрытии. В оптимальном варианте очистка не требует включения аффинной метки, такой как гексагистидин, MBP, FLAG и т.д. Рекомбинантные белки по настоящему раскрытию являются родственными в том, что все они включают по меньшей мере некоторую последовательность, полученную из субъединицы токсина CT-B Vibrio cholera или его искусственного функционального эквивалента. Предполагается, что очистку можно осуществлять путем применения моноклональных или поликлональных антител, однако получение моноклональных антител является дорогостоящим. Поликлональные антитела менее дорогостоящие, однако возможно, что будут наблюдаться различия в функциональных характеристиках между партиями от одного и того же животного и от отдельных животных. Иммуноаффинная очистка также требует жестких условий, таких как низкий pH, для элюирования белка-мишени, которые могут оказывать отрицательное влияние на белок-мишень и будут ограничивать повторное применение аффинной матрицы. Это также включает введение дополнительного белка в способ получения, чего предпочтительно избегать.
[0179] В случае нативного голотоксина CT токсин связывается с моноганглиозидом Gml (фигура 42), находящимся на поверхности большинства клеток млекопитающих, в том числе на эпителиальных клетках дыхательных путей и желудочно-кишечного тракта. Связывание осуществляется субъединицей B CT, и только олигомеры CT-B связываются с Gml. Таким образом предполагают, что CTB, иммобилизированный на подходящей подложке, можно применять для очистки иммуногенных рекомбинантных белков по настоящему раскрытию. Применение CTB не считают предпочтительным способом, несмотря на некоторые причины, примечательно, что CTB коммерчески доступен только в качестве материала, очищенного из мозга быка. Применение животного материала и, в частности, применение ткани мозга быка не подходит для применения в получении терапевтических продуктов.
[0180] Как известно, в связывании CTB с Gml задействован концевой галактозный фрагмент на разветвленной гликозилированной молекуле Gml, связывающейся с двумя прилежащими субъединицами CTB. Таким образом предполагают, что галактоза, иммобилизированная на подходящей твердой подложке, будет представлять общее средство очистки рекомбинантных белков по настоящему раскрытию. Для оценки целесообразности данного подхода ген, кодирующий CTB, клонировали в вектор экспрессии бактериального белка, сконструированный для извлечения периплазматического белка, с использованием методик, известных специалистам в данной области, и вводили в различные штаммы бактерий E. coli путем трансформации. Галактозно-сефарозную смолу (фигура 43) получали от Pierce (номер по каталогу Pierce 20372). Выращивали пятидесятимиллилитровые культуры клонов штаммов XL1-Blue, BL21 и TGI E. coli, экспрессирующих CTB, и индуцировали экспрессию ими рекомбинантного CTB в течение ночи при 37°C. Клетки собирали путем центрифугирования, и очищенную среду сохраняли для экстракции CTB. Содержимое периплазматического пространства высвобождали из сгустков клеток путем воздействия осмотического шока с использованием стандартных способов, известных специалистам в данной области, получая 10 мл на культуру.
[0181] Галактозно-сефарозную смолу промывали с помощью 200 мМ NaCl, 50 мМ Трис-HC1, 5 мМ ЭДТА при pH 7,5 (буфер TEN) в соответствии с инструкциями производителя. Добавляли NaCl, Трис-HCl при pH 7,5 и ЭДТА к кондиционированным средам и периплазматическим фракциям до конечной концентрации 200 мМ NaCl, 50 мМ Трис-HCl и 5 мМ ЭДТА. 0,5 мл промытой галактозо-сефарозы добавляли к каждой кондиционированной среде и периплазматическим фракциям и инкубировали с помешиванием при 4°C в течение 2-3 ч. Смолу извлекали в колонках BioRad и промывали 30 объемами слоя ледяного буфера TEN. Связанный белок элюировали путем повторного суспендирования смолы в 0,5 мл 1 M галактозы в PBS и инкубирования в течение 10 мин. Колонку опорожняли, а элюат оставляли для анализа. Этап элюирования повторяли несколько раз, и фракции анализировали на присутствие CTB. Практически все экспрессированные белки CTB обнаруживали в культуральной среде. Образцы предварительно очищенных кондиционированных сред и периплазматических фракций совместно с объединенными элюатами из колонок, содержащими очищенный CTB (из среды), анализировали с помощью SDS-PAGE и сравнивали с His-меченным CTB, очищенным с помощью IMAC (фигура 44). Видно, что CTB с высокой степенью очистки получали из надосадочных жидкостей культур всех трех штаммов, при этом клетки XL1-Blue давали самый высокий урожай (дорожки 4, 7 и 10). Чистота была вполне сравнима с той, которую наблюдали при очистке с помощью IMAC (дорожка 11), и включала значительное количество пентамерного белка.
[0182] Дополнительные варианты осуществления
[0183] Согласно настоящему документу в другом иллюстративном варианте осуществления раскрыта вакцина, состоящая из гомогенного рекомбинантного белка, для улучшения презентирования и увеличения количества эпитопов опухолевых антигенов в качестве элементов искусственного иммуногенного рекомбинантного белка. Согласно настоящему документу в одном иллюстративном варианте осуществления раскрыта вакцина, полученная из рекомбинантного белка, включающего всю последовательность полипептида и опухолевый антиген или их части.
[0184] В иллюстративном варианте осуществления рекомбинантные белки, раскрытые в настоящем документе, могут включать или содержать высокую долю белковых последовательностей, полученных из опухолевых антигенов и/или их эпитопов, в зависимости от общего молекулярного веса. Данные эпитопы опухолевых антигенов могут быть множественными копиями всего отдельного опухолевого антигена или его части или копиями всех нескольких различных опухолевых антигенов или их частей.
[0185] В иллюстративном варианте осуществления рекомбинантный белок представляет собой иммуногенную белковую молекулу, содержащую одну или несколько последовательностей, которые сворачиваются в физическую структуру, например, содержащую одну или несколько последовательностей белкового холерного токсина B (CT-B) Vibrio cholera или его искусственного эквивалента и содержащую одну или несколько последовательностей одного или нескольких опухолевых антигенов или их частей.
[0186] В иллюстративном варианте осуществления последовательность опухолевого антигена может включать в себя последовательность простатического специфического антигена (PSA) или его части. В других иллюстративных вариантах осуществления опухолевый антиген может включать один или несколько из следующих опухолевых антигенов, в том числе, без ограничения, PSA и другие опухолевые антигены полной длины или их части.
[0187] Согласно настоящему документу в другом иллюстративном варианте осуществления раскрыт белок, состоящий из гомогенного рекомбинантного белка, для улучшения презентирования и увеличения количества участков связывания рецептора в качестве элементов иммуногенного рекомбинантного белка. Согласно настоящему документу в одном иллюстративном варианте осуществления раскрыт рекомбинантный белок, содержащий всю последовательность полипептида и рецептор или их части.
[0188] В иллюстративном варианте осуществления рекомбинантные белки, раскрытые в настоящем документе, могут включать или содержать высокую долю белковых последовательностей, полученных из рецепторов и/или их участков связывания, в зависимости от общего молекулярного веса. Данные участки связывания могут быть множественными копиями всего отдельного рецептора или его части или копиями всех нескольких различных рецепторов или их частей.
[0189] В иллюстративном варианте осуществления рекомбинантный белок представляет собой иммуногенную белковую молекулу, содержащую одну или несколько последовательностей, которые сворачиваются в физическую структуру, например, содержащую одну или несколько последовательностей белкового холерного токсина B (CT-B) Vibrio cholera или его искусственного эквивалента, и содержащую одну или несколько последовательностей одного или нескольких рецепторов или их частей.
[0190] В иллюстративном варианте осуществления последовательность рецептора может включать в себя последовательность рецептора эпидермального фактора роста человека 2 (Her2) или его части и/или рецептора эпидермального фактора роста человека 3 (Her3) или его части. В других иллюстративных вариантах осуществления рецептор может включать один или несколько из следующих рецепторов, в том числе, без ограничения, Her2, Her3 и другие рецепторы полной длины или их части.
[0191] В других иллюстративных вариантах осуществления рекомбинантный белок представляет собой иммуногенную белковую молекулу, содержащую одну или несколько последовательностей, которые сворачиваются в физическую структуру, например, содержащую одну или несколько последовательностей CT-B или его искусственного модифицированного варианта и содержащую разнообразные сочетания одной или нескольких последовательностей одного или нескольких факторов роста или их частей, одной или нескольких последовательностей одного или нескольких опухолевых антигенов или их частей и одной или нескольких последовательностей одного или нескольких рецепторов или их частей.
[0192] В иллюстративном варианте осуществления рекомбинантный белок включает в себя включения или последовательности одного или нескольких факторов роста или их частей и одну или несколько последовательностей одного или нескольких опухолевых антигенов или их частей. В одном варианте осуществления рекомбинантный белок включает в себя одну или несколько последовательностей CT-B или его искусственного модифицированного варианта, PSA или его части и IGF-1 или его части.
[0193] В другом иллюстративном варианте осуществления рекомбинантный белок включает в себя включения или последовательности одного или нескольких факторов роста или их частей и одну или несколько последовательностей одного или нескольких рецепторов или их частей. В одном варианте осуществления рекомбинантный белок включает в себя одну или несколько последовательностей CT-B или его искусственного модифицированного варианта, Her2 или его части и IGF-1 или его части. В другом варианте осуществления рекомбинантный белок включает в себя одну или несколько последовательностей CT-B или его искусственного модифицированного варианта, Her2 или его части, Her2 или его части и PDGF или его части.
[0194] В другом иллюстративном варианте осуществления рекомбинантный белок включает в себя включения или последовательности одного или нескольких опухолевых антигенов или их частей и одну или несколько последовательностей одного или нескольких рецепторов или их частей.
[0195] В еще одном иллюстративном варианте осуществления рекомбинантный белок включает в себя включения или последовательности одного или нескольких факторов роста или их частей, одну или несколько последовательностей одного или нескольких опухолевых антигенов или их частей и одну или несколько последовательностей одного или нескольких рецепторов или их частей.
[0196] В любом из вариантов осуществления, упомянутых выше, помимо включения одной или нескольких копий отдельного опухолевого антигена, рецептора и/или фактора роста, представленных в виде отдельного опухолевого антигена, рецептора и/или фактора роста или его части на физический участок, и/или в виде цепей повторяющихся последовательностей опухолевого антигена, рецептора и/или фактора роста (например, n= 1-10), происходит следующее. Рекомбинантные белки согласно настоящему раскрытию могут также включать в себя включения одного или нескольких нейтрализующих доменов или участков связывания из двух или более различных опухолевых антигенов, рецепторов и/или факторов роста, которые представлены в виде отдельных таковых или в виде цепей в различных положениях в пределах последовательности рекомбинантных белков. Например, рекомбинантные белки могут включать в себя включения или последовательности двух-четырех различных опухолевых антигенов, рецепторов и/или факторов роста полной длины или их частей и/или одного или нескольких опухолевых антигенов, рецепторов и/или факторов роста полной длины или их частей в виде отдельных эпитопов или участков связывания или в виде двух или более тандемных повторов.
[0197] Полученные белки являются отдельными полипептидами, включающими опухолевый антиген, рецептор и/или фактор роста или один или несколько их эпитопов или участков связывания в пределах последовательностей рекомбинантных белков. В иллюстративном варианте осуществления последовательности рекомбинантных белков содержат одну или несколько частей последовательности CT-B и представляют собой включение(я) опухолевого антигена, рецептора и/или фактора роста, включающие по меньшей мере одно или несколько включений их эпитопов или участков связывания на поверхности иммуногенных рекомбинантных белков в естественной конформации.
[0198] Согласно настоящему раскрытию включения эпитопов опухолевых антигенов, участков связывания рецептора и/или эпитопов факторов роста должны быть свернуты с тем, чтобы их естественная конформация в значительной степени сохранялась и презентировалась компонентам иммунной системы хозяина таким образом, чтобы вызвать сильный иммунный ответ хозяина. Примеры подходящих природных белковых моделей включают, без ограничения, субъединицу B холерного токсина, токсин Listeria, столбнячный анатоксин, дифтерийный анатоксин, белок оболочки бактериофага, белок оболочки аденовируса и другие белки оболочки вирусов. Альтернативно, можно применять неприродные 'искусственные' полипептиды, что удовлетворяет условиям придания иммуногенности всему белку и обеспечения соответствующего презентирования эпитопов опухолевых антигенов, участков связывания рецептора и/или эпитопов факторов роста иммунной системе хозяина.
[0199] Адъювант
[0200] Определенные иллюстративные варианты осуществления, представленные в настоящем документе, включают рекомбинантные белки по настоящему раскрытию в вакцинных композициях и иммунологических адъювантных композициях, в том числе фармацевтических композициях, которые содержат, помимо рекомбинантных белков, по меньшей мере один адъювант, что означает компонент таких композиций, который обладает адъювантной активностью. Адъювант с такой адъювантной активностью включает композицию, которая при введении субъекту, такому как человек (например, пациент-человек), примат, отличный от человека, млекопитающее или другой высший эукариотический организм с узнаваемой иммунной системой, способна изменять (т.е., повышать или понижать статистически значимым образом и, в определенных предпочтительных вариантах осуществления, увеличивать или повышать) специфическую активность и/или долгосрочность иммунного ответа. В определенных иллюстративных вариантах осуществления, раскрытых в настоящем документе, необходимые антиген и/или антигены, находящиеся в белке-носителе, и необязательно один или несколько адъювантов могут таким образом изменять, например, вызывать или усиливать, иммунный ответ, который направлен против необходимых антигена и/или антигенов, которые могут быть введены в одно и то же время или могут быть разделены во времени и/или пространстве (например, в различные анатомические участки) при их введении, но конкретные иллюстративные варианты осуществления не предназначены быть ограниченными и, таким образом, также предусматривают введение рекомбинантного белка в композиции, которая не включает упомянутый антиген, но которая может также включать, без ограничения, один или несколько коадъювантов, имидазохинолиновый модификатор иммунного ответа.
[0201] Таким образом, и как отмечалось выше, адъюванты включают композиции, которые обладают адъювантными эффектами, такие как сапонины и миметики сапонинов, в том числе миметики QS21 и QS21 (см., например, патент США № 5057540; EP 0362279 B1; WO 95/17210), квасцы, растительные алкалоиды, такие как томатин, моющие средства, такие как (без ограничения) сапонин, полисорбат 80, спан 85 и стеарилтирозин, один или несколько цитокинов (например, GM-CSF, IL-2, IL-7, IL-12, TNF-альфа, IFN-гамма), имидазохинолиновый модификатор иммунного ответа и иммунные модификаторы со структурой типа двухцепочечный стебель-петля (dSLIM, например, Weeratna et al, 2005 Vaccine 23:5263).
[0202] Моющие средства, в том числе сапонины, изложены, например, в патенте США № 6544518; Lacaille-Dubois, M and Wagner H. (1996 Phytomedicine 2:363-386), патенте США № 5057540, Kensil, Crit. Rev Ther Drug Carrier Syst, 1996, 12 (1-2): 1-55 и EP 0362279 B1. Структуры в форме частиц, называемые иммуностимулирующими комплексами (ISCOMS), содержащие фракции Quil A (сапонина), являются гемолитическими, и их применяли в производстве вакцин (Morein, B., EP 0109942 B1). Как сообщалось, данные структуры обладают адъювантной активностью (EP 0109942 B1; WO 96/11711). Гемолитические сапонины QS21 и QS17 (очищенные с помощью ВЭЖХ фракции Quil A) описывали как эффективные системные адъюванты, и способы их получения раскрыты в патенте США № 5057540 и EP 0362279 B1. Также в этих литературных источниках описано применение QS7 (негемолитической фракции Quil-A), который действует в качестве эффективного адъюванта для системных вакцин. Применение QS21 также описано в Kensil et al. (1991 J. Immunology 146:431-437). Также известны комбинации QS21 и полисорбата или цклодекстрина (WO 99/10008). Определенные адъювантные системы, содержащие фракции QuilA, такие как QS21 и QS7, описаны в WO 96/33739 и WO 96/11711. Другие сапонины, которые использовали в исследованиях системной вакцинации, включают полученные из других видов растений, таких как Gypsophila и Saponaria (Bomford et al, Vaccine, 10(9):572-577, 1992).
[0203] Эсцин представляет собой другое моющее средство, родственное сапонинам, для использования в адъювантных композициях в вариантах осуществления, раскрытых в настоящем документе. Эсцин описан в справочнике Мерк (12.sup.th Ed.:запись 3737) в качестве смеси сапонинов, обнаруженной в семенах конского каштана, Aesculus hippocastanum. Описано его выделение с помощью хроматографии и очистки (Fiedler, Arzneimittel-Forsch. 4, 213 (1953)) и с применением ионнообменных смол (Erbring et al, патент США № 3238190). Фракции эсцина (также известные как аэсцин) очищали, и было показано, что они обладают биологической активностью (Yoshikawa M, et al. (Chem Pharm Bull (Tokyo) 1996 August; 44(8): 1454-1464)). Дигитонин является другим моющим средством, также описанным в справочнике Мерк (12th Ed., запись 3204) в качестве сапонина, полученного из семян Digitalis purpurea и очищенного согласно методике, описанной в Gisvold et al, J. Am. Pharm. Assoc., 1934, 23, 664; и Rubenstroth-Bauer, Physiol. Chem., 1955, 301, 621.
[0204] Другие адъюванты или коадъюванты для применения согласно конкретным описанным в настоящем документе вариантам осуществления включают блок-сополимер или биоразлагаемый полимер, которые относятся к классу полимерных соединений, известных специалистам в данной области. Примеры блок-сополимера или биоразлагаемого полимера, которые могут быть включены в вакцинную композицию или иммунологический адъювант, включают Pluronic.RTM. L121 (BASF Corp., Маунт-Олив, Нью-Джерси; см., например, Yeh et al, 1996 Pharm. Res. 13: 1693).
[0205] Некоторые дополнительные иллюстративные варианты осуществления предусматривают иммунологические адъюванты, которые включают, без ограничения, масло, которое в некоторых таких вариантах осуществления может способствовать коадъювантной активности, и в других таких вариантах осуществления можно дополнительно или альтернативно предусматривать фармацевтически приемлемый носитель или наполнитель. Известно любое количество подходящих масел, и они могут быть выбраны для включения в вакцинные композиции и иммунологические адъювантные композиции согласно настоящему раскрытию. Примеры таких масел, приводимые в целях иллюстрации, а не ограничения, включают сквален, сквалан, минеральное масло, оливковое масло, холестерин и моноолеат маннида.
[0206] Модификаторы иммунного ответа, такие как имидазохинолиновые модификаторы иммунного ответа, также известны в данной области техники и также могут быть включены в качестве адъювантов или коадъювантов в некоторые раскрытые в настоящем документе варианты осуществления.
[0207] Также, как отмечалось ранее, одним типом адъюванта или коадъюванта для применения в вакцинной композиции согласно настоящему раскрытию, как описано в настоящем документе, могут быть алюминиевые коадъюванты, которые обычно называют "квасцы". Квасцовые коадъюванты основаны на следующем: оксогидроксид алюминия; гидроксифосфат алюминия или разнообразные запатентованные соли. Квасцовые коадъюванты предпочтительны, поскольку они обладают хорошими показателями безопасности, усиливают гуморальный иммунный ответ, стабилизируют антигены, и их производство в больших масштабах является относительно простым. (Edelman 2002 Mol. Biotechnol. 21:129-148; Edelman, R. 1980 Rev. Infect. Dis. 2:370-383.)
[0208] Фармацевтические композиции
[0209] В некоторых иллюстративных вариантах осуществления фармацевтическая композиция представляет собой вакцинную композицию, которая как содержит рекомбинантный белок согласно настоящему раскрытию, так и может дополнительно содержать один или несколько компонентов, представленных в настоящем документе, которые выбраны из агониста TLR, коадъюванта (включающего, например, цитокин, имидазохинолиновый модификатор иммунного ответа и/или dSLIM) и т.п., и/или рекомбинантный экспрессионный конструкт в комбинации с фармацевтически приемлемым носителем, наполнителем или разбавителем.
[0210] Типичные носители будут нетоксичными для реципиентов при применяемых дозах и концентрациях. Что касается вакцин, содержащих рекомбинантный белок, их будут вводить в количестве от приблизительно 0,01 мкг/кг до приблизительно 100 мг/кг массы тела, как правило, посредством внутрикожного, подкожного, внутримышечного или внутривенного пути или посредством других путей.
[0211] Специалистам в данной области будет очевидно, что число и частота введений будет зависеть от ответа хозяина. "Фармацевтически приемлемые носители" для применения в терапевтических целях хорошо известны в области фармацевтики и описаны, например, в Remington's Pharmaceutical Sciences, Mack Publishing Co. (A. R. Gennaro edit. 1985). Например, при физиологическом значении pH можно применять стерильный солевой раствор и забуференный фосфатом солевой раствор. В фармацевтической композиции могут быть предусмотрены консерванты, стабилизаторы, красители и даже ароматизирующие средства. Например, в качестве консервантов можно добавлять бензоат натрия, аскорбиновую кислоту и сложные эфиры п-гидроксибензойной кислоты. В дополнение, можно применять антиоксиданты и суспендирующие средства.
[0212] Фармацевтические композиции могут быть в любой форме, которая предусматривает введение композиции пациенту. Например, композиция может быть в твердой, жидкой или газообразной (аэрозоль) форме. Обычные пути введения включают, без ограничения, пероральный, локальный, парентеральный (например, сублингвально или трансбуккально), сублингвальный, ректальный, вагинальный и интраназальный (например, в виде спрея). Выражение "парентеральный", применяемое в настоящем документе, включает ионофоретическое, сонофоретическое, пассивное трансдермальное введение, введение с помощью микроигл, а также подкожные инъекции, методики внутривенных, внутримышечных, интрастернальных, интракавернозных, интратекальных, внутрипросветных, внутриуретральных инъекций или инфузий. В конкретном варианте осуществления композицию, описанную в настоящем документе (включающую вакцинную и фармацевтическую композицию), вводят внутрикожно с помощью методики, выбранной из ионофореза, образования микрополостей, сонофореза или введения с помощью микроигл.
[0213] Фармацевтическая композиция составлена так, что обеспечивает биологическую доступность активных ингредиентов, содержащихся в ней, при введении композиции пациенту. Композиции, которые будут вводить пациенту, имеют форму одной или нескольких единиц дозирования, где, например, таблетка может быть отдельной единицей дозирования, а контейнер с одним или несколькими соединениями по настоящему изобретению в форме аэрозоля может содержать множество единиц дозирования.
[0214] Для перорального введения в композиции может присутствовать наполнитель и/или связующее вещество. Примерами являются сахароза, каолин, глицерин, крахмал, декстрины, альгинат натрия, карбоксиметилцеллюлоза и этилцеллюлоза. Могут присутствовать красящие и/или ароматизирующие средства. Можно использовать оболочку для покрытия.
[0215] Композиция может быть в форме жидкости, например, эликсира, сиропа, раствора, эмульсии или суспензии. Жидкость, в качестве двух примеров, может предназначаться для перорального введения или для доставки путем инъекции. В тех случаях, когда жидкость предназначена для перорального введения, предпочтительные композиции содержат один или несколько из подсластителя, консервантов, красителя/окрашивающего вещества и усилителя вкуса и запаха. В композицию, предназначенной для введения путем инъекции, могут быть включены один или несколько из поверхностно-активного вещества, консерванта, смачивающего средства, диспергирующего средства, суспендирующего средства, буфера, стабилизатора и изотонического средства.
[0216] Жидкая фармацевтическая композиция, применяемая в настоящем документе, независимо от того, находится ли она в форме раствора, суспензии или в любой другой форме, может включать один или несколько из следующих носителей или наполнителей: стерильные разбавители, такие как вода для инъекций, солевой раствор, предпочтительно физиологический солевой раствор, раствор Рингера, изотонический хлорид натрия, нелетучие масла, такие как сквален, сквалан, минеральное масло, моноолеат маннида, холестерин и/или синтетические моно- или диглицериды, которые могут служить растворителем или питательной взвесью, полиэтиленгликоли, глицерин, пропиленгликоль или другие растворители; антибактериальные средства, такие как бензиловый спирт или метилпарабен; антиоксиданты, такие как аскорбиновая кислота или бисульфит натрия; хелатообразующие средства, такие как этилендиаминтетрауксусная кислота; буферы, такие как ацетатные, цитратные или фосфатные буферы, и средства регуляции тоничности, такие как хлорид натрия или декстроза. Препараты для парентерального введения могут быть заключены в ампулы, шприцы одноразового использования или многодозовые флаконы, изготовленные из стекла или пластмассы. Инъекционные фармацевтические композиции предпочтительно являются стерильными.
[0217] В конкретном варианте осуществления фармацевтическая или вакцинная композиция по настоящему изобретению содержит стабильную водную суспензию с размером частиц менее 0,2 мкм и также содержит по меньшей мере один компонент, выбранный из группы, включающей фосфолипиды, жирные кислоты, поверхностно-активные вещества, моющие средства, сапонины, фторированные липиды и т.п.
[0218] Также может быть необходимо включение других компонентов в вакцинную или фармацевтическую композицию, таких как средства доставки, в том числе, без ограничения, соли алюминия, эмульсии типа "вода в масле", биоразлагаемое масло-основа, эмульсии типа "масло в воде", биоразлагаемые микрокапсулы и липосомы. Примеры дополнительных иммуностимулирующих веществ (коадъювантов) для применения в таких основах также описаны выше и могут включать N-ацетилмурамил-L-аланил-D-изоглутамин (MDP), глюкан, IL-12, GM-CSF, гамма-интерферон и IL-12.
[0219] Несмотря на то, что в фармацевтических композициях по настоящему изобретению можно применять любой подходящий носитель, известный специалистам в данной области, тип носителя будет меняться в зависимости от способа введения и необходимости замедленного высвобождения. В случае парентерального введения, такого как подкожная инъекция, носитель предпочтительно включает воду, солевой раствор, спирт, жир, воск или буфер. В случае перорального введения можно использовать любые из вышеупомянутых носителей или твердый носитель, такой как маннит, лактоза, крахмал, стеарат магния, сахарин натрия, тальк, целлюлоза, глюкоза, сахароза и карбонат магния. Также можно использовать биоразлагаемые микросферы (например, из сополимера лактида и галактида) в качестве носителей для фармацевтических композиций по настоящему изобретению.
[0220] Фармацевтическая композиция может также содержать разбавители, такие как буферы, антиоксиданты, такие как аскорбиновая кислота, низкомолекулярные (менее чем приблизительно 10 остатков) полипептиды, белки, аминокислоты, углеводы, в том числе глюкозу, сахарозу или декстрины, хелатообразующие средства, такие как ЭДТА, глутатион и другие стабилизаторы и наполнители. Нейтральный забуференный солевой раствор или солевой раствор, смешанный с неспецифическим сывороточным альбумином, являются иллюстративными подходящими разбавителями. Предпочтительно, продукт может быть составлен в качестве лиофилизата с применением подходящих растворов наполнителей (например, сахарозы) в качестве разбавителей.
[0221] В иллюстративном варианте осуществления домен рекомбинантного белка, несущий эпитоп или рецептор, вне зависимости от того, получен ли он из природной или из искусственной последовательности полипептида, должен обладать способностью к самоорганизации в олигомерные мультимеры при соответствующих химических/внешних условиях или к уменьшению до мономеров при альтернативных условиях. Оптимально, участвующие в мультимеризации домены будут собираться в стабильные мультимеры с небольшим числом субъединиц, например, димеры, тримеры, тетрамеры, пентамеры и т.д., так, чтобы образовывался продукт с частицами с равномерным размером. Примеры природных полипептидов включают, без ограничения, лейциновые застежки, белок lac-репрессор, стрептавидин/авидин, субъединицу B холерного токсина, участвующий в тримеризации домен Pseudomonas и вирусные капсидные белки.
[0222] В иллюстративном варианте осуществления раскрыт способ получения поливалентной молекулы. В данном иллюстративном варианте осуществления способ включает сборку мультимеров из мономерных субъединиц с получением искусственного белка, включающего в себя один или несколько опухолевых антигенов, рецепторов и/или факторов роста или их части.
[0223] В другом иллюстративном варианте осуществления раскрыт способ получения вакцинного состава. В данном иллюстративном варианте осуществления способ включает смешивание одного или нескольких отдельных моновалентных мультимеров вместе с получением поливалентной вакцины, содержащей рекомбинантный белок, включающий в себя один или несколько опухолевых антигенов, рецепторов и/или факторов роста или их части.
[0224] В еще одном иллюстративном варианте осуществления раскрыт способ лечения пациента. В данном иллюстративном варианте осуществления способ включает введение пациенту по отдельности одного или нескольких моновалентных рекомбинантных белков на основе одного опухолевого антигена, рецептора и/или фактора роста в один и тот же день или в чередующиеся дни или разы на протяжении периода вакцинации.
[0225] Несмотря на то, что рекомбинантный белок описан как включающий или содержащий одно или несколько из всей или части по меньшей мере одной последовательности опухолевых антигенов, факторов роста и/или рецепторов и последовательности CT-B, рекомбинантный белок может включать природную последовательность CT-B, или последовательность, по сути аналогичную природной последовательности CT-B, и/или искусственную последовательность.
[0226] Несмотря на то, что рекомбинантный белок описан как включающий или содержащий последовательность CT-B, рекомбинантный белок может включать или содержать производное последовательности CT-B или последовательности, которая по сути аналогична последовательности CT-B.
[0227] Несмотря на то, что применительно к определенным вариантам осуществления были описаны и показаны гомогенные рекомбинантные белки, содержащие или включающие один или несколько опухолевых антигенов, факторов роста и/или рецепторов, многие варианты и модификации будут очевидны для специалистов в данной области и могут быть произведены без отклонения от сущности и объема настоящего раскрытия. Таким образом, раскрытие не должно ограничиваться точными подробностями способа или конструкции, изложенных выше, поскольку предполагается, что такие варианты и модификации включены в объем настоящего раскрытия.
Реферат
Настоящее изобретение относится к области биотехнологии, конкретно к рекомбинантному белку для получения нейтрализующих антител против одного или нескольких факторов роста. Искусственно сконструированная молекула белка согласно настоящему изобретению предполагает наличие в своей структуре нескольких соединенных между собой коротким пептидным линкером фрагментов, выбираемых из иммуногенного пептида и нейтрализующего домена одного или более факторов роста человека, являющихся медиаторами пролиферации клеток в различных видах рака. Изобретение может быть использовано при получении вакцин для иммунотерапии опухолевых заболеваний. 4 н. и 11 з.п. ф-лы, 44 ил., 14 пр.

Комментарии