Способ получения l-треонина с использованием бактерии, принадлежащей к роду escherichia, в которой инактивирован ген tolc - RU2366703C2
Код документа: RU2366703C2
Чертежи
Описание
Область техники
Настоящее изобретение относится к микробиологической промышленности, в частности к способу получения L-аминокислоты с использованием бактерии семейства Enterobacteriaceae, модифицированной таким образом, что экспрессия гена tolC в указанной бактерии ослаблена.
Описание предшествующего уровня техники
Традиционно L-аминокислоты получают в промышленном масштабе методом ферментации с использованием штаммов микроорганизмов, выделенных из природных источников, или их мутантов. Как правило, микроорганизмы модифицируют для увеличения продукции L-аминокислот.
Для увеличения продукции L-аминокислот используются различные методики, включая трансформацию микроорганизма рекомбинантной ДНК (смотри, например, патент США 4278765). Другие методики для увеличения выхода продукта включают увеличение активностей ферментов, вовлеченных в биосинтез аминокислот, и/или устранение чувствительности целевого фермента к ингибированию продуцируемой аминокислотой по типу обратной связи (смотри, например, заявку РСТ WO 95/16042 или патенты США 4346170; 5661012 и 6040160).
Еще один путь для увеличения продукции L-аминокислот - ослабление экспрессии одного или нескольких генов, вовлеченных в деградацию целевой L-аминокислоты, генов, обеспечивающих отклонение предшественников целевой L-аминокислоты от пути биосинтеза L-аминокислоты, генов, вовлеченных в перераспределение потоков углерода, азота и фосфата, генов, кодирующих токсины, клеточные факторы и т.д.
TolC является порином внешней мембраны, участвующим в обеспечении потока нескольких гидрофобных и амфипатических молекул через мембрану. Белок TolC имеет бета-складчатую структуру и образует три цилиндра, каждый из которых состоит из 18-ти мембранных антипараллельных бета-тяжей. Белок TolC является мембранным компонентом, общим для нескольких систем выведения различных веществ.
Было установлено, что продукт гена tolC располагается на внешней мембране (Morona R., et al., J. Bacteriol., 153(2):693-699 (1983)). Белок TolC в виде триммера выделили из препарата внешней мембраны бактерии Escherichia coli и с помощью двухмерной проекции с разрешением 12 ангстрем установили его четвертичную структуру. Обнаружили, что белок TolC является белком внешней мембраны, каждый мономер которого входит в состав мембранного домена, предположительно имеет вторичную структуру бета-бочонка и С-концевой периплазматический домен. Связывание белка TolC с Sec-транслоказой для осуществления переноса через внутреннюю мембрану зависит от белка SecB (Baars L., et al., J. Biol. Chem., 281(15):10024-10034 (2006)).
Было показано, что мутации в гене tolC приводят к замедлению синтеза порина OmpF и к ускорению синтеза порина OmpC. Реконститугивные исследования подтвердили, что белок TolC образует во внешней мембране канал для пептидов. Обнаружили, что белок TolC необходим для функционирования многокомпонентной системы выведения ArcAB (Fralick J., J. Bacteriol, 178 (19):5803-5805 (1996)) и его гомологов AcrEF (Kobayashi K. et al. J. Bacteriol., 183(8): 2646-2653 (2001)) и YhiUV (Nishino K., et al., J. Bacteriol., 184(8):2319-2323 (2002)), системы выведения EmrAB (Borges-Walmsley M.L. et al., J. Biol. Chem., 278 (15):12903-12912 (2003)) и его гомолога EmrKY (Tanabe H., et al. J. Gen. Appt. Microbiol., 43:257-263 (1997)), системы выведения MdtABC (Nagakubo S., et al., J. Bacteriol., 184(15):4161-4167 (2002)) и системы экструзии макролида MacAB (Kobayashi N., et al., J. Bacteriol., 183(19):5639-5644 (2001)).
Штаммы с мутациями в гене tolC становятся толерантными к колицину Е1, у них нарушается чувствительность к бактериофагам, исчезает белок OmpF и возникает гиперчувствительность к детергентам, краскам и определенным антибиотикам.
Однако в настоящее время отсутствуют сообщения об инактивации гена tolC для целей получения L-аминокислот.
Описание изобретения
Целями настоящего изобретения являются повышение продуктивности штаммов-продуцентов L-аминокислот и предоставление способа получения L-аминокислоты с использованием указанных штаммов.
Данные цели были достигнуты путем обнаружения того факта, что ослабление экспрессии гена tolC может повысить продукцию L-аминокислот, таких как L-треонин, L-лизин, L-цистеин, L-метионин, L-лейцин, L-изолейцин, L-валин, L-гистидин, глицин, L-серин, L-аланин, L-аспарагин, L-аспарагиновая кислота, L-глутамин, L-глутаминовая кислота, L-пролин, L-аргинин, L-фенилаланин, L-тирозин и L-триптофан.
Настоящее изобретение предоставляет бактерию семейства Enterobacteriaceae, обладающую способностью к повышенной продукции аминокислот, таких как L-треонин, L-лизин, L-цистеин, L-метионин, L-лейцин, L-изолейцин, L-валин, L-гистидин, глицин, L-серин, L-аланин, L-аспарагин, L-аспарагиновая кислота, L-глутамин, L-глутаминовая кислота, L-пролин, L-аргинин, L-фенилаланин, L-тирозин и L-триптофан.
Целью настоящего изобретения является предоставление бактерии-продуцента L-аминокислоты семейства Enterobacteriaceae, при этом указанная бактерия была модифицирована таким образом, что экспрессия гена tolC в этой бактерии ослаблена.
Также целью настоящего изобретения является предоставление описанной выше бактерии, при этом экспрессия гена tolC ослаблена путем инактивации гена tolC.
Также целью настоящего изобретения является предоставление описанной выше бактерии, при этом указанная бактерия принадлежит к роду Escherichia.
Также целью настоящего изобретения является предоставление описанной выше бактерии, при этом указанная бактерия принадлежит к роду Pantoea.
Также целью настоящего изобретения является предоставление описанной выше бактерии, при этом указанная L-аминокислота выбрана из группы, состоящей из ароматической L-аминокислоты и неароматической L-аминокислоты.
Также целью настоящего изобретения является предоставление описанной выше бактерии, при этом указанная ароматическая L-аминокислота выбрана из группы, состоящей из L-фенилаланина, L-тирозина и L-триптофана.
Также целью настоящего изобретения является предоставление описанной выше бактерии, при этом указанная неароматическая L-аминокислота выбрана из группы, состоящей из L-треонина, L-лизина, L-цистеина, L-метионина, L-лейцина, L-изолейцина, L-валина, L-гистидина, глицина, L-серина, L-аланина, L-аспарагина, L-аспарагиновой кислоты, L-глутамина, L-глутаминовой кислоты, L-пролина и L-аргинина.
Также целью настоящего изобретения является предоставление способа получения L-аминокислоты, который включает в себя:
- выращивание описанной выше бактерии в питательной среде с целью продукции и выделения L-аминокислоты в культуральную жидкость, и
- выделение указанной L-аминокислоты из культуральной жидкости.
Также целью настоящего изобретения является предоставление описанного выше способа, при этом указанная L-аминокислота выбрана из группы, состоящей из ароматических L-аминокислот и неароматических L-аминокислот.
Также целью настоящего изобретения является предоставление описанного выше способа, при этом указанная ароматическая L-аминокислота выбрана из группы, состоящей из L-фенилаланина, L-тирозина и L-триптофана.
Также целью настоящего изобретения является предоставление описанного выше способа, при этом указанная неароматическая L-аминокислота выбрана из группы, состоящей из L-треонина, L-лизина, L-цистеина, L-метионина, L-лейцина, L-изолейцина, L-валина, L-гистидина, глицина, L-серина, L-аланина, L-аспарагина, L-аспарагиновой кислоты, L-глутамина, L-глутаминовой кислоты, L-пролина и L-аргинина.
Более детально настоящее изобретение описано ниже.
Наилучший способ осуществления настоящего изобретения
1. Бактерия согласно настоящему изобретению
Бактерия согласно настоящему изобретению - это бактерия, принадлежащая к семейству Enterobacteriaceae, обладающая способностью к продукции L-аминокислоты, при этом бактерия модифицирована таким образом, что экспрессия гена E.coli у этой бактерии ослаблена.
Согласно настоящему изобретению термин «бактерия, обладающая способностью к продукции L-аминокислоты» означает бактерию, обладающую способностью к продукции и выделению L-аминокислоты в питательную среду, когда бактерия согласно настоящему изобретению выращивается в указанной питательной среде.
Термин «бактерия, обладающая способностью к продукции L-аминокислоты» в качестве применяемого здесь термина также означает бактерию, способную продуцировать и вызывать накопление любой L-аминокислоты в питательной среде в больших количествах, по сравнению с диким типом или родительским штаммом E.coli, таким как штамм E.coli К-12, и, предпочтительно означает, что указанный микроорганизм способен накапливать в среде целевую L-аминокислоту в количестве не менее чем 0.5 г/л, более предпочтительно, не менее чем 1.0 г/л. Термин «L-аминокислота» включает в себя L-аланин, L-аргинин, L-аспарагин, L-аспарагиновую кислоту, L-цистеин, L-глутаминовую кислоту, L-глутамин, L-глицин, L-гистидин, L-изолейцин, L-лейцин, L-лизин, L-метионин, L-фенилаланин, L-пролин, L-серин, L-треонин, L-триптофан, L-тирозин и L-валин.
Термин «ароматическая L-аминокислота» включает в себя L-фенилаланин, L-тирозин и L-триптофан. Термин «неароматическая L-аминокислота» включает в себя L-треонин, L-лизин, L-цистеин, L-метионин, L-лейцин, L-изолейцин, L-валин, L-гистидин, L-глицин, L-серин, L-аланин, L-аспарагин, L-аспарагиновую кислоту, L-глутамин, L-глутаминовую кислоту, L-пролин и L-аргинин. Предпочтительными, в частности, являются L-треонин, L-лизин, L-цистеин, L-лейцин, L-гистидин, L-глутаминовая кислота, L-фенилаланин, L-триптофан, L-пролин и L-аргинин.
Семейство Enterobacteriaceae включает бактерии, принадлежащие к роду Escherichia, Enterobacter, Erwinia, Klebsiella, Pantoea, Photorhabdus, Providencia, Salmonella, Serratia, Shigella, Morganella, Yersinia и т.д. Более конкретно, могут быть использованы бактерии, классифицируемые как принадлежащие к семейству Enterobacteriaceae в соответствии с таксономией, используемой в базе данных NCBI (National Center for Biotechnology Information) (http://www.ncbi.nlm.nih.gov/htbinpost/Taxonomy/wgetorg?mode=Tree&id=1236&lvl=3&keep=l&srchmode=l&unlock). Бактерия, принадлежащая к роду Escherichia или Pantoea, предпочтительна.
Термин «бактерия, принадлежащая к роду Escherichia» означает, что бактерия относится к роду Escherichia в соответствии с классификацией, известной специалисту в области микробиологии. В качестве примера микроорганизма, принадлежащего к роду Escherichia, использованного в настоящем изобретении, но не ограничивается только ею, может быть упомянута бактерия Escherichia coli (E.coli).
Круг бактерий, принадлежащих к роду Escherichia, которые могут быть использованы в настоящем изобретении, не ограничен каким-либо образом, однако, например, бактерии, описанные в книге Neidhardt, F.C. et al. (Escherichia coli and Salmonella typhimurium, American Society for Microbiology, Washington D.C., 1208, Таблица 1), могут быть включены в число бактерий согласно настоящему изобретению.
Термин «бактерия, принадлежащая к роду Pantoea» означает, что бактерия относится к роду Pantoea в соответствии с классификацией, известной специалисту в области микробиологии. Недавно несколько видов Enterobacter agglomerans были заново классифицированы как Pantoea agglomerans, Pantoea ananatis, Pantoea stewartii или подобные им, на основании анализа нуклеотидной последовательности 16S рРНК и т.д. (Int. J. Syst. BacterioL, 43, 162-173 (1993)).
Термин «бактерия, модифицированная таким образом, что в указанной бактерии экспрессия гена tolC ослаблена», означает, что бактерия модифицирована таким образом, что модифицированная бактерия содержит меньшее количество белка TolC по сравнению с немодифицированной бактерией, или что модифицированная бактерия становится неспособной синтезировать белок TolC.
Термин "инактивация гена tolC" означают, что модифицированный ген кодирует полностью нефункциональный белок. Возможно также, что модифицированный участок ДНК неспособен нормально экспрессировать ген в результате делеции части гена, сдвига рамки считывания гена, введения missense/nonsense мутации(й) или модификации прилегающей к гену области, в результате включения последовательностей, контролирующих экспрессию гена, таких как промоторы, энхансеры, аттенуаторы, сайты связывания рибосомы и т.д.
Уровень экспрессии гена можно оценить путем измерения количества мРНК, транскрибируемой с гена, с использованием ряда известных методов, включая блотинг по Нозерну, количественную ОТ-ПЦР и подобные им. Количество белка, кодируемого геном, можно измерить известными методами, включая SDS-PAGE с последующим иммуноблотингом (Вестерн блотингом) и подобными им.
Ген tolC (синонимы - ЕСК3026, weeA, b3035, colE1-i, mtcB, mukA, refI, toc) кодирует белок TolC (синонимы: канал внешней мембраны TolC, B3035, WeeA, Toc, RefI, MukA, MtcB). Ген tolC (нуклеотиды с номерами с 3,176,137 по 3,177,618 в последовательности с инвентарным номером NC_000913.2; gi:49175990; в базе данных GenBank) располагается между генами ycal и lpxK на хромосоме штамма E.coli К-12. Нуклеотидная последовательность гена tolC и аминокислотная последовательность кодируемого им белка TolC, кодируемая геном tolC, показана на SEQ ID NO: 1 и SEQ ID NO: 2, соответственно.
Поскольку в последовательностях ДНК разных родов или штаммов семейства Enterobacteriaceae могут существовать некоторые различия, нуклеотидная последовательность гена tolC, подлежащего инактивации, не ограничивается последовательностью гена, приведенной в SEQ ID No: 1, но также может включать последовательности генов, гомологичных последовательности, приведенной в SEQ ID No: 1. Поэтому, вариант белка, кодируемого геном tolC, может быть представлен белком с гомологией не менее 80%, предпочтительней не менее 90%, и, наиболее предпочтительно, не менее 95%, по отношению к полной аминокислотной последовательности, кодируемой геном tolC и показанной на SEQ ID NO.2, до тех пор, пока активность белка TolC сохраняется на том же уровне, как до инактивации.
Кроме того, ген tolC может быть представлен вариантом, который гибридизуется с нуклеотидной последовательностью, приведенной в Перечне последовательностей под номером 1 (SEQ ID NO: 1), или с зондом, который может быть синтезирован на основе указанной нуклеотидной последовательности, в жестких условиях, при условии, что указанный вариант кодирует функциональный белок TolC таким, каким он был до инактивации. "Жесткие условия" включают такие условия, при которых образуются специфические гибриды, например гибриды, имеющие гомологию не менее чем 60%, более предпочтительно не менее чем 70%, наиболее предпочтительно не менее чем 80%, еще более предпочтительно не менее чем 90%, и в наибольшей степени предпочтительно не менее чем 95%, а неспецифические гибриды, например, гибриды, имеющие меньшую перечисленной выше гомологию - не образуются. Например, демонстрацией жестких условий может служить однократная или многократная отмывка, предпочтительно двух- или трехкратная отмывка при концентрации солей 1×SSC, 0.1% SDS, предпочтительно 0.1×SSC, 0.1% SDS, при температуре 60°С. Продолжительность отмывки зависит от типа мембраны, используемой для блотинга, и, как правило, указывается производителями наборов в инструкции. Например, рекомендуемая продолжительность отмывки для мембран Hybond™ N+nylon (Amersham) в жестких условиях составляет 15 минут. Более предпочтительно повторить отмывку 2-3 раза. Длина зонда может быть выбрана соответствующим образом, в зависимости от условий гибридизации, и обычно варьирует в диапазоне от 100 п.о. до 1 тыс.п.о.
Гомология между двумя аминокислотными последовательностями может быть установлена с помощью хорошо известных методов, например, компьютерной программы BLAST 2.0.
Экспрессия гена tolC может быть ослаблена путем введения мутации в ген на хромосоме таким образом, что количество внутриклеточного белка TolC, кодируемого этим геном, снизится по сравнению с немодифицированным штаммом. Такая мутация может быть достигнута введением гена лекарственной устойчивости или делецией части гена или полноразмерного гена (Qiu, Z. and Goodman, M.F., J. Biol. Chem., 272, 8611-8617 (1997); Kwon, D.H. et al J. Antimicrob. Chemother., 46, 793-796 (2000)). Экспрессия гена tolC может быть также ослаблена путем модификации экспрессии регуляторной последовательности, такой как промотор, последовательность Шайна-Дальгарно (SD) и т.д. (WO 95/34672, Carrier, T.A. and Keasling, J.D., Biotechnol Prog 15, 58-64 (1999)).
Например, следующие методы могут применяться для введения мутации путем генной рекомбинации. Конструируется мутантный ген и бактерия, которая должна быть модифицирована, трансформируется фрагментом ДНК, содержащим мутантный ген. Затем нативный ген на хромосоме замещается мутантным геном с использованием гомологичной рекомбинации, а полученный штамм отбирается путем селекции. Такое замещение гена с использованием гомологичной рекомбинации может быть проведено методами с использованием линейной ДНК, как, например, метод известный как "Red-зависимая интеграция" или "интеграция посредством Red-системы" (Datsenko, K.A., Wanner, B.L., Proc. Natl. Acad. Sci. USA, 97, 12, 6640-6645 (2000)) и метод с использованием плазмиды, репликация которой чувствительна к температуре (патент США 6,303,383 или заявка Японии 05-007491 А). Далее, введение сайт-специфической мутации путем замещения гена с использованием гомологичной рекомбинации, как сказано выше, может также быть осуществлено с использованием плазмиды с пониженной способностью к репликации в клетке хозяина.
Экспрессия гена может быть также ослаблена путем встраивания транспозона или IS-фактора в кодирующую область гена (патент США 5175107) или с помощью традиционных методов, таких как облучение УФ-лучами или обработка нитрозогуанидином (N-метил-N'-нитро-N-нитрозогуанидин), сайт-направленный мутагенез, разрушение гена с помощью гомологичной рекомбинации и/или за счет мутации сдвига рамки (Yu, D. et al., Proc. Natl. Acad. Sci. USA, 2000, 97:12: 5978-83 and Datsenko, K.A. and Wanner, B.L., Proc. Natl. Acad. Sci. USA, 2000, 97:12: 6640-45), также названной «Red-зависимая интеграция».
Продукция белка TolC в соединении с MFP-белками (Membrane Fusion Proteins - Мембранные Белки Слияния) обеспечивает облегченный транспорт веществ через внешнюю мембрану Escherichia coli. Штаммы с делениями в гене tolC становятся гиперчувствительными к гидрофобным агентам в результате инактивации системы выведения arcАВ, обеспечивающей резистентность к различным лекарственным препаратам (Fralick J., J. Bacteriol., 178 (19):5803-5805 (1996)). Поэтому снижение или отсутствие активности белка ТоlC в бактерии согласно настоящему изобретению может быть установлено путем сравнения с родительским немодифицированным штаммом бактерии.
Наличие или отсутствие гена tolC на хромосоме бактерии можно обнаружить хорошо известными методами, включая ПЦР, блотинг по Саузерну и подобными им. Кроме того, уровень экспрессии гена можно оценить путем измерения количества мРНК, транскрибируемой с гена, с использованием ряда известных методов, включая блотинг по Нозерну, количественную ОТ-ПЦР и подобные им. Количество белка, кодируемого геном, можно измерить известными методами, включая SDS-PAGE с последующим иммуноблотингом (Вестерн блотингом) и подобными им. Например, распознование продукта гена tolC проводили путем приготовления авторадиографических снимков гелей после электрофореза меченых образцов из мини-клеточного штамма бактерий (Моrona R., et al., J. Bacteriol., 153(2):693-699 (1983)).
Методами приготовления плазмидной ДНК, разрезания и лигирования ДНК, трансформации, выбора олигонуклеотидов в качестве праймеров и подобные им могут являться обычные методы, хорошо известные специалисту в данной области. Эти методы описаны, например, в книге Sambrook, J., Fritsch, E.F., and Maniatis, T., "Molecular Cloning A Laboratory Manual, Second Edition", Cold Spring Harbor Laboratory Press (1989).
Бактерии - продуценты L-аминокислоты
В качестве бактерии, согласно настоящему изобретению, которая модифицирована таким образом, что в ней ослаблена экспрессия гена tolC, может быть использована бактерия, способная продуцировать как ароматические, так и неароматические L-аминокислоты.
Бактерия, согласно настоящему изобретению, может быть получена путем инактивации гена tolC в бактерии, уже обладающей способностью продукцировать L-аминокислоты. С другой стороны, бактерия, согласно настоящему изобретению, может быть получена путем придания бактерии, в которой ген tolC уже инактивирован, способности продуцировать L-аминокислоты.
Бактерия-продуцент L-треонина
Примеры родительского штамма для получения бактерии-продуцента L-треонина, согласно настоящему изобретению, включают, но не ограничиваются штаммами, принадлежащими к роду Escherichia, такими как штамм E.coli TDH-6/pVIC40 (ВКПМ В-3996) (патенты США 5175107 и 5705371), штамм Е.coli 472T23/pYN7 (ATCC 98081) (патент США 5631157), штамм Е.coli NRRL-21593 (патент США 5939307), штамм Е.coli FERM ВР-3756 (патент США 5474918), штаммы E.coli FERM ВР-3519 и FERM ВР-3520 (патент США 5376538), штамм E.coli MG442 (Гусятинер и др., Генетика, 14, 947-956 (1978)), штаммы E.coli VL643 и VL2055 (Европейская патентная заявка ЕР 1149911 А) и подобными им.
Штамм TDH-6 является дефицитным по гену thrC, способен ассимилировать сахарозу и содержит ген ilvA с мутацией типа "leaky". Указанный штамм содержит мутацию в гене rhtA, которая обуславливает устойчивость к высоким концентрациям треонина и гомосерина. Штамм В-3996 содержит плазмиду pVIC40, которая была получена путем введения в вектор, производный от вектора RSF1010, оперона thrA*BC, включающего мутантный ген thrA, кодирующий аспартокиназа-гомосериндепидрогеназу I, у которой существенно снижена чувствительность к ингибированию треонином по типу обратной связи. Штамм В-3996 был депонирован 19 ноября 1987 года во Всесоюзном научном центре антибиотиков (РФ, 117105 Москва, Нагатинская ул., 3-А) с инвентарным номером РИА 1867. Указанный штамм также был депонирован во Всероссийской коллекции промышленных микроорганизмов (ВКПМ) (РФ, 117545 Москва, 1-й Дорожный проезд, 1) с инвентарным номером В-3996.
В качестве родительского штамма для получения бактерии-продуцента L-треонина, согласно настоящему изобретению, может также использоваться E.coli VKPM В-5318 (европейский патент EP 0593792 В). Штамм В-5318 является прототрофным по изолейцину и содержит плазмиду pVIC40, в которой регуляторная область треонинового оперона замещена чувствительным к температуре С1 репрессором фага λ и PR промотором. Штамм VKPM В-5318 был депонирован во Всероссийской коллекции промышленных микроорганизмов (ВКПМ) 3 мая 1990 г. с инвентарным номером VKPM В-5318.
Предпочтительно, чтобы бактерия согласно настоящему изобретению была далее модифицирована таким образом, чтобы иметь повышенную экспрессию одного или нескольких следующих генов:
- мутантного гена thrA, кодирующего аспартокиназа-гомосериндегидрогеназу I, устойчивую к ингибированию треонином по типу обратной связи;
- гена thrB, кодирующего гомосеринкиназу;
- гена thrC, кодирующего треонинсинтазу;
- гена rhtA, предположительно кодирующего трансмембранный белок;
- гена asd, кодирующего аспартат-β-семиальдегиддегидрогеназу, и
- гена aspC, кодирующего аспартатаминотрансферазу (аспартаттрансаминазу).
Нуклеотидная последовательность гена thrA, кодирующего аспартокиназа-гомосериндегидрогеназу I из Escherichia coli, известна (номера нуклеотидов с 337 по 2799 в последовательности с инвентарным номером NC_000913.2 в базе данных GenBank, gi: 49175990). Ген thrA расположен на хромосоме штамма E.coli К-12 между генами thrL и thrB. Нуклеотидная последовательность гена thrB, кодирующего гомосеринкиназу из Escherichia coli, известна (номера нуклеотидов с 2801 по 3733 в последовательности с инвентарным номером NC_000913.2 в базе данных GenBank, gi: 49175990). Ген thrB расположен на хромосоме штамма E.coli К-12 между генами thrA и thrC. Нуклеотидная последовательность гена thrC, кодирующего треонинсинтазу из Escherichia coli, известна (номера нуклеотидов с 3734 по 5020 в последовательности с инвентарным номером NC_000913.2 в базе данных GenBank, gi: 49175990). Ген thrC расположен на хромосоме штамма E.coli К-12 между геном thrB и открытой рамкой считывания yaaX. Все три указанных гена функционируют как один треониновый оперон. Для усиления экспрессии треонинового оперона желательно удалить из оперона область аттенюатора, который влияет на транскрипцию (заявка РСТ WO 2005/049808, заявка РСТ WO 2003/097839).
Мутантный ген thrA, кодирующий аспартокиназу-гомосериндегидрогеназу I, устойчивую к ингибированию треонином по типу обратной связи, так же, как и гены thrB и thrC могут быть получены в виде единого оперона из хорошо известной плазмиды pVIC40, которая представлена в штамме-продуценте E.coli ВКПМ В-3996. Плазмида pVIC40 подробно описана в патенте США 5705371.
Ген rhtA расположен на 18 минуте хромосомы E.coli около оперона glnHPQ, который кодирует компоненты транспортной системы глутамина, ген rhtA идентичен ORF1 (ген ybiF, номера нуклеотидов с 764 по 1651 в последовательности с инвентарным номером ААА218541 в базе данных GenBank, gi:440181), расположен между генами рехВ и оmpХ. Участок ДНК, экспрессирующийся с образованием белка, кодируемого рамкой считывания ORF1, был назван геном rhtA (rht: resistance to homoserine and threonine). Также было показано, что мутация rhtA23 представляет собой замену А-на-G в положении -1 по отношению к старт кодону ATG (тезисы 17th International Congress of Biochemistry and Molecular Biology, тезисы 1997 Annual Meeting of the American Society for Biochemistry and Molecular Biology, San Francisco, California August 24-29, 1997, abstract No.457, европейская заявка EP 1013765 A).
Нуклеотидная последовательность гена asd из E.coli известна (номера нуклеотидов с 3572511 по 3571408 в последовательности с инвентарным номером NC_000913.1 в базе данных GenBank, gi: 161313 07) и может быть получена с помощью ПЦР (полимеразная цепная реакция; ссылка на White, T.J. et al., Trends Genet., 5, 185 (1989)) с использованием праймеров, синтезированных на основе нуклеотидной последовательности указанного гена. Гены asd из других микроорганизмов могут быть получены сходным образом.
Также нуклеотидная последовательность гена aspC из E.coli известна (номера нуклеотидов с 983742 по 984932 в последовательности с инвентарным номером NC_000913.1 в базе данных GenBank, gi:16128895) и может быть получена с помощью ПЦР. Гены aspC из других микроорганизмов могут быть получены сходным образом.
Бактерия-продуцент L-лизина
Примеры бактерий-продуцентов L-лизина, принадлежащих к роду Escherichia, включают мутанты, обладающие устойчивостью к аналогу L-лизина. Аналог L-лизина ингибирует рост бактерий, принадлежащих к роду Escherichia, но это ингибирование полностью или частично снимается, когда в среде также присутствует L-лизин. Примеры аналога L-лизина включают, но не ограничиваются оксализином, лизингидроксаматом, S-(2-аминоэтил)-L-цистеином (АЕС), γ-метиллизном, α-хлорокапролактамом и так далее. Мутанты, обладающие устойчивостью к указанным аналогам лизина, могут быть получены путем обработки бактерий, принадлежащих к роду Escherichia, традиционными мутагенами. Конкретные примеры бактериальных штаммов, используемых для получения L-лизина, включают штамм Escherichia coli AJ 11442 (FERM BP-1543, NRRL B-12185; смотри патент США 4346170) и штамм Escherichia coli VL611. В этих микроорганизмах аспартокиназа устойчива к ингибированию L-лизином по принципу обратной связи.
Штамм WC 196 может быть использован в качестве бактерии-продуцента L-лизина Escherichia coli. Данный бактериальный штамм был получен путем селекции фенотипа устойчивости к АЕС у штамма W3110, производного от штамма Escherichia coli К-12. Полученный штамм был назван Escherichia coli AJ 13069 и был депонирован в Национальном Институте Биологических Наук и Человеческих Технологий, Агенство Промышленной Науки и Технологии, Министерство Международной Торговли и Промышленности (National Institute of Bioscience and Human-Technology, Agency of Industrial Science and Technology, Ministry of International Trade and Industry), в настоящее время называющийся Национальный Институт Прогрессивной Промышленной Науки и Технологии, Международный Депозитарий Организмов для Целей Патентования, Централ 6, 1-1, Хигаши 1-Чоме, Тсукуба-ши, Ибараки-кен, 305-8566, Япония (National Institute of Advanced Industrial Science and Technology, International Patent Organism Depositary, Central 6, 1-1, Higashi 1-Chome, Tsukuba-shi, Ibaraki-ken, 305-8566, Japan), 6 декабря 1994 года и получил инвентарный номер FERM Р-14690. Затем было произведено международное депонирование этого штамма согласно условиям Будапештского Договора 29 сентября 1995 года, и штамм получил инвентарный номер FERM BP-5252 (патент США 5827698).
Примеры родительских штаммов для получения бактерий, продуцирующих L-лизин согласно настоящему изобретению, также включают штаммы, в которых усилена экспрессия одного или нескольких генов, кодирующих ферменты биосинтеза L-лизина. Примеры ферментов, вовлеченных в биосинтез L-лизина, включают, но не ограничиваются ими, дигидродипиколинатсинтазу (dapA), аспартокиназу (lysC), дигидродипиколинатредуктазу (dapB), диаминопимелатдекарбоксилазу (lysA), диаминопимелатдегидрогеназу (ddh) (патент США. 6040160), фосфоенолпируваткарбоксилазу(pрс), аспартатсемиальдегиддегидрогеназу (asd), никотинамидадениндинуклеотидтрансгидрогеназу (pntAB) и аспартазу (aspA) (европейская заявка EP 1253195 A). Кроме того, родительские штаммы могут иметь повышенный уровень экспрессии гена, вовлеченного в процесс дыхания (суо) (европейская заявка EP 1170376 А), гена, кодирующего никотинамиднуклеотидтрансгидрогеназу (pntAB) (патент США 5830716), гена ybjE (заявка РСТ WO 2005/073390), или комбинации этих генов.
Примеры родительских штаммов для получения бактерий, продуцирующих L-лизин согласно настоящему изобретению, также включают штаммы, в которых снижена или отсутствует активность ферментов, которые катализируют реакции образования отличных от L-лизина соединений, ответвляющихся от основного пути биосинтеза L-лизина. Примеры ферментов, которые катализируют реакции образования отличных от L-лизина соединений, ответвляющихся от основного пути биосинтеза L-лизина, включают гомосериндегидрогеназу, лизиндекарбоксилазу (патент США 5827698) и малатдегидрогеназу (заявка РСТ WO 2005/010175).
Бактерия-продуцент L-цистеина
Примеры родительских штаммов, используемых для получения бактерии-продуцента L-цистеина согласно настоящему изобретению, включают в себя, но не ограничиваются штаммами, принадлежащими к роду Escherichia, такими как штамм E.coli JM15, трансформированный различными аллелями гена cysE, кодирующими устойчивые к ингибированию по типу обратной связи серинацетилтрансферазы (патент США 6218168; патентная заявка РФ 2003121601); штамм E.coli W3110, содержащий сверхэкспрессированные гены, кодирующие белок, способный к секреции соединений, токсичных для клетки (патент США 5972663); штаммы E.coli, содержащие цистеиндесульфогидразу со сниженной активностью (патент Японии JP 11155571 A2); штамм E.coli W3110 с повышенной активностью позитивного транскрипционного регулятора цистеинового регулона, кодируемого геном cysB (международная заявка РСТ WO 0127307 A1) и подобные им.
Бактерия-продуцент L-лейцина
Примеры родительских штаммов, используемых для получения бактерии-продуцента L-лейцина согласно настоящему изобретению, включают в себя, но не ограничиваются штаммами, принадлежащими к роду Escherichia, такими как штаммы E.coli, устойчивые к лейцину (например, штамм E.coli 57 (VKPM В-7386, патент США 6124121)) или к аналогам лейцина, включающих, например, β-2-тиенилаланин, 3-гидроксилейцин, 4-азалейцин и 5,5,5-трифлуоролейцин (выложенные патентные заявки Японии 62-34397 и 8-70879), штаммы E.coli, полученные с помощью генно-инженерных методов, описанных в заявке РСТ 96/06926; E.coli штамм Н-9068 (JP8-70879 A2) и подобные им.
Бактерия согласно настоящему изобретению может быть улучшена путем усиления экспрессии одного или нескольких генов, вовлеченных в биосинтез L-лейцина. Примеры таких генов включают в себя гены оперона leuABCD, и предпочтительно представлены мутантным геном leuA, кодирующим изопропилмалатсинтазу со снятым ингибированием L-лейцином по типу обратной связи (патент США 6403342). Кроме того, бактерия согласно настоящему изобретению может быть улучшена путем усиления экспрессии одного или нескольких генов, кодирующих белки, которые экспортируют L-аминокислоту из бактериальной клетки. Примеры таких генов включают в себя гены b2682 и b2683 (гены ygaZH) (европейская заявка EP 1239041 A2).
Бактерия-продуцент L-гистидина
Примеры родительских штаммов, используемых для получения бактерии-продуцента L-гистидина согласно настоящему изобретению, включают в себя, но не ограничиваются бактериями-продуцентами L-гистидина, принадлежащими к роду Escherichia, такими как штамм E.coli 24 (ВКПМ В-5945, патент РФ 2003677); штамм E.coli 80 (ВКПМ В-7270, патент РФ 2119536); штаммы E.coli NRRL B-12116-B12121 (патент США 4388405); штаммы E.coli H-9342 (FERM ВР-6675) и Н-9343 (FERM ВР-6676) (патент США 6344347); штамм E.coli H-9341 (FERM BP-6674) (Европейский патент 1085087); штамм E.coli AI80/pFM201 (патент США 6258554) и подобными им.
Примеры родительских штаммов для получения бактерий, продуцирующих L-гистидин согласно настоящему изобретению, также включают штаммы, в которых усилена экспрессия одного или нескольких генов, кодирующих ферменты биосинтеза L-гистидина. Примеры ферментов, вовлеченных в биосинтез L-гистидина, включают АТФ-фосфорибозилтрансферазу (hisG), фосфорибозил-АМФ-циклогидролазу (hisI), фосфорибозил-АТФ-фосфогидролазу (hisIE), фосфорибозилформимино-5-аминоимидазолкарбоксамидриботидизомеразу (hisA), амидотрансферазу (hisH), гистидинолфосфатаминотрансферазу (hisC), гистидинолфосфатазу (hisB), гистидинолдегидрогеназу (hisD) и т.д.
Известно, что гены, кодирующие ферменты биосинтеза L-гистидина (hisG, hisBHAFI), ингибируются L-гистидином, поэтому способность к продукции L-гистидина также может быть значительно усилена введением мутации, придающей устойчивость к ингибированию по типу обратной связи, в ген АТФ-фосфорибозидтрансферазы (hisG) (патенты РФ. 2003677 и 2119536).
Специфические примеры штаммов, обладающих способностью к продукции L-гистидина, включают E.coli FERM-P 5038 и 5048, в которые был введен вектор, содержащий ДНК, кодирующую фермент биосинтеза L-гистидина (заявка Японии 56-005099 А), штаммы E.coli, в которые введен ген rht, для экспорта аминокислоты (европейская заявка EP 1016710 А), штамм E.coli 80, которому придана устойчивость к сульфагуанидину, DL-1,2,4-триазол-3-аланину и стрептомицину (ВКПМ В-7270, патент РФ 2119536) и т.д.
Бактерия-продуцент L-глутаминовой кислоты
Примеры родительских штаммов, используемых для получения бактерии-продуцента L-глутаминовой кислоты согласно настоящему изобретению, включают в себя, но не ограничиваются штаммами, принадлежащими к роду Escherichia, такими как штамм E.coli VL334 thrС+ Европейский патент ЕР 1172433). Штамм E.coli VL334 (ВКПМ В-1641) является ауксотрофом по L-изолейцину и L-треонину с мутациями в генах thrC и ilvA (патент США 4278765). В этот штамм была перенесена природная аллель гена thrC методом общей трансдукции с использованием бактериофага Р1, выращенного на клетках природного штамма E.coli К12 (ВКПМ В-7). В результате был получен штамм, ауксотроф по L-изолейцину, VL334thrC+(BKПМ В-8961). Этот штамм обладает способностью к продукции L-глутаминовой кислоты.
Примеры родительских штаммов, используемых для получения бактерии-продуцента L-глутаминовой кислоты согласно настоящему изобретению, включают в себя, но не ограничиваются ими, штаммы, в которых усилена экспрессия одного или нескольких генов, кодирующих ферменты биосинтеза L-глутаминовой кислоты. Примеры ферментов, вовлеченных в биосинтез L-глутаминовой кислоты, включают глутаматдегидрогеназу, глутаминсинтетазу, глутаматсинтетазу, изоцитратдегидрогеназу, аконитатгидратазу, цитратсинтазу, фосфоенолпируваткарбоксилазу, пируваткарбоксилазу, пируватдегидрогеназу, пируваткиназу, фосфоенолпируватсинтазу, енолазу, фосфоглицеромутазу, фосфоглицераткиназу, глицеральдегид-3-фосфатдегидрогеназу, триозофосфатизомеразу, фруктозобифосфатальдолазу, фосфофруктониназу и глюкозофосфатизомеразу.
Примеры штаммов, модифицированных таким образом, что усилена экспрессия гена цитратсинтетазы, гена фосфоенолпируваткарбоксилазы и/или гена глутаматдегидрогеназы, включают описанные в европейских заявках EP 1078989 A, EP 955368 A и EP 952221 A.
Примеры родительских штаммов для получения продуцирующих L-глутаминовую кислоту бактерий, согласно настоящему исследованию, также включают штаммы, в которых снижена или отсутствует активность ферментов, которые катализируют синтез отличных от L-глутаминовой кислоты соединений, ответвляющихся от основного пути биосинтеза L-глутаминовой кислоты. Примеры таких ферментов включают изоцитратлиазу, α-кетоглутаратдегидрогеназу, фосфотрансацетилазу, ацетаткиназу, синтазу ацетогидроксикислот, ацетолактатсинтазу, форматацетилтрансферазу, лактатдегидрогеназу и глутаматдекарбоксилазу. Бактерии, принадлежащие к роду Escherichia, лишенные активности α-кетоглутаратдегидрогеназы или обладающие сниженной активностью α-кетоглутаратдегидрогеназы и способы их получения описаны в патентах США 5378616 и 5573945. Конкретно, примеры таких штаммов включают в себя следующие штаммы:
E.coli W311sucA::KmR
E.coli AJ 12624 (FERM ВР-3853)
E.coli AJ 12628 (PERM BP-3854)
E.coli AJ 12949 (FERM BP-4881)
E.coli W3110sucA::KmR- это штамм, полученный в результате разрушения гена α-кетоглутаратдегидрогеназы (далее называемого "ген sucA") в штамме E.coli W3110. У этого штамма активность α-кетоглутаратдегидрогеназы отсутствует полностью.
Другие примеры бактерии-продуцента L-глутаминовой кислоты включают в себя бактерии, принадлежащие к роду Escherichia и обладающие устойчивостью к антиметаболитам аспарагиновой кислоты и дефицитные по активности α-кетоглутаратдегидрогеназы, например, штамм AJ 13199 (FERM BP-5807) (патент США 5908768), или штамм FERM P-12379, дополнительно обладающий низкой активностью по расщеплению L-глутаминовой кислоты (патент США 5393671); штамм E.coli АЛЗ 138 (FERM BP-5565) (патент США 6110714) и подобные им.
Примеры бактерии-продуцента L-глутаминовой кислоты включают в себя мутантные штаммы, принадлежащие к роду Pantoea, которые лишенны активности α-кетоглутаратдегидрогеназы или имеют сниженную активность α-кетоглутаратдегидрогеназы, и могут быть получены описанным выше способом. Примерами таких штаммов являются штамм Pantoea ananatis AJ 13356 (патент США 6331419), штамм Pantoea ananatis AJ 13356, депонированный в Национальном Институте Биологических Наук и Человеческих Технологий, Агенство Промышленной Науки и Технологии, Министерство Международной Торговли и Промышленности (National Institute of Bioscience and Human-Technology, Agency of Industrial Science and Technology, Ministry of International Trade and Industry) (в настоящее время называющийся Национальный Институт Прогрессивной Промышленной Науки и Технологии, Международный Депозитарий Организмов для Целей Патентования, Централ 6, 1-1, Хигаши 1-Чоме, Тсукуба-ши, Ибараки-кен, 305-8566, Япония - National Institute of Advanced Industrial Science and Technology, International Patent Organism Depositary, Central 6,1-1, Higashi 1-Chome, Tsukuba-shi, Ibaraki-ken, 305-8566, Japan) 19 февраля, 1998 и получивший инвентарный номер FERM P-16645. Затем было произведено международное депонирование этого штамма согласно условиям Будапештского Договора от 11 января 1999 г., и штамм получил инвентарный номер FERM BP-6615. Штамм Pantoea ananatis АJ13356 не имеет α-KGDH активности в результате разрушения гена αKGDH-E1 субъединицы (sucA). Вышеупомянутый штамм при выделении был идентифицирован как Enterobacter agglomerans и депонирован как штамм Enterobacter agglomerans AJ13356. Тем не менее, позднее он был классифицирован как Pantoea ananatis на основе нуклеотидной последовательности 16S рРНК и других доказательств. Несмотря на то, что штамм AJ 13356, был депонирован в указанный выше депозитарий как Enterobacter agglomerans, для целей данного описания он будет упоминаться как Pantoea ananatis.
Бактерия-продуцент L-фенилаланина
Примеры родительских штаммов, используемых для получения бактерии-продуцента L-фенилаланина согласно настоящему изобретению, включают в себя, но не ограничиваются штаммами, принадлежащими к роду Escherichia, такими как штамм AJ12739 (tyrA::Tn10, tyrR) (ВКМП В-8197); штамм HW1089 (АТСС-55371), содержащий ген pheA34 (патент США 5354672); мутантный штамм MWEC101-b (KR8903681); штаммы NRRL B-12141, NRRL B-12145, NRRL В-12146 и NRRL В-12147 (патент США 4407952) и подобные им. Также в качестве родительских штаммов могут быть использованы бактерии, принадлежащие к роду Escherichia, - продуценты L-фенилаланина, такие как штамм E.coli K-12[W3110(tyrA)/pPHAB] (FERM BP-3566), штамм E.coli K-12[W3110(tyrA)/pPHAD] (FERM BP-12659), штамм E.coli K-12[W3110(tyrA)/pPHATerm] (FERM BP-12662) и штамм E.coli K-12[W3110(tyrA)/pBR-aroG4, рАСМАВ], названный как AJ12604 (FERM BP-3579) (Европейский патент EP 488424 B1). Кроме того, также могут быть использованы бактерии-продуценты L-фенилаланина, принадлежащие к роду Escherichia с повышенной активностью белков, кодируемых геном yedA или геном yddG (патентные заявки США 2003/0148473 A1 и 2003/0157667 A1).
Бактерия-продуцент L-триптофана
Примеры родительских штаммов, используемых для получения бактерии-продуцента L-триптофана согласно настоящему изобретению, включают в себя, но не ограничиваются бактериями-продуцентами L-триптофана, принадлежащими к роду Escherichia, такими как штаммы Е. coli JP4735/pMU3028 (DSM10122) и JP6015/pMU91 (DSM10123), лишенные активности триптофанил-тРНК синтетазы, кодируемой мутантным геном trpS (патент США 5756345); штамм E.coli SV164 (pGH5), содержащий аллель гена serA, кодирующего фермент фосфоглицератдегидрогеназу, не ингибируемый серином по типу обратной связи и аллель гена trpE, кодирующего фермент антранилатсинтазу, не ингибируемый триптофаном по типу обратной связи (патент США 6180373); штаммы E.coli AGX17 (pGX44) (NRRL В-12263) и AGX6(pGX50)aroP (NRRL B-12264), лишенные активности триптофаназы (патент США 4371614); штамм E.coli AGX17/pGX50, pACKG4-pps, в котором усилена способность к синтезу фосфоенолпирувата (заявка РСТ WO9708333, патент США 6319696), и подобные им. Бактерии-продуценты L-триптофана, принадлежащие к роду Escherichia и обладающие повышенной активностью идентифицированного белка, кодируемого геном yedA или геном yddG, могут быть также использованы в качестве родительских штаммов (патентные заявки США 2003/0148473 A1 и 2003/0157667 A1).
Примеры родительских штаммов, используемых для получения бактерии-продуцента L-триптофана согласно настоящему изобретению, также включают в себя штаммы, в которых увеличена активность одного или нескольких ферментов, выбранных из группы, состоящей из антранилатсинтазы, фосфоглицератдегидрогеназы и триптофансинтазы. И антранилатсинтаза, и фосфоглицератдегидрогеназа подвержены ингибированию L-триптофаном и L-серином по типу обратной связи, так что в эти ферменты могут быть введены мутации, снижающие чувствительность к ингибированию по типу обратной связи. Специфические примеры штаммов с такой мутацией включают E.coli SV164, антранилатсинтаза которой не чувствительна к ингибированию по типу обратной связи, и штамм-трансформант, полученный введением в E.coli SV164 плазмиды pGH5 (заявка РСТ WO 94/08031), которая содержит мутантный ген serA, кодирующий фосфоглицератдегидрогеназу, которая не чувствительна к ингибированию по типу обратной связи.
Примеры родительских штаммов, используемых для получения бактерии-продуцента L-триптофана согласно настоящему изобретению, также включают в себя штаммы, в которые введен триптофановый оперон, содержащий ген, кодирующий антранилатсинтазу, которая не чувствительна к ингибированию по типу обратной связи (заявка Японии 57-71397 А, заявка Японии 62-244382 А, патент США 4371614). Кроме того, способность к продукции L-триптофана может быть придана путем усиления экспрессии гена (из триптофанового оперона), кодирующего триптофансинтазу (trpBA). Триптофансинтаза состоит из двух субъединиц α и β, которые кодируются trpA и trpB соответственно. Кроме того, способность к продукции L-триптофана может быть увеличена усилением экспрессии оперона изоцитратлиазы-малатсинтазы (заявка РСТ WO 2005/103275).
Бактерия-продуцент L-пролина
Примеры бактерий-продуцентов L-пролина, используемых в качестве родительского штамма согласно настоящему изобретению, включают в себя, но не ограничиваются штаммами, принадлежащими к роду Escherichia, такими как штамм E.coli 702ilvA (ВКПМ В-8012), дефицитного по гену ilvA и способного к продукции L-пролина (Европейский патент EP 1172433). Бактерия согласно настоящему изобретению может быть улучшена путем усиления экспрессии одного или нескольких генов, вовлеченных в биосинтез L-пролина. Предпочтительно, примеры таких генов для бактерий-продуцентов L-пролина, включают ген proB, кодирующий глутаматкиназу с десенсибилизированной регуляцией L-пролином по типу обратной связи (патент Германии 3127361). Кроме того, бактерия согласно настоящему изобретению может быть улучшена путем усиления экспрессии одного или нескольких генов, кодирующих белки, экскретирующие L-аминокислоту из бактериальной клетки. Примерами таких генов являются гены b2682 и b2683 (ygaZH гены) (Европейская патентная заявка EP 1239041 A2).
Примеры бактерий, принадлежащих к роду Escherichia и обладающих способностью к продукции L-пролина, включают следующие штаммы E.coli: NRRL В-12403 и NRRL В-12404 (патент Великобритании GB 2075056), ВКПМ В-8012 (патентная заявка РФ 2000124295), плазмидные мутанты, описанные в патенте Германии DE 3127361, плазмидные мутанты, описанные у Bloom F.R. et al. (The 15th Miami winter symposium, 1983, p.34), и подобные им.
Бактерия-продуцент L-аргинина
Примеры родительских штаммов, используемых для получения бактерии-продуцента L-аргинина согласно настоящему изобретению, включают в себя, но не ограничиваются штаммами, принадлежащими к роду Escherichia, такими как штамм E.coli 237 (ВКПМ В-7925) (патентная заявка США 2002/058315 A1) и его производные, содержащие мутантную N-ацетилглутаматсинтазу (патентная заявка РФ 2001112869), штамм E.coli 382 (VKPM В-7926) (Европейская патентная заявка EP 1170358А1), штамм-продуцент аргинина, в который введен ген argA, кодирующий N-ацетилглутаматсинтетазу (Европейская патентная заявка EP 1170361 A1), и подобные им.
Примеры родительских штаммов, используемых для получения бактерии-продуцента L-аргинина согласно настоящему изобретению, также включают в себя штаммы, в которых усилена экспрессия одного или нескольких генов, кодирующих ферменты биосинтеза L- аргинина. Примеры таких генов включают гены, кодирующие N-ацетилглутамилфосфатредуктазу (argC), орнитинацетилтрансферазу (argJ), N-ацетилглутаматкиназу (argB), ацетилорнитинтрансаминазу (argD), орнитинкарбамоилтрансферазу (argF), синтетазу аргининсукциниловой кислоты (argG), лиазу аргининсукциниловой кислоты (argH) и карбамоилфосфатсинтетазу (carAB).
Бактерия-продуцент L-валина
Примеры родительских штаммов, используемых для получения бактерии-продуцента L-валина, согласно настоящему изобретению, включают в себя, но не ограничиваются ими, штаммы, модифицированные с целью сверхэкспрессии оперона ilvGMEDA (патент США 5998178). Желательно удалить область оперона ilvGMEDA, которая необходима для ослабления экспрессии, с тем чтобы экспрессия оперона не ослаблялась образующимся L-валином. Далее, желательно разрушить в опероне ген ilvA с тем, чтобы снизить активность треониндеаминазы.
Примеры родительских штаммов, используемых для получения бактерии-продуцента L-валина согласно настоящему изобретению, также включают в себя мутантные штаммы, имеющие мутацию аминоацил-тРНК-синтетазы (патент США 5658766). Например, может использоваться штамм E.coli VL1970, который имеет мутацию в гене ileS, кодирующем изолейцин-тРНК-синтетазу. Штамм E.coli VL1970 депонирован в Российской Национальной Коллекции Промышленных Микроорганизмов (ВКПМ) (Россия, 113545 Москва, 1-й Дорожный проезд) 24 июня 1988 г. с инвентарным номером ВКПМ В-4411.
Далее, в качестве родительских штаммов также могут использоваться мутантные штаммы, для роста которых требуется липоевая кислота, и/или с недостаточным количеством Н+-АТФазы (заявка РСТ WO 96/06926).
Бактерия-продуцент L-изолейцина
Примеры родительских штаммов, используемых для получения бактерии-продуцента L-изолейцина согласно настоящему изобретению, включают в себя, но не ограничиваются ими, мутантные штаммы с устойчивостью к 6-диметиламинопурину (заявка Японии 5-304969А), мутантные штаммы с устойчивость к аналогу изолейцина, такому как тиаизолейцин и гидроксамат изолейцина, и мутантные штаммы, дополнительно имеющие устойчивость к DL-этионину и/или гидроксамату аргинина (заявка Японии 5-130882А). Кроме того, в качестве родительских штаммов также могут использоваться рекомбинантные штаммы, трансформированные генами, кодирующими белки, вовлеченные в биосинтез L-изолейцина, такие как треониндеаминаза и ацетогидроксатсинтаза (заявка Японии 2-458А, патент Франции 0356739 и патент США 5998178).
2. Способ согласно настоящему изобретению.
Способом согласно настоящему изобретению является способ получения L-аминокислоты, включающий стадии выращивания бактерии согласно настоящему изобретению в питательной среде с целью продукции и накопления L-аминокислоты в питательной среде, и выделения L-аминокислоты из культуральной жидкости.
Согласно настоящему изобретению выращивание, выделение и очистка L-аминокислоты из культуральной или подобной ей жидкости может быть осуществлена способом, подобным традиционным способам ферментации, в которых аминокислота продуцируется с использованием бактерии.
Питательная среда, используемая для выращивания, может быть как синтетической, так и натуральной, при условии, что указанная среда содержит источники углерода, азота, минеральные добавки и, если необходимо, соответствующее количество питательных добавок, необходимых для роста микроорганизмов. К источникам углерода относятся различные углеводы, такие как глюкоза и сахароза, а также различные органические кислоты. В зависимости от характера ассимиляции используемого микроорганизма, могут использоваться спирты, такие как этанол и глицерин. В качестве источника азота могут использоваться различные неорганические соли аммония, такие как аммиак и сульфат аммония, другие соединения азота, такие как амины, природные источники азота, такие как пептон, гидролизат соевых бобов, ферментолизат микроорганизмов. В качестве минеральных добавок могут использоваться фосфат калия, сульфат магния, хлорид натрия, сульфат железа, сульфат марганца, хлорид кальция и подобные им соединения. В качестве витаминов могут использоваться тиамин, дрожжевой экстракт и т.п.
Выращивание осуществляется предпочтительно в аэробных условиях, таких как перемешивание культуральной жидкости на качалке, взбалтывание с аэрацией, при температуре в пределах от 20 до 40°С, предпочтительно в пределах от 30 до 38°С. pH среды поддерживают в пределах от 5 до 9, предпочтительно от 6.5 до 7.2. pH среды может регулироваться аммиаком, карбонатом кальция, различными кислотами, основаниями и буферными растворами. Обычно, выращивание в течение от 1 до 5 дней приводит к накоплению целевой L-аминокислоты в культуральной жидкости.
После выращивания твердые остатки, такие как клетки, могут быть удалены из культуральной жидкости методом центрифугирования или фильтрацией через мембрану, а затем L-аминокислота может быть выделена и очищена методами ионообменной хроматографии, концентрирования и/или кристаллизации.
Краткое описание фигур.
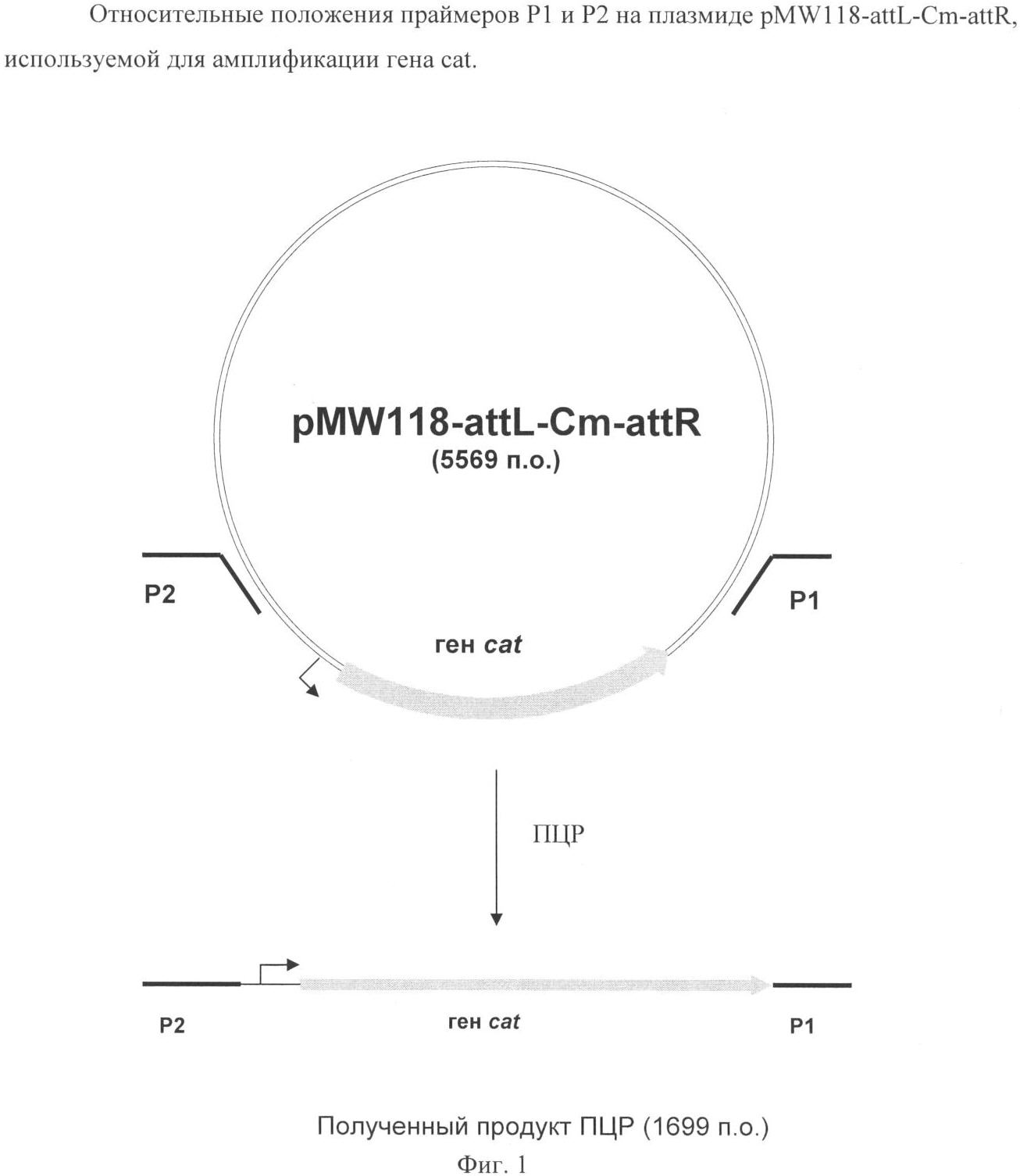
На Фиг.1 изображены относительные положения праймеров Р1 и Р2 на плазмиде pMW118-attL-Cm-attR, используемой для амплификации гена cat.
На Фиг.2 изображено конструирование фрагмента хромосомной ДНК, содержащего инактивированный ген tolC.
Примеры
Настоящее изобретение будет более подробно описано ниже со ссылкой на следующие не ограничивающие настоящее изобретение Примеры.
Пример 1. Конструирование штамма с инактивированным геном tolC
1. Деления гена tolC
Штамм, содержащий делецию гена tolC, был сконструирован с использованием методики, разработанной Datsenko, К.А. и Wanner, B.L. (Proc. Natl. Acad. Sci. USA, 2000, 97(12), 6640-6645), известной как "Red-зависимая интеграция". Фрагмент ДНК, содержащий маркер лекарственной устойчивости CmR, кодируемый геном cat, был получен методом ПЦР с использованием праймеров P1 (SEQ ID NO: 3) и Р2 (SEQ ID NO: 4) и плазмиды pMW118-attL-Cm-attR (WO 05/010175) в качестве матрицы. Праймер Р1 содержит как область, комплементарную области, расположенной на 5'-конце гена tolC, так и область, комплементарную attR участку. Праймер Р2 содержит как область, комплементарную области, расположенной на 3'-конце гена tolC, так и область, комплементарную участку attL. Использовался следующий температурный профиль для ПЦР: денатурация при 95°С в течение 3 мин; два первых цикла: 1 мин при 95°С, 30 сек при 50°С, 40 сек при 72°С; и последующие 25 циклов: 30 сек при 95°С, 30 сек при 54°С, 40 сек при 72°С; и заключительная полимеризация: 5 мин при 72°С.
Полученный продукт ПЦР длиной 1699 п.н. (Фиг.1), очищенный в агарозном геле, использовали для электропорации в штамм E.coli MG1655 (АТСС 700926), содержащий плазмиду pKD46 с термочувствительным репликоном. Плазмида pKD46 (Datsenko, K.A. and Wanner, B.L., Proc. Natl. Acad. Sci. USA, 2000, 97:12:6640-45) содержит фрагмент ДНК фага λ длиной 2154 нуклеотида (позиции с 31088 по 33241 нуклеотидной последовательности с инвентарным номером J02459 в базе данных GenBank), а также содержит гены λ Red-гомологичной системы рекомбинации (гены γ, β, exo) под контролем промотора ParaB; индуцируемого арабинозой. Плазмида pKD46 необходима для интеграции продукта ПЦР в хромосому штамма MG1655.
Электрокомпетентные клетки были получены следующим образом: ночную культуру штамма E.coli MG1655/pKD46 выращивали при 30°С в среде LB с добавкой ампициллина (100 мг/л), развели в 100 раз, добавив 5 мл среды SOB (Sambrook et al, "Molecular Cloning A Laboratory Manual, Second Edition", Cold Spring Harbor Laboratory Press (1989)), содержащей ампициллин и L-арабинозу (1 мМ). Полученную культуру растили с перемешиванием при 30°С до достижения OD600≈0.6, после чего делали клетки электрокомпетентными, путем концентрирования в 100 раз и трехкратного отмывания ледяной деионизированной H2O. Электропорацию проводили с использованием 70 мкл клеток и ≈100 нг продукта ПЦР. После электропорации клетки инкубировали в 1 мл среды SOC (Sambrook et al, "Molecular Cloning A Laboratory Manual, Second Edition", Cold Spring Harbor Laboratory Press (1989)) при 37°С в течение 2.5 часов, после чего высевали на чашки с L-агаром, содержащим хлорамфеникол (30 мкг/мл) и выращивали при 37°С для отбора CmR-рекомбинантов. Затем для удаления плазмиды pKD46 проводили 2 пассажа на L-агаре с Cm при 42°С, и полученные колонии проверяли на чувствительность к ампициллину.
2. Подтверждение делеции гена tolC с помощью ПЦР.
Мутанты с делегированным геном tolC, содержащие ген устойчивости к Cm, были проверены с помощью ПЦР. Локус-специфичные праймеры P3 (SEQ ID NO: 5) и P4 (SEQ ID NO: 6) использовались для проверки делеции с помощью ПЦР. Использовался следующий температурный профиль для ПЦР-проверки: денатурация при 94°С в течение 3 мин; профиль для 30 циклов: 30 сек при 94°С, 30 сек при 54°С, 1 мин при 72°С; заключительный шаг: 7 мин при 72°С. Длина продукта ПЦР, полученного в результате реакции с использованием в качестве матрицы клеток родительского штамма MG1655tolC+, составляет ~2.0 т.п.н. Длина продукта ПЦР, полученного в результате реакции с использованием в качестве матрицы клеток мутантного штамма, составляет ~1.7 т.п.о. (Фиг.2). Мутантный штамм назвали MG1655 ΔtolC::cat.
Пример 2. Продукция L-треонина штаммом E.coli B-3996-ΔtolC
Для оценки влияния инактивации гена tolC на продукцию треонина ДНК-фрагменты хромосомы описанного выше штамма E.coli MG1655 ΔtolC::cat были перенесены в штамм-продуцент L-треонина E.coli В-3996 (ВКПМ В-3996) с помощью Р1-трансдукции (Miller, J.H. (1972) Experiments in Molecular Genetics, Cold Spring Harbor Lab. Press, Plainview, NY), в результате чего был получен штамм В-3996-Δ tolC. Штамм В-3996 был депонирован 19 ноября 1987 г. во Всесоюзном научном центре антибиотиков (РФ, 117105 Москва, Нагатинская ул., 3-А) с инвентарным номером РИА 1867. Указанный штамм также был депонирован во Всероссийской коллекции промышленных микроорганизмов (ВКПМ) (РФ, 117545 Москва, 1-й Дорожный проезд, 1) с инвентарным номером В-3996.
Оба штамма E.coli В-3996 и B-3996-ΔtolC выращивали в течение 18-24 часов при температуре 37°С на чашках с L-агаром. Для получения посевной культуры указанные штаммы выращивали при 32°С в течение 18 часов на роторной качалке (250 об/мин) в пробирках размером 20×200 мм, содержащих 2 мл L-бульона с 4% глюкозой. Затем в ферментационную среду были внесены по 0.21 мл (10%) посевной культуры. Ферментацию проводили в 2 мл минимальной ферментационной среды в пробирках размером 20×200 мм. Клетки выращивали в течение 65 часов при 32°С с перемешиванием (250 об/мин).
После выращивания количество накопленного в среде L-треонина определяли с помощью бумажной хроматографии, с использованием подвижной фазы следующего состава: бутанол: уксусная кислота: вода = 4:1:1 (v/v). Раствор (2%) нингидрина в ацетоне использовали для визуализации. Пятно, содержащее L-треонин, было вырезано, L-треонин был элюирован 0.5% водным раствором CdCl2, после чего количество L-треонина оценивалось спектрофотометрическим методом при длине волны 540 нм. Результаты пяти независимых пробирочных ферментации приведены в Таблице 1. Как видно из Таблицы 1, штамм B-3996-ΔtolC накапливал большее количество L-треонина по сравнению со штаммом В-3996. Использовали следующий состав ферментационной среды (г/л):
Глюкозу и сульфат магния стерилизовали отдельно. СаСО3 стерилизовали сухим жаром при 180°С в течение 2 часов. pH доводили до 7.0. Антибиотик добавляли в среду после стерилизации.
Пример 3. Продукция L-лизина штаммом E.coli AJ11442-ΔtolC
Для оценки влияния инактивации гена tolC на продукцию лизина ДНК-фрагменты хромосомы описанного выше штамма E.coli MG1655 ΔtolC::cat могут быть перенесены в штамм-продуцент L-лизина Е. coli AJ11442 с помощью P1-трансдукции (Miller, J.H. (1972) Experiments in Molecular Genetics, Cold Spring Harbor Lab. Press, Plainview, NY), в результате чего может быть получен штамм AJ11442-ΔtolC.
Оба штамма E.coli, родительский AJ11442 и полученный AJ11442-ΔtolC, могут выращиваться в L-среде при 37°С, и 0.3 мл полученных культур может быть внесено в 20 мл ферментационной среды, содержащей необходимые антибиотики, в колбы объемом 500 мл. Культивирование может производиться при 37°С в течение 16 часов с использованием возвратно-поступательной качалки со скоростью перемешивания 115 об/мин. После выращивания количества L-лизина и остаточной глюкозы в среде могут быть измерены известным способом (Biotech-analyzer AS210, производитель - Sakura Seiki Co.). Затем, для каждого из штаммов может быть рассчитан выход L-лизина в пересчете на потребленную глюкозу. Состав ферментационной среды (г/л):
pH доводят до 7.0 в помощью КОН и среду автоклавируют при 115°С в течение 10 мин. Глюкозу и MgSO4·7H2O стерилизуют отдельно. Также добавляют 30 г/л CaCO3, предварительно простерилизованного сухим жаром при 180°С в течение 2 часов.
Пример 4. Продукция L-цистеина штаммом E.coli JM15(ydeD)-ΔtolC
Для оценки влияния инактивации гена tolC на продукцию L-цистеина ДНК-фрагменты хромосомы описанного выше штамма Е. coli MG1655 ΔtolC::cat могут быть перенесены в штамм-продуцент L-цистеина E.coli JM15(ydeD) с помощью Р1-трансдукции (Miller, J.H. (1972) Experiments in Molecular Genetics, Cold Spring Harbor Lab. Press, Plainview, NY), в результате чего может быть получен штамм JM15(ydeD)-ΔtolC.
Штамм E.coli JM15(ydeD) является производным штамма E.coli JM15 (патент США 6218168), который может быть трансформирован ДНК, содержащей ген ydeD, кодирующий мембранный белок, не вовлеченный в пути биосинтеза ни одной из L-аминокислот (патент США 5972663). Штамм JM15 (CGSC# 5042) может быть получен из генетической коллекции университета города Нью Хайвен в США (The E.coli Genetic Resource Center, Yale University, New Haven, USA (http://cgsc.biology.yale.edu/)).
Условия ферментации для оценки продукции L-цистеина детально описаны в Примере 6 патента США 6218168.
Пример 5. Продукция L-лейцина штаммом E.coli 57-ΔtolC
Для оценки влияния инактивации гена tolC на продукцию L-лейцина ДНК-фрагменты хромосомы описанного выше штамма E.coli MG1655 ΔtolC::cat могут быть перенесены в штамм-продуцент L-лейцина E.coli 57 (ВКПМ В-7386, патент США 6124121) с помощью Pl-трансдукции (Miller, J.H. (1972) Experiments in Molecular Genetics, Cold Spring Harbor Lab. Press, Plainview, NY), в результате чего может быть получен штамм 57-pMW-ΔtolC. Штамм E.coli 57 был депонирован во Всероссийской коллекции промышленных микроорганизмов (ВКПМ) (РФ, 117545 Москва, 1-й Дорожный проезд, 1) 19 мая 1997 года с инвентарным номером VKPM B-7386.
Оба штамма E.coli, 57 и 57-ΔtolC, могут быть выращены в течение 18-24 часов при температуре 37°С на чашках с L-агаром. Для получения посевной культуры указанные штаммы могут быть выращены на роторной качалке (250 об/мин) при 32°С в течение 18 часов в пробирках размером 20×200 мм, содержащих 2 мл L-бульона с 4% сахарозы. Затем в ферментационную среду может быть внесено по 0.21 мл (10%) посевной культуры. Ферментацию можно проводить в 2 мл минимальной ферментационной среды в пробирках размером 20×200 мм. Клетки могут выращиваться в течение 48-72 часов при 32°С с перемешиванием (250 об/мин).
Количество L-лейцина может быть измерено с помощью бумажной хроматографии (состав подвижной фазы: бутанол - уксусная кислота - вода = 4:1:1)
Может быть использован следующий состав ферментационной среды (г/л) (pH 7.2):
Глюкозу и мел следует стерилизовать отдельно.
Пример 6. Продукция L-гистидина штаммом E.coli 80-ΔtolC.
Для оценки влияния инактивации гена tolC на продукцию L-гистидина ДНК-фрагменты хромосомы описанного выше штамма E.coli MG1655 ΔtolC::cat могут быть перенесены в штамм-продуцент L-гистидина E.coli 80 с помощью P1-трансдукции (Miller, J.H. (1972) Experiments in Molecular Genetics, Cold Spring Harbor Lab. Press, Plainview, NY), в результате чего может быть получен штамм 80-ΔtolC. Штамм 80 описан в патенте РФ 2119536 и депонирован во Всероссийской коллекции промышленных микроорганизмов (Россия, 117545 Москва, 1-ый Дорожный проезд, 1) 15 октября 1999 г. с инвентарным номером ВКПМ В-7270, а затем 12 июля 2004 г. депонирован в соответствии с Будапештским Договором.
Оба штамма E.coli, родительский 80 и полученный 80-ΔtolC, могут выращиваться в L-бульоне при 29°С в течение 6 часов. Затем 0.1 мл полученных культур может быть внесено в 2 мл ферментационной среды в пробирки размером 20×200 мм и культуры могут быть выращены при 29°С в течение 65 часов на роторной качалке (350 об/мин). После выращивания количество накопленного в среде гистидина может быть определено с помощью бумажной хроматографии. Может быть использована подвижная фаза следующего состава: n-бутанол - уксусная кислота - вода = 4:1:1 (v/v). Раствор нингидрина (0.5%) в ацетоне может быть использован для визуализации.
Состав ферментационной среды (pH 6.0) (г/л):
Глюкозу, пролин, бетаин и CaCO3 стерилизуют отдельно. pH доводят до 6.0 перед стерилизацией.
Пример 7. Продукция L-глутаминовой кислоты штаммом E.coli VL334thrC+-ΔtolC
Для оценки влияния инактивации гена tolC на продукцию L-глутаминовой кислоты ДНК-фрагменты хромосомы описанного выше штамма E.coli MG1655 ΔtolC::cat могут быть перенесены в штамм-продуцент L-глутаминовой кислоты E. VL334thrC+(EP 1172433) с помощью P1-трансдукции (Miller, J.H. (1972) Experiments in Molecular Genetics, Cold Spring Harbor Lab. Press, Plainview, NY), в результате чего может быть получен штамм VL334thrC+-ΔtolC. Штамм VL334thrC+депонирован 6 декабря 2004 г. во Всероссийской коллекции промышленных микроорганизмов (ВКПМ) (Россия, 117545 Москва, 1-ый Дорожный проезд, 1) с инвентарным номером В-8961, а затем 8 декабря 2004 г. депонирован в соответствии с Будапештским Договором.
Оба штамма, родительский VL334thrC+и полученный VL334thrC+-ΔtolC, могут быть выращены на чашках с L-агаром при 37°С в течение 18-24 часов. Далее, одна петля клеток может быть перенесена в пробирки, содержащие 2 мл ферментационной среды. Ферментационная среда должна содержать глюкозу - 60 г/л, сульфат аммония - 25 г/л, KH2PO4 - 2 г/л, MgSO4 - 1 г/л, тиамин - 0.1 мг/мл, L-изолейцин - 70 мкг/мл и мел - 25 г/л (pH 7.2). Глюкозу и мел следует стерилизовать отдельно. Выращивание может производиться при 30°С в течение 3 дней с перемешиванием. После выращивания количество полученной L-глутаминовой кислоты может быть определено с помощью бумажной хроматографии (состав подвижной фазы: бутанол - уксусная кислота - вода = 4:1:1) с последующим окрашиванием нингидрином (1% раствор в ацетоне) и дальнейшим элюированием полученных соединений в 50% этаноле с 0.5% CdCl2.
Пример 8. Продукция L-фенилаланина штаммом E.coli AJ12739-ΔtolC
Для оценки влияния инактивации гена tolC на продукцию L-фенилаланина ДНК-фрагменты хромосомы описанного выше штамма E.coli MG1655 ΔtolC::cat могут быть перенесены в штамм-продуцент L-фенилаланина E.coli AJ12739 с помощью Р1-трансдукции (Miller, J.H. (1972) Experiments in Molecular Genetics, Cold Spring Harbor Lab. Press, Plainview, NY), в результате чего может быть получен штамм AJ12739-ΔtolC. Штамм AJ12739 депонирован во Всероссийской коллекции промышленных микроорганизмов (ВКПМ) (Россия, 117545 Москва, 1ый Дорожный проезд, 1) 6 ноября 2001 года с инвентарным номером ВКПМ В-8197, а затем 23 августа 2002 г. депонирован в соответствии с Будапештским Договором.
Оба штамма, родительский AJ12739 и полученный AJ12739-ΔtolC, могут быть выращены при 37°С в течение 18 часов в питательном бульоне, 0.3 мл полученных культур может быть внесено в 3 мл ферментационной среды в пробирки размером 20×200 мм, и культуры могут быть выращены при 37°С в течение 48 часов на роторной качалке. По окончании ферментации количество накопленного в среде фенилаланина может быть определено с помощью тонкослойной хроматографии (TLC). Для этой цели могут быть использованы TLC-пластинки размером 10×15 см, покрытые 0.11 мм-слоем силикагеля Сорбфил без флуоресцентного индикатора (Акционерное Общество Сорбполимер, Краснодар, Россия). Пластинки Сорбфил могут экспонироваться в подвижной фазе следующего состава: пропан-2-ол: этилацетат: 25% водного аммиака: вода = 40:40:7:16 (v/v). Раствор (2%) нингидрина в ацетоне может быть использован для визуализации.
Состав ферментационной среды (г/л):
Глюкозу и сульфат магния стерилизуют отдельно. CaCO3 стерилизуют сухим жаром при 180°С в течение 2 часов. pH доводят до 7.0.
Пример 9. Продукция L-триптофана штаммом E.coli SV164 (pGH5)-ΔtolC
Для оценки влияния инактивации гена tolС на продукцию L-триптофана ДНК-фрагменты хромосомы описанного выше штамма Е. coli MG1655 ΔtolC::cat могут быть перенесены в штамм-продуцент L-триптофана E.coli SV164 (pGH5) с помощью Р1-трансдукции (Miller, J.H. (1972) Experiments in Molecular Genetics, Cold Spring Harbor Lab. Press, Plainview, NY), в результате чего может быть получен штамм SV164(pGH5)-ΔtolC. Штамм SV164 имеет аллель гена trpE, кодирующего фермент антранилатсинтазу, не ингибируемый триптофаном по типу обратной связи. Плазмида pGH5 содержит мутантный ген sera, кодирующий фосфоглицератдегидрогеназу, не ингибируемую серином по типу обратной связи. Штамм SV164 (pGH5) подробно описан в патенте США 6180373 или Европейском патенте 0662143.
Оба штамма, полученный SV164(pGH5)-ΔtolC и родительский SV164(pGH5), могут быть выращены с перемешиванием при 37°С в течение 18 часов в 3 мл питательного бульона с добавлением тетрациклина (маркера плазмиды pGH5) (10 мг/мл). 0.3 мл полученных культур могут быть внесены в 3 мл ферментационной среды, содержащей тетрациклин (10 мг/мл) в пробирках размером 20×200 мм, и могут быть выращены при 32 С в течение 72 часов на роторной качалке при 250 об/мин. После выращивания количество накопленного в среде триптофана может быть определено с помощью TLC, как описано в Примере 8. Компоненты ферментационной среды представлены в Таблице 2, но группы компонентов А, В, С, D, Е, F и Н следует стерилизовать отдельно, как и показано в Таблице, чтобы избежать нежелательных взаимодействий во время стерилизации.
Пример 10. Продукция L-пролина штаммом E.coli 702ilvA-ΔtolC
Для оценки влияния инактивации гена tolC на продукцию L-пролина ДНК-фрагменты из хромосомы описанного выше штамма E.coli MG1655 ΔtolC::cat могут быть перенесены в штамм-продуцент L-пролина Е. coli 702ilvA с помощью Pl-трансдукции (Miller, J.H. (1972) Experiments in Molecular Genetics, Cold Spring Harbor Lab. Press, Plainview, NY), в результате чего может быть получен штамм 702ilvA-ΔtolC. Штамм 702ilvA депонирован 18 июля 2000 г. во Всероссийской коллекции промышленных микроорганизмов (ВКПМ) (Россия, 117545 Москва, 1ый Дорожный проезд, 1) с инвентарным номером ВКПМ В-8012, а затем 18 мая 2001 г. депонирован в соответствии с Будапештским Договором.
Оба штамма E.coli 702ilvA и 702ilvA-Δ tolC могут быть выращены в течение 18-24 часов при температуре 37°С на чашках с L-агаром. Затем ферментация с использованием этих штаммов может производиться в тех же условиях, как описано в Примере 7.
Пример 11. Продукция L-аргинина штаммом E.coli 382-ΔtolC
Для оценки влияния инактивации гена tolC на продукцию L-аргинина ДНК-фрагменты хромосомы описанного выше штамма E.coli MG1655 ΔtolC::cat, могут быть перенесены в штамм-продуцент L-аргинина E.coli 382 с помощью Pl-трансдукции (Miller, J.H. (1972) Experiments in Molecular Genetics, Cold Spring Harbor Lab. Press, Plainview, NY), в результате чего может быть получен штамм 382-ΔtolC. Штамм 382 депонирован во Всероссийской коллекции промышленных микроорганизмов (ВКПМ) (Россия, 117545 Москва, 1-ый Дорожный проезд, 1) 10 апреля 2000 года с инвентарным номером ВКПМ В-7926, а затем 18 мая 2001 г. депонирован в соответствии с Будапештским Договором.
Оба штамма, полученный 382-ΔtolC и родительский 382, могут быть выращены при 32°С в течение 18 часов в 2 мл LB-бульона, 0.3 мл полученных культур могут быть внесены в 2 мл ферментационной среды в пробирки размером 20×200 мм, и культуры могут быть выращены при 32°С в течение 48 часов на роторной качалке.
После выращивания количество накопленного в среде L-аргинина может быть определено с помощью бумажной хроматографии, при этом может использоваться следующий состав подвижной фазы: бутанол: уксусная кислота: вода = 4:1:1 (v/v). Раствор нингидрина (2%) в ацетоне может быть использован для визуализации. Пятно, содержащее L-аргинин, может быть вырезано, L-аргинин может быть элюирован 0.5% водным раствором CdCl2, после чего количество L-аргинина может быть определено спектрофотометрическим методом при длине волны 540 нм.
Состав ферментационной среды (г/л):
Глюкозу и сульфат магния стерилизуют отдельно. СаСО3 стерилизуют сухим жаром при 180°С в течение 2 часов. pH доводят до 7.0.
Пример 12. Удаление гена устойчивости к хлорамфиниколу Cm (cat gene) из хромосомы штаммов E.coli - продуцентов L-аминокислот.
Ген устойчивости Cm (ген cat) может быть удален из хромосомы штаммов-продуцентов L-аминокислот путем использования системы int-xis. С этой целью штамм-продуцент L-аминокислоты, в который были перенесены ДНК-фрагменты из вышеописанного штамма MG1655 ΔtolC::cat при помощи P1-трансдукции, может быть трансформирован плазмидой pMWts-Int/Xis. Селекция трансформированных клонов может быть произведена с использованием среды LB, содержащей ампициллин (100 мкг/мл). Клетки могут быть инкубированы при 30°С в течение ночи. Трансформированные клоны могут быть освобождены от гена cat путем выращивания отдельных колоний при 37°С (при этой температуре репрессор CIts в некоторой мере инактивируется, тогда как гены int/xis активируются) с последующей селекцией вариантов CmSApR. Удаление гена cat из хромосомы штаммов может быть подтверждено при помощи ПЦР. Локус-специфичные праймеры Р3 (SEQ ID NO:5) и P4 (SEQ ID NO:6) могут быть использованы для такого подтверждения путем ПЦР. Условия проведения ПЦР могут быть такими же, как описано выше. Продукт ПЦР, полученный в случае использования в качестве матрицы клеток с удаленным геном cat, должен быть намного короче (~0.3-0.5 т.п.о. в длину), чем в случае использования в качестве матрицы клеток штамма с неудаленным геном cat.
Хотя указанное изобретение описано в деталях со ссылкой на наилучший способ осуществления изобретения, для специалиста в указанной области техники очевидно, что могут быть совершены различные изменения и произведены эквивалентные замены, и такие изменения и замены не выходят за рамки настоящего изобретения. Каждому из упомянутых выше документов соответствует ссылка, и все цитируемые документы являются частью описания настоящего изобретения.
Группа А имеет pH, равный 7.1, который доводится с помощью аммиака. Каждая группа стерилизуется раздельно, охлаждается и затем смешивается друг с другом.




Реферат
Изобретение относится к биотехнологии и представляет собой способ получения L-треонина с использованием бактерии, принадлежащей к роду Escherichia, которая модифицирована таким образом, что ген tolC в указанной бактерии инактивирован. Изобретение позволяет получать L-треонин с высокой степенью эффективности. 2 н. и 1 з.п. ф-лы, 2 ил., 2 табл.
Формула
выращивание бактерии по любому из пп.1 и 2 в питательной среде, вызывающее продукцию и накопление L-треонина в культуральной жидкости, и
выделение L-треонина из культуральной жидкости.

Комментарии