Пептидные векторы - RU2005136221A
Код документа: RU2005136221A
Реферат
1. Соединение по формуле (I)
Х-В1-В2-В3-В4-Z,
(I)
где Х означает цитотоксический или цитостатический агент;
каждый из В1, В2, В3 и В4 означает, независимо для каждого случая, (Doc)m, (Aepa)n, -(C(О)-А1-А2-А3-А4-А5-С(О))s- или (аминокислота)р,
каждый из А1 и А5 означает, независимо для каждого случая, CR1R2;
каждый из R1 и R2 означает, независимо для каждого случая, Н, F, Br, Cl, I, C(1-30)алкил, C(2-30)алкенил, замещенный C(1-30)алкил, замещенный С(2-30)алкенил, SR3, S(O)R4 или S(O)2R5, или R1 и R2 вместе могут образовывать С(3-30)циклоалкил, С(3-30)гетероцикл или С(5-30)арильное кольцо;
каждый R3, R4 и R5 означает, независимо для каждого случая, C(1-30)алкил, C(2-30)алкенил, замещенный C(1-30)алкил или замещенный С(2-30)алкенил;
каждый из А2, А3 и А4 означает, независимо для каждого случая, CR6R7, O, S, (CH2)t или отсутствует;
каждый или R6 и R7 означает, независимо для каждого случая, H, F, Br, Cl, I, C(1-30)алкил, C(2-30)алкенил, замещенный C(1-30)алкил, замещенный С(2-30)алкенил, SR3, S(O)R4 или S(O)2R5, или R6 и R7 вместе могут образовывать кольцевую систему;
m равно, независимо для каждого случая, 0, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10;
n равно, независимо для каждого случая, 0, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10;
р равно, независимо для каждого случая, 0, 1 или 2;
s равно, независимо для каждого случая, 1, 2, 3, 4 и 5;
t равно, независимо для каждого случая, 0, 1, 2 или 3;
Z означает лиганд биологического рецептора, его аналог или производное указанного лиганда или указанного аналога;
при условии, что, когда Х является доксорубицином или производным доксорубицина, по меньшей мере одно из m и n не равно 0; и когда Х является паклитакселом или производным паклитаксела, В1 является (аминокислота)р и р равно 1 или 2,
или его фармацевтически приемлемая соль.
2. Соединение по п.1, в котором Х означает цитотоксическую часть молекулы, или его фармацевтически приемлемая соль.
3. Соединение по п.2, в котором Х означает антрациклин, или его фармацевтически приемлемая соль.
4. Соединение по п.3, в котором Х означает доксорубицин или производное доксорубицина, или его фармацевтически приемлемая соль.
5. Соединение по п.2, в котором Х означает камптотецин, производное камптотецина, паклитаксел или производное паклитаксела.
6. Соединение по п.5, в котором указанное производное камптотецина представляет собой
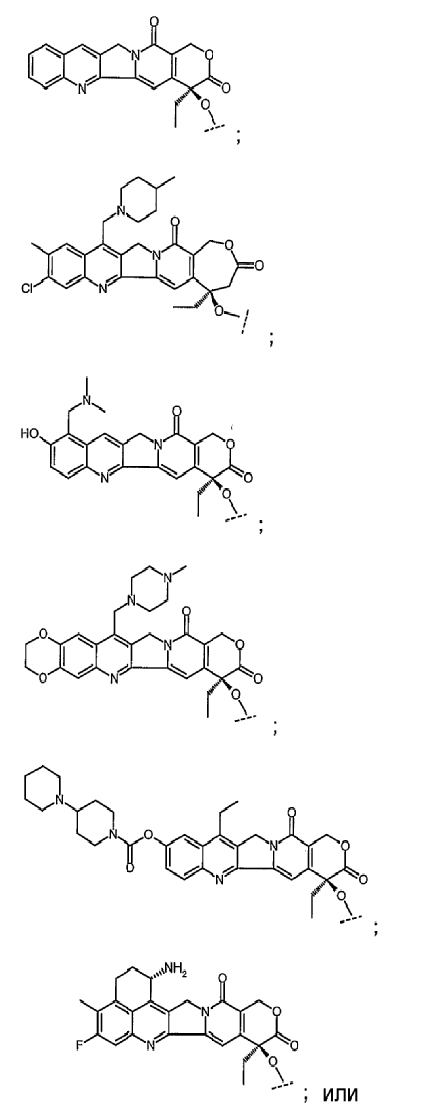
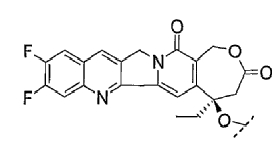
или его фармацевтически приемлемая соль.
7. Соединение по п.5, где или Х означает паклитаксел или производное паклитаксела, причем указанное производное паклитаксела представляет собой
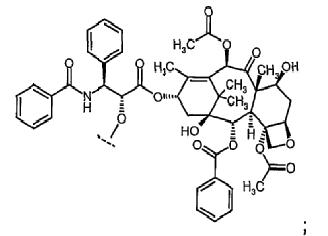
или его фармацевтически приемлемая соль.
8. Соединение по п.4, где Х означает доксорубицин или производное доксорубицина, причем указанное производное доксорубицина представляет собой
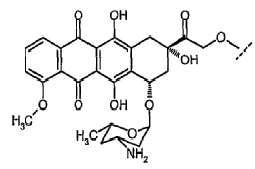
или его фармацевтически приемлемая соль.
9. Соединение по любому из пп.1-8, в котором Z означает соматостатин, бомбезин или LHRH или их аналог или производное указанного лиганда или указанного аналога; или его фармацевтически приемлемая соль.
10. Соединение по п. 9, где Z означает аналог соматостатина в соответствии с формулой
-DPhe-цикло(Cys-Tyr-DTrp-Lys-Abu-Cys)-Thr-NH2;
-DPhe-цикло(Cys-3ITyr-DTrp-Lys-Val-Cys)-Thr-NH2;
-DPhe-цикло(Cys-3ITyr-DTrp-Lys-Abu-Cys)-Thr-NH2;
-DPhe-цикло(Cys-3ITyr-DTrp-Lys-Thr-Cys)-Thr-NH2;
-Lys-DTyr-DTyr-цикло(Cys-Tyr-DTrp-Lys-Abu-Cys)-Thr-NH2;
-Caeg-цикло(DCys-Pal-DTrp-Lys-DCys)-Thr(Bzl)-Tyr-NH2;
-D2Nal-цикло[Cys-Tyr-DTrp-Lys-Val-Cys]-Thr-NH2;
-DPhe-цикло[Cys-Phe-DTrp-Lys-Thr-Cys]-Thr-ол;
-цикло({4-(-NH-C2H4-NH-CO-O)Pro}-Phg-DTrp-Lys-Tyr(4-Bzl)-Phe) или
-DPhe-цикло[Cys-Tyr-DTrp-Lys-Val-Cys]-Trp-NH2,
или его фармацевтически приемлемая соль.
11. Соединение по п.9, где Z означает аналог LHRH в соответствии с формулой
Glp-His-Trp-Ser-Tyr-DLys(-)-Leu-Arg-Pro-Gly-NH2;
Glp-His-Trp-Ser-Tyr-DOrn(-)-Leu-Arg-Pro-Gly-NH2;
Glp-His-Trp-Ser-Tyr-DDab(-)-Leu-Arg-Pro-Gly-NH2;
Glp-His-Trp-Ser-Tyr-DDap(-)-Leu-Arg-Pro-Gly-NH2;
Glp-His-Trp-Ser-Tyr-DApa(-)-Leu-Arg-Pro-Gly-NH2;
Glp-His-Trp-Ser-Tyr-DLys(-)-Leu-Arg-Pro-NHEt;
Glp-His-Trp-Ser-Tyr-DOrn(-)-Leu-Arg-Pro-NHEt;
Glp-His-Trp-Ser-Tyr-DDab(-)-Leu-Arg-Pro-NHEt;
Glp-His-Trp-Ser-Tyr-DDap(-)-Leu-Arg-Pro-NHEt;
Glp-His-Trp-Ser-His-DLys(-)-Trp-Tyr-Pro-Gly-NH2;
Glp-His-Trp-Ser-His-DOrn(-)-Trp-Tyr-Pro-Gly-NH2;
Glp-His-Trp-Ser-His-DDab(-)-Trp-Tyr-Pro-Gly-NH2 или
Glp-His-Trp-Ser-His-DDap(-)-Trp-Tyr-Pro-Gly-NH2,
или его фармацевтически приемлемая соль.
12. Соединение по п.9, где Z означает аналог бомбезина в соответствии с формулой
-Gln-Trp-Ala-Ala-βAla-His-Phe-Nle-NH2 (SEQ ID NO:1);
-Gln-Trp-Ala-Val-Gly-His-Leu-Ψ(CH2-NH)-Leu-NH2 (SEQ ID NO:2);
-Gln-Trp-Ala-Val-Gly-His-Leu-Ψ(CH2 -NH)-Phe-NH2 (SEQ ID NO:3);
-Gln-Trp-Ala-Ala-βAla-His-Leu-Leu-NH2 (SEQ ID NO:4);
-Gln-Trp-Ala-Ala-βAla-His-Leu-Nle-NH2 (SEQ ID NO:5);
-Gln-Trp-Ala-Val-βAla-His-Phe-Nle-NH2 (SEQ ID NO:6);
-Gln-Trp-Ala-Val-βAla-His-Ala-Nle-NH2 (SEQ ID NO:7);
-Gln-Trp-Ala-Val-βAla-Ala-Phe-Nle-NH2 (SEQ ID NO:8);
-Gln-Trp-Ala-Val-Gly-His-Leu-Leu-NH2 (SEQ ID NO:9);
-Gln-Trp-Ala-Val-Gly-His-Leu-Met-NH2 (SEQ ID NO:10);
-Gln-Trp-Ala-Val-Gly-His-Phe-Met-NH2 (SEQ ID NO:11);
-DAla-Gln-Trp-Ala-Val-β Ala-His-Phe-Nle-NH2;
-DPhe-Gln-Trp-Ala-Ala-βAla-His-Phe-Nle-NH2;
-DPhe-Gln-Trp-Ala-Val-βAla-Ala-Phe-Nle-NH2;
-DPhe-Gln-Trp-Ala-Val-βAla-His-Phe-Nle-NH2;
-DPhe-Gln-Trp-Ala-Val-βAla-His-Phe-Nle-NH2;
-DPhe-Gln-Trp-Ala-Val-β Ala-His-Ala-Nle-NH2;
-DPhe-Gln-Trp-Ala-Val-βAla-His-Leu-Leu-NH2;
-DPhe-Gln-Trp-Ala-Val-βAla-His-Leu-Nle-NH2;
-DPhe-Gln-Trp-Ala-Val-Gly-His-Leu-Ψ(CH2-NH)-Leu-NH2;
-DPhe-Gln-Trp-Ala-Val-Gly-His-Leu-Ψ(CH2-NH)-Phe-NH2;
-DPhe-Gln-Trp-Ala-Val-Gly-His-Leu-Met-NH2;
-DPhe-Gln-Trp-Ala-Val-Gly-His-Phe-Met-NH2;
-DPhe-Gln-Trp-Ala-Val-Gly-His-Leu-Leu-NH2,
или его фармацевтически приемлемая соль.
13. Соединение по п.1, в котором по меньшей мере одно из m и n не равно 0, или его фармацевтически приемлемая соль.
14. Соединение по п.1, где указанное соединение содержит формулу в соответствии с
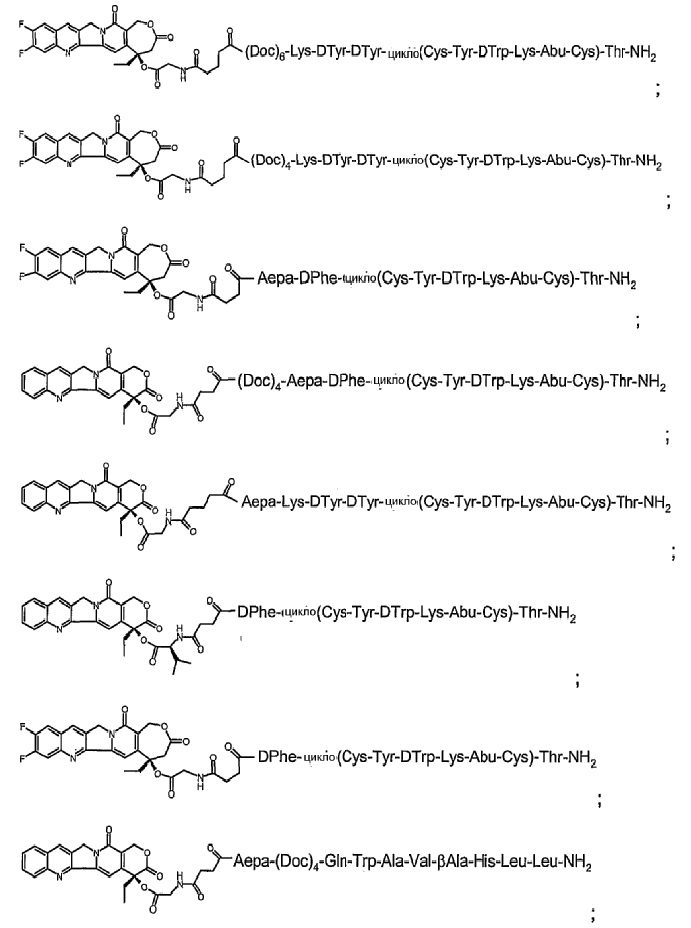
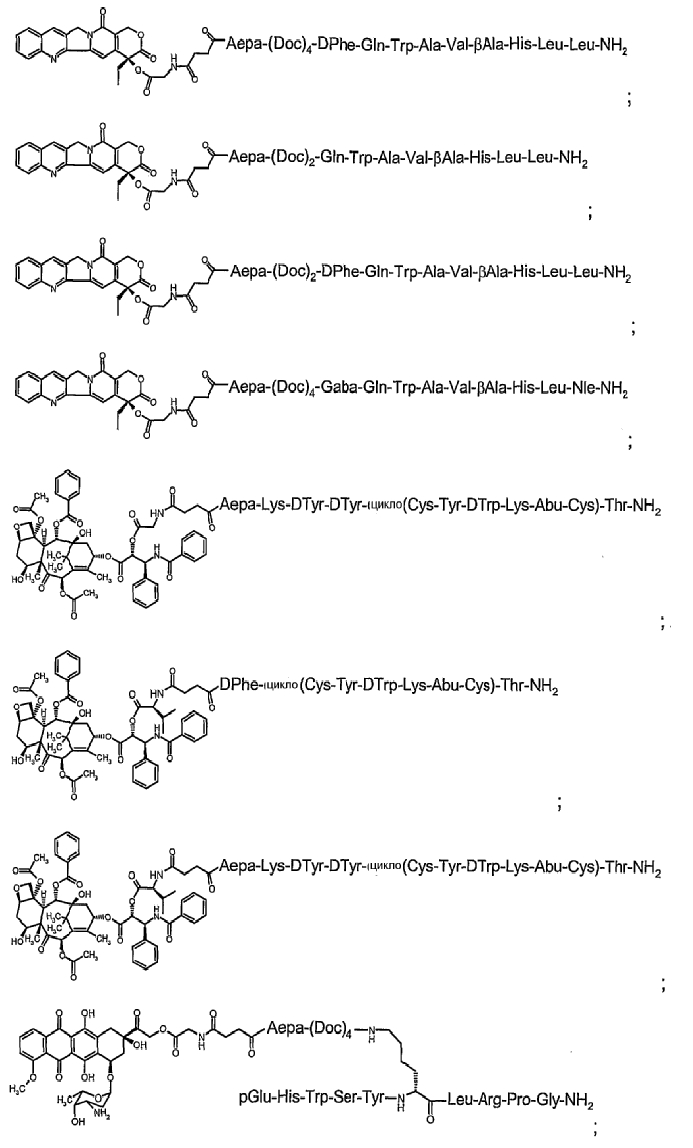
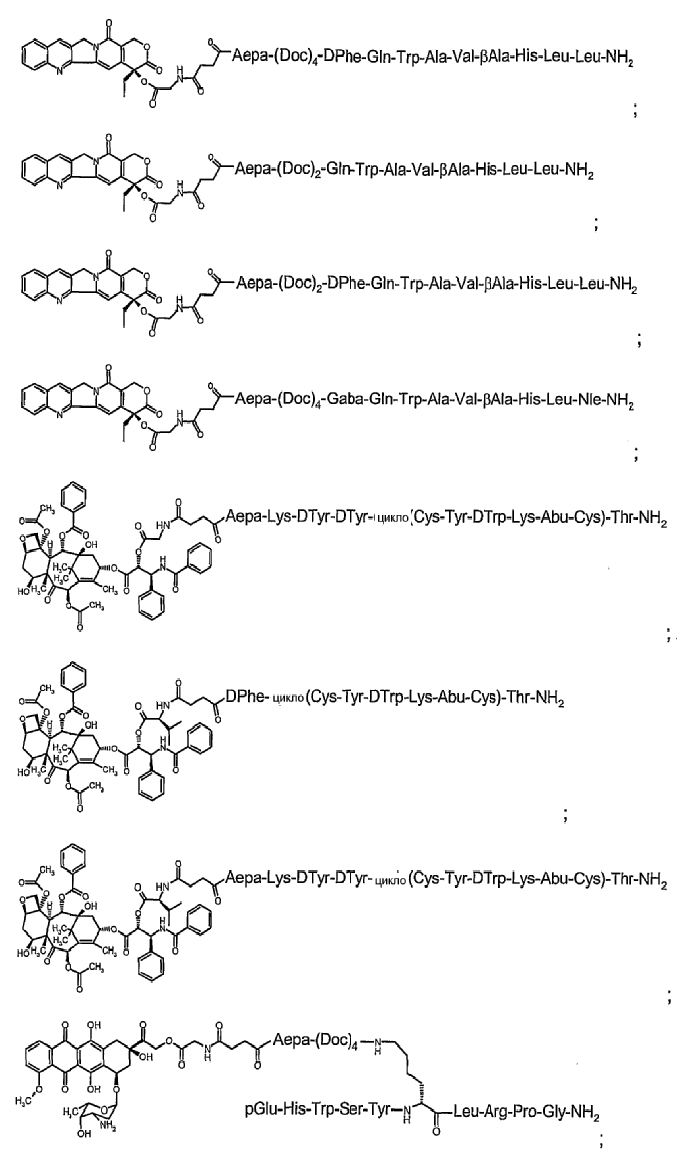
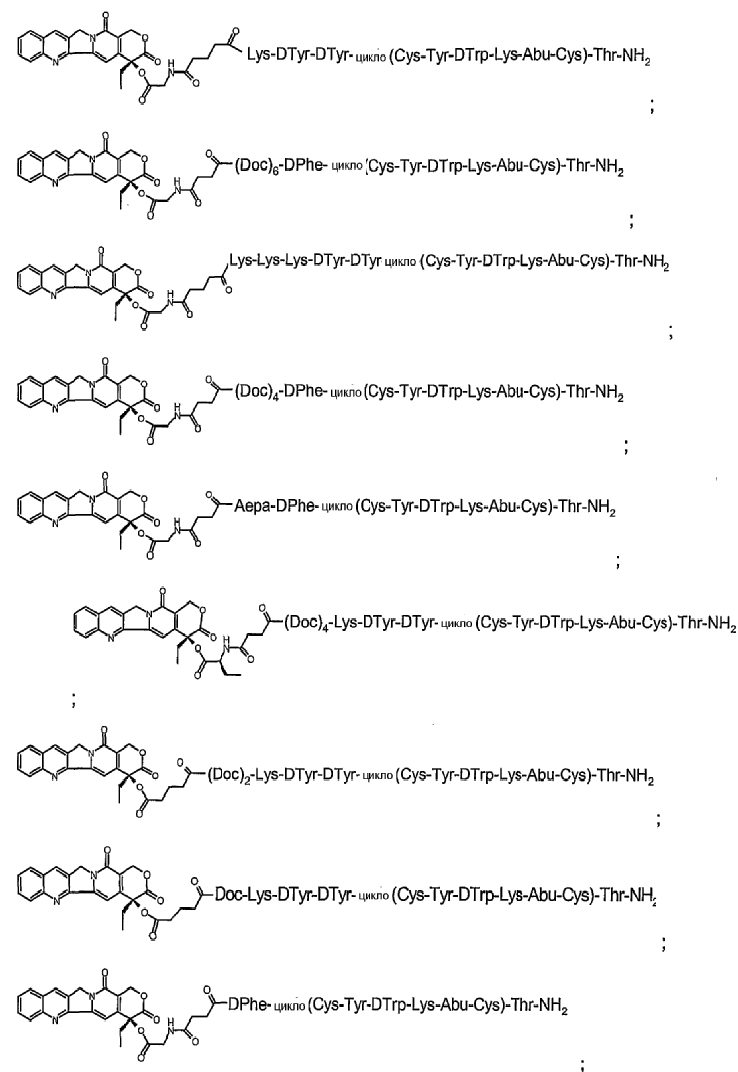
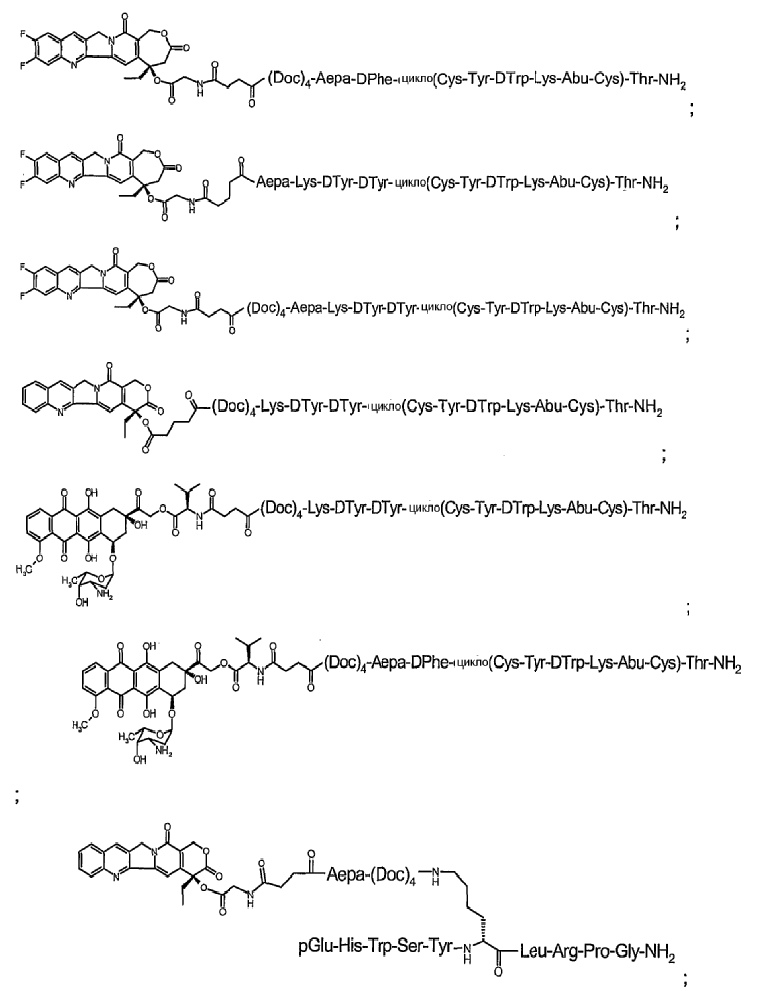
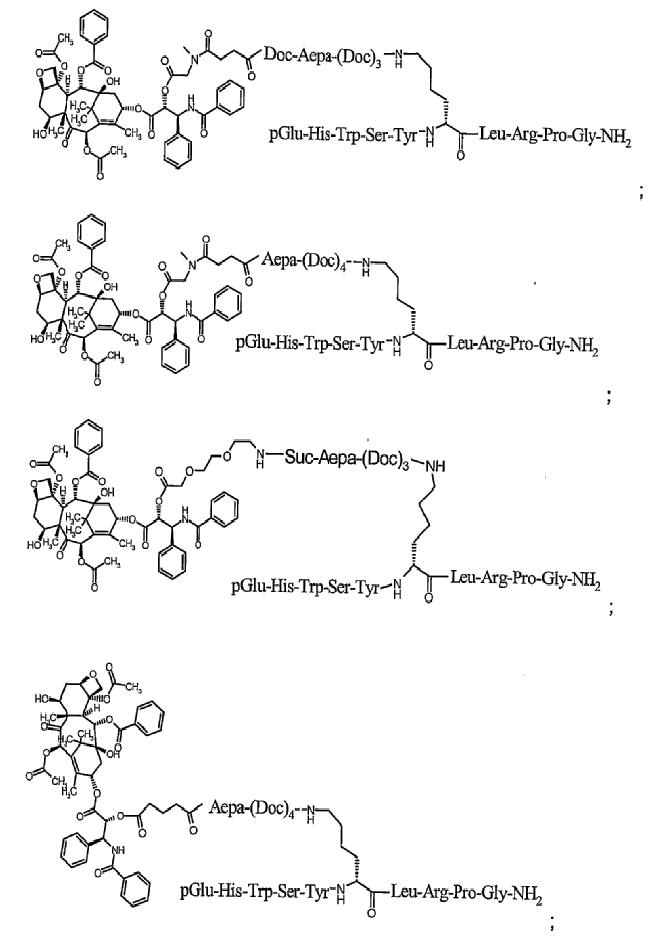
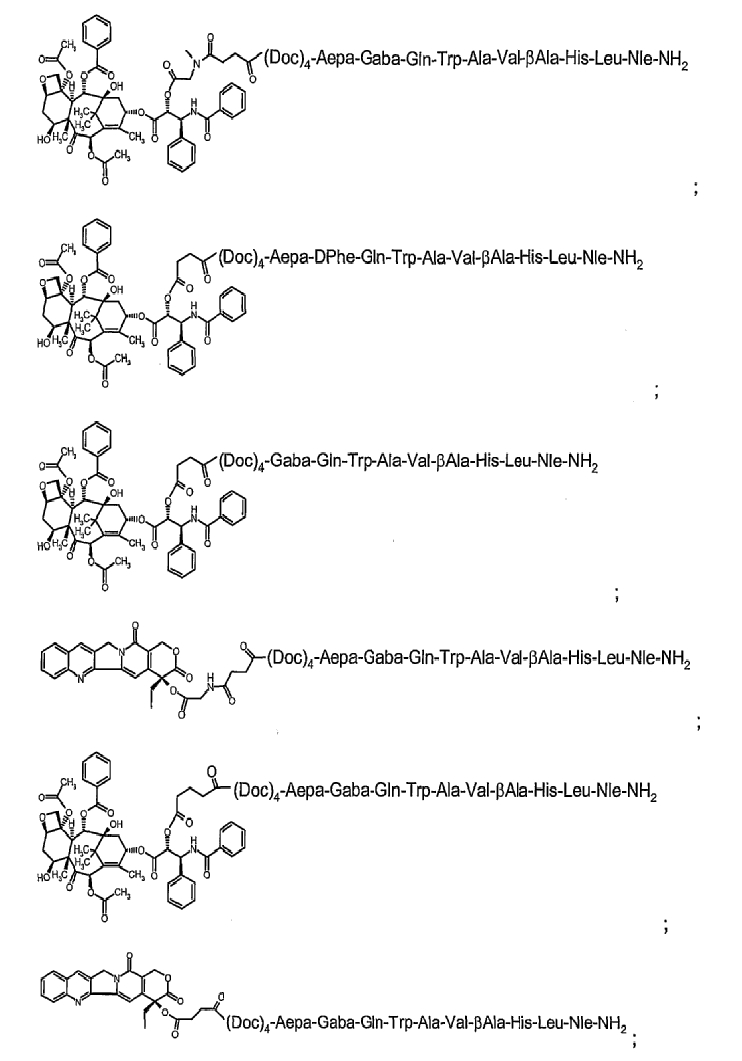
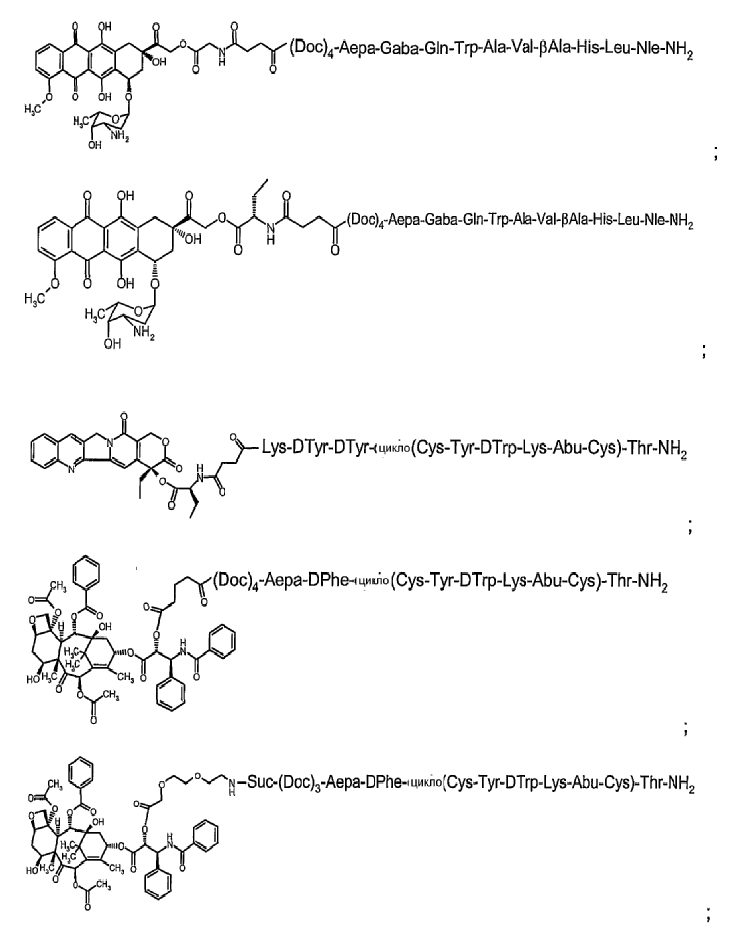

или его фармацевтически приемлемая соль.
15. Соединение по п.13, где эта формула содержит
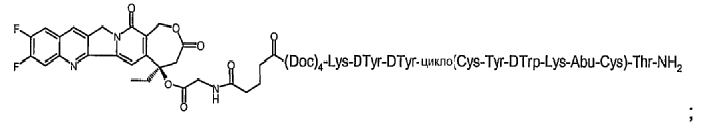
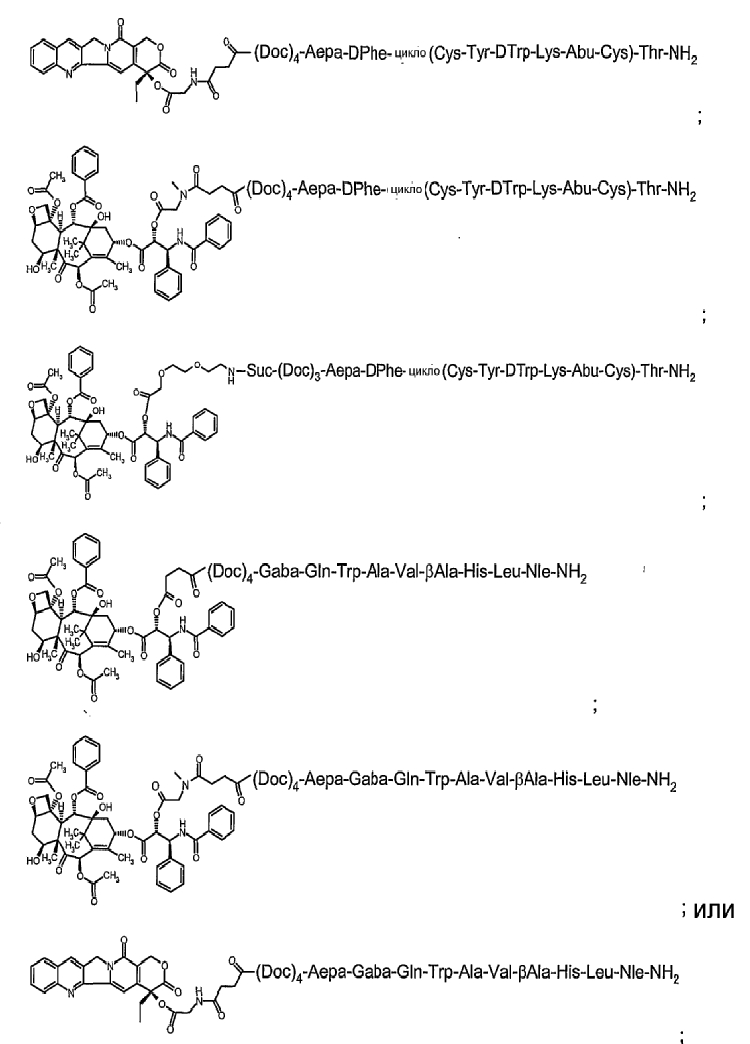
или его фармацевтически приемлемая соль.
16. Соединение по п.14, где указанное соединение содержит формулу:
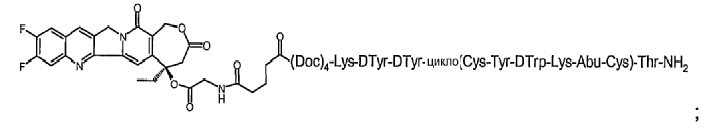
или его фармацевтически приемлемая соль.
17. Соединение по п.14, где указанное соединение содержит формулу
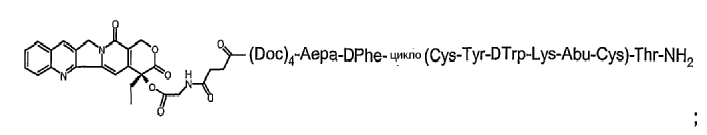
или его фармацевтически приемлемая соль.
18. Соединение, применимое в качестве промежуточного продукта в химическом синтезе, где указанный промежуточный продукт содержит соединение в соответствии с формулой


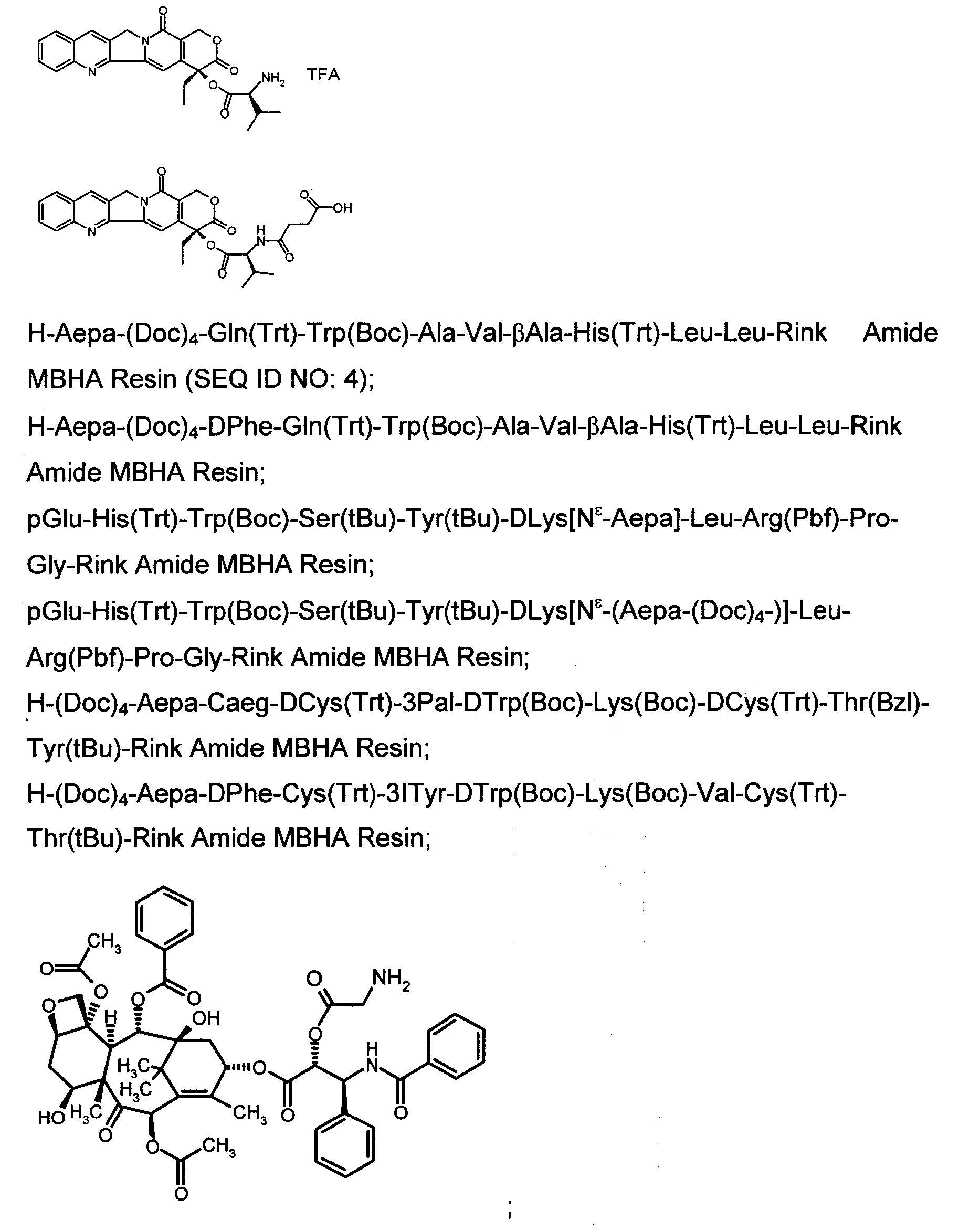
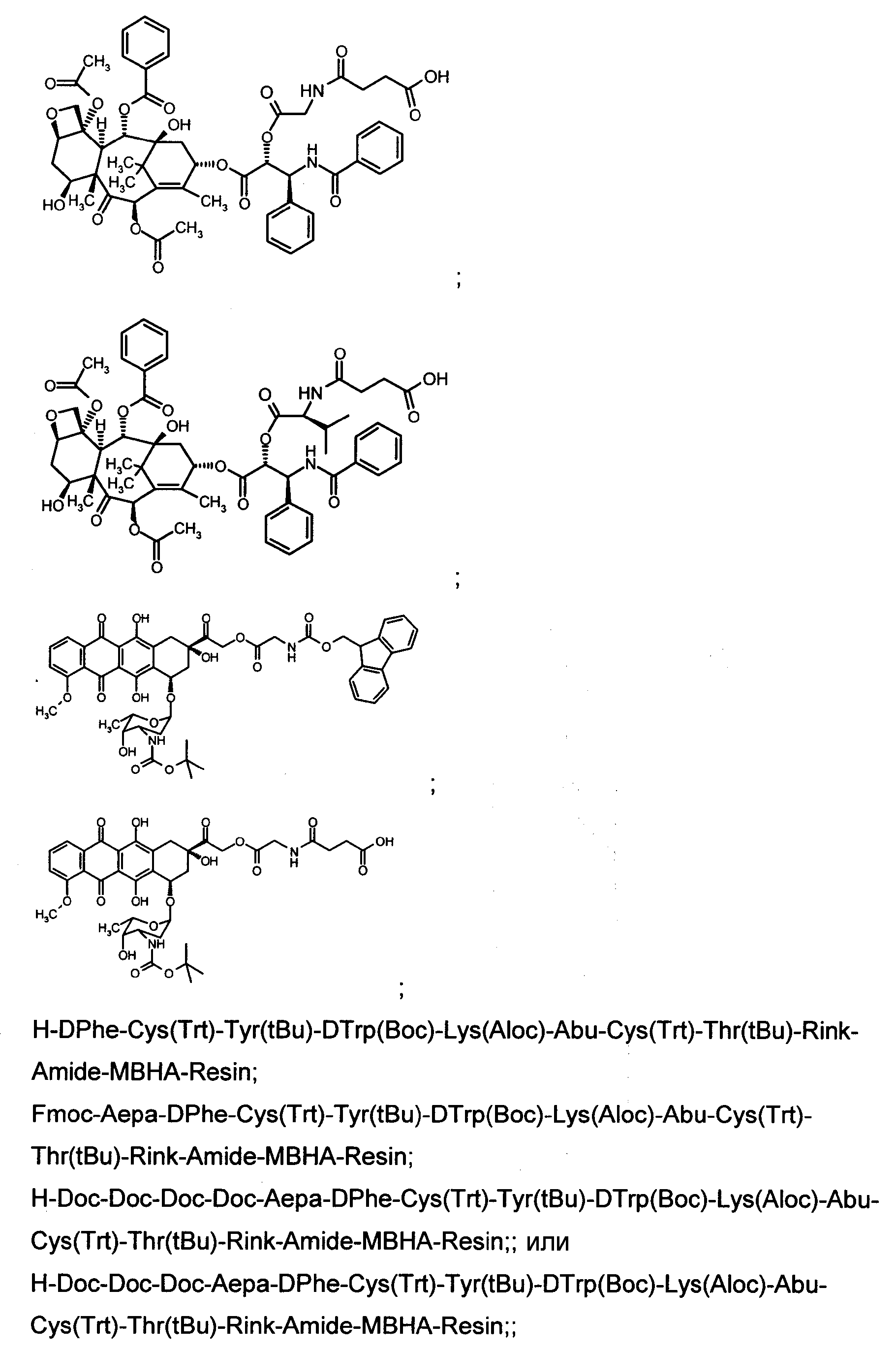
или его органическая или неорганическая соль.
19. Соединение по п.1, где указанное соединение содержит формулу






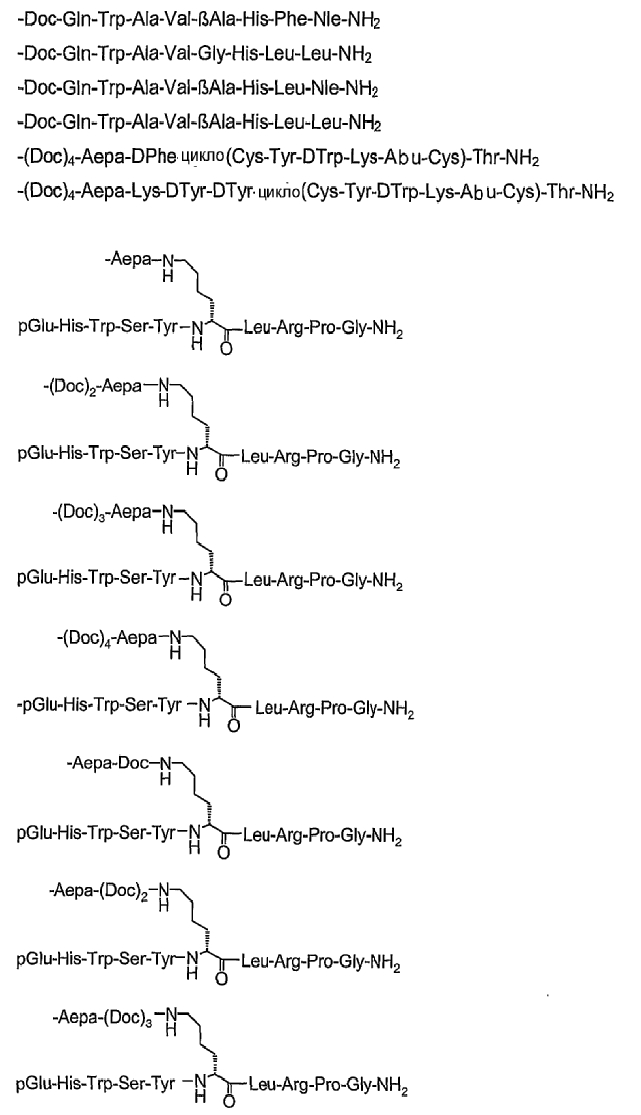
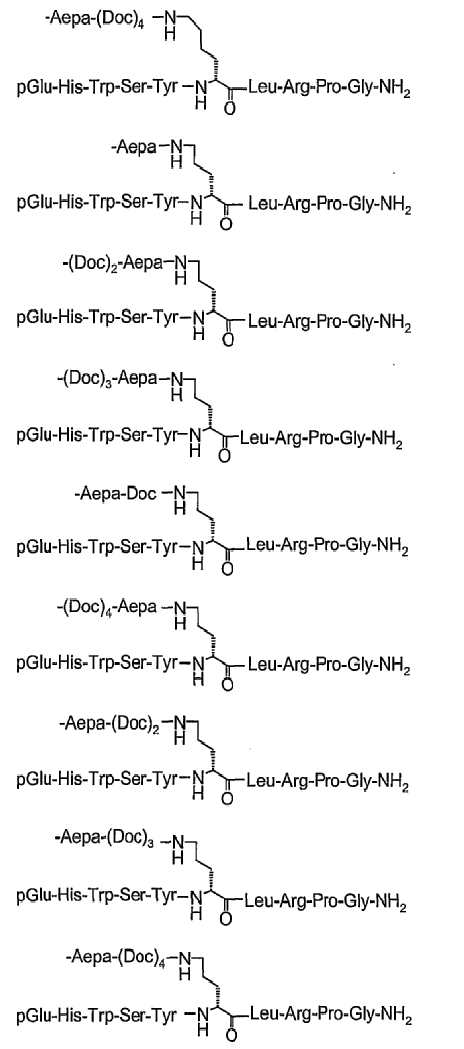



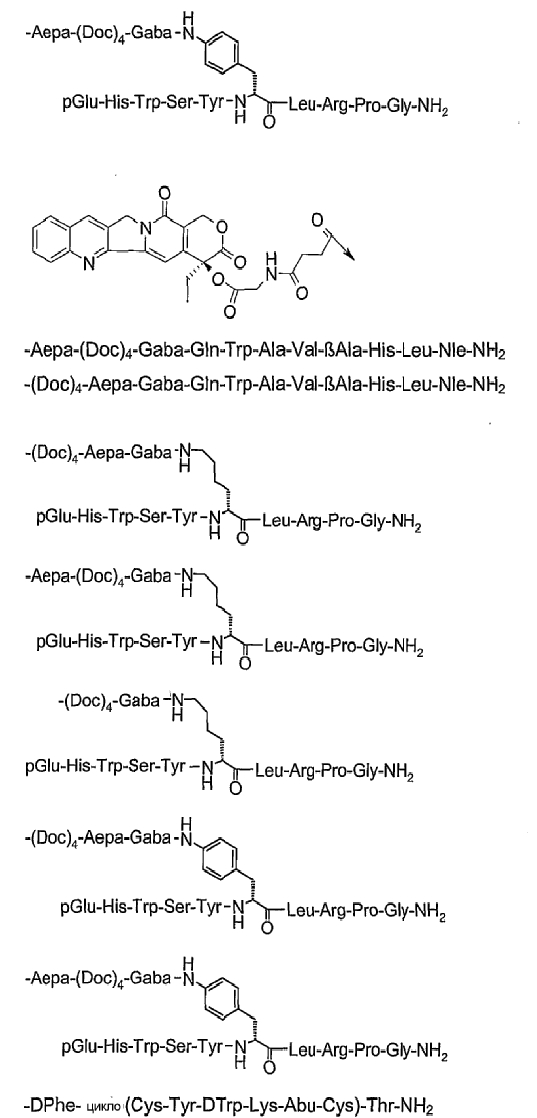
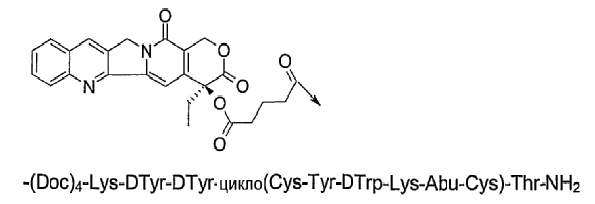
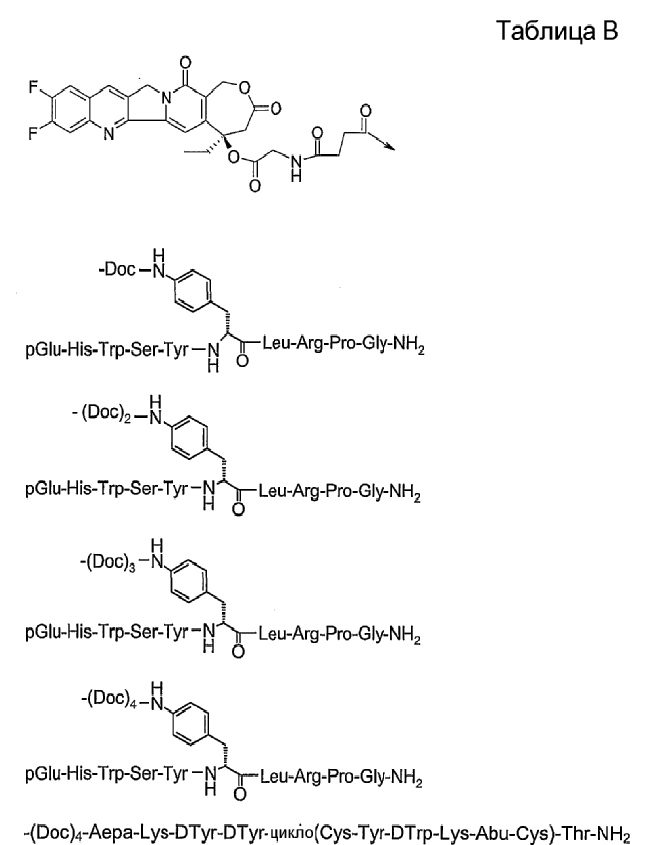





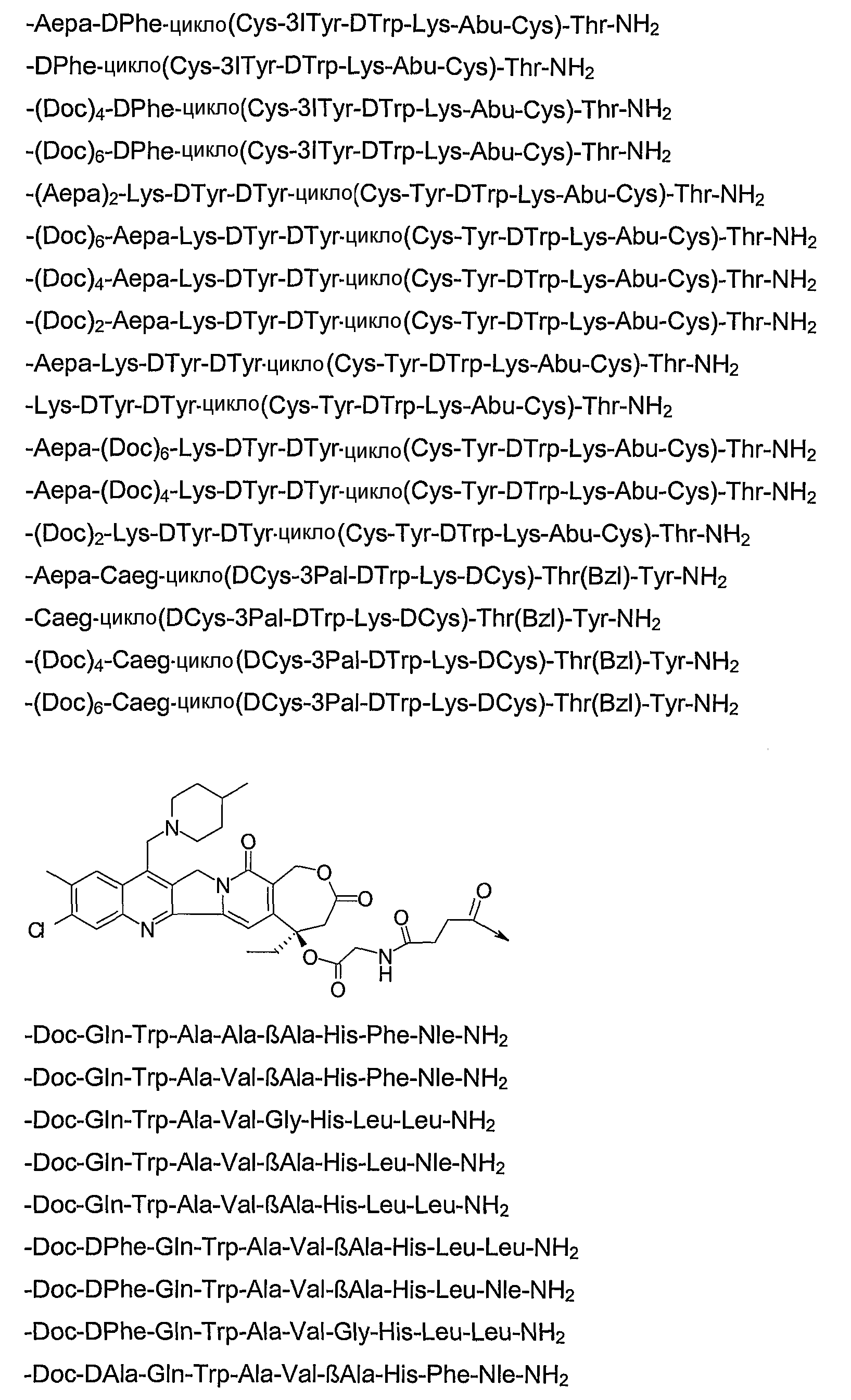



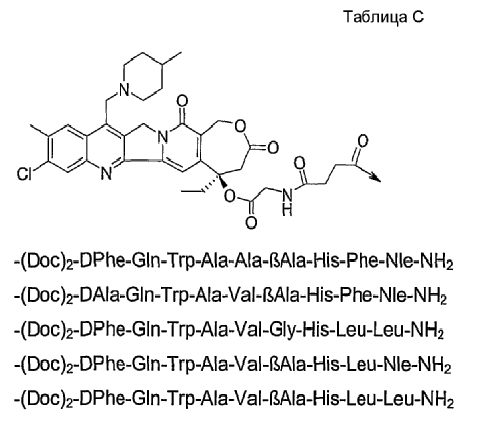


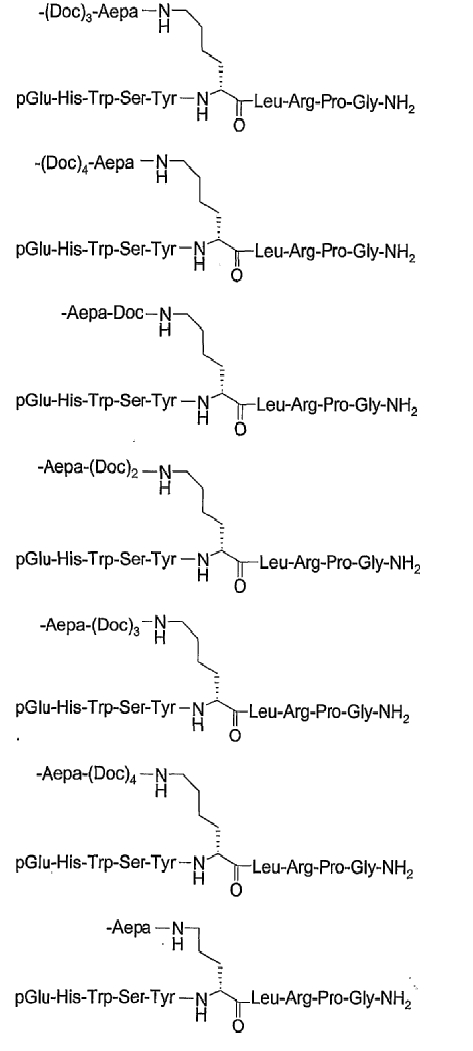

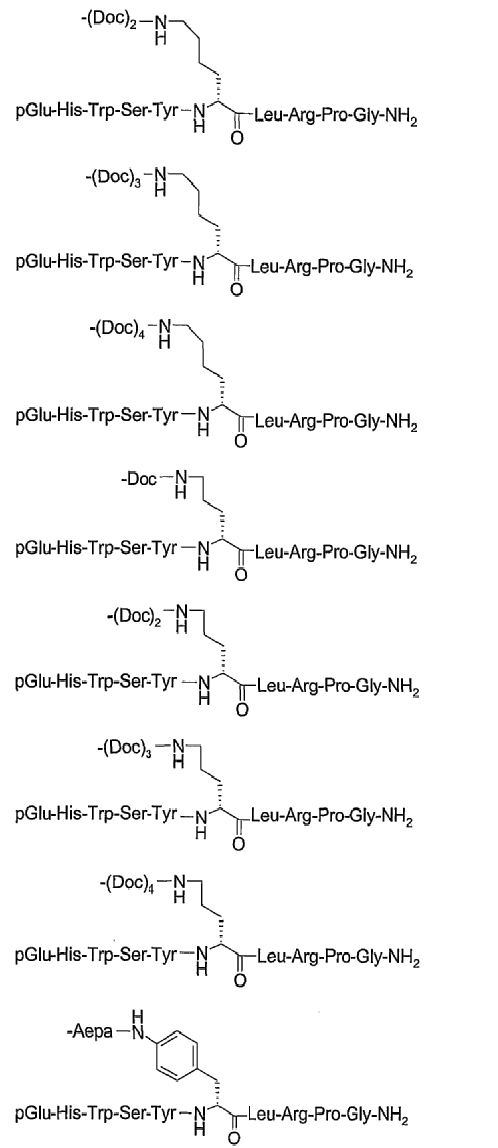
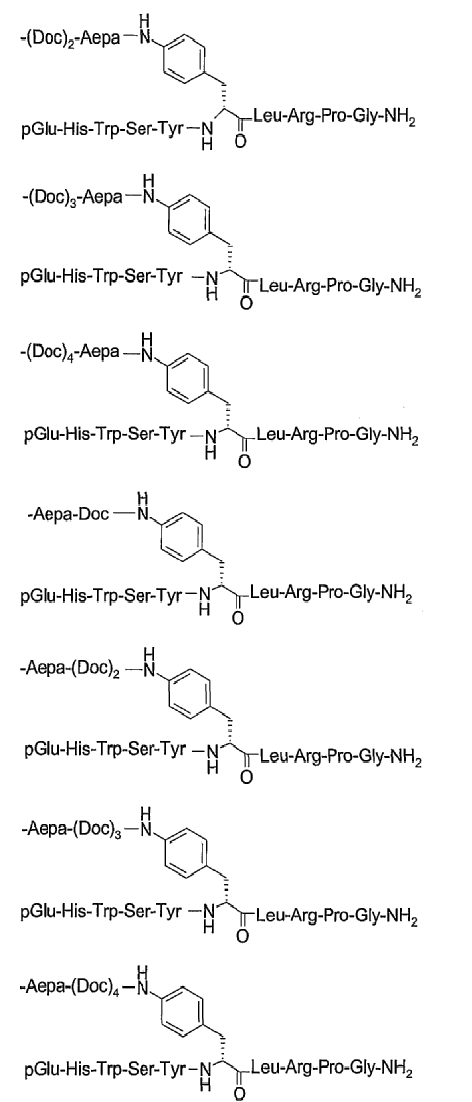








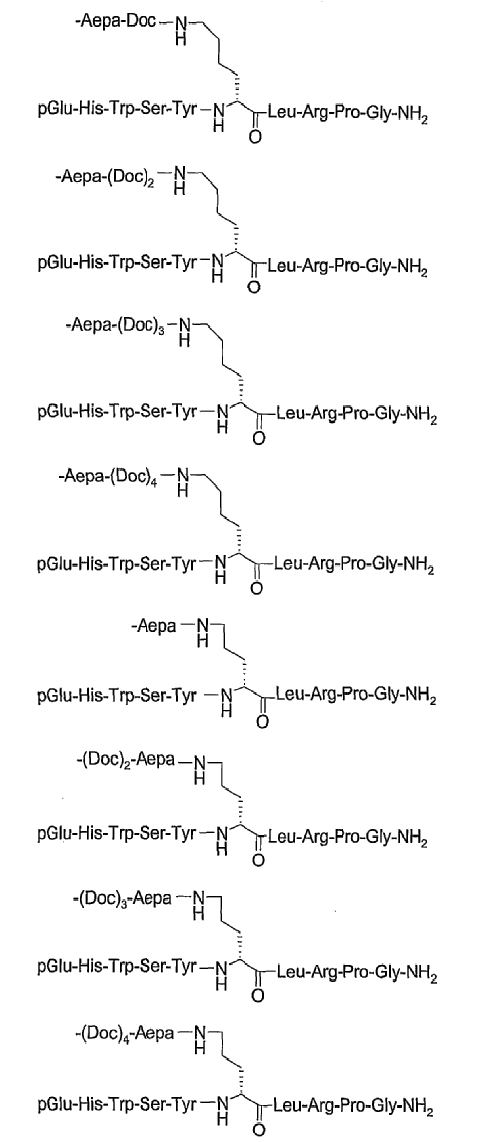

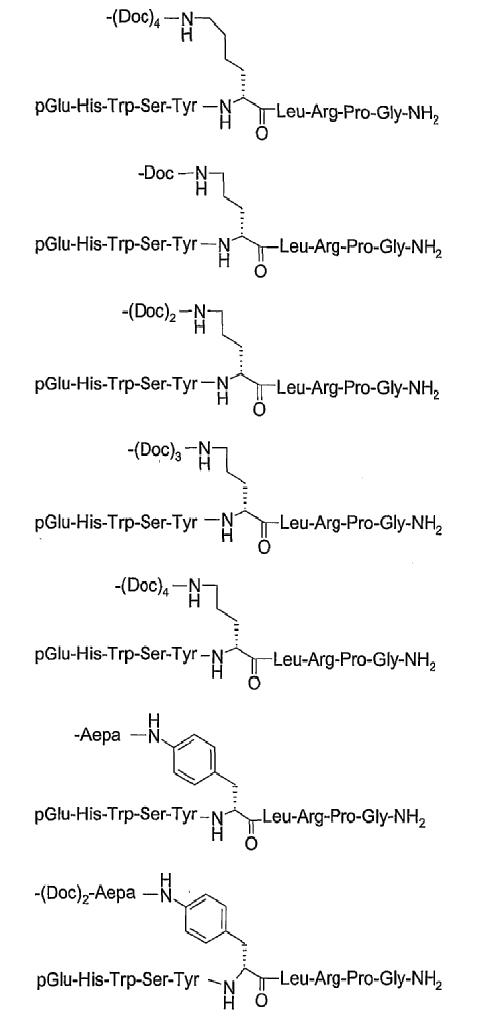
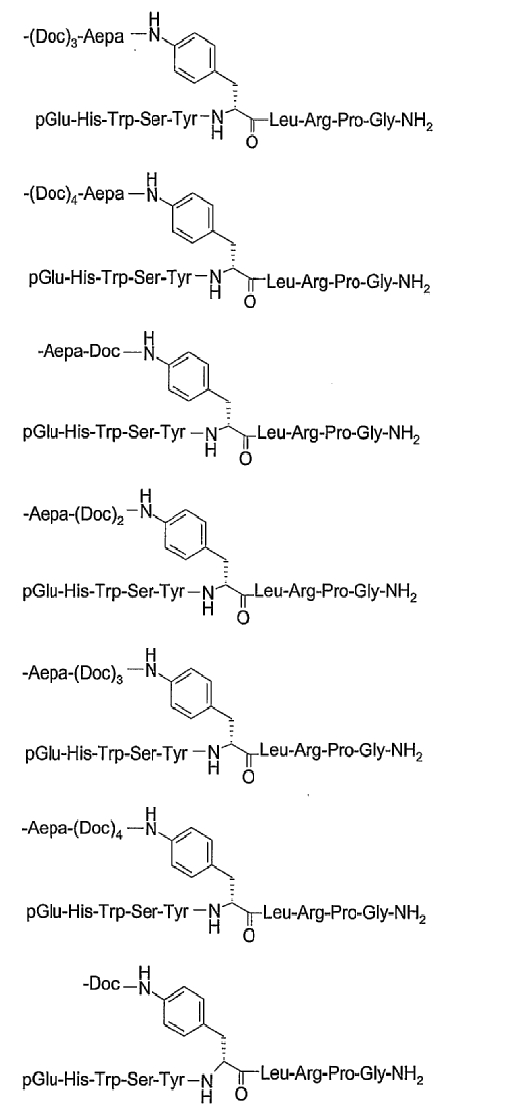




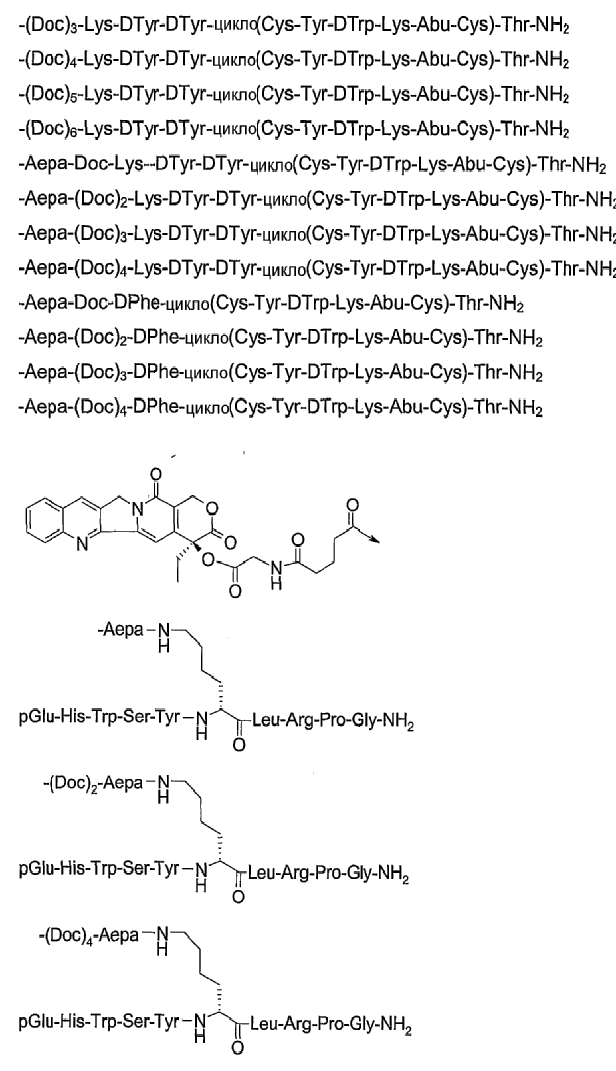
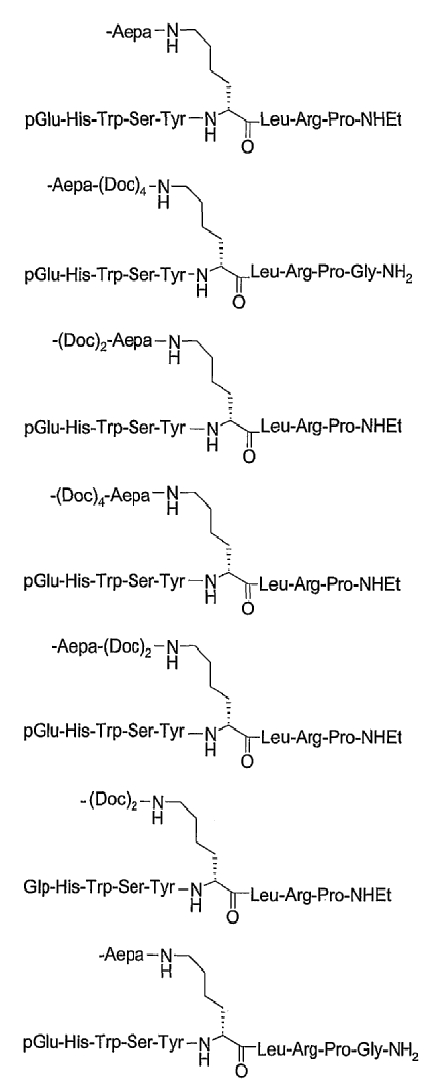
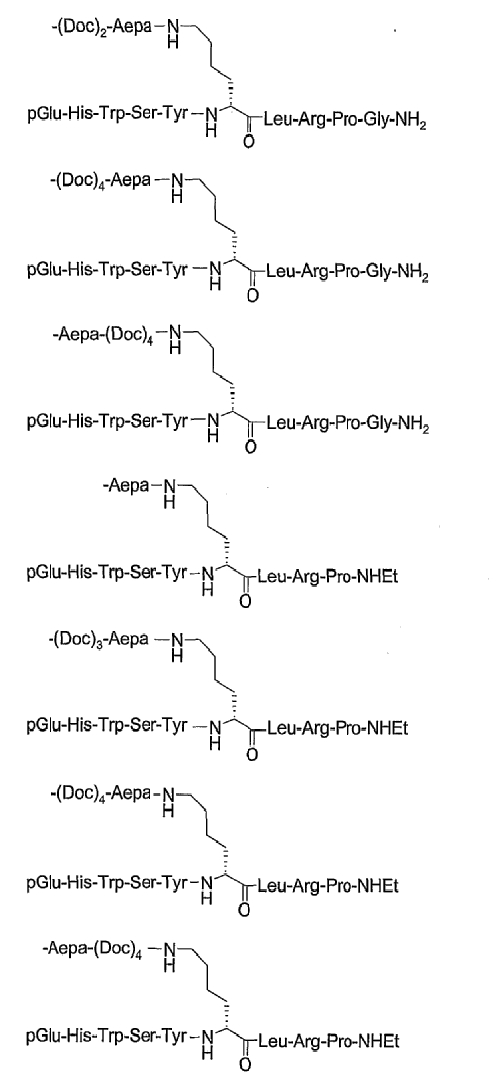
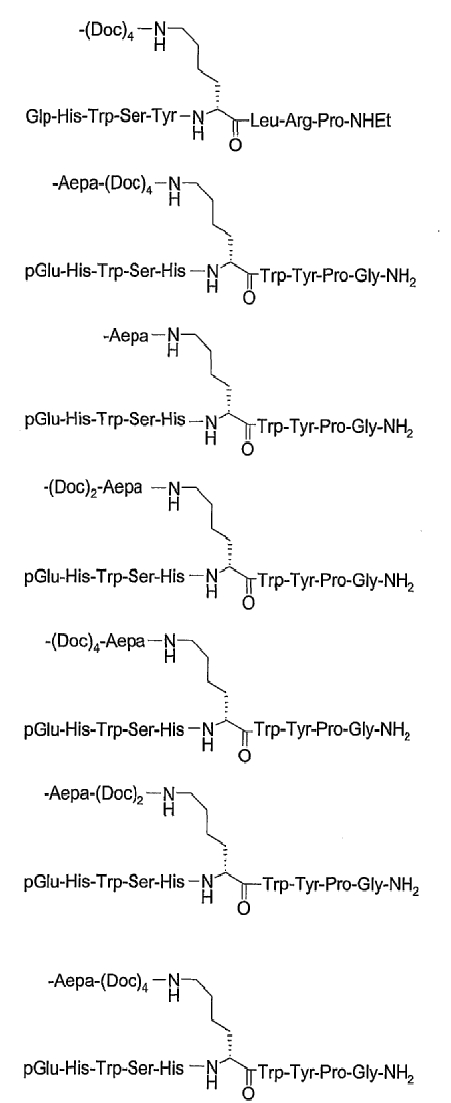
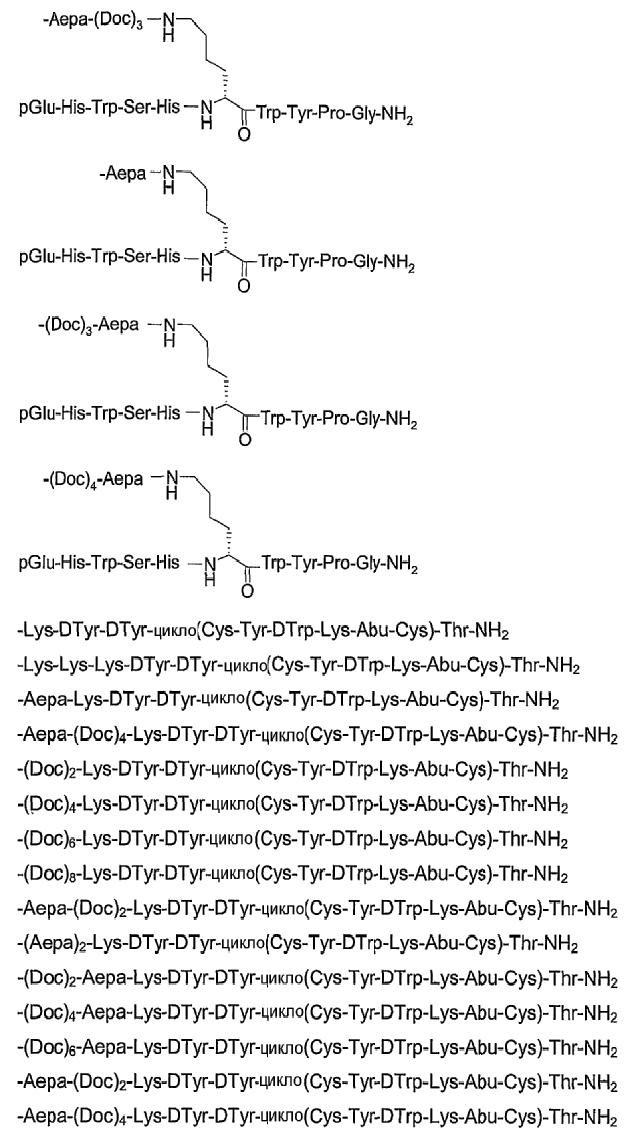
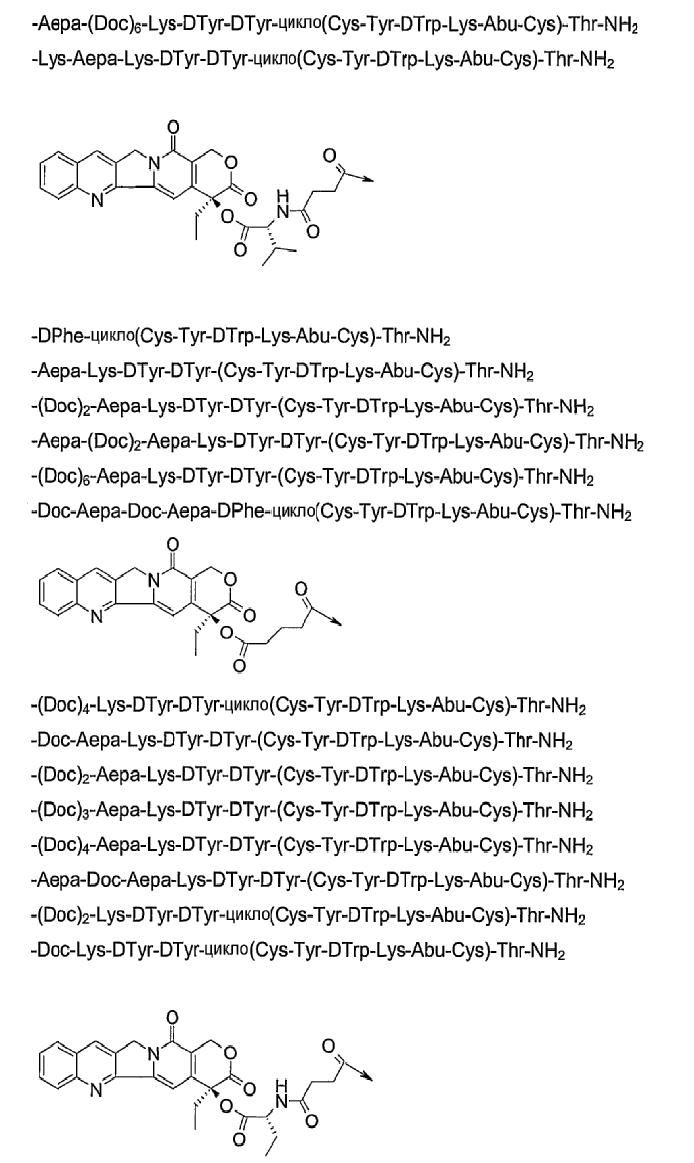
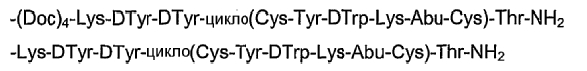

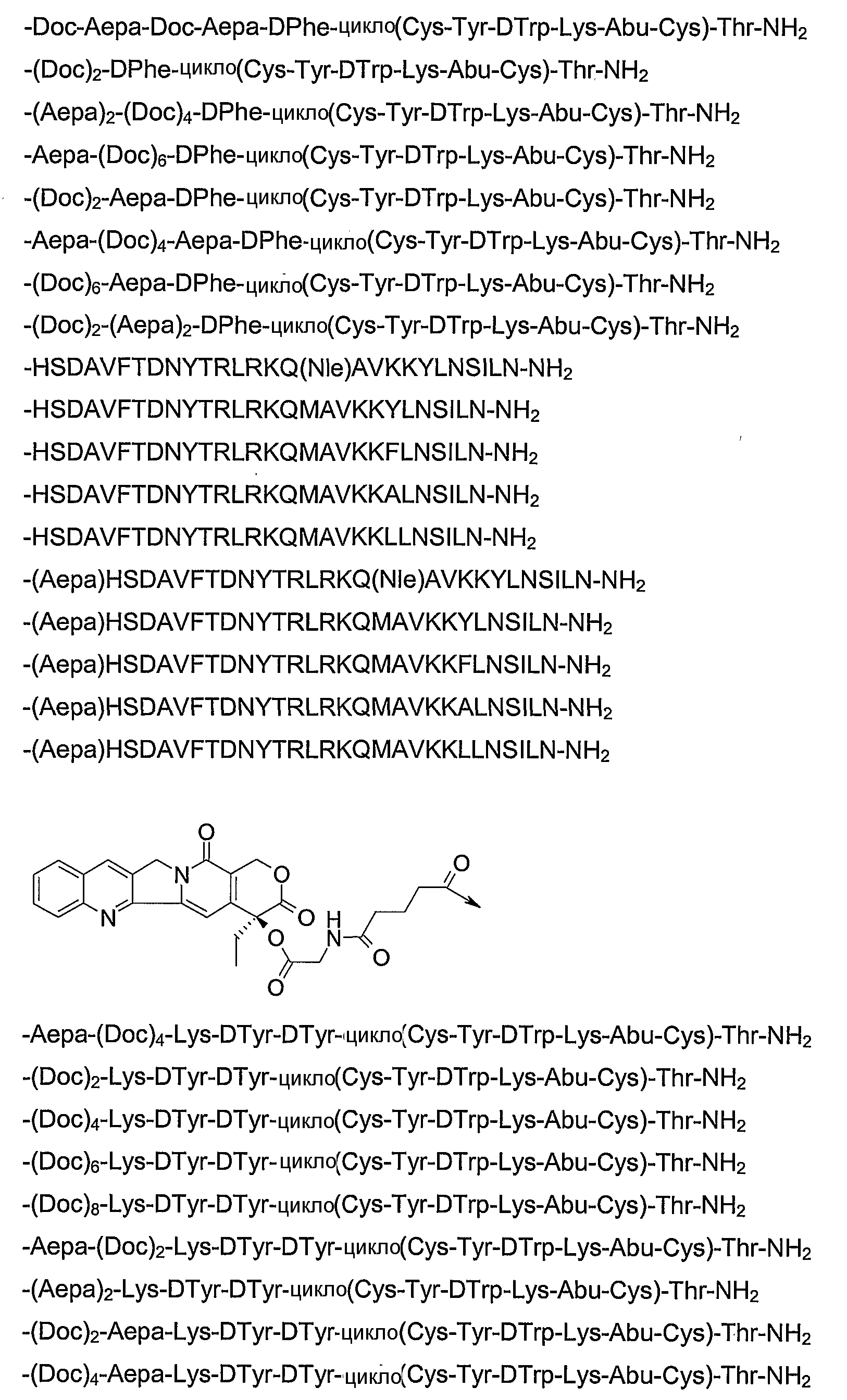
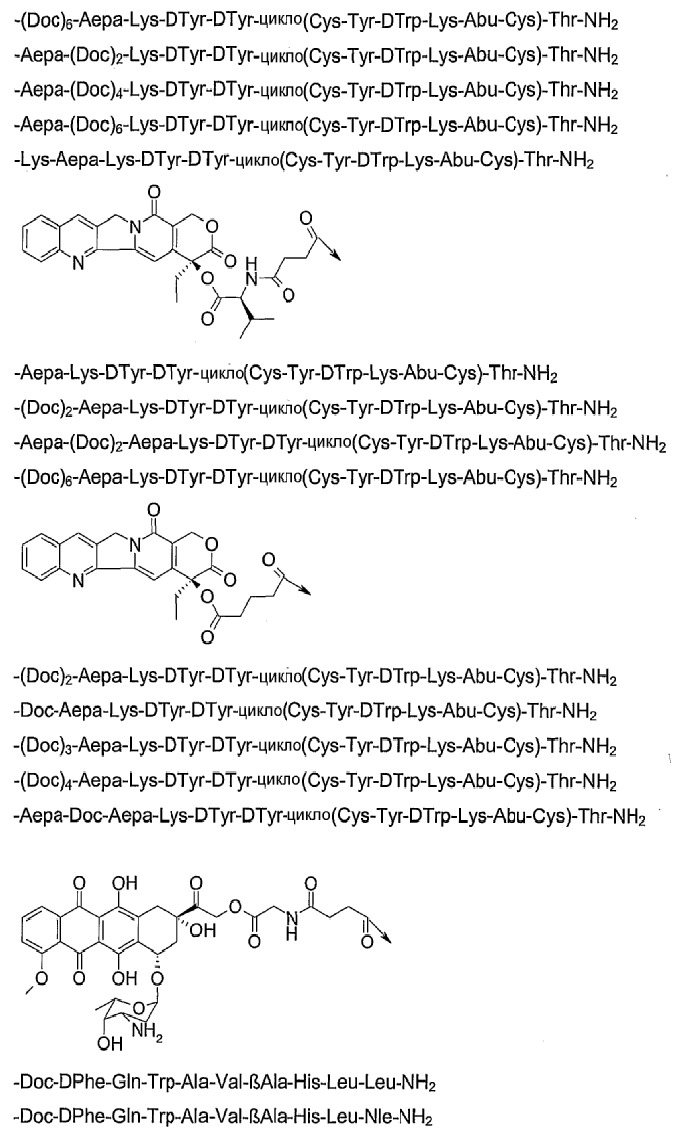






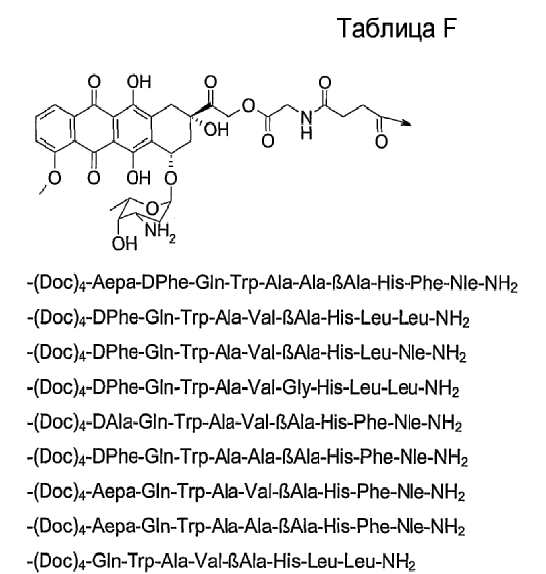


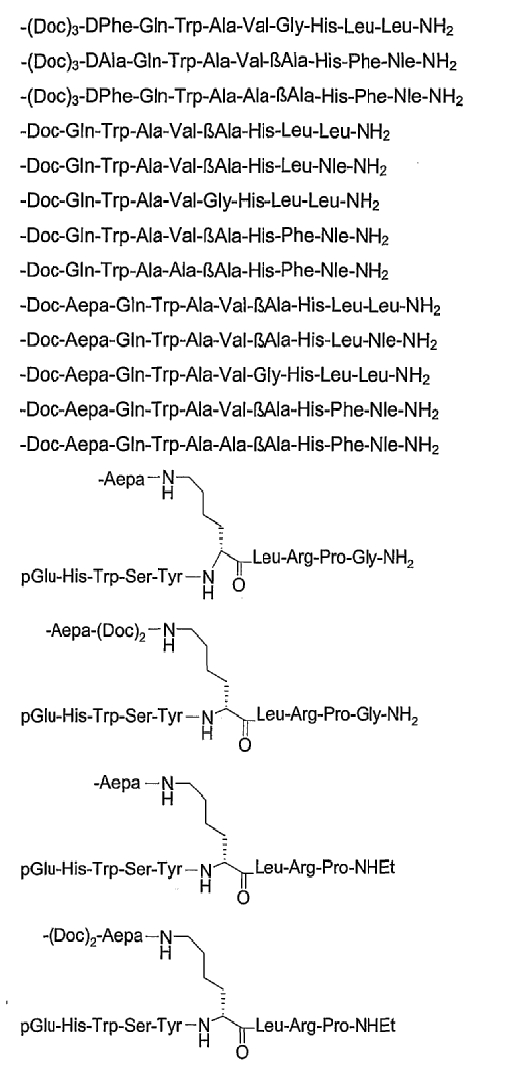
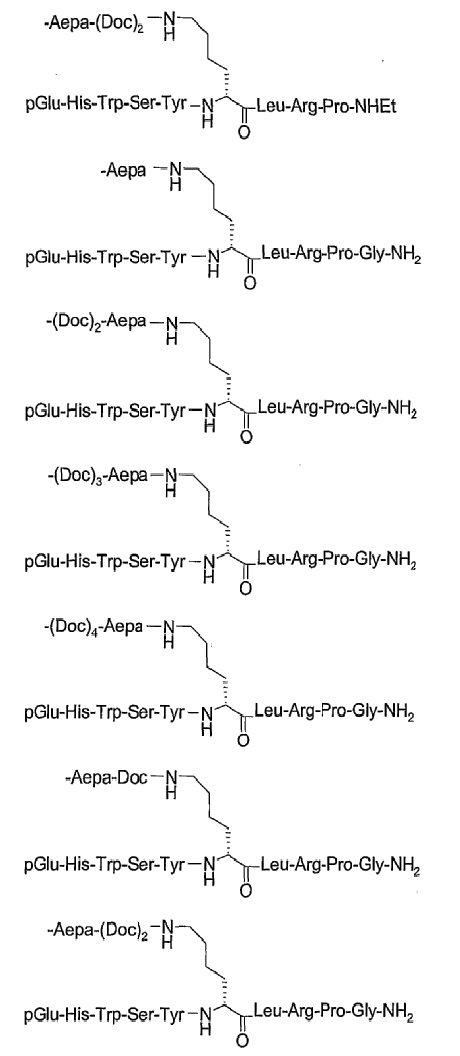
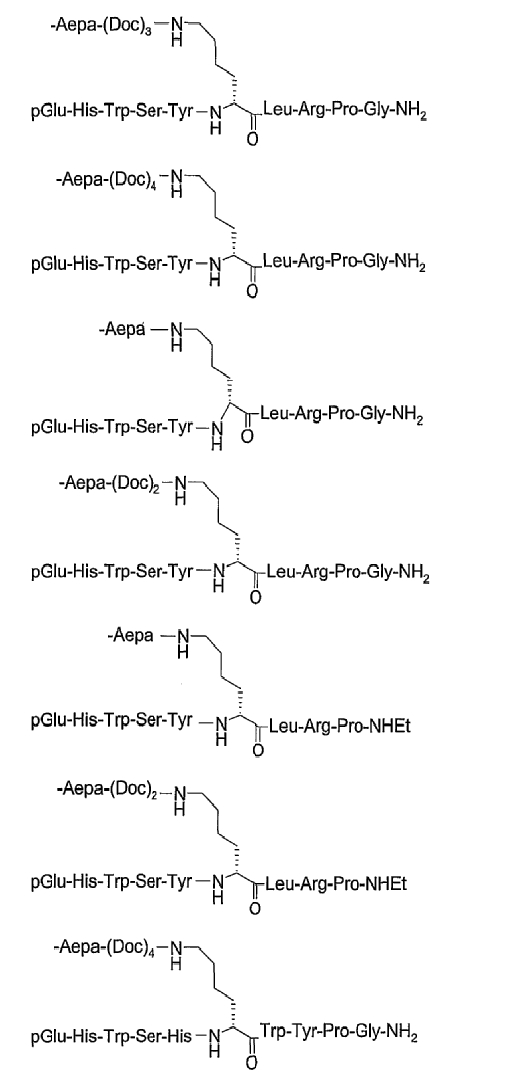
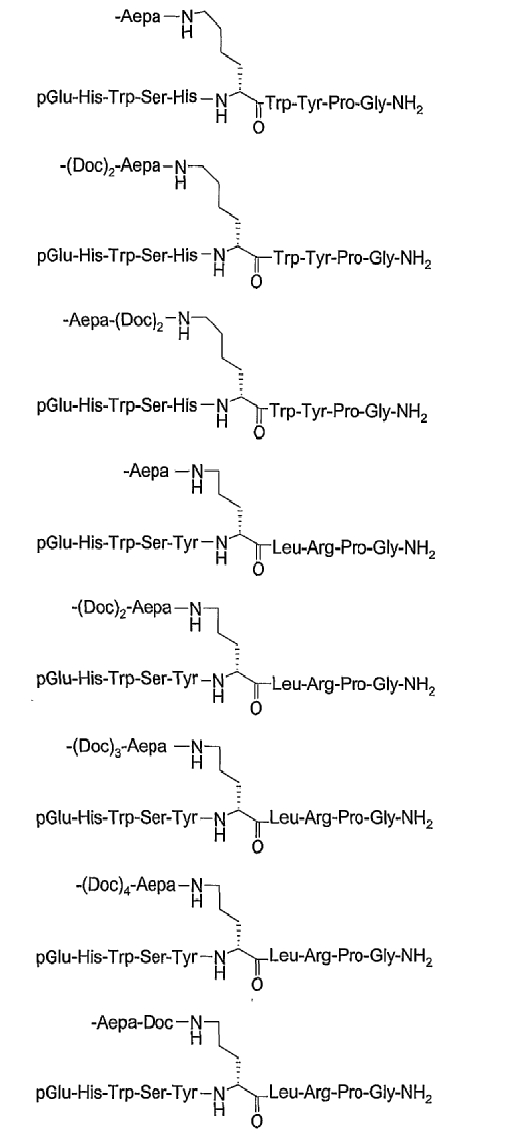
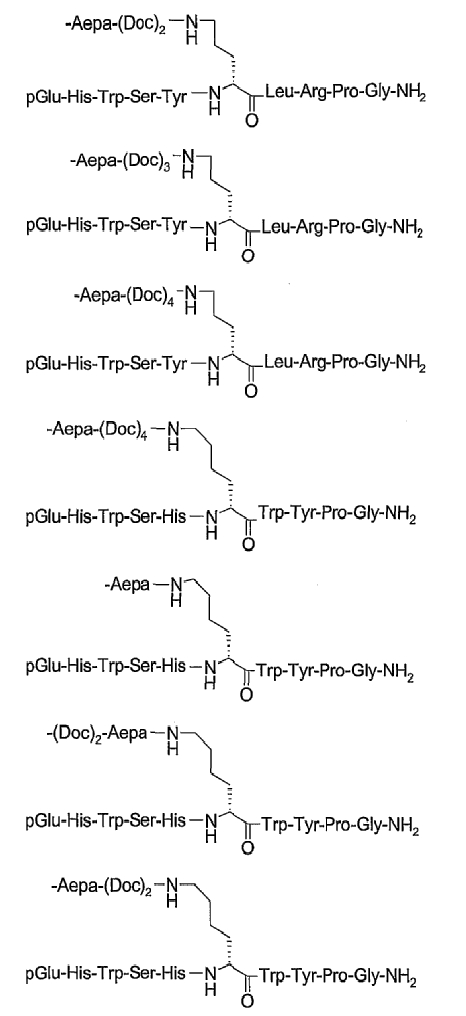
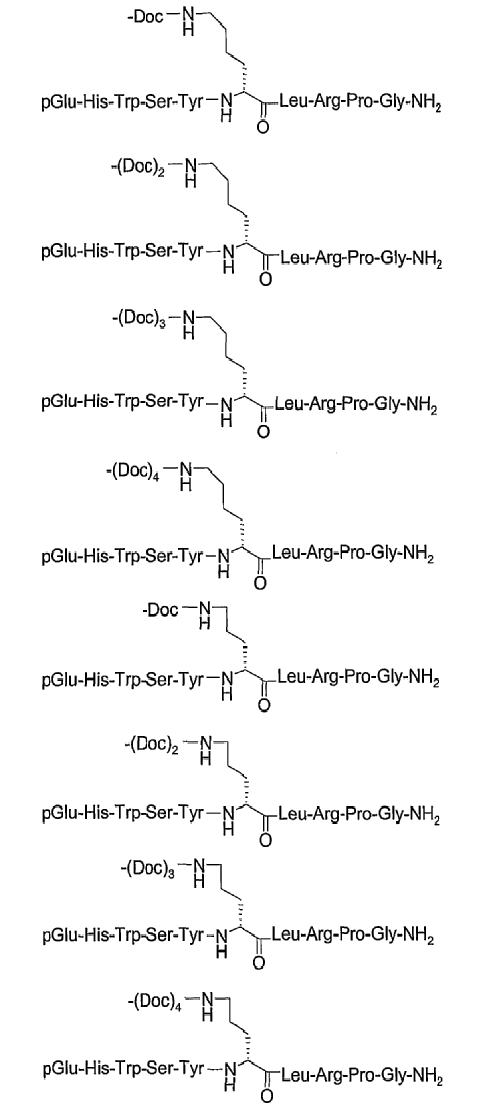
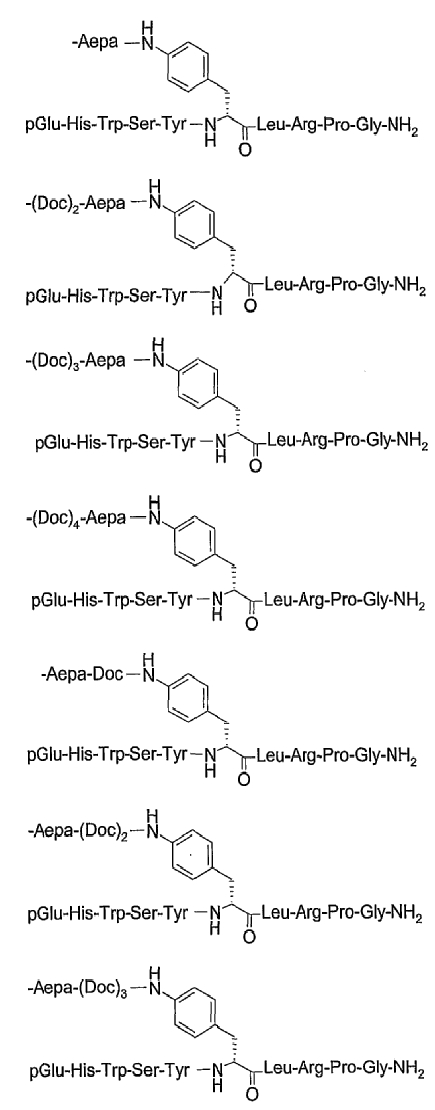
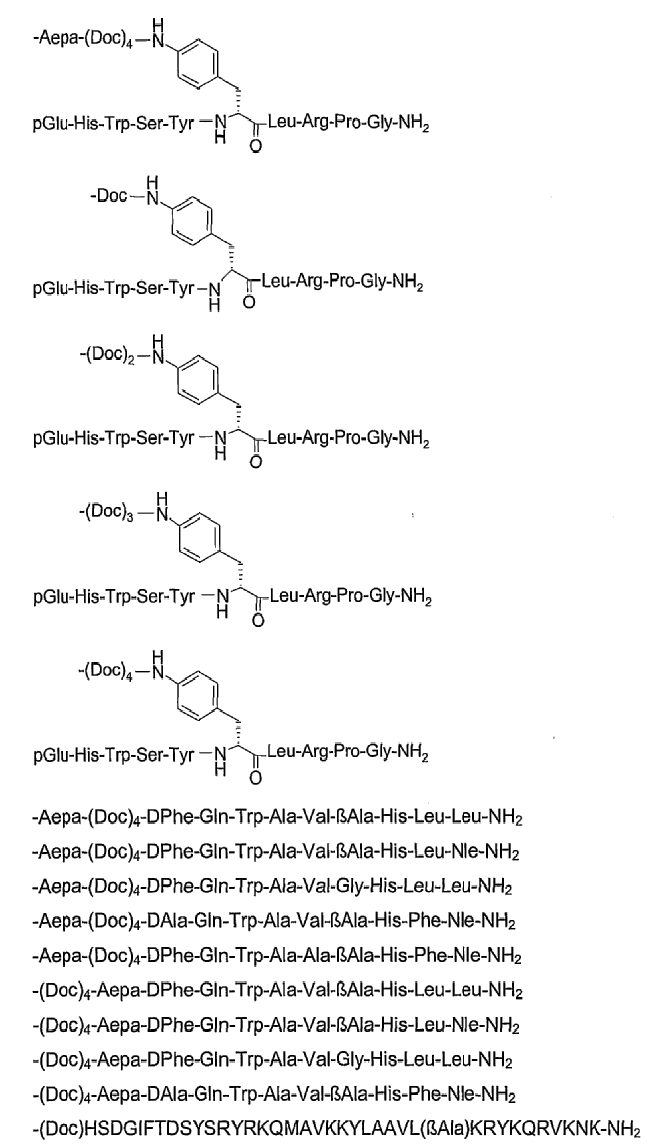
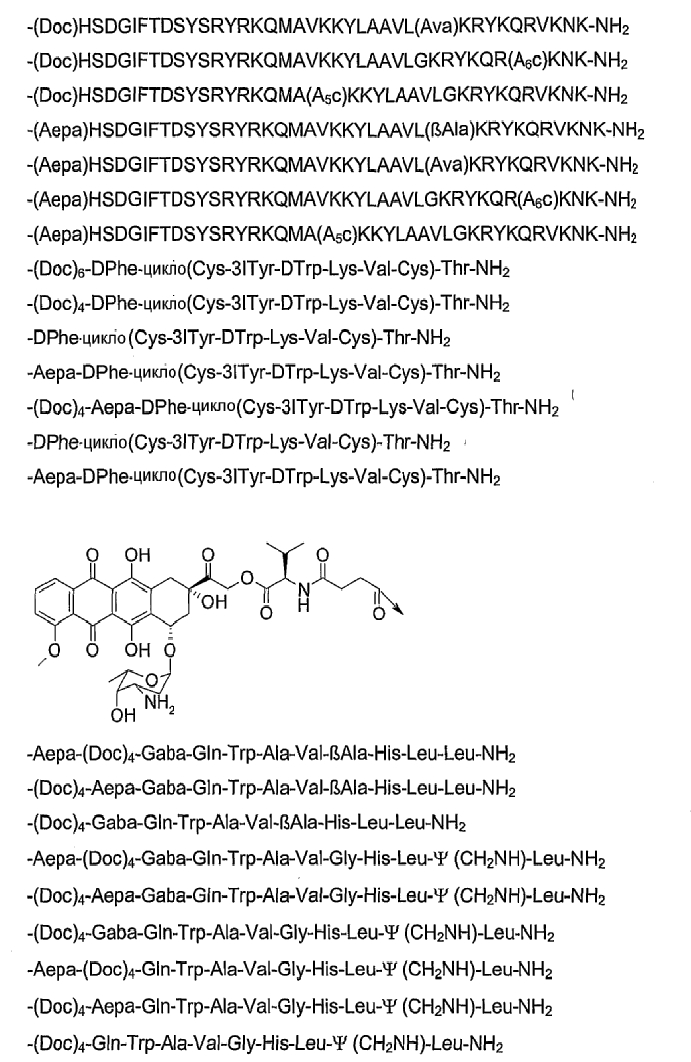
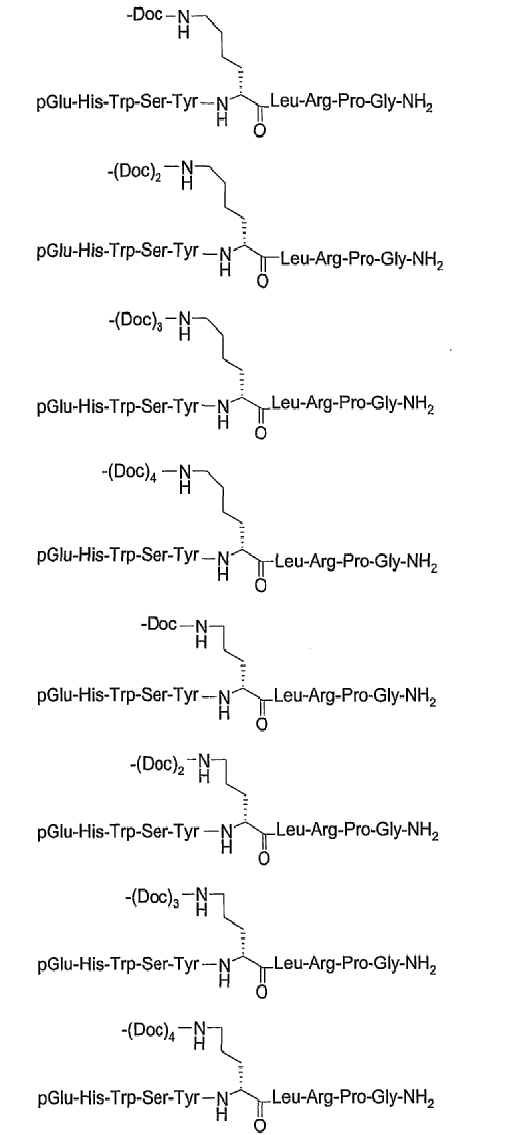
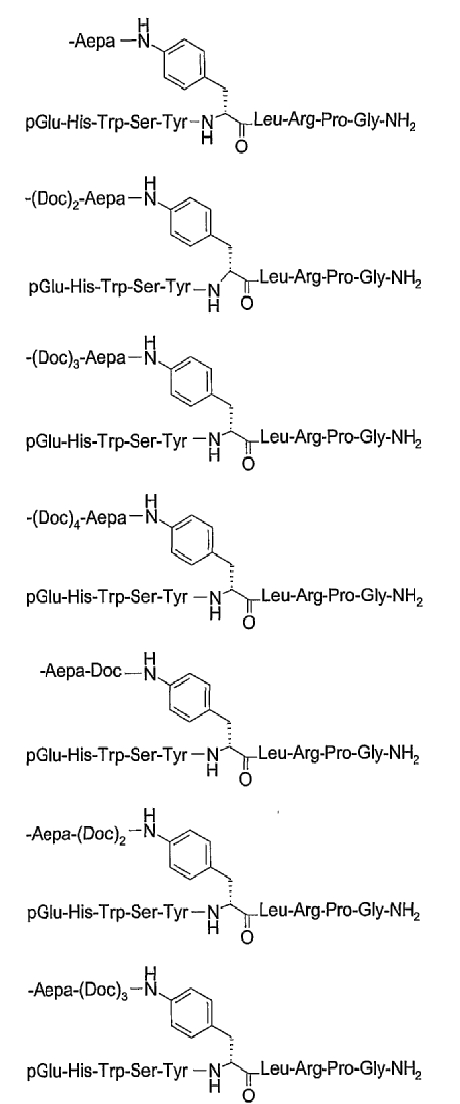
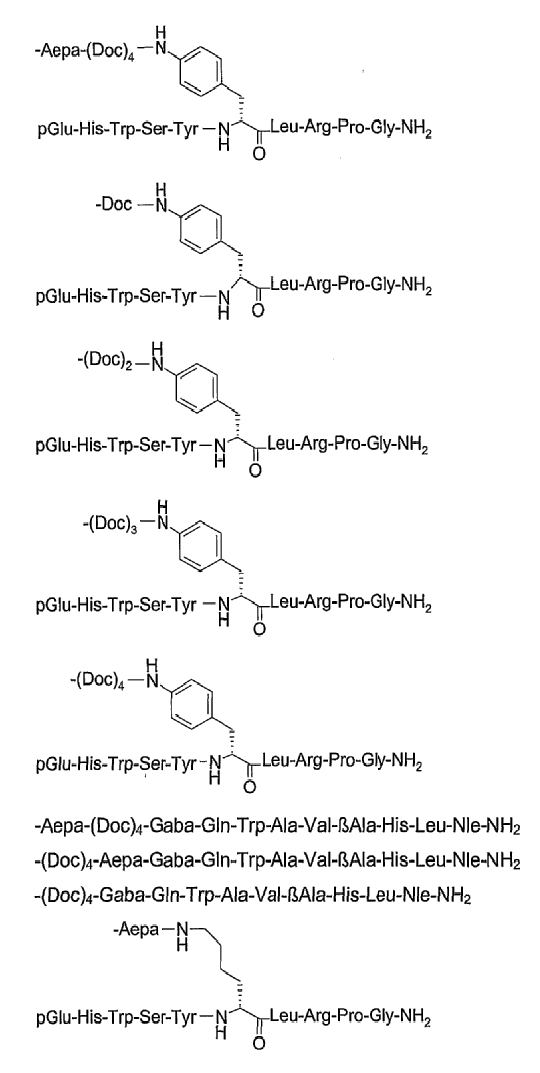
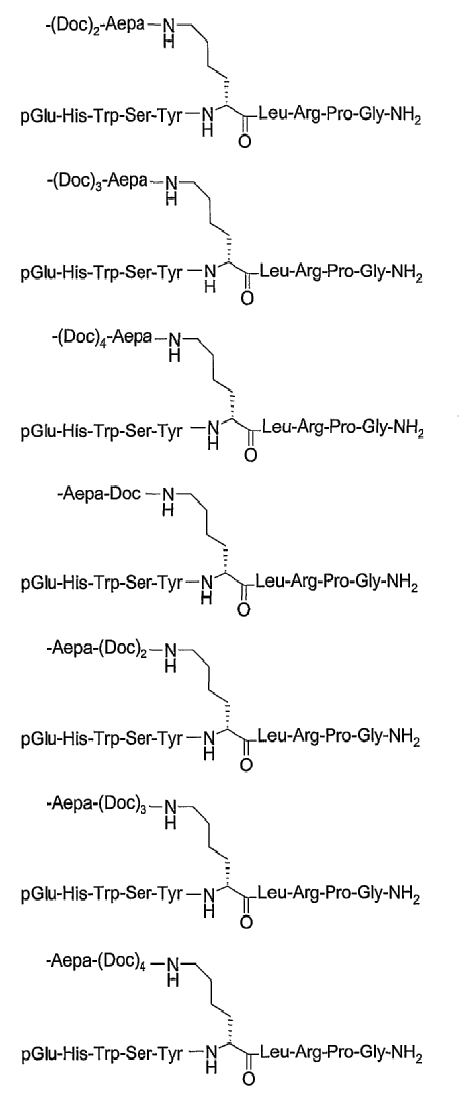
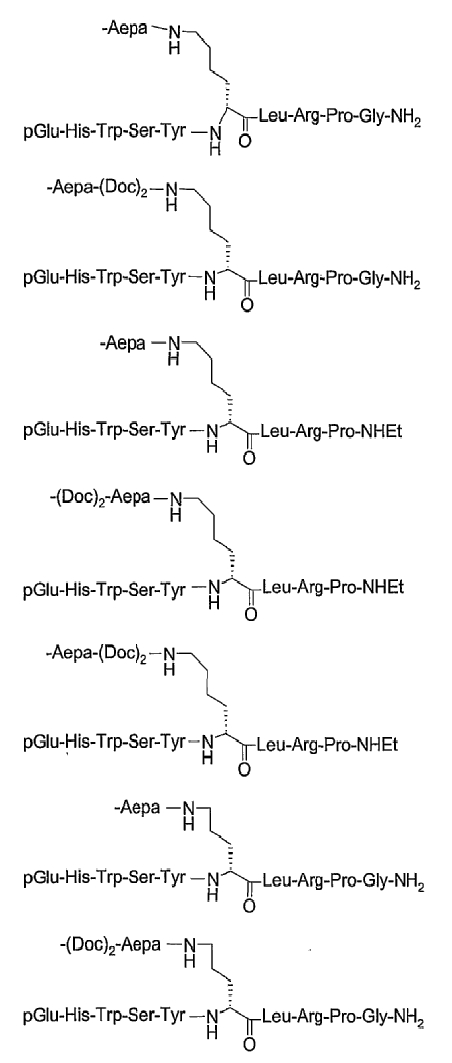
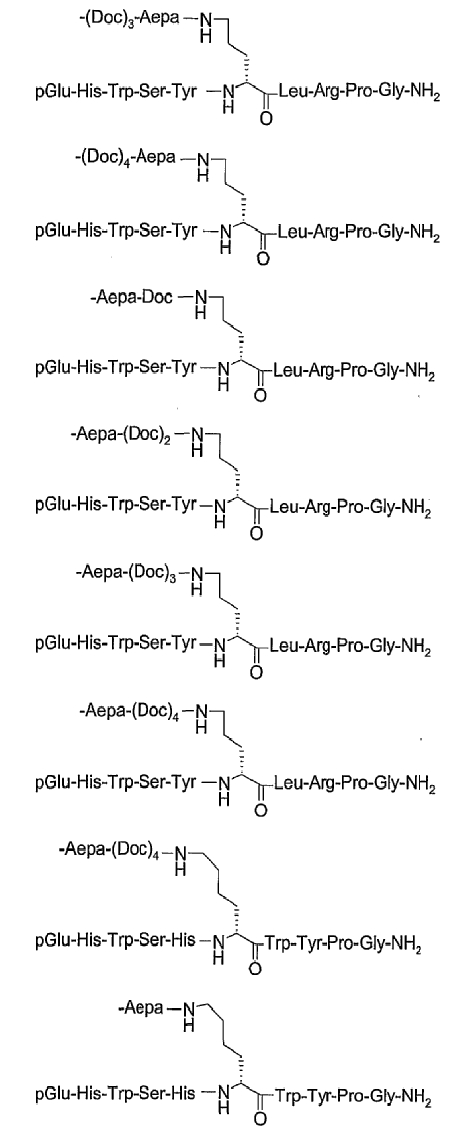
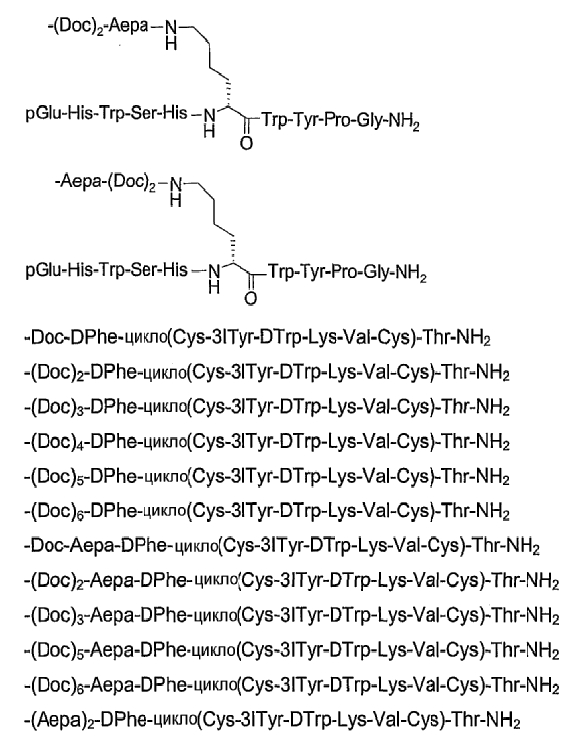
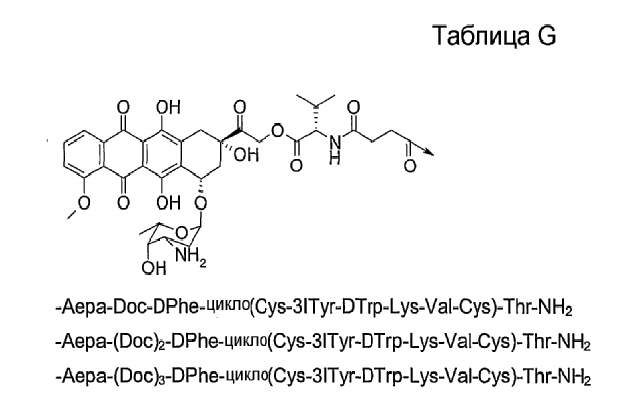








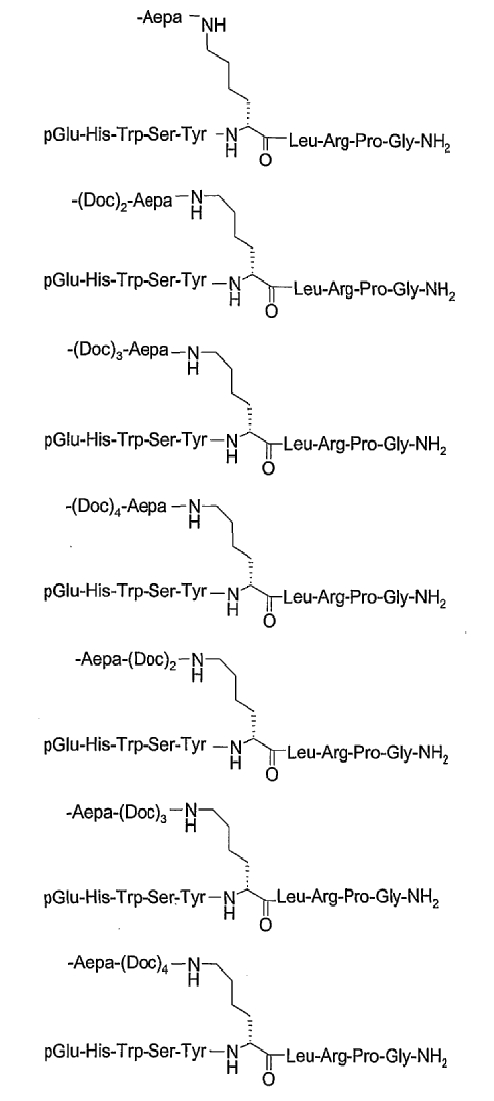
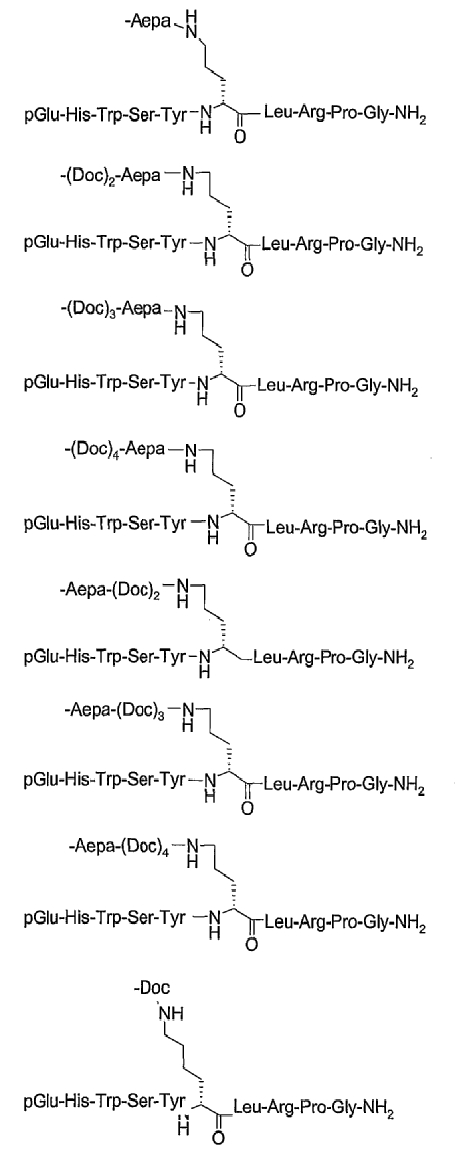
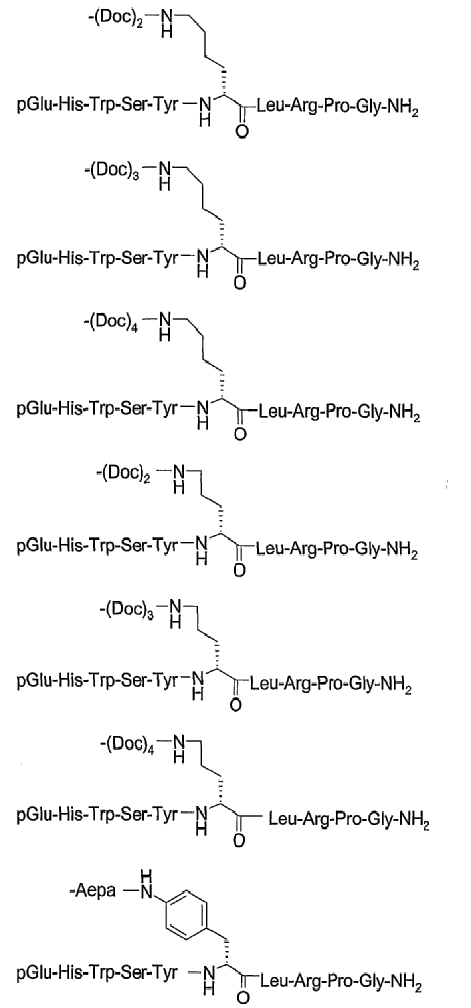
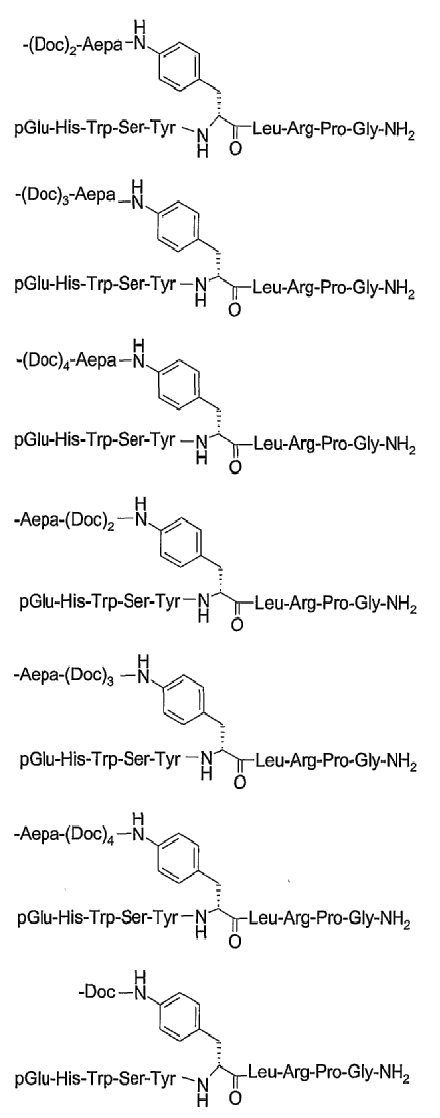

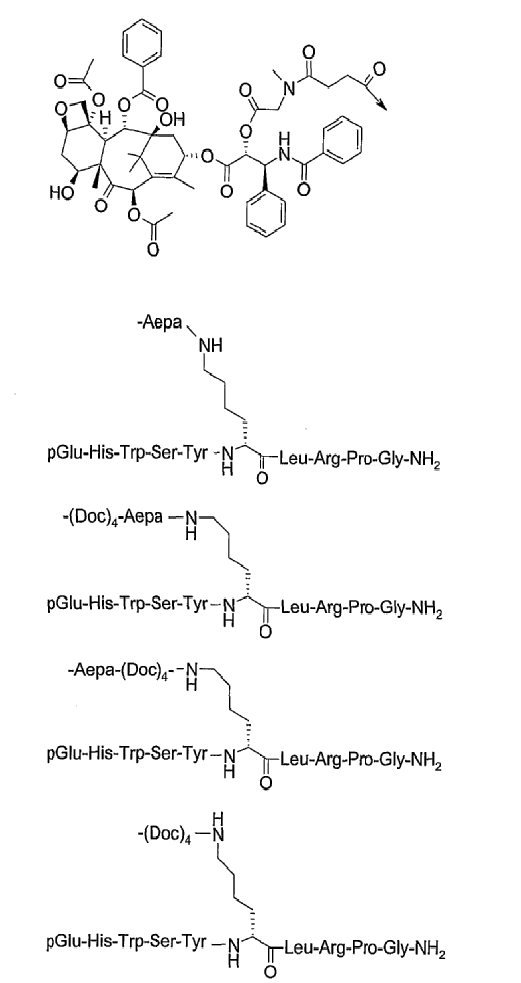
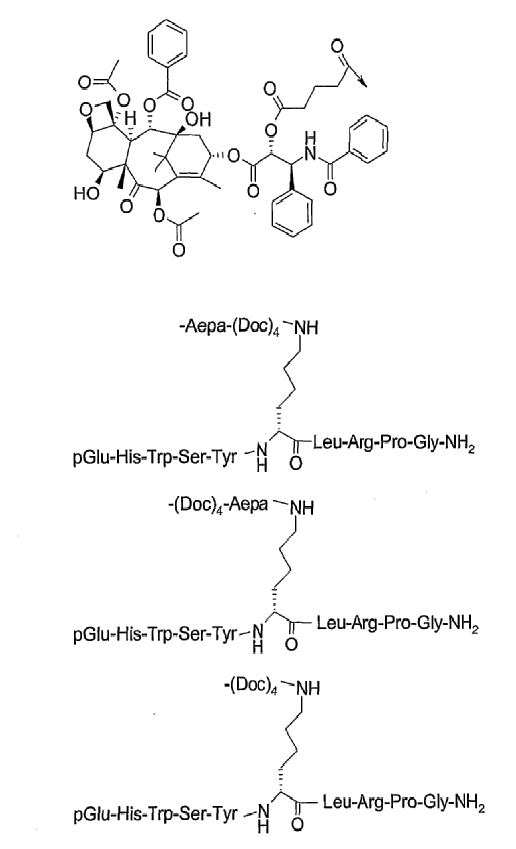
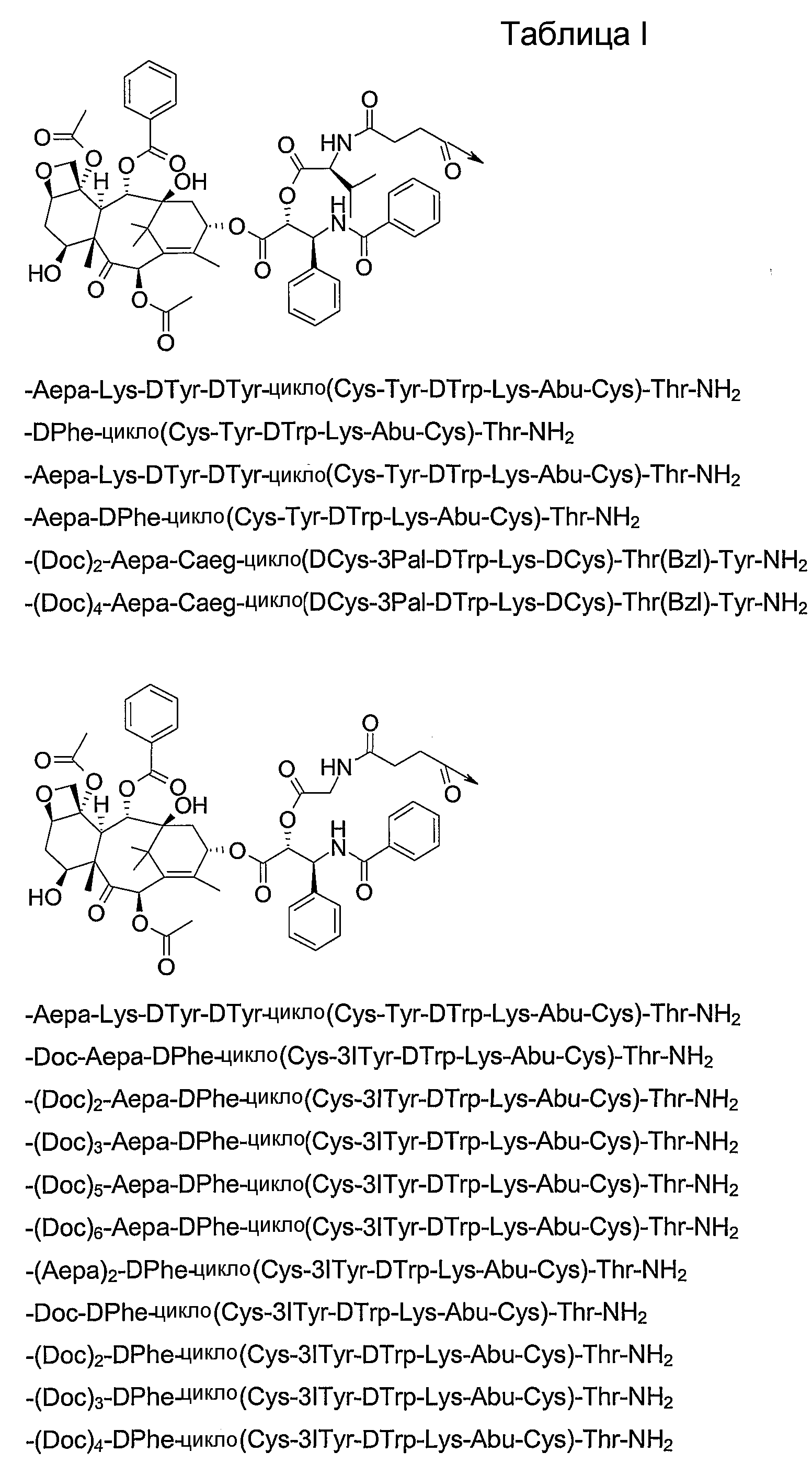



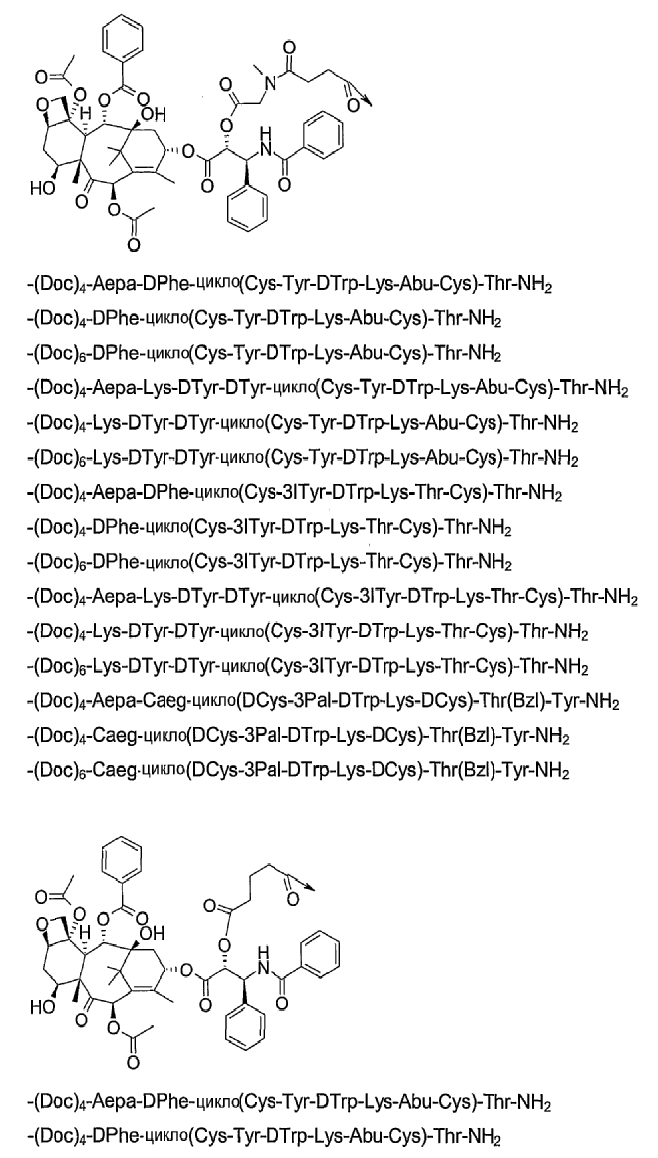

20. Фармацевтическая композиция, содержащая эффективное количество соединения по любому из пп.1-19 или его фармацевтически приемлемой соли и фармацевтически приемлемый носитель.
21. Способ лечения заболевания у субъекта, нуждающегося в этом, предусматривающий введение указанному субъекту терапевтически эффективного количества соединения по любому из пп.1-19 или его фармацевтически приемлемой соли, где указанное заболевание выбрано из группы, состоящей из фиброза, доброкачественной гиперплазии предстательной железы, атеросклероза, рестеноза, рака молочной железы, рака ободочной кишки, рака поджелудочной железы, рака предстательной железы, рака легкого, мелкоклеточного рака легкого, рака яичника, эпидермального рака и гемопоэтического рака.
22. Способ лечения заболевания у субъекта, нуждающегося в этом, предусматривающий введение указанному субъекту терапевтически эффективного количества соединения по любому из пп.1-19 или его фармацевтически приемлемой соли, где указанное заболевание выбрано из группы, состоящей из доброкачественной гиперплазии предстательной железы, рестеноза, рака молочной железы, рака ободочной кишки, рака поджелудочной железы, рака предстательной железы, рака легкого, мелкоклеточного рака легкого, рака яичника, эпидермального рака и гемопоэтического рака.
23. Способ лечения заболевания у субъекта, нуждающегося в этом, предусматривающий введение указанному субъекту терапевтически эффективного количества соединения по п.1 или его фармацевтически приемлемой соли, где указанное заболевание характеризуется нежелательной пролиферацей клеток, которые экспрессируют один или несколько рецепторов соматостатинового типа.
24. Способ лечения заболевания у субъекта, нуждающегося в этом, предусматривающий введение указанному субъекту терапевтически эффективного количества соединения по п.1 или его фармацевтически приемлемой соли, где указанное заболевание характеризуется нежелательной пролиферацей клеток, которые экспрессируют один или несколько рецепторов бомбезинового типа.
25. Способ лечения заболевания у субъекта, нуждающегося в этом, предусматривающий введение указанному субъекту терапевтически эффективного количества соединения по п.1 или его фармацевтически приемлемой соли, где указанное заболевание характеризуется нежелательной пролиферацей клеток, которые экспрессируют один или несколько рецепторов типа LHRH.
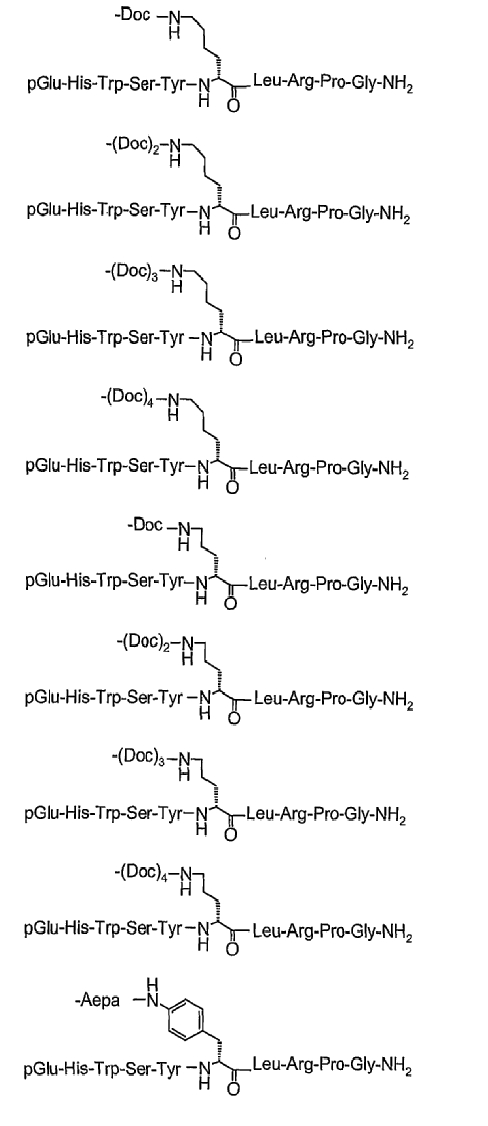
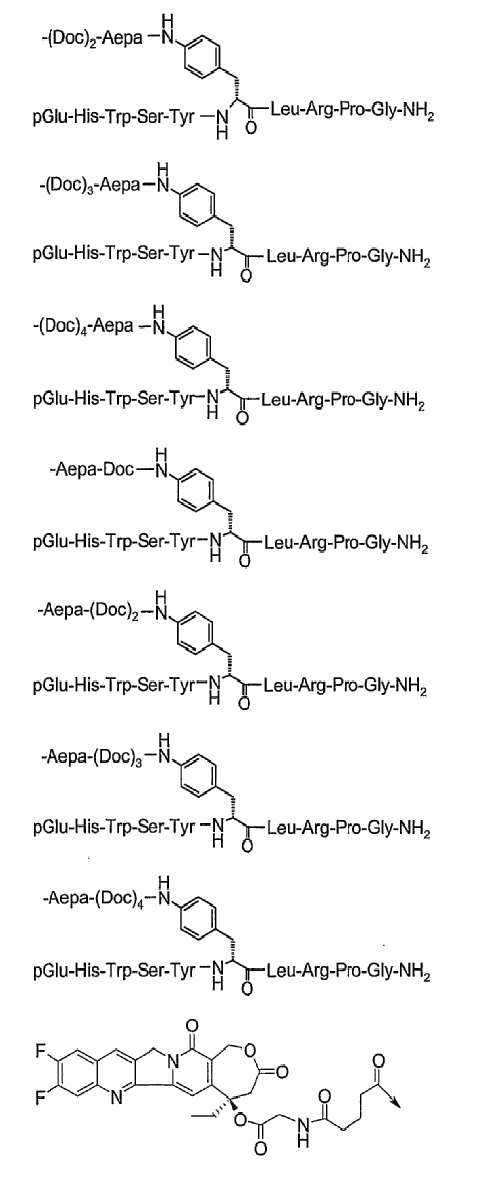
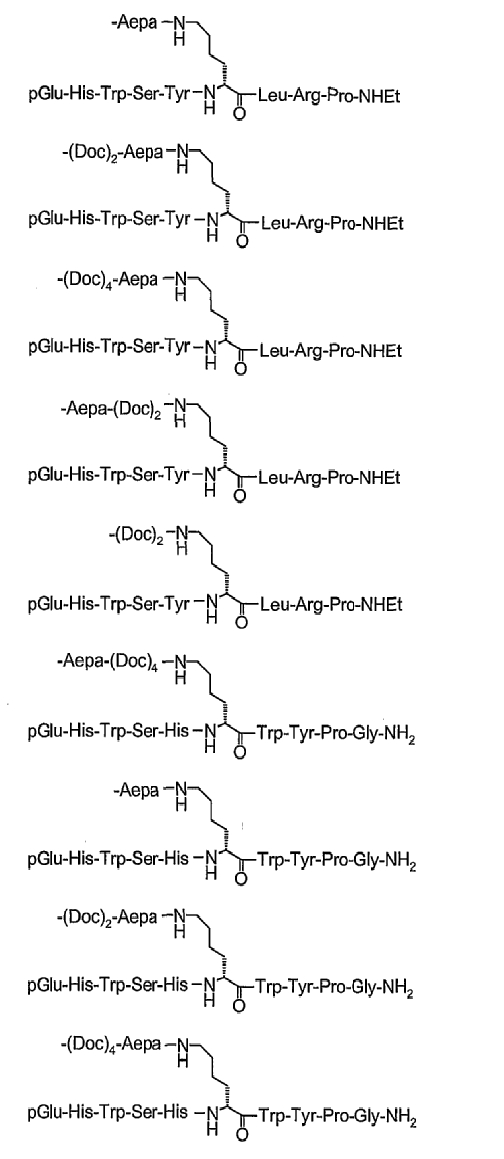
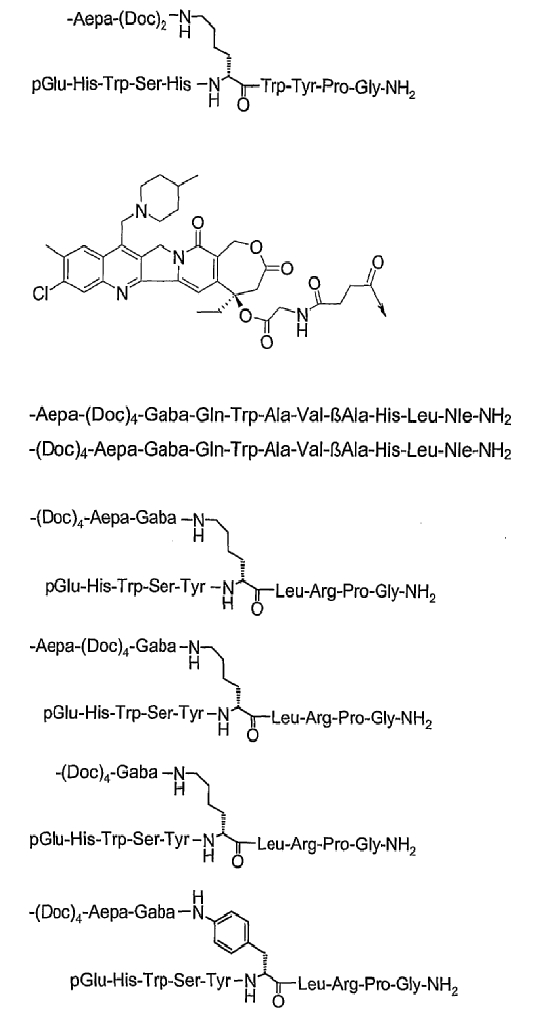
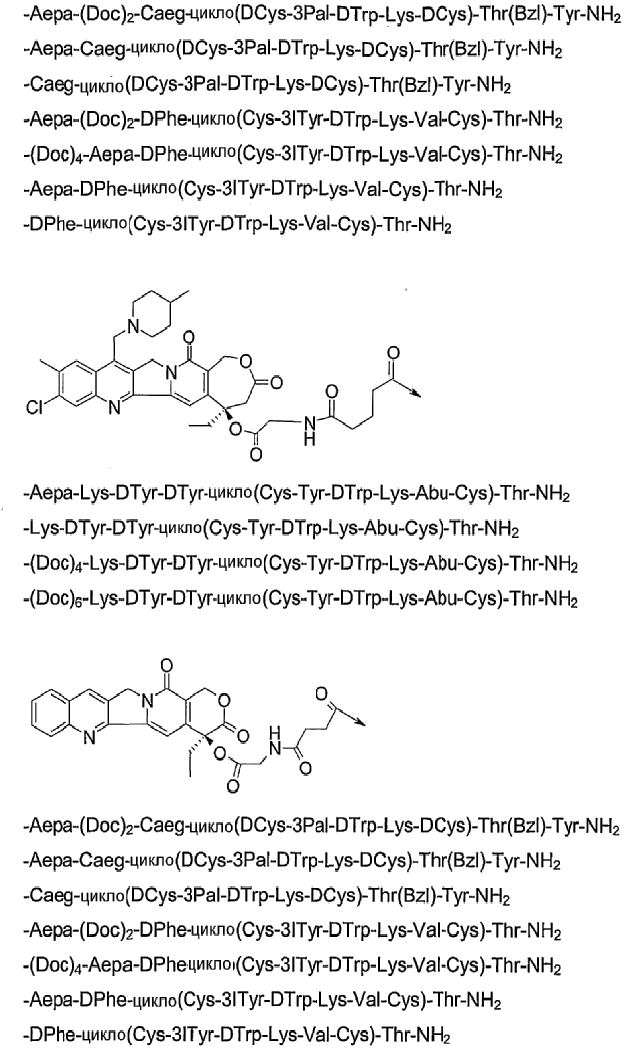
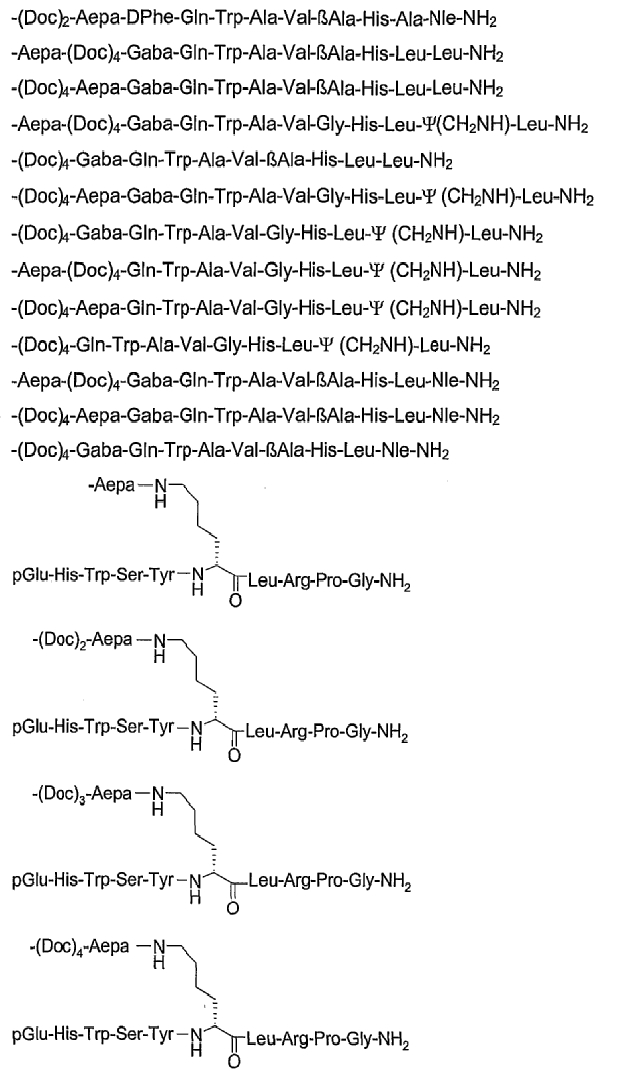
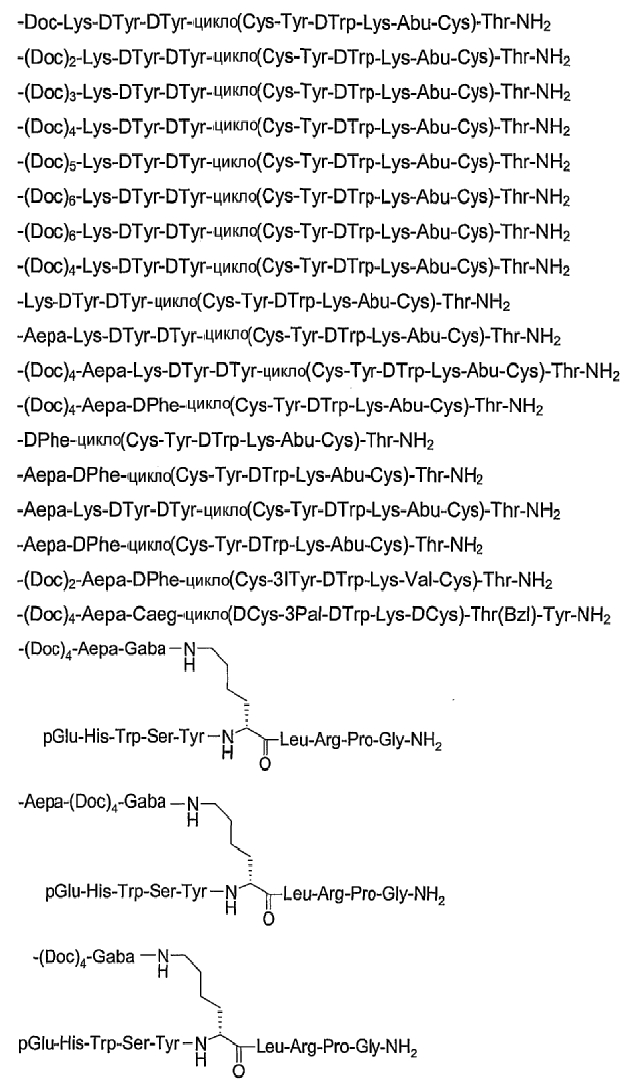
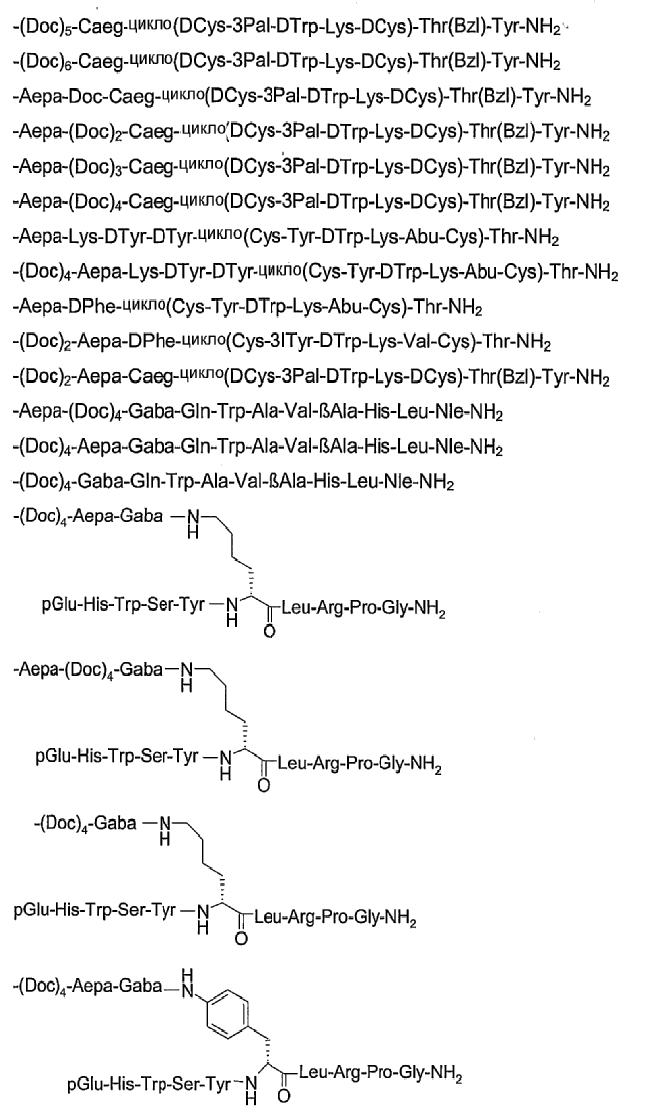
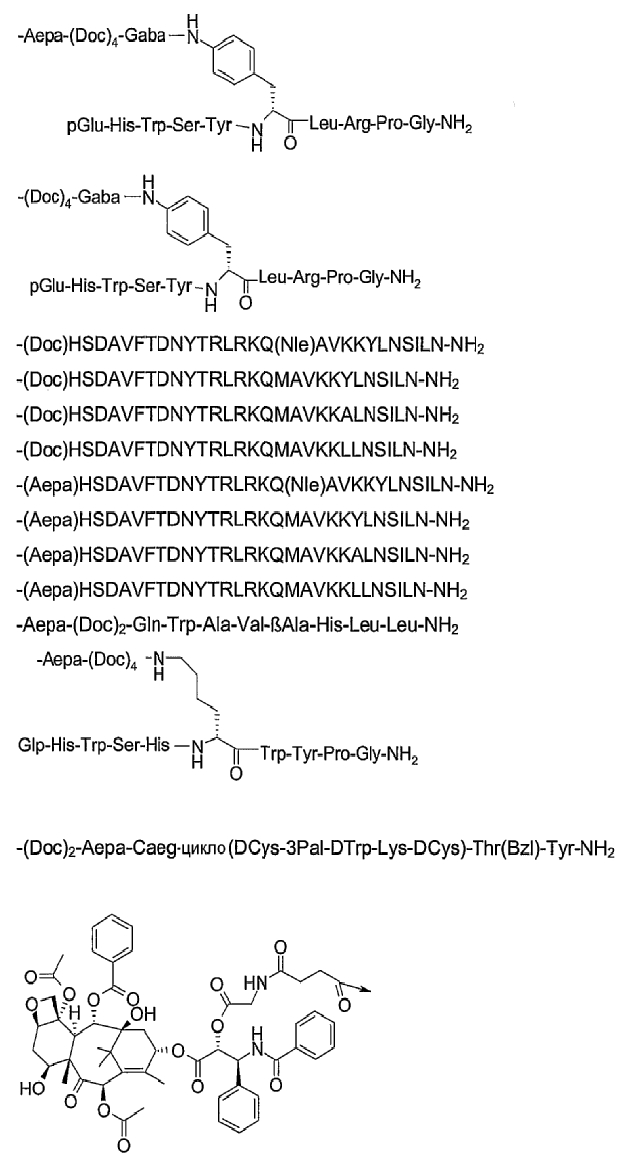
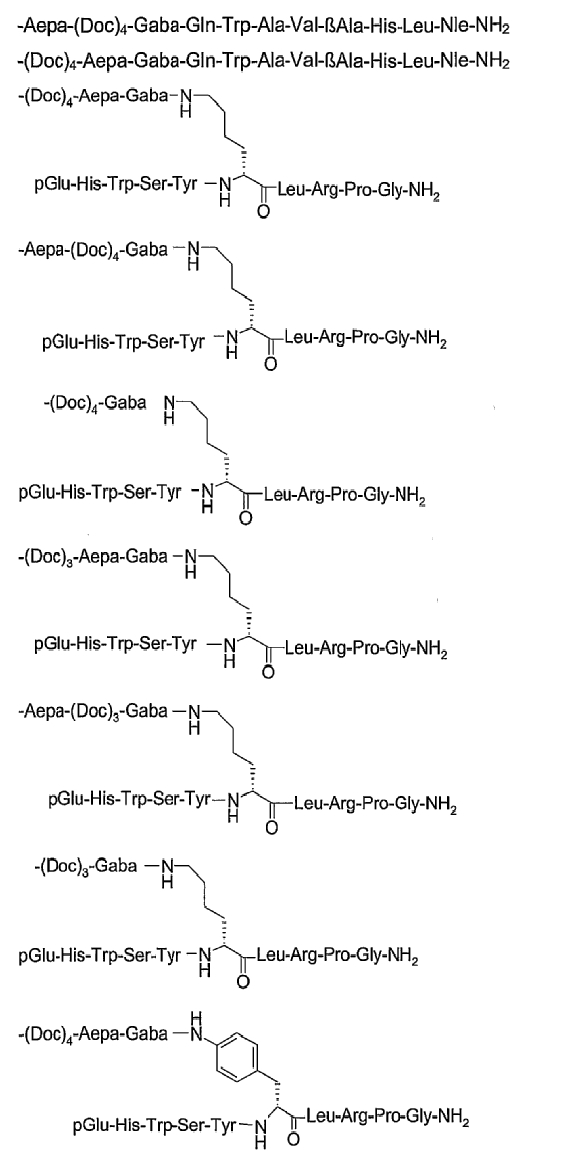
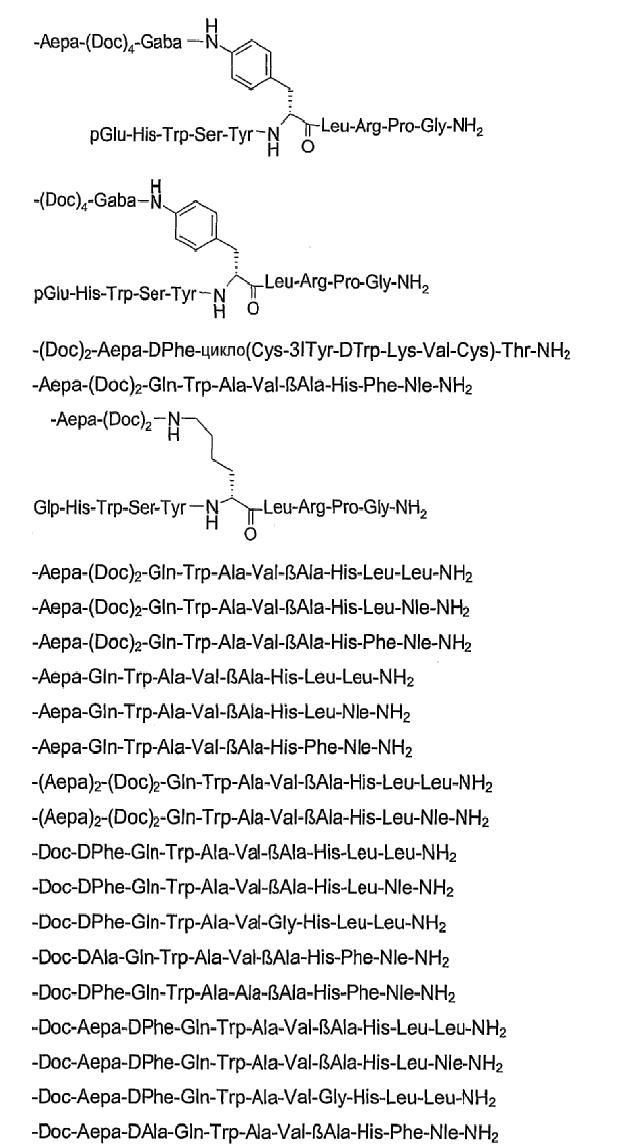
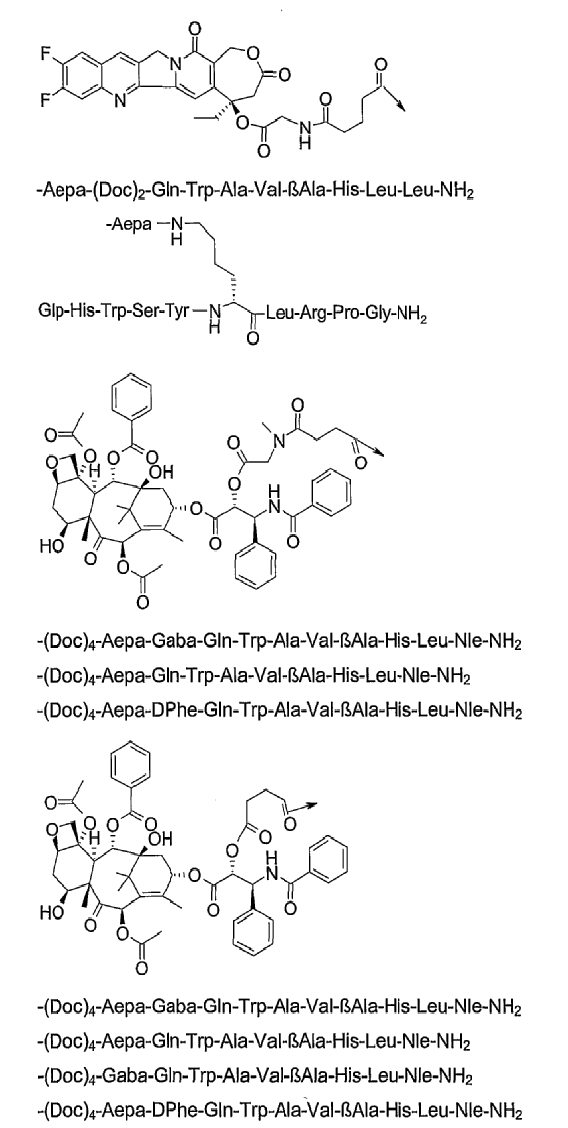
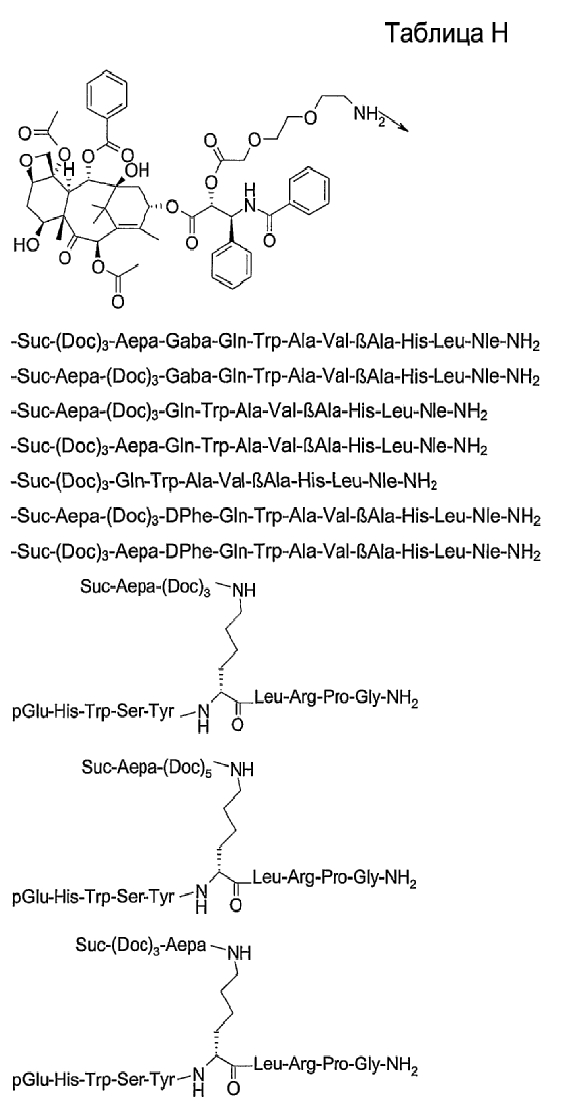
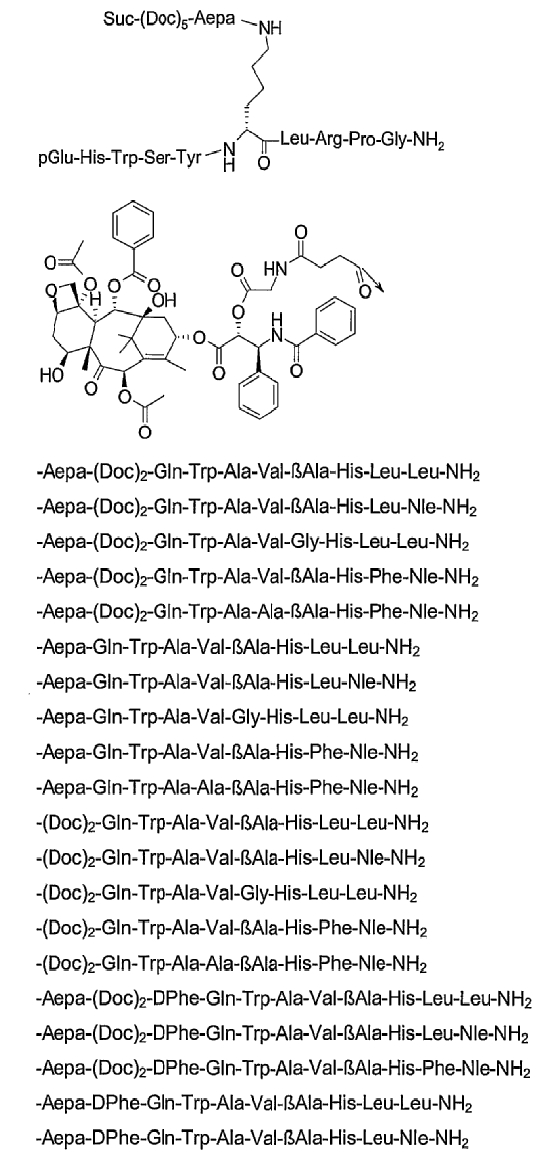
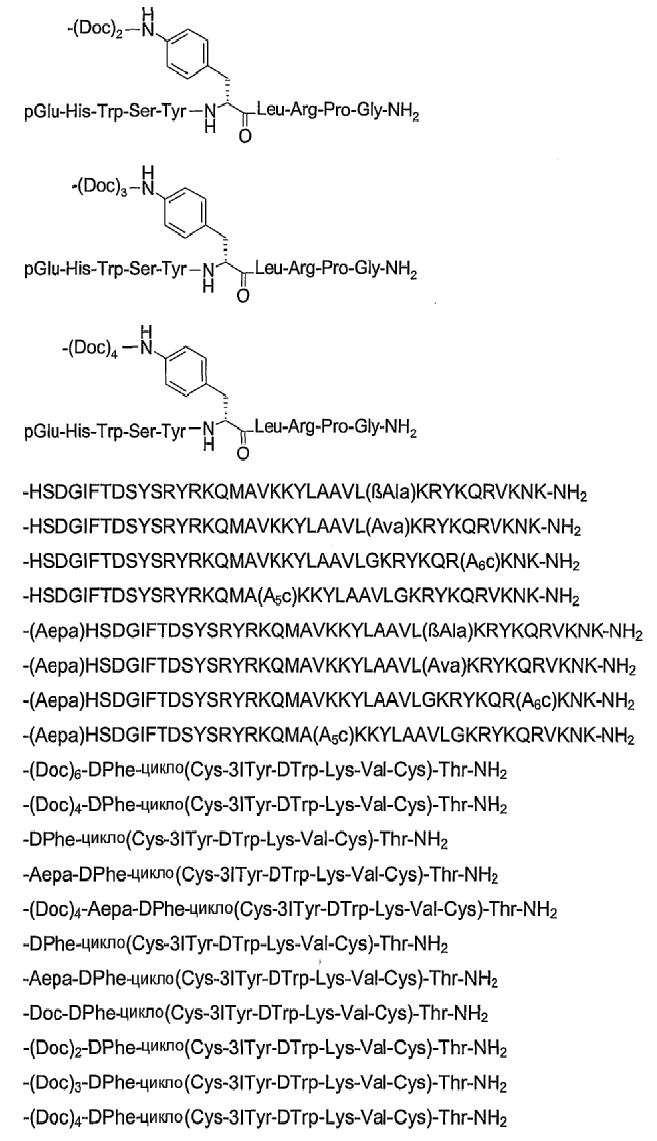
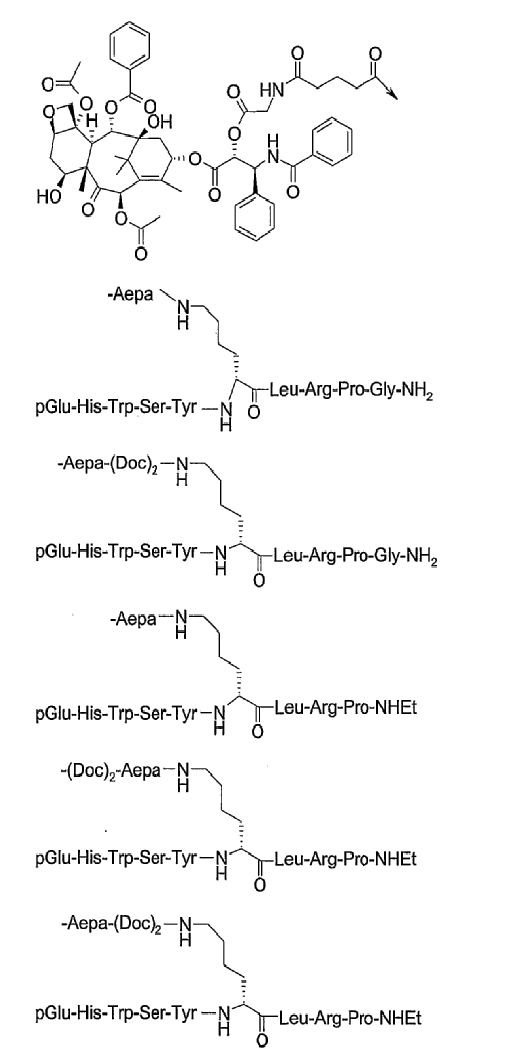
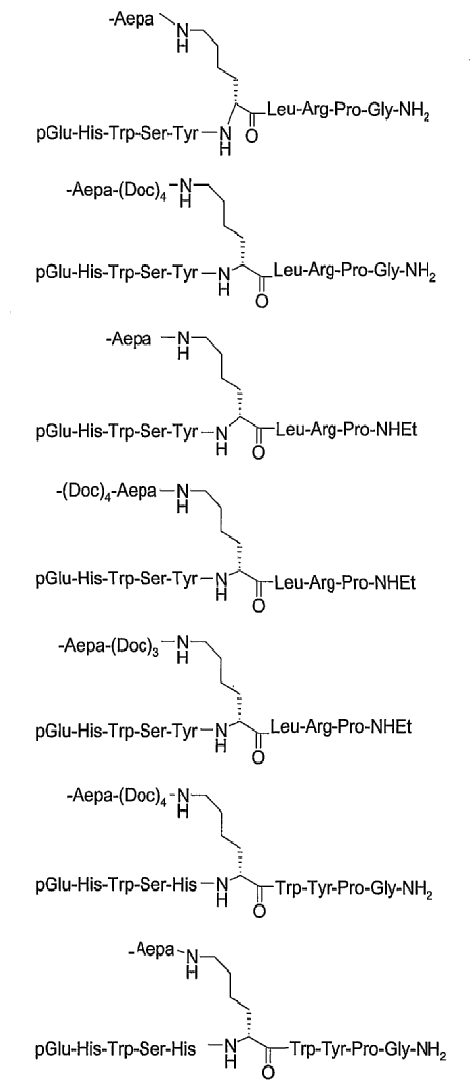
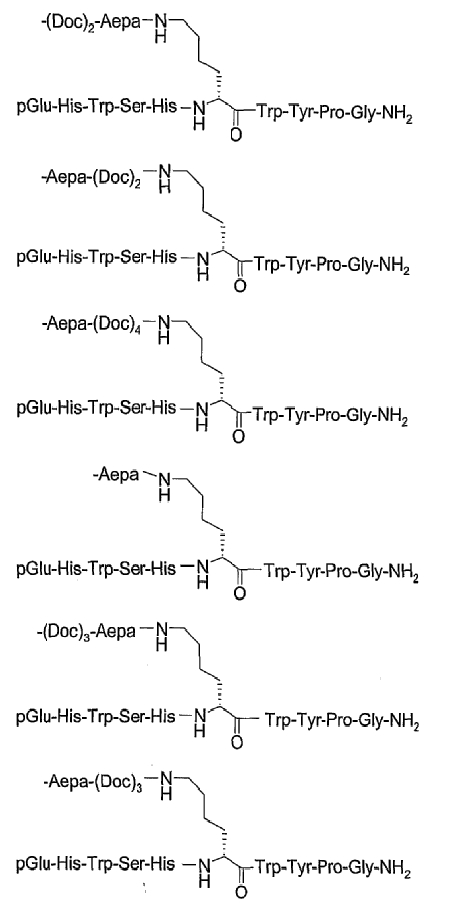
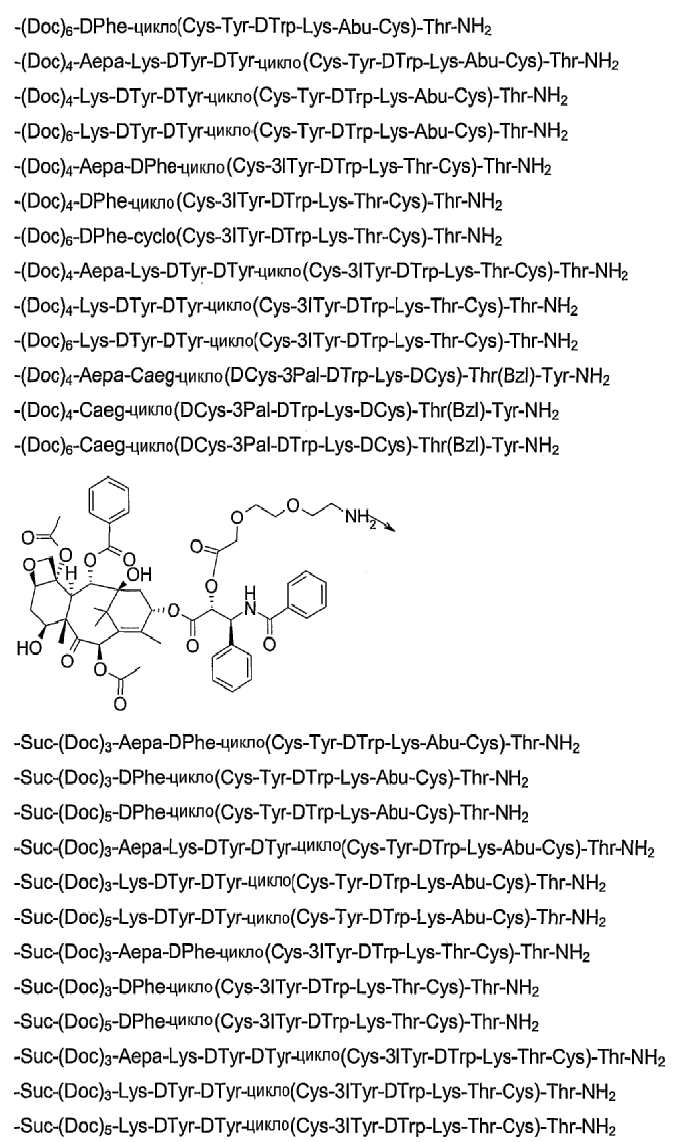
26. Соединение по п.1, которое представляет собой соединение, выбранное из группы следующих соединений:
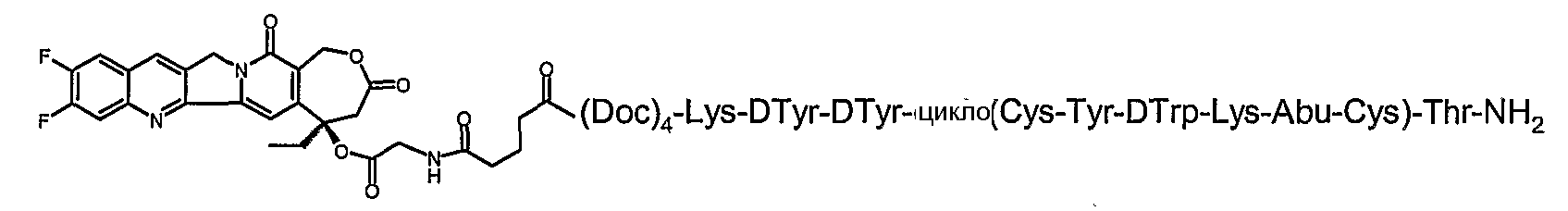
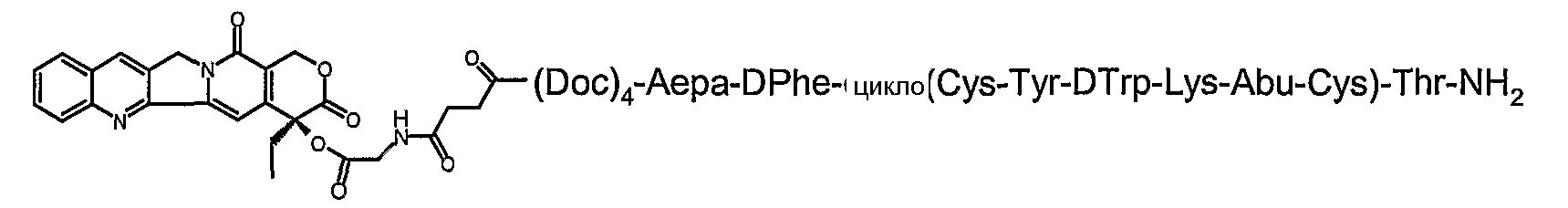
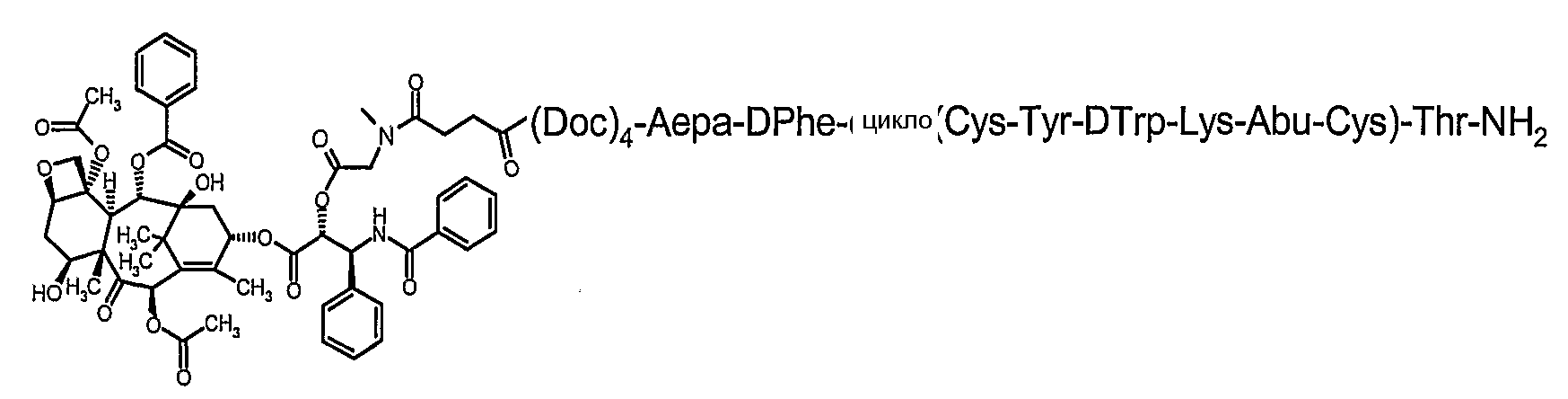
или его фармацевтически приемлемую соль.
27. Фармацевтическая композиция по п.20, содержащая эффективное количество соединения по п.26 или его фармацевтически приемлемой соли и фармацевтически приемлемый носитель.
28. Способ лечения заболевания у субъекта, нуждающегося в этом, предусматривающий введение указанному субъекту терапевтически эффективного количества соединения по п.26 или его фармацевтически приемлемой соли, где указанное заболевание выбрано из группы, состоящей из фиброза, доброкачественной гиперплазии предстательной железы, атеросклероза, рестеноза, рака молочной железы, рака ободочной кишки, рака поджелудочной железы, рака предстательной железы, рака легкого, мелкоклеточного рака легкого, рака яичника, эпидермального рака и гемопоэтического рака.
29. Способ лечения заболевания у субъекта, нуждающегося в этом, предусматривающий введение указанному субъекту терапевтически эффективного количества соединения по п.26 или его фармацевтически приемлемой соли, где указанное заболевание характеризуется нежелательной пролиферацией клеток, которые экспрессируют один или несколько рецепторов соматостатинового типа.
30. Способ лечения заболевания у субъекта, нуждающегося в этом, предусматривающий введение указанному субъекту терапевтически эффективного количества соединения по п.26 или его фармацевтически приемлемой соли, где указанное заболевание характеризуется нежелательной пролиферацией клеток, которые экспрессируют один или несколько рецепторов бомбезинового типа.
31. Способ лечения заболевания у субъекта, нуждающегося в этом, предусматривающий введение указанному субъекту терапевтически эффективного количества соединения по п.26 или его фармацевтически приемлемой соли, где указанное заболевание характеризуется нежелательной пролиферацией клеток, которые экспрессируют один или несколько рецепторов типа LHRH.
32. Соединение по п.1, которое представляет собой соединение
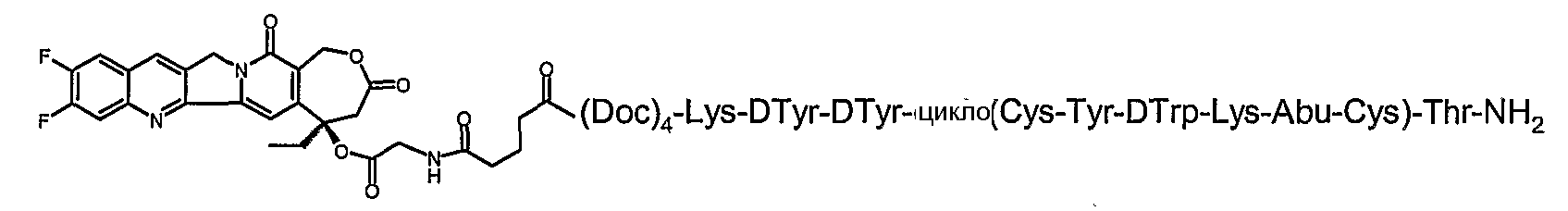
или его фармацевтически приемлемую соль.
33. Фармацевтическая композиция по п.20, содержащая эффективное количество соединения по п.32 или его фармацевтически приемлемой соли и фармацевтически приемлемый носитель.
34. Способ лечения заболевания у субъекта, нуждающегося в этом, предусматривающий введение указанному субъекту терапевтически эффективного количества соединения по п.32 или его фармацевтически приемлемой соли, где указанное заболевание выбрано из группы, состоящей из фиброза, доброкачественной гиперплазии предстательной железы, атеросклероза, рестеноза, рака молочной железы, рака ободочной кишки, рака поджелудочной железы, рака предстательной железы, рака легкого, мелкоклеточного рака легкого, рака яичника, эпидермального рака и гемопоэтического рака.
35. Способ лечения заболевания у субъекта, нуждающегося в этом, предусматривающий введение указанному субъекту терапевтически эффективного количества соединения по п.32 или его фармацевтически приемлемой соли, где указанное заболевание характеризуется нежелательной пролиферацией клеток, которые экспрессируют один или несколько рецепторов соматостатинового типа.
36. Способ лечения заболевания у субъекта, нуждающегося в этом, предусматривающий введение указанному субъекту терапевтически эффективного количества соединения по п.32 или его фармацевтически приемлемой соли, где указанное заболевание характеризуется нежелательной пролиферацией клеток, которые экспрессируют один или несколько рецепторов бомбезинового типа.
37. Способ лечения заболевания у субъекта, нуждающегося в этом, предусматривающий введение указанному субъекту терапевтически эффективного количества соединения по п.32 или его фармацевтически приемлемой соли, где указанное заболевание характеризуется нежелательной пролиферацией клеток, которые экспрессируют один или несколько рецепторов типа LHRH.
38. Соединение по п.1, которое представляет собой соединение
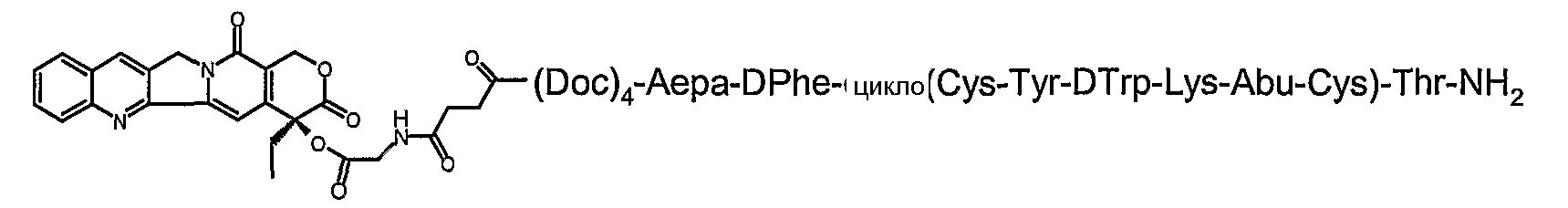
или его фармацевтически приемлемую соль.
39. Фармацевтическая композиция по п.20, содержащая эффективное количество соединения по п.38 или его фармацевтически приемлемой соли и фармацевтически приемлемый носитель.
40. Способ лечения заболевания у субъекта, нуждающегося в этом, предусматривающий введение указанному субъекту терапевтически эффективного количества соединения по п.38 или его фармацевтически приемлемой соли, где указанное заболевание выбрано из группы, состоящей из фиброза, доброкачественной гиперплазии предстательной железы, атеросклероза, рестеноза, рака молочной железы, рака ободочной кишки, рака поджелудочной железы, рака предстательной железы, рака легкого, мелкоклеточного рака легкого, рака яичника, эпидермального рака и гемопоэтического рака.
41. Способ лечения заболевания у субъекта, нуждающегося в этом, предусматривающий введение указанному субъекту терапевтически эффективного количества соединения по п.38 или его фармацевтически приемлемой соли, где указанное заболевание характеризуется нежелательной пролиферацией клеток, которые экспрессируют один или несколько рецепторов соматостатинового типа.
42. Способ лечения заболевания у субъекта, нуждающегося в этом, предусматривающий введение указанному субъекту терапевтически эффективного количества соединения по п.38 или его фармацевтически приемлемой соли, где указанное заболевание характеризуется нежелательной пролиферацией клеток, которые экспрессируют один или несколько рецепторов бомбезинового типа.
43. Способ лечения заболевания у субъекта, нуждающегося в этом, предусматривающий введение указанному субъекту терапевтически эффективного количества соединения по п.38 или его фармацевтически приемлемой соли, где указанное заболевание характеризуется нежелательной пролиферацией клеток, которые экспрессируют один или несколько рецепторов типа LHRH.
44. Соединение по п.1, которое представляет собой соединение
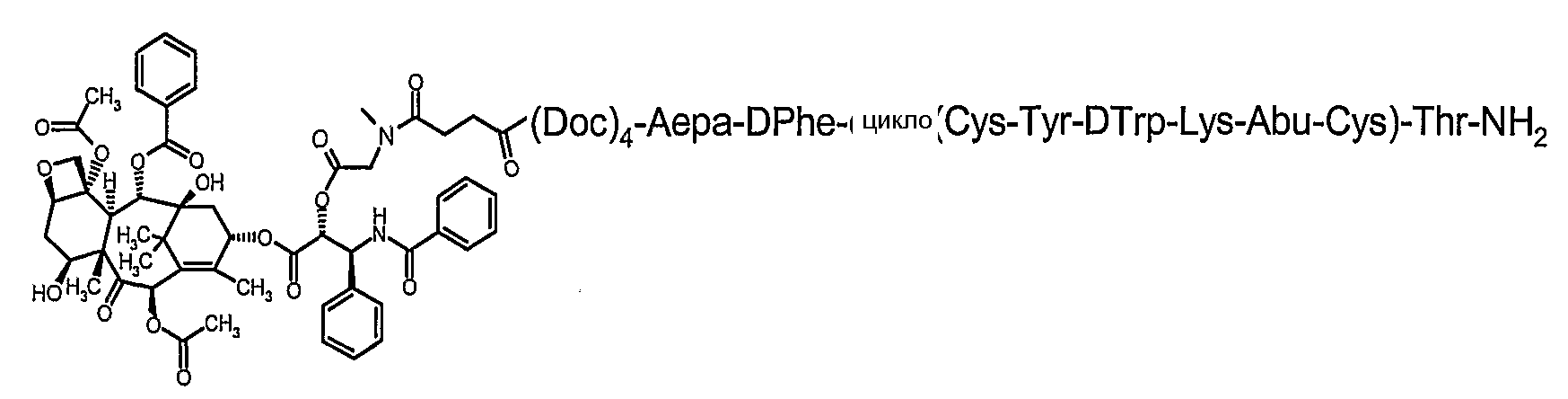
или его фармацевтически приемлемую соль.
45. Фармацевтическая композиция по п.20, содержащая эффективное количество соединения по п.44 или его фармацевтически приемлемой соли и фармацевтически приемлемый носитель.
46. Способ лечения заболевания у субъекта, нуждающегося в этом, предусматривающий введение указанному субъекту терапевтически эффективного количества соединения по п.44 или его фармацевтически приемлемой соли, где указанное заболевание выбрано из группы, состоящей из фиброза, доброкачественной гиперплазии предстательной железы, атеросклероза, рестеноза, рака молочной железы, рака ободочной кишки, рака поджелудочной железы, рака предстательной железы, рака легкого, мелкоклеточного рака легкого, рака яичника, эпидермального рака и гемопоэтического рака.
47. Способ лечения заболевания у субъекта, нуждающегося в этом, предусматривающий введение указанному субъекту терапевтически эффективного количества соединения по п.44 или его фармацевтически приемлемой соли, где указанное заболевание характеризуется нежелательной пролиферацией клеток, которые экспрессируют один или несколько рецепторов соматостатинового типа.
48. Способ лечения заболевания у субъекта, нуждающегося в этом, предусматривающий введение указанному субъекту терапевтически эффективного количества соединения по п.44 или его фармацевтически приемлемой соли, где указанное заболевание характеризуется нежелательной пролиферацией клеток, которые экспрессируют один или несколько рецепторов бомбезинового типа.
49. Способ лечения заболевания у субъекта, нуждающегося в этом, предусматривающий введение указанному субъекту терапевтически эффективного количества соединения по п.44 или его фармацевтически приемлемой соли, где указанное заболевание характеризуется нежелательной пролиферацией клеток, которые экспрессируют один или несколько рецепторов типа LHRH.

Комментарии