Меченый антиген е гепаднавируса и его применение в скрининге противовирусных веществ - RU2711750C2
Код документа: RU2711750C2
Чертежи




















































Описание
Данное изобретение выполнено с государственной поддержкой по контракту №R01AI094474, выделенной Национальным Институтом Здоровья. Государство обладает определенными правами на изобретение.
Данное изобретение относится к способам и применениям для скрининга веществ, направленных против гепаднавирусов, где вещества являются ингибиторами антигена Е вируса гепатита В (HBeAg), который в клеточных линиях, описанных в данном изобретении, преимущественно зависит от ковалентно замкнутой кольцевой ДНК (кзкДНК) и может служить суррогатным маркером кзкДНК при скрининге способности ингибировать кзкДНК гепаднавируса, такого как вирус гепатита В (HBV, от англ. Hepatitis В virus). В способах и применениях используют клетки, содержащие нуклеотидную последовательность, кодирующую меченый антиген Е гепаднавируса, такой как антиген Е вируса гепатита В (HBeAg). Кроме того, в данном изобретении изложены последовательности нуклеиновых кислот, кодирующие меченый антиген Е гепаднавируса, а также кодируемые ими белки. Также предложены наборы для применения в способах скрининга.
Хронический гепатит В в настоящее время представляет собой серьезную угрозу для здоровья населения и затрагивает приблизительно 350 миллионов человек во всем мире и по меньшей мере 1,2 миллиона жителей США. У данных пациентов существует повышенный риск развития цирроза, гепатоцеллюлярной карциномы (ГЦК) и других тяжелых клинических осложнений (1, 2, 12, 14). Ежегодно от заболеваний, связанных с HBV, в мире умирает приблизительно 1 миллион человек. Таким образом, лечение хронической HBV инфекции и предупреждение ее тяжелых последствий имеет первостепенное значения для охраны здоровья населения мира.
Вирус гепатита В (HBV) представляет собой нецитопатический гепатотропный ДНК-вирус, принадлежащий к семейству Hepadnaviridae. Гепаднавирусы представляют собой семейство оболочечных вирусов с двуцепочечной ДНК, которые могут вызывать инфекционные заболевания печени у человека и животных. Геном гепаднавирусов имеет схожую организацию. Они имеют небольшой геном, представленный двуцепочечной кольцевой ДНК. Геном состоит из двух цепей ДНК, одна из которых имеет минус-ориентацию, а другая плюс-ориентацию. Репликация включает обратную транскрипцию промежуточной РНК, обозначаемой прегеномной РНК (15, 19). У вируса известно три основных открытых рамки считывания (ОРС) и пять мРНК (18, 19).
При инфицировании вирусная геномная релаксированная кольцевая (рк) ДНК транспортируется в ядро клетки и конвертируется в эписомальную ковалентно замкнутую кольцевую (кзк) ДНК, которая служит матрицей для транскрипции для всех мРНК вируса, в частности, для мРНК прекорового белка размером 3,5-3,6 тпн, кодирующей прекоровый белок, который является предшественником HBeAg; прегеномной (пг) РНК размером 3,5 тпн, кодирующей коровый белок и полимеразу вируса; мРНК поверхностных белков размером 2,4 тпн/2,1 тпн, кодирующую белки оболочки вируса (антигены L (от англ. large), М (от англ. middle) и S (от англ. small)) и мРНК белка X размером 0,7 тпн, кодирующей белок X (18, 19). HBeAg образуется в результате двух протеолитических стадий, в результате которых удаляются N-концевой сигнальный пептид и С-концевая богатая аргинином последовательность прекорового белка (Wang (1991) J Virol 65(9), 5080 (10, 21). После транскрипции и перемещения в ядро цитоплазматическая вирусная пгРНК упаковывается вместе с полимеразой и белками капсида HBV в нуклеокапсид, внутри которого полимераза осуществляет обратную транскрипцию с образованием минус-цепи ДНК, с которой затем копируется плюс-цепь ДНК с образованием ркДНК генома потомства. Вновь синтезированные зрелые нуклеокапсиды либо упаковываются вместе с белками оболочки вируса и выходят в форме вирионов, либо поступают обратно в ядро для амплификации пула кзкДНК благодаря пути амплификации внутриклеточной кзкДНК (19). Таким образом, молекулярной основой хронического гепатита В является персистенция вирусной кзкДНК в ядрах инфицированных гепатоцитов.
Гепатит В полностью не излечивается. В настоящее время для лечения HBV одобрены к применению такие препараты, как интерферона альфа (IFN-α) и 5 аналогов нуклеозидов (нуклеотидов) (ламивудин, адефовир, энтекавир, телбивудин и тенофовир. Xu (2010) J Virol (84) 9332-9340 описывает воздействие мышиного интерферона на гепатоциты мыши. IFN-α позволяет достигнуть устойчивого вирусологического ответа лишь у небольшой группы пациентов через 48 недель стандартного лечения и вызывает тяжелые побочные эффекты (9). Все пять нуклеозидных (нуклеотидных) аналогов являются ингибиторами вирусной полимеразы, но редко позволяют излечить HBV инфекцию (6), а развитие резистентности чрезвычайно ограничивает их долгосрочную эффективность (16, 24). В настоящее время общепризнано, что основным ограничением существующей терапии является невозможность элиминировать существующий пул кзкДНК и/или предупредить образование кзкДНК вирусом дикого типа или устойчивым к лекарствам вирусом, присутствующим в следовых количествах. Таким образом, существует большая потребность в разработке новых терапевтических средств, которые бы направленно воздействовали на образование и персистенцию кзкДНК.
Cai (2013) Methods in Mol Biol 1030 (151-161) описывает саузерн блоттинг для определения кзкДНК HBV в клеточных культурах. До настоящего времени скрининг агентов, мишенью которых является кзкДНК, был ограничен в связи с отсутствием эффективных in vitro моделей HBV инфекции, и практическое определение кзкДНК с высокой или средней производительностью было невозможно. В альтернативном случае, образование кзкДНК может происходить в результате внутриклеточной амплификации в культурах клеток, стабильно трансфецированных HBV, с конститутивной или зависящей от условий репликацией генома HBV, таких как клетки HepG2.2.15 и HepAD38 (7, 11, 20).
При этом, непосредственная детекция кзкДНК в клеточных линиях HBV методом гибридизации с использованием саузерн-блоттинга или ПЦР в реальном времени не подходит для скрининга вследствие недостаточной чувствительности и специфичности, соответственно. С другой стороны, для кзкДНК в клетках HepG2.2.15 не существует подходящего суррогатного маркера, поскольку подавляющее большинство вирусных продуктов образуются с участием интегрированного вирусного трансгена и не отличимы от продуктов, образованных с участием кзкДНК. Ранее было показано, что продукция секретируемого HBeAg в клетках HepAD38 преимущественно зависит от кзкДНК и может служить суррогатным маркером кзкДНК (11, 23). Не так давно Cai et al. использовали усовершенствованный вариант линии клеток, продуцирующих HBeAg, зависимый исключительно от кзкДНК, обозначенных клетками HepDE19 (7), в 96-луночной тест-системе для скрининга ингибиторов кзкДНК и идентифицировали два низкомолекулярных соединения, которые ингибируют образование кзкДНК (3). Данная работа стала убедительным доказательством концепции, что биосинтез кзкДНК может быть непосредственной мишенью химических молекул и в результате высокопроизводительного скрининга можно идентифицировать ингибиторы кзкДНК. Однако определенные недостатки существующей тест-системы HepDE19 делают непрактичным скрининг более крупных библиотек. Например, общепринятый ELISA, используемый в настоящее время для определения HBeAg, требует множества манипуляций, демонстрирует некоторую перекрестную реактивность с коровым белком вируса вследствие гомологии аминокислотной последовательности и не подходит для более масштабного анализа на клетках.
Таким образом, данное изобретение решает техническую проблему обеспечения средств и способов для надежного скрининга ингибиторов кзкДНК гепаднавирусов.
Для решения технической проблемы предложены воплощения, охарактеризованные в формуле изобретения.
Соответственно, данное изобретение относится к способу оценки способности молекулы-кандидата ингибировать кзкДНК гепаднавируса, включающему стадии:
(а) приведения в контакт клетки, содержащей молекулу нуклеиновой кислоты, содержащую последовательность нуклеиновой кислоты, кодирующей меченый антиген Е гепаднавируса, с указанной молекулой-кандидатом;
(б) оценки уровня меченого антигена Е гепаднавируса и
(в) отбора молекулы-кандидата, если уровень меченого антигена Е гепаднавируса снижается по сравнению с контролем.
Способы общеприменимы для других гепаднавирусов млекопитающих и птиц, таких как репрезентативные вирус гепатита сурков (WHV) и вирус гепатита В уток (DHBV), схожие с вирусом гепатита В (HBV) по генной организации и принципу репликации. Таким образом, объяснения и эксперименты, приведенные в данном документе в отношении вируса гепатита В, применимы и к другим гепаднавирусам. Однако сведения, приведенные в данном документе, в предпочтительном воплощении относятся к вирусу гепатита В (HBV). Термины «гепаднавирус», «вирус гепатита В», «вирус гепатита В уток», «вирус гепатита В сурков» хорошо известны в области техники и используются в данном документе соответствующим образом. Аббревиатуры «HBV», «DHBV» или «WHV» используются в данном описании взаимозаменяемо и обозначают вирус гепатита В», «вирус гепатита В уток» и «вирус гепатита В сурков», соответственно.
Предпочтительным гепаднавирусом в данном документе является вирус гепатита В (HBV). Вирус гепатита В (HBV) представляет собой нецитопатический тропный к печени ДНК-вирус, принадлежащий к семейству Hepadnaviridae, т.е. HBV представляет собой гепаднавирус. Примеры последовательностей нуклеиновой кислоты генома HBV приведены в SEQ ID NO: 27, 28, 29, 30, 31, 32, 33 или 34.
Предпочтительным антигеном Е гепаднавируса в данном документе является антиген Е вируса гепатита В (HBeAg). Термины «антиген Е вируса гепатита В» и «HBeAg» в данном документе используют взаимозаменяемо. Примеры нуклеотидной последовательности и аминокислотной последовательности HBeAg приведены в SEQ ID NO: 16 и 18, соответственно. В данном описании «антиген Е гепаднавируса» (и аналогичный термин «антиген Е вируса гепатита В») относится преимущественно к белку/полипептиду, например, белку/полипептиду, имеющему аминокислотные последовательности, приведенные в SEQ ID NO: 18.
HBeAg может быть получен после инфицирования следующим образом: после инфицирования геномная релаксированная кольцевая (рк) ДНК вируса HBV транспортируется в ядро клетки и конвертируется в эписомальную кзкДНК, которая служит матрицей для транскрипции всех мРНК вируса, в том числе мРНК прекорового белка размером 3,5-3,6 тпн, кодирующей прекоровый белок, который является предшественником HBeAg. Термины «кзкДНК» и «ковалентно замкнутая кольцевая ДНК» в данном документе используют взаимозаменяемо.
Примеры нуклеотидной последовательности и аминокислотной последовательности прекорового белка HBV приведены в SEQ ID NO: 15 и 17, соответственно. Прекоровый белок HBV имеет N-концевой сигнальный пептид из 19 аминокислот, линкер из 10 аминокислот, центральный аминокислотный участок и С-концевой богатый аргинином домен из 34 аминокислот.
Примеры нуклеотидной последовательности и аминокислотной последовательности корового белка HBV приведены в SEQ ID NO: 23 и 24, соответственно. Коровый белок схож с прекоровым белок (см. SEQ ID NO: 17) в том, что он содержит С-концевую богатую аргинином последовательность прекорового белка; однако, коровый белок не содержит N-концевого сигнального пептида и линкерной последовательности прекорового белка, состоящей из 10 аминокислот.
HBeAg образуется в результате двух протеолитических стадий, в результате которых удаляются N-концевой сигнальный пептид и С-концевая богатая аргинином последовательность прекорового белка (Wang (1991) J Virol 65(9), 5080 (21). Таким образом, антиген Е вируса гепатита В (HBeAg) схож с прекоровым белок (см. SEQ ID NO: 17) в том, что он содержит N-концевой линкерный пептид прекорового белка, состоящий из 10 аминокислот; однако HBeAg не содержит С-концевую богатую аргинином последовательность прекорового белка.
Молекулярной основой хронического гепатита В является персистенция вирусной кзкДНК в ядрах инфицированных гепатоцитов.
Термины «кзкДНК» и «ковалентно замкнутая кольцевая ДНК» в данном документе используют взаимозаменяемо. Термины «кзкДНК» / «ковалентно замкнутая кольцевая ДНК» хорошо известны в области техники и используются в данном документе соответствующим образом. Как правило, «кзкДНК» / «ковалентно замкнутая кольцевая ДНК» в данном документе относится к ДНК, которая служит аутентичной эписомальной матрицей для транскрипции мРНК гепаднавируса.
Антиген Е вируса гепатита В (HBeAg) является принятым суррогатным маркером кзкДНК гепаднавируса HBV, которая в свою очередь свидетельствует о хронической гепаднавирусной инфекции. При этом, известные тесты на клетках, в которых используется HBeAg, имеют такие недостатки, как перекрестная реакция с коровым белком вируса.
Для улучшения специфичности и чувствительности определения репортера кзкДНК, создали клеточные линии, поддерживающие кзкДНК-зависимую продукцию рекомбинантного HBeAg с тагом (таким как встроенный N-концевой гемагглютининовый (НА) эпитоп). Кроме того, для детекции меченного (НА-) HBeAg разработали хемилюминесцентный ELISA (CLIA) и тест AlphaLISA. Тест-систему можно адаптировать для высокопроизводительного скрининга и полностью автоматизировать.
В способах, которые предложенные в данном описании, используют известные таги (такие как НА-таг или His-таг, Flag-таг, c-myc-таг, V5-таг или С9-таг, которые можно использовать вместо НА-тага или дополнительно к нему). Указанные таги можно использовать для очистки и детекции меченого антигена Е гепаднавируса. Используя антитела, специфически связывающиеся с тагом (например, в тестах ELISA, хемилюминесцентном ELISA (CLIA) и AlphaLISA), можно надежно и быстро оценивать уровень меченого антигена Е гепаднавируса и избегать перекрестной реакции с коровым белком.
В предложенных здесь способах используют клетки, содержащие молекулу нуклеиновой кислоты, содержащую нуклеотидную последовательность, кодирующую меченый антиген Е гепаднавируса. Чтобы отражать и обеспечивать образование кзкДНК гепаднавируса молекула нуклеиновой кислоты может содержать последовательность, кодирующую прекоровый белок гепаднавируса или даже геном гепаднавируса. В области техники известно, что геном HBV имеет очень компактную организацию и имеет перекрывающиеся открытые рамки считывания (ОРС) и множество cis элементов. Таким образом, считают, что вставка/делеция гена или замена последовательности с очень большой вероятностью будет влиять на репликацию вирусной ДНК (13, 22). (Liu, et al., J Virol. 2004; 78(2):642-9.) (Wang, et al., PLoS One. 2013 2; 8(4):e60306). В более ранних работах при получении рекомбинантного генома HBV в большинстве случаев производили замену последовательности HBV, такой как области, кодирующей полимеразу и белок оболочки, на GFP, однако для поддержки репликации вируса и сборки вириона была необходима транскомплементация по вирусным белкам (17) (Protzer, et al., PNAS (1999), 96: 10818-23). Кроме того, при применении для инфицирования пермиссивных клеток описанный геном рекомбинантного HBV может осуществлять только первый раунд синтеза кзкДНК, а внутриклеточная амплификация кзкДНК блокируется из-за дефекта репликации вирусной ДНК.
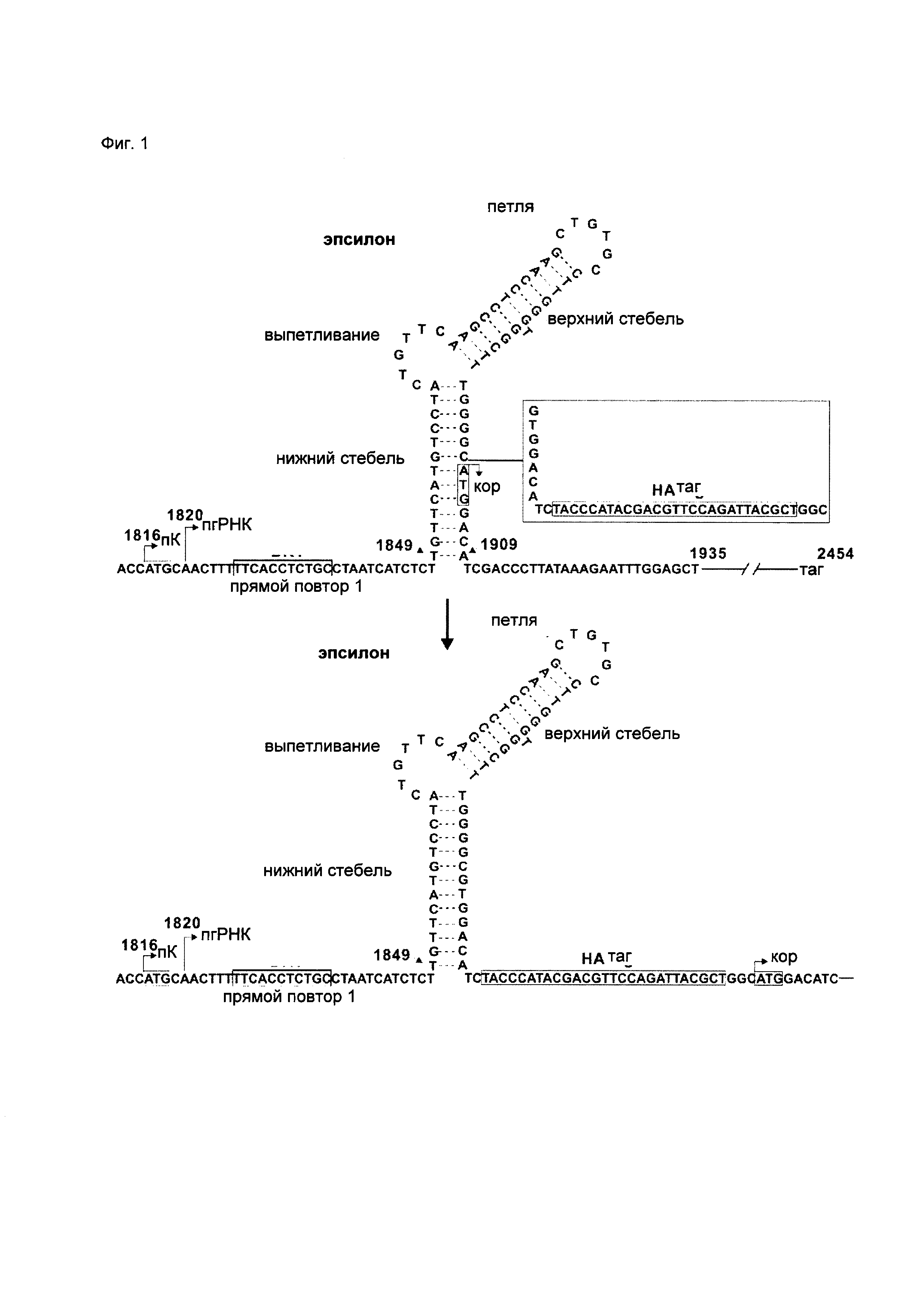
5' концевая структура стебель-петля (эпсилон) в пгРНК гепаднавируса, предпочтительно пгРНК HBV, является существенным для репликации вируса cis элементом. Она служит сигналом упаковки пгРНК и сайтом праймирования ДНК. Эпсилон перекрывается с 5' частью ОРС прекорового белка и содержит стартовый кодон ОРС белка капсида (корового белка). Для встраивания последовательности нуклеиновой кислоты, кодирующей таг, по ходу транскрипции относительно последовательности N-концевого сигнального пептида, в ОРС прекорового белка, не нарушая целостность эпсилон-структуры, кодируемой геномом HBV, встроили (НА-)таг с линкерной последовательность из трех аминокислот (GTG GAC АТС) на 5' конце, чтобы заменить исходную последовательность вируса (ATG GAC АТС) на правом плече у основания эпсилон-элемента, кодируемого геномом HBV. Таким образом, спаривание оснований эпсилон-элемента, кодируемого геномом HBV, сохранялось, а стартовый кодон ОРС корового белка сдвигался в позицию, расположенную по ходу транскрипции относительно эпсилон-элемента, кодируемого геномом HBV. Кроме того, исходная последовательность GGC размещалась между последовательностью НА-тага и AUG корового белка для сохранения аутентичного мотива Kozak стартового кодона корового белка (Фиг. 1). На Фиг. 1 показана часть генома HBV, кодирующая эпсилон-структуру, где нуклеотидная последовательность, кодирующая таг, встроена согласно данному изобретению.
Полагают, что указанные выше модификации оказывают минимальное влияние на пгРНК-зависимую экспрессию корового белка HBV и инкапсидирование пгРНК, поскольку экспрессионная кассета эпсилон-элемента и корового белка сохранилась, несмотря на то, что в матрице пгРНК сайт инициации трансляции корового белка был смещен на 39 нуклеотидов по ходу транскрипции. Действительно, геном рекомбинантного HBV поддерживал уровень репликации вирусной ДНК близкий к дикому типу и НА-меченный HBeAg успешно продуцировался при воссоздании ОРС прекорового белка в молекуле кзкДНК.
Встраивание олигонуклеотида, кодирующего таг, не влияло на репликацию вирусной ДНК, таким образом, предложенные в данном документе способы обеспечивают получение кзкДНК и, следовательно, оценку способности веществ/молекул-кандидатов ингибировать образование кзкДНК путем определения количества суррогатного маркера «меченого антигена Е гепаднавируса». Предложенные в данном документе способы и средства в первую очередь могут найти применение в скрининге и идентификации молекул-кандидатов, которые могут найти применение в терапии хронических заболеваний, ассоциированных с гепаднавирусами, такими как (хронический) гепатит и в особенности хронический гепатит В.
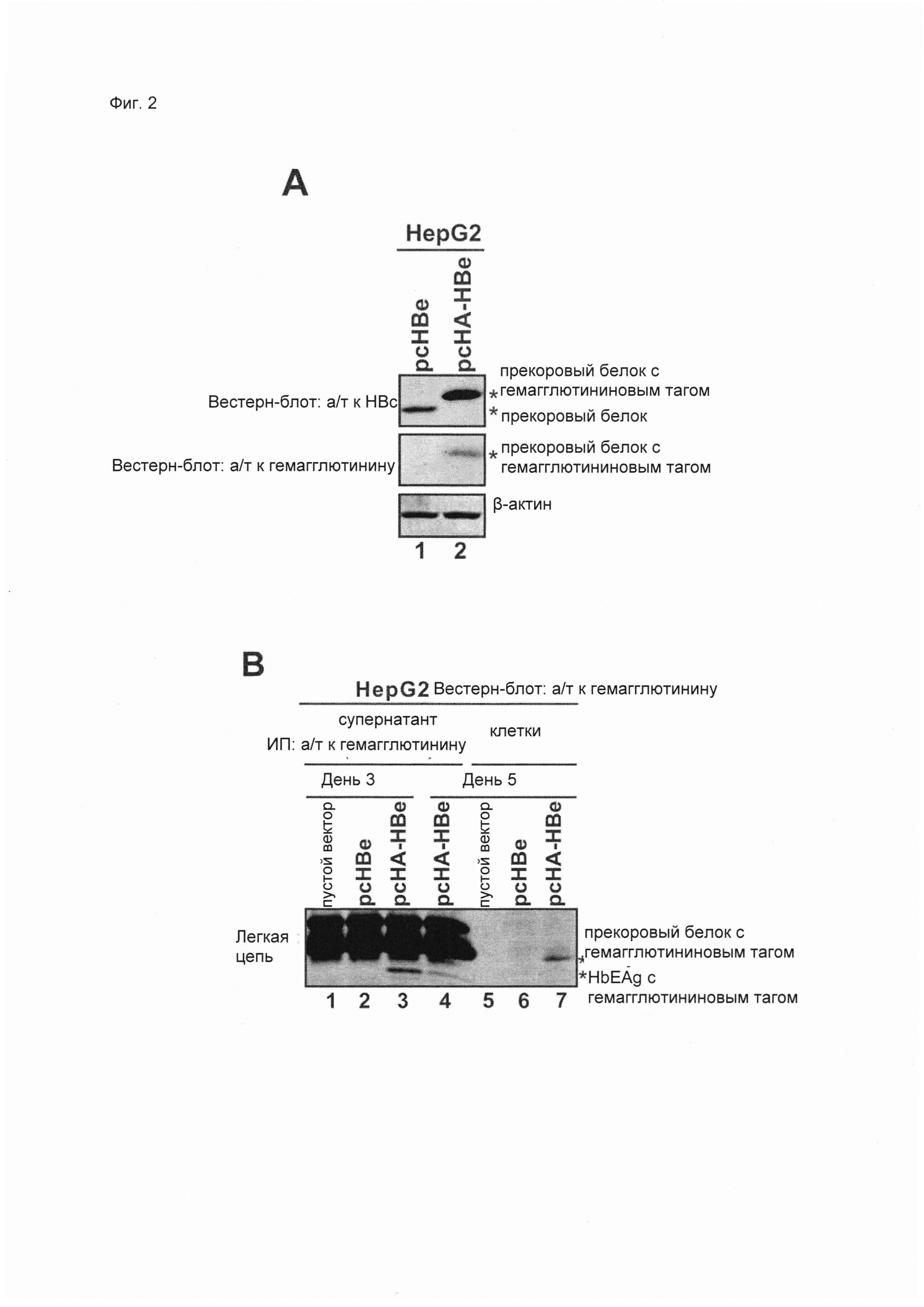
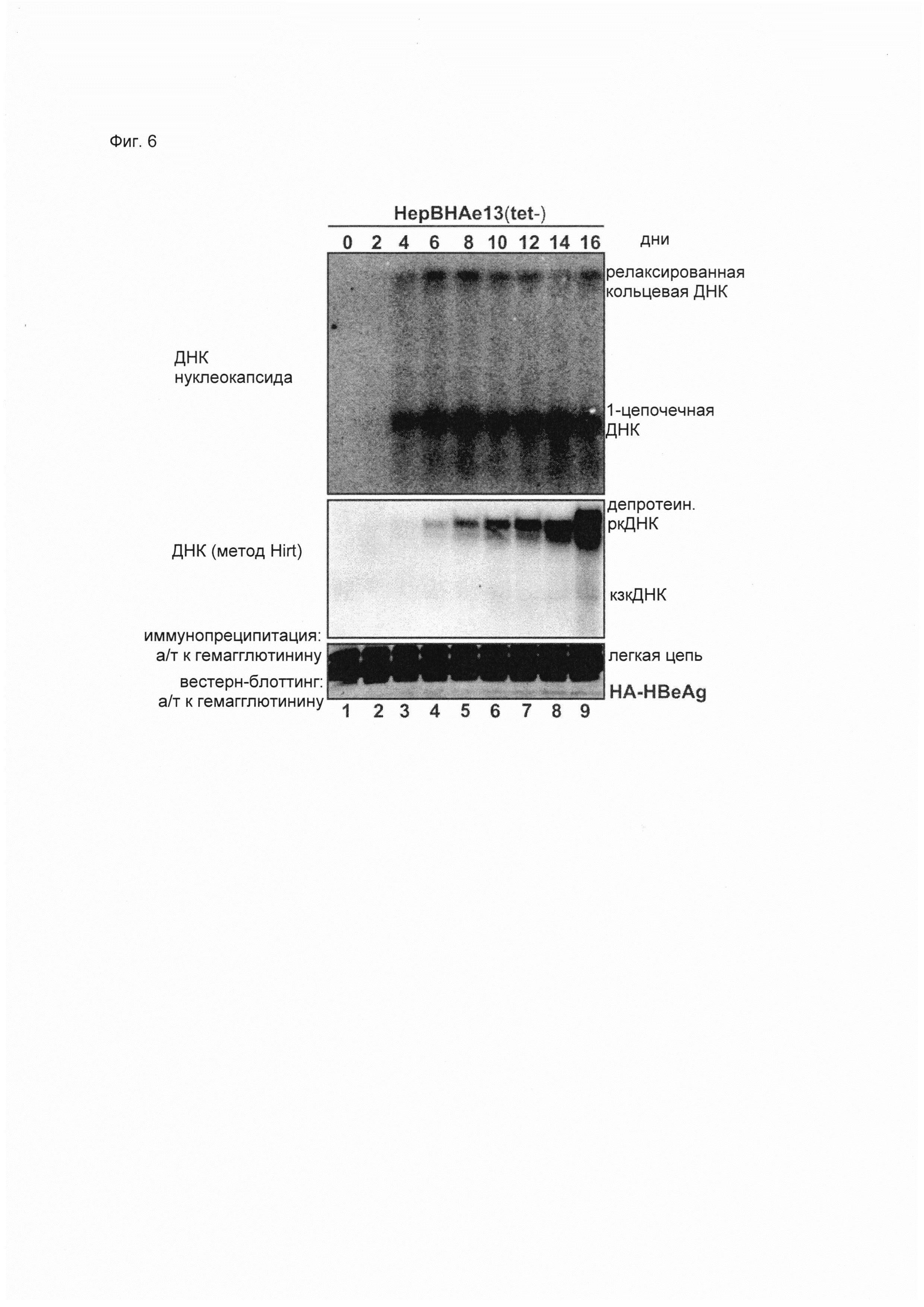
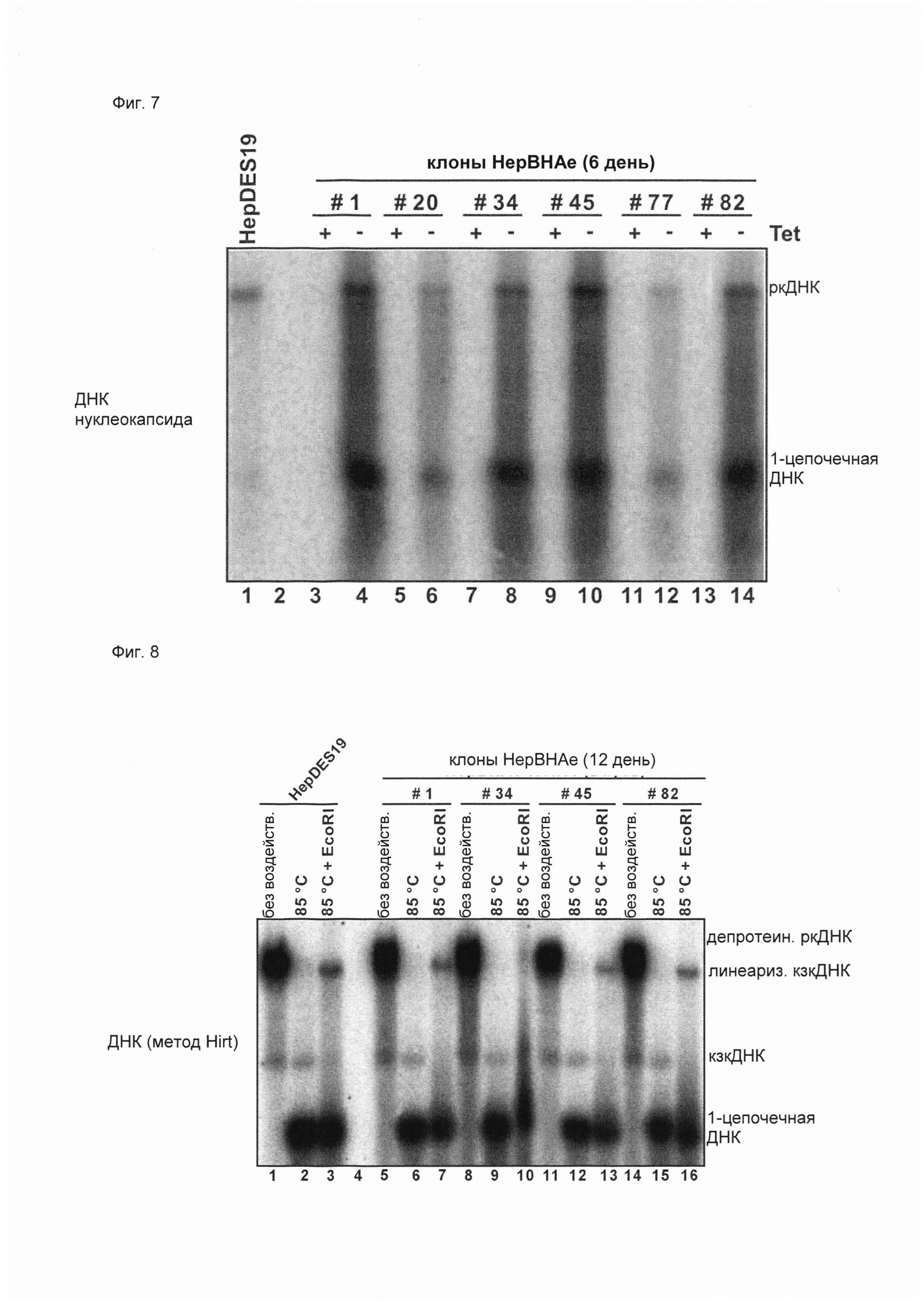
Встраивание последовательности нуклеиновой кислоты, кодирующей таг (такой как НА-таг), в ОРС прекорового белка гепаднавируса (такого как HBV) вызывает кзкДНК-зависимую продукцию меченого антигена Е гепаднавируса (такого как HBeAg). В поддержку данного изобретения было показано, что встраивание (НА-)тага не влияет на экспрессию прекорового белка и его посттрансляционную модификацию (отщепление N-концевого сигнального пептида и отщепление С-концевого домена) и секрецию зрелого HBeAg (Фиг. 2). Более того, было показано, что такая модификация в геноме гепаднавируса (такого как HBV) не препятствует инкапсидированию и обратной транскрипции вирусной пгРНК, необходимых для образования кзкДНК в результате внутриклеточной амплификации (Фиг. 4, 6-8, 12).
Данное изобретение относится к скринингу и оценке фармакологических агентов, активных в отношении гепаднавирусов. В частности, данное изобретение описывает дизайн и конструирование генома рекомбинантного вируса гепатита В (HBV) и новые клеточные линии для индуцируемой кзкДНК-зависимой экспрессии антигена Е HBV (HBeAg) с эпитопной меткой (например, меченного гемагглютинином вируса гриппа человека (НА)). Меченый HBeAg секретируется в культуральную жидкость и может быть определен количественно, например, с помощью хемилюминесцентного иммуноферментного анализа (CLIA) и/или AlphaLISA. В данном изобретении предложены эффективные клеточные репортерные системы HBV для скрининга соединений на предмет анти-гепаднавирусной активности, в особенности ингибирующих образование, сохранение кзкДНК и/или ее транскрипционную активность.
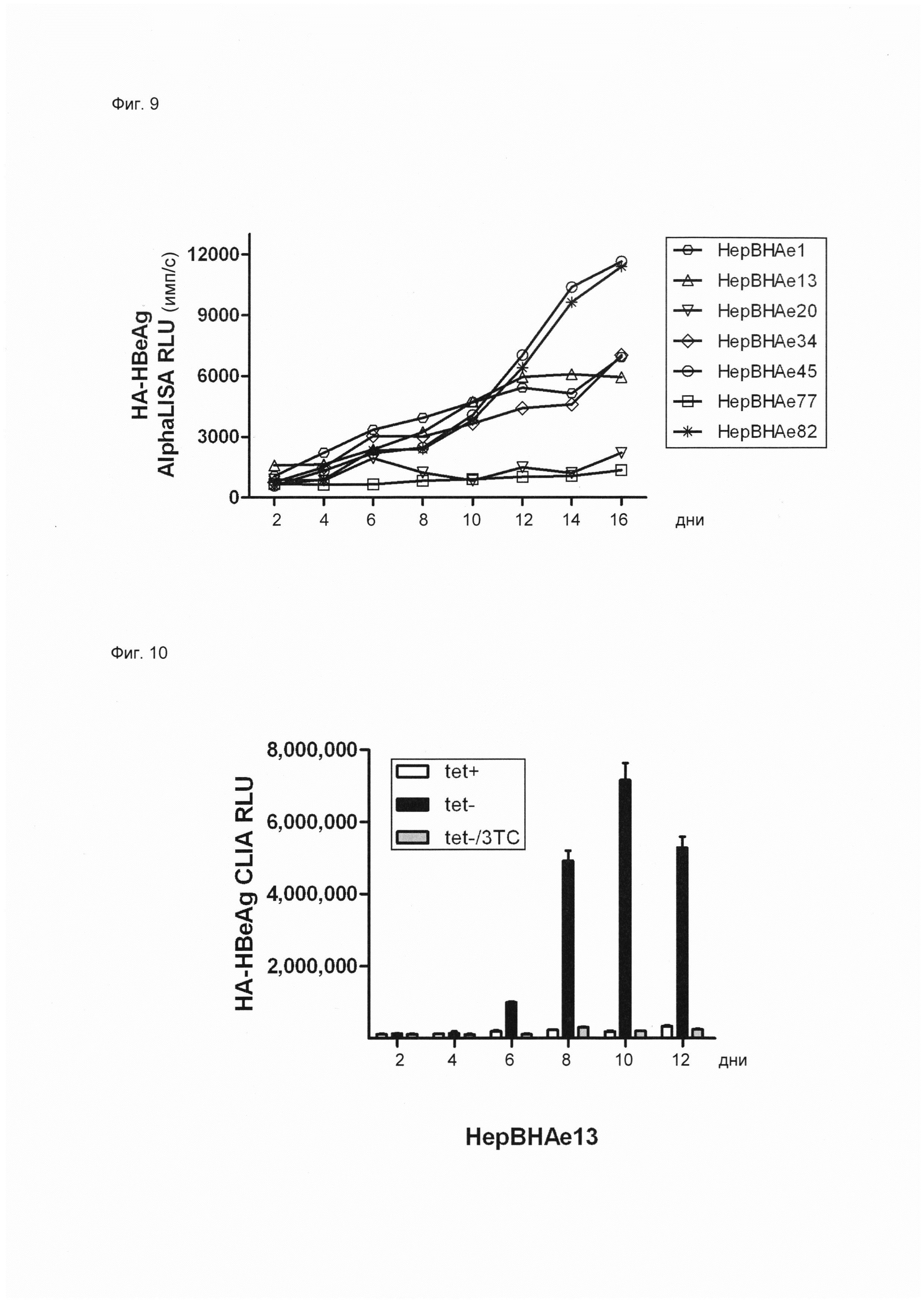
Фиг. 10 служит дополнительной иллюстрацией к данному изобретению. Так, было показано, что под воздействием 3ТС сигнал, обусловленный НА-HBeAg, в клетках НерВНАе13 не детектировали, хотя это происходило в экстремальных условиях, когда 3ТС блокировал репликацию вирусной ДНК и таким образом, кзкДНК не синтезировалась. Далее, с целью доказательства принципа, на клетках НерВНАе13 протестировали два ингибитора образования кзкДНК (ССС-0975 и ССС-0346). Оба соединения вызывали дозозависимое снижение уровня НА-HBeAg, см. Фиг 11.
Например, в соответствии с данным изобретением можно провести следующие исследования, направленные против гепаднавирусов, которые не являются ограничивающими:
1. Скрининг соединений/молекул-кандидатов, регулирующих стабильность кзкДНК и/или транскрипционную активность с использованием клеточных линий НерВНАе.
Согласно данному изобретению, способ определения in vitro можно применять для скрининга/оценки эффективности соединений/молекул-кандидатов в отношении регулирования стабильности кзкДНК и/или транскрипционной активности в ядре. Таким образом, соединения/молекулы-кандидаты изменяют уровень меченого антигена Е гепаднавируса (такого как НА-HBeAg) в культуральной надосадочной жидкости. Для выполнения теста клетки вначале можно высадить в культуральные планшеты в присутствии тетрациклина, и после того, как клетки достигнут конфлюентности, заменить среду на среду без тетрациклина для индукции репликации ДНК гепаднавируса (такого как HBV) и образования кзкДНК, что обычно занимает 6-8 суток. После этого можно вновь добавить тетрациклин для подавления репликации вирусной ДНК de novo из интегрированного генома HBV, совместно с добавлением 3ТС (или других ингибиторов полимеразы HBV) для блокирования пути внутриклеточной амплификации кзкДНК. В то же время, тестируемые соединения можно добавлять в культуральную среду на определенный период времени. Культуральную среду затем можно использовать для определения меченого антигена Е гепаднавируса (такого как НА-HBeAg) методом ELISA. Среду из лунок, не содержащих исследуемого соединения, можно использовать в качестве контроля. Эффективные соединения, снижающие уровень меченого антигена Е гепаднавируса (такого как НА-HBeAg) в культуральной среде, могут обладать активностью, способствующей круговороту кзкДНК или подавляющей транскрипцию кзкДНК. Выражение «эффективно» или «эффективный» в данном описании может использоваться для обозначения, что соединение, в определенной исследуемой концентрации, достаточно для предупреждения и, предпочтительно, снижения по меньшей мере на 50%, более предпочтительно по меньшей мере на 90%, продукции меченого антигена Е гепаднавируса (такого как НА-HBeAg) в тест-системе на клетках согласно данному изобретению. Прямое определение стационарных уровней кзкДНК и мРНК прекорового белка методом количественной ПЦР или гибридизации можно использовать для различения, снижает ли тестируемое соединение/ соединение-кандидат/молекула-кандидат стабильность кзкДНК или транскрипцию, соответственно.
2. Скрининг соединений/молекул-кандидатов, ингибирующих образование кзкДНК гепаднавируса (такого как HBV) с использованием линий клеток НерВНАе.
Согласно другому аспекту данного изобретения, способ определения in vitro можно применять для оценки соединений/молекул-кандидатов, подавляющих образование кзкДНК. Вкратце, клетки можно высаживать в лунки для культивирования и не добавлять тетрациклин в день, когда монослой становится конфлюентным. Одновременно можно добавлять исследуемое соединение и по окончании воздействия (приблизительно через 6 дней) определять в среде меченый антиген Е гепаднавируса (такой как НА-HBeAg) методом ELISA. Любое соединение, вызывающее снижение меченого антигена Е гепаднавируса (такого как НА-HBeAg) указывает, что оно может эффективно блокировать образование кзкДНК. В качестве дополнения к данному способу исследования in vitro следует отметить, что снижение меченого антигена Е гепаднавируса (такого как НА-HBeAg) в данном тесте может также указывать, что соединение имеет потенциал ингибировать репликацию ДНК гепаднавируса (такого как HBV). Указанную возможность можно исследовать путем непосредственного определения ДНК нуклеокапсида вируса методом саузерн блоттинга и/или количественной ПЦР. «Находки», сделанные по результатам описанного выше теста, могут также охватывать соединения, влияющие на стабильность и/или транскрипцию кзкДНК. В течение периода индукции мишенью исследуемых соединений может быть стабильность и/или транскрипционная активность ранее образованной кзкДНК.
3. Линии клеток НерНА-НВе служат в качестве системы для обратного скрининга.
Теоретически, соединения, «найденные» в вышеупомянутом тесте, могут непосредственно ингибировать трансляцию НА-меченого прекорового белка или посттрансляционную модификацию или секрецию меченого антигена Е гепаднавируса (такого как НА-HBeAg). Для исключения таких соединений, не ингибирующих кзкДНК, можно выполнить обратный скрининг «находок» в клетках НерНА-НВе, которые продуцируют меченый антиген Е гепаднавируса (такой как НА-меченый HBeAg), используя трансген в качестве матрицы. С другой стороны, клетки НерНА-НВе можно также использовать для скрининга ингибиторов HBeAg.
Термин «ингибировать ковалентно замкнутую кольцевую ДНК» и его грамматические производные может относиться к ингибированию стабильности ковалентно замкнутой кольцевой ДНК (т.е. сниженной стабильности ковалентно замкнутой кольцевой ДНК), к ингибированию транскрипционной активности ковалентно замкнутой кольцевой ДНК (т.е. сниженной транскрипции мРНК гепаднавируса при использовании ковалентно замкнутой кольцевой ДНК в качестве матрицы транскрипции) или к ингибированию образования ковалентно замкнутой кольцевой ДНК (т.е. отсутствие или уменьшенное образование кзкДНК).
Данные приведенные в качестве примера расшифровки и определения термина «ингибировать ковалентно замкнутую кольцевую ДНК» не являются взаимоисключающими. Например, ингибирование образования ковалентно замкнутой кольцевой ДНК может приводить или быть связанным со сниженной транскрипцией мРНК гепаднавируса, использующей ковалентно замкнутую кольцевую ДНК в качестве транскрипционной матрицы (т.е. с ингибированием транскрипционной активности ковалентно замкнутой кольцевой ДНК). Ингибирование стабильности ковалентно замкнутой кольцевой ДНК может привести или быть связанным со сниженной транскрипцией мРНК гепаднавируса, использующей ковалентно замкнутую кольцевую ДНК в качестве транскрипционной матрицы.
Таким образом, меченый антиген Е гепаднавируса можно использовать в качестве суррогатного маркера для любого подобного ингибирования кзкДНК гепаднавируса.
В соответствии с указанным выше, описанный в данном документе способ можно применять для оценки способности молекулы-кандидата ингибировать образование кзкДНК гепаднавируса. Для этого клетка может быть приведена в контакт с молекулой-кандидатом до образования кзкДНК.
Описанный в данном документе способ можно применять для оценки способности молекулы-кандидата снижать стабильность кзкДНК (например, количество или число кзкДНК) гепаднавируса. Для этого клетка может быть приведена в контакт с молекулой-кандидатом после образования кзкДНК.
Описанный в данном документе способ можно применять для оценки способности молекулы-кандидата снижать транскрипцию (транскрипционную активность) кзкДНК гепаднавируса. Для этого клетка может быть приведена в контакт с молекулой-кандидатом после образования кзкДНК.
Меченый антиген Е гепаднавируса, уровень которого подлежит оценке согласно данному изобретению, может содержать один или несколько тагов. Как показано в данном документе, надежная оценка меченого антигена Е гепаднавируса может достигаться с применением только одного тага, например, антитела, специфически связывающегося с тагом. Соответственно, предусматривают и предпочитают, что меченый антиген Е гепаднавируса содержит только один таг.
Это относится к одному или нескольким тагам, используемым в данном изобретении.
Термин «таг», используемый в данном документе, относится к любой химической структуре, которую можно использовать в качестве маркера. Прежде всего, термин «таг» относится к «белковому тагу». Термины «таг» и «белковый таг» известны в области техники, см., помимо прочего, Fritze СЕ, Anderson TR. "Epitope tagging: general method for tracking recombinant proteins". Methods Enzymol. 2000; 327: 3-16; Brizzard B, Chubet R. Epitope tagging of recombinant proteins. Curr Protoc Neurosci. 2001 May; Chapter 5: Unit 5.8; and/or Terpe K. Overview of tag protein fusions: from molecular and biochemical fundamentals to commercial systems. Appl Microbiol Biotechnol. 2003 Jan; 60(5):523-33.
Как правило, таг, используемый согласно данному описанию, представляет собой белковый таг, слитый с антигеном Е гепаднавируса. Например, нуклеиновая кислота, кодирующая таг, может быть слита с нуклеиновой кислотой, кодирующей антиген Е гепаднавируса, таким образом, чтобы экспрессировался химерный белок, содержащий таг и антиген Е гепаднавируса. Таг(и) могут быть слиты с 5'-концом нуклеиновой кислоты, кодирующей антиген Е гепаднавируса, встроены в нуклеиновую кислоту, кодирующую антиген Е гепаднавируса и/или слиты с 3'-концом нуклеиновой кислоты, кодирующей антиген Е гепаднавируса. Таким образом, полученный химерный белок может содержать таг(и) на N-конце, внутри (т.е. в составе антигена Е гепаднавируса / в виде внутреннего эпитопа) и/или на С-конце. Как показано в данном документе, таг, являющийся внутренним эпитопом, можно применять для надежной оценки уровня меченого антигена Е гепаднавируса и, следовательно, он является предпочтительным.
В области техники известны различные таги, которые можно применять согласно данному изобретению. Как правило, таг, применяемый в соответствии с данным описанием, имеет молекулярный вес приблизительно 1-3 кДа, предпочтительно около 1 кДа. Неисчерпывающими примерами низкомолекулярных тагов являются НА-таг, His-таг, Flag-таг, c-myc-таг, V5-таг или С9-таг. Предпочтительно применяют НА-таг. Применяемый Flag-таг может представлять собой 1×Flag-таг или 3×Flag-таг.
Низкий молекулярный вес проявляется в длине тага, т.е. числе аминокислотных остатков, из которых состоит таг. Например, в данном изобретении можно применять His-таг (6 аминокислот), НА-таг (9 аминокислот), FLAG-таг (8 аминокислот) или 3XFLAG-таг (22 аминокислоты). Приведенные в качестве примера таги поддерживают уровень репликации ДНК HBV близкий к дикому типу и, таким образом, могут найти применение в данном изобретении.
Соответственно, таги для применения в данном изобретении могут состоять из 6-22 аминокислот, например, из 6 аминокислот, 7 аминокислот, 8 аминокислот, 9 аминокислот, 10 аминокислот, 11 аминокислот, 12 аминокислот, 13 аминокислот, 14 аминокислот, 15 аминокислот, 16 аминокислот, 17 аминокислот, 18 аминокислот, 19 аминокислот, 20 аминокислот, 21 аминокислоты или 22 аминокислот.
Примеры нуклеотидных последовательностей, кодирующих таг для применения в данном изобретении, представляют собой нуклеотидную последовательность, кодирующую НА таг, приведенную в SEQ ID NO: 1, нуклеотидную последовательность, кодирующую His-таг, приведенную в SEQ ID NO: 2, нуклеотидную последовательность, кодирующую c-myc-таг, приведенную в SEQ ID NO: 4, нуклеотидную последовательность, кодирующую V5-таг, приведенную в SEQ ID NO: 5, нуклеотидную последовательность, кодирующую С9-таг, приведенную в SEQ ID NO: 6. Предпочтительным является применение НА тага, кодируемого SEQ ID NO: 1, или состоящего из аминокислотной последовательности, приведенной в SEQ ID NO: 8.
Примером нуклеотидной последовательности, кодирующей Flag-таг для применения в данном изобретении, является нуклеотидная последовательность, кодирующая 1×Flag таг, приведенная в SEQ ID NO: 3, или нуклеотидная последовательность, кодирующая 3×Flag-таг, приведенная в SEQ ID NO: 7.
Примерами аминокислотных последовательностей тагов для применения в данном изобретении, являются аминокислотная последовательность НА тага, приведенная в SEQ ID NO: 8, аминокислотная последовательность His-тага, приведенная в SEQ ID NO: 9, аминокислотная последовательность с-myc-тага, приведенная в SEQ ID NO: 11, аминокислотная последовательность V5-тага, приведенная в SEQ ID NO: 12, аминокислотная последовательность С9-тага, приведенная в SEQ ID NO: 13.
Примером аминокислотной последовательности Flag-тага для применения в данном изобретении, является аминокислотная последовательность 1×Flag-тага, приведенная в SEQ ID NO: 10, или аминокислотная последовательность 3×Flag-тага, приведенная в SEQ ID NO: 14.
Прежде всего предусматривается применение таких эпитопных тагов, как гемагглютининовый (НА) таг, His-таг, Flag-таг, c-myc-таг, V5-таг и/или С9-таг. Эпитопные таги представляют собой короткие пептидные последовательности, которые выбирают благодаря возможности надежно получать высокоаффинные антитела с использованием многих различных биологических видов. Указанные таги зачастую происходят от генов вирусов, что объясняет их высокую иммунореактивность. В частности, данные таги могут найти применение для вестерн-блоттинга, иммунофлуоресценции, иммуногистохимии, иммуноаффинной хроматографии и иммунопреципитации. Их также применяют для очистки антител. Указанные эпитопные таги наиболее пригодны, поскольку в данном изобретении можно применять известные и доступные для приобретения антитела, специфически связывающиеся с указанными тагами.
Аффинные таги присоединяют к белкам, так чтобы их можно было выделить их из естественного биологического источника с применением аффинной технологии. Они включают хитин-связывающий белок (СВР), мальтоза-связывающий белок (МВР) и глутатион-S-трансферазу (GST). Поли (His) таг представляет собой широко применяемый белковый таг; он связывается с металлическими матрицами.
Хроматографические таги применяют для изменения хроматографических свойств белка, чтобы обеспечить различную разрешающую способность благодаря определенной методике разделения. Зачастую, они состоят из полианионных аминокислот, таких как FLAG-таг.
По существу, в данном изобретении может применяться любой таг. Нуклеиновая кислота, кодирующая таг, входящая в состав молекулы нуклеиновой кислоты для применения в данном изобретении, должна поддерживать репликацию ДНК гепаднавируса, образование кзкДНК и кзкДНК-зависимое образование и секрецию антигена Е гепаднавируса. Данную способность легко проверить с помощью описанных в данном документе тестов, например, описанных в экспериментальной части. Например, показали, что при встраивании НА-тага репликация ДНК HBV происходила на уровне, характерном для дикого типа, и стабильные клеточные линии продуцировали НА-меченный HBeAg из кзкДНК. Указанную способность легко проверить и протестировать для других тагов. Встраивание His-таг и Flag-таг, например, не влияет на репликацию вирусной ДНК при транзиторной трансфекции.
Не отклоняясь от сущности изобретения, можно использовать другие таги.
Например, в данном изобретении в качестве тагов можно использовать репортерные белки, такие как люцифераза (например, люцифераза светлячка, люцифераза Renilla, люцифераза Gaussia и т.д.), зеленый флуоресцентный белок и т.п. Указанные репортерные белки позволяют легко оценить уровень меченых гепаднавирусов, например, путем визуального контроля, измерения флуоресценции и т.д. Флуоресцентные метки применяют для визуального снятия показаний по белку. GFP и его варианты представляют собой наиболее распространенные флуоресцентные метки.
Примерами репортерных белков, которые можно применять в скрининговых способах по изобретению, в числе прочих, являются люцифераза, (зеленый/красный) флуоресцентный белок и его варианты, EGFP (от англ. enhanced green fluorescent protein, улучшенный зеленый флуоресцентный белок), RFP (от англ. red fluorescent protein, красный флуоресцентный белок, такой как DsRed или DsRed2), CFP (от англ. cyan fluorescent protein, голубой флуоресцентный белок), BFP (от англ. blue green fluorescent protein, сине-зеленый флуоресцентный белок), YFP (от англ. yellow fluorescent protein, желтый флуоресцентный белок), β-галактозидаза или хлорамфениколацетилтрансфераза.
Люцифераза является хорошо известным репортером, см., например, Jeffrey (1987) Mol. Cell. Biol. 7(2), 725-737. Специалист в данной области может легко вывести дополнительные нуклеотидные и аминокислотные последовательности люциферазы для применения в контексте данного изобретения, используя соответствующие базы данных и классические учебники/обзоры.
Репортерный белок может обеспечить детекцию/оценку молекулы-кандидата для ингибирования кзкДНК, изменяя силу детектируемого сигнала. Указанный детектируемый сигнал может представлять собой сигнал резонансного переноса энергии флуоресценции (FRET, от англ. fluorescence resonance energy transfer), сигнал поляризации флуоресценции (FP, от англ. fluorescence polarization) или сигнал сцинтилляционного анализа сближения (SP, от англ. scintillation proximity). Детектируемый сигнал может быть связан с репортерным белком, согласно описанию выше. Например, GFP может быть получен из Aequorea victoria (US 5,491,084). Плазмида, кодирующая GFP из Aequorea victoria, зарегистрирована в АТСС под номером доступа 87451. Другие мутантные формы указанного GFP, включая среди прочих pRSGFP, EGFP, RFP/DsRed, DSRed2 и EYFP, BFP, YFP, но не ограничиваясь ими, доступны для приобретения, помимо прочего, у компании Clontech Laboratories, Inc. (Palo Alto, California).
В культивируемых клетках/тканях, содержащих молекулы нуклеиновых кислот, содержащие нуклеотидную последовательность, кодирующую антиген Е гепаднавируса, слитый с репортерным геном (таким как люцифераза, GFP и т.д.), можно отслеживать транскрипцию репортерного гена, зависящую от концентрации исследуемого соединения/молекулы-кандидата в культуральной среде. Изменение уровня транскрипции репортерного гена в зависимости от концентрации исследуемого соединения указывает на способность исследуемого соединения/молекулы-кандидата ингибировать кзкДНК.
Репортерные белки обычно крупнее, чем описанные в данном документе низкомолекулярные таги, такие как эпитопные таги. Из-за большей длины вставки, например, молекулы нуклеиновой кислоты, содержащей нуклеотидную последовательность, кодирующую люциферазу, по сравнению с последовательностью нуклеиновой кислоты, кодирующей меньшие (эпитопные) таги (такие как НА-таг), экспрессия расположенных по ходу транскрипции корового белка и полимеразы вируса из рекомбинантной прегеномной РНК может быть снижена, таким образом для восстановления репликации вируса может потребоваться транскомплементация по коровому белку и полимеразе. Например, согласно данному изобретению, можно применять клетки/клеточные линии, конститутивно экспрессирующие коровый белок гепаднавируса и полимеразу гепаднавируса (core/pol), в частности, при указанных обстоятельствах.
В данном изобретении предусмотрено применение меченого антигена Е гепаднавируса, содержащего два или более тагов. Применение двух или более тагов может обеспечить более надежное, а следовательно, более эффективное определение меченого антигена Е гепаднавируса. Например, если два или более тагов представляют собой различные таги (например, один таг представляет собой НА-таг, а второй таг представляет собой His-таг), можно использовать антитела, специфически связывающиеся с обоими тагами. Соответственно, в таком тесте можно использовать антитела для двух эпитопов, например, для определения методом ELISA для дальнейшего увеличения специфичности теста.
Обнаружили, что встраивание 3 × FLAG таг из 22 аминокислот поддерживает эффективную репликацию HBV. Соответственно, считается, что в данном изобретении также можно применять тандемные химерные эпитопные таги, например, такие как НА-линкер-FLAG.
В соответствии с описанием выше, когда применяют два или более тагов (например, два или более различных тагов), один таг может состоять из 6-22 аминокислот. В частности, предполагается, что общая длина тагов (т.е. сумма аминокислотных остатков двух или более тагов), применяемых в данном изобретении, не должна превышать максимум приблизительно 22 аминокислоты, поскольку экспрессия расположенного по ходу транскрипции корового белка и полимеразы вируса из рекомбинантной прегеномной РНК может быть снижена, как описано для репортерных белков (таких как люцифераза) выше. Если происходит такая сниженная экспрессия расположенных по ходу транскрипции корового белка и полимеразы вируса, например, когда общая длина двух или более тагов превосходит приблизительно 22 аминокислоты, для восстановления репликации вируса может потребоваться транскомплементация по коровому белку и полимеразе. Например, согласно данному изобретению, можно применять клетки/клеточные линии, конститутивно экспрессирующие коровый белок гепаднавируса и полимеразу гепаднавируса (core/pol), в частности, при указанных обстоятельствах.
Как и нуклеиновая кислота, кодирующая только один таг, нуклеиновая кислота, кодирующая два или более тагов, может быть слита с 5'-концом нуклеиновой кислоты, кодирующей антиген Е гепаднавируса, встроена в нуклеиновую кислоту, кодирующую антиген Е гепаднавируса и/или слита с 3'-концом нуклеиновой кислоты, кодирующей антиген Е гепаднавируса. Таги могут быть разделены ликером: таг-линкер-таг, если слиты два тага, таг-линкер-таг-линкер-таг, если слиты три тага и т.д.
Таким образом, получаемый химерный белок может содержать два или более тагов на N-конце, внутри (т.е. в составе антигена Е гепаднавируса / в виде внутреннего эпитопа) и/или на С-конце. Как показано в данном документе, таг, являющийся внутренним эпитопом, можно применять для надежной оценки уровня меченого антигена Е гепаднавируса и, следовательно, он является предпочтительным. В данном изобретении предусмотрено применение получаемого слитого белка с одним тагом, например, на N-конце и, например, вторым внутренним тагом и/или, например, третьим тагом на С-конце. Без отклонения от сущности изобретения, очевидными являются следующие комбинации, которые охвачены данным изобретением.
Два или более тагов могут представлять собой гемагглютининовый (НА)-таг, His-таг, Flag-таг, c-myc-таг, V5-таг и/или С9-таг. Flag-таг может представлять собой 1×Flag-таг или 3×Flag-таг.
Далее следует более подробное описание молекул нуклеиновой кислоты, которую применяют в данном изобретении.
Молекула нуклеиновой кислоты может содержать нуклеотидную последовательность, кодирующую прекоровый белок гепаднавируса, такой как прекоровый белок HBV. Пример нуклеотидной последовательности, кодирующей прекоровый белок гепаднавируса, приведен в SEQ ID NO: 15, а пример аминокислотной последовательности, кодирующей прекоровый белок гепаднавируса, приведен в SEQ ID NO: 17.
Молекула нуклеиновой кислоты может содержать нуклеотидную последовательность, кодирующую один или несколько тагов, как определено и описано выше. Последовательность, кодирующая один или несколько тагов, может быть (встроена) в направлении 3' по ходу транскрипции относительно нуклеотидной последовательности, кодирующей N-концевой сигнальный пептид и линкер прекорового белка гепаднавируса.
Применительно к вирусу гепатита В, N-концевой сигнальный пептид и линкер составляют 29 N-концевых аминокислот прекорового белка, как показано, например, в SEQ ID NO. 17. Соответственно, нуклеотидная последовательность, кодирующая один или несколько тагов, может быть (встроена) в направлении 3' по ходу транскрипции относительно нуклеотидной последовательности, кодирующей 29 N-концевых аминокислот прекорового белка вируса гепатита В. Другими словами, нуклеотидная последовательность, кодирующая один или несколько тагов, может быть (встроена) в направлении 3' по ходу транскрипции на расстоянии 87 нуклеотидов от 5' конца нуклеиновой кислоты, кодирующей прекоровый белок HBV (нуклеиновая кислота, кодирующая прекоровый белок, приведена, например, в SEQ ID NO. 15). На уровне белка, один или несколько тагов могут быть встроены в С-концевом направлении относительно аминокислотного остатка, соответствующего позиции 29 прекорового белка вируса гепатита В (аминокислоты прекорового белка показаны, например, в SEQ ID NO. 17).
Применительно к HBeAg, линкер составляет N-концевые 10 аминокислот HBeAg, как показано, например, в SEQ ID NO. 18. Применительно к HBeAg, нуклеотидная последовательность, кодирующая один или несколько тагов, может быть (встроена) в направлении 3' по ходу транскрипции относительно нуклеотидной последовательности, кодирующей N-концевые 10 аминокислот HBeAg. Другими словами, нуклеотидная последовательность, кодирующая один или несколько тагов, может быть (встроена) в направлении 3' по ходу транскрипции на расстоянии 30 нуклеотидов от 5' конца нуклеиновой кислоты, кодирующей HBeAg HBV (нуклеиновая кислота, кодирующая HBeAg, приведена, например, в SEQ ID NO. 16). На уровне белка, один или несколько тагов могут быть встроены в С-концевом направлении относительно аминокислотного остатка, соответствующего позиции 10 HBeAg (аминокислоты HBeAg показаны, например, в SEQ ID NO. 18).
Точнее, нуклеотидная последовательность, кодирующая один или несколько тагов, может быть (встроена) между нуклеотидами, соответствующими позициям 87 и 88 нуклеотидной последовательности, кодирующей прекоровый белок HBV (нуклеиновая кислота, кодирующая прекоровый белок HBV, приведена, например, в SEQ ID NO. 15). Указанные позиции ограничивают в эпсилон-структуре пгРНК гепаднавируса или в эпсилон-структуре, кодируемой геномом гепаднавируса, кодирующую последовательность линкера и стартовый кодон ОРС, кодирующей коровый белок гепаднавируса. Применительно к HBV, позиция 87 является последним 3' нуклеотидом последовательности, кодирующей линкер, а позиция 88 является первым нуклеотидом последовательности, кодирующей коровый белок.
На уровне белка, один или несколько тагов могут быть встроены в направлении между аминокислотными остатками, соответствующими позициям 29 и 30 прекорового белка вируса гепатита В (аминокислоты прекорового белка показаны, например, в SEQ ID NO. 17).
Аналогично, нуклеотидная последовательность, кодирующая один или несколько тагов, может быть (встроена) между нуклеотидами, соответствующими позициям 30 и 31 нуклеотидной последовательности, кодирующей HBeAg (нуклеотидная последовательность, кодирующая HBeAg, приведена, например, в SEQ ID NO. 16). На уровне белка, один или несколько тагов могут быть встроены между аминокислотными остатками, соответствующими позициям 10 и 11 HBeAg (аминокислоты HBeAg показаны, например, в SEQ ID NO. 18).
Нуклеиновая кислота, кодирующая один или несколько тагов, может быть (встроена) в направлении 5' против хода транскрипции относительно нуклеиновой кислоты, кодирующей коровый белок гепаднавируса, такого как коровый белок HBV. Пример нуклеотидной последовательности, кодирующей коровый белок HBV, приведен в SEQ ID NO: 23. Пример аминокислотной последовательности корового белка HBV, приведен в SEQ ID NO: 24.
Описанный выше сайт встраивания нуклеотидной последовательности, кодирующей один или несколько тагов, также можно определить в соответствии с позициями нуклеотидов в геноме гепаднавируса. По отношению к геному HBV молекула нуклеиновой кислоты, содержащая последовательность, кодирующую один или несколько тагов, может, согласно описанию выше, быть встроена между нуклеотидами, соответствующими позиции С1902 и позиции А1903 генома HBV. Указанные позиции можно определить в соответствии с номенклатурой, как описано, например, Galibert, F., et al. (1979), Nature 281:646-650.
Очевидно, что нуклеотиды (позиции) «С1902» и «А1903», упоминаемые в данном документе, относятся к последнему нуклеотиду кодирующей последовательности прекорового белка и первому нуклеотиду AUG кодирующей последовательности корового белка, соответственно. Они являются консервативными для последовательностей различных генотипов HBV (А-Н) (а также для приведенных здесь последовательностей SEQ ID NOs: 27-34). Соответственно, не являющиеся исчерпывающими примеры нуклеотидных последовательностей генома HBV, применяемые в данном изобретении, приведены в SEQ ID NO: 27, 28, 29, 30, 31, 32, 33 или 34. При этом, у некоторых редких (клинических) изолятов может отличаться нуклеотид «С», но не нуклеотид «А» в последовательности AUG корового белка или их позиции. Данные последовательности также входят в рамки изобретения.
Согласно данному изобретению, нуклеотидная последовательность, кодирующая один или несколько тагов, может быть встроена между нуклеотидами, соответствующими позиции С1902 и позиции А1903 генома гепаднавируса, отличного от генома HBV. Указанные соответствующие позиции генома гепаднавируса (т.е. позиции генома гепаднавируса, соответствующие позиции С1902 и позиции А1903 генома HBV) можно легко определить. Другими словами, нуклеотидная последовательность, кодирующая один или несколько тагов, может быть встроена между эпсилон-структурой пгРНК гепаднавируса, предпочтительно пгРНК HBV, или эпсилон-структурой, кодируемой геномом гепаднавируса (предпочтительно, геномом HBV), и стартовым кодоном ОРС нуклеотидной последовательности, кодирующей коровый белок гепаднавируса.
Например, если молекула нуклеиновой кислоты содержит нуклеотидную последовательность, кодирующую прекоровый белок гепаднавируса, последовательность, кодирующая один или несколько тагов, может быть (встроена) в направлении 3' по ходу транскрипции относительно нуклеотидной последовательности, кодирующей N-концевой сигнальный пептид и линкер прекорового белка гепаднавируса. Нуклеотидная последовательность, кодирующая N-концевой сигнальный пептид и линкер прекорового белка гепаднавируса, может быть легко определена. Последовательность начинается со стартового кодона (и, следовательно, включает стартовый кодон) ОРС нуклеотидной последовательности, кодирующей прекоровый белок гепаднавируса, и заканчивается перед стартовым кодоном ОРС нуклеотидной последовательности, кодирующей коровый белок гепаднавируса (т.е. кодирующая последовательность корового белка исключается). На уровне белка, один или несколько тагов могут быть встроены в С-концевом направлении относительно аминокислотного остатка, соответствующего С-концевому аминокислотному остатку линкера (линкера, следующего за N-концевым сигнальным пептидом).
Соответственно, нуклеотидная последовательность, кодирующая один или несколько тагов, может быть (встроена) в направлении 3' по ходу транскрипции относительно нуклеотидной последовательности, кодирующей N-концевые аминокислоты антигена Е гепаднавируса. Данные N-концевые аминокислоты составляют «линкер» прекорового белка гепаднавируса. На уровне белка, один или несколько тагов могут быть встроены в С-концевом направлении относительно С-концевого аминокислотного остатка линкера.
Точнее, нуклеотидная последовательность, кодирующая один или несколько тагов, может быть (встроена) между нуклеотидами, соответствующими позициям 87 и 88 нуклеотидной последовательности, кодирующей прекоровый белок HBV (нуклеиновая кислота, кодирующая прекоровый белок HBV, приведена, например, в SEQ ID NO. 15). На уровне белка, один или несколько тагов могут быть встроены в направлении между аминокислотными остатками, соответствующими позициям 29 и 30 прекорового белка вируса гепатита В (аминокислоты прекорового белка показаны, например, в SEQ ID NO. 17). Указанные позиции ограничивают в эпсилон-структуре пгРНК гепаднавируса, предпочтительно пгРНК HBV, или в эпсилон-структуре, кодируемой геномом гепаднавируса, предпочтительно геномом HBV, кодирующую последовательность линкера и стартовый кодон ОРС нуклеотидной последовательности, кодирующей коровый белок гепаднавируса. Применительно к HBV, позиция 87 является последним 3' нуклеотидом последовательности, кодирующей линкер, а позиция 88 является первым нуклеотидом последовательности, кодирующей коровый белок. Соответствующие позиции прекорового белка гепаднавируса HBV (т.е. позиции генома гепаднавируса, соответствующие позициям 87 и 88 нуклеотидной последовательности, кодирующей прекоровый белок HBV) можно легко определить.
Аналогично, нуклеотидная последовательность, кодирующая один или несколько тагов, может быть (встроена) между нуклеотидной последовательностью, кодирующей N-концевой сигнальный пептид и линкер прекорового белка гепаднавируса, и нуклеотидной последовательностью, кодирующей коровый белок гепаднавируса.
Например, нуклеотидная последовательность может быть (встроена) между нуклеотидами, соответствующими позициям 30 и 31 нуклеотидной последовательности, кодирующей HBeAg (нуклеотидная последовательность, кодирующая HBeAg, приведена, например, в SEQ ID NO. 16). На уровне белка один или несколько тагов могут быть встроены между аминокислотными остатками, соответствующими позициям 10 и 11 HBeAg (аминокислоты HBeAg показаны, например, в SEQ ID NO. 18). Указанные позиции ограничивают кодирующую последовательность N-концевого линкера гепаднавируса в прекоровом белке (или кодирующую последовательность N-концевого линкера гепаднавируса антигена Е гепаднавируса) и стартовый кодон ОРС нуклеотидной последовательности, кодирующей коровый белок гепаднавируса. Применительно к HBV, позиция 30 является последним 3' нуклеотидом последовательности, кодирующей линкер, в нуклеотидной последовательности, кодирующей HBeAg. Позиция 31 является первым нуклеотидом последовательности, кодирующей коровый белок. Соответствующие позиции нуклеотидной последовательности, кодирующей антиген Е гепаднавируса (т.е. позиции антигена Е гепаднавируса, соответствующие позициям 30 и 31 нуклеотидной последовательности, кодирующей HBeAg) можно легко определить.
Нуклеиновая кислота, кодирующая один или несколько тагов, может быть (встроена) в направлении 5' против хода транскрипции относительно нуклеиновой кислоты, кодирующей коровый белок гепаднавируса, такого как коровый белок HBV. Пример нуклеотидной последовательности, кодирующей коровый белок HBV, приведен в SEQ ID NO: 23. Пример аминокислотной последовательности корового белка HBV, приведен в SEQ ID NO: 24. Другими словами, нуклеотидная последовательность, кодирующая один или несколько тагов, может быть встроена между эпсилон-структурой пгРНК гепаднавируса, предпочтительно пгРНК HBV, или эпсилон-структурой, кодируемой геномом гепаднавируса (предпочтительно, геномом HBV), и стартовым кодоном ОРС нуклеотидной последовательности, кодирующей коровый белок гепаднавируса, предпочтительно, коровый белок HBV.
Как упоминалось выше, молекула нуклеиновой кислоты, которую применяют/предлагают в данном изобретении, может содержать последовательность, кодирующую один или несколько тагов, при этом указанная последовательность встроена в эпсилон-структуру пгРНК гепаднавируса, предпочтительно пгРНК HBV, или эпсилон-структуру, кодируемую геномом гепаднавируса, предпочтительно, геномом HBV. Приведенная в качестве примера эпсилон-структура, кодируемая геномом HBV, показана на Фиг. 1. Применительно к HBV, эпсилон-структура, кодируемая геномом HBV, начинается (и включает) позицию Т1849 и заканчивается (и включает) позицию А1909 генома HBV. Пример нуклеотидной последовательности эпсилон-структуры, кодируемой геномом HBV, приведен в SEQ ID NO: 25.
Как указано выше, молекула нуклеиновой кислоты, содержащая последовательность, кодирующую один или несколько тагов, может быть встроена в нижний стебель эпсилон-структуры пгРНК гепаднавируса, предпочтительно пгРНК HBV, или кодируемой геномом гепаднавируса, предпочтительно, геномом HBV. Пример нижнего стебля эпсилон-структуры, кодируемой геномом HBV, показан на Фиг. 1. Например, нуклеотидная последовательность, кодирующая один или несколько тагов, может быть встроена между нуклеотидами, соответствующими позициям 87 и 88 нуклеотидной последовательности, кодирующей прекоровый белок HBV (нуклеотидная последовательность, кодирующая прекоровый белок HBV, приведена, например, в SEQ ID NO. 15), или между нуклеотидами, соответствующими позициям 30 и 31 нуклеотидной последовательности, кодирующей HBeAg (нуклеотидная последовательность, кодирующая HBeAg, приведена, например, в SEQ ID NO. 16) или между нуклеотидами, соответствующими позиции С1902 и позиции А1903 генома HBV. Все указанные позиции находятся в нижнем стебле эпсилон-структуры пгРНК гепаднавируса, предпочтительно пгРНК HBV, или в нижнем стебле эпсилон-структуры, кодируемой геномом гепаднавируса, предпочтительно геномом HBV.
В данном изобретении предусмотрено и предпочтительно, что молекула нуклеиновой кислоты, содержит в направлении 5' от последовательности, кодирующей один или несколько тагов, последовательность, способную образовывать пары с основаниями нижнего стебля эпсилон-структуры пгРНК гепаднавируса, предпочтительно пгРНК HBV, или нижнего стебля эпсилон-структуры, кодируемой геномом гепаднавируса, предпочтительно, геномом HBV. Считают, что описанные в данном документе эксперименты и сведения, касающиеся вируса гепатита В/меченого антигена Е вируса гепатита В в целом применимы к гепаднавирусам/меченому антигену Е гепаднавирусов. Единственная модификация встраиваемой последовательности, применительно к HBV, может относиться к модификации 5' фланкирующей последовательности нуклеотидной последовательности, кодирующей (эпитопный) таг для образования пар с основаниями эпсилон-структуры пгРНК гепаднавируса, предпочтительно, пгРНК HBV, или эпсилон-структуры, кодируемой геномом гепаднавируса, предпочтительно геномом HBV, для каждого конкретного гепаднавируса, предпочтительно HBV. На основании сведений, изложенных в данном изобретении, специалист в области техники сможет легко сконструировать и получить нуклеотидную последовательность, расположенную в направлении 5' относительно нуклеотидной последовательности, кодирующей таг, для образования пар с основаниями эпсилон-структуры пгРНК гепаднавируса, предпочтительно, пгРНК HBV, или эпсилон-структуры, кодируемой геномом гепаднавируса, предпочтительно геномом HBV. В частности, в случае вируса гепатита В уток (DHBV), поскольку стартовый кодон ОРС корового белка расположен по ходу транскрипции относительно эпсилон-структуры, нет необходимости встраивать 5' фланкирующую последовательность для нуклеотидной последовательности, кодирующей (эпитопный) таг, для образования пар с основаниями эпсилон-структуры DHBV.
Как показано на Фиг. 1, нуклеотидную последовательность встраивали между нуклеотидами, соответствующими позициям С1902 и А1903 генома HBV, при этом указанная нуклеотидная последовательность содержала 5' фланкирующую область из 9 нуклеотидов (т.е. расположенную в 5' направлении относительно нуклеотидной последовательности, кодирующей один или несколько тагов), которая образовывала пары с основаниями нижнего стебля эпсилон-структуры пгРНК гепаднавируса, предпочтительно пгРНК HBV, или эпсилон-структуры, кодируемой геномом гепаднавируса, предпочтительно, геномом HBV, например, с нуклеотидами, соответствующими позициям Т1849-Т1855 генома HBV.
Важным и предпочтительным аспектом данного изобретения является то, что нуклеотидная последовательность, кодирующая один или несколько тагов, описанная в данном документе и/или встраиваемая, как описано выше в данном документе, дополнительно содержит нуклеотидную последовательность, которая способна образовывать пары с основаниями эпсилон-структуры пгРНК гепаднавируса, предпочтительно пгРНК HBV, или эпсилон-структуры, кодируемой геномом гепаднавируса, предпочтительно, геномом HBV, в частности, с основаниями нижнего стебля эпсилон-структуры пгРНК гепаднавируса, предпочтительно пгРНК HBV, или эпсилон-структуры, кодируемой геномом гепаднавируса, предпочтительно, геномом HBV. Применяя нуклеотидную последовательность, способную образовывать пары с основаниями эпсилон-структуры, преследуют цель сохранить эпсилон-структуру пгРНК гепаднавируса, предпочтительно пгРНК HBV, или эпсилон-структуру, кодируемую геномом гепаднавируса, предпочтительно, геномом HBV. Полагают, что эпсилон-структура, в свою очередь, имеет важное значение для репликации, продукции кзкДНК и экспрессии/продукции (меченого) антигена Е гепаднавируса, предпочтительно антигена Е HBV.
Предпочтительно, последовательность, способная образовывать пары с основаниями нижнего стебля эпсилон-структуры пгРНК гепаднавируса, предпочтительно пгРНК HBV, или эпсилон-структуры, кодируемой геномом гепаднавируса, предпочтительно, геномом HBV, способна образовывать пары с нуклеотидами, предпочтительно соответствующими позициям от Т1849 до А1854 или, возможно, соответствующими позициями от Т1849 до Т1855 генома HBV. Как правило, спаривание оснований в пгРНК происходит между комплементарными рибонуклеотидами, такими как A-U, G-C, а также может образовываться нестабильная пара между основаниями G-U. Если эпсилон-структура сохраняется, репликация, продукция кзкДНК и/или экспрессия/продукция меченого антигена Е гепаднавируса с молекул нуклеиновых кислот, применяемых/описанных в данном изобретении, не нарушается.
Следует отметить, что левое плечо эпсилон-структуры является частью нуклеотидной последовательности, кодирующей сигнальный пептид антигена Е гепаднавируса (такого как HBeAg) и, таким образом, должно оставаться неизменным. Встраивание в правое плечо эпсилон-структуры, созданное согласно описанию, не должно нарушать спаривание оснований нижнего стебля. В качестве примера приведено встраивание, показанное на Фиг. 1, в котором единственная замена нуклеотида относится к A1903G (т.е. замене А на G в позиции 1903 генома HBV). Точечная мутация в позиции 1903 сдвигает ОРС корового белка из эпсилон-структуры пгРНК гепаднавируса, предпочтительно пгРНК HBV, или эпсилон-структуры, кодируемой геномом гепаднавируса, предпочтительно геномом HBV, обеспечивая сохранение эпсилон-структуры и встраивание тага перед AUG корового белка. Коровый белок транслируется с прегеномной РНК, которая транскрибируется после стартового кодона ОРС прекорового белка, так что таг не будет включаться в коровый белок.
5' фланкирующая последовательность эпитопного тага, способная образовывать пары с основаниями (нижнего стебля) эпсилон-структуры пгРНК гепаднавируса, предпочтительно пгРНК HBV, или эпсилон-структуры, кодируемой геномом гепаднавируса, предпочтительно, геномом HBV, включает в себя до 3, 6 или 9 нуклеотидов, обычно 9 нуклеотидов.
Приведенная в качестве примера последовательность, способная образовывать пары с основаниями нижнего стебля эпсилон-структуры пгРНК гепаднавируса, предпочтительно пгРНК HBV, или эпсилон-структуры, кодируемой геномом гепаднавируса, предпочтительно, геномом HBV, состоит из последовательности, приведенной в SEQ ID No. 26. Приведенная в качестве примера последовательность, способная образовывать пары с основаниями нижнего стебля эпсилон-структуры пгРНК гепаднавируса, предпочтительно пгРНК HBV, или эпсилон-структуры, кодируемой геномом гепаднавируса, предпочтительно, геномом HBV, кодирует полипептид, приведенный в SEQ ID NO. 40.
Молекула нуклеиновой кислоты для применения в данном изобретении/предложенная в данном изобретении, дополнительно может содержать в направлении 3' относительно последовательности, кодирующей один или несколько тагов, нуклеотидную последовательность, кодирующую линкер. Линкер может состоять из одного или нескольких аминокислотных остатков. Предпочтительно, линкер состоит только из одного аминокислотного остатка, такого как остаток глицина.
Например, нуклеотидная последовательность, кодирующая линкер, состоит из последовательности GGC; или нуклеотидная последовательность кодирует остаток глицина. GGC копируется с 3 исходных нуклеотидов перед AUG открытой рамки считывания корового белка, которые вместе с AUG образуют типичный мотив Kozak для оптимальной инициации трансляции. Таким образом, линкер, который можно применять/встраивать, предпочтительно и целесообразно выбирать таким образом, чтобы сохранять аутентичный мотив Kozak стартового кодона корового белка.
Например, молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую меченый антиген Е гепаднавируса, может содержать нуклеотидную последовательность, приведенную в SEQ ID NO. 41. Например, молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую меченый антиген Е гепаднавируса, может содержать нуклеотидную последовательность, кодирующую аминокислотную последовательность, приведенную в SEQ ID NO. 42. Приведенная в качестве примера нуклеотидная последовательность, приведенная в SEQ ID NO: 41, состоит из нуклеотидной последовательности, способной спариваться с основаниями (нижнего стебля) эпсилон-структуры (GTGGACATC; в частности, нуклеотиды GTGGACAT спариваются с нуклеотидами, соответствующими позициям от Т1849 до Т1855 генома HBV), нуклеотидной последовательности, кодирующей НА-таг и нуклеотидной последовательности, кодирующей остаток глицина в качестве линкера (последняя нуклеотидная последовательность, прежде всего, целесообразна для сохранения аутентичного мотива Kozak стартового кодона корового белка).
Предполагают, что один или несколько тагов слиты в рамке считывания с антигеном Е гепаднавируса, предпочтительно, с антигеном Е вируса гепатита В (HBeAg). Аналогично, предполагают, что нуклеотидная последовательность, кодирующая один или несколько тагов (с возможной 5' фланкирующей нуклеотидной последовательностью, способной спариваться с основаниями (нижнего стебля) эпсилон-структуры и/или с возможной 3' нуклеотидной последовательностью, сохраняющей аутентичный мотив Kozak стартового кодона корового белка или кодирующей линкер) слита в рамке считывания с нуклеотидной последовательностью, кодирующей антиген Е гепаднавируса, предпочтительно, антиген Е вируса гепатита В (HBeAg).
Молекула нуклеиновой кислоты для применения в данном изобретении предложенная в данном изобретении, может содержать геном гепаднавируса, предпочтительно геном вируса гепатита В (HBV). Например, геном HBV представляет собой геном HBV генотипа А, В, С, D, Е, F, G или Н. Не являющиеся исчерпывающими примеры нуклеотидных последовательностей генома HBV, для применения в данном изобретении, приведены в SEQ ID NO: 27, 28, 29, 30, 31, 32, 33 или 34. Геном HBV может быть геномом HBV генотипа D, в частности, геномом HBV подтипа ayw (как геном HBV, приведенный в SEQ ID NO: 27).
Согласно данному изобретению, применяют только те молекулы нуклеиновых кислот, такие как геномы гепаднавируса, которые обеспечивают (существенную) экспрессию/продукцию (меченого) антигена Е гепаднавируса. Например, известны некоторые клинические варианты HBV, которые не обеспечивают существенной экспрессии/продукции антигена Е гепаднавируса. У некоторых клинических вариантов HBV, то, что они являются HBeAg-негативными, является следствием либо двойной мутации основного корового промотора (basal core promoter, ВСР) (A1764T/G1766A при генотипе D), либо мутации прекорового белка (G1898A при генотипе D). Тогда как мутации ВСР снижают HBeAg за счет снижения транскрипции мРНК прекорового белка, мутация прекорового белка приводит к появлению преждевременного стоп-кодона, останавливающего трансляцию прекорового белка. Такие варианты гепаднавируса в меньшей степени подходят для способов, предложенных в данном описании.
В предпочтительном воплощении данного изобретения меченый HBeAg содержит или состоит из аминокислотной последовательности, приведенной в SEQ ID NO: 22. Соответствующая нуклеотидная последовательность, кодирующая меченый HBeAg, приведена в SEQ ID NO: 20. Указанные последовательности особенно целесообразны в контексте данного изобретения, но являются всего лишь примерами предпочтительных воплощений.
Нуклеотидная последовательность, кодирующая меченый прекоровый белок, т.е. предшественник меченого HBeAg, приведена в SEQ ID NO: 19. Поскольку указанная нуклеотидная последовательность кодирует предшественник меченного HBeAg, ее можно считать нуклеотидной последовательностью, кодирующей меченный HBeAg. Соответствующая аминокислотная последовательность приведена в SEQ ID NO: 21.
Ниже следует более подробное описание, касающееся получения меченого антигена Е гепаднавируса и его применения для оценки способности молекулы-кандидата ингибировать кзкДНК гепаднавируса.
Нуклеиновая кислота для применения в данном изобретении/предложенная в данном изобретении может транскрибироваться в прегеномную (пг) РНК гепаднавируса, в частности, прегеномную (пг) РНК HBV.
Предусматривают, что указанная нуклеиновая кислота может быть сконструирована для предупреждения трансляции меченого антигена Е гепаднавируса. Например, нуклеиновая кислота не содержит стартового кодона ATG в 5' направлении относительно нуклеиновой кислоты, кодирующей меченый антиген Е гепаднавируса. Применительно к HBV, может быть произведена делеция или мутация стартового кодона нуклеиновой кислоты, кодирующей прекоровый белок. Например, указанный стартовый кодон (который подлежит делеции/мутации) может соответствовать нуклеотидам от позиции (и включая позицию) 1816 до позиции (и включая позицию) 1818 генома HBV, см., например, Фиг. 1.
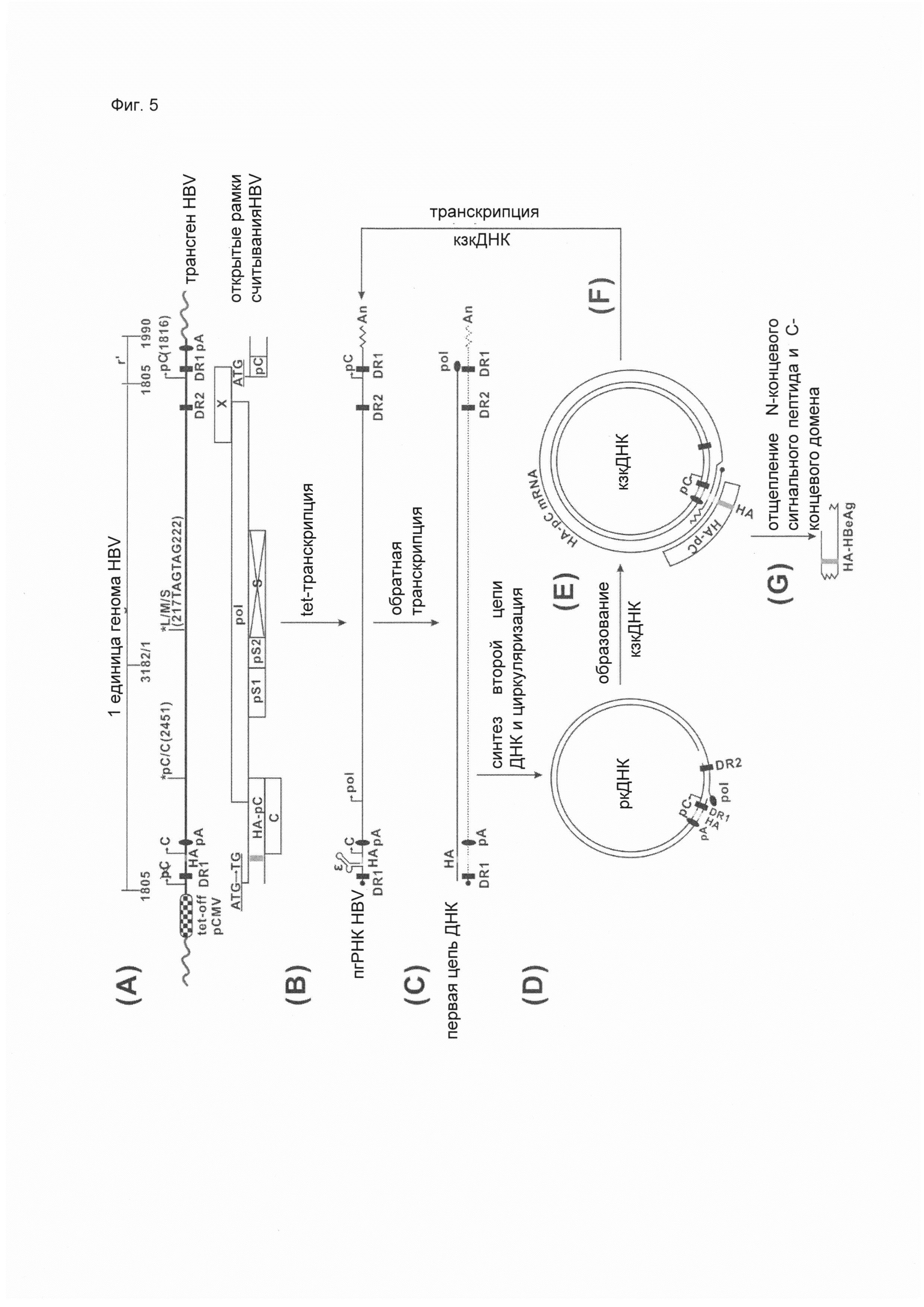
Недопущение трансляции меченого антигена Е гепаднавируса может быть целесообразным для недопущения его продукции/экспрессии в начале анализа. Целью данного изобретения является применение меченого антигена Е гепаднавируса в качестве суррогатного маркера кзкДНК. Если меченый антиген Е гепаднавируса образуется постоянно, его экспрессия/продукция не обязательно коррелируют с продукцией кзкДНК. Как показано на Фиг. 5, стартовый кодон можно восстановить на более поздней стадии анализа, когда/после того как образуется кзкДНК, так чтобы экспрессия/продукция (т.е. уровень) меченого антигена Е гепаднавируса справедливо отражала продукцию/экспрессию кзкДНК гепаднавируса. Таким образом, для более достоверной оценки способности молекулы-кандидата ингибировать кзкДНК, целесообразно, чтобы продукция/экспрессия меченого антигена Е гепаднавируса подавлялась в начале исследования, например, за счет удаления/мутации стартового кодона соответствующей нуклеиновой кислоты, кодирующей его, и чтобы продукция/экспрессия меченого антигена Е гепаднавируса становилась возможной позднее, чтобы отражать продукцию/уровень кзкДНК гепаднавируса.
Например, стартовый кодон ATG в 5' направлении относительно нуклеиновой кислоты, кодирующей меченый антиген Е гепаднавируса, согласно данному описанию, можно заменить нуклеотидами TG. Аналогично, молекула нуклеиновой кислоты для применения в данном изобретении и предложенная в данном изобретении, может быть модифицирована, например, за счет точечной мутации для предупреждения трансляции меченого антигена Е гепаднавируса.
Стадия (а) способа, применяемого согласно данному изобретению, может дополнительно включать стадию (аа), которая включает культивирование клетки, содержащей молекулу нуклеиновой кислоты, содержащую нуклеотидную последовательность, кодирующую меченый антиген Е гепаднавируса, в условиях, обеспечивающих
(i) синтез прегеномной (пг) РНК гепаднавируса;
(ii) обратную транскрипцию указанной синтезированной пгРНК в минус-цепь ДНК;
(iii) синтез второй плюс-цепи ДНК, чтобы указанная минус-цепь ДНК и указанная плюс-цепь ДНК образовывали двуцепочечную релаксированную кольцевую ДНК;
(iv) образование кзкДНК из указанной релаксированной кольцевой двуцепочечной ДНК;
(v) восстановление условий, обеспечивающих трансляцию меченого антигена Е гепаднавируса;
(vi) транскрипцию мРНК, кодирующей меченый антиген Е гепаднавируса;
(vii) трансляцию меченого антигена Е гепаднавируса;
Восстановление условий, обеспечивающих трансляцию меченого антигена Е гепаднавируса, может относиться к восстановлению или представлять собой восстановление стартового кодона, согласно объяснению и описанию, приведенным выше.
Молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую меченый антиген Е гепаднавируса, может содержаться в векторе, в частности, экспрессирующем векторе.
Вектор, например, может содержать последовательность, приведенную в SEQ ID NO: 35.
Молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую меченый антиген Е гепаднавируса, предпочтительно, антиген Е вируса гепатита В (HBeAg), может находиться под контролем индуцируемого промотора. Неисчерпывающими примерами индуцируемых промоторов для применения в данном изобретении являются тетрациклин-индуцируемый промотор, доксициклин-индуцируемый промотор, антибиотик-индуцируемый промотор, медь-индуцируемый промотор, спирт-индуцируемый промотор, стероид-индуцируемый промотор или гербицид-индуцируемый промотор. В описанных здесь экспериментах промотор, индуцируемый тетрациклином (доступный для приобретения в компании Clontech), работал по механизму tet-off (в присутствии тетрациклина экспрессия под контролем индуцируемого тетрациклином промотора подавляется). Полагают, что в данном изобретении также можно применять индуцируемый тетрациклином промотор, работающий по механизму tet-on. Например, системы tet-on/off, как на основе плазмиды, так и на основе вируса (ретровируса, аденовируса), можно приобрести в компаниях Clontech и Invitrogen. Помимо промоторов, индуцируемых тетрациклином/доксициклином, описанных выше, подходят и другие индуцируемые промоторы, которые, помимо прочих соединений, регулируются, например, антибиотиками, медью, спиртом, стероидами или гербицидами. Например, индуцируемым промотором является CMV промотор. Индуцируемый промотор может быть промотором tet-EF-1 альфа.
Кроме того, один или несколько стоп-кодонов могут быть встроены в кодирующую область одного или нескольких белков оболочки гепаднавируса, например, одного или нескольких белков оболочки гепаднавируса, являющихся одним или несколькими белками оболочки HBV. Один или несколько белков оболочки гепаднавируса (HBV) могут представлять собой один или несколько больших поверхностных белков (L), средних поверхностных белков (М) и малых поверхностных белков (S). В одном воплощении белок оболочки HBV представляет собой малый поверхностный белок (S). Приведенные в качестве примера кодирующие области одного или нескольких белков оболочки HBV показаны в SEQ ID NO: 36 (L), SEQ ID NO: 37 (M) и/или SEQ ID NO: 38 (S). В составе HBV нуклеотиды с 217 до 222 (TTGTTG) последовательности SEQ ID NO: 38 (S) могут быть мутированы, например, в TAGTAG, для предотвращения экспрессии белков оболочки.
Молекула-кандидат считается способной ингибировать кзкДНК гепаднавируса, если уровень (экспрессии) суррогатного маркера кзкДНК, меченого антигена Е гепаднавируса, снижается по сравнению с контролем.
Следует понимать, что оцениваемый уровень (экспрессии) меченого антигена Е гепаднавируса сравнивают с контролем, таким как стандартное или референтное значение уровня (экспрессии) меченого антигена Е гепаднавируса. Согласно данному описанию, контрольное (стандартное/референтное значение) можно оценивать в клетках, тканях или у животных, не являющихся человеком, которые не находились в контакте с молекулой-кандидатом. В альтернативном случае, согласно данному описанию, контрольное (стандартное/референтное значение) можно оценивать в клетках, тканях или у животных, не являющихся человеком, перед упомянутой выше стадией приведения в контакт. Снижение уровня (экспрессии) меченого антигена Е гепаднавируса при контакте с молекулой-кандидатом также можно сравнивать со снижением уровня (экспрессии) меченого антигена Е гепаднавируса под воздействием используемых в рутинной практике референтных соединений, таких как соединения, которые, как известно, не способны ингибировать кзкДНК. Специалист в данной области легко определит/оценит, снижается ли уровень (экспрессии) меченого антигена Е гепаднавируса.
И наоборот, не отклоняясь от сущности изобретения, в качестве положительного контроля можно использовать, например, референтные соединения, такие как соединения, которые, как известно, способны ингибировать кзкДНК. Молекула-кандидат считается способной ингибировать кзкДНК гепаднавируса, если уровень (экспрессии) суррогатного маркера кзкДНК, меченого антигена Е гепаднавируса, является эквивалентным или даже повышенным по сравнению с таким (положительным) контролем.
Согласно данному изобретению, в частности описанным здесь способам скрининга или выявления, клетка, ткань или животное, не являющееся человеком, подлежащие приведению в контакт с молекулой-кандидатом, содержат молекулу нуклеиновой кислоты, содержащую нуклеотидную последовательность, кодирующую меченый антиген Е гепаднавируса, согласно данному описанию.
Например, указанная клетка, ткань или животное, не являющееся человеком, могут быть способны экспрессировать меченный антиген Е гепаднавируса, согласно данному описанию. Как описано в данном изобретении, способность молекулы-кандидата ингибировать/быть антагонистом кзкДНК можно соответственно детектировать путем определения уровня экспрессии такого генного продукта нуклеотидной последовательности, кодирующей меченный антиген Е гепаднавируса, в частности, уровня экспрессии белка. Низкий уровень экспрессии (белка) (по сравнению с контролем (стандартным или референтным значением)) указывает на способность молекулы-кандидата действовать как ингибитор/антагонист.
Из-за пониженного транспорта/уровня экспрессии уровень транслируемого генного продукта (т.е. уровень белка) также будет снижен. Уровень (белка) описанного выше белка меченного антигена Е гепаднавируса обычно коррелирует с силой детектируемого сигнала, ассоциированного с белком - меченым антигеном Е гепаднавируса. Приведенные в качестве примера белки, меченые антигены Е гепаднавируса, могут содержать репортер, согласно описанию выше (например, люциферазу, (зеленый/красный) флуоресцентный белок и их варианты, улучшенный зеленый флуоресцентный белок EGFP и т.п.).
Аналогично, снижение сигнала репортера при контакте клетки/ткани/животного, не являющегося человеком, с молекулой-кандидатом будет указывать, что молекула-кандидат действительно является ингибитором/антагонистом и, следовательно, способна ингибировать кзкДНК. Молекулы-кандидаты, снижающие уровень меченного антигена Е гепаднавируса, согласно данному описанию, выбраны из исследуемых молекул-кандидатов, при этом предпочтительно выбирают те молекулы, которые значительно снижают уровень меченного антигена Е гепаднавируса (что выражается, например, в снижении сигнала репортера).
В контексте данного изобретения (в частности, описанных здесь способах скрининга/определения) предполагают, что в контакт также можно приводить клеточные экстракты (например, клеточные экстракты, содержащие молекулу нуклеиновой кислоты, содержащую нуклеотидную последовательность, кодирующую меченый антиген Е гепаднавируса, описанный и охарактеризованный в данном документе). Например, указанные клеточные экстракты можно получить из (трансгенных/генетически модифицированных) клеток, тканей и/или животных, не являющихся человеком, для применения в данном изобретении, в частности, для приведения в контакт с молекулой-кандидатом.
Применение указанных клеточных экстрактов особенно целесообразно, поскольку позволяет оценить активность молекулы-кандидата in vitro. Способы оценки/скрининга, в которых используют такие (клеточные) экстракты, можно, например, применять для предварительного скрининга молекул-кандидатов, при этом молекулы выбирают в ходе предварительного скрининга и затем подвергают последующему скринингу, например, описанными здесь способами с использованием клеток, в частности, способами, в которых (трансгенные) клетки, ткани и/или животные, не являющиеся человеком, приводят в контакт с молекулой-кандидатом. Соответственно, в данном контексте предпочтительно, чтобы молекула-кандидат была отобрана способом предварительного скрининга in vitro, как описано в данном документе выше и ниже.
Таким образом, термин «клетка», используемый в данном документе, охватывает (трансгенные/генетически модифицированные) клетки, (трансгенные/генетически модифицированные) ткани и/или (трансгенных/генетически модифицированных) животных, не являющихся человеком, а также клеточные экстракты, полученные из них.
Следует понимать, что при высокопроизводительном скрининге обычно проводят одновременный скрининг многих (зачастую тысяч) молекул-кандидатов. Соответственно, при (первом) скрининге отбирают молекулы-кандидаты, которые снижают уровень меченого антигена Е гепаднавируса.
Стадию (а) способа скрининга по данному изобретению, т.е. «стадию приведения в контакт» также можно осуществлять путем добавления (биологического) образца или композиции, содержащих указанную молекулу-кандидата или множество молекул-кандидатов (т.е. различные молекулы-кандидаты), к анализируемой клетке (клетке/ткани/животному, не являющемуся человеком, которые содержат молекулу нуклеиновой кислоты, содержащую нуклеотидную последовательность, кодирующую меченый антиген Е гепаднавируса).
Как правило, молекулы-кандидаты или композиции, содержащие/включающие в себя молекулы-кандидаты могут, например, быть добавлены к (трансфицированной) клетке, ткани или животному, не являющемуся человеком, содержащим молекулу нуклеиновой кислоты, содержащую нуклеотидную последовательность, кодирующую меченый антиген Е гепаднавируса. Согласно данному описанию и изложению, термин «содержащие молекулу нуклеиновой кислоты, содержащую нуклеотидную последовательность, кодирующую меченый антиген Е гепаднавируса» предполагает применение репортеров. Также в данном изобретении можно применять репортерные конструкции, содержащие промотор и/или энхансер.
Клетки, ткани и/или животные, не являющиеся человеком, для применения в данном изобретении или предложенные в данном изобретении, в частности, когда речь идет о способах скрининга/определения, могут быть стабильно или транзиторно трансфицированы молекулой нуклеиновой кислоты, содержащей нуклеотидную последовательность, кодирующую меченый антиген Е гепаднавируса.
Полагают, что соединения/молекулы, способные ингибировать кзкДНК (что выражается в снижении уровня меченого антигена Е гепаднавируса) будут эффективными агентами в фармацевтических приложениях, описанных в данном документе, и найдут применение в медицинских целях, в частности, в лечении заболеваний, связанных с гепаднавирусами, в частности, хронических заболеваний, связанных с гепаднавирусами, таких как хронический гепатит, и в частности, хронический гепатит В.
Молекулы-кандидаты/соединения, которые могут выполнять функцию специфических «антагонистов» или «ингибиторов» кзкДНК гепаднавируса, могут представлять собой низкомолекулярные связывающиеся соединения, такие как низкомолекулярные (органические) соединения.
Термин «низкомолекулярный» хорошо известен в контексте разработки лекарств и относится к медицинским соединениям, имеющим молекулярный вес менее 2500 Дальтон, предпочтительно менее 1000 Дальтон, более предпочтительно между 50 и 350 Дальтон. (Низкомолекулярные) связывающиеся соединения включают соединения естественного и искусственного происхождения. Термин «соединение» (или аналогичный термин «молекула») в контексте данного изобретения включает одиночные соединения или множество соединений. Указанные соединения/молекулы могут содержаться, например, в образцах, например, в клеточных экстрактах, например, растений, животных или микроорганизмов. Кроме того, указанные соединения могут быть известны в области техники, но их способность (отрицательно) влиять на кзкДНК гепаднавируса ранее не была известна. Множество соединений можно, например, добавлять к образцу in vitro, к культуральной среде или вводить в клетку.
Агенты-кандидаты могут также содержать функциональные группы, необходимые для структурного взаимодействия с белками, особенно для образования водородных связей, и, как правило, включают по меньшей мере аминогруппу, карбонильную группу, гидрокси-группу или карбоксильную группу, предпочтительно по меньшей мере две из функциональных химических групп. Агенты-кандидаты часто содержат карбоциклические или гетероциклические структуры и/или ароматические или полиароматические структуры, замещенные одной или несколькими из указанных выше функциональных групп.
Примеры классов агентов-кандидатов могут включать гетероциклы, пептиды, сахариды, стероиды и т.п. Соединения можно модифицировать для улучшения эффективности, стабильности, фармацевтической совместимости и т.п. Для идентификации, создания или скрининга дополнительных агентов можно устанавливать структуру агента. Например, когда идентифицируют пептиды, их можно различным образом модифицировать для улучшения их стабильности, например, с использованием аминокислот, не встречающихся в природе, таких как D-аминокислоты, в частности, D-аланин, за счет функционализации амино- или карбокси-конца, например, ацилирования или алкилирования аминогруппы или эстерификации или амидирования карбоксильной группы. Другие способы стабилизации могут включать инкапсулирование, например, в липосомы и т.д.
Как указано выше, агенты-кандидаты также находят среди других биомолекул, включая аминокислоты, жирные кислоты, пурины, пиримидины, нуклеиновые кислоты и производные, структурные аналоги или их комбинации. Агенты-кандидаты получают из многочисленных источников, включая библиотеки синтетических или естественных соединений. Например, существуют различные средства для случайного и направленного синтеза многочисленных органических соединений и биомолекул, включая экспрессию рандомизированных олигонуклеотидов и олигопептидов. В альтернативном случае, доступны и легко создаются библиотеки естественных соединений в форме экстрактов бактерий, грибов, растений и животных. Кроме того, естественные или полученные синтетическим путем библиотеки и соединения легко модифицировать с помощью стандартных химических, физических и биохимических средств, и можно применять для получения комбинаторных библиотек. Известные фармакологические агенты можно подвергать направленным или случайным химическим модификациям, таким как ацилирование, алкилирование, эстерификация, амидирование и т.д. для получения структурных аналогов.
В данном изобретении также предусмотрено, что для определения способности ингибировать кзкДНК можно исследовать соединения/молекулы, которые включают, помимо прочих, пептиды, белки, нуклеиновые кислоты (включая библиотеки, экспрессирующие кДНК), низкомолекулярные органические соединения, лиганды, пептидо-нуклеиновые кислоты (ПНК) и т.п. Указанные соединения также могут быть функциональными производными или аналогами.
Способы получения химических производных и аналогов хорошо известны специалистам в области техники и описаны, например, Beilstein, "Handbook of Organic Chemistry", Springer Edition New York, or in "Organic Synthesis", Wiley, New York. Кроме того, согласно данному изобретению можно исследовать влияние указанных производных и аналогов, т.е. их антагонистическое действие на кзкДНК.
Кроме того, можно использовать пептидомиметики соответствующих антагонистов или ингибиторов кзкДНК и/или применять для разработки компьютерные технологии. Компьютерные системы, подходящие для компьютерных разработок, например, белков и пептидов, известны в области техники и описаны, например, Berry (1994) Biochem. Soc. Trans. 22:1033-1036; Wodak (1987), Ann. N.Y. Acad. Sci. 501:1-13; Pabo (1986), Biochemistry 25:5987-5991. Результаты, полученные в указанном компьютерном анализе, можно применять в комбинации со способом по изобретению, например, для оптимизации известных соединений, веществ или молекул. Соответствующие соединения также можно идентифицировать посредством синтеза комбинаторных библиотек пептидомиметиков путем последовательной химической модификации и исследования получаемых соединений, например, в соответствии с описанными в данном документе способами. Способы получения и применения комбинаторных библиотек пептидомиметиков описаны на уровне техники, например, Ostresh (1996) Methods in Enzymology 267:220-234 and Dorner (1996) Bioorg. Med. Chem. 4:709-715. Кроме того, для дизайна антагонистов (пептидомиметиков) кзкДНК можно использовать трехмерную и/или кристаллографическую структуру антагонистов кзкДНК (Rose (1996) Biochemistry 35:12933-12944; Rutenber (1996) Bioorg. Med. Chem. 4:1545-1558).
Идентификацию/исследование молекул-кандидатов, способных ингибировать кзкДНК можно в том числе осуществлять при помощи трансфекции соответствующего хозяина молекулой нуклеиновой кислоты, содержащей нуклеотидную последовательность, кодирующую меченый антиген Е гепаднавируса, и приведения в контакт с молекулой-кандидатом.
Клетки-хозяева для применения в данном изобретении предпочтительно представляют собой клетки-эукариоты, в частности, клетки-эукариоты гепатоцитарного происхождения. Эукариотические клетки предпочтительно являются клетками гепатомы или клетками печени. Эукариотические клетки также могут происходить от клеток гепатомы или клеток печени. Предпочтительными клетками для применения в данном изобретении являются эукариотические клетки HepG2 (АТСС #НВ-8065). HepG2 известны своей способностью поддерживать образование и транскрипцию функциональной кзкДНК HBV. В данном изобретении предусмотрено и применение других клеток, таких как клеток, происходящих от гепатоцитов (например, Huh7). Также, в соответствии с изобретением, можно применять клетки непеченочного происхождения, при условии, что они поддерживают образование кзкДНК гепаднавируса (или, в более широком смысле, репликацию ДНК гепаднавируса). Например, такие клетки/хозяева непеченочного происхождения можно модифицировать, чтобы они поддерживали образование кзкДНК гепаднавируса (или репликацию ДНК гепаднавируса), если прегеномная РНК вводится в клетки или транскрибируется с матрицы ДНК с помощью экзогенного промотора. Транскрипция кзкДНК может иметь место, если осуществляют транскомплементацию таких непеченочных клеток по специфическим печеночным факторам транскрипции. Молекула нуклеиновой кислоты по изобретению или вектор, содержащий ее, могут быть стабильно интегрированы в геном клетки.
Молекула нуклеиновой кислоты для применения согласно данному изобретению (т.е. молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую меченый антиген Е гепаднавируса) или вектор, содержащий ее, предпочтительно состоят (по существу) из ДНК.
Объяснения, данные в данном документе выше применительно к «клеткам» также относятся и охватывают ткани/животных, не являющихся человеком, или производные этих клеток. Клетка для применения в данном изобретении также может содержаться в образце, например, биологическом, медицинском или патологическом образце. Например, предусматривается применение жидкостей, которые содержат клетки, тканей или клеточных культур. Такие жидкости могут представлять собой жидкости организма или выделения, а также могут быть культуральными образцами. Жидкости организма могут содержать кровь, сыворотку, плазму, мочу, слюну, синовиальную жидкость, спинальную жидкость, цереброспинальную жидкость, слезы, кал и т.п., но не ограничиваться ими.
Аналогично, молекулы-кандидаты могут содержаться в биологическом образце или композиции. Зачастую первому скринингу подвергают (множество) молекул-кандидатов. Образцы/композиции, оказавшиеся положительными при первом скрининге, могут подвергаться последующему скринингу для верификации предыдущих результатов и отбора наиболее эффективных ингибиторов/антагонистов. В ходе множества раундов скрининга и отбора выбирают такие молекулы-кандидаты, которые демонстрируют выраженную способность быть ингибиторами/антагонистами кзкДНК, как описано и изложено в данном документе. Например, партии (например, композиций/образцов), содержащие множество молекул-кандидатов, будут подвергаться повторному скринингу и партии, в которых молекулы-кандидаты не проявляют или проявляют недостаточную ингибиторную активность, будут отбрасываться без повторного тестирования.
Например, если тестируют (биологический) образец или композицию с множеством различных молекул-кандидатов и один (биологический) образец или одна композиция оказываются положительными, в этом случае можно провести повторный скрининг отдельных молекул из биологического образца или композиции, предпочтительно после выделения. Также можно провести последующий скрининг подгрупп (биологических) образцов или композиций, использованных в первом скрининге. Скрининг композиций с подгруппами тех молекул-кандидатов, которые исследовали в предыдущих раундах скрининга, таким образом, сузит круг возможных эффективных ингибиторов кзкДНК. Это может облегчить и ускорить процесс скрининга, в частности, когда проводят скрининг большого количества молекул. Соответственно, число раундов скрининга снижается по сравнению с тестированием каждой молекулы-кандидата в отдельности в первом и последующем скрининге (что, несомненно, также возможно). Таким образом, в зависимости от сложности или количества молекул-кандидатов, стадии способа скрининга, описанные в данном изобретении, можно осуществлять несколько раз до тех пор, как (биологический) образец или композиция, подлежащие скринингу, не будут содержать ограниченное число веществ, предпочтительно, одно вещество, что будет указывать на способность молекулы, проходящей скрининг, снижать уровень меченого антигена Е гепаднавируса.
В данном изобретении предусмотрено применение методов оптического измерения, например, флуоресцентных, обладающих разрешающей способностью на уровне одиночных клеток или тканей, например, на субклеточном уровне. Данные методы могут включать флуоресцентные методы, например, конфокальную микроскопию, цифровую регистрацию изображений, как в камерах на основе устройств с зарядовой связью, и соответствующее программное обеспечение для анализа изображений. Например, стадию (б) осуществляют после измерения стандартного ответа при выполнении контрольного эксперимента. Например, в клетке, ткани или у животного, не являющегося человеком, определяют уровень меченого антигена Е гепаднавируса без приведения в контакт с молекулой-кандидатом при первом скрининге. При втором скрининге, после приведения в контакт с молекулой-кандидатом, определяют/оценивают уровень меченного антигена Е гепаднавируса. Разница между уровнями указывает, является ли исследуемая молекула-кандидат антагонистом/ингибитором кзкДНК.
Уровень меченого антигена Е гепаднавируса можно определить путем измерения, например, уровня генных продуктов (в частности, уровня белка меченого антигена Е гепаднавируса) любым из описанных здесь способов, в частности, методом определения/детекции/оценки белка.
Например, можно определить экспрессию на уровне белка с помощью методов иммуноагглютинации, иммунопреципитации (например, иммунодиффузии, иммуноэлектрофореза, иммунной фиксации), вестерн-блоттинга (например, иммуногистохимии (in situ), иммуноцитохимии (in situ), аффинной хроматографии, иммуноферментных методов) и т.п. Количество очищенного полипептида в растворе можно определить физическими методами, например, фотометрией. Способы количественного определения конкретного белка в смеси основаны на специфическом связывании, например, антител. Специфические способы количественного и качественного определения, которые основаны на специфичности антител, включают, например, иммуногистохимию (in situ). Например, концентрация/уровень белка меченого антигена Е гепаднавируса в клетке, ткани или у животного, не являющегося человеком, можно определить методом иммуноферментного анализа (ELISA).
В данном изобретении предусмотрено, что оценку уровня меченого антигена Е гепаднавируса согласно стадии (б) можно осуществлять с помощью ELISA, CLIA или AlphaLISA.
В способах, которые предложены в данном описании, используют известные таги (такие как НА-таг или His-таг, Flag-таг, c-myc-таг, V5-таг или С9-таг, которые можно использовать вместо НА-тага или в дополнение к нему). Указанные таги можно использовать для очистки и детекции меченого антигена Е гепаднавируса. Используя антитела, специфически связывающиеся с тагом (например, в тестах ELISA, хемилюминесцентном ELISA (CLIA) и AlphaLISA), можно надежно и быстро оценивать уровень меченого антигена Е гепаднавируса и избегать перекрестной реакции с коровым белком.
Оценка уровня меченого антигена Е гепаднавируса согласно стадии (б) предложенного здесь способа может включать применение антитела, специфически распознающего указанный антиген Е гепаднавируса, предпочтительно антиген Е вируса гепатита В (такого как Anti-HBe: клон 29, лот 20110305, Autobio Diagnostics, не ограничиваясь им) и одного или нескольких антител, специфически распознающих один или несколько тагов (такого как Anti-HA: кат. номер А01244-100, Genscript, но не ограничиваясь им).
Согласно данному изобретению можно использовать следующие антитела, специфически распознающие антиген Е вируса гепатита В:
Imai, et al. Demonstration of two distinct antigenic determinants on hepatitis В e antigen by monoclonal antibodies. J. Immunol. 1982 Jan; 128(1):69-72.
Ferns and Tedder. Monoclonal antibodies to hepatitis В antigen (HBeAg) derived from hepatitis В core antigen (HBcAg): their use in characterization and detection of HBeAg. J Gen Virol. 1984 May; 65 (Pt 5):899-908.
Mondelli et al. Differential distribution of hepatitis В core and E antigens in hepatocytes: analysis by monoclonal antibodies. Hepatology. 1986 6(2): 199-204.
Stuckmann and Mushahwar. Re-examination and further characterization of a monoclonal antibody to hepatitis В e antigen (anti-HBe). J Virol Methods. 1986 Jul; 13(4):351-62.
Korec et al. Monoclonal antibodies against hepatitis В e antigen: production, characterization, and use for diagnosis. J Virol Methods. 1990 May; 28(2):165-9.
Usuda et al. A monoclonal antibody against a hepatitis В e antigen epitope borne by six amino acids encoded by the precore region. J Virol Methods. 1997 Nov; 68(2):207-15.
Sogut et al. Monoclonal antibodies specific for hepatitis В e antigen and hepatitis В core antigen. Hybridoma (Larchmt). 2011 Oct; 30(5):475-9.
В альтернативном случае, можно выполнять вестерн-блоттинг или иммуногистохимическое окрашивание. Вестерн-блоттинг сочетает разделение смеси белков путем электрофореза и специфическое определение с помощью антител. Электрофорез может быть многомерным, например, таким как двумерный электрофорез. Как правило, при двумерном электрофорезе полипептиды разделяют в одном измерении согласно их кажущейся молекулярной массе, а в другом измерении согласно их изоэлектрической точке.
Специалист в данной области способен определить количество полипептидов/белков, в частности, генных продуктов, описанных выше в данном документе, используя корреляцию, предпочтительно линейную корреляцию, между интенсивностью детектируемого сигнала и количеством, например, полипептидов/белков, подлежащих определению. Соответственно, уровень меченого антигена Е гепаднавируса можно определить по уровню белка меченого антигена Е гепаднавируса. Специалисту в данной области известны стандартные способы, применяемые для определения в образце уровня продукта экспрессии - количества/концентрации белка меченого антигена Е гепаднавируса или он может найти соответствующие способы в стандартных руководствах (например, Sambrook, 2001).
Молекулы-кандидаты отбирают, если уровень меченого антигена Е гепаднавируса (или соответствующего репортерного сигнала) сильно понижается, предпочтительно является очень низким или не детектируемым. Например, уровень меченого антигена Е гепаднавируса (или соответствующего репортерного сигнала) может быть снижен по меньшей мере на 50%, 60%, 70%, 80%, более предпочтительно по меньшей мере на 90% по сравнению с (контрольным) стандартным значением.
Способы трансфекции клеток или тканей известны в области техники. Соответственно, чтобы клетки или ткани экспрессировали указанные репортерные конструкции, для их трансфекции можно применять обработку фосфатом кальция или электропорацию (см. Sambrook (2001), loc. cit.). Кроме того, молекулы нуклеиновых кислот, экспрессирующие указанные репортерные конструкции, можно помещать в липосомы для доставки в клетки-мишени. В качестве другой альтернативы, чтобы клетки экспрессировали специфические репортерные конструкции, их можно трансдуцировать с помощью генетически модифицированных вирусных векторов.
В другом воплощении животное, не являющееся человеком, содержащее указанную репортерную конструкцию для детекции ингибирования кзкДНК, является трансгенным животным, отличным от человека. Не являющийся человеком организм для применения в описанных способах скрининга может быть выбран из группы, состоящей из С. elegans, дрожжей, дрозофил, данио, морских свинок, крыс и мышей. Получение такого трансгенного животного известно специалистам в данной области. Соответствующие методики описаны, помимо прочего, в главе 3.16 "Current Protocols in Neuroscience" (2001), John Wiley&Sons.
Соответственно, изобретение также относится к способу получения трансгенного животного, не являющегося человеком, который включает стадию введения молекулы нуклеиновой кислоты, содержащей нуклеотидную последовательность, кодирующую меченый антиген Е гепаднавируса, как описано в данном документе, в эмбриональную стволовую клетку или в половую клетку. Трансгенное животное, не являющееся человеком, предложенное и описанное в данном документе, наиболее эффективно применять в способах скрининга и фармакологических тестах, описанных выше. Трансгенное животное, не являющееся человеком, описанное в данном документе, можно применять в скрининге лекарств, а также в научных и медицинских исследованиях, в которых изучают, выбирают и/или выделяют антагонисты/ингибиторы кзкДНК для лечения заболеваний, ассоциированных с гепаднавирусами.
Трансгенные генетически модифицированные клетки, ткани и/или животные, не являющиеся человеком, для применения в контексте данного изобретения, в частности, способах скрининга/определения, содержат описанную и охарактеризованную в данном документе молекулу нуклеиновой кислоты, содержащую нуклеотидную последовательность, кодирующую меченый антиген Е гепаднавируса.
Данное изобретение относится к применению клетки, ткани или животного, не являющегося человеком, для скрининга и/или валидации соединения, которое предположительно является ингибитором кзкДНК гепаднавируса.
Термин «трансгенное животное, не являющееся человеком», «трансгенная клетка» или «трансгенная ткань» в данном документе относятся к отличному от человека животному, к ткани или клетке, которые не являются человеческими, содержащим иной генетический материал соответствующего животного, ткани или клетки дикого типа. Термин «генетический материал» в данном контексте может представлять собой любые разновидности молекул нуклеиновых кислот или их аналоги, например, молекулы нуклеиновых кислот или их аналоги, описанные в данном документе. Термин «иной» означает дополнительный или содержащийся в меньшем количестве генетический материал по отношению к геному животного или животной клетки дикого типа. Обзор различных систем экспрессии, которые применяют для создания трансгенных клеток/животных, приведен, например, в публикациях Methods in Enzymology 153 (1987), 385-516, in Bitter et al., (Methods in Enzymology 153 (1987), 516-544) и Sawers et al., (Applied Microbiology and Biotechnology 46 (1996), 1-9), Billman-Jacobe (Current Opinion in Biotechnology 7 (1996), 500-4), Hockney (Trends in Biotechnology 12 (1994), 456-463), Griffiths et al., (Methods in Molecular Biology 75 (1997), 427-440).
Данное изобретение относится к молекуле нуклеиновой кислоты, описанной выше в данном документе, т.е. молекуле нуклеиновой кислоты, содержащей нуклеотидную последовательность, кодирующую меченый антиген Е гепаднавируса. Объяснения и определения, приведенные в данном документе выше, применимы с учетом необходимых изменений. Антиген Е гепаднавируса, предпочтительно, представляет собой антиген Е вируса гепатита В (HBeAg).
Меченый антиген Е гепаднавируса может содержать только один таг. Таг состоит из 6-22 аминокислот. Типичный и предпочтительный (эпитопный) таг состоит из 8, 9, 10 или 11 аминокислот. 6xHis представляет собой минимальный эпитопный таг, который может применяться в данном изобретении. Допускается, чтобы вставка менее чем 6 аминокислот вместе с прилегающими аминокислотами HBeAg образовывала неоэпитоп, так чтобы в результате указанной вставки также образовался меченый гепаднавирус. Таг может представлять собой гемагглютининовый (НА) таг, His-таг, Flag-таг, c-myc-таг, V5-таг или С9-таг. Flag-таг может представлять собой 1×Flag-таг или 3×Flag-таг.
Меченый антиген Е гепаднавируса может содержать два или более тагов. Предпочтительно, два или более тагов являются различными тагами. Суммарная длина указанных двух или более тагов может составлять приблизительно от 12 до приблизительно 31 аминокислоты. Например, суммарная длина двух или более тагов может составлять 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30 или 31 аминокислоту. Два или более тагов могут представлять собой два или более гемагглютининовых (НА)-тагов, His-тагов, Flag-тагов, c-myc-тагов, V5-тагов и/или С9-тагов. Flag-таг может представлять собой 1×Flag-таг или 3×Flag-таг.
Примеры нуклеотидных последовательностей, кодирующих таг(и), представляют собой нуклеотидную последовательность, кодирующую НА таг, приведенную в SEQ ID NO: 1, нуклеотидную последовательность, кодирующую His-таг, приведенную в SEQ ID NO: 2, нуклеотидную последовательность, кодирующую c-myc-таг, приведенную в SEQ ID NO: 4, нуклеотидную последовательность, кодирующую V5-таг, приведенную в SEQ ID NO: 5, и/или нуклеотидную последовательность, кодирующую С9-таг, приведенную в SEQ ID NO: 6.
Примеры нуклеотидных последовательностей, кодирующих Flag-таг, представляют собой нуклеотидную последовательность, кодирующую 1×Flag-таг, приведенную в SEQ ID NO: 3, или нуклеотидную последовательность, кодирующую 3×Flag-таг, приведенную в SEQ ID NO: 7.
Примерами аминокислотных последовательностей тагов являются аминокислотная последовательность НА тага, приведенная в SEQ ID NO: 8, аминокислотная последовательность His-тага, приведенная в SEQ ID NO: 9, аминокислотная последовательность c-myc-тага, приведенная в SEQ ID NO: 11, аминокислотная последовательность V5-тага, приведенная в SEQ ID NO: 12, аминокислотная последовательность С9-тага, приведенная в SEQ ID NO: 13.
Примерами аминокислотных последовательностей Flag-тага являются аминокислотная последовательность 1×Flag-тага, приведенная в SEQ ID NO: 10, или аминокислотная последовательность 3×Flag-тага, приведенная в SEQ ID NO: 14.
Пример нуклеотидной последовательности, кодирующей HBeAg, приведен в SEQ ID NO: 16. Пример аминокислотной последовательности HBeAg приведен в SEQ ID NO: 18.
Молекула нуклеиновой кислоты может содержать нуклеотидную последовательность, кодирующую прекоровый белок гепаднавируса. Пример нуклеотидной последовательности, кодирующей прекоровый белок гепаднавируса, приведен в SEQ ID NO: 15. Пример аминокислотной последовательности прекорового белка гепаднавируса приведен в SEQ ID NO: 17.
Молекула нуклеиновой кислоты может содержать нуклеотидную последовательность, кодирующую один или несколько тагов, где указанная последовательность (встроена) в направлении 3' по ходу транскрипции относительно нуклеотидной последовательности, кодирующей N-концевой сигнальный пептид и линкер прекорового белка гепаднавируса.
Нуклеотидная последовательность, кодирующая один или несколько тагов, может быть (встроена) в направлении 3' по ходу транскрипции относительно нуклеотидной последовательности, кодирующей 29 N-концевых аминокислот прекорового белка вируса гепатита В.
Молекула нуклеиновой кислоты может содержать геном гепаднавируса. Предпочтительно, геном гепаднавируса представляет собой геном вируса гепатита В (HBV). Геном HBV может быть геномом HBV генотипа А, В, С, D, Е, F, G или Н. Геном HBV может быть геномом генотипа D. Предпочтительно, геном HBV является геномом HBV генотипа D подтипа ayw.
Нуклеиновая кислота, кодирующая один или несколько тагов, может быть (встроена) в направлении 5' против хода транскрипции относительно нуклеиновой кислоты, кодирующей коровый белок гепаднавируса, предпочтительно, коровый белок HBV. Пример нуклеотидной последовательности, кодирующей коровый белок HBV, приведен в SEQ ID NO: 23. Коровый белок может представлять собой коровый белок HBV. Пример аминокислотной последовательности корового белка HBV приведен в SEQ ID NO: 24.
Молекула нуклеиновой кислоты, содержащая последовательность, кодирующую один или несколько тагов, может быть встроена в эпсилон-структуру пгРНК гепаднавируса, предпочтительно пгРНК HBV, или в эпсилон-структуру, кодируемую геномом гепаднавируса, предпочтительно, геномом HBV, согласно данному описанию. Пример нуклеотидной последовательности эпсилон-структуры, кодируемой геномом HBV, приведен в SEQ ID NO: 25. Молекула нуклеиновой кислоты, содержащая последовательность, кодирующую один или несколько тагов, может быть встроена в нижний стебель эпсилон-структуры пгРНК гепаднавируса, предпочтительно пгРНК HBV, или в эпсилон-структуру, кодируемую геномом гепаднавируса, предпочтительно, геномом HBV.
Молекула нуклеиновой кислоты, содержащая последовательность, кодирующую один или несколько тагов, может быть встроена между нуклеотидами, соответствующими позициям С1902 и А1903 генома HBV.
Молекула нуклеиновой кислоты может содержать в направлении 5' от последовательности, кодирующей один или несколько тагов, последовательность, способную образовывать пары с основаниями нижнего стебля эпсилон-структуры пгРНК гепаднавируса, предпочтительно пгРНК HBV, или эпсилон-структуры, кодируемой геномом гепаднавируса, предпочтительно, геномом HBV. Последовательность, способная образовывать пары с основаниями нижнего стебля эпсилон-структуры генома (или кодируемая геномом) гепаднавируса, предпочтительно, HBV, прежде всего способна образовывать пары с нуклеотидами, соответствующими предпочтительно позициям генома HBV от Т1849 до А1854 или, возможно, соответствующими позициям от Т1849 до Т1855. Последовательность, способная образовывать пары с основаниями нижнего стебля эпсилон-структуры генома гепаднавируса, может включать в себя (вплоть до) 9 нуклеотидов.
Приведенная в качестве примера последовательность, способная образовывать пары с основаниями нижнего стебля эпсилон-структуры пгРНК гепаднавируса, предпочтительно пгРНК HBV, или эпсилон-структуры, кодируемой геномом гепаднавируса, предпочтительно, геномом HBV, состоит из последовательности, приведенной в SEQ ID No. 26. Приведенная в качестве примера последовательность, способная образовывать пары с основаниями нижнего стебля эпсилон-структуры пгРНК гепаднавируса, предпочтительно пгРНК HBV, или эпсилон-структуры, кодируемой геномом гепаднавируса, предпочтительно, геномом HBV, кодирует полипептид, приведенный в SEQ ID NO. 40.
Молекула нуклеиновой кислоты может содержать в направлении 3' относительно последовательности, кодирующей один или несколько тагов, последовательность, кодирующую линкер. Линкер может состоять из одного или нескольких аминокислотных остатков. Предпочтительно, линкер состоит только из одного аминокислотного остатка, такого как остаток глицина. Последовательность, кодирующая линкер, может состоять из последовательности GGC. Последовательность, кодирующая линкер, может кодировать остаток глицина. Кодирующая последовательность может быть целесообразна и подобрана соответствующим образом для сохранения аутентичного мотива Kozak стартового кодона корового белка.
Молекула нуклеиновой кислоты может содержать нуклеотидную последовательность, кодирующую меченый антиген Е гепаднавируса, которая содержит нуклеотидную последовательность, приведенную в SEQ ID NO. 41. Молекула нуклеиновой кислоты может содержать нуклеотидную последовательность, кодирующую меченый антиген Е гепаднавируса, которая содержит нуклеотидную последовательность, кодирующую аминокислотную последовательность, приведенную в SEQ ID NO. 42.
Предпочтительно, один или несколько тагов слиты в рамке считывания с антигеном Е гепаднавируса (или прекоровым белком Е гепаднавируса), предпочтительно, с антигеном Е вируса гепатита В (HBeAg) (или с прекоровым белком вируса гепатита В).
Пример нуклеотидной последовательности, кодирующей меченый HBeAg, приведен в SEQ ID NO: 20. Предпочтительная аминокислотная последовательность меченого HBeAg приведена в SEQ ID NO: 22.
Пример нуклеотидной последовательности, кодирующей меченый прекоровый белок вируса гепатита В, приведен в SEQ ID NO: 19. Пример аминокислотной последовательности прекорового белка вируса гепатита В приведен в SEQ ID NO: 21.
Примеры нуклеотидных последовательностей генома HBV приведены в SEQ ID NO: 27, 28, 29, 30, 31, 32, 33 или 34.
Нуклеиновая кислота может транскрибироваться в прегеномную (пг) РНК гепаднавируса. Предпочтительно, РНК гепаднавируса представляет собой РНК HBV.
Молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую меченый антиген Е гепаднавируса, может содержаться в векторе, таком как экспрессирующий вектор. Предпочтительно, антиген Е гепаднавируса, представляет собой антиген Е вируса гепатита В (HBeAg).
Как правило, нуклеиновая кислота обеспечивает трансляцию меченого антигена Е гепаднавируса, предпочтительно, антигена Е вируса гепатита В (HBeAg). Нуклеиновая кислота может содержаться в векторе, который содержит последовательность, приведенную в SEQ ID NO: 39.
В некоторых воплощениях нуклеиновая кислота сконструирована для предупреждения трансляции меченого антигена Е гепаднавируса. Например, нуклеиновая кислота не содержит стартового кодона ATG, расположенного в 5' направлении против хода транскрипции относительно нуклеиновой кислоты, кодирующей меченый антиген Е гепаднавируса. Например, стартовый кодон ATG, расположенный в 5' направлении против хода транскрипции относительно нуклеиновой кислоты, кодирующей меченый антиген Е гепаднавируса, может быть заменен нуклеотидами TG. Нуклеиновая кислота может быть модифицирована за счет точечной мутации для предупреждения трансляции меченого антигена Е гепаднавируса. Вектор может содержать последовательность, приведенную в SEQ ID NO: 35.
Молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую меченый антиген Е гепаднавируса, предпочтительно, антиген Е вируса гепатита В (HBeAg), может находиться под контролем индуцируемого промотора.
Индуцируемый промотор может представлять собой тетрациклин-индуцируемый промотор, доксициклин-индуцируемый промотор, антибиотик-индуцируемый промотор, медь-индуцируемый промотор, спирт-индуцируемый промотор, стероид-индуцируемый промотор или гербицид-индуцируемый промотор.
Индуцируемый промотор предпочтительно может быть промотором CMV. Индуцируемый промотор может быть промотором tet-EF-1 альфа.
В кодирующую область одного или нескольких белков оболочки гепаднавируса, предпочтительно, одного или нескольких белков оболочки HBV, могут быть встроены один или несколько стоп-кодонов.
Один или несколько белков оболочки HBV могут представлять собой один или несколько белков L, М и/или S. Белок оболочки HBV может представлять собой белок S.
Приведенные в качестве примера кодирующие области одного или нескольких (или приведенные в качестве примера нуклеотидные последовательности, кодирующие один или несколько) белков оболочки HBV, показаны в SEQ ID NO: 36 (L), SEQ ID NO: 37 (M) и/или SEQ ID NO: 38 (S). Нуклеотиды HBV с 217 до 222 (TTGTTG) последовательности SEQ ID NO: 38 (S) могут быть мутированы в TAGTAG для предотвращения экспрессии белков оболочки.
Данное изобретение относится к белку, кодируемому молекулой нуклеиновой кислоты, описанной и предложенной выше в данном документе.
Белок содержит меченый антиген Е гепаднавируса, предпочтительно, меченый антиген Е вируса гепатита В (HBeAg).
Антиген Е вируса гепатита В (HBeAg) может содержать аминокислотную последовательность, приведенную в SEQ ID NO: 18. Предпочтительно, меченый антиген Е гепаднавируса содержит только один таг.
Таг может состоять из 6-22 аминокислот. Таг может представлять собой гемагглютининовый (НА) таг, His-таг, Flag-таг, c-myc-таг, V5-таг или С9-таг. Flag-таг может представлять собой 1×Flag-таг или 3×Flag-таг.
Меченый антиген Е гепаднавируса может содержать два или более тагов. Предпочтительно, два или более тагов являются различными тагами. Суммарная длина указанных двух или более тагов составляет приблизительно от 14 до приблизительно 31 аминокислоты. Два или более тагов могут представлять собой два или более гемагглютининовых (НА)-тагов, His-тагов, Flag-тагов, c-myc-тагов, V5-тагов и/или С9-тагов. Flag-таг может представлять собой 1×Flag-таг или 3×Flag-таг.
Примеры нуклеотидных последовательностей, кодирующих таг, представляют собой нуклеотидную последовательность, кодирующую НА таг, приведенную в SEQ ID NO: 1, нуклеотидную последовательность, кодирующую His-таг, приведенную в SEQ ID NO: 2, нуклеотидную последовательность, кодирующую c-myc-таг, приведенную в SEQ ID NO: 4, нуклеотидную последовательность, кодирующую V5-таг, приведенную в SEQ ID NO: 5, и/или нуклеотидную последовательность, кодирующую С9-таг, приведенную в SEQ ID NO: 6.
Примеры нуклеотидных последовательностей, кодирующих Flag-таг, представляют собой нуклеотидную последовательность, кодирующую 1×Flag-таг, приведенную в SEQ ID NO: 3, или нуклеотидную последовательность, кодирующую 3×Flag-таг, приведенную в SEQ ID NO: 7.
Примерами аминокислотных последовательностей тагов являются аминокислотная последовательность НА тага, приведенная в SEQ ID NO: 8, аминокислотная последовательность His-тага, приведенная в SEQ ID NO: 9, аминокислотная последовательность c-myc-тага, приведенная в SEQ ID NO: 11, аминокислотная последовательность V5-тага, приведенная в SEQ ID NO: 12 и/или аминокислотная последовательность С9-тага, приведенная в SEQ ID NO: 13.
Примерами аминокислотных последовательностей Flag-тага являются аминокислотная последовательность 1×Flag-тага, приведенная в SEQ ID NO: 10, или аминокислотная последовательность 3×Flag-тага, приведенная в SEQ ID NO: 14.
Белок может содержать прекоровый белок гепаднавируса. Пример нуклеотидной последовательности, кодирующей прекоровый белок гепаднавируса, приведен в SEQ ID NO: 15. Пример аминокислотной последовательности прекорового белка гепаднавируса приведен в SEQ ID NO: 17.
Белок может содержать аминокислотную последовательность одного или нескольких тагов, где указанная последовательность находится в С-концевом направлении относительно аминокислотной последовательности сигнального пептида и линкера прекорового белка гепаднавируса. Белок может содержать аминокислотную последовательность одного или нескольких тагов, расположенную в С-концевом направлении относительно аминокислотной последовательности 29 N-концевых аминокислот прекорового белка вируса гепатита В.
Белок может содержать аминокислотную последовательность одного или нескольких тагов, где указанная последовательность находится в N-концевом направлении относительно аминокислотной последовательности корового белка гепаднавируса, предпочтительно в N-концевом направлении относительно аминокислотной последовательности корового белка HBV. Пример нуклеотидной последовательности, кодирующей коровый белок HBV, приведен в SEQ ID NO: 23. Пример аминокислотной последовательности корового белка HBV приведен в SEQ ID NO: 24.
Аминокислотная последовательность одного или нескольких тагов может быть встроена в аминокислотную последовательность, кодируемую эпсилон-структурой пгРНК гепаднавируса, предпочтительно пгРНК HBV, или эпсилон-структурой, кодируемой геномом гепаднавируса, предпочтительно, геномом HBV. Пример нуклеотидной последовательности эпсилон-структуры, кодируемой геномом HBV, приведен в SEQ ID NO: 25. Аминокислотная последовательность одного или нескольких тагов может быть встроена в аминокислотную последовательность, кодируемую нижним стеблем эпсилон-структуры пгРНК гепаднавируса, предпочтительно пгРНК HBV, или эпсилон-структуры, кодируемой геномом гепаднавируса, предпочтительно, геномом HBV, предпочтительно, в аминокислотную последовательность, кодируемую нижним стеблем эпсилон-структуры пгРНК гепаднавируса, предпочтительно пгРНК HBV, или эпсилон-структуры, кодируемой геномом гепаднавируса, предпочтительно, геномом HBV.
Аминокислотная последовательность одного или нескольких тагов может быть встроена между аминокислотными остатками, соответствующими позиции G29 и позиции М30 прекорового белка, например, такого, который показан в SEQ ID NO. 17.
Белок может дополнительно содержать в N-концевом направлении относительно аминокислотной последовательности одного или нескольких тагов аминокислотную последовательность из (до) 3 аминокислот, где указанная аминокислотная последовательность длиной до 3 аминокислот способна образовывать пары с основаниями нижнего стебля эпсилон-структуры пгРНК гепаднавируса, предпочтительно пгРНК HBV, или эпсилон-структуры, кодируемой геномом гепаднавируса, предпочтительно, геномом HBV. Предпочтительно, нуклеотидная последовательность, способная образовывать пары с основаниями нижнего стебля эпсилон-структуры пгРНК гепаднавируса, предпочтительно пгРНК HBV, или эпсилон-структуры, кодируемой геномом гепаднавируса, предпочтительно, геномом HBV, прежде всего способна образовывать пары с нуклеотидами, предпочтительно соответствующими позициям от Т1849 до А1854 или, возможно, соответствующими позициями от Т1849 до Т1855 генома HBV. Приведенная в качестве примера нуклеотидная последовательность, способная образовывать пары с основаниями нижнего стебля эпсилон-структуры пгРНК гепаднавируса, предпочтительно пгРНК HBV, или эпсилон-структуры, кодируемой геномом гепаднавируса, предпочтительно, геномом HBV, состоит из последовательности, приведенной в SEQ ID No. 26. Пример аминокислотной последовательности из (до) 3 аминокислот приведен в SEQ ID NO: 40.
Белок может дополнительно содержать линкер, расположенный в С-концевом направлении относительно аминокислотной последовательности одного или нескольких тагов. Линкер может состоять из одного или нескольких аминокислотных остатков. Предпочтительно, линкер состоит только из одного аминокислотного остатка, такого как остаток глицина.
Аминокислотная последовательность меченого антигена Е гепаднавируса может содержать аминокислотную последовательность, кодируемую нуклеотидной последовательностью, приведенной в SEQ ID NO. 41. Аминокислотная последовательность меченого антигена Е гепаднавируса может содержать аминокислотную последовательность, приведенную в SEQ ID NO. 42.
Предпочтительно, один или несколько тагов слиты в рамке считывания с антигеном Е гепаднавируса, предпочтительно, с антигеном Е вируса гепатита В (HBeAg).
Пример нуклеотидной последовательности, кодирующей меченый HBeAg, приведен в SEQ ID NO: 20. Предпочтительно, меченый HBeAg имеет аминокислотную последовательность, приведенную в SEQ ID NO: 22.
Пример нуклеотидной последовательности, кодирующей меченый прекоровый белок HBV, приведен в SEQ ID NO: 19. Пример аминокислотной последовательности меченого прекорового белка гепаднавируса приведен в SEQ ID NO: 21.
Данное изобретение относится к клетке-хозяину, содержащей молекулу нуклеиновой кислоты, описанную и предложенную в данном документе, и/или к клетке-хозяину, содержащей белок, описанный и предложенный в данном документе. Клетка-хозяин может быть эукариотической клеткой. Эукариотическая клетка может иметь гепатоцитарное происхождение. Эукариотическая клетка может быть клеткой гепатомы или может происходить от клетки гепатомы. В предпочтительном воплощении эукариотическая клетка представляет собой HepG2 (АТСС #НВ-8065).
Данное изобретение относится к процессу получения белка, описанного в данном изобретении, указанный процесс включает культивирование хозяина, как описано выше, при условиях, обеспечивающих экспрессию белка и выделение полученного белка из культуры.
Данное изобретение относится к набору для применения в способе данного изобретения. Также, данное изобретение относится к применению набора для скрининга молекул-кандидатов, предположительно способных ингибировать ковалентно замкнутую кольцевую ДНК гепаднавируса. Объяснения, приведенные в данном документе выше, касающиеся способа оценки способности молекулы-кандидата ингибировать кзкДНК гепаднавируса, применимы с соответствующими изменениями и к набору.
Набор может содержать антитело, специфически распознающее антиген Е гепаднавируса, описанный в данном документе, и одно или несколько антител, специфически распознающих один или несколько тагов, описанных в данном документе.
Набор (для применения при осуществлении) данного изобретения или способы и применения по изобретению могут дополнительно включать или сопровождаться инструкциями. Например, указанные инструкции могут служить ориентиром для специалиста в оценке способности молекул-кандидатов ингибировать кзкДНК и/или в оценке уровня меченого антигена Е гепаднавируса согласно данному изобретению. В частности, указанные инструкции могут содержать информацию о применении или использовании предложенных в данном документе способов и применений.
Набор (создаваемый при осуществлении) данного изобретения может дополнительно включать вещества/химические соединения и/или устройства, подходящие/необходимые для осуществления способов и применений данного изобретения. Например, указанные вещества/химические соединения и/или устройства представляют собой растворители, разбавители и/или буферы для стабилизации и/или хранения соединений, необходимых для специфического определения уровня ((экспрессии) белка) указанного меченого антигена Е гепаднавируса, как описано в данном документе.
Также, данное изобретение относится к применению молекулы нуклеиновой кислоты, описанной и предложенной в данном документе, белка, описанного и предложенного в данном документе, и/или клетки-хозяина, описанной и предложенной в данном документе, для скрининга молекул-кандидатов, предположительно способных ингибировать ковалентно замкнутую кольцевую ДНК гепаднавируса. Объяснения, приведенные в данном документе выше, касающиеся способа оценки способности молекулы-кандидата ингибировать кзкДНК гепаднавируса, применимы к ним с соответствующими изменениями.
В данном описании «содержащий» и «включающий» или их грамматические варианты следует понимать как характеристику указанных признаков, значений, стадий или компонентов, не исключающую добавление одного или нескольких дополнительных признаков, значений, стадий, компонентов или их групп. Указанный термин охватывает термины «состоящий из» и «состоящий по существу из». Так, термины «содержащий/включающий/имеющий» означают, что может присутствовать любой другой дополнительный компонент (равно как и признаки, значения, стадии и т.п.).
Термин «состоящий из» означает, что дополнительного компонента (равно как и признаков, значений, стадий и т.п.) присутствовать не может.
Термин «по существу состоящий из» или его грамматические варианты, используемые в данном описании, следует трактовать как характеристику указанных признаков, значений, стадий или компонентов, не исключающую добавление одного или нескольких дополнительных признаков, значений, стадий, компонентов или их групп, но только в том случае, если дополнительные признаки, значения, стадии, компоненты или их группы не изменяют существенным образом основные и новые характеристики заявленной композиций, устройства или способа.
Так, термин «по существу состоящий из» означает, что могут присутствовать определенные дополнительные компоненты (равно как и признаки, значения, стадии и т.п.), а именно те, которые существенным образом не влияют на основные характеристики композиции, устройства или способа. Другими словами, термин «по существу состоящий из» (который может использоваться взаимозаменяемо с термином «по существу содержащий») допускает присутствие иных компонентов в композиции, устройстве или способе в дополнение к обязательным компонентам (равно как и признакам, значениям, стадиям и т.п.), при условии, что присутствие других компонентов существенным образом не влияет на существенные характеристики устройства или способа.
Термин «способ» относится к методам, средствам, технологиям и процедурам для достижения заданной цели, включая такие методы, средства, технологии и процедуры, которые либо известны, либо могут быть легко выведены специалистом в области химии, биологии и биофизики из известных методов, средств, технологий и процедур.
В данном описании термин «выделенный» относится к композиции, которая отделена от своего окружения in vivo. Предпочтительно, выделенные композиции или соединения по данному изобретению по существу свободны от других веществ (например, других белков или других соединений), которые присутствуют в их окружении in vivo (т.е. очищенные или наполовину очищенные композиции или соединения).
Термин «приблизительно» в данном документе обозначает ± 10%.
Для более подробного описания данного изобретения приведены следующие графические материалы и примеры, которые не являются исчерпывающими.
Если не указано иное, использовали общепринятые генно-инженерные методики, описанные, например, Sambrook, Russell "Molecular Cloning, A Laboratory Manual", Cold Spring Harbor Laboratory, N.Y. (2001), включенные во всей полноте путем ссылки.
Данное изобретение проиллюстрировано следующими примерами.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Фиг. 1. Встраивание последовательности НА-тага в открытую рамку считывания прекорового белка HBV
Показана нуклеотидная последовательность ОРС прекорового белка HBV (генотип D, подтип ayw, нт 1816-2454) вместе с 5'-концевой частью (нуклеотиды 1816-1941). Последовательность между нуклеотидом 1941 и стоп-кодоном ОРС прекорового белка не показана. Стартовый кодон ОРС прекорового белка, последовательность прямого повтора 1 (direct repeat, DR1) и находящийся в рамке считывания стартовый кодон ОРС корового белка заключены в рамки. В плазмиде pTREHBV-HAe стартовый кодон 5' конца ОРС прекорового белка мутирован (ATG на TG). Аутентичный сайт инициации транскрипции пгРНК (нуклеотид 1820) указан стрелкой. Нумерация нуклеотидов HBV приведена в соответствии с номенклатурой Galibert (5). Показана ключевая структура стебель-петля (эпсилон, ε), которая выполняет роль важного cis-элемента в пгРНК HBV для последующей репликации ДНК, вместе с предсказанными внутренними структурами (нижний стебель, выпетливание, верхний стебель, петля). Для встраивания слитой в рамке считывания последовательности НА-тага в ОРС прекорового белка без нарушения спаривания оснований эпсилон-структуры, последовательность, содержащую ДНК НА-тага (gtggacatcTACCCATACGACGTTCCAGATTACGCTggc: SEQ ID NO: 41), встраивали в рамке считывания в позицию, примыкающую к стартовому кодону ОРС корового белка, в направлении против хода транскрипции (см. последовательность, заключенную в рамку). Модификация последовательности позволяет получить слитую в рамке считывания последовательность НА-тага, линкера и прекорового белка, а ОРС корового белка остается интактной и располагается по ходу транскрипции относительно эпсилон-структуры.
Фиг. 2. Экспрессия и секреция НА-меченного HBeAg
(А) Внутриклеточная экспрессия прекорового белка дикого типа и меченного гемагглютинином Клетки HepG2 трансфецировали плазмидой рсНВе или рсНА-НВе, через 5 дней клеточный лизат анализировали методом вестерн-блоттинг, используя антитела к НВс (верхняя панель) и к НА (средняя панель). β-актин служил контролем нанесения. Детектировали как прекоровый белок дикого типа, так и HA-меченный прекоровый белок (НА-прекоровый белок).
(В) Детекция НА-меченного HBeAg в культуральной жидкости Клетки HepG2 трансфицировали пустым вектором или плазмидой рсНВе или рсНА-НВе, отбирали образцы супернатанта в указанные точки времени и собирали клетки на 5 день после трансфекции. Образцы супернатанта подвергали иммунопреципитации (ИП) с использованием антитела к НА и детектировали НА-меченный HBeAg (НА-HBeAg) с помощью вестерн-блоттинга с использованием антитела к НА. Указана легкая цепь (LC) антитела. Вестерн-блоттинг выявил внутриклеточную экспрессию НА-прекорового белка.
Фиг. 3. Секреция НА-HBeAg линиями клеток НерНА-НВе
Клетки установленных линий, стабильно экспрессирующих НА-меченный HBeAg, в частности, клетки НерНА-НВе4 и НерНА-НВе47, высаживали в покрытые коллагеном 12-луночные планшеты в условиях конфлюентности. День, когда клетки высаживали, обозначали днем 0, среду обновляли каждый день. Образцы надосадочной жидкости собирали в указанные временные точки и определяли НА-HBeAg методом AlphaLISA, как описано в разделе Материалы и методы. Результаты AlphaLISA для соответствующих временных точек (ось X), выраженные в относительных световых единицах (relative light unit, RLU) (ось Y), представляли в виде гистограммы.
Фиг. 4. Репликация НА-рекомбинантного генома HBV в транзиторно трансфецированных клетках
Клетки HepG2 совместно трансфецировали pTREHBVDES или pTREHBV-HAe и плазмидой pTet-off. Клетки собирали через 5 дней после трансфекции и исследовали продукцию РНК HBV, корового белка, инкапсидированной пгРНК и репликацию вирусной ДНК с помощью нозерн-блоттинга, вестерн-блоттинга и саузерн-блот-гибридизации, соответственно. пгРНК: прегеномная РНК, РНК об: РНК белков оболочки; ркДНК: релаксированная кольцевая ДНК; 1-цеп ДНК: одноцепочечная ДНК.
Фиг. 5. Изображение разработанной схемы кзкДНК-зависимой экспрессии НА-меченного HBeAg HBV в стабильной линии клеток НерВНАе
В клетках, стабильно трансфецированных pTREHBV-HAe и pTet-off, трансген содержит избыточный (1,1 длины) геном HBV, находящийся под контролем промотора tet-CMV. Стартовый кодон (ATG) прекорового белка на 5' конце ДНК HBV был мутирован, а второй остался неизменным (3' концевая избыточность). Содержащий НА-таг фрагмент (обозначен серым) встроили в ОРС прекорового белка, как описано в разделе Материалы и методы. Трансген также содержит два тандемных стоп-кодона в ОРС малого (S) поверхностного белка для предупреждения экспрессии белка оболочки вируса. (В) После удаления тетрациклина (Tet) происходит транскрипция пгРНК и образуются коровый белок и полимераза, что приводит к упаковыванию пгРНК и (С) обратной транскрипции пгРНК в ркДНК. Благодаря механизму репарации ДНК (D) ркДНК конвертируется в кольцевую кзкДНК матрицу (Е), в которой восстанавливается открытая рамка считывания НА-прекорового белка, в результате чего образуются мРНК НА-прекорового белка (НА-рС mRNA) и пгРНК для репликации вируса de novo (F). (G) Трансляция НА-прекорового белка с мРНК НА-прекорового белка и процессинг с образованием секретируемого НА-HBeAg, который можно детектировать методом ELISA. preC, С, pol, L, М, S и X обозначают стартовые кодоны ОРС прекорового белка, корового белка, полимеразы, большого, среднего и малого антигенов и белка X, соответственно. DR обозначает прямые повторы последовательностей. CTD обозначает С-концевой домен.
Фиг. 6. Кинетика репликации вирусной ДНК, аккумуляции кзкДНК и продукции НА-меченого HBeAg в клетках НерВНАе13
Клетки НерВНАе13 высаживали в 6-луночные планшеты в присутствии тетрациклина. Когда монослой достигал конфлюентности, тетрациклин удаляли из культуральной среды, среду меняли каждые два дня. Клетки или образцы надосадочной жидкости собирали в указанные точки времени. Выделяли внутриклеточную ДНК нуклеокапсида (верхняя панель) и кзкДНК (нижняя панель) и анализировали методом саузерн-блот-гибридизации. Депротеин. ркДНК обозначает депротеинизированную (свободную от белка) релаксированную кольцевую ДНК. Секретированный НА-меченный HBeAg детектировали с помощью иммунопреципитации НА и вестерн-блоттинга, как описано выше.
Фиг. 7. Дополнительные индуцибельные линии клеток НерВНАе, поддерживающие репликацию НА-рекомбинантной ДНК HBV.
Клетки HepDES19 и вновь полученные клетки НерВНАе (разные номера клонов) высаживали в 6-луночные планшеты в одинаковой плотности присутствии тетрациклина. После достижения клетками конфлюентности одну группу клеток культивировали в присутствии тетрациклина, а другую группу клеток культивировали в отсутствие тетрациклина. Спустя 6 дней клетки собирали и анализировали ДНК нуклеокапсида вируса методом саузерн-блоттинга.
Фиг. 8. Подлинность кзкДНК в клетках линий НерВНАе
кзкДНК, полученную в клетках HepDES19 и указанных клетках НерВНАе, экстрагировали способом, предложенным Hirt, и подвергали электрофорезу в геле и саузерн-блот-гибридизации (дорожки 1, 5, 8, 11, 14). Для дальнейшей проверки подлинности кзкДНК HBV образцы ДНК, полученные согласно Hirt, нагревали до 85°С в течение 5 мин перед загрузкой в гель, в этих условиях происходила денатурация депротеинизированной ркДНК в 1-цепочечную ДНК, тогда как кзкДНК не подвергалась денатурации, и ее электрофоретическая подвижность оставалась неизменной (дорожки 2, 6, 9, 12, 15). Денатурированные нагреванием образцы ДНК далее расщепляли EcoRI, в этих условиях происходила линеаризация кзкДНК в полноразмерную двуцепочечную ДНК (дорожки 3, 7, 10, 13, 16).
Фиг. 9. Детекция НА-HBeAg в клетках линий НерНА-НВе методом AlphaLISA
Клетки НерВНАе высаживали в планшеты в присутствии тетрациклина. Когда клетки достигали конфлюентности, тетрациклин удаляли из культуральной среды, среду заменяли каждые два дня. Образцы надосадочной жидкости собирали в указанные точки времени и определяли НА-HBeAg с помощью AlphaLISA. Результаты AlphaLISA в относительных световых единицах (relative light unit, RLU) выражали в импульсах в секунду.
Фиг. 10. Ингибитор репликации HBV (3ТС) блокирует экспрессию НА-HBeAg в клетках НерВНАе13
Клетки НерВНАе13 культивировали в 6-луночных планшетах в присутствии тетрациклина до достижения конфлюентности. Одну группу клеток постоянно поддерживали в присутствии тетрациклина. Вторую группу клеток затем переводили на среду, не содержащую тетрациклин. Третью группу клеток затем культивировали в среде без тетрациклина, содержащей 10 мкМ 3ТС. Культуральную среду обновляли через день, в образцах надосадочной жидкости, собранных в указанные точки времени, определяли НА-меченный HBeAg с помощью хемилюминесцентного иммуноанализа (CLIA).
Фиг. 11. Ингибиторы образования кзкДНК HBV снижали уровень НА-HBeAg в клетках НерВНАе13.
Клетки высаживали в 96-луночные планшеты и удаляли тетрациклин из среды для индукции репликации вируса, когда клетки достигали конфлюентности. Клетки оставляли без воздействия или параллельно подвергали воздействию соединений в указанных концентрациях, концентрацию ДМСО нормализовали до 0,5% в группах без воздействия и с воздействием. Воздействие повторяли один раз в четыре дня. Через 12 дней после воздействия определяли НА-HBeAg в культуральной жидкости методом CLIA и результаты (среднее ± стандартное отклонение) откладывали в процентах относительно контроля.
Фиг. 12. Кинетика транскрипции РНК вируса, репликации ДНК и накопления кзкДНК в дополнительных клонах клеток НерВНАе
Указанные клетки НерВНАе высаживали в 6-луночные планшеты в присутствии тетрациклина. Когда монослой достигал конфлюентности, тетрациклин удаляли из культуральной среды, среду меняли каждые два дня. Клетки собирали в указанные точки времени. Выделяли общую РНК вируса (верхняя панель), цитоплазматическую ДНК нуклеокапсида (средняя панель) и анализировали методами нозерн- и саузерн-блот-гибридизации, соответственно. Выделенную кзкДНК денатурировали нагреванием при 85°С в течение 5 мин и подвергали линеаризации с использованием EcoR I, после чего анализировали методом саузерн-блоттинга (нижняя панель).
Фиг. 13. кзкДНК-зависимая экспрессия НА-HBeAg в дополнительных клонах клеток НерВНАе
Клетки НерВНАе культивировали в 96-луночных планшетах в присутствии тетрациклина до достижения конфлюентности. Одну группу клеток постоянно поддерживали в присутствии тетрациклина. Вторую группу клеток затем переводили на среду, не содержащую тетрациклин. Третью группу клеток затем культивировали в среде без тетрациклина, содержащей 10 мкМ 3ТС. Культуральную среду обновляли через день, через 9 дней после воздействия в образцах надосадочной жидкости определяли НА-меченный HBeAg с помощью хемилюминесцентного иммуноанализа (CLIA).
Данное изобретение проиллюстрировано следующими примерами.
Пример 1. Культивируемая клеточная линия с индуцибельной кзк-ДНК-зависимой экспрессией антигена Е вируса гепатита В с эпитопной меткой и ее применение для скрининга антивирусных веществ
Материалы и методы
Плазмиды
Для конструирования тетрациклин-индуцируемого поддерживающего репликацию HBV вектора, содержащего открытую рамку считывания прекорового белка, слитого с гемагглютинином вируса гриппа человека (НА), с нокаутом стартового кодона, химическим способом синтезировали фрагмент ДНК, содержащий мотив ТАТА-бокс промотора CMV-IE и расположенный по ходу транскрипции фрагмент HBV (генотип D, подтип ayw, нуклеотиды 1805-2335) с делецией нуклеотида 1816(A) и вставкой последовательности НА-тага в ОРС прекорового белка (Genscript Inc). В данном фрагменте ДНК сайт рестрикции фермента SacI находился на 5' конце, а аутентичный сайт рестрикции BspEI находился на 3' конце. Вектор pTREHBV-HAe конструировали путем встраивания синтезированного фрагмента ДНК между сайтами рестрикции SacI/BspEI в плазмиду pTREHBVDES. Полная последовательность pTREHBV-HAe приведена в SEQ ID NO: 35.
Для создания вектора, экспрессирующего слитый с НА прекоровый белок, ПЦР-фрагмент, содержащий нуклеотиды HBV 1816-2335 с встроенной последовательностью НА амплифицировали из pTREHBV-HAe с использованием праймеров 5'-ATTGGATCCACCATGCAACTTTTTCACCTCTGC-3' и
5'-ACAGTAGTTTCCGGAAGTGTTGATAGGATAGGGG-3'. ПЦР-фрагмент разрезали рестрикционными ферментами BamHI и BspEI и встраивали между теми же рестрикционными сайтами в вектор, экспрессирующий прекоровый белок (рсНВе) с получением плазмиды рсНА-НВе. Полная последовательность рсНА-НВе приведена в SEQ ID NO: 39.
Клеточные культуры
Клетки линии HepG2 (АТСС® НВ-8065™), линии клеток гепатобластомы, поддерживающих репликацию HBV, получили из АТСС. Линия клеток HepDES19, происходящих от HepG2, с индуцибельной экспрессией ДНК и кзкДНК HBV, описана ранее (7). Клеточные линии поддерживали в среде Дюльбекко в модификации Игла (DMEM)-F12 (Cellgro) с добавлением 10% эмбриональной телячьей сыворотки, 100 Ед/мл пенициллина и 100 мкг/мл стрептомицина.
Для установления клеточной линии НерВНАе клетки HepG2 трансфецировали плазмидой pTet-off (Clontech), экспрессирующей тетрациклин-контролируемый активатор транскрипции, и плазмидой pTREHBV-HAe, в которой транскрипция модифицированной пгРНК HBV находилась под контролем промотора CMV-IE с тетрациклин-контролируемыми элементами. Трансфецированные клетки HepG2 отбирали с использованием 500 мкг/мл G418 в присутствии 1 мкг/мл тетрациклина. Отбирали устойчивые к G418 колонии и выращивали из них клеточные линии. Репликацию HBV индуцировали путем культивирования клеток в среде без тетрациклина, а уровни промежуточных продуктов репликации вирусной ДНК определяли с помощью гибридизации методом саузерн-блоттинга. Выбирали линии клеток с высоким уровнем репликации HBV и обозначали НерВНАе, присваивая клонам различные номера.
Линию клеток НерНА-НВе, стабильно экспрессирующих меченный НА HBeAg, получали путем трансфекции клеток HepG2 плазмидой рсНА-НВе, для отбора колоний использовали 50 мкг/мл G418 и выявляли положительные колонии с помощью вестерн-блоттинга с использованием антитела к гемагглютинину.
Стабильные клеточные линии НерВНАе и НерНА-НВе культивировали так же, как и HepG2, за исключением добавления G418 в концентрации 500 мкг/мл. При культивировании клеток НерВНАе регулярно добавляли тетрациклин в концентрации 1 мкг/мл для подавления транскрипции пгРНК HBV.
Трансфекции клеток
Клетки (~1,0×106) высаживали в покрытые коллагеном 35-мм культуральные чашки в среде DMEM/F12 без антибиотика. После инкубации в течение ночи проводили трансфекцию, добавляя в каждую лунку в общей сложности 4 мкг плазмидной ДНК и липофектамин 2000 (Life Technologies), следуя инструкциям производителя. В указанные точки времени собирали трансфецированные клетки или образцы надосадочной жидкости.
Анализ нуклеиновых кислот вируса
Общую клеточную РНК выделяли с помощью реагента TRIzol (Life Technologies), следуя инструкциям производителя. Инкапсидированную вирусную пгРНК выделяли следующим образом: клетки в одной лунке 12-луночного планшета лизировали в 250 мкл лизирующего буфера, содержащего 10 мМ Tris-HCl (рН 8,0), 1 мМ ЭДТА, 1% NP-40 и 50 мМ NaCl при 37°С в течение 10 мин и удаляли ядра путем центрифугирования. Образец инкубировали с 6 Ед нуклеазы микрококков и 15 мкл 100 мМ CaCl2 и инкубировали в течение 15 мин при 37°С для расщепления свободных нуклеиновых кислот. Инкапсидированную вирусную пгРНК экстрагировали путем добавления 750 мкл реагента TRIzol LS (Invitrogen) согласно протоколу производителя. Проводили электрофорез образцов РНК в 1,5% агарозном геле, содержащем 2,2 М формальдегид, и переносили на мембрану Hybond-XL (GE Healthcare) в 20× буфере SSC (1× SSC представляет собой 0,15 М NaCl и 0,015 М цитрат натрия).
Цитоплазматическую вирусную ДНК нуклеокапсида экстрагировали следующим образом: клетки из чашки диаметром 35 мм лизировали в 0,5 мл лизирующего буфера, содержащего 10 мМ Tris-HCl, рН 8,0, 10 мМ ЭДТА, 1% NP40 и 2% сахарозы при 37°С в течение 10 мин. Клеточный дебрис и ядра удаляли путем центрифугирования и супернатант инкубировали с 3 мкл 1 М Mg(ОАс)2 и 5 мкл 10 мг/мл ДНКазы I (Calbiochem) в течение 30 мин при 37°С. Затем для преципитации нуклеокапсидов супернатант смешивали с 15 мкл 0,5 М ЭДТА и 130 мкл 35% раствора полиэтиленгликоля (ПЭГ) 8000, содержащего 1,5 М NaCl. После инкубации на льду в течение 1 ч вирусные нуклеокапсиды осаждали путем центрифугирования при 10000 об/мин в течение 5 мин при 4°С, с последующим расщеплением при 37°С в течение 1 ч в 400 мкл расщепляющего буфера, содержащего 0,5 мг/мл проназы (Calbiochem), 0,5% додецилсульфата натрия (ДСН), 100 мМ NaCl, 25 мМ Tris-HCl (рН 7,4) и 10 мМ ЭДТА. После расщепления смесь экстрагировали фенолом, осаждали ДНК этанолом и растворяли в буфере ТЕ (10 мМ Tris-HCl, рН 8,0, 1 мМ ЭДТА). Одну треть образца ДНК нуклеокапсида из каждой чашки разделяли путем электрофореза в 1,2% агарозном геле. Затем гель подвергали депуринизации в буфере, содержащем 0,2N HCl, денатурации в растворе, содержащем 0,5 М NaOH и 1,5 М NaCl, и нейтрализовали в буфере, содержащем 1 М Tris-HCl (рН 7,4) и 1,5 М NaCl. ДНК переносили на мембрану Hybond-XL в 20× буфере SSC.
Экстракцию вирусной ДНК, свободной от белков (кзкДНК и свободной от белков ркДНК), осуществляли путем модифицированной процедуры экстракции, предложенной Hirt (4, 8). Вкратце, клетки из одной чашки диаметром 35 мм лизировали в 3 мл 10 мМ Tris-HCl (рН 7,5), 10 мМ ЭДТА и 0,7% ДСН. После 30 мин инкубации при комнатной температуре лизат переносили в 15 мл пробирку и после этой стадии добавляли 0,8 мл 5 М NaCl и инкубировали при 4°С в течение ночи. Затем лизат просветляли путем центрифугирования при 10000 об/мин в течение 30 мин при 4°С и дважды экстрагировали фенолом и однократно смесью фенол : хлороформ : изоамиловый спирт (25:24:1). ДНК осаждали этанолом при комнатной температуре в течение ночи и растворяли в буфере ТЕ. Затем одну треть образца ДНК, свободной от белка, разделяли в 1,2% агарозном геле и переносили на мембрану Hybond-XL.
Для детекции РНК и ДНК HBV мембраны инкубировали с меченным [α-32Р]УТФ (800 кюри/ммоль; Perkin Elmer) полноразмерным рибозондом, специфическим к плюс- или минус-цепи HBV. Гибридизацию проводили в 5 мл буфера для гибридизации EKONO (Genotech) с предгибридизацией при 65°С в течение 1 ч и гибридизацией в течение ночи при 65°С, с последующей отмывкой в 0,1× SSC и 0,1% ДСН при 65°С в течение 1 ч. Мембрану помещали на фотостимулируемые пластины с нанесенным фосфором и регистрировали сигналы, формируемые в результате гибридизации, с помощью системы Typhoon FLA-7000 (GE Healthcare).
Вестерн-блоттинг
Клетки в 35-мм чашках отмывали однократно буфером ФСБ и лизировали в 500 мкл 1× буфера Laemmli. Клеточный лизат общим объемом 50 мкл разделяли путем электрофореза в 12% полиакриламидном геле и переносили на мембрану из поливинилидендифторида (Millipore). Мембраны блокировали блокирующим буфером Western Breeze (Life Technologies) и инкубировали с антителами к HBeAg (аа170-183), НА-тагу (Sigma-Aldrich, клон М2), β-актину (Sigma-Aldrich). Связанные антитела детектировали при помощи вторичных антител IRDye. Сигналы визуализировали и проводили количественную оценку результатов иммуноблота с помощью системы Li-COR Odyssey.
Иммунопреципитация
Клетки из одной чашки диаметром 35 мм лизировали в 0,5 мл лизирующего буфера, содержащего 10 мМ Tris-HCl, рН 8,0, 10 мМ ЭДТА, 1% NP40, 2% сахарозы и 1× коктейль ингибиторов протеаз (G-biosciences). После центрифугирования для удаления клеточного дебриса просветленный клеточный лизат инкубировали с 50 мкл Ezview Red Anti-HA (Sigma-Aldrich) при 4°C в течение ночи при плавном вращении. 0,5 мл образца среды из одной 35-мм чашки (всего 1 мл) немедленно подвергали иммунопреципитации. Частицы промывали буфером TBS (0,15 М NaCl, 0,05 М Tris-HCl [рН 7,4]) три раза при 4°С. Осажденные частицы использовали для приготовления образцов с использованием буфера Laemmli. Иммунопреципитированные НА-меченные белки детектировали с помощью вестерн-блоттинга с использованием антител, направленных против НА-тага (Sigma-Aldrich).
ELISA для определения НА-меченного HBeAg
Для определения НА-меченного HBeAg методом CLIA (хемилюминесцентного иммуноферментного анализа) покрытые стрептавидином высокочувствительные планшеты (черные, кат. номер 15525, Thermo Scientific) промывали ФСБ-Т (ФСБ с 0,05% Tween 20) три раза, а затем инкубировали с 50 мкл конъюгированного с биотином антитела к НА-тагу (кат. номер А00203, Genscript; 5 мкг/мл в ФСБ) при комнатной температуре в течение 30 мин с последующим 3-кратным отмыванием 200 мкл ФСБ-Т. После удаления промывочного буфера 50 мкл культуральной надосадочной жидкости добавляли в лунки планшета для ELISA и инкубировали при комнатной температуре в течение 30 мин с последующим 3-кратным отмыванием 200 мкл ФСБ-Т. В лунки добавляли 50 мкл конъюгированных с пероксидазой хрена (HRP) анти-НВе антител (из набора HBeAg CLIA, кат. номер: CL0312-2, Autobio Diagnostics) и инкубировали при комнатной температуре в течение 30 мин. После 5-кратного промывания 200 мкл ФСБ-Т добавляли по 25 мкл каждого субстрата А и В из набора CLIA и легко встряхивали планшет в течение 10 сек. Считывали показания в лунках планшета с помощью люминометра.
Для определения НА-меченного HBeAg методом AlphaLISA антитело к НА, конъюгированное с биотином (кат. номер А00203, Genscript), разводили до концентрации 2 мкг/мл в 1× буфере для анализа (25 мМ HEPES, 0,1 М NaCl, 0,1% БСА, рН 7,4) и вносили по 5 мкл в каждую лунку планшета Proxiplate-384 HS (кат. номер 6008279, Perkin Elmer). Затем в лунки добавляли по 5 мкл образцов культуральной жидкости и осторожно перемешивали, после чего инкубировали при комнатной температуре в течение 30 мин. Затем добавляли 5 мкл анти-НВе антитела в концентрации 0,2 мкг/мл (клон 29, лот 20110305, Autobio Diagnostics) и осторожно перемешивали, после чего инкубировали при комнатной температуре в течение 30 мин. Затем смешивали анализируемый раствор смешивали с 5 мкл разведенных акцепторных частиц AlphaLISA, покрытых антителами к IgG мыши (кат. номер AL105C, Perkin Elmer) (125 мкг/мл) и инкубировали при комнатной температуре в течение 30 мин, после чего инкубировали с 5 мкл донорных частиц AlphaScreen, покрытых стрептавидином (кат. номер 6760002S, Perkin Elmer) (125 мкг/мл), при комнатной температуре в течение 1 ч. После инкубации считывали показания в лунках планшета с помощью ридера Envision 2104 Multilabel (Perkin Elmer).
Результаты
В данном документе предложены два типа новых линий клеток, экспрессирующих НА-меченый HBeAg (НА-HBeAg) с трансгена и кзкДНК HBV, соответственно, и способы определения рекомбинантного HBeAg с помощью хемилюминесцентного иммунного анализа и теста AlphaLISA. Клеточные линии и анализы подходят для высокопроизводительного скрининга соединений, снижающих уровень кзкДНК HBV и/или подавляющих транскрипцию кзкДНК.
Небольшой размер компактной геномной ДНК HBV и наличие перекрывающихся открытых рамок считывания в геноме затрудняют встраивание репортерных генов без влияния на репликацию вирусной ДНК и последующее образование кзкДНК в трансфецированных клетках.
Клетки HepDE19 можно генетически модифицировать таким образом, чтобы экспрессия прекорового белка/HBeAg была кзкДНК-зависимой (3). В области техники известно, что геном HBV имеет очень компактную организацию и имеет перекрывающиеся открытые рамки считывания (ОРС) и множество cis-элементов. Таким образом, считают, что вставка/делеция гена или замена последовательности с очень большой вероятностью будет влиять на репликацию вирусной ДНК. В более ранних работах в большинстве случаев производили замену последовательности HBV, такой как область, кодирующая белок оболочки, на GFP для получения рекомбинантного генома HBV, но для поддержки репликации вируса и сборки вириона была необходима транскомплементация по вирусным белкам (Protzer, et al., PNAS (1999), 96: 10818-23). Кроме того, при применении для инфицирования пермиссивных клеток описанный рекомбинантный геном HBV может осуществлять только первый раунд синтеза кзкДНК, а внутриклеточная амплификация кзкДНК блокируется из-за дефекта репликации вирусной ДНК.
В отличие от предшествующего уровня техники, в данном изобретении была предпринята попытка продемонстрировать, что геном HBV выдерживает присутствие в открытой рамке считывания (ОРС) прекорового белка коротких экзогенных эпитопных тагов, слитых в рамке считывания, и их экспрессию с матрицы кзкДНК, таким образом, применение антитела к HBeAg в паре с антителом, специфическим к тагу, существенно улучшает специфичность определения методом ELISA.
Для конструирования тетрациклин-индуцируемого поддерживающего репликацию HBV вектора с открытой рамкой считывания, кодирующей прекоровый белок, слитый с гемагглютинином (НА) вируса гриппа человека, последовательность ДНК, содержащую НА-таг (gtggacatcTACCCATACGACGTTCCAGATTACGCTggc; SED ID NO.: 41), встроили в рамке считывания в позиции, примыкающей к стартовому кодону ОРС корового белка в направлении против хода транскрипции, в экспрессирующий HBV вектор pTREHBVDES, в котором экспрессия пгРНК HBV контролировалась тетрациклин (tet)-регулируемым промотором CMV-IE по механизму Tet-off. Фланкирующие последовательности (обозначены строчными буквами) НА-тага (обозначен заглавными буквами) были предназначены для сохранения спаривания оснований структуры стебель-петля (эпсилон, ε) генома HBV и мотива Kozak стартового кодона ОРС корового белка (Фиг. 1). Полученную рекомбинантную плазмиду обозначили pTREHBV-HAe (SEQ ID NO: 35). Помимо встроенного НА-тага плазмида pTREHBV-HAe содержала точечную делецию в 5' концевом стартовом кодоне ОРС прекорового белка (ATG на TG), за счет чего в плазмиде, служащей матрицей, предотвращалась экспрессия прекорового белка геномом HBV. Кроме того, для блокирования образования инфекционных частиц HBV в кодирующую область амино-конца малого (S) белка оболочки встроили два тандемных стоп-кодона (217TTGTTG222 на 217TAGTAG222; подчеркнуты мутации).
Для исследования возможности экспрессии прекорового белка HBV с эпитопной меткой и секреции HBeAg, последовательность ДНК, содержащую НА-таг, встраивали в ДНК вируса в той же позиции, как описано выше, в плазмиду рсНВе, экспрессирующую прекоровый белок, и обозначали конструкцию рсНА-НВе (SEQ ID NO: 39). Трансфекция клеток HepG2 рсНА-НВе приводила к внутриклеточной экспрессии НА-меченного прекорового белка и внеклеточной аккумуляции НА-меченного HBeAg (Фиг. 2), что подтверждало, что встраивание НА-тага в прекоровый белок не влияет на экспрессию прекорового белка, посттрансляционный процессинг и секрецию HBeAg. Также разработали хемилюминесцентный ELISA и AlphaLISA для детекции НА-меченного HBeAg (НА-HBeAg), как описано в разделе Материалы и методы.
Как описано выше, клеточная линия, конститутивно экспрессирующая НА-меченный HBeAg, была получена в результате стабильной трансфекции клеток HepG2 рсНА-НВе. С помощью теста AlphaLISA выбрали два клона с высоким уровнем экспрессии НА-меченного HBeAg и обозначили их НерНА-НВе4 и НерНА-НВе47, соответственно (Фиг. 3).
При транзиторной трансфекции плазмида pTREHBV-HAe, кодирующая рекомбинантный HBV, обеспечивала уровень репликации ДНК HBV, сопоставимый с тем, который обеспечивался pTREHBVDES (Фиг. 4), что означало, что встраивание НА-тага позволяло реплицироваться геному HBV. Затем осуществляли стабильную трансфекцию клеток HepG2 совместно pTREHBV-HAe и pTET-off (Clontech) для получения тетрациклин-индуцируемой клеточной линии, поддерживающей репликацию HBV. Согласно теории, в такой клеточной линии после индукции трансген не будет продуцировать прекоровый белок и его производное HBeAg вследствие выключения стартового кодона открытой рамки считывания прекорового белка. С транскрибированной пгРНК будут экспрессироваться коровый белок и полимераза вируса и запускаться обратная транскрипция с образованием ркДНК, приводящая к образованию кзкДНК в результате внутриклеточной амплификации. При 3' концевой избыточности пгРНК стартовый кодон неполной ОРС прекорового белка будет скопирован в последовательность ДНК вируса и при конверсии ркДНК в кзкДНК будет восстанавливаться интактная открытая рамка считывания НА-меченного прекорового белка. Таким образом, мРНК НА-меченного прекорового белка будет транскрибироваться только с кзкДНК, делая секретируемый НА-меченый HBeAg суррогатным маркером внутриклеточной кзкДНК (Фиг. 5).
Авторы изобретения получили 5 клеточных линий (HepBHAe1, НерВНАе13, НерВНАе34, НерВНАе45, НерВНАе82), которые поддерживают высокий уровень тетрациклин-зависимой репликации ДНК HBV (Фиг. 6 и 7).
В приведенной в качестве примера линии клеток НерВНАе13 при отмене тетрациклина кинетика синтеза и аккумуляции вирусных продуктов, включая промежуточные продукты репликации ДНК и кзкДНК, изменялась со временем. В культуральной жидкости клеток НерВНАе13 через 6 дней после удаления тетрациклина НА-меченый HBeAg также определялся с помощью вестерн-блоттинга, а затем уровень антигена постепенно снижался. Уровень НА-меченого HBeAg (НА-HBeAg) был пропорционален внутриклеточному уровню вирусной ДНК нуклеокапсида и кзкДНК (Фиг. 6). Подлинность кзкДНК, полученной из клеток линии НерВНАе, подтвердили с помощью денатурации нагреванием и последующего ферментативного расщепления рестриктазой (Фиг. 8). Таким образом, была получена индуцибельная клеточная линия, поддерживающая репликацию ДНК и образование кзкДНК рекомбинантного HBV с встроенным в прекоровый белок НА-тагом.
Исследование образцов надосадочной жидкости культивируемых клеток НерВНАе методом AlphaLISA показало повышенный уровень НА-меченного HBeAg при исследовании временной динамики на протяжении 16 дней (Фиг. 9). Для дальнейшей характеризации отобрали клетки НерНВАе13. Клетки культивировали в трех вариантах условий: 1) в присутствии тетрациклина для подавления экспрессии трансгена; 2) в отсутствие тетрациклина для индукции репликации вирусной ДНК; 3) в отсутствие тетрациклина, но при воздействии 3ТС для блокирования репликации вирусной ДНК и последующего образования кзкДНК. Хемилюминесцентный иммуноанализ (CLIA) показал, что НА-меченный HBeAg появлялся в культуральной среде через 6 дней после отмены тетрациклина и затем постепенно нарастал в результате формирования кзкДНК и экспрессии генов. Как и ожидали, в присутствии тетрациклина или под воздействием 3ТС (в отсутствие тетрациклина) НА-HBeAg не определялся в культуральной жидкости в какой-либо момент времени (Фиг. 10). Кроме того, два обнаруженных ранее ингибитора образования кзкДНК, а именно ССС-0975 и ССС-0346 (3), демонстрировали дозозависимое ингибирование образования НА-HBeAg клетками НерВНАе13 (Фиг. 11). Таким образом, продукция НА-меченого HBeAg в клетках НерВНАе13 является кзкДНК-зависимой.
Кроме того, исследование других клеточных линий НерВНАе, включая HepBHAe1, НерВНАе45 и НерВНАе82, показало, что после отмены тетрациклина мРНК HBV, цитоплазматическая ДНК нуклеокапсида и ядерная кзкДНК накапливались со временем (Фиг. 12). Как показано на Фиг. 13, на этих трех дополнительных линиях клеток НерВНАе подтверждали кзкДНК-зависимую продукцию НА-меченого HBeAg.
Резюмируя, были созданы новые индуцибельные клеточные линии, поддерживающие кзкДНК-зависимую экспрессию НА-меченого HBeAg HBV, который может служить суррогатным маркером кзкДНК HBV при скрининге антивирусных соединений с помощью способов детекции НА-HBeAg, описанных в данном документе.
Данное изобретение относится к следующим нуклеотидным и аминокислотным последовательностям:
Приведенные в данном документе последовательности размещены в базе данных NCBI и к ним можно получить доступ по адресу в интернете ncbi.nlm.nih.gov/sites/entrez?db=gene; Указанные последовательности также относятся к аннотированным и модифицированным последовательностям. В данном изобретении также предложены методы и способы, в которых применяют гомологичные последовательности и варианты конкретных последовательностей, приведенных в данном документе. Предпочтительно, указанные «варианты» представляют собой генетические варианты.
SEQ ID No. 1:
Нуклеотидная последовательность, кодирующая гемагглютининовый (НА)-таг

SEQ ID No. 2:
Нуклеотидная последовательность, кодирующая His-таг

SEQ ID No. 3:
Нуклеотидная последовательность, кодирующая Flag-таг

SEQ ID No. 4:
Нуклеотидная последовательность, кодирующая c-myc-таг

SEQ ID No. 5:
Нуклеотидная последовательность, кодирующая V5-таг

SEQ ID No. 6:
Нуклеотидная последовательность, кодирующая С9-таг

SEQ ID No. 7:
Нуклеотидная последовательность, кодирующая 3× Flag-таг


SEQ ID No. 8:
Аминокислотная последовательность НА-тага

SEQ ID No. 9:
Аминокислотная последовательность His-тага

SEQ ID No. 10:
Аминокислотная последовательность Flag-тага

SEQ ID No. 11:
Аминокислотная последовательность c-myc-тага

SEQ ID No. 12:
Аминокислотная последовательность V5-тага

SEQ ID No. 13:
Аминокислотная последовательность С9-тага

SEQ ID No. 14:
Аминокислотная последовательность 3× Flag-тага

SEQ ID No. 15:
Нуклеотидная последовательность, кодирующая прекоровый белок вируса гепатита В
Последовательность ОРС прекорового белка:

SEQ ID No. 16:
Нуклеотидная последовательность, кодирующая антиген Е вируса гепатита В (HBeAg)
Последовательность ДНК HBeAg:


SEQ ID No. 17:
Аминокислотная последовательность прекорового белка вируса гепатита В: аминокислотная последовательность прекорового белка:

SEQ ID No. 18:
Аминокислотная последовательность антигена Е вируса гепатита В (HBeAg)
Аминокислотная последовательность HBeAg (удалены N-концевой сигнальный пептид (19 аминокислот) и С-концевой богатый аргинином домен (34 аминокислоты) прекорового белка):

SEQ ID No. 19:
Нуклеотидная последовательность, кодирующая НА-меченный прекоровый белок вируса гепатита В.
Последовательность ДНК НА-меченного прекорового белка:


SEQ ID No. 20:
Нуклеотидная последовательность, кодирующая НА-меченный антиген Е вируса гепатита В (HBeAg)
Последовательность ДНК НА-меченного HBeAg:

SEQ ID No. 21:
Аминокислотная последовательность НА-меченного прекорового белка вируса гепатита В. Подчеркнут НА-таг.
Аминокислотная последовательность НА-меченного прекорового белка:


SEQ ID No. 22:
Аминокислотная последовательность НА-меченного антигена Е вируса гепатита В (HBeAg). Подчеркнут НА-таг.
Аминокислотная последовательность НА-меченного HBeAg:

SEQ ID No. 23:
Нуклеотидная последовательность, кодирующая коровый белок HBV

SEQ ID No. 24:
Аминокислотная последовательность корового белка HBV

SEQ ID No. 25:
Нуклеотидная последовательность эпсилон-структуры, кодируемой геномом HBV

SEQ ID No. 26:
Нуклеотидная последовательность, способная образовывать пары с основаниями нижнего стебля эпсилон-структуры генома гепаднавируса

SEQ ID No. 27:
Нуклеотидная последовательность генома HBV, генотип HBV D, подтип ayw. Номер доступа Genbank U95551 (С1902 и А1903 обозначены жирным шрифтом. Подчеркнута ОРС прекорового белка.)



SEQ ID No. 28:
Нуклеотидная последовательность генома HBV, генотип HBV А (номер доступа Genbank AP007263)


SEQ ID No. 29:
Нуклеотидная последовательность генома HBV, генотип HBV В (номер доступа Genbank AB602818)



SEQ ID No. 30:
Нуклеотидная последовательность генома HBV, генотип HBV С (номер доступа Genbank АВ540584)



SEQ ID No. 31:
Нуклеотидная последовательность генома HBV, генотип HBV E (номер доступа Genbank AP007262)


SEQ ID No. 32:
Нуклеотидная последовательность генома HBV, генотип HBV F (номер доступа Genbank НЕ974366)


SEQ ID No. 33:
Нуклеотидная последовательность генома HBV, генотип HBV G (номер доступа Genbank AP007264)



SEQ ID No. 34:
Нуклеотидная последовательность генома HBV, генотип HBV H (номер доступа Genbank АВ516393)



SEQ ID No. 35:
Нуклеотидная последовательность вектора pTREHBV-HAe (5 980 нт)
Вектор: pTRE2 (Clontech)
нт 356-452: нуклеотиды HBV 1805-1902 с делецией А1816
нт 453-491: встраивание НА-тага с фланкирующей последовательностью
нт 462-488: последовательность НА-тага
нт 492-3761: нуклеотиды HBV 1903-3182/1-1990



SEQ ID No. 36:
Нуклеотидная последовательность, кодирующая белок оболочки HBV, большой поверхностный белок (L)

SEQ ID No. 37:
Нуклеотидная последовательность, кодирующая белок оболочки HBV, средний поверхностный белок (М)


SEQ ID No. 38:
Нуклеотидная последовательность, кодирующая белок оболочки HBV, малый поверхностный белок (S)

SEQ ID No. 39:
Нуклеотидная последовательность экспрессирующего вектора рсНА-НВе (6 682 нт)
Вектор: pcDNA3.1/V5-His-TOPO (Invitrogen)
нт 929-1015: нуклеотиды HBV 1816-1902
нт 1016-1054: вставка
нт 1025-1051: последовательность НА-тага
нт 1055-2112: HBV 1903-2605/1573-1926






SEQ ID No. 40:
Аминокислотная последовательность, расположенная в N-концевом направлении относительно тага

SEQ ID No. 41:
Нуклеотидная последовательность, кодирующая НА-таг, содержащая
дополнительные 5'- и 3'- нуклеотиды. Подчеркнутые нуклеотиды обозначают последовательность, кодирующую НА-таг.

SEQ ID No. 42:
Аминокислотная последовательность НА-тага, содержащая дополнительные N-концевые и С-концевые аминокислоты. Подчеркнутые аминокислотные остатки обозначают последовательность НА-тага.

Документы, процитированные в данном описании
1. Arzumanyan, А., Н.М. Reis, and М.A. Feitelson. 2013. Pathogenic mechanisms in HBV- and HCV-associated hepatocellular carcinoma. Nature reviews. Cancer 13:123-135.
2. Block, Т.M., H. Guo, and J.T. Guo. 2007. Molecular virology of hepatitis В virus for clinicians. Clin Liver Dis 11:685-706, vii.
3. Cai, D., C. Mills, W. Yu, R. Yan, С.E. Aldrich, J.R. Saputelli, W.S. Mason, X. Xu, J.T. Guo, Т.M. Block, A. Cuconati, and H. Guo. 2012. Identification of disubstituted sulfonamide compounds as specific inhibitors of hepatitis В virus covalently closed circular DNA formation. Antimicrob Agents Chemother 56:4277-4288.
4. Cai, D., H. Nie, R. Yan, J.T. Guo, Т.M. Block, and H. Guo. 2013. A southern blot assay for detection of hepatitis В virus covalently closed circular DNA from cell cultures. Methods Mol Biol 1030:151-161.
5. Galibert, F., E. Mandart, F. Fitoussi, and P. Charnay. 1979. Nucleotide sequence of the hepatitis В virus genome (subtype ayw) cloned in E.coli. Nature 281:646-650.
6. Gish, R.G., A.S. Lok, Т.T. Chang, R.A. de Man, A. Gadano, J. Sollano, K.H. Han, Y.C. Chao, S.D. Lee, M. Harris, J. Yang, R. Colonno, and H. Brett-Smith. 2007. Entecavir therapy for up to 96 weeks in patients with HBeAg-positive chronic hepatitis B. Gastroenterology 133:1437-1444.
7. Guo, H., D. Jiang, T. Zhou, A. Cuconati, Т.M. Block, and J.T. Guo. 2007. Characterization of the intracellular deproteinized relaxed circular DNA of hepatitis В virus: an intermediate of covalently closed circular DNA formation. J Virol 81:12472-12484.
8. Hirt, B. 1967. Selective extraction of polyoma DNA from infected mouse cell cultures. J Mol Biol 26:365-369.
9. Hoofnagle, J.H., E. Doo, T.J. Liang, R. Fleischer, and A.S. Lok. 2007. Management of hepatitis B: summary of a clinical research workshop. Hepatology 45:1056-1075.
10. Ito, K., K.H. Kim, A.S. Lok, and S. Tong. 2009. Characterization of genotype-specific carboxyl-terminal cleavage sites of hepatitis В virus e antigen precursor and identification of furin as the candidate enzyme. J Virol 83:3507-3517.
11. Ladner, S.K., M.J. Otto, C.S. Barker, K. Zaifert, G.H. Wang, J.T. Guo, C. Seeger, and R.W. King. 1997. Inducible expression of human hepatitis В virus (HBV) in stably transfected hepatoblastoma cells: a novel system for screening potential inhibitors of HBV replication. Antimicrob Agents Chemother 41:1715-1720.
12. Liang, T.J. 2009. Hepatitis B: the virus and disease. Hepatology 49:S13-21.
13. Liu, N., L. Ji, M.L. Maguire, and D.D. Loeb. 2004. cis-Acting sequences that contribute to the synthesis of relaxed-circular DNA of human hepatitis В virus. J Virol 78:642-649.
14. McMahon, B.J. 2014. Chronic hepatitis В virus infection. The Medical clinics of North America 98:39-54.
15. Nassal, M. 2008. Hepatitis В viruses: reverse transcription a different way. Virus Res 134:235-249.
16. Pawlotsky, J.M., G. Dusheiko, A. Hatzakis, D. Lau, G. Lau, T.J. Liang, S. Locarnini, P. Martin, D.D. Richman, and F. Zoulim. 2008. Virologic monitoring of hepatitis В virus therapy in clinical trials and practice: recommendations for a standardized approach. Gastroenterology 134:405-415.
17. Protzer, U., M. Nassal, P.W. Chiang, M. Kirschfink, and H. Schaller. 1999. Interferon gene transfer by a hepatitis В virus vector efficiently suppresses wild-type virus infection. Proc Natl Acad Sci U S A 96:10818-10823.
18. Quasdorff, M., and U. Protzer. 2010. Control of hepatitis В virus at the level of transcription. J Viral Hepat 17:527-536.
19. Seeger, C, and W.S. Mason. 2000. Hepatitis В virus biology. Microbiol Mol Biol Rev 64:51-68.
20. Sells, M.A., M. Chen, and G. Acs. 1987. Production of hepatitis В virus particles in hepG2 cells transfected with cloned hepatitis В virus DNA. Proc. Natl. Acad. Sci. USA 84:1005-1009.
21. Wang, J., A.S. Lee, and J.H. Ou. 1991. Proteolytic conversion of hepatitis В virus e antigen precursor to end product occurs in a postendoplasmic reticulum compartment. J Virol 65:5080-5083.
22. Wang, Z., L. Wu, X. Cheng, S. Liu, B. Li, H. Li, F. Kang, J. Wang, H. Xia, C. Ping, M. Nassal, and D. Sun. 2013. Replication-competent infectious hepatitis В virus vectors carrying substantially sized transgenes by redesigned viral polymerase translation. PLoS One 8:e60306.
23. Zhou, Т., H. Guo, J.T. Guo, A. Cuconati, A. Mehta, and Т.M. Block. 2006. Hepatitis В virus e antigen production is dependent upon covalently closed circular (ccc) DNA in HepAD38 cell cultures and may serve as a cccDNA surrogate in antiviral screening assays. Antiviral Res 72:116-124.
24. Zoulim, F., and S. Locarnini. 2009. Hepatitis В virus resistance to nucleos(t)ide analogues. Gastroenterology 137:1593-1608 e1591-1592.
Все процитированные в данном описании документы включены во всей полноте путем ссылки. На основании полного описания изобретения специалисту в данной области будет очевидно осуществление изобретения в различных и аналогичных условиях, в широком диапазоне параметров и т.п., однако суть изобретения и объем изобретения и любого его воплощения останутся прежними.
В соответствии с тем, что описано выше и изложено в формуле изобретения, данное изобретение относится, в частности, к следующему:
1. Способ оценки способности молекулы-кандидата ингибировать ковалентно замкнутую кольцевую (кзк) ДНК гепаднавируса, включающий стадии:
(а) приведения в контакт клетки, содержащей молекулу нуклеиновой кислоты, содержащую нуклеотидную последовательность, кодирующую меченый антиген Е гепаднавируса, с указанной молекулой-кандидатом;
(б) оценки уровня меченого антигена Е гепаднавируса и
(в) отбора молекулы-кандидата, если уровень меченого антигена Е гепаднавируса снижается по сравнению с контролем.
2. Способ по п. 1, где указанный гепаднавирус представляет собой вирус гепатита В (HBV) и указанный антиген Е гепаднавируса представляет собой антиген Е вируса гепатита В (HBeAg).
3. Способ по п. 1 или 2, где указанный меченый антиген Е гепаднавируса содержит только один таг.
4. Способ по п. 3, где указанный таг состоит из 6-22 аминокислот.
5. Способ по п. 3 или 4, где указанный таг выбран из группы, состоящей из гемагглютининового (НА) тага, His-тага, Flag-тага, c-myc-тага, V5-тага и С9-тага.
6. Способ по п. 5, где указанный Flag-таг представляет собой ×Flag-таг или 3×Flag-таг.
7. Способ по п. 1 или 2, где указанный меченый антиген Е гепаднавируса содержит два или более тагов.
8. Способ по п. 7, где указанные два или более тагов представляют собой различные таги.
9. Способ по п. 7 или 8, где указанный таг состоит из 6-22 аминокислот.
10. Способ по любому из пп. 7-9, где указанные два или более тагов представляют собой два или более гемагглютининовых (НА)-тагов, His-тагов, Flag-тагов, с-myc-тагов, V5-тагов и/или С9-тагов.
11. Способ по п. 10, где указанный Flag-таг представляет собой 1×Flag-таг или 3×Flag-таг.
12. Способ по п. 5 или 10,
где нуклеотидные последовательности, кодирующие НА таг, приведены в SEQ ID NO: 1; где нуклеотидные последовательности, кодирующие His-таг, приведены в SEQ ID NO: 2; где нуклеотидные последовательности, кодирующие с-myc-таг, приведены в SEQ ID NO: 4; где нуклеотидные последовательности, кодирующие V5-таг, приведены в SEQ ID NO: 5; и/или где нуклеотидные последовательности, кодирующие С9-таг, приведены в SEQ ID NO: 6.
13. Способ по п. 6 или 11; где нуклеотидные последовательности, кодирующие 1×Flag-таг, приведены в SEQ ID NO: 3; или где нуклеотидные последовательности, кодирующие 3×Flag-таг, приведены в SEQ ID NO: 7.
14. Способ по п. 5 или 10,
где аминокислотная последовательность НА тага приведена в SEQ ID NO: 8;
где аминокислотная последовательность His-тага приведена в SEQ ID NO: 9; где аминокислотная последовательность c-myc-тага приведена в SEQ ID NO: 11;
где аминокислотная последовательность V5-тага приведена в SEQ ID NO: 12; и/или
где аминокислотная последовательность С9-тага приведена в SEQ ID NO: 13.
15. Способ по п. 6 или 11,
где аминокислотная последовательность 1×Flag-тага приведена в SEQ ID NO: 10; или
где аминокислотная последовательность 3×Flag-тага приведена в SEQ ID NO: 14.
16. Способ по любому из пп. 2-15; где нуклеотидная последовательность, кодирующая HBeAg, приведена в SEQ ID NO: 16.
17. Способ по любому из пп. 2-15; где аминокислотная последовательность HBeAg приведена в SEQ ID NO: 18.
18. Способ по любому из пп. 1-17; где молекула нуклеиновой кислоты содержит нуклеотидную последовательность, кодирующую прекоровый белок гепаднавируса.
19. Способ по п. 18, где нуклеотидная последовательность, кодирующая прекоровый белок гепаднавируса, приведена в SEQ ID NO: 15.
20. Способ по п. 18, где аминокислотная последовательность прекорового белка гепаднавируса приведена в SEQ ID NO: 17.
21. Способ по любому из пп. 1-17, где молекула нуклеиновой кислоты содержит нуклеотидную последовательность, кодирующую один или несколько тагов, где указанная последовательность находится в направлении 3' по ходу транскрипции относительно нуклеотидной последовательности, кодирующей N-концевой сигнальный пептид и линкер прекорового белка гепаднавируса.
22. Способ по п. 21, где указанная нуклеотидная последовательность, кодирующая один или несколько тагов, находится в направлении 3' по ходу транскрипции относительно нуклеотидной последовательности, кодирующей 29 N-концевых аминокислот прекорового белка вируса гепатита В.
23. Способ по любому из пп. 1-22, где молекула нуклеиновой кислоты содержит геном гепаднавируса.
24. Способ по п. 23, где указанный геном гепаднавируса представляет собой геном вируса гепатита В (HBV).
25. Способ по п. 24, где указанный геном HBV представляет собой геном HBV генотипа А, В, С, D, Е, F, G или Н.
26. Способ по п. 24, где указанный геном HBV представляет собой геном HBV генотипа D.
27. Способ по п. 26, где указанный геном HBV генотипа D представляет собой геном HBV подтипа ayw.
28. Способ по любому из пп. 1-17, где молекула нуклеиновой кислоты, кодирующая один или несколько тагов, находится в направлении 5' против хода транскрипции относительно нуклеотидной последовательности, кодирующей коровый белок гепаднавируса.
29. Способ по п. 28, где указанный коровый белок гепаднавируса представляет собой коровый белок HBV.
30. Способ по п. 29, где нуклеиновая кислота, кодирующая коровый белок HBV, приведена в SEQ ID NO: 23.
31. Способ по п. 29, где аминокислотная последовательность корового белка HBV приведена в SEQ ID NO: 24.
32. Способ по любому из пп. 1-31, где молекула нуклеиновой кислоты, кодирующая один или несколько тагов, встроена в эпсилон-структуру, кодируемую геномом гепаднавируса.
33. Способ по п. 32, где геном гепаднавируса представляет собой геном HBV.
34. Способ по п. 33, где нуклеотидная последовательность эпсилон-структуры, кодируемой геномом HBV, приведена в SEQ ID NO: 25.
35. Способ по любому из пп. 1-34, где молекула нуклеиновой кислоты, содержащая последовательность, кодирующую один или несколько тагов, встроена в нижний стебель эпсилон-структуры, кодируемой геномом гепаднавируса.
36. Способ по п. 35, где геном гепаднавируса представляет собой геном HBV.
37. Способ по любому из пп. 1-36, где молекула нуклеиновой кислоты, содержащая последовательность, кодирующую один или несколько тагов, встроена между нуклеотидами, соответствующими позициям С1902 и А1903 генома HBV.
38. Способ по любому из пп. 1-37, где молекула нуклеиновой кислоты содержит в направлении 5' относительно последовательности, кодирующей один или несколько тагов, последовательность, способную образовывать пары с основаниями нижнего стебля эпсилон-структуры, кодируемой геномом гепаднавируса.
39. Способ по п. 38, где последовательность, способная образовывать пары с основаниями нижнего стебля эпсилон-структуры, кодируемой геномом гепаднавируса, способна образовывать пары с нуклеотидами, соответствующими позициям от Т1849 до А1854 генома HBV.
40. Способ по п. 38 или 39, где последовательность, способная образовывать пары с основаниями нижнего стебля эпсилон-структуры, кодируемой геномом гепаднавируса, включает в себя вплоть до 9 нуклеотидов.
41. Способ по п. 40, в котором последовательность, способная образовывать пары с основаниями нижнего стебля эпсилон-структуры, кодируемой геномом гепаднавируса, состоит из последовательности, приведенной в SEQ ID No. 26; или где последовательность, которая способна образовывать пары с основаниями нижнего стебля эпсилон-структуры, кодируемой геномом гепаднавируса, кодирует полипептид, приведенный в SEQ ID NO. 40.
42. Способ по любому из пп. 1-41, где молекула нуклеиновой кислоты содержит в направлении 3' относительно последовательности, кодирующей один или несколько тагов, последовательность, кодирующую линкер.
43. Способ по п. 42, в котором указанный линкер состоит из одного или нескольких аминокислотных остатков.
44. Способ по п. 42, в котором указанный линкер состоит из одного аминокислотного остатка.
45. Способ по п. 44, в котором указанная аминокислота представляет собой остаток глицина.
46. Способ по любому из пп. 42-44, где указанная последовательность кодирующая линкер, состоит из последовательности GGC; или где указанная последовательность кодирует остаток глицина.
47. Способ по любому из пп. 1-46, где молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую меченый антиген Е гепаднавируса, содержит нуклеотидную последовательность, приведенную в SEQ ID NO. 41; или
где молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую меченый антиген Е гепаднавируса, содержит нуклеотидную последовательность, кодирующую аминокислотную последовательность, приведенную в SEQ ID NO. 42.
48. Способ по любому из пп. 1-47, где указанные один или несколько тагов слиты в рамке с антигеном Е гепаднавируса.
49. Способ по п. 48, где антиген Е гепаднавируса представляет собой антиген Е вируса гепатита В (HBeAg).
50. Способ по любому из пп. 2-49; где нуклеотидная последовательность, кодирующая меченый HBeAg, приведена в SEQ ID NO: 20.
51. Способ по любому из пп. 2-50, где аминокислотная последовательность меченого HBeAg приведена в SEQ ID NO: 22.
52. Способ по любому из пп. 2-51, где нуклеотидная последовательность, кодирующая меченый прекоровый белок HBV, приведена в SEQ ID NO: 19.
53. Способ по любому из пп. 2-52, где аминокислотная последовательность меченного прекорового белка HBV приведена в SEQ ID NO: 21.
54. Способ по любому из пп. 24-53, где нуклеотидная последовательность генома HBV приведена в любой из SEQ ID NO: 27, 28, 29, 30, 31, 32, 33 или 34.
55. Способ по любому из пп. 23-54, где нуклеиновая кислота может транскрибироваться в прегеномную (пг) РНК гепаднавируса, в частности, прегеномную (пг) РНК HBV.
56. Способ по любому из пп. 1-55, где указанная нуклеиновая кислота предотвращает трансляцию меченого антигена Е гепаднавируса.
57. Способ по п. 56, где указанная нуклеиновая кислота не содержит стартового кодона ATG в 5' направлении против хода транскрипции относительно нуклеиновой кислоты, кодирующей меченый антиген Е гепаднавируса.
58. Способ по п. 56 или 57, где стартовый кодон ATG в 5' направлении против хода транскрипции относительно нуклеиновой кислоты, кодирующей меченый антиген Е гепаднавируса, заменен нуклеотидами TG.
59. Способ по любому из пп. 56-58, где указанная нуклеиновая кислота модифицирована путем точечной мутации для предотвращения трансляции меченого антигена Е гепаднавируса.
60. Способ по любому из пп. 1-59, где молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую меченый антиген Е гепаднавируса, содержится в векторе.
61. Способ по п. 60, где вектор содержит последовательность, приведенную в SEQ ID NO: 35.
62. Способ по любому из пп. 1-61, где молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую меченый антиген Е гепаднавируса, находится под контролем индуцируемого промотора.
63. Способ по любому из пп. 56-62, где антиген Е гепаднавируса, представляет собой антиген Е вируса гепатита В (HBeAg).
64. Способ по п. 62 или 63, где индуцируемый промотор представляет собой тетрациклин-индуцируемый промотор, доксициклин-индуцируемый промотор, антибиотик-индуцируемый промотор, медь-индуцируемый промотор, спирт-индуцируемый промотор, стероид-индуцируемый или гербицид-индуцируемый промотор.
65. Способ по любому из пп. 62-64, где индуцируемый промотор представляет собой промотор CMV или промотор tet-EF-1 альфа.
66. Способ по любому из пп. 23-65, где один или несколько стоп-кодонов встроены в кодирующую область одного или нескольких белков оболочки гепаднавируса.
67. Способ по п. 66, где указанные один или несколько белков оболочки гепаднавируса представляют собой один или несколько белков оболочки HBV.
68. Способ по п. 67, где один или несколько белков оболочки HBV представляют собой один или несколько больших поверхностных белков (L), средних поверхностных белков (М) и малых поверхностных белков (S).
69. Способ по п. 67, где белок оболочки HBV представляет собой малый белок оболочки (S).
70. Способ по любому из пп. 67-69, где кодирующая область одного или нескольких белков оболочки HBV приведена в SEQ ID NO: 36 (L), SEQ ID NO: 37 (M) и/или SEQ ID NO: 38 (S).
71. Способ по п. 70, где нуклеотиды HBV с 217 до 222 (TTGTTG) последовательности SEQ ID NO: 38 (S) мутированы в TAGTAG для предотвращения экспрессии белков оболочки.
72. Способ по любому из пп. 1-71, где клетка представляет собой эукариотическую клетку.
73. Способ по п. 72, где эукариотическая клетка имеет гепатоцитарное происхождение.
74. Способ по п. 72 или 73, где эукариотическая клетка представляет собой клетку гепатомы или происходит из клетки гепатомы.
75. Способ по любому из пп. 72-74, где эукариотическая клетка представляет собой HepG2 (АТСС #НВ-8065).
76. Способ по любому из пп. 1-75, где молекула нуклеиновой кислоты или вектор, содержащий ее, стабильно интегрированы в геном клетки.
77. Способ по любому из пп. 1-76, в котором указанная стадия (а) дополнительно включает стадию (аа), которая включает культивирование клетки, содержащей молекулу нуклеиновой кислоты, содержащую нуклеотидную последовательность, кодирующую меченый антиген Е гепаднавируса, в условиях, обеспечивающих
(i) синтез прегеномной (пг) РНК гепаднавируса;
(ii) обратную транскрипцию указанной синтезированной пгРНК в минус-цепь ДНК;
(iii) синтез второй плюс-цепи ДНК, чтобы указанная минус-цепь ДНК и указанная плюс-цепь ДНК образовывали двуцепочечную релаксированную кольцевую ДНК;
(iv) образование кзкДНК из указанной релаксированной кольцевой двуцепочечной ДНК;
(v) возможно, восстановление условий, обеспечивающих трансляцию меченого антигена Е гепаднавируса;
(vi) транскрипцию мРНК, кодирующей меченый антиген Е гепаднавируса;
(vii) трансляцию меченого антигена Е гепаднавируса.
78. Способ по п. 77, где восстановление условий, обеспечивающих трансляцию меченого антигена Е гепаднавируса, представляет собой восстановление стартового кодона.
79. Способ по любому из пп. 1-78, где указанный способ предназначен для оценки способности молекулы-кандидата ингибировать образование кзкДНК гепаднавируса.
80. Способ по п. 79, в котором клетку приводят в контакт с молекулой-кандидатом перед образованием кзкДНК.
81. Способ по любому из пп. 1-78, где указанный способ предназначен для оценки способности молекулы-кандидата снижать количество или число кзкДНК гепаднавируса.
82. Способ по любому из пп. 1-78, где указанный способ предназначен для оценки способности молекулы-кандидата снижать транскрипцию кзкДНК гепаднавируса.
83. Способ по п. 81 или 82, где клетку приводят в контакт с молекулой-кандидатом после образования кзкДНК.
84. Способ по любому из пп. 1-83, в котором уровень меченого антигена Е гепаднавируса согласно стадии (б) оценивают с помощью ELISA, CLIA или AlphaLISA.
85. Способ по любому из пп. 1-84, в котором оценка уровня меченого антигена Е гепаднавируса согласно стадии (б) включает применение антитела, специфически распознающего указанный антиген Е гепаднавируса, и одного или нескольких антител, специфически распознающих один или несколько тагов.
86. Способ по любому из пп. 77-85, где указанный гепаднавирус представляет собой вирус гепатита В (HBV) и указанный антиген Е гепаднавируса представляет собой антиген Е вируса гепатита В (HBeAg).
87. Молекула нуклеиновой кислоты, содержащая последовательность нуклеиновой кислоты, кодирующей меченый антиген Е гепаднавируса.
88. Молекула нуклеиновой кислоты по п. 87, где указанный антиген Е гепаднавируса представляет собой антиген Е вируса гепатита В (HBeAg).
89. Молекула нуклеиновой кислоты по п. 87 или 88, где указанный меченый антиген Е гепаднавируса содержит только один таг.
90. Молекула нуклеиновой кислоты по п. 89, где указанный таг состоит из 6-22 аминокислот.
91. Молекула нуклеиновой кислоты по п. 89 или 90, где указанный таг выбран из группы, состоящей из гемагглютининового (НА) тага, His-тага, Flag-тага, с-myc-тага, V5-тага и С9-тага.
92. Молекула нуклеиновой кислоты по п. 91, где указанный Flag-таг представляет собой 1×Flag-таг или 3×Flag-таг.
93. Молекула нуклеиновой кислоты по п. 87 или 88, где указанный меченый антиген Е гепаднавируса содержит два или более тагов.
94. Молекула нуклеиновой кислоты по п. 93, где указанные два или несколько тагов представляют собой различные таги.
95. Молекула нуклеиновой кислоты по п. 93 или 94, где суммарная длина указанных двух или более тагов составляет приблизительно от 14 до 31 аминокислоты.
96. Молекула нуклеиновой кислоты по любому из пп. 93-95, где указанные два или более тагов представляют собой два или более гемагглютининовых (НА)-тагов, His-тагов, Flag-тагов, c-myc-тагов, V5-тагов и/или С9-тагов.
97. Молекула нуклеиновой кислоты по п. 96, где указанный Flag-таг представляет собой 1×Flag-таг или 3×Flag-таг.
98. Молекула нуклеиновой кислоты по любому из пп. 91 или 96,
где нуклеотидные последовательности, кодирующие НА таг, приведены в SEQ ID NO: 1; где нуклеотидные последовательности, кодирующие His-таг, приведены в SEQ ID NO: 2; где нуклеотидные последовательности, кодирующие с-myc-таг, приведены в SEQ ID NO: 4; где нуклеотидные последовательности, кодирующие V5-таг, приведены в SEQ ID NO: 5; и/или где нуклеотидные последовательности, кодирующие С9-таг, приведены в SEQ ID NO: 6.
99. Молекула нуклеиновой кислоты по п. 92 или 97,
где нуклеотидные последовательности, кодирующие 1×Flag-таг, приведены в SEQ ID NO: 3; или
где нуклеотидные последовательности, кодирующие 3×Flag-таг, приведены в SEQ ID NO: 7.
100. Молекула нуклеиновой кислоты по п. 91 или 96,
где аминокислотная последовательность НА тага приведена в SEQ ID NO: 8; где аминокислотная последовательность His-тага приведена в SEQ ID NO: 9; где аминокислотная последовательность c-myc-тага приведена в SEQ ID NO: 11;
где аминокислотная последовательность V5-тага приведена в SEQ ID NO: 12; и/или
где аминокислотная последовательность С9-тага приведена в SEQ ID NO: 13.
101. Молекула нуклеиновой кислоты по п. 92 или 97,
где аминокислотная последовательность 1×Flag-тага приведена в SEQ ID NO: 10; или
где аминокислотная последовательность 3×Flag-тага приведена в SEQ ID NO: 14.
102. Молекула нуклеиновой кислоты по любому из пп. 88-101, где нуклеотидная последовательность, кодирующая HBeAg, приведена в SEQ ID NO: 16.
103. Молекула нуклеиновой кислоты по любому из пп. 88-101, где аминокислотная последовательность HBeAg приведена в SEQ ID NO: 18.
104. Молекула нуклеиновой кислоты по любому из пп. 87-103, где молекула нуклеиновой кислоты содержит нуклеотидную последовательность, кодирующую прекоровый белок гепаднавируса.
105. Молекула нуклеиновой кислоты по п. 104, где нуклеотидная последовательность, кодирующая прекоровый белок гепаднавируса, приведена в SEQ ID NO:15.
106. Молекула нуклеиновой кислоты по п. 104, где аминокислотная последовательность прекорового белка гепаднавируса приведена в SEQ ID NO: 17.
107. Молекула нуклеиновой кислоты по любому из пп. 87-106, где молекула нуклеиновой кислоты содержит нуклеотидную последовательность, кодирующую один или несколько тагов, где указанная последовательность находится в направлении 3' по ходу транскрипции относительно нуклеотидной последовательности, кодирующей N-концевой сигнальный пептид и линкер («прекоровую» область) прекорового белка гепаднавируса.
108. Способ по п. 107, где указанная нуклеотидная последовательность, кодирующая один или несколько тагов, находится в направлении 3' по ходу транскрипции относительно нуклеотидной последовательности, кодирующей 29 N-концевых аминокислот прекорового белка вируса гепатита В.
109. Молекула нуклеиновой кислоты по любому из пп. 87-108, где молекула нуклеиновой кислоты содержит геном гепаднавируса.
110. Молекула нуклеиновой кислоты по п. 109, где указанный геном гепаднавируса представляет собой геном вируса гепатита В (HBV).
111. Молекула нуклеиновой кислоты по п. 110, где указанный геном HBV представляет собой геном HBV генотипа А, В, С, D, Е, F, G или Н.
112. Молекула нуклеиновой кислоты по п. 110, где указанный геном HBV представляет собой геном HBV генотипа D.
113. Молекула нуклеиновой кислоты по п. 112, где указанный геном HBV генотипа D представляет собой геном HBV подтипа ayw.
114. Молекула нуклеиновой кислоты по любому из пп. 87-113, где молекула нуклеиновой кислоты, кодирующая один или несколько тагов, находится в направлении 5' против хода транскрипции относительно нуклеотидной последовательности, кодирующей коровый белок гепаднавируса.
115. Молекула нуклеиновой кислоты по п. 114, где нуклеотидная последовательность кодирует коровый белок HBV.
116. Молекула нуклеиновой кислоты по п. 115, где нуклеотидная последовательность, кодирующая коровый белок HBV, приведена в SEQ ID NO: 23.
117. Молекула нуклеиновой кислоты по п. 114, где коровый белок представляет собой коровый белок HBV.
118. Молекула нуклеиновой кислоты по п. 116, где аминокислотная последовательность корового белка HBV приведена в SEQ ID NO: 24.
119. Молекула нуклеиновой кислоты по любому из пп. 87-118, где молекула нуклеиновой кислоты, содержащая последовательность, кодирующую один или несколько тагов, встроена в эпсилон-структуру, кодируемую геномом гепаднавируса.
120. Молекула нуклеиновой кислоты по п. 119, где указанный геном гепаднавируса представляет собой геном HBV.
121. Молекула нуклеиновой кислоты по п. 120, где нуклеотидная последовательность эпсилон-структуры, кодируемой геномом HBV, приведена в SEQ ID NO: 25.
122. Молекула нуклеиновой кислоты по любому из пп. 87-121, где молекула нуклеиновой кислоты, содержащая последовательность, кодирующую один или несколько тагов, встроена в нижний стебель эпсилон-структуры, кодируемой геномом гепаднавируса.
123. Молекула нуклеиновой кислоты по п. 122, где указанный геном гепаднавируса представляет собой геном HBV.
124. Молекула нуклеиновой кислоты по любому из пп. 87-123, где молекула нуклеиновой кислоты, содержащая последовательность, кодирующую один или несколько тагов, встроена между нуклеотидами, соответствующими позициям С1902 и А1903 генома HBV.
125. Молекула нуклеиновой кислоты по любому из пп. 87-124, где молекула нуклеиновой кислоты содержит в направлении 5' относительно последовательности, кодирующей один или несколько тагов, последовательность, способную образовывать пары с основаниями нижнего стебля эпсилон-структуры, кодируемой геномом гепаднавируса.
126. Молекула нуклеиновой кислоты по п. 125, где последовательность, способная образовывать пары с основаниями нижнего стебля эпсилон-структуры, кодируемой геномом гепаднавируса, способна образовывать пары с нуклеотидами генома HBV, соответствующими позициям от Т1849 до А1854.
127. Молекула нуклеиновой кислоты по п. 125 или 126, где последовательность, способная образовывать пары с основаниями нижнего стебля эпсилон-структуры, кодируемой геномом гепаднавируса, включает в себя вплоть до 9 нуклеотидов.
128. Молекула нуклеиновой кислоты по п. 127, в котором последовательность, способная образовывать пары с основаниями нижнего стебля эпсилон-структуры, кодируемой геномом гепаднавируса, состоит из последовательности, приведенной в SEQ ID No. 26; или где последовательность, которая способна образовывать пары с основаниями нижнего стебля эпсилон-структуры, кодируемой геномом гепаднавируса, кодирует полипептид, приведенный в SEQ ID NO. 40.
129. Молекула нуклеиновой кислоты по любому из пп. 87-128, где молекула нуклеиновой кислоты содержит в направлении 3' относительно последовательности, кодирующей один или несколько тагов, последовательность, кодирующую линкер.
130. Молекула нуклеиновой кислоты по п. 129, где указанный линкер состоит из одного или нескольких аминокислотных остатков.
131. Молекула нуклеиновой кислоты по п. 129, где указанный линкер состоит из одного аминокислотного остатка.
132. Молекула нуклеиновой кислоты по п. 131, где указанный аминокислотный остаток представляет собой остаток глицина.
133. Молекула нуклеиновой кислоты по любому из пп. 129-131, где указанная последовательность, кодирующая линкер, состоит из последовательности GGC; или где указанная последовательность кодирует остаток глицина.
134. Молекула нуклеиновой кислоты по любому из пп. 87-133, где молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую меченый антиген Е гепаднавируса, содержит нуклеотидную последовательность, приведенную в SEQ ID NO. 41; или
где молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую меченый антиген Е гепаднавируса, содержит нуклеотидную последовательность, кодирующую аминокислотную последовательность, приведенную в SEQ ID NO. 42.
135. Молекула нуклеиновой кислоты по любому из пп. 87-134, где указанные один или несколько тагов слиты в рамке с антигеном Е гепаднавируса.
136. Молекула нуклеиновой кислоты по п. 135, где указанный антиген Е гепаднавируса представляет собой антиген Е вируса гепатита В (HBeAg).
137. Молекула нуклеиновой кислоты по любому из пп. 88-136, где нуклеотидная последовательность, кодирующая меченый HBeAg, приведена в SEQ ID NO: 20.
138. Молекула нуклеиновой кислоты по любому из пп. 88-137, где аминокислотная последовательность меченого HBeAg приведена в SEQ ID NO: 22.
139. Молекула нуклеиновой кислоты по любому из пп. 88-138, где нуклеотидная последовательность, кодирующая меченный прекоровый белок HBV, приведена в SEQ ID NO: 19.
140. Молекула нуклеиновой кислоты по любому из пп. 88-139, где аминокислотная последовательность меченого прекорового белка HBV приведена в SEQ ID NO: 21.
141. Молекула нуклеиновой кислоты по любому из пп. 110-140, где нуклеотидная последовательность генома HBV приведена в любой из SEQ ID NO: 27, 28, 29, 30, 31, 32, 33 или 34.
142. Молекула нуклеиновой кислоты по любому из пп. 109-141, где молекула нуклеиновой кислоты может транскрибироваться в прегеномную (пг) РНК гепаднавируса.
143. Молекула нуклеиновой кислоты по п. 142, где указанная РНК гепаднавируса представляет собой РНК HBV.
144. Молекула нуклеиновой кислоты по любому из пп. 87-143, где молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую меченый антиген Е гепаднавируса, содержится в векторе.
145. Молекула нуклеиновой кислоты по п. 144, где указанный антиген Е гепаднавируса представляет собой антиген Е вируса гепатита В (HBeAg).
146. Молекула нуклеиновой кислоты по любому из пп. 87-145, где указанная молекула нуклеиновой кислоты обеспечивает трансляцию меченого антигена Е гепаднавируса.
147. Молекула нуклеиновой кислоты по п. 146, где указанный антиген Е гепаднавируса представляет собой антиген Е вируса гепатита В (HBeAg).
148. Нуклеиновая кислота по п. 147, где нуклеиновая кислота содержится в векторе, который содержит последовательность, приведенную в SEQ ID NO: 39.
149. Молекула нуклеиновой кислоты по любому из пп. 87-148, где указанная молекула нуклеиновой кислоты предотвращает трансляцию меченого антигена Е гепаднавируса.
150. Молекула нуклеиновой кислоты по п. 149, где указанная нуклеиновая кислота не содержит стартового кодона ATG в 5' направлении против хода транскрипции относительно нуклеиновой кислоты, кодирующей меченый антиген Е гепаднавируса.
151. Молекула нуклеиновой кислоты по п. 147 или 150, где стартовый кодон ATG в 5' направлении против хода транскрипции относительно нуклеиновой кислоты, кодирующей меченый антиген Е гепаднавируса, заменен нуклеотидами TG.
152. Молекула нуклеиновой кислоты по любому из пп. 147-151, где указанная нуклеиновая кислота модифицирована путем точечной мутации для предотвращения трансляции меченого антигена Е гепаднавируса.
153. Молекула нуклеиновой кислоты по любому из пп. 144, 145 и 149-152, где вектор содержит последовательность, приведенную в SEQ ID NO: 35.
154. Молекула нуклеиновой кислоты по любому из пп. 87-153, где молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую меченый антиген Е гепаднавируса, находится под контролем индуцируемого промотора.
155. Молекула нуклеиновой кислоты по любому из пп. 149-154, где антиген Е гепаднавируса представляет собой антиген Е вируса гепатита В (HBeAg).
156. Молекула нуклеиновой кислоты по п. 154 или 155, где индуцируемый промотор представляет собой тетрациклин-индуцируемый промотор, доксициклин-индуцируемый промотор, антибиотик-индуцируемый промотор, медь-индуцируемый промотор, спирт-индуцируемый промотор, стероид-индуцируемый промотор или гербицид-индуцируемый промотор.
157. Молекула нуклеиновой кислоты по любому из пп. 154-156, где индуцируемый промотор представляет собой промотор CMV или промотор tet-EF-1 альфа.
158. Молекула нуклеиновой кислоты по любому из пп. 110-157, где один или несколько стоп-кодонов встроены в кодирующую область одного или нескольких белков оболочки гепаднавируса.
159. Молекула нуклеиновой кислоты по п. 158, где указанные один или несколько белков оболочки гепаднавируса представляют собой один или несколько белков оболочки HBV.
160. Молекула нуклеиновой кислоты по п. 159, где указанные один или несколько белков оболочки HBV представляют собой L, М и/или S.
161. Молекула нуклеиновой кислоты по п. 159, где белок оболочки HBV представляет собой S.
162. Молекула нуклеиновой кислоты по любому из пп. 159-161, где кодирующая область одного или нескольких белков оболочки HBV приведена в SEQ ID NO: 36 (L), 37 (М) или 38 (S).
163. Молекула нуклеиновой кислоты по п. 162, где нуклеотиды HBV с 217 до 222 (TTGTTG) последовательности SEQ ID NO: 38 (S) мутированы в TAGTAG для предотвращения экспрессии белков оболочки.
164. Белок, кодируемый молекулой нуклеиновой кислоты, описанной в любом из пп. 87-163.
165. Белок, содержащий меченный антиген Е гепаднавируса.
166. Белок по п. 165, где указанный антиген Е гепаднавируса представляет собой антиген Е вируса гепатита В (HBeAg).
167. Белок по п. 166, где антиген Е вируса гепатита В (HBeAg) содержит аминокислотную последовательность, приведенную в SEQ ID NO: 18.
168. Белок по любому из пп. 165-167, где указанный меченый антиген Е гепаднавируса содержит только один таг.
169. Белок по п. 168, где указанный таг состоит из 6-22 аминокислот.
170. Белок по любому из пп. 165-169, где указанный таг выбран из группы, состоящей из гемагглютининового (НА) тага, His-тага, Flag-тага, с-myc-тага, V5-тага и С9-тага.
171. Белок по п. 170, где указанный Flag-таг представляет собой 1×Flag-таг или 3×Flag-таг.
172. Белок по любому из пп. 165-167, где указанный меченый антиген Е гепаднавируса содержит два или более тагов.
173. Способ по п. 172, где указанные два или более тагов представляют собой различные таги.
174. Белок по п. 172 или 173, где суммарная длина указанных двух или более тагов составляет приблизительно от 14 до 31 аминокислоты.
175. Белок по любому из пп. 172-174, где указанные два или более тагов представляют собой два или более гемагглютининовых (НА)-тагов, His-тагов, Flag-тагов, c-myc-тагов, V5-тагов и/или С9-тагов.
176. Белок по п. 175, где указанный Flag-таг представляет собой 1×Flag-таг или 3×Flag-таг.
177. Белок по п. 170 или 175,
где нуклеотидные последовательности, кодирующие НА таг, приведены в SEQ ID NO: 1; где нуклеотидные последовательности, кодирующие His-таг, приведены в SEQ ID NO: 2; где нуклеотидные последовательности, кодирующие с-myc-таг, приведены в SEQ ID NO: 4; где нуклеотидные последовательности, кодирующие V5-таг, приведены в SEQ ID NO: 5; и/или где нуклеотидные последовательности, кодирующие С9-таг, приведены в SEQ ID NO: 6.
178. Белок по п. 171 или 176,
где нуклеотидные последовательности, кодирующие 1×Flag-таг, приведены в SEQ ID NO: 3; или
где нуклеотидные последовательности, кодирующие 3×Flag-таг, приведены в SEQ ID NO: 7.
179. Белок по п. 170 или 175,
где аминокислотная последовательность НА тага приведена в SEQ ID NO: 8;
где аминокислотная последовательность His-тага приведена в SEQ ID NO: 9;
где аминокислотная последовательность c-myc-тага приведена в SEQ ID NO: 11;
где аминокислотная последовательность V5-тага приведена в SEQ ID NO: 12; и/или
где аминокислотная последовательность С9-тага приведена в SEQ ID NO: 13.
180. Белок по п. 171 или 176,
где аминокислотная последовательность 1×Flag-тага приведена в SEQ ID NO: 10; или
где аминокислотная последовательность 3×Flag-тага приведена в SEQ ID NO: 14.
181. Белок по любому из пп. 165-180, содержащий прекоровый белок гепаднавируса.
182. Белок по п. 181, где нуклеотидная последовательность, кодирующая прекоровый белок гепаднавируса, приведена в SEQ ID NO: 15.
183. Белок по п. 181, где аминокислотная последовательность прекорового белка гепаднавируса приведена в SEQ ID NO: 17.
184. Белок по любому из пп. 165-183, где белок содержит аминокислотную последовательность одного или нескольких тагов, где указанная последовательность находится в С-концевом направлении относительно аминокислотной последовательности сигнального пептида и линкера прекорового белка гепаднавируса.
185. Белок по п. 184, где указанный белок, содержащий аминокислотную последовательность одного или нескольких тагов, расположен в С-концевом направлении относительно аминокислотной последовательности 29 N-концевых аминокислот прекорового белка вируса гепатита В.
186. Белок по любому из пп. 165-183, где белок содержит аминокислотную последовательность одного или нескольких тагов, где указанная последовательность находится в N-концевом направлении относительно аминокислотной последовательности корового белка гепаднавируса.
187. Белок по п. 186, где коровый белок гепаднавируса представляет собой коровый белок HBV.
188. Белок по п. 187, где нуклеиновая кислота, кодирующая коровый белок HBV, приведена в SEQ ID NO: 23.
189. Белок по п. 187, где аминокислотная последовательность корового белка HBV приведена в SEQ ID NO: 24.
190. Белок по любому из пп. 165-189, где аминокислотная последовательность одного или нескольких тагов встроена в аминокислотную последовательность, кодируемую эпсилон-структурой, кодируемой геномом гепаднавируса.
191. Белок по п. 190, где геном гепаднавируса представляет собой геном HBV.
192. Белок по п. 191, где нуклеотидная последовательность эпсилон-структуры, кодируемой геномом HBV, приведена в SEQ ID NO: 25.
193. Белок по любому из пп. 165-192, где аминокислотная последовательность одного или нескольких тагов встроена в аминокислотную последовательность, кодируемую нижним стеблем эпсилон-структуры, кодируемой геномом гепаднавируса.
194. Белок по п. 193, где геном гепаднавируса представляет собой геном HBV.
195. Белок по любому из пп. 165-194, где аминокислотная последовательность одного или нескольких тагов встроена между аминокислотными остатками, соответствующими позиции G29 и позиции М30 прекорового белка HBV (например, такого, который приведен в SEQ ID NO. 17).
196. Белок по любому из пп. 165-195 дополнительно содержащий в N-концевом направлении относительно аминокислотной последовательности одного или нескольких тагов аминокислотную последовательность, включающую до 3 аминокислот, где указанная аминокислотная последовательность длиной до 3 аминокислот кодируется нуклеотидной последовательностью, которая способна образовывать пары с основаниями нижнего стебля эпсилон-структуры, кодируемой геномом гепаднавируса.
197. Белок по п. 196, в котором нуклеотидная последовательность, способная образовывать пары с основаниями нижнего стебля эпсилон-структуры, кодируемой геномом гепаднавируса, способна образовывать пары с нуклеотидами, соответствующими позициям генома HBV от Т1849 до А1854.
198. Белок по п. 198, где нуклеотидная последовательность, способная образовывать пары с основаниями нижнего стебля эпсилон-структуры, кодируемой геномом гепаднавируса, состоит из последовательности, приведенной в SEQ ID No. 26.
199. Белок по любому из пп. 196-198, где указанная аминокислотная последовательность, включающая до 3 аминокислот, приведена в SEQ ID NO: 40.
200. Белок по любому из пп. 165-199, дополнительно содержащий линкер в С-концевом направлении относительно аминокислотной последовательности одного или нескольких тагов.
201. Белок по п. 200, где указанный линкер состоит из одного или нескольких аминокислотных остатков.
202. Белок по п. 201, где указанный линкер состоит только из одного аминокислотного остатка.
203. Белок по п. 202, где указанный аминокислотный остаток представляет собой остаток глицина.
204. Белок по любому из пп. 1-46, где аминокислотная последовательность меченого антигена Е гепаднавируса содержит аминокислотную последовательность, кодируемую нуклеотидной последовательностью, приведенной в SEQ ID NO. 41; или
где аминокислотная последовательность меченого антигена Е гепаднавируса содержит аминокислотную последовательность, приведенную в SEQ ID NO. 42.
205. Белок по любому из пп. 165-204, где указанные один или несколько тагов слиты в рамке с антигеном Е гепаднавируса.
206. Белок по п. 205, где антиген Е гепаднавируса представляет собой антиген Е вируса гепатита В (HBeAg).
207. Белок по любому из пп. 166-206, где нуклеотидная последовательность, кодирующая меченый HBeAg, приведена в SEQ ID NO: 20.
208. Белок по любому из пп. 166-207, где аминокислотная последовательность меченого HBeAg приведена в SEQ ID NO: 22.
209. Белок по любому из пп. 166-208, где нуклеотидная последовательность, кодирующая меченый прекоровый белок HBV, приведена в SEQ ID NO: 19.
210. Белок по любому из пп. 166-209, где аминокислотная последовательность меченого прекорового белка HBV приведена в SEQ ID NO: 21.
211. Клетка-хозяин, содержащая молекулу нуклеиновой кислоты по любому из пп. 87-163 или белок по любому из пп. 164-210.
212. Клетка-хозяин по п. 211, где клетка представляет собой эукариотическую клетку.
213. Клетка-хозяин по п. 212, где клетка эукариотическая клетка имеет гепатоцитарное происхождение.
214. Клетка-хозяин по п. 212 или 213, где эукариотическая клетка является клеткой гепатомы или происходит от клетки гепатомы.
215. Клетка-хозяин по любому из пп. 212-214, где клетка эукариотическая клетка представляет собой HepG2 (АТСС #НВ-8065).
216. Способ получения белка, описанного в любом из пп. 164-210, указанный способ включает культивирование хозяина по любому из пп. 210-215 при условиях, обеспечивающих экспрессию белка и выделение полученного белка из культуры.
217. Набор для применения в способе по любому из пп. 1-86.
218. Набор, содержащий антитело, специфически распознающее антиген Е гепаднавируса, описанный в любом из пп. 165-167, и одно или несколько антител, специфически распознающих один или несколько тагов, описанных в любом из пп. 168-180.
219. Применение молекулы нуклеиновой кислоты по любому из пп. 87-163, белка по любому из пп. 164-210 и/или клетки-хозяина по любому из пп. 211-215 для скрининга молекул-кандидатов, предположительно способных ингибировать ковалентно замкнутую кольцевую ДНК гепаднавируса.
Реферат
Изобретение относится к области биотехнологии и молекулярной биологии. Предложен способ оценки способности молекулы-кандидата ингибировать ковалентно замкнутую кольцевую (кзк) ДНК гепаднавируса, представляющего собой вирус гепатита B (HBV). Способ обеспечивает надежный скрининг ингибиторов вируса гепатита В, что может быть использовано в медицине. 2 н. и 17 з.п. ф-лы, 13 ил., 1 пр.

Комментарии