Аналоги инсулина - RU2019100497A
Код документа: RU2019100497A
Формула
1. Аналог инсулина, содержащий пептид, представляющий собой А-цепь, и пептид, представляющий собой В-цепь, где В-цепь содержит ароматический или большой алифатический остаток в положении, соответствующем аминокислоте номер 20 в В-цепи человеческого инсулина, и/или ароматический или большой алифатический остаток в положении, соответствующем аминокислоте номер 15 в В-цепи человеческого инсулина, где аналог содержит по меньшей мере одну аминокислоту, которая встречается в человеческом инсулине, но отсутствует в соответствующем положении инсулина из яда Conus geographus, и где пептид, представляющий собой А-цепь, и пептид, представляющий собой В-цепь, связаны друг с другом посредством по меньшей мере одной пары цистеиновых остатков.
2. Аналог инсулина по п. 1, где ароматический или большой алифатический остаток в положении, соответствующем аминокислоте номер 20 в В-цепи человеческого инсулина, выбран из группы, состоящей из тирозина, фенилаланина, 4-метил фенилаланина, гистидина, триптофана, метионина, циклопентилаланина и циклогексилаланина.
3. Аналог инсулина по п. 1 или 2, где В-цепь усечена по С-терминальному концу по сравнению с человеческим инсулином.
4. Аналог инсулина по п. 3, где в В-цепи отсутствуют одна или несколько или все из девяти С-концевых аминокислот человеческого инсулина.
5. Аналог инсулина по п. 3 или 4, где в В-цепи отсутствует по меньшей мере РЬев24 человеческого инсулина.
6. Аналог инсулина по любому из пп. 1-5, где в В-цепи отсутствует по меньшей мере триплет ароматических аминокислот (аминокислоты PheB24-PheB25-TyrB26) человеческой В-цепи.
7. Аналог инсулина по любому из пп. 1-6, содержащий
пептид, представляющий собой А-цепь, содержащий последовательность Gly-XA2-XA3-XA4-XA5-CysA6-CysA7-XA8-XA9-XA10-CysA11-XA12-XA13-XA14-XA15-XA16-XA17-XA18-XA19-CysA20-XA21-XA22-XA23-XA24-XA25-XA26-XA27-XA28-XA29-XA30-XA31-XA32-XA33-XA34,
где XA2=Val или Ile; XA3=Val или Ala; XA4=Glu, Asp, Cys или гамма-карбоксиглутамат; XA5=Gln, Glu, гамма-карбоксиглутамат, His или Val; CysA6, CysA7 и CysA11 независимо представляют собой Cys или селеноцистеин; XA8=Thr, His, Asp, Gln, Tyr, Lys, Ala или Val; XA9=Ser, Arg, Asn, Gly, His или Lys; XA10=Ile, Pro, Tyr, Ala, Ser, Val, Phe, His или Thr; XA12=Ser или Thr; XA13=Leu, Asn, Val, Arg или Asp; XA14=Tyr, Ala, Gln, His, Asp или Glu; XA15=Gln, Glu или Thr; XA16=Phe, Leu или Ala; XA17=Glu, Gln, Lys, Arg, Ile, Met, Thr или Ser; XA18=Lys, Ser, Thr, Asn, Gln или Glu; XA19=Tyr или Phe; CysA20=Cys, селеноцистеин, амидированный Cys или амидированный селеноцистеин; XA21=Asn, Pro, His, Ser, Gly, Ala или отсутствует; XA22=Pro, Asn, Thr, Leu, Ser или отсутствует; XA23=Thr, Leu, Val, Ser или отсутствует; XA24=Arg, Thr, Met, Gln, Leu или отсутствует; XA25=Glu, Gly или отсутствует; XA26=Ser, Leu или отсутствует; XA27 - XA31 независимо представляют собой Ser или отсутствуют; XA32=Ala, Ser или отсутствует; XA33=Ala, Val или отсутствует; и XA34=Ala или отсутствует (SEQ ID NO: 1); и
пептид, представляющий собой В-цепь, содержащий последовательность XB1-XB2-XB3-XB4-XB5-XB6-XB7-XB8-CysB9-XB10-XB11-XB12-XB13-XB14-XB15-XB16-XB17-XB18-XB19-XB20-CysB21-XB22-XB23-XB24-XB25-XB26-XB27-XB28-XB29-XB30-XB31-XB32-XB33-XB34-XB35-XB36-XB37-XB38-XB39,
где XB1=Thr, Asn, Ser или отсутствует; XB2=Phe, Ser, Asn, Thr, Gln или отсутствует; XB3=Ala, Asp, Gly, Pro, Leu, Phe или His; XB4=Ala, Thr, Pro, Asp, Val или Gly; XB5=Asn, Pro, His, Thr, Arg, Lys, Ser или гидроксипролин; XB6=Lys, Glu, Asn, Asp, Arg, Gln или Gly; XB7=His, Tyr, Arg или Ile; XB8=Arg, Thr, Ile, Ser, Leu, Tyr или Lys; CysB9=Cys или селеноцистеин; XB10=Gly, Gln или Asp; XB11=Ser, Leu, Gly или Pro; XB12=His, Glu, гамма-карбоксиглутамат, Asp или Asn; XB13=Ile, Leu, Asp, Val или Ala; XB14=Thr, Ala, Pro, Val или Arg; XB15=Asn, Asp, Ala, Val, Thr, Pro или Glu; XB16=Ala, Ser, Gln, His, Thr, Tyr, Arg или Gly; XB17=Thr, Tyr, Pro, Leu или Gly; XB18=Tyr, Met, Val, Gln, Ile, Asp, Gly, Asn или Leu; XB19=Leu, Asp, Gln, Gly, Lys, Glu, Arg, Ser или Thr; XB20=Val, Leu или Lys; XB21=Cys, амидированный Cys, селеноцистеин или амидированный селеноцистеин; XB22=Val, Tyr, Phe, His, Gly, Gln, Leu, амидированный His, амидированный Val или отсутствует; XB23=Glu, Asp, Arg, Ser, Gly или отсутствует; XB24=Arg, Asp, Val или отсутствует; XB25=Gly, Leu, Val или отсутствует; XB26=Phe, Val, He или отсутствует; XB27=Phe, Asn, Pro, Glu или отсутствует; XB28=Tyr, Cys, His или отсутствует; XB29=Thr, His, ILe, Leu, Ser, Tyr или отсутствует; XB30=Pro, Glu, Leu, Ile, Arg или отсутствует; XB31=Ile, Lys или отсутствует; XB32=Ala, Asp, Ser, Thr, Lys, Leu, Gln или отсутствует; XB33=Cys или отсутствует; XB34=Glu, Pro, Val или отсутствует; XB35=Glu, Gly или отсутствует; XB36=Glu, Gly или отсутствует; XB37=Glu, Val или отсутствует; XB38=Ala, Asp или отсутствует; и XB39=Ala или отсутствует (SEQ ID NO: 2).
8. Аналог инсулина по п. 7, где пептид, представляющий собой В-цепь, содержит последовательность XB1-XB2-XB3-XB4-XB5-XB6-XB7-XB8-CysB9-XB10-XB11-XB12-XB13-XB14-XB15-XB16-XB17-XB18-XB19-XB20-CysB21-XB22-XB23-XB24-XB25-XB26-XB27-XB28-XB29-XB30-XB31-XB32-XB33-XB34-XB35-XB36-XB37-XB38-XB39,
где XB1=Thr, Asn, Ser или отсутствует; XB2=Phe, Ser, Asn, Thr, Gln или отсутствует; XB3=Asp, Gly, Pro, Leu, Phe или His; XB4=Thr, Pro, Asp, Val или Gly; XB5=Asn, Pro, His, Thr, Arg, Ser или гидроксипролин; XB6=Lys, Glu, Asn, Asp, Arg, Gln или Gly; XB7=His, Tyr, Arg или He; XB8=Arg, Thr, Ile, Ser, Leu, Tyr или Lys; CysB9=Cys или селеноцистеин; XB10=Gly, Gln или Asp; XB11=Ser, Leu, Gly или Pro; XB12=His, Glu, гамма-карбоксиглутамат, Asp или Asn; XB13=Ile, Leu, Asp, Val или Ala; XB14=Thr, Ala, Pro, Val или Arg; XB15=Asn, Asp, Ala, Val, Thr, Pro или Glu; XB16=Ala, Ser, Gln, His, Tyr, Arg или Gly; XB17=Tyr или Leu; XB18=Tyr, Met, Val, Gln, Ile, Asp, Gly, Asn или Leu; XB19=Leu, Asp, Gln, Gly, Lys, Glu, Arg или Thr; XB20=Val, Leu или Lys; CB21=Cys, амидированный Cys, селеноцистеин или амидированный селеноцистеин; XB22=Tyr, Phe или His; XB23=Glu, Arg, Ser, Gly или отсутствует; XB24=Arg, Asp, Val или отсутствует; XB25=Gly, Leu, Val или отсутствует; XB26=Phe, Val, Ile или отсутствует; XB27=Phe, Asn, Pro, Glu или отсутствует; XB28=Tyr, Cys, His или отсутствует; XB29=Thr, His, Leu, Tyr или отсутствует; XB30=Pro, Glu, Leu, Ile, Arg или отсутствует; XB31=Ile, Lys или отсутствует; XB32=Thr, Lys, Leu, Gln или отсутствует; XB33=Cys или отсутствует; XB34=Glu, Pro, Val или отсутствует; XB35=Glu, Gly или отсутствует; XB36=Glu, Gly или отсутствует; XB37=Glu, Val или отсутствует; XB38=Ala, Asp или отсутствует; и XB39=Ala или отсутствует (SEQ ID NO: 3).
9. Аналог инсулина по п. 7 или 8, где пептид, представляющий собой В-цепь, содержит последовательность XB1-XB2-XB3-XB4-XB5-XB6-XB7-XB8-CysB9-XB10-XB11-XB12-XB13-XB14-XB15-XB16-XB17-XB18-XB19-XB20-CysB21-XB22-XB23-XB24-XB25-XB26-XB27-XB28-XB29-XB30-XB32-XB32-XB33-XB34-XB35-XB36-XB37-XB38-XB39,
где XB1=Thr, Asn, Ser или отсутствует; XB2=Phe, Ser, Asn, Thr, Gln или отсутствует; XB3=Asp, Gly, Pro, Leu, Phe или His; XB4=Thr, Pro, Asp, Val или Gly; XB5=Asn, Pro, His, Thr, Arg, Ser или гидроксипролин; XB6=Lys, Glu, Asn, Asp, Arg, Gln или Gly; XB7=His, Tyr, Arg или Ile; XB8=Arg, Thr, Ile, Ser, Leu, Tyr или Lys; CysB9=Cys или селеноцистеин; XB10=Gly, Gln или Asp; XB11=Ser, Leu, Gly или Pro; XB12=His, Glu, гамма-карбоксиглутамат, Asp или Asn; XB13=Ile, Leu, Asp, Val или Ala; XB14=Thr, Ala, Pro, Val или Arg; XB15=Asn, Asp, Ala, Val, Thr, Pro или Glu; XB16=Ala, Ser, Gln, His, Tyr, Arg или Gly; XB17=Tyr или Leu; XB18=Tyr, Met, Val, Gln, Ile, Asp, Gly, Asn или Leu; XB19=Leu, Asp, Gln, Gly, Lys, Glu, Arg или Thr; XB20=Val, Leu или Lys; CB21=Cys, амидированный Cys, селеноцистеин или амидированный селеноцистеин; XB22=Tyr, Phe или His; XB23=Glu, Arg, Ser, Gly или отсутствует; и XB24, XB25, XB26, XB27, XB28, XB29, XB30, XB31, XB32, XB33, XB34, XB35, XB36, XB37, XB38 и XB39 отсутствуют (SEQ ID NO: 4).
10. Аналог инсулина по п. 7 или 8, где пептид, представляющий собой В-цепь, содержит последовательность XB1-XB2-XB3-XB4-XB5-XB6-XB7-XB8-CysB9-Gly-Ser-XB12-XB13-XB14-XB15-XB16-XB17-XB18-XB19-XB20-CysB21-XB22-XB23-XB24-XB25-XB26-XB27-XB28-XB29-XB30-XB31-XB32-XB33-XB34-XB35-XB36-XB37-XB38-XB39,
где XB1=Thr, Asn, Ser или отсутствует; XB2=Phe, Ser, Asn, Thr, Gln или отсутствует; XB3=Asp, Gly, Pro, Leu, Phe или His; XB7=Thr, Pro, Asp, Val или Gly; XB5=Asn, Pro, His, Thr, Arg, Ser или гидроксипролин; XB6=Lys, Glu, Asn, Asp, Arg, Gln или Gly; XB7=His, Tyr, Arg или He; XB8=Arg, Thr, Ile, Ser, Leu, Tyr или Lys; CysB9=Cys или селеноцистеин; XB12=His, Glu, гамма-карбоксиглутамат, Asp или Asn; XB13=Ile, Leu, Asp, Val или Ala; XB14=Thr, Ala, Pro, Val или Arg; XB15=Asn, Asp, Ala, Val, Thr, Pro или Glu; XB16=Ala, Ser, Gln, His, Tyr, Arg или Gly; XB17=Tyr или Leu; XB18=Tyr, Met, Val, Gln, Ile, Asp, Gly, Asn или Leu; XB19=Leu, Asp, Gln, Gly, Lys, Glu, Arg или Thr; XB20=Val, Leu или Lys; CB21=Cys, амидированный Cys, селеноцистеин или амидированный селеноцистеин; XB22=Tyr, Phe или His; XB23=Glu, Arg, Ser, Gly или отсутствует; XB24=Arg, Asp, Val или отсутствует; XB25=Gly, Leu, Val или отсутствует; XB26=Phe, Val, Не или отсутствует; XB27=Phe, Asn, Pro, Glu или отсутствует; XB28=Tyr, Cys, His или отсутствует; XB29=Thr, His, Leu, Tyr или отсутствует; XB30=Pro, Glu, Leu, Ile, Arg или отсутствует; XB31=Ile, Lys или отсутствует; XB32=Thr, Lys, Leu, Gln или отсутствует; XB33=Cys или отсутствует; XB34=Glu, Pro, Val или отсутствует; XB35=Glu, Gly или отсутствует; XB36=Glu, Gly или отсутствует; XB37=Glu, Val или отсутствует; XB38=Ala, Asp или отсутствует; и XB39=Ala или отсутствует (SEQ ID NO: 5).
11. Аналог инсулина по п. 7 или 8, где пептид, представляющий собой В-цепь, содержит последовательность XB1-XB2-XB3-XB4-XB5-XB6-XB7-XB8-CysB9-Gly-Ser-XB12-XB13-XB14-XB15-XB16-XB17-XB18-XB19-XB20-CysB21-XB22-XB23-XB24-XB25-XB26-XB27-XB28-XB29-XB30-XB31-XB32-XB33-XB34-XB35-XB36-XB37-XB38-XB39,
где XB1=Thr, Asn, Ser или отсутствует; XB2=Phe, Ser, Asn, Thr, Gln или отсутствует; XB3=Asp, Gly, Pro, Leu, Phe или His; XB4=Thr, Pro, Asp, Val или Gly; XB5=Asn, Pro, His, Thr, Arg, Ser или гидроксипролин; XB6=Lys, Glu, Asn, Asp, Arg, Gln или Gly; XB7=His или Tyr; XB8=Arg, Thr, Ile, Ser, Leu, Tyr или Lys; CysB9=Cys или селеноцистеин; XB12=His, Glu, гамма-карбоксиглутамат, Asp или Asn; XB13=Ile, Leu, Asp, Val или Ala; XB14=Thr, Ala, Pro, Val или Arg; XB15=Asn, Asp, Ala, Val, Thr, Pro или Glu; XB16=Ala, Ser, Gln, His, Tyr, Arg или Gly; XB17=Tyr или Leu; XB18=Tyr, Met, Val, Gln, Ile, Asp, Gly, Asn или Leu; XB19=Leu, Asp, Gln, Gly, Lys, Glu, Arg или Thr; XB20=Val или Leu; XB21=Cys, амидированный Cys, селеноцистеин или амидированный селеноцистеин; XB22=Tyr, Phe или His; XB23=Glu, Arg, Ser, Gly или отсутствует; XB24=Arg, Asp, Val или отсутствует; XB25=Gly, Leu, Val или отсутствует; XB26=Phe, Val, Ile или отсутствует; XB27=Phe, Asn, Pro, Glu или отсутствует; XB28=Tyr, Cys, His или отсутствует; XB29=Thr, His, Leu, Tyr или отсутствует; XB30=Pro, Glu, Leu, Ile, Arg или отсутствует; XB31=Ile, Lys или отсутствует; XB32=Thr, Lys, Leu, Gln или отсутствует; XB33=Cys или отсутствует; XB34=Glu, Pro, Val или отсутствует; XB35=Glu, Gly или отсутствует; XB36=Glu, Gly или отсутствует; XB37=Glu, Val или отсутствует; XB38=Ala, Asp или отсутствует; и XB39=Ala или отсутствует (SEQ ID NO: 6).
12. Аналог инсулина по п. 7, где пептид, представляющий собой В-цепь, содержит последовательность XB1-XB2-XB3-XB4-XB5-XB6-XB7-XB8-CysB9-Gly-Ser-XB12-XB13-XB14-XB15-XB16-XB17-XB18-XB19-XB20-CysB21-XB22-XB23, где XB1=Thr, Asn или отсутствует; XB2=Phe, Ser или отсутствует; XB3=Phe или Asp; XB4=Thr или Val; XB5=Pro, Asn или гидроксипролин; XB6=Lys, Asn или Gln; XB7=His или Tyr; XB8=Arg, Ile или Leu; CysB9=Cys или селеноцистеин; XB12=His, Asp, Glu или гамма-карбоксиглутамат; XB13Val, Ile или Leu; XB14=Thr, Ala, Pro или Val; XB15=Glu, Val, Asn или Asp; XB16=Ser, Gln, Tyr или Ala; XB17=Tyr или Leu; XB18=Tyr, Asp, Met или Val; XB19=Leu, Asp, Gln или Lys; XB20=Leu или Val; CysB21=Cys, амидированный Cys, селеноцистеин или амидированный селеноцистеин; XB22=Tyr или Gly; и XB23=Glu, Arg, Gly или отсутствует (SEQ ID NO: 7).
13. Аналог инсулина по п. 12, где пептид, представляющий собой В-цепь, содержит последовательность XB1-XB2-XB3-XB4-XB5-XB6-His-XB8-CysB9-Gly-Ser-XB12-XB13-XB14-XB15-XB16-XB17-XB18-XB19-XB20-CysB21-XB22-XB23, где XB1=Thr или отсутствует; XB2=Phe или отсутствует; XB3=Phe или Asp; XB4=Thr или Val; XB5=Pro, Asn или гидроксипролин; XB6=Lys или Gln; XB8=Arg или Leu; XB12=His, Glu или гамма-карбоксиглутамат; XB13=Ile или Leu; XB14=Thr или Val; XB15=Glu или Asn; XB16=Ser или Ala; XB17Tyr или Leu, XB18=Tyr или Met; XB19=Leu или Asp, XB20=Leu или Val; XB22=Tyr; и XB23=Glu или Arg (SEQ ID NO: 8).
14. Аналог инсулина по любому из пп. 7-12, где XB22 представляет собой Tyr.
15. Аналог инсулина по любому из пп. 1-14, где пептид, представляющий собой А-цепь, содержит последовательность Gly-XA2-XA3-XA4-XA5-CysA6-CysA7-XA8-XA9-XA10-CysA11-XA12-XA13-XA14-XA15-Phe-XA17-XA18-XA19-CysA20-XA21-XA22-XA23-XA24-XA25-XA26-XA27-XA28-XA29-XA30-XA31-XA32-XA33-XA34,
где XA2=Val или Ile; XA3=Val или Ala; XA4=Glu, гамма-карбоксиглутамат или Cys; XA5=Gln, Glu, гамма-карбоксиглутамат, His или Val; CysA6, CysA7 и CysA11 независимо представляют собой Cys или селеноцистеин; XA8=Thr, His, Asp, Gln, Tyr, Lys или Val; XA9=Ser, Arg, Asn, His или Lys; XA10=Ile, Pro, Tyr, Ala, Ser, Phe, His или Thr; XA12=Ser или Thr; XA13=Leu, Asn, Val или Asp; XA14=Tyr, Ala, Gln, Asp или Glu; XA15=Gln, Glu, или Thr; или Ala; XA17=Glu, Lys, Arg, Ile, Met, Thr или Ser; XA18=Lys, Thr, Asn, Gln или Glu; XA19=Tyr или Phe; CysA20=Cys, селеноцистеин, амидированный Cys или амидированный селеноцистеин; XA21=Asn, Pro, His, Ser, Gly, Ala или отсутствует; XA22=Pro, Asn, Thr, Leu, Ser или отсутствует; XA23=Thr, Leu, Val, Ser или отсутствует; XA24=Arg, Thr, Met, Gln, Leu или отсутствует; XA25=Glu, Gly или отсутствует; XA26=Ser, Leu или отсутствует; XA27-XA31 независимо представляют собой Ser или отсутствуют; XA32=Ala, Ser или отсутствует; XA33=Ala, Val или отсутствует; и XA34=Ala или отсутствует (SEQ ID NO: 9).
16. Аналог инсулина по любому из пп. 1-6, содержащий пептид, представляющий собой А-цепь, содержащий последовательность Gly-XA2-Val-XA4-XA5-CysA6-CysA7-XA8-XA9-XA10-CysA11-Ser-XA13-XA14-XA15-XA16-XA17-XA18-Tyr-CysA20-XA21, где XA2 представляет собой Val или Ile, XA4 представляет собой Glu или гамма-карбоксиглутамат, XA5 представляет собой His или Gln, XA8 представляет собой His или Thr, XA9 представляет собой Arg или Ser, XA10 представляет собой Pro или Ile, XA13 представляет собой Asn или Leu, XA14 представляет собой Ala или Tyr, XA15 представляет собой Glu или Gln, XA16 представляет собой Phe или Leu, XA17 представляет собой Lys или Glu, XA18 представляет собой Lys или Asn, и XA21 представляет собой Asn или отсутствует (SEQ ID NO: 10); и
пептид, представляющий собой В-цепь, содержащий последовательность XB21-XB2-XB3-XB4-XB5-XB6-His-XB8-CysB9-G1y-Ser-XB12-XB13-XB14-XB15-XB16-XB17-XB18-XB19-XB20-CysB21-XB22-XB23, где XB1=Thr или отсутствует; XB2=Phe или отсутствует; XB3=Phe или Asp; XB4=Thr или Val; XB5=Pro, Asn или гидроксипролин; XB6=Lys или Gln; XB8=Arg или Leu; XB12=His, Glu или гамма-карбоксиглутамат; XB13Ile или Leu; XB14=Thr или Val; XB15=Glu или Asn; XB16=Ser или Ala; XB17=Tyr или Leu; XB18=Tyr или Met; XB19=Leu или Asp, XB20=Leu или Val; XB22=Gly или Tyr; и XB23=Glu или Arg (SEQ ID NO: 11).
17. Аналог инсулина по п. 15 или 16, содержащий
пептид, представляющий собой А-цепь, содержащий последовательность Gly-XA2-Val-XA4XA5-CySA6-CysA7-XA8-XA9-XA10-CysA11-Ser-XA13-XA14-XA15-Phe-XA17-XA18-Tyr-CysA20-XA21, где XA2 представляет собой Val или Ile, XA4 представляет собой Glu или гамма-карбоксиглутамат, XA5 представляет собой His или Gln, XA8 представляет собой His или Thr, XA9 представляет собой Arg или Ser, XA10 представляет собой Pro или Ile, XA13 представляет собой Asn или Leu, XA14 представляет собой Ala или Tyr, XA15 представляет собой Glu или Gln, XA17 представляет собой Lys или Glu, XA18 представляет собой Lys или Asn, и XA21 представляет собой Asn или отсутствует (SEQ ID NO: 12); и
пептид, представляющий собой В-цепь, содержащий последовательность XB1-XB2-XB3-XB4-XB5-XB6-His-XB8-CysB9-Gly-Ser-XB12-XB13-XB14-XB15-XB16-XB17-XB18-XB19-XB20-CysB21-Tyr-XB23, где XB1=Thr или отсутствует; XB2=Phe или отсутствует; XB3=Phe или Asp; XB4=Thr или Val; XB5=Pro, Asn или гидроксипролин; XB6=Lys или Gln; XB8=Arg или Leu; XB12=His, Glu или гамма-карбоксиглутамат; XB13Ile или Leu; XB14=Thr или Val; XB15=Glu или Asn; XB16=Ser или Ala; XB17=Tyr или Leu; XB18=Tyr или Met; XB19=Leu или Asp, XB20=Leu или Val; и XB23=Glu или Arg (SEQ ID NO: 13).
18. Аналог инсулина по любому из пп. 15-17, содержащий
пептид, представляющий собой А-цепь, содержащий последовательность Gly-Val-Val-XA4-XA5-CysA6-CysA7-XA8-XA9-XA10-CysA11-Ser-XA13-XA14-XA15-Phe-XA17-XA18-Tyr-CysA20-XA21, где XA4 представляет собой Glu или гамма-карбоксиглутамат, XA5 представляет собой His или Gln, XA8 представляет собой His или Thr, XA9 представляет собой Arg или Ser, XA10 представляет собой Pro или Ile, XA13 представляет собой Asn или Leu, XA14 представляет собой Ala или Tyr, XA15 представляет собой Glu или Gln, XA17 представляет собой Lys или Glu, XA18 представляет собой Lys или Asn, и XA21 представляет собой Asn или отсутствует (SEQ ID NO: 14); и
пептид, представляющий собой В-цепь, содержащий последовательность XB1-XB2-XB3-XB4-XB5-XB6-His-Arg-CysB9-Gly-Ser-XB12-Ile-XB14-XB15-XB16-XB17-XB18-XB19-Leu-CysB21-Tyr-XB23, где XB1=Thr или отсутствует; XB2=Phe или отсутствует; XB3=Phe или Asp; XB4=Thr или Val; XB5=Pro, Asn или гидроксипролин; XB6=Lys или Gln; XB12=His, Glu или гамма-карбоксиглутамат; XB14=Thr или Val; Xbis=Glu или Asn; XB16=Ser или Ala; XB17Tyr или Leu; XB18=Tyr или Met; XB19=Leu или Asp, и XB23=Glu или Arg (SEQ ID NO: 15).
19. Аналог инсулина по любому из пп. 1-18, где применяется одно или несколько или все из следующего:
i) XA4 представляет собой гамма-карбоксиглутамат,
ii) XB5 представляет собой гидроксипролин; и
iii) XB12 представляет собой гамма-карбоксиглутамат.
20. Аналог инсулина по любому из пп. 1-19, содержащий
пептид, представляющий собой А-цепь, содержащий последовательность Gly-Ile-Val-Glu-Gln-Cys-Cys-Thr-Ser-Ile-Cys-Ser-Leu-Tyr-Gln-Leu-Glu-Asn-Tyr-Cys-Asn (SEQ ID NO: 16); и
пептид, представляющий собой В-цепь, содержащий последовательность Phe-Val-Asn-Gln-His-Leu-Cys-Gly-Ser-His-Leu-Val-Glu-Ala-Xaa-Tyr-Leu-Val-Cys-Gly-Glu, где Xaa представляет собой ароматический остаток или большой алифатический остаток (SEQ ID NO: 17).
21. Аналог инсулина по любому из пп. 1-19, содержащий
пептид, представляющий собой А-цепь, содержащий последовательность Gly-Ile-Val-Glu-Gln-Cys-Cys-Thr-Ser-Ile-Cys-Ser-Leu-Tyr-Gln-Leu-Glu-Asn-Tyr-Cys-Asn (SEQ ID NO: 18); и
пептид, представляющий собой В-цепь, содержащий последовательность Phe-Val-Asn-Gln-His-Leu-Cys-Gly-Ser-His-Leu-Val-Glu-Ala-Leu-Tyr-Leu-Val-Cys-Xaa-Glu, где Xaa представляет собой ароматический остаток или большой алифатический остаток (SEQ ID NO: 19).
22. Аналог инсулина по любому из пп. 1-21, где CysB9 из пептида, представляющего собой В-цепь, связан с CysA6 из пептида, представляющего собой А-цепь.
23. Аналог инсулина по любому из пп. 1-22, где CysB21 из пептида, представляющего собой В-цепь, связан с CysA20 из пептида, представляющего собой А-цепь.
24. Аналог инсулина по любому из пп. 1-23, где CysA7 связан с CysA11.
25. Аналог инсулина по любому из пп. 1-24, где пептид, представляющий собой А-цепь, и пептид, представляющий собой В-цепь, связаны друг с другом за счет одной пары их соответствующих терминальных концов.
26. Аналог инсулина по любому из пп. 1-25, где пептид, представляющий собой А-цепь, и пептид, представляющий собой В-цепь, связаны друг с другом за счет обоих терминальных концов.
27. Аналог инсулина по любому из пп. 1-26, который характеризуется IC50 в отношении человеческого рецептора IR-B, составляющей менее 10-6 М.
28. Аналог инсулина по любому из пп. 1-27, где в растворе аналог является на по меньшей мере 75% мономерным в растворе.
29. Аналог инсулина по любому из пп. 1-28, который характеризуется повышенной биодоступностью при введении человеку по сравнению с человеческим инсулином.
30. Аналог инсулина по п. 29, который характеризуется пиковой биодоступностью в диапазоне от 0,5 до 3 часов после введения человеку.
31. Аналог инсулина по п. 29 или 30, который характеризуется началом проявления активности в течение 10 минут после введения.
32. Аналог инсулина по любому из пп. 1-31, где аналог не связывается с человеческим IGF-IR или слабо связывается с человеческим IGF-IR.
33. Аналог инсулина по п. 32, где аналог характеризуется аффинностью (Kd) в отношении человеческого IGF-IR, составляющей менее 100 нМ.
34. Фармацевтическая композиция, содержащая аналог инсулина по любому из пп. 1-33 или его фармацевтически приемлемую соль и один или несколько фармацевтически приемлемых носителей.
35. Способ лечения и/или предупреждения связанного с инсулином состояния, предусматривающий введение терапевтически эффективного количества аналога инсулина по любому из пп. 1-33 субъекту, нуждающемуся в этом.
36. Способ по п. 35, где связанное с инсулином состояние представляет собой гипергликемию, инсулинорезистентность, диабет 1 типа, гестационный диабет или диабет 2 типа.
37. Способ снижения уровней глюкозы в крови, предусматривающий введение терапевтически эффективного количества аналога инсулина по любому из пп. 1-33 субъекту, нуждающемуся в этом.
38. Применение аналога инсулина по любому из пп. 1-33 в изготовлении лекарственного препарата для лечения и/или предупреждения связанного с инсулином состояния у субъекта.
39. Применение аналога инсулина по любому из пп. 1-33 в изготовлении лекарственного препарата для снижения уровней глюкозы в крови у субъекта.
40. Аналог инсулина по любому из пп. 1-33 для применения в лечении и/или предупреждении связанного с инсулином состояния у субъекта.
41. Аналог инсулина по любому из пп. 1-33 для применения в обеспечении снижения уровней глюкозы в крови у субъекта.
42. Способ изменения структуры или модификации полипептида, который, как известно, связывается с инсулиновым рецептором (IR), предусматривающий осуществление основанной на структуре оценки по отношению к структуре, определенной атомными координатами из приложения I или их подмножеством, и изменение структуры или химическую модификацию полипептида по результатам оценки.
43. Способ по п. 42, где основанная на структуре оценка предусматривает сравнение структуры, определенной атомными координатами из приложения I или их подмножеством, с атомными координатами инсулина или их подмножеством.
44. Способ по п. 42 или 43, где основанная на структуре оценка дополнительно предусматривает молекулярное моделирование комплекса, образованного структурой, определенной атомными координатами из приложения I или их подмножеством, и атомными координатами инсулинового рецептора или их подмножеством.
45. Способ по любому из пп. 42-44, дополнительно предусматривающий осуществление синтеза или получение полипептида, подвергнутого изменению структуры или химической модификации, и тестирование в отношении его способности связываться с IR.
46. Способ по любому из пп. 42-44, дополнительно предусматривающий осуществление синтеза или получение полипептида, подвергнутого изменению структуры или химической модификации, и определение способности полипептида, подвергнутого изменению структуры или химической модификации, модулировать активацию IR.
47. Способ по любому из пп. 42-44, дополнительно предусматривающий осуществление синтеза или получение полипептида, подвергнутого изменению структуры или химической модификации, и определение способности полипептида, подвергнутого изменению структуры или химической модификации, снижать уровни глюкозы в крови.
48. Способ по любому из пп. 42-47, где полипептид, который, как известно, связывается с IR, представляет собой инсулин.
49. Способ по п. 48, где инсулин представляет собой человеческий инсулин.
50. Полипептид, который был подвергнут изменению структуры или модификации с помощью способа по любому из пп. 42-49.
51. Полипептид по п. 50, который является мономерным.
52. Выделенная молекула, которая является агонистом IR, где молекула идентифицирована и/или сконструирована на основании 3D-структуры Con-Ins G1, определенной атомными координатами из приложения I или их подмножеством.
53. Молекула по п. 52, где молекула представляет собой пептид, полипептид или пептидомиметик.
54. Молекула по п. 52 или 53, которая является мономерной.
55. Молекула по любому из пп. 52-54, которая характеризуется IC50 в отношении человеческого рецептора IR-В, составляющей менее 10-6 М.
56. Способ идентификации соединения, которое связывается с IR, при этом способ включает:
i) создание модели трехмерной структуры полипептида, характеризующегося:
а) структурой, определенной атомными координатами из приложения I или их подмножеством, или
b) структурой, которая при наложении на соответствующие атомы остова структуры а) характеризуется среднеквадратическим отклонением, составляющим менее приблизительно 2,0
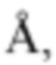 и
и
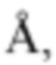
ii) конструирование соединения, которое потенциально связывается с IR, или осуществление скрининга в отношении него.
57. Способ по п. 56, где создание модели трехмерной структуры предусматривает создание модели полипептида, связанного с IR или его областями.
58. Способ по п. 56 или 57, дополнительно предусматривающий осуществление синтеза соединения, которое потенциально связывается с IR.
59. Способ по любому из пп. 56-58, где соединение модулирует по меньшей мере одну биологическую активность IR.
60. Способ по любому из пп. 56-59, где соединение является мономерным.
61. Способ по любому из пп. 56-60, который дополнительно предусматривает тестирование соединения, сконструированного или отобранного с помощью скрининга на стадии ii), в отношении его способности модулировать уровни глюкозы в крови.
62. Способ по любому из пп. 56-61, где i) и ii) осуществляют in silico.
63. Способ идентификации соединения, которое имитирует активность инсулина, с применением компьютера, при этом способ включает:
i) создание модели трехмерной структуры полипептида, характеризующегося
a) структурой, определенной атомными координатами из приложения I или их подмножеством, или
b) структурой, которая при наложении на соответствующие атомы остова структуры а) характеризуется среднеквадратическим отклонением, составляющим менее приблизительно 2,0
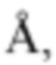 и
и
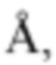
ii) конструирование соединения, которое имитирует активность инсулина, или осуществление скрининга в отношении него.
64. Способ по п. 63, где создание модели трехмерной структуры предусматривает создание модели полипептида, связанного с IR или его областями.
65. Способ по п. 63 или 64, дополнительно предусматривающий осуществление синтеза соединения, которое потенциально связывается с IR.
66. Способ по любому из пп. 63-65, где соединение модулирует по меньшей мере одну биологическую активность IR.
67. Способ по любому из пп. 63-66, где соединение является мономерным.
68. Способ по любому из пп. 63-67, при этом способ дополнительно предусматривает тестирование соединения, сконструированного или отобранного с помощью скрининга на стадии ii), в отношении его способности модулировать уровни глюкозы в крови.
69. Способ по любому из пп. 63-68, где i) и ii) осуществляют in silico.
70. Соединение, идентифицированное с применением способа по любому из пп. 56-69.
71. Кристалл полипептида Con-Ins G1, характеризующийся пространственной группой симметрии Р432 с размерами элементарной ячейки а=b=с=74,91
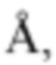 при этом отклонение размера любой ячейки составляет не более приблизительно 2%.
при этом отклонение размера любой ячейки составляет не более приблизительно 2%.
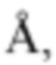
72. Структура полипептида Con-Ins G1, определенная атомными координатами из приложения I.
73. Применение структуры по п. 72 в качестве структурной модели.
74. Применение структурной модели по п. 73 для идентификации аналогов инсулина.
75. Аналог инсулина, идентифицированный с помощью применения по п. 74.
76. Фармацевтическая композиция, содержащая полипептид по п. 50 или 51, молекулу по любому из пп. 52-55, соединение по п. 70 или аналог инсулина по п. 75.
77. Пептид, включающий пептид, представляющий собой А-цепь инсулина, и пептид, представляющий собой В-цепь инсулина, где пептид, представляющий собой В-цепь, содержит замену по аминокислоте 10 и аминокислоте 20.
78. Пептид по п. 77, где замена по аминокислоте 20 представляет собой G20Y, G20F или G20P.
79. Пептид по п. 78, где замена по аминокислоте 20 представляет собой G20P, и пептид дополнительно содержит замену по аминокислоте 21, где замена по аминокислоте 21 представляет собой G21H.
80. Пептид по любому из пп. 77-79, где замена по аминокислоте 10 представляет собой Н10Е, H10D или H10Q.
81. Пептид по любому из пп. 77-80, дополнительно содержащий по меньшей мере одну замену в пептиде, представляющем собой А-цепь.
82. Пептид по п. 81, где по меньшей мере одна замена в пептиде, представляющем собой А-цепь, представляет собой Т8Н, T8Y, T8K или S9R.
83. Пептид по п. 82, дополнительно содержащий по меньшей мере две замены в пептиде, представляющем собой А-цепь.
84. Пептид по п. 81, где по меньшей мере две замены в пептиде, представляющем собой А-цепь, представляют собой две из замен, выбранных из Т8Н, T8Y, T8K и S9R.
85. Пептид по любому из пп. 77-84, где пептид представляет собой дезоктапептид-инсулин.
86. Пептид по любому из пп. 77-85, где пептид, представляющий собой В-цепь, содержит последовательность FVNQHLCGSELVEALYLVCYER (SEQ ID NO: 30).
87. Пептид по любому из пп. 77-86, где А-цепь содержит последовательность GIVEQCCHRICSLYQLENYCN (SEQ ID NO: 39).
88. Пептид по любому из пп. 77-87, где пептид, представляющий собой А-цепь, и пептид, представляющий собой В-цепь, связаны посредством по меньшей мере одной дисульфидной связи.
89. Пептид по любому из пп. 77-88, где пептид является мономерным.
90. Пептид по любому из пп. 77-89, где пептид, представляющий собой А-цепь инсулина, на по меньшей мере 70% идентичен пептиду, представляющему собой А-цепь человеческого инсулина дикого типа.
91. Фармацевтическая композиция, содержащая пептид по любому из пп. 77-90 и фармацевтически приемлемый носитель.
92. Способ повышения активации инсулинового рецептора у субъекта, предусматривающий введение терапевтически эффективного количества любого из пептидов по любому из пп. 77-90 субъекту, нуждающемуся в этом.
93. Способ снижения уровня сахара в крови у субъекта, предусматривающий введение терапевтически эффективного количества любого из пептидов по любому из пп. 77-90 субъекту, нуждающемуся в этом.
94. Способ лечения диабета 1 типа у субъекта, предусматривающий введение терапевтически эффективного количества любого из пептидов по любому из пп. 77-90 субъекту, нуждающемуся в этом.
95. Способ по п. 94, где у субъекта до введения пептида был диагностирован диабет 1 типа.
96. Терапевтический белок, содержащий пептид, представляющий собой А-цепь, связанный с пептидом, представляющим собой В-цепь, посредством по меньшей мере одной дисульфидной связи, где А-цепь содержит последовательность GIVEQCCHRICSLYQLENYCN (SEQ ID NO: 39), и где пептид, представляющий собой В-цепь, содержит последовательность FVNQHLCGSELVEALYLVCYER (SEQ ID NO: 30).

Комментарии