Гуманизированное антитело (н14.18) на основании антитела 14.18 мыши, связывающееся с gd2, и его слияние с il-2 - RU2366664C2
Код документа: RU2366664C2
Чертежи




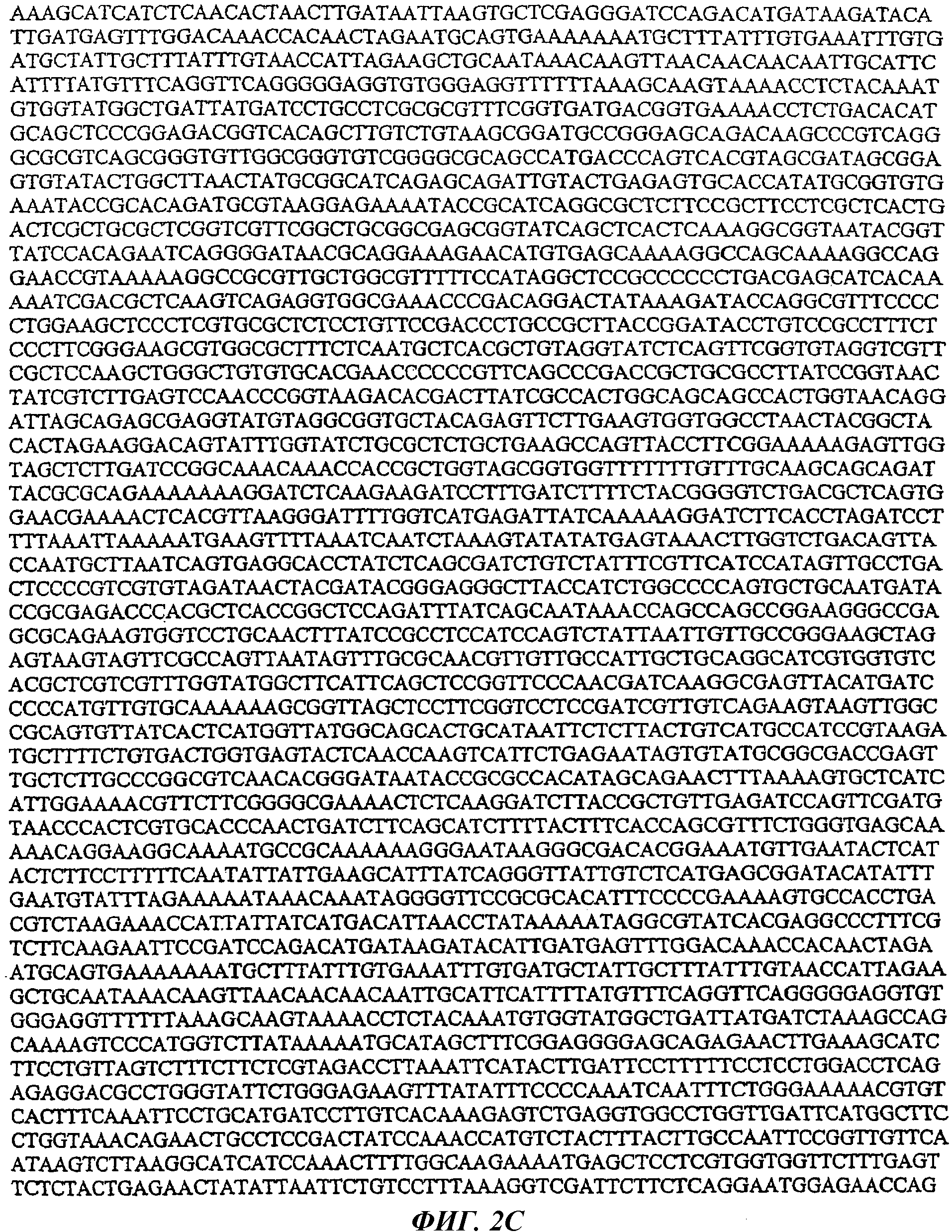


Описание
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение в целом относится к модифицированным антителам. Более конкретно, изобретение относится к модифицированным антителам со сниженной иммуногенностью, которые специфически связываются с поверхностным гликосфинголипидом GD2 клеток человека, и к их применению в качестве терапевтических средств.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
За последние годы достигнут значительный прогресс в разработке лекарственных средств на основе антител. Например, исследователи идентифицировали не только разнообразные маркеры, специфичные для рака, но и разнообразные антитела, которые специфически связываются с этими маркерами. Антитела можно использовать для доставки определенных молекул, например токсина или иммуностимулятора, например цитокина, к раковой клетке, экспрессирующей маркер, чтобы избирательно убить раковую клетку.
Антитело 14.18 - это полученное от мыши моноклональное антитело к гликосфинголипиду GD2 клеточной поверхности. GD2 - это дисиалоганглиозид, который в норме экспрессируется в значительном количестве только на наружной поверхности мембран нейрональных клеток, причем его предъявление иммунной системе ограничено гематоэнцефалическим барьером.
В противоположность этому, для многих опухолевых клеток характерны аномальные уровни экспрессии гликосфинголипидов клеточной поверхности. GD2, например, экспрессируется на поверхностях очень многих опухолевых клеток, включая нейробластомы, медуллобластомы, астроцитомы, меланомы, мелкоклеточный рак легких, остеосаркомы и другие саркомы мягких тканей. Соответственно, GD2 является удобным опухолеспецифичным маркером для нацеливания доменов иммуностимулирующих белков на опухолевые клетки с целью усиления эффективного иммунного ответа против опухолевых клеток для их разрушения. Хотя антитело мыши 14.18 (антитело m14.18) может способствовать нацеливанию этих доменов белков на опухолевые клетки, его аминокислотная последовательность, полученная от мыши, может оказывать вредное влияние на желаемый терапевтический эффект.
При введении пациенту антитела могут обладать сочетанной иммуногенностью для млекопитающего-реципиента. Это с большей вероятностью происходит в том случае, если антитела не являются аутологичными. Соответственно, эффективность лекарственных средств на основе антител часто ограничивается иммуногенной реакцией (ответом), направленной против терапевтического антитела. Эта иммуногенная реакция в типичном случае усиливается, если антитело полностью или частично получено от млекопитающего, отличающегося от млекопитающего-реципиента, например, если антитело получено от мыши, а реципиентом является человек.
Для клинического применения у людей может быть полезным модифицировать антитела, полученные от мыши, так, чтобы они больше напоминали антитела человека, для снижения или минимизации иммуногенности антитела, полученного от мыши. Иммуногенность антитела, полученного от мыши, можно снизить посредством создания химерного антитела, в котором константные области антитела человека слиты с вариабельными доменами мыши. Однако сохранившиеся вариабельные домены мыши обычно остаются иммуногенными для людей, и поэтому они могут снижать эффективность лекарственного средства на основе антитела.
Некоторые подходы к снижению иммуногенности, такие как «виниринг» и «гуманизация», включают в себя проведение замен многих аминокислот и могут нарушать связывание антитела с антигеном. Антитело m14.18 связывается с GD2 с умеренным сродством. Поэтому ожидается, что мутации, которые значительно понизят сродство m14.18 к GD2, будут снижать и его эффективность в терапевтических применениях у людей. Соответственно, в данной области техники существует потребность в терапевтических антителах, которые могут эффективно нацеливаться на GD2 и обладают сниженной иммуногенностью при введении людям.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В целом, настоящее изобретение предусматривает модифицированную форму антитела m14.18, которая является менее иммуногенной для людей, но сохраняет сродство связывания m14.18 с GD2 человека.
Более конкретно, изобретение предусматривает гуманизированную форму антитела m14.18 (антитело hu14.18), в котором несколько специфичных для мыши аминокислот в одном или нескольких каркасных участков заменены другими аминокислотами с целью снижения их иммуногенности для людей. Изобретение также предусматривает продукты слияния антитела hu14.18 с одной или несколькими неиммуноглобулиновыми частями для повышения эффекта направленной иммунной терапии.
В одном из аспектов настоящее изобретение предусматривает вариабельную область антитела, включающую последовательность аминокислот, представленную как SEQ ID NO: 1, которая определяет вариабельную область легкой цепи иммуноглобулина (VL область). В другом аспекте изобретение относится к вариабельной области антитела, включающей последовательность аминокислот, представленную как SEQ ID NO: 2, которая определяет вариабельную область тяжелой цепи иммуноглобулина (VH область). В одном из примеров осуществления изобретение относится к вариабельной области антитела, в которой последовательность аминокислот SEQ ID NO: 1 соединена с последовательностью аминокислот, представленной как SEQ ID NO: 2. Последовательности аминокислот могут быть соединены, например, дисульфидной связью или пептидной связью.
В следующем аспекте изобретение относится к вариабельной области антитела, которая специфически связывается с GD2 и содержит, по меньшей мере, аминокислоты 1-23 из SEQ ID NO: 1, аминокислоты 1-25 из SEQ ID NO: 2 или аминокислоты 67-98 из SEQ ID NO: 2. Эти последовательности определяют каркасные участки в вариабельных областях иммуноглобулина антитела hu14.18. Каркасные участки более подробно описаны ниже.
Один из аспектов изобретения относится к способу нацеливания на поверхность клетки, несущей GD2, и включает введение пациенту вариабельной области антитела согласно настоящему изобретению. В одном из примеров осуществления изобретения клеткой-мишенью является опухолевая клетка. Другие аспекты изобретения включают нуклеиновую кислоту, кодирующую вариабельную область антитела, или клетку, содержащую эту нуклеиновую кислоту, которые могут быть введены пациенту или использованы для продукции белка in vitro.
Изобретение также предусматривает полипептид, который содержит вариабельную область антитела согласно настоящему изобретению и Fc-фрагмент, содержащий, по меньшей мере, СН2-домен, нуклеиновые кислоты, кодирующие полипептид, клетки, содержащие нуклеиновые кислоты, и способы нацеливания на клетку, несущую GD2 на своей поверхности, посредством введения полипептида, нуклеиновой кислоты или клетки пациенту. В некоторых примерах осуществления изобретения Fc-фрагмент получен из IgG1.
Вариабельная область антитела может быть соединена (с внедрением Fc-фрагмента или без внедрения) с неиммуноглобулиновой частью. Более конкретно, неиммуноглобулиновая часть может быть цитокином, например - интерлейкином, гематопоэтическим фактором, лимфокином, интерфероном или хемокином. Интерлейкин может, например, быть интерлейкином-2 или интерлейкином-12. Гематопоэтический фактор и лимфокин могут быть, например, гранулоцитарно-макрофагальным колониестимулирующим фактором (GM-CSF) и лимфотоксином, соответственно. Интерферон может быть, например, интерфероном-α, интерфероном-β или интерфероном-γ. В некоторых примерах осуществления изобретения слитый белок включает вторую неиммуноглобулиновую часть, например - второй цитокин. В конкретном примере осуществления изобретения слитый белок включает вариабельную область антитела, IL-2 и IL-12.
Следует понимать, что признаки различных примеров осуществления изобретения, описанные в данной работе, не являются взаимоисключающими и могут существовать в различных комбинациях и перестановках.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Фигура 1 иллюстрирует последовательность аминокислот вариабельной области легкой цепи иммуноглобулина согласно настоящему изобретению.
Фигура 1 В иллюстрирует последовательность аминокислот вариабельной области тяжелой цепи иммуноглобулина согласно настоящему изобретению.
Фигуры 2A-D иллюстрируют нуклеотидную последовательность вектора экспрессии, включающую гибридные нуклеиновые кислоты, кодирующие слитый белок, состоящий из легкой цепи иммуноглобулина, тяжелой цепи иммуноглобулина и IL-2, согласно настоящему изобретению.
Фигура 3А иллюстрирует последовательность аминокислот легкой цепи иммуноглобулина согласно настоящему изобретению.
Фигура 3 В иллюстрирует последовательность аминокислот тяжелой цепи иммуноглобулина согласно настоящему изобретению.
СВЕДЕНИЯ, ПОДТВЕРЖДАЮЩИЕ ВОЗМОЖНОСТЬ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Настоящее изобретение предусматривает модифицированную форму антитела m14.18, которая менее иммуногенна для людей, но все еще способна специфически связываться с GD2 человека. Снижение иммуногенности обеспечивается посредством одной или нескольких измененных аминокислотных последовательностей вариабельных доменов иммуноглобулина. Антитело можно использовать для лечения GD2-позитивных опухолей, особенно - при слиянии его с цитокином или другим иммуномодулятором.
При использовании в данной работе термины «антитело» и «иммуноглобулин» следует понимать, как означающие: (1) интактное антитело (например - моноклональное антитело или поликлональное антитело), (2) его антигенсвязывающие участки, включающие, например, Fab-фрагмент, Fab'-фрагмент, (Fab')2-фрагмент, Fv-фрагмент, сайт связывания одноцепочечного антитела, sFv, (3) биспецифичные антитела и их антигенсвязывающие участки и (4) мультиспецифичные антитела и их антигенсвязывающие участки.
При использовании в данной работе термины «специфически связывается», «связывается специфически» и «специфическое связывание» следует понимать, как означающие то, что антитело имеет сродство связывания с конкретным антигеном по меньшей мере примерно 106 М-1, более предпочтительно - по меньшей мере примерно 107 М-1, еще более предпочтительно - по меньшей мере примерно 108 М-1, и наиболее предпочтительно - по меньшей мере примерно 1010 М-1.
При использовании в данной работе термины «каркасные участки» и «FR» следует понимать, как означающие участки вариабельной области иммуноглобулина, прилежащие к областям, определяющим комплементарность (CDR). CDR представляют собой участки вариабельной области иммуноглобулина, первично взаимодействующие с антигеном. Как показано на Фиг.1, VH и VL участки содержат по четыре FR и расположены в участках последовательностей аминокислот, взятых в рамки.
Более конкретно, со ссылкой на последовательность аминокислот, изображенную на Фиг.1А (SEQ ID NO: 1), FR-участки легкой цепи определены аминокислотными последовательностями от Asp1 до Cys23 (huVLFR1), от His39 до His54 (huVLFR2), от Gly62 до Cys93 (huVLFR3) и от Phe104 до Lys113 (huVLFR4). Со ссылкой на последовательность аминокислот, изображенную на Фиг.1 В (SEQ ID NO: 2), FR-участки тяжелой цепи определены аминокислотными последовательностями от Glu1 до Ser25 (huVHFR1), от Trp36 до Gly49 (huVHFR2), от Arg67 до Ser98 (huVHFR3) и от Trp103 до Ser113 (huVHFR4).
Белковые последовательности согласно настоящему изобретению
Отличительным признаком настоящего изобретения являются антитела, которые связываются, предпочтительно - специфически, с поверхностным гликосфинголипидом GD2 клетки человека и имеют модифицированные области, полученные из антитела мыши m14.18. Аминокислотные последовательности VH или VL (или обеих областей) модифицированы или гуманизированы с целью снижения их иммуногенности при введении человеку. Согласно настоящему изобретению, антитело m14.18 может быть гуманизировано, например, с использованием таких способов как деиммунизации, в которых потенциальные эпитопы Т-клеток удаляются или ослабляются посредством внедрения мутаций, которые снижают связывание эпитопа пептида с молекулой MHC класса II (см., например, WO98/52976 и WO00/34317). Альтернативно, мутируют эпитопы Т-клеток животных так, чтобы они соответствовали собственным эпитопам человека, присутствующим в антителах человека (см., например, Патент США №5,712,120). Настоящее изобретение предусматривает антитела к GD2, содержащие VL и VH области, которые содержат, по меньшей мере, одну гуманизированную FR-последовательность, за счет чего снижается их иммуногенность при введении человеку.
I. Вариабельные области тяжелой и легкой цепей
Как указано выше, hu14.18 содержит гуманизированные вариабельные области, полученные из m14.18, которые сохраняют способность к специфическому связыванию с антигеном GD2 человека. В некоторых примерах осуществления изобретения VL область антитела hu14.18 содержит следующий полипептид:
D-V-V-M-T-Q-T-P-L-S-L-P-V-T-P-G-E-P-A-S-I-S-C-R-S-S-Q-S-L-V-H-R-N-G-N-T-Y-L-H-W-Y-L-Q-K-P-G-Q-S-P-K-L-L-I-H-K-V-S-N-R-F-S-G-V-P-D-R-F-S-G-S-G-S-G-T-D-F-T-L-K-I-S-R-V-E-A-E-D-L-G-V-Y-F-C-S-Q-S-T-H-V-P-P-L-T-F-G-A-G-T-K-L-E-L-K (SEQ ID NO: 1).
В конкретных примерах осуществления изобретения антитело hu14.18 содержит FR1 легкой цепи, который определен остатками 1-23 из SEQ ID NO: 1, а именно, D-V-V-M-T-Q-T-P-L-S-L-P-V-T-P-G-E-P-A-S-I-S-C (huVLFR1).
В другом примере осуществления изобретения VH-область антитела hu14.18 содержит следующий полипептид:
E-V-Q-L-V-Q-S-G-A-E-V-E-K-P-G-A-S-V-K-I-S-C-K-A-S-G-S-S-F-T-G-Y-N-M-N-W-V-R-Q-N-I-G-K-S-L-E-W-I-G-A-I-D-P-Y-Y-G-G-T-S-Y-N-Q-K-F-K-G-R-A-T-L-T-V-D-K-S-T-S-T-A-Y-M-H-L-K-S-L-R-S-E-D-T-A-V-Y-Y-C-V-S-G-M-E-Y-W-G-Q-G-T-S-V-T-V-S-S (SEQ ID NO: 2).
В конкретных примерах осуществления изобретения антитело hu14.18 содержит FR1 тяжелой цепи, который определен остатками 1-25 из SEQ ID NO: 2, а именно: E-V-Q-L-V-Q-S-G-A-E-V-E-K-P-G-A-S-V-K-I-S-C-K-A-S (huVНFR1).
В других примерах осуществления изобретения антитело hu14.18 содержит FR3 тяжелой цепи, который представлен остатками 67-98 SEQ ID NO: 2, а именно: R-A-T-L-T-V-D-K-S-T-S-T-A-Y-M-H-L-K-S-L-R-S-E-D-T-A-V-Y-Y-C-V-S (huVНFR3).
В объем настоящего изобретения входят также различные комбинации вышеуказанных примеров осуществления изобретения. Например, антитело hu14.18 может включать VL-последовательность, представленную как SEQ ID NO: 1, и VH-последовательность, представленную как SEQ ID NO: 2. VL и VH-области могут быть соединены дисульфидной связью или пептидной связью, в зависимости от того, как построены последовательности кодирующих их нуклеиновых кислот.Обычно V-области связаны дисульфидной связью, если их последовательности кодируются различными рекомбинантными ДНК. В противоположность этому, V-области обычно связаны пептидной связью, если их последовательности кодируются одноцепочечной конструкцией ДНК.
Настоящее изобретение также включает в себя антитело, которое специфически связывает GD2 и содержит, по меньшей мере, один участок гуманизированных V-областей. Например, антитело hu14.18 может содержать VL-область, определенную как SEQ ID NO: 1, и VH-область, содержащую, по меньшей мере, один гуманизированный FR, например - huVНFR1 или huVНFR2. Альтернативно, антитело согласно настоящему изобретению может содержать VН-область, определенную как SEQ ID NO: 2, и VL-область, содержащую, по меньшей мере, один гуманизированный FR, например - huVLFR1. Антитело hu14.18 может также содержать VH-область, содержащую, по меньшей мере, один гуманизированный FR, и/или VL-область, содержащую, по меньшей мере, один гуманизированный FR.
В некоторых примерах осуществления изобретения вариабельная область легкой цепи и вариабельная область тяжелой цепи могут быть сшиты, соответственно, с константной областью легкой цепи и константной областью тяжелой цепи иммуноглобулина. Легкая цепь иммуноглобулина имеет константные области, которые обозначены как каппа- или лямбда-цепи. В частном примере осуществления изобретения константная область легкой цепи является каппа-цепью. Константные области тяжелой цепи и их различные модификации и комбинации более подробно обсуждены ниже.
II. Fc-фрагмент
Вариабельные домены антитела согласно настоящему изобретению по выбору сливают с Fc-фрагментом. Использованный в данной работе Fc-фрагмент охватывает домены, полученные из константной области тяжелой цепи иммуноглобулина, предпочтительно - иммуноглобулина человека, включая фрагменты, аналоги, варианты, мутанты или производные константной области. Константная область тяжелой цепи иммуноглобулина определена как естественно существующий или полученный посредством синтеза полипептид, гомологичный, по меньшей мере, одному участку С-терминальной области тяжелой цепи, включающему СН1, шарнир, СН2, СН3 и, для некоторых классов тяжелых цепей, СН4 домены. Область «шарнира» соединяет СН1-домен с СН2-СН3-участком Fc-фрагмента. Константная область тяжелых цепей всех иммуноглобулинов млекопитающих проявляет большое сходство последовательности аминокислот.Нуклеотидные последовательности ДНК этих областей иммуноглобулинов хорошо известны в данной области техники. (См., например, Gillies et al., (1989) J. Immunol. Meth. 125:191).
В настоящем изобретении Fc-фрагмент в типичном случае включает, по меньшей мере, CH2-домен. Например, Fc-фрагмент может включать всю константную область тяжелой цепи иммуноглобулина (СН1-шарнир-СН2-СН3). Альтернативно, Fc-фрагмент может включать всю шарнирную область или ее часть, СН2-домен и СН3-домен.
Константная область иммуноглобулина ответственна за многие важные эффекторные функции антитела, включая связывание с Fc-рецептором (FcR) и фиксацию комплемента. Существует 5 основных классов константной области тяжелой цепи, классифицируемых как IgA, IgG, IgD, IgE и IgM, каждый из которых обладает характерными эффекторными функциями, обозначаемыми как изотипы.
Например, IgG делится на четыре γ-изотипа: γ1, γ2, γ3 и γ4, также известных под названиями IgG1, IgG2, IgG3 и IgG4, соответственно. Молекулы IgG могут взаимодействовать со многими классами клеточных рецепторов, включая три класса Fcγ-рецепторов (FcγR), специфичных для IgG-класса антител, а именно - FcγRI, FcγRII и FcγRIII. Сообщалось, что последовательности, важные для связывания IgG с FcγR-рецепторами, находятся в СН2 и СН3 доменах.
На период полужизни антитела в сыворотке влияет способность этого антитела связываться с Fc-рецептором (FcR). Сходным образом, на период полужизни слитых белков, содержащих иммуноглобулины, также влияет их неспособность связываться с этими рецепторами (Gillies et al., Cancer Research (1999) 59:2159-66). СН2 и СН3 домены IgG2 и IgG4 обладают необнаружимым или сниженным сродством связывания с Fc-рецепторами, по сравнению с доменами IgG1. Соответственно, период полужизни в сыворотке сходного антитела может быть увеличен посредством использования СН2 и/или СН3 доменов от IgG2 или IgG4 изотипов. Альтернативно, антитело может содержать СН2 и/или СН3 домен от IgG1 или IgG3 с модификацией одной или нескольких аминокислот в этих доменах с целью снижения сродства связывания с Fc-рецепторами (см., например, Заявку на патент США 09/256,156, опубликованную как Заявка на патент США 2003-0105294-А1).
Шарнирная область Fc-фрагмента в норме расположена рядом с С-концом СН1-домена константной области тяжелой цепи. При включении в белки согласно настоящему изобретению, шарнир гомологичен естественно существующей области иммуноглобулина и в типичном случае включает остатки цистеина, связывающие две тяжелые цепи дисульфидными связями, как в природных иммуноглобулинах. Репрезентативные последовательности шарнирных областей иммуноглобулинов человека и мыши можно найти в ANTIBODY ENGINEERING, A PRACTICAL GUIDE (Borrebaeck, ed., W.H. Freeman and Co., 1992).
Подходящие для настоящего изобретения шарнирные области можно получить из IgG1, IgG2, IgG3, IgG4 и других изотипов иммуноглобулинов. Изотип IgG1 имеет в области шарнира две дисульфидные связи, обеспечивающие образование эффективных и устойчивых дисульфидных связей. Поэтому предпочтительная шарнирная область согласно настоящему изобретению получена из IgG1. По выбору, первый, наиболее близкий к N-концу цистеин шарнира IgG1 мутируют для повышения экспрессии и сборки антител или содержащих антитела слитых белков согласно настоящему изобретению (см, например, Заявку на патент США 10/093,958, опубликованную как Заявка на патент США 2003-0044423-А1).
Известно, что, в отличие от IgG1, шарнирная область IgG4 неэффективно образует дисульфидные связи между цепями (Angal et al., (1993), Mol. Immunol. 30:105-8). Аналогично, шарнирная область IgG2 содержит четыре дисульфидные связи, которые способствуют олигомеризации и, вероятно, некорректному дисульфидному связыванию во время секреции в рекомбинантных системах. Подходящая для настоящего изобретения шарнирная область может быть получена из шарнирной области IgG4, предпочтительно - содержащей мутацию, которая усиливает правильное образование дисульфидных связей между частями молекулы, полученными из тяжелых цепей (Angal et al., (1993), Mol. Immunol. 30(1):105-8). Другая предпочтительная шарнирная область получена из шарнирной области IgG2, в которой два первых цистеина мутированы в другие аминокислоты, например, в порядке предпочтительности, в серин, аланин, треонин, пролин, глутаминовую кислоту, глутамин, лизин, гистидин, аргинин, аспарагин, аспарагиновую кислоту, глицин, метионин, валин, изолейцин, лейцин, тирозин, фенилаланин, триптофан или селеноцистеин (см., например, публикацию Заявки на патент США 2003-0044423-А1).
Fc-фрагмент, слитый с вариабельной областью антитела согласно настоящему изобретению, может содержать СН2 и/или СН3 домены и шарнирную область, которые получены из различных изотипов антител. Например, Fc-фрагмент может содержать СН2 и/или СН3 домены IgG2 или IgG4 и шарнирную область IgG1. Сборка таких гибридных Fc-фрагментов описана в публикации Заявки на патент США 2003-0044423-А1.
При слиянии с вариабельной областью антитела согласно настоящему изобретению Fc-фрагмент предпочтительно содержит одну или несколько модификаций аминокислот, которые обычно увеличивают период полужизни слитого белка, содержащего Fc-фрагмент, в сыворотке. Такие модификации аминокислот включают мутации, значительно снижающие или устраняющие активность белка в отношении связывания с Fc-рецептором или фиксации комплемента. Например, один из типов таких мутаций удаляет сайт гликозилирования Fc-фрагмента тяжелой цепи иммуноглобулина. В IgG1 сайтом гликозилирования является Asn297 (см., например, Заявку на патент США 10/310,719, опубликованную как Заявка на патент США 2003-0166163-А1).
III. Соединительная область слитого белка
Вариабельные области согласно настоящему изобретению могут, по выбору, быть соединены или слиты с неиммуноглобулиновой частью, прямо или непрямо, например - через линкерный пептид (например -(Gly4-Ser)3 (SEQ ID NO: 3)). Иммуногенность слитых белков согласно изобретению можно снизить путем нарушения способности соединительной области слитого белка или соединительного эпитопа к взаимодействию с рецептором Т-клетки, как описано в публикации Заявки на Патент США 2003-0166877-А1. Даже при слиянии двух протеинов человека, например - Fc-фрагмента человека и IL-2 человека, область, окружающая соединительную область или соединительный эпитоп, содержит пептидную последовательность, которая в норме отсутствует в организме человека, и поэтому она может быть иммуногенной. Иммуногенность соединительного эпитопа можно снизить, например, посредством введения одного или нескольких сайтов гликозилирования вблизи соединительной области или посредством идентификации вероятного эпитопа Т-клеток, перекрывающего соединительную область, как описано в публикации Заявки на Патент США 2003-0166877-А1, и замены аминокислоты вблизи соединения с целью снижения способности вероятного эпитопа Т-клетки к взаимодействию с рецептором Т-клетки.
Период полужизни белка в сыворотке можно также увеличить путем введения мутаций в соединительную область слитого белка. Например, в белке, содержащем СН3-домен, слитый с неиммуноглобулиновой частью, можно заменить С-терминальный лизин СН3-домена на другую аминокислоту, например - на аланин, что может обеспечить значительное увеличение периода полужизни результирующего слитого белка в сыворотке.
В некоторых примерах осуществления изобретения протеолитическое расщепление соединительной области слитого белка является желательным. Соответственно, межгенная область может включать последовательность нуклеотидов, кодирующую сайт протеолитического расщепления. Этот сайт, расположенный между иммуноглобулином и цитокином, может быть предназначен для обеспечения протеолитического выделения цитокина в целевом месте. Например, хорошо известно, что плазмин и трипсин расщепляют пептидную цепь после остатков лизина и аргинина на участках, доступных для протеаз. Хорошо известны также другие сайт-специфические эндопротеазы и последовательности аминокислот, которые они распознают.
IV. Лечение болезней человека слитыми белками, содержащими антитело hu14.18
Вариабельные области антитела согласно настоящему изобретению могут быть присоединены к диагностическому и/или терапевтическому агенту. Агент может быть слит с антителом с получением слитого белка. Альтернативно, агент может быть химически сшит с антителом с получением иммуноконъюгата. Агентом может быть, например, токсин, радиоактивная метка, радиофармацевтический препарат, иммуностимулятор и т.п.
Вариабельную область антитела согласно настоящему изобретению можно присоединить к цитокину. Предпочтительные цитокины включают в себя интерлейкины, такие как интерлейкин-2 (IL-2), IL-4, IL-5, IL-6, IL-7, IL-10, IL-12, IL-13, IL-14, IL-15, IL-16 и IL-18, гематопоэтические факторы, такие как гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CSF), гранулоцитарный колониестимулирующий фактор (G-CSF) и эритропоэтин, факторы некроза опухолей (TNF), такие как TNF-α, лимфокины, такие как лимфотоксин, регуляторы метаболических процессов, такие как лептин, интерфероны, такие как интерферон-α, интерферон-β, интерферон-γ, и хемокины. Предпочтительно, чтобы слитый белок, состоящий из антитела и цитокина, или иммуноконъюгат проявлял биологическую активность цитокина. В одном из примеров осуществления изобретения вариабельный домен антитела слит с IL-2. Предпочтительно, несколько аминокислот в IL-2-части мутируют для снижения токсичности, как описано в публикации Заявки на Патент США 2003-0166163-А1.
Например, на Фиг.3А и 3 В изображены последовательности аминокислот из конкретного примера осуществления слитого белка на основе антитела согласно настоящему изобретению. Более конкретно, на Фиг.3А изображена пептидная последовательность гуманизированной легкой цепи иммуноглобулина, которая включает вариабельную и константную области. На Фиг.3 В изображена пептидная последовательность гуманизированной тяжелой цепи иммуноглобулина, соединенная с IL-2. Полипептиды обеспечивают слитый белок на основе гуманизированного антитела, способный специфически связываться с GD2 и стимулировать иммунную систему.
По выбору, протеиновые комплексы могут дополнительно содержать второе вещество, например - второй цитокин. В одном из примеров осуществления изобретения слитый белок на основе антитела hu14.18 содержит IL-12 и IL-2. Получение протеиновых комплексов, содержащих домен иммуноглобулина и два различных цитокина, подробно описано в Патенте США №6,617,135.
Слитые белки согласно настоящему изобретению можно использовать для лечения болезней человека, например - рака. При лечении опухолей человека особенно целесообразно вводить слитый белок на основе антитела и IL-2, содержащий V-области согласно настоящему изобретению, посредством инфузии или подкожной инъекции, используя дозы от 0,1 до 100 миллиграммов/метр2/пациента. В предпочтительном примере осуществления изобретения, в частности, целесообразно вводить слитый белок на основе антитела и IL-2, содержащий V-области согласно настоящему изобретению, посредством инфузии или подкожной инъекции, используя дозы от 0,1 до 10 миллиграммов/метр2/пациента, и более предпочтительно - примерно от 3 до 6 миллиграммов/метр2/пациента.
Клинические испытания показали, что после введения слитый белок hu14.18-IL-2 сохраняет свою способность активировать IL-2-реактивные клетки через IL-2 рецептор и способность связываться с GD2-позитивными опухолевыми клетками и доставлять IL-2 к их поверхности. Кроме того, введение слитого белка hu14.18-IL-2 больным раком приводило к прекращению прогрессирования заболевания у неожиданно большого числа пациентов (см. Пример 1).
Фармацевтические композиции согласно настоящему изобретению могут быть использованы в виде твердых, полутвердых или жидких дозировочных форм, например, таких как таблетки, капсулы, порошки, жидкости, суспензии и т.п., предпочтительно - в виде разовых дозировочных форм, подходящих для введения с точными дозировками. Композиции включают стандартный фармацевтический носитель или наполнитель, и, кроме того, они могут включать другие лекарственные агенты, фармацевтические агенты, носители, адъюванты и т.д. Такие наполнители могут содержать другие белки, например, такие как человеческий сывороточный альбумин или белки плазмы. Существующие способы приготовления таких дозировочных форм известны или очевидны специалистам в данной области техники. В любом случае композиция или рецептура для введения будет содержать активный компонент (или компоненты) в количестве, достаточном для получения желаемого эффекта у субъекта, подлежащего лечению.
Вводить композиции согласно настоящему изобретению можно с использованием любого признанного способа введения веществ, обладающих такой активностью. Эти способы включают пероральное, парентеральное или местное введение и другие системные формы. Предпочтительным способом введения является внутривенная инъекция в фармацевтически приемлемом носителе (см. Пример 1).
Введенное количество активного соединения будет, конечно же, зависеть от субъекта, подлежащего лечению, тяжести заболевания, способа введения и мнения назначающего препарат врача.
Нуклеиновые кислоты согласно настоящему изобретению
I. Рекомбинантные ДНК, кодирующие антитело hu14.18
Изобретение также включает в себя нуклеиновые кислоты, способные экспрессировать все перечисленные выше типы белков. Сюда относятся, например, нуклеиновые кислоты, кодирующие аминокислотную последовательность, представленную как SEQ ID NO: 1; аминокислотную последовательность, представленную как SEQ ID NO: 2; VL-область антитела hu14.18, которая включает аминокислотную последовательность huVLFR1; VH-область антитела hu14.18, которая включает аминокислотную последовательность huVHFR1; VH-область антитела hu14.18, которая включает аминокислотную последовательность huVHFR3; и слитые белки, содержащие антитело hu14.18, включающее, по меньшей мере, одну из вышеописанных гуманизированных FR-последовательностей и одно или несколько терапевтических средств.
Антитела hu14.18 согласно настоящему изобретению могут быть получены посредством методик генной инженерии, то есть посредством получения рекомбинантной нуклеиновой кислоты, кодирующей аминокислотную последовательность GD2-специфичного антитела, содержащего желаемые FR согласно настоящему изобретению. В одном из примеров осуществления изобретения генная конструкция, кодирующая антитело согласно настоящему изобретению, содержит (в 5'-3' ориентации) сегмент ДНК, кодирующий вариабельную область тяжелой цепи, содержащую, по меньшей мере, один гуманизированный FR, и сегмент ДНК, кодирующий константную область тяжелой цепи. В другом примере осуществления изобретения другой сегмент ДНК, кодирующий цитокин, слит с 3'-концом сегмента ДНК, кодирующего константную область тяжелой цепи. В следующем примере осуществления изобретения генная конструкция включает (в 5'-3' ориентации) сегмент ДНК, кодирующий вариабельную область тяжелой цепи, содержащую, по меньшей мере, один гуманизированный FR, и сегмент ДНК, кодирующий цитокин. Альтернативно, нуклеиновая кислота согласно настоящему изобретению может включать (в 5'-3' ориентации) сегмент ДНК, кодирующий вариабельную область легкой цепи, содержащую, по меньшей мере, один гуманизированный FR, и сегмент ДНК, кодирующий цитокин. В некоторых примерах осуществления изобретения нуклеиновую кислоту, кодирующую цитокин, присоединяют в рамке считывания к 3'-концу гена, кодирующего константную область (например, СН3 экзон), либо непосредственно, либо через интергенную область (например, с помощью соответствующих линкеров, таких как ДНК, кодирующая (Gly4-Ser)3 (SEQ ID NO: 3)).
II. Экспрессия рекомбинантных ДНК, кодирующих антитела hu14.18
Нуклеиновая кислота, кодирующая белки согласно настоящему изобретению, может быть введена или вставлена в один или несколько векторов экспрессии для введения в соответствующую реципиентную клетку, в которой она экспрессируется. Введение нуклеиновых кислот в векторы экспрессии может быть осуществлено с использованием стандартных способов молекулярной биологии. Предпочтительными векторами экспрессии являются такие векторы, с помощью которых кодируемый белок может экспрессироваться в бактериальной клетке или клетках млекопитающих.
Согласно настоящему изобретению вариабельная область тяжелой цепи антитела предпочтительно экспрессируется совместно с соответствующей легкой цепью в одной и той же клетке. Для слитых белков, которые содержат несколько полипептидных цепей, можно использовать больше одного вектора экспрессии. Способы совместной трансфекции, в которых используется, например, два вектора экспрессии, часто обеспечивают доставку обоих векторов в клетку-мишень. Альтернативно, иногда может быть целесообразным использовать один вектор, кодирующий несколько полипептидов, для их совместной экспрессии в одной клетке.
Например, на Фиг.2А-D изображена последовательность нуклеиновой кислоты вектора, кодирующего тяжелую и легкую цепи иммуноглобулина согласно настоящему изобретению. Вектор также включает нуклеиновую кислоту, кодирующую IL-2, слитый с 3'-концом тяжелой цепи иммуноглобулина. Соответственно, при введении в клетку один этот вектор может обеспечить слитый белок, состоящий из гуманизированного антитела и IL-2, который специфически связывается с GD2 и стимулирует иммунную функцию.
Кроме того, может быть удобно экспрессировать белки согласно настоящему изобретению как одноцепочечные молекулы. Например, вариабельная область антитела может экспрессироваться как одноцепочечное антитело или sFv, по выбору слитое с неиммуноглобулиновым белком. В другом примере осуществления изобретения тяжелую цепь (со слитым с ней цитокином или без цитокина) объединяют с комплементарной легкой (или тяжелой) цепью (со слитым с ней цитокином или без цитокина) с образованием моновалентных или дивалентных иммуноконъюгатов.
Реципиентными клеточными линиями предпочтительно являются лимфоидные клетки, такие как клетки миеломы (или гибридомы). Миеломные клетки могут синтезировать, собирать и секретировать иммуноглобулины, кодируемые трансфицированными генами, и могут гликозилировать белки. Особо предпочтительными реципиентными клетками являются клетки Sp2/0 миеломы, которые в норме не продуцируют эндогенный иммуноглобулин. После трансфекции клетка будет продуцировать только иммуноглобулины, кодируемые трансфицированными генными конструкциями. Трансфицированные клетки миеломы можно выращивать в культуре или в брюшине мышей, в последнем случае секретированные иммуноконъюгаты можно выделить из асцитной жидкости. Также в качестве реципиентных клеток можно использовать другие лимфоидные клетки, например - В-лимфоциты.
Существует несколько способов трансфекции лимфоидных клеток векторами, содержащими рекомбинантные нуклеиновые кислоты, кодирующие химерную Ig-цепь. Предпочтительным способом введения вектора в лимфоидные клетки является слияние со сферобластами (см., например, Gillies et al. (1989) Biotechnol. 7:798-804). Альтернативные способы включают электропорацию или преципитацию (осаждение) фосфатом кальция. Другими пригодными способами получения иммуноконъюгатов являются получение последовательности РНК, кодирующей рекомбинантную конструкцию, и ее трансляция в соответствующей системе in vivo или in vitro. После экспрессии белки согласно настоящему изобретению могут быть выделены с использованием стандартных процедур очистки белков (см., например, Патент США №5,650,150).
III. Лечение рака посредством генной терапии
Нуклеиновые кислоты согласно настоящему изобретению могут быть использованы в качестве генных терапевтических средств для лечения рака и других заболеваний, при которых желательно ориентировать иммунную систему на борьбу со специфическим типом клеток. Например, от человека или животного могут быть получены клетки, и в эти клетки могут быть трансфицированы одна или несколько нуклеиновых кислот, кодирующих антитело согласно настоящему изобретению. Затем клетки вводят обратно человеку или животному. Трансфицированными клетками могут быть нормальные или раковые клетки. Альтернативно, нуклеиновая кислота может быть введена в клетки in situ. После этого человек или животное дает иммунный ответ на раковые клетки, который может излечить рак или снизить тяжесть заболевания. Вариабельная область антитела согласно настоящему изобретению, сшитая (соединенная) с соответствующими регуляторными элементами для стимуляции экспрессии в клетках млекопитающих, может быть трансфицирована в клетки с помощью разнообразных способов, в том числе с помощью фосфата кальция, «генного ружья», аденовирусных векторов, катионных липосом, ретровирусных векторов или любых других эффективных способов трансфекции.
В конкретном примере осуществления изобретения антитело hu14.18 используется для избирательной доставки цитокина к клетке-мишени in vivo, так что цитокин может оказывать локальный биологический эффект, например - вызывать местный воспалительный ответ, стимулировать рост и активацию Т-клеток или активировать ADCC (антителозависимую клеточную цитотоксичность). В кровеносную систему субъекта, несущего клетки-мишени, вводят терапевтически эффективное количество антитела.
Изобретение проиллюстрировано далее не ограничивающими его примерами.
ОПИСАНИЕ ПРИМЕРОВ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Пример 1
Очистка hu14.18-IL-2 и составление рецептуры
В одном из опытов hu14.18-IL-2 экспрессировали в NS/0 клетках, супернатант культуры ткани собирали и выделяли белок hu14.18-IL-2 с использованием (последовательно) хроматографии на колонке с Abx Mixed Resin, хроматографии с рекомбинантным Белком А и хроматографии на колонке с Q Сефарозой с последующей диафильтрацией в тангенциальном потоке через Pellicon 2 для замены буфера в композиции. Подробности относительно этих стадий очистки описаны ниже. Стадии инактивации и удаления вируса чередовали с этими стадиями, как описано ниже. Стадии инактивации и удаления вируса не были нужны для самой очистки, но были использованы для того, чтобы обеспечить соответствие регулятивным требованиям.
рН двух литров супернатанта культуры ткани NS/0, содержащего hu14.18-IL-2, доводили до 5,9 с помощью 1М раствора уксусной кислоты, пропускали через Abx-колонку (J.T.Baker), промывали раствором, содержавшим 10 мМ MES и 100 мМ ацетата натрия, с рН 6,2 и элюировали раствором ацетата натрия (500 мМ) с рН 7. Этот материал загружали в колонку с рекомбинантным Белком А (Pharmacia), промывали раствором 100 мМ фосфата натрия и 150 мМ NaCl с рН 7, промывали раствором 100 мМ фосфата натрия и 150 мМ NaCl с рН 6, промывали раствором 10 мМ фосфата натрия с рН 7 и элюировали раствором 100 мМ фосфата натрия и 150 мМ NaCl с рН 3,5. рН элюированного материала был равен 4,2. Чтобы способствовать инактивации вируса, этот рН снижали до 3,8, и препарат инкубировали в течение 30 минут, после чего рН нейтрализовали до 7 с помощью 1М раствора NaOH. Для удаления нуклеиновой кислоты этот материал загружали на колонку с Q Сефарозой (Pharmacia) и промывали раствором 100 мМ фосфата натрия и 150 мМ NaCl с рН 7. Нуклеиновая кислота связывалась с колонкой, тогда как белок обнаруживался в потоке, прошедшем через колонку, и в промывных водах, причем промывки повторяли до тех пор, пока А280 не возвращался к исходной линии. Диафильтрацию через Pellicon 2 (Millipore) выполняли в соответствии с инструкциями производителя, и конечный продукт hu14.18-IL-2 помещали в следующую композицию:
рН буферной композиции доводили до 7 с помощью 1 М NaOH.
В качестве конечной стадии препарат фильтровали через мембрану Viresolve 180 (Millipore), которая отсекала вещества с молекулярной массой более 180.000 Дальтон. Это оказывало эффект «полировки» материала, в результате чего удалялись агрегированные димеры и олигомеры более высокого порядка.
Пример 2
Противоопухолевая активность слитого белка hu14.18-IL-2
Наблюдалась в клинических испытаниях Фазы I.
Для оценки безопасности и эффективности hu14.18-IL-2 было выполнено клиническое испытание Фазы I. Пригодные для участия в испытании пациенты имели гистологически подтвержденный диагноз меланомы, которая была признана неизлечимой хирургически и медикаментозно. Эти пациенты могли иметь пригодное для измерения или оценки метастатическое заболевание, или у них могло не быть признаков заболевания после хирургической резекции дистантных метастазов или регионального рецидива заболевания. Пациентов с несколькими (двумя или более) местными или региональными рецидивами включали в испытание только в том случае, если у них имелись ранее полученные доказательства поражения лимфатических узлов, и если рецидивы были разделены промежутком не менее 2 месяцев. От всех пациентов требовались адекватная функция костного мозга (определявшаяся по общему числу лейкоцитов (WBC)>3.500/мл или общему числу гранулоцитов>2000/мл, числу тромбоцитов>100.000/мл и содержанию гемоглобина>10,0 г/дл), адекватная функция печени (определявшаяся по уровню аспартатаминотрансферазы (AST)<3 х норма и общего билирубина<2,0 мг/дл) и адекватная функция почек (определявшаяся по уровню креатинина в сыворотке<2,0 мг/дл или клиренса креатинина>60 мл в минуту). Все пациенты по данным электрокортикографии (ECOG) имели статус, равный 0 или 1, и предполагаемый срок жизни не менее 12 недель. Пациентов, которые получали химиотерапию, лучевую терапию или иную иммунодепрессивную терапию в период до 4 недель до начала испытания, не включали в испытание. Пациенты могли ранее иметь метастазы в центральную нервную систему (ЦНС), если они подвергались лечению и были стабильными в течение, по меньшей мере, 4 недель до начала испытания. От всех пациентов было получено согласие, основанное на полученной информации.
Это испытание фазы I было спланировано как открытое, нерандомизированное испытание с повышением дозы, в котором группы, состоявшие из 3-6 пациентов, получали hu14.18-IL-2 в одной из следующих доз: 0,8, 1,6, 3,2, 4,8, 6,0 или 7,5 мг/м2/день. hu14.18-IL-2 вводили во время пребывания пациента в стационаре с виде 4-часовой внутривенной (IV) инфузии в течение 3-х последовательных дней на первой неделе каждого курса лечения. Слитый белок hu14.18-IL-2 вводили пациентам в композиции, содержавшей 4% маннитола, 100 мМ аргинина гидрохлогида, 5 мМ цитрата и 0,01% Твин 80 при рН, равном 7. Пациентов выписывали из госпиталя, при условии стабильности их состояния, примерно через 24 часа после завершения последней инфузии. Побочные явления и токсичность оценивали по общим критериям токсичности NCl (версия 2.0) и по оценочной шкале Висконсинского онкологического центра для IL-2 (общее состояние, прирост массы и температура). Дозолимитирующую токсичность (DLT) определяли как появление токсичности уровня 3 или 4, кроме лимфопении 3 степени, гипербилинерубинемии, гипофосфатемии или гипергликемии. Максимальную переносимую дозу (MTD) определяли как уровень дозы, при котором у двух из шести пациентов во время 1 курса лечения обнаруживалась DLT. Пациенты с симптомами токсичности уровня 3, связанной с лечением, должны были восстановиться, по меньшей мере, до уровня 1, прежде чем они могли продолжить лечение при 50%-ном снижении дозы в ходе курса 2. Пациентов с прогрессом заболевания ≥ 25% исключали из испытания. Пациентам со стабильным заболеванием проводили курс 2.
Фармакокинетические свойства hu14.18-IL-2 были оценены на пациентах. Когда уровни hu14.18-IL-2 были оценены в серийных пробах, взятых от всех 33 пациентов сразу же после первой 4-часовой инфузии (день 1, курс 1), было обнаружено, что период полужизни равен 3,7 часа (+/- SD (стандартное отклонение), равное 0,9 ч). Это значение является промежуточным между периодами полужизни 2-х его компонентов (примерно 45 минут для IL-2 и 3 дня для химерного антитела m14.18) и сопоставимо со значением, которое было получено для периода полужизни химерного белка m14.18-IL-2 у мышей. После клиренса hu14.18-IL-2 из сыворотки этих пациентов невозможно было обнаружить его компоненты - IL-2 и антитело hu14.18. Пиковое содержание в сыворотке и площадь под кривой (AUC) во время курса 1 обнаруживали достоверное дозозависимое возрастание (р<0,001).
В этом испытании лечение получили тридцать три пациента. В Таблице 1 перечислены клинические исходы болезни. Два пациента (6%) прошли только первые 2 дня курса 1. У одного из этих пациентов (уровень дозы 3) на 2-ой день лечения была обнаружена гипербилирубинемия степени 3, а у второго пациента (уровень дозы 6) возникла гипоксия степени 3 и гипотензия, что потребовало прекращения лечения. У обоих пациентов болезнь прогрессировала, и они не прошли второй курс терапии. У девятнадцати пациентов (58%) после первого курса терапии заболевание было стабильным, и они получили второй курс терапии. У пяти пациентов (15% от всех пациентов) для курса 2 потребовалось 50%-ное снижение дозы из-за побочных эффектов, возникших во время курса 1. Семнадцать пациентов (52% от всех пациентов) полностью прошли курс 2. Один пациент (уровень дозы 4) отказался от получения последней инфузии в ходе курса 2, а у одного пациента (уровень дозы 6) пришлось прекратить последнюю инфузию курса 2 из-за гипотензии. У восьми пациентов (24% от всех пациентов) после второго курса лечения заболевание было стабильным. Результаты показывают, что hu14.18-IL-2 вызывает стабилизацию прогресса заболевания у неожиданного большого числа пациентов.
У восьми из 33 пациентов заболевание оставалось стабильным после 2 курсов терапии, и 4 из этих 8 пациентов продолжали жить без признаков прогрессирования заболевания (1 со стабильным заболеванием и 3 без признаков заболевания) в течение 20-52 месяцев после завершения протокола лечения.
Пять из 33 пациентов были взяты в испытание без измеримых признаков заболевания после хирургической резекции рецидивов или метастазов. У двух из этих пяти пациентов болезнь прогрессировала, тогда как оставшиеся 3 пациента продолжали жить без признаков заболевания (20-52 месяца). Эти данные соответствуют гипотезе о том, что клиническая польза от иммунотерапевтического вмешательства наиболее вероятна у пациентов с низкой опухолевой нагрузкой. Кроме того, у одного из пациентов после двух курсов лечения наблюдалось объективное уменьшение размеров узла в легком, но общая реакция заболевания была оценена как прогресс болезни из-за роста дистантного узла. Узел был резецирован после терапии hu14.18-IL-2, и болезнь у данного пациента не прогрессировала в течение более чем 3 лет.
Иммуностимуляция in vivo с помощью hu14.18-IL-2 в клиническом испытании Фазы I
Пациентов, получавших лечение hu14.18-IL-2, исследовали также на признаки стимуляции иммунной системы. Лимфопения периферической крови наблюдалась на 2-ой-4-ый день, и за ней следовала «отдача» в виде лимфоцитоза на 5-ый-24-ый день. Оба этих изменения были дозозависимыми (р<0,01 и р<0,05, соответственно). Число лимфоцитов на 5-ый, 8-ой, 15-ый и 22-ой день было значительно больше исходного значения для курса 1. Исходное число лимфоцитов для курса 2 (29-ый день курса 1) превышало исходное число лимфоцитов для курса 1, что показывает, что эффект первого курса лечения еще сохранялся к 29-му дню. Кроме того, во время курса 2 число лимфоцитов на 5-ый, 8-ой и 15-ый день у этих 12 пациентов было больше соответствующих значений для 5-го, 8-го и 15-го дней курса 1.
Фенотип клеточной поверхности лимфоцитов обнаруживал экспансию CD16+и CD56+лимфоцитов (маркеры клеток натуральных киллеров (НК)) после первой недели терапии hu14.18-IL-2. Этот эффект все еще сохранялся на 29-ый день курса 1 (день 1 курса 2). У пациентов 19-33 (получавших 4,8-7,5 мг/м2/день) фенотип клеточной поверхности лимфоцитов, кроме 1-го и 8-го дня, определяли на 15-ый и на 22-ой день. Анализ продемонстрировал, что число CD56 и CD56/CD16 соэкспрессирующих клеток оставалось значительно повышенным (р<0,01) на 8-ой, 15-ый и 22-ой день.
В качестве меры активации иммунной системы были измерены уровни С-реактивного белка (CRP) у пациентов 13-33 и растворимого рецептора IL-2 (sIL-2R) у 31 пациента, завершивших курс 1. Достоверное повышение среднего уровня CRP присутствовало на 3-ий-5-ый день лечения в курсе 1 и в курсе 2, по сравнению с исходным уровнем для каждого курса. Это повышение уровня CRP возвращалось к исходным уровням к 8-му дню каждого курса лечения. Уровень sIL-2R достоверно повышался выше исходного уровня уже через 24 часа после инфузии hu14.18-IL-2 во время курса 1 и курса 2 и оставался повышенным до 8-го дня. Было обнаружено, что повышение уровня sIL-2R было дозозависимым (р=0,014). Значения sIL-2R для курса 2 возрастали по сравнению с соответствующими значениями для курса 1 в дни 1-5 у пациентов, получавших одинаковые дозы в ходе обоих курсов (р<0,05).
Линию клеток нейробластомы LA-N-5, экспрессирующую GD2 и связывающую hu14.18-IL-2, использовали для оценки активированной IL-2 функции НК и обусловленной антителами клеточной цитотоксичности (ADCC) на мононуклеарных клетках периферической крови (PBMC), полученных от 31 пациента, завершивших курс 1. Начиная с 8-го дня, в этих двух анализах наблюдалось достоверное повышение гибели клеток, опосредованной лимфоцитами, по сравнению с днем 1. 12 пациентов, получивших курс 2 в той же дозе, что и курс 1, показали результаты по ADCC, очень сходные с результатами, полученными во время курса 1. Единственным параметром, который, как было обнаружено, отличался в курсе 2 от курса 1, было повышение гибели клеток в присутствии IL-2 в день 1, что показывает, что стимулированная гибель клеток в этом анализе оставалась повышенной к 29-му дню (день 1 курса 2).
Поскольку LA-N-5-мишень относительно устойчива к свежим НК-клеткам, ее можно использовать для измерения гибели клеток, стимулированной IL-2, и ADCC. Однако, слабое уничтожение LA-N-5, опосредованное свежими PBMC в среде (без дополнительного IL-2 in vitro), не является достоверно большим на 8-ой день, по сравнению с днем 1.
Для пациентов 19-33 стандартные анализы с НК были выполнены в 1-ый, 8-ой, 15-ый и 22-ой день с использованием чувствительной к НК линии клеток-мишеней K562. Достоверное усиление лизиса натуральными киллерами (НК) клеток-мишеней К562, по сравнению с днем 1, при испытании в среде или в присутствии IL-2 наблюдалось на 8-ой и 22-ой день. Пробы сыворотки от избранных пациентов также оценивались с целью определения функциональной активности IL-2 и функциональной активности антитела к GD2.
Реагирующая на IL-2 клеточная линия Tf-1b продемонстрировала индуцированную IL-2 пролиферацию в ответ на сыворотку пациентов, полученную после инфузии hu14.18-IL-2. Прогрессивное усиление пролиферации обнаруживалось в течение первых 4 часов после 4-часовой инфузии. Значения возвращались к исходному уровню через 16 часов после этой инфузии, что совпадает с периодом полужизни hu14.18-IL-2, равным примерно 4 часам. Пробы сыворотки, взятые в эти моменты времени, также были посредством проточной цитометрии исследованы на присутствие интактного hu14.18-IL-2 иммуноцитокина (IC), который сохраняет IL-2 компонент и активность антитела к GD2. hu14.18-IL-2, способный связывать клеточную линию М21 (GD2-позитивную), можно было обнаружить в пробах сыворотки пациентов после инфузии IC. Количество IC, способного связываться с М21, прогрессивно возрастало в течение первых 4 часов после 4-часовой инфузии, а затем снижалось, что также соответствует периоду полужизни, примерно равному 4 часам. Наконец, были выполнены анализы in vitro проб, взятых у пациентов, для того, чтобы определить, приводит ли введение hu14.18-IL-2 к условиям in vivo, соответствующим условиям, необходимым для достижения ADCC. PBMC, взятые в день 8, обнаруживают повышенную цитотоксичность в отношении GD2+клеток-мишеней при добавлении hu14.18-IL-2 к анализу на цитотоксичность. Такой же ADCC-анализ был выполнен с PMBC, взятыми в день 8, однако вместо hu14.18-IL-2 к пробе была добавлена сыворотка пациента, полученная до или после введения hu14.18-IL-2. PBMC, полученные от пациентов на 8-ой день курса 2, были способны опосредовать усиленное уничтожение клеточной линии LA-N-5 в присутствии сыворотки, полученной после введения hu14.18-IL-2, по сравнению с результатами, полученными с сывороткой, взятой до инфузии. Таким образом, hu14.18-IL-2, циркулирующий у пациентов после внутривенного введения, может стимулировать ADCC с PMBC, активированных in vivo hu14.18-IL-2 от того же пациента.
Коротко говоря, эти результаты показывают, что с терапией hu14.18-IL-2 связаны иммунологические изменения, в том числе возрастание числа лимфоцитов, возрастание процентного содержания CD16+и CD56+PMBC, усиление лизиса НК и усиление ADCC. Дополнительное доказательство активации иммунной системы включает повышение уровней СРБ и sIL-2R в сыворотке. Лабораторные анализы сыворотки и PMBC показали, что молекула hu14.18-IL-2, циркулирующая в сыворотке пациента после внутривенного введения, сохраняет свою способность активировать IL-2-реактивные клетки через IL-2-рецептор, способность связываться с GD2-позитивными опухолевыми клетками и доставлять IL-2 к их поверхности, что было обнаружено с помощью проточной цитометрии. НК-клетки активируются in vivo, судя по их способности опосредовать НК и ADCC функции in vitro. Кроме того, НК-клетки, активированные in vivo hu14.18-IL-2, введенным этим пациентам, были способны опосредовать ADCC, усиленную hu14.18-IL-2, циркулирующим в сыворотке этих пациентов. Таким образом, условия для получения активации иммунной системы были достигнуты у всех пациентов в данном испытании.










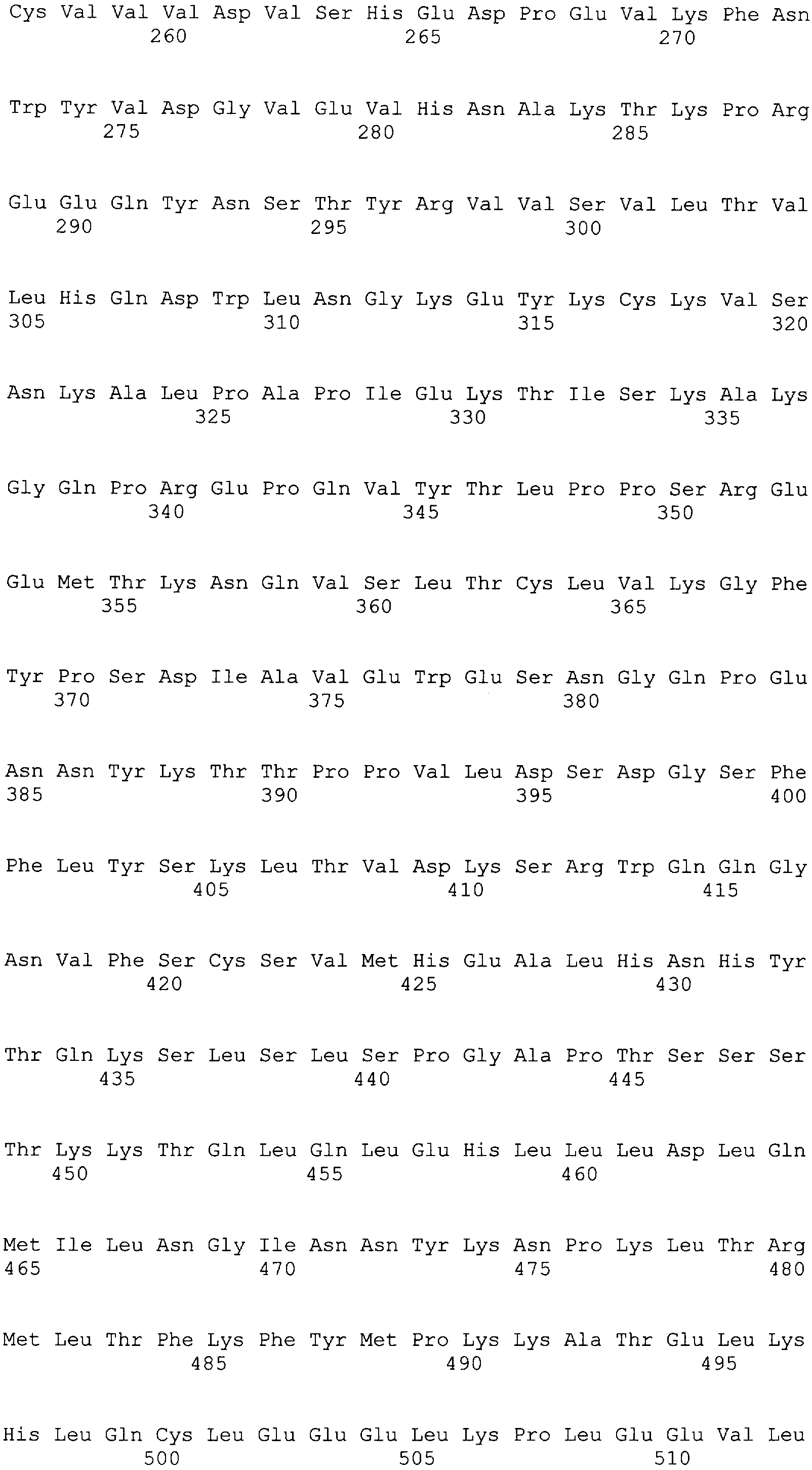

Реферат
Настоящее изобретение относится к иммунологии и биотехнологии. Предложено использование гуманизированного слитого белка для изготовления медикамента для стимулирования иммунного ответа и стабилизации прогрессирования заболевания у пациентов с GD2-позитивными опухолями. Антитело состоит из антитела Н14.18, связывающегося с поверхностным гликосфинголипидом GD2 клеток человека, и цитокина IL2. Описан способ усиления ADCC и лизисной активности НК-клеток у пациента, имеющего опухоль, путем введения слитого белка. Использование изобретения обеспечивает антитело с пониженной иммуногенностью по сравнению с антителом 14.18 мыши, что может найти применение для лечения опухолей со сверхэкспрессией GD2. 2 н.п. ф-лы, 3 ил., 1 табл.

Комментарии