Способ индукции конечной дифференцировки - RU2004133675A
Код документа: RU2004133675A
Реферат
1. Способ получения субероиланилида гидроксамовой кислоты (САГК), предусматривающий стадию перекристаллизации неочищенного препарата САГК из смеси метанола и воды.
2. Способ по п.1, отличающийся тем, что указанная смесь метанола и воды представляет собой смесь метанол/вода в соотношении примерно 2:1.
3. Субероиланилид гидроксамовой кислоты (САГК), получаемый по способу, предусматривающему стадию перекристаллизации неочищенного препарата САГК из смеси метанола и воды.
4. САГК по п.3, отличающийся тем, что указанная смесь метанола и воды представляет собой смесь метанол/вода в соотношении примерно 2:1.
5. Кристаллическая форма САГК, имеющая физические характеристики САГК, получаемая по способу, предусматривающему стадию перекристаллизации неочищенного препарата САГК из смеси метанола и воды.
6. Кристаллическая форма САГК по п.5, отличающаяся тем, что указанная смесь метанола и воды представляет собой смесь метанол/вода в соотношении примерно 2:1.
7. Способ синтеза субероиланилида гидроксамовой кислоты (САГК), предусматривающий стадии:
а. взаимодействия субериновой кислоты с анилином с образованием суберанилиновой кислоты или ее соли, имеющей структуру
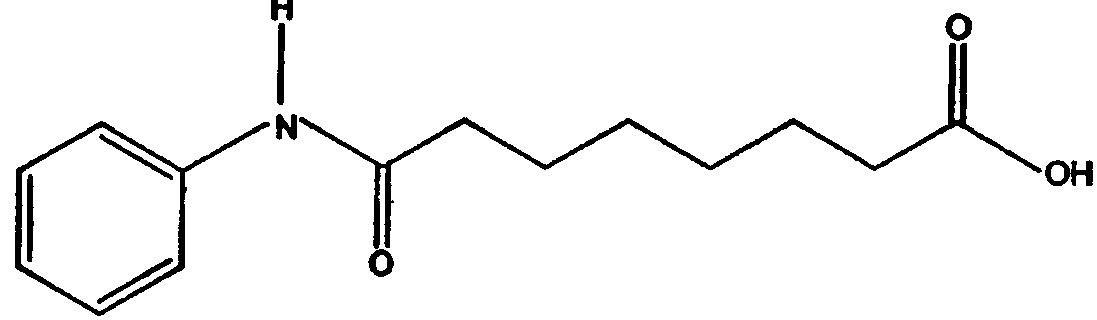
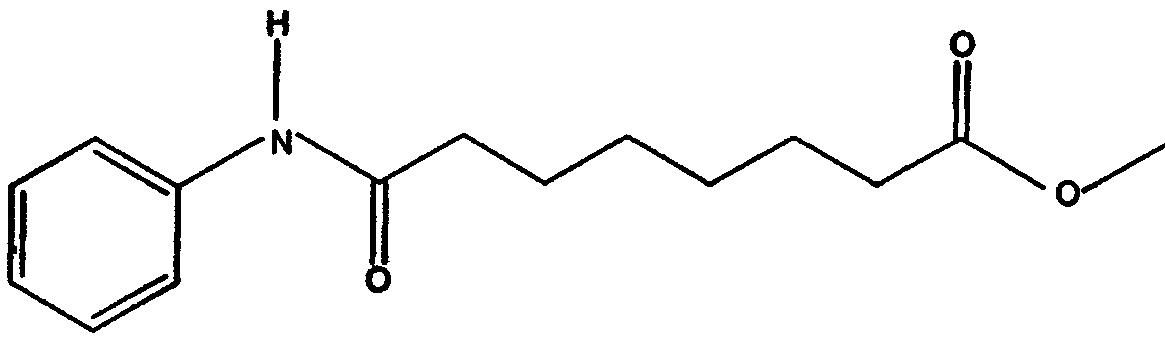
b. реакции суберанилиновой кислоты с метанолом с образованием метилсуберанилата, имеющего структуру
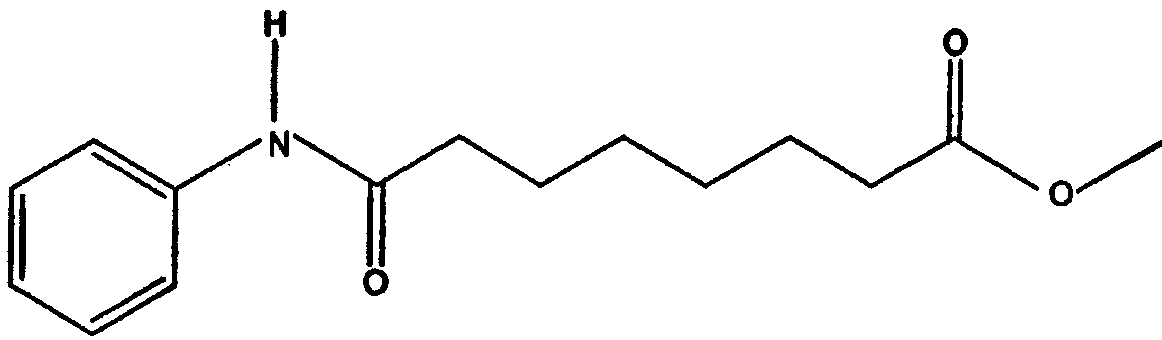
c. реакции метилсуберанилата с гидрохлоридом гидроксиламина с образованием неочищенного субероиланилида гидроксамовой кислоты в реакционной смеси и
d. перекристаллизации указанного неочищенного препарата САГК из смеси метанола и воды.
8. Способ по п.7, отличающийся тем, что указанная смесь метанола и воды представляет собой смесь метанол/вода в соотношении примерно 2:1.
9. Способ по п.7, отличающийся тем, что стадия (с) также предусматривает стадии:
(1) добавления к реакционной смеси метоксида натрия с получением прозрачного раствора и
(2) добавления ледяной уксусной кислоты к прозрачному раствору с образованием осадка.
10. Субероиланилид гидроксамовой кислоты (САГК), получаемый по способу, предусматривающему стадии:
а. взаимодействия субериновой кислоты с анилином с образованием суберанилиновой кислоты или ее соли, имеющей структуру
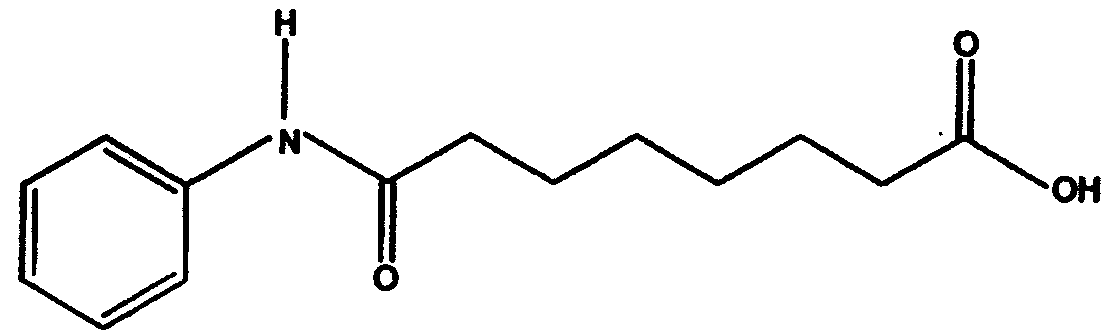
b. реакции суберанилиновой кислоты с метанолом с образованием метилсуберанилата, имеющего структуру

c. реакции метилсуберанилата с гидрохлоридом гидроксиламина с образованием неочищенного субероиланилида гидроксамовой кислоты в реакционной смеси и
d. перекристаллизации указанного неочищенного препарата САГК из смеси метанола и воды.
11. САГК по п.10, отличающийся тем, что указанная смесь метанола и воды представляет собой смесь метанол/вода в соотношении примерно 2:1.
12. Кристаллическая форма САГК, имеющая физические характеристики САГК, получаемая по способу, предусматривающему стадии:
а. реакции субериновой кислоты с анилином с образованием суберанилиновой кислоты или ее соли, имеющей структуру
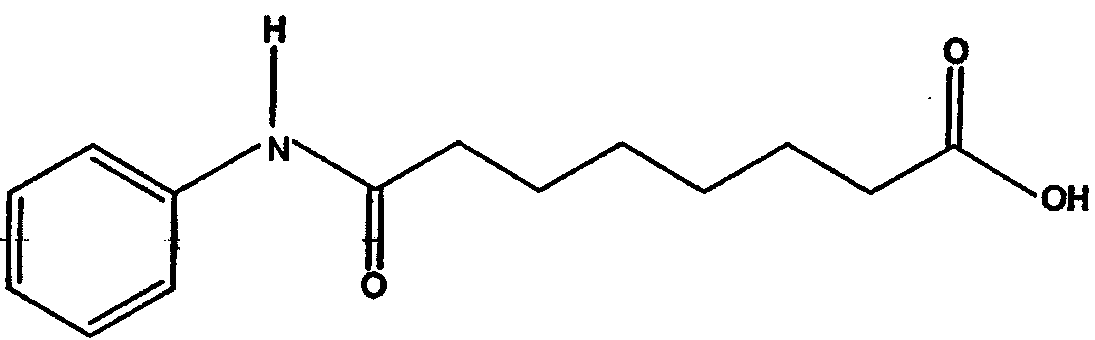
b. реакции суберанилиновой кислоты с метанолом с образованием метилсуберанилата, имеющего структуру
c. реакции метилсуберанилата с гидрохлоридом гидроксиламина с образованием неочищенного субероиланилида гидроксамовой кислоты в реакционной смеси и
d. перекристаллизации указанного неочищенного препарата САГК из смеси метанола и воды.
13. САГК по п.12, отличающийся тем, что указанная смесь метанола и воды представляет собой смесь метанол/вода в соотношении примерно 2:1.
14. Способ применения ингибитора гистондезацетилазы (HDAC) для получения лекарственного средства, используемого для достижения среднего значения концентрации указанного ингибитора HDAC в плазме, равной по меньшей мере примерно 10 нМ, у субъекта в течение периода времени, равного по меньшей мере двум часам после введения.
15. Способ применения ингибитора гистондезацетилазы (HDAC) при получении лекарственного средства, используемого для достижения среднего значения концентрации указанного ингибитора HDAC в плазме субъекта, равной по меньшей мере примерно 10 нМ, в течение периода времени, равного по меньшей мере двум часам после введения, и с достижением при этом селективной индукции конечной дифференцировки опухолевых клеток у указанного субъекта.
16. Способ применения ингибитора гистондезацетилазы (HDAC) при получении лекарственного средства, используемого для достижения среднего значенмя концентрации указанного ингибитора HDAC в плазме субъекта, равной по меньшей мере примерно 10 нМ, в течение периода времени, равного по меньшей мере двум часам после введения, и с достижением при этом конечной дифференцировки опухолевых клеток у указанного субъекта.
17. Способ применения ингибитора гистондезацетилазы (HDAC) при получении лекарственного средства, используемого для достижения среднего значения концентрации указанного ингибитора HDAC в плазме субъекта, равной по меньшей мере примерно 10 нМ, в течение периода времени, равного по меньшей мере двум часам после введения, и с достижением при этом индукции остановки клеточного роста опухолевых клеток у указанного субъекта.
18. Способ применения ингибитора гистондезацетилазы (HDAC) при получении лекарственного средства, используемого для достижения среднего значения концентрации указанного ингибитора HDAC в плазме субъекта, равной по меньшей мере примерно 10 нМ, в течение периода времени, равного по меньшей мере двум часам после введения, и с достижением при этом индукции апоптоза опухолевых клеток у указанного субъекта.
19. Способ по любому из пп. 14, 15, 16, 17 или 18, отличающийся тем, что указанная средняя концентрация указанного ингибитора HDAC в плазме поддерживается in vivo равной по меньшей мере примерно 10 нМ в течение по меньшей мере 10 часов после введения.
20. Способ по любому из пп. 14, 15, 16, 17 или 18, отличающийся тем, что указанное лекарственное средство обеспечивает суммарную дневную дозу указанного ингибитора HDAC в диапазоне примерно 25-4000 мг/м2.
21. Способ по любому из пп. 14, 15, 16, 17 или 18, отличающийся тем, что указанное лекарственное средство обеспечивает суммарную дневную дозу указанного ингибитора HDAC, равную примерно 200 мг.
22. Способ по любому из пп. 14, 15, 16, 17 или 18, отличающийся тем, что указанное лекарственное средство обеспечивает суммарную дневную дозу указанного ингибитора HDAC, равную примерно 400 мг.
23. Способ по любому из пп. 14, 15, 16, 17 или 18, отличающийся тем, что указанный ингибитор HDAC представляет собой субероиланилид гидроксамовой кислоты (САГК)

24. Способ по любому из пп. 14, 15, 16, 17 или 18, отличающийся тем, что указанный ингибитор HDAC представляет собой пироксамид, описываемый структурной формулой

25. Способ по любому из пп. 14, 15, 16, 17 или 18, отличающийся тем, что указанный ингибитор HDAC описывается структурной формулой
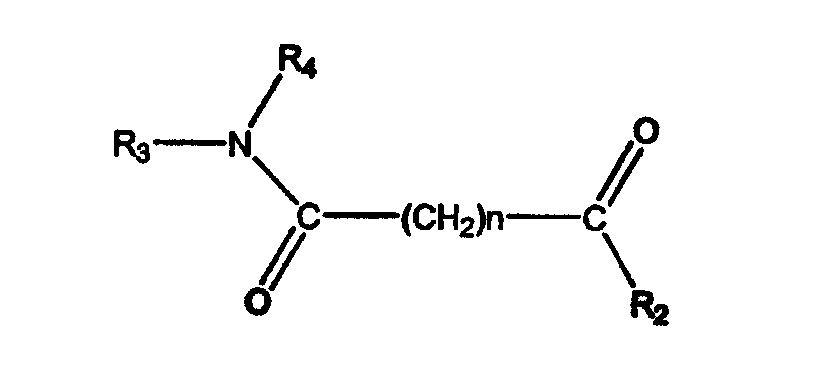
где R3 и R4 независимо обозначают замещенную или незамещенную разветвленную или неразветвленную алкильную, алкенильную, циклоалкильную, арильную, алкилокси, арилокси, арилалкилокси или пиридиновую группу, или R3 и R4 соединяются вместе с образованием пиперидиновой группы; R2 обозначает гидроксиламиногруппу; и n равно целому числу от 5 до 8.
26. Способ по любому из пп. 14, 15, 16, 17 или 18, отличающийся тем, что указанный ингибитор HDAC описывается структурной формулой

где R обозначает замещенный или незамещенный фенил, пиперидин, тиазол, 2-пиридин, 3-пиридин или 4-пиридин, и n равно целому числу от 4 до 8.
27. Способ по любому из пп. 14, 15, 16, 17 или 18, отличающийся тем, что указанный ингибитор HDAC описывается структурной формулой

где А обозначает амидный фрагмент, R1 и R2, каждый, выбирают из замещенного или незамещенного арила (например, фенила), арилалкила (например, бензила), нафтила, пиридинамино, 9-пурин-6-амино, тиазоламино, арилокси, арилалкилокси, пиридила, хинолинила или изохинолинила; R4 обозначает атом водорода, атом галогена, фенильную или циклоалкильную группировку, и n равно целому числу от 3 до 10.
28. Способ по любому из пп. 14, 15, 16, 17 или 18, отличающийся тем, что указанный ингибитор HDAC представляет собой субероиланилид гидроксамовой кислоты (САГК), получаемый по способу любого из пп. 1, 2, 7, 8 или 9.
29. Способ по любому из пп. 14, 15, 16, 17 или 18, отличающийся тем, что указанный ингибитор HDAC представляет собой субероиланилид гидроксамовой кислоты (САГК), получаемый в соответствии с любым из пп. 3, 4, 5, 6, 10, 11, 12 или 13.
30. Фармацевтическая композиция для перорального введения, содержащая ингибитор гистондезацетилазы (HDAC) или его фармацевтически приемлемую соль или гидрат, микрокристаллическую целлюлозу, натрий-кросскармеллозу и стеарат магния.
31. Композиция по п.30, отличающаяся тем, что указанный ингибитор HDAC представляет собой субероиланилид гидроксамовой кислоты (САГК)
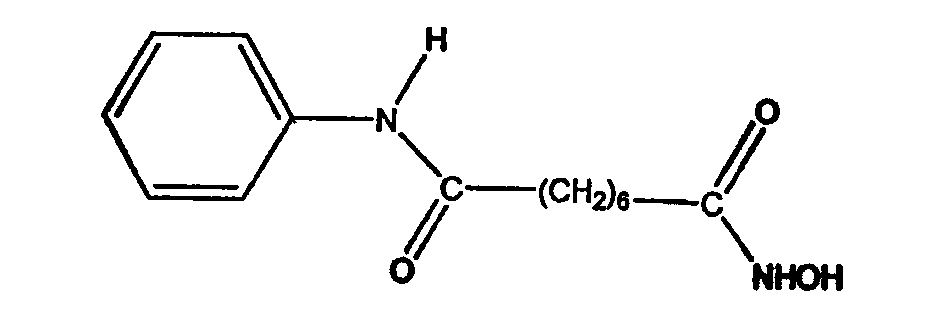
32. Композиция по п.30, содержащая
50-70 мас.% указанного ингибитора гистондезацетилазы (HDAC) или его фармацевтически приемлемой соли или гидрата;
20-40 мас.% микрокристаллической целлюлозы;
5-15 мас.% натрий-кросскармеллозы и
0,1-5 мас.% стеарата магния.
33. Композиция по п.30, содержащая примерно 50-200 мг указанного ингибитора HDAC.
34. Композиция по п.30, помещенная в желатиновую капсулу.
35. Фармацевтическая композиция для перорального введения, содержащая
субероиланилид гидроксамовой кислоты (САГК) или его фармацевтически приемлемую соль или гидрат;
микрокристаллическую целлюлозу;
натрий-кросскармеллозу и
стеарат магния.
36. Композиция по п.35, содержащая
50-70 мас.% САГК или его фармацевтически приемлемой соли или гидрата;
20-40 мас.% микрокристаллической целлюлозы;
5-15 мас.% натрий-кросскармеллозы и
0,1-5 мас.% стеарата магния.
37. Композиция по п.35, содержащая примерно 50-200 мг САГК.
38. Композиция по п.35, помещенная в желатиновую капсулу.
39. Композиция по п.30, отличающаяся тем, что указанный ингибитор HDAC представляет собой субероиланилид гидроксамовой кислоты (САГК), получаемый по способу, предусматривающему стадию перекристаллизации неочищенного препарата САГК из смеси метанола и воды.
40. Композиция по п.39, отличающаяся тем, что указанная смесь метанола и воды представляет собой смесь метанол/вода в соотношении примерно 2:1.
41. Композиция по п.30, отличающаяся тем, что указанный ингибитор HDAC представляет собой кристаллическую форму САГК, имеющую физические характеристики САГК, получаемую по способу, предусматривающему стадию перекристаллизации неочищенного препарата САГК из смеси метанола и воды.
42. Композиция по п.41, отличающаяся тем, что указанная смесь метанола и воды представляет собой смесь метанол/вода в соотношении примерно 2:1.
43. Композиция по п.30, отличающаяся тем, что указанный ингибитор HDAC представляет собой субероиланилид гидроксамовой кислоты (САГК), получаемый по способу, предусматривающему стадии:
а. реакции субериновой кислоты с анилином с образованием суберанилиновой кислоты или ее соли, имеющей структуру
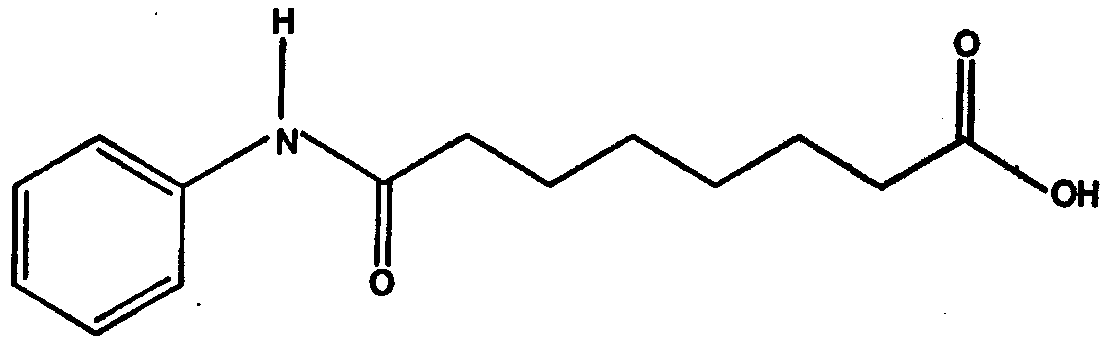
b. реакции суберанилиновой кислоты с метанолом с образованием метилсуберанилата, имеющего структуру
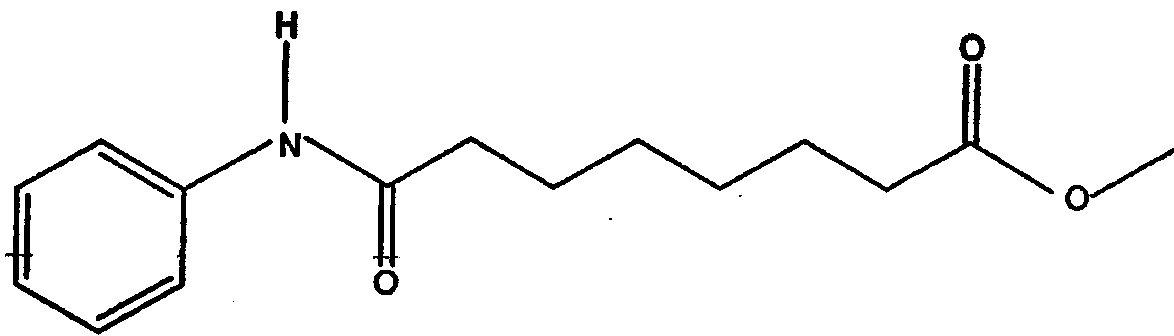
с. реакции метилсуберанилата с гидрохлоридом гидроксиламина с образованием неочищенного субероиланилида гидроксамовой кислоты в реакционной смеси и
d. перекристаллизации неочищенного препарата САГК из смеси метанола и воды.
44. Композиция по п.43, отличающаяся тем, что указанная смесь метанола и воды представляет собой смесь метанол/вода в соотношении примерно 2:1.
45. Композиция по п.30, отличающаяся тем, что указанный ингибитор HDAC представляет собой кристаллическую форму САГК, имеющую физические характеристики САГК, получаемую по способу, предусматривающему стадии:
а. реакции субериновой кислоты с анилином с образованием суберанилиновой кислоты или ее соли, имеющей структуру
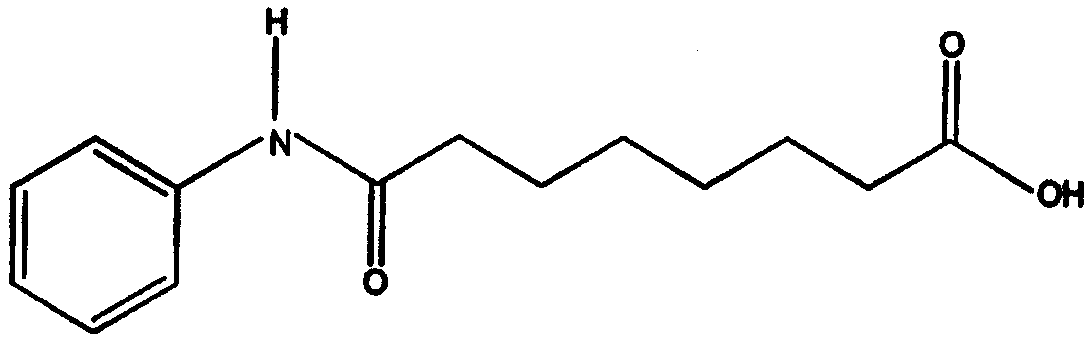
b. реакции суберанилиновой кислоты с метанолом с образованием метилсуберанилата, имеющего структуру
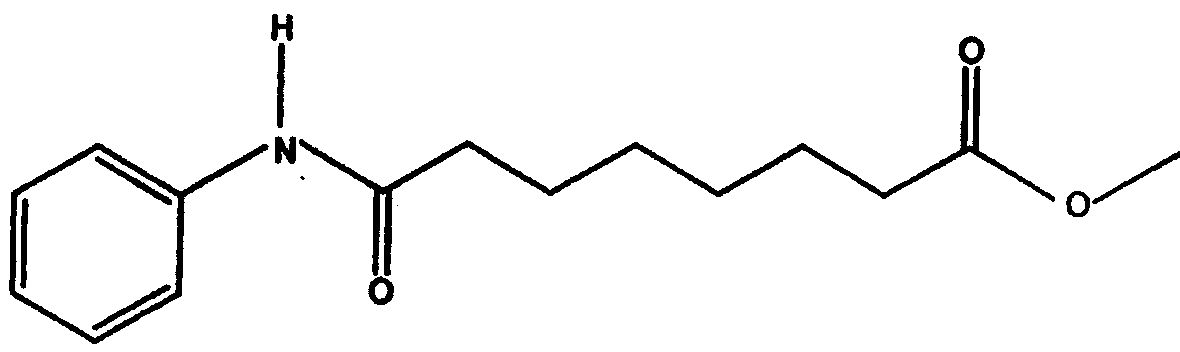
с. реакции метилсуберанилата с гидрохлоридом гидроксиламина с образованием неочищенного субероиланилида гидроксамовой кислоты в реакционной смеси и
d. перекристаллизации неочищенного препарата САГК из смеси метанола и воды.
46. Композиция по п.45, отличающаяся тем, что указанная смесь метанола и воды представляет собой смесь метанол/вода в соотношении примерно 2:1.

Комментарии