Антигенсвязывающая молекула, способная многократно связываться с множеством антигенных молекул - RU2642318C2
Код документа: RU2642318C2
Чертежи

































































































































































































Описание
[Уровень техники]
Антитела привлекают внимание в качестве лекарственных средств, так как они обладают высокой стабильностью в плазме и обладают малым количеством побочных эффектов. В настоящее время ряд подобных фармацевтических средств IgG-типа являются коммерчески доступными и на сегодняшний день разрабатываются многие лекарственные средства на основе антител (непатентные документы 1 и 2). Между тем, описаны различные способы, применимые для второго поколения лекарственных средств на основе антител, включающие способы, которые усиливают эффекторную функцию, антигенсвязывающую способность, фармакокинетику и стабильность, и способы, которые снижают риск развития иммуногенности (непатентный документ 3). Как правило, требуемая доза лекарственного средства на основе антитела является очень высокой. Это, в свою очередь, привело к возникновению проблем, таких как высокая стоимость производства, а также к трудностям при получении подкожных составов. В теории, доза фармацевтического средства на основе антитела может быть снижена путем улучшения фармакокинетики антитела или повышения аффинности между антителами и антигенами.
В литературе описаны способы улучшения фармакокинетики антител с использованием искусственных замен аминокислот в константных областях (непатентные документы 4 и 5). Аналогично описано созревание аффинности как способ улучшения антигенсвязывающей способности или активности нейтрализации антигена (непатентный документ 6). Этот способ дает возможность увеличения антигенсвязывающей способности посредством внесения аминокислотной мутации в область CDR вариабельной области или сходные с ней. Повышение антигенсвязывающей способности обеспечивает улучшение биологической активности in vitro или обеспечивает возможность снижения дозы и дополнительно обеспечивает повышенную эффективность in vivo (непатентный документ 7).
Между тем, способность одной молекулы антитела нейтрализовать антиген зависит от ее аффинности. Путем увеличения аффинности антиген можно нейтрализовать меньшим количеством антитела. Для увеличения аффинности антитела можно использовать различные способы (непатентный документ 6). Кроме того, если бы аффинность можно было сделать бесконечной посредством ковалентного связывания антитела с антигеном, одна молекула антитела могла бы нейтрализовать одну молекулу антигена (двухвалентное антитело могло бы нейтрализовать две молекулы антигена). Однако, стехиометрия нейтрализации одного антитела против одного антигена (одного двухвалентного антитела против двух антигенов) является лимитирующим фактором для предшествующих способов, и, таким образом, было невозможно полностью нейтрализовать антиген количеством антитела, меньшим, чем количество антигена. Другими словами, эффект, усиливающий аффинность, имеет лимитирующее значение (непатентный документ 9). Для увеличения периода действия нейтрализующего эффекта нейтрализующего антитела в течение определенного периода антитело должно быть введено в дозе, более высокой, чем количество антигена, продуцируемое в организме в течение такого же периода. Таким образом, в случае просто описанного выше улучшения фармакокинетики антител или технологии созревания аффинности существуют ограничения, когда дело доходит до снижения требуемой дозы антитела. Таким образом, для поддержания эффекта антител в отношении нейтрализации антигена в течение заданного периода времени с помощью антител в количестве, меньшем, чем количество антигена, одно антитело должно нейтрализовать множество антигенов.
Недавно было описано антитело, которое связывается с антигеном рН-зависимым образом, в качестве нового способа для достижения описанной выше задачи (патентный документ 1). Антитела с рН-зависимым связыванием антигена, которые прочно связываются с антигеном при нейтральных условиях в плазме и диссоциируют от антигена при кислых условиях в эндосоме, могут диссоциировать от антигена в эндосоме. Когда антитело с рН-зависимым связыванием антигена диссоциирует от антигена и рециркулирует в плазму посредством FcRn, оно может повторно связываться с другим антителом. Таким образом, антитело может многократно связываться с несколькими антигенами.
Кроме того, время удержания антигена в плазме является очень коротким по сравнению со временем удержания антител, рециркулирующих в плазму путем связывания с FcRn. Если антитело с продолжительным временем удержания в плазме связывает такой антиген с коротким удержанием в плазме, время удержания в плазме комплекса антиген-антитело увеличивается на тот же период, что и время удержания в плазме антитела. Таким образом, путем связывания с антителом повышается время удержания антигена, и таким образом концентрация антигена в плазме увеличивается. В таких случаях, даже если увеличивается аффинность антигена к антителу, не может быть увеличена элиминация антигена из плазмы. Опубликовано, что описанные выше pH-зависимые антигенсвязывающие антитела более эффективны как способ увеличения элиминации антигена плазмы по сравнению с типичными антителами (патентный документ 1).
Таким образом, одно антитело с рН-зависимым связыванием антигена связывает ряд антигенов и способно, по сравнению с типичными антителами, облегчать элиминацию антигена в плазме. Таким образом, антитела с рН-зависимым связыванием имеют действие, которое нельзя осуществить посредством типичных антител. Однако единственным известным способом достижения эффекта многократного связывания антитела с pH-зависимым связыванием антигена и эффекта ускорения элиминации антигена из плазмы было обеспечение зависимости от реакции антиген-антитело с использованием различий в pH между плазмой и эндосомой. Документы, касающиеся известного уровня техники, относящиеся к настоящему изобретению, представлены ниже:
Документы уровня техники
[Патентные документы]
[Патентный документ 1] WO 2009/125825, ANTIGEN-BINDING MOLECULE CAPABLE OF BINDING TO TWO OR MORE ANTIGEN MOLECULES REPEATEDLY
[Непатентные документы]
[Непатентный документ 1] Monoclonal antibody successes in the clinic, Janice M Reichert, Clark J Rosensweig, Laura B Faden & Matthew C Dewitz, Nature Biotechnology 23, 1073-1078 (2005)
[Непатентный документ 2] Pavlou AK, Belsey MJ., The therapeutic antibodies market to 2008, Eur J Pharm Biopharm. 2005 Apr; 59(3): 389-96
[Непатентный документ 3] Kim SJ, Park Y, Hong HJ., Antibody engineering for the development of therapeutic antibodies., Mol Cells. 2005 Aug 31; 20(1): 17-29. Review
[Непатентный документ 4] Hinton PR, Xiong JM, Johlfs MG, Tang MT, Keller S, Tsurushita N., An engineered human IgG1 antibody with longer serum half-life., J Immunol. 2006 Jan 1; 176(1): 346-56
[Непатентный документ 5] Ghetie V, Popov S, Borvak J, Radu C, Matesoi D, Medesan C, Ober RJ, Ward ES., Increasing the serum persistence of an IgG fragment by random mutagenesis., Nat Biotechnol. 1997 Jul; 15(7): 637-40
[Непатентный документ 6] Proc Natl Acad Sci U S A. 2005 Jun 14; 102(24): 8466-71. Epub 2005 Jun 6. A general method for greatly improving the affinity of antibodies by using combinatorial libraries. Rajpal A, Beyaz N, Haber L, Cappuccilli G, Yee H, Bhatt RR, Takeuchi T, Lerner RA, Crea R
[Непатентный документ 7] Wu H, Pfarr DS, Johnson S, Brewah YA, Woods RM, Patel NK, White WI, Young JF, Kiener PA. Development of Motavizumab, an Ultra-potent Antibody for the Prevention of Respiratory Syncytial Virus Infection in the Upper and Lower Respiratory Tract. J Mol Biol. (2007) 368: 652-665
[Непатентный документ 8] Hanson CV, Nishiyama Y, Paul S. Catalytic antibodies and their applications. Curr Opin Biotechnol. 2005 Dec; 16(6): 631-6
[Непатентный документ 9] Rathanaswami P, Roalstad S, Roskos L, Su QJ, Lackie S, Babcook J. Demonstration of an in vivo generated sub-picomolar affinity fully human monoclonal antibody to interleukin-8. Biochem Biophys Res Commun. 2005 Sep 9; 334(4): 1004-13.
[Сущность изобретения]
[Проблемы, решаемые изобретением]
Настоящее изобретение было осуществлено ввиду вышеуказанных обстоятельств. Задачей настоящего изобретения является предоставление способов ускорения захвата антигена в клетки с использованием антигенсвязывающих молекул, способов увеличения количества раз связывания антигена одной антигенсвязывающей молекулой, способов ускорения снижения концентрации антигена в плазме путем введения антигенсвязывающих молекул, способов увеличения удержания в плазме антигенсвязывающих молекул, антигенсвязывающих молекул, которые способствуют захвату антигена в клетки, антигенсвязывающих молекул, которые имеют увеличенное количество раз связывания антигена, антигенсвязывающих молекул, которые способны ускорять снижение концентрации антигена в плазме при введении, антигенсвязывающих молекул с увеличенным временем нахождения в плазме, фармацевтических композиций, содержащих антигенсвязывающие молекулы и способов их получения.
[Средства для решения проблем]
Авторы настоящего изобретения провели исследования, посвященные способам ускорения захвата антигена в клетки с помощью антигенсвязывающих молекул (молекулы, такие как полипептиды, имеющие активность связывания антигена), способам увеличения количества раз связывания антигена одной антигенсвязывающей молекулой, способам ускорения снижения концентрации антигена в плазме путем введения антигенсвязывающих молекул, и способам увеличения времени удержания в плазме антигенсвязывающей молекулы. В результате авторы настоящего изобретения сфокусировались на различиях в концентрациях кальция между плазмой и ранней эндосомой, а затем открыли, что: захват антигена в клетки с помощью антигенсвязывающих молекул может быть ускорен с использованием антигенсвязывающих молекул, которые обладают зависимой от кальция реактивностью антиген-антитело; количество раз связывания антигена одной антигенсвязывающей молекулой может быть увеличено путем многократного связывания антигена антигенсвязывающей молекулой; снижение концентрации антигена в плазме может быть ускорено путем введения антигенсвязывающих молекул; и удержание в плазме антигенсвязывающей молекулы может быть увеличено.
В частности, настоящее изобретение относится к способам ускорения захвата антигена в клетки с использованием антигенсвязывающих молекул, которые обладают зависимой от кальция реактивностью антиген-антитело, способам увеличения количества раз связывания антигена одной антигенсвязывающей молекулой, способам ускорения снижения концентрации антигена в плазме путем введения антигенсвязывающих молекул, и способам повышения удержания в плазме антигенсвязывающих молекул, а также к антигенсвязывающим молекулам, которые обеспечивают усиленный захват антигена в клетки, антигенсвязывающим молекулам с увеличенным количеством раз связывания антигена, к антигенсвязывающим молекулам, которые могут ускорять снижение концентрации антигена в плазме при введении, антигенсвязывающим молекулам с увеличенным удержанием в плазме, фармацевтическим композициям, содержащим описанные выше антигенсвязывающие молекулы, и способам их получения. Более конкретно, настоящее изобретение относится к следующему:
[1] антигенсвязывающая молекула, содержащая антигенсвязывающий домен и домен, связывающий FcRn человека, активность связывания антигена которой отличается в условиях двух различных концентраций кальция и является более низкой в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция, и которая обладает активностью связывания с FcRn человека в условиях нейтрального значения pH;
[2] антигенсвязывающая молекула согласно [1], где низкая концентрация кальция представляет собой концентрацию ионизированного кальция от 0,1 до 30 мкМ;
[3] антигенсвязывающая молекула согласно [1], где высокая концентрация кальция представляет собой концентрацию ионизированного кальция от 100 мкМ до 10 мМ;
[4] антигенсвязывающая молекула согласно [1] или [2], где низкая концентрация кальция представляет собой внутриэндосомальную концентрацию ионизированного кальция;
[5] антигенсвязывающая молекула согласно [1] или [3], где высокая концентрация кальция представляет собой концентрацию ионизированного кальция в плазме;
[6] антигенсвязывающая молекула согласно любому из [1]-[5], где FcRn-связывающий домен представляет собой Fc-область;
[7] антигенсвязывающая молекула согласно любому из [1]-[6], где, дополнительно, антигенсвязывающая активность является более низкой в условиях кислого значения pH, чем в условиях нейтрального значения pH;
[8] антигенсвязывающая молекула согласно [7], где по меньшей мере одна аминокислота заменена гистидином или по меньшей мере один гистидин встроен в антигенсвязывающую молекулу;
[9] антигенсвязывающая молекула согласно любому из [1]-[8], которая связывается с мембранным антигеном или растворимым антигеном;
[10] антигенсвязывающая молекула согласно любому из [1]-[9], где антиген представляет собой антиген, выбранный из группы, состоящей из IL-6R, IL-6, IgA, глипикана 3 человека и IgE;
[11] антигенсвязывающая молекула, содержащая антигенсвязывающий домен и FcRn-связывающий домен человека, активность связывания антигена которой отличается в двух различных условиях концентрации кальция и является более низкой в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция, и где легкая цепь или тяжелая цепь антигенсвязывающего домена содержит кальций-связывающий мотив, происходящий из антитела человека;
[12] антигенсвязывающая молекула согласно [11], где кальций-связывающий мотив содержится в CDR1, CDR2 и/или CDR3 легкой цепи антигенсвязывающего домена;
[13] антигенсвязывающая молекула согласно [12], где кальций-связывающий мотив содержится в положениях 30, 31 и/или 32 в соответствии с нумерацией по Kabat в CDR1 легкой цепи;
[14] антигенсвязывающая молекула согласно [12] или [13], где кальций-связывающий мотив содержится в положении 50 в соответствии с нумерацией по Kabat в CDR2 легкой цепи;
[15] антигенсвязывающая молекула согласно любому из [12]-[14], где кальций-связывающий мотив содержится в положении 92 в соответствии с нумерацией по Kabat в CDR3 легкой цепи;
[16] антигенсвязывающая молекула согласно любому из [12]-[15], которая представляет собой либо IgA, либо глипикан 3 человека;
[17] антигенсвязывающая молекула согласно [11], где кальций-связывающий мотив содержится в CDR1, CDR2 и/или CDR3 тяжелой цепи антигенсвязывающего домена;
[18] антигенсвязывающая молекула согласно [16], где кальций-связывающий мотив содержится в положениях 95, 96, 100a и/или 101 в соответствии с нумерацией по Kabat в CDR3 тяжелой цепи;
[19] антигенсвязывающая молекула согласно [17] или [18], которая представляет собой либо IL-6R, либо IL-6;
[20] антигенсвязывающая молекула согласно любому из [11]-[19], которая содержит FcRn-связывающий домен, который обладает активностью связывания FcRn при нейтральном диапазоне значений pH;
[21] антигенсвязывающая молекула согласно [20], где FcRn-связывающий домен представляет собой Fc-область;
[22] антигенсвязывающая молекула согласно любому из [1]-[10], [20] или [21], где одна или несколько аминокислот в положениях 248, 250, 252, 254, 255, 256, 257, 258, 265, 286, 289, 297, 303, 305, 307, 308, 309, 311, 312, 314, 315, 317, 332, 334, 360, 376, 380, 382, 384, 385, 386, 387, 389, 424, 428, 433, 434 и 436 (нумерация EU) в аминокислотной последовательности Fc-области отличаются от аминокислот в природной Fc-области;
[23] антигенсвязывающая молекула согласно [22], которая содержит любую или комбинацию из:
Met в положении аминокислоты 237;
Ile в положении аминокислоты 248;
Ala, Phe, Ile, Met, Gln, Ser, Val, Trp или Tyr в положении аминокислоты 250;
Phe, Trp или Tyr в положении аминокислоты 252;
Thr в положении аминокислоты 254;
Glu в положении аминокислоты 255;
Asp, Glu или Gln в положении аминокислоты 256;
Ala, Gly, Ile, Leu, Met, Asn, Ser, Thr или Val в положении аминокислоты 257;
His в положении аминокислоты 258;
Ala в положении аминокислоты 265;
Ala или Glu в положении аминокислоты 286;
His в положении аминокислоты 289;
Ala в положении аминокислоты 297;
Ala в положении аминокислоты 303;
Ala в положении аминокислоты 305;
Ala, Asp, Phe, Gly, His, Ile, Lys, Leu, Met, Asn, Pro, Gln, Arg, Ser, Val, Trp или Tyr в положении аминокислоты 307;
Ala, Phe, Ile, Leu, Met, Pro, Gln или Thr в положении аминокислоты 308;
Ala, Asp, Glu, Pro или Arg в положении аминокислоты 309;
Ala, His или Ile в положении аминокислоты 311;
Ala или His в положении аминокислоты 312;
Lys или Arg в положении аминокислоты 314;
Ala, Asp или His в положении аминокислоты 315;
Ala в положении аминокислоты 317;
Val в положении аминокислоты 332;
Leu в положении аминокислоты 334;
His в положении аминокислоты 360;
Ala в положении аминокислоты 376;
Ala в положении аминокислоты 380;
Ala в положении аминокислоты 382;
Ala в положении аминокислоты 384;
Asp или His в положении аминокислоты 385;
Pro в положении аминокислоты 386;
Glu в положении аминокислоты 387;
Ala или Ser в положении аминокислоты 389;
Ala в положении аминокислоты 424;
Ala, Asp, Phe, Gly, His, Ile, Lys, Leu, Asn, Pro, Gln, Ser, Thr, Val, Trp или Tyr в положении аминокислоты 428;
Lys в положении аминокислоты 433;
Ala, Phe, His, Ser, Trp или Tyr в положении аминокислоты 434; или
His, Ile, Leu или Val в положении аминокислоты 436;
в соответствии с нумерацией EU в Fc-области;
[24] антигенсвязывающая молекула согласно любому из [1]-[23], где антигенсвязывающая молекула представляет собой антитело;
[25] Способ получения антигенсвязывающей молекулы, имеющей по меньшей мере одну функцию, выбранную из следующего:
(i) функция ускорения захвата антигена в клетки,
(ii) функция связывания антигена два или более раз,
(iii) функция ускорения снижения концентрации антигена в плазме, и
(iv) функция улучшения удержания в плазме,
где способ включает стадии (a)-(e), указанные ниже:
(a) определение антигенсвязывающей активности антигенсвязывающей молекулы в условиях низкой концентрации кальция;
(b) определение антигенсвязывающей активности антигенсвязывающей молекулы в условиях высокой концентрации кальция;
(c) отбор антигенсвязывающей молекулы, которая имеет более низкую антигенсвязывающую активность в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция;
(d) получение гена, кодирующего антигенсвязывающую молекулу, отобранную на стадии (c); и
(e) продуцирование антигенсвязывающей молекулы с использованием гена, полученного на стадии (d);
[26] способ получения антигенсвязывающей молекулы, имеющей по меньшей мере одну функцию, выбранную из следующего:
(i) функция ускорения захвата антигена в клетки,
(ii) функция связывания антигена два или более раз,
(iii) функция ускорения снижения концентрации антигена в плазме, и
(iv) функция улучшения удержания в плазме,
где способ включает стадии (a)-(e), указанные ниже:
(a) приведение антигена в контакт с антигенсвязывающей молекулой или библиотекой антигенсвязывающих молекул в условиях высокой концентрации кальция;
(b) помещение антигенсвязывающей молекулы, которая связывает антиген на стадии (a), в условия низкой концентрации кальция;
(c) получение антигенсвязывающей молекулы, которая диссоциирует на стадии (b);
(d) получение гена, кодирующего антигенсвязывающую молекулу, полученную на стадии (c); и
(e) получение антигенсвязывающей молекулы с использованием гена, полученного на стадии (d);
[27] способ получения антигенсвязывающей молекулы, имеющей по меньшей мере одну функцию, выбранную из следующего:
(i) функция ускорения захвата антигена в клетки,
(ii) функция связывания антигена два или более раз,
(iii) функция ускорения снижения концентрации антигена в плазме, и
(iv) функция улучшения удержания в плазме,
где способ включает стадии (a)-(f), указанные ниже:
(a) приведение антигена в контакт с антигенсвязывающей молекулой или библиотекой антигенсвязывающих молекул в условиях низкой концентрации кальция;
(b) отбор антигенсвязывающей молекулы, которая не связывается с антигеном на стадии (a);
(c) обеспечение связывания антигенсвязывающей молекулы, отобранной на стадии (b), с антигеном в условиях высокой концентрации кальция;
(d) получение антигенсвязывающей молекулы, которая связалась с антигеном на стадии (c);
(e) получение гена, кодирующего антигенсвязывающую молекулу, полученную на стадии (d); и
(f) продуцирование антигенсвязывающей молекулы с использованием гена, полученного на стадии (e);
[28] способ получения по любому из [25]-[27], который дополнительно включает стадию обеспечения или увеличения активности связывания FcRn человека в условиях нейтрального значения pH путем модификации аминокислоты в антигенсвязывающей молекуле;
[29] способ получения согласно любому из [25]-[27], который дополнительно включает стадию снижения активности связывания в условиях кислого значения pH, чтобы она была более низкой, чем в условиях нейтрального значения pH, путем модификации аминокислоты в антигенсвязывающей молекуле;
[30] способ получения согласно любому из [25]-[27], где низкая концентрация кальция представляет собой концентрацию ионизированного кальция от 0,1 до 30 мкМ;
[31] способ получения согласно любому из [25]-[27], где высокая концентрация кальция представляет собой концентрацию ионизированного кальция от 100 мкМ до 10 мМ;
[32] способ получения согласно любому из [25]-[27], где низкая концентрация кальция представляет собой внутриэндосомальную концентрацию ионизированного кальция;
[33] способ получения согласно любому из [25]-[27], где высокая концентрация кальция представляет собой концентрацию ионизированного кальция в плазме;
[34] способ получения согласно [29], где модификация аминокислоты в антигенсвязывающей молекуле представляет собой модификацию путем замены по меньшей мере одной аминокислоты гистидином или встраивания по меньшей мере одного гистидина в антигенсвязывающую молекулу;
[35] способ получения согласно любому из [25]-[34], где антиген, связываемый антигенсвязывающей молекулой, представляет собой антиген, выбранный из группы, состоящей из IL-6R, IL-6, IgA, глипикана 3 человека и IgE;
[36] способ получения согласно любому из [25]-[35], где антигенсвязывающая молекула представляет собой антитело;
[37] фармацевтическая композиция, содержащая:
антигенсвязывающую молекулу согласно любому из [1]-[24] или антигенсвязывающую молекулу, полученную способом получения согласно любому из [25]-[36], и фармацевтически приемлемый носитель;
[38] фармацевтическая композиция согласно [37] для применения для ускорения интернализации антигена в клетки;
[39] фармацевтическая композиция согласно [37] для применения для ускорения снижения концентрации антигена в плазме;
[40] фармацевтическая композиция для применения для ускорения захвата антигена в клетки или снижения концентрации антигена в плазме, которая содержит антигенсвязывающую молекулу, содержащую антигенсвязывающий домен и FcRn-связывающий домен человека, активность связывания антигена которой отличается при двух различных концентрациях кальция и является более низкой в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция;
[41] фармацевтическая композиция согласно [40], где низкая концентрация кальция представляет собой концентрацию ионизированного кальция от 0,1 до 30 мкМ;
[42] фармацевтическая композиция согласно [40], где высокая концентрация кальция представляет собой концентрацию ионизированного кальция от 100 мкМ до 10 мМ;
[43] фармацевтическая композиция согласно [40] или [41], где низкая концентрация кальция представляет собой внутриэндосомальную концентрацию ионизированного кальция;
[44] фармацевтическая композиция согласно [40] или [42], где высокая концентрация кальция представляет собой концентрацию ионизированного кальция в плазме;
[45] фармацевтическая композиция согласно любому из [40]-[44], где FcRn-связывающий домен, содержащийся в антигенсвязывающей молекуле, представляет собой Fc-область;
[46] фармацевтическая композиция согласно любому из [40]- [45], где антигенсвязывающая активность антигенсвязывающей молекулы является более низкой в условиях кислого значения pH, чем в условиях нейтрального значения pH;
[47] фармацевтическая композиция согласно [46], где модификация аминокислоты в антигенсвязывающей молекуле представляет собой модификацию путем замены по меньшей мере одной аминокислоты гистидином или встраивания по меньшей мере одного гистидина в антигенсвязывающую молекулу;
[48] фармацевтическая композиция согласно любому из [40]-[47], где антиген, с которым связывается антигенсвязывающая молекула, представляет собой антиген, выбранный из группы, состоящей из IL-6R, IL-6, IgA, глипикана 3 человека и IgE;
[49] Способ скрининга антигенсвязывающей молекулы, которая имеет по меньшей мере одну функцию, выбранную из следующего:
(i) функция ускорения захвата антигена в клетки,
(ii) функция связывания антигена два или более раз,
(iii) функция ускорения снижения концентрации антигена в плазме, и
(iv) функция улучшения удержания в плазме,
где способ включает стадии (a)-(c), указанные ниже:
(a) определение антигенсвязывающей активности антигенсвязывающей молекулы в условиях низкой концентрации кальция;
(b) определение антигенсвязывающей активности антигенсвязывающей молекулы в условиях высокой концентрации кальция; и
(c) отбор антигенсвязывающей молекулы, антигенсвязывающая активность которой является более низкой в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция;
[50] способ скрининга антигенсвязывающей молекулы, которая имеет по меньшей мере одну функцию, выбранную из следующего:
(i) функция ускорения захвата антигена в клетки,
(ii) функция связывания антигена два или более раз,
(iii) функция ускорения снижения концентрации антигена в плазме, и
(iv) функция улучшения удержания в плазме,
где способ включает стадии (a)-(c), указанные ниже:
(a) приведение антигена в контакт с антигенсвязывающей молекулой или библиотекой антигенсвязывающих молекул в условиях высокой концентрации кальция;
(b) помещение антигенсвязывающей молекулы, которая связывает антиген на стадии (a) в условия низкой концентрации кальция; и
(c) получение антигенсвязывающей молекулы, которая диссоциирует на стадии (b);
[51] способ скрининга антигенсвязывающей молекулы, которая имеет по меньшей мере одну функцию, выбранную из следующего:
(i) функция ускорения захвата антигена в клетки,
(ii) функция связывания антигена два или более раз,
(iii) функция ускорения снижения концентрации антигена в плазме, и
(iv) функция улучшения удержания в плазме,
где способ включает стадии (a)-(d), указанные ниже:
(a) приведение антигена в контакт с антигенсвязывающей молекулой или библиотекой антигенсвязывающих молекул в условиях низкой концентрации кальция;
(b) отбор антигенсвязывающей молекулы, которая не связывает антиген на стадии (a);
(c) обеспечение связывания антигенсвязывающей молекулы, отобранной на стадии (b), с антигеном в условиях высокой концентрации кальция; и
(d) получение антигенсвязывающей молекулы, связавшейся с антигеном на стадии (c);
[52] способ скрининга согласно любому из [49]-[51], где низкая концентрация кальция представляет собой концентрацию ионизированного кальция от 0,1 до 30 мкМ;
[53] способ скрининга согласно любому из [49]-[51], где высокая концентрация кальция представляет собой концентрацию ионизированного кальция от 100 мкМ до 10 мМ;
[54] способ скрининга согласно любому из [49]-[52], где низкая концентрация кальция представляет собой внутриэндосомальную концентрацию ионизированного кальция;
[55] способ скрининга согласно любому из [49]-[51] или [53], где высокая концентрация кальция представляет собой концентрацию ионизированного кальция в плазме;
[56] способ скрининга согласно любому из [49]-[55], где антиген, с которым связывается антигенсвязывающая молекула, представляет собой антиген, выбранный из группы, состоящей из IL-6R, IL-6, IgA, глипикана 3 человека и IgE;
[57] способ скрининга согласно любому из [49]-[56], где антигенсвязывающая молекула представляет собой антитело;
[58] способ ускорения антигенсвязывающей молекулой захвата антигена в клетку путем введения антигенсвязывающей молекулы согласно любому из [1]-[24] или антигенсвязывающей молекулы, полученной способом получения согласно любому из [25]-[36];
[59] способ ускорения снижения концентрации антигена в плазме путем введения антигенсвязывающей молекулы согласно любому из [1]-[24] или антигенсвязывающей молекулы, полученной способом получения согласно любому из [25]-[36];
[60] способ увеличения количества раз связывания антигена одной антигенсвязывающей молекулой с использованием антигенсвязывающей молекулы согласно любому из [1]-[24] или антигенсвязывающей молекулы, полученной способом получения согласно любому из [25]-[36];
[61] способ увеличения удержания в плазме антигенсвязывающей молекулы с использованием антигенсвязывающей молекулы согласно любому из [1]-[24] или антигенсвязывающей молекулы, полученной способом получения согласно любому из [25]-[36];
[62] способ ускорения захвата антигена в клетку антигенсвязывающей молекулой путем введения антигенсвязывающей молекулы, содержащей антигенсвязывающий домен и FcRn-связывающий домен человека, антигенсвязывающая активность которой отличается при двух различных концентрациях кальция и является более низкой в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция;
[63] способ ускорения снижения концентрации антигена в плазме путем введения антигенсвязывающей молекулы, содержащей антигенсвязывающий домен и FcRn-связывающий домен человека, антигенсвязывающая активность которой отличается при двух различных концентрациях кальция и является более низкой в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция;
[64] способ увеличения количества раз связывания антигена одной антигенсвязывающей молекулой с использованием антигенсвязывающей молекулы, содержащей антигенсвязывающий домен и FcRn-связывающий домен человека, антигенсвязывающая активность которой отличается при двух различных концентрациях кальция и является более низкой в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция;
[65] способ увеличения удержания в плазме антигенсвязывающей молекулы с использованием антигенсвязывающей молекулы, содержащей антигенсвязывающий домен и FcRn-связывающий домен человека, антигенсвязывающая активность которой отличается при двух различных концентрациях кальция и является более низкой в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция;
[66] способ согласно любому из [62]-[65], где низкая концентрация кальция представляет собой концентрацию ионизированного кальция от 0,1 до 30 мкМ;
[67] способ согласно любому из [62]-[66], где высокая концентрация кальция представляет собой концентрацию ионизированного кальция от 100 мкМ до 10 мМ;
[68] способ согласно любому из [62]-[67], где низкая концентрация кальция представляет собой внутриэндосомальную концентрацию ионизированного кальция;
[69] способ согласно любому из [62]-[68], где высокая концентрация кальция представляет собой плазменную концентрацию ионизированного кальция;
[70] способ согласно любому из [62]-[69], где FcRn-связывающий домен антигенсвязывающей молекулы представляет собой Fc-область;
[71] способ согласно любому из [62]-[70], где, дополнительно, антигенсвязывающая активность антигенсвязывающей молекулы является более низкой в условиях кислого значения pH, чем в условиях нейтрального значения pH;
[72] способ согласно [71], где модификация аминокислот в антигенсвязывающей молекуле представляет собой модификацию путем замены по меньшей мере одной аминокислоты гистидином или встраивания по меньшей мере одного гистидина в антигенсвязывающую молекулу;
[73] способ согласно любому из [62]-[72], где антиген, с которым связывается антигенсвязывающая молекула, представляет собой антиген, выбранный из группы, состоящей из IL-6R, IL-6, IgA, глипикана 3 человека и IgE; и
[74] способ согласно любому из [62]-[73], где антигенсвязывающая молекула представляет собой антитело.
Более того, настоящее изобретение относится к наборам для применения в способах по настоящему изобретению, которые включают антигенсвязывающую молекулу по настоящему изобретению или антигенсвязывающую молекулу, полученную способами получения по настоящему изобретению. Настоящее изобретение также относится к средствам для ускорения антигенсвязывающей молекулой захвата антигена в клетки, средствам для ускорения снижения концентрации антигена в плазме, средствам для увеличения количества раз связывания антигена одной антигенсвязывающей молекулой и средствам для повышения удержания антигенсвязывающей молекулы в плазме, все из которых содержат в качестве активного ингредиента антигенсвязывающую молекулу по настоящему изобретению или антигенсвязывающую молекулу, полученную способом по настоящему изобретению. Более того, настоящее изобретение относится к применению антигенсвязывающей молекулы по настоящему изобретению или антигенсвязывающей молекулы, полученной способами получения по настоящему изобретению, для получения средств для ускорения антигенсвязывающей молекулой захвата антигена в клетки, средств для ускорения снижения концентрации антигена в плазме, средств для увеличения количества раз связывания антигена антигенсвязывающей молекулой или средств для увеличения удержания антигенсвязывающей молекулы в плазме. Настоящее изобретение также относится к антигенсвязывающим молекулам по настоящему изобретению или антигенсвязывающим молекулам, полученным способами получения по настоящему изобретению, для применения в способах по настоящему изобретению.
[Эффекты изобретения]
Настоящее изобретение относится к способам ускорения антигенсвязывающими молекулами захвата антигена в клетки, способам увеличения количества раз связывания антигена одной антигенсвязывающей молекулой, способам ускорения снижения концентрации антигена в плазме путем введения антигенсвязывающих молекул и способам увеличения удержания антигенсвязывающей молекулы в плазме. Ускорение захвата антигена в клетки антигенсвязывающими молекулами обеспечивает ускорение снижения концентрации антигена в плазме при введении антигенсвязывающих молекул, а также увеличение удержания в плазме антигенсвязывающей молекулы. Это может увеличить количество раз связывания антигена одной антигенсвязывающей молекулой. Таким образом, такие антигенсвязывающие молекулы могут обеспечивать превосходящие эффекты in vivo по сравнению с типичными антигенсвязывающими молекулами.
[Краткое описание чертежей]
На фиг.1 представлена диаграмма, на которой показано, что антитело с pH-зависимым связыванием многократно связывается с растворимыми антигенами. (i) антитело связывается с растворимыми антигенами; (ii) антитело неспецифически интернализуется в клетку путем пиноцитоза; (iii) антитело связывается с FcRn в эндосомах, а затем растворимые антигены диссоциируют от антитела; (iv) растворимые антигены переносятся в лизосомы и деградируются; (v) после диссоциации от растворимых антигенов антитело рециклирует в плазму через FcRn; (vi) рециклированное антитело может вновь связываться с растворимыми антигенами.
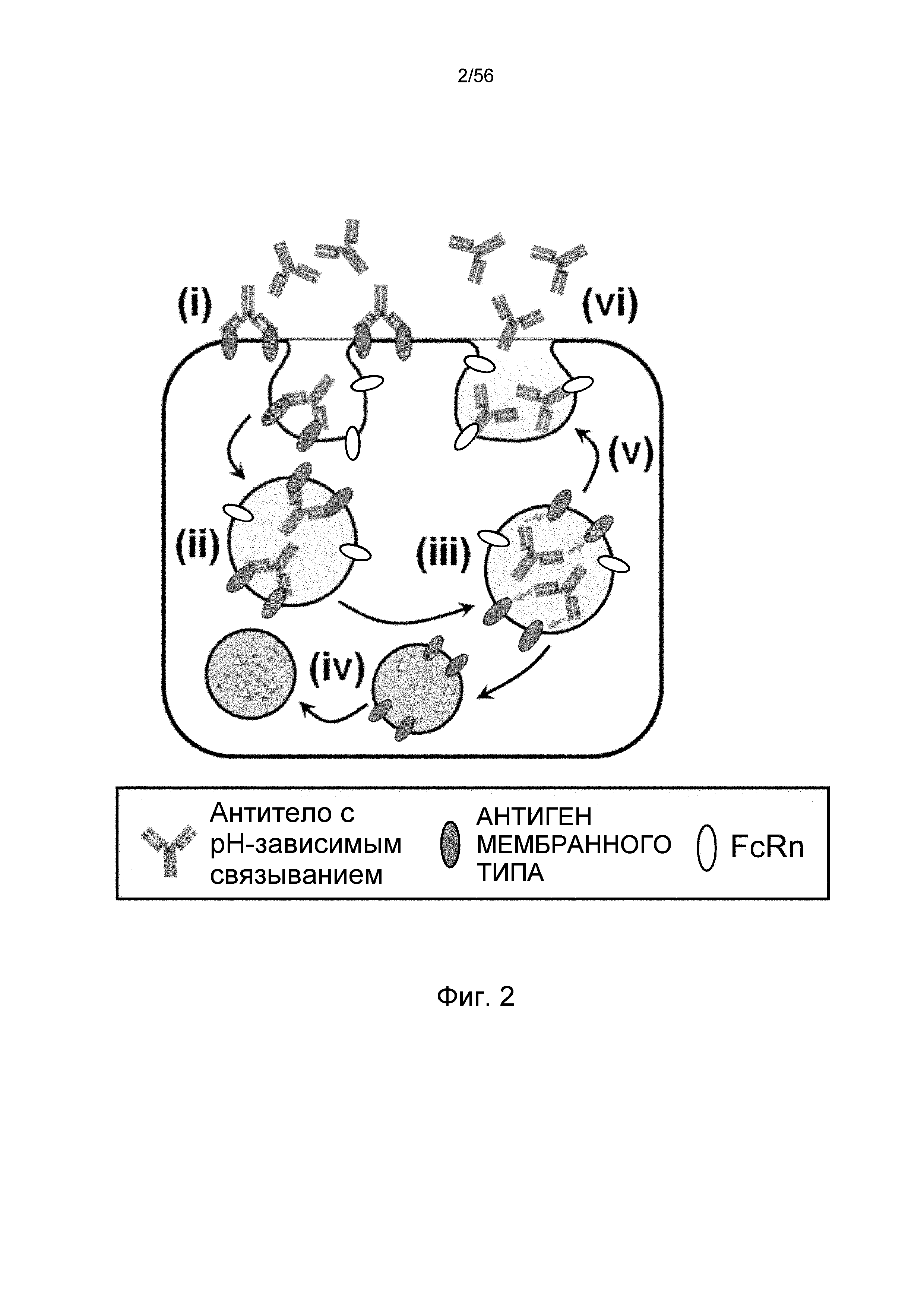
На фиг.2 представлена диаграмма, на которой показано, что антитело с pH-зависимым связыванием многократно связывается с мембранными антигенами. (i) Антитело связывается с мембранными антигенами; (ii) антитело интернализуется в клетку в комплексе с мембранными антигенами; (iii) антитело диссоциирует от мембранных антигенов в эндосоме; (iv) мембранные антигены переносятся в лизосому и деградируются; (v) после диссоциации от мембранных антигенов антитело рециклирует в плазму; (vi) рециклированное антитело может вновь связываться с мембранными антигенами.
На фиг.3 представлена диаграмма, на которой показаны способы взаимодействия в плазме (pH 7,4) и эндосоме (pH 6,0) антигена и антитела с pH-зависимым связыванием.
На фиг.4 представлена диаграмма, на которой показаны способы взаимодействия в плазме (Ca2+ 2 мМ) и эндосоме (Ca2+ 3 мкМ) антигена и антитела с кальций-зависимым связыванием.
На фиг.5 представлена диаграмма, на которой показаны способы взаимодействия в плазме (pH 7,4, Ca2+ 2 мМ) и эндосоме (pH 6,0, Ca2+ 3 мкМ) антигена и антитела с pH- и кальций-зависимым связыванием.
На фиг.6 представлены сенсограммы Biacore, на которых показано взаимодействие антител против рецептора IL-6 человека с растворимым рецептором IL-6 человека в условиях (Ca2+ 2 мМ) и (Ca2+ 3 мкМ).
На фиг.7 представлена сенсограмма Biacore, на которой показано взаимодействие H54/L28-IgG1 с растворимым рецептором IL-6 человека в условиях (Ca2+ 2 мМ) и (Ca2+ 3 мкМ).
На фиг.8 представлена сенсограмма Biacore, на которой показано взаимодействие FH4-IgG1 с растворимым рецептором IL-6 человека в условиях (Ca2+ 2 мМ) и (Ca2+ 3 мкМ).
На фиг.9 представлена сенсограмма Biacore, на которой показано взаимодействие 6RL#9-IgG1 с растворимым рецептором IL-6 человека в условиях (Ca2+ 2 мМ) и (Ca2+ 3 мкМ).
На фиг.10 представлена концентрация антитела в плазме с течением времени у мышей, которым вводили H54/L28-IgG1, FH4-IgG1 или 6RL#9-IgG1.
На фиг.11 представлен уровень в плазме растворимого рецептора IL-6 человека (hsIL-6R) с течением времени у нормальных мышей, которым вводили H54/L28-IgG1, FH4-IgG1 или 6RL#9-IgG1.
На фиг.12 представлена концентрация антитела в плазме с течением времени у нормальных мышей, которым вводили H54/L28-N434W, FH4-N434W или 6RL#9-N434W.
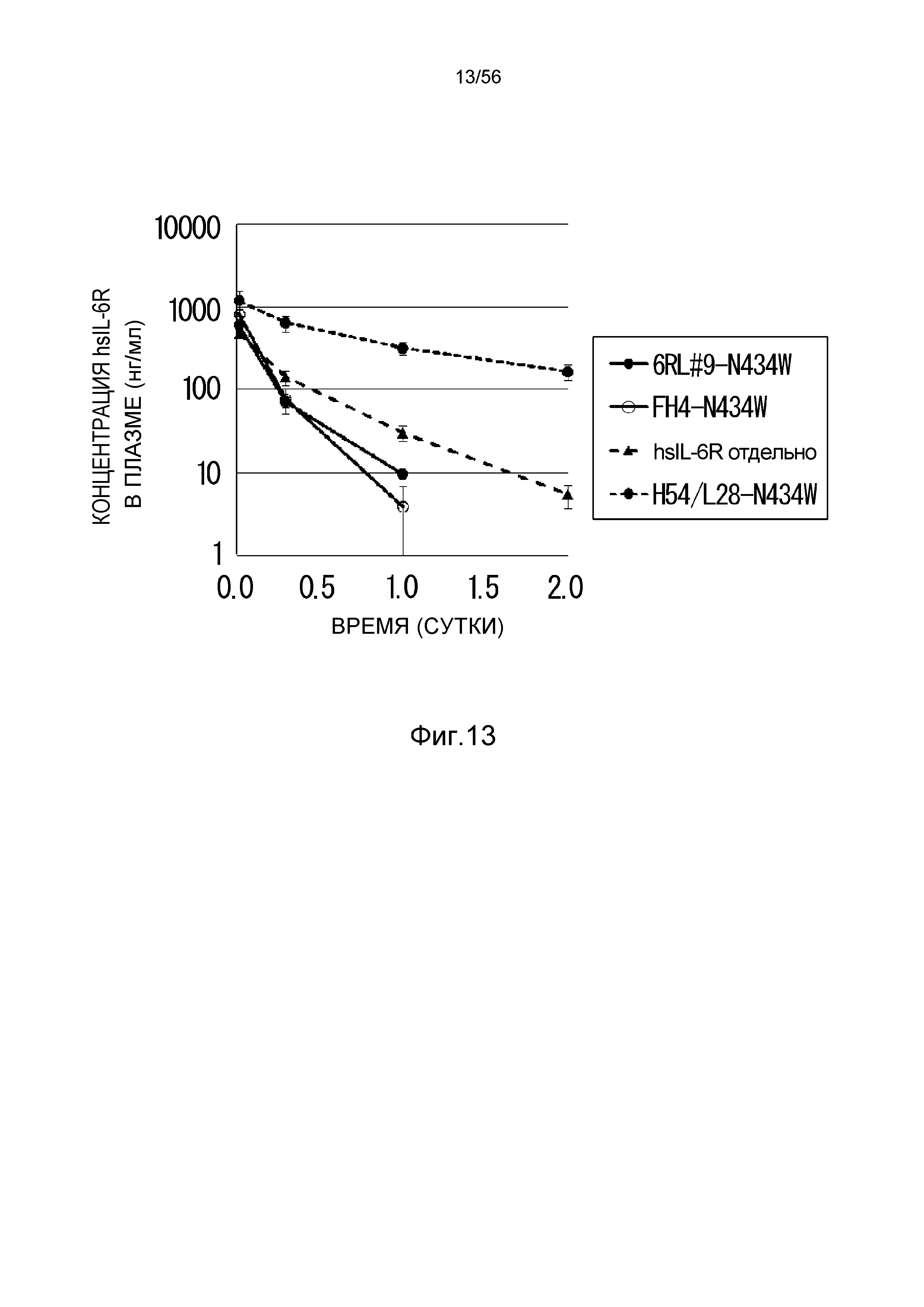
На фиг.13 представлен уровень в плазме растворимого рецептора IL-6 человека (hsIL-6R) с течением времени у нормальных мышей, которым вводили H54/L28-N434W, FH4-N434W или 6RL#9-N434W.
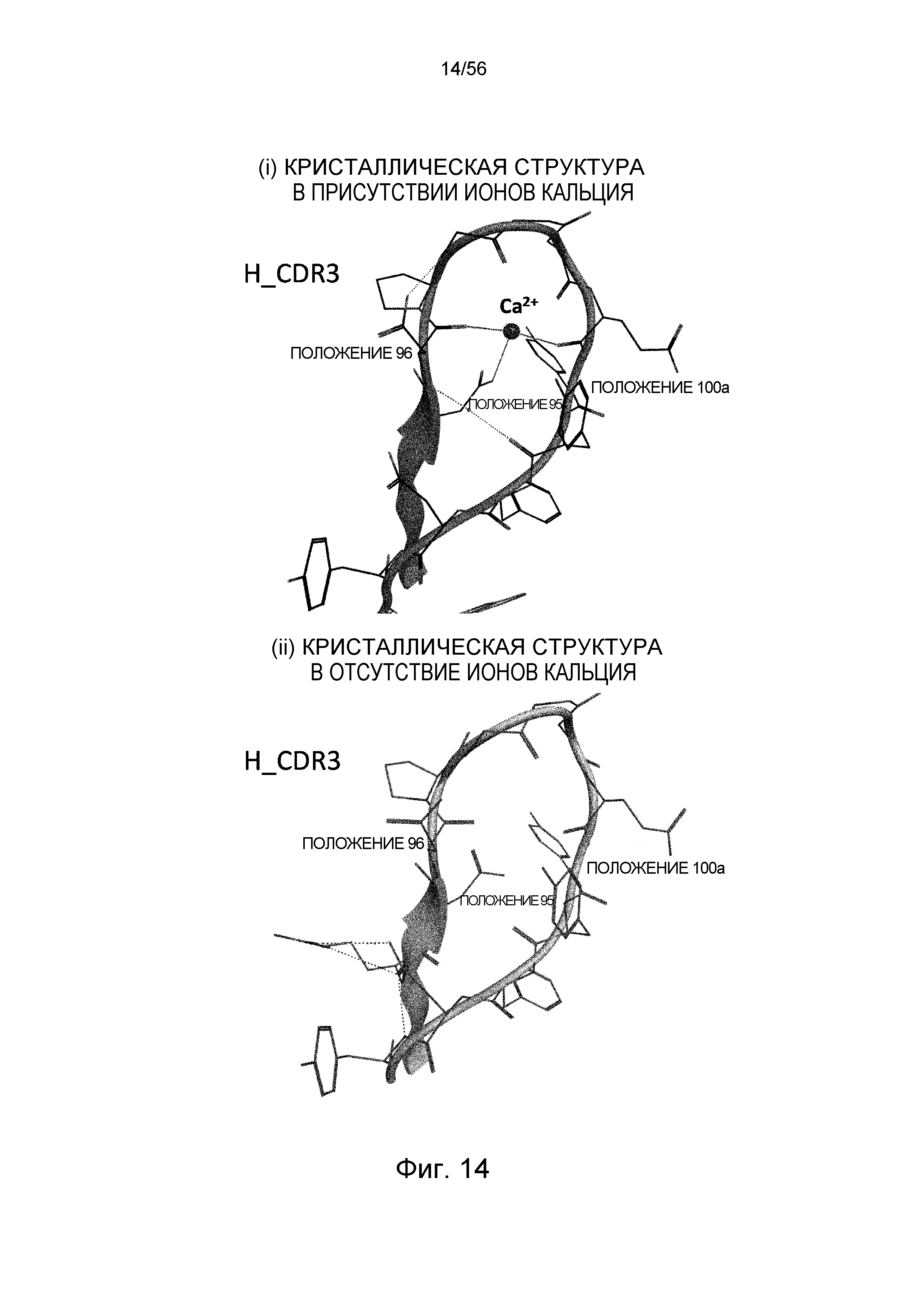
На фиг.14 представлена структура CDR3 тяжелой цепи Fab-фрагмента из антитела 6RL#9, определенная рентгеновской кристаллографией.
На фиг.15 представлены сенсограммы Biacore, на которых показано взаимодействие антител против IL-6 человека с IL-6 человека в условиях (Ca2+ 1,2 мМ) и (Ca2+ 3 мкМ).
На фиг.16 представлены ионообменные хроматограммы для антитела, имеющего последовательность человека Vk5-2, и антитела, имеющего последовательность h Vk5-2_L65, которая имеет модифицированную последовательность гликозилирования в последовательности человека Vk5-2. Сплошная линия указывает на хроматограмму для антитела, имеющего последовательность человека Vk5-2 (тяжелая цепь: CIM_H, SEQ ID NO: 48; легкая цепь: hVk5-2, слитая молекула между SEQ ID NO: 41 и 28); пунктирная линия указывает на хроматограмму для антитела, имеющую последовательность hVk5-2_L65 (тяжелая цепь: CIM_H (SEQ ID NO: 48); легкая цепь: hVk5-2_L65 (SEQ ID NO: 47)).
На фиг.17 показаны ионообменные хроматограммы для антитела, имеющего последовательность LfVk1_Ca (тяжелая цепь: GC_H, SEQ ID NO: 102; легкая цепь: LfVk1_Ca, SEQ ID NO: 61), и антитела, имеющего последовательность, в которой Asp (D) в последовательности LfVk1_Ca заменен на Ala (A), после хранения при 5°C (сплошная линия) или 50°C (пунктирная линия). После хранения при 5°C наиболее высокий пик в хроматограмме для каждого антитела определен как главный пик, и ось y каждой ионообменной хроматограммы нормализовали по главному пику.
На фиг.18 представлены ионообменные хроматограммы для антитела, имеющего последовательность LfVk1_Ca (тяжелая цепь: GC_H, SEQ ID NO: 102; легкая цепь: LfVk1_Ca, SEQ ID NO: 61), и антитела, имеющего последовательность LfVk1_Ca6 (тяжелая цепь: GC_H, SEQ ID NO: 102; легкая цепь: LfVk1_Ca6, SEQ ID NO: 75), в котором Asp (D) в положении 30 (система нумерации по Kabat) в последовательности LfVk1_Ca заменен на Ser (S), после хранения при 5°C (сплошная линия) или 50°C (пунктирная линия). После хранения при 5°C наиболее высокий пик в хроматограмме для каждого антитела определен как главный пик, и ось y каждой ионообменной хроматограммы нормализовали по главному пику.
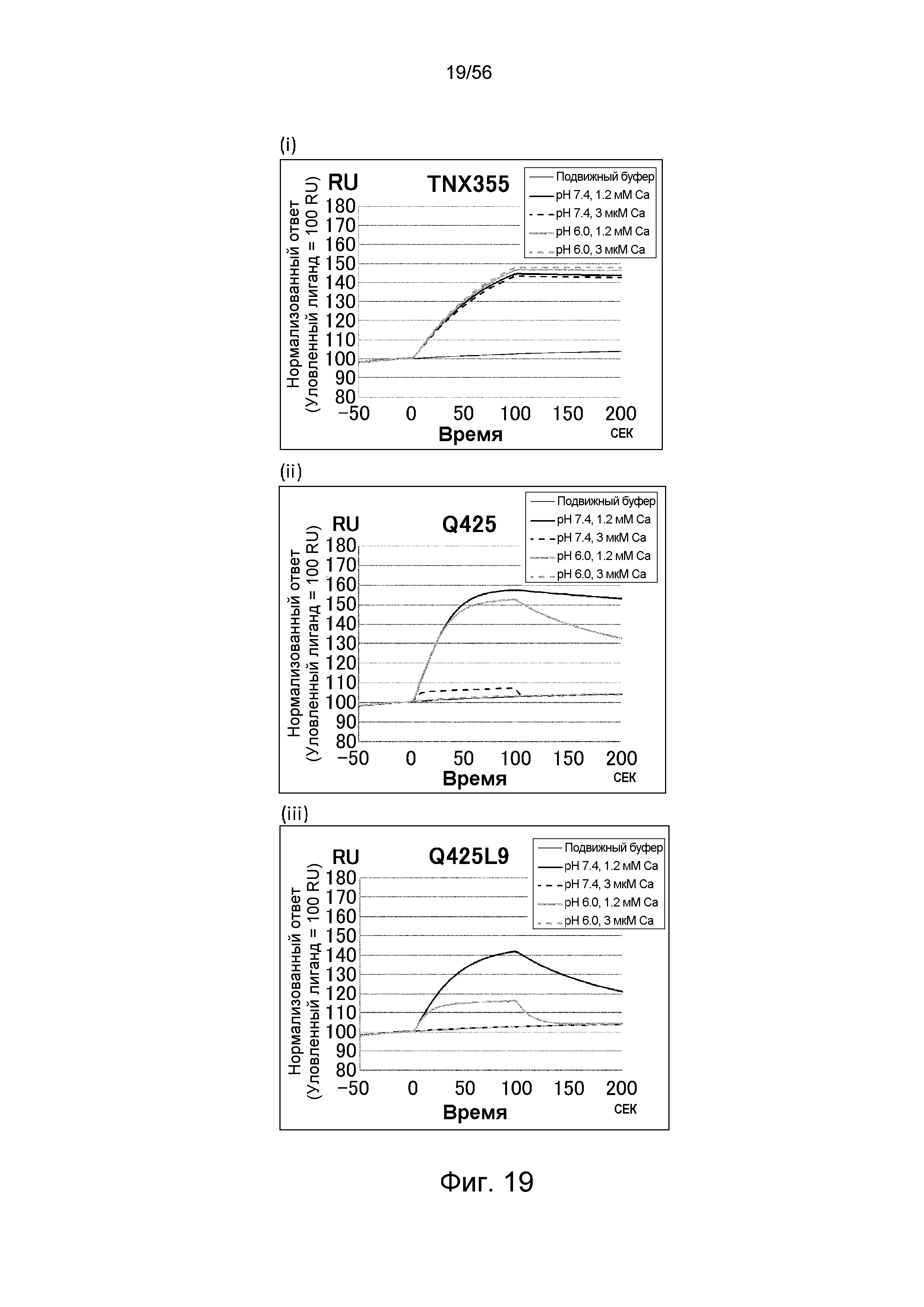
На фиг.19 представлены сенсограммы Biacore, на которых показано взаимодействие антител против CD4 человека с растворимым CD4 человека в условиях (Ca2+ 1,2 мМ) и (Ca2+ 3 мкМ).
На фиг.20 представлена концентрация в плазме антител против CD4 человека с течением времени у нормальных мышей.
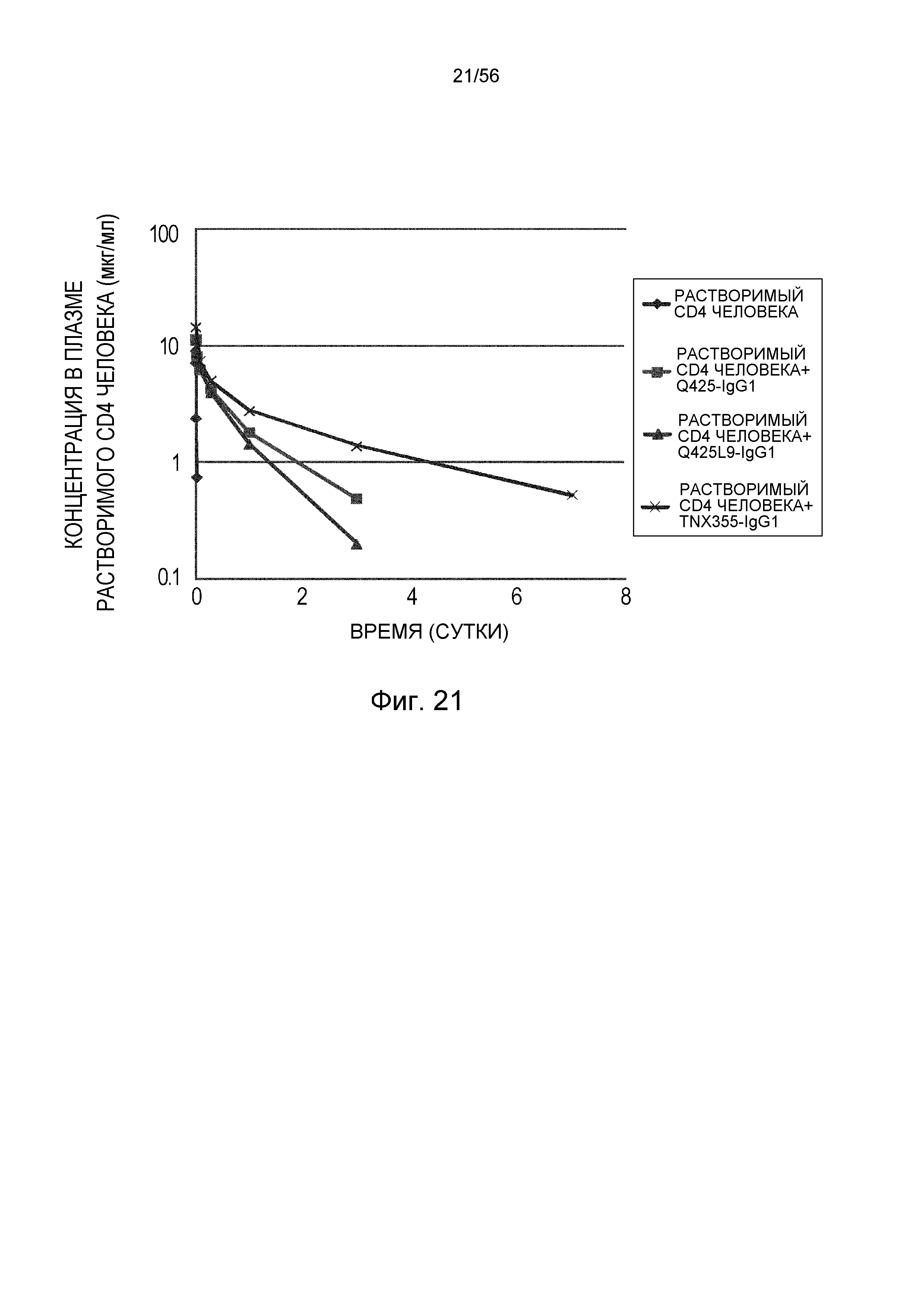
На фиг.21 описана концентрация в плазме растворимого CD4 человека с течением времени у нормальных мышей в группе, в которой вводили растворимый CD4 человека отдельно, в группе, в которой вводили антитело TNX355-IgG1, в группе, в которой вводили антитело Q425, и в группе, в которой вводили антитело Q425L9.
На фиг.22 представлены сенсограммы Biacore, на которых показано взаимодействие антител против IgA человека с IgA человека в условиях (Ca2+ 1,2 мМ) и (Ca2+ 3 мкМ).
На фиг.23 представлены концентрации антитела в плазме с течением времени у нормальных мышей для группы, в которой вводили антитело GA1-IgG1, группы, в которой вводили антитело GA2-IgG1, группы, в которой вводили антитело GA3-IgG1, и группы, в которой вводили GA2-N434W.
На фиг.24 представлена концентрация IgA человека в плазме с течением времени у нормальных для группы, в которой вводили IgA человека отдельно, группы, в которой вводили антитело GA1-IgG1, группы, в которой вводили GA2-IgG1, группы, в которой вводили антитело GA3-IgG1, и группы, в которой вводили антитело GA2-N434W.
На фиг.25 представлена концентрация в плазме несвязанного IgA человека с течением времени для группы, в которой вводили антитело GA1-IgG1, группы, в которой вводили антитело GA2-IgG1, группы, в которой вводили антитело GA3-IgG, и группы, в которой вводили антитело GA2-N434W.
На фиг.26 представлена иллюстративная диаграмма, на которой показана эффективность элиминации антигена на молекулу антитела для обычного антитела, которое образует большой иммунный комплекс с мультимерным антигеном.
На фиг.27 представлена иллюстративная диаграмма, на которой показана эффективность элиминации антигена на молекулу антитела для pH/Ca-зависимого антитела, имеющего константную область природного IgG1, которое формирует большой иммунный комплекс с мультимерным антигеном.
На фиг.28 представлена иллюстративная диаграмма, на которой показана эффективность элиминации антигена на молекулу антитела для pH/Ca-зависимого полиспецифического антитела, которое распознает два или более эпитопов в мономерном антигене и пригодно для образования большого иммунного комплекса.
На фиг.29 представлено взаимодействие антител против глипикана 3 с рекомбинантным глипиканом 3 человека в условиях (Ca2+ 1,2 мМ) и (Ca2+ 3 мкМ) в способе ELISA.
На фиг.30 представлено взаимодействие антител против IgE человека с рекомбинантным IgE человека в условиях (Ca2+ 2 мМ) и (Ca2+ 3 мкМ) в способе ELISA.
На фиг.31 представлены концентрации антитела в плазме с течением времени у трансгенных мышей с FcRn человека.
На фиг.32 представлена концентрация в плазме растворимого рецептора IL-6 человека с течением времени у трансгенных мышей с FcRn человека.
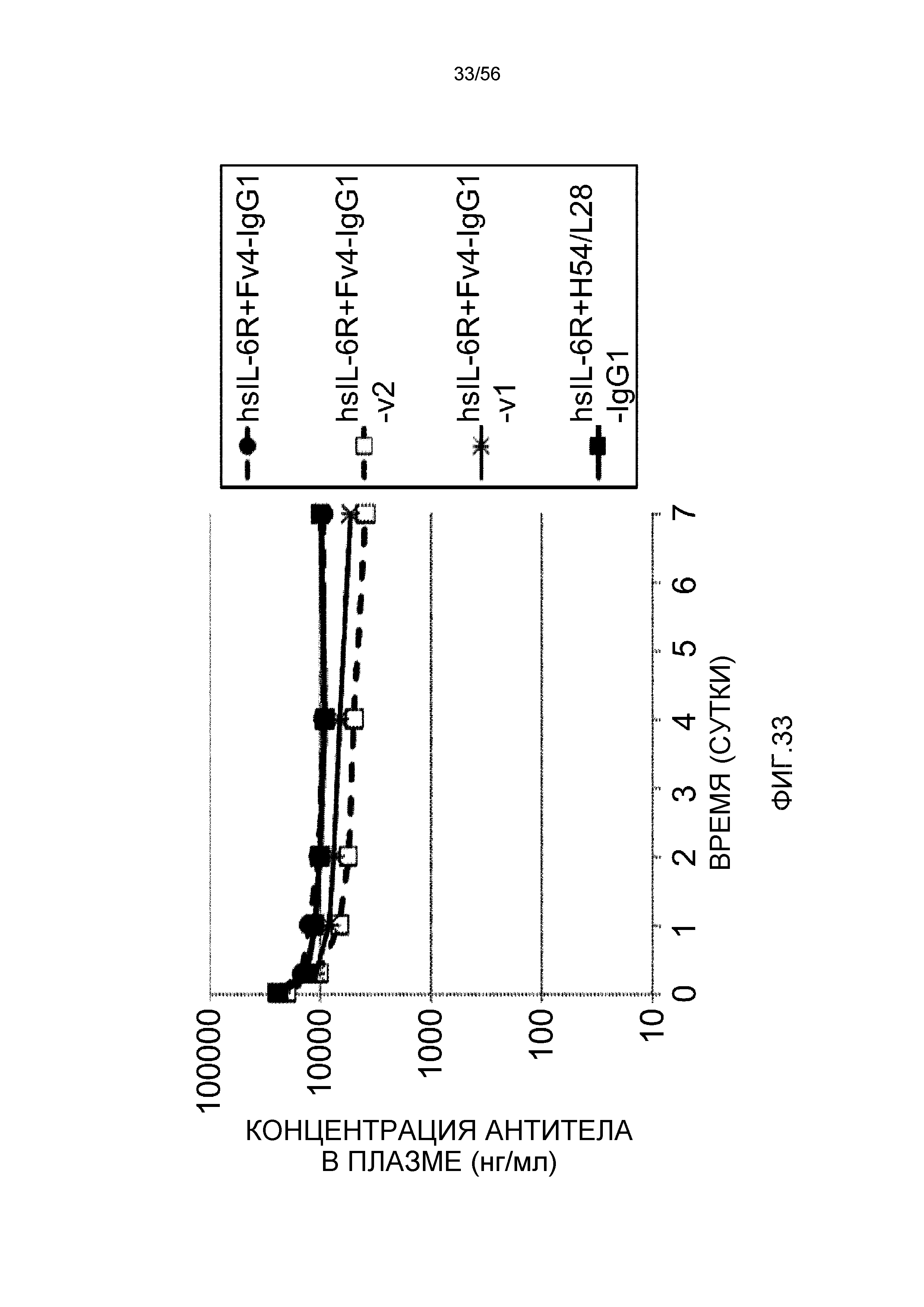
На фиг.33 представлены концентрации антитела в плазме с течением времени у нормальных мышей.
На фиг.34 представлена концентрация в плазме растворимого рецептора IL-6 человека у нормальных мышей.
На фиг.35 представлена концентрация в плазме несвязанного растворимого рецептора IL-6 человека с течением времени у нормальных мышей.
На фиг.36 представлена концентрация в плазме растворимого рецептора IL-6 человека с течением времени у трансгенных мышей с FcRn человека.
На фиг.37 представлена концентрация в плазме растворимого рецептора IL-6 человека с течением времени после введения Fv4-IgG1-F14 в более низкой дозе (0,01 мг/кг) или 1 мг/кг.
На фиг.38 представлены концентрации антитела в плазме с течением времени после введения Fv4-IgG1-F14 в более низкой дозе (0,01 мг/кг) или 1 мг/кг.
На фиг.39 представлена концентрация в плазме растворимого рецептора IL-6 человека с течением времени после введения антител против рецептора IL-6 человека нормальным мышам, у которых концентрация в плазме растворимого рецептора IL-6 человека является постоянной.
На фиг.40 представлена концентрация антитела в плазме с течением времени после совместного введения hsIL-6R и антитела против рецептора IL-6 человека трансгенным мышам с FcRn человека (линия 276).
На фиг.41 представлена концентрация в плазме с течением времени растворимого рецептора IL-6 человека после совместного введения hsIL-6R и антитела против рецептора IL-6 человека трансгенным мышам с FcRn человека (линия 276).
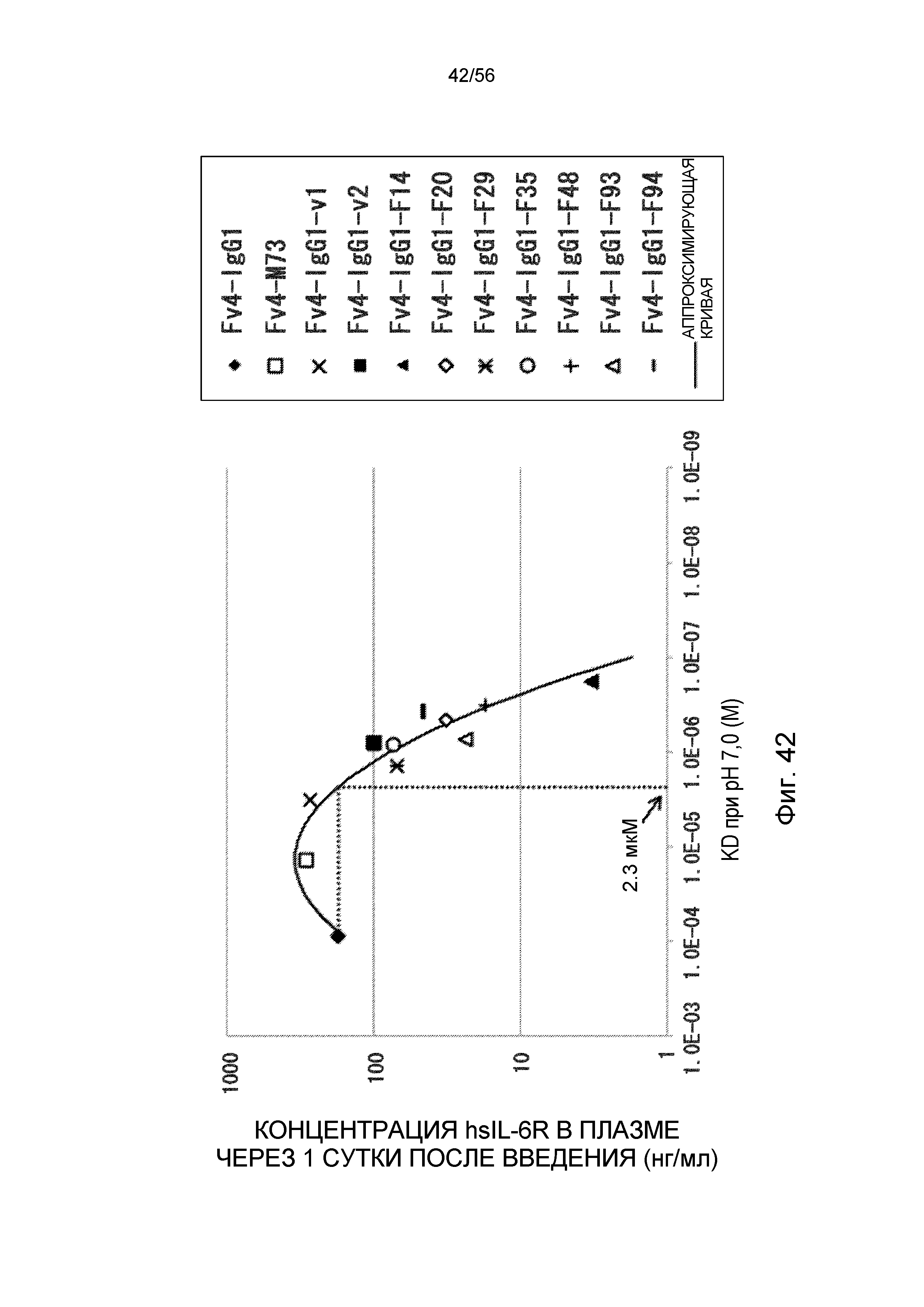
На фиг.42 представлена взаимосвязь между аффинностью связывания вариантов Fc с FcRn человека при pH 7,0 и концентрацией hsIL-6R в плазме через одни сутки после совместного введения hsIL-6R и антитела против рецептора IL-6 человека трансгенным мышам с FcRn человека (линия 276).
На фиг.43 представлена взаимосвязь между аффинностью связывания вариантов Fc с FcRn человека при pH 7,0 и концентрацией антитела в плазме через одни сутки после совместного введения hsIL-6R и антитела против рецептора IL-6 человека трансгенным мышам с FcRn человека (линия 276).
На фиг.44 представлено молярное соотношение антиген/антитело (значение C) с течением времени после совместного введения hsIL-6R и антитела против рецептора IL-6 человека трансгенным мышам с FcRn человека (линия 276).
На фиг.45 представлена взаимосвязь между аффинностью связывания вариантов Fc с FcRn человека при pH 7,0 и молярном соотношении антиген/антитело (значение C) на 1 сутки после совместного введения hsIL-6R и антитела против рецептора IL-6 человека трансгенным мышам с FcRn человека (линия 276).
На фиг.46 представлена концентрация в плазме hsIL-6R с течением времени после введения Fv4-IgG1-F14 при более низких дозах (0,01 или 0,2 мг/кг) или в дозе 1 мг/кг трансгенным мышам с FcRn человека (линия 276), у которых концентрация hsIL-6R в плазме является постоянной (стационарная инфузионная модель).
На фиг.47 представлена концентрация hsIL-6R в плазме с течением времени у трансгенных мышей с FcRn человека линии 276 и линии 32 после совместного введения hsIL-6R и антитела против рецептора IL-6 человека трансгенным мышам с FcRn человека (линии 276 и 32).
На фиг.48 представлена концентрации антитела в плазме с течением времени у трансгенных мышей с FcRn человека линии 276 и линии 32 после совместного введения hsIL-6R и антитела против рецептора IL-6 человека трансгенным мышам с FcRn человека (линии 276 и 32).
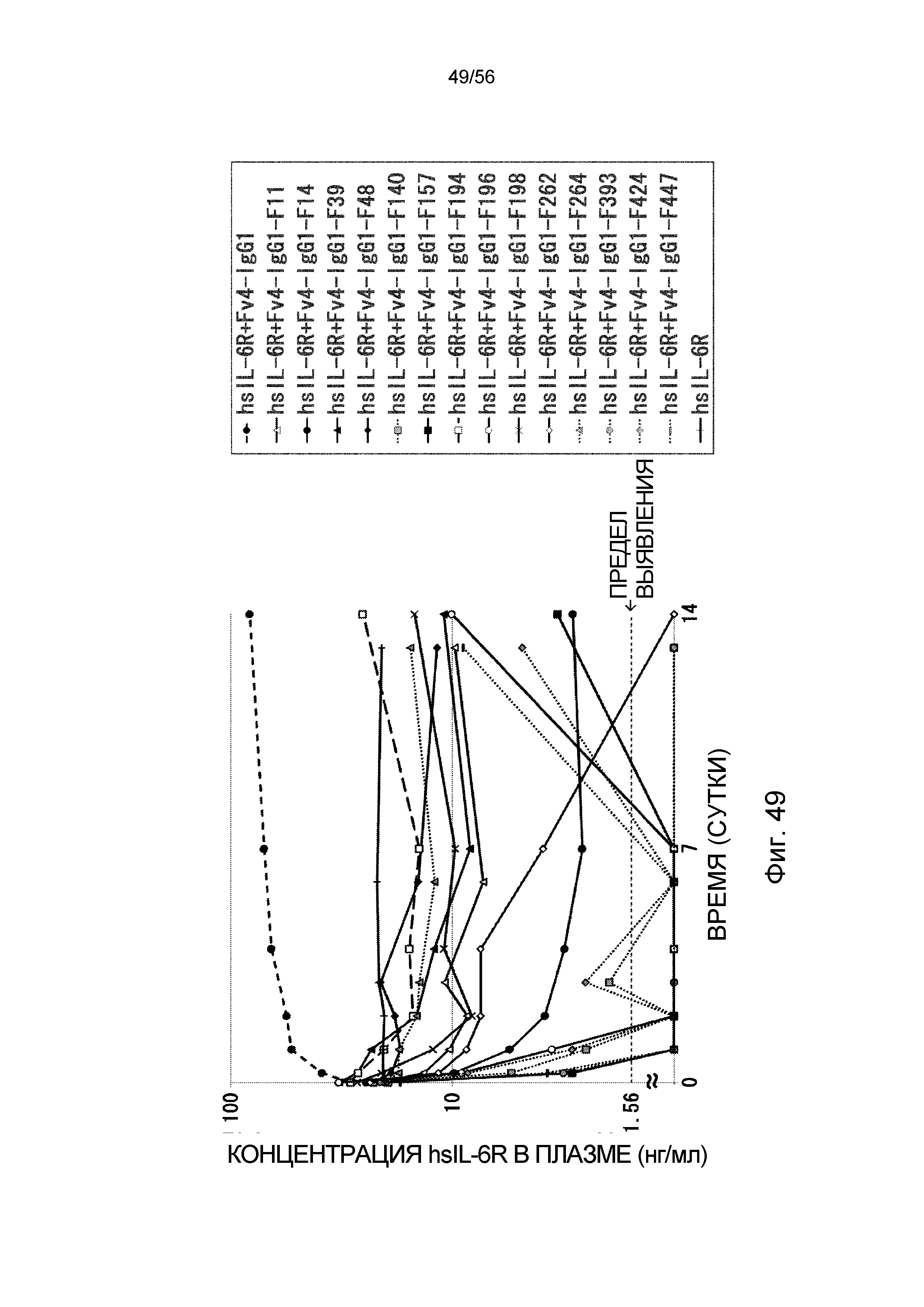
На фиг.49 представлена концентрация hsIL-6R в плазме с течением времени после введения антитела против рецептора IL-6 человека трансгенным мышам с FcRn человека, у которых концентрация hsIL-6R в плазме является постоянной (линия 32) (стационарная инфузионная модель).
На фиг.50 представлена концентрация антитела в плазме с течением времени после введения антитела против рецептора IL-6 человека трансгенным мышам с FcRn человека, у которых концентрация hsIL-6R в плазме является постоянной (линия 32) (стационарная инфузионная модель).
На фиг.51 представлено молярное соотношение антиген/антитело с течением времени (значение C) после введения антитела против рецептора IL-6 человека трансгенным мышам с FcRn человека, у которых концентрация hsIL-6R в плазме является постоянной (линия 32) (стационарная инфузионная модель).
На фиг.52 представлена взаимосвязь между аффинностью связывания вариантов Fc с FcRn человека при pH 7,0 и молярным соотношением антиген/антитело (значение C) на 1 сутки после введения антитела против рецептора IL-6 человека трансгенным мышам с FcRn человека (линия 32), у которых концентрация hsIL-6R в плазме является постоянной (стационарная инфузионная модель).
На фиг.53 представлен график концентрации антитела в плазме с течением времени после введения антител против рецептора IL-6 человека, имеющих вариант Fc: F11, F39, F48 и F264, трансгенным мышам с FcRn человека, у которых концентрация hsIL-6R в плазме является постоянной (линия 32) (стационарная инфузионная модель).
На фиг.54 представлен график концентрации в плазме hsIL-6R с течением времени после введения антител против IL-6 человека, имеющих вариант Fc: F11, F39, F48 и F264, трансгенным мышам с FcRn человека, у которых концентрация hsIL-6R в плазме является постоянной (линия 32) (стационарная инфузионная модель).
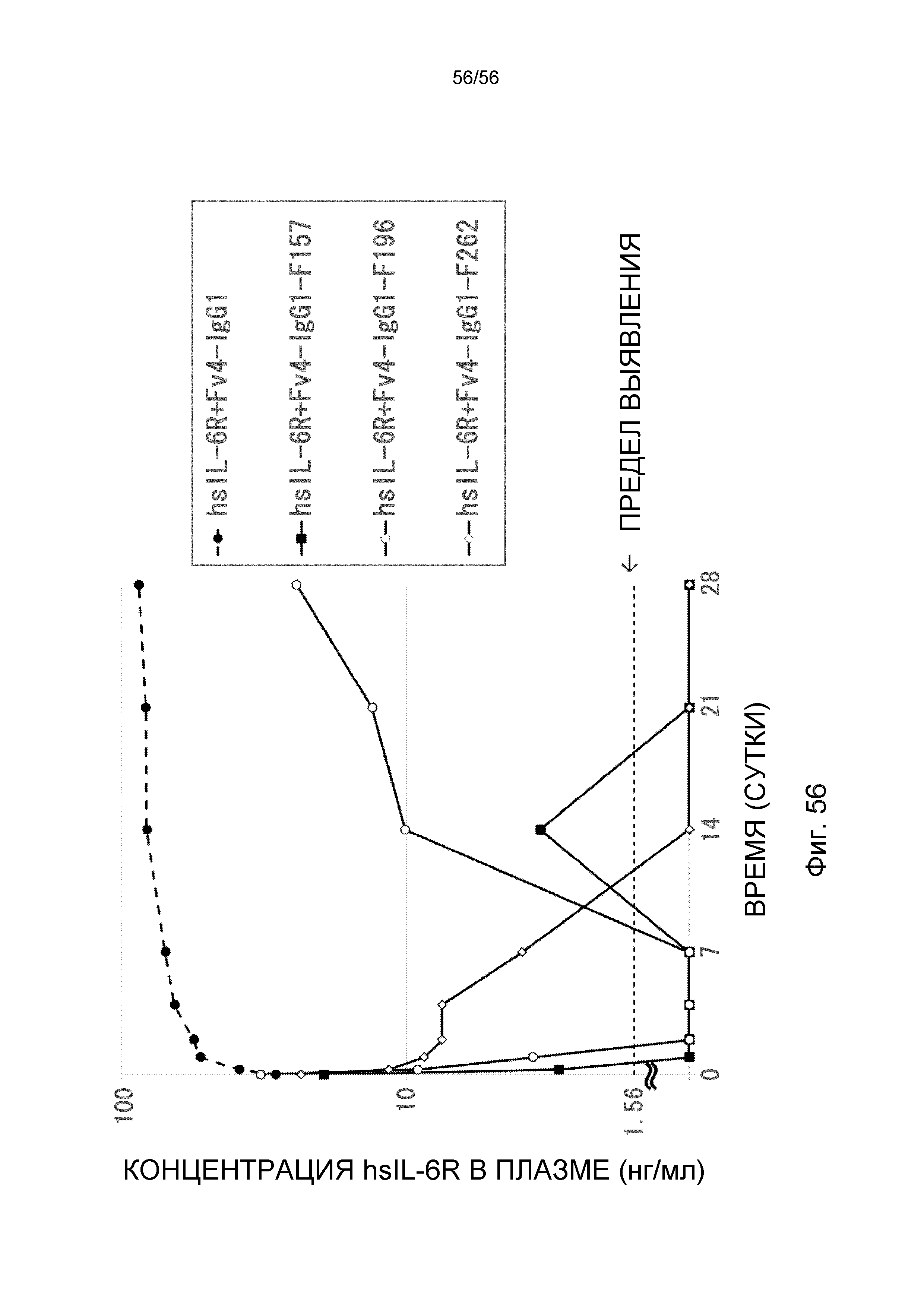
На фиг.55 представлена концентрация антитела в плазме с течением времени после введения антител против рецептора IL-6 человека, имеющих вариант Fc: F157, F196 и F262, трансгенным мышам с FcRn человека, к которых концентрация hsIL-6R в плазме является постоянной (линия 32) (стационарная инфузионная модель).
На фиг.56 представлена концентрация в плазме hsIL-6R с течением времени после введения антител против рецептора IL-6 человека, имеющих вариант Fc: F157, F196 и F262, трансгенным мышам с FcRn человека, у которых концентрация hsIL-6R в плазме является постоянной (линия 32) (стационарная инфузионная модель).
[Способы осуществления изобретения]
Настоящее изобретение относится к способам ускорения антигенсвязывающими молекулами захвата антигена в клетки, способам увеличения количества раз связывания антигена одной антигенсвязывающей молекулой, способам ускорения снижения концентрации антигена в плазме путем введения антигенсвязывающих молекул и способам увеличения удержания антигенсвязывающей молекулы в плазме. В частности, настоящее изобретение относится к способам ускорения захвата антигенсвязывающими молекулами антигена в клетки, способам увеличения количества раз связывания антигена одной антигенсвязывающей молекулой, способам ускорения снижения концентрации антигена в плазме путем введения антигенсвязывающих молекул и способам увеличения удержания антигенсвязывающих молекул в плазме, во всех из которых используется антигенсвязывающая молекула, которая имеет более низкую антигенсвязывающую активность (иногда называемую в настоящем описании "связывающей активностью") в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция.
Аминокислоты
В рамках настоящего изобретения аминокислоты описаны с помощью однобуквенного или трехбуквенного кодов или обоих из них, например, Ala/A, Leu/L, Arg/R, Lys/K, Asn/N, Met/M, Asp/D, Phe/F, Cys/C, Pro/P, Gln/Q, Ser/S, Glu/E, Thr/T, Gly/G, Trp/W, His/H, Tyr/Y, Ile/I или Val/V.
Антигены
В рамках настоящего изобретения "антигены" конкретно не ограничены по их структуре, при условии, что они содержат эпитопы, с которыми связываются антигенсвязывающие домены. Иными словами, антигены могут представлять собой неорганические или органические вещества; и Альтернативно, антигены могут представлять собой чужеродные или эндогенные вещества для организмов, которым проводят введение по настоящему изобретению. Примеры антигенов, которые связываются антигенсвязывающими доменам антигенсвязывающих молекул, фармакокинетика которых улучшается с помощью способов по настоящему изобретению, предпочтительно включают мембранные антигены, такие как рецепторные белки (мембраносвязанные рецепторы и растворимые рецепторы) и маркеры клеточной поверхности; растворимые антигены, такие как цитокины; и антигены с эпитопами, присутствующими только в чужеродных организмах. Такие антигены включают, например, следующие молекулы: 17-IA, 4-1 BB, 4Dc, 6-кето-PGF1a, 8-изо-PGF2a, 8-оксо-dG, рецептор аденозина A1, A33, ACE, ACE-2, активин, активин A, активин AB, активин B, активин C, активин RIA, активин RIA ALK-2, активин RIB ALK-4, активин RIIA, активин RIIB, ADAM, ADAM10, ADAM12, ADAM15, ADAM17/TACE, ADAM8, ADAM9, ADAMTS, ADAMTS4, ADAMTS5, адрессины, адипонектин, ADP рибозилциклаза-1, aFGF, AGE, ALCAM, ALK, ALK-1, ALK-7, аллерген, α1-антицимотрипсин, α1-антитрипсин, α-синуклеин, антагонист α-V/β-1, аминин, амилин, амилоид β, вариабельная область тяжелой цепи амилоидного иммуноглобулина, вариабельная область легкой цепи амилоидного иммуноглобулина, андроген, ANG, ангиотензиноген, лиганд ангиопоэтина 2, анти-Id, антитромбин III, антиген сибирской язвы, APAF-1, APE, APJ, апо-A1, апо-сывороточный амилоид A, Apo-SAA, APP, APRIL, AR, ARC, ART, артемин, ASPARTIC, предсердный натрийуретический фактор, предсердный натрийуретический пептид, предсердные натрийуретические пептиды A, предсердные натрийуретические пептиды B, предсердные натрийуретические пептиды C, интегрин av/b3, Axl, B7-1, B7-2, B7-H, BACE, BACE-1, защитный антиген Bacillus anthracis, Bad, BAFF, BAFF-R, Bag-1, BAK, Bax, BCA-1, BCAM, Bcl, BCMA, BDNF, b-ECGF, β-2-микроглобулин, β-лактамаза, bFGF, BID, Bik, BIM, BLC, BL-CAM, BLK, стимулятор B-лимфоцитов (BIyS), BMP, BMP-2 (BMP-2a), BMP-3 (остеогенин), BMP-4 (BMP-2b), BMP-5, BMP-6 (Vgr-1), BMP-7 (OP-1), BMP-8 (BMP-8a), BMPR, BMPR-IA (ALK-3), BMPR-IB (ALK-6), BMPR-II (BRK-3), BMPs, BOK, бомбезин, костный нейротрофический фактор, бычий гормон роста, BPDE, BPDE-DNA, BRK-2, BTC, молекула клеточной адгезии B-лимфоцитов, C10, ингибитор C1, C1q, C3, C3a, C4, C5, C5a (комплемент 5a), CA125, CAD-8, кадгерин-3, кальцитонин, cAMP, карбоангидраза IX, карциноэмбриональный антиген (CEA), карциномный антиген, кардиотрофин 1, катепсин A, катепсин B, катепсин C/DPPI, катепсин D, катепсин E, катепсин H, катепсин L, катепсин O, катепсин S, катепсин V, катепсин X/Z/P, CBL, CCI, CCK2, CCL, CCL1/I-309, CCL11/эотаксин, CCL12/MCP-5, CCL13/MCP-4, CCL14/HCC-1, CCL15/HCC-2, CCL16/HCC-4, CCL17/TARC, CCL18/PARC, CCL19/ELC, CCL2/MCP-1, CCL20/MIP-3-α, CCL21/SLC, CCL22/MDC, CCL23/MPIF-1, CCL24/эотаксин-2, CCL25/TECK, CCL26/эотаксин-3, CCL27/CTACK, CCL28/MEC, CCL3/M1P-1-α, CCL3Ll/LD-78-β, CCL4/MIP-1-β, CCL5/RANTES, CCL6/C10, CCL7/MCP-3, CCL8/MCP-2, CCL9/10/MTP-1-γ, CCR, CCR1, CCR10, CCR2, CCR3, CCR4, CCR5, CCR6, CCR7, CCR8, CCR9, CD1, CD10, CD105, CD11a, CD11b, CD11c, CD123, CD13, CD137, CD138, CD14, CD140a, CD146, CD147, CD148, CD15, CD152, CD16, CD164, CD18, CD19, CD2, CD20, CD21, CD22, CD23, CD25, CD26, CD27L, CD28, CD29, CD3, CD30, CD30L, CD32, CD33 (белки p67), CD34, CD37, CD38, CD3E, CD4, CD40, CD40L, CD44, CD45, CD46, CD49a, CD49b, CD5, CD51, CD52, CD54, CD55, CD56, CD6, CD61, CD64, CD66e, CD7, CD70, CD74, CD8, CD80 (B7-1), CD89, CD95, CD105, CD158a, CEA, CEACAM5, CFTR, cGMP, рецептор CGRP, CINC, CKb8-1, клаудин 18, CLC, токсин Clostridium botulinum, токсин Clostridium difficile, токсин Clostridium perfringens, c-Met, CMV, CMV UL, CNTF, CNTN-1, фактор комплемента 3 (C3), фактор комплемента D, кортикостероид-связывающий глобулин, рецептор колониестимулирующего фактора 1, COX, C-Ret, CRG-2, CRTH2, CT-1, CTACK, CTGF, CTLA-4, CX3CL1/фракталкин, CX3CR1, CXCL, CXCL1/Gro-α, CXCL10, CXCL11/I-TAC, CXCL12/SDF-1-α/β, CXCL13/BCA-1, CXCL14/BRAK, CXCL15/лангкин, CXCL16, CXCL16, CXCL2/Gro-β CXCL3/Gro-γ, CXCL3, CXCL4/PF4, CXCL5/ENA-78, CXCL6/GCP-2, CXCL7/NAP-2, CXCL8/IL-8, CXCL9/Mig, CXCL10/IP-10, CXCR, CXCR1, CXCR2, CXCR3, CXCR4, CXCR5, CXCR6, цистатин C, ассоциированный с опухолью антиген цитокератина, DAN, DCC, DcR3, DC-SIGN, ускоряющий распад фактор, лиганд Delta-подобного белка 4, дез(1-3)-IGF-l (IGF-1 головного мозга), Dhh, оксидаза DHICA, Dickkopf-1, дигоксин, дипептидилпептидаза IV, DKl, DNAM-1, ДНКаза, Dpp, DPPIV/CD26, Dtk, ECAD, EDA, EDA-A1, EDA-A2, EDAR, EGF, EGFR (ErbB-1), содержащий EGF-подобный домен белок 7, эластаза, эластин, EMA, EMMPRIN, ENA, ENA-78, эндосиалин, рецептор эндотелина, эндотоксин, энкефалиназа, eNOS, Eot, эотаксин, эотаксин-2, эотаксины, EpCAM, эфрин B2/EphB4, тирозинкиназный рецептор Epha2, рецептор эпидермального фактора роста (EGFR), рецептор ErbB2, тирозинкиназный рецептор ErbB3, ERCC, эритропоэтин (EPO), рецептор эритропоэтина, E-селектин, ET-1, Exodus-2, F-белок RSV, F10, F11, F12, F13, F5, F9, фактор Ia, фактор IX, фактор Xa, фактор VII, фактор VIII, фактор VIIIc, Fas, FcγR, Fc-эпсилон RI, FcγIIb, FcγRI, FcγRIIa, FcγRIIIa, FcγRIIIb, FcRn, FEN-1, ферритин, FGF, FGF-19, FGF-2, рецептор FGF-2, FGF-3, FGF-8, FGF-кислый, FGF-основный, FGFR, FGFR-3, фибрин, белок активации фибробластов (FAP), фибробластный фактор роста, фибробластный фактор роста-10, фибронектин, FL, FLIP, Flt-3, FLT3-лиганд, рецептор фолиевой кислоты, фолликулостимулирующий гормон (FSH), фракталкин (CX3C), свободная тяжелая цепь, свободная легкая цепь, FZD1, FZD10, FZD2, FZD3, FZD4, FZD5, FZD6, FZD7, FZD8, FZD9, G250, Gas 6, GCP-2, GCSF, G-CSF, рецептор G-CSF, GD2, GD3, GDF, GDF-1, GDF-15 (MIC-1), GDF-3 (Vgr-2), GDF-5 (BMP-14/CDMP-1), GDF-6 (BMP-13/CDMP-2), GDF-7 (BMP-12/CDMP-3), GDF-8 (миостатин), GDF-9, GDNF, гельсолин, GFAP, GF-CSF, GFR-α1, GFR-α2, GFR-α3, GF-β1, гликопротеин оболочки gH, GITR, глюкагон, рецептор глюкагона, рецептор глюкагон-подобного пептида 1, Glut 4, глутаматкарбоксипептидаза II, рецепторы гликопротеиновых гормонов, гликопротеин IIb/IIIa (GP IIb/IIIa), глипикан-3, GM-CSF, рецептор GM-CSF, gp130, gp140, gp72, гранулоцитарный CSF (G-CSF), GRO/MGSA, рилизинг-фактор гормона роста, GRO-β, GRO-γ, H. pylori, гаптен (NP-кэп или NIP-кэп), HB-EGF, HCC, HCC 1, гликопротеин оболочки gB HCMV, HCMV UL, гемопоэтический фактор роста (HGF), Hep B gp120, гепараназа, кофактор гепарина II, фактор роста печени, защитный антиген Bacillus anthracis, гликопротеин E2 вируса гепатита C, гепатит E, гепцидин, Her1, Her2/neu (ErbB-2), Her3 (ErbB-3), Her4 (ErbB-4), гликопротеин gB вируса простого герпеса (HSV), HGF, HGFA, высокомолекулярный ассоциированный с меланомой антиген (HMW-MAA), белки оболочки ВИЧ, такие как GP120, петля V3 gp 120 MIB ВИЧ, HLA, HLA-DR, HM1.24, HMFG PEM, HMGB-1, HRG, Hrk, HSP47, Hsp90, гликопротеин gD HSV, сердечный миозин человека, цитомегаловирус человека (HCMV), гормон роста человека (hGH), сывороточный альбумин человека, активатор плазминогена тканевого типа человека (t-PA), хантингтин, HVEM, IAP, ICAM, ICAM-1, ICAM-3, ICE, ICOS, IFN-α, IFN-β, IFN-γ, IgA, рецептор IgA, IgE, IGF, IGF-связывающие белки, IGF-1, IGF-1 R, IGF-2, IGFBP, IGFR, IL, IL-1, IL-10, рецепторы IL-10, IL-11, рецепторы IL-11, IL-12, рецепторы IL-12, IL-13, рецепторы IL-13, IL-15, рецепторы IL-15, IL-16, рецепторы IL-16, IL-17, рецепторы IL-17, IL-18 (IGIF), рецепторы IL-18, IL-1α, IL-1β, рецепторы IL-1, IL-2, рецепторы IL-2, IL-20, рецепторы IL-20, IL-21, рецепторы IL-21, IL-23, рецепторы IL-23, рецепторы IL-2, IL-3, рецепторы IL-3, IL-31, рецепторы IL-31, рецепторы IL-3, IL-4, рецепторы IL-4, IL-5, рецепторы IL-5, IL-6, рецепторы IL-6, IL-7, рецепторы IL-7, IL-8, рецепторы IL-8, IL-9, рецепторы IL-9, иммуноглобулиновый иммунный комплекс, иммуноглобулины, INF-α, рецепторы INF-α, INF-β, рецепторы INF-β, INF-γ, рецепторы INFγ, IFN типа I, рецептор IFN типа I, антиген вируса гриппа, ингибин, ингибин α, ингибин β, iNOS, инсулин, A-цепь инсулина, B-цепь инсулина, инсулиноподобный фактор роста 1, инсулиноподобный фактор роста 2, связывающие инсулиноподобный фактор роста белки, интегрин, интегрин α2, интегрин α3, интегрин α4, интегрин α4/β1, интегрин α-V/β-3, интегрин α-V/β-6, интегрин α4/β7, интегрин α5/β1, интегрин α5/β3, интегрин α5/β6, интегрин α-δ (αV), интегрин α-θ, интегрин β1, интегрин β2, интегрин β3 (GPIIb-IIIa), IP-10, I-TAC, JE, калликреин, калликреин 11, калликреин 12, калликреин 14, калликреин 15, калликреин 2, калликреин 5, калликреин 6, калликреин L1, калликреин L2, калликреин L3, калликреин L4, каллистатин, KC, KDR, фактор роста кератиноцитов (KGF), фактор роста кератиноцитов-2 (KGF-2), KGF, иммуноглобулин-подобный рецептор киллерных клеток, kit-лиганд (KL), Kit-тирозинкиназа, ламинин 5, LAMP, LAPP (амилин, амилоиный полипептид островков поджелудочной железы), LAP (TGF- 1), ассоциированный с латентностью пептид, латентный TGF-1, латентный TGF-1 bp1, LBP, LDGF, LDL, рецептор LDL, LECT2, Lefty, лептин, лютеинизирующий гормон (LH), антиген Льюиса Y, антиген, родственный антигену Льюиса Y, LFA-1, LFA-3, рецепторы LFA-3, Lfo, LIF, LIGHT, липопротеины, LIX, LKN, Lptn, L-селектин, LT-a, LT-b, LTB4, LTBP-1, сурфактант легких, лютеинизирующий гормон, лимфотактин, рецептор лимфотоксина β, рецептор лизосфинголипида, Mac-1, макрофагальный CSF (M-CSF), MAdCAM, MAG, MAP2, MARC, маспин, MCAM, MCK-2, MCP, MCP-1, MCP-2, MCP-3, MCP-4, MCP-I (MCAF), M-CSF, MDC, MDC (67 а.к.), MDC (69 а.к.), мегсин, Mer, семейство тирозинкиназных рецепторов MET, металлопротеазы, мембранный гликопротеин OX2, мезотелин, рецептор MGDF, MGMT, MHC (HLA-DR), микробный белок, MIF, MIG, MIP, MIP-1α, MIP-1β, MIP-3α, MIP-3β, MIP-4, MK, MMAC1, MMP, MMP-1, MMP-10, MMP-11, MMP-12, MMP-13, MMP-14, MMP-15, MMP-2, MMP-24, MMP-3, MMP-7, MMP-8, MMP-9, аттрактантный белок моноцитов, моноцитарный колониеингибирующий фактор, гонадотропин-ассоциированный пептид мыши, MPIF, Mpo, MSK, MSP, MUC-16, MUC18, муцин (Mud), мюллерово ингибирующее вещество, Mug, MuSK, ассоциированный с миелином гликопротеин, ингибирующий фактор миелоидного предшественника-1 (MPIF-I), NAIP, наноантитело, NAP, NAP-2, NCA 90, NCAD, N-кадгерин, NCAM, неприлизин, молекула адгезии нервных клеток, неросерпин, нейрональный фактор роста (NGF), нейротрофин-3, нейротрофин-4, нейротрофин-6, нейропилин 1, неуртурин, NGF-β, NGFR, NKG20, N-метионил-гормон роста человека, nNOS, NO, Nogo-A, рецептор Nogo, неструктурный белок типа 3 (NS3) из вируса гепатита C, NOS, Npn, NRG-3, NT, NT-3, NT-4, NTN, OB, OGG1, онкостатин M, OP-2, OPG, OPN, OSM, рецепторы OSM, остеоиндуктивные факторы, остеопонтин, OX40L, OX40R, окисленный LDL, p150, p95, PADPr, паратиреоидный гормон, PARC, PARP, PBR, PBSF, PCAD, P-кадгерин, PCNA, PCSK9, PDGF, рецептор PDGF, PDGF-AA, PDGF-AB, PDGF-BB, PDGF-D, PDK-1, PECAM, PEDF, PEM, PF-4, PGE, PGF, PGI2, PGJ2, PIGF, PIN, PLA2, плацентарный фактор роста, плацентарная щелочная фосфатаза (PLAP), плацентарный лактоген, ингибитор активатора плазминогена 1, тромбоцитарный фактор роста, plgR, PLP, полигликолевые цепи различного размера (например PEG-20, PEG-30, PEG40), PP14, прекалликреин, прионный белок, прокальцитонин, белок запрограммированной гибели клеток 1, проинсулин, пролактин, конвертаза пробелков PC9, прорелаксин, простатспецифический мембранный антиген (PSMA), белок A, белок C, белок D, белок S, белок Z, PS, PSA, PSCA, PsmAr, PTEN, PTHrp, Ptk, PTN, лиганд-1 P-селектинового гликопротеина, R51, RAGE, RANK, RANKL, RANTES, релаксин, A-цепь релаксина, B-цепь релаксина, ренин, F респираторно-синцитиального вируса (RSV), Ret, ретикулон 4, ревматоидные факторы, RLI P76, RPA2, RPK-1, RSK, RSV Fgp, S100, RON-8, SCF/KL, SCGF, склеростин, SDF-1, SDF1 α, SDF1 β, SERINE, сывороточный амилоид P, сывороточный альбумин, sFRP-3, Shh, шигаподобный токсин II, SIGIRR, SK-1, SLAM, SLPI, SMAC, SMDF, SMOH, SOD, SPARC, рецептор 1 сфингозин-1-фосфата, стафилококковая липотейхоевая кислота, Stat, STEAP, STEAP-II, фактор стволовых клеток (SCF), стрептокиназа, супероксиддисмутаза, синдекан-1, TACE, TACI, TAG-72 (ассоциированный с опухолью гликопротеин-72), TARC, TB, TCA-3, T-клеточный рецептор α/β, TdT, TECK, TEM1, TEM5, TEM7, TEM8, тенасцин, TERT, PLAP-подобная щелочная фосфатаза семенников, TfR, TGF, TGF-α, TGF-β, TGF-β панспецифический, TGF-β RII, TGF-β RIIb, TGF-β RIII, TGF-β Rl (ALK-5), TGF-β1, TGF-β2, TGF-β3, TGF-β4, TGF-β5, TGF-I, тромбин, тромбопоэтин (TPO), рецептор тимического стромального лимфопротеина, тимический Ck-1, тиреостимулирующий гормон (TSH), тироксин, тироксин-связывающий глобулин, Tie, TIMP, TIQ, тканевой фактор, ингибитор протеазы тканевого фактора, белок тканевого фактора, TMEFF2, Tmpo, TMPRSS2, рецептор I TNF, рецептор II TNF, TNF-α, TNF-β, TNF-β2, TNFc, TNF-RI, TNF-RII, TNFRSF10A (TRAIL R1 Apo-2/DR4), TNFRSF10B (TRAIL R2 DR5/KILLER/TRICK-2A/TRICK-B), TNFRSF10C (TRAIL R3 DcR1/LIT/TRID), TNFRSF10D (TRAIL R4 DcR2/TRUNDD), TNFRSF11A (RANK ODF R/TRANCE R), TNFRSF11B (OPG OCIF/TR1), TNFRSF12 (TWEAK R FN14), TNFRSF12A, TNFRSF13B (TACI), TNFRSF13C (BAFF R), TNFRSF14 (HVEM ATAR/HveA/LIGHT R/TR2), TNFRSF16 (NGFR p75NTR), TNFRSF17 (BCMA), TNFRSF18 (GITR AITR), TNFRSF19 (TROY TAJ/TRADE), TNFRSF19L (RELT), TNFRSF1A (TNF RI CD120a/p55-60), TNFRSF1B (TNF RII CD120b/p75-80), TNFRSF21 (DR6), TNFRSF22 (DcTRAIL R2 TNFRH2), TNFRSF25 (DR3 Apo-3/LARD/TR-3/TRAMP/WSL-1), TNFRSF26 (TNFRH3), TNFRSF3 (LTbR TNF RIII/TNFC R), TNFRSF4 (OX40 ACT35/TXGP1 R), TNFRSF5 (CD40 p50), TNFRSF6 (Fas Apo-1/APT1/CD95), TNFRSF6B (DcR3 M68/TR6), TNFRSF7 (CD27), TNFRSF8 (CD30), TNFRSF9 (4-1 BB CD137/ILA), TNFRST23 (DcTRAIL R1 TNFRH1), TNFSF10 (TRAIL Apo-2-лиганд/TL2), TNFSF11 (TRANCE/RANK-лиганд ODF/OPG-лиганд), TNFSF12 (TWEAK Apo-3-лиганд/DR3-лиганд), TNFSF13 (APRIL TALL2), TNFSF13B (BAFF BLYS/TALL1/THANK/TNFSF20), TNFSF14 (LIGHT HVEM-лиганд/LTg), TNFSF15 (TL1A/VEGI), TNFSF18 (GITR-лиганд AITR-лиганд/TL6), TNFSF1A (TNF-a коннектин/DIF/TNFSF2), TNFSF1B (TNF-b LTa/TNFSF1), TNFSF3 (LTb TNFC/p33), TNFSF4 (OX40-лиганд gp34/TXGP1), TNFSF5 (CD40-лиганд CD154/gp39/HIGM1/IMD3/TRAP), TNFSF6 (Fas-лиганд Apo-1-лиганд/APT1-лиганд), TNFSF7 (CD27-лиганд CD70), TNFSF8 (CD30-лиганд CD153), TNFSF9 (4-1 BB-лиганд CD137-лиганд), TNFα, TNF-β, TNIL-I, токсический метаболит, TP-1, t-PA, Tpo, TRAIL, TRAIL R, TRAIL-R1, TRAIL-R2, TRANCE, рецептор трансферрина, трансформирующие факторы роста (TGF), такие как TGF-α и TGF-β, трансмембранный гликопротеин NMB, транстиретин, TRF, Trk, TROP-2, трофобластный гликопротеин, TSG, TSLP, фактор некроза опухоли (TNF), ассоциированный с опухолью антиген CA 125, ассоциированный с опухолью антиген, экспрессирующий углевод, родственный антигену Льюиса Y, TWEAK, TXB2, Ung, uPAR, uPAR-1, урокиназа, VAP-1, сосудисто-эндотелиальный фактор роста (VEGF), васпин, VCAM, VCAM-1, VECAD, VE-кадгерин, VE-кадгерин-2, VEFGR-1 (flt-1), VEFGR-2, рецептор VEGF (VEGFR), VEGFR-3 (flt-4), VEGI, VIM, вирусные антигены, рецептор VitB12, рецептор витронектина, VLA, VLA-1, VLA-4, интегрин VNR, фактор фон Виллебранда (vWF), WIF-1, WNT1, WNT10A, WNT10B, WNT11, WNT16, WNT2, WNT2B/13, WNT3, WNT3A, WNT4, WNT5A, WNT5B, WNT6, WNT7A, WNT7B, WNT8A, WNT8B, WNT9A, WNT9B, XCL1, XCL2/SCM-l-β, XCLl/лимфотактин, XCR1, XEDAR, XIAP, XPD, HMGB1, IgA, Aβ, CD81, CD97, CD98, DDR1, DKK1, EREG, Hsp90, IL-17/IL-17R, IL-20/IL-20R, окисленный LDL, PCSK9, прекалликреин, RON, TMEM16F, SOD1, хромогранин A, хромогранин B, тау, VAP1, высокомолекулярный кининоген, IL-31, IL-31R, Nav1.1, Nav1.2, Nav1.3, Nav1.4, Nav1.5, Nav1.6, Nav1.7, Nav1.8, Nav1.9, EPCR, C1, C1q, C1r, C1s, C2, C2a, C2b, C3, C3a, C3b, C4, C4a, C4b, C5, C5a, C5b, C6, C7, C8, C9, фактор B, фактор D, фактор H, пропердин, склеростин, фибриноген, фибрин, протромбин, тромбин, тканевой фактор, фактор V, фактор Va, фактор VII, фактор VIIa, фактор VIII, фактор VIIIa, фактор IX, фактор IXa, фактор X, фактор Xa, фактор XI, фактор XIa, фактор XII, фактор XIIa, фактор XIII, фактор XIIIa, TFPI, антитромбин III, EPCR, тромбомодулин, TAPI, tPA, плазминоген, плазмин, PAI-1, PAI-2, GPC3, синдекан-1, синдекан-2, синдекан-3, синдекан-4, LPA и S1P и молекулы растворимых рецепторов для гормона или фактора роста в жидкостях организма, которые не заякорены на клетках.
"Эпитоп" означает антигенную детерминанту в антигене и относится к антигенному центру, с которым связывается антигенсвязывающий домен антигенсвязывающей молекулы, описанной в настоящем описании. Таким образом, например, эпитоп может быть определен в соответствии с его структурой. Альтернативно, эпитоп может быть определен в соответствии с антигенсвязывающей активностью антигенсвязывающей молекулы, которая распознает эпитоп. Когда антиген представляет собой пептид или полипептид, эпитоп может быть указан с помощью аминокислотных остатков, образующих эпитоп. Альтернативно, когда эпитоп представляет собой цепь сахара, эпитоп может быть указан с помощью его определенной структуры цепи сахаров.
Линейный эпитоп представляет собой эпитоп, который содержит эпитоп, в котором распознается его первичная аминокислотная последовательность. Такой линейный эпитоп, как правило, содержит по меньшей мере три и наиболее часто по меньшей мере пять, например, приблизительно 8-10 или 6-20 аминокислот в его конкретной последовательности.
В противоположность линейному эпитопу, "конформационный эпитоп" представляет собой эпитоп, в котором первичная аминокислотная последовательность, содержащая эпитоп, не является единственной детерминантой распознаваемого эпитопа (например, первичная аминокислотная последовательность конформационного эпитопа не обязательно распознается определяющим эпитоп антителом). Конформационные эпитопы могут содержать большее количество аминокислот по сравнению с линейными эпитопами. Антитело, распознающее конформационный эпитоп, распознает трехмерную структуру пептида или белка. Например, когда молекула белка сворачивается и формирует трехмерную структуру, аминокислоты и/или основные цепи полипептида, которые образуют конформационный эпитоп, располагаются рядом друг с другом, и эпитоп становится распознаваемым для антитела. Способы определения конформаций эпитопов включают, например, рентгеновскую кристаллографию, двумерный ядерный магнитный резонанс, сайт-специфическое спиновое мечение и электронный парамагнитный резонанс, он они не ограничиваются ими. См., например, Epitope Mapping Protocols in Methods in Molecular Biology (1996), Vol. 66, Morris (ed.).
Активность связывания
Примеры способа оценки связывания эпитопа исследуемой антигенсвязывающей молекулой, содержащей антигенсвязывающий домен для IL-6R, описаны ниже. В соответствии с примерами ниже, также можно соответствующим образом выполнять способы оценки связывания эпитопа исследуемой антигенсвязывающей молекулой, содержащей антигенсвязывающий домен, с антигеном, отличным от IL-6R.
Например, то, что исследуемая антигенсвязывающая молекула, содержащая антигенсвязывающий домен для IL-6R, распознает линейный эпитоп в молекуле IL-6R, можно подтвердить, например, как описано ниже. Для указанной выше цели синтезируют линейный пептид, содержащий аминокислотную последовательность, образующую внеклеточный домен IL-6R. Пептид можно синтезировать химически или его можно получать способами генетической инженерии с использованием области, кодирующей аминокислотную последовательность, соответствующую внеклеточному домену в кДНК IL-6R. Затем исследуемую антигенсвязывающую молекулу, содержащую антигенсвязывающий домен для IL-6R, оценивают в отношении ее активности связывания с линейным пептидом, содержащим аминокислотную последовательность, образующую внеклеточный домен. Например, иммобилизованный линейный пептид можно использовать в качестве антигена в ELISA для оценки активности связывания антигенсвязывающей молекулы с пептидом. Альтернативно, активность связывания с линейным пептидом можно оценивать, исходя из уровня, на котором линейный пептид ингибирует связывание антигенсвязывающей молекулы с клетками, экспрессирующими IL-6R. Эти исследования могут продемонстрировать активность связывания антигенсвязывающей молекулы с линейным пептидом.
Наличие распознавания исследуемой антигенсвязывающей молекулой, содержащей антигенсвязывающий домен для IL-6R, конформационного эпитопа можно оценивать следующим образом. Для указанной выше цели получают экспрессирующие IL-6R клетки. Наличие распознавания исследуемой антигенсвязывающей молекулой, содержащей антигенсвязывающий домен IL-6R, конформационного эпитопа, можно определять, когда она прочно связывается с экспрессирующими IL-6R клетками при контакте, но по существу не связывается с иммобилизованным линейным пептидом, содержащим аминокислотную последовательность, образующую внеклеточный домен IL-6R. В рамках настоящего изобретения "по существу не связывает" означает, что активность связывания составляет 80% или менее, как правило, 50% или менее, предпочтительно 30% или менее, и особенно предпочтительно 15% или менее по сравнению с активностью связывания с клетками, экспрессирующими IL-6R человека.
Способы оценки активности связывания исследуемой антигенсвязывающей молекулы, содержащей антигенсвязывающий домен для IL-6R, с экспрессирующими IL-6R клетками, включают, например, способы, описанные в Antibodies: A Laboratory Manual (Ed Harlow, David Lane, Cold Spring Harbor Laboratory (1988) 359-420). В частности, оценку можно проводить на основе принципа ELISA или активированной флуоресценцией сортировки клеток (FACS) с использованием в качестве антигена экспрессирующих IL-6R клеток.
В формате ELISA активность связывания исследуемой антигенсвязывающей молекулы, содержащей антигенсвязывающий домен для IL-6R, с экспрессирующими IL-6R клетками можно оценивать количественно путем сравнения уровней сигнала, генерируемого ферментативной реакцией. В частности, исследуемую антигенсвязывающую молекулу добавляют в планшет для ELISA, на котором иммобилизованы экспрессирующие IL-6R клетки. Затем антигенсвязывающую молекулу, связанную с клетками, выявляют с использованием меченного ферментом антитела, которое распознает исследуемую антигенсвязывающую молекулу. Альтернативно, когда используют FACS, приготавливают серии разведений исследуемой антигенсвязывающей молекулы и можно определять титр связывания антитела с экспрессирующими IL-6R клетками для сравнения активности связывания исследуемой антигенсвязывающей молекулы с экспрессирующими IL-6R клетками.
Связывание исследуемой антигенсвязывающей молекулы с антигеном, экспрессируемым на поверхности клеток, суспендированных в буфере или сходных с ним, можно выявлять с использованием проточного цитометра. Известные проточные цитометры включают, например, следующие устройства:
FACSCantoTM II
FACSAriaTM
FACSArrayTM
FACSVantageTM SE
FACSCaliburTM (все являются торговыми названиями BD Biosciences)
EPICS ALTRA HyPerSort
Cytomics FC 500
EPICS XL-MCL ADC EPICS XL ADC
Cell Lab Quanta/Cell Lab Quanta SC (все являются торговыми названиями Beckman Coulter).
Предпочтительные способы оценки активности связывания исследуемой антигенсвязывающей молекулы, содержащей антигенсвязывающий домен для IL-6R, с антигеном, включают, например, следующий способ. Сначала экспрессирующие IL-6R клетки подвергают реакции с исследуемой антигенсвязывающей молекулой, а затем их окрашивают меченным FITC вторичным антителом, которое распознает антигенсвязывающую молекулу. Исследуемую антигенсвязывающую молекулу надлежащим образом разбавляют подходящим буфером с получением молекулы с желаемой концентрацией. Например, молекулу можно использовать в концентрации в диапазоне от 10 мкг/мл до 10 нг/мл. Затем определяют интенсивность флуоресценции и количество клеток с использованием FACSCalibur (BD). Интенсивность флуоресценции, полученную с помощью анализа с использованием программного обеспечения CELL QUEST (BD), т.е. среднее геометрическое значение, отражает количество антитела, связанного с клетками. Следовательно, активность связывания исследуемой антигенсвязывающей молекулы, которую отражает количество связанной исследуемой антигенсвязывающей молекулы, можно определять путем определения геометрического среднего значения.
То, обладает ли исследуемая антигенсвязывающая молекула, содержащая антигенсвязывающий домен для IL-6R, общим эпитопом с другой антигенсвязывающей молекулой, можно оценивать на основе конкуренции между двумя молекулами за один и тот же эпитоп. Конкуренцию между антигенсвязывающими молекулами можно выявлять с помощью анализа перекрестного блокирования или сходных с ним. Например, предпочтительным анализом перекрестного блокирования является конкурентный анализ ELISA.
В частности, в анализе перекрестного блокирования белок IL-6R, иммобилизованный на лунках микропланшета для титрования, предварительно инкубируют в присутствии или в отсутствие являющейся кандидатом конкурентной антигенсвязывающей молекулы, а затем к ним добавляют антигенсвязывающую молекулу. Количество исследуемой антигенсвязывающей молекулы, связавшейся с белком IL-6R в лунках, непрямо коррелирует со связывающей способностью являющейся кандидатом конкурентной антигенсвязывающей молекулы, которая конкурирует за связывание с тем же эпитопом. Следовательно, чем более высокой является аффинность конкурентной антигенсвязывающей молекулы к тому же эпитопу, тем более низкой является активность связывания исследуемой антигенсвязывающей молекулы с покрытыми белком IL-6R лунками.
Количество исследуемой антигенсвязывающей молекулы, связанной с лунками через IL-6R, можно легко определить путем предварительного мечения антигенсвязывающей молекулы. Например, меченную биотином антигенсвязывающую молекулу определяют с использованием конъюгата авидин/пероксидаза и соответствующего субстрата. В частности, анализ перекрестного блокирования, в котором используются ферментные метки, такие как пероксидаза, называют "конкурентным анализом ELISA". Антигенсвязывающую молекулу также можно метить другими агентами для мечения, которые обеспечивают выявление или измерение. В частности, известны радиоактивные метки, флуоресцентные метки и т.п.
Когда являющаяся кандидатом конкурентная антигенсвязывающая молекула может блокировать связывание исследуемой антигенсвязывающей молекулой, содержащей антигенсвязывающий домен для IL-6R, по меньшей мере на 20%, предпочтительно по меньшей мере на 20-50%, и более предпочтительно по меньшей мере на 50% по сравнению с активностью связывания в контрольном эксперименте, исследованном в отсутствие конкурентной антигенсвязывающей молекулы, то определяют, что исследуемая антигенсвязывающая молекула по существу связывается с тем же эпитопом, с которым связывается конкурентная антигенсвязывающая молекула, или конкурирует за связывание с тем же эпитопом.
Когда структура эпитопа, с которым связывается исследуемая антигенсвязывающая молекула, содержащая антигенсвязывающий домен для IL-6R, уже идентифицирована, тогда то, имеют ли исследуемые и контрольные антигенсвязывающие молекулы общий эпитоп, можно оценивать путем сравнения активности связывания двух антигенсвязывающих молекул с пептидом, полученным путем внесения аминокислотных мутаций в пептид, формирующий эпитоп.
Для измерения указанной выше активности связывания, например, активность связывания исследуемых и контрольных антигенсвязывающих молекул в отношении линейного пептида, в который внесена мутация, сравнивают в описанном выше формате ELISA. Помимо способов ELISA, активность связывания с мутантным пептидом, связанным с колонкой, можно определять путем пропускания исследуемых и контрольных антигенсвязывающих молекул через колонку, а затем количественного определения антигенсвязывающей молекулы, элюированной в элюирующем растворе. Способы адсорбции мутантного пептида на колонку, например, в форме слитого пептида с GST, известны.
Альтернативно, когда идентифицированный эпитоп представляет собой конформационный эпитоп, тогда то, обладают ли исследуемые и контрольные антигенсвязывающие молекулы общим эпитопом, можно оценивать следующим способом. Сначала получают экспрессирующие IL-6R клетки и клетки, экспрессирующие IL-6R с мутацией, внесенной в эпитоп. Исследуемые и контрольные антигенсвязывающие молекулы добавляют в суспензию клеток, полученную суспендированием этих клеток в соответствующем буфере, таком как PBS. Затем клеточные суспензии надлежащим образом промывают буфером, и к ним добавляют меченное FITC антитело, которое распознает исследуемые и контрольные антигенсвязывающие молекулы. Интенсивность флуоресценции и количество клеток, окрашенных меченым антителом, определяют с использованием FACSCalibur (BD). Исследуемые и контрольные антигенсвязывающие молекулы надлежащим образом разбавляют с использованием подходящего буфера и используют в желаемых концентрациях. Например, их можно использовать в концентрации в диапазоне от 10 мкг/мл до 10 нг/мл. Интенсивность флуоресценции, определенная с помощью анализа с использованием программного обеспечения CELL QUEST (BD), т.е. геометрическое среднее значение, отражает количество меченого антитела, связанного с клетками. Следовательно, активность связывания исследуемых и контрольных антигенсвязывающих молекул, которую отражает количество связавшегося меченого антитела, можно определять путем измерения геометрического среднего значения.
В описанном выше способе то, что антигенсвязывающая молекула "по существу не связывается с клетками, экспрессирующими мутантный IL-6R," можно оценивать, например, следующим способом. Сначала исследуемые и контрольные антигенсвязывающие молекулы, связанные с клетками, экспрессирующими мутантный IL-6R, окрашивают меченым антителом. Затем определяют интенсивность флуоресценции клеток. Когда используют FACSCalibur для выявления флуоресценции проточной цитометрией, определенную интенсивность флуоресцении можно анализировать с использованием программного обеспечения CELL QUEST. Из геометрических средних значений в присутствии и в отсутствие антигенсвязывающей молекулы, можно вычислять сравнительное значение (ΔGeo-Mean) по следующей формуле для определения соотношения увеличения интенсивности флуоресценции в результате связывания антигенсвязывающей молекулой.
ΔGeo-Mean = Geo-Mean (в присутствии антигенсвязывающей молекулы)/ Geo-Mean (в отсутствие антигенсвязывающей молекулы)
Геометрическое среднее сравнительное значение (значение ΔGeo-Mean для мутантной молекулы IL-6R), определенное с помощью описанного выше анализа, которое отражает количество исследуемой антигенсвязывающей молекулы, связанной с клетками, экспрессирующими мутантный IL-6R, сравнивают со сравнительным значением ΔGeo-Mean, которое отражает количество исследуемой антигенсвязывающей молекулы, связавшейся с экспрессирующими IL-6R клетками. В этом случае, особенно предпочтительно, чтобы концентрации исследуемой антигенсвязывающей молекулы, используемой для определения сравнительных значений ΔGeo-Mean для экспрессирующих IL-6R клеток и клеток, экспрессирующих мутантный IL-6R, были скорректированы так, чтобы они были равными или по существу равными. В качестве контрольной антигенсвязывающей молекулы используют антигенсвязывающую молекулу, для которой подтверждено, что она распознает эпитоп в IL-6R.
Если сравнительное значение ΔGeo-Mean исследуемой антигенсвязывающей молекулы для клеток, экспрессирующих мутантный IL-6R, меньше, чем сравнительное значение ΔGeo-Mean исследуемой антигенсвязывающей молекулы для экспрессирующих IL-6R клеток, по меньшей мере на 80%, предпочтительно на 50%, более предпочтительно на 30%, и особенно предпочтительно на 15%, тогда исследуемая антигенсвязывающая молекула "по существу не связывается с клетками, экспрессирующими мутантный IL-6R". Формула для определения значения Geo-Mean (геометрического среднего значения) описана в руководстве пользователя программного обеспечения CELL QUEST (BD biosciences). Если сравнение показывает, что сравнительные величины по существу эквивалентны, то может быть определено, что эпитоп для исследуемой и контрольной антигенсвязывающих молекул является одним и тем же.
Антигенсвязывающий домен
В рамках настоящего изобретения "антигенсвязывающий домен" может представлять собой любую структуру, при условии, что она связывается с представляющим интерес антигеном. Такие домены предпочтительно включают, например:
вариабельные области тяжелых цепей и легких цепей антител;
модуль приблизительно из 35 аминокислот, называемый A-доменом, который содержится в мембранном белке клеток авимере in vivo (WO 2004/044011, WO 2005/040229);
аднектин, содержащий домен 10Fn3, который связывается с белковой частью фибронектина - гликопротеина, экспрессирующегося на клеточной мембране (WO 2002/032925);
аффитело, которое состоит из трехспирального пучка из 58-аминокислот на основе каркаса связывающего IgG домена белка A (WO 1995/001937);
Смоделированные белки анкиринового повтора (DARPin), которые представляют собой область, экспонированную на молекулярной поверхности анкириновых повторов (AR), имеющих структуру, в которой субъединица, состоящая из поворота, содержащего 33 аминокислотных остатка, две антипараллельных спирали и петлю многократно сложены в стопку (WO 2002/020565);
антикалины и т.п., которые представляют собой домены, состоящие из четырех петель, которые поддерживают одну сторону структуры бочки, состоящей из восьми расположенных по кругу антипараллельных нитей, которые являются высококонсервативными среди молекул липокалина, таких как ассоциированный с желатиной липокалин нейтрофилов (NGAL) (WO 2003/029462); и
вогнутая область, образованная структурой параллельных слоев внутри структуры в форме подковы, образованной уложенными в стопку повторами модуля лейцин-богатого повтора (LRR) вариабельного рецептора лимфоцитов (VLR), который не имеет иммуноглобулиновой структуры и используется в системе приобретенного иммунитета у бесчелюстных позвоночных, таких как минога и миксина (WO 2008/016854). Предпочтительные антигенсвязывающие домены по настоящему изобретению включают, например, антигенсвязывающие домены, имеющие вариабельные области тяжелых цепей и легких цепей антител. Предпочтительные примеры антигенсвязывающих доменов включают "одноцепочечный Fv (scFv)", "одноцепочечное антитело", "Fv", "одноцепочечный Fv 2 (scFv2)", "Fab" и "F(ab’)2".
Антигенсвязывающие домены антигенсвязывающих молекул по настоящему изобретению могут связываться с идентичным эпитопом. Такой эпитоп может присутствовать, например, в белке, содержащем аминокислотную последовательность SEQ ID NO: 15. Альтернативно, эпитоп может присутствовать в белке, содержащем аминокислоты в положениях 20-365 аминокислотной последовательности SEQ ID NO: 15. Альтернативно, каждый из антигенсвязывающих доменов антигенсвязывающих молекул по настоящему изобретению может связываться с отличающимся эпитопом. В рамках настоящего изобретения, отличающийся эпитоп может присутствовать, например, в белке, содержащем аминокислотную последовательность SEQ ID NO: 15. Альтернативно, эпитоп может присутствовать в белке, содержащем аминокислоты в положениях 20-365 аминокислотной последовательности SEQ ID NO: 15.
Кальций-связывающий мотив
Антигенсвязывающий домен антигенсвязывающей молекулы по настоящему изобретению содержит кальций-связывающий мотив. Кальций-связывающий мотив может быть расположен в любом месте антигенсвязывающего домена, при условии, что антигенсвязывающая активность является более низкой в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция. Когда антигенсвязывающий домен представляет собой вариабельную область антитела, кальций-связывающий мотив может содержаться в вариабельной области тяжелой цепи или вариабельной области легкой цепи. Альтернативно, кальций-связывающий мотив может содержаться как в тяжелых цепях, так и в легких цепях. В другом неограничивающем варианте осуществления кальций-связывающий мотив может содержаться в каркасной области или последовательности CDR вариабельной области. Альтернативно, кальций-связывающий мотив может содержаться в последовательностях как каркасной области, так и CDR.
В неограничивающем варианте осуществления настоящего изобретения кальций-связывающий мотив содержит аминокислотный остаток(-и), который изменяет антигенсвязывающую активность антигенсвязывающей молекулы, в зависимости от условий концентрации ионов кальция. Такие аминокислотные остатки предпочтительно включают, например, аминокислоты, обладающие активностью хелатирования металлов. Аминокислоты, обладающие активностью хелатирования металлов, предпочтительно включают, например, серин (Ser (S)), треонин (Thr (T)), аспарагин (Asn (N)), глутамин (Gln (Q)), аспарагиновую кислоту (Asp (D)), глутаминовую кислоту (Glu (E)), гистидин (His (H)) и тирозин (Tyr (Y)). Кальций-связывающие мотивы в существующих антигенсвязывающих доменах, которые обладают более низкой антигенсвязывающей активностью в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция, можно использовать в качестве подходящего кальций-связывающего мотива по настоящему изобретению. В качестве примеров таких существующих антигенсвязывающих доменов, предпочтительно можно использовать кальций-связывающие мотивы в вариабельных областях антител, которые обладают более низкой антигенсвязывающей активностью в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция; но они не ограничиваются ими. Такие антитела включают, но не ограничиваются ими, например, антитела против рецептора IL-6, содержащие SEQ ID NO: 1 и 2, и антитела против IL-6, содержащие SEQ ID NO: 25 и 26. Более того, известны тропонин C, кальмодулин, парвальбумин, легкая цепь миозина и т.п., которые имеют несколько участков связывания ионов кальция и предположительно происходят из общего источника в процессе их молекулярной эволюции. Их связывающие мотивы также можно использовать в качестве кальций-связывающего мотива по настоящему изобретению.
Когда антигенсвязывающий домен по настоящему изобретению представляет собой вариабельную область антитела, кальций-связывающий мотив может содержаться в его вариабельной области тяжелой цепи или вариабельной области легкой цепи. Альтернативно, кальций-связывающий мотив может содержаться как в тяжелых цепях, так и в легких цепях. В другом неограничивающем варианте осуществления кальций-связывающий мотив может содержаться в последовательности каркасной области или CDR вариабельной области. Альтернативно, кальций-связывающий мотив может содержаться в последовательностях как каркасной области, так и CDR. CDR1, CDR2 и/или CDR3 тяжелой цепи и легкой цепи можно конструировать так, чтобы они содержали такие кальций-связывающие мотивы. Например, в неограничивающем варианте осуществления настоящего изобретения вариабельную область легкой цепи антигенсвязывающей молекулы по настоящему изобретению можно конструировать так, чтобы она содержала кальций-связывающий мотив вариабельной области легкой цепи антитела человека SEQ ID NO: 41, 63 или 64. Такие кальций-связывающие мотивы включают мотивы, в которых любые одна или несколько из аминокислот в положениях 30, 31, 32, 50 и/или 92 в соответствии с нумерацией по Kabat обладают активностью хелатирования металла. В неограничивающем варианте осуществления такие кальций-связывающие мотивы предпочтительно включают кальций-связывающие мотивы, в которых те же аминокислоты, что и от одной до четырех аминокислот, выбранных из пяти аминокислот в положениях 30, 31, 32, 50 и/или 92 в соответствии с нумерацией по системе Kabat в вариабельной области легкой цепи антитела человека SEQ ID NO: 41, 63 или 64, находились в соответствующих аминокислотных положениях в соответствии с нумерацией по системе Kabat. В этом случае предпочтительно, чтобы аминокислоты, обладающие активностью хелатирования металлов, содержались в вариабельной области легкой цепи человека SEQ ID NO: 41, 63 или 64 в положении аминокислот, где аминокислоты в соответствующих положениях аминокислот из пяти положений аминокислот 30, 31, 32, 50 и/или 92 в соответствии с нумерацией по системе Kabat в вариабельной области легкой цепи, не являются идентичными аминокислотам в этих положениях. В другом неограничивающем варианте осуществления настоящего изобретения вариабельную область тяжелой цепи антигенсвязывающей молекулы по настоящему изобретению можно конструировать так, чтобы она имела, например, кальций-связывающий мотив вариабельной области тяжелой цепи SEQ ID NO: 1. Такие кальций-связывающие мотивы включают кальций-связывающие мотивы, в которых аминокислоты в положениях 95, 96 и/или 100a в соответствии с нумерацией по системе Kabat, имеют активность хелатирования металлов. В другом неограничивающем варианте осуществления настоящего изобретения вариабельную область тяжелой цепи антигенсвязывающей молекулы по настоящему изобретению можно конструировать так, чтобы она имела, например, кальций-связывающий мотив вариабельной области тяжелой цепи SEQ ID NO: 25. Такие кальций-связывающие мотивы включают мотивы, в которых аминокислоты в положениях 95 и/или 101 в соответствии с нумерацией по системе Kabat, обладают активностью хелатирования металлов. Аминокислоты, обладающие активностью хелатирования металлов, включают, например, серин (Ser (S)), треонин (Thr (T)), аспарагин (Asn (N)), глутамин (Gln (Q)), аспарагиновую кислоту (Asp (D)), глутаминовую кислоту (Glu (E)), гистидин (His (H)) и тирозин (Tyr (Y)). Более того, в связывании ионов кальция могут участвовать карбонильные группы основной цепи аминокислот в описанных выше положениях. Неожиданно, как описано в примерах ниже, активность связывания ионов кальция можно сообщать представляющему интерес антигенсвязывающему домену путем пересадки аминокислот из кальций-связывающего мотива в антигенсвязывающий домен. Также возможно соответствующим образом использовать мотив EF-hand, который содержится в кадгериновом домене и кальмодулине; C2-домен, который содержится в протеинкиназе C; Gla-домен, который содержится в белке фактора IX свертывания крови; лектин C-типа, который содержится в ациарогликопротеиновом рецепторе и маннозосвязывающем рецепторе; A-домен, который содержится в рецепторе LDL; аннексин, тромбоспондин домен 3 типа и EGF-подобный домен.
Специфичность
"Специфичный" означает, что молекула не проявляет никакого существенного связывания с молекулами, отличными от одной или нескольких молекул-партнеров по связыванию. Более того, "специфичный" также используют, когда антигенсвязывающий домен является специфичным к конкретному эпитопу среди множества эпитопов в антигене. Когда эпитоп, связываемый антигенсвязывающим доменом, содержится в нескольких различных антигенах, антигенсвязывающие молекулы, содержащие антигенсвязывающий домен, могут связываться с различными антигенами, которые имеют этот эпитоп.
Антитело
В рамках настоящего изобретения "антитело" относится к природному иммуноглобулину или иммуноглобулину, полученному частичным или полным синтезом. Антитела можно выделять из природных источников, таких как природная плазма и сыворотка, или из культуральных супернатантов продуцирующих антитела гибридом. Альтернативно, антитела можно частично или полностью синтезировать с использованием способов, таких как генетическая рекомбинация. Предпочтительные антитела включают, например, антитела изотипа иммуноглобулинов или принадлежащего ему подкласса. Известные иммуноглобулины человека включают антитела следующих девяти классов (изотипов): IgG1, IgG2, IgG3, IgG4, IgA1, IgA2, IgD, IgE и IgM. Из этих изотипов антитела по настоящему изобретению включают IgG1, IgG2, IgG3 и IgG4.
Способы получения антитела с желаемой активностью связывания известны специалистам в данной области. Ниже приведен пример, в котором описан способ получения антитела, которое связывается с IL-6R (антитело против IL-6R). Антитела, которые связываются с антигеном, отличным от IL-6R, также можно получать в соответствии с примером, описанным ниже.
Антитела против IL-6R можно получать в качестве поликлональных или моноклональных антител с использованием известных способов. Продуцируемые антитела против IL-6R предпочтительно представляют собой моноклональные антитела, происходящие из млекопитающих. Такие происходящие из млекопитающих моноклональные антитела включают антитела, продуцируемые гибридомами или клетками-хозяевами, трансформированными экспрессирующим вектором, несущим ген антитела, способами генетической инженерии. Моноклональные антитела по настоящему изобретению включают "гуманизированные антитела" или "химерные антитела".
Продуцирующие моноклональные антитела гибридомы можно получать с использованием известных способов, например, как описано ниже. В частности, млекопитающих иммунизируют общепринятыми способами иммунизации с использованием белка IL-6R в качестве сенсибилизирующего антигена. Полученные иммунные клетки подвергают слиянию с известными родительскими клетками общепринятыми способами слияния клеток. Затем гибридомы, продуцирующие антитело против IL-6R, можно отбирать путем скрининга продуцирующих моноклональное антитело клеток с использованием общепринятых способов скрининга.
В частности, моноклональные антитела получают так, как описано ниже. Сначала можно экспрессировать ген IL-6R, нуклеотидная последовательность которого представлена в SEQ ID NO: 16, для получения белка IL-6R, представленного в SEQ ID NO: 15, который будет использован в качестве сенсибилизирующего антигена для получения антитела. Для этого, последовательность гена, кодирующего IL-6R, встраивают в известный экспрессирующий вектор, и подходящие клетки-хозяева трансформируют этим вектором. Желаемый белок IL-6R человека очищают из клеток-хозяев или их культуральных супернатантов известными способами. Для получения растворимого IL-6R из культуральных супернатантов, например, белок, состоящий из аминокислот в положениях 1-357 в полипептидной последовательности IL-6R SEQ ID NO: 15, такой как описана в Mullberg et al. (J. Immunol. (1994) 152 (10), 4958-4968), экспрессируют в качестве растворимого IL-6R вместо белка IL-6R SEQ ID NO: 15. Также в качестве сенсибилизирующего антигена можно использовать очищенный природный белок IL-6R.
Очищенный белок IL-6R можно использовать в качестве сенсибилизирующего антигена для иммунизации млекопитающих. Также в качестве сенсибилизирующего антигена можно использовать неполный пептид IL-6R. В этом случае, неполный пептид можно получать путем химического синтеза на основе аминокислотной последовательности IL-6R человека, или путем встраивания неполного гена IL-6R в экспрессирующий вектор для экспрессии. Альтернативно, неполный пептид можно получать путем деградации белка IL-6R протеазой. Длина и область неполного пептида IL-6R не ограничены конкретными вариантами осуществления. Предпочтительная область может быть произвольным образом выбрана из аминокислотной последовательности в положениях аминокислот 20-357 аминокислотной последовательности SEQ ID NO: 15. Количество аминокислот, образующих пептид, подлежащий применению в качестве сенсибилизирующего антигена, предпочтительно составляет по меньшей мере пять или более, шесть или более, или семь или более. Более конкретно, в качестве сенсибилизирующего антигена можно использовать пептид из 8-50 остатков, более предпочтительно, из 10-30 остатков.
Альтернативно, для сенсибилизирующего антигена можно использовать слитый белок, полученный путем слияния желаемого неполного полипептида или пептида белка IL-6R с отличающимся полипептидом. Например, предпочтительно в качестве сенсибилизирующих антигенов используют Fc-фрагменты антител и пептидные метки. Векторы для экспрессии таких слитых белков можно конструировать путем слияния в рамке считывания генов, кодирующих два или более желаемых полипептидных фрагментов, и встраивания слитого гена в экспрессирующий вектор, как описано выше. Способы получения слитых белков описаны в Molecular Cloning 2nd ed. (Sambrook, J et al., Molecular Cloning 2nd ed., 9.47-9.58 (1989) Cold Spring Harbor Lab. Press). Способы получения IL-6R для применения в качестве сенсибилизирующего антигена и способы иммунизации с использованием IL-6R конкретно описаны в WO 2003/000883, WO 2004/022754, WO 2006/006693 и т.п.
Отсутствуют конкретное ограничение на млекопитающих, подлежащих иммунизации сенсибилизирующим антигеном. Однако предпочтительно выбирать млекопитающих, учитывая их совместимость с родительскими клетками, используемыми для слияния клеток. Как правило, предпочтительно используют грызунов, таких как мыши, крысы и хомячки, кроликов и обезьян.
Указанных выше животных иммунизируют сенсибилизирующим антигеном известными способами. Как правило, выполняемые способы иммунизации включают, например, внутрибрюшинное или подкожное введение сенсибилизирующего антигена млекопитающим. В частности, сенсибилизирующий антиген соответствующим образом разбавляют PBS (фосфатно-солевой буфер), физиологическим солевым раствором или сходными с ними. Если желательно, общепринятый адъювант, такой как полный адъювант Фрейнда, смешивают с антигеном и смесь эмульгируют. Затем сенсибилизирующий антиген вводят млекопитающем несколько раз с интервалами 4-21 суток. При иммунизации сенсибилизирующим антигеном можно использовать подходящие носители. В частности, когда в качестве сенсибилизирующего антигена используют низкомолекулярный неполный пептид, иногда желательно связывать сенсибилизирующий антигенный пептид с белком-носителем, таким как альбумин или гемоцианин лимфы улитки, для иммунизации.
Альтернативно, гибридомы, продуцирующие желаемое антитело, можно получать с использованием способов иммунизации ДНК, как описано ниже. Иммунизация ДНК представляет собой способ иммунизации, который обеспечивает стимуляцию иммунной системы путем экспрессии сенсибилизирующего антигена у животного, имунизированного в результате введения векторной ДНК, сконструированной для обеспечения экспрессии гена, кодирующего антигенный белок, у животного. По сравнению с общепринятыми способами иммунизации, в которых белковый антиген вводят животным, подлежащим иммунизации, иммунизация ДНК является лучшей в том, что:
- может быть обеспечена стимуляция иммунной системы при сохранении структуры мембранного белка, такого как IL-6R; и
- отсутствует необходимость в очистке антигена для иммунизации.
Для получения моноклонального антитела по настоящему изобретению с использованием иммунизации ДНК, сначала ДНК, экспрессирующую белок IL-6R, вводят животному, подлежащему иммунизации. ДНК, кодирующую IL-6R, можно синтезировать известными способами, такими как ПЦР. Полученную ДНК встраивают в соответствующий экспрессирующий вектор, а затем его вводят животному, подлежащему иммунизации. Предпочтительно используемые экспрессирующие векторы включают, например, коммерчески доступные экспрессирующие векторы, такие как pcDNA3.1. Векторы можно вводить в организм с использованием общепринятых способов. Например, иммунизацию ДНК проводят с использованием генной пушки для введения покрытых экспрессирующим вектором частиц золота в клетки организма животного, подлежащего иммунизации. Антитела, которые распознают IL-6R. также можно получать способами, описанными в WO 2003/104453.
После иммунизации млекопитающего, как описано выше, увеличение титра связывающего IL-6R антитела подтверждают в сыворотке. Затем иммунные клетки собирают от млекопитающего, а затем подвергают слиянию клеток. В частности, предпочтительно в качестве иммунных клеток используют спленоциты.
В качестве клетки, подлежащей слиянию с упомянутыми выше иммунными клетками, используют клетки миеломы млекопитающих. Клетки миеломы предпочтительно содержат подходящий селективный маркер для скрининга. Селективный маркер придает клеткам характеристики для их выживания (или гибели) в конкретных условиях культивирования. В качестве селективных маркеров известны дефицит гипоксантин-гуанин-фосфорибозилтрансферазы (далее сокращенно обозначаемый как дефицит HGPRT) и дефицит тимидинкиназы (далее сокращенно обозначаемый как дефицит TK). Клетки с дефицитом HGPRT или TK обладают чувствительностью к гипоксантину-аминоптерину-тимидину (далее сокращенно обозначаемой чувствительностью HAT). Чувствительные к HAT клетки не могут синтезировать ДНК в селективной среде HAT, и, таким образом, погибают. Однако, когда клетки слиты с нормальными клетками, они могут продолжать синтезировать ДНК с использованием пути спасения нормальных клеток, и, таким образом, они могут расти в селективной среде HAT.
Селекцию клеток с дефицитом HGPRT и TK можно проводить в среде, содержащей 6-тиогуанин, 8-азагуанин (далее сокращенно обозначаемый как 8AG) или 5’-бромдезоксиуридин, соответственно. Нормальные клетки погибают, поскольку они включают аналоги пиримидина в их ДНК. Между тем, клетки, которые являются дефицитными по этим ферментам, могут выживать в селективной среде, поскольку они не могут включать эти аналоги пиримидина. Кроме того, селективный маркер, называемый устойчивостью к G418, обеспечиваемый геном устойчивости к неомицину, обеспечивает устойчивость к 2-дезоксистрептаминовым антибиотикам (аналоги гентамицина). Известны различные типы миеломных клеток, которые пригодны для слияния клеток.
Например, предпочтительно можно использовать миеломные клетки, включающие следующие клетки:
P3(P3x63Ag8,653) (J. Immunol. (1979) 123 (4), 1548-1550);
P3x63Ag8U.1 (Current Topics in Microbiology и Immunology (1978)81, 1-7);
NS-1 (C. Eur. J. Immunol. (1976)6 (7), 511-519);
MPC-11 (Cell (1976) 8 (3), 405-415);
SP2/0 (Nature (1978) 276 (5685), 269-270);
FO (J. Immunol. Methods (1980) 35 (1-2), 1-21);
S194/5.XX0.BU.1 (J. Exp. Med. (1978) 148 (1), 313-323);
R210 (Nature (1979) 277 (5692), 131-133), и т.д.
Слияние клеток между иммуноцитами и клетками миеломы по существу проводят с использованием известных способов, например, способа Kohler and Milstein et al. (Methods Enzymol. (1981) 73: 3-46).
Более конкретно, слияние клеток можно проводить, например, в общепринятой культуральной среде в присутствии агента, обеспечивающего слияние клеток. Агенты, обеспечивающие слияние клеток, включают, например, полиэтиленгликоль (PEG) и вирус Сендай (HVJ). Если необходимо, также можно добавлять вспомогательное вещество, такое как диметилсульфоксид, для повышения эффективности слияния.
Соотношение иммунных клеток к клеткам миеломы можно определять самостоятельно, предпочтительно, например, оно составляет одну клетку миеломы на каждые от одного до десяти иммуноцитов. Культуральные среды, используемые для слияния клеток, включают, например, среды, которые пригодны для выращивания клеточных линий, такие как среда RPMI1640 и среда MEM, и другие общепринятые культуральные среды, используемые для этого типа клеточной культуры. Кроме того, предпочтительно в культуральную среду можно добавлять сывороточные добавки, такие как эмбриональная телячья сыворотка (FCS).
Для слияния клеток заданные количества указанных выше иммунных клеток и миеломных клеток смешивают в описанной выше культуральной среде. Затем добавляют раствор PEG (например, средняя молекулярная масса составляет приблизительно от 1000 до 6000), предварительно нагретый до приблизительно 37°C, в концентрации, как правило, от 30% до 60% (масс./об.). Затем эту смесь осторожно перемешивают для получения желаемых слитых клеток (гибридом). Затем к клеткам постепенно добавляют подходящую культуральную среду, упомянутую выше, и смесь многократно центрифугируют для удаления супернатанта. Таким образом, можно удалить агенты слияния клеток и т.п., которые являются неблагоприятными для роста гибридомы.
Селекцию полученных таким образом гибридом можно проводить путем культивирования с использованием общепринятой селективной среды, например, среды HAT (культуральная среда, содержащая гипоксантин, аминоптерин и тимидин). Клетки, отличные от желаемых гибридом (неслитые клетки) можно уничтожать путем продолжения культивирования в описанной выше среде HAT в течение достаточного периода времени. Как правило, период составляет от нескольких суток до нескольких недель. Затем, гибридомы, продуцирующие желаемое антитело, подвергают скринингу и клонируют по отдельности общепринятыми способами лимитирующих разведений.
Селекцию полученных таким образом гибридом можно проводить с использованием селективной среды на основе селективного маркера, которым обладает миелома, используемая для слияния клеток. Например, селекцию клеток с дефицитом HGPRT или TK можно проводить путем культивирования с использованием среды HAT (культуральная среда, содержащая гипоксантин, аминоптерин и тимидин). В частности, когда для слияния клеток используют чувствительные к HAT миеломные клетки, клетки, успешно слитые с нормальными клетками, могут селективно пролиферировать в среде HAT. Клетки, отличные от желаемых гибридом (неслитые клетки), можно уничтожать путем продолжения культивирования в описанной выше среде HAT в течение достаточного периода времени. В частности, селекцию желаемых гибридом можно проводить путем культивирования, как правило, в течение от нескольких суток до нескольких недель. Затем гибридомы, продуцирующие желаемое антитело, подвергают скринингу и по отдельности клонируют общепринятыми способами лимитирующих разведений.
Желаемые антитела можно предпочтительно отбирать и по отдельности клонировать способами скрининга на основе известной реакции антиген/антитело. Например, связывающее IL-6R моноклональное антитело может связываться с IL-6R, экспрессированным на поверхности клетки. Такое моноклональное антитело можно подвергать скринингу с помощью активированной флуоресценцией сортировки клеток (FACS). FACS представляет собой систему, которая оценивает связывание антитела с клеточной поверхностью путем анализа клеток, контактирующих с флуоресцентным антителом с использованием лазерного луча и измерения флуоресценции, испускаемой индивидуальными клетками.
Для скрининга гибридом, которые продуцируют моноклональные антитело по настоящему изобретению, с помощью FACS, сначала получают экспрессирующие IL-6R клетки. Клетки, предпочтительно используемые для скрининга, представляют собой клетки млекопитающих, в которых IL-6R экспрессируется вынужденным образом. В качестве контроля можно проводить селективное выявление активности антитела, которое связывается с IL-6R клеточной поверхности, с использованием в качестве клеток-хозяев нетрансформированных клеток млекопитающих. В частности, гибридомы, продуцирующие моноклональное антитело против IL-6R, можно выделять путем селекции гибридом, которые продуцируют антитело, которое связывает с клетками, в которых экспрессируется IL-6R вынужденным образом, но не с клетками-хозяевами.
Альтернативно, активность связывания антитела с иммобилизованными экспрессирующими IL-6R клетками можно оценивать на основе принципа ELISA. Например, экспрессирующие IL-6R клетки иммобилизуют на лунках планшета для ELISA. Культуральные супернатанты гибридом контактируют с иммобилизованными клетками в лунках, и выявляют антитела, которые связываются с иммобилизованными клетками. Когда моноклональные антитела происходят из мыши, антитела, связанные с клетками, можно выявлять с использованием антитела против иммуноглобулина мыши. Селекцию гибридом, продуцирующих желаемое антитело, обладающее антигенсвязывающей способностью, проводят с помощью описанного выше скрининга, и их можно клонировать способом лимитирующих разведений и т.п.
Продуцирующие моноклональное антитело гибридомы, полученные таким образом, можно пассировать в общепринятой культуральной среде и хранить в жидком азоте в течение длительного периода времени.
Описанные выше гибридомы культивируют общепринятым способом, и желаемые моноклональные антитела можно получать из культуральных супернатантов. Альтернативно, гибридомы вводят совместимым млекопитающим и выращивают в них, и моноклональные антитела получают из асцитной жидкости. Первый из этих способов пригоден для получения антител с высокой чистотой.
Предпочтительно также можно использовать антитела, кодируемые генами антител, которые клонированы из антителопродуцирующих клеток, таких как описанные выше гибридомы. Клонированный ген антитела встраивают в подходящий вектор, и его вводят в клетку-хозяина для экспрессии антитела, кодируемого геном. Способы выделения генов антител, встраивания генов в векторы и трансформации клеток-хозяев, уже разработаны, например, Vandamme et al. (Eur. J. Biochem. (1990) 192(3), 767-775). Способы продуцирования рекомбинантных антител также известны, как описано ниже.
Например, кДНК, кодирующую вариабельную область (V-область) антитела против IL-6R, получают из клеток гибридомы, экспрессирующих антитело против IL-6R. Для этой цели сначала из гибридом экстрагируют тотальную РНК. Способы, используемые для экстракции мРНК из клеток, включают, например:
- способ ультрацентрифугирования с гуанидином (Biochemistry (1979) 18(24), 5294-5299), и
- способ AGPC (Anal. Biochem. (1987) 162(1), 156-159)
Экстрагированные мРНК можно очищать с использованием набора для очистки мРНК mRNA Purification Kit (GE Healthcare Bioscience) и т.п. Альтернативно, также коммерчески доступны наборы для экстракции тотальной мРНК непосредственно из клеток, такие как набор для очистки мРНК QuickPrep mRNA Purification Kit (GE Healthcare Bioscience). мРНК можно получать из гибридом с использованием таких наборов. кДНК, кодирующие V-область антитела, можно синтезировать из полученных мРНК с использованием обратной транскриптазы. кДНК можно синтезировать с использованием набора для синтеза первой цепи кДНК с обратной транскриптазой AMV Reverse Transcriptase First-strand cDNA Synthesis Kit (Seikagaku Co.) и т.п. Более того, для синтеза и амплификации кДНК можно соответствующим образом использовать набор для амплификации кДНК SMART RACE cDNA amplification kit (Clontech) и способ 5’-RACE на основе ПЦР (Proc. Natl. Acad. Sci. USA (1988) 85(23), 8998-9002; Nucleic Acids Res. (1989) 17(8), 2919-2932). В таком способе синтеза кДНК на оба конца кДНК можно вносить подходящие участки для ферментов рестрикции, описанные ниже.
Представляющий интерес фрагмент кДНК очищают из полученного продукта ПЦР, а затем его лигируют в векторную ДНК. Таким образом, конструируют рекомбинантный вектор и вводят в E. coli и т.п. После селекции колоний из образующих колонии E. coli можно получать желаемый рекомбинантный вектор. Затем исследуют, имеет ли рекомбинантный вектор представляющую интерес нуклеотидную последовательность кДНК, известным способом, таким как способ с терминацией цепи дидезоксинуклеотидами.
Способ 5’-RACE, в котором используются праймеры для амплификации гена вариабельной области, удобно использовать для выделения гена, кодирующего вариабельную область. Сначала конструируют библиотеку кДНК 5’-RACE с помощью синтеза кДНК с использованием РНК, экстрагированных из клеток гибридом в качестве матрицы. Для синтеза библиотеки кДНК 5’-RACE соответствующим образом используют коммерчески доступный набор, такой как набор для амплификации кДНК SMART RACE.
Ген антитела амплифицируют способом ПЦР с использованием полученной библиотеки кДНК 5’-RACE в качестве матрицы. Праймеры для амплификации гена антитела мыши можно конструировать на основе известных последовательностей генов антител. Нуклеотидные последовательности праймеров варьируют, в зависимости от подкласса иммуноглобулинов. Таким образом, предпочтительно, чтобы подкласс был определен заранее с использованием коммерчески доступного набора, такого как набор для изотипирования моноклональных антител мыши Iso Strip mouse monoclonal antibody isotyping kit (Roche Diagnostics).
В частности, например, праймеры, которые обеспечивают амплификацию генов, кодирующих тяжелые цепи γ1, γ2a, γ2b и γ3 и легкие цепи κ и λ, используют для выделения генов, кодирующих IgG мыши. Как правило, для амплификации гена вариабельной области gG используют праймер, который гибридизуется с областью константной области вблизи вариабельной области, в качестве 3’-праймера. Между тем, в качестве 5’-праймера используют праймер, прилагаемый к набору для конструирования библиотеки кДНК 5’-RACE.
Продукты ПЦР, амплифицированные таким образом, используют для переформировывания иммуноглобулинов, состоящих из комбинации тяжелых и легких цепей. Селекцию желаемого антитела можно проводить с использованием активности связывания IL-6R переформированного иммуноглобулина в качестве индикатора. Например, когда задачей является выделение антитела против IL-6R, более предпочтительно, чтобы связывание антитела с IL-6R было специфическим. Скрининг связывающего IL-6R антитела можно проводить, например, с помощью следующих стадий:
(1) приведение экспрессирующей IL-6R клетки в контакт с антителом, содержащим V-область, кодируемую кДНК, выделенной из гибридомы;
(2) выявление связывания антитела с экспрессирующей IL-6R клеткой; и
(3) селекция антитела, которое связывается с экспрессирующей IL-6R клеткой.
Способы выявления связывания антитела с экспрессирующими IL-6R клетками известны. В частности, связывание антитела с экспрессирующими IL-6R клетками можно выявлять с помощью описанных выше способов, таких как FACS. Для оценки активности связывания антитела соответствующим образом используют иммобилизованные образцы экспрессирующих IL-6R клеток.
Предпочтительные способы скрининга антител, в которых в качестве индикатора используется активность связывания, также включают способы пэннинга с использованием фаговых векторов. Способы скрининга с использованием фаговых векторов являются преимущественными, когда гены антител выделяют из библиотек подклассов тяжелых цепей и легких цепей из популяции клеток, экспрессирующей поликлональное антитело. Гены, кодирующие вариабельные области тяжелых цепей и легких цепей, можно связывать соответствующей линкерной последовательностью с получением одноцепочечного Fv (scFv). Фаги, представляющие scFv на их поверхности, можно получать встраиванием гена, кодирующего scFv, в фаговый вектор. Фаги контактируют с представляющим интерес антигеном. Затем ДНК, кодирующую scFv, обладающие представляющей интерес активностью связывания, можно выделять путем сбора фагов, связанных с антигеном. Этот процесс можно повторять при необходимости для увеличения содержания scFv, обладающих представляющей интерес активностью связывания.
После выделения кДНК, кодирующей V-область представляющего интерес антитела против IL-6R, кДНК расщепляют ферментами рестрикции, которые распознают участки рестрикции, встроенные на обоих концах кДНК. Предпочтительные ферменты рестрикции распознают и расщепляют нуклеотидную последовательность, которая встречается в нуклеотидной последовательности гена антитела с низкой частотой. Более того, предпочтительно в представляющий интерес вектор вводят участок рестрикции для фермента, который образует липкий конец, для встраивания одной копии расщепленного фрагмента в правильной ориентации. Кодирующую кДНК V-область антитела против IL-6R расщепляют, как описано выше, и ее встраивают в соответствующий экспрессирующий вектор для конструирования экспрессирующего вектора для антитела. В этом случае, если ген, кодирующий константную область антитела (C-область), и ген, кодирующий описанную выше V-область, слить в рамке считывания, то получат химерное антитело. В рамках настоящего изобретения "химерное антитело" означает, что происхождение константной области отличается от вариабельной области. Таким образом, в дополнение к гетерохимерным антителам мыши/человека, химерные антитела по настоящему изобретению включают аллохимерные антитела человека/человека. Экспрессирующий вектор для химерного антитела можно конструировать путем встраивания гена V-области в экспрессирующий вектор, который уже имеет константную область. В частности, например, последовательность, распознаваемая первым ферментом рестрикции, который расщепляет выше гена V-области, можно соответствующим образом помещать на 5’-конец экспрессирующего вектора, содержащего ДНК, кодирующую желаемую константную область (C-область) антитела. Экспрессирующий вектор для химерного антитела конструируют путем слияния в рамке считывания двух генов, расщепленных одной и той же комбинацией ферментов рестрикции.
Для получения моноклонального антитела против IL-6R, гены антител встраивают в экспрессирующий вектор так, чтобы гены экспрессировались под контролем регулирующей экспрессию области. Регулирующая экспрессию область для экспрессии антитела включает, например, энхансеры и промоторы. Более того, на N-конец можно присоединять подходящую сигнальную последовательность, так чтобы экспрессируемое антитело секретировалось наружу клеток. Например, в качестве сигнальной последовательности можно использовать пептид, имеющий аминокислотную последовательность MGWSCIILFLVATATGVHS (SEQ ID NO: 113). Между тем, можно присоединять другие подходящие сигнальные последовательности. Экспрессированный полипептид расщепляется на С-конце описанной выше последовательности, и полученный полипептид секретируется из клеток в качестве зрелого полипептида. Затем подходящие клетки-хозяева трансформируют экспрессирующим вектором и получают рекомбинантные клетки, экспрессирущие ДНК, кодирующую антитело IL-6R.
ДНК, кодирующие тяжелую цепь (H-цепь) и легкую цепь (L-цепь) антитела, по отдельности встраивают в различные экспрессирующие векторы для экспрессии гена антитела. Молекулу антитела, имеющую H- и L-цепи, можно экспрессировать путем котрансфекции одной и той же клетки-хозяина векторами, в которые соответственно встроены гены H-цепи и L-цепи. Альтернативно, клетки-хозяева можно трансформировать одним экспрессирующим вектором, в который встроены ДНК, кодирующие H- и L-цепи (см. WO 1994011523).
Существуют различные известные комбинации клетка-хозяин/экспрессирующий вектор для получения антител путем введения выделенных генов антител в соответствующих хозяев. Все из этих экспрессирующих систем пригодны для выделения антигенсвязывающих доменов по настоящему изобретению. Подходящие эукариотические клетки, используемые в качестве клеток-хозяев, включают клетки животных, клетки растений и клетки грибов. В частности, клетки животных включают, например, следующие клетки.
(1) клетки млекопитающих: CHO, COS, клетки миеломы, клетки почки китайского хомячка (BHK), HeLa, Vero и т.п.;
(2) клетки земноводных: ооциты Xenopus и т.п.; и
(3) клетки насекомых: sf9, sf21, Tn5 и т.п.
Кроме того, в качестве клетки растений известна экспрессирующая система для генов антител с использованием клеток, происходящих из рода Nicotiana, таких как Nicotiana tabacum. Для трансформации клеток растений можно соответствующим образом использовать культивированные клетки каллуса.
Более того, в качестве клеток грибов можно использовать следующие клетки:
- дрожжи: род Saccharomyces, как например, Saccharomyces cerevisiae, и род Pichia, как например, Pichia pastoris; и
- нитчатые грибы: род Aspergillus, как например, Aspergillus niger.
Более того, также известны экспрессирующие системы для генов антител, в которых используются прокариотические клетки. Например, при использовании бактериальных клеток, в рамках настоящего изобретения можно подходящим образом использовать клетки E. coli, клетки Bacillus subtilis и т.п. Экспрессирующие векторы, несущие представляющие интерес гены антитела, вводят в клетки путем трансфекции. Трансфицированные клетки культивируют in vitro, и из культуры трансформированных клеток можно получать желаемое антитело.
В дополнение к описанным выше клеткам-хозяевам, также для получения рекомбинантного антитела можно использовать трансгенных животных. Следовательно, антитело можно получать из животного, которому введен ген, кодирующий представляющее интерес антитело. Например, ген антитела можно конструировать в качестве слитого гена путем встраивания в рамке считывания в ген, который кодирует белок, специфически продуцируемый в молоке. В качестве белка, секретируемого в молоке, можно использовать, например β-казеин козы и т.п. Фрагменты ДНК, содержащие слитый ген, в который встроен ген антитела, инъецируют в эмбрион козы, а затем этот эмбрион вводят в самку козы. Желаемые антитела можно получать в качестве белка, слитого с белком молока, из молока, продуцируемого трансгенной козой, родившейся от козы, являющейся реципиентом эмбриона (или ее потомства). Кроме того, для увеличения объема молока, содержащего желаемое антитело, продуцируемого трансгенной козой, трансгенной козе при необходимости можно вводить гормоны, Ebert, K. M. et al., Bio/Technology (1994) 12 (7), 699-702).
Когда антигенсвязывающую молекулу, описанную в настоящем описании, вводят человеку, антигенсвязывающий домен, происходящий из генетически рекомбинантного антитела, которое является искусственно модифицированным для снижения гетерологической антигенности против человека и т.п., можно соответствующим образом использовать в качестве антигенсвязывающего домена комплекса. Такие генетически рекомбинантные антитела включают, например, гуманизированные антитела. Эти модифицированные антитела получают соответствующим образом известными способами.
Вариабельная область антитела, используемая для получения антигенсвязывающего домена антигенсвязывающей молекулы, описанной в настоящем описании, как правило, образована тремя определяющими комплементарность областями (CDR) которые разделены четырьмя каркасными областями (FR). CDR представляет собой область, которая по существу определяет специфичность связывания антитела. Аминокислотные последовательности CDR являются в высокой степени разнообразными. С другой стороны, образующие FR аминокислотные последовательности часто обладают высокой идентичностью, даже среди антител с отличающейся специфичностью связывания. Таким образом, как правило, специфичность связывания определенного антитела можно вносить в другое антитело путем пересадки CDR.
Гуманизированное антитело также называют переформированным антителом человека. В частности, известны гуманизированные антитела, полученные пересадкой CDR антитела не являющегося человеком животного, такого как антитело мыши, в антитело человека и т.п. Также известны стандартные способы генной инженерии для получения гуманизированных антител. В частности, например, в качестве способа пересадки CDR антитела мыши в FR человека известна перекрывающаяся ПЦР с удлинением. В перекрывающейся ПЦР с удлинением, нуклеотидную последовательность, кодирующую CDR антитела мыши, подлежащую пересадке, добавляют к праймерам для синтеза FR антитела человека. Праймеры получают для каждой из четырех FR. Является общепризнанным, что при пересадке CDR мыши в FR человека, выбор FR человека, который имеет высокую идентичность FR мыши, является преимущественным для сохранения функции CDR. Таким образом, как правило, предпочтительно использовать FR человека, содержащую аминокислотную последовательность, которая обладает высокой идентичностью с аминокислотной последовательностью FR, соседней с CDR мыши, подлежащей пересадке.
Нуклеотидные последовательности, подлежащие лигированию, конструируют так, чтобы они были соединены друг с другом в рамке считывания. FR человека синтезируют по отдельности с использованием соответствующих праймеров. В результате получают продукты, в которых ДНК, кодирующая CDR мыши, связана с индивидуальными ДНК, кодирующими FR. Нуклеотидные последовательности, кодирующие CDR мыши, каждого продукта конструируют так, чтобы они перекрывались друг с другом. Затем проводят синтез комплементарной цепи для гибридизации перекрывающихся CDR-областей продуктов, синтезированных с использованием гена антитела человека в качестве матрицы. С помощью этой реакции FR человека лигируют через последовательности CDR мыши.
Полноразмерный ген V-области, в котором, в конечном итоге, лигированы три CDR и четыре FR, амплифицируют с использованием праймеров, которые гибридизуются с его 5’- или 3’-концом, в которые добавлены подходящие последовательности, распознаваемые ферментом рестрикции. Экспрессирующий вектор для гуманизированного антитела можно получать путем встраивания ДНК, полученной, как описано выше, и ДНК, которая кодирует C-область антитела человека, в экспрессирующий вектор, так чтобы они лигировались в рамке считывания. После трансфекции рекомбинантным вектором хозяина для получения рекомбинантных клеток, рекомбинантные клетки культивируют и ДНК, кодирующую гуманизированное антитело, экспрессируют с получением гуманизированного антитела в клеточной культуре (см., публикацию патента Европы № EP 239400 и международную публикацию патента № WO 1996/002576).
Путем качественного или количественного определения и оценки антигенсвязывающей активности гуманизированного антитела, полученного, как описано выше, можно пригодным образом отобрать FR антитела человека, которые позволяют CDR образовывать подходящий антигенсвязывающий центр при лигировании через CDR. Аминокислотные остатки в FR можно заменять при необходимости, так чтобы CDR переформированного анитетела человека образовывали соответствующий антигенсвязывающий центр. Например, мутации аминокислотной последовательности можно вносить в FR с использованием способа ПЦР, который используется для пересадки CDR мыши в FR человека. Более конкретно, в праймеры, которые гибридизуются с FR, можно вносить частичные мутации нуклеотидной последовательности. Мутации нуклеотидной последовательности вносятся в FR, синтезированные с использованием таких праймеров. Мутантные последовательности FR, имеющие желаемые характеристики, можно отбирать путем измерения и оценки активности мутанта антитела с замененной аминокислотой в отношении связывания с антигеном с помощью упомянутого выше способа (Cancer Res. (1993) 53: 851-856).
Альтернативно, желаемые антитела человека можно получать путем иммунизации трансгенных животных, имеющих полный набор генов антител человека (см. WO 1993/012227; WO 1992/003918; WO 1994/002602; WO 1994/025585; WO 1996/034096; WO 1996/033735) путем иммунизации ДНК.
Более того, также известны способы получения антител человека путем пэннинга с использованием библиотек антител человека. Например, V-область антитела человека экспрессируют в качестве одноцепочечного антитела (scFv) на поверхности фага способом фагового дисплея. Можно отбирать фаги, экспрессирующие scFv, которые связываются с антигеном. Последовательность ДНК, кодирующую V-область антитела человека, которая связывается с антигеном, можно определять путем анализа генов выбранных фагов. Определяют последовательность ДНК scFv, которая связывается с антигеном. Получают экспрессирующий вектор путем слияния последовательности V-области в рамке считывания с последовательностью C-области желаемого антитела человека и встраивания ее в соответствующий экспрессирующий вектор. Экспрессирующий вектор вводят в клетки, пригодные для экспрессии, такие как клетки, описанные выше. Антитело человека можно получать путем экспрессии гена, кодирующего антитело человека, в клетках. Эти способы уже известны (см. WO 1992/001047; WO 1992/020791; WO 1993/006213; WO 1993/011236; WO 1993/019172; WO 1995/001438; WO 1995/015388).
В дополнение к способам, описанным выше, для выделения генов антител можно соответствующим образом использовать способы клонирования B-клеток (идентификация каждой кодирующей антитело последовательности, ее клонирование и выделение; использование при конструировании экспрессирующего вектора для получения каждого антитела (IgG1, IgG2, IgG3 или IgG4, в частности); и т.п.), как описано, например Bernasconi et al. (Science (2002) 298: 2199-2202) или в WO 2008/081008.
Система нумерации EU
В соответствии со способами, используемыми в рамках настоящего изобретения, положения аминокислот, приписываемые CDR и FR антитела, указаны в соответствии с нумерацией по Kabat (Sequences of Proteins of Immunological Interest (National Institute of Health, Bethesda, Md., 1987 и 1991)). В рамках настоящего изобретения, когда антигенсвязывающая молекула представляет собой антитело или антигенсвязывающий фрагмент, аминокислоты вариабельной области указаны в соответствии с нумерацией по системе Kabat, в то время как аминокислоты константной области указаны в соответствии с системой нумерации EU на основе положений аминокислот по Kabat.
Захват антигена в клетки или ускорение захвата антигена в клетки
В рамках настоящего изобретения, "захват антигена в клетки", опосредуемый антигенсвязывающими молекулами, означает, что антигены включают в клетки путем эндоцитоза. В рамках настоящего изобретение, "ускорение захвата антигена в клетки" означает увеличение скорости захвата клетками антигенсвязывающей молекулы, которая связалась с антигеном в плазме, и/или снижение количество антигена, рециклирующего в плазму, после захвата. В рамках настоящего изобретения скорость захвата в клетки может быть увеличенной по сравнению со скоростью захвата в клетки антигенсвязывающей молекулы до снижения ее антигенсвязывающей активности в условиях низкой концентрации кальция так, чтобы она была ниже, чем в условиях высокой концентрации кальция. Таким образом, в рамках настоящего изобретения, то, способствует ли антигенсвязывающая молекула захвату антигена в клетки, можно оценивать на основе увеличения скорости захвата антигена в клетки. Скорость захвата антигена в клетки можно вычислять, например, путем мониторинга с течением времени снижения концентрации антигена в культуральной среде, содержащей клетки, экспрессирующие FcRn человека, после добавления антигена и антигенсвязывающей молекулы в среду, или путем мониторинга с течением времени величины захвата антигена в экспрессирующие FcRn человека клетки.
С использованием способов по настоящему изобретению для увеличения скорости опосредуемого антигенсвязывающей молекулой захвата антигена в клетки, например, путем введения антигенсвязывающих молекул, можно увеличивать скорость элиминации антигена из плазмы. Таким образом, оценку того, увеличивается ли опосредуемый антигенсвязывающей молекулой захват антигена в клетки, также можно проводить, например, путем исследования того, увеличивается ли скорость элиминации антигена из плазмы или снижается ли концентрация антигена в плазме при введении антигенсвязывающей молекулы. В частности, снижение концентрации антигена в плазме также можно ускорять путем введения антигенсвязывающих молекул по настоящему изобретению.
Количество раз связывания антигена одной антигенсвязывающей молекулой
В рамках настоящего изобретения, "количество раз связывания антигена одной антигенсвязывающей молекулой" означает количество раз связывания антигена, которое может быть достигнуто одной антигенсвязывающей молекулой до ее элиминации вследствие деградации. В рамках настоящего изобретения, "увеличение количества раз связывания антигена одной антигенсвязывающей молекулой" означает увеличение количества циклов, которые могут быть достигнуты одной антигенсвязывающей молекулой до ее элиминации вследствие деградации, если в качестве "одного цикла" определять процесс, при котором антигенсвязывающая молекула связывается с антигеном в плазме, и антигенсвязывающая молекула, связанная с антигеном, захватывается в клетки, и диссоциирует от антигена в эндосоме, а затем антигенсвязывающая молекула возвращается в плазму. В рамках настоящего изобретения, количество циклов может быть увеличено по сравнению с количеством циклов для антигенсвязывающей молекулы, антигенсвязывающая активность которой в условиях низкой концентрации кальция не является более низкой, чем в условиях высокой концентрации кальция, или количеством циклов антигенсвязывающей молекулы до снижения ее антигенсвязывающей активности в условиях низкой концентрации кальция так, чтобы она была ниже, чем антигенсвязывающая активность в условиях высокой концентрации кальция. Таким образом, оценку того, увеличивается ли количество циклов, можно проводить путем исследования того, "ускоряется ли захват в клетки", как описано выше, или того "увеличивается ли удержание в плазме", как описано ниже.
Увеличение удержания в плазме
В рамках настоящего изобретения, "увеличение удержания в плазме" является взаимозаменяемым с "повышением фармакокинетики", "улучшением фармакокинетики", "улучшенной фармакокинетикой", "усилением удержания в плазме", "повышением удержания в плазме" или "пролонгированием удержания в плазме". Эти выражения являются синонимами.
В рамках настоящего изобретения, "увеличение удержания в плазме" означает не только пролонгирование периода времени до элиминации из плазмы (например, пока антигенсвязывающая молекула не деградирует внутреклеточно и т.п. и может вернуться в плазму) после введения антигенсвязывающей молекулы животным, таким как человек, мыши, крысы, обезьяны, кролики и собаки, но также пролонгирование удержания в плазме антигенсвязывающих молекул в форме, которая обеспечивает связывание антигена (например, в свободной от антигена форме антигенсвязывающей молекулы) в ходе периода введения до элиминации вследствие деградации. В частности, "увеличение удержания в плазме" также включает пролонгирование периода времени до элиминации вследствие деградации антигенсвязывающей молекулы, не связанной с антигенами (свободная от антигена форма антигенсвязывающей молекулы).
Антигенсвязывающая молекула в плазме не может связываться с новым антигеном, если антигенсвязывающая молекула уже связалась с антигеном. Таким образом, чем более длительным является период времени, в ходе которого антигенсвязывающая молекула не связана с антигеном, тем более длительным является период времени, в ходе которого она может связываться с новым антигеном (более высокая вероятность связывания с другим антигеном). Это обеспечивает снижение периода времени, когда антиген свободен от антигенсвязывающей молекулы in vivo и пролонгирование периода времени, в ходе которого антиген связан с антигенсвязывающей молекулой. Путем ускорения элиминации антигена из плазмы при введении антигенсвязывающей молекулы может быть увеличена концентрация в плазме свободной от антигена формы антигенсвязывающей молекулы, и период времени, в ходе которого антиген связан с антигенсвязывающей молекулой, может быть пролонгирован. В частности, как используют в рамках изобретения, "повышение удержания в плазме антигенсвязывающей молекулы" включает улучшение любого фармакокинетического параметра (такое как пролонгирование времени полужизни в плазме, пролонгирование среднего времени удержания в плазме или снижение клиренса в плазме) свободной от антигена антигенсвязывающей молекулы по настоящему изобретению, пролонгирование периода времени, когда антиген связан с антигенсвязывающей молекулой, после введения антигенсвязывающей молекулы, и увеличение элиминации антигена из плазмы антигенсвязывающей молекулой, по сравнению со свободной от антигена антигенсвязывающей молекулой, антигенсвязывающая активность которой в условиях низкой концентрации кальция не является более низкой, чем в условиях высокой концентрации кальция, или свободной от антигена антигенсвязывающей молекулой до снижения ее антигенсвязывающей активности в условиях низкой концентрации кальция так, чтобы она была ниже, чем в условиях высокой концентрации кальция.
То, улучшаются ли фармакокинетические параметры, можно оценивать путем определения любого из параметров: время полужизни в плазме, среднее время удержания в плазме и клиренс из плазмы, для антигенсвязывающей молекулы или ее свободной от антигена формы ("Pharmacokinetics: Enshu-niyoru Rikai (Understanding through practice)" Nanzando). Например, концентрацию в плазме антигенсвязывающей молекулы или ее свободной от антигена формы определяют после введения антигенсвязывающей молекулы мышам, крысам, обезьянам, кроликам, собакам или человеку. Затем, определяют каждый параметр. Когда время полужизни в плазме или среднее время удержания в плазме пролонгируются, можно считать, что время удержания антигенсвязывающей молекулы в плазме повышается. Параметры можно определять способами, известными специалистам в данной области. Параметры можно оценивать соответствующим образом, например, с помощью некомпартментного анализа с использованием программного обеспечения для фармакокинетического анализа WinNonlin (Pharsight) в соответствии с инструкцией по применению. Концентрацию в плазме свободной от антигена формы антигенсвязывающей молекулы можно определять способами, известными специалистам в данной области, например, с использованием способа анализа, описанного в Clin Pharmacol. 2008 Apr; 48(4): 406-17.
В рамках настоящего изобретения, "повышение удержания в плазме" также включает пролонгирование периода, когда антиген связан с антигенсвязывающей молекулой, после введения антигенсвязывающей молекулы. Оценку того, пролонгируется ли период, когда антиген связан с антигенсвязывающей молекулой после введения антигенсвязывающей молекулы, можно проводить на основе времени до увеличения концентрации (соотношения) при измерении концентрации в плазме не связанного антигенсвязывающей молекулой антигена (свободного антигена) или отношения концентрации не связанного антигенсвязывающей молекулой антигена (концентрация свободного антигена) к общей концентрации антигена.
В рамках настоящего изобретения, "концентрацию антигена в плазме" можно определять путем измерения концентрации в плазме свободного от антигенсвязывающей молекулы антигена или отношения концентрации свободного от антигенсвязывающей молекулы антигена к общей концентрации антигена, с использованием способов, известных специалистам в данной области, например, способов измерения, описанных в Pharm Res. 2006 Jan; 23(1): 95-103.
Альтернативно, когда антиген проявляет конкретную функцию in vivo, оценку того, связан ли антиген с антигенсвязывающей молекулой, которая нейтрализует функцию антигена (антагонистическая молекула), можно проводить путем исследования того, нейтрализуется ли функция антигена. Оценку того, нейтрализуется ли функция антигена, можно проводить, путем анализа маркера in vivo, который отражает функцию антигена. Оценку того, связан ли антиген с антигенсвязывающей молекулой, которая активирует функцию антигена (молекула-агонист), можно проводить путем анализа маркера in vivo, который отражает функцию антигена.
Определение концентрации свободного от антигенсвязывающей молекулы антигена в плазме и отношения концентрации свободного от антигенсвязывающей молекулы антигена к общей концентрации антигена, анализ маркеров in vivo и сходные способы определения конкретно не ограничены; однако анализы предпочтительно проводят после того, как проходит определенный период времени после введения антигенсвязывающей молекулы. В рамках настоящего изобретения, период после введения антигенсвязывающей молекулы конкретно не ограничен; специалисты в данной области могут определить соответствующий период, в зависимости от свойств и т.п. вводимой антигенсвязывающей молекулы. Такие периоды включают, например, одни сутки после введения антигенсвязывающей молекулы, трое суток после введения антигенсвязывающей молекулы, семь суток после введения антигенсвязывающей молекулы, 14 суток после введения антигенсвязывающей молекулы и 28 суток после введения антигенсвязывающей молекулы.
В рамках настоящего изобретения является предпочтительным увеличение удержания в плазме у человека. Когда удержание в плазме у человека трудно определить, его также можно предсказать исходя из удержания в плазме у мышей (например, нормальных мышей, экспрессирующих антиген человека трансгенных мышей, экспрессирующих FcRn человека трансгенных мышей) или обезьян (например, яванских макаков).
Диссоциация антигена в клетке от связавшейся с ним внеклеточно антигенсвязывающей молекулы
Настоящее изобретение также применимо в качестве способа ускорения диссоциации антигена в клетке от связавшейся с ним внеклеточно антигенсвязывающей молекулы. В рамках настоящего изобретения, антиген может диссоциировать от антигенсвязывающей молекулы в любом отделе клетки; однако предпочтительно, чтобы антиген диссоциировал в ранней эндосоме. В рамках настоящего изобретения, выражение "антиген диссоциирует в клетке от связавшейся с ним внеклеточно антигенсвязывающей молекулы" не обязательно означает, что каждый антиген, захваченный в клетку путем связывания внеклеточно с антигенсвязывающей молекулой, диссоциирует от антигенсвязывающей молекулы в клетке. Приемлемо, чтобы доля антигена, который диссоциирует от антигенсвязывающей молекулы в клетке, была более высокой, по сравнению с антигенсвязывающей молекулой, антигенсвязывающая активность которой в условиях низкой концентрации кальция не является более низкой, чем в условиях высокой концентрации кальция, или антигенсвязывающей молекулой до снижения антигенсвязывающей активности в условиях низкой концентрации кальция так, чтобы она была более низкой, чем в условиях высокой концентрации кальция. Способ ускорения диссоциации антигена в клетке от связавшейся с ним внеклеточно антигенсвязывающей молекулы также может быть назван способом сообщения антигенсвязывающей молекуле свойства, которое способствует ускорению внутриклеточного захвата антигенсвязывающей молекулы, связанной с антигеном, и ускорению внутриклеточной диссоциации антигена от антигенсвязывающей молекулы.
Высвобождение из клетки в свободной от антигена форме антигенсвязывающей молекулы, захваченной в клетку в связанной с антигеном форме
Настоящее изобретение также применимо в качестве способа усиления высвобождения из клетки в свободной от антигена форме антигенсвязывающей молекулы, захваченной в клетку в связанной с антигеном форме. В рамках настоящего изобретения, "высвобождение из клетки в свободной от антигена форме антигенсвязывающей молекулы, захваченной в клетку в связанной с антигеном форме" не обязательно означает, что каждая антигенсвязывающая молекула, связанная с антигеном и захваченная в клетку, высвобождается в свободной от антигена форме из клетки. Приемлемо, чтобы доля антигенсвязывающей молекулы, которая высвобождается в свободной от антигена форме из клетки, была более высокой по сравнению с антигенсвязывающей молекулой, антигенсвязывающая активность которой в условиях низкой концентрации кальция не является более низкой, чем в условиях высокой концентрации кальция, или антигенсвязывающей молекулой до снижения ее антигенсвязывающей активности в условиях низкой концентрации кальция так, чтобы она была более низкой, чем в условиях высокой концентрации кальция. Предпочтительно, чтобы антигенсвязывающая молекула, высвободившаяся из клетки, сохраняла антигенсвязывающую активность. Способ ускорения высвобождения из клетки антигенсвязывающей молекулы в свободной от антигена форме, захваченной в клетку в связанной с антигеном форме, также может быть назван способом сообщения антигенсвязывающей молекуле свойства, которое способствует ускорению внутриклеточного захвата антигенсвязывающей молекулы, связанной с антигеном, и ускорения высвобождения из клетки антигенсвязывающей молекулы в свободной от антигена форме.
Условия концентрации кальция
В рамках настоящего изобретения условия низкой концентрации кальция, как правило, означают, что концентрация ионизированного кальция составляет от 0,1 мкМ до 30 мкМ, предпочтительно от 0,5 мкМ до 10 мкМ, и особенно предпочтительно от 1 мкМ до 5 мкМ, что сравнимо с концентрацией ионизированного кальция в ранней эндосоме in vivo. Между тем, в рамках настоящего изобретения, условия высокой концентрации кальция, как правило, означают, что концентрация ионизированного кальция составляет от 100 мкМ до 10 мМ, предпочтительно от 200 мкМ до 5 мМ, и особенно предпочтительно от 0,5 мМ до 2,5 мМ, что сравнимо с концентрацией ионизированного кальция в плазме (крови) in vivo.
Таким образом, в рамках настоящего изобретения, выражение "антигенсвязывающая активность антигенсвязывающей молекулы является более низкой в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция" означает, что антигенсвязывающая активность антигенсвязывающей молекулы является более низкой при концентрации ионизированного кальция от 0,1 мкМ до 30 мкМ, чем при концентрации ионизированного кальция от 100 мкМ до 10 мМ. Предпочтительно оно означает, что антигенсвязывающая активность антигенсвязывающей молекулы является более низкой при концентрации ионизированного кальция от 0,5 мкМ до 10 мкМ, чем при концентрации ионизированного кальция от 200 мкМ до 5 мМ. Особенно предпочтительно, оно означает, что антигенсвязывающая активность является более низкой при концентрации ионизированного кальция в ранней эндосоме in vivo, чем при концентрации ионизированного кальция в плазме in vivo; в частности, оно означает, что антигенсвязывающая активность антигенсвязывающей молекулы является более низкой при концентрации ионизированного кальция от 1 мкМ до 5 мкМ, чем при концентрации ионизированного кальция от 0,5 мМ до 2,5 мМ.
Между тем, как используют в рамках изобретения, выражение "антигенсвязывающая активность антигенсвязывающей молекулы является более низкой в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция" является взаимозаменяемым с выражением "антигенсвязывающая активность антигенсвязывающей молекулы является более высокой в условиях высокой концентрации кальция, чем в условиях низкой концентрации кальция". Выражение "антигенсвязывающая активность антигенсвязывающей молекулы является более низкой в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция" также означает, что антигенсвязывающая активность антигенсвязывающей молекулы в условиях низкой концентрации кальция снижена так, чтобы она была более низкой, чем в условиях высокой концентрации кальция, или антигенсвязывающая активность антигенсвязывающей молекулы в условиях высокой концентрации кальция увеличена так, чтобы она была более высокой, чем в условиях низкой концентрации кальция, путем модификации аминокислотной последовательности антигенсвязывающей молекулы, и т.д. Следовательно, в рамках настоящего изобретения, соотношение между антигенсвязывающей активностью антигенсвязывающей молекулы в условиях низкой концентрации кальция и антигенсвязывающей активностью в условиях высокой концентрации кальция может быть увеличено. Например, в одном варианте осуществления соотношение KD (приблизительно 3 мкМ)/KD (Ca 2 мМ) может быть увеличено, как описано ниже. Соотношение между антигенсвязывающей активностью антигенсвязывающей молекулы в условиях низкой концентрации кальция и антигенсвязывающей активностью в условиях высокой концентрации кальция может быть увеличено, например, путем снижения антигенсвязывающей активности в условиях низкой концентрации кальция с помощью выбора антигенсвязывающей молекулы с низкой антигенсвязывающей активностью в условиях низкой концентрации кальция или с помощью модификации аминокислотной последовательности в антигенсвязывающей молекуле; или путем увеличения антигенсвязывающей активности в условиях высокой концентрации кальция с помощью выбора антигенсвязывающей молекулы с высокой антигенсвязывающей активностью в условиях высокой концентрации кальция или с помощью модификации аминокислотной последовательности в антигенсвязывающей молекуле; или обоими из этих способов.
В рамках настоящего изобретения выражение "антигенсвязывающая способность является более слабой в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция", иногда используют вместо выражения "антигенсвязывающая активность является более низкой в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция". Более того, выражение "ослабление антигенсвязывающей способности в условиях низкой концентрации кальция так, чтобы она была более низкой, чем в условиях высокой концентрации кальция", иногда используют вместо выражения "снижение антигенсвязывающей активности в условиях низкой концентрации кальция так, чтобы она была более низкой, чем в условиях высокой концентрации кальция".
FcRn
В отличие от Fcγ-рецептора, принадлежащего семейству иммуноглобулинов, FcRn, в частности, FcRn человека, структурно сходен с полипептидами главного комплекса гистосовместимости (MHC) класса I, проявляя 22%-29% идентичность последовательности с молекулами MHC класса I (Ghetie el al., Immunol. Today (1997) 18 (12): 592-598). FcRn экспрессируется в качестве гетеродимера, состоящего из растворимой β- или легкой цепи (β2-микроглобулин) в комплексе с трансмембранной α- или тяжелой цепью. Подобно MHC, α-цепь FcRn содержит три внеклеточных домена (α1, α2 и α3), и ее короткий цитоплазматический домен заякоривает белок на клеточной поверхности. α1- и α2-домены взаимодействуют с FcRn-связывающим доменом Fc-области антитела (Raghavan et al., Immunity (1994) 1: 303-315).
FcRn экспрессируется в материнской плаценте и желточном мешке млекопитающих, и он вовлечен в перенос IgG от матери к плоду. Кроме того, в тонком кишечнике новорожденных грызунов, где FcRn экспрессируется, FcRn вовлечен в перенос материнских IgG через эпителий щеточной каемки из проглоченного молозива или молока. FcRn экспрессируется во множестве других тканей и системах эндотелиальных клеток различных видов. FcRn также экспрессируется у взрослого человека в эндотелии, кровеносных сосудах мышц и синусоидных капиллярах печени. Полагают, что FcRn участвует в поддержании концентрации IgG в плазме путем опосредования рециклирования IgG в сыворотку при связывании с IgG. Как правило, связывание FcRn с молекулами IgG строго зависит от pH. Оптимальное связывание наблюдают при кислом диапазоне pH ниже 7,0.
FcRn человека, предшественником которого является полипептид, имеющий сигнальную последовательность SEQ ID NO: 17 (полипептид с сигнальной последовательностью представлен в SEQ ID NO: 18), образует комплекс с β2-микроглобулином человека in vivo. Растворимый FcRn человека в комплексе с β2-микроглобулином получают с использованием общепринятых способов рекомбинантной экспрессии. FcRn-связывающие домены по настоящему изобретению можно оценивать в отношении их активности связывания с таким растворимым FcRn человека в комплексе с β2-микроглобулином. В рамках настоящего изобретения, если нет иных указаний, FcRn человека относится к форме, способной связываться с FcRn-связывающим доменом по настоящему изобретению. Примеры включают комплекс между FcRn человека и β2-микроглобулином человека.
FcRn-связывающий домен
Антигенсвязывающие молекулы по настоящему изобретению имеют антигенсвязывающий домен и FcRn-связывающий домен человека. FcRn-связывающий домен человека конкретно не ограничен, при условии, что антигенсвязывающие молекулы проявляют активность связывания FcRn человека при кислых значениях pH и/или при нейтральных значениях pH. Альтернативно, домен может иметь прямую или непрямую активность связывания FcRn человека. Такие домены включают, например, Fc-область иммуноглобулина IgG-типа, альбумин, домен 3 альбумина, антитела против FcRn человека, пептиды против FcRn человека и каркасные молекулы против FcRn человека, все из которых обладают активностью прямого связывания с FcRn человека; и молекулы, которые связываются с IgG или альбумином, которые обладают активностью непрямого связывания с FcRn человека. Такие предпочтительные домены по настоящему изобретению обладают активностью связывания FcRn человека в кислых и нейтральных диапазонах pH. Можно использовать домены без какого-либо изменения, при условии, что они уже обладают активностью связывания FcRn человека в кислых и нейтральных диапазонах pH. Когда домены имеют только слабую активность связывания FcRn человека в кислых и/или нейтральных диапазонах pH, или не имеют ее, активность связывания FcRn человека можно сообщать путем изменения аминокислот в антигенсвязывающих молекулах. Однако предпочтительно, чтобы активность связывания FcRn человека в кислых и/или нейтральных диапазонах pH сообщалась путем изменения аминокислот в FcRn-связывающем домене человека. Альтернативно, аминокислоты в доменах, которые уже обладают активностью связывания FcRn человека в кислых и/или нейтральных диапазонах pH, можно изменять для увеличения активности связывания FcRn человека. Желаемые аминокислотные изменения в FcRn-связывающем домене человека можно отбирать путем сравнения активности связывания FcRn человека в кислых и/или нейтральных диапазонах pH до и после изменения аминокислот.
Предпочтительным FcRn-связывающим доменом человека является область, которая прямо связывается с FcRn человека. Такие предпочтительные связывающие FcRn человека области включают, например, Fc-области антител. Между тем, области, способные связываться с полипептидом, таким как альбумин или IgG, который обладает активностью связывания FcRn человека, можно непрямо связывать с FcRn человека через альбумин, IgG и т.п. Таким образом, такая FcRn-связывающая область человека по настоящему изобретению может представлять собой область, которая связывается с полипептидом, обладающим активностью связывания с альбумином или IgG. В частности, предпочтительным является FcRn-связывающий домен человека с более высокой активностью связывания FcRn человека при нейтральных значениях pH. FcRn-связывающий домен человека с более высокой активностью связывания FcRn человека при нейтральных значениях pH можно отбирать заранее. Альтернативно, активность связывания FcRn человека при нейтральных значениях pH можно сообщать или увеличивать путем модификации аминокислот в антигенсвязывающей молекуле.
Подходящие условия, отличные от значения pH, при котором определяют активность связывания с FcRn человека, могут быть выбраны специалистами в данной области. Условия конкретно не ограничены. Например, измерения можно проводить при 37°C с использованием буфера MES, как описано в WO 2009/125825. Между тем, активность связывания FcRn человека у антигенсвязывающей молекулы можно определять способами, известными специалистам в данной области, например, с использованием Biacore (GE Healthcare) и т.п. Активность связывания между антигенсвязывающей молекулой и FcRn человека можно оценивать путем нанесения FcRn человека или антигенсвязывающей молекулы в качестве анализируемого образца на чип, на котором иммобилизованы антигенсвязывающая молекула или FcRn человека, соответственно.
В рамках настоящего изобретения, активность связывания FcRn человека при кислых значениях pH означает активность связывания FcRn человека при pH 4,0-6,5, предпочтительно активность связывания FcRn человека при pH 5,5-6,5, и особенно предпочтительно активность связывания FcRn человека при pH 5,8-6,0, что сравнимо с pH в ранней эндосоме in vivo. Между тем, активность связывания FcRn человека при нейтральных значениях pH означает активность связывания FcRn человека при pH 6,7-10,0, предпочтительно активность связывания с FcRn человека при pH 7,0-pH 8,0, и особенно предпочтительно активность связывания с FcRn человека при pH 7,4, что сравнимо с pH в плазме in vivo.
Активность связывания с FcRn человека при нейтральных значениях pH можно сообщать или увеличивать в антигенсвязывающей молекуле путем модификации аминокислоты в молекуле. Например, когда Fc-область иммуноглобулина IgG-типа используют в качестве FcRn-связывающего домена человека, активность связывания с FcRn человека при нейтральных значениях pH можно сообщать или увеличивать в антигенсвязывающей молекуле путем модификации аминокислоты в FcRn-связывающем домене человека. Предпочтительная Fc-область иммуноглобулина IgG-типа, подлежащая изменению, включает, например, Fc-область природного IgG (IgG1, IgG2, IgG3 или IgG4) человека. Аминокислоты в любых областях можно заменять другими аминокислотами при условии, что сообщается или увеличивается активность связывания с FcRn человека при нейтральных значениях pH. Когда антигенсвязывающая молекула имеет Fc-область IgG1 человека в качестве FcRn-связывающего домена человека, предпочтительно, чтобы молекула имела изменения, которые усиливают связывание с FcRn человека при нейтральных значениях pH по сравнению с природным IgG1 человека. Аминокислоты, в которых может быть достигнуто такое изменение, включают, например, аминокислоты в положениях 221-225, 227, 228, 230, 232, 233-241, 243-252, 254-260, 262-272, 274, 276, 278-289, 291-312, 315-320, 324, 325, 327-339, 341, 343, 345, 360, 362, 370, 375-378, 380, 382, 385-387, 389, 396, 414, 416, 423, 424, 426-438, 440 и 442 (нумерация EU). Более конкретно, такие изменения аминокислот включают, например, изменения, приведенные в таблице 1. С использованием изменений, описанных выше, может быть увеличено (усилено) связывание FcRn человека с Fc-областью иммуноглобулина IgG-типа при нейтральных значениях pH. Более того, изменения, которые могут усиливать связывание с FcRn человека в кислом диапазоне pH по сравнению с природным IgG1 человека, представлены в качестве примера в таблице 2. Когда из описанных выше изменений выбирают подходящие изменения, которые также могут усиливать связывание с FcRn человека при нейтральных значениях pH, они применимы для настоящего изобретения.
"Изменение аминокислот" или "аминокислотное изменение" FcRn-связывающего домена включает изменение аминокислотной последовательности в исходном FcRn-связывающем домене на отличающиеся аминокислотные последовательности. В качестве исходного FcRn-связывающего домена можно использовать любой FcRn-связывающий домен, при условии, что варианты, полученные путем модификации исходного FcRn-связывающего домена, могут связываться с FcRn человека в нейтральном диапазоне pH. Более того, также предпочтительно в качестве FcRn-связывающего домена по настоящему изобретению можно использовать FcRn-связывающий домен, модифицированный из исходного FcRn-связывающего домена, который уже модифицирован. "Исходный FcRn-связывающий домен" может относиться к самому полипептиду, композиции, содержащей исходный FcRn-связывающий домен или полинуклеотидной последовательности, кодирующей исходный FcRn-связывающий домен. Исходные FcRn-связывающие домены могут содержать известную Fc-область, полученную путем рекомбинации, кратко описанной в разделе "Антитела". Источник исходных FcRn-связывающих доменов не ограничен, и их можно получать из человека или любых не являющихся человеком организмов. Такие организмы предпочтительно включают мышей, крыс, морских свинок, хомячков, песчанок, кошек, кроликов, собак, коз, овец, животных семейства бычьи, лошадей, верблюдов и организмов, выбранных из не являющихся человеком приматов. В другом варианте осуществления исходные FcRn-связывающие домены также можно получать из яванских макаков, мартышек, макаков-резус, шимпанзе или людей. Исходные FcRn-связывающие домены можно предпочтительно получать из IgG1 человека; однако они не ограничиваются каким-либо конкретным классом IgG. Это означает, что в качестве исходного FcRn-связывающего домена можно соответствующим образом использовать Fc-область IgG1, IgG2, IgG3 или IgG4 человека, и в рамках настоящего изобретения это также означает, что предпочтительно в качестве исходного FcRn-связывающего домена можно использовать Fc-область произвольного класса или подкласса IgG, происходящую из любых организмов, описанных выше. Примеры встречающихся в природе мутантов или модифицированных форм IgG описаны в опубликованных документах (Curr. Opin. Biotechnol. (2009) 20 (6): 685-91; Curr. Opin. Immunol. (2008) 20 (4), 460-470; Protein Eng. Des. Sel. (2010) 23 (4): 195-202; WO 2009/086320; WO 2008/092117; WO 2007/041635; и WO 2006/105338); однако они не ограничиваются этими примерами.
Примеры изменений включают изменения с одной или несколькими мутациями, например, мутациями путем замены другими аминокислотными остатками аминокислот исходных FcRn-связывающих доменов, путем встраивания одного или нескольких аминокислотных остатков в исходные FcRn-связывающие домены или путем делеции одной или нескольких аминокислот из исходных FcRn-связывающих доменов. Предпочтительно, аминокислотные последовательности измененных FcRn-связывающих доменов включают по меньшей мере часть аминокислотной последовательности неприродного FcRn-связывающего домена. Такие варианты обязательно обладают идентичностью или сходством последовательности с их исходным FcRn-связывающим доменом, меньшим чем 100%. В предпочтительном варианте осуществления варианты обладают идентичностью или сходством аминокислотной последовательности приблизительно от 75% до менее чем 100%, более предпочтительно приблизительно от 80% до менее чем 100%, еще более предпочтительно приблизительно от 85% до менее чем 100%, еще более предпочтительно, приблизительно от 90% до менее чем 100%, и еще более предпочтительно приблизительно от 95% до менее чем 100% с аминокислотной последовательностью их исходного FcRn-связывающего домена. В неограничивающем варианте осуществления настоящего изобретения по меньшей мере одна аминокислота отличается между модифицированным FcRn-связывающим доменом по настоящему изобретению и его исходным FcRn-связывающим доменом. Аминокислотное отличие между модифицированным FcRn-связывающим доменом по настоящему изобретению и его исходным FcRn-связывающим доменом также может быть предпочтительно указано на основе аминокислотных отличий в описанных выше конкретных положениях аминокислот в соответствии с системой нумерации EU.
Более того, изменения, которые могут усиливать связывание с FcRn человека в кислом диапазоне pH по сравнению с исходным IgG человека, представлены в качестве примера в таблице 2. Когда соответствующие изменения, которые могут также усиливать связывание с FcRn человека в нейтральном диапазоне pH, выбирают из описанных выше изменений, они применимы к настоящему изобретению. Между тем, комбинации изменений, которые могут усиливать связывание Fv4-IgG1 с FcRn человека в кислых условиях, представлены в таблицах 6-1 и 6-2. Особенно предпочтительные аминокислоты, подлежащие изменению в исходной Fc-области IgG человека, включают, например, аминокислоты в положениях 237, 238, 239, 248, 250, 252, 254, 255, 256, 257, 258, 265, 270, 286, 289, 297, 298, 303, 305, 307, 308, 309, 311, 312, 314, 315, 317, 325, 332, 334, 360, 376, 380, 382, 384, 385, 386, 387, 389, 424, 428, 433, 434 и 436 (нумерация EU).
Особенно предпочтительные изменения включают, например,
замена аминокислоты Gly на Met в положении 237;
замена аминокислоты Pro на Ala в положении 238;
замена аминокислоты Ser на Lys в положении 239;
замена аминокислоты Lys на Ile в положении 248;
замена аминокислоты Thr на Ala, Phe, Ile, Met, Gln, Ser, Val, Trp или Tyr в положении 250;
замена аминокислоты Met на Phe, Trp или Tyr в положении 252;
замена аминокислоты Ser на Thr в положении 254;
замена аминокислоты Arg на Glu в положении 255;
замена аминокислоты Thr на Asp, Glu или Gln в положении 256;
замена аминокислоты Pro на Ala, Gly, Ile, Leu, Met, Asn, Ser, Thr или Val в положении 257;
замена аминокислоты Glu на His в положении 258;
замена аминокислоты Asp на Ala в положении 265;
замена аминокислоты Asp на Phe в положении 270;
замена аминокислоты Asn на Ala или Glu в положении 286;
замена аминокислоты Thr на His в положении 289;
замена аминокислоты Asn на Ala в положении 297;
замена аминокислоты Ser на Gly в положении 298;
замена аминокислоты Val на Ala в положении 303;
замена аминокислоты Val на Ala в положении 305;
замена аминокислоты Thr на Ala, Asp, Phe, Gly, His, Ile, Lys, Leu, Met, Asn, Pro, Gln, Arg, Ser, Val, Trp или Tyr в положении 307;
замена аминокислоты Val на Ala, Phe, Ile, Leu, Met, Pro, Gln или Thr положении 308;
замена аминокислоты Leu или Val на Ala, Asp, Glu, Pro или Arg в положении 309;
замена аминокислоты Gln на Ala, His или Ile в положении 311;
замена аминокислоты Asp на Ala или His в положении 312;
замена аминокислоты Leu на Lys или Arg в положении 314;
замена аминокислоты Asn на Ala или His в положении 315;
замена аминокислоты Lys на Ala в положении 317;
замена аминокислоты Asn на Gly в положении 325;
замена аминокислоты Ile на Val в положении 332;
замена аминокислоты Lys на Leu в положении 334;
замена аминокислоты Lys на His в положении 360;
замена аминокислоты Asp на Ala в положении 376;
замена аминокислоты Glu на Ala в положении 380;
замена аминокислоты Glu на Ala в положении 382;
замена аминокислоты Asn или Ser на Ala в положении 384;
замена аминокислоты Gly на Asp или His в положении 385;
замена аминокислоты Gln на Pro в положении 386;
замена аминокислоты Pro на Glu в положении 387;
замена аминокислоты Asn на Ala или Ser в положении 389;
замена аминокислоты Ser на Ala в положении 424;
замена аминокислоты Met на Ala, Asp, Phe, Gly, His, Ile, Lys, Leu, Asn, Pro, Gln, Ser, Thr, Val, Trp или Tyr в положении 428;
замена аминокислоты His на Lys в положении 433;
замена аминокислоты Asn на Ala, Phe, His, Ser, Trp или Tyr в положении 434;
и замена аминокислоты Tyr или Phe на His в положении 436 (нумерация EU) в исходной Fc-области IgG.
Между тем, количество аминокислот, подлежащее изменению, конкретно не ограничено; и можно изменять аминокислоты только в одном участке или в двух или более участках. Комбинации двух или более аминокислотных изменений включают, например, изменения, представленные в таблице 3. Между тем, комбинации изменений, которые могут усиливать связывание с FcRn человека в кислом диапазоне pH по сравнению с исходным IgG человека, представлены в таблицах 4-1 - 4-5. Когда также из описанных выше изменений выбирают соответствующие комбинаций изменений, которые также могут усиливать связывание с FcRn человека в нейтральном диапазоне pH, они применимы к настоящему изобретению. Более того, комбинации изменений, которые могут усиливать связывание Fv4-IgG1 с FcRn человека в нейтральных условиях, представлены в таблицах 5-1 и 5-2.
Активность связывания с FcRn человека антигенсвязывающей молекулы в нейтральном диапазоне pH может быть увеличена путем замены по меньшей мере одной аминокислоты, выбранной из этих аминокислот, другой аминокислотой.
Таблица 4-2 является продолжением таблицы 4-1.
Таблица 4-3 является продолжением таблицы 4-2.
Таблица 4-4 является продолжением таблицы 4-3.
Таблица 4-5 является продолжением таблицы 4-4.
Таблица 5-2 является продолжением таблицы 5-1.
Таблица 6-2 является продолжением таблицы 6-1.
Такие аминокислотные изменения можно соответствующим образом вносить с использованием известных способов. Например, изменения в Fc-домене природного IgG1 человека описаны в Drug Metab Dispos. 2007 Jan. 35(1): 86-94; Int Immunol. 2006 Dec. 18, (12): 1759-69; J Biol Chem. 2001 Mar. 2, 276(9): 6591-604; J Biol Chem. (2007) 282(3): 1709-17; J Immunol. (2002) 169(9): 5171-80; J Immunol. (2009) 182(12): 7663-71; Molecular Cell, Vol. 7, 867-877, April, 2001; Nat Biotechnol. 1997 Jul. 15, (7): 637-40; Nat Biotechnol. 2005 Oct. 23, (10): 1283-8; Proc Natl Acad Sci USA. 2006 Dec. 5, 103(49): 18709-14; EP 2154157; US 20070141052; WO 2000/042072; WO 2002/060919; WO 2006/020114; WO 2006/031370; WO 2010/033279; WO 2006/053301; и WO 2009/086320.
Согласно Journal of Immunology (2009) 182: 7663-7671, активность связывания природного IgG1 человека с FcRn человека в кислом диапазоне pH (pH 6,0) составляет KD 1,7 мкМ, и эта активность практически не поддается выявлению при нейтральном диапазоне pH. Таким образом, в предпочтительном варианте осуществления, антигенсвязывающая молекула, подлежащая применению в способах по настоящему изобретению, включает антигенсвязывающие молекулы, активность связывания которых с FcRn человека в кислом диапазоне pH составляет KD 20 мкМ или сильнее и является идентичной или более сильной, чем у природного IgG1 человека в нейтральном диапазоне pH. В более предпочтительном варианте осуществления антигенсвязывающая молекула включает антигенсвязывающие молекулы, активность связывания которых с FcRn человека составляет KD 2,0 мкМ или сильнее в кислом диапазоне pH и KD 40 мкМ или сильнее в нейтральном диапазоне pH. В еще более предпочтительном варианте осуществления антигенсвязывающая молекула включает антигенсвязывающие молекулы, активность связывания которых с FcRn человека составляет KD 0,5 мкМ или сильнее в кислом диапазоне pH и KD 15 мкМ или сильнее в нейтральном диапазоне pH. Особенно предпочтительно, чтобы антигенсвязывающая активность была более низкой в условиях кислых значений pH, чем в условиях нейтральных значений pH. Описанные выше величины KD определяют способом, описанным в Journal of Immunology (2009) 182: 7663-7671 (путем иммобилизации антигенсвязывающей молекулы на чип и нанесения FcRn человека в качестве анализируемого образца).
Константу диссоциации (KD) можно использовать в качестве величины активности связывания с FcRn человека. Однако природный IgG1 человека имеет низкую активность связывания с FcRn человека в нейтральном диапазоне pH (pH 7,4), и, таким образом, трудно вычислить активность в качестве KD. Способы оценки того, является ли активность связывания с FcRn человека более высокой, чем у природного IgG1 человека при pH 7,4, включают способы оценки путем сравнения интенсивности ответа в Biacore после нанесения анализируемых соединений в одинаковой концентрации. В частности, когда ответ после нанесения FcRn человека на чип, на котором иммобилизована антигенсвязывающая молекула при pH 7,4, является более сильным, чем ответ после нанесения FcRn человека на чип, на котором иммобилизован природный IgG1 при pH 7,4, активность связывания антигенсвязывающей молекулы с FcRn человека считают более высокой, чем активность связывания природного IgG1 человека при pH 7,4.
Также в качестве нейтрального диапазона pH можно использовать pH 7,0. Использование pH 7,0 в качестве нейтрального pH может способствовать слабому взаимодействию между FcRn человека и FcRn-связывающим доменом. Что касается температуры, используемой в условиях анализа, аффинность связывания можно оценивать при любой температуре от 10°C до 50°C. Предпочтительно, используют температуру от 15°C до 40°C для определения аффинности связывания между FcRn-связывающим доменом человека и FcRn человека. Более предпочтительно, также для определения аффинности связывания между FcRn-связывающим доменом и FcRn человека используют любую температуру от 20°C до 35°C, такую как любая из 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34 и 35°C. Одним из примеров этого варианта осуществления изобретения является температура 25°C, описанная в примере 5. В предпочтительном варианте осуществления взаимодействие между FcRn человека и FcRn-связывающим доменом можно измерять при pH 7,0 и при 25°C, как описано в примере 5. Аффинность связывания антигенсвязывающей молекулы с FcRn человека можно измерять с помощью Biacore, как описано в примере 3.
В более предпочтительном варианте осуществления антигенсвязывающие молекулы по настоящему изобретению обладают активностью связывания с FcRn человека при pH 7,0 и при 25°C, которая является более сильной, чем у природного IgG человека. В более предпочтительном варианте осуществления активность связывания с FcRn человека при pH 7,0 и при 25°C является в 28 раз более сильной, чем у природного IgG человека, или сильнее KD 3,2 мкМ. В более предпочтительном варианте осуществления активность связывания с FcRn человека при pH 7,0 и при 25°C является в 38 раз более сильной, чем у природного IgG человека, или сильнее KD 2,3 мкМ.
В качестве неизмененного IgG человека предпочтительно используют природный IgG1, IgG2, IgG3 или IgG4, чтобы он выполнял роль эталонного неизмененного IgG человека, подлежащего сравнению с антигенсвязывающими молекулами в отношении их активности связывания FcRn человека или активности связывания in vivo. Предпочтительно, в качестве FcRn-связывающего домена человека можно соответствующим образом использовать эталонную антигенсвязывающую молекулу, содержащую тот же антигенсвязывающий домен, что и у представляющей интерес антигенсвязывающей молекулы и природной Fc-области IgG человека. Более предпочтительно, природный IgG1 человека используют в качестве эталонного природного IgG человека, подлежащего сравнению с антигенсвязывающими молекулами в отношении их активности связывания FcRn человека или активности связывания in vivo.
Более конкретно, антигенсвязывающие молекулы с длительным эффектом в отношении активности элиминации антигена в плазме, описанные в рамках настоящего изобретения, обладают активностью связывания с FcRn человека при pH 7,0 и при 25°C в диапазоне от в 28 раз до в 440 раз более сильной активности, чем у природного IgG1 человека, или имеют KD в диапазоне от 3,0 мкМ до 0,2 мкМ. Концентрацию антигена в плазме в течение длительного времени определяют путем измерения концентрации общего или свободного антигена в плазме и молярного соотношения антиген/антигенсвязывающая молекула через 2, 4, 7, 14, 28, 56 или 84 суток после введения антигенсвязывающей молекулы для оценки длительного эффекта антигенсвязывающей молекулы по настоящему изобретению в отношении активности элиминации антигена из плазмы. Определение того, достигается ли антигенсвязывающей молекулой, описанной в рамках настоящего изобретения, снижение концентрации антигена в плазме или молярного соотношения антиген/антигенсвязывающая молекула, можно определять путем оценки снижения в любой или несколько моментов времени, описанных выше.
Еще более конкретно, антигенсвязывающие молекулы с кратковременным эффектом на активность в отношении элиминации антигена в плазме, описанные в рамках настоящего изобретения, обладают активностью связывания с FcRn человека при pH 7,0 и при 25°C, в 440 раз более сильной, чем у природного IgG человека, или имеют KD сильнее 0,2 мкМ. Концентрацию антигена в плазме в течение короткого периода времени определяют путем измерения концентрации общего или свободного антигена в плазме и молярного соотношения антиген/антигенсвязывающая молекула через 15 мин, 1, 2, 4, 8, 12 или 24 часов после введения антигенсвязывающей молекулы для оценки кратковременного эффекта антигенсвязывающей молекулы по настоящему изобретению на активность элиминации антигена из плазмы.
Способы по настоящему изобретению применимы к любым антигенсвязывающим молекулам, независимо от типа антигена-мишени.
Например, когда антигенсвязывающая молекула представляет собой антитело, которое связывается с мембранным антигеном, антитело, введенное в организм, связывается с антигеном, а затем захватывается путем интернализации в эндосомы в клетках вместе с антигеном, в то время как антитело продолжает быть связанным с антигеном. Затем антитело переносится в лизосомы, в то время как антитело продолжает быть связанным с антигеном, и антитело деградируется лизосомой вместе с антигеном. Опосредуемая интернализацией элиминация из плазмы называется антиген-зависимой элиминацией, и такая элиминация описана для многочисленных молекул антител (Drug Discov Today. 2006 Jan; 11(1-2): 81-8). Когда одна молекула IgG-антитела связывается с антигенами двухвалентным образом, одна молекула антитела интернализуется, антитело продолжает быть связанным с двумя молекулами антигена, и деградируется в лизосоме. Таким образом, в случае обычных антител, одна молекула IgG-антитела не может связываться с тремя или более молекулами антигена. Например, одна молекула IgG-антитела, имеющая нейтрализующую активность, не может нейтрализовать три или более молекулы антигена.
Относительно пролонгированное удержание (медленная элиминация) IgG-молекул в плазме является следствием функции FcRn человека, который известен как рецептор спасения для IgG-молекул. При захвате в эндосомы путем пиноцитоза, IgG-молекулы связываются с FcRn человека, экспрессированным в эндосомах, в кислых условиях в эндосомах. В то время как IgG-молекулы, которые не связались с FcRn человека, переносятся в лизосомы, где они деградируются, IgG-молекулы, которые связаны с FcRn человека, переносится на клеточную поверхность и вновь возвращаются в плазму путем диссоциации от FcRn человека в нейтральных условиях в плазме.
Альтернативно, когда антигенсвязывающая молекула представляет собой антитело, которое связывается с растворимым антигеном, антитело, введенное в организм, связывается с антигеном, а затем захватывается в клетки, в то время как антитело продолжает быть связанным с антигеном. Многие антитела, захватываемые в клетки, высвобождаются наружу клетки через FcRn. Однако поскольку антитела высвобождаются наружу клетки, когда антитела продолжают быть связанными с антигенами, антитела не могут вновь связываться с антигенами. Таким образом, аналогично антителам, которые связываются с мембранными антигенами, в случае обычных антител одна молекула IgG-антитела не может связываться с тремя или более молекулами антигена.
Антитела с зависимым от концентрации кальция связыванием антигена, которые сильно связываются с антигеном в условиях высокой концентрации кальция в плазме, но диссоциируют от антигена в условиях низкой концентрации кальция в эндосоме, могут диссоциировать от антигена в эндосоме. Такие антитела с зависимым от концентрации кальция связыванием антигена могут вновь связываться с антигенами, когда они рециклируют в плазму с помощью FcRn после диссоциации антигена; таким образом, каждое антитело может многократно связываться с множеством антигенов. Более того, антиген, связанный с антигенсвязывающей молекулой, диссоциирует в эндосоме и не рециклирует в плазму. Это способствует опосредуемому антигенсвязывающей молекулой захвату антигена в клетки. Таким образом, введение антигенсвязывающей молекулы может увеличить элиминацию антигена и, тем самым, снизить концентрацию антигена в плазме.
Антигенсвязывающие молекулы
Настоящее изобретение относится к антигенсвязывающим молекулам, имеющим антигенсвязывающий домен и FcRn-связывающий домен человека, где антигенсвязывающая активность антигенсвязывающих молекул отличается в двух различных условиях концентрации кальция и является более низкой в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция.
Антигенсвязывающие молекулы по настоящему изобретению конкретно не ограничены при условии, что они могут включать антигенсвязывающий домен, обладающий активностью связывания, специфичной к антигену мишени. Такие предпочтительные антигенсвязывающие домены включают, например, домены, имеющие антигенсвязывающую область антитела. Антигенсвязывающая область антитела содержит, например, CDR и вариабельные области. Когда антигенсвязывающая область антитела представляет собой CDR, она может содержать все шесть CDR из целого антитела или одну, две или более CDR. Когда CDR содержатся в антителе в качестве связывающей области, они могут содержать делеции, замены, вставки и/или инсерции аминокислот, или они могут быть частью CDR.
С другой стороны, антигенсвязывающие молекулы, подлежащие применению в способах по настоящему изобретению, включают антигенсвязывающие молекулы, которые обладают антагонистической активностью (антагонистические антигенсвязывающие молекулы), антигенсвязывающие молекулы, которые обладают агонистической активностью (агонистическая антигенсвязывающая молекула), и молекулы, обладающие цитотоксичностью. В предпочтительном варианте осуществления антигенсвязывающие молекулы включают антагонистические антигенсвязывающие молекулы, в частности, антагонистические антигенсвязывающие молекулы, которые распознают антиген, такой как рецептор или цитокин.
В рамках настоящего изобретения представляющая интерес антигенсвязывающая молекула конкретно не ограничена, и она может представлять собой любую антигенсвязывающую молекулу. Антигенсвязывающая молекула по настоящему изобретению предпочтительно обладает как антигенсвязывающей активностью (антигенсвязывающий домен), так и FcRn-связывающим доменом человека. В частности, предпочтительная антигенсвязывающая молекула по настоящему изобретению содержит FcRn-связывающий домен человека.
Антигенсвязывающая молекула, содержащая как антигенсвязывающий домен, так и FcRn-связывающий домен человека, включает, например, антитела. В контексте настоящего изобретения, предпочтительный пример антитела включает IgG-антитела. Когда антитело, подлежащее применению, представляет собой IgG-антитело, тип IgG не ограничен; и можно использовать IgG, принадлежащий любому изотипу (подклассу), такому как IgG1, IgG2, IgG3 или IgG4. Более того, антигенсвязывающие молекулы по настоящему изобретению могут содержать константную область антитела, и в константную область можно вносить аминокислотные мутации. Аминокислотные мутации, подлежащие внесению, включают, например, мутации, которые усиливают или нарушают связывание с Fcγ-рецептором (Proc Natl Acad Sci USA. 2006 Mar 14; 103(11): 4005-10), но они не ограничиваются этими примерами. Альтернативно, также можно изменять pH-зависимое связывание путем выбора соответствующей константной области, такой как константная область IgG2.
Когда представляющая интерес антигенсвязывающая молекула по настоящему изобретению представляет собой антитело, она может представлять собой антитело, происходящее из любого животного, такое как антитело мыши, антитело человека, антитело крысы, антитело кролика, антитело козы или антитело верблюда. Более того, антитело может представлять собой измененное антитело, например, химерное антитело, и в частности, измененное антитело, включающее аминокислотные замены в последовательности гуманизированного антитела и т.п. Антитела также включают биспецифические антитела, продукты модификации антител, связанные с различными молекулами, и полипептиды, содержащие фрагменты антител.
"Химерные антитела" представляют собой антитела, полученные путем комбинирования последовательностей, происходящих из различных животных. В частности, химерное антитело включает, например, антитела, имеющие вариабельные (V)-области тяжелых и легких цепей из антитела мыши и константные (C)-области тяжелых и легких цепей из антитела человека.
"Гуманизированные антитела", также называемые переформированными антителами человека, представляют собой антитела, в которых определяющие комплементарность области (CDR) антитела, происходящего из не являющегося человеком млекопитающего, например, мыши, трансплантированы в CDR антитела человека. Способы идентификации CDR известны (Kabat et al., Sequence of Proteins of Immunological Interest (1987), National Institute of Health, Bethesda, Md.; Chothia et al., Nature (1989) 342: 877). Общие способы генетической рекомбинации, пригодные для этой цели, также известны (см. патентную заявку Европы EP 125023; и WO 96/02576).
Биспецифическое антитело относится к антителу, которое имеет вариабельные области в той же молекуле антитела, которая распознает другие эпитопы. Биспецифическое антитело может представлять собой антитело, которое распознает два или более различных антигена, или антитело, которое распознает два или более различных эпитопа на одном и том же антигене.
Более того, полипептиды, содержащие фрагменты антител, включают, например, Fab-фрагменты, F(ab’)2-фрагменты, scFv (Nat Biotechnol. 2005 Sep; 23(9): 1126-36), доменные антитела (dAb) (WO 2004/058821; WO 2003/002609), scFv-Fc (WO 2005/037989), dAb-Fc и слитые белки Fc. Fc-область молекулы, содержащей Fc-область, можно использовать в качестве FcRn-связывающего домена человека. Альтернативно, FcRn-связывающий домен можно подвергать слиянию с этими молекулами.
Кроме того, антигенсвязывающие молекулы, которые применимы в рамках настоящего изобретения, могут представлять собой подобные антителам молекулы. Подобная антителу молекула (каркасная молекула, пептидная молекула) представляет собой молекулу, которая может проявлять функции связывания с молекулой-мишенью (Current Opinion in Biotechnology (2006) 17: 653-658; Current Opinion in Biotechnology (2007) 18: 1-10; Current Opinion in Structural Biology (1997) 7: 463-469; Protein Science (2006) 15: 14-27), и включает, например, DARPin (WO 2002/020565), аффитело (WO 1995/001937), авимер (WO 2004/044011; WO 2005/040229) и аднектин (WO 2002/032925). Эти подобные антителу молекулы могут связываться с молекулами-мишенями зависимым от концентрации кальция образом, способствовать захвату с помощью антигенсвязывающих молекул антигена в клетки, способствовать снижению концентрации антигена в плазме путем введения антигенсвязывающих молекул, и повышать удержание в плазме антигенсвязывающих молекул, и увеличивать количество раз связывания антигена одной антигенсвязывающей молекулой.
Более того, антигенсвязывающая молекула может представлять собой белок, полученный слиянием между FcRn-связывающим доменом человека и рецепторным белком, который связывается с мишенью, и включает, например, слитые белки TNFR-Fc, слитые белки IL1R-Fc, слитые белки VEGFR-Fc и слитые белки CTLA4-Fc (Nat Med. 2003, Jan; 9(1): 47-52; BioDrugs. (2006) 20(3): 151-60). Если эти слитые белки рецептора и FcRn-связывающего домена человека связываются с молекулой-мишенью зависимым от кальция образом, то это, возможно, способствует захвату антигена в клетки с помощью антигенсвязывающих молекул, способствует снижению концентрации антигена в плазме при введении антигенсвязывающих молекул, и повышает удержание в плазме антигенсвязывающих молекул, и увеличивает количество раз связывания антигена одной антигенсвязывающей молекулой.
Более того, антигенсвязывающая молекула может представлять собой слитый белок между искусственным белком-лигандом, который связывается с мишенью и имеет нейтрализующий эффект, и FcRn-связывающим доменом человека; и искусственный белок-лиганд включает, например, мутантный IL-6 (EMBO J. 1994 Dec 15; 13(24): 5863-70). Если такие слитые белки искусственного лиганда могут связываться с молекулами-мишенями зависимым от кальция образом, то это, возможно, способствует захвату антигена в клетки с помощью антигенсвязывающих молекул, способствует снижению концентрации антигена в плазме при введении антигенсвязывающих молекул, и повышает удержание в плазме антигенсвязывающих молекул, и увеличивает количество раз связывания антигена одной антигенсвязывающей молекулой
Более того, в антителах по настоящему изобретению можно модифицировать цепи сахаров. Антитела с измененными цепями сахаров включают, например, антитела с модифицированным гликозилированием (WO 99/54342 и т.п.), антитела с дефицитом связанной с цепью сахаров фукозы (WO 00/61739; WO 02/31140; WO 2006/067847; WO 2006/067913), и антитела, имеющие цепи сахаров с биссекторным GlcNAc (WO 02/79255).
Помимо концентрации ионизированного кальция, условия, используемые для измерения антигенсвязывающей активности, могут соответствующим образам выбирать специалисты в данной области, и они конкретно не ограничены. Например, для определения активности можно использовать условия с использованием буфера HEPES при 37°C. Например, для определения активности можно использовать Biacore (GE Healthcare) и т.п. Когда антиген представляет собой растворимый антиген, активность антигенсвязывающей молекулы в отношении связывания с растворимым антигеном можно определять путем нанесения антигена в качестве анализируемого соединения на чип, на который иммобилизована антигенсвязывающая молекула. Альтернативно, когда антиген представляет собой антиген мембранного типа, активность антигенсвязывающей молекулы в отношении связывания антигена мембранного типа можно определять путем нанесения антигенсвязывающей молекулы в качестве анализируемого соединения на чип с иммобилизованным антигеном.
В антигенсвязывающих молекулах по настоящему изобретению отношение антигенсвязывающей активности в условиях низкой концентрации кальция к антигенсвязывающей активности в условиях высокой концентрации кальция конкретно не ограничено, при условии, что антигенсвязывающая активность является более низкой в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция. Однако величина KD (Ca 3 мкМ)/KD (Ca 2 мМ), которая является соотношением констант диссоциации (KD) от антигена в условиях низкой концентрации кальция относительно диссоциации в условиях высокой концентрации кальция, предпочтительно равна 2 или более, более предпочтительно 10 или более, и еще более предпочтительно 40 или более. Верхний предел KD (Ca 3 мкМ)/KD (Ca 2 мМ) конкретно не ограничен, и она может представлять собой любую величину, например, 400, 1000 или 10000, при условии, что ее можно достигнуть с использованием технологий специалистов в данной области.
Когда антиген представляет собой растворимый антиген, величина антигенсвязывающей активности может быть представлена в значениях константы диссоциации (KD). С другой стороны, когда антиген представляет собой антиген мембранного типа, активность может быть представлена в значениях кажущейся константы диссоциации (кажущаяся KD). Константу диссоциации (KD) и кажущуюся константу диссоциации (кажущаяся KD) можно определять способами, известными специалистам в данной области, например, с использованием Biacore (GE Healthcare), графика Скэтчарда, проточного цитометра и т.п.
В антигенсвязывающих молекулах по настоящему изобретению другие параметры, которые отражают соотношение между антигенсвязывающей активностью в условиях низкой концентрации кальция и в условиях высокой концентрации кальция включают, например, константу скорости диссоциации kd. Когда константу скорости диссоциации (kd) используют вместо константы диссоциации (KD) в качестве параметра, отражающего соотношение активности связывания, величина kd (в условиях низкой концентрации кальция)/kd (в условиях высокой концентрации кальция), которая представляет собой соотношение между величинами kd (константа скорости диссоциации) для антигена в условиях низкой концентрации кальция и в условиях высокой концентрации кальция, предпочтительно равна 2 или более, более предпочтительно 5 или более, еще более предпочтительно 10 или более, и еще более предпочтительно 30 или более. Верхний предел величины kd (в условиях низкой концентрации кальция)/kd (в условиях высокой концентрации кальция) конкретно не ограничен, и он может представлять собой любую величину, например, 50, 100 или 200, при условии, что его можно достигнуть с использованием технологий специалистов в данной области.
Когда антиген представляет собой растворимый антиген, величина антигенсвязывающей активности может быть представлена с использованием константы скорости диссоциации (kd). Альтернативно, когда антиген представляет собой антиген мембранного типа, величина может быть представлена в значениях кажущейся kd (кажущаяся константа скорости диссоциации). Константу скорости диссоциации (kd) и кажущуюся константу скорости диссоциации (кажущаяся kd) можно определять способами, известными специалистам в данной области, например, с использованием Biacore (GE Healthcare), проточного цитометра и т.п.
В рамках настоящего изобретения при измерении антигенсвязывающей активности антигенсвязывающей молекулы при различных концентрациях кальция, предпочтительно использовать те же условия, за исключением концентрации кальция.
Отсутствуют конкретные ограничения способа снижения (ослабления) антигенсвязывающей активности антигенсвязывающей молекулы в условиях низкой концентрации кальция так, чтобы она была более низкой, чем в условиях высокой концентрации кальция (способ сообщения зависимой от кальция антигенсвязывающей активности) для получения антигенсвязывающей молекулы, которая имеет более низкую антигенсвязывающую активность в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция. Антигенсвязывающие молекулы, которые имеют более низкую (более слабую) антигенсвязывающую активность в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция (антигенсвязывающие молекулы, которые проявляют зависимое от концентрации кальция связывание) можно получать прямо, например, путем скрининга экспонированной in vitro библиотеки антител с использованием упомянутого выше зависимого от концентрации кальция связывания с антигеном в качестве индикатора.
Другие способы включают способы прямого выделения антигенсвязывающей молекулы, имеющей упомянутое выше свойство. Например, возможно прямо получить антитело, имеющее представляющее интерес свойство, путем иммунизации животных (мышей, крыс, хомяков, кроликов, трансгенных мышей с иммуноглобулином человека, трансгенных крыс с иммуноглобулином человека, трансгенных кроликов с иммуноглобулином человека, лам, верблюдов, и т.д.) антигеном, и скрининга полученных антител с использованием зависимого от концентрации кальция связывания антигена в качестве индикатора. Альтернативно, в аминокислотную последовательность антигенсвязывающей молекулы можно вносить случайные мутации, и антигенсвязывающую активность антигенсвязывающей молекулы в различных условиях концентрации кальция можно измерять с помощью описанного выше способа для отбора антигенсвязывающей молекулы, которая обладает более низкой антигенсвязывающей активностью в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция, по сравнению с антигенсвязывающей молекулой до модификации.
Когда антигенсвязывающая активность антигенсвязывающей молекулы в условиях низкой концентрации кальция снижена (ослаблена) так, чтобы она была более низкой, чем в условиях высокой концентрации кальция (величина KD (в условиях низкой концентрации кальция)/KD (в условиях высокой концентрации кальция) увеличена) с помощью упомянутого выше способа и т.п., величина KD (в условиях низкой концентрации кальция)/KD (в условиях высокой концентрации кальция), как правило, без конкретных ограничений, в два раза или более, предпочтительно в пять раз или более, и более предпочтительно в десять раз или более превышает величину KD исходного антитела.
Более того, с использованием способа сообщения зависимой от концентрации кальция антигенсвязывающей активности по настоящему изобретению, в комбинации со способом использования антигенсвязывающей молекулы, имеющей активность связывания с FcRn человека при нейтральных значениях pH, или способом сообщения или увеличения активности связывания с FcRn человека при нейтральных значениях pH, возможно усилить функцию ускорения захвата антигена в клетки, функцию увеличения количества раз связывания антигена одной антигенсвязывающей молекулой, функцию ускорения снижения концентрации антигена в плазме при введении антигенсвязывающей молекулы или функцию увеличения удержания в плазме антигенсвязывающей молекулы. Способы сообщения или увеличения активности связывания с FcRn человека при нейтральных значениях pH включают, например, описанные выше способы модификации аминокислоты в FcRn-связывающем домене человека. В рамках настоящего изобретения, "активность связывания с FcRn человека при нейтральных значениях pH" означает активность связывания с FcRn человека при pH 6,7-10,0. Предпочтительная активность связывания с FcRn человека представляет собой, например, активность связывания с FcRn человека при pH 7,0-8,0; и более предпочтительная активность связывания с FcRn человека представляет собой, например, активность связывания с FcRn человека при pH 7,4.
Более того, с использованием способа сообщения зависимой от концентрации кальция антигенсвязывающей активности по настоящему изобретению в комбинации со способом использования антигенсвязывающей молекулы, имеющей pH-зависимую антигенсвязывающую активность или способом сообщения pH-зависимой антигенсвязывающей активности, возможно усилить функцию ускорения захвата антигена в клетки, функцию увеличения количества раз связывания антигена одной антигенсвязывающей молекулой, функцию ускорения снижения концентрации антигена в плазме при введении антигенсвязывающей молекулы или функцию увеличения удержания в плазме антигенсвязывающей молекулы. Способы сообщения pH-зависимой антигенсвязывающей активности включают, например, способы, описанные в WO 2009/125825.
В частности, например, зависимую от концентрации кальция антигенсвязывающую молекулу по настоящему изобретению можно использовать в комбинации со способом снижения (ослабления) антигенсвязывающей активности антигенсвязывающей молекулы при кислых значениях pH так, чтобы она была ниже, чем при нейтральных значениях pH. В рамках настоящего изобретения, выражение "снижение (ослабление) антигенсвязывающей активности при кислых значениях pH так, чтобы она была ниже антигенсвязывающей активности при нейтральных значениях pH" означает снижение антигенсвязывающей активности антигенсвязывающей молекулы при pH 4,0-6,5 так, чтобы она была ниже чем при pH 6,7-10,0. Предпочтительно оно означает ослабление антигенсвязывающей активности антигенсвязывающей молекулы при pH 5,5-6,5 так, чтобы она была ниже, чем при pH 7,0-8,0, и в частности, предпочтительно означает ослабление антигенсвязывающей активности антигенсвязывающей молекулы при pH 5,8 так, чтобы она была ниже, чем при pH 7,4. В рамках настоящего изобретения, "кислое значение pH", как правило, относится к pH 4,0-6,5, предпочтительно pH 5,5-6,5, и особенно предпочтительно pH 5,8. Между тем, в рамках настоящего изобретения "нейтральное значение pH", как правило, относится к pH 6,7-10,0, предпочтительно pH 7,0-8,0, и особенно предпочтительно pH 7,4.
С другой стороны, выражение "снижение антигенсвязывающей активности антигенсвязывающей молекулы при кислых значениях pH так, чтобы она была ниже, чем при нейтральных значениях pH", является синонимичным с "увеличением антигенсвязывающей активности антигенсвязывающей молекулы при нейтральных значениях pH так, чтобы она была больше, чем при кислых значениях pH". В частности, в рамках настоящего изобретения, можно увеличивать различие между антигенсвязывающей активностью антигенсвязывающей молекулы при кислых значениях pH и нейтральных значениях pH (например, можно увеличивать величину KD (pH 5,8)/KD (pH 7,4), как описано ниже). Различие между активностью связывания антигена антигенсвязывающей молекулы при кислых значениях pH и нейтральных значениях pH можно увеличивать, например, путем снижения антигенсвязывающей активности при кислых значениях pH или увеличения антигенсвязывающей активности при нейтральных значениях pH, или обоих из них.
В рамках настоящего изобретения различие между активностью связывания антигена при кислых значениях pH и нейтральных значениях pH конкретно не ограничено, при условии, что антигенсвязывающая активность является более низкой при кислых значениях pH, чем при нейтральных значениях pH. Однако величина KD (pH 5,8)/KD (pH 7,4), которая представляет собой соотношение между константами диссоциации (KD) для антигена при pH 5,8 и pH 7,4, предпочтительно равна 2 или более, более предпочтительно 10 или более, и еще более предпочтительно 40 или более. Верхний предел величины KD (pH 5,8)/KD (pH 7,4) конкретно не ограничен, и он может представлять собой любую величину, например, 400, 1000 или 10000, при условии, что его можно достигнуть с использованием технологий специалистов в данной области.
В рамках настоящего изобретения другие параметры, которые отражают соотношение между антигенсвязывающей активностью при кислых значениях pH и при нейтральных значениях pH включают, например, константу скорости диссоциации kd. Когда константу скорости диссоциации (kd) используют вместо константы диссоциации (KD) в качестве параметра, отражающего соотношение активности связывания, kd (pH 5,8)/kd (pH 7,4), которая представляет собой соотношение между величинами kd (константа скорости диссоциации) для антигена при pH 5,7 и pH 7,4, предпочтительно равна 2 или более, более предпочтительно 5 или более, еще более предпочтительно 10 или более, и еще более предпочтительно 30 или более. Верхний предел величины kd (pH 5,8)/kd (pH 7,4) конкретно не ограничен, и он может представлять собой любую величину, например, 50, 100 или 200, при условии, что его можно достигнуть с использованием технологий специалистов в данной области.
Способы сообщения pH-зависимой антигенсвязывающей активности конкретно не ограничены. Такие способы включают, например, способы ослабления антигенсвязывающей активности при pH 5,8 так, чтобы она была ниже, чем при pH 7,4, путем замены по меньшей мере одной аминокислоты в антигенсвязывающей молекуле остатком гистидина или инсерции по меньшей мере одного остатка гистидина в антигенсвязывающую молекулу. Уже известно, что замена аминокислоты в антителе остатком гистидина может сообщить антителу pH-зависимую антигенсвязывающую активность (FEBS Letter, 309(1): 85-88, (1992)). В рамках настоящего изобретения, участки мутации (замены) или инсерции гистидина в антигенсвязывающую молекулу конкретно не ограничены, и можно использовать любой участок, при условии, что антигенсвязывающая активность при pH 5,8 становится слабее, чем при pH 7,4 (величина KD (pH 5,8)/KD (pH 7,4) увеличивается) по сравнению с величиной до мутации или инсерции. Например, когда антигенсвязывающая молекула представляет собой антитело, такие участки включают вариабельную область антитела. Количество встроенных (или созданных) участков мутации или инсерции гистидина может быть соответствующим образом определено специалистами в данной области. Только одни участок может быть заменен остатком гистидина, или остаток гистидина может быть встроен только в один участок. Альтернативно, два или более множественных участков могут быть заменены остатком гистидина, или остаток гистидина может быть встроен в два или более множественных участков. Также возможно в то же время вносить мутацию помимо мутации на остаток гистидина (мутация аминокислоты помимо гистидина). Более того, мутацию на остаток гистидина можно вносить одновременно со встраиванием остатка гистидина. Можно заменять или встраивать гистидин случайным образом с использованием способа, такого как сканирование гистидином, в котором используется гистидин вместо аланина в сканировании аланином, известном специалистам в данной области. Альтернативно, антигенсвязывающую молекулу, у которой KD (pH 5,8)/KD (pH 7,4) увеличена по сравнению с величиной до мутации, можно отбирать из библиотеки антигенсвязывающих молекул, в которые внесена случайная мутация или инсерция гистидина.
Когда по меньшей мере одна аминокислота в антигенсвязывающей молекуле заменена остатком гистидина, или по меньшей мере один остаток гистидина встроен в аминокислоты антигенсвязывающей молекулы, хотя отсутствует конкретное ограничение, предпочтительно, чтобы антигенсвязывающая активность антигенсвязывающей молекулы при pH 7,4 после замены или вставки гистидина была сравнима с антигенсвязывающей активностью при pH 7,4 до замены или инсерции гистидина. В рамках настоящего изобретения выражение "антигенсвязывающая активность антигенсвязывающей молекулы при pH 7,4 после замены или инсерции гистидина сравнима с антигенсвязывающей активностью при pH 7,4 до замены или вставки гистидина" означает, что антигенсвязывающая молекула после замены или инсерции гистидина сохраняет 10% или более, предпочтительно 50% или более, более предпочтительно 80% или более, и еще более предпочтительно 90% или более антигенсвязывающей активности до замены или инсерции гистидина. Когда антигенсвязывающая активность антигенсвязывающей молекулы нарушается путем замены или вставки гистидина, можно сделать так, чтобы антигенсвязывающая активность была сравнимой с антигенсвязывающей активностью до замены или инсерции гистидина путем внесения одной или нескольких аминокислотных замен, делеций, вставок и/или инсерций в антигенсвязывающую молекулу. Настоящее изобретение также включает антигенсвязывающие молекулы, имеющие сравнимую активностью связывания, полученную путем одной или нескольких замен, делеций, вставок и/или инсерций после замены или вставки гистидина.
Альтернативные способы ослабления антигенсвязывающей активности антигенсвязывающей молекулы при pH 5,8 так, чтобы она была ниже, чем при pH 7,4, включают способы замены аминокислоты в антигенсвязывающей молекуле неприродной аминокислотой или встраивания неприродной аминокислоты в аминокислоты антигенсвязывающей молекулы. Также известно, что с использованием неприродных аминокислот можно искусственно контролировать pKa (Angew. Chem. Int. Ed. 2005, 44, 34; Chem Soc Rev. 2004 Sep. 10; 33(7): 422-30; Amino Acids. 1999; 16(3-4): 345-79). Таким образом, в рамках настоящего изобретения, неприродные аминокислоты можно использовать вместо гистидина, упомянутого выше. Замену и/или инсерцию неприродной аминокислоты можно вносить одновременно с упомянутой выше заменой и/или инсерцией гистидина. В рамках настоящего изобретения можно использовать любые неприродные аминокислоты. Возможно использовать неприродные аминокислоты и т.п., известные специалистам в данной области.
Более того, когда антигенсвязывающая молекула представляет собой вещество, содержащее константную область антитела, альтернативные способы ослабления антигенсвязывающей активности антигенсвязывающей молекулы при pH 5,8 так, чтобы она была ниже, чем при pH 7,4, включают способы модификации константной области антитела, содержащейся в антигенсвязывающей молекуле. Примеры модификации константной области антитела включают способы замены константной области, описанные в WO 2009/125825.
Между тем, способы изменения константной области антитела включают, например, способы оценки различных изотипов константных областей (IgG1, IgG2, IgG3, и IgG4) и селекцию изотипов, которые снижают антигенсвязывающую активность при pH 5,8 (увеличивают скорость диссоциации при pH 5,8). Такие способы также включают способы снижения антигенсвязывающей активности при pH 5,8 (увеличения скорости диссоциации при pH 5,8) путем внесения аминокислотных замен в аминокислотные последовательности изотипов дикого типа (аминокислотные последовательности IgG1, IgG2, IgG3 или IgG4 дикого типа). Последовательность шарнирной области в константной области антитела значительно отличается среди изотипов (IgG1, IgG2, IgG3 и IgG4), и различие в аминокислотной последовательности шарнирной области имеет значительное влияние на антигенсвязывающую активность. Таким образом, возможно выбрать соответствующий изотип для снижения антигенсвязывающей активности при pH 5,8 (увеличения скорости диссоциации при pH 5,8) в зависимости от типа антигена или эпитопа. Более того, поскольку отличие в аминокислотной последовательности шарнирной области имеет значительное влияние на антигенсвязывающую активность, предполагают, что предпочтительные участки аминокислотной замены в аминокислотных последовательностях изотипов дикого типа расположены в шарнирной области.
Когда антигенсвязывающая активность антигенсвязывающего вещества при pH 5,8 ослабевает так, чтобы она была ниже, чем при pH 7,4 (когда величина KD (pH 5,8)/KD (pH 7,4) увеличивается) с помощью описанного выше способа и т.п., как правило, предпочтительно, чтобы величина KD (pH 5,8)/KD (pH 7,4) в два раза или более, предпочтительно в пять раз или более, и более предпочтительно в десять раз или более превышала величину KD исходного антитела, однако конкретно она не ограничивается этим.
Антигенсвязывающие молекулы
Более того, настоящее изобретение относится к антигенсвязывающим молекулам, антигенсвязывающая активность которых отличается при двух различных условиях концентрации кальция; т.е. антигенсвязывающая активность является более низкой в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция. Предпочтительно, настоящее изобретение относится к антигенсвязывающим молекулам, которые имеют более низкую антигенсвязывающую активность в условиях низкой концентрации кальция (концентрация ионизированного кальция от 0,1 мкМ до 30 мМ), чем в условиях высокой концентрации кальция (концентрация ионизированного кальция от 100 мкМ до 10 мМ). Более конкретно, антигенсвязывающие молекулы включают антигенсвязывающие молекулы, которые имеют более низкую антигенсвязывающую активность при концентрации ионизированного кальция в ранней эндосоме in vivo (низкая концентрация кальция, такая как от 1 мкМ до 5 мкМ), чем при концентрации ионизированного кальция в плазме in vivo (высокая концентрация кальция, такая как от 0,5 мМ до 2,5 мМ).
Что касается антигенсвязывающей активности антигенсвязывающей молекулы по настоящему изобретению, которая имеет более низкую антигенсвязывающую активность в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция, отсутствуют ограничения на отличия в антигенсвязывающей активности, при условии, что антигенсвязывающая активность является более низкой в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция. Приемлемо даже, чтобы антигенсвязывающая активность антигенсвязывающей молекулы была только немного более низкой в условиях низкой концентрации кальция.
В предпочтительном варианте осуществления для антигенсвязывающей молекулы по настоящему изобретению, которая имеет более низкую антигенсвязывающую активность в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция, величина KD (низкий уровень Ca)/KD (высокий уровень Ca), которая представляет собой соотношение KD между условиями низкой и высокой концентрации кальция, составляет 2 раза или более, предпочтительно величина KD (низкий уровень Ca)/KD (высокий уровень Ca) составляет 10 или более, и более предпочтительно величина KD (низкий уровень Ca)/KD (высокий уровень Ca) составляет 40 или более. Верхний предел величины KD (низкий уровень Ca)/KD (высокий уровень Ca) конкретно не ограничен, и он может представлять собой любую величину, такую как 400, 1000 и 10000, при условии, что он может быть достигнут способами, известными специалистам в данной области.
В другом предпочтительном варианте осуществления для антигенсвязывающей молекулы по настоящему изобретению, которая имеет более низкую антигенсвязывающую активность в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция, величина kd (низкий уровень Ca)/kd (высокий уровень Ca), которая представляет собой соотношение между величинами kd для антигена в условиях низкой концентрации кальция и условиях высокой концентрации кальция, составляет 2 или более, предпочтительно величина kd (низкий уровень Ca)/kd (высокий уровень Ca) составляет 5 или более, более предпочтительно величина kd (низкий уровень Ca)/kd (высокий уровень Ca) составляет 10 или более, и еще более предпочтительно величина kd (низкий уровень Ca)/kd (высокий уровень Ca) составляет 30 или более. Верхний предел величины kd (низкий уровень Ca)/kd (высокий уровень Ca) конкретно не ограничен, и он может представлять собой любую величину, такую как 50, 100 и 200, при условии, что его можно получать способами, известными специалистам в данной области.
Антигенсвязывающая молекула по настоящему изобретению, кроме того, может иметь упомянутую выше активность связывания с FcRn человека в условиях нейтральных значений pH. С использованием активности связывания с FcRn человека в условиях нейтральных значений pH в комбинации с зависимой от концентрации кальция антигенсвязывающей активности возможно усилить функцию ускорения захвата антигена в клетки, функцию увеличения количества раз связывания антигена одной антигенсвязывающей молекулой, функцию ускорения снижения концентрации антигена в плазме при введении антигенсвязывающей молекулы или функцию увеличения удержания в плазме антигенсвязывающей молекулы.
Антигенсвязывающая молекула по настоящему изобретению, дополнительно, может иметь упомянутую выше pH-зависимую антигенсвязывающую активность, т.е. более низкую антигенсвязывающую активность в условиях кислых значений pH, чем в условиях нейтральных значений pH. С использованием pH-зависимой антигенсвязывающей активности в комбинации с зависимой от концентрации кальция антигенсвязывающей активностью, возможно усилить функцию ускорения захвата антигена в клетки, функцию увеличения количества раз связывания антигена одной антигенсвязывающей молекулой, функцию ускорения снижения концентрации антигена в плазме при введении антигенсвязывающей молекулы или функцию увеличения удержания в плазме антигенсвязывающей молекулы.
Более того, антигенсвязывающая молекула по настоящему изобретению может иметь любое другое свойство, при условии, что она имеет более низкую антигенсвязывающую активность в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция. Например, антигенсвязывающая молекула может представлять собой агонистическую антигенсвязывающую молекулу или антагонистическую антигенсвязывающую молекулу. Предпочтительные антигенсвязывающие молекулы по настоящему изобретению включают, например, антагонистические антигенсвязывающие молекулы. Такая антагонистическая антигенсвязывающая молекула, как правило, представляет собой антигенсвязывающую молекулу, которая ингибирует рецептор-опосредуемую внутриклеточную передачу сигнала путем ингибирования связывания между лигандом (агонистом) и его рецептором.
Более того, антигенсвязывающая молекула, которой сообщают pH-зависимую антигенсвязывающую активность, может иметь замену по меньшей мере одной аминокислоты остатком гистидина или встраивание по меньшей мере одного остатка гистидина.
Между тем, отсутствует конкретное ограничение антигена, с которым связывается антигенсвязывающая молекула по настоящему изобретению, и антигенсвязывающая молекула может связываться с любым антигеном. Такие антигены включают, например, мембранные антигены, такие как рецепторные белки (рецепторы мембранного типа и растворимые рецепторы) и маркеры клеточной поверхности, и растворимые антигены, такие как цитокины. Конкретные примеры других антигенов описаны выше.
Способы скрининга
Настоящее изобретение относится к способам скрининга антигенсвязывающей молекулы, которая имеет более низкую антигенсвязывающую активность в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция. Настоящее изобретение также относится к способам скрининга антигенсвязывающей молекулы, имеющей по меньшей мере одну функцию, выбранную из:
(i) функция ускорения захвата антигена в клетки;
(ii) функция связывания с антигеном два или более раз;
(iii) функция ускорения снижения концентрации антигена в плазме; и
(iv) функция увеличения удержания в плазме.
В частности, настоящее изобретение относится к способам скрининга антигенсвязывающей молекулы, которые включают стадии (a)-(c) ниже:
(a) определение антигенсвязывающей активности антигенсвязывающей молекулы в условиях низкой концентрации кальция;
(b) определение антигенсвязывающей активности антигенсвязывающей молекулы в условиях высокой концентрации кальция; и
(c) отбор антигенсвязывающей молекулы, которая имеет более низкую антигенсвязывающую активность в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция.
Настоящее изобретение также относится к способам скрининга антигенсвязывающей молекулы, которые включают стадии (a)-(c) ниже:
(a) приведение антигена в контакт с антигенсвязывающей молекулой или библиотекой антигенсвязывающих молекул в условиях высокой концентрации кальция;
(b) помещение антигенсвязывающей молекулы, которая связывает антиген на стадии (a) в условия низкой концентрации кальция; и
(c) получение антигенсвязывающей молекулы, которая диссоциирует на стадии (b).
Настоящее изобретение также относится к способам скрининга антигенсвязывающей молекулы, которые включают стадии (a)-(d) ниже:
(a) приведение антигена в контакт с антигенсвязывающей молекулой или библиотекой антигенсвязывающих молекул в условиях низкой концентрации кальция;
(b) отбор антигенсвязывающей молекулы, которая не связывается с антигеном на стадии (a);
(c) обеспечение связывания антигенсвязывающей молекулы, отобранной на стадии (b), с антигеном в условиях высокой концентрации кальция; и
(d) получение антигенсвязывающей молекулы, которая связывается с антигеном на стадии (c).
Также настоящее изобретение относится к способам скрининга антигенсвязывающей молекулы, которые включают стадии (a)-(c) ниже:
(a) приведение антигенсвязывающей молекулы или библиотеки антигенсвязывающих молекул в контакт с колонкой с иммобилизованным на ней антигеном в условиях высокой концентрации кальция;
(b) элюирование антигенсвязывающей молекулы, которая связывается с колонкой на стадии (a), из колонки в условиях низкой концентрации кальция; и
(c) получение антигенсвязывающей молекулы, элюированной на стадии (b).
Настоящее изобретение также относится к способам скрининга антигенсвязывающей молекулы, которые включают стадии (a)-(d) ниже:
(a) пропускание антигенсвязывающей молекулы или библиотеки антигенсвязывающих молекул через колонку с иммобилизованным на ней антигеном в условиях низкой концентрации кальция;
(b) сбор антигенсвязывающей молекулы, элюированной без связывания с колонкой на стадии (a);
(c) обеспечение связывания антигенсвязывающей молекулы, собранной на стадии (b), с антигеном в условиях высокой концентрации кальция; и
(d) получение антигенсвязывающей молекулы, которая связывается с антигеном на стадии (c).
Настоящее изобретение также относится к способам скрининга антигенсвязывающей молекулы, которые включают стадии (a)-(d) ниже:
(a) приведение антигена в контакт с антигенсвязывающей молекулой или библиотекой антигенсвязывающих молекул в условиях высокой концентрации кальция;
(b) получение антигенсвязывающей молекулы, которая связывается с антигеном на стадии (a);
(c) помещение антигенсвязывающей молекулы, полученной на стадии (b), в условия низкой концентрации кальция; и
(d) получение антигенсвязывающей молекулы, антигенсвязывающая активность которой на стадии (c) является более низкой, чем антигенсвязывающая активность на стадии (b).
Описанные выше стадии можно повторять два или более раз. Таким образом, настоящее изобретение относится к способам скрининга, которые, кроме того, включают стадию повторения стадий (a)-(c) или (a)-(d) два или более раз в упомянутых выше способах скрининга. Количество повторений стадий (a)-(c) или (a)-(d) конкретно не ограничено, и как правило, оно равно десяти или менее.
В способах скрининга по настоящему изобретению антигенсвязывающая активность антигенсвязывающей молекулы в условиях низкой концентрации кальция конкретно не ограничена, при условии, что она представляет собой антигенсвязывающую активность при концентрации ионизированного кальция от 0,1 мкМ до 30 мкМ. Предпочтительно, антигенсвязывающая активность включает антигенсвязывающую активность при концентрации ионизированного кальция от 0,5 мкМ до 10 мкМ. Более предпочтительные концентрации ионизированного кальция включают концентрации ионизированного кальция в ранней эндосоме in vivo. В частности, антигенсвязывающая активность включает активность при 1 мкМ - 5 мкМ. Между тем, антигенсвязывающая активность антигенсвязывающей молекулы в условиях высокой концентрации кальция конкретно не ограничена, при условии, что она представляет собой антигенсвязывающую активность при концентрации ионизированного кальция от 100 мкМ до 10 мМ. Предпочтительно, антигенсвязывающая активность включает антигенсвязывающую активность при концентрации ионизированного кальция от 200 мкМ до 5 мМ. Более предпочтительные концентрации ионизированного кальция включают концентрации ионизированного кальция в плазме in vivo. В частности, антигенсвязывающая активность включает активность при от 0,5 мМ до 2,5 мМ.
Антигенсвязывающую активность антигенсвязывающей молекулы можно определять способами, известными специалистам в данной области. Подходящие условия, помимо концентрации ионизированного кальция, могут быть выбраны специалистами в данной области. Антигенсвязывающую активность антигенсвязывающей молекулы можно оценивать с использованием KD (константа диссоциации), кажущейся KD (кажущаяся константа диссоциации), kd скорости диссоциации (скорость диссоциации), кажущейся kd (кажущаяся диссоциация: кажущаяся скорость диссоциации) и т.п. Их можно определять способами, известными специалистам в данной области, например, с использованием Biacore (GE Healthcare), графика Скэтчарда, FACS и т.п.
В рамках настоящего изобретения стадия отбора антигенсвязывающей молекулы, которая имеет более высокую антигенсвязывающую активность в условиях высокой концентрации кальция, чем в условиях низкой концентрации кальция, является равнозначной стадии отбора антигенсвязывающей молекулы, которая имеет более низкую антигенсвязывающую активность в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция.
Отличие между антигенсвязывающей активностью в условиях высокой концентрации кальция и антигенсвязывающей активностью в условиях низкой концентрации кальция конкретно не ограничено, при условии, что антигенсвязывающая активность является более высокой в условиях высокой концентрации кальция, чем в условиях низкой концентрации кальция. Однако антигенсвязывающая активность в условиях высокой концентрации кальция предпочтительно в два раза или более, более предпочтительно в 10 раз или более, и еще более предпочтительно в 40 раз или более превышает антигенсвязывающую активность в условиях низкой концентрации кальция.
Антигенсвязывающие молекулы, подлежащие скринингу способом скрининга по настоящему изобретению, могут представлять собой любые антигенсвязывающие молекулы. Например, описанные выше антигенсвязывающие молекулы можно подвергать скринингу. Например, возможно проводить скрининг антигенсвязывающих молекул, имеющих природную последовательность, или антигенсвязывающих молекул, имеющих аминокислотную последовательность с заменой.
Антигенсвязывающие молекулы, подлежащие скринингу способом скрининга по настоящему изобретению, можно получать любыми способами. Можно использовать, например, предварительно существующие антитела, предварительно существующие библиотеки (фаговые библиотеки и т.п.), и антитела и библиотеки, полученные из B-клеток иммунизированных животных или гибридом, полученных иммунизацией животных, антитела или библиотеки, полученные внесением аминокислот, способных хелатировать кальций (например, аспарагиновая кислота или глутаминовая кислота), или неприродных аминокислотных мутаций в такие антитела или библиотеки (библиотеки с высоким содержанием неприродных аминокислот или аминокислот, способных хелатировать кальций (например, аспарагиновая кислота или глутаминовая кислота), библиотеки, в которые внесения мутации на неприродные аминокислоты или мутации на аминокислоты, способные хелатировать кальций (например, аспарагиновая кислота или глутаминовая кислота) в конкретных участках, и т.п.), и т.п.
Антигенсвязывающую молекулу, имеющую по меньшей мере одну функцию, выбранную из:
(i) функция ускорения захвата антигена в клетки,
(ii) функция связывания с антигеном два или более раз,
(iii) функция ускорения снижения концентрации антигена в плазме, и
(iv) функция увеличения удержания в плазме,
можно получать способами скрининга по настоящему изобретению путем введения животным, таким как люди, мыши и обезьяны. Таким образом, способы скрининга по настоящему изобретению можно использовать в качестве способа скрининга для получения антигенсвязывающей молекулы, имеющей по меньшей мере одну из описанных выше функций.
Более того, ожидается, что такие антигенсвязывающие молекулы, получаемые способами скрининга по настоящему изобретению, будут лучшими в качестве фармацевтических препаратов, поскольку доза и частота введения у пациентов могут быть снижены, и, в результате, может быть снижена общая дозировка. Таким образом, способы скрининга по настоящему изобретению можно использовать в качестве способов скрининга антигенсвязывающих молекул для применения в качестве фармацевтических композиций.
Способы получения антигенсвязывающих молекул
Настоящее изобретение относится к способам получения антигенсвязывающей молекулы, которая имеет более низкую антигенсвязывающую активность в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция. Настоящее изобретение также относится к способам получения антигенсвязывающей молекулы, имеющей по меньшей мере одну функцию, выбранную из:
(i) функция ускорения захвата антигена в клетки,
(ii) функция связывания с антигеном два или более раз,
(iii) функция ускорения снижения концентрации антигена в плазме, и
(iv) функция увеличения удержания в плазме.
В частности, настоящее изобретение относится к способам получения антигенсвязывающей молекулы, которые включают стадии (a)-(e) ниже:
(a) определение антигенсвязывающей активности антигенсвязывающей молекулы в условиях низкой концентрации кальция;
(b) определение антигенсвязывающей активности антигенсвязывающей молекулы в условиях высокой концентрации кальция;
(c) отбор антигенсвязывающей молекулы, которая имеет более низкую антигенсвязывающую активность в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция;
(d) получение гена, кодирующего антигенсвязывающую молекулу, отобранную на стадии (c); и
(e) продуцирование антигенсвязывающей молекулы с использованием гена, полученного на стадии (d).
Настоящее изобретение также относится к способам получения антигенсвязывающей молекулы, которые включают стадии (a)-(e) ниже:
(a) приведение антигена в контакт с антигенсвязывающей молекулой или библиотекой антигенсвязывающих молекул в условиях высокой концентрации кальция;
(b) помещение антигенсвязывающей молекулы, связавшейся с антигеном на стадии (a), в условия низкой концентрации кальция;
(c) получение антигенсвязывающей молекулы, которая диссоциирует на стадии (b);
(d) получение гена, кодирующего антигенсвязывающую молекулу, полученную на стадии (c); и
(e) продуцирование антигенсвязывающей молекулы с использованием гена, выделенного на стадии (d).
Стадии (a)-(d) можно повторять два или более раз. Таким образом, настоящее изобретение относится к способам, которые, кроме того, включают стадию повторения стадий (a)-(d) два или более раз в описанных выше способах. Количество повторений стадий (a)-(d) конкретно не ограничено, и как правило, оно равно десяти или менее.
Более того, настоящее изобретение относится к способам получения антигенсвязывающей молекулы, которые включают стадии (a)-(f) ниже:
(a) приведение антигена в контакт с антигенсвязывающей молекулой или библиотекой антигенсвязывающих молекул в условиях низкой концентрации кальция;
(b) отбор антигенсвязывающей молекулы, которая не связывается с антигеном на стадии (a);
(c) приведение антигена в контакт с антигенсвязывающей молекулой, отобранной на стадии (b), в условиях высокой концентрации кальция;
(d) получение антигенсвязывающей молекулы, которая связывается с антигеном на стадии (c);
(e) получение гена, кодирующего антигенсвязывающую молекулу, полученную на стадии (d); и
(f) продуцирование антигенсвязывающей молекулы с использованием гена, полученного на стадии (e).
Стадии (a)-(e) можно повторять два или более раз. Таким образом, настоящее изобретение относится к способам, которые дополнительно включают стадию повторения стадий (a)-(e) два или более раз в описанных выше способах. Количество повторений стадии (a)-(e) конкретно не ограничено, и как правило, оно равно десяти или менее.
Настоящее изобретение также относится к способам получения антигенсвязывающей молекулы, которые включают стадии (a)-(e) ниже:
(a) приведение антигенсвязывающей молекулы или библиотеки антигенсвязывающих молекул в контакт с колонкой с иммобилизованным на ней антигеном в условиях высокой концентрации кальция;
(b) элюирование антигенсвязывающей молекулы, связавшейся с колонкой на стадии (a), из колонки в условиях низкой концентрации кальция;
(c) получение антигенсвязывающей молекулы, элюированной на стадии (b);
(d) получение гена, кодирующего антигенсвязывающую молекулу, полученную на стадии (c); и
(e) продуцирование антигенсвязывающей молекулы с использованием гена, полученного на стадии (e).
Стадии (a)-(d) можно повторять два или более раз. Таким образом, настоящее изобретение относится к способам, которые дополнительно включают стадию повторения стадий (a)-(d) два или более раз в описанных выше способах. Количество повторений стадий (a)-(d) конкретно не ограничено, и как правило, оно равно десяти или менее.
Также настоящее изобретение относится к способам получения антигенсвязывающей молекулы, которые включают стадии (a)-(f) ниже:
(a) пропускание антигенсвязывающей молекулы или библиотеки антигенсвязывающих молекул через колонку с иммобилизованным на ней антигеном в условиях низкой концентрации кальция;
(b) сбор антигенсвязывающей молекулы, элюированной без связывания с колонкой на стадии (a);
(c) обеспечение связывания антигенсвязывающей молекулы, собранной на стадии (b), с антигеном в условиях высокой концентрации кальция;
(d) получение антигенсвязывающей молекулы, которая связывается с антигеном на стадии (c);
(e) получение гена, кодирующего антигенсвязывающую молекулу, полученную на стадии (d); и
(f) получение антигенсвязывающей молекулы с использованием гена, полученного на стадии (e).
Стадии (a)-(e) можно повторять два или более раз. Таким образом, настоящее изобретение относится к способам, которые дополнительно включают повторение стадий (a)-(e) два или более раз в описанных выше способах. Количество повторений стадий (a)-(e) конкретно не ограничено, и как правило, оно равно десяти или или менее.
Настоящее изобретение также относится к способам получения антигенсвязывающей молекулы, которые включают стадии (a)-(f) ниже:
(a) приведение антигена в контакт с антигенсвязывающей молекулой или библиотекой антигенсвязывающих молекул в условиях высокой концентрации кальция;
(b) получение антигенсвязывающей молекулы, которая связывается с антигеном на стадии (a);
(c) помещение антигенсвязывающей молекулы, полученной на стадии (b), в условия низкой концентрации кальция;
(d) получение антигенсвязывающей молекулы, которая имеет более низкую антигенсвязывающую активность на стадии (c), чем антигенсвязывающая активность на стадии (b);
(e) получение гена, кодирующего антигенсвязывающую молекулу, полученную на стадии (d); и
(f) продуцирование антигенсвязывающей молекулы с использованием гена, полученного на стадии (e).
Стадии (a)-(e) можно повторять два или более раз. Таким образом, настоящее изобретение относится к способам, которые дополнительно включают повторение стадий (a)-(e) два или более раз в описанных выше способах. Количество повторений стадий (a)-(e) конкретно не ограничено, и как правило, оно равно десяти или менее.
Антигенсвязывающие молекулы, используемые для способов получения по настоящему изобретению, можно получать любым способом, и они включают существующие антитела и библиотеки (фаговые библиотеки, и т.д.), антитела и библиотеки, полученные из гибридом, полученных иммунизацией животных, или из B-клеток иммунизированных животных, антитела и библиотеки, полученные встраиванием аминокислот, способных хелатировать кальций (например, аспарагиновая кислота и глутаминовая кислота), или мутаций на неприродные аминокислоты в библиотеки (библиотеки с увеличенным содержанием аминокислот, способных хелатировать кальций (например, аспарагиновая кислота и глутаминовая кислота) или неприродных аминокислот, библиотеки, в которые внесены аминокислоты, способные хелатировать кальций (например, аспарагиновая кислота и глутаминовая кислота), или мутации на неприродные аминокислоты в конкретных участках и т.п.).
В описанных выше способах получения антигенсвязывающая активность антигенсвязывающей молекулы в условиях низкой концентрации кальция конкретно не ограничена, при условии, что она представляет собой антигенсвязывающую активность при концентрации ионизированного кальция от 0,1 мкМ до 30 мкМ. Предпочтительно, антигенсвязывающая активность включает антигенсвязывающую активность при концентрации ионизированного кальция от 0,5 мкМ до 10 мкМ. Более предпочтительные концентрации ионизированного кальция включают концентрацию ионизированного кальция в ранней эндосоме in vivo. В частности, антигенсвязывающая активность включает активность связывания антигена при от 1 мкМ до 5 мкМ. Между тем, антигенсвязывающая активность антигенсвязывающей молекулы в условиях высокой концентрации кальция конкретно не ограничена, при условии, что она представляет собой антигенсвязывающую активность при концентрации ионизированного кальция от 100 мкМ до 10 мМ. Предпочтительно, антигенсвязывающая активность включает антигенсвязывающую активность при концентрации ионизированного кальция от 200 мкМ до 5 мМ. Более предпочтительные концентрации ионизированного кальция включают концентрацию ионизированного кальция в плазме in vivo. В частности, антигенсвязывающая активность включает антигенсвязывающую активность при от 0,5 мМ до 2,5 мМ.
Антигенсвязывающую активность антигенсвязывающей молекулы можно определять способами, известными специалистам в данной области. Подходящие условия, отличные от концентрации ионизированного кальция, могут быть определены специалистами в данной области.
Стадия отбора антигенсвязывающей молекулы, которая имеет более высокую антигенсвязывающую активность в условиях высокой концентрации кальция, чем в условиях низкой концентрации кальция, является тождественной стадии отбора антигенсвязывающей молекулы, которая имеет более высокую антигенсвязывающую активность в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция.
Отличие между антигенсвязывающей активностью в условиях высокой концентрации кальция и антигенсвязывающей активностью в условиях низкой концентрации кальция конкретно не ограничено, при условии, что антигенсвязывающая активность является более высокой в условиях высокой концентрации кальция, чем в условиях низкой концентрации кальция. Однако антигенсвязывающая активность в условиях высокой концентрации кальция предпочтительно в два раза или более, более предпочтительно в 10 раз или более, и еще более предпочтительно в 40 раз или более превышает антигенсвязывающую активность в условиях низкой концентрации кальция.
В способах получения, описанных выше, связывание антигена и антигенсвязывающей молекулы можно проводить в любом состоянии, и состояние конкретно не ограничено. Например, связывание антигена и антигенсвязывающей молекулы можно проводить путем приведения антигена в контакт с иммобилизованной антигенсвязывающей молекулой или путем приведения антигенсвязывающей молекулы в контакт с иммобилизованным антигеном. Альтернативно, связывание можно проводить путем приведения антигена в контакт с антигенсвязывающей молекулой в растворе.
Более того, способ получения по настоящему изобретению можно использовать для описанной выше антигенсвязывающей молекулы, имеющей активность связывания с FcRn человека при нейтральных значениях pH, или можно комбинировать со способом сообщения или увеличения активности связывания с FcRn человека при нейтральных значениях pH. Когда способ получения по настоящему изобретению комбинируют со способом сообщения или увеличения активности связывания с FcRn человека при нейтральных значениях pH, способ дополнительно может включать стадию изменения аминокислот в антигенсвязывающей молекуле для сообщения или увеличения активности связывания с FcRn человека в условиях нейтральных значений pH. Между тем, предпочтительный FcRn-связывающий домен человека антигенсвязывающей молекулы, обладающей активностью связывания с FcRn человека при нейтральных значениях pH, включает, например, описанные выше FcRn-связывающие домены человека, обладающие активностью связывания с FcRn человека при нейтральных значениях pH. Таким образом, способы получения по настоящему изобретению дополнительно могут включать стадию отбора заранее антигенсвязывающей молекулы, имеющей FcRn-связывающий домен человека с более высокой активностью связывания с FcRn человека при нейтральных значениях pH, и/или изменения аминокислот в антигенсвязывающей молекуле для сообщения или увеличения активности связывания с FcRn человека при нейтральных значениях pH.
Более того, способ получения по настоящему изобретению можно использовать для антигенсвязывающей молекулы, имеющей описанную выше pH-зависимую антигенсвязывающую активность, или его можно комбинировать со способом сообщения pH-зависимой антигенсвязывающей активности (WO 2009/125825). Когда способ получения по настоящему изобретению комбинируют со способом сообщения pH-зависимой антигенсвязывающей активности, способ дополнительно может включать стадию отбора заранее антигенсвязывающей молекулы, которая имеет более низкую антигенсвязывающую активность в условиях кислых значений pH, чем в условиях нейтральных значений pH, и/или изменения аминокислот в антигенсвязывающей молекуле для снижения антигенсвязывающей активности в условиях кислых значений pH так, чтобы она была ниже, чем в условиях нейтральных значений pH.
Предпочтительные антигенсвязывающие молекулы, обладающие pH-зависимой антигенсвязывающей активностью, включают, например, антигенсвязывающие молекулы, в которых по меньшей мере одна аминокислота антигенсвязывающей молекулы заменена остатком гистидина или по меньшей мере один остаток гистидина встроен в антигенсвязывающую молекулу. Таким образом, способ получения по настоящему изобретению дополнительно может включать стадию использования антигенсвязывающей молекулы, в которой по меньшей мере одна аминокислота заменена остатком гистидина или по меньшей мере один остаток гистидина встроен в антигенсвязывающую молекулу, или стадию замены по меньшей мере одной аминокислоты остатком гистидина или встраивания по меньшей мере одного остатка гистидина в антигенсвязывающую молекулу.
В способе получения по настоящему изобретению вместо гистидина можно использовать неприродные аминокислоты. Таким образом, настоящее изобретение может подразумевать неприродные аминокислоты вместо гистидина, описанного выше.
Способами получения по настоящему изобретению можно получать антигенсвязывающие молекулы, имеющие по меньшей мере одну функцию, выбранную из:
(i) функция ускорения захвата антигена в клетки,
(ii) функция связывания с антигеном два или более раз,
(iii) функция ускорения снижения концентрации антигена в плазме, и
(iv) функция увеличения удержания в плазме,
при введении животным, таким как человек, мыши и обезьяны. Таким образом, способы получения по настоящему изобретению можно использовать в качестве способа получения антигенсвязывающей молекулы, имеющей по меньшей мере одну из описанных выше функций.
Более того, особенно ожидается, что такие антигенсвязывающие молекулы будут лучшими в качестве фармацевтических препаратов, поскольку доза и частота введения у пациентов могут быть снижены и, в результате, может быть снижена общая дозировка. Таким образом, способы получения по настоящему изобретению можно использовать в качестве способов получения антигенсвязывающих молекул для применения в качестве фармацевтических композиций.
Гены, получаемые способом получения по настоящему изобретению, как правило, содержатся (встроены в) в соответствующих векторах, а затем их вводят в клетки-хозяева. Векторы конкретно не ограничены, при условии, что они стабильно сохраняют встроенные нуклеиновые кислоты. Например, когда в качестве хозяина используют E. coli, предпочтительные клонирующие векторы включают вектор pBluescript (Stratagene); однако можно использовать различные коммерчески доступные векторы. При использовании векторов для получения антигенсвязывающих молекул по настоящему изобретению особенно пригодными являются экспрессирующие векторы. Экспрессирующие векторы конкретно не ограничены, при условии, что векторы экспрессируют антигенсвязывающие молекулы in vitro, в E. coli, в клетках культуры, или в организме. Например, вектор pBEST (Promega) является предпочтительным для экспрессии in vitro; вектор pET (Invitrogen) является предпочтительным для E. coli; вектор pME18S-FL3 (номер доступа GenBank № AB009864) является предпочтительным для клеток в культуре; и вектор pME18S (Mol Cell Biol. (1988) 8: 466-472) является предпочтительным для организмов. ДНК по настоящему изобретению можно встраивать в векторы общепринятыми способами, например, путем лигирования с использованием участков ферментов рестрикции (Current protocols in Molecular Biology, edit. Ausubel et al., (1987) Publish. John Wiley & Sons, Section 11.4-11.11).
Описанные выше клетки-хозяева конкретно не ограничены, и можно использовать различные клетки-хозяева, в зависимости от назначения. Примеры клеток для экспрессии антигенсвязывающих молекул включают бактериальные клетки (такие как клетки Streptococcus, Staphylococcus, E. coli, Streptomyces и Bacillus subtilis), эукариотические клетки (такие как клетки дрожжей и Aspergillus), клетки насекомых (такие как Drosophila S2 и Spodoptera SF9), клетки животных (такие как CHO, COS, HeLa, C127, 3T3, BHK, HEK293 и клетки меланомы Bowes) и клетки растений. Векторы можно встраивать в клетки-хозяева известными способами, например, способами осаждения с фосфатом кальция, способами электропорации (Current protocols in Molecular Biology edit. Ausubel et al. (1987) Publish. John Wiley & Sons, Section 9.1-9.9), способами липофекции и способами микроинъекции.
Клетки-хозяева можно культивировать известными способами. Например, при использовании клеток животных в качестве хозяев, в качестве культуральной среды можно использовать DMEM, MEM, RPMI1640 или IMDM. Их можно использовать с сывороточными добавками, такими как FBS или эмбриональная телячья сыворотка (FCS). Клетки можно культивировать в бессывороточных культурах. Предпочтительное значение pH в ходе культивирования составляет приблизительно от 6 до 8. Инкубацию, как правило, проводят при приблизительно от 30 до 40°C в течение приблизительно от 15 до 200 часов. При необходимости среду заменяют, аэрируют или перемешивают.
В представляющие интерес полипептиды можно включать подходящие сигналы секреции, так чтобы антигенсвязывающие молекулы, экспрессированные в клетке-хозяине, секретировались в просвет эндоплазматической сети, периплазматическое пространство или внеклеточную среду. Эти сигналы могут быть эндогенными для представляющих интерес антигенсвязывающих молекул, или они могут представлять собой гетерологичные сигналы.
С другой стороны, например, в качестве систем для продуцирования полипептидов in vivo можно использовать системы продуцирования с использованием животных или растений. Представляющий интерес полинуклеотид вводят животному или в растение, и полипептид продуцируется в организме животного или в растении, а затем его извлекают. "Хозяева" по настоящему изобретению включают таких животных и растения.
Системы продуцирования с использованием животных включают системы с использованием млекопитающих или насекомых. Можно использовать млекопитающих, таких как козы, свиньи, овцы, мыши и животные семейства бычьих (Vicki Glaser SPECTRUM Biotechnology Applications (1993)). Млекопитающие могут быть трансгенными животными.
Например, полинуклеотид, кодирующий антигенсвязывающую молекула по настоящему изобретению, получают в качестве слитого гена с геном, кодирующим полипептид, специфично продуцируемый в молоке, такой как β-казеин козы. Далее в эмбрионы коз инъецируют полинуклеотидные фрагменты, содержащие слитый ген, а затем их трансплантируют самкам коз. Желаемые антигенсвязывающие молекулы можно получать из молока, продуцируемого трансгенными козами, которые рождены от коз, которым трансплантировали эмбрионы, или их потомками. При необходимости, для увеличения объема молока, содержащего антигенсвязывающую молекулу, трансгенными козами, можно вводить гормоны (Ebert et al., Bio/Technology (1994) 12: 699-702).
Для продуцирования антигенсвязывающих молекул по настоящему изобретению можно использовать насекомых, таких как тутовый шелкопряд. Когда используют тутового шелкопряда, бакуловирусы, несущие полинуклеотид, кодирующий представляющую интерес антигенсвязывающую молекулу, можно использовать для инфицирования тутового шелкопряда, и из их жидкостей организма можно получать представляющую интерес антигенсвязывающую молекулу.
Более того, когда для получения антигенсвязывающих молекул по настоящему изобретению используют растения, можно использовать, например, табак. Когда используют табак, полинуклеотид, кодирующий представляющую интерес антигенсвязывающую молекулу, встраивают в экспрессирующий вектор растений, например, pMON 530, а затем вектор вводят в бактерии, такие как Agrobacterium tumefaciens. Затем бактериям позволяют инфицировать табак, такой как Nicotiana tabacum, и желаемые антигенсвязывающие молекулы можно получать из их листьев (Ma et al., Eur. J. Immunol. (1994) 24: 131-138). Альтернативно, можно инфицировать ряску (Lemna minor) сходными бактериями. После клонирования из клеток ряски можно получать желаемые антигенсвязывающие молекулы (Cox KM et al., Nat. Biotechnol. 2006 Dec; 24(12): 1591-1597).
Полученные таким образом антигенсвязывающие молекулы можно выделять из клеток-хозяев или из окружающей среды клеток-хозяев (такой как среда или молоко) и очищать в качестве по существу чистых и гомогенных антигенсвязывающих молекул. Способы выделения и очистки антигенсвязывающих молекул конкретно не ограничены, и можно использовать способы выделения и очистки, обычно используемые для очистки полипептида. Антигенсвязывающие молекулы можно выделять и очищать путем соответствующего выбора и комбинирования, например, хроматографических колонок, фильтрации, ультрафильтрации, высаливания, осаждения растворителем, экстракции растворителем, дистилляции, иммунопреципитации, SDS-полиакриламидного гель-электрофореза, изоэлектрического фокусирования, диализа и перекристаллизации.
Хроматография включает, например, аффинную хроматографию, ионообменную хроматографию, гидрофобную хроматографию, гель-фильтрацию, обращенно-фазовую хроматографию и адсорбционную хроматографию (Strategies for Protein Purification and Characterization: A Laboratory Course Manual. Ed Daniel R. Marshak et al., (1996) Cold Spring Harbor Laboratory Press). Такие способы хроматографии можно выполнять с использованием жидкофазной хроматографии, такой как ВЭЖХ и FPLC. Колонки, используемые для аффинной хроматографии, включают колонки с белком A и колонки с белком G. Колонки с использованием белка A включают, например, Hyper D, POROS и Sepharose F. F. (Pharmacia).
Если необходимо, антигенсвязывающую молекулу можно модифицировать произвольным образом, и можно частично удалять пептиды, позволяя соответствующему модифицирующему белок ферменту действовать до или после очистки антигенсвязывающей молекулы. Такие модифицирующие белок ферменты включают, например, трипсин, химотрипсин, лизилэндопептидазы, протеинкиназы и глюкозидазы.
<Фармацевтические композиции>
Настоящее изобретение также относится к фармацевтическим композициям, которые включают антигенсвязывающие молекулы по настоящему изобретению, антигенсвязывающие молекулы, выделенные способами скрининга по настоящему изобретению, или антигенсвязывающие молекулы, полученные способами получения по настоящему изобретению. Антигенсвязывающие молекулы по настоящему изобретению, антигенсвязывающие молекулы, выделенные способом скрининга по настоящему изобретению, или антигенсвязывающие молекулы, полученные способом получения по настоящему изобретению, представляют собой антигенсвязывающие молекулы, имеющие по меньшей мере одну функцию, выбранную из:
(i) функция ускорения захвата антигена в клетки,
(ii) функция связывания с антигеном два или более раз,
(iii) функция ускорения снижения концентрации антигена в плазме, и
(iv) функция увеличения удержания в плазме,
пригодны в качестве фармацевтических композиций, поскольку ожидается, что может быть снижена частота введения. Более того, фармацевтическая композиция по настоящему изобретению может включать фармацевтически приемлемый носитель.
В рамках настоящего изобретения фармацевтические композиции, как правило, относятся к средствам для лечения или профилактики или исследования и диагностики заболеваний.
Фармацевтические композиции по настоящему изобретению могут быть составлены способами, известными специалистам в данной области. Например, их можно использовать парентерально в форме инъекций стерильных растворов или суспензий, включающих воду или другую фармацевтически приемлемую жидкость. Например, такие композиции могут быть составлены путем смешивания в форме единичной дозы, требуемой повсеместно одобренной практикой производства лекарственных средств, путем комбинирования надлежащим образом с фармакологически приемлемыми носителями или средами, в частности, со стерильной водой, физиологическим раствором, растительным маслом, эмульгатором, суспензией, поверхностно-активным веществом, стабилизатором, вкусовой добавкой, эксципиентом, носителем, консервантом, связующим веществом и т.п. В таких составах количество активного ингредиента корректируют так, чтобы получить соответствующее количество в заданном диапазоне.
Стерильные композиции для инъекций могут быть составлены с использованием носителей, таких как дистиллированная вода для инъекций, в соответствии со стандартной практикой составления.
Водные растворы для инъекций включают, например, физиологический солевой раствор и изотонические растворы, содержащие декстрозу или другие адъюванты (например, D-сорбит, D-маннозу, D-маннит и хлорид натрия). Также их можно использовать в комбинации с соответствующими солюбилизаторами, например, спиртами (этанол и т.п.), полиспиртами (пропиленгликоль, полиэтиленгликоль и т.п.), неионными поверхностно-активными веществами (полисорбат 80(TM), HCO-50 и т.п.).
Масла включают кунжутное масло и соевые масла. В комбинации с солюбилизаторами можно использовать бензилбензоат и/или бензиловый спирт. Также можно комбинировать буферы (например, фосфатный буфер натрий-ацетатный буфер), успокаивающие средства (например, прокаина гидрохлорид), стабилизаторы (например, бензиловый спирт и фенол) и/или антиоксиданты. Полученными инъекционными препаратами заполняют подходящие ампулы.
Фармацевтические композиции по настоящему изобретению предпочтительно вводят парентерально. Например, композиции могут быть в дозированной форме для инъекций, трансназального введения, введения через легкие или чрескожного введения. Например, их можно вводить системно или локально путем внутривенной инъекции, внутримышечной инъекции, внутрибрюшинной инъекции, подкожной инъекции и т.п.
Способы введения можно надлежащим образом выбирать, учитывая возраст и симптомы пациента. Доза фармацевтической композиции, содержащей антигенсвязывающую молекулу, может составлять, например, от 0,0001 до 1,000 мг/кг для каждого введения. Альтернативно, доза может составлять, например, от 0,001 до 100000 мг на пациента. Однако настоящее изобретение не ограничивается числовыми величинами, описанными выше. Дозы и способы введения варьируют, в зависимости от массы тела пациента, возраста, симптомов и т.п. Специалисты в данной области могут установить подходящие дозы и способы введения, учитывая факторы, описанные выше.
Более того, фармацевтическая композиция по настоящему изобретению может представлять собой фармацевтическую композицию, используемую для ускорения захвата антигена в клетки и снижения концентрации антигена в плазме.
Настоящее изобретение также относится к способам ускорения антигенсвязывающей молекулой захвата антигена в клетки и способам ускорения снижения концентрации антигена в плазме путем введения антигенсвязывающей молекулы по настоящему изобретению или антигенсвязывающей молекулы, полученной способом получения по настоящему изобретению. Антигенсвязывающую молекулу можно вводить in vivo или in vitro. Индивидуум, подлежащий введению, включает, например, не являющихся человеком животных (мышей, обезьян и т.д.) и человека.
Настоящее изобретение также относится к способам увеличения количества раз связывания антигена антигенсвязывающей молекулой и к способам увеличения удержания в плазме антигенсвязывающей молекулы с использованием антигенсвязывающей молекулы по настоящему изобретению или антигенсвязывающей молекулы, полученной способом получения по настоящему изобретению.
Аминокислоты, содержащиеся в аминокислотных последовательностях по настоящему изобретению, могут быть посттрансляционно модифицированными (например, модификация N-концевого глутамина в пироглутаминовую кислоту путем пироглутамилирования хорошо известна специалистам в данной области). Естественно, такие посттрансляционно модифицированные аминокислоты включены в аминокислотные последовательности по настоящему изобретению.
Более того, настоящее изобретение относится к наборам для применения в способах по настоящему изобретению, которые включают по меньшей мере антигенсвязывающую молекулу по настоящему изобретению. В дополнение к вышесказанному, также в наборы могут быть упакованы фармацевтически приемлемые носители, среды, инструкции, в которых описан способ применения, и т.п.
Также настоящее изобретение относится к средствам для ускорения захвата антигенсвязывающими молекулами антигена в клетки, средствам для ускорения снижения концентрации антигена в плазме, средствам для увеличения количества раз связывания антигена одной антигенсвязывающей молекулой, и средствам для увеличения удержания в плазме антигенсвязывающих молекул, все из которых содержат в качестве активного ингредиента антигенсвязывающую молекулу по настоящему изобретению или антигенсвязывающую молекулу, полученную способами получения по настоящему изобретению.
Настоящее изобретение также относится к применению антигенсвязывающих молекул по настоящему изобретению или антигенсвязывающих молекул, полученных способами получения по настоящему изобретению, для получения средств для ускорения захвата антигенсвязывающими молекулами антигена в клетки, средств для ускорения снижения концентрации антигена в плазме, средств для увеличения количества раз связывания антигена одной антигенсвязывающей молекулой, или средств для увеличения удержания антигенсвязывающих молекул.
Настоящее изобретение также относится к антигенсвязывающим молекулам по настоящему изобретению или антигенсвязывающим молекулам, полученным способами получения по настоящему изобретению, для применения в способах ускорения антигенсвязывающими молекулами захвата антигена в клетки, средствах для ускорения снижения концентрации антигена в плазме, способах увеличения количества раз связывания антигена одной антигенсвязывающей молекулой, и способах увеличения удержания антигенсвязывающих молекул в плазме.
Все цитированные в описании документы уровня техники включены в настоящее описание в качестве ссылок.
[ПРИМЕРЫ]
Ниже настоящее изобретение конкретно описано с помощью примеров, однако его не следует считать ограниченным ими.
[Пример 1] Концепция эффекта ускорения элиминации антигена кальций-зависимыми антигенсвязывающими антителами
(1-1) Эффект антител с pH-зависимым связыванием антигена на ускорение элиминации антигена
H54/L28-IgG1, описанное в WO 2009/125825, представляет собой гуманизированное антитело против рецептора IL-6. Fv4-IgG1 представляет собой гуманизированное антитело против рецептора IL-6, которое получено путем сообщения H54/L28-IgG1 свойства связывания с растворимым рецептором IL-6 человека pH-зависимым образом (которое связывается в нейтральных условиях, но диссоциирует в кислых условиях). Исследование in vivo, описанное в WO 2009/125825, с использованием мышей продемонстрировало, что элиминация растворимого рецептора IL-6 человека могла значительно ускоряться в группе, в которой вводили Fv4-IgG1 и растворимый рецептор IL-6 человека в качестве антигена, по сравнению с группой, в которой вводили смесь H54/L28-IgG1 и растворимого рецептора IL-6 человека в качестве антигена.
Растворимый рецептор IL-6 человека, связанный с обычным антителом, которое связывается с растворимым рецептором IL-6 человека, рециклирует в плазму вместе с антителом через FcRn. Между тем, антитело, которое связывается с растворимым рецептором IL-6 человека pH-зависимым образом, диссоциирует от растворимого рецептора IL-6 человека, связанного с антителом, в кислых условиях в эндосоме. Диссоциированный растворимый рецептор IL-6 человека деградируется в лизосоме. Это может значительно ускорить элиминацию растворимого рецептора IL-6 человека. Затем антитело, которое связывается с растворимым рецептором IL-6 человека pH-зависимым образом, рециклирует в плазму через FcRn. Рециклировавшее антитело может вновь связываться с растворимым рецептором IL-6 человека. Путем повторения этого цикла одна молекула антитела может многократно связываться с растворимыми рецепторами IL-6 человека (фиг.1).
Между тем, как описано в WO 2009/125825, после связывания с рецептором IL-6 человека мембранного типа, обычное гуманизированное антитело против рецептора IL-6 интернализуется в комплексе гуманизированного антитела против рецептора IL-6 и рецептора IL-6 человека мембранного типа, а затем деградируется в лизосоме. Напротив, гуманизированное антитело против рецептора IL-6, которое связывается с рецептором IL-6 pH-зависимым образом, рециклирует в плазму через диссоциацию от рецептора IL-6 человека мембранного типа в кислых условиях в эндосоме после интернализации в комплексе с рецептором IL-6 человека мембранного типа. Рециклировавшее антитело может вновь связываться с рецептором IL-6 человека мембранного типа. Путем повторения этого цикла одна молекула антитела может многократно связываться с рецептором IL-6 человека мембранного типа (фиг.2).
(1-2) pH и концентрации кальция в плазме и эндосоме
В механизме pH-зависимого связывания антитела, представленного на фиг.1 и 2, важно, чтобы антитело сильно связывалось с антигеном в плазме и диссоциировало от антигена в эндосоме на основе различий среды между плазмой и эндосомой, т.е. отличий pH (pH 7,4 в плазме; pH 6,0 в эндосоме). Степень различий среды между плазмой и эндосомой является важной для дифференциации антигенсвязывающей способности антитела с pH-зависимым связыванием в плазме и эндосоме. Отличие pH является следствием отличия в концентрации ионов водорода. В частности, концентрация ионов водорода в плазме (pH 7,4) составляет приблизительно 40 нМ, в то время как концентрация в эндосоме (pH 6,0) она составляет приблизительно 1000 нМ. Концентрация этого фактора (ионов водорода) отличается между плазмой и эндосомой приблизительно в 25 раз.
Авторы настоящего изобретения считают, что для легкого достижения механизма, проиллюстрированного на фиг.1 и 2, или для усиления этого механизма, может быть полезным использовать антитело, которое зависит от того фактора, который имеет большее различие в концентрации между плазмой и эндосомой, чем различие концентрации ионов водорода между ними. Таким образом, авторы изобретения провели поиск фактора, концентрация которого значительно отличается между плазмой и эндосомой. В результате был идентифицирован кальций. Концентрация ионизированного кальция составляет приблизительно от 1,1 до 1,3 мМ в плазме и приблизительно 3 мкМ в эндосоме. Концентрация этого фактора (кальция) отличается между ними приблизительно в 400 раз. Таким образом, было выявлено, что это соотношение является более высоким, чем отличие в концентрации ионов водорода (25 раз). В частности, ожидалось, что механизм, проиллюстрированный на фиг.1 и 2, будет легче достигнут или усилен при использовании антитела с зависимым от концентрации ионизированного кальция связыванием, которое связывается с антигеном в условиях высокой концентрации кальция (от 1,1 до 1,3 мМ), но диссоциирует от антигена в условиях низкой концентрации кальция (3 мкМ).
Более того, в WO 2009/125825 описано получение антител с pH-зависимым связыванием, свойства которых изменяются при pH между 7,4 и 6,0, путем встраивания гистидина. Гистидин является электрически нейтральным при нейтральных условиях в плазме, однако положительно заряжен в кислых условиях в эндосоме. Зависимость от pH можно сообщать взаимодействию антиген-антитело с использованием изменения электрического заряда гистидина. Между тем, как показано на фиг.3, когда используют гистидин, для связывания с антигеном в плазме и диссоциации от антигена в эндосоме остатки гистидина в антителе должны взаимодействовать с положительно заряженными аминокислотами антигена или аминокислотами, которые потенциально служат в качестве донора для образования водородных связей. Таким образом, эпитоп антигена, с которым связывается антитело с pH-зависимым связыванием, для обеспечения заданного эффекта должен содержать положительно заряженные аминокислоты или аминокислоты, которые потенциально служат в качестве донора для образования водородных связей.
С другой стороны, как показано на фиг.4, предполагается, что антитело с кальций-зависимым связыванием связывается с антигеном через ион кальция. В этом случае, эпитоп антигена содержит отрицательно заряженные аминокислоты или аминокислоты, которые потенциально служат в качестве акцептора для образования водородных связей, которые способны хелатировать ион кальция. Таким образом, такие антитела могут быть нацелены на эпитопы, на которые не нацеливаются антитела с pH-зависимым связыванием путем встраивания гистидина. Более того, как показано на фиг.5, ожидается, что с использованием антител как с зависимостью от кальция, так и с зависимостью от pH можно нацеливаться на эпитопы, которые обладают широким множеством свойств.
[Пример 2] Выделение антител с Ca-зависимым связыванием из библиотеки антител человека с использованием способа фагового дисплея
(2-1) Получение библиотеки фагового дисплея наивных антител человека
Было сконструировано несколько библиотек фагового дисплея антител, которые экспонируют Fab-домены, содержащие последовательности антител человека, с использованием в качестве матрицы поли-A-РНК, полученной из PBMC человека, поли-A-РНК человека, доступной в продаже и т.п., в соответствии с Methods Mol Biol. 2002, 178: 87-100.
(2-2) Выделение фрагментов антител с Ca-зависимым связыванием из библиотек с помощью пэннинга на гранулах
Первичную селекцию из сконструированных библиотек фагового дисплея антител человека обеспечивали путем обогащения фрагментами антител, имеющих связывающую способность антитела, или путем обогащения с использованием способности Ca-зависимого связывания в качестве индикатора. Обогащение фрагментами антител со способностью к Ca-зависимому связыванию осуществляли путем элюированием фагов путем хелатирования с помощью EDTA ионов Ca после связывания фрагментов антител с антигеном в присутствии ионов Ca. В качестве антигена использовали биотинилированный рецептор IL-6 человека.
Фаги получали с помощью E. coli, несущих фагмиды фагового дисплея, сконструированные так, как описано выше. Полученную культуральную среду осаждали с использованием 2,5 M NaCl/10% PEG. Затем осадок разбавляли TBS с получением раствора с фаговой библиотекой. К раствору с фаговой библиотекой добавляли BSA и CaCl2, так чтобы конечные концентрации BSA и ионизированного кальция составляли 4% и 1,2 мМ, соответственно. Пэннинг проводили в соответствии с общепринятым способом пэннинга с использованием магнитных гранул с иммобилизованным на них антигеном (J Immunol Methods. 2008 Mar 20, 332(1-2): 2-9; J Immunol Methods. 2001 Jan 1, 247(1-2): 191-203; Biotechnol Prog. 2002 Mar-Apr, 18(2): 212-20; Mol Cell Proteomics. 2003 Feb, 2(2): 61-9). Использованные магнитные гранулы представляли собой покрытые нейтравидином гранулы (Sera-Mag SpeedBeads NeutrAvidin-coated) и покрытые стрептавидином гранулы (Dynabeads M-280 Streptavidin).
В частности, 250 пмоль биотинилированного антигена добавляли к полученному раствору с фаговой библиотекой и приводили в контакт с антигеном при комнатной температуре в течение 60 минут. Добавляли блокированные BSA магнитные гранулы и инкубировали для связывания при комнатной температуре в течение 15 минут. Гранулы промывали один раз 1 мл 1,2 мМ CaCl2/TBS (TBS, содержащий 1,2 мМ CaCl2). Затем фаги собирали элюированием с использованием стандартного способа, для обогащения фрагментами антител, обладающими способностью связывания, или путем суспендирования гранул в 2 мМ EDTA/TBS (TBS, содержащий 2% EDTA) для обогащения фрагментами антител, имеющими способность к Ca-зависимому связыванию. E. coli инфицировали добавлением 10 мл штамма E. coli TG1 в фазе логарифмического роста (OD600 0,4-0,5) к полученной суспензии фага и культивированием при 37°C в течение одного часа при осторожном перемешивании. Инфицированные E. coli высевали в планшеты (225 мм × 225 мм). Вновь начинали культивирование этих E. coli для культивирования фагов.
При втором и последующих пэннингах, обогащения достигали с использованием способности к Ca-зависимому связыванию в качестве индикатора. В частности, 40 пмоль биотинилированного антигена добавляли к полученному раствору фаговой библиотеки. Фаги приводили в контакт с антигеном при комнатной температуре в течение 60 минут. К суспензии добавляли блокированные BSA магнитные гранулы и инкубировали для связывания при комнатной температуре в течение 15 минут. Гранулы промывали один раз 1,2 мМ CaCl2/TBST (TBS содержащий 1,2 мМ CaCl2 и 0,1% Tween-20) и 1,2 мМ CaCl2/TBS по 1 мл в каждом случае. Затем добавляли 0,1 мл 2 мМ EDTA/TBS (TBS, содержащий 2% EDTA) для суспендирования гранул при комнатной температуре, и сразу после суспендирования гранулы удаляли с использованием магнитного стенда, чтобы собрать суспензию фагов. Полученную суспензию фагов добавляли к 10 мл E. coli штамма TG1 в ходе логарифмической фазы роста (OD600 0,4-0,5) для инфицирования E. coli, которые затем культивировали при 37°C в течение одного часа при осторожном перемешивании. Инфицированные E. coli высевали в планшеты (225 мм × 225 мм). Вновь начинали культивирования этих E. coli, и фаги культивировали так, как описано выше. Пэннинг повторяли дважды.
(2-3) Оценка с помощью ELISA фагов
Из отдельных колоний E. coli, полученных способом, описанным выше, получали содержащие фаг культуральные суспернатанты в соответствии с Metods Mol Biol. 2002, 178: 133-145.
В содержащие фаг культуральные супернатанты добавляли BSA и CaCl2, так чтобы конечные концентрации BSA и кальция составляли 4% и 1,2 мМ, соответственно. Супернатанты подвергали ELISA. 96-луночные микропланшеты для титрования StreptaWell (Roche) покрывали с использованием 100 мкл PBS, содержавшего биотинилированный антиген. После промывания PBST (PBS, содержащий 0,1% Tween20) для удаления антигена, планшеты блокировали 250 мкл 4% BSA/TBS в течение одного часа или более. 4% BSA-TBS удаляли, а затем полученные культуральные супернатанты добавляли к планшетам. Планшеты выдерживали при 37°C в течение одного часа для обеспечения связывания антитела фагового дисплея. После промывания 1,2 мМ CaCl2/TBST (TBS, содержащий 1,2 мМ CaCl2 и 0,1% Tween20), в планшеты добавляли 1,2 мМ CaCl2/TBS или 1 мМ EDTA/TBS. Планшеты выдерживали при 37°C в ходе инкубации в течение 30 минут. После промывания 1,2 мМ CaCl2/TBST планшеты инкубировали в течение одного часа с конъюгированным с HRP антителом против M13 (Amersham Pharmacia Biotech), разбавленным TBS, содержавшим 4% BSA и 1,2 мМ ионизированный кальций. После промывания 2 мМ CaCl2/TBST, проводили детекцию с раствором только TMB (ZYMED). После остановки реакции добавлением серной кислоты определяли поглощение при 450 нм. Фрагменты антител, которые были оценены как имеющие способность к Ca-зависимому связыванию, анализировали в отношении их нуклеотидных последовательностей с использованием специфических праймеров.
(2-4) Экспрессия и очистка антител
Клоны, которые оценили как имеющие способность к Ca-зависимому связыванию с помощью ELISA фагов, вводили в экспрессирующие плазмиды клеток животных. Антитела экспрессировали с использованием следующего способа. Клетки линии, происходящей из клеток почки эмбриона FreeStyle 293-F (Invitrogen), суспендировали в среде для экспрессии FreeStyle 293 Expression Medium (Invitrogen), и аликвоты объемом 3 мл высевали в каждую ячейку планшетов с 6 ячейками с плотностью клеток 1,33×106 клеток/мл. Полученные плазмиды вводили в клетки способом липофекции. Клетки культивировали в инкубаторе CO2 (37°C, 8% CO2, 90 об/мин) в течение четырех суток. Из полученных культуральных супернатантов, антитела очищали с использованием rProtein A SepharoseTM Fast Flow (Amersham Biosciences) способом, известным специалистам в данной области. Концентрации очищенных антител определяли путем измерения поглощения при 280 нм с использованием спектрофотометра. Концентрации антител вычисляли из установленных величин на основе коэффициента экстинкции, определенного способом PACE (Protein Science 1995; 4: 2411-2423).
[Пример 3] Оценка полученных антител в отношении их активности Ca-зависимого связывания с рецептором IL-6 человека
Антитела 6RL#9-IgG1 (тяжелая цепь SEQ ID NO: 1; легкая цепь SEQ ID NO: 2), 6RK#12-IgG1 (тяжелая цепь SEQ ID NO: 66; легкая цепь SEQ ID NO: 67) и FH4-IgG1 (тяжелая цепь SEQ ID NO: 3; легкая цепь SEQ ID NO: 4), полученные согласно примеру 2, оценивали в отношении их активности связывания с рецептором интерлейкина 6 человека (hIL6R) при pH 7,4 с использованием Biacore T100 (GE Healthcare). Анализ проводили с использованием в качестве подвижного буфера 0,05% поверхностно-активного вещества P20, 10 ммоль/л ACES, 150 ммоль/л NaCl (pH 7,4 или 6,0), содержащего 3 мкМ или 2 мМ CaCl2.
После иммобилизации достаточного количества рекомбинантного белка A (Thermo Scientific) на сенсорном чипе CM4 (GE Healthcare) способом присоединения аминов, антителам позволяли связываться с сенсорным чипом. Подходящую концентрацию hIL-6R инжектировали в качестве анализируемого соединения для взаимодействия с антителами на сенсорном чипе. Затем инжектировали 10 ммоль/л глицина-HCl (pH 1,5) для регенерации сенсорного чипа. Измерения проводили при 37°C. Сенсограммы, полученные с помощью этого измерения, представлены на фиг.6. Результат продемонстрировал, что все из антител 6RL#9-IgG1, 6RK#12-IgG1 и FH4-IgG1 связывались с hIL6R слабее в условиях 3 мкМ концентрации Ca2+, чем условиях 2 мМ концентрации Ca2+.
Среди этих антител, в качестве антител, проявляющих зависимость от Ca, 6RL#9-IgG1 (тяжелая цепь SEQ ID NO: 1; легкая цепь SEQ ID NO: 2) и FH4-IgG1 (тяжелая цепь SEQ ID NO: 3; легкая цепь SEQ ID NO: 4) далее анализировали в отношении кинетики. H54/L28-IgG1 (тяжелая цепь SEQ ID NO: 5; легкая цепь SEQ ID NO: 6), описанное в WO 2009/125825, использовали в качестве антитела, не проявляющего зависимость от Ca. Использованные условия высокой и низкой концентрации ионов кальция представляли собой 2 мМ и 3 мкМ, соответственно. В качестве антигена использовали рецептор IL-6 человека (IL-6R). Соответствующее количество белка A (Invitrogen) иммобилизовывали на сенсорном чипе CM4 (GE Healthcare) способом присоединения аминов, и представляющие интерес антитела улавливали на чипе. Два типа использованных подвижных буферов представляли собой: [10 ммоль/л ACES, 150 ммоль/л NaCl, 0,05% (масс./об.) Tween20, 2 ммоль/л CaCl2 (pH 7,4)] или [10 ммоль/л ACES, 150 ммоль/л NaCl, 0,05% (масс./об.) Tween20, 3 мкмоль/л CaCl2 (pH 7,4)]. Все измерения проводили при 37°C. Каждый буфер также использовали для разбавления IL-6R.
H54L28-IgG1 анализировали путем инжекции каждого подвижного буфера в качестве пустого образца и разбавленного раствора IL-6R со скоростью потока 20 мкл/мин в течение трех минут. Таким образом, IL-6R позволяли взаимодействовать с антителом, уловленном на сенсорном чипе. Затем инжектировали подвижный буфер со скоростью потока 20 мкл/мин в течение десяти минут для выявления диссоциации IL-6R. Затем инжектировали 10 ммоль/л глицина-HCl (pH 1,5) со скоростью потока 30 мкл/мин в течение 30 секунд для регенерации сенсорного чипа. Константу скорости ассоциации ka (1/Мс) и константу скорости диссоциации kd (1/с), которые являются параметрами кинетики, вычисляли из сенсограммы, полученной с помощью измерения. Исходя из этих величин, вычисляли константу диссоциации KD (M) между каждым антителом и рецептором IL-6 человека. Каждый параметр вычисляли с использованием программного обеспечения Biacore T100 Evaluation Software (GE Healthcare).
FH4-IgG1 и 6RL#9-IgG1 анализировали путем инжектирования каждого подвижного буфера в качестве пустого образца и разбавленного раствора IL-6R со скоростью потока 5 мкл/мин в течение 15 минут. Таким образом, IL-6R позволяли взаимодействовать с антителом, уловленном на сенсорном чипе. Затем инжектировали 10 ммоль/л глицина-HCl (pH 1,5) со скоростью потока 30 мкл/мин в течение 30 секунд для регенерации сенсорного чипа. Исходя из модели аффинности стационарного состояния, из сенсограммы, полученной с помощью этого измерения, была вычислена константа диссоциации KD (M). Каждый параметр вычисляли с использованием программного обеспечения Biacore T100 Evaluation Software (GE Healthcare).
Константы диссоциации KD между IL-6R и каждым антителом в присутствии 2 мМ CaCl2, которые были определены описанными выше способами, представлены в таблице 7. H54/L28-IgG1 не продемонстрировал какого-либо различия в уровне связывания IL-6R вследствие различий в концентрации Ca. Между тем, FH4-IgG1 и 6RL#9-IgG1 проявляли значительное ухудшение связывания в условиях низкой концентрации Ca (фиг.7, 8 и 9).
В случае H54/L28-IgG1, KD при концентрации Ca 3 мкМ, может быть вычислена способами, сходными со способами, которые использовали для определения KD при концентрации Ca 2 мМ. В случае FH4-IgG1 и 6RL#9-IgG1, с другой стороны, трудно вычислить KD при концентрации Ca 3 мкМ способами, сходными со способами, описанными выше, поскольку связывание с IL-6R практически не выявлялось при концентрации Ca 3 мкМ. Однако KD можно предсказать с использованием формулы 1, представленной ниже (Biacore T100 Software Handbook, BR-1006-48, AE 01/2007).
[Формула 1]

Каждый символ в формуле 1, представленной выше, определен ниже.
Req (RU): уровни связывания в стационарном состоянии
Rmax (RU): способность поверхности связывать анализируемый образец
RI (RU): общий вклад рефракционного индекса в образце
C (M): концентрация анализируемого соединения
KD (M): равновесная константа диссоциации
Константа диссоциации KD между IL-6R и каждым антителом при концентрации Ca 3 мкмоль/л, которая может быть предсказана с использованием формулы 1, представленной выше, показана в качестве приблизительной оценки в таблице 8.
В таблице 8, представленной выше, величины Req, Rmax, RI и C оценены на основе результатов анализа.
На основе данных, описанных выше, было предсказано, что KD между IL-6R и FH4-IgG1 или 6RL#9-IgG1 увеличивалась приблизительно в 60 или 120 раз (аффинность была снижена в 60 или 120 раз или более), когда концентрацию CaCl2 изменяли с 2 мМ до 3 мкМ. В таблице 9 обобщенно представлены величины KD при концентрациях CaCl2 2 мМ и 3 мкМ и зависимость от Ca для трех типов H54/L28-IgG1, FH4-IgG1 и 6RL#9-IgG1.
[Пример 4] Оценка полученных антител в отношении связывания ими ионов кальция
Далее антитела исследовали в отношении связывания ими кальция с помощью дифференциальной сканирующей калориметрии (DSC) (MicroCal VP-Capillary DSC; MicroCal) для оценки средней температуры термической денатурации (величины Tm). Средняя температура термической денатурации (величина Tm) служит в качестве индикатора стабильности. Когда белок стабилизирован связыванием ионов кальция, средняя температура термической денатурации (величина Tm) является повышенной по сравнению со средней температурой термической денатурации, когда белок не связан с ионами кальция (J Bio Chem. 2008 Sep 12; Vol.283; No. 37: pp 25140-25149). Исходя из этого принципа, антитела оценивали в отношении связывания ими ионов кальция. Очищенные антитела подвергали диализу (EasySEP, TOMY) против раствора [20 мМ Tris-HCl, 150 мМ NaCl, 2 мМ CaCl2 (pH 7,4)] или [20 мМ Tris-HCl, 150 мМ NaCl, 3 мкМ CaCl2 (pH 7,4)]. Растворы белков доводили до 0,1 мг/мл с использованием того же буфера для диализа, который использовали при диализе раствора белка. Измерение DSC проводили при скорости нагревания 240°C/час от 20 до 115°C. Исходя из полученных кривых денатурации DSC, вычисляли среднюю температуру термической денатурации (величину Tm) для Fab-домена каждого антитела. Величины представлены в таблице 10.
Результат, представленный в таблице 10, демонстрирует, что для FH4 и 6RL#9, которые проявляют способность к кальций-зависимому связыванию, величины Tm их Fab варьируют, в зависимости от концентрации кальция, в то время как H54/L28, который не проявляет способности к кальций-зависимому связыванию, величина Tm не изменяется. Выявленные изменения величин Tm Fab в FH4 и 6RL#9 указывают на то, что Fab-домены антител были стабилизированы связыванием ионов кальция с антителами. Это подразумевает, что ион кальция связывается с FH4 и 6RL#9, в то время как ион кальция не связывается с H54/L28.
[Пример 5] Оценка антител с Ca-зависимым связыванием в отношении их эффекта на удержание антигена в плазме с использованием нормальных мышей
(5-1) Исследование in vivo с использованием нормальных мышей
Нормальным мышам (мышь 57BL/6J; Charles River Japan) вводили hsIL-6R (растворимый рецептор IL-6 человека: полученный, как описано в справочном примере 1), отдельно или в комбинации с антителом против рецептора IL-6 человека, а затем их оценивали в отношении динамики in vivo hsIL-6R и антитела против рецептора IL-6 человека. Раствор hsIL-6R (5 мкг/мл) или смешанный раствор hsIL-6R и антитела против рецептора IL-6 человека, вводили в количестве 10 мл/кг один раз в хвостовую вену. Используемые антитела против рецептора IL-6 человека представляли собой H54/L28-IgG1, 6RL#9-IgG1 и FH4-IgG1, описанные выше.
Концентрация hsIL-6R составляла 5 мкг/мл во всех смешанных растворах. Между тем, концентрация антитела против рецептора IL-6 человека отличалась в случае каждого антитела. Концентрация H54/L28-IgG1 составляла 0,1 мг/мл, в то время как концентрации 6RL#9-IgG1 и FH4-IgG1 составляли 10 мг/мл. Антитело против рецептора IL-6 человека присутствует в избытке относительно hsIL-6R, и, таким образом, предполагается, что практически каждый hsIL-6R связывается антителом. Взятие крови проводили через 15 минут, 7 часов, 1 сутки, 2 суток, 4 суток, 7 суток, 14 суток, 21 сутки и 28 сутки после введения. Взятую кровь сразу центрифугировали при 4°C и 12000 об/мин в течение 15 минут для отделения плазмы. Отделенную плазму хранили в морозильной камере при -20°C или ниже до измерения.
(5-2) Определение с помощью ELISA концентрации антитела против рецептора IL-6 человека в плазме нормальных мышей
Концентрацию антитела против рецептора IL-6 человека в плазме мыши определяли с помощью ELISA. Сначала F(ab’)2-фрагмент антитела против IgG человека (специфичный к γ-цепи) (SIGMA) распределяли в планшеты Nunc-Immuno Plates, MaxiSorp (Nalge nunc International) и выдерживали их в течение ночи при 4°C с получением планшетов с иммобилизованным антителом против IgG человека. Получали образцы для калибровочной кривой, имеющие плазменные концентрации 0,64, 0,32, 0,16, 0,08, 0,04, 0,02 и 0,01 мкг/мл, и образцы для анализа плазмы мыши, разбавленные в 100 раз или более, и разделяли их на аликвоты в планшеты с иммобилизованным антителом против IgG человека. Планшеты инкубировали при 25°C в течение одного часа, а затем проводили инкубацию с биотинилированным антителом против IL-6R человека (R&D) при 25°C в течение одного часа. Затем проводили реакцию со стрептавидин-PolyHRP80 (Stereospecific Detection Technologies) при 25°C в течение 0,5 часа. Проявление цвета проводили с использованием в качестве субстрата TMB One Component HRP Microwell Substrate (BioFX Laboratories). После остановки реакции 1 н. серной кислотой (Showa Chemical) измеряли поглощение при 450 нм на устройстве для считывания микропланшетов. Концентрации в плазме у мышей вычисляли из поглощения на калибровочной кривой с использованием аналитического программного обеспечения SOFTmax PRO (Molecular Devices). Концентрации антител H54/L28-IgG1, 6RL#9-IgG1 и FH4-IgG1 в плазме у нормальных мышей после внутривенного введения, определенные с помощью этого способа, представлены на фиг.10.
(5-3) Измерение концентрации hsIL-6R в плазме способом электрохемилюминесценции
Концентрацию hsIL-6R в плазме мышей определяли способом электрохемилюминесценции. Приготавливали образцы hsIL-6R для калибровочной кривой, доведенные до концентрации 2000, 1000, 500, 250, 125, 62,5 или 31,25 пг/мл, и анализируемые образцы плазмы мыши, разбавленные в 50 раз или более. Образцы смешивали с раствором моноклонального антитела против IL-6R человека (R&D), меченного рутением с помощью SULFO-TAG NHS Ester (Meso Scale Discovery), биотинилированного антитела против IL-6R человека (R&D) и тоцилизумаба (тяжелая цепь SEQ ID NO: 13; легкая цепь SEQ ID NO: 14), а затем позволяли им реагировать в течение ночи при 4°C. Буфер для анализа, используемый для этой реакции, содержит 10 мМ EDTA для снижения концентрации свободного Ca в образцах, так чтобы практические каждый hsIL-6R диссоциировал от 6RL#9-IgG1 или FH4-IgG1 в образцах и связывался с добавленным тоцилизумабом. Затем смеси разделяли на аликвоты в планшет со стрептавидином MA400 PR Streptavidine Plate (Meso Scale Discovery). После реакции в течение дополнительного часа при 25°C, планшет промывали. Сразу после добавления в планшет аликвот буфера для считывания T (×4) (Meso Scale Discovery), проводили измерение с использованием устройства для считывания SECTOR PR 400 (Meso Scale Discovery). Концентрацию hSIL-6R вычисляли, исходя из ответа на калибровочной кривой с использованием аналитического программного обеспечения SOFTmax PRO (Molecular Devices). Концентрации hsIL-6R в плазме у нормальных мышей с течением времени после внутривенного введения, определенные описанным выше способом, представлены на фиг.11.
Данные, описанные выше, продемонстрировали, что hsIL-6R, введенный отдельно, элиминировался очень быстро. Между тем, элиминация hsIL-6R была значительно замедлена, когда hsIL-6R вводили одновременно с основным антителом H54/L28-IgG1, которое не проявляет Ca-зависимого связывания hsIL-6R. Между тем, элиминация hsIL-6R была значительно ускорена, когда hsIL-6R одновременно вводили с 6RL#9-IgG1 или FH4-IgG1, которые имели в 100 раз или более высокое hsIL-6R Ca-зависимое связывание. Когда hsIL-6R вводили в комбинации с 6RL#9-IgG1 или FH4-IgG1, концентрация hsIL-6R в плазме на 1 сутки могла снижаться в 39 раз или в два раза, соответственно, по сравнению с тем, когда hsIL-6R вводили в комбинации с H54/L28-IgG1. Это демонстрирует, что антитела с кальций-зависимым связыванием могут ускорять элиминацию антигена из плазмы.
[Пример 6] Испытания по улучшению эффекта антитела с Ca-зависимым связыванием антигена (препарат антител) в отношении ускорения элиминации антигена
(6-1) Что касается связывания IgG-антитела с FcRn
IgG-антитела имеют более длительное время удержания в плазме в результате связывания FcRn. Связывание между IgG и FcRn наблюдают только в кислых условиях (pH 6,0). Напротив, связывание практически не поддается выявлению в нейтральных условиях (pH 7,4). IgG-антитело захватывается в клетки неспецифическим образом. Антитело возвращается на клеточную поверхность путем связывания с эндосомальным FcRn в кислых условиях эндосом, а затем диссоциирует от FcRn в нейтральных условиях плазмы. Когда связывание FcRn в кислых условиях утрачивается вследствие внесения мутаций в Fc-домен IgG, время удержания антитела в плазме значительно снижается, поскольку антитело более не рециклирует в плазму из эндосомы.
Описанным способом увеличения удержания в плазме IgG-антитела является усиление связывания FcRn в кислых условиях. Аминокислотные мутации вносят в Fc-домен IgG-антитела для увеличения его связывания с FcRn в кислых условиях. Это увеличивает эффективность рециклирования в плазму из эндосомы, что приводит к увеличению удержания в плазме. Важным требованием при замене аминокислоты является отсутствие усиления связывания FcRn в нейтральных условиях. Если IgG-антитело связывается с FcRn в нейтральных условиях, антитело не диссоциирует от FcRn в нейтральных условиях плазмы, даже если оно возвращается на клеточную поверхность путем связывания с FcRn в кислых условиях эндосом. В этом случае, удержание в плазме практически отсутствует, поскольку IgG-антитело не рециклирует в плазму.
Например, как описано в J Immunol. (2002) 169(9): 5171-80, IgG1-антитело, модифицированное внесением аминокислотных замен так, чтобы полученное антитело было способно связываться с FcRn мыши в нейтральных условиях (pH 7,4), проявляет очень низкое удержание в плазме при введении мышам. Более того, как описано в J Immunol. (2009) 182(12): 7663-71; J Biol Chem. 2007 Jan. 19, 282(3): 1709-17; и J Immunol. 2002 Nov. 1, 169(9): 5171-80, IgG1-антитело было модифицировано путем внесения аминокислотных замен так, чтобы полученное антитело проявляло увеличенное связывание FcRn человека в кислых условиях (pH 6,0) и в то же становилось способным связываться с FcRn человека в нейтральных условиях (pH 7,4). Было описано, что полученное антитело не демонстрирует ни улучшения, ни изменения удержания в плазме при введении яванским макакам. Таким образом, технология инженерии антител в отношении улучшения функция антител была сфокусирована только на увеличении удержания антитела в плазме путем усиления связывания с FcRn человека в кислых условиях без усиления связывания в нейтральных условиях (pH 7,4). На сегодняшний день отсутствует сообщение о преимуществе увеличения связывания FcRn человека в нейтральных условиях (pH 7,4) путем внесения аминокислотных замен в Fc-домен IgG-антитела.
Антитела, которые связываются с антигенами pH-зависимым образом, ускоряют элиминацию растворимого антигена. Антитела обеспечивают этот эффект путем многократного связывания с растворимыми антигенами. Таким образом, такие антитела очень полезны. Исследовали способ усиления связывания FcRn в нейтральных условиях (pH 7,4) для дальнейшего усиления эффекта способствования элиминации антигена.
(6-2) Получение антител с Ca-зависимым связыванием с рецептором IL-6 человека, имеющих активность связывания FcRn в нейтральных условиях
Аминокислотные мутации для усиления связывания FcRn в нейтральных условиях (pH 7,4) вносили в FH4-IgG1 и 6RL#9-IgG1, которые обладали способностью к кальций-зависимому связыванию антигена, и H54/L28-IgG1 в качестве контроля, которое не обладает способностью к кальций-зависимому связыванию антигена. Аминокислотные мутации вносили способом ПЦР, известным специалистам в данной области. В частности, FH4-N434W (тяжелая цепь SEQ ID NO: 7; легкая цепь SEQ ID NO: 8), 6RL#9-N434W (тяжелая цепь SEQ ID NO: 9; легкая цепь SEQ ID NO: 10), и H54/L28-N434W (тяжелая цепь SEQ ID NO: 11; легкая цепь SEQ ID NO: 12) конструировали путем замены Asn на Trp в положении 434 согласно системе нумерации EU в константной области тяжелой цепи IgG1. Способ замены аминокислоты является следующим. Мутантов получали с использованием набора для сайт-направленного мутагенеза QuikChange Site-Directed Mutagenesis Kit (Stratagene) способом, описанным в прилагаемых инструкциях. Полученные плазмидные фрагменты встраивали в экспрессирующие векторы клеток животных для конструирования желаемых экспрессирующих векторов. Экспрессию и очистку антител и определение их концентраций проводили способами, описанными в примере 2.
[Пример 7] Оценка эффекта антител с Ca-зависимым связыванием в отношении ускорения элиминации с использованием нормальных мышей
(7-1) Исследование in vivo с использованием нормальных мышей
Нормальным мышам (мышь C57BL/6J; Charles River Japan) вводили hsIL-6R (растворимый рецептор IL-6 человека: полученный, как описано в справочном примере 1), отдельно или в комбинации с антителом против рецептора IL-6 человека, а затем их оценивали в отношении динамики in vivo hsIL-6R и антитела против рецептора IL-6 человека. Раствор hsIL-6R (5 мкг/мл) или смешанные растворы hsIL-6R и антитела против рецептора IL-6 человека, вводили в количестве 10 мл/кг один раз в хвостовую вену. Используемые антитела против рецептора IL-6 человека представляли собой описанные выше H54/L28-N434W, 6RL#9-N434W и FH4-N434W.
Концентрация hsIL-6R составляла 5 мкг/мл во всех смешанных растворах. Между тем, концентрация антитела против рецептора IL-6 человека отличается в случае каждого антитела. Концентрации H54/L28-N434W, 6RL#9-N434W и FH4-N434W составляли 0,042, 0,55 и 1 мг/мл, соответственно. В этом случае, антитело против рецептора IL-6 человека присутствует в избытке относительно hsIL-6R в смешанных растворах, и, таким образом, предполагается, что практически каждый hsIL-6R связывается антителом. Взятие крови проводили через 15 минут, 7 часов, 1 сутки, 2 суток, 4 суток, 7 суток, 14 суток, 21 сутки и 28 сутки после введения. Взятую кровь сразу центрифугировали при 4°C и 12000 об/мин в течение 15 минут для отделения плазмы. Отделенную плазму хранили в морозильной камере при -20°C или ниже до измерения.
(7-2) Измерение с помощью ELISA концентрации антитела против рецептора IL-6 человека в плазме у нормальных мышей
Концентрацию антитела против рецептора IL-6 человека в плазме мыши измеряли с помощью ELISA, аналогично тому, как описано в примере 6. Концентрации антител H54/L28-N434W, 6RL#9-N434W и FH4-N434W в плазме с течением времени у нормальных мышей после внутривенного введения, определенные этим способом, представлены на фиг.12.
(7-3) Измерение концентрации hsIL-6R в плазме способом электрохемилюминесценции
Концентрацию hsIL-6R в плазме мышей определяли способом электрохемилюминесценции. Приготавливали образцы hsIL-6R для калибровочной кривой, доведенные до концентрации 2000, 1000, 500, 250, 125, 62,5 или 31,25 пг/мл, и анализируемые образцы плазмы мыши, разбавленные в 50 раз или более. Образцы смешивали с раствором моноклонального антитела против IL-6R человека (R&D), меченного рутением с помощью SULFO-TAG NHS Ester (Meso Scale Discovery) и биотинилированного антитела против IL-6R человека (R&D), а затем позволяли им реагировать в течение ночи при 4°C. Буфер для анализа, используемый для этой реакции, содержит 10 мМ EDTA для снижения концентрации свободного Ca в образцах, так чтобы практические каждый hsIL-6R диссоциировал от 6RL#9-N434W или FH4-N434W в образцах и существовал в свободной форме. Затем смеси разделяли на аликвоты в планшет со стрептавидином MA400 PR Streptavidine Plate (Meso Scale Discovery). После реакции в течение одного часа при 25°C, планшет промывали. Сразу после добавления в планшет аликвот буфера для считывания T (×4) (Meso Scale Discovery) проводили измерение с использованием устройства для считывания SECTOR PR 400 (Meso Scale Discovery). Концентрацию hSIL-6R вычисляли, исходя из ответа на калибровочной кривой с использованием аналитического программного обеспечения SOFTmax PRO (Molecular Devices). Концентрации hsIL-6R в плазме у нормальных мышей с течением времени после внутривенного введения, определенные описанным выше способом, представлены на фиг.13.
Данные, описанные выше, продемонстрировали, что связывание FcRn при pH 7,4 было усилено, однако, когда hsIL-6R одновременно вводили с основным антителом H54/L28-N434W, которое не проявляет Ca-зависимого связывания hsIL-6R, элиминация hsIL-6R была значительно замедлена по сравнению с тем, когда hsIL-6R вводили отдельно. Между тем, когда hsIL-6R вводили одновременно с 6RL#9-N434W или FH4-N434W, которые представляют собой антитела, которые обладают усиленным связыванием FcRn при pH 7,4 и в 100 раз или более увеличенным зависимым от Ca связыванием hsIL-6R, элиминация hsIL-6R была значительно ускоренной по сравнению с тем, когда hsIL-6R вводили отдельно. Когда hsIL-6R вводили одновременно с 6RL#9-N434W и FH4-N434W, концентрация hsIL-6R в плазме на 1 сутки могла снижаться в 3 и 8 раз, соответственно, по сравнению с тем, когда hsIL-6R вводили отдельно. Это демонстрирует, что элиминация антигена из плазмы может быть далее ускорена путем усиления способности связывания FcRn антитела с кальций-зависимым связыванием при pH 7,4.
По сравнению с основным антителом H54/L28-IgG1, которое не проявляет Ca-зависимое связывание hsIL-6R, было подтверждено, что антитело 6RL#9-IgG1 или FH4-IgG1, которые имеют в 100 раз или более увеличенное Ca-зависимое связывание hsIL-6R, обладает эффектом усиления элиминации hsIL-6R. Более того, по сравнению с тем, когда вводили hsIL-6R отдельно, было подтверждено, что hsIL-6R и антитело 6RL#9-N434W или FH4-N434W, которые проявляют усиленное связывание FcRn при pH 7,4 и имеют в 100 раз или более увеличенное зависимое от Ca связывание hsIL-6R, способны ускорить элиминацию hsIL-6R. Данные, описанные выше, указывают на то, что аналогично антителу, которое связывается с антигеном pH-зависимым образом, антитело, которое связывается с антигеном Ca-зависимым образом, диссоциирует от антигена в эндосоме, как проиллюстрировано на фиг.1. Как описано в примере 1, типы эпитопов, на которые направлены антитела с pH-зависимым связыванием антигена, являются ограниченными (фиг.3). Однако с использованием антител с Ca-зависимым связыванием антигеном, описанных в настоящем описании, считается, что можно расширить разнообразие эпитопов, на которые нацеливаются антитела, способные к зависимой от эндосом диссоциации антигена (фиг.4 и 5).
[Пример 8] Идентификация участка связывания ионов кальция в антителе 6RL#9 с помощью рентгеновской кристаллографии
(8-1) Рентгеновская кристаллография
Как описано в примере 4, измерение температуры термической денатурации Tm показало, что антитело 6RL#9 связывается с ионами кальция. Однако было непредсказуемо, какая часть антитела 6RL#9 связывается с ионом кальция. Следовательно, с использованием способа рентгеновской кристаллографии идентифицировали остатки антитела 6RL#9, которые взаимодействуют с ионом кальция.
(8-2) Экспрессия и очистка антитела 6RL#9
Антитело 6RL#9 экспрессировали и очищали для рентгеновской кристаллографии. В частности, плазмиды для экспрессии у животных, сконструированные так, чтобы они были способны экспрессировать тяжелую цепь (SEQ ID NO: 1) и легкую цепь (SEQ ID NO: 2) антитела 6RL#9, вводили временно в клетки животных. Сконструированные плазмиды вводили способом липофекции в клетки линии, происходящей из клеток почек эмбриона человека FreeStyle 293-F (Invitrogen), суспендированные в 800 мл среды для экспрессии FreeStyle 293 Expression Medium (Invitrogen) (конечная плотность клеток: 1×106 клеток/мл). Клетки с введенной плазмидой культивировали в инкубаторе с CO2 (37°C, 8% CO2, 90 об/мин) в течение пяти суток. Из культурального супернатанта, полученного, как описано выше, антитела очищали способом, известным специалистам в данной области, с использованием rProtein A SepharoseTM Fast Flow (Amersham Biosciences). Поглощение при 280 нм очищенных растворов антитела измеряли с использованием спектрофотометра. Из измеренных значений вычисляли концентрации антител с использованием коэффициента экстинкции, вычисленного способом PACE (Protein Science (1995) 4, 2411-2423).
(8-3) Очистка Fab-фрагмента антитела 6RL#9
Антитело 6RL#9 концентрировали до 21 мг/мл с использованием ультрафильтра с пределом молекулярной массы 10000 MWCO. Образец антитела в концентрации 5 мг/мл (2,5 мл) получали разбавлением раствора антитела с использованием буфера 4 мМ L-цистеин/5 мМ EDTA/20 мМ фосфат натрия (pH 6,5). К образцу добавляли 0,125 мг папаина (Roche Applied Science). После перемешивания образец инкубировали при 35°C в течение двух часов. После инкубации таблетку с ингибиторами протеаз Protease Inhibitor Cocktail Mini, не содержащую EDTA (Roche Applied Science), растворяли в 10 мл буфера 25 мМ MES (pH 6) и добавляли к образцу. Образец инкубировали на льду для остановки протеолитического расщепления папаином. Затем образец наносили на 1-мл катионнообменную колонку HiTrap SP HP (GE Healthcare), уравновешенную 25 мМ буфером MES (pH 6), ниже которой была последовательно подсоединена 1-мл колонка с белком A HiTrap MabSelect Sure Protein A column (GE Healthcare). Очищенную фракцию Fab-фрагмента антитела 6RL#9 получали, путем проведения элюирования с помощью линейного градиента концентрации NaCl вплоть до 300 мМ в описанном выше буфере. Затем полученную очищенную фракцию концентрировали до приблизительно 0,8 мл с использованием ультрафильтра 5000 MWCO. Концентрат наносили на колонку для гель-фильтрации Superdex 200 10/300 GL (GE Healthcare), уравновешенную 100 мМ буфером HEPES (pH 8), содержащим 50 мМ NaCl. Очищенный Fab-фрагмент антитела 6RL#9 для кристаллизации элюировали с колонки с использованием того же буфера. Все обработки колонок, описанные выше, проводили при низкой температуре от 6 до 7,5°C.
(8-4) Кристаллизация Fab-фрагмента антитела 6RL#9 в присутствии Ca
Затравочные кристаллы Fab-фрагмента 6RL#9 получали заранее согласно общим условиям. Затем очищенный Fab-фрагмент антитела 6RL#9 в 5 мМ CaCl2 концентрировали до 12 мг/мл с помощью ультрафильтра 5000 MWCO. Далее, образец, концентрированный, как описано выше, кристаллизовали способом висячей капли посредством диффузии в парах с использованием 100 мМ буфера HEPES (pH 7,5), содержавшего 20%-29% PEG4000, в качестве резервуарного раствора. Описанные выше затравочные кристаллы, дробили в 100 мМ буфере HEPES (pH 7,5), содержавшем 29% PEG4000 и 5 мМ CaCl2, и проводили серийное разведение в от 100 до 10000 раз. Затем 0,2 мкл разбавленных растворов комбинировали со смесью 0,8 мкл резервуарного раствора и 0,8 мкл концентрированного образца для получения кристаллизационных капель на покровном стекле. Каплям кристаллов позволяли держаться при 20°C в течение от двух до трех суток до получения плоских кристаллов. С использованием кристаллов получали данные рентгенодиффракции.
(8-5) Кристаллизация Fab-фрагмента антитела 6RL#9 в отсутствие Ca
Очищенный Fab-фрагмент антитела 6RL#9 концентрировали до 15 мг/мл с помощью ультрафильтра 5000 MWCO. Далее, образец, концентрированный, как описано выше, кристаллизовали способом висячей капли посредством диффузии в парах с использованием 100 мМ буфера HEPES (pH 7,5), содержавшего 18%-25% PEG4000, в качестве резервуарного раствора. Описанные выше затравочные кристаллы, дробили в 100 мМ буфере HEPES (pH 7,5), содержавшем 25% PEG4000, и проводили серийное разведение в от 100 до 10000 раз. Затем 0,2 мкл разбавленных растворов комбинировали со смесью 0,8 мкл резервуарного раствора и 0,8 мкл концентрированного образца для получения кристаллизационных капель на покровном стекле. Каплям кристаллов позволяли держаться при 20°C в течение от двух до трех суток до получения плоских кристаллов. С использованием кристаллов получали данные рентгенодиффракции.
(8-6) Рентгеновское кристаллографическое измерение кристалла Fab-фрагмента из антитела 6RL#9 в присутствии Ca
Кристаллы Fab-фрагмента антитела 6RL#9, полученные в присутствии Ca, смачивали 100 мМ раствором буфера HEPES (pH 7,5), содержавшим 35% PEG4000 и 5 мМ CaCl2. Удалив внешней раствор с поверхности монокристалла с помощью микробулавки в виде нейлоновой петли, монокристалл замораживали в жидком азоте. Данные рентгенодиффракции замороженного кристалла получали из линии пучка BL-17A Photon Factory в High Energy Accelerator Research Organization. Замороженный кристалл поддерживали в замороженном состоянии в ходе измерения путем постоянного помещения его в поток газообразного азота при -178°C. Всего было получено 180 дифракционных изображений с использованием CCD-детектора Quantum315r (ADSC), присоединенного к линии пучка, при вращении кристалла с интервалами 1°. Определение константы решетки, индексирование дифракционных пятен и анализ данных дифракции проводили с использованием программ Xia2 (CCP4 Software Suite), XDS Package (Walfgang Kabsch) и Scala (CCP4 Software Suite). Наконец, были получены данные интенсивности дифракции с разрешением вплоть до 2,2 ангстрем. Кристалл принадлежит к группе симметрии P212121 с константой решетки a=45,47 ангстрем, b=79,86 ангстрем, c=116,25 ангстрем, α=90°, β=90° и γ=90°.
(8-7) Рентгеновское кристаллографическое измерение кристалла Fab-фрагмента из антитела 6RL#9 в отсутствие Ca
Кристаллы Fab-фрагмента антитела 6RL#9, полученные в отсутствие Ca, смачивали 100 мМ раствором буфера HEPES (pH 7,5), содержавшим 35% PEG4000. Удалив внешней раствор с поверхности монокристалла с помощью микробулавки в виде нейлоновой петли, монокристалл замораживали в жидком азоте. Данные рентгенодиффракции замороженного кристалла получали из линии пучка BL-5A Photon Factory в High Energy Accelerator Research Organization. Замороженный кристалл поддерживали в замороженном состоянии в ходе измерения путем постоянного помещения его в поток газообразного азота при -178°C. Всего было получено 180 дифракционных изображений с использованием CCD-детектора Quantum210r (ADSC), присоединенного к линии пучка, при вращении кристалла с интервалами 1°. Определение константы решетки, индексирование дифракционных пятен и анализ данных дифракции проводили с использованием программ Xia2 (CCP4 Software Suite), XDS Package (Walfgang Kabsch)и Scala (CCP4 Software Suite). Наконец, были получены данные интенсивности дифракции с разрешением вплоть до 2,3 ангстрем. Кристалл принадлежит к группе симметрии P212121 с константой решетки a=45,40 ангстрем, b=79,63 ангстрем, c=116,07 ангстрем, α=90°, β=90° и γ=90°, и, таким образом, он структурно идентичен кристаллу, полученному в присутствии Ca.
(8-8) Измерение способом рентгеновской кристаллографии кристалла Fab-фрагмента из антитела 6RL#9 в присутствии Ca
Кристаллическую структуру Fab-фрагмента антитела 6RL#9 в присутствии Ca определяли способом молекулярного замещения с использованием программы Phaser (CCP4 Software Suite). Количество молекул в асимметричном элементе оценивали, исходя из размера кристаллической решетки и молекулярной массы Fab-фрагмента антитела 6RL#9. Исходя из гомологии первичной последовательности, часть из положений аминокислот 112-220 A-цепи и часть из положений аминокислот 116-218 B-цепи в конформационной координате PDB-кода 1ZA6, использовали в качестве модельных молекул для анализа областей CL и CH1. Затем часть из положений аминокислот 1-115 B-цепи в конформационной координате PDB-кода 1ZA6 использовали в качестве модельной молекулы для анализа VH-области. Наконец, часть из положений аминокислот 3-147 легкой цепи в конформационной координате PDB-кода 2A9M использовали в качестве модельной молекулы для анализа VL-области. Исходя из этого порядка, была получена первоначальная модель структуры Fab-фрагмента антитела 6RL#9 путем определения из функций сдвига и вращения положений и ориентаций модельных молекул для анализа кристаллической решетки. Кристаллографический фактор достоверности R для данных отражения при разрешении от 25 до 3,0 составлял 46,9%, и свободный R составлял 48,6% после детализации жесткого каркаса, где каждому из VH-, VL-, CH1- и CL-доменов позволяли отклоняться от первоначальной структурной модели. Затем детализации модели достигали путем повторения структурной детализации с использованием программы Refmac5 (CCP4 Software Suite) с последующей проверкой модели, проводимой с использованием программы Coot (Paul Emsley) на основании карт электронной плотности Fo-Fc и 2Fo-F, где коэффициенты Fo-Fc и 2Fo-Fc вычисляли с использованием экспериментально определенного структурного фактора Fo, структурного фактора Fc, вычисленного на основе этой модели, и фаз. Конечную детализацию проводили с использованием программы Refmac5 (CCP4 Software Suite) на основе карт электронной плотности Fo-Fc и 2Fo-F путем добавления молекулы воды и иона Ca в модель. С помощью 21020 данных отражения при разрешении от 25 до 2,2 ангстрем, в конечном итоге кристаллографический фактор достоверности R составил 20,0%, и свободный R составил 27,9% для модели, состоящей из 3440 атомов.
(8-9) Определение данных рентгенодиффракции кристалла Fab-фрагмента антитела 6RL#9 в отсутствие Ca
Кристаллическую структуру Fab-фрагмента антитела 6RL#9 в отсутствие Ca определяли на основе структуры кристалла, полученного в присутствии Ca. Молекулами воды и ионов Ca пренебрегали в конформационных координатах кристалла Fab-фрагмента антитела 6RL#9, полученного в присутствии Ca. Кристаллографический фактор достоверности R для данных отражения при разрешении от 25 до 3,0 ангстрем составил 30,3%, и свободный R составил 31,7% после детализации жесткого каркаса, где каждому из VH-, VL-, CH1- и CL-доменов позволяли отклоняться. Затем детализации модели достигали путем повторения структурной детализации с использованием программы Refmac5 (CCP4 Software Suite) с последующей проверкой модели, проводимой с использованием программы Coot (Paul Emsley) на основании карт электронной плотности Fo-Fc и 2Fo-F, где коэффициенты Fo-Fc и 2Fo-Fc вычисляли с использованием экспериментально определенного структурного фактора Fo, структурного фактора Fc, вычисленного на основе этой модели, и фаз. Конечную детализацию проводили с использованием программы Refmac5 (CCP4 Software Suite) на основе карт электронной плотности Fo-Fc и 2Fo-F путем добавления молекулы воды и иона Ca в модель. C помощью 18357 данных отражения при разрешении от 25 до 2,3 ангстрем, в конечном итоге кристаллографический фактор достоверности R составил 20,9%, и свободный R составил 27,7% для модели, состоящей из 3351 атомов.
(8-10) Сравнение данных рентгеновской кристаллографической дифракции Fab-фрагментов антитела 6RL#9 в присутствии и в отсутствие Ca
При сравнении кристаллографических структур Fab-фрагментов антитела 6RL#9 в присутствии и в отсутствие Ca, были выявлены значительные изменения в CDR3 тяжелой цепи. Структура CDR3 тяжелой цепи Fab-фрагмента антитела 6RL#9, определенная рентгеновской кристаллографией, представлена на фиг.14. В частности, ион кальция располагался в центре области петли CDR3 тяжелой цепи Fab-фрагмента антитела 6RL#9, полученного в присутствии Ca. Было предположено, что ион кальция взаимодействует с положениями 95, 96 и 100a (нумерация по Kabat) CDR3 тяжелой цепи. Было предположено, что петля CDR3 тяжелой цепи, которая является важной для связывания антигена, стабилизировалась связыванием кальция в присутствии Ca, и становилась оптимальной структурой для связывания антигена. Отсутствуют сообщения, демонстрирующие, что кальций связывается с CDR3 тяжелой цепи антитела. Таким образом, связанная с кальцием структура CDR3 тяжелой цепи антитела является новой структурой. Известно, что CDR3 тяжелой цепи является наиболее важной для связывания антигена. Мотив, для которого требуется ион кальция для поддержания структуры CDR3 тяжелой цепи, выявленный, как описано в настоящем примере, предполагает, что ион кальция играет важную роль в связывании антигена. В частности, в высокой степени вероятно, что антитела с этим мотивом связываются с антигеном зависимым от кальция образом. Например, когда получают синтетическую библиотеку, имеющую этот мотив, из этой библиотеки можно эффективно выделить антитела с кальций-зависимым связыванием.
[Пример 9] Получение антител, которые связываются с IL-6 Ca-зависимым образом, из библиотеки антител человека с использованием способов фагового дисплея
(9-1) Конструирование библиотеки фагового дисплея наивных антител человека
Библиотеку фагового дисплея антител человека, содержавшую множество фагов, которые экспонируют различные последовательности Fab-доменов антител человека, конструировали способом, известным специалистам в данной области с использованием, в качестве матрицы, поли-A-РНК, полученной из PBMC человека, коммерчески доступной поли-A-РНК человека и т.п.
(9-2) Получение фрагментов антител, которые связываются с антигеном Ca-зависимым образом, из библиотеки с помощью пэннинга на гранулах
Первичную селекцию из сконструированных библиотек фагового дисплея наивных антител человека проводили путем обогащения фрагментами антител, которые имеют активность связывания антигена (IL-6). Использованный антиген представлял меченный биотином IL-6.
Фаги получали с помощью E. coli, несущих фагмиды фагового дисплея. К осадку фагов, полученных с помощью E. coli, добавляли 2,5 M NaCl/10% PEG в культуральную среду для E. coli. Фракцию фагов разбавляли TBS для получения раствора с фаговой библиотекой. Затем к раствору с фаговой библиотекой добавляли BSA и CaCl2 до конечных концентраций 4% и 1,2 мМ ионов кальция, соответственно. Использованный способ пэннинга представлял собой общепринятый способ пэннинга с использованием магнитных гранул с иммобилизованным на них антигеном (J. Immunol. Methods. 2008 Mar 20, 332(1-2): 2-9; J. Immunol. Methods. 2001 Jan 1, 247(1-2): 191-203; Biotechnol Prog. 2002 Mar-Apr, 18(2): 212-20; Mol. Cell Proteomics. 2003 Feb, 2(2): 61-9). Использованные магнитные гранулы представляли собой покрытые нейтравидином гранулы (Sera-Mag SpeedBeads NeutrAvidin-coated) и покрытые стрептавидином гранулы (Dynabeads M-280 Streptavidin).
В частности, 250 пмоль биотинилированного антигена добавляли к полученному раствору с фаговой библиотекой. Таким образом, раствор приводили в контакт с антигеном при комнатной температуре в течение 60 минут. Добавляли блокированные BSA магнитные гранулы, и комплексу антиген-фаг позволяли связываться с магнитными гранулами при комнатной температуре в течение 15 минут. Гранулы промывали три раза 1,2 мМ CaCl2/TBS (TBS, содержащий 1,2 мМ CaCl2) и затем два раза 1 мл 1,2 мМ CaCl2/TBS (TBS, содержащий 1,2 мМ CaCl2). После этого к гранулам добавляли 0,5 мл трипсина в концентрации 1 мг/мл. После диспергирования в течение 15 минут при комнатной температуре, гранулы сразу разделяли с использованием магнитного стенда для сбора суспензии фагов. Полученную суспензию фагов добавляли к 10 мл E. coli штамма TG1 в фазе логарифмического роста (OD600=0,4-0,5). E. coli инкубировали при осторожном перемешивании при 37°C в течение одного часа для инфицирования фагами. Инфицированные E. coli высевали в чашку (225 мм × 225 мм). Затем из культуральной среды посеянных E. coli собирали фаги для получения раствора с фаговой библиотекой.
При втором и последующих пэннингах, фаги обогащали с использованием способности к Ca-зависимому связыванию в качестве индикатора. В частности, 40 пмоль меченного биотином антигена добавляли к полученному раствору фаговой библиотеки. Таким образом, фаговую библиотеку приводили в контакт с антигеном при комнатной температуре в течение 60 минут. Добавляли блокированные BSA магнитные гранулы и комплексу антиген-фаг позволяли связаться с магнитными гранулами при комнатной температуре в течение 15 минут. Гранулы промывали один раз 1 мл 1,2 мМ CaCl2/TBST и 1,2 мМ CaCl2/TBS. Затем к гранулам добавляли 0,1 мл 2 мМ EDTA/TBS. После диспергирования при комнатной температуре гранулы сразу отделяли с использованием магнитного стенда для сбора суспензии фагов. Белок pIII (белок pIII, происходящий из фага-помощника) отщепляли от фагов, которые не экспонировали Fab, добавлением 5 мкл трипсина в концентрации 100 мг/мл к собранной суспензии фага для устранения способности фагов, не экспонирующих Fab, инфицировать E. coli. Фаги, собранные из исходного раствора с фагом после обработки трипсином, добавляли к 10 мл клеток E. coli штамма TG1 в фазе логарифмического роста (OD600=0,4-0,7). E. coli инкубировали при осторожном перемешивании при 37°C в течение одного часа для инфицирования фагами. Инфицированные E. coli высевали в чашку (225 мм × 225 мм). Затем из культуральной среды посеянных E. coli собирали фаги для получения жидкого исходного раствора с фаговой библиотекой. Пэннинг проводили три раза с использованием активности Ca-зависимого связывания в качестве индикатора.
(9-3) Оценка с помощью ELISA фагов
Содержащие фаг культуральные супернатанты собирали из единичных колоний E. coli, полученных способом, описанным выше, в соответствии с общепринятым способом (Methods Mol. Biol. (2002) 178, 133-145). В содержащие фаг культуральные супернатанты добавляли BSA и CaCl2 до конечных концентраций 4% и 1,2 мМ ионов кальция, соответственно. Супернатанты подвергали ELISA по следующей методике. 96-луночные микропланшеты для титрования StreptaWell (Roche) покрывали в течение ночи с использованием 100 мкл PBS, содержащего меченный биотином антиген. Антиген удаляли из лунки путем промывания каждой лунки планшета PBST. Затем лунки блокировали 250 мкл 4% BSA-TBS в течение одного часа или более. После удаления 4% BSA-TBS в каждую лунку добавляли полученные культуральные супернатанты. Планшет инкубировали при 37°C в течение одного часа, так чтобы позволить экспонирующим антитело фагам связаться с антигеном на каждой лунке. После промывания каждой лунки 1,2 мМ CaCl2/TBST, добавляли 1,2 мМ CaCl2/TBS или 1 мМ EDTA/TBS. Планшет оставляли для инкубации при 37°C в течение 30 минут. После промывания 1,2 мМ CaCl2/TBST, в каждую лунку добавляли конъюгированное с HRP антитело против M13 (Amersham Pharmacia Biotech), разбавленное TBS, содержащим BSA и ионы кальция в конечных концентрациях 4% и 1,2 мМ ионов кальция, и планшет инкубировали в течение одного часа. После промывания 1,2 мМ CaCl2/TBST, в каждую лунку добавляли раствор только TMB (ZYMED). Хромогенную реакцию в растворе в каждой лунке останавливали добавлением серной кислоты. Затем проявившийся цвет оценивали путем измерения поглощения при 450 нм.
Из 96 выделенных клонов, с помощью ELISA фагов были получены антитела 6KC4-1#85, 6LC4-1#15 и 6LC4-2#16, имеющие Ca-зависимую активность связывания IL-6. С использованием фрагментов антител, для которых было предсказано, что они имеют Ca-зависимую антигенсвязывающую активность, исходя из результата фагового ELISA, описанного выше, в качестве матрицы, гены амплифицировали со специфическими праймерами, и их последовательности анализировали. Последовательности вариабельных областей тяжелой цепи и легкой цепи антитела 6KC4-1#85 представлены в SEQ ID NO: 25 и 26, соответственно. Полинуклеотид, кодирующий вариабельную область тяжелой цепи антитела 6KC4-1#85 (SEQ ID NO: 25) связывали с полинуклеотидом, кодирующим последовательность, происходящую из IgG1 (SEQ ID NO: 65), способом ПЦР. Полученный фрагмент ДНК встраивали в экспрессирующий вектор клеток животных для конструирования экспрессирующего вектора для тяжелой цепи SEQ ID NO: 27. Полинуклеотид, кодирующий вариабельную область легкой цепи антитела 6KC4-1#85 (SEQ ID NO: 26), связывали с полинуклеотидом, кодирующим константную область природной каппа-цепи (SEQ ID NO: 28), способом ПЦР. Фрагмент ДНК, содержащий связанную последовательность, представленную в SEQ ID NO: 29, встраивали в экспрессирующий вектор клеток животных. С использованием того же способа, антитело 6LC4-1#15 (тяжелая цепь SEQ ID NO: 68; легкая цепь SEQ ID NO: 69) и антитело 6LC4-2#16 (тяжелая цепь SEQ ID NO: 70; легкая цепь SEQ ID NO: 71) также встраивали в экспрессирующие векторы клеток. Последовательности сконструированных вариантов подтверждали способом, известным специалистам в данной области.
(9-4) Экспрессия и очистка антител
Клоны, которые были оценены как имеющие способность к Ca-зависимому связыванию с помощью ELISA фагов, вводили в экспрессирующие плазмиды клеток животных. Антитела экспрессировали с использованием следующего способа. Клетки линии, происходящей из клеток почки эмбриона FreeStyle 293-F (Invitrogen), суспендировали в среде для экспрессии FreeStyle 293 Expression Medium (Invitrogen), и аликвоты объемом 3 мл высевали в каждую ячейку планшетов с 6 ячейками с плотностью клеток 1,33×106 клеток/мл. Полученные плазмиды вводили в клетки способом липофекции. Клетки культивировали в инкубаторе CO2 (37°C, 8% CO2, 90 об/мин) в течение четырех суток. Из полученных культуральных супернатантов антитела очищали с использованием rProtein A SepharoseTM Fast Flow (Amersham Biosciences) способом, известным специалистам в данной области. Концентрации очищенных антител определяли путем измерения поглощения при 280 нм с использованием спектрофотометра. Концентрации антител вычисляли из установленных величин на основе коэффициента экстинкции, определенного способом PACE (Protein Science 1995; 4: 2411-2423).
(9-5) Анализ связывания кальций-зависимых антител против IL6
С использованием Biacore T100 (GE Healthcare), полученные антитела оценивали в отношении их активности связывания (константа диссоциации KD (M)) с интерлейкином 6 (hIL6) человека при pH 7,4. Измерение проводили с использованием в качестве подвижного буфера 0,05% Tween20, 10 ммоль/л ACES, 150 ммоль/л NaCl (pH 7,4), содержащего 3 мкМ или 1,2 мМ CaCl2.
После иммобилизации достаточного количества рекомбинантного белка A/G (Thermo Scientific) на сенсорном чипе CM5 (GE Healthcare) способом присоединения аминов, антителам позволяли связываться с ним. Соответствующую концентрацию hIL6 (интерлейкин 6 человека; Kamakura Techno-Science, Inc.) инжектировали в качестве анализируемого соединения для взаимодействия с антителами на сенсорном чипе. Затем сенсорный чип регенерировали путем инжекции 10 ммоль/л глицина-HCl (pH 1,5). Измерение проводили при 37°C. Сенсограмма, полученная с помощью этого измерения, представлена на фиг.15. Результат демонстрирует, что антитела 6LC4-1#15-IgG1, 6LC4-2#16-IgG1 и 6KC4-1#85-IgG1 имели более слабое связывание hIL6 в условиях 3 мкМ концентрации Ca2+, чем в условиях 1,2 мМ. Данные, описанные выше, указывают на то, что этот способ применим к другим антигенам, поскольку свойство кальций-зависимого связывания антигена было показано для IL-6, также как оно продемонстрировано и для IL-6R в примере 3.
[Пример 10] Оценка связывания антитела 6KC4-1#85 с ионом кальция
(10-1) Оценка связывания антитела 6KC4-1#85 с ионом кальция
Антитело 6KC4-1#85 с кальций-зависимым связыванием, которое было выделено из библиотеки антител человека, оценивали в отношении связывания им кальция. Оценку того, варьирует ли измеренная величина Tm, в зависимости от концентрации ионизированного кальция, проводили способом, описанным в примере 4.
Величины Tm для Fab-домена антитела 6KC4-1#85 представлены в таблице 11. Как показано в таблице 11, величина Tm для Fab-домена антитела 6KC4-1#85 варьировала, в зависимости от концентрации ионов кальция. Это демонстрирует, что антитело 6KC4-1#85 связывается с кальцием.
(10-2) Идентификация участка связывания ионов кальция в антителе 6KC4-1#85
Как показано в (10-1) примера 10, антитело 6KC4-1#85 связывается с ионом кальция. Однако 6KC4-1#85m не имеет кальций-связывающего мотива, такого как последовательность hVk5-2, описанная ниже. Таким образом, для идентификации остатков, ответственных за связывание ионов кальция антителом 6KC4-1#85, конструировали измененные тяжелые цепи (6_H1-11 (SEQ ID NO: 30), 6_H1-12 (SEQ ID NO: 31), 6_H1-13 (SEQ ID NO: 32), 6_H1-14 (SEQ ID NO: 33), 6_H1-15 (SEQ ID NO: 34)) и измененные легкие цепи (6_L1-5 (SEQ ID NO: 35) и 6_L1-6 (SEQ ID NO: 36)) путем замены остатка Asp (D) в CDR антитела 6KC4-1#85 остатком Ala (A), который не участвует в связывании или хелатировании ионов кальция. Способом, описанным в примере 2, измененные антитела очищали из культуральных супернатантов клеток животных, в которые введены экспрессирующие векторы, несущие гены измененных антител. Очищенные измененные антитела оценивали в отношении связывания ими кальция способом, описанным в примере 4. Результат измерения представлен в таблице 12.
Как показано в таблице 12, замена остатком Ala остатка в положении 95 или 101 (нумерация по Kabat) в CDR3 тяжелой цепи антитела 6KC4-1#85 привела к утрате активности связывания кальция антитела 6KC4-1#85. Это указывает на то, что эти остатки ответственны за связывание кальция. Было показано, что кальций-связывающий мотив в области основания петли CDR3 тяжелой цепи в антителе 6KC4-1#85, который был идентифицирован на основе активности связывания кальция антител, измененных относительно антитела 6KC4-1#85, также можно было использовать в качестве кальций-связывающего мотива в антигенсвязывающем домене антигенсвязывающей молекулы по настоящему изобретению. Подобно мотиву, выявленному, как описано в примере 8, этот кальций-связывающий мотив расположен в CDR3 тяжелой цепи. Таким образом, аналогично, например, когда конструируют синтетическую библиотеку, имеющею этот мотив, из библиотеки можно эффективно выделять антитела с кальций-зависимым связыванием.
[Пример 11] Поиск последовательностей человека эмбрионального типа, которые связываются с ионом кальция
(11-1) Выделение последовательностей человека эмбрионального типа
Антитела, связывающие ион кальция, содержащие последовательности человека эмбрионального типа, не были описаны. Таким образом, последовательности антител эмбрионального типа, имеющие последовательности человека эмбрионального типа, клонировали с использованием в качестве матрицы кДНК, полученной из поли-РНК селезенки эмбриона человека Human Fetal Spleen Poly RNA (Clontech), для оценки того, связывают ли антитела, имеющие последовательности человека эмбрионального типа, ион кальция. Клонированные фрагменты ДНК встраивали в экспрессирующие векторы клеток животных. Нуклеотидные последовательности сконструированных экспрессирующих векторов определяли способом, известным специалистам в данной области. SEQ ID представлены в таблице 13. С помощью ПЦР полинуклеотиды, кодирующие SEQ ID NO: 37 (Vk1), SEQ ID NO: 38 (Vk2), SEQ ID NO: 39 (Vk3), SEQ ID NO: 40 (Vk4) и SEQ ID NO: 41 (Vk5), связывали с полинуклеотидом, кодирующим природную константную область каппа-цепи (SEQ ID NO: 28). Связанные фрагменты ДНК встраивали в экспрессирующие векторы клеток животных. Более того, полинуклеотиды, кодирующие SEQ ID NO: 42 (Vk1), SEQ ID NO: 43 (Vk2), SEQ ID NO: 44 (Vk3), SEQ ID NO: 45 (Vk4) и SEQ ID NO: 46 (Vk5), связывали способом ПЦР с полинуклеотидом, кодирующим полипептид (SEQ ID NO: 65), имеющий делецию двух аминокислот на C-конце IgG1. Полученные фрагменты ДНК встраивали в экспрессирующие векторы клеток животных. Последовательности сконструированных вариантов подтверждали способом, известным специалистам в данной области.
(11-2) Экспрессия и очистка антител
Сконструированные экспрессирующие векторы клеток животных, в которые встроены фрагменты ДНК, имеющие пять типов последовательностей человека эмбрионального типа, вводили в клетки животных. Экспрессию антител проводили следующим способом. Клетки линии, происходящей из клеток почки эмбриона FreeStyle 293-F (Invitrogen), суспендировали в среде для экспрессии FreeStyle 293 Expression Medium (Invitrogen), и высевали с плотностью клеток 1,33×106 клеток/мл (3 мл) в каждую ячейку планшета с 6 ячейками. Полученные плазмиды вводили в клетки способом липофекции. Клетки культивировали в инкубаторе с CO2 (37°C, 8% CO2, 90 об/мин) в течение четырех суток. Из культуральных супернатантов, полученных, как описано выше, антитела очищали с использованием rProtein A SepharoseTM Fast Flow (Amersham Biosciences) способом, известным специалистам в данной области. Поглощение растворов очищенных антител измеряли при 280 нм с использованием спектрофотометра. Концентрации антител вычисляли из установленных величин на основе коэффициента экстинкции, определенного способом PACE (Protein Science 1995; 4: 2411-2423).
(11-3) Оценка антител, имеющих последовательности человека эмбрионального типа, в отношении их активности связывания ионов кальция
Очищенные антитела оценивали в отношении их активности связывания ионов кальция. Очищенные антитела подвергали диализу (EasySEP, TOMY) против раствора, содержавшего 20 мМ Tris-HCl, 150 мМ NaCl и 2 мМ CaCl2 (pH 7,4) или 20 мМ Tris-HCl, 150 мМ NaCl и 3 мкМ CaCl2 (pH 7,4). Растворы антитела в качестве исследуемого вещества доводили до 0,1 мг/мл с использованием того же раствора, который использовали для диализа, и проводили измерение DSC при скорости повышения температуры 240°C/ч от 20 до 115°C. Исходя из полученных кривых денатурации DSC, вычисляли среднюю температуру температурной денатурации (величину Tm) для Fab-домена каждого антитела. Величины Tm представлены в таблице 14.
Результат показал, что величины Tm для Fab-доменов антител, имеющих последовательность hVk1, hVk2, hVk3 или hVk4, не варьировали, в зависимости от концентрации ионов кальция в растворах, содержавших Fab-домен. Между тем, величина Tm для Fab-домена антитела, имеющего последовательность hVk5, варьировала, в зависимости от концентрации ионов кальция в растворе, содержавшем Fab-домен. Это демонстрирует, что последовательность hVk5 связывается с ионом кальция.
[Пример 12] Оценка последовательности Vk5 человека (hVk5)
(12-1) Последовательность hVk5
Единственной последовательностью hVk5, зарегистрированной в базе данных Kabat, является последовательность hVk5-2. Далее hVk5 и hVk5-2 используются в качестве синонимов.
(12-2) Конструирование, экспрессия и очистка негликозилированной формы последовательности hVk5-2
Последовательность hVk5-2 имеет последовательность для N-гликозилирования в положении аминокислоты 20 (нумерация по Kabat). Цепи сахаров, присоединенные к белкам, проявляют гетерогенность. Таким образом, желательно устранить гликозилирование с точки зрения гомогенности вещества. В этом контексте, конструировали вариант hVk5-2_L65 (SEQ ID NO: 47), в котором остаток Asn (N) в положении 20 (нумерация по Kabat) заменен Thr (T). Аминокислотную замену проводили способом, известным специалистам в данной области, с использованием набора для сайт-направленного мутагенеза QuikChange Site-Directed Mutagenesis Kit (Stratagene). ДНК, кодирующую вариант hVk5-2_L65, встраивали в экспрессирующий вектор животных. Экспрессирующий вектор животных, в который встроена конструированная ДНК, кодирующая вариант hVk5-2_L65, в комбинации с экспрессирующим вектором животных, имеющий вставку для экспрессии CIM_H (SEQ ID NO: 48) в качестве тяжелой цепи, встраивали в клетки животных способом, описанным в примере 2. Антитело, содержащее hVk5-2_L65 и CIM_H, которые экспрессировались в клетках животных, в которые были введены векторы, очищали способом, описанным в примере 2.
(12-3) Оценка антитела, имеющего негликозилированную последовательность hVk5-2, в отношении физических свойств
Выделенное антитело, имеющее модифицированную последовательность hVk5-2_L65, анализировали ионообменной хроматографией для исследования того, является ли она менее гетерогенной, чем антитело, имеющее исходную последовательность hVk5-2, до модификации. Методика ионообменной хроматографии представлена в таблице 15. Результат анализа показал, что hVk5-2_L65, модифицированное в участке гликозилирования, было менее гетерогенным, чем исходная последовательность hVk5-2, как показано на фиг.16.
Далее, оценку того, связывается ли антитело, содержащее менее гетерогенную последовательность hVk5-2_L65, с ионом кальция, оценивали способом, описанным в примере Пример 4. Результат показал, что величина Tm для Fab-домена антитела, имеющего hVk5-2_L65 с измененным участком гликозилирования, также варьировала, в зависимости от концентрации ионов кальция в растворах антител, как показано в таблице 16. В частности, было продемонстрировано, что Fab-домен антитела, имеющего hVk5-2_L65 с измененным участком гликозилирования, связывается с ионом кальция.
[Пример 13] Оценка активности связывания ионов кальция молекул антител, имеющих последовательность CDR из последовательности hVk5-2
(13-1) Конструирование, экспрессия и очистка модифицированных антител, имеющих последовательность CDR из последовательности hVk5-2
Последовательность hVk5-2_L65 представляет собой последовательность с измененными аминокислотами в участке гликозилирования каркасной области последовательности Vk5-2 человека. Как описано в примере 12, было продемонстрировано, что связывание ионов кальция происходило даже после изменения участка гликозилирования. Между тем, с точки зрения иммуногенности, главным образом, желательно, чтобы каркасная последовательность представляла собой последовательность эмбрионального типа. Таким образом, авторы настоящего изобретения оценивали, может ли каркасная последовательность антитела быть заменена каркасной последовательностью негликозилированной последовательности эмбрионального типа при сохранении активности антитела в отношении связывания ионов кальция.
Полинуклеотиды, кодирующие химически синтезированные последовательности, которые содержат измененную последовательность каркасной области из последовательности hVk5-2, hVk1, hVk2, hVk3 или hVk4 (CaVk1 (SEQ ID NO: 49), CaVk2 (SEQ ID NO: 50), CaVk3 (SEQ ID NO: 51) или CaVk4 (SEQ ID NO: 52), соответственно), связывали способом ПЦР с полинуклеотидом, кодирующим константную область (SEQ ID NO: 28) природной каппа-цепи. Связанные фрагменты ДНК встраивали в экспрессирующие векторы клеток животных. Последовательности сконструированных вариантов подтверждали способом, известным специалистам в данной области. Каждую плазмиду, сконструированную, как описано выше, встраивали в клетки животных в комбинации с плазмидой, в которую встроен полинуклеотид, кодирующий CIM_H (SEQ ID NO: 48), способом, описанным в примере 2. Экспрессированные молекулы представляющего интерес антитела очищали из культуральной среды клеток животных, в которых были введены плазмиды.
(13-2) Оценка измененных антител, имеющих последовательность CDR из последовательности hVk5-2, в отношении их активности связывания ионов кальция
Оценку того, связываются ли ионы кальция с измененными антителами, имеющими последовательность CDR из последовательности hVk5-2 и каркасные последовательности из последовательностей эмбрионального типа, отличные от hVk5-2 (hVk1, hVk2, hVk3 и hVk4), оценивали с использованием способа, описанного в примере 4. Результат оценки представлен в таблице 17. Было выявлено, что величина Tm Fab-домена каждого из измененных антител варьировала в зависимости от концентрации ионов кальция в растворах антител. Это демонстрирует, что антитела, имеющие каркасную последовательность, отличную от каркасных последовательностей из последовательности hVk5-2, также связываются с ионами кальция. В частности, было продемонстрировано, что мотив в последовательности CDR из последовательности hVk5-2 ответственен за связывание ионов кальция, в то время как каркасная последовательность может представлять собой любую каркасную последовательность.
Было продемонстрировано, что температура термической денатурации (величина Tm), в качестве индикатора термической стабильности Fab-домена каждого антитела, измененного так, чтобы оно имело последовательность CDR из последовательности hVk5-2 и каркасную последовательность эмбрионального типа, отличную от последовательности hVk5-2 (hVk1, hVk2, hVk3 или hVk4), является более высокой, чем температура термической денатурации Fab-домена исходного антитела, имеющего последовательность hVk5-2. Этот результат показывает, что антитела, имеющие последовательность CDR из последовательности hVk5-2 и каркасную последовательность hVk1, hVk2, hVk3 или hVk4, не только обладают активностью связывания ионов кальция, но также являются превосходными молекулами с точки зрения термической стабильности.
[Пример 14] Идентификация участка связывания ионов кальция в последовательности hVk5-2 человека эмбрионального типа
(14-1) Конструирование участка мутации в последовательности CDR из последовательности hVk5-2
Как описано в примере 13, также было показано, что антитела, имеющие легкую цепь, полученную в результате введения CDR-домена последовательности hVk5-2 в каркасную последовательность отличающейся последовательности эмбрионального типа, связываются с ионом кальция. Этот результат указывает на то, что в hVk5-2 участок связывания ионов кальция локализован в его CDR. Аминокислоты, которые связываются с ионом кальция, т.е. хелатируют ион кальция, включают отрицательно заряженные аминокислоты и аминокислоты, которые могут быть акцептором водородной связи. Таким образом, исследовали, связываются ли антитела, имеющие мутантную последовательность hVk5-2 с заменой остатком Ala (A) остатка Asp (D) или Glu (E) в последовательности CDR из последовательности hVk5-2, с ионом кальция.
(14-2) Конструирование последовательностей вариантов hVk5-2 с заменой на Ala, и экспрессия и очистка антител
Молекулы антител получали так, чтобы они содержали легкую цепь с заменой остатка Asp и/или Glu остатком Ala в последовательности CDR из последовательности hVk5-2. Как описано в примере 12, негликозилированный вариант hVk5-2_L65 проявлял связывание ионов кальция, и было предположено, что он является эквивалентным последовательности hVk5-2 с точки зрения связывания ионов кальция. В этом примере аминокислотные замены вносили в hVk5-2_L65 в качестве матричной последовательности. Сконструированные варианты представлены в таблице 18. Аминокислотные замены проводили способами, известными специалистам в данной области, такими как использование набора для сайт-направленного мутагенеза QuikChange Site-Directed Mutagenesis Kit (Stratagene), ПЦР или набора In fusion Advantage PCR Cloning Kit (TAKARA) для конструирования экспрессирующих векторов для измененных легких цепей, имеющих аминокислотную замену.
Нуклеотидные последовательности сконструированных экспрессирующих векторов подтверждали способом, известным специалистам в данной области. Экспрессирующие векторы, сконструированные для измененных легких цепей, временно вводили, в комбинации с экспрессирующим вектором для тяжелой цепи CIM_H (SEQ ID NO: 48), в клетки линии, происходящей из клеток почки эмбриона человека HEK293H (Invitrogen) или FreeStyle293 (Invitrogen) для экспрессии антител. Из полученных культуральных супернатантов антитела очищали с использованием rProtein A SepharoseTM Fast Flow (GE Healthcare) способом, известным специалистам в данной области. Поглощение растворов очищенного антитела при 280 нм измеряли с использованием спектрофотометра. Концентрации антител вычисляли из определенных величин с использованием коэффициента экстинкции, вычисленного способом PACE (Protein Science (1995) 4: 2411-2423).
(14-3) Оценка антител, имеющих замену Ala в последовательности hVk5-2, в отношении активности связывания ионов кальция
Проводили исследование, связываются ли полученные очищенные антитела с ионами кальция. В частности, очищенные антитела подвергали диализу (EasySEP, TOMY) против раствора 20 мМ Tris-HCl/150 мМ NaCl/2 мМ CaCl2 (pH 7,5) или раствора 20 мМ Tris-HCl/150 мМ NaCl (pH 7,5) (в таблице 19 указан в качестве концентрации ионов кальция 0 мкМ). Измерение DSC проводили при скорости увеличения температуры 240°C/ч от 20 до 115°C с использованием растворов антител, полученных в концентрации 0,1 мг/мл с помощью того же раствора, который использовали для диализа. Исходя из полученных кривых денатурации DSC, промежуточную температуру термической денатурации (величина Tm) вычисляли для Fab-домена каждого антитела, как показано в таблице 19. Было выявлено, что некоторые антитела, имеющие замену остатка Asp или Glu в последовательности CDR из последовательности hVk5-2 на остаток Ala, который не может быть вовлечен в связывание или хелатирование ионов кальция, имеют Fab-домен, Tm которого не варьировала в зависимости от концентрации ионов кальция в растворах антител. Было показано, что участки замены, в которых замена на Ala не изменяла Tm (положения 32 и 92 (нумерация по Kabat)), являются в значительной степени важными для связывания антителом ионов кальция.
[Пример 15] Оценка антител, имеющих последовательность hVk1 со связывающим ионы кальция мотивом, в отношении связывания ионов кальция
(15-1) Конструирование последовательности hVk1 со связывающим ионы кальция мотивом и экспрессия и очистка антител
Результат, описанный в примере 14, в отношении активности связывания кальция в случае замены Ala, демонстрирует, что остатки Asp или Glu в последовательности CDR из последовательности hVk5-2 были важными для связывания кальция. Таким образом, авторы настоящего изобретения оценивали, может ли антитело связываться с ионом кальция, когда остатки в положениях 30, 31, 32, 50 и 92 (нумерация по Kabat) отдельно вносили в другую последовательность вариабельной области эмбрионального типа. В частности, вариант LfVk1_Ca (SEQ ID NO: 61) конструировали путем замены остатками в положениях 30, 31, 32, 50 и 92 (нумерация по Kabat) в последовательности hVk5-2 остатков в положениях 30, 31, 32, 50 и 92 (нумерация по Kabat) последовательности hVk1 (последовательность человека эмбрионального типа). В частности, исследовали, могут ли антитела, имеющие последовательность hVk1, в которую встроено только 5 остатков из последовательности hVk5-2, связывать кальций. Варианты получали тем же способом, который описан в примере 2. Полученные варианты легкой цепи LfVk1_Ca и LfVk1, имеющие последовательность легкой цепи hVk1 (SEQ ID NO: 62) совместно экспрессировали с тяжелой цепью CIM_H (SEQ ID NO: 48). Антитела экспрессировали и очищали тем же способом, который описан в примере 14.
(15-2) Оценка антител, имеющих последовательность hVk1 человека со связывающим ионы кальция мотивом, в отношении активности связывания ионов кальция
Оценку того, связывает ли очищенное антитело, полученное, как описано выше, ионы кальция, проводили способом, описанным в примере 4. Результаты представлены в таблице 20. Величина Tm для Fab-домена антитела, имеющего LfVk1 с последовательностью hVk1, не варьировала, в зависимости от концентрации кальция в растворах антител. Между тем, Tm антитела, имеющего последовательность LfVk1_Ca сдвигалась на 1°C или более при изменении концентрации кальции в растворах антител. Таким образом, было показано, что антитело, имеющее LfVk1_Ca, связывается с кальцием. Результаты, описанные выше, демонстрирует, что полная последовательность CDR hVk5-2 не требуется, в то время как остатки, внесенные для конструирования последовательности LfVk1_Ca отдельно, являются достаточными для связывания ионов кальция.
(15-3) Конструирование, экспрессия и очистка устойчивой к деградации последовательности LfVk1_Ca
Как описано в (15-2) примера 15, вариант LfVk1_Ca (SEQ ID NO: 61) конструировали так, чтобы он имел замену остатками в положениях 30, 31, 32, 50 и 92 (нумерация по Kabat) в последовательности hVk5-2 остатков в положениях 30, 31, 32, 50 и 92 (нумерация по Kabat) в последовательности hVk1 (последовательность человека эмбрионального типа). Было продемонстрировано, что вариант связывается с ионом кальция. Таким образом, можно рассматривать Ca-зависимые антитела (Ca-связывающие антитела), имеющие последовательность LfVk1_Ca. Однако поскольку последовательность LfVk1_Ca является новой последовательностью, ее стабильность при хранении в качестве фармацевтического препарата неизвестна. Таким образом, применимость последовательности LfVk1_Ca в качестве фармацевтически препаратов еще предстоит установить. В этом контексте, стабильность LfVk1_Ca оценивали с помощью испытания с термическим ускорением. Антитело, имеющее LfVk1_Ca в качестве L-цепи, подвергали диализу против раствора 20 мМ гистидина-HCl/150 мМ NaCl (pH 6,0) в течение ночи при 4°C. Концентрацию антитела после диализа доводили до 0,5 мг/мл и хранили при 5°C или 50°C в течение трех суток. После хранения каждое антитело подвергали ионнобменной хроматографии способом, описанным в примере 12. Результат продемонстрировал, что LfVk1_Ca немного деградировало при хранении в течение трех суток при 50°C, как показано на фиг.17. Последовательность LfVk1_Ca имеет Asp в положениях 30, 31 и 32 (нумерация по Kabat), и таким образом его последовательность CDR1 содержит последовательность Asp-Asp, которая, как было описано, деградирует в кислых условиях (J. Pharm. Biomed. Anal. (2008) 47(1): 23-30). Это указывает на то, что аминокислоты в положениях 30, 31 и 32 (нумерация по Kabat) являются возможным участком деградации. Затем, чтобы избежать деградации LfVk1_Ca, конструировали варианты LfVk1_Ca1 (SEQ ID NO: 72), LfVk1_Ca2 (SEQ ID NO: 73) и LfVk1_Ca3 (SEQ ID NO: 74), чтобы они имели замену остатками Ala (A) трех остатков Asp (D), которые, возможно, являются чувствительными к деградации. Аминокислотную замену проводили способом, известным специалистам в данной области, с использованием набора для сайт-направленного мутагенеза QuikChange Site-Directed Mutagenesis Kit (Stratagene). ДНК, кодирующие варианты, встраивали в экспрессирующие векторы животных. В комбинации с экспрессирующим вектором животных, имеющим вставку для экспрессии GC H (SEQ ID NO: 102) в качестве тяжелой цепи, сконструированные экспрессирующие векторы животных, несущие вставки ДНК для вариантов, вводили в клетки животных способом, описанным в примере 14. Антитела, экспрессированные в клетках животных, в которые были введены векторы, очищали способом, описанным в примере 14.
(15-4) Оценка стабильности антител, имеющих устойчивую к деградации последовательность LfVk1_Ca
Оценку того, являлись ли антитела, полученные, как описано в (15-3) примера 15, более устойчивыми к деградации в растворах при pH 6,0, чем исходные антитела, имеющие последовательность LfVk1_Ca, предназначенную для модификации, проводили путем сравнения гетерогенности между соответствующими антителами после термического ускорения. Аналогично тому, как описано выше, антитела хранили при 5°C или 50°C в течение трех суток. Каждое антитело после хранения подвергали ионообменной хроматографии с использованием способа, описанного в примере 12. Как показано на фиг.17, результат анализа демонстрирует, что LfVk1_Ca1 с изменением в положении 30 (нумерация по Kabat) был менее гетерогенным и значительно более устойчивым к деградации при термическом ускорении, чем исходная последовательность LfVk1_Ca. В частности, было продемонстрировано, что деградация происходила по остатку Asp (D) в положении 30 последовательности LfVk1_Ca, однако ее можно было предотвратить изменением аминокислоты.
(15-5) Конструирование последовательности легкой цепи LfVk1_Ca, устойчивой к деградации по остатку Asp в положении 30, и экспрессия и очистка антител
Результат, описанный в (15-4) примера 15 в отношении устойчивости к деградации Ala-замещенной формы, демонстрирует, что в кислых условиях последовательность LfVk1_Ca деградировала по остатку Asp (D) в положении 30 (нумерация по Kabat) в ее последовательности CDR, и деградацию можно было предотвратить путем замены отличающейся аминокислотой (в (15-4), путем замены остатком Ala (A)) остатка Asp (D) в положении 30 (нумерация по Kabat). Затем, авторы настоящего изобретения исследовали, является ли устойчивой последовательность с заменой даже на Ser (S) - остаток, способный хелатировать ион кальция, остатка в положении 30 (нумерация по Kabat) (в отношении LfVk1_Ca6; SEQ ID NO: 75) к деградации при сохранении активности связывания кальция. Варианты получали способом, описанным в примере 14. Измененные легкие цепи последовательностей LfVk1_Ca6 и LfVk1_Ca экспрессировали в комбинации с тяжелой цепью GC_H (SEQ ID NO: 102). Антитела экспрессировали и очищали тем же способом, как описано в примере 14.
(15-6) Оценка последовательности легкой цепи LfVk1_Ca, устойчивой к деградации по остатку Asp в положении 30
Очищенные антитела, полученные, как описано выше, оценивали в отношении их стабильности при хранении в кислых условиях способом, описанным в (15-4) примера 15. Результат демонстрирует, что антитела, имеющие последовательность LfVk1_Ca6, являются более устойчивыми к деградации, чем антитела, имеющие исходную последовательность LfVk1_Ca, как показано на фиг.18.
Затем проводили исследование того, связывают ли антитела, имеющие последовательность LfVk1_Ca, и антитела, имеющие последовательность LfVk1_Ca6, ионы кальция способом, описанным в примере 15. Результат представлен в таблице 21. Величины Tm Fab-доменов антител, имеющих последовательность LfVk1_Ca, и антител, имеющих устойчивую к деградации последовательность LfVk1_Ca6, сдвигались на 1°C или более при изменении концентрации кальция в растворах антител.
Учитывая стабильность, результат, описанный выше, демонстрирует, что для связывающих ионы кальция антител важно, чтобы аминокислота в положении 30 представляла собой аминокислоту, способную взаимодействовать с ионом кальция (Asn, Glu, Gln, Ser, Thr, His, Tyr, и т.д.), отличную от Asp, и все или некоторые из аминокислот в положениях 31, 32, 50 и 92 (нумерация по Kabat) в последовательности были теми же, что и в hVk5-2, или представляли собой аминокислоты, способные взаимодействовать с кальцием (Asp, Asn, Glu, Gln, Ser, Thr, His, Tyr, и т.д.). Например, когда синтетическую библиотеку конструируют так, чтобы она имела такой мотив, из библиотеки можно эффективно выделить антитела с кальций-зависимым связыванием.
[Пример 16] Оценка с помощью ЯМР антител, имеющих последовательность hVk1 человека со связывающим ионы кальция мотивом, в отношении активности связывания ионов кальция
(16-1) Экспрессия и очистка антител
Антитело, имеющее LfVk1_Ca, и антитело, имеющее LfVk1, экспрессировали и очищали для измерений с помощью ЯМР. В частности, экспрессирующие плазмиды животных для антитела, имеющего LfVk1_Ca, конструировали так, чтобы они были способны экспрессировать его тяжелую цепь (SEQ ID NO: 13) и легкую цепь (SEQ ID NO: 61), и их временно вводили в клетки животных. Более того, экспрессирующие плазмиды животных для антитела, имеющего LfVk1, конструировали так, чтобы они были способны экспрессировать его тяжелую цепь (SEQ ID NO: 13) и легкую цепь (SEQ ID NO: 62), и их временно вводили в клетки животных. К 100 мл суспензии клеток, полученной суспендированием клеток, происходящих из клеток почки эмбриона человека FreeStyle 293-F (Invitrogen) с конечной плотностью клеток 1×106 клеток/мл в среде для экспрессии FreeStyle 293 Expression Medium (Invitrogen), добавляли меченые аминокислоты. В частности, раствор L-аспарагиновой кислоты-13C4,15N (10 мг), L-глутаминовой кислоты-13C5,15N (2,5 мг), L-глутамина-13C5,15N2 (60 мг), L-аспарагина-13C4,15N2·H2O (2,5 мг), и β-хлор-L-аланина (6 мг) в 10 мл воды фильтровали через 0,22-мкм фильтр и добавляли для получения Asp/Glu/Gln/Asn-меченных антител. Между тем, раствор L-лейцина-15N (30 мг) и β-хлор-L-аланина (6 мг) в 10 мл воды фильтровали через 0,22-мкм фильтр и добавляли для получения Leu-меченных антител. Сконструированные плазмиды вводили в клетки способом липофекции. Клетки, в которые введены плазмиды, культивировали в течение пяти суток в инкубаторе с CO2 (37°C, 8% CO2, 90 об/мин). Из культуральных супернатантов, полученных, как описано выше, антитела очищали с использованием rProtein A SepharoseTM Fast Flow (Amersham Biosciences) способом, известным специалистам в данной области. Поглощение растворов очищенных антител при 280 нм измеряли с использованием спектрофотометра. Концентрации антитела вычисляли из определенных величин с использованием коэффициента экстинкции, вычисленного способом PACE (protein Science (1995) 4: 2411-2423).
(16-2) Получение Fab-фрагмента
Каждое антитело концентрировали до 8,2-11,8 мг/мл с использованием ультрафильтра с пределом молекулярной массы 30000 MWCO. Антитела разбавляли до 8 мг/мл с использованием 50 мМ уксусной кислоты/125 мМ буфера Tris (pH 6,8), содержавшего 1 мМ L-цистеин и 2 мМ EDTA, для получения образцов. К каждому антителу добавляли папаин (Roche Applied Science) в количестве 1/240. После перемешивания образцы инкубировали при 37°C в течение одного часа. После инкубации каждый образец наносили на 1-мл HiTrap NHS-activated HP (GE Healthcare), на которую был иммобилизирован пептид Gly-Gly-Tyr-Arg (Sigma), и уравновешивали смесью 50 мМ уксусная кислота/125 мМ Tris-буфер (pH 6,8), а ниже ее последовательно была подсоединена 1-мл колонка HiTrap MabSelect Sure Protein A column (GE Healthcare). Очищенные фракции Fab-фрагментов получали путем удаления Fc-фрагмента, и нерасщепленные антитела удаляли в последующей колонке с белком A, в то время как активированный папаин удаляли с помощью выше расположенного пептида Gly-Gly-Tyr-Arg. К фракциям Fab добавляли ингибитор цистеиновых протеаз E64 (Sigma) в концентрации 10 мкМ для предотвращения активации неактивного папаина во фракциях Fab. Все действия на колонке, описанные выше, проводили при комнатной температуре от 20 до 25°C.
(16-3) Приготовление Fab-фрагментов антител LfVk1_Ca и LfVk1 в качестве образцов для ЯМР
Растворы антител концентрировали до 0,5 мл центрифугированием с использованием устройства для ультрафильтрации Vivaspin (Sartorius) с MWCO 5000. Затем в устройство для ультрафильтрации, описанное выше, помещали чашу для диафильтрации, и буфер заменяли на буфер для ЯМР: 5 мМ d-BisTris/20 мМ NaCl/0,001%(масс./об.) NaN3/5%(об./об.)2H2O (pH 7,0) (pH доводили с использованием NaOH и HCl) (через три цикла из: добавления 5 мл описанного выше буфера в чашу для диафильтрации, с последующим концентрированием до 0,5 мл центрифугированием). Растворы антител, в конечном итоге, концентрировали до 0,25 мл. Наконец, устройство для ультрафильтрации промывали буфером для ЯМР, и буфер объединяли с концентратом. Это давало 420 мкл и 270 мкл растворов антител для антитела LfVk1_Ca и антитела LfVk1, соответственно. На этой стадии, pH растворов вновь проверяли, и pH доводили до pH 7,0 с использованием NaOH и HCl, при необходимости. Поглощение при 280 нм измеряли с использованием УФ-спектрофотометра Nanodrop (Thermo Fisher Scientific) и концентрации Fab-фрагментов определяли с помощью коэффициента молярной экстинкции при 280 нм = 70000 M-1см-1. Концентрации Leu-меченных антител LfVk1_Ca и LfVk1 составляли 0,12 мМ, в то время как концентрации Asp-, Glu-, Asn- и Gln-меченных антител LfVk1_Ca и LfVk1 составляли 0,24 мМ. Из описанных выше образцов, антителом LfVk1_Ca заполняли пробирку для образца ЯМР диаметром 5 мм (shigemi), и антителом LfVk1 заполняли симметричную микропробирку для образца диаметром 5 мм (shigemi) для водного раствора с использованием пастеровской пипетки. В экспериментах по титрованию Ca2+ для антитела LfVk1_Ca, растворы CaCl2 добавляли к растворам антител последовательно так, чтобы количество Ca2+ составляло 1, 2, 5, 10 или 20 молярных эквивалентов относительно антитела. Добавленные растворы CaCl2 приготавливали в концентрациях 10, 20, 50 и 100 мМ CaCl2 с использованием буфера для ЯМР. Требуемые объемы растворов CaCl2 добавляли непосредственно к растворам антител в пробирки для образца для ЯМР с использованием микрошприца (ITO), который приспосабливали путем удлинения части шприца готового продукта, так чтобы объем загрузки находился в диапазоне от 3 до 10 мкл. После перемешивания с помощью вихревой мешалки, пробирки для образца центрифугировали с использованием ручной центрифуги (Shimadzu).
(16-4) Измерение ЯМР для выявления сигналов амидных групп в Fab-фрагментах антител LfVk1_Ca и LfVk1_Ca
Измерения ЯМР проводили с использованием ЯМР-спектрометра DRX750 (Bruker Biospin) с установленным на него TCI CryoProbe. Температура была установлена на 307K (поток газа 535 л/ч). В измерениях ЯМР для выявления сигналов амидных групп использовали1H-15N HSQC. Способ измерения проводили путем одновременного отделения13C от α и карбонильных атомов углерода и вычитания сигналов растворителя-воды в ходе периода изменения15N с использованием1H-15N FHSQC с группой импульсов 3-9-19. Для схемы контроля импульсов использовали стандартную программу, предоставленную изготовителем (Bruker Biospin). Условия измерений NMR были следующими. Ширина спектра: 12019 Гц (f2), 1976 Гц (f1); количество точек данных: 2048 (f2), 128 (f1). Данные обрабатывали с использованием Topspin 3.0 (Bruker Biospin) следующим образом. Перед преобразованием Фурье применяли функцию окна shifted square sine (QSINE) как в f2, так и в f1, и заполнение нулями для удвоения размера данных. Химические сдвиги сигналов вычисляли с использованием программного обеспечения для ЯМР-анализа Sparky (UCSF).
(16-5) Распределение сигнала ЯМР амидных групп главной цепи
80% сигналов ЯМР от амидных групп главной цепи Fab-фрагмента тоцилизумаба (тяжелая цепь SEQ ID NO: 13; легкая цепь SEQ ID NO: 14) были распределены ранее (данные не представлены). Аминокислотная последовательность Fab-фрагмента антитела LfVk1_Ca является такой же, как аминокислотная последовательность Fab-фрагмента тоцилизумаба, за исключением некоторых участков CDR1, CDR2, CDR3 легкой цепи и аминокислотных остатков в положениях 73 и 83 в легкой цепи. Аминокислотные последовательности, являющиеся общими для двух антител, дают сигналы ЯМР, которые проявляют одинаковые или сходные химические сдвиги. Вследствие этого информация о распределении для тоцилизумаба была применима для таких аминокислотных последовательностей. Для меченных Leu образцов, распределение, определенное как применимое, включает: 11, (33), (46), (47), (54), (78), 125, 135, 136, 154, 175, 179, 181 и 201 в легкой цепи, и 18, 46, 64, 71, 81, 83, 114, 144, 147, 165, 176, 181, 184 и 195 в тяжелой цепи. В указанных выше значениях, числа без скобок представляют собой номера остатков, в которых распределение является применимым, поскольку химические сдвиги являются общими с тоцилизумабом; номера в скобках соответствуют номерам остатков, для которых распределение является применимым, поскольку химические сдвиги являются сходными с химическими сдвигами тоцилизумаба и отсутствуют другие сигналы, дающие сходные химические сдвиги. Между тем, для Asp-, Glu-, Asn-, Gln-меченных образцов четыре сигнала были вновь выявлены в LfVk1_Ca, когда спектры сравнивали между антителами LfVk1_Ca и LfVk1. Было предположено, что они распределяются по четырем из пяти остатков, Asp30, Asp31, Asp32, Asp92 и Glu50, среди остатков Asp, Glu, Asn и Gln в легкой цепи, где последовательность, встроенная в качестве Ca2+-связывающего мотива, отличается между двумя антителами.
(16-6) Идентификация участка связывания Ca2+ в антителе LfVk1_Ca
Сигналы с отличающимся химическим сдвигом извлекали путем сравнения спектров1H-15N HSQC Fab-фрагмента антитела LfVk1_Ca в присутствии и в отсутствие 20 молярных эквивалентов Ca2+. Результат на Leu-меченных образцах показал, что только Leu33, но не другие Leu остатки, в легкой цепи вовлечены в связывание. Кроме того, в случае Asp-, Glu-, Asn-, Gln-меченных образцов, было выявлено, что четыре из пяти остатков Asp30, Asp31, Asp32, Asp92 и Glu50, в легкой цепи вовлечены в связывание, и все, за исключением одного из других остатков Asp, Glu, Asn и Gln, не были ответственны за связывание. Данные, описанные выше, демонстрируют, что в аминокислотной последовательности, встроенной в качестве Ca2+-связывающего мотива, некоторые аминокислоты по меньшей мере CDR1 легкой цепи и обеих или любой из CDR2 и CDR3 легкой цепи были вовлечены в связывание Ca2+. Это согласуется с данными, описанными в примере 15, что для связывания ионов кальция важно, чтобы аминокислоты в четырех положениях из положений 30, 31, 32, 50 и 92 (нумерация по Kabat) были идентичными аминокислотам в последовательности hVk5-2.
(16-7) Вычисление константны диссоциации для Ca2+ в эксперименте с титрованием
На основе спектров1H-15N HSQC при концентрациях Ca2+ 0, 1, 2, 5, 10 или 20 молярных эквивалентов относительно Fab-фрагмента антитела LfVk1_Ca был построен график с молярным эквивалентом Ca2+ по горизонтальной оси и с химическими сдвигами сигнала1H или15N для Leu33 легкой цепи, идентифицированного в качестве участка связывания, по вертикальной оси. С использованием функции, соответствующей формуле 2, представленной ниже, проводили аппроксимацию данных с помощью графического программного обеспечения Gnuplot.
[Формула 2]
f(x) = s * [1-0,5/a * {(a * x + a + Kd) - ((a * x + a + Kd)2 - 4 * x * a2)0,5} + t * [0,5/a * {(a * x + a + Kd) - ((a * x + a + Kd)2 - 4 * x * a2)0,5}
В функции, соответствующей формуле 2, "s" и "t" соответствуют химическому сдвигу [м.д.] для не связанного с Ca2+ состояния и оцененному химическому сдвигу [м.д.] для Ca2+-связанного насыщенного состояния, соответственно; "a" соответствует концентрации Fab-фрагмента антитела [M]; "Kd" соответствует константе диссоциации; и "x" соответствует молярным эквивалентам Ca2+, добавленным к Fab-фрагменту антитела. При аппроксимации данных параметрами аппроксимации были s, t и Kd. В результате, исходя из химических сдвигов1H и15N, Kd была оценена следующим образом: Kd=7,1×10-5 [M] и Kd=5,9×10-5 [M], соответственно.
[Пример 17] Оценка последовательности варианта hVk5-2 в отношении связывания кальция
Вариант 1 Vk5-2 (SEQ ID NO: 63) и вариант 2 Vk5-2 (SEQ ID NO: 64) получали в дополнение к Vk5-2 (SEQ ID NO: 41), все из которых классифицируют как Vk5-2. Эти варианты оценивали в отношении их связывания кальция. Каждый из фрагментов ДНК для Vk5-2, варианта 1 Vk5-2 и варианта 2 Vk5-2 встраивали в экспрессирующие векторы клеток животных. Нуклеотидные последовательности сконструированных экспрессирующих векторов определяли способом, известным специалистам в данной области. С помощью способа, описанного в примере 13, экспрессирующие векторы клеток животных, в которые встроены фрагменты ДНК для Vk5-2, варианта 1 Vk5-2 и варианта 2 Vk5-2, вводили в комбинации с экспрессирующим вектором животных, несущим вставку для экспрессии CIM_H (SEQ ID NO: 48) в качестве тяжелой цепи, в клетки животных, и антитела очищали. Очищенные антитела оценивали в отношении их активности связывания ионов кальция. Очищенные антитела подвергали диализу (EasySEP, TOMY) против 20 мМ Tris-HCl/150 мМ NaCl (pH 7,5) (в таблице 22 указано в качестве концентрации ионов кальция 0 мМ) или 20 мМ Tris-HCl/150 мМ NaCl/2 мМ CaCl2 (pH 7,5). Измерение DSC проводили при скорости увеличения температуры 240°C/ч от 20 до 115°C с использованием растворов антител, приготовленных в концентрации 0,1 мг/мл, с помощью того же раствора, который использовали для диализа. Исходя из полученных кривых денатурации DSC промежуточную температуру термической денатурации (величину Tm) вычисляли для Fab-домена каждого антитела. Величины Tm представлены в таблице 22.
Результат показал, что величина Tm для Fab-доменов антител, имеющих последовательность Vk5-2, варианта 1 Vk5-2 или варианта 2 Vk5-2 варьировала, в зависимости от концентрации ионов кальция в растворах, содержащих антитела, имеющие Fab-домены. Это демонстрирует, что антитела, имеющие последовательность, классифицированную как Vk5-2, связываются с ионами кальция.
[Пример 18] Антитела, которые связываются с CD4 человека кальций-зависимым образом
(18-1) Получение растворимого CD4 человека
Растворимый CD4 человека получали следующим образом. Последовательность ДНК, кодирующую последовательность (SEQ ID NO: 76), в которой Myc-метка связана с аминокислотной последовательностью CD4 человека, которая лишена трансмембранной области, встраивали в экспрессирующий вектор клеток животных. Последовательность сконструированного рекомбинантного CD4 человека подтверждали способом, известным специалистам в данной области.
(18-2) Экспрессия и очистка антител, которые связываются с растворимым CD4 человека
TNX355-IgG1 (тяжелая цепь SEQ ID NO: 77; легкая цепь SEQ ID NO: 78) и Q425 (тяжелая цепь SEQ ID NO: 79; легкая цепь SEQ ID NO: 80) представляют собой антитела против CD4 человека. Более того, Q425L9 (тяжелая цепь SEQ ID NO: 81; легкая цепь SEQ ID NO: 82) представляет собой вариант L-цепи из Q425. Последовательности ДНК, кодирующие аминокислоты TNX355-IgG1 (тяжелая цепь SEQ ID NO: 77; легкая цепь SEQ ID NO: 78), Q425 (тяжелая цепь SEQ ID NO: 79; легкая цепь SEQ ID NO: 80), и Q425L9 (тяжелая цепь SEQ ID NO: 81; легкая цепь SEQ ID NO: 82) встраивали в экспрессирующие плазмиды клеток животных. Антитела экспрессировали следующим способом. Клетки, происходящие из клеток почки эмбриона человека FreeStyle 293-F (Invitrogen), суспендировали в среде для экспрессии FreeStyle 293 Expression Medium (Invitrogen), и высевали с плотностью клеток 1,33×106 клеток/мл (3 мл) в каждую ячейку планшета с 6 ячейками. Полученные плазмиды вводили в клетки способом липофекции. Клетки культивировали в инкубаторе с CO2 (37°C, 8% CO2, 90 об/мин) в течение четырех суток. Из культуральных супернатантов, полученных, как описано выше, антитела очищали с использованием rProtein A SepharoseTM Fast Flow (Amersham Biosciences) способом, известным специалистам в данной области. Поглощение растворов очищенных антител измеряли при 280 нм с использованием спектрофотометра. Концентрации антител вычисляли из установленных величин на основе коэффициента экстинкции, определенного способом PACE (Protein Science 1995; 4: 2411-2423).
(18-3) Оценка активности полученных антител в отношении кальций-зависимого связывания с CD4 человека
Полученные антитела оценивали в отношении их активности кальций-зависимого связывания с растворимым CD4 человека с использованием Biacore T100 (GE Healthcare). Использованная высокая концентрация ионов кальция составляла 1,2 мМ, в то время как низкая концентрация ионов кальция составляла 3 мкМ. Растворимый CD4 человека (полученный, как описано в 18-1), использовали в качестве антигена. Достаточное количество белка G (Invitrogen) иммобилизовывали на сенсорном чипе CM4 (GE Healthcare) способом присоединения аминов, антителам позволяли связываться с сенсорным чипом, и затем представляющие интерес антитела улавливали. В качестве подвижного буфера использовали 10 ммоль/л ACES, 150 ммоль/л NaCl, 0,05% (масс./об.) Tween20, 1,2 ммоль/л CaCl2 (pH 7,4 или pH 6,0), содержавший 1,2 ммоль/л или 3 мкмоль/л CaCl2. Все измерения проводили при 37°C. CD4 человека разбавляли с использованием соответствующих буферов. Сенсограммы антител представлены на фиг.19. Как показано на фиг.19, форма сенсограммы антитела TNX355-IgG1 не изменялась даже тогда, когда изменяли условия подвижного буфера. Это демонстрирует, что TNX355-IgG1 представляет собой обычное антитело, которое не проявляет кальций-зависимую активность связывания с CD4 человека. Между тем, как для антитела Q425, так и для Q425L9, величина связывания антигена была более низкой при концентрации ионов кальция 3 мкМ (низкая концентрация ионов кальция), чем при 1,2 мМ (высокая концентрация ионов кальция), и таким образом, они проявляли активность Ca-зависимого связывания. В частности, не наблюдали фазы связывания для антитела Q425L9 при концентрации ионов кальция 3 мкМ даже при концентрации анализируемого соединения (растворимый CD4 человека) 200 нМ. В частности, было продемонстрировано, что Q425 и Q425L9 представляют собой антитела с кальций-зависимым связыванием, которые связываются с CD4 человека кальций-зависимым образом.
[Пример 19] Оценка антител с Ca-зависимым связыванием в отношении их эффекта на удержание антигена в плазме с использованием нормальных мышей
(19-1) Анализ in vivo с использованием нормальных мышей
Q425 и Q425L9, полученные, как описано в примере 18, представляют собой антитела, которые связываются с растворимым CD4 человека кальций-зависимым образом. Как уже описано в примерах 5 и 6 в отношении IL6R, было продемонстрировано, что при введении в комбинации с антигеном, антитело, имеющее свойство связывания с антигеном кальций-зависимым образом, обладает свойством ускорения элиминации антигена по сравнению с тем, когда антитело, которое связывается с антигеном кальций-независмым образом, вводят в комбинации с антигеном. Однако то, обладают ли антитела против других антигенов также свойством ускорения элиминации антигена, еще предстоит установить.
Затем растворимый CD4 человека (полученный, как описано в примере 18) вводили отдельно или в комбинации с антителом против CD4 человека нормальным мышам (мышь C57BL/6J; Charles River Japan). Мышей оценивали в отношении кинетики in vivo растворимого CD4 человека и антитела против CD4 человека после введения. Раствор растворимого CD4 человека (50 мкг/мл) или смешанный раствор растворимого CD4 человека и антитела против CD4 человека, вводили один раз в дозе 10 мл/кг в хвостовую вену. Использованные антитела против CD4 человека представляли собой TNX355-IgG1, Q425-IgG1 и Q425L9-IgG1, описанные выше.
Концентрация растворимого CD4 человека составляла 5 мкг/мл во всех смешанных растворах. Между тем, концентрации антител против CD4 человека варьировали, в зависимости от антитела: 0,264 мг/мл для TNX355-IgG1; 0,197 мг/мл для Q425-IgG1; и 2,594 мг/мл для Q425L9-IgG1. В этом случае, антитела против CD4 человека присутствовали в избыточном количестве по сравнению с растворимым CD4 человека, и, таким образом, предполагалось, что растворимый CD4 человека по большей части был связан с антителами. В группе, в которой вводили растворимый CD4 человека, взятие крови проводили через 2 минуты, 5 минут, 15 минут, 30 минут, один час и два часа после введения. В группе, в которой вводили растворимый CD4 человека в комбинации с TNX355-IgG1 без кальций-зависимой антигенсвязывающей активности, кровь собирали через 5 минут, 2 часа, 7 часов, 1 сутки, 3 суток, 7 суток, 14 суток и 28 сутки после введения. В группе, в которой вводили растворимый CD4 человека в комбинации с Q425-IgG1 или Q425L9-IgG1, имеющим кальций-зависимую антигенсвязывающую активность, взятие крови проводили через 5 минут, 30 минут, 2 часа, 7 часов, 1 сутки, 3 суток, 8 суток, 14 суток и 28 суток после введения. Непосредственно после взятия, кровь центрифугировали при 4°C и 12000 об/мин в течение 15 минут для выделения плазмы. Выделенную плазму хранили в морозильной камере при -20°C или ниже до измерений.
(19-2) Определение концентрации антитела против CD4 человека в плазме у нормальных мышей с помощью ELISA
Концентрации антител против CD4 человека в плазме мыши определяли с помощью ELISA. Сначала F(ab’)2-фрагмент антитела против IgG человека (специфичный к γ-цепи) (SIGMA) распределяли аликвотами в планшеты Nunc-Immuno Plates, MaxiSorp (Nalge nunc International). Планшет выдерживали в течение ночи при 4°C для получения планшетов с иммобилизованным антителом против IgG человека. Стандартные образцы получали в концентрациях 0,64, 0,32, 0,16, 0,08, 0,04, 0,02 и 0,01 мкг/мл в плазме. Образцы плазмы мыши для анализа получали путем разбавления в 100 раз или более. Образцы разделяли на аликвоты в планшеты с иммобилизованным антителом против IgG человека. Планшеты инкубировали при 25°C в течение одного часа. После инкубации образцы подвергали реакции с биотинилированным антителом против IL-6R человека (R&D) при 25°C в течение одного часа, а затем со стрептавидин-PolyHRP80 (Stereospecific Detection Technologies) при 25°C в течение 0,5 часа. Хромогенную реакцию проводили с использованием TMB One Component HRP Microwell Substrate (BioFX Laboratories) в качестве субстрата. После остановки реакции 1 н. серной кислотой (Showa Chemical) измеряли поглощение при 450 нм на устройстве для считывания микропланшетов. С использованием программного обеспечения для анализа SOFTmax PRO (Molecular Devices), концентрации в плазме мыши вычисляли на основе поглощения с помощью стандартной кривой.
Концентрации в плазме антител TNX355-IgG1, Q425-IgG1 и Q425L9-IgG1, определенные с помощью описанного выше способа после внутривенного введения нормальным мышам, представлены на фиг.20.
(19-3) Определение концентраций в плазме растворимого CD4 человека способом электрохимической люлминесценции
Концентрации растворимого CD4 человека определяли с помощью ELISA.
Для группы, в которой вводили sCD4 отдельно, и группы, в которой его вводили в комбинации с Q425 или Q425_L9, TNX распределяли аликвотами в планшет Nunc-Immuno Plate, MaxiSorp (Nalge nunc International). Планшет оставляли на ночь при 4°C для получения планшета с иммобилизованным на нем TNX. Стандартные образцы получали при концентрации в плазме 10, 5, 2,5, 1,25, 0,625, 0,3125 и 0,156 мкг/мл. Образцы плазмы мыши для анализа получали путем разбавления в 100 раз или более. Образцы получали с использованием буфера, содержащего 10 мМ EDTA, и распределяли аликвотами в планшет с иммобилизованным TNX. После инкубации в течение трех часов при 25°C образцы подвергали реакции с антителом против c-myc-HRP (Miltenyi Biotech) при 25°C в течение одного часа. Хромогенную реакцию проводили с использованием в качестве субстрата TMB One Component HRP Microwell Substrate (BioFX Laboratories). После остановки реакции 1 н. серной кислотой (Showa Chemical), проводили измерение поглощения при 450 нм с использованием устройства для считывания микропланшетов. С использованием программного обеспечения для анализа SOFTmax PRO (Molecular Devices), концентрации в плазме мыши вычисляли на основе поглощения с помощью стандартной кривой.
В группе, в которой введение проводили в комбинации с TNX, Q425 распределяли аликвотами в планшет Nunc-Immuno Plate, MaxiSorp (Nalge nunc International). Планшет оставляли на ночь 4°C для получения планшета с иммобилизованным на нем Q425. Стандартные образцы получали при концентрации в плазме 20, 10, 5, 2,5, 1,25, 0,625 и 0,3125 мкг/мл. Образцы плазмы мыши для анализа получали путем разведения в 100 раз или более. Образцы получали с использованием буфера, содержавшего 2 мМ Ca2+, и распределяли аликвотами в планшет с иммобилизованным на нем TNX. После инкубации в течение трех часов при 25°C образцы подвергали реакции с антителом против c-myc-HRP (Miltenyi Biotech) при 25°C в течение одного часа. Хромогенную реакцию проводили с использованием в качестве субстрата TMB One Component HRP Microwell Substrate (BioFX Laboratories). После остановки реакции 1 н. серной кислотой (Showa Chemical), проводили измерение поглощения при 450 нм с использованием устройства для считывания микропланшетов. С использованием программного обеспечения для анализа SOFTmax PRO (Molecular Devices), концентрации в плазме мыши вычисляли на основе поглощения с помощью стандартной кривой.
Концентрации растворимого CD4 человека в плазме с течением времени, определенные с помощью описанного выше способа, после внутривенного введения нормальным мышам, представлены на фиг.21.
Результат показал, что растворимый CD4 человека при введении отдельно элиминировался очень быстро. Между тем, элиминация растворимого CD4 человека была значительно замедленной при введении в комбинации с TNX355-IgG1, обычным антителом без активности Ca-зависимого связывания с растворимым CD4 человека. Напротив, элиминация растворимого CD4 человека была значительно ускорена при введении в комбинации с Q425-IgG1 или Q425L9-IgG1, имеющими активность Ca-зависимого связывания с растворимым CD4 человека. Элиминация растворимого CD4 человека могла ускоряться при введении в комбинации с Q425-IgG1 или Q425L9-IgG1 по сравнению с введением в комбинации с TNX355-IgG1. Эти данные демонстрируют, что не только для IL-6R, но также для CD4 человека, можно достигать элиминации из плазмы с помощью антитела с кальций-зависимым связыванием.
[Пример 20] Антитела, которые связываются с IgA человека кальций-зависимым образом
(20-1) Получение IgA человека (hIgA)
Антиген, рекомбинантный IgA человека (далее сокращенно обозначаемый как hIgA), получали следующим образом. hIgA, содержащий H(WT)-IgA1 (SEQ ID NO: 83) и L(WT) (SEQ ID NO: 14), экспрессировали и очищали ионообменной хроматографией и гель-фильтрацией с использованием способа, известного специалистам в данной области.
(20-2) Экспрессия и очистка антител, которые связываются с IgA человека
GA1-IgG1 (тяжелая цепь SEQ ID NO: 84; легкая цепь SEQ ID NO: 85), GA2-IgG1 (тяжелая цепь SEQ ID NO: 86; легкая цепь SEQ ID NO: 87), GA3-IgG1 (тяжелая цепь SEQ ID NO: 88; легкая цепь SEQ ID NO: 89), и GA4-IgG1 (тяжелая цепь SEQ ID NO: 90; легкая цепь SEQ ID NO: 91) представляют собой антитела, которые связываются с IgA человека. Следовательно, для дальнейшего усиления элиминации антигена (hIgA) из плазмы аналогично тому, как описано в примерах 6 и 7, конструировали GA2-N434W (тяжелая цепь SEQ ID NO: 92; легкая цепь SEQ ID NO: 87) путем внесений аминокислотной замены N434W в GA2-IgG1 для усиления связывания с FcRn мыши при pH 7,4. Последовательности ДНК, кодирующие GA1-IgG1 (тяжелая цепь SEQ ID NO: 84; легкая цепь SEQ ID NO: 85), GA2-IgG1 (тяжелая цепь SEQ ID NO: 86; легкая цепь SEQ ID NO: 87), GA3-IgG1 (тяжелая цепь SEQ ID NO: 88; легкая цепь SEQ ID NO: 89), GA4-IgG1 (тяжелая цепь SEQ ID NO: 90; легкая цепь SEQ ID NO: 91) и GA2-N434W (тяжелая цепь SEQ ID NO: 92; легкая цепь SEQ ID NO: 87) встраивали в экспрессирующие плазмиды животных способом, известным специалистам в данной области. Антитела экспрессировали следующим образом. Клетки, происходящие из клеток почки эмбриона человека FreeStyle 293-F (Invitrogen), суспендировали в среде для экспрессии FreeStyle 293 Expression Medium (Invitrogen), и высевали с плотностью клеток 1,33×106 клеток/мл (3 мл) в каждую ячейку планшета с 6 ячейками. Сконструированные плазмиды вводили в клетки способом липофекции. Клетки культивировали в инкубаторе с CO2 (37°C, 8% CO2, 90 об/мин) в течение четырех суток. Из полученных культуральных супернатантов антитела очищали с использованием rProtein A SepharoseTM Fast Flow (Amersham Biosciences) способом, известным специалистам в данной области. Концентрации очищенных антител определяли путем измерения поглощения при 280 нм с использованием спектрофотометра. Концентрации антител вычисляли из установленных величин на основе коэффициента экстинкции, определенного способом PACE (Protein Science 1995; 4: 2411-2423).
(20-3) Оценка полученных антител в отношении активности Ca-зависимого связывания с IgA человека
С использованием Biacore T200 (GE Healthcare) полученные антитела оценивали в отношении их активности связывания с IgA человека (константа диссоциации KD (M)). Измерение проводили с использованием в качестве подвижного буфера 0,05% Tween20, 20 ммоль/л ACES, 150 ммоль/л NaCl (pH 7,4 или pH 5,8), содержавшего 3 мкМ или 1,2 мМ CaCl2, или 0,05% tween20, 20 ммоль/л ACES, 150 ммоль/л NaCl (pH 8,0), содержавшего 0,1 мкМ или 10 мМ CaCl2.
После иммобилизации достаточного количества рекомбинантного белка A/G (Thermo Scientific) на сенсорный чип CM5 (GE Healthcare) способом присоединения аминов, антителам позволяли связаться с сенсорным чипом. Соответствующую концентрацию hIgA (описанного в (20-1)) инжектировали в качестве анализируемого соединения для взаимодействия с антителами на сенсорном чипе. Затем сенсорный чип регенерировали путем инжекции 10 ммоль/л глицина-HCl, pH 1,5. Измерение проводили при 37°C. Из результата анализа константу диссоциации KD (M) вычисляли на основе анализа с аппроксимацией кривой и анализа константы равновесия с использованием программного обеспечения Biacore T200 Evaluation Software (GE Healthcare). Результат представлен в таблице 23. Полученная сенсограмма представлена на фиг.22. Было продемонстрировано, что GA2-IgG1, GA3-IgG1 и GA4-IgG1 связываются с IgA человека сильно при концентрации Ca2+ 1,2 мМ и слабо при концентрации Ca2+ 3 мкМ.
[Пример 21] Оценка эффекта антител с Ca-зависимым связыванием IgA в отношении удержания антигена в плазме с использованием нормальных мышей
(21-1) Анализ in vivo с использованием нормальных мышей
IgA человека (IgA человека: полученный, как описано в примере 20) вводили отдельно или в комбинации с антителом против IgA человека нормальным мышам (мышь C57BL/6J; Charles River Japan). Мышей оценивали в отношении кинетики in vivo IgA человека и антитела против IgA человека после введения. Раствор IgA человека (80 мкг/мл) или смешанный раствор IgA человека и антитела против IgA человека вводили один раз в количестве 10 мл/кг в хвостовую вену. Использованные антитела против IgA представляли собой GA1-IgG1, GA2-IgG1, GA3-IgG1 и GA2-N434W, описанные выше.
Концентрация IgA человека в смешанном растворе составляла 80 мкг/мл. Между тем, концентрации антител против IgA человека варьировали, в зависимости от аффинности к hIgA: 100 мг/мл для GA1-IgG1; 28,9 мг/мл для GA2-IgG1; 53,8 мг/мл для GA3-IgG1; и 1 мг/мл для GA2-N434W. В этом случае, антитела против IgA человека присутствовали в избыточном количестве по сравнению с IgA человека, и предполагалось, что IgA человека по большей части был связан антителами. Взятие крови проводили через 5 минут, 7 часов, 1 сутки, 2 суток, 3 суток и 7 суток после введения. Сразу после взятия, кровь центрифугировали при 4°C и 12000 об/мин в течение 15 минут для выделения плазмы. Выделенную плазму хранили в морозильной камере при -20°C или ниже до измерений.
(21-2) Определение концентрации в плазме антитела против IgA человека у нормальных мышей с помощью ELISA
Концентрации антител против IgA человека в плазме мыши определяли с помощью ELISA. Сначала F(ab’)2-фрагмент антитела против IgG человека (специфичный к γ-цепи) (SIGMA) распределяли аликвотами в планшеты Nunc-Immuno Plates, MaxiSorp (Nalge nunc International). Планшет оставляли на ночь 4°C для получения планшета с иммобилизованным на нем антителом против IgG человека. Стандартные образцы получали при концентрации в плазме 0,5, 0,25, 0,125, 0,0625, 0,03125, 0,01563 и 0,07813 мкг/мл. Образцы плазмы мыши для анализа получали путем разведения в 100 раз или более. Образцы распределяли аликвотами в планшет с иммобилизованным на нем антителом против IgG человека. После инкубации в течение одного часа при 25°C, образцы подвергали реакции с конъюгатом антитела козы против IgG человека (специфичным к γ-цепи) с биотином (BIOT) (Southern Biotechnology Associats Inc.) при 25°C в течение одного часа. Затем образцы подвергали реакции со стрептавидин-PolyHRP80 (Stereospecific Detection Technologies) при 25°C в течение одного часа. Хромогенную реакцию проводили с использованием в качестве субстрата TMB One Component HRP Microwell Substrate (BioFX Laboratories). После остановки реакции 1 н. серной кислотой (Showa Chemical), проводили измерение поглощения при 450 нм с использованием устройства для считывания микропланшетов. С использованием программного обеспечения для анализа SOFTmax PRO (Molecular Devices), концентрации в плазме мыши вычисляли на основе поглощения с помощью стандартной кривой. Концентрации антител GA1-IgG1, GA2-IgG1, GA3-IgG1, и GA2-N434W в плазме с течением времени, определенные описанным выше способом, после внутривенного введения нормальным мышам представлены на фиг.23.
(21-3) Определение концентрации в плазме IgA человека с помощью ELISA
Концентрации IgA человека в плазме мыши определяли с помощью ELISA. Сначала антитело козы против IgA человека (BETHYL) распределяли аликвотами в планшет Nunc-Immuno Plate, MaxiSorp (Nalge nunc International). Планшет оставляли на ночь при 4°C для получения планшета, с иммобилизованным на нем антителом против IgA человека. Стандартные образцы IgA человека приготавливали при концентрациях в плазме 0,4, 0,2, 0,1, 0,05, 0,025, 0,0125 и 0,00625 мкг/мл. Образцы плазмы мыши для анализа получали путем разведения в 100 раз или более. 200 мкл hsIL-6R в концентрации 500 нг/мл добавляли к 100 мкл стандарта и образцов плазмы. Полученные смеси выдерживали при комнатной температуре в течение одного часа, а затем распределяли аликвотами в планшет с иммобилизованным на нем антителом против IgA человека и инкубировали при комнатной температуре в течение одного часа. После инкубации смеси подвергали реакции с биотинилированным антителом против IL-6R человека (R&D) при комнатной температуре в течение одного часа, а затем со стрептавидин-PolyHRP80 (Stereospecific Detection Technologies) при комнатной температуре в течение одного часа. Хромогенную реакцию проводили с использованием в качестве субстрата TMB One Component HRP Microwell Substrate (BioFX Laboratories). После остановки реакции 1 н. серной кислотой (Showa Chemical), проводили измерение поглощения при 450 нм с использованием устройства для считывания микропланшетов. С использованием программного обеспечения для анализа SOFTmax PRO (Molecular Devices), концентрации в плазме мыши вычисляли на основе поглощения с помощью стандартной кривой. Концентрации IgA человека в плазме с течением времени, определенные описанным выше способом, после внутривенного введения нормальным мышам, представлены на фиг.24.
Результат показал, что когда IgA человека вводили в комбинации с GA1-IgG1, антитело, зависимость которого от Ca при связывании с IgA человека является слабой (степень зависимости является низкой), элиминация IgA человека была замедлена по сравнению с введением отдельно. Между тем, элиминация IgA человека была значительно ускоренной при введении в комбинации с GA2-IgG1, которое проявляет в 100 раз или более увеличенную активность Ca-зависимого связывания IgA человека. Концентрацию в плазме несвязанного IgA человека определяли из концентрации антитела в плазме, представленной на фиг.23, концентрации IgA человека в плазме, представленной на фиг.24, и величины KD каждого антитела, представленной в таблице 23. Результат представлен на фиг.25. Как показано на фиг.25, концентрация несвязанного антигена (IgA человека) в группе, в которой вводили GA2-IgG1 или GA3-IgG1, была более низкой по сравнению с концентрацией не связанного антигена (IgA человека) в группе, в которой вводили GA1-IgG1. Это демонстрирует, что уровень несвязанного антигена (IgA человека) может быть снижен путем ускорения элиминации антигена с использованием антител с кальций-зависимым связыванием. Более того, GA2-N434W, которое проявляло усиленное связывание FcRn при pH 7,4, ускоряло элиминацию антигена в большей степени, чем GA2-IgG1. Уровень антигена снижался до уровня ниже предела выявления через 7 часов после введения.
Данные, описанные выше, демонстрируют, что антитела с кальций-зависимым связыванием могут ускорять элиминацию антигена из плазмы по сравнению с обычными антителами, которые связываются с антигеном pH- или кальций-независимым образом. Было выявлено, что это применимо не только к IL6R человека, описанному в примере 5, или CD4 человека, описанному в примере 19, но также к IgA человека. Более того, в дополнение к IL6R человека, описанному в примерах 6 и 7, было продемонстрировано для IgA человека, что элиминация антигена может быть далее ускорена путем усиления связывания FcRn антитела с кальций-зависимым связыванием при pH 7,4.
Как показано в справочном примере 31, Fv4-IgG1, которое связывается с рецептором IL-6 человека pH-зависимым образом, может ускорять элиминацию рецептора IL-6 человека по сравнению с H54/L28-IgG1, которое связывается с рецептором IL-6 человека pH-независимым образом; однако, Fv4-IgG1 не может ускорять элиминацию по сравнению с введением рецептора IL-6 человека отдельно. Для ускорения элиминации по сравнению с введением рецептора IL-6 человека отдельно следовало использовать Fv4-IgG1-v1 или Fv4-IgG1-v2 с усиленной активностью связывания FcRn.
Между тем, неожиданно было выявлено, что GA2-IgG1, которое связывается с IgA человека Ca-зависимым образом, ускоряет элиминацию IgA человека по сравнению с введением IgA человека отдельно, хотя оно имеет константную область природного IgG1, у которого связывание FcRn в нейтральном диапазоне не усилено. Полагают, что следующий механизм объясняет случай с GA2-IgG1.
В случае мономерных антигенов, таких как рецептор IL-6 человека, два антигена связываются с двухвалентным антителом. Это приводит к образованию комплекса антиген/антитело, состоящего из трех молекул антигена и антитела. С другой стороны, поскольку IgA человека представляет собой димерный антиген и антитело является двухвалентным, комплекс антиген/антитело между ними, вероятно, образует комплекс антиген/антитело (иммунный комплекс), состоящий из четырех или более молекул антигена и антитела.
Когда антитело природного IgG1-типа против мультимерного антигена образует объемный иммунный комплекс, иммунный комплекс может связываться с FcgR, FcRn, рецептором комплемента и т.п. через Fc-домен с авидностью по мультивалентному принципу. Таким образом, иммунный комплекс интернализуется в клетки, экспрессирующие такие рецепторы. Между тем, обычное pH/Ca-независимое антитело против мономерного антигена имеет недостаточно аффинности к рецептору природного IgG1-типа, и, таким образом, полученный иммунный комплекс интернализуется в клетки с низкой эффективностью. FcRn первоначально имеет роль рециклирования внутриклеточно интернализованных антител из эндосомы в плазму. Однако известно, что объемные иммунные комплексы, способные связываться с FcRn мультивалентным образом, переносятся из эндосомы с помощью FcRn и деградируются в лизосоме. В частности, как показано на фиг.26, обычное антитело против мультимерного антигена, которое образует объемный иммунный комплекс, может ускорять элиминацию антигена; однако антиген не диссоциирует от антитела в эндосоме и антитело также элиминируется одновременно с антигеном. Таким образом, эффективность элиминации антигена на молекулу антитела является низкой. Иными словами, обычное pH/Ca-независимое антитело против мономерного антигена может ускорять элиминацию антигена; однако предположительно его эффективность является низкой.
С другой стороны, когда pH/Ca-зависимое антитело, которое имеет природную константную область IgG1-типа, против мультимерного антигена образует объемный иммунный комплекс, иммунный комплекс связывается с FcgR, FcRn, рецептором комплемента и т.д. с авидностью через мультимерную Fc-область, как показано на фиг.27, и захватывается клетками, экспрессирующими рецепторы. Иммунный комплекс растворяется путем диссоциации антигена от pH/Ca-зависимого антитела в эндосоме. Антиген не может связываться с FcRn и переносится в лизосому для деградации. Между тем, антитело рециклирует в плазму посредством FcRn, поскольку оно не образует иммунный комплекс.
В частности, когда pH/Ca-зависимое антитело, которое имеет природную константную область IgG1-типа, против мультимерного антигена, может связываться с FcgR, FcRn, рецептором комплемента и т.п., с авидностью путем образования объемного иммунного комплекса, элиминация только антигена может быть селективно и значительно ускорена. Описанное выше явление предположительно также происходит в случае GA2-IgG1 против IgA человека. Ожидается, что это может быть пригодным в качестве способа значительного ускорения элиминации мультимерного антигена без использования способа аминокислотных замен для усиления связывания FcRn природным IgG1 в нейтральном диапазоне, как показано в справочном примере 31.
Для достижения эффекта, описанного выше, антиген и антитело должны формировать объемный иммунный комплекс и должны прочно связываться с FcgR/FcRn с авидностью, даже если антитело представляет собой IgG1. Когда антиген является димерным или представляет собой полимерный антиген более высокого порядка, путем скрининга pH/Ca-зависимых антител, которые образуют объемный иммунный комплекс и связываются с описанным выше рецептором, элиминация антигена может быть эффективно ускорена с использованием природной константной области IgG1 без проведения какой-либо аминокислотой замены. Как правило, считается, что антигены должны быть мультимерными (например, иммуноглобулины, такие как IgA и IgE, и суперсемейство TNF, как например, TNF и CD154), чтобы антитела и антигены образовывали объемные иммунные комплексы. Даже когда антиген является мономерным, объемный иммунный комплекс может быть образован с использованием смеси двух или более типов соответствующих pH/Ca-зависимых антител, которые распознают два или более эпитопов в мономерном антигене. Альтернативно, объемный иммунный комплекс может быть образован с использованием соответствующего полиспецифического pH/Ca-зависимого антитела, которое распознает два или более эпитопов в мономерном антигене (например, биспецифическое антитело, имеющее природную константную область IgG, в котором правое и левое плечи распознают эпитопы A и B, соответственно, как показано на фиг.28). В частности, если pH/Ca-зависимые антитела против мономерных антигенов можно подвергать скринингу, элиминацию антигена можно эффективно ускорять с использованием смеси антител, имеющих природную константную область IgG1, или полиспецифического антитела, имеющего природную константную область IgG1, без использования мутантного IgG1, имеющего аминокислотную замену.
[Пример 22] Антитела, которые связываются с глипиканом 3 человека кальций-зависимым образом
(22-1) Получение глипикана 3 человека (GPC3)
Рекомбинантный глипикан 3 человека (далее сокращенно обозначаемый как GPC3), который используют в качестве антигена, получали по следующей методике. Культивировали клетки CHO, в которые была конститутивно введения плазмида, которая экспрессирует последовательность, в которой шесть остатков гистидина связаны с аминокислотной последовательностью глипикана 3 человека без трансмембранного домена (SEQ ID NO: 93). Затем из собранных культуральных супернатантов GPC3 очищали ионообменной хроматографией, а затем аффинной хроматографией на основе His-метки и гель-фильтрацией.
(22-2) Экспрессия и очистка антител, которые связываются с GPC3 человека
Каждое из антител против глипикана 3 человека CSCM-01_005 (последовательность тяжелой цепи: 94; последовательность легкой цепи: 95), CSCM-01_009 (последовательность тяжелой цепи: 96; последовательность легкой цепи: 97), CSCM-01_015 (последовательность тяжелой цепи: 98, последовательность легкой цепи: 99), CSCM-01_023 (последовательность тяжелой цепи: 100; последовательность легкой цепи: 101) и GC-IgG1 (последовательность тяжелой цепи: 102; последовательность легкой цепи: 103) встраивали в экспрессирующие плазмиды животных. Антитела экспрессировали по следующей методике. Клетки, происходящие из клеток эмбриона почки человека FreeStyle 293-F (Invitrogen), суспендировали в среде для экспрессии FreeStyle 293 Expression Medium (Invitrogen), и высевали с плотностью клеток 1,33×106 клеток/мл (3 мл) в каждую ячейку планшета с 6 ячейками. Полученные плазмиды вводили в клетки способом липофекции. Клетки культивировали в инкубаторе с CO2 (37°C, 8% CO2, 90 об/мин) в течение четырех суток. Из полученных культуральных супернатантов антитела очищали с использованием rProtein A SepharoseTM Fast Flow (Amersham Biosciences) способом, известным специалистам в данной области. Концентрации очищенных антител определяли путем измерения поглощения при 280 нм с использованием спектрофотометра. Концентрации антител вычисляли из установленных величин на основе коэффициента экстинкции, определенного способом PACE (Protein Science 1995; 4: 2411-2423). Более того, антитело GC-IgG1 очищали из культуральных супернатантов клеток CHO, конститутивно экспрессирующих антитело GC-IgG1, и его концентрацию определяли тем же способом, как описано выше.
(22-3) Оценка выделенных антител в отношении активности Ca-зависимого связывания GPC3 человека
Выделенные антитела подвергали ELISA с использованием следующей методики. 96-луночный микропланшет для титрования StreptaWell (Roche) покрывали в течение ночи 100 мкл PBS, содержащего меченный биотином антиген. После смывания антигена из каждой лунки планшета с использованием буфера ACES (10 мМ ACES, 150 мМ NaCl, 100 мМ CaCl2, 0,05% Tween20, pH 7,4), лунки блокировали в течение одного часа или более 250 мкл буфера ACES, содержавшего 2% BSA. После удаления буфера ACES, содержавшего 2% BSA, из каждой лунки, очищенный IgG, подвергнутый серийному разведению с коэффициентом разбавления 4, начиная с 10 мкг/мл, получали заранее и распределяли аликвотами по 100 мкл в планшет. Планшет выдерживали в течение одного часа для обеспечения связывания IgG с антигеном в каждой лунке. После промывания буфером ACES в каждую лунку добавляли "10 мМ ACES, 150 мМ NaCl, 1,2 мМ CaCl2, pH 7,4", "10 мМ ACES, 150 мМ NaCl, 3 мкМ CaCl2, pH 7,4", "10 мМ ACES, 150 мМ NaCl, 1,2 мМ CaCl2, pH 5,8" или "10 мМ ACES, 150 мМ NaCl, 3 мкМ CaCl2, pH 5,8". Планшет инкубировали при 37°C в течение 30 минут. После промывания буфером ACES, в каждую лунку добавляли конъюгированное с HRP антитело против IgG человека (BIOSOURCE), разбавленное буфером ACES, содержавшим 2% BSA. Планшет инкубировали в течение одного часа. После промывания буфером ACES в каждую лунку добавляли раствор только TMB (ZYMED). Хромогенную реакцию в растворе в каждой лунке останавливали добавлением серной кислоты. Затем проводили оценку проявившегося цвета путем измерения поглощения при 450 нм.
Результат измерения представлен на фиг.29. В случае GC-IgG1, поглощение GC-IgG1 не изменялось, в зависимости от концентрации ионов кальция. Напротив, в случае CSCM-01_005, CSCM-01_009, CSCM-01_015 и CSCM-01_023, поглощение было значительно более низким при концентрации ионов кальция 3 мкМ (низкая концентрация ионов кальция), чем при 1,2 мМ (высокая концентрация ионов кальция). Результат, описанный выше, демонстрирует, что CSCM-01_005, CSCM-01_009, CSCM-01_015 и CSCM-01_023, обладают свойством варьирования связывания антигена в зависимости от концентрации ионов кальция. Это демонстрирует, что кальций-зависимые антитела против глипикана 3 человека также могут быть получены. По сравнению с типичными антителами против глипикана 3 человека, считается, что кальций-зависимые антитела против глипикана 3 могут ускорить элиминацию глипикана 3 человека, аналогично случаю с IL-6R человека, CD4 человека или IgA человека, описанными в примерах выше. Более того, считается, что элиминация глипикана 3 человека может быть далее ускорена путем усиления связывания с FcRn кальций-зависимых антител человека против глипикана 3 при pH 7,4.
[Пример 23] Антитела, которые связываются с IgE кальций-зависимым образом
(23-1) Получение биотинилированного IgE человека
IgE человека получали в качестве антигена по следующей методике. Получали экспрессирующий вектор клеток животных, в который встроена последовательность ДНК, кодирующая IgE-H (SEQ ID NO: 104, последовательность для биотинилирования связана с C-концом) и L(WT) (SEQ ID NO: 14). С использованием экспрессирующего вектора и FreeStyle293 (Invitrogen), полноразмерный белок IgE человека, с которым связана последовательность для биотинилирования на C-конце, экспрессировали в культуральном супернатанте. Из выделенного культурального супернатанта, получали биотинилированный IgE человека путем проведения ионообменной хроматографии, аффинной очистки на основе авидина и очистки гель-фильтрацией.
(23-2) Экспрессия и очистка антител, которые связываются с IgE человека
GEB0100 (тяжелая цепь, SEQ ID NO: 105; легкая цепь, SEQ ID NO: 106), GEB0220 (тяжелая цепь, SEQ ID NO: 107; легкая цепь, SEQ ID NO: 108), GEB0230 (тяжелая цепь, SEQ ID NO: 109; легкая цепь, SEQ ID NO: 110) и Xolair (тяжелая цепь, SEQ ID NO: 111; легкая цепь, SEQ ID NO: 112) представляли собой антитела, которые связываются с IgE человека. Каждое из GEB0100 (тяжелая цепь, SEQ ID NO: 105; легкая цепь, SEQ ID NO: 106), GEB0220 (тяжелая цепь, SEQ ID NO: 107; легкая цепь, SEQ ID NO: 108), GEB0230 (тяжелая цепь, SEQ ID NO: 109; легкая цепь, SEQ ID NO: 110), и Xolair (родовое наименование: Омализумаб) (тяжелая цепь, SEQ ID NO: 111; легкая цепь, SEQ ID NO: 112) встраивали в экспрессирующие плазмиды животных способом, известным специалистам в данной области. Антитела экспрессировали по следующей методике. Сконструированные плазмиды вводили в клетки, происходящие из клеток почки эмбриона человека FreeStyle 293-F (Invitrogen), способом липофекции. Клетки культивировали в течение от четырех до семи суток в инкубаторе с CO2 (37°C, 8% CO2, 90 об/мин). Из полученных культуральных суспернатантов антитела очищали с использованием rProtein A SepharoseTM Fast Flow (Amersham Biosciences) способом, известным специалистам в данной области.
Концентрации очищенных антител определяли путем измерения поглощения при 280 нм с использованием спектрофотометра. Концентрации антител вычисляли из установленных величин с использованием коэффициента экстинкции, вычисленного способом PACE (Protein Science (1995) 4: 2411-2423).
(23-3) Оценка выделенных антител в отношении активности Ca-зависимого связывания с IgE человека
Выделенные антитела оценивали в отношении их активности Ca-зависимого связывания с IgE человека с помощью ELISA. В частности, 40 мкл поликлонального антитела козы против IgG-Fc кролика (Bethyl laboratory; A120-111A) в концентрации 1 мкг/мл или поликлонального антитела козы против IgG-Fc человека (ICN biomedicals; 55071) в концентрации 1 мкг/мл добавляли в 384-луночный планшет MaxiSorp NUNC Immuno (Thermo fisher scientific; 464718). После инкубации в течение одного часа при комнатной температуре раствор удаляли и добавляли 50 мкл блокирующего реагента Blocking One Reagent (Nacalai Tesque; 03953-95), разбавленного до 20%. После инкубации в течение одного часа при комнатной температуре раствор удаляли и добавляли 40 мкл очищенных антител, разбавленных буфером Tris, содержавшим 1,2 мМ хлорид кальция. После инкубации в течение ночи при 4°C, планшет промывали три раза 80 мкл буфера Tris, содержащего 1,2 мМ хлорид кальция и 0,05% (масс./об.) Tween-20, и добавляли 40 мкл биотинилированного IgE человека (полученного, как описано в (23-1)), разбавленного до 500 нг/мл Tris-буфером, содержащим 1,2 мМ хлорид кальция. После инкубации в течение одного часа при комнатной температуре планшет промывали три раза 80 мкл Tris-буфера, содержавшего 1,2 мМ хлорид кальция и 0,05% (масс./об.) Tween-20. Добавляли 80 мкл буфера ACES (pH 7,4), содержавшего 2 мМ или 3 мкМ хлорид кальция, а затем сразу удаляли. Вновь в планшет добавляли 80 мкл буфера ACES (pH 7,4), содержавшего 2 мМ или 3 мкМ хлорид кальция. После инкубации в течение одного часа при 37°C, планшет промывали три раза 80 мкл Tris-буфера, содержавшего 1,2 мМ хлорид кальция и 0,05%(масс./об.) Tween-20, и добавляли 40 мкл меченного HRP стрептавидина (Thermo fisher scientific; 21132), разбавленного до 25 нг/мл Tris-буфером, содержавшим 1,2 мМ хлорид кальция. После инкубации в течение одного часа при комнатной температуре, планшет промывали три раза 80 мкл Tris-буфера, содержавшего 1,2 мМ хлорид кальция и 0,05%(масс./об.) Tween-20. Затем добавляли 40 мкл хромогенного субстрата (KPL; 50-66-06: компонент субстратной системы 1 пероксидаз ABTS). После инкубации в течение от 15 до 30 минут при комнатной температуре, измеряли поглощение при 405 нм (Molecular devices; SpectraMax Plus384).
Результат измерения представлен на фиг.30. В случае Xolair, поглощение не изменялось, в зависимости от концентрации ионов кальция. Напротив, для GEB0100, GEB0220 и GEB0230 поглощение было значительно более низким при концентрации ионов кальция 3 мкМ (низкая концентрация ионов кальция), чем при 1,2 мМ (высокая концентрация ионов кальция). Результат, описанный выше, демонстрирует, что GEB0100, GEB0220 и GEB0230 имеет свойства варьирования связывания антигена в зависимости от концентрации ионов кальция. Это указывает на то, что кальций-зависимые антитела против IgE человека также могут быть получены. По сравнению с типичными антителами против IgE человека, такими как Xolair, считается, что кальций-зависимые антитела против IgE человека могут ускорять элиминацию IgE человека аналогично случаю с IL-6R человека, CD4 человека или IgA человека, описанных в примерах выше. Более того, считается, что элиминация IgE человека может быть далее ускорена путем усиления связывания FcRn кальций-зависимых антител против IgE человека при pH 7,4.
[Справочный пример 1] Получение растворимого рецептора IL-6 человека (hsIL-6R)
Рекомбинантный рецептор IL-6 человека в качестве антигена получали следующим образом. Получали клеточную линию CHO, конститутивно экспрессирующую растворимый рецептор IL-6 человека (далее обозначаемый как hsIL-6R), имеющий аминокислотную последовательность из положений с 1 по 357 с N-конца, как описано в J. Immunol. 152: 4958-4968 (1994), способом, известным специалистам в данной области. Клетки культивировали для экспрессии hsIL-6R. hsIL-6R очищали из культурального супернатанта с помощью двух стадий: колоночная хроматография на Blue Sepharose 6 FF и гель-фильтрационная колоночная хроматография. Фракцию, элюированную в качестве главного пика на последней стадии, получали в качестве конечного продукта очистки.
[Справочный пример 2] Получение FcRn человека
FcRn представляет собой комплекс FcRn и β2-микроглобулина. Олиго-ДНК-праймеры получали на основе опубликованной последовательности гена FcRn человека (J Exp Med. 1994 Dec 1; 180(6): 2377-81). Фрагмент ДНК, кодирующий целый ген, получали способом ПЦР с использованием кДНК человека (Human Placenta Marathon-Ready cDNA, Clontech) в качестве матрицы и полученных праймеров. С использованием полученного фрагмента ДНК в качестве матрицы, фрагмент ДНК, кодирующий внеклеточный домен, содержащий сигнальную область (Met1-Leu290), амплифицировали способом ПЦР и встраивали в экспрессирующий вектор клеток млекопитающих. Аналогично, олиго-ДНК праймеры получали на основе опубликованной последовательности гена β2-микроглобулина человека (Proc. Natl. Acad. Sci. U.S.A. 99 (26): 16899-16903 (2002)). Фрагмент ДНК, кодирующий целый ген, получали способом ПЦР с использованием кДНК человека (Human Placenta Marathon-Ready cDNA, Clontech) в качестве матрицы и полученных праймеров. С использованием полученного фрагмента ДНК в качестве матрицы, фрагмент ДНК, кодирующий целый белок, содержащий сигнальную область (Met1-Met119) амплифицировали способом ПЦР и встраивали в экспрессирующий вектор клеток млекопитающих.
Растворимый FcRn человека экспрессировали по следующей методике. Плазмиды, сконструированные для экспрессии FcRn человека (SEQ ID NO: 17) и β2-микроглобулина (SEQ ID NO: 18), вводили в клетки клеточной линии, происходящей из рака почки эмбриона человека HEK293H (Invitrogen), способом липофекции с использованием PEI (Polyscience). Полученный культуральный супернатант собирали, и FcRn очищали с использованием IgG Sepharose 6 Fast Flow (Amersham Biosciences), а затем проводили дальнейшую очистку с использованием HiTrap Q HP (GE Healthcare) (J Immunol. 2002 Nov 1; 169(9): 5171-80).
[Справочный пример 3] Исследования по улучшению эффекта pH-зависимых антигенсвязывающих антител в отношении ускорения элиминации антигена (исследование in vivo)
(3-1) Получение антител с pH-зависимым связыванием рецептора IL-6 человека, которые связываются с FcRn в нейтральных условиях
Мутации вносили в Fv4-IgG1, содержащий VH3-IgG1 (SEQ ID NO: 19) и VL3-CK (SEQ ID NO: 20), для усиления связывания FcRn в нейтральных условиях (pH 7,4). В частности, VH3-IgG1-v1 (SEQ ID NO: 21) получали из константной области тяжелой цепи IgG1 путем замены Met на Tyr в положении 252, Ser на Thr в положении 254, и Thr на Glu в положении 256 согласно нумерации EU, в то время как VH3-IgG1-v2 (SEQ ID NO: 22) конструировали из константной области тяжелой цепи IgG1 путем замены Asn на Trp в положении 434 согласно нумерации EU. Мутанты конструировали путем аминокислотной замены с использованием набора для сайт-направленного мутагенеза QuikChange Site-Directed Mutagenesis Kit (Stratagene) или набора In-Fusion HD Cloning Kit (Clontech) в соответствии со способом, описанным в инструкциях. Полученные плазмидные фрагменты встраивали в экспрессирующие векторы клеток животных для конструирования экспрессирующих векторов для представляющей интерес H-цепи и L-цепи. Нуклеотидные последовательности сконструированных экспрессирующих векторов определяли способом, известным специалистам в данной области.
H54/L28-IgG1, содержащее H54 (SEQ ID NO: 5) и L28 (SEQ ID NO: 6), Fv4-IgG1, содержащее VH3-IgG1 (SEQ ID NO: 19) и VL3-CK (SEQ ID NO: 20), Fv4-IgG1-v1, содержащее VH3-IgG1-v1 (SEQ ID NO: 21) и VL3-CK (SEQ ID NO: 20), и Fv4-IgG1-v2, содержащее VH3-IgG1-v2 (SEQ ID NO: 22) и VL3-CK (SEQ ID NO: 20), экспрессировали и очищали способом, описанным ниже. Антитела экспрессировали с помощью FreestyleHEK293 (Invitrogen), как описано в протоколе, предоставленном изготовителем, или клеточной линии HEK293H (Invitrogen). Клетки клеточной линии, происходящей из рака почки эмбриона человека HEK293H (Invitrogen) суспендировали в DMEM (Invitrogen), дополненной 10% эмбриональной телячьей сывороткой (Invitrogen). Клетки высевали в количестве 10 мл на чашку в чашки для не прикрепляющихся клеток (диаметром 10 см; CORNING) с плотностью клеток 5-6 × 105 клеток/мл и культивировали в CO2-инкубаторе (37°C, 5% CO2) в течение всего дня и ночи. Затем среду удаляли аспирированием и добавляли 6,9 мл среды CHO-S-SFM-II (Invitrogen). Полученную плазмиду вводили в клетки способом липофекции. Полученные культуральные супернатанты собирали, центрифугировали (приблизительно 2000×g, 5 мин, комнатная температура) для удаления клеток и стерилизовали фильтрацией через 0,22-мкм фильтр MILLEX (зарегистрированный торговый знак)-GV (Millipore) с получением супернатантов. Антитела очищали из очищенных культуральных супернатантов способом, известным специалистам в данной области, с использованием rProtein A SepharoseTM Fast Flow (Amersham Biosciences). Для определения концентрации очищенного антитела измеряли поглощение при 280 нм с использованием спектрофотометра. Из определенных величин вычисляли концентрации антител с использованием коэффициента поглощения, вычисленного способом, описанным в Protein Science (1995) 4: 2411-2423.
(3-2) Исследование in vivo с использованием трансгенных мышей с FcRn человека и нормальных мышей
Кинетику in vivo hsIL-6R (растворимый рецептор IL-6 человека: получен, как описано в справочном примере 3) и антитела против рецептора IL-6 человека оценивали после введения трансгенным мышам с FcRn человека (B6.mFcRn-/-.hFcRn Tg линия 276 +/+ мышь, Jackson Laboratories; Methods Mol Biol. (2010) 602: 93-104) и нормальным мышам (мыши C57BL/6J; Charles River Japan) hsIL-6R по отдельности или hsIL-6R и антитела против рецептора IL-6 человека в комбинации. Раствор hsIL-6R (5 мкг/мл) или раствор смеси, содержавший hsIL-6R и антитела против рецептора IL-6 человека (5 мкг/мл и 0,1 мг/мл, соответственно), вводили один раз в дозе 10 мл/кг в хвостовую вену. В этом случае, антитела против рецептора IL-6 человека представлены в избытке над hsIL-6R, и таким образом, предполагается, что почти каждый hsIL-6R связываются с антителом. Кровь собирали через 15 минут, семь часов, одни сутки, двое суток, трое суток, четверо суток, семь суток, 14 суток, 21 сутки и 28 суток после введения. Собранную кровь немедленно центрифугировали при 15000 об/мин и 4°C в течение 15 минут для отделения плазмы. Отделенную плазму хранили в холодильнике при -20°C или ниже перед выполнением анализа. Используемые антитела против рецептора IL-6 человека представляют собой: описанные выше H54/L28-IgG1, Fv4-IgG1 и Fv4-IgG1-v2 для трансгенных мышей с FcRn человека и описанные выше H54/L28-IgG1, Fv4-IgG1, Fv4-IgG1-v1 и Fv4-IgG1-v2 для нормальных мышей.
(3-3) Измерение концентрации антител против рецептора IL-6 человека в плазме с помощью ELISA
Концентрацию антитела против рецептора IL-6 человека в плазме мыши измеряли посредством ELISA. (Fab')2-фрагмент антитела против IgG человека (специфичного к γ-цепи) (Sigma) распределяли в Nunc-ImmunoPlate MaxiSorp (Nalge Nunc International) и оставляли в течение ночи при 4°C для получения планшетов с иммобилизованными антителами против IgG человека. Получали образцы для калибровочной кривой при концентрации плазме 0,8, 0,4, 0,2, 0,1, 0,05, 0,025 и 0,0125 мкг/мл, и образцы плазмы мыши, разведенные в 100 раз и более. 200 мкл hsIL-6R в концентрации 20 нг/мл добавляли к 100 мкл образцов для калибровочной кривой и образцам плазмы, а затем образцы оставляли в течение одного часа при комнатной температуре. Затем образцы переносили на планшеты с иммобилизованными антителами против IgG человека и оставляли в течение одного часа при комнатной температуре. Затем добавляли биотинилированное антитело против IL-6R человека (R&D) для реакции в течение одного часа при комнатной температуре. Затем добавляли стрептавидин-PolyHRP80 (Stereospecific Detection Technologies) для реакции в течение одного часа при комнатной температуре, и хромогенную реакцию проводили с использованием в качестве субстрата TMP One Component HRP Microwell Substrate (BioFX Laboratories). После остановки реакции 1 н. серной кислотой (Showa Chemical), поглощение при 450 нм измеряли с помощью устройства для считывания микропланшетов. Концентрацию в плазме мыши рассчитывали из оптической плотности калибровочной кривой, используя аналитическое программное обеспечение SOFTmax PRO (Molecular Devices). Концентрации в плазме после внутривенного введения с течением времени, измеренные этим способом, представлены на фиг.31 для трансгенных мышей с FcRn человека и на фиг.33 для нормальных мышей.
(3-4) Измерение концентрации hsIL-6R в плазме с помощью электрохемилюминесцентного анализа
Концентрацию hsIL-6R в плазме мыши измеряли посредством электрохемилюминисценции. Получали образцы калибровочной кривой hsIL-6R, доведенные до концентрации 2000, 1000, 500, 250, 125, 62,5 и 31,25 пг/мл, и образцы плазмы мыши, разведенные в 50 раз или более. Образцы смешивали с раствором моноклонального антитела против IL-6R (R&D), меченного рутением, c SULFO-TAG NHS Ester (Meso Scale Discovery), биотинилированного антитела против IL-6R человека (R&D) и WT-IgG1, а затем оставляли для реакции в течение ночи при 37°C. Конечная концентрация WT-IgG1 в качестве антитела против рецептора IL-6 человека, содержащего H (WT) (SEQ ID NO: 13) и L (WT) (SEQ ID NO: 14), составила 333 мкг/мл, что является больше концентрации антитела против рецептора IL-6 человека, содержащегося в образцах, с целью связывания практически всех молекул hsIL-6R в образцах с WT-IgG1. Затем образцы переносили в планшет со стрептавидином MA400 PR (Meso Scale Discovery) и оставляли для реакции в течение одного часа при комнатной температуре, и проводили промывание. Сразу после добавления буфера для считывания T (×4) (Meso Scale Discovery) проводили измерения посредством Sector PR 400 Reader (Meso Scale Discovery). Концентрацию hsIL-6R вычисляли, основываясь на данных калибровочной кривой, используя аналитическое программное обеспечение SOFTmax PRO (Molecular Devices). Концентрация hsIL-6R в плазме с течением времени после внутривенного введения, как измерено в этом способе, представлена на фиг.32 для трансгенных мышей с FcRn человека и на фиг.34 для нормальных мышей.
(3-5) Определение концентрации свободного hsIL-6R в плазме с помощью электрохемилюминесцентного анализа
Для оценки степени нейтрализации растворимого рецептора IL-6 человека в плазме, концентрацию растворимого рецептора IL-6 человека, свободного от (не нейтрализованного посредством) антитела против рецептора IL-6 человека (концентрация свободного hsIL-6R) в плазме мыши, определяли электрохемилюминесцентным анализом. Все антитела типа IgG (IgG мыши, антитела против рецептора IL-6 человека и комплекс антитело против рецептора IL-6 человека-растворимый рецептор IL-6 человека) в плазме адсорбировали на белке A путем добавления 12 мкл каждого стандартного образца hsIL-6R, полученного из расчета 10000, 5000, 2500, 1250, 625, 312,5 или 156,25 пг/мл, и образцов плазмы мыши на соответствующее количество смолы rProtein A Sepharose Fast Flow (GE Healthcare), высушенной на 0,22-мкм чашке фильтра (Millipore). Затем, раствор в чашке осаждали с использованием высокоскоростной центрифуги для сбора раствора, который пропускали через смолу. Пропущенный через смолу раствор не содержал связанный с белком A комплекс антитело против рецептора IL-6 человека-растворимый рецептор IL-6 человека. Таким образом, концентрацию свободного hsIL-6R в плазме можно было определять, измеряя концентрацию hsIL-6R в пропущенном через смолу растворе. Затем пропущенный через смолу раствор смешивали с моноклональным антителом против IL-6R человека (R&D), меченным рутением, с Sulfo-Tag NHS Ester (Meso Scale Discovery) и биотинилированным антителом против IL-6R человека (R&D). Полученную в результате смесь инкубировали при комнатной температуре в течение одного часа, а затем добавляли на планшет со стрептавидином MA400 PR, разделяя на аликвоты (Meso Scale Discovery). После инкубации в течение одного часа при комнатной температуре планшет промывали и также в него распределяли аликвоты буфера для считывания T (×4) (Meso Scale Discovery). Результаты реакции на планшете сразу измеряли в устройстве для считывания планшетов SECTOR PR 400 Reader (Meso Scale Discovery). Концентрацию hsIL-6R рассчитывали, основываясь на данных в стандартной кривой с использованием анализа на программном обеспечении SOFTmax PRO (Molecular Devices). Концентрации свободного hsIL-6R в плазме нормальных мышей с течением времени после внутривенного введения определяли описанным выше способом, как показано на фиг.35.
(3-6) Эффект рН-зависимого связывания с рецептором IL-6 человека
H54/L28-IgG1 и Fv4-IgG1, которые связываются с рецептором IL-6 человека рН-зависимым образом, исследовали in vivo, и результаты сравнивали друг с другом. Как показано на фиг.31 и 33, удержание антитела в плазме было сравнимым. Между тем, как показано на фиг.32 и 34, hsIL-6R, введенный одновременно с Fv4-IgG1, который связывается с рецептором IL-6 человека рН-зависимым образом, как обнаружили, увеличивает элиминацию hsIL-6R по сравнению с hsIL-6R, введенным одновременно с H54/L28-IgG1. Тенденцию, описанную выше, наблюдали как для трансгенных мышей с FcRn человека, так и для нормальных мышей; таким образом, показано, что посредством сообщения способности рН-зависимого связывания с рецептором IL-6 человека, концентрация hsIL-6R в плазме через четверо суток после введения может быть снижена приблизительно в 17 и 34 раза, соответственно.
(3-7) Эффект связывания с FcRn в нейтральных условиях (pH 7,4)
Сообщалось, что природный IgG1 человека плохо связывался с FcRn человека (обладает очень низкой аффиностью связывания) в нейтральных условиях (pH 7,4). Связывание с FcRn человека в нейтральных условиях (pH 7,4), как сообщают, увеличивается при замене Asn на Trp в положении 434 (нумерация EU) в природном IgG1 человека (J Immunol. (2009) 182 (12): 7663-71). Fv4-IgG1-v2, полученный в результате внесения указанной выше аминокислотной замены в Fv4-IgG1, исследовали с помощью исследования in vivo с использованием трансгенных мышей с FcRn человека. Результаты исследования сравнивали с результатами, полученными для Fv4-IgG1. Как показано на фиг.31, время удержания антител являлось сравнимым между двумя антителами. Между тем, как показано на фиг.32, обнаружено, что hsIL-6R, введенный одновременно с Fv4-IgG1-v2, которое проявляет повышенное связывание с FcRn человека в нейтральных условиях (pH 7,4), элиминируется быстрее по сравнению с hsIL-6R, введенным одновременно с Fv4-IgG1. Таким образом, показано, что посредством сообщения способности связываться с FcRn человека в нейтральных условиях (pH 7,4), концентрация в плазме hsIL-6R через четверо суток после введения может быть снижена приблизительно в четыре раза.
Основываясь на гомологии между FcRn человека и FcRn мыши, полагают, что замена Asn на Trp в положении 434 согласно нумерации EU увеличивает связывание с FcRn мыши в нейтральных условиях (pH 7,4). Между тем, связывание с FcRn мыши в нейтральных условиях (pH 7,4), как сообщалось, увеличивается при замене Met на Tyr в положении 252, Ser на Thr в положении 254 и Thr на Glu в положении 256 согласно нумерации EU (J Immunol. (2002) 169(9): 5171-80). Fv4-IgG1-v1 и Fv4-IgG1-v2, которые получены в результате внесения описанных выше аминокислотных замен в Fv4-IgG1, исследовали in vivo, используя нормальных мышей. Результаты исследования сравнивали с результатами, полученными для Fv4-IgG1. Как показано на фиг.33, время удержания в плазме Fv4-IgG1-v1 и Fv4-IgG1-v2, которые усовершенствовали для увеличения связывания с FcRn мыши в нейтральных условиях (pH 7,4), являлось немного укороченным (концентрации в плазме нейтрализующего антитела через одни сутки после введения снижалась приблизительно в 1,5 и 1,9 раза, соответственно) по сравнению с Fv4-IgG1.
Как показано на фиг.34, было показано, что hsIL-6R, введенный одновременно с Fv4-IgG1-v1 или Fv4-IgG1-v2, которые были усовершенствованы для увеличения связывания с FcRn мыши в нейтральных условиях (pH 7,4), элиминируется явно быстрее по сравнению с hsIL-6R, введенным одновременно с Fv4-IgG1. Fv4-IgG1-v1 и Fv4-IgG1-v2 снижали концентрацию hsIL-6R в плазме через одни сутки после введения приблизительно в 32 и 80 раз, соответственно. Таким образом, выявили, что концентрацию в плазме можно снижать путем сообщения способности связывания с FcRn мыши в нейтральных условиях (pH 7,4). Как описано выше, путем сообщения способности связывания с FcRn мыши в нейтральных условиях (pH 7,4), концентрация антитела в плазме немного снижалась; однако был достигнут эффект снижения концентрации hsIL-6R в плазме, который в значительной степени превосходил снижение концентрации антитела. Кроме того, обнаружили, что hsIL-6R, введенный одновременно с Fv4-IgG1-v1 или Fv4-IgG1-v2, элиминируется даже быстрее по сравнению с группой, в которой hsIL-6R вводили отдельно. Как показано на фиг.34, hsIL-6R, введенный одновременно с Fv4-IgG1-v1 или Fv4-IgG1-v2, может снижать концентрацию hsIL-6R в плазме через одни сутки после введения приблизительно в 4 или 11 раз, соответственно, по сравнению с hsIL-6R отдельно. Конкретно, это означает, что элиминация растворимого рецептора IL-6 может быть ускорена посредством введения антитела, которое связывается с растворимым рецептором IL-6 рН-зависимым образом и которому сообщили способность связывания с FcRn мыши в нейтральных условиях (pH 7,4). Конкретно, концентрацию антигена в плазме можно снижать in vivo посредством введения такого антитела в организм.
Как показано на фиг.35, свободный hsIL-6R был представлен в диапазоне поддающейся детекции концентрации в течение семи суток после введения H54/L28-IgG1, в то время как hsIL-6R являлся неопределяемым через одни сутки после введения Fv4-IgG1. С другой стороны, свободный hsIL-6R являлся неопределяемым через семь часов после введения Fv4-IgG1-v1 или Fv4-IgG1-v2. Конкретно, концентрация свободного hsIL-6R была более низкой в присутствии Fv4-IgG1, который связывается с hsIL-6R рН-зависимым образом, по сравнению с H54/L28-IgG1, что предполагает более сильный нейтрализующий эффект hsIL-6R, которого достигают посредством обеспечения рН-зависимого связывания с hsIL-6R. Кроме того, свободная концентрация hsIL-6R была более низкой в присутствии Fv4-IgG1-v1 или Fv4-IgG1-v2, оба из которых были модифицированы из Fv4-IgG1 для повышения способности связывания с FcRn при pH 7,4. Это демонстрирует, что путем увеличения активности связывания с FcRn при pH 7,4 можно достигать более сильного нейтрализующего эффекта hsIL-6R.
При введении обычное нейтрализующее антитело, такое как H54/L28-IgG1, снижает клиренс связанного антигена, что приводит к пролонгированному времени удержания антигена в плазме. Не является предпочтительным, чтобы введенные антитела пролонгировали время удержания антигена, действие которого должно быть нейтрализовано антителами. Время удержания антигена в плазме можно укорачивать посредством сообщения связыванию антигена зависимости от pH (антитело связывается в нейтральных условиях, но подвергается диссоциации в кислых условиях). В рамках настоящего изобретения время удержания антигена в плазме можно было дополнительно укоротить путем дополнительного сообщения способности связывания с FcRn человека в нейтральных условиях (pH 7,4). Кроме того, показано, что, по сравнению с клиренсом антигена отдельно, клиренс антигена можно было увеличивать путем введения антитела, которое связывается с антигеном рН-зависимым образом и которому сообщена способность связывания с FcRn в нейтральных условиях (pH 7,4). В настоящее время, не существует способа, пригодного для увеличения клиренса антигена путем введения антитела, относительно клиренса антигена отдельно. Таким образом, способы, осуществленные, как описано в настоящем примере, являются в высокой степени полезными в качестве способа элиминации антигенов из плазмы путем введения антител. Кроме того, авторы настоящего изобретения первыми открыли преимущество увеличения способности связывания с FcRn в нейтральных условиях (pH 7,4). Кроме того, и v4-IgG1-v1 и Fv4-IgG1-v2, которые имеют различные аминокислотные замены, увеличивающие способность связывания с FcRn в нейтральных условиях (pH 7,4), производили сравнимый эффект. Это позволяет предположить, что, несмотря на тип аминокислотных замен, каждая аминокислотная замена, которая увеличивает способность связывания с FcRn человека в нейтральных условиях (pH 7,4), потенциально обладает эффектом, увеличивающим элиминацию антигена. Конкретно, молекулы антитител, которые при введении элиминируют антигены из плазмы, можно получать, используя следующие аминокислотные замены как в отдельности, так и в комбинации:
замена аминокислоты Pro на Ile в положении 257 и замена аминокислоты Gln на Ile в положении 311 согласно нумерации EU, каждая из которых описана в J Biol Chem. 2007, 282(3): 1709-17; замена аминокислоты Asn на Ala, Tyr или Trp в положении 434, замена аминокислоты Met на Tyr в положении 252, замена аминокислоты Thr на Gln в положении 307, замена аминокислоты Val на Pro в положении 308, замена аминокислоты Thr на Gln в положении 250, замена аминокислоты Met на Leu в положении 428, замена аминокислоты Glu на Ala в положении 380, замена аминокислоты Ala на Val в положении 378, замена аминокислоты Tyr на Ile в положении 436 согласно нумерации EU, каждая из которых описана в J Immunol. (2009) 182(12): 7663-71; замена аминокислоты Met на Tyr в положении 252, замена аминокислоты Ser на Thr в положении 254, замена аминокислоты Thr на Glu в положении 256 согласно нумерации EU, каждая из которых описана в J Biol Chem. 2006 Aug. 18, 281(33): 23514-24; замена аминокислоты His на Lys в положении 433, замена аминокислоты Asn на Phe в положении 434, и замена аминокислоты Tyr на His в положении 436 согласно нумерации EU, каждая из которых описана в Nat Biotechnol. 2005 октября 23(10): 1283-8; и т.п.
[Справочный пример 4] Оценка активности связывания с FcRn человека
Для системы анализа, основанной на Biacore для исследования взаимодействия между антителом и FcRn, система, в которой антитело иммобилизовано на сенсорном чипе и используется FcRn человека в качестве анализируемого соединения, описана J Immunol. (2009) 182(12): 7663-71. Для этой цели, FcRn человека получали, как описано в справочном примере 2. Fv4-IgG1, Fv4-IgG1-v1 и Fv4-IgG1-v2 оценивали в отношении активности связывания с FcRn человека (константа диссоциации (KD)) при pH 6,0 и pH 7,4 с использованием описанной выше системы. Антитела исследовали в качестве исследуемого соединения после прямой иммобилизации на сенсорный чип Series S CM5. С использованием набора для присоединения аминов по инструкции изготовителя, антитела иммобилизовали на сенсорном чипе так, чтобы обеспечить величину иммобилизации 500 RU. Используемый подвижный буфер представлял собой 50 ммоль/л Na-фосфат/150 ммоль/л NaCl, содержащий 0,05% (об./об.%) поверхностно-активного вещества P20 (pH 6,0).
С помощью полученных сенсорных чипов, проводили анализ с использованием в качестве подвижного буфера, 50 ммоль/л Na-фосфат/150 ммоль/л NaCl, содержащего 0,05% поверхностно-активного вещества P20 (pH 6,0), или 50 ммоль/л Na-фосфат/150 ммоль/л NaCl, содержащего 0,05% поверхностно-активного вещества P20 (pH 7,4). Анализы проводили исключительно при 25°C. Разбавленные растворы FcRn человека и подвижный буфер в качестве контрольного раствора инжектировали со скоростью потока 5 мкл/мин в течение десяти минут для обеспечения взаимодействия FcRn человека с антителом на чипе. Затем инжектировали подвижный буфер со скоростью потока 5 мкл/мин в течение одной минуты для контроля диссоциации FcRn. Затем сенсорный чип регенерировали посредством двух раундов инжектирования 20 ммоль/л Tris-HCl/150 ммоль/л NaCl (pH 8,1) при скорости потока 30 микролитров/мин в течение 15 секунд.
Результаты анализа анализировали с использованием программного обеспечения Biacore T100 Evaluation (Ver. 2.0.1). С помощью аффинного способа стационарного состояния рассчитывали константу диссоциации (KD) из анализа результатов при шести различных концентрациях FcRn. Результаты активности связывания с FcRn человека (константы диссоциации (KD)) Fv4-IgG1, Fv4-IgG1-v1 и Fv4-IgG1-v2 при pH 6,0 и pH 7,4 представлены в таблице 24 ниже.
При pH 7,4, связывание FcRn человека с Fv4-IgG1 было слишком слабым для определения значения KD (NA). Между тем наблюдали, что Fv4-IgG1-v1 и Fv4-IgG1-v2 связывается с FcRn человека при pH 7,4, и было определено, что значение KD составляет 36,55 и 11,03 мкМ, соответственно. Было определено, что значения KD для FcRn человека при pH 6,0 составляют 1,99, 0,32 и 0,11 мкМ. Как показано на фиг.31, при сравнении с Fv4-IgG1, Fv4-IgG1-v2 усиливалась элиминация hsIL-6R у трансгенных мышей с FcRn человека. Таким образом, можно прогнозировать, что элиминация антигена будет ускоряться путем усиления связывания с FcRn человека при pH 7,4, по меньшей мере так, чтобы она была более высокой, чем 11,03 мкМ, посредством изменения IgG1 человека. Между тем, как описано в J Immunol. (2002) 169(9): 5171-80, IgG1 человека связывается приблизительно в десять раз сильнее с FcRn мыши, чем с FcRn человека. По этой причине, Fv4-IgG1-v1 и Fv4-IgG1-v2, как прогнозируют, тоже будет связываться приблизительно в десять раз более сильно с FcRn мыши, чем FcR человека, при pH 7,4. Ускорение элиминации hsIL-6R посредством Fv4-IgG1-v1 или Fv4-IgG1-v2 у нормальной мыши, показанное на фиг.34, является более значимым, чем ускорение элиминации посредством Fv4-IgG1-v2 у трасгенных мышей с FcRn человека, показанное на фиг.32. Это позволяют предположить, что степень ускорения элиминации hsIL-6R увеличивается, в зависимости от силы связывания с FcRn при pH 7,4.
[Справочный пример 5] Получение рН-зависимых антител, связывающих рецептор IL-6 человека, с увеличенным связыванием FcRn человека в нейтральных условиях
(5-1) Получение мутантов константной области тяжелой цепи Fv4-IgG1
Различные изменения для увеличения связывания с FcRn человека в нейтральных условиях вносили в Fv4-IgG1 для дополнительного увеличения эффекта рН-зависимых антител, связывающих рецептор IL-6 человека, в отношении элиминации антигена у трасгенных мышей с FcRn человека. Конкретно, аминокислотные изменения, представленные в таблицах 25-1 и 25-2, вносили в константную область тяжелой цепи Fv4-IgG1 для получения различных мутантов (номера аминокислот участков мутаций представлено согласно нумерации EU). Аминокислотные замены вносили способами, известными специалистам в данной области, как описано в справочном примере 3.
Таблица 25-2 является продолжением таблицы 25-1.
Каждый вариант, содержащий полученную тяжелую цепь и L (WT) (SEQ ID NO: 14) экспрессировали и очищали способами, известными специалистам в данной области, как описано в справочном примере 3.
(5-2) Оценка связывания с FcRn человека
Связывание между антителом и FcRn человека анализировали кинетически с использованием Biacore T100 (GE Healthcare). Для этой цели FcRn человека получали, как описано в справочном примере 2. Достаточное количество белка L (ACTIGEN) иммобилизовали на сенсорном чипе CM4 (GE Healthcare) посредством способа присоединения аминов, и обеспечивали улавливание на чипе представляющих интерес антител. Затем, разбавленные растворы FcRn и подвижный буфер (в качестве контрольного раствора) инжектировали для обеспечения взаимодействия FcRn человека с антителом, уловленном на сенсорным чипе. Используемый подвижный буфер содержал 50 ммоль/л фосфат натрия, 150 ммоль/л NaCl и 0,05% (масс./об.) Tween20 (pH 7,0). FcRn разбавляли с использованием каждого буфера. Чип регенерировали с использованием 10 ммоль/л глицина-HCl (pH 1,5). Анализы проводили исключительно при 25°C. Константу скорости ассоциации ka (1/Мс) и константу скорости диссоциации kd (1/с), каждая из которых представляет собой кинетические параметры, рассчитывали, основываясь на сенсограммах, полученных в анализах, и из этих значений определяли KD (M) каждого антитела для FcRn человека. Каждый параметр рассчитывали с использованием программного обеспечения Biacore T100 Evaluation (GE Healthcare).
Результат оценки связывания FcRn человека в нейтральных условиях (pH 7,0) посредством Biacore представлен в таблицах 6-1 и 6-2. KD природного IgG1 невозможно было рассчитать, так как оно продемонстрировало только очень слабое связывание. Таким образом, KD представлено как ND в таблице 6-1.
[Справочный пример 6] Исследование in vivo рН-зависимых антител, связывающих рецептор IL-6 человека, с усиленным связыванием FcRn человека в нейтральных условиях
Зависимые от рН антитела, связывающие рецептор IL-6 человека, обладающие способностью связывания FcRn человека в нейтральных условиях, получали с использованием тяжелых цепей, полученных, как описано в справочном примере 4, для сообщения способности связывания с FcRn человека в нейтральных условиях. Антитела оценивали в отношении их эффекта элиминации антигена in vivo. Конкретно, антитела, перечисленные ниже, экспрессировали и очищали способами, известными специалистам в данной области, как описано в справочном примере 3:
Fv4-IgG1, содержащее VH3-IgG1 и VL3-CK;
Fv4-IgG1-v2, содержащее VH3-IgG1-v2 и VL3-CK;
Fv4-IgG1-F14, содержащее VH3-IgG1-F14 и VL3-CK;
Fv4-IgG1-F20, содержащее VH3-IgG1-F20 и VL3-CK;
Fv4-IgG1-F21, содержащее VH3-IgG1-F21 и VL3-CK;
Fv4-IgG1-F25, содержащее VH3-IgG1-F25 и VL3-CK;
Fv4-IgG1-F29, содержащее VH3-IgG1-F29 и VL3-CK;
Fv4-IgG1-F35, содержащее VH3-IgG1-F35 и VL3-CK;
Fv4-IgG1-F48, содержащее VH3-IgG1-F48 и VL3-CK;
Fv4-IgG1-F93, содержащее VH3-IgG1-F93 и VL3-CK; и
Fv4-IgG1-F94, содержащее VH3-IgG1-F94 и VL3-CK.
С помощью таких же способов, как описано в справочном примере 3, полученные зависимые от рН антитела, связывающие рецептор IL-6 человека, исследовали in vivo с использованием трансгенных мышей с FcRn человека (B6.mFcRn-/-.hFcRn Tg линия 276 +/+ мышь, Jackson Laboratories; Methods Mol Biol. (2010) 602: 93-104).
Концентрации в плазме растворимого рецептора IL-6 человека с течением времени после внутривенного введения трансгенным мышам с FcRn человека представлена на фиг.36. Результаты исследования показали, что концентрация в плазме растворимого рецептора IL-6 человека поддерживалась на низком уровне с течением времени в присутствии любого из рН-зависимых антител, связывающих рецептор IL-6 человека, с увеличенным связыванием FcRn человека в нейтральных условиях, по сравнению со связыванием в присутствии Fv4-IgG1, которое почти не обладает способностью связывания с FcRn человека в нейтральных условиях. Среди прочих, антитела, которые проявляли заметный эффект, включают, например, Fv4-IgG1-F14. Было показано, что концентрация в плазме растворимого рецептора IL-6 человека, введенного одновременно с Fv4-IgG1-F14, снизилась приблизительно в 54 раза через одни сутки после введения по сравнению с концентрацией растворимого рецептора IL-6 человека, введенного одновременно с Fv4-IgG1. Кроме того, было показано, что концентрация в плазме растворимого рецептора IL-6 человека, введенного одновременно с Fv4-IgG1-F21, снизилась приблизительно в 24 раза через семь часов после введения по сравнению с концентрацией растворимого рецептора IL-6 человека, введенного одновременно с Fv4-IgG1. Кроме того, концентрация в плазме растворимого рецептора IL-6 человека, введенного одновременно с Fv4-IgG1-F25 через семь часов после введения, была ниже предела выявления (1,56 нг/мл). Таким образом, ожидалось, что Fv4-IgG1-F25 обеспечит значительное снижение, составляющее 200 или более раз, концентрации растворимого рецептора IL-6 человека относительно концентрации растворимого рецептора IL-6 человека, введенного одновременно с Fv4-IgG1. Полученные результаты, описанные выше, продемонстрировали, что увеличение связывания с FcRn человека антител с pH-зависимым связыванием антигена в нейтральных условиях является высокоэффективным для усиления эффекта элиминации антигена. Между тем, тип аминокислотных изменений для усиления связывания FcRn человека в нейтральных условиях, которые вносят для усиления эффекта элиминации антигена, конкретно не ограничен; и такие изменения включают изменения, которые представлены в таблицах 6-1 и 6-2. Усиление эффекта элиминации антигена in vivo можно предсказать с помощью любого внесенного изменения.
Более того, концентрация в плазме растворимого рецептора IL-6 человека, введенного одновременно с одним из четырех типов зависимых от рН антител, связывающих рецептор IL-6 человека, Fv4-IgG1-F14, Fv4-IgG1-F21, Fv4-IgG1-F25 и Fv4-IgG1-F48, сохранялась на более низком уровне в течение времени, чем концентрация растворимого рецептора IL-6 человека, введенного отдельно. Такие pH-зависимые антитела, связывающие рецептор IL-6 человека, можно вводить в организм, где концентрацию в плазме растворимого рецептора IL-6 человека поддерживают постоянной (стационарное состояние) для поддержания в плазме концентрации растворимого рецептора IL-6 человека на более низком уровне, чем стационарная концентрация в плазме. Конкретно, концентрацию антигена в плазме in vivo можно снижать путем введения такого антитела в организм.
[Справочный пример 7] Оценка эффективности низких доз (0,01 мг/кг) Fv4-IgG1-F14
Fv4-IgG1-F14, полученный, как описано в справочном примере 6, исследовали в низких дозах (0,01 мг/кг) с помощью такого же способа исследования in vivo, как описано в справочном примере 6. Результаты (представленные на фиг.37 и 38) сравнивали с результатами, описанными в справочном примере 6, которые получали путем введения Fv4-IgG1 и Fv4-IgG1-F14 при 1 мг/кг.
Результаты продемонстрировали, что, хотя концентрация антитела в плазме в группе, в которой вводили Fv4-IgG1-F14 в концентрации 0,01 мг/кг, являлась приблизительно в 100 раз более низкой по сравнению с группой, в которой вводили 1 мг/кг (фиг.38), показатели концентрации в плазме растворимого рецептора IL-6 человека с течением времени были сравнимыми друг с другом (фиг.37). Кроме того, показано, что концентрация в плазме растворимого рецептора IL-6 человека через семь часов после введения в группе, в которой вводили Fv4-IgG1-F14 из расчета 0,01 мг/кг, снижалась приблизительно в три раза по сравнению с концентрацией в группе, в которой вводили Fv4-IgG1 из расчета 1 мг/кг. Кроме того, в присутствии Fv4-IgG1-F14 концентрация в плазме растворимого рецептора IL-6 человека, который вводили в различных дозах, была более низкой с течением времени в обеих группах, по сравнению с группой, в которой вводили растворимый рецептор IL-6 человека отдельно (фиг.37).
Результаты демонстрируют, что даже при введении в дозе, составляющей одну сотую от дозы Fv4-IgG1, Fv4-IgG1-F14, которое было получено в результате модификации Fv4-IgG1 для усиления связывания с FcRn человека в нейтральных условиях, эффективно снижает концентрацию в плазме растворимого рецептора IL-6 человека. В частности, предсказано, что антигены могут быть эффективно элиминированы даже при более низкой дозе, если антитела с pH-зависимым связыванием антитела модифицировать для усиления их способности связывания с FcRn в нейтральных условиях.
[Справочный пример 8] Исследование in vivo, основанное на стационарной модели с использованием нормальных мышей
(8-1) Оценка связывания с FcRn мыши в нейтральных условиях
VH3/L (WT)-IgG1, содержащее VH3-IgG1 (SEQ ID NO: 19) и L (WT) (SEQ ID NO: 14), VH3/L (WT)-IgG1-v2, содержащее VH3-IgG1-v2 (SEQ ID NO: 22) и L (WT) (SEQ ID NO: 14) и VH3/L (WT)-IgG1-F20, содержащее VH3-IgG1-F20 (SEQ ID NO: 23) и L (WT) (SEQ ID NO: 141), каждое из которых получали, как описано в справочном примере 5, оценивали в отношении связывания с FcRn мыши в нейтральных условиях (pH 7,4) с помощью способа, описанного ниже.
Связывание между антителом и FcRn мыши анализировали кинетически с использованием Biacore T100 (GE Healthcare). Подходящее количество белка L (ACTIGEN) иммобилизовали на сенсорном чипе CM4 (GE Healthcare) с помощью способа присоединения аминов, и обеспечивали улавливание на чипе представляющего интерес антигена. Затем инжектировали разбавленные растворы FcRn и подвижный буфер (в качестве контрольного раствора) для обеспечения взаимодействия FcRn мыши с антителом, уловленном на сенсорном чипе. Используемый подвижный буфер содержал 50 ммоль/л фосфата натрия, 150 ммоль/л NaCl и 0,05% (масс./об.) Tween 20 (pH 7,4). FcRn разбавляли с использованием каждого буфера. Чип подвергали регенерации с использованием 10 ммоль/л глицина-HCl (pH 1,5). Анализы проводили исключительно при 25°C. Константу скорости ассоциации ka (1/Mc) и константу скорости диссоциации kd (1/с), каждая из которых представляет собой кинетические параметры, рассчитывали, основываясь на сенсограммах, полученных в анализах, и из этих значений определяли KD (M) каждого антитела для FcRn мыши. Каждый параметр рассчитывали с использованием программного обеспечения Biacore T100 Evaluation (GE Healthcare).
Результаты представлены в таблице 26 (аффинность в отношении FcRn мыши при pH 7,4). VH3/L (WT)-IgG1 (IgG1 в таблице 26), константная область которого представляет собой константную область природного IgG1, проявлял только очень слабое связывание с FcRn мыши. Таким образом, KD было невозможно рассчитать, и она обозначена как ND в таблице 26. Анализ результатов показал, что измененные антитела с усиленным связыванием с FcRn человека в нейтральных условиях также продемонстрировали усиленное связывание с FcRn мыши в нейтральных условиях.
(8-2) Исследование in vivo с использованием нормальных мышей с постоянной концентрацией в плазме растворимого рецептора IL-6 человека
С использованием H54/L28-IgG1, Fv4-IgG1, Fv4-IgG1-v2 и Fv4-IgG1-F20, полученных, как описано в примере 3 и справочном примере 5, проводили исследование in vivo способом, описанным ниже.
Инфузионный насос (MINI-OSMOTIC PUMP MODEL 2004; alzet), содержавший растворимый рецептор IL-6 человека, имплантировали под кожу спины нормальных мышей (мыши C57BL/6J; Charles River Japan) для получения модели на животных, где концентрация в плазме растворимого рецептора IL-6 человека поддерживается постоянной. Антитела против рецептора IL-6 человека вводили модельным животным для оценки кинетики in vivo после введения растворимого рецептора IL-6 человека. Моноклональное антитело против CD4 мыши (R&D) вводили в количестве 20 мг/кг один раз в хвостовую вену для подавления продукции нейтрализующего антитела против растворимого рецептора IL-6 человека. Затем, инфузионный насос, содержавший 92,8 мкг/мл растворимого рецептора IL-6 человека, имплантировали под кожу спины мыши. Через трое суток после имплантации инфузионного насоса, антитела против рецептора IL-6 человека вводили в количестве 1 мг/кг один раз в хвостовую вену. Кровь собирали через 15 минут, семь часов, одни сутки, двое суток, трое суток, четверо суток, семь суток, 14 суток, 21 сутки и через 28 суток после введения антитела против рецептора IL-6 человека. Собранную кровь немедленно центрифугировали при 15000 об/мин и 4°C в течение 15 минут для отделения плазмы. Отделенную плазму хранили в холодильнике при -20°C или ниже до проведения анализа.
(8-3) Определение концентрации в плазме антитела против рецептора IL-6 человека посредством ELISA
Используемый способ был таким же, как описано в справочном примере 5.
(8-4) Определение концентрации в плазме hsIL-6R с помощью электрохемилюминесцентного анализа
Используемый способ был таким же, как описано в справочном примере 1.
Как показано на фиг.39, концентрация в плазме растворимого рецептора IL-6 человека повышалась до 650 нг/мл (в 15 раз относительно концентрации до введения), когда H54/L28-IgG1, нейтрализующее антитело против растворимого рецептора IL-6 человека, вводили нормальным мышам (группа hsIL-6R), у которых концентрацию в плазме растворимого рецептора IL-6 человека поддерживали постоянной приблизительно на уровне 40 нг/мл. С другой стороны, в группе, в которой вводили Fv4-IgG1, которое было получено в результате сообщения H54/L28-IgG1 pH-зависимой способности связывания с антигеном, концентрацию в плазме растворимого рецептора IL-6 человека поддерживали на уровне приблизительно 70 нг/мл. Это позволяет предположить, что увеличение концентрации в плазме растворимого рецептора IL-6 человека, вызванное введением H54/L28-IgG1, типичного нейтрализующего антитела, может быть снижено до приблизительно одной десятой путем сообщения способности к рН-зависимому связыванию.
Кроме того, показано, что концентрация в плазме растворимого рецептора IL-6 человека сохраняется постоянной на уровне одной десятой или ниже одной десятой от стационарной концентрации при введении Fv-IgG1-v2 или Fv-IgG1-F20, каждое из которых получено в результате внесения изменения в pH-зависимые, связывающие рецептор IL-6, для усиления связывания FcRn в нейтральных условиях. Когда вводили Fv-IgG1-v2, концентрация в плазме растворимого рецептора IL-6 человека через 14 суток после введения составляла приблизительно 2 нг/мл. Таким образом, Fv-IgG1-v2 могло снижать концентрацию до 1/20 от уровня до введения. Между тем, когда вводили Fv-IgG1-F20, концентрация в плазме растворимого рецептора IL-6 человека через семь часов, одни сутки, двое суток и четверо суток после введения была ниже предела выявления (1,56 нг/мл). Это позволяет предположить, что Fv-IgG1-F20 снижало концентрацию до 1/25 или ниже 1/25 от уровня до введения.
Данные, описанные выше, демонстрируют, что концентрацию антигена в плазме можно значительно снизить посредством увеличения скорости элиминации антигена в плазме, путем введения антитела, обладающего как рН-зависимой антигенсвязывающей способностью, так и активностью связывания с FcRn в нейтральных условиях, в модели на животных, в которой концентрацию антигена в плазме поддерживают постоянной.
Обычные антитела, такие как H54/L28-IgG1, могут нейтрализовать действие антигена-мишени только путем связывания с антигеном-мишенью, и даже более того, они увеличивают концентрацию антигена в плазме. Напротив, было обнаружено, что, антитела, обладающие как способностью к рН-зависимому связыванию антигена, так и активностью связывания с FcRn в нейтральных условиях, способны не только нейтрализовать антиген-мишень, но также снижать концентрацию в плазме антигена-мишени. Можно ожидать, что эффект удаления антигена из плазмы является более существенным, чем нейтрализация. Кроме того, удаление антигена также может действовать для антигенов-мишеней, для которых удаление путем одной нейтрализации является недостаточно эффективным.
[Справочный пример 9] Идентификация порогового уровня аффинности связывания с FcRn человека при нейтральных значениях pH, требуемых для увеличения элиминации антигена, и взаимосвязь между элиминацией антигена и аффинностью связывания с FcRn человека при нейтральных значениях pH
(9-1) Получение антитела для исследования in vivo
Получали варианты Fc Fv4-IgG1, содержащего VH3-IgG1 (SEQ ID NO: 19) и VL3-CK (SEQ ID NO: 20), с увеличенным связыванием с FcRn в условиях нейтральных значений pH. Конкретно, получали VH3-M73 (SEQ ID NO: 24) и VH3-IgG1-v1 (SEQ ID NO: 21). Замены аминокислот вносили способами, известными специалистам в данной области, как описано в ссылочном примере 3.
H54/L28-IgG1, содержащее H54 (SEQ ID NO: 5) и L28 (SEQ ID NO: 6), Fv4-IgG1, содержащее VH3-IgG1 (SEQ ID NO: 19) и VL3-CK (SEQ ID NO: 20), Fv4-M73, содержащее VH3-M73 (SEQ ID NO: 24) и VL3-CK (SEQ ID NO: 20), Fv4-IgG1-v1, содержащее VH3-IgG1-v1 (SEQ ID NO: 21) и VL3-CK (SEQ ID NO: 20), и Fv4-IgG1-v2, содержащее VH3-IgG1-v2 (SEQ ID NO: 22) и VL3-CK (SEQ ID NO: 20), экспрессировали и очищали способом, известным специалистам в данной области, описанным в ссылочном примере 3.
(9-2) Оценка аффинности связывания антитела с FcRn человека в условиях нейтральных значений pH
VH3/L (WT)-IgG1, содержащее VH3-IgG1 (SEQ ID NO: 19) и L (WT) (SEQ ID NO: 14), VH3/L (WT)-M73, содержащее VH3-M73 (SEQ ID NO: 24) и L (WT) (SEQ ID NO: 14), VH3/L (WT)-IgG1-v1, содержащее VH3-IgG1-v1 (SEQ ID NO: 21) и L (WT) (SEQ ID NO: 14), и VH3/L (WT)-IgG1-v2, содержащее VH3-IgG1-v2 (SEQ ID NO: 22) и L (WT) (SEQ ID NO: 14), каждый из которых получали, как описано в справочном примере 3, оценивали в отношении связывания с FcRn человека в условиях нейтральных pH (pH 7,0).
Активность связывания VH3/L (WT)-IgG1-v1 и VH3/L (WT)-IgG1-v2 с FcRn человека измеряли с использованием способа, описанного в справочном примере 5. Вследствие низкой активности связывания VH3/L (WT)-IgG1 и VH3/L (WT)-M73 c FcRn человека, активность связывания c FcRn человека нельзя было измерить с использованием способа, описанного в примере 5, таким образом, эти антитела оценивали с помощью способа, описанного ниже. Связывание между антителом и FcRn человека анализировали кинетически с использованием Biacore T100 (GE Healthcare). Достаточное количество белка L (ACTIGEN) иммобилизовали на сенсорном чипе CM4 (GE Healthcare) с помощью способа на основе связанных аминов, и обеспечивали захват представляющего интерес антитела на чипе. Затем, инжектировали разбавленные растворы FcRn и подвижный буфер в качестве контрольного раствора для обеспечения взаимодействия FcRn человека с антителом, уловленном на сенсорном чипе. Используемый подвижный буфер содержал 50 ммоль/л фосфата натрия, 150 ммоль/л NaCl и 0,05% (масс./об.) Tween 20 (pH 7,0). FcRn разбавляли с использованием каждого буфера. Чип регенерировали с использованием 10 ммоль/л глицин-HCl (pH 1,5). Анализы проводили при 25°C.
KD (M) каждого антитела получали из данных сенсограммы с использованием программного обеспечения Biacore T100 Evaluation (GE Healthcare), которая одновременно аппроксимирует фазы ассоциации и диссоциации сенсограмм и осуществляет общую аппроксимацию всех кривых в рабочем наборе. Сенсограммы аппроксимировали модели связывания 1:1 - модели "связывания Ленгмюра", осуществляемой с помощью программного обеспечения Biacore T100 Evaluation. Для некоторых из связывающих взаимодействий, KD получали посредством нелинейного регрессионного анализа графиков Req, равновесного связывающего ответа, против log концентрации анализируемого соединения, с использованием равновесного подхода.
Результаты связывания с FcRn человека в нейтральных условиях (pH 7,0) с помощью Biacore представлены в таблице 27.
(9-3) Исследование in vivo эффекта антитела в отношении элиминацию антигена в модели совместного введения с использованием трансгенной линии 276 мышей с FcRn человека
Исследование антител in vivo с использованием модели совместного введения проводили, как описано в справочном примере 3. Антитела против рецептора IL-6 человека, использованные в этом исследовании, представляют собой описанные выше H54/L28-IgG1, Fv4-IgG1, Fv4-M73, Fv4-IgG1-v1 и Fv4-IgG1-v2. Мыши, использованные в этом исследовании, представляют собой трансгенных мышей с FcRn человека (B6.mFcRn-/-.hFcRn Tg линия 276 +/+ мышь, Jackson Laboratories; Methods Mol Biol. (2010) 602: 93-104).
Как показано на фиг.40, фармакокинетика H54/L28-IgG1, Fv4-IgG1, Fv4-M73, Fv4-IgG1-v1 и Fv4-IgG1-v2 была сравнимой, и эти антитела поддерживались в сходной концентрации в плазме в ходе исследования.
Концентрация hsIL-6R в плазме с течением времени представлена на фиг.41. По сравнению с hsIL-6R, введенным с Fv4-IgG1, hsIL-6R, введенный с Fv4-IgG1-v2, продемонстрировал увеличенный клиренс, в то время как hsIL-6R, введенный с Fv4-M73 и Fv4-IgG1-v1, продемонстрировал сниженный клиренс. Хотя все варианты Fc, M73, v1 и v2 обладают повышенной аффинностью связывания с FcRn человека в нейтральных условиях pH (pH 7,0), показано, что только Fv4-IgG1-v2, но не Fv4-M73 и Fv4-IgG1-v1, продемонстрировало повышенный клиренс hsIL-6R. Это показывает, что для увеличения клиренса антигена аффинность связывания антитела с FcRn человека при pH 7,0 должна быть по меньшей мере большей, чем для IgG1-v1, аффинность связывания которого с FcRn человека при pH 7,0 составляет KD 3,2 мкМ или в 28 раз более высокая, чем у интактного IgG1 человека (аффинность связывания с FcRn человека составляет KD 88 мкМ).
На фиг.42 описана взаимосвязь между аффинностью связывания вариантов Fc с FcRn человека при pH 7,0 и концентрацией в плазме hsIL-6R через 1 сутки после совместного введения hsIL-6R и вариантов Fc. Варианты Fc, описанные в этом примере и справочном примере 6 (Fv4-IgG1, Fv4-M73, Fv4-IgG1-v1, Fv4-IgG1-v2, Fv4-IgG1-F14, Fv4-IgG1-F20, Fv4-IgG1-F21, Fv4-IgG1-F25, Fv4-IgG1-F29, Fv4-IgG1-F35, Fv4-IgG1-F48, Fv4-IgG1-F93 и Fv4-IgG1-F94), представлены на графике. Путем повышения аффинности связывания антитела с FcRn человека при pH 7,0, концентрация в плазме hsIL-6R, которая отражает клиренс антигена, сначала увеличивается, а затем стремительно снижается. Это показывает, что для увеличения клиренса антигена, по сравнению с неизмененным IgG1 человека, аффинность связывания антитела с FcRn человека при pH 7,0 предпочтительно должна быть более высокой, чем KD, равная 2,3 мкМ (значение, полученное из кривой аппроксимации, фиг.42). Аффинность связывания антитела с FcRn человека между KD, равной 88 мкМ, и KD, равной 2,3 мкМ, будет скорее снижать клиренс антигена (более высокая концентрация hsIL-6R). Иными словами, аффинность связывания антитела с FcRn человека при pH 7,0 предпочтительно должна быть в 38 раз более высокой, чем для природного IgG1 человека, чтобы усилить элиминацию антигена, или в ином случае будет снижаться клиренс антигена.
На фиг.43 представлена зависимость между аффинностью связывания вариантов Fc с FcRn человека при pH 7,0 и концентрацией антитела в плазме через 1 сутки после совместного введения hsIL-6R и вариантов Fc. Варианты Fc, описанные в этом примере и справочном примере 6 (Fv4-IgG1, Fv4-M73, Fv4-IgG1-v1, Fv4-IgG1-v2, Fv4-IgG1-F14, Fv4-IgG1-F20, Fv4-IgG1-F21, Fv4-IgG1-F25, Fv4-IgG1-F29, Fv4-IgG1-F35, Fv4-IgG1-F48, Fv4-IgG1-F93 и Fv4-IgG1-F94), представлены на графике. Посредством увеличения аффинности связывания антитела с FcRn человека при pH 7,0, концентрация в плазме антитела, которая отражает фармакокинетику антител (клиренс), вначале увеличивается, но затем стремительно снижается. Это демонстрирует, что для поддержания фармакокинетики антитела, аналогичной природному IgG1 человека (аффинность связывания с FcRn человека составляет KD 88 мкМ), аффинность антитела по отношению к FcRn человека при pH 7,0 должна быть более слабой, чем KD, равная 0,2 мкМ (значение, полученное в результате аппроксимации кривой на фиг.43). Аффинность связывания антитела для FcRn человека, превышающая KD 0,2 мкМ, увеличивала клиренс антитела (т.е. более быстрая элиминация антитела из плазмы). Иными словами, аффинность связывания антитела с FcRn человека при pH 7,0 должна быть в 440 раз более высокой, чем для природного IgG1 человека, чтобы проявлять фармакокинетику антител, сходную с природным IgG1 человека, или в ином случае это будет приводить к быстрой элиминации антитела из плазмы.
Принимая во внимание как фиг.42, так и фиг.43, для увеличения клиренса антигена (т.е. снижения концентрации антигена в плазме) по сравнению с IgG1, при сохранении фармакокинетики антител, аналогичной природному IgG1 человека, аффинность связывания антитела с FcRn человека при pH 7,0 должна составлять от 2,3 мкМ до 0,2 мкМ, или иными словами, аффинность связывания антитела с FcRn человека при pH 7,0 должна быть в пределах диапазона от 38 раз до 440 раз более высокой, чем для неизмененного IgG1 человека. Такое антитело с фармакокинетикой, сходной с IgG1, с длительной активностью элиминации антигена может быть полезным для терапевтических средств на основе антитела, для которых требуются более длительные интервалы между введениями, как например, в случае хронического заболевания вследствие его свойства длительного действия.
С другой стороны, путем увеличения аффинности связывания антитела с FcRn человека при pH 7,0 более чем KD 0,2 мкМ, или иными словами, путем увеличения аффинности связывания антитела с FcRn человека при pH 7,0 более чем в 440 раз по сравнению с природным IgG1 человека, происходит в большей степени кратковременное увеличение клиренса антигена, хотя антитело элимируются из плазмы быстрее, чем природный IgG1 человека. Такое антитело со способностью индуцировать быстрое и сильное снижение концентрации антигена будет являться полезным для терапевтического средства на основе антитела, как например, для острого заболевания, где связанный с заболеванием антиген необходимо удалять из плазмы вследствие его свойства быстрого действия.
Количество антигена, элиминируемое из плазмы посредством антитела, представляет собой важный фактор для оценки эффективности элиминации антигена путем введения вариантов Fc антитела, обладающих повышенной аффинностью связывания с FcRn человека при pH 7,0. Для оценки эффективности элиминации антигена с помощью антитела проводили следующий расчет в каждый момент времени исследования in vivo, описанный в этом примере и справочном примере 6.
Значение A: молярная концентрация антигена в каждый момент времени;
Значение B: молярная концентрация антигена в каждый момент времени;
Значение C: молярная концентрация антигена по отношению к молярной концентрации антитела (молярное отношение антигена/антитело) в каждый момент времени
C=A/B
Зависимость от времени значения C (молярное отношение антиген/антитело) для каждого антитела описана на фиг.44. Низкие значения C показывают высокую элиминацию антигена с помощью антитела, тогда как высокое значение C показывает низкую эффективность элиминации антигена по отношению к антителу. Низкое значение C по сравнению с IgG1 показывает, что более высокая эффективность элиминации антигена достигается с помощью вариантов Fc, в то время как высокие значения C по сравнению с IgG1 показывают, что варианты Fc обладают отрицательным эффектом на эффективность элиминации антигена. Все варианты Fc, за исключением Fv4-M73 и Fv4-IgG1-v1 продемонстрировали повышенную эффективность элиминации антигена по сравнению с Fv4-IgG1. Fv4-M73 и Fv4-IgG1-v1 продемонстрировали отрицательное влияние на эффективность элиминации антигена, что согласуется с фиг.42.
На фиг.45 представлена зависимость между аффинностью связывания Fc-вариантов с FcRn человека при pH 7,0 и значением C (молярное отношение антиген/антитело) через 1 сутки после совместного введения hsIL-6R и вариантов Fc. Варианты Fc, описанные в этом примере и справочном примере 6 (Fv4-IgG1, Fv4-M73, Fv4-IgG1-v1, Fv4-IgG1-v2, Fv4-IgG1-F14, Fv4-IgG1-F20, Fv4-IgG1-F21, Fv4-IgG1-F25, Fv4-IgG1-F29, Fv4-IgG1-F35, Fv4-IgG1-F48, Fv4-IgG1-F93, и Fv4-IgG1-F94), представлены на графике. Это показывает, что для достижения более высокой эффективности элиминации антигена по сравнению с природным IgG1 человека, аффинность антитела к FcRn человека при pH 7,0 должна быть более высокой, чем KD 3,0 мкМ (значение, полученное из аппроксимирующей кривой на фиг.45). Другими словами, для достижения более высокой эффективности элиминации антигена по сравнению с природным IgG1 человека аффинность связывания антитела с FcRn человека при pH 7,0 должна быть по меньшей мере в 29 раз более высокой, чем для природного IgG1 человека.
В заключение, группа вариантов антител, обладающая аффинностью связывания с FcRn при pH 7,0 от KD 3,0 мкМ до 0,2 мкМ, или иными словами, группа вариантов антител, обладающих аффинностью связывания с FcRn при pH 7,0 в пределах диапазона, от 29 раз до 440 раз более высокого, чем для природного IgG1 человека, обладает фармакокинетикой, аналогичной фармакокинетике антител для IgG1, но имеет повышенную способность к элиминации антитела из плазмы. Таким образом, такое антитело демонстрирует повышенную эффективность элиминации антигена по сравнению с IgG1. Фармакокинетика, аналогичная IgG1, будет обеспечивать длительную элиминацию антигена из плазмы (элиминация антигена длительного действия), и более длительные интервалы дозирования, что может являться преимуществом для терапевтических средств на основе антител, предназначенных для лечения хронических заболеваний. Группа вариантов антител, обладающих аффинностью связывания с FcRn при pH 7,0, превышающей KD 0,2 мкМ, или иными словами, группа вариантов антител, обладающая аффинностью связывания с FcRn при pH 7,0, в 440 раз более высокой, чем для природного IgG1 человека, обладает ускоренным клиренсом антигена (кратковременная элиминация антитела). Тем не менее, поскольку такое антитело, обеспечивает еще более быстрый клиренс антитела (быстрая элиминация антигена), таким образом, такое антитело также демонстрирует повышенную эффективность элиминации антигена по сравнению с IgG1. Как показано в справочном примере 8, Fv4-IgG1-F20 у нормальных мышей будет индуцировать значительную элиминацию антигена из плазмы в очень короткий период, но эффект элиминации антигена не является продолжительным. Такой профиль будет предпочтительным в случае острого заболевания, где необходимо, чтобы антиген, связанный с заболеванием, был удален из плазмы быстро и в значительной степени в очень короткий период.
[Справочный пример 10] Исследование in vivo Fv4-IgG1-F14 с помощью инфузионной модели стационарного состояния с использованием трансгенной линии 276 мышей с FcRn человека
Исследование in vivo Fv4-IgG1-F14 с помощью инфузионной модели стационарного состояния с использованием трансгенных мышей линии 276 с FcRn человека проводили, как описано ниже. Исследуемая группа состоит из контрольной группы (без антитела), Fv4-IgG1 в дозе 1 мг/кг и Fv4-IgG1-F14 в дозе 1 мг/кг, 0,2 мг/кг и 0,01 мг/кг.
Инфузионный насос (MINI-OSMOTIC PUMP MODEL 2004; alzet), содержавший растворимый рецептор IL-6 человека, имплантировали под кожу спины трансгенных мышей 276 с FcRn человека (мыши B6.mFcRn-/-.hFcRn Tg линии 276 +/+ (B6.mFcRn-/- hFCRN Tg276 B6.Cg-Fcgrt
Концентрацию hsIL-6R в плазме мыши измеряли посредством электрохемилюминисценции. Получали образцы калибровочной кривой hsIL-6R, доведенные до концентрации 2000, 1000, 500, 250, 125, 62,5 и 31,25 пг/мл, и образцы плазмы мыши, разведенные в 50 раз или более. Образцы смешивали с раствором моноклонального антитела против IL-6R человека (R&D), меченного рутением, с SULFO-TAG NHS Ester (Meso Scale Discovery), биотинилированного антитела против IL-6R человека (R&D) и WT-IgG1, а затем оставляли для реакции в течение ночи при 37°C. Конечная концентрация WT-IgG1 в качестве антитела против рецептора IL-6 человека, содержащего тоцилизумаб (тяжелая цепь SEQ ID NO: 13; легкая цепь SEQ ID NO: 14), составила 333 мкг/мл, что является больше концентрации антитела против рецептора IL-6 человека, содержащегося в образцах, с целью связывания практически всех молекул hsIL-6R в образцах с WT-IgG1. Затем образцы переносили в планшет со стрептавидином MA400 PR (Meso Scale Discovery) и оставляли для реакции в течение одного часа при комнатной температуре, и проводили промывание. Затем сразу добавляли буфер для считывания T (×4) (Meso Scale Discovery), измерения проводили посредством Sector PR 400 Reader (Meso Scale Discovery). Концентрацию hsIL-6R вычисляли, основываясь на данных калибровочной кривой, используя аналитическое программное обеспечение SOFTmax PRO (Molecular Devices).
На фиг.46 представлен профиль концентрации hsIL-6R в плазме с течением времени после введения антитела. По сравнению с исходным уровнем hsIL-6R без антитела, введение 1 мг/кг Fv4-IgG1 приводило к повышению в несколько раз концентрации hsIL-6R в плазме. С другой стороны, введение 1 мг/кг Fv4-IgG1-F14 привело к значительному снижению концентрации в плазме по сравнению с группой Fv4-IgG1 и контрольной группой. Через 2 суток концентрация в плазме hsIL-6R не определялась (нижний предел определения концентрации в плазме hsIL-6R составляет 1,56 нг/мл в этой системе измерения), и это длилось вплоть до 14 суток.
H54/L28-IgG1-F14 проявляло снижение концентрации в плазме hsIL-6R по сравнению с H54/L28-IgG1, но степень снижения была небольшой. Степень снижения была более высокой для вариабельной области Fv4, которая обладала свойством рН-зависимого связывания с hsIL-6R. Это демонстрирует, что, хотя увеличение аффинности связывания с FcRn человека при pH 7,0 является эффективным для снижения концентрации антигена в плазме, комбинация рН-зависимого связывания антигена и повышенной аффинности связывания с FcRn человека при нейтральных значениях pH значительно увеличивает элиминацию антигена.
Исследование с использованием более низких доз Fv4-IgG1-F14 продемонстрировало, что даже при 0,01 мг/кг, что составляет 1/100 от 1 мг/кг, концентрация антигена в плазме снижается ниже исходного уровня, демонстрируя значительную эффективность этой молекулы в отношении удаления антигена из плазмы.
[Справочный пример 11] Сравнение трансгенной линии 276 и линии 32 мышей с FcRn человека в модели совместного введения
Предшествующие исследования in vivo проводили с использованием трансгенной линии 276 мышей с FcRn человека (Jackson Laboratories). Для сравнения различий между трансгенной линией 276 мышей с FcRn человека и другой трансгенной линией, линией 32, проводили исследование совместного введения H54/L28-IgG1, Fv4-IgG1 и Fv4-IgG1-v2 с использованием трансгенной линии 32 мышей с FcRn человека (B6.mFcRn-/-.hFcRn Tg линия 32 +/+ мышь (B6.mFcRn-/- hFCRN Tg32; B6.Cg-Fcgrt
На фиг.47 представлена концентрация в плазме hsIL-6R с течением времени как у трансгенной линии 276 мышей с FcRn человека, так и у в трансгенной линии 32 мышей с FcRn человека. H54/L28-IgG1, Fv4-IgG1 и Fv4-IgG1-v2 продемонстрировали сходный профиль концентраций в плазме hsIL-6R с течением времени. В обеих линиях мышей увеличение аффинности связывания с FcRn человека при pH 7,0 увеличивало элиминацию антигена из плазмы (сравнение Fv4-IgG1 и Fv4-IgG1-v2) в одинаковой степени.
На фиг.48 представлена концентрация антитела в плазме с течением времени как у трансгенной линии 276 мышей с FcRn человека, так и у трансгенной линии 32 мышей с FcRn человека. H54/L28-IgG1, Fv4-IgG1 и Fv4-IgG1-v2 продемонстрировали сходный профиль концентрации антител в плазме с течением времени.
В заключение, незначимое отличие наблюдали между линией 276 и линией 32, что показало, что вариант Fc для увеличения аффинности связывания с FcRn человека при pH 7,0 был эффективным в двух различных трансгенных линиях мышей, экспрессирующих FcRn человека, в отношении увеличения элиминации антигена из плазмы.
[Справочный пример 12] Получение различных вариантов Fc антител, имеющих увеличенную аффинность связывания с FcRn при нейтральных значениях pH
(12-1) Получение вариантов Fc
Различные мутации для увеличения аффинности связывания с FcRn человека при нейтральных значениях pH вносили в Fv4-IgG1 для дальнейшего улучшения профиля элиминации антигена. В частности, мутации аминокислот, представленные в таблице 15, вносили в константную область тяжелой цепи Fv4-IgG1 для получения вариантов Fc (номера аминокислот участков мутации представлены в соответствии с нумерацией EU). Аминокислотные замены вносили способом, известным специалистам в данной области, описанным в справочном примере 3.
Дополнительные варианты (с IgG1-F100 по IgG1-F1052), каждый из которых содержит полученную тяжелую цепь и L (WT) (SEQ ID NO: 14), экспрессировали и очищали способами, известными специалистам в данной области, как описано в справочном примере 3.
(12-2) Оценка связывания FcRn человека
Связывание между антителом и FcRn человека анализировали кинетически, как описано в справочном примере 5 для IgG1-v1, IgG1-v2 и с IgG1-F2 по IgG1-F1052 или в справочном примере 9 для IgG1 и M73. Результат связывания FcRn человека в нейтральных условиях (pH 7,0) при исследовании с помощью Biacore представлен в таблицах с 28-1 по 28-21.
Таблица 28-2 является продолжением таблицы 28-1.
Таблица 28-3 является продолжением таблицы 28-2.
Таблица 28-4 является продолжением таблицы 28-3.
Таблица 28-5 является продолжением таблицы 28-4.
Таблица 28-6 является продолжением таблицы 28-5.
Таблица 28-7 является продолжением таблицы 28-6.
Таблица 28-8 является продолжением таблицы 28-7.
Таблица 28-9 является продолжением таблицы 28-8.
Таблица 28-10 является продолжением таблицы 28-9.
Таблица 28-11 является продолжением таблицы 28-10.
Таблица 28-12 является продолжением таблицы 28-11.
Таблица 28-13 является продолжением таблицы 28-12.
Таблица 28-14 является продолжением таблицы 28-13.
Таблица 28-15 является продолжением таблицы 28-14.
Таблица 28-16 является продолжением таблицы 28-15.
Таблица 28-17 является продолжением таблицы 28-16.
Таблица 28-18 является продолжением таблицы 28-17.
Таблица 28-19 является продолжением таблицы 28-18.
Таблица 28-20 является продолжением таблицы 28-19.
Таблица 28-21 является продолжением таблицы 28-20.
[Справочный пример 13] Исследование in vivo различных антител с вариантами Fc с помощью инфузионной модели стационарного состояния с использованием трансгенных мышей линии 32 с FcRn человека
Варианты Fc, полученные согласно справочному примеру 12, исследовали в отношении их способности элиминировать антиген из плазмы в инфузионной модели стационарного состояния с использованием трансгенных мышей линии 32 с FcRn человека. Инфузионную модель стационарного состояния in vivo осуществляли, как описано в примере 1, но вместо линии 276 использовали трансгенных мышей линии 32 с FcRn человека, и моноклональное антитело против CD4 вводили два раза (до имплантации инфузионного насоса и через 14 суток после введения антитела) или три раза (до имплантации инфузионного насоса и через 10 и 20 суток после введения антитела).
Из вариантов Fc, описанных в таблицах с 28-1 по 28-21, выбранные антитела с вариантами Fc, приведенные ниже, экспрессировали и очищали способами, известными специалистам в данной области, как описано в справочном примере 3:
Fv4-IgG1, содержащее VH3-IgG1 и VL3-CK;
Fv4-IgG1-F11, содержащее VH3-IgG1-F11 и VL3-CK;
Fv4-IgG1-F14, содержащее VH3-IgG1-F14 и VL3-CK;
Fv4-IgG1-F39, содержащее VH3-IgG1-F39 и VL3-CK;
Fv4-IgG1-F48, содержащее VH3-IgG1-F48 и VL3-CK;
Fv4-IgG1-F140, содержащее VH3-IgG1-F140 и VL3-CK;
Fv4-IgG1-F157, содержащее VH3-IgG1-F157 и VL3-CK;
Fv4-IgG1-F194, содержащее VH3-IgG1-F194 и VL3-CK;
Fv4-IgG1-F196, содержащее VH3-IgG1-F196 и VL3-CK;
Fv4-IgG1-F198, содержащее VH3-IgG1-F198 и VL3-CK;
Fv4-IgG1-F262, содержащее VH3-IgG1-F262 и VL3-CK;
Fv4-IgG1-F264, содержащее VH3-IgG1-F264 и VL3-CK;
Fv4-IgG1-F393, содержащее VH3-IgG1-F393 и VL3-CK;
Fv4-IgG1-F424, содержащее VH3-IgG1-F434 и VL3-CK; и
Fv4-IgG1-F447, содержащее VH3-IgG1-F447 и VL3-CK.
Эти антитела вводили трансгенным мышам линии 32 с FcRn человека в дозе 1 мг/кг.
На фиг.49 представлена концентрация hsIL-6R в плазме у мышей с течением времени. По сравнению с Fv4-IgG1, все варианты Fc, имеющие увеличенную аффинность связывания с FcRn человека при pH 7,0, проявляли снижение концентрации hsIL-6R в плазме и, таким образом, усиленную элиминацию антигена из плазмы. Хотя степень и продолжительность снижения концентрации антигена отличалась среди вариантов Fc, все варианты неизменно снижали концентрацию hsIL-6R в плазме по сравнению с IgG1, демонстрируя, что увеличенная аффинность связывания с FcRn человека при pH 7,0 универсальным образом усиливает элиминацию антигена из плазмы. На фиг.50 представлена концентрация антитела с течением времени у мышей. Фармакокинетика антител отличалась среди вариантов Fc.
Как описано в справочном примере пример 9, количество антигена, элиминированного из плазмы, на антитело является важным фактором увеличения эффективности элиминации антигена при введении антител с вариантами Fc, имеющих увеличенную аффинность связывания с FcRn человека при pH 7,0. Таким образом, величина C (молярное соотношение антиген/антитело) для каждого антитела с течением времени представлена на фиг.51. На фиг.52 описана взаимосвязь между аффинностью связывания вариантов Fc с FcRn человека при pH 7,0 и величина C (молярное соотношение антиген/антитело) на 1 сутки после введения антител. Это демонстрирует, что все антитела с вариантами Fc, исследованные в этом исследовании, имеют более низкую величину C по сравнению с Fv4-IgG1. Поскольку все из вариантов Fc, исследованных в этом исследовании, имеют аффинность связывания с FcRn человека при pH 7,0, более сильную, чем KD 3,0 мкМ, они достигали более высокой эффективности элиминации антигена по сравнению с природным IgG1 человека. Это согласовывалось с результатами, полученными в справочном примере 9 (фиг.42).
На фиг.53 описано, что среди вариантов Fc, исследованных в этом исследовании, антитела, имеющие вариант Fc F11, F39, F48 и F264, проявляли сходную фармакокинетику с IgG1. Поскольку это исследование проводили с использованием трансгенных мышей с FcRn человека, то ожидается, что эти варианты Fc имеют длительное время полужизни, сходное с IgG1, также и у человека. На фиг.54 описана концентрация hsIL-6R в плазме с течение времени у мышей, которым вводили антитела, имеющие сходную фармакокинетику с природным IgG1 человека (F11, F39, F48 и F264). Эти варианты снижали концентрацию hsIL-6R в плазме по сравнению с IgG1 приблизительно в 10 раз. Более того, эти антитела снижали концентрацию hsIL-6R ниже исходной концентрации hsIL-6R (концентрация без антитела). Таким образом, эти антитела могут обеспечить длительную элиминацию антигена из плазмы, и, таким образом, длительные интервалы между введениями доз, которые являются предпочтительными для лекарственных средств на основе антител от хронических заболеваний.
На фиг.55 и 56 представлена концентрация антитела в плазме и концентрация hsIL-6R в плазме с течением времени для IgG1, и вариантов Fc F157, F196 и F262, соответственно. Неожиданно, хотя фармакокинетика антител F157 и F262 показала значительно более быстрый клиренс из плазмы по сравнению с природным IgG1 человека, F157 и F262 проявляли значительную элиминацию hsIL-6R из плазмы. В частности, концентрация hsIL-6R в плазме в случае F157 была ниже предела выявления (1,56 нг/мл), с 1 по 28 сутки (за исключением 14 суток), и концентрация hsIL-6R в плазме в случае F262 была ниже предела выявления (1,56 нг/мл) с 14 по 28 сутки. С другой стороны, для F196 с более медленным клиренсом антитела по сравнению с F157, концентрация антигена начинала увеличиваться на 14 сутки и возвращалась обратно на 28 сутки. Среди вариантов Fc, исследованных в этом исследования, F157 и F262 были единственными вариантами Fc, которые были способны снижать концентрацию hsIL-6R в плазме ниже 1,56 нг/мл на 28 сутки.
Такой длительный эффект F157 и F262 является неожиданным, исходя из фармакокинетики антител, поскольку антитела элиминировались из плазмы очень быстро по сравнению с природным IgG1 человека. В частности, концентрация антитела F157 в плазме не определялась на 21 сутки. Тем не менее, концентрация hsIL-6R в плазме продолжала быть сниженной до уровня ниже предела выявления 1,56 нг/мл на 21 и 28 сутки. Настоящее изобретение не ограничивается конкретной теорией, однако этот неожиданный эффект считают следствием присутствия антитела на поверхности клетки эндотелия сосудов в качестве связанной с FcRn формы. Хотя эти антитела продемонстрировали низкую концентрацию в плазме, эти антитела все еще присутствует в сосудистом отделе в связанной с FcRn форме (которую нельзя измерить в качестве концентрации антитела в плазме). Это связанное с FcRn антитело все еще может связываться с антигеном в плазме и после опосредуемого FcRn захвата комплекса антиген/антитело, антиген высвобождается в эндосоме и деградируется лизосомой, в то время как антитело рециклирует обратно на клеточную поверхность в связанной с FcRn форме. Таким образом, это связанное с FcRn участвует в элиминации антигена. Это объясняет причину, почему эти антитела поддерживают способность элиминации антигена даже после того, как концентрация антитела в плазме становится низкой.
Промышленная применимость
Настоящее изобретение относится к способам ускорения захвата антигена в клетки с использованием антигенсвязывающих молекул, способам увеличения количества раз связывания антигена одной антигенсвязывающей молекулой, способам ускорения снижения концентрации антигена в плазме путем введения антигенсвязывающих молекул, и способам увеличения удержания в плазме антигенсвязывающих молекул. Путем ускорения захвата антигена в клетки с помощью антигенсвязывающей молекулы, стало возможным не только ускорить снижение уровня антигена в плазме путем введения антигенсвязывающей молекулы, но и увеличить удержания в плазме антигенсвязывающей молекулы и увеличить количество раз связывания антигена каждой антигенсвязывающей молекулой. Такие антигенсвязывающие молекулы могут проявлять более благоприятные эффекты in vivo, чем типичные антигенсвязывающие молекулы.
Реферат
Изобретение относится к биохимии. Описано антитело для снижения концентрации антигена в плазме, содержащее антигенсвязывающий домен и FcRn-связывающий домен человека, активность связывания антигена которого отличается в двух различных условиях концентрации кальция и является более низкой в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция, где низкая концентрация кальция представляет собой концентрацию ионизированного кальция от 0,1 до 30 мкМ, а высокая концентрация кальция представляет собой концентрацию ионизированного кальция от 100 мкМ до 10 мМ, где указанное антитело содержит по крайней мере четыре аминокислоты, выбранные из группы, включающей аминокислоты в положениях 30, 31, 32, 50 и 92 в соответствии с нумерацией по Kabat в легкой цепи, которые обладают хелатирующей активностью в отношении металла. А также описана фармацевтическая композиция, содержащая данное антитело. Изобретение может быть использовано для ускорения захвата антигенсвязывающими молекулами антигена в клетки, увеличения количества раз связывания антигена одной антигенсвязывающей молекулой, ускорения снижения концентрации антигена в плазме и увеличения удержания антигенсвязывающей молекулы в плазме, а также антигенсвязывающих молекул. 2 н. и 3 з.п. ф-лы, 56 ил., 28 табл., 25 пр.
Формула
Документы, цитированные в отчёте о поиске
Способы и композиции для модуляции взаимодействия между apj-рецептором и вирусом иммунодефицита человека (вич)
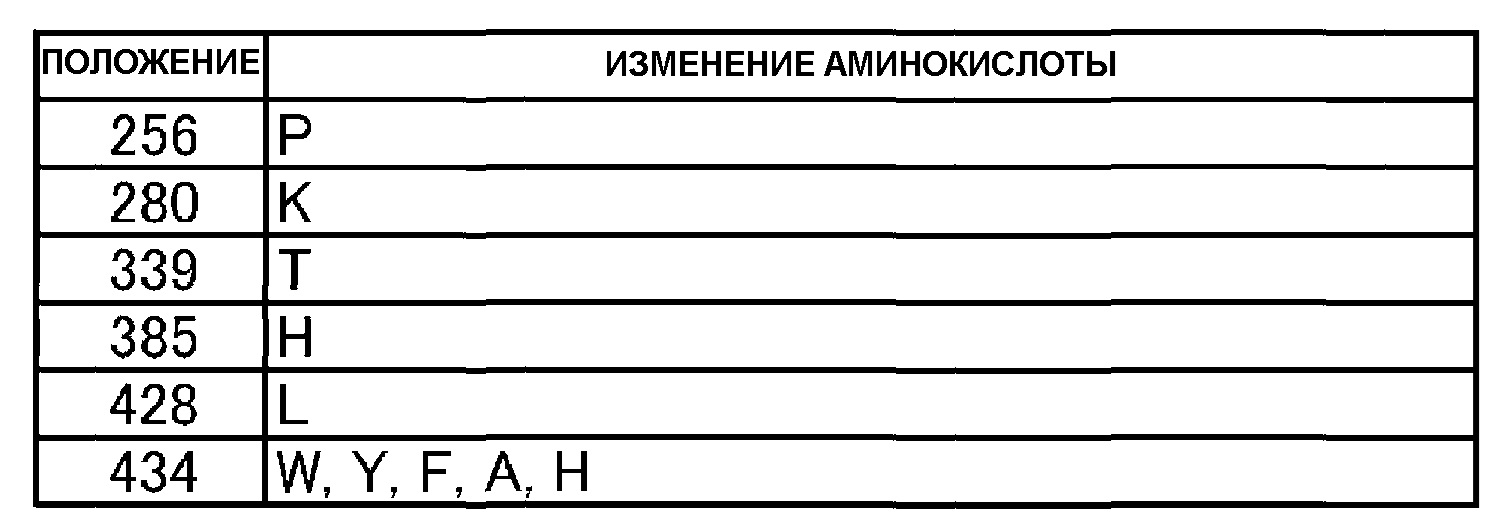








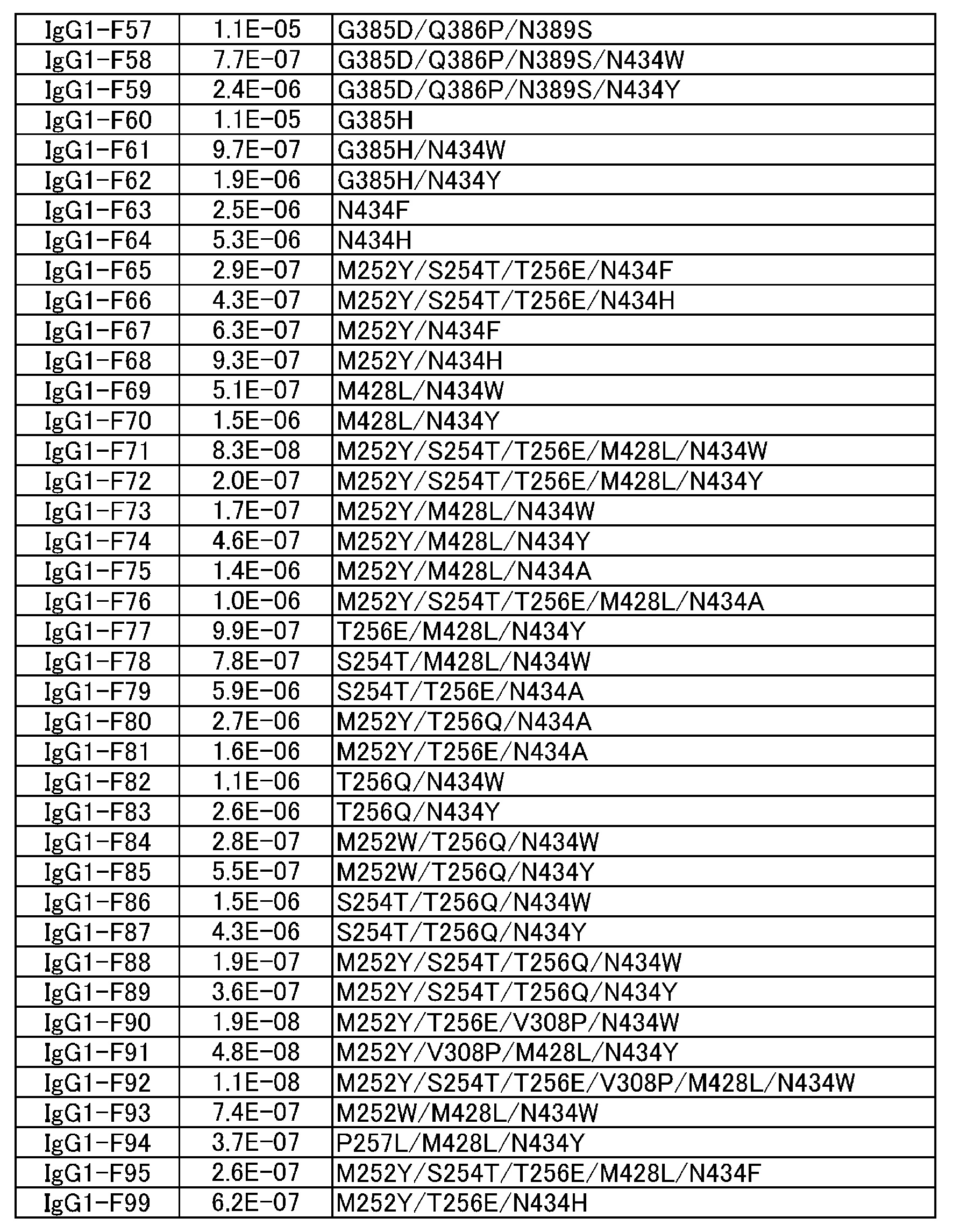
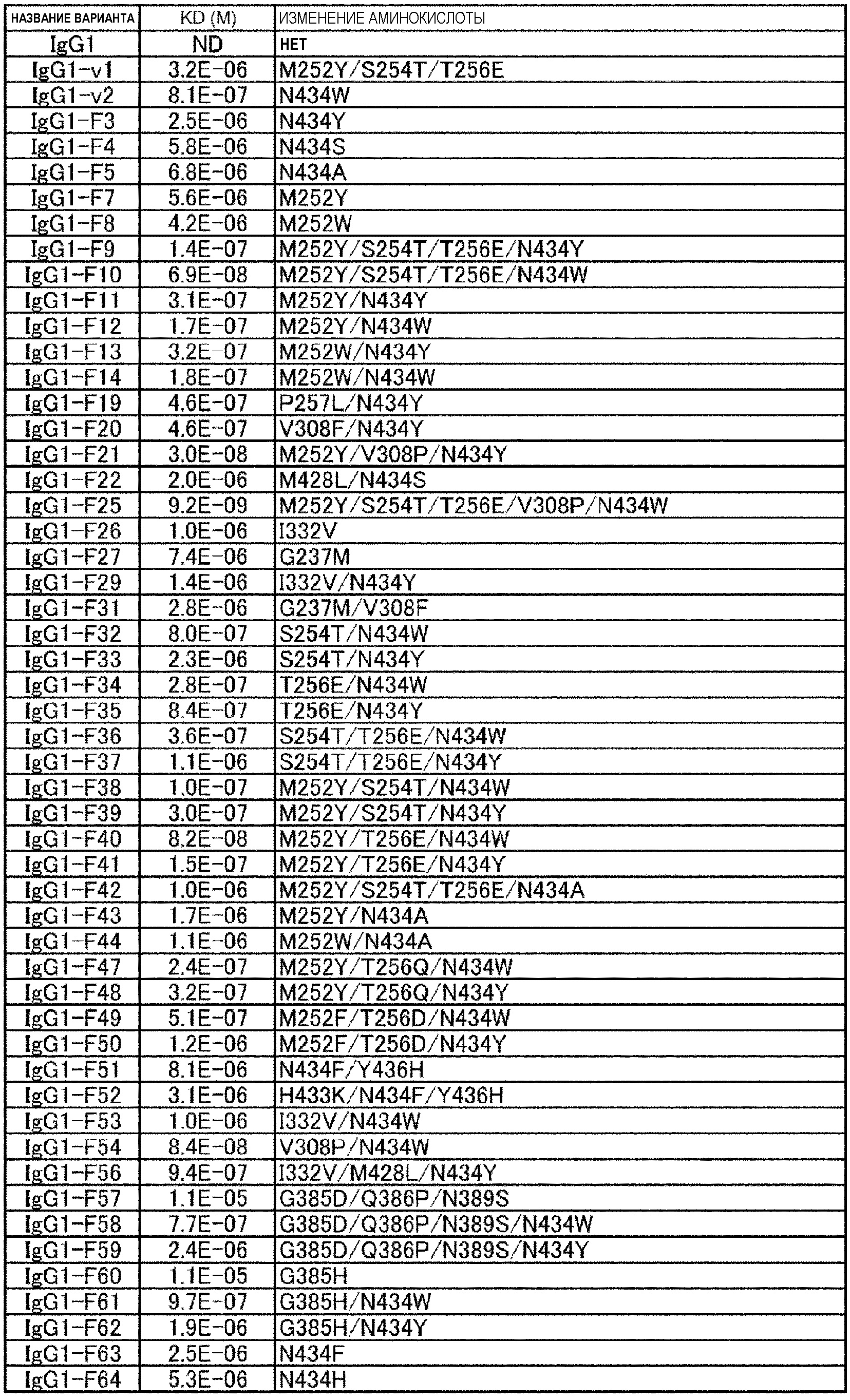


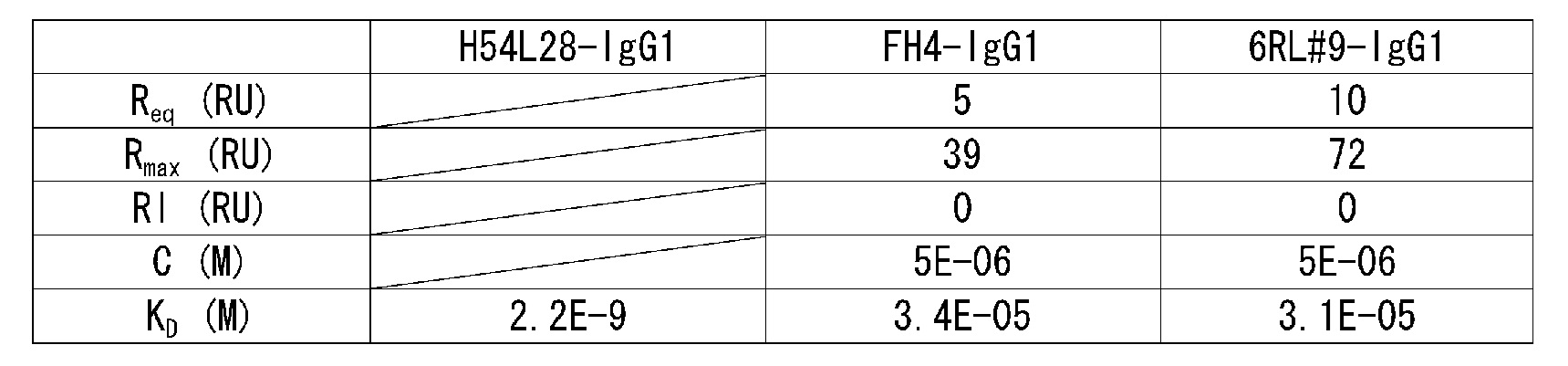
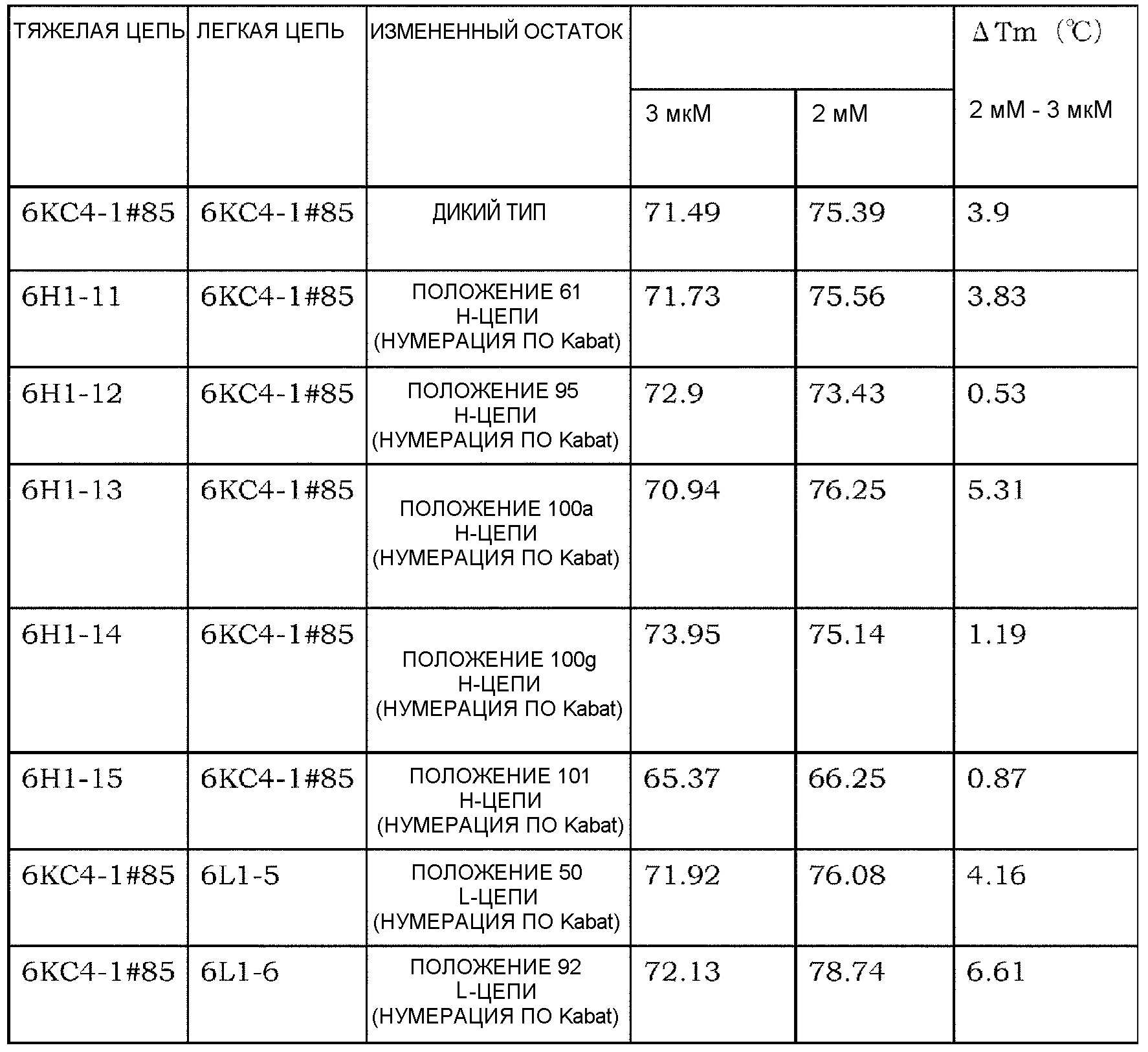

























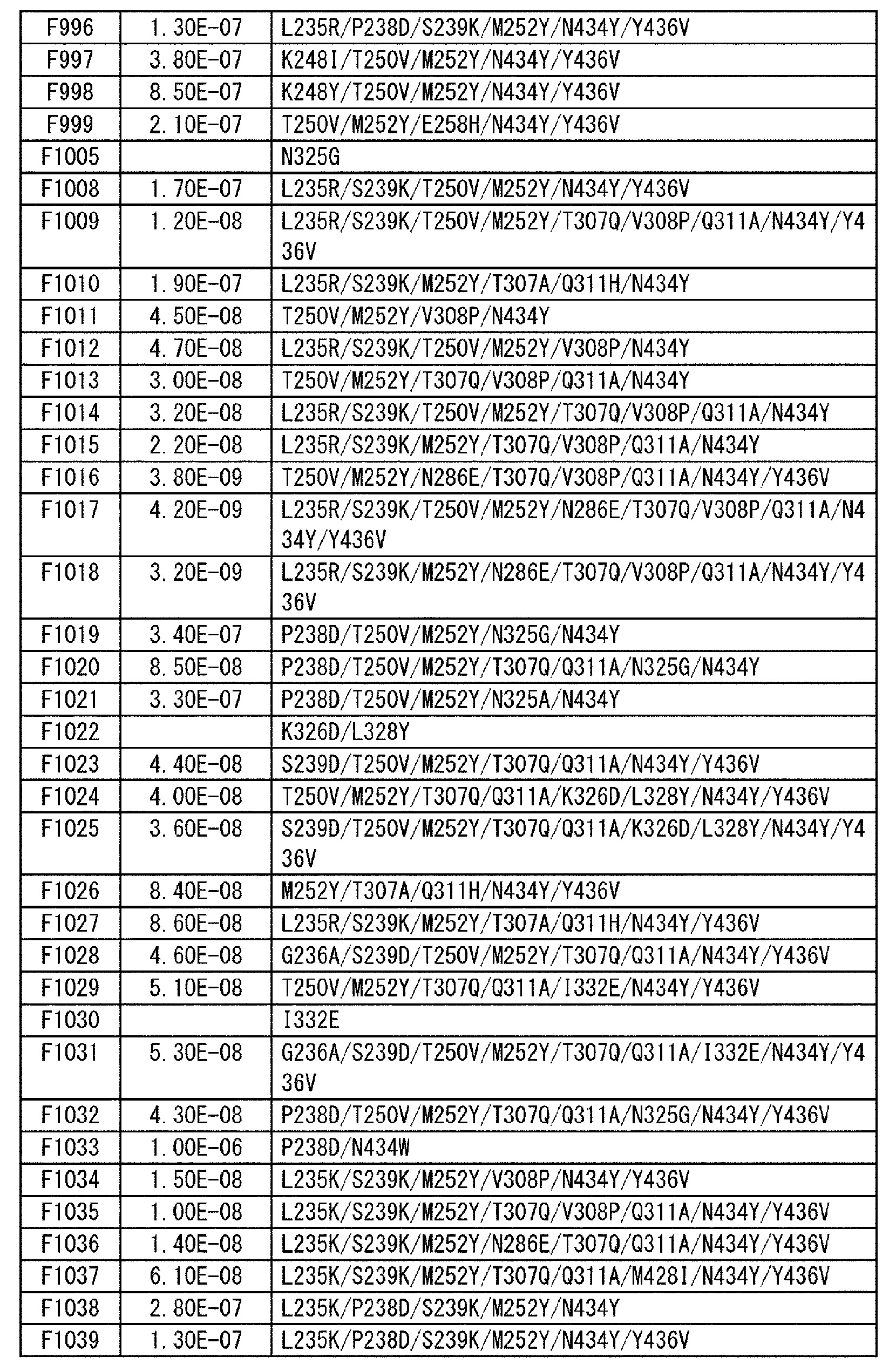


Комментарии