Смесь аналогов циклоспорина и ее применение в качестве иммуномодулирующего агента - RU2004110941A
Код документа: RU2004110941A
Реферат
1. Композиция, включающая изомерную смесь аналога циклоспорина, модифицированного в 1-м аминокислотном остатке заместителем 1,3-диеном, где интервал содержания 1,3-диенового заместителя в изомерной смеси составляет от приблизительно 10% до приблизительно 90% для Е-изомера и от приблизительно 90% до приблизительно 10% для Z-изомера.
2. Композиция по п.1, отличающаяся тем, что недейтерированные изомеры представляют собой изомеры Е- и Z-, как они определены ниже
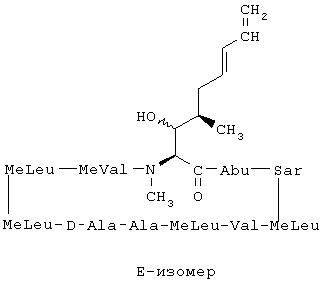
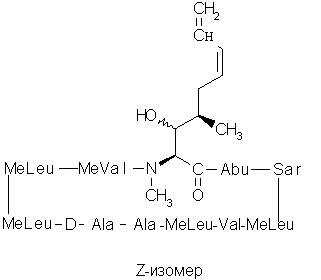
3. Композиция по п.2, отличающаяся тем, что изомерная смесь содержит от приблизительно 15% до приблизительно 85% Е-изомера и от приблизительно 85% до приблизительно 15% Z-изомера.
4. Композиция по п.2, отличающаяся тем, что изомерная смесь содержит от приблизительно 25% до приблизительно 75% Е-изомера и от приблизительно 75% до приблизительно 25% Z-изомера.
5. Композиция по п.2, отличающаяся тем, что изомерная смесь содержит от приблизительно 35% до приблизительно 65% Е-изомера и от приблизительно 65% до приблизительно 35% Z-изомера.
6. Композиция по п.2, отличающаяся тем, что изомерная смесь содержит от приблизительно 45% до приблизительно 55% Е-изомера и от приблизительно 55% до приблизительно 45% Z-изомера.
7. Композиция по п.2, отличающаяся тем, что изомерная смесь содержит от приблизительно 45% до приблизительно 50% Е-изомера и от приблизительно 55% до приблизительно 50% Z-изомера.
8. Композиция по п.2, отличающаяся тем, что изомерная смесь содержит от приблизительно 55% до приблизительно 50% Е-изомера и от приблизительно 45% до приблизительно 50% Z-изомера.
9. Композиция по п.2, отличающаяся тем, что изомерная смесь содержит от приблизительно 55% до приблизительно 65% Е-изомера и от приблизительно 45% до приблизительно 35% Z-изомера.
10. Композиция по п.2, отличающаяся тем, что изомерная смесь содержит от приблизительно 65% до приблизительно 75% Е-изомера и от приблизительно 35% до приблизительно 25% Z-изомера.
11. Композиция по п.2, отличающаяся тем, что изомерная смесь содержит от приблизительно 75% до приблизительно 85% Е-изомера и от приблизительно 25% до приблизительно 15% Z-изомера.
12. Композиция по п.2, отличающаяся тем, что изомерная смесь содержит от приблизительно 85% до приблизительно 90% Е-изомера и от приблизительно 15% до приблизительно 10% Z-изомера.
13. Композиция по п.2, отличающаяся тем, что изомерная смесь содержит от приблизительно 90% до приблизительно 95% Е-изомера и от приблизительно 10% до приблизительно 5% Z-изомера.
14. Фармацевтическая композиция, содержащая изомерную смесь аналога циклоспорина в соответствии с любым из пп.1-13 и фармацевтически приемлемый наполнитель.
15. Фармацевтическая композиция по п.14, отличающаяся тем, что она содержит жидкий раствор, содержащий поверхностно-активное вещество, этанол, липофильный и/или амфифильный растворитель.
16. Фармацевтическая композиция по п.15, отличающаяся тем, что она содержит d-альфа-токоферил-полиэтиленгликоль 1000 сукцинат (витамин Е TPGS), масло триглицерида со средней длиной цепи (МСТ), твин 40 и этанол.
17. Фармацевтическая композиция по п.14, отличающаяся тем, что она включает желатиновую капсулу, содержащую изомерную смесь аналогов, жидкий раствор, содержащий поверхностно-активное вещество, этанол, липофильный и/или амфифильный растворитель.
18. Фармацевтическая композиция по п.16, отличающаяся тем, что она представляет собой дозированную форму на один прием.
19. Фармацевтическая композиция по п.17, отличающаяся тем, что она представляет собой дозированную форму на один прием.
20. Фармацевтическая композиция по п.19, отличающаяся тем, что она содержит от приблизительно 5 мг до приблизительно 500 мг активного ингредиента.
21. Фармацевтическая композиция по п.15, отличающаяся тем, что она содержит приблизительно 50 мг изомерной смеси.
22. Фармацевтическая композиция по п.14, отличающаяся тем, что раствор содержит приблизительно 50 мг/мл изомерной смеси.
23. Фармацевтическая композиция по п.15, отличающаяся тем, что раствор содержит 50 мг/мл изомерной смеси.
24. Фармацевтическая композиция по п.14, отличающаяся тем, что она приспособлена для перорального введения.
25. Способ осуществления иммуносупрессии, включающий введение животному, в случае такой необходимости, эффективного количества изомерной смеси аналога циклоспорина в соответствии с любым из пп.1-13.
26. Способ по п.25, отличающийся тем, что указанное животное является человеком.
27. Способ по п.25, отличающийся тем, что количество вводимой изомерной смеси аналога циклоспорина составляет от приблизительно 0,05 мг на килограмм веса тела в день до приблизительно 50 мг на килограмм веса тела в день.
28. Способ по п.27, отличающийся тем, что количество вводимой изомерной смеси аналога циклоспорина составляет от приблизительно 0,1 мг на килограмм веса тела в день до приблизительно 10 мг на килограмм веса тела в день.
29. Способ по п.27, отличающийся тем, что количество вводимой изомерной смеси аналога циклоспорина составляет от приблизительно 0,5 мг/кг/деньдо приблизительно 10 мг/кг/день.
30. Способ по п.29, отличающийся тем, что количество вводимой изомерной смеси аналога циклоспорина составляет от приблизительно 2 мг/кг/день до приблизительно 6 мг/кг/день, вводимых перорально два раза в день.
31. Способ по п.30, отличающийся тем, что количество вводимой изомерной смеси аналога циклоспорина составляет от приблизительно 0,5 мг/кг/день до приблизительно 3 мг/кг/день, вводимых перорально два раза в день.
32. Способ повышения эффективности иммуносупрессорного аналога циклоспорина путем приготовления изомерной смеси аналога для применения в качестве иммуносупрессорного агента.
33. Способ по п.32, отличающийся тем, что указанная изомерная смесь содержит композицию по любому из пп.1-13.
34. Способ по п.33, отличающийся тем, что количество вводимой изомерной смеси аналога циклоспорина составляет от приблизительно 0,05 мг на килограмм веса тела в день до приблизительно 50 мг на килограмм веса тела в день.
35. Способ по п.25, отличающийся тем, что указанная иммуносупрессия предназначена для лечения или облегчения острого отторжения трансплантата органа или ткани.
36. Способ по п.35, отличающийся тем, что указанный трансплантат выбран из группы, состоящей из трансплантатов сердца, легкого, объединенных сердца-легкого, печени, почки, поджелудочной железы, кожи, кишечника и роговицы.
37. Способ п.25, отличающийся тем, что указанные иммуносупрессия или иммуносупрессорный агент предназначены для лечения или облегчения опосредованного Т-клетками отторжения.
38. Способ по п.25, отличающийся тем, что указанные иммуносупрессия или иммуносупрессорный агент предназначены для лечения или облегчения реакции "трансплантат против хозяина".
39. Способ по п.35, отличающийся тем, что указанное отторжение трансплантата органа или ткани является следствием трансплантации костного мозга.
40. Способ по п.25, отличающийся тем, что указанная иммуносупрессия предназначена для лечения или облегчения хронического отторжения трансплантированного органа.
41. Способ по п.37, отличающийся тем, что указанное хроническое отторжение представляет собой заболевание сосудов трансплантата.
42. Способ по п.25, отличающийся тем, что указанная иммуносупрессия предназначена для лечения или облегчения отторжения ксенотрансплантата.
43. Способ по п.42, отличающийся тем, что указанное отторжение ксенотрансплантата выбрано из группы, состоящей из острого, подострого и хронического отторжения органа, происходящего в том случае, когда донор органа принадлежит к иному биологическому виду, чем реципиент.
44. Способ по п.42, отличающийся тем, что указанное отторжение ксенотрансплантата представляет собой отторжение, опосредованное В-клетками или антителами.
45. Способ по п.25, отличающийся тем, что указанные иммуносупрессия или иммуносупрессорный агент предназначены для лечения или облегчения аутоиммунного заболевания или болезненного состояния, или воспалительного заболевания или болезненного состояния.
46. Способ по п.45, отличающийся тем, что указанное заболевание или болезненное состояние выбрано из группы, состоящей из артрита, ревматоидного артрита, хронического прогрессирующего артрита, деформирующего артрита и других ревматических заболеваний.
47. Способ по п.45, отличающийся тем, что указанное заболевание или болезненное состояние выбрано из группы, состоящей из гематологических расстройств (гемолитической анемии, гипопластической анемии, истинной эритроцитарной анемии, идиопатической тромбоцитопении), системной красной волчанки, полихондрии, склеродемы, гранулематоза Вегенера, дерматомиозита, хронического активного гепатита, миастении, псориаза, синдрома Стивенса-Джонсона, синдрома идиопатической мальабсорбции, (аутоиммунного) воспаления кишечника, язвенного колита, болезни Крона, эндокринной офтальмопатии, болезни Грейвса, саркоидоза, рассеянного склероза, первичного цирроза печени, юношеского диабета (сахарного диабета 1 типа), увеита (предшествующего и последующего), кератоконъюнктивита (keratoconjunctivitis sicca и vernal keratoconjunctivitis), интерстициального склероза легких, псориазного артрита, гломерулонефрита, идиопатического нефротического синдрома, нефропатии минимальных изменений и юношеского дерматомиозита.
48. Способ по п.45, отличающийся тем, что указанное заболевание или болезненное состояние выбрано из группы, состоящей из псориаза, контактного дерматита, атопического дерматита, очаговой алопеции, полиморфной эритемы, герпетиформного дерматита, склеродермии, витилиго, ангиита гиперчувствительности, крапивницы, буллезного пемфигоида, красной волчанки, пузырчатки, врожденного буллезного эпидермолиза, других воспалительных или аллергических болезненных состояний кожи, воспалительных болезненных состояний легких и дыхательных путей, астмы, аллергий и пневмокониоза.
49. Композиция, как она определена в любом из пп.1-13, в качестве терапевтической композиции.
50. Применение композиции, как она определена в любом из пп.1-13, для изготовления лекарственного средства для обеспечения иммуносупрессии с целью предотвращения отторжения аллотрансплантата или ксенотрансплантата, предпочтительно почки, сердца, печени, или предотвращения или лечения аутоиммунных болезненных состояний, в частности, ревматоидного артрита или псориаза.
51. Применение изомерной смеси аналога цикпоспорина в соответствии с любым из пп.1-13 для получения лекарственного средства для создания иммуносупрессии при введении животному.
52. Применение по п.51, отличающееся тем, что животное является человеком.
53. Применение по п.52, отличающееся тем, что количество подлежащей введению изомерной смеси аналога циклоспорина составляет от приблизительно 0,05 мг на килограмм веса тела в день до приблизительно 50 мг на килограмм веса тела в день.
54. Применение по п.52, отличающееся тем, что количество подлежащей введению изомерной смеси аналога циклоспорина составляет от приблизительно 0,1 мг на килограмм веса тела в день до приблизительно 10 мг на килограмм веса тела в день.
55. Применение по п.52, отличающееся тем, что количество подлежащей введению изомерной смеси аналога циклоспорина составляет от приблизительно 0,5 мг/кг/день до приблизительно 10 мг/кг/день.
56. Применение по п.52, отличающийся тем, что количество подлежащей введению изомерной смеси аналога циклоспорина составляет от приблизительно 2 мг/кг/день до приблизительно 6 мг/кг/день, вводимых перорально два раза в день.
57. Применение по п.52, отличающийся тем, что количество подлежащей введению изомерной смеси аналога циклоспорина составляет от приблизительно 0,5 мг/кг/день до приблизительно 3 мг/кг/день, вводимых перорально два раза в день.
58. Композиция, включающая изомерную смесь аналога циклоспорина, модифицированного в 1-м аминокислотном остатке заместителем 1,3-диеном, характеризующаяся тем, что изомерная смесь содержит не менее чем приблизительно 55% Е-изомера и не более чем приблизительно 45% Z-изомера.
59. Композиция по п.58, отличающаяся тем, что недейтерированные изомеры представляют собой изомеры Е- и Z-, как они определены ниже
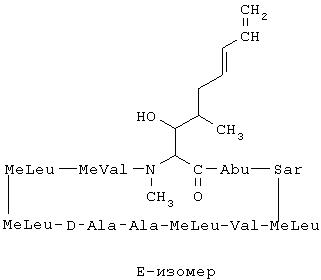
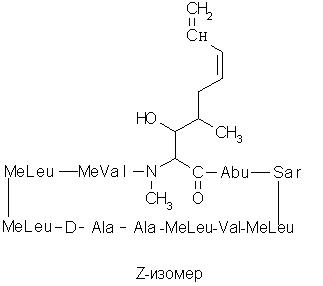
60. Композиция по п.59, отличающаяся тем, что изомерная смесь содержит от приблизительно 55% до приблизительно 65% Е-изомера и от приблизительно 35% до приблизительно 45% Z-изомера.
61. Композиция по п.59, отличающаяся тем, что изомерная смесь содержит от приблизительно 65% до приблизительно 75% Е-изомера и от приблизительно 25% до приблизительно 35% Z-изомера.
62. Композиция по п.59, отличающаяся тем, что изомерная смесь содержит от приблизительно 75% до приблизительно 85% Е-изомера и от приблизительно 15% до приблизительно 25% Z-изомера.
63. Композиция по п.59, отличающаяся тем, что изомерная смесь содержит от приблизительно 85% до приблизительно 90% Е-изомера и от приблизительно 10% до приблизительно 15% Z-изомера.
64. Композиция по п.59, отличающаяся тем, что изомерная смесь содержит от приблизительно 90% до приблизительно 95% Е-изомера и от приблизительно 10% до приблизительно 5% Z-изомера.
65. Композиция по п.59, отличающаяся тем, что изомерная смесь содержит не менее 95% Е-изомера и не более 5% Z-изомера.
66. Композиция, включающая изомерную смесь аналога циклоспорина, модифицированного в 1-м аминокислотном остатке заместителем 1,3-диеном, характеризующаяся тем, что изомерная смесь содержит не более чем приблизительно 45% Е-изомера и не менее чем приблизительно 55% Z-изомера.
67. Композиция по п.66, отличающаяся тем, что недейтерированные изомеры представляют собой изомеры Е- и Z-, как они определены ниже

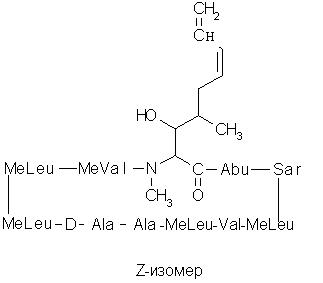
68. Композиция по п.67, отличающаяся тем, что изомерная смесь содержит от приблизительно 75% до приблизительно 65% Z-изомера и от приблизительно 25% до приблизительно 35% Е-изомера.
69. Композиция по п.67, отличающаяся тем, что изомерная смесь содержит от приблизительно 65% до приблизительно 55% Z-изомера и от приблизительно 35% до приблизительно 45% Е-изомера.
70. Фармацевтическая композиция, содержащая изомерную смесь аналога циклоспорина в соответствии с любым из пп.58-69 и фармацевтически приемлемый наполнитель.
71. Фармацевтическая композиция по п.70, отличающаяся тем, что она содержит жидкий раствор, содержащий поверхностно-активное вещество, этанол, липофильный и/или амфифильный растворитель.
72. Фармацевтическая композиция по п.70, отличающаяся тем, что она содержит d-альфа-токоферил-полиэтиленгликоль 1000 сукцинат (витамин Е TPGS), масло триглицерида со средней длиной цепи (МСТ), твин 40 и этанол.
73. Фармацевтическая композиция по п.70, отличающаяся тем, что она включает желатиновую капсулу, содержащую изомерную смесь аналогов, жидкий раствор, содержащий поверхностно-активное вещество, этанол, липофильный и/или амфифильный растворитель.
74. Фармацевтическая композиция по п.72, отличающаяся тем, что она представляет собой дозированную форму на один прием.
75. Фармацевтическая композиция по п.73, отличающаяся тем, что она представляет собой дозированную форму на один прием.
76. Фармацевтическая композиция по п.74, отличающаяся тем, что она содержит от приблизительно 5 мг до приблизительно 500 мг активного ингредиента.
77. Фармацевтическая композиция по п.75, отличающаяся тем, что она содержит от приблизительно 5 мг до приблизительно 500 мг активного ингредиента.
78. Фармацевтическая композиция по п.73, отличающаяся тем, что она содержит приблизительно 50 мг изомерной смеси.
79. Фармацевтическая композиция по п.71, отличающаяся тем, что раствор содержит 50 мг/мл изомерной смеси.
80. Фармацевтическая композиция по п.72, отличающаяся тем, что раствор содержит 50 мг/мл изомерной смеси.
81. Фармацевтическая композиция по п.70, отличающаяся тем, что она приспособлена для перорального введения.
82. Фармацевтическая композиция для осуществления иммуносупрессии при введении животному, включающая терапевтически эффективное количество изомерной смеси аналога циклоспорина в соответствии с любым из пп.58-69.
83. Фармацевтическая композиция по п.72, отличающаяся тем, что указанное животное является человеком.
84. Фармацевтическая композиция по п.73, отличающаяся тем, что указанное животное является человеком.
85. Фармацевтическая композиция по п.72, отличающаяся тем, что количество вводимой изомерной смеси аналога циклоспорина составляет от приблизительно 0,05 мг на килограмм веса тела в день до приблизительно 50 мг на килограмм веса тела в день.
86. Фармацевтическая композиция по п.73, отличающаяся тем, что количество вводимой изомерной смеси аналога циклоспорина составляет от приблизительно 0,05 мг на килограмм веса тела в день до приблизительно 50 мг на килограмм веса тела в день.
87. Фармацевтическая композиция для осуществления иммуносупрессии, включающая терапевтически эффективное количество изомерной смеси иммуносупрессорного аналога циклоспорина, в которой получение изомерной смеси снижает токсичность аналога циклоспорина, причем указанная изомерная смесь содержит композицию в соответствии с любым из пп.58-69.
88. Фармацевтическая композиция по п.70, отличающаяся тем, что она пригодна для лечения заболевания или состояния, выбранного из группы, состоящей из артрита, ревматоидного артрита, хронического прогрессирующего артрита, деформирующего артрита и других ревматических заболеваний.
89. Фармацевтическая композиция по п.70, отличающаяся тем, что она пригодна для лечения заболевания или состояния, выбранного из группы, состоящей из гематологических расстройств, гемолитической анемии, гипопластической анемии, истинной эритроцитарной анемии, идиопатической тромбоцитопении, системной красной волчанки, полихондрии, склеродемы, гранулематоза Вегенера, дерматомиозита, хронического активного гепатита, миастении, псориаза, синдрома Стивенса-Джонсона, синдрома идиопатической мальабсорбции, (аутоиммунного) воспаления кишечника, язвенного колита, болезни Крона, эндокринной офтальмопатии, болезни Грейвса, саркоидоза, рассеянного склероза, первичного цирроза печени, юношеского диабета (сахарного диабета 1 типа), увеита (предшествующего и последующего), кератоконъюнктивита (keratoconjunctivitis sicca и vernal keratoconjunctivitis), интерстициального склероза легких, псориазного артрита, гломерулонефрита, идиопатического нефротического синдрома, нефропатии минимальных изменений и юношеского дерматомиозита.
90. Фармацевтическая композиция по п.70, отличающаяся тем, что она пригодна для лечения заболевания или состояния, выбранного из группы, состоящей из псориаза, контактного дерматита, атопического дерматита, очаговой алопеции, полиморфной эритемы, герпетиформного дерматита, склеродермии, витилиго, ангиита гиперчувствительности, крапивницы, буллезного пемфигоида, красной волчанки, пузырчатки, врожденного буллезного эпидермолиза, других воспалительных или аллергических болезненных состояний кожи, воспалительных болезненных состояний легких и дыхательных путей, астмы, аллергий и пневмокониоза.
91. Применение композиции, как она определена в любом из пп.58-69, для изготовления лекарственного средства для обеспечения иммуносупрессии с целью предотвращения отторжения аллотрансплантата или ксенотрансплантата, предпочтительно почки, сердца, печени, или предотвращения или лечения аутоиммунных болезненных состояний, в частности, ревматоидного артрита или псориаза.

Комментарии