Библиотека зависимых от концентрации ионов связывающих молекул - RU2732151C2
Код документа: RU2732151C2
Чертежи
















Описание
ОБЛАСТЬ ТЕХНИКИ
РОДСТВЕННАЯ ЗАЯВКА
По настоящей заявке испрашивается приоритет на основе заявок на патент Японии № 2011-218006 (поданная 30 сентября 2011 года) и 2012-123479 (поданная 30 мая 2012 года), содержание которых включено в настоящее описание в качестве ссылки в полном объеме.
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к библиотеке антигенсвязывающих молекул, антигенсвязывающая активность которых изменяется в зависимости от условий концентрации ионов, к способу получения библиотеки, способу селекции таких антигенсвязывающих молекул, способу получения таких антигенсвязывающих молекул и к фармацевтической композиции, содержащей такую антигенсвязывающую молекулу.
УРОВЕНЬ ТЕХНИКИ
Антитела привлекли внимание в качестве фармацевтических средств вследствие их высокой стабильности в плазме и малых неблагоприятных реакций. Среди прочего, множество лекарственных средств на основе IgG-антител уже выпускается, и большое количество лекарственных средств на основе антител находятся на стадии разработки (непатентные документы 1 и 2). Между тем, были разработаны различные технологии, применимые для лекарственных средств на основе антител второго поколения. Например, описаны способы улучшения эффекторных функций, способности связывать антиген, фармакокинетики или стабильности, или снижения риска иммуногенности (непатентный документ 3). Возможными проблемами таких лекарственных средств на основе антител являются трудность получения препаратов для подкожного введения (поскольку лекарственные средства на основе антител обычно вводят в очень высоких дозах), высокая стоимость получения и т.д. Способы улучшения фармакокинетики антител и способы повышения аффинности антител к их антигенам можно использовать для снижения доз лекарственных средств на основе антител.
В качестве способа улучшения фармакокинетики антител была описана искусственная замена аминокислот в константных областях (непатентные документы 4 и 5). Ранее описанное созревание аффинности, способ усиления антигенсвязывающей способности и способности нейтрализовать антиген (непатентный документ 6), вовлекает мутацию аминокислот, например, в областях CDR вариабельных областей, для того, чтобы тем самым достигнуть усиленной антигенсвязывающей активности. Такое усиление антигенсвязывающей способности может улучшить биологическую активность in vitro или снизить дозы и может далее повышать эффективность лекарственного средства in vivo (непатентный документ 7).
Количество антигена, которое может быть нейтрализовано одной молекулой антитела, зависит от аффинности. Более высокая аффинность позволяет антителу в меньшем количестве нейтрализовывать антиген. Аффинность антитела можно повышать различными способами (непатентный документ 6). Антитело, способное ковалентно связываться с антигеном с неограниченной аффинностью, способно нейтрализовать, на одну молекулу, одну молекулу антигена (или два антигена в случае двухвалентного антитела). Однако предшествующие способы имеют стехиометрическое ограничение реакции нейтрализации вплоть до одной молекулы антигена (или две молекулы антигена в случае двухвалентного антитела) на молекулу антитела и неспособны полностью нейтрализовать антиген при использовании антитела в количестве ниже количества антигена. Кратко, существует ограничение эффекта повышения аффинности (непатентный документ 9). Присущая длительность нейтрализующего эффекта нейтрализующего антитела требует введения антитела в количестве выше количества антигена, продуцируемого in vivo за период времени. Единственно упомянутого выше способа улучшения фармакокинетики антител или созревания аффинности недостаточно для снижения необходимых доз антител. В этом отношении, одно антитело должно нейтрализовать множество антигенов для сохранения эффекта нейтрализации антигена в течение представляющего интерес периода времени в количестве ниже количества антигена.
Для достижения этой задачи недавно в качестве нового подхода было описано антитело, связывающееся с антигеном зависимым от pH образом (патентный документ 1). В указанном документе описано, что в антигенсвязывающую молекулу вносят остаток гистидина для получения антитела с pH-зависимым связыванием антигена, свойства которого изменяются между условиями нейтральных значений pH и кислых значений pH. Это антитело с pH-зависимым связыванием антигена прочно связывается с антигеном в нейтральных условиях в плазме и диссоциирует от антигена в кислых условиях в эндосоме. Таким образом, антитело с pH-зависимым связыванием антигена может диссоциировать от антигена в эндосоме. Антитело с pH-зависимым связыванием антигена, диссоциировавшее таким образом от антигена, может связываться с антигеном после рециклирования обратно в плазму через FcRn. Это позволяет одному антителу связываться с множеством антигенов многократно.
Антигены обладают очень коротким временем удержания в плазме по сравнению с антителами, которые рециклируют путем связывания с FcRn. Комплексы антитело-антиген в случае антител, имеющих длительное время полужизни в плазме (длительное время удержания в плазме), и таких антигенов, имеющих короткое время полужизни в плазме (короткое время удержания в плазме), имеют такое же длительное время удержания в плазме, как и антитела. Таким образом, связывание антигена с антителом скорее продлевает его время удержания в плазме и увеличивает концентрацию антигена в плазме. В таком случае, даже повышение аффинности антитела к антигену не может ускорить выведение антигена из плазмы. Таким образом, антитело с pH-зависимым связыванием антигена, упомянутое выше, также является более эффективным в качестве подхода для ускорения выведения антигена из плазмы, чем обычные антитела (патентный документ 1).
Таким образом, антитело с pH-зависимым связыванием антигена может связываться с множеством антигенов посредством одной молекулы антитела, ускоряя выведение антигенов из плазмы, по сравнению с обычными антителами, и само по себе имеет эффекты, которые не могут быть достигнуты с помощью обычных антител. Аминокислота в существующей последовательности антитела может быть заменена, чтобы тем самым придать ему активность pH-зависимого связывания антигена. Между тем, для получения такого нового антитела можно использовать способ получения антител из иммунизированных животных или способ получения антител из библиотеки антител человека, однако он имеет возможные ограничения, как описано ниже.
Способ, который вовлекает иммунизацию не являющих человеком животных, может обеспечить антитело с pH-зависимым связыванием, но редко может обеспечить антитела с pH-зависимым связыванием антигена против различных типов антигенов за короткий период времени или селективно обеспечить антитела, специфически связывающиеся с конкретными эпитопами. Альтернативно антитело может быть получено обогащением библиотеки антител человека со способностью к pH-зависимому связыванию антигена в качестве показателя. Однако общеизвестно, что частота появления остатков гистидина в вариабельных областях антитела человека (зарегистрированных в базе данных Кабат), не является высокой, как можно видеть, исходя из 5,9% для CDR1 тяжелой цепи, 1,4% для CDR2 тяжелой цепи, 1,6% для CDR3 тяжелой цепи, 1,5% для CDR1 тяжелой цепи, 0,5% для CDR2 тяжелой цепи и 2,2% для CDR3 легкой цепи, что указывает на то, что библиотека антител человека содержит только очень небольшое количество последовательностей, которые могут обладать способностью к pH-зависимому связыванию антигена. Таким образом, существует потребность в библиотеки антител, которая обладает увеличенной частотой встречаемости гистидина в антигенсвязывающих центрах и обогащена последовательностями, которые обладают способностью к pH-зависимому связыванию антигена.
Эффектов, таких как ускорение выведения антигена из плазмы, можно достигнуть, если антителу придать зависимость способности связывания антигена от фактора (отличного от pH), отличающегося между условиями плазмы и ранней эндосомы.
Ниже приведен список литературы в соответствии с настоящим изобретением.
Список литературы
Патентная литература
Патентный документ 1: WO2009125825
Непатентный документ
Непатентный документ 1: Janice M Reichert, Clark J Rosensweig, Laura B Faden & Matthew C Dewitz, Monoclonal antibody successes in the clinic, Nat. Biotechnol. (2005) 23, 1073-1078.
Непатентный документ 2: Pavlou AK, Belsey MJ., The therapeutic antibodies market to 2008, Eur J Pharm Biopharm. (2005) 59 (3), 389-396.
Непатентный документ 3: Kim SJ, Park Y, Hong HJ., Antibody engineering for the development of therapeutic antibodies, Mol Cells. (2005) 20 (1), 17-29.
Непатентный документ 4: Hinton PR, Xiong JM, Johlfs MG, Tang MT, Keller S, Tsurushita N., An engineered human IgG1 antibody with longer serum half-life, J Immunol. (2006) 176 (1), 346-356.
Непатентный документ 5: Ghetie V, Popov S, Borvak J, Radu C, Matesoi D, Medesan C, Ober RJ, Ward ES., Increasing the serum persistence of an IgG fragment by random mutagenesis, Nat. Biotechnol. (1997) 15 (7), 637-640.
Непатентный документ 6: Rajpal A, Beyaz N, Haber L, Cappuccilli G, Yee H, Bhatt RR, Takeuchi T, Lerner RA, Crea R., A general method for greatly improving the affinity of antibodies by using combinatorial libraries, Proc. Natl. Acad. Sci. USA. (2005) 102 (24), 8466-8471.
Непатентный документ 7: Wu H, Pfarr DS, Johnson S, Brewah YA, Woods RM, Patel NK, White WI, Young JF, Kiener PA. Development of Motavizumab, an Ultra-potent Antibody for the Prevention of Respiratory Syncytial Virus Infection in the Upper and Lower Respiratory Tract, J. Mol. Biol. (2007) 368, 652-665.
Непатентный документ 8: Hanson CV, Nishiyama Y, Paul S. Catalytic antibodies and their applications. Curr Opin Biotechnol, (2005) 16 (6), 631-6.
Непатентный документ 9: Rathanaswami P, Roalstad S, Roskos L, Su QJ, Lackie S, Babcook J. Demonstration of an in vivo generated sub-picomolar affinity fully human monoclonal antibody to interleukin-8, Biochem. Biophys. Res. Commun. (2005) 334 (4), 1004-13.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
ТЕХНИЧЕСКАЯ ПРОБЛЕМА
Настоящее изобретение было осуществлено с учетом такой ситуации, и задачей настоящего изобретения является предоставление библиотеки, по существу состоящей из множества антигенсвязывающих молекул, отличающихся друг от друга последовательностью, где антигенсвязывающий домен в каждой из антигенсвязывающих молекул содержит по меньшей мере один аминокислотный остаток, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов, композиции, содержащей множество полинуклеотидных молекул, каждая из которых кодирует антигенсвязывающие молекулы, композиции, содержащей множество векторов, каждый из которых содержит полинуклеотидные молекулы, способа селекции антигенсвязывающих молекул, способа выделения полинуклеотидных молекул, способа получения антигенсвязывающих молекул и фармацевтической композиции, содержащей любую из антигенсвязывающих молекул.
РЕШЕНИЕ ПРОБЛЕМЫ
Авторы настоящего изобретения провели тщательные исследования библиотеки, содержащей множество антигенсвязывающих молекул, отличающихся друг от друга последовательностью, где антигенсвязывающий домен в каждой из указанных антигенсвязывающих молекул содержит по меньшей мере один аминокислотный остаток, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от различий средового фактора in vivo. В результате, авторы настоящего изобретения сфокусировались на различиях в концентрации ионов, в частности в концентрации ионов кальция, между плазмой и ранней эндосомой, или pH этих сред и открыли, что использование антигенсвязывающих молекул, обладающих активностью кальций-зависимого или pH-зависимого связывания антигена, обеспечивает ускорение клеточного захвата антигенов антигенсвязывающими молекулами, и на получении библиотеки, по существу состоящей из антигенсвязывающих молекул, которые снижают концентрацию антигена в плазме.
В частности, настоящее изобретение относится к библиотеке, по существу состоящей из множества антигенсвязывающих молекул, отличающихся друг от друга последовательностью, где антигенсвязывающий домен в каждой из антигенсвязывающих молекул содержит по меньшей мере один аминокислотный остаток, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов, к композиции, содержащей множество полинуклеотидных молекул, каждая из которых кодирует антигенсвязывающую молекулу, композиции, содержащей множество векторов, каждый из которых содержит полинуклеотидные молекулы, к способу селекции антигенсвязывающих молекул, к способу выделения полинуклеотидных молекул, к способу получения антигенсвязывающих молекул, к фармацевтической композиции, содержащей любую из антигенсвязывающих молекул и т.д. Более конкретно, настоящее изобретение относится к следующему:
[1] Библиотека, по существу состоящая из множества антигенсвязывающих молекул, отличающихся друг от друга последовательностью, где антигенсвязывающий домен в каждой из антигенсвязывающих молекул содержит по меньшей мере один аминокислотный остаток, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов.
[2] Библиотека согласно [1], где концентрация ионов представляет собой концентрацию ионов кальция.
[3] Библиотека согласно [2], где аминокислотный остаток содержится в антигенсвязывающем домене тяжелой цепи антигенсвязывающей молекулы.
[4] Библиотека согласно [3], где антигенсвязывающий домен в тяжелой цепи представляет собой вариабельную область тяжелой цепи.
[5] Библиотека согласно [4], где аминокислотный остаток содержится в CDR3 вариабельной области тяжелой цепи.
[6] Библиотека согласно любому из [2]-[5], где аминокислотный остаток расположен в любом одном или более из положений 95, 96, 100a и 101, определяемых посредством нумерации по Кабату, в CDR3 тяжелой цепи.
[7] Библиотека согласно любому из [2]-[6], где аминокислотная последовательность, за исключением указанного аминокислотного остатка, содержит аминокислотную последовательность наивной последовательности.
[8] Библиотека согласно любому из [3]-[7], где вариабельная область легкой цепи антигенсвязывающей молекулы содержит аминокислотную последовательность наивной последовательности.
[9] Библиотека согласно [2], где аминокислотный остаток содержится в антигенсвязывающем домене легкой цепи антигенсвязывающей молекулы.
[10] Библиотека согласно [9], где антигенсвязывающий домен в легкой цепи представляет собой вариабельную область легкой цепи.
[11] Библиотека согласно [10], где аминокислотный остаток находится в CDR1 вариабельной области легкой цепи.
[12] Библиотека согласно [11], где аминокислотный остаток расположен в любом одном или более из положений 30, 31 и 32, определяемых посредством нумерации по Кабату, в CDR1.
[13] Библиотека согласно любому из [10]-[12], где аминокислотный остаток находится в CDR2 вариабельной области легкой цепи.
[14] Библиотека согласно [13], где аминокислотный остаток расположен в положении 50, определяемом посредством нумерации по Кабату, в CDR2 легкой цепи.
[15] Библиотека согласно любому из [10]-[14], где аминокислотный остаток находится в CDR3 легкой цепи.
[16] Библиотека согласно [15], где аминокислотный остаток расположен в положении 92, определяемом посредством нумерации по Кабату, в CDR3 легкой цепи.
[17] Библиотека согласно любому из [2] и [9]-[16], где каркасная область легкой цепи в антигенсвязывающей молекуле содержит каркасную последовательность эмбрионального типа.
[18] Библиотека согласно любому из [2] и [9]-[17], где вариабельная область тяжелой цепи антигенсвязывающей молекулы содержит аминокислотную последовательность наивной последовательности.
[19] Библиотека согласно любому из [1]-[18], где аминокислотный остаток формирует кальций-связывающий мотив.
[20] Библиотека согласно [19], где кальций-связывающий мотив представляет собой любой кальций-связывающий мотив, выбранный из домена кадгерина, EF hand, домена C2, домена Gla, лектина C-типа, домена A, аннексина, домена тромбоспондина 3 типа, EGF-подобного домена, домена Vk5, домена, представленного SEQ ID NO: 10, и домена, представленного SEQ ID NO: 11.
[21] Библиотека согласно любому из [2]-[20], где аминокислотный остаток представляет собой аминокислоту, обладающую эффектом хелатирования металлов.
[22] Библиотека согласно [21], где аминокислота, обладающая эффектом хелатирования металлов, представляет собой любую одну или более аминокислот, выбранных из серина, треонина, аспарагина, глутамина, аспарагиновой кислоты и глутаминовой кислоты.
[23] Библиотека согласно [1], где условия концентрации ионов представляют собой условия pH.
[24] Библиотека согласно [23], где аминокислотный остаток находится в антигенсвязывающем домене тяжелой цепи антигенсвязывающей молекулы.
[25] Библиотека согласно [24], где антигенсвязывающий домен тяжелой цепи представляет собой вариабельную область тяжелой цепи.
[26] Библиотека согласно [25], где аминокислотный остаток расположен в любом одном или более из положений 27, 31, 32, 33, 35, 50, 52, 53, 55, 57, 58, 59, 61, 62, 95, 96, 97, 98, 99, 100a, 100b, 100d, 100f, 100h, 102 и 107, определяемых посредством нумерации по Кабату, в вариабельной области тяжелой цепи.
[27] Библиотека согласно [26], где аминокислотная последовательность, за исключением аминокислотного остатка в любом одном или более из положений 27, 31, 32, 33, 35, 50, 52, 53, 55, 57, 58, 59, 61, 62, 95, 96, 97, 98, 99, 100a, 100b, 100d, 100f, 100h, 102 и 107, определяемых посредством нумерации по Кабату, в вариабельной области тяжелой цепи содержит аминокислотную последовательность наивной последовательности.
[28] Библиотека согласно любому из [23]-[27], где вариабельная область легкой цепи антигенсвязывающей молекулы содержит последовательность эмбрионального типа.
[29] Библиотека согласно [23], где аминокислотный остаток находится в антигенсвязывающем домене легкой цепи антигенсвязывающей молекулы.
[30] Библиотека согласно [29], где антигенсвязывающий домен в легкой цепи представляет собой вариабельную область легкой цепи.
[31] Библиотека согласно [30], где аминокислотный остаток расположен в любом одном или более из положений 24, 27, 28, 30, 31, 32, 34, 50, 51, 52, 53, 54, 55, 56, 89, 90, 91, 92, 93, 94 и 95a, определяемых посредством нумерации по Кабату, в вариабельной области легкой цепи.
[32] Библиотека согласно [30] или [31], где аминокислотный остаток находится в CDR1 вариабельной области легкой цепи.
[33] Библиотека согласно [32], где аминокислотный остаток расположен в любом одном или более из положений 24, 27, 28, 30, 31, 32 и 34, определяемых посредством нумерации по Кабату, в CDR1 легкой цепи.
[34] Библиотека согласно любому из [30]-[33], где аминокислотный остаток находится в CDR2 легкой цепи.
[35] Библиотека согласно [34], где аминокислотный остаток расположен в любом одном или более из положений 50, 51, 52, 53, 54, 55 и 56, определяемых посредством нумерации по Кабату, в CDR2 легкой цепи.
[36] Библиотека согласно любому из [30]-[35], где аминокислотный остаток находится в CDR3 легкой цепи.
[37] Библиотека согласно [36], где аминокислотный остаток расположен в любом одном или более из положений 89, 90, 91, 92, 93, 94 и 95a, определяемых посредством нумерации по Кабату, в CDR3 легкой цепи.
[38] Библиотека согласно любому из [29]-[37], где каркасная область легкой цепи содержит каркасную последовательность эмбрионального типа.
[39] Библиотека согласно любому из [29]-[38], где вариабельная область тяжелой цепи имеет наивную последовательность.
[40] Библиотека согласно любому из [23]-[39], где аминокислотный остаток представляет собой аминокислоту, имеющую pKa боковой цепи от 4,0 до 8,0.
[41] Библиотека согласно любому из [23]-[40], где аминокислотный остаток представляет собой глутаминовую кислоту.
[42] Библиотека согласно любому из [23]-[39], где аминокислотный остаток представляет собой аминокислоту, имеющую pKa боковой цепи от 5,5 до 7,0.
[43] Библиотека согласно любому из [23]-[40] и [42], где аминокислотный остаток представляет собой гистидин.
[44] Библиотека, по существу состоящая из множества слитых полипептидов, каждый из которых содержит антигенсвязывающие молекулы согласно любому из [1]-[43], где каждый из слитых полипептидов представляет собой продукт слияния вариабельной области тяжелой цепи антигенсвязывающей молекулы и по меньшей мере части белка вирусной оболочки.
[45] Библиотека согласно [44], где белок вирусной оболочки выбран из группы, состоящей из белка pIII, основного белка оболочки pVIII, pVII, pIX, Soc, Hoc, gpD, pv1 и их вариантов.
[46] Композиция, содержащая множество полинуклеотидных молекул, каждая из которых кодирует антигенсвязывающие молекулы, отличающиеся друг от друга последовательностью, согласно любому из [1]-[43] или слитые полипептиды, отличающиеся друг от друга последовательностью, согласно [44] или [45].
[47] Композиция, содержащая множество векторов, каждый из которых содержит множество полинуклеотидных молекул согласно [46] в функционально связанном состоянии.
[48] Композиция согласно [47], где векторы представляют собой экспрессирующие векторы, которые можно реплицировать.
[49] Композиция согласно [48], где каждый из экспрессирующих векторов, которые можно реплицировать, представляет собой экспрессирующий вектор, в котором полинуклеотид функционально связан с промоторной областью, выбранной из группы, состоящей из промоторной системы lacZ, промотора щелочной фосфатазы phoA (Ap), промотора бактериофага λPL (чувствительный к температуре промотор), промотора tac, промотора триптофана, промотора pBAD и промотора бактериофага T7.
[50] Композиция согласно [48] или [49], где каждый из экспрессирующих векторов, которые можно реплицировать, представляет собой фаг M13, f1, fd или Pf3 или его производное, или лямбдоидный фаг или его производное.
[51] Композиция, содержащая множество вирусов, каждый из которых содержит векторы согласно любому из [47]-[50].
[52] Композиция, содержащая множество вирусов, каждый из которых экспонирует на своей поверхности антигенсвязывающие молекулы, отличающиеся друг от друга последовательностью, согласно любому из [1]-[43] или слитые полипептиды, отличающиеся друг от друга последовательностью, согласно [44] или [45].
[53] Библиотека, содержащая антигенсвязывающие молекулы, отличающиеся друг от друга последовательностью, согласно любому из [1]-[43] или слитые полипептиды, отличающиеся друг от друга последовательностью, согласно [44] или [45], где библиотека имеет от 1×106 до 1×1014 различных последовательностей вариабельной области.
[54] Библиотека согласно [53], где библиотека имеет 1×108 или более различных последовательностей вариабельной области.
[55] Способ получения библиотеки, по существу состоящей из множества антигенсвязывающих молекул, отличающихся друг от друга последовательностью, причем способ включает получение множества антигенсвязывающих молекул, сконструированных так, что антигенсвязывающий домен в каждой из антигенсвязывающих молекул содержит по меньшей мере один аминокислотный остаток, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов.
[56] Способ получения согласно [55], где антигенсвязывающие молекулы представляют собой антигенсвязывающие молекулы согласно любому из [2]-[43].
[57] Способ получения согласно [55] или [56], где вариабельная область тяжелой цепи каждой из антигенсвязывающих молекул является слитой по меньшей мере с частью белка вирусной оболочки.
[58] Способ получения согласно любому из [55]-[57], где белок вирусной оболочки выбран из группы, состоящей из белка pIII, основного белка оболочки pVIII, pVII, pIX, Soc, Hoc, gpD, pv1 и их вариантов.
[59] Способ селекции антигенсвязывающей молекулы, антигенсвязывающая активность которой изменяется в зависимости от условий концентрации ионов, причем способ включает стадии:
a) получение библиотеки, по существу состоящей из антигенсвязывающих молекул, отличающихся друг от друга последовательностью, согласно любому из [1]-[43] или слитых полипептидов, отличающихся друг от друга последовательностью, согласно [44] или [45];
b) приведение библиотеки в контакт с антигенами при двух или более различных условиях концентрации ионов;
c) сортировка из библиотеки субпопуляции антигенсвязывающих молекул, антигенсвязывающая активность которых изменяется в зависимости от условий концентрации ионов; и
d) выделение каждой антигенсвязывающей молекулы, антигенсвязывающая активность которой изменяется в зависимости от условий концентрации ионов, из субпопуляции, отсортированной на стадии c).
[60] Способ выделения полинуклеотида, кодирующего антигенсвязывающую молекулу, антигенсвязывающая активность которой изменяется в зависимости от условий концентрации ионов, причем способ включает стадии:
a) получение библиотеки, содержащей множество экспрессирующих векторов, которые можно реплицировать, каждый из которых содержит в функционально связанном состоянии множество полинуклеотидов, каждый из которых кодирует антигенсвязывающие молекулы, отличающиеся друг от друга последовательностью, согласно любому из [1]-[43] или слитые полипептиды, отличающиеся друг от друга последовательностью, согласно [44] или [45];
b) обеспечение возможности множеству вирусов, каждый из которых трансформирован экспрессирующими векторами, содержащимися в библиотеке, экспрессировать на своей поверхности антигенсвязывающие молекулы или слитые полипептиды, отличающиеся друг от друга последовательностью, кодируемые полинуклеотидами;
c) приведение множества вирусов в контакт с антигенами при двух или более различных условиях концентрации ионов;
d) сортировка из библиотеки субпопуляции вирусов, антигенсвязывающая активность которых изменяется в зависимости от условий концентрации ионов;
e) выделение каждого вируса, антигенсвязывающая активность которого изменяется в зависимости от условий концентрации ионов, из субпопуляции вирусов, отсортированных на стадии d); и
f) выделение полинуклеотидов из выделенного вируса.
[61] Способ согласно [60], где стадии c) и d) дополнительно повторяют по меньшей мере один раз.
[62] Способ согласно любому из [59]-[61], где концентрация ионов представляет собой концентрацию ионов кальция.
[63] Способ согласно [62], где отбирают антигенсвязывающую молекулу, имеющую более низкую антигенсвязывающую активность в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция.
[64] Способ согласно [63], где условия низкой концентрации кальция представляют собой условия от 0,1 мкМ до 30 мкМ.
[65] Способ согласно [63] или [64], где условия высокой концентрации кальция представляют собой условия от 100 мкМ до 10 мМ.
[66] Способ согласно любому из [59]-[61], где условия концентрации ионов представляют собой условия pH.
[67] Способ согласно [66], где отбирают антигенсвязывающую молекулу, имеющую более низкую антигенсвязывающую активность в условиях кислых значений pH, чем в условиях нейтральных значений pH.
[68] Способ согласно [66], где условия кислых значений pH представляют собой условия pH от 4,0 до 6,5.
[69] Способ согласно [67] или [68], где условия нейтральных значений pH представляют собой условия pH от 6,7 до 10,0.
[70] Способ получения антигенсвязывающей молекулы, антигенсвязывающая активность которой изменяется в зависимости от условий концентрации ионов, причем способ включает стадии:
a) получение библиотеки, содержащей множество экспрессирующих векторов, которые можно реплицировать, каждый из которых содержит в функционально связанном состоянии множество полинуклеотидов, каждый из которых кодирует антигенсвязывающие молекулы, отличающиеся друг от друга последовательностью, согласно любому из [1]-[43] или слитые полипептиды, отличающиеся друг от друга последовательностью, согласно [44] или [45];
b) обеспечение возможности множеству вирусов, каждый из которых трансформирован экспрессирующими векторами, содержащимися в библиотеке, экспрессировать на своей поверхности антигенсвязывающие молекулы или слитые полипептиды, отличающиеся друг от друга последовательностью, кодируемые полинуклеотидами;
c) приведение множества вирусов в контакт с антигенами при двух или более различных условиях концентрации ионов;
d) сортировка из библиотеки субпопуляции вирусов, антигенсвязывающая активность которых изменяется в зависимости от условий концентрации ионов;
e) выделение каждого вируса, антигенсвязывающая активность которого изменяется в зависимости от условий концентрации ионов, из субпопуляции вирусов, отсортированных на стадии d);
f) выделение полинуклеотидов из выделенного вируса;
g) культивирование клетки-хозяина, трансфицированной вектором, имеющим функционально связанную вставку выделенных полинуклеотидов; и
h) сбор антигенсвязывающих молекул из культур клеток, культивируемых на стадии g).
[71] Способ получения антигенсвязывающей молекулы, антигенсвязывающая активность которой изменяется в зависимости от условий концентрации ионов, причем способ включает стадии:
a) получение библиотеки, содержащей множество экспрессирующих векторов, которые можно реплицировать, каждый из которых содержит в функционально связанном состоянии множество полинуклеотидов, каждый из которых кодирует антигенсвязывающие молекулы, отличающиеся друг от друга последовательностью, согласно любому из [1]-[43] или слитые полипептиды, отличающиеся друг от друга последовательностью, согласно [44] или [45];
b) обеспечение возможности множеству вирусов, каждый из которых трансформирован экспрессирующими векторами, содержащимися в библиотеке, экспрессировать на своей поверхности антигенсвязывающие молекулы или слитые полипептиды, отличающиеся друг от друга последовательностью, кодируемые полинуклеотидами;
c) приведение множества вирусов в контакт с антигенами при двух или более различных условиях концентрации ионов;
d) сортировка из библиотеки субпопуляции вирусов, антигенсвязывающая активность которых изменяется в зависимости от условий концентрации ионов;
e) выделение каждого вируса, антигенсвязывающая активность которого изменяется в зависимости от условий концентрации ионов, из субпопуляции вирусов, отсортированных на стадии d);
f) выделение полинуклеотидов из выделенного вируса;
g) связывание выделенных полинуклеотидов в рамке считывания с полинуклеотидом, кодирующим константную область антитела;
h) культивирование клетки-хозяина, трансфицированной вектором, имеющим функционально связанную вставку полинуклеотидов, связанных на стадии g); и
i) выделение антигенсвязывающих молекул из культур клеток, культивируемых на стадии h).
[72] Способ получения согласно [70] или [71], где стадии c) и d) дополнительно повторяют по меньшей мере один раз.
[73] Способ получения согласно любому из [70]-[72], где концентрация ионов представляет собой концентрацию ионов кальция.
[74] Способ получения согласно [73], где выбирают антигенсвязывающую молекулу, имеющую более низкую антигенсвязывающую активность в условиях низкой концентрации кальция, чем в условиях высокой концентрации кальция.
[75] Способ получения согласно [74], где условия низкой концентрации кальция представляют собой условия от 0,1 мкМ до 30 мкМ.
[76] Способ получения согласно [74] или [75], где условия высокой концентрации кальция представляют собой условия от 100 мкМ до 10 мМ.
[77] Способ получения согласно любому из [70]-[72], где условия концентрации ионов представляют собой условия pH.
[78] Способ получения согласно [77], где отбирают антигенсвязывающую молекулу, имеющую более низкую антигенсвязывающую активность в условиях кислых значений pH, чем в условиях нейтральных значений pH.
[79] Способ получения согласно [78], где условия кислых значений pH представляют собой условия pH от 4,0 до 6,5.
[80] Способ получения согласно [78] или [79], где условия нейтральных значений pH представляют собой условия от pH 6,7 до 10,0.
[81] Антигенсвязывающая молекула, полученная способом получения согласно любому из [70]-[80].
[82] Фармацевтическая композиция, содержащая антигенсвязывающую молекулу согласно [81] или ее модифицированную форму.
Краткое описание чертежей
[Фиг. 1] На фиг. 1 представлен график, на котором показана взаимосвязь между распределением аминокислот (указано как библиотека) для информации о последовательности приблизительно 132 клонов, выделенных из E. coli, трансформированных библиотекой генов антител, связывающихся с антигенами pH-зависимым образом, и модельным распределением аминокислот (обозначено как модель). На оси абсцисс представлено положение аминокислоты, определяемое посредством нумерации по Кабату. На оси ординат представлена доля каждой аминокислоты в распределении.
[Фиг. 2] На фиг. 2 представлены сенсограммы для антитела против IL-6R (тоцилизумаб), антитела 6RpH#01, антитела 6RpH#02 и антитела 6RpH#03 при pH 7,4. На оси абсцисс представлено время. На оси ординат представлены величины RU.
[Фиг. 3] На фиг. 3 представлены сенсограммы для антитела против IL-6R (тоцилизумаб), антитела 6RpH#01, антитела 6RpH#02 и антитела 6RpH#03 при pH 6,0. На оси абсцисс представлено время. На оси ординат представлены величины RU.
[Фиг. 4A] На фиг. 4A представлена диаграмма, на которой показан профиль взаимодействия между антителом с pH-зависимым связыванием и его антигеном в плазме (pH 7,4) и в эндосоме (pH 6,0).
[Фиг. 4B] На фиг. 4B представлена диаграмма, на которой показан профиль взаимодействия между антителом с кальций-зависимым связыванием и его антигеном в плазме (2 мМ Ca2+) и в эндосоме (3 мкМ Ca2+).
[Фиг. 4C] На фиг. 4C представлена диаграмма, на которой показан профиль взаимодействия между антителом с pH- и кальций-зависимым связыванием и его антигеном в плазме (2 мМ Ca2+) и в эндосоме (3 мкМ Ca2+).
[Фиг. 5] На фиг. 5 представлены ионообменные хроматограммы для антитела, содержащего последовательность Vk5-2 человека, и антитела, содержащего последовательность hVk5-2_L65, модифицированную из последовательности Vk5-2 человека в участке последовательности гликозилирования. Сплошная линия соответствует хроматограмме для антитела, содержащего последовательность Vk5-2 человека (тяжелая цепь: CIM_H (SEQ ID NO: 4) и легкая цепь: hVk5-2 (SEQ ID NO: 1, слитая с SEQ ID NO: 26)). Пунктирная линия соответствует хроматограмме для антитела, имеющего последовательность hVk5-2_L65 (тяжелая цепь: CIM_H (SEQ ID NO: 4) и легкая цепь: hVk5-2_L65 (SEQ ID NO: 5)).
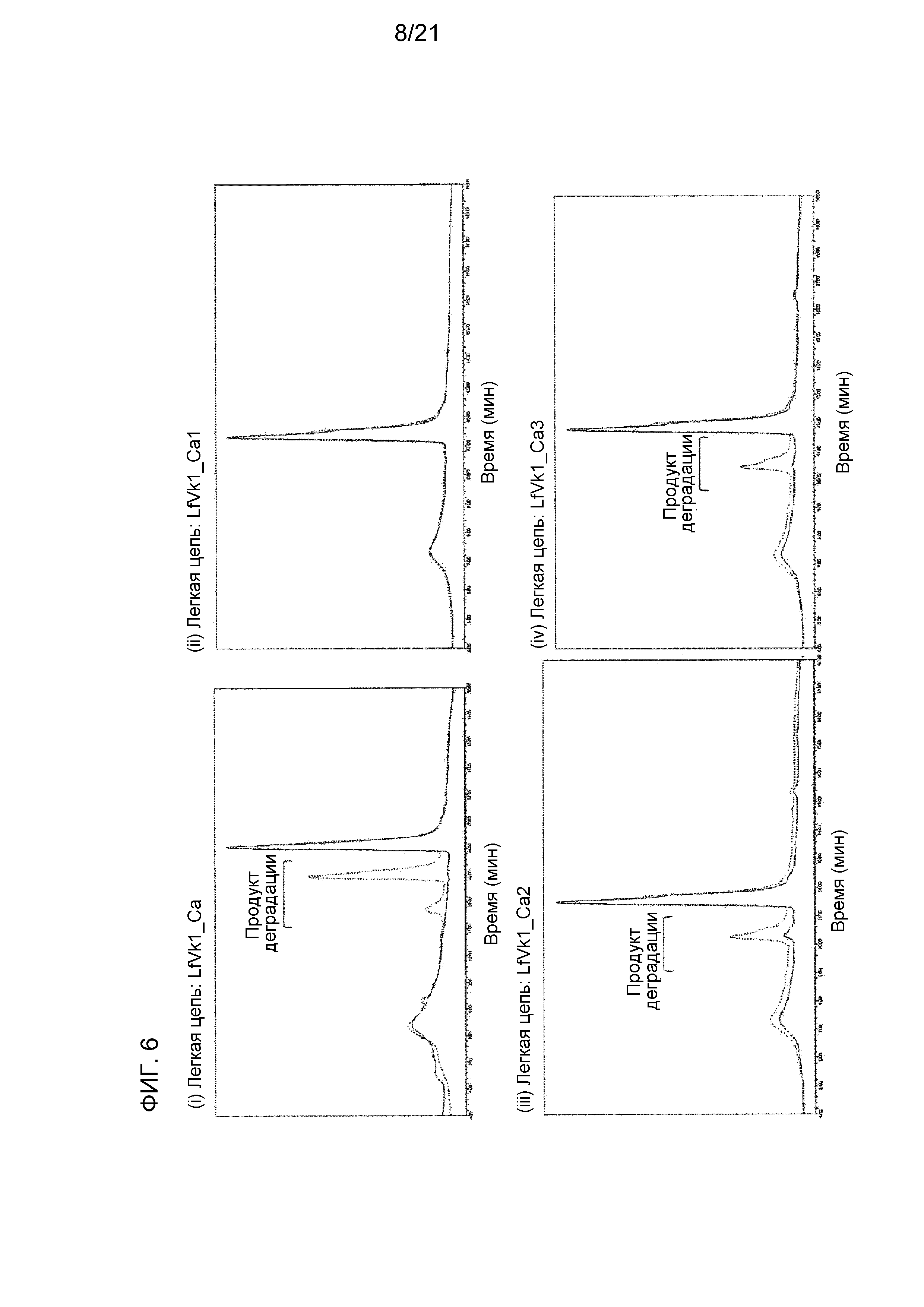
[Фиг. 6] На фиг. 6 представлены ионообменные хроматограммы для антитела, содержащего последовательность LfVk1_Ca (тяжелая цепь: GC_H (SEQ ID NO: 48) и легкая цепь: LfVk1_Ca (SEQ ID NO: 43)), и антитела, содержащего последовательность, модифицированную из последовательности LfVk1_Ca путем замены остатка Asp (D) на остаток Ala (A), после хранения при 5°C (сплошная линия) или после хранения при 50°C (пунктирная линия). Наиболее высокий пик на каждой ионообменной хроматограмме после хранения при 5°C определяют как основной пик. На диаграмме ось y нормализована по основному пику.
[Фиг. 7] На фиг. 7 представлены ионообменные хроматограммы для антитела, содержащего последовательность LfVk1_Ca (тяжелая цепь: GC_H (SEQ ID NO: 48) и легкая цепь: LfVk1_Ca (SEQ ID NO: 43)), и антитела, содержащего последовательность LfVk1_Ca6 (тяжелая цепь: GC_H (SEQ ID NO: 48) и легкая цепь: LfVk1_Ca6 (SEQ ID NO: 49)), модифицированную из последовательности LfVk1_Ca путем замены остатка Asp (D) в положении 30 (определяемом посредством нумерации по Кабату) на остаток Ser (S) после хранения при 5°C (сплошная линия) или после хранения при 50°C (пунктирная линия). Наиболее высокий пик на каждой ионообменной хроматограмме после хранения при 5°C определяют как основной пик. На диаграмме ось y нормализована по основному пику.
[Фиг. 8] На фиг. 8 представлен график, на котором показана взаимосвязь между распределением аминокислот (указано как библиотека) для информации о последовательности приблизительно 290 клонов, выделенных из E. coli, трансформированных библиотекой генов антител, связывающихся с антигенами Ca-зависимым образом, и модельным распределением аминокислот (указано как модель). На оси абсцисс представлено положение аминокислоты, определяемое посредством нумерации по Кабату. На оси ординат представлена доля каждой аминокислоты в распределении.
[Фиг. 9] На фиг. 9 представлены сенсограммы для антитела против IL-6R (тоцилизумаб), антитела 6RC1IgG_010, антитела 6RC1IgG_012 и антитела 6RC1IgG_019 в условиях высокой концентрации ионов кальция (1,2 мМ). На оси абсцисс представлено время. На оси ординат представлены величины RU.
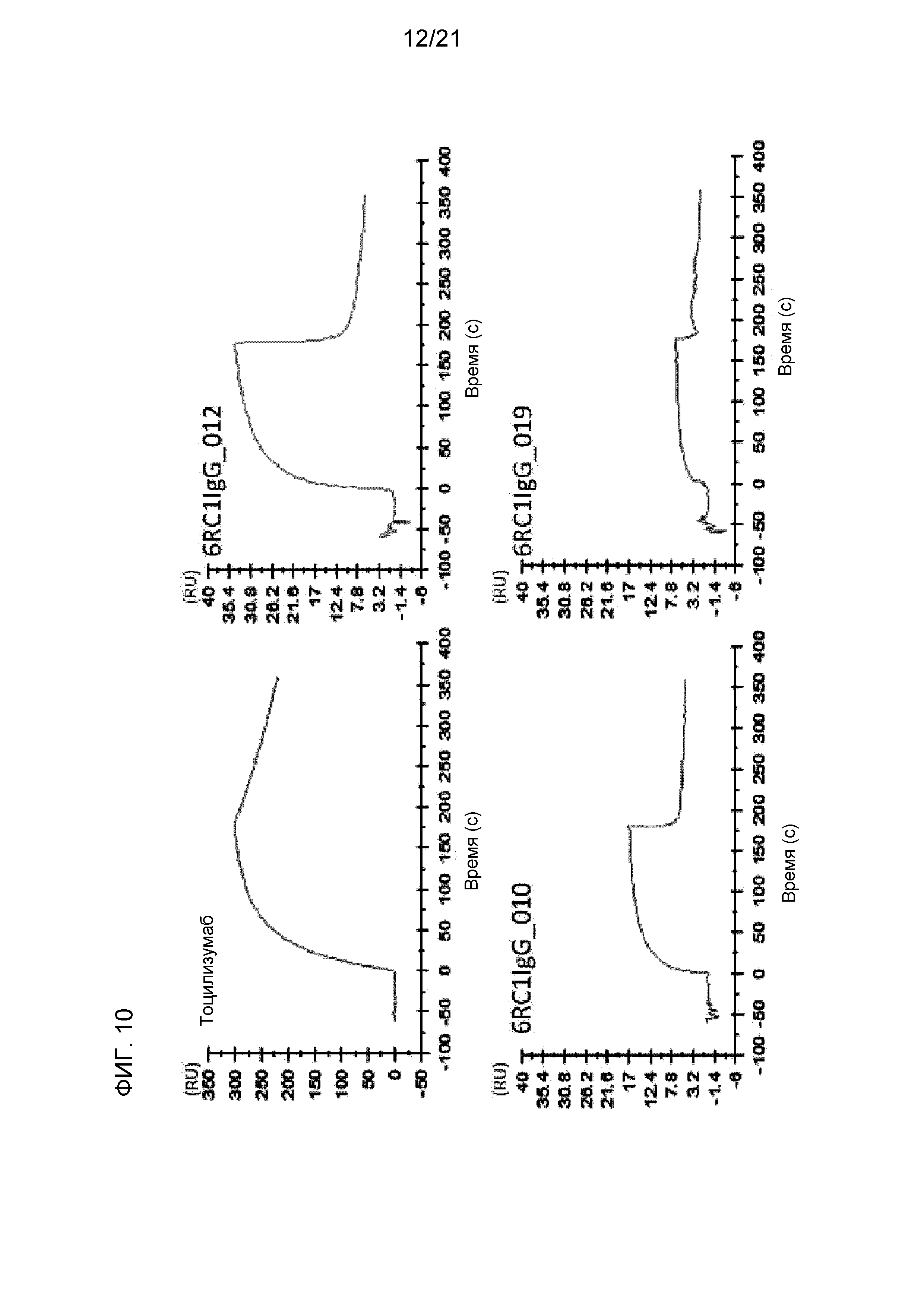
[Фиг. 10] На фиг. 10 представлены сенсограммы для антитела против IL-6R (тоцилизумаб), антитела 6RC1IgG_010, антитела 6RC1IgG_012 и антитела 6RC1IgG_019 в условиях низкой концентрации ионов кальция (3 мкМ). На оси абсцисс представлено время. На оси ординат представлены величины RU.
[Фиг. 11] На фиг. 11 представлена структура CDR3 тяжелой цепи в Fab-фрагменте антитела 6RL#9, определенная рентгеноструктурным анализом. На фиг. 11(i) представлена диаграмма, на которой показана CDR3 тяжелой цепи с кристаллической структурой, полученной в условиях кристаллизации в присутствии ионов кальция. На фиг. 11(ii) представлена диаграмма, на которой показана CDR3 тяжелой цепи с кристаллической структурой, полученной в условиях кристаллизации в отсутствие ионов кальция.
[Фиг. 12] На фиг. 12 представлена сенсограмма, отражающая взаимодействие между антителом против IgA человека и IgA человека при 1,2 мМ Ca2+ и при 3 мкМ Ca2+ с использованием Biacore.
[Фиг. 13] На фиг. 13 представлена диаграмма, отражающая взаимодействие между антителом против глипикана 3 человека и рекомбинантным глипиканом 3 человека при 1,2 мМ Ca2+ и при 3 мкМ Ca2+ с использованием ELISA.
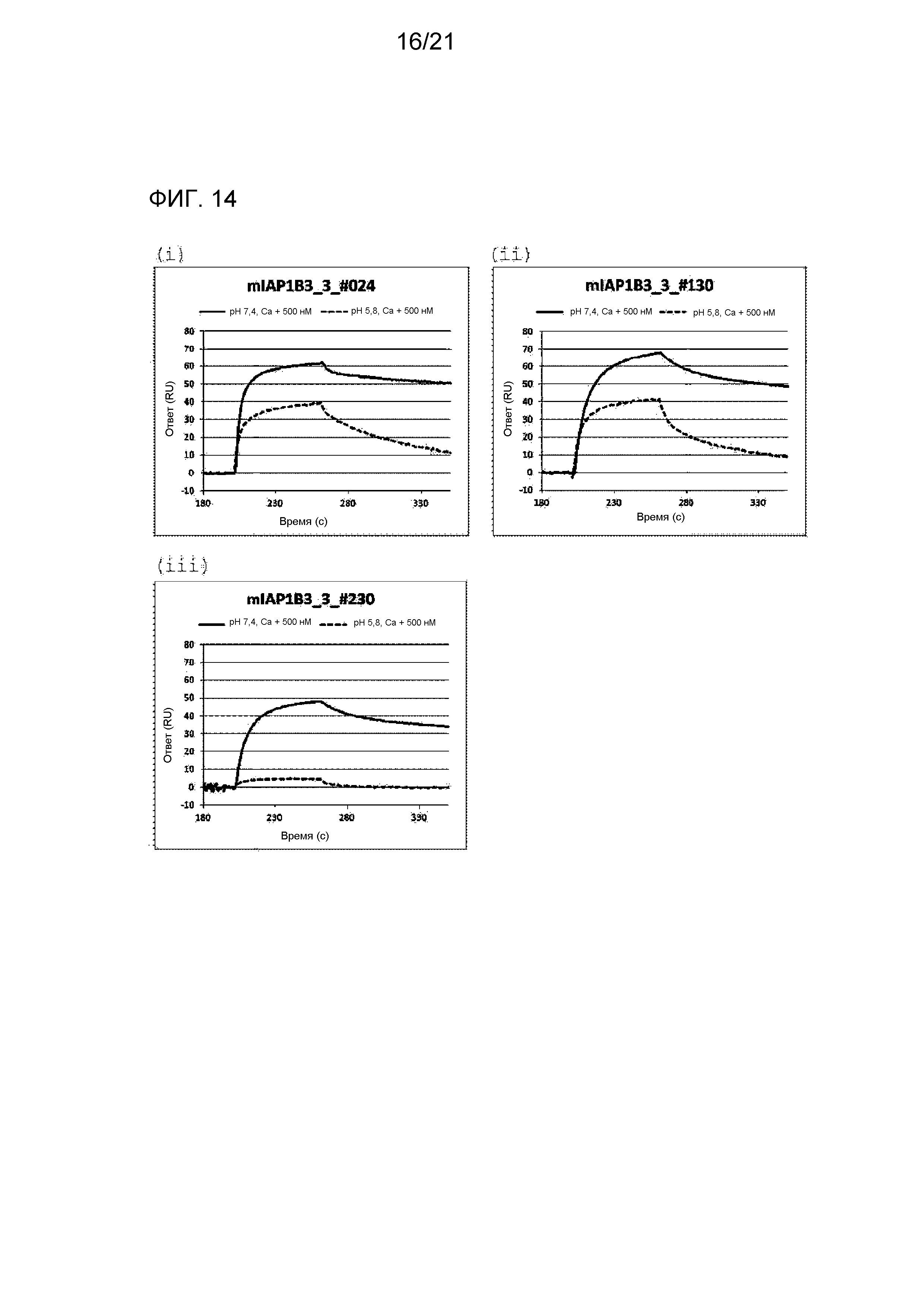
[Фиг. 14] На фиг. 14 представлена сенсограмма, отражающая взаимодействие между антителом против IgA мыши и IgA мыши при pH 7,4 и при pH 5,8 с использованием Biacore. Сплошная линия соответствует результатам в условиях приблизительно pH 7,4. Пунктирная линия соответствует результатам в условиях приблизительно pH 5,8.
[Фиг. 15] На фиг. 15 представлена сенсограмма, отражающая взаимодействие между антителом против HMGB1 человека и HMGB1 человека при pH 7,4 и при pH 5,8 с использованием Biacore. Сплошная линия соответствует результатам в условиях приблизительно pH 7,4. Пунктирная линия соответствует результатам в условиях приблизительно pH 5,8.
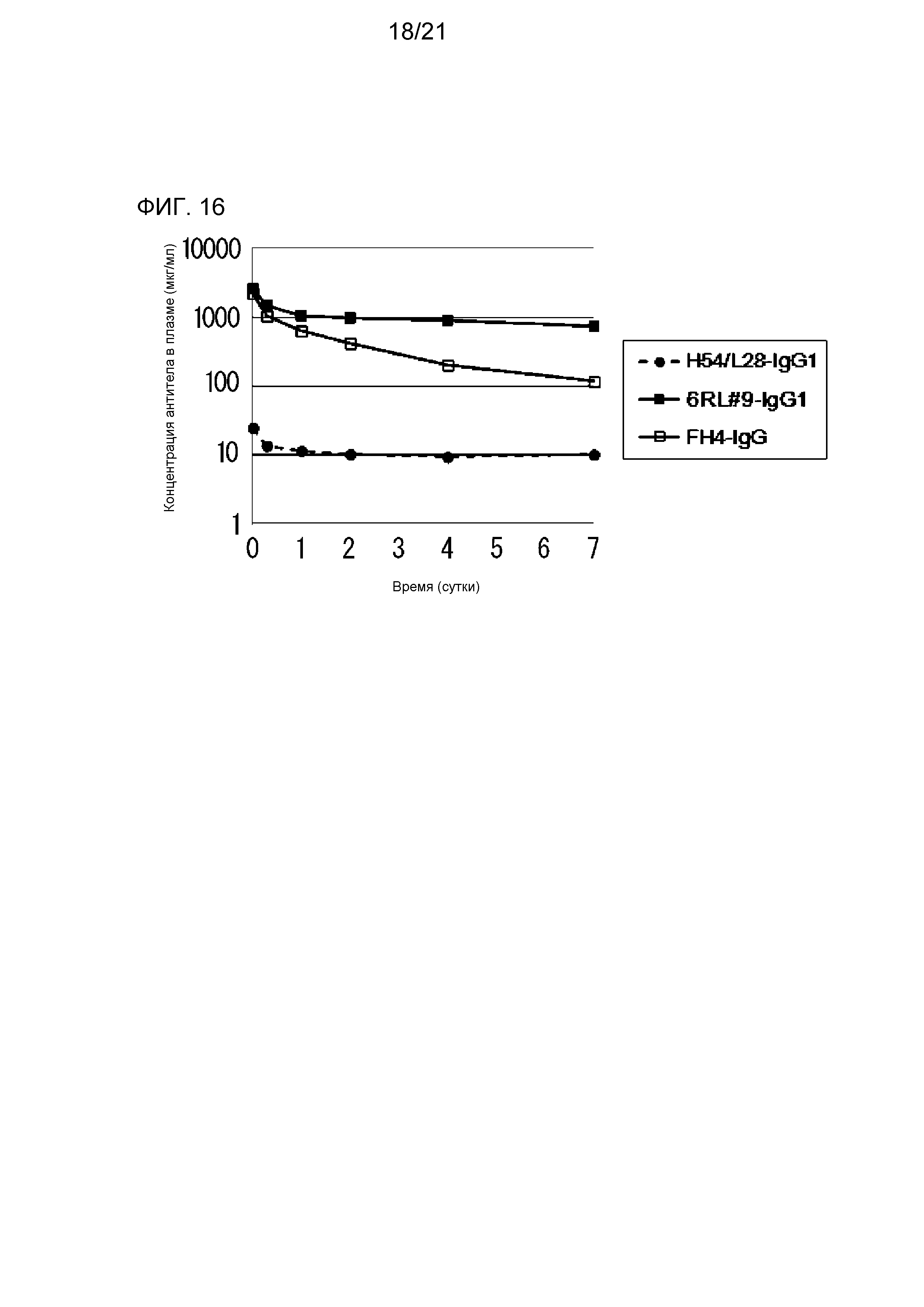
[Фиг. 16] На фиг. 16 представлена диаграмма, на которой показана концентрация в плазме антитела H54/L28-IgG1, антитела FH4-IgG1 и антитела 6RL#9-IgG1 у нормальной мыши.
[Фиг. 17] На фиг. 17 представлена диаграмма, на которой показана концентрация растворимого рецептора IL-6 человека (hsIL-6R) в плазме нормальной мыши, которой вводили антитело H54/L28-IgG1, антитело FH4-IgG1 или антитело 6RL#9-IgG1.
[Фиг. 18] На фиг. 18 представлена диаграмма, на которой показаны концентрации в плазме антитела H54/L28-N434W, антитела FH4-N434W и антитела 6RL#9-N434W у нормальной мыши.
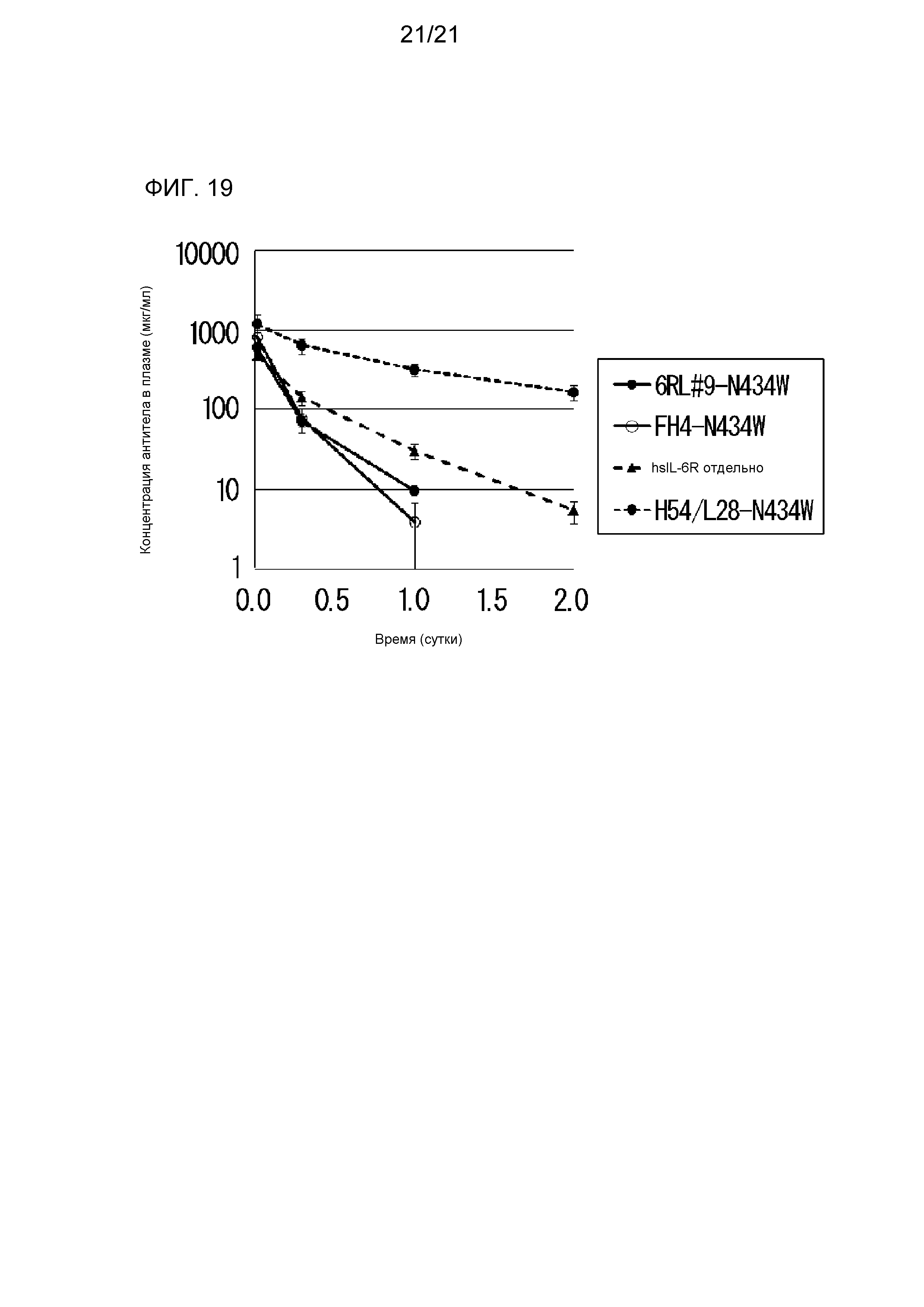
[Фиг. 19] На фиг. 19 представлена диаграмма, на которой показана концентрация растворимого рецептора IL-6 человека (hsIL-6R) в плазме нормальной мыши, которой вводили антитело H54/L28-N434W, антитело FH4-N434W и антитело 6RL#9-N434W.
ОПИСАНИЕ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
Настоящее изобретение относится к библиотеке, по существу состоящей из множества антигенсвязывающих молекул, отличающихся друг от друга последовательностью, где антигенсвязывающая активность каждой антигенсвязывающей молекулы изменяется в зависимости от условий концентрации ионов и т.п. Также настоящее изобретение относится к новому системному способу получения библиотеки, по существу состоящей из множества антигенсвязывающих молекул, отличающихся друг от друга последовательностью, где антигенсвязывающая активность каждой антигенсвязывающей молекулы изменяется в зависимости от условий концентрации ионов металлов и/или концентрации ионов водорода. Такую библиотеку можно использовать в качестве комбинаторной библиотеки, которая помогает проводить селекцию и/или скрининг синтетического клона антигенсвязывающей молекулы с желаемой активностью, например аффинностью связывания и авидностью, подходящей, например, для условий концентрации ионов металла и/или концентрации ионов водорода.
Эти библиотеки пригодны для идентификации полипептидной последовательности антигенсвязывающей молекулы, которая может взаимодействовать с любым из антигенов-мишеней различных типов. Например, библиотека, содержащая полипептиды разнообразных антигенсвязывающих молекул по настоящему изобретению, экспрессируемые с помощью фагового дисплея, является особенно пригодной для селекции и/или скрининга представляющей интерес антигенсвязывающей молекулы. Также настоящее изобретение относится к эффективной высокопроизводительной автоматической системе для этого. Способ по настоящему изобретению может обеспечить антигенсвязывающую молекулу, связывающуюся с антигеном-мишенью зависимым от условий образом. Кроме того, настоящее изобретение относится к фармацевтической композиции, содержащей антигенсвязывающую молекулу в качестве активного ингредиента.
ОПРЕДЕЛЕНИЕ
Аминокислота
Каждая аминокислота указана в настоящем описании посредством однобуквенного кода или трехбуквенного кода, или обоих из них, например, как обозначают посредством Ala/A, Leu/L, Arg/R, Lys/K, Asn/N, Met/M, Asp/D, Phe/F, Cys/C, Pro/P, Gln/Q, Ser/S, Glu/E, Thr/T, Gly/G, Trp/W, His/H, Tyr/Y, Ile/I и Val/V.
Нумерация EU и нумерация по Кабату
В соответствии со способом, используемым в рамках настоящего изобретения, положения аминокислот, приписываемые CDR и FR антитела, определяют в соответствии со способом Кабат (Sequences of Proteins of Immunological Interest, National Institute of Health, Bethesda, Md., 1987 and 1991). Когда антигенсвязывающая молекула, описанная в настоящем описании, представляет собой антитело или антигенсвязывающий фрагмент, аминокислоты в вариабельных областях указаны в соответствии с нумерацией по Кабату, и аминокислоты в константных областях указаны в соответствии с нумерацией EU, соответствующей положениям аминокислот по Кабату.
Модификация аминокислот
Аминокислоты в аминокислотных последовательностях антигенсвязывающих молекул могут быть модифицированы с помощью подходящим образом выбранного способа, известного в данной области, такого как сайт-направленный мутагенез (Kunkel et al., Proc. Natl. Acad. Sci. USA (1985) 82, 488-492) или перекрывающаяся ПЦР. Также аминокислоты могут быть заменены неприродными аминокислотами с использованием множества способов модификации, известных в данной области (Annu. Rev. Biophys. Biomol. Struct. (2006) 35, 225-249; и Proc. Natl. Acad. Sci. U.S.A. (2003) 100 (11), 6353-6357). Например, также предпочтительно используют содержащую тРНК бесклеточную систему трансляции (Clover Direct (Protein Express, an R & D oriented company)), содержащую неприродную аминокислоту, связанную с тРНК янтарь-супрессора, комплементарной кодону UAG (янтарь-кодон), который представляет собой стоп-кодон. Кроме того, для обозначения аминокислотной модификации можно использовать выражение, в котором используют однобуквенные коды аминокислот до и после модификации перед и за номером, соответствующим конкретному положению. Например, модификация P238D, используемая для добавления аминокислотной замены к Fc-области, содержащейся в константной области антитела, соответствует замене Pro в положении 238, определяемом посредством нумерации EU, на Asp. В частности, число соответствует положению аминокислоты, определяемому посредством нумерации EU; однобуквенный код аминокислоты, предшествующий числу, соответствует аминокислоте до замены; и однобуквенный код аминокислоты, следующий после числа, соответствует аминокислоте после замены.
И/или
Термин “и/или”, описанный в настоящем описании, включает каждую комбинацию, отображаемую, соответственно, посредством “и” и “или”. В частности, например, выражение “аминокислоты 33, 55, и/или 96 заменены” включает следующие варианты модификации аминокислот: (a) положение 33, (b) положение 55, (c) положение 96, (d) положения 33 и 55, (e) положения 33 и 96, (f) положения 55 и 96, и (g) положения 33, 55 и 96.
Антигенсвязывающая молекула
Термин “антигенсвязывающая молекула”, описанный в настоящем описании, используют для обозначения молекулы, содержащей антигенсвязывающий домен в наиболее широком значении и, конкретно, она включает различные молекулярные формы при условии, что эти формы проявляют антигенсвязывающую активность. Примеры молекулы, содержащей антигенсвязывающий домен, связанный с FcRn-связывающим доменом, включают антитела. Антитела могут включать простые моноклональные антитела (включая агонистические и антагонистические антитела), антитела человека, гуманизированные антитела, химерные антитела, и т.п. Альтернативно, можно использовать фрагмент такого антитела. Предпочтительные примеры фрагмента могут включать антигенсвязывающие домены и антигенсвязывающие фрагменты (например, Fab, F(ab')2, scFv и Fv). Антигенсвязывающая молекула по настоящему изобретению также может включать каркасные молекулы, содержащиеся в библиотеке для конструирования антигенсвязывающих доменов, содержащие только частичные структуры существующих стабильных конформаций (например, белковая структура α/β-бочонка), используемые в качестве каркасов.
“Антигенсвязывающий домен”, описанный в настоящем описании, может представлять собой домен, имеющий любую структуру при условии, что используемый домен связывается с представляющим интерес антигеном. Предпочтительные примеры такого домена включают вариабельные области тяжелой и легкой цепей антител, происходящий из мембранного белка in-vivo модуль, называемый доменом A, размером приблизительно 35 аминокислот, содержащийся в авимере (WO2004044011 и WO2005040229), аднектин, содержащий домен 10Fn3 в качестве связывающего белок домена, происходящего из гликопротеина фибронектина, экспрессируемого на клеточных мембранах (WO2002032925), аффиантитело, содержащее каркас IgG-связывающего домена, состоящий из трехспирального пучка, состоящего из 58 аминокислот белка A (WO1995001937), DARPin (смоделированные белки с анкириновыми повторами), которые представляют собой экспонированные на поверхности молекул области анкириновых повторов (AR), каждая из которых имеет структуру из 33 аминокислотных остатков, уложенную в субъединицу из поворота, двух антипараллельных спиралей и петли (WO2002020565), антикалин, имеющий четыре области петли, соединяющие восемь антипараллельных цепей, изогнутых в направлении центральной оси на одном конце структуры бочонка, высококонсервативной среди молекул липокалинов, таких как ассоциированный с желатином липокалин нейтрофилов (NGAL) (WO2003029462), и вогнутую область во внутренней структуре параллельных слоев в укладке в форме подковы, образованной повторяющимися модулями богатых лейцином повторов (LRR) вариабельного рецептора лимфоцитов (VLR), который не имеет иммуноглобулиновой структуры, как наблюдают для приобретенной иммунной системы бесчелюстных позвоночных, таких как минога и миксина (WO2008016854). Предпочтительные примеры антигенсвязывающего домена по настоящему изобретению включают антигенсвязывающие домены, содержащие вариабельные области тяжелой и легкой цепей антител.
Термин “антитело”, описанный в настоящем описании, относится к природному иммуноглобулину или иммуноглобулину, полученному частичным или полным синтезом. Антитело можно выделять из природных источников (например, плазма и сыворотка), в которых антитело встречается естественным образом, или из культуральных супернатантов продуцирующих антитела гибридом. Альтернативно антитела можно частично или полностью синтезировать с использованием такого подхода, как генетическая рекомбинация. Предпочтительные примеры антитела включают изотипы иммуноглобулинов и подклассы этих изотипов. Известно, что имуноглобулины человека имеют 9 классов (изотипов): IgG1, IgG2, IgG3, IgG4, IgA1, IgA2, IgD, IgE и IgM. Из этих изотипов, антитело по настоящему изобретению может включать IgG1, IgG2, IgG3 и IgG4. В Sequences of proteins of immunological interest, NIH Publication No. 91-3242, описано множество аллотипических последовательностей, вследствие полиморфизма, в качестве константных областей IgG1 человека, IgG2 человека, IgG3 человека и IgG4 человека, любую из которых можно использовать в рамках настоящего изобретения. В частности, IgG1 человека может иметь последовательность с DEL или EEM в качестве аминокислотной последовательности в положениях 356-358, определяемых посредством нумерации EU. В Sequences of proteins of immunological interest, NIH Publication No. 91-3242, описано множество аллотипических последовательностей вследствие полиморфизма, в качестве константных областей IgK (каппа) человека и IgL7 (лямбда) человека, любую из которых можно использовать в рамках настоящего изобретения. Антитело, имеющее желаемую активность связывания, получают способом, общеизвестным специалистам в данной области.
Антитело можно получать в качестве поликлонального или моноклонального антитела с использованием способов, известных в данной области. В качестве моноклонального антитела предпочтительно можно получать происходящее из млекопитающего моноклональное антитело. Происходящее из млекопитающего моноклональное антитело охватывает, например, антитела, продуцируемые гибридомами, и антитела, продуцируемые клетками-хозяевами, трансформированными экспрессирующими векторами, содержащими гены антитела, с помощью подхода генной инженерии.
Гибридомы, продуцирующие моноклональные антитела, можно получать с использованием способа, известного в данной области. В частности, млекопитающих иммунизируют сенсибилизирующими антигенами в соответствии с обычным способом иммунизации. Полученные иммуноциты подвергают слиянию с родительскими клетками, известными в данной области, с помощью обычного способа слияния клеток. Далее, эти слитые клетки можно подвергать скринингу в отношении клеток, продуцирующих моноклональное антитело, с помощью обычного способа скрининга для отбора гибридом, продуцирующих антитела против сенсибилизирующих антигенов.
Млекопитающие, подлежащие иммунизации сенсибилизирующими антигенами, не ограничиваются каким-либо конкретным животным, и их предпочтительно выбирают для применения в слиянии клеток, учитывая совместимость с родительскими клетками. Как правило, предпочтительно используют грызунов, например, мышей, крыс, хомяков или кроликов, или других млекопитающих, таких как обезьяны.
Этих животных иммунизируют сенсибилизирующими антигенами в соответствии со способом, известным в данной области. Например, общий способ может вовлекать иммунизацию млекопитающих сенсибилизирующими антигенами путем введения посредством внутрибрюшинной или подкожной инъекции. В частности, сенсибилизирующие антигены, разбавленные PBS (фосфат-солевой буфер), солевым раствором, и т.п., с соответствующей степенью разбавления, смешивают, если желательно, с обычным адъювантом, например, полным адъювантом Фрейнда, и эмульгируют, а затем полученную эмульсию сенсибилизирующих антигенов вводят млекопитающим несколько раз с интервалами от 4 до 21 суток. Также для иммунизации сенсибилизирующими антигенами можно использовать подходящий носитель. В частности, в случае использования частичных пептидов, имеющих низкую молекулярную массу, в качестве сенсибилизирующих антигенов, для иммунизации желательно использовать сенсибилизирующие антигенные пептиды, связанные с белками-носителями, такими как альбумин или гемоцианин лимфы улитки.
Гибридомы, продуцирующие антитела против желаемого полипептида, также можно получать путем иммунизации посредством ДНК, как описано ниже. Иммунизация посредством ДНК относится к способу стимуляции иммунитета, который вовлекает: иммунизацию животных путем введения векторных ДНК, которые сконструированы в форме, способной экспрессировать гены, кодирующие антигенный белок, у иммунизированных животных; и стимуляцию иммунитета животных путем экспрессии in vivo сенсибилизирующих антигенов. Можно ожидать, что иммунизация ДНК является лучшей по следующим характеристикам относительно общих способов иммунизации, которые вовлекают иммунизацию животных путем введения белковых антигенов:
- когда антиген представляет собой мембранные белки, иммунизация ДНК может обеспечить стимуляцию иммунитета при сохранении структур мембранных белков; и
- иммунизация ДНК устраняет потребность в очистке иммунизирующих антигенов.
В клеточном слиянии с иммуноцитами используют клетки миеломы млекопитающих. Клетки миеломы предпочтительно имеют подходящий селективный маркер для скрининга. Селективный маркер относится к признаку, который может сохраниться (или не может сохраниться) в конкретных условиях культивирования. Например, в качестве селективного маркера в данной области известны дефицит гипоксантин-гуанин-фосфорибозилтрансферазы (далее в настоящем описании сокращенно обозначаемый как дефицит HGPRT) или дефицит тимидинкиназы (далее в настоящем описании сокращенно обозначаемый как дефицит TK). Клетки, имеющие дефицит HGPRT или TK, являются чувствительными к гипоксантин-аминоптерин-тимидину (далее в настоящем описании сокращенно обозначаются как чувствительные к HAT). Чувствительные к HAT клетки погибают в селективной среде HAT, поскольку клетки не синтезируют ДНК. Напротив, эти клетки, когда они слиты с нормальными клетками, становятся способными расти даже в селективной среде HAT, поскольку слитые клетки могут продолжать синтез ДНК с использованием пути спасения из нормальных клеток.
Селекцию клеток, имеющих дефицит HGPRT или TK, можно проводить в среде, содержащей 6-тиогуанин или 8-азагуанин (далее в настоящем описании сокращенно обозначаемый как 8AG) или 5'-бромдезоксиуридин, соответственно. Нормальные клетки погибают при включении этих аналогов пиримидинов в их ДНК. Напротив, клетки с дефицитом этих ферментов могут выжить в селективной среде, поскольку эти клетки не могут включать аналоги пиримидина в их ДНК. Кроме того, селективный маркер, называемый маркером устойчивости G418, обеспечивает устойчивость к антибиотику 2-дезоксистрептамину (аналог гентамицина) через ген устойчивости к неомицину. В данной области известны различные клетки миеломы, пригодны для слияния клеток.
Например, в качестве таких клеток миеломы можно предпочтительно использовать P3 (P3x63Ag8,653) (J. Immunol. (1979) 123 (4), 1548-1550), P3x63Ag8U.1 (Current Topics in Microbiology and Immunology (1978) 81, 1-7), NS-1 (C. Eur. J. Immunol. (1976) 6 (7), 511-519), MPC-11 (Cell (1976) 8 (3), 405-415), SP2/0 (Nature (1978) 276 (5685), 269-270), FO (J. Immunol. Methods (1980) 35 (1-2), 1-21), S194/5.XX0.BU.1 (J. Exp. Med. (1978) 148 (1), 313-323) или R210 (Nature (1979) 277 (5692), 131-133).
В основном, клеточное слияние между иммуноцитами и клетками миеломы проводят в соответствии со способом, известным в данной области, например, способом Kohler and Milstein et al. (Methods Enzymol. (1981) 73, 3-46).
Более конкретно, слияние клеток можно проводить, например, в обычной питательной культуральной среде в присутствии ускорителя слияния клеток. Например, в качестве ускорителя слияния можно использовать полиэтиленгликоль (PEG) или японский гемагглютинирующий вирус (HVJ). Кроме того, если желательно, добавляют вспомогательное вещество, такое как диметилсульфоксид, и его используют для повышения эффективности слияния.
Соотношение между используемыми иммуноцитами и клетками миеломы можно выбирать произвольно. Например, количество иммуноцитов предпочтительно выбирают так, чтобы оно в 1-10 раз превышало количество клеток миеломы. В качестве культуральной среды для слияния клеток можно использовать, например, среды RPMI1640 или MEM, пригодные для выращивания клеточной линии миеломы, или любую другую обычную культуральную среду для применения в клеточной культуре указанного типа, и ее можно далее дополнять раствором, дополненным сывороткой, такой как эмбриональная телячья сыворотка (FCS).
Для слияния клеток иммуноциты и клетки миеломы хорошо перемешивают в заданных количествах в культуральной среде, и к ним обычно добавляют раствор PEG (например, имеющего среднюю молекулярную массу порядка от 1000 до 6000), предварительно нагретый приблизительно до 37°C, в концентрации от 30 до 60% (масс./об.). Смешанный раствор осторожно перемешивают для формирования желаемых представляющих интерес слитых клеток (гибридом). Затем в суспензии клеток последовательно добавляют подходящую культуральную среду, проиллюстрированную выше, и супернатант удаляют центрифугированием. Эту процедуру можно повторять, чтобы тем самым удалить агенты для слияния клеток и т.п., неблагоприятные для роста гибридом.
Полученные таким образом гибридомы можно культивировать для селекции с использованием обычной селективной среды, например, среды HAT (культуральная среда, содержащая гипоксантин, аминоптерин и тимидин). Культивирование с использованием среды HAT можно продолжать достаточно долго (как правило, в течение от нескольких суток до нескольких недель) для обеспечения гибели клеток (неслитых клеток), отличных от желаемых гибридом. Затем, гибридомы, продуцирующие желаемое антитело, подвергают скринингу в отношении единичных клонов и клонируют в качестве единичных клонов обычным способом лимитирующих разведений.
Гибридомы, полученные таким образом, можно подвергать селекции с использованием селективной среды, подходящей для селективного маркера, который содержится в клетках миеломы, используемых для слияния клеток. Например, селекцию клеток, имеющих дефицит HGPRT или TK, можно проводить путем культивирования в среде HAT (культуральная среда, содержащая гипоксантин, аминоптерин и тимидин). В частности, в случае чувствительных к HAT клеток миеломы, используемых для слияния клеток, в среде HAT способны селективно расти только клетки, успешно слитые с нормальными клетками. Культивирование с использованием среды HAT продолжают в течение времени, достаточно длительного для обеспечения гибели клеток (неслитых клеток), отличных от желаемых гибридом. В частности, для селекции желаемых гибридом культивирование можно, в основном, проводить в течение от нескольких суток до нескольких недель. Затем, гибридомы, продуцирующие желаемое антитело, подвергают скринингу в отношении единичных клонов и клонируют в качестве единичных клонов обычным способом лимитирующих разведений.
Скрининг желаемого антитела и клонирование в качестве единичных клонов предпочтительно можно проводить с помощью способа скрининга на основе реакции антиген-антитело, известного в данной области. Скрининг такого моноклонального антитела можно проводить, например, с помощью FACS (активированная флуоресценцией сортировка клеток). FACS относится к системе, которая может анализировать клетки, подвергнутые контакту с флуоресцентными антителами, с помощью лазерного излучения, и измерять флуоресценцию, испускаемую индивидуальными клетками, тем самым анализируя связывание антител с поверхностью клеток.
Альтернативно антитело можно оценивать в отношении его активности связывания с иммобилизованными антигенами на основе принципов ELISA. Например, антигены иммобилизуют на лунках планшета для ELISA. Культуральный супернатант гибридом приводят в контакт с антигенами в лунках для выявления антитела, связавшегося с антигеном. В случае происходящего из мыши моноклонального антитела, связавшееся с антигеном антитело можно выявлять с использованием антитела против иммуноглобулинов мыши. Эти отобранные с помощью скрининга гибридомы, продуцирующие желаемое антитело, обладающие антигенсвязывающей способностью, можно клонировать способом лимитирующих разведений и т.п. Гибридомы, продуцирующие моноклональное антитело, полученные таким образом, можно субклонировать в обычной культуральной среде. Также гибридомы можно хранить в течение длительного периода времени в жидком азоте.
Гибридомы можно культвировать обычным способом. Желаемое моноклональное антитело можно получать из их культурального супернатанта. Альтернативно гибридомы можно вводить млекопитающим, совместимым с ними, и выращивать, и из их асцитной жидкости можно получать моноклональное антитело. Первый из этих способов пригоден для получения высокочистых антител.
Также предпочтительно можно использовать антитела, кодируемые генами антител, клонированными из клеток, продуцирующих антитело, таких как гибридомы. Клонированные гены антител встраивают в подходящие векторы и переносят хозяевам для экспрессии антител, кодируемых генами. Способы выделения генов антител, встраивания в векторы и трансформации клеток-хозяев, уже разработаны, например, Vandamme et al. (Eur. J. Biochem. (1990) 192 (3), 767-775). Способ получения рекомбинантных антител также известен в данной области, как указано ниже.
Например, кДНК, кодирующие вариабельные области (V-области) представляющего интерес антитела, получают из клеток гибридомы, продуцирующих это антитело. Для этой цели обычно сначала из гибридом экстрагируют тотальную РНК. Например, для экстракции мРНК из клеток можно использовать следующие способы:
- способ ультрацентрифугирования с гуанидином (Biochemistry (1979) 18 (24), 5294-5299), и
- способ AGPC (Anal. Biochem. (1987) 162 (1), 156-159).
Экстрагированную мРНК можно очищать с использованием набора для очистки мРНК (GE Healthcare Bio-Sciences Corp.) и т.п. Альтернативно также коммерчески доступен набор для прямой экстракции тотальной мРНК из клеток, такой как набор для очистки мРНК QuickPrep (GE Healthcare Bio-Sciences Corp.). С использованием такого набора можно получать мРНК из гибридом. Из полученных мРНК можно синтезировать кДНК, кодирующие V-область антитела, с использованием обратной транскриптазы. кДНК можно синтезировать с использованием набора для синтеза первой цепи кДНК с обратной транскриптазой AMV (Seikagaku Corp.) и т.п. Альтернативно для синтеза и амплификации кДНК можно использовать набор для амплификации кДНК SMART RACE (Clontech Laboratories, Inc.) и 5'-RACE ПЦР (Proc. Natl. Acad. Sci. USA (1988) 85 (23), 8998-9002; и Nucleic Acids Res. (1989) 17 (8), 2919-2932). В ходе такого синтеза кДНК, на оба конца кДНК можно вносить соответствующие участки рестрикции, описанные ниже.
Представляющие интерес фрагменты кДНК очищают из полученных продуктов ПЦР, а затем связывают с векторными ДНК. Полученные таким образом рекомбинантные векторы переносят в E. coli и т.п., а затем проводят селекцию колоний. Затем из E. coli, которые образовали колонии, можно получать рекомбинантный вектор. Затем присутствие или отсутствие нуклеотидной последовательности представляющей интерес кДНК в рекомбинантном векторе подтверждают способом, известным в данной области, например, способом терминации цепи дидезоксинуклеотидами.
Гены, кодирующие вариабельную область, удобно получать способом 5'-RACE с использованием праймеров для амплификации генов вариабельной области. Сначала синтезируют кДНК с помощью РНК, экстрагированных из клеток гибридомы, в качестве матрицы для получения библиотеки кДНК для 5'-RACE. Для синтеза библиотеки кДНК для 5'-RACE соответствующим образом используют доступный набор, такой как набор для амплификации кДНК SMART RACE.
Гены антител амплифицируют способом ПЦР с использованием полученной библиотеки кДНК для 5'-RACE в качестве матрицы. Праймеры для амплификации генов антител мыши можно конструировать на основе последовательностей генов антител, известных в данной области. Эти праймеры имеют нуклеотидную последовательность, которая отличается для каждого подкласса иммуноглобулинов. Таким образом, подкласс представляющего интерес антитела желательно определять заранее с использованием коммерчески доступного набора, такого как набор для изотипирования моноклональных антител мыши Iso Strip (Roche Diagnostics K.K.).
В частности, можно использовать праймеры, способные амплифицировать гены, кодирующие тяжелые цепи γ1, γ2a, γ2b и γ3 и легкие цепи κ и λ, например, для цели получения генов, кодирующих IgG мыши. Праймеры, отжигающиеся на частях, соответствующих константным областям вблизи вариабельных областей, обычно используют в качестве 3'-праймеров для амплификации генов вариабельной области IgG. С другой стороны, праймеры, включенные в набор для получения библиотеки кДНК для 5' RACE, используют в качестве 5'-праймеров.
Продукты ПЦР, амплифицированные таким образом, можно использовать для реконструкции иммуноглобулинов, состоящих из тяжелых и легких цепей в комбинации. Реконструированные иммуноглобулины можно подвергать скринингу в отношении желаемого антитела с их антигенсвязывающей активностью в качестве показателя. Например, для цели получения антитела против антигена, более предпочтительно, антитело специфически связывается с антигеном. Антитело, связывающееся с антигеном, можно подвергать скринингу, например, с помощью следующих стадий:
(1) приведение в контакт антител, содержащих V-области, кодируемые кДНК, полученными из гибридом, с антигенами;
(2) выявление связывания антиген-антитело; и
(3) селекция связывающего антиген антитела.
Выявление связывания антиген-антитело проводят способом, известным в данной области. В частности, связывание антиген-антитело можно выявлять с помощью подхода, такого как FACS или ELISA, описанные выше.
После получения каждой кДНК, кодирующей представляющую интерес V-область антитела, кДНК расщепляют ферментами рестрикции, которые распознают участки рестрикции, встроенные на обоих концах кДНК. Предпочтительно, ферменты рестрикции распознают и расщепляют нуклеотидную последовательность, которая встречается с низкой частотой в нуклеотидных последовательностях, составляющих гены антител. Более предпочтительно, ферменты рестрикции расщепляют встроенные участки с образованием липких концов, для встраивания в вектор одной копии расщепленного фрагмента в правильном направлении. кДНК, кодирующие V-область антитела, расщепленные таким образом, можно встраивать в соответствующие экспрессирующие векторы для получения экспрессирующих векторов для антител. В этом случае, гены, кодирующие константную область антитела (C-область), подвергают слиянию в рамке считывания с генами, кодирующими V-область, для получения химерных антител. В этом контексте, химерные антитела относятся к антителам, содержащим константные и вариабельные области различного происхождения. Таким образом, химерное антитело в соответствии с настоящим изобретением также охватывает гетерогенные (например, мыши-человека) химерные антитела, а также гомогенные химерные антитела человека-человека. Гены V-области можно встраивать в экспрессирующие векторы, предварительно имеющие гены константных областей, конструируя экспрессирующие векторы для химерных антител. В частности, например, последовательности распознавания для ферментов рестрикции, которые расщепляют гены V-области, могут быть соответствующим образом расположены на 5'-стороне экспрессирующих векторов, содержащих ДНК, кодирующие константные области (C-области) желаемого антитела. Полученные экспрессирующие векторы и гены V-области, расщепленные той же комбинацией ферментов рестрикции, подвергают слиянию в рамке считывания друг с другом, конструируя экспрессирующие векторы для химерных антител.
Для получения желаемого антитела ген антитела можно встраивать в экспрессирующие векторы, так чтобы ген был функционально связан с контрольными последовательностями. Контрольные последовательности для экспрессии антител охватывают, например, энхансеры и промоторы. Также, на N-конец антитела можно добавлять сигнальную последовательность для внеклеточной секреции экспрессируемого антитела. Например, в качестве сигнальной последовательности можно использовать пептид, имеющий аминокислотную последовательность MGWSCIILFLVATATGVHS (SEQ ID NO: 13). К антителу можно добавлять любую другую подходящую сигнальную последовательность. Экспрессируемый полипептид расщепляется на C-конце сигнальной последовательности, и отщепленный полипептид может секретироваться внеклеточно в качестве зрелого полипептида. С помощью этих экспрессирующих векторов можно трансформировать подходящие клетки-хозяева, получая рекомбинантные клетки, экспрессирующие ДНК, кодирующую желаемое антитело.
Для эксперессии генов антител ДНК, кодирующую тяжелую цепь (H-цепь), и ДНК, кодирующую легкую цепь (L-цепь), по отдельности встраивают в различные экспрессирующие векторы. Одну и ту же клетку-хозяина можно котрансфицировать вектором, в который встроена тяжелая цепь, и вектором, в который встроена легкая цепь, и тем самым можно обеспечивать экспрессию молекул антител, содержащих H- и L-цепи. Альтернативно ДНК, кодирующие тяжелую цепь и легкую цепь, можно встраивать в единичный экспрессирующий вектор, которым затем можно трансформировать клетку-хозяина (см. WO1994011523).
В данной области известно множество комбинаций клеток-хозяев и экспрессирующих векторов для получения антитела путем переноса выделенных генов антител в подходящих хозяев. Все из этих экспрессирующих систем можно использовать для выделения антигенсвязывающих молекул по настоящему изобретению. В случае использования эукариотических клеток в качестве клеток-хозяев, можно соответственно использовать клетки животных, растений или грибов. В частности, примеры клеток животных могут включать следующие клетки:
(1) клетки млекопитающих, такие как CHO (линия клеток яичника китайского хомячка), COS (линия клеток почки обезьяны), клетки миеломы (Sp2/O, NS0, и т.д.), BHK (линия клеток почки детенышей хомячка), HEK293 (линия клеток почки эмбриона человека с расщепленной аденовирусной (Ad)5 ДНК), клетки PER.C6 (линия клеток сетчатки эмбриона человека, трансформированная генами аденовируса типа 5 (Ad5) E1A и E1B), Hela и Vero (Current Protocols in Protein Science, May, 2001, Unit 5.9, Table 5.9.1);
(2) клетки земноводных, такие как ооциты Xenopus; и
(3) клетки насекомых, такие как sf9, sf21 и Tn5.
Альтернативно, в качестве растительных клеток в данной области известны экспрессирующие системы для генов антител с использованием клеток, происходящих из рода Nicotiana (например, Nicotiana tabacum). Для трансформации клеток растений можно соответствующим образом использовать культивируемые клетки каллюса.
В качестве клеток грибов можно использовать следующие клетки:
- клетки, происходящие из дрожжей рода Saccharomyces (например, Saccharomyces cerevisiae) и рода Pichia (например, Pichia pastoris), и
- клетки, происходящие из нитчатых грибов рода Aspergillus (например, Aspergillus niger).
Также, в данной области известны экспрессирующие системы для генов антител с использованием прокариотических клеток. В случае использования, например, бактериальных клеток, можно соответствующим образом использовать клетки бактерий, таких как E. coli и Bacillus subtilis. Экспрессирующие векторы, содержащие ген представляющего интерес антитела, переносят в эти клетки путем трансформации. Трансформированные клетки культивируют in vitro, и из полученных культур трансформированных клеток можно получать желаемое антитело.
В дополнение к клеткам-хозяевам, для получения рекомбинантных антител можно использовать трансгенных животных. В частности, желаемое антитело можно получать из животных, трансфицированных геном, кодирующим это антитело. Например, гены антител можно встраивать в рамке считывания в гены, кодирующие белки, специфически продуцируемые в молоке, конструируя слитые гены. В качестве белка, секретируемого в молоке, можно использовать, например, β-казеин козы и т.п. Фрагменты ДНК, содержащие слитые гены, имеющие вставку гена антитела, инъецируют в эмбрионы козы, которые в свою очередь имплантируют самкам коз. Из молока, продуцируемого трансгенными козами (или их потомками), рожденными козами, которым имплантировали эмбрионы, можно получать желаемое антитело в качестве слитого белка с белком молока. Кроме того, для увеличения количества молока, содержащего желаемое антитело, продуцируемого трансгенными козами, трансгенным козам можно вводить гормоны (Bio/Technology (1994), 12 (7), 699-702).
В случае введения антигенсвязывающей молекулы, описанной в настоящем описании, человеку, в качестве антигенсвязывающего домена для молекулы можно соответствующим образом выбирать антигенсвязывающий домен, происходящий из генетически рекомбинантного антитела, которое сконструировано искусственным образом, например, для снижения гетероантигенности человека. Генетически рекомбинантное антитело охватывает, например, гуманизированные антитела. Эти сконструированные антитела соответствующим образом получают с использованием способа, известного в данной области.
Каждая вариабельная область антитела, используемая для получения антигенсвязывающего домена в антигенсвязывающей молекуле, описанной в настоящем описании, как правило, состоит из трех определяющих комплементарность областей (CDR), фланкированных четырьмя каркасными областями (FR). CDR представляют собой области, которые по существу определяют специфичность связывания антитела. CDR имеют разнообразные аминокислотные последовательности. С другой стороны, FR по большей части образованы аминокислотными последовательностями, которые являются высокоидентичными даже среди антител с различной специфичностью связывания. Таким образом, как правило, специфичность связывания определенного антитела можно трансплантировать в другие антитела путем пересадки CDR.
Гуманизированные антитела также называют реконструированными антителами человека. В частности, в данной области известно, например, гуманизированное антитело, состоящее антитела человека, в которое пересажены CDR антитела не являющегося человеком животного (например, мыши). Также для получения гуманизированных антител известны общие подходы рекомбинации генов. В частности, например, перекрывающаяся ПЦР известна в данной области в качестве способа пересадки CDR антител мыши в FR человека. В перекрывающейся ПЦР, к праймерам для синтеза FR антител человека добавляют нуклеотидную последовательность, кодирующую каждую CDR антитела мыши, подлежащую пересадке. Праймеры получают для каждой из четырех FR. Для пересадки CDR мыши в FR человека, обычно считается преимущественным выбор FR человека, высокоидентичных FR мыши, для сохранения функций CDR. В частности, как правило, предпочтительно используют FR человека, содержащие аминокислотные последовательности, высокоидентичные аминокислотным последовательностям FR, соседних с CDR мыши, подлежащими пересадки.
Нуклеотидные последовательности, подлежащие связыванию, конструируют так, чтобы последовательности были связаны в рамке считывания друг с другом. Нуклеотидные последовательности, кодирующие FR человека, синтезируют по отдельности с использованием соответствующих им праймеров. Полученные продукты содержат ДНК, кодирующую CDR мыши, присоединенную к каждой последовательности, кодирующей FR человека. Нуклеотидные последовательности, кодирующие CDR мыши, конструируют так, чтобы нуклеотидная последовательность в каждом продукте перекрывалась с другой нуклеотидной последовательностью. Затем перекрывающиеся участки CDR в продуктах, синтезированных с генов антител человека в качестве матриц, подвергают отжигу друг с другом для реакции синтеза комплементарной цепи. С помощью этой реакции последовательности FR человека связывают через последовательности CDR мыши.
Наконец, полноразмерную последовательность гена V-области, содержащей связанные три CDR и четыре FR, амплифицируют с использованием праймеров, каждый из которых отжигается с ее 5'- и 3'-концами и имеет присоединенную последовательность распознавания для соответствующего фермента рестрикции. Полученную таким образом ДНК и ДНК, кодирующую C-область антитела человека, можно встраивать в экспрессирующие векторы, так что эти ДНК подвергаются слиянию в рамке считывания с получением векторов для экспрессии гуманизированного антитела. Эти векторы, имеющие вставки, переносят в хозяев, получая рекомбинантные клетки. Затем рекомбинантные клетки культивируют для экспрессии ДНК, кодирующей гуманизированное антитело, для продукции гуманизированных антител в культуры культивируемых клеток (EP239400 и WO1996002576).
Полученные таким образом гуманизированные антитела можно оценивать в отношении их антигенсвязывающей активности с помощью количественного или качественного анализа, тем самым отбирая подходящие FR антител человека, которые позволяют CDR формировать подходящий антигенсвязывающий центр, когда их связывают через CDR. Если необходимо, аминокислотный остаток(и) FR можно заменять так, чтобы CDR полученного реконструированного антитела человека формировали подходящий антигенсвязывающий центр. Например, в аминокислотную последовательность FR можно вносить мутацию с использованием способа ПЦР, используемого при пересадке CDR мыши в FR человека. В частности, мутацию частичной нуклеотидной последовательности можно вносить в праймеры, отжигающиеся на нуклеотидной последовательности FR. Нуклеотидная последовательность FR, синтезированная с использованием таких праймеров, содержит мутацию, внесенную таким образом. Такие варианты антител, имеющие замененную аминокислоту(ы), можно оценивать в отношении их антигенсвязывающей активности с помощью того же анализа, как описано выше, чтобы тем самым выбрать варианты последовательностей FR, имеющие желаемые свойства (Sato et al., Cancer Res (1993) 53, 851-856).
Альтернативно желаемое антитело человека можно получать путем иммунизации ДНК с использованием трансгенных животных, имеющих все репертуары генов антител человека (см. WO1993012227, WO1992003918, WO1994002602, WO1994025585, WO1996034096 и WO1996033735), в качестве иммунизированных животных.
Кроме того, также известен способ получения антител человека путем пэннинга с использованием библиотек антител человека. Например, V-области антител человека экспрессируют в качестве одноцепочечного антитела (scFv) на поверхности фагов способом фагового дисплея. Можно отбирать фаг, экспрессирующий связывающее антиген scFv. Ген отобранного фага можно анализировать для определения последовательностей ДНК, кодирующих V-области связывающегося с антигеном антитела человека. После определения последовательности ДНК связывающего антиген scFv, последовательности V-областей можно подвергать слиянию в рамке считывания с последовательностями C-областей желаемого антитела человека, а затем встраивать в соответствующие экспрессирующие векторы, получая экспрессирующие векторы. Экспрессирующие векторы переносят в предпочтительные экспрессирующие клетки, как проиллюстрировано выше. Гены, кодирующие антитела человека, экспрессируются клетками, обеспечивая получение антител человека. Эти способы уже известны в данной области (см. WO1992001047, WO19992020791, WO1993006213, WO1993011236, WO1993019172, WO1995001438 и WO1995015388).
“Антигенсвязывающий домен”, описанный в настоящем описании, относится к области, которая специфично связывается с частью или всем антигеном по принципу комплементарности. Примеры антигенсвязывающего домена могут включать домены, имеющие антигенсвязывающий домен антитела. Примеры антигенсвязывающего домена антитела могут включать CDR и вариабельные области. В случае использования CDR в качестве антигенсвязывающего домена антитела, антигенсвязывающий домен может содержать все из 6 CDR, содержащихся в антителе, или он может содержать одну или две, или более из этих CDR. Каждая CDR, содержащаяся в качестве связывающей области антитела, может иметь, например, делецию, замену, вставку и/или инсерцию аминокислот, или можно использовать часть CDR при условии, что содержащаяся CDR имеет антигенсвязывающую активность. Антитело, направленное против антигена, имеющего большую молекулярную массу, может связываться только с конкретным участком в антигене. Этот конкретный участок называют эпитопом. Антигенсвязывающий домен может быть образован одним или более вариабельными доменами антитела. Предпочтительно, антигенсвязывающий домен содержит вариабельную область легкой цепи (VL) антитела и вариабельную область тяжелой цепи (VH) антитела. Предпочтительные примеры такого антигенсвязывающего домена включают “scFv (одноцепочечный Fv)”, “одноцепочечное антитело”, “Fv”, “scFv2 (одноцепочечный Fv2)”, “Fab”, “диантитело”, “линейное антитело” и “F(ab')2”.
“Вариабельная область антитела”, как используют в рамках изобретения, относится к области, которая содержится в каждой из легкой и тяжелой цепей молекулы антитела и содержит аминокислотные последовательности определяющих комплементарность областей (CDR; т.е. CDR1, CDR2 и CDR3) и каркасных областей (FR). VH представляет собой вариабельную область тяжелой цепи. VL представляет собой вариабельную область легкой цепи. В соответствии со способом, используемым в рамках настоящего изобретения, положения аминокислот, приписываемые CDR и FR, определяют в соответствии со способом Кабат (Sequence of Proteins of Immunological Interest, National Institute of Health, Bethesda, Md., 1987 and 1991). В настоящем описании, аминокислоты в антителе или антигенсвязывающем фрагменте также пронумерованы в соответствии с нумерацией по Кабату, соответствующей положениям аминокислот по Кабату.
Термин “определяющие комплементарность области (CDR; т.е. CDR1, CDR2 и CDR3)”, как используют в рамках изобретения, относится к аминокислотным остаткам в вариабельной области антитела, существование которых необходимо для связывания антигена. Каждая вариабельная область содержит три области CDR, в основном обозначаемые как CDR1, CDR2 и CDR3. Каждая определяющая комплементарность область может содержать аминокислотные остатки из “определяющей комплементарность области”, как описано Кабат (т.е. остатки 24-34 (CDR1), 50-56 (CDR2) и 89-97 (CDR3) в вариабельной области легкой цепи и остатки 31-35 (CDR1), 50-65 (CDR2) и 95-102 (CDR3) в вариабельной области тяжелой цепи; Kabat et al., Sequences of Proteins of Immunological Interest, 5th edition, Public Health Service, National Institute of Health, Bethesda, MD. (1991)) и/или остатки из “гипервариабельной петли” (т.е. остатки 26-32 (CDR1), 50-52 (CDR2) и 91-96 (CDR3) в вариабельной области легкой цепи и остатки 26-32 (CDR1), 53-55 (CDR2) и 96-101 (CDR3) в вариабельной области тяжелой цепи; Chothia and Lesk, J. Mol. Biol. (1987) 196, 901-917). В некоторых случаях каждая определяющая комплементарность область может содержать аминокислоты как из области CDR, так и из гипервариабельной петли, определяемой способом Кабат.
Термин “Fab”-фрагмент включает вариабельные и константные области легкой цепи и вариабельную область и первую константную область (CH1) тяжелой цепи. F(ab')2-фрагмент антитела содержит пару Fab-фрагментов, как правило ковалентно связанных в участках вблизи их C-концов между остатками цистеина в шарнирной области. Также в данной области известны другие химические связи фрагментов антител, к которым относится настоящее изобретение.
Термин “одноцепочечный Fv” или “scFv” фрагмент антитела включает области VH и VL антитела, которые в свою очередь образуют единую полипептидную цепь. Обычно полипептид Fv, кроме того, содержит полипептидный линкер между областями VH и VL. Этот линкер позволяет образование структуры, желательной для связывания антигена посредством scFv. scFv рассмотрены, например, в Pluckthun, The Pharmacology of Monoclonal Antibodies (1994) Vol. 113, 269-315 (Rosenburg and Moore ed., Springer-Verlag, New York).
Термин “диантитело” относится к небольшому фрагменту антитела, имеющему два антигенсвязывающих центра. Этот фрагмент антитела содержит вариабельную область тяжелой цепи (VH), связанную с вариабельной областью легкой цепи (VL), в одной полипептидной цепи (VH и VL). Линкер, который является слишком коротким, чтобы образовать пару этих двух областей на одной и той же полипептидной цепи, используют, чтобы вынудить эти области образовывать пару с их определяющими комплементарность областями на другой полипептидной цепи, так чтобы образовывалось два антигенсвязывающих центра. Диантитело подробно описано, например, в патентных документах, таких как патент Европы № 404097 и WO1993011161 и непатентные документы, такие как Holliger et al., Proc. Natl. Acad. Sci. USA (1993) 90, 6444-6448.
Термин “линейное антитело” относится к антителу, описанному в Zapata et al., Protein Eng. (1995) 8 (10), 1057-1062. В кратком изложении, это антитело содержит пару тандемных сегментов Fd (VH-CH1-VH-CH1), которые образуют пару антигенсвязывающих доменов с комплементарным полипептидом легкой цепи. Линейное антитело может быть биспецифическим или моноспецифическим.
Антиген
“Антиген”, описанный в настоящем описании, не ограничен конкретной структурой при условии, что антиген содержит эпитоп, с которым связывается антигенсвязывающий домен. С другой стороны, антиген может представлять собой неорганическое вещество или он может представлять собой органическое вещество. Примеры антигена могут включать следующие молекулы: 17-IA, 4-1BB, 4Dc, 6-кето-PGF1a, 8-изо-PGF2a, 8-оксо-dG, рецептор аденозина A1, A33, ACE, ACE-2, активин, активин A, активин AB, активин B, активин C, активин RIA, активин RIA ALK-2, активин RIB ALK-4, активин RIIA, активин RIIB, ADAM, ADAM10, ADAM12, ADAM15, ADAM17/TACE, ADAM8, ADAM9, ADAMTS, ADAMTS4, ADAMTS5, аддрессин, aFGF, ALCAM, ALK, ALK-1, ALK-7, альфа-1-антитрипсин, антагонист альфа-V/бета-1, ANG, Ang, APAF-1, APE, APJ, APP, APRIL, AR, ARC, ART, артемин, анти-Id, ASPARTIC, предсердный натрийуретический фактор, интегрин av/b3, Axl, b2M, B7-1, B7-2, B7-H, стимулитор B-лимфоцитов (BlyS), BACE, BACE-1, Bad, BAFF, BAFF-R, Bag-1, BAK, Bax, BCA-1, BCAM, Bcl, BCMA, BDNF, b-ECGF, bFGF, BID, Bik, BIM, BLC, BL-CAM, BLK, BMP, BMP-2 BMP-2a, остеогенин BMP-3, BMP-4 BMP-2b, BMP-5, BMP-6 Vgr-1, BMP-7 (OP-1), BMP-8 (BMP-8a, OP-2), BMPR, BMPR-IA (ALK-3), BMPR-IB (ALK-6), BRK-2, RPK-1, BMPR-II (BRK-3), BMP, b-NGF, BOK, бомбезин, нейротрофический фактор костей, BPDE, BPDE-ДНК, BTC, фактор комплемента 3 (C3), C3a, C4, C5, C5a, C10, CA125, CAD-8, кальцитонин, cAMP, карциноэмбриональный антиген (CEA), ассоциированные со злокачественной опухолью антигены, катепсин A, катепсин B, катепсин C/DPPI, катепсин D, катепсин E, катепсин H, катепсин L, катепсин O, катепсин S, катепсин V, катепсин X/Z/P, CBL, CCI, CCK2, CCL, CCL1, CCL11, CCL12, CCL13, CCL14, CCL15, CCL16, CCL17, CCL18, CCL19, CCL2, CCL20, CCL21, CCL22, CCL23, CCL24, CCL25, CCL26, CCL27, CCL28, CCL3, CCL4, CCL5, CCL6, CCL7, CCL8, CCL9/10, CCR, CCR1, CCR10, CCR10, CCR2, CCR3, CCR4, CCR5, CCR6, CCR7, CCR8, CCR9, CD1, CD2, CD3, CD3E, CD4, CD5, CD6, CD7, CD8, CD10, CD11a, CD11b, CD11c, CD13, CD14, CD15, CD16, CD18, CD19, CD20, CD21, CD22, CD23, CD25, CD27L, CD28, CD29, CD30, CD30L, CD32, CD33 (p67 белок), CD34, CD38, CD40, CD40L, CD44, CD45, CD46, CD49a, CD52, CD54, CD55, CD56, CD61, CD64, CD66e, CD74, CD80 (B7-1), CD89, CD95, CD123, CD137, CD138, CD140a, CD146, CD147, CD148, CD152, CD164, CEACAM5, CFTR, cGMP, CINC, ботулинический токсин, токсин Clostridium perfringens, CKb8-1, CLC, CMV, CMV UL, CNTF, CNTN-1, COX, C-Ret, CRG-2, CT-1, CTACK, CTGF, CTLA-4, CX3CL1, CX3CR1, CXCL, CXCL1, CXCL2, CXCL3, CXCL4, CXCL5, CXCL6, CXCL7, CXCL8, CXCL9, CXCL10, CXCL11, CXCL12, CXCL13, CXCL14, CXCL15, CXCL16, CXCR, CXCR1, CXCR2, CXCR3, CXCR4, CXCR5, CXCR6, цитокератиновые ассоциированные с опухолью антигены, DAN, DCC, DcR3, DC-SIGN, фактор, ускоряющий распад, дез-(1-3)-IGF-I (IGF-1 головного мозга), Dhh, дигоксин, DNAM-1, ДНК-аза, Dpp, DPPIV/CD26, Dtk, ECAD, EDA, EDA-A1, EDA-A2, EDAR, EGF, EGFR (ErbB-1), EMA, EMMPRIN, ENA, рецептор эндотелина, энкефалиназа, eNOS, Eot, эотаксин 1, EpCAM, эфрин B2/EphB4, EPO, ERCC, E-селектин, ET-1, фактор IIa, фактор VII, фактор VIIIc, фактор IX, активирующий фибробласты белок (FAP), Fas, FcR1, FEN-1, ферритин, FGF, FGF-19, FGF-2, FGF3, FGF-8, FGFR, FGFR-3, фибрин, FL, FLIP, Flt-3, Flt-4, фоликулостимулирующий гормон, фракталкин, FZD1, FZD2, FZD3, FZD4, FZD5, FZD6, FZD7, FZD8, FZD9, FZD10, G250, Gas6, GCP-2, GCSF, GD2, GD3, GDF, GDF-1, GDF-3 (Vgr-2), GDF-5 (BMP-14, CDMP-1), GDF-6 (BMP-13, CDMP-2), GDF-7 (BMP-12, CDMP-3), GDF-8 (миостатин), GDF-9, GDF-15 (MIC-1), GDNF, GDNF, GFAP, GFRa-1, GFR-альфа 1, GFR-альфа 2, GFR-альфа 3, GITR, глюкагон, Glut4, гликопротеин IIb/IIIa (GPIIb/IIIa), GM-CSF, gp130, gp72, GRO, рилизинг-фактор гормона роста, гаптен (NP-cap или NIP-cap), HB-EGF, HCC, гликопротеин оболочки HCMV gB, гликопротеин оболочки HCMV gH, HCMV UL, гемопоэтический фактор роста (HGF), Hep B gp120, гепараназа, Her2, Her2/neu (ErbB-2), Her3 (ErbB-3), Her4 (ErbB-4), гликопротеин gB вируса простого герпеса (HSV), гликопротеин gD HSV, HGFA, высокомолекулярный ассоциированный с меланомой антиген (HMW-MAA), gp120 HIV, петля V3 gp 120 IIIB HIV, HLA, HLA-DR, HM1,24, HMFG PEM, HRG, Hrk, сердечный миозин человека, цитомегаловирус человека (HCMV), гормон роста человека (HGH), HVEM, I-309, IAP, ICAM, ICAM-1, ICAM-3, ICE, ICOS, IFNg, Ig, рецептор IgA, IgE, IGF, IGF-связывающий белок, IGF-1R, IGFBP, IGF-I, IGF-II, IL, IL-1, IL-1R, IL-2, IL-2R, IL-4, IL-4R, IL-5, IL-5R, IL-6, IL-6R, IL-8, IL-9, IL-10, IL-12, IL-13, IL-15, IL-18, IL-18R, IL-23, интерферон (INF)-альфа, INF-бета, INF-гамма, ингибин, iNOS, A-цепь инсулина, B-цепь инсулина, инсулиноподобный фактор роста 1, интегрин альфа 2, интегрин альфа 3, интегрин альфа 4, интегрин альфа 4/бета 1, интегрин альфа 4/бета 7, интегрин альфа 5 (альфа V), интегрин альфа 5/бета 1, интегрин альфа 5/бета 3, интегрин альфа 6, интегрин бета 1, интегрин бета 2, интерферон-гамма, IP-10, I-TAC, JE, калликреин 2, калликреин 5, калликреин 6, калликреин 11, калликреин 12, калликреин 14, калликреин 15, калликреин L1, калликреин L2, калликреин L3, калликреин L4, KC, KDR, фактор роста кератиноцитов (KGF), ламинин 5, LAMP, LAP, LAP (TGF-1), латентный TGF-1, латентный TGF-1 bp1, LBP, LDGF, LECT2, lefty, антиген Lewis-Y, родственный Lewis-Y антиген, LFA-1, LFA-3, Lfo, LIF, LIGHT, липопротеин, LIX, LKN, Lptn, L-селектин, LT-a, LT-b, LTB4, LTBP-1, белок поверхности легких, лютеинизирующий гормон, рецептор лимфотоксина-бета, Mac-1, MAdCAM, MAG, MAP2, MARC, MCAM, MCAM, MCK-2, MCP, M-CSF, MDC, Mer, металлопротеиназы, рецептор MGDF, MGMT, MHC (HLA-DR), MIF, MIG, MIP, MIP-1-альфа, MK, MMAC1, MMP, MMP-1, MMP-10, MMP-11, MMP-12, MMP-13, MMP-14, MMP-15, MMP-2, MMP-24, MMP-3, MMP-7, MMP-8, MMP-9, MPIF, Mpo, MSK, MSP, муцин (Muc1), MUC18, мюллерово ингибиторное вещество, Mug, MuSK, NAIP, NAP, NCAD, N-C адгерин, NCA 90, NCAM, NCAM, неприлизин, нейротрофин-3, -4 или -6, нейротурин, фактор роста нервов (NGF), NGFR, NGF-бета, nNOS, NO, NOS, Npn, NRG-3, NT, NTN, OB, OGG1, OPG, OPN, OSM, OX40L, OX40R, p150, p95, PADPr, паратиреоидный гормон, PARC, PARP, PBR, PBSF, PCAD, P-кадгерин, PCNA, PDGF, PDGF, PDK-1, PECAM, PEM, PF4, PGE, PGF, PGI2, PGJ2, PIN, PLA2, плацентарная щелочная фосфатаза (PLAP), PlGF, PLP, PP14, проинсулин, прорелаксин, белок C, PS, PSA, PSCA, простатспецифический мембранный антиген (PSMA), PTEN, PTHrp, Ptk, PTN, R51, RANK, RANKL, RANTES, RANTES, A-цепь релаксина, B-цепь релаксина, ренин, F респираторно-синцитиального вируса (RSV), RSV Fgp, Ret, ревматоидный фактор, RLIP76, RPA2, RSK, S100, SCF/KL, SDF-1, SERINE, сывороточный альбумин, sFRP-3, Shh, SIGIRR, SK-1, SLAM, SLPI, SMAC, SMDF, SMOH, SOD, SPARC, Stat, STEAP, STEAP-II, TACE, TACI, TAG-72 (ассоциированный с опухолью гликопротеин-72), TARC, TCA-3, T-клеточный рецептор (например, T-клеточный рецептор альфа/бета), TdT, TECK, TEM1, TEM5, TEM7, TEM8, TERT, PLAP-подобная щелочная фосфатаза семенников, TfR, TGF, TGF-альфа, TGF-бета, панспецифический TGF-бета, TGF-бета RI (ALK-5), TGF-бета RII, TGF-бета RIIb, TGF-бета RIII, TGF-бета 1, TGF-бета 2, TGF-бета 3, TGF-бета 4, TGF-бета 5, тромбин, Ck-1 тимуса, тиреостимулирующий гормон, Tie, TIMP, TIQ, тканевой фактор, TMEFF2, Tmpo, TMPRSS2, TNF, TNF-альфа, TNF-альфа/бета, TNF-бета 2, TNFc, TNF-RI, TNF-RII, TNFRSF10A (TRAIL R1 Apo-2, DR4), TNFRSF10B (TRAIL R2 DR5, KILLER, TRICK-2A, TRICK-B), TNFRSF10C (TRAIL R3 DcR1, LIT, TRID), TNFRSF10D (TRAIL R4 DcR2, TRUNDD), TNFRSF11A (RANK ODF R, TRANCER), TNFRSF11B (OPG OCIF, TR1), TNFRSF12 (TWEAK R FN14), TNFRSF13B (TACI), TNFRSF13C (BAFF R), TNFRSF14 (HVEM ATAR, HveA, LIGHT R, TR2), TNFRSF16 (NGFR p75NTR), TNFRSF17 (BCMA), TNFRSF18 (GITR AITR), TNFRSF19 (TROY TAJ, TRADE), TNFRSF19L (RELT), TNFRSF1A (TNF RI CD120a, p55-60), TNFRSF1B (TNF RII CD120b, p75-80), TNFRSF26 (TNFRH3), TNFRSF3 (LTbR TNF RIII, TNFC R), TNFRSF4 (OX40 ACT35, TXGP1 R), TNFRSF5 (CD40 p50), TNFRSF6 (Fas Apo-1, APT1, CD95), TNFRSF6B (DcR3 M68, TR6), TNFRSF7 (CD27), TNFRSF8 (CD30), TNFRSF9 (4-1BB CD137, ILA), TNFRSF21 (DR6), TNFRSF22 (DcTRAIL R2 TNFRH2), TNFRST23 (DcTRAIL R1 TNFRH1), TNFRSF25 (DR3 Apo-3, LARD, TR-3, TRAMP, WSL-1), TNFSF10 (TRAIL Apo-2 ligand, TL2), TNFSF11 (лиганд TRANCE/RANK ODF, лиганд OPG), TNFSF12 (лиганд TWEAK Apo-3, лиганд DR3), TNFSF13 (APRIL TALL2), TNFSF13B (BAFF BLYS, TALL1, THANK, TNFSF20), TNFSF14 (лиганд LIGHT HVEM, LTg), TNFSF15 (TL1A/VEGI), TNFSF18 (лиганд GITR лиганда AITR, TL6), TNFSF1A (TNF-a конектин, DIF, TNFSF2), TNFSF1B (TNF-b LTa, TNFSF1), TNFSF3 (LTb TNFC, p33), TNFSF4 (лиганд OX40 gp34, TXGP1), TNFSF5 (лиганд CD40 CD154, gp39, HIGM1, IMD3, TRAP), TNFSF6 (Fas-лиганд лиганда Apo-1, лиганд APT1), TNFSF7 (CD27-лиганд CD70), TNFSF8 (CD30-лиганд CD153), TNFSF9 (лиганд 4-1BB лиганда CD137), TP-1, t-PA, Tpo, TRAIL, TRAIL R, TRAIL-R1, TRAIL-R2, TRANCE, рецептор трансферрина, TRF, Trk, TROP-2, TSG, TSLP, ассоциированный с опухолью антиген CA125, ассоциированный с опухолью антиген, экспрессирующий родственный Lewis-Y углевод, TWEAK, TXB2, Ung, uPAR, uPAR-1, урокиназа, VCAM, VCAM-1, VECAD, VE-кадгерин, VE-кадгерин-2, VEFGR-1 (flt-1), VEGF, VEGFR, VEGFR-3 (flt-4), VEGI, VIM, вирусные антигены, VLA, VLA-1, VLA-4, интегрин VNR, фактор фон Виллебранда, WIF-1, WNT1, WNT2, WNT2B/13, WNT3, WNT3A, WNT4, WNT5A, WNT5B, WNT6, WNT7A, WNT7B, WNT8A, WNT8B, WNT9A, WNT9A, WNT9B, WNT10A, WNT10B, WNT11, WNT16, XCL1, XCL2, XCR1, XCR1, XEDAR, XIAP, XPD, HMGB1, IgA, Aβ, CD81, CD97, CD98, DDR1, DKK1, EREG, Hsp90, IL-17/IL-17R, IL-20/IL-20R, окисленный LDL, PCSK9, прекалликреин, RON, TMEM16F, SOD1, хромогранин A, хромогранин B, белок тау, VAP1, высокомолекулярный кининоген, IL-31, IL-31R, Nav1.1, Nav1.2, Nav1.3, Nav1.4, Nav1.5, Nav1.6, Nav1.7, Nav1.8, Nav1.9, EPCR, C1, C1q, C1r, C1s, C2, C2a, C2b, C3, C3a, C3b, C4, C4a, C4b, C5, C5a, C5b, C6, C7, C8, C9, фактор B, фактор D, фактор H, пропердин, склеростин, фибриноген, фибрин, протромбин, тромбин, тканевой фактор, фактор V, фактор Va, фактор VII, фактор VIIa, фактор VIII, фактор VIIIa, фактор IX, фактор IXa, фактор X, фактор Xa, фактор XI, фактор XIa, фактор XII, фактор XIIa, фактор XIII, фактор XIIIa, TFPI, антитромбин III, EPCR, тромбомодулин, TAPI, tPA, плазминоген, плазмин, PAI-1, PAI-2, GPC3, синдекан-1, синдекан-2, синдекан-3, синдекан-4, LPA, S1P, рецептор ацетилхолина, AdipoR1, AdipoR2, рибозилциклаза-1 ADP, интегрин альфа-4/бета-7, интегрин альфа-5/бета-1, интегрин альфа-v/бета-6, интегрин альфа-v/бета-1, лиганд-2 ангиопоэтина, Angptl2, возбудитель сибирской язвы, кадгерин, карбоангидраза-IX, CD105, CD155, CD158a, CD37, CD49b, CD51, CD70, CD72, клаудин 18, токсин Clostridium difficile, CS1, лиганд 4 дельта-подобного белка, оксидаза DHICA, лиганд Dickkopf-1, дипептидилпептидаза IV, EPOR, F-белок RSV, фактор Ia, FasL, альфа-рецептор фолата, рецептор глюкагона, рецептор глюкагон-подного пептида 1, глутамат карбоксипептидаза II, GMCSFR, гликопротеин E2 вируса гепатита C, гепцидин, рецептор IL-17, рецептор IL-22, рецептор IL-23, рецептор IL-3, тирозинкиназа Kit, лейцин-богатый альфа-2-гликопротеин 1 (LRG1), рецептор лизосфинголипида, мембранный гликопротеин OX2, мезотелин, MET, MICA, MUC-16, ассоциированный с миелином гликопротеин, нейропилин-1, нейропилин-2, рецептор Nogo, PLXNA1, PLXNA2, PLXNA3, PLXNA4A, PLXNA4B, PLXNB1, PLXNB2, PLXNB3, PLXNC1, PLXND1, лиганд запрограммированной клеточной гибели 1, конвертаза пробелков PC9, лиганд-1 гликопротеина P-селектина, RAGE, ретикулон 4, RF, RON-8, SEMA3A, SEMA3B, SEMA3C, SEMA3D, SEMA3E, SEMA3F, SEMA3G, SEMA4A, SEMA4B, SEMA4C, SEMA4D, SEMA4F, SEMA4G, SEMA5A, SEMA5B, SEMA6A, SEMA6B, SEMA6C, SEMA6D, SEMA7A, шигаподобный токсин II, рецептор-1 сфингозин-1-фосфата, ST2, стафилококковаая липотейхоевая кислота, тенасцин, TG2, рецептор тимического стромального лимфопоэтина, рецептор 12A суперсемейства TNF, трансмембранный гликопротеин NMB, TREM-1, TREM-2, трофобластный гликопротеин, рецептор TSH, TTR, тубулин, ULBP2 и рецепторы для гормонов или факторов роста. Другие примеры антигена могут включать растворимые молекулы рецепторов, описанных выше, которые существуют в жидкостях организма in vivo, не являясь заякоренными на клетках.
Эпитоп, который означает антигенную детерминанту, находящуюся в антигене, означает участок на антигене, с которым связывается антигенсвязывающий домен в антигенсвязывающей молекуле, описанной в настоящем описании. Таким образом, например, эпитоп может определяться его структурой. Альтернативно эпитоп определяется антигенсвязывающей активностью антигенсвязывающей молекулы, которая распознает эпитоп. Эпитоп в антигенном пептиде или полипептиде может определяться аминокислотными остатками, составляющими эпитоп. Альтернативно эпитоп, состоящий из цепи сахаров, может определяться конкретной структурой цепи сахаров.
Линейный эпитоп относится к эпитопу, содержащему эпитоп, который распознается через его первичную последовательность аминокислот. Линейный эпитоп как правило содержит по меньшей мере 3 и наиболее часто по меньшей мере 5, например, от приблизительно 8 до приблизительно 10 или от 6 до 20 аминокислот, в уникальной последовательности.
В противоположность линейному эпитопу, конформационный эпитоп относится к эпитопу, который содержится в первичной последовательности аминокислот, содержащей компонент, отличный от одного определенного компонента распознаваемого эпитопа (например, эпитоп, первичная последовательность аминокислот может не распознаваться антителом, которое определяет эпитоп). Конформационный эпитоп может содержать увеличенное количество аминокислот по сравнению с линейным эпитопом. Антитело распознает конформационный эпитоп путем распознавания трехмерной структуры антигенного пептида или белка. Например, молекула белка может быть свернута с образованием трехмерной структуры. В таком случае, определенные аминокислоты и/или полипептидный остов, образующий конформационный эпитоп, расположены параллельно, чтобы позволить антителу распознавать эпитоп. Конформацию эпитопа определяют способом, включающим, например, но не ограничивающимся ими, рентгеновскую кристаллографию, двумерную ядерную магнитно-резонансную спектроскопию и сайт-специфическое спиновое мечение и спектроскопию электронного парамагнитного резонанса. См., например, Epitope Mapping Protocols in Methods in Molecular Biology (1996), Vol. 66, Morris ed.
Подход рекомбинации генов
Термин “набор кодонов” относится к набору различных нуклеотидных триплетных последовательностей, которые используют для кодирования желаемой аминокислоты. Один набор олигонуклеотидов включает последовательности, которые отражают каждую возможную комбинацию нуклеотидных триплетов, обеспечиваемых набором кодонов, и кодируют желаемую группу аминокислот. Такой набор олигонуклеотидов можно синтезировать, например, с помощью твердофазного способа. IUB обеспечивает стандартную систему обозначения кодонов. Этот код известен в данной области. Набор кодонов обычно указывают с помощью трех прописных букв, например, NNK, NNS, DVK или DVD.
Код IUB
G: гуанин
A: аденин
T: тимин
C: цитозин
R (A или G)
Y (C или T)
M (A или C)
K (G или T)
S (C или G)
W (A или T)
H (A, C или T)
B (C, G или T)
V (A, C или G)
D (A, G или T)
N (A, C, G или T)
Например, в наборе кодонов DVK, D представляет собой нуклеотид A, G или T; V представляет собой A, G или C; и K представляет собой G или T. Этот набор кодонов представляет собой 18 различных кодонов и может кодировать аминокислоты Ala, Trp, Tyr, Lys, Thr, Asn, Lys, Ser, Arg, Asp, Glu, Gly и Cys.
Олигонуклеотид, имеющий “вырожденный” нуклеотид в конкретном положении, конструируют способом, известным в области, к которой относится настоящее изобретение (например, Garrard and Henner, Gene (1993) 128, 103-109). Набор олигонуклеотидов, имеющих такой определенный тип набора кодонов, можно синтезировать с использованием коммерчески доступного устройства для синтеза нуклеиновых кислот (доступного, например, от Applied Biosystems, Inc., Foster City, CA), или его можно получать в качестве коммерчески доступных продуктов (например, Life Technologies, Rockville, MD). Таким образом, набор синтетических олигонуклеотидов, имеющих конкретный набор кодонов, обычно содержит множество олигонуклеотидов, отличающихся по последовательности. В неограничивающем аспекте настоящего изобретения олигонуклеотиды могут содержать, например, участки ферментов рестрикции, пригодные для клонирования.
Термины “клетка”, “клеточная система” и “клеточная культура” используют в настоящем описании синонимично. Такие обозначения могут включать каждого потомка клеток или клеточных систем. Таким образом, например, термины “трансформант” и “трансформированная клетка” включают первичные клетки-мишени и культуры, происходящие из них, не зависимо количества пассажей. Также следует понимать, что каждый потомок может не иметь точно идентичные содержащиеся в них ДНК, вследствие преднамеренной или случайной мутации. Эти термины могут включать потомка варианта, имеющего по существу те же функции или биологическую активность, что и при скрининге первоначально трансформированных клеток. Если подразумевается другое обозначение, это будет очевидно из контекста.
Термин “последовательность контроля”, используемый для указания на экспрессию кодирующей последовательности, относится к нуклеотидной последовательности ДНК, необходимой для экспрессии функционально связанной кодирующей последовательности в конкретном организме-хозяине. Последовательности контроля, пригодные, например, для прокариот, включают промоторы, необязательные последовательности операторов, участки связывания рибосом и, вероятно, другие последовательности, которые все еще предстоит изучить. Использование промотора, сигнала полиаденилирования и энхансера известно в данной области для экспрессии кодирующей последовательности в эукариотических клетках.
Выражение “функционально связанный” в отношении нуклеиновой кислоты означает, что нуклеиновая кислота имеет функциональную взаимосвязь с другой последовательностью нуклеиновой кислоты. Например, препоследовательность или секреторная лидерную ДНК функционально связана с ДНК полипептида, когда он экспрессируется в качестве белка-предшественника, вовлеченного в секрецию полипептида. Промотор или энхансер, когда они влияют на транскрипцию кодирующей последовательности, функционально связаны с последовательностью. Альтернативно, участок связывания рибосом, когда он расположен так, чтобы способствовать трансляции, функционально связан с кодирующей последовательностью. Обычно выражение “функционально связанный” означает, что последовательности связанных ДНК расположены последовательно и что секреторная лидерная последовательность, например, в последовательном порядке присутствует в рамке считывания. Однако энхансер не должен располагаться последовательно. Такую связь достигают путем лигирования в соответствующих участках лигирования. В отсутствие таких участков используют синтетический олигонуклеотидный адаптер или линкер в соответствии с общепринятой практикой. Альтернативно связанные нуклеиновые кислоты можно получать с помощью подхода перекрывающейся ПЦР, описанного ниже.
“Лигирование” относится к способу формирования фосфодиэфирной связи между двумя фрагментами нуклеиновой кислоты. Для лигирования двух фрагментов концы этих фрагментов должны быть совместимыми друг с другом. В некоторых случаях эти концы обладают совместимостью сразу после расщепления эндонуклеазой. Однако совместимость для лигирования требует, чтобы сначала липкие концы, обычно образующиеся при расщеплении эндонуклеазой, были преобразованы в тупые концы. Для преобразования в тупые концы каждую ДНК обрабатывают приблизительно 10 единицами фрагмента Кленова ДНК-полимеразы I или ДНК-полимеразой T4 при 15°C в течение по меньшей мере 15 минут в присутствии четырех дезоксирибонуклеотидтрифосфатов в соответствующем буферном растворе. Далее ДНК очищают экстракцией фенолом-хлороформом и преципитацией этанолом, или очисткой на диоксиде кремния. Фрагменты ДНК, подлежащие слиянию, добавляют в эквимолярных количествах к раствору. Этот раствор содержит ATP и буфер лигазы, а также приблизительно 10 единиц лигазы (например, ДНК-лигаза T4) на 0,5 мкг ДНК. В случае связывания ДНК с вектором, вектор сначала линеаризуют посредством расщепляющего действия соответствующей эндонуклеазы рестрикции. Затем линеаризованный фрагмент обрабатывают бактериальной щелочной фосфатазой или фосфатазой кишечника теленка, тем самым препятствуя самолигированию фрагмента на стадии лигирования.
Термин “белок оболочки” относится к белку, по меньшей мере часть которого присутствует на поверхности вирусной частицы. С точки зрения функциональности, белок оболочки представляет собой произвольный белок, который связывается с вирусными частицами в процессе конструирования вирусов в клетках-хозяевах и сохраняет его связанное состояние до тех пор, пока не произойдет инфицирование вирусом других клеток-хозяев. Белок оболочки может представлять собой основной белок оболочки или может представлять собой минорный белок оболочки. Минорный белок оболочки обычно представляет собой белок оболочки, присутствующий в вирусном капсиде в количестве предпочтительно по меньшей мере приблизительно 5, более предпочтительно по меньшей мере приблизительно 7, еще более предпочтительно по меньшей мере приблизительно 10 или более копий белка на вирион. Основной белок оболочки может присутствовать в количестве десятков, сотен или тысяч копий на вирион. Примеры основного белка оболочки включают белок p8 нитчатого фага.
Термин “предел выявления” для химического объекта, такого как неорганический объект, органический объект или организм в конкретном анализе относится к минимальной концентрации объекта, выявляемой выше фонового уровня для анализа. Например, в ELISA фагов, “предел выявления” для конкретного фага, экспонирующего конкретный антигенсвязывающий фрагмент, относится к концентрации фага, при которой конкретный фаг генерирует больше сигналов ELISA, чем сигналы, генерируемые контрольным фагом, который не экспонирует антигенсвзывающий фрагмент.
Термин “фаговый дисплей” относится к подходу, посредством которого варианты полипептидов экспонируются в качестве слитых белков по меньшей мере с частью белков оболочки на поверхности частиц фагов, например, нитчатых фагов. Фаговый дисплей является полезным, поскольку большую библиотеку рандомизированных вариантов белка можно быстро и эффективно подвергать скринингу в отношении связывания последовательности с антигеном-мишенью с высокой аффинностью. Дисплей библиотек пептидов и белков на фагах используют для скрининга миллионов полипептидов в отношении полипептидов с конкретными свойствами связывания. Способ поливалентного фагового дисплея используют для дисплея небольших случайных пептидов и небольших белков путем слияния с геном III или геном VIII нитчатого фага (Wells and Lowman, Curr. Opin. Struct. Biol. (1992) 3, 355-362; и ссылки, цитированные в указанном документе). Одновалентный фаговый дисплей вовлекает слияние библиотеки белков или пептидов с геном III или его частью, и экспрессию слитых белков на низких уровнях в присутствии белка гена III дикого типа, так что каждая фаговая частица экспонирует одну копию или ни одной копии слитых белков. Одновалентные фаги имеют более низкий эффект авидности, чем у поливалентных фагов, и, таким образом, их подвергают скринингу на основе эндогенной аффинности лиганда с использованием фагмидных векторов, которые упрощают манипулирование с ДНК (Lowman and Wells, Methods: A Companion to Methods in Enzymology (1991) 3, 205-216).
“Фагмида” относится к плазмидному вектору, обладающему бактериальным ориджином репликации, например Co1E1, и копией межгенной области бактериофага. В качестве фагмиды можно соответствующим образом использовать любой бактериофаг, известный в данной области, включая, например, нитчатые бактериофаги и лямбдоидные бактериофаги. Обычно плазмида дополнительно содержит селективный маркер устойчивости к антибиотику. Фрагменты ДНК, клонированные в эти векторы, можно выращивать в качестве плазмид. Когда клетки, трансформированные этими векторами, обладают всеми генами, необходимыми для продуцирования фаговых частиц, профиль репликации плазмид сдвигается на профиль репликации по принципу “катящегося кольца” с образованием копий одной цепи плазмидной ДНК и упаковыванием фаговых частиц. Фагмида может образовывать инфекционные или неинфекционные фаговые частицы. Этот термин включает фагмиды, содержащие ген белка оболочки фага или его фрагмент, связанный с геном гетерологичного полипептида путем слияния генов, так что гетерологичный пептид экспонируется на поверхности фаговой частицы.
Термин “фаговый вектор” означает двухцепочечный репликативный бактериофаг, который содержит гетерологичный ген и способен реплицироваться. Фаговый вектор имеет ориджин репликации фага, который позволяет репликацию фага и образование фаговых частиц. Предпочтительно фаг является нитчатым бактериофагом, например, фаг M13, f1, fd или Pf3 или их производное, или лямбдоидным фагом, например, лямбда, 21, phi80, phi81, 82, 424, 434, или любым другим фагом или его производным.
Термин “олигонуклеотид” относится к короткому одноцепочечному или двухцепочечному полидезоксинуклеотиду, который химически синтезируют способом, известным в данной области (например, химия фосфотриэфиров, фосфитов или фосфорамидитов с использованием твердофазного подхода, такого как подход, описанный в EP266032; или способ через промежуточное соединение дезоксинуклеотид H-фосфонат, описанный в Froeshler et al., Nucl. Acids. Res. (1986) 14, 5399-5407). Другие способы синтеза олигонуклеотидов включают полимеразную цепную реакцию, описанную ниже, и другие автоматические способы с праймерами и олигонуклеотидный синтез на твердой подложке. Все из этих способов описаны в Engels et al., Agnew. Chem. Int. Ed. Engl. (1989) 28, 716-734. Эти способы используют при условии, что вся последовательность нуклеиновой кислоты гена известна, и при условии, что доступна последовательность нуклеиновой кислоты, комплементарная кодирующей цепи. Альтернативно возможные последовательности нуклеиновых кислот можно соответствующим образом предсказывать с использованием известных и предпочтительных остатков, кодирующих каждый аминокислотный остаток, если известна заданная аминокислотная последовательность. Олигонуклеотид можно очищать с использованием полиакриламидных гелей, или колонки с молекулярными ситами, или путем преципитации.
Термины “слитый белок” и “слитый полипептид” относятся к полипептиду, имеющему два сегмента, ковалентно связанны друг с другом. Этот полипептид имеет различные признаки, определяемые этими сегментами. Эти признаки могут представлять собой в каждом случае, например, биологическое свойство, такое как активность in vitro или in vivo. Альтернативно эти признаки могут представлять собой в каждом случае химическое или физическое свойство, например, связывание с антигеном мишенью или катализ реакции. Эти два сегмента могут быть связаны либо прямо через одинарную пептидную связь, либо через пептидный линкер, содержащий один или более аминокислотных остатков. Обычно эти два сегмента и линкер присутствуют в одной рамке считывания. Предпочтительно, два сегмента полипептида получают из гетерологичных или различающихся полипептидов.
Термин “гетерологичная ДНК” относится к произвольной ДНК, которую переносят в клетки-хозяева. ДНК может происходить из различных источников, включая геномные ДНК, кДНК, синтетические ДНК и их слитые конструкции или комбинации. ДНК может включать ДНК из тех же клеток или того же типа клеток, что и клетки-хозяева или реципиентные клетки, или ДНК из отличающегося типа клеток, например, из млекопитающего или растения. ДНК необязательно может содержать маркерный или селективный ген, например, ген устойчивости к антибиотику или ген температурной устойчивости, и т.п.
Термин “положение с высокой степенью разнообразия”, как используют в рамках изобретения, относится к положению аминокислоты в вариабельных областях легкой и тяжелой цепи, имеющему несколько различных аминокислот, присутствующих в этом положении, когда сравнивают аминокислотные последовательности известных и/или природных антител или антигенсвязывающие фрагменты. Положение с высокой степенью разнообразия обычно находится в областях CDR. В одном аспекте положение с высокой степенью разнообразия в известных и/или природных антителах эффективно определяют, исходя из данных, предоставленных в Кабат, Sequences of Proteins of Immunological Interest (National Institutes of Health, Bethesda, Md., 1987 and 1991). Во множестве баз данных (http://vbase.mrc-cpe.cam.ac.uk/ и http://www.bioinf.org.uk/abs/index.html) в интернете предоставлена обширная коллекция множества последовательностей легких и тяжелых цепей человека и их выравнивание. Информация об этих последовательностях и их выравнивании является полезной для определения положения с высокой степенью разнообразия в соответствии с настоящим изобретением. В соответствии с настоящим изобретением, положение аминокислоты считается положением с высокой степенью разнообразия, если положение аминокислоты имеет разнообразие предпочтительно от приблизительно 2 до приблизительно 20, предпочтительно от приблизительно 3 до приблизительно 19, предпочтительно от приблизительно 4 до приблизительно 18, предпочтительно от 5 до 17, предпочтительно от 6 до 16, предпочтительно от 7 до 15, предпочтительно от 8 до 14, предпочтительно от 9 до 13, или предпочтительно от 10 до 12 возможных аминокислотных остатков в этом положении. В некоторых вариантах осуществления положение аминокислоты может иметь разнообразие предпочтительно по меньшей мере приблизительно 2, предпочтительно по меньшей мере приблизительно 4, предпочтительно по меньшей мере приблизительно 6, предпочтительно по меньшей мере приблизительно 8, предпочтительно приблизительно 10, предпочтительно приблизительно 12 возможных различных аминокислотных остатков. В настоящем описании такие аминокислотные остатки также называют нестрогими остатками. Термин “неслучайный набор кодонов” относится к набору кодонов, кодирующему выбранную аминокислоту, которая частично (предпочтительно, полностью) удовлетворяет критериям выбора аминокислот, описанным в настоящем описании. Термин “случайный набор кодонов”, как используют в рамках изобретения, относится к набору кодонов, имеющему комбинацию кодонов, кодирующих произвольную аминокислоту, выбранную из 20 аминокислот (Ala/A, Leu/L, Arg/R, Lys/K, Asn/N, Met/M, Asp/D, Phe/F, Cys/C, Pro/P, Gln/Q, Ser/S, Glu/E, Thr/T, Gly/G, Trp/W, His/H, Tyr/Y, Ile/I и Val/V).
Библиотека
В соответствии с одним аспектом, настоящее изобретение относится библиотеке, по существу состоящей из множества антигенсвязывающих молекул, отличающиеся друг от друга последовательностью, где антигенсвязывающий домен в каждой из антигенсвязывающих молекул содержит по меньшей мере один аминокислотный остаток, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов. Предпочтительные примеры концентрации ионов включают концентрацию ионов металлов и концентрацию ионов водорода.
Термин “библиотека”, описанный в настоящем описании, относится к множеству антигенсвязывающих молекул, множеству слитых полипептидов, каждый из которых содержит антигенсвязывающие молекулы, или нуклеиновым кислотам или полинуклеотидам, каждый из которых кодирует свою последовательность. Множество антигенсвязывающих молекул, содержащихся в библиотеке, или множество слитых полипептидов, каждый из которых содержит антигенсвязывающие молекулы, не имеют одну и ту же последовательность, и представляют собой антигенсвязывающие молекулы, отличающиеся друг от друга последовательностью, или слитые полипептиды, каждый из которых содержит эти антигенсвязывающие молекулы.
Термин “ион металла”, описанный в настоящем описании, относится к иону элемента, принадлежащему к любой из группы I, включая щелочные металлы, за исключением водорода и семейства меди, группы II, включая щелочноземельные металлы и семейство цинка, группы III, за исключением бора, группы IV, за исключением углерода и кремния, группы VIII, включая семейство железа и семейство платины, и подгруппы A групп V, VI и VII, или металлический элемент, такой как сурьма, висмут или полоний. Атомы металлов имеют свойство высвобождать валентные электроны, становясь катионами. Это свойство называют тенденцией к ионизации. Металлы, имеющие высокую тенденцию к ионизации, согласно сообщениям, имеют высокую химическую активность.
Примеры иона металла, предпочтительного в рамках настоящего изобретения, включают ионы кальция. Ионы кальция вовлечены в регуляцию множества жизненно-важных явлений, включая сокращение мышц, таких как скелетная мышца, гладкая мышца и сердечная мышца, активацию (например, движение и фагоцитоз) лейкоцитов, активацию (например, деформация и секреция) тромбоцитов, активацию лимфоцитов, активацию (например, секреция гистамина) тучных клеток, клеточный ответ, опосредуемый α-рецептором катехоламинов или рецептором ацетилхолина, экзоцитоз, высвобождение трансмиттеров из окончаний нейронов, и аксональный поток в нейронах. Например, в качестве внутриклеточных рецепторов ионов кальция известны тропонин C, кальмодулин, парвальбумин и легкая цепь миозина, которые имеют несколько участков связывания ионов кальция и, возможно, происходят из общего источника с точки зрения молекулярной эволюции. Также известно большое количество их связывающих мотивов. Хорошо известными связывающими мотивами являются, например, домен кадгерина, EF hand, содержащийся в кальмодулине, домен C2, содержащийся в протеинкиназе C, домен Gla, содержащийся в факторе свертывания крови IX, лектин C-типа, содержащийся в рецепторе асиалогликопротеинов или манноза-связывающем рецепторе, домен A, содержащийся в рецепторе LDL, аннексин, домен тромбоспондина 3 типа и EGF-подобный домен.
Когда ион металла в соответствии с настоящим изобретением представляет собой ион кальция, примеры условий концентрации ионов кальция включают условия низкой концентрации ионов кальция и условия высокой концентрации ионов кальция. Выражение “активность связывания меняется, в зависимости от условий концентрации ионов кальция” означает, что антигенсвязывающая активность каждой антигенсвязывающей молекулы изменяется, в зависимости от различий между условиями низкой концентрации ионов кальция и условиями высокой концентрации ионов кальция. Примеры этого случая включают более высокую антигенсвязывающую активность антигенсвязывающей молекулы в условиях высокой концентрации ионов кальция, чем в условиях низкой концентрации ионов кальция. Другой его пример включает более высокую антигенсвязывающую активность антигенсвязывающей молекулы в условиях низкой концентрации ионов кальция, чем в условиях высокой концентрации ионов кальция.
В рамках настоящего описания высокая концентрация ионов кальция конкретно не ограничена однозначной численной величиной и предпочтительно может представлять собой концентрацию, выбранную из диапазона от 100 мкМ до 10 мМ. В другом аспекте высокая концентрация ионов кальция может представлять собой концентрацию, выбранную из диапазона от 200 мкМ до 5 мМ. В другом аспекте высокая концентрация ионов кальция также может представлять собой концентрацию, выбранную из диапазона от 500 мкМ до 2,5 мМ. В альтернативном аспекте высокая концентрация ионов кальция также может представлять собой концентрацию, выбранную из диапазона от 200 мкМ до 2 мМ. Кроме того, эта концентрация также может представлять собой концентрацию, выбранную из диапазона от 400 мкМ до 1,5 мМ. Ее особенно предпочтительные примеры включают концентрации, выбранные из диапазона от 500 мкМ до 2,5 мМ, которые близки к концентрации ионов кальция в плазме (в крови) in vivo.
В настоящем описании низкая концентрация ионов кальция конкретно не ограничена однозначной численной величиной, и предпочтительно она может представлять собой концентрацию, выбранную из диапазона от 0,1 мкМ до 30 мкМ. В другом аспекте низкая концентрация ионов кальция может представлять собой концентрацию, выбранную из диапазона от 0,2 мкМ до 20 мкМ. В другом аспекте низкая концентрация ионов кальция также может представлять собой концентрацию, выбранную из диапазона от 0,5 мкМ до 10 мкМ. В альтернативном аспекте низкая концентрация ионов кальция также может представлять собой концентрацию, выбранную из диапазона от 1 мкМ до 5 мкМ. Кроме того, эта концентрация также может представлять собой концентрацию, выбранную из диапазона от 2 мкМ до 4 мкМ. Ее особенно предпочтительные примеры включают концентрации, выбранные из диапазона от 1 мкМ до 5 мкМ, которые являются близкими к концентрациям ионизированного кальция в ранней эндосоме in vivo.
В рамках настоящего изобретения выражение “антигенсвязывающая активность антигенсвязывающей молекулы является более низкой в условиях низкой концентрации ионов кальция, чем в условиях высокой концентрации ионов кальция” означает, что антигенсвязывающая активность антигенсвязывающей молекулы при концентрации ионов кальция, выбранной из диапазона от 0,1 мкМ до 30 мкМ, является более слабой, чем при концентрации ионов кальция, выбранной из диапазона от 100 мкМ до 10 мМ. Это выражение предпочтительно означает, что антигенсвязывающая активность антигенсвязывающей молекулы при концентрации ионов кальция, выбранной из диапазона от 0,5 мкМ до 10 мкМ, является более слабой, чем при концентрации ионов кальция, выбранной из диапазона от 200 мкМ до 5 мМ. Особенно предпочтительно выражение означает, что антигенсвязывающая активность при концентрации ионов кальция в ранней эндосоме in vivo является более слабой, чем при концентрации ионов кальция в плазме in vivo. В частности, это означает, что антигенсвязывающая активность антигенсвязывающей молекулы при концентрации ионов кальция, выбранной из диапазона от 1 мкМ до 5 мкМ, является более слабой, чем при концентрации ионов кальция, выбранной из диапазона от 500 мкМ до 2,5 мМ.
Определение того, изменяется ли антигенсвязывающая активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов металлов, можно проводить с использованием способа анализа, известного в данной области. Например, антигенсвязывающую активность антигенсвязывающей молекулы сравнивают между условиями низкой концентрации ионов кальция и условиями высокой концентрации ионов кальция, чтобы подтвердить, что антигенсвязывающая активность антигенсвязывающей молекулы изменяется до более высокого уровня в условиях высокой концентрации ионов кальция, чем в условиях низкой концентрации ионов кальция.
В рамках настоящего изобретения выражение “антигенсвязывающая активность антигенсвязывающей молекулы является более низкой в условиях низкой концентрации ионов кальция, чем в условиях высокой концентрации ионов кальция” может быть выражено как “антигенсвязывающая активность антигенсвязывающей молекулы является более высокой в условиях высокой концентрации ионов кальция, чем в условиях низкой концентрации ионов кальция”. В рамках настоящего изобретения выражение “антигенсвязывающая активность является более низкой в условиях низкой концентрации ионов кальция, чем в условиях высокой концентрации ионов кальция” также описывается как “антигенсвязывающая способность является более слабой в условиях низкой концентрации ионов кальция, чем в условиях высокой концентрации ионов кальция”. Кроме того, выражение “антигенсвязывающая активность в условиях низкой концентрации ионов кальция является сниженной относительно антигенсвязывающей активности в условиях высокой концентрации ионов кальция” также описывается как “антигенсвязывающая способность в условиях низкой концентрации ионов кальция ослаблена относительно антигенсвязывающей активности в условиях высокой концентрации ионов кальция”.
Условия, отличные от концентрации ионов кальция для анализа антигенсвязывающей активности, могут соответствующим образом выбирать специалисты в данной области без конкретных ограничений. Антигенсвязывающую активность можно анализировать в условиях, например, буфера HEPES и 37°C. Также антигенсвязывающую активность можно анализировать с использованием, например, Biacore (GE Healthcare Bio-Sciences Corp.). В анализе антигенсвязывающей активности, антигенсвязывающую молекулу можно оценивать в отношении ее связывающей способности против, например, растворимых антигенов, путем инжекции антигенов в качестве анализируемого соединения на чип, на котором иммобилизована антигенсвязывающая молекула. Альтернативно антигенсвязывающую молекулу можно оценивать в отношении ее связывающей способности против, например, мембранных антигенов, путем инжекции молекулы в качестве анализируемого соединения на чип с иммобилизованным антигеном.
В антигенсвязывающей молекуле по настоящему изобретению соотношение между антигенсвязывающей активностью в условиях низкой концентрации ионов кальция и антигенсвязывающей активностью в условиях высокой концентрации ионов кальция конкретно не ограничено, при условии, что антигенсвязывающая активность в условиях низкой концентрации ионов кальция является более слабой, чем в условиях высокой концентрации ионов кальция. Отношение константы диссоциации KD в условиях низкой концентрации ионов кальция к KD в условиях высокой концентрации ионов кальция (KD (3 мкМ Ca)/KD (2 мМ Ca)) для антигенов предпочтительно составляет 2 или выше, более предпочтительно 10 или выше, еще более предпочтительно 40 или выше. Верхней предел отношения KD (3 мкМ Ca)/KD (2 мМ Ca) конкретно не ограничен, и оно может представлять собой любую величину, включая 400, 1000, 10000 и т.д. при условии, что итоговая антигенсвязывающая молекула может быть технически получена специалистами в данной области. Альтернативно отношение может определяться величиной KD (3 мкМ Ca)/KD (1,2 мМ Ca). В частности, отношение KD (3 мкМ Ca)/KD (1,2 мМ Ca) равно 2 или выше, более предпочтительно 10 или выше, еще более предпочтительно 40 или выше. Верхний предел отношения KD (3 мкМ Ca)/KD (1,2 мМ Ca) конкретно не ограничен и может представлять собой величину, включающую 400, 1000, 10000 и т.д. при условии, что итоговая антигенсвязывающая молекула может быть технически получена специалистами в данной области.
Константу диссоциации KD можно использовать в качестве величины антигенсвязывающей активности для растворимых антигенов. Альтернативно для мембранных антигенов можно использовать кажущуюся KD (кажущаяся константа диссоциации). KD (константа диссоциации) и кажущуюся KD (кажущаяся константа диссоциации) можно измерять способом, общеизвестным специалистам в данной области, например, с использованием Biacore (GE Healthcare Bio-Sciences Corp.), графика Скэтчарда или проточного цитометра.
Альтернативно, предпочтительно можно использовать, например, константу скорости диссоциации kd в качестве другого показателя, который указывает на соотношение между антигенсвязывающей активностью в условиях низкой концентрации кальция и антигенсвязывающей активностью в условиях высокой концентрации кальция для антигенсвязывающей молекулы по настоящему изобретению. В случае использования kd (константа скорости диссоциации) вместо KD (константа диссоциации) в качестве отношения активностей связывания, отношение kd (константа скорости диссоциации) в условиях низкой концентрации ионов кальция к kd (константа скорости диссоциации) в условиях высокой концентрации кальция (kd (в условиях низкой концентрации ионов кальция)/kd (в условиях высокой концентрации кальция)) для антигенов предпочтительно составляет 2 или выше, более предпочтительно 5 или выше, еще более предпочтительно 10 или выше, еще более предпочтительно 30 или выше. Верхний предел отношения kd (в условиях низкой концентрации ионов кальция)/kd (в условиях высокой концентрации кальция) конкретно не ограничен и он может представлять собой любую величину, включающую 50, 100, 200 и т.д., при условии что итоговая антигенсвязывающая молекула может быть получена в соответствии с техническим здравым смыслом специалистов в данной области.
Константу скорости диссоциации kd можно использовать в качестве величины антигенсвязывающей активности для растворимых антигенов. Альтернативно для мембранных антигенов можно использовать кажущуюся kd (кажущаяся константа скорости диссоциации). kd (константа скорости диссоциации) и кажущуюся kd (кажущаяся константа скорости диссоциации) можно измерять способом, общеизвестным специалистам в данной области, например, с использованием Biacore (GE Healthcare Bio-Sciences Corp.) или проточного цитометра. В рамках настоящего изобретения антигенсвязывающая активность антигенсвязывающей молекулы при различных концентрациях ионов кальция предпочтительно анализируют при условии, что другую концентрацию кальция сохраняют постоянной.
В рамках настоящего изобретения условия концентрации для протона, т.е. атомного ядра водорода, используют синонимично с условиями водородного показателя (pH). Когда активную массу ионов водорода в водном растворе указывают как aH+, pH определяется как -log10aH+. В водном растворе, имеющем низкую ионную силу (например, ниже 10-3), aH+ практически равна ионной силе водорода. Например, ионное произведение воды при 25°C и давлении, равном 1 атмосферу, составляет Kw=aH+aOH=10-14 и, таким образом, aH+=aOH=10-7 для чистой воды. В этом случае, pH 7 соответствует нейтральному водному раствору; pH меньше 7 соответствует кислому водному раствору; и pH более 7 соответствует щелочному водному раствору.
В случае использования условий pH в качестве условий концентрации ионов водорода в соответствии с настоящим изобретением, примеры условий pH включают условия кислых значений pH и условия нейтральных значений pH. Выражение “активность связывания изменяется в зависимости от условий pH” означает, что антигенсвязывающая активность каждой антигенсвязывающей молекулы изменяется в зависимости от различий между условиями кислых значений pH и условиями нейтральных значений pH. Примеры этого случая включают более высокую антигенсвязывающую активность антигенсвязывающей молекулы в условиях нейтральных значений pH, чем в условиях кислых значений pH. Другой его пример включает более высокую антигенсвязывающую активность антигенсвязывающей молекулы в условиях кислых значений pH, чем в условиях нейтральных значений pH.
В настоящем описании нейтральные значения pH конкретно не ограничены однозначной численной величиной и предпочтительно они могут быть выбраны из диапазона от pH 6,7 до pH 10,0. В другом аспекте нейтральные значения pH могут быть выбраны из диапазона от pH 6,7 до pH 9,5. В другом аспекте нейтральные значения pH могут быть выбраны из диапазона от pH 7,0 до pH 9,0. В альтернативном аспекте это значение pH может быть выбрано из диапазона от pH 7,0 до pH 8,0. Его особенно предпочтительные примеры включают значение pH 7,4, которое является близким к значению pH плазмы (крови) in vivo.
В настоящем описании кислое значение pH конкретно не ограничено однозначной численной величиной и предпочтительно оно может быть выбрано из диапазона от pH 4,0 до pH 6,5. В другом аспекте кислое значение pH может быть выбрано из диапазона от pH 4,5 до pH 6,5. В другом аспекте кислоте значение pH может быть выбрано из диапазона от pH 5,0 до pH 6,5. В альтернативном аспекте это значение pH может быть выбрано из диапазона от pH 5,5 до pH 6,5. Его особенно предпочтительные примеры включают значение pH 5,8, которое является близким к значению pH в ранней эндосоме in vivo.
В рамках настоящего изобретения выражение “антигенсвязывающая активность антигенсвязывающей молекулы является более низкой в условиях кислых значений pH, чем в условиях нейтральных значений pH”, означает, что антигенсвязывающая активность антигенсвязывающей молекулы при значении pH, выбранном из диапазона от pH 4,0 до pH 6,5, является более слабой, чем при значении pH, выбранном из диапазона от pH 6,7 до pH 10,0. Это выражение предпочтительно означает, что антигенсвязывающая активность антигенсвязывающей молекулы при значении pH, выбранном из диапазона от pH 4,5 до pH 6,5, является более слабой, чем при значении pH, выбранном из диапазона от pH 6,7 до pH 9,5. Более предпочтительно, выражение означает, что антигенсвязывающая активность антигенсвязывающей молекулы при значении pH, выбранном из диапазона от pH 5,0 до pH 6,5, является более слабой, чем при значении pH, выбранном из диапазона от pH 7,0 до pH 9,0. Кроме того, выражение предпочтительно означает, что антигенсвязывающая активность антигенсвязывающей молекулы при значении pH, выбранном из диапазона от pH 5,5 до pH 6,5, является более слабой, чем при pH, выбранном из диапазона от pH 7,0 до pH 8,0. Особенно предпочтительно это выражение означает, что антигенсвязывающая активность при значении pH в ранней эндосоме in vivo является более слабой, чем при значении pH в плазме in vivo. В частности, это означает, что антигенсвязывающая активность антигенсвязывающей молекулы при pH 5,8 является более слабой, чем при pH 7,4.
Определение того, изменяется ли антигенсвязывающая активность антигенсвязывающей молекулы в зависимости от условий pH, можно определять, например, в соответствии со способом анализа активности связывания при различных условиях pH, описанных выше. Например, антигенсвязывающую активность антигенсвязывающей молекулы сравнивают между условиями кислых значений pH и условиями нейтральных значений pH для подтверждения того, что антигенсвязывающая активность антигенсвязывающей молекулы изменяется до более высокого уровня в условиях нейтральных значений pH, чем условиях кислых значений pH.
В рамках настоящего изобретения выражение “антигенсвязывающая активность антигенсвязывающей молекулы является более низкой в условиях кислых значений pH, чем в условиях нейтральных значений pH”, может быть выражено как “антигенсвязывающая активность антигенсвязывающей молекулы является более высокой в условиях нейтральных значений pH, чем в условиях кислых значений pH”. В рамках настоящего изобретения выражение “антигенсвязывающая активность является более низкой в условиях кислых значений pH, чем в условиях нейтральных значений pH”, также описывается как “антигенсвязывающая способность является более слабой в условиях кислых значений pH, чем в условиях нейтральных значений pH”. Кроме того, выражение “антигенсвязывающая активность в условиях кислых значений pH снижена в отношении антигенсвязывающей активности в условиях нейтральных значений pH” также описывается как “антигенсвязывающая способность в условиях кислых значений pH ослаблена относительно антигенсвязывающей способности в условиях нейтральных значений pH”.
Когда ион металла представляет собой, например, ион кальция, тип аминокислотного остатка, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов, как описано выше, не ограничен, при условии, что аминокислота формирует кальций-связывающий мотив. Кальций-связывающий мотив хорошо известен специалистам в данной области и подробно описан (например, Springer et al., Cell (2000) 102, 275-277; Kawasaki and Kretsinger, Protein Prof. (1995) 2, 305-490; Moncrief et al., J. Mol. Evol. (1990) 30, 522-562; Chauvaux et al., Biochem. J. (1990) 265, 261-265; Bairoch и Cox, FEBS Lett. (1990) 269, 454-456; Davis, New Biol. (1990) 2, 410-419; Schaefer et al., Genomics (1995) 25, 638-643; Economou et al., EMBO J. (1990) 9, 349-354; и Wurzburg et al., Structure. (2006) 14, 6, 1049-1058). В частности, антигенсвязывающая молекула по настоящему изобретению может содержать любой кальций-связывающий мотив, известный в данной области, включая лектины C-типа, такие как ASGPR, CD23, MBR и DC-SIGN. Другие предпочтительные примеры такого кальций-связывающего мотива могут включать кальций-связывающий мотив, содержащийся в домене Vk5, находящемся в вариабельной области легкой цепи антитела, имеющей последовательность эмбрионального типа, такую как Vk5-2, как описано ниже.
В качестве альтернативного примера в качестве аминокислотного остатка, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов кальция предпочтительно можно использовать аминокислоту, обладающую эффектом хелатирования металлов. Предпочтительные примеры аминокислоты, обладающей эффектом хелатирования металлов, включают серин (Ser (S)), треонин (Thr (T)), аспарагин (Asn (N)), глутамин (Gln (Q)), аспарагиновую кислоту (Asp (D)) и глутаминовую кислоту (Glu (E)).
Положение аминокислотного остатка, содержащегося в антигенсвязывающем домене, не ограничено конкретным положением и может представлять собой любое положение в вариабельной области тяжелой и легкой цепей, составляющей антигенсвязывающий домен, при условии, что итоговый аминокислотный остаток изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов кальция. В одном аспекте настоящее изобретение относится к библиотеке, по существу состоящей из антигенсвязывающих молекул, отличающихся друг от друга последовательностью, где аминокислотный остаток, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов кальция, содержится в антигенсвязывающем домене тяжелой цепи. В другом аспекте настоящее изобретение относится к библиотеке, по существу состоящей из антигенсвязывающих молекул, отличающихся друг от друга последовательностью, где аминокислотный остаток содержится в CDR3 тяжелой цепи. В альтернативном аспекте настоящее изобретение относится к библиотеке, по существу состоящей из антигенсвязывающих молекул, отличающихся друг от друга последовательностью, где аминокислотный остаток расположен в любом одном или более из положений 95, 96, 100a, и 101, определяемых посредством нумерации по Кабату, в CDR3 тяжелой цепи.
В одном аспекте настоящее изобретение относится к библиотеке, по существу состоящей из антигенсвязывающих молекул, отличающихся друг от друга последовательностью, где аминокислотный остаток, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов кальция, находится в антигенсвязывающем домене легкой цепи. В другом аспекте настоящее изобретение относится к библиотеке, по существу состоящей из антигенсвязывающих молекул, отличающихся друг от друга последовательностью, где аминокислотный остаток находится в CDR1 легкой цепи. В альтернативном аспекте, настоящее изобретение относится к библиотеке, по существу состоящей из антигенсвязывающих молекул, отличающихся друг от друга последовательностью, где аминокислотный остаток расположен в любом одном или более из положений 30, 31 и 32, определяемых посредством нумерации по Кабату, в CDR1 легкой цепи.
В альтернативном аспекте настоящее изобретение относится к библиотеке, по существу состоящей из антигенсвязывающих молекул, отличающихся друг от друга последовательностью, где аминокислотный остаток находится в CDR2 легкой цепи. В следующем альтернативном аспекте настоящее изобретение относится к библиотеке, по существу состоящей из антигенсвязывающих молекул, отличающихся друг от друга последовательностью, где аминокислотный остаток расположен в положении 50, определяемом посредством нумерации по Кабату, в CDR2 легкой цепи.
В альтернативном аспекте настоящее изобретение относится к библиотеке, по существу состоящей из антигенсвязывающих молекул, отличающихся друг от друга последовательностью, где аминокислотный остаток находится в CDR3 легкой цепи. В следующем альтернативном аспекте настоящее изобретение относится к библиотеке, по существу состоящей из антигенсвязывающих молекул, отличающихся друг от друга последовательностью, где аминокислотный остаток расположен в положении 92, определяемом посредством нумерации по Кабату, в CDR3 легкой цепи.
В отличающемся аспекте настоящее изобретение также относится к библиотеке, по существу состоящей из антигенсвязывающих молекул, отличающихся друг от друга последовательностью, где аминокислотный остаток находится в двух или трех CDR, выбранных из CDR1, CDR2 и CDR3 легкой цепи, описанных выше. Кроме того, настоящее изобретение относится к библиотеке, по существу состоящей из антигенсвязывающих молекул, отличающихся друг от друга последовательностью, где аминокислотный остаток расположен в любом одном или более из положений 30, 31, 32, 50 и 92, определяемых посредством нумерации по Кабату, в легкой цепи.
В особенно предпочтительном варианте осуществления желательно, чтобы каркасная последовательность в вариабельных областях легкой цепи и/или тяжелой цепи каждой антигенсвязывающей молекулы имела каркасную последовательность человека эмбрионального типа. Таким образом, в одном аспекте настоящего изобретения антигенсвязывающая молекула по настоящему изобретению, имеющая каркасные последовательности, все из которых представляют собой полностью человеческие последовательности, вероятно, вызывает небольшой иммунный ответ или не вызывает иммуногенного ответа при введении человеку (например, для лечения заболевания). В этом контексте выражение “содержащий последовательность эмбрионального типа” в соответствии с настоящим изобретением означает, что по меньшей мере часть каркасной последовательности по настоящему изобретению идентична части каркасной последовательности человека эмбрионального типа. Например, последовательность FR2 тяжелой цепи в антигенсвязывающей молекуле по настоящему изобретению может представлять собой последовательность, состоящую из комбинации последовательностей FR2 тяжелой цепи из множества различных каркасных последовательностей человека эмбрионального типа. Такая антигенсвязывающая молекула также включена в антигенсвязывающую молекулу, “содержащую последовательность эмбрионального типа”, по настоящему изобретению.
Предпочтительные примеры каркасной области включают последовательности известных в настоящее время полностью человеческих каркасных областей, приведенные на таком web-сайте, как V-Base (http://vbase.mrc-cpe.cam.ac.uk/). Любую из последовательностей этих каркасных областей можно соответствующим образом использовать в качестве последовательности эмбрионального типа, содержащейся в антигенсвязывающей молекуле по настоящему изобретению. Последовательности эмбрионального типа можно классифицировать на основе их аналогии (Tomlinson et al., J. Mol. Biol. (1992) 227, 776-798; Williams and Winter, Eur. J. Immunol. (1993) 23, 1456-1461; и Cox et al., Nat. Genetics (1994) 7, 162-168). Предпочтительную последовательность эмбрионального типа можно соответствующим образом выбирать из Vκ, подразделяемых на 7 подгрупп, Vλ, классифицируемых на 10 подгрупп, и VH, подразделяемых на 7 подгрупп.
Предпочтительные примеры полностью человеческих последовательностей VH включают, но не ограничиваются ими, последовательности VH подгруппы VH1 (например, VH1-2, VH1-3, VH1-8, VH1-18, VH1-24, VH1-45, VH1-46, VH1-58 и VH1-69), подгруппы VH2 (например, VH2-5, VH2-26 и VH2-70), подгруппы VH3 (VH3-7, VH3-9, VH3-11, VH3-13, VH3-15, VH3-16, VH3-20, VH3-21, VH3-23, VH3-30, VH3-33, VH3-35, VH3-38, VH3-43, VH3-48, VH3-49, VH3-53, VH3-64, VH3-66, VH3-72, VH3-73 и VH3-74), подгруппы VH4 (VH4-4, VH4-28, VH4-31, VH4-34, VH4-39, VH4-59 и VH4-61), подгруппы VH5 (VH5-51), подгруппы VH6 (VH6-1) и подгруппы VH7 (VH7-4 и VH7-81). Эти последовательности также описаны в общедоступной литературе (Matsuda et al., J. Exp. Med. (1998) 188, 1973-1975) и т.д. Специалисты в данной области могут соответствующим образом конструировать антигенсвязывающую молекулу по настоящему изобретению на основе информации о последовательности. Предпочтительно можно использовать любую другую полностью человеческую каркасную область или субобласть каркасной области.
Предпочтительные примеры полностью человеческих последовательностей VK включают, но не ограничиваются ими, A20, A30, L1, L4, L5, L8, L9, L11, L12, L14, L15, L18, L19, L22, L23, L24, O2, O4, O8, O12, O14 и O18, принадлежащие подгруппе Vk1, A1, A2, A3, A5, A7, A17, A18, A19, A23, O1 и O11, принадлежащие подгруппе Vk2, A11, A27, L2, L6, L10, L16, L20 и L25, принадлежащие подгруппе Vk3, B3, принадлежащую подгруппе Vk4, B2, принадлежащую подгруппе Vk5 (также обозначаемая в настоящем описании как Vk5-2), и A10, A14 и A26, принадлежащие подгруппе VK6 (Kawasaki et al., Eur. J. Immunol. (2001) 31, 1017-1028; Schable and Zachau, Biol. Chem. Hoppe Seyler (1993) 374, 1001-1022; и Brensing-Kuppers et al., Gene (1997) 191, 173-181).
Предпочтительные примеры полностью человеческих последовательностей VL включают, но не ограничиваются ими, V1-2, V1-3, V1-4, V1-5, V1-7, V1-9, V1-11, V1-13, V1-16, V1-17, V1-18, V1-19, V1-20 и V1-22, принадлежащие подгруппе VL1, V2-1, V2-6, V2-7, V2-8, V2-11, V2-13, V2-14, V2-15, V2-17 и V2-19, принадлежащие подгруппе VL2, V3-2, V3-3 и V3-4, принадлежащие подгруппе VL3, V4-1, V4-2, V4-3, V4-4 и V4-6, принадлежащие подгруппе VL4, и V5-1, V5-2, V5-4 и V5-6, принадлежащие подгруппе VL5 (Kawasaki et al., Genome Res. (1997) 7, 250-261).
Эти каркасные последовательности отличатся друг от друга одним или более аминокислотными остатками. Эти каркасные последовательности можно использовать вместе “по меньшей мере с одним аминокислотным остатком, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов” по настоящему изобретению. Примеры полностью человеческих каркасных областей, используемых вместе “по меньшей мере с одним аминокислотным остатком, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов” по настоящему изобретению, включают, но не ограничиваясь ими, KOL, NEWM, REI, EU, TUR, TEI, LAY и POM (например, Kabat et al., (1991); и Wu et al., J. Exp. Med. (1970) 132, 211-250).
Хотя настоящее изобретение не связано с какой-либо конкретной теорией, ожидается, что использование последовательности эмбрионального типа предотвратит неблагоприятный иммунный ответ практически у всех индивидуумов, вероятно, частично благодаря следующему: соматические мутации часто встречаются в вариабельных областях иммуноглобулинов в результате стадии созревания аффинности, которая существует в ходе нормального иммунного ответа. Эти мутации встречаются, главным образом, рядом с CDR, имеющими гипервариабельную последовательность, но также влияют на остатки в каркасных областях. Эти мутации в каркасных областях отсутствуют в генах эмбрионального типа и не маловероятно, что они будут иммунногенными у пациентов. С другой стороны, обычные популяции людей подвергаются воздействию большого количества каркасных последовательностей, экспрессируемых генами эмбрионального типа. В результате иммунологической толерантности, предполагается, что эти каркасные области эмбрионального типа являются низкоиммуногенными или неиммуногенными для пациентов. Для максимизации возможности иммунологической толерантности, последовательность эмбрионального типа можно выбирать из функциональных кластеров генов эмбрионального типа, где обычно присутствуют гены, кодирующие вариабельную область.
Антигенсвязывающую молекулу, содержащую “по меньшей мере один аминокислотный остаток, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов” по настоящему изобретению в каркасной последовательности, можно получать путем выбора соответствующим образом способа, известного в данной области, такого как сайт-направленный мутагенез (Kunkel et al., Proc. Natl. Acad. Sci. USA (1985) 82, 488-492) или перекрывающаяся ПЦР.
Например, вариабельные области легкой цепи, выбранные в качестве каркасных последовательностей, заранее содержащие “по меньшей мере один аминокислотный остаток, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов”, можно комбинировать с вариабельными областями тяжелой цепи, полученными в качестве рандомизированной библиотеки последовательностей вариабельной области, получая библиотеку по настоящему изобретению, содержащую множество антигенсвязывающих молекул, отличающихся друг от друга последовательностью. Когда концентрация ионов представляет собой концентрацию ионов кальция, неограничивающие примеры такой библиотеки предпочтительно включают библиотеку, содержащую в комбинации последовательность вариабельной области легкой цепи, представленную в SEQ ID NO: 1 (Vk5-2), и вариабельные области тяжелой цепи, полученные в качестве рандомизированной библиотеки последовательностей вариабельных областей. В качестве предпочтительного примера, последовательность вариабельной области легкой цепи, описанную в SEQ ID NO: 1 (Vk5-2), а также вариант 1 Vk5-2, представленный SEQ ID NO: 2, или вариант 2 Vk5-2, представленный SEQ ID NO: 3, описанные ниже, соответствующим образом используют в качестве последовательности вариабельной области легкой цепи, содержащей домен Vk5, присутствующий в вариабельной области легкой цепи антитела, имеющего последовательность эмбрионального типа, такую как Vk5-2. Домен Vk5-2, содержащий “по меньшей мере один аминокислотный остаток, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов”, находящийся в этих молекулах, можно использовать в качестве домена, содержащего кальций-связывающий мотив по настоящему изобретению. В неограничивающем аспекте настоящего изобретения по меньшей мере одну аминокислоту, которая формирует кальций-связывающий мотив, можно использовать в качестве “по меньшей мере одного аминокислотного остатка, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов” по настоящему изобретению.
Также последовательности вариабельных областей легкой цепи, выбранные в качестве каркасных последовательностей, заранее содержащих “по меньшей мере один аминокислотный остаток, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов” можно конструировать так, чтобы они содержали разнообразные аминокислоты в качестве остатков, отличных от указанного аминокислотного остатка. В рамках настоящего изобретения такие остатки называют нестрогими остатками. Количество и положения нестрогих остатков не ограничивается каким-либо конкретным аспектом при условии, что антигенсвязывающая активность антигенсвязывающей молекулы по настоящему изобретению изменяется, в зависимости от условий концентрации ионов. В частности, каждая из последовательностей CDR и/или FR тяжелой цепи и/или легкой цепи может содержать один или более нестрогих остатков. Когда концентрация ионов представляет собой, например, концентрацию ионов кальция, неограничивающие примеры нестрогих остатков, внесенных в последовательность вариабельной области легкой цепи, представленной в SEQ ID NO: 1 (Vk5-2), включают аминокислотные остатки, описанные в таблицах 13, 14, 17 и 18.
Альтернативно вариабельные области легкой цепи, в которые внесен “по меньшей мере один аминокислотный остаток, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов”, можно комбинировать с вариабельными областями тяжелой цепи в качестве рандомизированной библиотеки вариабельных областей, получая библиотеку по настоящему изобретению, содержащую множество антигенсвязывающих молекул, отличающихся друг от друга последовательностью. Когда концентрация ионов кальция представляет собой концентрацию ионов кальция, неограничивающие примеры такой библиотеки предпочтительно включают библиотеку, содержащую в комбинации последовательности вариабельной области легкой цепи, происходящие из последовательности эмбрионального типа SEQ ID NO: 6 (Vk1), SEQ ID NO: 7 (Vk2), SEQ ID NO: 8 (Vk3), SEQ ID NO: 9 (Vk4), или т.п. путем замены конкретного остатка “по меньшей мере одним аминокислотным остатком, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов кальция”, и вариабельные области тяжелой цепи, полученные в качестве рандомизированной библиотеки последовательностей вариабельной области. Неограничивающие примеры указанного аминокислотного остатка включают аминокислотные остатки, содержащиеся в CDR1 легкой цепи. Другие неограничивающие примеры аминокислотного остатка включают аминокислотные остатки, содержащиеся в CDR2 легкой цепи. Следующие неограничивающие примеры указанного аминокислотного остатка включают аминокислотные остатки, содержащиеся в CDR3 легкой цепи.
Неограничивающие примеры аминокислотного остатка, содержащегося в CDR1 легкой цепи, как описано выше, включают аминокислотные остатки 30, 31 и/или 32, определяемые посредством нумерации по Кабату, в вариабельной области легкой цепи CDR1. Неограничивающие примеры аминокислотного остатка, содержащегося в CDR2 легкой цепи, включают аминокислотный остаток 50, определяемый посредством нумерации по Кабату, в вариабельной области легкой цепи CDR2. Неограничивающие примеры аминокислотного остатка, содержащегося в CDR3 легкой цепи, включают аминокислотный остаток 92, определяемый посредством нумерации по Кабату, в вариабельной области легкой цепи CDR3. Эти аминокислотные остатки могут содержаться отдельно или в комбинации из двух или более из этих аминокислот при условии, что эти аминокислотные остатки образуют кальций-связывающие мотивы и/или антигенсвязывающая активность антигенсвязывающей молекулы изменяется в зависимости от условий концентрации ионов кальция. Например, известны тропонин C, кальмодулин, парвальбумин и легкая цепь миозина, которые имеют несколько участков связывания ионов кальция и, вероятно, происходят из общего источника с точки зрения молекулярной эволюции. CDR1, CDR2 и/или CDR3 легкой цепи можно конструировать так, чтобы они содержали любой из их связывающих мотивов. Например, для этих целей можно соответствующим образом использовать домен кадгерина, EF hand, содержащийся в кальмодулине, доме C2, содержащийся в протеинкиназе C, домен Gla, содержащийся в факторе свертывания крови IX, лектин C-типа, содержащийся в рецепторе асиалогликопротеинов или манноза-связывающем рецепторе, домен A, содержащийся в рецепторе LDL, аннексин, домен тромбоспондина 3 типа и EGF-подобный домен.
В случае комбинирования вариабельных областей легкой цепи, в которые внесен “по меньшей мере один аминокислотный остаток который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов”, с вариабельными областями тяжелой цепи, полученными в качестве рандомизированной библиотеки последовательностей вариабельных областей, последовательности вариабельных областей легкой цепи можно конструировать так, чтобы они содержали нестрогие остатки, как и в описанном выше случае. Количество и положения нестрогих остатков не ограничиваются каким-либо конкретным аспектом при условии, что антигенсвязывающая активность антигенсвязывающей молекулы по настоящему изобретению изменяется в зависимости от условий концентрации ионов. В частности, каждая из последовательностей CDR и/или FR тяжелой цепи и/или легкой цепи может содержать один или более нестрогих остатков. Когда концентрация представляет собой, например, концентрацию ионов кальция, неограничивающие примеры нестрогих остатков, внесенных в последовательности вариабельной области легкой цепи, включают аминокислотные остатки, описанные в таблицах 13, 14, 17 и 18.
Предпочтительные примеры вариабельных областей тяжелой цепи для комбинирования с ними включают рандомизированную библиотеку вариабельных областей. Рандомизированную библиотеку вариабельных областей получают путем соответствующего комбинирования способов, известных в данной области. В неограничивающем аспекте настоящего изобретения в качестве рандомизированной библиотеки вариабельных областей предпочтительно можно использовать иммунную библиотеку, сконструированную на основе генов антител, происходящих из лимфоцитов животных, иммунизированных конкретными антигенами, пациентов с инфекционным заболеванием, людей, имеющих увеличенный титр антител в крови в результате вакцинации, пациентов со злокачественной опухолью или аутоиммунными заболеваниями.
В неограничивающем аспекте настоящего изобретения также в качестве рандомизированной библиотеки вариабельных областей предпочтительно можно использовать синтетическую библиотеку, получаемую путем замены последовательностей CDR V-генов геномной ДНК или реконструированных функциональных V-генов синтетическим набором олигонуклеотидов, содержащим последовательности, кодирующие набор кодонов, имеющий соответствующую длину. В этом случае, ими можно заменять только последовательности CDR3, поскольку разнообразие наблюдают в последовательности гена CDR3 тяжелой цепи. Разнообразие аминокислот, обеспечивающее вариабельные области антигенсвязывающих молекул, основано на разнообразии, сообщенном аминокислотным остаткам в положениях, экспонированных на поверхности антигенсвязывающих молекул. Положения, экспонированные на поверхности, относятся к положениям, которые считаются экспонируемыми на поверхности и/или доступными для антигенов, исходя из структур, набора структур и/или смоделированных структур антигенсвязывающих молекул, и обычно они расположены в их CDR. Предпочтительно, положения, экспонированные на поверхности, определяют с использованием компьютерной программы, такой как программа Insight II (Accelrys Inc.), и координат из трехмерных моделей антигенсвязывающих молекул. Положения, экспонированные на поверхности, можно определять с использованием алгоритма, известного в данной области (например, Lee and Richards, J. Mol. Biol. (1971) 55, 379-400; и Connolly, J. Appl. Cryst. (1983) 16, 548-558). Положения, экспонированные на поверхности, можно определять с использованием программного обеспечения, пригодного для моделирования белков, и информации о трехмерной структуре, полученной для антител. Предпочтительные примеры программного обеспечения, которое можно использовать для такой цели, включают программное обеспечение SYBYL biopolymer module (Tripos Associates Inc.). Как правило и предпочтительно, ʺразмерʺ зондов, используемых для вычисления, устанавливают приблизительно на 1,4 ангстрема или ниже в значениях радиуса, когда алгоритм требует, чтобы пользователь ввел параметры размера. Способ определения экспонированных на поверхности областей и площадей с использованием программного обеспечения для персональных компьютеров, описан в Pacios, Comput. Chem. (1994) 18 (4), 377-386, и J. Mol. Model. (1995) 1, 46-53.
В следующем неограничивающем аспекте настоящего изобретения в качестве рандомизированной библиотеки вариабельных областей используют наивную библиотеку, состоящую из наивных последовательностей, которые представляют собой наборы последовательностей антител без смещений, сконструированные из генов антител, происходящих из лимфоцитов здоровых людей (Gejima et al., Human Antibodies (2002) 11, 121-129; и Cardoso et al., Scand. J. Immunol. (2000) 51, 337-344). Аминокислотная последовательность, содержащая наивную последовательность, как описано в рамках настоящего изобретения, относится к аминокислотной последовательности, полученной из такой наивной библиотеки.
В одном аспекте настоящего изобретения вариабельные области тяжелой цепи, выбранные в качестве каркасных последовательностей, заранее содержащих “по меньшей мере один аминокислотный остаток, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов”, можно комбинировать с вариабельными областями легкой цепи, полученными в качестве рандомизированной библиотеки последовательностей вариабельных областей, чтобы получить библиотеку по настоящему изобретению, содержащую множество антигенсвязывающих молекул, отличающихся друг от друга последовательностью. Когда концентрация ионов представляет собой концентрацию ионов кальция, неограничивающие примеры такой библиотеки предпочтительно включают библиотеку, содержащую в комбинации последовательность вариабельной области тяжелой цепи, описанную в SEQ ID NO: 10 (6RL#9H-IgG1) или SEQ ID NO: 11 (6KC4-1#85H-IgG1), и вариабельные области легкой цепи, полученные в качестве рандомизированной библиотеки последовательностей вариабельных областей. Альтернативно библиотеку можно получать с использованием соответствующим образом выбранных вариабельных областей легкой цепи, имеющих последовательность эмбрионального типа, вместо вариабельных областей легкой цепи, полученных в качестве рандомизированной библиотеки последовательностей вариабельных областей. Ее предпочтительные примеры включают библиотеку, содержащую в комбинации последовательность вариабельной области тяжелой цепи, представленную в SEQ ID NO: 10 (6RL#9H-IgG1) или SEQ ID NO: 11 (6KC4-1#85H-IgG1), и вариабельные области легкой цепи, имеющие последовательность эмбрионального типа.
Также, последовательности вариабельных областей тяжелой цепи, выбранные в качестве каркасных последовательностей, заранее содержащих “по меньшей мере один аминокислотный остаток, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов”, можно конструировать так, чтобы они содержали нестрогие остатки. Количество и положения нестрогих остатков не ограничиваются каким-либо конкретным аспектом при условии, что антигенсвязывающая активность антигенсвязывающей молекулы по настоящему изобретению изменяется в зависимости от условий концентрации ионов кальция. В частности, каждая из последовательностей CDR и/или FR тяжелой цепи и/или легкой цепи может содержать один или более нестрогих остатков. Когда концентрация ионов представляет собой, например, концентрацию ионов кальция, неограничивающие примеры нестрогих остатков, внесенных в последовательность вариабельной области тяжелой цепи, описанную в SEQ ID NO: 10 (6RL#9H-IgG1), включают все аминокислотные остатки CDR1 и CDR2 тяжелой цепи, а также аминокислотные остатки CDR3 тяжелой цепи, за исключением положений 95, 96 и/или 100a. Альтернативно неограничивающие примеры нестрогих остатков, внесенных в последовательность вариабельной области тяжелой цепи, представленную в SEQ ID NO: 11 (6KC4-1#85H-IgG1), включают все аминокислотные остатки CDR1 и CDR2 тяжелой цепи, а также аминокислотные остатки CDR3 тяжелой цепи, за исключением положений 95 и/или 101.
Альтернативно вариабельные области тяжелой цепи, в которые внесен “по меньшей мере один аминокислотный остаток, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов”, можно комбинировать с вариабельными областями легкой цепи, полученными в качестве рандомизированной библиотеки последовательностей вариабельных областей, или вариабельными областями легкой цепи, имеющими последовательность эмбрионального типа, чтобы получить библиотеку по настоящему изобретению, содержащую множество антигенсвязывающих молекул, отличающихся друг от друга последовательностью. Когда концентрация ионов представляет собой концентрацию ионов кальция, неограничивающие примеры такой библиотеки предпочтительно включают библиотеку, содержащую в комбинации последовательности вариабельной области тяжелой цепи, образованные из вариабельных областей тяжелой цепи путем замены конкретного остатка “по меньшей мере одним аминокислотным остатком, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов кальция”, и вариабельные области легкой цепи, полученные в качестве рандомизированной библиотеки последовательностей вариабельных областей, или вариабельные области легкой цепи, имеющие последовательность эмбрионального типа. Неограничивающие примеры указанного аминокислотного остатка включают аминокислотные остатки, содержащиеся в CDR1 тяжелой цепи. Другие неограничивающие примеры указанного аминокислотного остатка включают аминокислотные остатки, содержащиеся в CDR2 тяжелой цепи. Следующие неограничивающие примеры указанного аминокислотного остатка включают аминокислотные остатки, содержащиеся в CDR3 тяжелой цепи. Неограничивающие примеры аминокислотного остатка, содержащегося в CDR3 тяжелой цепи, включают аминокислоты в положениях 95, 96, 100a и/или 101, определяемых посредством нумерации по Кабату, в вариабельной области тяжелой цепи CDR3. Эти аминокислотные остатки могут содержаться отдельно или в комбинации из двух или более из этих аминокислот при условии, что эти аминокислотные остатки образуют кальций-связывающие мотивы и/или антигенсвязывающая активность антигенсвязывающей молекулы изменяется в зависимости от условий концентрации ионов кальция.
В случае комбинирования вариабельных областей тяжелой цепи, в которые внесен “по меньшей мере один аминокислотный остаток, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов”, с вариабельными областями легкой цепи, полученными в качестве рандомизированной библиотеки последовательностей вариабельных областей, или вариабельными областями легкой цепи, имеющими последовательность эмбрионального типа, последовательности вариабельных областей тяжелой цепи можно конструировать так, чтобы они содержали нестрогие остатки, как и в описанном выше случае. Количество и положения нестрогих остатков не ограничиваются каким-либо конкретным аспектом при условии, что антигенсвязывающая активность антигенсвязывающей молекулы по настоящему изобретению изменяется в зависимости от условий концентрации ионов. В частности, каждая из последовательностей CDR и/или FR тяжелой цепи может содержать один или более нестрогих остатков. Также в качестве аминокислотных последовательностей CDR1, CDR2 и/или CDR3 вариабельной области тяжелой цепи можно использовать рандомизированную библиотеку вариабельных областей предпочтительно, за исключением “аминокислотного остатка, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов”. В случае использования последовательностей эмбрионального типа в качестве вариабельных областей легкой цепи, их неограничивающие примеры могут включать последовательности эмбрионального типа SEQ ID NO: 6 (Vk1), SEQ ID NO: 7 (Vk2), SEQ ID NO: 8 (Vk3) и SEQ ID NO: 9 (Vk4).
В качестве аминокислотного остатка, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов кальция предпочтительно можно использовать любой аминокислотный остаток при условии, что аминокислотный остаток формирует кальций-связывающий мотив. Конкретные примеры такого аминокислотного остатка включают аминокислоты, имеющие электронодонорные свойства. Предпочтительные примеры аминокислот, имеющих электронодонорные свойства, включают серин, треонин, аспарагин, глутамин, аспарагиновую кислоту и глутаминовую кислоту.
В одном аспекте настоящего изобретения вариабельные области легкой цепи, в которые внесен “по меньшей мере один аминокислотный остаток, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов водорода”, также можно комбинировать с вариабельными областями тяжелой цепи, полученными в качестве рандомизированной библиотеки последовательностей вариабельных областей, чтобы получить библиотеку по настоящему изобретению, содержащую множество антигенсвязывающих молекул, отличающихся друг от друга последовательностью.
Неограничивающие примеры указанного аминокислотного остатка включают аминокислотные остатки, содержащиеся в CDR1 легкой цепи. Другие неограничивающие примеры указанного аминокислотного остатка включают аминокислотные остатки, содержащиеся в CDR2 легкой цепи. Следующие неограничивающие примеры указанного аминокислотного остатка включают аминокислотные остатки, содержащиеся в CDR3 легкой цепи.
Неограничивающие примеры аминокислотного остатка, содержащегося в CDR1 легкой цепи, как описано выше, включают аминокислотные остатки 24, 27, 28, 30, 31, 32 и/или 34, определяемые посредством нумерации по Кабату, в вариабельной области легкой цепи CDR1. Неограничивающие примеры аминокислотного остатка, содержащегося в CDR2 легкой цепи, включают аминокислотные остатки 50, 51, 52, 53, 54, 55 и/или 56, определяемые посредством нумерации по Кабату, в вариабельной области легкой цепи CDR2. Неограничивающие примеры аминокислотного остатка, содержащегося в CDR3 легкой цепи, включают аминокислотные остатки 89, 90, 91, 92, 93, 94 и/или 95a, определяемые посредством нумерации по Кабату, в вариабельной области легкой цепи CDR3. Эти аминокислотные остатки могут содержаться отдельно или в комбинации из двух или более из этих аминокислот при условии, что антигенсвязывающая активность антигенсвязывающей молекулы, содержащей аминокислотный остаток(остатки) изменяется в зависимости от условий концентрации ионов водорода.
В случае комбинирования вариабельных областей легкой цепи, в которые внесен “по меньшей мере один аминокислотный остаток, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов водорода”, с вариабельными областями тяжелой цепи, полученными в качестве рандомизированной библиотеки последовательностей вариабельных областей, последовательности вариабельных областей легкой цепи можно конструировать так, чтобы они содержали нестрогие остатки, как и в описанном выше случае. Количество и положения нестрогих остатков не ограничиваются каким-либо конкретным аспектом при условии, что антигенсвязывающая активность антигенсвязывающей молекулы по настоящему изобретению изменяется в зависимости от условий концентрации ионов. В частности, каждая из последовательностей CDR и/или FR тяжелой цепи и/или легкой цепи может содержать один или более нестрогих остатков. Неограничивающие примеры нестрогих остатков, внесенных в последовательности вариабельной области легкой цепи, включают аминокислотные остатки, описанные в таблицах 4 и 5. В качестве неограничивающего примера, в качестве аминокислотных последовательностей вариабельных областей легкой цепи предпочтительно можно использовать последовательность эмбрионального типа Vk1 (SEQ ID NO: 6), Vk2 (SEQ ID NO: 7), Vk3 (SEQ ID NO: 8), Vk4 (SEQ ID NO: 9) и т.п., за исключением аминокислотного остатка, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов водорода, или нестрогих остатков.
Предпочтительные примеры вариабельных областей тяжелой цепи, подлежащие комбинированию с ними, включают рандомизированную библиотеку вариабельных областей. Рандомизированную библиотеку вариабельных областей получают путем соответствующего комбинирования способов, известных в данной области. В неограничивающем аспекте настоящего изобретения в качестве рандомизированной библиотеки вариабельных областей предпочтительно можно использовать иммунную библиотеку, сконструированную на основе генов антител, происходящих из лимфоцитов животных, иммунизированных конкретными антигенами, пациентов с инфекционным заболеванием, людей, имеющих увеличенный титр антител в крови в результате вакцинации, пациентов со злокачественной опухолью или аутоиммунными заболеваниями.
В неограничивающем аспекте настоящего изобретения также в качестве рандомизированной библиотеки вариабельных областей предпочтительно можно использовать синтетическую библиотеку, получаемую путем замены последовательностей CDR V-генов геномной ДНК или реконструированных функциональных V-генов синтетическим набором олигонуклеотидов, содержащим последовательности, кодирующие набор кодонов, имеющий соответствующую длину, как и в описанном выше случае.
В следующем неограничивающем аспекте настоящего изобретения в качестве рандомизированной библиотеки вариабельных областей используют наивную библиотеку, состоящую из наивных последовательностей, которые представляют собой наборы последовательностей антител без смещений, сконструированные из генов антител, происходящих из лимфоцитов здоровых людей (Gejima et al., Human Antibodies (2002) 11, 121-129; и Cardoso et al., Scand. J. Immunol. (2000) 51, 337-344).
В альтернативном аспекте настоящего изобретения вариабельные области тяжелой цепи, в которые внесен “по меньшей мере один аминокислотный остаток, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов водорода”, можно комбинировать с вариабельными областями легкой цепи, полученными в качестве рандомизированной библиотеки последовательностей вариабельных областей, или вариабельными областями легкой цепи, имеющими последовательность эмбрионального типа, чтобы получить библиотеку по настоящему изобретению, содержащую множество антигенсвязывающих молекул, отличающихся друг от друга последовательностью. Неограничивающие примеры такой библиотеки предпочтительно включают библиотеку, содержащую в комбинации последовательности вариабельной области тяжелой цепи, образованные из вариабельных областей тяжелой цепи путем замены конкретного остатка “по меньшей мере одним аминокислотным остатком, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов водорода”, и вариабельные области легкой цепи, полученные в качестве рандомизированной библиотеки последовательностей вариабельных областей, или вариабельные области легкой цепи, имеющие последовательность эмбрионального типа. Неограничивающие примеры указанного аминокислотного остатка включают аминокислотные остатки, содержащиеся в CDR1 тяжелой цепи. Другие неограничивающие примеры указанного аминокислотного остатка включают аминокислотные остатки, содержащиеся в CDR2 тяжелой цепи. Следующие неограничивающие примеры аминокислотного остатка включают аминокислотные остатки, содержащиеся в CDR3 тяжелой цепи.
Неограничивающие примеры аминокислотного остатка, содержащегося в CDR1 тяжелой цепи, включают аминокислотные остатки 27, 31, 32, 33 и/или 35, определяемые посредством нумерации по Кабату, в вариабельной области тяжелой цепи CDR1. Неограничивающие примеры аминокислотного остатка, содержащегося в CDR2 тяжелой цепи, включают аминокислотные остатки 50, 52, 53, 55, 57, 58, 59, 61 и/или 62, определяемые посредством нумерации по Кабату, в вариабельной области тяжелой цепи CDR2. Неограничивающие примеры аминокислотного остатка, содержащегося в CDR3 тяжелой цепи, включают аминокислотные остатки 95, 96, 97, 98, 99, 100a, 100b, 100d, 100f, 100h, 102 и/или 107, определяемые посредством нумерации по Кабату, в вариабельной области тяжелой цепи CDR3. Эти аминокислотные остатки могут содержаться отдельно или в комбинации из двух два или более из этих аминокислот при условии, что антигенсвязывающая активность антигенсвязывающей молекулы, содержащей аминокислотный остаток(остатки), изменяется в зависимости от условий концентрации ионов водорода.
В случае комбинирования вариабельных областей тяжелой цепи, в которые внесен “по меньшей мере один аминокислотный остаток, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов водорода”, с вариабельными областями легкой цепи, полученными в качестве рандомизированной библиотеки последовательностей вариабельных областей, или вариабельными областями легкой цепи, имеющими последовательность эмбрионального типа, последовательности вариабельных областей тяжелой цепи можно конструировать так, чтобы они содержали нестрогие остатки, как и в описанном выше случае. Количество и положения нестрогих остатков не ограничиваются каким-либо конкретным аспектом при условии, что антигенсвязывающая активность антигенсвязывающей молекулы по настоящему изобретению изменяется в зависимости от условий концентрации ионов водорода. В частности, каждая из последовательностей CDR и/или FR тяжелой цепи может содержать один или более нестрогих остатков. Также рандомизированную библиотеку вариабельных областей предпочтительно можно использовать в качестве аминокислотных последовательностей CDR1, CDR2 и/или CDR3 вариабельной области тяжелой цепи, за исключением “аминокислотного остатка, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов водорода”. В случае использования последовательностей эмбрионального типа в качестве вариабельных областей легкой цепи, их неограничивающие примеры могут включать последовательности эмбрионального типа SEQ ID NO: 6 (Vk1), SEQ ID NO: 7 (Vk2), SEQ ID NO: 8 (Vk3) и SEQ ID NO: 9 (Vk4).
В качестве аминокислотного остатка, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов водорода, предпочтительно можно использовать любой аминокислотный остаток. Конкретные примеры такого аминокислотного остатка включают аминокислоты, имеющие pKa боковой цепи от 4,0 до 8,0. Предпочтительные примеры аминокислот, имеющих такие электронодонорные свойства, включают природные аминокислоты, такие как гистидин и глутаминовая кислота, а также неприродные аминокислоты, такие как аналоги гистидина (US20090035836), m-NO2-Tyr (pKa: 7,45), 3,5-Br2-Tyr (pKa: 7,21), и 3,5-I2-Tyr (pKa: 7,38) (Bioorg. Med. Chem. (2003) 11 (17), 3761-2768). Особенно предпочтительные примеры аминокислотного остатка включают аминокислоты, имеющие pKa боковой цепи от 5,5 до 7,0. Предпочтительные примеры аминокислот, имеющих такие электронодонорные свойства, включают гистидин.
Аминокислоты в антигенсвязывающих доменах можно модифицировать с помощью соответствующим образом выбранного способа, известного в данной области, такого как сайт-направленный мутагенез (Kunkel et al., Proc. Natl. Acad. Sci. USA (1985) 82, 488-492) или перекрывающаяся ПЦР. Также аминокислоты могут быть заменены неприродными аминокислотами с использованием множества способов модификации, известных в данной области (Annu. Rev. Biophys. Biomol. Struct. (2006) 35, 225-249; и Proc. Natl. Acad. Sci. U.S.A. (2003) 100 (11), 6353-6357). Например, также предпочтительно используют содержащую тРНК бесклеточную систему трансляции (Clover Direct (Protein Express, an R & D oriented company)), содержащую неприродную аминокислоту, связанную с тРНК янтарь-супрессора, комплементарной кодону UAG (янтарь-кодон), который представляет собой стоп-кодон.
Предпочтительные примеры вариабельных областей тяжелой цепи для комбинирования с ними включают рандомизированную библиотеку вариабельных областей. Рандомизированную библиотеку вариабельных областей получают путем соответствующего комбинирования способов, известных в данной области. В неограничивающем аспекте настоящего изобретения в качестве рандомизированной библиотеки вариабельных областей предпочтительно можно использовать иммунную библиотеку, сконструированную на основе генов антител, происходящих из лимфоцитов животных, иммунизированных конкретными антигенами, пациентов с инфекционным заболеванием, людей, имеющих увеличенный титр антител в крови в результате вакцинации, пациентов со злокачественной опухолью или аутоиммунными заболеваниями.
В неограничивающем аспекте настоящего изобретения также в качестве рандомизированной библиотеки вариабельных областей предпочтительно можно использовать синтетическую библиотеку, получаемую путем замены последовательностей CDR V-генов геномной ДНК или реконструированных функциональных V-генов синтетическим набором олигонуклеотидов, содержащим последовательности, кодирующие набор кодонов, имеющий соответствующую длину. В этом случае, ими можно заменять только последовательности CDR3, поскольку разнообразие наблюдают в последовательности гена CDR3 тяжелой цепи. Разнообразие аминокислот, обеспечивающее вариабельные области антигенсвязывающих молекул, основано на разнообразии, сообщенном аминокислотным остаткам в положениях, экспонированных на поверхности антигенсвязывающих молекул. Положения, экспонированные на поверхности, относятся к положениям, которые считаются экспонируемыми на поверхности и/или доступными для антигенов, исходя из структур, набора структур и/или смоделированных структур антигенсвязывающих молекул, и обычно они расположены в их CDR. Предпочтительно, положения, экспонированные на поверхности, определяют с использованием компьютерной программы, такой как программа Insight II (Accelrys Inc.) и координат из трехмерных моделей антигенсвязывающих молекул. Положения, экспонированные на поверхности, можно определять с использованием алгоритма, известного в данной области (например, Lee and Richards, J. Mol. Biol. (1971) 55, 379-400; и Connolly, J. Appl. Cryst. (1983) 16, 548-558). Положения, экспонированные на поверхности, можно определять с использованием программного обеспечения, пригодного для моделирования белков, и информации о трехмерной структуре, полученной для антител. Предпочтительные примеры программного обеспечения, которое можно использовать для такой цели, включают программное обеспечение SYBYL biopolymer module (Tripos Associates Inc.). Как правило и предпочтительно, “размер” зондов, используемых для вычисления, устанавливают приблизительно на 1,4 ангстрема или ниже в значениях радиуса, когда алгоритм требует, чтобы пользователь ввел параметры размера. Способ определения экспонированных на поверхности областей и площадей с использованием программного обеспечения для персональных компьютеров, описан в Pacios, Comput. Chem. (1994) 18 (4), 377-386, и J. Mol. Model. (1995) 1, 46-53.
В следующем неограничивающем аспекте настоящего изобретения в качестве рандомизированной библиотеки вариабельных областей используют наивную библиотеку, состоящую из наивных последовательностей, которые представляют собой наборы последовательностей антител без смещений, сконструированные из генов антител, происходящих из лимфоцитов здоровых людей (Gejima et al., Human Antibodies (2002) 11, 121-129; и Cardoso et al., Scand. J. Immunol. (2000) 51, 337-344).
В качестве аминокислот, отличных от аминокислотного остатка, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов, можно использовать любую аминокислоту, при условии что антигенсвязывающая молекула по настоящему изобретению связывается с антигенами. В качестве предпочтительного примера, для этого можно использовать технологию библиотек фагового дисплея антител, известную в данной области (например, J. D. Marks et al., J. Mol. Biol. (1991) 222, 581-597). В частности, с помощью фаговой библиотеки выбирают аминокислотные последовательности, за исключением аминокислотного остатка, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов.
Термин “отличающиеся друг от друга последовательностью” во множестве антигенсвязывающих молекул, отличающихся друг от друга последовательностью, как описано в рамках настоящего изобретения, означает, что индивидуальные антигенсвязывающие молекулы в библиотеке имеют различные последовательности. В частности, количество различных последовательностей в библиотеке отражает количество независимых клонов, последовательности которых отличаются в библиотеке, и также называется “размером библиотеки”. Размер библиотеки для обычной библиотеки фагового дисплея составляет от 106 до 1012 и может быть расширен до 1014 с использованием способа, известного в данной области, такой как способ рибосомного дисплея. Однако истинное число фаговых частиц, используемых при селекции с использованием пэннинга, обычно в 10-10000 раз превышает размер библиотеки. Этот множитель избыточности, также называемый “числом эквивалентов библиотеки”, отражает тот факт, что от 10 до 10000 индивидуальных клонов могут иметь одинаковую аминокислотную последовательность. Таким образом, термин “отличающиеся друг от друга последовательностью”, описанный в рамках настоящего изобретения, означает, что индивидуальные антигенсвязывающие молекулы в библиотеке за исключением количества эквивалентов в библиотеке, имеют отличающиеся последовательности, и, более конкретно, означает, что библиотека имеет 106-1014, предпочтительно 107-1012, более предпочтительно 108-1011, особенно предпочтительно 108-1010 антигенсвязывающих молекул, отличающихся друг от друга последовательностью.
Термин “множество” в библиотеке, по существу состоящей из множества антигенсвязывающих молекул, как описано в рамках настоящего изобретения, обычно относится к набору из двух или более типов веществ, например, таких как антигенсвязывающая молекула, слитый полипептид, полинуклеотидная молекула, вектор или вирус по настоящему изобретению. Например, если два или более вещества отличаются друг от друга конкретным признаком, вещества существуют в качестве двух или более типов. Их примеры могут включать варианты аминокислот, наблюдаемые в конкретном положении аминокислоты в аминокислотной последовательности. Например, две или более антигенсвязывающих молекулы по настоящему изобретению, имеющие по существу одинаковые, предпочтительно идентичные, последовательности, за исключением нестрогих остатков или за исключением конкретных вариантов аминокислот в экспонированных на поверхности положениях аминокислот с высокой степенью разнообразия, считаются множеством антигенсвязывающих молекул по настоящему изобретению. В другом примере, две или более полинуклеотидных молекулы по настоящему изобретению, имеющих по существу одинаковые, предпочтительно идентичные последовательности, за исключением оснований, кодирующих нестрогие остатки, или за исключением оснований, кодирующих конкретные варианты аминокислот в экспонированных на поверхности положениях аминокислот с высокой степенью разнообразия, считаются множеством полинуклеотидных молекул по настоящему изобретению.
Термин “по существу состоящий из” в библиотеке, по существу состоящей из множества антигенсвязывающих молекул, как описано в рамках настоящего изобретения, отражает количество антигенсвязывающих молекул, антигенсвязывающая активность которых различается, в зависимости от условий концентрации ионов, среди независимых клонов, последовательности которых отличаются, в библиотеке. В частности, предпочтительно библиотека имеет по меньшей мере 104 антигенсвязывающих молекул, которые обладают такой активностью связывания. Более предпочтительно, настоящее изобретение относится к библиотеке, имеющей по меньшей мере 105 антигенсвязывающих молекул, которые обладают такой активностью связывания. Еще более предпочтительно, настоящее изобретение относится к библиотеке, имеющей по меньшей мере 106 антигенсвязывающих молекул, которые обладают такой активностью связывания. Особенно предпочтительно, настоящее изобретение относится к библиотеке, имеющей по меньшей мере 107 антигенсвязывающих молекул, которые обладают такой активностью связывания. Также предпочтительно, настоящее изобретение относится к библиотеке, имеющей по меньшей мере 108 антигенсвязывающих молекул, которые обладают такой активностью связывания. Иными словами, этот термин предпочтительно может быть указан с помощью соотношения антигенсвязывающих молекул, антигенсвязывающая активность которых отличается в зависимости от условий концентрации ионов, и количества независимых клонов, последовательность которых различается, в библиотеке. В частности, настоящее изобретение относится к библиотеке, содержащей антигенсвязывающие молекулы, которые обладают такой активностью связывания в соотношении от 0,1% до 80%, предпочтительно от 0,5% до 60%, более предпочтительно от 1% до 40%, еще более предпочтительно от 2% до 20%, особенно предпочтительно от 4% до 10% относительно количества независимых клонов, последовательность которых различается, в библиотеке. Слитые полипептиды, полинуклеотидные молекулы или векторы также могут быть указаны с помощью количества молекул или соотношения по отношению ко всем молекулам, как и в описанном выше случае. Также вирусы могут быть указаны с помощью количества индивидуальных вирусов или соотношения по отношению ко всем индивидуальным вирусам, как и в описанном выше случае.
Слитый полипептид, содержащий антигенсвязывающую молекулу
В одном варианте осуществления настоящего изобретения можно получать слитую молекулу антигенсвязывающей молекулы по настоящему изобретению и гетерлогичный полипептид. В одном варианте осуществления антигенсвязывающую молекулу по настоящему изобретению можно подвергать слиянию по меньшей мере с частью белка вирусной оболочки, выбранного из группы, состоящей, например, из белков вирусной оболочки pIII, pVIII, pVII, pIX, Soc, Hoc, gpD и pVI и их вариантов, с образованием слитого полипептида.
В одном варианте осуществления антигенсвязывающая молекула по настоящему изобретению может представлять собой ScFv, Fab-фрагмент, F(ab)2 или F(ab')2. В другом варианте осуществления настоящее изобретение относится к библиотеке, по существу состоящей из множества слитых молекул, отличающихся друг от друга последовательностью, причем каждая из слитых молекул содержит любую из этих антигенсвязывающих молекул и гетерологичный полипептид. В частности, настоящее изобретение относится к библиотеке, по существу состоящей из множества слитых молекул, отличающихся друг от друга последовательностью, причем каждый их слитых белков содержит любую из этих антигенсвязывающих молекул и по меньшей мере часть белка вирусной оболочки, выбранного из группы, состоящей, например, из белков вирусной оболочки pIII, pVIII, pVII, pIX, Soc, Hoc, gpD и pVI и их вариантов. Антигенсвязывающая молекула по настоящему изобретению, кроме того, может содержать домен димеризации. В одном варианте осуществления домен димеризации может быть расположен между вариабельной областью тяжелой или легкой цепи антитела и по меньшей мере частью белка вирусной оболочки. Этот домен димеризации может содержать по меньшей мере одну последовательность димеризации и/или последовательность, содержащую один или более остатков цистеина. Этот домен димеризации предпочтительно может быть связан с C-концом вариабельной области или константной области тяжелой цепи. Домен димеризации может иметь различные структуры в зависимости от того, получают ли вариабельную область антитела в качестве компонента слитого белка с компонентом в виде белка вирусной оболочки (янтарный стоп-кодон после домена димеризации отсутствует), или в зависимости от того, получают ли вариабельную область антитела в основном без наличия компонента в виде белка вирусной оболочки (например, янтарный стоп-кодон после домена димеризация домен присутствует). Когда вариабельную область антитела получают в основном в качестве слитого белка с компонентом в виде белка вирусной оболочки, двухвалентный дисплей осуществляют с помощью одной или более дисульфидных связей и/или одной последовательности димеризации. Предпочтительно, антигенсвязывающая молекула по настоящему изобретению имеет домен димеризации, содержащий как остаток цистеина, так и последовательность димеризации, когда вариабельная область антитела получена в основном без слияния с компонентом в виде белка вирусной оболочки (например, янтарный стоп-кодон присутствует). В одном варианте осуществления тяжелые цепи F(ab)2 димеризуются в домене димеризации, не содержащем шарнирную область. Этот домен димеризации может содержать, например, последовательность лейциновой молнии, известную в данной области, такую как последовательность GCN4: GRMKQLEDKVEELLSKNYHLENEVARLKKLVGERG (SEQ ID NO: 12).
Полинуклеотид, кодирующий антигенсвязывающую молекулу
Набор олигонуклеотидов или праймеров для применения в целях получения полинуклеотида, кодирующего каждую антигенсвязывающую молекулу, можно синтезировать с использованием стандартного способа. Например, один набор олигонуклеотидов, содержащий последовательности, которые включают каждую возможную комбинацию нуклеотидных триплетов, обеспечиваемую набором кодонов, и кодируют желаемую группу аминокислот, можно синтезировать твердофазным способом. Таким образом, набор синтетических олигонуклеотидов, имеющий конкретный набор кодонов, как правило, содержит множество олигонуклеотидов, отличающихся друг от друга последовательностью. Это различие обеспечивается набором кодонов в целой последовательности. Синтез олигонуклеотидов, имеющих выбранные “вырожденные” нуклеотиды в определенных положениях, известен в данной области. Такой набор нуклеотидов, имеющих такой определенный тип набора кодонов, можно синтезировать с использованием коммерчески доступного устройства для синтеза нуклеиновых кислот (Applied Biosystems, Inc.) или его можно получать в качестве коммерчески доступных продуктов (например, Life Technologies). Как используют в рамках настоящего изобретения, олигонуклеотиды имеют последовательность, которая позволяет гибридизацию с нуклеиновой кислотой-матрицей вариабельного домена, и также могут содержать участки ферментов рестрикции, пригодные для клонирования.
Библиотека может быть сформирована с использованием наборов вышележащих и нижележащих олигонуклеотидов. Каждый набор олигонуклеотидов имеет множество олигонуклеотидов, имеющих различные последовательности, определяемые набором кодонов, предоставленным в олигонуклеотидной последовательности. Наборы вышележащих и нижележащих олигонуклеотидов можно использовать, вместе с последовательностями нуклеиновых кислот-матриц вариабельного домена, для получения “библиотеки” продуктов ПЦР. Продукты ПЦР можно подвергать слиянию с другими родственными или неродственными последовательностями нуклеиновых кислот, например, последовательностями нуклеиновых кислот, кодирующими компоненты в виде белка вирусной оболочки и домены димеризации, с использованием общеизвестного молекулярно-биологического подхода. Таким образом, такой набор олигонуклеотидов может называться “кассетой нуклеиновой кислоты”.
Последовательность каждого праймера ПЦР содержит один или более наборов кодонов, сконструированных для нестрогих остатков с высокой степенью разнообразия, экспонированных на поверхности антигенсвязывающей молекулы. Как описано выше, каждый набор кодонов представляет собой набор различных последовательностей нуклеотидных триплетов, которые используют для кодирования желаемых вариантов аминокислот. Также набор олигонуклеотидов имеет последовательность достаточной длины для гибридизации с нуклеиновой кислотой-матрицей и необязательно может иметь участки рестрикции. ДНК-матрицы формируют с помощью векторов, происходящих из векторов бактериофага M13 или векторов, содержащих ориджин репликации одноцепочечного фага, описанного Viera et al. (Meth. Enzymol. (1987) 153, 3). Таким образом, ДНК, подлежащую внесению мутации, встраивают в один из этих векторов для формирования одноцепочечной матрицы. Получение одноцепочечной матрицы описано в справочнике Sambrook et al.
Способы внесения выбранных аминокислот в антигенсвязывающие молекулы, как описано в неограничивающем варианте осуществления настоящего изобретения, уже известны в данной области. Некоторые из этих способов описаны в настоящем описании. Например, “по меньшей мере один аминокислотный остаток, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов” или нестрогие остатки с высокой степенью разнообразия можно экспонировать на поверхности по меньшей мере одной антигенсвязывающей молекулы и/или вносить в нее с использованием способа Kunkel, предоставленного Kunkel et al. (Methods Enzymol. (1987) 154, 367-382) с получением библиотеки. Такой способ можно соответствующим образом выбирать в случае получения, например, библиотеки по настоящему изобретению, содержащей множество антигенсвязывающих молекул, отличающихся друг от друга последовательностью, путем комбинирования вариабельных областей легкой цепи, в которые внесен “по меньшей мере один аминокислотный остаток, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов” по настоящему изобретению, с вариабельными областями тяжелой цепи, полученными в качестве рандомизированной библиотеки последовательностей вариабельных областей. Когда ион металла представляет собой ион кальция, неограничивающие примеры такого случая включают получение последовательностей вариабельной области легкой цепи, образованных из последовательности эмбрионального типа SEQ ID NO: 6 (Vk1), SEQ ID NO: 7 (Vk2), SEQ ID NO: 8 (Vk3), SEQ ID NO: 9 (Vk4) и т.п. путем замены конкретного остатка “по меньшей мере одним аминокислотным остатком, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов кальция”. Способ, как описано выше, можно выбирать для получения таких вариабельных областей легкой цепи.
В этом случае, наборы олигонуклеотидов можно использовать в качестве праймеров в реакции ПЦР с использованием матричных последовательностей нуклеиновых кислот вариабельной области в качестве матриц для получения кассет нуклеиновых кислот. Каждая используемая матричная последовательность нуклеиновой кислоты, предпочтительно представляет собой последовательность, которая кодирует любой участок в легкой или тяжелой цепи иммуноглобулина и содержит заданную последовательность нуклеиновой кислоты (т.е. последовательность нуклеиновой кислоты, кодирующая аминокислоту, подлежащую замене). Ссылаясь на описанный выше пример, в качестве последовательности матрицы можно использовать нуклеиновую кислоту, кодирующую вариабельную область в последовательности эмбрионального типа SEQ ID NO: 6 (Vk1), SEQ ID NO: 7 (Vk2), SEQ ID NO: 8 (Vk3), SEQ ID NO: 9 (Vk4) и т.п. Матричная последовательность нуклеиновой кислоты вариабельной области кодирует по меньшей мере часть вариабельной области и кодирует по меньшей мере одну CDR. В некоторых случаях матричная последовательность нуклеиновой кислоты вариабельной области кодирует множество CDR. Вышележащие и нижележащие участки последовательности нуклеиновой кислоты-матрицы вариабельной области могут быть мишенями для гибридизации представителей наборов вышележащих и нижележащих олигонуклеотидных праймеров. Первый олигонуклеотид набора вышележащих праймеров может гибридизоваться с первой цепью нуклеиновой кислоты, в то время как второй олигонуклеотид набора нижележащих праймеров может гибридизоваться со второй цепью нуклеиновой кислоты. Олигонуклеотидные праймеры можно конструировать так, чтобы они содержали один или более наборов кодонов и гибридизовались с частью матричной последовательности нуклеиновой кислоты вариабельной области. Использование этих олигонуклеотидов в ПЦР может внести два или более набора кодонов в продукт ПЦР (т.е. кассету нуклеиновой кислоты). Олигонуклеотидные праймеры, которые гибридизуются с областями в последовательности нуклеиновой кислоты, кодирующей вариабельную область антитела, могут включать участки, кодирующие остатки CDR, подлежащие замене другими аминокислотами.
Как описано в настоящем описании, также в качестве способа внесения выбранных аминокислот в антигенсвязывающие молекулы можно соответствующим образом выбирать перекрывающуюся ПЦР, как описано для неограничивающих вариантов осуществления настоящего изобретения (WO1993003151). “По меньшей мере один аминокислотный остаток, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов” или нестрогие остатки с высокой степенью разнообразия можно экспонировать на поверхности по меньшей мере одной антигенсвязывающей молекулы и/или вносить в нее для получения библиотеки. Наборы вышележащих и нижележащих олигонуклеотидов, используемых в перекрывающейся ПЦР, могут содержать каркасную последовательность достаточной длины, подлежащую гибридизации с матричной последовательностью нуклеиновой кислоты вариабельной области, вместе с последовательностью, кодирующей “по меньшей мере один аминокислотный остаток, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов” или нестрогие остатки с высокой степенью разнообразия.
Например, получают наборы олигонуклеотидов, кодирующие наборы кодонов для “по меньшей мере одного аминокислотного остатка, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов” и дополнительных нестрогих остатков, для получения полинуклеотидных молекул, каждая из которых кодирует вариабельные области легкой цепи, в которые внесен аминокислотный остаток, как описано в неограничивающем варианте осуществления настоящего изобретения. Каркасную последовательность достаточной длины, подлежащую гибридизации с матричной последовательностью нуклеиновой кислоты вариабельной области, связывают выше или ниже в рамке считывания с наборами олигонуклеотидов.
В случае внесения аминокислотного остатка или дополнительных нестрогих остатков, например, в CDR2 и CDR3 вариабельной области легкой цепи, олигонуклеотид достаточной длины, кодирующий аминокислотную последовательность FR2, соседнюю с CDR2, связывают с 5'-концами набора олигонуклеотидов, в то время как олигонуклеотид, кодирующий аминокислотную последовательность FR3, соседнюю с CDR2, связывают с их 3'-концами, для получения праймеров. Кроме того, олигонуклеотид достаточной длины, кодирующий аминокислотную последовательность FR4, соседнюю с CDR3, связывают с 5'-концами набора олигонуклеотидов, комплементарного указанному выше набору олигонуклеотидов, в то время как олигонуклеотид, кодирующий аминокислотную последовательность FR3, соседнюю с CDR3, связывают с его 3'-концами, для получения комплементарных праймеров. Когда олигонуклеотид, кодирующий аминокислоты FR3, в праймерах и олигонуклеотид, кодирующий аминокислоты FR3, в комплементарных праймерах содержат перекрывающиеся последовательности достаточной длины, чтобы они гибридизовались друг с другом, вариабельные области легкой цепи, содержащие этот аминокислотный остаток или дополнительные нестрогие остатки, внесенные в CDR2 и CDR3, можно получать путем реакции ПЦР в условиях, не вовлекающих матричную последовательность. Когда эти олигонуклеотиды не содержат таких перекрывающихся последовательностей, вариабельные области легкой цепи, содержащие этот аминокислотный остаток или дополнительные нестрогие остатки, внесенные в CDR2 и CDR3, можно аналогичным образом получать посредством реакции ПЦР с использованием, например, нуклеиновой кислоты вариабельной области с последовательностью эмбрионального типа SEQ ID NO: 6 (Vk1), SEQ ID NO: 7 (Vk2), SEQ ID NO: 8 (Vk3), SEQ ID NO: 9 (Vk4) и т.п. в качестве матричной последовательности.
В случае получения, например, библиотеки, содержащей вариабельные области легкой цепи, имеющие CDR3 с внесенным в нее аминокислотным остатком или дополнительными нестрогими остатками и рандомизированные CDR1 и CDR2, олигонуклеотид достаточной длины, кодирующий аминокислотную последовательность FR4, соседнюю с CDR3, связывают с 5'-концами набора олигонуклеотидов, комплементарных указанному набору олигонуклеотидов, в то время как олигонуклеотид, кодирующий аминокислотную последовательность FR3, соседнюю с CDR3, связывают с его 3'-концами, для получения праймеров. Аналогичным образом библиотеку полинуклеотидов, кодирующих вариабельные области легкой цепи, имеющие CDR3 с внесенным в нее аминокислотным остатком или дополнительными нестрогими остатками, и рандомизированные CDR1 и CDR2, можно получать аналогичным образом с помощью ПЦР с использованием полученных праймеров, праймеров, имеющих нуклеотидную последовательность, кодирующую FR1, и библиотеки, содержащей рандомизированные нуклеиновые кислоты вариабельной области (например, наивная последовательность) в качестве матричных последовательностей. Эти способы получения библиотеки полинуклеотидов легких цепей, в которые внесены “по меньшей мере один аминокислотный остаток, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов” и/или нестрогие остатки, также соответствующим образом выбирают для получения библиотеки полинуклеотидов тяжелых цепей, в которое внесен аминокислотный остаток и дополнительные нестрогие остатки.
Альтернативно наборы вышележащих и нижележащих олигонуклеотидов можно синтезировать так, чтобы каждая олигонуклеотидная последовательность содержала участки рестрикции. Эти участки рестрикции способствуют встраиванию кассеты нуклеиновой кислоты (т.е. продукта реакции ПЦР) в экспрессирующие векторы, имеющие дополнительные последовательности антитела. Предпочтительно, участки рестрикции конструируют так, чтобы облегчать клонирование кассеты нуклеиновой кислоты без внесения чужеродных последовательностей нуклеиновых кислот или без удаления исходных последовательностей нуклеиновых кислот CDR или каркасных областей.
Полученную кассету нуклеиновой кислоты можно клонировать в соответствующий вектор для экспрессии частичной или целой последовательности легкой или тяжелой цепи, составляющей антигенсвязывающую молекулу по настоящему изобретению. В соответствии со способом, подробно описанным в рамках настоящего изобретения, кассету нуклеиновой кислоты клонируют в вектор, который позволяет продукцию частичной или полной последовательности легкой или тяжелой цепи, слитой с целым белком вирусной оболочки или его частью (т.е. формирование слитого белка). Такой вектор, как описано ниже, может представлять собой экспрессирующий вектор, сконструированный так, чтобы частицы или клетки экспонировали слитый белок на их поверхности. Для такой цели несколько типов векторов получают и используют для осуществления настоящего изобретения. Фагмидные векторы представляют собой векторы, предпочтительно используемые в рамках настоящего изобретения. Как общеизвестно специалистам в данной области, фагмидные векторы обычно могут содержать различные компоненты, включая последовательности контроля (например, промоторы и сигнальные последовательности), гены для фенотипической селекции, участки ориджина репликации и другие необходимые компоненты.
В неограничивающем варианте осуществления для экспрессии конкретных вариантов аминокислот в комбинации, кассета нуклеиновой кислоты может кодировать целую или частичную вариабельную область тяжелой или легкой цепи. Например, в случае конструирования кассеты нуклеиновой кислоты так, чтобы CDR3 тяжелой цепи содержала “по меньшей мере один аминокислотный остаток, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов” и/или нестрогие остатки, как описано в неограничивающем аспекте настоящего изобретения, можно получать кассеты нуклеиновых кислот, имеющие разнообразие последовательности CDR3 тяжелой цепи, а затем связывать с кассетами нуклеиновых кислот, кодирующими рандомизированные вариабельные области, такие как наивные последовательности. Как и в библиотеке, кассеты нуклеиновых кислот можно встраивать в экспрессирующие векторы, содержащие дополнительные последовательности антител, например, целые или частичные вариабельные или константные области легкой и тяжелой цепи, для получения антигенсвязывающих молекул, содержащих эти варианты аминокислот или комбинации вариантов аминокислот. Эти дополнительные последовательности в антигенсвязывающих молекулах можно подвергать слиянию с другими последовательностями нуклеиновых кислот, например, последовательностями, кодирующими компонент белка вирусной оболочки. В результате, можно получать слитые белки.
Вектор
Один неограничивающий аспект настоящего изобретения включает экспрессирующий вектор, который можно реплицировать, содержащий последовательность нуклеиновой кислоты, кодирующую слитый ген, где слитый ген кодирует слитый белок, содержащий одну вариабельную область антигенсвязывающей молекулы или одну вариабельную область антигенсвязывающей молекулы и одну константную область, слитые с целым белком вирусной оболочки или его частью. Один неограничивающий аспект настоящего изобретения также включает библиотеку разнообразных экспрессирующих векторов, которые можно реплицировать, каждый из которых содержит множество слитых генов, каждый из которых кодирует множество различных слитых белков, содержащих вариабельные области с разнообразными последовательностями, сформированными, как описано выше, во множестве антигенсвязывающих молекул, отличающихся друг от друга последовательностью. Векторы могут содержать различные компоненты и предпочтительно сконструированы так, чтобы гены вариабельной области антигенсвязывающих молекул можно было переносить между различными векторами и/или слитые белки можно было экспонировать в различных форматах.
Предпочтительные примеры векторов включают фаговые векторы. Фаговые векторы имеют ориджин репликации, который позволяет репликацию фага и формирование фаговой частицы. Предпочтительные примеры фага могут включать нитчатые бактериофаги, включающие фаги M13, f1, fd и Pf3 и их производные, и лямбдоидные фаги, включающие фаг лямбда, 21, phi80, phi81, 82, 424, 434 и другие фаги и их производные.
Примеры белка вирусной оболочки включают инфекционный белок PIII, основной белок оболочки PVIII, pVII, pIX, Soc (T4), Hoc (T4), gpD (бактериофаг λ), и минорный белок оболочки бактериофага 6 (pVI) (нитчатый фаг (J. Immunol. Methods. (1999) 231 (1-2), 39-51); и вариант основного белка бактериофага M13 (P8) (Protein Sci. (2000) 9 (4), 647-654)). Cлитый белок экспонируется на поверхности фага. Подходящие фаговые системы включают хелперный фаг M13KO7, M13R408, M13-VCS и Phi X 174, фаговую систему pJuFo (J. Virol. (2001) 75 (15), 7107-7113), гиперфаг (Nat. Biotechnol. (2001) 19 (1), 75-78) и KM13 (Fold Des. (1998) 3 (5), 321-328). Предпочтительным хелперным фагом является M13KO7. Предпочтительным белком оболочки является белок оболочки гена III фага M13. Предпочтительным хозяином является E. coli, и штамм E. Coli с дефицитом протеазы. Например, для экспрессии слитого белка могут быть пригодны векторы, такие как векторы fth1 (Nucleic Acids Res. (2001) 29 (10) e50).
Экспрессирующий вектор также может содержать секреторную сигнальную последовательность, слитую с ДНК, кодирующей вариабельную область тяжелой или легкой цепи антигенсвязывающей молекулы или ее фрагмента. Эта последовательность, как правило, расположена с 5'-стороны гена, кодирующего слитый белок и, таким образом, транскрибируется на N-конце слитого белка. Однако в некоторых случаях было продемонстрировано, что сигнальная последовательность располагается в положении, отличном от положения с 5'-стороны от гена, кодирующего белок, подлежащий секреции. Эта последовательность направляет белок, с которым эта последовательность связана, через внутреннюю мембрану бактериальной клетки. ДНК, кодирующую сигнальную последовательность, получают в качестве фрагмента, отщепляемого эндонуклеазой рестрикции, из любого гена, кодирующего белок, имеющий сигнальную последовательность. Например, в качестве подходящих прокариотических сигнальных последовательностей можно использовать ген, кодирующий LamB или OmpF (Wong et al., Gene (1983), 68 (2), 193-203), MalE или PhoA и другие гены. Предпочтительной прокариотической сигнальной последовательностью для осуществления настоящего изобретения является сигнальная последовательность термостабильного энтеротоксина II (STII) E. coli, описанная Chang et al. (Gene (1987) 55 (2-3), 189-196), pelB или malE.
Вектор обычно содержит промотор в качестве последовательности контроля, который обеспечивает экспрессию слитого белка. Промоторы, обычно используемые в прокариотических векторах, включают промоторную систему lacZ, промотор щелочной фосфатазы phoA (Ap), промотор бактериофага λPL (чувствительный к температуре промотор), промотор tac (гибридный промотор trp-lac, который регулируется репрессором lac), триптофановый промотор, промотор pBAD и промотор бактериофага T7. Промоторы рассмотрены в справочнике Sambrook et al. (выше). Хотя эти промоторы используют наиболее часто, аналогично можно использовать другие подходящие микробные промоторы.
Также вектор может содержать другие последовательности нуклеиновых кислот, например, последовательности, кодирующие gD-метки, эпитопы c-Myc, полигистидиновые метки, флуоресцентные белки (например, GFP) или белок β-галактозидазы, пригодный для обнаружения и очистки слитого белка, экспрессируемого на поверхности фага или клетки. Например, gD-метка, кодирующая последовательность нуклеиновой кислоты, также обеспечивает положительную или отрицательную селекцию клеток или вирусов, экспрессирующих слитый белок. В некоторых вариантах осуществления gD-метку предпочтительно подвергают слиянию с антигенсвязывающей молекулой вариабельной области, неслитой с компонентом в виде белка вирусной оболочки. Например, последовательность нуклеиновой кислоты, кодирующая полигистидиновую метку, пригодна для идентификации слитого белка, содержащего вариабельную область антигенсвязывающей молекулы, которая связывается с конкретным антигеном, с использованием иммуногистохимического подхода. Такую метку, пригодную для обнаружения связывания антигена, можно подвергать слиянию с вариабельной областью антигенсвязывающей молекулы, неслитой с компонентом в виде белка вирусной оболочки, или вариабельной областью антигенсвязывающей молекулы, слитой с компонентом в виде белка вирусной оболочки.
Предпочтительные примеры других пригодных компонентов в векторе, используемом для осуществления настоящего изобретения, включают гены для фенотипической селекции. Типичный ген для фенотипической селекции представляет собой ген, кодирующий белок, который сообщает клеткам-хозяевам устойчивость к антибиотикам. В качестве такого примера, предпочтительно можно использовать ген устойчивости к ампициллину (ampr) и ген устойчивости к тетрациклину (tetr).
Также вектор может содержать последовательность нуклеиновой кислоты, содержащую уникальные участки рестрикции и супрессируемый стоп-кодон. Уникальные участки рестрикции пригодны для переноса гена вариабельной области антигенсвязывающей молекулы между различными векторами и экспрессирующими системами и особенно пригодны для продуцирования полноразмерной антигенсвязывающей молекулы или антигенсвязывающего фрагмента клеточной культурой. Супрессируемый стоп-кодон пригоден для регуляции уровня экспрессии слитого белка и способствует очистке растворимого фрагмента антигенсвязывающей молекулы. Например, янтарный стоп-кодон может транслироваться в Gln в хозяине supE, способном к фаговому дисплею, в то время как в хозяине, не являющемся supE, тот кодон интерпретируется как стоп-кодон, обеспечивая продукцию растворимого фрагмента антигенсвязывающей молекулы, неслитого с белком оболочки фага. Эти синтетические последовательности можно подвергать слиянию с генами, кодирующими одну или более вариабельных областей антигенсвязывающей молекулы, в векторе.
Предпочтительно можно использовать вектор, который позволяет нуклеиновой кислоте, кодирующей представляющую интерес последовательность антигенсвязывающей молекулы, быть без труда извлеченной из вектора и помещенной в другой вектор. Например, подходящие участки рестрикции можно встраивать в вектор для облегчения извлечения последовательности нуклеиновой кислоты, кодирующей антигенсвязывающую молекулу по настоящему изобретению или ее вариабельную область. Последовательности рестрикции обычно выбирают в качестве уникальных последовательностей в векторе, чтобы способствовать эффективному вырезанию и лигированию в новые векторы. Затем антигенсвязывающая молекула или ее вариабельную область могут экспрессироваться с векторов в качестве молекулы, имеющей структуру, свободную от слитых чужеродных последовательностей, например, белок вирусной оболочки или другие метки последовательности.
ДНК, кодирующую кодон терминации или стоп-кодон, можно встраивать между нуклеиновой кислотой, кодирующей вариабельную область или константную область антигенсвязывающей молекулы (ген 1), и нуклеиновой кислотой, кодирующей компонент в виде белка вирусной оболочки (ген 2). Такой кодон терминации включает UAG (янтарь), UAA (охра) и UGA (опал) (Davis et al., Microbiology (1980), p. 237, 245-247 и 374, Harper & Row, New York). Кодон терминации или стоп-кодон, экспрессируемые в клетках-хозяевах дикого типа, приводят к синтезу белкового продукта гена 1, не связанного с белком гена 2. Однако слитый белок синтезируется в поддающемся выявлению количестве при выращивании в супрессорных клетках-хозяевах. Такие супрессорные клетки-хозяева известны в данной области и описаны в качестве штаммов с супрессорными генами E. coli (Bullock et al., BioTechniques (1987) 5, 376-379) и т.д. Такой кодон терминации можно встраивать в мРНК, кодирующую слитый полипептид.
Супрессируемый кодон можно встраивать между первым геном, кодирующим вариабельную или константную область антигенсвязывающей молекулы, и вторым геном, кодирующим по меньшей мере часть белка оболочки фага. Альтернативно супрессируемый кодон терминации можно встраивать рядом с участком слияния путем замены триплета последней аминокислоты в вариабельной области антигенсвязывающей молекулы или триплета первой аминокислота в белке оболочки фага. Супрессируемый кодон терминации можно встраивать в положении или после положения, соответствующего C-концу домена димеризации. Репликация плазмиды, содержащей супрессируемый кодон в супрессорных клетках-хозяевах, обеспечивает слитый полипептид, содержащий полипептид и белок оболочки, в поддающемся выявлению количестве. Таким образом, репликация плазмиды в несупрессорных клетках-хозяевах завершает трансляцию на встроенном супрессируемом триплете UAG, UAA или UGA и, таким образом, приводит к синтезу вариабельной области антигенсвязывающей молекулы по существу без слияния с белком оболочки фага. Таким образом, вариабельная область антигенсвязывающей молекулы, экспрессируемая в несупрессорных клетках, секретируется из клеток-хозяев после синтеза вследствие отсутствия слитого белка оболочки фага, подлежащего заякориванию на мембране хозяина.
Вариабельные или константные области легкой цепи и/или тяжелой цепи антигенсвязывающей молекулы можно далее подвергать слиянию с пептидной последовательностью, которая обеспечивает взаимодействие одного или более слитых полипептидов на вирусной частице или клеточной поверхности. Эту пептидную последовательность называют в настоящем описании “доменом димеризации”. Домен димеризации может содержать по меньшей мере одну или более последовательностей димеризации или по меньшей мере одну последовательность, содержащую остаток цистеина, или обе из них. Подходящие последовательности димеризации включают последовательности димеризации белков, имеющих амфипатические α-спирали, которые содержат регулярно расположенные гидрофобные остатки и позволяют образование димера путем взаимодействия гидрофобных остатков каждого белка. Такие белки и части белков содержат, например, области лейциновых молний. Домен димеризации также может содержать один или более остатков цистеина (например, предоставляемых последовательностью шарнирной области антитела, содержащейся в домен димеризации). Остатки цистеина обеспечивают димеризацию путем образования одной или более дисульфидных связей. В одном варианте осуществления, где стоп-кодон расположен ниже последовательности, кодирующей домен димеризации, домен димеризации содержит по меньшей мере один остаток цистеина. Домен димеризации предпочтительно расположен между вариабельным или константным доменом антитела и компонентом в виде белка вирусной оболочки.
В некоторых случаях вектор кодирует, например, фаговый полипептид одной антигенсвязывающей молекулы в одноцепочечной форме, содержащей вариабельные области тяжелой и легкой цепей, слитые с белком оболочки. В этих случаях вектор считается “моноцистронным”, так что один транскрипт экспрессируется под контролем определенного промотора. Примеры такого вектора включают векторы, в которых используется промотор щелочной фосфатазы (AP) или промотор Tac для обеспечения экспрессии моноцистронной последовательности, кодирующей вариабельную область легкой цепи (VL-домен) и вариабельную область тяжелой цепи (VH-домен), между которыми расположен линкерный пептид. Такая цистронная последовательность связана на ее 5'-конце с сигнальной последовательностью malE или термостабильного энтеротоксина II (STII) E. coli и на ее 3'-конце с целым белком вирусной оболочки или его частью (например, белок pIII). В некоторых вариантах осуществления, вектор может дополнительно содержать последовательность, кодирующую домен димеризации (например, лейциновая молния), как показано в SEQ ID NO: 12, на ее 3'-конце между второй последовательностью вариабельной области и последовательностью белка вирусной оболочки.
В других случаях вариабельные области тяжелой и легкой цепей могут экспрессироваться в качестве отдельных полипептидов. Такой вектор является ʺбицистроннымʺ и позволяет экспрессию отдельных транскриптов. В этом векторе подходящий промотор, например, промотор tac или PhoA, можно использовать для обеспечения экспрессии бицистронной мРНК. Первый цистрон, кодирующий, например, вариабельные и константные области легкой цепи, связывают на его 5'-конце с сигнальной последовательностью malE, pelB или термостабильного энтеротоксина II (STII) E. coli и на его 3'-конце с последовательностью нуклеиновой кислоты, кодирующей gD-метку. Второй цистрон, кодирующий, например, вариабельную область и константную область CH1 тяжелой цепи, связывают на его 5'-конце с сигнальной последовательностью malE или термостабильного энтеротоксина II (STII) E. coli и на его 3'-конце с целым белком вирусной оболочки или его частью.
В векторе, который образует бицистронную мРНК и обеспечивает дисплей F(ab')2-pIII, подходящий промотор, например промотор tac или PhoA (AP), обеспечивает экспрессию первого цистрона, который кодирует вариабельные и константные области легкой цепи, и функционально связан на его 5'-конце с сигнальной последовательностью malE или термостабильного энтеротоксина II (STII) E. coli и на его 3'-конце с последовательностью нуклеиновой кислоты, кодирующей gD-метку. Второй цистрон кодирует, например, вариабельные и константные области тяжелой цепи и функционально связан на его 5'-конце с сигнальной последовательностью malE или термостабильного энтеротоксина II (STII) E. coli и на его 3'-конце с последовательностью, кодирующей домен димеризации, содержащий последовательность шарнирной области IgG и последовательность лейциновой молнии, за которой следует по меньшей мере часть белка вирусной оболочки.
Дисплей слитого полипептида
Слитый полипептид вариабельной области антигенсвязывающей молекулы можно экспонировать в различных формах на поверхности клетки, вируса или фагмидной частицы. Эти формы включают одноцепочечные Fv-фрагменты (scFv), F(ab)-фрагменты и поливалентные формы этих фрагментов. Поливалентные формы предпочтительно представляют собой димер ScFv, Fab или F(ab'), которые обозначают в настоящем описании как (ScFv)2, F(ab)2 и F(ab')2, соответственно. Дисплей поливалентных форм является предпочтительным, возможно, поскольку экспонированные поливалентные формы обычно обеспечивают идентификацию низкоаффинных клонов и/или имеют множество антигенсвязывающих участков, которые обеспечивают более эффективную селекцию редких клонов в ходе селекции.
Способы экспонирования слитых полипептидов, содержащих фрагменты антител, на поверхности бактериофагов, известны в данной области и описаны, например, в WO1992001047 и в настоящем описании. Другие сходные способы описаны в WO1992020791, WO1993006213, WO1993011236 и 1993019172. Специалисты в данной области могут соответствующим образом использовать эти способы. В другой общедоступной литературе (H.R. Hoogenboom & G. Winter (1992) J. Mol. Biol. 227, 381-388, WO1993006213 и WO1993011236) описана идентификация антител с использованием искусственно реаранжированных репертуаров генов вариабельной области против различных антигенов, экспонированных на поверхности фагов.
В случае конструирования вектора для дисплея в форме scFv, этот вектор содержит последовательности нуклеиновых кислот, кодирующие вариабельные области легкой и тяжелой цепей антигенсвязывающей молекулы. Как правило, последовательность нуклеиновой кислоты, кодирующую вариабельную область тяжелой цепи антигенсвязывающей молекулы, подвергают слиянию с последовательностью нуклеиновой кислоты, кодирующей компонент в виде белка вирусной оболочки. Последовательность нуклеиновой кислоты, кодирующую вариабельную область легкой цепи антигенсвязывающей молекулы, связывают с нуклеиновой кислотой вариабельной области тяжелой цепи антигенсвязывающей молекулы через последовательность нуклеиновой кислоты, кодирующую пептидный линкер. Пептидный линкер обычно содержит приблизительно от 5 до 15 аминокислот. Необязательно, дополнительную последовательность, кодирующую, например, метку, пригодную для очистки или выявления, можно подвергать слиянию с 3'-концом последовательности нуклеиновой кислоты, кодирующей вариабельную область легкой цепи антигенсвязывающей молекулы, или последовательности нуклеиновой кислоты, кодирующей вариабельную область тяжелой цепи антигенсвязывающей молекулы, или с обеими из них.
В случае конструирования вектора для дисплея в форме F(ab), этот вектор содержит последовательности нуклеиновых кислот, кодирующие вариабельные и константные области антигенсвязывающей молекулы. Последовательность нуклеиновой кислоты, кодирующую вариабельную область легкой цепи, подвергают слиянию с последовательностью нуклеиновой кислоты, кодирующей константную область легкой цепи. Последовательность нуклеиновой кислоты, кодирующую вариабельную область тяжелой цепи антигенсвязывающей молекулы, подвергают слиянию с последовательностью нуклеиновой кислоты, кодирующей константную область CH1 тяжелой цепи. Как правило, последовательность нуклеиновой кислоты, кодирующую вариабельные и константные области тяжелой цепи, подвергают слиянию с последовательностью нуклеиновой кислоты, кодирующей целый белок вирусной оболочки или его часть. Вариабельные и константные области тяжелой цепи предпочтительно экспрессируются в качестве слитого продукта по меньшей мере с частью белка вирусной оболочки, в то время как вариабельные и константные области легкой цепи экспрессируются отдельно от слитого белка тяжелая цепь-вирусный белок оболочки. Тяжелая и легкая цепи могут ассоциировать друг с другом через ковалентную связь или нековалентную связь. Необязательно, дополнительная последовательность, кодирующая, например, полипептидную метку, пригодную для очистки или выявления, может быть слита с 3'-концом последовательности нуклеиновой кислоты, кодирующей константную область легкой цепи антигенсвязывающей молекулы, или последовательности нуклеиновой кислоты, кодирующей константную область тяжелой цепи антигенсвязывающей молекулы, или обе из них.
Перенос вектора в клетку-хозяина
Векторы, сконструированные таким образом, переносят в клетки-хозяева для амплификации и/или экспрессии. Векторы можно переносить в клетки с помощью способов трансформации, известных в данной области, включая электропорацию, осаждение с фосфатом кальция и т.п. Когда векторы представляют собой инфекционные частицы, такие как вирусы, векторы сами по себе проникают в клетки-хозяева. Слитые белки экспонируют на поверхности фаговых частиц путем трансфекции клеток-хозяев экспрессирующимися векторами, которые можно реплицировать, имеющими вставки полинуклеотидов, кодирующих белок, и продукции фаговых частиц с помощью подхода, известного в данной области.
Экспрессирующие векторы, которые можно реплицировать, можно переносить в клетки-хозяева с использованием различных способов. В неограничивающем варианте осуществления векторы можно переносить в клетки путем электропорации, как описано в WO2000106717. Клетки культивируют при 37°C, необязательно в течение приблизительно 6-48 часов (или до тех пор, пока OD при 600 нм не достигнет 0,6-0,8) в стандартной культуральной среде. Далее, культуральную среду центрифугируют и культуральный супернатант удаляют (например, путем переливания). На начальной стадии очистки клеточный осадок предпочтительно ресуспендируют в буферном растворе (например, 1,0 мМ HEPES (pH 7,4)). Далее, суспензию вновь центрифугируют для удаления супернатанта. Полученный клеточный осадок ресуспендируют в глицерине, разбавленном, например, до 5-20% об./об. Суспензию вновь центрифугируют для удаления супернатанта, тем самым, получая клеточный осадок. Полученный клеточный осадок ресуспендируют в воде или разбавленном глицерине. Исходя из результата измерения полученной концентрации клеток, конечную концентрацию клеток доводят до желаемой концентрации с использованием воды или разбавленного глицерина.
Примеры предпочтительных рецепторных клеток включают штамм SS320 E. coli, способный отвечать на электропорацию (Sidhu et al., Methods Enzymol. (2000) 328, 333-363). Штамм SS320 E. coli получен путем скрещивания клеток MC1061 с клетками XL1-BLUE в условиях, достаточных для переноса эписомы фертильности (F'-плазмида) из XL1-BLUE в клетки MC1061. Штамм SS320 E. coli депонирован в ATCC (10801 University Boulevard, Manassas, Virginia) под номером депозита № 98795. В рамках настоящего изобретения можно использовать любую F'-эписому, которая обеспечивает репликацию фага в этом штамме. Подходящую эписому можно получать из штаммов, депонированных в ATCC, или можно получать в качестве коммерчески доступных продуктов (TG1, CJ236, CSH18, DHF', ER2738, JM101, JM103, JM105, JM107, JM109, JM110, KS1000, XL1-BLUE, 71-18 и т.д.).
Использование более высоких концентраций ДНК (приблизительно в 10 раз) при электропорации повышает частоту трансформации и увеличивает количество ДНК, трансформирующих клетки-хозяева. Использование высоких концентраций клеток также повышает эффективность (приблизительно в 10 раз). Увеличенное количество перенесенных ДНК может обеспечить библиотеку, имеющую большее разнообразие и большее количество независимых клонов, отличающихся последовательностью. Трансформированные клетки обычно выбирают, исходя из присутствия или отсутствия роста на среде, содержащей антибиотик.
Способ селекции антигенсвязывающей молекулы, активность связывания которой изменяется в зависимости от условий, и способ выделения полинуклеотида, кодирующего молекулу
Способы использования фагового дисплея для идентификации антигенсвязывающих молекул, которые проявляют желаемую активность связывания против антигенов, уже разработаны в данной области, также включая их различным образом модифицированные способы. В одном неограничивающем аспекте соответствующие клетки-хозяева трансформируют библиотекой экспрессирующих векторов, которые можно реплицировать, сконструированных так, чтобы они содержали элементы регуляции транскрипции, функционально связанные со слитыми генами, кодирующими слитые полипептиды. Трансформированные клетки культивируют для формирования фаговых частиц, экспонирующих слитые полипептиды на их поверхности. Затем проводят стадию “селекции связывающих молекул”, которая охватывает селекцию и сортировку путем приведения рекомбинантных фаговых частиц в контакт с антигенами-мишенями, так чтобы по меньшей мере часть субпопуляции частиц связывалась с антигенами, для цели увеличения содержания связанных с антигеном частиц в субпопуляции относительно не связанных с антигеном частиц в ходе селекции. Для другого раунда скрининга в отличающихся или таких же условиях реакции, отсортированную субпопуляцию амплифицируют, например, путем инфицирования субпопуляцией свежих клеток-хозяев, таких как клетки XL1-Blue. Далее проводят стадию приведения амплифицированной таким образом субпопуляции полученных антигенсвязывающих молекул в контакт с антигенами в отличающихся концентрациях ионов для скрининга антигенсвязывающих молекул, которые связываются с антигенами в желаемых условиях. Эту стадию приведения в контакт субпопуляции с антигенами при различных концентрациях ионов можно проводить в качестве начальной стадии способа селекции. Комбинирование стадии “селекции связывающих молекул” и стадии селекции связывающих молекул, активность связывания которых изменяется в различных условиях концентрации ионов, можно соответствующим образом изменять. Также, стадию селекции и сортировки можно проводить столько раз, сколько желательно. Эти антигенсвязывающие молекулы, которые связываются с антигенами в различных условиях концентрации ионов, пригодны в качестве терапевтических лекарственных средств, способных быстро устранять патогенные антигены из организмов при введении в организмы.
Слитые полипептиды вариабельных областей или их частей, содержащих аминокислоту, которая изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов, и/или нестрогие остатки в соответствии с настоящим изобретением экспонируют на поверхности фагов, фагмидных частиц или клеток. Далее, представителей, составляющих субпопуляцию слитых полипептидов, можно выбирать и/или сортировать в отношении их способности связываться с антигенами в различных концентрациях ионов. Способ селекции, сортировки и скрининга слитых полипептидов также включает способ селекции, сортировки и скрининга на общих белках, обладающих аффинностью в отношении вариабельных областей антигенсвязывающих молекул, таких как белок L или меченые антитела, способные связываться с антигенсвязывающими молекулами или их фрагментами, экспонированными на фагах. Такой способ можно использовать для увеличения размера библиотеки и числа эквивалентов библиотеки, которая экспонирует правильно свернутые антигенсвязывающие молекулы (или слитые полипептиды, содержащие молекулы).
Для описанной выше селекции, сортировки и скрининга можно использовать две основных стратегии. Первая стратегия представляет собой способ на твердой подложке, скрининг в чашках или скрининг с иммобилизованным антигеном. Второй стратегией является способ связывания в растворе.
В “способе на твердой подложке” антигены можно связывать с соответствующей твердой или полутвердой матрицей, известной в данной области, например, агарозными гранулами, акриламидными гранулами, стеклянными гранулами, целлюлозой, различными акриловыми сополимерами, гидроксиалкилметакрилатными гелями, полиакриловыми и полиметакриловыми сополимерами, нейлоном, и нейтральными и ионными носителями. Присоединение антигенов к матрице можно обеспечивать способом, описанным в Methods in Enzymology (1976) 44 или другими способами, известными в данной области.
После присоединения антигена к матрице иммобилизованные антигены контактируют с библиотекой, экспрессирующей слитые полипептиды, в условиях, подходящих для связывания по меньшей мере одной субпопуляции фаговых частиц с иммобилизованными антигенами. Обычно условия, включая pH, ионную силу, температуру и т.п., выбирают так, чтобы они имитировали физиологические условия. Связанные частицы (“связывающиеся элементы”) с иммобилизованными антигенами отделяют от частиц, не связанных с мишенью, путем промывания водой. Условия промывания можно корректировать так, чтобы удалять все, кроме высокоаффинных связывающихся элементов. Связывающиеся элементы можно диссоциировать от иммобилизованной мишени различными способами. Эти способы включают, например, конкурентную диссоциацию с использованием лигандов дикого типа (например, избыточные антигены), изменение pH и/или ионной силы, и способы, известные в данной области. Как правило, связывающиеся элементы можно элюировать с аффинной матрицы с помощью соответствующего материала для элюирования, такого как кислота (например, 0,1 M HCl) или лиганды. Элюирование при увеличенных концентрациях лиганда может элюировать экспонированные связывающиеся молекулы с более высокой аффинностью.
Подходящие клетки-хозяева можно инфицировать выделенными связывающимися элементами, т.е. вирусными частицами (и, если необходимо, хелперными фагами, например, когда вирусные частицы представляют собой фагмидные частицы) для повторной амплификации связывающихся элементов в клетках. Полученные таким образом клетки-хозяева культивируют в условиях, пригодных для амплификации частиц, которые экспонируют желаемый слитый полипептид. Далее, фаговые частицы собирают, и стадию селекции повторяют один или более раз до тех пор, пока связывающиеся антиген элементы не увеличатся в количестве настолько, чтобы достигнуть значительной доли. Селекцию и скрининг можно проводить столько раз, сколько желательно. Один из способов селекции или скрининга может вовлекать выделение связывающихся элементов, которые связываются с общими аффинными белками, такими как белок L или антитела против полипептидных меток, присутствующих в экспонированных полипептидах, например, антителах против gD-белка или полигистидиновых меток.
В одном аспекте настоящего изобретения можно соответствующим образом использовать способ скрининга в жидкой фазе, называемый “способом связывания в растворе”. Способ связывания в растворе можно использовать для выявления улучшенных связывающихся элементов из случайной библиотеки, нацеленной на повышение активности связывания желаемого связывающегося клона или группы клонов. Этот способ вовлекает приведение в контакт множества полипептидов, например, полипептидов, экспонированных на фаговых или фагмидных частицах (библиотека), с антигенами, мечеными или слитыми с молекулами меток. В качестве метки можно использовать биотин или другие конкретные молекулы для связывания. Жесткость фазы раствора можно варьировать с использованием постепенно снижающихся концентраций меченых или слитых антигенов в первой фазе раствора для связывания. Для дальнейшего увеличения жесткости, после связывания с первыми антигенами, меченными молекулами меток или слитыми с мечеными молекулами меток в первой фазе раствора, может соответствующим образом следовать дополнительный контакт со второй фазой раствора, имеющей высокую концентрацию антигенов, немеченых молекулами меток или неслитых с мечеными молекулами меток. В этом случае, антигены, немеченые молекулами меток или неслитые с мечеными молекулами меток, обычно используют в количестве, в от 100 до 1000 раз превышающем количество меченой мишени во второй фазе. Время инкубации первой фазы раствора находится в диапазоне от нескольких минут до 1-2 часов или более до достижения равновесия. Поскольку связывающиеся элементы, имеющие высокую скорость ассоциации, имеют тенденцию к тому, чтобы иметь свойство связываться с мишенью быстро на этой первой фазе, можно выбирать условия приведения в контакт так, чтобы укоротить время связывания. Время инкубации и температуру второй фазы можно варьировать для увеличения жесткости. Такое варьирование условий инкубации обеспечивает смещение селекции в отношении связывающихся элементов, которые отсоединяются от мишени с медленной скоростью (скорость диссоциации). После контакта множества полипептидов, экспонированных на фаговых или фагмидных частицах, с антигенами, фаговые или фагмидные частицы, связанные с антигенами, меченными молекулами меток или слитыми с мечеными молекулами меток, отделяют от не связавшихся фаговых или фагмидных частиц. Смеси фаговая или фагмидная частица-антиген выделяют из фазы раствора путем приведения в контакт фаговых или фагмидных частиц с антигенами в течение короткого периода времени (например, от 2 до 5 минут), который обеспечивает связывание с антигенами, меченными молекулами меток или слитыми с мечеными молекулами меток. Первоначальная концентрация антигенов, меченных молекулами меток или слитых с мечеными молекулами меток, находится в диапазоне от приблизительно 0,1 нМ до приблизительно 1000 нМ. Частицы можно элюировать из смеси, а затем выращивать в течение следующего раунда скрининга. Предпочтительно множество раундов скрининга повторяют с использованием более низкой концентрации антигенов, меченных молекулами меток или слитых с мечеными молекулами меток, в каждом раунде скрининга. Как описано ниже в разделе “Примеры”, например, покрытые стрептавидином гранулы можно соответствующим образом использовать в способе связывания в растворе с использованием биотина в качестве меченой молекулы метки.
Способ на твердой подложке и способ связывания в растворе можно соответствующим образом осуществлять отдельно или в комбинации для выделения связывающихся элементов, имеющих желаемый признак. После двух, трех или четырех раундов селекции и скрининга в отношении антигенов, субпопуляцию, отобранную для идентификации конкретных связывающихся элементов, имеющих желаемое свойство или признак, обычно подвергают скринингу в отношении индивидуальных клонов. Предпочтительно, процесс скрининга можно проводить с использованием автоматической системы, которая обеспечивает высокопроизводительный скрининг библиотеки.
После идентификации связывающихся элементов на основе связывания антигена, из связывающихся элементов можно экстрагировать нуклеиновые кислоты. Затем экстрагированные ДНК используют для прямой трансформации клеток-хозяев E. coli. Альтернативно их кодирующие последовательности можно амплифицировать, например, с помощью ПЦР с использованием соответствующих праймеров, а затем секвенировать типичным способом секвенирования. Далее, ДНК связывающихся элементов, кодирующие вариабельную область, можно встраивать в векторы, расщепленные ферментами рестрикции, для экспрессии кодируемых антигенсвязывающих молекул.
Для селекции и скрининга фаговых частиц, экспрессирующих антигенсвязывающую молекулу по настоящему изобретению, антигенсвязывающая активность которой изменяется в зависимости от условий концентрации ионов, или ее слитый полипептид, субпопуляцию фаговых частиц, антигенсвязывающая активность которых изменяется, сортируют путем варьирования условий для приведения в контакт иммобилизованных антигенов с библиотекой, содержащей фаговые частицы, экспрессирующие антигенсвязывающие молекулы или слитые полипептиды.
Если взять ион кальция в качестве предпочтительного примера иона металла, примеры условий концентрации ионов кальция включают условия низкой концентрации ионов кальция и условия высокой концентрации ионов кальция. Выражение “активность связывания изменяется в зависимости от условий концентрации ионов кальция” означает, что антигенсвязывающая активность каждой антигенсвязывающей молекулы изменяется в зависимости от различий между условиями низкой концентрации ионов кальция и условиями высокой концентрации ионов кальции. Примеры этого случая включают более высокую антигенсвязывающую активность антигенсвязывающей молекулы в условиях высокой концентрации ионов кальция, чем в условиях низкой концентрации ионов кальция. Другой его пример включает более высокую антигенсвязывающую активность антигенсвязывающей молекулы в условиях низкой концентрации ионов кальция, чем в условиях высокой концентрации ионов кальция.
В настоящем описании высокая концентрация ионов кальция конкретно не ограничена однозначной численной величиной и предпочтительно может представлять собой концентрацию, выбранную из диапазона от 100 мкМ до 10 мМ. В другом аспекте высокая концентрация ионов кальция может представлять собой концентрацию, выбранную из диапазона от 200 мкМ до 5 мМ. В другом аспекте высокая концентрация ионов кальция также может представлять собой концентрацию, выбранную из диапазона от 500 мкМ до 2,5 мМ. В альтернативном аспекте высокая концентрация ионов кальция также может представлять собой концентрацию, выбранную из диапазона от 200 мкМ до 2 мМ. Кроме того, эта концентрация также может представлять собой концентрацию, выбранную из диапазона от 400 мкМ до 1,5 мМ. Ее особенно предпочтительные примеры включают концентрации, выбранные из диапазона от 500 мкМ до 2,5 мМ, которые являются близкими к концентрациям ионов кальция в плазме (крови) in vivo.
В настоящем описании низкая концентрация ионов кальция конкретно не ограничена однозначной численной величиной и предпочтительно может представлять собой концентрацию, выбранную из диапазона от 0,1 мкМ до 30 мкM. В другом аспекте низкая концентрация ионов кальция может представлять собой концентрацию, выбранную из диапазона от 0,2 мкМ до 20 мкМ. В другом аспекте низкая концентрация ионов кальция также может представлять собой концентрацию, выбранную из диапазона от 0,5 мкМ до 10 мкМ. В альтернативном аспекте низкая концентрация ионов кальция также может представлять собой концентрацию, выбранную из диапазона от 1 мкМ до 5 мкМ. Кроме того, эта концентрация также может представлять собой концентрацию, выбранную из диапазона от 2 мкМ до 4 мкМ. Особенно предпочтительные ее примеры включают концентрации, выбранные из диапазона от 1 мкМ до 5 мкМ, которые являются близкими к концентрациям ионизированного кальция в ранней эндосоме in vivo.
В рамках настоящего изобретения выражение “антигенсвязывающая активность антигенсвязывающей молекулы является более низкой в условиях низкой концентрации ионов кальция, чем в условиях высокой концентрации ионов кальция” означает, что антигенсвязывающая активность антигенсвязывающей молекулы при концентрации ионов кальция, выбранной из диапазона от 0,1 мкМ до 30 мкМ, является более слабой, чем при концентрации ионов кальция, выбранной из диапазона от 100 мкМ до 10 мМ. Это выражение предпочтительно означает, что антигенсвязывающая активность антигенсвязывающей молекулы при концентрации ионов кальция, выбранной из диапазона от 0,5 мкМ до 10 мкМ, является более слабой, чем при концентрации ионов кальция, выбранной из диапазона от 200 мкМ до 5 мМ. Особенно предпочтительно, это выражение означает, что антигенсвязывающая активность при концентрации ионов кальция в ранней эндосоме in vivo является более слабой, чем при концентрации ионов кальция в плазме in vivo. В частности, это означает, что антигенсвязывающая активность антигенсвязывающей молекулы при концентрации ионов кальция, выбранной из диапазона от 1 мкМ до 5 мкМ, является более слабой, чем при концентрации ионов кальция, выбранной из диапазона от 500 мкМ до 2,5 мМ.
Для селекции и скрининга, например, фаговых частиц, экспрессирующих антигенсвязывающие молекулы, антигенсвязывающая активность которых является более высокой в условиях высокой концентрации ионов кальция, чем в условиях низкой концентрации ионов кальция, или их слитые полипептиды, сначала сортируют субпопуляцию фаговых частиц, связывающихся с иммобилизованными антигенами в условиях высокой концентрации кальция. Затем отсортированную субпопуляцию (библиотека, содержащая фаговые частицы, экспрессирующие антигенсвязывающие молекулы или слитые полипептиды), приводят в контакт с иммобилизованными антигенами в условиях низкой концентрации ионов кальция. Фаговые частицы, которые не связываются с иммобилизованными антигенами в условиях низкой концентрации ионов кальция, сортируют и отделяют в супернатант или последующие промывочные жидкости. Условия высокой концентрации кальция и условия низкой концентрации кальция можно соответствующим образом выбирать из диапазонов, описанных выше. В неограничивающем аспекте субпопуляцию можно сортировать на основе различий между антигенсвязывающей активностью при концентрации ионов кальция, выбранной из диапазона от 0,1 мкМ до 30 мкМ, и антигенсвязывающей активностью при концентрации ионов кальция, выбранной из диапазона от 100 мкМ до 10 мМ. В другом неограничивающем аспекте субпопуляцию можно сортировать на основе различий между антигенсвязывающей активностью при концентрации ионов кальция, выбранной из диапазона от 0,5 мкМ до 10 мкМ, и антигенсвязывающей активностью при концентрации ионов кальция, выбранной из диапазона от 200 мкМ до 5 мМ. В альтернативном неограничивающем аспекте субпопуляцию можно сортировать на основе различий между антигенсвязывающей активностью при концентрации ионов кальция в ранней эндосоме in vivo и антигенсвязывающей активностью при концентрации ионов кальция в плазме in vivo, в частности, различий между антигенсвязывающей активностью при концентрации ионов кальция, выбранной из диапазона от 1 мкМ до 5 мкМ, и антигенсвязывающей активностью при концентрации ионов кальция, выбранной из диапазона от 500 мкМ до 2,5 мМ.
Если взять концентрацию ионов водорода в качестве предпочтительного примера концентрации ионов, примеры условий концентрации ионов водорода включают условия кислых значений pH и условия нейтральных значений pH. Выражение “активность связывания изменяется в зависимости от условий pH” означает, что антигенсвязывающая активность каждой антигенсвязывающей молекулы изменяется в зависимости от различий между кислыми значениями pH и нейтральными значениями pH. Примеры этого случая включают более высокую антигенсвязывающую активность антигенсвязывающей молекулы при нейтральных значениях pH, чем при кислых значениях pH. Другой его пример включает более высокую антигенсвязывающую активность антигенсвязывающей молекулы при кислых значениях pH, чем при нейтральных значениях pH.
В настоящем описании нейтральное значение pH конкретно не ограничивается однозначной численной величиной и предпочтительно оно может быть выбрано из диапазона от pH 6,7 до pH 10,0. В другом аспекте нейтральное значение pH может быть выбрано из диапазона от pH 6,7 до pH 9,5. В другом аспекте нейтральное значение pH может быть выбрано из диапазона от pH 7,0 до pH 9,0. В альтернативном аспекте это значение pH может быть выбрано из диапазона от pH 7,0 до pH 8,0. Особенно предпочтительные его примеры включают значение pH 7,4, которое является близким pH в плазме (крови) in vivo.
В настоящем описании кислое значение pH конкретно не ограничено однозначной численной величиной и предпочтительно оно может быть выбрано из диапазона от pH 4,0 до pH 6,5. В другом аспекте кислое значение pH может быть выбрано из диапазона от pH 4,5 до pH 6,5. В другом аспекте кислое значение pH может быть выбрано из диапазона от pH 5,0 до pH 6,5. В альтернативном аспекте это значение pH может быть выбрано из диапазона от pH 5,5 до pH 6,5. Особенно предпочтительные его примеры включают значение pH 5,8, которое является близким к концентрации ионизированного кальция в ранней эндосоме in vivo.
В рамках настоящего изобретения выражение “антигенсвязывающая активность антигенсвязывающей молекулы является более низкой в условиях нейтральных значений pH, чем в условиях кислых значений pH” означает, что антигенсвязывающая активность антигенсвязывающей молекулы при значении pH, выбранном из диапазона от pH 4,0 до pH 6,5, является более слабой, чем при значении pH, выбранном из диапазона от pH 6,7 до pH 10,0. Это выражение предпочтительно означает, что антигенсвязывающая активность антигенсвязывающей молекулы при значении pH, выбранном из диапазона от pH 4,5 до pH 6,5, является более слабой, чем при значении pH, выбранном из диапазона от pH 6,7 до pH 9,5. Более предпочтительно, выражение означает, что антигенсвязывающая активность антигенсвязывающей молекулы при значении pH, выбранном из диапазона от pH 5,0 до pH 6,5, является более слабой, чем при значении pH, выбранном из диапазона от pH 7,0 до pH 9,0. Кроме того, выражение предпочтительно означает, что антигенсвязывающая активность антигенсвязывающей молекулы при значении pH, выбранном из диапазона от pH 5,5 до pH 6,5, является более слабой, чем при значении pH, выбранном из диапазона от pH 7,0 до pH 8,0. Особенно предпочтительно, это выражение означает, что антигенсвязывающая активность при pH в ранней эндосоме in vivo является более слабой, чем при pH в плазме in vivo. В частности, это означает, что антигенсвязывающая активность антигенсвязывающей молекулы при pH 5,8 является более слабой, чем при pH 7,4.
Определение того, изменяется ли антигенсвязывающая активность антигенсвязывающей молекулы в зависимости от условий pH можно проводить, например, в соответствии со способом анализа активности связывания при различных условиях pH, описанных выше. Например, антигенсвязывающую активность антигенсвязывающей молекулы сравнивают между условиями кислых значений pH и условиями нейтральных значений pH для подтверждения того, что антигенсвязывающая активность антигенсвязывающей молекулы изменяется до более высокого уровня в условиях нейтральных значений pH, чем в условиях кислых значений pH.
Для селекции и скрининга, например, фаговых частиц, экспрессирующих антигенсвязывающие молекулы, антигенсвязывающая активность которых является более высокой в условиях нейтральных значений pH, чем в условиях кислых значений pH, или их слитые полипептиды, сначала сортируют субпопуляцию фаговых частиц, связывающихся с иммобилизованными антигенами в условиях нейтральных значений pH. Затем отсортированную субпопуляцию (библиотека, содержащая фаговые частицы, экспрессирующие антигенсвязывающие молекулы или слитые полипептиды) приводят в контакт с иммобилизованными антигенами в условиях кислых значений pH. Фаговые частицы, которые не связываются с иммобилизованными антигенами в условиях кислых значений pH, сортируют и отделяют в супернатант или последующие промывочные жидкости. Условия нейтральных значений pH и условия кислых значений pH можно соответствующим образом выбирать из диапазонов, описанных выше. В неограничивающем аспекте субпопуляцию можно сортировать на основе различий между антигенсвязывающей активностью при значении pH, выбранном из диапазона от pH 4,0 до pH 6,5, и антигенсвязывающей активностью при значении pH, выбранном из диапазона от pH 6,7 до pH 10,0. В другом неограничивающем аспекте субпопуляцию можно сортировать на основе различий между антигенсвязывающей активностью при значении pH, выбранном из диапазона от pH 4,5 до pH 6,5, и антигенсвязывающей активностью при значении pH, выбранном из диапазона от pH 6,7 до pH 9,5. В альтернативном неограничивающем аспекте, субпопуляцию можно сортировать на основе различий между антигенсвязывающей активностью при значении pH, выбранном из диапазона от pH 5,0 до pH 6,5, и антигенсвязывающей активностью при значении pH, выбранном из диапазона от pH 7,0 до pH 9,0. Кроме того, субпопуляцию можно сортировать на основе различий между антигенсвязывающей активностью при значении pH, выбранном из диапазона от pH 5,5 до pH 6,5, и антигенсвязывающей активностью при значении pH, выбранном из диапазона от pH 7,0 до pH 8,0. В следующем альтернативном неограничивающем аспекте, субпопуляцию можно сортировать на основе различий между антигенсвязывающей активностью при pH в ранней эндосоме in vivo и антигенсвязывающей активностью при pH в плазме in vivo, в частности, различий между антигенсвязывающей активностью при pH 5,8 и антигенсвязывающей активностью при pH 7,4.
Способ получения антигенсвязывающей молекулы, активность связывания которой изменяется в зависимости от условий
В неограничивающем аспекте настоящего изобретения полинуклеотид, кодирующий отобранную таким образом антигенсвязывающую молекулу, активность связывания которой изменяется в зависимости от условий, выделяют, а затем встраивают в соответствующий экспрессирующий вектор. В частности, после получения каждой кДНК, кодирующей представляющую интерес вариабельную область антигенсвязывающей молекулы, кДНК расщепляют ферментами рестрикции, которые распознают участки рестрикции, встроенные на обоих концах кДНК. Предпочтительно, ферменты рестрикции распознают и расщепляют нуклеотидную последовательность, которая встречается с низкой частотой в нуклеотидных последовательностях, составляющих гены антигенсвязывающих молекул. Кроме того, предпочтительно ферменты рестрикции расщепляют участки, встроенные в них, с образованием липких концов, для встраивания в вектор одной копии расщепленного фрагмента в правильном направлении. кДНК, кодирующие вариабельную область антигенсвязывающей молекулы, расщепленные таким образом, можно встраивать в соответствующие экспрессирующие векторы с получением экспрессирующих векторов для антигенсвязывающей молекулы по настоящему изобретению. В этом случае, гены, кодирующие константную область (C-область) антитела, можно подвергать слиянию в рамке считывания с генами, кодирующими вариабельную область.
Для получения желаемой антигенсвязывающей молекулы, полинуклеотид, кодирующий антигенсвязывающую молекулу, встраивают в экспрессирующие векторы в форме, функционально связанной с последовательностями контроля. Последовательности контроля охватывают, например, энхансеры и промоторы. Также с его амино-концом можно связывать подходящую сигнальную последовательность для внеклеточной секреции экспрессируемой антигенсвязывающей молекулы. Например, в качестве сигнальной последовательности можно использовать пептид, имеющий аминокислотную последовательность MGWSCIILFLVATATGVHS (SEQ ID NO: 13). Можно присоединять любую подходящую сигнальную последовательность. Экспрессируемый полипептид расщепляется на C-конце сигнальной последовательности, и отщепленный полипептид может внеклеточно секретироваться в качестве зрелого полипептида. Подходящие клетки-хозяева можно трансформировать этими экспрессирующими векторами с получением рекомбинантных клеток, экспрессирующих полинуклеотид, кодирующий желаемую антигенсвязывающую молекулу.
Для экспрессии полинуклеотида, кодирующего антигенсвязывающую молекулу, полинуклеотид, кодирующий тяжелую цепь, и полинуклеотид, кодирующий легкую цепь, антигенсвязывающей молекулы по отдельности встраивают в различные экспрессирующие векторы. Одну и ту же клетку-хозяина можно котрансфицировать вектором, в который встроена тяжелая цепь, и вектором, в который встроена легкая цепь, и, тем самым, обеспечивать экспрессию антигенсвязывающих молекул, содержащих тяжелые и легкие цепи. Альтернативно полинуклеотиды, кодирующие тяжелую цепь и легкую цепь, можно встраивать в один экспрессирующий вектор, которым затем трансформируют клетку-хозяина (см. WO1994011523).
В данной области известны многие комбинации клеток-хозяев и экспрессирующих векторов для получения антигенсвязывающей молекулы путем переноса выделенного полинуклеотида, кодирующего антигенсвязывающую молекулу, в соответствующих хозяев. Все из этих экспрессирующих систем можно использовать для выделения антигенсвязывающей молекулы по настоящему изобретению. В случае использования эукариотических клеток в качестве клеток-хозяев, можно соответствующим образом использовать клетки животных, растений или грибов. В частности, примеры клеток-животных могут включать следующие клетки:
(1) клетки млекопитающих, такие как CHO (линия клеток яичника китайского хомячка), COS (линия клеток почки обезьяны), клетки миеломы (Sp2/O, NS0, и т.д.), BHK (линия клеток детенышей хомячка), HEK293 (линия клеток почки эмбриона человека с расщепленной ДНК аденовируса (Ad)5), клетки PER.C6 (линия клеток сетчатки эмбриона человека, трансформированных генами E1A и E1B аденовируса 5 типа (Ad5)), Hela и Vero (Current Protocols in Protein Science (май 2001 года, раздел 5.9, таблица 5.9.1));
(2) клетки земноводных, такие как ооциты Xenopus; и
(3) клетки насекомых, такие как sf9, sf21 и Tn5.
Альтернативно в данной области известны системы экспрессии генов антител с использованием клеток, происходящих из рода Nicotiana (например, Nicotiana tabacum) в качестве растительных клеток. Для трансформации клеток растений можно соответствующим образом использовать культивируемые клетки каллюса.
В качестве клеток грибов можно использовать следующие клетки:
- клетки, происходящие из дрожжей рода Saccharomyces (например, Saccharomyces cerevisiae) и рода Pichia (например, Pichia pastoris), и
- клетки, происходящие из нитчатых грибов рода Aspergillus (например, Aspergillus niger).
Также в данной области известны экспрессирующие системы для полинуклеотидов, кодирующих антигенсвязывающие молекулы, с использованием прокариотических клеток. В случае использования, например, бактериальных клеток, можно соответствующим образом использовать клетки бактерий, таких как E. coli и Bacillus subtilis. Экспрессирующие векторы, содержащие представляющий интерес полинуклеотид, кодирующий антигенсвязывающую молекулу, переносят в эти клетки путем трансформации. Трансформированные клетки культивируют in vitro, и из полученных культур трансформированных клеток можно получать желаемую антигенсвязывающую молекулу.
В дополнение к клеткам-хозяевам, для получения рекомбинантной антигенсвязывающей молекулы можно использовать трансгенных животных. В частности, желаемую антигенсвязывающую молекулу можно получать из животных, трансфицированных полинуклеотидом, кодирующим эту антигенсвязывающую молекулу. Например, полинуклеотид, кодирующий антигенсвязывающую молекулу, можно встраивать в рамке считывания в гены, кодирующие белки, специфически продуцируемые в молоке, конструируя слитые гены. В качестве белков, секретируемых в молоке, можно использовать, например, β-казеин козы и т.п. Фрагменты ДНК, содержащие слитые гены, имеющие вставку полинуклеотида, кодирующего антигенсвязывающую молекулу, инъецируют в эмбрионы козы, которые в свою очередь имплантируют самкам коз. Из молока, продуцируемого трансгенными козами (или их потомками), рожденными козами, которым имплантировали эмбрионы, можно получать желаемую антигенсвязывающую молекулу в качестве слитого белка с белком молока. Кроме того, для увеличения количества молока, содержащего желаемую антигенсвязывающую молекулу, продуцируемую трансгенными козами, трансгенным козам можно вводить гормоны (Bio/Technology (1994), 12 (7), 699-702).
В случае введения антигенсвязывающей молекулы, описанной в настоящем описании, человеку, в качестве антигенсвязывающего домена для молекулы можно соответствующим образом выбирать антигенсвязывающий домен, происходящий из генетически рекомбинантного антитела, которое сконструировано искусственным образом, например, для снижения гетероантигенности человека. Генетически рекомбинантное антитело охватывает, например, гуманизированные антитела. Эти сконструированные антитела соответствующим образом получают с использованием способа, известного в данной области.
Каждая вариабельная область антигенсвязывающей молекулы, используемая для получения антигенсвязывающего домена в антигенсвязывающей молекуле, описанной в настоящем описании, как правило, состоит из трех определяющих комплементарность областей (CDR), фланкированных четырьмя каркасными областями (FR). CDR представляют собой области, которые по существу определяют специфичность связывания антигенсвязывающей молекулы. CDR имеют разнообразные аминокислотные последовательности. С другой стороны, FR по большей части образованы аминокислотными последовательностями, которые являются высокоидентичными даже среди антигенсвязывающих молекул с различной специфичностью связывания. Таким образом, как правило, специфичность связывания определенной антигенсвязывающей молекулы можно трансплантировать в другие антигенсвязывающие молекулы путем пересадки CDR.
Гуманизированные антитела также называют реконструированными антителами человека. В частности, в данной области известно, например, гуманизированное антитело, состоящее из антитела человека, в которое пересажены CDR антитела не являющегося человеком животного (например, мыши). Также для получения гуманизированных антител известны общие подходы рекомбинации генов. В частности, например, перекрывающаяся ПЦР известна в данной области в качестве способа пересадки CDR антител мыши в FR человека. В перекрывающейся ПЦР, к праймерам для синтеза FR антител человека добавляют нуклеотидную последовательность, кодирующую каждую CDR антитела мыши, подлежащую пересадке. Праймеры получают для каждой из четырех FR. Для пересадки CDR мыши в FR человека, обычно считается преимущественным выбор FR человека, высокоидентичных FR мыши, для сохранения функций CDR. В частности, как правило, предпочтительно используют FR человека, содержащие аминокислотные последовательности, высокоидентичные аминокислотным последовательностям FR, соседних с CDR мыши, подлежащими пересадке.
Нуклеотидные последовательности, подлежащие связыванию, конструируют так, чтобы последовательности были связаны в рамке считывания друг с другом. Нуклеотидные последовательности, кодирующие FR человека, синтезируют по отдельности с использованием соответствующих им праймеров. Полученные продукты содержат ДНК, кодирующую CDR мыши, присоединенную к каждой последовательности, кодирующей FR человека. Нуклеотидные последовательности, кодирующие CDR мыши, конструируют так, чтобы нуклеотидная последовательность в каждом продукте перекрывалась с другой нуклеотидной последовательностью. Затем перекрывающиеся участки CDR в продуктах, синтезированных с генов антител человека в качестве матриц, подвергают отжигу друг с другом для реакции синтеза комплементарной цепи. С помощью этой реакции последовательности FR человека связывают через последовательности CDR мыши.
Наконец, полноразмерную последовательность гена V-области, содержащей связанные три CDR и четыре FR, амплифицируют с использованием праймеров, каждый из которых отжигается с ее 5'- и 3'-концами и имеет присоединенную последовательность распознавания для соответствующего фермента рестрикции. Полученную таким образом ДНК и ДНК, кодирующую C-область антитела человека, можно встраивать в экспрессирующие векторы, так чтобы осуществить слияние этих ДНК в рамке считывания, с получением векторов для экспрессии гуманизированного антитела. Эти векторы, имеющие вставки, переносят в хозяев, получая рекомбинантные клетки. Затем рекомбинантные клетки культивируют для экспрессии ДНК, кодирующей гуманизированное антитело, для продукции гуманизированных антител в культуры культивируемых клеток (EP239400 и WO1996002576).
Полученные таким образом гуманизированные антитела можно оценивать в отношении их антигенсвязывающей активности с помощью количественного или качественного анализа, тем самым отбирая подходящие FR антител человека, которые позволяют CDR формировать подходящий антигенсвязывающий центр, когда их связывают через эти CDR. Если необходимо, аминокислотный остаток(и) FR можно заменять так, чтобы CDR полученного реконструированного антитела человека формировали подходящий антигенсвязывающий центр. Например, в аминокислотную последовательность FR можно вносить мутацию с использованием способа ПЦР, используемого при пересадке CDR мыши в FR человека. В частности, мутацию частичной нуклеотидной последовательности можно вносить в праймеры, отжигающиеся на нуклеотидной последовательности FR. Нуклеотидная последовательность FR, синтезированная с использованием таких праймеров, содержит мутацию, внесенную таким образом. Такие варианты антител, имеющие замененную аминокислоту(ы), можно оценивать в отношении их антигенсвязывающей активности с помощью того же анализа, как описано выше, чтобы тем самым выбрать варианты последовательностей FR, имеющие желаемые свойства (Sato et al., Cancer Res (1993) 53, 851-856).
В неограничивающем аспекте настоящего изобретения модифицированную форму выделенного таким образом полинуклеотида, кодирующего выбранную антигенсвязывающую молекулу, активность связывания которой изменяется в зависимости от условий, затем встраивают в соответствующие экспрессирующие векторы. Один предпочтительный пример такой модифицированной формы включает гуманизированную форму полинуклеотидной последовательности, кодирующей антигенсвязывающую молекулу по настоящему изобретению, найденную путем скрининга с использованием, в качестве рандомизированной библиотеки вариабельных областей, синтетической библиотеки или иммунной библиотеки, полученной из не являющихся человеком животных в качестве источника. Гуманизированную форму антигенсвязывающей молекулы можно получать путем выбора способа, сходного со способом получения гуманизированного антитела, описанным выше.
В других аспектах предпочтительные примеры модифицированной формы включают модифицированные формы выделенной полинуклеотидной последовательности, которая модифицирована так, чтобы обеспечить повышение аффинности связывания антигена (созревание аффинности) антигенсвязывающей молекулы по настоящему изобретению, найденной путем скрининга с использованием синтетической библиотеки или наивной библиотеки в качестве рандомизированной библиотеки вариабельных областей. Такие модифицированные формы можно получать с помощью различных способов созревания аффинности, известных в данной области, включая мутагенез CDR (Yang et al., J. Mol. Biol. (1995) 254, 392-403), шаффлинг цепей (Marks et al., Bio/Technology (1992) 10, 779-783), использование штаммов-мутаторов E. coli (Low et al., J. Mol. Biol. (1996) 250, 359-368), шаффлинг ДНК (Patten et al., Curr. Opin. Biotechnol. (1997) 8, 724-733), фаговый дисплей (Thompson et al., J. Mol. Biol. (1996) 256, 77-88) и половую ПЦР (Clameri et al., Nature (1998) 391, 288-291).
Примеры антигенсвязывающей молекулы, полученной способом получения по настоящему изобретению, включают антигенсвязывающие молекулы, содержащие домен, связывающий FcRn (в частности, FcRn человека), как описано выше. Домен, связывающий FcRn (в частности, FcRn человека), можно использовать в различных модифицированных формах. В одном аспекте предпочтительные примеры модифицированной формы по настоящему изобретению также включают полинуклеотид, кодирующий антигенсвязывающую молекулу, имеющую тяжелую цепь, где с полинуклеотидом, кодирующим выбранную антигенсвязывающую молекулу, активность связывания которой изменяется, в зависимости от условий, связан в рамке считывания полинуклеотид, кодирующий такую модифицированную форму домена, связывающего FcRn (в частности, FcRn человека).
В неограничивающем аспекте настоящего изобретения предпочтительные примеры домена, связывающего FcRn (в частности, FcRn человека), включают константные области антител, таких как IgG1, соответствующий SEQ ID NO: 14 (AAC82527.1 с добавленным Ala на N-конце), IgG2, соответствующий SEQ ID NO: 15 (AAB59393.1 с добавленным Ala на N-конце), IgG3, соответствующий SEQ ID NO: 16 (CAA27268.1), и IgG4, соответствующий SEQ ID NO: 17 (AAB59394.1 с добавленным Ala на N-конце). Относительно длительное время удержания в плазме молекул IgG (медленное исчезновение из плазмы) обуславливается функциями FcRn, известным как рецептор спасения, для молекул IgG. Молекулы IgG, захватываемые в эндосому через пиноцитоз, связываются с FcRn, экспрессируемым в эндосоме, в кислых условиях эндосомы. Молекулы IgG, которые не связались с FcRn, удаляются в лизосому и деградируются в ней, в то время как связанные с FcRn молекулы IgG мигрируют к клеточной поверхности и диссоциируют от FcRn в нейтральных условиях в плазме, возвращаясь в плазму.
“Антигенсвязывающая молекула, антигенсвязывающая активность которой изменяется в зависимости от условий концентрации ионов кальция” по настоящему изобретению прочно ассоциирована с антигеном в условиях высокой концентрации кальция в плазме и диссоциирует от антигена в условиях низкой концентрации ионов кальция в эндосоме. Таким образом, эта антигенсвязывающая молекула может диссоциировать от антигена в эндосоме. Таким образом, “антигенсвязывающая молекула, антигенсвязывающая активность который изменяется в зависимости от условий концентрации ионов кальция”, по настоящему изобретению, которая прочно ассоциирована с антигеном в условиях высокой концентрации кальция в плазме и диссоциирует от антигена в условиях низкой концентрации ионов кальция в эндосоме, диссоциирует от антигена и может вновь ассоциировать с антигеном после рециклирования в плазму с помощью FcRn. Это позволяет одной молекуле антигенсвязывающей молекулы связываться с множеством антигенов многократно. Также антиген, связанный с антигенсвязывающей молекулой, диссоциирует от нее в эндосоме и, таким образом, не рециклирует в плазму. Это обеспечивает клеточный захват антигенов антигенсвязывающей молекулой. Введение антигенсвязывающей молекулы может ускорять исчезновение антигена и снижать концентрацию антигена в плазме.
“Антигенсвязывающая молекула, антигенсвязывающая активность которой изменяется в зависимости от условий pH” по настоящему изобретению, прочно ассоциирована с антигеном в условиях нейтральных значений pH в плазме и диссоциирует от антигена в кислых условиях в эндосоме. Таким образом, эта антигенсвязывающая молекула может диссоциировать от антигена в эндосоме. “Антигенсвязывающая молекула, антигенсвязывающая активность которой изменяется в зависимости от условий pH” по настоящему изобретению, которая прочно ассоциирована с антигеном в условиях нейтральных значений pH в плазме и диссоциирует от антигена в кислых условиях в эндосоме, таким образом, диссоциирует от антигена и может вновь ассоциировать с антигеном после рециклирования в плазму с помощью FcRn. Это позволяет одной молекуле антигенсвязывающей молекулы связываться с множеством антигенов многократно. Также антиген, связанный с антигенсвязывающей молекулой, диссоциирует от нее в эндосоме и, таким образом, не рециклирует в плазму. Это обеспечивает клеточный захват антигенов антигенсвязывающей молекулой. Введение антигенсвязывающей молекулы может ускорять исчезновение антигена и снижать концентрацию антигена в плазме.
Способность связываться с FcRn в условиях высокой концентрации кальция в плазме может быть сообщена “антигенсвязывающей молекуле, антигенсвязывающая активность которой изменяется в зависимости от условий концентрации ионов кальция” по настоящему изобретению, которая прочно ассоциирована с антигеном в условиях высокой концентрации кальция в плазме и диссоциирует от антигена в условиях низкой концентрации ионов кальция в эндосоме. Это обеспечивает клеточный захват комплекса антигенсвязывающей молекулы и антигена. Таким образом, введение антигенсвязывающей молекулы может ускорить исчезновение антигена из плазмы и снизить концентрацию антигена в плазме.
Способность связываться с FcRn в условиях нейтральных значений pH в плазме можно сообщать “антигенсвязывающей молекуле, антигенсвязывающая активность которой изменяется в зависимости от условий pH” по настоящему изобретению, которая прочно ассоциирована с антигеном в условиях нейтральных значений pH в плазме и диссоциирует от антигена в условиях кислых значений pH в эндосоме. Это ускоряет клеточный захват комплекса антигенсвязывающей молекулы и антигена. Таким образом, введение антигенсвязывающей молекулы может ускорить исчезновение антигена из плазмы и снизить концентрацию антигена в плазме.
Обычное антитело, содержащее Fc-область, не обладает активностью связывания FcRn в условиях нейтральных значений pH в плазме. Обычное антитело и комплекс антитело-антиген, таким образом, захватываются в клетки через неспецифический эндоцитоз и транспортируются на клеточную поверхность путем связывания с FcRn в условиях кислых значений pH в эндосоме. Поскольку FcRn ответственен за транспорт антитела из эндосомы на клеточную поверхность, считается, что некоторые рецепторы FcRn также существуют на клеточной поверхности. Антитело диссоциирует от FcRn в условиях нейтральных значений pH на клеточной поверхности и, таким образом, рециклирует в плазму.
Учитывая кинетику in vivo антитела, содержащего Fc-область (FcRn-связывающий домен), “антигенсвязывающая молекула, антигенсвязывающая активность которой изменяется в зависимости от условий концентрации ионов кальция” по настоящему изобретению, которая прочно ассоциирована с антигеном в условиях высокой концентрации кальция в плазме и диссоциирует от антигена в условиях низкой концентрации ионов кальция в эндосоме, ассоциирует с антигеном в плазме и диссоциирует от связанного антигена в эндосоме. Таким образом, скорость исчезновения антигена считается равной скорости клеточного захвата через неспецифический эндоцитоз. В случае недостаточной зависимости связывания антигена антигенсвязывающей молекулой от концентрации ионов кальция, антигены, не диссоциировавшие в эндосоме, рециклируют в плазму. Напротив, в случае достаточной зависимости связывания антигена антигенсвязывающей молекулой от концентрации ионов кальция, скорость исчезновения антигена определяется скоростью клеточного захвата через неспецифический эндоцитоз.
“Антигенсвязывающая молекула, антигенсвязывающая активность которой изменяется в зависимости от условий pH” по настоящему изобретению, которая прочно ассоциирована с антигеном в условиях нейтральных значений pH в плазме и диссоциирует от антигена в условиях кислых значений pH в эндосоме, ассоциирует с антигеном в плазме и диссоциирует от связанного антигена в эндосоме. Таким образом, скорость исчезновения антигена считается равной скорости клеточного захвата через неспецифический эндоцитоз. В случае недостаточной зависимости от pH связывания антигена антигенсвязывающей молекулой, антигены, не диссоциировавшие в эндосоме, рециклируют в плазму. Напротив, в случае достаточной зависимости от pH связывания антигена антигенсвязывающей молекулой, скорость исчезновения антигена определяется скоростью клеточного захвата через неспецифический эндоцитоз.
Таким образом, антигенсвязывающей молекуле, содержащей FcRn-связывающий домен, можно сообщать способность связывания с FcRn при нейтральных значениях pH. Полученная антигенсвязывающая молекула захватывается в клетки зависимым от FcRn образом через связывание с FcRn, присутствующим на клеточной поверхности. Скорость опосредуемого FcRn клеточного захвата является более высокой, чем скорость клеточного захвата через неспецифический эндоцитоз. В этом отношении, сообщение способности связываться с FcRn при нейтральных значениях pH может далее увеличить скорость исчезновения антигена из плазмы. В частности, антигенсвязывающая молекула, обладающая способностью связываться с FcRn при нейтральных значениях pH, доставляет антиген быстрее в клетки, чем обычная антигенсвязывающая молекула, содержащая Fc-область (не обладающая активностью связывания FcRn в условиях нейтральных значений pH в плазме) и диссоциирует от антигена в эндосоме. Диссоциировавшая антигенсвязывающая молекула рециклирует на клеточную поверхность или в плазму, где молекула вновь ассоциирует с антигеном, что вновь приводит к опосредуемому FcRn клеточному захвату. Более высокая способность связываться с FcRn при нейтральных значениях pH может увеличивать скорость оборота указанного цикла и, таким образом, увеличить скорость исчезновения антигена из плазмы. Антигенсвязывающая активность антигенсвязывающей молекулы при кислых значениях pH может быть снижена относительно антигенсвязывающей активности при нейтральных значениях pH, тем самым далее усиливая эффективность. Увеличенное количество оборотов указанного цикла на антигенсвязывающую молекулу, возможно, позволит одной антигенсвязывающей молекуле связаться с более высоким количеством антигенов.
Антигенсвязывающая молекула по настоящему изобретению может содержать антигенсвязывающий домен и домен, связывающий FcRn (в частности, FcRn человека). FcRn-связывающий домен ни влияет на связывание антигена, ни зависит от типа антигена, как также понятно из механизма, упомянутого выше. Антигенсвязывающая активность (способность связывания) антигенсвязывающей молекулы в условиях низкой концентрации ионов кальция является сниженной относительно антигенсвязывающей активности в условиях высокой концентрации ионов кальция, и/или активность связывания FcRn этой молекулы при нейтральных значениях pH в плазме является увеличенной. Это может ускорить клеточный захват антигенов антигенсвязывающей молекулой и ускорить скорость исчезновения антигенов.
Как описано выше, антигенсвязывающая молекула по настоящему изобретению может содержать антигенсвязывающий домен и FcRn-связывающий домен, который ни влияет на связывание антигена, ни зависит от типа антигена, как также понятно из механизма, упомянутого выше. Антигенсвязывающая активность (способность связывания) антигенсвязывающей молекулы в условиях кислых значений pH является сниженной относительно антигенсвязывающей активности в условиях нейтральных значений pH, и/или активность связывания FcRn этой молекулы при нейтральных значениях pH в плазме является увеличенной. Это может ускорить клеточный захват антигенов антигенсвязывающей молекулой и ускорить скорость исчезновения антигенов.
Активность связывания FcRn FcRn-связывающего домена (например, константная область антитела) можно анализировать способом, общеизвестным специалистам в данной области, как упоминалось выше в абзаце об активности связывания. Условия, отличные от pH, могут соответствующим образом определять специалисты в данной области. Антигенсвязывающая активность и активность связывания FcRn человека антигенсвязывающей молекулы можно оценивать, например, на основе KD (константа диссоциации), кажущейся KD (кажущаяся константа диссоциации), kd (скорость диссоциации), или кажущейся kd (кажущаяся скорость диссоциации). Эти показатели можно измерять способом, общеизвестным специалистам в данной области, например, с использованием Biacore (GE Healthcare Bio-Sciences Corp.), графика Скэтчарда или проточного цитометра.
Условия, отличные от pH, для анализа активности связывания FcRn человека FcRn-связывающего домена (например, константная область антитела), могут быть соответствующим образом выбраны специалистами в данной области без конкретных ограничений. Активность связывания FcRn человека можно анализировать в условиях, например, буфера MES и 37°C, как описано в WO2009125825. Также активность связывания FcRn человека FcRn-связывающего домена (например, константная область антитела) можно анализировать способом, общеизвестным специалистам в данной области, например, с использованием Biacore (GE Healthcare Bio-Sciences Corp.). В анализе активности связывания FcRn человека, FcRn-связывающий домен (например, константная область антитело) можно оценивать в отношении его связывающей способности путем инжекции анализируемого FcRn человека на чип с иммобилизованным FcRn-связывающим доменом или антигенсвязывающей молекулой по настоящему изобретению, содержащей FcRn-связывающий домен, или путем инжекции анализируемого FcRn-связывающего домена или антигенсвязывающей молекулы по настоящему изобретению, содержащей FcRn-связывающий домен, на чип с иммобилизованным FcRn человека.
Нейтральные значения pH в качестве условий, в которых FcRn-связывающий домен (например, константная область антитела) или антигенсвязывающая молекула, содержащая FcRn-связывающий домен, имеют активность связывания FcRn, обычно означают условия от pH 6,7 до pH 10,0. Нейтральное значение pH предпочтительно представляет собой диапазон, указываемый с помощью любой величины pH от pH 7,0 до pH 8,0 и предпочтительно оно выбрано из pH 7,0, 7,1, 7,2, 7,3, 7,4, 7,5, 7,6, 7,7, 7,8, 7,9 и 8,0, особенно предпочтительно pH 7,4, которое является близким к pH в плазме (крови) in vivo. Аффинность связывания FcRn-связывающего домена человека в отношении FcRn человека при pH 7,4 может быть трудно оценить вследствие его низкой аффинности связывания. В таком случае, вместо pH 7,4 можно использовать pH 7,0. В рамках настоящего изобретения кислое значение pH в качестве условий, в которых FcRn-связывающий домен человека или антигенсвязывающая молекула, содержащая FcRn-связывающий домен человека, имеют активность связывания FcRn, обычно означает от pH 4,0 до pH 6,5. Кислое значение pH предпочтительно означает от pH 5,5 до pH 6,5 и особенно предпочтительно означает от pH 5,8 до pH 6,0, которые являются близкими к pH в ранней эндосоме in vivo. Температура, используемая в условиях анализа, может представлять собой любую температуру от 10°C до 50°C, при которой FcRn-связывающий домен человека или антигенсвязывающую молекулу, содержащую FcRn-связывающий домен человека, оценивают в отношении их аффинности связывания FcRn человека. Предпочтительно, для определения аффинности связывания FcRn человека FcRn-связывающего домена человека или антигенсвязывающей молекулы, содержащей FcRn-связывающий домен человека, используют температуру от 15°C до 40°C. Более предпочтительно, также для определения аффинности связывания FcRn человека FcRn-связывающего домена человека или антигенсвязывающей молекулы, содержащей FcRn-связывающий домен человека, используют любую температуру от 20°C до 35°C, например, любую из температур 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34 и 35°C. В одном аспекте настоящего изобретения одним неограничивающим примером является температура 25°C.
Согласно Journal of Immunology (2009) 182: 7663-7671, активность связывания природного IgG1 человека с FcRn человека в кислом диапазоне pH (pH 6,0) составляет KD 1,7 мкМ, однако эта активность практически не поддается выявлению при нейтральных значениях pH. Таким образом, в предпочтительном аспекте, можно проводить скрининг антигенсвязывающей молекулы по настоящему изобретению, обладающей активностью связывания FcRn человека при кислых значениях pH и при нейтральных значениях pH, которая включает антигенсвязывающую молекулу, имеющую активность связывания FcRn человека, составляющую KD 20 мкМ или сильнее при кислых значениях pH и активность связывания FcRn человека, эквивалентную или более сильную, чем активность связывания активность FcRn человека у природного IgG при нейтральных значениях pH. В более предпочтительном аспекте, можно проводить скрининг антигенсвязывающей молекулы, обладающей активностью связывания FcRn человека, составляющей KD 2,0 мкМ или сильнее, при кислых значениях pH, и активностью связывания FcRn человека, составляющей KD 40 мкМ или сильнее, при нейтральных значениях pH. В следующем предпочтительном аспекте можно проводить скрининг антигенсвязывающей молекулы, обладающей активностью связывания FcRn человека, составляющей KD 0,5 мкМ или сильнее, при кислых значениях pH и активностью связывания FcRn человека, составляющей KD 15 мкМ или сильнее, при нейтральных значениях pH. Эти величины KD определяют способом, описанным в The Journal of Immunology (2009) 182: 7663-7671 (который вовлекает иммобилизацию антигенсвязывающих молекул на чип и инжекцию на него FcRn человека в качестве анализируемого соединения).
В рамках настоящего изобретения FcRn-связывающий домен предпочтительно обладает активностью связывания FcRn человека при кислых значениях pH и при нейтральных значениях pH. FcRn-связывающий домен, естественным образом обладающий активностью связывания FcRn человека при кислых значениях pH и при нейтральных значениях pH, можно прямо использовать в качестве домена. Когда домен не имеет или имеет слабую активность связывания FcRn человека при кислых значениях pH и/или при нейтральных значениях pH, аминокислоту(ы) в антигенсвязывающей молекуле можно модифицировать для получения FcRn-связывающего домена, обладающего желаемой активностью связывания FcRn человека. Альтернативно аминокислоту(ы) в FcRn-связывающем домене человека можно предпочтительно модифицировать для получения FcRn-связывающего домена, обладающего желаемой активностью связывания FcRn человека при кислых значениях pH и/или при нейтральных значениях pH. Также, аминокислоту(ы) в FcRn-связывающем домене, природным образом имеющем активность связывания FcRn человека при кислых значениях pH и/или при нейтральных значениях pH, можно модифицировать для получения FcRn-связывающего домена, обладающего желаемой активностью связывания FcRn человека. Такая аминокислотная модификация, которая сообщает желаемую активность связывания FcRn-связывающему домену человека, может быть выявлена путем сравнения активности связывания FcRn человека при кислых значениях pH и/или при нейтральных значениях pH до и после модификации аминокислоты. Специалисты в данной области могут соответствующим образом проводить аминокислотную модификацию с использованием подхода, известного в данной области.
В рамках настоящего изобретения термин “модификация аминокислоты(аминокислот)” или “аминокислотная модификация” в FcRn-связывающем домене включает модификацию в аминокислотную последовательность, отличную от аминокислотной последовательности исходного FcRn-связывающего домена. В качестве исходного домена можно использовать любой FcRn-связывающий домен при условии, что полученная модифицированная форма исходного FcRn-связывающего домена может связываться с FcRn человека при кислых значениях pH и/или при нейтральных значениях pH (таким образом, не обязательно требуется, чтобы исходный FcRn-связывающий домен имел активность связывания FcRn человека в условия кислых значений pH и/или нейтральных значений pH). Предпочтительные примеры исходного FcRn-связывающего домена включают константные области IgG-антител, т.е. природные константные области, соответствующие любой из SEQ ID NO: 14-17. Альтернативно, в качестве модифицированного FcRn-связывающего домена по настоящему изобретению предпочтительно можно использовать FcRn-связывающий домен, дополнительно модифицированный из уже модифицированного FcRn-связывающего домена в качестве исходного FcRn-связывающего домена. Исходный FcRn-связывающий домен может означать сам полипептид, композицию, содержащую исходный FcRn-связывающий домен, или аминокислотную последовательность, кодирующую исходный FcRn-связывающий домен. Исходный FcRn-связывающий домен может включать FcRn-связывающие домены IgG-антител, известные в данной области, получаемые путем рекомбинации, рассмотренной в абзаце, касающемся антитела. Исходный FcRn-связывающий домен не ограничивается по его происхождению, и он может быть получен из произвольного не являющегося человеком организма животного или человека. Предпочтительные примеры произвольного организма включают организм, выбранный из мышей, крыс, морских свинок, хомяков, песчанок, кошек, кроликов, собак, коз, овец, крупного рогатого скота, лошадей, верблюдов и не являющихся человеком приматов. В другом аспекте исходный FcRn-связывающий домен можно получать из яванского макака, мартышки, макака-резус, шимпанзе или человека. Предпочтительно, исходную Fc-область можно получать из IgG1 человека, хотя исходный FcRn-связывающий домен по настоящему изобретению не ограничивается конкретным классом IgG. Это означает, что в качестве исходной Fc-области можно использовать Fc-область IgG1, IgG2, IgG3 или IgG4 человека. В Sequences of Proteins of Immunological interest, NIH Publication No. 91-3242, описано множество аллотипических последовательностей, присущих полиморфизму, в качестве Fc-областей IgG1 человека, IgG2 человека, IgG3 человека и IgG4 человека, любую из которых можно использовать в рамках настоящего изобретения. В частности, IgG1 человека может иметь последовательность с DEL или EEM в качестве аминокислотной последовательности в положениях 356-358, определяемых посредством нумерации EU. Аналогично, в рамках настоящего изобретения это означает, что в качестве исходного FcRn-связывающего домена предпочтительно можно использовать FcRn-связывающий домен произвольного класса или подкласса IgG из произвольного организма. Примеры вариантов встречающихся в природе IgG или их подвергнутых манипулированию форм описаны в общедоступной литературе (Curr. Opin. Biotechnol. (2009) 20 (6), 685-91; Curr. Opin. Immunol. (2008) 20 (4), 460-470; Protein Eng. Des. Sel. (2010) 23 (4), 195-202; WO2009086320, WO2008092117, WO2007041635 и WO2006105338), хотя варианты или подвергнутые манипулированию формы по настоящему изобретению не ограничиваются вариантами, описанными в указанных документах.
В аминокислоту(ы) в FcRn-связывающем домене, вовлеченную в связывание FcRn, соответствующим образом вносят мутации для сообщения способности связывания с FcRn (в частности, FcRn человека) при нейтральных значениях pH антигенсвязывающей молекуле, содержащей домен, связывающий FcRn (в частности, FcRn человека). В случае использования константной области молекулы IgG-антитела в качестве FcRn-связывающего домена, примеры такого модифицированного FcRn-связывающего домена включают константные области, происходящие из природных константных областей IgG, путем модификации аминокислот в положениях 221-225, 227, 228, 230, 232, 233-241, 243-252, 254-260, 262-272, 274, 276, 278-289, 291-312, 315-320, 324, 325, 327-339, 341, 343, 345, 360, 362, 370, 375-378, 380, 382, 385-387, 389, 396, 414, 416, 423, 424, 426-438, 440 и 442, определяемых посредством нумерации EU, на аминокислоты, отличающиеся от соответствующих встречающихся в природе аминокислот. Более конкретно, их примеры включают модифицированные формы константных областей, содержащие Pro в положении аминокислоты 256, Lys в положении аминокислоты 280, Thr в положении аминокислоты 339, His в положении аминокислоты 385, Leu в положении аминокислоты 428, и/или Trp, Tyr, Phe, Ala или His в положении аминокислоты 434 (все определены посредством нумерации EU). Использование этих модифицированных форм может усилить активность Fc-области IgG-иммуноглобулина в отношении связывания FcRn человека при нейтральных значениях pH.
Альтернативно, можно соответствующим образом использовать модифицированную форму, способную связываться с FcRn человека более сильно при кислых значениях pH, чем у константной области природного IgG. Такую модифицированную форму можно соответствующим образом выбирать, исходя из ее способности также сильно связываться с FcRn человека при нейтральных значениях pH, и использовать в рамках настоящего изобретения. Примеры такой модифицированной формы включают константные области, образованные из константных областей природного IgG, путем модификации аминокислот, определяемых посредством нумерации EU, на аминокислоты, отличные от соответствующих встречающихся в природе аминокислот. В качестве примера такой аминокислотной модификации, предпочтительно можно использовать модифицированные константные области, содержащие аминокислоты, приведенные в таблице 1.

Примеры особенно предпочтительной аминокислотной модификации включают модификацию, которая заменяет аминокислоты в положениях 237, 238, 239, 248, 250, 252, 254, 255, 256, 257, 258, 265, 270, 286, 289, 297, 298, 303, 305, 307, 308, 309, 311, 312, 314, 315, 317, 325, 332, 334, 360, 376, 380, 382, 384, 385, 386, 387, 389, 424, 428, 433, 434 и 436, определяемых посредством нумерации EU, аминокислотами, отличающимися от соответствующих аминокислот в константной области природного IgG. По меньшей мере одну аминокислоту, выбранную из этих аминокислот, можно модифицировать в другую аминокислоту, тем самым усиливая активность FcRn-связывающего домена в отношении связывания FcRn человека при нейтральных значениях pH.
Примеры особенно предпочтительной модификации включают модификацию константной области природного IgG, которая приводит к:
Met в положении аминокислоты 237,
Ala в положении аминокислоты 238,
Lys в положении аминокислоты 239,
Ile в положении аминокислоты 248,
Ala, Phe, Ile, Met, Gln, Ser, Val, Trp или Tyr в положении аминокислоты 250,
Phe, Trp или Tyr в положении аминокислоты 252,
Thr в положении аминокислоты 254,
Glu в положении аминокислоты 255,
Asp, Glu или Gln в положении аминокислоты 256,
Ala, Gly, Ile, Leu, Met, Asn, Ser, Thr или Val в положении аминокислоты 257,
His в положении аминокислоты 258,
Ala в положении аминокислоты 265,
Phe в положении аминокислоты 270,
Ala или Glu в положении аминокислоты 286,
His в положении аминокислоты 289,
Ala в положении аминокислоты 297,
Gly в положении аминокислоты 298,
Ala в положении аминокислоты 303,
Ala в положении аминокислоты 305,
Ala, Asp, Phe, Gly, His, Ile, Lys, Leu, Met, Asn, Pro, Gln, Arg, Ser, Val, Trp или Tyr в положении аминокислоты 307,
Ala, Phe, Ile, Leu, Met, Pro, Gln или Thr в положении аминокислоты 308,
Ala, Asp, Glu, Pro или Arg в положении аминокислоты 309,
Ala, His, или Ile в положении аминокислоты 311,
Ala или His в положении аминокислоты 312,
Lys или Arg в положении аминокислоты 314,
Ala или His в положении аминокислоты 315,
Ala в положении аминокислоты 317,
Gly в положении аминокислоты 325,
Val в положении аминокислоты 332,
Leu в положении аминокислоты 334,
His в положении аминокислоты 360,
Ala в положении аминокислоты 376,
Ala в положении аминокислоты 380,
Ala в положении аминокислоты 382,
Ala в положении аминокислоты 384,
Asp или His в положении аминокислоты 385,
Pro в положении аминокислоты 386,
Glu в положении аминокислоты 387,
Ala или Ser в положении аминокислоты 389,
Ala в положении аминокислоты 424,
Ala, Asp, Phe, Gly, His, Ile, Lys, Leu, Asn, Pro, Gln, Ser, Thr, Val, Trp или Tyr в положении аминокислоты 428,
Lys в положении аминокислоты 433,
Ala, Phe, His, Ser, Trp или Tyr в положении аминокислоты 434, и
His в положении аминокислоты 436
(все определяются посредством нумерации EU).
Количество аминокислот, подлежащих модификации, конкретно не ограничено. Может быть модифицирована только одна аминокислота, или могут быть модифицированы две или более аминокислот. Примеры комбинации двух или более аминокислот, подлежащих модификации, включают комбинации, как показано в таблице 2.





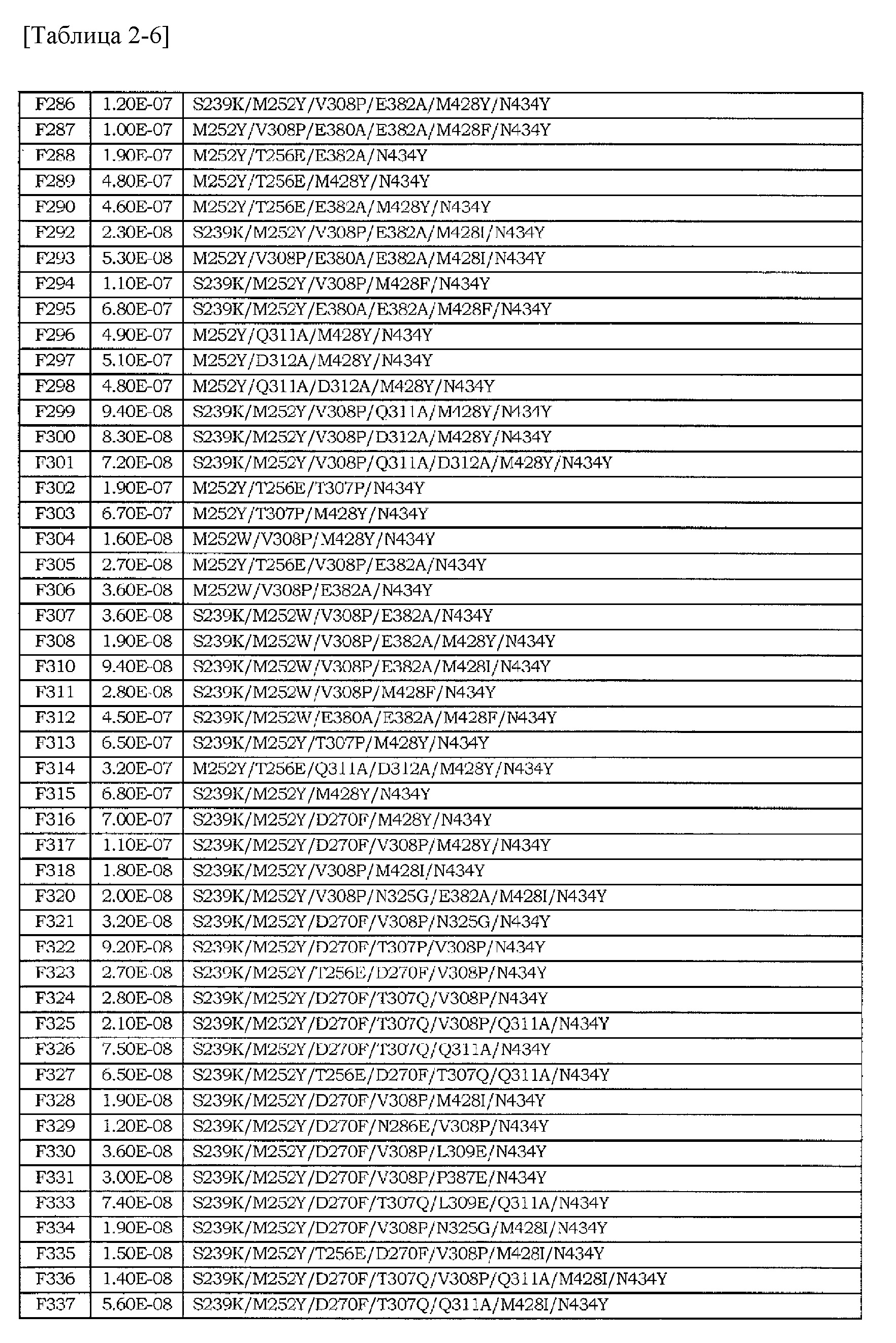

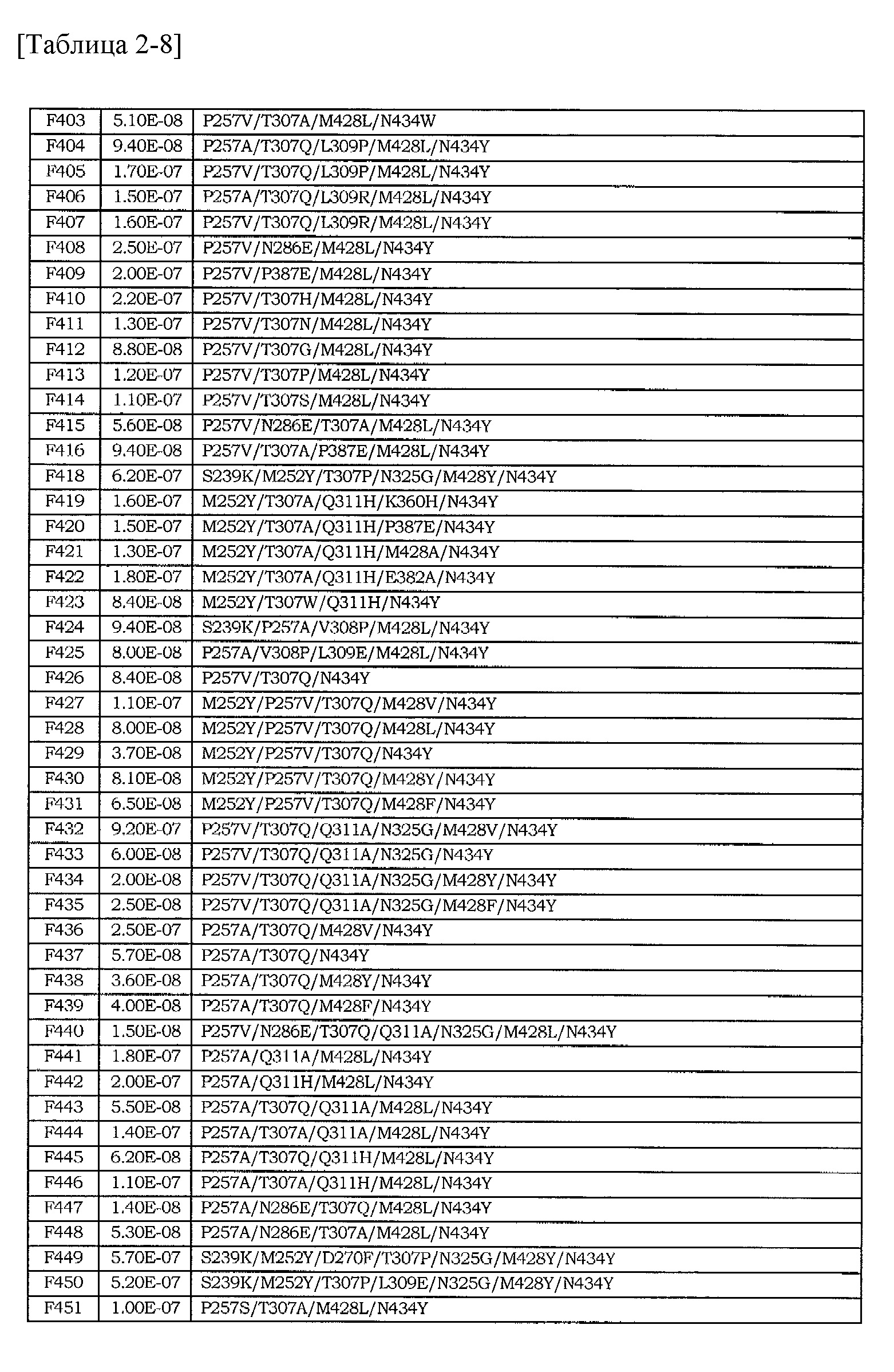


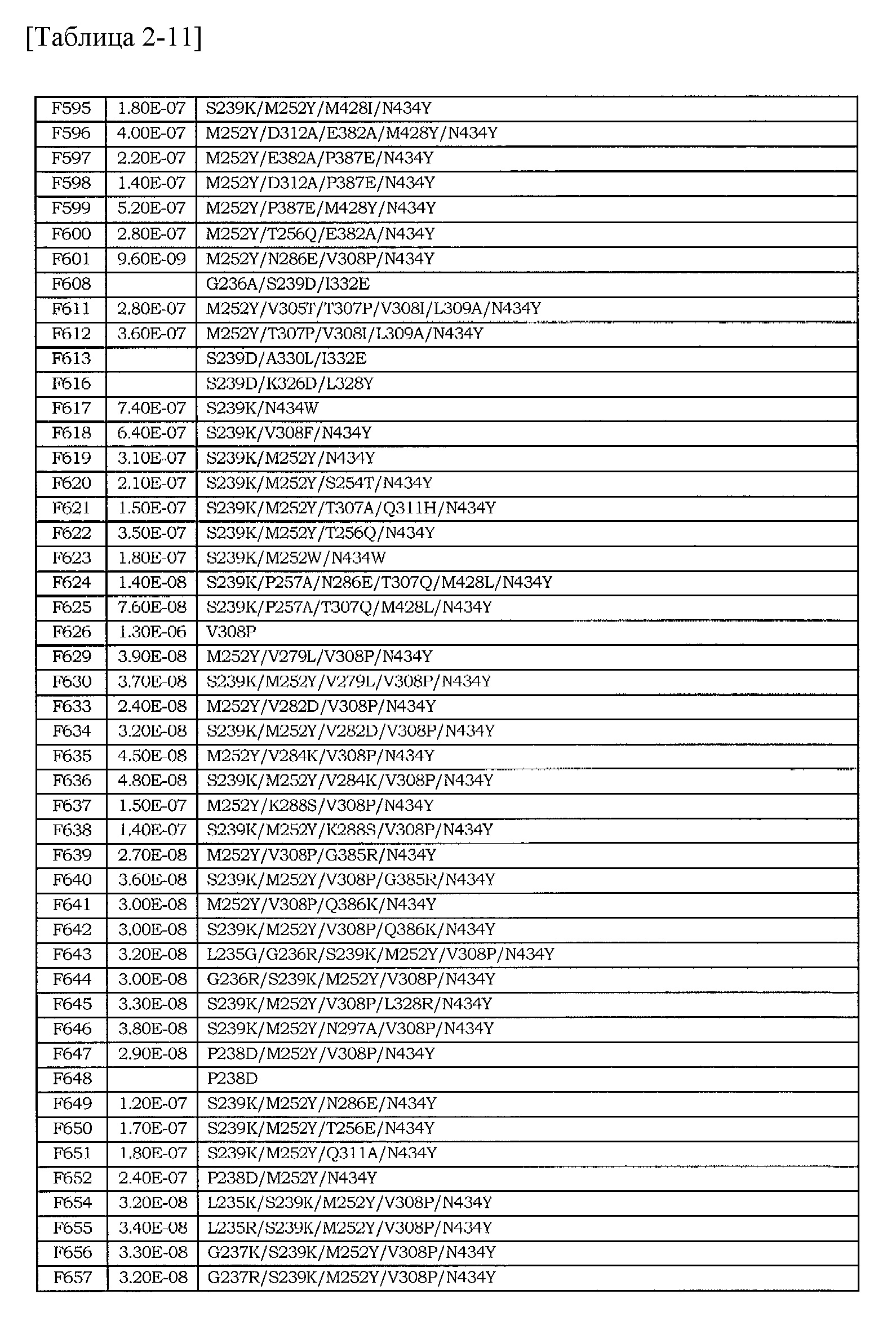


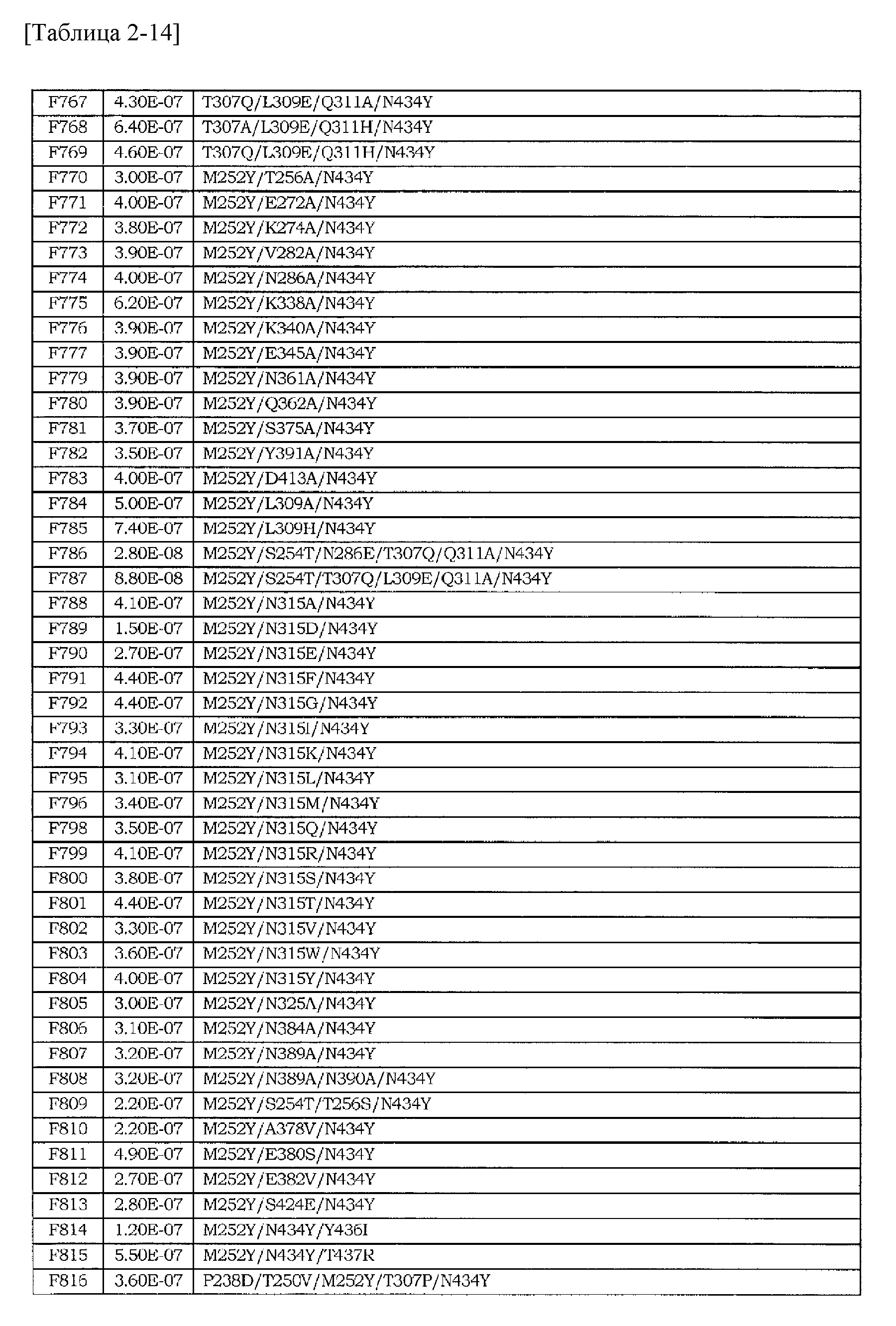
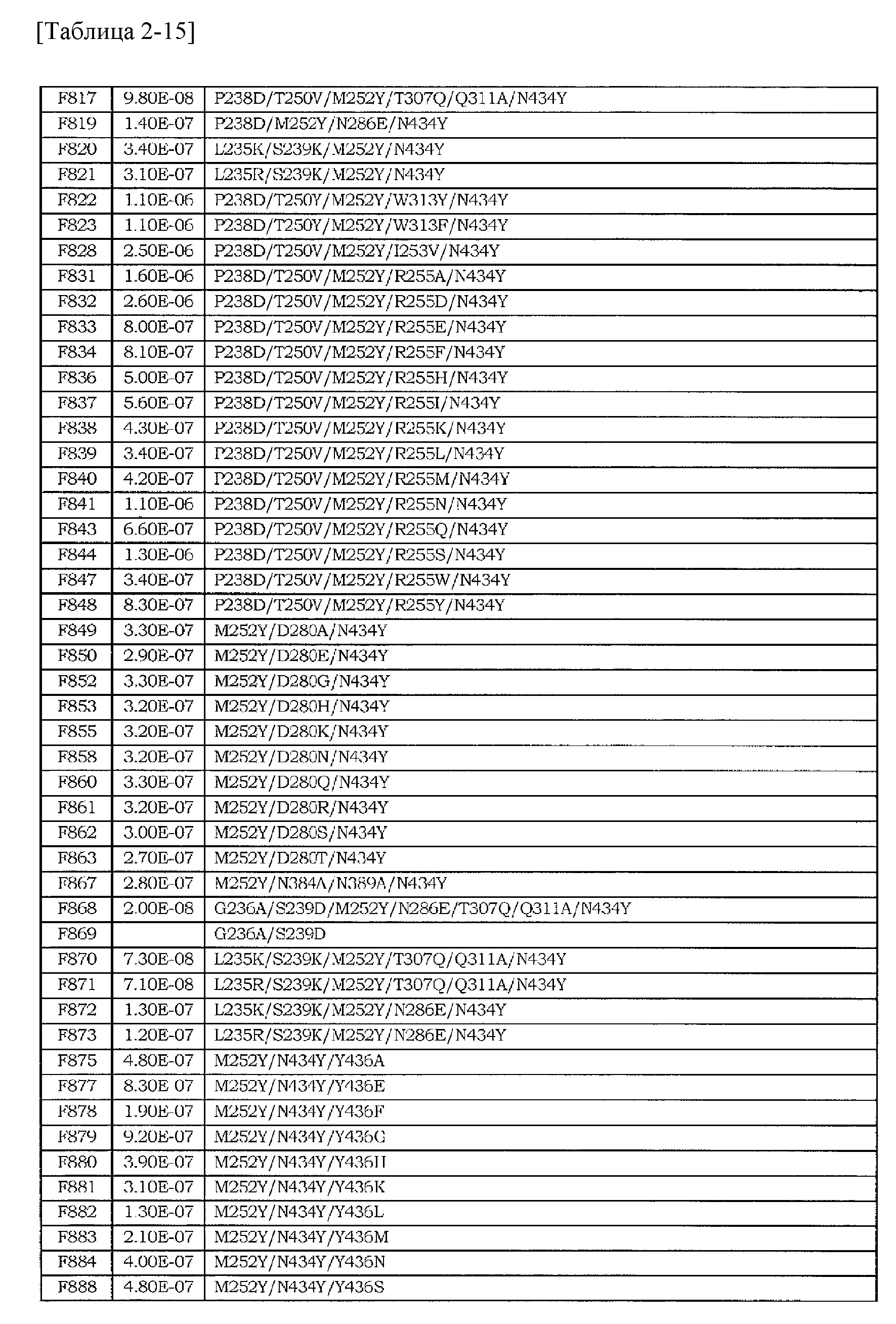


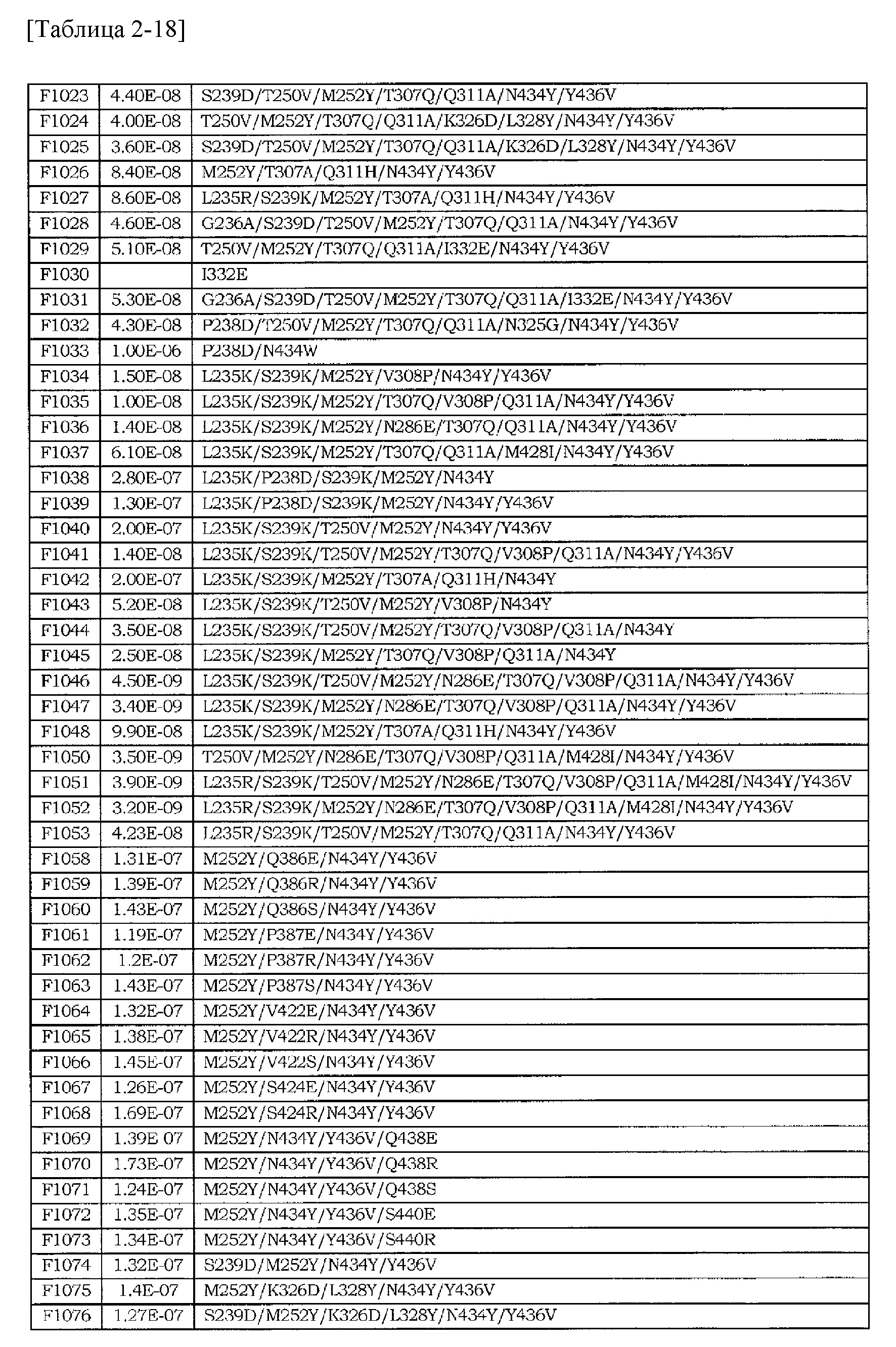
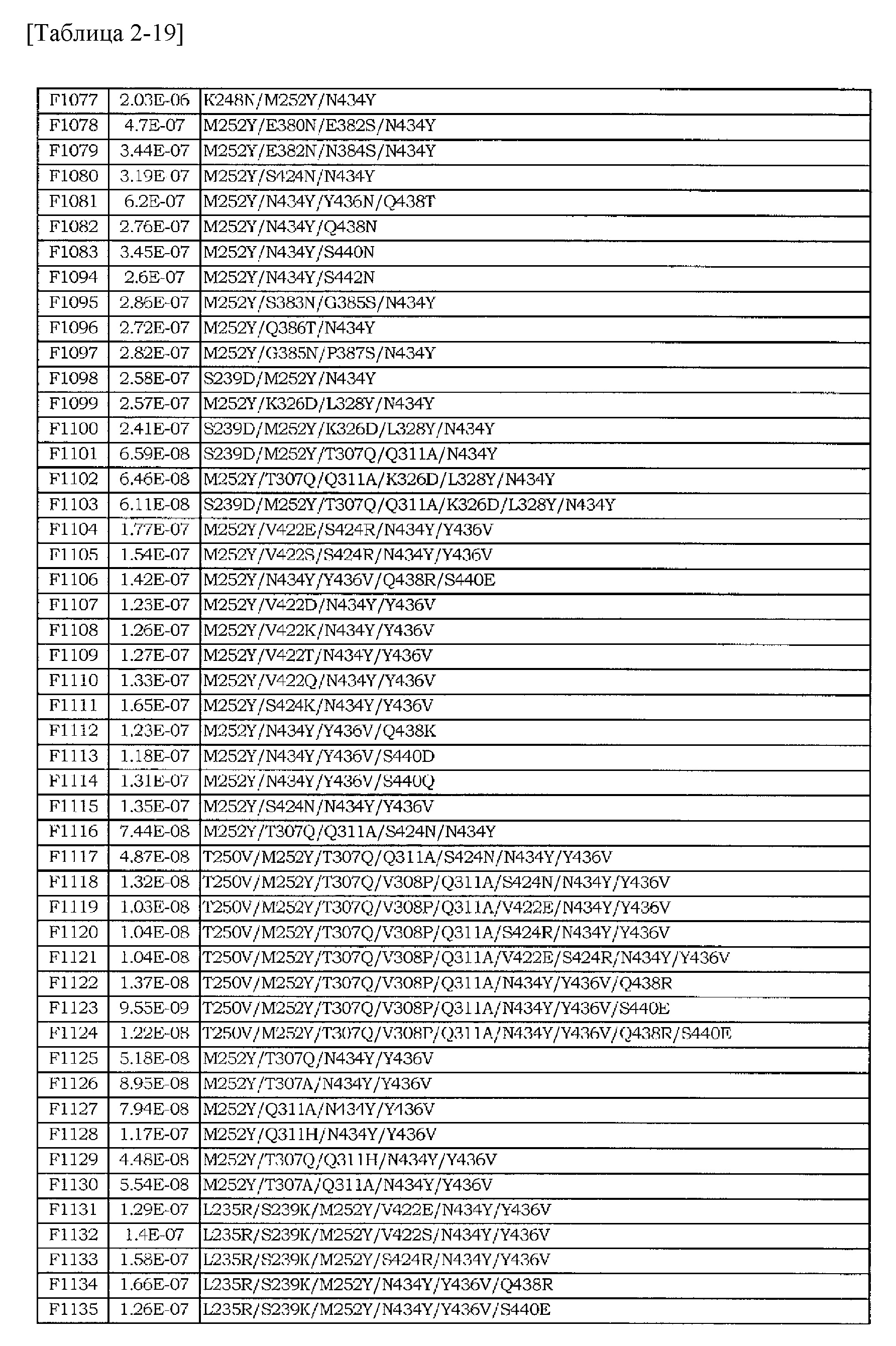






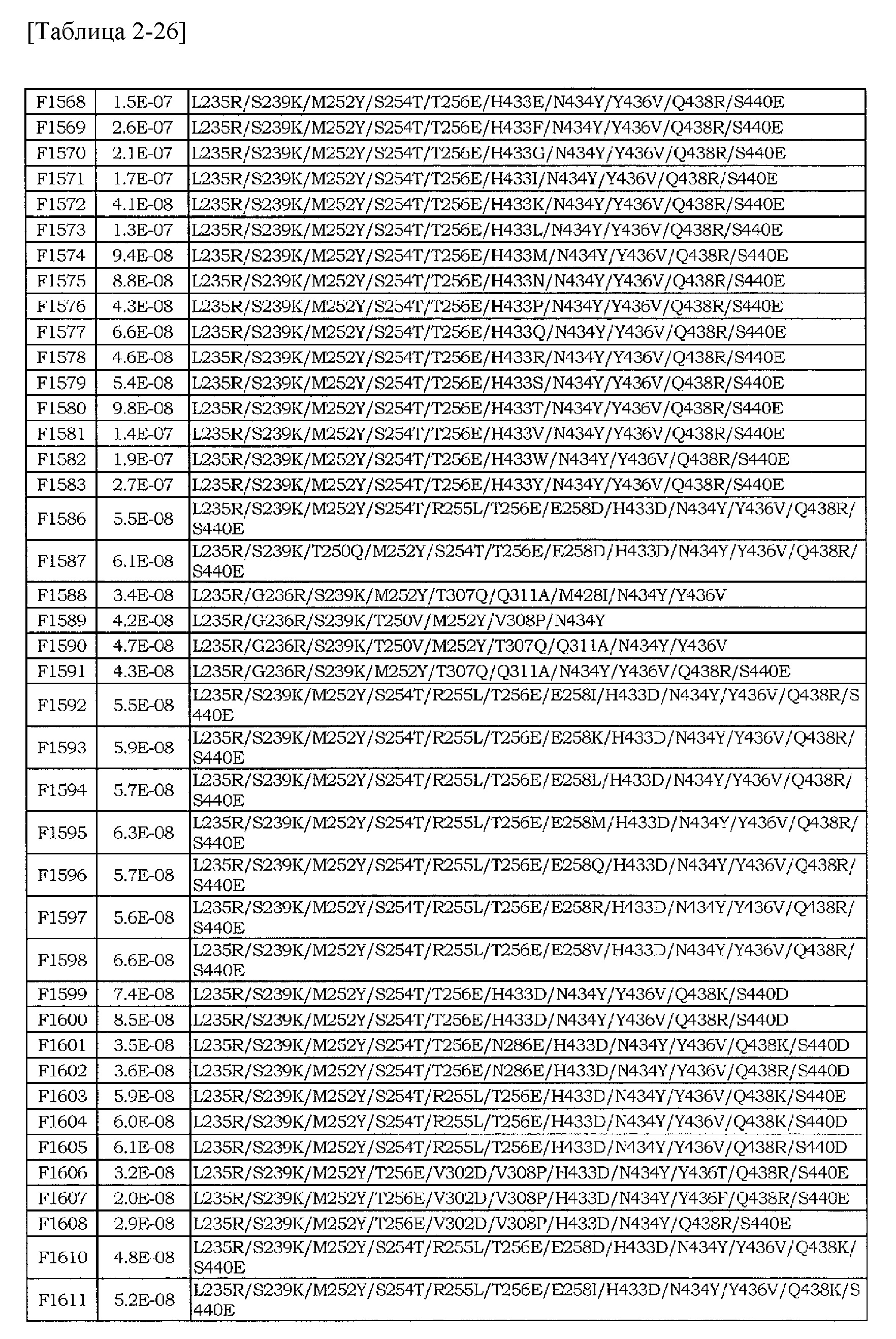



Примеры модификации включают одну или более мутаций, например, мутацию, которая заменяет аминокислоту(ы) в исходной Fc-области, на аминокислотный остаток(остатки), отличающийся от нее, инсерцию одного или более аминокислотных остатков в аминокислотную последовательность исходной Fc-области, и делецию одной или более аминокислот из аминокислотной последовательности исходной Fc-области. Предпочтительно, аминокислотная последовательность Fc-области, модифицированной таким образом, содержит аминокислотную последовательность, содержащую по меньшей мере неприродную часть Fc-области. Такой вариант неизбежно имеет менее чем 100% идентичность последовательности с исходной Fc-областью. В предпочтительном варианте осуществления вариант имеет аминокислотную последовательность с приблизительно от 75% до менее чем 100% идентичностью или сходством последовательностей, более предпочтительно с приблизительно от 80% до менее чем 100%, еще более предпочтительно с приблизительно от 85% до менее чем 100%, еще более предпочтительно с приблизительно от 90% до менее чем 100%, наиболее предпочтительно с приблизительно от 95% до менее чем 100% идентичностью или сходством последовательности с аминокислотной последовательностью исходной Fc-области. В неограничивающем аспекте настоящего изобретения исходная Fc-область и модифицированная Fc-область по настоящему изобретению отличаются по меньшей мере одной аминокислотой. Отличие аминокислоты между исходной Fc-областью и модифицированной Fc-областью предпочтительно может определяться отличием аминокислоты в указанном положении ее аминокислотного остатка, определяемом, в частности, посредством системы нумерации EU.
Аминокислоту(ы) в Fc-области можно модифицировать с помощью соответствующим образом выбранного способа, известного в данной области, такого как сайт-направленный мутагенез (Kunkel et al., Proc. Natl. Acad. Sci. USA (1985) 82, 488-492) или перекрывающаяся ПЦР. Также аминокислота(ы) может быть заменена неприродными аминокислотами с использованием множества способов модификации, известных в данной области (Annu. Rev. Biophys. Biomol. Struct. (2006) 35, 225-249; и Proc. Natl. Acad. Sci. U.S.A. (2003) 100 (11), 6353-6357). Например, также предпочтительно используют содержащую тРНК бесклеточную систему трансляции (Clover Direct (Protein Express, an R & D oriented company)), содержащую неприродную аминокислоту, связанную с тРНК янтарь-супрессора, комплементарной кодону UAG (янтарь-кодон), который представляет собой стоп-кодон.
В одном аспекте модифицированной формы по настоящему изобретению, получают полинуклеотид, кодирующий антигенсвязывающую молекулу, имеющую тяжелую цепь, в которой полинуклеотид, кодирующий модифицированный FcRn-связывающий домен, имеющий аминокислоту(ы), в которую таким образом внесена мутация, связан в рамке считывания с полинуклеотидом, кодирующим выбранную антигенсвязывающую молекулу, активность связывания которой изменяется в зависимости от условий.
Настоящее изобретение относится к способу получения антигенсвязывающей молекулы, включающему выделение антигенсвязывающей молекулы из культур клеток, трансфицированных вектором, имеющим функционально связанную вставку, в которой полинуклеотид, кодирующий FcRn-связывающий домен, связан в рамке считывания с полинуклеотидом, выделенным из вируса по настоящему изобретению. Настоящее изобретение также относится к способу получения антигенсвязывающей молекулы, включающему выделение антигенсвязывающей молекулы из культур клеток, трансфицированных вектором, имеющим функционально связанную вставку, в которой полинуклеотид, кодирующий FcRn-связывающий домен, заранее функционально связанный с вектором, связан в рамке считывания с полинуклеотидом, выделенным из вируса по настоящему изобретению.
Фармацевтическая композиция
Хотя настоящее изобретение не связано с какой-либо конкретной теорией, например, количество антигенов, которые могут быть связаны на одну антигенсвязывающую молекулу, увеличивается и ускоряется исчезновение антигена из плазмы, в результате ускорения клеточного захвата в организме, в который ввели антигенсвязывающую молекулу, содержащую антигенсвязывающий домен, антигенсвязывающая активность которого изменяется в зависимости от условий концентрации ионов так, что антигенсвязывающая активность является более низкой в условиях кислых значений pH, чем в условиях нейтральных значений pH, и, кроме того, содержащую FcRn-связывающий домен (например, константная область антитела), обладающий активностью связывания FcRn человека в условиях нейтральных значений pH. Возможно, причина этому состоит в следующем.
Когда антитело, связывающееся с мембранным антигеном, например, вводят в качестве антигенсвязывающей молекулы в организм, антитело ассоциирует с антигеном и захватывается, вместе с антигеном (при сохранении его состояния связывания с антигеном), во внутриклеточную эндосому путем интернализации. Затем антитело мигрирует в лизосому при сохранении его состояния связывания с антигеном, и комплекс антиген-антитело деградируется лизосомой. Опосредуемое интернализацией исчезновение из плазмы называют антигензависимым исчезновением, и оно описано в отношении множества молекул антител (Drug Discov Today (2006) 11 (1-2), 81-88). После того, как одна молекула IgG-антитела двухвалентным образом связывается с антигенами, эта одна молекула антитела в состоянии, связанном с молекулами антигена, интернализуется и деградируется в этом состоянии в лизосоме. Таким образом, одна молекула общепринятого IgG-антитела не может связываться с тремя или более молекулами антигена. Например, одна молекула IgG антитела, обладающая активностью нейтрализации, не может нейтрализовать три или более молекул антигена.
Относительно длительное время удержания в плазме IgG-молекул (медленное исчезновение) свойственно функциям FcRn человека, известного как рецептор спасения, для молекул IgG. Молекулы IgG, захватываемые в эндосому через пиноцитоз, связываются с FcRn человека, экспрессируемым в эндосоме, в кислых условиях эндосомы. Затем молекулы IgG, которые не связались с FcRn человека, мигрируют в лизосому и деградируются в ней. С другой стороны связанные с FcRn человека молекулы IgG мигрируют к клеточной поверхности. Молекулы IgG диссоциируют от FcRn человека в нейтральных условиях в плазме и, таким образом, рециклируют в плазму.
Когда антигенсвязывающая молекула представляет собой растворимое антигенсвязывающее антитело, антитело, введенное в организм, ассоциирует с антигеном, а затем захватывается в клетки при сохранении ее связанного с антигеном состояния. Большинство антител, захваченных таким образом в клетки, ассоциируют с FcRn в эндосоме, а затем мигрируют к клеточной поверхности. Эти антитела диссоциируют от FcRn человека в нейтральных условиях в плазме и, таким образом, высвобождаются из клеток. Однако антитело, содержащее общепринятый антигенсвязывающий домен, антигенсвязывающая активность которого не изменяется в зависимости от условий концентрации ионов (например, pH), высвобождается из клеток при сохранении ее связанного с антигеном состояния. Таким образом, это антитело не может вновь ассоциировать с антигеном. Таким образом, как и в случае антитела, связывающегося с мембранным антигеном, одна молекула обычного IgG-антитела, антигенсвязывающая активность которого не изменяется в зависимости от условий концентрации ионов (например, pH), не может связываться с тремя или более молекулами антигенов.
Антитело с pH-зависимым связыванием антигена, которое прочно ассоциировано с антигеном в условиях нейтральных значений pH в плазме и диссоциирует от антигена в условиях кислых значений pH в эндосоме (антитело, способное связываться с антигеном в условиях нейтральных значений pH и отделяться от антигена в условиях кислых значений pH) или антитело с зависимым от концентрации ионов кальция связыванием, которое прочно ассоциировано с антигеном в условиях высокой концентрации ионов кальция в плазме и диссоциирует от антигена в условиях низкой концентрации ионов кальция в эндосоме (антитело, способное связываться с антигеном в условиях высокой концентрации ионов кальция и отделяться от антигена в условиях низкой концентрации ионов кальция) может диссоциировать от антигена в эндосоме. Антитело с pH-зависимым связыванием антигена или антитело с зависимым от концентрации ионов кальция связыванием антигена, диссоциировавшее таким образом от антигена, может вновь ассоциировать с антигеном после рециклирования в плазму с помощью FcRn. Это позволяет одной молекуле антитела связываться с множеством молекул антигена многократно. Также, антиген, связанный с антигенсвязывающей молекулой, диссоциирует от антитела в эндосоме и, таким образом, деградируется в лизосоме без рециклирования в плазму. Введение такой антигенсвязывающей молекулы в организм может ускорить клеточный захват антигенов и снизить концентрацию антигена в плазме.
Способность связываться с FcRn человека в условиях нейтральных значений pH (pH 7,4) можно сообщать антителу с pH-зависимым связыванием антигена, которое прочно ассоциировано с антигеном в условиях нейтральных значений pH в плазме и диссоциирует от антигена в условиях кислых значений pH в эндосоме (антитело, способное связываться с антигеном в условиях нейтральных значений pH и отделяться от антигена в условиях кислых значений pH), или антителу с зависимым от концентрации ионов кальция связыванием антигена, которое прочно ассоциировано с антигеном в условиях высокой концентрации ионов кальция в плазме и диссоциирует от антигена в условиях низкой концентрации ионов кальция в эндосоме (антитело, способное связываться с антигеном в условиях высокой концентрации ионов кальция и отделяться от антигена в условиях низкой концентрации ионов кальция). Полученная антигенсвязывающая молекула далее ускоряет клеточный захват антигенов, связанных с ней. Введение такой антигенсвязывающей молекулы в организм может ускорить исчезновение антигена и снизить концентрацию антигена в плазме. Обычное антитело, не обладающее ни способностью к pH-зависимому связыванию антигена, ни способностью к зависимому от концентрации ионов кальция связыванию антигена, и его комплекс антитело-антиген захватываются в клетки через неспецифический эндоцитоз и транспортируются на клеточную поверхность путем связывания с FcRn в условиях кислых значений pH в эндосоме. Антитело диссоциирует от FcRn в условиях нейтральных значений pH на клеточной поверхности и, таким образом, рециклирует в плазму. Когда антитело, которое связывается с антигеном достаточно pH-зависимым образом (т.е. которое ассоциирует с антигеном в условиях нейтральных значений pH и диссоциирует от него в условиях кислых значений pH) или достаточно зависимым от концентрации ионов кальция образом (т.е. которое ассоциирует с антигеном в условиях высокой концентрации ионов кальция и диссоциирует от него в условиях низкой концентрации ионов кальция), ассоциирует с антигеном в плазме и диссоцитирует от связанного с ним антигена в эндосоме, скорость исчезновения антигена считается равной скорости клеточного захвата антитела и его комплекса антитело-антиген через неспецифический эндоцитоз. В случае недостаточной зависимости связывания антитела с антигеном от pH или зависимости его от концентрации ионов кальция, антигены, не диссоциировавшие в эндосоме, рециклируют в плазму вместе с антителом. Напротив, в случае достаточной зависимости от pH связывания антигена, скорость исчезновения антигена определяется скоростью клеточного захвата через неспецифический эндоцитоз. Поскольку FcRn ответственен за транспорт антител из эндосомы на клеточную поверхность, считается, что некоторые FcRn-рецепторы также существуют на клеточной поверхности.
Обычно, IgG-иммуноглобулин, который является одной из форм антигенсвязывающей молекулы, почти не обладает активностью связывания FcRn при нейтральных значениях pH. Авторы настоящего изобретения предположили, что IgG-иммуноглобулин, обладающий активностью связывания FcRn при нейтральных значениях pH, способен связываться с FcRn, присутствующим на клеточной поверхности, и захватываться в клетки зависимым от FcRn образом путем связывания с FcRn, присутствующим на клеточной поверхности. Скорость опосредуемого FcRn клеточного захвата является более быстрой, чем скорость клеточного захвата через неспецифический эндоцитоз. Это указывает на то, что сообщение способности связываться с FcRn при нейтральных значениях pH может далее ускорять скорость исчезновения антигена с помощью антигенсвязывающей молекулы. В частности, антигенсвязывающая молекула, обладающая способностью связываться с FcRn при нейтральных значениях pH, доставляет антиген в клетки быстрее, чем обычный (природный человеческий) IgG-иммуноглобулин, и диссоциирует от антигена в эндосоме. Диссоциировавшая антигенсвязывающая молекула рециклирует на клеточную поверхность или в плазму, где молекула реассоциирует с антигеном, что вновь приводит к опосредуемому FcRn клеточному захвату. Более высокая способность связываться с FcRn при нейтральных значениях pH может увеличить скорость оборота указанного цикла и, таким образом, ускоряет скорость исчезновения антигена из плазмы. Антигенсвязывающая активность антигенсвязывающей молекулы при кислых значениях pH можно снижать относительно антигенсвязывавющей активности при нейтральных значениях pH, чтобы тем самым далее увеличивать скорость исчезновения антигена из плазмы. Увеличенная скорость оборота указанного цикла может приводить к увеличенному количеству циклов, которые, вероятно, позволят одной антигенсвязывающей молекуле связаться с более высоким количеством молекул антигена. Антигенсвязывающая молекула по настоящему изобретению может содержать антигенсвязывающий домен и FcRn-связывающий домен. FcRn-связывающий домен ни влияет на связывание антигена, ни зависит от типа антигена, как также понятно из механизма, упомянутого выше. Антигенсвязывающая активность (способность связывания) антигенсвязывающей молекулы в условиях низкой концентрации ионов, таких как условия кислых значений pH или низкой концентрации ионов кальция, является сниженной относительно антигенсвязывающей активности в условиях концентрации ионов, таких как условия нейтральных значений pH или высокой концентрации ионов кальция, и/или активность связывания FcRn этой молекулы при pH в плазме является усиленной. Это может ускорить клеточный захват антигенов антигенсвязывающей молекулой и ускорить скорость исчезновения антигенов. Таким образом, можно ожидать, что антигенсвязывающая молекула по настоящему изобретению будет проявлять улучшенные эффекты по сравнению с обычными терапевтическими антителами, например, в отношении снижения неблагоприятной реакции, вызываемой антигенами, увеличением дозы антитела, и улучшения кинетики антитела in vivo.
В частности, настоящее изобретение относится к фармацевтической композиции, содержащей антигенсвязывающую молекулу по настоящему изобретению, антигенсвязывающую молекулу, выделенную способом скрининга по настоящему изобретению, или антигенсвязывающую молекулу, продуцированную способом получения по настоящему изобретению. Антигенсвязывающая молекула по настоящему изобретению или антигенсвязывающая молекула, полученная способом получения по настоящему изобретению, пригодна в качестве фармацевтической композиции, поскольку ее введение обеспечивает высокий эффект, состоящий в снижении концентрации антигена в плазме по сравнению с общепринятыми антигенсвязывающими молекулами. Фармацевтическая композиция по настоящему изобретению может содержать фармацевтически приемлемый носитель.
В рамках настоящего изобретения фармацевтическая композиция обычно относится к средству для лечения или профилактики заболевания, или обследования, или диагностики.
Фармацевтическая композиция по настоящему изобретению может быть составлена с использованием способа, общеизвестного специалистам в данной области. Например, фармацевтическую композицию по настоящему изобретению можно парентерально использовать в форме инъекции в стерильном растворе или суспензии с водой или любым другим фармацевтически приемлемым раствором. Например, активный ингредиент можно соответствующим образом комбинировать с фармакологически приемлемыми носителями или средами, в частности, стерильной водой или солевым раствором, растительным маслом, эмульгатором, суспендирующим веществом, поверхностно-активным веществом, стабилизатором, вкусовой добавкой, эксципиентом, носителем, антисептиком, связующим веществом, и т.п. и смешивать с ними в единичной дозированной форме, требуемой в соответствии с общепринятой фармацевтической практикой для получения препарата. Количество активного ингредиента в этих препаратах выбирают так, чтобы вводить подходящий объем в пределах назначенного диапазона.
Стерильные композиции для инъекции можно составлять в соответствии с обычной фармацевтической практикой с использованием носителя, такого как дистиллированная вода для инъекций. Примеры инъецируемых водных растворов включают солевой раствор и изотонические растворы, содержащие глюкозу или другие адъюванты (например, D-сорбит, D-манноза, D-маннит и хлорид натрия). В комбинации с ними можно использовать подходящий солюбилизатор, например, спирт (этанол, и т.д.), полиспирт (пропиленгликоль, полиэтиленгликоль, и т.д.), или неионное поверхностно-активное вещество (полисорбат 80(TM), HCO-50, и т.д.).
Примеры масляных растворов включают кунжутное масло и соевое масло. В комбинации можно использовать бензилбензоат и/или бензиловый спирт в качестве солюбилизаторов. Эти инъецируемые растворы можно смешивать с буфером (например, фосфатно-солевой буфер и натрий-ацетатный буферный раствор), успокаивающим средством (например, прокаина гидрохлорид), стабилизатором (например, бензиловый спирт и фенол) и антиоксидантом. Полученными инъекциями обычно заполняют подходящие ампулы.
Фармацевтическую композицию по настоящему изобретению предпочтительно вводят парентеральным путем. Например, композицию вводят в дозированной форме инъекции, трансназального средства, транспульмонального средства или чрескожного средства. Композицию можно вводить системно или локально, например, путем внутривенной инъекции, внутримышечной инъекции, внутрибрюшинной инъекции или подкожной инъекции.
Способ введения можно соответствующим образом выбирать в зависимости от возраста и симптомов пациента. Единичная доза фармацевтической композиции, содержащей антигенсвязывающую молекулу, может быть выбрана из диапазона, например, от 0,0001 мг до 1000 мг на кг массы тела. Альтернативно доза может быть выбрана из диапазона, например, от 0,001 до 100000 мг на пациента, хотя доза по настоящему изобретению не обязательно ограничена этими численными величинами. Доза и способ введения варьируют в зависимости от массы тела, возраста, симптомов и т.д. пациента. Специалисты в данной области могут выбрать подходящую дозу и способ введения, учитывая эти условия.
Аминокислоты, содержащиеся в аминокислотных последовательностях, описанных в рамках настоящего изобретения, могут претерпевать посттрансляционную модификацию (например, модификация N-концевого глутамина в пироглутаминовую кислоту путем пироглутамилирования, которая хорошо известна специалистам в данной области). Даже такие формы, имеющие посстрансляционно модифицированные аминокислоты, естественно, включены в аминокислотные последовательности, описанные в рамках настоящего изобретения.
Все документы уровня техники, цитированные в настоящем описании, включены в настоящее описание в качестве ссылок.
Как используют в рамках изобретения, аспект, отражаемый выражением с термином “содержащий”, охватывает аспект, отражаемый выражением с термином “по существу состоящий из”, и аспект, отражаемый выражением с термином “состоящий из”.
Примеры
Далее настоящее изобретение описано более конкретно с помощью примеров. Однако настоящее изобретение не ограничивается этими примерами.
[Пример 1] Конструирование библиотеки антител с pH-зависимым связыванием
(1-1) Способ получение антитела с pH-зависимым связыванием
В WO2009125825 описано, что в антигенсвязывающую молекулу вносят гистидин для получения антитела с pH-зависимым связыванием антигена, свойство которого изменяется между областями нейтральных значений pH и кислых значений pH. Описанное антитело с pH-зависимым связыванием получают путем модификации, которая осуществляет замену части аминокислотной последовательности желаемой антигенсвязывающей молекулы на гистидин. Возможный способ более эффективного получения антитела с pH-зависимым связыванием без получения заранее антигенсвязывающей молекулы, подлежащей модификации, включает внесение гистидина в вариабельные области (более предпочтительно, положения, которые могут быть вовлечены в связывание антигена) и получение антигенсвязывающей молекулы, связывающейся с желаемым антигеном, из полученной совокупности антигенсвязывающих молекул (называемых His-библиотекой). Антигенсвязывающая молекула, полученная из His-библиотеки, имеет более высокую частоту встречаемости гистидина, чем обычные библиотеки антител, что указывает на то, что можно эффективно получать антигенсвязывающие молекулы, обладающие желаемым свойством.
(1-2) Конструирование совокупности (His-библиотека) молекул антител, содержащих остатки гистидина в вариабельных областях, которые позволяют эффективное получение связывающего антитела, которое связывается с антигеном pH-зависимым образом
Сначала для His-библиотеки были выбраны положения внесения гистидина. В WO2009125825 описано, что антитела с pH-зависимым связыванием антигена были получены путем замены аминокислотных остатков в последовательностях антитела против рецептора IL-6, антитела против IL-6 и антитела против рецептора IL-31 на гистидин. Кроме того, были получены антитело против лизоцима яичного белка (FEBS Letter 11483, 309, 1, 85-88) и антитело против гепцидина (WO2009139822), обладающие способностью к pH-зависимому связыванию антигена, путем замены аминокислот в аминокислотных последовательностях антигенсвязывающих молекул на гистидин. В таблице 3 представлены положения внесения гистидина в антитело против рецептора IL-6, антитело против IL-6, антитело против рецептора IL-31, антитело против лизоцима яичного белка и антитело против гепцидина. Положения, представленные в таблице 3, могут служить в качестве положений-кандидатов, которые могут контролировать связывание антиген-антитело. В дополнение к положениям, представленным в таблице 3, положения, в высокой степени доступные для антигена, также считались подходящими в качестве положений внесения гистидина.
В His-библиотеке, сконструированной с помощью вариабельных областей тяжелых и легких цепей, используемые вариабельные области тяжелой цепи представляли собой последовательности антител человека, в то время как в вариабельные области легкой цепи вносили остаток гистидина. Положения, приведенные выше, и положения, которые могут быть вовлечены в связывание антигена, т.е. положения 30, 32, 50, 53, 91, 92 и 93 (определяемые посредством нумерации по Кабату; Kabat EA et al., 1991. Sequence of Proteins of Immunological Interest. NIH) в легких цепях отбирали в качестве положений внесения гистидина для His-библиотеки. Также, последовательность Vk1 выбирали в качестве матричной последовательности вариабельной области легкой цепи для внесения гистидина. Множеству аминокислот позволяли появиться в каждом данном положении в матричной последовательности для увеличения разнообразия антигенсвязывающих молекул, составляющих библиотеку. Экспонированные на поверхности положения в вариабельных областях, которые вероятно будут взаимодействовать с антигенами, выбирали в качестве положения, в котором оказывалось множество аминокислот. В частности, в качестве таких нестрогих остатков были выбраны положения 30, 31, 32, 34, 50, 53, 91, 92, 93, 94 и 96 (определяемые посредством нумерации по Кабату; Kabat EA et al. 1991. Sequences of Proteins of Immunological Interest. NIH) в легких цепях.
Далее, выбирали типы и встречаемость появляющихся аминокислотных остатков. Аминокислоты нестрогих остатков анализировали в отношении их частоты встречаемости в последовательностях hVk1 и hVk3, зарегистрированных в базе данных Кабат (KABAT, E.A. et al.: “Sequences of Proteins of Immunological interest”, vol. 91, 1991, NIH PUBLICATION). Исходя из результатов анализа, типы аминокислот, появляющихся в His-библиотеке, выбирали из аминокислот с высокой частотой появления в каждом положении. По этой методике также выбирали аминокислоты, для которых было подтверждено, что они обладают низкой частотой встречаемости, исходя из результатов анализа, чтобы предотвратить нарушение баланса свойств аминокислот. Частота встречаемости выбранных аминокислот была выбрана на основании результатов анализа базы данных Кабат.
Учитывая выбранные таким образом аминокислоты и их частоту встречаемости, было сконструировано две His-библиотеки: His-библиотека 1, фиксированная на условии, что каждая CDR содержала один остаток гистидина без исключения; и His-библиотека 2, которая была более акцентирована на разнообразии последовательностей, чем His-библиотека 1. Детальная конструкция His-библиотеки 1 и His-библиотеки 2 представлена в таблицах 4 и 5 (“Положение” в каждой таблице отражает нумерацию по Кабату). Частота появления аминокислот, описанных в таблицах 4 и 5, может исключать Ser (S) в положении 94, определяемом посредством нумерации по Кабату, в случае Asn (N) в положении 92.

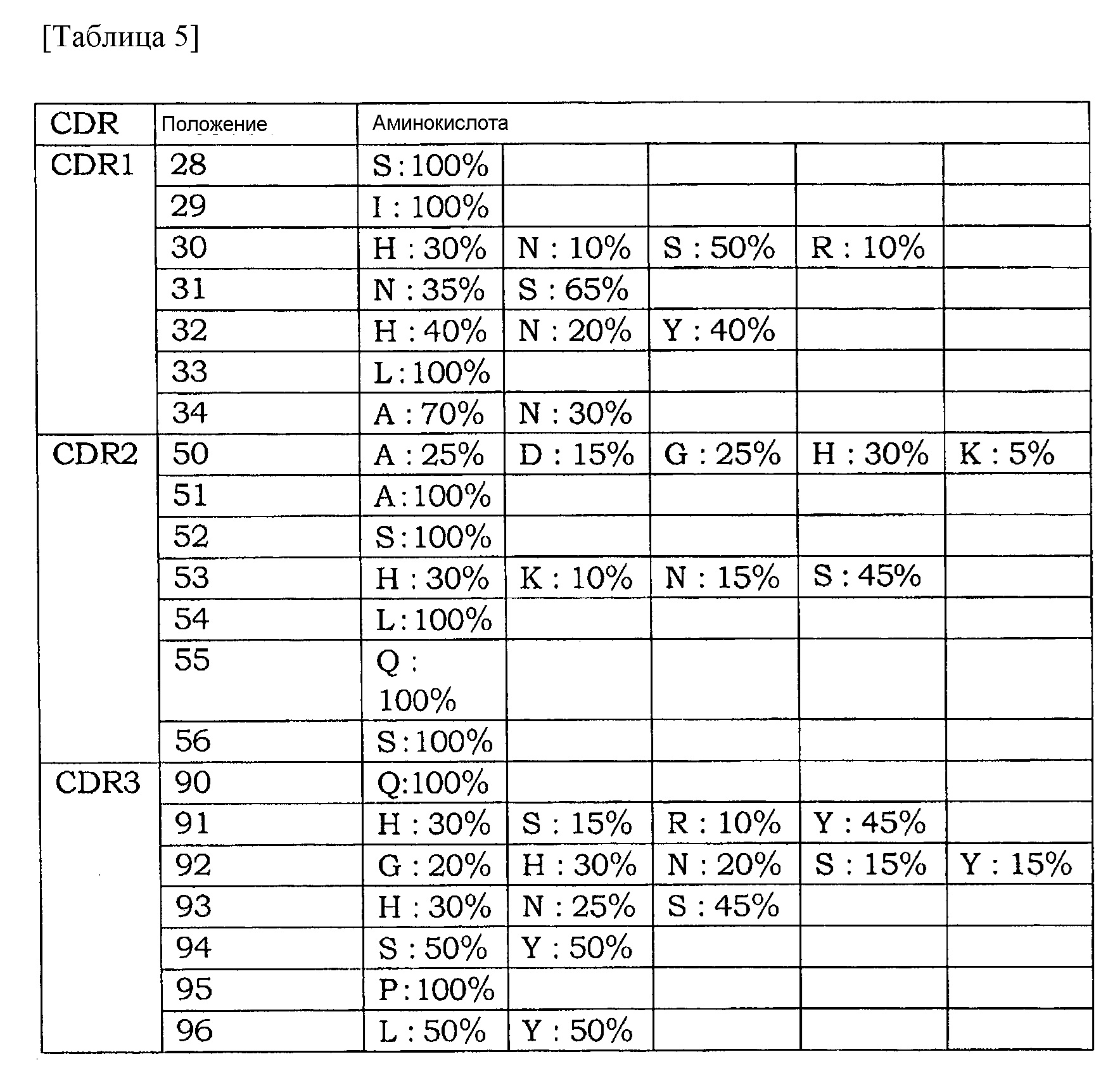
[Пример 2] Получение библиотеки фагового дисплея антител человека (His-библиотека 1) для получения антитела, связывающегося с антигеном pH-зависимым образом
Библиотеку генов вариабельных областей тяжелой цепи антитела амплифицировали способом ПЦР с использованием поли-A РНК, полученной из PBMC человека, коммерчески доступной поли-A РНК человека, и т.п. в качестве матрицы. Библиотеку генов вариабельных областей легкой цепи антитела, сконструированную в качестве His-библиотеки 1, описанной в примере 1, амплифицировали с использованием ПЦР. Комбинации последовательностей в библиотеке генов вариабельных областей тяжелых цепей антител и библиотеке генов вариабельных областей легких цепей антител, полученных таким образом, встраивали в фагмидные векторы для конструирования библиотеки фагового дисплея антител человека, экспонирующих Fab-домены, состоящие из последовательностей антител человека. Способ конструирования выполняли в соответствии с Methods Mol Biol. (2002) 178, 87-100. При конструировании этой библиотеки использовали последовательность библиотеки фагового дисплея, которая содержала линкерную часть для связывания Fab фагмиды и белка pIII фага, и последовательность для расщепления трипсином, встроенную между доменами N2 и CT белка pIII хелперного фага. Части генов антител, выделенные из E. coli, трансформированных библиотекой генов антител, секвенировали, получая информацию о последовательности приблизительно для 132 клонов. На фиг. 1 представлено модельное распределение аминокислот и распределение аминокислот в подтвержденной последовательности. Конструировали библиотеку, содержащую разнообразные последовательности, соответствующие модельному распределению аминокислот.
[Пример 3] Получение антитела, связывающегося с IL-6R pH-зависимым образом
(3-1) Получение фрагмента антитела, связывающегося с антигеном pH-зависимым образом, из библиотеки с помощью пэннинга на гранулах
Первый раунд скрининга сконструированной His-библиотеки 1 проводили путем увеличения содержания только фрагментов антител, обладающих способностью связывать антиген (IL-6R).
Фаги получали из E. coli, содержавших сконструированную фагмиду для фагового дисплея. К культурам E. coli, которые продуцировали фаги, добавляли 2,5 M NaCl/10% PEG, и совокупность фагов, преципитированных таким образом, разбавляли TBS, получая раствор с фаговой библиотекой. К раствору с фаговой библиотекой добавляли BSA и CaCl2, (конечная концентрация: 4% BSA и 1,2 мМ ионы кальция). Способ пэннинга проводили в соответствии с общепринятым способом пэннинга с использованием антигенов, иммобилизованных на магнитных гранулах (J. Immunol. Methods. (2008) 332 (1-2), 2-9; J. Immunol. Methods. (2001) 247 (1-2), 191-203; Biotechnol. Prog. (2002) 18 (2) 212-20; и Mol. Cell Proteomics (2003) 2 (2), 61-9). Использованные магнитные гранулы представляли собой покрытые нейтравидином гранулы (Sera-Mag SpeedBeads NeutrAvidin-coated) или покрытые стрептавидином гранулы (Dynabeads M-280 Streptavidin).
В частности, 250 пмоль меченных биотином антигенов добавляли к полученному раствору с фаговой библиотекой и, тем самым, приводили в контакт с раствором с фаговой библиотекой при комнатной температуре в течение 60 минут. Добавляли блокированные BSA магнитные гранулы, а затем комплексы антиген-фаг связывали с магнитными гранулами при комнатной температуре в течение 15 минут. Гранулы промывали три раза 1 мл 1,2 мМ CaCl2/TBS (TBS, содержащий 1,2 мМ CaCl2 и 0,1% Tween 20), а затем дополнительно промывали два раза 1 мл 1,2 мМ CaCl2/TBS (pH 7,6). После добавления 0,5 мл 1 мг/мл трипсина, гранулы суспендировали при комнатной температуре в течение 15 минут, и сразу после этого гранулы отделяли с использованием магнитного стенда для получения раствора с фагами. Полученный раствор с фагами добавляли к 10 мл штамма E. coli ER2738 на логарифмической фазе роста (OD600: 0,4-0,7). Штамм E. coli инфицировали фагами при осторожном вращении культуры штамма при 37°C в течение 1 часа. Инфицированные E. coli инокулировали на чашку 225 мм × 225 мм. Далее из культур инокулированных E. coli собирали фаги, получая раствор с фаговой библиотекой.
На втором и последующих раундах пэннинга увеличивали содержание фагов с антигенсвязывающей способностью или способностью pH-зависимого связывания в качестве показателя. В частности, 40 пмоль меченных биотином антигенов добавляли к полученному раствору с фаговой библиотекой и, тем самым, приводили в контакт с раствором с фаговой библиотекой при комнатной температуре в течение 60 минут. Добавляли блокированные BSA магнитные гранулы, а затем комплексы антиген-фаг связывали с магнитными гранулами при комнатной температуре в течение 15 минут. Гранулы промывали несколько раз 1 мл 1,2 мМ CaCl2/TBST и 1,2 мМ CaCl2/TBS. Для увеличения содержания с антигенсвязывающей способностью в качестве показателя, гранулы, дополненные 0,5 мл 1 мг/мл трипсина, суспендировали при комнатной температуре в течение 15 минут, и сразу после этого гранулы отделяли с использованием магнитного стенда для получения раствора с фагами. Для увеличения содержания со способностью к pH-зависимому связыванию антигена в качестве показателя, гранулы, дополненные 0,1 мл 50 мМ MES/1,2 мМ CaCl2/150 мМ NaCl (pH 5,5), суспендировали при комнатной температуре. Сразу после этого гранулы отделяли с использованием магнитного стенда для получения вновь раствора с фагами. Добавление 5 мкл 100 мг/мл трипсина к полученному раствору с фагами расщепляло белки pIII (белки pIII, происходящие из хелперного фага) не экспонирующих Fab фагов для устранения способности не экспонирующих Fab фагов инфицировать E. coli. Полученные фаги добавляли к 10 мл штамма E. coli ER2738 на логарифмической фазе роста (OD600: 0,4-0,7). Штамм E. coli инфицировали фагами при осторожном вращении культуры штамма при 37°C в течение 1 часа. Инфицированные E. coli инокулировали на чашку 225 мм × 225 мм. Далее из культур инокулированных E. coli собирали фаги, получая раствор с фаговой библиотекой. Этот пэннинг с антигенсвязывающей способностью или способностью к pH-зависимому связыванию в качестве показателей проводили всех в течение 2 раундов.
(3-2) Оценка с помощью ELISA фагов
Содержащий фаг культуральный супернатант получали в соответствии с общепринятым способом (Methods Mol. Biol. (2002) 178, 133-145) из каждой единичной колонии E. coli, полученной с помощью описанного выше способа.
После добавления BSA и CaCl2 (конечная концентрация: 4% BSA и 1,2 мМ ионы кальция), содержащий фаг культуральный супернатант подвергали ELISA по следующей методике: микропланшет для титрования StreptaWell 96 (F. Hoffmann-La Roche Ltd.) покрывали в течение ночи 100 мкл PBS, содержавшего меченные биотином антигены. Каждую лунку планшета промывали PBST (PBS, содержащий 0,1% Tween 20), для удаления не связавшихся антигенов. Затем лунку блокировали 250 мкл 4% BSA-TBS в течение 1 часа или более. После удаления 4% BSA-TBS, полученный супернатант добавляли в каждую лунку, и планшет оставляли стоять при 37°C в течение 1 часа для связывания экспонируемых фагом антител с антигенами, содержащимися в каждой лунке. Каждую лунку промывали 1,2 мМ CaCl2/TBST, и добавляли 1,2 мМ CaCl2/TBS (pH 7,6) или 1,2 мМ CaCl2/TBS (pH 5,5). Планшеты оставляли стоять при 37°C в течение 30 минут для инкубации. После промывания 1,2 мМ CaCl2/TBST в каждую лунку добавляли конъюгированные с HRP антитела против M13 (Amersham Pharmacia Biotech Inc.), разбавленные TBS, имеющим 4% BSA, и ионизированный кальций в концентрации 1,2 мМ. Планшет инкубировали в течение 1 часа. После промывания 1,2 мМ CaCl2/TBST, в каждую лунку добавляли простой раствор TMB (ZYMED Laboratories, Inc.). Хромогенную реакцию раствора в каждой лунке завершали добавлением серной кислоты. Затем развитие цвета анализировали на основе поглощения при 450 нм.
17 клонов были ELISA-положительными специфическим к антигену образом в результате ELISA фагов для 96 клонов (после 2 раундов пэннинга), содержание которых было увеличено с антигенсвязывающей способностью в качестве показателя. Таким образом, анализировали образцы, полученные в 3 раундах пэниннга. С другой стороны, 70 клонов были ELISA-положительными в результате ELISA фагов для 94 клонов (после 2 раундов пэннинга), содержание которых было увеличено со способностью к pH-зависимому связыванию антигена в качестве показателя. Таким образом, анализировали эти образцы, полученные в 2 раундах пэннинга.
Гены клонов, подвергнутых ELISA фагов, амплифицировали с использованием специфических праймеров, а затем анализировали в отношении их нуклеотидных последовательностей.
Результаты фагового ELISA и анализа последовательностей представлены в таблице 6 ниже.
Антитела, обладающие способностью к pH-зависимому связыванию антигена, получали сходным способом, из библиотеки фагового дисплея наивных антител человека. 13 типов антител с pH-зависимым связыванием было получено путем оценки 88 клонов, содержание которых было увеличено с антигенсвязывающей способностью в качестве показателя. Также было получено 27 типов антител с pH-зависимым связыванием путем оценки 83 клонов, содержание которых было увеличено со способностью к pH-зависимому связыванию антигена в качестве показателя.
Эти результаты продемонстрировали, что His-библиотека 1 продуцирует больше вариантов клонов, обладающих способностью к pH-зависимому связыванию антигена, чем библиотека фагового дисплея наивных антител человека.
(3-3) Экспрессия и очистка антитела
Ген каждого клона, оцененного как обладающий способностью к pH-зависимому связыванию антигена в результате ELISA фагов, встраивали в плазмиды для экспрессии в клетках животных. Экспрессию антител проводили следующим способом: линию FreeStyle 293-F, происходящую из почки эмбриона человека, (Invitrogen Corp.) суспендировали в среде для экспрессии FreeStyle 293 Expression Medium (Invitrogen Corp.). Суспензию, имеющую плотность клеток 1,33×106 клеток/мл, инокулировали в концентрации 3 мл/лунка в планшет с 6 ячейками. Полученные плазмиды переносили в клетки путем липофекции. Клетки культивировали в течение 4 суток в инкубаторе с CO2 (37°C, 8% CO2, 90 об./мин.). Антитела очищали из полученного культурального супернатанта способом, общеизвестным специалистам в данной области, с использованием rProtein A Sepharose(TM) Fast Flow (Amersham Biosciences, Inc.). Поглощение очищенного раствора антител измеряли при 280 нм с использованием спектрофотометра. Концентрацию антитела вычисляли из полученной величины измерения с использованием коэффициента экстинкции, вычисленного с помощью PACE (Protein Science (1995) 4, 2411-2423).
(3-4) Оценка полученного антитела в отношении его способности к pH-зависимому связыванию с рецептором IL-6 человека
Для оценки зависимости от pH активности связывания рецептора IL-6 человека антител 6RpH#01 (тяжелая цепь: SEQ ID NO: 18 и легкая цепь: SEQ ID NO: 19), 6RpH#02 (тяжелая цепь: SEQ ID NO: 20 и легкая цепь: SEQ ID NO: 21), и 6RpH#03 (тяжелая цепь: SEQ ID NO: 22 и легкая цепь: SEQ ID NO: 23), полученных на стадии (3-3), эти антитела анализировали в отношении их взаимодействия с рецепторами IL-6 человека с использованием Biacore T100 (GE Healthcare Bio-Sciences Corp.). В качестве контрольного антитела, не обладающего активностью pH-зависимого связывания с рецепторами IL-6 человека, использовали тоцилизумаб (тяжелая цепь: SEQ ID NO: 24 и легкая цепь: SEQ ID NO: 25). Взаимодействие в реакции антиген-антитело анализировали в растворах с pH 7,4 и pH 6,0 в качестве условий нейтральных значений pH и кислых значений pH, соответственно. Приблизительно 300 RU каждого представляющего интерес антитела улавливали на сенсорном чипе CM5 (GE Healthcare Bio-Sciences Corp.) с иммобилизованным на нем белком A/G (Invitrogen Corp.), в соответствующем количестве способом присоединения аминов. В качестве подвижных буферов использовали два типа буферных растворов: 20 мМ ACES, 150 мМ NaCl, 0,05% (масс./об.) Tween 20, и 1,2 мМ CaCl2 (pH 7,4); и 20 мМ ACES, 150 мМ NaCl, 0,05% (масс./об.) Tween 20, и 1,2 мМ CaCl2(pH 6,0). Рецепторы IL-6 человека также разбавляли с помощью каждого из этих буферов. Весь анализ проводили при 37°C.
В анализе взаимодействия в реакции антиген-антитело с использованием контрольного антитела тоцилизумаба, антитела 6RpH#01, антитела 6RpH#02 и антитела 6RpH#03, разбавленный раствор рецептора IL-6 или пустой подвижный буфер инжектировали со скоростью потока 5 мкл/мин в течение 3 минут для взаимодействия рецепторов IL-6 с антителом тоцилизумабом, антителом 6RpH#01, антителом 6RpH#02 или антителом 6RpH#03, уловленными на сенсорном чипе. Затем на него инжектировали 10 мМ глицин-HCl (pH 1,5) со скоростью потока 30 мкл/мин в течение 30 секунд, чтобы регенерировать сенсорный чип.
На фиг. 2 представлены сенсограммы антител, проанализированных при pH 7,4 с помощью описанного выше способа. На фиг. 3 представлены сенсограммы антител в условиях pH 6,0, полученных сходным способом.
В результате, было выявлено, что способность связывания рецептора IL6 у антитела 6RpH#01, антитела 6RpH#02 и антитела 6RpH#03 значительно снижалась при изменении pH буфера от pH 7,4 до pH 6,0.
[Пример 4] Получение библиотеки фагового дисплея антител человека (His-библиотека 2) для получения антитела, связывающегося с антигеном pH-зависимым образом
Библиотеку генов вариабельных областей тяжелой цепи антитела амплифицировали способом ПЦР с использованием поли-A РНК, полученной из PBMC человека, коммерчески доступной поли-A РНК человека, и т.п. в качестве матрицы. Для повышения частоты встречаемости антител, обладающих способностью к pH-зависимому связыванию антигена, как описано в примере 1, части легких цепей с вариабельными областями антитела конструируют так, чтобы в этих частях легких цепей увеличивалась частота встречаемости остатков гистидина в участках, вероятно выполняющих роль участка приведения в контакт с антигеном. Библиотеку вариабельных областей легкой цепи приводят в контакт так, чтобы аминокислоты с высокой частотой встречаемости, определенные из информации о частоте встречаемости аминокислот в природных антителах человека, были равномерно распределены в качестве аминокислотных остатков, отличных от остатков с внесенным гистидином среди нестрогих остатков. Библиотеку можно получать путем привлечения для ее синтеза коммерческой уполномоченной компании и т.п. Комбинации последовательностей библиотеки генов вариабельных областей тяжелой цепи антитела и библиотеки генов вариабельных областей легкой цепи антитела, полученные таким образом, встраивают в фагмидные векторы. Библиотеку фагового дисплея антител человека, экспонирующую Fab-домены, состоящие из последовательностей антител человека, конструируют в соответствии со способом, известным в данной области (Methods Mol Biol. (2002) 178, 87-100). Части генов антител, выделенные из E. coli, трансформированных библиотекой генов антител, секвенируют в соответствии со способом, описанным в примере 2.
[Пример 5] Получение антитела, связывающегося с IL-6R pH-зависимым образом
(5-1) Получение фрагмента антитела, связывающегося с антигеном pH-зависимым образом, из библиотеки с помощью пэннинга на гранулах
Первый раунд скрининга сконструированной His-библиотеки 2 проводят путем увеличения содержания только фрагментов антител, обладающих способностью связывать антиген (IL-6R).
Фаги получают из E. coli, содержащих сконструированную фагмиду для фагового дисплея. К культурам E. coli, которые продуцируют фаги, добавляют 2,5 M NaCl/10% PEG, и совокупность фагов, преципитированных таким образом, разбавляют TBS, получая раствор с фаговой библиотекой. Затем к раствору с фаговой библиотекой добавляют BSA и обезжиренное молоко в качестве блокирующего агента. Способ пэннинга проводят в соответствии с общепринятым способом пэннинга с использованием антигенов, иммобилизованных на магнитных гранулах (J. Immunol. Methods. (2008) 332 (1-2), 2-9; J. Immunol. Methods. (2001) 247 (1-2), 191-203; Biotechnol. Prog. (2002) 18 (2) 212-20; и Mol. Cell Proteomics (2003) 2 (2), 61-9). Используемые магнитные гранулы представляют собой покрытые нейтравидином гранулы (Sera-Mag SpeedBeads NeutrAvidin-coated) или покрытые стрептавидином гранулы (Dynabeads M-280 Streptavidin).
В частности, 250 пмоль меченных биотином антигенов добавляют к полученному раствору с фаговой библиотекой и, тем самым, приводят в контакт с раствором с фаговой библиотекой при комнатной температуре в течение 60 минут. Добавляют магнитные гранулы, блокированные блокирующим агентом, а затем комплексы антиген-фаг связывают с магнитными гранулами при комнатной температуре в течение 15 минут. Гранулы промывают три раза 1 мл TBST, а затем дополнительно промывают два раза 1 мл TBS. После добавления магнитных гранул, блокированных блокирующим агентом, комплексы антиген-фаг связывают с магнитными гранулами при комнатной температуре в течение 15 минут. Гранулы промывают три раза 1 мл TBST, а затем дополнительно промывают два раза 1 мл TBS. После добавления 0,5 мл 1 мг/мл трипсина, гранулы суспендируют при комнатной температуре в течение 15 минут, и сразу после этого гранулы отделяют с использованием магнитного стенда для получения раствора с фагами. Собранный раствор с фагами добавляют к 10 мл штамма E. coli ER2738 на логарифмической фазе роста (OD600: 0,4-0,7). Штамм E. coli инфицируют фагами при осторожном вращении культуры штамма при 37°C в течение 1 часа. Инфицированные E. coli инокулируют на чашку 225 мм × 225 мм. Далее из культур инокулированных E. coli собирают фаги, получая раствор с фаговой библиотекой.
На втором и последующих раундах пэннинга увеличивают содержание фагов с антигенсвязывающей способностью или способностью pH-зависимого связывания в качестве показателя. В частности, 40 пмоль меченных биотином антигенов добавляют к полученному раствору с фаговой библиотекой и, тем самым, приводят в контакт с раствором с фаговой библиотекой при комнатной температуре в течение 60 минут. Добавляют блокированные BSA или обезжиренным молоком магнитные гранулы, а затем комплексы антиген-фаг связывают с магнитными гранулами при комнатной температуре в течение 15 минут. Гранулы промывают 1 мл TBST и TBS. Для увеличения содержания с антигенсвязывающей способностью в качестве показателя, гранулы, дополненные 0,5 мл 1 мг/мл трипсина, суспендируют при комнатной температуре в течение 15 минут, и сразу после этого гранулы отделяют с использованием магнитного стенда для получения раствора с фагами. Для увеличения содержания со способностью к pH-зависимому связыванию антигена в качестве показателя, гранулы, дополненные 0,1 мл 50 мМ MES/1,2 мМ CaCl2/150 мМ NaCl (pH 5,5), суспендируют при комнатной температуре. Сразу после этого гранулы отделяют с использованием магнитного стенда для получения раствора с фагами. Добавление 5 мкл 100 мг/мл трипсина к собранному раствору с фагами расщепляет белки pIII (белки pIII, происходящие из хелперного фага) не экспонирующих Fab фагов для устранения способности не экспонирующих Fab фагов инфицировать E. coli. Собранные фаги добавляют к 10 мл штамма E. coli ER2738 на логарифмической фазе роста (OD600: 0,4-0,7). Штамм E. coli инфицируют фагами при осторожном вращении культуры штамма при 37°C в течение 1 часа. Инфицированные E. coli инокулируют на чашку 225 мм × 225 мм. Далее из культур инокулированных E. coli собирают фаги, получая раствор с фаговой библиотекой. Этот пэннинг с антигенсвязывающей способностью или способностью к pH-зависимому связыванию в качестве показателей повторяют несколько раз.
(5-2) Оценка с помощью ELISA фагов
Содержащий фаг культуральный супернатант получают в соответствии с общепринятым способом (Methods Mol. Biol. (2002) 178, 133-145) из каждой единичной колонии E. coli, полученной с помощью описанного выше способа.
После добавления BSA и CaCl2, содержащий фаг культуральный супернатант подвергали ELISA по следующей методике: микропланшет для титрования StreptaWell 96 (F. Hoffmann-La Roche Ltd.) покрывают в течение ночи 100 мкл PBS, содержащего меченные биотином антигены. Каждую лунку планшета промывают PBST для удаления не связавшихся антигенов. Затем лунку блокируют 250 мкл 4% BSA-TBS в течение 1 часа или более. После удаления 4% BSA-TBS, полученный супернатант добавляют в каждую лунку, и планшет оставляют стоять при 37°C в течение 1 часа для связывания экспонируемых фагом антител с антигенами, содержащимися в каждой лунке. Каждую лунку промывают 1,2 мМ CaCl2/TBST, и добавляют 1,2 мМ CaCl2/TBS (pH 7,6) или 1,2 мМ CaCl2/TBS (pH 5,5). Планшет оставляют стоять при 37°C в течение 30 минут для инкубации. После промывания 1,2 мМ CaCl2/TBST в каждую лунку добавляют конъюгированные с HRP антитела против M13 (Amersham Pharmacia Biotech Inc.), разбавленные TBS, имеющим 4% BSA и ионизированный кальций в концентрации 1,2 мМ. Планшет инкубируют в течение 1 часа. После промывания 1,2 мМ CaCl2/TBST, в каждую лунку добавляют простой раствор TMB (ZYMED Laboratories, Inc.). Хромогенную реакцию раствора в каждой лунке завершают добавлением серной кислоты. Затем развитие цвета анализируют на основе поглощения при 450 нм.
Гены фрагментов антител, оцененных как имеющие способность к pH-зависимому связыванию антигена в результате ELISA фагов, амплифицируют в качестве матрицы с использованием специфических праймеров, а затем анализируют в отношении их нуклеотидных последовательностей.
(5-3) Экспрессия и очистка антител
Ген каждого клона, оцененного как обладающий способностью к pH-зависимому связыванию антигена в результате ELISA фагов, встраивают в плазмиды для экспрессии в клетках животных. Экспрессию антител проводят следующим способом: линию FreeStyle 293-F, происходящую из почки эмбриона человека, (Invitrogen Corp.) суспендируют в среде для экспрессии FreeStyle 293 Expression Medium (Invitrogen Corp.). Суспензию, имеющую плотность клеток 1,33×106 клеток/мл, инокулируют в концентрации 3 мл/лунка в планшет с 6 ячейками. Полученные плазмиды переносят в клетки путем липофекции. Клетки культивируют в течение 4 суток в инкубаторе с CO2 (37°C, 8% CO2, 90 об./мин.). Антитела очищают из полученного культурального супернатанта способом, общеизвестным специалистам в данной области, с использованием rProtein A Sepharose(TM) Fast Flow (Amersham Biosciences, Inc.). Поглощение очищенного раствора антител измеряют при 280 нм с использованием спектрофотометра. Концентрацию антитела вычисляют из полученной величины измерения с использованием коэффициента экстинкции, вычисленного с помощью PACE (Protein Science (1995) 4, 2411-2423).
(5-4) Оценка полученного антитела в отношении его способности к pH-зависимому связыванию с рецептором IL-6 человека
Для оценки зависимости от pH активности связывания рецептора IL-6 человека антител, полученных согласно примеру 5, эти антитела анализируют в отношении их взаимодействия с рецепторами IL-6 человека с использованием Biacore T100 (GE Healthcare Bio-Sciences Corp.). В качестве контрольного антитела, не обладающего pH-зависимой активностью связывания с рецепторами IL-6 человека, используют тоцилизумаб (тяжелая цепь: SEQ ID NO: 24 и легкая цепь: SEQ ID NO: 25). Взаимодействие в реакции антиген-антитело анализируют в растворах с pH 7,4 и pH 6,0 в качестве условий нейтральных значений pH и кислых значений pH, соответственно. Каждое представляющее интерес антитело улавливают на сенсорном чипе CM5 (GE Healthcare Bio-Sciences Corp.) с иммобилизованным на нем белком A/G (Invitrogen Corp.), в соответствующем количестве способом присоединения аминов. В качестве подвижных буферов используют два типа буферных растворов: 20 мМ ACES, 150 мМ NaCl, 0,05% (масс./об.) Tween 20, и 1,2 мМ CaCl2 (pH 7,4); и 20 мМ ACES, 150 мМ NaCl, 0,05% (масс./об.) Tween 20, и 1,2 мМ CaCl2(pH 6,0). Рецепторы IL-6 человека также разбавляют с помощью каждого из этих буферов. Весь анализ проводят при 37°C.
В анализе взаимодействия в реакции антиген-антитело с использованием контрольного антитела тоцилизумаба и антител, полученных согласно примеру 5, разбавленный раствор рецептора IL-6 или пустой подвижный буфер инжектируют, чтобы рецепторы IL-6 взаимодействовали с антителами, иммобилизованными на сенсорном чипе. Затем на него инжектируют 10 мМ глицин-HCl (pH 1,5) при скорости потока 30 мкл/мин в течение 30 секунд, чтобы регенерировать сенсорный чип. Сенсограммы в условиях pH 6,0 также получают сходным способом.
[Пример 6] Поиск последовательности человека эмбрионального типа, связывающейся с ионом кальция
(6-1) Антитело, связывающееся с антигеном кальций-зависимым образом
Антитело, связывающееся с антигеном кальций-зависимым образом (антитело с кальций-зависимым связыванием антигена), представляет собой антитело, взаимодействие которого с антигеном изменяется в зависимости от концентрации ионов кальция. Поскольку считается, что антитело с кальций-зависимым связыванием антигена связывается с антигеном через ионы кальция, аминокислоты, составляющие антигенные эпитопы, представляют собой отрицательно заряженные аминокислоты, способные хелатировать ионы кальция, или аминокислоты, которые могут служить в качестве акцепторов водородных связей (фиг. 4B). Благодаря свойствам таких составляющих эпитоп аминокислот, антитело с кальций-зависимым связыванием антигена способно нацеливаться на эпитоп, отличный от эпитопа pH-зависимой антигенсвязывающей молекулы, полученной путем встраивания остатков гистидина, как показано на фиг. 4A. Кроме того, использование антигенсвязывающих молекул, обладающих свойством связывания с антигенами как кальций-зависимым, так и pH-зависимым образом, как показано на фиг. 4C, может обеспечивать получение антигенсвязывающих молекул, способных индивидуально нацеливаться на разнообразные эпитопы, имеющих широкий диапазон свойств. Это указывает на то, что антитело с кальций-зависимым связыванием антигена может быть эффективно получено путем конструирования набора молекул, содержащих кальций-связывающие мотивы (Ca-библиотека) и получения антигенсвязывающих молекул из указанного набора молекул.
(6-2) Получение последовательности человека эмбрионального типа
Возможным примером набора молекул, содержащих кальций-связывающие мотивы, является набор антител в качестве таких молекул. Иными словами, возможным примером Ca-библиотеки является библиотека антител, содержащая кальций-связывающие мотивы.
Ни одно из описанных ранее антител, содержащих последовательности человека эмбрионального типа, не связывается с ионами кальция. Таким образом, для определения того, связываются ли антитела, содержащие последовательности человека эмбрионального типа, с ионами кальция, последовательности ДНК эмбрионального типа антител, содержащих последовательности человека эмбрионального типа, клонировали с использованием, в качестве матрицы, кДНК, полученных из поли-РНК селезенки эмбриона человека (Clontech Laboratories, Inc.). Клонированные фрагменты ДНК встраивали в экспрессирующие векторы для клеток животных. Полученные экспрессирующие векторы секвенировали способом, общеизвестным специалистам в данной области. SEQ ID NO аминокислотных последовательностей, кодируемых определенными нуклеотидными последовательностями, представлены в таблице 7. Полинуклеотид, кодирующий последовательность SEQ ID NO: 6 (Vk1), SEQ ID NO: 7 (Vk2), SEQ ID NO: 8 (Vk3), SEQ ID NO: 9 (Vk4) или SEQ ID NO: 1 (Vk5), связывали способом ПЦР с полинуклеотидом, кодирующим природную константную область цепи каппа (SEQ ID NO: 26). Полученные фрагменты ДНК по отдельности встраивали в векторы для экспрессии в клетках животных. Также полинуклеотид вариабельной области тяжелой цепи, кодирующий последовательность SEQ ID NO: 27 (Vk1), SEQ ID NO: 28 (Vk2), SEQ ID NO: 29 (Vk3) или SEQ ID NO: 30 (Vk4), связывали способом ПЦР с полинуклеотидом, кодирующим IgG1, лишенный 2 C-концевых аминокислот в последовательности SEQ ID NO: 14. Полученные фрагменты ДНК по отдельности встраивали в векторы для экспрессии в клетках животных. Последовательности полученных модифицированных форм подтверждали способом, общеизвестным специалистам в данной области. В этом контексте Vk1 человека также обозначают как hVk1; Vk2 человека также обозначают как hVk2; Vk3 человека также обозначают как hVk3; и Vk4 человека также обозначают как hVk4.
(6-3) Экспрессия и очистка антител
Векторами для экспрессии в клетках животных, имеющими вставку фрагмента ДНК, кодирующего каждый из 5 типов последовательностей человека эмбрионального типа, полученных таким образом, трансфицировали клетки животных. Экспрессию антител проводили следующим способом: линию FreeStyle 293-F, происходящую из почки эмбриона человека, (Invitrogen Corp.) суспендировали в среде для экспрессии FreeStyle 293 Expression Medium (Invitrogen Corp.). Суспензию, имеющую плотность клеток 1,33×106 клеток/мл, инокулировали в концентрации 3 мл/лунка в планшет с 6 ячейками. Полученные плазмиды переносили в клетки путем липофекции. Клетки культивировали в течение 4 суток в инкубаторе с CO2 (37°C, 8% CO2, 90 об./мин.). Антитела очищали из полученного культурального супернатанта способом, общеизвестным специалистам в данной области, с использованием rProtein A Sepharose(TM) Fast Flow (Amersham Biosciences, Inc.). Поглощение очищенного раствора антител измеряли при 280 нм с использованием спектрофотометра. Концентрацию антитела вычисляли из полученной величины измерения с использованием коэффициента экстинкции, вычисленного с помощью PACE (Protein Science (1995) 4, 2411-2423).
(6-4) Оценка антитела, содержащего последовательность человека эмбрионального типа, в отношении его активности связывания ионов кальция
Очищенные антитела оценивали в отношении их активности связывания ионов кальция. Среднюю температуру термической денатурации (Tm) измеряли с помощью дифференциальной сканирующей калориметрии (DSC) (MicroCal VP-Capillary DSC, MicroCal) в качестве показателя для оценки связывания антителами ионов кальция. Средняя температура термической денатурации (Tm) служит в качестве показателя стабильности и становится более высокой, когда белок стабилизирован через связывание ионов кальция, по сравнению со средней температурой термической денатурации (Tm) не связанного с ионом кальция белка (J. Biol. Chem. (2008) 283, 37, 25140-25149). Для оценки активности связывания антитела с ионами кальция оценивали изменение величины Tm каждого антитела в зависимости от изменения концентрации ионов кальция в растворе антитела. Очищенные антитела подвергали диализу (EasySEP, Tomy Seiko Co., Ltd.) против раствора, содержащего 20 мМ Tris-HCl, 150 мМ NaCl и 2 мМ CaCl2 (pH 7,4) или содержащего 20 мМ Tris-HCl, 150 мМ NaCl и 3 мкМ CaCl2 (pH 7,4) в качестве внешнего раствора. Каждый раствор антитела доводили приблизительно до 0,1 мг/мл с помощью раствора, использованного в диализе, и подвергали в качестве исследуемого вещества анализу DSC при от 20°C до 115°C со скоростью повышения температуры, установленной на 240°C/ч. В таблице 8 представлена средняя температура термической денатурации (Tm) для каждого Fab-домена антитела, вычисленная на основе полученной кривой денатурации DSC.
В результате величина Tm Fab-домена антитела, содержащего последовательность hVk1, hVk2, hVk3 или hVk4, не изменялась в зависимости от концентрации ионов кальция в растворе, содержавшем Fab-домен. Напротив, величина Tm Fab-домена антитела, содержащего последовательность hVk5, изменялась в зависимости от концентрации ионов кальция в растворе антитела, содержавшем Fab-домен, что указывает на то, что последовательность hVk5 связывается с ионами кальция.
(6-5) Оценка последовательности hVk5-2 в отношении связывания кальция
В дополнение к Vk5-2 (SEQ ID NO: 1, слитая с SEQ ID NO: 26), получали вариант 1 Vk5-2 (SEQ ID NO: 2) и вариант 2 Vk5-2 (SEQ ID NO: 3), классифицируемые как Vk5-2, согласно примеру 6(6-2). Эти варианты также оценивали в отношении связывания ими кальция. Фрагменты ДНК Vk5-2, варианта 1 Vk5-2 и варианта 2 Vk5-2 по отдельности встраивали в экспрессирующие векторы для клеток животных. Полученные экспрессирующие векторы секвенировали способом, общеизвестным специалистам в данной области. Клетки животных котрансфицировали каждым экспрессирующим вектором для клеток животных, имеющим вставку фрагмента ДНК Vk5-2, варианта 1 Vk5-2 или варианта 2 Vk5-2, и вектором для экспрессии в клетках животных, имеющим вставку ДНК, кодирующей тяжелую цепь CIM_H (SEQ ID NO: 4), для экспрессии, способом, описанным в примере 6(6-3). Полученные антитела очищали. Очищенные антитела оценивали в отношении их активности связывания ионов кальция. Очищенные антитела подвергали диализу (EasySEP, Tomy Seiko Co., Ltd.) против раствора, содержавшего 20 мМ Tris-HCl, 150 мМ NaCl, и 2 мМ CaCl2 (pH 7,5) или содержавшего 20 мМ Tris-HCl и 150 мМ NaCl (pH 7,5) (последний раствор указан как “концентрация ионов кальция”: 0 мМ в таблице 9) в качестве внешнего раствора. Каждый раствор антитела доводили приблизительно до 0,1 мг/мл с помощью раствора, используемого для диализа, и подвергали в качестве исследуемого вещества анализу DSC при от 20°C до 115°C со скоростью повышения температуры, установленной на 240°C/ч. В таблице 9 представлена средняя температура термической денатурации (Tm) каждого Fab-домена антитела, вычисленная на основе полученной кривой денатурации DSC.
В результате, величина Tm для Fab-домена антитела, содержащего последовательность Vk5-2, варианта 1 Vk5-2 или варианта 2 Vk5-2, изменялась в зависимости от концентрации ионов кальция в растворе антитела, содержащего Fab-домен, что указывает на то, что антитело, обладающее последовательностью, классифицируемой как Vk5-2, связывается с ионами кальция.
[Пример 7] Оценка последовательности Vk5 (hVk5) человека
(7-1) Последовательность hVk5
В базе данных Кабат в качестве последовательности hVk5 зарегистрирована только последовательность hVk5-2. Далее hVk5 и hVk5-2 будут использоваться синонимично. В WO2010136598 описано, что относительная распространенность последовательности hVk5-2 среди последовательностей эмбрионального типа составляет 0,4%. В других сообщениях также утверждается, что относительная распространенность последовательности hVk5-2 среди последовательностей эмбрионального типа составляет от 0 до 0,06% (J. Mol. Biol. (2000) 296, 57-86; и Proc. Natl. Acad. Sci. (2009) 106, 48, 20216-20221). Поскольку последовательность hVk5-2 имеет низкую частоту встречаемости среди последовательностей эмбрионального типа, как описано выше, получение антител со связыванием кальция из библиотеки антител, состоящей из последовательностей человека эмбрионального типа, или из B-клеток, полученных путем иммунизации мышей, экспрессирующих антитела человека, оказалось неэффективным. Это может обеспечить обоснованность конструирования Ca-библиотеки, содержащей последовательности hVk5-2 человека. Однако ранее описанные библиотеки синтетических антител (WO2010105256 или WO2010136598), не включали последовательности hVk5. Кроме того, физико-химические свойства последовательности hVk5-2 не были описаны, и ее применимость была неизвестна.
(7-2) Конструирование, экспрессия и очистка негликозилированной последовательности hVk5-2
Последовательность hVk5-2 имеет последовательность с потенциальной N-гликозилированной аминокислотой в положении 20 (определяемом посредством нумерации по Кабату). С точки зрения гомогенности вещества является желательным избегание того, чтобы белки были гликозилированными, поскольку цепи сахаров, присоединенные к белкам, вызывают гетерогенность. Таким образом, модифицированную форму hVk5-2_L65 (SEQ ID NO: 5) получали путем замены остатка Asn (N) в положении 20 (определяемом посредством нумерации по Кабату) на остаток Thr (T). Аминокислотную замену проводили способом, общеизвестным специалистам в данной области, с использованием набора для сайт-направленного мутагенеза QuikChange (Stratagene Corp.). ДНК, кодирующую модифицированную форму hVk5-2_L65, встраивали в векторы для экспрессии в клетках животных. Клетки животных котрансфицировали полученным вектором для экспрессии в клетках животных, имеющим вставку ДНК модифицированной формы hVk5-2_L65, и вектором для экспрессии в клетках животных, имеющим вставку ДНК, кодирующую тяжелую цепь CIM_H (SEQ ID NO: 4) для экспрессии, способом, описанным в примере 6. Антитело, содержащее hVk5-2_L65 и CIM_H, экспрессировалось трансфицированными клетками животных и его очищали способом, описанным в примере 6.
(7-3) Оценка антитела, содержащего негликозилированную последовательность hVk5-2, в отношении его физико-химических свойств
Анализ того, была ли снижена гетерогенность полученного антитела, содержащего модифицированную последовательность hVk5-2_L65, относительно антитела, содержащего исходную последовательность hVk5-2, которую подвергали модификации, проводили с использованием ионообменной хроматографии. Ионообменную хроматографию проводили способом, представленным в таблице 10. Результаты анализа продемонстрировали, что, как показано на фиг. 5, hVk5-2_L65, модифицированное в участке гликозилирования из исходной последовательности hVk5-2, имеет меньшую гетерогенность, чем исходная последовательность hVk5-2.
Далее, антитело, содержащее последовательность hVk5-2_L65, имеющую уменьшенную гетерогенность, оценивали в отношении ее способности связываться с ионами кальция способом, описанным в примере 6. В результате, как показано в таблице 11, величина Tm Fab-домена антитела, содержащего hVk5-2_L65, модифицированную в участке гликозилирования, также варьировала в зависимости от изменения концентрации ионов кальция в растворе антитела. Это показало, что ионы кальция связываются с Fab-доменом антитела, содержащего hVk5-2_L65, модифицированную в участке гликозилирования.
[Пример 8] Оценка молекулы антитела, содержащей последовательность CDR hVk5-2, в отношении ее активности связывания ионов кальция
(8-1) Получение, экспрессия и очистка сконструированного антитела, содержащего последовательность CDR hVk5-2
Последовательность hVk5-2_L65 представляет собой последовательность, модифицированную из последовательности Vk5-2 человека путем аминокислотной замены в участке гликозилирования в каркасной области. В примере 7 показано, что ионы кальция связываются даже с антителом, содержащим последовательность, модифицированную в участке гликозилирования. Как правило, последовательности эмбрионального типа были желательными в качестве каркасных последовательностей, с точки зрения иммуногенности. Таким образом, проводили исследование в отношении того можно ли заменить каркасные последовательности антитела негликозилированными каркасными последовательностями эмбрионального типа при сохранении активности связывания антителом ионов кальция.
Полинуклеотид, кодирующий последовательность, модифицированную из химически синтезированной последовательности hVk5-2, путем замены в ней каркасных последовательностей на последовательности hVk1, hVk2, hVk3 или hVk4 (модифицированные последовательности конструировали в качестве CaVk1 (SEQ ID NO: 31), CaVk2 (SEQ ID NO: 32), CaVk3 (SEQ ID NO: 33) и CaVk4 (SEQ ID NO: 34), соответственно) связывали способом ПЦР с полинуклеотидом, кодирующим природную константную область цепи каппа (SEQ ID NO: 26). Полученные фрагменты ДНК по отдельности встраивали в векторы для экспрессии в клетках животных. Последовательности полученных модифицированных форм подтверждали способом, общеизвестным специалистам в данной области. Клетки животных котрансфицировали каждой плазмидой, полученной таким образом, и плазмидой, имеющей вставку полинуклеотида, кодирующего CIM_H (SEQ ID NO: 4), способом, описанным в примере 6. Желаемые молекулы антител, экспрессированные таким образом, очищали из культуральной жидкости трансфицированных клеток животных.
(8-2) Оценка сконструированного антитела, содержащего последовательность hVk5-2 CDR, в отношении его активности связывания ионов кальция
Сконструированные антитела, содержащие каркасные последовательности из последовательности эмбрионального типа (hVk1, hVk2, hVk3 или hVk4), отличной от последовательности hVk5-2, и последовательности CDR из последовательности hVk5-2, оценивали в отношении их способности связываться с ионами кальция способом, описанным в примере 6. Результаты оценки представлены в таблице 12. Было показано, что величина Tm для Fab-домена каждого полученного антитела варьирует в зависимости от изменения концентрации ионов кальция в растворе антитела. Эти результаты продемонстрировали, что антитело, содержащее каркасные последовательности, отличные от каркасных последовательностей hVk5-2, также связывается с ионами кальция.
Как далее очевидно из результатов, температура термической денатурации (Tm), показатель термической стабильности, Fab-домена каждого антитела, модифицированного так, чтобы оно содержало каркасные последовательности из последовательности эмбрионального типа (hVk1, hVk2, hVk3, или hVk4), отличной от последовательности hVk5-2, и последовательности CDR из последовательности hVk5-2, была более высокой, чем у Fab-домена антитела, содержащего исходную последовательность hVk5-2, которую подвергали модификации. Из этого результата, было выявлено, что антитело, содержащее каркасные последовательности hVk1, hVk2, hVk3 или hVk4 и последовательности CDR hVk5-2, представляет собой молекулу, которая обладает свойством связывания ионов кальция и также является превосходным с точки зрения термической стабильности.
[Пример 9] Идентификация участка связывания ионов кальция, присутствующего в последовательности эмбрионального типа человека hVk5-2
(9-1) Конструирование участка мутации в последовательности CDR последовательности hVk5-2
Как описано в примере 8, также показано, что антитела, содержащие легкие цепи с доменами CDR последовательности hVk5-2, встроенными в каркасные последовательности отличающейся последовательности эмбрионального типа, связываются с ионами кальция. Этот результат указывает на то, что участок связывания ионов кальция, присутствующий в hVk5-2, был расположен в CDR. Примеры аминокислот, связывающихся с ионами кальциями, т.е. хелатирующих ионы кальция, включают отрицательно заряженные аминокислоты и аминокислоты, которые могут служить в качестве акцепторов водородной связи. Таким образом, антитела, содержащие вариант последовательности hVk5-2, полученный мутацией последовательности hVk5-2 путем замены остатков Asp (D) и/или Glu (E) в последовательностях CDR на остатки Ala (A), оценивали в отношении их способности связываться с ионами кальция.
(9-2) Получение варианта последовательности hVk5-2 с заменой на Ala и экспрессия и очистка антител
Получали молекулы антител, которые содержали модифицированные легкие цепи с остатками Ala вместо остатков Asp и/или Glu, присутствующих в последовательностях CDR hVk5-2. Как описано в примере 7, негликозилированная модифицированная форма hVk5-2_L65 сохраняла связывание ионов кальция и, таким образом, оказалась эквивалентной последовательности hVk5-2 с точки зрения свойства связывания ионов кальция. В этом примере аминокислотную замену проводили с hVk5-2_L65 в качестве матричной последовательности. Полученные модифицированные формы представлены в таблице 13. Аминокислотную замену проводили способом, общеизвестным специалистам в данной области, с использованием набора для сайт-направленного мутагенеза QuikChange (Stratagene Corp.), набора для клонирования способом ПЦР In fusion Advantage PCR cloning kit (Takara Bio Inc.) и т.п. Конструировали экспрессирующие векторы для легких цепей, модифицированные посредством аминокислотной замены.
Полученные экспрессирующие векторы секвенировали способом, общеизвестным специалистам в данной области. Линию клеток, происходящих из почки эмбриона человека HEK293H (Invitrogen Corp.) или клетки FreeStyle 293 (Invitrogen Corp.) временно котрансфицировали полученным экспрессирующим вектором для каждой модифицированной легкой цепи и экспрессирующим вектором для тяжелой цепи CIM_H (SEQ ID NO: 4) для экспрессии антител. Каждое антитело очищали от полученного культурального супернатанта способом, общеизвестным специалистам в данной области, с использованием rProtein A Sepharose(TM) Fast Flow (GE Healthcare Bio-Sciences Corp.). Поглощение очищенного раствора антител измеряли при 280 нм с использованием спектрофотометра. Концентрацию антитела вычисляли из полученной величины измерения с использованием коэффициента экстинкции, вычисленного с помощью PACE (Protein Science (1995) 4, 2411-2423).
(9-3) Оценка антитела, содержащего вариант последовательности hVk5-2 с заменой на Ala, в отношении его активности связывания ионов кальция
Определение того, связываются ли полученные очищенные антитела с ионами кальция, проводили способом, описанным в примере 6. Результаты представлены в таблице 14. Величины Tm для Fab-доменов некоторых антител не изменялись в зависимости от концентрации ионов кальция в растворах антител, в результате замены Asp и/или Glu, присутствующих в последовательностях CDR последовательности hVk5-2, на остатки Ala, которые были неспособны участвовать в связывании или хелатировании ионов кальция. Было показано, что участки замены, которые не вызывали изменение величин Tm даже при замене на Ala (положения 32 и 92 (определяемые посредством нумерации по Кабату)), являются особенно важными для связывания антителами ионов кальция.
[Пример 10] Оценка антитела, содержащего последовательность hVk1, имеющую мотив, связывающий ион кальция
(10-1) Получение последовательности hVk1, имеющей мотив, связывающий ионы кальция, и экспрессия и очистка антител
Результаты для активности связывания кальция у вариантов с заменой на Ala, описанных в примере 9, показали, что остатки Asp и Glu последовательностей CDR в последовательности hVk5-2 важны для связывания кальция. Таким образом, антитела, полученные путем встраивания только остатков 30, 31, 32, 50 и 92 (определяемых посредством нумерации по Кабату) в последовательность вариабельной области отличающейся последовательности эмбрионального типа, оценивали в отношении их способности связываться с ионами кальция. В частности, модифицированную форму LfVk1_Ca (SEQ ID NO: 43) получали путем замены остатков 30, 31, 32, 50 и 92 (определяемых посредством нумерации по Кабату) в последовательности эмбрионального типа человека hVk1 на остатки 30, 31, 32, 50 и 92 (определяемые посредством нумерации по Кабату) в последовательности hVk5-2. Присутствие или отсутствие способности связывать кальций определяли в отношении антитела, содержащего последовательность hVk1 только с этими пятью встроенными в нее остатками, происходящими из последовательности hVk5-2. Получение модифицированной формы проводили аналогично примеру 9. Полученную таким образом модифицированную легкую цепь LfVk1_Ca или LfVk1 (SEQ ID NO: 44), содержащую последовательность легкой цепи hVk1, коэкспрессировали с тяжелой цепью CIM_H (SEQ ID NO: 4). Экспрессию и очистку антител проводили аналогично тому, как в примере 9.
(10-2) Оценка антитела, содержащего последовательность человека hVk1, имеющую мотив, связывающий ионы кальция, в отношении его активности связывания ионов кальция
Определение того, связываются ли очищенные антитела, полученные таким образом, с ионами кальция, проводили способом, описанным в примере 6. Результаты представлены в таблице 15. Величина Tm Fab-домена антитела, содержащего LfVk1, имеющую последовательность hVk1, не изменялась в зависимости от изменения концентрации ионов кальция в растворе антитела. Напротив, величина Tm последовательности антитела, содержащего LfVk1_Ca, изменялась на 1°C или более в зависимости от изменения концентрации кальция в растворе антитела, что указывает на то, что антитело, содержащее LfVk1_Ca, связывается с кальцием. Эти результаты продемонстрировали, что не вся последовательность CDR hVk5-2 требуется для связывания ионов кальция и для связывания достаточно только остатков, внесенных для конструирования последовательности LfVk1_Ca.
(10-3) Конструирование, экспрессия и очистка недеградируемой последовательности LfVk1_Ca
В примере 10(10-1) модифицированную форму LfVk1_Ca (SEQ ID NO: 43) получали путем замены остатков 30, 31, 32, 50 и 92 (определяемых посредством нумерации по Кабату) в последовательности человека эмбрионального типа hVk1 на остатки 30, 31, 32, 50, и 92 (определяемые посредством нумерации по Кабату) в последовательности hVk5-2, и показано, что она связывалась с ионами кальция. Это может обеспечить обоснованность конструирования Ca-библиотеки, содержащей последовательности LfVk1_Ca. Поскольку физико-химические свойства последовательности LfVk1_Ca не описаны, ее применимость неизвестна. Последовательность LfVk1_Ca содержала Asp в положениях 30, 31 и 32 (определяемые посредством нумерации по Кабату) и содержала в ее последовательности CDR1 последовательность Asp-Asp, которая, согласно сообщениям, является деградируемой в кислых условиях (J. Pharm. Biomed. Anal. (2008) 47 (1), 23-30). С точки зрения стабильности при хранении, желательно избежать деградации в кислых условиях. Таким образом, модифицированные формы LfVk1_Ca1 (SEQ ID NO: 45), LfVk1_Ca2 (SEQ ID NO: 46) и LfVk1_Ca3 (SEQ ID NO: 47) получали путем замены деградируемых остатков Asp (D) на остатки Ala (A). Замену аминокислот проводили способом, общеизвестным специалистам в данной области, с использованием набора для сайт-направленного мутагенеза QuikChange (Stratagene Corp.). ДНК, кодирующую каждую форму, встраивали в векторы для экспрессии в клетках животных. Клетки животных котрансфицировали полученным вектором для экспрессии в клетках животных, имеющих вставку ДНК каждой модифицированной формы, и вектором для экспрессии в клетках животных, имеющим вставку ДНК, кодирующую тяжелую цепь GC_H (SEQ ID NO: 48) для экспрессии, способом, описанным в примере 6. Антитела, экспрессируемые в трансфицированных клетках животных очищали способом, описанным в примере 6.
(10-4) Оценка стабильности антитела, содержащего недеградируемую последовательность LfVk1_Ca
Оценку того, снижалась ли деградация каждого антитела, полученного согласно примеру 10(10-3), в растворе при pH 6,0 по сравнению с антителом, содержащим исходную последовательность LfVk1_Ca, подвергнутую модификации, проводили путем сравнения гетерогенности антител после термического ускорения. Каждое антитело подвергали диализу в течение ночи против раствора, содержавшего 20 мМ гистидин-HCl и 150 мМ NaCl (pH 6,0) в условиях 4°C. Подвергнутое диализу антитело доводили до 0,5 мг/мл и хранили при 5°C или 50°C в течение 3 суток. Каждое антитело, хранившееся таким образом, подвергали ионообменной хроматографии способом, описанным в примере 7. Результаты анализа продемонстрировали, что, как показано на фиг. 6, LfVk1_Ca1, модифицированная в участке деградации, имеет меньшую гетерогенность, чем исходная последовательность LfVk1_Ca, и ее деградация при термическом ускорении значительно снижается. Эти результаты продемонстрировали, что деградация происходит в остатке Asp (D), расположенном в положении 30 в последовательности LfVk1_Ca, и ее можно избежать путем модификации аминокислот.
(10-5) Получение недеградируемой по остатку Asp30 последовательности легкой цепи LVk1_Ca и экспрессия и очистка антител
Результаты ингибирования деградации варианта с заменой Ala, описанного в примере 10(10-4), показали, что деградация в кислых условиях происходит по остатку Asp (D) в положении 30 (определяемом посредством нумерации по Кабату) в последовательности CDR последовательности LfVk1_Ca и ее можно ингибировать путем замены остатка 30 (определяемого посредством нумерации по Кабату) на другую аминокислоту (в примере 10(10-4), на остаток Ala (A)). Таким образом, последовательность (обозначаемая как LfVk1_Ca6; SEQ ID NO: 49), полученную путем замены остатка 30 (определяемого посредством нумерации по Кабату) на остаток Ser (S) - типичный остаток, способный хелатировать ионы кальция, оценивали в отношении присутствия или отсутствия ингибирования деградации. Получение модифицированной формы проводили аналогично тому, как в примере 10. Полученную модифицированную последовательность легкой цепи LfVk1_Ca6 или последовательность легкой цепи LfVk1_Ca коэкспрессировали с тяжелой цепью GC_H (SEQ ID NO: 48). Экспрессию и очистку антитела проводили аналогично тому, как в примере 10.
(10-6) Оценка недеградируемой по остатку Asp30 последовательности легкой цепи LVk1_Ca
Стабильность при хранении очищенных антител, полученных таким образом, в кислых условиях определяли способом, описанным в примере 10(10-4). Результаты продемонстрировали, что, как показано на фиг. 7, деградация антитела, содержащего последовательность LfVk1_Ca6, в большей степени ингибировалась, чем деградация антитела, содержащего исходную последовательность LfVk1_Ca.
Кроме того, определение того, связывается ли антитело, содержащее последовательность LfVk1_Ca, и антитело, содержащее последовательность LfVk1_Ca6, с ионами кальция, проводили способом, описанным в примере 6. Результаты представлены в таблице 16. Величины Tm для Fab-доменов антитела, содержащего последовательность LfVk1_Ca и антитела, содержащего недеградируемую последовательность LfVk1_Ca6, в каждом случае изменялись на 1°C или более в зависимости от концентрации кальция в растворах антител.
[Пример 11] Конструирование набора (Ca-библиотека) молекул антител, содержащих мотивы, связывающие ионы кальция, в вариабельных областях, которые позволяют эффективное получение связывающего антитела, которое связывается с антигеном зависимым от концентрации ионов кальция образом
Предпочтительные примеры кальций-связывающих мотивов включают последовательность hVk5-2 и ее последовательности CDR, и, кроме того, выбранные остатки 30, 31, 32, 50 и 92 (определяемые посредством нумерации по Кабату). Кроме того, мотив EF hand (кальмодулин, и т.д.) кальций-связывающего белка и лектин C-типа (ASGPR, и т.д.) также соответствуют кальций-связывающим мотивам.
Ca-библиотеку конструируют с помощью вариабельных областей тяжелых и легких цепей. Используемые вариабельные области тяжелой цепи представляли собой последовательности антител человека, в то время как в вариабельные области легкой цепи встраивали кальций-связывающие мотивы. Последовательность hVk1 была выбрана в качестве матричной последовательности вариабельной области тяжелой цепи для внесения кальций-связывающего мотива. Как показано в примере 10, было показано, что антитело, содержащее последовательность LfVk1_Ca, в которой в последовательность hVk1 в качестве кальций-связывающего мотива внесена последовательность CDR hVk5-2, связывается с ионами кальция. В матричной последовательности в каждом данном положении позволяли появиться различным аминокислотам для расширения разнообразия антигенсвязывающих молекул, составляющих библиотеку. Экспонированные на поверхности положения в вариабельных областях, которые вероятно будут взаимодействовать с антигенами, выбирали в качестве положения для появления множества аминокислот. В частности, в качестве таких нестрогих остатков были выбраны положения 30, 31, 32, 34, 50, 53, 91, 92, 93, 94 и 96 (определяемые посредством нумерации по Кабату).
Далее, выбирали типы и встречаемость аминокислотных остатков, подлежащих появлению. Аминокислоты нестрогих остатков анализировали в отношении их частоты встречаемости в последовательностях hVk1 и hVk3, зарегистрированных в базе данных Кабат (KABAT, E.A. et al.: “Sequences of Proteins of Immunological interest”, vol. 91, 1991, NIH PUBLICATION). Исходя из результатов анализа, типы аминокислот, появляющихся в Ca-библиотеке, выбирали из аминокислот с высокой частотой появления в каждом положении. В этой методике также выбирали аминокислоты, для которых было подтверждено, что они обладают низкой частотой встречаемости, исходя из результатов анализа, чтобы предотвратить нарушение баланса свойств аминокислот. Частота встречаемости выбранных аминокислот была выбрана на основании результатов анализа базы данных Кабат.
Учитывая выбранные таким образом аминокислоты и их частоту встречаемости, была сконструирована следующая Ca-библиотека: Ca-библиотека, которая была акцентирована на разнообразии последовательностей так, чтобы она содержала кальций-связывающие мотивы и множество аминокислот в каждом остатке, отличном от мотивов. Детальная конструкция Ca-библиотеки представлена в таблицах 17 и 18 (“Положение” в каждой таблице отражает нумерацию по Кабату). Частота появления аминокислот, описанных в таблицах 17 и 18, может включать Leu (L) вместо Ser (S) в положении 94, определяемом посредством нумерации по Кабату, в случае Asn (N) в положении 92.


[Пример 12] Получение Ca-библиотеки
Библиотеку генов вариабельных областей тяжелой цепи антитела амплифицировали способом ПЦР с использованием поли-A РНК, полученной из PBMC человека, коммерчески доступной поли-A РНК человека, и т.п. в качестве матрицы. Части легких цепей для вариабельных областей антитела конструировали так, чтобы увеличить частоту встречаемости антител, которые сохраняли кальций-связывающие мотивы и были способны связываться с антигенами зависимым от концентрации кальция образом, как описано в примере 11. Библиотеку вариабельных областей легкой цепи антитела конструировали в соответствии с информацией о частоте встречаемости аминокислот в природных антителах человека (KABAT, E.A. et al.: “Sequences of Proteins of Immunological interest”, vol. 91, 1991, NIH PUBLICATION), так что аминокислоты с высокой частотой встречаемости в природных последовательностях антител человека были равномерно распределены в качестве аминокислотных остатков, отличных от остатков с встроенным кальций-связывающим мотивом, среди нестрогих остатков. Комбинации последовательностей в библиотеке генов вариабельных областей тяжелой цепи антител и в библиотеке генов вариабельных областей легкой цепи антитела, полученные таким образом, встраивали в фагмидные векторы. Конструировали библиотеку фагового дисплея антител человека, экспонирующую Fab-домены, состоящие из последовательностей антител человека (Methods Mol Biol. (2002) 178, 87-100).
Части генов антител, выделенные из E. coli, трансформированных библиотекой генов антител, секвенировали в соответствии со способом, описанным в примере 2. На фиг. 8 представлено распределение аминокислот в последовательностях 290 типов клонов, полученных таким образом, и модельное распределение аминокислот.
[Пример 13] Оценка молекулы, содержащейся в Ca-библиотеке, в отношении ее активности связывания ионов кальция
(13-1) Активность связывания ионов кальция молекулы, содержащейся в Ca-библиотеке
Поскольку последовательность hVk5-2, для которой показано, что она связывается с ионами кальция, имеет низкую частоту встречаемости среди последовательностей эмбрионального типа, как показано в примере 7, получение связывающих кальций антител из библиотеки антител, состоящей из последовательностей человека эмбрионального типа или из B-клеток, полученных путем иммунизации мышей, экспрессирующих антитела человека, оказалось неэффективным. Таким образом, конструировали Ca-библиотеку согласно примеру 12. Сконструированную Ca-библиотеку оценивали в отношении присутствия или отсутствия клонов, проявляющих связывание кальция.
(13-2) Экспрессия и очистка антитела
Ген каждого клона, содержащегося в Ca-библиотеке, встраивали в плазмиды для экспрессии в клетках животных. Экспрессию антител проводили следующим способом: линию FreeStyle 293-F, происходящую из почки эмбриона человека, (Invitrogen Corp.) суспендировали в среде для экспрессии FreeStyle 293 Expression Medium (Invitrogen Corp.). Суспензию, имеющую плотность клеток 1,33×106 клеток/мл, инокулировали в концентрации 3 мл/лунка в планшет с 6 ячейками. Полученные плазмиды переносили в клетки путем липофекции. Клетки культивировали в течение 4 суток в инкубаторе с CO2 (37°C, 8% CO2, 90 об./мин.). Антитела очищали из полученного культурального супернатанта способом, общеизвестным специалистам в данной области, с использованием rProtein A Sepharose(TM) Fast Flow (Amersham Biosciences, Inc.). Поглощение очищенного раствора антител измеряли при 280 нм с использованием спектрофотометра. Концентрацию антитела вычисляли из полученной величины измерения с использованием коэффициента экстинкции, вычисленного с помощью PACE (Protein Science (1995) 4, 2411-2423).
(13-3) Оценка полученного антитела в отношении связывания им ионов кальция
Определение того, связывались ли очищенные антитела, полученные таким образом, с ионами кальция, проводили способом, описанным в примере 6. Результаты представлены в таблице 19. Величины Tm для Fab-доменов множества антител, содержащихся в Ca-библиотеки, изменялись в зависимости от концентрации ионов кальция, указывая на то, что Ca-библиотека содержит молекулы, связывающиеся с ионами кальция.
[Пример 14] Получение антитела, связывающегося с рецептором IL-6 Ca-зависимым образом
(14-1) Получение фрагмента антитела, связывающегося с антигеном Ca-зависимым образом, из библиотеки способом пэннинга на гранулах
Первый раунд скрининга сконструированной Ca-библиотеки проводили путем увеличения содержания только фрагментов антител, обладающих способностью связывать антиген (IL-6R).
Фаги получали из E. coli, содержавших сконструированную фагмиду для фагового дисплея. К культурам E. coli, которые продуцировали фаги, добавляли 2,5 M NaCl/10% PEG, и совокупность фагов, преципитированных таким образом, разбавляли TBS, получая раствор с фаговой библиотекой. К раствору с фаговой библиотекой добавляли BSA и CaCl2, (конечная концентрация: 4% BSA и 1,2 мМ ионы кальция). Способ пэннинга проводили в соответствии с общепринятым способом пэннинга с использованием антигенов, иммобилизованных на магнитных гранулах (J. Immunol. Methods. (2008) 332 (1-2), 2-9; J. Immunol. Methods. (2001) 247 (1-2), 191-203; Biotechnol. Prog. (2002) 18 (2) 212-20; и Mol. Cell Proteomics (2003) 2 (2), 61-9). Использованные магнитные гранулы представляли собой покрытые нейтравидином гранулы (Sera-Mag SpeedBeads NeutrAvidin-coated) или покрытые стрептавидином гранулы (Dynabeads M-280 Streptavidin).
В частности, 250 пмоль меченных биотином антигенов добавляли к полученному раствору с фаговой библиотекой и, тем самым, приводили в контакт с раствором с фаговой библиотекой при комнатной температуре в течение 60 минут. Добавляли блокированные BSA магнитные гранулы, а затем комплексы антиген-фаг связывали с магнитными гранулами при комнатной температуре в течение 15 минут. Гранулы промывали три раза 1 мл 1,2 мМ CaCl2/TBST (TBST, содержащий 1,2 мМ CaCl2), а затем дополнительно промывали два раза 1 мл 1,2 мМ CaCl2/TBS (TBS, содержащий 1,2 мМ CaCl2). После добавления 0,5 мл 1 мг/мл трипсина, гранулы суспендировали при комнатной температуре в течение 15 минут, и сразу после этого гранулы отделяли с использованием магнитного стенда для сбора раствора с фагами. Собранный раствор с фагами добавляли к 10 мл штамма E. coli ER2738 на логарифмической фазе роста (OD600: 0,4-0,7). Штамм E. coli инфицировали фагами при осторожном вращении культуры штамма при 37°C в течение 1 часа. Инфицированные E. coli инокулировали на чашку 225 мм × 225 мм. Далее из культур инокулированных E. coli собирали фаги, получая раствор с фаговой библиотекой.
На втором раунде пэннинга увеличивали содержание фагов с антигенсвязывающей способностью или способностью к Ca-зависимому связыванию в качестве показателя.
В частности, для увеличения содержания с антигенсвязывающей способностью в качестве показателя, 40 пмоль меченных биотином антигенов добавляли к полученному раствору с фаговой библиотекой и, тем самым, приводили в контакт с раствором с фаговой библиотекой при комнатной температуре в течение 60 минут. Добавляли блокированные BSA магнитные гранулы, а затем комплексы антиген-фаг связывали с магнитными гранулами при комнатной температуре в течение 15 минут. Гранулы промывали несколько раз 1 мл 1,2 мМ CaCl2/TBST и 1,2 мМ CaCl2/TBS. Затем гранулы, дополненные 0,5 мл 1 мг/мл трипсина, суспендировали при комнатной температуре в течение 15 минут, и сразу после этого гранулы отделяли с использованием магнитного стенда для сбора раствора с фагами. Добавление 5 мкл 100 мг/мл трипсина к собранному раствору с фагами расщепляло белки pIII (белки pIII, происходящие из хелперного фага) не экспонирующих Fab фагов для устранения способности не экспонирующих Fab фагов инфицировать E. coli. Собранный раствор с фагами добавляли к 10 мл штамма E. coli ER2738 на логарифмической фазе роста (OD600: 0,4-0,7). Штамм E. coli инфицировали фагами при осторожном вращении культуры штамма при 37°C в течение 1 часа. Инфицированные E. coli инокулировали на чашку 225 мм × 225 мм. Далее из культур инокулированных E. coli собирали фаги, получая раствор с фаговой библиотекой.
Для увеличения содержания со способностью к Ca-зависимому связыванию в качестве показателя, 40 пмоль меченных биотином антигенов добавляли к полученному раствору с фаговой библиотекой и, тем самым, приводили в контакт с раствором с фаговой библиотекой при комнатной температуре в течение 60 минут. Добавляли блокированные BSA магнитные гранулы, а затем комплексы антиген-фаг связывали с магнитными гранулами при комнатной температуре в течение 15 минут. Гранулы промывали 1 мл 1,2 мМ CaCl2/TBST и 1,2 мМ CaCl2/TBS. Затем гранулы, дополненные 0,1 мл 2 мМ EDTA/TBS (TBS, содержащий 2 мМ EDTA), суспендировали при комнатной температуре. Сразу после этого гранулы отделяли с использованием магнитного стенда для сбора раствора с фагами. Добавление 5 мкл 100 мг/мл трипсина к собранному раствору с фагами расщепляло белки pIII (белки pIII, происходящие из хелперного фага) не экспонирующих Fab фагов для устранения способности не экспонирующих Fab фагов инфицировать E. coli. Собранный раствор с фагами добавляли к 10 мл штамма E. coli ER2738 на логарифмической фазе роста (OD600: 0,4-0,7). Штамм E. coli инфицировали фагами при осторожном вращении культуры штамма при 37°C в течение 1 часа. Инфицированные E. coli инокулировали на чашку 225 мм × 225 мм. Далее из культур инокулированных E. coli собирали фаги, получая раствор с фаговой библиотекой.
(14-2) Оценка с помощью ELISA фагов
Содержащий фаг культуральный супернатант получали в соответствии с общепринятым способом (Methods Mol. Biol. (2002) 178, 133-145) из каждой единичной колонии E. coli, полученной с помощью описанного выше способа.
После добавления BSA и CaCl2, содержащий фаг культуральный супернатант подвергали ELISA по следующей методике: микропланшет для титрования StreptaWell 96 (F. Hoffmann-La Roche Ltd.) покрывали в течение ночи 100 мкл PBS, содержавшего меченные биотином антигены. Каждую лунку планшета промывали PBST для удаления не связавшихся антигенов. Затем лунку блокировали 250 мкл 4% BSA-TBS в течение 1 часа или более. После удаления 4% BSA-TBS, полученный супернатант добавляли в каждую лунку, и планшет оставляли стоять при 37°C в течение 1 часа для связывания экспонируемых фагом антител с антигенами, содержащимися в каждой лунке. Каждую лунку промывали 1,2 мМ CaCl2/TBST, и добавляли 1,2 мМ CaCl2/TBS или 1 мМ EDTA/TBS. Планшет оставляли стоять при 37°C в течение 30 минут для инкубации. После промывания 1,2 мМ CaCl2/TBST в каждую лунку добавляли конъюгированные с HRP антитела против M13 (Amersham Pharmacia Biotech Inc.), разбавленные TBS, имеющим ионизированный кальций в концентрации 1,2 мМ. Планшет инкубировали в течение 1 часа. После промывания 1,2 мМ CaCl2/TBST, в каждую лунку добавляли простой раствор TMB (ZYMED Laboratories, Inc.). Хромогенную реакцию раствора в каждой лунке завершали добавлением серной кислоты. Затем развитие цвета анализировали на основе поглощения при 450 нм.
Гены клонов, подвергнутых ELISA фагов, амплифицировали с использованием специфических праймеров, а затем анализировали в отношении их нуклеотидных последовательностей. Результаты ELISA фагов и анализа последовательностей представлены ниже в таблице 20.
(14-3) Экспрессия и очистка антитела
Ген каждого клона, оцененного как обладающий способностью к Ca-зависимому связыванию антигена в результате ELISA фагов, встраивали в плазмиды для экспрессии в клетках животных. Экспрессию антител проводили следующим способом: линию FreeStyle 293-F, происходящую из почки эмбриона человека, (Invitrogen Corp.) суспендировали в среде для экспрессии FreeStyle 293 Expression Medium (Invitrogen Corp.). Суспензию, имеющую плотность клеток 1,33×106 клеток/мл, инокулировали в концентрации 3 мл/лунка в планшет с 6 ячейками. Полученные плазмиды переносили в клетки путем липофекции. Клетки культивировали в течение 4 суток в инкубаторе с CO2 (37°C, 8% CO2, 90 об./мин.). Антитела очищали из полученного культурального супернатанта способом, общеизвестным специалистам в данной области, с использованием rProtein A Sepharose(TM) Fast Flow (Amersham Biosciences, Inc.). Поглощение очищенного раствора антител измеряли при 280 нм с использованием спектрофотометра. Концентрацию антитела вычисляли из полученной величины измерения с использованием коэффициента экстинкции, вычисленного с помощью PACE (Protein Science (1995) 4, 2411-2423).
(14-4) Оценка полученного антитела в отношении его способности к Ca-зависимому связыванию с рецептором IL-6 человека
Для оценки зависимости от Ca активности связывания рецептора IL-6 человека антител 6RC1IgG_010 (тяжелая цепь: SEQ ID NO: 72 и легкая цепь: SEQ ID NO: 73), 6RC1IgG_012 (тяжелая цепь: SEQ ID NO: 74 и легкая цепь: SEQ ID NO: 75) и 6RC1IgG_019 (тяжелая цепь: SEQ ID NO: 76 и легкая цепь: SEQ ID NO: 77), полученных согласно примеру 14, эти антитела анализировали в отношении их взаимодействия с рецепторами IL-6 человека с использованием Biacore T100 (GE Healthcare Bio-Sciences Corp.). В качестве контрольного антитела, не обладающего активностью Ca-зависимого связывания с рецепторами IL-6 человека, использовали тоцилизумаб (тяжелая цепь: SEQ ID NO: 24 и легкая цепь: SEQ ID NO: 25). Взаимодействие анализировали в растворах с концентрациями ионов кальция 1,2 мМ и 3 мкМ в качестве условий высокой концентрации ионов кальция и низкой концентрации ионов кальция, соответственно. Каждое представляющее интерес антитело улавливали на сенсорном чипе CM5 (GE Healthcare Bio-Sciences Corp.) с иммобилизованным на нем белком A/G (Invitrogen Corp.), в соответствующем количестве способом присоединения аминов. Использовали два типа подвижных буферов: 20 мМ ACES, 150 мМ NaCl, 0,05% (масс./об.) Tween 20, и 1,2 мМ CaCl2 (pH 7,4); и 20 мМ ACES, 150 мМ NaCl, 0,05% (масс./об.) Tween 20, и 3 мкМ CaCl2(pH 7,4). Рецепторы IL-6 человека также разбавляли с помощью каждого из этих буферов. Эти анализы все проводили при 37°C.
В анализе взаимодействия в реакции антиген-антитело с использованием контрольного антитела тоцилизумаба, антитела 6RC1IgG_010, антитела 6RC1IgG_012 и антитела 6RC1IgG_019, разбавленный раствор рецептора IL-6 или пустой подвижный буфер инжектировали со скоростью потока 5 мкл/мин в течение 3 минут для взаимодействия рецепторов IL-6 с антителом тоцилизумабом, антителом 6RC1IgG_010, антителом 6RC1IgG_012 или антителом 6RC1IgG_019, уловленными на сенсорном чипе. Затем на него инжектировали 10 мМ глицин-HCl (pH 1,5) со скоростью потока 30 мкл/мин в течение 30 секунд, чтобы регенерировать сенсорный чип.
На фиг. 9 представлены сенсограммы для антител, проанализированных при высокой концентрации ионов кальция с помощью этого способа.
Сенсограммы для антитела тоцилизумаба, антитела 6RC1IgG_010, антитела 6RC1IgG_012 и антитела 6RC1IgG_019 в условиях низкой концентрации ионов кальция также получали сходным способом. На фиг. 10 представлены сенсограммы антител при низкой концентрации ионов кальция.
В результате, было выявлено, что способность связывать рецептор IL6 антитела 6RC1IgG_010, антитела 6RC1IgG_012 и антитела 6RC1IgG_019 значительно снижалась при изменении концентрации ионов кальция в буфере от 1,2 мМ до 3 мкМ.
[Пример 15] Получение антитела, связывающегося с рецептором IL-6 Ca-зависимым образом, из библиотеки антител человека с использованием технологии фагового дисплея
(15-1) Получение библиотеки фагового дисплея наивных антител человека
Библиотеку фагового дисплея антител человека, состоящую из множества фагов, экспонирующих Fab-домены, обладающие различными последовательностями антител человека, конструировали в соответствии со способом, общеизвестным специалистам в данной области, с использованием поли-A РНК, полученной из PBMC человека, коммерчески доступной поли-A РНК человека, и т.п. в качестве матрицы.
(15-2) Получение фрагмента антитела, связывающегося с антигеном Ca-зависимым образом, из библиотеки способом пэннинга на гранулах
Первый раунд скрининга сконструированной библиотеки фагового дисплея наивных антител человека проводили путем увеличения содержания только фрагментов антител, обладающих способностью связывать антиген (IL-6R), или путем увеличения содержания фрагментов антител со способностью к зависимому от концентрации Ca связыванию антигена (рецептора IL-6). Увеличение содержания фрагментов антител со способностью к зависимому от концентрации Ca связыванию антигена (рецептор IL-6) в качестве показателя проводили путем элюирования фагов из фаговой библиотеки, связанной с рецепторами IL-6, в присутствии ионов Ca с использованием EDTA хелатирующих Ca ионов. Используемые антигены представляли собой меченные биотином рецепторы IL-6.
Фаги получали из E. coli, содержавших сконструированную фагмиду для фагового дисплея. К культурам E. coli, которые продуцировали фаги, добавляли 2,5 M NaCl/10% PEG, и совокупность фагов, преципитированных таким образом, разбавляли TBS, получая раствор с фаговой библиотекой. Далее, к раствору с фаговой библиотекой добавляли BSA и CaCl2, (конечная концентрация: 4% BSA и 1,2 мМ ионы кальция). Способ пэннинга проводили в соответствии с общепринятым способом пэннинга с использованием антигенов, иммобилизованных на магнитных гранулах (J. Immunol. Methods. (2008) 332 (1-2), 2-9; J. Immunol. Methods. (2001) 247 (1-2), 191-203; Biotechnol. Prog. (2002) 18 (2) 212-20; и Mol. Cell Proteomics (2003) 2 (2), 61-9). Использованные магнитные гранулы представляли собой покрытые нейтравидином гранулы (Sera-Mag SpeedBeads NeutrAvidin-coated) или покрытые стрептавидином гранулы (Dynabeads M-280 Streptavidin).
В частности, 250 пмоль меченных биотином антигенов добавляли к полученному раствору с фаговой библиотекой и, тем самым, приводили в контакт с раствором с фаговой библиотекой при комнатной температуре в течение 60 минут. Добавляли блокированные BSA магнитные гранулы, а затем комплексы антиген-фаг связывали с магнитными гранулами при комнатной температуре в течение 15 минут. Гранулы промывали один раз 1 мл 1,2 мМ CaCl2/TBS (TBS, содержащий 1,2 мМ CaCl2). Затем собирали раствор с фагом путем элюирования в соответствии с общим способом для увеличения содержания фрагментов антител, обладающих способностью связывания рецептора IL-6, или путем элюирования с гранул, суспендированных в 2 мМ EDTA/TBS (TBS, содержащий 2 мМ EDTA) для увеличения содержания фрагментов антител со способностью к зависимому от концентрации Ca связыванию рецептора IL-6 в качестве показателя. Собранный раствор с фагами добавляли к 10 мл штамма E. coli TG1 на логарифмической фазе роста (OD600: 0,4-0,7). Штамм E. coli инфицировали фагами при осторожном вращении культуры штамма при 37°C в течение 1 часа. Инфицированные E. coli инокулировали на чашку 225 мм × 225 мм. Далее из культур инокулированных E. coli собирали фаги, получая раствор с фаговой библиотекой.
На втором и последующих раундах пэннинга увеличивали содержание фагов со способностью к Ca-зависимому связыванию в качестве показателя. В частности, 40 пмоль меченных биотином антигенов добавляли к полученному раствору с фаговой библиотекой и, тем самым, приводили в контакт с раствором с фаговой библиотекой при комнатной температуре в течение 60 минут. Добавляли блокированные BSA магнитные гранулы, а затем комплексы антиген-фаг связывали с магнитными гранулами при комнатной температуре в течение 15 минут. Гранулы промывали 1 мл 1,2 мМ CaCl2/TBST и 1,2 мМ CaCl2/TBS. Затем гранулы, дополненные 0,1 мл 2 мМ EDTA/TBS, суспендировали при комнатной температуре. Сразу после этого гранулы отделяли с использованием магнитного стенда для сбора раствора с фагами. Собранный раствор с фагами добавляли к 10 мл штамма E. coli TG1 на логарифмической фазе роста (OD600: 0,4-0,7). Штамм E. coli инфицировали фагами при осторожном вращении культуры штамма при 37°C в течение 1 часа. Инфицированные E. coli инокулировали на чашку 225 мм × 225 мм. Далее из культур инокулированных E. coli собирали фаги, получая раствор с фаговой библиотекой. Пэннинг со способностью к Ca-зависимому связыванию в качестве показателя повторяли несколько раз.
(15-3) Оценка с помощью ELISA фагов
Содержащий фаг культуральный супернатант получали в соответствии с общепринятым способом (Methods Mol. Biol. (2002) 178, 133-145) из каждой единичной колонии E. coli, полученной с помощью описанного выше способа.
После добавления BSA и CaCl2(конечная концентрация: 4% BSA и 1,2 мМ ионы кальция), содержащий фаг культуральный супернатант подвергали ELISA по следующей методике: микропланшет для титрования StreptaWell 96 (F. Hoffmann-La Roche Ltd.) покрывали в течение ночи 100 мкл PBS, содержавшего меченные биотином антигены. Каждую лунку планшета промывали PBST для удаления не связавшихся антигенов. Затем лунку блокировали 250 мкл 4% BSA-TBS в течение 1 часа или более. После удаления 4% BSA-TBS, полученный супернатант добавляли в каждую лунку, и планшет оставляли стоять при 37°C в течение 1 часа для связывания экспонируемых фагом антител с антигенами, содержащимися в каждой лунке. Каждую лунку промывали 1,2 мМ CaCl2/TBST, и добавляли 1,2 мМ CaCl2/TBS или 1 мМ EDTA/TBS. Планшет оставляли стоять при 37°C в течение 30 минут для инкубации. После промывания 1,2 мМ CaCl2/TBST в каждую лунку добавляли конъюгированные с HRP антитела против M13 (Amersham Pharmacia Biotech Inc.), разбавленные TBS, имеющим 4% BSA и ионизированный кальций в концентрации 1,2 мМ (все указаны в конечных концентрациях). Планшет инкубировали в течение 1 часа. После промывания 1,2 мМ CaCl2/TBST, в каждую лунку добавляли простой раствор TMB (ZYMED Laboratories, Inc.). Хромогенную реакцию раствора в каждой лунке завершали добавлением серной кислоты. Затем развитие цвета анализировали на основе поглощения при 450 нм.
Гены фрагментов антител, оцененных как обладающие способностью к Ca-зависимому связыванию антигена в результате ELISA фагов, амплифицировали в качестве матриц с использованием специфических праймеров, а затем анализировали в отношении их нуклеотидных последовательностей.
(15-4) Экспрессия и очистка антитела
Ген каждого клона, оцененного как обладающий способностью к Ca-зависимому связыванию антигена в результате ELISA фагов, встраивали в плазмиды для экспрессии в клетках животных. Экспрессию антител проводили следующим способом: линию FreeStyle 293-F, происходящую из почки эмбриона человека, (Invitrogen Corp.) суспендировали в среде для экспрессии FreeStyle 293 Expression Medium (Invitrogen Corp.). Суспензию, имеющую плотность клеток 1,33×106 клеток/мл, инокулировали в концентрации 3 мл/лунка в планшет с 6 ячейками. Полученные плазмиды переносили в клетки путем липофекции. Клетки культивировали в течение 4 суток в инкубаторе с CO2 (37°C, 8% CO2, 90 об./мин.). Антитела очищали из полученного культурального супернатанта способом, общеизвестным специалистам в данной области, с использованием rProtein A Sepharose(TM) Fast Flow (Amersham Biosciences, Inc.). Поглощение очищенного раствора антител измеряли при 280 нм с использованием спектрофотометра. Концентрацию антитела вычисляли из полученной величины измерения с использованием коэффициента экстинкции, вычисленного с помощью PACE (Protein Science (1995) 4, 2411-2423).
[Пример 16] Оценка полученного антитела в отношении его способности к Ca-зависимому связыванию с рецептором IL-6 человека
Для оценки зависимости от Ca активности связывания рецептора IL-6 человека антител 6RL#9-IgG1 (тяжелая цепь: SEQ ID NO: 78 (последовательность SEQ ID NO: 10, связанная с происходящей из IgG1 константной областью) и легкая цепь: SEQ ID NO: 79) и FH4-IgG1 (тяжелая цепь: SEQ ID NO: 80 и легкая цепь: SEQ ID NO: 81), полученных согласно примеру 15, эти антитела подвергали кинетическому анализу в отношении их реакции антиген-антитело с рецепторами IL-6 человека с использованием Biacore T100 (GE Healthcare Bio-Sciences Corp.). В качестве контрольного антитела, не обладающего активностью Ca-зависимого связывания с рецепторами IL-6 человека, использовали H54/L28-IgG1, описанное в WO2009125825 (тяжелая цепь: SEQ ID NO: 82 и легкая цепь: SEQ ID NO: 83). Кинетический анализ реакции антиген-антитело проводили в растворах с концентрациями ионов кальция 2 мМ и 3 мкМ в качестве условий высокой концентрации ионов кальция и низкой концентрации ионов кальция, соответственно. Каждое представляющее интерес антитело улавливали на сенсорном чипе CM4 (GE Healthcare Bio-Sciences Corp.) с иммобилизованным на нем белком A (Invitrogen Corp.), в соответствующем количестве способом присоединения аминов. В качестве подвижных буферов использовали два типа буферных растворов: 10 мМ ACES, 150 мМ NaCl, 0,05% (масс./об.) Tween 20, и 2 мМ CaCl2 (pH 7,4); и 10 мМ ACES, 150 мМ NaCl, 0,05% (масс./об.) Tween 20, и 3 мколь/л CaCl2(pH 7,4). Рецепторы IL-6 человека также разбавляли с помощью каждого из этих буферов. Весь анализ проводили при 37°C.
В кинетическом анализе реакции антиген-антитело с использованием антитела H54/L28-IgG1, разбавленный раствор рецептора IL-6 или пустой подвижный буфер инжектировали со скоростью потока 20 мкл/мин в течение 3 минут для взаимодействия рецепторов IL-6 с антителом H54/L28-IgG1, уловленном на сенсорном чипе. Затем инжектировали подвижный буфер со скоростью потока 20 мкл/мин в течение 10 минут, и наблюдали диссоциацию рецепторов IL-6. Затем на него инжектировали 10 мМ глицин-HCl (pH 1,5) со скоростью потока 30 мкл/мин в течение 30 секунд, чтобы регенерировать сенсорный чип. Константу скорости ассоциации ka (1/M с) и константу скорости диссоциации kd (1/с) вычисляли в качестве кинетических параметров из сенсограммы, полученной в анализе. Эти величины использовали для вычисления константы диссоциации KD (M) антитела H54/L28-IgG1 в отношении рецептора IL-6 человека. Каждый параметр вычисляли с использованием программного обеспечения Biacore T100 Evaluation Software (GE Healthcare Bio-Sciences Corp.).
В кинетическом анализе реакции антиген-антитело с использованием антитела FH4-IgG1 и антитела 6RL#9-IgG1, разбавленный раствор рецептора IL-6 или пустой подвижный буфер инжектировали со скоростью потока 5 мкл/мин в течение 15 минут для взаимодействия рецепторов IL-6 с антителом FH4-IgG1 и антителом 6RL#9-IgG1, уловленными на сенсорном чипе. Затем на него инжектировали 10 мМ глицин-HCl (pH 1,5) со скоростью потока 30 мкл/мин в течение 30 секунд, чтобы регенерировать сенсорный чип. Константу диссоциации KD (M) вычисляли с использованием модели аффинности в стационарном состоянии из сенсограмм, полученных в анализе. Каждый параметр вычисляли с использованием программного обеспечения Biacore T100 Evaluation Software (GE Healthcare Bio-Sciences Corp.).
В таблице 21 представлена константа диссоциации KD для каждого антитела в отношении рецептора IL-6, определенная этим способом в присутствии 2 мМ CaCl2.
KD антитела H54/L28-IgG1 в условиях концентрации Ca 3 мкМ можно вычислять аналогично тому, как и в присутствии Ca в концентрации 2 мМ. Выявлено, что антитело FH4-IgG1 и антитела 6RL#9-IgG1 почти не связывались с рецептором IL-6 в условиях концентрации Ca 3 мкМ. Таким образом, KD трудно вычислить указанным выше способом. Вместо этого, величины KD этих антител в условиях концентрации Ca 3 мкМ можно вычислять в соответствии с выражением 1 (Biacore T100 Software Handbook, BR-1006-48, AE 01/2007).
[Выражение 1]
Req=C×Rmax/(KD+C)+RI
В указанном выше выражении 1, каждый символ определяют следующим образом:
Req (RU): Уровни связывания в стационарном состоянии
Rmax (RU): Способность поверхности связывать анализируемое соединение
RI (RU): Совокупный вклад индекса рефракции в образце
C (M): Концентрация анализируемого соединения
KD (M): Равновесная константа диссоциации
В таблице 22 представлены результаты приближенной оценки константы диссоциации KD каждого антитела в отношении рецептора IL-6 при концентрации Ca 3 мкмоль/л в соответствии с выражением 1. В таблице 22, Req, Rmax, RI и C соответствуют величинам, гипотетически предположенным, исходя из результатов анализа.
В результате было предсказано, что антитело FH4-IgG1 и антитело 6RL#9-IgG1 имеют величины KD в отношении рецептора IL-6, которые увеличиваются приблизительно в 60 раз и приблизительно 120 раз, соответственно (аффинность снижалась в 60 раз и 120 раз или более) при снижении концентрации CaCl2 в буфере от 2 мМ до 3 мкМ.
В таблице 23 обобщенно представлены величины KD трех типов антител: H54/L28-IgG1, FH4-IgG1 и 6RL#9-IgG1, в присутствии 2 мМ CaCl2 и в присутствии 3 мкМ CaCl2, и зависимость от Ca величин KD.
Было выявлено, что антитело H54/L28-IgG1 не отличается в отношении связывания рецептора IL-6 в зависимости от отличий в концентрации Ca. Напротив, значительное ослабление связывания рецептора IL-6 наблюдали для антитела FH4-IgG1 и антитела 6RL#9-IgG1 в условиях низкой концентрации Ca (таблица 23).
[Пример 17] Оценка полученного антитела в отношении связывания им ионов кальция
Далее, среднюю температуру термической денатурации (Tm) измеряли с помощью дифференциальной сканирующей калориметрии (DSC) (MicroCal VP-Capillary DSC, MicroCal) в качестве показателя для оценки связывания антителами ионов кальция. Средняя температура термической денатурации (Tm) служит в качестве показателя стабильности и становится более высокой, когда белок стабилизирован через связывание ионов кальция, по сравнению со средней температурой термической денатурации (Tm) не связанного с ионом кальция белка (J. Biol. Chem. (2008) 283, 37, 25140-25149). Оценивали изменение величины Tm каждого антитела в зависимости от изменения концентрации ионов кальция в растворе антитела для оценки активности связывания антитела с ионами кальция. Очищенные антитела подвергали диализу (EasySEP, Tomy Seiko Co., Ltd.) против раствора, содержащего 20 мМ Tris-HCl, 150 мМ NaCl и 2 мМ CaCl2 (pH 7,4) или содержащего 20 мМ Tris-HCl, 150 мМ NaCl, и 3 мкМ CaCl2 (pH 7,4) в качестве внешнего раствора. Каждый раствор антитела доводили приблизительно до 0,1 мг/мл антитела с помощью раствора, использованного в диализе, и подвергали в качестве исследуемого вещества анализу DSC при от 20°C до 115°C со скоростью повышения температуры, установленной на 240°C/ч. В таблице 24 представлена средняя температура термической денатурации (Tm) для каждого Fab-домена антитела, вычисленная на основе полученной кривой денатурации (DSC).
Результаты, представленные в таблице 24, показали, что величины Tm для Fab-доменов антитела FH4-IgG1 и антитела 6RL#9-IgG1, обладающих способностью к кальций-зависимому связыванию, варьировали в зависимости от изменения концентрации ионов кальция, в то время как величина Tm для Fab-домена антитела H54/L28-IgG1, не обладающего способностью к кальций-зависимому связыванию, не изменялась в зависимости от изменения концентрации ионов кальция. Такое изменение величин Tm для Fab-доменов антитела FH4-IgG1 и антитела 6RL#9-IgG1 указывает на то, что Fab-домены были стабилизированы через связывание ионов кальция с этими антителами. Эти результаты продемонстрировали, что антитело FH4-IgG1 и антитело 6RL#9-IgG1 связывается с ионами кальция, в то время как антитело H54/L28-IgG1 не связывается с ионами кальция.
[Пример 18] Идентификация связывающего ионы кальция участка в антителе 6RL#9 с помощью рентгеноструктурного анализа
(18-1) Рентгеноструктурный анализ
Как показано в примере 17, анализ температуры термической денатурации Tm показал, что антитело 6RL#9 связывалось с ионами кальция. Однако участок, через который антитело 6RL#9 связывалось с ионами кальция, был непредсказуемым. Таким образом, остаток, ответственный за взаимодействие с ионами кальция, идентифицировали в последовательности антитела 6RL#9 с использованием подхода рентгеноструктурного анализа.
(18-2) Экспрессия и очистка антитела 6RL#9
Антитело 6RL#9, экспрессированное для анализа с использованием рентгеновской кристаллографии, очищали. В частности, клетки животных временно трансфицировали плазмидами для экспрессии в клетках животных, полученных так, чтобы обеспечить соответствующую экспрессию тяжелой цепи (SEQ ID NO: 78) и легкой цепи (SEQ ID NO: 79) антитела 6RL#9. Полученные плазмиды трансфицировали способом липофекции в 800 мл клетки линии, происходящей из клеток почек эмбриона человека FreeStyle 293-F (Invitrogen Corp.), суспендированные до конечной плотности клеток 1×106 клеток/мл в среде для экспрессии FreeStyle 293 Expression Medium (Invitrogen Corp.). Клетки, трансфицированные плазмидами, культивировали в течение 5 суток в инкубаторе с CO2 (37°C, 8% CO2, 90 об./мин.). Антитела очищали из полученного культурального супернатанта способом, общеизвестным специалистам в данной области, с использованием rProtein A Sepharose(TM) Fast Flow (Amersham Biosciences, Inc.). Поглощение очищенного раствора антител измеряли при 280 нм с использованием спектрофотометра. Концентрацию антитела вычисляли из полученной величины измерения с использованием коэффициента экстинкции, вычисленного с помощью PACE (Protein Science (1995) 4, 2411-2423).
(18-3) Очистка Fab-фрагмента из антитела 6RL#9
Антитело 6RL#9 концентрировали до 21 мг/мл с использованием ультрафильтрационной мембраны с пределом молекулярной массы 10000 MWCO. Антитело разбавляли до 5 мг/мл с использованием буфера 4 мМ L-цистеин/5 мМ EDTA/20 мМ фосфат натрия (pH 6,5), получая 2,5 мл образца антитела. После добавления 0,125 мг папаина (Roche Applied Science), образец перемешивали, а затем оставляли стоять при 35°C в течение 2 часов. Образец, оставленный стоять таким образом, далее дополняли одной таблеткой коктейля ингибиторов протеаз Protease Inhibitor Cocktail Mini, EDTA-Free (Roche Applied Science), растворенной в 10 мл 25 мМ буферного раствора MES (pH 6), и оставляли стоять на льду для завершения протеазной реакции с папаином. Далее образец добавляли в 1-мл катионообменную колонку HiTrap SP HP (GE Healthcare Bio-Sciences Corp.) (уравновешенную 25 мМ буферным раствором MES (pH 6)), ниже которой была последовательно подсоединена 1-мл колонка с белком A-носителем HiTrap MabSelect Sure (GE Healthcare Bio-Sciences Corp.). Очищенную фракцию Fab-фрагмента антитела 6RL#9 получали путем элюирования на линейном градиенте концентрации NaCl вплоть до 300 мМ в этом буферном растворе. Далее, полученную очищенную фракцию концентрировали приблизительно до 0,8 мл с использованием ультрафильтрационной мембраны 5000 MWCO. Концентрат добавляли в колонку для гель-фильтрации Superdex 200 10/300 GL (GE Healthcare Bio-Sciences Corp.), уравновешенную 100 мМ буферным раствором HEPES (pH 8), содержавшим 50 мМ NaCl. Очищенный Fab-фрагмент антитела 6RL#9 для кристаллизации элюировали с колонки с использованием указанного буферного раствора. Все действия на колонке проводили при низкой температуре, составляющей от 6 до 7,5°C.
(18-4) Кристаллизация Fab-фрагмента антитела 6RL#9 в присутствии ионов кальция
Затравочные кристаллы Fab-фрагмента 6RL#9 получали заранее согласно общепринятым условиям. Далее очищенный Fab-фрагмент антитела 6RL#9 доводили добавлением CaCl2 до 5 мМ и концентрировали до 12 мг/мл с использованием ультрафильтрационной мембраны 5000 MWCO. Затем образец, концентрированный таким образом, кристаллизовали способом висячей капли посредством диффузии в парах. В качестве резервуарного раствора использовали 100 мМ буферный раствор HEPES (pH 7,5), содержавший 20-29% PEG4000. Затравочные кристаллы дробили в 100 мМ буферном растворе HEPES (pH 7,5), содержавшем 29% PEG4000 и 5 мМ CaCl2, и разбавляли в 100-10000 раз, и 0,2 мкл каждого раствора этой серии разведений добавляли к смешанному раствору 0,8 мкл резервуарного раствора и 0,8 мкл концентрированного образца на покровном стекле для получения кристаллизационных капель. Кристаллизационные капли оставляли стоять при 20°C в течение от 2 суток до 3 суток. На полученных кристаллах, подобных тонким пластинам, определяли данные рентгенодифракции.
(18-5) Кристаллизация Fab-фрагмента антитела 6RL#9 в отсутствие ионов кальция
Очищенный Fab-фрагмент антитела 6RL#9 концентрировали до 15 мг/мл с использованием ультрафильтрационной мембраны 5000 MWCO. Затем образец, концентрированный таким образом, кристаллизовали способом висячей капли посредством диффузии в парах. В качестве резервуарного раствора использовали 100 мМ буферный раствор HEPES (pH 7,5), содержавший 18-25% PEG4000. Кристаллы Fab-фрагмента антитела 6RL#9, полученные в присутствии Ca, дробили в 100 мМ буферном растворе HEPES (pH 7,5), содержавшем 25% PEG4000, и разбавляли в 100-10000 раз, и 0,2 мкл каждого раствора этой серии разведений добавляли к смешанному раствору 0,8 мкл резервуарного раствора и 0,8 мкл концентрированного образца на покровном стекле для получения кристаллизационных капель. Кристаллизационные капли оставляли стоять при 20°C в течение от 2 суток до 3 суток. На полученных кристаллах, подобных тонким пластинам, определяли данные рентгенодифракции.
(18-6) Получение данных рентгенодифракции на кристалле Fab-фрагмента антитела 6RL#9, полученного в присутствии ионов кальция
Один из монокристаллов (полученных в присутствии Ca) Fab-фрагмента антитела 6RL#9, погруженный в 100 мМ буферный раствор HEPES (pH 7,5), содержавший 35% PEG4000 и 5 мМ CaCl2 вычерпывали, вместе с внешним раствором, с использованием очень мелкой булавки в виде нейлоновой петли и замораживали в жидком азоте. Данные рентгенодифракции на замороженном кристалле анализировали с использованием линии пучка BL-17A от Photon Factory, Institute Materials Structure Science, High Energy Accelerator Research Organization (KEK). В процессе анализа, замороженный кристалл держали все время в потоке азота при -178°C для сохранения его замороженного состояния. Было получено всего 180 дифракционных изображений при вращении кристалла на 1° для каждого изображения, с использованием CCD-детектора Quantum 315r (Area Detector Systems Corporation (ADSC)), оборудованного линией пучка. Определение константы решетки, индексирование дифракционных пятен и обработку данных дифракции проводили с использованием программы Xia2 (CCP4 Software Suite), XDS Package (Wolfgang Kabsch), и Scala (CCP4 Software Suite). Наконец, были получены данные интенсивности дифракции с разрешением вплоть до 2,2 ангстрем. Этот кристалл принадлежал к пространственной группе P212121 и имел константы решетки a=45,47 ангстрем, b=79,86 ангстрем, c=116,25 ангстрем, α=90°, β=90° и γ=90°.
(18-7) Получение данных рентгенодифракции на кристалле Fab-фрагмента антитела 6RL#9, полученного в отсутствие ионов кальция
Один из монокристаллов (полученных в присутствие Ca) Fab-фрагмента антитела 6RL#9, погруженный в 100 мМ буферный раствор HEPES (pH 7,5), содержавший 35% PEG4000, вычерпывали, вместе с внешним раствором, с использованием очень мелкой булавки в виде нейлоновой петли и замораживали в жидком азоте. Данные рентгенодифракции на замороженном кристалле анализировали с использованием линии пучка BL-5A от Photon Factory, Institute Materials Structure Science, High Energy Accelerator Research Organization (KEK). В процессе анализа, замороженный кристалл держали все время в потоке азота при -178°C для сохранения его замороженного состояния. Было получено всего 180 дифракционных изображений при вращении кристалла на 1° для каждого изображения, с использованием CCD-детектора Quantum 210r (Area Detector Systems Corporation (ADSC)), оборудованного линией пучка. Определение константы решетки, индексирование дифракционных пятен и обработку данных дифракции проводили с использованием программы Xia2 (CCP4 Software Suite), XDS Package (Wolfgang Kabsch), и Scala (CCP4 Software Suite). Наконец, были получены данные интенсивности дифракции с разрешением вплоть до 2,3 ангстрем. Этот кристалл, который представлял собой кристалл того же типа, что и кристалл, полученный в присутствии Ca, принадлежал к пространственной группе P212121 и имел константы решетки a=45,40 ангстрем, b=79,63 ангстрем, c=116,07 ангстрем, α=90°, β=90° и γ=90°.
(18-8) Структурный анализ кристалла Fab-фрагмента антитела 6RL#9, полученного в присутствии ионов кальция
Структуру кристалла Fab-фрагмента антитела 6RL#9, полученного в присутствии Ca, определяли способом молекулярного замещения с использованием программы Phaser (CCP4 Software Suite). Количество молекул в асимметричном элементе оценивали, исходя из размера полученной кристаллической решетки и молекулярной массы Fab-фрагмента антитела 6RL#9. Исходя из гомологии первичной последовательности, аминокислотные остатки в положениях 112-220 в цепи A и в положениях 116-218 цепи B, установленные из структурной координаты с кодом PDB: 1ZA6, были выбраны в качестве модельных молекул для поиска областей CL и CH1. Далее, аминокислотные остатки в положениях 1-115 в цепи B, извлеченные из структурной координаты с кодом PDB: 1ZA6, были выбраны в качестве модельной молекулы для поиска области VH. Наконец, аминокислотные остатки в положениях 3-147 в легкой цепи, установленные из структурной координаты с кодом PDB: 2A9M, были выбраны в качестве модельной молекулы для поиска области VL. Исходя из этого порядка, были определены ориентация и положение каждой модельной молекулы для поиска в кристаллической решетке с помощью функций вращения и сдвига для получения исходной структурной модели Fab-фрагмента антитела 6RL#9. Исходную структурную модель подвергали детализации жесткого каркаса, смещая каждый из доменов VH, VL, CH1 и CL, с получением кристаллографического фактора достоверности R, составляющего 46,9%, и величины свободного R, составляющей 48,6%, для данных отражения 25-3,0 ангстрем. Кроме того, модель детализировали с помощью коррекции модели в программе повторений Coot (Paul Emsley) на основании карт электронной плотности с коэффициентами 2Fo-Fc и Fo-Fc, вычисленными с использованием детализации структуры с помощью программы Refmac5 (CCP4 Software Suite), экспериментально определенного структурного фактора Fo, структурного фактора Fc, вычисленного из этой модели, и фазы. Конечную детализацию проводили с использованием программы Refmac5 (CCP4 Software Suite) путем включения в модель ионов Ca и молекул воды на основе карт электронной плотности с коэффициентами 2Fo-Fc и Fo-Fc. Наконец, получали кристаллографический фактор достоверности R, составляющий 20,0%, и величину свободного R, составляющую 27,9%, для модели из 3440 атомов с использованием 21020 данных об отражении с разрешением 25-2,2 ангстрем.
(18-9) Структурный анализ кристалла Fab-фрагмента антитела 6RL#9, полученного в отсутствие ионов кальция
Структуру кристалла Fab-фрагмента антитела 6RL#9, полученного в отсутствие Ca, определяли с использованием структуры кристалла, которая представляла собой структуру такого же типа, как и структура, полученная в присутствии Ca. Молекулы воды и ионы кальция Ca были исключены из структурных координат кристалла Fab-фрагмента антитела 6RL#9, полученного в присутствии Ca, с последующей детализацией жесткого каркаса со смещением каждого из доменов VH, VL, CH1 и CL, с получением кристаллографического фактора достоверности R, составляющего 30,3%, и величины свободного R, составляющего 31,7%, для данных отражения при 25-3,0 ангстрем. Кроме того, модель детализировали с помощью коррекции модели в программе повторений Coot (Paul Emsley) на основании карт электронной плотности с коэффициентами 2Fo-Fc и Fo-Fc, вычисленными с использованием детализации структуры с помощью программы Refmac5 (CCP4 Software Suite), экспериментально определенного структурного фактора Fo, структурного фактора Fc, вычисленного из этой модели, и фазы. Конечную детализацию проводили с использованием программы Refmac5 (CCP4 Software Suite) путем включения в модель молекул воды на основе карт электронной плотности с коэффициентами 2Fo-Fc и Fo-Fc. Наконец, получали кристаллографический фактор достоверности R, составляющий 20,9%, и величину свободного R, составляющую 27,7%, для модели из 3351 атомов с использованием 18357 данных отражения с разрешением 25-2,3 ангстрем.
(18-10) Сравнение данных рентгенодифракции между кристаллами Fab-фрагмента антитела 6RL#9, полученными в присутствии Ca и в отсутствие Ca
В результате структурного сравнения кристаллов Fab-фрагмента антитела 6RL#9, полученных в присутствии Ca и в отсутствие Ca, наблюдали значительное изменение в CDR3 тяжелой цепи. На фиг. 11 представлена структура CDR3 тяжелой цепи Fab-фрагмента антитела 6RL#9, определенная с помощью рентгеноструктурного анализа. В частности, ион кальция присутствовал в центральной области части петли CDR3 тяжелой цепи в кристалле Fab-фрагмента антитела 6RL#9, полученном в присутствии Ca. Было предположено, что ион кальция взаимодействует с аминокислотными остатками 95, 96 и 100a (определяемые посредством нумерации по Кабату) в CDR3 тяжелой цепи. Это позволяет предположить, что в присутствии Ca петля CDR3 тяжелой цепи, которая важна для связывания антигена, стабилизирована посредством связывания с кальцием, принимая структуру, оптимальную для связывания антигена. Ни в одном из предшествующих сообщений не было показано, что кальций связывается с CDR3 тяжелой цепи антитела. Эта структура CDR3 тяжелой цепи антитела, связывающаяся с кальцием, является новой структурой.
Кальций-связывающие мотивы, присутствующие в CDR3 тяжелой цепи, которые были выявлены из структуры Fab-фрагмента антитела 6RL#9, также могут служить в качестве новых факторов для конструирования Ca-библиотеки, как описано в примере 11. Хотя кальций-связывающие мотивы вносили в вариабельную область легкой цепи в примере 11, другая возможная библиотека содержит, например, CDR3 тяжелой цепи антитела 6RL#9 и содержит нестрогие остатки в других CDR, включая CDR легкой цепи.
[Пример 19] Получение антитела, связывающегося с рецептором IL-6 Ca-зависимым образом, из библиотеки антител человека с использованием технологии фагового дисплея
(19-1) Получение библиотеки фагового дисплея наивных антител человека
Библиотеку фагового дисплея антител человека, состоящую из множества фагов, экспонирующих Fab-домены, обладающие различными последовательностями антител человека, конструировали в соответствии со способом, общеизвестным специалистам в данной области, с использованием поли-A РНК, полученной из PBMC человека, коммерчески доступной поли-A РНК человека, и т.п. в качестве матрицы.
(19-2) Получение фрагмента антитела, связывающегося с антигеном Ca-зависимым образом, из библиотеки способом пэннинга на гранулах
Первый раунд скрининга сконструированной библиотеки фагового дисплея наивных антител человека проводили путем увеличения содержания только фрагментов антител, обладающих способностью связывать антиген (IL-6R). Использованные антигены представляли собой меченный биотином IL-6.
Фаги получали из E. coli, содержавших сконструированную фагмиду для фагового дисплея. К культурам E. coli, которые продуцировали фаги, добавляли 2,5 M NaCl/10% PEG, и совокупность фагов, преципитированных таким образом, разбавляли TBS, получая раствор с фаговой библиотекой. Далее, к раствору с фаговой библиотекой добавляли BSA и CaCl2, (конечная концентрация: 4% BSA и 1,2 мМ ионы кальция). Способ пэннинга проводили в соответствии с общепринятым способом пэннинга с использованием антигенов, иммобилизованных на магнитных гранулах (J. Immunol. Methods. (2008) 332 (1-2), 2-9; J. Immunol. Methods. (2001) 247 (1-2), 191-203; Biotechnol. Prog. (2002) 18 (2) 212-20; и Mol. Cell Proteomics (2003) 2 (2), 61-9). Использованные магнитные гранулы представляли собой покрытые нейтравидином гранулы (Sera-Mag SpeedBeads NeutrAvidin-coated) или покрытые стрептавидином гранулы (Dynabeads M-280 Streptavidin).
В частности, 250 пмоль меченных биотином антигенов добавляли к полученному раствору с фаговой библиотекой и, тем самым, приводили в контакт с раствором с фаговой библиотекой при комнатной температуре в течение 60 минут. Добавляли блокированные BSA магнитные гранулы, а затем комплексы антиген-фаг связывали с магнитными гранулами при комнатной температуре в течение 15 минут. Гранулы промывали три раза 1 мл 1,2 мМ CaCl2/TBST (TBST, содержащий 1,2 мМ CaCl2), а затем дополнительно промывали два раза 1 мл 1,2 мМ CaCl2/TBS (TBS, содержащий 1,2 мМ CaCl2). После добавления 0,5 мл 1 мг/мл трипсина, гранулы суспендировали при комнатной температуре в течение 15 минут, и сразу после этого гранулы отделяли с использованием магнитного стенда для сбора раствора с фагами. Собранный раствор с фагами добавляли к 10 мл штамма E. coli TG1 на логарифмической фазе роста (OD600: 0,4-0,7). Штамм E. coli инфицировали фагами при осторожном вращении культуры штамма при 37°C в течение 1 часа. Инфицированные E. coli инокулировали на чашку 225 мм × 225 мм. Далее из культур инокулированных E. coli собирали фаги, получая раствор с фаговой библиотекой.
На втором и последующих раундах пэннинга увеличивали содержание фагов со способностью к Ca-зависимому связыванию в качестве показателя. В частности, 40 пмоль меченных биотином антигенов добавляли к полученному раствору с фаговой библиотекой и, тем самым, приводили в контакт с раствором с фаговой библиотекой при комнатной температуре в течение 60 минут. Добавляли блокированные BSA магнитные гранулы, а затем комплексы антиген-фаг связывали с магнитными гранулами при комнатной температуре в течение 15 минут. Гранулы промывали 1 мл 1,2 мМ CaCl2/TBST и 1,2 мМ CaCl2/TBS. Затем гранулы, дополненные 0,1 мл 2 мМ EDTA/TBS, суспендировали при комнатной температуре. Сразу после этого гранулы отделяли с использованием магнитного стенда для сбора раствора с фагами. Добавление 5 мкл 100 мг/мл трипсина к собранному раствору с фагами расщепляло белки pIII (белки pIII, происходящие из хелперного фага) не экспонирующих Fab фагов для устранения способности не экспонирующих Fab фагов инфицировать E. coli. Фаги, собранные из обработанного трипсином раствора с фагами, добавляли к 10 мл штамма E. coli TG1 на логарифмической фазе роста (OD600: 0,4-0,7). Штамм E. coli инфицировали фагами при осторожном вращении культуры штамма при 37°C в течение 1 часа. Инфицированные E. coli инокулировали на чашку 225 мм × 225 мм. Далее из культур инокулированных E. coli собирали фаги, получая раствор с фаговой библиотекой. Этот пэннинг со способностью к Ca-зависимому связыванию в качестве показателя проводили всего в течение 3 раундов.
(19-3) Оценка с помощью ELISA фагов
Содержащий фаг культуральный супернатант получали в соответствии с общепринятым способом (Methods Mol. Biol. (2002) 178, 133-145) из каждой единичной колонии E. coli, полученной с помощью описанного выше способа.
После добавления BSA и CaCl2 (конечная концентрация: 4% BSA и 1,2 мМ ионы кальция), содержащий фаг культуральный супернатант подвергали ELISA по следующей методике: микропланшет для титрования StreptaWell 96 (F. Hoffmann-La Roche Ltd.) покрывали в течение ночи 100 мкл PBS, содержавшего меченные биотином антигены. Каждую лунку планшета промывали PBST для удаления не связавшихся антигенов. Затем лунку блокировали 250 мкл 4% BSA-TBS в течение 1 часа или более. После удаления 4% BSA-TBS, полученный супернатант добавляли в каждую лунку, и планшет оставляли стоять при 37°C в течение 1 часа для связывания экспонируемых фагом антител с антигенами, содержащимися в каждой лунке. Каждую лунку промывали 1,2 мМ CaCl2/TBST, и добавляли 1,2 мМ CaCl2/TBS или 1 мМ EDTA/TBS. Планшет оставляли стоять при 37°C в течение 30 минут для инкубации. После промывания 1,2 мМ CaCl2/TBST в каждую лунку добавляли конъюгированные с HRP антитела против M13 (Amersham Pharmacia Biotech Inc.), разбавленные TBS, имеющим 4% BSA и ионизированный кальций в концентрации 1,2 мМ (все указаны в конечных концентрациях). Планшет инкубировали в течение 1 часа. После промывания 1,2 мМ CaCl2/TBST, в лунки добавляли простой раствор TMB (ZYMED Laboratories, Inc.). Хромогенную реакцию раствора в каждой лунке завершали добавлением серной кислоты. Затем развитие цвета анализировали на основе поглощения при 450 нм.
С помощью ELISA было получено антитело 6KC4-1#85, обладающее способностью к Ca-зависимому связыванию IL-6, с использованием 96 выделенных клонов. Ген фрагмента антитела, оцененный как обладающий способностью к Ca-зависимому связыванию антигена в результате ELISA фагов, амплифицировали в качестве матрицы с использованием специфических праймеров, а затем анализировали в отношении его нуклеотидной последовательности. Последовательность вариабельной области тяжелой цепи антитела 6KC4-1#85 представлена в SEQ ID NO: 11, и ее последовательность вариабельной области легкой цепи представлена в SEQ ID NO: 84. Полинуклеотид, кодирующий вариабельную область тяжелой цепи (SEQ ID NO: 11) антитела 6KC4-1#85, связывали способом ПЦР с полинуклеотидом, кодирующим последовательность, происходящую из IgG1. Полученный фрагмент ДНК встраивали в векторы для экспрессии в клетках животных для конструирования векторов, которые позволяют экспрессию тяжелой цепи, соответствующей SEQ ID NO: 85. Полинуклеотид, кодирующий вариабельную область легкой цепи (SEQ ID NO: 84) антитела 6KC4-1#85, связывали способом ПЦР с полинуклеотидом, кодирующим природную константную область цепи каппа (SEQ ID NO: 26). Полученный фрагмент ДНК встраивали в векторы для экспрессии в клетках животных. Последовательность полученной модифицированной формы подтверждали способом, общеизвестным специалистам в данной области. Последовательность полученной модифицированной формы подтверждали способом, общеизвестным специалистам в данной области.
(19-4) Экспрессия и очистка антитела
Ген клона 6KC4-1#85, оцененного как обладающий способностью к Ca-зависимому связыванию антигена в результате ELISA фагов, встраивали в плазмиды для экспрессии в клетках животных. Экспрессию антител проводили следующим способом: линию FreeStyle 293-F, происходящую из почки эмбриона человека, (Invitrogen Corp.) суспендировали в среде для экспрессии FreeStyle 293 Expression Medium (Invitrogen Corp.). Суспензию, имеющую плотность клеток 1,33×106 клеток/мл, инокулировали в концентрации 3 мл/лунка в планшет с 6 ячейками. Полученные плазмиды переносили в клетки путем липофекции. Клетки культивировали в течение 4 суток в инкубаторе с CO2 (37°C, 8% CO2, 90 об./мин.). Антитела очищали из полученного культурального супернатанта способом, общеизвестным специалистам в данной области, с использованием rProtein A Sepharose(TM) Fast Flow (Amersham Biosciences, Inc.). Поглощение очищенного раствора антител измеряли при 280 нм с использованием спектрофотометра. Концентрацию антитела вычисляли из полученной величины измерения с использованием коэффициента экстинкции, вычисленного с помощью PACE (Protein Science (1995) 4, 2411-2423).
[Пример 20] Оценка антитела 6KC4-1#85 в отношении его связывания ионов кальция
Антитело 6KC4-1#85 с кальций-зависимым связыванием антигена, полученное из библиотеки антител, оценивали в отношении связывания им кальция. Оценку того, изменялась ли измеренная величина Tm при различных концентрациях ионизированного кальция, оценивали способом, описанным в примере 6.
В таблице 25 представлена величина Tm для Fab-домена антитела 6KC4-1#85. Как показано в таблице 25, величина Tm Fab-домена антитела 6KC4-1#85 изменялась в зависимости от концентрации ионов кальция, демонстрируя, что антитело 6KC4-1#85 связывается с кальцием.
[Пример 21] Идентификация участка связывания иона кальция в антителе 6KC4-1#85
Как показано в примере 20, было показано, что антитело 6KC4-1#85 связывается с ионами кальция, но не обладает кальций-связывающими мотивами, выявленными в исследовании последовательности hVk5-2. Таким образом, для подтверждения того, что ионы кальция связывались с тяжелой или легкой цепью антитела 6KC4-1#85, или обеими из них, сконструированные антитела, содержащие либо тяжелую, либо легкую цепь, замененную соответствующей цепью антитела против глипикана 3 (последовательность тяжелой цепи GC_H (SEQ ID NO: 48) и последовательность легкой цепи GC_L (SEQ ID NO: 86)), неспособной связываться с ионами кальция, оценивали в отношении их связывания ионов кальция. В таблице 26 представлены величины Tm для сконструированных антител, измеренные в соответствии со способом, представленным в примере 6. В результате величина Tm сконструированного антитела, имеющего тяжелую цепь антитела 6KC4-1#85, изменялась в зависимости от концентрации ионов кальция, что указывает на то, что антитело 6KC4-1#85 связывается с кальцием через его тяжелую цепь.
Для дальнейшей идентификации остатка, через который тяжелая цепь антитела 6KC4-1#85 связывается с ионами кальция, получали модифицированные тяжелые цепи (6_H1-11 (SEQ ID NO: 87), 6_H1-12 (SEQ ID NO: 88), 6_H1-13 (SEQ ID NO: 89), 6_H1-14 (SEQ ID NO: 90), и 6_H1-15 (SEQ ID NO: 91)) или модифицированные легкие цепи (6_L1-5 (SEQ ID NO: 92) и 6_L1-6 (SEQ ID NO: 93)) путем замены остатков Asp (D), присутствующих в CDR антитела 6KC4-1#85, на остатки Ala (A), которые были неспособны участвовать в связывании или хелатировании ионов кальция. Сконструированные антитела очищали в соответствии со способом, описанным в примере 19, из культур клеток животных, трансфицированных экспрессирующими векторами, содержащими сконструированные гены антител. Связывание кальция очищенными сконструированными антителами анализировали способом, описанным в примере 6. Результаты анализа представлены в таблице 27. Как показано в таблице 27, антитело 6KC4-1#85 утрачивало его способность связывания кальция при замене остатка 95 или 101 (определяемые посредством нумерации по Кабату) в CDR3 тяжелой цепи на остаток Ala, что указывает на то, что эти остатки важны для связывания кальция. Кальций-связывающие мотивы, присутствующие вблизи основания петли CDR3 тяжелой цепи в антителе 6KC4-1#85, которые были выявлены, исходя из свойства связывания кальция сконструированного антитела 6KC4-1#85, также могут служить в качестве новых факторов для конструирования Ca-библиотеки, как описано в примере 11. Хотя кальций-связывающие мотивы вносили в вариабельную область легкой цепи в примере 11, другая возможная библиотека содержит, например, CDR3 тяжелой цепи антитела 6KC4-1#85 и содержит нестрогие остатки в других CDR, включая CDR легкой цепи.
[Пример 22] Получение антитела, связывающегося с IgA человека Ca-зависимым образом
(22-1) Получение MRA-hIgA, GC-hIgA и биотинилированного IgA-Fc человека
MRA-hIgA (тяжелая цепь: SEQ ID NO: 97 и легкая цепь: SEQ ID NO: 25), GC-hIgA (тяжелая цепь: SEQ ID NO: 98 и легкая цепь: SEQ ID NO: 99), и биотинилированное IgA-Fc (также обозначаемое как меченное биотином hIgA-Fc; hIgA_CH2-CH3-Avitag: SEQ ID NO: 100) получали в качестве IgA человека следующим образом:
(22-1-1) Получение MRA-hIgA
Рекомбинантный IgA человека MRA-hIgA (далее обозначаемый как MRA-hIgA) получали следующим образом: экспрессированный hIgA, содержащий H(WT)-IgA1 (SEQ ID NO: 97) и L(WT) (SEQ ID NO: 25), очищали способом, общеизвестным специалистам в данной области, с использованием ионообменной хроматографии и гель-фильтрации.
(22-1-2) Получение GC-hIgA
Рекомбинантный IgA человека GC-hIgA получали следующим образом: фрагмент гена, кодирующий GC-hIgA (тяжелая цепь: SEQ ID NO: 98 и легкая цепь: SEQ ID NO: 99), встраивали в вектор для экспрессии в клетках животных. FreeStyle 293 (Invitrogen Corp.) котрансфицировали сконструированным плазмидным вектором и геном, кодирующим EBNA1, подлежащим экспрессии, с использованием 293Fectin (Invitrogen Corp.). Затем клетки, трансфицированные этими генами, культивировали при 37°C в течение 6 суток в атмосфере 8% CO2 для секреции белков GC-hIgA в культуральный супернатант.
Содержащие GC-hIgA клеточные культуры фильтровали через 0,22-мкм фильтр на горловину бутылки, получая культуральный супернатант. Культуральный супернатант разбавляли 20 мМ Tris-HCl (pH 8,0) и наносили на HiTrap Q HP (GE Healthcare Bio-Sciences Corp.), уравновешенную этом раствором, а затем GC-hIgA элюировали на градиенте концентрации NaCl. Затем проводили удаление ассоциатов гель-фильтрацией с использованием Superdex 200 и замену буфера на 20 мМ His-HCl и 150 мМ NaCl (pH 6,0), получая очищенный GC-hIgA.
(22-1-3) Получение меченного биотином hIgA-Fc
Для добавления биотина на C-конец представляющего интерес белка (IgA-Fc человека), фрагмент гена, кодирующий специфическую последовательность (последовательность Avitag) для опосредуемого биотинлигазой биотинилирования, присоединяли ниже фрагмента гена, кодирующего область IgA-Fc человека. Фрагмент гена, кодирующий белок IgA человека, связанный с последовательностью Avitag (hIgA_CH2-CH3-Avitag (SEQ ID NO: 100)), встраивали в векторы для экспрессии в клетках животных. FreeStyle 293 (Invitrogen Corp.) трансфицировали сконструированными плазмидными векторами с использованием 293Fectin (Invitrogen Corp.). Эту трансфекцию проводили одновременно с геном, кодирующим EBNA1, подлежащий экспрессии, и геном, кодирующим биотинлигазу (BirA), подлежащую экспрессии для биотинилирования, чтобы пометить белок биотином. Клетки, трансфицированные этими генами в соответствии с описанными выше методиками, культивировали при 37°C в течение 6 суток в атмосфере 8% CO2 для секреции представляющего интерес белка в культуральный супернатант.
Клеточные культуры, содержащие представляющий интерес IgA-Fc человека, фильтровали через 0,22-мкм фильтр на горлышко бутылки с получением культурального супернатанта. Культуральный супернатант разбавляли 20 мМ Tris-HCl (pH 7,4) и наносили на HiTrap Q HP (GE Healthcare Bio-Sciences Corp.), уравновешенную этим раствором, а затем представляющий интерес IgA-Fc человека элюировали на градиенте концентрации NaCl. Элюат с HiTrap Q HP разбавляли 50 мМ Tris-HCl (pH 8,0) и наносили на колонку SoftLink Avidin, уравновешенную этим раствором, а затем проводили элюирование 5 мМ биотином, 150 мМ NaCl, и 50 мМ Tris-HCl (pH 8,0). Затем проводили удаление ассоциатов гель-фильтрацией с использованием Superdex 200 и замену буфера на 20 мМ His-HCl и 150 мМ NaCl (pH 6,0), получая очищенное IgA-Fc человека.
(22-2) Получение фрагмента антитела, связывающегося с антигеном зависимым от Ca образом из библиотеки с помощью пэннинга на гранулах
Первый раунд скрининга сконструированной библиотеки с Ca-зависимым связыванием антигена (Ca-библиотека) проводили со способностью связывать антиген (IgA-Fc человека) в качестве показателя.
Фаги получали из E. coli, содержавших сконструированную фагмиду для фагового дисплея. К культурам E. coli, которые продуцировали фаги, добавляли 2,5 M NaCl/10% PEG, и совокупность фагов, преципитированных таким образом, разбавляли TBS, получая раствор с фаговой библиотекой. Далее к раствору с фаговой библиотекой добавляли BSA или обезжиренное молоко и CaCl2 (конечная концентрация: 4% BSA и 1,2 мМ ионы кальция; или 3% обезжиренное молоко и 1,2 мМ ионы кальция), получая раствор с блокированной фаговой библиотекой. Способ пэннинга проводили в соответствии с общепринятым способом пэннинга с использованием антигенов, иммобилизованных на магнитных гранулах (J. Immunol. Methods. (2008) 332 (1-2), 2-9; J. Immunol. Methods. (2001) 247 (1-2), 191-203; Biotechnol. Prog. (2002) 18 (2) 212-20; и Mol. Cell Proteomics (2003) 2 (2), 61-9). Использованные магнитные гранулы представляли собой покрытые нейтравидином гранулы (Sera-Mag SpeedBeads NeutrAvidin-coated) или покрытые стрептавидином гранулы (Dynabeads M-280 Streptavidin).
В частности, 250 пмоль меченных биотином антигенов (меченный биотином IgA-Fc) добавляли к полученному раствору с фаговой библиотекой и, тем самым, приводили в контакт с раствором с фаговой библиотекой при комнатной температуре в течение 60 минут. Добавляли блокированные BSA или обезжиренным молоком магнитные гранулы, а затем комплексы антиген-фаг связывали с магнитными гранулами при комнатной температуре в течение 15 минут. Гранулы промывали 1 мл 1,2 мМ CaCl2/TBST (TBS, содержащий 1,2 мМ CaCl2 и 0,1% Tween 20) и 1 мл 1,2 мМ CaCl2/TBS (TBS, содержащий 1,2 мМ CaCl2). После добавления 0,5 мл 1 мг/мл трипсина, гранулы суспендировали при комнатной температуре в течение 15 минут, и сразу после этого гранулы отделяли с использованием магнитного стенда для сбора раствора с фагами. Собранный раствор с фагами добавляли к 10 мл штамма E. coli ER2738 на логарифмической фазе роста (OD600: 0,4-0,7). Штамм E. coli инфицировали фагами при осторожном вращении культуры штамма при 37°C в течение 1 часа. Инфицированные E. coli инокулировали на чашку 225 мм × 225 мм. Далее из культур инокулированных E. coli собирали фаги, получая раствор с фаговой библиотекой.
На втором и третьем раундах пэннинга увеличивали содержание фагов со способностью к зависимому от концентрации ионов Ca связыванию антигена в качестве показателя. В частности, 40 пмоль меченных биотином антигенов добавляли к раствору с фаговой библиотекой, полученному путем блокирования аналогично тому, как и на первом раунде пэниннга, и, тем самым, приводили в контакт с раствором с фаговой библиотекой при комнатной температуре в течение 60 минут. Добавляли блокированные BSA магнитные гранулы, а затем комплексы антиген-фаг связывали с магнитными гранулами при комнатной температуре в течение 15 минут. Гранулы промывали 1 мл 1,2 мМ CaCl2/TBST и 1,2 мМ CaCl2/TBS. Затем гранулы, дополненные 0,1 мл 2 мМ EDTA/TBS (TBS, содержащий 2 мМ EDTA), суспендировали при комнатной температуре. Сразу после этого гранулы отделяли с использованием магнитного стенда для сбора раствора с фагами. Добавление 5 мкл 100 мг/мл трипсина к собранному раствору с фагами расщепляло белки pIII (белки pIII, происходящие из хелперного фага) не экспонирующих Fab фагов для устранения способности не экспонирующих Fab фагов инфицировать E. coli. Собранный раствор с фагами добавляли к 10 мл штамма E. coli ER2738 на логарифмической фазе роста (OD600: 0,4-0,7). Штамм E. coli инфицировали фагами при осторожном вращении культуры штамма при 37°C в течение 1 часа. Инфицированные E. coli инокулировали на чашку 225 мм × 225 мм. Далее из культур инокулированных E. coli собирали фаги, получая раствор с фаговой библиотекой.
(22-3) Скрининг антитела, связывающего IgA человека, с использованием Biacore
Гены фрагментов антител, экстрагированные из фагмид, полученных из E. coli, полученных после завершения второго раунда пэннинга, встраивали в векторы для экспрессии в клетках животных. Экспрессию антител проводили следующим способом: линию клеток, происходящих из почки эмбриона человека, FreeStyle 293-F (Invitrogen Corp.) суспендировали в среде для экспрессии FreeStyle 293 Expression Medium (Invitrogen Corp.). Суспензию, имеющую плотность клеток 2,63×105 клеток/мл, инокулировали в концентрации 190 мкл/лунка в 96-луночный планшет. Полученные плазмиды переносили в клетки способом липофекции. Клетки культивировали в течение 4 в инкубаторе с CO2 (37°C, 8% CO2).
Культуральный супернатант, полученный описанным выше способом, использовали для анализа способности к связыванию GC-hIgA с использованием Biacore A100. Антитела в культуральном супернатанте иммобилизировали на сенсорный чип CM5 (GE Healthcare Bio-Sciences Corp.) с иммобилизованном на нем белком A (Invitrogen Corp.) в подходящем количестве способом присоединения аминов. В качестве подвижного буфера использовали буферный раствор, содержащий 20 мМ ACES, 150 мМ NaCl, 0,05% (масс./об.) Tween 20, и 1,2 мМ CaCl2 (pH 7,4). GC-hIgA также разбавляли этим буфером. Весь анализ проводили при 25°C.
Гены антител, оцененные как обладающие способностью связывать GC-hIgA в результате анализа способности связывать IgG с помощью Biacore, амплифицировали с использованием специфических праймеров из векторов для экспрессии в клетках животных, использованных для их экспрессии, а затем анализировали в отношении их нуклеотидных последовательностей.
(22-4) Скрининг связывающего hIgA антитела с помощью ELISA фагов
Содержащий фаг культуральный супернатант получали с помощью культуры фага в соответствии с общепринятым способом (Methods Mol. Biol. (2002) 178, 133-145) из каждой единичной колонии E. coli, полученной после третьего раунда пэннинга, проведенного на стадии (22-2). После добавления BSA и CaCl2(конечная концентрация: 4% BSA и 1,2 мМ ионы кальция), содержащий фаг культуральный супернатант подвергали ELISA по следующей методике: микропланшет для титрования StreptaWell 96 (F. Hoffmann-La Roche Ltd.) покрывали в течение ночи 100 мкл PBS, содержавшего меченный биотином IgA-Fc. Каждую лунку планшета промывали PBST для удаления не связавшихся антигенов. Затем лунку блокировали 250 мкл 4% BSA-TBS в течение 1 часа или более. После удаления 4% BSA-TBS, полученный супернатант добавляли в каждую лунку, и планшет оставляли стоять при 37°C в течение 1 часа для связывания экспонируемых фагом антител с IgA-Fc, содержащимся в каждой лунке. Каждую лунку промывали 1,2 мМ CaCl2/TBST, и добавляли 1,2 мМ CaCl2/TBS или 1 мМ EDTA/TBS. Планшет оставляли стоять при 37°C в течение 30 минут для инкубации. После промывания 1,2 мМ CaCl2/TBST в каждую лунку добавляли конъюгированные с HRP антитела против M13 (Amersham Pharmacia Biotech Inc.), разбавленные TBS, имеющим 4% BSA и ионизированный кальций в концентрации 1,2 мМ (все указаны в конечных концентрациях). Планшет инкубировали в течение 1 часа. После промывания 1,2 мМ CaCl2/TBST, в лунки добавляли простой раствор TMB (ZYMED Laboratories, Inc.). Хромогенную реакцию раствора в каждой лунке завершали добавлением серной кислоты. Затем развитие цвета анализировали на основе поглощения при 450 нм.
Клоны, оцененные как обладающие способностью связывать IgA-Fc, изменяющейся в зависимости от концентрации ионов Ca, в результате ELISA фагов, анализировали в отношении нуклеотидных последовательности их генов фрагментов антител.
(22-5) Получение фрагмента антитела, связывающегося с антигеном Ca-зависимым образом, из библиотеки с помощью пэннинга на гранулах
Первый раунд скрининга сконструированной библиотеки с Ca-зависимым связыванием антигена (Ca-библиотеки) проводили со способностью связывать антиген (IgA-Fc человека) в качестве показателя.
Фаги получали из E. coli, содержавших сконструированную фагмиду для фагового дисплея. К культурам E. coli, которые продуцировали фаги, добавляли 2,5 M NaCl/10% PEG, и совокупность фагов, преципитированных таким образом, разбавляли TBS, получая раствор с фаговой библиотекой. Далее к раствору с фаговой библиотекой добавляли BSA или обезжиренное молоко и CaCl2 (конечная концентрация: 4% BSA и 1,2 мМ ионы кальция; или 3% обезжиренное молоко и 1,2 мМ ионы кальция), получая раствор с блокированной фаговой библиотекой. В первом раунде пэннинга способ пэннинга проводили в соответствии с общепринятым способом пэннинга с использованием антигенов, иммобилизованных на магнитных гранулах (J. Immunol. Methods. (2008) 332 (1-2), 2-9; J. Immunol. Methods. (2001) 247 (1-2), 191-203; Biotechnol. Prog. (2002) 18 (2) 212-20; и Mol. Cell Proteomics (2003) 2 (2), 61-9). Использованные магнитные гранулы представляли собой покрытые нейтравидином гранулы (Sera-Mag SpeedBeads NeutrAvidin-coated) или покрытые стрептавидином гранулы (Dynabeads M-280 Streptavidin).
В частности, 250 пмоль меченных биотином антигенов (меченный биотином IgA-Fc) добавляли к полученному раствору с фаговой библиотекой и, тем самым, приводили в контакт с раствором с фаговой библиотекой при комнатной температуре в течение 60 минут. Добавляли блокированные обезжиренным молоком магнитные гранулы, а затем комплексы антиген-фаг связывали с магнитными гранулами при комнатной температуре в течение 15 минут. Гранулы промывали 1 мл 1,2 мМ CaCl2/TBST (TBS, содержащий 1,2 мМ CaCl2 и 0,1% Tween 20) и 1 мл 1,2 мМ CaCl2/TBS (TBS, содержащий 1,2 мМ CaCl2). После добавления 0,5 мл 1 мг/мл трипсина, гранулы суспендировали при комнатной температуре в течение 15 минут, и сразу после этого гранулы отделяли с использованием магнитного стенда для сбора раствора с фагами. Собранный раствор с фагами добавляли к 10 мл штамма E. coli ER2738 на логарифмической фазе роста (OD600: 0,4-0,7). Штамм E. coli инфицировали фагами при осторожном вращении культуры штамма при 37°C в течение 1 часа. Инфицированные E. coli инокулировали на чашку 225 мм × 225 мм. Далее из культур инокулированных E. coli собирали фаги, получая раствор с фаговой библиотекой.
Второй раунд пэннинга проводили с использованием антигенов, иммобилизованных на планшете. В частности, меченные биотином антигены добавляли в концентрации 5 пмоль/лунка в покрытой стрептавидину планшет с 10 ячейками (StreptaWell, F. Hoffmann-La Roche Ltd.) и приводили в контакт с ним при комнатной температуре в течение 60 минут. Затем планшет промывали три раза TBST (TBS, содержащий 0,1% Tween 20), получая планшет с иммобилизованным на нем антигеном. В него добавляли фаговую библиотеку, блокированную обезжиренным молоком, содержащим 1,2 мМ Ca, и тем самым приводили в контакт с антигенами при комнатной температуре в течение 60 минут. Планшет промывали три раза 1,2 мМ CaCl2/TBST с использованием устройства для промывания планшетов (Skan WASHER, SKARON). Затем планшет далее погружали в 2 л 1,2 мМ CaCl2/TBST и осторожно встряхивали в течение 60 минут. Фаги в каждой лунке, дополненные 0,1 мл 2 мМ EDTA/TBS (TBS, содержащий 2 мМ EDTA), суспендировали при комнатной температуре, а затем собирали раствор с фагами. Добавление 5 мкл 100 мг/мл трипсина к собранному раствору с фагами расщепляло белки pIII (белки pIII, происходящие из хелперного фага) не экспонирующих Fab фагов для устранения способности не экспонирующих Fab фагов инфицировать E. coli. Собранный раствор с фагами добавляли к 10 мл штамма E. coli ER2738 на логарифмической фазе роста (OD600: 0,4-0,7). Штамм E. coli инфицировали фагами при осторожном вращении культуры штамма при 37°C в течение 1 часа. Инфицированные E. coli инокулировали на чашку 225 мм ×225 мм.
(22-6) Скрининг связывающего hIgA антитела с помощью ELISA фагов
Содержащий фаг культуральный супернатант получали с помощью культуры фагов в соответствии с общепринятым способом (Methods Mol. Biol. (2002) 178, 133-145) из каждой единичной колонии E. coli, полученной после пэннинга. ELISA фагов проводили способом, описанным для стадии (22-4). Гены клонов, оцененных как обладающие способностью к Ca-зависимому связыванию антигена, анализировали в отношении их нуклеотидных последовательностей, затем встраивали в векторы для экспрессии в клетках животных и экспрессировали в качестве антител, которые затем очищали.
[Пример 23] Оценка полученного антитела в отношении его способности к Ca-зависимому связыванию с IgA человека
(23-1) Экспрессия и очистка полученного антитела против IgA человека
Среди полученных антител, оцененных как обладающие способностью связывать IgA человека в примере 22, антитела GA1-IgG1 (полученное на стадии (22-3); тяжелая цепь: SEQ ID NO: 101 и легкая цепь: SEQ ID NO: 102), GA2-IgG1 (полученное на стадии (22-4); тяжелая цепь: SEQ ID NO: 103 и легкая цепь: SEQ ID NO: 104), GA3-IgG1 (полученное на стадии (22-6); тяжелая цепь: SEQ ID NO: 105 и легкая цепь: SEQ ID NO: 106), и GA4-IgG1 (полученное на стадии (22-3); тяжелая цепь: SEQ ID NO: 107 и легкая цепь: SEQ ID NO: 108) экспрессировали с использованием следующего способа, а затем очищали: линию FreeStyle 293-F, происходящую из почки эмбриона человека, (Invitrogen Corp.) суспендировали в среде для экспрессии FreeStyle 293 Expression Medium (Invitrogen Corp.). Суспензию, имеющую плотность клеток 1,33×106 клеток/мл, инокулировали в концентрации 3 мл/лунка в планшет с 6 ячейками. Полученные плазмиды трансфицировали в клетки путем липофекции. Клетки культивировали в течение 4 суток в инкубаторе с CO2 (37°C, 8% CO2, 90 об./мин.). Антитела очищали из полученного культурального супернатанта способом, общеизвестным специалистам в данной области, с использованием rProtein A Sepharose(TM) Fast Flow (Amersham Biosciences, Inc.). Поглощение очищенного раствора антител измеряли при 280 нм с использованием спектрофотометра. Концентрацию антитела вычисляли из полученной величины измерения с использованием коэффициента экстинкции, вычисленного с помощью PACE (Protein Science (1995) 4, 2411-2423).
(23-2) Оценка полученного антитела в отношении его способности к Ca-зависимому связыванию IgA
Антитела (GA1-IgG1, GA2-IgG1, GA3-IgG1 и GA4-IgG1), полученные на стадии (23-1), оценивали в отношении их активности связывания IgA человека (константа диссоциации KD (M)) с использованием Biacore T200 (GE Healthcare Bio-Sciences Corp.). Активность связывания анализировали с использованием 0,05% Tween 20, 20 ммоль/л ACES и 150 ммоль/л NaCl с добавлением 3 мкМ или 1,2 мМ CaCl2 (pH 7,4 и pH 5,8) или 0,05% Tween 20, 20 ммоль/л ACES и 150 ммоль/л NaCl (pH 8,0) с добавлением 0,1 мкМ или 10 мМ CaCl2 в качестве подвижного буфера.
Каждое антитело связывали с рекомбинантным белком A/G (Thermo Fisher Scientific K.K.), иммобилизованным в соответствующем количестве на сенсорный чип CM5 (GE Healthcare Bio-Sciences Corp.) способом присоединения аминов. Соответствующую концентрацию MRA-hIgA (описанного на стадии (22-1)) инжектировали на него в качестве анализируемого соединения и подвергали взаимодействию с антителом на сенсорном чипе. Затем инжектировали 10 ммоль/л глицин-HCl (pH 1,5), чтобы регенерировать сенсорный чип. Анализ проводили при 37°C. Константу диссоциации KD (M) вычисляли с помощью анализа с аппроксимацией кривой и анализа равновесной величины на основе результатов анализа с использованием Biacore T200 Evaluation Software (GE Healthcare Bio-Sciences Corp.). Результаты представлены в таблице 28. Также, полученные сенсограммы представлены на фиг. 12. Как явно показано, GA2-IgG1, GA3-IgG1 и GA4-IgG1 прочно связываются с IgA человека при концентрации Ca2+ 1,2 мМ, но слабо связываются с IgA человека при концентрации ионов Ca 3 мкМ.
[Таблица 28]

Хотя антитела, взаимодействие которых с антигенами (рецепторы IL6) изменялось в зависимости от концентрации ионов Ca, были получены из Ca-библиотеки согласно примеру 14, было выявлено, что антитела, связывающиеся с антигенами зависимым от концентрации ионов Ca образом, могут быть получены не только с использованием рецепторов IL6, но и с использованием IgA человека.
[Пример 24] Получение антитела, связывающегося с глипиканом 3 человека (GPC3) зависимым от Ca образом
(24-1) Получение глипикана 3 человека
Рекомбинантный глипикан 3 человека (далее обозначаемый как GPC3) для применения в качестве антигена получали следующим образом: культуральный супернатант собирали из клеток CHO, стабильно трансфицированных плазмидами, для экспрессии не содержащей трансмембранной области аминокислотной последовательности глипикана 3 человека, связанной с 6 остатками гистидина (SEQ ID NO: 109). Полученный культуральный супернатант очищали ионообменной хроматографией, затем подвергали аффинной очистке на основе His-метки, и очищали гель-фильтрацией с получением GPC3. GPC3 метили биотином с использованием EZ-Link NHS-PEG4-Biotin (Thermo Fisher Scientific K.K.) для получения меченного биотином GPC3.
(24-2) Получение фрагмента антитела, связывающегося с антигеном зависимым от Ca образом из библиотеки с помощью пэннинга на гранулах
Первый раунд скрининга сконструированной библиотеки антител с Ca-зависимым связыванием GPC3 проводили со способностью связывать антиген (GPC3) в качестве показателя.
Фаги получали из E. coli, содержавших сконструированную фагмиду для фагового дисплея. К культурам E. coli, которые продуцировали фаги, добавляли 2,5 M NaCl/10% PEG, и совокупность фагов, преципитированных таким образом, разбавляли TBS, получая раствор с фаговой библиотекой. Далее к раствору с фаговой библиотекой добавляли BSA или обезжиренное молоко и CaCl2 (конечная концентрация: 4% BSA и 1,2 мМ ионы кальция; или 3% обезжиренное молоко и 1,2 мМ ионы кальция), получая раствор с блокированной фаговой библиотекой. Способ пэннинга проводили в соответствии с общепринятым способом пэннинга с использованием антигенов, иммобилизованных на магнитных гранулах (J. Immunol. Methods. (2008) 332 (1-2), 2-9; J. Immunol. Methods. (2001) 247 (1-2), 191-203; Biotechnol. Prog. (2002) 18 (2) 212-20; и Mol. Cell Proteomics (2003) 2 (2), 61-9). Использованные магнитные гранулы представляли собой покрытые нейтравидином гранулы (Sera-Mag SpeedBeads NeutrAvidin-coated) или покрытые стрептавидином гранулы (Dynabeads M-280 Streptavidin).
В частности, 250 пмоль меченных биотином антигенов (меченный биотином GPC3) добавляли к полученному раствору с фаговой библиотекой и, тем самым, приводили в контакт с раствором с фаговой библиотекой при комнатной температуре в течение 60 минут. Добавляли блокированные BSA или обезжиренным молоком магнитные гранулы, а затем комплексы антиген-фаг связывали с магнитными гранулами при комнатной температуре в течение 15 минут. Гранулы промывали 1 мл 1,2 мМ CaCl2/TBST (TBS, содержащий 1,2 мМ CaCl2) и 1 мл 1,2 мМ CaCl2/TBS (TBS, содержащий 1,2 мМ CaCl2). После добавления 0,5 мл 1 мг/мл трипсина, гранулы суспендировали при комнатной температуре в течение 15 минут, и сразу после этого гранулы отделяли с использованием магнитного стенда для сбора раствора с фагами. Собранный раствор с фагами добавляли к 10 мл штамма E. coli ER2738 на логарифмической фазе роста (OD600: 0,4-0,7). Штамм E. coli инфицировали фагами при осторожном вращении культуры штамма при 37°C в течение 1 часа. Инфицированные E. coli инокулировали на чашку 225 мм × 225 мм. Далее из культур инокулированных E. coli собирали фаги, получая раствор с фаговой библиотекой.
На втором и последующих раундах пэннинга увеличивали содержание фагов со способностью к Ca-зависимому связыванию антигена в качестве показателя. В частности, 40 пмоль меченных биотином антигенов добавляли к раствору с фаговой библиотекой, полученному путем блокирования аналогично тому, как и на первом раунде пэниннга, и, тем самым, приводили в контакт с раствором с фаговой библиотекой при комнатной температуре в течение 60 минут. Добавляли блокированные BSA или обезжиренным молоком магнитные гранулы, а затем комплексы антиген-фаг связывали с магнитными гранулами при комнатной температуре в течение 15 минут. Гранулы промывали 1 мл 1,2 мМ CaCl2/TBST и 1,2 мМ CaCl2/TBS. Затем гранулы, дополненные 0,1 мл 2 мМ EDTA/TBS (TBS, содержащий 2 мМ EDTA), суспендировали при комнатной температуре. Сразу после этого гранулы отделяли с использованием магнитного стенда для сбора раствора с фагами. Добавление 5 мкл 100 мг/мл трипсина к собранному раствору с фагами расщепляло белки pIII (белки pIII, происходящие из хелперного фага) не экспонирующих Fab фагов для устранения способности не экспонирующих Fab фагов инфицировать E. coli. Собранный раствор с фагами добавляли к 10 мл штамма E. coli ER2738 на логарифмической фазе роста (OD600: 0,4-0,7). Штамм E. coli инфицировали фагами при осторожном вращении культуры штамма при 37°C в течение 1 часа. Инфицированные E. coli инокулировали на чашку 225 мм × 225 мм. Далее из культур инокулированных E. coli собирали фаги, получая раствор с фаговой библиотекой.
(24-3) Скрининг связывающего GPC3 антитела с помощью ELISA фагов
Содержащий фаг культуральный супернатант получали с помощью культуры фага в соответствии с общепринятым способом (Methods Mol. Biol. (2002) 178, 133-145) из каждой единичной колонии E. coli, полученной после второго и третьего раундов пэннинга, проведенных описанным выше способом.
После добавления BSA и CaCl2(конечная концентрация: 4% BSA и 1,2 мМ ионы кальция), содержащий фаг культуральный супернатант подвергали ELISA по следующей методике: микропланшет для титрования StreptaWell 96 (F. Hoffmann-La Roche Ltd.) покрывали в течение ночи 100 мкл PBS, содержавшего меченные биотином антигены. Каждую лунку планшета промывали PBST (PBS, содержащий 0,1% Tween 20) для удаления не связавшихся антигенов. Затем лунку блокировали 250 мкл 4% BSA-TBS в течение 1 часа или более. После удаления 4% BSA-TBS, полученный супернатант добавляли в каждую лунку, и планшет оставляли стоять при 37°C в течение 1 часа для связывания экспонируемых фагом антител с антигенами, содержащимися в каждой лунке. Каждую лунку промывали 1,2 мМ CaCl2/TBST, и добавляли 1,2 мМ CaCl2/TBS или 1 мМ EDTA/TBS. Планшет оставляли стоять при 37°C в течение 30 минут для инкубации. После промывания 1,2 мМ CaCl2/TBST в каждую лунку добавляли конъюгированные с HRP антитела против M13 (Amersham Pharmacia Biotech Inc.), разбавленные TBS, имеющим 4% BSA и ионизированный кальций в концентрации 1,2 мМ (все указаны в конечных концентрациях). Планшет инкубировали в течение 1 часа. После промывания 1,2 мМ CaCl2/TBST, в лунки добавляли простой раствор TMB (ZYMED Laboratories, Inc.). Хромогенную реакцию раствора в каждой лунке завершали добавлением серной кислоты. Затем развитие цвета анализировали на основе поглощения при 450 нм.
Гены фрагментов антител, оцененные как обладающие способностью к Ca-зависимому связыванию антигена в результате ELISA фагов, амплифицировали в качестве матрицы с использованием специфических праймеров, а затем анализировали в отношении их нуклеотидных последовательностей.
(24-4) Экспрессия и очистка антитела, связывающегося с GPC3 человека
Гены четырех антител, оцененных как обладающие способностью к Ca-зависимому связыванию антигена в результате ELISA фагов, т.е. CSCM-01_005 (последовательность тяжелой цепи: 110 и последовательность легкой цепи: 111), CSCM-01_009 (последовательность тяжелой цепи: 112 и последовательность легкой цепи: 113), CSCM-01_015 (последовательность тяжелой цепи: 114 и последовательность легкой цепи: 115), и CSCM-01_023 (последовательность тяжелой цепи: 116 и последовательность легкой цепи: 117), и антитела против GPC3 человека GC-IgG1 (последовательность тяжелой цепи: 118 и последовательность легкой цепи: 119) в качестве контроля по отдельности встраивали в плазмиды для экспрессии в клетках животных. Экспрессию антител проводили следующим способом: линию FreeStyle 293-F, происходящую из почки эмбриона человека, (Invitrogen Corp.) суспендировали в среде для экспрессии FreeStyle 293 Expression Medium (Invitrogen Corp.). Суспензию, имеющую плотность клеток 1,33×106 клеток/мл, инокулировали в концентрации 3 мл/лунка в планшет с 6 ячейками. Полученные плазмиды переносили в клетки путем липофекции. Клетки культивировали в течение 4 суток в инкубаторе с CO2 (37°C, 8% CO2, 90 об./мин.). Антитела очищали из полученного культурального супернатанта способом, общеизвестным специалистам в данной области, с использованием rProtein A Sepharose(TM) Fast Flow (Amersham Biosciences, Inc.). Поглощение очищенного раствора антител измеряли при 280 нм с использованием спектрофотометра. Концентрацию антитела вычисляли из полученной величины измерения с использованием коэффициента экстинкции, вычисленного с помощью PACE (Protein Science (1995) 4, 2411-2423). Антитело GC-IgG1 очищали аналогично тому, как описано выше, из культурального супернатанта клеток CHO, стабильно экспрессирующих антитело GC-IgG1, и его концентрацию вычисляли.
(24-5) Оценка полученного антитела в отношении способности к Ca-зависимому связыванию с GPC3 человека
Полученные антитела подвергали ELISA по следующей методике: микропланшет для титрования StreptaWell 96 (F. Hoffmann-La Roche Ltd.) покрывали в течение ночи 100 мкл PBS, содержавшим антигены, меченные биотином. Каждую лунку планшета промывали буфером ACES (10 мМ ACES, 150 мМ NaCl, 100 мМ CaCl2 и 0,05% Tween 20 (pH 7,4)) для удаления не связанных антигенов. Затем лунку блокировали 250 мкл буфера ACES, содержавшего 2% BSA, в течение 1 часа или более. После удаления буфера ACES, содержавшего 2% BSA, 100 мкл каждого из 4-кратных серийных разведений очищенного IgG, заранее разбавленного от 10 мкг/мл, добавляли в каждую лунку, и планшет оставляли стоять в течение 1 часа для связывания IgG с антигенами, содержавшимися в каждой лунке. Каждую лунку промывали буфером ACES, и добавляли “10 мМ ACES, 150 мМ NaCl и 1,2 мМ CaCl2 (pH 7,4)”, “10 мМ ACES, 150 мМ NaCl и 3 мкМ CaCl2 (pH 7,4)”, “10 мМ ACES, 150 мМ NaCl и 1,2 мМ CaCl2 (pH 5,8)” или “10 мМ ACES, 150 мМ NaCl и 3 мкМ CaCl2 (pH 5,8)”. Планшет оставляли стоять при 37°C в течение 30 минут для инкубации. После промывания буфером ACES, в каждую лунку добавляли конъюгированные с HRP антитела против IgG человека (BioSource International, Inc.), разбавленные буфером ACES, содержавшим 2% BSA. Планшет инкубировали в течение 1 часа. После промывания буфером ACES, в лунки добавляли простой раствор TMB (ZYMED Laboratories, Inc.). Хромогенную реакцию раствора в каждой лунке завершали добавлением серной кислоты. Затем анализировали развитие цвета на основе поглощения при 450 нм.
Результаты анализа представлены на фиг. 13. Поглощение было постоянным для GC-IgG1, независимо от концентрации ионов кальция, в то время как поглощение было значительно более низким для CSCM-01_005, CSCM-01_009, CSCM-01_015 и CSCM-01_023 при концентрации ионов кальция 3 мкМ (низкая концентрация ионов кальция), чем при концентрации ионов кальция 1,2 мМ (высокая концентрация ионов кальция). Из этих результатов было показано, что CSCM-01_005, CSCM-01_009, CSCM-01_015, и CSCM-01_023 обладают свойством связывания антигена, которое изменяется в зависимости от концентрации ионов кальция, что указывает на то, что кальций-зависимое антитело также может быть получено против глипикана 3 человека.
[Пример 25] Получение антитела, связывающегося с IgA мыши зависимым от pH образом
(25-1) Получение GC-mIgA и биотинилированного IgA-Fc мыши
GC-mIgA (тяжелая цепь: SEQ ID NO: 120 и легкая цепь: SEQ ID NO: 121) и биотинилированное IgA-Fc мыши (также обозначаемое как меченное биотином mIgA-Fc; mIgA_CH2-CH3-Avitag: SEQ ID NO: 122) получали в качестве IgA мыши следующим образом:
(25-1-1) Получение GC-mIgA
Рекомбинантное IgA GC-mIgA мыши получали следующим образом: фрагмент гена, кодирующий GC-mIgA (тяжелая цепь: SEQ ID NO: 120 и легкая цепь: SEQ ID NO: 121), встраивали в вектор для экспрессии в клетках животных. FreeStyle 293 (Invitrogen Corp.) котрансфицировали сконструированным плазмидным вектором и геном, кодирующим EBNA1, подлежащим экспрессии, с использованием 293Fectin (Invitrogen Corp.). Затем клетки, трансфицированные этими генами, культивировали при 37°C в течение 4 суток в атмосфере 8% CO2 для секреции белков GC-mIgA в культуральный супернатант.
Содержащие GC-mIgA клеточные культуры фильтровали через 0,22-мкм фильтр на горловину бутылки, получая культуральный супернатант. Культуральный супернатант разбавляли 20 мМ Tris-HCl (pH 8,0) и наносили на HiTrap Q HP (GE Healthcare Bio-Sciences Corp.), уравновешенную этом раствором, а затем GC-mIgA элюировали на градиенте концентрации NaCl. Затем проводили удаление ассоциатов гель-фильтрацией с использованием Superdex 200 и замену буфера на 20 мМ His-HCl и 150 мМ NaCl (pH 6,0), получая очищенный GC-mIgA.
(25-1-2) Получение меченного биотином mIgA-Fc
Для добавления биотина на C-конец представляющего интерес белка (IgA-Fc мыши), фрагмент гена, кодирующий специфическую последовательность (последовательность Avitag) для опосредуемого биотинлигазой биотинилирования, присоединяли ниже фрагмента гена, кодирующего область IgA-Fc мыши. Фрагмент гена, кодирующий белок IgA мыши, связанный с последовательностью Avitag (mIgA_CH2-CH3-Avitag (SEQ ID NO: 122)), встраивали в векторы для экспрессии в клетках животных. FreeStyle 293 (Invitrogen Corp.) трансфицировали сконструированными плазмидными векторами с использованием 293Fectin (Invitrogen Corp.). Эту трансфекцию проводили одновременно с геном, кодирующим EBNA1, подлежащим экспрессии, и геном, кодирующим биотинлигазу (BirA), подлежащим экспрессии для биотинилирования, чтобы пометить белок биотином. Клетки, трансфицированные этими генами в соответствии с описанными выше методиками, культивировали при 37°C в течение 6 суток в атмосфере 8% CO2 для секреции представляющего интерес белка в культуральный супернатант.
Клеточные культуры, содержащие представляющий интерес IgA-Fc мыши, фильтровали через 0,22-мкм фильтр на горлышко бутылки с получением культурального супернатанта. Культуральный супернатант разбавляли 20 мМ Tris-HCl (pH 7,4) и наносили на HiTrap Q HP (GE Healthcare Bio-Sciences Corp.), уравновешенную этим раствором, а затем представляющий интерес IgA-Fc мыши элюировали на градиенте концентрации NaCl. Далее, элюат с HiTrap Q HP разбавляли 50 мМ Tris-HCl (pH 8,0) и наносили на колонку SoftLink Avidin, уравновешенную этим раствором, а затем представляющее интерес IgA-Fc мыши элюировали 5 мМ биотином, 150 мМ NaCl, и 50 мМ Tris-HCl (pH 8,0). Затем проводили удаление ассоциатов гель-фильтрацией с использованием Superdex 200 и полученный содержащий IgA-Fc мыши буфер заменяли на 20 мМ His-HCl и 150 мМ NaCl (pH 6,0), получения очищенное IgA-Fc мыши.
(25-2) Получение фрагмента антитела, связывающегося с антигеном pH-зависимым образом, из His-библиотеки с помощью пэннинга на гранулах
Первый раунд скрининга сконструированной библиотеки с pH-зависимым связыванием антигена (His-библиотека 1) проводили со способностью связывать антиген (IgA-Fc мыши) в качестве показателя.
Фаги получали из E. coli, содержавших сконструированную фагмиду для фагового дисплея. К культурам E. coli, которые продуцировали фаги, добавляли 2,5 M NaCl/10% PEG, и совокупность фагов, преципитированных таким образом, разбавляли TBS, получая раствор с фаговой библиотекой. Далее к раствору с фаговой библиотекой добавляли обезжиренное молоко (конечная концентрация: 3% обезжиренное молоко), получая раствор с блокированной фаговой библиотекой. Способ пэннинга проводили в соответствии с общепринятым способом пэннинга с использованием антигенов, иммобилизованных на магнитных гранулах (J. Immunol. Methods. (2008) 332 (1-2), 2-9; J. Immunol. Methods. (2001) 247 (1-2), 191-203; Biotechnol. Prog. (2002) 18 (2) 212-20; и Mol. Cell Proteomics (2003) 2 (2), 61-9). Использованные магнитные гранулы представляли собой покрытые нейтравидином гранулы (Sera-Mag SpeedBeads NeutrAvidin-coated) или покрытые стрептавидином гранулы (Dynabeads M-280 Streptavidin).
В частности, меченные биотином антигены (меченный биотином mIgA-Fc) добавляли к полученному раствору с фаговой библиотекой и, тем самым, приводили в контакт с раствором с фаговой библиотекой при комнатной температуре в течение 60 минут. Меченные биотином антигены использовали в пэннинге в количестве 250 пмоль для первого раунда, 40 пмоль для второго раунда и 10 пмоль для третьего раунда. После добавления блокированных молоком магнитных гранул, комплексы антиген-фаг связывали с магнитными гранулами при комнатной температуре в течение 15 минут. Гранулы промывали 1 мл 1,2 мМ CaCl2/TBST (TBS, содержащий 1,2 мМ CaCl2 и 0,1% Tween 20 (pH 7,6)) и 1 мл 1,2 мМ CaCl2/TBS (TBS, содержащий 1,2 мМ CaCl2 (pH 7,6)). После добавления 0,5 мл 1 мг/мл трипсина, гранулы суспендировали при комнатной температуре в течение 15 минут, и сразу после этого гранулы отделяли с использованием магнитного стенда для сбора раствора с фагами. Собранный раствор с фагами добавляли к 10 мл штамма E. coli ER2738 на логарифмической фазе роста (OD600: 0,4-0,7). Штамм E. coli инфицировали фагами при осторожном вращении культуры штамма при 37°C в течение 1 часа. Инфицированные E. coli инокулировали на чашку 225 мм × 225 мм. Далее из культур инокулированных E. coli собирали фаги, получая раствор с фаговой библиотекой. Этот пэннинг проводили всего в течение 3 раундов.
(25-3) Оценка антитела, связывающего IgA мыши, в отношении его связывающей способности с использованием Biacore
Гены фрагментов антител, экстрагированные из фагмид, полученных из E. coli, полученных после завершения третьего раунда пэннинга, встраивали в векторы для экспрессии в клетках животных. Экспрессию антител проводили следующим способом: линию клеток, происходящих из почки эмбриона человека, FreeStyle 293-F (Invitrogen Corp.) суспендировали в среде для экспрессии FreeStyle 293 Expression Medium (Invitrogen Corp.). Суспензию, имеющую плотность клеток 2,63×105 клеток/мл, инокулировали в концентрации 190 мкл/лунка в 96-луночный планшет. Полученные плазмиды переносили в клетки способом липофекции. Клетки культивировали в течение 4 в инкубаторе с CO2 (37°C, 8% CO2).
Культуральный супернатант, полученный описанным выше способом, использовали для анализа способности к связыванию GC-mIgA с использованием Biacore A100. Антитела в культуральном супернатанте улавливали на сенсорный чип CM5 (GE Healthcare Bio-Sciences Corp.) с белком A/G (Invitrogen Corp.), иммобилизованным на нем в подходящем количестве, способом присоединения аминов. В качестве подвижных буферов использовали два типа буферных растворов: 20 мМ ACES, 150 мМ NaCl, 0,05% (масс./об.) Tween 20 и 1,2 мМ CaCl2 (pH 7,4); и 20 мМ ACES, 150 мМ NaCl, 0,05% (масс./об.) Tween 20 и 1,2 мМ CaCl2 (pH 5,8). Взаимодействие в реакции антиген-антитело анализировали в условиях нейтральных значений pH и кислых значений pH. GC-mIgA также разбавляли каждым из этих буферов и инжектировали при скорости потока 10 мкл/мин в течение 60 секунд для взаимодействия антигена с антителами, уловленными на сенсорном чипе. Затем, на него инжектировали 10 мМ глицин-HCl (pH 1,5) со скоростью потока 30 мкм/мин в течение 30 секунд, чтобы регенерировать сенсорный чип. Весь анализ проводили при 25°C.
В результате оценки связывания с помощью Biacore mIAP1B3-3_#024 (тяжелая цепь: SEQ ID NO: 123 и легкая цепь: SEQ ID NO: 124), mIAP1B3-3_#130 (тяжелая цепь: SEQ ID NO: 125 и легкая цепь: SEQ ID NO: 126), и mIAP1B3-3_#230 (тяжелая цепь: SEQ ID NO: 127 и легкая цепь: SEQ ID NO: 128) были получены в качестве антител, оцененных как обладающие способностью к pH-зависимому связыванию с GC-mIgA. На фиг. 14 представлены сенсограммы для этих антител при pH 7,4 и pH 5,8. Было выявлено, что способность этих антител связывать IgA мыши снижалась при изменении pH буфера от pH 7,4 до pH 5,8.
Гены этих антител из векторов для экспрессии в клетках животных, использованных для их экспрессии, анализировали в отношении их нуклеотидных последовательностей.
Хотя антитела, взаимодействие которых с антигенами (IL-6R) изменялось, в зависимости от pH, были получены из His-библиотеки 1 в примере 3, было выявлено, что антитела, связывающиеся с антигенами pH-зависимым образом, могут быть получены не только с использованием IL-6R, но и с использованием IgA мыши.
[Пример 26] Получение антитела, связывающегося с HMGB1 человека зависимым от pH образом
(26-1) Получение HMGB1 человека и биотинилированного HMGB1 человека
HMGB1 человека (SEQ ID NO: 129) и биотинилированный HMGB1-Avi человека (также обозначаемый как меченный биотином hHMGB1; hHMGB1-Avitag: SEQ ID NO: 130) получали следующим образом:
(26-1-1) Получение HMGB1 человека
Рекомбинантный HMGB1 человека hHMGB1 получали следующим образом: фрагмент гена, кодирующий hHMGB1 (SEQ ID NO: 129), встраивали в вектор для экспрессии в клетках животных. FreeStyle 293 (Invitrogen Corp.) котрансфицировали сконструированным плазмидным вектором и геном, кодирующим EBNA1, подлежащим экспрессии, с использованием 293Fectin (Invitrogen Corp.). Затем клетки, трансфицированные этими генами, культивировали при 37°C в атмосфере 8% CO2 для секреции белков hHMGB1 в культуральный супернатант. Полученный таким образом культуральный супернатант наносили на HiTrap SP Sepharose HP (GE Healthcare Bio-Sciences Corp.), заранее уравновешенную PBS, и колонку промывали PBS, а затем белки, адсорбированные на колонке, элюировали на линейном градиенте концентрации хлорида натрия. После уравновешивания 20 мМ гистидин-HCl (pH 5,0), элюированную фракцию, содержащую hHMGB1, разбавленную в 3 раза этим буферным раствором, наносили на колонку. Колонку промывали этим буфером, а затем белки, адсорбированные на колонке, элюировали на линейном градиенте концентрации хлорида натрия. Содержащую hHMGB1 фракцию концентрировали с помощью ультрафильтрационной мембраны, а затем наносили на колонку Superdex 200 (GE Healthcare Bio-Sciences Corp.), уравновешенную 300 мМ NaCl и 20 мМ гистидином (pH 6,0). Очищенную фракцию hHMGB1 получали путем разделения с использованием того же буферного раствора.
(26-1-2) Получение меченного биотином HMGB1 человека
Для добавления биотина на C-конец представляющего интерес белка (HMGB1 человека), фрагмент гена, кодирующий специфическую последовательность (последовательность Avitag) для опосредуемого биотинлигазой биотинилирования, присоединяли ниже фрагмента гена, кодирующего область HMGB1 человека. Фрагмент гена, кодирующий белок HMGB1 человека, связанный с последовательностью Avitag (hHMGB1-Avitag (SEQ ID NO: 130)), встраивали в векторы для экспрессии в клетках животных. FreeStyle 293 (Invitrogen Corp.) трансфицировали сконструированными плазмидными векторами с использованием 293Fectin (Invitrogen Corp.). Эту трансфекцию проводили одновременно с геном, кодирующим EBNA1, подлежащим экспрессии, и геном, кодирующим биотинлигазу (BirA), подлежащим экспрессии для биотинилирования, чтобы пометить белок биотином. Клетки, трансфицированные этими генами в соответствии с описанными выше методиками, культивировали при 37°C в атмосфере 8% CO2 для секреции представляющего интерес белка в культуральный супернатант.
Полученный таким образом культуральный супернатант наносили на HiTrap SP Sepharose HP (GE Healthcare Bio-Sciences Corp.), заранее уравновешенную PBS, и колонку промывали PBS, а затем белки, адсорбированные на колонке, элюировали на линейном градиенте концентрации хлорида натрия. Фракцию, содержавшую HMGB1-Avi, разбавленную в 2 раза 100 мМ Tris-HCl (pH 7,4), наносили на колонку SoftLink Soft Release Avidin Resin column (Promega Corp.), уравновешенную TBS. Колонку промывали TBS, а затем белки, адсорбированные на колонке, элюировали с использованием TBS (pH 8,0), содержащего 5 мМ биотин. Фракцию, содержавшую HMGB1-Avi, концентрировали через ультрафильтрационную мембрану, а затем наносили на колонку Superdex 200 (GE Healthcare Bio-Sciences Corp.), уравновешенную 300 мМ NaCl и 20 мМ гистидином (pH 6,0). Очищенную фракцию биотинилированного HMGB1-Avi получали путем разделения с использованием того же буферного раствора.
(26-2) Получение фрагмента антитела, связывающегося с антигеном pH-зависимым образом, из His-библиотеки с помощью пэннинга на гранулах
Первый раунд скрининга сконструированной библиотеки с pH-зависимым связыванием антигена (His-библиотека 1) проводили со способностью связывать антиген (HMGB1 человека) в качестве показателя.
Фаги получали из E. coli, содержавших сконструированную фагмиду для фагового дисплея. К культурам E. coli, которые продуцировали фаги, добавляли 2,5 M NaCl/10% PEG, и совокупность фагов, преципитированных таким образом, разбавляли TBS, получая раствор с фаговой библиотекой. Далее к раствору с фаговой библиотекой добавляли BSA и CaCl2 (конечная концентрация: 4% BSA и 1,2 мМ ионы кальция), получая раствор с блокированной фаговой библиотекой. Способ пэннинга проводили в соответствии с общепринятым способом пэннинга с использованием антигенов, иммобилизованных на магнитных гранулах (J. Immunol. Methods. (2008) 332 (1-2), 2-9; J. Immunol. Methods. (2001) 247 (1-2), 191-203; Biotechnol. Prog. (2002) 18 (2) 212-20; и Mol. Cell Proteomics (2003) 2 (2), 61-9). Использованные магнитные гранулы представляли собой покрытые нейтравидином гранулы (Sera-Mag SpeedBeads NeutrAvidin-coated) или покрытые стрептавидином гранулы (Dynabeads M-280 Streptavidin).
В частности, 250 пмоль меченных биотином антигенов (меченный биотином hHMGB1) добавляли к полученному раствору с фаговой библиотекой и, тем самым, приводили в контакт с раствором с фаговой библиотекой при комнатной температуре в течение 60 минут. Добавляли блокированные BSA магнитные гранулы, а затем комплексы антиген-фаг связывали с магнитными гранулами при комнатной температуре в течение 15 минут. Гранулы промывали 1 мл 1,2 мМ CaCl2/TBST (50 мМ Tris, 300 мМ NaCl, 1,2 мМ CaCl2 и 0,1% Tween 20 (pH 7,6)) и 1 мл 1,2 мМ CaCl2/TBS (50 мМ Tris, 300 мМ NaCl, и 1,2 мМ CaCl2 (pH 7,6)). После добавления 0,5 мл 1 мг/мл трипсина, гранулы суспендировали при комнатной температуре в течение 15 минут, и сразу после этого гранулы отделяли с использованием магнитного стенда для сбора раствора с фагами. Собранный раствор с фагами добавляли к 10 мл штамма E. coli ER2738 на логарифмической фазе роста (OD600: 0,4-0,7). Штамм E. coli инфицировали фагами при осторожном вращении культуры штамма при 37°C в течение 1 часа. Инфицированные E. coli инокулировали на чашку 225 мм × 225 мм. Далее из культур инокулированных E. coli собирали фаги, получая раствор с фаговой библиотекой.
На втором и последующих раундах пэннинга увеличивали содержание фагов с антигенсвязывающей способностью или способностью к pH-зависимому связыванию в качестве показателя. В частности, 40 пмоль меченных биотином антигенов добавляли к полученному раствору с фаговой библиотекой, и, тем самым, приводили в контакт с раствором с фаговой библиотекой при комнатной температуре в течение 60 минут. Добавляли блокированные BSA магнитные гранулы, а затем комплексы антиген-фаг связывали с магнитными гранулами при комнатной температуре в течение 15 минут. Гранулы промывали несколько раз 1 мл 1,2 мМ CaCl2/TBST и 1,2 мМ CaCl2/TBS. Для увеличения содержания с антигенсвязывающей способностью в качестве показателя, гранулы, дополненные 0,5 мл 1 мг/мл трипсина, суспендировали при комнатной температуре в течение 15 минут, и сразу после этого гранулы отделяли с использованием магнитного стенда для сбора раствора с фагами. Для увеличения содержания со способностью к pH-зависимому связыванию антигена в качестве показателя, к гранулам добавляли 0,4 мл (раунд 2) или 0,1 мл (раунд 3 или далее) 50 мМ MES/1,2 мМ CaCl2/150 мМ NaCl (pH 5,5) и полученные гранулы суспендировали при комнатной температуре. Затем гранулы отделяли с использованием магнитного стенда, получая раствор с фагами. Добавление 20 мкл (раунд 2) или 5 мкл (раунд 3 или далее) 100 мг/мл трипсина к собранному раствору с фагами расщепляло белки pIII (белки pIII, происходящие из хелперного фага) не экспонирующих Fab фагов для устранения способности не экспонирующих Fab фагов инфицировать E. coli. Собранные фаги добавляли к 10 мл штамма E. coli ER2738 на логарифмической фазе роста (OD600: 0,4-0,7). Штамм E. coli инфицировали фагами при осторожном вращении культуры штамма при 37°C в течение 1 часа. Инфицированные E. coli инокулировали на чашку 225 мм × 225 мм. Далее из культур инокулированных E. coli собирали фаги, получая раствор с фаговой библиотекой. Этот пэннинг с антигенсвязывающей способностью или способностью к pH-зависимому связыванию в качестве показателя проводили всего в течение 3 раундов.
(26-3) Скрининг связывающего HMGB1 человека с помощью ELISA фагов
Содержащий фаг культуральный супернатант получали с помощью культуры фага в соответствии с общепринятым способом (Methods Mol. Biol. (2002) 178, 133-145) из каждой единичной колонии E. coli, полученной после третьего и четвертого раундов пэннинга, проведенных на стадии (26-2). После добавления BSA и CaCl2(конечная концентрация: 4% BSA и 1,2 мМ ионы кальция), содержащий фаг культуральный супернатант подвергали ELISA по следующей методике: микропланшет для титрования StreptaWell 96 (F. Hoffmann-La Roche Ltd.) покрывали в течение четырех часов или более 100 мкл PBS, содержавшего меченный биотином hHMGB1. Каждую лунку планшета промывали PBST для удаления не связавшихся антигенов. Затем лунку блокировали 250 мкл 4% BSA-TBS (50 мМ Tris, 300 мМ NaCl, 2,5 мМ CaCl2 и 4% BSA) в течение 1 часа или более. После удаления 4% BSA-TBS, полученный супернатант добавляли в каждую лунку, и планшет оставляли стоять при 37°C в течение 1 часа для связывания экспонируемых фагом антител с HMGB1, содержащимся в каждой лунке. Каждую лунку промывали 1,2 мМ CaCl2/TBST (pH 7,6) и добавляли 1,2 мМ CaCl2/TBS (pH 7,6) или 1,2 мМ CaCl2/150 мМ NaCl/50 мМ MES (pH 5,5). Планшет оставляли стоять при 37°C в течение 30 минут для инкубации. После промывания 1,2 мМ CaCl2/TBST в каждую лунку добавляли конъюгированные с HRP антитела против M13 (Amersham Pharmacia Biotech Inc.), разбавленные 4% BSA-TBS. Планшет инкубировали в течение 1 часа. После промывания 1,2 мМ CaCl2/TBST (pH 7,6), в лунки добавляли простой раствор TMB (Invitrogen Corp.). Хромогенную реакцию раствора в каждой лунке завершали добавлением серной кислоты. Затем развитие цвета анализировали на основе поглощения при 450 нм.
Гены фрагментов антител, содержащиеся в клонах, оцененных как обладающие способностью связывать HMGB1 человека, изменяющейся в зависимости от pH на основе результатов ELISA фагов, анализировали в отношении их нуклеотидных последовательностей.
(26-4) Экспрессия и очистка антитела, связывающегося с HMGB1 человека
Гены трех антител, оцененных как обладающих способностью к pH-зависимому связыванию антигена в результате ELISA фагов, т.е. HM_3_2_R_017 (тяжелая цепь: SEQ ID NO: 131 и легкая цепь: SEQ ID NO: 132), HM_3_2_R_054 (тяжелая цепь: SEQ ID NO: 133 и легкая цепь: SEQ ID NO: 134) и HM_4_1_R_001 (тяжелая цепь: SEQ ID NO: 135 и легкая цепь: SEQ ID NO: 136), по отдельности встраивали в плазмиды для экспрессии в клетках животных. Экспрессию этих антител проводили следующим способом: линию FreeStyle 293-F, происходящую из почки эмбриона человека, (Invitrogen Corp.) суспендировали в среде для экспрессии FreeStyle 293 Expression Medium (Invitrogen Corp.). Суспензию, имеющую плотность клеток 1,33×106 клеток/мл, инокулировали в концентрации 3 мл/лунка в планшет с 6 ячейками. Полученные плазмиды переносили в клетки путем липофекции. Клетки культивировали в течение 4 суток в инкубаторе с CO2 (37°C, 8% CO2, 90 об./мин.). Антитела очищали из полученного культурального супернатанта способом, общеизвестным специалистам в данной области, с использованием rProtein A Sepharose(TM) Fast Flow (Amersham Biosciences, Inc.). Поглощение очищенного раствора антител измеряли при 280 нм с использованием спектрофотометра. Концентрацию антитела вычисляли из полученной величины измерения с использованием коэффициента экстинкции, вычисленного с помощью PACE (Protein Science (1995) 4, 2411-2423).
(26-5) Оценка полученного антитела в отношении его способности к pH-зависимому связыванию с HMGB1 человека
Для оценки зависимости от pH активности связывания hHMGB1 антител HM_3_2_R_017 (тяжелая цепь: SEQ ID NO: 131 и легкая цепь: SEQ ID NO: 132), HM_3_2_R_054 (тяжелая цепь: SEQ ID NO: 133 и легкая цепь: SEQ ID NO: 134) и HM_4_1_R_001 (тяжелая цепь: SEQ ID NO: 135 и легкая цепь: SEQ ID NO: 136), полученных на стадии (26-4), эти антитела анализировали в отношении их взаимодействия с hHMGB1 с использованием Biacore T100 (GE Healthcare Bio-Sciences Corp.). Взаимодействие в реакции антиген-антитело анализировали в растворах pH 7,4 и pH 5,8 в качестве условий нейтральных значений pH и кислых значений pH, соответственно. Приблизительно 200 RU каждого представляющего интерес антитела улавливали на сенсорном чипе CM4 (GE Healthcare Bio-Sciences Corp.) с белком A/G (Pierce Biotechnology Inc.), иммобилизованным на нем в подходящем количестве, способом присоединения аминов. В качестве подвижных буферов использовали два типа буферных растворов: 20 мМ ACES, 150 мМ NaCl, 0,05% (масс./об.) Tween 20 и 1,2 мМ CaCl2 (pH 7,4); и 20 мМ ACES, 150 мМ NaCl, 0,05% (масс./об.) Tween 20 и 1,2 мМ CaCl2 (pH 5,8). hHMGB1 также разбавляли каждым из этих буферов. Весь анализ проводили при 25°C.
В анализе взаимодействия в реакции антиген-антитело с использованием антитела HM_3_2_R_017, антитела HM_3_2_R_054 и антитела HM_4_1_R_001 разбавленный раствор hHMGB1 или пустой подвижный буфер инжектировали со скоростью потока 10 мкл/мин в течение 60 секунд для улавливания антигена на сенсорный чип. Антитело HM_3_2_R_017, антитело HM_3_2_R_054 и антитело HM_4_1_R_001 подвергали взаимодействию с hHMGB1. Затем инжектировали 10 мМ глицин-HCl (pH 1,5) со скоростью потока 30 мкл/мин в течение 30 секунд, чтобы регенерировать сенсорный чип.
На фиг. 15 представлены сенсограммы этих антител, проанализированных описанным выше способом при pH 7,4 и pH 5,8.
Из этих результатов, было выявлено, что способность антитела HM_3_2_R_017, антитела HM_3_2_R_054 и антитела HM_4_1_R_001 связывать hHMGB1 снижалась при изменении pH буфера от pH 7,4 до pH 5,8, что указывает на то, что антитела с pH-зависимым связыванием также можно получать против HMGB1 человека.
[Справочный пример 1] Оценка антитела с Ca-зависимым связыванием в отношении его влияния на время удержания в плазме антигена с использованием нормальной мыши
(1-1) Испытание in vivo с использованием нормальной мыши
hsIL-6R (растворимый рецептор IL-6 человека; полученный согласно справочному примеру 4), вводили отдельно или одновременно с каждым антителом против рецептора IL-6 человека каждой нормальной мыши (мышь C57BL/6J, Charles River Laboratories Japan, Inc.). Затем hsIL-6R и антитело против рецептора IL-6 человека оценивали в отношении их фармакокинетики in vivo. Раствор hsIL-6R (5 мкг/мл) или смешанный раствор hsIL-6R и антитело против рецептора IL-6 человека вводили в однократной дозе 10 мл/кг в хвостовую вену. Использованное антитело против рецептора IL-6 человека представляло собой H54/L28-IgG1, 6RL#9-IgG1 или FH4-IgG1, описанные выше.
Смешанный раствор имел фиксированную концентрацию hsIL-6R 5 мкг/мл, но имел концентрацию антитела против рецептора IL-6 человека, отличающуюся среди антител: 0,1 мг/мл для H54/L28-IgG1 и 10 мг/мл для 6RL#9-IgG1 и FH4-IgG1. В этом случае, в смешанном растворе присутствовало избыточное количество антитела против рецептора IL-6 человека, чтобы его было достаточно для связывания hsIL-6R. Таким образом, значительное большинство антигенов hsIL-6R, по-видимому, связывалось с антителами. Взятие крови проводили через 15 минут, 7 часов, 1 сутки, 2 суток, 4 суток, 7 суток, 14 суток, 21 суток и 28 суток после введения. Собранную кровь сразу центрифугировали при 12000 об./мин. при 4°C в течение 15 минут для получения плазмы. Отделенную плазму хранили в морозильной камере, установленной на -20°C или ниже, до применения в анализе.
(1-2) Измерение концентрации антитела против рецептора IL-6 человека в плазме нормальной мыши с помощью ELISA
Концентрацию антитела против рецептора IL-6 человека в плазме мыши определяли с помощью ELISA. Сначала F(ab')2-фрагмент антитела против IgG человека (специфичный к γ-цепи) (Sigma-Aldrich Corp.) распределяли в планшеты Nunc-Immuno Plate, MaxiSoup (Nalge nunc International) и позволяли им стоять в течение ночи при 4°C с получением планшетов с антителом против IgG человека в твердой фазе. Образцы для калибровочной кривой, имеющие концентрации в плазме 0,64, 0,32, 0,16, 0,08, 0,04, 0,02 или 0,01 мкг/мл, и образцы плазмы мыши для анализа, разбавленные в 100 раз или более, распределяли в планшет с антителом против IgG человека на твердой фазе, а затем проводили инкубацию при 25°C в течение 1 часа. Затем планшету позволяли реагировать с биотинилированным антителом против IL-6 R человека (R&D Systems, Inc.) при 25°C в течение 1 часа. Затем проводили реакцию со стрептавидин-PolyHRP80 (Stereospecific Detection Technologies GmbH) при 25°C в течение 0,5 часа. TMB One Component HRP Microwell Substrate (BioFX Laboratories Inc.) использовали в качестве субстрата в хромогенной реакции. Хромогенную реакцию останавливали добавлением 1н серной кислоты (Showa Chemical Industry Co., Ltd.). Затем измеряли поглощение цветного раствора при 450 нм с использованием устройства для считывания микропланшетов. Концентрации антител в плазме у мышей вычисляли из величин поглощения на калибровочной кривой с использованием аналитического программного обеспечения SOFTmax PRO (Molecular Devices, LLC). На фиг. 16 представлено изменение концентраций антител H54/L28-IgG1, 6RL#9-IgG1 и FH4-IgG1, измеренных этим способом, в плазме нормальных мышей после внутривенного введения.
(1-3) Измерение концентрации hsIL-6R в плазме способом электрохемилюминесценции
Концентрацию hsIL-6R в плазме мыши определяли способом электрохемилюминесценции. Образцы для калибровочной кривой hsIL-6R, приготовленные в концентрации 2000, 1000, 500, 250, 125, 62,5 или 31,25 пг/мл, и образец плазмы мыши для анализа, разбавленный в 50 раз или выше, подвергали реакции при 4°C в течение ночи со смешанным раствором моноклонального антитела против IL-6R человека (R&D Systems, Inc.), меченного рутением с помощью SULFO-TAG NHS Ester (Meso Scale Discovery), биотинилированного антитела против IL-6R человека (R&D Systems, Inc.) и раствором тоцилизумаба (тяжелая цепь SEQ ID NO: 24, легкая цепь SEQ ID NO: 25). Концентрация свободного Ca в образцах была снижена, чтобы позволить практически всем из антигенов hsIL-6R в образцах диссоциировать от 6RL#9-IgG1 или FH4-IgG1, а затем ассоциировать с добавленным тоцилизумабом. Для этой цели буфер для анализа содержал 10 мМ EDTA. Затем реакционный раствор распределяли в планшет MA400 PR Streptavidin Plate (Meso Scale Discovery). После последующей реакции при 25°C в течение 1 часа, каждую лунку планшета промывали, а затем в каждую лунку распределяли буфер для считывания T (×4) (Meso Scale Discovery). Сразу после этого реакционный раствор анализировали с использованием устройства для считывания SECTOR PR 400 (Meso Scale Discovery). Концентрацию hsIL-6R вычисляли из ответа калибровочной кривой с использованием программного обеспечения для анализа SOFTmax PRO (Molecular Devices, LLC). На фиг. 17 представлено изменение концентрации hsIL-6R, измеренной этим способом в плазме нормальных мышей после внутривенного введения.
В результате hsIL-6R отдельно выводилось из крови быстро, в то время как его одновременное введение с обычным антителом H54/L28-IgG1, не обладающим Ca-зависимым связыванием hsIL-6R, значительно продлевало выведение hsIL-6R. Напротив, его одновременное введение с антителом 6RL#9-IgG1 или FH4-IgG1, обладающим в 100 раз или более высоким зависимым от Ca связыванием hsIL-6R, значительно ускоряло выведение hsIL-6R. Антитела 6RL#9-IgG1 и FH4-IgG1, одновременно введенные с hsIL-6R, снижали концентрацию hsIL-6R в плазме через 1 сутки в 39 раз и 2 раза, соответственно, по сравнению с H54/L28-IgG1, одновременно введенным с ними. Это продемонстрировало, что антитело с кальций-зависимым связыванием может ускорять выведение антигенов из плазмы.
[Справочный пример 2] Исследование улучшения эффекта ускорения выведения антигена антитела с Ca-зависимым связыванием антигена (получение антитела)
(2-1) Связывание FcRn с IgG-антителом
IgG-антитело имеет более длительное время удержания в плазме в результате связывания FcRn. Связывание между IgG и FcRn наблюдают только в кислых условиях (pH 6,0), и практически не поддается выявлению в нейтральных условиях (pH 7,4). IgG-антитело захватывается в клетки неспецифическим образом, но рециклирует на клеточную поверхность путем связывания с эндосомальным FcRn в кислых условиях эндосом, и диссоциирует от FcRn в нейтральных условиях плазмы. IgG, который утратил связывание FcRn в кислых условиях в результате мутации в Fc-области, более не рециклирует в плазму из эндосомы, что приводит к значительному снижению времени удержания антитела в плазме.
Описанные ранее способы увеличения времени удержания в плазме IgG-антитела вовлекают повышение связывания FcRn в кислых условиях. Аминокислотную замену вносят в Fc-область IgG-антитела для увеличения его связывания с FcRn в кислых условиях, тем самым повышая эффективность рециклирования IgG-антитела в плазму из эндосомы. В результате время удержания IgG-антитела в плазме увеличивается. При внесении замены считается важным не увеличить связывание с FcRn в нейтральных условиях. Полагают, что время удержания в плазме такого IgG-антитела, связывающегося с FcRn в нейтральных условиях, скорее снижается, поскольку IgG-антитело может рециклировать на клеточную поверхность через связывание FcRn в кислых условиях в эндосоме, но оно не может ни диссоциировать от FcRn в нейтральных условиях в плазме, ни рециклировать в плазму.
Например, как описано в Dall' Acqua et al. (J. Immunol. (2002) 169 (9), 5171-5180), IgG1-антитело, которое стало способным связываться с FcRn мыши в нейтральных условиях (pH 7,4) вследствие внесения аминокислотной замены, согласно сообщениям, проявляет ухудшенное время удержания в плазме при введении мыши. Как описано Yeung et al. (J. Immunol. (2009) 182 (12), 7663-7671), Datta-Mannan et al. (J. Biol. Chem. (2007) 282 (3), 1709-1717), и Dall' Acqua et al. (J. Immunol. (2002) 169 (9), 5171-5180), было подтверждено, что сконструированное IgG1-антитело, обладающее улучшенной способностью связываться с FcRn человека в кислых условиях (pH 6,0) в результате внесения аминокислотной замены также связывается с FcRn человека в нейтральных условиях (pH 7,4). В соответствии с сообщениями, антитело, введенное яванскому макаку, не проявляло улучшения времени удержания в плазме или изменения времени удержания в плазме. Общепринятые способы инженерии антител для улучшения функций антител были сфокусированы на повышение времени удержания в плазме антител путем усиления связывания с FcRn человека в кислых условиях без усиления связывания с FcRn человека в нейтральных условиях (pH 7,4). В частности, ни в одном из предшествующих сообщений не упомянуто о преимуществах IgG1-антитела, обладающего усиленным связыванием с FcRn человека в нейтральных условиях (pH 7,4) вследствие внесения аминокислотной замены в Fc-область.
Антитела с Ca-зависимым связыванием антигена являются в высокой степени полезными, вследствие их эффектов ускорения выведения растворимых антигенов и связывания одной молекулы антитела с растворимыми антигенами многократно. Способ усиления связывания FcRn в нейтральных условиях (pH 7,4) исследовали для дальнейшего улучшения указанного эффекта ускорения выведения антигена.
(2-2) Получение антитела с Ca-зависимым связыванием рецептора IL-6 человека, обладающего активностью связывания FcRn в нейтральных условиях
Аминокислоты в Fc-областях FH4-IgG1 и 6RL#9-IgG1, обладающие способностью к кальций-зависимому связыванию антигена, и H54/L28-IgG1, использованное в качестве контроля, не обладающего способностью к кальций-зависимому связыванию антигену, подвергали мутации, получая модифицированные формы, обладающие связыванием FcRn в нейтральных условиях (pH 7,4). Мутацию аминокислот вносили способом ПЦР с использованием способа, общеизвестного специалистам в данной области. В частности, FH4-N434W (тяжелая цепь: SEQ ID NO: 94 и легкая цепь: SEQ ID NO: 81), 6RL#9-N434W (тяжелая цепь: SEQ ID NO: 95 и легкая цепь: SEQ ID NO: 79) и H54/L28-N434W (тяжелая цепь: SEQ ID NO: 96 и легкая цепь: SEQ ID NO: 83) получали путем замены Asn в аминокислоте 434, определяемой нумерацией EU, в константной области тяжелой цепи IgG1 на Trp. Экспрессирующие векторы для клеток животных, имеющие вставку полинуклеотида, кодирующего каждый из этих вариантов с заменой аминокислоты, получали с использованием набора для сайт-направленного мутагенеза QuikChange (Stratagene Corp.) в соответствии со способом, описанном в руководстве, прилагаемом к набору. Экспрессию и очистку антитела, и измерение концентрации проводили способом, описанным в примере 15.
[Справочный пример 3] Оценка антитела с Ca-зависимым связыванием в отношении его эффекта ускорения исчезновения с использованием нормальной мыши
(3-1) Испытание in vivo с использованием нормальной мыши
hsIL-6R (растворимый рецептор IL-6 человека; полученный согласно справочному примеру 4) вводили отдельно или одновременно с каждым антителом против рецептора IL-6 человека каждой нормальной мыши (мышь C57BL/6J, Charles River Laboratories Japan, Inc.). Затем hsIL-6R и антитело против рецептора IL-6 человека оценивали в отношении их кинетики in vivo. Раствор hsIL-6R (5 мкг/мл) или смешанный раствор hsIL-6R и антитела против рецептора IL-6 человека, вводили в однократной дозе 10 мл/кг в хвостовую вену. Использованное антитело против рецептора IL-6 человека представляло собой H54/L28-N434W, 6RL#9-N434W или FH4-N434W, описанные выше.
Смешанный раствор имел фиксированную концентрацию hsIL-6R 5 мкг/мл, но имел концентрацию антитела против рецептора IL-6 человека, отличающуюся среди типов антител: 0,042 мг/мл для H54/L28-N434W, 0,55 мг/мл для 6RL#9-N434W и 1 мг/мл для FH4-N434W. В этом случае, антитело против рецептора IL-6 человека присутствовало в избыточном количестве, достаточном для hsIL-6R. Таким образом, значительное большинство антигенов hsIL-6R, по-видимому, связывалось с антителами. Взятие крови проводили через 15 минут, 7 часов, 1 сутки, 2 суток, 4 суток, 7 суток, 14 суток, 21 суток и 28 суток после введения. Собранную кровь сразу центрифугировали при 12000 об./мин. при 4°C в течение 15 минут для получения плазмы. Отделенную плазму хранили в морозильной камере, установленной на -20°C или ниже, до применения в анализе.
(3-2) Измерение концентрации антитела против рецептора IL-6 человека в плазме нормальной мыши с помощью ELISA
Концентрацию антитела против рецептора IL-6 человека в плазме мыши измеряли с помощью ELISA аналогично тому, как в справочном примере 1. На фиг. 18 представлено изменение концентраций антител H54/L28-N434W, 6RL#9-N434W и FH4-N434W, измеренных этим способом, в плазме нормальных мышей после внутривенного введения.
(3-3) Измерение концентрации hsIL-6R в плазме способом электрохемилюминесценции
Концентрацию hsIL-6R в плазме мыши определяли способом электрохемилюминесценции. Образцы для калибровочной кривой hsIL-6R, приготовленные в концентрации 2000, 1000, 500, 250, 125, 62,5 или 31,25 пг/мл, и образцы плазмы мыши для анализа, разбавленные в 50 раз или выше, подвергали реакции при 4°C в течение ночи со смешанным раствором моноклонального антитела против IL-6R человека (R&D Systems, Inc.), меченного рутением с помощью SULFO-TAG NHS Ester (Meso Scale Discovery) и биотинилированного антитела против IL-6R человека (R&D Systems, Inc.). Концентрация свободного Ca в образцах была снижена, чтобы позволить практически всем из антигенов hsIL-6R в образцах диссоциировать от 6RL#9-N434W или FH4-N434W, чтобы они находились в свободной форме. Для этой цели буфер для анализа содержал 10 мМ EDTA. Затем реакционный раствор распределяли в планшет MA400 PR Streptavidin Plate (Meso Scale Discovery). После последующей реакции при 25°C в течение 1 часа, каждую лунку планшета промывали, а затем в каждую лунку распределяли буфер для считывания T (×4) (Meso Scale Discovery). Сразу после этого реакционный раствор анализировали с использованием устройства для считывания SECTOR PR 400 (Meso Scale Discovery). Концентрацию hsIL-6R вычисляли из ответа калибровочной кривой с использованием программного обеспечения для анализа SOFTmax PRO (Molecular Devices, LLC). На фиг. 19 представлено изменение концентрации hsIL-6R, измеренной этим способом в плазме нормальных мышей после внутривенного введения.
В результате одновременное введение hsIL-6R с антителом H54/L28-N434W, обладающим активностью связывания FcRn при pH 7,4, но не активностью Ca-зависимого связывания с hsIL-6R, значительно замедляло исчезновение hsIL-6R по сравнению с введением hsIL-6R отдельно. Напротив, одновременное введение его с антителом 6RL#9-N434W или антителом FH4-N434W, обладающим в 100 раз или более Ca-зависимым связыванием hsIL-6R, а также связыванием FcRn при pH 7,4, ускоряло исчезновение hsIL-6R, по сравнению с введением hsIL-6R отдельно. Антитело 6RL#9-N434W и антитело FH4-N434W, введенные одновременно с hsIL-6R, снижали концентрацию hsIL-6R в плазме в 3 раза и 8 раз в течение одних суток после введения, соответственно, по сравнению с hsIL-6R, введенным отдельно. Эти результаты продемонстрировали, что антитело с кальций-зависимым связыванием антигеном, обладающее активностью связывания FcRn при pH 7,4, может дополнительно ускорить исчезновение антигенов из плазмы.
Было подтверждено, что антитело 6RL#9-IgG1 или антитело FH4-IgG1, обладающие в 100-раз или более Ca-зависимой активностью связывания hsIL-6R, обладают эффектом увеличения исчезновения hsIL-6R, по сравнению с антителом H54/L28-IgG1, не обладающим Ca-зависимым связыванием hsIL-6R. Было подтверждено, что антитело 6RL#9-N434W или антитело FH4-N434W, обладающие в 100-раз или более Ca-зависимой активностью связывания hsIL-6R и также связыванием FcRn при pH 7,4 ускоряет исчезновение hsIL-6R, по сравнению с hsIL-6R, введенным отдельно. Эти данные указывают на то, что, как и в случае антитела с pH-зависимым связыванием антигена, антитело с Ca-зависимым связыванием антитела диссоциирует от антигена в эндосоме.
[Справочный пример 4] Получение растворимого рецептора IL-6 человека (hsIL-6R)
Рекомбинантный антиген рецептора IL-6 человека получали следующим образом: клеточную линию CHO, стабильно экспрессирующую растворимый рецептор IL-6 человека (далее обозначаемый как hsIL-6R), состоящий из N-концевой аминокислотной последовательности в положениях от 1 до 357, как описано Mullberg et al. (J. Immunol. (1994) 152, 4958-4968), конструировали способом, общеизвестным специалистам в данной области. Экспрессирующую линию культивировали для экспрессии hsIL-6R. hsIL-6R очищали из полученного культурального супернатанта колоночной хроматографией Blue Sepharose 6 FF и гель-фильтрационной колоночной хроматографией. Фракцию, элюированную в качестве основного пика на конечной стадии, использовали в качестве конечного очищенного продукта.
[Справочный пример 5] ЯМР-анализ антитела, содержащего последовательность hVk1 человека, обладающую мотивом связывания ионов кальция, в отношении его активности связывания ионов кальция
(5-1) Экспрессия и очистка антитела
Антитело, содержащее LfVk1_Ca, и антитело, содержащее LfVk1, экспрессировали для анализа с помощью ЯМР и очищали. В частности, клетки животных временно трансфицировали плазмидами для экспрессии в клетках животных, полученными так, чтобы они обеспечивали экспрессию тяжелой цепи (SEQ ID NO: 24) и легкой цепи (SEQ ID NO: 43) антитела, содержащего LfVk1_Ca (также обозначаемого как антитело LfVk1_Ca). Также, клетки животных временно трансфицировали плазмидами для экспрессии в клетках животных, полученными так, чтобы они обеспечивали соответствующую экспрессию тяжелой цепи (SEQ ID NO: 24) и легкой цепи (SEQ ID NO: 44) антитела, содержащего LfVk1 (также обозначаемого как антитело LfVk1). Аминокислоты для мечения добавляли к 100 мл суспензии клеток линии клеток, происходящей из почки эмбриона человека, FreeStyle 293-F (Invitrogen Corp.), суспендированных при конечной плотности клеток 1×106 клеток/мл в среде для экспрессии FreeStyle 293 Expression Medium (Invitrogen Corp.). В частности, для метки Asp/Glu/Gln/Asn, L-аспарагиновую кислоту-13C4,15N (10 мг), L-глутаминовую кислоту-13C5,15N (2,5 мг), L-глутамин-13C5,15N2 (60 мг), L-аспарагин-13C4,15N2⋅H2O (2,5 мг) и β-хлор-L-аланин (6 мг) суспендировали в 10 мл воды, и полученный раствор фильтровали через 0,22-мкм фильтр, а затем добавляли к суспензии клеток. В случае метки Leu, L-лейцин-15N (30 мг) и β-хлор-L-аланин (6 мг) суспендировали в 10 мл воды, и полученный раствор фильтровали через 0,22-мкм фильтр, а затем добавляли к суспензии клеток. Полученными плазмидами трансфицировали клетки способом липофекции. Клетки, трансфицированные плазмидами, культивировали в течение 5 суток в инкубаторе с CO2 (37°C, 8% CO2, 90 об./мин.). Антитела очищали из полученного культурального супернатанта способом, общеизвестным специалистам в данной области, с использованием rProtein A Sepharose(TM) Fast Flow (Amersham Biosciences, Inc.). Поглощение очищенного раствора антител измеряли при 280 нм с использованием спектрофотометра. Концентрацию антитела вычисляли из полученной величины измерения с использованием коэффициента экстинкции, вычисленного с помощью PACE (Protein Science (1995) 4, 2411-2423).
(5-2) Получение Fab-фрагмента
Каждое антитело концентрировали до 8,2-11,8 мг/мл с использованием ультрафильтрационной мембраны, обладающей пределом молекулярной массы 30000 MWCO. Антитело разбавляли до 8 мг/мл смесью 1 мМ L-цистеина, 2 мМ EDTA и 50 мМ уксусной кислоты/125 мМ tris буферный раствор (pH 6,8), получая образец антитела. После добавления папаина (Roche Applied Science) в 1/240 количества каждого антитела, образец перемешивали, а затем оставляли стоять при 37°C в течение 1 часа. Образец, оставленный таким образом, добавляли в конъюгированную с пептидом Gly-Gly-Tyr-Arg (Sigma-Aldrich Corp.) 1-мл HiTrap NHS-activated HP (GE Healthcare Bio-Sciences Corp.) (уравновешенную смесью 50 мМ уксусная кислота/125 мМ tris буферный раствор (pH 6,8)), последовательно подсоединенную к нижеследующей 1 мл-колонке с белком A-носителем HiTrap MabSelect Sure (GE Healthcare Bio-Sciences Corp.). Активированный папаин удалялся с помощью вышерасположенного пептида Gly-Gly-Tyr-Arg, в то время как Fc-фрагменты и нерасщепленные антитела удалялись в нижерасположенной колонке с белком A-носителем, получая очищенную фракцию Fab-фрагмента. К фракции Fab добавляли 10 мкМ ингибитор цистеиновых протеаз E64 (Sigma-Aldrich Corp.), чтобы предотвратить активацию неактивного папаина, содержащегося во фракции Fab. Все действия на колонке проводили при комнатной температуре от 20 до 25°C.
(5-3) Получение образцов для ЯМР Fab-фрагментов антител LfVk1_Ca и LfVk1
Каждый раствор антитела концентрировали до 0,5 мл центрифугированием с использованием ультрафильтра MWCO 5000 Vivaspin (Sartorius). Далее в ультрафильтр помещали чашу для диафильтрации, и буферный раствор заменяли буферным раствором для ЯМР: 5 мМ d-BisTris, 20 мМ NaCl, 0,001% (масс./об.) NaN3, и 5% (об./об.)2H2O (pH 7,0) (с доведенным pH с использованием NaOH или HCl) (5 мл буферного раствора добавляли в чашу для диафильтрации, содержимое которой концентрировали до 0,5 мл центрифугированием; это действие повторяли три раза). В итоге полученный раствор концентрировали до 0,25 мл. Наконец, ультрафильтр тщательно промывали буферным раствором для ЯМР. Промывочные жидкости объединяли с концентратом, получая 420 мкл раствора антитела LfVk1_Ca и 270 мкл раствора антитела LfVk1. На этой стадии pH каждого раствор вновь подтверждали и корректировали, если необходимо, до pH 7,0 с помощью NaOH или HCl. Поглощение измеряли при 280 нм с использованием устройства для измерения в УФ-области Nanodrop (Thermo Fisher Scientific K.K.). Каждый Fab-фрагмент количественно определяли с использованием коэффициента молярной экстинкции при 280 нм, установленного как 70000 M-1⋅см-1, и, следовательно, было определено, что для меченного Leu антитела LfVk1_Ca и меченного Leu антитела LfVk1 количество составляет 0,12 мМ и для меченного Asp/Glu/Asn/Gln антитела LfVk1_Ca и меченного Asp/Glu/Asn/Gln антитела LfVk1 количество составляет 0,24 мМ. Из этих образцов, каждое антитело LfVk1_Ca помещали в пробирку для ЯМР-образца (Shigemi Co., Ltd.) диаметром 5 мм, в то время как каждое антитело LfVk1 помещали в симметричную пробирку для водных растворов микрообразцов (Shigemi Co., Ltd.) диаметром 5 мм с использованием пастеровской пипетки. В эксперименте по титрованию с Ca2+ антитела LfVk1_Ca, растворы CaCl2 последовательно добавляли к раствору антитела в количестве 1, 2, 5, 10 и 20 молярных эквивалентов Ca2+ относительно антитела. Растворы CaCl2, использованные для добавления, получали в качестве 10, 20, 50 и 100 мМ растворов CaCl2, растворенных в буфере для ЯМР. Необходимые количества растворов CaCl2 прямо добавляли в объемах в диапазоне от 3 до 10 мкл к растворам антител, помещенным в пробирки для ЯМР-образца с использованием изготовленного на заказ микрошприца (Ito Corp.), где шприцевая часть выступала из готовой части. Пробирки для образцов перемешивали с использованием вихревого смесителя, а затем центрифугировали в ручной центрифуге (Shimadzu Corp.).
(5-3) Анализ ЯМР для выявления сигналов амидных групп в Fab-фрагментах антител LfVk1_Ca и LfVk1_Ca
Анализ ЯМР проводили с использованием ЯМР-спектроскопа DRX750 (Bruker Biospin K.K.), оборудованного TCI CryoProbe. Температура была установлена на 307 K (34°C) (поток газа: 535 л/ч). Для выявления сигналов амидных групп в анализе ЯМР использовали1H-15N HSQC. В способе анализа использовали1H-15N FHSQC, вовлекающий одновременное13C-отщепление α-углерода и углерода карбонила в периоде эволюции15N, и группу импульсов 3-9-19 для погашения сигналов водного растворителя. Для их контроля использовали импульсную программу, включенную в качестве стандарта изготовителем (Bruker Biospin K.K.). Условия анализа ЯМР были следующими: ширина спектра: 12019 Гц (f2) и 1976 Гц (f1), и количество точек данных: 2048 (f2) и 128 (f1). Для обработки данных использовали Topspin 3.0 (Bruker Biospin K.K.). Условия обработки данных были следующими: как для f2, так и для f1, данные перемножали на основе функции окна shifted sine (QSINE)-bell и заполняли нулями для удвоения количества точек данных, с последующим преобразованием Фурье. Химические сдвиги сигналов вычисляли с использованием программного обеспечения для анализа ЯМР Sparky (UCSF).
(5-4) Распределение сигнала ЯМР амидных групп основной цепи
80% сигналов ЯМР амидных групп основной цепи в Fab-фрагменте тоцилизумаба (тяжелая цепь: SEQ ID NO: 24 и легкая цепь: SEQ ID NO: 25) уже были распределены (данные не опубликованы). Аминокислотная последовательность Fab-фрагмента антитела LfVk1_Ca, является такой же, как и аминокислотная последовательность Fab-фрагмента тоцилизумаба, за исключением части CDR1, CDR2 и CDR3 легкой цепи и аминокислотных остатков 73 и 83 легкой цепи. Поскольку сигналы ЯМР одинаковых частей в аминокислотных последовательностей этих антител, обладают идентичными или сходными химическими сдвигами, информацию о распределении в тоцилизумабе можно было применить к антителу LfVk1_Ca. Распределение остатков 11, (33), (46), (47), (54), (78), 125, 135, 136, 154, 175, 179, 181 и 201 легкой цепи и остатков 18, 46, 64, 71, 81, 83, 114, 144, 147, 165, 176, 181, 184 и 195 тяжелой цепи можно было применить к меченному Leu образцу. Числа без скобок соответствуют номерам остатков, для которых можно было применить распределение, поскольку их химические сдвиги идентичны химическим сдвигам тоцилизумаба. Числа в скобках соответствуют номерам остатков, для которых можно было применить распределение, поскольку их химические сдвиги были сходны с химическими сдвигами тоцилизумаба и отсутствовали другие сигналы, имеющие сходные химические сдвиги. Для образца, меченного Asp/Glu/Asn/Gln, было вновь выявлено четыре сигнала в LfVk1_Ca посредством спектрального сравнения между антителом LfVk1_Ca и антителом LfVk1. Эти сигналы были успешно классифицированы как сигналы, исходящие от любых 4 из 5 остатков, внесенных в качестве Ca2+-связывающих мотивов, т.е. Asp30, Asp31, Asp32, Asp92 и Glu50 в легкой цепи, последовательности которых отличаются между антителами, среди остатков Asp, Glu, Asn и Gln.
(5-5) Идентификация Ca2+-связывающего участка на антителе LfVk1_Ca
Сигналы с измененным химическим сдвигом извлекали путем сравнения спектров1H-15N HSQC между Fab-фрагментом антитела LfVk1_Ca, без добавления Ca2+, и Fab-фрагмента, дополненного 20 молярными эквивалентами Ca2+. Результаты для меченных Leu образцов продемонстрировали, что Leu33 легкой цепи вовлечен в связывание, в то время как другие остатки Leu не вовлечены в связывание. Результаты для меченных Asp/Glu/Asn/Gln образцов продемонстрировали, что любые 4 из 5 остатков (Asp30, Asp31, Asp32, Asp92 и Glu50 легкой цепи) вовлечены в связывание, в то время как другие остатки Asp, Glu, Asn и Gln, за исключением 1 остатка, не вовлечены в связывание. Исходя из этих результатов, было идентифицировано, что аминокислоты по меньшей мере в CDR1 легкой цепи в аминокислотной последовательности, встроенной в качестве Ca2+-связывающих мотивов, а также в одной или обеих из CDR2 и CDR3 легкой цепи, участвуют в связывании Ca2+. Это согласовывалось с результатами, подтвержденными в примере 15, указывающими на то, что для связывания ионов кальция важно то, чтобы 4 из остатков 30, 31, 32, 50 и 92 (определяемых посредством нумерации по Кабату) представляли собой аминокислоты последовательности hVk5-2.
(5-6) Вычисление константы диссоциации Ca2+в эксперименте с титрованием
Использовали спектры1H-15N HSQC, которые получали, когда концентрация Ca2+ составляла 0, 1, 2, 5, 10 или 20 молярных эквивалентов относительно Fab-фрагмента антитела LfVk1_Ca. Химический сдвиг1H или15N в сигнале Leu33 легкой цепи, идентифицированном как участок связывания, наносили на график в качестве ординаты, в то время как указанные выше молярные эквиваленты Ca2+ наносили на график в качестве абсциссы. Данные аппроксимировали к функции, соответствующей следующему выражению 2 с использованием программного обеспечения для построения графиков Gnuplot:
[Выражение 2]
f(x)=s×[1-0,5/a×{(a×x+a+Kd)-((a×x+a+Kd)2-4×x×a2)0,5}+t×[0,5/a×{(a×x+a+Kd)-((a×x+a+Kd)2-4×x×a2)0,5}
В функции, соответствующей выражению 2, s и t соответствуют химическому сдвигу [м.д.] в отсутствие связанного Ca2+ и предполагаемому химическому сдвигу [м.д.] в присутствии связанного при насыщении Ca2+, соответственно; a соответствует концентрации [M] Fab-фрагмента антитела; Kd соответствует константе диссоциации; и x соответствует молярному эквиваленту Ca2+, добавленного к Fab-фрагменту антитела. Для аппроксимации, в качестве параметров аппроксимации использовали s, t и Kd. В результате из химического сдвига1H была получена оценка Kd=7,1×10-5 [M], и из химического сдвига15N была получена оценка Kd=5,9×10-5 [M].
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Chugai Seiyaku Kabushiki Kaisha
<120> Библиотека зависимых от концентрации ионов связывающих молекул
<130> PCG-9036WO
<150> JP 2011-218006
<151> 2011-09-30
<150> JP 2012-123479
<151> 2012-05-30
<160> 136
<170> PatentIn version 3.1
<210> 1
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 1
Glu Thr Thr Leu Thr Gln Ser Pro Ala Phe Met Ser Ala Thr Pro Gly
1 5 10 15
Asp Lys Val Asn Ile Ser Cys Lys Ala Ser Gln Asp Ile Asp Asp Asp
20 25 30
Met Asn Trp Tyr Gln Gln Lys Pro Gly Glu Ala Ala Ile Phe Ile Ile
35 40 45
Gln Glu Ala Thr Thr Leu Val Pro Gly Ile Ser Pro Arg Phe Ser Gly
50 55 60
Ser Gly Tyr Gly Thr Asp Phe Thr Leu Thr Ile Asn Asn Ile Glu Ser
65 70 75 80
Glu Asp Ala Ala Tyr Tyr Phe Cys Leu Gln His Asp Asn Phe Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 2
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 2
Glu Thr Thr Leu Thr Gln Ser Pro Ala Phe Met Ser Ala Thr Pro Gly
1 5 10 15
Asp Lys Val Asn Ile Ser Cys Lys Ala Ser Gln Asp Ile Asp Asp Asp
20 25 30
Met Asn Trp Tyr Gln Gln Lys Pro Gly Glu Ala Ala Ile Phe Ile Ile
35 40 45
Gln Glu Ala Thr Thr Leu Val Pro Gly Ile Pro Pro Arg Phe Ser Gly
50 55 60
Ser Gly Tyr Gly Thr Asp Phe Thr Leu Thr Ile Asn Asn Ile Glu Ser
65 70 75 80
Glu Asp Ala Ala Tyr Tyr Phe Cys Leu Gln His Asp Asn Phe Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 3
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 3
Glu Thr Thr Leu Thr Gln Ser Pro Ala Phe Met Ser Ala Thr Pro Gly
1 5 10 15
Asp Lys Val Asn Ile Ser Cys Lys Ala Ser Gln Asp Ile Glu Asp Asp
20 25 30
Met Asn Trp Tyr Gln Gln Lys Pro Gly Glu Ala Ala Ile Phe Ile Ile
35 40 45
Gln Glu Ala Thr Thr Leu Val Pro Gly Ile Ser Pro Arg Phe Ser Gly
50 55 60
Ser Gly Tyr Gly Thr Asp Phe Thr Leu Thr Ile Asn Asn Ile Glu Ser
65 70 75 80
Glu Asp Ala Ala Tyr Tyr Phe Cys Leu Gln His Asp Asn Phe Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 4
<211> 445
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 4
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Ile Met Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Leu Ile Asn Pro Tyr Asn Gly Gly Thr Asp Tyr Asn Pro Gln Phe
50 55 60
Gln Asp Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gly Tyr Asp Asp Gly Pro Tyr Thr Leu Glu Thr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Asn Phe Gly Thr Gln Thr Tyr Thr Cys Asn Val Asp His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Thr Val Glu Arg Lys Ser Cys
210 215 220
Val Glu Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu
260 265 270
Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Phe Arg Val Val Ser
290 295 300
Val Leu Thr Val Val His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gly Leu Pro Ala Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Thr Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Met Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
<210> 5
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 5
Glu Thr Thr Leu Thr Gln Ser Pro Ala Phe Met Ser Ala Thr Pro Gly
1 5 10 15
Asp Lys Val Thr Ile Ser Cys Lys Ala Ser Gln Asp Ile Asp Asp Asp
20 25 30
Met Asn Trp Tyr Gln Gln Lys Pro Gly Glu Ala Ala Ile Phe Ile Ile
35 40 45
Gln Glu Ala Thr Thr Leu Val Pro Gly Ile Ser Pro Arg Phe Ser Gly
50 55 60
Ser Gly Tyr Gly Thr Asp Phe Thr Leu Thr Ile Asn Asn Ile Glu Ser
65 70 75 80
Glu Asp Ala Ala Tyr Tyr Phe Cys Leu Gln His Asp Asn Phe Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 6
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 6
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Phe
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 7
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 7
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asn Gly Asp Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Val
85 90 95
Leu Arg Asn Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Gln
100 105 110
<210> 8
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 8
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Asn Trp Pro Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 9
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 9
Asp Ile Val Met Thr Gln Ser Pro Glu Ser Leu Val Leu Ser Leu Gly
1 5 10 15
Gly Thr Ala Thr Ile Asn Cys Arg Ser Ser Gln Ser Val Leu Tyr Ser
20 25 30
Ser Asn Asn Lys Asn Tyr Leu Thr Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Thr Leu Leu Phe Ser Trp Ala Ser Ile Arg Asp Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Ala Ser Gly Ser Gly Thr Glu Phe Thr Leu Thr
65 70 75 80
Ile Ser Asp Leu Gln Ala Glu Asp Ala Ala Val Tyr Tyr Cys Gln Gln
85 90 95
Tyr Tyr Arg Ala Pro Ser Phe Gly Gln Gly Thr Lys Leu Gln Ile Lys
100 105 110
<210> 10
<211> 121
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 10
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Gly Gly Ser Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Asp Pro Gly Gly Gly Glu Tyr Tyr Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 11
<211> 126
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 11
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Glu Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Tyr Ile Ser Ser Ser Gly Ser Thr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Pro Tyr Tyr Tyr Asp Ser Ser Gly Tyr Thr Asp Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 12
<211> 35
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 12
Gly Arg Met Lys Gln Leu Glu Asp Lys Val Glu Glu Leu Leu Ser Lys
1 5 10 15
Asn Tyr His Leu Glu Asn Glu Val Ala Arg Leu Lys Lys Leu Val Gly
20 25 30
Glu Arg Gly
35
<210> 13
<211> 19
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 13
Met Gly Trp Ser Cys Ile Ile Leu Phe Leu Val Ala Thr Ala Thr Gly
1 5 10 15
Val His Ser
<210> 14
<211> 330
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 14
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
100 105 110
Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
115 120 125
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
130 135 140
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
145 150 155 160
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
165 170 175
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
180 185 190
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
195 200 205
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
210 215 220
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu
225 230 235 240
Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
245 250 255
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
260 265 270
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
275 280 285
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
290 295 300
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
305 310 315 320
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
325 330
<210> 15
<211> 326
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 15
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Asn Phe Gly Thr Gln Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Thr Val Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys Pro Ala Pro
100 105 110
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
115 120 125
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
130 135 140
Val Ser His Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly
145 150 155 160
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn
165 170 175
Ser Thr Phe Arg Val Val Ser Val Leu Thr Val Val His Gln Asp Trp
180 185 190
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro
195 200 205
Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Gln Pro Arg Glu
210 215 220
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn
225 230 235 240
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
245 250 255
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
260 265 270
Thr Pro Pro Met Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
275 280 285
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
290 295 300
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
305 310 315 320
Ser Leu Ser Pro Gly Lys
325
<210> 16
<211> 377
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 16
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Thr Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Arg Val Glu Leu Lys Thr Pro Leu Gly Asp Thr Thr His Thr Cys Pro
100 105 110
Arg Cys Pro Glu Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg
115 120 125
Cys Pro Glu Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys
130 135 140
Pro Glu Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys Pro
145 150 155 160
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
165 170 175
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
180 185 190
Val Val Asp Val Ser His Glu Asp Pro Glu Val Gln Phe Lys Trp Tyr
195 200 205
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
210 215 220
Gln Tyr Asn Ser Thr Phe Arg Val Val Ser Val Leu Thr Val Leu His
225 230 235 240
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
245 250 255
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Gln
260 265 270
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met
275 280 285
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
290 295 300
Ser Asp Ile Ala Val Glu Trp Glu Ser Ser Gly Gln Pro Glu Asn Asn
305 310 315 320
Tyr Asn Thr Thr Pro Pro Met Leu Asp Ser Asp Gly Ser Phe Phe Leu
325 330 335
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Ile
340 345 350
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn Arg Phe Thr Gln
355 360 365
Lys Ser Leu Ser Leu Ser Pro Gly Lys
370 375
<210> 17
<211> 327
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 17
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Ser Cys Pro Ala Pro
100 105 110
Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
115 120 125
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
130 135 140
Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp
145 150 155 160
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe
165 170 175
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
180 185 190
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu
195 200 205
Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
210 215 220
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys
225 230 235 240
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
245 250 255
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
260 265 270
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
275 280 285
Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser
290 295 300
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
305 310 315 320
Leu Ser Leu Ser Leu Gly Lys
325
<210> 18
<211> 458
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 18
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ser Ile Tyr Cys Ser Ser Thr Ser Cys Tyr Glu Pro Pro
100 105 110
Tyr Tyr Tyr Tyr Met Asp Val Trp Gly Lys Gly Thr Met Val Thr Val
115 120 125
Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser
130 135 140
Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys
145 150 155 160
Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu
165 170 175
Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu
180 185 190
Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr
195 200 205
Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val
210 215 220
Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro
225 230 235 240
Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe
245 250 255
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
260 265 270
Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe
275 280 285
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
290 295 300
Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr
305 310 315 320
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
325 330 335
Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala
340 345 350
Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg
355 360 365
Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly
370 375 380
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
385 390 395 400
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
405 410 415
Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln
420 425 430
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
435 440 445
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
450 455
<210> 19
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 19
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser His
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser His Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser His Asn Tyr Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 20
<211> 447
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 20
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Met Ile Asn Gly Val Trp Glu Gly Gly Met Asp Val Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
<210> 21
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 21
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile His Ser His
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr His Ala Ser Lys Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Gly Asn Ser Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 22
<211> 451
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 22
Glu Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met Ile Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Lys Ser Lys Val Asp Gly Gly Thr Thr Asp Tyr Ala Ala
50 55 60
Pro Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asp Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Ala Asp Val Pro Ala Ser Asn Pro Tyr Gly Phe Asp Tyr
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly
115 120 125
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
130 135 140
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
145 150 155 160
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
165 170 175
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
180 185 190
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
195 200 205
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys
210 215 220
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu
225 230 235 240
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
245 250 255
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
260 265 270
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
275 280 285
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser
290 295 300
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
305 310 315 320
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
325 330 335
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
340 345 350
Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln
355 360 365
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
370 375 380
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
385 390 395 400
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu
405 410 415
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
420 425 430
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
435 440 445
Leu Ser Pro
450
<210> 23
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 23
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Asn Ser His
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Asp Ala Ser His Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Asn Asn Tyr Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 24
<211> 449
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 24
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Arg Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Tyr Ser Ile Thr Ser Asp
20 25 30
His Ala Trp Ser Trp Val Arg Gln Pro Pro Gly Arg Gly Leu Glu Trp
35 40 45
Ile Gly Tyr Ile Ser Tyr Ser Gly Ile Thr Thr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Met Leu Arg Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Arg Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Leu Ala Arg Thr Thr Ala Met Asp Tyr Trp Gly Gln Gly
100 105 110
Ser Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys
<210> 25
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 25
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Thr Ser Arg Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 26
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 26
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
1 5 10 15
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
20 25 30
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
35 40 45
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
65 70 75 80
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
85 90 95
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
100 105
<210> 27
<211> 128
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 27
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Gly Gly Ser Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gly Thr Leu Tyr Asp Phe Trp Ser Gly Tyr Tyr Ser Tyr
100 105 110
Asp Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 28
<211> 122
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 28
Gln Met Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Leu Asp Thr Gly Pro Tyr Tyr Tyr Gly Met Asp Val Trp
100 105 110
Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 29
<211> 124
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 29
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ser Pro Val Pro Gly Val Tyr Tyr Tyr Tyr Gly Met Asp
100 105 110
Val Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120
<210> 30
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 30
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Lys Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Ser Tyr
20 25 30
Trp Ile Gly Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Tyr Pro Gly Asp Ser Asp Thr Arg Tyr Ser Pro Ser Phe
50 55 60
Gln Gly Gln Val Thr Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu Gln Trp Ser Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg His Arg Ala Gly Asp Leu Gly Gly Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 31
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 31
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Ile Asp Asp Asp
20 25 30
Met Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Glu Ala Thr Thr Leu Val Pro Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln His Asp Asn Phe Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 32
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 32
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Lys Ala Ser Gln Asp Ile Asp Asp Asp
20 25 30
Met Asn Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro Gln Leu Leu Ile
35 40 45
Tyr Glu Ala Thr Thr Leu Val Pro Gly Val Pro Asp Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala
65 70 75 80
Glu Asp Val Gly Val Tyr Tyr Cys Leu Gln His Asp Asn Phe Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 33
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 33
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Lys Ala Ser Gln Asp Ile Asp Asp Asp
20 25 30
Met Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Glu Ala Thr Thr Leu Val Pro Gly Ile Pro Asp Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Leu Gln His Asp Asn Phe Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 34
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 34
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ala Ser Gln Asp Ile Asp Asp Asp
20 25 30
Met Asn Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu Leu Ile
35 40 45
Tyr Glu Ala Thr Thr Leu Val Pro Gly Val Pro Asp Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Ala
65 70 75 80
Glu Asp Val Ala Val Tyr Tyr Cys Leu Gln His Asp Asn Phe Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 35
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 35
Glu Thr Thr Leu Thr Gln Ser Pro Ala Phe Met Ser Ala Thr Pro Gly
1 5 10 15
Asp Lys Val Thr Ile Ser Cys Lys Ala Ser Gln Asp Ile Ala Asp Asp
20 25 30
Met Asn Trp Tyr Gln Gln Lys Pro Gly Glu Ala Ala Ile Phe Ile Ile
35 40 45
Gln Glu Ala Thr Thr Leu Val Pro Gly Ile Ser Pro Arg Phe Ser Gly
50 55 60
Ser Gly Tyr Gly Thr Asp Phe Thr Leu Thr Ile Asn Asn Ile Glu Ser
65 70 75 80
Glu Asp Ala Ala Tyr Tyr Phe Cys Leu Gln His Asp Asn Phe Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 36
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 36
Glu Thr Thr Leu Thr Gln Ser Pro Ala Phe Met Ser Ala Thr Pro Gly
1 5 10 15
Asp Lys Val Thr Ile Ser Cys Lys Ala Ser Gln Asp Ile Asp Ala Asp
20 25 30
Met Asn Trp Tyr Gln Gln Lys Pro Gly Glu Ala Ala Ile Phe Ile Ile
35 40 45
Gln Glu Ala Thr Thr Leu Val Pro Gly Ile Ser Pro Arg Phe Ser Gly
50 55 60
Ser Gly Tyr Gly Thr Asp Phe Thr Leu Thr Ile Asn Asn Ile Glu Ser
65 70 75 80
Glu Asp Ala Ala Tyr Tyr Phe Cys Leu Gln His Asp Asn Phe Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 37
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 37
Glu Thr Thr Leu Thr Gln Ser Pro Ala Phe Met Ser Ala Thr Pro Gly
1 5 10 15
Asp Lys Val Thr Ile Ser Cys Lys Ala Ser Gln Asp Ile Asp Asp Ala
20 25 30
Met Asn Trp Tyr Gln Gln Lys Pro Gly Glu Ala Ala Ile Phe Ile Ile
35 40 45
Gln Glu Ala Thr Thr Leu Val Pro Gly Ile Ser Pro Arg Phe Ser Gly
50 55 60
Ser Gly Tyr Gly Thr Asp Phe Thr Leu Thr Ile Asn Asn Ile Glu Ser
65 70 75 80
Glu Asp Ala Ala Tyr Tyr Phe Cys Leu Gln His Asp Asn Phe Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 38
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 38
Glu Thr Thr Leu Thr Gln Ser Pro Ala Phe Met Ser Ala Thr Pro Gly
1 5 10 15
Asp Lys Val Thr Ile Ser Cys Lys Ala Ser Gln Asp Ile Asp Asp Asp
20 25 30
Met Asn Trp Tyr Gln Gln Lys Pro Gly Glu Ala Ala Ile Phe Ile Ile
35 40 45
Gln Ala Ala Thr Thr Leu Val Pro Gly Ile Ser Pro Arg Phe Ser Gly
50 55 60
Ser Gly Tyr Gly Thr Asp Phe Thr Leu Thr Ile Asn Asn Ile Glu Ser
65 70 75 80
Glu Asp Ala Ala Tyr Tyr Phe Cys Leu Gln His Asp Asn Phe Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 39
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 39
Glu Thr Thr Leu Thr Gln Ser Pro Ala Phe Met Ser Ala Thr Pro Gly
1 5 10 15
Asp Lys Val Thr Ile Ser Cys Lys Ala Ser Gln Asp Ile Ala Asp Ala
20 25 30
Met Asn Trp Tyr Gln Gln Lys Pro Gly Glu Ala Ala Ile Phe Ile Ile
35 40 45
Gln Glu Ala Thr Thr Leu Val Pro Gly Ile Ser Pro Arg Phe Ser Gly
50 55 60
Ser Gly Tyr Gly Thr Asp Phe Thr Leu Thr Ile Asn Asn Ile Glu Ser
65 70 75 80
Glu Asp Ala Ala Tyr Tyr Phe Cys Leu Gln His Asp Asn Phe Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 40
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 40
Glu Thr Thr Leu Thr Gln Ser Pro Ala Phe Met Ser Ala Thr Pro Gly
1 5 10 15
Asp Lys Val Thr Ile Ser Cys Lys Ala Ser Gln Asp Ile Ala Asp Asp
20 25 30
Met Asn Trp Tyr Gln Gln Lys Pro Gly Glu Ala Ala Ile Phe Ile Ile
35 40 45
Gln Ala Ala Thr Thr Leu Val Pro Gly Ile Ser Pro Arg Phe Ser Gly
50 55 60
Ser Gly Tyr Gly Thr Asp Phe Thr Leu Thr Ile Asn Asn Ile Glu Ser
65 70 75 80
Glu Asp Ala Ala Tyr Tyr Phe Cys Leu Gln His Asp Asn Phe Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 41
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 41
Glu Thr Thr Leu Thr Gln Ser Pro Ala Phe Met Ser Ala Thr Pro Gly
1 5 10 15
Asp Lys Val Thr Ile Ser Cys Lys Ala Ser Gln Asp Ile Ala Asp Ala
20 25 30
Met Asn Trp Tyr Gln Gln Lys Pro Gly Glu Ala Ala Ile Phe Ile Ile
35 40 45
Gln Ala Ala Thr Thr Leu Val Pro Gly Ile Ser Pro Arg Phe Ser Gly
50 55 60
Ser Gly Tyr Gly Thr Asp Phe Thr Leu Thr Ile Asn Asn Ile Glu Ser
65 70 75 80
Glu Asp Ala Ala Tyr Tyr Phe Cys Leu Gln His Asp Asn Phe Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 42
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 42
Glu Thr Thr Leu Thr Gln Ser Pro Ala Phe Met Ser Ala Thr Pro Gly
1 5 10 15
Asp Lys Val Thr Ile Ser Cys Lys Ala Ser Gln Asp Ile Asp Asp Asp
20 25 30
Met Asn Trp Tyr Gln Gln Lys Pro Gly Glu Ala Ala Ile Phe Ile Ile
35 40 45
Gln Glu Ala Thr Thr Leu Val Pro Gly Ile Ser Pro Arg Phe Ser Gly
50 55 60
Ser Gly Tyr Gly Thr Asp Phe Thr Leu Thr Ile Asn Asn Ile Glu Ser
65 70 75 80
Glu Asp Ala Ala Tyr Tyr Phe Cys Leu Gln His Ala Asn Phe Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 43
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 43
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Asp Asp Asp
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Glu Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Asp Ser Thr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 44
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 44
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 45
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 45
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ala Asp Asp
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Glu Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Asp Ser Thr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 46
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 46
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Asp Ala Asp
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Glu Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Asp Ser Thr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 47
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 47
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Asp Asp Ala
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Glu Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Asp Ser Thr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 48
<211> 443
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 48
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ala Leu Asp Pro Lys Thr Gly Asp Thr Ala Tyr Ser Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro
115 120 125
Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val
130 135 140
Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala
145 150 155 160
Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly
165 170 175
Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly
180 185 190
Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys
195 200 205
Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys
210 215 220
Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu
225 230 235 240
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
245 250 255
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
260 265 270
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
275 280 285
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
290 295 300
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
305 310 315 320
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
325 330 335
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
340 345 350
Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
355 360 365
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
370 375 380
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
385 390 395 400
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
405 410 415
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
420 425 430
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440
<210> 49
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 49
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Asp Asp
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Glu Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Asp Ser Thr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 50
<211> 456
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 50
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Ser
20 25 30
Ser Tyr Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Ser Ile Tyr Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg Val Pro Pro Tyr Ser Ser Ser Ser Tyr Tyr Tyr Tyr Tyr
100 105 110
Tyr Tyr Met Asp Val Trp Gly Lys Gly Thr Thr Val Thr Val Ser Ser
115 120 125
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
130 135 140
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
145 150 155 160
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
165 170 175
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
180 185 190
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
195 200 205
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
210 215 220
Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
225 230 235 240
Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
245 250 255
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
260 265 270
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
275 280 285
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
290 295 300
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
305 310 315 320
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
325 330 335
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
340 345 350
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu
355 360 365
Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
370 375 380
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
385 390 395 400
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
405 410 415
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
420 425 430
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
435 440 445
Gln Lys Ser Leu Ser Leu Ser Pro
450 455
<210> 51
<211> 452
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 51
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Ala Pro Gly Ile Gln Leu Trp Leu Arg Pro Ser Tyr Phe Asp
100 105 110
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys
115 120 125
Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly
130 135 140
Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
145 150 155 160
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
165 170 175
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
180 185 190
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn
195 200 205
Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro
210 215 220
Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
225 230 235 240
Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
245 250 255
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
260 265 270
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
275 280 285
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
290 295 300
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
305 310 315 320
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
325 330 335
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
340 345 350
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro
450
<210> 52
<211> 447
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 52
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Trp Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ala Gly Asp Ser Ile Lys Tyr Ser
20 25 30
Ser Asp Tyr Trp Gly Trp Val Arg Gln Ser Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Ser Ser Tyr Leu Ser Gly Thr Thr Gln Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Met Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Arg Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg His Arg Gly Pro Thr Gly Val Asp Gln Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
<210> 53
<211> 449
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 53
Glu Val Gln Leu Val Gln Ser Gly Gly Gly Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Thr Leu Ser Cys Val Gly Tyr Gly Phe Thr Phe His Glu Asn
20 25 30
Asp Met His Trp Leu Arg Gln Pro Leu Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser His Ile Gly Trp Asn Asn Asn Arg Val Ala Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Ala Val Ser Arg Asp Asn Ala Lys Asn Ser Leu Phe
65 70 75 80
Leu His Met Asn Ser Leu Arg Pro Asp Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Asp Leu Gly Asn Pro Ile Tyr Asp Val Phe Asp Val Trp Gly
100 105 110
Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro
<210> 54
<211> 452
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 54
Gln Pro Ala Leu Ala Gln Met Gln Leu Val Glu Ser Gly Gly Gly Leu
1 5 10 15
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
20 25 30
Thr Phe Asp Asp Tyr Ala Met His Trp Val Arg Gln Ala Pro Gly Lys
35 40 45
Gly Leu Glu Trp Val Ser Gly Ile Ser Trp Asn Ser Gly Ser Ile Gly
50 55 60
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
65 70 75 80
Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
85 90 95
Ala Leu Tyr Tyr Cys Ala Arg Glu Gly Val Leu Gly Asp Ala Phe Asp
100 105 110
Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys
115 120 125
Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly
130 135 140
Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
145 150 155 160
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
165 170 175
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
180 185 190
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn
195 200 205
Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro
210 215 220
Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
225 230 235 240
Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
245 250 255
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
260 265 270
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
275 280 285
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
290 295 300
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
305 310 315 320
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
325 330 335
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
340 345 350
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro
450
<210> 55
<211> 454
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 55
Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp Ser Val Ser Ser Asn
20 25 30
Ser Ala Ala Trp Asn Trp Ile Arg Gln Ser Pro Ser Arg Gly Leu Glu
35 40 45
Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Lys Trp Tyr Asn Asp Tyr Ala
50 55 60
Val Ser Val Lys Ser Arg Ile Thr Ile Asn Pro Asp Thr Ser Lys Asn
65 70 75 80
Gln Phe Ser Leu Gln Leu Asn Ser Val Thr Pro Glu Asp Thr Ala Val
85 90 95
Tyr Tyr Cys Ala Arg Arg Val Arg Ser Gly Ser Tyr Tyr Tyr Tyr Gly
100 105 110
Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val
210 215 220
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
225 230 235 240
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
245 250 255
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
260 265 270
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
275 280 285
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
290 295 300
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
305 310 315 320
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
325 330 335
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
340 345 350
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr
355 360 365
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
370 375 380
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
385 390 395 400
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
405 410 415
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
420 425 430
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
435 440 445
Ser Leu Ser Leu Ser Pro
450
<210> 56
<211> 450
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 56
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Ile Ser Gly Asp Ser Val Ser Ser Asn
20 25 30
Ser Ala Ala Trp Asn Trp Ile Arg Gln Ser Pro Ser Arg Gly Leu Glu
35 40 45
Trp Leu Gly Arg Thr Tyr Tyr Arg Ser Lys Trp Tyr Asn Asp Tyr Ala
50 55 60
Val Ser Val Lys Ser Arg Ile Thr Ile Ile Pro Asp Thr Ser Lys Asn
65 70 75 80
Gln Phe Ser Leu Gln Leu Asn Ser Val Thr Pro Glu Asp Thr Ala Val
85 90 95
Tyr Tyr Cys Ala Arg Lys Asp Pro Arg Val Trp Ala Phe Asp Ile Trp
100 105 110
Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser
210 215 220
Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu
225 230 235 240
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
245 250 255
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
260 265 270
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
275 280 285
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr
290 295 300
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
305 310 315 320
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
325 330 335
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
340 345 350
Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val
355 360 365
Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
370 375 380
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
385 390 395 400
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr
405 410 415
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
420 425 430
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
435 440 445
Ser Pro
450
<210> 57
<211> 449
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 57
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile Ile Pro Val Leu Ala Ile Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr His Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Gly Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ser Gly Tyr Ser Ala Gly Tyr Gly Gly Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro
<210> 58
<211> 447
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 58
Glu Val Gln Leu Val Glu Ser Gly Gly Asp Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Lys Thr Tyr
20 25 30
Trp Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Asn Ile Arg Ala Asp Gly Gly Gln Met Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asp Ser Leu Tyr
65 70 75 80
Leu Gln Met Ile Ser Leu Arg Pro Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Arg Asp Pro Phe Ala Ser Gly Gly Leu Asp Gln Trp Gly Gln Gly
100 105 110
Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
<210> 59
<211> 450
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 59
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met Glu Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Leu Ile Ser His Asp Gly Asn Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Glu Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Asp Arg Val Arg Tyr Phe Asp Ser Tyr Gly Met Asp Val Trp
100 105 110
Gly His Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser
210 215 220
Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu
225 230 235 240
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
245 250 255
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
260 265 270
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
275 280 285
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr
290 295 300
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
305 310 315 320
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
325 330 335
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
340 345 350
Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val
355 360 365
Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
370 375 380
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
385 390 395 400
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr
405 410 415
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
420 425 430
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
435 440 445
Ser Pro
450
<210> 60
<211> 449
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 60
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Glu
1 5 10 15
Ser Leu Arg Ile Ser Cys Lys Gly Ser Gly Tyr Ser Phe Thr Ser Phe
20 25 30
Trp Ile Asn Trp Val Arg Gln Met Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Asn Ile Asp Pro Ser Asp Ser Tyr Thr Asn Tyr Ser Pro Ser Phe
50 55 60
Gln Gly His Val Ala Ile Ser Ala Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Leu His Trp Asn Ser Leu Lys Ala Ser Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg His Arg Tyr Leu Gly Gln Leu Ala Pro Phe Asp Pro Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro
<210> 61
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 61
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Glu Asp Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Glu Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Arg Asp Asn Tyr Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 62
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 62
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Glu Asp Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr His Ala Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Asp Ser Ser Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 63
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 63
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Glu Asp Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Glu Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Ser Asn Tyr Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 64
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 64
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Glu Asp Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Glu Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Asp Gly Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 65
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 65
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Glu Asp Asp
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Glu Ala Ser Asn Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Ser Ser Ser Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 66
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 66
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Glu Asp Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Glu Ala Ser Asn Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asp Ser Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 67
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 67
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Asp Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr His Ala Ser His Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asp Asn Ser Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 68
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 68
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Asp Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr His Ala Ser Asn Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asp Asn Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 69
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 69
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Glu Asp Asp
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Glu Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Arg Asp Ser Ser Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 70
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 70
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Glu Asp Asp
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Glu Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Asn Asp Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 71
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 71
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Glu Asp Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Glu Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Asp Asn Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 72
<211> 453
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 72
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ala Phe Leu Glu Trp Pro Ile Trp Gly Ser Glu Tyr Phe
100 105 110
Gln His Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr
115 120 125
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
130 135 140
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
145 150 155 160
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
165 170 175
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
180 185 190
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
195 200 205
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu
210 215 220
Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
225 230 235 240
Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
245 250 255
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
260 265 270
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
275 280 285
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
290 295 300
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
305 310 315 320
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
325 330 335
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
340 345 350
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys
355 360 365
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
370 375 380
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
385 390 395 400
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
405 410 415
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
420 425 430
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
435 440 445
Leu Ser Leu Ser Pro
450
<210> 73
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 73
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Glu Asp Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr His Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Arg Asp Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 74
<211> 451
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 74
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Gly Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Ser Ala Tyr Asn Gly Asn Thr Asn Tyr Ala Gln Lys Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Thr Tyr Tyr Tyr Asp Ser Ser Ala Pro Ala Phe Asp Ile
100 105 110
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly
115 120 125
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
130 135 140
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
145 150 155 160
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
165 170 175
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
180 185 190
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
195 200 205
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys
210 215 220
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu
225 230 235 240
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
245 250 255
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
260 265 270
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
275 280 285
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser
290 295 300
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
305 310 315 320
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
325 330 335
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
340 345 350
Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln
355 360 365
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
370 375 380
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
385 390 395 400
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu
405 410 415
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
420 425 430
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
435 440 445
Leu Ser Pro
450
<210> 75
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 75
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Glu Asp Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Glu Ala Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Asp Asp Ser Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 76
<211> 452
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 76
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Arg Gly Ser Gly Phe Asn Trp Gly Asn Tyr Ala Phe Asp
100 105 110
Ile Trp Gly Gln Gly Phe Ser Val Thr Val Ser Ser Ala Ser Thr Lys
115 120 125
Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly
130 135 140
Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
145 150 155 160
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
165 170 175
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
180 185 190
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn
195 200 205
Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro
210 215 220
Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
225 230 235 240
Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
245 250 255
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
260 265 270
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
275 280 285
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
290 295 300
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
305 310 315 320
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
325 330 335
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
340 345 350
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro
450
<210> 77
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 77
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Glu Asp Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Glu Ala Ser Asn Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asp Arg Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 78
<211> 449
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 78
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Gly Gly Ser Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Asp Pro Gly Gly Gly Glu Tyr Tyr Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro
<210> 79
<211> 217
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 79
Gln Ser Val Leu Thr Gln Pro Pro Ser Val Ser Gly Ala Pro Gly Gln
1 5 10 15
Arg Val Thr Ile Ser Cys Thr Gly Ser Arg Ser Asn Met Gly Ala Gly
20 25 30
Tyr Asp Val His Trp Tyr Gln Leu Leu Pro Gly Ala Ala Pro Lys Leu
35 40 45
Leu Ile Ser His Asn Thr His Arg Pro Ser Gly Val Pro Asp Arg Phe
50 55 60
Ser Gly Ser Lys Ser Gly Ala Ser Ala Ser Leu Ala Ile Thr Gly Leu
65 70 75 80
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Gln Ser His Asp Ser Ser
85 90 95
Leu Ser Ala Val Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Ser
100 105 110
Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser Glu
115 120 125
Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp Phe
130 135 140
Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro Val
145 150 155 160
Lys Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn Lys
165 170 175
Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys Ser
180 185 190
His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val Glu
195 200 205
Lys Thr Val Ala Pro Thr Glu Cys Ser
210 215
<210> 80
<211> 453
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 80
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Arg Asp Tyr Tyr Asp Ser Ser Gly Tyr Tyr Asp Ala Phe
100 105 110
Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr
115 120 125
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
130 135 140
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
145 150 155 160
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
165 170 175
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
180 185 190
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
195 200 205
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu
210 215 220
Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
225 230 235 240
Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
245 250 255
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
260 265 270
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
275 280 285
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
290 295 300
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
305 310 315 320
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
325 330 335
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
340 345 350
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys
355 360 365
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
370 375 380
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
385 390 395 400
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
405 410 415
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
420 425 430
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
435 440 445
Leu Ser Leu Ser Pro
450
<210> 81
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 81
Glu Thr Thr Val Thr Gln Ser Pro Ser Phe Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Ile Thr Thr Thr Asp Ile Asp Asp Asp
20 25 30
Met Asn Trp Phe Gln Gln Glu Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Ser Glu Gly Asn Ile Leu Arg Pro Gly Val Pro Ser Arg Phe Ser Ser
50 55 60
Ser Gly Tyr Gly Thr Asp Phe Thr Leu Thr Ile Ser Lys Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Ser Asp Asn Leu Pro Phe
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 82
<211> 447
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 82
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Asp Asp
20 25 30
Gln Ala Trp Ser Trp Val Arg Gln Pro Pro Gly Glu Gly Leu Glu Trp
35 40 45
Ile Gly Tyr Ile Ser Tyr Ser Gly Ile Thr Asn Tyr Asn Pro Ser Leu
50 55 60
Lys Gly Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Ala Tyr Tyr Cys
85 90 95
Ala Arg Ser Leu Ala Arg Thr Thr Ala Met Asp Tyr Trp Gly Glu Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
<210> 83
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 83
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Ser Val Thr Ile Thr Cys Gln Ala Ser Gln Asp Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Glu Leu Leu Ile
35 40 45
Tyr Tyr Gly Ser Glu Leu His Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Glu Ala
65 70 75 80
Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Gly Asn Ser Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Glu Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 84
<211> 106
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 84
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Phe Asp Ala Ser Asn Arg Ala Ala Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Asp Lys Trp Val Thr
85 90 95
Phe Gly Gly Gly Thr Thr Val Glu Ile Arg
100 105
<210> 85
<211> 454
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 85
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Glu Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Tyr Ile Ser Ser Ser Gly Ser Thr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Pro Tyr Tyr Tyr Asp Ser Ser Gly Tyr Thr Asp Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val
210 215 220
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
225 230 235 240
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
245 250 255
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
260 265 270
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
275 280 285
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
290 295 300
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
305 310 315 320
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
325 330 335
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
340 345 350
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr
355 360 365
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
370 375 380
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
385 390 395 400
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
405 410 415
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
420 425 430
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
435 440 445
Ser Leu Ser Leu Ser Pro
450
<210> 86
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 86
Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Asn
85 90 95
Thr His Val Pro Pro Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 87
<211> 454
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 87
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Glu Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Tyr Ile Ser Ser Ser Gly Ser Thr Ile Tyr Tyr Ala Ala Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Pro Tyr Tyr Tyr Asp Ser Ser Gly Tyr Thr Asp Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val
210 215 220
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
225 230 235 240
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
245 250 255
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
260 265 270
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
275 280 285
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
290 295 300
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
305 310 315 320
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
325 330 335
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
340 345 350
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr
355 360 365
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
370 375 380
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
385 390 395 400
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
405 410 415
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
420 425 430
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
435 440 445
Ser Leu Ser Leu Ser Pro
450
<210> 88
<211> 454
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 88
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Glu Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Tyr Ile Ser Ser Ser Gly Ser Thr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Ala Pro Tyr Tyr Tyr Asp Ser Ser Gly Tyr Thr Asp Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val
210 215 220
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
225 230 235 240
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
245 250 255
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
260 265 270
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
275 280 285
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
290 295 300
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
305 310 315 320
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
325 330 335
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
340 345 350
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr
355 360 365
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
370 375 380
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
385 390 395 400
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
405 410 415
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
420 425 430
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
435 440 445
Ser Leu Ser Leu Ser Pro
450
<210> 89
<211> 454
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 89
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Glu Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Tyr Ile Ser Ser Ser Gly Ser Thr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Pro Tyr Tyr Tyr Ala Ser Ser Gly Tyr Thr Asp Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val
210 215 220
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
225 230 235 240
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
245 250 255
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
260 265 270
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
275 280 285
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
290 295 300
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
305 310 315 320
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
325 330 335
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
340 345 350
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr
355 360 365
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
370 375 380
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
385 390 395 400
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
405 410 415
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
420 425 430
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
435 440 445
Ser Leu Ser Leu Ser Pro
450
<210> 90
<211> 454
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 90
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Glu Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Tyr Ile Ser Ser Ser Gly Ser Thr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Pro Tyr Tyr Tyr Asp Ser Ser Gly Tyr Thr Ala Ala
100 105 110
Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val
210 215 220
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
225 230 235 240
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
245 250 255
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
260 265 270
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
275 280 285
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
290 295 300
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
305 310 315 320
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
325 330 335
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
340 345 350
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr
355 360 365
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
370 375 380
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
385 390 395 400
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
405 410 415
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
420 425 430
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
435 440 445
Ser Leu Ser Leu Ser Pro
450
<210> 91
<211> 454
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 91
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Glu Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Tyr Ile Ser Ser Ser Gly Ser Thr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Pro Tyr Tyr Tyr Asp Ser Ser Gly Tyr Thr Asp Ala
100 105 110
Phe Ala Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser
115 120 125
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr
130 135 140
Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
145 150 155 160
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
165 170 175
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
180 185 190
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile
195 200 205
Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val
210 215 220
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
225 230 235 240
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
245 250 255
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
260 265 270
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
275 280 285
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
290 295 300
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
305 310 315 320
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
325 330 335
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
340 345 350
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr
355 360 365
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
370 375 380
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
385 390 395 400
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
405 410 415
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
420 425 430
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
435 440 445
Ser Leu Ser Leu Ser Pro
450
<210> 92
<211> 213
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 92
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Phe Ala Ala Ser Asn Arg Ala Ala Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Asp Lys Trp Val Thr
85 90 95
Phe Gly Gly Gly Thr Thr Val Glu Ile Arg Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys
210
<210> 93
<211> 213
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 93
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Phe Asp Ala Ser Asn Arg Ala Ala Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Phe Ala Lys Trp Val Thr
85 90 95
Phe Gly Gly Gly Thr Thr Val Glu Ile Arg Arg Thr Val Ala Ala Pro
100 105 110
Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly Thr
115 120 125
Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala Lys
130 135 140
Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln Glu
145 150 155 160
Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser Ser
165 170 175
Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr Ala
180 185 190
Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser Phe
195 200 205
Asn Arg Gly Glu Cys
210
<210> 94
<211> 453
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 94
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Arg Asp Tyr Tyr Asp Ser Ser Gly Tyr Tyr Asp Ala Phe
100 105 110
Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr
115 120 125
Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser
130 135 140
Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu
145 150 155 160
Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His
165 170 175
Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser
180 185 190
Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys
195 200 205
Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu
210 215 220
Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
225 230 235 240
Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
245 250 255
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
260 265 270
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
275 280 285
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
290 295 300
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
305 310 315 320
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
325 330 335
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
340 345 350
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys
355 360 365
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
370 375 380
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
385 390 395 400
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
405 410 415
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
420 425 430
Cys Ser Val Met His Glu Ala Leu His Trp His Tyr Thr Gln Lys Ser
435 440 445
Leu Ser Leu Ser Pro
450
<210> 95
<211> 449
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 95
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ile Ile Asn Pro Ser Gly Gly Ser Thr Ser Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Asp Pro Gly Gly Gly Glu Tyr Tyr Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Trp His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro
<210> 96
<211> 447
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 96
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Asp Asp
20 25 30
Gln Ala Trp Ser Trp Val Arg Gln Pro Pro Gly Glu Gly Leu Glu Trp
35 40 45
Ile Gly Tyr Ile Ser Tyr Ser Gly Ile Thr Asn Tyr Asn Pro Ser Leu
50 55 60
Lys Gly Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Ala Tyr Tyr Cys
85 90 95
Ala Arg Ser Leu Ala Arg Thr Thr Ala Met Asp Tyr Trp Gly Glu Gly
100 105 110
Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Trp His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
<210> 97
<211> 464
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 97
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Arg Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Tyr Ser Ile Thr Ser Asp
20 25 30
His Ala Trp Ser Trp Val Arg Gln Pro Pro Gly Arg Gly Leu Glu Trp
35 40 45
Ile Gly Tyr Ile Ser Tyr Ser Gly Ile Thr Thr Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Met Leu Arg Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Arg Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Leu Ala Arg Thr Thr Ala Met Asp Tyr Trp Gly Gln Gly
100 105 110
Ser Leu Val Thr Val Ser Ser Ala Ser Pro Thr Ser Pro Lys Val Phe
115 120 125
Pro Leu Ser Leu Cys Ser Thr Gln Pro Asp Gly Asn Val Val Ile Ala
130 135 140
Cys Leu Val Gln Gly Phe Phe Pro Gln Glu Pro Leu Ser Val Thr Trp
145 150 155 160
Ser Glu Ser Gly Gln Gly Val Thr Ala Arg Asn Phe Pro Pro Ser Gln
165 170 175
Asp Ala Ser Gly Asp Leu Tyr Thr Thr Ser Ser Gln Leu Thr Leu Pro
180 185 190
Ala Thr Gln Cys Leu Ala Gly Lys Ser Val Thr Cys His Val Lys His
195 200 205
Tyr Thr Asn Pro Ser Gln Asp Val Thr Val Pro Cys Pro Val Pro Ser
210 215 220
Thr Pro Pro Thr Pro Ser Pro Ser Thr Pro Pro Thr Pro Ser Pro Ser
225 230 235 240
Cys Cys His Pro Arg Leu Ser Leu His Arg Pro Ala Leu Glu Asp Leu
245 250 255
Leu Leu Gly Ser Glu Ala Asn Leu Thr Cys Thr Leu Thr Gly Leu Arg
260 265 270
Asp Ala Ser Gly Val Thr Phe Thr Trp Thr Pro Ser Ser Gly Lys Ser
275 280 285
Ala Val Gln Gly Pro Pro Glu Arg Asp Leu Cys Gly Cys Tyr Ser Val
290 295 300
Ser Ser Val Leu Pro Gly Cys Ala Glu Pro Trp Asn His Gly Lys Thr
305 310 315 320
Phe Thr Cys Thr Ala Ala Tyr Pro Glu Ser Lys Thr Pro Leu Thr Ala
325 330 335
Thr Leu Ser Lys Ser Gly Asn Thr Phe Arg Pro Glu Val His Leu Leu
340 345 350
Pro Pro Pro Ser Glu Glu Leu Ala Leu Asn Glu Leu Val Thr Leu Thr
355 360 365
Cys Leu Ala Arg Gly Phe Ser Pro Lys Asp Val Leu Val Arg Trp Leu
370 375 380
Gln Gly Ser Gln Glu Leu Pro Arg Glu Lys Tyr Leu Thr Trp Ala Ser
385 390 395 400
Arg Gln Glu Pro Ser Gln Gly Thr Thr Thr Phe Ala Val Thr Ser Ile
405 410 415
Leu Arg Val Ala Ala Glu Asp Trp Lys Lys Gly Asp Thr Phe Ser Cys
420 425 430
Met Val Gly His Glu Ala Leu Pro Leu Ala Phe Thr Gln Lys Thr Ile
435 440 445
Asp Arg Leu Ala Gly Lys Glu Gln Lys Leu Ile Ser Glu Glu Asp Leu
450 455 460
<210> 98
<211> 458
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 98
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Pro Lys Thr Gly Asp Thr Ala Tyr Ser Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser Ala Ser Pro Thr Ser Pro Lys Val Phe Pro Leu Ser Leu
115 120 125
Cys Ser Thr Gln Pro Asp Gly Asn Val Val Ile Ala Cys Leu Val Gln
130 135 140
Gly Phe Phe Pro Gln Glu Pro Leu Ser Val Thr Trp Ser Glu Ser Gly
145 150 155 160
Gln Gly Val Thr Ala Arg Asn Phe Pro Pro Ser Gln Asp Ala Ser Gly
165 170 175
Asp Leu Tyr Thr Thr Ser Ser Gln Leu Thr Leu Pro Ala Thr Gln Cys
180 185 190
Leu Ala Gly Lys Ser Val Thr Cys His Val Lys His Tyr Thr Asn Pro
195 200 205
Ser Gln Asp Val Thr Val Pro Cys Pro Val Pro Ser Thr Pro Pro Thr
210 215 220
Pro Ser Pro Ser Thr Pro Pro Thr Pro Ser Pro Ser Cys Cys His Pro
225 230 235 240
Arg Leu Ser Leu His Arg Pro Ala Leu Glu Asp Leu Leu Leu Gly Ser
245 250 255
Glu Ala Asn Leu Thr Cys Thr Leu Thr Gly Leu Arg Asp Ala Ser Gly
260 265 270
Val Thr Phe Thr Trp Thr Pro Ser Ser Gly Lys Ser Ala Val Gln Gly
275 280 285
Pro Pro Glu Arg Asp Leu Cys Gly Cys Tyr Ser Val Ser Ser Val Leu
290 295 300
Pro Gly Cys Ala Glu Pro Trp Asn His Gly Lys Thr Phe Thr Cys Thr
305 310 315 320
Ala Ala Tyr Pro Glu Ser Lys Thr Pro Leu Thr Ala Thr Leu Ser Lys
325 330 335
Ser Gly Asn Thr Phe Arg Pro Glu Val His Leu Leu Pro Pro Pro Ser
340 345 350
Glu Glu Leu Ala Leu Asn Glu Leu Val Thr Leu Thr Cys Leu Ala Arg
355 360 365
Gly Phe Ser Pro Lys Asp Val Leu Val Arg Trp Leu Gln Gly Ser Gln
370 375 380
Glu Leu Pro Arg Glu Lys Tyr Leu Thr Trp Ala Ser Arg Gln Glu Pro
385 390 395 400
Ser Gln Gly Thr Thr Thr Phe Ala Val Thr Ser Ile Leu Arg Val Ala
405 410 415
Ala Glu Asp Trp Lys Lys Gly Asp Thr Phe Ser Cys Met Val Gly His
420 425 430
Glu Ala Leu Pro Leu Ala Phe Thr Gln Lys Thr Ile Asp Arg Leu Ala
435 440 445
Gly Lys Asp Tyr Lys Asp Asp Asp Asp Lys
450 455
<210> 99
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 99
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Asn
85 90 95
Thr His Val Pro Pro Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 100
<211> 233
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 100
Cys His Pro Arg Leu Ser Leu His Arg Pro Ala Leu Glu Asp Leu Leu
1 5 10 15
Leu Gly Ser Glu Ala Asn Leu Thr Cys Thr Leu Thr Gly Leu Arg Asp
20 25 30
Ala Ser Gly Val Thr Phe Thr Trp Thr Pro Ser Ser Gly Lys Ser Ala
35 40 45
Val Gln Gly Pro Pro Glu Arg Asp Leu Cys Gly Cys Tyr Ser Val Ser
50 55 60
Ser Val Leu Pro Gly Cys Ala Glu Pro Trp Asn His Gly Lys Thr Phe
65 70 75 80
Thr Cys Thr Ala Ala Tyr Pro Glu Ser Lys Thr Pro Leu Thr Ala Thr
85 90 95
Leu Ser Lys Ser Gly Asn Thr Phe Arg Pro Glu Val His Leu Leu Pro
100 105 110
Pro Pro Ser Glu Glu Leu Ala Leu Asn Glu Leu Val Thr Leu Thr Cys
115 120 125
Leu Ala Arg Gly Phe Ser Pro Lys Asp Val Leu Val Arg Trp Leu Gln
130 135 140
Gly Ser Gln Glu Leu Pro Arg Glu Lys Tyr Leu Thr Trp Ala Ser Arg
145 150 155 160
Gln Glu Pro Ser Gln Gly Thr Thr Thr Phe Ala Val Thr Ser Ile Leu
165 170 175
Arg Val Ala Ala Glu Asp Trp Lys Lys Gly Asp Thr Phe Ser Cys Met
180 185 190
Val Gly His Glu Ala Leu Pro Leu Ala Phe Thr Gln Lys Thr Ile Asp
195 200 205
Arg Leu Ala Gly Lys Gly Gly Gly Gly Ser Gly Leu Asn Asp Ile Phe
210 215 220
Glu Ala Gln Lys Ile Glu Trp His Glu
225 230
<210> 101
<211> 450
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 101
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Val Ala Pro Gly Asn Trp Gly Ser Pro Tyr Phe Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser
210 215 220
Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu
225 230 235 240
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
245 250 255
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
260 265 270
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
275 280 285
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr
290 295 300
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
305 310 315 320
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
325 330 335
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
340 345 350
Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val
355 360 365
Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
370 375 380
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
385 390 395 400
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr
405 410 415
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
420 425 430
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
435 440 445
Ser Pro
450
<210> 102
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 102
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Glu Asp Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Glu Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Arg Asp Ser Ser Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 103
<211> 451
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 103
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Pro Arg Trp Glu Thr Ala Ile Ser Ser Asp Ala Phe Asp Ile
100 105 110
Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly
115 120 125
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
130 135 140
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
145 150 155 160
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
165 170 175
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
180 185 190
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
195 200 205
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys
210 215 220
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu
225 230 235 240
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
245 250 255
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
260 265 270
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
275 280 285
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser
290 295 300
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
305 310 315 320
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
325 330 335
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
340 345 350
Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln
355 360 365
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
370 375 380
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
385 390 395 400
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu
405 410 415
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
420 425 430
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
435 440 445
Leu Ser Pro
450
<210> 104
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 104
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Asp Asp
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Glu Ala Ser Asn Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Ser Ser Ser Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 105
<211> 448
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 105
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asn Gly Asp Tyr Leu Glu Tyr Phe Gln His Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
<210> 106
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 106
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Asp Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Glu Ala Ser Asn Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Arg Asp Ser Ser Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 107
<211> 452
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 107
Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Ile Leu Gly Gly Ser Ile Ser Gly His
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Thr Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asp Tyr Ser Gly Ser Thr His Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Met Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Met Tyr Tyr Cys Ala
85 90 95
Arg Asp Asn Trp Asp Phe Gly Ser Gly Ser Tyr Tyr Asn Trp Phe Asp
100 105 110
Pro Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys
115 120 125
Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly
130 135 140
Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
145 150 155 160
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
165 170 175
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
180 185 190
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn
195 200 205
Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro
210 215 220
Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
225 230 235 240
Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
245 250 255
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
260 265 270
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
275 280 285
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
290 295 300
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
305 310 315 320
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
325 330 335
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
340 345 350
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro
450
<210> 108
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 108
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Glu Asp Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr His Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Asp Asn Ser Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 109
<211> 545
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 109
Gln Pro Pro Pro Pro Pro Pro Asp Ala Thr Cys His Gln Val Arg Ser
1 5 10 15
Phe Phe Gln Arg Leu Gln Pro Gly Leu Lys Trp Val Pro Glu Thr Pro
20 25 30
Val Pro Gly Ser Asp Leu Gln Val Cys Leu Pro Lys Gly Pro Thr Cys
35 40 45
Cys Ser Arg Lys Met Glu Glu Lys Tyr Gln Leu Thr Ala Arg Leu Asn
50 55 60
Met Glu Gln Leu Leu Gln Ser Ala Ser Met Glu Leu Lys Phe Leu Ile
65 70 75 80
Ile Gln Asn Ala Ala Val Phe Gln Glu Ala Phe Glu Ile Val Val Arg
85 90 95
His Ala Lys Asn Tyr Thr Asn Ala Met Phe Lys Asn Asn Tyr Pro Ser
100 105 110
Leu Thr Pro Gln Ala Phe Glu Phe Val Gly Glu Phe Phe Thr Asp Val
115 120 125
Ser Leu Tyr Ile Leu Gly Ser Asp Ile Asn Val Asp Asp Met Val Asn
130 135 140
Glu Leu Phe Asp Ser Leu Phe Pro Val Ile Tyr Thr Gln Leu Met Asn
145 150 155 160
Pro Gly Leu Pro Asp Ser Ala Leu Asp Ile Asn Glu Cys Leu Arg Gly
165 170 175
Ala Arg Arg Asp Leu Lys Val Phe Gly Asn Phe Pro Lys Leu Ile Met
180 185 190
Thr Gln Val Ser Lys Ser Leu Gln Val Thr Arg Ile Phe Leu Gln Ala
195 200 205
Leu Asn Leu Gly Ile Glu Val Ile Asn Thr Thr Asp His Leu Lys Phe
210 215 220
Ser Lys Asp Cys Gly Arg Met Leu Thr Arg Met Trp Tyr Cys Ser Tyr
225 230 235 240
Cys Gln Gly Leu Met Met Val Lys Pro Cys Gly Gly Tyr Cys Asn Val
245 250 255
Val Met Gln Gly Cys Met Ala Gly Val Val Glu Ile Asp Lys Tyr Trp
260 265 270
Arg Glu Tyr Ile Leu Ser Leu Glu Glu Leu Val Asn Gly Met Tyr Arg
275 280 285
Ile Tyr Asp Met Glu Asn Val Leu Leu Gly Leu Phe Ser Thr Ile His
290 295 300
Asp Ser Ile Gln Tyr Val Gln Lys Asn Ala Gly Lys Leu Thr Thr Thr
305 310 315 320
Ile Gly Lys Leu Cys Ala His Ser Gln Gln Arg Gln Tyr Arg Ser Ala
325 330 335
Tyr Tyr Pro Glu Asp Leu Phe Ile Asp Lys Lys Val Leu Lys Val Ala
340 345 350
His Val Glu His Glu Glu Thr Leu Ser Ser Arg Arg Arg Glu Leu Ile
355 360 365
Gln Lys Leu Lys Ser Phe Ile Ser Phe Tyr Ser Ala Leu Pro Gly Tyr
370 375 380
Ile Cys Ser His Ser Pro Val Ala Glu Asn Asp Thr Leu Cys Trp Asn
385 390 395 400
Gly Gln Glu Leu Val Glu Arg Tyr Ser Gln Lys Ala Ala Arg Asn Gly
405 410 415
Met Lys Asn Gln Phe Asn Leu His Glu Leu Lys Met Lys Gly Pro Glu
420 425 430
Pro Val Val Ser Gln Ile Ile Asp Lys Leu Lys His Ile Asn Gln Leu
435 440 445
Leu Arg Thr Met Ser Met Pro Lys Gly Arg Val Leu Asp Lys Asn Leu
450 455 460
Asp Glu Glu Gly Phe Glu Ala Gly Asp Cys Gly Asp Asp Glu Asp Glu
465 470 475 480
Cys Ile Gly Gly Ala Gly Asp Gly Met Ile Lys Val Lys Asn Gln Leu
485 490 495
Arg Phe Leu Ala Glu Leu Ala Tyr Asp Leu Asp Val Asp Asp Ala Pro
500 505 510
Gly Asn Ser Gln Gln Ala Thr Pro Lys Asp Asn Glu Ile Ser Thr Phe
515 520 525
His Asn Leu Gly Asn Val His Ser Pro Leu Lys His His His His His
530 535 540
His
545
<210> 110
<211> 443
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 110
Glu Val Gln Leu Val Glu Thr Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr
100 105 110
Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro
115 120 125
Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val
130 135 140
Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala
145 150 155 160
Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly
165 170 175
Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly
180 185 190
Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys
195 200 205
Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys
210 215 220
Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu
225 230 235 240
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
245 250 255
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
260 265 270
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
275 280 285
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
290 295 300
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
305 310 315 320
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
325 330 335
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
340 345 350
Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
355 360 365
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
370 375 380
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
385 390 395 400
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
405 410 415
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
420 425 430
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440
<210> 111
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 111
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Glu Asp Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Glu Ala Ser Asn Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Asp Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 112
<211> 459
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 112
Gln Val Gln Leu Val Gln Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Pro Ala Gly Arg His Tyr Tyr Asp Ser Ser Gly Tyr Tyr
100 105 110
Asp Tyr Tyr Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Met Val Thr
115 120 125
Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro
130 135 140
Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val
145 150 155 160
Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala
165 170 175
Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly
180 185 190
Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly
195 200 205
Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys
210 215 220
Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys
225 230 235 240
Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu
245 250 255
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
260 265 270
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
275 280 285
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
290 295 300
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
305 310 315 320
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
325 330 335
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
340 345 350
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
355 360 365
Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
370 375 380
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
385 390 395 400
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
405 410 415
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
420 425 430
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
435 440 445
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
450 455
<210> 113
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 113
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Asp Asp
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Glu Ala Ser Asn Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Leu Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 114
<211> 451
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 114
Gln Val Gln Leu Val Glu Thr Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ala Ile Ser Gly Ser Gly Gly Ser Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Asp Arg Thr Pro Tyr Asp Phe Trp Ser Gly Tyr Leu Asp Tyr
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly
115 120 125
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
130 135 140
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
145 150 155 160
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
165 170 175
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
180 185 190
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
195 200 205
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys
210 215 220
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu
225 230 235 240
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
245 250 255
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
260 265 270
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
275 280 285
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser
290 295 300
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
305 310 315 320
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
325 330 335
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
340 345 350
Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln
355 360 365
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
370 375 380
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
385 390 395 400
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu
405 410 415
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
420 425 430
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
435 440 445
Leu Ser Pro
450
<210> 115
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 115
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Glu Asp Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Glu Ala Ser Asn Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Arg Asp Ser Ser Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 116
<211> 451
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 116
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Gly Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Ser Ala Tyr Asn Gly Asn Thr Asn Tyr Ala Gln Lys Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ser Pro Leu Leu Trp Phe Gly Glu Pro Phe Phe Asp Tyr
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly
115 120 125
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
130 135 140
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
145 150 155 160
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
165 170 175
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
180 185 190
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
195 200 205
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys
210 215 220
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu
225 230 235 240
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
245 250 255
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
260 265 270
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
275 280 285
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser
290 295 300
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
305 310 315 320
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
325 330 335
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
340 345 350
Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln
355 360 365
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
370 375 380
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
385 390 395 400
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu
405 410 415
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
420 425 430
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
435 440 445
Leu Ser Pro
450
<210> 117
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 117
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Glu Asp Asp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr His Ala Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Asp Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 118
<211> 445
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 118
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Ala Leu Asp Pro Lys Thr Gly Asp Thr Ala Tyr Ser Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro
115 120 125
Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val
130 135 140
Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala
145 150 155 160
Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly
165 170 175
Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly
180 185 190
Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys
195 200 205
Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys
210 215 220
Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu
225 230 235 240
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
245 250 255
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
260 265 270
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
275 280 285
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
290 295 300
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
305 310 315 320
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
325 330 335
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
340 345 350
Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
355 360 365
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
370 375 380
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
385 390 395 400
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
405 410 415
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
420 425 430
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440 445
<210> 119
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 119
Asp Val Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Asn
85 90 95
Thr His Val Pro Pro Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 120
<211> 449
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 120
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Glu Met His Trp Ile Arg Gln Pro Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Asp Pro Lys Thr Gly Asp Thr Ala Tyr Ser Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Phe Tyr Ser Tyr Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ser Ala Ser Ala Arg Asn Pro Thr Ile Tyr Pro Leu Thr Leu
115 120 125
Pro Pro Val Leu Cys Ser Asp Pro Val Ile Ile Gly Cys Leu Ile His
130 135 140
Asp Tyr Phe Pro Phe Gly Thr Met Asn Val Thr Trp Gly Lys Ser Gly
145 150 155 160
Lys Asp Ile Thr Thr Val Asn Phe Pro Pro Ala Leu Ala Ser Gly Gly
165 170 175
Arg Tyr Thr Met Ser Ser Gln Leu Thr Leu Pro Ala Val Glu Cys Pro
180 185 190
Glu Gly Glu Ser Val Lys Cys Ser Val Gln His Asp Ser Asn Pro Val
195 200 205
Gln Glu Leu Asp Val Asn Cys Ser Gly Pro Thr Pro Pro Pro Pro Ile
210 215 220
Thr Ile Pro Ser Cys Gln Pro Ser Leu Ser Leu Gln Arg Pro Ala Leu
225 230 235 240
Glu Asp Leu Leu Leu Gly Ser Asp Ala Ser Ile Thr Cys Thr Leu Asn
245 250 255
Gly Leu Arg Asn Pro Glu Gly Ala Ala Phe Thr Trp Glu Pro Ser Thr
260 265 270
Gly Lys Asp Ala Val Gln Lys Lys Ala Ala Gln Asn Ser Cys Gly Cys
275 280 285
Tyr Ser Val Ser Ser Val Leu Pro Gly Cys Ala Glu Arg Trp Asn Ser
290 295 300
Gly Ala Ser Phe Lys Cys Thr Val Thr His Pro Glu Ser Gly Thr Leu
305 310 315 320
Thr Gly Thr Ile Ala Lys Val Thr Val Asn Thr Phe Pro Pro Gln Val
325 330 335
His Leu Leu Pro Pro Pro Ser Glu Glu Leu Ala Leu Asn Glu Leu Leu
340 345 350
Ser Leu Thr Cys Leu Val Arg Ala Phe Asn Pro Lys Glu Val Leu Val
355 360 365
Arg Trp Leu His Gly Asn Glu Glu Leu Ser Pro Glu Ser Tyr Leu Val
370 375 380
Phe Glu Pro Leu Lys Glu Pro Gly Glu Gly Ala Thr Thr Tyr Leu Val
385 390 395 400
Thr Ser Val Leu Arg Val Ser Ala Glu Thr Trp Lys Gln Gly Asp Gln
405 410 415
Tyr Ser Cys Met Val Gly His Glu Ala Leu Pro Met Asn Phe Thr Gln
420 425 430
Lys Thr Ile Asp Arg Leu Ser Gly Lys Asp Tyr Lys Asp Asp Asp Asp
435 440 445
Lys
<210> 121
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 121
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Arg Asn Thr Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala
35 40 45
Pro Arg Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Asn
85 90 95
Thr His Val Pro Pro Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Ala Asp Ala Ala Pro Thr Val Ser Ile Phe Pro Pro Ser Ser Glu
115 120 125
Gln Leu Thr Ser Gly Gly Ala Ser Val Val Cys Phe Leu Asn Asn Phe
130 135 140
Tyr Pro Lys Asp Ile Asn Val Lys Trp Lys Ile Asp Gly Ser Glu Arg
145 150 155 160
Gln Asn Gly Val Leu Asn Ser Trp Thr Asp Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Met Ser Ser Thr Leu Thr Leu Thr Lys Asp Glu Tyr Glu
180 185 190
Arg His Asn Ser Tyr Thr Cys Glu Ala Thr His Lys Thr Ser Thr Ser
195 200 205
Pro Ile Val Lys Ser Phe Asn Arg Asn Glu Cys
210 215
<210> 122
<211> 233
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 122
Cys Gln Pro Ser Leu Ser Leu Gln Arg Pro Ala Leu Glu Asp Leu Leu
1 5 10 15
Leu Gly Ser Asp Ala Ser Ile Thr Cys Thr Leu Asn Gly Leu Arg Asn
20 25 30
Pro Glu Gly Ala Ala Phe Thr Trp Glu Pro Ser Thr Gly Lys Asp Ala
35 40 45
Val Gln Lys Lys Ala Ala Gln Asn Ser Cys Gly Cys Tyr Ser Val Ser
50 55 60
Ser Val Leu Pro Gly Cys Ala Glu Arg Trp Asn Ser Gly Ala Ser Phe
65 70 75 80
Lys Cys Thr Val Thr His Pro Glu Ser Gly Thr Leu Thr Gly Thr Ile
85 90 95
Ala Lys Val Thr Val Asn Thr Phe Pro Pro Gln Val His Leu Leu Pro
100 105 110
Pro Pro Ser Glu Glu Leu Ala Leu Asn Glu Leu Leu Ser Leu Thr Cys
115 120 125
Leu Val Arg Ala Phe Asn Pro Lys Glu Val Leu Val Arg Trp Leu His
130 135 140
Gly Asn Glu Glu Leu Ser Pro Glu Ser Tyr Leu Val Phe Glu Pro Leu
145 150 155 160
Lys Glu Pro Gly Glu Gly Ala Thr Thr Tyr Leu Val Thr Ser Val Leu
165 170 175
Arg Val Ser Ala Glu Thr Trp Lys Gln Gly Asp Gln Tyr Ser Cys Met
180 185 190
Val Gly His Glu Ala Leu Pro Met Asn Phe Thr Gln Lys Thr Ile Asp
195 200 205
Arg Leu Ser Gly Lys Gly Gly Gly Gly Ser Gly Leu Asn Asp Ile Phe
210 215 220
Glu Ala Gln Lys Ile Glu Trp His Glu
225 230
<210> 123
<211> 449
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 123
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Gly Ser Ile Ser Lys Thr
20 25 30
Tyr Ser Tyr Trp Ala Trp Ile Arg Gln His Pro Val Lys Gly Leu Glu
35 40 45
Trp Ile Gly Tyr Ile Ser Tyr Gly Gly Gly Thr His Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Ser Asp Thr Ser Lys Asn His Phe
65 70 75 80
Ser Leu Asn Leu Asn Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg Ser Gly Phe Arg Val Phe Gly Ala Phe Asp Ile Trp Gly
100 105 110
Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro
<210> 124
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 124
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Arg Ser His
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Asp Ala Ser His Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Asn Ser Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 125
<211> 450
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 125
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Ser
20 25 30
Ser Tyr Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Ser Ile Tyr Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg His Gly Pro Ser Gly Ser Tyr Tyr Ala Phe Asp Ile Trp
100 105 110
Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro
115 120 125
Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr
130 135 140
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
145 150 155 160
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
165 170 175
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
180 185 190
Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn
195 200 205
His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser
210 215 220
Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu
225 230 235 240
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
245 250 255
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
260 265 270
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
275 280 285
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr
290 295 300
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
305 310 315 320
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
325 330 335
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
340 345 350
Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val
355 360 365
Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
370 375 380
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
385 390 395 400
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr
405 410 415
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
420 425 430
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
435 440 445
Ser Pro
450
<210> 126
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 126
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser His
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Lys Ala Ser His Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Arg His His Ser Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 127
<211> 452
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 127
Gln Val Gln Leu Gln Gln Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Ser Leu Ser Leu Thr Cys Asn Val Ser Gly Tyr Tyr Ile Ser Ser Gly
20 25 30
Tyr Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Ser Ile Tyr Pro Ser Gly Thr Ser His Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Leu Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Leu Ser Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ala Gly Val Ile Ala Gly Gly Pro Arg Thr Tyr Ala Phe Asp
100 105 110
Ile Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys
115 120 125
Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly
130 135 140
Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
145 150 155 160
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
165 170 175
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
180 185 190
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn
195 200 205
Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro
210 215 220
Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
225 230 235 240
Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
245 250 255
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
260 265 270
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
275 280 285
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
290 295 300
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
305 310 315 320
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
325 330 335
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
340 345 350
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro
450
<210> 128
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 128
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Arg Ser His
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Lys Ala Ser His Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser His His Ser Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 129
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 129
Gly Lys Gly Asp Pro Lys Lys Pro Arg Gly Lys Met Ser Ser Tyr Ala
1 5 10 15
Phe Phe Val Gln Thr Cys Arg Glu Glu His Lys Lys Lys His Pro Asp
20 25 30
Ala Ser Val Asn Phe Ser Glu Phe Ser Lys Lys Cys Ser Glu Arg Trp
35 40 45
Lys Thr Met Ser Ala Lys Glu Lys Gly Lys Phe Glu Asp Met Ala Lys
50 55 60
Ala Asp Lys Ala Arg Tyr Glu Arg Glu Met Lys Thr Tyr Ile Pro Pro
65 70 75 80
Lys Gly Glu Thr Lys Lys Lys Phe Lys Asp Pro Asn Ala Pro Lys Arg
85 90 95
Pro Pro Ser Ala Phe Phe Leu Phe Cys Ser Glu Tyr Arg Pro Lys Ile
100 105 110
Lys Gly Glu His Pro Gly Leu Ser Ile Gly Asp Val Ala Lys Lys Leu
115 120 125
Gly Glu Met Trp Asn Asn Thr Ala Ala Asp Asp Lys Gln Pro Tyr Glu
130 135 140
Lys Lys Ala Ala Lys Leu Lys Glu Lys Tyr Glu Lys Asp Ile Ala Ala
145 150 155 160
Tyr Arg Ala Lys Gly Lys Pro Asp Ala Ala Lys Lys Gly Val Val Lys
165 170 175
Ala Glu Lys Ser Lys Lys Lys Lys Glu Glu Glu Glu Asp Glu Glu Asp
180 185 190
Glu Glu Asp Glu Glu Glu Glu Glu Asp Glu Glu Asp Glu Asp Glu Glu
195 200 205
Glu Asp Asp Asp Asp Glu
210
<210> 130
<211> 234
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 130
Gly Lys Gly Asp Pro Lys Lys Pro Arg Gly Lys Met Ser Ser Tyr Ala
1 5 10 15
Phe Phe Val Gln Thr Cys Arg Glu Glu His Lys Lys Lys His Pro Asp
20 25 30
Ala Ser Val Asn Phe Ser Glu Phe Ser Lys Lys Cys Ser Glu Arg Trp
35 40 45
Lys Thr Met Ser Ala Lys Glu Lys Gly Lys Phe Glu Asp Met Ala Lys
50 55 60
Ala Asp Lys Ala Arg Tyr Glu Arg Glu Met Lys Thr Tyr Ile Pro Pro
65 70 75 80
Lys Gly Glu Thr Lys Lys Lys Phe Lys Asp Pro Asn Ala Pro Lys Arg
85 90 95
Pro Pro Ser Ala Phe Phe Leu Phe Cys Ser Glu Tyr Arg Pro Lys Ile
100 105 110
Lys Gly Glu His Pro Gly Leu Ser Ile Gly Asp Val Ala Lys Lys Leu
115 120 125
Gly Glu Met Trp Asn Asn Thr Ala Ala Asp Asp Lys Gln Pro Tyr Glu
130 135 140
Lys Lys Ala Ala Lys Leu Lys Glu Lys Tyr Glu Lys Asp Ile Ala Ala
145 150 155 160
Tyr Arg Ala Lys Gly Lys Pro Asp Ala Ala Lys Lys Gly Val Val Lys
165 170 175
Ala Glu Lys Ser Lys Lys Lys Lys Glu Glu Glu Glu Asp Glu Glu Asp
180 185 190
Glu Glu Asp Glu Glu Glu Glu Glu Asp Glu Glu Asp Glu Asp Glu Glu
195 200 205
Glu Asp Asp Asp Asp Glu Gly Gly Gly Gly Ser Gly Leu Asn Asp Ile
210 215 220
Phe Glu Ala Gln Lys Ile Glu Trp His Glu
225 230
<210> 131
<211> 449
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 131
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ser Val Ser Gly Gly Pro Ile Ser Ser Ser
20 25 30
Gly Tyr Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu
35 40 45
Trp Ile Gly Thr Val Tyr Phe Asn Gly Asp Thr Tyr Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
65 70 75 80
Ser Leu Lys Leu Asn Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Arg Glu Glu Gly Tyr Tyr Tyr Tyr Tyr Met Asp Val Trp Gly
100 105 110
Lys Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
115 120 125
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
130 135 140
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
145 150 155 160
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
165 170 175
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
180 185 190
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
195 200 205
Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys
210 215 220
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
225 230 235 240
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
245 250 255
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
260 265 270
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
275 280 285
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
290 295 300
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
305 310 315 320
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
325 330 335
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
340 345 350
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
355 360 365
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
370 375 380
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
385 390 395 400
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
405 410 415
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
420 425 430
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
435 440 445
Pro
<210> 132
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 132
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Asn Ser His
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Gly Ala Ser His Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser His Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 133
<211> 459
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 133
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Gly Thr Phe Ser Ser Tyr
20 25 30
Ala Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Gly Thr Ala Asn Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Asn Arg Thr Leu Thr Tyr Tyr Asp Phe Trp Ser Gly Tyr
100 105 110
Ser Phe Trp Asp Ala Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr
115 120 125
Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro
130 135 140
Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val
145 150 155 160
Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala
165 170 175
Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly
180 185 190
Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly
195 200 205
Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys
210 215 220
Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys
225 230 235 240
Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu
245 250 255
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
260 265 270
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
275 280 285
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
290 295 300
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
305 310 315 320
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
325 330 335
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
340 345 350
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
355 360 365
Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
370 375 380
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
385 390 395 400
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
405 410 415
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
420 425 430
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
435 440 445
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
450 455
<210> 134
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 134
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile His Ser His
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Gly Ala Ser His Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Arg His Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 135
<211> 452
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 135
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Glu Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Ser Tyr Ile Ser Ser Ser Gly Arg Thr Phe Ser Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ser Gly Tyr Ser Asp Gly Trp Tyr Pro Ser Trp Phe Asp
100 105 110
Ser Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys
115 120 125
Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly
130 135 140
Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro
145 150 155 160
Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr
165 170 175
Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val
180 185 190
Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn
195 200 205
Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro
210 215 220
Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
225 230 235 240
Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
245 250 255
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
260 265 270
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
275 280 285
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
290 295 300
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
305 310 315 320
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
325 330 335
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
340 345 350
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
405 410 415
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Pro
450
<210> 136
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> модифицированный фрагмент антитела
<400> 136
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Asn Ser His
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr His Ala Ser Asn Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Ser Ser Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<---
Реферат
Изобретение относится к биотехнологии. Описана библиотека, по существу состоящая из множества антигенсвязывающих молекул, отличающихся друг от друга последовательностью, где антигенсвязывающий домен в каждой из антигенсвязывающих молекул содержит по меньшей мере один аминокислотный остаток, который изменяет антигенсвязывающую активность антигенсвязывающей молекулы в зависимости от условий концентрации ионов. Также описаны композиция, содержащая множество полинуклеотидных молекул, каждая из которых кодирует антигенсвязывающие молекулы, композиция, содержащая множество векторов, каждый из которых содержит полинуклеотидные молекулы, способ селекции антигенсвязывающих молекул, способ выделения полинуклеотидных молекул, способ получения антигенсвязывающих молекул, и фармацевтическая композиция, содержащая любую из антигенсвязывающих молекул. 8 н. и 21 з.п. ф-лы, 19 ил., 28 табл., 31 пр.

Комментарии