Способ получения (8r)-8,13-цикло-13,14-секо-5β-прегн-2-ен-6,14,20-триона - RU2677344C2
Код документа: RU2677344C2
Описание
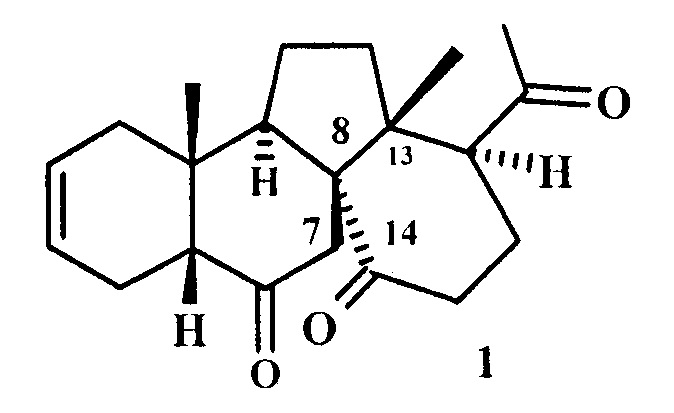
Изобретение относится к способу получения abeo-экдистероидов, конкретно - синтезу (8R)-13(14→8)-abeo-экдистероида формулы (1).
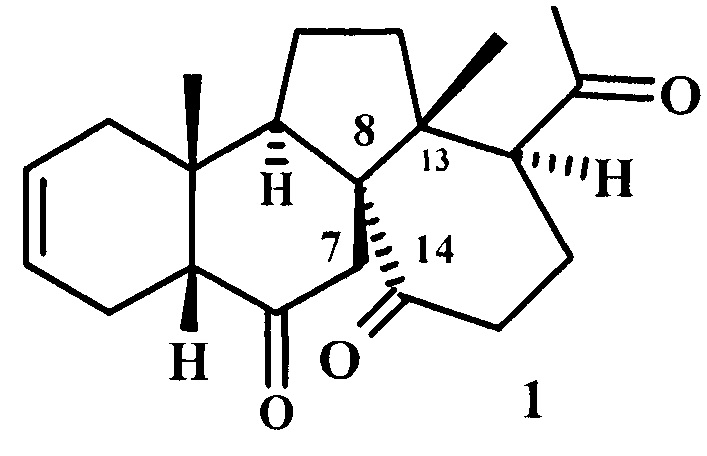
Стероиды, тетрациклический остов которых образуется в результате смещения в положение С(13)-С(8) связи С(13)-С(14) с нор-гомо-трансформацией колец С и D относятся к новому классу стероидов - abeo-стероидам. Впервые abeo-стероиды выделены в минорных количествах из морских организмов Synoicum adareanum [Miyata Y., Diyabalanage Т., Amsler C.D., McClintock J.B., Valeriote F.A., Baker B.J., J. Nat. Prod., 2007, 70, 1859-1864] и Halichondria japonica [Amagata Т., Doi M., Tohgo M., Minoura K., Numata A., Chem.commun., 1999, 1321-1322] и проявили высокую цитотоксическую активность. Экдистероиды, впервые выделенные в нанограммовых количествах из насекомых, а затем обнаруженные во многих видах растений в многократно более высоких концентрациях (1-3% от воздушно-сухой массы растений), являются гормонами линьки и метаморфоза насекомых и составляют обширную группу соединений (около 500), структурно-родственных стероидам.
Известно об образовании (8R)-13(14→8)-abeo-20-гидроксиэкдизона (3) при УФ-облучении водного раствора 20-гидроксиэкдизона (2) (λ>290 нм, 12 часов), наряду с другими соединениями [Canonica L., Danieli В., Lesma G., Palmisano G., Helv. Chim. Acta, 1987, 70, 701-716]. Согласно этому известному методу, выход целевого (8R)-13(14→8)-abeo-экдистероида (3) невысок (23%).
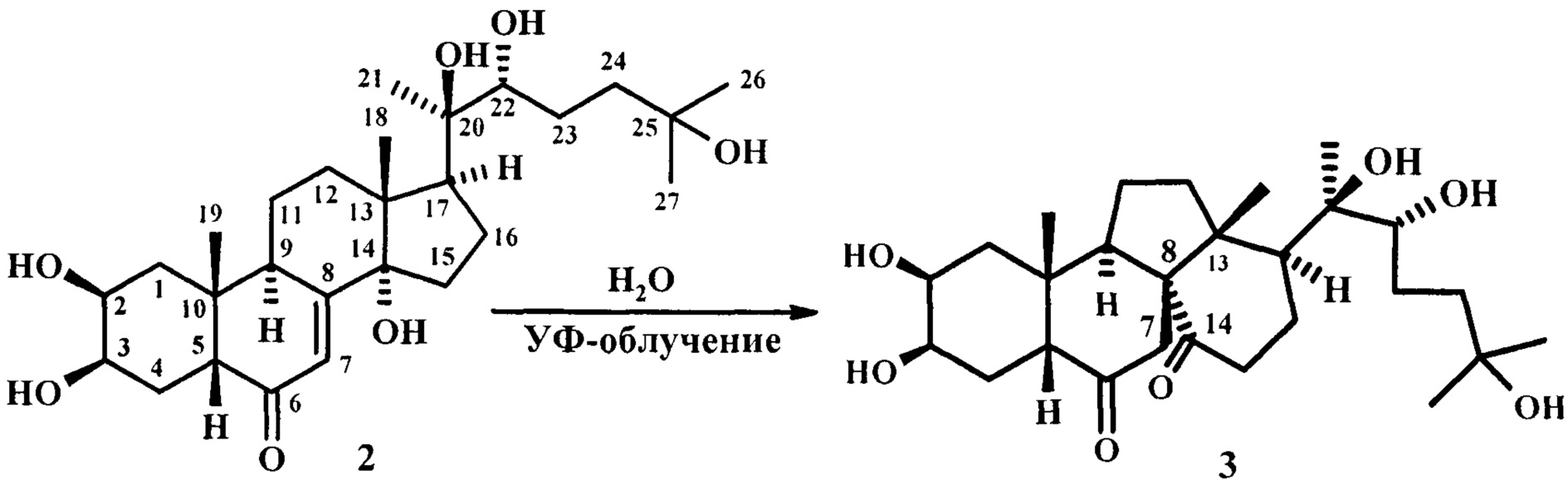
Известным способом не может быть получен (8R)-13(14→8)-abeo-экдистероид формулы (1).
Таким образом, в литературе отсутствуют сведения о селективном получении (8R)-13(14→8)-abeo-экдистероида формулы (1).
Задачей предлагаемого изобретения является разработка эффективного метода синтеза нового представителя (8R)-13(14→8)-abeo-экдистероидов-(8R)-8,13-цикло-13,14-секо-5β-прегн-2-ен-6,14,20-триона (1).
Это достигается тем, что (8R)-8,13-цикло-13,14-секо-5β-прегн-2-ен-6,14,20-трион (1) образуется в одну стадию с выходом 97% при ультразвуковом облучении (22 кГц, 20 Вт) 2,3-О-мезилата постстерона (4) в растворе диметилформамида (ДМФА) в присутствии 12 эквивалентов йодистого натрия и 12 эквивалентов цинка в течение 4 ч. Выделенный и хроматографически очищенный abeo-экдистероид (1) является кристаллическим (т.пл. 282-284°С),
Реакция проходит по схеме:

Существенные отличия предлагаемого способа:
1. В предлагаемом способе используется ультразвуковое излучение (22 кГц, 20 Вт), в то время как, в известном способе - ультрафиолетовое (λ>290 нм);
2. В предлагаемом способе, в качестве исходного субстрата, используется 2,3-O-мезилат постстерона, в то время как, в известном способе - 20-гидроксиэкдизон;
3. В предлагаемом способе используется NaI, Zn и ДМФА.
Предлагаемый способ обладает следующими преимуществами:
1. Разработанный способ открывает путь к получению труднодоступных abeo-экдистероидов, выделяемых в минорных количествах из морских организмов и обладающих потенциальной противоопухолевой активностью ([1] Miyata Y., Diyabalanage Т., Amsler C.D., McClintock J.B., Valeriote F.A., Baker B.J., J. Nat. Prod., 2007, 70, 1859-1864; [2] Amagata Т., Doi M., Tohgo M., Minoura K., Numata A., Chem.commun., 1999, 1321-1322];
2. Способ обеспечивает селективное получение нового соединения - (8R)-13(14→8)-abeo-экдистероида (1);
3. Высокий выход (8R)-13(14→8)-abeo-экдистероида (1)-97%;
4. Малое время реакции.
Сущность способа демонстрируется следующим примером:
Пример. На раствор 2,3-О-мезилата постстерона (4) (0.365 г, 0.75 мМ) в 8 мл диметилформамида (ДМФА) в присутствии йодистого натрия (1.35 г, 9 мМ) и цинка (0.59 г, 9 мМ) воздействовали ультразвуком (22 кГц, 20 Вт) в течение 4 ч. Далее в реакционную смесь добавляли 8 мл дистиллированной воды и экстрагировали CHCl3 (3×30 мл), органический слой промывали насыщенным раствором NaCl, упаривали. Сухой остаток хроматографировали на колонке (12 г SiO2, элюент смесь (5:1) гексан-этилацетат). Выделяли 0.239 г (97%) соединения (1) (Rf 0.41, Sorbfil, CHCl3-МеОН, 20:1), т.пл. 282-284°С,
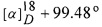
Спектральные характеристики (8R)-8,13-цикло-13,14-секо-5β-прегн-2- ен-6,14,20-триона (1):
1Н ЯМР (500 МГц, CDCl3), δ, м.д.: 0.88 с (3Н, Н3С18), 1.10 с (3Н, Н3С19), 1.47 д.д (1Н, H4, J 4.0 и 17.0 Гц), 1.69 м (1Н, Н12), 1.72 м (1Н, Н4), 1.88 м(1Н, Н1), 1.94 д (1Н, Н7α, J 13.5 Гц), 2.12 м (2Н, Н16), 2.15 м (1H, Н11), 2.21 м (1Н, Н12), 2.25 с (3Н, Н3С21), 2.35 м (1Н, Н11), 2.42 д.т (1Н, Н15, J6.5 и 13.0 Гц), 2.56 уш.д (1H, Н5, J 6.0 Гц), 2.64 м (1Н, H1), 2.89 м (1Н, Н15), 2.93 д (1Н, Н7β, J 13.5 Гц), 2.97 м (1Н, Н9), 3.24 д.д (1Н, Н17, J 5.0 и 12.0 Гц), 5.37 м (1Н, H3), 5.61 уш.д (1Н, Н2, J 8.0 Гц).13С ЯМР (500 МГц, CDCl3), δ, м.д.: 15.32 (С18), 20.74 (С1), 24.06 (С11), 25.24 (С19), 27.35 (С16), 31.75 (С21), 34.43 (С12), 34.56 (С4), 37.04 (С15), 39.30 (С10), 39.71 (С7), 46.82 (С5), 52.78 (С17), 53.23 (С9), 56.99 (С13), 66.01 (С8), 123.20 (С3), 124.55 (С2), 207.94 (С6), 209.89 (С20), 213.10 (С14).
Реферат
Изобретение относится к способу получения (8R)-8,13-цикло-13,14-секо-5β-прегн-2-ен-6,14,20-триона формулы (1), в котором 2,3-O-мезилат постстерона облучают ультразвуком (22 кГц, 20 Вт) в растворе диметилформамида в присутствии 12 эквивалентов йодистого натрия и 12 эквивалентов цинка в течение 4 ч с последующей водной обработкой реакционной смеси и выделением целевого продукта с помощью колоночной хроматографии на силикагеле. Технический результат: разработан способ получения (8R)-8,13-цикло-13,14-секо-5β-прегн-2-ен-6,14,20-триона с высоким выходом. 1 пр.
Формула

Комментарии