Новый способ синтеза 3-о-сульфамата 16,16-диметил-d-гомоэквиленина - RU2752064C1
Код документа: RU2752064C1
Описание
Изобретение относится к области органической химии и химико-фармацевтической промышленности и касается лекарственных средств для лечения онкологических заболеваний, в том числе, рака молочной железы.
В настоящее время отмечена отчетливая тенденция к возрастанию частоты злокачественных новообразований, среди которых рак молочной железы занимает одну из ведущих позиций.
Известно, что активность эстрогенов in situ в раковой опухоли может главным образом регулироваться стероидной сульфатазой. Стероидная сульфатаза катализирует гидролиз сульфата эстрона до эстрона и сульфата DHEA до DHEA (Dibbelt L., Kuss Е. Biol. Chem. Hoppe-Seyler, 1991, vol. 372, no. 3, p.173-185; Stein C., et al. J. Biol. Chem., 1989, 264(23), 13865-13872). Следовательно, контроль ее активности является важным шагом в предотвращении развития эстрогензависимых опухолей.
Самым известным ингибитором стероидной сульфатазы является ЕМАТЕ-сульфамат эстрона (Ahmed S., et al. Cur. Med. Chem., 2002, vol. 9, no. 2, p. 263-273). Однако он обладает существенным недостатком. Под действием ингибиторов сульфатазы эстрона, имеющих в своем составе сульфаматную группу, происходит необратимая дезактивация фермента с высвобождением свободного лиганда [Howarth N.M., Purohit A., Reed M.J.J. Med. Chem., 1994, vol. 37, no. 2, p. 219-221]. В частности, сульфамат эстрона ингибирует сульфатазу эстрона, однако высвобождение свободного гормона приводит к появлению сильной утеротропной активности, что, в свою очередь приводит к пролиферации опухолей [Shields-Botella J. et al., J Steroid Biochem. Mol. Biol., 2003, vol. 84, no. 2-3, p. 327-335].
Таким образом, при поиске новых противоонкологических агентов исследователи должны учесть, что носитель сульфаматной группы ингибитора сульфатазы эстрона не должен обладать гормональной (утеротропной) активностью.
Известны способы синтеза производных D-гомоэквиленина с различным сочленением колец, в том числе, содержащих метальные группы при С-16, с использованием реакции с никелем Ренея (Глуздиков И.А. Синтез ингибиторов сульфатазы эстрона: Автореф. дисс. на соискание ученой степени кандидата химических наук. - Санкт-Петербург: 2007).
Одним из перспективных производных D-гомоэквиленина представляется соединение, раскрытое в международной заявке WO 2020096486 (А1), опубл. 2020-05-14, где описан метод синтеза 3-О-сульфамата 16,16-диметил-D-гомоэквиленина, который ингибирует сульфатазу эстрона, активен в моделях in vitro и in vivo против рака молочной железы, включая трижды-негативную форму. Производное представляет собой соединение формулы (1):
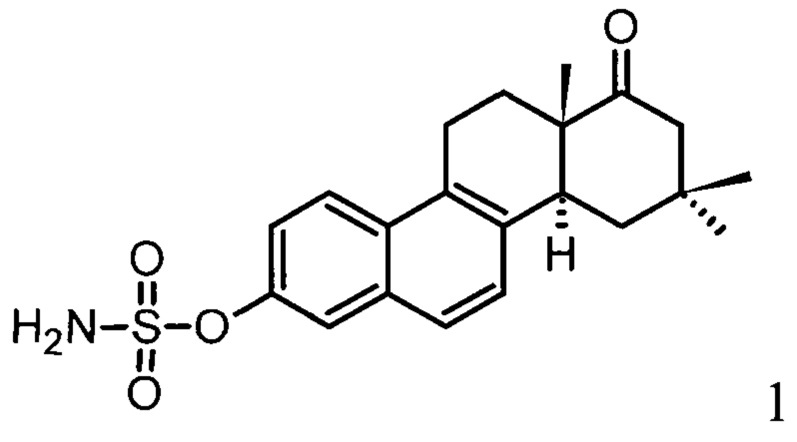
Способ осуществляют путем проведения реакции известной изотиурониевой соли с 2,4,4-триметилциклопентан-1,3-дионом, что приводит к образованию секостероида, циклодегидратация которого позволяет получить эстрапентаен, который обрабатывают Ni/Ra с последующим выделением метилового эфира 16,16-диметил-D-гомоэквиленина. Данный источник может быть указан в качестве ближайшего аналога. Недостатком описанного метода синтеза соединения является наличие стадии окисления оксидом хрома в пиридине, что приводит к малым выходам и сложности выделения продукта реакции.
Задачей настоящего изобретения является разработка нового усовершенствованного способа синтеза целевого соединения (1).
Задача решается тем, что кето-группу эстрапентаена защищают диоксолановой группой, после чего проводят стадию ароматизации под действием Никеля Ренея. Снятие защиты и метоксигруппы происходит одновременно при кипячении в смеси уксусной и бромистоводородной кислот.
Преимуществом нового метода синтеза является также возможность использовать промежуточные соединения без дополнительной очистки.
Схема получения 3-О-сульфамата 16,16-диметил-D-гомоэквиленина (соединение 1) представлена ниже:
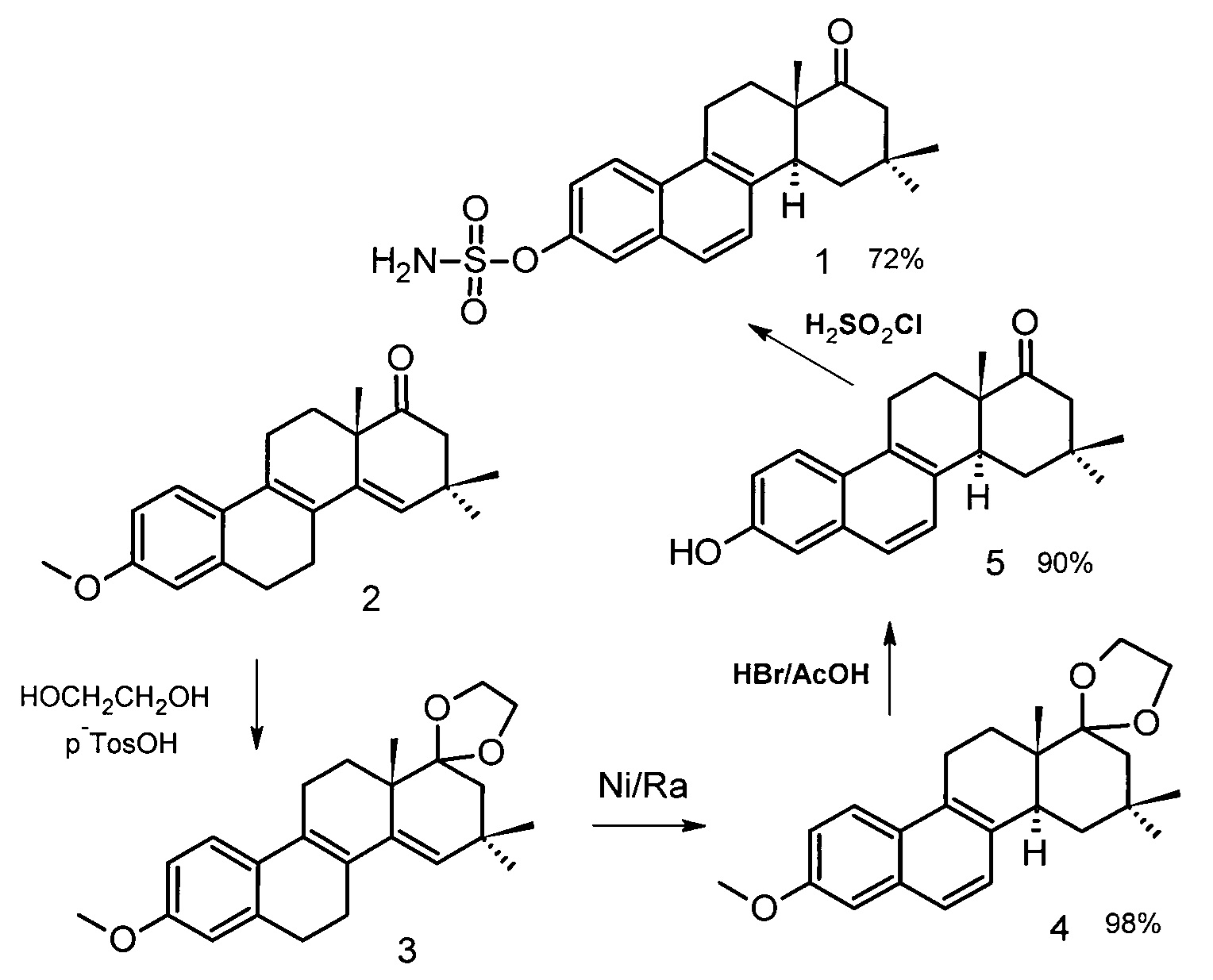
Соединение 2: 16,16-диметил-3-метокси-D-гомоэстра-1,3,5(10),8,14-пентаен-17а-он;
Соединение 3: 16,16-диметил-3-метокси-D-гомоэстра-1,3,5(10),8,14-пентаен-17а-[1,3-диоксалан]
Соединение 4: 16,16-Диметил-3-метокси-D-гомоэстра-1,3,5(10),6,8-пентаен-17а-[1,3-диоксалан]
Соединение 5: 16,16-диметил-D-гомоэквиленин
Технические результаты:
- усовершенствован метод синтеза,
- увеличен общий выход соединения (в среднем на 34%),
- исключены стадии с опасными для людей и окружающей среды реактивами и растворителями.
Пример 1.
Экспериментальная часть.
В круглодонной колбе растворяют 6,44 г (20 ммоль) эстрапентаена в 50 мл бензола, добавляют 2,5 г (40 ммоль) этиленгликоля и 1.0 г п-толуолсульфокислоты. Реакционную массу кипятят с насадкой Дина-Старка до прекращения выделения воды (10 ч). Контроль за ходом реакции осуществляют методом ТСХ. Реакционную смесь промывают водой, нас. раствором бикарбоната натрия и водой. Сушат безводным сульфатом натрия. После отгонки растворителя получают 7,4 г (100%) маслообразного слегка желтого продукта. Полученный диоксолан можно использовать в следующей стадии без очистки (по ЯМР продукт индивидуален).
Стадия с Никелем Ренея. Соотношение субстрат : Никель Ренея 1:5. 1.0 г диоксолана растворяют в 15 мл диоксана и перемешивают при комнатной температуре 20 мин, затем нагревают до 70°С. Контроль за ходом реакции осуществляют методом ТСХ. Выход ароматизированного продукта 4 количественный.
Снятие защиты и метоксигруппы происходит одновременно при кипячении в смеси уксусной и бромистоводородной кислот 1:1 в течении 8-10 часов. Контроль за ходом реакции осуществляют методом ТСХ. Продукт получают перекристаллизацией из метанола. Выход продукта 5 90%.
Целевой сульфамат 1 получали реакцией с сульфамолихлоридом. Сульфамоилхлорид, 150 мг, добавляли под аргоном к раствору 154 мг (0,50 ммоль) соединения 5 в 1,3 мл безводного ДМФА при охлаждении льдом. Через 12 ч смесь выливали в насыщенный раствор NaCl (6 мл) и экстрагировали этилацетатом (4×3 мл). Объединенные экстракты промывали насыщенным раствором NaCl и сушили над безводным сульфатом натрия, растворитель удаляли, а остаток подвергали перекристаллизации из метанола. Выход 0,14 г (74%), т.пл. 212-213.0°С. Найдено, %: С 65.00; Н 6.60; N 3.56. C20H27NO4S. Вычислено, %: С 65.09; Н 6.50; N 3.61.
Пример 2.
Фармакологическая активность.
Исследования противоопухолевой активности проводилось в экспериментах на мышах линии FVB, трансгенной по HER-2/neu (ER-/PR-HER2+), с опухолями молочных желез. Для моделирования карциномы молочной железы в исследование было включено 48 мышей линии FVB/N, с инкорпорированным онкогеном HER2/neu, массой тела 25-30 г. Вводили соединение (1) однократно в сутки орально в дозе 1-10 мг/кг. Наблюдалось ингибирование роста опухоли на 68-82% соответственно.
Таким образом, полученные новым способом субстанции могут быть использованы как эффективные противоопухолевые препараты в медицинской практике.
Реферат
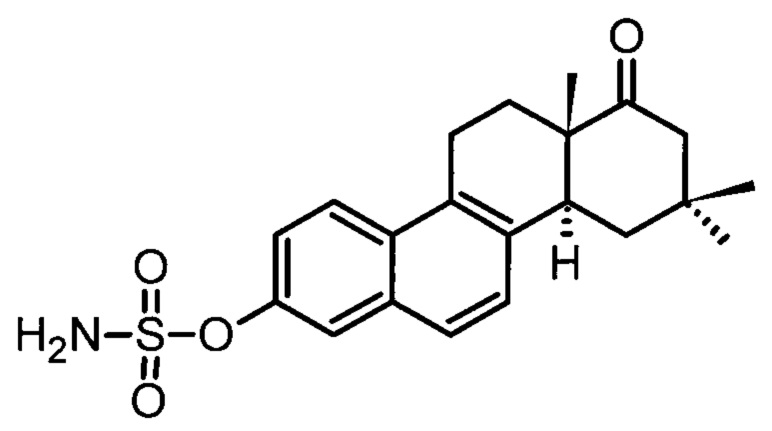
Изобретение относится к способу получения 3-О-сульфамата 16,16-диметил-D-гомоэквиленина формулы (1), в котором кето-группу 16,16-диметил-3-метокси-D-гомоэстра-1,3,5(10),8,14-пентаен-17а-она защищают диоксолановой группой путем реакции этиленгликоля и п-толуолсульфокислоты с образованием 16,16-диметил-3-метокси-D-гомоэстра-1,3,5(10),8,14-пентаен-17а-[1,3-диоксалана], после чего проводят стадию ароматизации под действием Никеля Ренея, снятие защиты и метоксигруппы 16,16-диметил-3-метокси-D-гомоэстра-1,3,5(10),6,8-пентаен-17а-[1,3-диоксалана] проводят одновременно при кипячении в смеси уксусной и бромистоводородной кислот, к раствору очищенного перекристаллизацией 16,16-диметил-D-гомоэквиленина добавляют сульфамолихлорид и получают целевой продукт (1). Технический результат: разработан новый способ получения 3-О-сульфамата 16,16-диметил-D-гомоэквиленина формулы (1) с высоким выходом, в котором исключены стадии с опасными реактивами и растворителями и в котором промежуточные продукты используют без дополнительной очистки. 2 пр.(1)
Формула

Комментарии