Последовательность днк (варианты), рекомбинантная днк, протеин, способ получения протеина, способ получения микроорганизмов, способ получения клеток гриба, способ получения линейных α -1,4-глюканов и/или фруктозы и способ получения линейных α-1,4-глюканов - RU2201963C2
Код документа: RU2201963C2
Чертежи







Описание
Настоящее изобретение относится к методам рекомбинантных ДНК для получения растений и микроорганизмов, способных к внутри- или внеклеточной экспрессии протеина, обладающего амилосахаразной активностью и катализирующего синтез линейных α-1,4-глюканов из сахарозы.
Кроме того, настоящее изобретение относится к новым последовательностям ДНК и плазмидам, содержащим указанные последовательности ДНК, которые после интеграции в геном растения или после трансформации в микроорганизмах, в частности в бактериях или в грибах, приводят к экспрессии фермента, катализирующего синтез линейных α-1,4-глюканов из сахарозы, а также к трансгенным организмам (т. е. растениям, грибам и микроорганизмам), содержащим вышеуказанные последовательности ДНК.
Линейные α-1,4-глюканы представляют собой полисахариды, состоящие из мономеров глюкозы, причем последние связаны друг с другом исключительно через α-1,4-глюкозидные связи. Наиболее часто встречающимся природным α-1,4-глюканом является амилоза - компонент крахмала растений. В последнее время все большее и большее значение придается коммерческому применению линейных α-1,4-глюканов. Вследствие своих физико-химических свойств амилоза может быть использована для получения бесцветных, не имеющих запаха и вкуса, нетоксичных и биологически разложимых пленок. В настоящее время уже существуют различные возможности применения, например, в пищевой промышленности, текстильной промышленности, в производстве стекловолокна и в производстве бумаги.
Также достигнуты определенные успехи в производстве волокон из амилозы, свойства которых сходны с таковыми природных целлюлозных волокон и которые позволяют частично или даже полностью заменить последние в производстве бумаги.
Являясь наиболее важным представителем линейных α -1,4-глюканов, амилоза, в частности, находит применение в качестве связующего вещества при изготовлении таблеток, в качестве загустителя для пудингов и кремов, в качестве заменителя желатина, в качестве связующего вещества при производстве звукоизолирующих панелей стен и для улучшения текучести низкозастывающих масел.
Другим свойством α-1,4-глюканов, которое недавно привлекло повышенное внимание, является способность их молекул образовывать вещества, включенные в органические комплексные соединения, вследствие их спирального строения. Это свойство позволяет применять α-1,4-глюканы для разнообразных целей. Указанные свойства определяют возможность их применения для молекулярного инкапсулирования витаминов, фармацевтических соединений и ароматических веществ, а также их применения для хроматографического разделения смеси веществ на иммобилизованных линейных α-1,4-глюканах.
Амилоза также служит в качестве исходного материала при получении так называемых циклодекстринов (также называемых циклоамилазами, цикломальтозами), которые в свою очередь находят широкое применение в фармацевтической промышленности, в технологии изготовления пищевых продуктов, при производстве косметики и в технологии аналитического разделения. Указанные циклодекстрины представляют собой циклические мальтолигосахариды, составленные из 6-8 моносахаридных фрагментов и обладающие способностью легко растворяться в воде, но включающие гидрофобные полости, что может использоваться для получения включенных соединений.
В настоящее время линейные α-1,4-глюканы получают в виде амилозы из крахмала. Сам крахмал состоит из двух компонентов. Первым компонентом является амилоза в виде неразветвленной цепи, состоящей из остатков глюкозы, соединенных α-1,4-связями. Другим компонентом является амилопектин, представляющий собой полимер с высокой степенью ветвления, который состоит из остатков глюкозы и в котором кроме α-1,4-связей глюкозные цепи также могут быть разветвлены с помощью α-1,6-связей. Вследствие своего различного строения и обусловленных этим различных физико-химических свойств эти два компонента также находят применение для различных целей. Чтобы иметь возможность непосредственно использовать свойства отдельных компонентов, необходимо получить их в чистом виде. Оба компонента могут быть получены из крахмала, однако этот процесс требует нескольких стадий очистки, занимает много времени и является дорогостоящим.
Следовательно, существует необходимость в получении обоих компонентов крахмала в однородном виде. Для этой цели вырабатывающие крахмал растения изменяли путем селекции или с помощью генной инженерии с целью получить крахмал с измененной пропорцией амилозы/амилопектина. Хотя обычно процентное содержание амилопектина в кукурузном крахмале составляет, например, 70%, с помощью селекции удалось получить сорт кукурузы (восковую кукурузу), крахмал которой состоит практически на 100% из амилопектина (Akatsuka и Nelson, 1966, J. Biol. Chem. 241: 2280-2285).
Кроме того, путем селекции было получено несколько сортов кукурузы, обладающих повышенным содержанием амилозы (60-70%), например сорта amylose extender и dull (Wolf и др., 1955, J. Am. Chem. Soc. 77: 1654-1659; Boyer и др. , 1976, Die Stärke: 28: 405-410). Для получения сортов, которые синтезируют однородный крахмал в виде амилопектина, использовали другие виды растений, например, рис (Sano, 1984, Theor. Appl. Genet. 68: 467-473) и ячмень (Shannon и Garwood, 1984, в Whistler, Bemiller, Paschall, Starch: Chemistry and Technology, Academic Press, Orlando, 2-е изд., 25-86), или таковые, которые синтезируют крахмал с высоким содержанием амилозы (например, различные виды гороха). Помимо указанных выше методик классического скрещивания опубликованы методики, основанные на генетическом воздействии на вырабатывающие крахмал растения.
Например, у Visser и др., (1991, Mol. Gen. Genet. 255: 289-296) говорится, что сорта картофеля, синтезирующие практически чистый амилопектиновый крахмал, могут быть получены путем антисмыслового ингибирования гена, который кодирует крахмал-синтетазу, необходимую для связывания гранул крахмала.
В международной заявке WO 92/14827 описано получение растений картофеля, которые вследствие анитсмыслового ингибирования экспрессии фермента разветвления вырабатывают крахмал с повышенной пропорцией амилозы/аминопектина. Однако растения, описанные в WO 92/14827, не обладают способностью производить крахмал с более высоким содержанием амилозы.
Несмотря на многочисленные попытки и разнообразные подходы до сих пор никому не удалось добиться успеха в получении растений, производящих чистый амилозный крахмал.
Также до сих пор не описаны возможности получения амилозы с высокой степенью чистоты или чистых линейных α-1,4-глюканов с использованием других способов, например генной инженерией микроорганизмов.
Кроме того, до сих пор не были обнаружены последовательности ДНК, кодирующие ферменты, которые обладали бы способностью катализировать синтез линейных α-1,4-глюканов в растениях, грибах, микроорганизмах или in vitro.
Таким образом, целью настоящего изобретения является получение последовательностей ДНК и разработка способов, дающих возможность получать растения, грибы и микроорганизмы, способные синтезировать линейные α-1,4-глюканы.
Задачи настоящего изобретения решены посредством различных вариантов выполнения изобретения, представленных в пунктах формулы изобретения.
Следовательно, изобретение относится к последовательностям ДНК, кодирующим протеины, обладающие ферментативной активностью амилосахаразы.
В частности изобретение относится к последовательностям ДНК, кодирующим протеин, который имеет аминокислотную последовательность, представленную в SEQ ID No.1, и к кодирующей ДНК-последовательности, представленной в SEQ ID No.1. Кроме того, настоящее изобретение относится к последовательностям ДНК, гибридизирующимся с вышеуказанными последовательностями по изобретению и кодирующим протеин, обладающий ферментативной активностью амилосахаразы, а также к последовательностям ДНК, которые вследствие генетического кода являются вырожденными по сравнению с вышеуказанными последовательностями ДНК по изобретению.
В этом контексте термин "гибридизация" обозначает гибридизацию в обычных условиях гибридизации, предпочтительно в строгих условиях, таких, как описано, например, у Sambrook и др. (1989, Molecular Cloning, A Laboratory Manual, 2-е изд., Cold Spring Hatbor Laboratory Press, Cold Spring Harbor, NY).
В другом варианте осуществления изобретение относится к последовательностям ДНК, кодирующим протеин, обладающий
ферментативной активностью амилосахаразы, и получаемым с помощью способа, включающего следующие стадии:
(а) получение библиотеки геномной или кДНК на основе геномной ДНК или мРНК клеток
организма;
(б) трансформацию приемлемого хозяина с помощью библиотеки, созданной на стадии (а);
(в) обработку трансформированных клеток парами йода;
(г) выявление клеток,
окрашенных в голубой цвет;
(д) выделение и культивирование клеток, выявленных на стадии (г); и
(е) выделение геномной ДНК-вставки или кДНК-вставки из трансформированных клеток.
Приемлемым хозяином, упомянутым в стадии (б), является, например, Е. coli.
В предпочтительном варианте осуществления изобретение относится к последовательностям ДНК, кодирующим амилосахаразу из микроорганизмов, в частности из грамотрицательных микроорганизмов, предпочтительно из бактерий рода Neisseria и наиболее предпочтительно из Neisseria polysaccharea.
Также представляется возможным модифицировать последовательности ДНК по изобретению путем мутации или с помощью последовательности, измененной путем инсерции (вставки), делеции, замещения или рекомбинации с целью изменить определенное свойство протеина, подлежащего экспрессии. Одной из этих модификаций, среди прочего, является делеция сигнальной последовательности, обеспечивающей секрецию фермента, и вставки других сигнальных последовательностей или последовательностей ДНК, кодирующих транзитные пептиды и тем самым влияющих на локализацию экспрессируемого протеина.
Последовательности ДНК по изобретению, в частности последовательность ДНК по изобретению, представленная в SEQ ID No.1, или ее часть, могут применяться для определения, присутствуют ли гомологичные последовательности ДНК в определенных организмах или экспрессируются ими. Для достижения этого образцы ДНК или мРНК конкретного организма гибридизируют с последовательностью ДНК по изобретению в пригодных для этой цели условиях гибридизации в соответствии с обычными способами.
В соответствии со стандартными методиками из генома различных организмов также можно выделять гомологичные последовательности, которые также кодируют амилосахаразы или ферменты, обладающие аналогичными свойствами, используя последовательность ДНК по изобретению. В данном контексте гомология означает идентичность последовательности по крайней мере на 40-60%, предпочтительно более чем на 60%, особенно предпочтительно более чем на 80%, наиболее предпочтительна идентичность последовательности более чем на 95%. Кроме того, гомология означает, что соответствующие последовательности ДНК или кодируемые аминокислотные последовательности являются функционально и/или структурно эквивалентными. Последовательности, которые гомологичны последовательностям по изобретению и которые отличаются от последовательности ДНК или кодируемой аминокислотной последовательности по изобретению по одному или нескольким позициям, являются нормальными вариантами указанной последовательности, представляющими собой модификации, имеющие такую же функцию. Это могут быть варианты, встречающиеся в естественных условиях, такие как последовательности из других организмов, или мутации. Указанные мутации могут возникать естественным путем, или их можно получать с помощью специфичного мутагенеза. Кроме того, эти варианты могут быть последовательностями, полученными синтетическим путем. Все эти последовательности ДНК равным образом подпадают под объем изобретения.
Протеины, кодируемые различными вариантами последовательности ДНК по изобретению, обладают общими специфичными характеристиками, такими как ферментативная активность, иммунологическая реактивность, конформация и т.д., а также физическими свойствами, такими как электрофоретическая подвижность, хроматографическое свойства, коэффициент седиментации, растворимость, спектроскопические свойства, стаблильность и т.д.
Чтобы выявить родственные последовательности ДНК, должны быть получены библиотеки генов организма, подлежащего исследованию, которые являются характерными для присущих организму генов, или генов, полученных в результате экспрессии в организме или в определенной ткани организма. К первому из вышеуказанных типов относятся геномные библиотеки, к последнему относятся библиотеки кДНК.
Идентификацию и выделение гомологичных последовательностей ДНК из таких библиотек осуществляют путем гибридизации в соответствии со стандартными методиками (см. , например, у Sambrook и др., 1989, Molecular Cloning, A Laboratory Manual, 2-е изд., Cold Spring Hatbor Laboratory Press, Cold Spring Harbor, NY).
В качестве гибридизирующего зонда могут быть использованы молекулы ДНК, которые имеют точно такую же или практически такую же последовательность ДНК, как и последовательность, представленная в SEQ ID No.1, или часть указанной последовательности. Фрагменты ДНК, используемые в качестве гибридизирующих зондов, также могут представлять собой синтетические фрагменты ДНК, которые были получены в соответствии с обычными методами синтеза ДНК и являются практически идентичными последовательности по изобретению. После идентификации и выделения генов, гибридизирующих с последовательностью ДНК по изобретению, необходимо определить последовательность и проанализировать свойства протеинов, кодируемых указанной последовательностью.
Амилосахараза (также обозначаемая как сахароза: α-1,
4-глюкан-4-α-глюкозилтрансфераза, К. Ф. 2.4.1.4.) представляет собой фермент, для которого предложена следующая реакционная схема:
сахароза + (α-1,4-D-глюкозил)n
-->
D-фруктоза+(α-1,4-D-глюкозил)n+1
Эта реакция представляет собой реакцию трансглюкозилирования. Продуктами этой реакции являются линейные α-1,
4-глюканы и фруктоза. Кофакторы при этом не требуются. До сих пор амилосахаразная активность была обнаружена только у нескольких видов бактерий, в частности у видов рода Neisseria (MacKenzie и др. ,
1978, Can. J. Microbiol. 24: 357-362), а фермент был оценен только с точки зрения его ферментативной активности. По данным Okada и др. частично очищенный фермент из Neisseria perflava после добавления
сахарозы приводит к синтезу гликогенподобных полисахаридов, которые являются слабо разветвленными (Okada и др., 1974, J. Biol. Chem. 249: 126-135). Аналогично этому синтезируемые внутри- или
внеклеточно глюканы Neisseria perflava и Neisseria polysaccharea обладают определенной степенью разветвленности (Riou и др., 1986, Can. J. Microbiol. 32: 909-911). До настоящего времени остается
неясным, получаются ли эти разветвления вследствие действия амилосахаразы или благодаря другому ферменту, присутствующему в препаратах очищенной амилосахаразы в качестве примеси. Поскольку фермент,
вызывающий разветвление, до сих пор не выявлен, предполагают, что амилосахараза катализирует как реакцию полимеризации, так и реакцию разветвления (Okada и др., 1974, J. Biol. Chem. 249: 126-135).
Фермент, который экспрессируют присущим ему образом в Neisseria, является особенно стабильным, очень сильно связывается с продуктами полимеризации и конкурентно ингибируется продуктом фруктозой (MacKenzie и др., 1978, Can. J. Microbiol. 24: 357-362). Вид Neisseria, а именно, Neisseria polysaccharea, секретирует амилосахаразу (Riou и др., 1986, Can. J. Microbiol. 32: 909-911), в то время как у другого вида Neisseria она сохраняется в клетке.
Ферменты, обладающие амилосахаразной активностью, могут быть обнаружены только в микроорганизмах. Растения, имеющие амилосахаразы, неизвестны.
В соответствии с изобретением можно показать, что продуктом реакции, катализируемой амилосахаразой, являются линейные α-1,4-глюканы, которые не являются разветвленными, как это предполагалось до сих пор (см. выше).
Обнаружение ферментативной активности амилосахаразы может быть осуществлено путем обнаружения синтезированных глюканов, как описано ниже в примере 3. Обнаружение обычно осуществляют, используя окрашивание йодом. Бактериальные колонии, экспрессирующие амилосахаразу, можно идентифицировать с помощью, например, обработки парами йода. Колонии, синтезирующие линейные α-1,4-глюканы, окрашиваются в голубой цвет.
Ферментативная активность очищенного фермента может быть обнаружена, например, на содержащих сахарозу агарозных пластинках. Если протеин наносят на такую пластинку и инкубируют в течение 1 ч или более при 37oС, он диффундирует в агарозу и катализирует синтез линейных глюканов. Последние могут быть обнаружены при обработке парами йода. Кроме того, протеин может быть обнаружен в нативных полиакриламидных гелях. После электрофореза в нативном полиакриламидном геле гель уравновешивают в натрий-цитратном буфере (50 мМ, рН 6,5) и инкубируют в течение ночи в растворе сахарозы (5%-ной в натрий-цитратном буфере). Если гель после этого окрашивают раствором Люголя, то зоны, в которых локализованы протеины, обладающие амилосахаразной активностью, окрашиваются в голубой цвет вследствие синтеза линейных α-1,4-глюканов.
С помощью последовательностей ДНК по изобретению можно получить растения, способные производить чистый амилозный крахмал, т.е. линейные α-1,4-глюканы, и модифицировать вырабатывающие крахмал растения таким образом, чтобы они имели более высокое содержание крахмала и в то же время увеличенную пропорцию амилозы/амилопектина. Последовательности ДНК по изобретению могут применяться для получения микроорганизмов и грибов, в частности дрожжей, способных производить фермент, катализирующий синтез линейных α-1,4-глюканов из сахарозы.
Кроме того, с помощью последовательностей ДНК по изобретению или кодируемых ими протеинов при небольших затратах на производство можно получать чистый фруктозный сироп.
Согласно другому варианту
осуществления изобретение относится к рекомбинантным молекулам ДНК, таким как векторы, в частности плазмиды, содержащие последовательности ДНК по изобретению или их части, например плазмида pNB2,
которая была депонирована под каталожным номером DSM No. 9196. В частности изобретение относится к рекомбинантным молекулам ДНК, в которых последовательность ДНК по изобретению сцепляют с
последовательностями, обеспечивающими экспрессию протеина, обладающего амилосахаразной активностью, в микроорганизмах, грибах или растениях, например, к плазмидам, содержащим следующие
последовательности ДНК:
(а) соответствующий промотор, активный в микроорганизмах и обеспечивающий транскрипцию кодирующей последовательности в микроорганизмах в прямом направлении от него,
и
(б) последовательность ДНК, кодирующая полипептид, обладающий амилосахаразной активностью и сцепленный с промотором таким образом, чтобы обеспечить образование транслируемой РНК в
полипептиде,
или к плазмидам, содержащим следующие последовательности ДНК:
(а) соответствующий промотор, активный в растениях, обеспечивающий транксрипцию кодирующей
последовательности в прямом направлении от него в соответствующее время или на соответствующей стадии развития трансгенного растения или в определенных тканях трансгенного растения, и
(б)
последовательность ДНК, кодирующую полипептид, обладающий амилосахаразной активностью и сцепленный с промотором таким образом, чтобы обеспечить образование транслируемой РНК в полипептиде.
Кроме того, предметом изобретения являются микроорганизмы, грибы и растения, содержащие рекомбинантые молекулы ДНК по изобретению.
Еще одним предметом изобретения являются обладающие ферментативной активностью амилосахаразы протеины, которые кодируются одной из последовательностей ДНК по изобретению, в частности таковые, имеющие происхождение из микроорганизмов, предпочтительно из грамотрицательных микроорганизмов, в частности рода Neisseria и наиболее предпочтительно из Neisseria polysaccharea. Кроме того, предметом изобретения являются амилосахаразы, имеющие по данным гель-электрофореза молекулярную массу 63±20 кДа, предпочтительно 63±15 кДа и наиболее предпочтительно 63±10 кДа.
Далее предметом изобретения являются конкретные протеины, которые обладают ферментативной активностью амилосахаразы и аминокислотная последовательность которых представлена в SEQ ID No.1. Кроме того, изобретение относится к протеинам, имеющим аминокислотные последовательности, которые практически идентичны аминокислотной последовательности, приведенной в SEQ ID No. 1, или которые отличаются от указанной последовательности по одной или нескольким позициям. Эти отличия предпочтительно представляют собой обмены консервативными аминокислотами, так что протеин обладает ферментативной активностью амилосахаразы. Таким образом, изобретение также относится к амилосахаразам, аминокислотная последовательность которых имеет высокую гомологичность аминокислотной последовательности, приведенной в SEQ ID No.1, в частности гомологичность по крайней мере на 70%, предпочтительно более чем на 80%, более предпочтительно более чем на 90%, особенно предпочтительна гомологичность по крайней мере на 99%.
Кроме того, один из вариантов выполнения изобретения относится к применению последовательности ДНК по изобретению и молекул ДНК, в частности плазмид, содержащих указанные последовательности ДНК, для трансформации клеток прокариот или эукариот, а также для экспрессии амилосахаразы в клетках прокариот или эукариот, а также к способу получения протеинов по изобретению путем выращивания в соответствующей питательной среде микроорганизма, содержащего рекомбинантную молекулу ДНК по изобретению.
В частности предметом настоящего изобретения является способ получения растений, которые способны синтезировать линейные α-1,4-глюканы, характеризующийся введением в клетки растения последовательности ДНК по изобретению, содержащей область, кодирующую протеин, обладающий ферментативной активностью амилосахаразы, и сцепленную с последовательностями ДНК, обеспечивающими экспрессию в клетках растений и регенерацию целых растений из трансформированных клеток.
Кроме того, настоящее изобретение относится к способу получения растительных клеток и растений, способных синтезировать линейные α-1,4-глюканы,
включающему следующие стадии:
(а) получение полигенного экспрессирующего кластера, имеющего следующие частичные последовательности:
(I) промотор, активный в растениях и
обеспечивающий образование РНК в соответствующей ткани-мишени или в клетках-мишенях;
(II) по крайней мере одну последовательность ДНК, кодирующую протеин, обладающий ферментативной
активностью амилосахаразы, и слитую с промотором в смысловой ориентации;
(III) функционирующий в растениях сигнал для прекращения транскрипции и полиаденилирования молекулы РНК;
(б)
перенос полигенного экспрессирующего кластера в клетки растений; и
(в) регенерацию целых интактных растений из трансформированных растительных клеток.
Пригодными для этой цели промоторами являются такие промоторы, которые обеспечивают конститутивную экспрессию гена во всех тканях растений, такие как промотор 35S вируса мозаики цветной капусты (CaMV), a также таковые, которые обеспечивают экспрессию только в определенных органах или только на определенных стадиях развития растения. Известны промоторы, обеспечивающие специфичную экспрессию в клубнях растений картофеля, такие как промотор В33 (Liu и др., 1990, Mol. Gen. Genet. 223: 401-406), или таковые, которые обеспечивают специфичную экспрессию в корнеплодах сахарной свеклы. Кроме того, в литературе описаны последовательности ДНК, обеспечивающие зависящую от света и тканеспецифичную экспрессию в клетках листьев последовательностей ДНК, расположенных ниже по ходу транскрипции (Orozco и Ogren, 1993, Plant Mol. Biol. 23: 1129-1138).
Последовательность ДНК, указанная в пункте (II) на стадии (а) процесса по существу может представлять собой любую последовательность ДНК, содержащую кодирующую область, которая кодирует протеин, обладающий ферментативной активностью амилосахаразы. Пригодные для этой цели последовательности ДНК, в частности, представляют собой последовательности ДНК, имеющие происхождение из микроорганизмов, предпочтительно из грамотрицательных микроорганизмов, прежде всего из бактерий рода Neisseria и в частности из Neisseria polysaccharea.
Предпочтительный вариант осуществления способа по изобретению включает применение последовательностей ДНК, кодирующих протеин, обладающий ферментативной активностью амилосахаразы, причем протеин имеет аминокислотную последовательность, представленную в SEQ ID No.1, или аминокислотную последовательность, практически идентичную таковой.
Предпочтительно применять последовательности ДНК, имеющие высокую степень гомологичности последовательности ДНК, представленной в SEQ ID No.1, и кодирующие амилосахаразу. Также могут применяться последовательности ДНК, которые могут быть получены из указанных последовательностей путем замещения, инсерции или делеции, в том случае, если не ухудшена их ферментативная активность.
Особенно предпочтительный вариант осуществления способа относится к применению последовательности ДНК, имеющей нуклеотидную последовательность, представленную в SEQ ID No.1, или ее части, при условии, что длина этих частей достаточна для того, чтобы кодировать протеин, обладающий ферментативной активностью амилосахаразы.
В соответствии с изобретением последовательность ДНК, кодирующую амилосахаразу, сцепляют в смысловой ориентации с промотором (3'-конец промотора с 5'-концом кодирующей последовательности). Указанная последовательность может быть модифицирована до или после сцепления с элементами, контролирующими транскрипцию (промотором и сигналом окончания транскрипции), чтобы изменять при необходимости свойства полипептида или его локализацию, как это более подробно описано ниже. Последовательность ДНК, представленная в SEQ ID No.1, например, кодирует внеклеточную амилосахаразу. Секреция обеспечивается сигнальной последовательностью, включающей 16 N-концевых остатков аминокислот, кодируемых нуклеотидами с 939 по 986 последовательности, представленной в SEQ ID No.1. Поскольку такие сигнальные последовательности прокариот обычно приводят к секреции протеина также и в растительных клетках, экспрессируемый протеин транспортируют в апопласт растения, когда используют последовательность, представленную в SEQ ID No.1.
Для осуществления экспрессии фермента в цитозоле растительных клеток сигнальная последовательность, оказывающая воздействие на секрецию, должна быть удалена. Если фермент, подлежащий экспрессии, должен быть связан с определенными внутренними компартменами, такими как хлоропласты, амилопласты, митохондрии или вакуоли, сигнальная последовательность, оказывающая воздействие на секрецию, должна быть заменена на сигнальную последовательность или на последовательность, кодирующую транзитный пептид, который обеспечивает транспорт экспрессируемого протеина к соответствующему компартменту. Подобные последовательности известны. Для транспорта в пластиды, например, пригодны транзитные пептиды пептидов-предшественников малой субъединицы рибулозобифосфаткарбоксилазы (рибулозо-1,5-бифосфаткарбоксилаза/оксигеназа RUBISCO) из картофеля (Wolter и др., 1988, Proc. Acad. Sci. USA 85: 846-850) или протеин-носитель ацила (АСР). Для транспорта в вакуооли, например, может быть использована сигнальная последовательность пататина (Sonnewald и др., 1991, Plant' J. 1: 95-106). Применяемые последовательности должны быть слиты в матрице с последовательностью ДНК, кодирующей фермент.
Перенос полигенного экспрессирующего кластера, сконструированного на стадии (а) способа, в растительные клетки предпочтительно осуществляют с использованием плазмид, например бинарных плазмид.
Предпочтительно использовать методики, гарантирующие стабильную интеграцию полигенного экспрессирующего кластера в геном трансформированной растительной клетки.
Способ по изобретению в основном может быть применен к любым видам растений. Интерес представляют как однодольные, так и двудольные растения. Методики трансформации были описаны ранее для различных видов однодольных и двудольных растений.
Последовательности ДНК по изобретению дают возможность модифицировать растения так, что они экспрессируют протеины, обладающие ферментативной активностью амилосахаразы, позволяя тем самым осуществлять в растениях синтез линейных α-1,4-глюканов. Поскольку α-1,4-глюканы с точки зрения их строения идентичны синтезируемой в растениях амилозе, то возможно получать растения, которые синтезируют чистую амилозу, и модифицировать растения, вырабатывающие крахмал, таким образом, чтобы они синтезировали крахмал с более высокой пропорцией амилозы.
В большинстве растений продукты, образовавшиеся в результате поглощения света в процессе фотосинтеза, транспортируются по растению к соответствующим органам-мишеням в виде сахаров, более конкретно в основном в виде сахарозы. Поскольку субстратом для реакции полимеризации амилосахаразы является сахароза, указанный выше способ главным образом дает возможность модифицировать в отношении экспрессии амилосахаразы все растения, как двудольные, так и однодольные. Предпочтительными являются культурные растения, такие как кукуруза, рис, пшеница, ячмень, сахарная свекла, сахарный тростник, табак, картофель или маниок, а также определенные виды фруктовых и овощных культур, в том числе яблоневые, сливы, морковь или томаты.
Экспрессия амилосахаразной активности в растениях может, среди прочего, применяться для изменения в результате синтеза линейных α-1,4-глюканов вязкости получаемых из растений экстрактов. В этой связи интерес представляют томаты. В результате экспрессии амилосахаразы в плодах томатов происходит синтез линейных α-1,4-глюканов, что приводит к увеличению вязкости экстрактов, получаемых из этих плодов.
Экспрессия амилосахаразы, кроме того, особенно целесообразна в тех органах растений, в которых запасается большое количество сахарозы. Такими органами являются, например, корнеплод сахарной свеклы или стебель сахарного тростника. Поскольку эти растения в норме не синтезируют какое-либо заметное количество крахмала, из этих растений могут быть выделены в чистом виде синтезируемые амилозой α-1,4-глюканы.
Местом биосинтеза сахарозы в растительных клетках является цитозоль. Однако местом ее запасания является вакуоль. В процессе транспорта к запасающей ткани сахарной свеклы или картофеля или в процессе транспорта в эндосперм семян сахароза должна пройти через апопласт. Следовательно, все три компартмента клетки, т.е. цитозоль, вакуоль и апопласт, могут рассматриваться как пригодные для экспрессии амилосахаразы при синтезе линейных глюканов.
В растениях, вырабатывающих крахмал, таких, как картофель или кукуруза, у которых синтез крахмала и накопление крахмала обычно происходит в амилопластах, экспрессия амилосахаразы в апопласте, цитозоле или в вакуоли должна привести к дополнительному синтезу глюканов в этих компартментах, что означает значительное увеличение полезной продуктивности.
Поскольку картофель в процессе выделения крахмала дает возможность отделить крахмал, синтезированный в амилопластах, от линейных α-1,4-глюканов, синтезированных с помощью амилосахаразы в апопласте, в цитозоле или в вакуоли, одно и то же растение может использоваться для получения как крахмала, так и линейных α-1,4-глюканов.
Кроме того, известны трансгенные растения картофеля и растения кукурузы, в которых путем ингибирования АДФ-глюкозопирофосфорилазы с помощью антисмыловой конструкции полностью подавляют синтез крахмала в клубнях и зернах соответственно. Вместо этого, например, у картофеля в клубнях аккумулируются растворимые сахара, в частности сахароза и глюкоза (Müller-Röber и др., 1992, EMBO J. 11: 1229-1238; ЕР-А-0455316). С помощью экспрессии амилосахаразы в цитозоле, вакуоли или апопласте этих растений, т.е. в компартментах, в которых отсутствуют разветвленные ферменты, можно достигнуть синтеза крахмала с высоким содержанием амилозы, т.е. крахмала, состоящего в основном из линейных α-1,4-глюканов. Механизм реакции, которая катализируется амилосахаразой, характеризуется тем, что остаток глюкозы непосредственно переносится от сахаразы к линейному глюкану. В процессе биосинтеза линейных глюканов из сахарозы в растениях сахароза сначала разлагается на глюкозу и фруктозу, которые в свою очередь превращаются в активированную промежуточную форму АДФ-глюкозы. Остаток глюкозы из АДФ-глюкозы с помощью фермента синтеза крахмала переносится к уже существующему глюкану, высвобождая при этом АДФ. Превращение сахарозы в две молекулы АДФ-глюкозы происходит в несколько стадий с поглощением энергии.
Следовательно, энергетический баланс реакции, катализируемой амилосахаразой, значительно лучше энергетического баланса синтеза сахарозы из амилозы в растительных клетках, что приводит к увеличению выхода синтезированных глюканов в растениях, экспрессирующих амилосахаразную активность.
Известно много клонирующих векторов, содержащих в доступной форме сигнал репликации для E.coli и ген-маркер для отбора трасформированных бактериальных клеток, которые могут применяться для достижения интродукции чужеродных генов в высшие растения. Примерами таких векторов являются pBR322, серии pUC, серии M13mp, pACYC184 и т.д. Требуемая последовательность может быть интродуцирована в вектор в соответствующем сайте рестрикции. Полученную плазмиду применяют для трансформации клеток E.coli. Трансформированные клетки E. coli культивируют в соответствующей среде и затем собирают и подвергают лизису. Плазмиду регенерируют. Методами анализа, обычно применяемыми для характеризации получаемых плазмид ДНК, являются рестрикционный анализ, гель-электрофорез, реакции секвенирования и другие способы, известные в биохимии и молекулярной биологии. После каждой операции ДНК плазмиды может быть расщеплена и сцеплена с другими последовательностями ДНК. Каждая последовательность плазмидной ДНК может быть клонирована в такой же или в других плазмидах.
Для интродукции ДНК в растительную клетку-хозяина пригодны многочисленные методики. Эти методики включают трансформацию растительных клеток с помощью Т-ДНК с использованием Agrobacterium tumefaciens или Agrobacterium rhizogenes в качестве трансформирующих агентов, слияние протопластов, инъекцию, электропорацию ДНК, интродукцию ДНК биобаллистическим методом, а также другие возможные методики. В зависимости от способа интродукции требуемых генов в растительные клетки могут быть необходимы другие последовательности ДНК. Если, например, для трансформации растительных клеток применяют Ti- или Ri-плазмиду, то по крайней мере правая пограничная последовательность, хотя часто и правая, и левая пограничные последовательности Т-ДНК Ti- или Ri-плазмид должны быть сцеплены с генами, подлежащими интродукции в качестве фланкирующей области.
Если для трансформации применяют Agrobacteria, то интродукцируемую ДНК необходимо клонировать в специальных плазмидах, т.е. либо в промежуточном векторе, либо в бинарном векторе. Промежуточные векторы могут быть интегрированы в Ti- или Ri-плазмиду Agrobacteria путем гомологичной рекомбинации, поскольку их последовательности гомологичны последовательностям Т-ДНК. Промежуточные векторы не способны реплицироваться в Agrobacteria. Промежуточный вектор может быть перенесен в Agrobacterium tumefaciens с использованием плазмиды-хелпера (конъюгация). Бинарные векторы способны реплицироваться как в E.coli, так и в Agrobacteria. Они содержат ген-маркер селекции и линкер или полилинкер, которые ограничены справа и слева пограничными областями Т-ДНК. Они могут быть непосредственно трансформированы в Agrobacteria (Holsters и др., 1978, Mol. Gen. Genet. 163: 181-187). Agrobacterium, которая служит в качестве клетки-хозяина, может содержать плазмиду, несущую vir-область. vir-Область необходима для переноса Т-ДНК в клетку растения. В ней может присутствовать дополнительная Т-ДНК. Трансформированную таким образом Agrobacterium используют для трансформации растительных клеток.
Применение Т-ДНК для трансформации растительных клеток интенсивно исследовалось и достаточно полно описано в ЕР 120516; у Hoekema и др. в The Binary Plant Vector System, Offsetdrukkerij Kanters B.V. Alblasserdam, 1985, глава V; Fraley и др., Crit. Rev. Plant. Sci, 4: 1-46, и у An и др.; 1985, EMBO J. 4: 277-287.
Для переноса ДНК в растительные клетки может оказаться целесообразным культивировать эксплантаты растений совместно с Agrobacterium tumefaciens или Agrobacterium rhizogenes. Из зараженного растительного материала (например, из кусочков листьев, сегментов стеблей, корней, а также протопластов или клеток растений, выращенных в суспензии) в соответствующей среде, которая может содержать антибиотики или биоциды для отбора трансформированных клеток, может быть регенерировано целое растение. Полученные таким образом растения могут быть подвергнуты исследованию на присутствие интродуцированной ДНК.
Для плазмид, используемых для инъекции и электропорации ДНК в растительных клетках, не существует конкретных требований. Могут применяться простые плазмиды, такие как производные pUC. Однако, если требуется регенерировать целые растения из таких трансформированных клеток, необходимо присутствие селектируемого маркера.
Если интродуцированнную ДНК интегрируют в геном растительной клетки, она обычно сохраняет там стабильность и также может быть обнаружена в следующем поколении первоначально трансформированной клетки. Обычно она содержит маркер селекции, который придает трансформированным растительным клеткам устойчивость к биоциду или антибиотику, такому как канамицин, G 418, блеомицин, гигромицин или глуфозинат и т.д. Таким образом, индивидуально подобранный маркер должен давать возможность отличать трансформированные клетки от клеток, лишенных интродуцированной ДНК.
Трансформированные клетки развиваются внутри растения как обычные клетки (ср. , например, McCormick и др., 1986, Plant Cell Reports 5: 81-84). Такие растения могут быть выращены обычным образом и могут быть скрещены с растениями, которые имеют такой же трансформированный генетический код или другие генетические коды. Образовавшиеся в результате этого гибридные особи обладают соответствующими фенотипическими свойствами.
Чтобы гарантировать стабильное закрепление и наследование фенотипических особенностей, необходимо получить два или несколько поколений. Кроме того, для подтверждения стабильного закрепления соответствующего фенотипа или других характеристик должен быть собран урожай семян.
Еще одним предметом изобретения являются модифицированные растительные клетки и растения, полученные с помощью вышеуказанного процесса по изобретению, в частности растительные клетки и растения, содержащие последовательность ДНК по изобретению в сочетании с последовательностями ДНК, которые позволяют осуществлять экспрессию последовательности ДНК по изобретению в растительных клетках. Указанные растительные клетки характеризуются наличием экспрессии протеина, обладающего ферментативной активностью амилосахаразы, приводящей тем самым к синтезу линейных α-1,4-глюканов в клетках или растениях. Для трансгенных растительных клеток и растений, кроме того, характерно то, что они содержат рекомбинантную молекулу ДНК, которая стабильно интегрирована в их геном и которая содержит полигенный экспрессирующий кластер, причем полигенный экспрессирующий кластер содержит последовательность ДНК, кодирующую амилосахаразу.
Линейные α-1,4-глюканы, образованные в трансгенных растительных клетках и растениях с помощью амилосахаразы, могут быть выделены из трансгенных растительных клеток и растений таким же образом, что и образующийся нормальным образом крахмал. Они также составляют предмет настоящего изобретения.
Кроме того, изобретение относится к применению последовательностей ДНК по изобретению или их частей для экспрессии полипептида, обладающего амилосахаразной активностью, предпочтительно в микроорганизмах, не обладающих собственной амилосахаразной активностью.
В настоящей заявке под микроорганизмами понимают бактерии, а также все одноклеточные организмы, как они определены, например, у Schlegel "Allgemeine Mikrobiologie" (Georg Thieme Veriag, 1985, с. 1-2).
В настоящее время в биотехнологических исследованиях для синтеза и получения огромного разнообразия веществ в большой степени используются микроорганизмы. Это стало возможным благодаря разработке множества различных систем для эффективной экспрессии генов прокариот и эукариот в микроорганизмах (см. , например, обзор Methods in Enzymology 153: 385-516). Широкое применение нашли, например, штаммы таких видов бактерий, как Eschenchia coli и Bacillus subtilis. Для получения последовательностей ДНК по изобретению, в частности последовательности ДНК, представленной в SEQ ID No.1, в настоящее время возможно экспрессировать протеин, обладающий ферментативной активностью амилосахаразы, в микроорганизмах, для которых доступны соответствующие системы экспрессии.
Настоящее изобретение, в частности, относится к способу получения микроорганизмов, способных
синтезировать внутриклеточно или внеклеточно линейные α-1,4-глюканы, в соответствии с которым последовательность ДНК по изобретению интродуцируют и экспрессируют в микроорганизме. Указанный
процесс, например, может включать следующие стадии:
(а) получение полигенного экспрессирующего кластера, имеющего следующие частичные последовательности:
(I) промотор, активный в
выбранном микроорганизме и обеспечивающий транскрипцию последовательности ДНК в прямом направлении от него;
(II) последовательность ДНК, кодирующую амилосахаразу и слитую с промотором в
смысловой ориентации;
(III) функционирующий в микроорганизмах сигнал для прекращения транскрипции;
(б) трансформацию соответствующего микроорганизма с помощью полигенного
экспрессирующего кластера, полученного на стадии (а).
Векторы экспресии подробно описаны в данной области техники. В дополнение к гену-маркеру селекции и собственному репликону, обеспечивающему репликацию в выбранном хозяине, они обычно содержат бактериальный или вирусный промотор и сигнал прекращения траскрипции. Между промотором и сигналом прекращения траскрипции присутствует по крайней мере один сайт рестрикции или один полилинкер, который позволяет осуществить инсерцию кодирующей последовательности ДНК. В качестве промоторной последовательности можно применять последовательность ДНК, которая обычно контролирует транскрипцию соответствующего гена, при условии, что она проявляет активность в выбранном организме. Эта последовательность может быть замещена другими промоторными последовательностями. Могут применяться промоторы, которые оказывают воздействие на конститутивную экспрессию гена, или индуцируемые промоторы, позволяющие селективно регулировать экспрессию гена в прямом направлении от него. Бактериальные и вирусные промоторные последовательности, обладающие указанными свойствами, подробно описаны в данной области техники. К промоторам, позволяющим осуществлять наиболее сильную экспрессию гена в прямом направлении от него, относятся например, Т7-промотор (Studier и др., 1990, в Methods in Enzymology 185: 60-89), lacuv5, trp, trp-lacUV5 (DeBoer и др., в Rodriguez, R. L. и Chamberlin, M.J. (ред.), Promoters, Structure and Function; Praeger, New York, 1982, с. 462-481; DeBoer и др., 1983, Proc. Natl. Acad. Sci. USA 80: 21-25), lp1, гас (Boros и др., 1986, Gene 42: 97-100) или промотор ompF.
Последовательность ДНК, указанная в пункте (II) стадии (а) процесса, может представлять собой любую последовательность ДНК, кодирующую протеин, обладающий ферментативной активностью амилосахаразы. Предпочтительно применяют последовательности ДНК, которые имеют происхождение из микроорганизмов, в частности грамотрицательных бактерий, предпочтительно рода Neisseria и особенно предпочтительно из Neisseria polysaccharea. В особенно предпочтительном варианте осуществления последовательность ДНК имеет нуклеотидную последовательность, представленную в SEQ ID No.1, или последовательность ДНК, которую гибридизируют с ней и которая кодирует протеин, обладающий ферментативной активностью амилосахаразы, причем эта последовательность сцеплена с промотором в смысловой ориентации (3'-конец промотора с 5'-концом кодирующей последовательности).
Применяемая последовательность может быть модифицирована либо до, либо после интеграции в вектор экспрессии, чтобы при необходимости изменять свойства полипептида или его локализацию, как более подробно описано выше.
Вместо последовательности, представленной в последовательности SEQ ID No. 1, могут применяться последовательности ДНК, которые могут быть получены из указанной последовательности путем замещения, инсерции или делеции, если при этом не ухудшается ферментативная активность кодируемого протеина.
Трансформация микроорганизмов на стадии (б) обычно может быть осуществлена с помощью стандартных методик, таких, как описанные у Maniatis и др. (Molecular Cloning: A Laboratory Manual, 1982, New York: Cold Spring Harbor Laboratory Press).
Трансформированный микроорганизм культивируют в среде, которая должна быть пригодной для потребностей конкретного используемого хозяина. Особенное внимание необходимо уделять значению рН, температуре, вентилированию и т.д.
Еще одним предметом изобретения являются микроорганизмы, которые получены описанным выше способом и которые характеризуются наличием последовательности ДНК, кодирующей амилосахаразу, причем последовательность является частью рекомбинантной молекулы ДНК. Указанная рекомбинантная молекула ДНК в зависимости от использованного способа трансформации может присутствовать в клетках либо вне генома, либо может быть стабильно интегрирована в геном клеток использованного микроорганизма.
Амилосахараза, экспрессированная Neisseria polysaccharea, представляет собой внеклеточный фермент, который синтезирует линейные α-1,4-глюканы на основе сахарозы вне клеток. Для этого в отличие от большинства путей синтеза полисахаридов, протекающих внутри клетки, не требуются ни активированные производные глюкозы, ни кофакторы. Энергию, необходимую для образования α-1,4-глюкозидной связи между конденсированными остатками глюкозы, получают непосредственно за счет гидролиза связи между фрагментом глюкозы и фруктозы в молекуле сахарозы.
Поэтому оказывается возможным выращивать секретирующие амилосахаразу микроорганизмы, которые были получены на стадиях описанного выше процесса, в среде, содержащей сахарозу, причем секретируемая амилоза приводит к синтезу линейных α-1,4-глюканов из сахарозы среды. Эти глюканы могут быть выделены из питательной среды.
Кроме того, представляется возможным синтезировать α-1,4-глюканы in vitro путем получения фермента, лишенного клеток. В этом случае микроорганизмы, секретирующие амилосахаразу, выращивают в среде без сахарозы, давая возможность продолжать экспрессию амилосахаразы до достижения стационарной фазы роста. После удаления клеток из питательной среды путем центрифугирования секретированный фермент может быть получен из супернатанта. Затем для синтеза линейных α-1,4-глюканов фермент может быть добавлен в растворы, содержащие сахарозу. По сравнению с синтезом линейных α-1,4-глюканов непосредственно в питательной среде, содержащей сахарозу, преимуществом этого метода является то, что в этом случае условия реакции можно лучше контролировать и что продукты реакции оказываются существенно более чистыми и легче поддаются последующей очистке.
Фермент может быть очищен из питательной среды с помощью обычных методов очистки, таких как осаждение, ионообменная хроматография, аффинная хроматография, гель-фильтрация, ЖХВД-хроматография с обращенной фазой и т.д. Кроме того, возможно осуществлять экспрессию полипептида с помощью модифицированной последовательности ДНК, встроенной в вектор экспрессии, что приводит к получению полипептида, который вследствие своих определенных свойств может быть более легко выделен из питательной среды. Кроме того, возможно экспрессировать фермент в виде протеина, слитого с другой полипептидной последовательностью, чьи специфические характеристики связывания позволяют выделять слитый протеин с помощью аффинной хроматографии.
Известными методами являются, например, экспрессия протеина, слитого с глутатион-S-трансферазой, и последующая очистка с помощью аффинной хроматографии на колонке с глутатионом, основанной на сродстве глутатион-S-трансферазы к глутатиону (Smith и Johnson, 1988, Gene 67: 31-40). Другим известным методом является экспрессия протеина, слитого с протеином, связывающим мальтозу, (ПСМ) и последующая очистка на амилозной колонке (Guan и др., 1988, Gene 67: 21-30; Maina и др., 1988, Gene 74: 365-373).
Помимо возможности синтеза линейных α-1,4-глюканов путем непосредственного добавления очищенного фермента в раствор, содержащий сахарозу, существует другой способ, основанный на иммобилизации фермента на носителе. Преимущества такой иммобилизации состоят в том, что фермент как катализатор синтеза может быть легко возвращен в исходное состояние и может применяться несколько раз. Поскольку очистка ферментов обычно требует много времени и является дорогостоящей, иммобилизация и повторное использование фермента приводят к существенному снижению затрат. Другим преимуществом является высокая степень чистоты продуктов реакции, что, среди прочего, является следствием того факта, что условия реакции можно лучше контролировать в случае, когда используются иммобилизованные ферменты. Нерастворимые линейные глюканы, получаемые в виде продуктов реакции, затем легко могут быть подвергнуты дальнейшей очистке.
Существует множество веществ, пригодных в качестве носителей для иммобилизации протеинов, которые могут быть связаны с носителем либо через ковалентные, либо через нековалентные связи (см. обзор Methods in Enzymology, тома 135, 136 и 137). Широко применяемыми в качестве носителей материалами являются, например, агароза, целлюлоза, полиакриламид, двуокись кремния или найлон.
По аналогии с очищенным ферментом микроорганизмы, экспрессирующие необходимый полипептид или секретирующие конкретный метаболит, также могут быть иммобилизованы. Обычно иммобилизация достигается путем включения клеток в соответствующее вещество, такое, как, например, альгинат, полиакриламид, желатин, целлюлозу или хитозан. Однако также можно адсорбировать или ковалентно связывать клетки с носителем (см. Brodelius и Mosbach, в Methods in Enzymology, том 135: 173-175). Преимуществом иммобилизации клеток является то, что в этом случае может быть получена существенно более высокая плотность клеток по сравнению с культиварованием в жидкой среде, приводящая к более высокой продуктивности. В этом случае затраты на смешение и вентиляцию культуры, а также на поддержание ее стерильности являются более низкими. Важным аспектом является то, что иммобилизация дает возможность организации непрерывного производства, поскольку при этом можно избежать или существенно сократить продолжительные непродуктивные фазы, которые обычно имеют место в процессах ферментации.
Подобно микроорганизмам последовательности ДНК по изобретению также могут применяться для экспрессии амилосахаразной активности в грибах, в частности в дрожжевых грибах, например, в Saccharomyces cerevisiae. Векторы, применяемые для экспрессии гетерологичных генов в дрожжах, описаны в литературе (например, у Bitter и др., Methods in Enzymology, 153: 516-544). В дополнение к гену-маркеру селекции и сайту инициации репликации для культивирования в бактериях эти векторы содержат по крайней мере один дополнительный ген-маркер селекции, позволяющий идентифицировать трансформированные клетки дрожжей, последовательность ДНК, позволяющую осуществлять репликацию в дрожжах, и полилинкер для встраивания требуемого полигенного экспрессирующего кластера. Полигенный экспрессирующий кластер конструируют из промотора, последовательности ДНК, подлежащей экспрессии, и последовательности ДНК, осуществляющей окончание транскрипции и полиаденилирование транскрипта. Промоторы и сигналы окончания транскрипции из Saccharomyces также описаны в литературе и являются доступными. Вектор экспрессии может быть интродуцирован в клетки дрожжей путем трансформации в соответствии с обычными методами (см. Methods in Yeast Genetics, A Laboratory Course Manual, Cold Spring Harbor Laboratory Press, 1990). Клетки, содержащие вектор, отбирают и культивируют в соответствующей селекционной среде. Кроме того, клетки дрожжей дают возможность интегрировать полигенный экспрессирующий кластер в геном клетки путем гомологичной рекомбинации с использованием соответствующего вектора, приводящего к стабильному наследованию признаков.
По аналогии с микроорганизмами для получения секретируемой амилосахаразы также могут использоваться штаммы дрожжей, экспрессирующие амилосахаразу. Методы культивирования дрожжей в литературе описаны достаточно полно (см., например. Methods in Yeast Genetics, A Laboratory Course Manual, Cold Spring Harbor Laboratory Press, 1990). Также возможна иммобилизация дрожжей, и этот метод уже нашел применение для получения этанола в экономически значимых масштабах (Nagashima и др., в Methods in Enzymology, том 136: 394-405; Nojima и Yamada, в Methods in Enzymology, том 136: 380-394).
Однако применение дрожжей, секретирующих амилосахаразу, для синтеза линейных α-1,4-глюканов в среде, содержащей сахарозу, пока представляется проблематичным, поскольку дрожжи секретируют инвертазу, осуществляющую гидролиз внеклеточной сахарозы. Дрожжи получают образовавшиеся гексозы с помощью переносчика гексозы. Однако у Gozalbo и Hohmann (1990, Current Genetics 17, 77-79) описан штамм дрожжей, который несет дефектный ген suc2 и в результате не может секретировать инвертазу. Кроме того, эти клетки дрожжей не имеют транспортной системы для доставки сахарозы в клетки. Если указанный штамм модифицируют с помощью последовательности ДНК по изобретению таким образом, чтобы он секретировал амилосахаразу в среде для культивирования, амилосахараза осуществляет синтез линейных α-1, 4-глюканов, если питательная среда содержит сахарозу. Фруктоза, образующаяся в качестве продукта реакции, затем может поступать в клетки дрожжей.
Таким образом, настоящее изобретение
также отосится к способу получения клеток грибов, способных синтезировать либо внутриклеточно, либо внеклеточно линейные α-1,4-глюканы, при этом последовательность ДНК по изобретению
интродуцируют в клетки грибов и экспрессируют. Указанный процесс в качестве примера может включать следующие стадии:
(а) получение полигенного экспрессирующего кластера, имеющего следующие
частичные последовательности:
(I) промотор, активный в выбранном грибе и обеспечивающий транскрипцию последовательности ДНК в прямом направлении от него;
(II) последовательность ДНК,
кодирующую амилосахаразу и слитую с промотором в смысловой ориентации;
(III) функционирующий в клетках гриба сигнал для прекращения транскрипции; и
(б) трансформацию клеток гриба с
помощью полигенного экспрессирующего кластера, сконструированного на стадии (а).
Еще одним предметом настоящего изобретения является возможность получать чистый фруктозный сироп недорогим путем при использовании последовательностей ДНК по изобретению. Традиционные способы получения фруктозы предполагают либо ферментативный гидролиз сахарозы с использованием инвертазы, либо разложение крахмала до фрагментов глюкозы, часто путем ацидолиза, и последующее ферментативное превращение глюкозы во фруктозу при помощи глюкозоизомеразы. Оба метода приводят к получению смесей глюкозы и фруктозы. Оба компонента должны быть отделены друг от друга с помощью хроматографических методов.
Получение чистой фруктозы или чистого фруктозного сиропа с использованием протеина, обладающего ферментативной активностью амилосахаразы, предпочтительно осуществляют в лишенной клеток системе с использованием очищенного фермента. Последний может быть иммобилизован на соответствующем носителе или может присутствовать в растворенном виде. Наличие сахарозы приводит к синтезу линейных глюканов и к высвобождению фруктозы. Отделение субстрата от продуктов реакции или разделение двух продуктов реакции может быть достигнуто, например, с помощью мембран, проницаемых для фруктозы, но не проницаемых для сахарозы или глюканов. Если фруктозу непрерывно удаляют с помощью такой мембраны, сахароза более или менее полно превращается во фруктозу и линейные глюканы.
Кроме того, амилосахараза предпочтительно может быть иммобилизована на носителе, расположенном между двумя мембранами, одна из которых проницаема для фруктозы, но не для сахарозы или глюканов, а другая позволяет проникать сахарозе, но не глюканам. Субстрат вводят через мембрану, проницаемую для сахарозы. Синтезируемые глюканы остаются в пространстве между двумя мембранами, а высвобожденная фруктоза может непрерывно удаляться из реакционной среды через мембрану, проницаемую только для фруктозы. Такое устройство позволяет эффективно разделять продукты реакции и, таким образом, получать, среди прочего, чистую фруктозу.
Преимущества применения амилосахараз для получения чистой фруктозы состоят в том, что в качестве исходного материала может применяться относительно дешевый сахарозный субстрат, а также в том, что фруктоза может быть выделена из реакционной смеси простым путем без применения хроматографических методов.
Изобретение, кроме того, относится к применению протеинов, обладающих ферментативной активностью амилосахаразы, для получения фруктозы.
Еще одной возможностью применения протеинов, обладающих амилосахаразной активностью, является их использование для получения циклодекстринов. Циклодекстрины получают путем разложения крахмала с помощью фермента циклодекстрин-трансглюкозилазы (КФ 2.4.1.19), который получают из бактерий Bacillus macerans. Вследствие разветвленности крахмала только приблизительно 40% остатков глюкозы может быть превращено в циклодекстрины с использованием этой системы. При использовании практически чистых протеинов, обладающих амилосахаразной активностью, оказывается возможным синтезировать циклодекстрины на основе сахарозы при одновременном действии амилосахаразы и циклодекстрин-трансглюкозилазы, причем амилосахараза катализирует синтез линейных глюканов из сахарозы, а циклодекстрин-трансглюкозилаза катализирует превращение этих глюканов в циклодекстрины.
Плазмиду pNB2 по изобретению в соответствии с Будапештским Договором депонировали в Немецкой коллекции микроорганизмов (Deutsche Sammlung von Mikroorganismen (DSM)), Брауншвейг, Германия, 6 мая 1994 г. под каталожным номером DSM 9196.
Используемые
сокращения
ИПТП - изопропил-β-D-тиогалактопиранозид.
Используемые среды и растворы
YT-среда - 8 г бактотриптона, 5 г дрожжевого экстракта, 5 г NaCl, до 1000
мл ddH2O.
YT-планшеты - YT-среда с 15 г бактоагара/1000 мл;
раствор Люголя - 12 г KI, 6 г I2, до 1,8 л ddH2.
Описание
чертежей
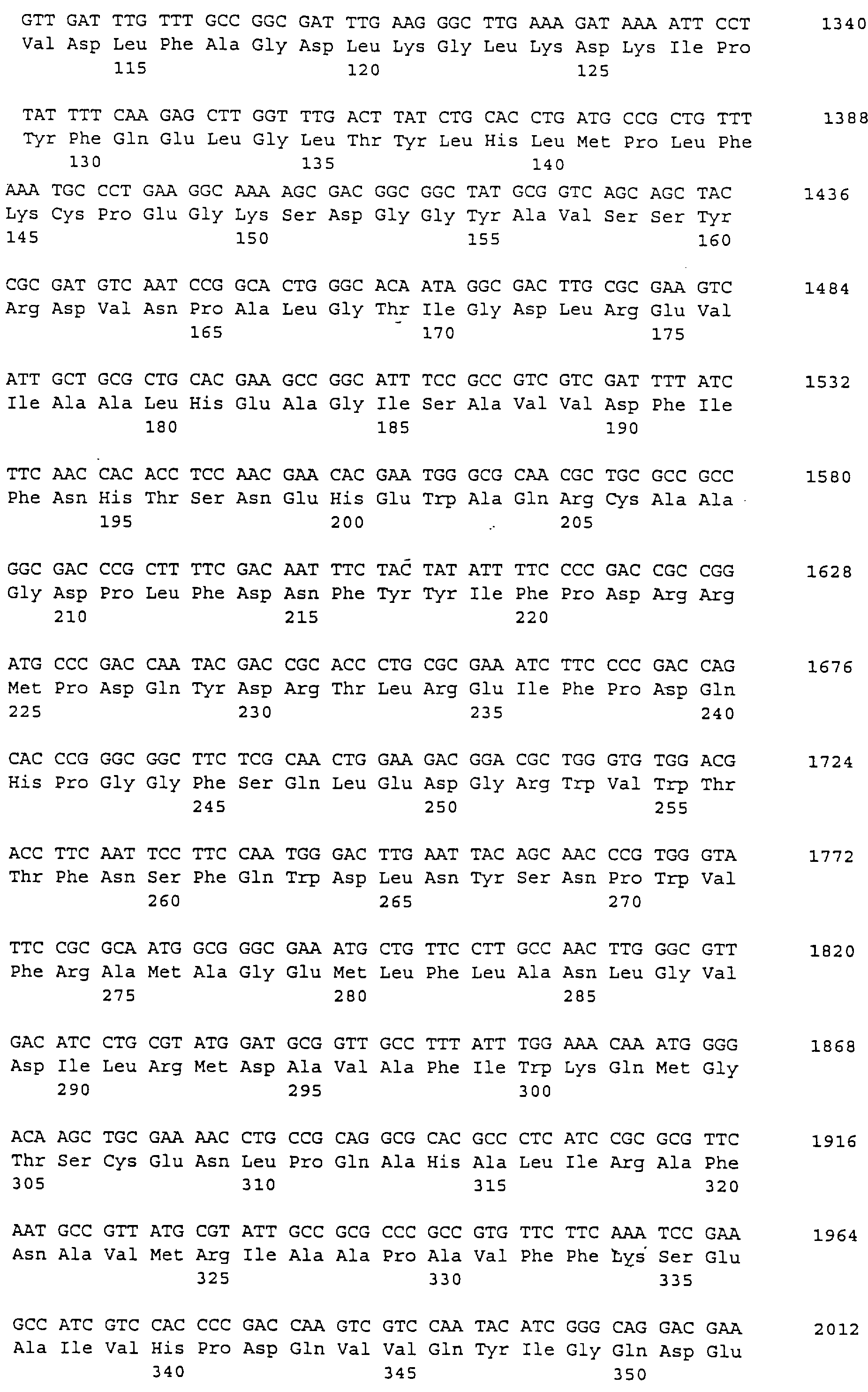
На фиг. 1 представлена схема плазмиды pNB2 (DSM 9196). Тонкая линия соответствует последовательности вектора клонирования pBluescript SK(-). Жирная линия соответствует геномной
ДНК-вставке Neisseria polysaccharea длиной приблизительно 4,2 т.п.н. Кодирующая область амилосахаразы изображена в виде стрелки, расположенной под вставкой. Над вставкой изображена секвенируемая
область. Все количественные значения соотнесены с этой областью длиной 2883 пары оснований.
На фиг. 2 показано проявление амилосахаразной активности в трансформированных клетках E. coli, подвергнутых действию паров йода. Клетки E.coli, трансформированные плазмидой pBluescript II SK (стрелка А) и клетки E.coli, трансформированные плазмидой pNB2, (стрелка В) помещали на YT-планшеты (1,5%-ный агар; 100 мкг/мл ампициллина; 5%-ная сахароза; 0,2 мМ ИПТП) и инкубировали в течение ночи при 37oС. Затем планшеты подвергали действию паров йода. У колоний клеток, трансформированных плазмидой pNB2, видно выраженное голубое кольцо.
Ниже изобретение проиллюстрировано на примерах.
Пример 1
Выделение из Neisseria
polysaccharea последовательности геномной ДНК. кодирующей амилосахаразную активность
Для выделения из Neisseria polysaccharea последовательности ДНК, кодирующей амилосахаразную активность,
сначала создавали библиотеку
геномной ДНК. Клетки Neisseria polysaccharea выращивали на "Колумбийском кровяном агаре" (Columbia blood agar, фирма Difco) в течение 2 дней при 37oС.
Образовавшиеся колонии собирали с планшетов. Геномную ДНК выделяли в соответствии с методом Ausubel и др. (в Current Protocols in Molecular Biology (1987), J. Wiley & Sons, NY) и подвергали
процессингу. Полученную таким образом ДНК частично разлагали с помощью рестрикционной эндонуклеазы Sau3A. Образовавшиеся фрагменты ДНК лигировали с разложенным с помощью BamHI вектором pBluescript
SK(-). Продукты лигирования трансформировали в клетках E.coli штамма XL1-Blue. Для их отбора клетки помещали на YT-планшеты с добавлением ампициллина в
качестве маркера селекции. Селекционная
среда дополнительно содержала 5%-ную сахарозу и 1 мМ ИПТП. После инкубации в течение ночи при 37oС образовавшиеся бактериальные колонии окрашивали йодом, помещая кристаллический йод под
крышку чашки Петри и помещая культуральные планшеты с колониями бактерий на 10 мин каждый в другую половину чашки Петри. Йод, который испаряется при комнатной температуре, окрашивал в голубой цвет
некоторые области культуральных планшетов, содержащих амилозоподобные глюканы. Из колоний бактерий, имевших голубое кольцо, выделяли ДНК плазмиды в соответствии с методом Birnboim & Doly (1979,
Nucleic Acids Res. 7: 1513-1523). Эту ДНК ретрансформировали в клетках Е.coli штамма SURE. Трансформированные клетки помещали на YT-планшеты с ампициллином в качестве маркера селекции. Выделяли
положительные клоны.
Пример 2
Анализ последовательности геномной ДНК-вставки плазмиды pNB2
Из клона Е. coli, полученного в соответствии с методикой из примера 1,
выделяли рекомбинантную плазмиду. Рестрикционный анализ показал, что указанная плазмида представляла собой продукт лигирования, состоящий из двух молекул вектора и геномного фрагмента длиной
приблизительно 4,2 т.п.н. Плазмиду разлагали с помощью рестрикционной эндонуклеазы PstI и выделяли геномный фрагмент (GeneClean, Bio101). Полученный таким образом фрагмент лигировали с вектором
pBluescript II SK, линеаризованным с помощью PstI, что приводит к удвоению сайтов рестрикции PstI и SmaI. Продукт лигирования трасформировали в клетках E.coli и затем помещали на планшеты с
ампициллином для отбора. Выделяли позитивные клоны. Из одного из этих клонов выделяли плазмиду pNB2 (фиг. 1), а часть последовательности ее геномной ДНК-вставки определяли стандартными методиками,
используя дидезокси-метод (Sanger и др., 1977, Proc. Natl. Acad. Sci. USA 74: 5463-5467).
Длина всей вставки составляет приблизительно 4,2 т.п.н. Определяли нуклеотидную последовательность частичной последовательности, имеющей длину 2883 пары оснований. Эта нуклеотидная последовательность указана ниже (SEQ ID No.1). Локализация секвенированной области в геномной вставке показана на фиг.1.
Пример 3
Экспрессия внеклеточной амилосахаразной активности в трансформированных клетках E.coli
(а) Обнаружение амилосахаразной активности
во время роста на YT-планшетах
Для экспрессии внеклеточной амилосахаразной активности клетки E.coli трансформировали вектором pNB2 в соответствии со стандартными методиками. Колонию
трансформированного штамма инкубировали на YT-планшетах (1,5%-ный агар; 100 мкг/мл ампициллина; 5%-ная сахароза; 0,2 мМ ИПТП) и инкубировали в течение ночи при 37oС. Амилосахаразную
активность определяли, подвергая колонию действию паров йода (фиг.2). У колоний, экспрессирующих амилосахаразу, проявляется голубое кольцо. Амилосахаразную активность можно обнаружить даже при
отсутствии ИПТП, вероятно вследствие активности эндогенных промоторов амилосахаразы.
(б) Обнаружение амилосахаразной активности во время роста в YT-среде
Для экспрессии
внеклеточной амилосахаразной активности E.coli трансформировали вектором pNB2 в соответствии со стандартными методиками. YT-среду (100 мкг/мл ампициллина; 5%-ная сахароза) инокулировали колонией
трансформированного штамма. Клетки инкубировали в течение ночи при 37oС при постоянном перемешивании (роторный смеситель; 150-200 об/мин). Продукты реакции, катализируемой амилосахаразой,
обнаруживали путем добавления раствора Люголя к супернатанту культуры, что приводило к окрашиванию в голубой цвет.
(в) Обнаружение амилосахаразной активности в супернатантах культуры
трансформированных клеток E.coli, которые культивировали без сахарозы
Для экспрессии внеклеточной амилосахаразной активности клетки E.coli трансформировали вектором pNB2 в соответствии со
стандартными методиками. YT-среду (100 мг/мл ампициллина) инокулировали колонией трансформированного штамма. Клетки инкубировали в течение ночи при 37oС при постоянном перемешивании
(роторный смеситель; 150-200 об/мин). Затем клетки отделяли путем центрифугирования (30 мин, 4oС, 5500 об/мин, ротор JA10 фирмы Beckmann). Супернатант фильтровали через фильтр с размером
пор 0,2 мкм (Schleicher & Schuell) в стерильных условиях.
Обнаружение амилосахаразной активности проводили путем:
(I) инкубирования супернатанта на агаровом планшете с
добавлением сахарозы. В одну лунку в агаровом планшете (5%-ная сахароза в 50 мМ натрий-цитратном буфере, рН 6,5) помещали 40 мкл супернатанта и инкубировали по крайней мере в течение 1 часа при 37oС. Продукты реакции, катализируемой амилосахаразой, обнаруживали с помощью окрашивания парами йода. Присутствующие продукты реакции дают голубую окраску.
(II) или путем электрофоретического разделения протеинов в супернатантах в нативном геле и обнаружения продуктов реакции в геле после инкубирования с сахарозой. Разделяли 40-80 мкл супернатанта с помощью гель-электрофореза на 8%-ном нативном полиакриламидном геле (0,375 М Трис, рН 8,8) при напряжении 100 вольт. Затем гель дважды уравновешивали в течение 15 минут с помощью приблизительно 100 мл 50 мМ натрий-цитратного буфера (рН 6,5) и инкубировали в течение ночи при 37oС в натрий-цитратном буфере с рН 6,5/5%-ной сахарозе. Чтобы визуализировать реакционный продукт катализируемой амилосахаразой реакции гель промывали раствором Люголя. Полосы, имеющие амилосахаразную активность, окрашивались в голубой цвет.
Пример 4
Получение глюканов in vitro с
помощью частично очищенной амилосахаразы
Для экспрессии внеклеточной амилосахаразной активности клетки E.coli трансформировали вектором pNB2 в соответствии со стандартными методиками.
YT-среду (100 мг/мл ампициллина) инокулировали колонией трансформированного штамма. Клетки инкубировали в течение ночи при 37oС при постоянном перемешивании (роторный смеситель; 150-200
об/мин). Затем клетки отделяли путем центрифугирования (30 мин, 4oС, 5500 об/мин, ротор JA10 фирмы Beckmann). Супернатант фильтровали через фильтр с размером пор 0,2 мкм (Schleicher &
Schuell) в стерильных условиях.
Затем супернатант концентрировали, уменьшая объем в 200 раз, с использованием камеры Amicon (мембрана типа YM30 с размером эксклюзии 30 кДа, компания Amicon) при избыточном давлении (p=3 бар). Концентрированный супернатант добавляли к 50 мл раствора сахарозы (5%-ная сахароза в 50 мМ натрий-цитратном буфере с pH 6,5). Весь раствор инкубировали при 37oC. При этом образуются белесые нерастворимые полисахариды.
Пример 5
Характеризация продуктов реакции, синтезированных с помощью амилосахаразы из примера 4
Нерастворимые продукты реакции, описанные в примере 4, растворимы в 1М NaOH. Продукты реакции характеризовали путем измерения максимума абсорбции. Приблизительно 100 мг выделенных продуктов
реакции (масса в сыром состоянии) растворяли в 200 мкл 1 М NaOH и разбавляли водой в соотношении 1:10. К 100 мкл этого разбавленного раствора добавляли 900 мкл 0,1 М NaOH и 1 мл раствора Люголя.
Абсорбционный спектр измеряли в диапазоне от 400 до 700 нм. Максимум соответствует 605 нм (максимум абсорбции амилозы: приблизительно 614 нм).
Анализ реакционной смеси, полученной в примере 4, с помощью ЖХВД на колонке CARBOPAC PA1 (фирма DIONEX) показал, что кроме нерастворимых продуктов также образуются растворимые продукты. Эти растворимые продукты предствляют собой полисахариды с короткой цепью. Длина цепи составляла от приблизительно 5 до приблизительно 60 остатков глюкозы. Также можно было обнаружить, хотя и в меньшем количестве, даже более короткие или более длинные молекулы.
Доступные аналитические методы не позволили обнаружить разветвление в продуктах синтеза.
Пример 6
Экспрессия внутриклеточной
амилосахаразной активности в трансформированных клетках E.coli
Применяя полимеразно-цепьевую реакцию (ПЦР) амплифицировали фрагмент плазмиды pNB2, содержащий нуклеотиды с 981 по 2871
последовательности, представленной в SEQ ID No.1. В качестве праймеров использовали следующие олигонуклеотиды:
TPN2 5'-CTC ACC ATG GGC ATC TTG GAC ATC-3' (SEQ ID No.3);
ТРС1 5'-CTG
CCA TGG TTC AGA CGG CAT TTG G-3' (SEQ ID No.4).
Образовавшийся фрагмент содержит кодирующую область для амилосахаразы за исключением нуклеотидов, кодирующих 16 N-концевых аминокислот. Эти аминокислоты включают последовательности, необходимые для выделения фермента из клетки. Кроме того, этот ПЦР-фрагмент содержит 88 пар оснований 3'-нетранслируемой области. С помощью использованных праймеров сайты рестрикции NcoI вводили в оба конца фрагмента.
После разложения с помощью рестрикционной энедонуклеазы NcoI образовавшийся фрагмент лигировали с разложенным с помощью NcoI вектором экспрессии рМех 7. Продукты лигирования трансформировали в клетках E.coli и отбирали трансформированные клоны. Позитивные клоны инкубировали в течение ночи при 37oС на YT-планшетах (1,5%-ный агар; 100 мкг/мл ампициллина; 5%-ная сахароза; 0,2 мМ ИПТП). После воздействия на планшеты паров йода в области, окружающей бактериальные колонии, не было обнаружено никакого голубого окрашивания, но можно было обнаружить образование гликогена внутри клеток (коричневое окрашивание трансформированных клеток в противоположность неокрашенным нетрансформированным клеткам XL1-Blue). Чтобы оценить функциональные свойства протеина, трансформированные клетки, которые выращивали на YT-среде, разрушали ультразвуком, а полученный неочищенный экстракт вносили с помощью пипетки на агаровые планшеты, содержащие сахарозу. После обработки планшетов парами йода можно было обнаружить голубое окрашивание.
Реферат
Изобретение относится к генной инженерии и может быть использовано для получения растений, грибов и микроорганизмов, обогащенных линейными α-1,4-глюканами. Последовательности ДНК, кодирующие протеин, обладающий ферментативной активностью амилосахаразы, и сцепленные с регуляторными последовательностями, вводят в клетки прокариот или эукариот. Из клеток растений затем регенерируют целые растения, в которых синтез линейных α-1,4-глюканов протекает более интенсивно, чем в нетрансформированных растениях. Экспрессированные α-1-4-глюконы и/или фруктозу затем выделяют из организма хозяина. 10 с. и 7 з.п.ф-лы, 2 ил.
Формула
18.05.1994 - по п.1, в части признаков (а) и (б); 3-13, 15, 14 и 16, в части, касающейся α-1,4-глюканов, и п.17;
22.12.1994 - по п.1, в части признаков (в)-(д); 2, 14 и 16, в части, касающейся фруктозы.

Комментарии