Моно- или диацилфосфиноксиды - RU2057759C1
Код документа: RU2057759C1
Чертежи


Описание
Изобретение относится к моно- и диацилфосфиноксидам, а также к их применению в качестве фотоинициаторов фотополимеризации этиленненасыщенных соединений.
Известны
моноацилфосфиноксиды, которые могут использоваться в качестве фотоинициаторов (см.
европейский патент А-7508) [1] Бисацилфосфиноксиды и их применение в качестве фотоинициаторов описано в европейском
патенте А-184095 [2] Авторами изобретения получены новые моно- и бисацилфосфиноксиды,
отличающиеся от известных соединений наличием у них определенных заместителей. При этом имеются в виду соединения
формулы I


-X-

R3 С1-С18-алкил, С2-С6-алкенил, фенилвинил, одно- или многозамещенный фенилом, С2-С5-алкоксикарбонилом, галоге- ном, С1-С12-алкокси-, фенокси-, С1-С12 -алкилтио- и/или фенилтио-группами С1-С8-алкил, незамещенный или замещенный С1-С12 -алкилом, фенилом, фенокси-, С1-С12 -алкокси-группами, С2-С5-алкоксикарбонилом, С1-С4-алкилтио-группой и/или галогеном С5 -С10-циклоалкил, незамещенный или многозамещенный С1-С12-алкилом, С1-С12-алкокси-группой, С1-С12-алкоксиалкилом, С1-С4-алкилтио-группой и/или галогеном С6-С12-арил или содержащий один или несколько атомов О, S или N 5- или 6-звенный одновалентный гетероциклический остаток, который может быть одно- или многозамещенным галогеном, С1-С4-алкилом или С1-С4-алкокси-группой, а
R4 С1-С18-алкил, фенил-С1-С4-алкил, С5-С8-циклоалкил или С6-С10-арил, при условии, что по меньшей мере один из остатков R1, R2 и R3 означает замещенный алкил или R1 и R2 вместе с атомом фосфора образуют би- или трициклическое кольцо, или R3 означает замещенный циклоалкил, в котором однако, алкильные остатки не могут быть единственными заместителями.
R1, R2, R3 и R4 в значении С1-С15-алкил могут быть прямыми или разветвленными и могут означать, например, метил, этил, пропил, изопропил, н-бутил, втор-бутил, трет-бутил, пентил, гексил, гептил, октил, 2-этилгексил, 2,4,4-триметилфенил, децил, додецил, тетрадецил, гептадецил или октадецил.
R3 в значении алкил предпочтительно является третичным алкилом, например, трет-бутилом, 1,1-диметилпропилом, 1,1-диметилбутилом или 1,1, 3,3-тетраметилбутилом.
R1 и R2 в значении С2-С18-алкенил могут означать, например, винил, аллил, металлил, 1,1-диметилаллил, 2-бутенил, 2-гексенил, октенил, ундеценил, додеценил или октадеценил. R4 в значении С2-С18-алкенил может означать, кроме того, винил.
R3 в значении С2-С6 -алкенил может означать, например, винил, пропенил или бутенил.
R1 и R2 в значении одно- или многозамещенного, например, одно-трех-, предпочтительно одно-двухзамещенного С1-С8-алки- ла, могут означать, например, бензил, 1-фенилэтил, 2-фенилэтил,α,α-диметилбензил, бенгидрил, п-толилметил, 1-(п-бутилфе- нил)-этил, п-хлорбензил, 2,4-дихлорбензил, п-метоксибензил, м-этоксибензил, 2-цианоэтил, 2-цианопропил, 2-метоксикарбонилэтил, 2-бутоксикарбонилпропил, 1,2-ди(ме- токсикарбонил)-этил, 2-метоксиэтил, 1, 3-диоксолан-2-ил, 1,3-диоксан-2-ил, 2-метил-1,3-диоксолан-2-ил, 4-метил-1,3-диоксолан-2- ил, 2-изопропоксиэтил, 2-бутоксипропил, 2-октилоксиэтил, хлорметил, 2-хлорэтил, трихлорметил или трифторметил, предпочтительно бензил.
R3 в качестве одно- или многозамещенного, например, одно-трех-, предпочтительно одно-двухзамещенного С1-С8 -алкила может означать, например, бензил, фенилэтил, α,α-диметилбензил, бензгидрил, 1,1-дихлорэтил, трихлорметил, трифторметил, 1,1-диметил-2-хлорэтил, 2-метоксиизопропил, 2-этоксиэтил, бутилтиометил, 2-додецилтиоэтил или 2-фенилтиоэтил.
R4 в качестве одно- или многозамещенного, например, одно-трех-, предпочтительно одно-двухзамещенного С1-С8 -алки- ла, может означать, например, бензил, 2-фенилэтил, 3-фенилпропил, 2-метоксиэтил, 2-бутоксиэтил, 2-гексилоксиэтил, 2-изопро- поксипропил, 2-хлорэтил или 2,2,2-трифторэтил.
R1, R2, R3 и R4 в качестве С5-С8-циклоалкила могут означать, например, циклопентил, циклогексил или циклооктил. R3 в качестве замещенного, например, одно-четырехзамещенного С5-С10-циклоалкила может означать, например, метилциклопентил, диметилциклопентил, метилциклогексил, диметилциклогексил, диэтилцик- логексил, бутилциклогексил, метоксициклогексил, диметоксициклогексил, диэтоксициклогексил, бутилтиоциклогексил, хлорциклогексил, дихлорциклогексил или дихлорциклопентил, а также насыщенную или ненасыщенную бициклическую систему, такую как, например, норборнил или норборненил.
R1, R2, R3 и R4 в качестве С6-С12-арила могут означать, например, фенил, α-нафтил, β-нафтил или 4-дифенилил, в частности, фенил. R1, R2 и R3 в качестве замещенного С6 -С12-арила могут означать, например, хлорфенил, дихлорфенил, трихлорфенил, дифторфенил, толил, этилфенил, третбутилфенил, додецилфенил, метоксифенил, диметоксифенил, этоксифенил, гексилоксифенил, метилнафтил, изопропилнафтил, хлорнафтил или этоксинафтил. R3 в качестве замещенного арила может, кроме того, означать, например, метоксиэтилфенил, этоксиметилфенил, метилфенил, изопропилтиофенил или третбутилтиофенил. Предпочтительным замещенным арилом также является замещенный фенил.
R1, R2 и R3 в качестве гетероциклического остатка могут означать, например, фурил, тиенил, пиррил, пиридил, индолил, бензоксазолил, диоксолил, диоксил, бензимидазолил или бензтиазолил. Предпочтительно такой гетероциклический остаток содержит 3-12, в частности, 3-5 атомов углерода. Замещенным (например 1-3, предпочтительно одним или двумя заместителями) гетероциклическими остатками являются, например, диметилпиридил, метилхинолил, диметилпиррил, метоксифурил, диметоксипиридил или дифторпиридил.
Х в качестве С1-С8-алкилена может означать, например, метилен, 1, 2-этилен, 2,2-диметил-1,3-пропилен, три-, тетра-, пента- и гексаметилен или фенилметилен.
В том случае, если R1 и R2 вместе с атомом Р образуют моноциклическое кольцо, то предпочтительно им является фосфациклопентановое кольцо.
В том случае, если R1 и R2 вместе с атомом Р образуют бициклическое кольцо, то предпочтительно им является фосфабициклогексановое или фосфабициклононановое кольцо.
В том случае, если R1 и R2 вместе с атомом Р образуют трициклическое кольцо, то предпочтительно им является (6Н)-дибенз-[c,e] [1,2]-оксафосфорное кольцо.
Предпочтительным являются те из соединений формулы I, у которых R1 означает С1-С12-алкил, одно-трехзамещенный фенилом, (С1-С4-алкил)-фенилом, хлорфенилом, (С1-С4-адкокси)-фенилом и/или С1-С4-алкокси-группой
С1-С4-алкил, циклогексил, С6-С10-арил или одно-трехзамещенный хлором, С1-С12-алкилом и/или С1-С4
-алкокси-группой
С6-С10-арил или содержащий один или несколько атомов О, S или N 5- или 6-звенный одновалентный гетероциклический остаток; R2 имеет те же значения,
что и R1,
или означает остаток -СО- R3 или -ОR4, или R1 и R2 или R1 и R4 вместе с атомом Р образуют моно- или
бициклический остаток с 4-8
атомами углерода; R3 означает С1-С8-алкил, одно- или двухзамещенный фенилом, С1-С4-алкокси-группой, С2
-С5-алкоксикарбонилом
и/или хлором С1-С6-алкил, незамещенный или замещенный фенилом, С1-С4-алкокси-группой, С2-С5
-алкоксикарбонилом и/или хлором С5-С6-циклоалкил, С6-С10-арил или одно-трехзамещенный С1-С12-алкилом, С1-С4
-алкокси-группой и/или хлором С6
-С10-арил, а R4 С1-С8-алкил, циклогексил, бензил или фенил, предпочтительно, у которых R1 означает
С1-С8-алкил, одно- или
двухзамещенный фенилом, (С1-С4-алкил)-фенилом или С1-С4-алкокси группой С1-С4-алкил,
циклогексил,
фенил или
одно-трехзамещенный С1-С4-алкилом или С1-С4-алкокси-группой фенил; R2 имеет те же значения, что и R1,
или означает остаток -СО-R3 или -ОR4, или R1 и R2 или R1 и R4 вместе с атомом Р образуют моно- или бициклическое кольцо; R3
означает незамещенный или
замещенный фенилом, хлором и/или С1-С4-алкокси-группой С1-С6-алкил, незамещенный или замещенный фенилом, С1-С4- алкокси-группjq, С2-С5-алкоксикарбонилом и/или хлором С5-С6- циклоалкил, фенил или одно-трехзамещенный С1-С4-алкилом, С1-С4
-алкокси-группой и/или хлором фенил, а R4 С1-С4-алкил, циклогексил или фенил.
Предпочтительно R1 означает замещенный алкил в соответствии с указанным определением, в частности, одно-двух- замещенный (С1-С4-алкил)-фенилом, фенилом или С1-С4-алкокси-группой С1 -С4-алкил, наиболее предпочтительно бензил.
R3, в частности, означает фенил, замещенный в обоих ортоположениях С1-С4-алкилом, С1 -С4 -алкокси-группой или хлором.
Предпочтительным далее являются бициклические соединения формулы II или III
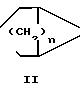


Примерами соединений формулы I являются: дибензил-(2,4,6-триметилбензил)-фосфиноксид; бис(2-фенилэтил)-(2,6- дихлорбензоил)-фосфиноксид; бис(2-фенилпропил)-(2,6-диметоксибензоил)-фосфинок- сид; бис(2-фенилпропил)-(2,4,6-триметилбензоил)-фосфиноксид; бис(2-цианоэтил)-(2,4,6-триметилбензоил)-фосфиноксид; метиловый эфир 2-фенилпропил-(2, 4, 6-триме- тилбензоил)-фосфиновой кислоты; 6-бис(хлорметил)пропионил-(6Н)-дибенз[c,e][1,2] оксафосфорин-6-оксид; метиловый эфир фенил-(2,2-диметил-3-фенилпропионил)-фосфиновой кислоты; дифенил-(2, 2-диметил-3-финилпропионил)-фосфиноксид; дифенил-2,6-диметоксициклогексаноил-фо- сфиноксид; дибутил-(2-метил-2-фенилбутирил)-фосфиноксид; бутил-1,1-диэтоксиэтил-2,4,6-триметилбезоил-фосфиноксид; бис(циклогексил)-(2-метил-2-фенилтиопро- пионил)-фосфиноксид; дифенил -(2-октилокси-2-фенилпропионил)-фосфиноксид; 1-(2,6-диметилбензоил)-фосфолан-1-оксид; 6-(2,6-дихлорбензоил)-6-фосфабицикло[2.1.1] гексан-6-оксид; 9-(2,6-дихлорбензоил)-9-фосфабицикло[3.3.1]нонан-9-оксид; 9-(2.4.6-триметилбензоил)-9-фосфабицикло[4,2,1] но- нан-9-оксид; бис(2,6-дихлорбензоил)-2-фенилпропилфосфиноксид; бис(2, 6-диметоксибензоил)-бензилфосфиноксид; бис(2,6-диме- токсибензоил)-2-фенилпропилфосфиноксид; бис(2,6-диметоксибензоил)-2-фенилэтилфос- финоксид; бис(2,6-дихлорбензоил)-бензилфосфиноксид; бис(2, 6- дихлорбензоил)-2-фенилэтилфосфиноксид; бис(2,4,6-триметилбензоил)-бензилфосфи- ноксид; бис(2,4,6-триметилбензоил)-2-фенилпропилфосфиноксид; бис(2,4,6-триметилбензоил)-2-фенилэтилфосфиноксид; бис(2, 4,6-триметилбензоил)-2-цианоэтилф- осфиноксид; бис(2,6-дихлорбензоил)-2-цианоэтилфосфиноксид; бис(2,6-диметоксибензоил)-2-цианоэтилфосфиноксид; бис(2-метилтиобензоил)-2-фенилпропилфо- сфиноксид; бис(2-метил-1-нафтоил)-2-фенилпропилфосфиноксид; бис(2-метил-2-фенилпропионил)-циклогексилфосфиноксид; бис(2-метил-2-фенилбутирил)-фенилфосфи- ноксид; бис(2,2-диметил-4-фенилбутирил)-фенилфосфиноксид; бис(2-метокси -2-фенилбутирил)-4-пропилфенилфосфиноксид; бис(2-метилтио-2-фенилбутирил)- циклогексилфосфиноксид; бис(2-метил-2-фенилтиопропионил)-2-фенилпропилфосфиноксид; бис(2-метил-2-фенилбутирил)-2-фенилпро-пилфосфиноксид; бис(2-метил-2,-фенилбутирил)-2-циклогексилфосфиноксид; (2,6-дихлорбензоил)-(1,3-диоксолан-2-ил)-фенил- фосфиноксид; дифенил-(3-фенил-бицикло[2.2.1] гепт-5-ен-2-илкарбонил)-фосфинок- сид; дифенил(2-метил-3-фенил-бицикло[2.2.1] гептан-2-илкарбонил)-фосфиноксид; 2,4,6-триметилбензоил-бензил-бути- лфосф- иноксид; 2, 6-дихлорбензоил-бензил-бутирилфосфиноксид; 2,6-диметоксибензоил-бензил-бутилфосфиноксид; 2,6-диметоксибензоил-бензил-октилф-осфиноксид; 2,6-дихлоррбензоил-бензил-октилфосфиноксид; 2,4, 6-триметилбензоил-бензил-октилфосфиноксид; 2,4,6-триме-тилбензоил-бензил-метилфос- финоксид; 2,4,6-триметилбензоил-бензил-циклогексилфосфиноксид; 2,6-дихлорбензоил-бензил-циклогексилфосфиноксид; 2, 6-диметоксибензоил-бензил-циклогекси- лфосфиноксид.
Соединения формулы I, в которых R2 означает остаток -ОR4, могут быть получены по реакции Арбузова-Михайлиса,
при взаимодействии соответствующего фосфонита формулы IV с хлорангидридом карбоновой кислоты формулы V по следующей схеме:
R1-



Реакцию можно проводить в среде растворителя или без него. В том случае, если исходные реагенты IV и V являются жидкими, предпочтительно реакцию проводить без использованиями растворителя. Подходящими растворителями являются прежде всего углеводороды, например, алканы и их смеси, бензол, толуол или ксилол. Предпочтительно реакцию проводить при 20-120оС. Образующийся R4Cl предпочтительно отгонять в ходе реакции. При использовании растворителя его отгоняют в конце реакции. Полученный сырой продукт может быть очищен, например, с помощью перегонки, кристаллизации или хроматографии.
Фосфониты формулы IV могут быть получены известным образом, путем взаимодействия дихлорфосфина R1-PCl2 с как минимум 2 молями R4ОН в присутствии акцептора НСl (см. Houben-Weyl, Methoden d. Org. Chemie XII/1, 324-327 (1963), Штутгарт).
Соединения формулы I, в которых R2 означает остаток -СОR3, могут быть получены путем двойного
ацилирования первичного фосфина формулы VI по меньшей мере двумя эквивалентами хлорангидрида кислоты формулы V в присутствии по меньшей мере двух эквивалентов основания и последующего окисления
образующегося диацилфосфина формулы VII до фосфиноксида по следующей схеме



В качестве основания можно использовать, например, третичные амины, щелочные металлы, диизопропиламид лития, алкоголяты или гидриды щелочных металлов. Первую стадию предпочтительно проводят в среде растворителя. В качестве растворителей можно использовать в первую очередь углеводороды, например, алканы, бензол, толуол или ксилол. После отделения образующегося хлорида основания фосфин VII можно выделить путем упаривания реакционной смеси или же вторую стадию проводят не отделяя VII, а используя раствор сырого продукта. В качестве окислителя для осуществления второй стадии можно использовать прежде всего перекись водорода и органические перекисные соединения, например, надуксусную кислоту.
Используемые в качестве исходного материала первичные фосфины формулы VI являются известными соединениями или они могут быть получены аналогично известным соединениям (см. Houben Weyl, Methoden der Org. Chemie XII/1, 60-63 (1963), G. Thieme Verlag, Штутгарт).
Соединения формулы I, у которых R2 не является ни одним из остатков -ОR4 или -СОR3, могут быть получены путем ацилирования
вторичных фосфинов формулы VIII и последующего окисления по схеме:



Исходные фосфины формулы VIII могут быть получены известными методами, например, путем восстановления монохлорфосфинов (R1) (R2) PCl и AlH4 (см. Ноuben Weyl, Methoden der Org. Chemie XII/1, 60-63 (1963), G. Thieme Verlag, Штутграт).
По другому варианту эти соединения могут быть получены по реакции Арбузова-Михаэлиса, путем взаимодействия фосфинитов формулы IX c V
по следующей схеме:



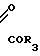
В этой схеме R5 означает алкил.
Исходные соединения формулы IX могут быть получены известными методами, например, путем алкоголиза монохлорфосфинов (R1) (R2) PCl спиртом R5ОН в присутствии основания (см. Ноuben Weyl, Methoden d. Org. Chemie XII/1, 208-210 (1963), G. Thieme Verlag, Штутгарт).
В соответствии с изобретением соединения формулы I могут использоваться в качестве фотоинициаторов фотополимеризации этиленненасыщенных соединений или смесей, содержащих такие соединения. Такие ненасыщенные соединения могут содержать одну или несколько олефиновых двойных связей. Они могут быть низкомолекулярными (мономеры) или высокомолекулярными (олигомеры). Примерами мономеров с одной двойной связью являются алкил или оксиалкилакрилаты или алкил- или оксиалкилметакрилаты, такие как метил-, этил-, бутил-, 2-этилгексил- или 2-оксиэтилакрилаты, изоборнилакрилат, метил- или этилметакрилаты. Другими примерами таких соединений являются акрилнитрил, акриламид, метакриламид, N-замещенные (мет)акриламиды, виниловые эфиры, такие как винилацетат, простые виниловые эфиры, например, изобутилвиниловый эфир, стирол, алкил- и галогенстиролы, N-винилпирролидон, винилхлорид или винилиденхлорид.
Примерами мономеров с несколькими двойными связями являются этиленгликоль-, пропиленгликоль-, неопентилгликоль-, гексаметиленгликоль- или бисфенил-А- диакрилаты, 4, 4'-бис(2-акрилоил-оксиэтокси)-дифенилпропан, триметилолпропан- триакрилат, пентаэритриттриакрилат, пента- эритриттетраакрилат, винилакрилат, дивинилбезол, дивинилсукцинат, диаллил- фталат, триаллилфосфат, триаллилизоцианурат или трис-(2-акрилоилэтил)изоцианурат.
Примерами высокомолекулярных (олигомерных) соединений со многими ненасыщенными связями являются акрилированные эпоксидные смолы, акрилированные полиуретаны или акрилированные полиэфиры. Другими примерами ненасыщенных олигомеров являются ненасыщенные полиэфирные смолы, получаемые обычно из малеиновой, фталевой кислот и одного или нескольких диолов, имеющих мол.м. примерно 500-3000. Такие ненасыщенные олигомеры можно назвать также предполимерами.
Часто используют двухкомпонентные смеси предполимера с мономером с несколькими ненасыщенными связями или трехкомпонентные смеси, которые кроме того содержат еще мономер с одной ненасыщенной связью. Предполимер в этом случае определяет в первую очередь свойства образующейся лаковой пленки. Подбирая тот или иной предполимер, специалист может изменять свойства отверждаемой пленки. Мономеры с несколькими ненасыщенными связями играют роль сшивателя, который делает пленку нерастворимой. Мономер с одной ненасыщенной связью играет роль реакционноспособного разбавителя, с помощью которого можно снизить вязкость без использования растворителя.
Такие двух- трехкомпонентные системы на основе предполимеров используют при получении печатных красок, а также лаков, фоторезисторов или других фотоотверждаемых масс. В качестве связующих для печатных красок применяются также однокомпонентные системы на основе фотоотверждаемых преполимеров.
Ненасыщенные полиэфирные смолы чаще всего применяются в двухкомпонентных системах в комбинации с ненасыщенными мономерами с одной связью, предпочтительно со стиролом. Для получения фоторезисторов часто применяются специальные однокомпонентные системы, например, полималеинимиды, полихалконы или полиимиды.
Ненасыщенные соединения могут применяться также в смеси с нефотополимеризующимися пленкообразующими компонентами. Это могут быть, например, физически высыхающие полимеры или их растворы в органических растворителях, также как нитроцеллюлоза или ацетобутиратцеллюлоза. К таким компонентам относятся также химически или термически отверждающиеся смолы, такие, как, например, полиизоцианаты, полиэпоксидные или меламиновые смолы. Использование в таких комбинациях термически отверждаемых смол играет важную роль при применении так называемых гибридных систем, которые на первой стадии фотополимеризуются, а на второй стадии сшиваются с помощью дополнительной термической обработки.
Фотополимеризующиеся смеси помимо фотоинициатора могут содержать также различные добавки. Примерами таких добавок являются термические ингибиторы, назначение которых состоит в предотвращении преждевременной полимеризации, в частности, гидрохинон или стерически затрудненные фенолы. Для повышения стабильности при хранении в темноте можно использовать, например, соединения меди, фосфора, четвертичные аммониевые основания или производные гидроксиламина. Для исключения влияния в процессе полимеризации кислорода воздуха можно добавлять парафин или аналогичные воскообразные материалы, которые в начале полимеризации выходят на поверхность. В качестве фотостабилизаторов можно добавлять небольшие количества УФ-абсорберов, например, типа бензтриазола, бензофенона или оксаланилида. Еще более эффективными являются добавки фотостабилизаторов, не абсорбирующих УФ, таких как стерически затрудненные амины (НАLS).
В некоторых случаях может оказаться целесообразным применять смеси двух или нескольких фотоинициаторов в соответствии с изобретением. Разумеется, можно применять также смеси с известными фотоинициаторами, например смеси с бензофеноном, производными ацетофенона, бензиновыми эфирами или бензилкеталями.
Для ускорения фотополимеризации можно применять добавки аминов, например, триэтаноламина, N-метилдиэтаноламина, этилового эфира п-диметиламинобензойной кислоты или кетона Мехлера. Действие аминов можно усилить путем добавки ароматических кетонов типа бензофенона.
Ускорения фотополимеризации можно добиться также путем добавки фотосенсибилизаторов, смещающих или расширяющих спектральную чувствительность. Такими добавками являются, в частности, ароматические карбонильные соединения, такие как, например, производные бензофенона, тиоксантона, антрахинона и 3-ацилкумарина, а также 3-(ароилмети- лен)-тиазолины.
Другими обычно используемыми добавками в зависимости от целей применения являются наполнители, пигменты, красители, смачиватели или вспомогательные средства, способствующие растеканию.
Соединения использованы в фотополимеризующихся композициях, содержащих: (а) по меньшей мере одно этиленненасыщенное соединение и (в) в качестве фотоинициатора по меньшей мере одно соединение формулы I, причем такие композиции могут содержать кроме того и другой фотоинициатор и/или другие добавки.
Содержание фотоинициатора (в) в заявляемых фотополимеризующихся композициях предпочтительно составляет 0,05-15, наиболее предпочтительно 0,2-5 мас. в расчете на массу композиции.
Заявляемые фотополимеризующиеся композиции могут использоваться для различных целей, например в качестве печатных красок, белой эмали, пигментированных лакокрасочных материалов, красок для наружных работ, для получения фоторепродукций, фотоизображений или печатных плат, в качестве масс для зубных пломб, клеящих веществ, покрытий оптических волокон, для печатных схем или для нанесения покрытий на электронные детали.
Полимеризацию осуществляют известными методами фотополимеризации, путем облучения солнечным светом или светом с большим содержанием коротковолнового излучения. В качестве источников облучения можно использовать, например ртутные излучатели высокого, среднего и низкого давления, суперактиновые люминисцентные лампы или лазеры, максимум излучения которых находится в интервале 250-450 нм. В случае комбинаций фотосенсибилизаторов можно использовать также источники света с большей длиной волны или лазерное излучение с длиной должны до 600 нм.
В следующих примерах, если это не оговорено, приведенные части и проценты, как в описании и формуле изобретения, являются массовыми.
П р и м е р 1. Получение бис(2-фенилпропил)-(2,6-диметоксибензоил)-фосфинокс- ида.
К раствору 1,1 г (0,011 моль) диизопропиламина в 10 мл абсолютного тетрагидрофурана (ТГФ) добавляют по каплям в течение 10 мин в атмосфере аргона при 0оС 6,9 мл (0,011 моля 1,6 М) бутиллития. Этот раствор при (-20)-(-30)оС добавляют по каплям в течение примерно 40 мин к раствору 2,2 г (0,011 моль) 2, 6-диметоксибензоилхлорида и 2,7 г (0,01 моль) бис(2-фенилпропил)-фосфина в 20 мл абсолютного ТГФ. После перемешивания в течение 2 ч при -30оС желтый раствор нагревают до комнатной температуры, разбавляют 100 мл толуола и промывают один раз водой и один раз насыщенным раствором бикарбоната натрия. Органическую фазу высушивают над сульфатом магния, фильтруют и концентрируют в ротационном выпарном аппарате. Остаток растворяют в 40 мл ацетонитрила и смешивают с 1,1 г (0,01 моль) 30%-ной перекиси водорода. После перемешивания в течение 1 ч при 50оС реакционную смесь разбавляют толуолом, промывают рассолом и насыщенным раствором карбоната натрия, высушивают с помощью сульфата магния и упаривают в ротационном выпарном аппарате. После очистки с помощью хроматографии (элюент:смесь гексана и уксусного эфира в соотношении 1: 1) получают 3,1 г (68,9% от теоретического выхода) целевого соединения в виде маслянистой жидкости.
Вычислено, C 71,98; H 6,94.
Найдено, С 71,45; Н 7,05.
П р и м е р 2. Получение бис(2-фенилпропил)-(2,4,6-триметилбензоил)-фосфинок-сида.
Указанный фосфиноксид получают аналогичным описанному в примере 1 способом.
Вычислено, С 77,75; Н 7,69.
Найдено, С 77,24; Н 7,72.
П р и м е р 3. Получение дифенил-[2, 2-бис(хлорметил)пропионил]-фосфиноксида 3,9 г (0,02 моль) дихлорпропионилхлорида добавляют к 20 мл толуола и нагревают смесь до 80оС. В течение примерно 5 мин к полученному раствору добавляют по каплям 4,3 г (0,02 моль) метоксидифенилфосфина, причем при этом отгоняется метилхлорид. После перемешивания в течение 1 ч при 80оС желтоватый раствор охлаждают по комнатной температуры и упаривают в ротационном выпарном аппарате. После хроматографической очистки (элюент:смесь гексана и уксусного эфира в соотношении 3:1) получают 1,6 г (22,8% от теоретического выхода) целевого соединения в виде желтой смолы.
Вычислено, C 57,48; H 4,82; Cl 19,96.
Найдено, С 57,37; Н 5,16; Сl 18,84.
П р и м е р 4. Получение этокси-(2, 6-диметоксибензоил)-(диэтоксиметил)-фосфиноксида.
Указанное соединение получают аналогичным описанному в примере 3 способом. Полученное соединение имеет температуру плавления 81оС.
Вычислено, С 53,33; Н 6,99; Р 8,60.
Найдено, С 53,15; Н 6,94; Р 9,24.
П р и м е р 5. Получение дифенил-[1,2, 2-триметил-3-метоксикарбонил)-циклопент-1-ил]-фосфиноксида.
Указанное соединение получают аналогичным описанному в примере 3 способом. Полученное соединение представляет собой маслянистую жидкость (выход 28,2% от теоретического).
Вычислено, C 69,33; Н 6,83.
Найдено, С 69,75; Н 6, 87.
П р и м е р 5а. Получение бис(2,
6-диметоксибензоил)-бензилфосфиноксида
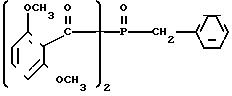
Точка плавления: 193-194оС
Вычислено, С 64,10; Н 5,
38.
Найдено, С 64,16; Н 5,40.
П р и м е р 5b. Получение бис(2,
6-дихлорбензоил)-бензилфосфиноксида

Точка плавления 149-151оС.
Вычислено, C 51,89; H 2,70; Cl 29,17.
Найдено, С 51, 82; Н 2,80; Сl 28,94.
П р и м е р 5с. Получение бис(2,4,
6-триметилбензоил)-бензилфосфиноксида


Вычислено, С 74,92; Н 6,76.
Найдено, С 73, 90; Н 6,89.
П р и м е р 5d.

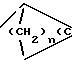
(I): n 4, m 2
(II): n 3; m 3 К 20,7 г (0,146 моля) смеси изомеров 9Н-9-фосфабицикло[3,3,1] -нонан и 9Н-9-фосфабицикло[4,2,1]-нонан (®Proban фир- мы НOECHST), растворенной в 100 мл абсолютного тетрагидрофурана, добавляют в течение 30 мин при 20-30оС 100 мл (0,16 моля) бутиллития (1,6 молярно в гексане). После этого реакционную смесь нагревают до 40оС и при этой температуре перемешивают в течение 1 ч. При -30оС этот раствор в течение 60 мин добавляют к раствору 29,2 г (0,146 моля) 2,4, 6-триметилбензоилхлорида в 150 мл абсолютного тетрагидрофурана. Для совершенствования превращения, реакционную смесь перемешивают в течение 3 ч. После этого смеси дают нагреваться до комнатной температуры и промывают ее два раза водой и насыщенным раствором бикарбоната. После высушивания органической фазы над сульфатом магния, ее упаривают в вакууме. Остаток растворяют в 200 мл толуола и при перемешивании и охлаждении в течение 20 мин при 20-30оС добавляют по каплям к 16,5 г (0,146 моля) 30% -ной перекиси водорода. Для совершенствования реакции реакционную смесь еще перемешивают в течение 1 ч при той же самой температуре. После этого промывают ее два раза водой и разбавленным раствором бикарбоната. После высушивания над сульфатом магния и фильтрации остаток упаривают в вакууме. Оба изомера выделяют с помощью хроматографии (элемент: смесь гексана и этилового эфира уксусной кислоты в соотношении 4:1) и перекристаллизуют от циклогексана. Получают 10,0 г (22% от теоретического выхода) целевого соединения (I), имеющего точку плавления (82-83оС, и 6,0 г (13,5% от теоретического выхода) целевого соединения (II), имеющего точку плавления 90-91оС.
Соединение I. Вычислено, C 71,03; Н 8,28.
Найдено, С 70,88; Н 8,49.
Соединение II. Вычислено, С 71,03; Н 8,28.
Найдено, С 69,99; Н 8,17.
П р и м е р 5е.


(I): n 4; m 2
(II): n 3; m 3
Соединение примера 5е получают аналогичным к описанному в примере 5а способом получения, причем 2,4,6-триметилбен- зоилхлорид замещают смесью изомеров 9Н-9-фосфабицикло[3,3,1] -нонана и 9Н-9-фосфабицикло[4,2,1]-нонана (®Proban фирмы НОЕСНST). Оба изомерных продуктов реакции выделяют с помощью хроматографии, как описано в примере 5с.
Точки
плавления:
Соединение (I) 127-128оС
Соединение
(II) 163-164оС
Результаты элементарного анализа:
Соединение (I) Вычислено, С 63,35; Н 7,19.
Найдено, С 63,22; Н 7,11.
Соединение (II) Вычислено, С 63,35; Н 7,19.
Найдено, С 63,14; Н 7,13.
П р и м е р 5f. Получение
9-пивалоил-9-фосфабицикло[4,2,1]нонан-9-оксида (I) и 9-пивалоил-9-фосфабицикло[3,3,
1]нонан-9- оксида (II)
CH3-

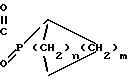
(I): 4,0 г (16,5% от теоретического выхода) в виде воскообразного продукта.
(II): 7,3 (30,2% от теоретического выхода) в виде белого порошка, имеющего точки плавления 77-78оС.
П р и м е р 6. Реакционная способность инициатора в покровном слое из белой эмали.
30 ч. H7C

15 ч. триметилолпропантрисакрилата
5 ч. N-винилпирролидона
50 ч. диоксида титана (рутия)
Полученную белую эмаль перемешивают с двумя массовыми процентами испытуемого инициатора и приготовленную композицию наносят слоем толщиной 100 мкм на алюминиевую жесть, предварительно загрунтованную белой Соil Coat-эмалью. Образцы отверждают, облучая их ртутной лампой среднего давления (Наnovia 30 Вт/см). Отверждение происходит после высыхания нижний стороны отделенной пленки эмали. Реакционную способность определяют по числу проходов под лампой при определенной скорости движения ленты. Кроме того, реакционную способность определяют после предварительного освещения в течение минуты под 5 лампами мощностью 40 Вт (Рhilips TL 03). Сразу же после отверждения и после дополнительного облучения в течение 15 мин или соответственно 16 ч (блеск) под 5 лампами мощностью 40 Вт (Рhilips TL 03) измеряют твердость по маятниковому прибору (по Konig, DIN 53157), пожелтение (индекс пожелтения, А S TM D 1925-70) и блеск при 20 и 60о С (Multiglossgerat, A S TM D 523). Полученные результаты приведены в табл. 1 и 2.
П р и м е р 7.
Реакционная способность в прозрачном лаке.
Прозрачный лак получают из 99,5 ч.

0,5 ч.

Приготовленный лак смешивают с 2 мас. испытуемого инициатора и композицию наносят слоем толщиной 100 мкм на зажимные плиты, покрытые слоем белой синтетической смолы.
Образцы облучают в РРС-приборе ртутной лампой среднего давления (2х60 Вт/см). При этом определяют скорость движения ленты в м/мин, необходимую для получения стойкой к истиранию поверхности. Твердость определяют в единицах твердости по маятниковому прибору по Konig (DIN 53157), а также измеряют пожелтение в единицах индекса пожелтения (A S TM D 1925-70). Полученные результаты приведены в табл. 3.
Примеры использования с сравнительными данными.
П р и м е р 8. Реакционная способность инициатора в белом лаке.
В качестве соединения по уровню техники (ЕР-А 184095)
подвергают испытанию соединение формулы А,
®Ebecryl а в качестве соединений по изобретению испытывают соединения, используемые в примерах 5а, 5b и 5с.
Инициаторы в концентрациях 1 мас. перемешивают с композицией белого лака, состоящей из 67,5 ч.

Образцы наносят ракелем толщиной 100 мкм на зажимные плиты и, с целью их отверждения, направляют 4 раза под ртутной лампой среднего давления (типа Hanovia) при скорости движения ленты 10 м/мин. Твердость по маятниковому прибору определяют по методике Кonig (DIN 53157). После этого дополнительно облучают образцы под 5 лампами типа ТL 40/03 и после 15 мин или соответственно 16 ч снова определяют твердость по маятниковому прибору. Чем выше величины, тем лучше активность испытуемого инициатора. Полученные результаты приведены в табл. 4 и показывают значительное превосходство соединения по изобретению.
П
р и м е 9. Реакционная способность инициатора в белом лаке
В
качестве соединения по уровню техники подвергают испытанию описанное в примере 8 соединение А, а в качестве соединений по
изобретению испытывают используемые в примере 5d соединения (I) и (II).
Испытуемые соединения в концентрации 2 мас. перемешивают с композицией лака фирмы SIRCA, свободно от пигментов. К полученной смеси добавляют 20 вес. белой пасти пигмента (TiO2 ).
Смеси наносят ракелем толщиной 150 μм на зажимные плиты и до отверждения обрабатывают воздухом в течение 1 мин при 50оС, чтобы удалить долю растворителя лаковой композиции.
В течение нескольких проходов облучают образцы под ртутной лампой среднего давления (типа Наnovia) при скорости движения ленты 10 м/мин. Реакционную способность инициатора определяют количеством проходов до того, что отвержденный слой лака является прочным на истирание. Чем ниже количество проходов, тем больше реакционная способность инициатора. После отверждения измеряют пожелтения (Yellowness Ingex, VI) по ASTM D 1925-70. Чем ниже полученные значения, тем меньше пожелтение. Полученные значения приведены в табл. 5. Они показывают превосходство соединений по изобретению по сравнению с прототипом.
Реферат
Использование: в химии фосфорорганических веществ, в частности в качестве фотоинициаторов этиленоненасыщенных соединений. Сущность изобретения: продукт - моно- или диацилфосфиноксиды ф-лы: R1R2 P(O)-C(O)-R3, где R1- замещенный алкоксигруппой C1-C8 - алкил или фенил; R2 означает R1 или означает остаток: -C(O)-R3 или OR4, или R1 и R2 - вместе с P образуют моно-, ди- или трициклическое кольцо с 4-15 атомами углерода; R3 - алкил, C5-C10 циклоалкил, фенил; R4 - алкил. Реагент 1: R1P(OR4)2 или R1PH2. Реагент 2: R3C(O)Cl. Реагент 3: окислитель. Условия реакции: в среде растворителя при 20-120oС. 9 з.п. ф-лы, 5 табл.
Формула

где R1 замещенный фенилом или С1 - С12-алкоксигруппой С1 С8-алкил или фенил;
R2 имеет указанное для R1 значение или означает остаток - СО-R3 , или ОR4, или R1 и R2 вместе с атомом фосфора образуют моно-, ди- или трициклическое кольцо с 4 15 атомами углерода;
R3 незамещенный или замещенный галогеном С1 - С8-алкил, незамещенный или замещенный С1 С12-алкилом или/и С2 С5-алкоксикарбонилом С5 - С10-циклоалкил, незамещенный или одно- или многозамещенный С1 С12-алкилом, С1 С12-алкоксигруппой или/и галогеном фенил;
R4 С1 С4-алкил при условии, что по меньшей мере один из остатков R1, R2 и R3 означает замещенный алкильный остаток или что R1 и R2 вместе с атомом фосфора образуют би- или трициклическое кольцо, или что R3 замещенный циклоалкильный остаток, который не может содержать алкильные остатки в качестве единственных заместителей.

или

где n 1 4;
R3 имеет одно из указанных в п. 1 значений.

Комментарии