Производные эктеинасцидинов, фармацевтическая композиция на их основе и применение - RU2306316C2
Код документа: RU2306316C2
Описание
Данное изобретение относится к способам синтеза, соединениям, полученным: с использованием этих способов, и их применению в качестве противоопухолевых агентов. В частности, оно относится к синтетическим способам получения природно встречающихся производных эктеинасцидина и родственных аналогов, в том числе новых промежуточных продуктов, которые образуют часть таких синтетических способов.
Кроме того, данное изобретение относится к новым, ранее не раскрытым применениям аналогов эктеинасцидина.
Патент Соединенных Штатов №5089273 описывает новые композиции, полученные путем экстракции из тропического морского беспозвоночного, Ecteinascidia turbinata, и обозначаемого как эктеинасцидины 729, 743, 745, 759 А, 759 В и 770. Эти соединения применимы в качестве антибактериальных и/или противоопухолевых агентов для млекопитающих. Эктеинасцидин 743 проходит клинические испытания в качестве противоопухолевого агента.

Ограниченная доступность природного материала привела к поиску альтернативных синтетических способов, необходимых для получения этих природных соединений и родственных аналогов.
Синтетический способ получения соединений эктеинасцидина описан в патенте США 5721362. Заявленный способ является многостадийным, приведено 38 примеров, каждый из которых описывает одну или несколько стадий в схеме получения эктеинасцидина 743.
Способы получения эктеинасцидина 743, содержащие меньшее количество стадий, описаны в WO 0069862 и WO 0187895 и включают в себя использование цианосафрацина В в качестве исходного материала.
Однако все еще существует необходимость в создании более экономичных способов получения других эктеинасцидинов, в частности в создании более экономичных способов получения известных противоопухолевых агентов, таких как ЕТ-729, а также способов, позволяющих получать новые соединения.
Синтетические соединения эктеинасцидина известны из различных ранее поданных заявок РСТ, в том числе, например, WO 0018233, WO 0177115, WO 0187894, WO 0187895, WO 99 51238 и WO 9846080. Все эти патентные заявки специально включены в данное описание в качестве ссылок, определяющих пути разработки способов и синтеза соединений эктеинасцидина. В частности, они выявляют взаимосвязь структуры и активности соединений данного изобретения. См. также J. Am. Chem. Soc., 1996, vol.118, № 38, pp.9017-9023 в отношении соединений эктеинасцидина. Синтетические соединения и природные эктеинасцидины имеют конденсированную циклическую систему:

Во многих эктеинасцидинах имеется 1, 4-мостик через эту конденсированную циклическую систему. В случае природных эктеинасцидинов 1,4-мостик является иногда 1,4-спироаминовым мостиком, например, в эктеинасцидине 729, 736 или 743.
В одном аспекте данное изобретение относится к хиноновым соединениям эктеинасцидина, имеющим группу хинона в кольце Е. Такие соединения обычно имеют формулу (Ab):
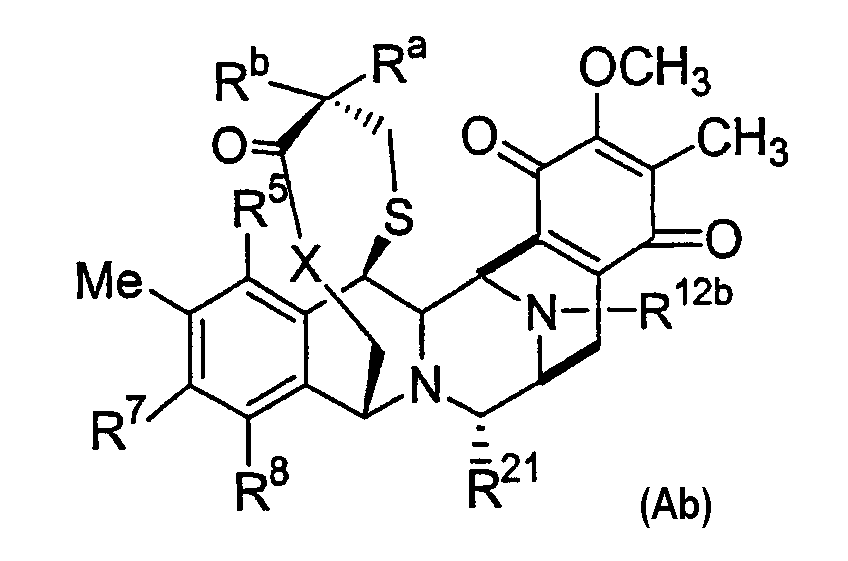
где Rа, Rb, R5, R7, R8, R21, Х и кольцо Е имеют определенные здесь значения, сера в 1,4-мостике может быть окисленной и R12b имеет значения, определенные для R12 или R12a.
Эти хиноновые соединения представляют особенный интерес в связи с их активностью, в особенности в связи с активностью хинона эктеинасцидина 637. Они могут быть получены окислением соединения эктеинасцидина, имеющего кольцо Е, которое является фенольным кольцом, как, например, в эктеинасцидине 743, имеющем 16-метил-, 17-метокси-, 18-гидроксифенильное кольцо в кольце Е. Могут быть использованы и другие заместители. Подходящие окисляющие агенты включают в себя соль Фреми.
Данное изобретение относится также к способу получения эктеинасцидина 729 и его производных, имеющих водород в положении N-12. Способ в соответствии с изобретением предусматривает получение эктеинасцидина с заместителем в положении N-12 и удаление этого заместителя. После этого N-Н-группа в положении 12 может быть дериватизована, например, группой R12а.
Кроме того, данное изобретение относится к способу, являющемуся модификацией способа получения эктеинасцидина, описанного в заявке автора данного изобретения WO 0187895. Таким образом, данное изобретение относится к способу получения соединения эктеинасцидина, в котором 1,4-мостик образуется при использовании циклического соединения-предшественника, конденсированного с ди-6,8-еноном, имеющим лабильную группу в положении 1, гидрокси в положении 10, защищенную группу в положении 12, защищенную гидроксигруппу в положении 18.
1,4-Мостик может быть спироамином, например, как в эктеинасцидине 729, но наличие такой группы необязательно. Обычно 1,4-мостик имеет формулу:
-(1)СН2-Х-С(=О)-С(Ra)(Rb)-S(4)-,
где -СН2- находится в положении 1, а -S- находится в положении 4 соединения эктеинасцидина, причем группы Х, Ra и Rb имеют определенные здесь значения.
Данное изобретение относится к соединению эктеинасцидина, которое имеет формулу (А):
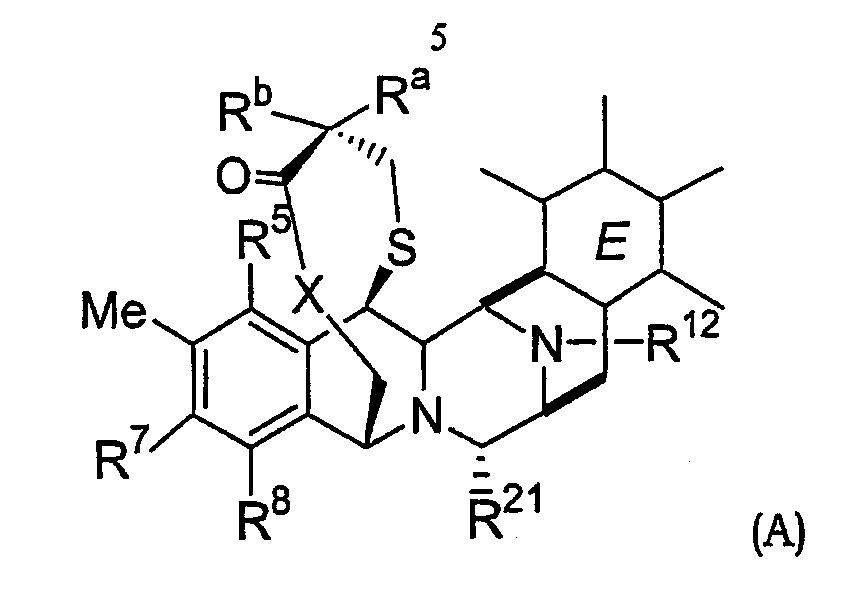
где:
Ra и Rb вместе с атомом углерода, к которому они присоединены, образуют группу -С(=О)-; группу -СН(Rc)-, где Rс обозначает ОХ1 или N(Х1Х2), где Х1 или каждый из Х1, Х2 обозначает независимо Н, -С(=О)-R', замещенный или незамещенный углеводород; или спирокольцо;
R5 обозначает -ОН-группу, которая может быть защищена или ее производное;
R7 обозначает -ОСН3 и R8 обозначает -ОН или R7 и R8 вместе образуют группу -О-СН2-О-;
R12 обозначает защитную группу;
R21 обозначает -Н, -ОН или -CN;
Х обозначает -NH- или -О-;
кольцо Е имеет формулу:

где R18 обозначает -ОН-группу, которая может быть защищена, или ее производное; и сера в 1,4-мостике может быть окислена.
1,4-Мостик может отсутствовать, в частности, для новых хиноновых соединений. В этом случае заместитель в положении 1, R1 , может быть таким, как в заявке авторов данного изобретения WO 0187894.
Защитная группа на N-12 может быть удалена с образованием водорода и необязательно заменена другим заместителем с образованием других соединений данного изобретения. Примеры таких дериватизованных соединений включают в себя соединения, в которых группа N-12 является алкилом, таким как метил или этил, в частности метил, или является ацилом, в частности ацетилом.
Данное изобретение относится дополнительно к соединениям формулы (Аа):

где Rа, Rb, R5, R7, R8, R21, Х и кольцо Е имеют определенные здесь значения, сера в 1,4-мостике может быть окисленной и R12а обозначает водород, замещенный или незамещенный углеводород, замещенный или незамещенный ацил, но предпочтительно не является метилом.
В другом аспекте данное изобретение относится к соединениям эктеинасцидина, имеющим 1,4-мостик, где кислород β в положении 1 заменен изостерой. Подходящие изостеры включают в себя -NH-.
Таким образом, данное изобретение относится к соединениям эктеинасцидина, имеющим 1,4-мостик, где 1,4-мостик имеет формулу:
-(1) СН2-Х-С(=О)-С(Ra)(Rb)-S(4)-,
где -СН2- находится в положении 1, а -S- находится в положении 4 соединения эктеинасцидина, причем группа Х обозначает NH и Ra и Rb имеют определенные здесь значения.
Такие соединения включают в себя соединения формулы (Ас):

где Rа, Rb, R5, R7, R8, R12b, R21 и кольцо Е имеют определенные здесь значения и сера в 1,4-мостике может быть окисленной.
Эти соединения могут быть получены способом в соответствии с данным изобретением, который является модификацией способа WO 0187895, с 1 лабильным заместителем, который является предпочтительно группой формулы:
-СН2-NProt1-C(=О)-CHNProt2-S-H,
где Prot1 и Prot2 являются аминозащитными группами.
Эти защитные группы могут быть затем удалены по отдельности или вместе, и соответствующие атомы азота могут быть дериватизованы подходящим образом.
Подходящие процедуры могут быть проведены, как раскрыто в WO 0187894, WO0187895, WO 0177115, которые включены здесь специальной ссылкой.
Предпочтительные варианты
Хиноновые соединения данного изобретения предпочтительно получают способом, который предусматривает окисление эктеинасцидина, имеющего фенол в качестве кольца Е, где гидроксигруппа фенола находится в положении 18 и может быть замещенной.
Такая реакция происходит в соответствии со следующей схемой:
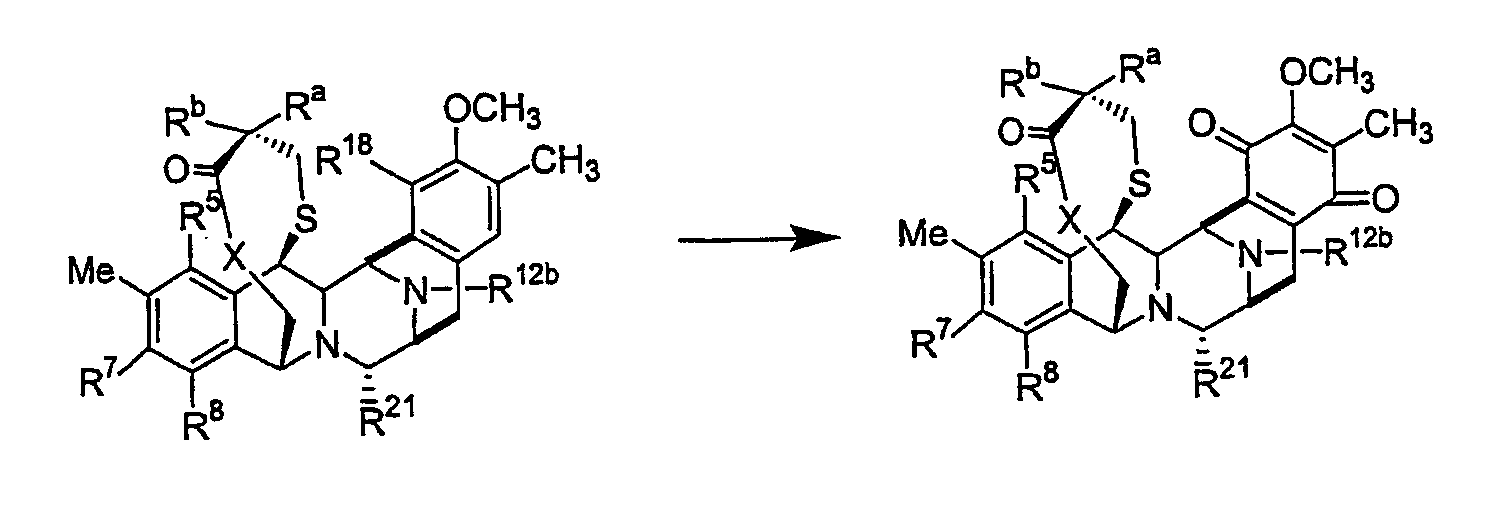
Альтернативно хиноновые соединения данного изобретения могут быть получены модификацией синтетических процедур, известных из более ранних заявок авторов, исходя из сафрацина В или родственного соединения в качестве исходного соединения. В частности, данное изобретение относится к способу, основанному на способе, описанном в заявке авторов WO 00699862, где кольцо Е является хиноновым кольцом в исходном материале, причем кольцо Е не превращают в фенольную систему, как упоминается на странице 24 указанной заявки WO 00699862.
1,4-Мостик необязателен в хиноновых соединениях данного изобретения.
В соединениях данного изобретения, в структуре которых присутствует 1,4-мостик, предпочтительные примеры группы, образованной Ra и Rb вместе с углеродом, к которому они присоединены, включают в себя:
-С(=О)-;
-CHNH2-группу, которая может быть защищена, или ее производное;
-СНОН-группу, которая может быть защищена, или ее производное;
группу формулы:

где Rd и Х1 имеют определенные ниже значения;
группу формулы:
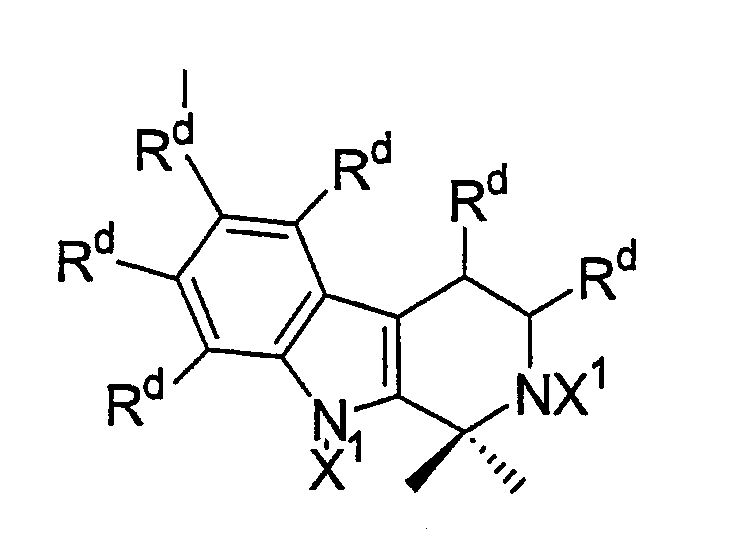
где Rd и Х1 имеют определенные ниже значения.
Rd и Х1 в этих группах предпочтительно выбраны из водорода или замещенного или незамещенного R', OR', -С(=О)R', углеводорода, углеводородокси или гидрокарбоила, в частности водорода, незамещенного или замещенного алкила или алкокси, незамещенного или замещенного алкенила, замещенного или незамещенного алкинила, незамещенного или замещенного арила, незамещенного или замещенного аралкила; предпочтительно водорода, алкила или алкокси, более предпочтительно водорода, метила или метокси, наиболее предпочтительно оба являются водородом.
Предпочтительные определения включают в себя определения, которые дают группу формулы:
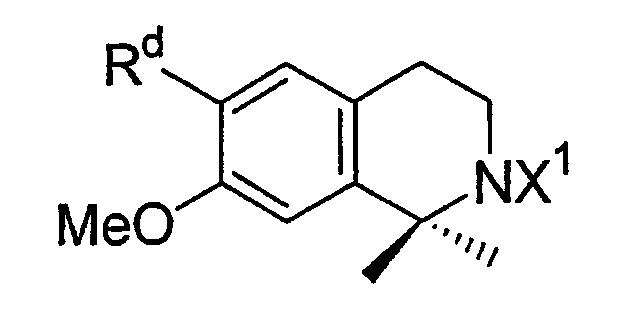
где Rd и Х1 имеют определенные выше значения; или
группа формулы:

где Rd и Х1 имеют определенные выше значения.
В частности, Ra и Rb могут быть выбраны с получением группы формулы:
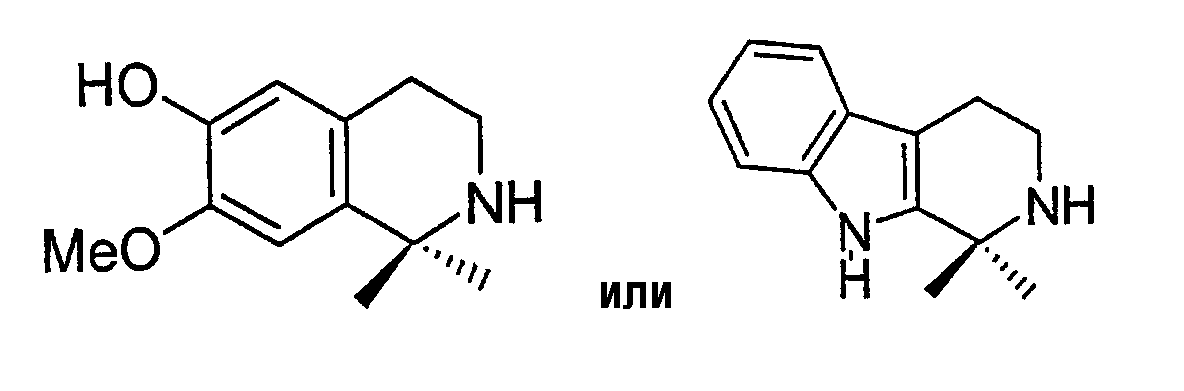
где Ra и Rb вместе с атомом углерода, к которому они присоединены, образуют группу -CHNH2, которая может быть защищена, или ее производное, и эта группа может быть группой формулы -CHNHX1 или -CHN(X1X2), где Х1, Х2 обозначает Н, С(=О)R', замещенный или незамещенный С1-18алкил, замещенный или незамещенный С2-18алкенил, замещенный или незамещенный С2-18алкинил, замещенный или незамещенный арил или защитную группу. Предпочтительные определения включают в себя водород, ацил, такой как ацетил, или защитную группу.
Один из Ra или Rb часто является водородом, а другой предпочтительно является Н; -NHCO-алкилом, в частности, где алкил имеет до 16 атомов углерода, например 1, 4, 7, 15 атомов углерода, и может быть галогензамещенным, необязательно пергалогензамещенным; -NH-алкил-СООН, в частности, где алкил имеет до 4 атомов углерода; защищенным -NHCOCH(NH2)CH2SH, где NH2 и/или SH являются защищенными; -NH-биотином; -NH-арилом; -NH(aa)y, где аа обозначает ацил аминокислоты, а y обозначает предпочтительно 1, 2 или 3 и где любая группа NH2 является необязательно дериватизованной или защищенной, например, амидной концевой группой или группой Doc; фталимидо, образованным -NX2-; алкилом, предпочтительно имеющим 1-4 атома углерода; арилалкенилом, в частности циннамоилом, который может быть замещенным, например, 3-трифторметилом.
Предпочтительные примеры группы Ra или Rb включают в себя NHAc, NHCO(CH2)2COOH, NHCOCH(NHAlloc)CH2SFm, NHCO(CH2CH)14CH3, NHTFA, NHCO(CH2)2CH3, NHCOCH2CH(CH3)2, NHCO(CH2)6CH3, NH-биотин, NHBz, NHCOCinn, NHCO-(p-F3C)-Cinn, NHCOVal-NH2, NHCOVal-N-Ac, NHCOVal-N-COCinn, NHCOVal-Ala-NH2, NHCOVal-Ala-N-Ac, NHCOAla-NH2, OH, OAc, NHAc, NHCO(CH2)2COOH, NHCOCH(NH2)CH2SFm, NPhth, NH-(m-CO2Me)-Dz, NHCO(CH2)14CH3, NMe2, NHAlloc, NHTroc, NHBz, NHCO-(P-F3C)-Cinn, NHCOVal-NH2, NHCOVal-N-Ac, NHCOVal-Ala-N-COCinn, NHCOAla-N-Ac, NHCOAla-N-COCinn, Nphth, вместе со сходными группами, где число атомов углерода варьируется или аминокислота изменена или другое изменение этого рода произведено с образованием сходной группы.
В случаях, когда Ra и Rb вместе с атомом углерода, к которому они присоединены, образуют группу -СНОН или защищенную или дериватизованную версию такой группы, эта группа может быть группой формулы -СНОХ1, где Х1 имеет определенное здесь значение.
Другие предпочтительные примеры включают в себя ОН, ОАс, OCOCF3, OCOCH2CH2CH3, OCO(CH2)6CH3, ОСО(СН2)14СН3, OCOCH=CHPh, OSO2CH3 вместе со сходными группами, где число атомов углерода варьируется или введены отличающиеся группы-заместители или другое изменение этого рода произведено с образованием сходной группы.
Сера в 1,4-мостике может быть окислена с образованием, например, группы -S(=O)-.
В случае, когда 1,4-мостик отсутствует, группа в положении 1, R1, является подходящим образом необязательно защищенной аминометиленовой группой или ее производным, или необязательно защищенной гидроксиметиленовой группой или ее производным; а группа в положении 4, R4, обычно является водородом.
R1 обозначает предпочтительно гидрофобную группу, которая, следовательно, не содержит свободной амино-, гидроксигруппы или другой гидрофильной группы. Обычно R1 обозначает группу -CH2-NH2-CO-R', где R' имеет определенное здесь значение, но предпочтительно имеет длину линейной цепи менее чем 20 атомов, более предпочтительно менее чем 15 или 10 атомов, где 1,4-фенил считается длиной из четырех атомов, и подобные соображения относятся и к другим циклическим группам (например, 1,2-циклогексил является длиной цепи из двух атомов), и эта линейная цепь из менее чем 10, 15 или 20 атомов сама может быть замещенной. В частности, эти данные предполагают, что равновесие должно достигаться между отсутствием такой группы Ra-CO- и наличием большой, объемной группы.
В особенно предпочтительных соединениях группа R1 ацилирована на -NH2-группе, и, например, N-ацильные производные могут быть образованы из групп -CH2NH2 и -CH2-NH-aa, где аа обозначает аминокислоту. Ацильные производные могут быть N-ацильными или N-тиоацильными производными. Ацильные группы могут быть группами формулы -СО-R', где R' имеет определенные здесь значения и выбран таким образом, чтобы удовлетворять указанным критериям. Подходящие ацильные группы включают в себя аланил, аргинил, аспартил, аспарагил, цистил, глутамил, глутаминил, глицил, гистидил, гидроксипролил, изолейцил, лейцил, лизил, метионил, фенилаланил, пролил, серил, треонил, тиронил, триптофил, тирозил, валил, а также другие аминокислотные ацильные группы, которые могут быть L- или D-. Такие аминокислотные ацильные группы предпочтительно являются дериватизованными на аминогруппе для создания гидрофобности.
В вариации группа R1 является производным гидроксиметиленовой группы. Аналогичное можно отнести к производному аминометиленовой группы.
В одном предпочтительном аспекте, по меньшей мере, один из R5, R18 и R' в группе Rd выбран из водорода, R', С=OR' или COOR', где R' обозначает необязательно замещенный алкил или алкенил, причем эти необязательные заместители выбраны из галогена, амино, в том числе амино, произведенного из аминокислоты, арила или гетероциклила.
R5 обозначает предпочтительно -ОН, которая может быть защищена, или ее производное. В частности, он может быть группой -ОХ1. Особенно предпочтительный R5 является ацилоксигруппой, в частности ацетилоксигруппой. Другие примеры включают в себя циннамоилокси и гептаноилокси.
R7 обозначает -ОСН3 и R8 обозначает -ОН, или более предпочтительно R7 и R8 вместе образуют группу -О-СН2-О-.
R12 обозначает защитную группу для атома азота аминогруппы. Подходящие защитные группы для таких аминогрупп включают в себя карбаматы, амиды и другие защитные группы, такие как алкил, арилалкил, сульфо- или галогенарилалкил, галогеналкил, алкилсилилалкил, арилалкил, циклоалкилалкил, алкиларилалкил, гетероциклилалкил, нитроарилалкил, ациламиноалкил, нитроарилдитиоарилалкил, дициклоалкилкарбоаксамидоалкил, циклоалкил, алкенил, арилалкенил, нитроарилалкенил, гетероциклилалкенил, гетероциклил, гидроксигетероциклил, алкилдитио, алкокси-, или галоген-, или алкилсульфиниларилалкил, гетероциклилацил, и другие карбаматы, и алканоил, галогеналканоил арилалканоил, алкеноил, гетероциклилацил, ароил, арилароил, галогенароил, нитроароил и другие амиды, а также алкил, алкенил, алкилсилилалкоксиалкил, алкоксиалкил, цианоалкил, гетероциклил, алкоксиарилалкил, циклоалкил, нитроарил, арилалкил, алкокси- или гидроксиарилалкил и многие другие группы. Такие группы могут быть необязательно замещенными. Дополнительные примеры приведены в более ранних патентных описаниях авторов данного изобретения.
Предпочтительный класс соединений включает производное эктеинасцидина, где N-12-защитная группа R12 выбрана из галогеналкила, алкоксиалкила, галогеналкоксиалкила, арилалкилена, галогеналкиларилалкилена, ацила, галогенацила, необязательно замещенного галогеналкоксиалкила, необязательно замещенного галоген- или алкиларилалкенилацила, алкенилацила, карбоната, карбамата, арилалкила, алкенила, ангидрида карбоновой кислоты и аминокислоты.
Особенно предпочтительным является производное эктеинасцидина, где N-12-защитная группа R12 выбрана из аллила, ацетила, трифторацетила, 2,2, 2-трихлорэтоксикарбонила, изовалерилкарбонила, транс-3-(трифторметил)циннамоилкарбонила, гептафторбутирилкарбонила, деканоилкарбонила, транс-циннамоилкарбонила, бутирилкарбонила, 3-хлорпропионилкарбонила, циннамоилкарбонила, 4-метилциннамоилкарбонила, гидроциннамоилкарбонила или транс-гексеноилкарбонила, или аланила, аргинила, аспартила, аспарагила, цистила, глутамила, глутаминила, глицила, гистидила, гидроксипролила, изолейцила, лейцила, лизила, метионила, фенилаланила, пролила, серила, треонила, тиронила, триптофила, тирозила, валила или другой аминокислотной ацильной группы, фталимидо или другой циклической амидогруппы.
R18 имеет предпочтительно значения, определенные для R5, хотя наиболее предпочтительным значением является гидрокси.
R21 обозначает -Н или более предпочтительно -ОН или -CN.
Кольцо Е имеет формулу:
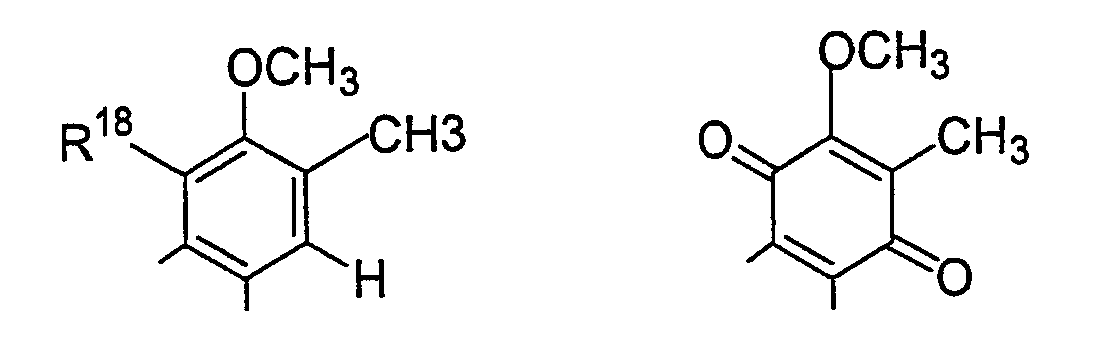
где R18 обозначает -ОН-группу, которая может быть защищена, или ее производное; и предпочтительно имеет формулу -ОХ1. Примеры, кроме -ОН, включают в себя циннамоилокси.
Х1 и Х2, когда они являются аминозащитными группами, и Prot1 и Prot2 могут иметь значения, определенные для R12, и в отношении дополнительной информации делается ссылка на WO 0187895.
Х1, когда он является гидроксизащитной группой, и Prot3 могут быть известными защитными группами для гидроксигруппы. Подходящие защитные группы для гидроксигрупп включают в себя простые и сложные эфиры, такие как алкиловый, алкоксиалкиловый, арилоксиалкиловый, алкоксиалкоксиалкиловый, алкилсилилалкоксиалкиловый, алкилтиоалкиловый, арилтиоалкиловый, азидоалкиловый, цианоалкиловый, хлоралкиловый, гетероциклический, арилациловый, галогенарилациловый, циклоалкилалкиловый, алкениловый, циклоалкиловый, алкиларилалкиловый, алкоксиарилалкиловый, нитроарилалкиловый, галогенарилалкиловый, алкиламинокарбониларилалкиловый, алкилсульфиниларилалкиловый, алкилсилиловый и другие простые эфиры и арилациловый, арилалкилкарбонатный, алифатический карбонатный, алкилсульфиниларилалкиловый карбонатный, алкилкарбонатный, арилгалогеналкилкарбонатный, арилалкенилкарбонатный, арилкарбаматный, алкилфосфиниловый, алкилфосфинотиоиловый, арилфосфинотиоиловый, арилалкилсульфонатный и другие сложные эфиры. Такие группы могут быть необязательно замещенными. Дополнительные примеры приведены в более ранних патентных описаниях авторов.
Каждая группа R' независимо выбрана из группы, состоящей из Н, ОН, NO2, NH2, SH, CN, галогена, =О, С(=О)Н, С(=О)СН3, СО2Н, СО2СН3, С1-С6алкила, алкинила, алкенила, арила, аралкила и гетероциклила. Предпочтительные определения включают в себя Н, ацил, алкил, в особенности Н и алканоил или циннамоил.
Предпочтительные соединения данного изобретения включают в себя соединения, согласующиеся с одним или более из следующих определений:
R1 обозначает -СН2NH2 или -СН2ОН, которые могут быть защищены, или их производные (в отношении которой см., в частности, WO 0187894, включенный специальной ссылкой в этом месте для описания R1, и, следовательно, все описание WO 0187894 в отношении R1 образует часть данного текста) и R4 обозначает -Н; или R1 и R4 вместе образуют группу формулы (II), (III), (IV), (V) или (VI), где Х обозначает О, NH или NR и Y обозначает O, S или S=O и R обозначает азотзащитную группу и R' обозначает Н, или ОН, или ОМе, или Ме.

R5 обозначает -ОН, -ОАс или -О-аллил или -О-циннамоил или О-октаноил;
R7 и R8 вместе образуют группу -О-СН2-О-;
R12b обозначает Н, алкил, галогеналкил, алкоксиалкил, галогеналкоксиалкил, арилалкилен, галогеналкиларилалкилен, ацил, галогенацил, карбонат, карбамат, арилалкил, алкенил и аминокислоту. Предпочтительно R12b обозначает Н, метил, аллил, ацетил, трифторацетил, 2,2,2-трихлорэтоксикарбонил, изовалерилкарбонил, транс-3-(трифторметил)циннамоилкарбонил, гептафторбутирилкарбонил, деканоилкарбонил, транс-циннамоилкарбонил, бутирилкарбонил, 3-хлорпропионилкарбонил, циннамоилкарбонил, 4-метилциннамоилкарбонил, гидроциннамоилкарбонил или транс-гексеноилкарбонил, или аланил, аргинил, аспартил, аспарагил, цистил, глутамил, глутаминил, глицил, гистидил, гидроксипролил, изолейцил, лейцил, лизил, метионил, фенилаланил, пролил, серил, треонил, тиронил, триптофил, тирозил, валил, а также другие менее обычные аминокислотные ацильные группы, а также фталимидо или другие циклические амидогруппы.
Кольцо Е имеет формулу:

Подходящие заместители-галогены в соединениях данного изобретения включают в себя F, Cl, Br и I.
Алкильные группы имеют предпочтительно 1-24 атома углерода. Один более предпочтительный класс алкильных групп имеет от 1 до приблизительно 12 атомов углерода, еще более предпочтительно от 1 до приблизительно 8 атомов углерода, даже более предпочтительно от 1 до приблизительно 6 атомов углерода и наиболее предпочтительно 1, 2, 3 или 4 атома углерода. Другой предпочтительный класс алкильных групп имеет от 12 до приблизительно 24 атомов углерода, более предпочтительно от 12 до приблизительно 18 атомов углерода и наиболее предпочтительно 13, 15 или 17 атомов углерода. Метил, этил и пропил, в том числе изопропил, являются особенно предпочтительными алкильными группами в соединениях данного изобретения. В применении здесь термин «алкил», если нет иной модификации, относится как к циклическим, так и к нециклическим группам, хотя циклические группы будут содержать по меньшей мере три углеродных кольцевых члена.
Предпочтительные алкенильные и алкинильные группы в соединениях данного изобретения имеют одну или более ненасыщенных связей и от 2 до приблизительно 12 атомов углерода, более предпочтительно от 2 до приблизительно 8 атомов углерода, еще более предпочтительно от 2 до приблизительно 6 атомов углерода, даже еще более предпочтительно 1, 2, 3 или 4 атома углерода. Термины «алкенил» и «алкинил», используемые здесь, относятся как к циклическим, так и к нециклическим группам, хотя обычно более предпочтительными являются прямые или разветвленные нециклические группы.
Предпочтительные алкоксигруппы в соединениях данного изобретения включают в себя группы, имеющие одну или более кислородных связей и от 1 до приблизительно 12 атомов углерода, более предпочтительно от 1 до приблизительно 8 атомов углерода и еще более предпочтительно от 1 до приблизительно 6 атомов углерода и наиболее предпочтительно 1, 2, 3 или 4 атома углерода.
Предпочтительные алкилтиогруппы в соединениях данного изобретения имеют одну или более простых тиоэфирных связей и от 1 до приблизительно 12 атомов углерода, более предпочтительно от 1 до приблизительно 8 атомов углерода и еще более предпочтительно от 1 до приблизительно 6 атомов углерода. Алкилтиогруппы, имеющие 1, 2, 3 или 4 атома углерода, являются особенно предпочтительными.
Предпочтительные алкилсульфинильные группы в соединениях данного изобретения включают в себя группы, имеющие одну или более сульфоксидных (SO) групп и от 1 до приблизительно 12 атомов углерода, более предпочтительно от 1 до приблизительно 8 атомов углерода и еще более предпочтительно от 1 до приблизительно 6 атомов углерода. Алкилсульфинильные группы, имеющие 1, 2, 3 или 4 атома углерода, являются особенно предпочтительными.
Предпочтительные алкилсульфонильные группы в соединениях данного изобретения включают в себя группы, имеющие одну или более сульфонильных (SO2) групп и от 1 до приблизительно 12 атомов углерода, более предпочтительно от 1 до приблизительно 8 атомов углерода и еще более предпочтительно от 1 до приблизительно 6 атомов углерода. Алкилсульфонильные группы, имеющие 1, 2, 3 или 4 атома углерода, являются особенно предпочтительными.
Предпочтительные аминоалкильные группы включают в себя группы, имеющие одну или более первичных, вторичных и/или третичных аминогрупп и от 1 до приблизительно 12 атомов углерода, более предпочтительно от 1 до приблизительно 8 атомов углерода, еще более предпочтительно от 1 до приблизительно 6 атомов углерода, даже более предпочтительно 1, 2, 3 или 4 атома углерода. Вторичные и третичные аминогруппы являются обычно более предпочтительными, чем первичные аминогруппы.
Гетероциклические группы включают в себя гетероароматические и гетероалициклические группы. Подходящие гетероароматические группы в соединениях данного изобретения содержат один, два или три гетероатома, выбранных из атомов N, O или S, и включают в себя, например, кумаринил, в том числе 8-кумаринил, хинолинил, в том числе 8-хинолинил, пиридил, пиразинил, пиримидил, фурил, пирролил, тиенил, тиазолил, оксазолил, имидазолил, индолил, бензофуранил и бензотиазол. Подходящие гетероалициклические группы в соединениях данного изобретения содержат один, два или три гетероатома, выбранных из атомов N, O или S, и включают в себя, например, группы тетрагидрофуранил, тетрагидропиранил, пиперидинил, морфолино и пирролидинил.
Подходящие карбоциклические арильные группы в соединениях данного изобретения включают в себя соединения с одним кольцом или с множественными кольцами, в том числе соединения с множественными кольцами, которые содержат отдельные и/или конденсированные арильные группы. Типичные карбоциклические арильные группы содержат 1-3 отдельных или конденсированных колъца и от 6 до приблизительно 18 атомов углерода кольца. Особенно предпочтительные карбоциклические арильные группы включают в себя фенил, в том числе замещенный фенил, такой как 2-замещенный фенил, 3-замещенный фенил, 2,3-замещенный фенил, 2,5-замещенный фенил, 2,3, 5-замещенный и 2,4,5-замещенный фенил, в том числе, когда один или более из фенильных заместителей являются электрон-акцепторной группой, такой как галоген, циано, нитро, алканоил, сульфинил, сульфонил и т.п.; нафтил, в том числе 1-нафтил и 2-нафтил; бифенил; фенантрил и антрацил.
Предпочтительными ацильными группами являются R'-CO-, в том числе алкил-СО, алкенил-СО, алкинил-СО, арил-СО, гетероциклил-СО, среди прочих.
Ссылки здесь на замещенные группы в соединениях данного изобретения относятся к указанной части молекулы, которая может быть замещена в одном или более доступных положениях одной или более подходящими группами, как упомянуто выше, такими как, например, галоген, такой как фтор, хлор, бром и йод; циано; гидроксил; нитро; азидо; алканоил, такой как С1-6алканоильная группа, такая как ацил и т.п.; карбоксамидо; алкильные группы, в том числе группы, имеющие от 1 до приблизительно 2 атомов углерода или от 1 до приблизительно 6 атомов углерода и более предпочтительно 1-3 атома углерода; алкенильные и алкинильные группы, в том числе группы, имеющие одну или более ненасыщенных связей и от 2 до приблизительно 12 атомов углерода или от 2 до приблизительно 6 атомов углерода; алкоксигруппы, имеющие одну или более кислородных связей и от 1 до приблизительно 12 атомов углерода или от 1 до приблизительно 6 атомов углерода; арилоксигруппа, такая как фенокси; алкилтиогруппы, в том числе группы, имеющие одну или более простых тиоэфирных связей и от 1 до приблизительно 12 атомов углерода или от 1 до приблизительно 6 атомов углерода; алкилсульфинильные группы, в том числе группы, имеющие одну или более сульфинильных связей и от 1 до приблизительно 12 атомов углерода или от 1 до приблизительно 6 атомов углерода; алкилсульфонильные группы, в том числе группы, имеющие одну или более сульфонильных связей и от 1 до приблизительно 12 атомов углерода или от 1 до приблизительно 6 атомов углерода; аминоалкильные группы, такие как группы, имеющие один или более атомов N и от 1 до приблизительно 12 атомов углерода или от 1 до приблизительно 6 атомов углерода; карбоциклический арил, имеющий 6 или более атомов углерода, в частности фенил (например, R является замещенной или незамещенной бифенильной группой); и аралкил, такой как бензил.
Предпочтительные R'-группы присутствуют в группах формулы R', COR' или OCOR' и включают в себя алкил или алкенил, которые могут быть замещены в одном или более доступных положениях одной или более подходящими группами, такими как, например, галоген, такой как фтор, хлор, бром и йод, в частности, ω-хлор или перфтор; аминоалкильные группы, такие как группы, имеющие один или более атомов N- и от 1 до приблизительно 12 атомов углерода или от 1 до приблизительно 6 атомов углерода, и, в частности, включающие в себя аминокислоту, особенно глицин, аланин, аргинин, аспарагин, аспарагиновую кислоту, цистеин, глутамин, глутаминовую кислоту, гистидин, изолейцин, лейцин, лизин, метионин, фенилаланин, пролин, серин, треонин, триптофан, тирозин или валин, в частности, защищенные формы таких аминокислот; карбоциклический арил, имеющий 6 или более атомов углерода, в частности фенил; и аралкил, такой как бензил; гетероциклические группы, в том числе гетероалициклические и гетероароматические группы, в частности, с 5-10 атомами кольца, из которых 1-4 являются гетероатомами, более предпочтительно гетероциклические группы с 5 или 6 атомами колец и 1 или 2 гетероатомами или 10 атомами кольца и 1-3 гетероатомами, причем эти гетероциклические группы являются необязательно замещенными одним или несколькими заместителями, допускаемыми для R', и, в частности, амино, например диметиламино или кето.
Ацильные производные, такие как -СО-R', могут быть N-ацильными или N-тиоацильными производными, а также циклическими амидами. Ацильные группы могут быть, в качестве иллюстрации, алканоильными, галогеналканоильными, арилалканоильными, алкенильными, гетероциклилацильными, ароильными, арилароильными, галогенароильными, нитроароильными или другими ацильными группами. R' или подобная группа ацила могут быть различными группами, такими как алкил, алкокси, алкилен, арилалкил, арилалкилен, ацил аминокислоты или гетероциклил, каждая из которых замещена галогеном, циано, нитро, карбоксиалкилом, алкокси, арилом, арилокси, гетероциклилом, гетероциклилокси, алкилом, амино или замещенным амино. Другие ацилирующие агенты включают в себя изотиоцианаты, такие как арилизотиоцианаты, в частности фенилизотиоцианат. Алкильная, алкокси или алкиленовая группы предпочтительно имеют 1-6 или 12 атомов углерода и могут быть линейными, разветвленными или циклическими. Арильные группы обычно являются фенилом, бифенилом или нафтилом. Гетероциклильные группы могут быть ароматическими или частично или полностью ненасыщенными и предпочтительно имеют 4-8 атомов кольца, более предпочтительно 5 или 6 атомов кольца с одним или несколькими гетероатомами, выбранными из атомов азота, серы и кислорода.
Не ограничиваясь, типичные группы R' в ацильных группах включают в себя алкил, галогеналкил, алкоксиалкил, галогеналкоксиалкил, арилалкилен, галогеналкиларилалкилен, ацил, галогенацил, арилалкил, алкенил и аминокислоту. Например, R'-СО- может быть ацетилом, трифторацетилом, 2,2,2-трифторэтоксикарбонилом, изовалерилкарбонилом, транс-3-(трифторметил)циннамоилкарбонилом, гептафторбутирилкарбонилом, деканоилкарбонилом, транс-циннамоилкарбонилом, бутирилкарбонилом, 3-хлорпропионилкарбонилом, циннамоилкарбонилом, 4-метилциннамоилкарбонилом, гидроциннамоилкарбонилом, или транс-гексеноилкарбонилом, или аланилом, аргинилом, аспартилом, аспарагилом, цистилом, глутамилом, глутаминилом, глицилом, гистидилом, гидроксипролилом, изолейцилом, лейцилом, лизилом, метионилом, фенилаланилом, пролилом, серилом, треонилом, тиронилом, триптофилом, тирозилом, валилом, а также другими менее обычными аминокислотными ацильными группами, а также фталимидо или другими циклическими амидами.
Один класс предпочтительных соединений данного изобретения включает в себя соединения данного изобретения, которые имеют один или несколько из следующих заместителей:
R1 и R4 образуют мостик, как описано, или R1 имеет указанное выше значение, а R4 является водородом.
R5 обозначает водород;
алкил, более предпочтительно алкил из 1-6 атомов углерода;
С(=О)R', где R' обозначает алкил, предпочтительно алкил из 1-24 атомов углерода, в частности 1-8 или 12-18 атомов углерода; галогеналкил, более предпочтительно ω -хлор- или перфторалкил из 1-4 атомов углерода, в частности ω-хлорэтил или перфторметил, этил или пропил; гетероциклилалкил, более предпочтительно алкил из 1-6 атомов углерода с ω -гетероциклическим заместителем, предпочтительно имеющим 5-10 атомов кольца и 1-4 гетероатома, в том числе конденсированный гетероалициклил с 3 гетероатомами, такой как биотин; аминоалкил, более предпочтительно алкил из 1-6 атомов углерода, в частности 2 атомов углерода, с ω-аминогруппой, необязательно замещенной, например, алкоксикарбонилом, таким как (СН3)3 С-О-С=О-, или другой защитной группой;
арилалкилен, в частности циннамоил; алкилен, в частности винил или аллил; аралкил, такой как бензил; или
С(=О)OR', где R' обозначает алкил, более предпочтительно алкил из 1-6 атомов углерода, в частности разветвленный алкил; алкенил, более предпочтительно аллил;
R12 обозначает водород, метил или защитную группу, в том числе алкоксикарбонил, такой как (СН3)3С-О-С=О-.
R18, когда он присутствует, обозначает водород;
алкил, более предпочтительно алкил из 1-6 атомов углерода;
С(=О)R', где R' обозначает алкокси, в частности, с алкильной группой из 1-6 атомов углерода; алкил, более предпочтительно алкил из 1-24 атомов углерода, предпочтительно 1-8 или 12-18 атомов углерода; галогеналкил, более предпочтительно перфторалкил из 1-4 атомов углерода, в частности перфторметил, этил или пропил; арилалкилен, в частности циннамоил; гетероциклилалкил, более предпочтительно алкил из 1-6 атомов углерода с ω-гетероциклическим заместителем, предпочтительно имеющим 5-12 атомов кольца и 1-4 гетероатома, в том числе конденсированный гетероциклил с 3 гетероатомами, такой как биотин; гетероциклилалкил предпочтительно с 1 атомом углерода в алкильной группе, и более предпочтительно гетероалициклилметил с 5-10 атомами кольца и 1-4 атомами кольца, в частности конденсированный гетероциклил с 1-4 гетероатомами, такой как диметиламинокумарин или кумарин; алкилен, в частности аллил; аралкил, такой как бензил;
С(=О)OR', где R' обозначает алкил, более предпочтительно алкил из 1-6 атомов углерода; алкилен, в частности винил или аллил; аралкил, такой как бензил.
Rd обозначает ОС(=О)R', где R' обозначает алкил, более предпочтительно алкил из 1-24 атомов углерода, предпочтительно 1-8 или 12-18 атомов углерода; галогеналкил, более предпочтительно ω -хлор- или перфторалкил из 1-4 атомов углерода, в частности ω-хлорэтил или перфторметил, этил или пропил; аралкил, такой как бензил или фенетил; арилалкилен, в частности циннамоил; аминоалкил, в частности аминокислота, более предпочтительно защищенная аминокислота, в том числе защищенный цистеин, особенно Fm-S-CH2CH(NHBOC)-cys или аланин, в частности (СН3)3 С-О-С=О-ala; гетероциклилалкил, предпочтительно алкил из 1-6 атомов углерода с ω-гетероциклическим заместителем, предпочтительно имеющим 5-12 атомов кольца и 1-4 гетероатома, в том числе конденсированный гетероцикл с 3 атомами кольца, такой как биотин; гетероциклилалкил предпочтительно с 1 атомом углерода в алкильной группе и более предпочтительно гетероалициклилметил с 5-10 атомами кольца и 1-4 атомами кольца, особенно конденсированный гетероцикл с 1-4 гетероатомами, такой как кумарин или диметиламинокумарин; алкилен, особенно аллил; аралкил, такой как бензил;
О(С=О)OR', где R' обозначает алкил, более предпочтительно алкил из 1-6 атомов углерода; алкилен, в частности винил или аллил; аралкил, такой как бензил;
ОР=О(OR')2, где R' обозначает бензил.
Х1 обозначает водород;
алкил, более предпочтительно алкил из 1-6 атомов углерода;
(С=О)OR', где R' обозначает алкилен, в частности винил;
R21 обозначает водород, гидрокси или циано.
Соединения с изменениями в R5 являются частью данного изобретения, в частности, со сложноэфирными группами, R1=R'СО-, где R' обозначает длинную алифатическую или ароматическую группу.
Имеются соединения, которые имеют хорошие свойства ADME (абсорбции-распределения-метаболизма-секреции), которые являются хорошими признаками фармакокинетики.
В варианте данного изобретения эти соединения имеют один или более из следующих признаков:
R1 обозначает -СН2-N(R')2 или -СН2OR', где каждый из R' обозначает Н; алкил-СО-; галогеналкил-СО-; циклоалкилалкил-СО-; галогеналкил-О-СО-; арилалкил-СО-; арилалкенил-СО-; гетероарил-СО-; алкенил-СО-; алкенил; ацил аминокислоты; или защитную группу;
R5 обозначает ацетил или другой ацил. Предпочтительно он имеет, по меньшей мере, 4, 5 или 6 атомов углерода, например до 18 или 24 атомов углерода. Подходящие заместители включают в себя сложные эфиры COR', где R' обозначает алкил, алкенил, часто с одним или несколькими заместителями. Алкил, замещенный алкил, алкенил и арилалкенил являются предпочтительными, причем предпочтительные заместители включают в себя арил, гетероциклил. Другие определения для R5 включают в себя эфиры формулы COR', произведенные из аминокислоты, необязательно замещенной аминокислоты.
R18 обозначает гидрокси, или он представляет OR', OCOR' или OCOOR', где R' является заместителем с некоторым объемом. Такие объемные заместители включают в себя заместители с группами с разветвленными цепями, ненасыщенные группы или циклические группы, в том числе ароматические группы. Таким образом, разветвленный алкил, циклоалкил, разветвленный алкенил, арил, гетероароматическая группа и родственные группы являются предпочтительными для включения в этой структуре заместителя R18. Предпочтительно общее количество атомов углерода равно 2-24, более предпочтительно 6-18 атомам углерода. Обычно R18 является сложным эфиром, простым эфиром или карбонатом, имея формулу OCOR', OR' или OCOOR'.
Rd обозначает гидрокси или метокси. Альтернативно он обозначает OR', OCOR' или OCOOR', где R' является заместителем с некоторым объемом. Такие объемные заместители включают в себя заместители с группами с разветвленными цепями, ненасыщенные группы или циклические группы, в том числе ароматические группы. Таким образом, разветвленный алкил, циклоалкил, разветвленный алкенил, арил, гетероароматическая группа и родственные группы являются предпочтительными для включения в структуре этого заместителя. Предпочтительно общее количество атомов углерода равно 2-24, более предпочтительно 6-18 атомов углерода.
Не ограничиваясь, другой класс предпочтительных соединений данного изобретения имеет одно или несколько из следующих определений: R21 обозначает Н, -CN или -ОН, наиболее предпочтительно -ОН или -CN.
R5 обозначает предпочтительно Н или ацетил; арилалкил, в частности бензил; алкил-СО- (причем алкил имеет до 25 атомов углерода, например до 17, 19 или 21 атома углерода, и предпочтительно нечетное число атомов углерода, соответствующее жирной карбоновой кислоте с четным числом атомов углерода, или еще более низкое количество атомов углерода, такое как 1-6), в частности, СН3 -(СН2)n-CO-, где n равно, например, 1, 2, 4, 6, 12, 14 или 16; галогеналкил-СО-, в частности трифторметилкарбонил, арилалкил-СО-, в частности бензил-СО-; арилалкенил-СО-, в частности циннамоил-СО-; наиболее предпочтительно R1 обозначает Н, ацетил или циннамоил.
R12 обозначает Н; алкил, в частности метил; алкил-О-СО-, в частности трет-бутил-О-СО- или алкенил-О-СО-, в частности аллил-О-СО-.
R18 обозначает предпочтительно Н или ацетил; алкил (причем алкил имеет 1-6 атомов углерода), в частности С1-С3алкил; алкенил, в частности аллил; арилалкил, в частности бензил; алкил-СО- (причем алкил имеет до 25 атомов углерода, например до 17, 19 или 21 атома углерода, и предпочтительно нечетное число атомов углерода, соответствующее жирной карбоновой кислоте с четным количеством атомов углерода, или еще более низкое количество атомов углерода, например 1-6), в частности СН3-(СН2)n-CO-, где n равно, например, 1, 2, 4, 6, 12, 14 или 16, и его производные, такие как биотин-(СН2)4-СО-; арилалкенил-СО-, в частности циннамоил-СО-; алкил-О-СО-, в частности трет-бутил-О-СО-; арилалкил-О-СО-, в частности бензил-О-СО-; алкенил-О-СО-, в частности аллил-О-СО-.
Rd обозначает предпочтительно ОН, О-ацетил, О-алкил (причем алкил имеет 1-6 атомов углерода), в частности С1-С3алкил; О-алкенил, в частности аллил; арилалкил-О-, в частности бензил; алкил-СО-О- (причем алкил имеет до 25 атомов углерода, например до 17, 19 или 21 атома углерода, и предпочтительно нечетное число атомов углерода, соответствующее жирной карбоновой кислоте с четным количеством атомов углерода, или еще более низкое количество атомов углерода, например 1-6), в частности СН3-(СН2)n-CO-О-, где n равно, например, 1, 2, 4, 6, 12, 14 или 16, и его производные, такие как биотин-(СН2)4-СОО-; галогеналкил-СО-О-, в частности трифторметилкарбонил; ацил аминокислоты или его производное, такое как FmSCH2CH(NHBOC)CO-O-; арилалкенил-СО-О, в частности циннамоил-СО-О-; алкил-О-СО-О-, в частности трет-бутил-О-СО-О-; алкенил-О-СО-О-, в частности аллил-О-СО-О-; арилалкил-О-СО-О-, в частности бензил-О-СО-О-; защитную группу, такую как РО(OBn)2; наиболее предпочтительно R4 обозначает ОН, ацилокси, например, циннамоилокси.
Х1 обозначает Н или алкил (причем алкил имеет 1-6 атомов углерода) и R5 является наиболее предпочтительно Н или С1-С3алкилом.
Способ, который предусматривает получение эктеинасцидина с заместителем N-12 и удаление этого заместителя, обычно проводят с использованием соединения эктеинасцидина с метильной группой в положении N-12. Примеры таких соединений могут быть найдены в опубликованных и ожидающих одновременного рассмотрения заявках авторов на патент РСТ, относящихся к соединениям эктеинасцидина. Эти заявки включены здесь в качестве специальной ссылки в их полном объеме. Удаление метильной группы в положении N-12 может быть достигнуто с использованием известных процедур деметилирования.
В данную реакцию включен также способ, в котором заместителем является защитная группа, и эту защитную группу удаляют.
Группа N-H в положении 12 может быть дериватизована группой R12а. Подходящие примеры являются такими же, которые приведены в определении для R4, за исключением водорода. Предпочтительные примеры включают в себя ацил, в частности алкил-СО-; алкенил, в частности аллил; или алкил-О-СО-, в частности трет-BOC.
Способ получения эктеинасцидина 729 и родственных соединений может моделироваться на основе синтетических процедур, приведенных в WO 0187895. Обычно этот способ может использовать исходное соединение с метильной группой при N-12, которая замещена защитной группой.
Например, согласно способу данного изобретения соединение формулы (В):

где R21 имеет значение, определенное ранее, и Prot3 является защитной группой, подвергают превращению -СН2NH2 в положении 1 в -СН2ОН, защите -СН2ОН в положении 1, защите -ОН в положении 18, удалению метильной группы в положении 12, удалению защитной группы в положении 5, образованию 10-гидрокси-ди-6,8-енона, защите положения 12, удалению защитной группы в положении 1, образованию лабильной группы в положении 1, установленной для образования 1,4-мостика, образованию 1,4-мостика, удалению защиты положения 18, необязательной модификации 1,4-мостика, удалению защитной группы в положении 12 и необязательной дополнительной модификации этой структуры.
-СН2ОН в положении 1 защищают, например, трет-бутилдифенилсилилоксигруппой. -ОН в положении 18 защищают, например, метоксиэтоксиметильной группой. Положение 12 защищают, например, аллильной группой. Лабильную группу в положении 1 образуют обычно с использованием реагента формулы:
-СН2 -X'-C(=O)-CHNProt2-SH,
где X' обозначает -О- или -NProt1 и Prot1 и Prot2 имеют определенные выше значения. 1,4-мостик может быть модифицирован, например, удалением защиты из -NProt1- с получением группы -NH-, которая может быть затем дополнительно дериватизована, удалением защиты -NProt2- с получением группы -NH- и необязательно превращением в группу -С(=О)-, которая может быть затем дополнительно дериватизована, с получением, таким образом, диапазона возможностей для 1,4-мостика, определенного приведенной формулой -(1)СН2-Х-С(=О)-С(Ra)(Rb)-S(4)-.
Примеры дополнительных модификаций, которые могут проводиться на этой структуре, включают в себя одно или более изменений заместителя в положении 1, например, превращение нитрильной группы 21 в гидроксигруппу 21, изменение заместителя в положении 5, изменение заместителя в положении 18, окисление серы в 1,4-мостике, присоединение заместителя в положении 12 и превращение кольца Е в хинон.
Дополнительные подробности изобретения
Промежуточные продукты 1 и 16 (обозначаемые как промежуточные продукты 21 и 36 соответственно в заявках на патенты WO 0069862 и WO 0187895) применимы для получения других соединений эктеинасцидина, как подробно описано здесь. Здесь описаны также другие родственные хинону аналоги, получаемые из промежуточных продуктов 16 и 18 (обозначаемых как промежуточный продукт 35 в заявках на патенты WO 0069862 и WO 0187895).
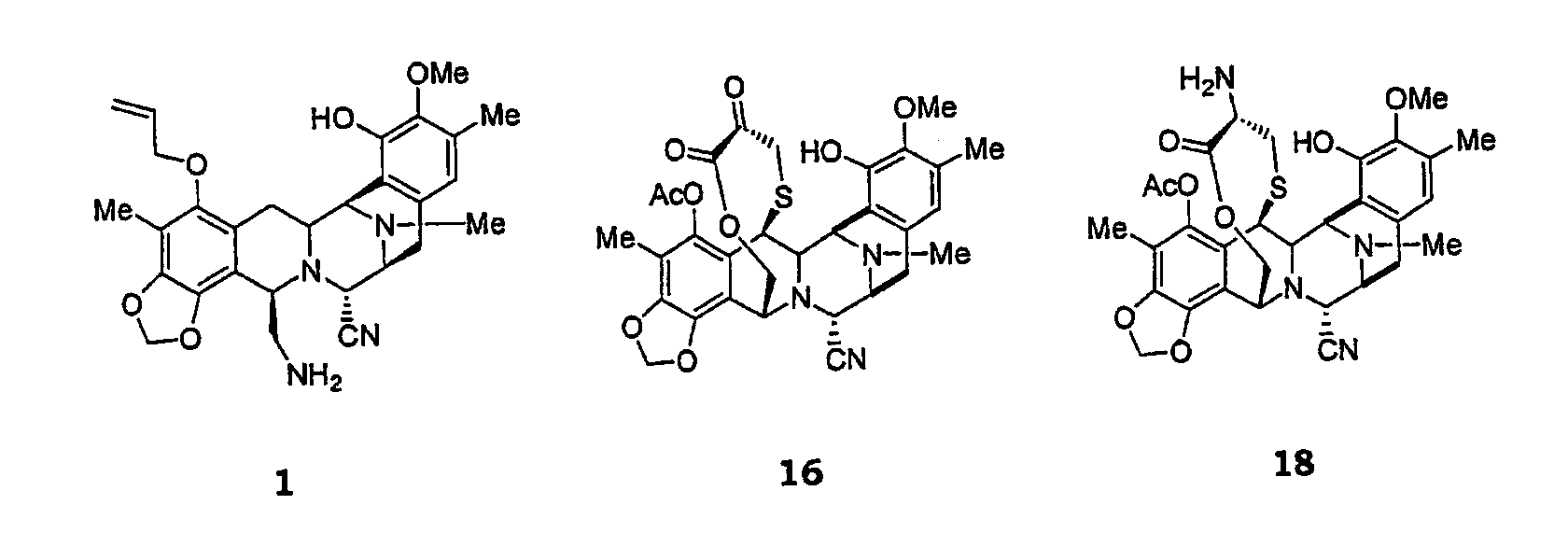
В частности, из промежуточного продукта 1 можно синтезировать природно встречающееся производное эктеинасцидина ЕТ729.

Подобным образом из промежуточного продукта 16 можно синтезировать природно встречающиеся производные эктеинасцидина ЕТ594, ЕТ745 и ЕТ759В (через ЕТ770 и ЕТ743 в качестве промежуточных продуктов) и хиноны, родственные ЕТ594 и ЕТ736 соответственно. Хинон, родственный ЕТ637, получают из промежуточного продукта 18.
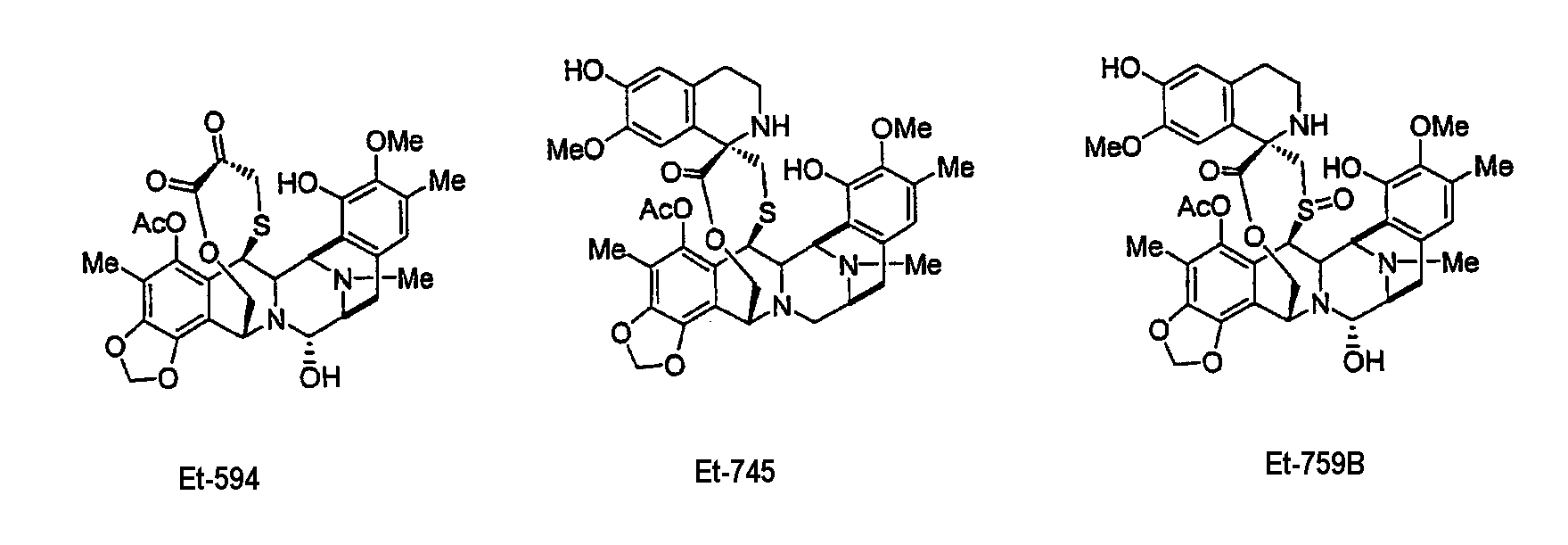
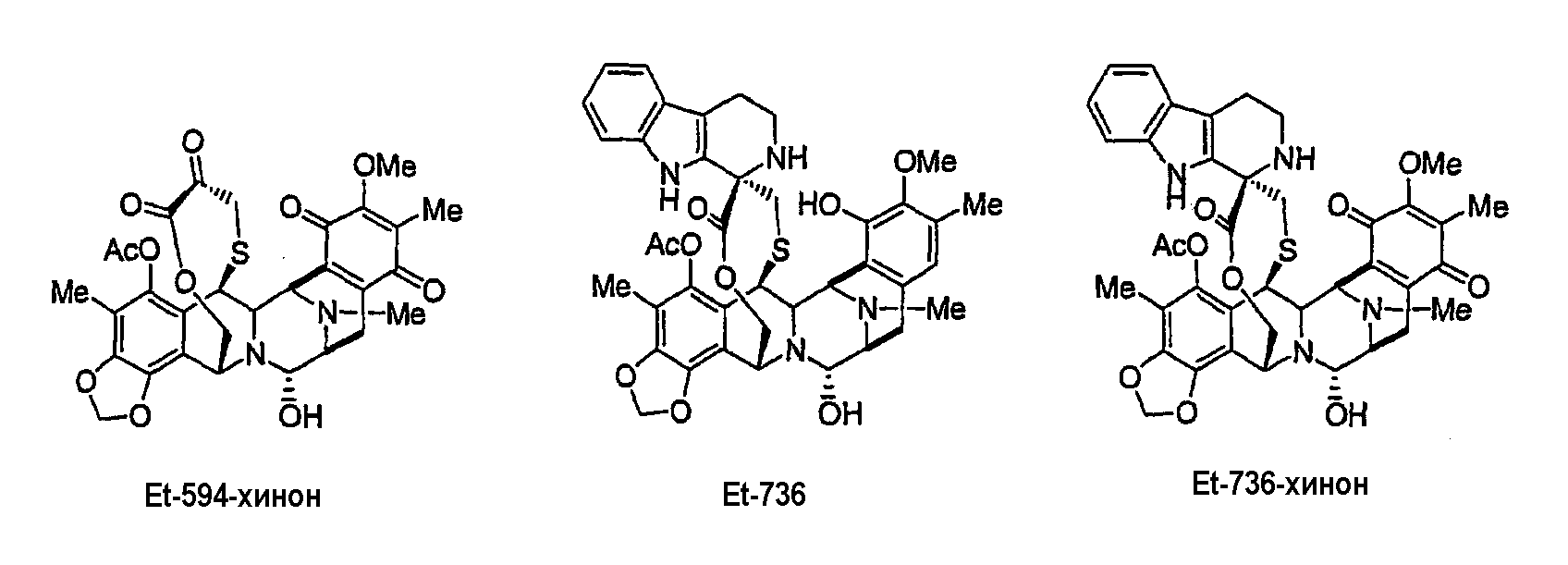
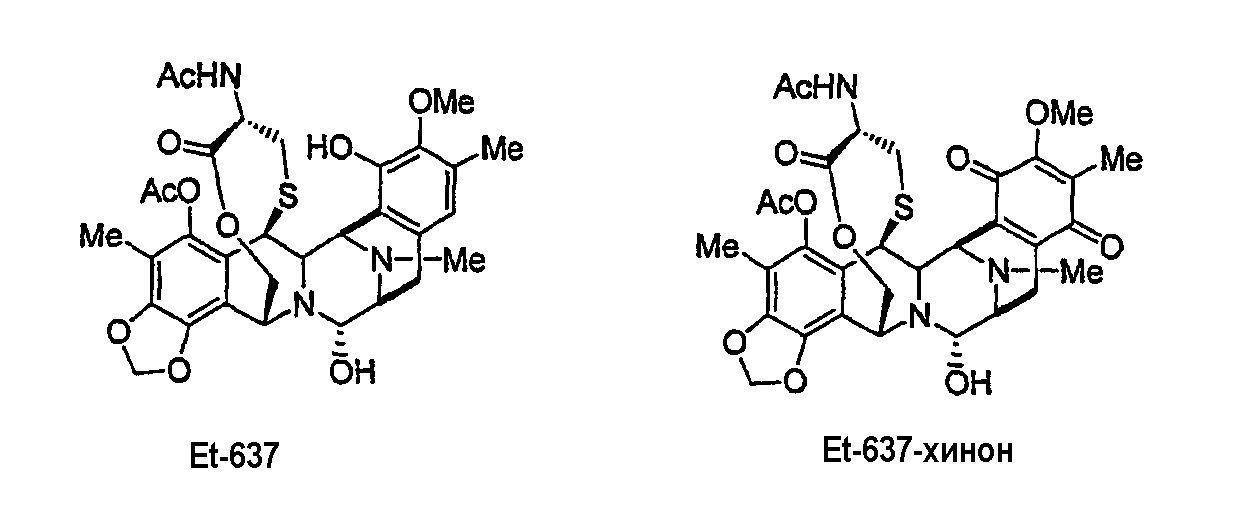
Синтез ЕТ729 описан здесь; данное изобретение относится также к получению новых аналогов ЕТ729 из промежуточного продукта 12 с использованием сходной последовательности синтеза.
В следующем аспекте данного изобретения промежуточный продукт 1 используют в синтезе нового семейства аналогов эктеинасцидина (таких как 77), в котором 1,4-мостик включает в себя амидную связь, а не лактонную связь, обнаруживаемую в ЕТ-743.
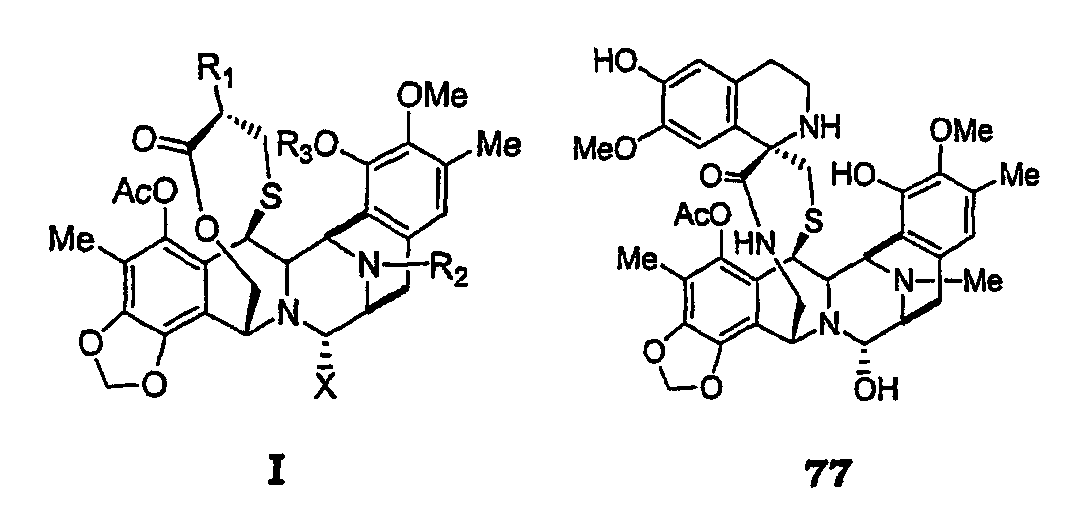
Таким образом, согласно данному изобретению заявляются производные эктеинасцидина, имеющие амидную связь, а не лактонную связь, обнаруживаемую в ЕТ-743, или у которых отсутствует этот мостик. Определение этих новых соединений исключает известные соединения эктеинасцидина. Эти новые соединения включают в себя соединения, представленные в таблице в конце этого описания, и их аналоги. Эти аналоги могут отличаться одним или несколькими заместителями от соединений, приведенных в примерах в заявках авторов WO 0187894, WO 0187895 или WO 0069862, и в общем находятся в релевантных формулах, приведенных в заявках авторов WO 0187894, WO 0187895 или WO 0069862.
Таким образом, общая формула для соединений данного изобретения получена идентификацией нового соединения в данном описании, в частности в таблице, и обобщением в соответствии с этими определениями остальной части этой молекулы на основе общей формулы предыдущих заявок. Предпочтительные определения, приведенные в более ранних заявках WO авторов данного изобретения, будут также использоваться в дальнейшем.
Синтетические способы данного изобретения обеспечивают первые способы для получения ЕТ729, ЕТ594, ЕТ745 и ЕТ759В; и хинонов, родственных ЕТ594, ЕТ637, ЕТ736, и имеющего мостиковую связь аналога-лактама ЕТ743 и родственных промежуточных продуктов. Кроме того, данное изобретение относится к синтетическим способам получения различных аналогов ЕТ729.
Такие синтетические способы могут обеспечить более экономичные пути к известным противоопухолевым агентам, а также позволить получать новые активные соединения.
Подходящие исходные материалы для этих новых синтетических способов включают в себя соединения, родственные природным бис(тетрагидроизохинолиновым) алкалоидам. Такие исходные материалы могут быть получены либо из различных классов антибиотиков сафрамицина и сафрацина, доступных из различных культуральных бульонов, как подробно описано в заявках на патенты WO 0187894 и WO 0187895, или с использованием других синтетических или биохимических процессов.
В одном конкретном аспекте данное изобретение относится к применению промежуточного продукта 1 (промежуточного продукта 21 в заявках на патенты WO 0187894 и WO 0187895) в новом синтетическом способе получения эктеинасцидина 729, как подробно изображено в схеме I.




Реагенты: а) NaNO2, AcOH, THF; b) TBDPSCI, Im, DMAP, DMF; c) MEMCl, NaH, THF/Н2О; d) m-CPBA, TEA, TFFA, DCM; e) HSnBu3, AcOH, (PPh3)2PdCl2, DCM; f) (PhSeO)2O, DCM; g) Cs2CO3, аллилBr, DMF; h) TBAF, THF; i) производное цистеина, EDC.HCl, DMAP, DIPEA, DCM; j) DMCO; Tf2O, DIPEA, трет-BuOH, трет-бутилтетраметилгуанидин, Ас2О, DCM; k) пара-TsOH, CHCl3; l) N-метилпиридин-4-карбоксальдегидйодид, DBU, оксалиловая кислота; m) 3-гидрокси-4-метоксифенетиламин, силикагель, EtOH; n) HSnBu3, (PPh3)2PdCl2, AcOH, DCM; o) AgNO3, CH3CN, Н2О
Обычно превращение промежуточного продукта 1 или родственного соединения в эктеинасцидин, такой как ЕТ729, включает в себя следующие превращения:
(а) Превращение NH2 в ОН, например, реакцией с нитритом натрия в уксусной кислоте.
(b) Защиту первичного ОН и фенольного Е-кольца.
(с) Деметилирование мостикового вторичного амина с последующим удалением защиты и окислением фенола А-кольца и последующим аллилированием мостикового амина.
(d) Удаление защиты и этерификацию первичного спирта защищенной боковой цепью цистеина с образованием промежуточного продукта 10.
(е) Образование мостикового кольца реакцией циклизации (с образованием 11) и последующие реакции удаления защиты N и О с образованием промежуточного продукта 12.
(f) Введение остатка допамина переаминированием и реакции Пикте-Шпенглера с образованием промежуточного продукта 14.
(g) Удаление N-аллилзащитной группы и превращение CN в ОН.
Таким образом, теперь можно превращать промежуточный продукт 1 (получаемый из цианосафрацина В) в ЕТ-729, что обеспечивает первый синтетический подход к этому природно встречающемуся эктеинасцидину.
Высокая активность промежуточных продуктов требует использование защитных групп для фенольного Е-кольца, боковой цепи цистеина, мостикового азота и первичного спирта для предотвращения нежелательных побочных реакций.
Таким образом, некоторое количество альтернативных промежуточных продуктов может образовываться в зависимости от конкретного выбора защитных групп. Применение других защитных групп, не описанных в описании подробно, также является частью данного изобретения.
В следующем аспекте, данное изобретение относится к новым способам превращения промежуточного продукта 16 (обозначаемого как промежуточный продукт 36 в заявках на патенты WO 0069862 и WO 0187895) в соединения эктеинасцидина ЕТ594, ЕТ745 и ЕТ759В, встречающиеся в природе, представленные подробно в схеме 2.
Промежуточный продукт 16 получают из промежуточного продукта 1, как описано в вышеупомянутых заявках на патенты, и он имеет структуру промежуточного продукта 13 схемы 1 с -Ме, присоединенным к N, вместо -аллила.
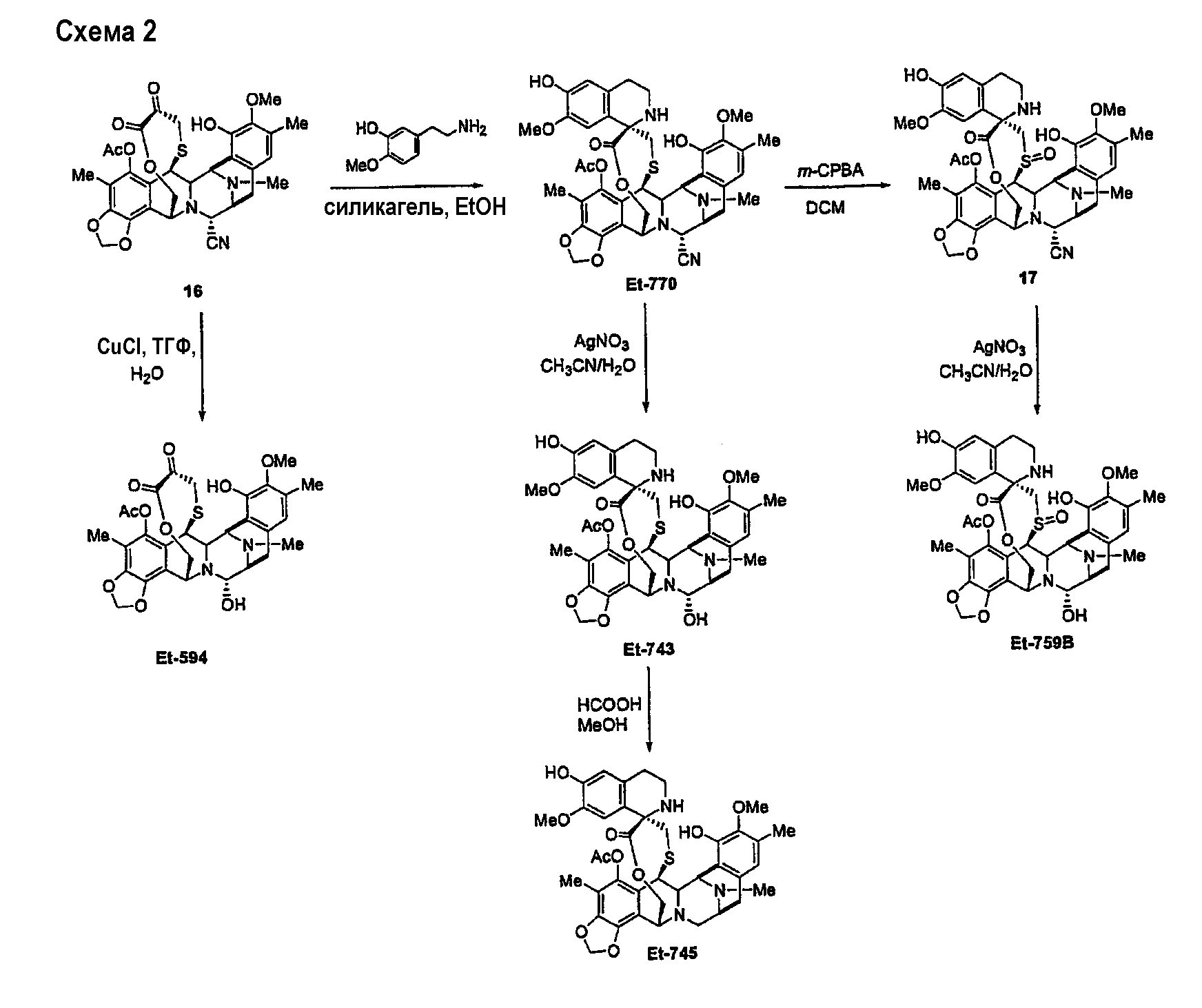
Более подробно, эти процессы включают в себя следующие превращения.
(а) Образование ЕТ594 из промежуточного продукта 16 в одностадийный превращением группы CN в группу ОН.
(b) Синтез ЕТ745 из ЕТ743 (получаемого в две стадии из промежуточного продукта 16) восстановительным отщеплением вторичной спиртовой группы.
(с) Образование ЕТ759В из промежуточного продукта 16 в трех стадиях, включающих в себя образование ЕТ770 с последующим окислением и превращением нитрильной группы в гидроксигруппу.
Таким образом, данное изобретение относится также к простым новым способам получения соединений эктеинасцидина ЕТ594, ЕТ745 и ЕТ759В, встречающихся в природе, из промежуточного соединения 16 (получаемого из цианосафрацина В).
Кроме того, данное изобретение относится к способу синтеза хиноновых производных ЕТ594, ЕТ637 и ЕТ736 из промежуточного соединения 16 (обозначаемого как промежуточное соединение 36 в заявках на патенты WO 0187894 и WO 0187895) и промежуточного соединения 18 (обозначаемого как промежуточное соединение 35 в заявках на патенты WO 0069862 и WO 0187895), (схема 3).

Более подробно, такие способы включают в себя следующие превращения.
(а) Образование ЕТ637-хинона из промежуточного продукта 18 в трех стадиях, включающих в себя образование промежуточного продукта 19 ацетилированием аминогруппы с последующим окислением фенольного кольца и превращением нитрильной группы в гидроксильную группу.
(b) Синтез ЕТ594-хинона в двух стадиях из промежуточного продукта 16 через реакцию окисления фенольного кольца и превращение нитрильной группы в гидроксильную группу.
(с) Синтез ЕТ736-хинона в трех стадиях из промежуточного продукта 16, включающих в себя введение триптаминовой части молекулы для образования промежуточного продукта 22, реакцию окисления и превращение нитрильной группы в гидроксильную группу.
Таким образом, данное изобретение относится к малостадийным и новым способам получения окисленных производных соединений эктеинасцидина ЕТ594, ЕТ637 и ЕТ736 встречающихся в природе промежуточных продуктов 16 и 18 (оба из которых могут быть получены из цианосафрацина В).
В следующем варианте и в соответствии с последовательностью синтеза ЕТ729 данное изобретение относится к способам получения новых и различных аналогов ЕТ729 из промежуточного продукта 12. Предпочтительные способы получения соединений формул I, II и III описаны ниже в следующих реакционных схемах с примерами типичных групп-заместителей.

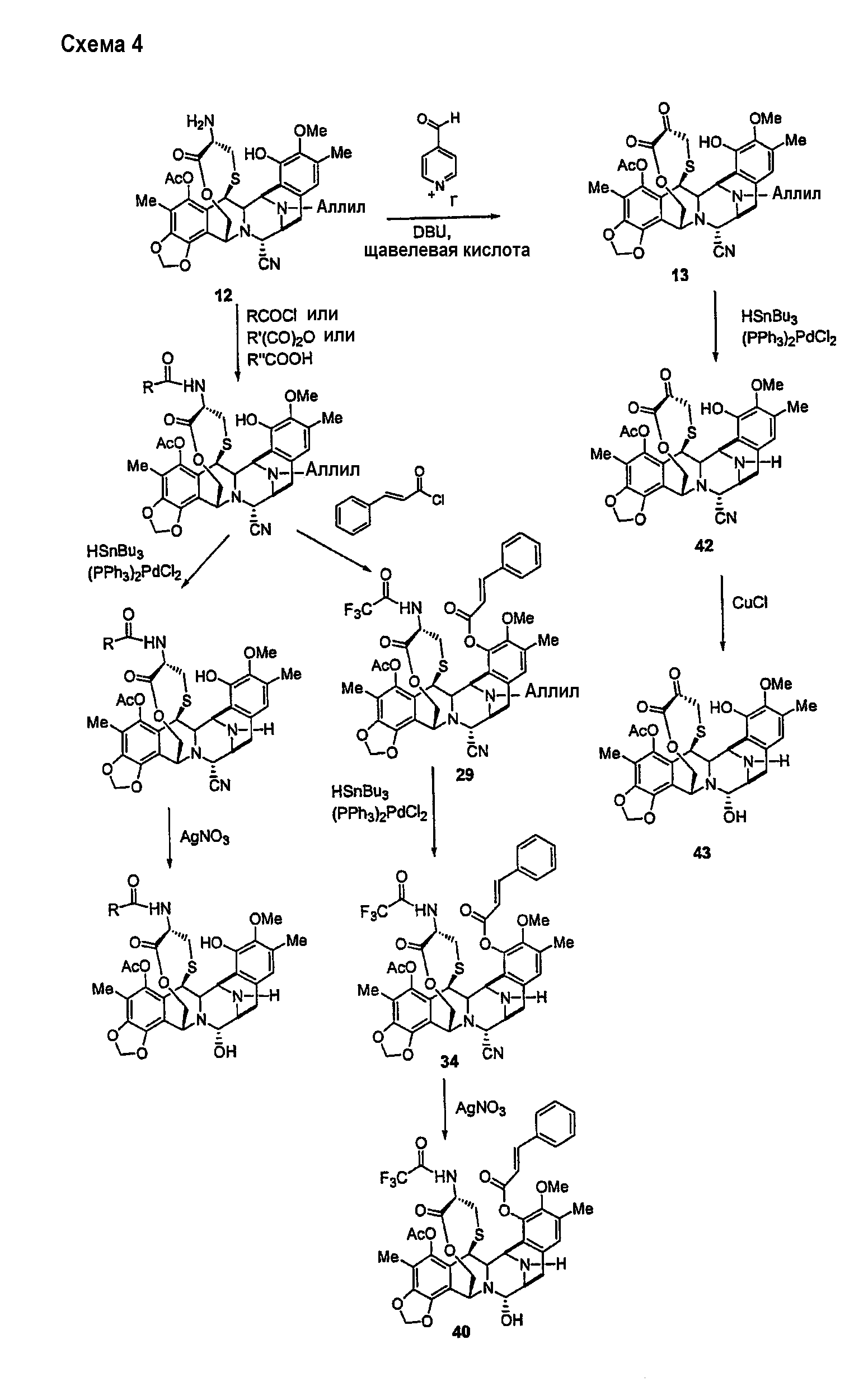
Обычно превращение промежуточного продукта 12 или 13 в различные аналоги ЕТ729 включает в себя следующие превращения:
(а) Реакции ацилирования посредством различных процедур, описанных в экспериментальной части, реакции деаллилирования при N-12 и взаимопревращение нитрильной группы в гидроксильную группу. Соединение 40 является примером промежуточного продукта с типичными группами-заместителями, где определено место двух последовательных реакций ацилирования, с последующими двумя последними стадиями, описанными выше.
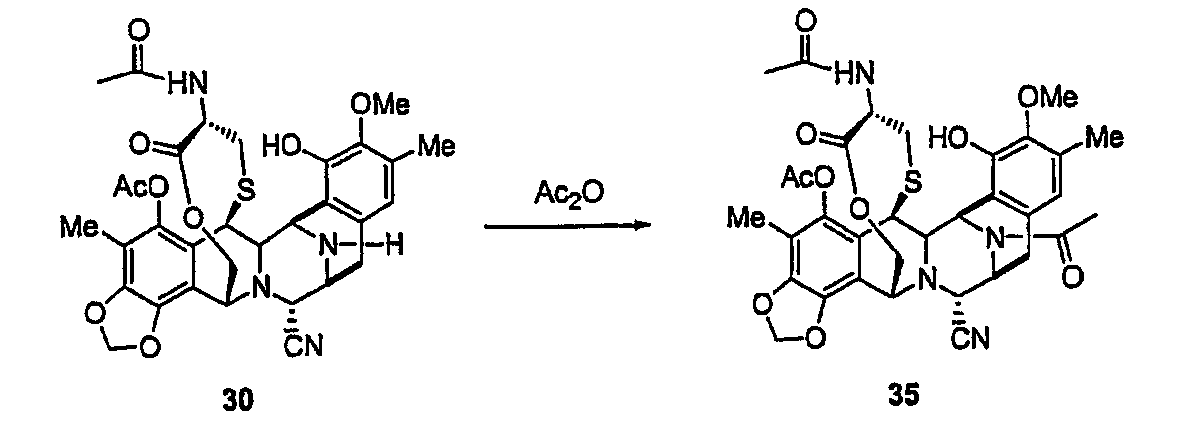
(b) Образование соединения 35 из промежуточного продукта 30 одностадийной реакцией ацетилирования в положении N-12.
(с) Синтез соединения 43 из соединения 13 реакцией деаллилирования и превращением нитрильной группы в гидроксильную группу с использованием CuCl.
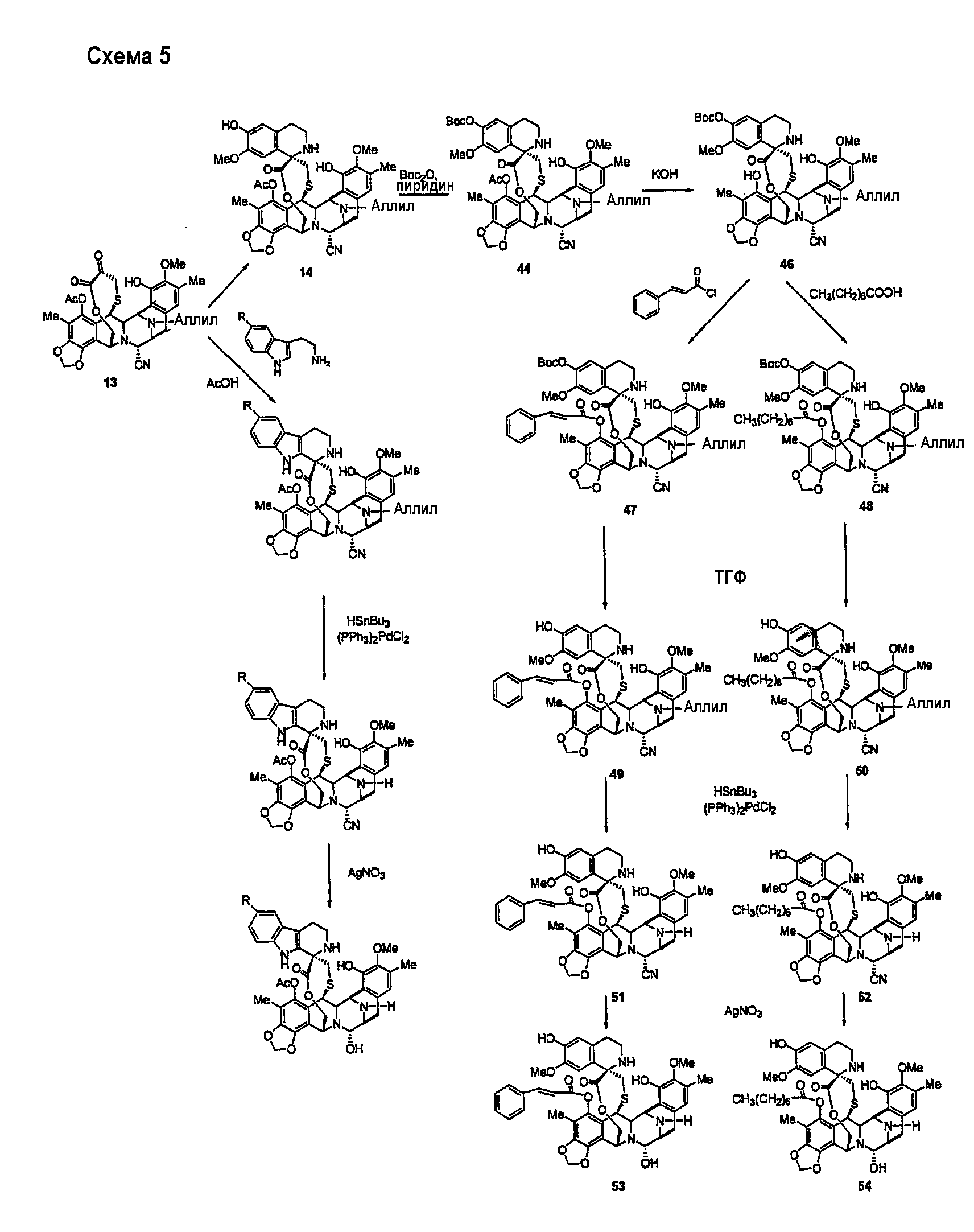
Более подробно, эти процессы включают в себя следующие превращения из промежуточного продукта 13.
(а) Двухстадийное образование промежуточного продукта 46 из соединения 14 посредством защиты гидроксильной группы в виде Вос-карбоната и деацетилирования при С-5 с использованием КОН.
(b) Синтез соединений 53 и 54 из промежуточного продукта 46 с использованием той же самой последовательности синтеза: реакция ацилирования при С-5 циннамоилхлоридом или октановой кислотой, удаление карбонатной группы, реакция деаллилирования при N-12 и, наконец, превращение нитрильной группы в гидроксильную группу.
(с) Синтез других аналогов ЕТ729 из промежуточного продукта 13, включающий в себя три стадии: введение триптаминовой группы, реакцию деаллилирования и превращение нитрильной группы в гидроксильную группу.
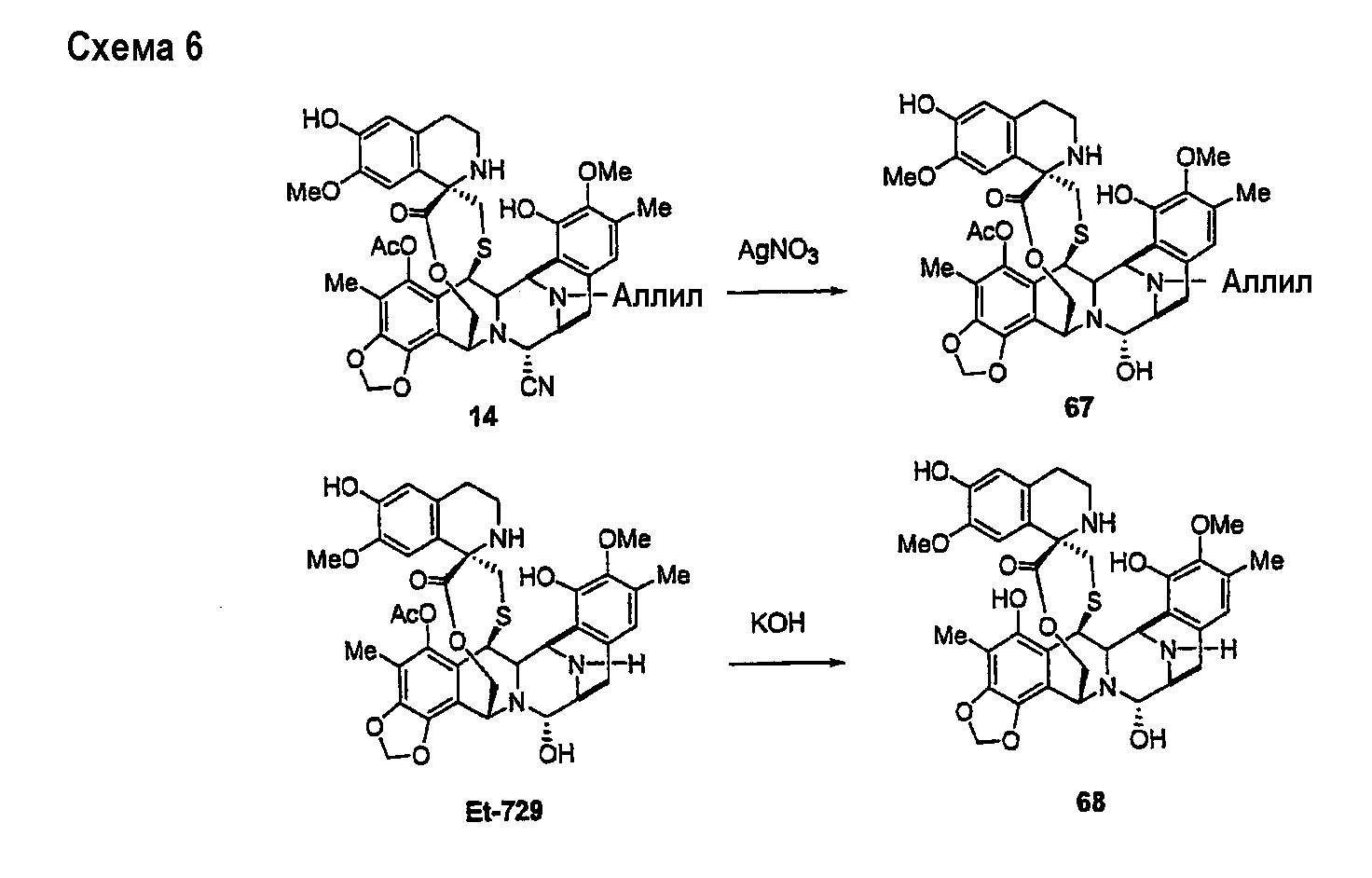
Более подробно, схема 6 описывает синтез соединения 67 и соединения 68 из промежуточного продукта 14 и ЕТ729 соответственно.
В следующем варианте данное изобретение относится к способу синтеза нового семейства соединений эктеинасцидина, в котором лактонная связь 1,4-мостика ЕТ743 и родственных промежуточных продуктов заменена амидной связью, как подробно показано в схеме 7.
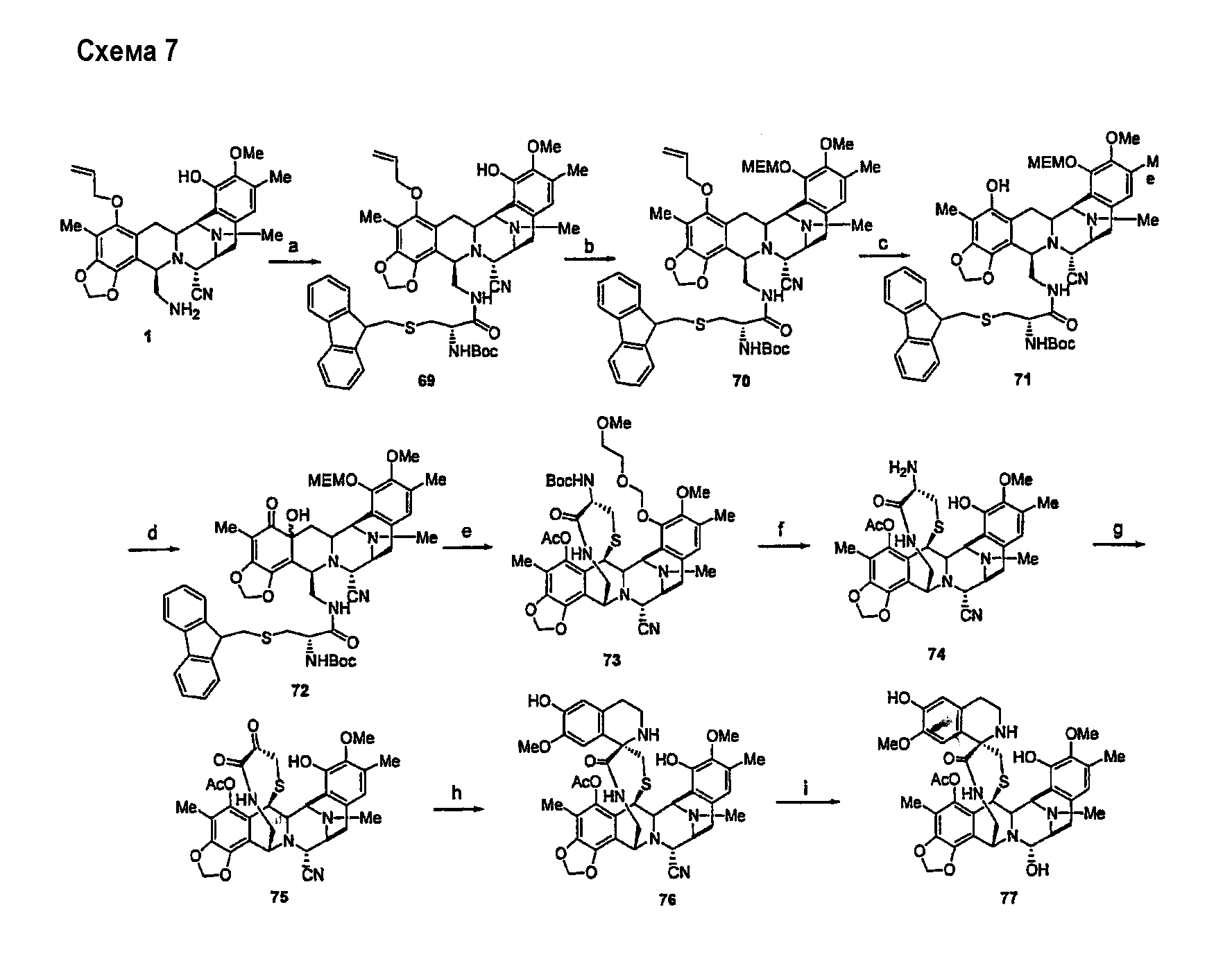
Более подробно, промежуточный продукт 1 (промежуточный продукт 21 в заявках на патенты WO 0069862 и WO 0187895) может быть превращен в такие соединения с использованием следующей последовательности стадий:
(а) Одностадийное введение фрагмента защищенного цистеина путем связывания с группой первичного амина промежуточного продукта 1.
(b) Манипулирование защитными группами и реакция окисления с образованием промежуточного продукта 72.
(с) Циклизация с получением желаемой лактамной мостиковой структуры с последующим удалением защиты первичного амина.
(d) Завершение синтеза трансаминированием, реакцией Пикте-Шпенглера и превращением нитрила в гидроксильную группу.
Таким образом, данное изобретение относится к способу синтеза большого семейства соединений, родственных ЕТ743, в которых лактонная связь мостиковой структуры заменена лактамной связью.
Реакционные схемы, описанные в данном описании, могут быть модифицированы и/или комбинированы различными путями, и альтернативные последовательности реакционных стадий и получаемые соединения являются частью данного изобретения.
Таким образом, этими и другими путями можно превращать цианосафрацин В в ряд промежуточных продуктов и производных с потенциальной противоопухолевой терапевтической активностью. Эти промежуточные продукты могут быть получены с использованием уже описанных соединений в качестве исходных материалов или с использованием альтернативных путей.
Новые активные соединения
Авторы изобретения обнаружили также, что некоторые из соединений данного изобретения, которые авторы первоначально получали в качестве промежуточных продуктов, имеют исключительно высокую активность в лечении раков, таких как лейкозы, рак легкого, рак ободочной кишки, рак почки и меланома.
Таким образом, данное изобретение относится к способу лечения любого млекопитающего, в частности человека, пораженного раком, предусматривающий введение пораженному индивидууму терапевтически эффективного количества соединения данного изобретения или его фармацевтической композиции.
Данное изобретение относится также к фармацевтическим препаратам, которые содержат в качестве активного ингредиента соединение или соединения данного изобретения, а также способам их приготовления.
Примеры фармацевтических композиций включают в себя любое твердое вещество (таблетки, пилюли, капсулы, гранулы и т.д.) или жидкость (растворы, суспензии или эмульсии) с подходящим составом или пероральным, местным или парентеральным введением, и они могут содержать чистое соединение или соединение в комбинации с любым носителем или другими фармакологически активными соединениями. Эти композиции могут требовать стерилизации при парентеральном введении.
Введение соединений или композиций данного изобретения может выполняться любым подходящим способом, таким как внутривенное вливание (инфузия), введение пероральных препаратов, внутрибрюшинное и внутривенное введение. Авторы предпочитают использование времени инфузии до 24 часов, более предпочтительно 2-12 часов, причем наиболее предпочтительными являются периоды инфузии 2-6 часов. Особенно желательными являются короткие периоды времени инфузии, которые могут выполняться без оставления пациента на ночь в больнице. Однако, если требуется, инфузия может продолжаться 12-24 часа или даже в течение более продолжительного времени. Инфузия может выполняться с подходящими интервалами, например в течение 2-4 недель. Фармацевтические композиции данного изобретения могут доставляться инкапсулированными в липосомах или наносферах, в композициях пролонгированного высвобождения или другими стандартными средствами доставки.
Точная доза этих соединений будет варьироваться в соответствии с конкретной формой, способом введения и конкретным положением органа в теле, хозяином и подлежащей лечению опухолью. Следует принимать во внимание и другие факторы, такие как возраст, масса тела, пол, пищевой рацион, время введения, скорость экскреции, состояние пациента, комбинации лекарственных веществ, чувствительность к препаратам и тяжесть заболевания. Введение может проводиться непрерывно или периодически в максимальной переносимой дозе.
Соединения и композиции данного изобретения могут быть использованы с другими лекарственными средствами для обеспечения комбинаторной терапии. Другие лекарственные средства могут образовывать часть той же самой композиции или могут быть обеспечены в виде отдельной композиции для введения одновременно или в другое время. Идентичность другого лекарственного средства особо не ограничивается и подходящие кандидаты таких лекарственных средств включают в себя:
а) лекарственные средства с антимитотическими действиями, в частности, такие, которые нацелены на элементы цитоскелета, в том числе модуляторы микротрубочек, такие как таксановые лекарственные средства (такие как таксол, паклитаксел, таксотере, доцетаксел), подофилотоксины или винкаалкалоиды (винкристин, винбластин);
b) лекарственные средства-антиметаболиты, такие как 5-фторурацил, цитарабин, гемцитабин, аналоги пуринов, такие как пентостатин, метотрексат);
с) алкилирующие агенты, такие как азотные аналоги горчичного газа (такие как циклофосфамид или ифофосфамид);
d) лекарственные средства, которые нацелены на ДНК, такие как антрациклиновые лекарственные средства адриамицин, доксорубицин, фарморубицин или эпирубицин;
е) лекарственные средства, которые нацелены на топоизомеразы, такие как этопозид;
f) гормоны и агонисты или антагонисты гормонов, такие как эстрогены, антиэстрогены (тамоксифен и родственные соединения) и андрогены, флутамид, лейпрорелин, гозерелин, ципротрон или октреотид;
g) лекарственные средства, которые нацелены на трансдукцию сигналов в опухолевых клетках, в том числе производные антител, такие как герцептин;
h) алкилирующие лекарственные средства, такие как содержащие платину лекарственные средства (цисплатин, карбонплатин, оксалиплатин, параплатин) или нитрозомочевины;
i) лекарственные средства, потенциально влияющие на метастазирование опухолей, такие как ингибиторы металлопротеиназ клеточного матрикса;
j) агенты генотерапии и антисмысловые агенты;
k) содержащие антитела терапевтические средства;
l) другие биологически активные соединения морского происхождения, в особенности дидемнины, такие как аплидин;
m) аналоги стероидов, в частности дексаметазон;
n) противовоспалительные лекарственные средства, в частности дексаметазон; и
о) противорвотные лекарственные средства, в частности дексаметазон.
Данное изобретение относится также к соединениям данного изобретения для применения в способе лечения и для применения этих соединений в приготовлении композиции для лечения рака.
ПРИМЕРЫ
Данное изобретение иллюстрируется следующими примерами.
Экспериментальная часть
Пример 1

Раствор соединения 1 (9,84 г, 18,97 ммоль) в ТГФ (569 мл) и Н2О (285 мл) охлаждали при 0°С при помощи бани со льдом. Затем добавляли NaNO2 (1,96 г, 28,45 ммоль) и 90% водного АсОН (18,97 мл, 0,33 моль) при 0°С и эту смесь перемешивали при 23°С в течение 18 часов. После охлаждения реакционной смеси до 0°С добавляли насыщенный водный раствор бикарбоната натрия (300 мл, щелочной рН) и дихлорметан (500 мл). После экстракции водную фазу дополнительно экстрагировали дихлорметаном (2×300 мл). Объединенные органические экстракты сушили над сульфатом натрия и упаривали досуха при пониженном давлении. Затем неочищенное твердое вещество растворяли в МеОН (379 мл) и добавляли 1 М NaOH (38 мл) при 0°С. Эту смесь перемешивали при 23°С в течение 4 часов. После разбавления EtOAC (600 мл) при 0°С органический слой промывали смесью воды (400 мл), насыщенного водного раствора бикарбоната натрия (100 мл, щелочной рН). После экстракции водную фазу дополнительно экстрагировали EtOAC (3×300 мл). Объединенные органические экстракты сушили над Na2SO4, фильтровали и концентрировали в вакууме. Остаток очищали колоночной флэш-хроматографией (SiO2, градиент гексан:EtOAC от 3:1 до 2:1) с получением 2 (4,55 г, 46%) в виде белого твердого вещества.
Rf: 0,33 (гексан:EtOAC 1:1).
1H ЯМР (300 МГц, CDCl3) 6,48 (c, 1H), 6,15-6,02 (м, 1H), 5,92 (д, 1H), 5,86 (д, 1H), 5,77 (c, 1H), 5,39 (дд, 1H), 5,26 (дд, 1H), 4,24-4,15 (м, 3H), 4,04 (д, 1H), 3,97 (т, 1H), 3,74 (c, 3H), 3,64 (дт, 1H), 3,43 (дд, 1H), 3,38-3,34 (м, 2H), 3,31 (т, 1H), 3,22 (дд, 1H), 3,10 (дд, 1H), 2,49 (д, 1H), 2,34 (c, 3H), 2,24 (c, 3H), 2,11 (c, 3H), 1,88 (дд, 1H).
13С ЯМР (75 МГц, CDCl3) 148,6, 146,7, 144,4, 143,0, 138,9, 133,9, 130,2, 129,1, 121,1, 120,9, 117,7, 117,4, 116,8, 113,3, 112,3, 101,1, 74,3, 63,7, 60,6, 60,1, 58,1, 56,9, 56,7, 55,4, 41,7, 26,2, 25,7, 15,7, 9,3.
ESI-MC m/z: Вычислено для С29Н33N3O6: 519,59. Найдено (М+1)+: 520,3.
Пример 2
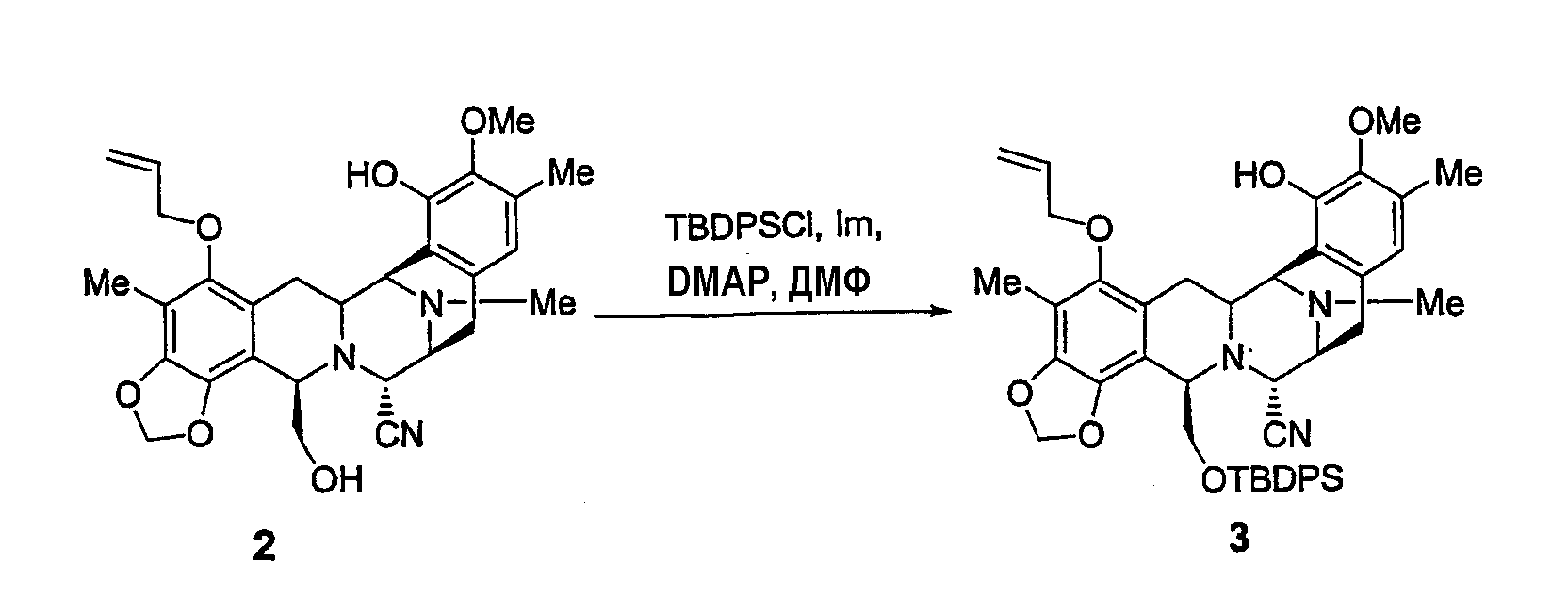
К раствору соединения 2 (9,33 г, 0,018 моль) в безводном ДМФ (40 мл, 0,45 М) добавляли при 23°С имидазол (3,05 г, 0,045 моль) и DMAP (219 мг, 0,0018 моль). Раствор охлаждали при 0°С и добавляли по каплям TBDPSCl (7,0 мл, 0,027 моль) в атмосфере аргона. Реакционной смеси давали достичь 23°С и оставляли ее при этой температуре на 1 час и 15 минут. После этого периода времени добавляли воду (350 мл) и смесь этилацетат/гексан (3:2, 250 мл). Органическую фазу отделяли, сушили над сульфатом натрия и фильтровали и растворитель удаляли при пониженном давлении. Неочищенный материал очищали колоночной флэш-хроматографией (смеси элюентов этилацетат/гексан в градиенте от 15:85 до 2:3) с получением 3 (11,8, 87%) в виде желтого твердого вещества.
Rf: 0,36 (этилацетат/гексан 2:3).
1H ЯМР (300 МГц, CDCl3): δ 7,55 (д, 2H), 7,41-7, 22 (м, 8H), 6,45 (c, 1H), 6,18-6,02 (м, 1H), 6,78 (c, 2H), 6,61 (c, 1H), 5,35 (д, 1H), 5,21 (д, 1H), 4,42 (д, 1H), 4,18 (м, 2H), 4,05 (м, 2H), 3,78 (c, 3H), 3,64 (дд, 1H), 3,41-3,31 (м, 2H), 3,29-3,20 (м, 2H), 3,02 (дд, 1H), 2,70 (д, 1H), 2,30 (c, 3H), 2,28 (c, 3H), 2,08 (c, 3H), 2,02 (дд, 1H), 0,90 (c, 9H).
13С ЯМР (75 МГц, CDCl3) δ: 148,69, 146,94, 144, 33, 142,90, 139,35, 135,98, 135,67, 134,27, 133,56, 132,94, 131,49, 129,84, 129,70, 128,59, 127,79, 127,73, 122,13, 121,24, 118,94, 117,61, 117,55, 113,22, 112,04, 101,12, 74,52, 68,24, 61,89, 60,93, 59,29, 57,68, 57,06, 55,73, 42,01, 26,93, 26,79, 25,84, 19,19, 16,07, 9,56.
ESI-MC m/z: Вычислено для С45Н51N3O6Si: 757,3. Найдено (М+Na)+: 780,3.
Пример 3
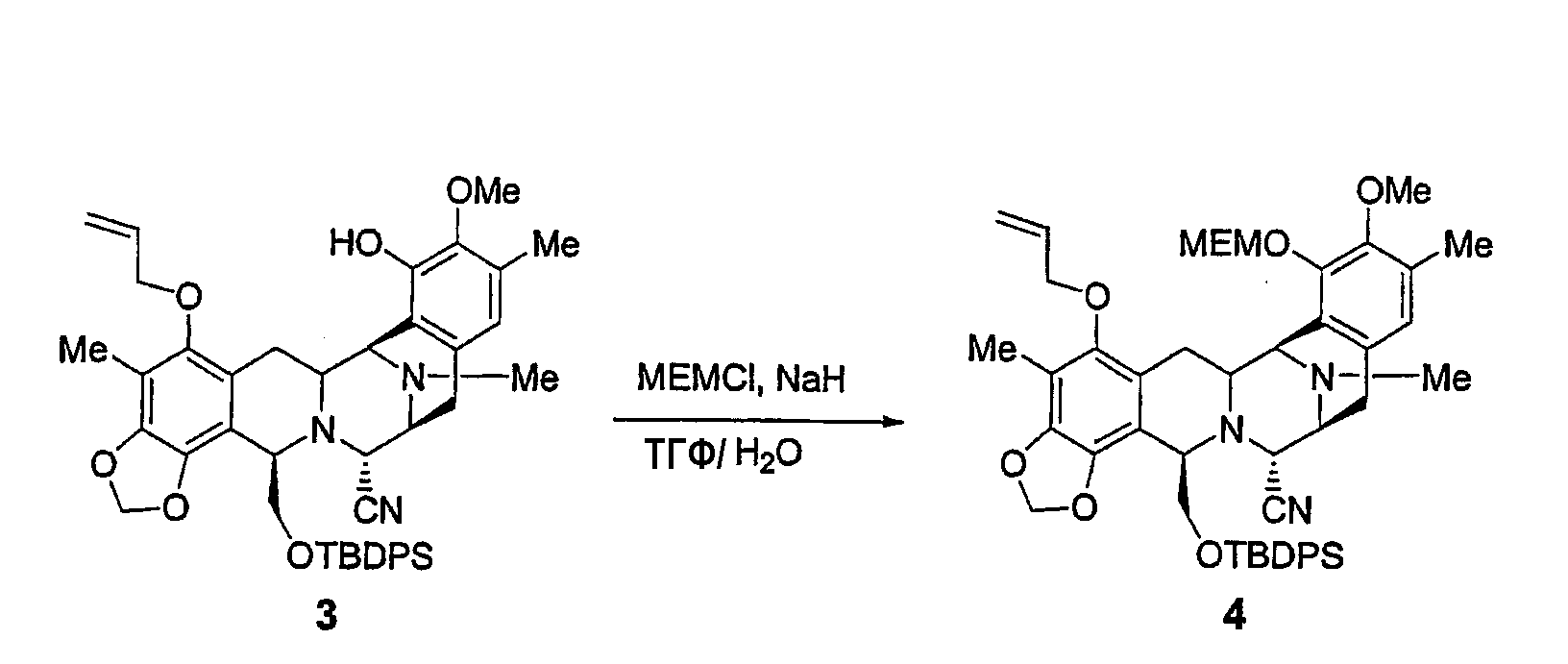
К раствору промежуточного продукта 3 (11,75 г, 0,016 моль) в смеси ТГФ/Н2О (113 мл/0,31 мл, 0,14 М) добавляли МЕМ-хлорид (3,0 мл, 0,026 моль). Раствор охлаждали при 0°С и добавляли в виде порций гидрида натрия (930 мг, 0,023 моль) (в течение 1 часа и 15 минут). Реакционную смесь оставляли при 0°С в атмосфере аргона на 1 час. После этого периода времени добавляли воду (150 мл) и водную фазу экстрагировали дихлорметаном (2×150 мл). Объединенные органические слои сушили над сульфатом натрия, фильтровали и растворитель удаляли при пониженном давлении с получением промежуточного продукта 4 (13,4 г, 100%) в виде желтого твердого вещества. Это соединение использовали на следующей стадии без очистки.
Rf: 0,32 (этилацетат/гексан 1:2).
1H ЯМР (300 МГц, CDCl3): δ 7,58 (д, 2H), 7,38 (м, 6H), 7,27 (м, 2H), 6,70 (c, 1H), 6,18-6,02 (м, 1H), 5,75 (c, 1H), 5,60 (c, 1H), 5,40 (д, 1H), 5,28 (д, 1H), 5,24 (д, 1H), 5,19 (д, 1H), 4,50 (ушир.c, 1H), 4,38 (ушир.c, 1H), 4,20-3,97 (м, 4H), 3,85 (м, 1H), 3,70 (c, 3H), 3,58 (м, 3H), 3,38 (c, 3H), 3,38 (м, 2H), 3,22 (м, 2H), 3,02 (дд, 1H), 2,70 (д, 1H), 2, 38 (c, 3H), 2,24 (c, 3H), 2,05 (c, 3H), 1,93 (дд, 1H), 0,84 (c, 9H).
13С ЯМР (75 МГц, CDCl3) δ: 148,76, 148,60, 148,49, 139,29, 135,87, 135,63, 134,18, 133, 23, 132,89, 130,85, 130,49, 129,89, 129,77, 127,82, 127,73, 125,45, 121,76, 118,45, 117,55, 113,23, 111,97, 101,13, 98,49, 95,79, 74,26, 71,98, 71,95, 69,57, 67,44, 67,37, 66,95, 61,32, 59,85, 59,18, 59,10, 57,50, 57,16, 55,58, 41,69, 29,87, 26,83, 26,83, 26,12, 19,05, 16,07, 9,46.
ESI-MC m/z: Вычислено для С49Н59N3O8Si: 845,4. Найдено (М+1)+: 846,3.
Пример 4
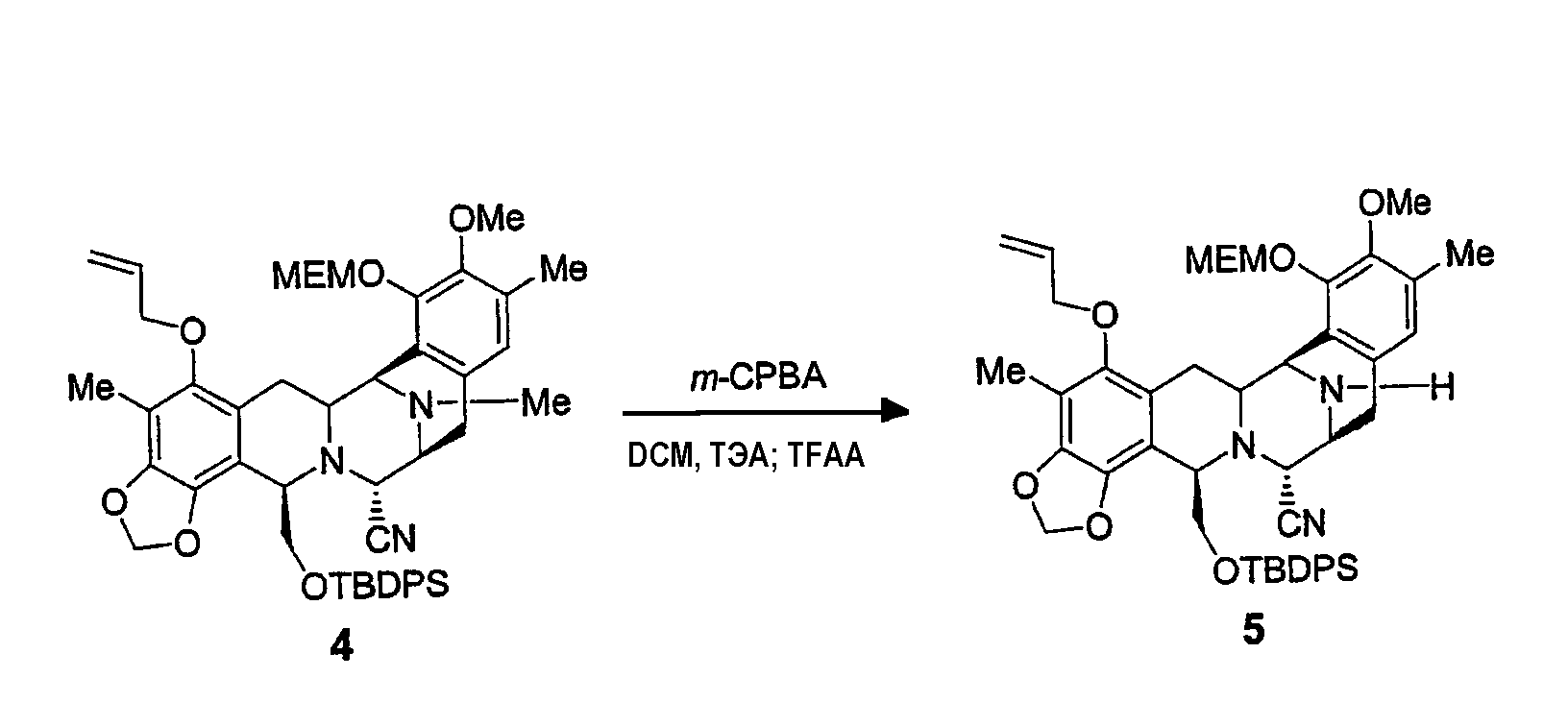
К раствору промежуточного продукта 4 (2,51 г, 0,003 моль) в безводном дихлорметане (25 мл, 0,12 М) добавляли m-CPBA (1,33 г, 0,006 моль) при -20°С в атмосфере аргона. Раствору давали достичь -10°С в течение 25 минут, добавляли ТЭА (4,14 мл, 0,03 моль) и реакционную смесь оставляли при 0°С, наконец, добавляли по каплям TFAA (6,29 мл, 0,045 моль) и этот раствор выдерживали при 0°С в течение 30 минут. После этого периода времени добавляли воду и водную фазу отделяли, сушили над сульфатом натрия, фильтровали и растворитель удаляли при пониженном давлении. Неочищенный материал очищали колоночной флэш-хроматографией (смеси элюентов этилацетат/гексан в градиенте от 1:4 до 6:1 и конечные промывки метанолом) с получением промежуточного продукта 5 (2,1 г, 85%) в виде желтого твердого вещества.
Rf: 0,19 (этилацетат/гексан 1:1).
1H ЯМР (300 МГц, CDCl3): δ 7,55 (д, 2H), 7,45-7,28 (м, 8H), 6,70 (c, 1H), 6, 14-6,02 (м, 1H), 5,81 (д, 1H), 5,67 (д, 1H), 5,43-5,35 (м, 2H), 5,26 (м, 2H), 5,03 (ушир.c, 1H), 4,73 (ушир.c, 1H), 4,68 (м, 1H), 4,22-4,09 (м, 3Н), 3,81 (ушир.с, 2Н), 3,73 (с, 3Н), 3,61 (дд, 1Н), 3, 53 (ушир.с, 4Н), 3,46-3,28 (м, 2Н), 3,34 (с, 3Н), 2,97 (д, 1Н), 2,25 (с, 3Н), 2,11 (с, 3Н), 1,95 (дд, 1Н), 0,94 (с, 9Н).
ESI-MC m/z: Вычислено для С48Н57N3O8Si: 831,4. Найдено (М+Na)+: 832,3.
Пример 5
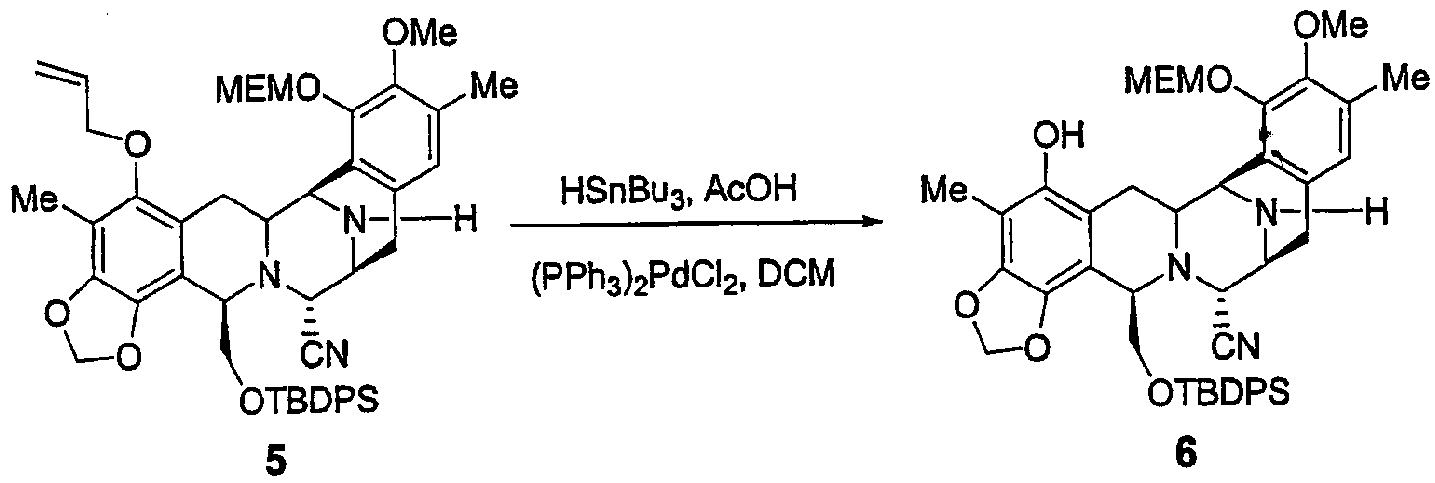
К раствору промежуточного продукта 5 (5,9 г, 7,09 ммоль), (PPh3)2PdCl2 (399 мг, 0,57 ммоль), уксусной кислоты (2,03 мл, 35,47 ммоль) в безводном дихлорметане (45 мл, 0,16 М) добавляли по каплям при 23°С гидрид трибутилолова (6,7 мл, 24,83 ммоль). Реакционную смесь оставляли при 23°С в атмосфере аргона на 35 минут. Реакционную смесь выливали на колонку (смеси элюентов этилацетат/гексан в градиенте от 1:4 до 8,1) с получением промежуточного продукта 6 (3,97 г, 71%) в виде желтого твердого вещества.
Rf: 0,17 (этилацетат/гексан 1:1).
1H ЯМР (300 МГц, CDCl3): δ 7,57 (д, 2H), 7,43-7,24 (м, 8H), 6,68 (c, 1H), 5,73 (д, 1H), 5,58 (д, 1H), 5,47 (д, 1H), 5,22 (д, 1H), 4,54 (д, 1H), 4,47 (д, 1H), 4,14 (м, 1H), 4,04 (дд, 1H), 3,94 (м, 1H), 3,73-3,65 (м, 4H), 3,70 (c, 3H), 3,39 (c, 3H), 3,38-3,30 (м, 2H), 3,25 (м, 1H), 3,11 (дд, 1H), 2,91 (д, 1H), 2,24 (c, 3H), 2,06 (c, 3H), 1,84 (дд, 1H), 0,91 (c, 9H).
ESI-MC m/z: Вычислено для С45Н53N3O8Si: 791,4. Найдено (М+Na)+: 814,3.
Пример 6
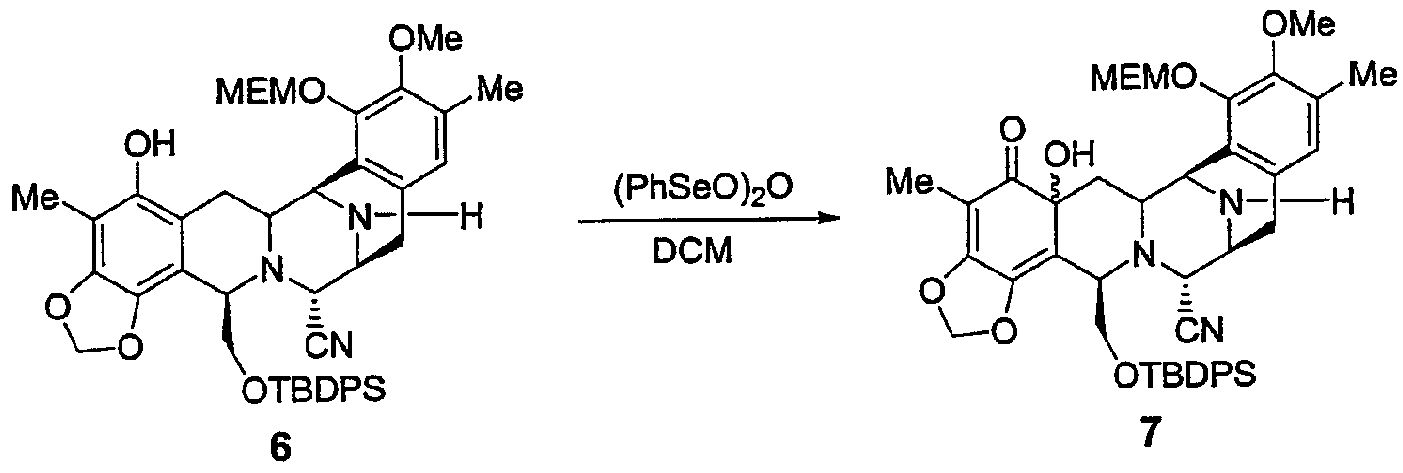
К раствору промежуточного продукта 6 (1,87 г, 2,36 ммоль) в безводном дихлорметане (20 мл, 0,12 М) добавляли по каплям при -15°С в атмосфере аргона раствор бензолселенинового ангидрида (1,82 г, 3,53 ммоль) в безводном дихлорметане (20 мл). Раствор оставляли при -15°С на 25 минут. Реакционную смесь разбавляли дихлорметаном и добавляли насыщенный раствор бикарбоната натрия при -10°С. Водную фазу экстрагировали дихлорметаном, объединенные органические слои сушили над сульфатом натрия, фильтровали и растворитель удаляли при пониженном давлении. Неочищенный продукт этой реакции очищали колоночной флэш-хроматографией (смеси элюентов этилацетат/гексан в градиенте от 1:6 до 6:1) с получением промежуточного продукта 7 (1,53 г, 80%) в виде желтого твердого вещества и в виде смеси изомеров 3:1 согласно1Н ЯМР.
Rf: 0,24 (этилацетат/гексан 2:1).
1H ЯМР (300 МГц, CDCl3): δ 7,64 (дд, 6H), 7,57 (д, 2H), 7,40-7,25 (м, 12H), 6,65 (c, 1H), 6,53 (c, 1H), 5,65 (c, 1H), 5,42 (c, 1H), 5,25 (c, 1H), 5,23 (c, 1H), 5,22 (м, 1H), 5,19 (д, 1H), 5,11 (д, 1H), 5,06 (д, 1H), 4,80 (c, 1H), 4,73 (c, 1H), 4,43 (д, 1H), 4,36 (м, 1H), 4,32 (м, 1H), 4,25 (д, 1H), 3,97 (дд, 1H), 3,89 (c, 3H), 3,86-3,77 (м, 4H), 3,74-3,60 (м, 4H), 3,59 (c, 3Н), 3,55-3,48 (м, 4H), 3,38-3,35 (м, 2H), 3,34 (c, 3H), 3,31 (c, 3Н), 3,18-3,03 (м, 2H), 2,96 (дд, 1H), 2,73 (д, 1H), 2,57 (д, 1H), 2,21 (c, 3H), 2,14 (c, 3Н), 2,17-1,86 (м, 2H), 1,75 (c, 3Н), 1,70 (c, 3Н), 1,07 (c, 9H), 0,99 (c, 9H).
13C ЯМР (75 МГц, CDCl3): δ 201,05, 197,78, 160,43, 158,64, 148,81, 147,84, 146,88, 146,70, 140,01, 137,97, 135,99, 135,97, 135,79, 133,64, 133,00, 132,80, 131,33, 131,25, 130,61, 130,41, 130,05, 129,98, 129,91, 129,04, 127,95, 127,91, 127,77, 127,60, 125,98, 125,82, 117,38, 117,26, 113,51, 111,22, 104,50, 104,37, 101,39, 100,55, 98,16, 95,84, 92,51, 73,09, 71,96, 71,94, 71,92, 70,48, 69,67, 69,60, 67,65, 66,99, 64,65, 60,68, 60,23, 60,12, 60,02, 59,35, 59,26, 59,24, 59,22, 59,19, 59,03, 56,81, 56,44, 50,30, 49,99, 49,73, 49,61, 43,24, 36,30, 31,30, 27,10, 19,57, 19,23, 16,03, 16,01, 7,55, 7,27.
ESI-MC m/z: Вычислено для С45Н53N3O9Si: 807,4. Найдено (М+1)+: 808,3.
Пример 7

К раствору промежуточного продукта 7 (3,78 г, 4,68 ммоль) в безводном ДМФ (30 мл, 0,16 М) добавляли при 23°С в атмосфере аргона карбонат цезия (5,35 г, 16,39 ммоль) и аллилбромид (2,03 мл, 23,42 ммоль). Реакционную смесь оставляли при 23°С в течение 16 часов, охлаждали при 0°С и по каплям добавляли уксусную кислоту для разрушения избытка основания. Раствор разбавляли дихлорметаном и добавляли по каплям насыщенный водный раствор бикарбоната натрия. Водную фазу экстрагировали дихлорметаном, объединенные органические слои сушили над сульфатом натрия. Неочищенный продукт очищали колоночной флэш-хроматографией (смеси элюентов этилацетат/гексан в градиенте от 100/0 до 2:1) с получением промежуточного продукта 8 (3,62 г, 91%) в виде желтого твердого вещества.
Rf: 0,40 (этилацетат/гексан 1:1).
1H ЯМР (300 МГц, CDCl3): δ 7,65 (м, 3Н), 7,43-7,28 (м, 7H), 6,54 (c, 1H), 5,88 (м, 1H), 5,31-5,10 (м, 2H), 5,24 (c, 1H), 5,19 (c, 1H), 5,12 (д, 1H), 5,02 (д, 1H), 4,47 (д, 1H), 4,34 (дд, 1H), 3,99 (дд, 1H), 3,93-3,86 (м, 2H), 3,81-3,73 (м, 2H), 3,62-3,53 (м, 2H), 3,61 (c, 3Н), 3,41 (м, 1H), 3,37 (c, 3Н), 3,23 (м, 1H), 3,08-2,97 (м, 2H), 2,79 (ддд, 2H), 2,39 (д, 1H), 2,24-1,95 (м, 1H), 2,17 (c, 3Н), 1,71 (c, 3Н), 1,07 (c, 9H).
ESI-MC m/z: Вычислено для С48Н57N3O9Si: 847,4. Найдено (М+1)+: 848,2.
Пример 8
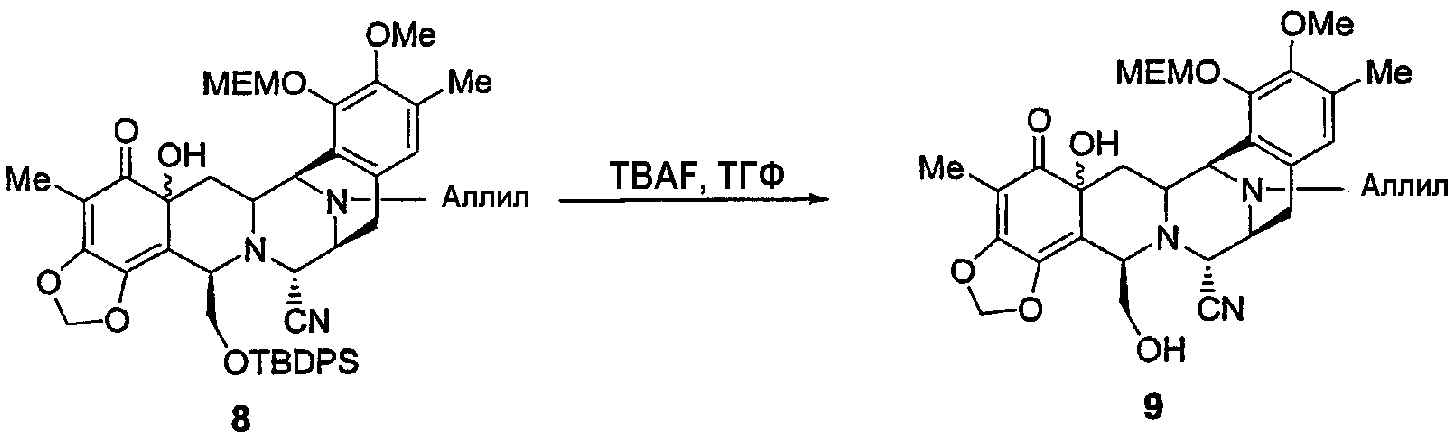
К раствору промежуточного продукта 8 (942 мг, 1,11 ммоль) в безводном ТГФ (10 мл, 0,1 М) в атмосфере аргона добавляли по каплям TBAF (3,33 мл, 3,33 ммоль) при 23°С. Реакционную смесь оставляли при 23°С в атмосфере аргона на 2 часа и 20 минут. Раствор разбавляли этилацетатом и добавляли насыщенный солевой раствор. Органическую фазу отделяли, сушили над сульфатом натрия, фильтровали и растворитель удаляли при пониженном давлении. Неочищенный продукт очищали колоночной флэш-хроматографией (смеси элюентов этилацетат/гексан в градиенте от 1:2 до 2:1) с получением промежуточного продукта 9 (461 мг, 68%) в виде желтого твердого вещества.
Rf: 0, 26 (этилацетат/гексан 2:1).
1H ЯМР (300 МГц, CDCl3): δ 6,66 (c, 1H), 6,60 (c, 1H), 5,88-5,80 (м, 1H), 5,81 (c, 3H), 5,80 (c, 3H), 5,20 (д, 2H), 5,12 (д, 1H), 5,07 (д, 1H), 4,12 (м, 1H), 4,07 (м, 1H), 3,91-3,67 (м, 4H), 3,85 (c, 3H), 3,59-3,49 (м, 4H), 3,41 (ушир.д, 1H), 3,34 (м, 1H), 3,31 (c, 3H), 3,24 (дт, 1H), 3,09 (дд, 1H), 2,86 (ддд, 2H), 2,53 (д, 2H), 2,18 (c, 3H), 2,05 (д, 2H), 1,75 (c, 3H).
13C ЯМР (75 МГц, CDCl3): δ 198,81, 159,04, 149,01, 148,23, 140,94, 135,34, 131,42, 130,99, 125,74, 123,58, 117,99, 117,21, 111,06, 104,41, 101,86, 98,52, 71,86, 70,57, 69,43, 62,25, 60,63, 59,22, 59,19, 58,46, 56,68, 56,22, 55,74, 51,89, 36,57, 25,79, 15,98, 7,52.
ESI-MC m/z: Вычислено для С32Н39N3O9: 609,3. Найдено (М+Na)+: 632,3.
Пример 9

К раствору промежуточного продукта 9 (1,43 г, 2,34 ммоль) и производного цистеина (1,40 г, 3,51 ммоль) в безводном дихлорметане (20 мл, 0,12 М) добавляли при 23°С EDC.HCl (1,12 г, 5,85 ммоль), DMAP (114 мг, 1,17 ммоль) и DIPEA (0,24 мл, 1,36 ммоль). Реакционную смесь оставляли в атмосфере аргона на 2 часа. Добавляли насыщенный раствор бикарбоната натрия и водную фазу экстрагировали дихлорметаном, объединенные органические слои сушили над сульфатом натрия, фильтровали и растворитель удаляли при пониженном давлении. Неочищенный продукт очищали колоночной флэш-хроматографией (смеси элюентов этилацетат/гексан в градиенте от 1:4 до 2:1) с получением промежуточного продукта 10 (1,42 г, 61%, некоторое количество исходного материала регенерировалось) в виде желтого твердого вещества и в виде смеси из 4 изомеров.
Rf: 0,26 (этилацетат/гексан 2:1).
1H ЯМР (300 МГц, CDCl3): δ 7,70 (д, 8Н), 7,66-7,58 (м, 8Н), 7,37-7,23 (м, 16Н), 6,59 (ушир.c, 2H), 6,49 (c, 1H), 6,47 (c, 1H), 5,87-5,79 (м, 4H), 5,69, 5,67, 5,65 (ушир.c, 6H), 5,56 (c, 2H), 5, 38-4,97 (м, 20H), 4,61-4,37 (м, 12H), 4,18-3,85 (м, 28H), 3,78 (c, 3H), 3,77-3,66 (м, 2H), 3,59 (c, 3H), 3,58 (c, 3H), 3,58 (c, 3H), 3,53 (м, 8H), 3,35 (м, 2H), 3,35 (c, 3H), 3,35 (c, 3H), 3,32 (c, 3H), 3,31 (c, 3H), 3,21-2,55 (м, 36H), 2,43- 2,30 (м, 4H), 2,17 (c, 6H), 2,12 (c, 3H), 2,10 (c, 3H), 1,74, 1,74, 1,73 (c, 12H), 1,22 (c, 36H).
ESI-MC m/z: Вычислено для С54 Н62N4O12S: 990,4. Найдено (М+1)+: 991,2.
Пример 10
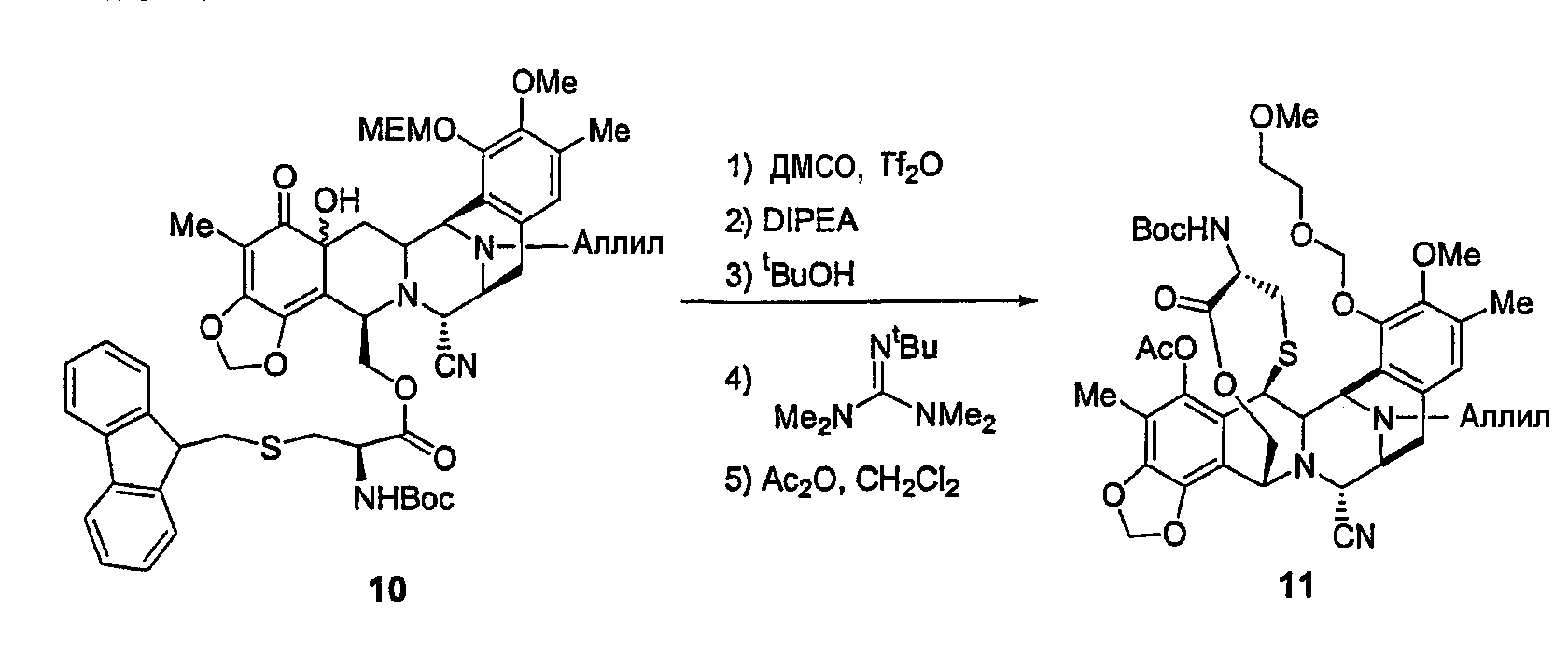
Реакционную колбу обрабатывали пламенем два раза, откачивали воздух, продували аргоном несколько раз и хранили в атмосфере аргона для реакции. К раствору ДМСО (43,0 мкл) в безводном CH2Cl2 (4,0 мл) по каплям добавляли трифторметансульфоновый ангидрид (20,3 мкл) при -78°С. Реакционную смесь перемешивали при -78°С в течение 20 минут, затем добавляли через канюлю раствор соединения 10 (основного изомера) (60 мг, 0,06 ммоль) в безводном CH2Cl2 (2,0 мл) при -78°С. Во время добавления температуру в обеих колбах поддерживали при -78°С. Реакционную смесь перемешивали при -40°С в течение 35 минут. После этого периода времени добавляли по каплям изо-Pr2NEt (160 мкл) и реакционную смесь выдерживали при 0°С в течение 45 минут. Затем добавляли по каплям трет-BuOH (57 мкл) и гуанидин (96 мкл) и реакционную смесь перемешивали при 23°С в течение 40 минут. После этого периода времени добавляли по каплям уксусный ангидрид (86 мкл) и реакционную смесь выдерживали при 23°С в течение еще 1 часа. Затем эту реакционную смесь разбавляли CH2Cl2 и промывали водным насыщенным раствором NH4Cl, NaHCO3 и NaCl. Объединенные органические слои сушили над Na2SO4, фильтровали и концентрировали.
Остаток очищали колоночной флэш-хроматографией (смеси элюентов этилацетат/гексан в градиенте от 1:4 до 1:1) с получением соединения 11 (34 мг, 67%) в виде бледно-желтого твердого вещества.
Rf: 0,43 (этилацетат/гексан 1:1).
1H ЯМР (300 МГц, CDCl3): δ 6,79 (c, 1H), 6,08 (д, 1H), 5,98 (д, 1H), 5,92-5,82 (м, 1H), 5,32 (д, 1H), 5,18 (м, 1H), 5,17 (д, 1H), 5,12 (д, 1H), 5,01 (д, 1H), 4,62 (д, 1H), 4,52 (ушир.c, 1H), 4,41 (д, 1H), 4,28 (м, 2H), 4,20 (д, 1H), 4,14 (дд, 1H), 3,91 (окт, 2H), 3,76 (c, 3H), 3,59 (т, 2H), 3,54 (м, 1H), 3,44 (д, 1H), 3,37 (c, 3H), 3,00 (м, 2H), 2,90-2,72 (м, 3H), 2,37-2,24 (м, 1H), 2,31 (c, 3H), 2,29 (c, 3H), 2,02 (c, 3H), 1,45 (c, 9H).
13С ЯМР (75 МГц, CDCl3): δ 170,89, 168,86, 155,36, 149,40, 148,60, 145,97, 141,19, 140,64, 135,47, 131,65, 131,15, 125,54, 125,24, 120,68, 118,18, 118,09, 113,78, 113,54, 102,21, 98,33, 79,95, 71,93, 69,35, 61,60, 60,60, 60,44, 59,93, 59,39, 59,30, 55,90, 54,14, 54,03, 51,18, 41,95, 33,06, 28,72, 28,45, 23,93, 20,59, 16,11, 14,42, 9,83.
ESI-MC m/z: Вычислено для С42Н52N4O12S: 836,3. Найдено (М+1)+: 837,1.
Пример 11

К раствору промежуточного продукта 11 (29 мг, 0,035 ммоль) в CHCl3 (1 мл, 0,03 М) добавляли при 23°С p -TsOH (40 мг, 0,21 ммоль). Реакционную смесь оставляли при 23°С в атмосфере аргона на 15 часов. Реакционную смесь разбавляли дихлорметаном и добавляли насыщенный водный раствор бикарбоната натрия. Водную фазу экстрагировали дихлорметаном, объединенные органические слои сушили над сульфатом натрия, фильтровали и растворитель удаляли при пониженном давлении. Неочищенный продукт очищали колоночной флэш-хроматографией (смеси элюентов этилацетат/гексан в градиенте от 1:4 до 2:1 и конечные промывки метанолом) с получением промежуточного продукта 12 (16 мг, 71%) в виде желтого твердого вещества.
Rf: 0,07 (этилацетат/гексан 1:1).
1H ЯМР (300 МГц, CDCl3): δ 6,52 (c, 1H), 6,07 (д, 1H), 5,98 (д, 1H), 5,85 (м, 1H), 5, 13-5,06 (м, 2H), 5,01 (д, 1H), 4,52 (ушир.c, 1H), 4,33 (д, 1H), 4,26 (c, 1H), 4,19 (д, 1H), 4,12 (м, 1H), 3,77 (c, 3H), 3,53 (ушир.д, 1H), 3,40 (д, 1H), 3,28 (м, 1H), 2,95-2,75 (м, 4H), 2,30 (c, 3H), 2,28 (c, 3H), 2,21 (ушир.c, 2H), 2,03 (c, 3H).
13С ЯМР (75 МГц, CDCl3): δ 174,59, 168,91, 147,85, 145,86, 143,10, 141,22, 140,56, 135,21, 131,27, 129,53, 121,11, 120,72, 118,93, 118,30, 114,01, 113,54, 102,15, 61,55, 60,44, 60,30, 59,73, 59,53, 56,09, 54,22, 53,31, 52,07, 41,95, 34,58, 24,23, 20,82, 15,89, 9,86.
ESI-MC m/z: Вычислено для С33Н36N4O8S: 648,2. Найдено (М+1)+: 649,1.
Пример 12

К раствору соли пиридиния (211 мг, 0,85 ммоль) в ДМФ (2,3 мл) добавляли при 23оС раствор промежуточного продукта 12 (55 мг, 0,085 ммоль) в дихлорметане (2,9 мл, конечная концентрация 0,016 М). Реакционную смесь оставляли при 23°С в атмосфере аргона на 4 часа и 15 минут, затем добавляли DBU (13 мкл, 0,085 ммоль) и этот раствор перемешивали при 23°С в атмосфере аргона в течение 15 минут. После этого периода времени добавляли насыщенный раствор щавелевой кислоты (2 мл) и реакционную смесь оставляли при 23°С в атмосфере аргона на 30 минут. Реакционную смесь охлаждали при 0°С, разбавляли Et2O и добавляли насыщенный раствор бикарбоната натрия до достижения рН 5. Водную фазу экстрагировали Et2O (×4), дополнительно подщелачивали дополнительным количеством бикарбоната натрия и экстрагировали дополнительным количеством Et2O (×4). Объединенные органические слои сушили над сульфатом натрия, фильтровали и растворитель удаляли при пониженном давлении. Неочищенный продукт очищали колоночной флэш-хроматографией (смеси элюентов этилацетат/гексан в градиенте от 1:2 до 2:1) с получением промежуточного продукта 13 (28 мг, 51%) в виде желтого твердого вещества.
Rf: 0,66 (этилацетат/гексан 2:1).
1H ЯМР (300 МГц, CDCl3): δ 6,49 (c, 1H), 6,11 (д, 1H), 6,01 (д, 1Н), 5,88-5,77 (м, 1Н), 5,70 (с, 1Н), 5,09 (м, 3Н), 4,66 (ушир.c, 1H), 4,40 (c, 1H), 4,36 (д, 1H), 4,20 (дд, 1H), 4,17 (д, 1H), 3,75 (c, 3H), 3,55 (м, 2H), 2,88-2,67 (м, 5H), 2,56 (д, 1H), 2,32 (c, 3H), 2,25 (c, 3H), 2,04 (c, 3H).
ESI-MC m/z: Вычислено для С33Н33N3O9S: 647,1. Найдено (М+1)+: 648,1.
Пример 13

К раствору промежуточного продукта 13 (26 мг, 0,04 ммоль) и производного допамина (24 мг, 0,14 ммоль) в EtOH (0,7 мл, 0,06 М) добавляли при 23°С силикагель (56 мг). Реакционную смесь оставляли при 23°С в атмосфере аргона на 15 часов. Растворитель этой реакции удаляли при пониженном давлении и неочищенный продукт очищали колоночной флэш-хроматографией (смеси элюентов этилацетат/гексан в градиенте от 1:1 до 4:1) с получением промежуточного продукта 14 (30 мг, 94%) в виде бледно-желтого твердого вещества.
Rf: 0,37 (этилацетат/гексан 2:1).
1H ЯМР (300 МГц, CDCl3): δ 6,60 (c, 1H), 6,46 (c, 1H), 6,44 (c, 1H), 6,04 (д, 1H), 5,96 (д, 1H), 5,94-5,80 (м, 1H), 5,73 (c, 1H), 5,48 (ушир.c, 1H), 5,11 (м, 2H), 5,02 (д, 1H), 4,57 (ушир.c, 1H), 4,36 (д, 1H), 4,33 (c, 1H), 4,19 (д, 1H), 4,11 (дд, 1H), 3,78 (c, 3H), 3,61 (c, 3H), 3,55 (м, 1H), 3,50 (д, 1H), 3,09 (м, 1H), 2,99-2,74 (м, 5Н), 2,59 (м, 1H), 2,47 (дт, 1H), 2,32 (c, 3H), 2,25 (c, 3H), 2,23-2,13 (м, 2H), 2,04 (c, 3H).
ESI-MC m/z: Вычислено для С42Н44N4 O10S: 796,3. Найдено (М+1)+: 797,2.
Пример 14

К раствору промежуточного продукта 14 (30 мг, 0,038 ммоль), (PPh3)2PdCl2 (3 мг, 0,003 ммоль), уксусной кислоты (11 мкл, 0,188 ммоль) в безводном дихлорметане (1 мл, 0,04 М) добавляли по каплям при 23°С в атмосфере аргона HSnBu3 (36 мкл, 0,13 ммоль). Реакционную смесь оставляли при 23°С и в атмосфере аргона на 20 минут. После этого периода времени реакционную смесь выливали на колонку (смеси элюентов дихлорметан/метанол в градиенте от 100/0 до 30:1) с получением промежуточного продукта 15 (12 мг, 42%) в виде бледно-желтого твердого вещества. Некоторая часть исходного материала (17 мг) выделялась в неочищенном виде со следами производных бутилолова.
Rf: 0,22 (дихлорметан/метанол 20:1).
1H ЯМР (300 МГц, CDCl3): δ 6,62 (c, 1H), 6,47 (c, 1H), 6,44 (c, 1H), 6,06 (д, 1H), 5,98 (д, 1H), 5,03 (д, 1H), 4,57 (ушир.c, 1H), 4,50 (д, 1H), 4,34 (c, 1H), 4,20 (д, 1H), 4,15 (дд, 1H), 3,85 (д, 1H), 3,78 (c, 3H), 3,62 (c, 3H), 3,52 (д, 1H), 3,15-2,95 (м, 3H), 2,77 (м, 1H), 2,60 (м, 1H), 2,46 (дт, 1H), 2,35 (д, 1H), 2,31 (c, 3H), 2,26 (c, 3H), 2, 15 (д, 1H), 2,04 (c, 3H).
13С ЯМР (75 МГц, CDCl3): δ 172,84, 172,12, 145,98, 145,60, 144,77, 144,53, 142,98, 141,59, 140,36, 131,49, 129,81, 129,36, 125,84, 124,60, 121,57, 121,32, 118,34, 114,33, 114,17, 109,99, 102,10, 64,79, 61,46, 60,66, 60,17, 59,25, 59,01, 55,40, 48,84, 47,86, 42,13, 39,87, 29,00, 28,33, 20,67, 16,01, 9,97.
ESI-MC m/z: Вычислено для С39Н40N4O10S: 756,2. Найдено (М+1)+: 757,3.
Пример 15

К раствору промежуточного продукта 15 (12 мг, 0,016 ммоль) в ацетонитриле (0,66 мл) добавляли при 23°С воду (0,44 мл, 0, 015 М, конечная концентрация) и AgNO3 (81 мг, 0,47 ммоль). Реакционную смесь оставляли при 23°С в атмосфере аргона на 23 часа. Реакционную смесь разбавляли дихлорметаном и добавляли насыщенный раствор бикарбоната натрия и насыщенный раствор хлорида натрия. Водную фазу экстрагировали дихлорметаном и объединенные органические слои сушили над сульфатом натрия, фильтровали и растворитель удаляли при пониженном давлении. Неочищенный Et-729 очищали колоночной флэш-хроматографией (смеси элюентов дихлорметан/метанол в градиенте от 100/0 до 3:1) с получением конечного продукта (8,3 мг, 70%) в виде белого твердого вещества.
Rf: 0,07 (дихлорметан/метанол 95:5).
1H ЯМР (300 МГц, CD3OD): δ 6,59 (c, 1H), 6, 44 (c, 1H), 6,40 (c, 1H), 6,13 (c, 1H), 6,02 (c, 1H), 5,20 (д, 1H), 4,73 (c, 1H), 4,58 (д, 2H), 4,26 (д, 1H), 4,13 (дд, 1H), 3,80 (ушир.д, 1H), 3,73 (c, 3H), 3,67 (д, 1H), 3,59 (c, 3H), 3,22-3,02 (м, 3H), 2,78 (м, 1H), 2,59 (м, 1H), 2,42 (м, 2H), 2,31 (c, 3H), 2,30 (c, 3H), 2,05 (м, 1H), 2,04 (c, 3H).
13С ЯМР (75 МГц, CD3OD): δ 173,52, 170,26, 148,13, 147,01, 146,92, 146,86, 145,04, 142,67, 141,95, 132,04, 129,28, 125,79, 122,77, 122,42, 121,40, 116,29, 115,89, 111,63, 103,54, 90,94, 65,53, 61,80, 60,38, 58,23, 57,23, 55,76, 47,35, 43,15, 40,70, 28, 85, 27,79, 20,49, 16,07, 9,38.
ESI-MC m/z: Вычислено для С38Н41N3O11S: 747,2. Найдено (М+1)+: 748,1.
Пример 16
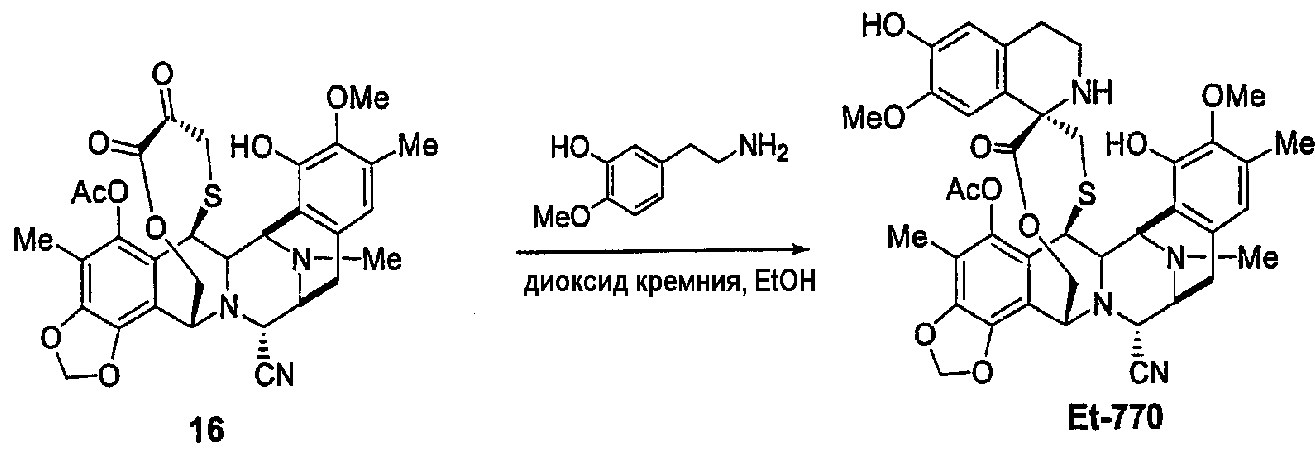
К раствору соединения 16 (0,5 г, 0,80 ммоль), 3-гидрокси-4-метоксифенетиламина (924 мг, 2,8 ммоль) в этиловом спирте добавляли при 23°С силикагель (1 г). Реакционную смесь перемешивали при 23°С в атмосфере аргона в течение 16 часов. После этого периода времени растворитель удаляли при пониженном давлении и неочищенный продукт этой реакции очищали колоночной флэш-хроматографией (смеси элюентов этилацетат/метиленхлорид в градиенте от 1:2 до 100% в этилацетате, конечные промывки в смеси метиленхлорид/метиловый спирт 9:1) с получением Et-770 (564 мг, 91%) в виде бледно-желтого твердого вещества.
1H ЯМР (300 МГц, CDCl3): 6,60 (c, 1H), 6,47 (c, 1H), 6,45 (c, 1H), 6,05 (c, 1H), 5,98 (c, 1H), 5,02 (д, 1H), 4,57 (ушир.c, 1H), 4,32 (ушир.c, 1H), 4,28 (д, 1H), 4,18 (д, 1H), 4,12 (дд, 1H), 3,78 (c, 3H), 3,62 (c, 3H), 3,50 (д, 1H), 3,42 (м, 1H), 3,10 (ддд, 1H), 2,94 (м, 2H), 2,79 (м, 1H), 2,61 (м, 1H), 2,47 (м, 1H), 2,35 (м, 1H), 2,32 (c, 3H), 2,27 (c, 3H), 2,20 (c, 3H), 2,09 (м, 1H), 2,04 (c, 3H).
ESI-MC m/z: Вычислено для С40Н42N4O10S: 770,7. Найдено (М+Н)+: 771,2.
Пример 17
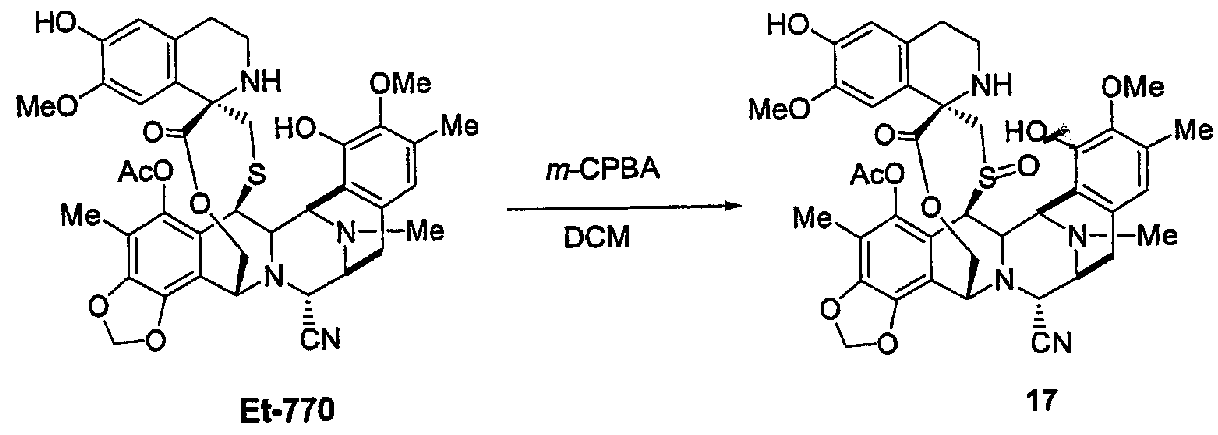
К раствору Et-770 (45 мг, 0,058 ммоль) в CH2Cl2 (3 мл, 0,03 М) добавляли при 0°С в атмосфере аргона mCPBA (15,1 мг, 0,087 ммоль). Реакционную смесь перемешивали при 0°С в течение 30 минут, затем добавляли насыщенный водный раствор бикарбоната натрия, затем водную фазу экстрагировали CH2Cl2, органические слои сушили над сульфатом натрия и растворитель удаляли при пониженном давлении. Неочищенный продукт очищали колоночной флэш-хроматографией (элюент: этилацетат/гексан 3:1) с получением соединения 17 (45,6 мг, 99%).
Rf: 0,18 (этилацетат/гексан 2:1).
1H ЯМР (300 МГц, CDCl3): δ 6,63 (c, 1H), 6,51 (c, 1H), 6,47 (c, 1H), 6,19 (c, 1H), 6,05 (c, 1H), 6,00 (c, 1H), 4,66 (д, 1H), 4,61 (д, 1H), 4,30-4,28 (м, 1H), 4,19 (c, 1H), 4,07 (c, 1H), 3,82 (c, 1H), 3,73 (д, 1H), 3,65 (д, 1H), 3,60 (c, 3H), 3,43 (д, 1H), 3,04-2,95 (м, 2H), 2,88-2,81 (м, 1H), 2,72-2,55 (м, 3Н), 2,48-2,41 (м, 1H), 2,30 (c, 3Н), 2,25 (c, 3H), 2,23 (c, 3Н), 2,05 (c, 3Н).
13С ЯМР (75 МГц, CDCl3): δ 172,0, 169,2, 148,2, 146,8, 146,3, 145,1, 144,8, 142,3, 140,8, 130,8, 129,6, 129,5, 124,5, 122,6, 120,2, 120,0, 117,8, 114,6, 111,8, 109,5, 102,4, 70,9, 67,8, 61,8, 61,7, 60,9, 60,6, 60,0, 55,3, 54,9, 54,7, 41,9, 40,0, 29,9, 29,1, 25,0, 21,0, 16,2, 10,3.
ESI-MC m/z: Вычислено для С40Н42N4O11S: 786,2. Найдено (М+Na)+: 809,3.
Пример 18
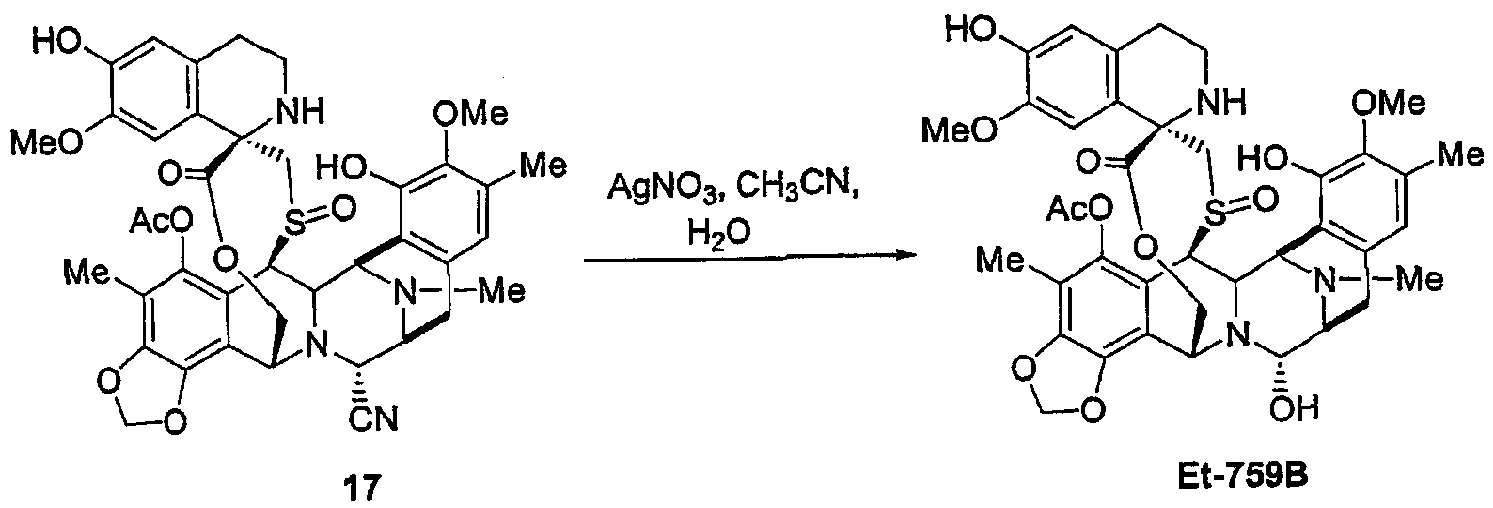
К раствору соединения 17 (45 мг, 0,057 ммоль) в CH3CN/Н2О (6 мл/2 мл, 0,007 М) добавляли при 23°С AgNO3 (287,1 мг, 1,71 ммоль). Реакционную смесь перемешивали в атмосфере аргона и защищали от света в течение 24 часов. Реакционную смесь разбавляли CH2Cl2 и гасили насыщенным водным раствором бикарбоната натрия и насыщенным водным солевым раствором 1:1. Водную фазу экстрагировали CH2Cl2, органические слои сушили над сульфатом натрия и растворитель удаляли при пониженном давлении. Неочищенный продукт очищали колоночной флэш-хроматографией с получением Et-759В (23,2 мг, 52%) бледно-желтого твердого вещества и некоторого количества регенерированного исходного материала (18,7 мг, 42%).
Rf: 0,36 (CH2Cl2/МеОН 8:0,5).
1H ЯМР (300 МГц, CDCl3): δ 6,65 (c, 1H), 6,48 (c, 1H), 6,43 (c, 1H), 6, 20 (c, 1H), 6,04 (д, 1H), 5,97 (c, 1H), 4,78 (c, 1H), 4,70 (д, 1H), 4,55 (д, 1H), 4,36 (д, 1H), 4,07-3,98 (м, 1H), 3,83 (c, 3H), 3,77 (д, 1H), 3,69-3,63 (м, 1H), 3,61 (c, 3H), 3,46 (д, 1H), 3,22 (д, 1H), 3,06-2,82 (м, 4H), 2,66-2,43 (м, 4H), 2,31 (c, 3H), 2,26 (c, 3H), 2,21 (c, 3H), 2,04 (c, 3H).
13С ЯМР (75 МГц, CDCl3): δ 171,9, 169,3, 148,0, 146,9, 145,0, 144,7, 142,2, 141,0, 130,7, 130,1, 129,6, 124,9, 123,0, 120,9, 120,1, 114,6, 113,7, 109,5, 102,2, 82,9, 67,9, 63,1, 61,8, 60,5, 57,7, 57,6, 55,9, 55,3, 55,1, 41,7, 40,0, 29,9, 29,2, 24,7, 21,0, 16,1, 14,3, 10,2.
ESI-MC m/z: Вычислено для С39Н43N3O12S: 777,84. Найдено (М-Н2О+H)+: 760,2.
Пример 19
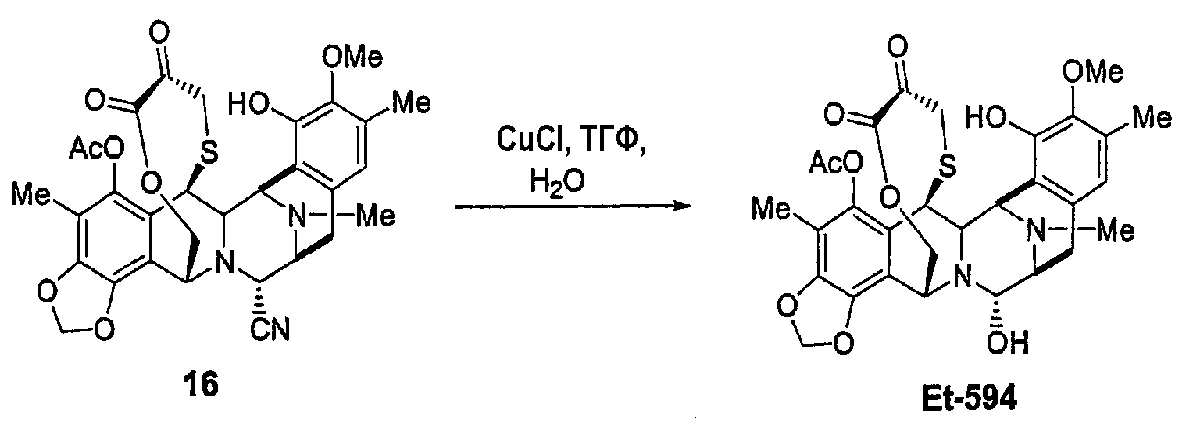
К раствору соединения 16 (100 мг, 0,16 ммоль) в смеси ТГФ/Н2 О (4,26 мл/1,06 мл, 0,03 М) добавляли при 23°С в атмосфере аргона CuCl (79,5 мг, 0,80 ммоль). Реакционную смесь перемешивали при 23°С в атмосфере аргона и защищали от света в течение 24 часов. Реакционную смесь разбавляли CH2Cl2, реакцию гасили насыщенным водным раствором хлорида аммония. Водную фазу отделяли и органическую фазу промывали насыщенным водным раствором бикарбоната натрия. Водную фазу экстрагировали CH2Cl2, органические слои сушили над сульфатом натрия и растворитель удаляли при пониженном давлении. Неочищенный продукт очищали колоночной флэш-хроматографией (элюент CH2Cl2/МеОН 60:1) с получением Et-594 (70 мг, 71%) в виде желтого твердого вещества.
Rf: 0,44 (CH2Cl2/МеоН 60:1).
1H ЯМР (300 МГц, CDCl3): δ 6,53 (c, 1H), 6,49 (c, 1H), 6,07 (c, 1H), 6,05 (c, 1H), 5,98 (c, 1H), 5,94 (c, 1H), 5,71 (c, 2H), 5,18 (д, 1Н), 5,12 (д, 1H), 4,85 (c, 1H), 4,77 (c, 1H), 4,55-4,36 (м, 3H), 4,17-4,11 (м, 4H), 3,77 (c, 3H), 3,75 (c, 3H), 3,58 (д, 1H), 3,47 (c, 4H), 3,19 (c, 2H), 3,07 (c, 3H), 2,87-2,54 (м, 6H), 2,31 (c, 3H), 2,30 (c, 3H), 2,28 (c, 3H), 2,23 (c, 3H), 2,18-2,05 (м, 2H), 2,15 (c, 3H), 2,11 (c, 3H), 2,05 (c, 3H), 1,98 (c, 3H).
ESI-MC m/z: Вычислено для С30Н32N2O10S: 612,1. Найдено (М-Н2О+Н)+: 595,5.
Пример 20
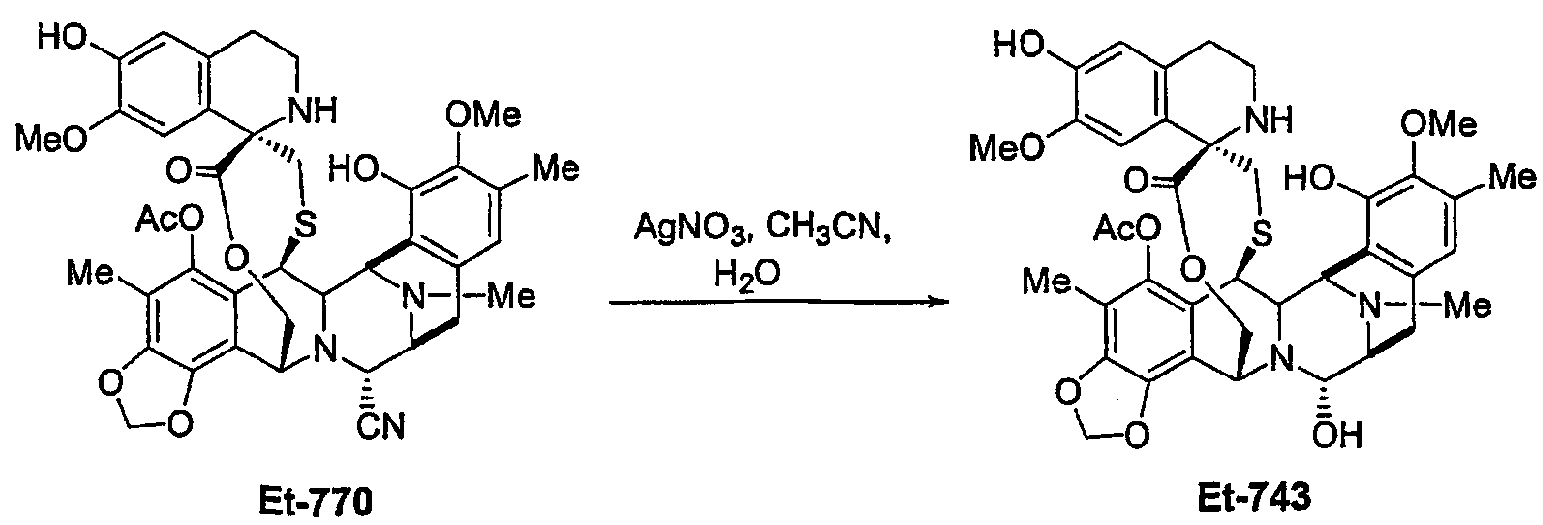
К раствору Et-770 (1,25 г, 1,62 ммоль) в CH3CN/Н2О (64,8 мл/43,2 мл, 0,015 М) добавляли при 23°С AgNO3 (8,27 г, 1,71 ммоль). Реакционную смесь перемешивали в атмосфере аргона и защищали от света в течение 24 часов. Реакционную смесь разбавляли CH2Cl2 и реакцию гасили насыщенным водным раствором бикарбоната натрия и водным насыщенным солевым раствором 1:1. Водную фазу экстрагировали CH2Cl2, органические слои сушили над сульфатом натрия и растворитель удаляли при пониженном давлении. Неочищенный продукт очищали колоночной флэш-хроматографией (CHCl3/EtOAC/МеОН в градиенте от 49:49:2 до 48:40:12) с получением Et-743 (1,09 г, 88%) в виде желтого твердого вещества и некоторого количества регенерированного исходного материала (75 мг, 6%).
Rf: 0,2 (CHCl3/EtOAC/МеОН 49:49:2).
1H ЯМР (300 МГц, CDCl3): δ 6,60 (c, 1H), 6,46 (c, 1H), 6,44 (c, 1H), 6,02 (д, 1H), 5,94 (ушир.д, 1H), 5,13 (д, 1H), 4,81 (ушир.c, 1H), 4,50 (ушир.c, 1H), 4,49 (ушир.c, 1H), 4,16 (дд, 1H), 4,04 (дд, 1H), 3,79 (c, 3H), 3,61 (c, 3H), 3,57 (ушир.д, 1H), 3,22 (ушир.д, 1H), 3,12 (ддд, 1H), 2,87 (ушир.c, 1H), 2,85 (ушир.c, 1H), 2,80 (м, 1H), 2,60 (ддд, 1H), 2,47 (ддд, 1H), 2,38 (ушир.c, 1H), 2,26 (c, 3H), 2,18 (м, 1H), 2,17 (c, 3H), 2,03 (c, 3H).
13С ЯМР (75 МГц, CDCl3): δ 172,6, 168,3, 147,7, 145,1, 144,4, 143,0, 141,3, 140,5, 131,5, 129,2, 126,1, 121,9, 120,9, 118,0, 116,0, 114,0, 112,5, 109,8, 101,6, 82,1, 64,7, 61,3, 60,3, 57,8, 56,0, 55,1, 54,9, 42,2, 41,4, 39,7, 28,8, 24,0, 20,4, 15,8, 9,6.
ESI-MC m/z: Вычислено для С39Н43N3O11S: 761,3. Найдено (М-Н2О+Н)+: 744,4.
Пример 21

К раствору Et-743 (25 мг, 0,03 ммоль) в метиловом спирте (1,5 мл, 0,02 М) добавляли при 23°С муравьиную кислоту (11 мкл, 0,3 ммоль). Этот раствор перемешивали при 23°С в течение 6 часов, затем растворитель удаляли при пониженном давлении и неочищенный продукт очищали колоночной флэш-хроматографией (CHCl3/EtOAC/МеОН 49:49:2) с получением Et-745 (15,8 мг, 64%).
Rf: 0,17 (CHCl3/EtOAC/МеОН 49:49:2).
1H ЯМР (300 МГц, CDCl3): δ 6,61 (c, 1H), 6,49 (c, 1H), 6,42 (c, 1H), 6,00 (д, 1H), 5,95 (д, 1H), 5,10 (д, 1H), 4,50 (ушир.c, 1H), 4,38 (д, 1H), 4,09 (дд, 1H), 3,79 (c, 3H), 3, 60 (c, 3H), 3,38-3,21 (м, 3H), 3,17-2,81 (м, 5H), 2,71 (м, 1H), 2,52 (м, 2H), 2,41 (д, 1H), 2,33 (c, 3H), 2,24 (c, 3H), 2,22 (c, 3H), 2,12 (м, 1H), 2,02 (c, 3H).
13С ЯМР (75 МГц, CDCl3): δ 172,43, 168,19, 147,72, 144,79, 144,60, 144,50, 142,64, 141,03, 139,77, 131,61, 128,61, 126,07, 122,09, 120,50, 118,51, 115,41, 114,50, 112,63, 109,94, 101,41, 64,26, 64,06, 62,21, 60,83, 60,01, 55,00, 42,39, 41,76, 40,78, 39,29, 31,39, 29,50, 28,53, 25,45, 22,45, 20,30, 15,62, 13,92, 9,48.
ESI-MC m/z: Вычислено для С39Н43N3O10S: 745,3. Найдено (М+H)+: 746,2.
Пример 22

К раствору соединения 18 (520,8 мг, 0,84 ммоль) в CH2Cl2 (17 мл, 0,05 М) в атмосфере аргона при комнатной температуре добавляли уксусный ангидрид (0,08 мл, 0,88 ммоль). Реакционную смесь перемешивали в течение 30 минут и затем реакцию гасили водным насыщенным раствором NaHCO3. Водный слой экстрагировали CH2Cl2 и органический слой сушили над Na2SO4. Флэш-хроматография (гексан/EtOAC, 1:2, 2:5, 1:3) дает чистое соединение 19 (96%).
Rf: 0,2 (гексан/этилацетат 2:3).
1H ЯМР (300 МГц, CDCl3): δ 6,56 (c, 1H), 6,04 (дд, 2H), 5,78 (c, 1H), 5,52 (ушир.д, 1H), 5,02 (д, 1H), 4,58 (ддд, 1H), 4,53 (ушир.c, 1H), 4,27-4,25 (м, 2H), 4,19-4,15 (м, 2H), 3,77 (c, 3H), 3,44-3,43 (м, 2H), 2,92-2,90 (м, 2H), 2,36-2,02 (м, 2H), 2,36 (c, 3H), 2,30 (c, 3H), 2,16 (c, 3H), 2,02 (c, 3H), 1,88 (c, 3H).
13С ЯМР (75 МГц, CDCl3): δ 170,5, 168,8, 168,4, 148,1, 145,8, 143,1, 141,0, 140,3, 130,7, 129,9, 129,0, 120,3, 119,0, 117,9, 113,5, 102,0, 61,3, 60,3, 60,2, 59,3, 58,9, 54,7, 54,5, 51,9, 41,8, 41,4, 32,4, 23,7, 22,8, 20,4, 16,0, 9,5.
ESI-MC m/z: Вычислено для С33Н36N4O9S: 664,2. Найдено (М+Н)+: 665,2.
Пример 23

К раствору соединения 19 (100 мг, 0,15 ммоль) в ацетоне (15 мл, 0,01 М) добавляли раствор соли Фреми (141 мг, 0,52 ммоль) в буферном растворе KH2PO4/Na2НРО4 (15 мл, 0,035 М). После 24 часов при 23° С реакционную смесь экстрагировали CH2Cl2 и сушили над Na2SO4. Хроматография (гексан/этилацетат 1:2) дает чистое соединение 20 (101 мг, 99%).
Rf: 0,38 (гексан/этилацетат 1:1).
1H ЯМР (300 МГц, CDCl3): δ 6,10 (д, 1H), 6,01 (д, 1H), 5,68 (д, 1H), 4,98 (д, 1H), 4,54-4,50 (м, 1H), 4,43 (c, 1H), 4,21 (c, 1H), 4,15-4,07 (м, 3H), 4,09 (c, 3H), 3,47 (c, 1H), 3,42 (д, 1H), 2,88-2,78 (м, 2H), 2,47 (д, 1H), 2,25 (c, 3H), 2,22-2,18 (м, 1H), 2,18 (c, 3H), 2,02 (c, 3H), 2,01 (c, 3H), 1, 87 (c, 3H).
ESI-MC m/z: Вычислено для С33Н34N4O10S: 678,2. Найдено (М+H)+: 679,1.
Пример 24

К раствору соединения 20 (100 мг, 0,14 ммоль) в смеси ТГФ/Н2О 4:1 (5,6 мг, 0,009 М) добавляли CuCl (145 мг, 1,47 ммоль). Спустя 24 часа при 23°С реакцию гасили насыщенным водным раствором NH4Cl, промывали солевым раствором и водным насыщенным раствором NaHCO3, разбавляли и экстрагировали CH2Cl2. Органический слой сушили над Na2SO4. Хроматография (CH2Cl2/МеОН 32:1) дает чистое соединение ЕТ-637-хинон (60 мг, 61%).
Rf: 0,54 (CH2Cl2/МеОН 32:1).
1H ЯМР (300 МГц, CDCl3): δ 6,07 (д, 1H), 5,97 (д, 1H), 5,72 (д, 1H), 5,08 (д, 1H), 4,71 (c, 1H), 4,52-4,33 (м, 3H), 4,08 (c, 3H), 4,08-4,01 (м, 3H), 3,53 (д, 1H), 3,24 (д, 1H), 2,83-2,69 (м, 2H), 2,46-2,33 (м, 1H), 2,24 (c, 3H), 2, 16 (c, 3H), 2,02 (c, 3H), 2,00 (c, 3H), 1,87 (c, 3H).
13С ЯМР (75 МГц, CDCl3): δ 175,5, 162,6, 162,2, 150,0, 138,9, 134,2, 133,7, 130,9, 129,9, 119,9, 111, 7, 107,5, 94,9, 75,2, 55,3, 53,6, 50,4, 48,6, 46,0, 45,8, 34,1, 33,6, 26,8, 22,6, 15,9, 13,4, 12,7.
ESI-MC m/z: Вычислено для С32Н35N3O11S: 669,2. Найдено (М-Н2О+Н)+: 652,1.
Пример 25
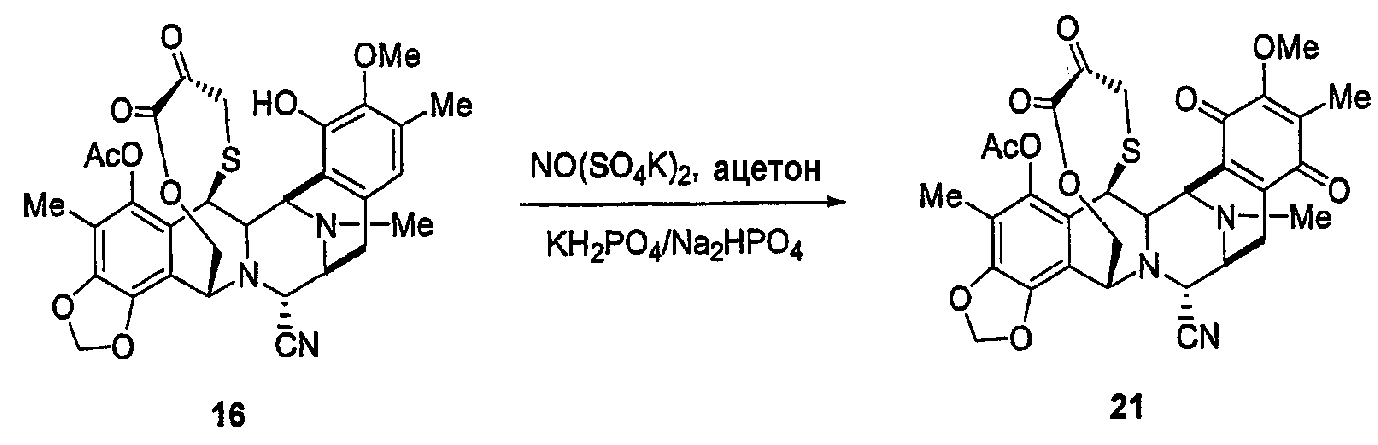
К раствору соединения 16 (100 мг, 0,16 ммоль) в ацетоне (16 мл, 0,01 М) добавляли раствор соли Фреми (151 мг, 0,56 ммоль) в буферном растворе KH2PO4/Na2 НРО4 (16 мл, 0,035 М). После 24 часов при 23°С реакционную смесь экстрагировали CH2Cl2 и сушили над Na2SO4. Хроматография (гексан/этилацетат 1:1) дает чистое соединение 21 (79 мг, 78%).
Rf: 0,3 (гексан/этилацетат 1:1).
1H ЯМР (300 МГц, CDCl3): δ 6,12 (д, 1Н), 6,03 (д, 1Н), 5,05 (д, 1Н), 4,48 (c, 1H), 4,28 (д, 1H), 4,24 (c, 1H), 4,20-4,16 (м, 1H), 4,05-4,00 (м, 1H), 3,98 (c, 3H), 3,59 (т, 1H), 3,38 (д, 1H), 3,35 (д, 1H), 2,84-2,64 (м, 2H), 2,40-2, 27 (м, 1H), 3,30 (c, 3H), 2,18 (c, 3H), 2,03 (c, 3H), 2,02 (c, 3H).
ESI-MC m/z: Вычислено для С31Н29N3O10S: 635,2. Найдено (М+Н)+ : 636,1.
Пример 26
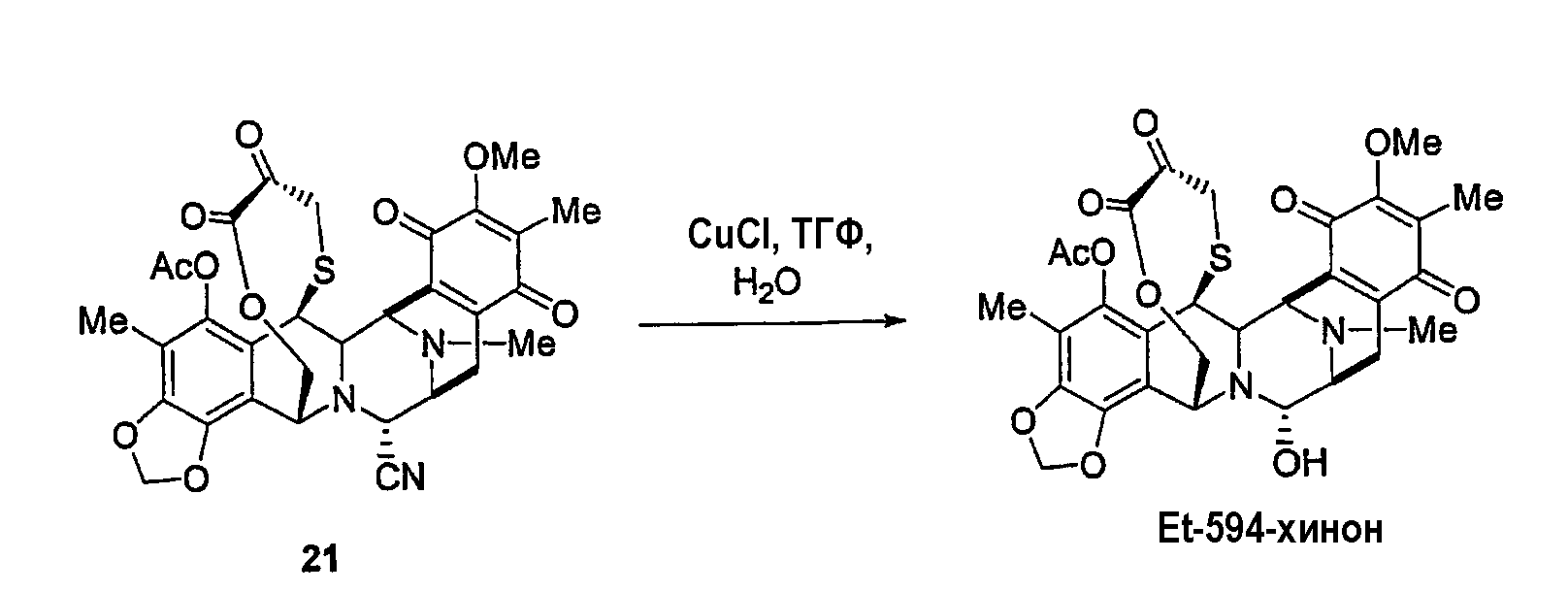
К раствору соединения 21 (79 мг, 0, 12 ммоль) в смеси ТГФ/Н2О 4:1 (4,4 мг, 0,009 М) добавляли CuCl (123 мг, 1,24 ммоль). Спустя 24 часа при 23°С реакцию гасили насыщенным водным раствором NH4Cl, промывали солевым раствором и водным насыщенным раствором NaHCO3, разбавляли и экстрагировали CH2Cl2. Органический слой сушили над Na2SO4. Хроматография (CH2Cl2/МеОН 32:1) дает чистое соединение Et-594-хинон (45 мг, 59%).
Rf: 0,6 (CH2Cl2/МеОН 32:1).
1H ЯМР (300 МГц, CDCl3): δ 6,10-5,97 (м, 4Н), 5,12 (д, 1Н), 5,05 (д, 1H), 4,74-4,63 (м, 2H), 4,43-4,26 (м, 2H), 4,22-4,11 (м, 2H), 4,06 (c, 6H), 4,05-3,91 (м, 2H), 3,82-3,71 (м, 2H), 3, 55-3,20 (м, 2H), 3,03 (c, 4H), 2,75-2,62 (м, 2H), 2,56-2,42 (м, 2H), 2,35-2,23 (м, 2H), 2,29 (c, 3H), 2,27 (c, 3H), 2,18 (c, 3H), 2,17 (c, 3H), 2,03 (c, 3H), 2,02 (c, 3H), 2,00 (c,3H), 1,98 (c, 3H).
13С ЯМР (75 МГц, CDCl3): δ 187,6, 187,2, 186,3, 186,1, 170,0, 169,3, 158,5, 158,4, 156,5, 146,6, 146,6, 142,0, 141,9, 140,9, 140,7, 137,4, 137,1, 136, 7, 129,7, 129,4, 118,6, 117,9, 117,7, 115,1, 114,9, 102,5, 102,4, 92,4, 83,0, 82,7, 65,3, 64,6, 60,7, 60,6, 58,8, 58,5, 58,1, 57,5, 57,4, 56,0, 55,8, 55,1, 53,7, 53,3, 53,1, 52,6, 42,6, 42,4, 40,9, 40, 8, 35,5, 35,2, 29,9, 20,9, 20,8, 20,2, 9,9, 9,8.
ESI-MC m/z: Вычислено для С30Н30N2O11S: 626,2. Найдено (М-Н2О+Н)+: 609,1.
Пример 27
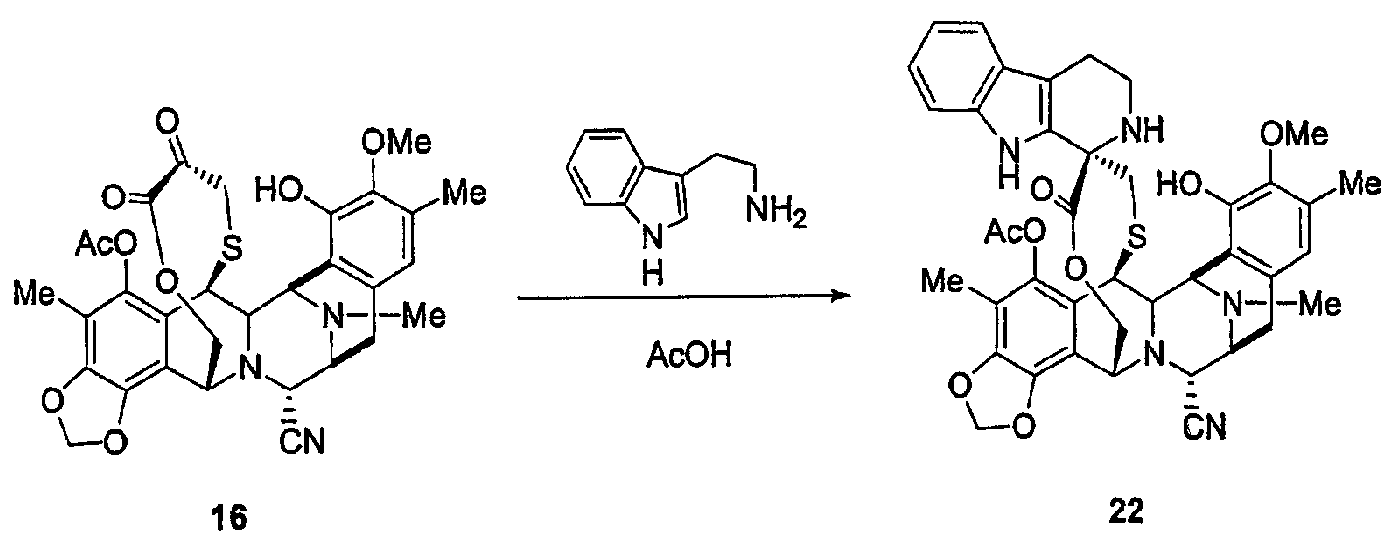
К раствору соединения 16 (75 мг, 0,12 ммоль) в уксусной кислоте (1,5 мл, 0,08 М) в атмосфере аргона при 23°С добавляли триптамин (68 мг, 0,42 ммоль). Реакционную смесь перемешивали при 23°С в течение 24 часов и затем уксусную кислоту выпаривали. Добавляли водный насыщенный раствор NaHCO3 и смесь экстрагировали CH2Cl2. Объединенные органические слои сушили над Na2SO4. Флэш-хроматография (гексан/этилацетат 1:1) дает чистое соединение 22 (90 мг, 99%).
Rf: 0,4 (гексан/этилацетат 1:1).
1H ЯМР (300 МГц, CDCl3): δ 7,74 (c, 1H), 7,38 (д, 1H), 7,25 (д, 1H), 7,08 (т, 1H), 7,00 (т, 1H), 6,66 (c, 1H), 6,22 (д, 1H), 6,02 (д, 1H), 5,79 (c, 1H), 5,08 (д, 1H), 4,55(c, 1H), 4,32 (c, 1H), 4,27 (д, 1H), 4,21 (c, 1H), 4,19 (д, 1H), 3,81 (c, 3H), 3,44-3,40 (м, 2H), 3,18-2,78 (м, 4H), 2,71-2,51 (м, 3H), 2,37 (c, 3H), 2,26 (c, 3H), 2,21 (c, 3H), 2,06 (c, 3H).
13С ЯМР (75 МГц, CDCl3): δ 171,7, 168,9, 148,2, 145,9, 143,2, 141,3, 140,5, 135,7, 130,8, 130,6, 129,5, 127,0, 122,2, 120,9, 120,8, 119,5, 118,6, 118,4, 113,8, 111,1, 110,5, 102,2, 62,5, 61, 5, 60,8, 60,5, 59,7, 55,9, 54,8, 42,1, 41,7, 40,0, 39,5, 29,9, 24,0, 21,7, 20,8, 16,1, 9,9.
ESI-MC m/z: Вычислено для С41Н41N5O8S: 763,3. Найдено (М+Н)+: 764,2.
Пример 28

К раствору соединения 22 (100 мг, 0,13 ммоль) в ацетоне (13 мл, 0,01 М) добавляли раствор соли Фреми (122 мг, 0,45 ммоль) в буферном растворе KH2PO4/Na2НРО4 (13 мл, 0, 035 М). После 24 часов при 23°С реакционную смесь экстрагировали CH2Cl2 и сушили над Na2SO4. Хроматография (гексан/этилацетат 1:1) дает чистое соединение 23 (85 мг, 85%).
Rf: 0,4 (гексан/этилацетат 1:1).
1H ЯМР (300 МГц, CDCl3): δ 7,76 (c, 1H), 7,39 (д, 1H), 7,24 (д, 1H), 7,09 (ддд, 1H), 7,01 (ддд, 1H), 6,22 (д, 1H), 6,02 (д, 1H), 4,98 (д, 1H), 4,44 (c, 1H), 4,22 (c, 1H), 4,19-4,18 (м, 1H) 3,13 (д, 1H), 4,11 (c, 3H), 4,04 (д, 1H), 3,48 (c, 1H), 3,39 (д, 1H), 3,16-3,09 (м, 1H), 2,88-2,78 (м, 2H), 2,70-2,47 (м, 5H), 2,23 (c, 3H), 2,21 (c, 3H), 2,08 (c, 3H), 2,05 (c, 3Н).
ESI-MC m/z: Вычислено для С41Н39N5O9 S: 777,3. Найдено (М+Н)+: 778,2.
Пример 29
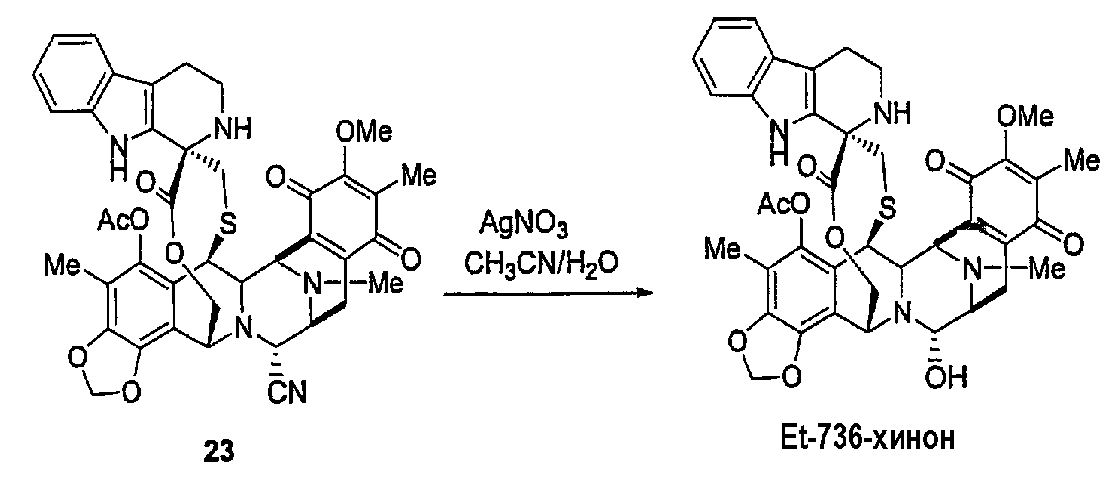
К раствору соединения 23 (85 мг, 0,10 ммоль) в смеси CH3CN/Н2О 3:2 (5,8 мл, 0,009 М) добавляли AgNO3 (549 мг, 3,27 ммоль). После 24 часов при 23°С реакцию гасили смесью 1:1 водного насыщенного солевого раствора и NaHCO3, перемешивали в течение 10 минут и разбавляли и экстрагировали CH2Cl2. Органический слой сушили над Na2SO4. Хроматография (CH2Cl2/МеОН 32:1) дает чистое соединение ЕТ-736-хинон (40 мг, 50%).
Rf: 0,6 (CH2Cl2/МеОН 32:1).
1H ЯМР (300 МГц, CDCl3): δ 7,71 (c, 1H), 7,39 (д, 1H), 7,26 (д, 1H), 7,10 (ддд, 1H), 7,01 (ддд, 1H), 6,22 (д, 1H), 6,01 (д, 1H), 5,12 (д, 1H), 4,76 (c, 1H), 4,42-4,37 (м, 2H), 4,11-4,04 (м, 2H) 4,10 (c, 3H), 3,56 (c, 1H), 3,35-3,11 (м, 2H), 2,85-2,65 (м, 3H), 2,60-2,36 (м, 4Н), 2,23 (c, 3H), 2,19 (c, 3H), 2,09 (c, 3H), 2,05 (c, 3H).
13C ЯМР (75 МГц, CDCl3): δ 186,6, 182,8, 170,9, 169,0, 157,1, 146,1, 141,7, 140,9, 137,5, 136,9, 135,7, 130,6, 128,2, 127,0, 122,4, 119,2, 119,4, 118,7, 115,3, 111,2, 82,7, 62,9, 62,8, 60,9, 58,6, 57,7, 55,9, 53,3, 41,5, 41,1, 40,9, 40,3, 29,9, 22,0, 20,8, 20,0, 14,4, 9,9, 9,1.
ESI-MC m/z: Вычислено для С40Н40N4O10S: 768,3. Найдено (М-Н2О+Н)+: 751,2.
Пример 30
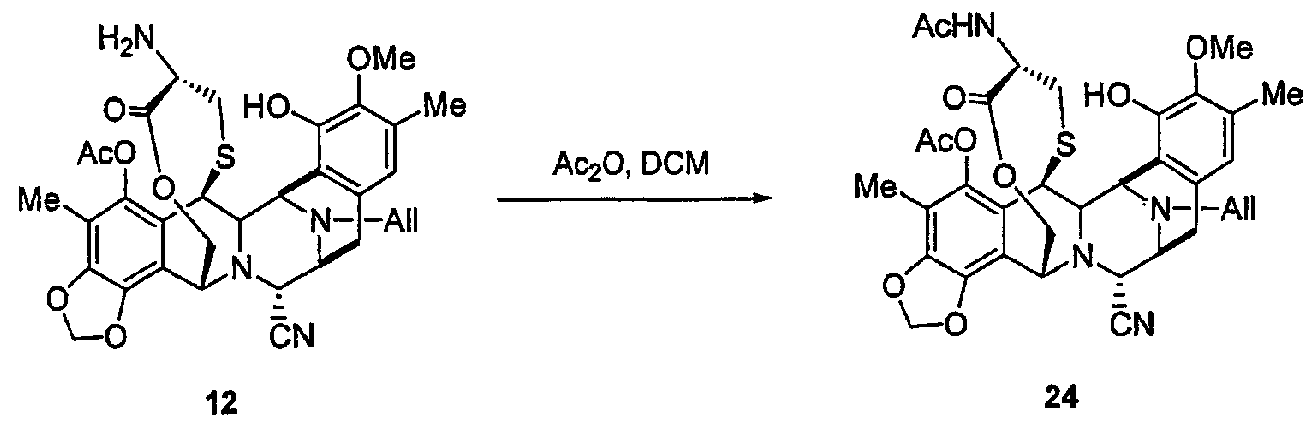
К раствору соединения 12 (99,1 мг, 0,15 ммоль) в CH2Cl2 (3 мл, 0,05 М) в атмосфере аргона при 23°С добавляли уксусный ангидрид (0,015 мл, 0,16 ммоль). Реакционную смесь перемешивали в течение 45 минут и затем реакцию гасили водным насыщенным раствором NaHCO3. Водный слой экстрагировали CH2Cl2 и органический слой сушили над Na2SO4. Флэш-хроматография (гексан/EtOAC, в градиенте 3:2 - 1:2) дает чистое соединение 24 (97 мг, 91%).
Rf: 0,3 (гексан/этилацетат 3:2).
1H ЯМР (300 МГц, CDCl3): δ 6,54 (c, 1H), 6,02 (д, 2H), 5,96 (c, 1H), 5,89-5,76 (м, 1H), 5,52 (д, 1H), 5,11-4,99 (м, 3H), 4,58-4,55 (м, 1H), 4,52 (м, 1H), 4,33 (д, 1H), 4,26 (c, 1H), 4,18 (c, 1H), 4,16 (д, 1H), 3,74 (c, 3Н), 3,54 (ушир.д, 1H), 3,41 (д, 1H), 2,94-2,71 (м, 4H), 2,30-2,25 (м, 1H), 2,30 (c, 3Н), 2,25 (c, 3Н), 2,10 (д, 1H), 2,00 (c, 3Н), 1,87 (c, 3Н).
13С ЯМР (75 МГц, CDCl3): δ 170,5, 168,8, 168,4, 147,8, 145,7, 143,0, 140,9, 140,3, 134,8, 131,1, 129,0, 120,3, 120,1, 119, 4, 118,1, 117,8, 113,4, 113,3, 101,9, 61,2, 60,3, 60,2, 59,4, 59,1, 55,7, 53,0, 51,8, 51,7, 41,7, 32,4, 23,8, 22,8, 20,4, 16,0, 9,5.
ESI-MC m/z: Вычислено для С35Н38N4O9S: 690,2. Найдено (М+Н)+: 691,5.
Пример 31
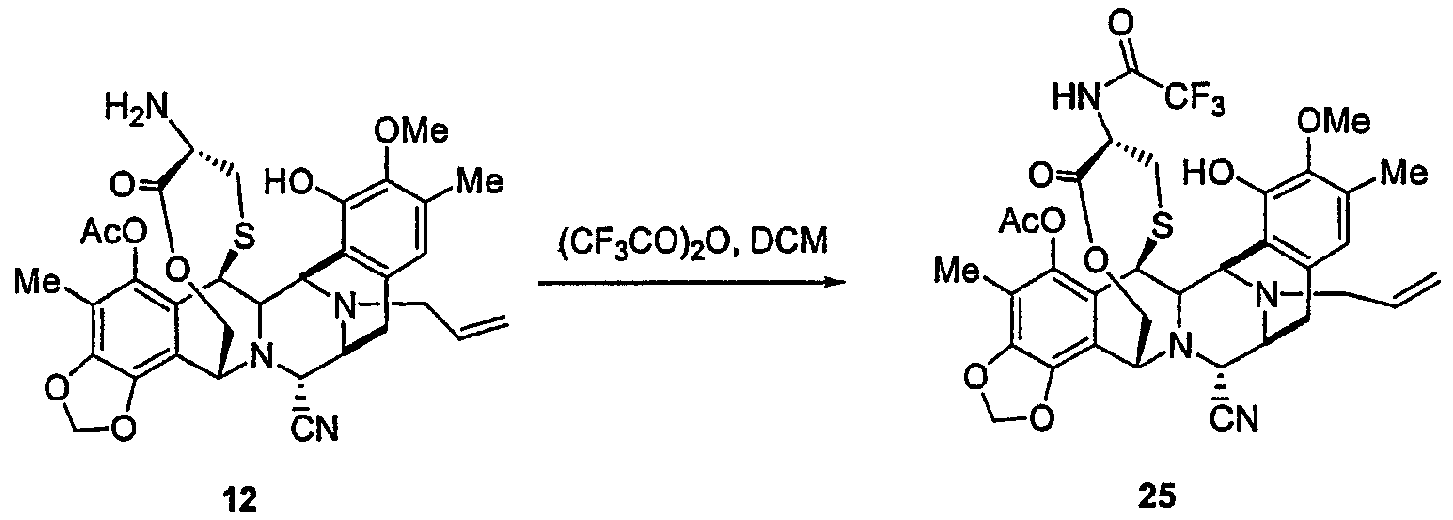
К раствору соединения 12 (130 мг, 0,20 ммоль) в CH2Cl2 (3 мл, 0,03 М) в атмосфере аргона добавляли трифторуксусный ангидрид (0,057 мл, 0,40 ммоль). Реакционную смесь перемешивали в течение 30 минут при 23°С, затем разбавляли CH2Cl2, промывали водным насыщенным раствором NaHCO3 и органическую фазу сушили над Na2SO4. Флэш-хроматография (гексан/EtOAC, 3:2) дает чистое соединение 25 (104 мг, 73%).
Rf: 0,68 (гексан/этилацетат 1:1).
1H ЯМР (300 МГц, CDCl3): δ 6,55 (c, 1H), 6,41 (д, 1H), 6,09 (д, 1H), 5,99 (д, 1H), 5,90-5,77 (м, 1H), 5,72 (c, 1H), 5,12-5,03 (м, 3H), 4,60 (ушир.п, 1H), 4,54-4,51 (м, 1H), 4,34 (дд, 1H), 4,33 (c, 1H), 4,21 (дд, 1H), 4,19 (д, 1H), 3,73 (c, 3H), 3,57-3,55 (м, 1H), 3,44 (д, 1H), 2,87-2,71 (м, 4H), 2,43-2,38 (м, 1H), 2,28 (c, 3H), 2,27 (c, 3H), 2, 11-2,04 (м, 1H), 2,02 (c, 3H).
ESI-MC m/z: Вычислено для С35Н35F3N4O9S: 744,2. Найдено (М+Н)+: 745,5.
Пример 32
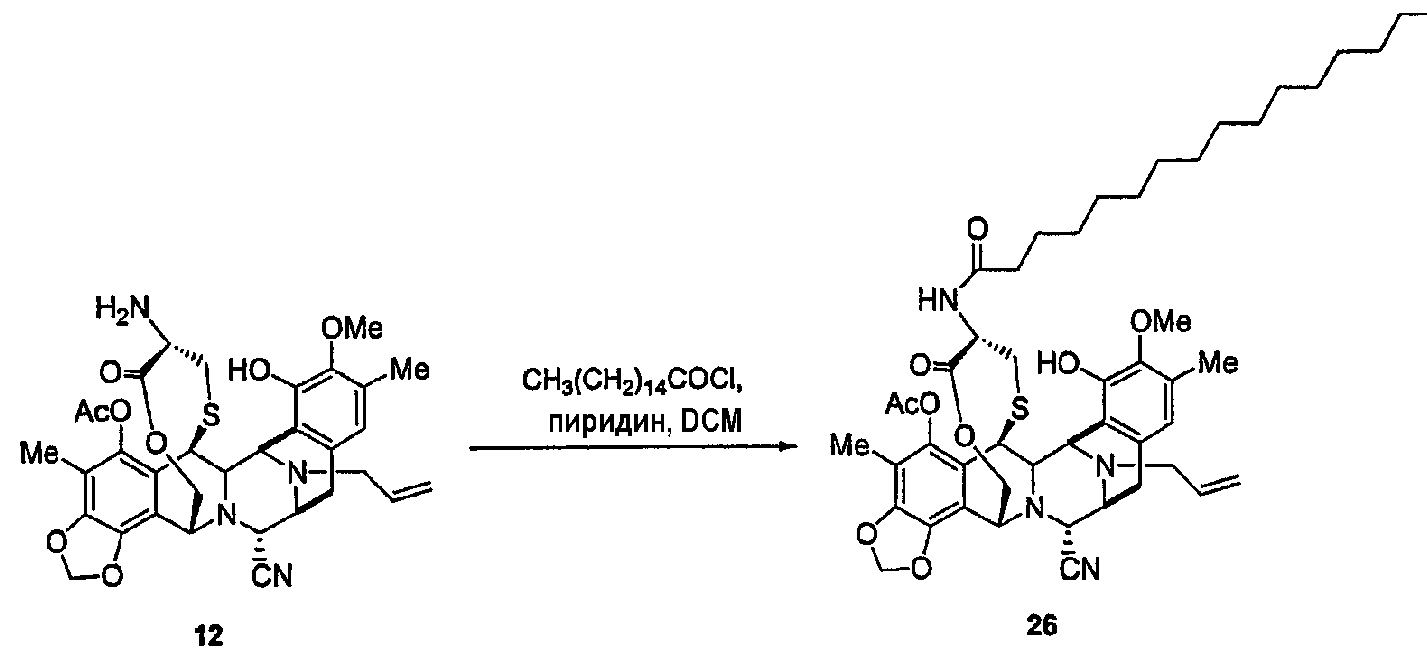
К раствору соединения 12 (60 мг, 0,09 ммоль) в CH2 Cl2 (3,2 мл, 0,03 М) в атмосфере аргона добавляли пиридин (0,008 мл, 0,09 ммоль) и пальмитоилхлорид (0,03 мл, 0,09 ммоль). Реакционную смесь перемешивали в течение 30 минут при 23°С, затем разбавляли CH2Cl2 и промывали водным насыщенным раствором NaHCO3. Органическую фазу сушили над Na2SO4. Флэш-хроматография (гексан/EtOAC, 3:2) дает чистое соединение 26 (71 мг, 90%).
Rf: 0,62 (гексан/этилацетат 1:1).
1H ЯМР (300 МГц, CDCl3): δ 6,55 (c, 1H), 6,08 (д, 1H), 5,98 (д, 1H), 5,89-5,77 (м, 1H), 5,75 (c, 1H), 5,47 (д, 1H), 5,11 (д, 1H), 5,07 (д, 1H), 5,02 (д, 1H), 4,62-4,58 (м, 1H), 4,53 (c, 1H), 4,34 (д, 1H), 4,28 (c, 1H), 4,19 (д, 1H), 4,17 (дд, 1H), 3, 76 (c, 3H), 3,55 (д, 1H), 3,43 (д, 1H), 2,96-2,72 (м, 4H), 2,32 (c, 3H), 2,27 (c, 3H), 2,14-1,98 (м, 1H), 2,02 (c, 3H), 1,62-1,56 (м, 2H), 1,32-1,28 (м, 24H), 0,87 (т, 3H).
ESI-MC m/z: Вычислено для С49Н66N4O9S: 886,5. Найдено (М+H)+: 887,9.
Пример 33
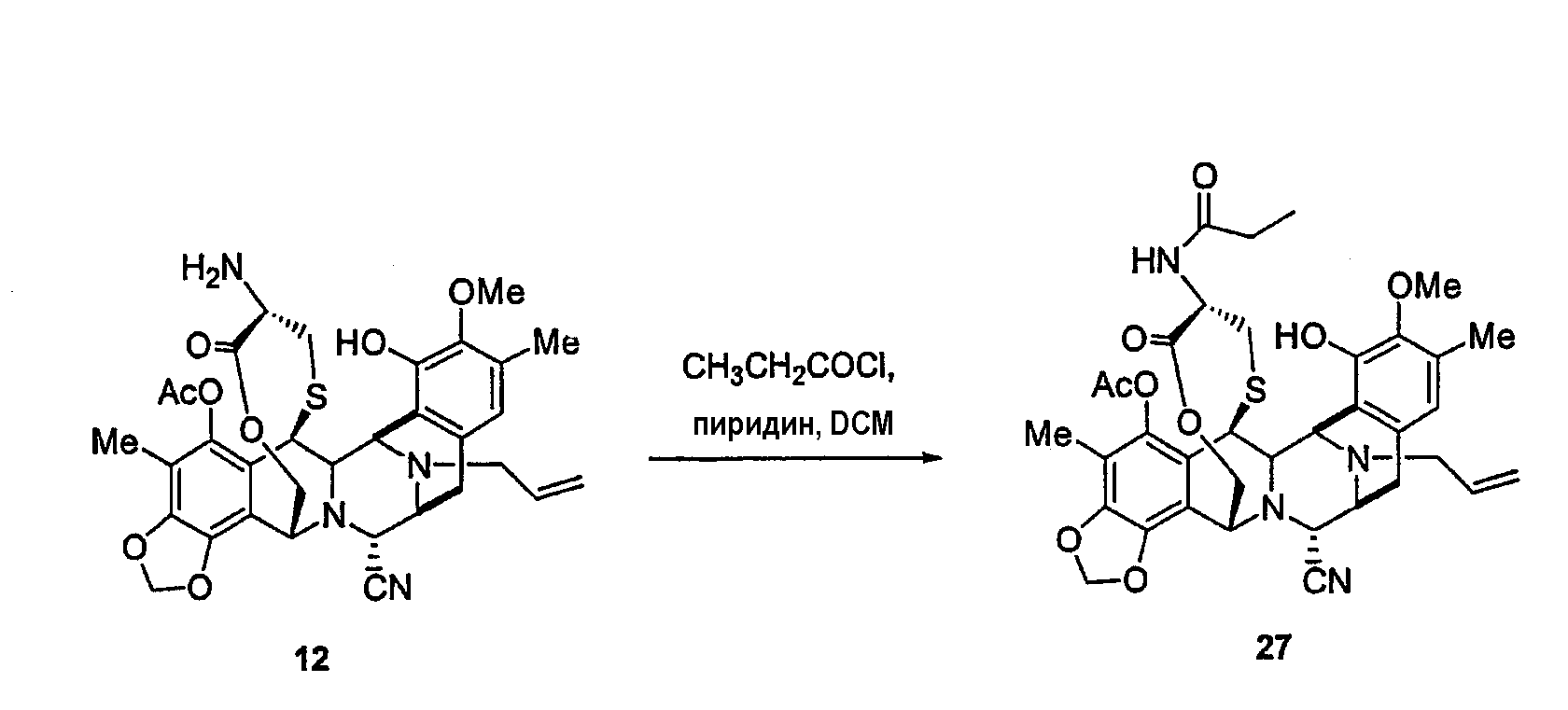
К раствору соединения 12 (65 мг, 0,1 ммоль) в CH2Cl2 (1,6 мл, 0,06 М в атмосфере аргона добавляли пиридин (0,009 мл, 0,11 ммоль) и пропионилхлорид (0,009 мл, 0,11 ммоль). Реакционную смесь перемешивали в течение 15 минут при 23°С, затем разбавляли CH2Cl2 и промывали водным насыщенным раствором NaHCO3. Органическую фазу сушили над Na2SO4. Флэш-хроматография (гексан/EtOAC в градиенте 1:1 - 1:2) дает чистое соединение 27 (41 мг, 59%).
Rf: 0,66 (гексан/этилацетат 1:4).
1H ЯМР (300 МГц, CDCl3): δ 6,55 (c, 1H), 6,08 (д, 1H), 5,98 (д, 1H), 5,90-5,77 (м, 1H), 5,51 (д, 1H), 5,12 (д, 2H), 5,03 (д, 2H), 4,61-4,54 (м, 2Н), 4,36 (д, 1Н), 4,29 (c, 1H), 4,16 (дд, 2H), 3,76 (c, 3H), 3,55 (д, 1H), 3,43 (д, 1H), 2,89-2,76 (м, 5H), 2,31 (c, 3H), 2,24 (c, 3H), 2,15-2, 04 (м, 2H), 2,02 (c, 3H), 1,10 (т, 3H).
ESI-MC m/z: Вычислено для С36Н40N4O9S: 704,3. Найдено (М+Н)+: 705,6.
Пример 34

К раствору соединения 12 (64 мг, 0,1 ммоль) в CH2 Cl2 (2 мл, 0,05 М) в атмосфере аргона добавляли кумариновую кислоту (23 мг, 0,13 ммоль), DIPEA (0,05 мл, 0,15 ммоль) и EDC.HCl (60 мг, 0,15 ммоль). Реакционную смесь перемешивали в атмосфере аргона при 23°С в течение 4 часов, затем разбавляли CH2Cl2, промывали водным насыщенным раствором NaHCO3. Органическую фазу сушили над Na2 SO4. Флэш-хроматография (гексан/EtOAC, 1:1) дает чистое соединение 28 (40 мг, 49%).
Rf: 0,5 (гексан/этилацетат 1:2).
1H ЯМР (300 МГц, CDCl3): δ 8,98 (д, 1H), 7,69-7,62 (м, 2H), 7,44 (7,33 (м, 2H), 6,65 (c, 1H), 6,10 (c, 1H), 5,99 (c, 1H), 5,89-5,80 (м, 1H), 5,60 (д, 1H), 5,11-5,05 (м, 4H), 4,69 (дд, 1H), 4,59 (ушир.c, 1H), 4,35-4,16 (м, 5Н), 3,67 (3Н), 3,58 (д, 1H), 3,45 (д, 2H), 2,93-2,62 (м, 5H), 2,27 (c, 3Н), 2,13 (c, 3Н), 2,03 (c, 3Н).
ESI-MC m/z: Вычислено для С43Н40N4O11S: 820,2. Найдено (М+H)+: 821,8.
Пример 35
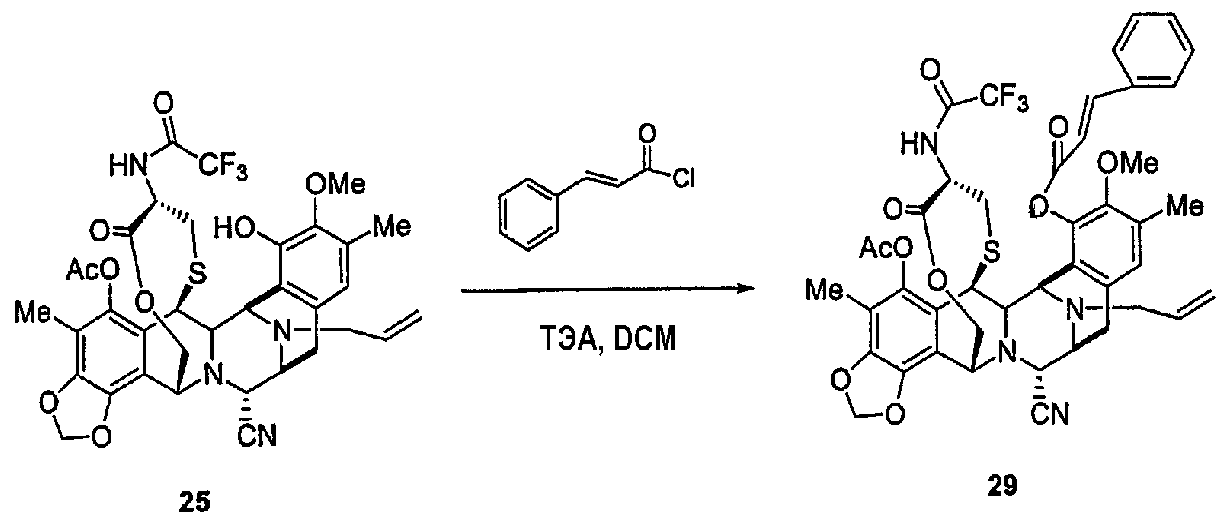
К раствору соединения 25 (40 мг, 0,05 ммоль) в CH2Cl2 (1,5 мл, 0,03 М) в атмосфере аргона добавляли Et3N (0,035 мл, 0,24 ммоль) и циннамоилхлорид (27,7 мг, 0,016 ммоль). После 30 минут при 23°С реакционную смесь разбавляли CH2Cl2, промывали водным насыщенным раствором NaHCO3 и органическую фазу сушили над Na2SO4. Флэш-хроматография (гексан/EtOAC, 3:2) дает чистое соединение 29 (46 мг, 99%).
Rf: 0,5 (гексан/этилацетат 2:1).
1H ЯМР (300 МГц, CDCl3): δ 7,93 (д, 1H), 7,62-7,59 (м, 2H), 7,46-7,44 (м, 3H), 6,91 (c, 1H), 6,63 (д, 1H), 6,44 (д, 1H), 6,11 (д, 1H), 6,01 (д, 1H), 5,84-5,71 (м, 1H), 5,19-5,05 (м, 3H), 4,59-4,53 (м, 1H), 4,35 (c, 1H), 4,25-4,21 (м, 2H), 4,00 (д, 1H), 3,71 (c, 3H), 3,64-3,62 (м, 1H), 3,49 (д, 1H), 2,95-2,88 (м, 3H), 2,77-2,70 (м, 1H), 2,52-2,48 (м, 1H), 2, 36 (c, 3H), 2,30 (c, 3H), 2,14-2,04 (м, 1H), 2,06 (c, 3H).
ESI-MC m/z: Вычислено для С44Н41F3N4O10S: 874,3. Найдено (М+H)+: 875,6.
Общая экспериментальная процедура для синтеза соединений 30, 32, 33 и 34: реакция деаллилирования
К раствору исходного материала в CH2Cl2 (0,04 М) добавляли (PPh3)2PdCl2 (0,08 экв.) и уксусную кислоту (5 экв.). Добавляли по каплям HSnBu3 (исходное количество 8 экв.) при 23°С в атмосфере аргона. Во время реакции (1 час и 45 минут) добавляли по каплям дополнительное количество HSnBu3 (конечное количество 48 экв.). После этого периода времени раствор выливали на колонку. Флэш-хроматография (смеси гексан/этилацетат) дает чистые соединения.
Пример 36

Rf: 0,3 (гексан/этилацетат 2:5).
1H ЯМР (300 МГц, CDCl3): δ 6,57 (c, 1H), 6,04 (д, 2H), 5,51 (д, 1H), 5,03 (д, 1H), 4,60-4,57 (м, 1H), 4,52 (ушир.п., 1H), 4,47 (д, 1H), 4,27 (c, 1H), 4,19-4,15 (м, 2H), 3,84 (ушир.д, 1H), 3,75 (c, 3H), 3,43 (д, 1H), 3,07 (c, 1H), 2,96 (кв, 1Н), 2, 34-2,27 (м, 1H), 2,30 (c, 3H), 2,27 (c, 3H), 2,13 (д, 1H), 2,02 (c, 3H), 1,87 (c, 3H).
ESI-MC m/z: Вычислено для С32Н34N4O9S: 650,2. Найдено (М+Н)+: 651,4.
Пример 37

Rf: 0,3 (гексан/этилацетат 1:1).
1H ЯМР (300 МГц, CDCl3): δ 6,54 (c, 1H), 6,40 (д, 1H), 6,10 (д, 1H), 6,00 (д, 1H), 5,05 (д, 1H), 4,60 (ушир.п, 1H), 4,54-4,51 (м, 1H), 4,48 (д, 1H), 4,32 (c, 1H), 4,22 (дд, 1H), 4,19 (д, 1H), 3,86-3,84 (м, 1H), 3,73 (c, 3H), 3,46 (д, 1H), 2,99-2,98 (м, 2H), 2,44-2,39 (м, 1H), 2,29 (c, 3H), 2,26 (c, 3H), 2,13-2,08 (м, 1H), 2,03 (c, 3H).
ESI-MC m/z: Вычислено для С32Н31F3N4O9S: 704,2. Найдено (М+Н)+: 705,6.
Пример 38
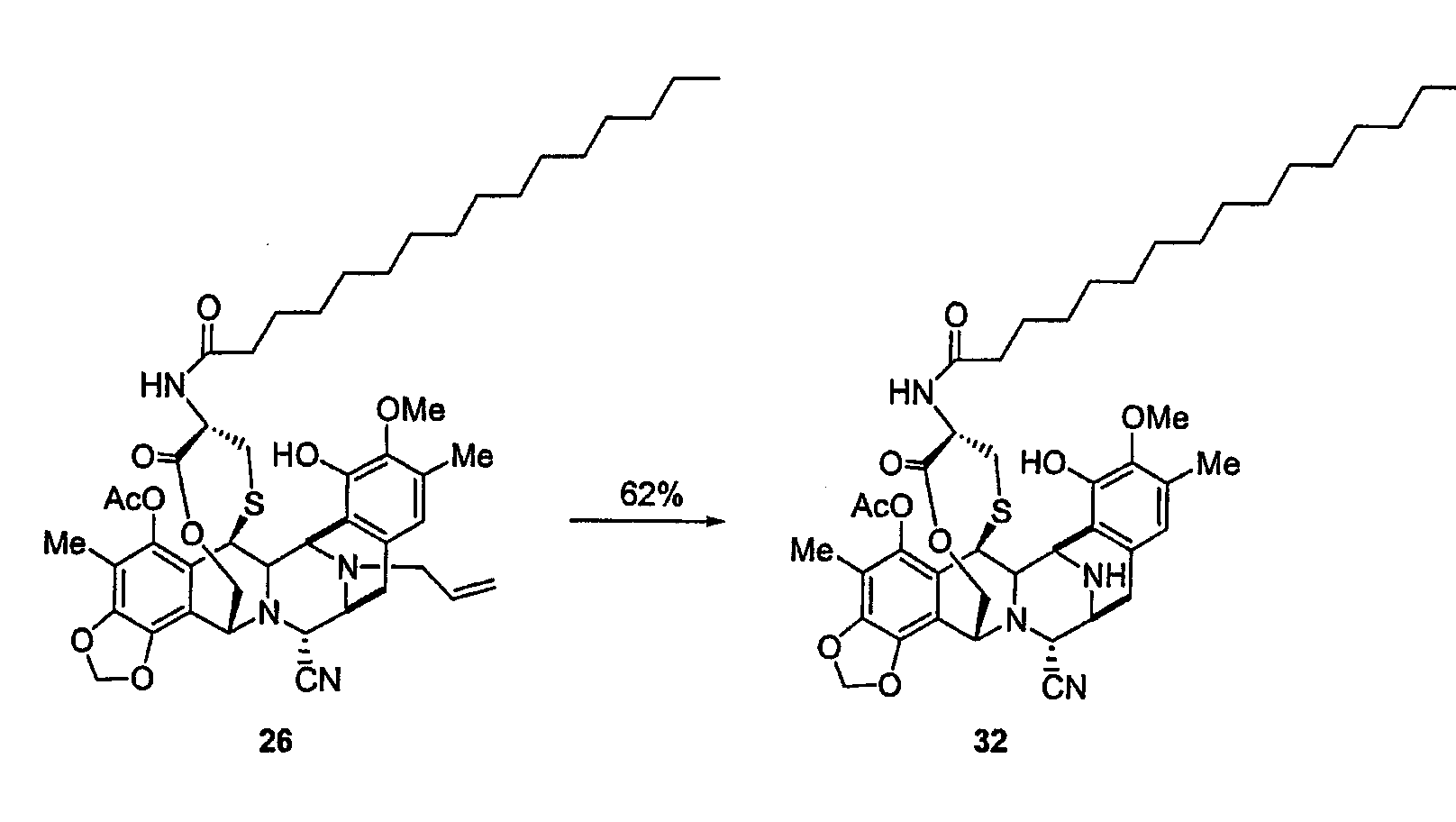
Rf: 0,4 (гексан/этилацетат 1:1).
1H ЯМР (300 МГц, CDCl3): δ 6,57 (c, 1H), 6,09 (д, 1H), 5,99 (д, 1H), 5,78 (c, 1H), 5,47 (д, 1H), 5,03 (д, 1H), 4,62-4,60 (м, 1H), 4,53 (c, 1H), 4,47 (д, 1H), 4,28 (c, 1H), 4,19 (д, 1H), 4,17 (дд, 1H), 3,85 (д, 1H), 3,76 (c, 3H), 3,44 (д, 1H), 3,11-2,91 (м, 2H), 2,31 (c, 3H), 2,28 (c, 3H), 2,16-1,96 (м, 3H), 2,02 (c, 3H), 1,62-1,56 (м, 2H), 1,38-1,28 (м, 24H), 0,87 (т, 3H).
ESI-MC m/z: Вычислено для С46Н62N4O9S: 846,4. Найдено (М+H)+: 847,0.
Пример 39

Rf: 0,2 (гексан/этилацетат 1:1).
1H ЯМР (300 МГц, CDCl3): δ 6, 57 (c, 1H), 6,01 (c, 1H), 5,74 (д, 1H), 5,52 (д, 1H), 5,10-4,83 (м, 2H), 4,61-4,54 (м, 1H), 4,48 (д, 1H), 4,34-4,15 (м, 4H), 3,76 (c, 3Н), 3,59-3,34 (м, 3H), 3,10-2,89 (м, 3H), 2,30 (c, 3H), 2,29 (c, 3H), 2,12 (дд, 2H), 2,03 (c, 3Н), 1,10 (т, 3H).
ESI-MC m/z: Вычислено для С33Н36N4O9S: 664,2. Найдено (М+H)+: 665,6.
Пример 40

Rf: 0,4 (гексан/этилацетат 1:1).
1H ЯМР (300 МГц, CDCl3): δ 7,93 (д, 1H), 7,62-7,59 (м, 2H), 7,46-7,44 (м, 3H), 6,87 (c, 1H), 6,65 (д, 1H), 6,43 (д, 1H), 6,12 (д, 1H), 6,03 (д, 1H), 5,03 (д, 1H), 4,56-4,49 (м, 1H), 4,35 (c, 1H), 4,23-4,1 (м, 3H), 3,72 (c, 3H), 3,49 (д, 1H), 3,19-2,90 (м, 3H), 2,52-2,43 (м, 1H), 2,30 (c, 3H), 2,147-2,08 (м, 1H), 2,06 (c, 3H), 2,03 (c, 3H).
ESI-MC m/z: Вычислено для С41Н37F3N4O10S: 834,2. Найдено (М+H)+: 836,0.
Пример 41
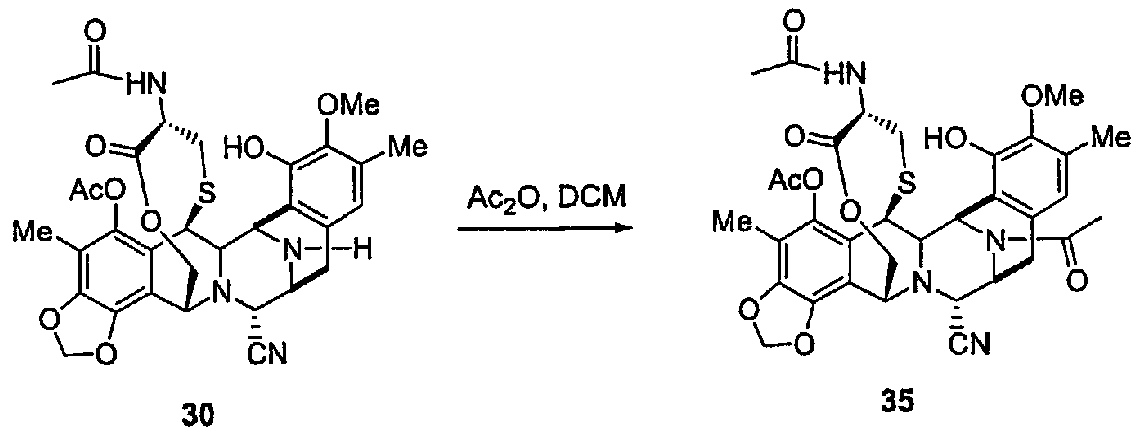
К раствору соединения 30 (25 мг, 0,04 ммоль) в CH2Cl2 (0,8 мл, 0,05 М) в атмосфере азота добавляли при 23°С уксусный ангидрид (0,005 мл, 0,042 ммоль). Спустя 1 час при 23°С добавляли дополнительное количество уксусного ангидрида (0,005 мл, 0,042 ммоль). Реакционную смесь перемешивали в течение еще 4 часов и затем реакцию гасили водным насыщенным раствором NaHCO3. Водный слой экстрагировали CH2Cl2 и органический слой сушили над Na2SO4. Флэш-хроматография (гексан/EtOAc, в градиенте от 2:5 до 1:5) дает чистое соединение 35 (24 мг, 90%).
Rf: 0,15 (гексан/этилацетат 2:7).
1H ЯМР (300 МГц, CDCl3): δ 6,56, 6,54 (2c, 1H), 6,36, 6,15-6,00 (м, 3H), 5,52-5,42 (м, 1,6H), 5,29-5,25 (м, 0,6H), 5,07-5,01 (м, 1H), 4,71-4,58 (м, 2, 4H), 4,30-4,16 (м, 3,4H), 3,76, 3,74 (2c, 3H), 3,41-3,13 (м, 3H), 2,40-2,35 (м, 1H), 2,13 (д, 1H), 2,28, 2,27, 2,19, 2,07, 2,02, 1,98, 1,87, 1,86 (8c, 15H).
ESI-MC m/z: Вычислено для С34Н36N4O10S: 692,2. Найдено (М+Н)+: 693,3.
Общая экспериментальная процедура для синтеза соединений 36, 32, 38, 39, 40 и 41: превращение нитрильной группы в гидроксильную группу
К раствору исходного материала в смеси ТГФ/Н2О 4:1 (0,03 М) добавляли 10 экв. CuCl. Реакционную смесь перемешивали в течение 24 часов с защитой от света. После него реакцию гасили водным насыщенным раствором NH4Cl и разбавляли CH2Cl2. Органическую фазу промывали солевым раствором и водным насыщенным раствором NaHCO3 и водную фазу экстрагировали CH2Cl2. Объединенные органические слои сушили над Na2SO4. Флэш-хроматография (смеси CH2Cl2/МеОН) дает чистые соединения.
Пример 42

Rf: 0,11 (CH2Cl2/МеОН 30:1).
1H ЯМР (300 МГц, CD3OD): δ 6,56 (c, 1H), 6,05 (д, 2H), 5,23 (д, 1H), 4,71 (c, 1H), 4,51 (м, 1H), 4,50-4,40 (м, 2H), 4,14-4,11 (м, 2H), 3,71 (c, 3H), 3,62-3,60 (м, 1H), 3,52-3,50 (м, 1H), 3,00 (д, 2H), 2,30 (c, 3H), 2,28 (c, 3H), 2,28-2,05 (м, 2H), 2,00 (c, 3H), 1,90 (c, 3H).
ESI-MC m/z: Вычислено для С31Н35N3O10S: 641,2. Найдено (М-Н2О+Н)+: 624,3.
Пример 43

Rf: 0,35 (CH2Cl2/МеОН 16:1).
1H ЯМР (300 МГц, CDCl3): δ (6,55 (c, 1H), 6,49-6,47 (м, 1Н), 6,07 (д, 1H), 5,97 (д, 1H), 5,18 (д, 1H), 4,83 (c, 1H), 4,52-4,49 (м, 2H), 4,35 (ca, 1H), 4,15-4,08 (м, 2H), 3,73 (c, 3H), 3,60-3,45 (м, 2H), 2,96-2,85 (м, 2H), 2,47-2,39 (м, 1H), 2,29 (c, 3H), 2,27 (c, 3H), 2,17-2,08 (м, 1H), 2,02 (c, 3H).
13C ЯМР (75 МГц, CDCl3): δ 169,0, 156,4, 156,1, 146,0, 142,9, 141,3, 141,1, 131,8, 130,1, 129,0, 121,7, 120,8, 115,1, 114,6, 102,1, 81,1, 68,4, 62,2, 60,4, 57,2, 56,1, 53,1, 42,5, 32,1, 32,0, 29,6, 28,1, 22,9, 20,7, 14,3, 9,8.
ESI-MC m/z: Вычислено для С31Н32F3N3O10S: 695,2. Найдено (М-Н2О+Н)+: 678,4.
Пример 44
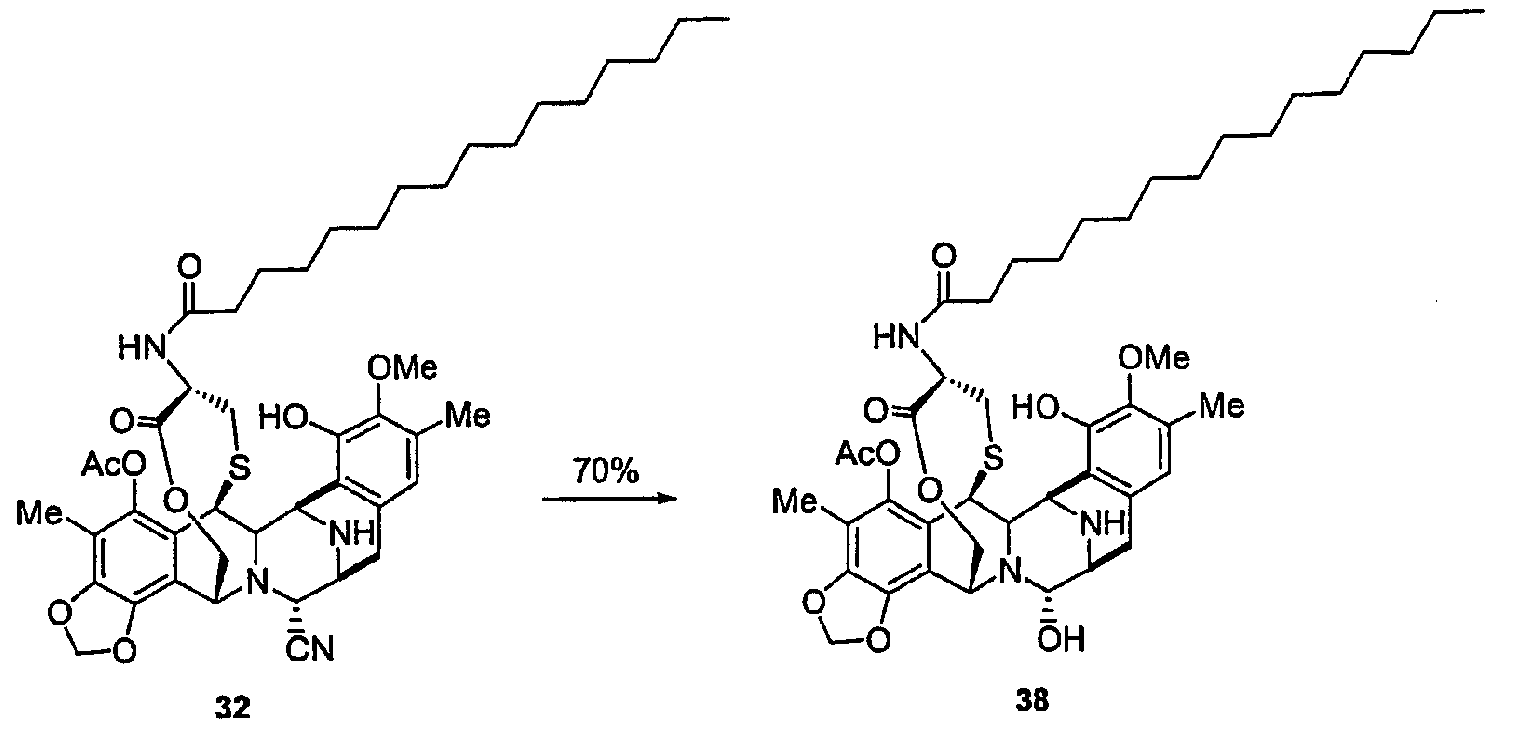
Rf: 0,4 (CH2Cl2 /МеОН 16:1).
1H ЯМР (300 МГц, CDCl3): δ 6,57 (c, 1H), 6,06 (д, 1H), 5,96 (д, 1H), 5,53 (д, 1H), 5,15 (д, 1H), 4,78 (c, 1H), 4,59-4,56 (м, 1H), 4,48-4,42 (м, 1H), 4,35 (д, 1H), 4,07 (дд, 1H), 3,98 (дд, 1H), 3,76 (c, 3H), 3,60-3,57 (м, 1H), 3,52 (д, 1H), 3,02-2,79 (м, 2H), 2,31 (c, 3H), 2,28 (c, 3H), 2,17-2,05 (м, 1H), 2,01 (c, 3H), 1,70-1,63 (м, 2H), 1, 36-1,24 (м, 24H), 0,87 (т, 3H).
13C ЯМР (75 МГц, CDCl3): δ 172,2, 170,7, 146,1, 145,8, 142,9, 141,2, 141,0, 132,1, 129,2, 125,5, 125,0, 121,4, 121,0, 115,4, 112,8, 102,0, 81,2, 61,8, 60,6, 57,0, 56,1, 52,0, 51,3, 48,1, 42,4, 36,6, 32,5, 32,1, 30,0, 29,9, 29,8, 29,7, 29,6, 28,0, 27,4, 25,6, 22,9, 20,8, 16,2, 14,3, 9,8.
ESI-MC m/z: Вычислено для С45Н63N3O10S: 837,4. Найдено (М-Н2О+Н)+: 820,8.
Пример 45
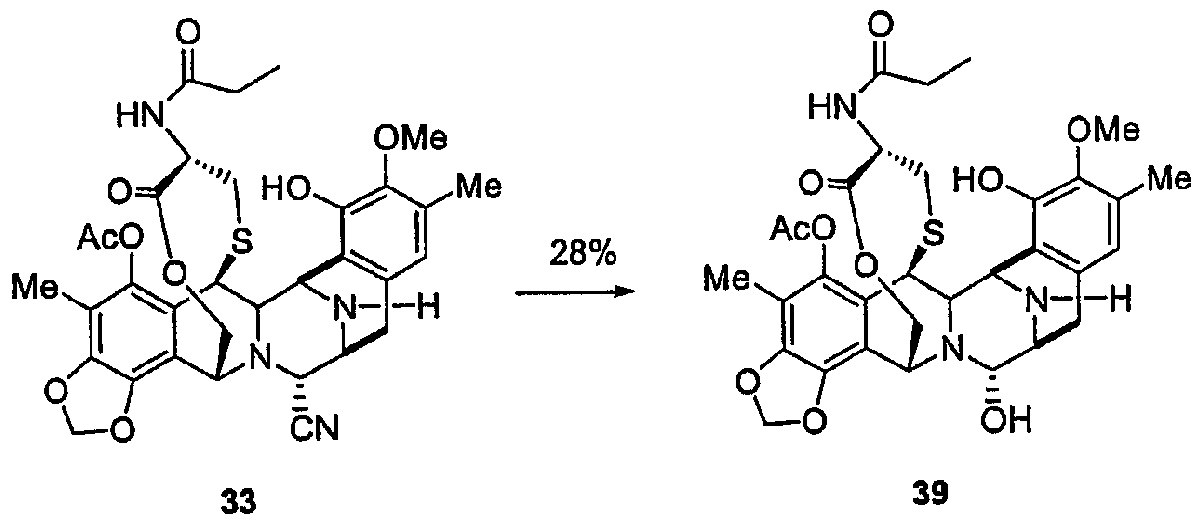
Rf: 0,22 (CH2Cl2/МеОН 5:1).
1H ЯМР (300 МГц, CDCl3): δ 6,58 (c, 1H), 6,07 (c, 1H), 5,97 (c, 1H), 5,76 (ушир.c, 1H), 5,57 (д, 1H), 5,16 (д, 1H), 4,79 (c, 1H), 4,60-4'35 (м, 4H), 4,08 (д, 1H), 3,76 (c, 3H), 3,64-3,50 (м, 2H), 3,00 (д, 1H), 2,84 (дд, 1H), 2,30 (c, 3H), 2,28 (c, 3H), 2,35-2,28 (м, 1H) 2,17-2,04 (м, 3H), 2,01 (c, 3H),1,10 (т, 3H).
ESI-MC m/z: Вычислено для С32Н37 N3O10S: 655,2. Найдено (М-Н2О+Н)+: 638,4.
Пример 46
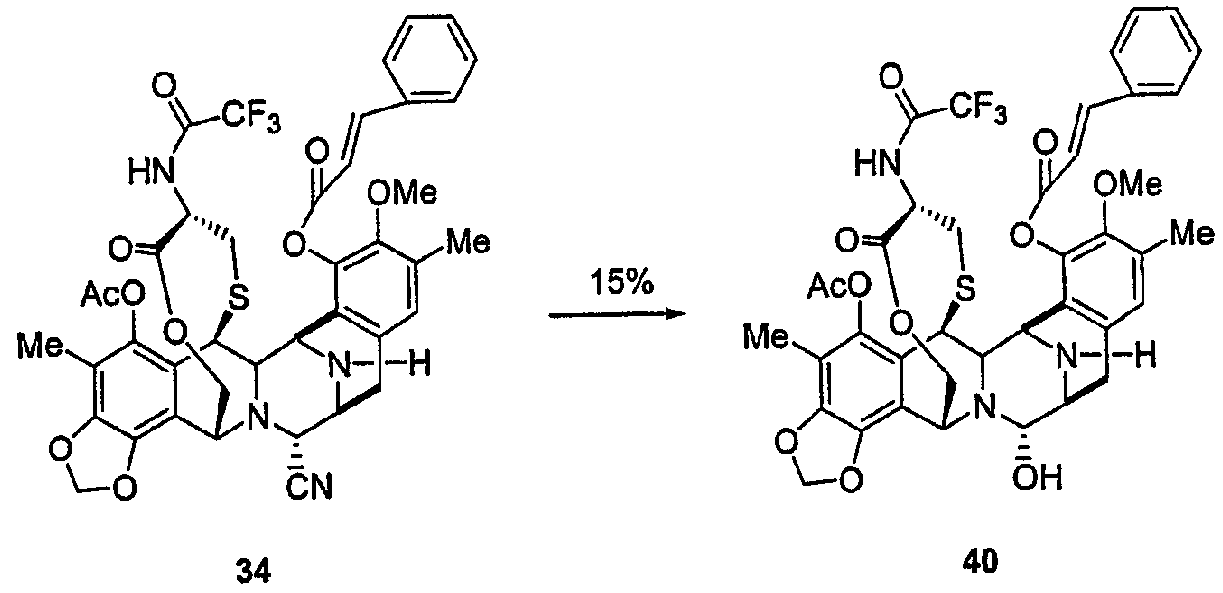
Rf: 0,35 (CH2Cl2/МеОН 16:1).
1H ЯМР (300 МГц, CDCl3): δ 7,94 (д, 1H), 7, 62-7,59 (м, 2H), 7,46-7,44 (м, 3H), 6,87 (c, 1H), 6,65 (д, 1H), 6,45 (д, 1H), 6,09 (д, 1H), 6,00 (д, 1H), 5,15 (д, 1H), 4,83 (c, 1H), 4,52-4,49 (м, 2H), 4,35 (ca, 1H), 4,15-4,08 (м, 2H), 3,73 (c, 3H), 3,60-3,45 (м, 2H), 2,96-2,85 (м, 2H), 2,47-2,39 (м, 1H), 2,29 (c, 3H), 2,27 (c, 3H), 2,17-2,08 (м, 1H), 2,02 (c, 3H).
ESI-MC m/z: Вычислено для С40Н38F3 N3O11S: 825,2. Найдено (М-Н2О+Н)+: 809,5.
Пример 47
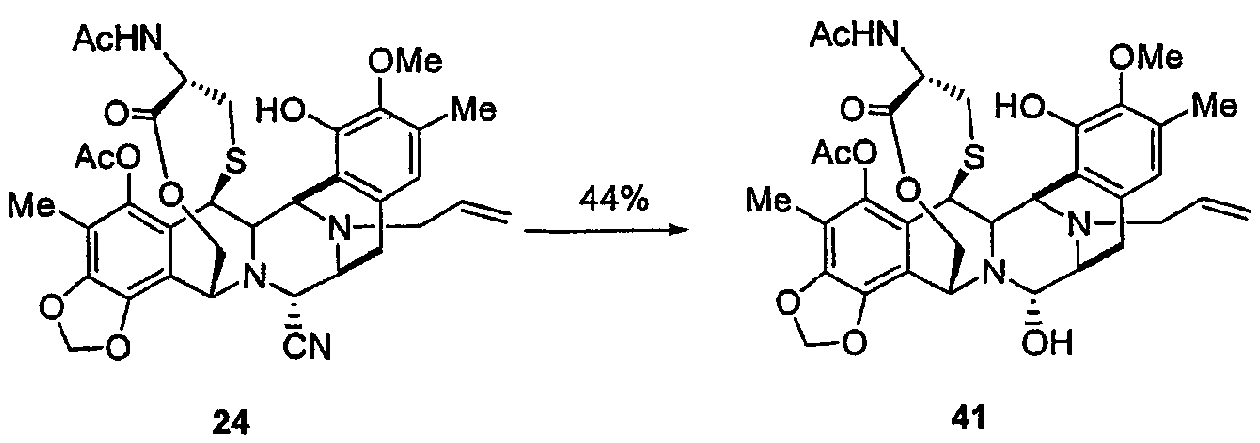
Rf: 0,2 (CH2Cl2/МеОН 60:1).
1H ЯМР (300 МГц, CDCl3): δ 6,58 (c, 1H), 6,02 (д, 2H), 5,83-5,69 (м, 1H), 5,69 (c, 1H), 5,59 (д, 1H), 5,17-4,96 (м, 3Н), 4,78 (c, 1H), 4,57-4,53 (м, 1H), 4,47-4,25 (м, 3Н), 4,09 (дд, 1H), 3,77 (c, 3H), 3,47 (д, 1H), 3,34-3,31 (м, 1H), 2,92-2,73 (м, 4H), 2,32-2,27 (м, 1H), 2,32 (c, 3Н), 2,27 (c, 3Н), 2,14 (д, 1H), 2,01 (c, 3Н), 1,88 (c, 3H).
ESI-MC m/z: Вычислено для С34Н39N3O10S: 681,2. Найдено (М-Н2О+Н)+: 664,6.
Пример 48
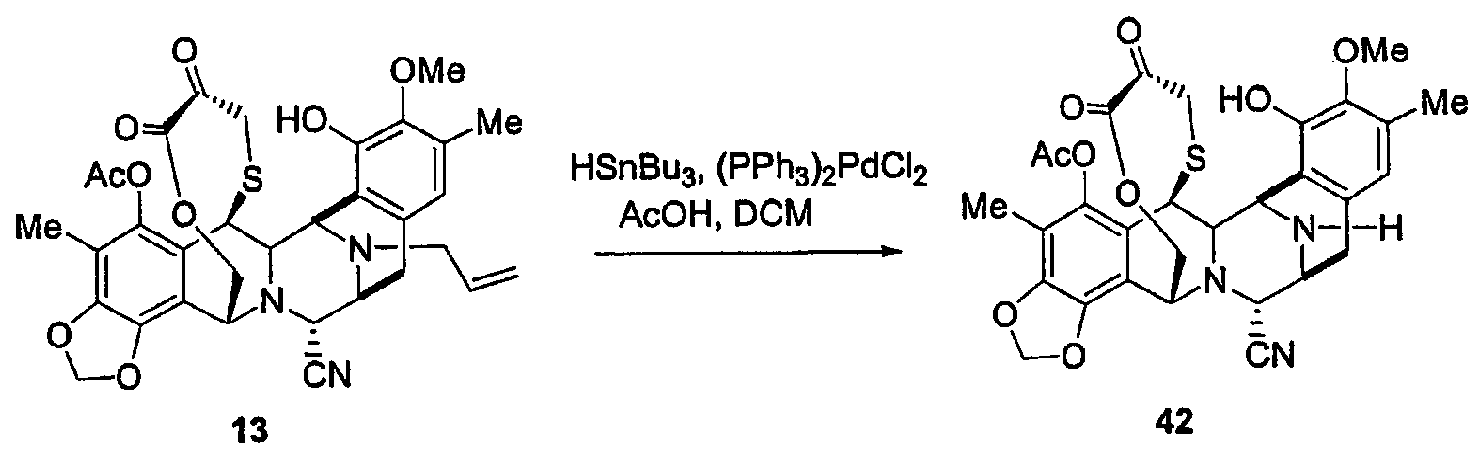
К раствору соединения 13 (39 мг, 0,06 ммоль) в CH2Cl2 (1,5 мл, 0,040 М) добавляли (PPh3)2PdCl2 (3,4 мг, 0,004 ммоль), уксусную кислоту (0,02 мл, 0,30 ммоль) и, наконец, HSnBu3 (0,05 мл, 0,2 ммоль). После 30 минут при 23°С реакционную смесь выливали на колонку. Хроматография (гексан/этилацетат в градиенте от 4:1 до 1:2) дает чистое соединение 42 (31 мг, 86%).
Rf: 0,38 (гексан/этилацетат 3:4).
1H ЯМР (300 МГц, CDCl3): δ 6,58 (c, 1H), 6, 51 (с, 1H), 6,11 (д, 1H), 6,08 (д, 1H), 6,02 (д, 1H), 5,99 (д, 1H), 5,78 (ca, 2H), 5,10 (д, 1H), 5,05 (д, 1H), 4,65 (c, 1H), 4,54 (c, 1H), 4,50 (д, 1H), 4,47 (д, 1H), 4,40 (c, 1H), 4,26 (c, 1H), 4,24 (c, 1H), 4,20 (c, 1H), 4,18 (д, 1H), 4,01 (дд, 1H), 3,87-3,81 (м, 2H), 3,76 (c, 3H), 3,74 (c, 3H), 3,56 (д, 1H), 3,42 (д, 1H), 3,13-2,81 (м, 6H), 2,57 (д, 2H), 2,32 (c, 3H), 3,31 (c, 3H), 2,28 (c, 3H), 2,24 (c, 3H), 2,19-2,15 (м, 1H), 2,04 (c, 3H), 2,03 (c, 3H).
ESI-MC m/z: Вычислено для С30Н29N3O9S: 607,2. Найдено (М+Н)+: 608, 3.
Пример 49

К раствору соединения 42 (30 мг, 0,05 ммоль) в смеси ТГФ/Н2О 4:1 (1,7 мг, 0,009 М) добавляли CuCl (49 мг, 0,5 ммоль). Спустя 24 часа при 23°С реакционную смесь гасили насыщенным водным раствором NH4Cl, разбавляли CH2Cl2 и промывали солевым раствором и водным насыщенным раствором NaHCO3 и водную фазу экстрагировали CH2Cl2. Органический слой сушили над Na2SO4. Хроматография (CH2Cl2/МеОН 16:1) дает чистое соединение 43 (3 мг, 10%).
Rf: 0,2 (CH2Cl2 /МеОН 16:1).
1H ЯМР (300 МГц, CDCl3): δ 6,58 (с, 1Н), 6,05 (д, 1Н), 5,96 (д, 1Н), 5,78 (ca, 1H), 5,17 (д, 1H), 4,78 (c, 1H), 4,51-4,35 (м, 3H), 4,07 (дд, 1H), 4,00 (м, 2H), 3,77 (c, 3H), 3,64-3,53 (м, 2H), 3,07-2,80 (м, 3H), 2,31 (c, 3H), 2,17-2,10 (м, 1H), 2,02 (c, 3H).
ESI-MC m/z: Вычислено для С29Н30N2 O10S: 598,2. Найдено 583,1 (М+Н2О+Ме).
Пример 50
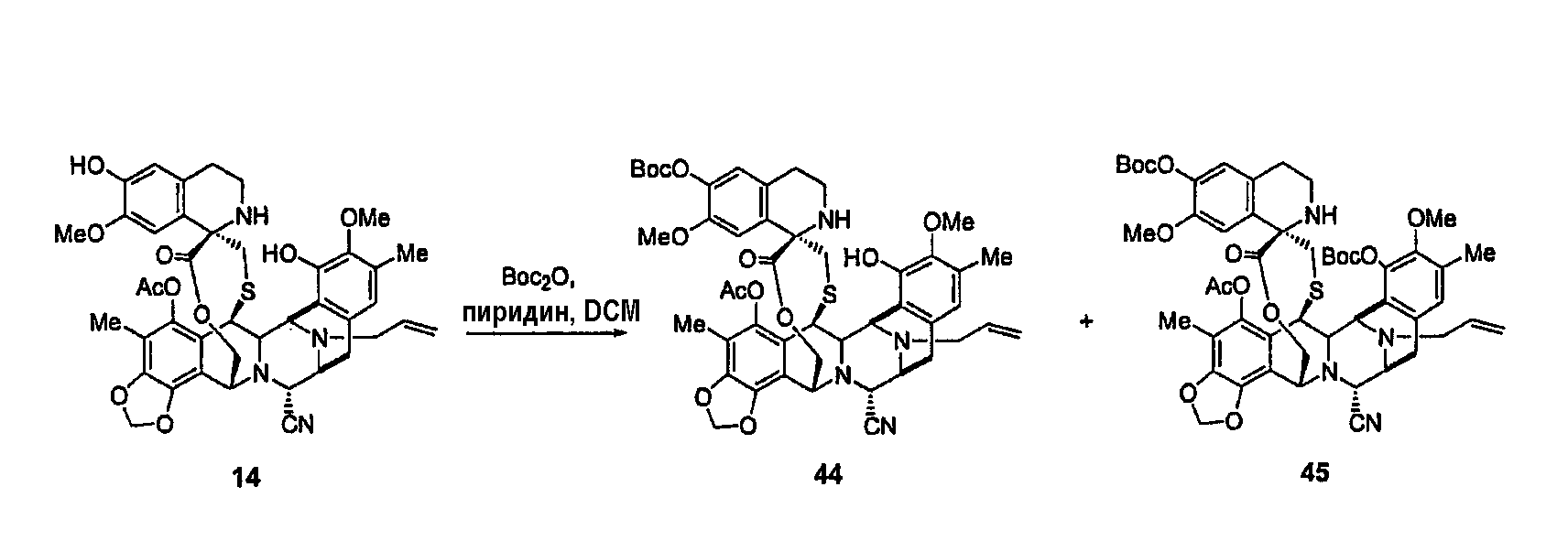
К раствору соединения 14 (414 мг, 0,5 ммоль) в CH2Cl2 (9,5 мл, 0,032 М) в атмосфере аргона добавляли Вос2О (113 мг, 0,5 ммоль) и пиридин (0,04 мл, 0,5 ммоль). После 2 часов при 23°С добавляли дополнительное количество Вос2О (113 мг, 0,5 ммоль) и пиридина (0,04 мл, 0,05 ммоль). Спустя 3 часа добавляли дополнительное количество Вос2О (113 мг, 0,5 ммоль) и пиридина (0,04 мл, 0,05 ммоль). Общее время реакции: 6 часов. Реакцию гасили водным насыщенным раствором NaHCO3, водную фазу экстрагировали CH2Cl2 и органические слои сушили над Na2SO4. Флэш-хроматография (гексан/этилацетат 1:1) дает чистые соединения 44 (365 мг, 78%) и 45 (105 мг, 20%).
Соединение 44
Rf: 0,5 (гексан/этилацетат 1:1).
1H ЯМР (300 МГц, CDCl3): δ 6,68 (c, 1H), 6,59 (c, 1H), 6,57 (c, 1H), 6,03 (д, 1H), 5,96 (д, 1H), 5,93-5,80 (м, 1H), 5,73 (c, 1H), 5,13-5,07 (м, 2H), 5,00 (д, 1H), 4,55 (c, 1H), 4,36 (д, 1H), 4,32 (c, 1H), 4,18 (д, 1H), 4,09 (дд, 1H), 3,78 (c, 3H), 3,58 (c, 3H), 3, 57-3,49 (м, 2H), 3,14-3,05 (м, 1H), 2,98-2,76 (м, 4H), 2,68-2,59 (м, 1H), 2,50-2,45 (м, 1H), 2,35-2,14 (м, 2H), 2,31 (c, 3H), 2,26 (c, 3H), 2,02 (c, 3H), 1,50 (c, 9H).
ESI-MC m/z: Вычислено для С47Н52N4O12S: 896,3. Найдено (М+Н)+: 897,0.
Соединение 45
Rf: 0,6 (гексан/этилацетат 1:1).
1H ЯМР (300 МГц, CDCl3): δ 6,92 (c, 1H), 6,68 (c, 1H), 6,55 (c, 1H), 6,03 (д, 1H), 5,96 (д, 1H), 5,87-5,75 (м, 1H), 5,22-5,07 (м, 2H), 5,00 (д, 1H), 4,55 (c, 1H), 4,33 (c, 1H), 4,18 (д, 1H), 4,10 (дд, 1H), 4,06 (д, 1H), 3,80 (c, 3H), 3,58 (c, 3H), 3,52 (д, 1H), 3,12-3,00 (м, 1H), 2,93-2,75 (м, 4H), 2,68-2,58 (м, 1H), 2,51-2,46 (м, 1H), 2,32 (c, 3H), 2,31 (c, 3H), 2,27-2,23 (м, 2H), 2,05 (c, 3H), 1,50 (c, 9H), 1,49 (c, 9H).
ESI-MC m/z: Вычислено для С52Н60N4O14S: 996,4. Найдено (М+Н)+: 997,7.
Пример 51
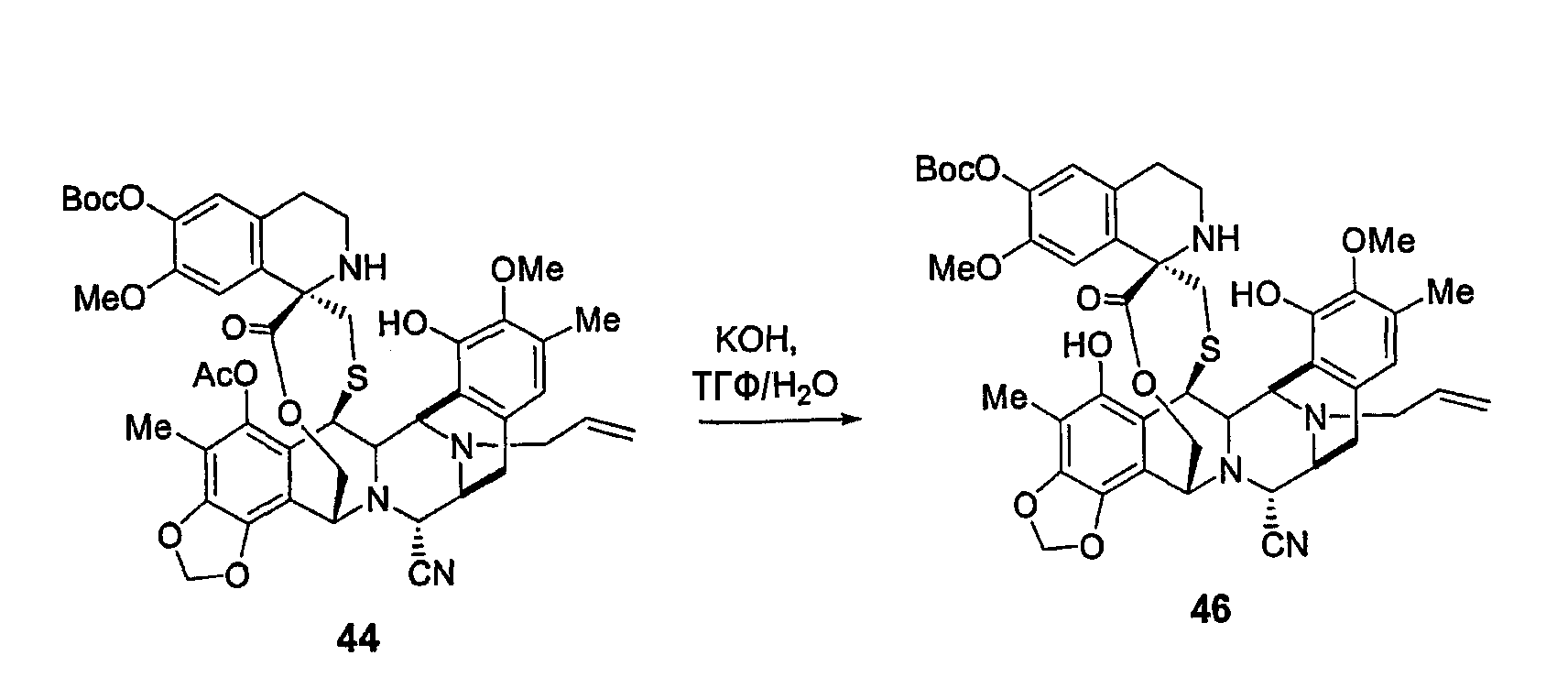
К раствору соединения 44 (275 мг, 0,30 ммоль) в смеси ТГФ/Н2О 2:1 (15 мл, 0,027 М) добавляли водный раствор КОН (4 мл, 1,1 М). Реакционную смесь перемешивали при 23°С в течение 2 часов. После этого периода времени реакцию гасили солевым раствором и экстрагировали CH2Cl2. Органический слой сушили над Na2SO4. Хроматография (гексан/этилацетат 1:1) дает чистое соединение 46 (216 мг, 82%).
Rf: 0,48 (гексан/этилацетат 1:1).
1H ЯМР (300 МГц, CDCl3): δ 6, 70 (c, 1H), 6,59 (c, 1H), 6,55 (c, 1H), 6,25 (c, 1H), 5,95 (д, 1H), 5,89 (д, 1H), 5,87-5,77 (м, 1H), 5,72 (c, 1H), 5,10-5,03 (м, 2H), 4,99 (д, 1H), 4,49 (д, 1H), 4,38-4,36 (м, 2H), 4,17 (д, 1H), 4,05 (дд, 1H), 3,68 (c, 3H), 3,59-3,53 (м, 2H), 3,56 (c, 3H), 3,13-3,04 (м, 1H), 2,99-2,71 (м, 4H), 2,68-2,46 (м, 3H), 2,40 (д, 1H), 2,30 (c, 3H), 2,16 (c, 3H), 1,50 (c, 9H).
ESI-MC m/z: Вычислено для С45Н50N4O11S: 854,3. Найдено (М+Н)+: 855,6.
Пример 52

К раствору соединения 46 (108 мг, 0,13 ммоль) в CH2Cl2 (4 мл, 0,032 М) в атмосфере аргона при 23° С добавляли пиридин (0,02 мл, 0,26 ммоль) и циннамоилхлорид (21 мл, 0,13 ммоль). Реакционную смесь оставляли на 2 часа при 23°С и реакцию гасили после этого периода времени водным насыщенным раствором NaHCO3, водную фазу экстрагировали CH2Cl2 и органические слои сушили над Na2SO4. Флэш-хроматография (гексан/этилацетат 2:1) дает чистое соединение 47 (53 мг, 43%).
Rf: 0,67 (гексан/этилацетат 1:1).
1H ЯМР (300 МГц, CDCl3): δ 7,88 (д, 1H), 7,59-7,57 (м, 2H), 7,44-7, 39 (м, 3Н), 6,71 (c, 1H), 6,589 (д, 1H), 6,58 (c, 1H), 6,54 (c, 1H), 6,06 (д, 1H), 5,97 (д, 1H), 5,92-5,79 (м, 1H), 5,46 (c, 1H), 5,13-5,05 (м, 2H), 5,01 (д, 1H), 4,57 (c, 1H), 4,37-4,34 (м, 2H), 4,20 (c, 1H), 4,11 (д, 1H), 3,61 (c, 3Н), 3,55 (д, 2H), 3,45 (c, 3Н), 3,15-3,09 (м, 1H), 2,96-2,62 (м, 4H), 2,51-2,31 (м, 3Н), 2,25 (c, 3Н), 2,09 (c, 3Н), 1,51 (c, 9H).
ESI-MC m/z: Вычислено для С55Н56N4O12S: 984,4. Найдено (М+Н)+: 986,0.
Пример 53

К раствору соединения 46 (108 мг, 0,13 ммоль) в CH2Cl2 (4 мл, 0,032 ммоль) в атмосфере аргона добавляли октановую кислоту (0,02 мл, 0,13 ммоль), DMAP (31 мг, 0,26 ммоль) и EDC.HCl (48 мг, 0,26 ммоль). Реакционную смесь перемешивали при 23°С в течение 2 часов. После этого периода времени реакционную смесь разбавляли CH2Cl2, промывали солевым раствором и органический слой сушили над Na2SO4. Флэш-хроматография (гексан/этилацетат 2:1) дает чистое соединение 48 (86 мг, 69%).
Rf: 0,85 (гексан/этилацетат 1:1).
1H ЯМР (300 МГц, CDCl3): δ 6,68 (c, 1H), 6,58 (c, 1H), 6,56 (c, 1H), 6,03 (д, 1H), 5,95 (д, 1H), 5,93-5,79 (м, 1H), 5,65 (c, 1H), 5,13-5,07 (м, 2H), 5,00 (д, 1H), 4,53 (д, 1H), 4,36-4,32 (м, 2H), 4,17 (д, 1H), 4,09 (дд, 1H), 3,76 (c, 3H), 3,58 (c, 3H), 3,57-3, 50 (м, 2H), 3,14-3,06 (м, 1H), 2,97-2,75 (м, 4H), 2,68-2,45 (м, 3H), 2,35-2,14 (м, 2H), 2,31 (c, 3H), 2,01 (c, 3H), 1,75-1,71 (м, 2H), 1,50 (c, 9H), 1,36-1,24 (м, 10H), 0,89 (т, 3H).
ESI-MC m/z: Вычислено для С53Н64N4O12S: 980,4. Найдено (М+Н)+: 982,0.
Пример 54
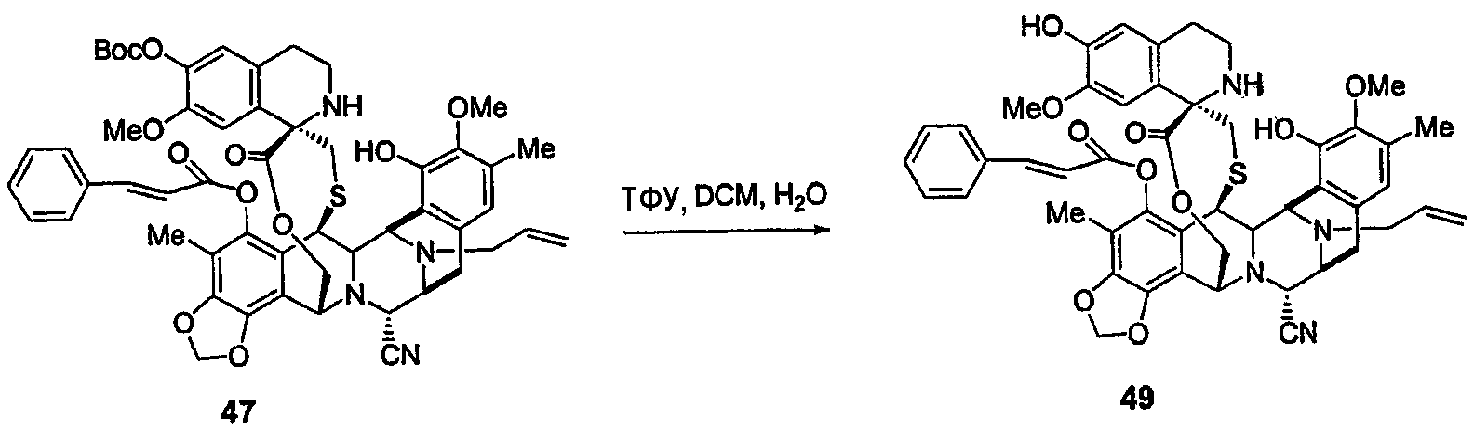
Раствор соединения 47 (38 мг, 0,03 ммоль) в смеси CH2Cl2/Н2О/ТФУ 2:1:3,3 (3,1 мл, 0, 013 М) перемешивали при 23°С в течение 64 часов. Реакционную смесь нейтрализовали водным насыщенным раствором NaHCO3, экстрагировали CH2Cl2 и органические слои сушили над Na2SO4. Флэш-хроматография (гексан/этилацетат 3:2) дает чистое соединение 49 (34 мг, 99%).
Rf: 0,56 (гексан/этилацетат 1:1).
1H ЯМР (300 МГц, CDCl3): δ 7,86 (д, 1H), 7,58-7,54 (м, 2H), 7,46-7,44 (м, 3H), 6,57 (д, 1H), 6,55 (c, 1H), 6,49 (c, 1H), 6,45 (c, 1H), 6,07 (д, 1H), 5,99 (д, 1H), 5,90-5, 79 (м, 1H), 5,42 (c, 1H), 5,13-5,04 (м, 2H), 5,03 (д, 1H), 4,60 (c, 1H), 4,37-4,34 (м, 2H), 4,23-4,20 (м, 2H), 4,13 (д, 1H), 3,64 (c, 3H), 3,55 (д, 2H), 3,44 (c, 3H), 3,15-3,06 (м, 1H), 2,97-2,77 (м, 4H), 2,64-2,34 (м, 4H), 2,24 (c, 3H), 2,09 (c, 3H).
ESI-MC m/z: Вычислено для С49Н48N4O10S: 884,3. Найдено (М+Н)+: 885,0.
Пример 55
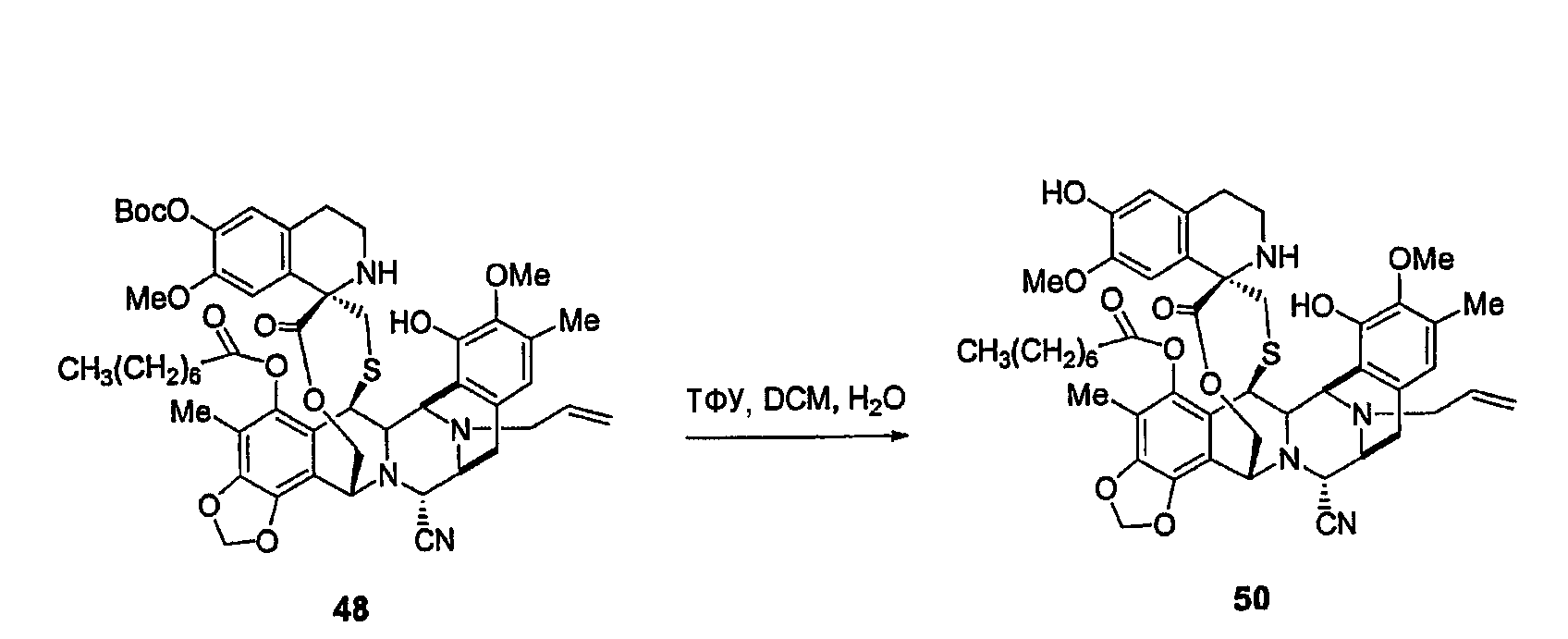
Раствор соединения 48 (65 мг, 0,06 ммоль) в смеси CH2Cl2/Н2О/ТФУ 2:1:3,3 (5,3 мл, 0,013 М) перемешивали при 23°С в течение 64 часов. Реакционную смесь нейтрализовали водным насыщенным раствором NaHCO3 , экстрагировали CH2Cl2 и органические слои сушили над Na2SO4. Флэш-хроматография (гексан/этилацетат 3:2) дает чистое соединение 50 (57 мг, 99%).
Rf: 0,64 (гексан/этилацетат 1:1).
1H ЯМР (300 МГц, CDCl3): δ 6,59 (c, 1H), 6,47 (c, 1H), 6,43 (c, 1H), 6,04 (д, 1H), 5,96 (д, 1H), 5, 91-5,80 (м, 1H), 5,64 (c, 1H), 5,14-5,07 (м, 2H), 5,00 (д, 1H), 4,55 (д, 1H), 4,36-4,33 (м, 2H), 4,20 (д, 1H), 4,11 (дд, 1H), 3,77 (c, 3H), 3,62 (c, 3H), 3,58-3,50 (м, 2H), 3,12-3,07 (м, 1H), 2,98-2, 76 (м, 4H), 2,63-2,43 (м, 3H), 2,36-2,10 (м, 2H), 2,31 (c, 3H), 2,02 (c, 3H), 1,73-1,65 (м, 2H), 1,34-1,20 (м, 10H), 0,89 (т, 3H).
ESI-MC m/z: Вычислено для С48Н56 N4O10S: 880,4. Найдено (М+Н)+: 882,0.
Синтез соединений 51 и 52 в соответствии с общей экспериментальной процедурой реакций деаллилирования
Пример 56
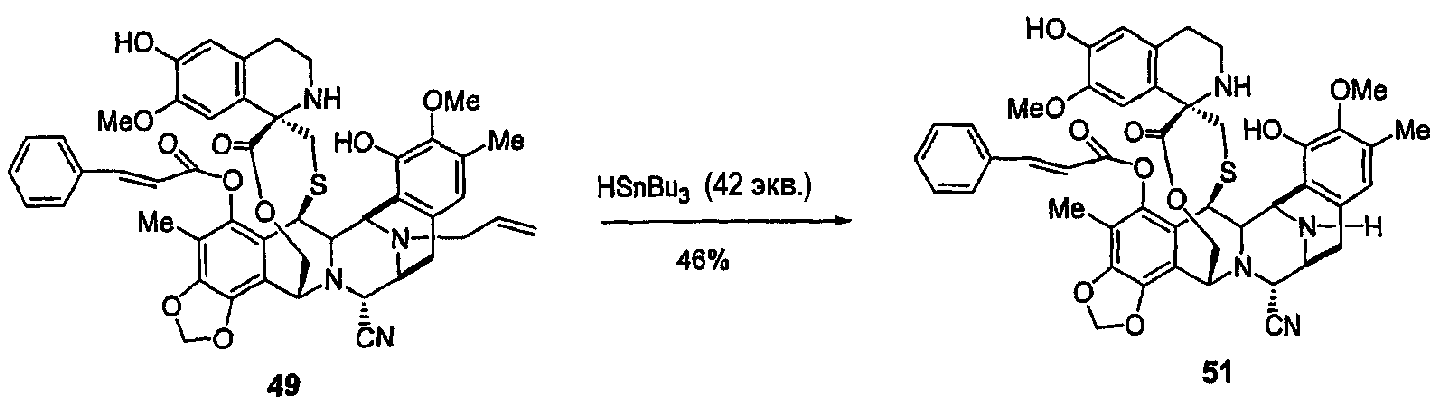
Rf: 0,26 (гексан/этилацетат 1:1).
1H ЯМР (300 МГц, CDCl3): δ 7,87 (д, 1H), 7,59-7,54 (м, 4H), 7,51-7,44 (м, 6H), 6,60-6,43 (м, 8H), 6,07 (д, 2H), 5,97 (д, 2H), 5,03 (д, 2H), 4,59 (c, 2H), 4,50 (д, 1H), 4,37-4,34 (м, 2H), 4,23-4,09 (м, 4H), 3,84 (д, 2H), 3,65 (c, 3H), 3,64 (c, 3H), 3,61 (c, 6H), 3,57-3,52 (м, 2H), 3,43-3,40 (м, 2H), 3,14-2,97 (м, 6H), 2,93-2,80 (м, 6H), 2,68-2,58 (м, 2H), 2, 48-2,20 (м, 4H), 2,29 (c, 3H), 2,23 (c, 3H), 2,09 (c, 3H), 1,94 (c, 3H).
ESI-MC m/z: Вычислено для С46Н44N4O10S: 844,3. Найдено (М+Н)+: 845,0.
Пример 57
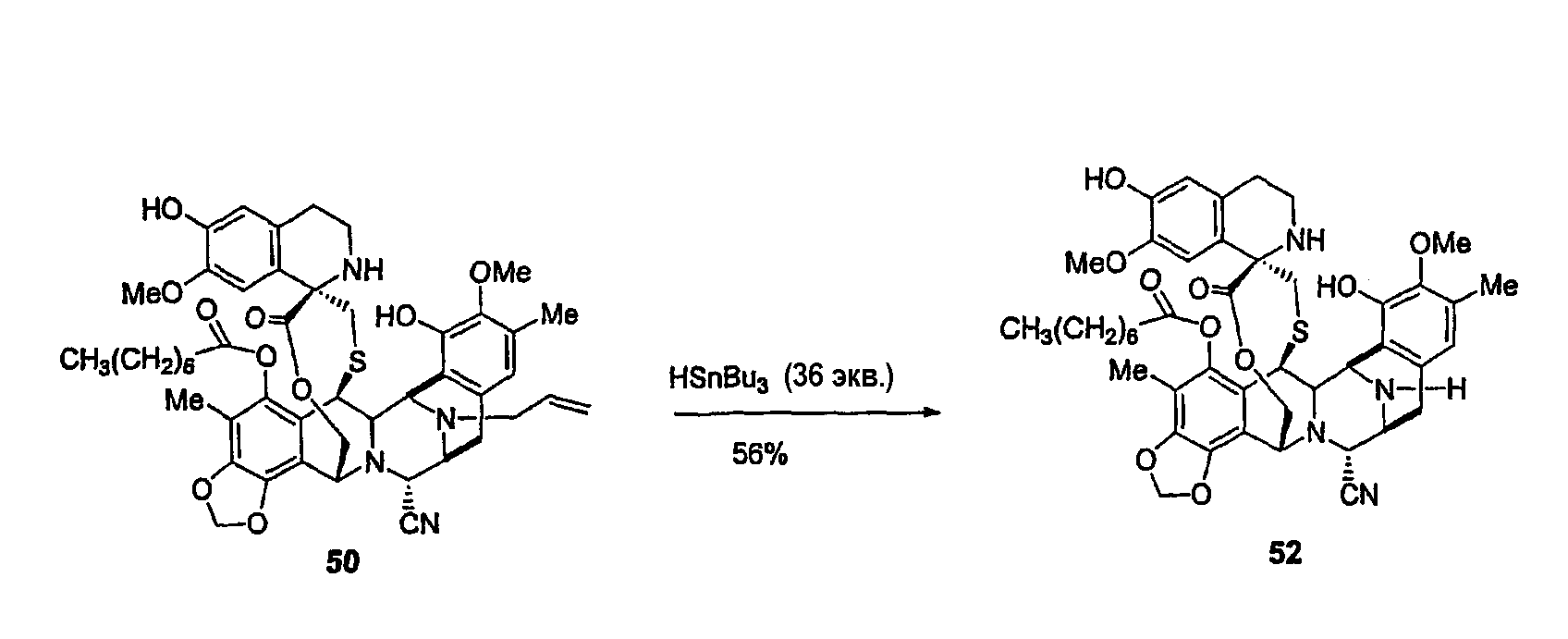
Rf: 0,36 (гексан/этилацетат 1:1).
1H ЯМР (300 МГц, CDCl3): δ 6,61 (c, 1H), 6,47 (c, 1H), 6,43 (c, 1H), 6,05 (д, 1H), 5,97 (д, 1H), 5,72 (c, 1H), 5,02 (д, 1H), 4,55 (д, 1H), 4,50 (д, 1H), 4,33 (c, 1H), 4,19 (д, 1H), 4,11 (дд, 1H), 3,85 (д, 1H), 3,76 (c, 3H), 3,61 (c, 3H), 3,52 (д, 1H), 3,14-2,97 (м, 3H), 2,81-2,76 (м, 1H), 2,67-2,48 (м, 3H), 2,43-2,33 (м, 1H), 2, 30 (c, 3H), 2,17-2,09 (м, 1H), 2,02 (c, 3H), 1,74-1,70 (м, 2H), 1,38-1,20 (м, 10H), 0,89 (т, 3H).
ESI-MC m/z: Вычислено для С45Н52N4O10S: 840,3. Найдено (М+Н)+: 841,1.
Общая экспериментальная процедура для синтеза соединений 53 и 54. Взаимопревращение нитрильной группы в гидроксильную группу
К раствору исходного материала в CH3CN/Н2О 3:2 (0,015 М) добавляли AgNO3 (30 экв.). После 24 часов при 23°С реакцию гасили смесью 1:1 насыщенных водных растворов рассола и NaHCO3, перемешивали в течение 10 минут, разбавляли и экстрагировали CH2Cl2. Органический слой сушили над Na2SO4. Хроматография (смеси CH2Cl2:МеОН) дает чистые соединения 53 и 54.
Пример 58
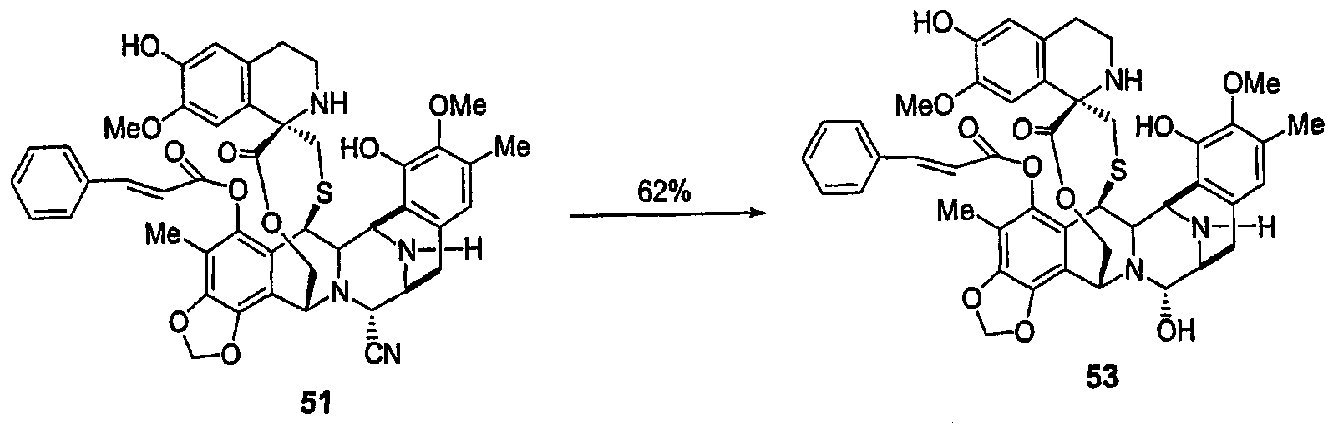
Rf: 0,46 (CH2Cl2/МеОН 8:0,5).
1H ЯМР (300 МГц, CDCl3): δ 7,87 (д, 1H), 7,59-7,54 (м, 4H), 7,51-7,44 (м, 6H), 6,60-6,43 (м, 8H), 6,05 (д, 2H), 5,97 (д, 2H), 5,14 (д, 2H), 4,87 (c, 2H), 4,54-4,37 (м, 4H), 4,06-4,02 (м, 2H), 3,74-3,60 (м, 4H), 3,64 (c, 3H), 3, 63 (c, 3H), 3,61 (c, 3H), 3,48 (c, 3H), 3,48-3,43 (м, 2H), 3,18-3,01 (м, 6H), 2,91-2,83 (м, 6H), 2,70-2,58 (м, 2H), 2,49-2,22 (м, 4H), 2,29 (c, 3H), 2,24 (c, 3H), 2,08 (c, 3H), 1,93 (c, 3H).
13C-ЯМР (75 МГц, CDCl3): δ 145,7, 144,6, 144,5, 131,1, 129,4, 129,0, 128,9, 128,5, 127,1, 126,7, 125,0, 121,6, 117,3, 114,9, 114,2, 110,0, 101,9, 81,5, 68,4, 61, 4, 60,6, 57,3, 56,2, 55,3, 51,4, 48,0, 42,4, 40,0, 38,9, 37,3, 36,0, 33,0, 32,1, 32,0, 31,2, 30,5, 29,6, 29,1, 27,6, 27,3, 23,9, 23,2, 22,9, 20,0, 16,0, 14,4, 11,2, 9,8.
ESI-MC m/z: Вычислено для С45Н45N3O11S: 835,3. Найдено (М+Н)+: 836,0.
Пример 59
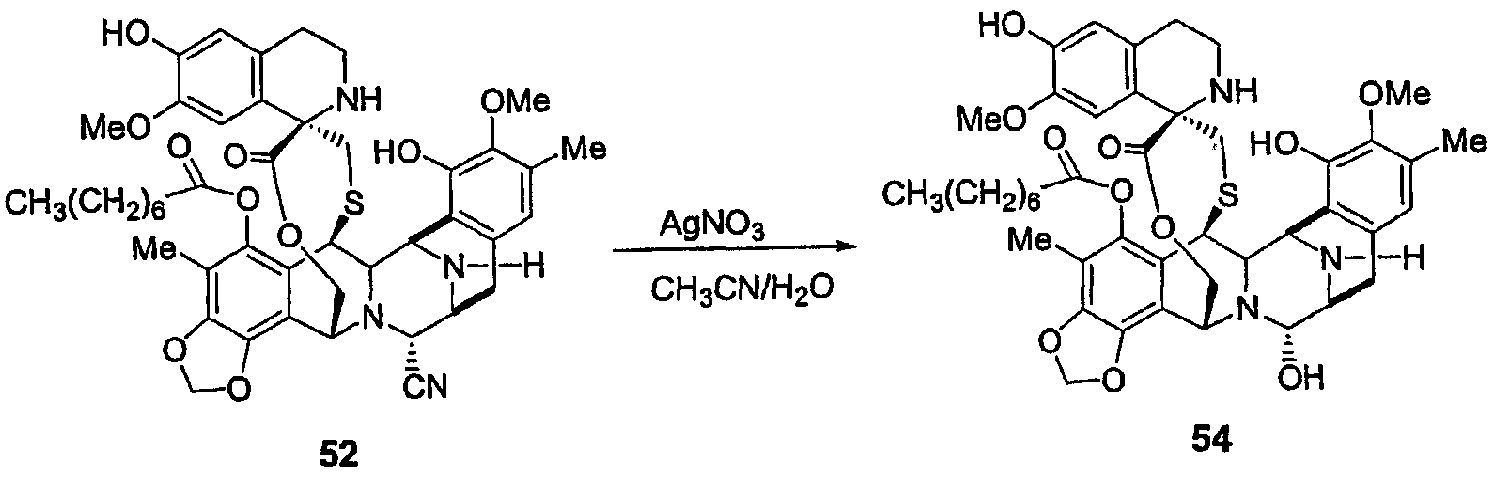
Rf: 0,31 (CH2Cl2/МеОН 8:0,5).
1H ЯМР (300 МГц, CDCl3): δ 6,60 (c, 1H), 6,45 (c, 1H), 6,42 (c, 1H), 6,02 (д, 1H), 5,95 (д, 1H), 5,12 (д, 1H), 4,83 (c, 1H), 4,52 (д, 1H), 4,45 (c, 1H), 4,40-4,36 (м, 1H), 4,06-3,99 (м, 2H), 3,76 (c, 1H), 3,63-3,60 (м, 2H), 3,61 (c, 3H), 3,46 (д, 1H), 3,15-3,00 (м, 3H), 2,90-2,77 (м, 2H), 2,63-2,49 (м, 3H), 2,43-2,35 (м, 1H), 2,30 (c, 3Н), 2,18-2,06 (м, 1H), 2,00 (c, 3Н), 1,74-1,70 (м, 2H), 1,34-1,20 (м, 10Н), 0,89 (т, 3Н).
ESI-MC m/z: Вычислено для С44Н53N3O11S: 831,3. Найдено (М+Н)+: 832,0.
Общая экспериментальная процедура для введения триптаминовой части молекулы, реакции Пикте-Шпенглера; синтеза соединений 55, 56, 57 и 58
К раствору соединения 13 в уксусной кислоте (0,5 10-4М) в атмосфере аргона при 23°С добавляли триптаминовый реагент. Реакционную смесь перемешивали в течение 24 часов при 23°С (для соединений 57 и 58 температура реакции 60°С) и затем уксусную кислоту выпаривали. Добавляли водный насыщенный раствор NaHCO3 и смесь экстрагировали CH2Cl2 и органические слои сушили над Na2 SO4. Флэш-хроматография (смеси гексан/этилацетат) дает чистые соединения.
Пример 60
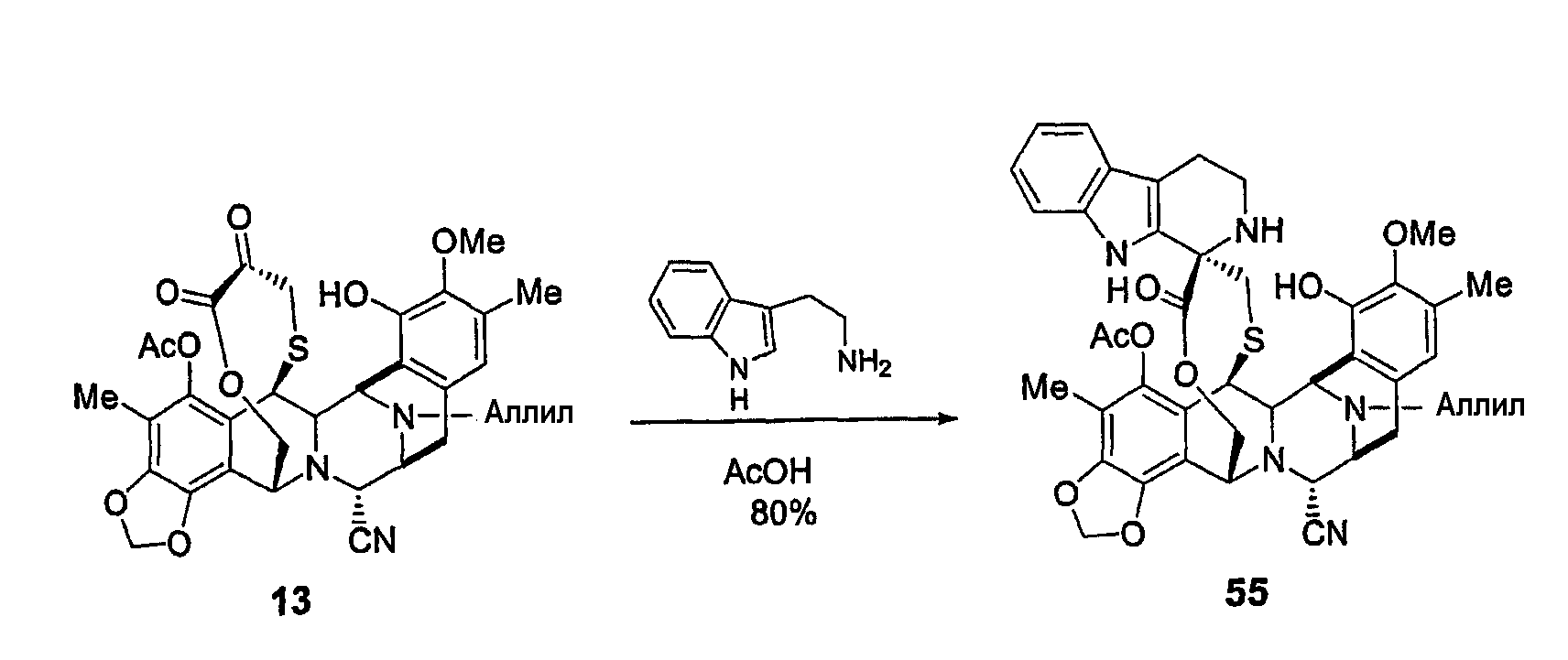
Rf: 0,45 (гексан/этилацетат 1:1).
1H ЯМР (300 МГц, CDCl3): δ 7,74 (c, 1H), 7,38 (д, 1H), 7,24 (д, 1H), 7,09 (т, 1H), 7,00 (т, 1H), 6,66 (c, 1H), 6,22 (д, 1H), 6,01 (д, 1H), 5,94-5,80 (м, 1H), 5,78 (c, 1H), 5,15-5,07 (м, 3H), 4,56 (c, 1H), 4,37 (д, 1H), 4,33 (c, 1H), 4,23 (д, 1H), 4,19 (дд, 1H), 3, 80 (c, 3H), 3,55 (д, 1H), 3,44 (д, 1H), 3,17-2,80 (м, 6H), 2,71-2,52 (м, 3H), 2,37 (c, 3H), 2,25 (c, 3H), 2,06 (c, 3H).
ESI-MC m/z: Вычислено для С43Н43N5O8S: 789,3. Найдено (М+Н)+: 790,0.
Пример 61

Rf: 0,18 (гексан/этилацетат 1:1).
1H ЯМР (300 МГц, CDCl3): δ 7,65 (c, 1H), 7,11 (д, 1H), 6,81 (д, 1H), 6,73 (дд, 1H), 6, 66 (c, 1H), 6,19 (д, 1H), 5,99 (д, 1H), 5,92-5,83 (м, 1H), 5,78 (c, 1H), 5,15-5,06 (м, 3H), 4,55 (c, 1H), 4,36 (д, 1H), 4,32 (c, 1H), 4,22 (д, 1H), 4,18 (дд, 1H), 3,81 (c, 3H), 3,79 (c, 3H), 3,54 (д, 1H), 3,44 (д, 1H), 3,16-3,03 (м, 2H), 2,96-2,78 (м, 4H), 2,65-2,50 (м, 3H), 2,38 (c, 3H), 2,25 (c, 3H), 2,05 (c, 3H).
ESI-MC m/z: Вычислено для С44Н45N5 O9S: 819,3. Найдено (М+Н)+: 820,5.
Пример 62
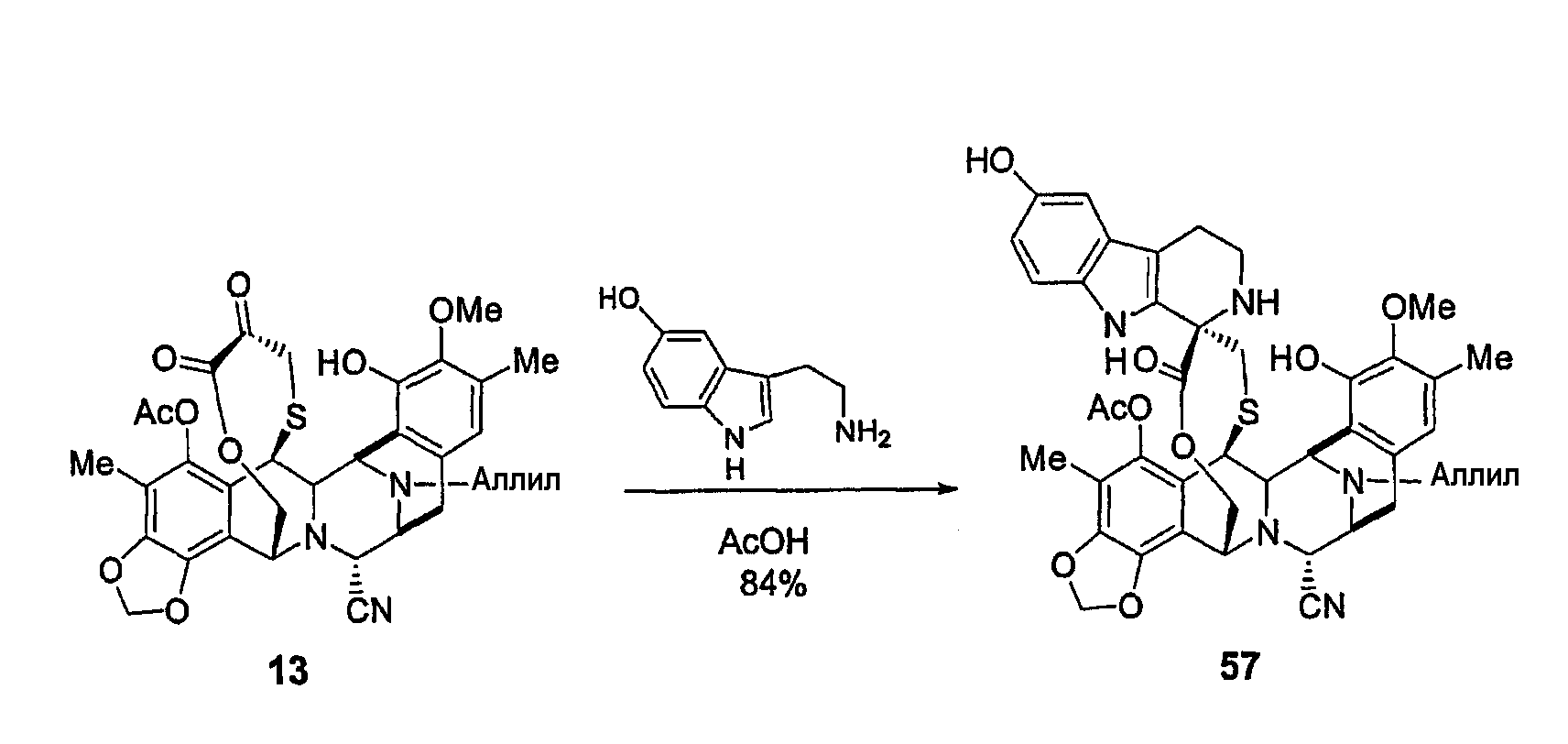
Rf: 0,10 (гексан/этилацетат 1:1).
1H ЯМР (300 МГц, CDCl3): δ 7,72 (c, 1H), 6,88 (д, 1H), 6,65 (д, 1H), 6,60 (д, 1H), 6,52 (дд, 1H), 6,10 (c, 1H), 5,94 (c, 1H), 5,94-5,81 (м, 1H), 5,82 (c, 1H), 5,14-5,03 (м, 3H), 4,53 (c, 1H), 4,35 (д, 1H), 4,29 (c, 1H), 4,20 (д, 1H), 4,17 (дд, 1H), 3,80 (c, 3H), 3,53 (д, 1H), 3,41 (д, 1H), 3,09-3, 01 (м, 2H), 2,91-2,72 (м, 5H), 2,56-2,51 (м, 2H), 2,37 (c, 3H), 2,23 (c, 3H), 2,03 (c, 3H).
ESI-MC m/z: Вычислено для С43Н43N5O9S: 805,3. Найдено (М+Н)+: 806,5.
Пример 63

Rf: 0,48 (гексан/этилацетат 1:1).
1H ЯМР (300 МГц, CDCl3): δ 7,66 (c, 1H), 7,14 (с, 1H), 7,13 (д, 1H), 6,91 (д, 1H), 6,66 (C, 1H), 6,21 (c, 1H), 6,00 (c, 1H), 5,92-5,81 (м, 1H), 5,80 (c, 1H), 5,15-5,06 (м, 3H), 4,55 (c, 1H), 4,37 (д, 1H), 4,32 (c, 1H), 4,21 (д, 1H), 4,16 (д, 1H), 3,81 (c, 3H), 3,54 (д, 1H), 3,43 (д, 1H), 3,17-3,03 (м, 2H), 2,96-2, 77 (м, 5H), 2,68-2,42 (м, 4H), 2,37 (c, 3H), 2,25 (c, 3H), 2,06 (c, 3H).
ESI-MC m/z: Вычислено для С44Н45N5O8S: 803,3. Найдено (М+Н)+: 804,4.
Синтез соединений 59, 60, 61 и 62 в соответствии с общей экспериментальной процедурой для реакций деаллилирования
Пример 64

Rf: 0,21 (гексан/этилацетат 1:1).
1H ЯМР (300 МГц, CDCl3): δ 7,74 (c, 1H), 7,38 (д, 1H), 7,24 (д, 1H), 7,09 (т, 1H), 7,00 (т, 1H), 6,68 (c, 1H), 6,23 (д, 1H), 6,02 (д, 1H), 5,10 (д, 1Н), 4,55 (c, 1H), 4,51 (д, 1H), 4,33 (c, 1H), 4,23 (д, 1H), 4,19 (дд, 1H), 3,84 (д, 1H), 3,80 (c, 3Н), 3,45 (д, 1H), 3,25-2,79 (м, 6H), 2,71-2,53 (м, 3Н), 2,36 (c, 3Н), 2,26 (c, 3Н), 2,07 (c, 3Н).
ESI-MC m/z: Вычислено для С40Н39N5O8S: 749,3. Найдено (М+Н)+: 749,9.
Пример 65

Rf: 0,15 (гексан/этилацетат 1:2).
1H ЯМР (300 МГц, CDCl3): δ 7,65 (c, 1H), 7,12 (д, 1H), 6,81 (д, 1H), 6,73 (дд, 1H), 6,67 (c, 1H), 6,20 (c, 1H), 6,00 (c, 1H), 5,08 (д, 1H), 4,55 (c, 1H), 4,49 (д, 1H), 4,31 (c, 1H), 4,31-4,16 (м, 2H), 3,83 (д, 1H), 3,80 (c, 3H), 3,79 (c, 3H), 3, 44 (д, 1H), 3,24-3,11 (м, 2H), 3,03-2,94 (м, 1H), 2,83-2,80 (м, 1H), 2,65-2,50 (м, 4H), 2,36 (c, 3H), 2,26 (c, 3H), 2,06 (c, 3Н).
ESI-MC m/z: Вычислено для С41Н41 N5O9S: 779,3. Найдено (М+Н)+: 780,0.
Пример 66
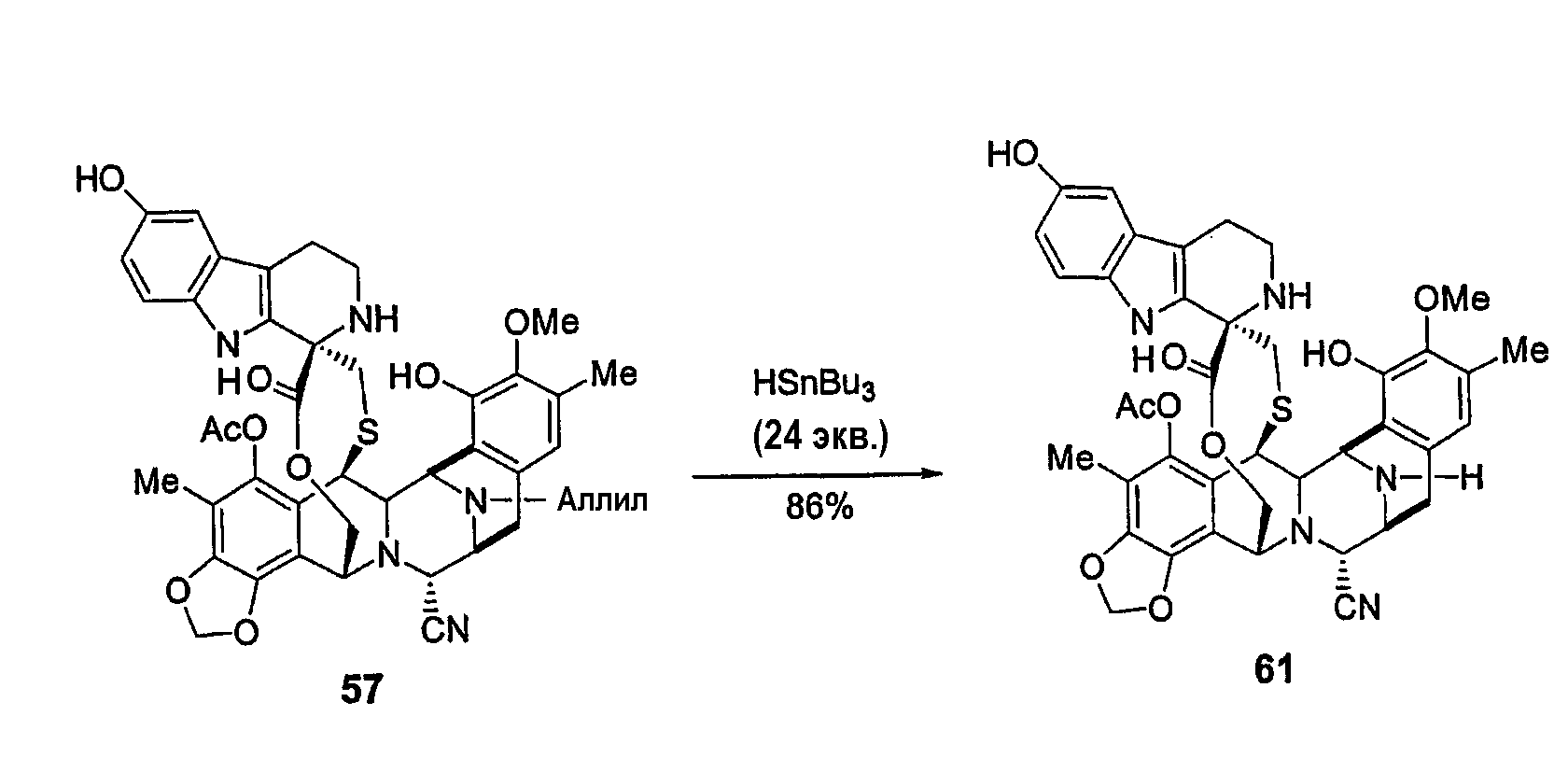
Rf: 0,10 (гексан/этилацетат 1:2).
1H ЯМР (300 МГц, CDCl3): δ 7,67 (c, 1H), 6,93 (д, 1H), 6,66 (c, 2H), 6,55 (дд, 1H), 6,15 (c, 1H), 5,98 (c, 1H), 5,06 (д, 1H), 4,53 (c, 1H), 4,48 (д, 1H), 4,29 (c, 1H), 4,19 (д, 1H), 3,82 (д, 1H), 3,78 (c, 3H), 3,42 (д, 1H), 3,22-2,96 (м, 5H), 2,76-2,73 (м, 2H), 2, 57-2,43 (м, 3H), 2,35 (c, 3H), 2,25 (c, 3H), 2,04 (c, 3H).
ESI-MC m/z: Вычислено для С40Н39N5O9S: 765,3. Найдено (М+Н)+: 766, 4.
Пример 67
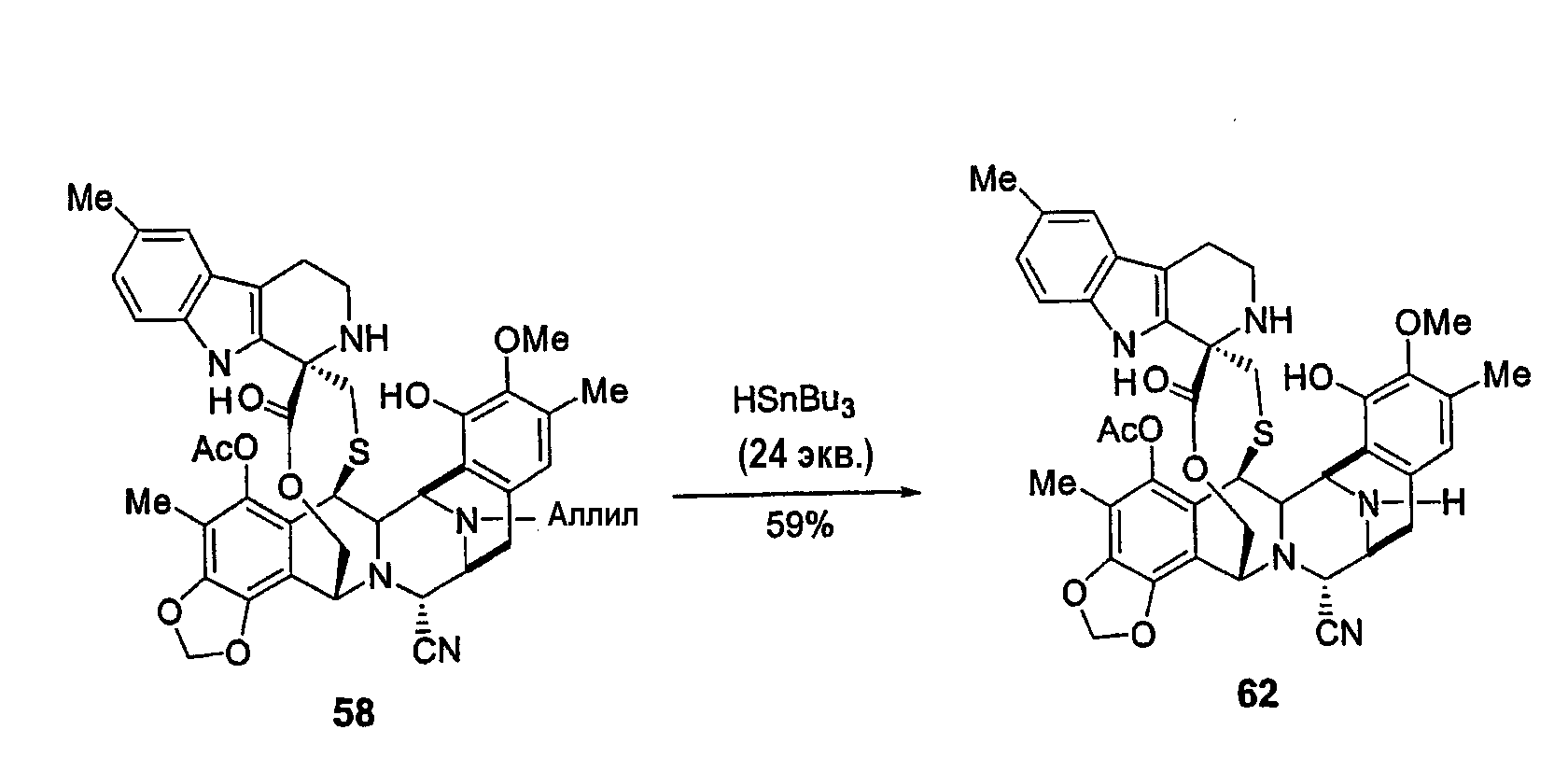
Rf: 0,35 (гексан/этилацетат 1:2).
1H ЯМР (300 МГц, CDCl3): δ 7,63 (c, 1H), 7,26 (c, 1H), 7,15 (д, 1H), 6,91 (д, 1H), 6,68 (c, 1H), 6,22 (д, 1H), 6,02 (д, 1H), 5,09 (д, 1H), 4,55 (c, 1H), 4,50 (д, 1H), 4,32 (c, 1H), 4,22 (д, 1H), 4,18 (дд, 1H), 3,83 (д, 1H), 3,80 (c, 3H), 3,44 (д, 1H), 3,25-3,10 (м, 3H), 3,03-2,94 (м, 1H), 2,83-2,77 (м, 1H), 2,66-2,51 (м, 4H), 2,37 (c, 3H), 2,36 (c, 3H), 2,26 (c, 3H), 2,07 (c, 3H).
ESI-MC m/z: Вычислено для С41Н41N5O8S: 763,3. Найдено (М+Н)+: 764,0.
Общая экспериментальная процедура для синтеза соединений 63, 64, 65, 66 и 67. Взаимопревращение нитрильной группы в гидроксильную группу
К раствору исходного материала в CH3CN/Н2О 3:2 (0,015 М) добавляли AgNO3 (30 экв.). После 24 часов при 23°С реакцию гасили смесью 1:1 насыщенных водных растворов рассола и NaHCO3, перемешивали в течение 10 минут, разбавляли и экстрагировали CH2Cl2. Органический слой сушили над Na2SO4. Хроматография (смеси CH2Cl2:МеОН) дает чистые соединения 63, 64, 65, 66 и 67.
Пример 68
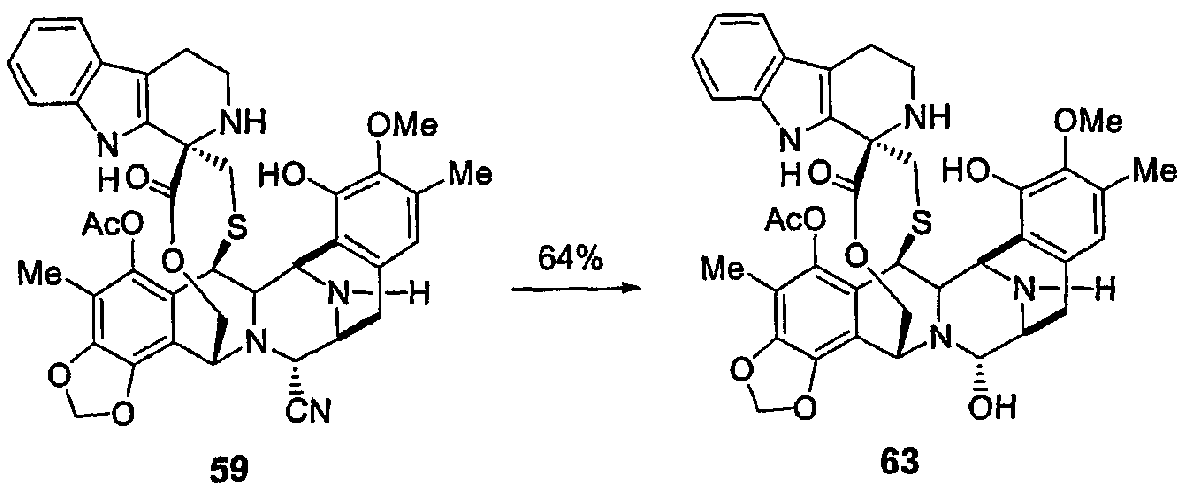
Rf: 0,13 (CH2Cl2/МеОН 16:1).
1H ЯМР (300 МГц, CDCl3): δ 7,72 (c, 1H), 7,38 (д, 1H), 7,24 (д, 1H), 7,09 (т, 1H), 7,00 (т, 1H), 6,68 (c, 1H), 6,21 (д, 1H), 6,00 (д, 1H), 5,21 (д, 1H), 4,85 (c, 1H), 4,53-4,38 (м, 3H), 4,13-4,08 (м, 2H), 3,80 (c, 3H), 3,64-3,57 (м, 3H), 3,17-3,08 (м, 2H), 2,91-2,82 (м, 2H), 2, 69-2,54 (м, 3H), 2,36 (c, 3H), 2,25 (c, 3H), 2,08 (c, 3H).
13С ЯМР (75 МГц, CDCl3): δ 171,7, 146,0, 145,7, 142,8, 141,4, 140,9, 135,7, 132,0, 131,1, 129,5, 127,1, 125,0, 124,6, 122,1, 121,8, 121,5, 119,4, 118,6, 115,7, 111,2, 110,4, 102,0, 81,7, 62,6, 62,1, 60,6, 57,2, 56,1, 51,4, 48,1, 42,6, 40,0, 39,4, 29,9, 27,4, 21,8, 20,8, 16,6, 9,9.
ESI-MC m/z: Вычислено для С39Н40N4O9S: 740,3. Найдено (М-Н2О+Н)+: 723,0.
Пример 69
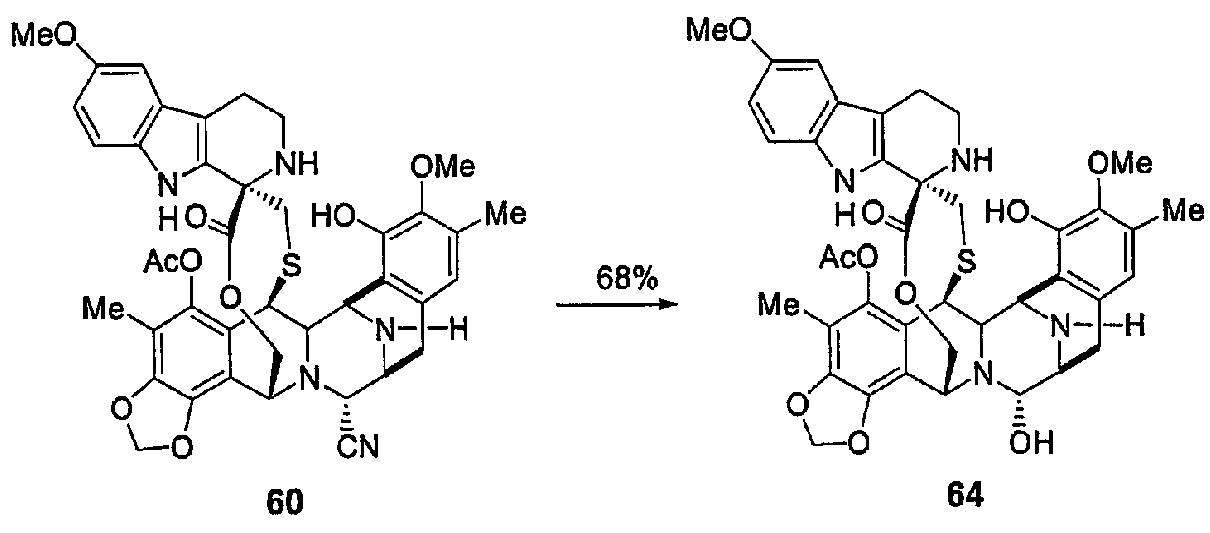
Rf: 0,36 (CH2Cl2/МеОН 8:1).
1H ЯМР (300 МГц, CDCl3): δ 7,60 (c, 1H), 7,12 (д, 1H), 6,81 (д, 1H), 6,74 (дд, 1H), 6,68 (c, 1H), 6,19 (c, 1H), 6,00 (дд, 1H), 5,20 (д, 1H), 4,84 (c, 1H), 4,53-4,37 (м, 3H), 4,12-4,07 (м, 2H), 3,80 (c, 3H), 3,78 (c, 3H), 3,60-3,53 (м, 3H), 3,18-3,11 (м, 2H), 2,90-2,79 (м, 2H), 2,66-2,49 (м, 3Н), 2,36 (c, 3Н), 2,25 (c, 3Н), 2,05 (c, 3H).
13С ЯМР (75 МГц, CDCl3): δ 171,7, 168,9, 154,0, 146,1, 145,7, 142,9, 141,4, 140,9, 134,0, 131,9, 130,9, 129,6, 129,3, 127,4, 124,5, 121,8, 121,5, 115,7, 113,1, 111,9, 110,1, 102,1, 100,6, 81,7, 62,6, 62,0, 60,6, 57,1, 56,1, 51,4, 48,0, 42,6, 40,1, 39,4, 29,9, 27,4, 21,8, 20,8, 16,0, 9,9.
ESI-MC m/z: Вычислено для С40Н42N4O10S: 770,3. Найдено (М-Н2О+Н)+: 753,2.
Пример 70
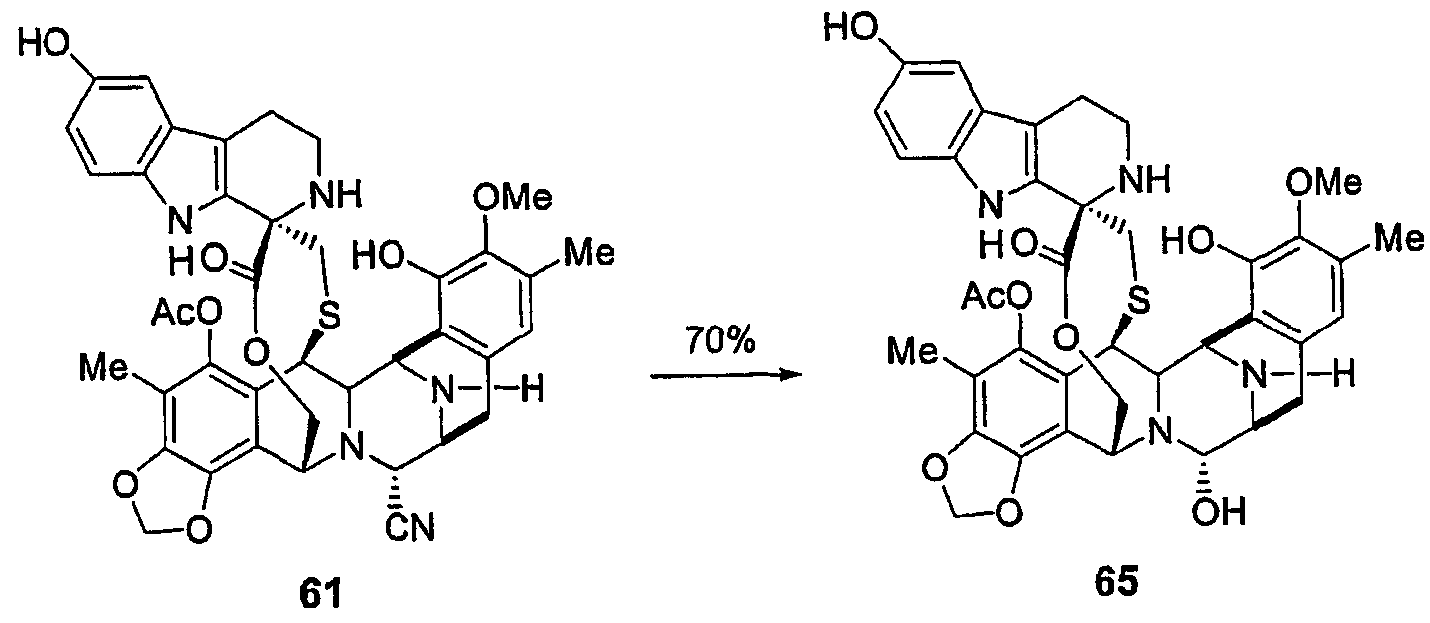
Rf: 0,15 (CH2Cl2/МеОН 8:1).
1H ЯМР (300 МГц, CDCl3): δ 7,59 (c, 1H), 7,03 (д, 1H), 6,72 (д, 1H), 6,68 (т, 1H), 7, 00 (т, 1H), 6,68 (c, 1H), 6,61 (дд, 1H), 6,18 (c, 1H), 5,97 (c, 1H), 5,20 (д, 1H), 4,84 (c, 1H), 4,52-4,36 (м, 3H), 4,12-4,09 (м, 2H), 3,80 (c, 3H), 3,60-3,48 (м, 3H), 3,16-3,10 (м, 3H), 2,91-2,77 (м, 2H), 2,57-2,43 (м, 3H), 2,36 (c, 3H), 2,26 (c, 3H), 2,05 (c, 3H).
13C ЯМР (75 МГц, CDCl3): δ 171,7, 169,2, 149,6, 146,1, 142,8, 141,3, 141,0, 132,1, 132,0, 131,1, 131,0, 129,6, 129,0, 127,7, 124,6, 121,8, 121,5, 115,7, 113,1, 111,7, 109,8, 103,4, 102,1, 81,7, 68,3, 62,0, 60,6, 57,1, 56,1, 51,4, 48,0, 42,5, 40,0, 39,2, 32,1, 27,4, 20,8, 16,0, 9,9.
ESI-MC m/z: Вычислено для С39Н40N4O10S: 756,3. Найдено (М-Н2О+Н)+: 739,0.
Пример 71
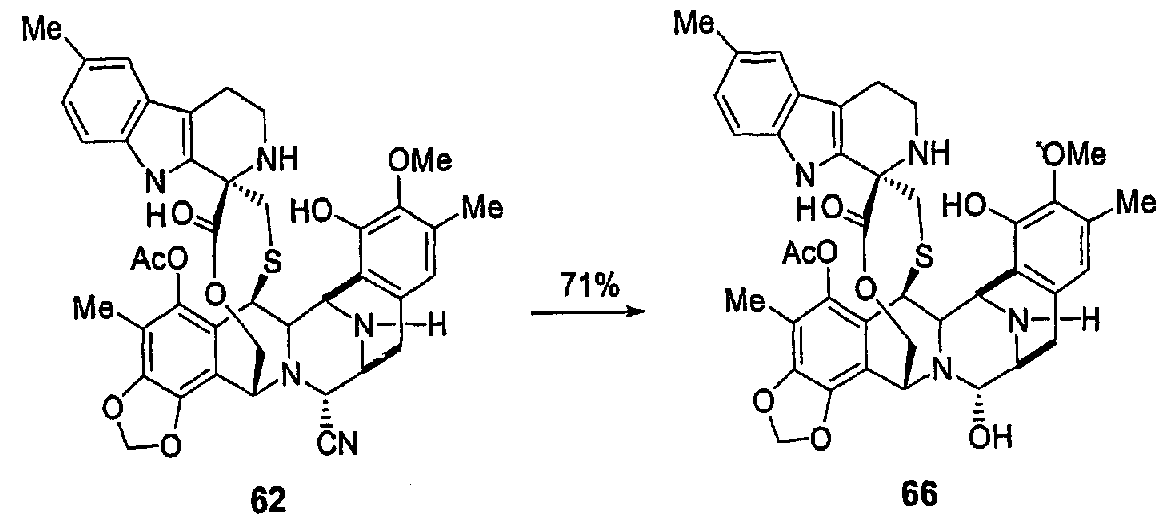
Rf: 0,47 (CH2Cl2/МеОН 8:1).
1H ЯМР (300 МГц, CDCl3): δ 7,61 (c, 1H), 7,14 (c, 1H), 7,13 (д, 1H), 6,91 (д, 1H), 6,66 (c, 1H), 6,20 (c, 1H), 6,01 (д, 1H), 5,19 (д, 1H), 4,85 (c, 1H), 4,54-4,40 (м, 3H), 4,12-4,08 (м, 2H), 3,80 (c, 3H), 3,62 (д, 2H), 3,54 (м, 1H), 3,17-3,08 (м, 2H), 2,90-2,78 (м, 2H), 2,64-2,47 (м, 3H), 2,37 (c, 3H), 2,36 (c, 3H), 2,25 (c, 3H), 2,06 (c, 3H).
13C ЯМР (75 МГц, CDCl3): δ 171,7, 168,9, 146,2, 145,7, 142,9, 141,4, 140,9, 134,1, 132,4, 132,3, 131,2, 129,6, 128,6, 127,3, 123,7, 121,7, 121,4, 118,4, 115,7, 113,1, 110,8, 109,9, 102,1, 81,6, 62,0, 60,6, 56,1, 51,4, 48,0, 42,5, 39,4, 32,1, 29,2, 28,1, 27,3, 21,8, 20,8, 16,0, 13,8, 9,9.
ESI-MC m/z: Вычислено для С40Н42N4O9S: 754,3. Найдено (М-Н2О +Н)+: 737,3.
Пример 72

Rf: 0,26 (CH2Cl2/МеОН 30:1).
1H ЯМР (300 МГц, CDCl3): δ 6,62 (c, 1H), 6,47 (c, 1H), 6,45 (c, 1H), 6,03 (c, 1H), 5,95 (c, 1H), 5,78 (м, 1H), 5,67 (c, 1H), 5,38 (м, 1H), 5,14 (д, 2H), 5,05 (ушир.c, 1H), 4,99 (ушир.c, 1H), 4,83 (ушир.c, 1H), 4,49 (ушир.c, 1H), 4,28 (ушир.c, 1H), 4,05 (д, 1H), 3,79 (c, 3H), 3,61 (c, 3H), 3,57 (м, 1H), 3,35 (м, 1H), 3,12 (м, 1H), 2,85 (м, 4H), 2,60 (м, 2H), 2,51 (м, 1H), 2,32 (c, 3H), 2,26 (c, 3H), 2,18 (м, 4H), 2,03 (c, 3H).
ESI-MC m/z: Вычислено для С41Н45N3O11S: 787,8. Найдено (М-Н2О+Н)+: 770,4.
Пример 73
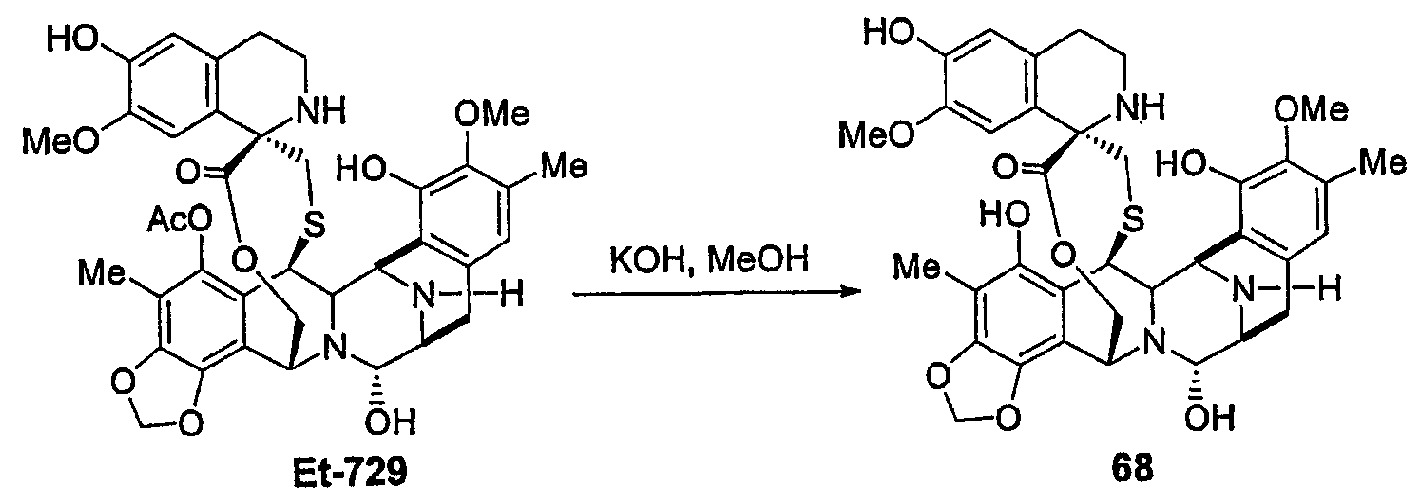
Раствор Et-729 (19,9 мг, 0,03 ммоль) в метанольном растворе КОН (5,21 мл, 0,95 ммоль, 0,1817 М) перемешивали в атмосфере аргона при 23°С. После 1 часа реакционную смесь разбавляли CH2Cl2 и экстрагировали. Органический слой сушили над Na2SO4. Хроматография дает чистое соединение.
Rf: 0,18 (CH2Cl2/МеОН 10:1).
1H ЯМР (300 МГц, CDCl3): δ 6,61 (c, 1H), 6,39 (c, 1H), 6,33 (c, 1H), 6,03 (c, 1H), 5,88 (c, 1H), 5,45-5,44 (м, 1H), 5,13 (д, 1H), 4,81 (c, 1H), 4,71-6,67 (м, 2H), 4,30 (д, 1H), 4,08 (дд, 1H), 3,92 (д, 1H), 3,79 (д, 1H), 3,73 (c, 3H), 3,55 (c, 3H), 3,18-3,05 (м, 3H), 2,83-2,79 (м, 1H), 2,70-2,56 (м, 1H), 2,38 (д, 1H), 2,30 (c, 3H), 2,20 (д, 1H), 2,14 (c, 3H).
ESI-MC m/z: Вычислено для С36Н39N3O10S: 705,2. Найдено (М-Н2О+Н)+: 688,4.
Пример 74

К раствору промежуточного продукта 1 (1,17 г, 2,26 ммоль) и производного цистеина (0,9 г, 2,26 ммоль) в безводном дихлорметане (45 мл, 0,05 М) добавляли при 23°С в атмосфере аргона EDC.HCl (0,87 г, 4,52 ммоль) и DMAP (0,55 г, 4,52 ммоль). Реакционную смесь оставляли при 23°С в атмосфере аргона на 1 час. Добавляли насыщенный водный раствор бикарбоната натрия и водную фазу экстрагировали дихлорметаном, объединенные органические слои сушили над сульфатом натрия, фильтровали и растворитель удаляли при пониженном давлении. Неочищенный продукт очищали колоночной флэш-хроматографией (смеси элюентов дихлорметан/метанол в градиенте от 100:0 до 80:1) с получением промежуточного продукта 69 (1,43 г, 70%) в виде желтого твердого вещества.
Rf: 0,5 (дихлорметан/МеОН 60:1).
1H ЯМР (300 МГц, CDCl3): δ 7,63 (д, 2H), 7,47 (дд, 2H), 7,34 (м, 2H), 7,23 (м, 2H), 6,35 (c, 1H), 6,09 (д, 1H), 5,91 (м, 2H), 5,85 (д, 1H), 5,62 (м, 1H), 5,58 (c, 1H), 5,30 (дд, 1H), 5,20 (дд, 1H), 4,15 (д, 1H), 4,06-3,91 (м, 4H), 3,78 (дд, 1H), 3,69 (ушир.т, 1H), 3,49 (c, 3H), 3,44 (м, 2H), 3,30 (д, 1H), 3,18 (дд, 1H), 3,07 (м, 3H), 2,81 (м, 2H), 2,29-2,21 (м, 1H), 2,22 (c, 3H), 2,15 (c, 3H), 2,08 (c, 3H), 1,45 (c, 9H), 1,44 (м, 1H).
13C ЯМР (75 МГц, CDCl3): δ 169,95, 154,83, 148,77, 146,74, 145,06, 144,19, 142,48, 141,30, 141,22, 138,49, 134,24, 131,47, 128,76, 127,46, 127,33, 126,98, 126,76, 124,36, 124,09, 121,29, 121,08, 119,82, 119,62, 118,03, 116,76, 116,41, 112,89, 112,44, 101,03, 79,65, 73,46, 60,38, 58,76, 57,85, 56,21, 55,27, 51,76, 46,66, 41,49, 38,59, 34,48, 33,85, 31,55, 28,37, 26,41, 24,29, 22,61, 15,51, 14,08, 9,53.
ESI-MC m/z: Вычислено для С51Н57N5O8S: 899,4. Найдено (М+Н)+: 900,4.
Пример 75
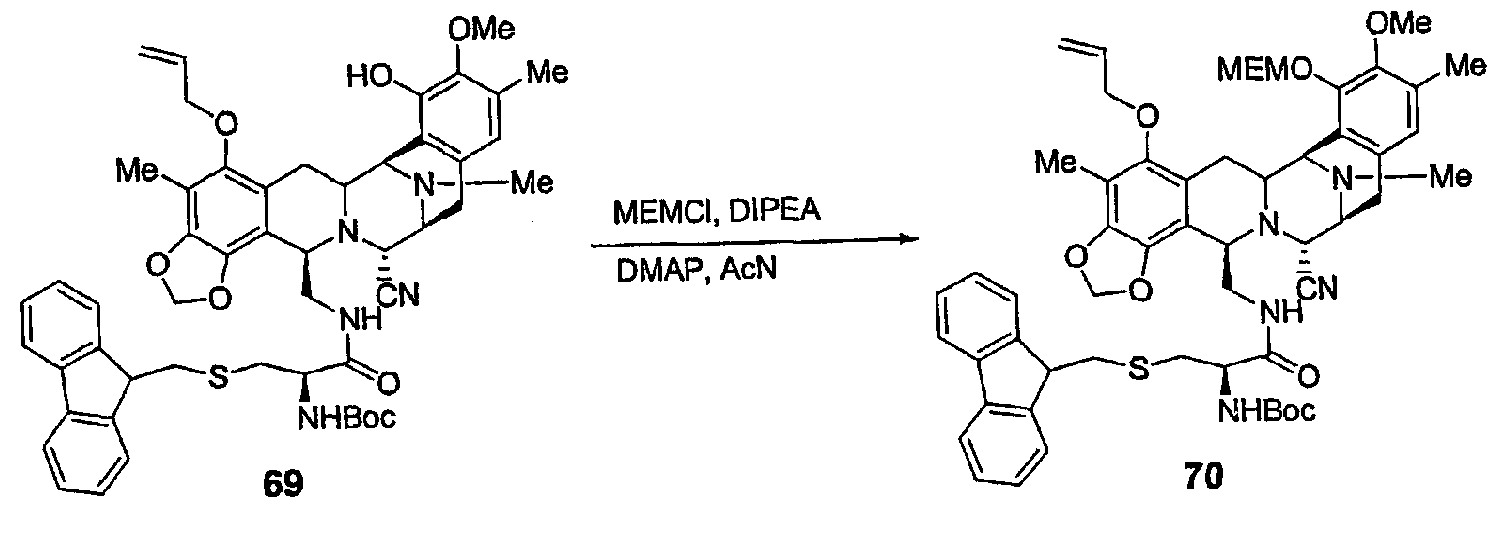
К раствору промежуточного продукта 69 (1,37 г, 1,52 ммоль) в безводном ацетонитриле (8 мл, 0,19 М) добавляли при 0°С в атмосфере аргона DIPEA (5,31 мл, 30,4 ммоль), MEMCl (2,59 мл, 22,8 ммоль) и DMAP (18,63 мг, 0,15 ммоль). Реакционную смесь оставляли при 23°С в атмосфере аргона в течение 5 часов. Добавляли насыщенный водный раствор хлорида аммония, водную фазу экстрагировали дихлорметаном, объединенные органические слои сушили над сульфатом натрия, фильтровали и растворитель удаляли при пониженном давлении. Неочищенный продукт очищали колоночной флэш-хроматографией (элюент этилацетат/гексан 2:3) с получением промежуточного продукта 70 (1,38 г, 92%) в виде желтого твердого вещества. Другую фракцию 130 мг выделяли после колонки в виде смеси исходного материала и соединения 70 в соотношении 2:1.
Rf: 0,48 (этилацетат/гексан 2:3).
1H ЯМР (300 МГц, CDCl3): δ 7,62 (д, 2H), 7,50 (д, 1H), 7,40 (т, 1H), 7,33 (м, 2H), 7,21 (м, 2H), 6,55 (c, 1H), 6,08 (д, 1H), 5,97 (м, 1H), 5,95-5,86 (м, 1H), 5,84 (д, 1H), 5,66 (ушир.д, 1H), 5,31 (дд, 1H), 5,21 (дд, 1H), 5,14 (д, 1H), 5,04 (д, 1H), 4,16 (д, 1H), 4,06-3,92 (м, 3H), 3,87 (м, 2H), 3,73 (м, 4H), 3,54 (м, 2H), 3,41 (c, 3H), 3,34 (c, 3H), 3,30 (м, 2H), 3,20 (дд, 1H), 3,04 (м, 3H), 2,82 (м, 2H), 2,27 (м, 1H), 2,24 (c, 3H), 2,09 (c, 3H), 2,07 (c, 3H), 1,49 (c, 9H), 1,43 (м, 1H).
13C ЯМР (75 МГц, CDCl3): δ 170,19, 155,14, 148,96, 148,83, 148,31, 145,37, 145,23, 144,43, 141,61, 141,55, 138,70, 134,42, 131,13, 131,02, 127,76, 127,59, 127,23, 127,01, 125,58, 124,58, 124,27, 123,93, 121,42, 120,09, 119,88, 118,29, 116,82, 113,03, 112,68, 101,31, 98,34, 95,88, 92,55, 79,97, 73,50, 71,98, 71,88, 69,54, 67,68, 67,01, 59,73, 59,27, 58,94, 58,27, 56,86, 56,35, 55,52, 51,90, 46,95, 41,63, 38,37, 34,87, 33,67, 28,65, 26,70, 24,47, 15, 83, 9,73.
ESI-MC m/z: Вычислено для С55Н65N5O10S: 987,4. Найдено (М+1)+: 988,6.
Пример 76

К раствору промежуточного продукта 70 (1,38 г, 1,39 ммоль) в безводном дихлорметане (36 мл, 0, 04 М) добавляли при 23°С в атмосфере аргона (PPh3)2PdCl2 (0,11 г, 8% по массе), уксусную кислоту (0,39 мл, 6,98 ммоль) и гидрид трибутилолова (1,31 мл, 4,88 ммоль). Реакционную смесь оставляли при 23°С в атмосфере аргона на 30 минут, разбавляли гексаном и выливали на колонку (смеси элюентов этилацетат/гексан в градиенте от 0:100 до 3:2) с получением промежуточного продукта 71 (1,16 г, 87%) в виде желтого твердого вещества.
Rf: 0,28 (этилацетат/гексан 1:1).
1H ЯМР (300 МГц, CDCl3): δ 7,69 (т, 2H), 7,54 (т, 2H), 7,39-7,23 (м, 4H), 6,61 (c, 1H), 5,98 (м, 1H), 5,96 (c, 1H), 5,87 (c, 1H), 5,80 (c, 1H), 5,39 (т, 2H), 5,21 (д, 1H), 4,11 (м, 3H), 4,01 (м, 1H), 3,92 (м, 3H), 3,66 (c, 3H), 3,55 (м, 2H), 3,39 (c, 3H), 3,37 (м, 3H), 3,26-3,12 (м, 4H), 2,90 (д, 1H), 2,88 (м, 1H), 2,78 (д, 1H), 2,27 (c, 3H), 2,15 (c, 3H), 2,06 (c, 3H), 1,73 (дд, 1H), 1,39 (c, 9H).
ESI-MC m/z: Вычислено для С52Н61N5O10S: 947,4. Найдено (М+1)+: 948,8.
Пример 77
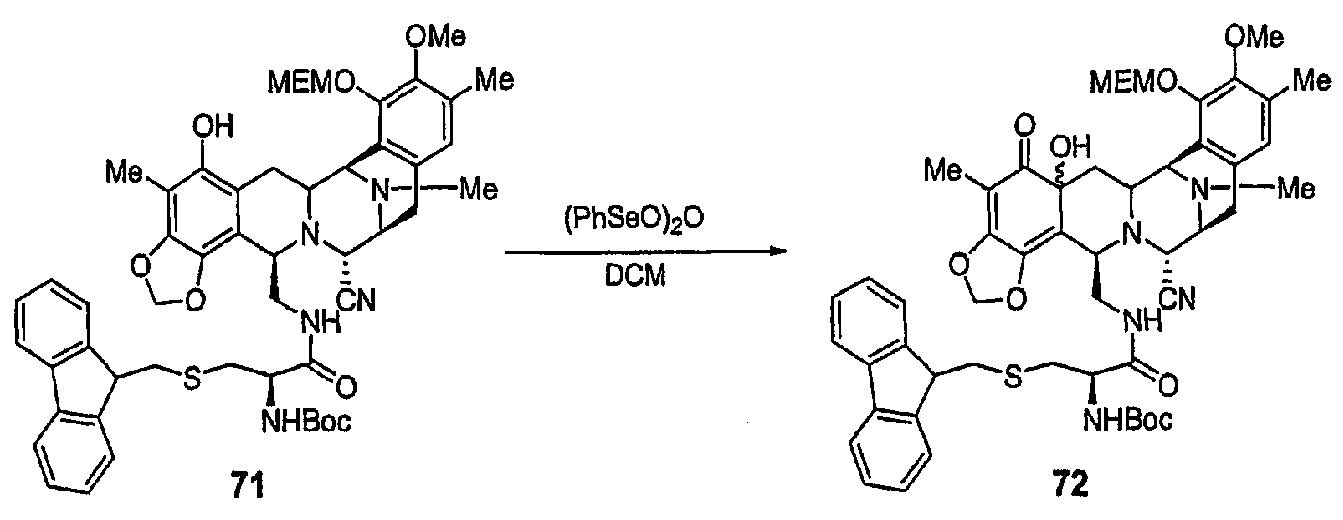
К раствору соединения 71 (39 мг, 0,041 ммоль) в безводном CH2Cl2 (1,2 мл, 0, 03 М) добавляли при -10°С в атмосфере аргона раствор бензолселенинового ангидрида (21,14 мг, 0,041 ммоль) в безводном CH2Cl2 (0,6 мл). Реакционную смесь перемешивали при -10°С в атмосфере аргона в течение 30 минут. Реакционную смесь разбавляли CH2Cl2 и реакцию гасили насыщенным водным раствором бикарбоната натрия, водную фазу экстрагировали CH2Cl2 и органические слои сушили над сульфатом натрия. Растворитель удаляли при пониженном давлении и неочищенный продукт этой реакции очищали колоночной флэш-хроматографией с получением соединения 72 (33 мг, 83%) в виде бледно-желтого твердого вещества и смеси изомеров в соотношении 1,3:1 согласно1Н ЯМР.
Rf: 0,21 и 0,11 (этилацетат/гексан 2:1).
1H ЯМР (300 МГц, CDCl3): δ 7,74 (д, 4H), 7,70-7,62 (м, 4H), 7,39 (т, 4H), 7,31 (т, 4H), 6,72 (м, 2H), 6,61 (c, 1H), 6,46 (c, 1H), 5,78 (c, 1H), 5,77 (c, 1H), 5,61 (c, 1H), 5,58 (c, 1H), 5,38 (ушир.д, 1H), 5,23 (д, 1H), 5,12 (д, 2H), 5,04 (д, 1H), 4,83 (c, 1H), 4,41 (c, 1H), 4,11 (м, 2H), 4,03 (м, 4H), 3,90-3,86 (м, 2H), 3, 86 (c, 3H), 3,78-3,71 (м, 5H), 3,55 (м, 6H), 3,52 (c, 3H), 3,38 (c, 3H), 3,35 (c, 3H), 3,27 (м, 4H), 3,12 (м, 3H), 2,81 (м, 6H), 2,44 (м, 4H), 2,26 (c, 3H), 2,22 (c, 3H), 2,14 (c, 3H), 2,14-2,10 (м, 2H), 2,04 (c, 3H), 1,78 (c, 3H), 1,77 (c, 3H), 1,39 (c, 9H), 1,34 (c, 9H).
ESI-MC m/z: Вычислено для С52Н61N5O11S: 963,4. Найдено (М+1)+: 964,9.
Пример 78

Реакционную колбу обрабатывали пламенем два раза, откачивали воздух, продували аргоном несколько раз и хранили в атмосфере аргона для реакции. К раствору ДМСО (220,8 мкл) в безводном CH2Cl2 (20,7 мл) по каплям добавляли трифторметансульфоновый ангидрид (104,7 мкл) при -78°С. Реакционную смесь перемешивали при -78°С в течение 20 минут, затем добавляли через канюлю раствор 72 (300 мг, 0,31 ммоль) в безводном CH2Cl2 (10,4 мл) при -78°С. Во время добавления температуру в обеих колбах поддерживали при -78°С. Реакционную смесь перемешивали при -40°С в течение 35 минут. После этого периода времени добавляли по каплям изо-Pr2NEt (812,9 мкл) и реакционную смесь выдерживали при 0°С в течение 45 минут. Затем добавляли по каплям трет-BuOH (293,4 мкл) и гуанидин (534,9 мкл) и реакционную смесь выдерживали при 23°С в течение 40 минут. После этого добавляли по каплям уксусный ангидрид (441,1 мкл) и реакционную смесь выдерживали при 23°С в течение еще 1 часа. Затем эту реакционную смесь разбавляли CH2Cl2 и промывали водным насыщенным раствором NH4Cl, NaHCO3 и NaCl. Объединенные органические слои сушили над Na2SO4, фильтровали и концентрировали.
Остаток очищали колоночной флэш-хроматографией (смеси элюентов этилацетат/гексан в градиенте от 1:4 до 1:1) с получением 73 (160 мг, 64%) в виде бледно-желтого твердого вещества.
Rf: 0,13 (этилацетат/гексан 1:1).
1H ЯМР (300 МГц, CDCl3): δ 6,76 (c, 1H), 6,06 (д, 1H), 5,98 (c, 1H), 5,32 (д, 1H), 5,17 (д, 1H), 4,81 (c, 1H), 4,48 (ушир.c, 1H), 4,36 (ушир.д, 1H), 4,18 (c, 1H), 3,95-3,82 (м, 3H), 3,75 (c, 3H), 3,72-3,68 (м, 1H), 3,59-3,52 (м, 4H), 3,37 (c, 3H), 3,36 (c, 3H), 2,96 (м, 2H), 2,56 (ушир.д, 1H), 2,29 (c, 3H), 2,28 (c, 3H), 2,19 (c, 3H), 1,98 (c, 3H), 1,69 (м, 1H), 1,42-1,37 (м, 1H), 1,38 (c, 9H).
ESI-MC m/z: Вычислено для С40Н51N5O11S: 809,3. Найдено (М+1)+: 810,2.
Пример 79
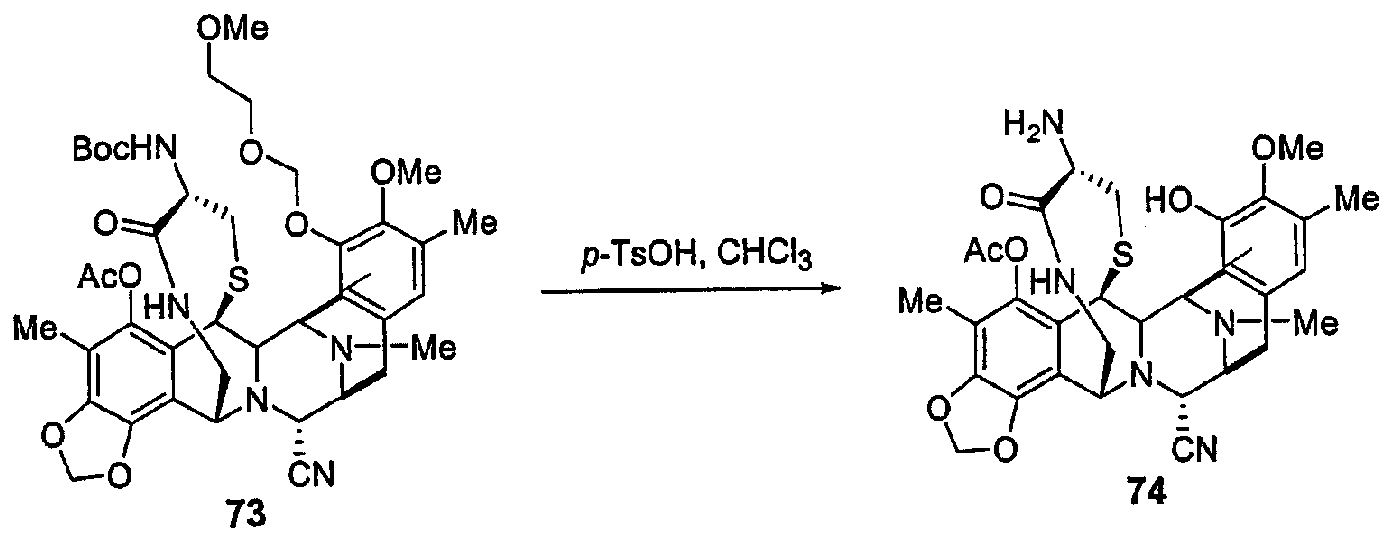
К раствору промежуточного продукта 73 (169 мг, 0,21 ммоль) в CHCl3 (11 мл, 0,02 М) добавляли при 23°С p-TsOH (243 мг, 1,25 ммоль). Реакционную смесь оставляли при 23°С и в атмосфере аргона на 14 часов. Реакционную смесь разбавляли дихлорметаном и добавляли насыщенный водный раствор бикарбоната натрия. Водную фазу экстрагировали дихлорметаном, объединенные органические слои сушили над сульфатом натрия, фильтровали и растворитель удаляли при пониженном давлении. Неочищенный продукт очищали колоночной флэш-хроматографией (смеси элюентов метиленхлорид/метиловый спирт в градиенте от 100:0 до 9:1) с получением промежуточного продукта 74 (123 мг, 95%) в виде оранжевого твердого вещества.
Rf: 0,17 (метиленхлорид/метиловый спирт 95:5).
1H ЯМР (300 МГц, CDCl3): δ 6,81 (ушир.c, 1H), 6,49 (c, 1H), 6,06 (д, 1H), 6,00 (д, 1H), 4,43 (ушир.c, 1H), 4,27 (д, 2H), 4,17 (c, 1H), 4,04 (д, 1H), 3,77 (c, 3H), 3,62 (д, 1H), 3,39 (д, 1H), 3,18 (м, 1H), 3,00 (дд, 2H), 2,65 (д, 1H), 2,57 (м, 1H), 2,33 (c, 3H), 2,27 (c, 3H), 2,17 (c, 3H), 1,97 (c, 3H), 1,80 (д, 1H).
ESI-MC m/z: Вычислено для С31Н35N5O7S: 621,2. Найдено (М+1)+: 622,2.
Пример 80
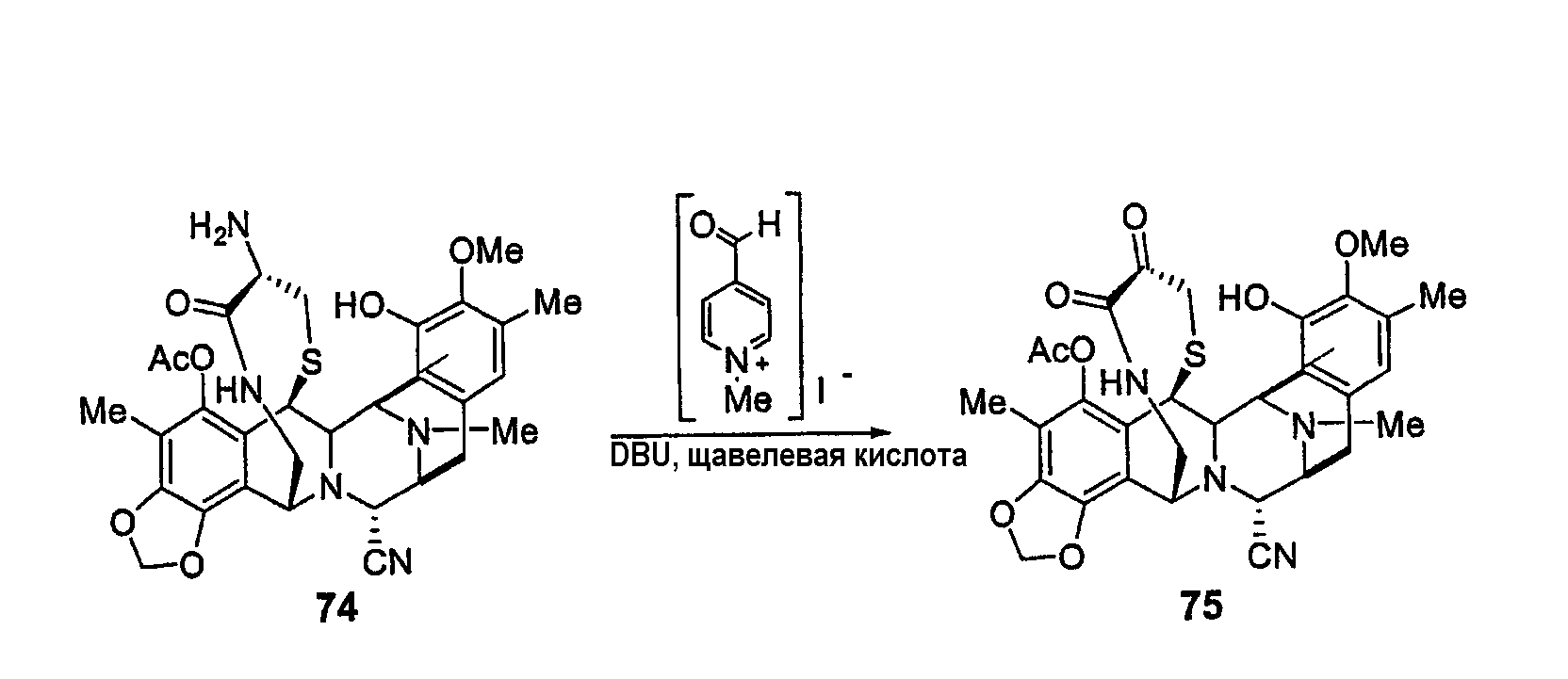
К раствору соли пиридиния (285 мг, 1,14 ммоль) в ДМФ (6 мл) добавляли при 23°С раствор промежуточного продукта 74 (71 мг, 0,114 ммоль) в дихлорметане (6 мл, конечная концентрация 0,01 М). Реакционную смесь оставляли при 23°С и в атмосфере аргона на 4 часа и 15 минут, затем добавляли DBU (0,17 мл, 1,14 моль) и этот раствор перемешивали при 23°С и в атмосфере аргона в течение 15 минут. После этого периода времени добавляли насыщенный раствор щавелевой кислоты (11 мл) и реакционную смесь оставляли при 23°С в атмосфере аргона на 30 минут. Реакционную смесь охлаждали при 0°С, разбавляли Et2O и добавляли насыщенный раствор бикарбоната натрия до достижения рН 5. Водную фазу экстрагировали Et2O (×4), дополнительно подщелачивали дополнительным количеством бикарбоната натрия и экстрагировали дополнительным количеством Et2O (×4). Объединенные органические слои сушили над сульфатом натрия, фильтровали и растворитель удаляли при пониженном давлении. Неочищенный продукт очищали колоночной флэш-хроматографией (смеси элюентов метиленхлорид/метиловый спирт в градиенте от 100:0 до 20:1) с получением промежуточного продукта 75 (38 мг, 55%) в виде желтого твердого вещества.
Rf: 0,7 и 0,5 (метиленхлорид/метиловый спирт 8:1).
1H ЯМР (300 МГц, CDCl3): δ (смесь изомера) 6,49 (c, 1H), 6,06 (д, 1H), 6,01 (д, 1H), 5,78 (c, 1H), 4,55 (c, 1H), 4,37-4,23 (м, 3H), 4,05 (д, 1H), 3,80 (c, 3H), 3,65 (д, 1H), 3,40 (ушир.д, 1H), 3,06-3,00 (м, 2H), 2,66 (дд, 2H), 2,34 (c, 3H), 2,29 (c, 3H), 2,18 (c, 3H), 1,99 (c, 3H).
ESI-MC m/z: Вычислено для С31Н32N4O8S: 620,2. Найдено (М+1)+: 621,1.
Пример 81

К раствору промежуточного продукта 75 (23 мг, 0, 037 ммоль) в уксусной кислоте (1,3 мл) добавляли после 1 часа производное допамина (25 мг, 0,10 ммоль). Реакционную смесь оставляли при 23°С в атмосфере аргона на 50 часов. Растворитель этой реакции удаляли при пониженном давлении и остаток разбавляли CH2Cl2, промывали насыщенным водным раствором бикарбоната натрия. Органическую фазу сушили над сульфатом натрия, растворитель удаляли при пониженном давлении и неочищенный продукт очищали колоночной флэш-хроматографией (смеси элюентов CH2Cl2/этилацетат в градиенте от 100:0 до 1:2) с получением промежуточного продукта 76 (18 мг, 63%) в виде бледно-желтого твердого вещества и смеси изомеров.
Rf: 0,26 (CH2Cl2/этилацетат 1:3).
1H ЯМР (300 МГц, CDCl3): δ 6,54 (c, 1H), 6,48 (д, 1H), 6,43 (c, 1H), 6,08 (д, 1H), 6,06 (д, 1H), 6,04 (д, 1H), 6,01 (д, 1H), 5,80 (c, 1H), 5,75 (c, 1H), 5,41 (м, 1H), 4,60-4,16 (м, 7H), 4,04 (м, 2H), 3,80 (c, 3H), 3,79 (c, 3H), 3,77 (c, 3H), 3,76 (c, 3H), 3,65 (д, 2H), 3,42 (м, 2H), 3,07-2,84 (м, 5H), 2,70 (д, 2H), 2,61-2,47 (м, 4H), 2,36 (c, 3H), 2,34 (c, 3H), 2,31 (c, 3H), 2,19 (c, 3H), 2,16 (c, 3H), 2,04 (c, 3H), 2,00 (c, 3H), 1,99 (c, 3H), 1,66 (м, 2H).
ESI-MC m/z: Вычислено для С40Н43N5O9S: 769,3. Найдено (М+1)+: 770,0.
Пример 82
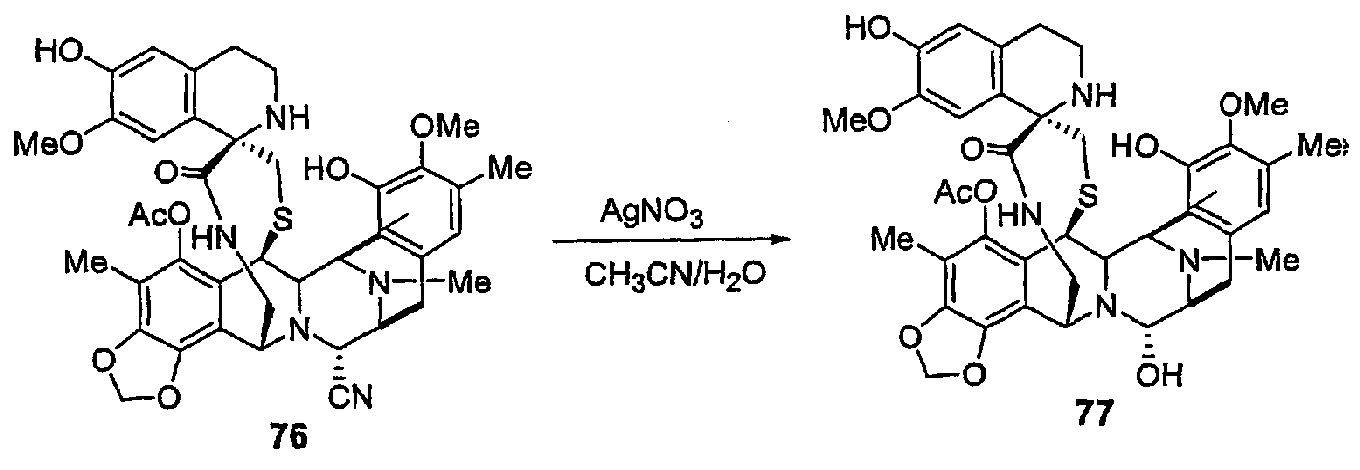
К раствору промежуточного продукта 76 (7 мг, 0,009 ммоль) в ацетонитриле (0,6 мл) добавляли при 23°С воду (0,4 мл, 0,015 М, конечная концентрация) и AgNO3 (46 мг, 0,27 ммоль). Реакционную смесь оставляли в атмосфере аргона при 23°С на 31 час. Реакционную смесь разбавляли дихлорметаном и насыщенным раствором бикарбоната натрия и добавляли насыщенный раствор хлорида натрия. Водную фазу экстрагировали дихлорметаном и объединенные органические слои сушили над сульфатом натрия, фильтровали и растворитель удаляли при пониженном давлении. Неочищенный продукт очищали колоночной флэш-хроматографией (смеси элюентов дихлорметан/этилацетат в градиенте 1/9 - 100% в этилацетате) с получением конечного продукта 77 (4 мг, 58%) в виде бледно-желтого твердого вещества.
Rf: 0,17 (дихлорметан/этилацетат 1:9).
1H ЯМР (300 МГц, CDCl3): δ 6,54 (c, 1H), 6,20 (м, 1H), 6,03 (д, 1H), 6,01 (д, 1H), 5,72 (c, 1H), 5,41 (ушир.c, 1H), 4,65 (ушир.c, 1H), 4,40-4,29 (м, 3H), 4,16 (д, 2H), 3,83 (м, 1H), 3,77 (c, 3H), 3,76 (c, 3H), 3,49 (c, 1H), 3,21 (м, 2H), 2,94 (м, 4H), 2,66 (д, 1H), 2,51 (д, 2H), 2,36 (м, 2H), 2,31 (c, 6H), 2,17 (c, 3H), 2,00 (c, 3H).
ESI-MC m/z: Вычислено для С39Н44N4O10S: 760,3. Найдено (М-Н2О+1)+: 743, 0.
Биопробы в противоопухолевом скрининге
Заключительное действие этих исследований состоит в прекращении роста in vitro культуры опухолевых клеток посредством непрерывного исследования этих клеток в испытуемой пробе (тест-пробе).
1°. - Ингибирование роста клеток путем подсчета количества клеток
Этот анализ использует 24-луночные мультичашки с диаметром 16 мм (Bergeron, 1984; Schroeder, 1981). Использованными линиями опухолевых клеток являются: Р-388 (АТСС CCL 46), суспензионная культура лимфоидной неоплазмы из мыши DBA/2; А-549 (АТСС CCL 185), монослойная культура рака легкого человека; НТ-29 (АТСС НТВ-38), монослойная культура рака ободочной кишки человека; MEL-28 (ATCC HTB-72), монослойная культура меланомы человека и DU-145 (ATCC HTB-81), монослойная культура рака предстательной железы человека.
Клетки поддерживали в логарифмической фазе роста в минимальной эссенциальной среде Игла со сбалансированными солями Эрла, с неэссенциальными аминокислотами, с 2,0 мМ L-лутамином, без бикарбоната натрия (ЕМЕМ/neaa), дополненной 10% фетальной телячьей сывороткой (ФТС), 10-2 М. Для экспериментов клетки собирали из субконфлюентных культур с использованием трипсина и ресуспендировали в свежей среде перед посевом.
Клетки Р-388 высевали в лунки с диаметром 16 мм при 1×104клеток на лунку в аликвотах 1 мл ЕМЕМ-5% ФТС, содержащие различные концентрации испытуемой пробы. Отдельный ряд культур без лекарственного средства засевали в качестве контроля роста для гарантии того, что клетки остаются в экспоненциальной фазе роста. Все определения проводили в двух повторностях. После трех дней инкубирования при 37°С 5% СО2 в атмосфере с влажностью 98% приблизительно определяли IC50 путем сравнения роста в лунках с лекарственным средством с ростом в контрольных лунках.
Клетки А-549, НТ-29, MEL-28 и DU-145 высевали в лунки с диаметром 16 мм при 1×104 клеток на лунку в аликвотах 1 мл ЕМЕМ-5% ФТС, содержащие различные концентрации испытуемой пробы. Отдельный ряд культур без лекарственного средства высевали в качестве контроля роста для гарантии того, что клетки остаются в экспоненциальной фазе роста. Все определения проводили в двух повторностях. После трех дней инкубирования при 37оС, 5% СО2 в атмосфере с влажностью 98%, клетки окрашивали 0,1% кристаллическим фиолетовым красителем. Приблизительно определяли IC50 путем сравнения роста клеток в лунках с лекарственным средством с ростом клеток в контрольных лунках.
Для количественного определения активности после инкубационного периода клетки трипсинизировали и подсчитывали в счетчике Коултера ZM. Все количества (общее количество клеток на одну лунку) представляют собой среднее из двух повторностей лунок. % G, процент роста относительно культур без лекарственного средства. Результаты этих анализов использовали для построения кривых доза-ответ, из которых определяли более точные величины IC50 (концентрацию пробы, которая дает 50% ингибирование роста клеток).
Основываясь на полученных результатах, можно предположить возможность применимости определенных лекарственных средств в качестве потенциального лечения рака. Для этого способа соединения, которые обнаруживают величины IC50, меньшие, чем 1 мкг/мл, отбирают для продолжения дополнительных исследований. Данные IC50 позволяют предсказать не только то, что лекарственное средство является цитостатическим, но также и то, что может ли оно иметь потенциал уменьшения опухоли.
2о. - Ингибирование роста клеток колориметрическим анализом
Колориметическая проба, использующая реакцию сульфородамина В (SRB), была адаптирована для количественного измерения роста и жизнеспособности клеток (согласно способу, описанному Philip Skehan, et al. (1990), New colorimetric cytotoxicity assay for anticancer drug screening, J. Natl. Cancer Instr., 82:1107-1112)).
Этот анализ использует 96-луночные культуральные микропланшеты с диаметром 9 мм (Faircloth, 1988; Mosmann, 1983). Большинство клеточных линий получают из Американской Коллекции Типовых Культур (АТСС), полученных из различных типов раков человека.
Клетки поддерживают в среде RPMI 1640 с 10% ФТС, дополненной 0,1 г/л пенициллина и 0,1 г/л стрептомицин-сульфата, и затем инкубируют при 37°С, 5% СО2 и влажности 98%. Для экспериментов клетки собирают из субконфлюэнтной культуры, используя трипсин, и ресуспендируют в свежей среде перед посевом в чашки Петри.
Клетки высевают в 96-луночные микротитрационные планшеты при 5×104 клеток на лунку в аликвотах 195 мкл среды и им дают прикрепляться к поверхности планшета выращиванием в среде, не содержащей лекарственного средства, в течение 18 часов. После этого добавляют пробы в аликвотах 5 мкл в диапазоне 10-10-8мкг/мл, растворенные в ДМСО/EtOH/ЗФР (0,5:0,5:99). После 48 часов экспозиции противоопухолевое действие измеряют SRB-методологией: клетки фиксируют добавлением 50 мкл холодной 50% (масса/объем) трихлоруксусной кислоты (ТХУ) и инкубированием в течение 60 минут при 4°С. Планшеты промывают деионизированной водой и сушат. В каждую микротитрационную лунку добавляют 100 мкл раствора SRB (0,4% масса/объем в 1% уксусной кислоте) и инкубируют в течение 10 минут при комнатной температуре. Несвязанный SRB удаляют промыванием 1% уксусной кислотой. Планшеты сушат на воздухе и связанный краситель солюбилизируют Трис-буфером. Оптические плотности считывают на автоматическом спектрофотометрическом планшет-ридере при единственной длине волны 490 нм.
Рассчитывают величины для среднего ±SD (стандартное отклонение) из трех повторностей лунок. Могут быть рассчитаны некоторые параметры для клеточных ответных реакций: GI = ингибирование роста, TGI = общее ингибирование роста (цитостатическое действие) и LC = убивание клеток (цитотоксическое действие).
По полученным результатам можно прогнозировать применимость определенного лекарственного средства для потенциального лечения рака. Для этого способа соединения, которые обнаруживают величины GI50, меньшие, чем 10 мкг/мл, отбирают для продолжения дополнительных исследований. Данные GI50 позволяют делать предсказания не только о том, является ли лекарственное средство цитостатическим, но также и о том, может ли оно иметь потенциал уменьшения опухоли.
Данные активности (молярные)
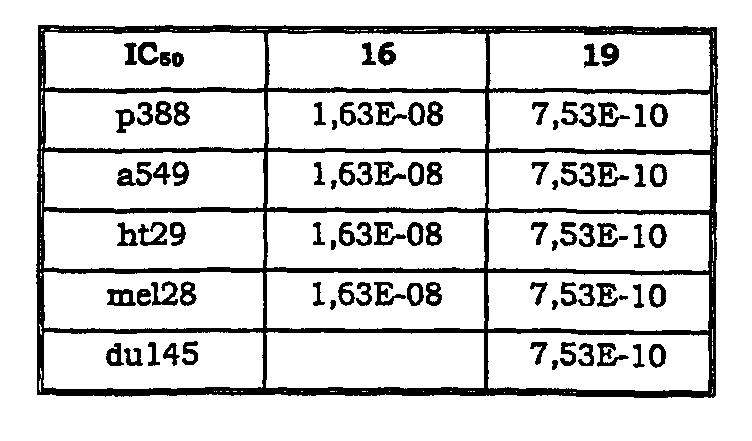


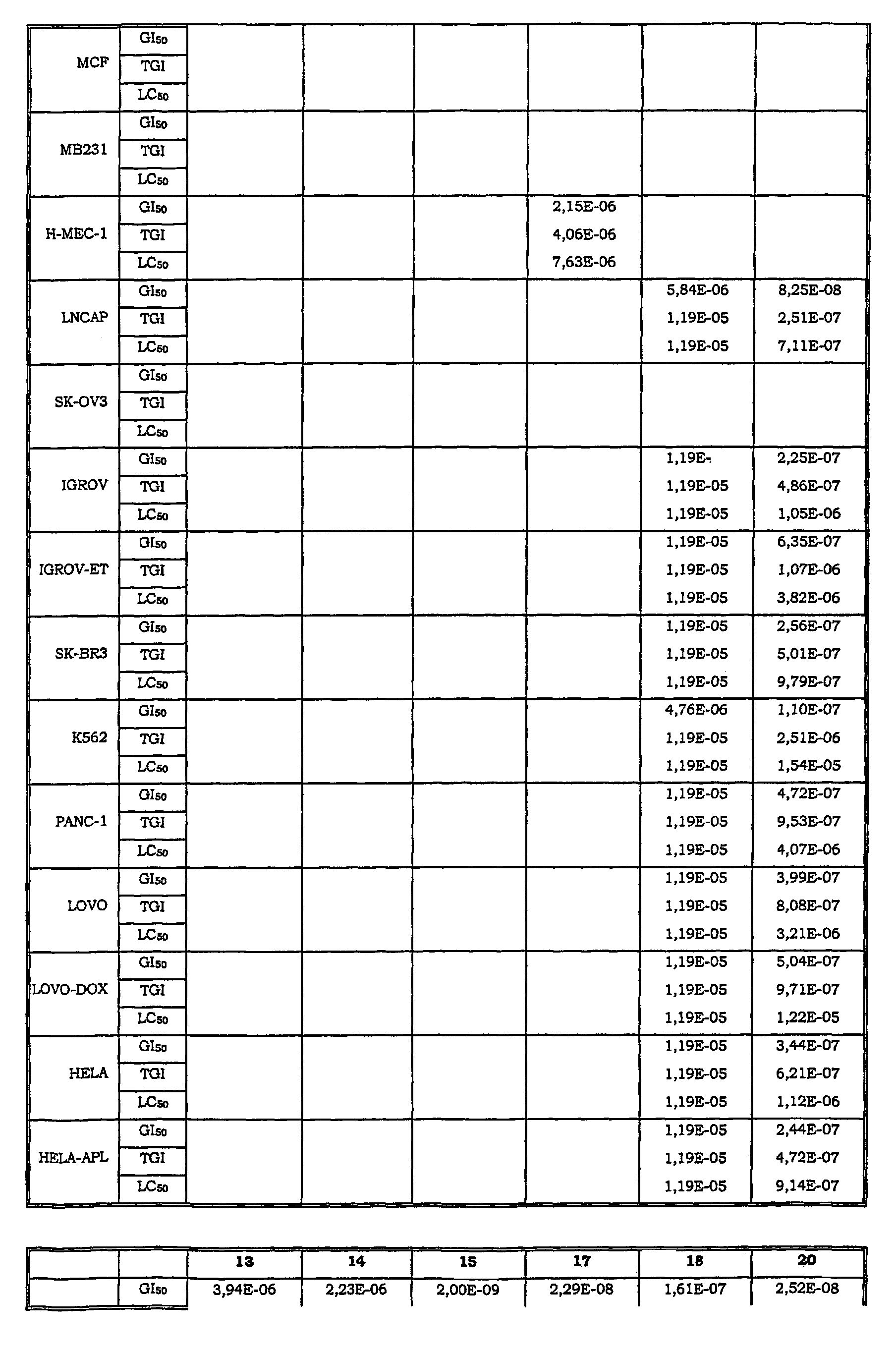
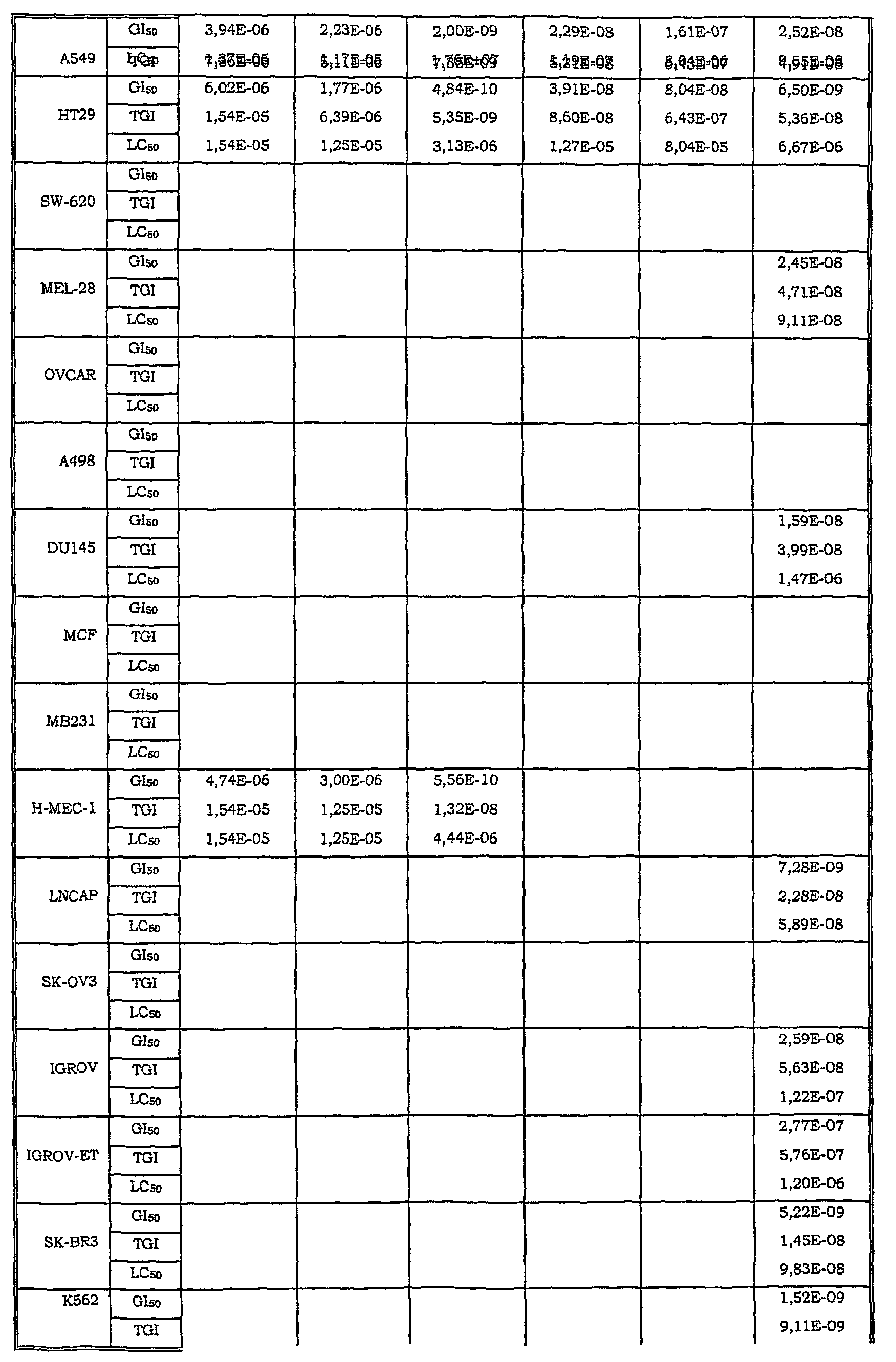
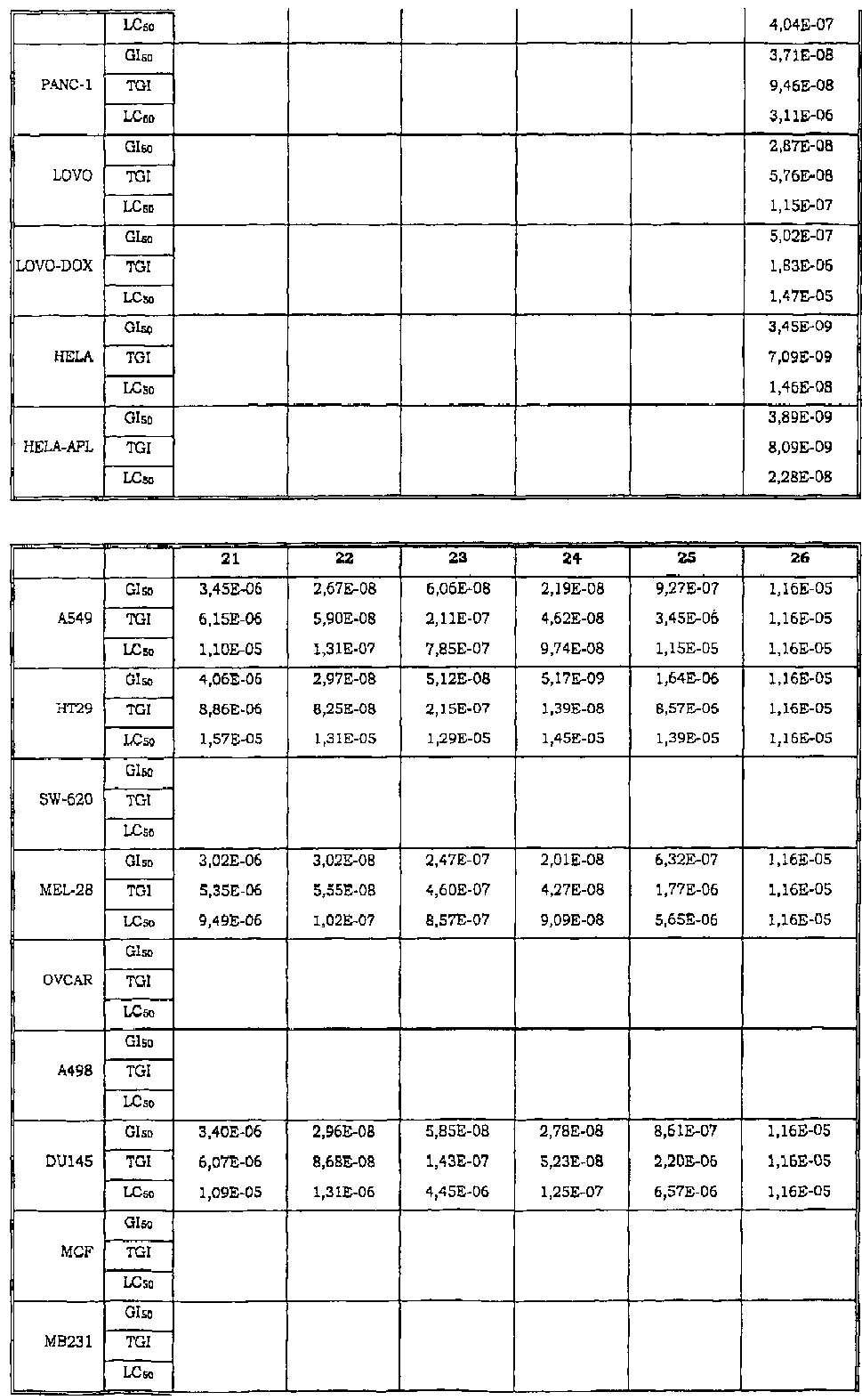
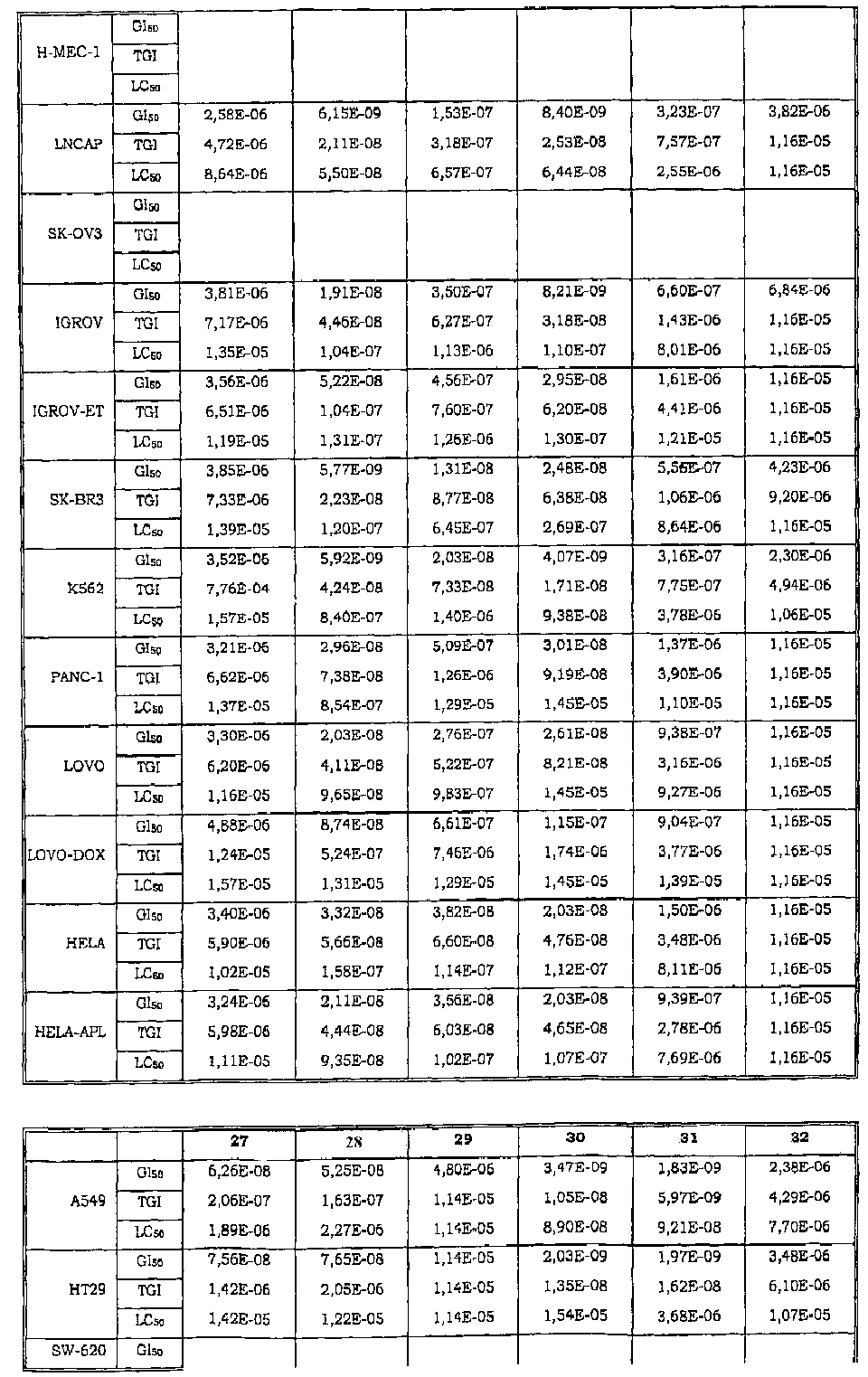

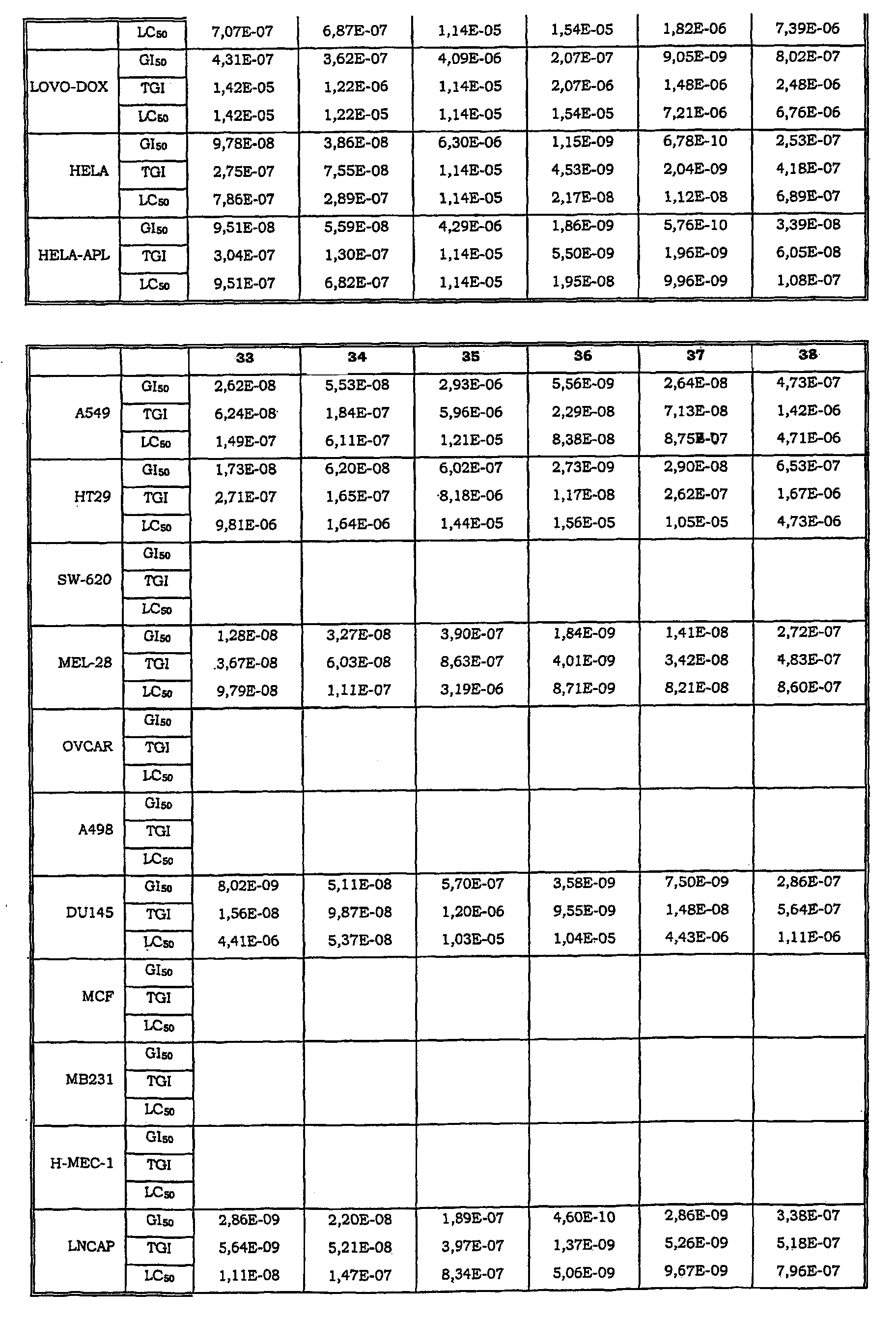

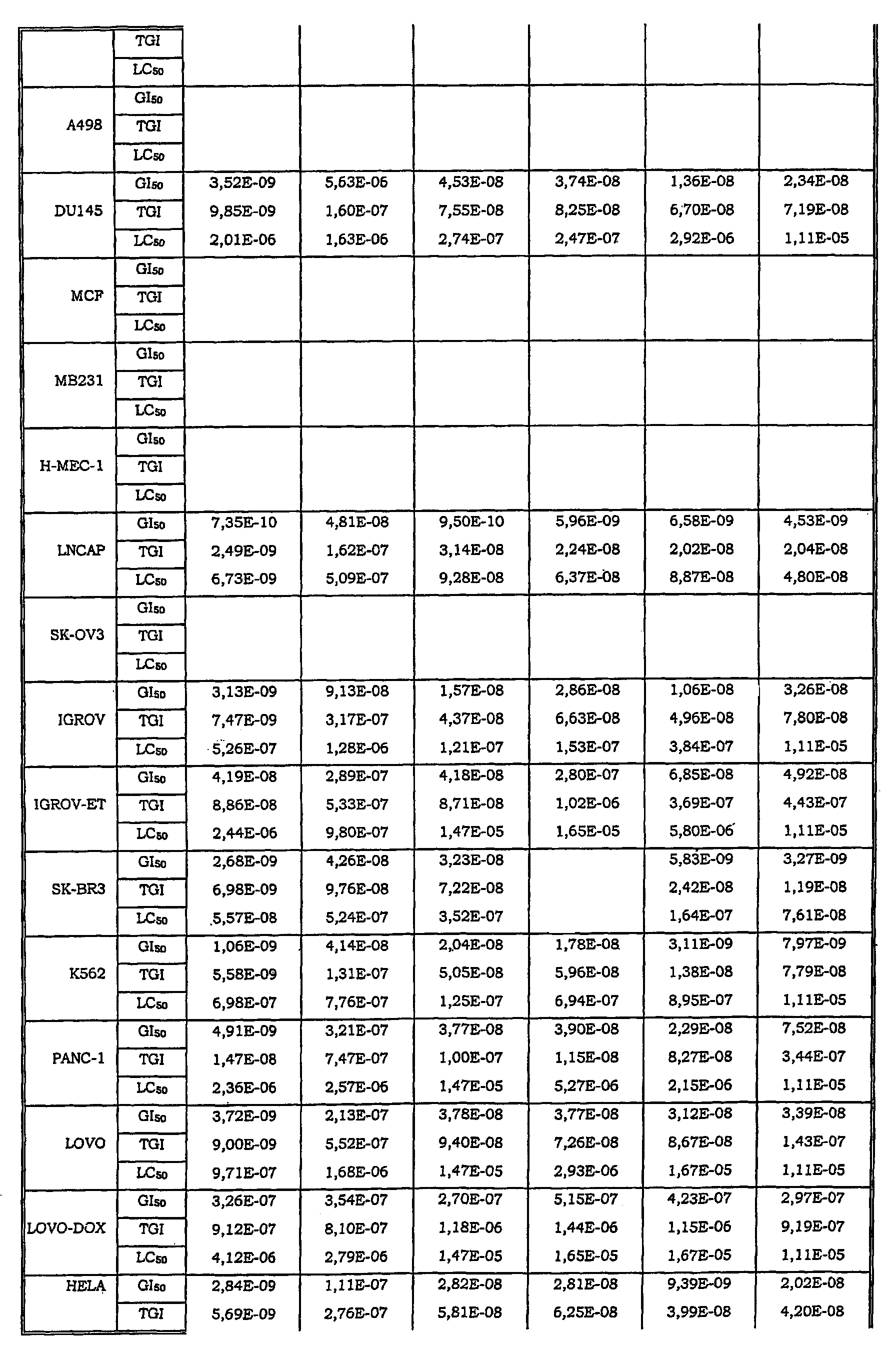

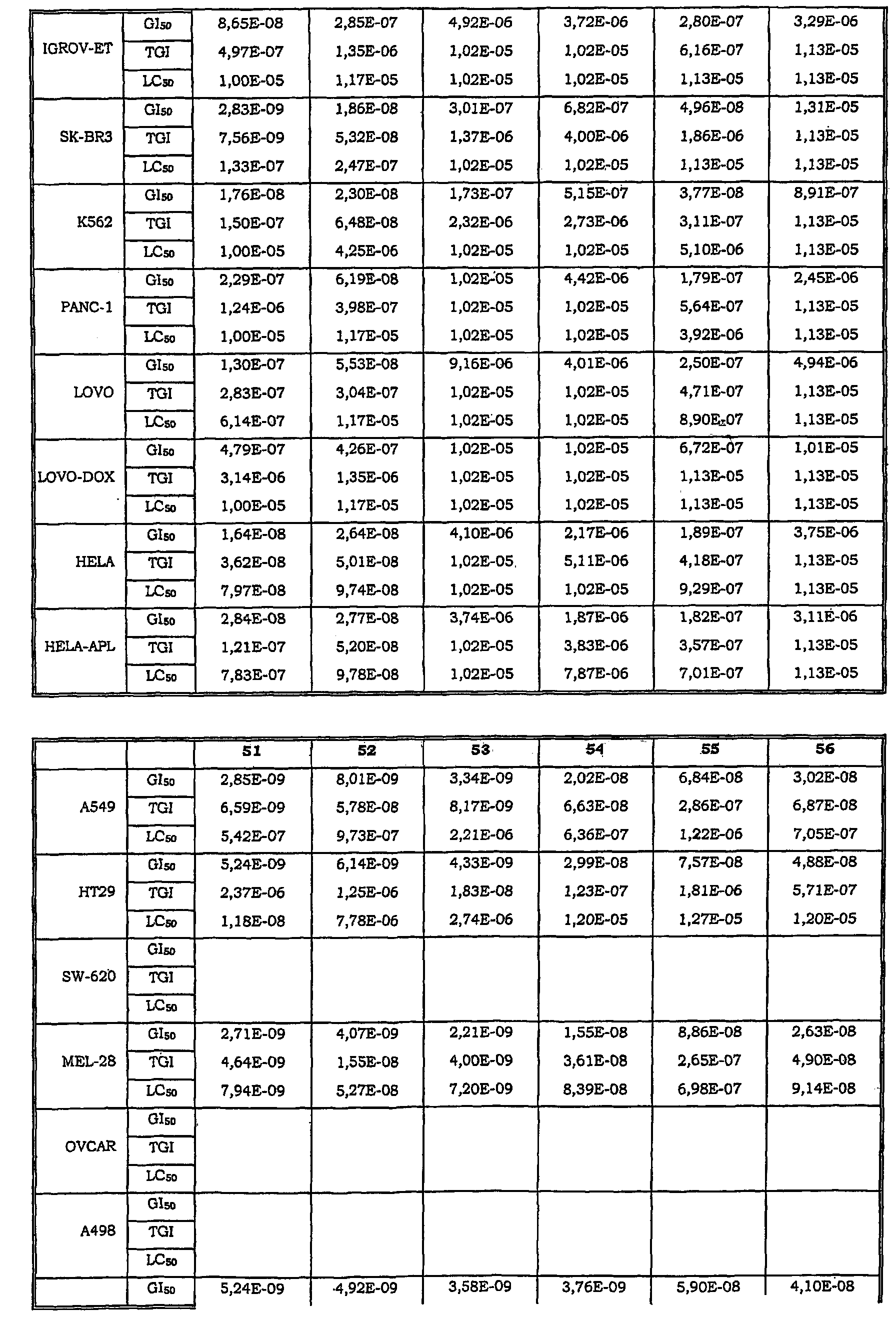
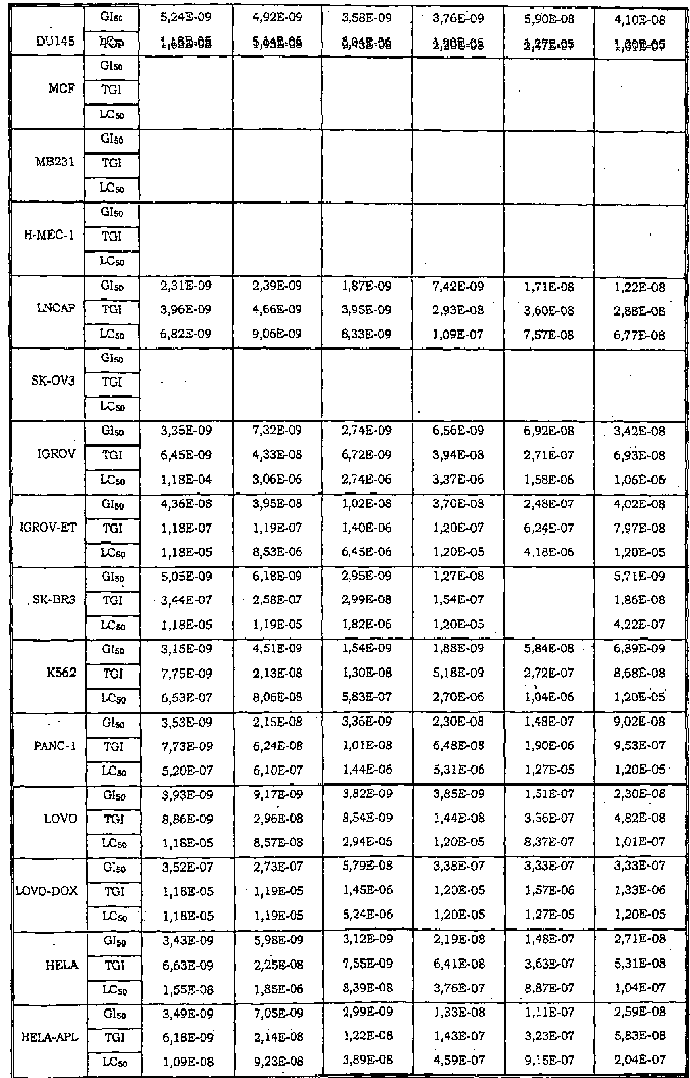
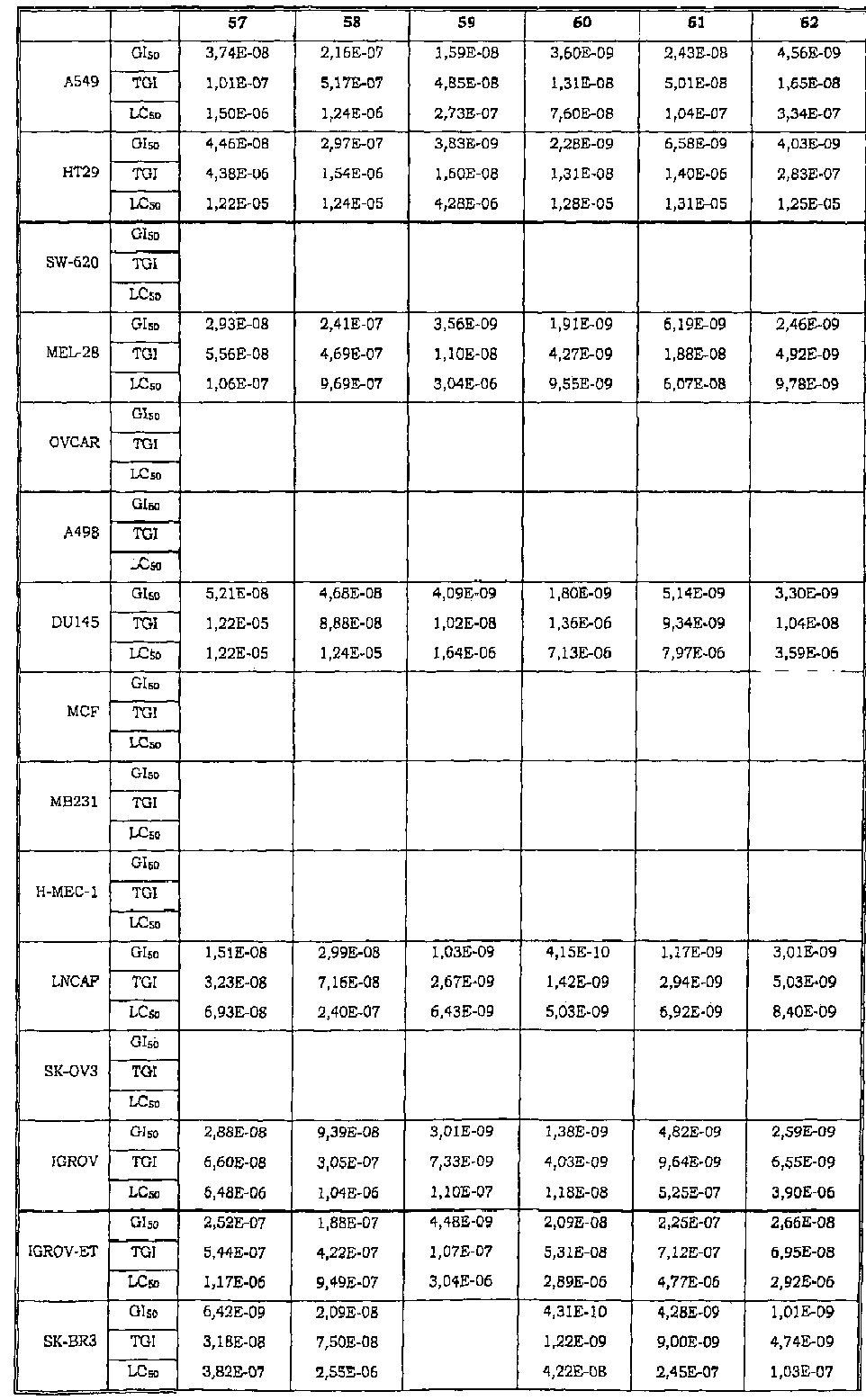
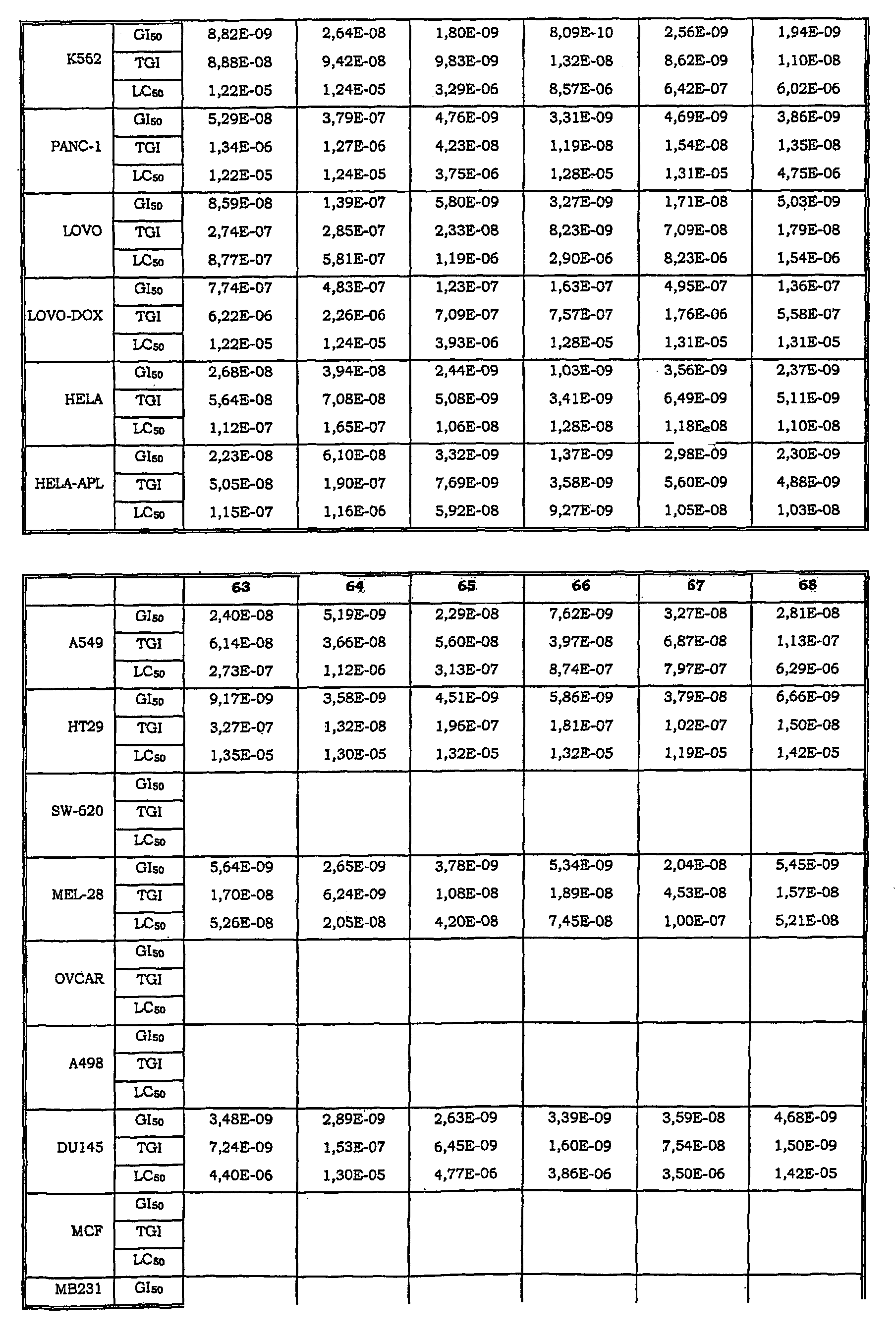
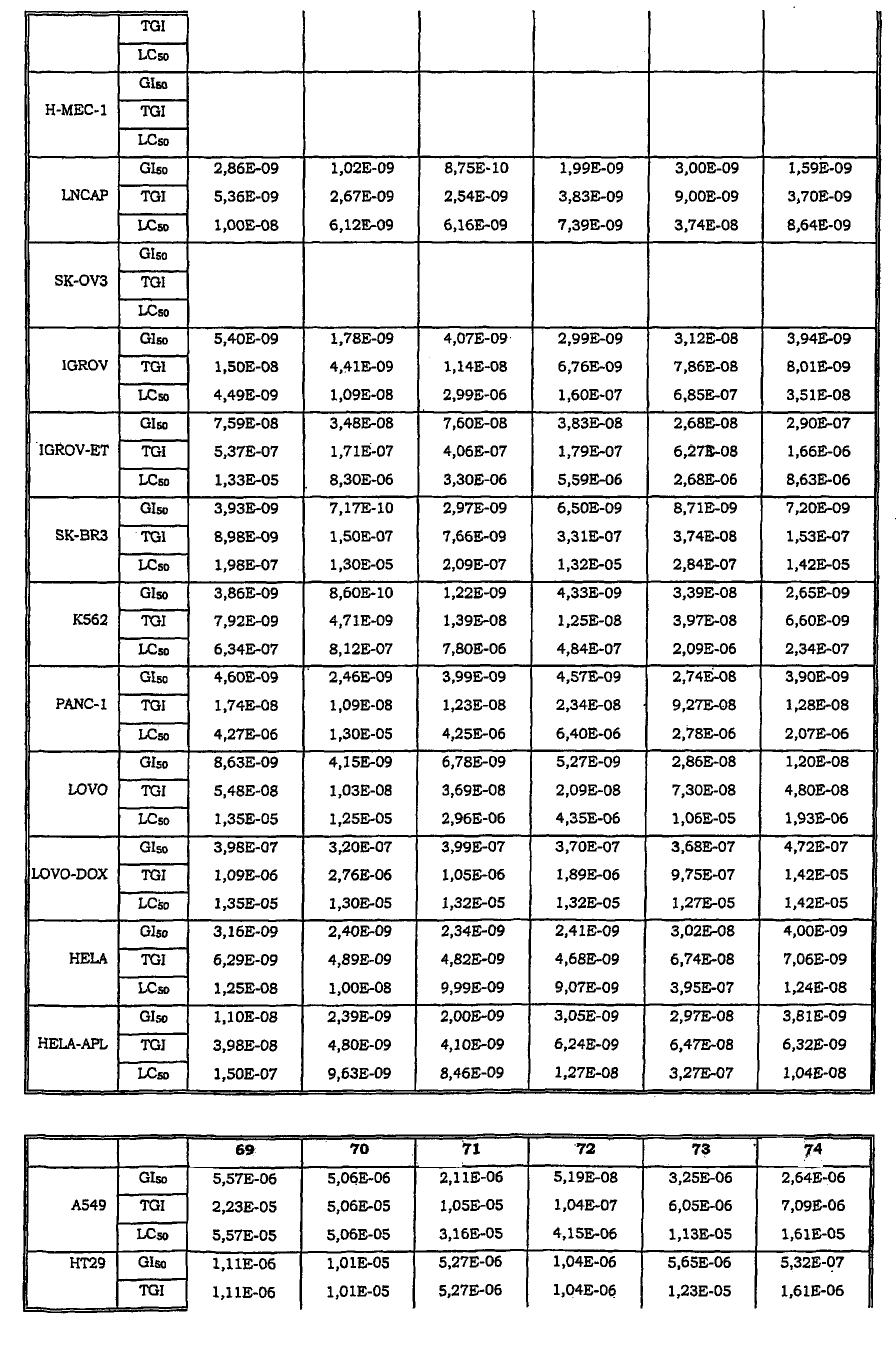
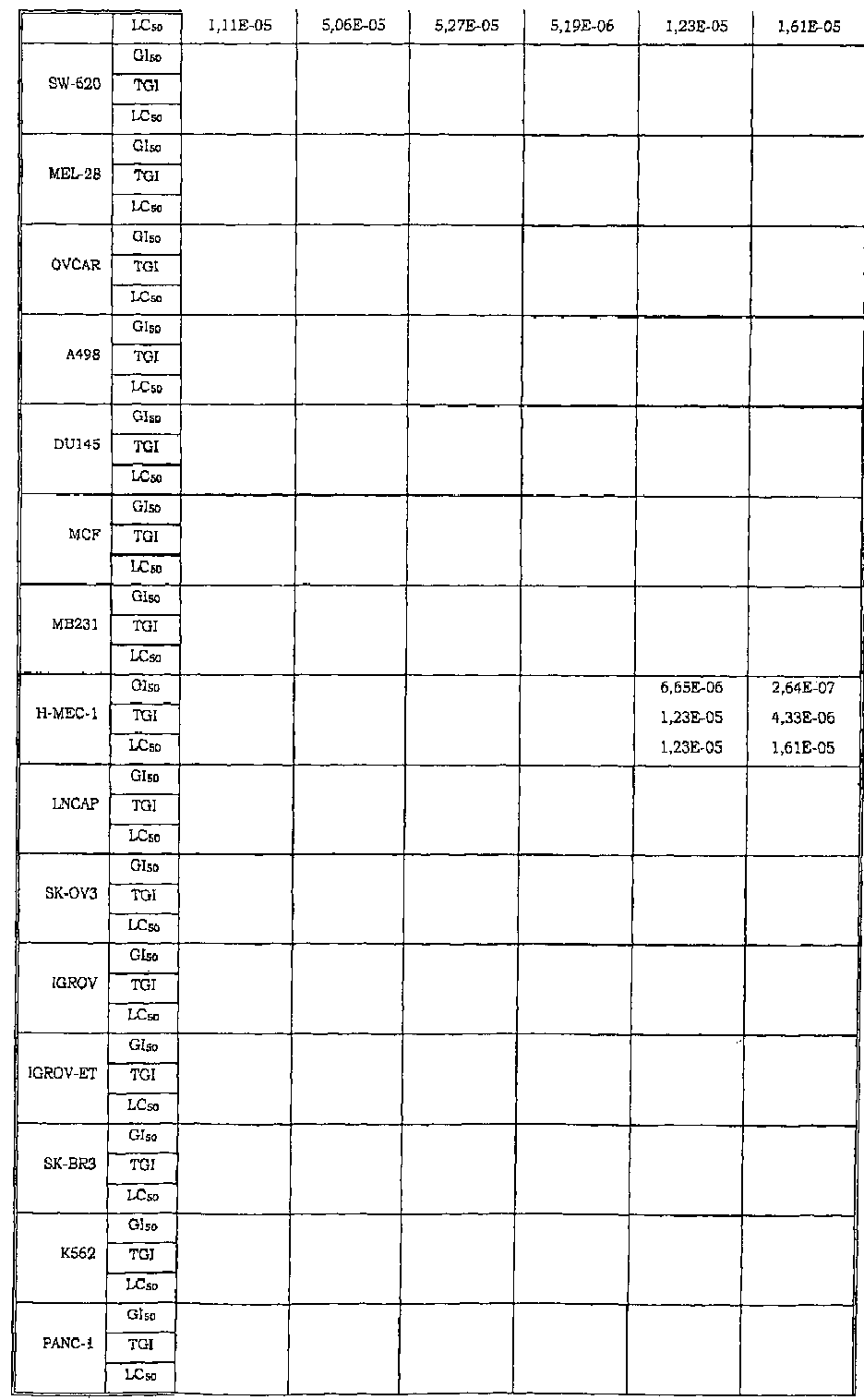
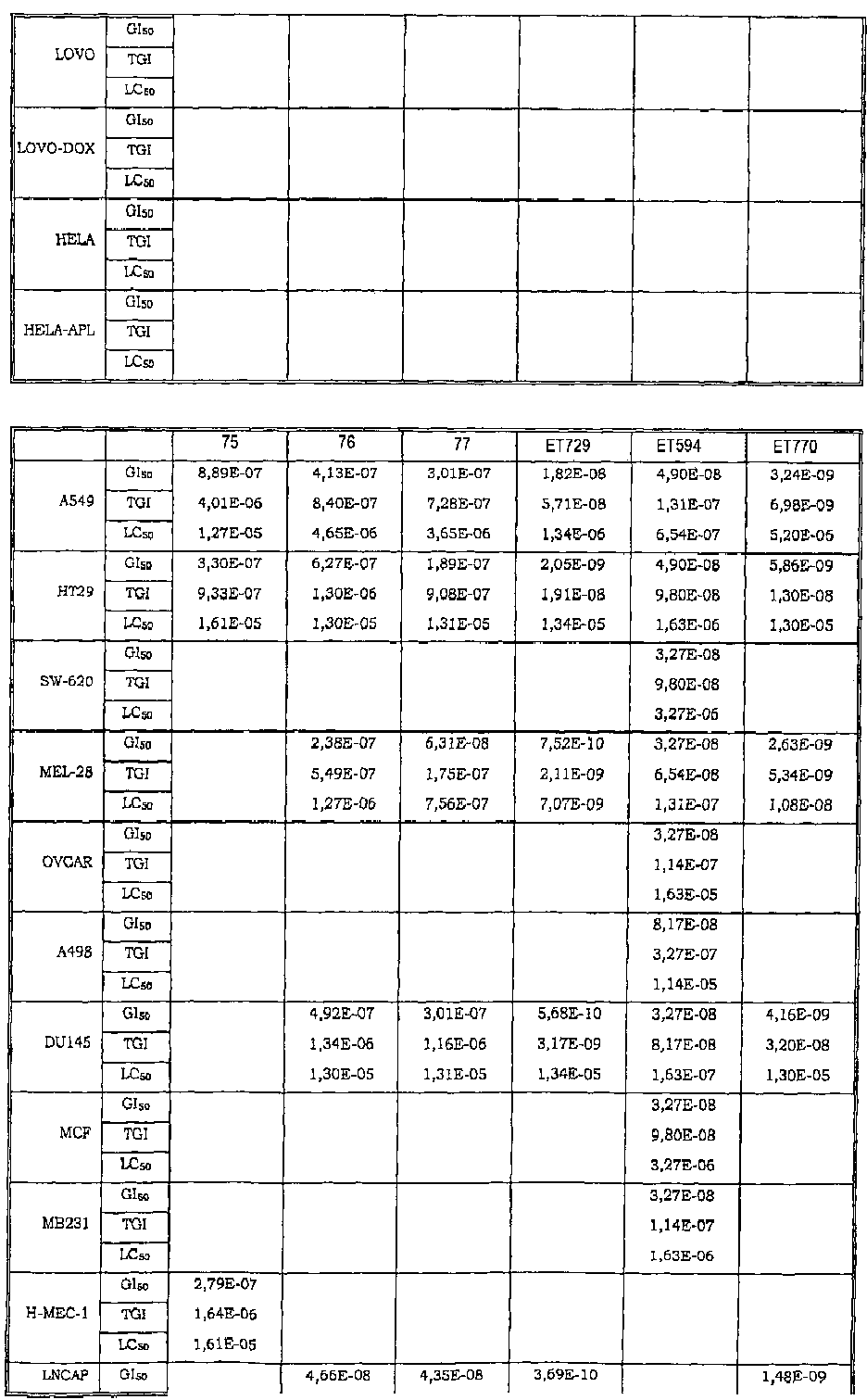

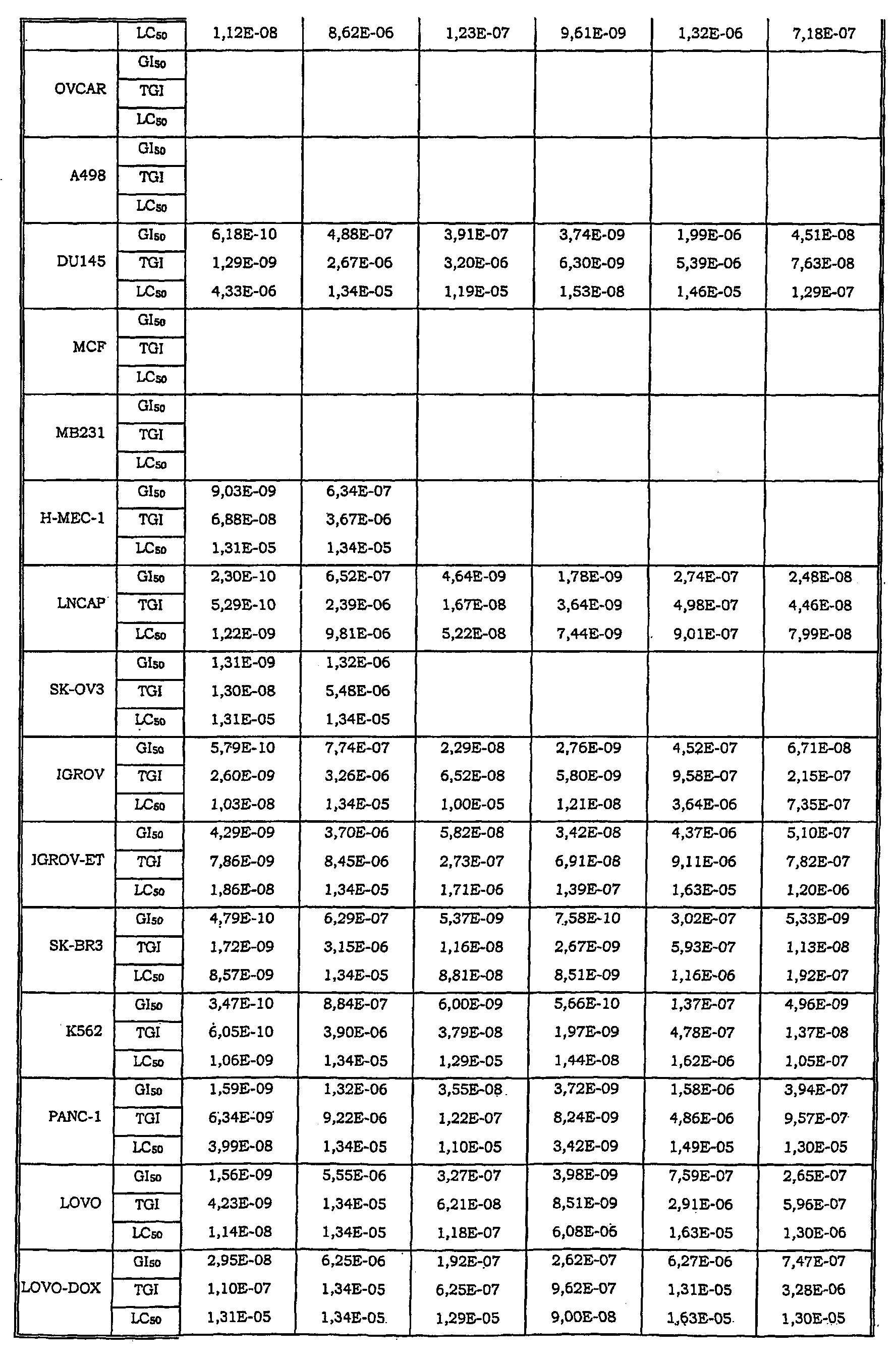

Реферат
Изобретение относится к новым производным эктеинасцидинов, имеющим хиноновую группу в кольце Е, формулы
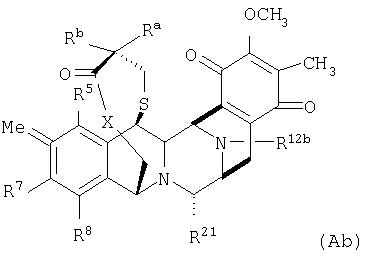
где Ra и Rb вместе с углеродом, к которому они присоединены, образуют группу:
-С(=O)-; -CH(OX1) или -CHN(X1X2), где каждый X1 и Х2 обозначает независимо Н, С1-18алкил, С2-18алкенил или С2-18алкинил или -C(=O)R', где R' независимо выбрана из группы, состоящей из Н, C1-C6алкила, С2-6алкинила, С2-6алкенила, гетероциклила, содержащего один или два гетероатома O; группу формулы:

где Rd и X1 выбраны из водорода или С1-12алкила или алкокси, С2-12алкенила, С2-12алкинила, С6-18арила; Х представляет -NH- или -О-; R5 обозначает -OX1 группу, где X1обозначает Н или -C(=O)R', где R' независимо выбрана из группы, состоящей из C1-С6алкила, С2-6алкинила, С2-6алкенила; R7 и R8 вместе образуют группу -O-СН2-O-; R12bобозначает водород, С1-12алкил или С2-12алкенил; и R обозначает -Н, -ОН или -CN, а также фармацевтической композиции на их основе для лечения рака и их применению для приготовления лекарственных средств для лечения рака. 3 н. и 13 з.п. ф-лы, 2 табл.
Формула
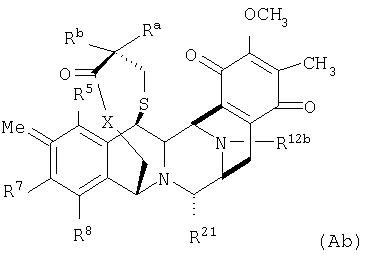
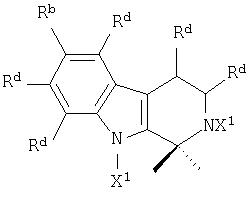
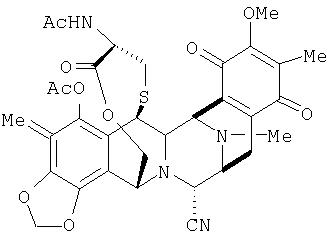
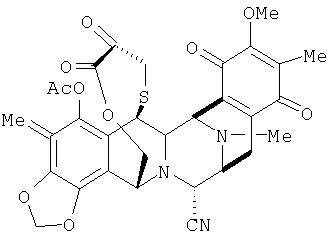

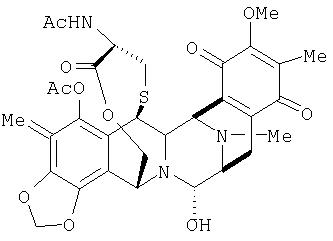
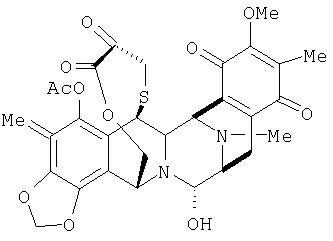
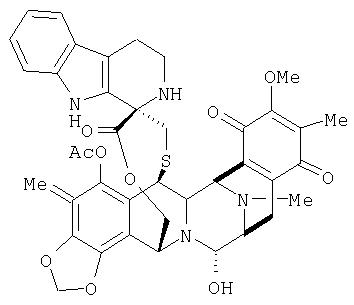

Комментарии