Способ получения 0-дезащетил-7-n-ациламиноцефалоспорановых кислот или их солей - SU406363A3
Код документа: SU406363A3
Описание
СПОСОБ ПОЛУЧЕНИЯ O-ДEЗAЦETИЛ-7-N-AЦИЛAMИHOЦЕФАЛОСПОРАНОВЫХ КИСЛОТ ИЛИ ИХ СОЛЕЙ
Изобретение относится к способу получения новых производных ациламиноцефалоспорановой кислоты, которые превосходят по своим свойствам известные аналоги, применяемые в фармацевтической промышленности.
Основанный на известной реакции ацилирования оксисоед.и«ений карбоновыми кислотами или их реаюционноспособным.и производными предлагаемый способ получения О-дезацетил-7-Ы-ацила .миНоцвфалоспорановых кислот или их солей общей формулы
CH-iOCO-NH
соон ol где RI - ацильный остаток циклически замещенной низшей алкаикар боновой кислоты, содержащей аминогруппу, связанную с атомом углерода алифатической цепи;
R2 - водород, незамещенный или замещен«ый на один или несколько атомов галоида низший а л кил;
п - О .или 1,
заключается в том, что цефалоспорин общей формулы
2
jf-N J-СН-гОСОСНъ
о СООН
где Rl - Rb в котором свободная аминогруппа защищена отщепляемой защитной группой, или его соль дезацетилируют известным способом и полученное соединение общей формулы
YN
RiH«-к ..он
о
где Rl имеет вышеуказанные значения, или его соль обраоатывают изоцианатом общей формулы
и
0п
где Ra и п - как указано выше, с последующим отщеплением защитной группы известными приемами. Продукты выделяют в свободном виде или в виде солл известным способом . При необходимости получеиную смесь .изомеров разделяют на отдельные изомеры.
Циклически замещенной низшей алканка-рбоновой кислотой является, например, соответственно замещенная .муравьиная, пропионовая , масляная, .изомасляная, валериановая , изовалериановая, метилэтилуксусная, триметилуксусная или капроиовая .кислота, предпочтительно уксусная кислота.
Циклический заместитель низшей алканкарбоно .вой кислоты может -быть (Насыщенным или ненасыщенным, циклоалифатическ:им .или ароматическим и может содержать гетероатомы , такие, .как сера, кислород или азот.
Циклические заместител.и -представл-яют собой замещенные ц.икл.оалифатические остатки, содержащие 3-8, лучще 5 или 6 атомов углерода в цикле, напр.им€р циклопропил, цнклобутил , циклопентил, циклогексил, циклогептил , циклооктил, 1-, 2- или 3-(циклолентил, 1-, 2- или 3-циклогексенил, 1- 2-, 3- или 4-циклогептенил .
Из циклических аро.матичебких заместителей можно назвать фенил, тт.ир.идил, тиенил или фурил.
Циклические остатки могут быть замещены на .Н.ИЗШ.ИЙ алкил, такой, как метил, этил, н-прОПил, изопропил, н-бутил, грег-бутил, низшую алкоксигрутюу, такую, как .метокси, этокс-и , w-нронилокси, изопропилокси, галоид, например фтор, хлор, бром, трифтометил и нитрогруппу . Аминогруппа может находиться как в остатке низшей алкан,карбоно-вой кислоты , так и в циклическом циклоалифатическом заместителе.
Остаток R2 представляет собой незамещенный или замещенный на галолд низший алкил , в котором за.меститель находится предпочтительно в р- или -положении.
Для защ.иты аминогруппу обычно ацили ру .ют, например сложным полуэфиром угольной кислоты, ацилыный остаток кото(рого можно отщеплять .в кислой среде, например при обработке сильной органической карбоиовой кислотой, такой, как галоидалканкарбоновая кислота, в первую очередь трифто.руксусной кислотой. Ац.ильные остатки, например карбалкоксиостатки , в которых низший алкил содержит в «-положении алифатические или циклические заместители ароматического характера , такие, как фенил, бифенилил (4-:бифенилил ), ИЛ.И гетероциклические группы ароматического характера, например 2-фурил, в частности карбо-грег-бутилокси-, карбо-третчентилокси- , карбодифенилметокси-, карбо-2 (4-бифен-ллил) -2-пропилокси-, карбо-1,1 -дифеКИЛЭТОКСИ- , карбо-2-фурфурилокси- или карбоциклоал1ко1ксиостатки , В которых циклоалкил представляет собой предпочтительно полициклический циклоалкил, в частности карбоадамантилоксиостаток. Ацильные остатки сложных полуефиров угольной кислоты у1ожно отщеплять при восстановлении водородом в пр.исутствии никелевых или палладиевых катализаторов .или водородом в момент выделения , который образуется при обработке металлов, например цинка, их сплавов, амальга ,м или солей кислотой, в частности низшей алка.нкарбоновой кислотой, в нер.вую очередь уксусной кислотой, или спиртом, таким, как низший алканол, в кот-оро.м низший алкил замещен в а-положени.и арО.матически.ми группами , в частности фенильными остатками, или в у -лоложен.ии атомами галоида, в частности
.хлара, и представляет собой кар1бо-2,2,2-трихлорэтокси- , карбо-2-йо.дэт.окси- или карбобензилокси- остаток. Карбо- низшую алко.ксигруппу , в которой низший алкил содержит в к-положении низщую алкоксигруппу, например .метоксифенил, в первую очередь ж-метоксифенил , предпочтительно 3,5-диметоксифенил , можно отщеплять фотолитическим путем, ванример при освещении УФ-лучами.
Защитными группами могут быть полиарилметильные группы, в которых арил - замещенный фенил, в ча.стности тритил.
Такие группы .можно отщеплять обычным , например при обработке сильной неорганической кислотой, напр.имер соляной, или
органической кислотой, например муравьиной или уксусной.
При восстановлении водародом с гарисутсивии катализато1ра или (в 1момвнт выделения можно переводить авидо- и нитрогру п1пы в
свободную аминогруппу и этерицифровамные карбоксигруппы в свободную карбоксильную тр.уипу.
Предлагаемые соединения -могут быть выделены в виде соли щелоч1Н.ого металла, напр .имер натрия или калия, щелочноземельнбго металла, например магния или кальция, соли аммония, включая аммониевые соли с органическими оснОВани.ям,и такими, как триметиламин , триэтиламин, 1-метилпи.рролидин, 1-этилпиперидин , ди.бензилэтилвндиамин или про., «айн. Их можно получать, например, обработкой свободных оснований или внутренних солей основными сое:динвн.иями, в данном случае с по.мощью ионоо5мвН1НИ|КОв.
Кислотно-аддитивные соли образуются при обработке оснований .неорганическими кислота .ми, такими, как соляная, бромистоводородная или серная, или органическими кислотами , такими, как .метансульфоновая, 2-оксиэтансуль1фоновая , л-толуолсульфонновая, трифторуксусная . Внутренние соли образуются при обработке кислотно-аддитивных солей слабоо сновньгм .ионнооб.менником, при титровании основания до изоэлектрической точки или обработке кислотой соли с основанием. Получаемые смеси изо.меров можно разделить известным cnocoi6QM на отдельные изомеры.
Предлагаемые соединения получают в присутствии или отсутствие разбавителей или
растворителей или их смесей, в присутств.ии конденсируюш,его агента и/.чли катализаторов, пр.и охлаждении или нагревании, в закрытом сосуде под давлением и/или в атмосфере инертного газа, например азота.
Для анализа веществ во всех примерах иопользуют томкослойку.ю хроматографию яа силикагеле (проявление з парах йода) в системе 1 - этила/цетат - пиридин - ледяная уксусная кислота - вода (62:21:6:11) -И системе 2 - н-бутанол - ледяная уксусная кислота - вода (67 : 10 : 23). Пример 1. КСуспензии 1 г (2 ммоль) 7-М-: К-карбо-трет-бутилокси -D-(-) -а-фенллгли .цил -аминоцефалоспорановой кислоты в 80 мл дистиллированной воды прибавляют 20 ял (2 ммоль) 0,1 н. едкого натра, к Болученно ,му раствору добавляют 0,05 г ацетилзстеразы из Bacillus АТСС 6633 и перемешивают 2 час при 37° С, поддерживая рН 7,3. Выделяющуюся при ферментативном расщеплении уксусную кислоту нейтрализуют ,20 мл 0,1 н. едкого «атра, ф|ильтруют раствор по окончании омыления через инфузорную землю , -подвергают фильтрат лиофильной сущке и получают натриевую соль О-дезацетил-7-N Ы-карбо-г/оет-бутилокси -D- (-) -а- фенилглицил -аминоцефалоспо;рановой кислоты. К раствору 2,27 г (4 ммоль), содержащего анетат натрия сырого лиофилизата натриевой соли О-дезацетил-7-М- М-карбо-трег-бутилокси-1 )-(-)-а-фенилгли1цил - аминоцефалоспорановой кислоты .в 20 мл абсолютного дегазированного диметилформамида, содержащего 5,6 мл (40 ммоль) абсолютного триэтиламина, прибавляют 3,36 мл (40 ммоль) р-хлорэтилизоцианата , взбалтывают 30 мин при 25° С, выпаривают в высоком вакууме досуха и .дигерируют остаток 3 раза, употребляя по 100 мл простого эфира. Остаток, не растворивщийся в простом эфире, обрабатывают 50 мл 10%-ного водного фосфатного буфера (рН 6,7), прибавляют зтилацетат, доводя рН до 2,5, и экстрагируют 3X200 мл этила/цетата. Органические экстракты промывают водой и насыщенным водным раствором поваренной соли, сущат над сульфатом натрия и выпаривают в вакууме. Остаток хроматографируют на 30-к,ратно.м количество - силикагеля (размер зерен 0,05-.0,2 мм), элюируя смесью бензол- этилацетат (6:4), ,и получают чистую 0-дезацетил-О- (N-p-хлорэтилкарбамоил) -7-N N-карбо-грет-бутилокси -D-(-)-а- фенилглицил -аминоцефалоспорановую кислоту. При 5° С и хороще.м перемещивании растворяют 0,57 г (1 ммоль) О-дезацетил-О-(М-рхлорэтилкарбамоил )-7-.Ы- Ы-карбо -трет- бутилокси-О- (-)-сс-фенилглицил - аминоцефалоспорановой кислоты в 1,91 мл (25 ммоль) трифторуксусной кислоты, но окончании выделения газа (3 мин) выливаьот на 30 мл охлажденного простого эфира и отделяют центрифугированием объемистый а-морфный осадок, который промывают 4 раза свежи.м простым эфиром и сущат в высоком вакууме Получают трифтор ацетат О-деза цетил-О-(Нр-хло ,рэтилкарбамоил)-7-Ы )-а- фенил глйцил - аминоцефалоспорановой кислоты R/, 0,08; Яг2 0,24. Раствор 0,1 г (0,173 ммоль) полученного трифторацетата в 0,4 мл (0,2 ммоль) 0,5 н. со яной КИСЛОТЫ промывают 3X1 мл этилацетаа , промывают оргаявчеакие ;раст1воры 1 мл оды и выбрасывают их. К объединенным одным растворам добавляют 2 н. водный аствор карбоната «атрия до ,рН 4,6 (изоэлекрическая точка), отфильтровывают осадок, рОМывают его очень небольщим количеством оды и получают О-дезадетил-0-(Ы-|3-хлортилкарбамоил ) -7-N- D(-)-а- фенилглицил миноцефалоспо .рановую .кислоту в Виде внутренней соли. R/i 0,08; R/2 0,24. УФ-снектр (0,1 н. водный раствор бикароната натрия): макс. 258 ммк (е 8050). ИК-спектр (вазелиновое масло), мк: 3,13; 5,62; 5,69; 5,85; 5,91; 6,20; 6,45; 6,60; 7,40; 7,78; ,98; 8,42; 8,78; 9,35; 9,67; 10,30; 12,27; 12,97 14,43. Пример 2. К раствору 113 г (2Q млюль) содержащего ацетат натрия сырого лиофилизата натриевой соли О-дезацетил-7-Ы- Ы-карбо -трет- бутилокси -D-(-)-а- фенилглицил амииоцефалоспорановой кислоты в 200 мл абсолютного дегазированного диметилформамида , содержащего 28 мл (200 ммоль) абсолютного триэтиламина, прибавляют 11,8 мл (200 ммоль) метилизоцианата, взбалтывают 30 мин при 25° С, выпаривают раствор в высоком вакууме досуха, добавляют к остатку 600 М.Л 10%-ного водного фосфатного буфера (рН 6,7), прибавляют этилацетат, доводя рЫ до 2,5, и экстрагируют (3X300 мл этилацетата . Органические экстракты промывают водой и насыщенным водным раствором поваренной соли, сушат над сульфато м натрия и выпаривают в вакууме. Остаток хроматографируют на 30-кратном количестве силикагеля (размер зерен 0,05-0,2 мм), элюируя смесью бензол-этилацетат (1:1), и получают чистую 0-дезацетил-О- (N-мeтилKalpбalмoил)-7-NМ-карбо-грег-бутилокси -D-(-)-«- фенилглицил -аминО|Цефалоспораиовую кислоту, R/i 0,50; R;2 0,50. При 5° С и хорошем перемешивании растворяют 0,50 г 0-дeзaцeтал-O-(N-мeтилкapбaмоил )-7-Ы- М-карбо-г/;ег - бутилокси -D-(-)а-фенилглицил -амино цефалоспорановой кислоты в 2,0 мл трифторуксусной кислоты, по окончании выделения газа ( мин) выливают на 30 мл охлажденного простого эфира и отделяют объемистый аморфный осадок центрифугированием, промывают 4 раза свежим .простым эфиром ;н сущат в высоком вакууме . Получают трифторацетат О-деза-.-т:.-O- (N - метилкарбамоил)-7-К- -(-)-сх-фенилглицил - а.миноцефалоспорановой кислоты, R/1 0,05; R/20,13. 1,66 г (3,1 ммоль) трифтор ацетата 0-дезацетил-О- (N - метилкарбамоил) - (-)а-фенилглицил -аминоцефалосно .рановой кислоты растворяют в 40 мл метанола и 40 мл воды, добавляют 0,1 н. 50%-ный .метанольный раствор едкого натра до рН 4,5, прибавляют этанол и выпаривают досуха. Остаток дигерируют 10 раз, употребляя но 5 мл спирта, растворяют в 40 мл метанола и 40 мл воды я
7
Обрабатывают 400.. мг ло,рита SX LF. После фильтрадии через «гйфло, удаления метанола в высоком вакууме я лиофильной сушки водного раствора О-дезацетил-О-,(Н-метилкарбам ,оил)-7-М-11)-(-)-а-|фен:илглнцил - аминоцефалоспорановую кислоту в виде внутренней соли, R/1 0,,05; 0,13.
УФ-спектр (вода): Я.,,,, 26Q лшк (7900).
ИК-снектр (вазелиновое масло), мк:3,08, 5,65, 5,91, 6,24, 6,42, 7,93, -8,85, 9,36, 9,72, 10,33, Г2,26.
Пример 3. К раст.во,ру 19,8 г (35 ммоль) содержащего ацетат натрия сырого лиофилизата .натриевой сол.и 0-дeзa:цeтил-7-N- N-кapбoТуОег-бутилокси-D (-)-сс-феНИЛГлицил - аминОЦефалоспорановой кислоты в 300 мл абсолютного дегазированного диметилфор.мамида, содержащего 49 лл (350 ммоль) абсолютного триэтиламина, прибавляют 27,7 ,ил (350 ммоль) этилизоцианата, взбалтывают 30 шн при 25°С, выпаривают в высоком вакууме досуха, добавляют к остатку 600 мл 10%-ного водного фосфатного буфера (рН 6,7), прибавляют этилацетат , доводят рН до 2,5 и экстрагируют 3X300 мл этилацетата. Объедииенные органические экстракты промывают водой и насыщенным водным раствором поваренной соли, сушат над сульфатом натрия и выпаривают в вакууме. Остаток хроматографируют на 30кратно м количестве силикагеля (размер зерен 0,05-0,2 мм), элюируя смесью бензол-этилацетат (6:4), и получают чистую 0-дезацетил0- (К-:Этилкарбамоил) - 7-N - N-Kap6o-r/7er-6yтилокси - D- (-) -сс-фенилглицил - аминоцефалоспорановую кислоту, R/ ,0,55; R/2 0,52.
При 5°С и перемешивании растворяют 0,50 г О-дезацетил-0-(М-этилкарбамоил)-7-М М-;карбо-г/7е7--бутилокси-/ - (-) - сс-фенилглицил -аминоцефалоапорановой .кислоты в 2,0 .ил трифторуксусной кислоты, по окончании выделения газа (3 мин) выливают на 30 лгл охлажденного простого эфира и отделяют объемистый а.морфный осадок центрифугированием, промывают его 4 раза свежим простым эфиром и сушат в высоком вакууме. Получают трифторацетат О - дезацетил-О - (N-этилкарбомoил-7-N-Z )-(-)-а-фенилглицил - аминоцефалоснорановой кислоты, R/, 0,07; R/2 0,18.
3,10 г (5,6 ммоль) полученного трифторацетата растворяют в 80 лы метанола и 80 мл воды, добавляют 0,1 н. 50%-ный метанольный раствор едкого натра до рН 4,3, удаляют метанол в высоком вакууме и проводят лиофильную сушку. Остаток дигерируют 4 раза, используя 30 мл этилацетата, и 8 раз, употребляя 15 мл спирта, добавляют 30 мл -метанола и 30 мл воды и обрабатывают 400 ме норита SX LF. После фильтрования через «гифло, удаления метанола и лиофильной сушки получают О - дезацетил-О- (N-этилкарбамоил) (-) -сс-фенилглицил - аминоцефалоспорановую кислоту в виде внутренней соли. R/, 0,07; R/2 0,18.
УФ-спектр ( вода) :Амакс 261 ммк (27800).
ИК-спектр (вазелиновое масло), мк: 3,10;
8
5,63; 5,90; 6,23; 7,98; 9,00; 9,,32; 9,68; 12,25 и 14,4.
При .м е р 4. iK раствору 11,3 г (20 ммоль) содержащего ацетат натрия сырого лиофилизата натриевой соли О-дезацетил-7-Ы- М-карбо-трег-бутилокси - D-(-) - а - фенилглицил аминоцефалоспорановой кислоты в 200 мл абсолютного дегазированного диметилформамида , содержащего 28 мл (200 ммоль) абсолютного триэтиламина, прибавляют 15,6 мл (200 ммоль) ацетилизоцианата, взбалтывают 30 мин при 25° С, выпаривают в высоком вакууме досуха, обрабатывают остаток 600 мл 10%-ного водного фосфатного буфера (рН
6,7), прибавляют этилацетат, доводя рН до 2,5, и экстрагируют 3X300 мл этилацетата.
Объединенные экстракты промывают водой и (Насыщенным водным растворо.м поваренной соли, сушат над сульфатО.м натрия и
выпаривают в вакууме. Остаток хро матографируют иа 30-кратном количестве силикагеля (размер зерен 0,05-0,2 мм), элюируя смесью бензол-этилацетат (1 : 1), и получают чистую О-деза1цетил-О-(Ы-ацетилкарбамоил) - 7-N-JNкарбо-г/рег-бутилокси- )-(-)-а-фенилглицил аминощефалоснорановую кислоту.
При 5° С и перемешивании растворяют О,-50 г О-дезацетил-О-(М-ацетилкарбамоил)-7К- М-карбо-:г/5ег-бутилокси- - (-)-а-фенилглицил -аминоцефалоспорановой кислоты в 2,0 мл трифторуисусной кислоты, по окоячании выделения газа (--3 мин) выливают на 30 мл охл-ажденного простого эфира и отделяют объемистый аморфный осадок центрифугированием , промывают 4 раза свежим простым эфиром и сушат в высоком вакууме. Получают трнфторацетат 0-дезацетил-Ь-(М-ацетилкарбачМОИл )-7-КТ - (-)-а-фенилглицил аминоцефалоспорановой кислоты.
1,5 г полученного трифторацетата растворяют в 40 мл .метанола и 40 мл воды, добавляют 0,1 н. 50%-иый метанольный раствор едкого натра до рН 4,5, прибавляют этанол и выпаривают досуха. Остаток растирают 10 раз
с 5 мл снирта, обрабатывают 40 мл .метанола ч 40 мл воды, затем 400 мг норита SX-LF, фильтруют через «гифло, удаляют метанол в высоком вакууме и подвергают водный раствор лиофильной сушке. 0-дезацетил-0-(Мацетилкарбамоил )-7-Ы- Э-(-) - фенилглицил аминоцефалоспорановую кислоту получают в виде внутренней соли.
Предмет изобретения
Способ получения 0-дезацетил-7-М-а,циламиноцефалоспорановых кислот или их солей обпдей формулы
R,
j N CH OCONH/С -Б-i
II 0/га
О
соон
где RI - ацилвный остаток циклически замещенной низшей алканкарбоновой кислоты, содержащей аминогруппу, связанную с атомом углерода алифатической цеаи;
R2-водород, низш-ий алкил, незамещенный .или замещенный на .один или несколько .атомов галолда;
п - О или 1,
отличающийся тем, что цефалоспорин общей формулы
R;HN
N х СН ОСОСНь
}
соон
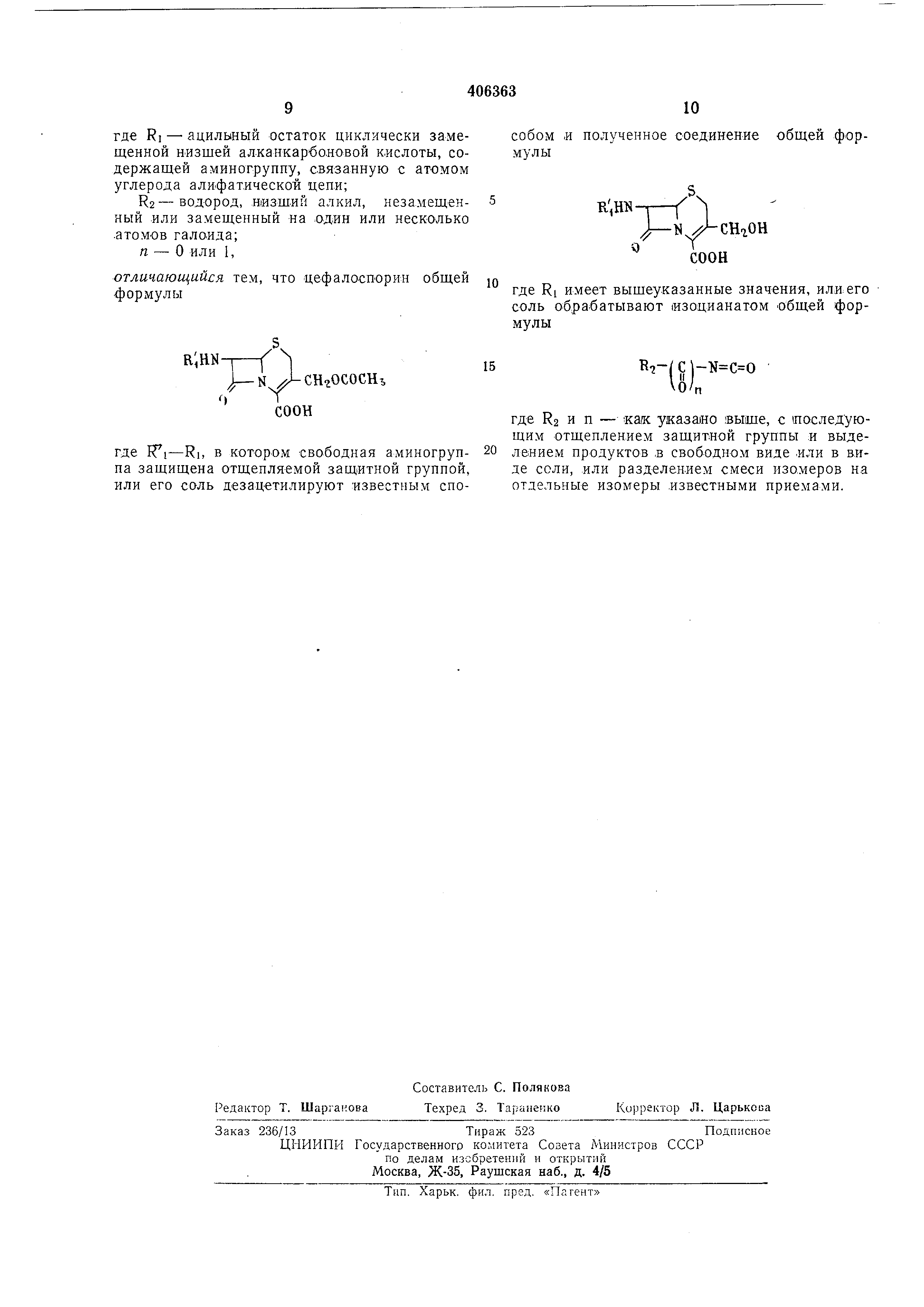
где Rl-Ri, в котором свободная аминогруппа защищена отщепляемой защитной группой, или его соль дезацетилируют известным способом и полученное соединение общей формулы
Т1,да
соон
где RI имеет вышеу.казанные значения, или его соль обрабатывают изоцианатом общей формулы
15
где R2 и п - как указано выше, с (последующим отщеплен.ием защитной группы .и выделением продуктов .в свободном виде или в в.иде соли, .или разделением смеси изо.меров на отдельные изомеры .известными приемами.




Реферат

Формула


Комментарии