Способ, средство, тест-система для колориметрического определения аналита и нитрозоанилиновые соединения - RU2114914C1
Код документа: RU2114914C1
Чертежи







Описание
Изобретение относится к способу колориметрического определения аналита посредством ферментативного окисления с помощью PQQ-зависимой дегидрогеназы (PQQ - пирролохинолинхинон) в присутствии акцептора электронов из группы обогащенных электронами ароматических нитрозосоединений и определения восстановленного акцептора электронов за счет появления окраски как меры количества аналита. Далее, изобретение относится к средству для колориметрического определения аналита путем ферментативного окисления, содержащему PQQ-зависимую дегидрогеназу, обогащенное электронами ароматическое нитрозосоединение, а также цветообразующий неокислительный индикатор для иминосоединения, образующегося из обогащенного электронами, ароматического нитрозосоединения при восстановлении. Далее, изобретение относится к новым нитрозоанилиновым соединениям, их получению, а также к их применению для колориметрического определения аналита.
Ферментативное окисление в аналитике делает возможным обнаружение и определение веществ в самых различных испытуемых материалах. При этом окисляющий фермент в присутствии принимающего электроны реакции окисления акцептора воздействует на соответствующий ферментативный субстрат. Восстановление акцептора электронов указывает на наличие ферментативного субстрата. При этом до сих пор как особенно предпочтительное оказывалось, что восстановленный акцептор электронов можно обнаруживать за счет образования окраски, так как это возможно не только при необходимости использования дорогостоящих измерительных приборов, но и в случае необходимости можно осуществлять также визуально.
В известных методах колориметрического определения веществ посредством окисляюще действующих ферментов применяют оксидазы или дегидрогеназы. Обе группы ферментов относятся к основной группе оксидоредуктаз (Römpps Chemielexikon, Francksche Verlagsbuchhandlund, Штутгард, 8-е изд., 1985, т.4, с. 2952; Lexikon Biochemie, Herausgeber H.D. Jakubke, Verlag Chemie, Вайнхайм, 2-е изд. , 1981, с.194), члены которой могут различаться своими природными акцепторами электронов.
Природным акцептором электронов для оксидов является молекулярный кислород (Römpps Chemielexikon, Francksche Verlagsbuchhandlung, Штутгард, 8-е изд., 1985, т.4, с.2946). В случае определений аналитов при этом аналит окисляется оксидазой и O2. Образующийся пероксид водорода с помощью пероксидазы используется для окисления лейкокрасителя. Об уровне техники в отношении использования оксидаз для колориметрического определения аналитов следует цитировать A. Kunst и др. в "Methods of enzymatic analysis", Hrsg.H.U.Bergmeyer, Verlag Chemie, Вайнхайм, 3-е изд., 1984, т.6, с.178-185. Там определяют глюкозу в сыворотке, плазме или депротеинизированной крови путем введения во взаимодействие с глюкозооксидазой и кислородом воздуха тем, что образующийся при этой реакции за счет восстановления кислорода пероксид водорода восстанавливается в присутствии пероксидазы и тем самым вызывает окрашивание также имеющегося в реакционной смеси фенола и 4-аминофеназона. Высокий редокспотенциал (окислительно-восстановительный потенциал) перекиси водорода и неселективность и нестабильность пероксидазы чаще всего приводят к ограничениям такого теста. Мешающе действуют, например, ионы переходных металлов или гем или гемопротеины, которые легко могут попадать в получаемые из крови пробы, так как они разлагают перекись водорода. Ингредиенты проб, как например билирубин, или также медикаменты, как например метилдиоксифенилаланин, которые встречаются в получаемых из крови пробах или в моче, могут приводить к окрашиванию с перекисью водорода и пероксидазой, и, таким образом, к ошибочным результатам, однако также они могут снова восстанавливать уже образовавшийся краситель и таким образом обесцвечивать.
В особенности при осуществлении вышеуказанных методов определения на твердых носителях, в так называемом сухом тесте, дополнительно потребность в кислороде оксидаз оказалась отрицательно сказывающейся. Прежде всего тогда, когда требуется много кислорода для окисления высоких концентраций ферментативного субстрата, диффузия кислорода из воздуха в реакционную среду может становиться определяющей скорость стадией и приводить к длительным реакционным временам или в особенности при кинетических методах определения - к ошибочным результатам.
Дегидрогеназы в общем можно подразделять на такие, которые необходимы для окисления ферментативных субстратов никотинамид-аденин-динуклеотид (NAD) или никотинамид-аденин-динуклеотид-фосфат (NADP) в качестве прямых природных акцепторов электронов, и на такие, которые независимы от NAD или NADP и которые также используют другие вещества, чем природные прямые акцепторы электронов, при ферментативных реакциях окисления. Под группу независимых от NAD или NADP дегидрогеназ подпадают в особенности PQQ- и флавин-зависимые дегидрогеназы.
Использование NAD-зависимых дегидрогеназ для колориметрических измерений известно, например, из патента ФРГ А-2147466. Там описывается, что лактат при катализе лактатдегидрогеназой с никотинамин-аденин-динуклеотидом превращается в пируват и восстановленный никотинамид-аденин-динуклеотид. Образовавшийся NADH реагирует затем, например в присутствии фермента диафоразы, с солями тетразолия при образовании NAD и окрашенных формазанов, концентрацию которых можно определять фотометрически. Вместо диафоразы также можно назвать N-метилфеназиний-метосульфат в качестве катализатора восстановления для переноса электронов от NADH к соли тетразолия.
Недостатки этого способа следует видеть в том, что вместо NADH также другие, возможно присутствующие в биологических пробах, как например кровь, сыворотка, плазма или моча, восстанавливающе действующие вещества, как глутатион, или медикаменты, как метилдиоксифенилаланин или добезилат, в присутствии неспецифических катализаторов восстановления, как диафораза или N-метилфеназиний-метосульфат, переводят соли тетразолия в соответствующие формазаны и таким образом приводят к ошибочным положительным результатам, хотя они не так быстро реагируют с солями тетразолия в отсутствие катализаторов восстановления.
Из европейского патента EP-A-0354441 известно окислительное, ферментативное обнаружение аналитов посредством флавин-зависимых оксидаз или NAD-независимых дегидрогеназ, как PQQ-зависимые дегидрогеназы, с помощью обогащенных электронами, ароматических нитрозосоединений. В случае этих методов обнаружения, ароматическое нитрозосоединение ферментативно восстанавливается до соответствующего, обогащенного электронами, ароматического амина, который либо обнаруживается с помощью осаждающейся, труднорастворимой гетерополикислоты за счет образования гетерополи-синего, либо в присутствии окислителя вводится в реакцию сочетания с цветообразующим реагентом с образованием красителя. Сине-серые градации цвета при образовании гетерополи-синего, правда, мало пригодны для точной визуальной оценки. Для колориметрического обнаружения в общем неокрашенных или только очень слабо окрашенных ароматических аминов с помощью цветообразующего реагента отрицательным является то, что дополнительно требуется окислитель. Так как такой окислитель мешает ферментативному восстановлению ароматического нитрозосоединения до ароматического амина, то реакцию обнаружения нужно проводить в две отдельные стадии; в первой стадии ароматическое нитрозосоединение ферментативно восстанавливается до ароматического амина и в отдельной от нее второй стадии добавляется окислитель для окислительного сочетания ароматического амина с цветообразующим реагентом.
Другой недостаток этого способа обнаружения заключается в том, что для восстановления каждого эквивалента ароматического нитрозосоединения до ароматического амина нужно окислять два эквивалента аналита. Это в особенности в случае незначительных концентраций аналита может приводить к неудовлетворительной чувствительности такого способа обнаружения.
Поэтому задачей изобретения являлось устранение вышеуказанных недостатков уровня техники и разработка более простого, с меньшим количеством помех, чувствительного и визуально лучше оцениваемого способа и нахождения средства для окислительного обнаружения аналитов, который в особенности можно осуществлять в одну стадию и который дает во всей видимой области длин волн визуально хорошо оценниваемые окраски (цвета).
Задача решается благодаря изобретению, которое охарактеризовано в формуле изобретения.
Соответственно этому найден способ колориметрического определения аналита посредством ферментативного окисления аналита с помощью оксидоредуктазы в присутствии прямого акцептора электронов из группы обогащенных электронами ароматических нитрозосоединений, при котором определение восстановленного акцептора электронов осуществляют за счет появления окраски как меры количества аналита, отличающийся тем, что обогащенное электронами ароматическое нитрозосоединение при окислении аналита в присутствии PQQ-зависимой дегидрогеназы восстанавливается до иминосоединения и оно без дальнейшего ферментативного восстановления до ароматического амина обнаруживается за счет появления окраски.
Предметом изобретения, в частности, является способ колориметрического определения аналита с помощью оксидоредуктазы в присутствии прямого акцептора электронов из группы обогащенных электронами, ароматических нитрозосоединений, при котором определение восстановленного акцептора электронов осуществляют за счет появления окраски как меры количества аналита, который отличается тем, что обогащенное электронами ароматическое нитрозосоединение при окислении аналита в присутствии PQQ-зависимой дегидрогеназы восстанавливается до иминосоединения и оно, вместо ферментативного дальнейшего восстановления до ароматического амина, путем взаимодействия с неокислительным цветообразующим индикатором определяется колориметрически.
Кроме того, найдено средство для колориметрического определения аналита путем ферментативного окисления аналита, содержащее PQQ-зависимую дегидрогеназу и прямой акцептор электронов из группы обогащенных электронами, ароматических нитрозосоединений, которое отличается тем, что оно либо содержит обогащенное электронами ароматическое нитросоединение, которое при ферментативном восстановлении образует окрашенное иминосоединение, либо оно, далее, содержит неокислительный цветообразующий реагент (индикатор) для иминосоединения, образующегося из обогащенного электронами ароматического нитрозосоединения путем восстановления.
Согласно изобретению под термином "аналит" понимают такое вещество, которое ферментативно окисляется. Во многих случаях аналитом является такое вещество, которое нужно обнаружить прямо или определить количественно в исследуемой пробе. Например, глюкозу можно окислять прямо с помощью PQQ-зависимой глюкозодегидроредуктазы (глюкозо-краситель-оксидоредуктаза) и колориметрически определять. Однако также возможно, что аналит образуется лишь путем одной или нескольких предварительных реакций из другого вещества, так что путем колориметрического определения аналита косвенно можно делать вывод о концентрации исходного вещества.
Аналит в изобретении представляет собой такое вещество, которое акцептуется (признается) в качестве субстрата используемой PQQ-зависимой дегидрогеназы.
PQQ-зависимые дегидрогеназы содержат в качестве кофактора пирролхинолинхинон. Обзор таких "хинопротеинов" представлен J.A. Jongejahn и др. в "PQQ и хинопротеины", Kluver Academic Publ. Dordrecht, Нидерланды, 1989. Примерами используемых согласно изобретению ферментов являются PQQ-зависимая глюкозодегидрогеназа [глюкозо-краситель-оксидоредуктаза, Е.С. 1.1.1.50/1.1.1.91/1.1.1.97], спиртодегидрогеназа или лактат-дегидрогеназа. В предлагаемом в изобретении способе в особенности можно использовать PQQ-зависимую глюкозодегидрогеназу предпочтительно для колориметического определения глюкозы.
В качестве прямых акцепторов электронов, которые принимают электроны от системы фермент /система кофактор дегидрогеназа/ PQQ, используют обогащенные электронами ароматические нитрозосоединения, которые известны в качестве акцепторов электронов для оксидаз и NADH-независимых дегидрогеназ из европейского патента A-0-354441 и европейского патента EP-A-0441222 и в случае которых нитрозогруппа непосредственно связана с обогащенным электронами ароматическим ядром. Термин "прямые" акцепторы электронов означает, что электроны прямо катализируемые ферментами, без необходимости в катализаторе восстановления, принимаются системой фермент/ кофактор.
В смысле изобретения, используемые в качестве восстанавливаемых, обогащенных электронами ароматических нитрозосоединений соединения представляют собой таковые, которые принимают электроны, получающиеся при окислении соответствующего используемой PQQ-зависимой дегидрогеназе субстрата, от фермента и при этом образуют иминосоединения. Соответствующее иминосоединение содержит иминогруппу = NH, которая через свою двойную связь связана с первоначальным ароматическим ядром и сопряжена с его электронами двойной связи. Обогащенные электронами ароматические нитрозосоединения содержат один или несколько электронодонорных остатков или групп, на или в ароматическом ядре, которые благоприятствуют образованию иминосоединения тем, что они вступают в сопряжение с иминогруппой за счет отдачи электронов через первоначальное ароматическое ядро.
Это относится к заместителям, которые оказывают +M-эффект на ароматическое ядро. Например,
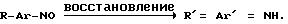
Примерами связанных с ароматическим ядром остатков R c +M-эффектом являются такие заместители, как гидроксильный, алкоксильный, арилокси-, алкилтио-, арилтио-, амино-, моноалкиламино-, моноариламино-, диалкиламино- и диариламиноостатки.
В случае производных нитрозобензола эти заместители, например, особенно проявляют свое действие тогда, когда они находятся в орто- и/или параположении к нитрозогруппе.
Группы с электронодонорным и благоприятствующим иминоструктуре эффектом также могут быть составной частью гетероароматической циклической системы.
Примерами являются гетероциклические ароматические нитрозосоединения с избытком π-электронов, в которых ароматическая циклическая система настолько обогащена электронами, что внешний +M-заместитель является лишним для образования стабилизированной за счет мезомерии иминогруппы после восстановления. Избыток π -электронов образуется вследствие того, что имеется больше ароматических π -электронов, чем дают атомы кольца, через которые могут распределяться π -электроны. Такого рода гетероциклы известны специалисту.
Примерами таких ароматических гетероциклов являются антипирин, пиразольные гетероциклы и пиразолы.
Избыток электронов, используемых согласно
изобретению, обогащенных электронами ароматических нитрозосоединений имеет дополнительный эффект, заключающийся в том, что эти нитрозосоединения в известной мере через кето-енольную таутомерию
находятся в равновесии с эквивалентной оксимной предельной структурой
R-Ar-N=O ←____→ R′= Ar′ = N-OH
Обе таутомерные
предельные структуры в рамках изобретения должны охватываться понятием "ароматические нитрозосоединения" в качестве используемых согласно изобретению веществ.
В случае вышеуказанных +M-заместителей имеются в виду алкоксильные, алкилтио-, моноалкиламино- и диалкиламиноостатки, в которых алкил представляет собой углеводородный остаток с 1-6 C-атомами, который, со своей стороны, может быть замещен гидроксильной группой, в случае необходимости замещенной одно- или многократно алкилом с 1-6 C-атомами аминогруппой, PO3H2, SO3H или CO2 H. Кислотные остатки PO3H2, SO3H и CO2H могут быть как таковые или находиться в солевой форме, как соли аммония, щелочных или щелочно-земельных металлов.
Арилокси- и арилтиоостатки содержат ароматические остатки с 6-10 C-атомами, причем особенно предпочтительны фенокси- и фенилтиоостатки.
Аммониевыми солями являются таковые, которые содержат ион аммония, или таковые, которые содержат катионы аммония, одно- или многократно замещенные алкильными, арильными или аралкильными остатками. Алкил в алкильных или арилкильных остатках, обозначает углеводородный остаток с 1-6 C-атомами. Арил в арильных и аралкильных остатках представляет собой с 6-10-ю C-атомами ароматическую циклическую систему, причем предпочтителен фенил. Предпочтительным аралкильным остатком является бензил.
Солями щелочных металлов предпочтительно являются соли лития, натрия или калия. Соли щелочно-земельных металлов предпочтительно представляют собой соли магния или кальция.
Вышеуказанные примеры +M-заместителей не нужно понимать как полный перечень. Специалисту в каждом отдельном случае известно, является ли данный остаток +M-заместителем и в каком месте он оказывает это действие на ароматическую систему, или какие ароматические гетероциклы в циклической системе содержат соответствующую группировку и насколько все эти остатки могут быть возможными заместителями в ароматических нитрозосоединениях, которые могут использоваться согласно настоящему изобретению.
Ароматическая основная структура используемого ароматического нитрозосоединения предпочтительно представляет собой обогащенное электронами ароматическое кольцо с 5-7, особенно предпочтительно с 5-6, атомами углерода или гетероатомами, которое может быть анеллировано с одним или двумя ароматическими и/или алициклическими кольцами. Для ароматических анеллированных колец при этом принимают во внимание как углеродные ароматические системы, так и также гетероароматические системы с количеством атомов углерода или гетероатомов по 5-7, предпочтительно 5-6.
Под алициклическими кольцами понимают насыщенные или ненасыщенные циклоалифатические соединения с 5-7 C-атомами или гетероатомами, предпочтительно с 5- или 6-ю атомами углерода. Под гетероатомами понимают азот, кислород или серу.
Предпочтительными, используемыми согласно изобретению нитрозосоединениями, являются производные нитрозобензола.
Под производными нитрозобензола понимают также нитрозобензол, который анеллирован с одним или несколькими ароматическими и/или алициклическими кольцами. В качестве ароматических колец при этом принимают во внимание как углеродные ароматические системы, так и также гетероароматические соединения с количеством в цикле по 5-7, предпочтительно 5 или 6. Примерами являются анеллированные бензольные или нафталиновые циклы или анеллированное пиридиновое кольцо.
Особенно предпочтительны нитрозобензольные производные общей формулы I
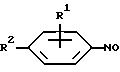
где R1 - водород, гидроксил; алкил, в случае необходимости замещенный гидроксилом, COOH, PO3H2, или SO3H; алкоксил, алкилтио, арилокси, арилтио, галоген, или аминогруппа, которая в случае необходимости одно- или многократно замещена алкилом, в случае необходимости замещенным гидроксилом, PO3H2, диалкилфосфинилом, SO3H или CO2H; и
R2 - гидроксильная группа, алкоксильная, арилокси-, арилтио- или алкилтиогруппа, причем алкильный остаток в случае необходимости со своей стороны замещен гидроксильной группой, алкоксильной группой, в случае необходимости одно- или многократно замещенной алкилом аминогруппой, PO3H2, SO3H или CO2H как таковыми или в солевой форме в виде солей аммония, щелочных или щелочно-земельных металлов, или аминогруппа NR3R4,
в которой R3 и R4 могут быть одинаковыми или разными и обозначают водород, арильную или алкильную группу, которая со своей стороны может быть замещена гидроксилом, алкоксилом, гидроксиалкоксилом, в случае необходимости замещенной гидроксилом полиалкоксильной группой, PO3H2, SO3H, COOH как таковыми или в солевой форме или в случае необходимости одно- или многократно замещенной алкилом аминогруппой; или
в которой R3 и R4 могут представлять собой алкиленовый остаток, который в случае необходимости прерывается кислородом, серой или азотом, причем азот замещен алкильным, гидроксиалкильным, гидроксиалкоксиалкильным, алкоксигидроксилалкильным, алкоксикарбонилалкильным, диоксанилилалкильным или полиалкоксиалкильным остатком, который, со своей стороны, смотря по обстоятельствам, в алкильной части может быть замещен гидроксильным остатком; или,
когда R1 находится в ортоположении к NR3R4, то R3 или R4 также вместе с R1 может представлять собой алкиленовый остаток.
При этом галоген обозначает фтор, хлор, бром или иод. Особенно предпочтительны фтор и хлор.
Алкил в алкильном, алкоксильном или алкилтиоостатке обозначает углеводородный остаток с 1-6 C-атомами, причем особенно предпочтительны остатки с 1-3 C-атомами. Вышеуказанное определение
для алкила также относится к алкильной части в гидроксиалкильном, диалкиламиноалкильном, гидроксиалкоксиалкильном, алкоксиалкильном, полиалкоксиалкильном, алкоксигидроксиалкильном и
диоксанилилалкильном остатках. Диоксанилильный остаток представляет собой остаток, в случае которого диоксановая циклическая система связана с алкильным остатком. Предпочтительно речь идет о 1,
4-диоксановой циклической системе

Полиалкоксиалкильным остатком является остаток -алкил-(алкокси)n-алкокси, в котором n = 1-10. Предпочтительно n = 1-4. Особенно предпочтительно n 1-3. Алкиленовый остаток представляет собой линейную или разветвленную, предпочтительно линейную, насыщенную или ненасыщенную, предпочтительно насыщенную, углеводородную цепь из 2-5, предпочтительно 2-4 C-атомов, с двумя свободными местами связывания.
Арил в арильном и аралкильном остатках представляет собой содержащую 6-10 C-атомов ароматическую циклическую систему, причем предпочтителен фенил.
Аммониевыми солями являются такие, которые содержат ион аммония NH , или такие, которые содержат катионы аммония, одно- или многократно замещенные алкильными, арильными или аралкильными остатками.
Солями щелочных металлов предпочтительно являются соли лития, натрия или калия. Солями щелочно-земельных металлов предпочтительно являются соли магния или кальция.
Предпочтительными остатками R1 являются водород и алкил, предпочтительно водород.
Предпочтительными остатками R2 являются алкоксильные остатки и аминогруппа NR3R4.
В значении образованного R1 и R3, прерываемого кислородом, серой или азотом алкиленового остатка предпочтителен образованный путем включения атома азота согласно общей формуле I морфолиновый, соответственно тиоморфолиновый, соответственно пиперазиновый остаток. Особенно предпочтителен пиперазиновый остаток.
В значении образованного R1 и R3 алкиленового остатка предпочтителен образованный путем включения ароматического кольца согласно общей формуле I индолиновый или 1,2,3,4-тетрагидрохинолиновый остаток.
Для получения соли предлагаемого согласно изобретению нитрозоанилинового производного общей формулы I предпочтительны в особенности такие сильные кислоты, в особенности неорганические кислоты, как соляная кислота, серная кислота, азотная кислота, фосфорная кислота. Особенно предпочтительны гидрохлориды, которые являются солями соляной кислоты.
Предпочтительными нитрозосоединениями общей формулы I являются: N,N'-бис-/2-гидроксиэтил/-n-нитрозоанилин, N, N'-диметил-n-нитрозоанилин, N, N'-диэтил-n-нитрзоанилин, N-метил-N'-/4-нитрозофенил/-пиперазин, N-/2-гидроксиэтил/5-нитрозоиндолин, 2,4-диметокси-нитрозобензол, N,N'-бис-/2-метоксиэтил/-4-нитрозоанилин, N-/4-нитрозофенил/-морфолин, N-/2,2-диэтокси-этил/-N'-/4-нитрозофенил/-пиперазин, n-нитрозофенол, 3-метокси-4-нитрозофенол.
Из обогащенных электронами гетероароматических нитрозосоединений, ароматическая
циклическая система которых настолько обогащена электронами, что излишним является внешний +M-заместитель для нитрозо-/оксимтаутомерии и для образования имина, в предлагаемом согласно изобретению
способе особенно пригодны замещенные нитрозогруппой пиразолоны, пиразолы и в особенности нитрозозамещенные пиразольные соединения, которые, например, описаны в Ullmann's Enzyclopedia of Industrial
Chemistry, 5-е изд., т. А 20, с. 72-74. При этом предпочтительны 3-нитрозопиразольные соединения общей формулы II

Эти соединения большей частью известны, в качестве предстадий для препаративного синтеза соответствующих 3-аминопиразольных соединений, из европейской патентной заявки EP-A-0433854.
В формуле II X-Y - NR5CO или N = CR6;
R5 - водород; алкил, в случае необходимости замещенный гидроксилом, карбоксилом,
SO3H, PO3H2, диалкилфосфинилом;
R6 - водород, алкил, алкенил, алкоксил, алкилтио, арил, арилтио, аралкил, в случае необходимости, смотря по
обстоятельствам, замещенный гидроксилом, карбоксилом, SO3H, PO3H2, солью одного из этих кислотных остатков и/или алкоксикарбонилом; или аминогруппа, которая в случае
необходимости замещена одним или двумя, содержащими в случае необходимости один или несколько гидроксильных, карбоксильных и/или алкоксикарбонильных остатков алкильными остатками, причем когда
аминогруппа замещена двумя алкильными остатками, то эти остатки также могут быть циклизованы до кольца, которое, кроме N-атома аминогруппы, в случае необходимости может прерываться также кислородом,
серой или другим атомом азота; или аминогруппа, которая в случае необходимости замещена одной или двумя ацильными группами, алкокси- и/или аралкоксикарбонильными группами, H2N-CO, алкил-,
аралкил- и/или арилкарбамоильными группами; или карбоксил, алкоксикарбонил, карбоксамидогруппа или галоген; и
R7 - алкил, тиоалкил или аралкил, в случае необходимости замещенный
гидроксилом, карбоксилом, SO3H или PO3H2, или аминогруппа, которая в случае необходимости замещена одной или двумя алкильными группами, которые со своей стороны опять
могут быть замещены гидроксилом, карбоксилом, SO3H, диалкилфосфинилом или PO3H2; причем по меньшей мере R6 и/или R7 представляет собой
аминогруппу; и
R8 - алкильная или аралкильная группа, которая в случае необходимости может быть замещена гидроксилом, карбоксилом, SO3H или PO3H2;
или
R7 и R8 вместе образуют насыщенную или ненасыщенную 3- или 4-членную цепь из атомов азота или атомов углерода и в случае необходимости одного или нескольких атомов
азота или серы, причем атомы углерода в случае необходимости замещены алкилом, алкоксилом, алкилтио, гидроксилом, аралкилом, арилом, карбоксилом, карбоксамидо, алкоксикарбонилом, цианогруппой,
галогеном, аминогруппой, которая в случае необходимости замещена одним или двумя, в случае необходимости содержащими один или несколько гидроксильных, карбоксильных и/или алкоксикарбонильных остатков,
алкильными остатками; и причем атомы азота, которые не связаны через двойную связь, замещены алкилом или аралкилом, в случае необходимости замещенным гидроксилом, SO3H, PO3H2, карбоксилом или диалкилфосфинилом; или два соседних заместителя цепи в случае необходимости образуют алкиленовую группу, которая со своей стороны в случае необходимости замещена арилом или
анеллирована с ним;
а также в случае необходимости соответствующие таутомерные формы и их соли.
При этом "алкил" - также в алкилтио-, диалкилфосфинильном, алкилкарбамоильном и аралкильном остатках - обозначает линейный или разветвленный алкильный остаток с 1-6, предпочтительно 1-4 C-атомами. Примерами являются метильная, этильная, пропильная, изобутильная или трет-бутильная группы.
Если аминогруппа замещена двумя алкильными остатками, то эти остатки также могут быть циклизованы в кольцо так, что в целом они представляют собой прерываемое атомом азота кольцо. При этом предпочтительны такие аминогруппы, которые представляют собой в целом 5- или 6-членное кольцо и которое со своей стороны в случае необходимости прерывается кислородом, серой или азотом. Особенно предпочтителен морфолиновый остаток.
"Алкокси" - также в алкокси- и аралкоксикарбонильных остатках - обозначает линейный или разветвленный алкоксильный остаток с 1-6, предпочтительно 1-4 C-атомами. Примерами являются метокси-, этокси-, пропилокси-, изо-бутилокси- или трет-бутилоксигруппы.
"Арил" - также в арилкарбамоильных группах - обозначает углеродный ароматический или гетероароматический остаток, предпочтительно таковой с 6-10 атомами в кольце, в особенности фенильную или нафтильную группу, которые дополнительно могут быть еще замещены алкилом, алкоксилом и/или галогеном. Особенно предпочтителен фенильный остаток.
"Аралкильный остаток" - также в аралкилкарбамоильной группе - обозначает остаток, в котором вышеуказанная алкильная группа замещена вышеохарактеризованным арильным остатком. Предпочтительна бензильная группа.
"Аралкоксильный" остаток, например в аралкоксикарбонильных группах, обозначает остаток, в котором вышеуказанная алкоксильная группа замещена вышеохарактеризованным арильным остатком. Предпочтительна бензилоксигруппа.
"Галоген" обозначает остатки: фтор,
хлор, бром и йод. Предпочтительны фтор и хлор,
"Ацильная группа" обозначает остаток карбоновой кислоты, который может содержать алкильные, аралкильные или арильные остатки. Предпочтительны
ацетильные, фенилацетильные или бензоильные остатки.
Под алкиленовой группой понимают линейную или разветвленную, насыщенную или ненасыщенную углеводородную цепь из 3-5, предпочтительно 3-х или 4-х C-атомов с двумя свободными местами связывания.
Примерами являются: -CH2-CH= CH-,
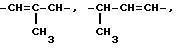
Предпочтительны бутадиендиильный остаток (-CH=CH-CH=CH-) и тетраметиленовый остаток [-(CH2 )4-].
Алкенильный остаток представляет собой линейный или разветвленный углеводородный остаток из 2-5 C-атомов по меньшей мере с одной двойной связью. Предпочтителен,
например, винильный остаток. Под диалкилфосфинильной группой понимают остаток
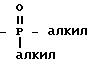
причем "алкил" имеет указанное ранее значение.
Предпочтителен диметилфосфинильный остаток.
В качестве солей SO3H-, PO3H2- и карбоксильных остатков
можно использовать соли щелочных или щелочно-земельных металлов или аммония. Под солями щелочных металлов понимают соли лития, натрия, калия, рубидия и цезия, причем предпочтительны соли лития, натрия
и калия, прежде всего, однако, соли натрия и калия. Солями щелочно-земельных металлов являются соли бериллия, магния, кальция, стронция или бария. Предпочтительны соли магния и кальция, причем
особенно предпочтительны кальциевые соли. В качестве солей аммония могут найти применение таковые незамещенного иона аммония, NH
В качестве карбоксамидного остатка понимают остаток CONH2, однако также такие остатки, в которых аминогруппа замещена в случае необходимости одним или двумя содержащими в случае необходимости один или несколько гидроксильных, карбоксильных и/или алкоксикарбонильных остатка алкильными остатками.
Из используемых согласно изобретению нитрозосоединений общей формулы II предпочтительны такие соединения, в которых R7 и R8 образуют насыщенную или ненасыщенную цепь, как описано выше. Особенно предпочтительно при этом, когда эта цепь ненасыщена и электроны двойной связи и свободная электронная пара азота ненасыщенной цепи сопряжены с двойной связью или мостичным N-атомом общей формулы II так, что в результате образуется анеллированное ароматическое кольцо.
В случае необходимости для вещества общей формулы II также возможны таутомерные формы. Они также должны охватываться общей формулой II.
Согласно изобретению предпочтительны нитрозосоединения общих формул III - XII

При этом X-Y имеет такое же значение, как указывалось раньше. R9, R10, R11 и R12, которые являются одинаковыми или разными, обозначают водород, гидроксил, алкил, алкоксил, алкилтио, арилкил, арил, карбоксил, алкоксикарбонил, карбоксамидогруппу, цианогруппу, аминогруппу, которая в случае необходимости замещена одним или двумя, в случае необходимости содержащими один или несколько гидроксильных, карбоксильных и/или алкоксикарбонильных остатков, алкильными остатками, или галоген, причем два соседних остатка в случае необходимости образуют алкиленовую группу, которая со своей стороны в случае необходимости замещена арилом или анеллирована с ним, и
R13 представляет собой алкил или аралкил, который в случае необходимости может быть замещен гидроксилом, карбоксилом, SO3H, PO3H2 или диалкилфосфинилом. Определения остатков соответствуют указанным для соединений общей формулы II.
Для предлагаемого согласно изобретению применения особенно предпочтительны вещества общих формул III, IV, V, VII, VIII и IX, в случае необходимости соответствующие таутомерные формы и их соли. Особенно предпочтительны такие вещества, в которых X-Y имеет значение N=CR6, причем R6 может иметь значение, как указанное для общей формулы II.
В качестве исключительно пригодных для применения согласно изобретению оказались в особенности такие соединения, как 3-нитрозо-2-метил-пиразол-(1,5а)-пиридин, 3-нитрозо-пиразоло(1,5-а)-пиридин и 3-нитрозо-пиразоло(3.2-с)-S-триазол и их соли, в особенности гидрохлорид.
Как указано выше, согласно предлагаемому в изобретении способу ароматические нитрозосоединения вводят в контакт с исследуемой пробой и PQQ-зависимой дегидрогеназой. В европейских патентах EP-A-0354441 и EP-A-0441222 описывается, что оксидазы и NAD-независимые дегидрогеназы восстанавливают ароматические нитрозосоединения до обогащенных электронами ароматических аминосоединений, которые, с другой стороны, можно обнаружить с помощью цветообразующего реагента и окислителя путем окислительного сочетания.
Неожиданно оказалось, что в присутствии неокислительного цветообразующего индикатора для хиноидных иминосоединений и PQQ-зависимой дегидрогеназы, ароматическое нитрозосоединение при окислении аналита не проходит через стадию полного, катализированного PQQ-зависимой дегидрогеназой, ферментативного восстановления до обогащенного электронами ароматического амина, а может останавливаться на промежуточной стадии образующегося после частичного ферментативного восстановления имина за счет неокислительного цветообразующего индикатора и может быть обнаружено.
Еще неожиданнее оказалось, что, если выбирают определенные ароматические нитрозосоединения, которые уже содержат хромогенный остаток, эти ароматические нитрозосоединения в присутствии PQQ-зависимой дегидрогеназы, правда, восстанавливаются до окрашенного иминосоединения, ферментативное дальнейшее восстановление до ароматического амина по существу, однако, не происходит, так что также окрашенное иминосоединение, даже без необходимости реакции с краскообразующим индикатором, можно определять как меру количества аналита. Примеры соответствующих используемых согласно изобретению, хромогенных нитрозосоединений приводятся ниже.
Хотя ассортимент пригодных, обогащенных электронами, ароматических нитрозосоединений очень большой, все они акцептируются PQQ-зависимыми дегидрогеназами как прямые акцепторы электронов. Существенной, по-видимому, является лишь нитрозогруппа, которая связана с обогащенным электронами ароматическим остатком.
Предлагается, что реакцию можно представить по следующей реакционной схеме на примере нитрозоанилина

Ароматическое нитрозосоединение (1) при окислении аналита восстанавливается до ароматического гидроксиламина (2), последний спонтанно отщепляет воду, благодаря чему возникает хиноидная промежуточная иминостадия (3). Прежде, чем она восстанавливается далее ферментативно благодаря PQQ-зависимой дегидрогеназе до ароматического амина, как это известно из европейских патентов A-0354441 и A-0441222, ее можно, например, благодаря цветообразующему реагенту (HP) улавливать и в виде окрашенного продукта сочетания (4) колориметрически определять, или она содержит хромогенный остаток продукта сочетания уже в исходном соединении (5) и, таким образом, после ферментативного восстановления ее можно колориметрически определять прямо в виде иминосоединения (4).
Неожиданным является то, что специфически при применении PQQ-дегидрогеназ можно улавливать или прямо обнаруживать промежуточную иминостадию (3) согласно изобретению с помощью индикатора, не осуществляя дальнейшее, известное из европейского патента A-0354441 ферментативное восстановление до амина. При применении флавин-зависимых оксидаз, которые согласно европейскому патенту A-0354441 также восстанавливают ароматические нитрозосоединения, удается обнаружить промежуточную иминостадию только в очень незначительном количестве, в то время как большая часть промежуточной иминостадии при окислении аналита очень быстро ферментативно восстанавливается далее до ароматического амина.
Согласно изобретению обнаружение хиноидного иминосоединения также можно осуществлять с помощью окрашивающего неокислительного реагента. Термин "окрашивающий" обозначает, что благодаря реакции цветообразующего реагента с иминосоединением получается окрашенное вещество, максимум поглощения которого отличен от такового используемого нитрозосоединения и цветообразующего реагента до реакции. Под неокислительным окрашивающим индикатором понимают, что индикатор реагирует с обнаруживаемым соединением при возникновении окраски, причем индикатор не действует окисляюще на обнаруживаемое соединение, (например, за счет содержащегося в индикаторе дополнительного окислителя).
Обнаружение образующегося в способе согласно изобретению иминосоединения можно осуществлять путем реакции цветообразующего реагента с иминосоединением. При этом получается окрашенное вещество, которое содержит иминосоединение в качестве частичной структуры. Обнаружение, однако, также можно осуществлять таким образом, что иминосоединение окисляет молекулу лейкокрасителя до окрашенной молекулы.
Также возможна комбинация обоих принципов обнаружения тем, что цветообразующий реагент сочетают с молекулой обнаруживаемого иминосоединения до получения неокрашенной молекулы лейкокрасителя, которая окисляется другой молекулой иминосоединения до красителя.
Такие окрашивающие индикаторы для иминосоединений известны в большом количестве. Принимают во внимание все вещества, которые реагируют с окисленными производными п-фенилендиамина с возникновением окраски.
Примерами окрашивающих за счет реакции сочетания индикаторов являются ароматические соединения, предпочтительно фенольные и нафтольные соединения, которые замещены хорошими удаляемыми группами, и таким образом эти удаляемые группы легко и очень быстро могут замещаться обнаруживаемым иминосоединением с возникновением окраски. Предпочтительными примерами являются 1-нафтол-4-сульфокислота, 2,4,6-трибром-3-гидроксибензойная кислота, 2,4-дихлор-1-нафтол, тетразин или Оранж 1.
В предлагаемом согласно изобретению способе для обнаружения иминосоединения также используются индикаторы, которые не сочетаются с иминосоединением, а которые при восстановлении иминосоединения до амина образуют окрашенное соединение. Чаще всего это происходит путем димеризации лейкокрасителя. Пригодные лейкокрасители известны специалисту из способа обнаружения пероксида водорода или пероксидазы. Примерами таких лейкокрасителей являются 1-нафтиламиносульфокислоты, триарилимидазолы (патент ФРГ 2735690), диарилимидазолы (патент США 4-919890), аминокарбазолы (патенты ФРГ 2205733, 2338932), оксазолы, тиазолы (европейский патент A-0167973), и т.д.
Пригодны все лейкокрасители, которые на основании своего редокспотенциала в состоянии восстанавливать иминосоединения.
Наконец, можно комбинировать принципы обнаружения - сочетание с индикатором и окисление лейкокрасителя - тем, что в качестве цветообразующей компоненты для иминосоединений используются реагент, который с иминосоединением образует бесцветное лейкосоединение, которое лишь за счет второй молекулы иминосоединения при его восстановлении до соответствующего ароматического амина окисляется до красителя. Наиболее употребительными, очень хорошо известными из цветной фотографии так называемыми "компонентами цветного проявления" являются фенолы, нафтолы, анилины, нафтиламины, а также их производные и метиленактивные соединения. Обзор о такого рода компонентах цветного проявления дается T.H.James в "The Theory of the Photographic Process", 3-е изд., Mc Millan, Нью-Йорк, 1966, глава 17, с. 385-390.
Предлагаемый согласно изобретению способ осуществляют таким образом, что исследуемая проба одновременно контактирует с PQQ-зависимой дегидрогеназой, одним или несколькими вышеописанными, обогащенными электронами, ароматическими нитрозосоединениями и индикатором для иминосоединений. Если проба содержит аналит, который окисляется PQQ-зависимой дегидрогеназой, то ароматическое нитросоединение при ферментативном восстановлении реагирует до образования соответствующего иминосоединения. Последнее реагирует с цветообразующим индикатором так, что возникающую окраску можно корректировать с концентрацией аналита в пробе. Колориметрию можно осуществлять визуально за счет сравнительных окрасок или фотометрически.
Особенно простой способ окислительного обнаружения аналитов имеет место тогда, когда образующееся за счет восстановления ароматического нитрозосоединения иминосоединение само окрашено и его не нужно обнаруживать сначала путем сочетания с окрашивающим индикатором или путем окисления лейкокрасителя. Окрашенные иминосоединения, как описано выше, сами по себе известны специалисту из цветной фотографии и из аналитических способов обнаружения.
Для предлагаемого в
изобретении способа окислительного обнаружения аналита за счет прямого определения окрашенного хиноидного иминосоединения в качестве особенно пригодных оказались нитрозоанилиновые соединения формулы
XIII как прямые хромогенные акцепторы электронов, которые восстанавливаются до окрашенного хинондиимина формулы XIV
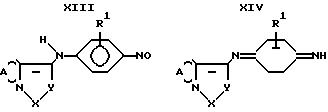
где R1 (в общей формуле XIII) - водород, гидроксил, галоген, алкоксил, алкилтио, арилокси или арилтио; алкил, в случае необходимости замещенный гидроксилом, карбоксилом, PO3H2 или SO3H; аминогруппа, в случае необходимости одно- или многократно замещенная алкилом, который в свою очередь в случае необходимости может быть замещен гидроксилом, PO3H2, диалкилфосфинилом, SO3H или карбоксилом;
X - Y - NR5-CO или N=CR6, причем R5 и R6 имеют такое же значение, что и указанное в общей формуле II;
A - насыщенная или ненасыщенная трехчленная цепь с одним атомом азота или серы и двумя атомами углерода или двумя атомами азота и одним атомом углерода, причем атомы углерода в случае необходимости замещены алкилом, алкоксилом, алкилтио, гидроксилом, аралкилом, арилом, карбоксилом, карбоксамидо, алкоксикарбонилом, цианогруппой, галогеном, аминогруппой, которая в случае необходимости замещена одним или двумя, содержащими в случае необходимости один или несколько гидроксильных, карбоксильных и/или алкоксикарбонильных остатков, алкильными остатками; и причем атомы азота, которые не связаны через двойную связь, замещены водородом, алкилом, замещенным в случае необходимости SO3H или диалкилфосфинилом, или аралкилом; или два соседних заместителя цепи в случае необходимости образуют алкиленовую группу, которая со своей стороны в случае необходимости замещена арилом или анеллирована с ним;
а также в случае необходимости соответствующие таутомерные формы и их соли.
Значение отдельных заместителей при этом такое же, как и в соединениях общей формулы II. Предпочтительными остатками R1 при этом являются водород или алкил, а X-Y предпочтительно обозначает группу N=CR6.
Особенно предпочтительно образует A с соседним гетероциклом имидазольное, триазольное, бензимидазольное, тиазольное или дигидроимидазольное кольцо, атомы углерода которого могут нести указанное в общем определении для значения A заместители. При этом исключительно предпочтительно имидазольное кольцо.
Особенно предпочтительными соединениями являются:
1) [2,4-диметил-пиразол-(1,5-а)-имидазол-3-ил]-(4-нитрозофенил)- амин;
2) [4-метил-пиразол-(1,5-а)-имидазол-3-ил]-(4-нитрозофенил)- амин;
3) [4-(диметилфосфинилметил)-2-метил-пиразол-(1,5-а)имидазол-3- ил] -(4-нитрозофениламин);
5) [5,
6-дигидро-4-диметилфосфинилметил-2-метил-пиразол-(1,5-а) имидазол-3-ил]-(4-нитрозофенил)-амин;
6) [4-(диметилфосфинилметил)-2-метил-пиразол-(1,5-а) имидазол-3-ил] -(4-нитрозофенил)-амин;
7) [2,6-диметил-4-диметилфосфинилметил-пиразол(3,2-с)-S-триазол- 3-ил] -(4-нитрозофенил)-амин.
Если предлагаемый в изобретении способ осуществляют так, что путем восстановления ароматического нитрозосоединения образуется прямо окрашенное хинондииминное соединение формулы XVII, то исследуемую пробу одновременно вводят в контакт с PQQ-зависимой дегидрогеназой и одним или несколькими, обогащенными электронами ароматическими нитрозосоединениями общей формулы XVI. Если проба содержит аналит, который окисляется PQQ-зависимой дегидрогеназой, то обогащенное электронами ароматическое нитрозосоединение реагирует до образования соответствующего окрашенного хинондиимина. Дополнительный избыток электронов наконденсированного на хромогенное, обогащенное электронами пиразольное кольцо кольца A способствует тому, что неожиданно образовавшееся хинондииминное соединение далее больше не восстанавливается ферментативно до соответствующего амина, а окрашенное хинондииминное соединение прямо можно определять в форме измерения световой абсорбции и коррелировать с концентрацией аналита в пробе. Для того чтобы достичь быстрого ферментативного восстановления хромогенных ароматических нитрозосоединений, особенно предпочтительно, когда они достаточно хорошо растворимы. Особенно предпочтительным для предлагаемого в изобретении способа при использовании хромогенных нитрозоармоатических соединений формулы XIII является тот случай, когда их концентрация в растворе составляет по меньшей мере 10-3 моль/л, предпочтительно по меньшей мере 10-2 моль/л.
Хорошей растворимости можно достигать в особенности тем, что хромогенное нитрозосоединение снабжается гидрофильными группами.
Соответственно, исключительно хорошо пригодными в способе изобретения хромогенными нитрозосоединениями являются, например, вышеуказанные соединения 3, 4 и 7.
Способ можно осуществлять по так называемому мокрому тесту, например в кювете, или в виде так называемого сухого теста на соответствующем носителе реагента, причем необходимые тест-реагенты находятся на тест-носителе, в особенности на поглощающем или набухающем материале. Такие тест-носители известны, например, из патента ФРГ A-3247608, европейского патента EP-A-0262445 или европейского патента EP-A-0256806.
Другим предметом изобретения является средство для колориметрического определения аналита путем ферментативного окисления, которое охарактеризовано в формуле изобретения. Такое средство содержит наряду с необходимой для ферментативного окисления определяемого аналита PQQ-зависимой дегидрогеназой и наряду по меньшей мере с одним ароматическим нитрозосоединением в качестве прямого акцептора электронов, который принимает высвобождающиеся при ферментативном окислении аналита электроны от системы PQQ/дегидрогеназа, далее дополнительно дающий окраску неокислительный индикатор для иминосоединений.
В качестве PQQ-дегидрогеназ, ароматических нитрозосоединений и цветообразующих индикаторов для хиноидных иминосоединений используют описанные выше для предлагаемого в изобретении способа вещества. Если используют в предлагаемом согласно изобретению способе обогащенные электронами ароматические нитрозосоединения формулы XIII, которые уже содержат связанный с анилиновым азотом хромогенный остаток, то средство предпочтительно не содержит никакого цветообразующего индикатора для иминосоединений, так как образующийся при восстановлении хинондиимин формулы XIV уже окрашен.
Для установления пригодного для осуществления способа pH-значения, которое рекомендуется в особенности для используемых ферментов и индикатора для иминосоединения, предлагаемое согласно изобретению средство содержит буферную систему. Предпочтительно средство содержит буферную систему, которая в тест-растворе устанавливает pH-значение 4-9. В особенности предпочтительно слега кислое pH-значение, равное 5-6,5.
Предлагаемое согласно изобретению средство может быть в форме раствора в нанесенном на поглощающий или набухающий носитель виде. В форме раствора средство содержит предпочтительно все необходимые для способа изобретения реагенты. В качестве растворителя предпочтительно речь идет о воде, однако, также о смеси с водорастворимыми органическими растворителями, как например метанол, этанол, ацетон или диметилформамид. Из соображений устойчивости может быть предпочтительным распределение необходимых для теста реагентов на два или несколько растворов, которые смешивают лишь при непосредственном исследовании. Однако следует обратить внимание на то, что ароматическое нитрозосоединение и индикатор для иминосоединения перед началом теста находились в растворе. В случае концентрации используемых ароматических нитрозосоединений руководствуются концентрацией определяемого аналита.
Типичные концентрации определяемых согласно способу изобретения аналитов представляют собой 10-6 - 10-2 моль/л, в особенности 10-5 - 10-3 моль/л. Соответственно типичные концентрации используемых нитрозосоединений составляют 10-4 - 10-1 моль/л. Для того чтобы достигать достаточно быстрого ферментативного восстановления, особенно предпочтительны концентрации нитрозосоединений, в особенности хромогенных нитрозосоединений формулы XIV выше 10-3 моль/л. В случае концентрации используемой PQQ-зависимой дегидрогеназы руководствуются ее активностью и концентрацией аналита. Типичными величинами концентраций фермента являются 1 mU/мл - 1 U/мл при тесте в кювете.
Индикаторы для иминосоединений используются по меньшей мере в стехиометрическом соотношении к используемым нитрозосоединениям, предпочтительно в 1,5 - 2-кратном избытке.
Предлагаемое согласно изобретению средство также может быт в форме тест-полосы. Такие тест-полосы известны в самых различных видах выполнения, например из европейского патента EP-A-016387, патента ФРГ EP-A-3247608, европейских патентов EP-A-0262445 или A-0256806. В тест-полосах (индикаторных бумагах) необходимые для осуществления способа определения реагенты находятся на твердых слоях носителя. В качестве слоев-носителей принимают во внимание в особенности поглощающие и/или набухающие материалы, которые смачиваются исследуемой жидкостью. Примерами являются желатина, целлюлоза или прочее из химических волокон. Внутри или на этих носителях находятся реагенты в твердой форме. При нанесении исследуемой жидкости на тест-полосы или при окунании тест-полосы в исследуемую жидкость на полосах образуется жидкая среда, в которой протекает реакция обнаружения. Вызванное реакцией образование окраски можно оценивать визуально или фотометрически, например отражательно/фотометрически.
Предпочтительные концентрации индивидуальных
реагентов на тест-полосах составляют, моль:
Аналит - Обычно 10-4 - 10-1
Нитрозосоединение - 10-3 - 1
Неокислительный индикатор - 10-3 - 1
Фермент, ед. на тест-поле - 0,1 - 100
Предлагаемое изобретение обладает тем преимуществом, что нет необходимости ни в каких неспецифических катализаторах восстановления,
как диафораза или метилфеназиний-метосульфат, для восстановления акцептора электронов, а его восстановление осуществляется прямо за счет специфической системы аналит/фермент. Таким образом, можно
избегать мешающих побочных реакций. Благодаря использованию нитрозоосединений в качестве акцепторов электронов более нет никакого ограничения акцептора электронов, например, из-за слишком медленной
диффузии, как это имеет место в случае кислорода в качестве акцептора электронов. На один эквивалент обнаруживаемой промежуточной иминостадии окисляется только один эквивалент аналита. Это
способствует высокой чувствительности обнаружения аналита. Нет необходимости ни в каком окислителе для реакции с окрашивающим реагентом. Поэтому также всю реакцию обнаружения можно осуществлять без
помех в одну стадию и в общем растворе. Большой ассортимент используемых цветообразующих индикаторов, между прочим таких, которые известны из цветной фотографии, позволяет почти свободно выбирать
длину волны, при которой должно осуществляться измерение, и коэффициент экстинкции, который определяет чувствительность измерения.
Особенно просто осуществляется предлагаемый в изобретении способ тогда, когда образуется прямо окрашенное иминосоединение и нет необходимости в реакции с окрашивающим реагентом.
Следующим предметом изобретения является новое
хромогенное нитрозоанилиновое соединение формулы XIII

где R1 - водород, гидроксил, галоген, алкоксил или алкилтио, арилокси или арилтио, алкил, в случае необходимости замещенный гидроксилом, карбоксилом, PO3H2, диалкилфосфинилом или SO3H, аминогруппа, которая в случае необходимости одно- или многократно замещена алкилом, который в свою очередь в случае необходимости может быть замещен гидроксилом, PO3H2, SO3H или карбоксилом; и NR5-CO или N=CR6,
X-Y - NR5-CO или N=CR6, причем R5 - водород, алкил, в случае необходимости замещенный гидроксилом, карбоксилом, SO3H, PO3H2, диалкилфосфинилом, и R6 - водород, алкил, в случае необходимости, смотря по обстоятельствам, замещенный гидроксилом, диалкилфосфинилом, карбоксилом, SO3H, PO3H2, солью одного из этих кислотных остатков и/или алкоксикарбонилом, или аминогруппа, которая в случае необходимости замещена одним или двумя, содержащими в случае необходимости один или несколько гидроксильных, карбоксильных и/или алкоксикарбонильных остатков алкильными остатками; причем, когда аминоостаток замещен двумя алкильными остатками, то эти остатки также могут быть циклизованы до образования кольца, которое кроме N-атома аминогруппы в случае необходимости также может прерываться атомом кислорода, серы или другим атомом азота, или аминогруппа, которая в случае необходимости замещена одной или двумя ацильными группами, алкокси- и/или аралкоксикарбонильными группами, H2N-CO, алкил-, аралкил- и/или арилкарбамоильными группами; или водород, карбоксил, алкоксикарбонил, карбоксамидо или галоген; и
A - насыщенная или ненасыщенная трехчленная цепь из одного атома азота или атома серы и двух атомов углерода или двух атомов азота и одного атома углерода, причем атомы углерода в случае необходимости замещены алкилом, алкоксилом, алкилтио, гидроксилом, аралкилом, арилом, карбоксилом, карбоксамидогруппой, алкоксикарбонилом, цианогруппой, галогеном, аминогруппой, которая в случае необходимости замещена одним или двумя, в случае необходимости содержащими один или несколько гидроксильных, карбоксильных и/или алкоксикарбонильных остатков алкильными остатками; и причем атомы азота, которые не связаны через двойную связь, замещены водородом, алкилом, в случае необходимости замещенным гидроксилом, SO3H, карбоксилом, PO3H2 или диалкилфосфинилом; или аралкилом, или два соседних заместителя цепи в случае необходимости образуют алкиленовую группу, которая со своей стороны в случае необходимости замещена арилом или анеллирована с ним;
а также в случае необходимости соответствующие таутомерные формы и их соли.
Значение отдельных заместителей при этом такое же, как в соединении общей формулы II.
Предпочтительными остатками R1 являются водород и незамещенный или замещенный алкил. X-Y предпочтительно образует группу N=CR6, причем R6 - предпочтительно водород или незамещенный или замещенный алкил.
Предпочтительно A вместе с соседним гетероциклом образует имидазольное, триазольное, бензимидазольное, тиазольное или дигидроимидазольное кольцо, в которых значение заместителей кольца соответствует таковым общей формулы III.
Исключительно предпочтительно A образует имидазольное кольцо. Особенно предпочтительными соединениями являются:
1) [2,5-диметил-пиразол-(1,
5-a)-имидазол-3-ил]-(4-нитрозофенил)-амин;
2) [4-метил-пиразол-(1,5-a)-имидазол-3-ил]-(4-нитрозофенил)-амин;
3) [4-(диметилфосфинилметил)-2-метил-пиразол-(1,5-a)-имидазол-3-ил]
- (4-нитрозофениламин);
5) [5,6-дигидро-4-диметилфосфинилметил-2-метил-пиразол-(1,5-a) имидазол-3-ил]-(4-нитрозофенил)-амин;
6) (4-(диметилфосфинилметил)-2-метил-пиразол-[1,5-a]
- имидазол-3-ил)-(4-нитрозофенил)-амин;
7) (2,6-диметил-4-диметилфосфинилметил-пиразол[3,2-c]-s-триазол-3-ил)-(4-нитрозофени)-амин.
Получение предлагаемых согласно изобретению соединений формулы XIII осуществляют само по себе известными способами, которые описаны в публикации J. T. Hays и др. в J.Org.Chem. 32, 158 (1967). Для этой цели простые эфиры, предпочтительно простые метиловые эфиры, п-нитрозофенильных производных при протонном катализе вводят во взаимодействие с соответствующими 3-аминогетероциклами. При замещении метоксигруппы образуются вторичные амины формулы XIII.
Используемые гетероариламины либо описаны в литературе, либо могут получаться аналогично известным способам. В особенности в европейском патенте A-0433854 описаны аминосоединения, которые в качестве основной структуры содержат пиразольные гетероциклы.
Необходимые в качестве промежуточных продуктов аминосоединения как правило по причинам устойчивости находятся в виде солей сильных кислот, например неорганических кислот. Для взаимодействия с п-нитрозоанизолами предпочтительно используются свободные основания аминосоединений, которые получают обычными способами, например путем растворения солей в воде, добавления основания вплоть до pH 8-10 и экстракции свободного основания с помощью органического растворителя, например уксусного эфира или метиленхлорида. Альтернативно для этой цели, в особенности в случае трудно экстрагируемых аминосоединений, можно поступать следующим образом: аминосоединение растворяют в метаноле, затем добавляют основание, например раствор NaHCO3, триэтиламин и т.д., вплоть до достижения pH-значения метанольного раствора согласно влажной индикаторной pH-бумаги примерно 5-6. Затем добавляют вторую реакционную компоненту, п-нитрозоанизол.
Пример 1. Определение глюкозы с помощью PQQ-зависимой глюкоза-краситель-оксидоредуктазы и 1-нафтол-сульфокислоты в качестве компоненты цветного проявления.
В кювете смешивают мл:
Цитратный буфер/пирофосфатный буфер (50 ммоль) pH 7,5 - 0,38
N,N-Бис-(2-гидроксиэтил)-4-нитрозоанилин (5 ммоль,
в буфере) - 0,40
1-Нафтол-4-сульфокислота (10 ммоль в H2O) в качестве реагента цветного проявления - 0,20
Раствор пробы (0-40 ммоль глюкозы) - 0,01
Тест начинают
путем добавки 0,01 мл раствора фермента (глюкоза-краситель-оксидоредуктаза, EC 1.1.99.17, 900 ед/мг, 800 ед/мл) и измеряют изменение экстинкции при длине волны 606 нм. Постоянные значения экстинкции
достигаются спустя максимально 5 мин (фиг.1).
Пример 2. Обнаружение глюкозы с помощью PQQ-зависимой глюкоза-краситель-оксидоредуктазы и 2,4,6-трибром-3-гиброксибензойной кислоты в качестве индикатора.
Измеряемая смесь (конечные концентрации):
Цитратный буфер, pH 5,8, ммоль - 100
2,4,6,-трибром-3-гидроксибензойная кислота, ммоль - 10
N,
N-бис-(2-гидроксиэтил)-4-нитрозоанилин, ммоль - 1
Глюкоза-краситель-оксидоредуктаза, ед/мл - 10
Нитрат натрия, моль - 0,1
Глюкоза, ммоль - 100-500
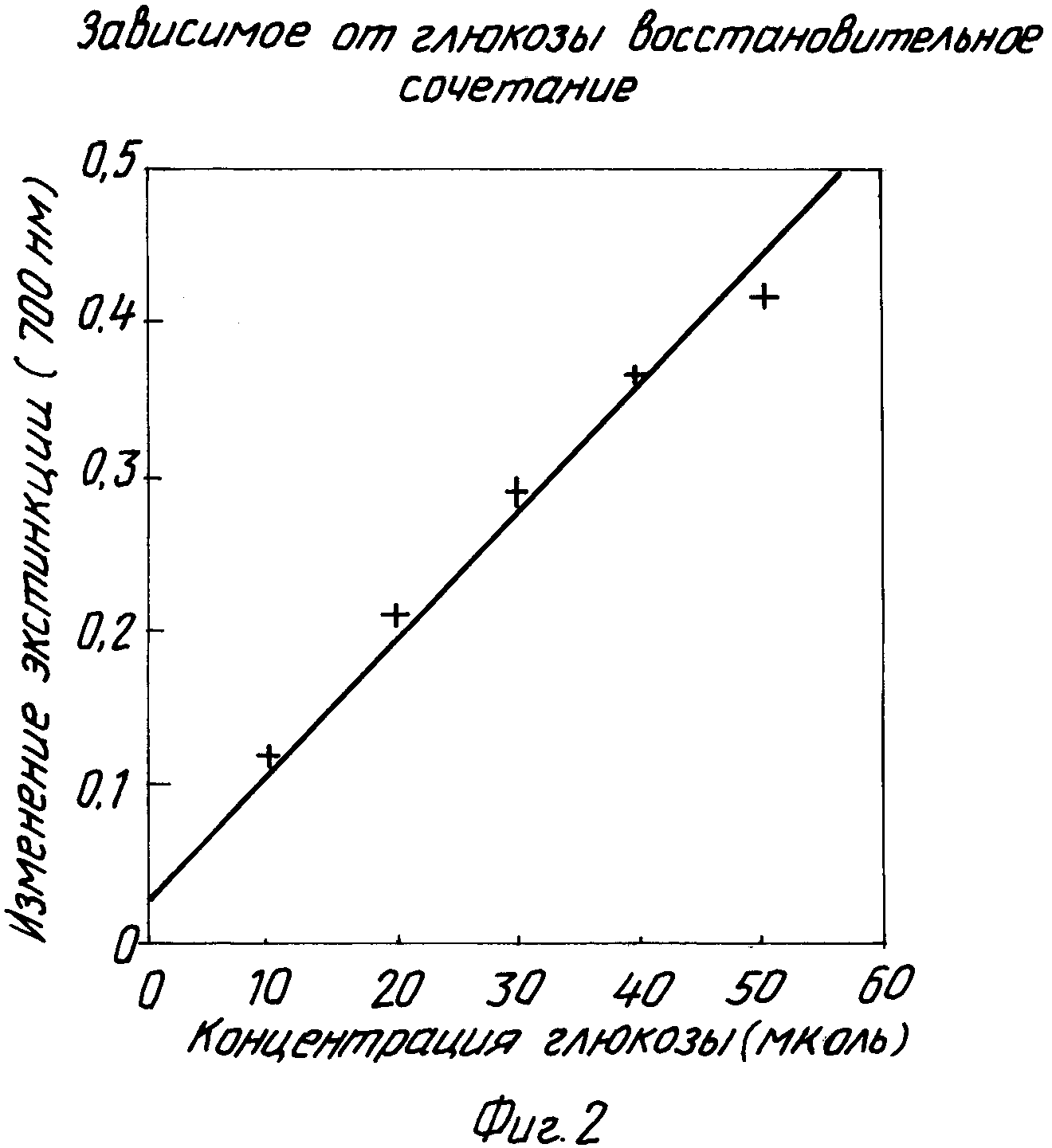
С увеличением
концентрации глюкозы наблюдают увеличивающееся образование зеленого красителя (максимум = 700 нм, фиг.2).
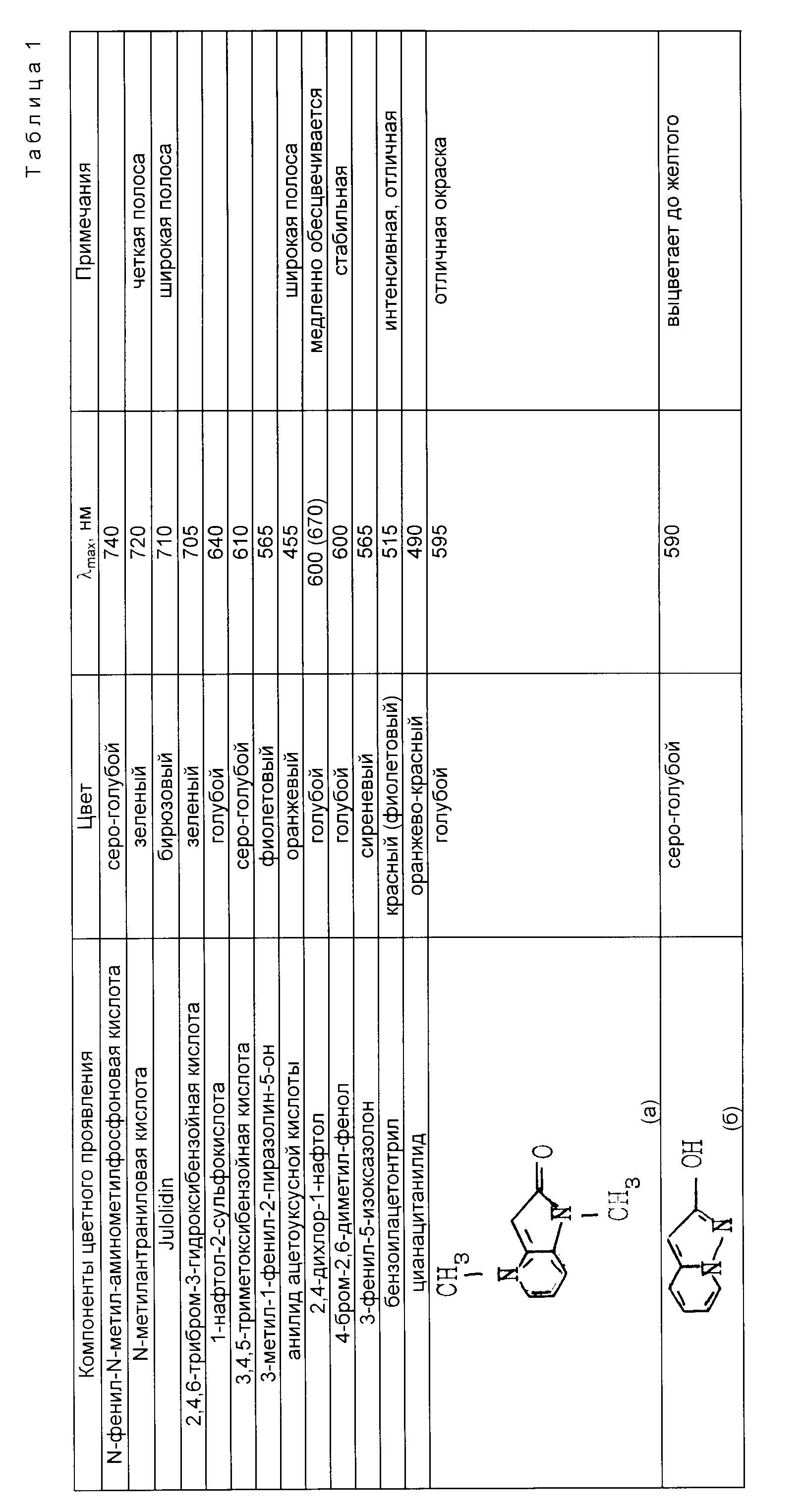
Пример 3. Таким же образом можно использовать указанные в табл. 1 другие реагенты цветного проявления для иминов. В табл. 1 представлены максимумы поглощения, полученные после сочетания N,N-бис-(2-гидроксиэтил)-п-хинондиимина с указанными компонентами цветного проявления.
Пример 4. Аналогично примеру 1 используют различные, указанные в табл. 2, обогащенные электронами ароматические нитрозосоединения. В табл. 2 представлены окраски, соответственно максимумы поглощения, полученные после проявления с 1-нафтол-2-сульфокислотой или 1-нафтол-4-сульфокислотой.
Пример 5. Сравнение определения глюкозы посредством обнаружения иминосоединений путем восстановительного проявления между PQQ-зависимой глюкоза-краситель-оксидоредуктазой и глюкоза-оксидазой.
В кювету помещают, ммоль:
Фосфатный буфер, pH 7,5 - 100
N,N-бис-(2-гидроксиэтил)-4-нитрозоанилин - 1
1-Нафтол-4-сульфокислота - 10
Глюкоза-краситель-оксидоредуктоза, ед./мл - 100
Путем
добавки глюкозы (0-60 ммоль) получают соответствующие количества красителя (фиг. 3).
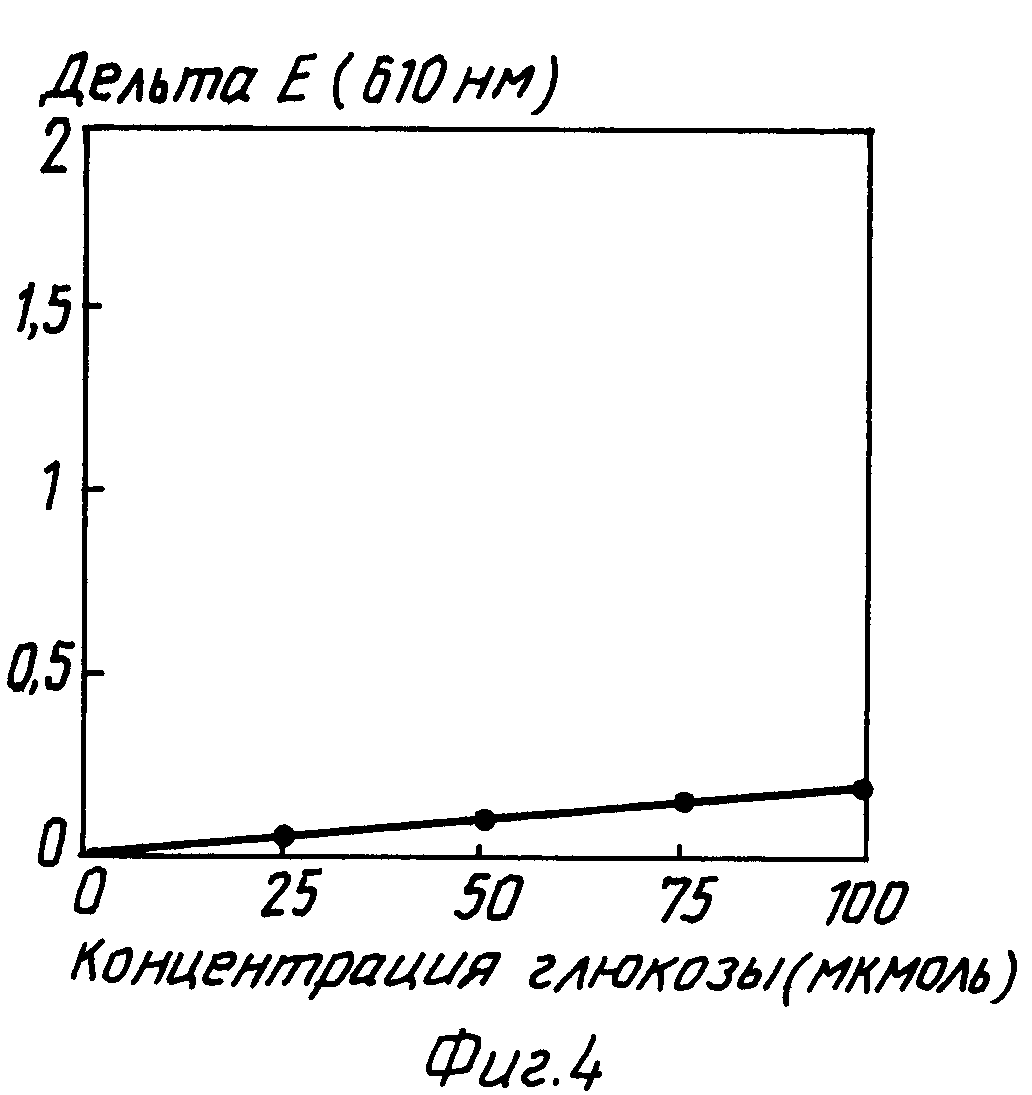
Если глюкоза-краситель-оксидоредуктазу заменяют таким же количеством глюкоза-оксидазы, то получают, напротив, только в 8 раз меньший выход красителя, так как большая часть образовавшейся промежуточной стадии хинондиимина восстанавливается далее глюкозооксидазой при расходе глюкозы с образованием фенилендиамина (фиг. 4).
Пример 6. Определение глюкозы с помощью PQQ-зависимой глюкоза-краситель-оксидоредуктазы посредством восстановительного образования окрашенных иминосоединений.
Уравнение реакции

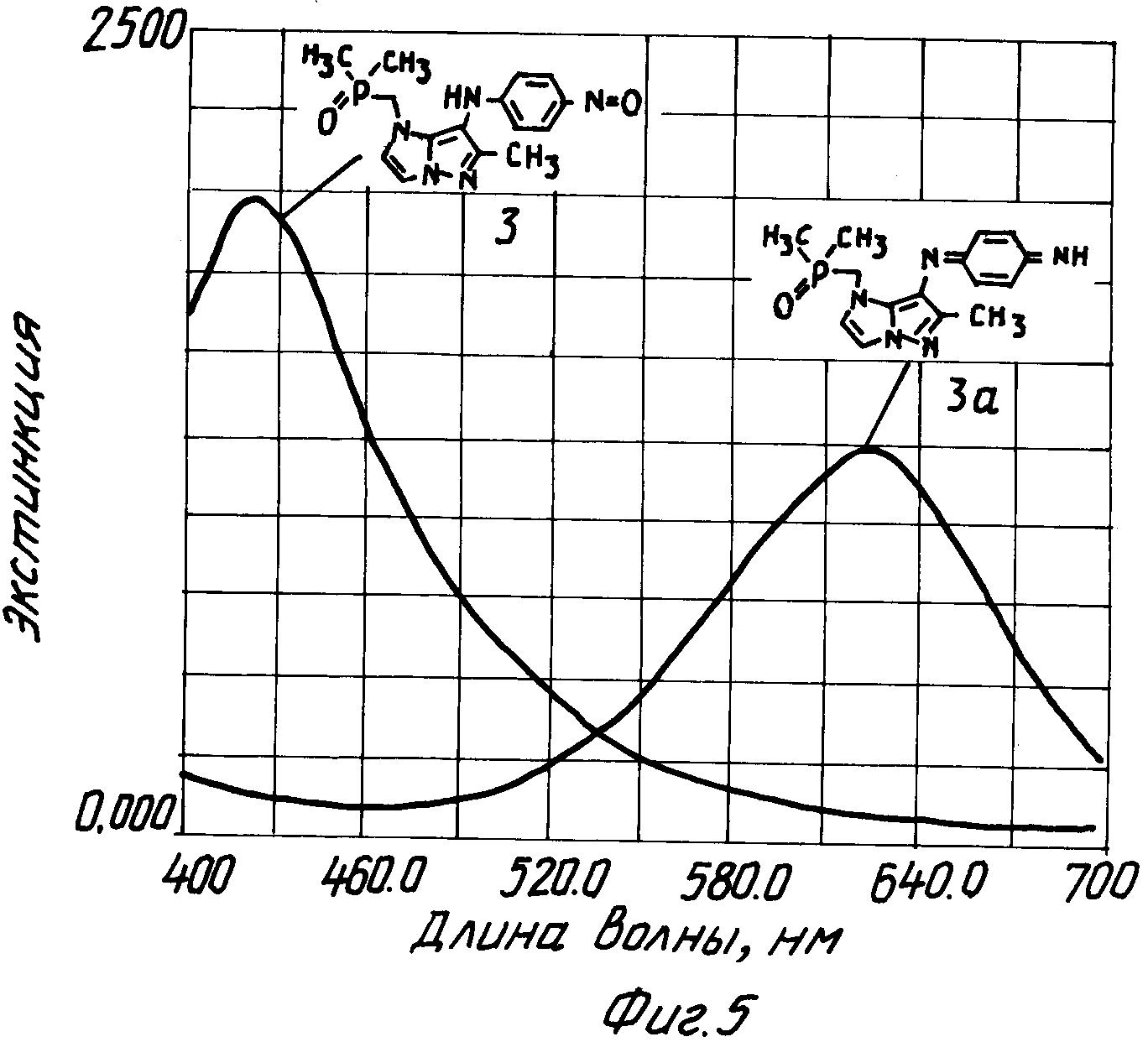
Спектры соединения 3 и соединения 3а представлены на фиг. 5.
Измеряемая смесь (конечная концентрация):
Цитратный буфер, pH 6, ммоль - 200
п-Нитрозоанилин (N 3 из табл. 3), ммоль - 1
CaCl2 , ммоль - 1
Мутаротаза, ед./мл - 20
Глюкоза-краситель-оксидоредуктаза, ед./мл - 10
После добавки различных количеств глюкозы между 0 и конечной концентрацией 50
мкмоль, спустя 5 мин измеряют изменения экстинкции (фиг. 6).
Аналогично используют соединения из табл. 3. В табл. 3 представлены максимумы поглощения используемых нитрозосоединений и полученных окрашенных хинондииминов.
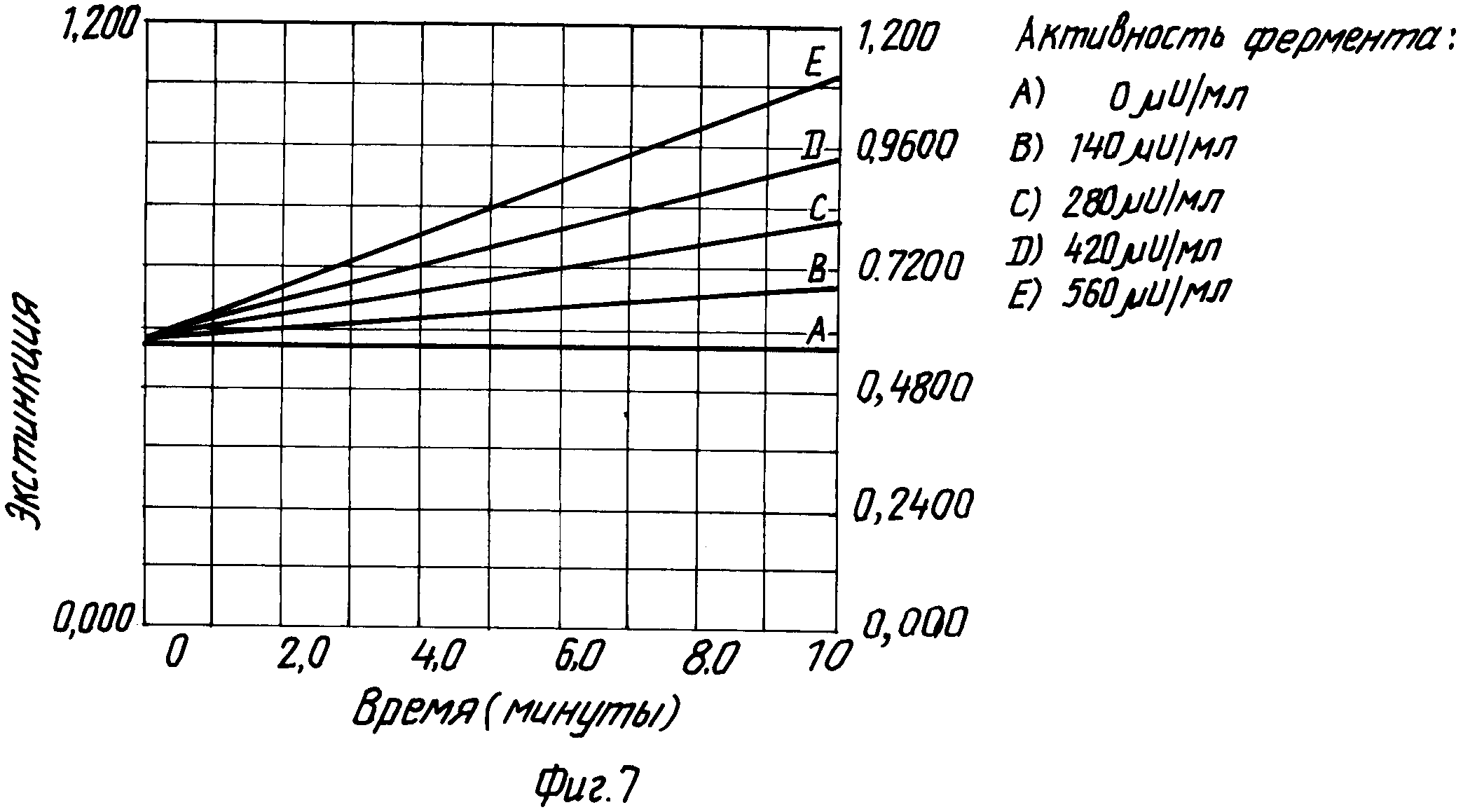
Пример 7. Определение ферментной активности PQQ-зависимой глюкоза-краситель-оксидоредуктаза путем восстановительного образования окрашенного иминосоединения из ароматического нитрозосоединения.
Описанную в примере 6 реакцию также можно использовать для измерения ферментной активности PQQ-зависимой дегидрогеназы.
Измеряемая смесь (конечная концентрация), ммоль:
Цитратный буфер, pH 5,8 - 200
п-Нитрозоанилин (3) из примера 6 - 1
Хлорид кальция - 1
Глюкоза - 30
Кинетическое измерение начинают с помощью 0-1 mU глюкоза-краситель-оксидоредуктазы и измеряют во времени изменение окраски (фиг. 7).
Пример 8. (4-(Диметилфосфинилметил)-2-метил-пиразол-(1,5-а)-имидазол-3-ил) -(4-нитрозофенил)-амин (3).
13,7 г 3-Амино-2-метил-4-(диметилфосфинилметил)-пиразол-[1,5-а]-имидазол-дигидрохлорида растворяют в 350 мл метанола. Раствор охлаждают примерно до 5oC и смешивают с концентрированным водным раствором бикарбоната натрия, пока мокрая индикаторная pH-бумага не покажет pH-значение примерно 6. Затем к полученной смеси в течение 30 мин прикапывают раствор 7,8 г п-нитрозоанизола в 35 мл метанола. Перемешивают смесь в течение 4 ч при комнатной температуре и путем добавки дальнейшего количества раствора NaHCO3 поддерживают pH-значение равным 6.
Реакционную смесь отфильтровывают, смешивают примерно со 150 мл силикагеля и выпаривают досуха. Силикагель вносят в колонку и продукт выделяют путем элюирования с помощью смеси толуола с метанолом = 2:1. Получают 10,3 г черно-коричневой массы, которую снова хроматографируют на силикагеле с помощью смеси метиленхлорида с метанолом = 12:1. Получают 4,9 г целевого соединения с т. пл. 204oC (с разложением).
Rf (силикагель) толуол/метанол (2: 1) = 0,3; CH2Cl2/метанол (12:1) = 0,21.

Получение исходного продукта.
a) 4-Диметилфосфинилметил-2-метил-пиразол-(1,5-a)-имидазол.
37 г 2-Метил-пиразол-(1,5-a)-имидазола (J. Het. Chem. 10, 441/(1973)) растворяют в 370 мл безводного диметилформамида и смешивают с 54,2 г хлорметилдиметилфосфаноксида и 119 г карбоната калия. Смесь перемешивают 10 ч при 115oC (температура бани). Осадок отсасывают и фильтрат выпаривают. Остаток хроматографируют на силикагеле (элюирующее средство этилацетат/метанол = 2: 1). Получают в целом 36,6 г целевого соединения в виде смеси коричневых кристаллов с коричневым маслом.
РСХ (силикагель, этилацетат/метанол = 2:1): Rf=0,2.
c). 3-Амино-4-диметилфосфинилметил-2-метил-пиразол-(1,5-a)-имидазол х 2HCl.
18 г вышеполученного соединения растворяют в 25 мл концентрированной соляной кислоты и 50 мл воды. Затем к полученному раствору при 0oC прикапывают раствор 6,2 г нитрита натрия в 25 мл воды. Спустя 30 мин при 0oC раствор слегка подщелачивают путем добавления раствора бикарбоната натрия и после этого порциями добавляют 21,4 г дитионита натрия. Смесь перемешивают еще 30 мин и смешивают ее с раствором 17 г ди-трет-бутил-дикарбоната в 100 мл диоксана. Реакционную смесь перемешивают в течение ночи при комнатной температуре, диоксан отгоняют и остаток многократно экстрагируют смесью н-бутанола с этилацетатом в соотношении 3:1. Остающийся после высушивания и выпаривания органической фазы остаток растворяют в 320 мл насыщенного хлороводородом метанола. Перемешивают еще 2 ч, охлаждают на ледяной бане и отфильтровывают выделившиеся кристаллы. В целом получают 18,1 г целевого соединения.
ТСХ (силикагель, толуол/метанол = 3:1): Rf = 0,1.
Пример 9. (4-Нитрозофенил)-2-метил-(4-сульфопропил-пиразол-(1,5-a)-имидазол-3-ил)-амин (4).
Аналогично примеру 7 3-амино-4-сульфопропил-пиразол-(1,5-a)-имидазол вводят во взаимодействие с п-нитрозоанизолом в метаноле. Реакционную смесь отфильтровывают и фильтрат выпаривают. Остаток хроматографируют на силикагеле с помощью смеси толуол/метанол = 2:1. Продукт затем для дальнейшей очистки вносят в колонку с адсорбирующей смолой HP 20SS (фирма Mitsubishi) и элюируют с помощью ступенчатого градиента смеси метанол/вода = от 1:9 до 2: 8. Содержащие продукт фракции объединяют, концентрируют, обрабатывают небольшим количеством этанола и продукт осаждают путем добавки эфира. Получают целевое соединение в форме коричневого порошка.
ТСХ (силикагель, этанол: Rf = 0,6, смесь изопропанол/бутилацетат/вода = 5:3:2 Rf = 0,48).
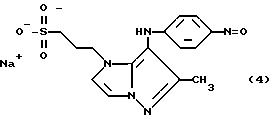
Получение исходного продукта.
a). 2-Метил-4-сульфопропил-пиразол-(1,5-a)-имидазол.
2-Метил-пиразол-(1,5-a)-имидазол вводят во взаимодействие с солью фенилдиазония, которую получают обычным образом путем диазотирования анилина, при pH 2 - 5. Полученный 2-метил-3-фенилазо-пиразол-(1,5-a)-имидазол (5,6 г) растворяют в 60 мл диметилформамида, смешивают с 3,4 г пропансультона и 7 г карбоната калия. Смесь перемешивают 6 ч при 110oC, снова добавляют 5 г пропансультона и 7 г карбоната калия и перемешивают следующие 8 ч при 110oC. После охлаждения отфильтровывают и остаток хорошо промывают дважды метанолом. Раствор концентрируют и остаток хроматографически разделяют на силикагеле (элюирующее средство этилацетат/метанол/вода = 75:15:10). Выход: 5,3 г кристаллов желто-киричневого цвета.
ТСХ (силикагель, этилацетат/метанол/вода = 75:15:10): Rf = 0,3.
б). 3-Амино-2-метил-4-сульфопропил-пиразол-(1,5-a)-имидазол.
4,3 г вышеполученного азосоединения растворяют в 40 мл ледяной уксусной кислоты и в течение 1 ч порциями смешивают с 4 г цинкового порошка. Смесь перемешивают еще 30 мин, отсасывают и выпаривают. Остаток растирают с 30 мл этилацетата, отсасывают и фильтрат отбрасывают. Получают 10,2 г серо-коричневого порошка, который достаточно чист для дальнейшей переработки.
ТСХ (силикагель, этилацетат/ацетон/ледяная уксусная кислота/ вода=5:2:2: 1): Rf=0,14.
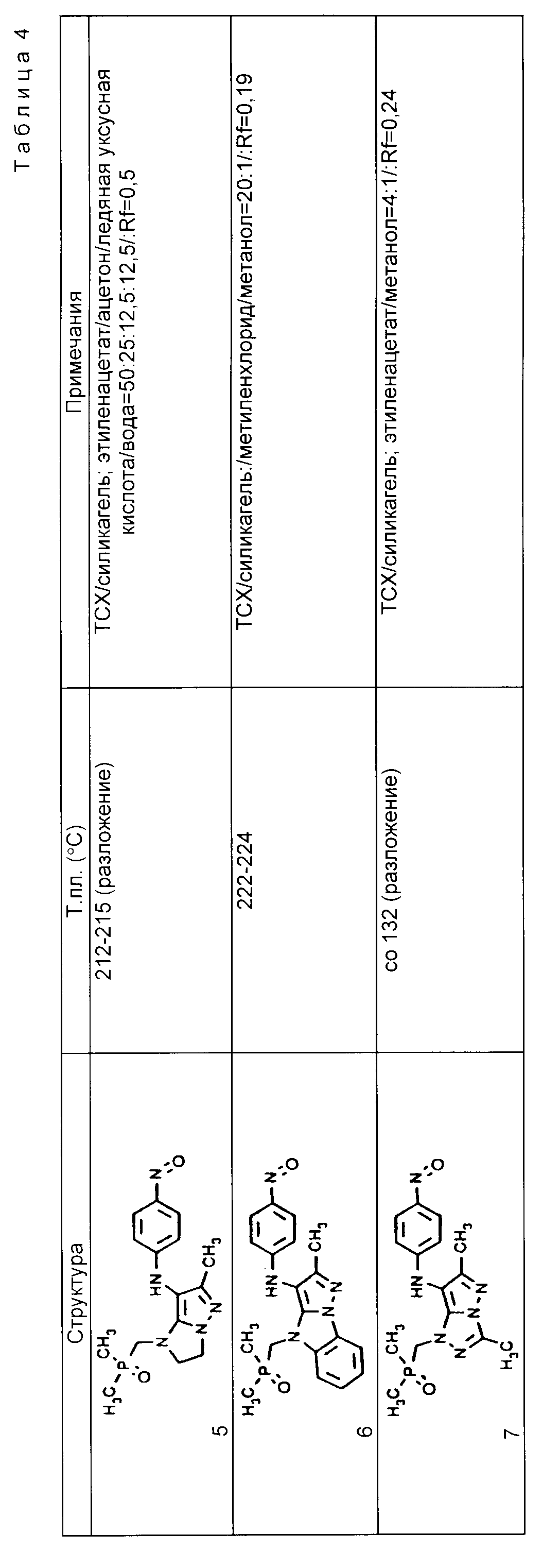
Пример 10. Аналогично
примеру 8 или 9 получают соединения из табл.4. Синтез исходных аминосоединений осуществляют следующим образом:
a) Получение исходного соединения для соединения 5 табл.4: 3-амино-5,6-дигидро-,
4-диметилфосфинилметил-2-метил-пиразол-(1,5-a)- имидазол.
3,9 г 2-метил-пиразол-(1,5-a)-имидазолина, 2,7 г ацетата натрия и 7,4 г тетрафторбората п-метоксибензолдиазония растворяют в 40 мл ледяной уксусной кислоты и раствор в течение 1 ч нагревают при 40-50oC. Реакционную смесь выпаривают, остаток обрабатывают раствором бикарбоната натрия и этилацетатом. Экстрагируют этилацетатом, высушивают и выпаривают. Остаток очищают путем хроматографии на силикагеле (элюирующее средство: этилацетат/лигроин= 1: 1 - 2:1, этилацетат, этилацетат/метанол = 95:5). Получают 4,12 г соответствующего 3-азосоединения (ТСХ: силикагель, этилацетат/метанол = 95:5: Rf = 0,5), которое алкилируют на азоте имидазолинового кольца с помощью хлорметилдиметилфосфаноксида. Переведение в 3-аминосоединение осуществляют путем восстановления азогруппы аналогично примеру 8,б).
Для выделения и очистки, сырое амино-соединение растворяют в небольшом количестве воды, смешивают с твердым бикарбонатом натрия и добавляют раствор трехкратного молярного количества ди-трет-бутил-дикарбоната в диоксане. Смесь перемешивают в течение ночи, выпаривают, экстрагируют сначала эфиром, чтобы удалить побочные продукты, и затем 5 раз с помощью метиленхлорида, чтобы выделить продукт. Получают кристаллическое трет-бутилоксикарбонильное соединение (ТСХ: этилацетат/ацетон/ледяная уксусная кислота/вода= 50:25:12: 5: Rf=0,5), которое для отщепления трет-бутилоксикарбонильной группы растворяют в 50 мл метанольного раствора хлороводорода. Спустя 1 ч при комнатной температуре концентрируют наполовину и продукт осаждения эфиром. Получают целевое соединение в виде гидрохлорида.
ТСХ (н-бутанол/ледяная уксусная кислота/вода = 2:1:1): Rf=0,3.
б). Получение исходного соединения для соединения 6 в табл.4: 3-амино-4-диметилфосфинилметил-2-метил-пиразол-(1,5-a)-бензимидазол.
Целевое соединение получают аналогично примеру 10 путем взаимодействия 2-метил-пиразол-(1,5-a)-бензимидазола (J.prakt.Chem. 326, 829 (1984) с солью фенилдиазония, N-алкилирования с помощью хлорметил-диметил-фосфаноксида и восстановления азогруппы с помощью цинка в ледяной уксусной кислоте. Получают целевое соединение в виде тригидрохлорид-дигидрата с т. пл.192oC (разложение).
ТСХ (силикагель; изопропанол/бутилацетат/вода = 50:30:20):Rf = 0,38.
в). Получение исходного соединения для соединения 7 в табл.4: 3-амино-2, 6-диметил-4-диметилфосфинил-пиразол-(3,2-c)-s-триазол.
6 г 2,6-Диметил-пиразол-(3,2-c)-c-триазола растворяют в 65 мл диметилформамида и смешивают раствор с 3,9 г хлорметил-диметилфосфаноксида и 8 г карбоната калия. Смесь перемешивают 2 ч при 100oC, отсасывают горячей и фильтрат выпаривают. Остаток хроматографируют на силикагеле (элюирующее средство: этилацетат/метанол = 4:1). Для омыления и декарбоксилирования продукт кипятят с обратным холодильником в течение 7 ч в концентрированной соляной кислоте. Реакционную смесь выпаривают. Получают светло-коричневое масло.
ТСХ (силикагель: этилацетат/метанол = 2:1): Rf =0,37.
Превращение вышеполученного продукта в 3-амино-соединение осуществляют аналогично способу, описанному в примере 8 для соответствующего 3-аминопиразол-(1,5-a)-имидазола (8,б). Получают целевое соединение в виде гидрохлорида с т.пл.255oC (разложение).
ТСХ (силикагель; этилацетат/метанол = 3:1): Rf =0,2.
Реферат
Изобретение может быть использовано для обнаружения и определения веществ
в различных испытуемых материалах. Способ определения аналита включает ферментативное окисление аналита с помощью PQQ-зависимой дегидрогеназы в присутствии акцептора электронов. Акцептор электронов
- обогащенные электронами ароматические нитрозосоединения, которые восстанавливают до иминосоединения при окислении аналита. Восстановленный акцептор обнаруживают путем цветового проявления. В случае,
если акцептор не способен к цветовому проявлению, обнаружение проводят в присутствии неокислительного окрашивающего индикатора для иминосоединений или в присутствии лейкокрасителя. При этом
лейкокраситель окисляется в присутствии иминосоединений до красителя. Средство для способа содержит PQQ-зависимую дегидрогеназу и прямой акцептор электронов - обогащенные электронами ароматические
нитрозосоединения, неокислительный окрашивающий индикатор для иминосоединений или лейкокраситель. Тест-система для способа представляет собой инертный носитель, содержащий реагенты предлагаемого
средства. Нитрозоанилиновые соединения (новые) формулы
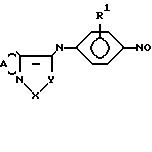
где R1 - Н, ОН, галоген, C1-C6-алкил, С1-C6-алкоксил, Х - У - N=СR6, R6 - Н, А - насыщенная или ненасыщенная трехчленная цепь с одним атомом N или S и двумя атомами углерода, или с двумя атомами азота и одним атомом углерода, атомы углерода могут быть замещены или образуют алкиленовую цепь. Эти соединения могут быть использованы в качестве хромогенных акцепторов электронов при определении аналита. Изобретение делает возможным обнаружение и определение веществ в самых различных испытуемых материалах. Способ отличается простотой. Он одностадиен, имеет меньше помех, высокочувствителен. 4 с. и 18 з.п. ф-лы, 4 табл., 7 ил.

Формула

где R1 означает водород, гидроксил, алкил, в случае необходимости замещенный гидроксилом, COOH или PO3H2, SO3H, алкокси, алкилтио, арилокси, арилтио, галоген или аминогруппу, которая в случае необходимости одно- или многократно замещена алкилом, замещенным в случае необходимости гидроксилом, PO3H2, диалкилфосфинилом, SO3H или COOH;
R2 означает гидроксильную группу, алкоксил, арилокси-, арилтио- или алкилтиогруппу, причем алкильный остаток в случае необходимости со своей стороны замещен гидроксильной группой, алкоксигруппой, в случае необходимости одно- или многократно замещенной алкилом, аминогруппой, PO3H2, SO3H или COOH как таковыми или в солевой форме, как соли аммония, щелочных или щелочноземельных металлов, или обозначает аминогруппу, NR3R4, в которой К3 и R4 могут быть одинаковыми или разными и обозначают водород, арильную или алкильную группу, которая со своей стороны может быть замещена гидроксильной, алкоксильной, гидроксиалкоксигруппой, в случае необходимости гидроксизамещенной полиалкоксигруппой, PO3H2, SO3H,COOH как таковыми или в форме соли, в случае необходимости, одно- или многократно замещенной алкилом, аминогруппой, или в которой R3 и R4 могут представлять собой алкиленовый остаток, который в случае необходимости прерывается кислородом, серой или азотом, причем азот замещен алкильным, гидроксиалкильным, гидроксиалкоксиалкильным, алкоксигидроксиалкильным, алкоксикарбонилалкильным, диоксанилилалкильным или полиалкоксиалкильным остатком, который со своей стороны, смотря по обстоятельствам, в алкильной части может быть замещен гидроксилом, или если R1 находится в ортоположении к NR3R4, то R3 или R4 также вместе с R1 может представлять собой алкиленовый остаток.

в которой X-Y - NR5-CO или N = CR6, причем R5 - водород, алкил, в случае необходимости замещенный гидроксилом, карбоксилом, SO3H, PO3H2, диалкилфосфинилом;
R6 означает водород, алкил, алкенил, алкоксил, алкилтио, арил, арилтио, аралкил, в случае необходимости, смотря по обстоятельствам, замещенный гидроксилом, диалкилфосфинилом, карбоксилом, SO3H, PO3H2, солью одного из этих кислотных остатков и/или алкоксикарбонилом, или обозначает аминогруппу, которая в случае необходимости замещена одним или двумя, в случае необходимости несущими один или несколько гидроксильных, карбоксильных и/или алкоксикарбонильных остатков, алкильными остатками, причем если аминогруппа замещена двумя алкильными остатками, то эти остатки также могут быть закрыты до образования кольца, которое, кроме N-атома аминогруппы в случае необходимости, также может прерываться кислородом, серой или другим атомом азота, или аминогруппу, которая в случае необходимости замещена одной или двумя алкильными группами, алкокси- и/или аралкоксикарбонильными группами, H2N-CO, алкил-, аралкил- и/или арилкарбамоильными группами, или обозначает водород, карбоксил, алкоксикарбонил, карбоксамидо или галоген;
R7 обозначает алкил, тиоалкил или аралкил, в случае необходимости замещенный гидроксилом, карбоксилом, SO3H или PO3H2, или аминогруппу, которая в случае необходимости замещена одной или двумя алкильными группами, которые, в свою очередь, могут быть замещены гидроксилом, карбоксилом, SO3H, диалкилфосфинилом или PO3H2, причем по меньшей мере R6 и/или R7 представляет собой аминогруппу;
R8 обозначает алкильную или аралкильную группу, которая в случае необходимости может быть замещена гидроксилом, карбоксилом, SO3H или PO3H2,
или B7 и R8 обозначают насыщенную или ненасыщенную трех- или четырехчленную цепь из атомов азота или из атомов углерода и в случае необходимости одного или нескольких атомов азота или атомов серы, причем атомы углерода в случае необходимости замещены алкилом, алкоксилом, алкилтио, гидроксилом, аралкилом, арилом, карбоксилом, карбоксамидо, алкоксикарбонилом, цианогруппой, галогеном, аминогруппой, которая в случае необходимости замещена одним или двумя, в случае необходимости несущими один или несколько гидроксильных, карбоксильных и/или алкоксикарбонильных остатков, арильными остатками, и причем атомы азота, которые не связаны через двойную связь, замещены алкилом, или аралкилом, или диалкилфосфинилом, или два соседних заместителя цепи в случае необходимости образуют алкиленовую группу, которая со своей стороны в случае необходимости замещена арилом или анеллирована с ним,
а также, в случае необходимости, соответствующие таутомерные формы и их соли.
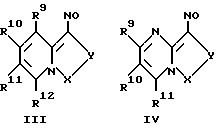
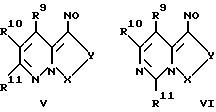


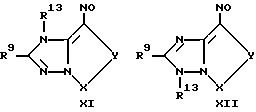
где R9, R10, R11 и R12, которые являются одинаковыми или различными, обозначают водород, гидроксил, алкил, алкоксил, алкилтио, аралкил, арил, карбоксил, алкоксикарбонил, карбоксамидо, цианогруппу, аминогруппу, которая в случае необходимости замещена одним или двумя, несущими в случае необходимости один или несколько гидроксильных, карбоксильных или/и алкоксикарбонильных остатков, алкильными остатками, или галоген, причем два соседних остатка в случае необходимости образуют алкиленовую группу, которая со своей стороны в случае необходимости замещена арилом или анеллирована с ним;
R13 обозначает алкил или аралкил, который в случае необходимости может быть замещен гидроксилом, карбоксилом, SO3H, PO3H2 или диалкилфосфинилом.
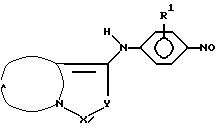
где R1 обозначает водород, гидроксил, галоген, алкоксил, алкилтио, арилокси или арилтио, в случае необходимости замещенный гидроксилом, карбоксилом, PO3H2 или SO3H, аминогруппу, в случае необходимости одно- или многократно замещенную алкилом, который, в свою очередь, в случае необходимости, может быть замещен гидроксилом, PO3H2, диалкилфосфинилом, SO3H или карбоксилом;
X-Y обозначает NR5-CO или N = CR6, причем R5 обозначает водород, алкил, в случае необходимости замещенный гидроксилом, карбоксилом, SO3H, PO3H2, диалкилфосфинилом, R6 обозначает водород, алкил, алкенил, алкоксил, алкилтио, арил, арилтио, в случае необходимости, смотря по обстоятельствам, замещенный гидроксилом, карбоксилом, SO3H, PO3 H2, соль одного из этих кислотных остатков и/или алкоксикарбонил, или обозначает аминогруппу, которая в случае необходимости замещена одним или двумя, несущими один или несколько гидроксильных, карбоксильных и/или алкоксикарбонильных остатков, алкильными остатками, причем когда аминогруппа замещена двумя алкильными остатками, то эти остатки также могут замыкаться до кольца, которое, кроме N-атома аминогруппы, в случае необходимости, также может прерываться кислородом, серой или другим атомом азота, или аминогруппу, которая в случае необходимости, замещена одной или двумя ацильными группами, алкокси- и/или аралкоксикарбонильными группами, H2N-CO, алкил-, аралкил- и/или арилкарбамоильными группами, или обозначает карбоксил, алкоксикарбонил, карбоксамидо или галоген,
A представляет собой насыщенную или ненасыщенную трехчленную цепь с одним атомом азота или серы и двумя атомами углерода или двумя атомами азота и одним атомом углерода, причем атомы углерода, в случае необходимости, замещены алкилом, алкоксилом, алкилтио, гидроксилом, аралкилом, арилом, карбоксилом, карбоксамидо, алкокикарбо.

X-Y - N=CR6, причем R6 - водород;
А обозначает насыщенную или ненасыщенную трехчленную цепь с одним атомом азота или серы и двумя атомами углерода или с двумя атомами азота и одним атомом углерода, причем атомы углерода, в случае необходимости, замещены C1-C6-алкилом, C1-C6-алкоксилом, C1-C6-алкилтио, гидроксилом, галогеном, и причем атомы азота, которые не связаны через двойную связь, возможно замещены C1-C6-алкилом, в случае необходимости, замещены SO3H, C1-C6-диалкилфосфинилом или два соседних атома углерода в этой трехчленной цепи образуют алкиленовую цепь.

Комментарии