Способ получения производных глутаминовой кислоты или их фармацевтически приемлемых солей - RU2002747C1
Код документа: RU2002747C1
Описание
кислоты ут-3-иновой кислоты и гепт-6-ено- вой кислоты, соответственно, и диметил-L- глутамата.
Пример 2. Диметил-М-{6-{2-пивалои- ламино-4-гидрокси-5,6.7,8-тетрагидропи- ридо 2,3-о пиримидин-6-ил)гексаноил -1 - глутамат.
К раствору 1,0 г диметил-М-{6-{2-пивало- иламино-4-гидроксипиридо(2.3-с1 пирими- дин- 6-ил)гекс-5-иноил}-1.-глутамата в 20 мл ледяной уксусной кислоты добавляют 300 мг оксида платины. Полученную смесь гидрируют при атмосферном давлении при перемешивании в течение 4 ч, катализатор отфильтровывают, а- полученный фильтрат концентрируют при пониженном давлении. После хроматографической обработки на силикагеле при элюировании смесью: 1:19 метанол-хлороформ получают 0,84 г (82,7%) диметил-М-{6-(2-пивалоиламино-4-гидрок- си-5.6,7,8- тетрагидропиридоС2,3-(Цпири- мидин-6-ил)гексаноил -Ь-глутамэта, т.пл. 162-166°С.
Вычислено, %: С 57.57; Н 7,54; N 13.43.
С25Н39№07.
Найдено, %: С 57,31; Н 7.25; N 14,15.
Аналогичным образом получают из ди- метил-М-{5-{2-пиаэлоия-амино-4-гидроксиг пиридо{2,3-(13 пиримидин-6-ил)пент-4-ино- ил}-Ьглутамата диметил-М-|5-(2-пиваяоила- мино-4-гидрокси-5,6,7,8-тетрагидропиридо 2,3-0 пиримидин-6-ил)пентаноилН- Глута мат. т.пл. 151-159°С.
Вычислено. %: С 56,79; Н 7,35; N 13.80.
C24H37N5O
Найдено, %: С 57.06; Н 7.22; N 13,66.
Аналогичным образом получают диме- тил-М-{3-{2 -пи8алоил амино-4-гидрокси-5)6 ,7.8-тетрагидропиридо {2.3-б пиримидин- 6-ил)-пропмонил}-и-глутамат и диметил- N (2-п и валои ламино-4-ги дрокси-5,6,7, 8-тетрагидропиридо 2,3-б пиримидин-6- ил)бутирил -Ьглутамат из М-(3-(2-пивало- иламино-4-гидроксипиридо 2,3- пири- мидин-6-ил) акрилоилН-глутамата и диме- тил-М- 4-(2-пивалоиламино-4-гидроксипир ,3-с пиримидин- 6-ил)бут-3-иноил}4 - глутамата, соответственно.
Используя эквивалентное количество диметил-М- 7-(2-пивалоиламино-4-гидрокс ипиридо 2,3-Ь пиримидин- 6-ил)гепт-6-ено- ил -1-глутамата, получают диметил-Ы- 7-(2- пиваяоиламино-4-гидрокси-5,6,7,8-тетра- гидропиридо 2,3-Ь пиримидин-6-ил}-геп- таноил -Ьглутамат, т.пл. 152-160°С,
Вычислено. %: С 58,30; Н 7,72; N 13.08,
C26H41N50
Найдено, %: С 58,51; Н 7,61; N 12.87. Пример 3. Диэтил-М-{4- 2-(2-пивало- иламино-4-гидрокси-5,6,7,8-тетрагидропиридо 2,3-с1 пиримидин-6-ил)этил}циклогек- сил-1 -ил J-L-глутамат
A.5 г 2-пивалоиламино-4-гидрокси-6-(4- 5 карбоксифенилэтинил)пиридо 2,3 пиримидина и 1,60 г оксида платины в 200 мл трифторуксусной кислоты гидрируют в аппарате Парра при комнатной температуре и
ю 4,2 эти в течение 24 ч. После удаления катализатора фильтрованием и концентрирования полученного фильтрата получают 2-пивалоиламино-4-гидрокси-6- 2-{4-кар5 боксициклогекс-1-ил) 5,6,7,8-тетра- гидропиридо 2,3-б пиримидина в виде белого твердого продукта, который далее очищают на хроматографической колонке
0 (water 200), элюируя смесью 1:9 мета- нол:дихлорметан. т.пл. 218-234°С,
Вычислено, %: С 63,35; 7,97; N 13.85.
C21H32N404
5 Найдено, %: С 63,30; Н 7,48; N 13,57.
B.К раствору 2,40 г 2-пивалоиламино-4- гидрокси-6-{2-(4-карбоксициклогекс-1-ил) 5,б,7.8-тетрдгидропиридо 2,3о (пиримидина в 50 мл сухого N-метил- пирролидона и 2,25 мл N-метилморфолина добавляют 2,75 г фенил-Ы-фенилфосфоами- нохлоридата. Полученную смесь перемеши5 вают при 0°С в атмосфере азота в течение 45 мин. а затем добавляют 2,45 г диэтил-L- гяутамата и после этого продолжают перемешивание при комнатной температуре в
0 течение 72 ч.
Растворитель отгоняют при 0,2 мм рт.ст./60°С, а остаток хроматографируют на силикагеле, элюируя смесью 1:19 метанол5 хлороформ до получения 1,67 г (48%) диэ- тил-Ы-{4-{2-(2-пивалоиламино-4-гидрокси-5 ,6,7,8-тетрагидропиридо 2.3 с1 пиримидин- 6-ил этил циклогекс-1-ил}-Ь-глутамата, т.пл.
o 160-170°С.
Вычислено, %: С 61,10; Н 8.03; N 11,87.
C30H47N50
Найдено. %: С 61,38; Н 7.90; N 11,84. 5 Пример 4. (2-амино-4-гидрокси- 5,6,7,8-тетрагидролиридо 2,3-с1 пирими- дин-б-ил)гексаноил -1 -глутаминовая кислота .
Раствор 0,5 г димедил-М- 6-{2-пивалои- ламино-4-гидрокси-5,6,7,8-тетрагидропи- ридо .З- пиримид н-б-илУексаноил Ь- глутамата в 75 мл 1.0 н. водном гидроксиде натрия перемешивают при комнатной температуре в течение -120 ч, а затем рН 7,0 устанавливают осторожным добавлением 5,0 н. соляной кислоты. Воду отгоняют при пониженном давлении, а концентрирован- ный раствор охлаждают затем на ледяной бане. Образующуюся твердую часть отфильтровывают и сушат при 80°С, получают (2-амино-4-ги дрокси-5,6,7,8-тетрагидропиридо 2 ,3-с1 пиримидин-3-ил)-гексаноилЗ-Ь глутаминоаую кислоту, т.пл. (вспенивание) 135°С, при 180-195°С.
ЯМР (ДМСО-de. 300 МГц) 6 : 9,80 (с. шир. 1Н), 7,90 (с, J - 8 Гц. 1Н), 6,20 (с, 1Н). 5,95 (с, 2Н), 4,08 (м, 1Н). 3.10 (м. 1Н), 2,63 (т, J 10 Гц, 1Н). 2,40 (м. 1Н, 2,20 Ст, J - 9 Гц, 2Н), 2,05 (т, J - 9 Гц, 2Н), 1,84 (м/1 Н), 1,70 (м, 2Н), 1,55 (м, ЗН), 1.20 {м, 6Н).
Аналогичным образом получают из ди- метил- 5-{2-пивалоиламино-4-гидр0кси-5.6 ,7,8-тетрагидропиридо 2,3-й пиримидин-б- ,ил)пентаноил -Ьглутамата М-ЈН2-амино-4- ги д рокси-5,6,7,8-тетрагидроп1фи ,3-d) пиримидин- 6-ил)пентаноия|Ч.-глутамино- вую кислоту, т.пл. 144°С (размягчение и вспенивание);
ЯМР (ДМСО-de, 300 МГц) д : 9,70 (с. шир, 1Н). 8,01 (д, J - 6 Гц. 1Н), 6.17 (с, 1Н). 5,88(с, 2Н), 4,13 (м. 1Н), 3,17 (м, 1Н), 2.68(т, J - 6 Гц, 1Н), 2,42 (м, 1Н), 2,22 (т, J - 5 Гц, 2Н), 2,07(т, J -5 Гц, 2Н), 1,86(м, 1 Н), 1,70(м, 2Н), 1.44 (м, ЗН), 1,24 (м. 4Н).
(2-амино-4-гидрокси-5,6.7,8-тет ра- гидропиридо 2.3-3 пиримидин- 6- ил)про«иомил -1 -глутаминовую кислоту и N -{4 - (2 -амино-4-гидрокси-5,6,7,8-тетра- гидропиридо 2,3 пиримидин- 6-ил)бути- р«л -1--глутаминовую кислоту получают аналогичным образом из диметил-М-{3-(2-пи- валоилэмино-4-гидрокси-5,6,7,8-тетрагидроп иридо 12,3-й пиримидмн-6-ил)пропионилН-- глутамата и диметил-М- 4-(2-пивалойламино- 4-гидрокеи-5,6,7,8-тетрагидропиридо 2,3-й пиримидин-6-ил)бутмрил -и-гпутамата соответственно..
Аналогичным образом, (2-амино-4- гидрокси-5,б,7,8-тетрагмдропиридо{2,3-0} пириммдин-б-ил)гептано«яЗ-1.-гдутамино- вую кислоту получают из д«метил-М- 7-(2- пивалоиламино-4-гидрокс«-amp;,6,7,8-тетраг идроп иридо (2,3-й п |дамидин-б-илЗ-гепта- номлЗ-Ьглутамата, т.пл, 185-195°С (со вспениванием );
ЯМР (ДМСО-de. 300 МГц) б : 9,68 (с, 1шр, Ш), 8,01 (д. J - 10 Гц, 1Н)( 6,20 (с, 1Н), 5,88 (с, 2Н), 4,14 (м, 1 Н), 3,10 (м , 1 Н), 2,66 (т, J - 9 Гц, 1Н), 2,35 (м, 1Н). 2,20 (т, J - 5 Гц, 2Н), 2,05 (т, J - 5 Гц, 2Н). 1,89 (м, 1 Н), 1,67 (м, 2Н), 1.45 (м, ЗН), 1.20 (м, 8Н).
Аналогичным образом, используя диэ- шл М-4-{2-{2-пивалоиламино-4-гадрокси-5 ,6,7,8-тетрагидропиридо 2,3-й пиримидин- 6:ил)этил}циклогекс-1 -ил-1 -глутамат, получают Ы-4-{2-(2-амино-4-гидрокси-5.6,7,8-тетраги- дропиридо 2,3-а1 пириммдин-б-ил)этилЗциклогекс-1-ил -Ьглутаминовую кислоту, т.пл. 210- 225°С.
ЯМР (ДМСО-de, 300 МГц) д : 9.70 (с, шир. 1Н),7,90(м, 1Н),6,23(с, 1Н),5,92(с.2Н). 4,17 (м, 1 Н), 3,18 (м, 1 Н). 2,72 (т, J 9 Гц, 1 Н), 2,45(м, 1 Н), 2,27 (т. J - 6 Гц, 2Н), 2.09 (м, 1 Н). 1.96 (м, 1 Н). 1.74 (м, ЗН), 1,45 (м. 5Н), 1,27 (м, 8Н).
Пример 5. Диметил-М-{5-(2-пи8алои- flaMHHO-4-rMApOKcnnnpHAot2.3-d nMpHMM- дин- 6-ил)этинилХтиен 2-илкарбонил)-1 -глу- тамат
A.Раствор 1,50 г (7.25 ммоль) 5-бром-2- тиофенкзрбоновой кислоты, несколько капель диметилформамида и 2,21 мл тионилхлорида нагревают с обратным холодильником в течение 2,5 ч. Растворитель удаляют при пониженном давлении, а остаток растворяют в -10 мл сухого метиленхло- рида. Этот раствор добавляют по каплям к осажденному льдом раствору 1,62 г диме- тил-1 -глутаматгидрохлорида, 10 мг димети- ламинопиридина и 2,11 мл триэтиламина в 25 мл сухого метиленхлорида. После завершения добавления полученную смесь перемешивают при комнатной температуре в течение 12 ч, а затем разбавляют водой и экстрагируют метиленхлоридом. Органические экстракты промывают 0,1 н. соляной кислотой и насыщенным раствором бикарбоната натрия, а затем выпаривают, получают 2.71 т (100%) диметил-1 -(5-бромтеег- 2-илкар- бонил)-1--глутамата в виде вязкого масла, которое можно использовать в дальнейшем без последующей очистки.
Диметил-М-(5-бромофур-2-илкарбонил) -L-глутамат, также в виде вязкого масла, получают аналогичным образом из 5-бром- 2-фуранкарбоновой кислоты
Диметил-М-(5-бромтиен-3-илкарбонил) -L-глутаМат можно получить аналогичным образом из 5-бромтиенилкарбоновой ки слоты ,
B.Смесь 1,70 г (6,32 ммоля) 2-пивалои- ламино-4-шдрокси-6-этинилпиридо 2, пиримидана, 2,30. г (6,32 ммоль) диметил-1- (5-бромтиен-2-илкарбонил)-1 -глутамата, 44 мг палладий-хлорида, 130 мг трифенилфос- фина, 25 мг иодида меди (I) и 1,13 мл триэтиламина в 30 мл ацетонитрила нагревают с обратным холодильником в течение 3 ч, а затем охлаждают до комнатной температуры . Растворитель удаляют при пониженном давлении, а остаток обрабатывают на хро- матографической колонке (Waters 500), злю- ируя смесью 1:19 метанол :метиленхлорид до получения диметил-М- 5-(2-пивалоилами- но 4-гидроксипиридо 2,3-й пиримидин-б- ил)этинилХтиен-2-илкарбонил)-1.-глутамата, т.пл. 228-230°С.
Вычислено, %: С56,41 ;Н 4,92; N12,65; S 5,79.
C26H27N507S
Найдено, %: С 56.64; Н 4.77; N 12,88; S 5.58.
Аналогичным образом, заменяя эквивалентным количеством диметил-М-(5-бром- фур-2-илкарбонил)-1 -глутамата диметил-М-(5-бромотиен-2-илкарбонил)-1.- глутамат в вышеописанной процедуре, получают диметил-М- 5-(2-пивалоиламино-4- гидроксипиридо 2,3-с 3пиримидин- 6-ил(фур-2-илкарбонил)-1 -глутамат, т.пл. 135°С (с потемнением), 181°С (разложение).
Вычислено. %: С 58,32; Н 4J1; N 13,08.
C26H25N508
Найдено, %: С 58.58; Н 4,92; N 1ff.11.
Аналогично, заменяя эквивалентным количеством диметил-М-(5-бромтиен-3-ил- карбонил)-1 -глутамата диметил М-(5-бром- тиен-2-илкарбонил)-1 -глутаматв вышеописанной процедуре, получают диме- тил-М-{5-{2-пивалоиламино-4-гидрокс«яи- .3-6 пиримидин- б-йл)этил(тиен-3- илкарбонил)-1 -глутамат.
Пример 6. Диметил-Г4-{5-{2-(2-пива- лоиламино-4-гидрокси-5,6,7,8- тетрагидро- пи , и рими дин-6-ил) н-2 -илкарбонил-L- глутамат
К раствору 0,5 г диметия-Ь{5-{2-пивало- иламино-4-гидроксипиридо 2,3- пирими- дин-6- ил этинил тиен-2-илкарбонил)-Ь-глу- тамата в 3amp; мл ледяной уксусной кисл ты добавляют 1,5 г 5% палладия на угле. Полученную смесь гидрируют при давлении 1 ати при перемешивании в течение 18ч, катализатор отфильтровывают, а полученный фильтрат концентрируют при пониженном давлении. После хроматографической обработки на -силикагеяе при элюировакии смесью 1:19 метанол:хлороформ, получают 100 мг 19,7% диметил-М-{5- 2-(2-пивалоила- мино4-гидроксипиридо{2,3-ч1 пиримидив- 6-ил)этил тиен-2-илкарбонил}-1,-тлутамата и 204 мг (40.2%) целевого диметил-М-{5-{2-{2- пивалоиламиио-4-гидрокси-5,6,7,8- тетра- гидропиридо 2,3 пиримидин-6-ил)этил тмен-2-иякарбонил}-1.- глутамата, т.пл. 152-160°С.
Вычислено, %: С 55,60; Н 6,28; N 12,47.
C25H35N50
Найдено, %: С 55,76: Н 6,23; N 12,26, Частично1 гидрированные побочные продукты можно повторно гидрировать до получения дополнительного количества целевого продукта.
. Аналогичным образом получают из ди- метил-М-(5-пивалоиламино-4-гидроксипи- ,3-й пиримидин-б-ил) этинил(фур-2- илкарбонил)-Ьглутзмата диметил-г4-{542- (2-пивалоилэмино-4-гидрокси-5,6.7,8-тетрагидропиридо 2,3- 1 пиримидин-6-ил)- 9тил фур-2-илкарбонил}-Ь-глутамат, т.пл, 155-162°С. Вычислено, %: С 57,45; Н 6.12; N 12,88.
C26H33N508
Найдено. %: С 57.22: Н 6.08; N 12.66. Аналогичным образом можно получить
диметил-Ы-{5-{2-{2-пивалоиламино-4-гид- рокси-5,6,7,8-тетрагидропиридо 2, римидин-6-ил)этия тиен-3-илкарбонил}-1. глутамат из диметил-Ы- 5-{2-пивалоиламино-4-гидроксипиридо 2 ,3-с1}пиримидин-6- ил)этинил тион-3-илкар6онил-и-глутамата.
ГГр и м е р 7. М-{5-{2-{2-амино-4-гидро- кси-5,6,7.8-тетрагидропиридо 2,3-б пиримидин-6-ил )этил тиен-2-илкарбонил}-1--глу- таминовая кислота
Раствор 100 мг диметил-ЬЬ{5 {2-{2-пива- лоиламино-4-гидрокси-5,6,7,8-тетрагидропиридо 2.3-Ь пиримидин-6-ил)этил}тиен- 2-илкарбония}-1-глутамата в 15 мл 1,0 н. водного гидроксида натрия перемешивают при комнатной температуре в течение 120 ч,
а затем рН 7.0 устанавливают путем осторожного добавления 5,0 н. соляной кислоты, Образующийся твердый продукт собирают фильтрованием и сушат при 80°С. получают
61,5 мг (76,8%) М-{5-{2-{2-амино-4-гидрокси- 5.6,7,8-тетрагидропиридо 2,3-с1 пирими- дин-6-ил)этил тион-2-ил карбон ил)-и-глута- миновой кислоты, т.пл. 226-240°С (вспенивание и разложение).
ЯМР(ДМСО-ае) (5:9,80(с.шир, Ж). 8.45 (д, J 9 Гц, 1Н), 7,62 (д. J - 3 Гц. 1 Н). 6,87 (д, J - 3 Гц, 1 Н), 6.30 (с, 1 Н), 6,04 (с. 2Н). 4,28 (ш,
1Н),3.12(м, 1Н),2,84(м.ЗН),2-.36(м, 1Н),2.02 (м, 1Н). 1,83 (м, 2Н), 1,57 (м, ЗН).
Аналогичным образом из диметил-М-{5-{2- (2 -пивалоиламино-4-гидрокси- 5,6,7,8-тетрагидропиридо (2,)пиримидин-6-ил) 2-илкарбонил}-и-глутамата получают Ы-{5-{2- С2-амино-4-гидрокси-5,6,7,8-тетрагидропири пиримидин-6-ил)этил фур-2-илкарбонил}Ч .-глутаминовую кислоту, т.пл. 204-230°С (со вспениванием).
ПМР (ДМСО-de. 300 МГц) д : 9,80 (с, шир, 1Н). 8.27 (д, J - 9 Гц. 1 Н). 7,03 (д. J - 4 Гц, 1 Н), 6.30 (с, 1 Н), 6,25 (д. J - 4 Гц, 1 Н). 6,04
(с, 2Н), 4.03 (м, 1Н),3,15(м, 1Н). 2,65 (м.ЗН), 2,42 (м, 1 Н), 2.16 (т, J - 7 Гц, 2Н). 2.01 (м, 1Н), 1,84(м,2Н). 1.57 (м.ЗН).
1Ч-{5Ч2-(2-амино-4-гидрокси-5,6,7,8-те- трагидропиридо(2-,3-й1 пиримидин-6- ил)зтил}тиенил-3-илкарбонил}-1.-глутами- новую кислоту можно получить аналогичным способом из диметил-ЈЦ5-{2-{2-пивало- иламино-4-гидрокси-5,6,7,8-тетрагидропи - ридо М- 2,3-б пиримидин-6-ил)этил тиен-3- иякарбонил}-и-глутамата.
Пример 8. HKso для линии клеток лейкемии человека CCR FCEM М-{5-{2-(2- амино- -гидрокси-бДТ.б-тетрагИдропири- ,3-d пиримидин-6-ил)этилЗтиен-2-ил- карбонияН--глутаминовой кислоты составляет 0,0015 Mkr/мл.
MKso (2-амино-4-гидрокси- 5,б,7.8-тетрап1Дролмридо 2,3-йЗ пирими- дин-6-ил)этил фур-2-иякарбонил}-1.-глута- миновой кислоты составляет 0,010 мкг/мл И Kso М-4-(2-(2-амино-4-гидрокси-5,б,7.8-тет- рагидропиридо 2,3-сП пиримидин-6- .ил)этил тибн-2-илкарбонил}-С-глутамино- вой кислоты составляет 0,0756 мкг/мл.
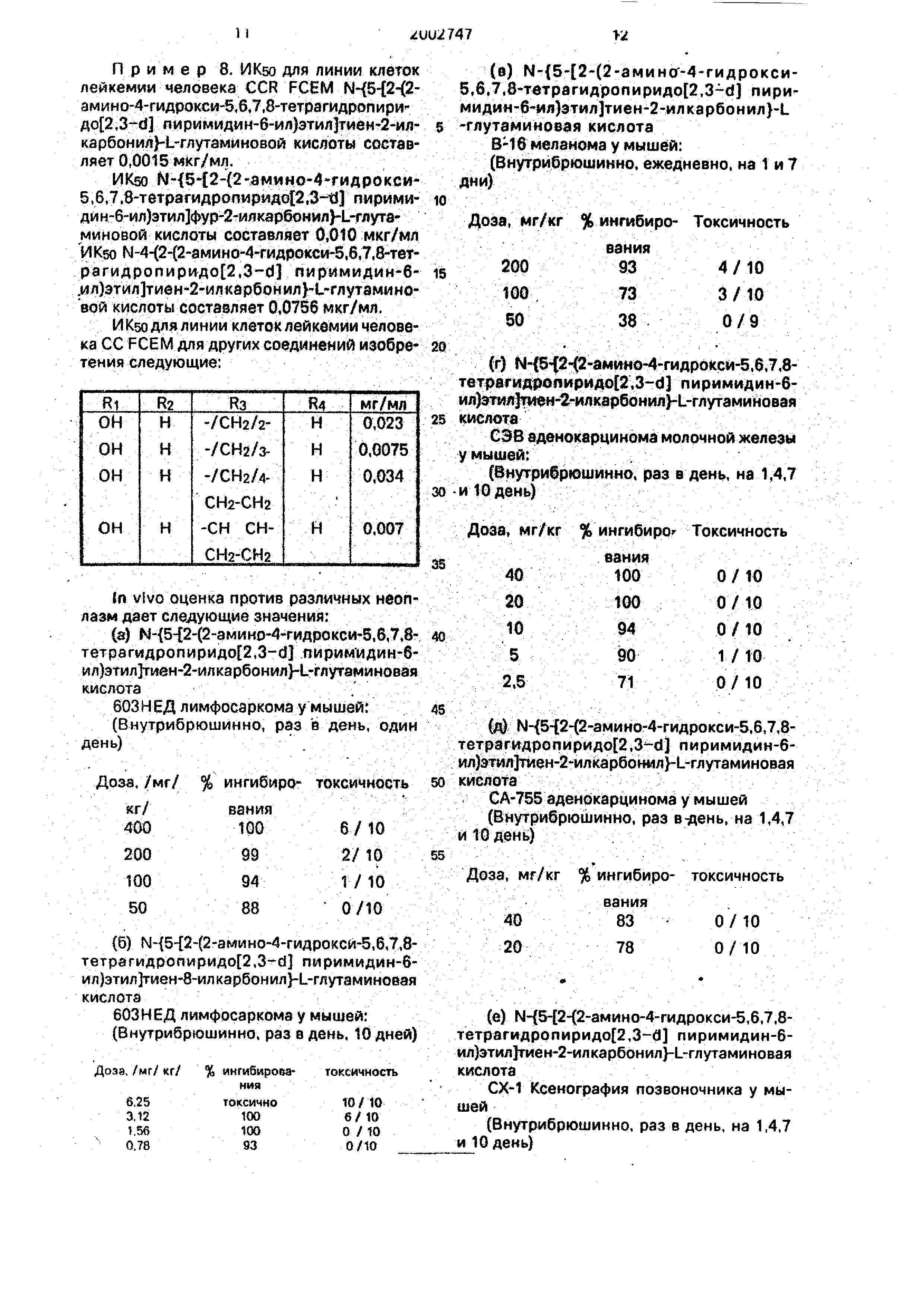
И Kso для линии клеток лейкемии человека СС FCEM для других соединений изобретения следующие:
(в) М-{5- 2-(2-аминог-4-гидрокси- 5,6,7,8-тетрагидролиридо 2, пири- мидин-6-ия)этил тиен-2-илкарбонил}-1 -глутаминоеая кислота
В-16 меланома у мышей:
(Внутрибрюшинно, ежедневно, на 1 и 7 дни)
Доза, мг/кг % ингибиро- Токсичность
20
(г) 4-{5-{2-(2-ами«о-4-гидрокси-5,6,7,8- тетрагидропиридо 2,3-(1} пиримидин-6- ил)этил}тиен-2-илкарбонил}-1-глутаминовая 25 кислота
СЭВ аденокарцинома молочной железы у мышей:
(Внутрибрюшинно, раз в день, на 1,4,7 зо -и 10 день)





Реферат

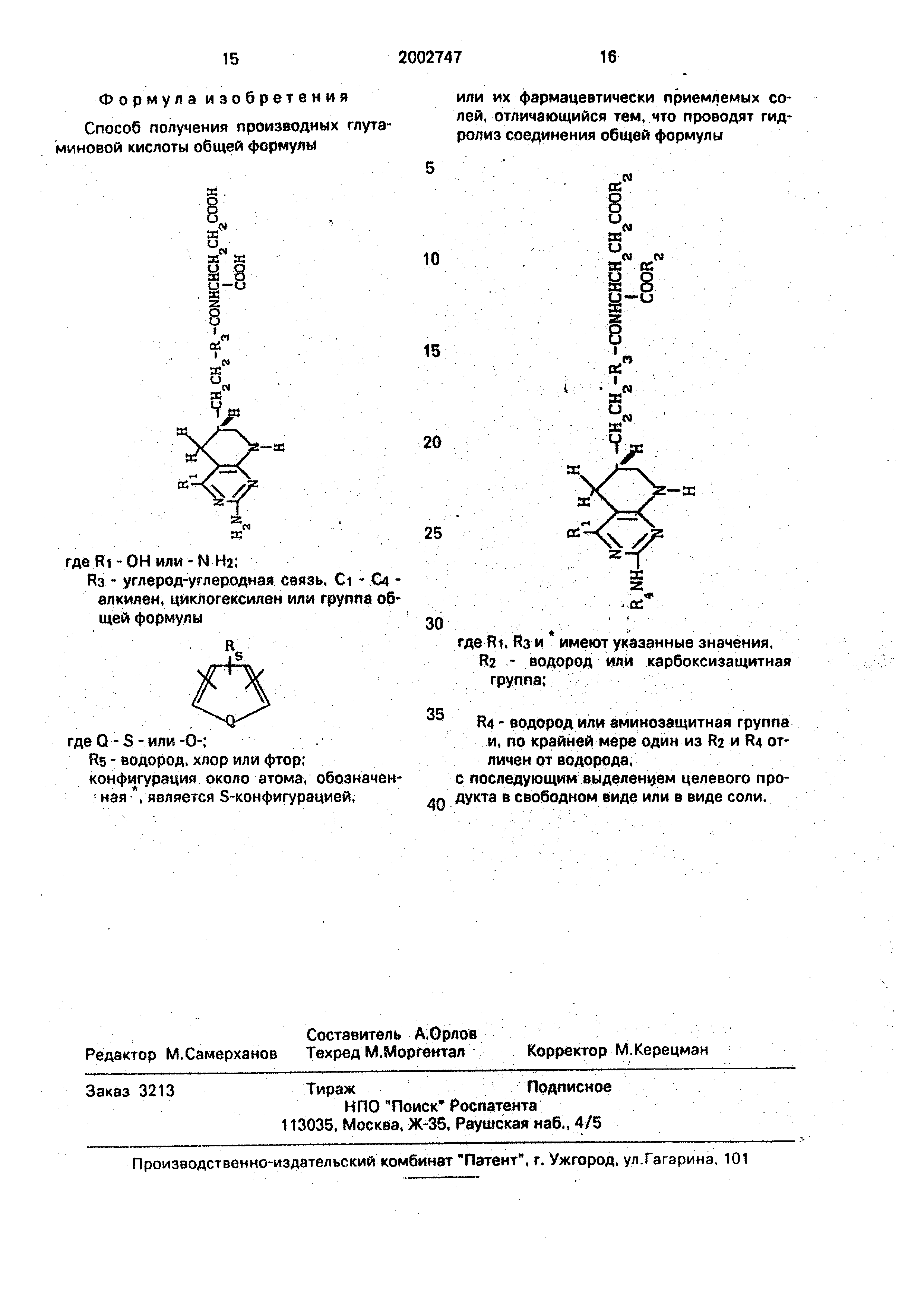
Формула

Комментарии