Способ получения амидов лизергиновой кислоты или их солей - SU468419A3
Код документа: SU468419A3
Описание
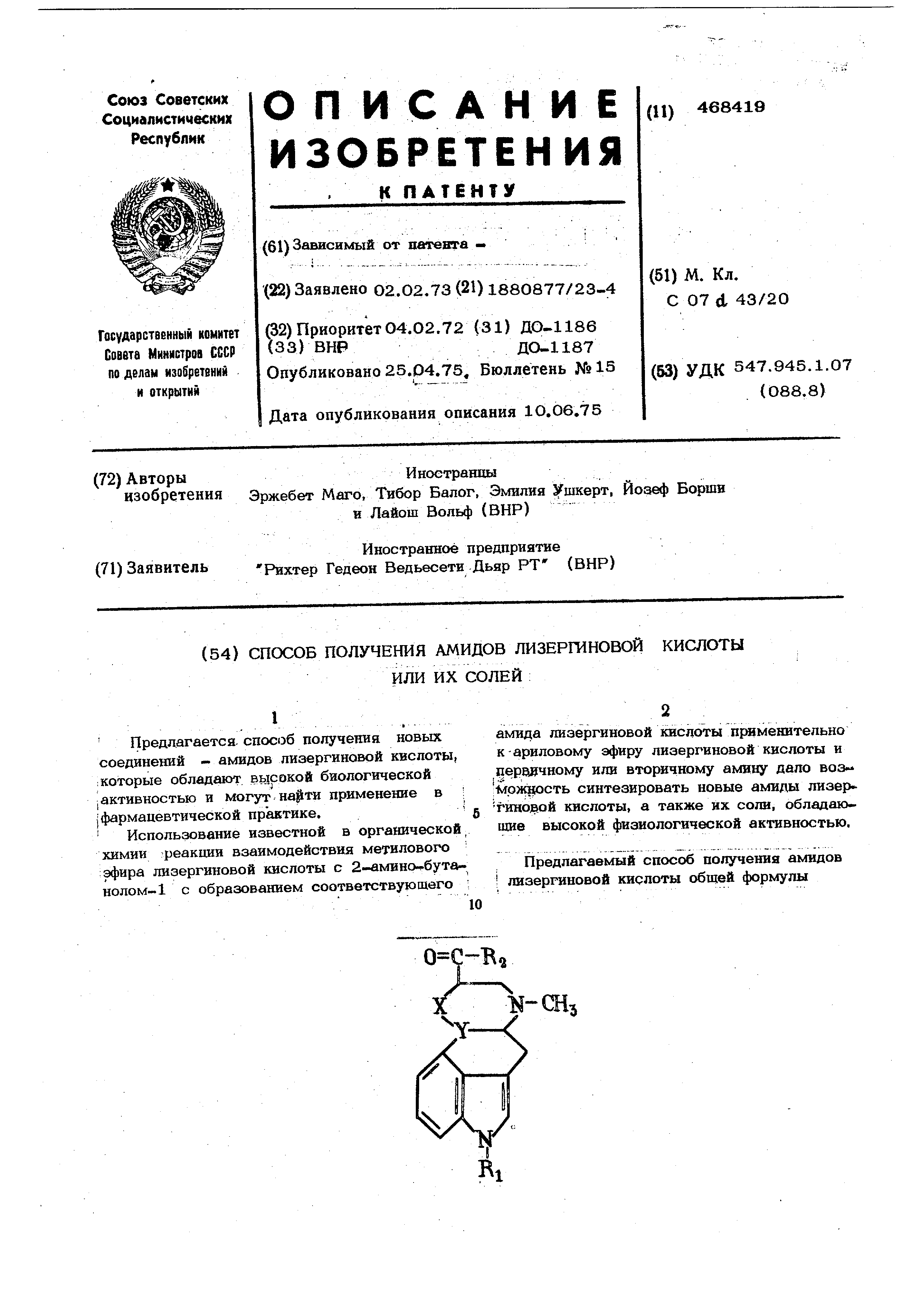
(54) СПОСОБ ПОЛУЧЕНИЯ АМИДОВ ЛИЗЕРШНОВОЙ КИСЛОТЫ
ИЛИ ИХ СОЛЕЙ



Реферат

Формула
где X - V др)едставляют собой группу
iX;
( или -СН водород или метил;
группа аминоспирта.сложного эфира
аминокислоты, алкилаклина, ариламина,: .замещенного ариламина или эаме- ; щенная гитероциклическая rpyrmai
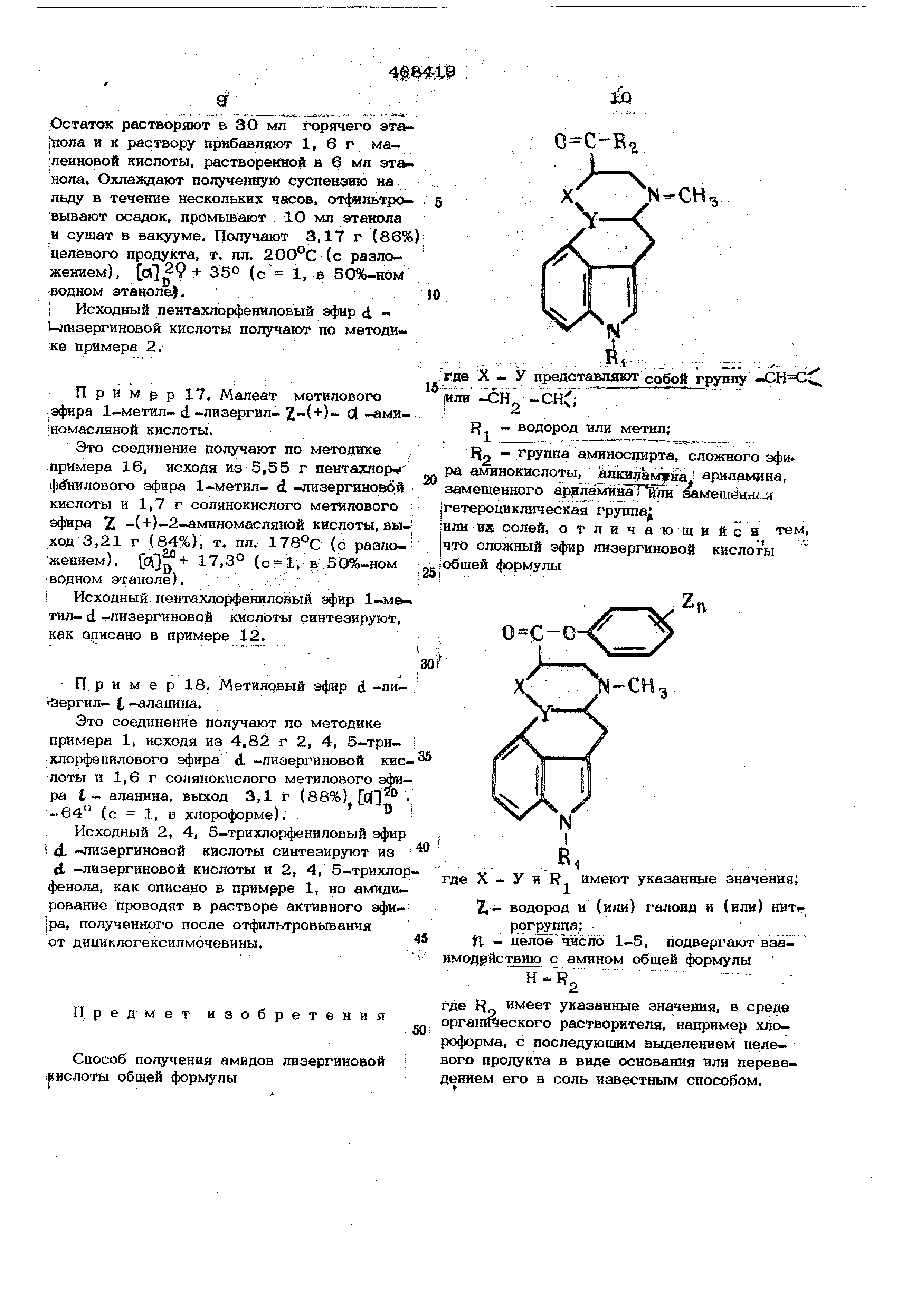
или их солей заключается в том, что сложный эфир лизергиновой кислоты общей фор-, мулы
где X - У и R имеют указанные значения; Т.- водород и (или)галоид и (или) нитрогруппа;
Л, - целое число 1-5,
подвергают взаимодействию с амином общей формулы
Н - R
где R имеет указанные значения;
i
в среде органического растворителя, например
хлороформа, с последующим выделением целевого продукта в виде основания или переведением
его в соль известным способом;
Предлагаемый способ позволяет получать
очень чистый продукт с хорошим выходом в i мягких условиях реакции без образования побочных продуктов.
Во время реакции не происходит ни изо- ;меризации, ни рацемизации, выход почти
количественный. Этот способ может быть
1
|арименен для получения любых амидов лизергиновой . кислоты, N -алкиллизергино-
вых кислот, 9, 1 б-дигидролизергиновой .кислоты и -алкил-9, 10-дигидролизергиновых кислот..
Особенно выгодно использовать в качестве активных сложных эфиров лизергиновой
кислоты пентахлорфениловый эфир. Реакцию |предпочтительно проводить в присутствии
Инертного растворителя, такого как хлоро:форм , тетрагидрофуран, ацетонитрил, мети|ленхлорид
и диметилформамнд. Активные i с ложные эфиры лизергиновой кислоты могут
I быть употреблены в выделенной форме, но 5; реакцию можно также проводить, используя
i реакционную смесь, в которой были образованы эти активные эфиры, i В качестве аминных реагентов можно
: применять любые замещенные аминосоеди-
10нения, например моно- и полиокеиаминоспир ты
, моно- и дизамещенные алкиламины, аминокислоты, ди- и трйпептиды, монозаме
щенные пиперазины, ариламины, например анилин и производные анилина, аминопири15 дины и т. п.
Пример. 4-метоксианилид 1-ме |тил-9, 10-дигидро- d. -лизергиновой кисло5
,53 г пентахлорфенилового эфира I-Me20 тил-9, 10-дигидро- d-лизергиновой кислоты
растворяют в 100 мл сухого хлороформа при перемешивании, затем раствор охлаждают
в ледяной воде и прибавляют по каплям 1,35 г 4-метоксианилина, раство-
25 ранного в 10 мл хлороформа. Раствор 1 ча перемешивают при комнатной температуре,
затем экстрагируют 6 х 25 мл 1%-ным водным раствором винной кислоты. Объеди
няют водные экстракты и устанавливают
30 рН объединенных экстрактов 8 добавлением
нескольких миллилитров 10%-ного водного раствора гидроокиси аммония. Водный раствор
встряхивают с хлороформом 5x50 мл. Объединяют хлороформные экстракты,
сушат сульфатом натрия, фильтруют и упаривают в вакууме. Остаток растворяют в
1О мл бензола и бензольный раствор выливают в ЗОО мл сухого петролейного эфира.
Отфильтровывают выпавший осшафок, промывают его небольшим количеством петролейного
эфира и сушат в вакууме. Продукт хроматографируют на колонке с окисью алю.
миния, используя смесь бензола и хлорофор ма (3:2) в качестве элюирующего агента.
рТаким путем получают 3,56 г (91%) 4I -мётоксианилида 1-метил-9,1О-дигидро-с1
-лизергиновой кислрты, т. пл, 159 С.
Исходное соединение; 1-метил-9, 10-дигидро-
d -лизергановую кислоту в виде пентахлорфенилового сложного эфира,получают
следующим образом; 1,43 г высушенной от воды 1-метил-9,-1О-дигидро-d-дизергиновой
кислоты суспендируют в 6О мл. абсолюного металенхлорида, затем прибавляют
1,35 I пентахлорфенола. Полученный раство охлаждают при перемешивании до О -50с
и прибавляют маленькими порциями в тече 5- ; , .; 6 ние 2 час 1,25 г дидаклогексалкарбодтшми- нилового эфира 9, 1О-дигидро d лизергида
. Раствор постепенно нагревают до 20°С новой кислоты и 2,0 г 2-амино-5-бромпичи
перемешивают еще 2 час. Отфильтровы-ридина, 3,4 г (80%), т. пл. 132°С. вают кристаллы дициклогексилмочевины и ,Исходный 2, 4, 5-трихлорфениловый
промывают 10 мл тетрагидрофурана. Объеди- 9, 10-дигидро-d -лизергнновой кисняют
фильтрат и промьтную жидкость и вы- лоты синтезируют из 9, 1О-дигидро- Ы паривают
досуха при пониженном давлении. ; -лизергиновой кислоты и трихлорфено а по Сухой остаток растворяют в горячем состою: методике примера 1.
ЯНИН в 5 мл бензола и полученный растворП р и м е р 6. 1 етил-9, Ю-дигидвыливают при перемешивании в 50 глппет- юро- d--лизергилгяицилтирозинол,
ролейного эфира. Получетшую суспензию Это соединение получают по методике
обрабатывают на льду в течение 24 час;,примера 1, исходя из 5,53 г пентахлорфепосле
чего продукт фильтруют, промьшаютнилового эфира ,;1-к:егал-9, Ю-дигидро2О
мл холодного петролвйногр эфира и сут-; d -лизергиновой KHcnoTW и 2,8 г глицилшат
в вакууме, выход 2,О г (75%),.t 15.тирозннола, выход 4,Э г (89%), т. пл. 152°С. 2О° (с 0,5, этанол). :Исходнь1й пентахлорфениловый эфир 1
„ X .. 4-метил. 9, 10-дигидро-cL -лизергиновой П р и м е р 2. 4-Метоксианилид d. -. « «к и.
, кис лоты синтезируют по методике примера, -лизергиновой кислоты..,„ , h-
Пример 7, 3-Трифторметиланилид Это соединение получают по методике , -г t- « ,
.i 20 9, lO-дигидро- А -лизергиновой кислоты, примера 1, исходя из 5,37 г пентахлорфе-. м «j- и-t
, ., „Это соединение получают по Методике нилового эфира d -лизергиновой кислоты.1
1 0 0/примера 1, исходя из 5,39 г пентахлорфеи 1,5 г р -метокснанилина, выход 84%- „ -, л
Го 1x1 т,„ 10-70,-нилового эфира 9, 10-дигидро- d-лизерги 3jX T Г/ Т пл J. / ч,огч ,,
„,о V Iновой кислоты и 2, о г 3-трифторметиланиИсходный пентахлорфениловыи эфир d -.. /-TOO/ -I«/ O
/ ; , 25 лина, выход 3,1 г (72%), т. пл. 13О°С. -лизергиновой кчслоты синтезируют из4-,.„.-j. ,
„1Исходный пентахлорфениловыи эфир 9. -лизергиновой кислрты и пентахлорфенола , i
по методике, опиской в примере 1, вькод Ю-дигидро- d -лизергиновой кислоты син62% .Га} + 31 . (с 0.5. этанол).. - зируют, как описано в примере 1.
П р е р 3. 4-Метоксианилид 9,Ю- i „ 3-Трифторметиланилид -дигидро-а. -лизергиновой кислоты. . 10-дигидро- d -лизергиновой
KWf JTfTPF Эго соединение получают по методике . , с or,J. Это соединение получают, как описано
примера 1. исходя из 5,39 г пентахлорфе- Аг , „ .,В примере 1. исходя из 4.О5 г 4-нитронилового
эфира 9. 10-дигидро- d -лизерги- ,.,./ -.г-фенилового эфира 1-метил-9, 10-дигндроновой
кислоты и 1,5 г л-метоксианилина, j м мн 0-1 00 со/ ioxiO 35 - Л лизергиновой кислоты и 2,0 г 3-трив
количестве 3.1 г (82,5%), т. пл. 164 С. ., о /c. .. „,. л. п 1 п фторметиланилина, выход 2,9 г (68%).
Исходный пентахлорфениловыи эфир 9,1О-;д -дигидро- d -лизергиновой кислоты получа- , „ . ,
v . „Исходный 4-нитрофениловыи эфир 1-меют из 9, 10-дигидро- d-лизергиновой кис-гч i , 5 ,
тил-9,10-дигидро-d -лизергиновой кислолоты и пентахлорфенола по методике, опи-. . v, ... , ,.
n/ L оО40 ты получают из 1-метил-9,10-дигидро-d санной в примере 1. выход 69,5%.LC(J +3 „ .
/ г- .тизергиновои кислоты и 4-нитрофенола по ( с О,5. этанол).„ ,
т-г . о / и V c методике, описанной в примере 1. но амиП р и м е р 4. 6-(4-Хлор-5-нитропи-« , t- ,
, „дирование проводят в растворе активного римидино) амид а -лизергиновой кислоты.-. эфира
, полученного после отфильтровывания Это соединение синтезируют, как описано. 45 дициклогексилмочевины.
в примере 1, исходя из 5,37 г пентахлор- , фенилового эфира d -лизергиновой кислотыП р и м е р 9. Алпиламидмалеат-d и
2,0 г 4-хлор-5-нитро-6-аминошфИмидина ..-яизергино вой. кислоты.... „. .„ гГ/4.п, Свободное основание получают по методив
количестве 3,2 г (74%), т. пл 240Ос.: г пента . Исходный пентахлорфениловыи эфир-d- во;хЛорфенилового эфира d -лизергиновой кис.
-лизергиновой кислоты получают, как | и 1. О г { -аллиламина. Свободное описано в примере 2.i- - -
,,с .-. / - основание, синтезированное после хромато11 р и м е р о, 2-I Ь-Бромпиридино)-,щ;
- „ Р J Р м пи/графин, растворяют в 20 мл горячего этаамид 9, 1О-дигидро-d -лизергиновой кис-, г- -г г-г
. нола и к раствору прибавляют раствор 1,2г . СЕ„г. .., 00 малеиновой кислоты в 5 мл этанола. От-
Соеаине,ше получают по методике приме- . ф„„ьтровывают выпавшую в осадок кристалра
1, иг:ходя из 4,7 г 2, 4, 5.трихлорфе-|„„ ескую соль и промывают небольшим ко. 4684IS
7личеством холодного этанола, потом сушат.
Получают 3,6 г (84%) целевого продукта, т. пп. 179°С. Исходный пентахлорфениловый эфир d
,.лизергиновой кислоты получают по методи- ке примера «Пример 1О. Аллиламид 1-метил-9
, 10-дигидро- 4- -лизергиновой кислоты. Это соединение синтезируют по методике
примера 1, исходя из 5,53 г пентахлор фенилового эфира 1-метил-9, 10 дигидро-
- d -лнзергиновой кислоты и 1,О г t -аллиламина . Получают 3, 1 г (96%) пелевого продукта, т, пл. 189 С.
Исходное соединение пентахлорфенило- вый эфир 1-метил-9,1О-дигидро d-лизергиновой
кислоты получают по методике примера 1. П р и м е р 11. 2-(1-Оксибутил) амид малеат
d -лизергиновой кислоты. Это соединение получают по методике
примера 9, исходя из 5,37 г пентахлорфенилового эфира d -лизергиновой кислоты
и 1, 1 г (+)- -окси-Яминобутана, выход 3,85 г (84,5%), т. пл. 2ОО°С, +
47,0° (с 1,0, вода).° Исходный пентахлорфениловый эфир А -лизергиновой
кислоты синтезируют по методике примера 2. При мер 12. 2-( 1-Оксибутил) амид
малеат 1-метил- d -лизергиновой кислоты. Это соединение получают по методике
9, исходя из 5,51 г пентахлорфенилоБого эфира 1-метил- d -лизергиновой
кислоты и 1,1 г (+)-1-окси-2-аминобутана , выход 4,12 г (83%), т. пл. 183°С,
;№)+ 42,0°(с 0,4. вода). Исходный пентахлорфениловый эфир 1-ме
тил- it -лизергиновой кислоты, синтезируют из 1-метил- d -лизергиновой кислоты и
пентахлорфенола по методике примера 1. Пример 13. 4-( j3 -Оксипропил)пиперазидмалеат
9, 1О-дигидро- 4- -пизер;гиновой кислоты. Это соединение получают по методике
примера 9, исходя из 5,;39 г пентахлорфенилового эфира 9, 1О-дигндро- d -лизергиновой
кислоты и 1,75 г ( J8 -оксипропил пиперазина, выход 4,9 г (93%), т. пл. 207
M|° -4 9°(с 0,5, водный этанол). Исходный пентахлорфениловый эфир 9, 1О
Q -дйгидро- d -лизергиновой кислоты синтезируют , как описано в примере 3. .
П р и. 14..Метиловый эфир 1-метил- .б,: 1р-диг«дар ; зергт1л- СО -нитро--2-арРИНИНй| .- ,:;. .
Растворяют;5,53 г пентахлорфенилового эфира 1-метил-9, 1О-дигидро- d -лизергиновой
кислоты в смеси 5 О мл хлороформа и 50 мл тетрагидрофурана при перемешивании
и к холодному раствору прибавляют 3,5 г солянокислого метилового эфира- Z - со -нитро-
2. -аргинина, растворенного в смеси .-хлороф9рма 9 мл триэтиламина.
Реакционную смесь пе|)емешивают при комнатной температуре 2 час, затем экстрагируют
(5 X 30 мл) 1%-ным водным раствором винной кислоты, далее поступают, как
в примере 1. Получают 4,2 г (86,5%) целевого продукта, т. пл. 220 С.
Исходный пентахлорфениловый эфир 1-метил-9 , 10-дигидрсЦлизергиновой кислоты
получают по методТ ке примера 1. При мер 15, Диметиламид d -лизергиновой кислоты.
Это соединение получают по методике примера 1, исходя из 2,7 г пентахлорфенилового
эфира 4 -лизергиновой кислоты и 0,5 г диметиламина, выход 1,3 г (88%), о
Lcajjj + ЗО (в пиридине). Исходный пентахлорфениловый эфирй -лизергиновой
кислоты синтезируют по методике примера 2. П р и м е р 16. Малеат метилового эфира
d -лизергил- Х-(+)-С1- миномасляной кислоты. 1,7 г солянокислого метилового эфира
(+)-2-аминомасляной кислоты (т. пл. |94-960с, 21°, с 5, в 20%-ной
соляной кислоте) суспендируют в 15О мл хлороформа и охлаждают суспензию до 1О С.
К перемешиваемой суспензии прикапывают ,4 мл триэтиламина, после чего к полученному
раствору прибавляют 5,37 г пентахлорфенилового эфира d -лизергиновой кислоты, реакционную
смесь перемешивают еше 30 мин. Реакционную массу разбавляют ЗОО мл хлороформа
и экстрагируют (2 х 50 мл) 1% нь1М водным раствором винной кислоты.
Устанавливают рН объединенных водных экстрактов, равным 7-7,5, используя 10%ную
водную гидроокись аммония, и этот водный раствор экстрагируют хлороформом
(4 X 50 мл). Объединяют органические фазы , сушат безводным сульфатом магнмя,
фильтруют и упаривают досуха в вакууме.



Комментарии