Модифицированные цитоксины и их терапевтическое применение - RU2018107843A
Код документа: RU2018107843A
Формула
1. Соединение формулы (I)

где A1 представляет собой органическую группу; или A1представляет собой гидрофильную группу или атом водорода;
A2 представляет собой фрагмент цитотоксического лекарственного средства, который имеет молекулярную массу не более 1600 Да;
X1 представляет собой гидрофобную группу; и
X2 представляет собой простую связь, органическую группу, -O-, -S-, -S(=O)-, -S(=O)2-, -S-S-, -N=, =N-, -N(H)-, -N=N-N(H)-, -N(H)-N=N-, -N(OH)- или -N(=O)-.
2. Соединение по п.1, где A1 представляет собой группу карбоновой кислоты, карбоксилатный анион или карбоксилатный эфир.
3. Соединение по п.2, где A1 представляет собой группу карбоновой кислоты.
4. Соединение по любому из пп.1-3, где фрагмент цитотоксического лекарственного средства имеет молекулярную массу не более 1500 Да, или не более 1400 Да, или не более 1300 Да, или не более 1200 Да, или не более 1100 да, или не более 1000 Да.
5. Соединение по любому из пп.1-4, где фрагмент цитотоксического лекарственного средства представляет собой органический фрагмент.
6. Соединение по любому из пп.1-5, где фрагмент цитотоксического лекарственного средства представляет собой часть лекарственного средства, выбранного из группы, состоящей из: фрагмента паклитаксела, фрагмента этопозида, фрагмента гемцитабина, фрагмента циклофосфамида, фрагмента хлорамбуцила, фрагмента доксорубицина, фрагмента даунорубицина, фрагмента 5-фторурацила, фрагмента дактиномицина, фрагмента амифостина, фрагмента флударабина, фрагмента топотекана, фрагмента ифосфамида, фрагмента винкристина, фрагмента карбоплатина, фрагмента винбластина, фрагмента иматиниба, фрагмента леналидомида, фрагмента пеметрекседа, фрагмента абиратерона, фрагмента эрлотиниба, фрагмента бортезомиба, фрагмента оксалиплатина, фрагмента метотрексата, фрагмента карфилзомиба, фрагмента кризотиниба, фрагмента висмодегиба, фрагмента пoнатиниба, фрагмента тивозаниба, фрагмента карбозантиниба, фрагмента эпирубицина, фрагмента доцетаксела, фрагмента цисплатина, фрагмента эрибулуна, фрагмента иксабепилона, фрагмента винорелбина, фрагмента эверолимуса, фрагмента митомицина С, фрагмента сунитиниба, фрагмента иринотекана, фрагмента леиковорима, фрагмента третиноина, фрагмента аллопуринола, фрагмента аспарагиназы, фрагмента бендамустина, фрагмента блеомицина, фрагмента фолиновой кислоты, фрагмента капецитабина, фрагмента цитарабина, фрагмента дакарбазина, фрагмента филграстима, фрагмента гидроксикарбамида, фрагмента меркаптопурина, фрагмента месна, фрагмента прокарбазина, фрагмента тиогуанина и фармацевтически приемлемые соли любого из вышеперечисленных фрагментов, предпочтительно, фрагмент цитотоксического лекарственного средства представляет собой часть лекарственного средства, выбранного из группы, состоящей из: фрагмента паклитаксела, фрагмента этопозида, фрагмента гемцитабина, фрагмента циклофосфамида, фрагмента хлорамбуцила, фрагмента доксорубицина, фрагмента даунорубицина, фрагмента 5-фторурацила, фрагмента дактиномицина, фрагмента амифостина, фрагмента флударабина, фрагмента топотекана, фрагмента ифосфамида, фрагмента винкристина, фрагмента винбластина, фрагмента иматиниба, фрагмента леналидомида, фрагмента пеметрекседа, фрагмента абиратерона, фрагмента эрлотиниба, фрагмента бортезомиба, фрагмента метотрексата, фрагмента карфилзомиба, фрагмента кризотиниба, фрагмента висмодегиба, фрагмента понатиниба, фрагмента тивозаниба, фрагмента карбозантиниба, фрагмента эпирубицина, фрагмента доцетаксела, фрагмента эрибулуна, фрагмента иксабепилона, фрагмента винорелбина, фрагмента эверолимуса, фрагмента митомицина С, фрагмента сунитиниба, фрагмента иринотекана, фрагмента лейковорима и фармацевтически приемлемые соли любого из вышеперечисленных фрагментов.
7. Соединение по п.6, где фрагмент лекарственного средства выбран из группы, состоящей из фрагмента паклитаксела, фрагмента метотрексата, фрагмента 5-фторурацила, фрагмента гемцитабина, фрагмента пеметрекседа и фармацевтически приемлемых солей любого из вышеуказанных фрагментов.
8. Соединение по п.7, где фрагмент лекарственного средства представляет собой фрагмента паклитаксела.
9. Соединение по п.8, где фрагмент паклитаксела представляет собой фрагмент формулы:
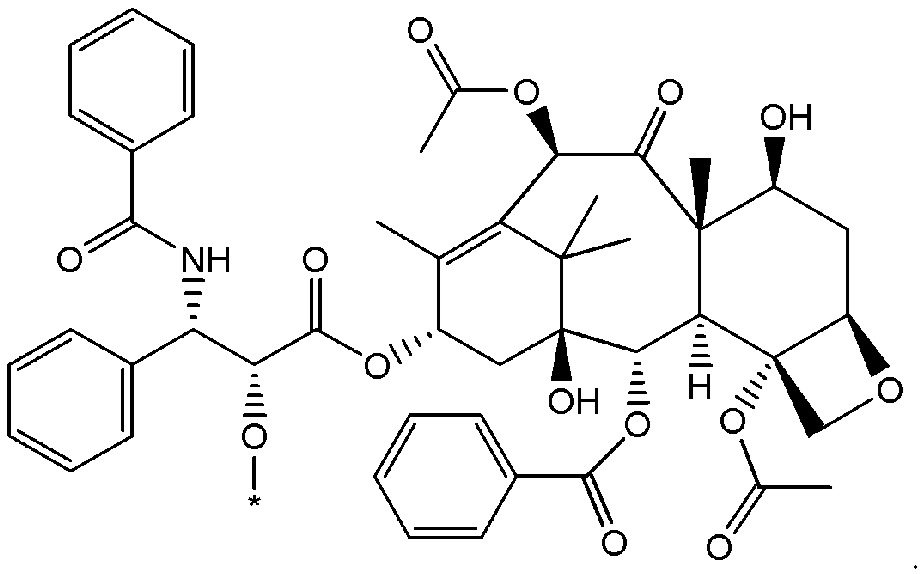
10. Соединение по п.8, где фрагмент паклитаксела представляет собой фрагмент формулы:

11. Соединение по любому из пп.1-10, где X1 представляет собой C12-22гидрокарбилен, который может быть необязательно замещен.
12. Соединение по п.11, где X1 представляет собой C12-22алкиленовую группу.
13. Соединение по п.12, где X1 представляет собой -(CH2)12-, -(CH2)14-, -(CH2)16-, -(CH2)18-, -(CH2)20- или -(CH2)22-.
14. Соединение по п.13, где X1 представляет собой -(CH2)16-.
15. Соединение по п.14, где X2 представляет собой -C(=O)-.
16. Соединение по п.1, которое представляет собой соединение формулы
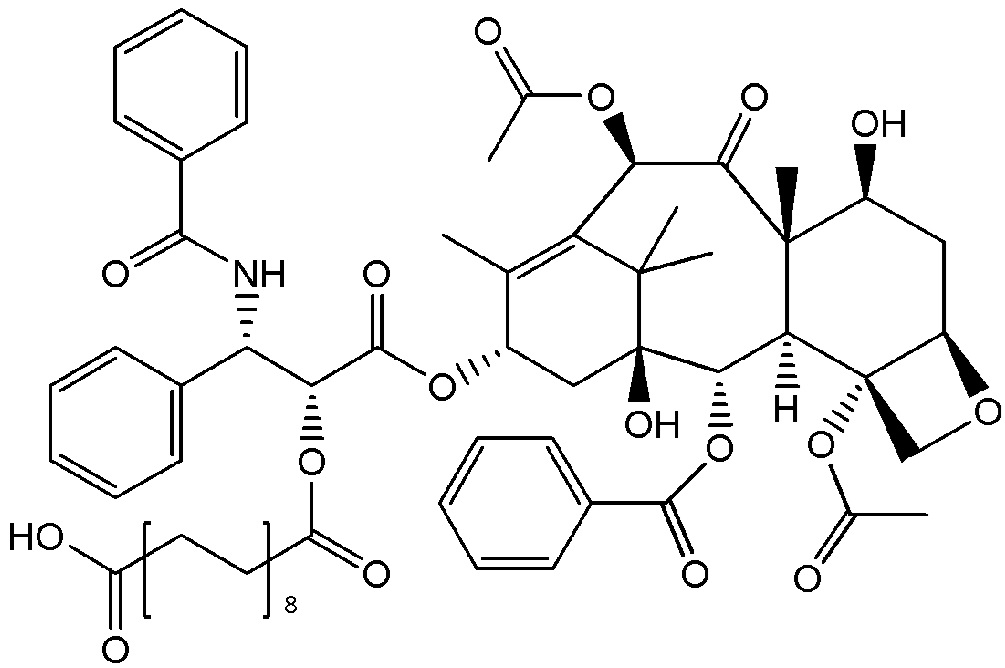
или его фармацевтически приемлемую соль.
17. Фармацевтическая композиция, содержащая
соединение по любому из пп.1-16 и
белок, где белок представляет собой сывороточный альбумин человека или белок, последовательность которого по меньшей мере на 50% эквивалентна последовательности сывороточного альбумина человека.
18. Фармацевтическая композиция по п.17, где белок представляет собой сывороточный альбумин человека.
19. Фармацевтическая композиция по п. 17 или 18, дополнительно содержащая носитель.
20. Фармацевтическая композиция по п.19, где носитель содержит воду.
21. Фармацевтическая композиция по п.20, где соединение и белок нековалентно связаны друг с другом с константой связывания (Kb) равной по меньшей мере 102 М-1, или по меньшей мере 103 М-1, или по меньшей мере 104 М-1, или по меньшей мере 105 М-1.
22. Фармацевтическая композиция по любому из пп. 19-21, где соединение и белок сольватированы носителем.
23. Фармацевтическая композиция по любому из пп. 19-22, которая содержит одно или несколько соединений по любому из пп. 1-16 и один или несколько белков, где по меньшей мере 90 мас. %, или по меньшей мере 95 мас. %, или по меньшей мере 97 мас. %, или по меньшей мере 99 мас. %, соединений в композиции связаны с белками с константой связывания (Kb) равной по меньшей мере 102 М-1, или по меньшей мере 103 М-1, или по меньшей мере 104 М-1, или по меньшей мере 105 М-1.
24. Фармацевтическая композиция по п.23, где по меньшей мере 90 мас. %, или по меньшей мере 95 мас. %, или по меньшей мере 97 мас. %, или по меньшей мере 99 мас. %, частиц связанных с белком в композиции имеют радиус не более 5 нм, или радиус не более 4 нм, измеренный методом динамического рассеяния света.
25. Фармацевтическая композиция по любому из пп. 19-24, где фармацевтическая композиция пригодна для парентерального введения млекопитающему, например человеку.
26. Фармацевтическая композиция по любому из пп. 19-24, где фармацевтическая композиция пригодна для внутривенного введения млекопитающему, например человеку.
27. Фармацевтическая композиция, содержащая
соединение, которое содержит фрагмент цитотоксического лекарственного средства и фрагмент, связывающийся с белком;
белок, где белок представляет собой сывороточный альбумин человека или белок, последовательность которого по меньшей мере на 50% эквивалентна последовательности сывороточного альбумина человека; и
носитель, который содержит воду;
где соединение и белок нековалентно связаны друг с другом с константой связывания (Kb) равной по меньшей мере 102 М-1, или по меньшей мере 103 М-1, или по меньшей мере 104 М-1, или по меньшей мере 105 М-1: и
где соединение и белок сольватированы носителем.
28. Фармацевтическая композиция по п.27, где соединение представляет собой соединение по любому из пп.1-16.
29. Фармацевтическая композиция по п. 27 или 28, где белок представляет собой сывороточный альбумин человека.
30. Фармацевтическая композиция по любому из пп. 27-29, которая содержит одно или несколько соединений по любому из пп. 1-16 и один или несколько белков, где по меньшей мере 90 мас. %, или по меньшей мере 95 мас. %, или по меньшей мере 97 мас. %, или по меньшей мере 99 мас. %, соединений в композиции связаны с белками с константой связывания (Kb) равной по меньшей мере 102 М-1, или по меньшей мере 103 М-1, или по меньшей мере 104 М-1, или по меньшей мере 105 М-1.
31. Фармацевтическая композиция по п.30, где по меньшей мере 90 мас. %, или по меньшей мере 95 мас. %, или по меньшей мере 97 мас. %, или по меньшей мере 99 мас. %, частиц связанных с белком в композиции имеют радиус не более 5 нм, или радиус не более 4 нм, измеренный методом динамического рассеяния света.
32. Фармацевтическая композиция по любому из пп. 27-31, где фармацевтическая композиция пригодна для парентерального введения млекопитающему, например человеку.
33. Фармацевтическая композиция по любому из пп. 27-31, где фармацевтическая композиция пригодна для внутривенного введения млекопитающему, например человеку.
34. Способ лечения рака, включающий:
введение субъекту соединения по любому из пп. 1-16 или композиции по любому из пп. 17-33.
35. Способ индуцирования апоптоза в раковой клетке включающий:
контактирование раковой клетки с соединением по любому из пп. 1-16 или с композицией по любому из пп. 17-33.
36. Способ ингибирования пролиферации злокачественной опухоли, включающий:
контактирование злокачественной опухоли с соединением по любому из пп. 1-16 или с композицией по любому из пп. 17-33.
37. Применение соединения по любому из пп. 1-16 или композиции по любому из пп. 17-33 в качестве лекарственного средства.
38. Применение соединения по любому из пп. 1-16 или композиции по любому из пп. 17-33 для лечения рака.
39. Применение соединения по любому из пп. 1-16 для изготовления лекарственного средства.
40. Применение соединения по любому из пп. 1-16 для изготовления лекарственного средства для лечения рака.

Комментарии