3-(3,4-динитропиразол-5-ил)-4-нитрофуразан и способ его получения - RU2760680C1
Код документа: RU2760680C1
Чертежи
Описание
Настоящее изобретение относится к новому соединению - 3-(3,4-динитропиразол-5-ил)-4-нитрофуразану формулы:

и способу его получения.
Предлагаемое соединение - 3-(3,4-динитропиразол-5-ил)-4-нитрофуразан является плавким термостойким взрывчатым веществом и может найти применение во взрывчатых составах, изготавливаемых методом литья, а также в качестве компонента твердых ракетных топлив и энергоемких составов различного назначения, эксплуатируемых при повышенных температурах. Соединение 1 также может быть использовано в качестве полупродукта для синтеза аналогов или найти применение в органическом синтезе.
3-(3,4-Динитропиразол-5-ил)-4-нитрофуразан является соединением, молекула которого содержит до сих пор не встречавшуюся одновременно последовательность атомов и связей, представляющее тринитропроизводное, полученное на основе молекулы, включающей связанные между собой простой связью пиразол-5-ильный фрагмент и фуразановый цикл. Объединение в одной молекуле нитрофуразанильного и динитропиразольного фрагментов придает ей положительные качества, присущие как производным фуразана, так и пиразола. Соединение 1 и его свойства, а также способ его получения в литературе не описаны. В литературе описано изомерное вещество, состоящее из связанных нитрофуразанильного и динитропиразольного фрагментов (2) (А.Б. Шереметев, И.Л. Юдин. 3-(3,5-Динитропиразол-4-ил)-4-нитрофуразан, способ его получения и применение его в качестве термостойкого взрывчатого вещества. Пат. Российской федерации №2343150 от 27.06.08; А.В. Sheremetev, I.L. Yudin, Ν.V. Palysaeva, К.Yu. Suponitsky, The Synthesis of 4-(3-Nitrofurazan-4-yl)-3,5-dinitropyrazole and its Salts, J. Heterocycl. Chem., 2012, 49, (2), 394-401 DOI: 10.1002/jhet.708), принятое нами за прототип.Однако связывание гетероциклов осуществляется с участием положения 4 пиразольного цикла. Соединение 2 является термостойким высокоплавким взрывчатым веществом (см. таблицу) и не может быть использовано для приготовления взрывчатых составов методом литья. Синтез соединения 2 осуществляют по представленной ниже трех-стадийной схеме. На первой стадии из 3-нитрофуразан-4-уксусной кислоты (3), диметилформамида и хлорокиси фосфора получали триметиниевую соль (4). На второй стадии при конденсации соли 4 с гидразином осуществляли формирование пиразольного цикла. При этом формировался базовый остов молекулы, где положение 4 пиразольного цикла участвует в связывании с нитрофуразанильным фрагментом, приводя к соединению 5. На последней стадии нитрование пиразольного фрагмента серно-азотной смесью использовалось для введения двух нитрогрупп в положения 3 и 5 пиразольного цикла, давая целевой продукт 2. Таким образом, получается соединение, где нитрогруппы удалены друг от друга и разделены другим заместителем, нитрофуразанильным.
Процесс протекает по следующей схеме:

Получить указанным способом соединение 1 не представляется возможным, так как в предлагаемом соединении пиразольный цикл связан другим положением, а именно, положением 5, с нитрофуразанильным, то есть является позиционным изомером соединения 2.
Технической задачей настоящего изобретения является создание нового нитросоединения, содержащего в своем составе как фуразановый, так и пиразольный циклы, являющегося новым термостойким взрывчатым веществом и обладающим при этом низкой температурой плавления с сохранением хороших взрывчатых характеристик и имеющим большой интервал термической безопасности, и разработка способа его получения. Поставленная техническая задача достигается новым соединением - 3-(3,4-динитропиразол-5-ил)-4-нитрофуразаном формулы:
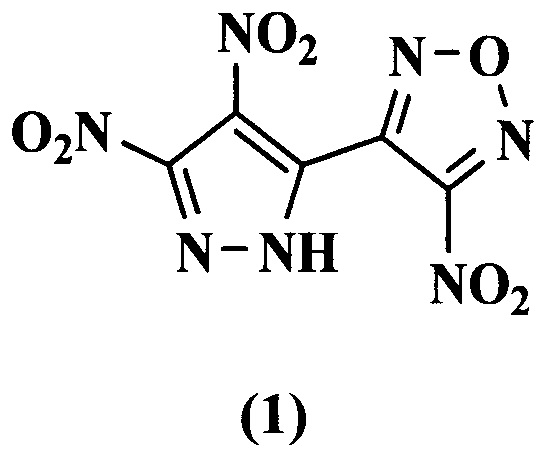
являющимся плавким термостойким взрывчатым веществом, и способом его получения, заключающимся в том, что 3-амино-4-ацетилфуразан подвергают взаимодействию с диметилацеталем диметилформамида (DMADMF) в среде инертного органического растворителя при 8- 110°С с последующим упариванием реакционной массы и обработкой полученного при этом остатка солью гидразина в среде органического растворителя или его смеси с водой, образующийся при этом 3-амино-4-(пиразол-5-ил)фуразан подвергают обработке смесью водного раствора перекиси водорода с органическими кислотами и/или их ангидридами, или неорганическими кислотами, с последующим взаимодействием полученного при этом 3-(пиразол-3-ил)-4-нитрофуразана со смесью концентрированной азотной кислоты или ее соли и ангидрида органической кислоты, и промежуточно образующийся N-нитропродукт подвергают термообработке в среде органического высококипящего растворителя с последующими обработкой полученного при этом 3-(3-нитропиразол-5-ил)-4-нитрофуразана нитрующей смесью, состоящей из концентрированной азотной кислоты и концентрированной сильной неорганической кислоты, при нагревании, и выделением целевого продукта.
Процесс протекает по следующей схеме:

Предложенный способ получения 3-(3,4-динитропиразол-5-ил)-4-нитрофуразана (1) включает следующие стадии.
Первая стадия. Исходный 3-амино-4-ацетилфуразан (6) получают обработкой 3,4-диацетилфуроксана водным аммиаком (А.Б. Шереметев, С.Г. Забусов, Т.Р. Тухбатшин, Н.В. Палысаева, К.Ю. Супоницкий. Синтез 3-амино-4-ацилфуразанов из 3,4-диацилфуроксанов. Химия гетероцикл. соедин., 2014, (8), 1250-1262 [А.В. Sheremetev, S.G. Zabusov, T.R. Tukhbatshin, N.V. Palysaeva, and K.Yu. Suponitsky. Synthesis of 4-Acyl-3-aminofurazans from 3,4-Diacylfuroxans. Chem. Heterocycl. Compounds., 2014, 50, (8), 1154-1165]). Взаимодействие соединения (6) с диметилацеталем диметилформамида (DMADMF) в кипящем инертном растворителе, например, бензоле, толуоле, ксилоле, хлорбензоле и др., может протекать при температуре от 80 до 110°С. По завершению реакции (контроль по ТСХ) все летучие компоненты смеси упаривают при пониженном давлении, а остаток обрабатывают раствором соли гидразина, например, гидрохлоридом, сульфатом, нитратом, ацетатом и др., в органическом растворителе или его смеси с водой, что дает 3-замещенный пиразол (7).
Вторая стадия. Окисление аминогруппы соединения 7 осуществляют смесями 30-50%-ной перекиси водорода с органическими кислотами и/или их ангидридами, или неорганическими кислотами. Возможно использование различных добавок, ускоряющих и улучшающих протекание процесса, например, таких как Na2WO4×2H2O, (NH4)2S2O8 и др.
Третья стадия. Введение первой нитрогруппы необходимо провести в положение 3 пиразольного цикла. Для этого соединение 8 обрабатывают смесью 95-100%-ной азотной кислоты с ангидридом органической кислоты, например, Ac2O, (CF3CO)2О и др. при температуре от -10 до +18°С. Реакция может протекать в присутствии растворителя, например, АсОН, CF3CO2H, CH2Cl2 и др. При этом образуется N-нитро интермедиат, т.е. соединение, где нитрогруппа присоединена к атому азота пиразольного цикла. Этот интермедиат нагревают в инертном растворителе, например, хлорбензоле, декалине, тетрахлорэтане и др., что приводит к N→С-миграции нитрогруппы, давая соединение 9.
Четвертая стадия. Введение второй нитрогруппы в пиразольный цикл осуществляется при нитровании нитрующей смесью, состоящей из концентрированной азотной кислоты в смеси с концентрированными сильными неорганическими кислотами, например, H2SO4, Н3РО4. Процесс можно вести при температуре от 50°С до температуры кипения азотной кислоты. Для усиления активности нитрующей смеси серную кислоту можно укреплять или заменять олеумом.
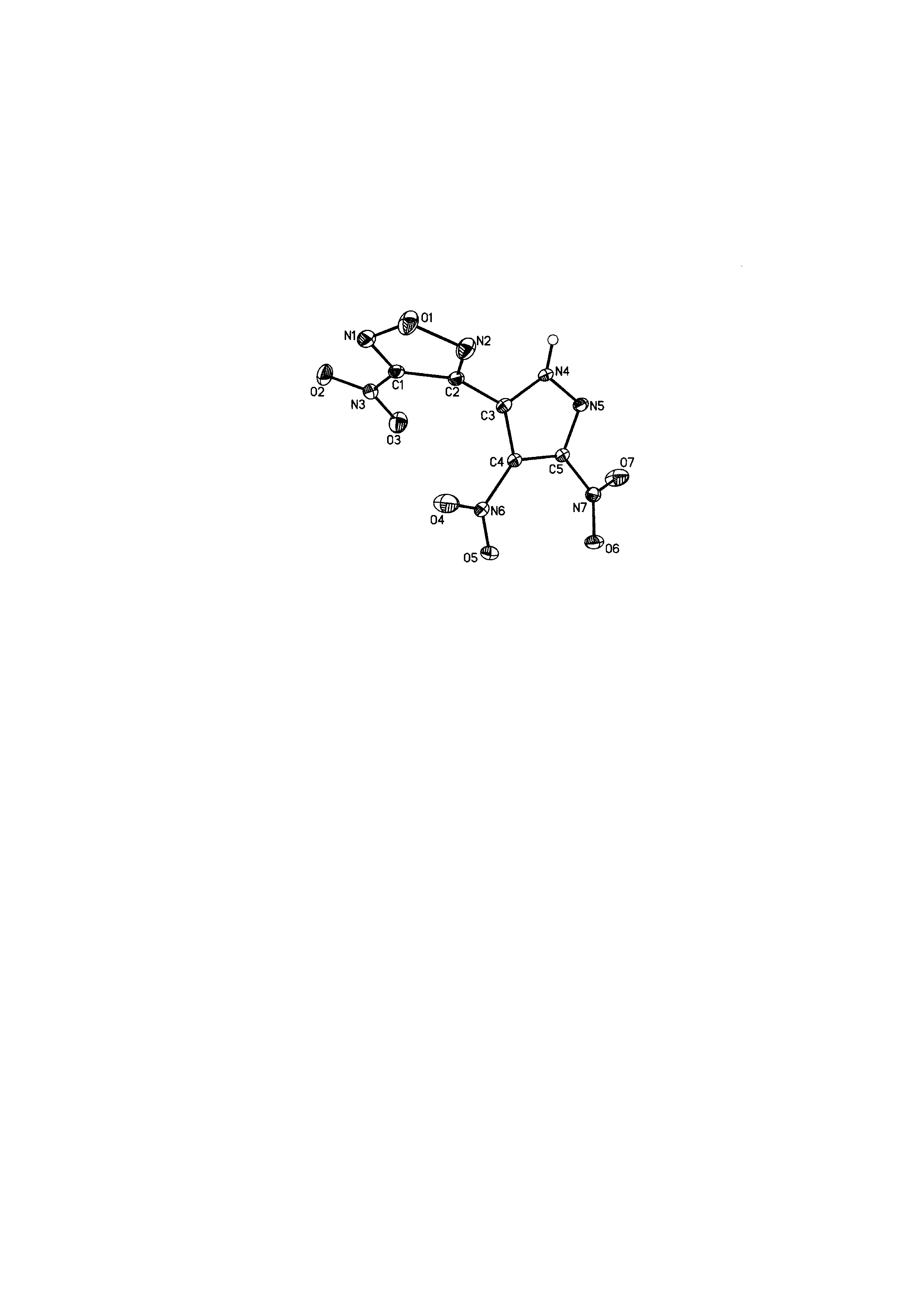
Строение полупродуктов и целевого соединения доказано данными элементного анализа, масс-, ИК-, ЯМР-спектров. Для соединения 1 из раствора азотной кислоты выращен кристалл (гидрат) и выполнен его рентгеноструктурный анализ. На рис. показана молекулярная структура соединения 1 по данным РСА.
Таким образом, заявляемое соединение представляет собой производное неизвестной ранее комбинации фуразанового и пиразольного циклов с тремя нитрогруппами. В целевом тринитропроизводном, тип связывания гетероциклов, а именно за счет положения 5 пиразольного цикла, приводит к образованию центронесимметричной молекулы, что обеспечивает ей пониженную температуру плавления. Наличие в структуре заявляемого соединения N-H фрагмента, позволяет замещать протон, синтезируя различные производные, корректируя тем самым свойства молекулы. Предложенный способ основан на целесообразном сочетании трех последовательных реакций. Первая, циклоконденсация - формирование пиразольного цикла из ацетильной группы обработкой диметилацеталем диметилформамида (DMADMF), а затем гидразином. Вторая, окисление аминогруппы до нитрогруппы. Последняя, нитрование пиразольного цикла - постадийное введение двух нитрогрупп при нитровании сначала (i) смесью азотной кислоты с ангидридом органической кислоты, с последующим термолизом, и, затем, (ii) смесью азотной кислоты с сильными неорганическими кислотами.
Лишь совокупность взятых для синтеза соединения формулы (1) последовательности действий и условий и выбранное исходное соединение дали возможность добиться одной из указанных целей - получить тринитропроизводное, содержащее в своей основе связанные простой связью фуразановый цикл и пиразол-5-ильный фрагмент.
Предлагаемое соединение может найти применение в качестве плавкого компонента взрывчатых составов, твердых ракетных топлив и энергоемких составов различного назначения, эксплуатируемых при повышенных температурах.
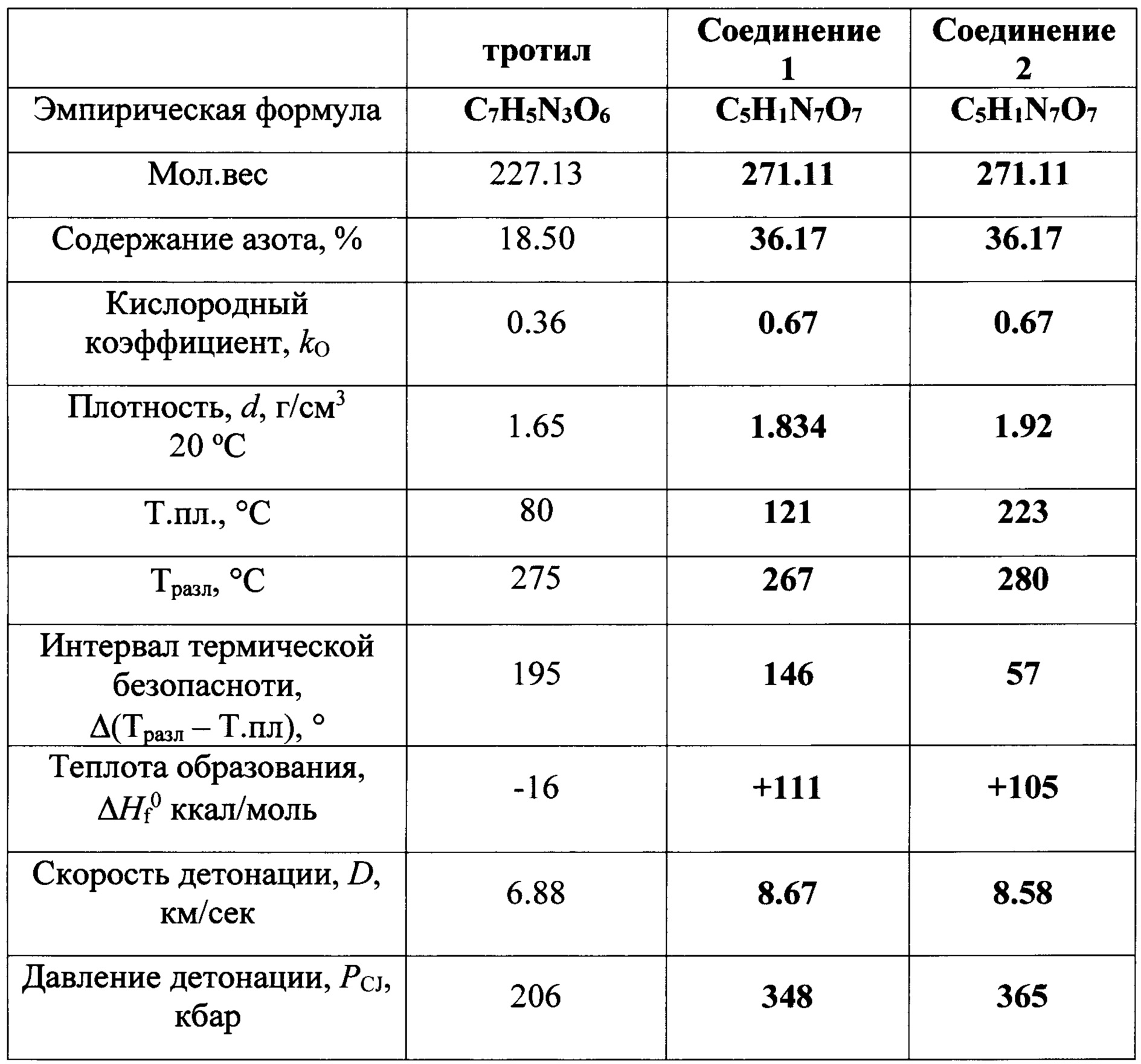
В качестве базового плавкого компонента штатных взрывчатых веществ в настоящее время используются тринитротолуол (тротил) [Энергетические конденсированные системы. Краткий энциклопедический словарь. По ред. Б.П. Жукова, Изд. 2-е, М: Янус-К, 2000; J. Kohler, R. Meyer, Explosives. 4 ed., Weinheim: VCH, 1993].

Как видно из таблицы, тротил обладает широким интервалом термической безопасности, однако имеет средние энергетические и взрывчатые характеристики (теплота образования,


Известно термостойкое взрывчатое вещество, являющееся позиционным изомером заявляемого соединения, в котором нитрофуразановый цикл связан с динитропиразольным фрагмента, за счет положения 4 пиразольного цикла (2) (А.Б. Шереметев, И.Л. Юдин. 3-(3,5-Динитропиразол-4-ил)-4-нитрофуразан, способ его получения и применение его в качестве термостойкого взрывчатого вещества. Пат. Российской федерации №2343150 от 27.06.08; А.В. Sheremetev, I.L. Yudin, Ν.V. Palysaeva, К.Yu. Suponitsky, The Synthesis of 4-(3-Nitrofurazan-4-yl)-3,5-dinitropyrazole and its Salts, J. Heterocycl. Chem., 2012, 49, (2), 394-401 DOI: 10.1002/jhet.708).
Соединение 2 является более мощным взрывчатым веществом, чем тротил, однако имеет слишком высокую температуру плавления и узкий интервал термической безопасности (см. таблицу).
Как видно из таблицы, характеристики соединения 1 занимают промежуточное положение между соединениями 2 и тротилом, превышая характеристики последнего, но соединение 1 имеет существенно более низкую температуру плавления, чем соединение 2. Имея высокие энергетические характеристики и широкий интервал термической безопасности соединение 1, в отличие от изомерного соединения 2, может найти применение в качестве плавкой основы для энергоемких составов, изготавливаемых методом литья.
Таким образом, получено новое соединение, построенное из связанных между собой простой связью фуразанового и присоединенного положением 5 пиразольного циклов, включающее три нитрогруппы, являющееся термостойким взрывчатым веществом, и разработан способ его получения. Необходимо отметить, что производные фуразана и пиразола широко используются при конструировании взрывчатых веществ, однако ранее не использовались комбинация, включающая (i) оба эти гетероцикла, связь между которыми осуществляется с участием положения 5 пиразольного цикла; (ii) три нитрогруппы; (iii) незамещенный NH-фрагмент пиразола, обеспечивающий образование стабилизирующих водородных связей.
Настоящее изобретение иллюстрируется следующими примерами, не ограничивающий его объем.
Пример 1. Смесь 3-амино-4-ацетилфуразана (соединение 6) (10 г, 78.7 ммоля) и DMADMF (20.4 г, 171.2 ммоля) в 100 мл бензола кипятили 7-9 ч (ТСХ контроль). Во время кипения раствор постепенно окрашивается сначала в желтый, а затем - красный цвет. Затем упаривали растворитель и летучие примеси в вакууме досуха, остаток промывали эфиром. К оставшемуся черному маслу (~18 г) добавляли 100 мл этанола и солянокислый гидразин (24.82 г, 236.4 ммоля) и полученную смесь перемешивали при 40-50°С в течении 4 ч. Реакционную смесь оставляли на ночь при комнатной температуре. Растворитель упаривали в вакууме досуха и получали оранжевое масло, которое перекристаллизовали из воды с углем. Получено 8.2 г (69%) 3-амино-4-(пиразол-5-ил)фуразана (соединение 7) в виде светло-коричневых игольчатых кристаллов, т.пл. 170-172°С. ИК-спектр (KBr, ν,см-1): 3438, 3333, 3222, 3050, 2967, 2851, 1630, 1599, 1565, 1530, 1345, 1204, 1139, 1087, 1000, 951, 923, 899, 872, 779. Спектр ЯМР1Н (DMSO-d6, δ, м.д.): 13.54 (с, 1Н, ΝΗ), 8.00 (с, 1Н), 6.83 (с, 1Н), 6.37 (с, 2Н, ΝΗ2). Спектр ЯМР13С (DMSO-d6, δ, м.д.): 154.8, 141.0, 139.0, 130.4, 104.1. Масс-спектр, m/z (%): 151 [М+] (64), 94 (100), 68 (23), 58 (14). Найдено, %: С, 39.86; Н, 3.39; N, 46.25. C5H5N5O (151.13). Вычислено, %: С, 39.74; Н, 3.33; N, 46.34.
Смесь соединения 7 (2.0 г, 13.24 ммоля), Na2WO4×2H2O (4.24 г, 12.88 ммоля), 50%-ной Н2О2 (30 мл) и конц. H2SO4 (15 мл), приготовленную при комнатной температуре, нагревали до 45°С за 20 мин и перемешивали при этой температуре 3 ч. Затем смесь охладили до комнатной температуры, разбавляли холодной водой (20 мл) и экстрагировали этилацетатом (3×20 мл). Экстракты объединяли, промывали водой и сушили над MgSO4. Растворитель удаляли в вакууме, что давало масло, которое при затирании в воде кристаллизуется, и отфильтровывали. После перекристаллизации из воды получили 1.99 г (83%) 3-(пиразол-3-ил)-4-нитрофуразана (соединение 8), белый порошок, т.пл. 105-106°С.ИК-спектр (KBr, ν, см-1): 3163, 3059, 2976, 2916, 1588, 1550, 1487, 1406, 1389, 1362, 1267, 1119, 1066, 955, 825, 782, 767. Спектр ЯМР1Н (DMSO-d6, δ, м.д.): 13.76 (с, 1Н, ΝΗ), 8.06 (с, 1Н, СН), 6.98 (с, 1Н, СН). Спектр ЯМР13С (DMSO-d6, δ, м.д.): 158.9, 144.3, 134.2, 130.6, 107.0. Масс-спектр, m/z (%):181 [М+] (58), 135 (17), 105 (100), 76 (54), 50 (67). Найдено, %: С, 33.23; Η, 1.70; Ν, 38.58. C5H3N5O3 (181.11). Вычислено, %: С, 33.16; Η, 1.67; Ν, 38.67.
К раствору соединения 8 (5.0 г, 28 ммоля) в трифторуксусной кислоте (56 мл) при -5-0°С по каплям добавили ΗΝΟ3 {d 1.50 г/см3, 3.5 мл), а затем Ac2O (11.2 мл). Реакционную смесь перемешивали при этой температуре 2.5 ч, вылили в ледяную воду (200 мл), экстрагировали хлористым метиленом (3×40 мл). Объединенные экстракты сушили безводным Na2SO4 и растворитель удаляли при пониженном давлении. Оставшееся светло-желтое масло (~6 г) разбавляли тетрахлорэтаном (50 мл). Смесь кипятили в течение 10 ч, охладили до комнатной температуры, выпавший осадок отфильтровали, промыли гексаном (10 мл). Получили 5.4 г (90%) 3-(3-нитропиразол-5-ил)-4-нитрофуразана (соединение 9), светло-бежевого порошка с т.пл. 78°С. ИК-спектр (KBr, ν, см-1): 3380, 3160, 1608, 1564, 1552, 1472, 1420, 1392, 1356, 1268, 1242, 1200, 1164, 1040, 988, 960, 896, 836, 816, 760, 720, 612. Спектр ЯМР1Н (DMSO-d6, δ, м.д.): 15.30 (уш. с, 1Н, NH); 7.61 (с, 1H, Н-4). Спектр ЯМР13С (DMSO-d6, δ, м.д.): 159.3 (уш. с, CFz-NO2); 155.8 (уш. с, CPz-NO2); 141.5 (CFz); 128.2 (С-5); 106.1 (СН-4). Спектр ЯМР14N (DMSO-d6, δ, м.д.): -30.49 (уш. с, ΝO2). Найдено, m/z: 225.0017 [М-Н]-. C5HN6O5. Вычислено, m/z\ 225.0014.
К раствору соединения 9 (0.60 г, 2.7 ммоля) в H2SO4 (d 1.827 г/см3, 6 мл) по каплям прибавили HNO3 (d 1.50 г/см3, 1.3 мл) и перемешивали при нагревании до 100°С 5 ч. Реакционную смесь охлаждали, выливали в 30 мл ледяной воды, отфильтровывали выпавший осадок, промывали водой. Фильтрат экстрагировали эфиром (2×25 мл), объединенные экстракты сушили безводным MgSO4. Растворитель удаляли при пониженном давлении, что давало твердый остаток. Оба осадка объединяли и кристаллизовали из хлороформа. Получили 0.51 г (71%) целевого 3-(3,4-динитропиразол-5-ил)-4-нитрофуразана (1) в виде белого порошка с т.пл. 121°С. ИК-спектр (KBr, ν, см-1): 3678, 3464, 1622, 1581, 1560, 1536, 1494, 1432, 1406, 1366, 1334, 1299, 1171, 1098, 1036, 971, 906, 853, 830, 814, 753, 528. Спектр ЯМР13С (DMSO-d6, δ, м.д.): 159.7 (уш. с, CFz-NO2); 150.0 (уш. с, C-3-NO2); 141.8 (CFz); 128.5 (С-5); 126.1 (уш. с, C-4-NO2). Спектр ЯМР14N (DMSO-d6, δ, м.д.): -25.13 (CPz-NO2); -35.47 (CFz-NO2). Найдено, m/z: 269.9872 [M-H]-. C5N7O7. Вычислено, m/z: 269.9865.
Пример 2. Смесь 3-амино-4-ацетилфуразана (соединение 6) (10 г, 78.7 ммоля) и DMADMF (20.4 г, 171.2 ммоля) в 100 мл ксилола нагревали до 110°С 9 ч (ТСХ контроль). Во время кипения раствор постепенно окрашивается сначала в желтый, а затем - красный цвет. Затем упаривали растворитель и летучие примеси в вакууме досуха, остаток промывали эфиром. К оставшемуся черному масла (~18 г) добавляли 100 мл 50% раствора MeCN в H2O и сернокислый гидразин (30.73 г, 236.4 ммоля) и полученную смесь перемешивали при 40-50°С в течении 5 ч. Реакционную смесь оставляли на ночь при комнатной температуре. Растворитель упаривали в вакууме досуха и получали оранжевое масло, которое кристаллизовали из воды с углем. Получено 7.5 г (63%) 3-амино-4-(пиразол-5-ил)фуразана (соединение 7) в виде светло-коричневых игольчатых кристаллов, т.пл. 170-172°С. Спектр ЯМР1Н (DMSO-d6, δ, м.д.): 13.53 (с, 1H, ΝΗ), 8.02 (с, 1Н), 6.83 (с, 1Н), 6.38 (с, 2Н, ΝΗ2).
Смесь соединения 7 (2.0 г, 13.24 ммоля), 30%-ной H2O2 (30 мл), трифторуксусной кислоты (10 мл) и трифторуксусного ангидрида (10 мл), приготовленную при комнатной температуре, нагревали до 45°С за 20 мин и перемешивали при этой температуре 7 ч. Затем смесь охладили до комнатной температуры, разбавляли холодной водой (120 мл) и экстрагировали этилацетатом (3×20 мл). Экстракты объединяли, промывали водой и сушили над MgSO4. Растворитель удаляли в вакууме, что давало масло, которое при затирании в воде кристаллизуется, и отфильтровывали. После перекристаллизации из воды получили 1.68 г (70%) 3-(пиразол-3-ил)-4-нитрофуразана (соединение 8), белый порошок, т.пл. 105-106°С. Спектр ЯМР1Н (DMSO-d6, δ, м.д.): 13.76 (с, 1Н, ΝΗ), 8.06 (с, 1H, СН), 6.98 (с, 1Н, СН).
К суспензии соединения 8 (5.0 г, 28 ммоля) в CH2Cl2 (70 мл) при 15-18°С добавили ΝΗ4ΝΟ3 (8.96 г, 112 ммоль), а затем по каплям добавили (CF3CO)2О (15.6 мл). Реакционную смесь перемешивали при этой температуре 5 ч, вылили в ледяную воду (200 мл), экстрагировали хлористым метиленом (3×40 мл). Объединенные экстракты сушили безводным Na2SO4 и растворитель удаляли при пониженном давлении. Оставшееся светло-желтое масло (~6 г) разбавляли бензонитрилом (50 мл). Смесь нагрели до 120°С, грели 6 часов, затем кипятили в течение 6 ч, охладили до комнатной температуры, выпавший осадок отфильтровали, промыли гексаном (10 мл). Получили 3.8 г (76%) 3-(3-нитропиразол-5-ил)-4-нитрофуразана (9) в виде светло-бежевого порошка с т.пл. 78°С.Спектр ЯМР1H (DMSO-d6, δ, м.д.): 15.30 (уш. с, 1H, NH); 7.61 (с, 1Н, Н-4).
К раствору соединения 9 (0.60 г, 2.7 ммоля) в 5-20% олеуме (6 мл) по каплям прибавили ΗΝΟ3 (d 1.50 г/см3, 1.3 мл) и перемешивали при нагревании до 80°С 6 ч. Реакционную смесь охлаждали, выливали в 40 мл ледяной воды, отфильтровывали выпавший осадок, промывали водой. Фильтрат экстрагировали эфиром (3×25 мл), объединенные экстракты сушили безводным MgSO4. Растворитель удаляли при пониженном давлении, что давало твердый остаток. Оба осадка объединяли и кристаллизовали из хлороформа. Получили 0.48 г (67%) целевого 3-(3,4-динитропиразол-5-ил)-4-нитрофуразана (1) в виде белого порошка с т.пл. 121°С. Спектр ЯМР13С (DMSO-d6, δ, м.д.): 159.7 (уш. с, CFz-NO2); 150.0 (уш. с, C-3-NO2); 141.8 (CFz); 128.5 (С-5); 126.1 (уш. с, C-4-NO2).
Техническим результатом предлагаемого изобретения является создание нового соединения, которое представляет собой динитропроизводное, сформированное на основе молекулы, включающей связанные между собой простой связью фуразановый циклы и пиразол-5-ильный фрагмент, имеющего существенно более низкую температуру плавления, чем известный аналог, и более высокие энергетические характеристики, чем у штатного взрывчатого вещества, такого как тротил, и разработка способа его получения. Предлагаемое соединение 1 является мощным плавким термостойким взрывчатым веществом.
Реферат
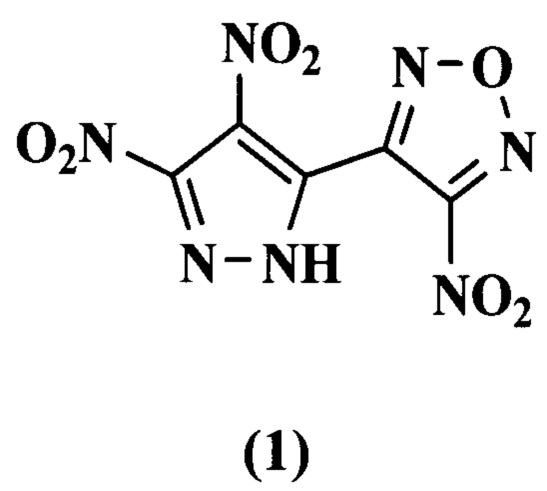
Изобретение относится к новому соединению - 3-(3,4-динитропиразол-5-ил)-4-нитрофуразану формулы:

являющемуся плавким термостойким взрывчатым веществом, и к способу его получения. Технический результат: получено новое соединение, которое имеет существенно более низкую температуру плавления, чем известный аналог, и более высокие энергетические характеристики, чем у штатного взрывчатого вещества, такого как тротил. Соединение 1 может найти применение во взрывчатых составах, изготавливаемых методом литья, а также в качестве компонента твердых ракетных топлив и энергоемких составов различного назначения, эксплуатируемых при повышенных температурах. Соединение 1 также может быть использовано в качестве полупродукта для синтеза аналогов или найти применение в органическом синтезе. 2 н. и 1 з.п. ф-лы, 1 ил., 1 табл., 1 пр.
Формула

Комментарии