Производные гидроксиметилфуразанкарбоновой кислоты и фармацевтический препарат - RU2134687C1
Код документа: RU2134687C1
Описание
Настоящее изобретение относится к производным гидроксиметилфуразанкарбоновой кислоты, способу ее получения и ее применению.
Различные производные 2-окси- и 5-оксифуразанкарбоновой кислоты, которые в качестве заместителей в фуразановом кольце несут метильную группу, известны и описаны, в частности, в европейских заявках EP-B 38438 и EP-B 54873. Однако производные 2-окси- и 5-оксифуразанкарбоновой кислоты, которые несут гидроксиметильную группу в качестве заместителя, на сегодняшний день не известны.
Настоящее изобретение относится к производным
гидроксиметилфуразановой кислоты общей формулы I

в которой один из радикалов R1 и R2 представляет собой гидроксиметил, а другой представляет собой

R3 и R4 независимо друг от друга обозначают водород, (C1-C20)алкил, 1-фенил(C2-C4 )алкил, 2-фенил(C3-C4)алкил, (C3-C6)алкенил, (C3-C7)циклоалкил, -(CH2)n-NR5R6, -(CH2)n-OR5, -(CH2)m-COOR5, -CH(Alk)-COOR5, -(CH2)m-CONR5R6,
CH(Alk)-CONR5R6,

-(CH2)n-NR5(COAlk), -(CH2 )n-Ar или -(CH2)n-Het, или R3 и R4 оба вместе со связывающим их атомом азота образуют гетероцикл, который также может быть однократно либо многократно замещен на (C1-C6)алкил, (C3-C7)циклоалкил, (C1-C4-алкоксигруппу, аминогруппу, (C1-C4 )алкиламиногруппу, ди((C1-C4)-алкил)аминогруппу, гидроксильную группу, ацетоксигруппу, бензил, фенетил или Ar;
R5 и R6 независимо друг от друга обозначают водород, (C1-C6) алкил, (C3-C7)циклоалкил, бензил, фенетил или Ar;
R7 обозначает (C1-C6)алкил, (C3-C7)циклоалкил, бензил, фенил, который может быть однократно либо многократно замещен на (C1-C4)алкил;
Alk обозначает (C1-C6 )алкил;
Ar представляет собой фенил, который может быть однократно либо многократно замещен на (C1-C4)алкил, (C1-C4)алкоксигруппу или сульфамоил;
Het является гетероциклическим радикалом с числом азота 1-3, который может быть однократно либо многократно замещен на (C1-C4)алкил;
n обозначает 0, 1, 2, 3 или 4;
m обозначает 1, 2, 3 или 4;
p обозначает 1, 2 или 3;
а также к их фармацевтически приемлемым солям.
Таким образом, настоящее изобретение включает в
себя как соединения общей формулы Ia, так и соединения общей формулы Ib

где X представляет собой NR3R4, OH или OR7, а R3, R4 и R7 имеют значения, указанные выше; изобретение включает в себя также смеси соединений общих формул Ia и Ib в любых количественных соотношениях компонентов.
Кроме вышеперечисленных обозначений для R5 и R6 указанные радикалы также могут обозначать (C3 -C6)алкенил.
Ar также может являться арильным радикалом с числом C-атомов до 12.
Кроме вышеназванных заместителей Ar может также содержать следующие заместители: аминогруппу, (C1-C4)алкиламиногруппу, ди(C1-C4)алкиламиногруппу, (C1-C6)алканоиламиногруппу, фтор, хлор, бром, гидроксильную группу, ацетоксигруппу, нитрогруппу, трифторметил или цианогруппу.
В качестве заместителей для Het следует упомянуть также и такие заместители, как (C1-C4)алкоксигруппу, аминогруппу, (C1-C4)алкиламиногруппу, ди[(C1-C4)алкил] аминогруппу, (C1-C6)алканоиламиногруппу, фтор, хлор, бром, гидроксильную группу, ацетоксигруппу, нитрогруппу, цианогруппу и Ar.
Алкильные группы могут быть линейными или разветвленными. Это относится также к тем случаям, когда они замещены или имеются, например, в алкоксигруппах или алкиламиногруппах либо представлены в качестве заместителей в других остатках. Примерами алкильных групп, представляющих собой одно из значений R3, R4, R5, R6, R7 или Alk, являются метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор.-бутил, трет.-бутил. пентил, гексил или 1-метилпентил, а алкильные группы, входящие в число значений R3 или R4, могут представлять собой еще и октил, децил, додецил, гексадецил, октадецил или эйкозил.
(C3-C6)алкенильные группы, составляющие одно из значений R3, R4, R5 и R6, также могут быть линейными или разветвленными. Примерами таких групп являются аллил, 2-бутенил, 3-бутенил, 2-метил-2-бутенил, 3-метил-2-бутенил, 2,3-диметил-2-бутенил, 2-гексенил, 5-гексенил.
(C3-C7)циклоалкильный радикал, входящий в число значений R3, R4, R5, R6 или R7 или используемый в качестве заместителя в гетероцикле, образованном из R3 и R4 и связывающего их атома азота, представляет собой, например, циклопропил, циклобутил, циклопентил, циклогексил или циклогептил. Предпочтительными циклоалкильными радикалами являются циклопентиловый и циклогексиловый радикал.
Содержащийся в -(CH2)n-Ar-группе, в R5 и R6 и используемый в качестве заместителя в гетероциклическом кольце Het и в образованном из R3 и R4 и связывающего их атома азота гетероцикле арильный радикал с 6-12 C-атомами может представлять собой, например, незамещенный либо замещенный фенил, 1-нафтил, 2-нафтил, 3-бифенилил или 4-бифенилил. Предпочтителен из названных незамещенный либо замещенный фенильный радикал.
-(CH2)n-Ar обозначает предпочтительно фенил, бензил и фенетил, который может быть незамещенным либо одно- или двукратнозамещенным в фенильном кольце.
Содержащийся в -(CH2 )n-Het-группе гетероциклический радикал с числом гетероатомов 1-3 может быть ароматическим, частично ненасыщенным и насыщенным и может быть аннелирован. Предпочтительные формы гетероцикла представляют собой 5-звенные, 6-звенные и 7-звенные кольца. Предпочтительным гетероатомом является азот. Кроме того, гетероатомом может являться кислород и сера. В качестве примеров гетероциклов, из которых образуется радикал Het, следует назвать азетидин, пирролидин, пиррол, индол, пиразол, имидазолидин, имидазолин, имидазол, 1,2,3-триазол, 1,2,4-триазол, тетрагидрофуран, фуран, 1,3-диоксолан, тетрагидротиофен, тиофен, бензотиофен, 1,3-дитиолан, 1,3-оксазолин, 1,3-оксазол, 1,3,4-оксадиазол, фуразан, 1,3-тиазолидин, 1,3-тиазол, пиперидин, 1,2,5,6-тетрагидропиридин, 1,4-дигидропиридин, пиридин, хинолин, изохинолин, пиридазин, пиримидин, пиперазин, 1,2,3-триазин, 1,3,5-триазин, пергидропиран, 1,3-диоксан, 1,4-диоксан, 1,3-дитиан, дигидро-1,3-оксазин, морфолин, пергидро-1,4-тиазин, пергидроазепин. Het может представлять собой, например, тетразолильный радикал. Азотные гетероциклы могут быть соединены атомом азота или атомом углерода. К предпочтительным гетероциклическим радикалам Het относятся 1-пирролил, 1- и 2-имидазолил, 2-, 3- и 4-пиридил, 4-пиперидинил и связанные через атом азота радикалы ненасыщенных гетероциклов, как, например, пирролидинил, пиперидинил, пиперазинил, морфолинил и пергидро-1,4-тиазин-4-ил.
Арильные радикалы Ar и гетероциклические радикалы Het могут быть также одно- или многократно замещены. Примерами возможных (C1-C4)алкильных заместителей могут служить метил, этил, н-пропил, изопропил, изобутил или трет.-бутил; примерами возможных заместителей (C1-C4)алкоксигруппами могут служить метокси, этокси, н-пропокси, н-бутокси или изобутокси; примерами возможных заместителей (C1-C4)алкиламиногруппами могут служить метиламино, этиламино, изопропиламино, изобутиламино или трет.-бутиламино; примерами возможных заместителей ди[C1-C4)алкил] аминогруппами могут служить диметиламино, диэтиламино, диизопропиламино, метилэтиламино, метил-трет.-бутиламино; примерами заместителей (C1-C6)алканоиламиногруппами могут служить формиламино, ацетиламино, пропиониламино, н-бутириламино, изобутириламино, пивалоиламино или гексаноиламино. Примерами замещенных производных фенила, предпочтительно в качестве арильного радикала, являются 2-, 3- или 4-метилфенил, 4-трет.-бутилфенил, 2-, 3- или 4-метоксифенил, 3-этоксифенил, 2,3-, 3,4- или 3,5-диметоксифенил, 3,4,5-триметоксифенил, 3-аминофенил, 3- или 4-диметиламинофенил, 4-ацетиламинофенил, 2-, 3- или 4-фторфенил, 2,3- или 3, 4-дифторфенил, 2-, 3- или 4-хлорфенил, 2,3-, 3,4-, 3,5- или 2,6-дихлорфенил, 4-бромфенил, 4-гидроксифенил, 3-гидрокси-4-метоксифенил, 2-, 3- или 4-нитрофенил, 4-хлор-3-нитрофенил, 3- или 4-трифторметилфенил, 2-, 3- или 4-цианфенил. Примерами замещенных гетероциклических радикалов Het являются 2,5-диметил-1-пирролил, 2,5-диметилпирролидино, 2,6-диметилпиперидино, 4-метилпиперазино, 4-фенилпиперазино, 4-(2-метоксифенил)-пиперазино, 4-гидроксипиперидино, 4-аминопиперидино, 4-ацетилпиперазино.
Образованный из R3 и R4 и связывающего их атома азота гетероцикл представляет собой, например, пирролидин, пиперидин, морфолин или пиперазин, причем из заместителей, которые этот гетероцикл может нести, у второго атома азота пиперазина предпочтительны (C1-C6)алкил, (C3-C7)циклоалкил, бензил, фенетил и Ar.
R7 представляет собой предпочтительно линейный либо разветвленный (C1-C4)алкильный радикал, например, метил, этил, н-пропил, изопропил, н-бутил, изобутил, трет.-бутил, прежде всего метил.
Радикал X может быть хиральным или ахиральным. При наличии хирального радикала X соединение может быть представлено в рацемической форме или в форме оптических антиподов либо диастереомеров.
Предпочтительны соединения, в которых X представляет собой NR3R4 и один из радикалов R3 и R4 обозначает водород, а другой имеет одно из указанных выше значений или же оба радикала R3 и R4 вместе со связывающим их атомом азота образуют гетероцикл, который также может быть одно- или многократно замещен на (C1-C6)алкил, (C3-C7)циклоалкил, (C1-C4)алкоксигруппу, аминогруппу, (C1-C4)алкиламиногруппу, ди[(C1-C4 )алкил]аминогруппу, гидроксильную группу, ацетоксигруппу, бензил, фенетил или фенил. Особенно предпочтительны соединения формулы I, в которых X представляет собой NR3R4 и один из радикалов R3 и R4 представляет водород, тогда как другой из них представляет собой водород, (C1-C6)алкил, -(CH2)nNR5R6, причем n обозначает 1, 2, 3 или 4, а R5 и R6 обозначают (C1-C6)алкил, -(CH2)nOR5, причем n обозначает 2, 3 или 4, а R5 обозначает водород или (C1-C4)алкил, или представляет собой -(CH2)nAr, причем n обозначает 0, 1, 2, 3 или 4, а Ar является одно- или многократно замещенным фенилом, заместители которого определены выше; или представляют собой -(CH2)nHet, причем n обозначает 1, 2 3 или 4, а Het обозначает гетероциклическое кольцо, которое в качестве гетероатомов содержит 1 или 2 атома азота, которое может быть одно- или многократно замещено метилом, или радикалы R3 и R4 вместе со связывающим их атомом азота образуют гетероцикл, который также может быть одно- или многократно замещен метилом.
Предпочтительны, кроме того, соединения формулы I, в которых X представляет собой NR3R4 и один из радикалов R3 и R4 представляет собой водород, а другой представляет собой водород, (C1-C6)алкил, -(CH2)nNR5R6, причем n обозначает 1, 2 или 3, а R5 и R6 обозначают (C1-C6)алкил, -(CH2)nAr, причем n обозначает 1 или 2, а Ar обозначает незамещенный либо одно- или многократно замещенный фенильный радикал, или (CH2)nHet, причем n обозначает 1, 2 или 3, а Het обозначает пиридил или имидазолил, или оба R3 и R4 вместе со связывающим их атомом азота образуют пирролидиновое или пиперазиновое кольцо, замещенное метилом.
К предпочтительным
соединениям общей формулы I относятся далее такие, в которых один из радикалов R1 и R2 представляет собой гидроксиметил, а другой представляет собой

или предпочтительно

Особенно предпочтительными являются такие соединения общей формулы I, в которой R1 представляет собой гидроксиметил, либо R2 представляет собой гидроксиметил. Наиболее предпочтительным является амид-4-гидроксиметил-2-оксифуразан-3-карбоновой кислоты.
Предлагаемые согласно изобретению соединения общей формулы I, в которых
один из радикалов R1 и R2 представляет собой -CONR3R4, могут быть получены, например, путем окисления известного из публикаций соединения формулы II (см.
Synthesis 1977, стр. 977) с помощью окислителя до соединения формулы III или формулы IV или же до смеси соединений формул III или IV

после чего соединения формулы III и/или IV подвергают взаимодействию с амином HNR3R4, где R3 и R4 имеют указанные выше значения.
В качестве окислителей в названной реакции могут использоваться традиционные реагенты, такие как, например, галогены, N-хлор- и N-бромсукцинимид, гипохлориты щелочных и щелочноземельных металлов, алкилгипохлориты, такие как, например, трет.-бутилгипохлорит, соединения четыреххлористого свинца, такие как, например, ацетат четыреххлористого свинца, соли железа (III), такие как, например, красная кровяная соль, или нитрозные газы, как, например, N2O3 или N2O4. Предпочтительными окислителями являются гипохлориты щелочных и щелочноземельных металлов и алкилгипохлориты. Обменную реакцию осуществляют предпочтительно в растворителе, таком как, например, вода, спирт, таком как, например, метанол или этанол, простой эфир, сложный эфир, таком как, например, этилацетат, карбоновая кислота, такая как, например, уксусная кислота, метиленхлорид, хлороформ, циклогексан, бензол, толуол, хлорбензол, дихлорбензол, диметилформамид (ДМФА) или диметилсульфоксид (ДМСО), или в смеси растворителей в диапазоне температур от -10oC до 50oC, предпочтительно от -5oC до 25oC. Соединения формул III и/или IV могут непосредственно, без выделения, использоваться в последующей реакции.
Соединения формул III и/или IV с помощью спиртов R7OH, причем R7 имеет указанные выше значения, могут быть также превращены сначала в предлагаемые по изобретению сложные эфиры общих формул Ic и/или Id. Алкоголиз может осуществляться также без выделения соединений формул III и/или IV. Так, например, окисление соединений формулы II можно проводить таким образом, что в результате получают непосредственно соединения общих формул Ic и/или Id.

Предлагаемые согласно изобретению сложные эфиры общих формул Ic и/или Id при определенных условиях в свою очередь могут переводиться с помощью аминов R3R4NH в амиды по изобретению. Этот аминолиз, равно как и аминолиз соединений III и/или IV, может осуществляться в растворителе или без него. В качестве растворителей могут использоваться, например, вода, спирты, такие как метанол, этанол, н- или изопропанол, н- или изобутанол, сложные эфиры, такие как этил- или изопропилацетат, простые эфиры, такие как диэтиловый, дипропиловый, дибутиловый эфир, трет.-бутилметиловый эфир, тетрагидрофуран, диоксан или моно- либо диалкиловый эфир этиленгликоля либо диэтиленгликоля, углеводороды, такие как толуол или ксилол, хлористые углеводороды, такие как дихлорметан, хлорбензол или дихлорбензол либо, например, диметилформамид, N-метилпирролидон или диметилсульфоксид. Температура реакции лежит в диапазоне от -10oC до 140oC, предпочтительно от 0oC до 80oC.
Соединения
общей формулы I, в которых один из радикалов R1 и R2 представляет собой -CON3R4, могут быть получены также следующим путем: сначала соединение формулы II с
помощью аминов R3R4NH, где R3 и R4 имеют указанное выше значение, превращают в соединение общей формулы V

которое затем окисляют до соединений общей формулы I, причем и в этом случае на каждой из стадий могут использоваться растворители и окислители, приведенные в качестве примеров при описании предыдущих вариантов осуществления способа.
При определенных условиях соединения общей формулы I по изобретению, получаемые по одному из вышеописанных способов, путем модифицирования заместителей могут быть превращены в другие предлагаемые согласно изобретению соединения общей формулы I. Так, например, боковую цепь -CO-NH-(CH2)mCOOR5 взаимодействием с амином HNR5R6 можно превратить в боковую цепь -CO-NH-(CH2)mCONR5R6. Аналогичное превращение возможно также и в отношении боковой цепи -CO-NH-CH(Alk)-COOR5.
Соединения общей формулы I, в которых один из радикалов R1 и
R2 представляет собой -CON3R4, могут быть получены взаимодействием соединений общей формулы VI

в которой один из радикалов R8 и R9 является гидроксиметилом, а другой представляет собой реакционноспособную кислотную группу, такую как, например,

c амином HNR3R4, где R3 и R4 имеют указанное выше значение. Предпочтительно реакцию осуществляют в присутствии основания, нейтрализующего образующиеся кислоты. В качестве таких оснований предпочтительно используют карбонаты щелочных металлов, такие как гидрокарбонат натрия или калия или карбонат натрия или калия, гидроксиды щелочных металлов, такие как гидроксид натрия, калия или лития, алкоголяты щелочных металлов, такие как метилат натрия или калия, этилат натрия или калия либо трет.-бутилат калия, гидриды щелочных металлов, такие как гидрид натрия или калия, амиды щелочных металлов, такие как амид натрия или диизопропиламид лития, или же органические основания, такие как пиридин или триэтиламин. Эти основания применяют преимущественно в молярных количествах. В качестве растворителей в зависимости от типа реакционноспособной кислотной группы могут использоваться вода, спирты, такие как метанол, этанол, н- или изопропанол, н- или изобутанол, простые эфиры, такие как диэтиловый, дипропиловый, дибутиловый эфир, тетрагидрофуран, диоксан или моно- либо диалкиловый эфир этиленгликоля либо диэтиленгликоля, углеводороды, такие как толуол или ксилол, хлористые углеводороды, такие как дихлорметан, хлорбензол или дихлорбензол, либо, например, диметилформамид, N-метилпироллидон или диметилсульфоксид. Температура реакции лежит в диапазоне от -10oC до 80oC.
В названных реакциях получения соединений общей формулы I эти последние или промежуточные соединения общих формул III/IX, Ic/Id и VI получают, как правило, в виде смеси изомеров, и в случае соединений общей формулы I речь идет о смеси соединений общих формул Ia и Ib. Их, однако, можно разделять с помощью известных методов, таких, как перекристаллизация или хроматография, в частности колоночная хроматография. Разделение, следовательно, может проводиться на стадии получения промежуточного продукта или же на стадии получения соединений общей формулы I по изобретению. Если разделяемые соединения несут основную или кислотную группу, может оказаться целесообразным перевести их сначала в соль, а затем уже разделять смесь изомерных солей. Смеси изомеров получают также в тех случаях, когда чистый изомер после его растворения в субстанции или в инертном растворителе подвергают нагреву до температуры в диапазоне от 50 до 200oC или фотолизу при температуре в диапазоне от 0 до 50oC. Тем самым разделением полученной таким путем смеси появляется возможность один изомер перевести в другой.
Предлагаемые по изобретению соединения общей формулы I, содержащие основную группу, могут образовывать с помощью неорганических или органических кислот кислотно-аддитивные соли. Пригодными для образования фармацевтически приемлемых солей кислотами являются, например, хлористый водород, бромистый водород, нафталиндисульфоновые кислоты, прежде всего нафталиндисульфоновая кислота (1,5), фосфорная, азотная, серная, щавелевая, молочная, винная, уксусная, салициловая, бензойная, муравьиная, пропионовая, пивалевая, диэтилуксусная, малоновая, янтарная, пимелиновая, фумаровая, малеиновая, яблочная, сульфаминовая, фенилпропионовая, глюконовая, аскорбиновая, изоникотиновая, метансульфоновая, п-толуолсульфоновая, лимонная или адипиновая кислоты. Аддитивные соли кислот могут быть получены по обычной методике, а именно смешиванием соответствующих компонентов, предпочтительно в пригодном для таких целей растворителе или разбавителе. Аддитивные соли кислот, получаемые для разделения изомеров из соединений общей формулы I, можно соответственно при определенных условиях непосредственно путем анионного обмена или с помощью свободного основания перевести, если таковое диктуется целями применения веществ, в фармацевтически приемлемые аддитивные соли кислот.
Предлагаемые согласно изобретению соединения общей формулы I, содержащие кислотную группу, например, карбоксигруппу, могут образовывать с помощью неорганических или органических оснований соли. Приемлемыми для применения в фармакологии солями являются, например, соли натрия, соли калия, соли магния, соли кальция, соли аммония или соли, образуемые с помощью органических аминов, в частности этаноламина или аминокислот.
Производные гидроксиметилфуразанкарбоновой кислоты общей формулы I и их фармацевтически приемлемые соли обладают ценными фармакологическими свойствами, основанными на образовании окиси азота и его действии. В гладких мышцах они обусловливают релаксацию, а в тромбоцитах проявляют противоадгезивное и противоагрегационное действие. Кроме того, окись азота играет решающую роль в регуляции функций почек, в защите иммунной системы или при эректильных дисфункциях. Таким образом, соединения общей формулы I могут применяться при названных показаниях, и прежде всего при лечении, соответственно предупреждении, заболеваний сердечно-сосудистой системы, в частности при стенокардии.
Фармакологическое действие соединений формулы I выявляли с помощью модифицированного метода Godfraind и Kaba (Arch. Int. Pharmacodyn. Ther. 196, (Suppl. ), стр. 35-49, 1972 г.) и Schueman et al. (Naunyn-Schmiedeberg's Arch. Pharmacol. 289, стр. 409-418, 1975 г.). При этом спиральные полосы пульмональной артерии морской свинки деполяризовали после уравновешивания в бескальциевом растворе Тироде 40 ммоль/л калия. После добавки 0,5 ммоль/л CaCl2 происходило сокращение. Введением кумулятивной добавки испытуемого вещества определяли его расслабляющее действие. На основании графической кривой концентрации (ось абсцисс: log концентрации (моль/л) испытуемого вещества, ось ординат: % подавления максимального сокращения, среднее значение 4-6 полос сосудов) определяли концентрацию испытуемого вещества, которая подавляет сокращение на 50% (=IC50, моль/л).
Ниже наряду с полученными описанным методом значений IC50 соединений по изобретению приведены соответствующие
значения для молсидомина и изосорбид-5-мононитрата, двух часто применяемых при лечении стенокардии (Angina pectoris) биологически активных веществ. По сравнению с этими веществами соединения по
изобретению отличаются заметно более высокой эффективностью: - IC50 (моль/л)
Соединение 1 I (пример 1) - 8•10-6
Соединение 3 I (пример 3) - 1,2•
10-5
Соединение из примера 4 I - 7,3•10-6
Соединение из примера 8 - 8•10-6
Соединение из примера 18 - 8•10-6
Соединение из примера 23 - 1,5•10-5
Соединение из примера 24 - 2•10-6
Соединение из примера 26 - 1,1•10-5
Молсидомин - 3•10-4
Изосорбид-5-мононитрат - > 1•10-4
Соединения общей формулы I и их фармацевтически приемлемые соли могут поэтому
применяться в качестве лекарственных средств для людей как таковые, а также в смесях друг с другом или в виде фармацевтических композиций, которые позволяют вводить их энтерально или парентерально и
которые в качестве активного ингредиента содержат эффективную дозу по крайней мере одного соединения общей формулы I или одной из его солей наряду с обычными фармацевтически приемлемыми наполнителями
и добавками.
Лекарственные средства могут вводиться орально, например в форме таблеток, пилюль, лаковых таблеток, драже, мягкожелатиновых и твердожелатиновых капсул, растворов, сиропов, эмульсий либо суспензий или же в виде аэрозольных смесей. Введение может проводиться также ректально, например в форме суппозиториев, или парентерально, например в форме растворов для инъекций или растворов для внутривенного введения, или же через кожу, например в форме мазей или настоек.
Для изготовления фармацевтических препаратов могут использоваться инертные в фармацевтическом отношении неорганические либо органические наполнители. Для изготовления пилюль, таблеток, драже и капсул с твердожелатиновой оболочкой можно использовать, например, лактозу, кукурузный крахмал или его производные, тальк, стеариновую кислоту или ее соли и т.п. В качестве наполнителей для капсул с мягкожелатиновой оболочкой и суппозиториев могут служить, например, жиры, воск, полутвердые и жидкие полиолы, природные или отвержденные масла и т. п. В качестве наполнителей при изготовлении растворов и сиропов могут использоваться, например, вода, сахароза, инвертный сахар, глюкоза, полиолы и т.п. В качестве наполнителей при изготовлении растворов для инъекций пригодны, например, вода, спирты, глицерин, полиолы или растительные масла.
Наряду с биологически активными веществами и наполнителями фармацевтические препараты могут содержать еще и добавки, такие как, например, разбавители, увлажнители, связывающие вещества, мягчители, смачивающие средства, стабилизаторы, эмульгаторы, консерванты, сладкие вещества, красители, вещества, улучшающие вкус и запах, буферы, далее растворители или вещества, улучшающие растворимость, или вещества для получения эффекта продленного действия, а также соли для изменения осмотического давления, средства для оболочек или антиоксиданты. Фармацевтические препараты могут содержать, кроме того, два или более соединений общей формулы I или их фармацевтически приемлемых солей, а также другие терапевтически эффективные вещества. К таковым относятся, в частности, блокаторы β -рецепторов, такие как, например, пропанолол, пиндолол, метопролол; вазодилататоры, такие как, например, карбохромен; успокоительные средства, такие как, например, производные барбитуровой кислоты, 1,4-бензодиазепины и мепробамат; мочегонные средства, такие как, например, хлортиазид; кардиотонизирующие средства, такие как, например, препараты из наперстянки; средства, снижающие кровяное давление, такие как, например, гидралазин, дигидралазин, рамиприл, празозин, клонидин, алкалоиды раувольфии; средства, снижающие уровень жирной кислоты в крови, такие как, например, безафибрат, фенофибрат; средства для профилактики тромбоза, такие как, например, фенпрокумон.
Производные гидроксиметилфуразанкарбоновой кислоты общей формулы I, их фармацевтически приемлемые соли и фармацевтические препараты, содержащие в качестве биологически активных веществ соединения общей формулы I или их фармацевтически приемлемые аддитивные соли кислот, могут применяться для лечения, соответственно предупреждения, заболеваний сердечно-сосудистой системы человека, например, в качестве противогипертонических лекарственных средств при различных формах высокого кровяного давления, при лечении, соответственно предупреждении, стенокардии (Angina pectoris) и т.д. Кроме того, они могут применяться также при лечении эректильных дисфункций. Их дозировка может варьировать в широких пределах, но в каждом отдельном случае она определяется индивидуальными особенностями пациента.
Как правило, при оральном введении суточная доза для одного человека составляет 0,5-100 мг, предпочтительно 1-20 мг. При других формах введения суточную дозу также назначают примерно в тех же количественных пределах, т.е., как правило, 0,5-100 мг на человека. Эту суточную дозу можно вводить в несколько приемов, например, разделить ее на 2-4 части.
Примеры.
Спектры1H-ЯМР измеряли в D6-ДМСО, используемом в качестве растворителя. Ниже указаны химический сдвиг δ в част/млн, множественность спектральных линий (s = синглет, d = дублет, t = триплет, m = мультиплет) и протонное число сигналов.
1.
4-Гидроксиметил-N-изопропил-2-оксифуразан-3-карбоксамид и 4-гидроксиметил-N-изопропил-5-оксифуразан-3-карбоксамид
а) 4-гидрокси-N-изопропил-2,3-диоксиминобутирамид
9,4 г 3,
4-диоксимино-2-оксотетрагидрофурана суспендируют в 50 мл метанола и смешивают с 4,2 г изопропиламина. Смесь перемешивают в течение 3 ч и охлаждают в ледяной бане. Твердое вещество отсасывают и затем
перекристаллизовывают из метанола.
Выход: 8,5 г; Tтек 133-134oC.
б) 4-гидроксиметил-N-изопропил-2-оксифуразан-3-карбоксамид и
4-гидроксиметил-N-изопропил-5-оксифуразан-3-карбоксамид
Смесь, состоящую из 10 г соединения, полученного на стадии а), 120 мл метиленхлорида и 22 г тетраацетата свинца, перемешивают в течение
5 ч. Водорастворимые компоненты трижды экстрагируют путем встряхивания с помощью воды, порциями по 100 мл соответственно, органическую фазу сушат над сульфатом натрия и концентрируют в вакууме.
Оставшееся масло разделяют посредством колоночной хроматографии (силикагель, система растворителей: метилехлорид/метанол 99:1). Таким путем получают:
Соединение 1 I: 2-оксипроизводное, выход
3,6 г (масло)
1H-ЯМР: 1,20 (d, 6H), 4,08 (m, 1H), 4,69 (d, 2H), 5,77 (t, 1H), 8,25 (m, 1H)
Соединение 1 II: 5-оксипроизводное, выход 1,8 г (масло)
1
H-ЯМР: 1,20 (d, 6H), 4,08 (m, 1H), 4,57 (d, 2H), 5,68 (t, 1H), 9,04 (m, 1H)
2. Метиловый эфир 4-гидроксиметил-2-оксифуразан-3-карбоновой кислоты и метиловый эфир
4-гидроксиметил-5-оксифуразан-3-карбоновой кислоты
В смесь, состоящую из 2,9 г 3,4-диоксимино-2-оксотетрагидрофурана, 30 мл метиленхлорида и 10 мл метанола, при охлаждении льдом добавляют 8,9
г тетраацетата свинца. После перемешивания в течение 2 ч при комнатной температуре добавляют 3 мл триэтиламина, после чего перемешивание продолжают еще в течение 30 мин, затем разбавляют 30 мл
метиленхлорида и дважды промывают соответственно порциями по 30 мл воды. Органическую фазу сушат над сульфатом натрия и концентрируют в вакууме. Остаток тщательно смешивают с трет.-бутилметиловым
эфиром и полученное твердое вещество отсасывают. Для разделения изомеров проводят перекристаллизацию из трет.-бутилметилового эфира. Таким путем получают:
Соединение 2 I: 2-оксипроизводное,
выход 1,9 г, Tтек 92-94oC.
1H-ЯМР: 3,86 (s, 3H), 4,70 (s, 2H), 5,76 (m, 1H)
Соединение 2 II: 5-оксипроизводное содержится в маточном растворе
перекристаллизации.
3. 4-Гидроксиметил-2-оксифуразан-3-карбоксамид и 4-гидроксиметил-5-оксифуразан-3-карбоксамид
а) 4-гидроксиметил-2-оксифуразан-3-карбоксамид
(Соединение 3 I)
1,9 г метилового эфира 4-гидроксиметил-2-оксифуразан-3-карбоновой кислоты из примера 2) смешивают в 25 мл метанола с 7,2 г концентрированного водного раствора аммиака. Через
1 ч смесь концентрируют в вакууме и остаток перекристаллизовывают из воды.
Выход: 1,1 г; Tтек 128-130oC.
1H-ЯМР: 4,72 (d, 2H), 5,73 (t,
1H), 7,85 (m, 1H), 8,41 (m, 1H)
Структура была подтверждена рентгеноанализом.
б) 4-гидроксиметил-5-оксифуразан-3-карбоксамид
(Соединение 3 II)
Соответственно
тому, как это описано в а), содержащийся в маточном растворе перекристаллизации метиловый эфир 4-гидроксиметил-5-оксифуразан-3-карбоновой кислоты из примера 2) подвергали взаимодействию с аммиаком.
Полученный продукт очищали посредством колоночной хроматографии (силикагель, система растворителей: метиленхлорид/метанол 98:2). Tтек 145-147oC.
1H-ЯМР:
4,57 (d, 2H), 5,60 (t, 1H), 8,20 (m, 1H), 8,50 (m, 1H)
Аналогичным путем получают:
4 I. 4-гидроксиметил-N-метил-2-оксифуразан-3-карбоксамид
Tтек 104-106oC
1H-ЯМР: 2,80 (s, 3H), 4,72 (s, 2H), 5,70 (m, 1H), 8,41 (m, 1H)
4 II. 4-гидроксиметил-N-метил-5-оксифуразан-3-карбоксамид
Tтек 86-88o
C
1H-ЯМР: 2,91 (d, 3H), 4,57 (d, 2H), 5,63 (t, 1H), 9,12 (m, 1H)
5. Гидрохлорид 4-метилпиперазида 4-гидроксиметил-2-оксифуразан- 3-карбоновой кислоты
Tтек 210oC (разложение)
1H-ЯМР: 2,82 (s, 3H), 3,0-4,4 (m, 8H), 4,62 (s, 2H), 9,0-10,0 (m, 2H)
6. Гидрохлорид
N-(2-диизопропиламиноэтил)-4-гидроксиметил-2- оксифуразан-3-карбоксамида
Tтек 189-191oC
1H-ЯМР: 1,40 (d, 12H), 3,2 (m, 2H), 3,70 (m, 4H), 4,74 (s, 2H),
5,75 (m, 1H), 8,84 (m, 1H), 10,30 (m, 1H)
7. N-бутил-4-гидроксиметил-2-оксифуразан-3-карбоксамида
Масло
1H-ЯМР: 0,91 (t, 3H), 1,30 (m, 2H), 1,45 (m, 2H), 3,26 (m,
2H), 4,72 (s, 2H), 5,75 (m, 1H), 8,45 (m, 1H)
8. Гидрохлорид 4-гидроксиметил-N-(3-пиридилметил)-2-оксифуразан- 3-карбоксамида
Tтек 185oC (разложение)
1H-ЯМР: 4,68 (d, 2H), 4,72 (s, 2H), 8,0 (m, 1H), 8,51 (m, 1H), 8,80 (m, 1H), 8,90 (s, 1H), 9,30 (m, 1H)
9. N-бензил-4-гидроксиметил-2-оксифуразан-3-карбоксамида
Tтек 94-96oC
1H-ЯМР: 4,48 (s, 2H), 4,73 (s, 2H), 5,80 (m, 1H), 7,30 (m, 5H), 8,85 (m, 1H)
10.
N-карбамоилметил-4-гидроксиметил-2-оксифуразан-3-карбоксамид
Tтек 186-188oC
1H-ЯМР: 3,85 (d, 2H), 4,74 (t, 2H), 5,73 (t, 1H), 7,20 (m, 1H), 7,50 (m,
1H), 8,60 (m, 1H)
11. Пирролидид 4-гидроксиметил-2-оксифуразан-3-карбоновой кислоты
Масло
1H-ЯМР: 1,85 (m, 4H), 3,47 (m, 4H), 4,60 (d, 2H), 5,78 (t, 1H)
12. 4-гидроксиметил-N-изобутил-2-оксифуразан-3-карбоксамид
Масло
1H-ЯМР: 0,89 (d, 6H), 1,84 (m, 1H), 3,12 (m, 2H), 4,72 (d, 2H), 5,77 (t, 1H)
13.
4-гидроксиметил-N-(2-гидроксиэтил)-2-оксифуразан-3-карбоксамид
Tтек 69-71oC
1H-ЯМР: 3,36 (m, 2H), 3,53 (m, 2H), 4,72 (d, 2H), 4,86 (t, 1H), 5,72 (t,
1H), 8,40 (m, 1H)
14. Гидрохлорид 4-гидроксиметил-N-(2-диизопропиламиноэтил)-5-оксифуразан-3-карбоксамида
Tтек 167-170oC
1H-ЯМР: 1,35 (q,
12H), 3,20 (m, 2H), 3,69 (m, 4H), 4,57 (s, 2H), 5,69 (m, 1H), 9,48 (m, 1H), 10,23 (m, 1H)
15. 4-гидроксиметил-N-(3-(имидазол-1-ил)-пропил)-5-оксифуразан- 3-карбоксамид
Tтек
145-147oC
1H-ЯМР: 1,95 (m, 2H), 3,25 (m, 2H), 4,00 (m, 2H), 4,54 (s, 2H), 5,71 (m, 1H), 6,87 (s, 1H), 7,18 (s, 1H), 7,62 (s, 1H), 9,27 (m, 1H)
16.
4-гидроксиметил-N-(2-гидроксиэтил)-5-оксиифуразан-3-карбоксамид
Tтек масло
1H-ЯМР: 3,32 (m, 2H), 3,52 (m, 2H), 4,55 (d, 2H), 4,70 (m, 1H), 5,67 (t, 1H), 9,09 (m,
1H)
17. 4-гидроксиметил-N,N-диметил-2-оксифуразан-3-карбоксамид
Tтек масло
1H-ЯМР: 2,98 (d, 6H), 4,58 (d, 2H), 5,84 (t, 1H)
18.
4-гидроксиметил-N-(2-метоксиэтил)-2-оксифуразан-3-карбоксамид
Tтек масло
1H-ЯМР: 3,26 (s, 3H), 3,47 (s, 4H), 4,73 (s, 2H), 5,77 (m, 1H), 8,48 (m, 1H)
19. Изопропиловый эфир 4-гидроксиметил-2-оксифуразан-3-карбоновой кислоты
Масло
1H-ЯМР: 1,30 (d, 6H), 4,69 (d, 2H), 5,17 (m, 1H), 5,70 (t, 1H)
20.
4-гидроксиметил-N-(3-(имидазол-1-ил)-пропил)-2-оксифуразан- 3-карбоксамид
Tтек 122-125oC
1H-ЯМР: 1,93 (m, 2H), 3,23 (m, 2H), 4,00 (m, 2H), 4,72 (s,
2H), 5,89 (m, 1H), 6,90 (s, 1H), 7,18 (s, 1H), 7,63 (s, 1H), 8,60 (m, 1H)
21. 4-гидроксиметил-N-(3-гидроксипропил)-5-оксифуразан-3-карбоксамид
масло
1H-ЯМР: 1,69
(m, 2H), 3,33 (m, 2H), 3,47 (m, 2H), 4,52 (m, 3H), 5,65 (t, 1H), 9,10 (m, 1H)
22. 4-гидроксиметил-N-(3-пиридилметил)-5-оксифуразан-3-карбоксамид
Tтек 154-156o
C
1H-ЯМР: 4,51 (d, 2H), 4,59 (d, 2H), 5,63 (t, 1H), 7,39 (m, 1H), 7,75 (m, 1H), 8,49 (m, 1H), 8,59 (s, 1H), 9,78 (m, 1H)
23.
4-гидроксиметил-N-((S)-1-фенилэтил)-2-оксифуразан-3-карбоксамид
Tтек масло
α = +17,5 (c=5,472, MeOH)
1H-ЯМР: 1,48 (d, 3H), 4,69 (d, 2H), 5,10 (m, 1H), 5,87 (t, 1H), 7,33 (m, 5H), 8,84 (d, 1H)
24.
4-гидроксиметил-N-((R)-1-фенилэтил)-2-оксифуразан-3-карбоксамид
Масло
α
1H-ЯМР: 1,48 (d, 3H), 4,69 (d, 2H), 5,10 (m, 1H), 5,87 (t, 1H), 7,33 (m, 5H), 8,84 (d, 1H)
25.
4-гидроксиметил-N-октадецил-2-оксифуразан-3-карбоксамид
Tтек 75-77oC
1H-ЯМР: 0,6-1,6 (m, 35H), 3,30 (m, 2H), 4,70 (m, 2H), 5,76 (m, 1H), 8,50 (m,
1H)
26. 4-гидроксиметил-N-[2-(4-сульфамоилфенил)-этил] -2-оксифуразан- 3-карбоксамид
Tтек 152-154oC
1H-ЯМР: 2,90 (m, 2H), 3,53 (m, 2H), 4,72
(s, 2H), 5,80 (m, 1H), 7,23 (m, 2H), 7,42 (d, 2H), 7,77 (d, 2H), 8,57 (m, 1H)
27. Метиловый эфир 4-гидроксиметил-2-оксифуразан-3-карбоновой кислоты
а) 3,
4-диоксимино-2-оксотетрагидрофуран
В смесь, состоящую из 49 г тетроновой кислоты, 43,4 г концентрированной соляной кислоты и 100 мл воды, при охлаждении льдом добавляют по каплям раствор 30,4
г нитрита натрия в 60 мл воды. Затем смесь перемешивают в течение 30 мин, после чего смешивают с раствором 30,6 г гидрохлорида гидроксиламина в 60 мл воды. При охлаждении льдом продолжают
перемешивание еще в течение 3 ч, после чего продукт отсасывают, промывают водой и после сушки отсасывают.
Выход: 76,3 г (влажный)
Tтек 160-180oC
(разложение)
3,4-диоксимино-2-оксотетрагидрофуран получают также из этилового эфира 4-трет. -бутоксиацетуксусной кислоты путем обработки водной серной кислотой либо соляной кислотой,
нитрозирования образовавшейся в качестве промежуточного продукта тетроновой кислоты и взаимодействия с гидрохлоридом гидроксиламина с выходом 60%.
б) Метиловый эфир
4-гидроксиметил-2-оксифуразан-3-карбоновой кислоты
В охлажденную в ледяной бане смесь, состоящую из 27 г 3,4-диоксимино-2-оксотетрагидрофурана и 210 мл метанола, быстро добавляют по каплям
раствор 18,9 г трет.-бутилгипохлорита в 25 мл этилацетата. Затем небольшими порциями при охлаждении производят добавку ацетата калия (18,5 г) и смесь, помещенную в постепенно нагревающуюся до
комнатной температуры ледяную баню, перемешивают в течение ночи. Затем смесь концентрируют в вакууме, остаток растворяют в воде и полученный продукт экстрагируют с помощью этилацетата. После сушки и
концентрирования этилацетатной фазы проводят перекристаллизацию из изопропилацетата.
Выход: 14,7 г
Tтек 97-98oC
Вышеописанным способом получают
также метиловый эфир 4-гидроксиметил-2-оксифуразан-3-карбоновой кислоты, с той лишь разницей, что вместо раствора трет. -бутилгипохлорита в этилацетате используют твердый 70%-ный гипохлорит
кальция.
28. 4-гидроксиметил-N-циклогексил-2-оксифуразан-3-карбоксамид
Tтек 97-98oC
1H-ЯМР: 1,10-1,85 (m, 10H), 3,74 (m, 1H), 4,72 (s,
2H), 5,82 (m, 1H), 8,25 (m, 1H)
29. 4-гидроксиметил-N-этоксикарбонилметил-2-оксифуразан-3-карбоксамид
Tтек масло
1H-ЯМР: 1,23 (t, 3H), 4,08 (d, 2H), 4,
15 (q, 2H), 4,74 (d, 2H), 5,73 (t, 1H), 8,81 (m, 1H)
30. 4-гидроксиметил-N-(2-ацетиламиноэтил)-2-оксифуразан-3-карбоксамид
Tтек 126-128oC
1
H-ЯМР: 1,79 (s, 1H), 3,20 (m, 2H), 3,33 (m, 2H), 4,75 (s, 2H), 5,76 (m, 1H), 7,80 (m, 1H), 8,51 (m, 1H)
31. 4-гидроксиметил-N-аллил-2-оксифуразан-3-карбоксамид
Tтек
масло
1H-ЯМР: 3,90 (s, 2H), 4,76 (s, 2H), 5,17 (m, 2H), 5,83 (m, 1H), 5,78 (m, 1H), 8,67 (m, 1H)
32. 4-гидроксиметил-N-(1-этоксикарбонилэтил)-2-оксифуразан-3-карбоксамид
Tтек масло
1H-ЯМР: 1,32 (t, 3H), 1,40 (d, 3H), 4,32 (q, 2H), 4,50 (m, 1H), 4,73 (d, 2H), 5,71 (t, 1H), 8,81 (m, 1H)
33.
4-гидроксиметил-N-[3-(2-оксопирролидин-1-ил)-пропил] -2- оксифуразан-3-карбоксамид
Tтек 120-122oC
1H-ЯМР: 1,65 (m, 2H), 1,92 (m, 2H), 2,22 (m, 2H), 3,
21 (m, 4H), 3,38 (m, 2H), 4,74 (s, 2H), 5,73 (m, 1H), 8,55 (m, 1H)
34. 4-гидроксиметил-N-[2-(3,4-диметоксифенил)-этил] -2- оксифуразан-3-карбоксамид
Tтек 128-130oC
1H-ЯМР: 2,77 (t, 2H), 3,46 (t, 2H), 3,73 (s, 3H), 3,74 (s, 3H), 4,70 (s, 2H), 5,72 (m, 1H), 6,70-6,91 (m, 3H), 8,44 (m, 1H)
В нижеследующих примерах А-Е
представлено описание фармацевтических препаратов
Пример А
Капсулы с мягкожелатиновой оболочкой, содержащие 5 мг биологически активного вещества в одной капсуле: - на 1 капсулу
Активное вещество - 5 мг
Фракционированная триглицеридная смесь из кокосового масла - 150 мг
Содержимое капсулы - 155 мг
Пример Б
Раствор для инъекций,
содержащий 1 мг биологически активного вещества на 1 мл: - на 1 мл
Активное вещество - 1,0 мг
Полиэтиленгликоль 400 - 0,3 мл
Хлорид натрия - 2,7 мг
Вода для
инъекций - до 1,0 мл
Пример В
Эмульсия, содержащая 3 мг биологически активного вещества на 5 мл - на 100 мл эмульсии
Активное вещество - 0,06 г
Нейтральное масло
- q.s.
Натрийкарбоксиметилцеллюлоза - 0,6 г
Стеарат полиоксиэтилена - q.s.
Глицерин чистый - 0,2-2,0 г
Вкусовое вещество - q.s.
Вода
(опресненная или дистиллированная) - до 100 мл
Пример Г
Ректальный препарат, содержащий 4 мг биологически активного вещества на один суппозиторий - на 1 суппозиторий
Активное вещество - 4 мг
Основа суппозитория - до 2 г
Пример Д
Таблетки, содержащие 2 мг биологически активного вещества в одной таблетке - на 1 таблетку
Активное
вещество - 2 мг
Лактат (тонкоизмельченный) - 2 мг
Кукурузный крахмал (белый) - 150 мг
Молочный сахар - 60 мг
Микрокристаллическая целлюлоза - 50 мг
Поливинилпирролидон - 20 мг
Стеарат магния - 2 мг
Натрийкарбоксиметиловый крахмал - 25 мг - 311 мг
Пример Е
Драже, содержащие 1 мг биологически активного вещества в
одной пилюле - на 1 пилюлю
Активное вещество - 1 мг
Кукурузный крахмал - 100 мг
Лактоза - 60 мг
Втор.-фосфат кальция - 30 мг
Растворимый крахмал - 3 мг
Стеарат магния - 2 мг
Коллоидная кремниевая кислота - 4 мг - 200 мгH
Реферат
Описываются новые производные гидроксиметилфуразанкарбоновой кислоты общей формулы I, в которой один из радикалов R1 и R2 представляет собой гидроксиметил, а другой представляет собой
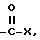
-(CH2)m COOR5, -CH(Alk)-COOR5, -(CH2)m-CONR5R6, CH(Alk)-CONR5R6,

Формула
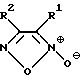
в которой один из радикалов R1 и R2 представляет собой гидроксиметил, а другой представляет собой

R3 и R4 независимо друг от друга обозначают водород, (С1-С20)-алкил, 1-фенил (С2-С4)-алкил, 2-фенил-(С3-С4)-алкил, (С3-С6)-алкенил, (С3-С7)-циклоалкил, -(СН2)n-NR5 R6, -(СН2)n-ОR5, -(СН2)m-COOR5,
-СН(Alk)-СООR5, -(СН2)m-СОNR5R6, СН(Alk)-CONR5R6,

-(СН2)n-NR5 (COAlk), -(СН2)n-Ar или -(СН2)n-Неt; или R3 и R4 вместе со связывающим их атомом азота образуют гетероцикл, который также может быть однократно либо многократно замещен на (С1-С6)-алкил, (С3-С7)-циклоалкил, (С1-С4)-алкоксигруппу, аминогруппу, (С1-С4)-алкиламиногруппу, ди-((С1-С4)алкил)-аминогруппу, гидроксильную группу, бензил, фенетил или фенил;
R5 и R6 независимо друг от друга обозначают водород, (С1-С6)-алкил, (С3-С7)-циклоалкил, бензил, фенетил или фенил;
R7 обозначает (С1-С6)-алкил, (С3-С7)-циклоалкил, бензил, фенил, который может быть однократно либо многократно замещен на (С1-С4)-алкил;
Alk обозначает (C1-C6)-алкил;
Ar представляет собой фенил, который может быть однократно либо многократно замещен на (С1-С4)-алкил, (С1-С4)-алкоксигруппу или сульфамоил;
Het является гетероциклическим радикалом с 1-3 атомами азота, который может быть ароматическим, частично ненасыщенным или насыщенным, а также может быть однократно либо многократно замещен на (С1-С4)-алкил;
n обозначает 0, 1, 2, 3 или 4;
m обозначает 1, 2, 3 или 4;
р обозначает 1, 2 или 3;
а также их фармацевтически приемлемые соли.

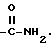
6. Соединения по пп.1-5, в которых R1 представляет собой гидроксиметил.

Комментарии