Способ получения производных пиримидина, промежуточные продукты и способ их получения - RU2174978C2
Код документа: RU2174978C2
Описание
Изобретение относится, во-первых, к способу получения 5,
6-диметил-2-(4-фторфениламино)-4-(1-метил-1,2,3,4-тетрагидроизохинолин-2-ил)пиримидина, представленного следующей формулой (I) и его солей присоединения кислот; во-вторых, к способу получения
промежуточных соединений для получения соединения (1); и, в-третьих, к новому промежуточному соединению. Более конкретно, настоящее изобретение относится, во-первых, к способу получения 5,
6-диметил-2-(4-фторфениламино)-4-(1-метил-1,2,3,4-тетрагидроизохинолин-2-ил)пиримидина, представленного следующей формулой (I),

и его солей присоединения кислот, где производное пиримидина, представленное нижеследующей формулой (II-A),

в котором Hal представляет галоген, подвергают взаимодействию с 1-метил-1,2,3,4-тетрагидроизохинолином, представленным следующей формулой (III);

во-вторых, к способу получения производного пиримидина, представленного формулой (II-А), и соединения формулы (III); и, в-третьих, к новому промежуточному соединению, включая производное пиримидина, представленное формулой (II-A).
5, 6-Диметил-2-(4-фторфениламино)-4-(1-метил-1,2,3,4- тетрагидроизохинолин-2-ил) пиримидин вышеприведенной формулы (I) ингибирует выделение желудочной кислоты посредством обратимого эффекта торможения протонного насоса и благодаря этому может быть использован как противоязвенный агент. Это соединение было разработано авторами настоящего изобретения, которые затем подали заявки на патент на соединение и/или способ его получения в Корее и других странах (см. Международную публикацию WO 96/05177).
По способу, описанному в ранее поданных патентных заявках 5,
6-диметил-2-(4-фторфениламино)-4-(1-метил-1,2,3,4- тетрагидроизохинолин-2-ил) пиримидин получают по следующей реакционной схеме A:
Реакционная схема A

Поскольку исходный продукт на вышеприведенной реакционной схеме имеет два реакционно-активных участка (т.е. два атома Cl), первая реакция неизбежно дает побочный продукт, который снижает выход целевого соединения.
Авторы настоящего изобретения провели большую работу для того, чтобы разработать новый способ получения 5,6-диметил-2-(4-фторфениламино)-4-(1-метил-1,2,3,4-тетрагидроизохинолин-2-ил)пиримидина формулы (I) без образования побочных продуктов. В результате было обнаружено, что целевое соединение формулы (I) может быть эффективно получено без образования побочных продуктов путем взаимодействия производного пиримидина, представленного формулой (II-A), с 1-метил-1,2,3,4-тетрагидроизохинолином, представленным формулой (III), и, таким образом, разработали настоящее изобретение.
Настоящее изобретение относится к новому способу получения 5, 6-диметил-2-(4-фторфениламино)-4-(1-метил-1,2,3,4-тетрагидроизохинолин-2-ил)пиримидина, представленного формулой (I) и его солей присоединения кислот.
Более конкретно, настоящее
изобретение относится к способу получения 5,6-диметил-2-(4-фторфениламино)-4-(1-метил-1,2,3,4-тетрагидроизохинолин-2-ил)пиримидина, представленного формулой (I)
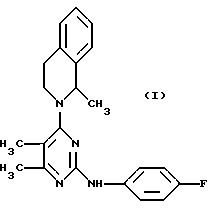
и его солей присоединения кислот, где производное пиримидина, представленное следующей формулой (II-A),
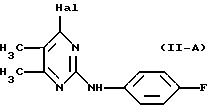
в котором Hal представляет галоген, подвергают взаимодействию с 1-метил-1,2,3,4-тетрагидроизохинолином, представленным формулой (III);
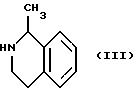
Кроме того, настоящее изобретение относится к способу получения производного пиримидина формулы (II-A) и соединения формулы (III). Далее настоящее изобретение относится к новому промежуточному соединению, представленному следующей формулой (II), которое включает производное пиримидина, представленное формулой (II-A),

в котором R представляет гидрокси или галоген.
По настоящему изобретению соединение формулы (I) может быть получено путем взаимодействия соединения формулы (II-A) с 1-метил-1,2,3,4-тетрагидроизохинолином
формулы (III), как изображено на следующей реакционной схеме 1:
Реакционная схема 1
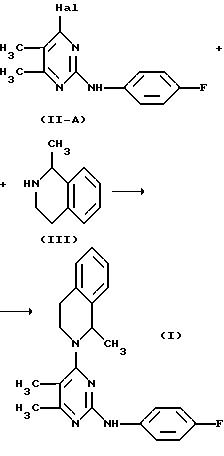
Поскольку исходный продукт на реакционной схеме 1 (т.е. соединение формулы (II-A)) имеет единственный реакционно-активный участок (т.е. Hal), эта реакционная схема не дает никаких побочных продуктов и таким образом оптимизирует выход соединения формулы (I), целевого продукта.
Настоящее изобретение более подробно описано ниже.
Хотя 4-галоген-2-(4-фторфениламино)-5, 6-диметилпиримидин, представленный формулой (II-A), в соответствии с настоящим изобретением может быть подвергнут взаимодействию с эквивалентным количеством 1-метил-1,2,3,4-тетрагидроизохинолина, представленного формулой (III), предпочтительно проводить реакцию, используя избыток, а не эквивалентное количество последнего. Поскольку последний в условиях реакции является жидкостью, непрореагировавший 1-метил-1,2,3,4-тетрагидроизохинолин может быть легко удален после того, как реакция будет завершена.
Реакцию по настоящему изобретению предпочтительно проводить в присутствии растворителя. Растворители, которые могут быть использованы для этой цели, включают N,N-диметилформамид, н-бутанол, н-пентанол, н-гексанол, диметилсульфоксид, этиленгликоль, 1, 2-пропиленгликоль и их смеси. Наиболее предпочтительными из них являются пропиленгликоль и этиленгликоль, поскольку использование любого из них минимизирует и время реакции, и образование побочных продуктов.
По способу настоящего изобретения реакционную схему 1 обычно осуществляют в присутствии основания. Основания, которые могут быть использованы для этой цели, включают триэтиламин, N,N-диметиланилин, пиридин и ацетат калия. Температура реакции для взаимодействия соединения формулы (II-A) и 1-метил-1,2,3,4-тетрагидроизохинолина формулы (III) предпочтительно лежит в интервале от 110oC до 160oC, и время реакции предпочтительно находится в интервале от 16 часов до 72 часов.
5,6-Диметил-2-(4-фторфениламино)-4-(1-метил-1,2,3, 4-тетрагидроизохинолин- 2-ил) пиримидин формулы (I), полученный по вышеописанному способу, может быть преобразован в его соль присоединения кислот, предпочтительно в гидрохлоридную соль, обычными способами. Полученный продукт может быть очищен обычными методами обработки, такими как перекристаллизация, хроматография и т.п.
Поскольку соединение формулы (I), полученное по способу настоящего изобретения, содержит асимметричный атом углерода (т.е. атом углерода, помеченный значком* в приведенной ниже формуле), это соединение может присутствовать в форме (R)-(+)-изомера и (S)-(-)-изомера, или в форме рацемата, где R- и S-изомеры смешаны в соотношении 1:1. Если не указано другое, то соединение формулы (I) должно пониматься как включающее все эти изомеры.
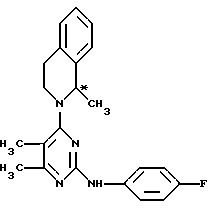
(R)-(+)- и (S)-(-)-изомеры соединения формулы (I) могут быть легко получены из R- и S-изомеров, соответственно, соединения формулы (III).
Соединение формулы (II-A), которое используется как исходный продукт по способу настоящего изобретения, является новым
соединением, которое может быть получено по способу, представленному следующей реакционной схемой 2:
Схема реакций 2

На реакционной схеме 2 Hal представляет галоген.
Как изображено на реакционной схеме 2, взаимодействие 4- фторфенилгуанидинкарбоната формулы (IV) с этил-2-метилацето- ацетатом формулы (V) дает 4-гидрокси-2-(4-фторфениламино)-5,6- диметилпиримидин формулы (II-B), который может затем взаимодействовать с галогенирующим агентом для получения 4- галоген-2-(4-фторфениламино)-5,6-диметилпиримидина формулы (II-A).
4-Фторфенилгуанидинкарбонат формулы (IV), который используется в качестве исходного продукта для получения соединения формулы (II-A) по реакционной схеме 2, может быть легко получен из 4-фторанилина с использованием известных способов (см., например. Европейский патент N 0560726). В частности, желаемый 4-фторфенилгуанидинкарбонат может быть получен взаимодействием 4-фторанилина с 50% раствором цианамида в кислых условиях с использованием 30-37% соляной кислоты и при поддержании температуры в интервале от 75oC до 95oC.
Первая стадия реакционной схемы 2 может быть осуществлена в присутствии растворителя. Растворители, которые могут быть использованы для этой цели, включают ацетонитрил, N,N-диметилформамид и диметилсульфоксид. Эта реакция предпочтительно проводится при температуре в интервале от 110oC до 160oC.
На второй стадии реакционной схемы 2 4-гидрокси-2-(4-фторфениламино)-5,6-диметилпиримидин формулы (II-B), полученный на первой стадии реакционной схемы 2, преобразуют в соединение формулы (II-A) путем взаимодействия первого с галогенирующим агентом. Галогенирующие агенты, которые могут быть использованы для этой цели, включают оксихлорид фосфора, оксалилхлорид, тионилхлорид и трибромид фосфора. Эта реакция галогенирования проводится в присутствии растворителя. Реакционные растворители, которые могут быть использованы для этой цели, включают, предпочтительно, N,N-диметилформамид, диметилсульфоксид, 1,2-дихлорэтан и 1,2-дихлорбензол. Предпочтительно поддерживать температуру реакции в интервале от 75oC до 95oC.
Хотя вторая стадия реакционной схемы 2 может быть проведена путем выделения промежуточного продукта после того, как завершена первая стадия реакции, предпочтительно проводить первую и вторую стадии в одном сосуде. В частности, 4-гидрокси-2-(4-фторфениламино)-5,6-диметилпиримидин формулы (II-B) получают из 4-фторфенилгуанидинкарбоната и затем может быть без выделения успешно подвергнут взаимодействию с галогенирующим агентом с получением 4-галоген-2-(4-фторфенил-амино)-5,6-диметилпиримидина (II-A).
Соединение формулы (II-A), которое используют как исходный материал для получения соединения формулы (I) по настоящему изобретению, является новым, как и соединение формулы (II-B), полученное в качестве промежуточного соединения по реакционной схеме 2. Оба новых соединения могут быть представлены следующей формулой (II), которая входит в объем настоящего изобретения.

в которой R представляет гидрокси или галоген.
1-Метил-1,2,3,4-тетрагидроизохинолин формулы (III), который также используется как исходный продукт по реакционной схеме 1, является известным соединением и может быть получен известными способами (см., например. Международную публикацию WO 94/14795). По этому известному способу (R)- или (S)-1-метил-1,2,3,4-тетрагидроизохинолин получают взаимодействием (R)- или (S)-метилбензиламина с α-хлор-α-метилтио)ацетилхлоридом и хлоридом олова (SnCl2) с получением (R)- или (S)- 1-метил-4-метилтио-1,2,3,4-тетрагидроизохинолин-3-она, соответственно, с последующим взаимодействием полученного соединения с никелем Ренея для удаления метилтиогруппы и с добавлением в конце восстанавливающего агента. Однако этот способ является невыгодным, поскольку α-хлор-α-(метилтио)ацетилхлорид, который используется в качестве исходного продукта, является и нестабильным, и взрывоопасным, поэтому этот способ не может быть использован в промышленном масштабе. Кроме того, поскольку стадия реакции продолжительна, общий выход низок, что делает этот способ неэкономичным.
Авторы настоящего изобретения долгое время работали над поиском более эффективного способа получения 1-метил-1,2,3,4-тетрагидроизохинолина. Было установлено, что 1-метил-1,2,3,4-тетрагидроизохинолин может быть получен экономично и безопасно последовательным взаимодействием α-метилбензиламина с 2-бромэтанолом, бромирующим агентом и кислотой Льюиса. Такой способ получения 1-метил-1,2,3,4-тетрагидроизохинолина является новым и входит в объем изобретения. Этот новый способ получения 1-метил-1,2,3,4-тетрагидроизохинолина более подробно объяснен ниже.
По настоящему изобретению 1-метил-1,2,3, 4-тетрагидроизохинолин формулы (III) может быть получен последовательным взаимодействием α-метилбензиламина с 2-бромэтанолом, бромирующим агентом и кислотой Льюиса. Способ по настоящему изобретению соответствует следующей реакционной схеме 3.
Реакционная схема 3

Все использованные в реакционной схеме 3 исходные продукты и реагенты являются известными соединениями и могут быть получены как промышленные продукты. На первой стадии α-метилбензиламин взаимодействует с 2-бромэтанолом с получением N-(2-гидроксиэтил)-α-метилбензиламин, который в свою очередь, взаимодействует с бромирующим агентом с получением гидробромида М-(2-бромэтил)-α-метилбензиламина. На третьей стадии гидробромид N-(2-бромэтил)-α-метилбензиламина взаимодействует с кислотой Льюиса с получением желаемого 1-метил-1,2,3, 4-тетрагидроизохинолина формулы (III).
Реакционные растворители, которые могут быть использованы на первой стадии, включают ацетонитрил, N,N-диметилформамид, дихлорметан и 1, 2-дихлорэтан, и температуру реакции предпочтительно поддерживают в интервале от 40oC до 60oC. Реакционные растворители, которые могут быть использованы на второй стадии, включают 1,2-дихлорэтан, уксусную кислоту, воду и 1,2-дихлорбензол, и температуру реакции предпочтительно поддерживают в интервале от 110oC до 145oC. Бромирующие агенты, которые могут быть использованы в этой реакции, включают бром, бромноватую кислоту, водный раствор бромноватой кислоты и трибромид фосфора.
Хотя первая и вторая стадия реакционной схемы 3 могут быть проведены с выделением N-(2-гидроксиэтил)-α-метилбензиламина, полученного в качестве промежуточного соединения после завершения первой стадии реакции, предпочтительно осуществлять первую и вторую стадии реакции без выделения промежуточного продукта. Таким образом, бромирующий агент добавляют в сосуд, который содержит продукты первой стадии реакции.
Затем N-(2-бромэтил)-α-метилбензиламин, полученный на второй стадии реакции, циклизуют путем взаимодействия с кислотой Льюиса для получения целевого 1-метил-1,2,3,4-тетрагидроизохинолина формулы (III). Реакционные растворители, которые могут быть использованы в этой реакции, включают декалин, 1,2-дихлорэтан и 1,2-дихлорбензол, и кислоты Льюиса для этой реакции циклизации включают хлорид алюминия (III), хлорид цинка и хлорид железа.
Поскольку 1-метил-1,2,3,4-тетрагидроизохинолин может быть экономично получен согласно вышеописанному способу, в соответствии с настоящим изобретением при использовании этого соединения в качестве реагента может быть также экономично получен целевой 5,6-диметил-2-(4-фторфениламино)-4-(1-метил- 1,2,3,4-тетрагидроизохинолин-2-ил)пиримидин формулы (I).
Для того, чтобы использовать соединение формулы (III) в виде (R)-(+)- или (S)-(-)-изомера в качестве исходного продукта для получения соединения формулы (I) по настоящему изобретению, каждая изомерная форма соединения формулы (III) может быть эффективно получена при использовании соответствующего (R)-(+)- или (S)-(-)-метилбензиламина в качестве исходного продукта, используемого по способу, представленному на реакционной схеме 3.
Настоящее изобретение будет подробно пояснено в следующих примерах. Следует, однако, учесть, что настоящее изобретение никоим образом не ограничивается этими примерами.
Препаративный пример: 4-фторфенилгуанидинкарбонат
882 г (747 мл) 32% cоляной кислоты добавляют к 1000 г (8,9 моль)
4-фторанилина, смесь нагревают до 87oC и в течение 2 часов добавляют к ней по каплям 780 мл (9,9 моль) 50% раствора цианамида. Реакционную смесь доводят до pH 2,4 добавлением в нее 120 мл
32% соляной кислоты, перемешивают в течение 3 часов и охлаждают до 60oC. К реакционному раствору в течение 30 минут добавляют по каплям раствор Na2CO3 (Na2
CO3/вода 578 г/1640 мл). Реакционную смесь перемешивают в течение 40 минут и затем охлаждают до 15oC. Полученный серый твердый продукт фильтруют, промывают сначала 600 мл воды и
затем 2000 мл этилацетата и, наконец, сушат, получая 1395 г указанного в заголовке соединения, имеющего светло-серый цвет.
Выход: 81,4%
Т.пл.: 175oC
ЯМР
(ДМСО-d6, м.д.): 5,50-6,88 (уш.с, 5H), 6,87 (м, 2H), 7,17 (м, 2H)
Пример 1: 4-Гидрокси-2-(4-фторфениламин)-5,6-диметилпиримидин
54,5 г (253,2 ммоль)
4-Фторфенилгуанидинкарбоната, полученного в Препаративном примере выше, суспендируют в 50 мл N,N-диметилформамида и 37,8 г (262,2 ммоль) этил-2-метил-ацетоацетата, и полученную суспензию кипятят с
обратным холодильником при 140oC в течение 3 часов. Реакционный раствор вновь разбавляют 100 мл N,N-диметилформамида и охлаждают до 80oC. Добавляют к нему 160 мл изопропилового
спирта и полученную смесь перемешивают в течение 30 минут. Образовавшийся твердый продукт отфильтровывают, промывают 150 мл ацетона и в конце сушат, получая 41 г названного в заголовке соединения.
Выход: 61,4%
Т.пл.: 256oC
ЯМР (ДМСО-d6, м.д.): 1,83 (с, 3H), 2,19 (с, 3H), 7,18 (т, 2H), 7,68 (м, 2H), 9,36 (уш.с, 1H), 10,63 (уш.с, 1H).
Пример 2: 4-Хлор-2-(4-фторфениламино)-5,6-диметилпиримидин
40,5 г (174,1 ммоль) 2-(4-Фторфениламино)-4-гидрокси-5,6- диметилпиримидина, полученного в примере 1, суспендируют в 80 мл
N,N-диметилформамида и полученную суспензию нагревают до 80oC. В течение одного часа добавляют 31,9 г (19,4 мл, 210,1 ммоль) оксихлорида фосфора при постоянной температуре 85oC.
Реакционный раствор перемешивают в течение 30 минут и затем при перемешивании к нему добавляют 400 г воды со льдом. Смесь доводят до pH 11 добавлением гидроксида натрия и затем отфильтровывают
полученный твердый продукт. Выделенный твердый продукт промывают 150 мл 50% водного раствора метанола и затем сушат, получая 42,3 г названного в заголовке соединения.
Выход: 96,7%
Т.пл.: 114oC
ЯМР (CDCl3, м.д.): 2,21 (с, 3H), 2,41 (с, 3H), 7,01 (т, 2H), 7,18 (уш.с, 1H), 7,56 (т, 2H).
Пример 3: 4-Хлор-2-(4-фторфениламино)-5,
6-диметилпиримидин
1390 г (7,6 моль) 4-Фторфенилгуанидин карбоната, полученного в Препаративном примере выше, суспендируют в 1300 мл N,N-диметилформамида и 1206 г (8,4 моль)
этил-2-метилацето-ацетата. Полученную суспензию нагревают при кипячении с обратным холодильником в течение одного часа, перегоняют под нормальным давлением до 1100 мл и затем отгоняют до тех пор, пока
температура реакционного раствора не достигнет 160oC. К остатку добавляют 1600 мл N, N-диметилформамида и затем охлаждают до 80oC. К смеси за один час добавляют при постоянной
температуре 80-85oC 1388 г (840 мл, 9,1 моль) оксихлорида фосфора. Реакционный раствор перемешивают в течение 30 минут и затем разбавляют 2000 мл N,N-диметилформамида. К разбавленному
раствору в течение 40 минут добавляют при перемешивании 7000 мл воды. Реакционный раствор перемешивают в течение 4 часов, полученный продукт отфильтровывают, промывают 1500 мл 50% водного раствора
метанола и затем сушат. Полученный таким образом высушенный желтовато-коричневый порошок растворяют в 4000 мл метанола при кипячении с обратным холодильником и затем охлаждают до 10oC.
Полученный твердый продукт отфильтровывают и сушат, получая 1186 г названного в заголовке соединения.
Выход: 62,4%
Т.пл.: 114oC
ЯМР (CDCl3,
м.д.): 2,21 (с, 3H), 2,41 (с, 3H), 7,01 (т, 2H), 7,18 (уш. с, 1H), 7,56 (т, 2H).
Пример 4: 4-Бром-2-(4-фторфениламино)-5,6-диметилпиримидин
5 г (21,44 ммоль)
2-(4-Фторфениламино)-4-гидрокси-5,6-диметилпиримидина, полученного в примере 1, суспендируют в 40 мл N,N-диметилформамида и полученную суспензию нагревают до 65oC. К ней добавляют по каплям
за 20 минут 8,1 г (30 ммоль) трибромида фосфора и полученную смесь оставляют для протекания реакции на 30 минут при 75oC. Реакционный раствор охлаждают до комнатной температуры, выливают на
500 г воды со льдом, доводят до pH 11 раствором гидроксида натрия, перемешивают в течение 30 минут и затем вновь доводят pH до 5,5 разбавленной соляной кислотой. Полученный желтый твердый продукт
промывают 100 мл воды и сушат, получая 4,1 г указанного в заголовке соединения.
Выход: 64,58%
Т.пл.: 123oC
ЯМР (CDCl3, м. д.): 2,21 (с, 3H), 2,
42 (с, 3H), 6,98 (т, 2H), 7,24 (с, 1H), 7,54 (кв, 2H).
Пример 5: 1-Метил-1,2,3,4-тетpaгидpoизoxинoлин
(1) Получение N-(2-гидроксиэтил)-α-метилбензиламина:
103,
08 г (0,86 моль) α-Метилбензиламина растворяют в 110 мл дихлорметана и добавляют 127,56 г (1,02 моль) 2-бромэтанола. Смесь перемешивают в течение 50 часов при 52oC до полного
завершения реакции. Реакционный раствор концентрируют под пониженным давлением и остаток подвергают фракционной перегонке, получая 109 г указанного в заголовке соединения, имеющего бледно-желтый
цвет.
Выход: 76,7%
Т.кип.: 60oC/0,5 мм рт.ст.
ЯМР (CDCl3, м. д.): 1,38 (д, 3H), 2,40 (уш. с, 1H), 2,61 (м, 2H), 3,58 (м, 2H), 3,78 (кв, 1H), 7,18-7,38 (м, 5H).
(2) Получение гидробромида N-(2-бромэтил)-α-метилбензиламина:
100 г (605,32 ммоль) N-(2-Гидроксиэтил)-α-метилбензиламина, полученного в
примере 5 (1) выше, суспендируют в 515 мл 48% водного раствора бромоводородной кислоты и ведут реакцию в полученной суспензии при 126oC в течение 30 минут при кипячении с обратным
холодильником. Затем реакционный раствор перегоняют в течение 2 часов при нормальном давлении при постоянной температуре и удаляют 465 мл водного раствора бромоводородной кислоты и воды побочных
продуктов реакции. Остаток растворяют в 550 мл ацетона, и добавляют к нему 500 мл этилацетата и 670 мл эфира. Реакционный раствор перемешивают в течение 30 минут, охлаждают до 0oC и затем
дают ему постоять в течение 3 часов. Полученный твердый продукт отфильтровывают, промывают 400 мл этилацетата и затем сушат, получая 97 г первой фракции указанного в заголовке соединения. Затем
фильтрат концентрируют. Остаток растворяют в 450 мл ацетона, разбавляют 680 мл эфира и затем дают ему постоять при 0oC в течение 12 часов. Полученный твердый продукт отфильтровывают,
собирают и промывают 450 мл этилацетата, получая 32,5 г второй фракции указанного в заголовке соединения.
Выход: 69,23%
Т.пл.: 186-187oC
ЯМР (CDCl3, м.д.): 1,94 (д, 3H), 3,21 (м, 2H), 3,82 (м, 2H), 4,42 (кв, 1H), 7,40-7,72 (м, 5H), 9,51 (уш.с, 1H), 9,91 (уш.с, 1H).
(3) Получение 1-метил-1,2,3,4-тетрагидроизохинолина:
50,0 г (161,8 ммоль) Гидробромида N-(2-бромэтил)-α-метилбензиламина, полученного в примере 5 (2) выше, суспендируют в 450 мл декалина и затем нагревают до 140oC. К суспензии за
40 минут добавляют 64,70 г (485,4 ммоль) безводного хлорида алюминия (AlCl3). Реакционный раствор дополнительно перемешивают в течение 30 минут при постоянной температуре и затем охлаждают
до комнатной температуры. Удаляют супернатант и нижний слой добавляют к 800 г воды со льдом при перемешивании. Добавляют туда 150 мл концентрированной соляной кислоты и смесь перемешивают в течение 10
минут. Этот раствор промывают трижды, каждый раз 1000 мл этилацетата, полученный водный слой отделяют, доводят до pH 12 гидроксидом натрия и затем трижды экстрагируют, каждый раз 2100 мл этилацетата.
Экстракты объединяют, промывают 420 мл насыщенного солевого раствора, обезвоживают безводным сульфатом магния и затем выпаривают при пониженном давлении, чтобы удалить этилацетат. Остаток перегоняют,
получая 18,1 г указанного в заголовке соединения.
Выход: 75,99%
Т.кип.: 79-80o/0,5 мм рт.ст.
ЯМР (CDCl3, м. д. ): 1,59 (д, 3H), 2,14 (с, 1H), 2,76-3,02 (м, 2H), 3,10-3,22 (м, 1H), 3,34-3,45 (м, 1H), 4,22 (кв, 1H), 7,18-7,31 (м, 4H).
Пример 6: 1-Метил-1,2,3,4-тетрагидроизохинолин
(1) Получение гидробромида
N-(2-бромэтил)-α-метилбензиламина:
76,61 г (630 ммоль) α-Метилбензиламина растворяют в 77 мл дихлорметана и добавляют туда 94,8 г (760 ммоль) 2-бромэтанола. Смесь перемешивают
при 51oC в течение 50 часов для полного завершения реакции. Реакционный раствор концентрируют при пониженном давлении, добавляют к нему 286,4 мл (2500 ммоль) 48% водного раствора
бромоводородной кислоты и оставляют реагировать при 126oC в течение 30 минут при кипячении с обратным холодильником. Затем реакционный раствор перегоняют в течение 2 часов при нормальном
давлении при постоянной температуре и удаляют 250 мл водной бромоводородной кислоты и воды, побочного продукта реакции. Остаток растворяют в 350 мл изопропилового спирта при кипячении с обратным
холодильником в течение 30 минут, и этот раствор охлаждают до 10oC и затем дают ему постоять в течение 3 часов. Образовавшийся твердый продукт отфильтровывают, промывают 50 мл этилацетата и
затем сушат, получая 128,9 г названного в заголовке соединения.
Выход: 66,2%
Т.пл.: 186-187oC
ЯМР (CDCl3, м.д.): 1,94 (д, 3H), 3,21 (м, 2H), 3,
82 (м, 2H), 4,42 (кв, 1H), 7,40-7,72 (м, 5H), 9,51 (уш.c, 1H), 9,91 (уш.с, 1H).
(2) Получение 1-метил-1,2,3,4-тетрагидроизохинолина:
10,0 г (30,1 ммоль) Гидробромида
N-(2-бромэтил)-α-метилбензиламина, полученного в примере 6 (1) выше, суспендируют в 60 мл 1,2-дихлорбензола и затем нагревают до 145oC. Добавляют в течение 40 минут 13,47 г (96,54
ммоль) безводного хлорида алюминия. Реакционный раствор перемешивают еще 30 минут при постоянной температуре, охлаждают до комнатной температуры и при перемешивании выливают на 250 г воды со льдом.
Добавляют 30 мл концентрированной соляной кислоты и смесь перемешивают в течение 10 минут Этот раствор промывают трижды, каждый раз 130 мл дихлорметана, полученный водный слой отделяют, доводят до pH
12 гидроксидом натрия и затем экстрагирую трижды, каждый раз 250 мл этилацетата.
Экстракты объединяют, промывают 40 мл насыщенного солевого раствора, обезвоживают безводным сульфатом магния и затем
выпаривают при пониженном давлении, чтобы удалить этилацетат. Остаток перегоняют, получая 2,90 г указанного в заголовке соединения
Выход: 65,39%
Т.кип.: 79-80oC/0,5 мм
рт.ст.
ЯМР (CDCl3, м. д. ): 1,59 (д, 3H), 2,14 (с, 1H), 2,76-3,02 (м, 2H), 3,10-3,22 (м, 1H), 3,34-3,45 (м, 1H), 4,22 (кв, 1H), 7,18- 7,31 (м, 4H).
Пример 7:
1-Метил-1,2,3,4-тетрагидроизохинолин
200 г (647,17 ммоль) Гидробромида N-(2-бромэтил)-α-метилбензиламина, полученного в примере 5 (2) или в примере 6 (1) выше, суспендируют в 700 мл
декалина и затем нагревают до 150oC. К суспензии в течение 40 минут добавляют 261,5 г (1961 ммоль) безводного хлорида алюминия. Реакционный раствор перемешивают еще 30 минут при постоянной
температуре и затем охлаждают до комнатной температуры. Удаляют супернатант и нижний слой при перемешивании выливают на 3500 г воды со льдом. Добавляют 210 мл концентрированной соляной кислоты и смесь
перемешивают в течение 10 минут. Этот раствор промывают трижды, каждый раз 2500 мл этилацетата, затем водный слой отделяют, доводят до pH 12 гидроксидом натрия и затем экстрагируют трижды, каждый раз
3000 мл этилацетата. Экстракты объединяют, промывают 550 мл насыщенного солевого раствора, обезвоживают безводным сульфатом магния и затем выпаривают при пониженном давлении, чтобы удалить этилацетат.
Остаток перегоняют, получая 78,9 г названного в заголовке соединения.
Выход: 82,8%
Т.кип.: 79-80oC/0,5 мм рт.ст.
ЯМР (CDCl3, м. д. ): 1, 59 (д, 3H), 2,14 (с, 1H), 2,76-3,02 (м, 2H), 3,10-3,22 (м, 1H), 3,34-3,45 (м, 1H), 4,22 (кв, 1H), 7,18-7,31 (м, 4H).
Пример 8: (R)-(+)-1-Метил-1,2,3,4-тетрагидроизохинолин
(1)
Получение (R)-(+)-N-(2-гидроксиэтил)-α-метилбензиламина:
51,45 г (0,43 ммоль) (R)-(+)-α-Метилбензиламина растворяют в 52 мл дихлорметана и добавляют туда 63,78 г (0,51 ммоль)
2-бромэтанола. Эту смесь перемешивают при 51oC в течение 50 часов для полного завершения реакции. Реакционный раствор концентрируют при пониженном давлении и остаток подвергают фракционной
перегонке, получая 54 г указанного в заголовке соединения, имеющего бледно-желтый цвет.
Выход: 76%
Т.пл.: 60oC/0,5 мм рт.ст.
[α]: +55° (с=1, в CHCl3)
ЯМР (CDCl3, м.д.): 1,38 (д, 3H),
2,40 (уш.с, 1H), 2,61 (м, 2H), 3,58 (м, 2H), 3,78 (кв, 1H), 7,18-7,38 (м, 5H).
(2) Получение гидробромида (R)-(+)-N-(2-бромэтил)-α-метилбензиламина:
11,0 г (66,58
ммоль) (R)-(+)-N-(2-Гидроксиэтил)-α-метил-бензиламина, полученного в примере 8 (1) выше, суспендируют в 52 мл 48% водного раствора бромоводородной кислоты и в полученной суспензии проводят
реакцию при 126oC в течение 30 минут при кипячении с обратным холодильником. Реакционный раствор перегоняют в течение 2 часов при нормальном давлении и постоянной температуре и удаляют 47
мл водной бромоводородной кислоты и воды, побочного продукта реакции. Остаток растворяют в 55 мл ацетона и добавляют туда 50 мл этилацетата и 70 мл эфира. Реакционный раствор перемешивают в течение 30
минут, охлаждают до 0oC и затем дают ему постоять в течение 3 часов. Образующийся твердый продукт отфильтровывают, промывают 30 мл этилацетата и затем сушат, получая 10 г первой фракции
названного в заголовке соединения. Фильтрат затем концентрируют. Остаток растворяют в 60 мл этанола и полученную смесь концентрируют при пониженном давлении. Остаток растворяют в 50 мл ацетона,
разбавляют 70 мл эфира и затем дают постоять при 0oC в течение 12 часов. Полученный твердый продукт отфильтровывают, собирают и промывают 30 мл этилацетата, получая вторую фракцию
указанного в заголовке соединения.
Выход: 64%
Т.пл.: 186-187oC
[α]
ЯМР (CDCl3, м.д.): 1,94 (д, 3H), 3,21 (м, 2H), 3,82 (м, 2H), 4,42 (кв, 1H), 7,40-7,72 (м, 5H), 9,51
(уш.с, 1H), 9,91 (уш.с, 1H).
(3) Получение (R)-(+)-1-метил-1,2,3,4-тетрагидроизохинолина:
5,0 г (16,18 ммоль) Гидробромида (R)-(+)-N-(2-бромэтил)-α-метилбензиламина,
полученного в (2) выше, суспендируют в 50 мл декалина и полученную суспензию нагревают до 140oC. Добавляют к ней за 40 минут 6,470 г (48,54 ммоль) безводного хлорида алюминия (AlCl3). Реакционный раствор перемешивают еще 30 минут при постоянной температуре и охлаждают до комнатной температуры. Супернатант удаляют и нижний слой при перемешивании добавляют к 70 г воды со
льдом. Добавляют туда 20 мл концентрированной соляной кислоты и смесь перемешивают в течение 10 минут. Этот раствор промывают трижды, каждый раз 100 мл этилацетата, полученный водный слой отделяют,
доводят до pH 12 гидроксидом натрия и затем экстрагируют трижды, каждый раз 250 мл этилацетата. Экстракты объединяют, промывают 40 мл насыщенного солевого раствора, обезвоживают безводным сульфатом
магния и затем выпаривают при пониженном давлении, чтобы удалить этилацетат. Остаток перегоняют, получая 1,70 г указанного в заголовке соединения.
Выход: 71,4%
Т.кип.:
79-80oC/0,5 мм рт.ст.
[α]
ЯМР (CDCl3, м. д. ): 1,59 (д, 3H), 2,14 (с, 1H), 2,76-3,02 (м, 2H), 3,10-3,22 (м, 1H), 3,34-3,45 (м, 1H), 4,22 (кв, 1H), 7,18-7,31 (м, 4H).
Пример 9:
(R)-(+)-1-Метил-1,2,3,4-тетpaгидpoизoxинoлин
(1) Получение гидробромида (R)-(+)-N-(2-бромэтил)-α-метилбензиламина:
76,61 г (630 ммоль) (R)-(+)-α-Метилбензиламина
растворяют в 77 мл дихлорметана и добавляют к нему 94,8 г (760 ммоль) 2-бромэтанола. Эту смесь перемешивают при 51oC в течение 50 часов для полного завершения реакции. Этот реакционный
раствор концентрируют под пониженным давлением и добавляют к нему 286,4 г (2500 ммоль) 48% водного раствора бромоводородной кислоты и затем проводят реакцию при 126oC в течение 30 минут при
кипячении с обратным холодильником. Реакционный раствор затем перегоняют в течение 2 часов при нормальном давлении при постоянной температуре и удаляют 250 мл водной бромоводородной кислоты и воды,
побочного продукта реакции. Остаток растворяют в 350 мл изопропилового спирта при кипячении с обратным холодильником в течение 30 минут, этот раствор охлаждают до 10oC и затем дают ему
постоять в течение 3 часов. Полученный твердый продукт отфильтровывают, промывают 50 мл этилацетата и затем сушат, получая 127,5 г указанного в заголовке соединения.
Выход: 65,5%
Т.пл.: 186-187oC
[α]
ЯМР (CDCl3, м.д.): 1,94 (д, 3H), 3,21 (м, 2H), 3,82 (м, 2H), 4,42 (кв, 1H), 7,40-7,72 (м, 5H), 9,51 (уш.с, 1H), 9,91 (уш.с, 1H).
(2) Получение
(R)-(+)-1-метил-1,2,3,4-тетрагидроизохинолина:
10,0 г (30,1 ммоль) Гидробромида (R)-(+)-N-(2-бромэтил)-α-метилбензиламина, полученного в Примере 9 (1) выше, суспендируют в 60 мл 1,
2-дихлорбензола и затем нагревают до 145oC. К суспензии за 40 минут добавляют 13,47 г (96,54 ммоль) безводного хлорида алюминия (AlCl3). Реакционный раствор перемешивают еще 30
минут при той же температуре, охлаждают до комнатной температуры и выливают при перемешивании на 250 г воды со льдом. Добавляют туда 30 мл концентрированной соляной кислоты и смесь перемешивают в
течение 10 минут. Этот раствор промывают трижды, каждый раз 130 мл дихлорметана, полученный водный слой отделяют, доводят до pH 12 гидроксидом натрия и затем экстрагируют трижды, каждый раз 250 мл
этилацетата. Экстракты объединяют, промывают 40 мл насыщенного солевого раствора, обезвоживают безводным сульфатом магния и затем выпаривают при пониженном давлении, чтобы удалить этилацетат. Остаток
перегоняют, получая 3,06 г названного в заголовке соединения.
Выход: 69%
Т.кип.: 79-80o/0,5 мм рт.ст.
[α]
ЯМР (CDCl3, м. д. ): 1,59 (д, 3H), 2,14 (с, 1H), 2,
76-3,02 (м, 2H), 3,10-3,22 (м, 1H), 3,34-3,45 (м, 1H), 4,22 (кв, 1H), 7,18- 7,31 (м, 4H).
Пример 10: (R)-(+)-1-метил-1,2,3,4-тетрагидроизохинолин
73,45 г (240 моль)
Гидробромида (R)-(+)-N-(2-бромэтил)-α-метилбензиламина, полученного в примере 9 (1) выше, суспендируют в 260 мл декалина и полученную суспензию нагревают до 150oC. К суспензии за 40
минут добавляют 95,10 г (710 ммоль) безводного хлорида алюминия. Реакционный раствор перемешивают еще 30 минут при той же температуре и затем охлаждают до комнатной температуры. Удаляют супернатант и
нижний слой выливают при перемешивании на 1600 г воды со льдом. Добавляют туда 70 мл концентрированной соляной кислоты и полученную смесь перемешивают в течение 10 минут. Этот раствор промывают трижды,
каждый раз 700 мл этилацетата, полученный водный слой отделяют, доводят до pH 12 гидроксидом натрия и экстрагируют трижды, каждый раз 900 мл этилацетата. Экстракты объединяют, промывают 200 мл
насыщенного солевого раствора, обезвоживают безводным сульфатом магния и выпаривают при пониженном давлении, чтобы удалить этилацетат. Остаток перегоняют, получая 28,2 г указанного в заголовке
соединения.
Выход: 79,7%
Т.кип.: 79-80oC/0,5 мм рт.ст.
[α]
ЯМР (CDCl3, м. д. ): 1,59 (д, 3H), 2,14 (с, 1H), 2,76-3,02 (м, 2H), 3,10-3,22 (м, 1H), 3,34-3,45 (м, 1H),
4,22 (кв, 1H), 7,18- 7,31 (м, 4H).
Пример 11: (S)-(-)-1-метил-1,2,3,4-тетрагидроизохинолин
(1) Получение (S)-(-)-N-(2-гидроксиэтил)-α-метилбензиламина:
108,23
г (0,903 ммоль) (S)-(-)-α-Метилбензиламина растворяют в 140 мл дихлорметана и добавляют туда 144,0 г (1,071 ммоль) 2-бромэтанола. Эту смесь перемешивают при 51oC в течение 52 часов
для полного завершения реакции. Реакционный раствор концентрируют при пониженном давлении и остаток подвергают фракционной перегонке, получая 117,4 г указанного в заголовке соединения, имеющего
бледно-желтый цвет.
Выход: 78,7%
Т.пл.: 60oC/0,5 мм рт.ст.
[α]
ЯМР (CDCl3, м.д.): 1,38 (д, 3H), 2,40 (уш.с, 1H), 2,61 (м, 2H), 3,58 (м, 2H), 3,78 (кв, 1H), 7,18-7,38 (м,
5H).
(2) Получение гидробромида (S)-(-)-N-(2-бромэтил)-α-метилбензиламина:
22,1 г (133,16 ммоль) (S)-(-)-N- (2-Гидроксиэтил)-α-метилбензиламина, полученного в
примере 11 (1) выше, суспендируют в 105 мл 48% водного раствора бромоводородной кислоты и в полученной суспензии проводят реакцию при 126oC в течение 30 минут при кипячении с обратным
холодильником. Реакционный раствор перегоняют в течение 2 часов при нормальном давлении при постоянной температуре и удаляют 95 мл водной бромоводородной кислоты и воды, побочного, продукта реакции.
Остаток растворяют в 112 мл ацетона и добавляют туда 100 мл этилацетата и 150 мл эфира. Реакционный раствор перемешивают в течение 30 минут, охлаждают до 0oC и затем дают ему постоять в
течение 3 часов. Образующийся твердый продукт отфильтровывают, промывают 70 мл этилацетата и затем сушат, получая 20 г первой фракции указанного в заголовке соединения. Фильтрат затем концентрируют.
Остаток растворяют в 130 мл этанола и полученную смесь концентрируют при пониженном давлении. Остаток растворяют в 104 мл ацетона, разбавляют 143 мл эфира и затем дают постоять при 0oC в
течение 12 часов. Полученный твердый продукт отфильтровывают, собирают и промывают 75 мл этилацетат, получая 6,7 г второй фракции указанного в заголовке соединения.
Выход: 64,8%
Т.пл.: 186-187oC
[α]
ЯМР (CDCl3, м.д.): 1,94 (д, 3H), 3,21 (м, 2H), 3,82 (м, 2H), 4,42 (кв, 1H), 7,40-7,72 (м, 5H), 9,51 (уш.с, 1H), 9,91 (уш.с, 1H).
(3) Получение
(S)-(-)-1-метил-1,2,3,4-тетрагидроизохинолина:
5,0 г (16,18 ммоль) Гидробромида (S)-(-)-N-(2-бромэтил)-α-метилбензиламина, полученного в примере (2) выше, суспендируют в 50 мл декалина
и полученную суспензию нагревают до 140oC. Добавляют в течение 40 минут 6,47 г (48,54 ммоль) безводного хлорида алюминия (AlCl3). Реакционный раствор перемешивают еще 30 минут
при постоянной температуре и охлаждают до комнатной температуры. Супернатант удаляют и нижний слой при перемешивании добавляют к 70 г воды со льдом. Добавляют туда 20 мл концентрированной соляной
кислоты и смесь перемешивают в течение 10 минут. Этот раствор промывают трижды, каждый раз 100 мл этилацетата, полученный водный слой отделяют, доводят до pH 12 гидроксидом натрия и затем экстрагируют
трижды, каждый раз 250 мл этилацетата. Экстракты объединяют, промывают 40 мл насыщенного солевого раствора, обезвоживают безводным сульфатом магния и затем выпаривают при пониженном давлении, чтобы
удалить этилацетат. Остаток перегоняют, получая 1,75 г указанного в заголовке соединения.
Выход: 73,5%
Т.кип.: 79-80oC/0,5 мм рт.ст.
[α
]
ЯМР (CDCl3, м. д. ): 1,
59 (д, 3H), 2,14 (с, 1H), 2,76-3,02 (м, 2H), 3,10-3,22 (м, 1H), 3,34-3,45 (м, 1H), 4,22 (кв, 1H), 7,18- 7,31 (м, 4H).
Пример 12: (S)-(-)-1-метил-1,2,3,4-тетрагидроизохинолин
(1) Получение гидробромида (S)-(-)-N-(2-бромэтил)-α-метилбензиламина:
176,20 г (1449 ммоль) (S)-(-)-α-Метилбензиламина растворяют в 185 мл дихлорметана и добавляют к нему 218,04
г (1748 ммоль) 2-бромэтанола. Эту смесь перемешивают при 51oC в течение 50 часов для полного завершения реакции. Этот реакционный раствор концентрируют при пониженном давлении и добавляют к
нему 685 мл (5750 ммоль) 48% водного раствора бромоводородной кислоты и затем проводят реакцию при 126oC в течение 30 минут при кипячении с обратным холодильником. Реакционный раствор затем
перегоняют в течение 2 часов при нормальном давлении при постоянной температуре и удаляют 580 мл водной бромоводородной кислоты и воды, побочного продукта реакции. Остаток растворяют в 760 мл
изопропилового спирта при кипячении с обратным холодильником в течение 30 минут, этот раствор охлаждают до 10oC и затем дают ему постоять в течение 3 часов. Полученный твердый продукт
отфильтровывают, промывают 150 мл этилацетата и затем сушат, получая 306,5 г указанного в заголовке соединения.
Выход: 68,4%
Т.пл.: 185oC
[α]
ЯМР (CDCl3, м.д.): 1,94 (д, 3H),
3,21 (м, 2H), 3,82 (м, 2H), 4,42 (кв, 1H), 7,40-7,72 (м, 5H), 9,51 (уш.с, 1H), 9,91 (уш.с, 1H).
(2) Получение (S)-(-)-1-метил-1,2,3,4-тетрагидроизохинолина:
10,0 г (30,1
ммоль) Гидробромида (S)-(-)-N-(2-бромэтил)-α-метилбензиламина, полученного в примере 12 (1) выше, суспендируют в 60 мл 1,2-дихлорбензола и затем нагревают до 145oC. К суспензии за 40
минут добавляют 13,47 г (96,54 ммоль) безводного хлорида алюминия (AlCl3). Реакционный раствор перемешивают еще 30 минут при постоянной температуре, охлаждают до комнатной температуры и
выливают при перемешивании на 250 г воды со льдом. Добавляют туда 30 мл концентрированной соляной кислоты и смесь перемешивают в течение 10 минут. Этот раствор промывают трижды, каждый раз 130 мл
дихлорметана, полученный водный слой отделяют, доводят до pH 12 гидроксидом натрия и затем экстрагируют трижды, каждый раз 250 мл этилацетата. Экстракты объединяют, промывают 40 мл насыщенного
солевого раствора, обезвоживают безводным сульфатом магния и затем выпаривают при пониженном давлении, чтобы удалить этилацетат. Остаток перегоняют, получая 3,10 г указанного в заголовке
соединения.
Выход: 69,96%
Т.кип.: 79-80oC/0,5 мм рт.ст.
[α]
ЯМР (CDCl3, м. д. ): 1,59 (д, 3H), 2,14 (с, 1H), 2,76-3,02 (м, 2H), 3,10-3,22 (м, 1H), 3,34-3,45 (м, 1H),
4,22 (кв, 1H), 7,18- 7,31 (м, 4H).
Пример 13: (S)-(-)-1-метил-1,2,3,4-тетрагидроизохинолин
73,45 г (240 моль) Гидробромида (S)-(-)-N-(2-бромэтил)-α-метилбензиламина,
полученного в Примере 12 (1) выше, суспендируют в 260 мл декалина и полученную суспензию нагревают до 150oC. К суспензии за 40 минут добавляют 95,10 г (710 ммоль) безводного хлорида
алюминия. Реакционный раствор перемешивают еще 30 минут при постоянной температуре и затем охлаждают до комнатной температуры. Удаляют супернатант и нижний слой выливают при перемешивании на 1600 г
воды со льдом. Добавляют туда 70 мл концентрированной соляной кислоты и полученную смесь перемешивают в течение 10 минут. Этот раствор промывают трижды, каждый раз 700 мл этилацетата, полученный
водный слой отделяют, доводят до pH 12 гидроксидом натрия и экстрагируют трижды, каждый раз 900 мл этилацетата. Экстракты объединяют, промывают 200 мл насыщенного солевого раствора, обезвоживают
безводным сульфатом магния и выпаривают под пониженным давлением, чтобы удалить этилацетат. Остаток перегоняют, получая 27,6 г указанного в заголовке соединения.
Выход: 78,1%
Т.кип.: 79-80oC/0,5 мм рт.ст.
[α]
ЯМР (CDCl3, м. д. ): 1,59 (д, 3H), 2,14 (с, 1H), 2,76-3,02 (м, 2H), 3,10-3,22 (м, 1H), 3,34-3,45 (м, 1H), 4,22 (кв, 1H), 7,18- 7,31 (м, 4H).
Получение 5,6-диметил-2-(4-фторфениламино)-4-(1-метил-1,2,3,4- тетpaгидpoизoxинoлин-2-ил)пиримидина и его гидрохлорида
В примерах с 14 по 20 включительно в качестве реагента
используют 1-метил-1,2,3,4-тетрагидроизохинолин, полученный по способу, описанному в международной публикации WO 94/14795.
Пример 14
2,65 г (27 ммоль) Ацетата калия и 4,0 г
(26,9 ммоль) 1-метил-1,2,3,4-тетрагидроизохинолина добавляют к 85 мл н-гексанола и затем нагревают до 80oC. Туда же добавляют 6,17 г (24,5 ммоль) 4-хлор-2-(4-фторфениламино)-5,
6-диметилпиримидина и затем проводят реакцию при 140oC в течение 28 часов при кипячении с обратным холодильником с получением 5,6-диметил-2- (4-фторфениламино)-4-(1-метил-1,2,3,
4-тетрагидроизохинолин-2-ил)пиримидина.
Реакционный раствор охлаждают до комнатной температуры, разбавляют 20 мл ацетона и затем при перемешивании добавляют по каплям к 120 мл воды. После перемешивания смеси в течение 2 часов полученный твердый продукт отфильтровывают, промывают 30 мл воды, растворяют в 150 мл дихлорметана и затем промывают последовательно 20 мл 4н HCl, 20 мл воды и затем 20 мл 4н раствора гидроксида натрия. Дихлорметановый слой обезвоживают безводным сульфатом магния, концентрируют при пониженном давлении и затем разбавляют 100 мл этанола. К этому реакционному раствору добавляют 30 г концентрированной соляной кислоты и полученную таким образом смесь перемешивают в течение 5 часов. Полученный твердый продукт отфильтровывают, промывают 20 мл этанола и затем сушат, получая 6,1 г очищенного гидрохлорида 5,6-диметил-2-(4-фторфениламино)-4-(1-метил-1,2,3,4-тетрагидроизохинолин-2-ил)пиримидина.
Выход: 62,4%
Т.пл.:
255oC
ЯМР (CDCl3, м. д.): 1,58 (д, 3H), 2,21 (с, 3H), 2,38 (с, 3H), 2,84 (м, 1H), 3,12 (м, 1H), 3,61 (м, 2H), 4,23 (м, 1H), 5,38 (кв, 1H), 7,25 (м, 6H), 7,61 (м, 2H), 10,
33 (с, 1H), 13,43 (уш.с, 1H).
Пример 15
8,12 г (11,2 мл, 80,3 ммоль) Триэтиламина, 30 мл н-бутанола и 6,58 г (44,1 ммоль) 1-метил-1,2,3,4-тетрагидроизохинолина добавляют к 40
мл этиленгликоля. Туда же добавляют 10,1 г (40,1 ммоль) 4-хлор-2-(4-фторфениламино)-5,6-диметилпиримидина и затем проводят реакцию при 130oC в течение 30 часов при кипячении с обратным
холодильником для получения 5,6-диметил-2-(4-фторфениламино)-4-(1-метил-1,2,3,4-тетрагидроизохинолин-2-ил)пиримидина. Этот продукт обрабатывают согласно методике, описанной в Примере 14, получая 14,7
г очищенного гидрохлорида 5,6-диметил-2-(4-фторфениламино)-4-(1-метил-1,2,3,4-тетрагидроизохинолин-2-ил)пиримидина.
Выход: 91%
Т.пл.: 256oC
ЯМР (CDCl3, м. д.): 1,58 (д, 3H), 2,21 (с, 3H), 2,38 (с, 3H), 2,84 (м, 1H), 3,12 (м, 1H), 3,61 (м, 2H), 4,23 (м, 1H), 5,38 (кв, 1H), 7,25 (м, 6H), 7,61 (м, 2H), 10,33 (с, 1H), 13,43 (уш.с, 1H).
Пример 16
45 мл Триэтиламина, 50 мл н-бутанола и 32 г (217 ммоль) 1-метил-1,2,3,4-тетрагидроизохинолина добавляют к 150 мл этиленгликоля. Туда же добавляют 51,3 г (203,8 ммоль)
4-хлор-2- (4-фторфениламино)-5,6-диметилпиримидина и затем проводят реакцию при 135oC в течение 28 часов при кипячении с обратным холодильником с получением 5,
6-диметил-2-(4-фторфениламино)-4- (1-метил-1,2,3,4-тетрагидроизохинолин-2-ил)пиримидина. Этот продукт обрабатывают согласно методике, описанной в примере 14, получая 66 г очищенного гидрохлорида 5,
6-диметил-2-(4-фторфениламино)-4-(1-метил-1,2,3,4-тетрагидроизохинолин-2-ил)пиримидина.
Выход: 81,1%
Т.пл.: 256oC
ЯМР (CDCl3, м. д.): 1,58 (д,
3H), 2,21 (с, 3H), 2,38 (с, 3H), 2,84 (м, 1H), 3,12 (м, 1H), 3,61 (м, 2H), 4,23 (м, 1H), 5,38 (кв, 1H), 7,25 (м, 6H), 7,61 (м, 2H), 10,33 (с, 1H), 13,43 (уш.с, 1H).
Пример 17
75 мл триэтиламина и 65 г (442 ммоль) 1-метил-1,2,3,4- тетрагидроизохинолина добавляют к 100 мл 1,2-пропиленгликоля. Туда же добавляют 100,9 г (0,40 моль) 4-хлор-2-(4-фторфениламино)-5,
6-диметилпиримидина и затем проводят реакцию при 120oC в течение 64 часов при кипячении с обратным холодильником с получением 5,6-диметил-2-(4-фторфениламино)-4-(1-метил-1,2,3,
4-тетрагидроизохинолин-2-ил)пиримидина. Этот продукт обрабатывают согласно методике, описанной в примере 14, получая 91 г очищенного гидрохлорида 5,6-диметил-2-(4-фторфениламино)-4-(1-метил-1,2,3,
4-тетрагидроизохинолин-2-ил)пиримидина.
Выход: 57,1%
Т.пл.: 258oC
ЯМР (CDCl3, м. д.): 1,58 (д, 3H), 2,21 (с, 3H), 2,38 (с, 3H), 2,84 (м, 1H), 3,
12 (м, 1H), 3,61 (м, 2H), 4,23 (м, 1H), 5,38 (кв, 1H), 7,25 (м, 6H), 7,61 (м, 2H), 10,33 (с, 1H), 13,43 (уш.с, 1H).
Пример 18
720 мл триэтиламина и 695 г (4,72 моль) 1-метил-1,
2,3,4-тетрагидроизохинолина добавляют к 2100 мл 1,2-пропиленгликоля. Туда же добавляют 1179 г (4,68 моль) 4-хлор-2-(4-фторфениламино)-5,6-диметилпиримидина и в полученной таким образом смеси проводят
реакцию при 130oC в течение 58 часов с получением 5,6-диметил-2-(4-фторфениламино)-4-(1-метил-1,2,3,4-тетрагидроизохинолин-2-ил)пиримидина. Этот продукт обрабатывают согласно методике,
описанной в примере 14, получая 1250 г очищенного гидрохлорида 5,6-диметил-2-(4-фторфениламино)-4-(1-метил-1,2,3,4-тетрагидроизохинолин-2-ил)пиримидина.
Выход: 66,9%
Т.пл.:
258oC
ЯМР (CDCl3, м. д.): 1,58 (д, 3H), 2,21 (с, 3H), 2,38 (с, 3H), 2,84 (м, 1H), 3,12 (м, 1H), 3,61 (м, 2H), 4,23 (м, 1H), 5,38 (кв, 1H), 7,25 (м, 6H), 7,61 (м, 2H), 10,
33 (с, 1H), 13,43 (уш.с, 1H).
Пример 19
110 мл н-бутанола, 240 мл триэтиламина и 236 г (1,60 моль) 1-метил-1,2,3,4-тетрагидроизохинолина добавляют к 600 мл этиленгликоля.
Туда же добавляют 400 г (1,59 моль) 4-хлор-2-(4-фторфениламино)-5,6-диметилпиримидина и затем проводят реакцию при 140oC в течение 48 часов с получением 5,
6-диметил-2-(4-фторфениламино)-4-(1-метил-1,2,3,4-тетрагидроизохинолин-2-ил)пиримидина. Этот продукт обрабатывают согласно методике, описанной в примере 14, получая 485 г очищенного гидрохлорида 5,
6-диметил-2-(4-фторфениламино)-4-(1-метил-1,2,3,4-тетрагидроизохинолин-2-ил)пиримидина.
Выход: 76,5%
Т.пл.: 257oC
ЯМР (CDCl3, м. д.): 1,58 (д,
3H), 2,21 (с, 3H), 2,38 (с, 3H), 2,84 (м, 1H), 3,12 (м, 1H), 3,61 (м, 2H), 4,23 (м, 1H), 5,38 (кв, 1H), 7,25 (м, 6H), 7,61 (м, 2H), 10,33 (с, 1H), 13,43 (уш.с, 1H).
Пример 20
240 мл Триэтиламина и 9,7 г (65,8 ммоль) 1-метил-1,2,3,4-тетрагидроизохинолина добавляют к 25 мл 1,2-пропиленгликоля. Затем туда же добавляют 15 г (51 ммоль) 4-бром-2-(4-фторфениламино)-5,
6-диметилпиримидина и в полученной таким образом смеси ведут реакцию при 110oC в течение 28 часов. Полученный продукт обрабатывают согласно методике, описанной в Примере 14, получая 15,86 г
очищенного гидрохлорида 5,6-диметил-2-(4-фторфениламино)-4-(1-метил-1,2,3,4-тетрагидроизохинолин-2-ил)пиримидина.
Выход: 78%
Т.пл.: 257oC
ЯМР (CDCl3, м. д.): 1,58 (д, 3H), 2,21 (с, 3H), 2,38 (с, 3H), 2,84 (м, 1H), 3,12 (м, 1H), 3,61 (м, 2H), 4,23 (м, 1H), 5,38 (кв, 1H), 7,25 (м, 6H), 7,61 (м, 2H), 10,33 (с, 1H), 13,43 (уш.с, 1H).
Пример 21
8,12 г (11,2 мл, 80,3 ммоль) Триэтиламина, 30 мл н-бутанола и 6,58 г (44,1 ммоль) 1-метил-1,2,3,4-тетрагидроизохинолина, полученного в примере 5, добавляют к 40 мл
этиленгликоля. Туда же добавляют 10,1 г (40,1 ммоль) 4-хлор-2-(4-фторфениламино)-5,6-диметилпиримидина и ведут реакцию при 130oC в течение 30 часов при кипячении с обратным холодильником,
получая 5,6-диметил-2-(4-фторфениламино)-4-(1-метил-1,2,3,4-тетрагидроизохинолин-2-ил)пиримидин.
Реакционный раствор охлаждают до комнатной температуры, разбавляют 30 мл ацетона и затем при перемешивании добавляют по каплям 200 мл воды. После перемешивания в течение 2 часов образовавшийся твердый продукт отфильтровывают, промывают 60 мл воды, растворяют в 250 мл дихлорметана и промывают последовательно сначала 35 мл 4н HCl, 35 мл воды, и затем 40 мл 4н раствора гидроксида натрия. Дихлорметановый слой дегидратируют безводным сульфатом магния, концентрируют при пониженном давлении и затем разбавляют 200 мл этанола. К этому реакционному раствору добавляют 45 г концентрированной соляной кислоты и смесь перемешивают в течение 5 часов. Полученный твердый продукт отфильтровывают, промывают 30 мл этанола и затем сушат, получая 9,82 г очищенного гидрохлорида 5,6-диметил-2-(4-фторфениламино)-4-(1-метил-1, 2, 3, 4-тетрагидроизохинолин-2-ил)пиримидина.
Выход: 66,53%
Т.пл.: 255oC
ЯМР (CDCl3, м. д.): 1,58 (д, 3H), 2,21 (с, 3H), 2,38 (с, 3H), 2,84 (м, 1H), 3,12 (м, 1H), 3,61 (м, 2H), 4,23 (м, 1H), 5,38
(кв, 1H), 7,25 (м, 6H), 7,61 (м, 2H), 10,33 (с, 1H), 13,43 (уш.с, 1H).
Пример 22
75 мл триэтиламина и 65 г (442 ммоль) 1-метил-1,2,3,4-тетрагидроизохинолина, полученного в
примере 7, добавляют к 100 мл 1,2-пропиленгликоля. Туда же добавляют 100,9 г (0,40 моль) 4-хлор-2-(4-фторфениламино)-5,6-диметилпиримидина и ведут реакцию при 120oC в течение 64 часов,
чтобы получить 5,6-диметил-2-(4-фторфениламино)-4-(1-метил-1,2,3,4-тетрагидроизохинолин-2-ил) пиримидин. Этот продукт обрабатывают согласно методике, описанной в примере 21, получая 95,1 г очищенного
гидрохлорида 5,6-диметил-2-(4-фторфениламино)-4-(1-метил-1,2,3,4-тетрагидроизохинолин-2-ил)пиримидина.
Выход: 59,67%
Т.пл.: 258oC
ЯМР (CDCl3,
м. д.): 1,58 (д, 3H), 2,21 (с, 3H), 2,38 (с, 3H), 2,84 (м, 1H), 3,12 (м, 1H), 3,61 (м, 2H), 4,23 (м, 1H), 5,38 (кв, 1H), 7,25 (м, 6H), 7,61 (м, 2H), 10,33 (с, 1H), 13,43 (уш.с, 1H).
Пример 23
14 мл триэтиламина и 9,7 г (65,8 ммоль) 1-метил-1,2,3,4-тетрагидроизохинолина, полученного в примере 7, добавляют к 25 мл 1,2-пропиленгликоля. Туда же добавляют 15 г (51 ммоль)
4-бром-2-(4-фторфениламино)-5,6-диметилпиримидина и ведут реакцию при 120oC в течение 28 часов, чтобы получить 5,6-диметил-2-(4-фторфениламино)-4-(1-метил-1,2,3,
4-тетрагидроизохинолин-2-ил)пиримидин. Этот продукт обрабатывают согласно методике, описанной в примере 21, получая 14,9 г очищенного гидрохлорида 5,6-диметил-2-(4-фторфениламино)-4-(1-метил-1,2,3,
4-тетрагидроизохинолин-2-ил)пиримидина.
Выход: 73,28%
Т.пл.: 257oC
ЯМР (CDCl3, м. д.): 1,58 (д, 3H), 2,21 (с, 3H), 2,38 (с, 3H), 2,84 (м, 1H),
3,12 (м, 1H), 3,61 (м, 2H), 4,23 (м, 1H), 5,38 (кв, 1H), 7,25 (м, 6H), 7,61 (м, 2H), 10,33 (с, 1H), 13,43 (уш.с, 1H).
Пример 24
8,12 г (11,2 мл, 80,3 ммоль) Триэтиламина, 30
мл н-бутанола и 6,58 г (44,1 ммоль) (R)-(+)-1-метил-1,2,3,4-тетрагидроизохинолина, полученного в примере 9, добавляют к 40 мл этиленгликоля. Туда же добавляют 10,1 г (40,1 ммоль)
4-хлор-2-(4-фторфениламино)-5,6-диметилпиримидина и затем проводят реакцию при 130oC в течение 30 часов при кипячении с обратным холодильником для получения 5,
6-диметил-2-(4-фторфениламино)-4-(1-метил-1,2,3,4-тетрагидроизохинолин-2-ил)пиримидина.
Реакционный раствор охлаждают до комнатной температуры, разбавляют 30 мл ацетона и затем при перемешивании добавляют по каплям 200 мл воды. После перемешивания смеси в течение 2 часов полученный твердый продукт отфильтровывают, промывают 60 мл воды, растворяют в 250 мл дихлорметана и затем промывают последовательно 35 мл 4н HCl, 35 мл воды и затем 40 мл 4н раствора гидроксида натрия. Дихлорметановый слой обезвоживают безводным сульфатом магния, концентрируют при пониженном давлении и затем разбавляют 200 мл этанола. К этому реакционному раствору добавляют 45 г концентрированной соляной кислоты и полученную таким образом смесь перемешивают в течение 5 часов. Полученный твердый продукт отфильтровывают, промывают 30 мл этанола и затем сушат, получая 9,21 г очищенного гидрохлорида (R)-(+)-5,6-диметил-2-(4-фторфениламино)-4-(1-метил-1,2,3, 4-тетрагидроизохинолин-2-ил)пиримидина.
Выход: 62,4%
Т.пл.: 255oC
[α]
ЯМР (CDCl3, м. д.): 1,58 (д, 3H), 2,21 (с, 3H), 2,38 (с, 3H), 2,84 (м, 1H), 3,12 (м, 1H), 3,61
(м, 2H), 4,23 (м, 1H), 5,38 (кв, 1H), 7,25 (м, 6H), 7,61 (м, 2H), 10,33 (с, 1H), 13,43 (уш.с, 1H).
Пример 25
23 мл Триэтиламина и 16 г (108,5 ммоль) (R)-(+)-1-метил-1,2,3,
4-тетрагидроизохинолина, полученного в примере 10, добавляют к 75 мл этиленгликоля. Туда же добавляют 25,7 г (101,8 ммоль) 4-хлор-2-(4-фторфениламино)-5,6-диметилпиримидина и в полученной таким
образом смеси проводят реакцию при 135oC в течение 28 часов при кипячении с обратным холодильником с получением (R)-(+)-5,6-диметил-2-(4-фторфениламино)-4-(1-метил-1,2,3,
4-тетрагидроизохинолин-2-ил)пиримидина. Этот продукт обрабатывают согласно методике, описанной в примере 24, получая 33 г очищенного гидрохлорида 5,6-диметил-2-(4-фторфениламино)-4-(1-метил-1, 2, 3,
4-тетрагидроизохинолин-2-ил)пиримидина.
Выход: 81,1%
Т.пл.: 257oC
[α]
ЯМР (CDCl3, м. д.): 1,58 (д, 3H), 2,21 (с, 3H), 2,38 (с, 3H), 2,84 (м, 1H), 3,12 (м, 1H), 3,61
(м, 2H), 4,23 (м, 1H), 5,38 (кв, 1H), 7,25 (м, 6H), 7,61 (м, 2H), 10,33 (с, 1H), 13,43 (уш.с, 1H).
Пример 26
14 мл
Триэтиламина и 9,7 г (65,8 ммоль) (R)-(+)-1-метил-1,2,3,
4-тетрагидроизохинолина, полученного в примере 10, добавляют к 25 мл 1,2-пропиленгликоля. Затем туда же добавляют 15 г (51 ммоль) 4-бром-2-(4-фторфениламино)-5,6-диметилпиримидина и в полученной
таким образом смеси ведут реакцию при 120oC в течение 28 часов. Продукт реакции затем обрабатывают согласно методике, описанной в примере 24, получая 16,2 г очищенного гидрохлорида 5,
6-диметил-2-(4-фторфениламино)-4-(1-метил-1,2,3,4-тетрагидроизохинолин-2-ил)пиримидина.
Выход: 79,97%
Т.пл.: 257oC
[α]
ЯМР (CDCl3, м. д.): 1,58 (д, 3H), 2,21 (с, 3H), 2,38
(с, 3H), 2,84 (м, 1H), 3,12 (м, 1H), 3,61 (м, 2H), 4,23 (м, 1H), 5,38 (кв, 1H), 7,25 (м, 6H), 7,61 (м, 2H), 10,33 (с, 1H), 13,43 (уш.с, 1H).
Пример 27
8,12 г (11,2 мл, 80,3
ммоль) Триэтиламина, 30 мл н-бутанола и 6,58 г (44,1 ммоль) (S)-(-)-1-метил-1,2,3,4-тетрагидроизохинолина, полученного в примере 13, добавляют к 40 мл этиленгликоля. Туда же добавляют 10,1 г (40,1
ммоль) 4-хлор-2-(4-фторфениламино)-5,6-диметилпиримидина и ведут реакцию при 130oC в течение 30 часов при кипячении с обратным холодильником с получением (S)-(-)-5,
6-диметил-2-(4-фторфениламино)-4-(1-этил-1,2,3,4-тетрагидроизохинолин-2-ил)пиримидина.
Реакционный раствор охлаждают до комнатной температуры, разбавляют 30 мл ацетона и затем при перемешивании добавляют по каплям 200 мл воды. После перемешивания в течение 2 часов образовавшийся твердый продукт отфильтровывают, промывают 60 мл воды, растворяют в 250 мл дихлорметана и промывают последовательно 35 мл 4н HCl, 35 мл воды и 40 мл 4н раствора гидроксида натрия. Дихлорметановый слой обезвоживают безводным сульфатом магния, концентрируют под пониженным давлением и затем разбавляют 200 мл этанола. К этому реакционному раствору добавляют 45 г концентрированной соляной кислоты и смесь перемешивают в течение 5 часов. Полученный твердый продукт отфильтровывают, промывают 30 мл этанола и затем сушат, получая 8,95 г очищенного гидрохлорида (S)-(-)-5,6-диметил-2-(4-фторфениламино)-4-(1-метил-1,2,3,4-тетрагидроизохинолин-2-ил)пиримидина.
Выход: 60,6%
Т.пл.: 255oC
[α]
ЯМР (CDCl3, м. д.): 1,58 (д, 3H), 2,21 (с, 3H), 2,38 (с, 3H), 2,84 (м, 1H), 3,12 (м, 1H), 3,61 (м, 2H), 4,23 (м, 1H), 5,38 (кв, 1H), 7,25 (м, 6H), 7,61 (м, 2H), 10,33 (с, 1H), 13,43
(уш.с, 1H).
Пример 28
15 мл Триэтиламина и 9,7 г (65,8 ммоль) (S)-(-)-1-метил-1,2,3,4-тетрагидроизохинолина, полученного в примере 13, добавляют к 25 мл 1,2-пропиленгликоля.
Туда же добавляют 15 г (51 ммоль) 4-бром-2-(4-фторфениламино)-5,6-диметилпиримидина и затем ведут реакцию при 110oC в течение 38 часов. Продукт реакции затем обрабатывают согласно методике,
описанной в примере 27, получая 15,86 г очищенного гидрохлорида 5,6-диметил-2-(4- фторфениламино)-4-(1-метил-1,2,3,4-тетрагидроизохинолин-2- ил)пиримидина.
Выход: 78%
Т.пл.:
257oC
[α]
ЯМР (CDCl3, м. д.): 1,58 (д, 3H), 2,21 (с, 3H), 2,38 (с, 3H), 2,84 (м, 1H), 3,12 (м, 1H), 3,61 (м, 2H), 4,23 (м, 1H), 5,38 (кв, 1H), 7,25 (м, 6H), 7,61 (м, 2H), 10,33 (с, 1H), 13,43 (уш.с,
1H).
Реферат
Изобретение относится к улучшенному способу получения 5,6-диметил-2-(4-фторфениламино)-4-(1-метил-1,2,3,
4-тетрагидроизохинолин-2-ил)пиримидина формулы I
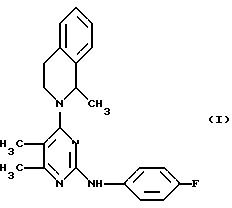
возможно в виде R(+) или S(-) изомеров, или солей его присоединения кислоты. Указанное соединение обладает противоязвенным действием, ингибирует выделение желудочной кислоты и может быть использовано в фармацевтической промышленности. Соединение формулы I получают взаимодействием соединения, формулы II-А

с 1-метил-1,2,3, 4-тетрагидроизохинолином формулы III

возможно в виде R(+) или S(-) изомера, возможно в присутствии растворителя, такого, как N,N-диметилформамид, диметилсульфоксид, н.бутанол, этиленгликоль и др., в присутствии основания, такого как триэтиламин, N,N-диметиланилин, пиридин, ацетат калия. Изобретение также относится к новым соединениям формулы II
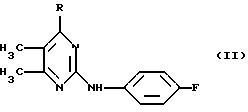
где R означает гидрокси или галоген, и способу получения соединения IIа. 3 с. и 7 з.п. ф-лы.
Формула

и его солей присоединения кислот, отличающийся тем, что производное пиримидина, представленное следующей формулой II-A:

котором Hal представляет галоген, взаимодействует с 1-метил-1,2,3,4-тетрагидроизохинолином, представленным следующей формулой III:

2. Способ по п.1, отличающийся тем, что соль присоединения кислоты является гидрохлоридом.

в которой Hal представляет галоген, отличающийся тем, что 4-фторфенилгуанидинкарбонат, представленный следующей формулой IV:

взаимодействует с этил-2-метилацетоацетатом, представленным следующей формулой V:

с получением 4-гидрокси-2-(4-фторфениламино)-5, 6-диметилпиримидина, представленного следующей формулой II-В:
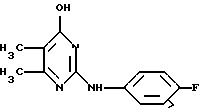
которое затем взаимодействует с галогенирующим агентом.

в которой R представляет гидрокси или галоген.
04.05.1996, 29.10.1996 по пп.1 - 6, 9 - 10;
29.10.1996 по пп.7 и 8.
Документы, цитированные в отчёте о поиске
Способ получения производных 2-анилинопиримидина или их кислотно-аддитивных солей
Способ получения производных 2-анилинопиримидина

Комментарии