Способ получения гидроксилированных циклопентилпиримидиновых соединений - RU2643811C2
Код документа: RU2643811C2
Описание
ПРИОРИТЕТ ИЗОБРЕТЕНИЯ
[0001] Эта заявка заявляет приоритет предварительной заявки Соединенных Штатов под номером 61/648473, поданной 17 мая 2012 года, и предварительной заявки Соединенных Штатов под номером 61/785122, поданной 14 марта 2013 года. Полное описание этих предварительных заявок включено в данный документ посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ
[0002] В данном документе описываются способы получения и очистки циклопентилпиримидиновых соединений, обладающих терапевтической активностью против заболеваний, таких как рак, в качестве ингибиторов активности АКТ киназы.
УРОВЕНЬ ТЕХНИКИ
[0003] Ферменты протеинкиназа B/Akt являются группой серин/треонинкиназ, которые чрезмерно экспрессируются в некоторых опухолях людей. Международная патентная заявка под номером публикации WO 2008/006040 и патент US №8063050 описывают ряд ингибиторов AKT, включая (S)-2-(4-хлорфенил)-1-(4-((5R,7R)-7-гидрокси-5-метил-6,7-дигидро-5H-циклопента[d]пиримидин-4-ил)пиперазин-1-ил)-3-(изопропиламино)пропан-1-он (GDC-0068).
Наряду с тем, что в WO 2008/006040 и патенте US №8063050 описываются способы, пригодные для получения гидроксилированных циклопента[d]пиримидиновых соединений в качестве ингибиторов AKT протеинкиназы, необходимы альтернативные или улучшенные способы получения этих соединений, включая промышленные способы.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0004] Представлен способ получения, разделения и очистки соединений, описанных в данном документе. Соединениями, описанными здесь, являются ингибиторы AKT протеинкиназы, их соли и промежуточные соединения, пригодные при получении таких соединений.
[0005] Один аспект включает способ, включающий циклизацию соединения формулы II

или его соли с образованием соединения формулы I

или его соли, где:
R1 представляет собой водород или аминозащитную группу;
R2 представляет собой -CN, -COORa или -CONRaRb;
Ra и Rb независимо представляют собой водород, -ORc, замещенный или незамещенный C1-12 алкил, замещенный или незамещенный С2-12 алкенил, замещенный или незамещенный С2-12 алкинил, замещенный или незамещенный С3-8 циклоалкил, замещенный или незамещенный фенил или замещенный или незамещенный 3-12-членный гетероциклил; или
Ra и Rb взяты вместе с атомом, к которому они присоединены, с образованием 3-7-членного гетероциклила;
Rc независимо представляет собой водород или необязательно замещенный С1-12 алкил; и
М представляет собой Li или Mg.
[0006] Другой аспект включает способ, включающий приведение в контакт соединения формулы III или его соли с магниевым или литиевым металлирующим агентом:

где R3 представляет собой бром или йод; с образованием соединения формулы I или его соли.
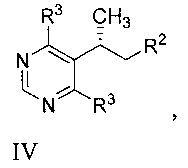
[0007] Другой аспект включает способ, включающий приведение в контакт соединения формулы IV

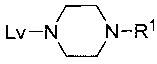
или его соли с соединением

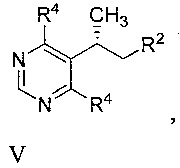
[0008] Другой аспект включает способ, включающий бромирование или йодирование соединения формулы V
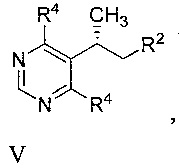
или его соли, где R4 представляет собой -Cl или -ОН, с образованием соединения формулы IV.
[0009] Другой аспект включает соединение формулы II

или его соль, где:
R1 представляет собой водород или аминозащитную группу;
R2 представляет собой -CN, -COORa или -CONRaRb;
Ra и Rb независимо представляют собой водород, -ORc, замещенный или незамещенный С1-12 алкил, замещенный или незамещенный С2-12 алкенил, замещенный или незамещенный С2-12 алкинил, замещенный или незамещенный С3-8 циклоалкил, замещенный или незамещенный фенил или замещенный или незамещенный 3-12-членный гетероциклил; или
Ra и Rb взяты вместе с атомом, к которому они присоединены, с образованием 3-7-членного гетероциклила;
Rc независимо представляет собой водород или необязательно замещенный С1-12 алкил; и
М представляет собой Li или Mg.
[0010] Другой аспект включает соединение формулы III

или его соли, где:
R1 представляет собой водород или аминозащитную группу;
R2 представляет собой -CN, -COORa или -CONRaRb;
Ra и Rb независимо представляют собой водород, -ORb, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный циклоалкил, замещенный или незамещенный фенил или замещенный или незамещенный гетероциклил; или
Ra и Rb взяты вместе с атомом, к которому они присоединены, с образованием 3-7-членного гетероциклила; и
R3 представляет собой бром или йод.
[0011] Другой аспект включает соединение формулы IV

или его соль, где:
R2 представляет собой -CN, -COORa или -CONRaRb; и каждый R3 независимо представляет собой йод или бром.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0012] Далее будет приведено детальное описание некоторых вариантов реализации изобретения, примеры которых раскрыты с помощью сопутствующих структур и формул. Ввиду того, что изобретение будет описано в комбинации с перечисленными вариантами реализаций, следует понимать, что они не предназначены для ограничения изобретения этими вариантами реализации. Более того, изобретение охватывает все альтернативы, модификации и эквиваленты, которые могут быть включены в рамки представленного изобретения, как определено в формуле изобретения. Специалистам в данной области техники понятны многочисленные способы и материалы, подобные или эквивалентные описанным в данном документе, которые могут быть использованы в практике настоящего изобретения. Настоящее изобретение никоим образом не ограничено описанными способами и материалами. В случае если один или большее количество включенных литературных источников информации и подобных материалов отличается от или противоречит данной заявке, включая, но не ограничиваясь ими, определенные термины, используемые термины, описанные методики или т.д., данная заявка является руководством.
[0013] Термин «ацил» означает карбонил-содержащий заместитель, представленный формулой -C(O)-R, в которой R представляет собой водород, алкил, циклоалкил, гетероциклил, циклоалкил-замещенный алкил или гетероциклил-замещенный алкил, в котором алкил, алкокси, циклоалкил и гетероциклил независимо являются необязательно замещенными и такими, как определено в данном документе. Ацильные группы включают алканоил (например, ацетил), ароил (например, бензоил) и гетероароил (например, пиридиноил).
[0014] Термин «алкил», в контексте данного документа, касается насыщенного линейного или разветвленного моновалентного углеводородного радикала, включающего от одного до двенадцати атомов углерода, и в другом варианте реализации от одного до шести атомов углерода, где алкильный радикал может быть необязательно независимо замещен одним или большим количеством заместителей, описанных в данном документе. Примеры алкильных групп включают, но не ограничиваясь ими, метил (Me, -CH3), этил (Et, -СН2СН3), 1-пропил (n-Pr, н-пропил, -СН2СН2СН3), 2-пропил (i-Pr, изо-пропил, -СН(CH3)2), 1-бутил (n-Bu, н-бутил, -СН2СН2СН2СН3), 2-метил-1-пропил (i-Bu, изо-бутил, -СН2СН(СН3)2), 2-бутил (s-Bu, втор-бутил, -СН(СН3)СН2СН3), 2-метил-2-пропил (t-Bu, трет-бутил, -С(СН3)3), 1-пентил (н-пентил, -СН2СН2СН2СН2СН3), 2-пентил (-СН(СН3)СН2СН2СН3), 3-пентил (-СН(СН2СН3)2), 2-метил-2-бутил (-С(СН3)2СН2СН3), 3-метил-2-бутил (-СН(СН3)СН(СН3)2), 3-метил-1-бутил (-СН2СН2СН(CH3)2), 2-метил-1-бутил (-СН2СН(СН3)СН2СН3), 1-гексил (-СН2СН2СН2СН2СН2СН3), 2-гексил (-СН(СН3)СН2СН2СН2СН3), 3-гексил (-СН(СН2СН3)(СН2СН2СН3)), 2-метил-2-пентил (-С(СН3)2СН2СН2СН3), 3-метил-2-пентил (-СН(СН3)СН(СН3)СН2СН3), 4-метил-2-пентил (-СН(СН3)СН2СН(СН3)2), 3-метил-3-пентил (-С(СН3)(СН2СН3)2), 2-метил-3-пентил (-СН(СН2СН3)СН(СН3)2), 2,3-диметил-2-бутил (-С(СН3)2СН(СН3)2), 3,3-диметил-2-бутил (-СН(СН3)С(СН3)3, 1-гептил, 1-октил и тому подобные.
[0015] Термин «алкилен», в контексте данного документа, касается линейного или разветвленного насыщенного бивалентного углеводородного радикала, включающего от одного до двенадцати атомов углерода, и в другом варианте реализации изобретения от одного до шести атомов углерода, где алкиленовый радикал может быть необязательно независимо замещен одним или большим количеством заместителей, описанных в данном документе. Примерами являются, но не ограничиваясь ими, метилен, этилен, пропилен, 2-метилпропилен, пентилен и т.п.
[0016] Термин «алкенил», в контексте данного документа, касается линейного или разветвленного моновалентного углеводородного радикала, включающего от двух до двенадцати атомов углерода, и в другом варианте реализации от двух до шести атомов углерода, по меньшей мере с одной ненасыщенной связью, то есть, углерод-углерод, sp2 двойной связью, где алкенильный радикал может быть необязательно независимо замещен одним или большим количеством заместителей, описанных в данном документе, и включает радикалы, имеющие «цис» и «транс» ориентации, или, альтернативно, «Е» и «Z» ориентации. Примеры включают, но не ограничиваясь ими, этиленил или винил (-СН=СН2), аллил (-СН2СН=СН2),, 1-пропенил, 1-бутен-1-ил, 1-бутен-2-ил и т.п.
[0017] Термин «алкинил», в контексте данного документа, касается линейного или разветвленного моновалентного углеводородного радикала, включающего от двух до двенадцати атомов углерода, и в другом варианте реализации от двух до шести атомов углерода, по меньшей мере с одной ненасыщенной связью, то есть, углерод-углерод, sp тройной связью, где алкинильный радикал может быть необязательно независимо замещен одним или большим количеством заместителей описанных здесь. Примеры включают, но не ограничиваясь ими, этинил (-С≡СН) и пропинил (пропаргил, -СН2С≡СН).
[0018] Термин «алкокси» касается линейного или разветвленного моновалентного радикала, представленного формулой -OR, в которой R представляет собой алкил, алкенил, алкинил или циклоалкил, который может быть дополнительно необязательно замещен, как определено в данном документе. Алкокси-группы включают метокси, этокси, пропокси, изопропокси, моно-, ди- и три-фторметокси и циклопропокси.
[0019] Термин «амино» означает первичные (то есть, -NH2), вторичные (то есть -NRH), третичные (то есть -NRR) и четвертичные (то есть, -N+RRRX-) амины, которые необязательно замещены, и в которых R независимо представляет собой алкил, алкокси, циклоалкил, гетероциклил, циклоалкил-замещенный алкил или гетероциклил-замещенный алкил, где алкил, алкокси, циклоалкил и гетероциклил являются такими как определено в данном документе. Специфическими вторичными и третичными аминами являются алкиламин, диалкиламин, ариламин, диариламин, аралкиламин и диаралкиламин, где алкилы и арилы являются такими, как определено в данном документе, и необязательно независимо замещены. Специфическими вторичными и третичными аминами являются метиламин, этиламин, пропиламин, изопропиламин, фениламин, бензиламин диметиламин, диэтиламин, дипропиламин и диизопропиламин.
[0020] Термины «циклоалкил», «карбоцикл», «карбоциклил» и «карбоциклическое кольцо», в контексте данного документа, применяются взаимозаменяемо и касаются насыщенного или частично ненасыщенного цикличного углеводородного радикала, имеющего от трех до двенадцати атомов углерода, и в другом варианте реализации - от трех до восьми атомов углерода. Термин «циклоалкил» включает моноциклические и полициклические (например, бициклические и трициклические) циклоалкильные структуры, которые необязательно включают насыщенное или частично ненасыщенное циклоалкильное кольцо, конденсированное с насыщенным, частично ненасыщенным или ароматическим циклоалкильным или гетероциклическим кольцом. Примеры циклоалкильных групп включают, но не ограничиваясь ими, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклогексенил, циклогексадиенил, циклогептенил и т.п. Бициклические карбоциклы включают системы, имеющие 7-12 циклических атомов, организованных, например, как бицикло [4,5], [5,5], [5,6] или [6,6] система, или как мостиковые системы, такие как бицикло[2.2.1]гептан, бицикло[2.2.2]октан и бицикло[3.2.2]нонан. Циклоалкил может быть необязательно независимо замещен одним или большим количеством заместителей, описанных в данном документе.
[0021] Термин «арил», в контексте данного документа, означает моновалентный ароматический углеводородный радикал с 6-20 атомами углерода, полученный удалением одного атома водорода с одного атома углерода исходной ароматической циклической системы. Арил включает бициклические радикалы, содержащие ароматическое кольцо, конденсированное с насыщенным, частично ненасыщенным кольцом или ароматическим карбоциклическим или гетероциклическим кольцом. Примеры арильных групп включают, но не ограничиваются ими, радикалы, производные от бензола, нафталина, антрацена, бифенила, индена, индана, 1,2-дигидронафталина, 1,2,3,4-тетрагидронафталина и т.п. Арильные группы могут быть необязательно независимо замещены одним или большим количеством заместителей, описанных в данном документе.
[0022] Термины «гетероцикл», «гетероциклил» и «гетероциклическое кольцо», в контексте данного документа, применяются взаимозаменяемо и касаются насыщенного или частично ненасыщенного карбоциклического радикала с 3-12-членными кольцевыми атомами, в котором по меньшей мере один кольцевой атом является гетероатомом, независимо выбранным из азота, кислорода и серы, а оставшиеся кольцевые атомы представляют собой С, где один или большее количество кольцевых атомов может быть необязательно независимо замещено одним или большим количеством заместителей, описанных ниже. Один из вариантов реализации изобретения включает гетероциклы с 3-7-членными кольцевыми атомами, в которых по меньшей мере один кольцевой атом является гетероатомом, независимо выбранным из азота, кислорода и серы, а оставшиеся кольцевые атомы представляют собой С, где один или большее количество кольцевых атомов может быть необязательно независимо замещено одним или большим количеством заместителей, описанных ниже. Радикал может быть углеродным радикалом или гетероатомным радикалом. Термин «гетероцикл» включает гетероциклоалкокси. «Гетероциклил» также включает радикалы, где гетероциклильные радикалы являются конденсированными с насыщенным, частично ненасыщенным или ароматическим карбоциклическим или гетероциклическим кольцом. Примеры гетероциклических колец включают, но не ограничиваясь ими, пирролидинил, тетрагидрофуранил, дигидрофуранил, тетрагидротиенил, тетрагидропиранил, дигидропиранил, тетрагидротиопиранил, пиперидино, морфолино, тиоморфолино, тиоксанил, пиперазинил, гомопиперазинил, азетидинил, оксетанил, тиетанил, гомопиперидинил, оксепанил, тиепанил, оксазепанил, диазепинил, тиазепинил, 2-пирролинил, 3-пирролинил, индолинил, 2Н-пиранил, 4Н-пиранил, диоксанил, 1,3-диоксоланил, пиразолинил, дитианил, дитиоланил, дигидропиранил, дигидротиенил, дигидрофуранил, пиразолидинил, имидазолинил, имидазолидинил, 3-азабицикло[3.1.0]гексанил, 3-азабицикло[4.1.0]гептанил, азабицикло[2.2.2]гексанил, 3Н-индолил хинолизинил и N-пиридилмочевины. Спирофрагменты также включены в рамки этого определения. Гетероцикл может быть С-присоединенным или N-присоединенным, если это возможно. Например, производной группой от пиррола может быть пиррол-1-ил (N-присоединенный) или пиррол-3-ил (С-присоединенный). Кроме того, производной группой от имидазола может быть имидазол-1-ил (N-присоединенный) или имидазол-3-ил (С-присоединенный). Примерами гетероциклических групп, в которых 2 кольцевых атома углерода замещены оксо (=O) заместителями, являются изоиндолин-1,3-дионил и 1,1-диоксо-тиоморфолинил. Гетероциклические группы здесь необязательно независимо замещены одним или большим количеством заместителей, описанных в данном документе.
[0023] Термин «гетероарил», в контексте данного документа, касается моновалентного ароматического радикала с 5-, 6- или 7-членным кольцом и включает конденсированные циклические системы (по меньшей мере одна из которых является ароматической) из 5-10 атомов, содержащих по меньшей мере один гетероатом, независимо выбранный из азота, кислорода и серы. Примеры гетероарильных групп включают, но не ограничиваясь ими, пиридинил, имидазолил, имидазопиридинил, пиримидинил, пиразолил, триазолил, пиразинил, тетразолил, фурил, тиенил, изоксазолил, тиазолил, оксазолил, изотиазолил, пирролил, хинолинил, изохинолинил, индолил, бензимидазолил, бензофуранил, циннолинил, индазолил, индолизинил, фталазинил, пиридазинил, триазинил, изоиндолил, птеридинил, пуринил, оксадиазолил, триазолил, тиадиазолил, тиадиазолил, фуразанил, бензофуразанил, бензотиофенил, бензотиазолил, бензоксазолил, хиназолинил, хиноксалинил, нафтиридинил и фуропиридинил. Спирофрагменты также включены в рамки этого определения. Гетероарильные группы могут быть необязательно независимо замещены одним или большим количеством заместителей, описанных в данном документе.
[0024] «Уходящая группа» относится к части первого реагента в химической реакции, который вытесняется из первого реагента в ходе химической реакции. Примеры уходящих групп включают, но не ограничиваясь ими, водород, галоген, гидроксильные группы, сульфгидрильные группы, аминогруппы (например, -NRR, где R независимо представляет собой алкил, алкенил, алкинил, циклоалкил, фенил или гетероциклил, и R независимо является необязательно замещенным), силильные группы (например, -SiRRR, где R независимо представляет собой алкил, алкенил, алкинил, циклоалкил, фенил или гетероциклил, и R независимо является необязательно замещенным), -N(R)OR (где R независимо представляет собой алкил, алкенил, алкинил, циклоалкил, фенил или гетероциклил, и R независимо является необязательно замещенным), алкокси-группы (например, -OR, где R независимо представляет собой алкил, алкенил, алкинил, циклоалкил, фенил или гетероциклил, и R независимо является необязательно замещенным), тиоловые группы (например, -SR, где R независимо представляет собой алкил, алкенил, алкинил, циклоалкил, фенил или гетероциклил, и R независимо является необязательно замещенным), сульфонилокси-группы (например, -OS(O)1-2R, где R независимо представляет собой алкил, алкенил, алкинил, циклоалкил, фенил или гетероциклил, и R независимо является необязательно замещенным), сульфаматные группы (например, -OS(O)1-2NRR, где R независимо представляет собой алкил, алкенил, алкинил, циклоалкил, фенил или гетероциклил, и R независимо является необязательно замещенным), карбаматные группы (например, -OC(O)2NRR, где R независимо представляет собой алкил, алкенил, алкинил, циклоалкил, фенил или гетероциклил, и R независимо является необязательно замещенным) и карбонатные группы (например, -OC(O)2RR, где R независимо представляет собой алкил, алкенил, алкинил, циклоалкил, фенил или гетероциклил, и R независимо является необязательно замещенным). Примеры сульфонилокси-групп включают, но не ограничиваясь ими, алкилсульфонилокси-группы (например, метилсульфонилокси (мезилатная группа) и трифторметилсульфонилокси (трифлатная группа)) и арилсульфонилокси-группы (например, n-толуолсульфонилокси (тозилатная группа) и n-нитросульфонилокси (нозилатная группа)). Другие примеры уходящих групп включают замещенные и незамещенные аминогруппы, такие как амино, алкиламино, диалкиламино, гидроксиламино, алкоксиламино, N-алкил-N-алкоксиамино, ациламино, сульфониламино и т.п.
[0025] «Аминозащитная группа», в контексте данного документе, касается групп, обычно используемых для предотвращения реакций аминогрупп во время реакций, проводимых на других функциональных группах. Примеры таких защитных групп включают карбаматы, амиды, алкильные и арильные группы, имины, так же как многочисленные производные по N-гетероатому, которые могут быть удалены для регенерирования заданной аминогруппы. Конкретными аминозащитными группами являются Ас (ацетил), трифторацетил, фталимид, Bn (бензил), Tr (трифенилметил или тритил), бензилиденил, п-толуолсульфонил, Pmb (п-метоксибензил), Boc (трет-бутилоксикарбонил), Fmoc (9-флуоренилметилоксикарбонил) и Cbz (карбобензилокси). Дополнительные примеры этих групп можно найти в публикации: Wuts, P.G.М. and Greene, T.W. (2006) Frontmatter, в книге Greene, Protective Groups in Organic Synthesis, четвертое издание, John Wiley & Sons, Inc., Хобокен, штат Нью-Джерси, США. Термин «защищенная амино» касается аминогруппы, замещенной одной из упомянутых выше аминозащитных групп.
[0026] Термин «замещенный», в контексте данного документа, означает любую из упомянутых выше групп (например, алкил, алкилен, алкенил, алкинил, циклоалкил, арил, гетероциклил и гетероарил), в которой по меньшей мере один атом водорода заменен заместителем. В случае оксозаместителя («=O») замещены два атома водорода. «Заместители», в контексте настоящего изобретения, включают, но не ограничиваясь ими, галоген, гидрокси, оксо, циано, нитро, амино, алкиламино, диалкиламино, алкил, алкенил, алкинил, циклоалкил, алкокси, замещенный алкил, тиоалкил, галоалкил (включая пергалоалкил), гидроксиалкил, аминоалкил, замещенный алкенил, замещенный алкинил, замещенный циклоалкил, арил, замещенный арил, гетероарил, замещенный гетероарил, гетероцикл, замещенный гетероцикл, -NReRf, -NReC(=O)Rf, -NReC(=O)NReRf, -NReC(=O)ORf-NReSO2Rf, -ORe, -C(=O)Re-C(=O)ORe, -C(=O)NReRf, -OC(=O)NReRf, -SRe, -SORe, -S(=O)2Re, -OS(=O)2Re, -S(=O)2ORe, где Re и Rf являются одинаковыми или разными и независимо представляют собой водород, алкил, замещенный алкил, алкенил, замещенный алкенил, алкинил, замещенный алкинил, циклоалкил, замещенный циклоалкил, арил, замещенный арил, гетероарил, замещенный гетероарил, гетероцикл, замещенный гетероцикл.
[0027] Термин «гало» или «галоген», в контексте данного документа, означает фтор, хлор, бром или йод.
[0028] Термины в единственном числе, при использовании в настоящем документе, означают один или более.
[0029] В данном документе ссылка на «около» в отношении значения или параметра включает (и описывает) варианты реализаций изобретения, которые касаются значения или параметра per se, и в одном из вариантов реализации изобретения плюс или минус 20% от приведенного значения. Например, описание, ссылаясь на «около X», включает описание «X».
[0030] Термин «фармацевтически приемлемые соли» включает соли присоединения кислот и оснований. Примерами солей являются, но не ограничиваясь ими, сульфаты, цитраты, ацетаты, оксалаты, хлориды, бромиды, йодиды, нитраты, бисульфаты, фосфаты, гидрофосфаты, изоникотинаты, лактаты, салицилаты, гидроцитраты, тартраты, олеаты, таннаты, пантотенаты, битартраты, аскорбаты, сукцинаты, малеаты, гентисинаты, фумараты, глюконаты, глюкуронаты, сахараты, формиаты, бензоаты, глутаматы, метансульфонаты, этансульфонаты, бензолсульфонаты, n-толуолсульфонаты и памоаты (то есть, 1,1'-метиленбис-(2-гидрокси-3-нафтоаты)). Фармацевтически приемлемая соль может содержать включение другой молекулы, такой как ацетатный ион, сукцинатный ион или другой противоион. Противоион может быть любым органическим или неорганическим фрагментом, стабилизирующим заряд основного соединения.
[0031] Термин «фармацевтически приемлемая кислотно-аддитивная соль» касается солей, которые сохраняют биологическую эффективность и свойства свободного основания и которые не являются биологически или иным путем нежелательными, и образованы с помощью неорганических кислот, таких как хлористоводородная кислота, бромистоводородная кислота, серная кислота, азотная кислота, угольная кислота, фосфорная кислота и т.д., а органические кислоты могут быть выбраны из алифатических, циклоалифатических, ароматических, аралифатических, гетероциклических, карбоциклических и сульфоновых органических кислот, таких как муравьиная кислота, уксусная кислота, пропионовая кислота, гликолевая кислота, глюконовая кислота, молочная кислота, пировиноградная кислота, щавелевая кислота, яблочная кислота, малеиновая кислота, малоновая кислота, янтарная кислота, фумаровая кислота, винная кислота, лимонная кислота, аспарагиновая кислота, аскорбиновая кислота, глутаминовая кислота, антраниловая кислота, бензойная кислота, коричная кислота, миндальная кислота, эмбоновая кислота, фенилуксусная кислота, метансульфоновая кислота, этансульфоновая кислота, бензолсульфоновая кислота, п-толуолсульфоновая кислота, салициловая кислота и т.п.
[0032] Термин «фармацевтически приемлемые основно-аддитивные соли» включает соли, являющиеся производными неорганических оснований, такие как натриевые, калиевые, литиевые, аммониевые, кальциевые, магниевые, железные, цинковые, медные, марганцевые, алюминиевые соли и т.п. Особенно предпочтительными основно-аддитивными солями являются соли аммония, калия, натрия, кальция и магния. Соли, производные от фармацевтически приемлемых органических нетоксичных оснований, включают соли первичных, вторичных и третичных аминов, замещенных аминов, включая встречающиеся в природе замещенные амины, циклических аминов и основных ионообменных смол, таких как изопропиламин, триметиламин, диэтиламин, триэтиламин, трипропиламин, этаноламин, 2-диэтиламиноэтанол, трометамин, дициклогексиламин, лизин, аргинин, гистидин, кофеин, прокаин, гидрабамин, холин, бетаин, этилендиамин, глюкозамин, метилглюкамин, теобромин, пурины, пиперазин, пиперидин, N-этилпиперидин, полиаминовые смолы и т.п. Особенно предпочтительными органическими нетоксичными основаниями являются изопропиламин, диэтиламин, этаноламин, трометамин, дициклогексиламин, холин и кофеин.
[0033] Соединения представленного изобретения, если не указано иное, включают соединения, которые отличаются только присутствием одного или большего количества атомов изотопов. Например, в рамки этого изобретения попадают соединения представленного изобретения, в которых один или большее количество атомов водорода заменено дейтерием или тритием, или один или большее количество атомов углерода заменено13С или14С атомами углерода, или один или большее количество атомов азота заменено15N атомом азота, или один или большее количество атомов серы заменено33S,34S или36S атомом серы, или один или большее количество атомов кислорода заменено17О или18O атомом кислорода.
[0034] Один аспект включает способ, включающий циклизацию соединения формулы II
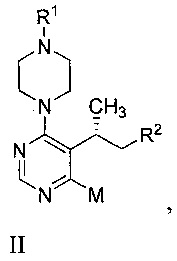
или его соли с образованием соединения формулы I

или его соли, где:
R1 представляет собой водород или аминозащитную группу;
R2 представляет собой -CN, -COORa или -CONRaRb;
Ra и Rb независимо представляют собой водород, -ORc, замещенный или незамещенный C1-12 алкил, замещенный или незамещенный С2-12 алкенил, замещенный или незамещенный С2-12 алкинил, замещенный или незамещенный С3-8 циклоалкил, замещенный или незамещенный фенил или замещенный или незамещенный 3-12-членный гетероциклил; или
Ra и Rb взяты вместе с атомом, к которому они присоединены, с образованием 3-7-членного гетероциклила;
Rc независимо представляет собой водород или необязательно замещенный С1-12 алкил; и
М представляет собой Li или Mg.
[0035] Другой аспект включает соединение формулы I или его соль, полученные в соответствии со способом, включающим циклизацию соединения формулы II или его соли.
[0036] В другом аспекте представлен способ, включающий приведение в контакт соединения формулы III

или его соли, где:
R1 представляет собой водород или аминозащитную группу;
R2 представляет собой -CN, -COORa или -CONRaRb;
Ra и Rb независимо представляют собой водород, -ORc, замещенный или незамещенный С1-12 алкил, замещенный или незамещенный С2-12 алкенил, замещенный или незамещенный С2-12 алкинил, замещенный или незамещенный С3-8 циклоалкил, замещенный или незамещенный фенил или замещенный или незамещенный 3-12-членный гетероциклил; или
Ra и Rb взяты вместе с атомом, к которому они присоединены, с образованием 3-7-членного гетероциклила;
Rc независимо представляет собой водород или необязательно замещенный С1-12 алкил; и
R3 представляет собой бром или йод;
с металлирующим агентом, содержащим магний или литий, с образованием соединения формулы I или его соли.
[0037] Другой аспект включает соединение формулы I или II или его соль, полученные в соответствии со способом, включающим приведение в контакт соединения формулы III с металлирующим агентом, содержащим магний или литий.
[0038] В другом варианте реализации описанные выше способы дополнительно включают приведение в контакт соединения формулы IV:
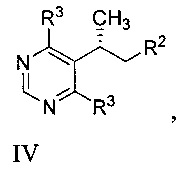
или его соли с соединением

R1 представляет собой водород или аминозащитную группу;
R2 представляет собой -CN, -COORa или -CONRaRb;
Ra и Rb независимо представляют собой водород, -ORc, замещенный или незамещенный С1-12 алкил, замещенный или незамещенный С2-12 алкенил, замещенный или незамещенный С2-12 алкинил, замещенный или незамещенный С3-8 циклоалкил, замещенный или незамещенный фенил или замещенный или незамещенный 3-12-членный гетероциклил; или
Ra и Rb взяты вместе с атомом, к которому они присоединены, с образованием 3-7-членного гетероциклила;
Rc независимо представляет собой водород или необязательно замещенный С1-12 алкил; и
каждый R3 независимо представляет собой бром или йод; и
Lv представляет собой уходящую группу.
[0039] Другой аспект включает соединение формулы III или его соль, полученные в соответствии со способом, включающим приведение в контакт соединения формулы IV или его соли с соединением
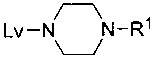
[0040] В другом варианте реализации описанные выше способы дополнительно включают бромирование или йодирование соединения формулы V
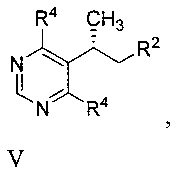
или его соли, с образованием соединения Формулы IV или его соли, где R4 представляет собой -Cl или -ОН.
[0041] В одном варианте реализации описанные выше способы дополнительно включают бромирование соединения формулы V или его соли, где R4 представляет собой -OH.
[0042] В одном варианте реализации описанное выше бромирование дополнительно включает приведение в контакт соединения формулы V или его соли с бромирующим агентом, с образованием соединения формулы IV или его соли, где R3 в формуле IV представляет собой Br.
[0043] Бромирующие агенты включают, например, PBr3, PBr5, O=PBr3, Р(ОН)Br3, Br2 (в одном примере с фосфином, таким как PR3, где R представляет собой алкил, циклоалкил, арильную или гетероциклильную группу), HBr, O=SBr2, другие бромидные соли, такие как NaBr, KBr и CuBr2 (в одном примере с фторирующими агентами, такими как 1-хлорметил-4-фтор-1,4-диазониабицикло[2.2.2]октана бис(тетрафторборат) или Selectfluor®), и гексабромацетон (в одном примере с алкилтрибромацетатом, таким как этилтрибромацетат).
[0044] В одном варианте реализации бромирующий агент содержит бром и фосфор, например, PBr3, PBr5, O=PBr3, Р(OH)Br3 и Br2 в комбинации с фосфином, таким как PR3, где R представляет собой алкил, циклоалкил, арильную или гетероциклильную группу.
[0045] В одном варианте реализации описанные выше способы дополнительно включают йодирование соединения формулы V, где R4 представляет собой -Cl.
[0046] В одном варианте реализации описанное выше йодирование дополнительно включает приведение в контакт соединения формулы V или его соли с йодирующим агентом, с образованием соединения формулы IV или его соли, где R3 в формуле IV представляет собой I.
[0047] Йодирующие агенты включают, например, йодидные соли, такие как NaI, ΚΙ или HI (в одном примере полученные in situ из йодидной соли и кислоты, например, из йодида натрия или калия и кислоты, такой как метансульфоновая кислота).
[0048] Другой аспект включает соединение формулы IV или его соль, полученные в соответствии со способом, включающим бромирование или йодирование соединения формулы V.
[0049] В некоторых вариантах реализации, в которых R1 в формуле I представляет собой аминозащитную группу, указанный способ дополнительно включает снятие защиты аминозащитной группы с получением соединения формулы I, где R1 представляет собой Н. В одном примере R1 представляет собой трет-бутоксикарбонил (Boc), а способ дополнительно включает удаление группы Воc за счет взаимодействия соединения формулы I с кислотой, например, хлористоводородной, серной, трифторметансульфоновой или трифторуксусной кислотой.
[0050] В некоторых вариантах реализации R1 представляет собой аминозащитную группу, например, удаляемую карбамоильную группу (например, трет-бутоксикарбонил и бензилоксикарбонил). В некоторых вариантах реализации R1 в формуле (II) и/или формуле (I) представляет собой замещенную ацильную группу, такую как замещенный -С(O)-алкил.
[0051] В некоторых вариантах реализации R1 представляет собой -C(O)-Rd или -C(O)ORd, а Rd независимо представляет собой водород, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный циклоалкил, замещенный или незамещенный фенил или замещенный или незамещенный гетероциклил.
[0052] В некоторых вариантах реализации Rc представляет собой С1-6 алкил или водород, при этом указанный алкил необязательно замещено оксо-группой, галогеном или фенилом.
[0053] В некоторых вариантах реализации Rd представляет собой C1-6 алкил или водород, при этом указанный алкил необязательно замещено оксо-группой, галогеном или фенилом. В некоторых вариантах реализации Rd представляет собой трет-бутил.
[0054] В некоторых вариантах реализации R1 представляет собой водород.
[0055] В некоторых вариантах реализации R2 представляет собой -COORa или -CONRaRb.
[0056] В некоторых вариантах реализации R2 представляет собой -СООН или -СООСН3.
[0057] В некоторых вариантах реализации R2 представляет собой -C(O)N(Ra)ORb. В некоторых вариантах реализации R2 представляет собой -С(O)N(CH3)OCH3.
[0058] В некоторых вариантах реализации R2 представляет собой -CN, -СООН или -CONRaRb. В некоторых вариантах реализации R2 представляет собой -COOMe или -COOEt. В некоторых вариантах реализации R2 представляет собой -COOPr.
[0059] В некоторых вариантах реализации Ra и Rb независимо представляют собой водород, -ORc, замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, замещенный или незамещенный циклоалкил, замещенный или незамещенный фенил или замещенный или незамещенный гетероциклил.
[0060] В некоторых вариантах реализации Ra и Rb независимо представляют собой водород, С1-6 алкил или -O(C1-6 алкил).
[0061] В некоторых вариантах реализации Ra и Rb взяты вместе с атомом, к которому они присоединены, с образованием 3-7-членного гетероциклила.
[0062] В некоторых вариантах реализации Ra и Rb независимо представляют собой водород или С1-6 алкил, при этом указанный алкил необязательно замещен оксо-группой, галогеном или фенилом.
[0063] В некоторых вариантах реализации Ra и Rb представляют собой метил.
[0064] В некоторых вариантах реализации Ra и Rb взяты вместе с атомом, к которому они присоединены, с образованием морфолинильной группы.
[0065] В некоторых вариантах реализации M представляет собой Mg.
[0066] В некоторых вариантах реализации M представляет собой Li.
[0067] В некоторых вариантах реализации R3 представляет собой йод. В некоторых вариантах реализации R3 представляет собой бром.
[0068] В некоторых вариантах реализации R4 представляет собой Cl. В некоторых вариантах реализации R4 представляет собой Cl.
[0069] В некоторых вариантах реализации металлирующий агент содержит один или более из лития и магния. В некоторых вариантах реализации металлирующий агент представляет собой магнийорганическое соединение, такое как реактив Гриньяра (например, C1-С6 галогенид алкилмагния, например, iPrMgCl.) В некоторых вариантах реализации металлирующий агент представляет собой литийорганическое соединение, такое как C1-С6 алкиллитий (например, н-бутиллитий и трет-бутиллитий).
[0070] В некоторых вариантах реализации металлирующий агент представляет собой один или более из (i) LiR и (ii) MgR2, где каждый R независимо представляет собой галоген, необязательно замещенный C1-6 алкил, необязательно замещенный С3-7 циклоалкил, необязательно замещенный арил, необязательно замещенный гетероарил или необязательно замещенный гетероциклил, или две группы R взяты вместе с атомом, к которому они присоединены, с образованием 5-7-членного, необязательно замещенного кольца. В некоторых вариантах реализации каждый R независимо представляет собой галоген, необязательно замещенный C1-6 алкил или необязательно замещенный С3-7 циклоалкил.
[0071] В одном аспекте способ получения соединения формулы I или его соли из соединения формул II или III может быть осуществлен в эфирном или углеводородном растворителе или в смеси этих растворителей (например, тетрагидрофуран (ТГФ), метил-трет-бутиловый эфир (МТБЭ), циклопентил-метиловый эфир (ЦПМЭ), диэтиловый эфир, диизопропиловый эфир, дифениловый эфир, толуол, этилбензол, ксилол, кумол, пентан или гептан). Могут быть использованы другие подходящие условия (например, температура реакции равна или ниже 20°С, такое значение как около -10°С или около -78°С), выполнение реакции практически в безводной среде (например, менее, чем около 100 м.д., 50 м.д. или менее, чем около 10 м.д. воды) и выполнение реакции под инертной атмосферой, например, под атмосферой гелия, неона, аргона или азота). В конкретном варианте реализации способ получения соединения формулы I или его соли из соединения формул II или III осуществляют под атмосферой азота в ТГФ при температуре от около -25°С до около -5°С или около -10±2°С, в безводной среде.
[0072] В другом варианте реализации соединения формулы I используют для получения ингибиторов киназы АКТ для лечения заболеваний и расстройств, восприимчивых к ингибированию АКТ, как описано в патенте США №8063050, выданном Митчеллу (Mitchell, et al).
[0073] Другой аспект включает способ получения соединения формулы 2.2 или его соли,
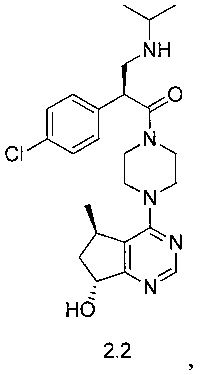
включающий стереоселективное восстановление соединения формулы I или его соли,

с получением соединения формулы 2.1 или его соли,
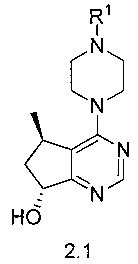
и взаимодействие соединения формулы 2.1 или его соли с соединением формулы
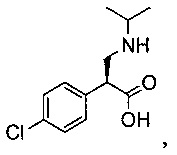
или его солью с образованием соединения формулы 2.2.
[0074] Другой аспект включает соединение формулы 2.2 или его соль, полученные в соответствии со способом, включающим стереоселективное восстановление соединения формулы I или его соли, с образованием соединения формулы 2.1 или его соли, и взаимодействие соединения формулы 2.1 или его соли с соединением формулы
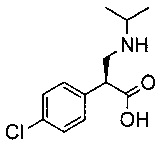
[0075] Соединения, раскрытые в данном документе, могут содержать один или большее количество хиральных центров. Соответственно, при желании, такие соединения могут быть получены или выделены в форме чистых стереоизомеров (таких как индивидуальные энантиомеры или диастереомеры, или в форме стереоизомерно обогащенных смесей). Все такие стереоизомеры (и обогащенные смеси) включены в рамки данного изобретения, если не указано иное. Чистые стереоизомеры (или обогащенные смеси) можно получить, используя, например, оптически активные исходные материалы или стереоселективные реагенты, хорошо известные в данной области. Альтернативно, рацемические или стереоизомерно обогащенные смеси таких соединений можно разделить, используя, например, хроматографию на хиральной колонке, хиральные разделяющие агенты и т.п.
[0076] В иллюстративных целях на Схеме 1 показан общий способ получения соединений настоящего изобретения, а также основные промежуточные соединения. Более подробное описание отдельных стадий реакций представлено ниже в разделе «Примеры». Специалистам в данной области техники понятно, что могут быть использованы другие способы синтеза для получения соединений по настоящему изобретению. Хотя на Схеме показаны, а ниже описаны конкретные исходные материалы и реагенты, для получения многочисленных производных могут быть легко использованы другие исходные материалы и реагенты и/или условия реакции. Кроме того, многие соединения, полученные по способам, описанным ниже, могут быть дополнительно модифицированы в свете представленного описания, с использованием стандартных химических методик, общеизвестных специалистам в данной области техники.

[0077] Схема 1 иллюстрирует способ получения соединения формулы I, где R1, Ra и Rb независимо являются такими, как описано выше для формулы I. Реакция соединения 1.1 с йодирующим агентом (например, с йодидной солью, такой как NaI, и необязательно с кислотой) приводит к образованию дийодпиримидина 1.2, который взаимодействует с монозащищенным пиперазином с образованием метилового эфира 1.3. Метиловый эфир превращают в амид 1.5 через кислотное промежуточное соединение 1.4, полученное щелочным гидролизом указанного сложного эфира. Амид 1.5 металлируют металлирующим агентом, таким как реактив Гриньяра (например,iPrMgCl), и циклизуют с получением циклопентилкетона I.
[0078] В другом аспекте представлено применение соединений формулы I в качестве промежуточных соединений при получении фармацевтически активных соединений, таких как ингибиторы AKT, описанные в патенте US 8063050, выданном 22 ноября 2011 года Митчеллу (Mitchell). Например, как показано на приведенной ниже Схеме 2, соединения формулы I могут быть использованы для получения (S)-2-(4-хлорфенил)-1-(4-((5R,7R)-7-гидрокси-5-метил-6,7-дигидро-5H-циклопента[d]пиримидин-4-ил)пиперазин-1-ил)-3-(изопропиламино)пропан-1-она, как описано в патенте US 8063050, выданном 22 ноября 2011 года, как описано, например, в Примере 14, который включен в данный документ посредством ссылки.
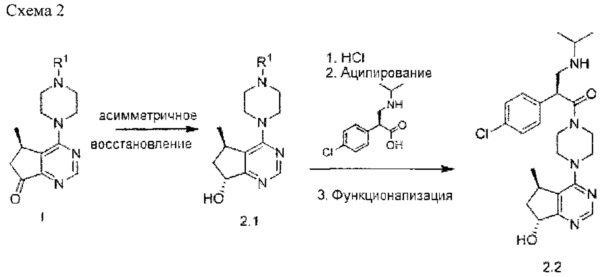
[0079] Схема 2 раскрывает способ получения соединения формулы 2.2. Асимметричное восстановление соединений формулы I приводит к образованию соединений формулы 2.1, где R1 является таким, как описано выше для формулы I. Если R1 представляет собой защитную группу, например, группу Boc, то соединение 2.1 может затем взаимодействовать с HCl, может быть ацилировано и функционализировано, например, посредством дальнейшего снятия защиты, с образованием соединения 2.2.
[0080] Другой аспект включает продукт, полученный по любому способу, схеме или примеру, представленному в настоящем документе.
ПРИМЕРЫ
[0081] Изобретение далее раскрывается со ссылкой на следующие примеры, которые приведены с целью иллюстрации и не предназначены для ограничения изобретения.
[0082] Сокращения, используемые здесь, имеют следующие значения:
вод.: водный;
DIPA: диизопропиламин;
DIPEA: диизопропилэтиламин;
МТВЕ: метил-трет-бутиловый эфир;
TMSCl: триметилхлорсилан;
MsDPEN: N-метансульфонил-1,2-дифенилэтилендиамин;
TsDACH: N-(п-толуолсульфонил)-1,2-диаминоциклогексан;
Dppp: 1,3-Бис(дифенилфосфино)пропан;
NMM: 4-метилморфолин;
PhME: толуол;
СРМЕ: циклопентилметиловый эфир;
DBU: 1,8-диазобицикло[5,4]ундец-7-ен;
CDI: 1,1'-карбонилдиимидазол;

(R)-метил 3-(4,6-дихлорпиримидин-5-ил)бутаноат
[0083] В смесь (R)-метил 3-(4,6-дигидроксипиримидин-5-ил)бутаноата (1,00 кг, 4,70 моль), толуола (4,00 л) и 2,6-диметилпиридина (0,550 л, 4,70 моль) медленно добавляли оксихлорид фосфора (0,960 л, 10,6 моль) при 50°С. Смесь перемешивали при 70°С в течение 24 часов. Раствор охладили до 0°С. К этой смеси медленно добавляли 20% водный раствор гидроксида натрия (около 40,0 моль, 1,60 кг в 8,00 л H2O), поддерживая внутреннюю температуру ниже 30°С, с получением конечного значения pH от 5 до 6. Добавляли этилацетат (2,50 л), перемешивали в течение 0,5 часа, и затем слои разделяли. Водную фазу экстрагировали этилацетатом (3×1,00 л). Органические растворы объединяли и промывали 1 N соляной кислотой (2×2,50 л) и насыщенным раствором соли (2,50 л). Органические растворы объединяли и сушили над сульфатом натрия, и фильтровали через стеклянный фильтр. Раствор концентрировали до около 3,00 мл/г и разводили ацетонитрилом до около 7,00 мл/г. Последовательность действий повторяли дважды для удаления остатков этилацетата и толуола (подтверждали1Н ЯМР анализом). Оставшийся неочищенный раствор непосредственно использовали на следующей стадии без дополнительной очистки или выделения.1H ЯМР (300 МГц, CDCl3) δ 8,62 (s, 1Н), 4,15 (ddq, J=8,1, 7,2, 7,2 Гц, 1Н), 3,64 (s, 3Н), 3,08 (dd, J=16,5, 8,1 Гц, 1H), 2,86 (dd, J=16,5, 7,2 Гц, 1H), 1,45 (d, J=7,2 Гц, 3Н). Расчетное значение МСВР для C9H11Cl2N2O2 [М+Н]+: 249,0192, найдено 249,0190.

(R)-метил 3-(4,6-дийодпиримидин-5-ил)бутаноат
[0084] В раствор (R)-метил 3-(4,6-дихлорпиримидин-5-ил)бутаноата (36,0 г, 145 ммоль) в ацетонитриле (540 мл) добавляли йодид натрия (152 г, 1,02 моль). Смесь перемешивали при 25°С в течение 30 минут, затем охлаждали до около 5°С. Добавляли метансульфоновую кислоту (9,41 мл, 1,00 экв.) за 5 минут. Смесь перемешивали при температуре около 5°С в течение 3 часов. Реактор охлаждали до температуры около 5°С и добавляли N,N-диизопропилэтиламин (20,3 мл, 116 ммоль). Смесь перемешивали в течение 1 часа, нагревая смесь до 20°С. Добавляли насыщенный раствор сульфита натрия до прекращения дальнейшего изменения цвета, чтобы удалить йод. Добавляли воду (540 мл) и доводили pH до значения от 5 до 7. Двухфазную смесь концентрировали под пониженным давлением при температуре менее 40°С для удаления ацетонитрила. Водную суспензию отфильтровали с получением 48,8 г (выход 78%) грязновато-белого твердого продукта.1Н ЯМР (300 МГц, CDCl3) δ 8,21 (s, 1H), 4,02 (ddq, J=7,8, 7,5, 7,2 Гц, 1H), 3,67 (s, 3Н), 3,18 (dd, J=16,5, 7,8 Гц, 1H), 2,91 (dd, J=16,5, 7,5 Гц, 1H), 1,47 (d, J=7,2 Гц, 3Н). Расчетное значение МСВР для C9H11I2N2O2 [М+Н]+: 432,8904, найдено 432,8906.

(R)-трет-6утил 4-(6-йод-5-(4-метокси-4-оксобутан-2-ил)пиримидин-4-ил)пиперазин-1-карбоксилат
[0085] В раствор (R)-метил 3-(4,6-дийодпиримидин-5-ил)бутаноата (212 г, 491 ммоль) и Boc-пиперазина (101 г, 540 ммоль) в метаноле (424 мл) добавляли N,N-диизопропилэтиламин (94,3 мл, 540 ммоль). Смесь нагревали при 60°С в течение 24 часов. Метанол удаляли перегонкой под пониженным давлением при температуре ниже 40°С. К смеси добавляли 318 мл тетрагидрофурана. Описанный выше прием замены растворителя повторяли дважды. К смеси добавляли 424 мл тетрагидрофурана, 212 мл насыщенного водного раствора хлорида аммония и 21,2 мл воды. Органический слой промывали с помощью 212 мл (1,00 об.) насыщенного водного раствора хлорида аммония. Этот тетрагидрофурановый раствор использовали на следующей стадии без дополнительной очистки (аналитический выход 91% по массе).1Н ЯМР (300 МГц, CDCl3) δ 8,25 (s, 1Н), 3,80-3,67 (m, 1Н), 3,65 (s, 3Н), 3,60-3,56 (m, 4Н), 3,21-3,18 (m, 4Н), 3,14 (dd, J=16,2, 9,0 Гц, 1H), 2,81 (dd, J=16,2, 5,7 Гц, 1Н), 1,48 (s, 9Н), 1,47 (d, J=7,2 Гц, 3Н). Расчетное значение МСВР для C18H28IN4O4 [М+Н]+: 491,1150, найдено 491,1154.

(R)-3-(4-(4-(трет-бутоксикарбонил)пиперазин-1-ил)-6-йод-пиримидин-5-ил)бутановая кислота
[0086] В раствор (R)-трет-бутил 4-(6-йод-5-(4-метокси-4-оксобутан-2-ил)пиримидин-4-ил)пиперазин-1-карбоксилата (219 г, 0,447 моль) в тетрагидрофуране (657 мл) добавляли раствор моногидрата гидроксида лития (56,2 г, 1,34 моль) в 329 мл воды при 25°С. Смесь перемешивали при 25°С в течение 5 часов. Нижний водный слой отбросили. Смесь подкислили 1 N соляной кислотой при 5°C с получением конечного значения pH от около 1 до 2. Слои разделили. Затем верхний слой экстрагировали изопропилацетатом (440 мл × 3), объединили с нижним слоем и промыли водой (220 мл × 2). Растворители удалили перегонкой при пониженном давлении при температуре ниже 50°С. Оставшийся изопропилацетат удалили азеотропной перегонкой с гептаном под пониженным давлением при температуре ниже 50°С. Продукт постепенно выпал в осадок, его отфильтровали с получением порошка от грязновато-белого до светло-желтого цвета (196 г, выход 84%).1Н ЯМР (300 МГц, CDCl3) δ 8,27 (s, 1H), 3,80-3,68 (m, 1H), 3,59-3,56 (m, 4Н), 3,23-3,14 (m, 5Н), 2,86 (dd, J=16,5, 5,4 Гц, 1H), 1,50 (d, J=7,2 Гц, 3Н), 1,48 (s, 9Н). Расчетное значение МСВР для C17H26IN4O4 [М+Н]+: 477,0993, найдено 477,0995.

(R)-трет-бутил 4-(6-йод-5-(4-(метокси(метил)амино)-4-оксобутан-2-ил)пиримидин-4-ил)пиперазин-1-карбоксилат
[0087] В раствор (R)-3-(4-(4-(трет-бутоксикарбонил)пиперазин-1-ил)-6-йодпиримидин-5-ил)бутановой кислоты (100 г, 210 ммоль) в тетрагидрофуране (700 мл) частями добавляли 1,1'-карбонилдиимидазол (40,9 г, 252 ммоль). Реакционную смесь перемешивали при 20°С в течение 1 часа и охлаждали до 5°С. Частями добавляли N,O-диметилгидроксиамина гидрохлорид (41,0 г, 420 ммоль), затем N-метилморфолин (6,94 мл, 63,0 ммоль). Смесь перемешивали при 5°С в течение около 1 часа, медленно нагревали до комнатной температуры и перемешивали в течение 24 часов. Добавляли насыщенный водный раствор хлорида аммония (500 мл) и воду (150 мл) до четкого разделения фаз. Органический слой промывали насыщенным водным раствором хлорида аммония (500 мл) и насыщенным раствором соли (200 мл). Оставшуюся воду удаляли азеотропной перегонкой до содержания менее 500 м.д. при помощи совместного выпаривания с тетрагидрофураном. Продукт в виде раствора в тетрагидрофуране использовали на следующей стадии без дополнительной очистки или выделения (аналитический выход по массе: >99%).1Н ЯМР (300 МГц, CDCl3) δ 8,23 (s, 1H), 3,84 (ddq, J=9,0, 7,2, 5,1 Гц, 1H), 3,72 (s, 3Н), 3,61-3,57 (m, 4Н), 3,42 (dd, J=16,5, 9,0 Гц, 1H), 3,25-3,21 (m, 4Н), 3,17 (s, 3Н), 2,76 (dd, J=16,5, 5,1 Гц, 1H), 1,47 (s, 9Н), 1,47 (d, J=7,2 Гц, 3Н). Расчетное значение МСВР для C19H31IN5O4 [М+Н]+: 520,1415, найдено 520,1413.

(R)-трет-бутил 4-(5-метил-7-оксо-6,7-дигидро-5H-циклопента[d]пиримидин-4-ил)пиперазин-1-карбоксилат
Способ А:
[0088] Раствор (R)-трет-бутил 4-(6-йод-5-(4-(метил(фенил)амино)-4-оксобутан-2-ил)пиримидин-4-ил)пиперазин-1-карбоксилата (109 г, 210 ммоль) в тетрагидрофуране (600 мл) продували азотом в течение 30 минут. По каплям добавляли раствор изопропилмагния хлорида (159 мл, 210 ммоль, 1,32 М в тетрагидрофуране) при -15°С. Смесь перемешивали при -10°С в течение 1 часа и медленно переносили в холодный 20 масс. % водный раствор хлорида аммония (600 мл) при перемешивании, поддерживая внутреннюю температуру ниже 10°С. Затем органический слой промывали насыщенным водным раствором хлорида аммония (500 мл). Тетрагидрофуран удаляли перегонкой при пониженном давлении при температуре ниже 40°С. Медленно добавляли метил трет-бутиловый эфир (350 мл), поддерживая внутреннюю температуру от 35°С до 40°С, затем гептан (350 мл). Смесь медленно охлаждали до 20°С, а продукт постепенно выпадал в осадок во время этого процесса. Суспензию отфильтровали, а осадок на фильтре высушивали при 40°С под вакуумом с получением серого твердого вещества (52,3 г, выход 75% за две стадии).1Н ЯМР (300 МГц, CDCl3) δ 8,73 (s, 1Н), 3,92-3,83 (m, 2H), 3,73-3,49 (m, 7H), 2,96 (dd, J=16,5, 7,2 Гц, 1H), 2,33 (dd, J=16,5, 1,8 Гц, 1H), 1,50 (s, 9H), 1,32 (d, J=6,9 Гц, 3Н). Расчетное значение МСВР для C17H25N4O3 [М+Н]+: 333,1921, найдено 333,1924.
Способ В:
[0089] В Таблице 1 показаны иллюстративные вещества, которые были использованы для получения (R)-трет-бутил 4-(5-метил-7-оксо-6,7-дигидро-5H-циклопента[d]пиримидин-4-ил)пиперазин-1-карбоксилата, в соответствии с описанной выше методикой. Соединение в колонке «Вещество» использовали вместо (R)-трет-бутил 4-(6-йод-5-(4-(метил(фенил)амино)-4-оксобутан-2-ил)пиримидин-4-ил)пиперазин-1-карбоксилата в описанном выше способе, условия реакции представлены в колонке «Масштаб и условия», при этом все остальные условия были по существу такими же. Количество, показанное в колонке «Выход», представляет собой процентную площадь пика циклизованного продукта в неочищенной реакционной смеси, по результатам измерения с помощью ВЭЖХ-МС. Количество, показанное в скобках, представляет собой выделенный выход. Конечный продукт, (R)-трет-бутил 4-(5-метил-7-оксо-6,7-дигидро-5H-циклопента[d]пиримидин-4-ил)пиперазин-1-карбоксилат, не выделяли из описанных ниже реакций.


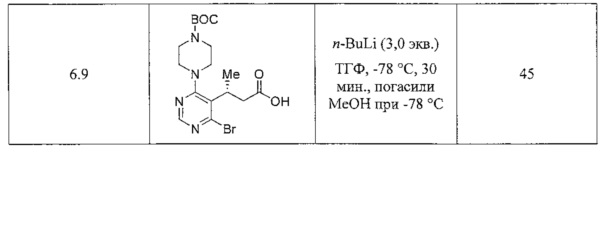
[0090] Эксперименты, описанные в Примерах 1-6а, выполняли в килограммовых масштабах с получением сравнимого или улучшенного выхода.
[0091] Все патенты, патентные заявки, документы и статьи, упомянутые здесь, включены в данный документ посредством ссылки в полном объеме.
Реферат
Изобретение относится к новому способу получения соединения формулы I и его солей. Соединения формулы I могут быть использованы для получения соединений, обладающих свойствами ингибитора АКТ киназы и предназначенных для лечения таких заболеваний, как рак. Способ получения соединения формулы Iвключает циклизацию соединения формулы II или его соли, где Rпредставляет собой трет-бутоксикарбонил; Rпредставляет собой -COOR, где Rпредставляет собой водород или незамещенный Салкил, или Rпредставляет собой -CONRR, где Rпредставляет собой незамещенный Салкил и Rпредставляет собой -OR, фенил; или Rи Rвзяты вместе с атомом, к которому они присоединены, с образованием 5-7-членного гетероциклила, дополнительно включающего атом кислорода; Rпредставляет собой Cалкил; и M представляет собой Li или Mg. При этом используют соединение формулы II или его соль, полученное путем приведения в контакт соединения формулы III или его солигде Rпредставляет собой бром или йод, с магниевым или литиевым металлирующим агентом, например галогенидом алкилмагния. Соединение формулы III получают обычно взаимодействием соединения формулы IV или его соли с соединениемс получением соединения формулы V или его соли, где Rпредставляет собой -Cl или -OH, RRимеют значения, указанные выше. Изобретение также относится к новым промежуточным соединениям - соединению формулы III и соединению формулы IV. Способ позволяет получать продукты в промышленном масштабе с сопоставимым или повышенным выходом и качеством продуктов. 3 н. и 19 з.п. ф-лы, 1 табл., 6 пр.
Формула


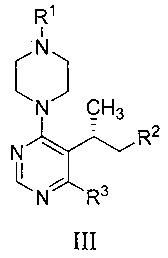




Комментарии