Производные 3(2н)-пиридазинона или их фармацевтически приемлемые соли и фармацевтическая композиция на их основе - RU2054004C1
Код документа: RU2054004C1
Чертежи



Описание
Изобретение относится к новым производным 3(2Н)-пиридазинона и к их фармацевтически приемлемым солям, обладающим ингибиторной активностью по отношению к агрегированию тромбоцитов, кардиотонической активностью, вазодилаторной активностью, противо-SRS-А-активностью, к способам их получения и к фармацевтическим композициям, содержащим их в качестве активного компонента.
Характеристика известного уровня техники:
1) В области веществ,
обладающих противотромботическим действием.
Известно, что агрегирование тромбоцитов играет важную роль в образовании тромбов, связанном с болезненным состоянием. Основными болезнями, которые вызываются образованием тромбов, являются тромбоз головного мозга, тромбоз легких, инфаркт миокарда, закупорка периферийной артерии, стенокардия и т.п. и для лечения всех этих болезней необходимо разрабатывать новые полезные лекарства. Внимание широкой публики привлекло использование в качестве профилактического и терапевтического средства противотромботического агента, обладающего ингибиторной активностью по отношению к агрегированию тромбоцитов. До настоящего времени широко изучено действие аспирина, а не так давно прошли клинические исследования тиклопидин и циклостазол. Однако имеется необходимость в препаратах с более сильным эффектом.
Помимо упомянутых различных, связанных с тромбозом, заболеваний существует ряд заболеваний, связанных с тромбоцитами. Примерами таких заболеваний являются нефрит, метастазы раковых опухолей и т.п. и в последнее время проводились различные исследования, какое профилактическое и терапевтическое действие оказывают на эти заболевания главным образом противотромботические агенты, обладающие способностью контролировать функцию тромбоцитов ("Journal of Poyal College of Physicians", v. 7, N 1, р. 5-18, 1972; "Japan clinics, hihon Rinsho)", v.4, N 6, р. 130-136, 1988; Anticancer Research, vol, 6,р. 543-548, 1986).
2) В области кардиотонических средств.
Кардиотоники, повышающие сократительную силу миокарда, использовались издавна в качестве терапевтического средства против недостатка прилива крови к сердцу. Однако обычные кардиотоники, такие как сердечные гликозиды, представителями которых являются препараты наперстянки-аминофилин и катехоламины, дают сильные побочные эффекты, вследствие чего недавно были разработаны в клиниках такие лекарства, как милринон и денопамин.
3) В области сосудорасширяющих средств
Известно много сосудорасширяющих средств, но в настоящее время имеется только несколько лекарственных препаратов, обладающих
благоприятными фармакологическими характеристиками для кровеносной системы, в частности, удовлетворительной ингибиторной активностью по отношению к агрегированию тромбоцитов.
4) В области средств, обладающих противодействием по отношению к SRS-A.
SRS-A (медленно реагирующая субстанция аллергии) представляют собой химический медиатор, высвобождающийся вместе с гистамином, например, в результате аллергической реакции, и обладающий фармакологической активностью в смысле способности вызывать сильное и продолжительное сокращение гладкой мускулатуры трахеи. Их существование давно известно в таком феноменологическом аспекте.
В 1979 г было обнаружено, что сама SRS-A представляет собой смесь лейкотриена С4 (далее называемого LTC4), лейкотриена D4 (далее называемого LTD4) и лейкотриена Е4 (далее называемого LTE4) [как, правило, называется пептидным лейкотриеном]
Проведены обширные исследования SRS-A в смысле ее связи с болезненным состоянием. В результате стала ясной связь SRS-A с аллергическими заболеваниями немедленного типа, такими как бронхиальная астма,
аллергический ринит, крапивница и сенная лихорадка.
Кроме того, было высказано предположение о связи SRS-A с различными воспалительными заболеваниями, например с ишемической болезнью сердца и т.д.
Таким образом, можно ожидать, что соединение, обладающее ингибиторной активностью по отношению к SRS-A, окажется полезным в качестве профилактического или терапевтического лекарственного средства против расстройств, вызываемых либо LTC4, LTD4 или LTE4, либо их смесями.
Как об антагонистах SRS-A, сообщалось о многих используемых в медицине веществах ("Drugs of the Future", v.12, р.453-474, 1987); "Annual Reoports in Medical chemistry", vol. 22, р.73-84, 1987 и "Annual Reviews in Pharmacological Toxicology", vol. 29, р.123-143, 1989).
Не сообщалось однако, никаких примеров их практического клинического применения.
Далее будет рассмотрена связь 6- ω -замещенных алкилокси-3-(2Н)-пиридазинонов формулы (1) и их фармацевтически приемлемых солей согласно изобретению с соединениями, раскрываемыми в опубликованных источниках.
а) Выложенная заявка Германии N 1 670 169), далее называемая источником (а)), раскрывает 3(2Г)-пиридазиноны, содержащие водород или алифатическую, циклоалифатическую, арилалифатическую или ароматическую группу в 2-положении, хлор или бром в 4-положении, алкиламино-группу в 5-положении и атом хлора или брома либо гидрокси- или С1-С4-алкокси-группу в 6-положении.
Указанный источник (а) раскрывает способ синтеза производных 3(2Н)-пиридазинона, их применение как промежуточных при синтезе медикаментов или красителей, а также применение как промежуточных продуктов синтеза различных соединений. Однако не упоминается об их фармакологической активности и не приводится конкретных примеров таких соединений. Кроме того, такие соединения не описаны конкретно.
(б) Не прошедшая экспертизу заявка на патент Японии N 183675) 1983 (далее упоминаемая как источник (б)) раскрывает производные 3(2Н)-пиридазинона, несущие низшую алкильную группу в 2-положении, атом водорода в 4-положении, замещенную или незамещенную анилиновую группу в положении 5 и гидроксильную группу или низшую алкокси-группу в 6-положении.
Раскрывается, что производные 3(2Н)-пиридазинона обладают анальгезирующим действием, противовоспалительным действием, противоаллергическим действием, противоревматическим действием, но не раскрывается их фармакологическая активность. (в) Не прошедшая экспертизу опубликованная заявка на патент Японии N 30187/1988, выложенная для открытого ознакомления опубликованная заявка на Европатент N 0275997 (далее упоминаемая как источник (в)) раскрывает производные 6-замещенный алкокси-5-замещенный бензиламино-3(2Н)-пиридазинона и их применение в качестве агента, обладающего анти-SPS-A активностью, который в некотором отношении аналогичен соединениям данного изобретения.
В результате обширных исследований было открыто, что производные 3(2Н)-пиридазинона и их фармацевтически приемлемые соли по изобретению, отличающиеся от любого из соединений, описанных в приведенных источниках (а)-(в), представляют собой великолепные соединения в смысле противотромботических агентов, стимуляторов сердечной деятельности, сосудорасширяющих агентов и/или анти-SRS-A агентов, и что они могут входить в качестве активных ингредиентов в профилактические или терапевтические лекарственные препараты для лечения упомянутых различных связанных с тромбозом заболеваний, сердечной недостаточности, гипертонии и/или астмы или аллергических заболеваний немедленного типа. На основании этого открытия было разработано изобретение.
Таким образом, изобретение относится к производным 3(2Н)-пиридазинона и к их фармацевтически приемлемым солям, к способу их получения и к
фармацевтическим композициям, содержащим их в качестве активного ингредиента, причем производное 3(2Н)-пиридазинона описывается следующей общей формулой (1)
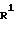
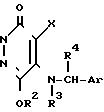
R2 это А1-Y1/A1 это алкиленовая группа С1-С12 с прямой или разветвленной цепью, Y1 это СО2R5 (R5 как определено выше), циано-группа, CR6 (R6 это атом водорода, алкильная группа С1-С4 с прямой или разветвленной цепью либо фенильная группа) или группа тиенила или пиридила, которая может быть замещена в любом положении,
CON
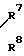
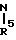
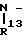

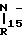
N
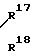
N
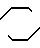

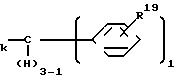
O

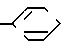
где R3 и R4 соответственно и независимо атом водорода либо прямая или разветвленная алкильная группа С1-С3;
Х это атом хлора, атом брома, атом водорода или цианогруппа; и Ar это
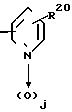
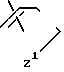
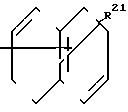
где R21 атом водорода или OR5, где R5 определено выше, или
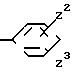
CON
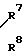
Значения R1, R2, R3, R4, X и Ar в приведенной общей формуле I, описывающей соединение изобретения, будут объяснены ниже.
Примеры R1 включают: атом водорода, метильную группу, этильную группу, н-пропильную группу, изо-пропильную группу, н-бутильную группу, изо-бутильную группу, втор-бутильную группу, трет-бутильную группу, группы: 2-пропенил, 2-метил-2-пропенил, карбоксиметил, 2-карбоксиэтил, 3-карбоксипропил, 4-карбоксибутил, метоксикарбонилметил, 2-метоксикарболнилэтил, 3-метоксикарбонилпропил, 4-метоксикарбонилбутил, этоксикарбонил- метил, 2-этоксикарбонилэтил, 3-этоксикарбонилпропил, 4-этоксикарбонилбутил, н-пропоксикарбонилметил, изо-пропокси- карбонилметил, 2-н-пропоксикарбонилэтил, 2-изо-пропоксикарбонилэтил, 3-н-пропоксикарбонилпропил, 3-изо-пропокси- карбонилпропил, 4-н-пропоксикарбонилбутил, 4-изо-пропоксикарбонилбутил, н-бутоксикарбонилметил, изо-бутоксикарбонилметил, втор-бутоксикарбонилметил, трет- бутоксикарбонилметил, 2-н-бутоксикарбонилэтил, 2-изо-бутоксикарбонилэтил, 2-втор-бутоксикарбонилэтил, 2-трет- бутоксикарбонилэтил, 3-н-бутоксикарбонилпропил, 3-изо-бутоксикарбонилпропил, 3-втор-бутоксикарбонилпропил, 3-трет-бутоксикарбонилпропил, 4-н-бутоксикарбонилбутил, 4-изо-бутоксикарбонилбутил, 4-втор-бутоксикарбонилбутил, 4-трет-бутоксикарбонилбутил и т.п. предпочтительно это атом водорода, этильная группа и изо-пропильная группа, и более предпочтительно атом водорода.
Примеры R2 включают А1-Y1 или A2-Y2, где А1 алкиленовая группа С1 -С12 с прямой или разветвленной цепью, а А2 алкиленовая группа С2-С10, которая может быть замещена алкильной группой С1-С3 с прямой цепью, за исключением случая, когда углеродная цепь, соединяющая атом кислорода с группой Y2, содержит один атом углерода.
Примеры Y1 включают группы: карбоксил, метоксикарбонил, этоксикарбонил, н-пропоксикарбонил, изо-пропоксикарбонил, н-бутоксикарбонил, изо-бутоксикарбонил, втор-бутоксикарбонил, трет-бутоксикарбонил, 2-тиенил, 3-тиенил, 2-пиридил, 3-пиридил, 4-пиридил, циано-группа, гидроксил, метокси-группа, этокси-группа, н-пропокси-группа, изо-пропокси-группа, н-бутокси-группа, изо-бутокси-группа, втор-бутокси- группа, трет-бутокси-группа, фенокси-группа, карбамоил, N-метиламинокарбонил, N-этиламинокарбонил, N-н-пропилами- нокарбонил, N-изо-пропиламинокарбонил, N-н-бутиламинокарбонил, N-втор-бутиламинокарбонил, N-изо-бутиламинокарбонил, трет-бутиламинокарбонил, N-циклопропиламинокарбонил, N-циклобутиламинокарбонил, N-циклопентиламинокарбонил, N-циклогексиаминокарбонил, N-циклогептиламинокарбонил, N-циклооктиламинокарбонил, N-фениламинокарбонил, N-2-тиа- золиламинокарбонил, N-4-тиазолиламинокарбонил, N-5-тиазолиламинокарбонил, N-2-тиадиазолиламинокарбонил, N-5-тиадиазолиламинокарбонил, 1-азиридинокарбонил, 1-азетидинокарбонил, 1-пирролидинокарбонил, 1-пипериди- нокарбонил, 1-гомопиперидинокарбонил, 1-(2,5-диметил)пирролидинокарбонил, 1-(2,6-диметил)пиперидинокарбонил, 1-(3-фенил)-пи- рролидинокарбонил, 1-(4-фенил)пиперидинокарбонил, N-метилсульфониламино-группа, N-этилсульфониламино-группа, N-н-пропилсульфонил, N-изо-пропилсульфониламиногруппа, N-н-бутилсуль- фониламино-группа, N-изо-бутилсульфониламино-группа, N-втор-бутилсульфониламина-группа, N-трет-бутилсуль- фониламино-группа, 1-морфолинокарбонил, N-фенилсульфониламино-группа, замещенная по азоту фенил- сульфониламино-группа (замещенная метилом, этилом, н-пропилом, изо-пропилом, н-бутильной группой, изо-бутильной группой, втор-бутильной группой, трет-бутильной группой, атомом фтора, атомом хлора, атомом брома или атомом йода в орто- мета- или пара-положении бензольного кольца), замещенная фенильная группа (замещенная метильной группой, этильной группой, н-пропильной группой, изо-пропильной группой, н-бутильной группой, изо-бутильной группой, вторбутильной группой, трет-бутильной группой, атомом фтора, атомом хлора, атомом брома, атомом иода, формиламино-группой, ацетиламино-группой, пропиониламино-группой, бутириламино-группой, метилсульфониламино-группой, этилсульфониламино-группой, N-н-пропилсульфониламино-группой, N-изо-пропилсульфониламино-группой, N-н-бутилсульфониламино-группой, N-изо-бутилсульфониламино-группой, N-втор-бутилсульфониламино-группой, N-трет-бутилсульфониламино-группой, N-фенилсульфониламиногруппой, гидрокси-группой, метокси-группой, этокси-группой, н-пропокси-группой, изо-пропокси-группой, изо-бутокси-группой, н-бутокси-группой, втор-бутокси-группой, трет-бутокси-группой, замещенной по азоту фенилсульфониламино-группой (которая замещена метильной группой, этильной группой, н-пропильной группой, изо-пропильной группой, н-бутильной группой, изо-бутильной группой, втор-бутильной группой, трет-бутильной группой, атомом фтора, атомом хлора, атомом брома или атомом иода в орто-, мета- или пара-положении бензольного кольца), метилтио-группой, этилтио-группой, н-пропилтио-группой, изопропилтио-группой, н-бутилтио-группой, изо-бутилтио-группой, втор-бутилтио-группой, трет-бутилтио-группой, метилсульфоксигруппой, этилсульфокси-группой, н-пропилсульфокси-группой, изо-пропил- сульфокси-группой, втор-бутилсульфокси-группой, н-бутилсульфокси-группой, изо-бутилсульфокси-группой, трет-бутилсульфокси-группой, метилсульфонильной группой, этилсульфонильной группой, н-пропилсульфонильной группой, изо-пропилсульфонильной группой, н-бутилсульфонильной группой, втор-бутилсульфонильной группой, изо-бутилсульфонильной группой, втор-бутилсульфонильной группой, изо-бутилсульфонильной группой, или третбутилсульфонильной группой в орто-, мета- или пара-положении бензольного кольца), N-фенилкарбониламино-группа, 1-(2-оксо) азетидинил, 1-(2-оксо)-пирролидинил, 1-(2-оксо-пиперидинил, 1-(2-оксо)гомопиперидинил, 1-(2-оксо-3,3-диметил)пирролидинил, 1-(2-оксо-5,5-диметил)пирролидинил, N-метокси- карбониламино-группа, N-этоксикарбониламино-группа, N-н-пропоксикарбониламино-группа, N-изо-пропоксикар- бониламино-группа, N-н-бутоксикарбониламино-группа, N-изо-бутоксикарбониламино-группа, N-втор-бутоксикар -бониламино-группа, N-трет-бутоксикарбониламино-группа, 3-(2-оксо)-оксазолидинил, 3-(2-оксо-5,5-диметил)оксазолидинил, 3-2(2-оксо-4,4-диэтил)оксазолидинил, 3-(2-оксо-5,5-диэтил)оксазолидинил, N,N-двузамещенная амино-группа (включающая необязательное сочетание метильной группы, этильной группы, н-пропильной группы, н-бутильной группы, вторбутила и группы трет-бутила), 1-азетидино-группа, 1-пирролидино-группа, 1-пиперидино-группа, 1-(2,5-диметил)пирролидино-, 1-(3,4-диметил)пирролидино-, 1-(4,4-диметил)пиперидино-, 1-(4-фенилметил)пиперадино-, 1-(4-дифенилметил)пипе- радино-группа, 1-(4-замещенный фенилметил)пиперадинил или 1-(4-двузамещенный фенилметил)пиперадинил (замещенный атомом фтора, атомом хлора, атомом брома или атомом иода в орто- мета- или пара-положении бензольного кольца), группа фениламинокарбоксила, группа N,N-двуза- мещенного аминокарбонила (включающая необязательное сочетание линейной или циклической алкильной группы, фенильной группы, группы тиазолила или тиадиазолила в вышеописанных N-замещенных аминокарбонильных группах), N-алкил-N-фенилсульфониламино-, N-N-диалкил- сульфониламино- или N-алкил-N-алкоксикарбониламино-группа (несущие линейный или разветвленный С1-С4-алкильный заместитель на атоме азота описанной N-фенилсульфониламино-, N-алкилсуль- фониламино- или N-алкоксикарбониламино-группы), двузамещенные фенильные группы (которые замещены в орто-, мета- или пара-положении бензольного кольца необязательным сочетанием атома галогена, линейной алкильной группы, ациламино-группы, гидрокси-группы, алкокси-группы, N-фенилсульфониламино-группы, N-алкилсульфониламино-группы, в вышеописанных замещенных фенильных группах) и т.п.
Примеры Y2 включают фенильную группу.
Примеры R3 и R4 включают атом водорода, группу метила, группу этила, группу н-пропила и группу изо-пропила, предпочтительно R3 и R4представляют собой атом водорода.
Примеры Х включают атом водорода, атом хлора, атом брома и циано-группу, в предпочтительном варианте каждый заместитель отличен от атома водорода.
Примеры Ar включают группу 2-пиридила, группу 3-пиридила, группу 4-пиридила, группы замещенного 2-пиридила, 3-пиридила или 4-пиридила (замещенного атомом фтора, атомом хлора, атомом брома и атомом иода, метокси-группой, этокси-группой, н-пропокси-группой, изо-про- покси-группой, н-бутокси-группой, изо-бутокси-группой, втор-бутокси-группой или трет-бутокси-группой в 2-, 3-, 4-, 5- или 6-положении пиридинового кольца, группу N-оксидопиризила, соответствующую описанным группам пиридила или замещенного пиридила, группу 2-фурила, группу 2-фурила, группу 2-тианила, группу 3-тианила, группу 1-нафтила, группу 2-нафтила, группы 1-нафтила, или 2-нафтила (замещенные гидрокси-группой, метокси-группой, этокси-группой, н-пропокси-группой, изо-пропокси-группой, н-бутокси-группой, изо-бутокси-группой, втор-бутокси-группой или трет-бутокси-группой в необязательном положении нафталинового кольца) либо замещенные фенильные группы, несущие один или два заместителя в необязательном сочетании в необязательном положении. Примеры заместителей включают атом водорода, атом фтора, атом хлора, атом брома, атом иода, группу метила, группу этила, группу н-пропила, группу изо-пропила, группу н-бутила, группу изо-бутила, группу втор-бутила, группу трет-бутила, гидрокси-группу, алкокси-группу, содержащую линейную или разветвленную алкильную группу С1-С8, группу диоксиэтилена, 1,2-диоксиэтилена или 1,3-диоксипропилена (которая представляет собой два соседних заместителя, соединенных вместе) или группу 0-А1-Y3. А1 представляет собой линейную или разветвленную алкиленову группу С1-С10, Y3 фенильная группа, замещенная фенильная группа, [замещенная метильной группой, этильной группой, группой н-пропила, группой изо-пропила, группой н-бутила, группой изо-бутила, группой втор-бутила, группой трет-бутила, атомом фтора, атомом хлора, атомом брома или атомом иода в орто-, мета- или пара-положении бензольного кольца] либо упомянутая (в связи с Y1) группа карбоксила, алкоксикарбонила, 1-циклоаминокарбонила, 1-морфолинокарбонила или карбамоила, группу N-замещенного или N, N-двузамещенного аминокарбонила, несущая на атоме азота необязательное сочетание двух заместителей, которыми могут быть атом водорода, линейная, разветвленная или циклическая алкильная группа, фенильная группа, группа тиазолила и группа тиадиазолила. Предпочтительные примеры включают группу 3-пиридила или группу типа 3-замещенного-4-метоксифенила, но не следует ограничивать данное изобретение этими примерами.
В приведенном описании "h", "изо", "втор" и "трет" заменяют, соответственно, "нормальный", "изо", "вторичный" и "третичный".
Предпочтительные соединения среди соединений, отвечающих общей формуле (I) изобретения, описываются следующей общей формулой IC,
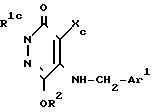
R2 A1 Y3', A1 представляет собой алкиленовую группу С1-С12 с прямой или разветвленной цепью; Y3' СО2R5, R5 алкильная группа С1-С4с прямой или разветвленной цепью),
CON
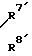
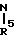
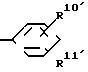
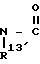
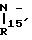
N
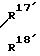
N

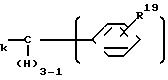
или
O

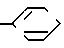
Хс' это атом хлора, атом брома, или циано-группа; и
А' это группа 3-пиридила или
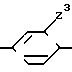
CON
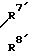
Соединения общей формулы I согласно изобретению включают оптические изомеры и стереоизомеры на основе 1-6 асимметричных атомов углерода.
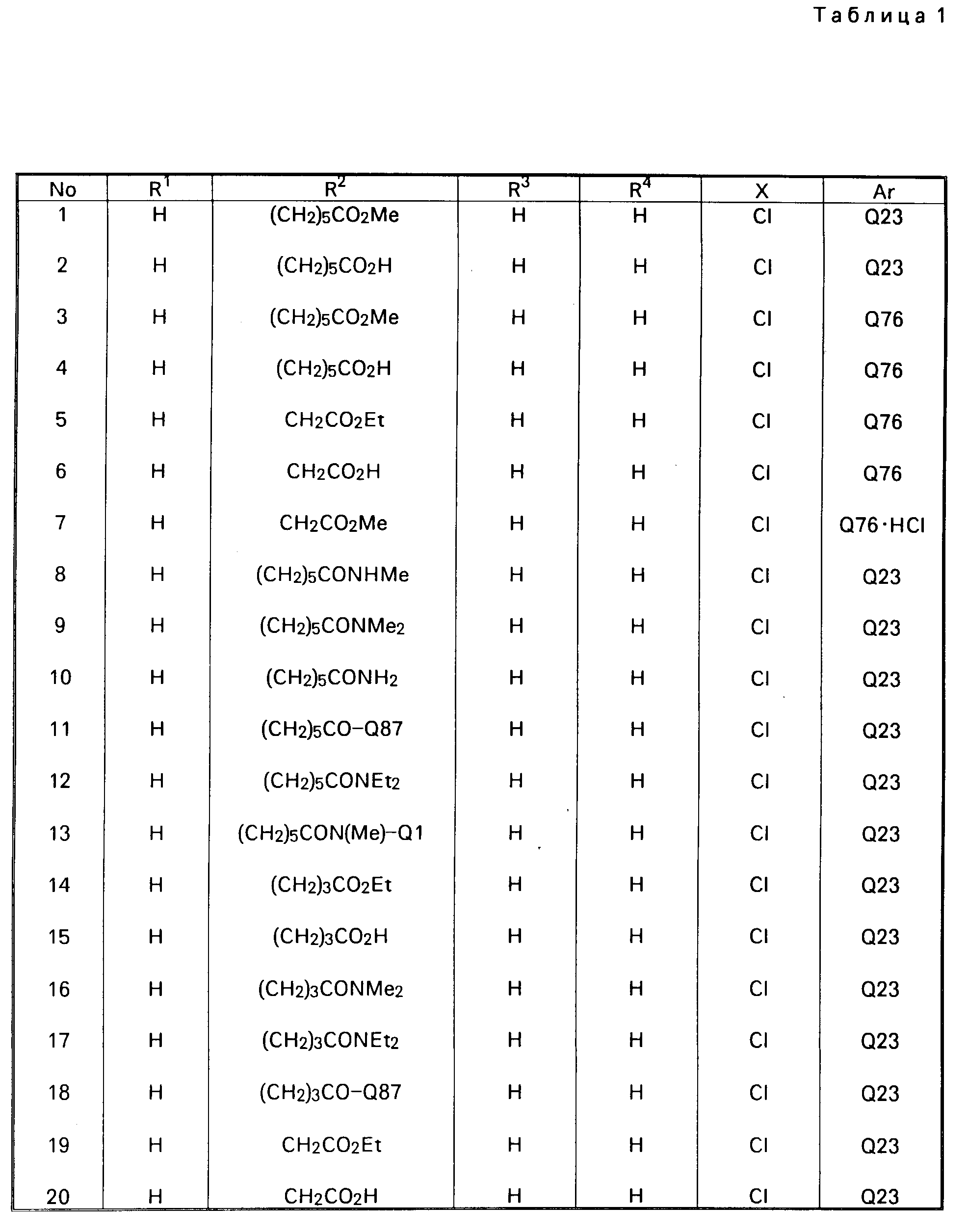
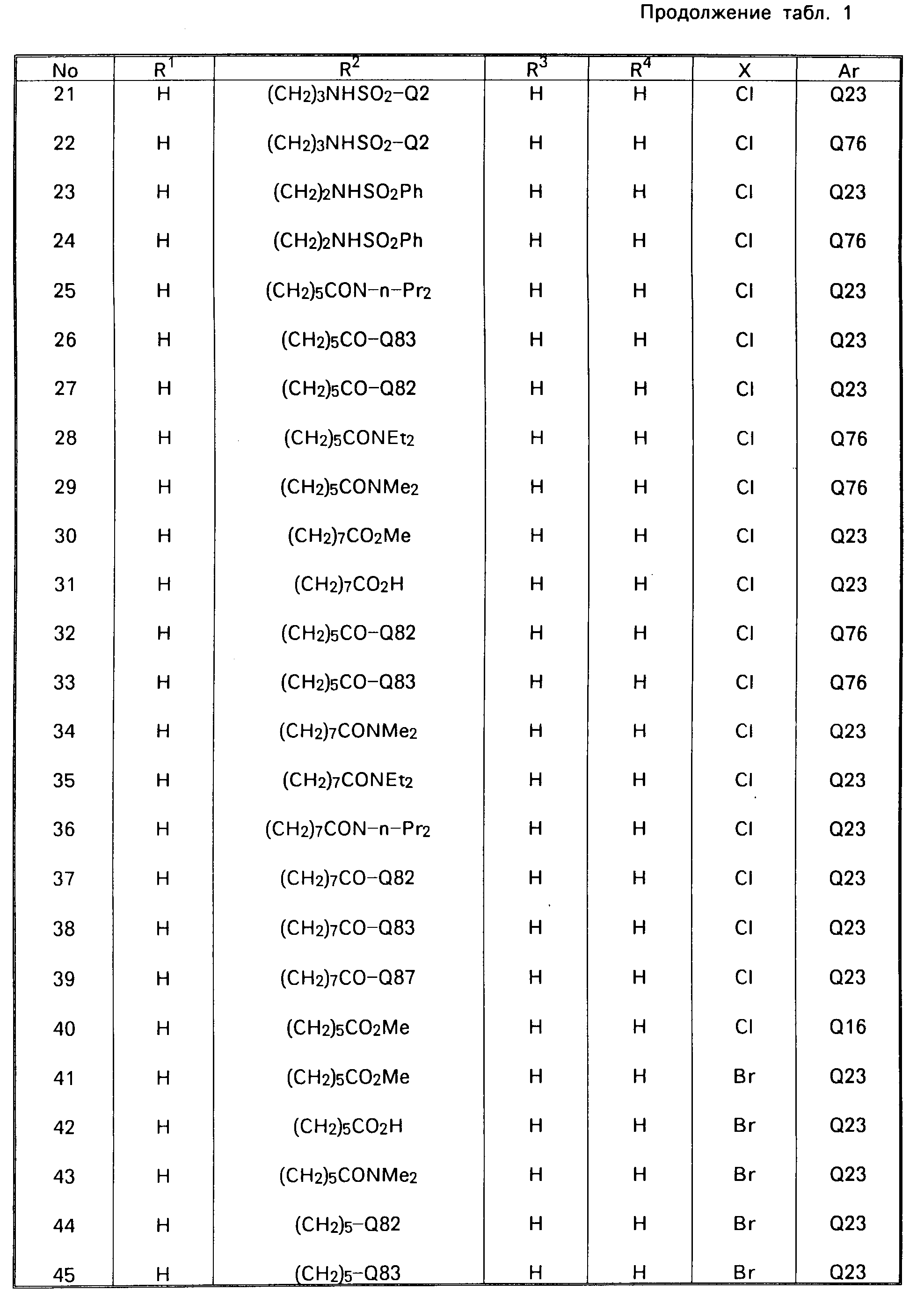
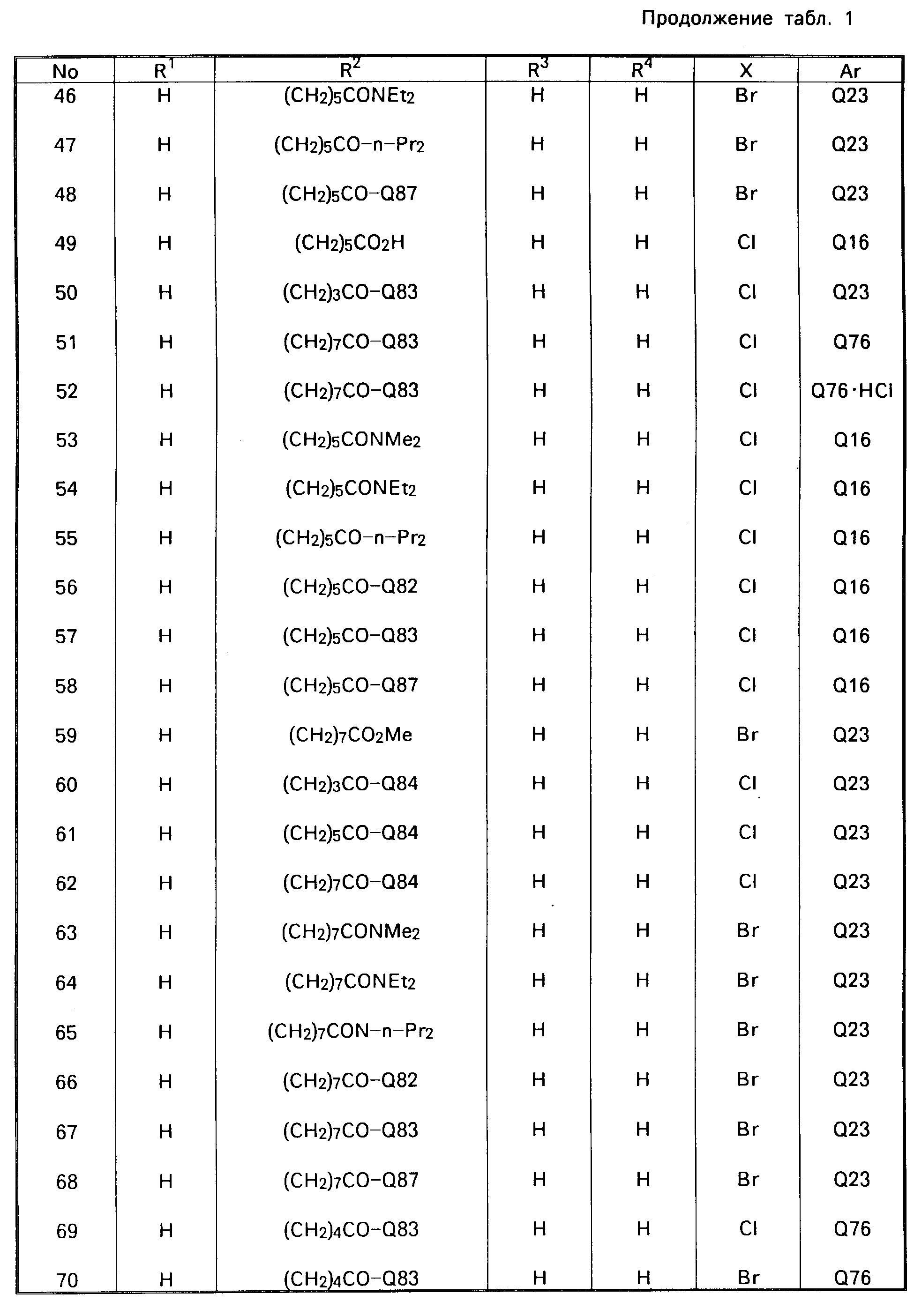
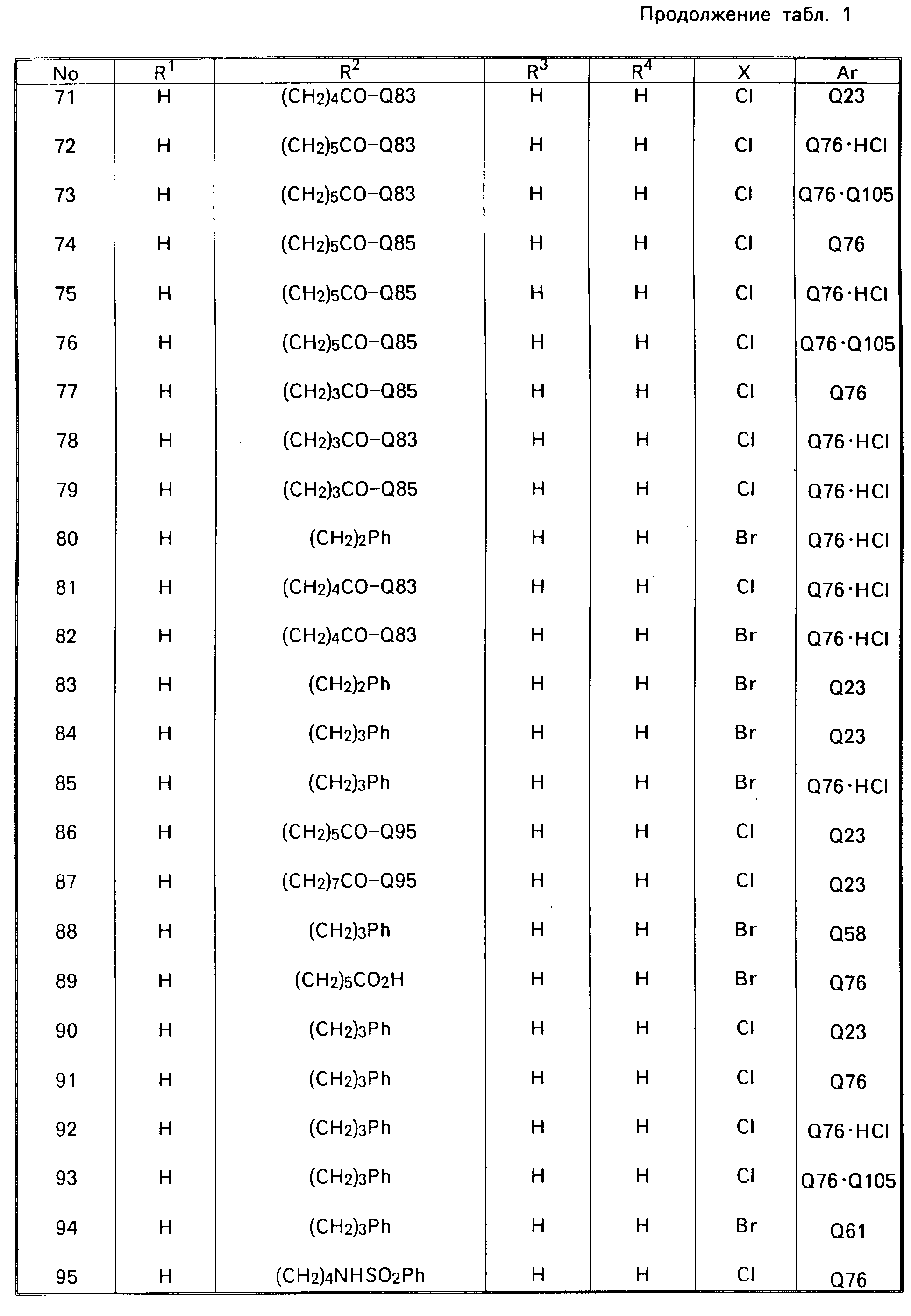
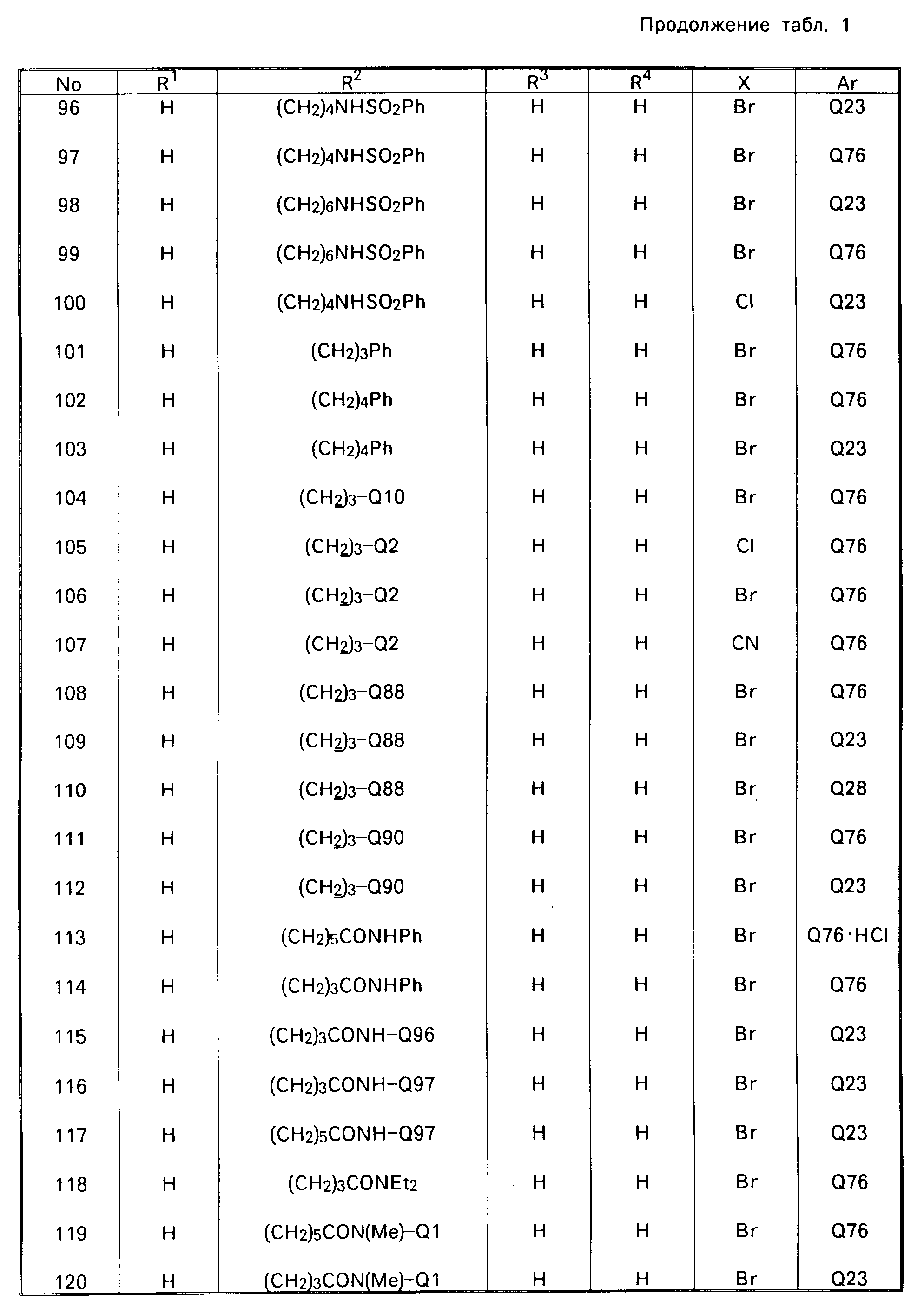
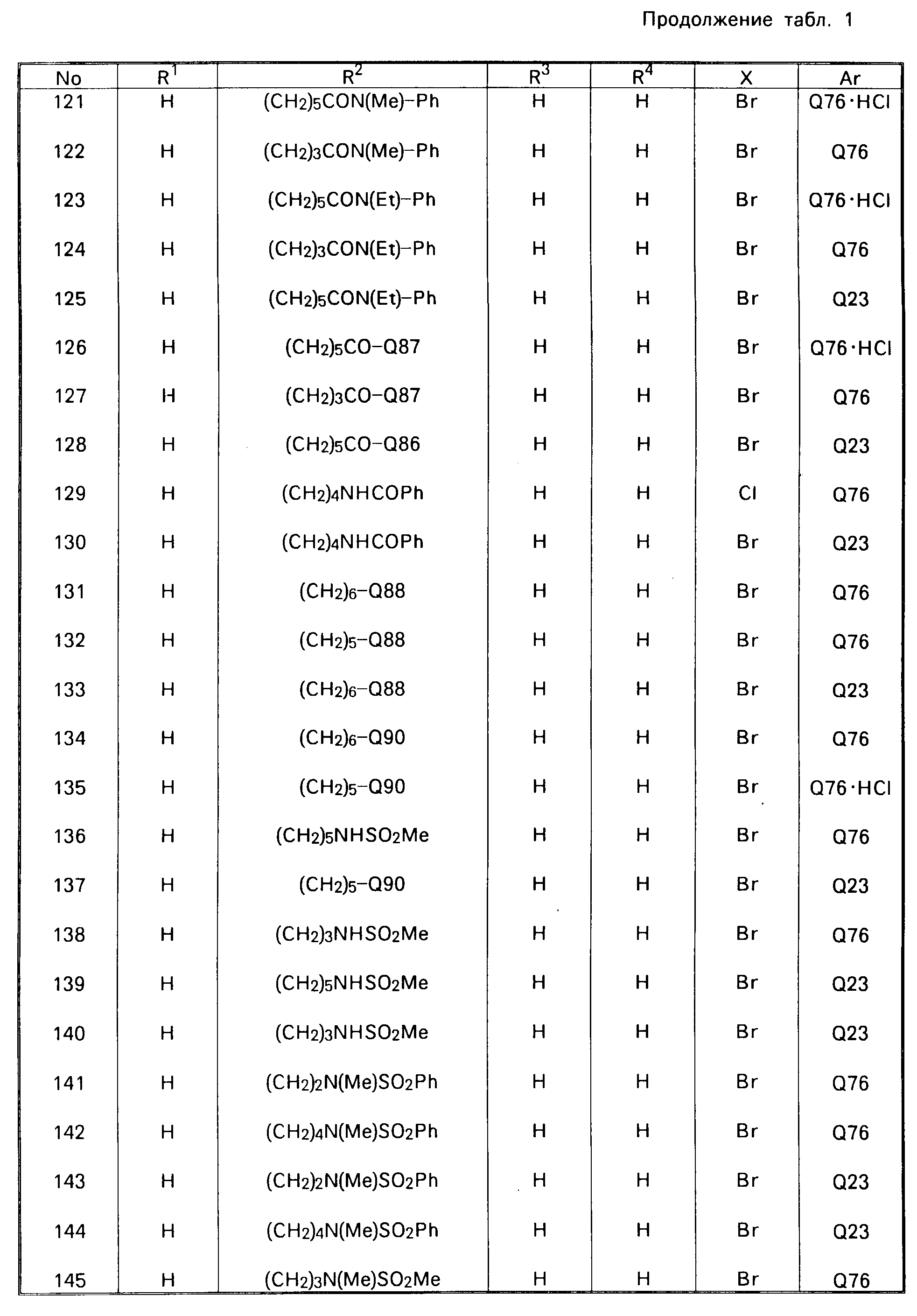
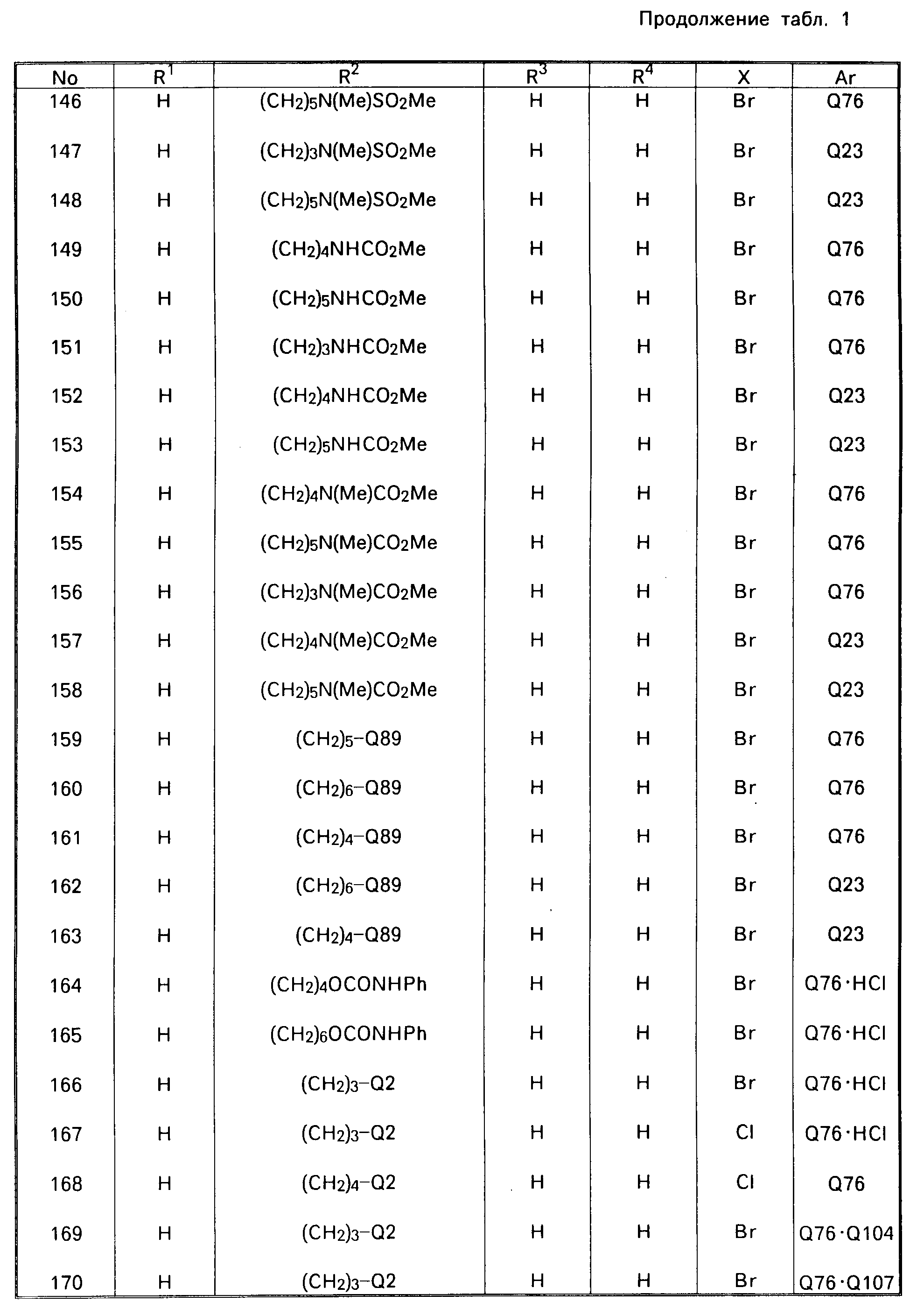
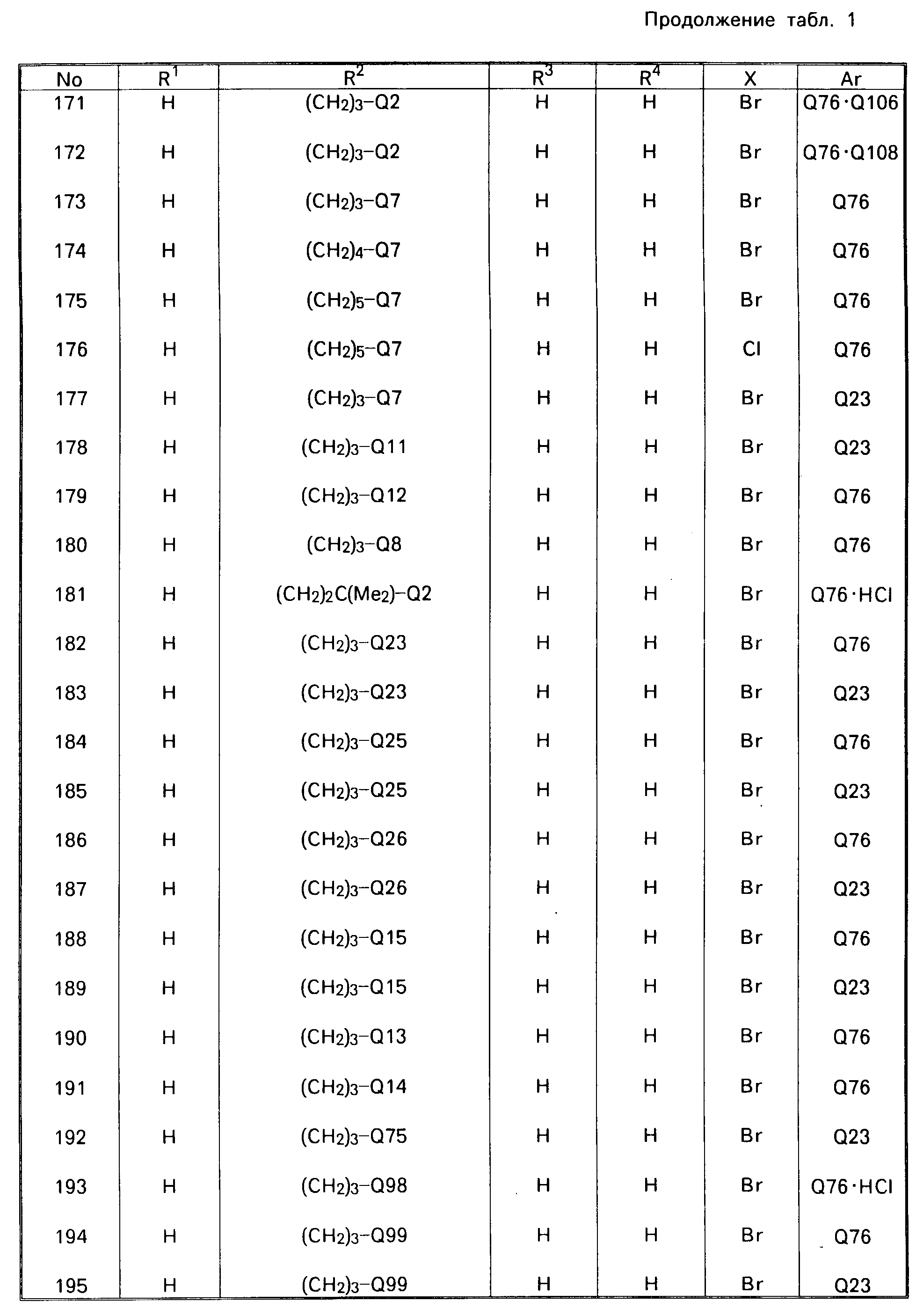
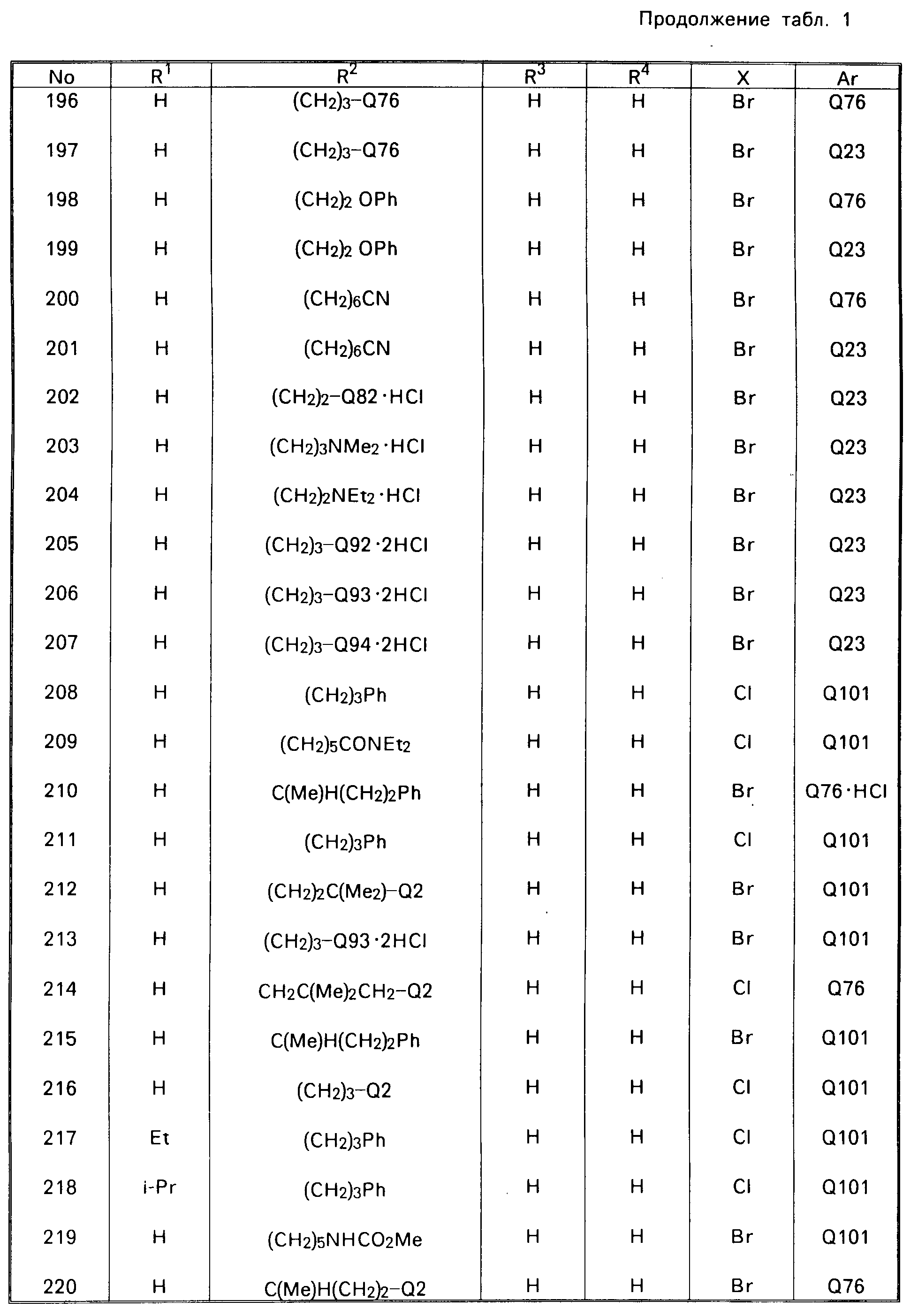
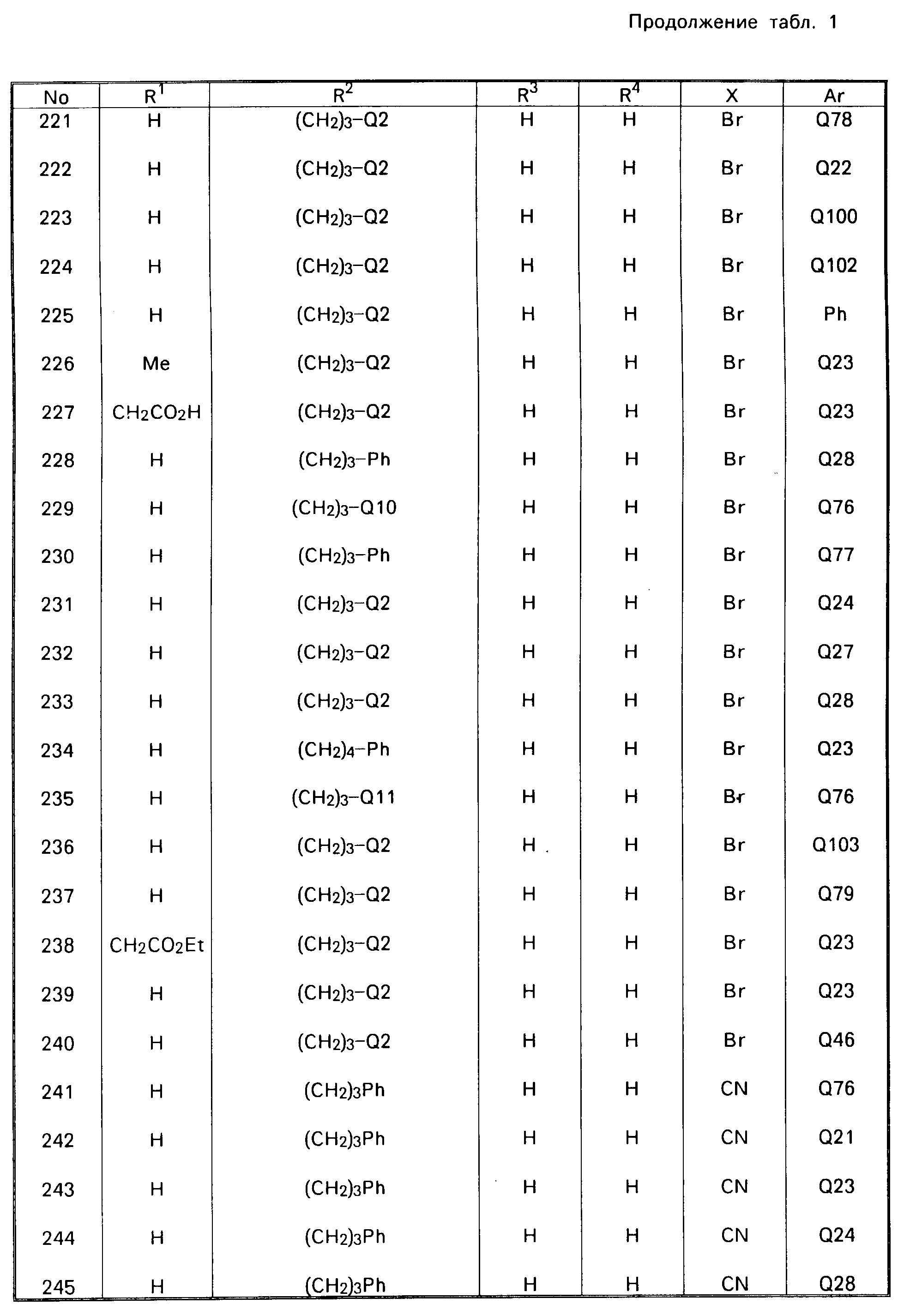
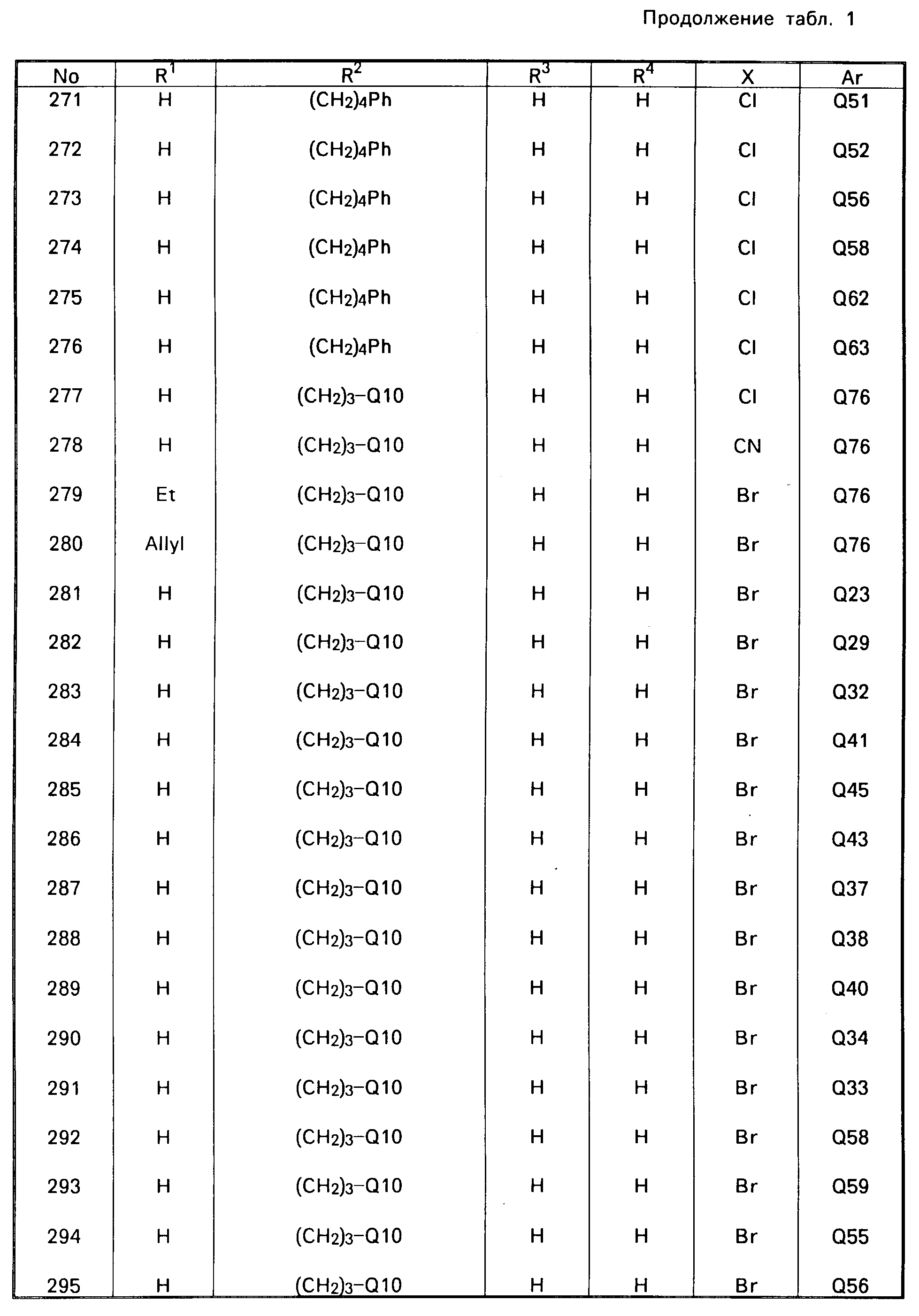
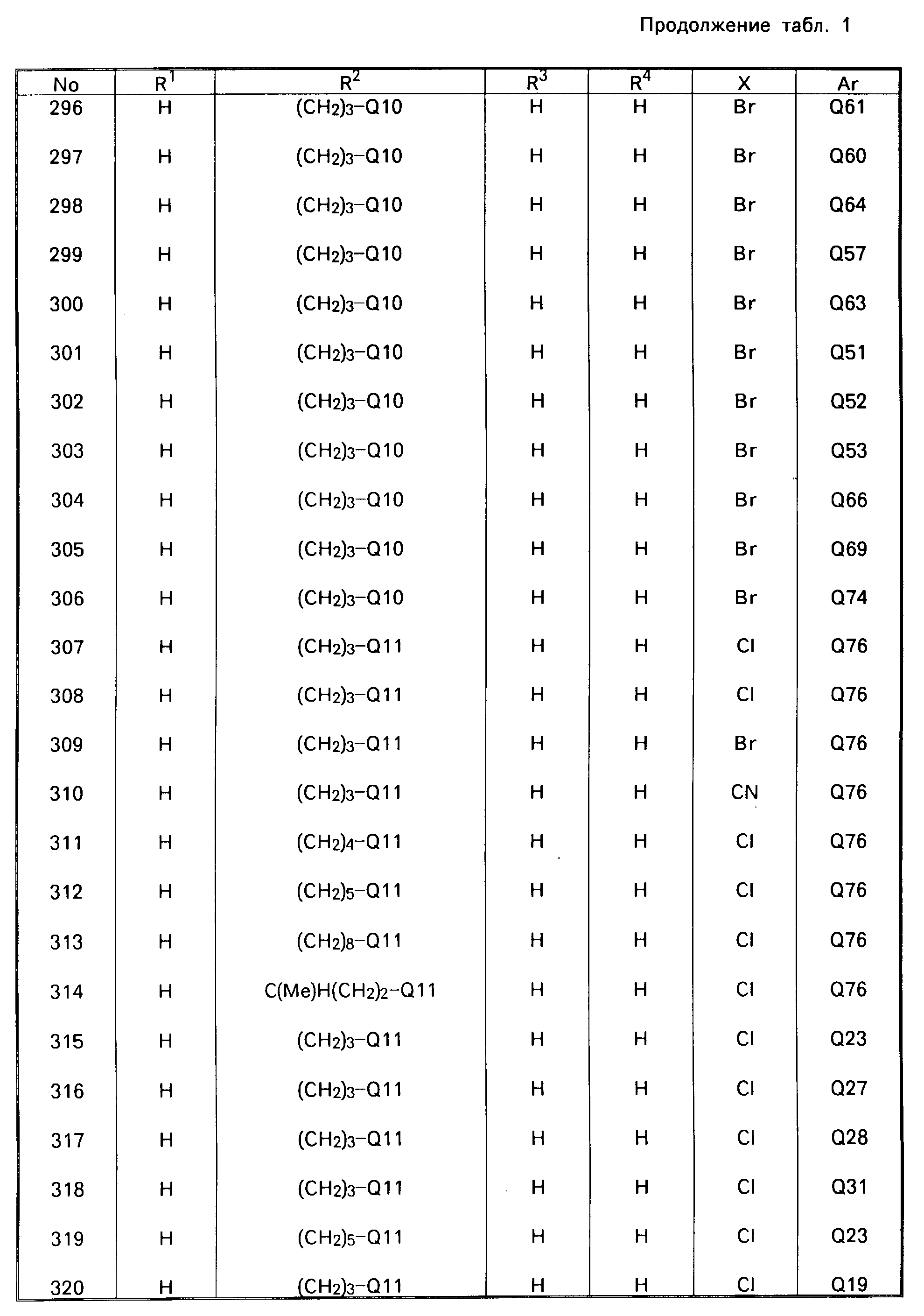
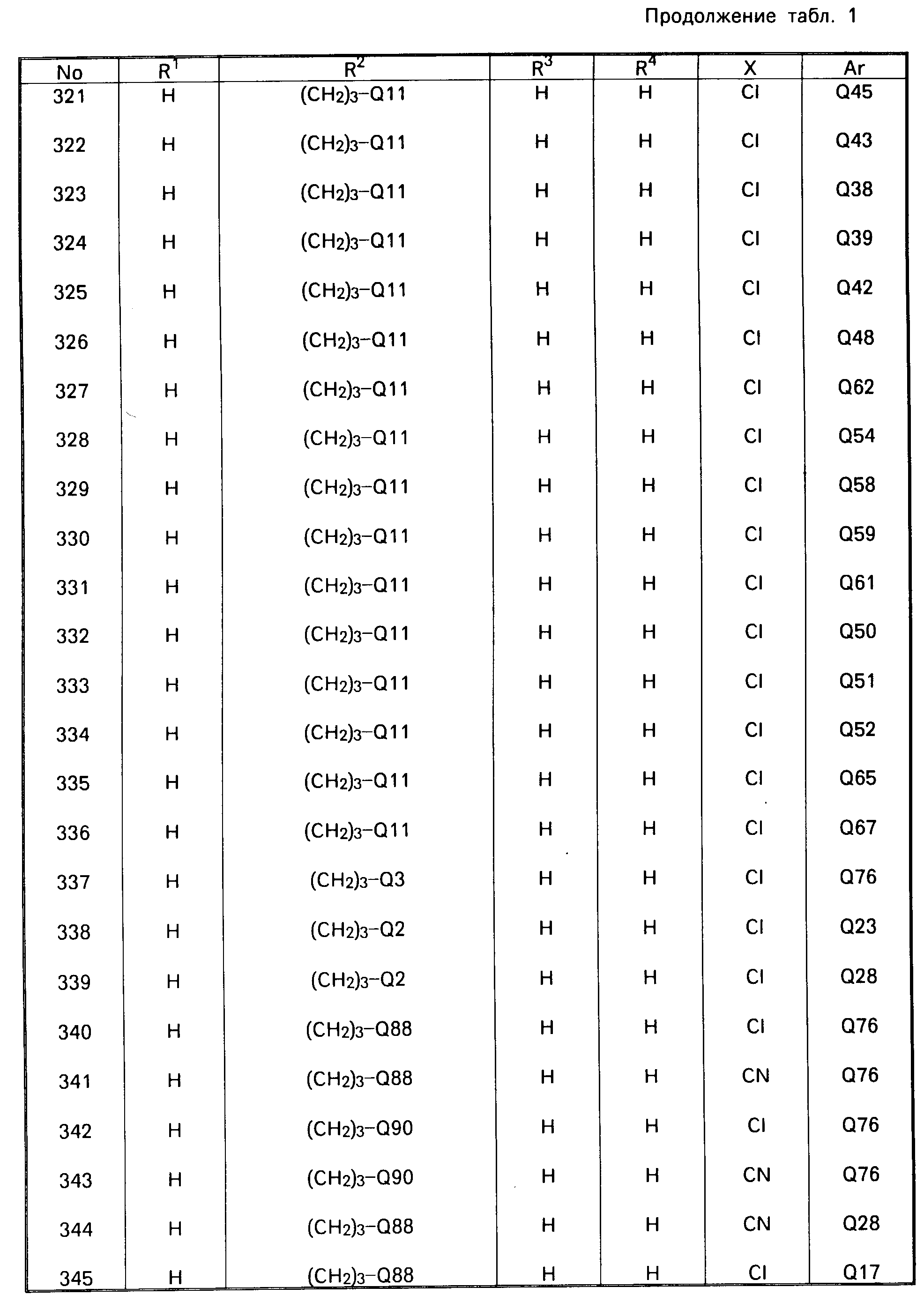
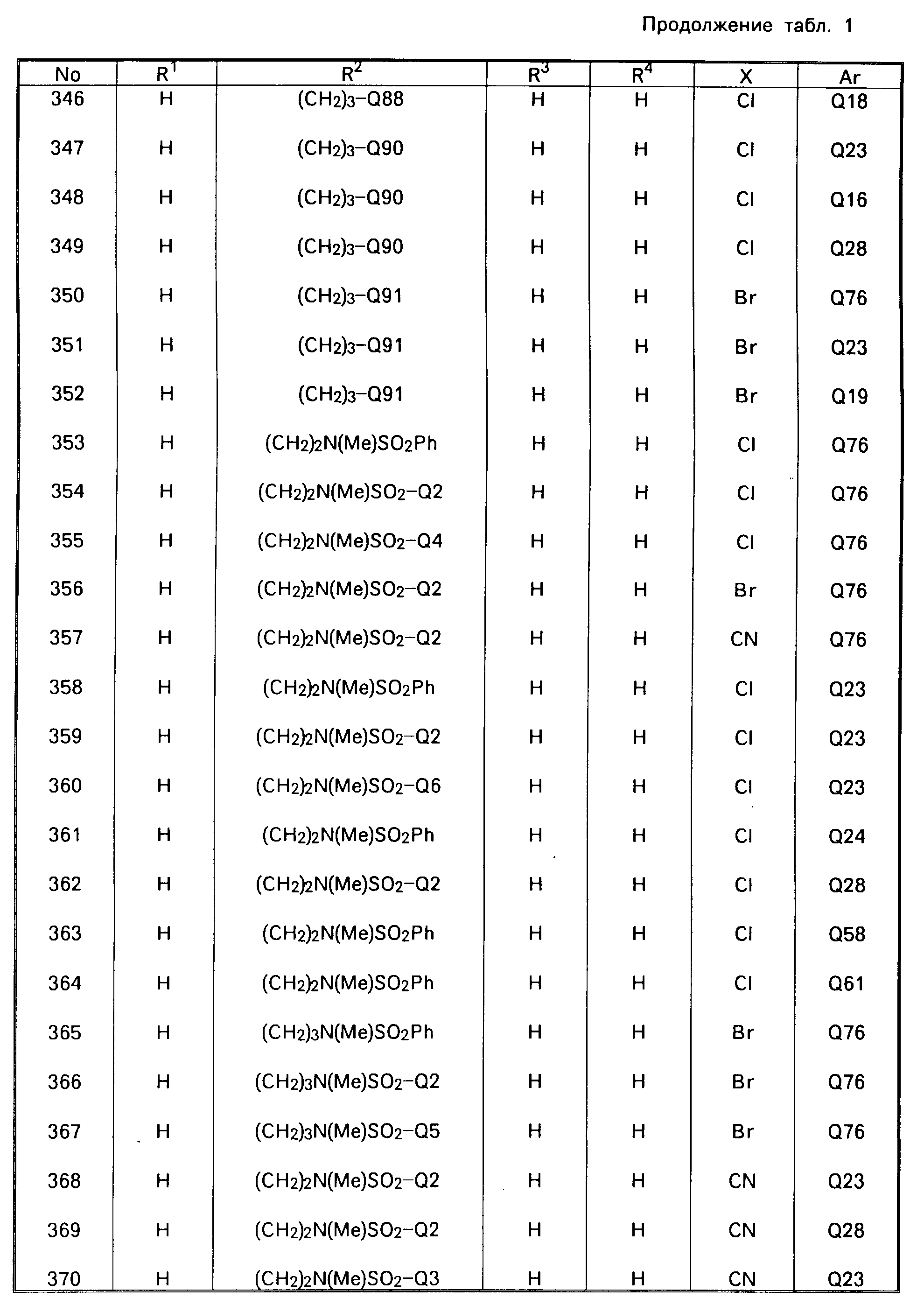
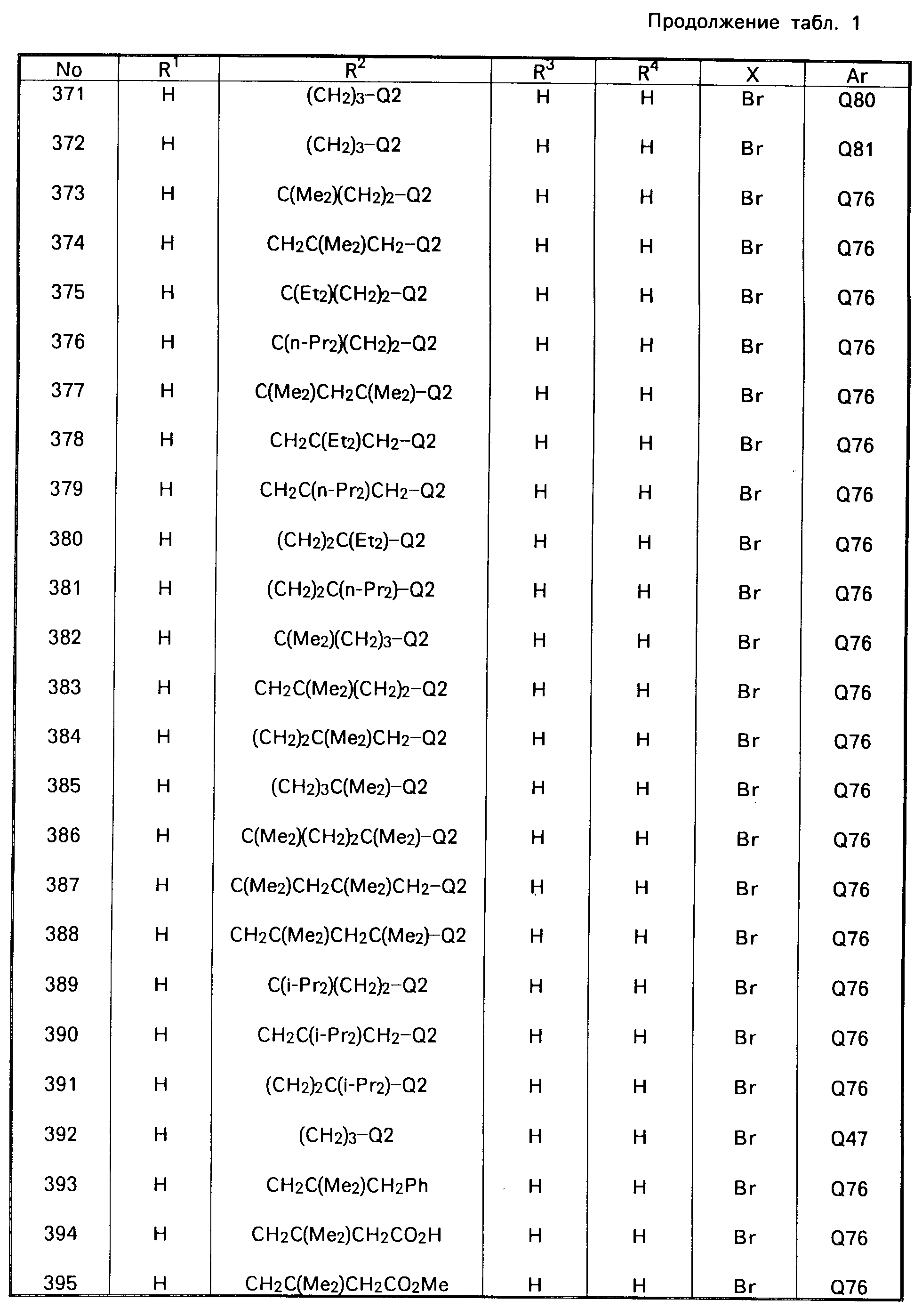
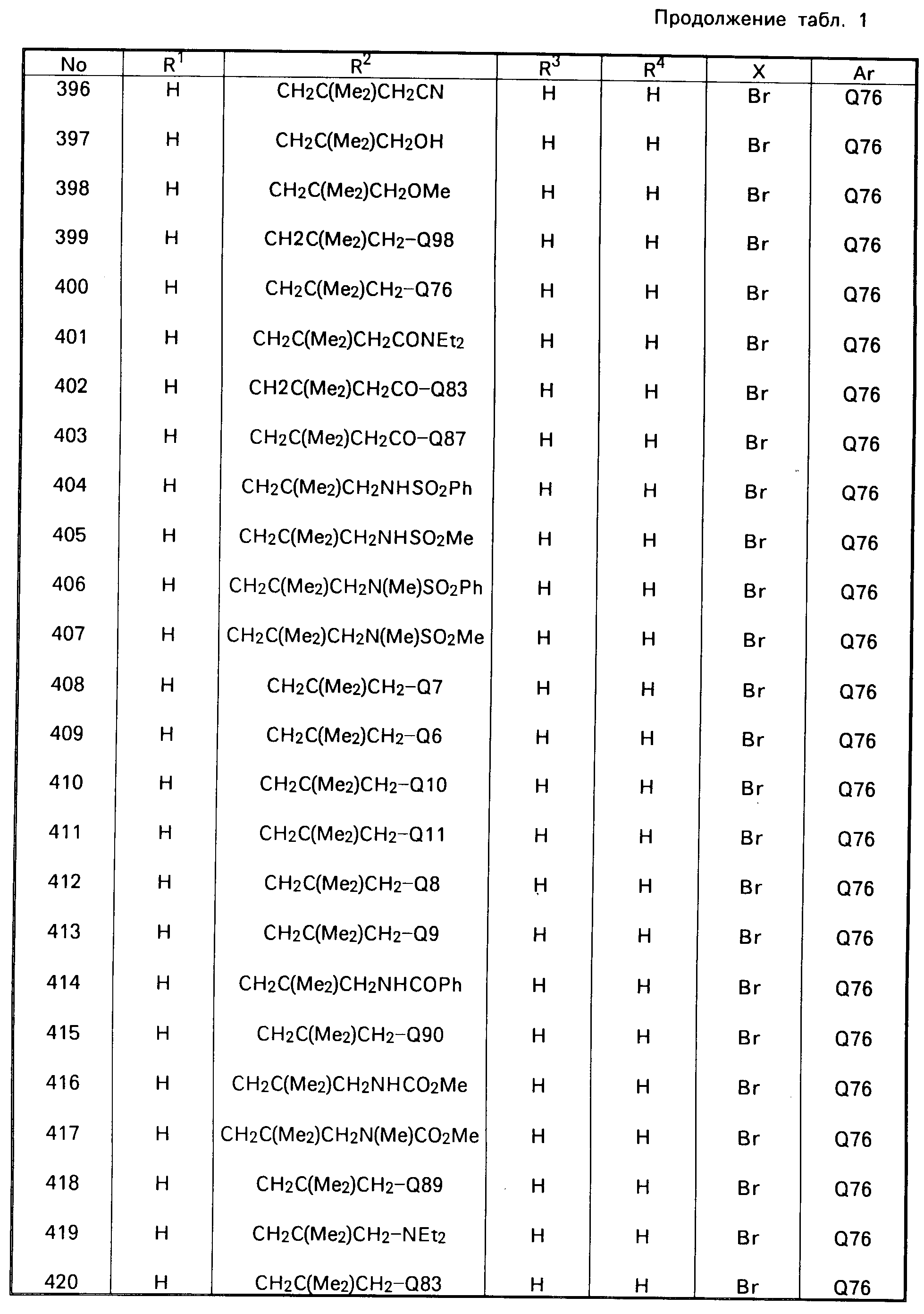
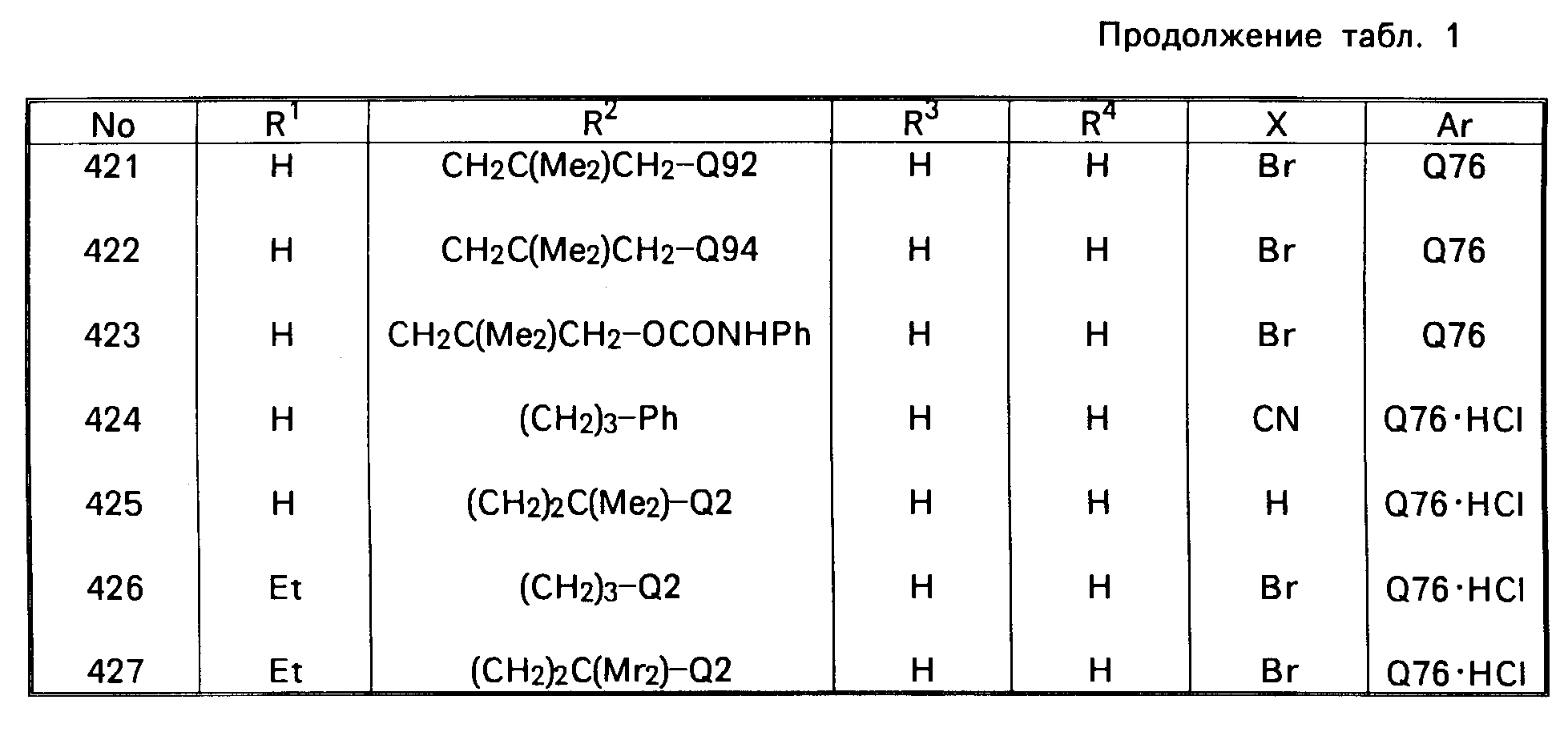
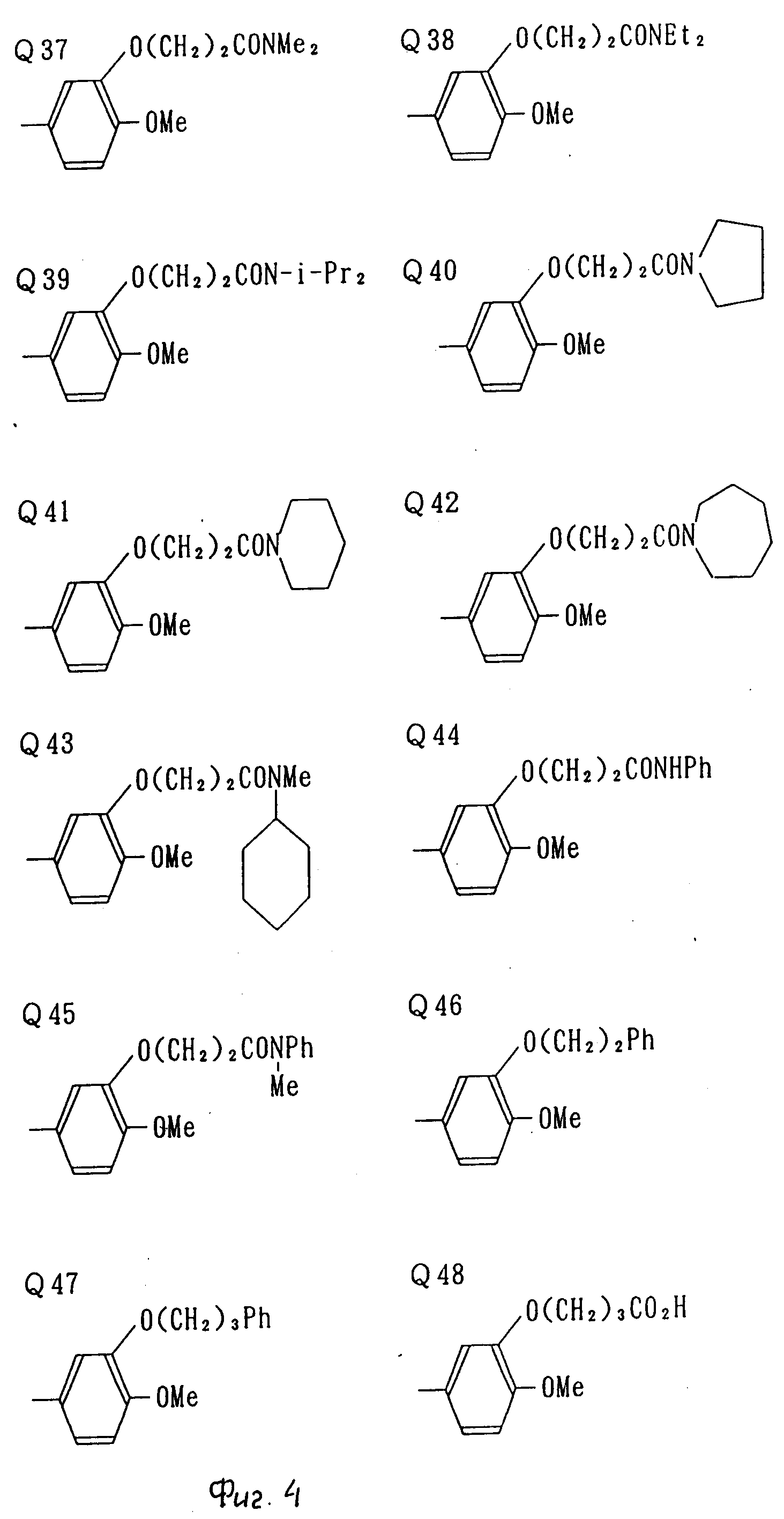
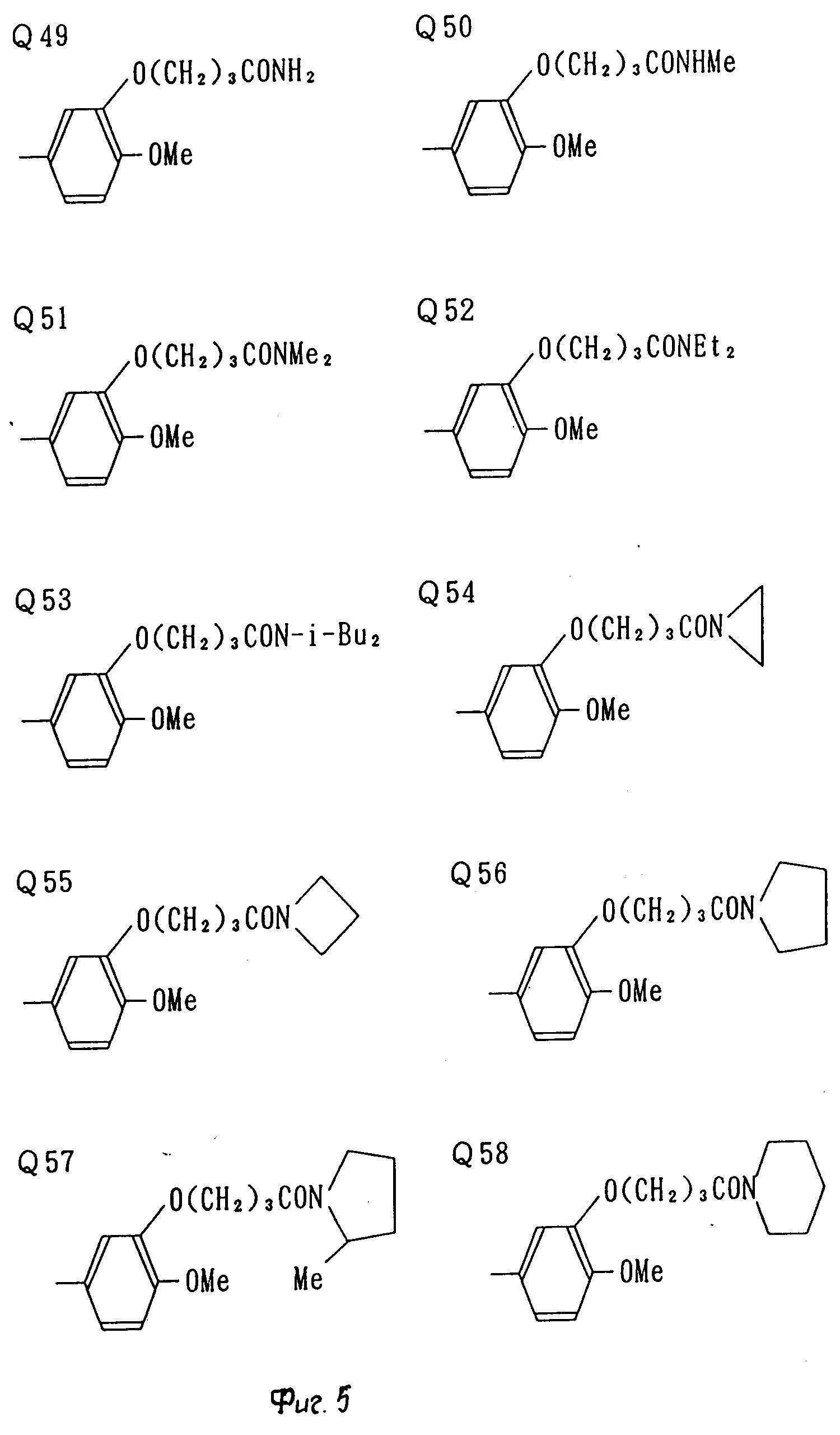
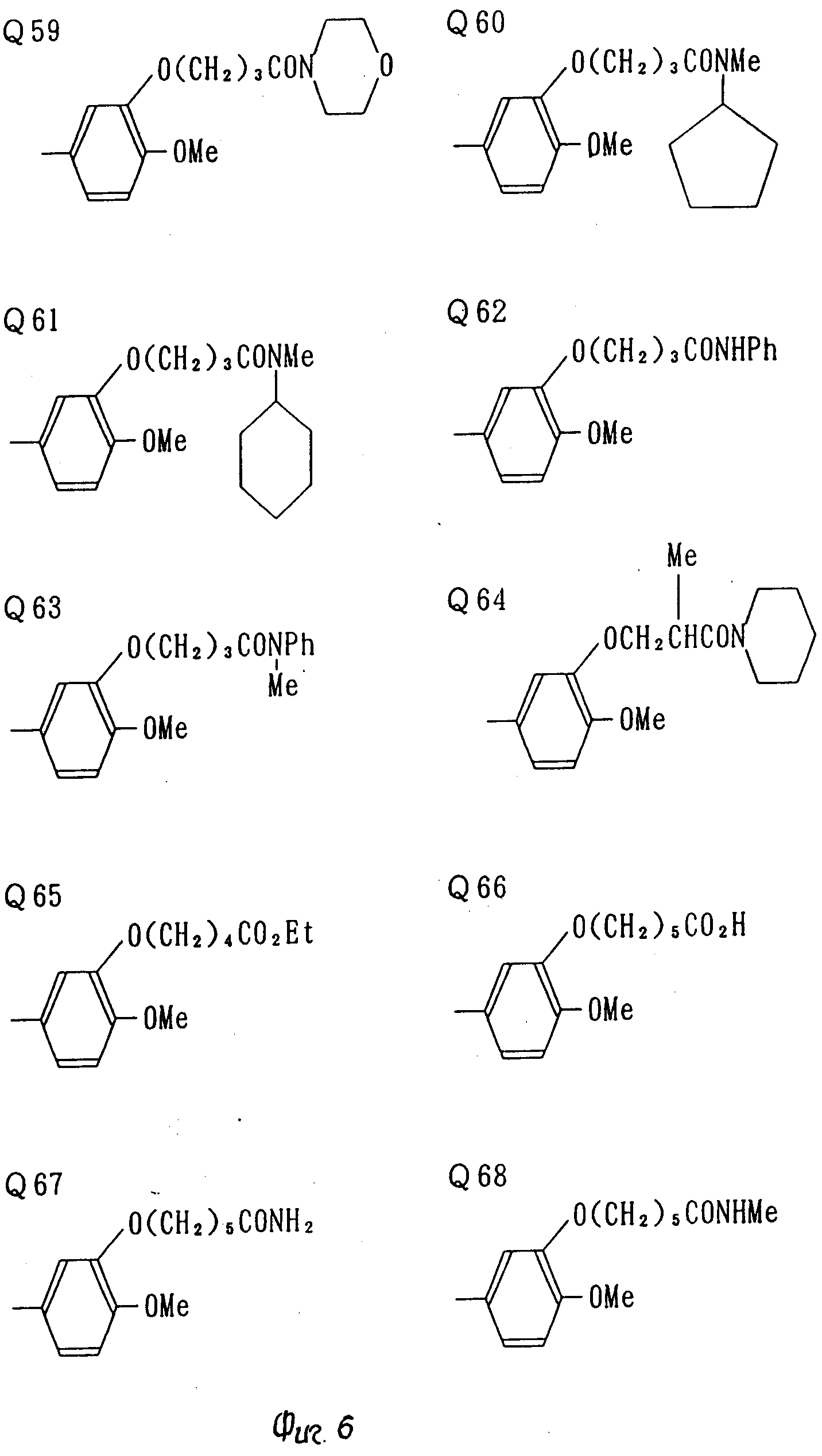
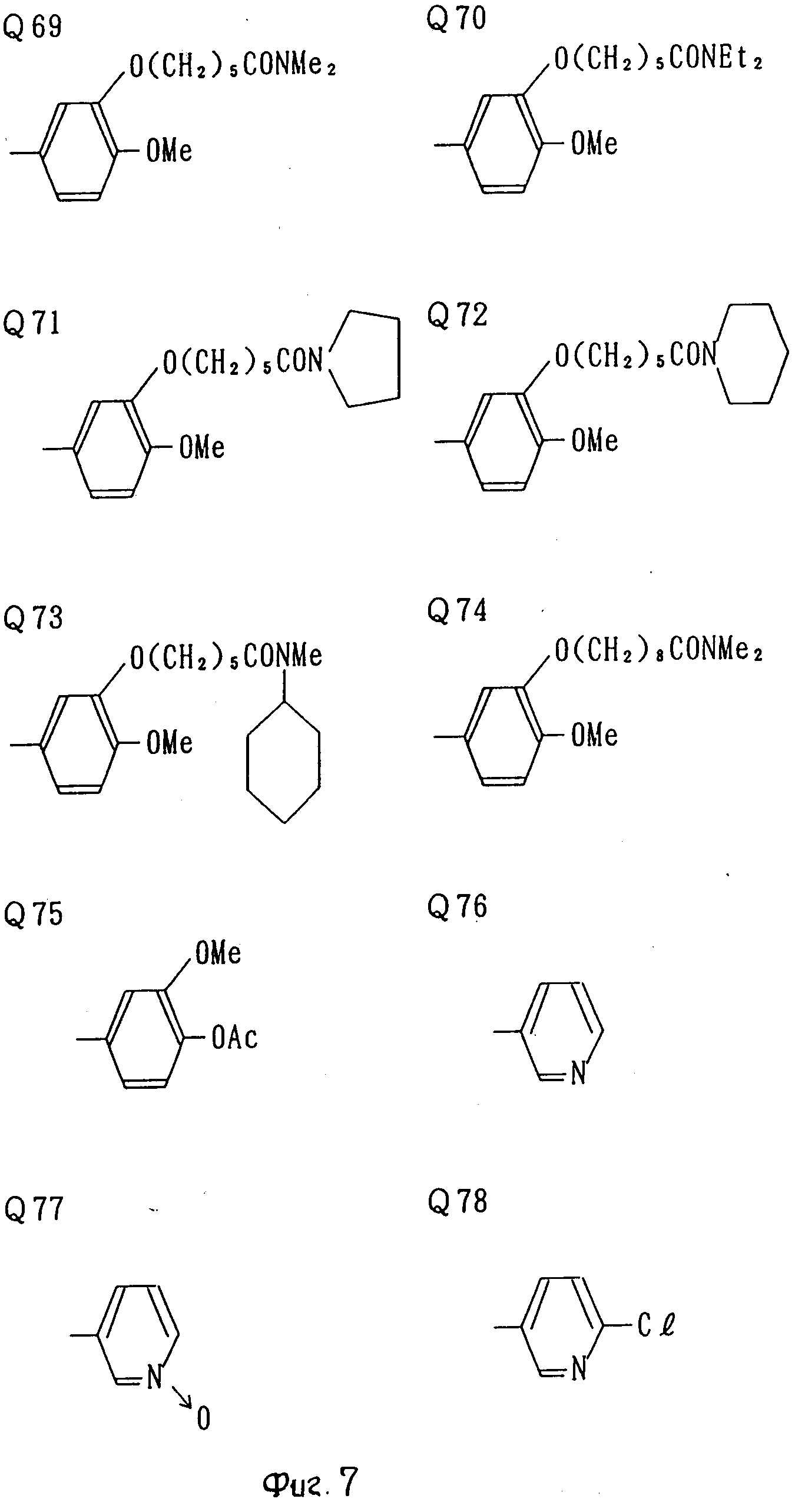
В табл. 1 приводятся типичные представители соединений, являющихся производными, являющихся производными 3(2Н)-пиридазинона общей формулы I и их фармацевтически приемлемых солей согласно изобретению, но не следует ограничивать изобретение только приведенными соединениями.
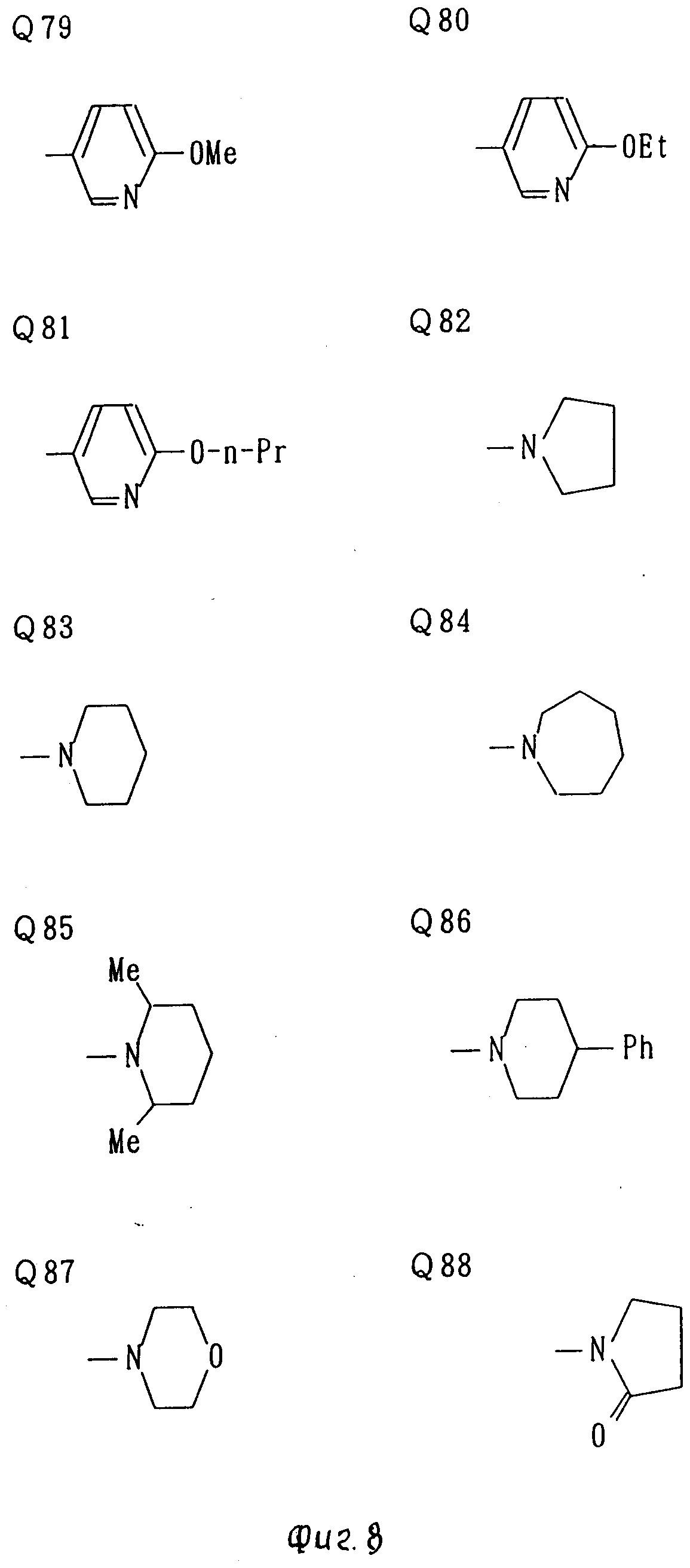
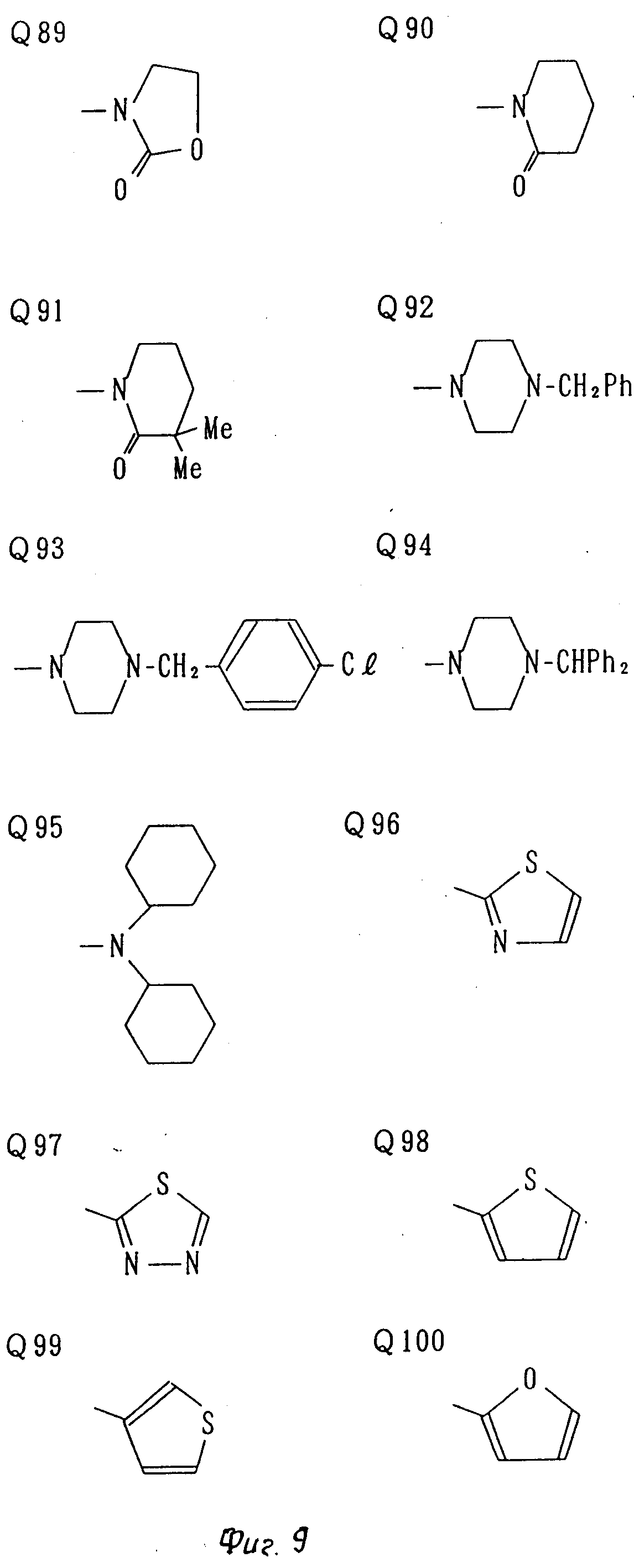
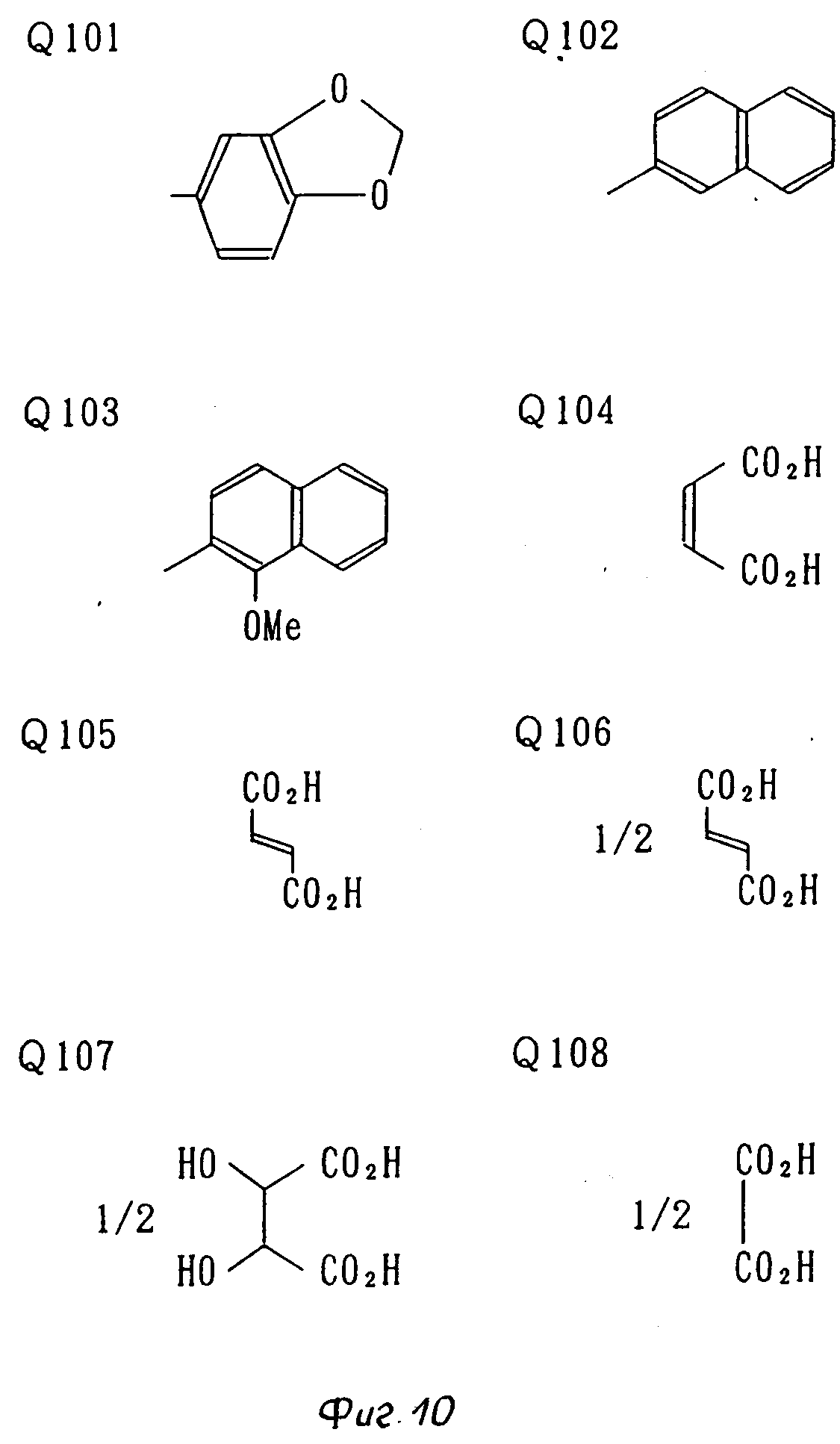
В таблице 1: "n" обозначает нормальный, "i" обозначает изо "sec" обозначает вторичный, "Ме" обозначает метильную группу, "Et" обозначает этильную группу, "Pr" обозначает группу пропила, "Bu" обозначает группу бутила, "Pen" обозначает группу пентила, "Hex" обозначает группу гексила, "Hep" обозначает группу гептила, "Oct" обозначает группу октила, "Ас" обозначает группу ацетила и "Ph" обозначает фенильную группу.
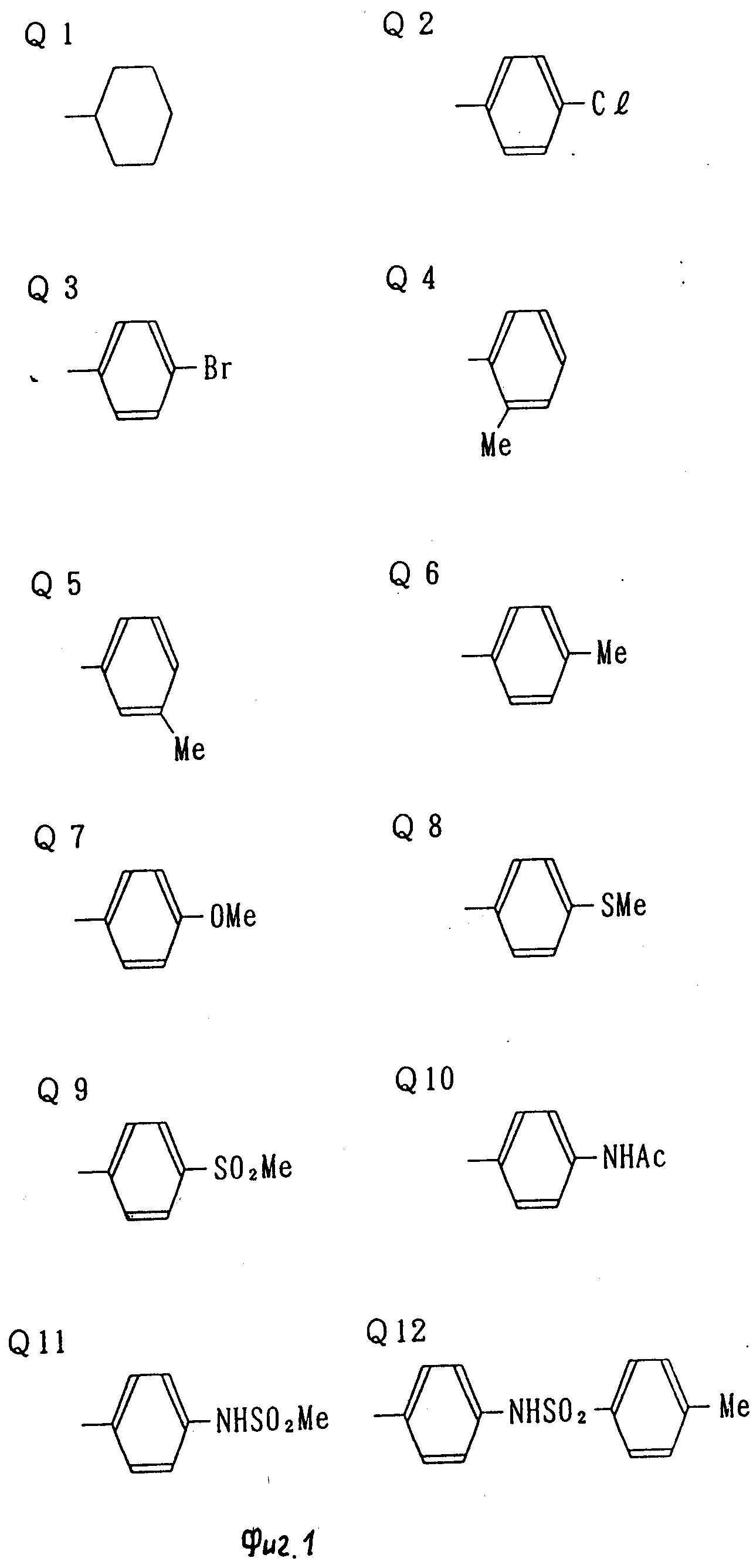
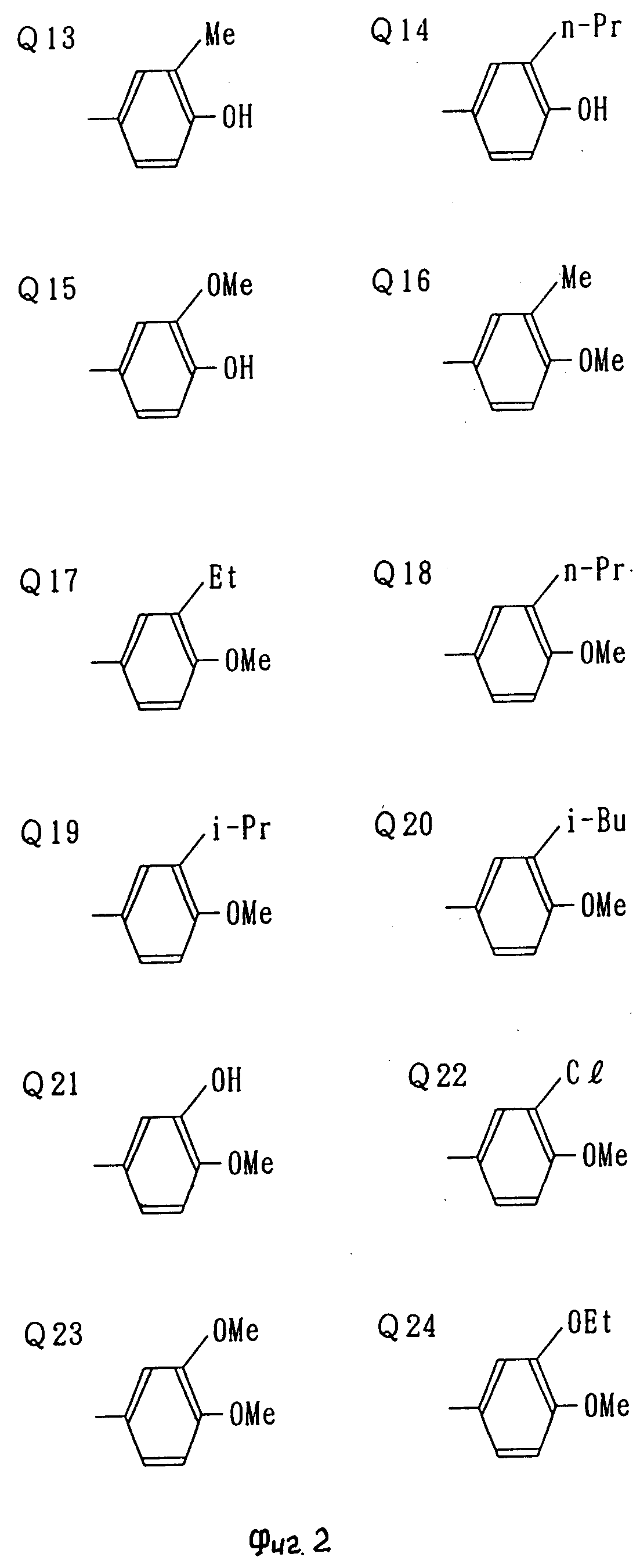
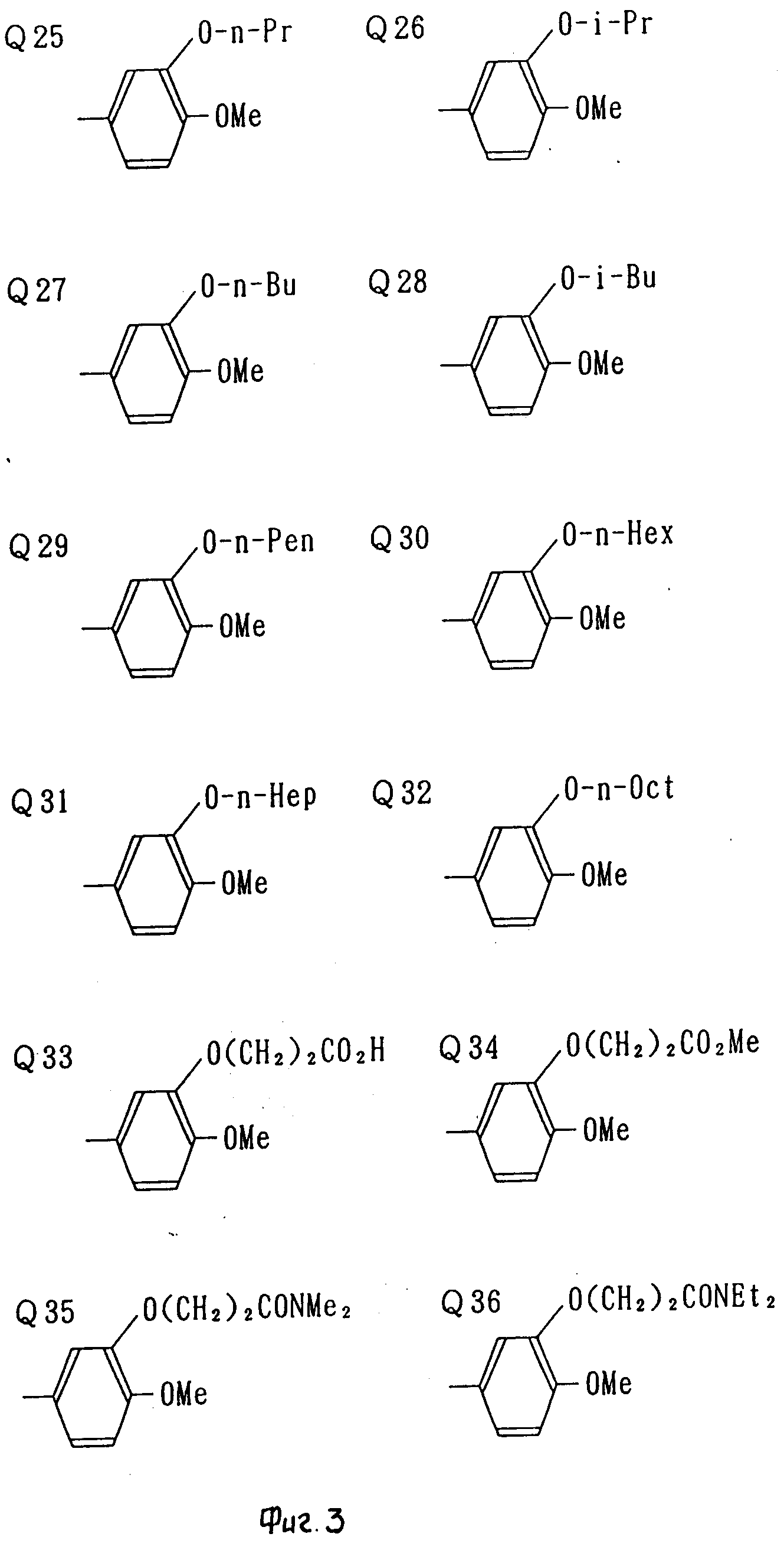
Q1-Q108 в табл. 1 это группы, отвечающие формулам, приведенным на фиг. 1-10.
Далее поясняется способ получения соединений по изобретению.
Производные 3(2Н)-пиридазинона общей формулы (1) и их фармацевтически приемлемые соли согласно изобретению могут быть получены следующими способами в соответствии со схемами реакций (1) (9).
Схема реакции (1)
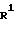
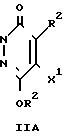
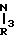

____→
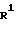
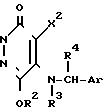
где Х1 атом хлора или атом брома; Х2 атом хлора, атом брома или атом водорода; R1, R2, R3, R4 и Ar определено выше.
По способу получения, соответствующему схеме реакции (I), соединение формулы (11А) 4,5-дигалоген- или 5-галоген-3(2Н)пиридазинона взаимодействует с производным арилметиламина формулы (III) или с его солью в присутствии дегидрогалогенирующего агента, необязательно в инертном растворителе, с образованием соединения формулы (IA), в структуре которого атом углерода в 4-положении соединения формулы (I) согласно данному изобретению связан с Х2.
атом хлора или атом брома, образуется в качестве побочного продукта позиционный изомер соединения формулы (IA), т.е. соединение
формулы (VA)
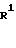
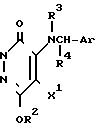
А именно, при использовании высокополярного растворителя имеется тенденция к высокому значению отношения производительности соединения (IA) согласно изобретению. Напротив, в тех случаях, когда используется растворитель с низкой полярностью, такой как бензол, толуол или гексан, имеется тенденция к высокому значению отношения производительности соединения (VA).
Следовательно, в качестве растворителей, обеспечивающих подавление образования в качестве побочного продукта соединения формулы (VA) и эффективное получение соединений (IA) по изобретению можно упомянуть растворители типа эфира, такие, как тетрагидрофуран или 1,4-диоксан, растворители амидного типа такие, как формамид, N,N-диметилформамид, N,N-диметилацетамид или N-метилпирролидон, ацетонитрил, диметилсульфоксид, растворители спиртового типа, такие как метанол, этанол или пропанол, органические амины, такие как пиридин, триэтиламин, N,N-диметиламиноэтанол или триэтаноламин, воду или смеси перечисленных веществ.
Желаемые соединения формулы (IA) согласно данному соединению можно легко выделить из смеси соединений формул (IA) и (VA) и очистить с помощью обычных методов, известных per Sl в органическом синтезе, таких как дробная перекристаллизация или различные разновидности хроматографии на силикагеле.
В случае использования соединения формулы (IIA), в которой Х2 это атом водорода, например 5-галоген-3(2Н)-пиридазинона, в качестве растворителей при проведении реакции можно использовать, помимо упомянутых растворителей, а также и бензол, толуол, ксилол, н-гексан, н-гептан и т.п.
В процессе реакции между соединением формулы (IIA) и соединением формулы (III) образуется бромистый водород. Как правило, имеется возможность повысить выход за счет введения в реакционную систему дегидрогалогенирующего агента, связывающего такой галогеноводород.
Можно использовать любой дегидрогалогенирующий агент, не влияющий неблагоприятным образом на реакцию и способный улавливать галогенид водорода. В качестве таких дегидрогалогенирующих агентов можно упомянуть неорганические основания, такие как карбонат калия, карбонат натрия, гидрокарбонат калия или гидрокарбонат натрия, либо органические основания, такие как N,N-диметиланилин, N, N-диэтиланилин, триметиламин, триэтиламин, N,N-диметиламиноэтанол или пиридин.
С другой стороны, в качестве дегидрогалогенирующего агента можно использовать исходное арилметиламино-производное формулы (III), взятое в избытке. Во многих случаях это обеспечивает повышение выхода.
Температура реакции может колебаться от 10оС до температуры кипения растворителя, используемого для проведения реакции.
Молярное соотношение между исходными веществами можно установить произвольно. Однако арилметиламино- производное формулы (III) или его соль обычно может использоваться в количестве 1 10 молей, предпочтительно 1,2 5 молей, на моль 4,5-дигалоген- или 5-галогенпроизводного 3(2Н)-пиридазинона формулы (IIA).
4,5-Дигалоген- или 5-галоген-производное 3(2Н)-пиридазинона формулы (IIA) можно получить традиционным способом или по обычной реакции органического синтеза, как описано ниже.
А именно, 4,5-дигалоген- или 5-галоген-производное 3-(2Н)-пиридазинона формулы (IIa) можно получить по способу, раскрытому в упомянутом источнике (в).
Те из арилметиламино-производных формулы (III) и их солей в способе (I), которые не поступают на рынок как промышленные продукты, можно получить по способу, раскрываемому в не прошедшей экспертизу опубликованной заявке на патент Японии N 267560/1986. Схема реакции (2):
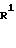
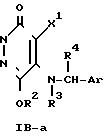
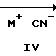
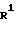
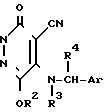

где R1, R2, R3, R4, X1 и Ar определены выше.
Приведенная схема реакции (2) иллюстрирует способ получения 4-циано-5-арилметиламино-производного формулы (IB) данного изобретения путем реакции замещения галогена между 4-галоген-5-арилметиламино-производным формулы (IВ-а) и цианитом металла формулы (IV).
Примеры металла М включают атом лития, атом натрия, атом калия, атом меди и т.п.
В качестве растворителя реакции предпочтительно используются растворители амидного типа, такие как N,N-диметилформамид, N,N-диметилацетамид, N-метилпирролидон и др. растворители спиртового типа, такие как метанол, этанол, н-пропанол, н-бутанол и др. диметилсульфоксид и их водосодержащие растворители.
Температуру реакции меняют в зависимости от используемых реагентов, но обычно она колеблется от комнатной температуры до точки кипения растворителя, используемого для проведения реакции. Как правило, реакция с участием соединения, атом галогена в 4-положении формулы которого представляет собой бром, протекает в более мягких температурных условиях по сравнению с реакцией с участием атома хлора.
Молярное соотношение между исходными веществами можно определить произвольно, и достаточно, что цианид металла формулы (IV) используется в количестве 1,2 10 молей на один моль 4-галоген-5-арилметиламино-производного формулы (IB-a).
Желаемое соединение можно легко выделить и очистить известным в органическом синтезе методом, например, перекристаллизацией, хроматографией на силикагеле различного типа или дистилляцией.
Схема реакции (3)

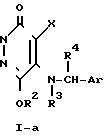
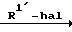
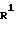
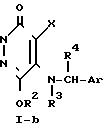
где R1' алкильная группа С1-С4 с линейной или разветвленной цепью, алкенильная группа С3-С4 или (СН2)nСO2R5, это атом хлора, атом брома, атом иода или другие элюминируемые функциональные группы; h, R2, R3, R4, R5, X и Ar определены выше.
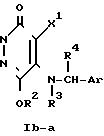
Приведенная схема реакции (3) иллюстрирует способ получения продукта замещения в 2-положении формулы (1-b) согласно изобретению в результате взаимодействия соединения формулы (I-a), в котором 2-положение пиридазинона занято атомом водорода, являющегося разновидностью соединений формулы (I) изобретения, с реакционноспособным производным, содержащим элиминируемую группу, таким как галогенпроизводное, алкилсульфонатное производное или фенилсульфонатное производное, отвечающее формуле R1' hal.
Данную реакцию можно в общем случае проводить в присутствии неорганического основания, такого как карбонат калия, карбонат натрия, карбонат лития, гидрокарбонат калия, гидрокарбонат натрия, гидроксид лития и др. либо в присутствии органического основания, такого как триэтиламин, три-н-пропиламин и др.
В случае, когда R3 в соединении формулы (I-a) представляет собой алкил, могут быть использованы, помимо перечисленных неорганических оснований, гидриды металлов и металлоорганические соединения, такие как гидрид натрия, н-бутиллитий и др.
В качестве растворителя реакции можно с успехом использовать, в случае применения неорганического или органического основания, растворитель типа кетонов (ацетон, метилэтилкетон, диэтилкетон и др.), растворитель амидного типа (формамид, N,N-диметилформамид, N,N-диметилацетамид и др.), растворитель спиртового типа (метанол, этанол и др.), воду и их смеси, а в случае использования гидрида металла растворитель типа эфира.
При использовании неорганического основания или органического основания температура реакции обычно колеблется от 0оС до температуры кипения растворителя, а при использовании гидрида металла она обычно колеблется от -78 до 60оС.
Молярное соотношение между исходными материалами можно определять произвольно. Однако достаточно, чтобы
реакционноспособное производное формулы R1 hal использовалось в количестве от 1 до 5 молей на один моль соединения формулы (I-a)
Желаемое соединение можно выделить и очистить
согласно способу, описание которого приводилось в связи со схемой реакции (2).
Схема реакции (4)
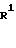
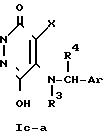
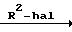
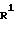
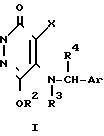
где R1, R2, R3, R4, X, Ar и hal определено выше.
Приведенная схема реакции (4) иллюстрирует способ получения соединения формулы (I) по изобретению путем взаимодействия 6-гидрокси-5-арилметиламино-производного формулы (10-а) с реакционноспособным производным формулы R2-hal. 6-Гидрокси-5-арилметил-производное формулы (10-а), используемое в данной реакции в качестве исходного материала, можно получить по способам, раскрываемым в упомянутом источнике (в) и схеме реакции (2).
Что касается условий проведения реакции, то можно ее проводить в условиях, аналогичных используемым при проведении реакции согласно приведенной схеме (3).
Схема реакции (5)
(i)
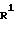
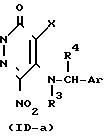
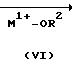
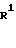
(ii)
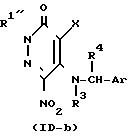
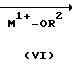


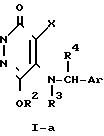
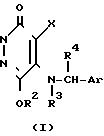
Приведенная схема реакции (5) иллюстрирует способ получения 6-алкокси-5-арилметиламино-производного формулы (I) или формулы (I-a) изобретения путем реакции замещения нитро-группы 6-нитро-5-арилметиламино-производного формулы (ID-a) или (ID-b) с алкоксидом щелочного металла формулы (VI). Используемые в качестве исходного материала для данной реакции 6-нитро-производное формулы (ID-a) и (ID-b) можно получить в соответствии со способом, описанным в упомянутом источнике (в).
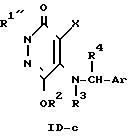
Соединение с атомом водорода в 2-положении пиридазинона, являющееся одним из желательных соединений, можно получить прямым путем, как показано в схеме реакции (5)-(i), где R1 в формуле (1D-a) и (I) представляет собой водород, или путем, показанным в схеме реакции (5)-(ii), которая представляет собой превращение 6-нитро-5-арилметиламино-производного формулы (ID-b), защищенного в 2-положении группой R1'', в соединение формулы (ID-c), с последующим удалением защитной группы R1'', целью чего является получение желаемого соединения. Во многих случаях выход обычно лучше при получении по последнему способу.
В качестве защитной группы R1'' предпочтительно использовать тетрагидропиранил, тетрагидрофуранил, 2-триметил- силилэтоксиметил (Ме3SiCH2 CH2OCH2-), пивалоилоксиметил (Me3C-CO2CH2-), бензи- локсиметил (
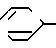
Удаление защитной группы R1'' можно легко осуществить обычным способом, применяемым для удаления таких защитных групп.
Здесь щелочной металл в формуле М1 представляет собой литий, натрий или калий.
Следовательно, алкоксиды щелочного металла в формуле (VI), используемые в качестве нуклеофильного агента, включают алкоксиды металлов, соответствующие данному выше определению М1 и R2.
Относительно растворителей реакции нет каких-либо особенных ограничений до тех пор, пока растворитель инертен по отношению к реакции, и можно перечислить растворители амидного типа (такие как N-метилпирролидон, формамид, N, N-диметилформамид или N, N-диметилацетамид), растворители типа простых эфиров (такие как диэтиловый эфир, 1, 2-диметоксиэтан, тетрагидрофуран или 1,4-диоксан), растворители типа бензола (такие как бензол, толуол или ксилол), а также смеси перечисленных веществ.
Температура реакции изменяется в зависимости от используемых реагентов. Обычно она колеблется в пределах от -15оС до температуры кипения используемого для реакции растворителя.
Молярное соотношение между исходными материалами можно определить произвольно, и достаточно, чтобы алкоксид щелочного металла формулы (VI) использовался в количестве от 1,2 до 10 молей на один моль 6-нитро-5-арилметаламино-производного формулы (ID-a) или (1D-b).
Желаемое соединение можно легко выделить и очистить известным в органическом синтезе способом, например, перекристаллизацией, хроматографией на силикагале различного типа или дистилляцией.
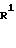
где R1, R2, R3, R4, X1 и Ar определено выше.
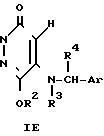
Приведенная схема реакции (6) иллюстрирует способ получения соединения формулы (IE) по изобретению, в структуре которого 4-положение занято атомом водорода, путем восстановительного удаления атома галогена 4-галоген-производного формулы (IB-a).
В качестве способа восстановления обычно применяют каталитическое гидрирование. В качестве катализаторов можно перечислить палладий, оксид платины, никелевый катализатор Рэнея и т.п. и реакция протекает относительно гладко при давлении водорода от 1 до 10 атм.
В тех случаях, когда R2 содержит атом, который отравляет катализатор, предпочтительный результат иногда обеспечивает использование гидрида металла, такого как гидрид три-н-бутилового или литий-алюминийгидрид.
В качестве растворителя реакции используют проточные растворители в случае реакции каталитического гидрирования, а при использовании гидрида металла используют, как правило, растворитель типа простого эфира.
Температура реакции может колебаться в пределах обычно от -10 до 100оС, и реакция обычно протекает ровно.
Схема реакции (7)
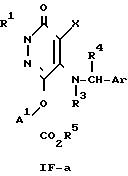
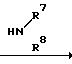
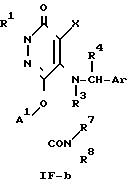
где R1, R3, R4, R5, R7, R8, A1, X и Ar определено выше.
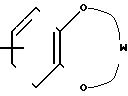
Приведенная схема реакции (7) иллюстрирует способ получения 6-аминокарбонилалкиленокси-производного формулы (IF-b) путем проведения реакции конденсации, включающей дегидратацию, 6- ω-карбоксиалкиленокси-производного или 6- ω-алкоксикарбонилалкиленокси-производного формулы (IF-a) и амина формулы (VII).
В случае, когда R5 представляет собой атом водорода, процесс конденсации можно осуществить по способу, известному из синтеза пептидов, например, хлорангидридным способом, смешанным хлорангидридным методом или по методу, предусматривающему использование конденсационного агента, такого как дициклогексилкарбодимид, карбонилдиимидазол или имид N-гидрокси-янтарной кислоты, и метод конденсации выбирают в зависимости от реакционноспособности аминов формулы (VII). Реакцию можно проводить в обычно применяемых для таких реакций условиях.
В случае реакции с высоконуклеофильными аминами, которые отвечают формуле (VII), конденсация может протекать даже при использовании сложных эфиров, в формуле которых R5 представляет собой
алкильную группу. В таком случае тип растворителя не ограничивается специально, и может быть использован любой растворитель, если он не влияет неблагоприятно на реакцию. В некоторых случаях реакция
может протекать в отсутствие растворителя. Температура реакции колеблется в пределах от комнатной до 200оС, более обычно от 50 до 150оС. Схема реакции (8)
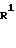
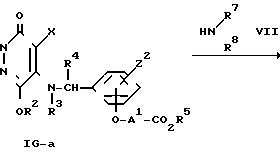
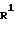
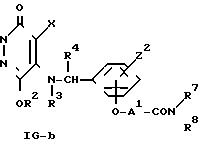
где R1, R2, R3, R4, R5, R7, R8, X, Z2 и AI определены выше.
Проведенная схема реакции (8) иллюстрирует способ получения амидо-пpоизводного формулы (IG-b) путем реакции конденсации между 5-( ω -карбоксиалкиленокси)фенилметиламино- или 5-( ω -алкоксикарбонилалкиленокcи)фенилметиламино-производным формулы (IG-a) и амином формулы (VII).
Данную реакцию можно осуществить точно так же, как и реакцию по схеме (7).
Схема реакции (9)
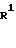
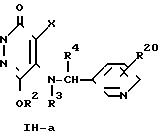
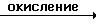
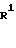
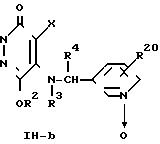
где R1, R2, R3, R4, R20 и Х определено выше.
Приведенная схема реакции (9) иллюстрирует способ получения N-оксипиридилметиламино-производного формулы (IН) путем окисления атома азота в пиридиновом кольце 5-пиридилметиламино-производного формулы (IН-a). Примеры окислителей включают надмуравьиную кислоту, надуксусную кислоту, надбензойную кислоту, метахлорнадбензойную кислоту, трет-бутилгидропероксид, водную перекись водорода и т.п.
В качестве растворителей реакции можно перечислить растворители галогенного типа (тетрахлорид углерода, хлороформ, дихлометан, 1,2-дихлоэтан и др. ), растворители типа простых эфиров (диэтиловый эфир, тетрагидрофуран, 1,4-диоксан и др.), растворители типа бензола (бензол, толуол и др.), растворители типа спиртов (метанол, этанол, трет-бутанол и др.), уксусную кислоту, муравьиную кислоту и т.п. В некоторых случаях добавляют в качестве катализатора комплекс переходного металла.
Температура реакции обычно колеблется в пределах от -20оС до температуры кипения используемого растворителя.
Молярное соотношение между исходными материалами можно устанавливать произвольно, но окислитель используется, как правило, в количестве от 1 до 10 моль, предпочтительно от 1,2 до 5 молей, на один моль 5 пиридилметиламино-производного формулы (IН-а).
Желаемое соединение можно легко выделить и очистить известными в органическом синтезе методами, например перекристаллизацией, хроматографией на силикагеле или дистилляцией.
В качестве способов употребления 3(2Н)-пиридазинонов формулы (I) или их фармацевтически приемлемых солей согласно изобретению можно упомянуть не пероральное употребление в виде инъекций (подкожных, внутривенных, внутримышечных или внутрибрюшинных), мазей, суппозиториев или аэрозолей и пероральное употребление в виде таблеток, капсул, гранул, пилюль, сиропов, жидкостей, эмульсий или суспензий.
Упомянутая фармакологическая композиция содержит соединение по изобретению в количестве приблизительно 0,1 99,5 мас. предпочтительно приблизительно 0,5-99,5 мас. в расчете на общую массу композиции.
К соединению по изобретению или к композиции, содержащей соединение по изобретению, могут быть добавлены другие фармакологически активные соединения.
Кроме того, композиция по изобретению может содержать множество соединений по изобретению.
Клиническая доза соединений согласно изобретению изменяется в зависимости от возраста массы тела, чувствительности или наблюдаемых у пациента симптомов и т.д. Обычно, однако, эффективная дневная доза составляет 0,003 1,5 г, предпочтительно 0,01 0,6 г для взрослого пациента.
При необходимости, однако, можно использовать дозы вне указанного диапазона.
В зависимости от способа употребления, соединения согласно изобретению можно вводить в различные подходящие композиции, в соответствии с обычными методами, применяемыми при приготовлении фармацевтических формул.
А именно, можно изготовить таблетки, капсулы, гранулы или пилюли для перорального употребления, используя такие эксципиенты, как сахар, лактоза, глюкоза, крахмал или маннит; такие связующие, как сиропы, гуммиарабик, желатин, сорбит, трагакант, метилцеллюлоза или поливинилпирролидон; дезинтегранты, такие как крахмал, карбоксиметилцеллюлоза или ее кальциевые соли, порошок кристаллической целлюлозы или полиэтиленгликоль; придающие скользкость агенты, такие как тальк, стеарат магния или кальция либо двуокись кремния; либо смазку, такую как лаурат натрия или глицерин.
Растворы для инъекций, растворы, эмульсии, суспензии, сиропы или аэрозоли можно приготовить, растворяя активный ингредиент в растворителе, например, в воде, этиловом спирте, изопропиловом спирте, пропиленгликоле, 1,3-бутиленгликоле, или полиэтиленгликоле; вводя поверхностно активную добавку, например, эфир сорбита и жирной кислоты, эфир полиоксиэтилена, сорбита и жирной кислоты, эфир полиоксиэтилена, сорбита и жирной кислоты, эфир полиоксиэтилена и жирной кислоты, полиоксиэтиленовый эфир гидрогенизированного касторового масла или лецитина, суспензирующую добавку, например натриевую соль карбоксиметилцеллюлозы, производное целлюлозы, такое как метилцеллюлоза, либо натуральный каучук, такой как трагакант или гуммиарабик; или консервант, например эфир параоксибензойной кислоты, бензалконийхлорид или соль сорбиновой кислоты.
Аналогичным образом можно изготовить суппозитории, используя, например, полиэтиленгликоль, ланоин или кокосовое масло.
Наилучший способ реализации изобретения (примеры получения, примеры формул и примеры испытаний).
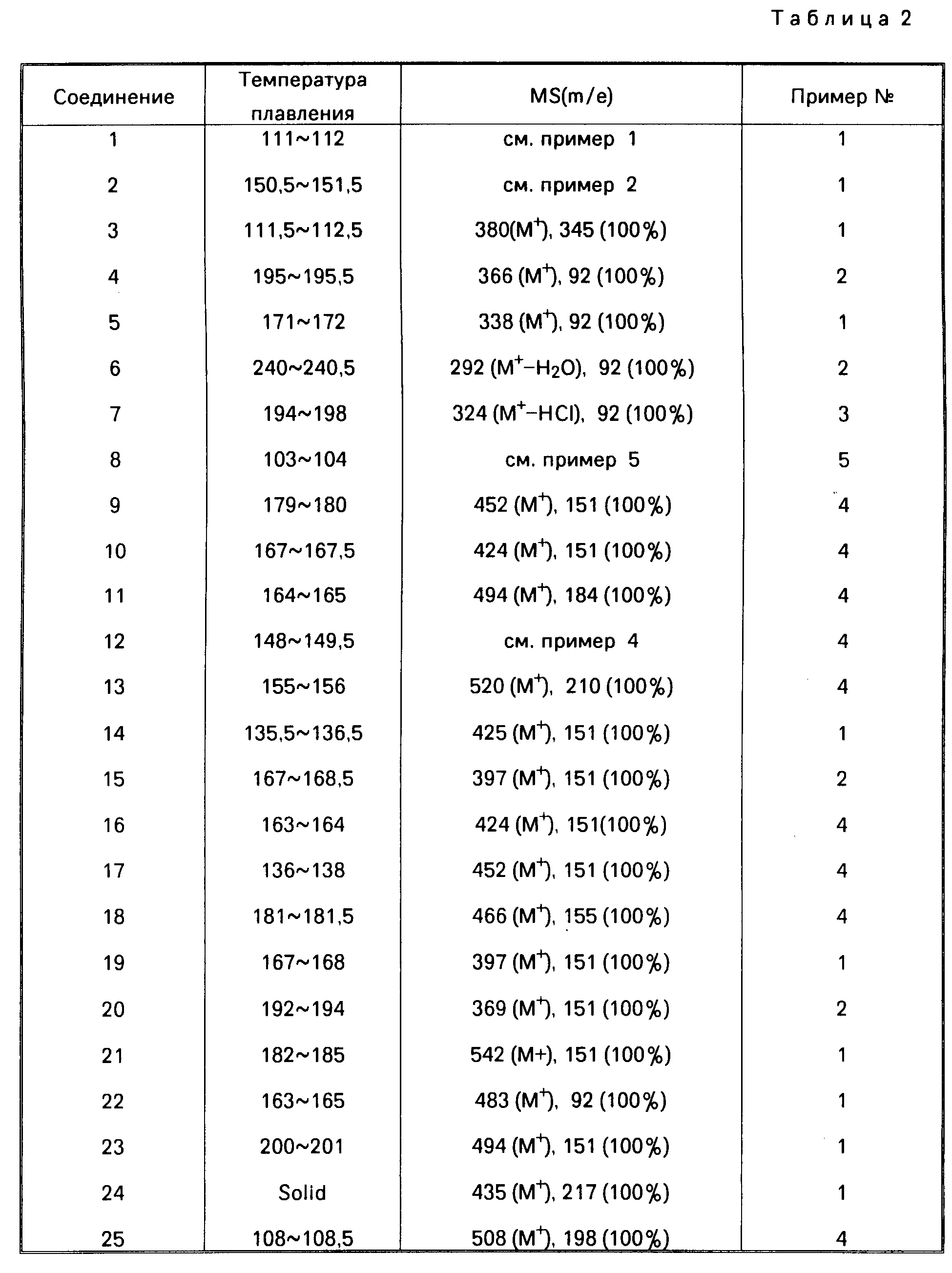
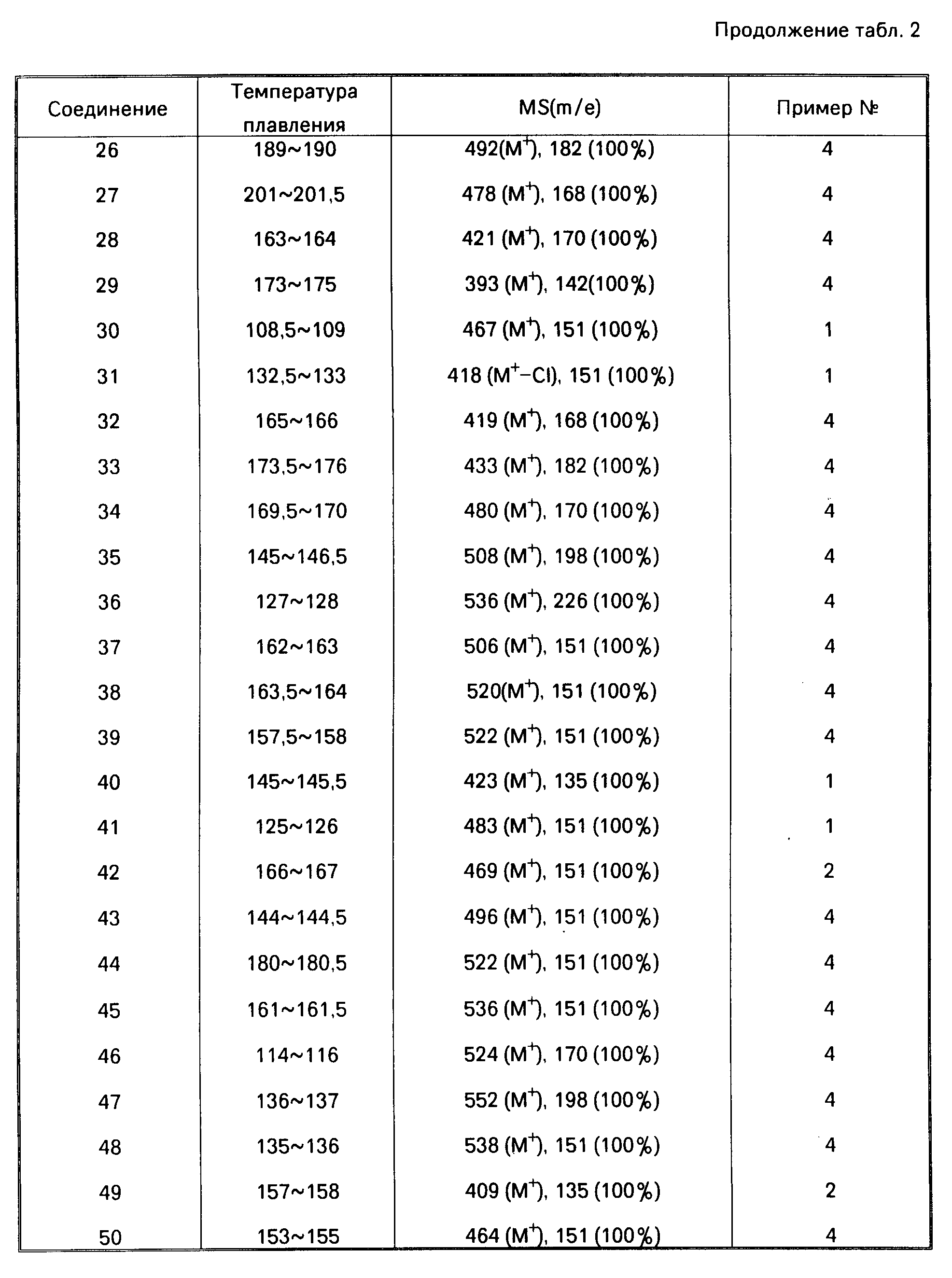
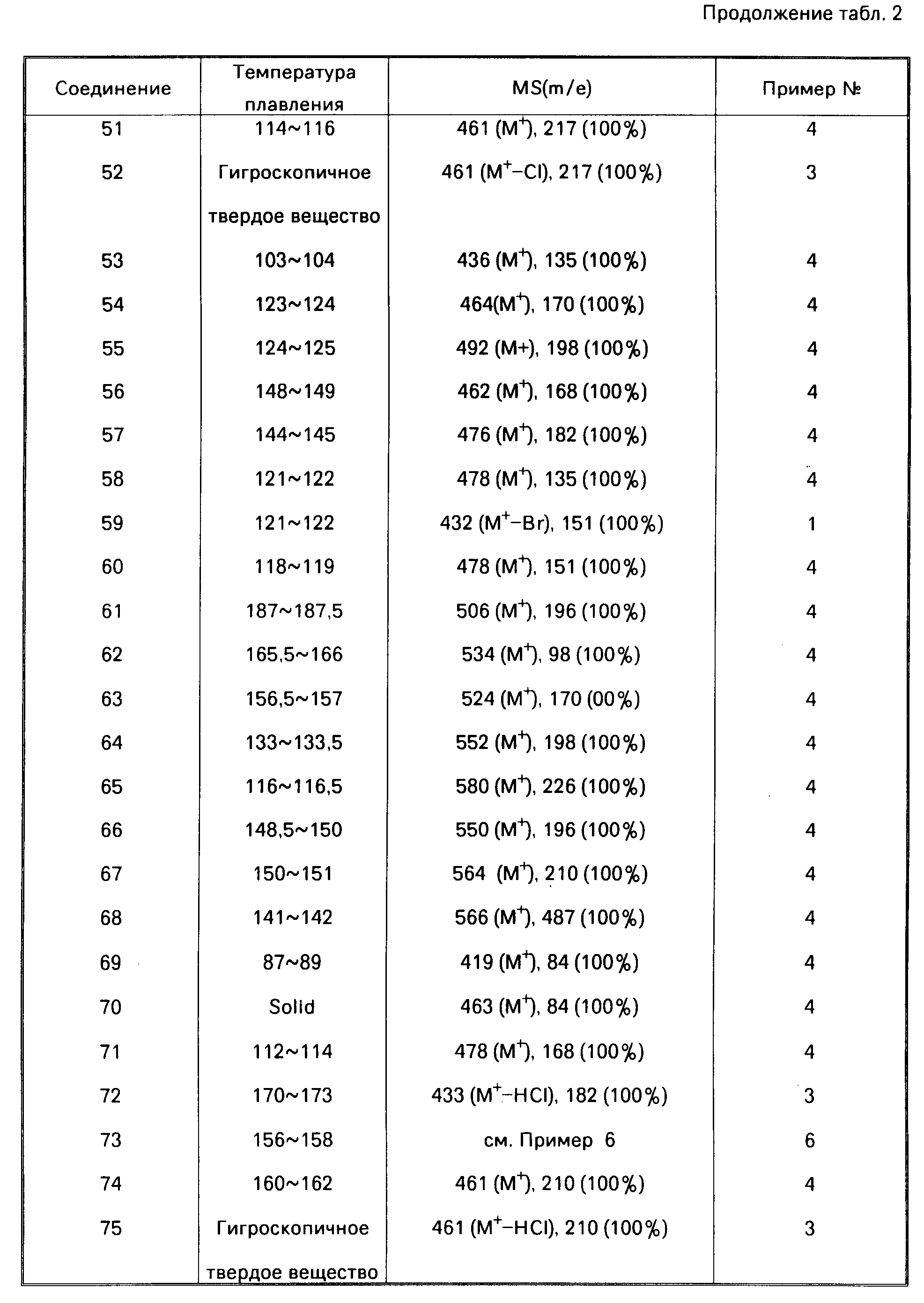
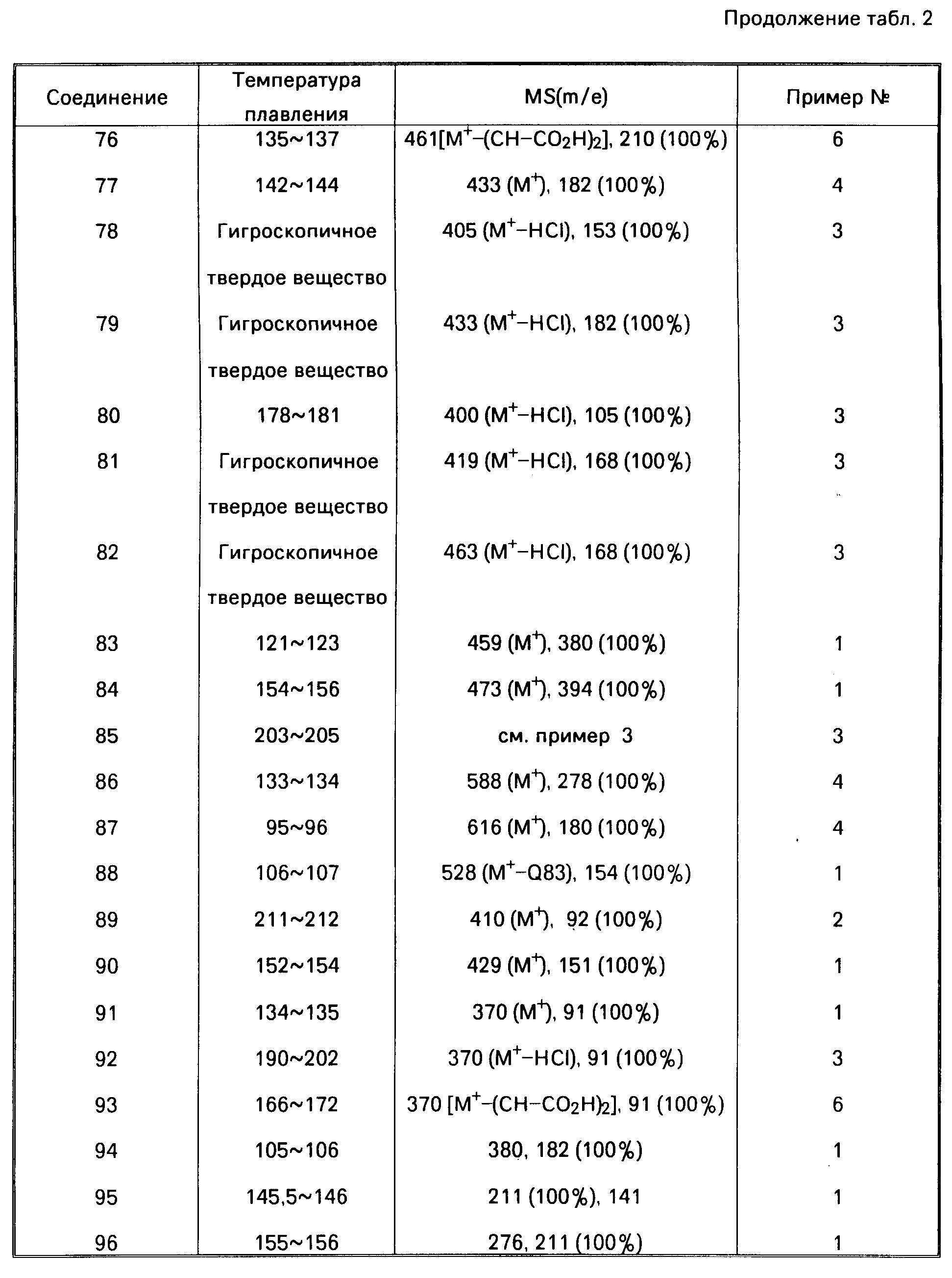
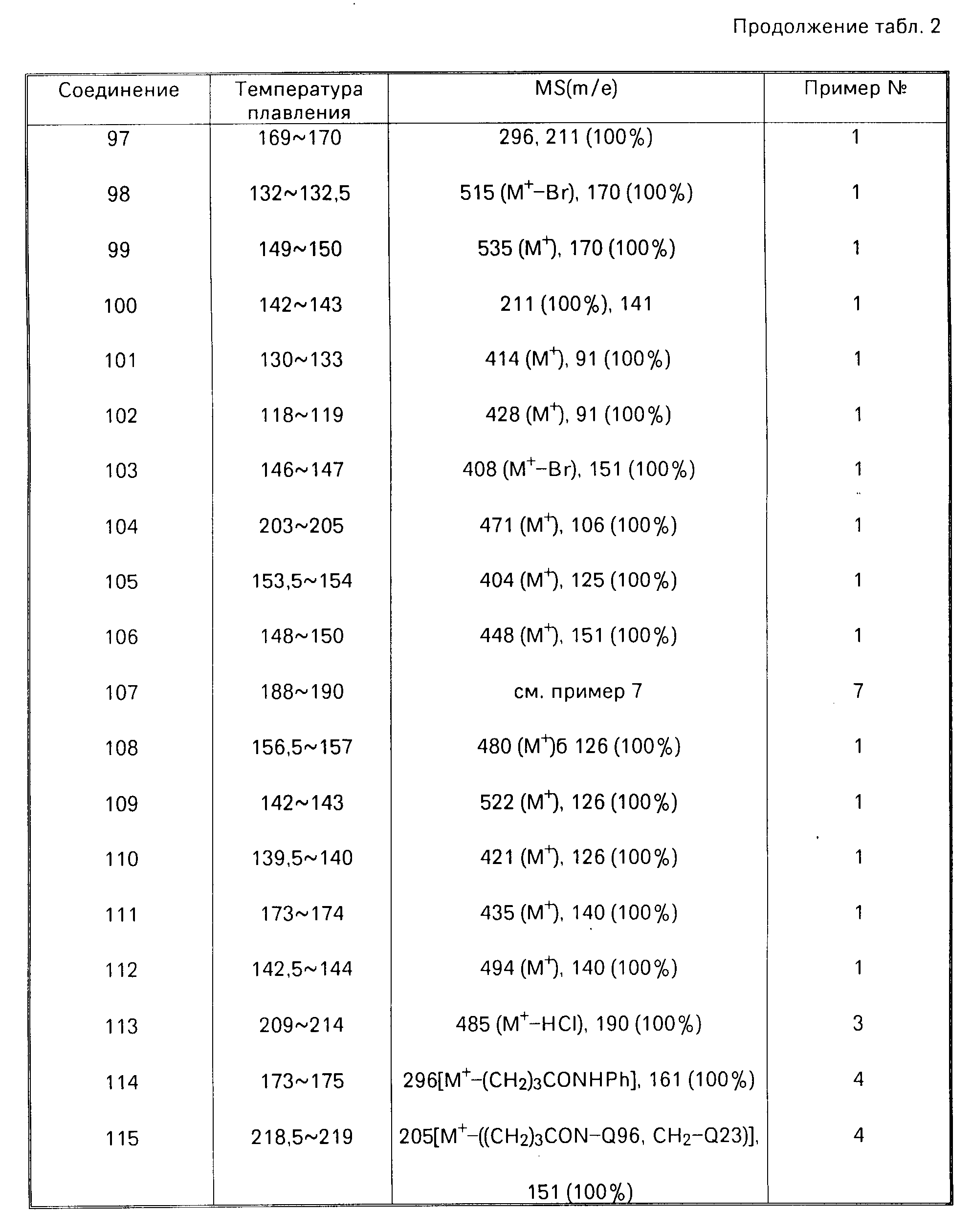
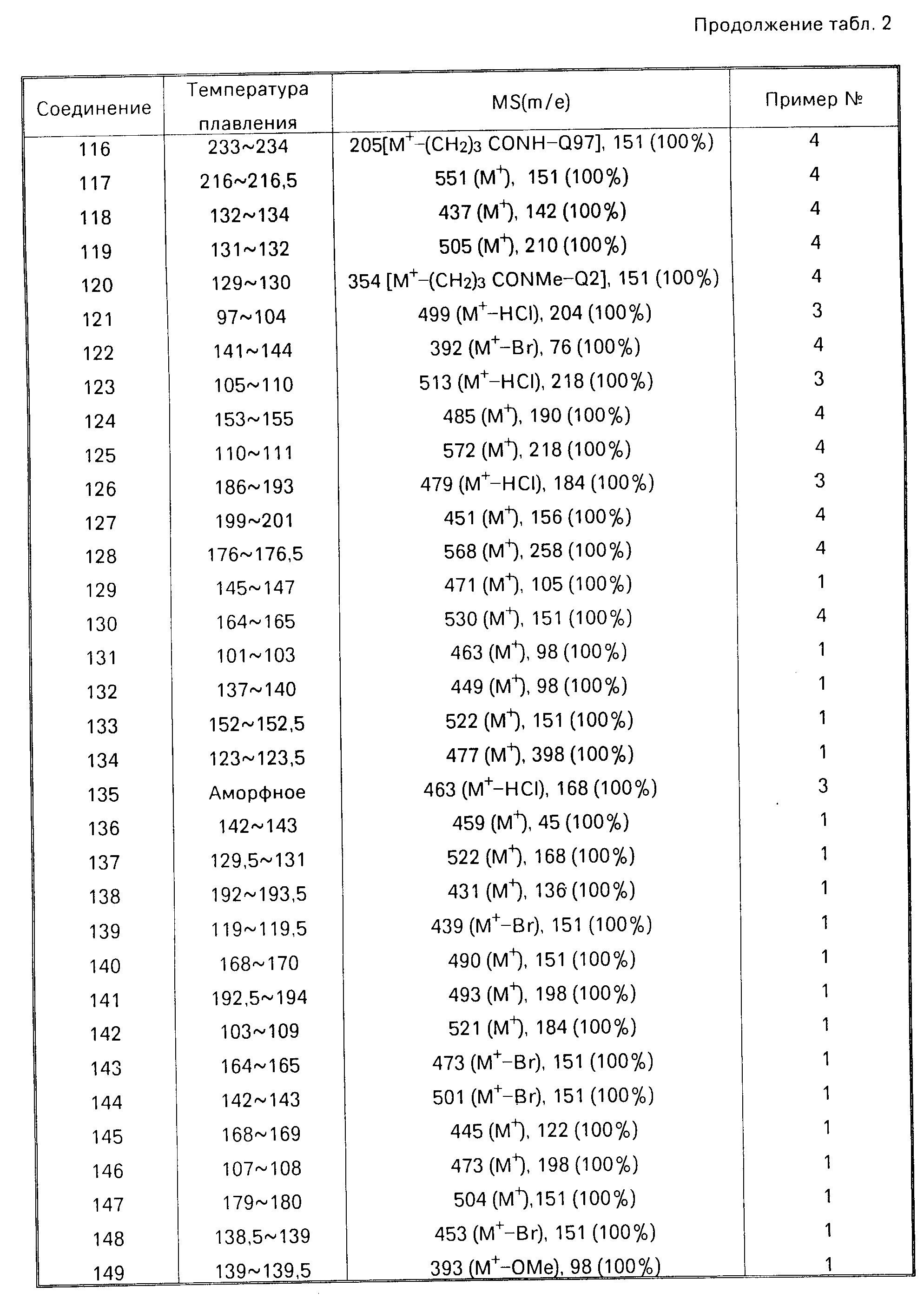
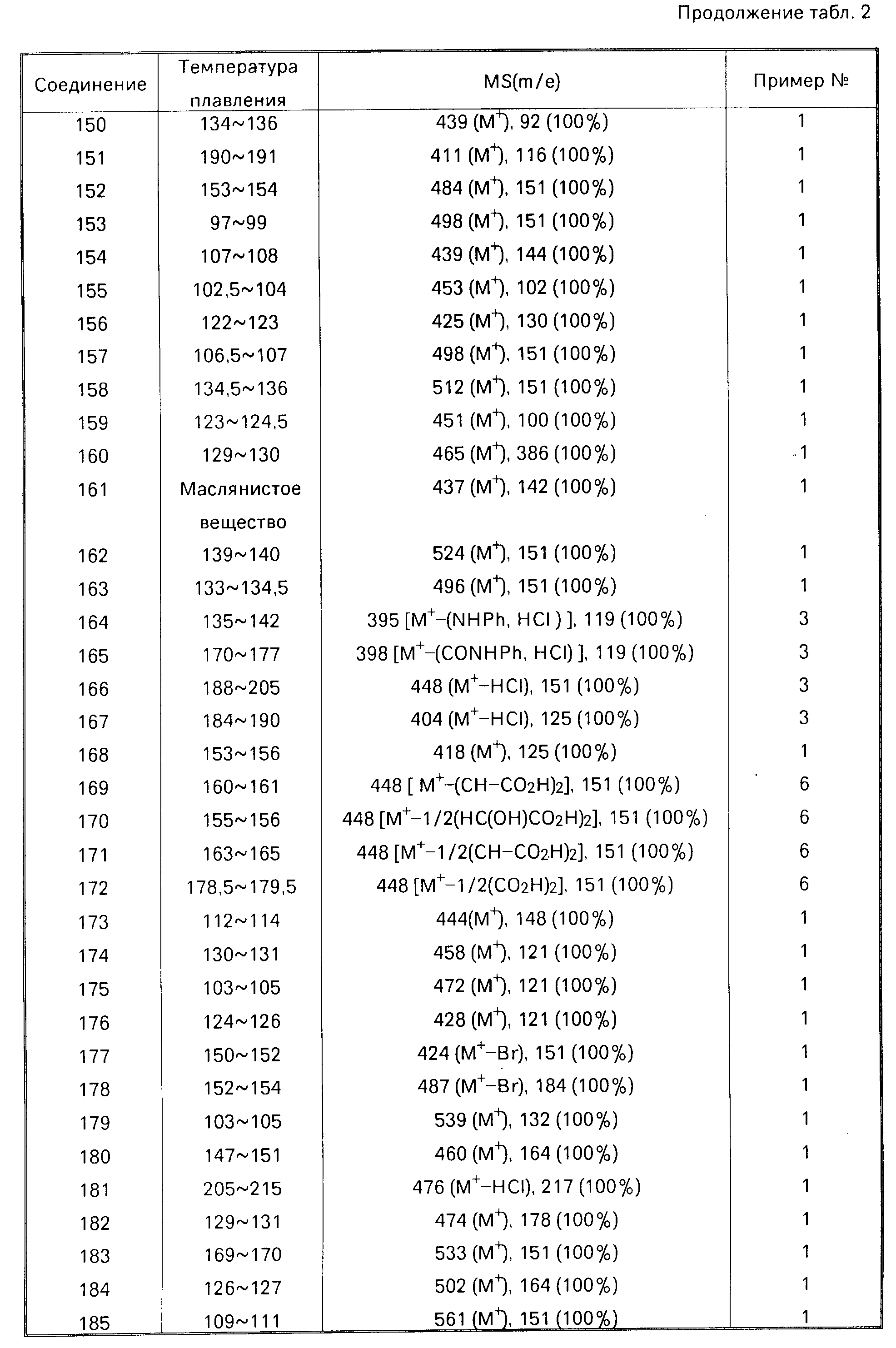
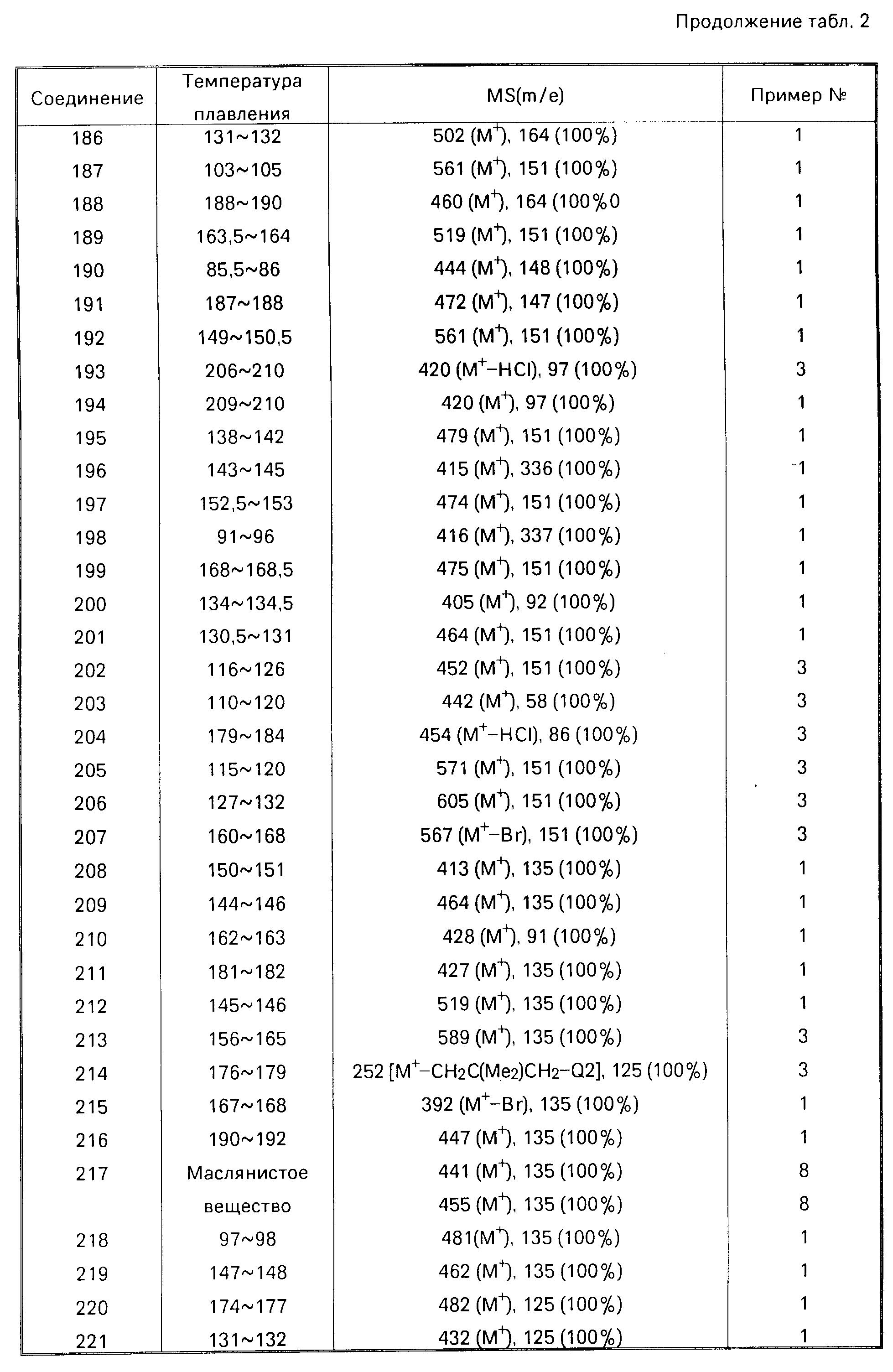
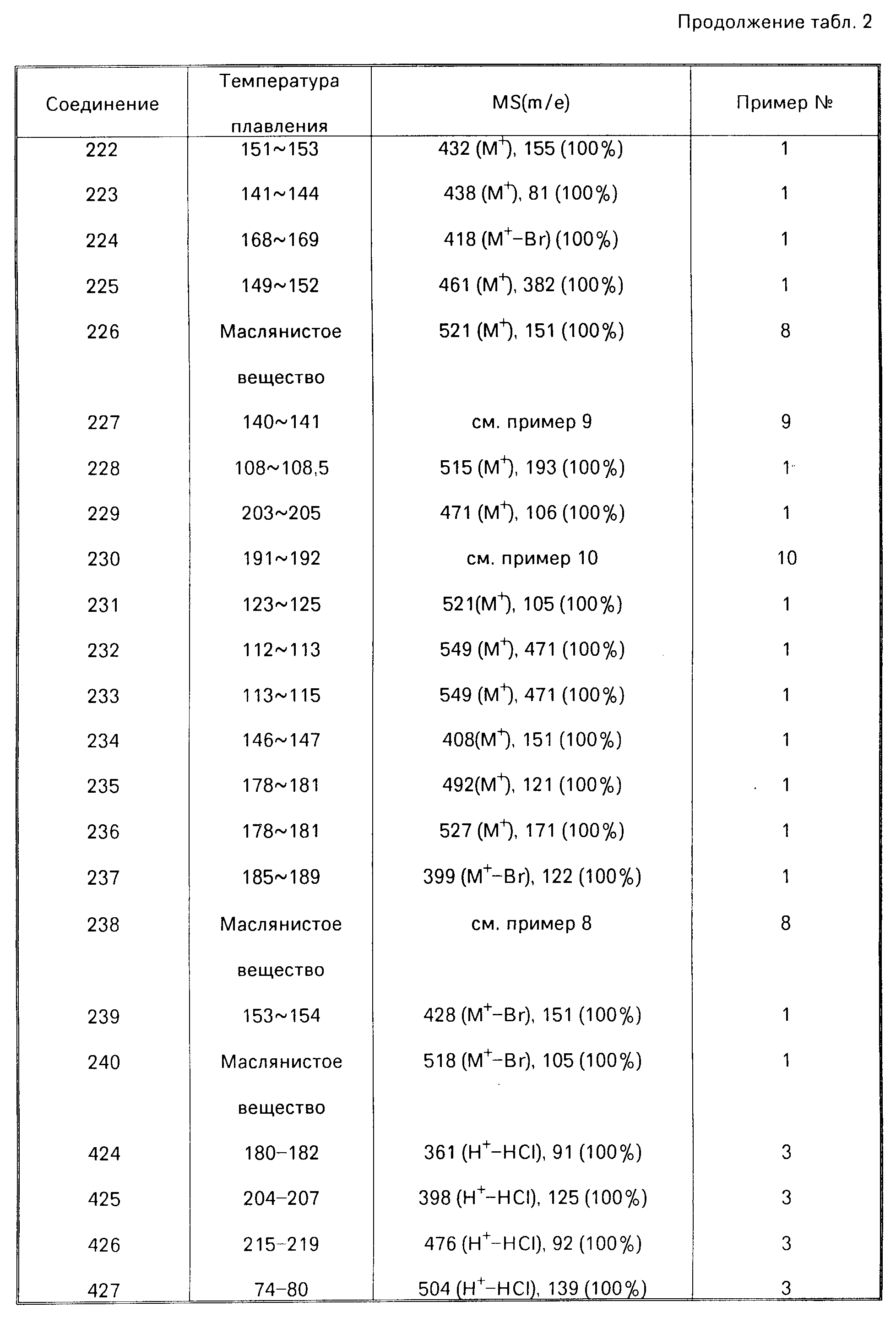
Далее дается детальное описание изобретения со ссылками на примеры, включая примеры получения, примеры формул и примеры испытаний. Следует однако понимать, что данное изобретение ни в коей мере не ограничивается этими конкретными примерами. В описании примеров получения, а также в табл.2, символы "NMP", "IR" и "MS" означают "спектр ядерного магнитного резонанса", "инфра-красный спектр" и "масс-спектрометрия" соответственно. ИК-спектры снимались методом диска из бромида калия, а ЯМР в хлороформе, содержащем тяжелый водород, за исключением особо оговоренных случаев.
В данных масс-спектрометрии в табл.2 приводятся только основные пики, или типичные пики фрагментов.
Пример получения 1. 4-Хлор-5-(3,4-диметоксибензиламино)-6-(5-метоксикарбонилпентилокси)-3(2Н)-пи ридазинон (соединение I).

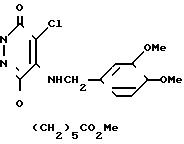
Смесь, состоящую из 4,13 г 4,5-дихлор-6-(5-метоксикарбонилпентилокси)-3(2Н)-пи- ридазинона, 6,70 г 3,4-диметоксибензиламина, 130 мл 1,4-диоксана и 130 мл воды, нагревали в течение ночи с обратным холодильником при перемешивании. Выпарили растворитель при пониженном давлении, в остаток налили воды, после чего экстрагировали продукт хлороформом. Экстракт промыли разбавленной хлористоводородной кислотой, водой и солевым раствором в перечисленном порядке и высушили над сульфатом натрия. Затем отогнали pаствоpитель и кристаллизовали остаток из смеси хлороформ(н-гексан)диэтиловый эфир, получив в результате вышеуказанное соединение в виде бесцветных кристаллов с температурой плавления от 111 до 112оС.
ЯМР: δ 11,71 (1Н, широкий синглет), 6,71 (3Н, синглет), 5,02 (1Н, сжатый триплет), 4,76 (2Н, дублет), 4,11 (2Н, триплет), 3,80 (6Н, синглет), 3,57 (3Н, синглет), 2,26 (2Н, триплет), 2,1-1,2 (6Н, мультиплет).
МС (m/e): 439 (М+), 404, 151 (100%).
Пример получения 2. 4-Хлор-5-(3,4-диметоксибензиламино)-6-(5-карбоксипентилокси)-3(2Н)-пиридази- нон(соединение 2).

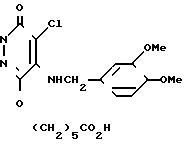
Смесь, состоящую из 240 мг 4-хлор-5-(3,4-диметоксибензиламино)-6-(5-метоксикарбонилпентилокси)-3(2Н)-пи рида(соединение I), полученного согласно методике примера получения 1, 65 мг гидроксида натрия, 10 мл метанола и 1 мл воды, перемешивали при 60 70оС в течение 1 ч. После проведения реакции маточник выпарили при пониженном давлении, в остаток налили воды и довели рН полученного раствора до 1-2 с помощью разбавленной хлористоводородной кислоты, после чего продукт экстрагировали хлороформом. Промыли экстракт водой и соляным раствором в перечисленном порядке и высушили над сульфатом натрия. Затем отогнали растворитель и кристаллизовали остаток из смеси хлороформ (диэтиловый эфир, что дало 192 мг названного соединения в виде бесцветных кристаллов с точкой плавления 150, 5-151,5оС.
ЯМР δ 6,70 (3Н, синглет), 5,14 (1Н, сжатый триплет), 4,75 (2Н, дублет), 4,10 (2Н, триплет), 3,79 ( 6Н, синглет), 2,29 (2Н, триплет), 2,0-1,2 (6Н, мультиплет).
ИК: ( ν·см-1 ): 3100, 2910, 1720, 1610.
МС (m/e): 425 (М+), 390, 151 (100%).
Пример получения 3. 4-Бром-5-(3-пиридилметиламино)-6-(3-фенилпропокси)-3(2Н)-пиридазинона гидрохлорид
(соединение N 85)

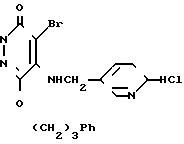
Растворили 2,50 г 4-бром-(3-пиридилметиламино)-6-(3-фенилпропокси)-3(2Н)-пи- ридазинона (соединение 101) в 150 мл 10%-ного раствора хлористого водорода в метаноле и перемешивали полученный раствор при комнатной температуре в течение 1 ч. Выпарили растворитель при пониженном давлении и кристаллизовали остаток из смеси метанол/диэтиловый эфир, что дало 2,68 г названного соединения в виде бесцветных кристаллов с температурой плавления от 203 до 205оС.
МС (m/e): 414 (М+ -НСl), 335, 322, 296, 217, 118 (100%).
Пример получения 4. 4-Хлор-5-(3,4-диметоксибензиламино)-6-(5-N,N- диэтиламинокарбонилпентилокси)
-3(2Н)-пиридазинон (соединение 12)

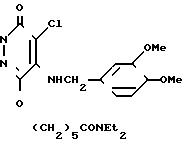
60 мг этилхлоркарбоната добавили к смеси, состоящей из 200 мг 4-хлор-5-(3,4-диметоксибензиламино)-6-(5-карбоксипенти- локси)-3(2Н)-пиридазинона (соединение 2), полученного по методике примера получения 2, 60 мг триэтиламина и 10 мл тетрагидрофурана, причем смесь охлаждали льдом и перемешивали полученную смесь при той же температуре в течение 1,5 ч. Далее к ней добавили 100 мг диэтиламина и полученную смесь далее перемешивали в течение 2,5 ч, убрав ледяную баню, после чего выпарили растворитель при пониженном давлении. К остатку добавили воду и экстрагировали продукт хлороформом. Экстракт промыли соляным раствором и высушили над сульфатом натрия. Затем растворитель удалили дистилляцией и кристаллизовали остаток из смеси хлороформ/диэтиловый эфир, получив в результате 209 мг названного соединения в виде бесцветных кристаллов с температурой плавления от 148 до 149,5оС.
ЯМР, δ 6,75 (3Н, синглет), 5,15 (1Н, сжатый триплет), 4,79 (2Н, дублет), 4,15 (2Н, триплет), 3,83 (6Н, синглет), 3,81, 3,76 (каждый 2Н, квартет), 2,27 (2Н, триплет), 2,1-1,9 (6Н, мультиплет), 1,15, 1,10 (каждый 3Н, триплет).
МС(m/e): 480 (М+), 445, 310, 275, 170 (100%), 151.
Пример получения 5.
4-Хлор-5-(3,4-диметоксибензиламино)- -(5-N-метиламинокарбонилпентилокси)-3(2Н)-(соединение 8)

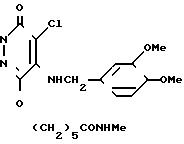
Смесь, состоящую из 200 мг 4-хлор-5-(3, 4-диметоксибензиламино)-6- 5-метокси-карбонилпентилокси)-3(2Н)-пиридазинона (соединение I), полученного по методике примера получения 1,2 мл 40%-ного водного раствора метиламина и 6 мл метанола, нагревали с обратным холодильником в течение 8 ч. Выпарили реакционную смесь при пониженном давлении и экстрагировали продукт хлороформом. Экстракт промыли по очереди водой и солевым раствором, а затем высушили над сульфатом натрия. Затем отогнали растворитель и кристаллизовали остаток из смеси хлороформ/диэтиловый эфир, так что получилось 146 мг вышеназванного соединения в виде бесцветных кристаллов с температурой плавления 103-104оС.
ЯМР δ 11,75 (1Н, широкий синглет), 6,73 (3Н, синглет), 6,0-5,5) 1Н, широкий мультиплет), 5,02 (1Н, сжатый триплет), 4, 76 (2Н, дублет), 4,10 (2Н, триплет), 3,81 (6Н, синглет) 2,74 (8Н, дублет), 2,12 (2Н, сжатый триплет), 1,9-1,3 (6Н, мультиплет).
МС (m/e): 438 (М+), 403, 310, 274, 151 (100%), 128.
Пример получения 6.
4-Хлор-5-(3-пиридилметиламино)-6-[5- (1-пиперидинокарбонилпентокси)]-3(2Н)- пиридазинона фумарат (соединение 73)

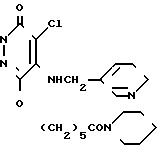
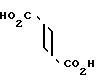
Смесь, состоящую из 1,0 г 4-хлор-5-(3-пиридилметиламино-6-[5-(1-пиперидинокарбонилпентилокси)]-3(2Н)-п ирид(соединение 33), 268 г фумаровой кислоты и 20 мл метанола, перемешивали при комнатной температуре в течение 1 ч. Выпарили реакционную смесь при пониженном давлении и перекристаллизовали твердый остаток из смеси хлороформ/этилацетат, получив в результате 1,06 г названного соединения в виде бесцветных кристаллов с температурой плавления от 156 до 158оС.
MC(m/e): 433 (М+- (СН-СО2Н2)2), 398, 287, 251, 216, 182 (100%).
Пример получения 7.
4-Циано-5-(3-пиридилметиламино)-6-[3- (4-хлорфенилпропокси)]-3(2Н)-пиридазин-он (соединение 107).

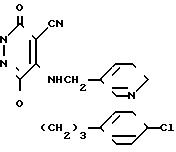
Смесь, состоящую из 1,0 г 4-бром-5-(3-пиридилметиламино)-6-[3-(4-хлорфенилпро- покси)]-3-(2Н)-пиридазинона (соединение 106), 587 мг цианида меди и 20 мл N-метилпирролидона, перемешивали в течение 6 ч при 120-130оС. После охлаждения полученной смеси до комнатной температуры к ней добавили насыщенный водный раствор хлорида аммония, после чего продукт экстрагировали хлороформом. Экстракт промыли солевым раствором и высушили над сульфатом натрия. Затем растворитель отогнали и кристаллизовали остаток из ацетонитрила, получив 313 мг вышеназванного соединения в виде слегка желтоватых кристаллов с температурой плавления от 188 до 190оС.
МС (m/e): 395 (М+), 350, 243, 152 (100%), 124.
ИК:( ν
Пример получения 8. 2-Этоксикарбонилметали-4-бром-5-(3, 4-диметоксибензиламино)-6-[3-(4-хлорбен- зилфенилпропокси)]-3(2Н)-пиридазинон (соединение 238).
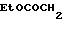
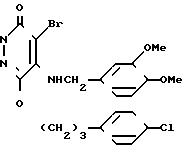
Смесь, состоящую из 100 мг 4-бром-5-(3,4-диметоксибензиламино)-6 -[3-(4-хлорфенилпропокси)] -3(2Н)-пиридазинона (соединение N 239), 33 мг карбоната калия, 49 мг этилбромацетата, 316 мг иодида натрия и 5 мл метилэтилкетона, перемешивали при нагревании с обратным холодильником в течение 5 ч. После того, как нерастворившийся материал удалили фильтрацией,выпарили растворитель при пониженном давлении и к остатку добавили воду, после чего экстрагировали продукт хлороформом. Экстракт промыли солевым раствором и высушили над сульфатом натрия. Затем отогнали растворитель, а остаток подвергли очистке способом колоночной хроматографии на силикагеле (элюант: н-гексан)этилацетат -1(1), что дало 82 мг вышеназванного соединения в виде бесцветного масла.
МС (m'e): 593 (М+), 514, 288, 259, 151 (100%).
Пример получения 9. 2-(Карбоксиметил)-4-бром-5-(3, 4- диметоксибензиламино)-6-[3-(4-хлорфенилпропокси)] -(2Н)-пиридазинон (соединение 227).
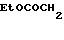
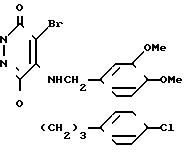
Смесь, состоящую из 80 мг 2-этоксикарбонилметил-4-бром-5(3, 4- диметоксибензиламино)-6-[3-(4-хлорфенилпропокси)] 3(2Н)-пиридазинона (соединение 238), полученного по методике примера получения 8, 16 мг гидроксида натрия, 2 мл метанола и 0,2 мл воды, перемешивали при комнатной температуре в течение 2 ч. После окончания реакции маточник выпарили при пониженном давлении, в остаток налили воды и довели рН полученного раствора до 1-2 с помощью разбавленной хлористоводородной кислоты, после чего экстрагировали продукт хлороформом. Экстракт промыли солевым раствором и высушили над сульфатом натрия. Затем растворитель отогнали, а остаток кристаллизовали из смеси хлороформ (диэтиловый эфир, получив 49 мг вышеназванного соединения в виде бесцветных кристаллов с температурой плавления 140-141оС.
МС (m/e): 486 (М+ -Br), 427, 371, 151 (100%).
Пример получения 10. 4-Бром-5-[3-(N-оксипиридилметиламино)] -6-(3-фенилпропокси)-3(2Н)пиридазинон (соединение 230).

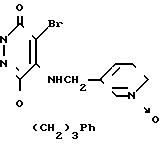
Смесь, состоящую из 250 мг 4-бром-5-(3-пиридилметиламино)-6-(34фенилпропокси)-3(2Н)-пиридазинона, 167 мг мета-хлорбензойной кислоты и 10 мл дихлорметана, перемешивали при комнатной температуре в течение 6 ч. К полученной смеси добавили насыщенный водный раствор гидрокарбоната натрия и хлороформ, после чего отделили органический слой. Оставшийся водный слой реэкстрагировали хлороформом и соединили полученный экстракт с первым органическим слоем. Объединенный экстракт промыли водой и солевым раствором по очереди и высушили над сульфатом натрия. Затем отогнали растворитель, и полученный твердый остаток перекристаллизовали из смеси хлороформ/диэтиловый эфир, что дало вышеназванное соединение в виде бесцветных кристаллов с температурой плавления 191-192оС, МС (m/e): 414 (М+ -С), 335, 323, 295, 217, 91 (100%).
Соединения, описанные в нижеследующей табл. 2, были получены в соответствии с приведенными примерами получения. Структуры соединений следует определять по номерам соединений в табл.1. Самый правый столбец в табл.2 указывает номер примера получения, согласно которому было получено соединение.
Пример формулы 1 (таблетки) Соединение N
85 10 г Лактоза 20 г Крахмал 4 г Крахмал для пасты 1 г Стеарат магния 0,1 г Кальциевая соль карбоксиметилцеллюлозы 7 г Всего 42,1 г
Перечисленные компоненты смешивают обычным способом и
формулируют в виде покрытых сахаром таблеток, каждая из которых содержит 50 мг активного ингредиента.
Пример формулы 2 (капсулы) Соединение N 88 10 г Лактоза 20 г Микрокристаллическая
целлюлоза 10 г Стеарат магния 1 г Всего 41 г
Перечисленные компоненты смешали обычным способом и смесью наполнили желатиновые капсулы, так что получились капсулы, в каждой из которых
содержалось по 50 мг активного ингредиента.
Пример формулы 3 (мягкие капсулы) Соединение 94 10 г Кукурузное масло 35 г Всего 45 г
Перечисленные компоненты смешали и
формулировали обычным способом, так чтобы получить мягкие капсулы.
Пример формулы 4 (мазь) Соединение N 55 1,0 г Оливковое масло 20 г Белый вазелин 79 г Всего 100 г
Перечисленные выше компоненты смешали обычным способом, так чтобы получить 1%-ную мазь.
Пример формулы 5 (аэрозольная суспензия). (А) Соединение N 11 0,25 Изопропилмиристат 0,10%
Этанол 26,40% (Б) 60-40 смесь 1,2 дихлортетрафтор- этана и 1-хлорпента- фторэтана 73,25%
Смешали указанную композицию (А). Полученную таким образом растворенную смесь загрузили в контейнер,
снабженный клапаном, и пропеллант (Б) подавали из сопла клапана до манометрического давления примерно от 2,46 до 2,81 мг/см2, так чтобы получить аэрозольную суспензию.
Методика испытаний
1. Эффект подавления слипания тромбоцитов
1). Тест in vitro
(А). Эффект подавления слипания тромбоцитов у крыс.
Собрали кровь из центральной артерии самцов белой японской крысы (масса 1,8-2,5 кг) в пипетку, 1/10 объема которой было занято 3,8% цитратом натрия.
Полученную таким образом кровь подвергли центрифугированию при 200g в течение 7 мин при комнатной температуре, что имело целью получение обогащенной тромбоцитами плазмы (ОТП). Остаток далее подвергли центрифугированию при 2000q в течение 10 минут с целью получения бедной тромбоцитами плазмы (БТП). Измерения проводили на разбавленных до 300 000/мм3 БТП и ОТП. Плазму ОТП и БТП помещали в кювету и устанавливали интервал пропускания на 0% в случае ОТП и на 100% для БТП. Затем к ОТП добавили образец испытываемого лекарства, растворенный в 100% диметилсульфоксиде (ДМСО): конечная концентрация ДМСО 0,25% После термостатирования (37оС, 900 обмин в течение 2 мин) добавили агент, способствующий слипанию, с целью снятия кривой слипания. Вызываемый испытываемым образцом лекарства эффект подавления слипания тромбоцитов оценивали как концентрацию (IC50 μM), при которой агрегирование контрольного образца подавлялось на 50% Агенты, способствующие агрегированию ADP и арахидоновую кислоту (А.А) вводили в минимальных концентрациях (ADP: 5-10 μM; A.A. 0,2-0,3 мМ), вызывающих максимально интенсивное агрегирование. Измерение степени агрегирования осуществляли с помощью NBS НЕМА TRACER 601.
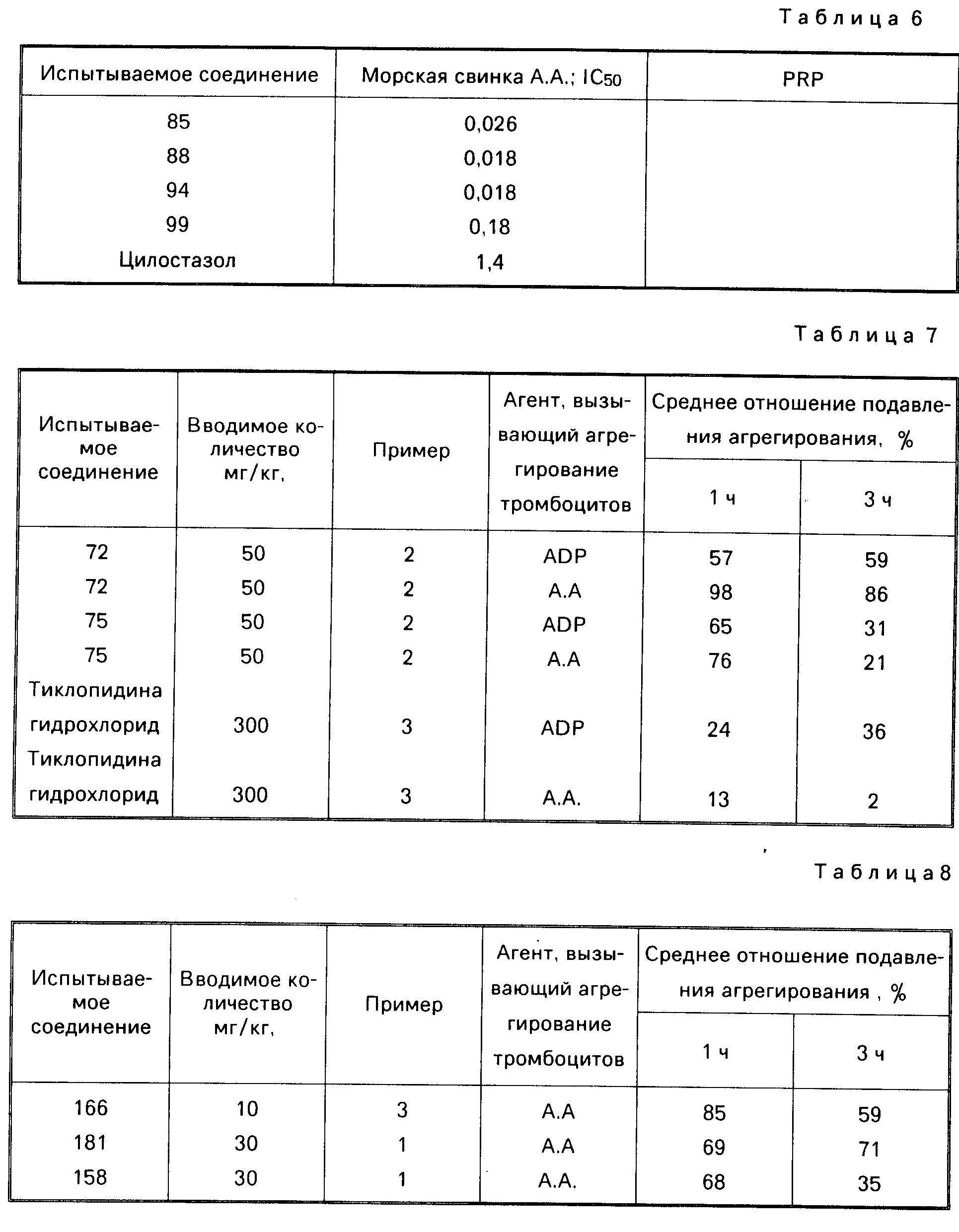
(Б) Эффект подавления агрегирования тромбоцитов у морских свинок
Собрали кровь из центральной артерии самца морской свинки типа Hartley (массой около 300 г)
точно так же, как описывалось выше, и подвергли центрифугированию при 160g в течение 10 мин при комнатной температуре с целью получения ОТП. Остаток далее подвергли центрифугированию при 3000g в
течение 10 мин. ОТП для измерений приготовили таким же способом, как и в вышеописанном эксперименте на крысах, и добавили, с целью вычисления значения концентрации IC50, при которой на
контрольном образце наблюдается 50%-е подавление агрегирования тромбоцитов, образец испытываемого лекарства растворенный в 100% ДМСО (конечная концентрация ДМСО: 0,5). В качестве агента, вызывающего
агрегирование тромбоцитов, использовали А.А. при конечной концентрации 0,1 мМ.
2. Тест in vivo.
(А) Эффект подавления слипания тромбоцитов у крыс.
После того, как самец японского белого кролика (вес: 1,8-2,5 кг) голодал в течение 18 ч, ему ввели перорально образец испытываемого лекарства в виде суспензии в 0,5% метилцеллюлозе. После введения
лекарства из ушной артерии периодически собирали кровь, и для оценки слипания тромбоцитов, вызываемого каждым агрегирующим агентом, приготовили ОТП точно так же, как и в вышеописанном испытании in
vitro. Эффект, вызываемый испытываемым лекарством, оценивали по соотношению подавляемого агрегирования, которое вычисляется при допущении, что до введения лекарства агрегирование тромбоцитов
составляло 100%
(Б) Эффект подавления слипания тромбоцитов у морских свинок
(1) После того, как самец морской свинки типа Хартли (вес: около 350 г) голодал в течение 18 ч, ему
перорально ввели образец испытываемого лекарства в виде суспензии в 5%-ном растворе гуммиарабика. После введения лекарства из центральной артерии периодически отбирали кровь и приготовили ОТП, как в
вышеописанном испытании in vitro, для измерения агрегирования тромбоцитов, вызываемого каждым агрегирующим агентом. Эффект от введения испытываемого лекарства оценивали по отношению подавления
агрегирования, которое вычислялось в предположении, что до введения лекарства агрегирование составляло 100
(2) После того, как самец морской свинки типа Хартли (вес: около 350 г) голодал в
течение 18 ч, ему перорально ввели образец испытываемого лекарства в виде суспензии в 5%-ном растворе гуммиарабика. Через час после введения собрали кровь из центральной артерии и приготовили ОТП
таким же способом, как в вышеописанном испытании in vitro, с целью измерения агрегирования тромбоцитов, вызванного каждым из агрегирующих агентов. Эффект, обусловленный введением образца испытываемого
лекарства, оценивали по величине отношения подавленного агрегирования, вычисленного в предположении, что до введения лекарства агрегирование тромбоцитов составляло 100%
(В) Имитация
тромбоцитопении у мышей
Коллаген (Hormon-Chemie Co. Ltd.), разведенный в изотоническом растворе хлорида натрия, ввели самцу мыши ICR (масса 24-30 г) через хвостовую вену в количестве 1 мг/5
мл/кг. Через 5 мин, под анестезией центобарбитала, отобрали 5 объемов крови из нижней полой вены в пластиковый шприц, в котором содержался один объем 3,8% цитрата натрия. Образец испытываемого
лекарства ввели перорально за час до введения коллагена. Собранную таким образом кровь развели в 20 раз Изотоном II и подвергли центрифугированию при 60g в течение 5 мин. Затем верхний слой опять
разбавили Изотоном II для измерения числа тромбоцитов с помощью счетчика Coulter (модель ZM).
В вышеописанных испытаниях 1-1 и 1-2 в качестве контрольных препаратов использовались тиклопидина гидрохлорид (Dauchi Seiyaku Co. Ltd) и Цилостазол (Otsuka Pharmaceutical Co. Ltd).
II. Кардиотонический эффект.
После обескровливания самца морской свинки (тип Хартли, 250-400 г) сердце извлекли и немедленно погрузили в питательный раствор (раствор Кребса-Хенселейта: NaCl 118,4 мМ, KCl 4,7 мМ, MgSO4·7Н2О 1,18 мМ, CaCl2·2H2O 2,5 мМ, KH2PO4 1,2 мМ, NaHCO3 24,9 мМ, глюкоза 11,1 мМ), аэрированный кислородом (в котором содержалось 5% диоксида углерода). Затем, чтобы получить образец для испытаний, поместили аэрированный кислородом питательный раствор в лабораторную кювету при непрерывном аэрировании кислородом. После быстрого отделения предсердия и желудочка, из правого желудочка приготовили препарат сосковидной мышцы и подвесили его в ванне для органов, наполненной аэрированным кислородом питательным раствором, при постоянной температуре 31оС, а затем приложили нагрузку на растяжение 500 мг.
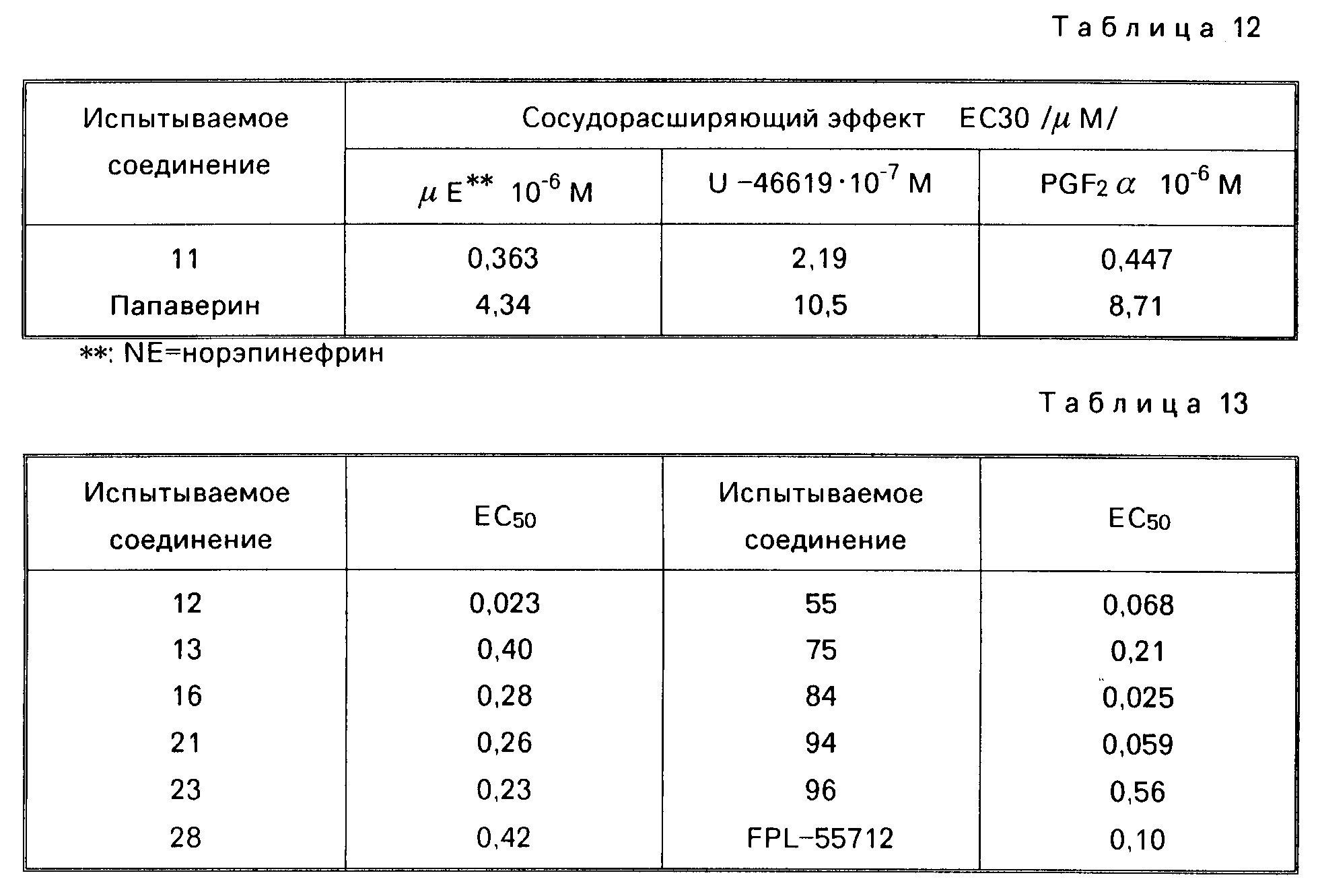
Через 20 мин после подвешивания препарата сосковидной мышцы питательный раствор заменили, а также через 40 мин, и после наблюдения еще в течение 20 мин, кумулятивным образом ввели изопротеренол (конечная концентрация 3 х 10-7 М) чтобы наблюдать его влияние на сократительную силу мышцы. После того, как операцию повторили еще раз вышеописанным образом, сменили питательный раствор через 20 мин и через 40 мин, и после наблюдения в течение еще 20 мин, кумулятивным способом ввели образец испытываемого лекарства. Эффект, который оказывало каждое испытываемое лекарство на сократительную силу, оценивали по величине относительного изменения (%), вызываемого испытываемым лекарством, в предположении, что разница величины сократительной силы при втором введении изопротеренола составляет 100% и вычисляли концентрацию ЕС30(μМ), необходимую для 30% увеличения.
Измерение сократительной силы осуществлялось путем наложения импульсов прямоугольной формы [напряжение: пороговая величина х 2 (V), продолжительность: 3 (мс), частота: 1 (Гц)] на сосковидную мышцу через биполярные платиновые электроды от электронного стимулятора (hihon Kohden SEN-3201) с целью регистрации возникающего напряжения на записывающем устройстве с помощью проволочного тензометра и F-D-захвата.
В качестве контрольного кардиотоника использовали милринон (Wintrop Co. ).
III. Вазодилаторный эффект
Самца крысы (тип белой японской крысы, 2-2,
5 кг) подвергли анестезии путем внутривенной инъекции нембутала [масса, кг х 0,5 + 0,5 мл] После обескровливания извлекли грудную аорту и погрузили ее немедленно в питательный раствор (раствор
Кребса-Хенселейта: NaCl 118,4 мМ, КСl 4,7 мМ, MgSO4 · 7H2O 1,188 мМ, СaCl2 · 2H2O 2,5 мМ, KH2PO4 1,2 мМ, NaHCO3 24,9 мМ, глюкоза 11,1 мМ), аэрированный кислородом (в котором содержалось 5% диоксида углерода). Затем ее поместили, с целью приготовления препарата, в лабораторную кювету, наполненную
аэрированным кислородом питательным раствором, и фиксировали оба конца кровеносного сосуда булавками с целью удаления жира и соединительной ткани. Спиралевидный препарат (ширина: 3 мм, длина: около 1
см) вырезали ножницами. Фиксировали скобой обе стороны препарата, и подвесили его в ванне для органов, наполненной аэрированным кислородом питательным раствором, при постоянной температуре 37оС, после чего приложили к нему растягивающее напряжение 2 г.
Растяжение кровеносного сосуда регистрировали с помощью записывающего устройства [hihon Kohden] путем F-D-захвата
[hihon Kohden 611-T] и проволочного тензометра [hihon Kohden AP-600G]
После подвешивания образца питательный раствор меняли через 20 и через 40 мин, наблюдая каждый образец еще в течение 20
мин (в течение которых растягивающее усилие составляло 2 г). Затем ввели норэпинефрин (конечная концентрация: 10-6 М) и наблюдали состояние кровеносного сосуда под воздействием напряжения.
После того, как образец наблюдали еще в течение 20 мин, вызвали сокращение кровеносного сосуда с помощью контрактильного агента. После установления стабильной степени сокращения ввели кумулятивным
способом образец испытываемого лекарства. По окончании испытания ввели папаверин (конечная концентрация: 10-4 М) для обеспечения полной релаксации.
Влияние образца
испытываемого лекарства на сокращение, вызываемое контрактильным агентом, оценивали по величине относительного изменения (%), вызываемого введением образца испытываемого лекарства, в предположении,
что разница между растягивающим усилием во время введения контрактильного агента и после введения папаверина составляет 100%
IV. Эффект противодействия SRS-A (эффект расширения бронхов)
Лекарство:
Образец испытываемого лекарства использовали в виде раствора в 100% диметилсульфоксиде (ДМСО, Wako Junyaku), Лейкотриен D4 (LTD4, Hetrafine) разбавляли
дистиллированной водой.
Индометацин (Indo, Sigma) растворяли в 100% этаноле (EtOH, Comune Kagaku). Аминофиллин (АР, Sigma), гистамина гидрохлорид (His, Wako Junyaku) растворяли в дистиллированной воде. Конечные концентрации ДМСО и EtOH в ванне не превышали, соответственно, 0,25% об/об и 0,1% об/об.
Методика.
Обескровили морскую свинку весом 300-450 г и извлекли трахею. После удаления жира и соединительной ткани ее разрезали на спиральные полоски шириной около 2 мм и разделили на 2-3 куска, каждый из которых содержал ткани 4 гладких мышц. Полученный таким образом препарат подвесили в ванне для органов емкостью 8 мл, в которой содержался модифицированный раствор Тироде, аэрированный смесью 95% О2 + 5% СО2 при 37оС, и к нему приложили нагрузку 1 г. Релаксацию мышцы регистрировали самописцем (Yokogama Hokushin Electric, тип 3066) с помощью изотонического преобразователя (Nihon Kohden TD-112S).
Модифицированный раствор Тироде имел следующий состав (мМ):
NaCl 1137, KCl 2,7, CaCl2 1,8, MgCl2 1,0, NaHCO3 20, NaH2PO4,
0,32, глюкоза 11.
Образец выдерживали в течение 50-60 мин, а затем вызывали его сокращение действием гистамина гидрохлорида (100 μМ). После установления постоянной реакции препарат промыли и выдержали в течение 20-30 мин. К препарату добавили индометацин (5 μМ), и после термостатирования в течение 30 мин вызвали сокращение препарата, добавили к нему LTD4 (30 nM). После того, как реакция стала стабильной, кумулятивным путем ввели испытываемое лекарство. И. наконец, добавили АР (1 мМ) для достижения выражались в процентах релаксации, в предположении, что релаксация под действием АР составила 100% и измеряли концентрацию, обеспечивающую достижение 50% релаксации (ЕС50, μМ).
В качестве контроля
использовали FPL-55712, известный как препарат, обладающий избирательным антагонистическим действием по отношению к SPS-A [Fisons LtD/; Journal of Medicinal Chemistry, Jol. 20, рр. 371-379, 1977]
Результаты испытаний
I. Эффект подавления агрегирования тромбоцитов.
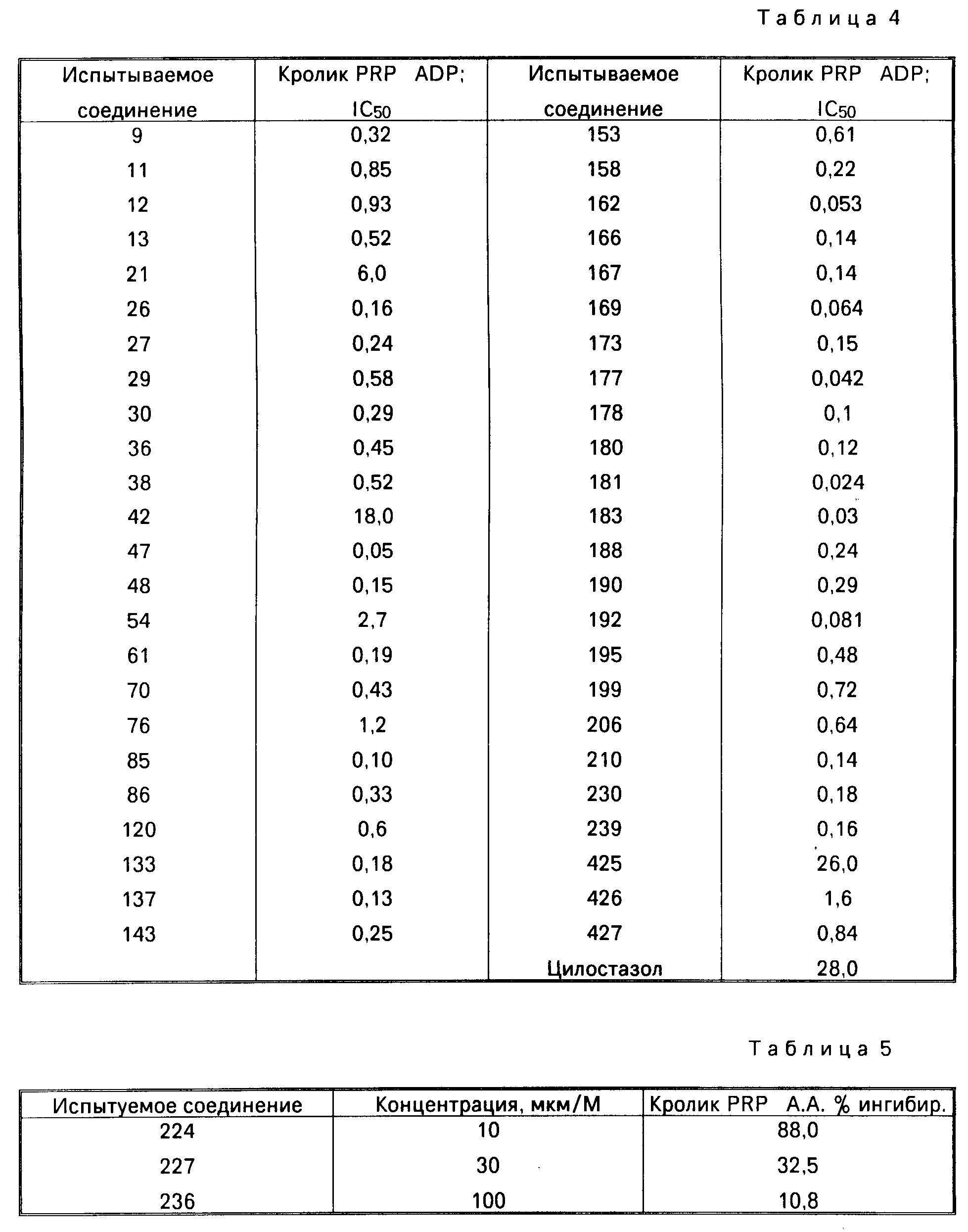
1. Испытания in vitro: (А), (Б)
Табл. 3-6 показывают эффект подавления агрегирования
тромбоцитов, вызываемый испытываемыми соединениями, который оценивался по величине IC50 (μМ).
2. Испытания in vivo.
(А) Эффект подавления агрегирования тромбоцитов у крыс приведен в табл. 7.
(Б) Эффект подавления агрегирования тромбоцитов у морских свинок (1) приведен в табл. 8, 9.
Эффект подавления агрегирования тромбоцитов у морских свинок (2).
(В) Эффект ингибирования редукции тромбоцитов мыши приведен в табл.10.
II. Кадиотонический эффект приведен в табл.11.
III. Сосудорасширяющий эффект приведен в табл.12.
IV. Эффект противодействия SRS-A приведен в табл.12.
Возможное применение в промышленности.
Как с очевидностью следует из приведенных результатов, соединения по данному изобретению обладают великолепным действием подавления агрегирования тромбоцитов, кардиотоническим действием, сосудорасширяющим действием и противодействием по отношению к SRS-А. Таким образом, соединения по данному изобретению могут быть использованы в качестве профилактических и терапевтических лекарственных препаратов для лечения различных связанных с тромбозом заболеваний, гипертонии, стенокардии, сердечной недостаточности и аллергических заболеваний немедленного типа, включая астму.
Реферат
Использование: в химико-фармацевтической промышленности.
Сущность изобретения: производные 3(2Н)пиридазинона ф-лы 1 или их фармацевтически приемлемые соли при определенных значениях радикалов и фармацевтическая композиция, обладающая противотромбической,
инотропной, сосудорасширяющей и антагонистической по отношению к медиатору активностью, содержащая в качестве активного ингредиента соединение ф-лы 1 или его фармацевтически приемлемую соль в
количестве 0,5 - 95 мас.%. 2 с. п. ф-лы. Структура соединения ф-лы 1:
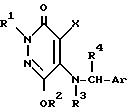
10 ил., 12 табл.
Формула
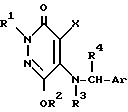
где R1 - водород, алкильная группа С1 - С4, группа общей формулы
-(СН2)n CO2R5,
где n = 1, 2 или 3;
R5 - водород или алкильная группа С1 - С4,
R2 - группа формулы A1 - Y1, где А1 - алкилен С1 - С12 с прямой или разветвленной цепью, Y1 - группа СО2R5, где R5 имеет указанные значения, цианогруппа, фенокси, тиенил, пиридил
или группа общей формулы
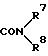
где R7 и R8 независимо - водород, алкил С1 - С4, циклогексил, фенил, или группа тиазолила или тиадиазолила или R7 и R8 вместе образуют алкиленовую группу С2 - С8, которая может быть замещена алкильной группой С1 - С3 или фенильной группой, или R7 и R8 вместе в атомом азота, к которому они присоединены, образуют морфолиновое кольцо,
или группа общей формулы
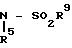
где R5 имеет указанные значения,
R9 - алкильная С1 - С4 или фенильная группа, необязательно замещенная галогеном,
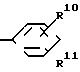
или общей группа формулы
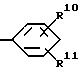
где R10 и R11 представляют независимо водород, галоген, С1 - С4-алкил, С1 - С4-алкокси, С1 - С4-алкилтио, гидроксил, С1 - С4 -алканоиламино, С1 - С4-алканоилокси или группу общей формулы NHSO2R9, где R9 имеет указанные значения,
или группа общей формулы
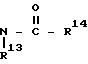
где R13 - водород, R14 - фенильная группа или R13 и R14 вместе образуют алкиленовую группу С2 - С8,
или группа общей формулы
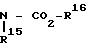
где R15 - водород или алкильная группа С1 - С4, R16 - алкильная группа С1 - С4, или R15 и R16 вместе образуют алкиленовую группу С2 - С8,
или группа общей формулы
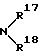
где R17 и R18 - независимо алкильная группа С1 - С4 или R17 и R18 вместе с атомом азота, к которому они присоединены, образуют пирролидино, пиперидино, оксазолидино, необязательно замещенные оксогруппой или они могут образовывать пиперазиногруппу, замещенную на другом атоме азота дифенилметилом или бензилом, которые в фенильном кольце могут быть замещены галогеном;
или группа формулы
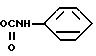
R3 - водород или С1 - С3-алкил;
R4 - водород;
Х - хлор, бром, водород или цианогруппа
Аг - группа общей формулы
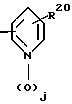
где j = 0 или 1;
R20 - водород, галоген или С1 - С4-алкоксигруппа или группа формулы
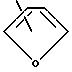
или группа общей формулы
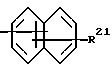
где R21 - водород или С1 - С4 -алкоксигруппа или группа общей формулы
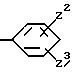
где Z2 и Z3 - независимо водород, галоген, алкильная группа С1 - С4 или С1 - С7-алкокси, причем последняя необязательно замещена фенилом, пиперидинокарбонилом или аминокарбонилом, при этом аминогруппа замещена С1 - С4-алкилом и циклогексилом,
или группа формулы
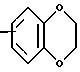
при условии, что если в группе A1 - Y1 Y1 - фенил, тогда А1 не может означать метилен,
или их фармацевтически приемлемые соли.

Комментарии