Средство для изменения скорости роста или репродукции клеток, способ его получения, способ стимуляции заживления ран или лечения ожогов, способ коррекции косметического дефекта, способ ингибирования старения кожи и способ стимуляции роста волос - RU2280459C2
Код документа: RU2280459C2
Чертежи




Описание
1. Введение
Настоящее изобретение относится к композициям, содержащим клеточную культуральную среду, кондиционированную клетками, выращенными в двухмерной культуре (то есть в монослое) или в трехмерной культуре. Клетки, используемые для кондиционирования среды, могут быть генетически модифицированы в целях изменения концентрации белков, присутствующих в данной среде. Кондиционированную клеточную среду обрабатывают для использования в различных целях, включая обработку ран, применение в качестве косметических добавок, пищевых добавок и добавок в корм животных, культивирование клеток, фармацевтическое применение, а также для использования в композициях и методах для стимуляции роста волос. Настоящее изобретение также относится к композициям, содержащим белки внеклеточного матрикса и/или другие очищенные белки, происходящие от данной кондиционированной среды.
2. Предпосылки создания изобретения
2.1. Кондиционированная клеточная среда
Композиции, содержащие культуральную среду, обычно включают незаменимые аминокислоты, соли, витамины, минералы, следовые количества металлов, сахара, липиды и нуклеозиды. Были сделаны попытки создать среду для культивирования клеток, являющуюся источником компонентов, необходимых для удовлетворения потребностей в питательных веществах, требующихся для роста клеток в контролируемой, искусственной и in vitro-среде. Питательные композиции, рН и осмомолярность варьируется в соответствии с такими параметрами, как тип клеток, клеточная плотность и система, используемая для культивирования. Многие композиции, содержащие клеточные культуральные среды, описаны в литературе, а некоторые среды являются коммерчески доступными. Специалистам известно, что после инкубирования культуральной среды с клетками эта среда становится "истощенной" или "кондиционированной" средой. Кондиционированные среды содержат много исходных компонентов самой среды, а также различные клеточные метаболиты и секретированные белки, включая, например, биологически активные факторы роста, медиаторы воспаления и другие внеклеточные белки. Клеточные линии растут в виде монослоя или на гранулах в отличие от клеток, растущих в трехмерной среде, в которой отсутствуют взаимодействия клеток друг с другом и клеток с внеклеточным матриксом, характерные для всех тканей in vivo. Поэтому такие клетки секретируют ряд клеточных метаболитов, хотя они необязательно должны секретировать эти метаболиты, и уровни секретированных белов приближаются к физиологическим уровням. Стандартную кондиционированную клеточную культуральную среду, то есть среду, культивированную клеточными линиями, растущими в виде монослоя или на гранулах, обычно отбрасывают, а иногда используют в манипуляциях с культурами, таких как снижение плотности клеток.
2.2. Системы для культивирования тканей
Большинство клеточных культур позвоночных выращивают in vitro в виде монослоев на искусственном субстрате, погруженном в культуральную среду. Субстраты, на которых растут указанные монослои, могут быть, по своей природе, твердыми, такими как пластик, или полутвердыми гелями, такими как коллаген или агар. В настоящее время предпочтительными субстратами, используемыми при культивировании тканей или клеток, являются пластики для одноразового применения.
Несколько специалистов провели исследования по использованию природных субстратов для компонентов базальных мембран. Базальные мембраны включают смесь гликопротеинов и протеогликанов, окружающих большинство клеток in vivo. Так, например, Reid & Rojkund, 1979, Methods in Enzymology, Vol.57, Cell Culture, Jakoby & Fasten, eds., New York, Acad. Press, pp.263-278; Viodavsky et al., 1980, Cell 19:607-617; Yang et al., 1979, Proc.Nati.Acad.Sci. USA 76:3401 использовали коллаген для культивирования гепатоцитов, эпителиальных клеток и эндотелиальной ткани. В попытке стимулировать терминальную дифференцировку использовали рост клеток на флотирующем коллагене (Michalopoulos & Pitot, 1975, Fed. Proc. 34:826) и на мембранах с нитратом целлюлозы (Savage & Bonney, 1978, Exp.Cell.Res. 114:307-315). Однако пролонгированная клеточная регенерация и культивирование таких тканей в указанных системах до сих пор не были осуществлены.
Для усиления роста клеток, а особенно при низкой плотности, были использованы культуры фибробластов эмбрионов мышей. Предполагается, что этот эффект обусловлен отчасти пополнением данной среды, но он может быть также обусловлен кондиционированием субстрата клеточными продуктами. В этих системах питающие слои фибробластов росли как конфлюентные монослои, которые делают данную поверхность подходящей для прикрепления других клеток. Так, например, сообщалось о росте глиомы на конфлюентных питающих слоях нормальных фетальных клеток кишечника (Lindsay 1979, Nature 228:80).
Хотя культивирование клеток в двухмерной среде является стандартным способом получения, наблюдения и исследования клеток в культуре, позволяющим достигать высокой степени пролиферации клеток, однако, он является нехарактерным для целых тканей In vivo. Для исследования таких функциональных и морфологических взаимодействий некоторые исследователи использовали трехмерные субстраты, такие как коллагеновый гель (Douglas et al., 1980, In Vitro 16:306-312; Yang et al., 1979, Proc. Natl. Acad. Sci. 76:3401; Yang et al., 1980, Proc. Natl. Acad. Sci. 77:2088-2092; Yang et al., 1981, Cancer Res. 41:1021-1027); целлюлозная губка, взятая отдельно (Leighton et al., 1951, J. Natl. Cancer. Inst. 12:545-561) или покрытая коллагеном (Leighton et al., 1968, Cancer Res. 28:286-296); желатиновая губка, Gelfoam (Sorour et al., 1975, J.Neurosurg. 43:742-749).
В основном эти трехмерные субстраты инокулировали культивируемыми клетками. Сообщалось, что многие клетки этих типов проникали в матрикс и создавали "тканеподобную" гистологию. Так, например, трехмерные коллагеновые гели были использованы для культивирования эпителия молочной железы (Yang efc al., 1981, Cancer. Res. 41:1021-1027) и нейронов симпатической нервной системы (Ebendal, 1978, Exp.Cell Res. 98:159-169). Кроме того, были предприняты различные попытки регенерации тканеподобной архитектуры из диспергированных культур монослоев. Kruse & Miedema (1965, J.Cell Biol. 27:273) сообщали, что перфузионные монослои могли расти до глубины более чем в десять клеток, а в том случае, когда проводили подпитку соответствующей средой в многослойных культурах могли развиваться органоидные структуры (см. также Schneider et al., 1963, Exp.Cell Res. 30:449-459; Bell et al., 1979, Proc.Natl. Acad. Sci., USA, 76:1274-1279; Green, 1979, Science 200:1385-1388). Сообщалось, что эпидермальные кератиноциты человека могут образовывать дерматоглифы (фрикционныие гребешки, если они выдерживаются в течение нескольких недель без переноса); Folkmann и Haudenschild (1980, Nature 288:551-556) сообщали об образовании капиллярных канальцев в культурах сосудистых эндотелиальных клеток, культивированных в присутствии эндотелиального фактора роста и среды, кондиционированной опухолевыми клетками; Sirica и др. (1979, Proc.Natl. Acad. Sci., USA, 76:283-287; 1980, Cancer Res. 40:3259-3267) поддерживали гепатоциты в первичной культуре в течение приблизительно 10-13 дней на найлоновых ситах, покрытых тонким слоем коллагена. Однако в таких системах не была получена долгоживущая культура и не была достигнута пролиферация клеток.
Была предпринята попытка создания долгоживущей культуры тканей, таких как костный мозг. В целом все полученные результаты были разочаровывающими, то есть, хотя слой стромальных клеток, содержащих клетки различного типа, образовывался быстро, однако, какой-либо значимый гемопоэз не мог поддерживаться в течение какого-либо реального времени (обзор см. Dexter et al., In Long Term Bone Marrow Culture, 1984, Alan R. Liss, Inc., pp.57-96).
Некоторые группы исследователей предприняли попытки вырастить ткани кожи и соединительной ткани in vitro для трансплантации in vivo. В одной из таких систем гидратированная бычья коллагеновая решетка образует субстрат, в который внедряются клетки, такие как фибробласты, что приводит к стягиванию этой решетки в ткань (Bell et al., патент США №4485096). В другой системе для культивирования клеток фибробластов использовалась пористая перекрестно сшитая коллагеновая губка (Eisenberg, WO 91/16010). Был также описан каркас, состоящий из синтетических полимеров и предназначенный для регулирования клеточного роста и пролиферации in vitro так, чтобы после начала роста фибробластов и присоединения их к матриксу, их можно было трансплантировать пациенту (Vacanti et al., патенты США №5759830; 5770193; 5736372).
В качестве каркаса для роста клеток были также сконструированы и разработаны синтетические матрицы, состоящие из биологически разлагаемых, биологически совместимых сополимеров полиэфиров и аминокислот (патент США №5654381; 5709854). Биологически неразлагаемые каркасы также способны поддерживать рост клеток. Были также разработаны трехмерные системы культивирования клеток, которые состоят из стромального матрикса, поддерживающего рост клеток из любой нужной ткани с образованием зрелой ткани (Naughton et al., патенты США №№4721096 и 5032508). Другой метод предусматривает получение медленно полимеризующихся гидрогелей, содержащих большое число клеток нужного типа, которые внедряются в матрикс после их введения пациенту (патент США №5709854). Были сконструированы внеклеточные матриксные препараты, которые состоят из стромальных клеток, обеспечивающих трехмерную систему для культивирования клеток нужного типа, и которые могут быть инъецированы пациенту для точного включения данного биоматериала в организм пациента (Naughton et al. WO 96/39101).
2.3. Клеточные цитокины и факторы роста
Секреция внеклеточных белков, таких как факторы роста, цитокины и белки стрессов, в кондиционированные клеточные среды открывает новые возможности в получении продуктов для использования в различных целях, включая репарацию тканей, например, при лечении ран и других дефектов ткани, таких как косметические дефекты, а также для использования в качестве пищевых добавок в пищу человека и в корм животных. Так, например, известно, что факторы роста играют важную роль в процессе заживления ран. В основном, очевидно, что при лечении ран желательно увеличить уровень поставляемых факторов роста путем прямого введения этих факторов.
Клеточные цитокины и факторы роста участвуют в ряде важных клеточных процессов, включая пролиферацию клеток, адгезию клеток, морфологию клеток, дифференцировку клеток, миграцию клеток, воспалительные реакции, ангиогенез и гибель клеток. Исследования продемонстрировали, что гипоксический стресс и повреждение клеток индуцирует ответную реакцию, включая повышение уровней мРНК и белков, соответствующих факторам роста, таким как PDGF (тромбоцит-производный фактор роста), VEGF (сосудистый эндотелиальный фактор роста), FGF (фактор роста тромбоцитов) и IGF (инсулиноподобный фактор роста)(Gonzalez-Rubio, M. et al., 1996, Kidney Int. 50(1):164-73; Abramovitch, R. et al., 1997, Int. J. Exp. Pathol. 78(2):57-70; Stein I. et al., 1995, Mol.Cell.Biol. 15(10):5363-8; Yang W. et al., 1997, FEBS Lett. 403(2):139-42; West, N.R. et al. 1995, J.Neurosci. Res. 40 (5):647-59).
Факторы роста, такие как трансформирующий фактор роста-β, также известные специалистам как TGF-β, индуцируются некоторыми белками стрессов в процессе заживления ран. Известны два белка стрессов, GRP78 и HSP90. Эти белки стабилизируют клеточные структуры и сообщают клеткам резистентность к неблагоприятным условиям. Семейство димерных белков TGF-β включает TGF-β1, TGF-β2 и TGF-β3 и регулирует рост и дифференцировку клеток многих типов. Кроме того, это семейство белков обладает рядом биологических эффектов, стимулирующих рост клеток некоторых типов (Noda et al., 1989, Endocrinology 124:2991-2995) и ингибирующих рост клеток других типов (Goey et al., 1989, J.Immunol. 143:877-880; Pietenpol et al., 1990, Proc.Natl.Acad.Sci.USA 87:3758-3762). Было также показано, что TGF-β способствует повышению экспрессии белков внеклеточного матрикса, включая коллаген и фибронектин (Ignotz et al., 1986, J.Biol.Chem. 261:4337-4345), и ускорению заживления ран (Mustoe et al., 1987, Science 237:1333-1335).
Другим таким фактором роста является PDGF. PDGF был первоначально обнаружен как сильный митоген для мезенхимных клеток. (Ross R. et al., 1974, Proc.Natl. Acad. Sci., USA, 71(4):1207-1210; Kohler N. et al., 1974, Exp.Cell Res. 87:297-301). Последующие исследования показали, что PDGF способствует увеличению уровня насыщенности клетками и грануляции ткани при ее образовании. Раны, заживляемые с помощью PDGF, на ранней стадии имеют внешний вид воспалительного ответа, заключающегося в увеличении количества клеток типов нейтрофилов и макрофагов в области раны. В этих ранах также наблюдается повышенная функция фибробластов (Pierce G.F. et al., 1988, J.Exp.Med. 167:974-987). При исследовании животных было показано, что как PDGF, так и TGF-β способствуют стимуляции образования коллагена, увеличению содержания ДНК и уровней белков (Grotendorst G.R. et al., 1985, J. Clin. Invest. 76:2323-2329; Sporn, M.B. et al., 1983, Science (Wash DC) 219:1329). Было показано, что PDGF является эффективным для лечения ран у человека. В ранах человека, например в пролежнях, подвергающихся заживлению, экспрессия PDGF-AA усиливается. Такое увеличение PDGF-AA соответствует увеличению активированных фибробластов, отложению межклеточного матрикса и активной васкулялизации раны. Кроме того, такое увеличение PDGF-AA не наблюдается в хронических незаживающих ранах (Principles of Tissue Engineering, R. Lanza et al. (eds.) pp.133-141 (R.G. Landes Co. TX 1997). Рядом других факторов роста, обладающих способностью к индуцированию ангиогенеза и к заживлению ран, являются VEGF, KGF и основный FGF.
В настоящее время не существует простых эффективных методов или композиций для применения сред, содержащих различные цитокины, факторы роста или другие регуляторные белки, обнаруживаемые в кондиционированных средах настоящего изобретения.
3. Краткое описание изобретения
Заявителями настоящего изобретения описаны новые композиции кондиционированной клеточной культуральной среды. Кроме того, настоящее изобретение относится к использованию этих новых композиций. Настоящее изобретение также относится к композициям, содержащим конкретные белковые продукты, происходящие от кондиционированной клеточной среды настоящего изобретения.
Композиции кондиционированной клеточной среды настоящего изобретения могут состоять из любой известной определенной или неопределенной среды и могут быть кондиционированы с использованием любых эукариотических клеток. Эта среда может быть кондиционирована стромальными клетками, паренхимными клетками, мезенхимными стволовыми клетками, резервными клетками печени, стволовыми нервными клетками, стволовыми клетками поджелудочной железы и/или эмбриональными стволовыми клетками. Предпочтительной является трехмерная тканевая конструкция. Клетки этого типа, независимо от того, присутствуют они в монослое или в трехмерном пространстве, будут влиять на свойства кондиционированной среды. Так, например, среда, кондиционированная астроцитами и нейронами, будет вырабатывать некоторые характерные метаболиты и белки, а поэтому такая кондиционированная среда является предпочтительной для некоторых применений в целях репарации нервной ткани. В предпочтительных вариантах осуществления изобретения среда кондиционирована трехмерной клеточной и тканевой культурой. В другом предпочтительном варианте осуществления изобретения среда кондиционирована стромальными клетками, использованными в продуцировании TransCyte™ (Smith & Nephew PLC., United Kingdom). В наиболее предпочтительном варианте осуществления изобретения клетками трехмерной тканевой культуры являются стромальные клетки, а конструкцией тканевой культуры является Dermagraft™ (Advanced Tissue Sciences, Inc., La Jolla CA) с добавлением или без добавления специфических паренхимных клеток. Такая кондиционированная клеточная среда дает уникальную комбинацию факторов и конкретных отношений, которая отличается от монослойных культур и которая наиболее близка к средам, наблюдаемым in vivo. Эта трехмерная стромальная культура может быть затем культивирована с паренхимными клетками, такими как клетки кожи, кости, печени, нервной системы, поджелудочной железы и т.п., с получением кондиционированной среды, содержащей характерные внеклеточные белки и другие метаболиты тканей этого типа. Кроме того, каждая клетка этого типа может быть также генетически модифицирована. Такая генетическая модификация может быть использована для изменения концентрации одного или нескольких компонентов в указанной среде, например, для позитивной регуляции белка, для введения нового белка или для регуляции концентрации ионов.
После кондиционирования клеточной среды настоящего изобретения она может быть использована в любом состоянии. Физическими вариантами этой кондиционированной среды являются, но не ограничиваются ими, жидкая или твердая среда, замороженная среда, лиофилизованная среда или среда, высушенная до порошкообразного состояния. Кроме того, эта среда может быть приготовлена в сочетании с фармацевтически приемлемым наполнителем, используемым в качестве носителя для внутреннего введения, для введенния непосредственно в пищу или пищевой продукт, для получения мази или растирания для местного применения или, например, она может быть изготовлена в виде хирургического клея или добавлена в него для ускорения заживления швов после хирургического вмешательства. Кроме того, указанная среда может быть дополнительно обработана для увеличения или уменьшения концентрации одного или нескольких факторов или компонентов, содержащихся в данной среде. Так, например, кондиционированная среда может быть обогащена факторами роста с использованием иммуноаффинной хроматографии.
В одном из вариантов настоящего изобретения кондиционированная среда настоящего изобретения используется для заживления ран. Примерами применения такой кондиционированной среды являются, но не ограничиваются ими, использование в марлевых повязках (адгезивных или неадгезивных) и местное применение для стимуляции и/или ускорения заживления ран. В этом случае указанная кондиционированная среда может быть обработана для увеличения или уменьшения концентрации одного или нескольких компонентов в целях ускорения заживления ран. Эти композиции могут быть лиофилизованы/высушены замораживанием и добавлены в наполнитель для ран, либо они могут быть добавлены в уже имеющиеся композиции для заполнения ран в целях ускорения их заживления. Альтернативно, указанная среда может быть добавлена в гидрогелевую композицию и использована в качестве пленки для местной обработки раны и в антиадгезивных компрессах. Композиции, содержащие среду настоящего изобретения, могут быть кондиционированы клетками, которые экспрессируют генные продукты с улучшенными свойствами, способствующими заживлению ран, то есть сконструированными клетками, которые экспрессируют генные продукты, обладающие свойствами, препятствующими образованию рубцов.
В другом варианте осуществления изобретения композиции, содержащие кондиционированную клеточную среду настоящего изобретения, могут быть использованы для коррекции врожденных патологий и устранения физических дефектов. Кроме того, композиции в форме препаратов для инъекций или гидрогелей могут быть использованы для разглаживания морщин и складок у бровей, устранения рубцов и других повреждений кожи. В другом варианте осуществления изобретения кондиционированная клеточная среда может быть также добавлена в тени для век, румяна, компактные пудры или в другие косметические препараты.
В еще одном варианте осуществления изобретения композиции, содержащие кондиционированную клеточную среду настоящего изобретения, могут быть использованы в качестве пищевых добавок или диетических добавок. Указанная кондиционированная среда содержит множество питательных веществ, включая незаменимые аминокислоты, витамины и минералы. Кондиционированная среда настоящего изобретения может быть, например, концентрирована и/или лиофилизована, а предпочтительно введена в капсулы или таблетки для проглатывания. Кроме того, указанные композиции могут быть также добавлены непосредственно в пищу для увеличения в ней питательных веществ.
В еще одном варианте осуществления изобретения указанные композиции могут быть использованы в качестве добавки в корм животных так, чтобы он содержал различные белки, витамины, антибиотики, полисахариды и другие факторы, благоприятно влияющие на рост крупного рогатого скота и других жвачных животных.
Еще в одном варианте осуществления изобретения композиции настоящего изобретения могут быть использованы для культивирования клеток. Кондиционированные клеточные среды настоящего изобретения содержат факторы, благоприятствующие прикреплению и росту клеток. Кроме того, клеточная среда может быть кондиционирована клетками, которые были трансформированы методами генной инженерии и которые могут, например, содержать повышенные концентрации фибронектина или коллагена, стимулирующие прикрепление клеток к каркасу или к поверхности культуры.
В еще одном варианте осуществлении изобретения композиции кондиционированной клеточной среды используются в фармацевтических целях. Настоящее изобретение относится к клеточным средам, культивируемым с трехмерными тканевыми конструкциями так, чтобы факторы роста и другие белки секретировались в данной среде в соотношениях, близких к наблюдаемым in vivo. Поэтому кондиционированные среды настоящего изобретения являются подходящими для различных фармацевтических применений.
И, наконец, композиции настоящего изобретения могут быть изготовлены в виде препаратов местного применения для стимуляции роста волос.
3.1. Определения
Используемые в настоящем описании термины имеют следующие значения:
Адгезивный слой: клетки, прикрепленные непосредственно к трехмерному носителю или связанные опосредованно путем прикрепления к клеткам, которые сами непосредственно прикреплены к носителю.
Кондиционированная среда: композиция, содержащая внеклеточный(е) белок(ки) и клеточные метаболиты, которые ранее поддерживали рост нужных эукариотических клеток любого типа, где указанные клетки были культивированы либо в двух-, либо в трехмерной среде. Эта среда иногда также называется "кондиционированной клеточной средой" или "кондиционированной средой для культивирования клеток или тканей".
Стромальные клетки: фибробласты вместе с другими клетками и/или элементами или без них, обнаруживаемые в рыхлой соединительной ткани, включая, но не ограничиваясь ими, эндотелиальные клетки, перициты, макрофаги, моноциты, клетки плазмы, тучные клетки, адипоциты, мезенхимные стволовые клетки, резервные клетки печени, нервные стволовые клетки, панкреатические стволовые клетки, хондроциты, прехондроциты и т.п.
Тканеспецифические или паренхимные клетки: клетки, которые образуют основную и отличительную ткань органа, отличающуюся от ее каркаса-носителя.
Трехмерный носитель: трехмерный каркас, состоящий из любого материала и/или имеющий любую форму, которая (а) позволяет клеткам прикрепляться к нему (либо он может быть модифицирован так, чтобы клетки могли прикрепляться к нему); и (b) способствует росту клеток более чем в одном слое. Этот носитель инокулирован стромальными клетками с образованием живой трехмерной стромальной ткани. Структура такого каркаса может быть типа сита, губки или она может быть образована из гидрогеля.
Трехмерная стромальная ткань или "живой" стромальный матрикс: трехмерный каркас, который был инокулирован стромальными клетками, выращенными на носителе. Белки внеклеточного матрикса, вырабатываемые стромальными клетками, осаждаются на указанном носителе, образуя, тем самым, "живую" стромальную ткань. Указанная живая стромальная ткань может поддерживать рост тканеспецифических клеток, которые затем инокулируют с образованием трехмерной клеточной культуры.
Тканеспецифическая трехмерная клеточная культура или тканеспецифическая трехмерная конструкция: трехмерная "живая" стромальная ткань, которая была инокулирована тканеспецифическими клетками и культивирована. В основном, тканеспецифическими клетками, используемыми для инокуляции трехмерного стромального матрикса, являются "стволовые" клетки (или "резервные" клетки) для данной ткани, то есть клетки, генерирующие новые клетки, которые при их созревании становятся "специализированными" клетками, образующими паренхиму ткани.
Нижеуказанные сокращения имеют следующие значения:
BCS = телячья сыворотка
BFU-E = эритроидная "взрывообразующая" единица
TGF-β = трансформирующий фактор роста β
CFU-C (КОЕ-К) = колониеобразующая единица в культуре
CFU-GEMM (КОЕ-ГЭММ) = колониеобразующая единица гранулоцитов, эритроцитов, моноцитов, мегакариоцитов
CSF (КСФ) = колониестимулирующий фактор
DMEM = модифицированная по методу Дульбекко среда Игла
EDTA = этилендиамин-тетрауксусная кислота
FBS = фетальная телячя сыворотка
FGF (ФРФ) = фактор роста фибробластов
GAG = гликозаминогликан
GM-CSF = гранулоцитарный/макрофагальный колониестимулирующий фактор
HBSS = сбалансированный солевой раствор Хэнкса
HS = лошадиная сыворотка
IGF (ИПФ) = инсулиноподобный фактор
LTBMC = долгоживущая культура клеток костного мозга
MEM = минимальная поддерживающая среда
PBL (ЛПК) = лейкоциты периферической крови
PBS = забуференный фосфатом физиологический раствор
PDGF (ТФР) = тромбоцит-производный фактор роста
RPMI 1640 = среда под номером 1640, разработанная Roswell Park Memorial Institute (GIBCO, Inc., Grand Island, N.Y.)
SEM - сканирующий электронный микроскоп
VEGF = сосудистый эндотелиальный фактор роста.
4. Описание графического материала
На фиг.1 представлен график, описывающий кинетику отложения гликозаминогликанов и коллагена, осаждаемых в зависимости от времени продуктами трехмерной ткани Transcyte™ и Dermagraft®. Объем отложения гликозаминогликанов зависит от периода роста, тогда как отложение коллагена не зависит от периода роста.
На фиг.2 представлен график влияния внеклеточного матрикса (удаленного из Transcyte™) и добавленного при разведении 1:2, 1:5, 1:10 и 1:100 к монослойным культурам человеческих фибробластов и кератиноцитов. Наиболее значимый эффект проиллюстрирован при разведении матрикса в отношении 1:10.
На фиг.3 представлен график относительной пролиферации человеческих фибробластов и кератиноцитов, экспонированных кондиционированной средой (клеточная культуральная среда, на которой были предварительно выращены клетки в Transcyte™). Усиление клеточного ответа наблюдалось минимум через три дня.
На фиг.4 представлен график влияния кондиционированной среды 1х (среда для культивирования клеток, которая ранее поддерживала рост клеток в Transcyte™) на отложение коллагена из клеток, культивированных в трех измерениях по сравнению с основной средой DMEM (содержащей среду, дополненную 10% BCS и содержащую 2 мМ L-глутамина и 1х антибиотик/противогрибковый агент), в которую была добавлена бессывороточная среда и основная среда с конечной концентрацией 1х. Отложение коллагена в культурах, обработанных кондиционированной средой в течение 10 дней, возрастало почти на 50% по сравнению с каждым контролем со статистической значимостью (р=0,05).
На фиг.5 представлен график противоокислительной активности в кондиционированной клеточной среде (среда для культивирования клеток, которая ранее поддерживала рост клеток в Transcyte™) по отношению к эпидермальным кератиноцитам человека в культуре. При экспонировании кератиноцитов человека кондиционированной средой, которая ранее поддерживала рост клеток в Transcyte™, в течение трех дней, было отмечено, что внутриклеточное окисление снижалось почти на 50% со статистической значимостью (р<0,0003).
5. Подробное описание изобретения
Настоящее изобретение относится к новым композициям, содержащим любую кондиционированную определенную или неопределенную среду, культивированную с использованием эукариотических клеток любого типа или трехмерной тканевой конструкции, и к способам применения указанных композиций. Указанные клетки культивируют в монослое, на гранулах (то есть в двухмерной среде) или, предпочтительно, в трехмерной среде. Указанные клетки, предпочтительно, представляют собой клетки человека для снижения риска возникновения иммунного ответа, и такими клетками являются стромальные клетки, паренхимные клетки, мезенхимные стволовые клетки, резервные клетки печени, стволовые нервные клетки, панкреатические стволовые клетки и/или эмбриональные стволовые клетки. Среда, кондиционирования клеточной и тканевой культурами, будет содержать различные естественным образом секретированные белки, такие как биологически активные факторы роста, а среды, культивированные в трех измерениях, будут содержать эти белки в соотношениях, приближающихся к физиологическим уровням. Настоящее изобретение также относится к новым композициям, содержащим конкретные продукты белков, происходящих от кондиционированной клетками среды настоящего изобретения, и к использованию этих композиций.
"Предварительно кондиционированная" клеточная культуральная среда для культивирования клеток может быть любой средой для культивирования клеток, которая адекватно соответствует потребностям культивируемых клеток в питательных элементах. Примерами таких сред являются, но не ограничиваются ими, модифицированная по методу Дульбекко среда Игла (DMEM), среда Хэма F12, RPMI 1640, среда Исков, среда Маккой и другие композиции сред, известные специалистам, включая среды, описанные в работах Methods For Preparation of Media, Supplements and Substrate For Serum-Free Animal Cell Culture Alan R.Liss, New York (1984) и Cell & Tissue Culture: Laboratory Procedures, John Wiley & Sons Ltd., Chichester, England 1996, которые во всей своей полноте вводятся в настоящее описание посредством ссылки. Указанная среда может быть дополнена любыми компонентами, необходимыми для поддержания нужной клеточной или тканевой культуры. Если это необходимо, то дополнительно может быть добавлена сыворотка, такая как бычья сыворотка, которая представляет собой комплексный раствор альбуминов, глобулинов, стимуляторов роста и ингибиторов роста. Такая сыворотка не должна содержать патогенов и должна быть тщательно скринирована на загрязнение микоплазмой, бактериями, грибками и вирусами. Эта сыворотка должна быть также получена, в основном, из Соединенных Штатов и не должна поставляться из стран, в которых местный скот несет агенты-возбудители болезней. Добавление гормонов в среду может быть желательным, а может быть и нежелательным.
Другие ингредиенты, такие как витамины, факторы роста и адгезии, белки и т.п. могут быть выбраны специалистами в соответствии с целями применения. В настоящем изобретении могут быть использованы клетки любого типа, подходящие для получения нужной кондиционированной среды. Для культивирования среды могут быть использованы генетически сконструированные клетки. Такие клетки могут быть модифицированы, например, для экспрессии нужного белка или белков так, чтобы концентрация экспрессированного белка или белков в данной среде была оптимизирована для конкретной цели применения. В соответствии с настоящим изобретением клетки и тканевые культуры, используемые для кондиционирования среды, могут быть сконструированы так, чтобы они экспрессировали нужный генный продукт, который может быть наделен широким рядом функций, включая, но не ограничиваясь ими, повышенную способность экспрессировать белки, имеющие аналогичные физиологические реакции и повышенную экспрессию конкретного белка, подходящего для конкретного применения, такого как белок, способствующий заживлению раны, или белок, ингибирующий некоторые другие белки, такие как протеаза, молочная кислота и т.п.
Указанные клетки могут быть сконструированы так, чтобы они экспрессировали нужный генный продукт, который является биологически активным и обладает выбранной биологической функцией, который действует как репортер для выбранного физиологического состояния, который усиливает недостаточную или дефектную экспрессию генного продукта или который обладает антивирусной, антибактериальной или противораковой активностью. В соответствии с настоящим изобретением целевым генным продуктом может быть пептид или белок, такой как фермент, гормон, цитокин, антиген или антитело, регуляторный белок, такой как транскрипционный фактор или ДНК-связывающий белок, структурный белок, такой как белок клеточной поверхности, либо таким целевым генным продуктом может быть нуклеиновая кислота, такая как рибосома или антисмысловая молекула. Указанными целевыми генными продуктами являются, но не ограничиваются ими, генные продукты, стимулирующие рост клеток. Так, например, генетическая модификация может обеспечивать позитивную регуляцию содержания эндогенных белков, введение нового белка или регуляцию концентрации ионов путем гетерологичной экспрессии ионных каналов или изменения функции эндогенных ионов. В качестве примеров могут служить, но не ограничиваются ими, сконструированные ткани, которые экспрессируют генные продукты для системной доставки (например, секретированные генные продукты, такие как белки, включая факторы роста, гормоны, фактор VIII, фактор IX, нейромедиаторы и энкафалины).
В соответствии с настоящим изобретением предпочтительно, чтобы указанные клетки были культивированы на трехмерном стромальном носителе и выращены в множественных слоях, образующих клеточный матрикс. Эта матриксная система в более высокой степени приближается к физиологическим условиям, наблюдаемым in vivo, чем ранее описанные монослойные системы тканевых культур. Трехмерные культуры, такие как Dermagraft® (Advanced Tissue Science, Inc., La Jolla, CA), и Transcyte™ (Smith & Nephew, PLC, United Kingdom), продуцируют множество факторов роста и других белков, которые секретируются в среду в физиологических отношениях и концентрациях. Dermagraft® состоит из аллогенных неонатальных фибробластов, культивированных на биологически разлагаемом полиглицине. Transcyte™ представляет собой временной (промежуточный) заменитель "живой" кожи, состоящий из трехмерной стромальной ткани, связанной с временным покрытием, как описано в патенте США 5460939. Кроме того, трехмерные тканевые культуры, которые кондиционируют клеточную среду, могут содержать мезенхимные стволовые клетки, резервные клетки печени, нервные стволовые клетки, панкреатические стволовые клетки, и/или эмбриональные стволовые клетки, и/или паренхимные клетки, и/или паренхимные стволовые клетки, обнаруживаемые в тканях многих типов, включая, но не ограничиваясь ими, ткани костного мозга, кожи, печени, поджелудочной железы, почек, надпочечника и нервной ткани, а также ткани желудочно-кишечного тракта и мочеполовых путей. См. патенты США №№4721096, 4963489, 5032508, 5266480, 5160490 и 5559022, каждый из которых во всей своей полноте вводится в настоящее описание посредством ссылки.
5.1. Клеточные среды
Композиции клеточных культуральных сред описаны в литературе и многие из них являются коммерчески доступными.
Ингредиентами предварительно кондиционированной среды являются, но не ограничиваются ими, ингредиенты, описанные ниже. Кроме того, концентрации этих ингредиентов хорошо известны каждому специалисту. См. например, Methods For Preparation of Media, Supplements and Substrate for Serum-free Animal Cell Culture, как указано выше. Указанными ингредиентами являются аминокислоты (D- и/или L-аминокислоты), такие как глутамин, аланин, аргинин, аспарагин, цистеин, глутаминовая кислота, глицин, гистидин, изолейцин, лейцин, лизин, метионин, фенилаланин, пролин, серин, треонин, триптофан, тирозин, валин и их производные; подгруппы растворимых кислот, таких как тиамин, аскорбиновая кислота, соединения железа(3), соединения железа(2), пурины, глутатион и одноосновные фосфаты натрия.
Другими ингредиентами являются сахара, дезоксирибоза, рибоза, нуклеозиды, водорастворимые витамины, рибофлавин, соли, металлы в следовых количествах, липиды, соли уксусной кислоты, соли фосфорной кислоты, HEPES, феноловый красный, соли пировиноградной кислоты и буферы.
Другими ингредиентами, часто используемыми в композициях сред, являются жирорастворимые витамины (включая A, D, Е и К), стероиды и их производные, холестерин, жирные кислоты и липиды, твин 80, 2-меркаптоэтанолпирамидины, а также ряд добавок, включая сыворотку (фетальную, лошадиную, телячью и т.п.), белки (инсулин, трансферрин, факторы роста, гормоны и т.п.), антибиотики (гентамицин, пенициллин, стрептамицин, амфотерицин В и т.п.), ультафильтрат цельного яйца и факторы адгезии (фибро-нектины, витронектины, коллагены, ламенины, тенасцины и т.п.).
Само собой разумеется, что в указанные среды могут или нет быть добавлены факторы роста и другие белки, такие как факторы адгезии, поскольку многие из этих клеточных конструкций, а, в частности, трехмерные конструкции клеточных и тканевых культур, описанные в настоящей заявке, сами вырабатывают такие факторы роста и факторы адгезии и другие белки, секретируемые в среды, описанные более подробно ниже, см. Раздел 5.8.
5.2. Клеточные культуры
5.2.1. Клетки
Данная среда может быть кондиционирована стромальными клетками, паренхимными клетками, мезенхимными стволовыми клетками (клетками, коммитированными или некоммитированными в отношении направления дифференцировки), резервными клетками печени, стволовыми нервными клетками, стволовыми клетками поджелудочной железы и/или эмбриональными стволовыми клетками. Такими клетками, среди прочих, являются, но не ограничиваются ими, клетки костного мозга, кожи, печени, поджелудочной железы, почек, нервной ткани, надпочечника, эпителия слизистой и гладких мышц. Фибробласты и подобные фибробластам клетки и другие клетки и/или элементы клеток, которые составляют строму, могут происходить от плода или зрелого организма и могут быть получены из соответствующих источников, таких как кожа, печень, поджелудочная железа, слизистая оболочка, артерии, вены, пупочный канатик и плацентарные ткани и т.п. Такие ткани и/или органы могут быть получены путем соответствующей биопсии или после аутопсии. Действительно, органы трупов могут быть использованы в качестве крупных источников стромальных клеток и элементов.
Эмбриональные стволовые клетки и/или другие элементы, которые составляют строму, могут быть выделены известными методами. Так, например, популяции человеческих эмбриональных стволовых клеток и методы их выделения и использования были недавно описаны Keller et al., Nature Med., 5:151-152 (1999), Smith Curr. Biol. 8:R802-804 (1998); выделенные первичные половые клетки были описаны Shamblatt et al., PNAS 95:13726-1373 (1998), клетки, выделенные из бластоцитов были описаны Thomason et al. Science 282:1145-1147 (1988). Методы выделения и культивирования мезенхимных стволовых клеток известны специалистам. См., Mackay et al. Tissue Eng. 4:415-428 (1988); William et al, Am.Surg. 65:22-26 (1999). Инокуляция этих клеток описана ниже, см. Раздел 5.3. Аналогичным образом стволовые клетки нервной ткани могут быть выделены способом, описанным Flax et al., Nature Biotechnol., 16:1033-1039 (1998); и Frisen et al., Cell. Mol. Life Sci., 54:935-945 (1998).
Эти клетки могут быть культивированы любым известным способом, например, в монослое, на гранулах или в трехмерном слое и любым другим способом (т.е. в чашках для культивирования, в роллер-флаконах, в системах с непрерывным потоком и т.п.). Методы культивирования клеток и тканей хорошо известны специалистам и описаны, например, в Cell & Tissue Culture: Laboratory Procedures, см.выше; Freshney (1987), Culture of Animal Cells: A Manual of Basic Techniques, cm. ниже.
В основном, используемые клеточные линии тщательно скринируют на патогены человека и животных. В зависимости от применения такой скрининг может иметь решающее значение, в том случае, когда пригодными являются лишь клетки, не содержащие патогенов (например, для лечения ран, для пищевых добавок и т.п.). Методы скрининга на патогены хорошо известны специалистам. Клетки такого типа, независимо от того, культивированы они в двух или в трех измерениях, будут оказывать влияние на свойства данной кондиционированной среды. Предпочтительной является трехмерная конструкция.
5.2.2. Трехмерные клеточные культуры
Стромальными клетками, используемыми в указанных трехмерных культурах, являются фибробласты, мезенхимные стволовые клетки, резервные клетки печени, нервные стволовые клетки, панкреатические стволовые клетки и/или эмбриональные стволовые клетки вместе с дополнительными клетками и/или элементами, описанными более подробно в данном описании, или без них.
Фибробласты будут поддерживать рост множества различных клеток и тканей в указанной трехмерной системе культивирования, и следовательно, они могут быть инокулированы в матрицу с образованием "общей" стромальной матрицы-основы для культивирования клеток и тканей любых типов. Однако в некоторых случаях может оказаться предпочтительным использование "специфической", а не "общей" стромальной матрицы-основы, и в данном случае стромальные клетки и элементы могут быть получены из конкретной ткани, органа или индивидуума. Кроме того, фибробласты и другие стромальные клетки и/или элементы могут быть получены из клеток того же типа, культивированных в указанной трехмерной системе. Это может быть предпочтительным при культивировании тканей, в которых "специализированные" стромальные клетки могут играть конкретную структурную/функциональную роль; например, клетки гладкой мышцы артерии, глиальные клетки нервной ткани, клетки печени Купфера и т.п.
При инокуляции на трехмерный носитель стромальные клетки будут пролиферировать на данном каркасе и выделять белки соединительной ткани, обычно секретируемые этими стромальными клетками, такие как факторы роста, регуляторные факторы и белки внеклеточного матрикса. Эти стромальные клетки и их естественнно секретируемые белки соединительной ткани, в основном, создают каркас, образуя таким образом живую стромальную ткань, которая будет поддерживать рост тканеспецифических клеток, инокулированных в данной трехмерной культуральной системе настоящего изобретения. Действительно, при инокуляции тканеспецифическими клетками данная трехмерная стромальная ткань будет поддерживать активную пролиферацию культуры в течение длительного промежутка времени. Это является очень важным фактором, поскольку поры в ситах позволяют стромальным клеткам проникать в культуру, не подвергая конфлюэнтные стромальные культуры контактному ингибированию, и стромальные клетки продолжают расти, делиться и при этом остаются функционально активными.
Факторы роста и регуляции вырабатываются стромальной тканью и секретируются в данную среду. Факторы роста (которыми являются, но не ограничиваются ими, αFGF, βFGF, инсулиновый фактор роста или TGF-бета), либо природные или модифицированные продукты крови или другие биологически активные молекулы (которыми являются, но не ограничиваются ими, гиалуроновая кислота или гормоны) усиливают колонизацию на трехмерной матрице или каркасе и кондиционирование куль-туральной среды.
Степень, с которой растут эти стромальные клетки перед использованием культур in vivo, может варьироваться в зависимости от типа ткани, культивируемой в трехмерной тканевой культуре. Живые стромальные ткани, которые кондиционируют среду, могут быть использованы в качестве корректирующих структур путем их имплантации in vivo. Эти стромальные клетки могут быть генетически модифицированы с доведением количества белковых продуктов, секретированных в культуральную среду, до такого уровня, при котором увеличивается концентрация выделенного продукта, полученного из кондиционированной среды. Таким продуктом являются противоспалительные факторы, например, антитело против GM-CSF, антитело против TNF, антитело против IL-1, IL-2 и т.п. Альтернативно, стромальные клетки могут быть генетически модифицированы для "нокаут"-экспрессии продуктов нативного гена, которые стимулируют воспаление, например, GM-CSF, TNF, IL-1, IL-2, или "нокаут"-экспрессии МНС для снижения риска отторжения.
Рост стромальных клеток в трех измерениях будет поддерживать активную пролиферацию как стромальных, так и тканеспецифических клеток в культуре в течение значительно более продолжительного времени, чем в монослойных системах. Более того, трехмерная система обеспечивает созревание, дифференцировку и сегрегацию клеток в культуре in vitro с образованием компонентов зрелых тканей, аналогичных аналогам, обнаруживаемым in vivo, и сохранение белков в кондиционированной среде в соотношениях, более близких к физиологическим отношениям.
Хотя заявители не должны или не обязаны объяснять механизм, посредством которого действует трехмерная клеточная и тканевая система, однако, успешному функционированию трехмерной культуральной системы способствуют ряд присущих ей следующих факторов:
(a) трехмерный каркас обеспечивает большую площадь поверхности для прикрепления белков, а следовательно, для адгезии стромальных клеток; и
(b) вследствие трехмерности каркаса стромальные клетки продолжают активный рост, в противоположность клеткам в монослойных культурах, которые растут до конфлюентности, испытывают контактное ингибирование и прекращают рост и деление. Продуцирование факторов роста и регуляторных факторов благодаря репликации стромальных клеток может быть частично ответственно за стимуляцию пролиферации и регуляцию дифференцировки клеток в культуре;
(c) этот трехмерный каркас позволяет осуществлять пространственное распределение клеточных элементов, которые являются более схожими с элементами, обнаруживаемыми в ткани-аналоге in vivo;
(d) увеличение потенциального объема роста для клеток в трехмерной системе может способствовать созданию локального микроокружения, стимулирующего созревание клеток;
(e) трехмерный каркас максимизирует межклеточное взаимодействие благодаря тому, что он дает больше возможностей для перемещения мигрирующих клеток, таких как макрофаги, моноциты и, возможно, лимфоциты в адгезивном слое;
(f) было установлено, что поддержание фенотипа дифференцированных клеток требует не только присутствия факторов роста/дифференцировки, но также и соответствующих клеточных взаимодействий. Настоящее изобретение позволяет эффективно воссоздавать микроокружение тканей, что приводит к образованию превосходной кондиционированной среды.
5.3. Создание трехмерной стромальной ткани
Трехмерный носитель или каркас может представлять собой любой материал и/или иметь любую форму, которые (а) позволяют клеткам прикрепляться к нему (либо он может быть модифицирован так, чтобы клетки прикреплялись к нему); и (b) позволяют клеткам расти более чем в одном слое. Для создания каркаса может быть использован ряд различных материалов, включая, но не ограничиваясь ими: биологически неразлагаемые материалы, например, найлон (полиамиды), дакрон (полиэфиры), полистирол, полипропилен, полиакрилаты, поливиниловые соединения (например, поливинилхлорид), поликарбонат (PVC), политетрафторэтилен (PTFE; тефлон), терманокс (ТРХ), нитроцеллюлоза, хлопок; и биологически разлагаемые материалы, например, полигликолевая кислота (PGA), коллаген, коллагеновые губки, кетгутовый материал для швов, целлюлоза, желатин, декстран, полиалканоаты и т.п. Любой из этих материалов может быть тканным, сплетенным, связанным и т.п. с получением сита, например, с образованием трехмерного каркаса. Этому каркасу может быть, в свою очередь, придана любая необходимая форма в качестве корректирующей структуры, например, форма трубок, шнуров, нитей и т.п. Некоторые материалы, такие как найлон, полистирол и т.п., являются плохими субстратами для прикрепления клеток. При использовании этих материалов в качестве трехмерного каркаса указанный каркас желательно предварительно обработать перед инокуляцией стромальных клеток в целях стимуляции прикрепления стромальных клеток к носителю. Так, например, перед инокуляцией стромальными клетками, найлоновые каркасы могут быть обработаны 0,1 М уксусной кислотой и инкубированы в полилизине, FBS, и/или в коллагене для покрытия ими найлона. Полистирол может быть аналогичным образом обработан с использованием серной кислоты.
При трансплантации in vivo культур, кондиционирующих среду, может оказаться предпочтительным использовать биологически разлагаемые матрицы, например, такие как полигликолевая кислота, коллаген, коллагеновые губки, тканный коллаген, материал для кетгутового шва, желатин, полимолочная кислота или полигликолевая кислота и их сополимеры. При поддерживании этих культур в течение длительных промежутков времени или при криоконсервации предпочтительными могут быть неразлагаемые материалы, такие как найлон, дакрон, полистирол, полиакрилаты, поливинилы, тефлоны, хлопок и т.п. Подходящим найлоновым ситом, которое может быть использовано в соответствии с настоящим изобретением, является нитекс (Nitex), найлоновый фильтр, имеющий средний размер пор 210 мкм и средний диаметр найлонового волокна 90 мкм (#3-210/36, Tetko, Inc., N.Y.).
Стромальные клетки, включая фибробласты, мезенхимные стволовые клетки, резервные клетки печени, нервные стволовые клетки, панкреатические стволовые клетки и/или эмбриональные стволовые клетки, вместе с дополнительными клетками и/или элементами, описанными ниже, или без них, инокулируют в каркас. Кроме того, клетки, обнаруживаемые в рыхлой соединительной ткани, могут быть инокулированы на трехмерный носитель вместе с фибробластами. Такими клетками являются, но не ограничиваются ими, клетки гладких мышц, эндотелиальные клетки, перициты, макрофаги, моноциты, клетки плазмы, тучные клетки, адипоциты и т.п. Как объяснялось ранее, фетальные фибробласты могут быть использованы для образования "общей" трехмерной стромальной матрицы, которая будет поддерживать рост различных клеток и/или тканей. Однако "специфическая" стромальная ткань может быть получена путем инокуляции трехмерного каркаса фибробластами, происходящими от культивируемой ткани того же типа и/или от конкретного индивидуума, которому позднее вводят эти клетки и/или ткани, выращенные в культуре в соответствии с трехмерной системой настоящего изобретения.
Таким образом, в одном из вариантов осуществления изобретения могут быть культивированы стромальные клетки, которые являются "специализированными" клетками для конкретной ткани. Так, например, стромальные клетки гемопоэтической ткани, включая, но не ограничиваясь ими, фибробласты, эндотелиальные клетки, макрофаги/моноциты, адипоциты и ретикулярные клетки, могут быть использованы для образования трехмерной субконфлюэнтной стромы для долгоживущей культуры костного мозга in vivo. Гемопоэтические стромальные клетки могут быть легко получены из "лейкоцитной пленки", образуемой в суспензии костного мозга путем центрифугирования при низкой центробежной силе, например при 3000 × g. В данном стромальном слое, который образует внутреннюю стенку артерии, могут быть добавлены большие количества недифференцированных клеток гладкой мышцы для получения эластичного белка. Стромальными клетками печени могут быть фибробласты, клетки Купфера и эндотелиальные клетки сосудов и желчных протоков. Аналогичным образом, в качестве стромы для поддержания пролиферации нервных клеток и тканей могут быть использованы глиальные клетки; причем глиальные клетки для этих целей могут быть получены путем трипсинизации или расщепления коллагеназой головного мозга эмбриона или взрослого индивидуума (Ponten & Westermark, 1980, in Federof, S.Hertz, L., eds, "Advances in Cellular Neurobiology, "Vol.1, New York, Academic Press, pp.209-227). Рост клеток в трехмерной стромальной клеточной культуре может быть дополнительно усилен путем добавления белков в данный каркас или путем покрытия носителя данными белками (например коллагенами, эластичными волокнами, ретикулярными волокнами), гликопротеинами, гликозаминогликанами (например гепаринсульфатом, хондроитин-4-сульфатом, хондроитин-6-сульфатом, дерматансульфатом, кератинсульфатом и т.п.), клеточным матриксом и/или другими материалами.
Кроме того, мезенхимные стволовые клетки (клетки, коммитированные или некоммитированные в отношении направления дифференцировки), являются преимущественными "стромальными" клетками для инокуляции в данный каркас. Эти клетки могут дифференцироваться в остеоциты, фибробласты сухожилий и связок, стромальные клетки костного мозга, адипоциты и другие клетки соединительной ткани, и хондроциты, в зависимости от времени, после добавления эндогенных или дополнительных факторов роста и регуляторных факторов, и других факторов, включая простагландины, интерлейкины и природные халоны, регулирующие пролиферацию и/или дифференцировку.
Фибробласты могут быть легко выделены путем дезагрегации соответствующего органа или ткани, который служит источником фибробластов. Это может быть легко осуществлено методами, известными специалистам. Так, например, данная ткань или орган могут быть дезинтегрированы механически и/или обработаны расщепляющими ферментами и/или хелатообразующими агентами, которые ослабляют связи между соседними клетками, что дает возможность диспергировать данную ткань в суспензию отдельных клеток без значительного разрушения клетки. Ферментативная диссоциация может быть осуществлена путем измельчения ткани и обработки указанной измельченной ткани любыми из ряда расщепляющих ферментов, взятых либо отдельно, либо в комбинации. Такими ферментами являются, но не ограничиваются ими, трипсин, хемотрипсин, коллагеназа, эластаза и/или гиалуронидаза, ДНКаза, проназа, диспаза и т.п. Механическое разрушение может быть также осуществлено рядом способов, включая, но не ограничиваясь ими, использование дезинтеграторов, смесителей, сит, гомогенизаторов, ячеек под давлением или ультразвуковых устройств и т.п. Обзор некоторых способов дезагрегации тканей см. Freshney, Culture of Animal Cells: A Manual of Basic Technique, 2d Ed., A.R. Liss, Inc. New York, 1987, Ch.9, pp.107-126.
После измельчения отдельных клеток с образованием суспензии эта суспензия может быть фракционирована с получением субпопуляций клеток, из которых могут быть получены фибробласты и/или другие стромальные клетки и/или элементы. Это может быть также осуществлено с использованием стандартной техники для разделения клеток, включая, но не ограничиваясь ими, клонирование и отбор клеток определенного типа, селективную деструкцию нежелательных клеток (негативный отбор), разделение на основе отличающихся агглютинирующих свойств клеток в смешанной популяции, процедуры замораживания-оттаивания, разделение на основе различных адгезивных свойств клеток в смешанной популяции, фильтрацию, стандартное и зональное центрифугирование, элютриационное центрифугирование (проточное центрифугирование), гравитационное разделение, противоточное распределение, электрофорез и сортинг флуоресцентно-активированных клеток. Обзор методов клонального отбора и разделения клеток см. Freshney, Culture of Animal Cells: A Manual of Basic Technique, 2d Ed., A.R. Liss, Inc. New York, 1987, Ch.ll and 12, pp.137-168.
Выделение фибробластов может быть, например, осуществлено следующим образом: свежие образцы ткани тщательно промывают и измельчают в сбалансированном растворе Хэнкса (HBSS) для удаления сыворотки. Измельченную ткань инкубируют 1-12 часов в свежеприготовленном растворе диссоциирующего фермента, такого как трипсин. После такого инкубирования диссоциированные клетки суспендируют, осаждают путем центрифугирования и высевают на чашки для культивирования. Все фибробласты прикрепляются раньше других клеток, а поэтому соответствующие стромальные клетки могут быть селективно выделены и выращены. Затем выделенные фибробласты могут быть культивированы до конфлюэнтности, перенесены из конфлюэнтной среды и инокулированы в трехмерный матрикс (см., Naughton et al., 1987, J.Med. 18 (3 and 4) 219-250). Инокуляция трехмерного каркаса высоконцентрированными стромальными клетками, например, приблизительно 106-5×106 клеток/мл, приводит к созданию трехмерной стромальной ткани за более короткие промежутки времени.
После инокуляции стромальных клеток трехмерный каркас должен быть инкубирован в подходящей питательной среде. Как упоминалось ранее, подходящими для использования могут быть многие коммерчески доступные среды, такие как RPMI 1640, среда Фишера, среда Исков, среда Маккой и т.п. Важно отметить, что трехмерные стромальные клеточные культуры могут быть суспендированы или флотированы в данной среде в процессе инкубирования для максимизации пролиферирующей активности. Эту культуру периодически "подпитывают", а кондиционированные среды настоящего изобретения выделяют и обрабатывают, как описано ниже в разделах 5.6 и 5.7. Таким образом, в зависимости от культивируемой ткани и от нужного типа коллагена соответствующие стромальные клетки могут быть отобраны для инокуляции трехмерного матрикса.
В процессе инкубирования трехмерных стромальных клеточных культур пролиферирующие клетки могут высвобождаться из данного матрикса. Эти высвобожденные клетки могут прилипать к стенкам сосуда для культивирования, где их пролиферация может продолжаться с образованием конфлюэнтного монослоя. Это событие должно быть предотвращено или сведено к минимуму, например, путем удаления высвобожденных клеток в процессе подпитки или путем переноса трехмерной стромальной культуры в новый сосуд для культивирования. Присутствие конфлюентного монослоя в сосуде будет "останавливать" рост клеток в трехмерном матриксе и/или культуре. Удаление конфлюэнтного монослоя или перенос культуры в новый сосуд со свежей средой будет восстанавливать пролиферирующую активность данной трехмерной культуральной системы. Следует отметить, что кондиционированные среды настоящего изобретения обрабатывают, при необходимости, так, чтобы они не содержали каких-либо целых клеток (если, конечно, эти целые клетки не используются для конкретных целей). Такое удаление или перенос должны быть проведены в любом сосуде для культивирования, который имеет стромальный монослой, конфлюэнтность которого превышает 25%. Альтернативно, указанная культуральная система может перемешиваться для предотвращения слипания высвобожденных клеток, либо вместо периодической подпитки культур, данная культуральная система может быть сформирована так, чтобы свежие среды непрерывно проходили через данную систему. Скорость потока может быть скорректирована для максимизации пролиферации в данной трехмерной культуре и для отмывки и удаления клеток, высвобожденных из этой культуры, так, чтобы они не прилипали к стенкам сосуда и не продолжали расти до конфлюэнтности.
Другие клетки, такие как паренхимные клетки, могут быть инокулированы и выращены на трехмерной живой стромальной ткани.
5.4. Инокуляция тканеспецифических клеток в трехмерный стромальный матрикс и поддерживание культур
После того, как трехмерная культура стромальных клеток достигнет соответствующего уровня роста, то дополнительные клетки, такие как тканеспецифические клетки (паренхимные клетки) или клетки поверхностного слоя, желательные для культивирования, могут быть также инокулированы в живую стромальную ткань. Эти клетки культивируют на живой стромальной ткани in vitro с образованием культивированного аналога нативной ткани и кондиционированием среды благодаря высвобождению в эту среду внеклеточных продуктов в отношениях, близких к физиологическим уровням. Высокая концентрация клеток в инокуляте будет преимущественно приводить к усилению пролиферации в культуре гораздо быстрее, чем низкая концентрация. Выбор клеток для инокуляции зависит от культивируемой ткани, которой может быть, но не ограничивается ею, костный мозг, кожа, печень, поджелудочная железа, почки, нервная ткань, надпочечник, эпителий слизистой оболочки и гладкая мышца и т.п. Эти клетки благодаря вырабатыванию в данных средах характерных внеклеточных белков, таких как определенные факторы роста, позволяют получать среды, оптимизированные для данных конкретных тканей.
В качестве неограничивающего примера может служить ряд эпителиальных клеток, которые могут быть культивированы на трехмерной живой стромальной ткани. Примерами таких эпителиальных клеток являются, но не ограничиваются ими, кератиноциты, клетки слизистой оболочки полости рта и клетки желудочно-кишечного тракта (ЖКТ). Такие эпителиальные клетки могут быть выделены ферментативной обработкой ткани известными методами с последующим размножением этих клеток в культуре и нанесением этих эпителиальных клеток на трехмерный матрикс-носитель стромальных клеток. Стромальный носитель обеспечивает присутствие факторов роста и других белков, которые стимулируют нормальное деление и дифференцировку эпителиальных клеток.
В основном, этот инокулят должен включать "стволовую" клетку (также называемую "резервной" клеткой) для этой ткани, то есть такие клетки, которые генерируют новые клетки, которые при созревании становятся специализированньми клетками, формирующими различные компоненты ткани.
Паренхимные клетки или другие клетки поверхностного слоя, используемые в данном инокуляте, могут быть получены из клеточных суспензий, приготовленных путем дезагрегации нужной ткани стандартными методами, описанными выше в Разделе 5.3 для получения стромальных клеток. Для инокуляции трехмерной живой стромальной ткани может быть использована сама суспензия целых клеток. В результате этого регенеративные клетки, содержащиеся в гомогенате, в отличие от не-регенеративных клеток, будут подвергаться пролиферации, созреванию и соответствующей дифференцировке на данной матрице. Альтернативно, клетки конкретного типа могут быть выделены из соответствующих фракций клеточной суспензии стандартными методами, описанными выше в Разделе 5.1 для фракционирования стромальных клеток. Если указанные "стволовые" клетки или "резервные" клетки могут быть легко выделены, то они могут быть использованы для преимущественной инокуляции трехмерного стромального носителя. Так, например, при культивировании костного мозга эта трехмерная строма может быть инокулирована клетками костного мозга, либо свежими клетками, либо клетками, полученными из криоконсервированного образца. При культивировании кожи трехмерная строма может быть инокулирована меланоцитами и кератиноцитами. При культивировании печени трехмерная строма может быть инокулирована гепатоцитами. При культивировании поджелудочной железы трехмерная строма может быть инокулирована эндокринными клетками поджелудочной железы. Обзор методов, которые могут быть использованы для получения паренхимных клеток из различных тканей, см. Freshney, Culture of Animal Cells: A Manual of Basic Technique, 2d Ed., A.R. Liss, Inc. New York, 1987, Ch.20, pp.257-288.
Фактически, различные соотношения коллагена различных типов, осажденного на стромальный матрикс до инокуляции, могут влиять на рост позже инокулированных тканеспецифических клеток. Так, например, для оптимального роста гемопоэтических клеток данный матрикс должен предпочтительно содержать коллаген типа III, IV и I в отношении приблизительно 6:3:1 в исходном матриксе. Для трехмерных систем культивирования клеток кожи в исходном матриксе предпочтительно осаждается коллаген типа I и III. Соотношения осажденных коллагенов различных типов могут быть изменены или увеличены путем отбора фибробластов, которые вырабатывают коллаген соответствующего типа. Это может быть осуществлено с использованием моноклональных антител соответствующего изотипа или подкласса, которые способны активировать комплемент и которые определяют коллаген данного типа. Указанные антитела и комплемент могут быть использованы для негативного отбора фибробластов, экспрессирующих коллаген нужного типа. Альтернативно, стромальные клетки, используемые для инокуляции матрицы, могут представлять собой смесь клеток, синтезирующих коллаген соответствующего типа. Распределение и происхождение коллагенов различных типов показаны в таблице 1.



В процессе инкубирования трехмерная клеточная культуральная система должна быть суспендирована или флотирована в питательной среде. Культуры должны периодически подпитываться свежей средой. И в этом случае следует позаботиться о предотвращении прилипания клеток, высвобожденных из культуры к стенкам сосуда, где они могут пролиферировать и образовывать конфлюэнтный монослой. Очевидно, что при культивировании диффузных тканей, в отличие от структурированных тканей, высвобождение клеток из трехмерной культуры становится более легким. Так, например, в соответствии с настоящим изобретением, трехмерная культура кожи является гистологически и морфологически нормальной; тогда как отдельные дермальные и эпидермальные слои не высвобождают клетки в поддерживающие среды. В противоположность этому трехмерные культуры костного мозга настоящего изобретения высвобождают зрелые не-адгезивные клетки в среду почти так же, как эти клетки высвобождаются в костном мозге In vivo. Как уже объяснялось ранее, если эти высвобожденные клетки будут прилипать к сосуду с культурой и образовывать конфлюэнтный монослой, то пролиферация трехмерной культуры будет "остановлена". Этого можно избежать путем удаления высвобожденных клеток во время подпитки или переноса трехмерной культуры в новый сосуд путем перемешивания культуры для предупреждения прилипания высвобожденных клеток к стенке сосуда, или путем непрерывной подачи потока свежей среды при скорости, достаточной для восполнения питательных веществ в культуре и удаления высвобожденных клеток. Как упоминалось ранее, кондиционированную среду обрабатывают, если это необходимо, так, чтобы в ней не содержалось целых клеток и клеточного дебриса.
На рост и активность клеток в культуре может негативно влиять ряд факторов роста, таких как инсулин, гормон роста, соматомедины, колониестимулирующие факторы, эритропоэтин, эпидермальный фактор роста, эритропоэтический фактор печени (гепатопоэтин) и фактор роста клеток печени. Другими факторами, регулирующими пролиферацию и/или дифференцировку, являются простагландины, интерлейкины и природные халоны.
5.5. Генетически сконструированные конструкции
В другом варианте осуществления изобретения трехмерные конструкции, кондиционирующие данные среды могут действовать как носители для введения генных продуктов в среды, которые, например, стимулируют репарацию и/или регенерацию дефектов ткани. Эти клетки могут быть генетически сконструированы для экспрессии, например, медиаторов воспаления, таких как IL-6, IL-8 и G-CSF. Кроме того, или альтернативно, эти клетки могут быть генетически сконструированы для экспрессии противовоспалительных факторов, например, антитела против GM-CSF, антитела против TNF, антитела против IL-1, IL-2 и т.п.
В другом варианте осуществления изобретения эти клетки могут быть генетически сконструированы для экспрессии гена в средах так, чтобы они обладали терапевтическим действием, например, при продуцировании TGF-β, стимуляцией генерирования хряща, при продуцировании других факторов, таких как BMP-13, стимуляцией формирования хряща, или при продуцировании стимулирующих факторов, стимулирующих миграцию стромальных клеток и/или отложение матрикса. Поскольку эти конструкции включают эукариотические клетки, то генный продукт может быть соответствующим образом экспрессирован и процессирован с образованием активного продукта. Такая экспрессия используемых регуляторных элементов, предпочтительно, должна обеспечивать регулируемую экспрессию гена так, чтобы в культуре мог происходить сверхсинтез данного продукта. В основном, выбор транскрипционного промотора и промоторных элементов зависит, отчасти, от типа ткани и культивированных клеток. При этом предпочтительными являются клетки и ткани, которые способны секретировать белки (например, которые обогащены такими органеллами, как шероховатый эндоплазматический ретикулум и комплекс Гольджи). Сверхпродуцированный генный продукт затем секретируется сконструированной клеткой в кондиционированную среду.
Клетки, используемые для кондиционирования данной среды могут быть генетически сконструированы в целях регуляции одного или более генов; либо регуляция экспрессии гена может быть кратковременной или длительной; либо активность гена может быть не-индуцибельной или индуцибельной.
Клетки, которые кондиционируют данную среду, могут быть также генетически модифицированы для "нокаут"-экспрессии факторов, которые стимулируют воспаление. Методы негативной модуляции, применяемые для снижения уровней экспрессии гена-мишени или уровней активности нужного генного продукта, обсуждаются ниже. Используемый здесь термин "негативная модуляция" означает снижение уровней генного продукта в отсутствии модулирующей обработки. Экспрессия гена, который является нативным для данной клетки, может быть снижена или прекращена различными способами, например, эта экспрессия может быть ингибирована путем полной инактивации гена (обычно называемой "нокаутом") с использованием стандартной техники гомологичной рекомбинации. Обычно, экзон, кодирующий важную область белка (или экзон с 5'-стороны от этой области цепи) прерывается позитивным селектируемым маркером (например, neo), что предупреждает продуцирование нормальной мРНК от гена-мишени и приводит к инактивации этого гена. Ген может быть также инактивирован путем создания делении или инактивирующей инсерции части гена, или путем делении целого гена. При использовании конструкции, имеющей две области гомологии с геном-мишенью, которые в данном геноме находятся на значительном расстоянии друг от друга, последовательности, находящиеся между этими двумя областями, могут быть делегированы. Mombaerts et al., 1991, Proc.Natl. Acad. Sci., USA, 88:3084-3087. Альтернативно, ген может быть также инактивирован путем делеции выше- или нижерасположенных экспрессионных элементов.
В соответствии с настоящим изобретением антисмысловые и рибозимные молекулы, ингибирующие экспрессию гена-мишени, могут быть также использованы для снижения уровня активности гена-мишени. Так, например, было показано, что антисмысловые РНК-молекулы, ингибирующие экспрессию гена главных комплексов гистосовместимости (ГКС), обнаруживают наибольший разброс в отношении иммунных ответов. Кроме того, могут быть сконструированы соответствующие рибозимные молекулы, описанные, например, Haseloff et al., 1988, Nature 334:585-591; Zaug et al., 1984, Science 224:574-578; и Zaug & Cech, 1986, Science 231:470-475. Кроме того, для снижения уровня активности гена-мишени могут быть использованы молекулы с тройной спиралью. Эти методы подробно описаны L.G.Davis et al., eds, Basic Methods in Molecular Biology, 2nd ed., Appleton & Lange, Norwalk, Conn. 1994.
Методы, которые могут быть использованы для генетического конструирования клеток настоящего изобретения, хорошо известны специалистам, и более подробно описаны в имеющих общего владельца патентах Соединенных штатов 4963489 и 5785964, содержание которых вводится в настоящее описание посредством ссылки. Так, например, рекомбинантная ДНК-конструкция или вектор, содержащий экзогенную нуклеиновую кислоту, например, кодирующую нужный генный продукт, могут быть сконструированы и использованы для трансформации или трансфекции стромальных клеток настоящего изобретения. Такие трансформированные или трансфицированные клетки, которые несут данную экзогенную нуклеиновую кислоту и которые способны экспрессировать указанную нуклеиновую кислоту, отбирают и клонально размножают в указанных трехмерных конструкциях настоящего изобретения.
Методы получения ДНК-конструкций, содержащих нужный ген, в целях трансформации или трансфекции клеток, в целях отбора клеток, несущих и экспрессирующих нужный ген, хорошо известны специалистам. См. например, методы, описанные Maniatis et al., 1989, Molecular Cloning. - A Laboratory Manual, Cold Spring Harbor Laboratory N.Y., Ausubel et al., 1989, Current Protocols in Molecular Biology, Greene Publisching Associates & Wiley Interscience, N.Y.; и Sambrook et al., 1989, Molecular Cloning: A Laboratory Manual, 2nd Ed., Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y.
Указанные клетки могут быть сконструированы с использованием ряда векторов, включая, но не ограничиваясь ими, интегрирующие вирусные векторы, например, ретровирусный вектор или аденоассоциированные вирусные векторы; или неинтегрирующие реплицирующиеся векторы, например, векторы на основе вируса папилломы, SV40-векторы, аденовирусные векторы; или дефектные по репликации вирусные векторы. Если требуется кратковременная экспрессия, то могут оказаться предпочтительными не-интегрирующие векторы и дефектные по репликации векторы, поскольку в этих системах для регуляции экспрессии нужного гена могут быть использованы либо индуцибельные, либо конститутивные промоторы. Альтернативно, интегрирующие векторы могут быть использованы для обеспечения кратковременной экспрессии, при условии, что нужный ген регулируется индуцибельным промотором. Другими методами введения ДНК в клетки является использование липосом, липофекция, электропорации, использование "дробовика" для выстреливания частиц или прямая инжекция ДНК.
Указанные клетки предпочтительно трансформируют или трансфецируют нуклеиновой кислотой, например, регулируемой ДНК, то есть функционально соединенной с одним или несколькими подходящими экспрессионными регуляторными элементами, такими как промоторные или энхансерные последовательности, терминаторы транскрипции, сайты полиаденилирования и т.п., и селектируемым маркером. После введения чужеродной ДНК сконструированные клетки могут быть культивированы в обогащенных средах, а затем могут быть перенесены на селективные среды. Селектируемый маркер в данной чужеродной ДНК сообщает резистентность для отбора и позволяет клеткам стабильно интегрировать чужеродную ДНК, например, в плазмиду или в свои хромосомы, а также расти с образованием фокусов, которые, в свою очередь, могут быть клонированы и размножены в клеточные линии. Этот метод может оказаться преимущественным для конструирования клеточных линий, экспрессирующих генные продукты в указанных средах.
Для регуляции экспрессии встроенного гена может быть использован любой промотор. Так, например, вирусными промоторами являются, но не ограничиваются ими, промотор/энхансер CMV, SV40, папилломавирус, вирус Эпштейна-Барра, промотор гена эластина и промотор гена β -глобина. Предпочтительно, регуляторные элементы, используемые для регуляции экспрессии нужного гена, должны обеспечивать регуляцию экспрессии данного гена так, чтобы данный продукт синтезировался in vivo только при необходимости. Если желательна кратковременная экспрессия, то в не-интергирующем и/или дефектном по репликации векторе, предпочтительно, использовать конститутивные промоторы. Альтернативно, для регуляции экспрессии встроенного гена, если это необходимо, могут быть использованы индуцибельные промоторы. Индуцибельные промоторы могут быть сконструированы в интергирующих и/или реплицирующихся векторах. Так, например, индуцибельными промоторами являются, но не ограничиваются ими, промоторы металлотиониена и промотор белков теплового шока.
В соответствии с настоящим изобретением индуцибельными промоторами, используемыми для экспрессии нужных экзогенных генов, являются нативные промоторы регуляторных белков, описанных в настоящей заявке, которые индуцируются в результате криоконсервации и последующего оттаивания. Так, например, промотор TGF-β, VEGF или известные белки теплового шока могут быть использованы в качестве экспрессионного регуляторного элемента, то есть они могут быть функционально присоединены к нужному экзогенному гену в целях экспрессии нужного генного продукта в тканевых конструкциях, кондиционирующих клеточные среды.
Для осуществления конститутивной или кратковременной экспрессии генных продуктов, сконструированных в клетках, может быть использован ряд методов. Так, например, может быть использован метод транскариотической трансформации, описанный Seldon et al., 1987, Science 236:714-718. Используемый здесь термин "транскариотический" предполагает, что ядра имплантированных клеток были модифицированы путем добавления ДНК-последовательностей посредством стабильной или кратковременной трансфекции. Клетки, предпочтительно, сконструируют так, чтобы под кратковременным и/или индуцибельным контролем, осуществляемым во время постоперативного выделения, экспрессировались такие генные продукты, как химерный гибридный белок, заякоренный на стромальных клетках, например химерная молекула, состоящая из внутриклеточного и/или трансмембранного домена рецепторной или рецепторподобной молекулы, слитой с генным продуктом в виде внеклеточного домена.
Кроме того, может оказаться предпочтительным получить конструкцию, имеющую внеклеточный матрикс, содержащий чужеродный генный продукт, фактор роста, регуляторный фактор и т.п., который затем будет присутствовать в кондиционированной среде. Этот вариант осуществления изобретения был разработан, исходя из обнаружения того факта, что во время роста человеческих стромальных клеток на трехмерном каркасе-носителе клетки синтезируют и осаждают на этом каркасе человеческий внутриклеточный матрикс так, как это происходит в нормальной человеческой ткани. Внеклеточный матрикс локально секретируется клетками, и не только связывает клетки и ткани вместе, но также влияет на развитие и поведение контактирующих клеток. Внутриклеточный матрикс содержит различные белки соединительной ткани, например волокнообразующие белки, внедренные в гидратированный гель, состоящий из сети цепей гликозаминогликанов. Эти гликозаминогликаны представляют собой гетерогенную группу длинных отрицательно заряженных полисахаридных цепей, которые (за исключением гиалуроновй кислоты) ковалентно связаны с белком с образованием молекулы протеогликанов. В соответствии с этим вариантом осуществления изобретения, стромальные клетки могут быть генетически сконструированы для экспрессии нужного генного продукта или модифицированных форм генного продукта, который будет присутствовать во внеклеточном матриксе и, в конечном счете, в клеточной среде.
5.6. Выделение кондиционированной среды
Клетки могут быть культивированы любыми способами, известными специалистам. Предпочтительно, чтобы клетки были культивированы в окружении, которое способно обеспечить асептическую обработку и транспортировку. Стандартные способы культивирования клеток и тканей ограничены тем, что данная среда должна находиться под наблюдением и контролем человека. Это ограничивает количество клеток и тканей, которое может быть культивировано за один промежуток времени, а следовательно, и объем кондиционированной среды, который может быть получен за один промежуток времени. По этой причине предпочтительно, чтобы данная среда была кондиционирована таким способом, который позволял бы проводить крупномасштабное культивирование (получение больших количеств кондиционированной среды) с использованием, например, аппарата для асептического крупномасштабного культивирования, подобно тому, который описан в принадлежащем соавторам патенте США 5763267 (патент '267), содержание которого во всей своей полноте вводится в настоящее описание посредством ссылки. С использованием асептически закрытой системы, описанной в патенте '267, предварительно кондиционированные культуральные среды переносят из резервуара с жидкостью во впускной коллектор, равномерно распределяют в культурах в системе с непрерывным потоком и используют для культивирования в трехмерных клеточных и тканевых культурах, например, таких как Dermagraft®. В частности, аппарат, описанный в патенте '267, включает множество гибких или полугибких камер для обработки, содержащих один или несколько отдельных карманов для культивирования, множество жестких разделителей, впускной жидкостный коллектор, выпускной жидкостный коллектор, резервуар для жидкости и приспособление для транспортировки жидкости в системе.
Во время обработки жидкая среда транспортируется из жидкостного резервуара во впускной коллектор, который, в свою очередь, равномерно распределяет данные среды по каждой из присоединенных к нему камер для обработки и по внутренним карманам для культивирования. Выпускной жидкостный коллектор также обеспечивает равномерное заполнение каждой камеры для обработки и удаление из указанных камер для обработки всех пузырьков воздуха, образовавшихся во время обработки. Камеры для обработки являются гибкими или полугибкими, так, чтобы конечный потребитель мог легко обращаться с ними во время промывания и введения культивированных трансплантатов. Благодаря гибкости указанных камер для обработки они могут быть также снабжены жесткими разделителями, которые обеспечивают равномерное распределение жидкости в этих камерах во время обработки. При необходимости (то есть после кондиционирования данной среды так, чтобы внеклеточные белки, такие как факторы роста, достигали в данной среде нужного уровня), среду для "кондиционирования" откачивают из системы и обрабатывают для использования. Предпочтительно, кондиционированную клеточную среду собирают из данного аппарата на более поздних стадиях роста ткани, если уровень некоторых факторов роста и секреция белков соединительной ткани достигает своего наиболее высокого уровня (см. Фиг.1). В предпочтительном варианте осуществления изобретения среду, кондиционированную трехмерной клеточной культурой, собирают после обработки этой среды клетками во время культивирования в течение 10-14 дней.
В другом варианте осуществления изобретения трехмерную ткань культивируют в аппарате для асептического роста трехмерных тканевых культур, как описано в патенте США №5843766 (патент '766), который во всей своей полноте вводится в настоящее описание посредством ссылки. В патенте '766 описана камера для тканевой культуры, где указанная камера представляет собой корпус, обеспечивающий рост трехмерной ткани, которая может быть выращена, сохранена в замороженном виде и доставлена конечному потребителю в том же самом асептическом контейнере. Камера для культивирования тканей включает корпус, в котором содержится субстрат, и который сконструирован для облегчения роста трехмерной ткани на поверхности этого субстрата. Указанный корпус включает впускное и выпускное отверстие, которое служит для подачи и выпуска среды. Этот корпус также включает, по крайней мере, один распределитель потока. В одном из вариантов осуществления изобретения этот распределитель потока представляет собой перегородку, которая используется для распределения потока среды в камере в целях создания непрерывного однородного фрагмента трехмерной ткани. Во втором варианте осуществления изобретения распределитель потока представляет собой комбинацию отклоняющих пластин, распределительных каналов и проточного канала. В каждом из описанных вариантов указанный корпус, кроме того, является герметичным так, чтобы он обеспечивал асептические условия внутри камеры во время роста и хранения ткани. И в этом случае, предпочтительно, среду собирают из данного аппарата на более поздних стадиях роста ткани, если уровень некоторых факторов роста и секреция белков соединительной ткани достигает своего наиболее высокого уровня, (см. Фиг.1). В предпочтительном варианте осуществления изобретения среду, кондиционированную трехмерной клеточной культурой, собирают после обработки этой среды клетками во время культивирования в течение 10-14 дней.
5.7. Концентрирование кондиционированной среды
После удаления кондиционированной клетками среды она может быть необходима для последующего процесса получения супернатанта. Такой процесс может включать, но не ограничивается ими, концентрированно с помощью устройства для фильтрации потока воды или путем дефильграции методами, описанными в Cell & Tissue Culture: Laboratory Procedure, см. выше, pp. 29D:0,1-29 D:0,4.
Кроме того, данная среда может быть подвергнута 10-20-кратному концентрированию с использованием концентрирующего устройства, работающего при избыточном давлении и имеющего фильтр с отсечкой 10000 мол. масс. (Amicon, Beverly, MA).
Кроме того, кондиционированная среда может быть также обработана для выделения и очистки продукта, например, в целях удаления нежелательных протеаз. Используемые методы выделения и очистки продукта, которые позволяют сохранить оптимальную активность, хорошо известны специалистам. Так, например, может оказаться желательной очистка фактора роста, регуляторного фактора, пептидного гормона, антитела и т.п. Такими методами являются, но не ограничиваются ими, гель-хроматография (с использованием матриц, таких как сефадекс), ионообменная хроматография, аффинная хроматография на хелате металла с нерастворимой матрицей, такой как перекрестно-сшитая агароза, ВЭЖХ-очистка и гидрофобная хроматография кондиционированной среды. Эти методы более подробно описаны в Cell & Tissue Culture: Laboratory Procedure, см. выше. Само собой разумеется, что в зависимости от целей применения кондиционированной среды и/или полученных из нее продуктов должны быть приняты соответствующие меры для поддержания стерильности. Альтернативно, может оказаться необходимой стерилизация, и она может быть осуществлена методами, известными специалистам, такими как, например, нагревание и/или стерилизация с помощью фильтра, при этом следует обеспечить сохранение нужной биологической активности.
5.7.1. Выделение коллагена
Как упоминалось ранее, кондиционированная среда настоящего изобретения содержит множество продуктов, которые могут быть из нее выделены и очищены. Так, например, фибробласты человеческой кожи синтезируют и секретируют предшественники коллагена и фракции этих предшественников включаются в трехмерный внеклеточный матрикс. Это включение требует удаления концевых пептидов (N- и С-пептидов), которые значительно снижают растворимость коллагеновых молекул (остальная часть секретированного коллагена остается в растворе из-за отсутствия протеолиза). В основном, растворимый коллаген может быть получен при нейтральных условиях рН и при высоких концентрациях соли. См., Kielty, С.М., I. Hopkinson, et al. (1993), Collagen: The Collagen Family: Structure, Assembly and Organization in the Extracellular Matrix, Connective Tissue and Its Heritable Disorders: molecular, genetics and medical aspects. P.M.Royce & B. Steinmann. New York, Wiley-Liss, Inc.:103-149). Заявителями представлены данные, иллюстрирующие действие кондиционированной среды (среды, которая ранее поддерживала рост клеток, культивированных в трех измерениях) на приготовление и состав трехмерных тканей, и полученные путем измерения количества коллагена, секретированного во внеклеточный матрикс тканей, культивированных в присутствии бессывороточной среды, питательной среды или трехмерной кондиционированной среды (см. Раздел 6.3). Кондиционированная среда настоящего изобретения значительно увеличивает отложение коллагена в ткани in vitro, как показано на фиг.4.
Кроме того, заявителями было неожиданно обнаружено, что отложение коллагена не носит линейный характер, а секретируется в возрастающих количествах в процессе культивирования (см. фиг.1). В соответствии с этим заявителями было использовано это открытие при сборе коллагена.
Следует отметить, что нижеследующий протокол приводится в качестве примера и может быть модифицирован методами, известными специалистам. Для очистки коллагена добавляют 240 мл среды, кондиционированной фибробластами к 240 мл 5 М NaCl (в отношении среды к соли 1:1) и осаждают в течение 16 часов при температуре 4°С. Суспензию центрифугируют приблизительно 20 минут при 4000 × g. Супернатант отбрасывают. Осадок промывают 10 мл раствора 50 мМ Трис-HCl (рН 7,5) и 2,4 М NaCl. Затем осуществляют центрифугирование в течение 20 минут при 4000 × g и супернатант отбрасывают. Осадок ресуспендируют в 10 мл 5М уксусной кислоты. Для удаления пропептидов добавляют 1 мл пепсина (100 мг/мл) (Sigma Chemical, St.Louis, МО) и гидролизуют в течение 16 часов при 4°С (при этом, пропептиды удаляются, а тройная спираль остается интактной). Суспензию центрифугируют в течение 20 минут при 4000 × g. Затем выделяют супернатант и осадок отбрасывают. После этого добавляют 2,1 мл 5М NaCl и 0,5М уксусной кислоты до конечного объема 15 мл (конечная концентрация NaCl 0,7 М). Затем его осаждают в течение примерно 16 часов при 4°С. Суспензию центрифугируют в течение 20 минут при 4000 × g и супернатант отбрасывают. Полученный осадок растворяют в 0,5 мл 0,5М раствора уксусной кислоты. Полученный коллаген должен иметь чистоту, по крайней мере, 90%, и эта чистота может быть проанализирована стандартными методами, известными специалистам, такими как, например, электрофорез в ПААГ с ДСН.
5.8. Применения кондиционированной среды
5.8.1. Использование для заживления ран
Кондиционированная среда настоящего изобретения может быть применена для стимуляции заживления ран и лечения ожогов. При повреждении ткани полипептидные факторы роста, обладающие определенным спектром биологических активностей, высвобождаются и стимулируют заживление раны. Заживление раны представляет собой сложный процесс, который включает несколько стадий и который способен регулируемым образом закрывать раневые полости с образованием наружного покрова и с формированием функционально компетентной ткани. Этот процесс начинается с гемостаза с последующей фазой воспаления, в котором участвуют нейтрофилы и макрофаги. Этот процесс продолжается с развитием гранулированной ткани и реэпитализации с закрытием раны. Затем образуется рубцовая ткань, которая в течение последующих месяцев ремодулируется с образованием почти исходной анатомической структуры. В идеальном случае рубцовая ткань является минимальной настолько, что на ее основе может образовываться здоровая функционально компетентная ткань, которая гистологически и физиологически подобна исходной нормальной ткани.
Каждая стадия процесса заживления регулируется клеточными взаимодействиями, опосредованными регуляторными белками, такими как цитокины, факторы роста и медиаторы воспаления, а также механизмами контактирования клеток. Так, например, медиаторы воспаления, такие как IL-6, IL-8 и G-CSF индуцируют дифференцировку лимфоцитов и образование белков острой фазы, а также инфильтрацию, созревание и активацию нейтрофилов, то есть процессы, которые играют важную роль в воспалительных стадиях заживления ран. Другими примерами регуляторных белков, участвующих в процессе заживления ран, являются VEGF, который индуцирует ангиогенез во время воспаления и грануляции ткани; BMP, который индуцирует образование кости; KGF, который активирует кератиноциты и TGF-β1, который индуцирует отложение внеклеточного матрикса. В таблице 2 (см. ниже) проиллюстрированы концентрации ряда факторов роста, определенные с помощью ELISA (твердофазного иммуноферментного анализа) и присутствующие в кондиционированной среде настоящего изобретения, которая ранее поддерживала рост клеток, выращенных в тканевой культуре Dermagraft®. Следует отметить, что нижеследующий список не является полным перечнем факторов и приводится лишь для дополнительной характеризации кондиционированной среды в отношении концентрации некоторых из биологически активных факторов, присутствующих в среде настоящего изобретения.
При незаживающих ранах процесс заживления раны прерывается в момент после гемостаза и до реэпитализации и, по-видимому, не способен к возобновлению. Большинство воспалений, обнаруживаемых в полости раны, вызваны инфекциями, однако, указанное воспаление способствует образованию окружения, богатого протеазами, которые разлагают регуляторные белки и, таким образом, препятствуют процессу заживления ран.
Для количественной оценки и характеризации главных молекулярных компонентов, секретируемых фибробластами, обнаруженными в трехмерных тканевых культурах TransCyte™ и Dermagraft™, был использован ряд методов. Белками матрикса человека и гликозаминогликанами (GAG), присутствующими в Transcyte™ и Dermagraft®, являются но не ограничиваются ими, коллаген I, III, фибронектин, тенасцин, декорин, версикан, бетагликан, синдекан, а также другие компоненты (данные не приводятся). Эти секретированные белки и GAG обладают главными структурными функциями, а также стимулируют деление, миграцию и адгезию клеток и передачу сигнала. Отложение гликозаминогликанов (объем отложения зависит от периода роста) и коллагена (объем отложения не зависит от периода роста) в трехмерных культуральных системах проиллюстрировано на фиг.1. Эти компоненты были измерены с помощью ELISA, Вестерн-блот-анализа, иммуногистохимии и ПЦР. Так, например, некоторыми из компонентов, обнаруживаемых в Transcyte™, являются коллаген I, III и VII (РНК), фибронектин, тенасцин, тромбоспондин 2, эластин, протеогликаны, декорин, версикан, а также другие компоненты (данные не приводятся). Активность этих компонентов при развитии, заживлении и нормальной функции тканей хорошо описана. Кроме того, заявителями описано некоторые действия биологически сконструированного матрикса человека на клеточную функцию in vitro. Так, например, заявители отмечают, что при добавлении биологически сконструированного матрикса пролиферация клеток усиливается. Для исследования этого действия на пролиферацию клеток матрикс был физически удален из Transcyte™ и Dermagraft® и добавлен в различных разведениях к монослойным культурам человеческих фибробластов и кератиноцитов. Повышенная в результате этого пролиферация клеток проиллюстрирована на фиг.2.
Кроме того, как подробно описано в Разделе 6.3, заявители сообщают, что влияние трехмерной кондиционированной среды на приготовление и состав трехмерных тканей было оценено путем измерения количества коллагена, секретированного во внутриклеточный матрикс тканей, культивированных в присутствии бессывороточной среды, питательной среды или трехмерной кондиционированной среды. Это влияние трехмерной кондиционированной среды на приготовление и состав трехмерных тканей было оценено путем измерения количества коллагена, секретированного во внутриклеточный матрикс тканей, культивированных в присутствие бессывороточной среды, питательной среды или трехмерной кондиционированной среды. В указанной кондиционированной среде настоящего изобретения уровень отложения коллагена в ткани in vitro значительно возрастает, как показано на фиг.4. Поскольку настоящее изобретение относится ко многим регуляторным белкам, которые, очевидно, играют важную роль в заживлении раны, то было показано, что они истощаются в in vivo-моделях заживления ран. Кроме того, при некоторых клинических состояниях, таких как диабет, обеспечение некоторыми регуляторными белками, необходимыми для заживления ран, является недостаточным. Так, например, на мышиной модели инсулин-независимого диабета (например, на мышах db/db) было показано, что в ранах этих мышей уровни секреции VEGF и PDGF и экспрессии рецептора PDGF были пониженными по сравнению с уровнями в ранах нормальных мышей.
Кроме того, кондиционированная среда настоящего изобретения может быть также использована для обработки других типов повреждений тканей, например, травматических или врожденных, где желательна репарация и/или регенерация дефектной или поврежденной ткани, так как в указанной кондиционированной среде настоящего изобретения было обнаружено много факторов роста, включая, например, факторы роста фибробластов (FGF), тромбоцитпроизводные факторы роста (PDGF), эпидермальные факторы роста (EGF), морфогенные белки костей (BMP) и трансформирующие факторы роста (TGF); а также факторы, модулирующие васкуляризацию, такие как VEGF (сосудистый эндотелиальный фактор роста), KGF (фактор роста кератиноцитов) и основный FGF; факторы ангиогенеза и факторы антиангиогенеза. Белки стрессов, такие как GR78 и MSP90 индуцируют факторы роста, такие как TGF-β, TGF-β, включая TGF-β-1, TGF-β-2, TGF-β-3, TGF-β-4 и TGF-β-5, регулируют рост и дифференцировку и ускоряют заживление ран (Noda et al. 1989, Endocrin. 124:2991-2995; Goey et al. 1989, J.Immunol. 143:877-880, Mutoe et al. 1987, Science 237:1333-1335). Митогены, такие как PDGF, способствуют увеличению степени насыщенности и грануляции при образовании ткани (Kohler et al. 1974, Exp. Cell. Res. 87:297-301). Как было упомянуто ранее, эти клетки, а предпочтительно клетки человека минимизируют проблемы, связанные с иммуногенностью.
Поскольку кондиционированная среда настоящего изобретения содержит ряд факторов заживления ран, то указанная кондиционированная среда преимущественно используется при обработке ран и лечении ожогов, включая раны на коже, переломы костей, язвы желудка, поражения поджелудочной железы, печени, почек, селезенки, кровеносных сосудов и другие внутренние раны. Кроме того, указанные кондиционированные среды могут быть объединены с другими лекарственными ингредиентами, такими как антибиотики и аналгетики. В некоторых вариантах своего осуществления настоящее изобретение относится к композициям кондиционированных сред в виде лечебных мазей или растираний для местного применения. Фактически, было показано, что кондиционированная среда настоящего изобретения для местного применения индуцирует пролиферацию фибробластов и кератиноцитов человека. Усиление клеточного ответа наблюдалось для клеток, экспонированных кондиционированной средой, по крайней мере, в течение трех дней in vitro (фиг.3).
Альтернативно, кондиционированная среда может быть включена в повязку (адгезивную или неадгезивную повязку) для стимуляции и/или ускорения заживления ран. Кондиционированные среды могут быть использованы в любой форме, то есть в виде жидкости или в твердом виде, в виде замороженного, лиофилизованного или высушенного порошка, в виде пленки для местной обработки раны и антиадгезивных аппликаций и в виде инъекций, см. заявку РСТ WO 96/39101, которая во всей своей полноте вводится в настоящее описание посредством ссылки.
Альтернативно, кондиционированная клеточная среда настоящего изобретения может быть приготовлена с использованием полимеризуемых или структурированных гидрогелей, как описано в патентах США №№5709854; 5516532; 5654381; и в WO 98/52543, каждый из которых во всей своей полноте вводится в настоящее описание посредством ссылки. Примерами материалов, которые могут быть использованы для образования гидрогеля, являются модифицированные альгинаты. Альгинат представляет собой углеводный полимер, выделенный из морских водорослей, который может быть структурирован с образованием гидрогеля путем обработки двухвалентным катионом, таким как кальций, как описано, например, в заявке WO 94/25080, описание которой вводится в настоящее описание посредством ссылки. Альгинат подвергают ионному структурированию в присутствии двухвалентных катионов в воде, при комнатной температуре, с образованием гидрогелевой матрицы. Используемый здесь термин "модифицированные альгинаты" означает химически модифицированные альгинаты, обладающие модифицированными гидрогелевыми свойствами.
Кроме того, полисахариды, которые образуют гель под действием одновалентных катионов, включая бактериальные полисахариды, такие как геллан, и полисахариды растений, такие как карагенаны, могут быть структурированы с образованием гидрогеля методами, аналогичными известным методам структурирования альгинатов, описанных выше.
Особенно подходящими являются модифицированные производные гиалуроновой кислоты. Используемый здесь термин "гиалуроновые кислоты" означает природные и химически модифицированные гиалуроновые кислоты. Модифицированные гиалуроновые кислоты могут быть сконструированы и синтезированы с использованием предварительно выбранных химических модификаций для коррекции скорости и степени перекрестного сшивания и биологического разложения.
Могут быть также использованы ковалентно сшитые предшественники гидрогеля. Так, например, водорастворимый полиамин, такой как хитозан, может быть перекрестно сшит с водорастворимым диизотиоцианатом, таким как диизотиоцианат полиэтиленгликоля.
Альтернативно, могут быть использованы полимеры, которые включают заместители и являются перекрестно сшитыми посредством свободнорадикальной реакции после контактирования с инициатором свободнорадикальной реакции. Так, например, могут быть использованы полимеры, которые включают этиленоненасыщенные группы и могут быть структурированы фотохимическим методом, как описано в WO 93/17669, содержание которого вводится в настоящее описание посредством ссылки. В этом варианте осуществления изобретения получают водорастворимые макромеры, которые включают, по крайней мере, одну водорастворимую область, биологически разлагаемую область и, по крайней мере, две свободнорадикально полимеризуемые области. Примерами таких макромеров являются ПЭГ-олиголактилакрилаты, где указанные акрилатные группы полимеризуют с использованием систем инициации свободнорадикальной реакции, таких как эозиновый краситель, или путем кратковременного экспонирования светом ультрафиолетового или видимого диапазона. Кроме того, могут быть использованы водорастворимые полимеры, включающие циннамоильные группы, которые могут быть структурированы фотохимическими методами, как описано Matsuba et al., ASAID Trans., 38:154-157 (1992).
Предпочтительными полимеризуемыми группами являются акрилаты, диакрилаты, олигоакрилаты, диметакрилаты, олигометакрилаты и другие биологически приемлемые фотополимеризуемые группы. Наиболее предпочтительным типом активной полимеризуемой группы являются акрилаты.
Природные и синтетические полимеры могут быть модифицированы посредством химических реакций, известных специалистам и описанных, например, March, "Advanced Organic Chemistry", 4th Edition 1992, Wiley-Interscience Publication, New York.
Полимеризацию, предпочтительно, инициируют с использованием фотоинициаторов. Подходящими являются фотоинициаторы, которые могут быть использованы для инициации полимеризации макромеров без цитотоксического действия и за короткий период времени, то есть за несколько минут, а наиболее предпочтительно за секунды.
Для фотополимеризации может быть использовано множество красителей. Подходящие красители хорошо известны специалистам. Предпочтительными красителями являются эритрозин, флоксим, бенгальский розовый, тонин, камфорхинон, этилэозин, эозин, метиленовый синий, рибофлавин, 2, 2-диметил-2-фенилацетофенон, 2-метокси-2-фенилацетофенон, 2,2-диметокси-2-фенилацетофенон, другие ацетофеноновые производные и камфорхинон. Подходящими сокатализаторами являются амины, такие как N-метилдиэтаноламин, N,N-диметилбензиламин, триэтаноламин, триэтиламин, дибензиламин, N-бензилэтаноламин, N-изопропилбензиламин. Предпочтительным сокатализатором является триэтаноламин.
В другом варианте осуществления изобретения кондиционированные среды настоящего изобретения или, альтернативно, конкретные белки внеклеточного матрикса, высвобождаемые в данные среды, используют для получения превосходного материала для наложения швов. Природный секретированный внеклеточный матрикс обеспечивает данные кондиционированные среды коллагенами типа I и типа III, фибронектином, терасцином, гликозаминогликанами, кислотными и основными FGF, TGF-α и TGF-β, KGF, версиканом, декорином и различными другими секретируемыми белками кожного матрикса человека. Аналогичным образом кондиционированные клеточные среды настоящего изобретения или белки внеклеточного матрикса, полученные из этих кондиционированных сред, могут быть использованы для нанесения на стандартные устройства для имплантации, включая сосудистые протезы, а в хирургии - для устранения физических дефектов, что позволяет получить превосходные устройства для имплантации. Имплантаты должны быть изготовлены из биосовместимых, инертных материалов, которые могут заменять или возмещать утраченную функцию, и могут быть изготовлены либо из биологически неразлагаемых материалов, либо из биологически разлагаемых материалов. При покрытии устройств для имплантации средой, содержащей указанные внеклеточные белки, этот имплантат обеспечивает прикрепление к нему соответствующих клеток, что приводит к образованию превосходной ткани в области имплантации. Таким образом, швы, бандажи и имплантаты, покрытые кондиционированной клеточной средой или белками, полученными из этой среды, способствуют усилению рекрутинга клеток, таких как лейкоциты и фибробласты, в поврежденные области и индуцируют пролиферацию и дифференцировку клеток, что приводит к лучшему заживлению раны.
В другом варианте осуществления изобретения кондиционированная среда может быть приготовлена в комбинации с фармацевтически приемлемым наполнителем, который служит носителем для внутреннего введения. Кроме того, данная среда может быть дополнительно обработана в целях увеличения или снижения количества одного или нескольких факторов или компонентов, содержащихся в данной среде, например, обогащена фактором роста с использованием иммуноаффинной хроматографии или, наоборот, удален компонент, который является менее желательным для данного применения, описанного в настоящей заявке.
Само собой разумеется, что для заживления ран в конкретных тканях может потребоваться среда, кондиционированная конкретной тканью. Так, например, повреждения нервной ткани могут требовать присутствия белков, содержащихся в среде, кондиционированной культурами нервных клеток. Конкретные продукты могут быть получены или, альтернативно, кондиционированная среда может быть обогащена иммунноаффинной хроматографией или усилением экспрессии нужного белка из специфической среды, такого как, например, фактор роста нервной ткани (NGF). NGF-регулируемыми параметрами являются, но не ограничиваются ими, функция холинергического нейромедиатора (ацетил-холинэстеразы (AChE) и ацетил-холин-синтезирующего фермента (ChAT)), размер нервной клетки и экспрессии NGF-рецепторов типа II; причем NGF секретируется в среду, которая кондиционирована глиальными и другими нервными клетками, культивированными на трехмерной стромальной ткани, и которая может быть затем использована в приготовлении композиции для заживления нервной ткани.
Дефицит эндогенного NGF приводит к осложнению некоторых нейродегенеративных расстройств и при этом наблюдается явная неспособность поврежденных зрелых нейронов ЦНС к регенерации. В частности, повреждение нервной ткани с последующей дегенерацией нервных волокон, находящихся на значительном расстоянии от места повреждения, приводит к отделению аксона от клеточного тела. В центральной нервной системе значительного роста в месте повреждения не происходит, что обычно приводит к гибели пораженного нейрона. NGF играет решающую роль в способности к регенерации зрелых холинергических нейронов ЦНС на уровне клеточного тела (например, в перегородке мозговой ткани), промежуточного тканевого пространства (нейронного мостика) и в области реиннервации (например, при образовании гиппокампа). Кроме того, NGF могут успешно способствовать улучшению познавательной способности. Среда, кондиционированная глиальными клетками, может, например, поставлять экзогенный NGF и другие факторы роста нервной ткани так, чтобы новые аксоны могли расти от отрезанных концов поврежденного нерва (например, с развитием конуса роста) с удлинением до исходного участка сцепления.
Кроме того, повреждение головного мозга и спинного мозга часто сопровождается глиальным клеточным ответом на сопутствующую дегенерацию аксона, что приводит к образованию рубцовой ткани. Ранее считалось, что эта рубцовая ткань является физическим барьером для роста нервной ткани, однако оказалось, что большее значение имеет присутствие или отсутствие нейротропных факторов в тканях, окружающих нервную ткань. Очевидно, что астроциты способны синтезировать ламинин в ответ на повреждение ткани (ламинин может быть также обнаружен в кондиционированной среде, как более подробно обсуждается в Разделе 5.8.2, касающегося белков внеклеточного матрикса). Было обнаружено, что коллаген и фибронектин, а особенно ламинин, стимулируют рост нейритов из культивированных нейронов или эксплантатов нервной ткани in vitro. Очевидно, что эти белки внеклеточного матрикса обеспечивают адгезивный субстрат, который облегчает продвижение конуса роста и удлинение аксона. Таким образом, присутствие нейротропных факторов и поддерживающего субстрата необходимо для успешной регенерации нервной ткани, поскольку для такой регенерации, очевидно, требуется, чтобы клеточное тело нейрона было способно продуцировать соответствующий биосинтетический ответ; а среда, окружающая поврежденный участок, была способна поддерживать элонгацию и в конечном счете функциональное повторное сцепление аксона. Среда, кондиционированная нервными клетками, такими как астроциты и глиальные клетки, содержит нейротропные факторы роста и белки внеклеточного матрикса, необходимые для регенерации нервной ткани в поврежденном головном мозге и спинном мозге. Таким образом, в одном из вариантов осуществления изобретения кондиционированную среду получают для лечения таких повреждений.
В другом варианте осуществления изобретения обработка кожи, костей, печени, поджелудочной железы, хряща и других конкретных тканей может быть осуществлена средой, кондиционированной клетками соответствующего типа, предпочтительно, культивированных в трех измерениях, что приводит к получению кондиционированной среды, содержащей характерные внеклеточные белки и другие метаболиты тканей этого типа, используемые для лечения ран в тканях соответствующего типа.
Кондиционированная клеточная среда может быть также добавлена в устройства, используемые в периодонтальной хирургии для стимуляции однородной репарации ткани, для получения биологически разлагаемых контактных линз, для защиты роговицы или имплантантов костей, для изготовления хирургических объемных наполнителей, для стимуляции увеличения мягкой ткани, а в частности кожи, в целях разглаживания морщин на коже и в целях увеличения сфинктера мочевого пузыря для лечения недержания мочи.
В другом варианте осуществления изобретения указанные композиции могут быть лиофилизованы/высушены замораживанием и добавлены в качестве наполнителя для ран (например, для заполнения полостей, остающихся после удаления волосяных луковиц при пересадке волос) или добавлены к существующим композициям для заполнения ран в целях ускорения их заживления. В другом варианте осуществления изобретения среду кондиционируют генетически сконструированными клетками для увеличения концентрации в данной среде белков, способствующих заживлению ран. Так, например, клетки могут сконструированы для экспрессии генных продуктов, таких как любые факторы роста, перечисленные выше.
5.8.2. Репарация и коррекция врожденных аномалий, приобретенных дефектов и косметических дефектов
Композиции, содержащие указанную среду, могут быть также использованы для исправления и коррекции ряда аномалий, как врожденных, так и приобретенных, а также косметических дефектов, как поверхностных, так и проникающих. Так, например, указанные композиции могут быть добавлены в любой форме и могут быть использованы в гидрогелях, инъекциях, кремах, мазях, и даже могут быть добавлены в тени для век, румяна, компактные пудры или в другие косметические препараты местного применения для укрепления кожи.
В другом варианте осуществления изобретения препараты для местного применения или для нанесения кондиционированной среды известным методом, таким как инъекция, пероральное введение и т.п. изготавливают, например, в целях разглаживания и/или предупреждения образования морщин и устранения ряда нежелательных эффектов, индуцированных действием УФ-света и загрязняющих веществ и в целях предупреждения естественного старения кожи.
Кроме того, в другом варианте осуществления изобретения среду настоящего изобретения используют для уменьшения старения клеток и ингибирования активности факторов, вызывающих рак кожи. Эта кондиционированная среда обладает противоокислительной активностью как показано в Разделе 7.1. И в этом случае введение млекопитающему может быть осуществлено местно либо любым известным методом, таким как инъекция, пероральное введение и т.п. Заявителями было установлено, что статистически значимое снижение (р<0,003) внутриклеточного окисления, составляющего приблизительно 50 процентов, наблюдалось в кератиноцитах человека, экспонированных кондиционированной средой настоящего изобретения.
Таким образом, помимо индуцирования пролиферации клеток эпидермиса и кожи и секреции коллагена in vitro, кондиционированная среда настоящего изобретения обладает сильной противоокислительной активностью (фиг.5). Кроме того, указанные факторы являются относительно стабильными, и содержание TGF-β, VEGF и коллагена было стабильным после хранения в течение 21 дня при 37°С и при рН 7,4 и 5,5. В растворах, хранившихся в течение 2 лет при -20°С, поддерживались стабильные уровни TGF-β и VEGF.
Этот стерильный обогащенный питательными веществами раствор представляет собой биологически сконструированный косметический продукт, который может быть легко получен в больших объемах и может быть использован в качестве добавки к различным продуктам для ухода за кожей, к косметическим и дерматологическим продуктам, в целях пополнения уровней факторов роста и матриксных молекул в коже, волосах и ногтях человека. В этих продуктах предусматривается их использование в сочетании с альфа-оксикислотами, способствующими отшелушиванию кожи, для потенциальной оптимизации проникновения факторов роста и других биомолекул в кожу, и в сочетании с химическим средством для отшелушивания в целях потенциального ускорения лечения и ослабления воспаления.
Указанная кондиционированная среда может быть приготовлена в целях разглаживания морщин и складок у бровей, удаления рубцов и других дефектов кожи вместо использования силиконовых или других продуктов и т.п. Указанная кондиционированная среда содержит факторы роста и медиаторы воспаления, такие как, например, VEGF, HGF, IL-6, IL-8, G-CSF и TGF-β1 (см. таблицу 3 в Разделе 5.8.1), а также белки внеклеточного матрикса, такие как коллаген типа I и III, фибронектин, тенасцин, гликозаминогликаны, кислотные и основные FGF, TGF-α и TGF-β, KGF, версикан, декорин, бетаглицены, синдекан и различные другие секретированные белки кожного матрикса человека, которые могут быть использованы для исправления физических и косметических дефектов. Как подробно описано в Разделе 6.3, заявители сообщают, что действие трехмерной кондиционированной среды на получение и композицию трехмерных тканей было оценено путем измерения количества коллагена, секретированного во внутриклеточный матрикс тканей, культивированных в присутствие бессывороточной среды, питательной среды или трехмерной кондиционированной среды. В указанной кондиционированной среде настоящего изобретения уровень отложения коллагена в ткани in vitro значительно возрастает, как показано на фиг.4. Действие трехмерной кондиционированной среды на получение и композицию трехмерных тканей было оценено путем измерения количества коллагена, секретированного во внутриклеточный матрикс тканей, культивированных в присутствии бессывороточной среды, питательной среды или трехмерной кондиционированной среды. Само собой разумеется, что клетки, используемые для кондиционирования данной среды, могут быть генетически сконструированы для экспрессии повышенных концентраций указанных белков в среде.
Кондиционированные среды настоящего изобретения могут быть приготовлены в виде препаратов для инъекций. Альтернативно, могут быть приготовлены продукты, происходящие от указанных кондиционированных сред. Так, например, биологически активные вещества, такие как белки и лекарственные средства, могут быть включены в композиции настоящего изобретения для высвобождения или регулируемого высвобождения этих активных веществ после инъекции данной композиции. Примерами биологически активных веществ могут служить факторы роста тканей, такие как TGF-β и т.п., которые стимулируют заживление и репарацию ткани в области инъекции. Методами очистки продукта являются, но не ограничиваются ими, гель-хроматография (с использованием матриц, таких как Сефадекс®), ионообменная хроматография, аффинная хроматография на хелате металла с нерастворимой матрицей, такой как перекрестно-сшитая агароза, ВЭЖХ-очистка и гидрофобная хроматография кондиционированной среды. Такие методы более подробно описаны в Cell & Tissue Culture: Laboratory Procedures, см.выше; Sanbrook et al., 1989, Molecular Cloning: A Laboratory Manual, 2nd Ed., Cold Spring Harbor Lab Press, Cold Spring Harbor, NY.
В варианте осуществления изобретения, относящемуся к инъекциям, используют водную суспензию, и композиция данной водной суспензии обычно имеет физиологический рН (т.е. приблизительно 6,8-7,5). Кроме того, средство для местной анестезии, такое как лидокаин (обычно в концентрации около 0,3 масс.%) обычно добавляют для ослабления локальной боли при инъекции. Конечная композиция также обычно содержит жидкий смазывающий агент, такой как мальтоза, к которому организм должен быть толерантным. Примерами смазывающих компонентов являются глицерин, гликоген, мальтоза и т.п. В качестве смазывающих агентов могут быть также использованы органические полимерные материалы-основы, такие как полиэтиленгликоль и гиалуроновая кислота, а также нефибриллярный коллаген, а предпочтительно сукцинилированный коллаген. Такие смазывающие агенты обычно используют для улучшения инъецируемости, введения и дисперсии инъецированного биоматериала в области инъекции и для снижения количества поверхностных включений этого материала путем модификации вязкости данной композиции. Конечный состав композиции определяется количеством обработанной кондиционированной среды в фармацевтически приемлемом носителе.
Обработанную кондиционированную среду затем набирают в шприц или в другое приспособление для инъекций для точного введения кондиционированной среды в область дефекта ткани. В случае композиции для стимуляции роста кожи, термин "инъецируемый" относится к композиции, которая может быть инъецирована из шприцев, имеющих калибр 25, при нормальных условиях и при нормальном давлении без какого-либо значительного повреждающего прокалывания. Такое прокалывание может вызывать попадание композиции, вытекающей из шприца, на поверхность, а не ее инъецирование в ткань. Для точного введения желательно использовать тонкие иглы калибра 27 (внут. диаметр 200 мк) или даже 30 (внут. диаметр 150 мк). Максимальный размер частиц, которые могут быть экструдированы через такие иглы, в целом зависит, по крайней мере, от следующих параметров: максимального размера частиц, отношений размера частиц (длина:ширина), жесткости частиц, шероховатости поверхности частиц и подобных факторов, влияющих на адгезию частиц друг с другом, вязкоупругих свойств суспендирующей жидкости и скорости потока через иглу. Самым простым случаем являются жесткие сферические гранулы, суспендированные в ньютоновской жидкости, а более сложным случаем являются волокнистые или разветвленные частицы в вязкоупругой жидкости.
Нижеописанные стадии в способе получения инъецируемой человеку секретированной кондиционированной среды предпочтительно осуществляют в стерильных условиях с использованием стерильных материалов. Обработанная кондиционированная среда в фармацевтически приемлемом носителе может быть инъецирована чрезкожно или подкожно для наращивания мягкой ткани в целях исправления или коррекции врожденных аномалий, приобретенных дефектов или косметических дефектов. Примерами таких состояний являются врожденные аномалии, такие как гемифациальная микросомия, гипоплазия щек и скул, односторонняя гипоплазия молочной железы, впалая грудь, недоразвитость грудной клетки (аномалия Поланда) и небоглоточная недостаточность после репарации небной расщелины или подслизистой небной расщелины (при ведении заглоточного имплантата); приобретенные дефекты (посттравматические, послеоперационные и постинфекционные дефекты), такие как глубокие шрамы, подкожная атрофия (например, вторичная, вызванная дискоидной красной волчанкой), кератозные поражения, энофтальм в глазу с западающим яблоком (также называемый синдромом верхней борозды), угревые свищи на лице, лентовидная склеродермия с подкожной атрофией, дефект в виде седловидного носа, болезнь Ромберга и односторонний паралич голосовых связок; и косметические дефекты, такие как складки у бровей в области переносицы, глубокие складки в носогубной области, характерная сеть морщин вокруг рта, впалые щеки и гипоплазия молочной железы. Композиции настоящего изобретения могут быть также инъецированы во внутренние ткани, такие как ткани, определяющие сфинктеры организма для наращивания этих тканей.
Другими типами тканей, используемых для кондиционирования среды, являются, но не ограничиваются ими, костный мозг, кожа, эпителиальные клетки и хрящи, однако, совершенно очевидно, что трехмерная культуральная система может быть использована с клетками и тканями других типов.
Альтернативно, кондиционированная клеточная среда настоящего изобретения может быть приготовлена с использованием полимеризуемых или структурированных гидрогелей, описанных в предыдущем разделе, касающемся обработки ран.
5.8.3. Пищевые и диетические добавки
Указанная кондиционированная среда может быть использована в качестве пищевых добавок и приготовлена в виде диетической добавки. Кондиционированная среда настоящего изобретения содержит много питательных компонентов, включая незаменимые аминокислоты, минералы и витамины в избыточном количестве и таких видов, которые обычно не встречаются в отдельных пищевых продуктах или в группе продуктов. Заявителям неизвестен какой-либо еще сбалансированный пищевой продукт (кроме грудного молока), содержащий широкий ряд питательных веществ, хотя были предприняты такие попытки изготовления дорогостоящих жидких составов, предназначенных для взрослых и детей. Кондиционированная среда и продукты, вырабатываемые этой средой, могут быть использованы в качестве недорогого источника сбалансированной пищевой добавки для похудения или, альтернативно, для повышения питательных веществ в пище, а в частности, в пище, поставляемой в страны третьего мира. Указанная среда является стерильной и не загрязнена человеческими патогенами (то есть является асептической). Кондиционированная среда может быть концентрированной и/или лиофилизованной, а предпочтительно вводится в виде капсул или таблеток для проглатывания. Альтернативно, указанные композиции могут быть непосредственно добавлены в пищу взрослого человека или ребенка в целях увеличения содержания в ней питательных веществ. Указанный богатый питательными веществами источник может быть подвергнут относительно недорогостоящей обработке и может быть бесценной добавкой для людей пожилого возраста с недостаточным питанием, а в частности для детей в неразвитых странах, где возрастающая смертность, обусловленная слабым иммунитетом по отношению к инфекциям, ассоциируется с недоеданием.
Кроме того, многие микроэлементы, обнаруживаемые в кондиционированных средах, такие как железо и магний, имеют важное значение для выживания и размножения млекопитающих, и считается, что крайний дефицит микроэлементов может серьезно сказаться на здоровье людей. Предполагается, что различные важные микроэлементы способствуют снижению уровня инфекции и риска заболевания раком благодаря модификации конкретных фаз онкогенеза. Микроэлементы также усиливают функциональную активность иммунной системы и ее механизмы взаимодействия Т-клеток и В-клеток, M⌀s и клеток-киллеров путем специфического усиления продуцирования различных цитокинов в целях облегчения их фагоцитарного и цитотоксического действия, направленного против инвазивных патогенов и/или в целях предотвращения возникновения предраковых клеток в различных жизненно важных органах. См. Chandra, R.K. ed.(1988), Nutrition and Immunology: Contemporary Issues in Clinical Nutrition, Alan R. Liss, New York. Таким образом, существует крайняя необходимость в получении относительно недорогостоящего источника в сбалансированных питательных веществах. Идеальными пищевыми продуктами для обогащения указанной кондиционированной средой являются хлеб, злаки и другие зерновые продукты, такие как пасты, крекеры и т.п. Кроме того, указанная среда может быть дополнительно обработана для увеличения или снижения количества одного или нескольких факторов или компонентов, содержащихся в данной среде, например, для обогащения факторами роста с использованием иммуноаффинной хроматографии или, наоборот, для удаления менее желательного компонента в любом из применений, описанных в данном разделе.
5.8.4. Добавки в корм для животных
Указанные композиции могут быть использованы в качестве добавок в корм для животных. В одном из вариантов осуществления изобретения кондиционированная среда содержит бычью сыворотку, которая является источником белка и других факторов, благоприятно влияющих на млекопитающих, таких как крупный рогатый скот и другие жвачные животные, такие как коровы, олени и т.п. Указанную среду скринируют на патогены и на отсутствие бычьих патогенов и микоплазмы. Кондиционированную среду настоящего изобретения предпочтительно получают от коров, выращенных в Соединенных Штатах для минимизации вероятности загрязнения патогенами.
5.8.5. Клеточная культуральная среда
Композиции, содержащие указанную среду, могут быть "повторно использованы" для культивирования клеток, а в частности клеток, которые трудно культивировать in vitro. В стандартную ростовую среду обычно добавляют множество факторов, уже присутствующих в кондиционированной среде настоящего изобретения. Кроме того, указанная кондиционированная среда также содержит факторы, стимулирующие прикрепление и рост клеток, такие как белки внеклеточного матрикса, описанные выше. Увеличение концентраций фибронектина и коллагена может благоприятно влиять на стимуляцию прилипания клеток к каркасу или поверхности культуры. Вместо добавления этих факторов в среду может быть использована кондиционированная среда для культивирования клеток и получения трехмерных тканевых структур, таких как Dermagraft®. Заявителями было продемонстрировано, что указанная кондиционированная среда способствует усилению пролиферации фибробластов и кератиноцитов, см. фиг.3. Клеточный дебрис или другие частицы, а также протеазы, молочная кислота и другие компоненты, которые, по всей вероятности, негативно влияют на рост клеток, могут быть удалены из данной среды с последующим ее повторным использованием в качестве клеточной культуральной среды. В этих целях может также оказаться желательным, чтобы данная кондиционированная среда содержала сыворотку. Сыворотка также может содержать адгезивные факторы, такие как фибронектин и фактор распределения сыворотки, который стимулирует прикрепление клеток к субстрату. Такое прикрепление необходимо для роста некоторых, но не всех, клеток in vitro. Помимо поставки веществ, необходимых для клеточного роста, сыворотка может также играть определенную роль в стабилизации и дезинтоксикации культуральной среды. Так, например, сыворотка может обладать значительной забуферивающей способностью и содержать специфические ингибиторы протеазы, такие как α1-антитрипсин и α2-макроглобулин. Альбумин сыворотки, присутствующий в высоких концентрациях в среде, содержащей, например, 10% сыворотку, также может действовать как неспецифический ингибитор протеолиза, а также связывать жирорастворимые витамины и стероидные гормоны, которые, в своей свободной форме, могут оказаться токсичными. Компоненты сыворотки могут также связывать и устранять токсичные тяжелые металлы и реакционно-способные органические соединения, которые могут присутствовать в компонентах данной среды.
5.8.6. Фармацевтические применения
Кондиционированная среда настоящего изобретения содержит ряд ценных фармацевтических факторов и компонентов, таких как факторы роста, регуляторные факторы, пептидные гормоны, антитела и т.п., подробно описанные в данном описании, а поэтому они могут быть использованы в различных фармацевтических препаратах. Продуктами, которые могут быть также добавлены, являются, но не ограничиваются ими, антибиотики, антивирусные агенты, противогрибковые агенты, стероиды, аналгетики, противоопухолевые лекарственные средства, лекарственные препараты, проходящие клинические испытания, или любые соединения, которые должны приводить к образованию комбинации с присутствующими в кондиционированной среде факторами, обладающей усиливающим или синергическим действием. Как обсуждалось ранее, клетки культивируют и среду выделяют в асептических условиях. Кроме того, данная среда может быть протестирована на патогены. Если осуществляют стерилизацию, то она должна быть проведена в условиях, которые минимально влияют на биологическую активность, как описано выше. Эта среда может быть дополнительно обработана для увеличения или снижения концентрации одного или нескольких факторов или компонентов, содержащихся в данной среде, например, для обогащения факторами роста с использованием иммуноаффинной хроматографии, или, наоборот, для удаления менее желательного компонента в любом из применений, описанных в данном разделе. В предпочтительном варианте осуществления изобретения, композиции изготавливают из среды, кондиционированной трехмерной клеточной конструкцией. Указанные трехмерные культуры продуцируют множество факторов роста и других белков, которые секретируются в среду при оптимальных физиологических отношениях и концентрациях. См., например, таблицу 2 в Разделе 5.8.1. Следовательно, данная среда дает уникальную комбинацию факторов и их конкретных отношений, которые близки к обнаруживаемым in vivo. Для указанных целей бычья сыворотка обычно не является предпочтительной. Она может быть предпочтительной для удаления клеточного дебриса или других частиц, таких как протеазы, молочная кислота или другие компонентны, которые, вероятно, негативно влияют на рост клеток.
Кондиционированная среда может быть приготовлена в виде фармацевтических препаратов в форме таблеток, капсул, кожных пластырей, ингаляторов, глазных капель, капель в нос, ушных капель, суппозиториев, кремов, мазей, инъекций, гидрогелей и в форме любой другой подходящей композиции, известной специалистам. Для перорального введения указанные фармацевтические композиции могут быть приготовлены в форме, например, таблеток или капсул, изготовленных стандартными способами с использованием фармацевтически приемлемых наполнителей, таких как связующие агенты (например, прежелатинизированный кукурузный крахмал, поливинилпирролидон или гидроксипропилметилцеллюлоза); наполнители (например, лактоза, микрокристаллическая целлюлоза или бифосфат кальция); смазывающие агенты (например, стеарат магния, тальк или двуокись кремния); дезинтеграторы (например, картофельный крахмал или натрий-гликолят крахмала); или смачивающие агенты (например, лаурилсульфат натрия). Таблетки могут быть покрыты хорошо известными способами. Жидкие препараты для перорального введения могут быть изготовлены, например, в виде растворов, сиропов или суспензий, либо они могут представлять собой сухой продукт для разведения водой или другим подходящим носителем перед его использованием. Такие жидкие препараты могут быть получены стандартными способами с использованием фармацевтически приемлемых добавок, таких как суспендирующие агенты (например, сорбитный сироп, производные целлюлозы или гидрогенизированные пищевые жиры); эмульгирующие агенты (например, лецитин или камедь акации); безводные носители (например, миндальное масло, жирные сложные эфиры, этиловый спирт или фракционированные растительные масла); и консерванты (например, метил- или пропил-п-гидроксибензоаты или сорбиновая кислота). Эти препараты могут также содержать буферные соли, отдушки, красители и подслащивающие агенты, если это необходимо.
Фармацевтические композиции настоящего изобретения могут быть введены пациенту различными способами с использованием стандартных процедур, хорошо известных специалистам. Так, например, указанное введение может быть местным, пероральным, интраназальным, внутривенным, подкожным, внутридермальным, чрезкожным, внутримышечным или внутрибрюшинным. Кроме того, указанные фармацевтические композиции могут быть изготовлены так, чтобы они функционировали как носители с регулируемым пролонгированным высвобождением.
Терапевтическими продуктами, содержащимися в указанных кондиционированных средах, являются но не ограничиваются ими, ферменты, гормоны, цитокины, антигены, антитела, факторы свертывания крови и регуляторные белки. Терапевтическими белками являются, но не ограничиваются ими, медиаторы воспаления, ангиогенные факторы, фактор VIII, фактор IX, эритропоэтин (ЭПО), альфа-1-антитрипсин, кальцитонин, глюкоцереброзидаза, человеческий гормон роста и его производные, липопротеин низкой плотности (ЛНП) и аполипопротеин Е, рецептор IL-2 и его антагонисты, инсулин, глобин, иммуноглобулины, каталитические антитела, интерлейкины (IL), инсулиноподобные факторы роста, супероксид-дисмутаза, модификаторы иммунного ответа, BMP (костные морфогенные белки), паратиреоидный гормон и интерферон, факторы роста нервной ткани, тканевые активаторы плазминогена и колониестимулирующие факторы (КСФ). Само собой разумеется, что указанная среда может быть дополнительно обработана для увеличения или снижения концентрации одного или нескольких факторов или компонентов, содержащихся в данной среде, например, для обогащения факторами роста с использованием иммуноаффинной хроматографии или, наоборот, для удаления менее желательного компонента в любом из применений, описанных в данном разделе.
Для определения активности конкретного фактора или конкретных факторов могут быть проведены анализы, обычно используемые специалистами для гарантии того, что приемлемый уровень биологической активности (например, терапевтически эффективной активности) будет сохранен при связывании молекулы или при инкапсуляции молекулы.
Таким образом, кондиционированные клеточные среды и продукты, полученные из сред настоящего изобретения, могут быть использованы, например, для получения инсулина для лечения диабета, фактора роста нервной ткани для лечения болезни Альцгеймера, фактора VIII и других факторов свертывания крови для лечения гемофилии, допамина для лечения болезни Паркинсона, энкефалинов, вырабатываемых хромафиннными клетками надпочечников, для лечения хронических болей, дистрофина для лечения мышечной дистрофии, и человеческого гормона роста для лечения аномального роста.
Дозы указанных терапевтических белковых агентов хорошо известны специалистам и их можно найти в фармацевтических справочниках, таких как Physician Desk Reference, Medical Economics Data Publishers; Remington's Pharmaceutical Sciences, Mack Publishing Co.; Goodman & Oilman, The Pharmacological Basic Of Therapeutics, McGraw Hill Publ., The Chemotherapy Source Book, Williams & Wilkens Publishers.
Терапевтически эффективные дозы любого из вышеописанных лекарственных средств или агентов могут быть легко определены стандартными способами, известными специалистам. Термин "терапевтически эффективная" доза означает количество данного соединения, достаточное для ослабления, по крайней мере, одного симптома патологического процесса и/или заболевания, подвергаемого лечению.
Токсичность и терапевтическая эффективность лекарственных средств может быть определена с использованием стандартных фармацевтических процедур, проводимых на клеточных культурах или экспериментальных животных, например, путем определения LD50 (доза, которая является летальной для 50% особей) и ED50 (доза, дающая терапевтический эффект у 50% особей). Дозовое отношение токсического и терапевтического эффектов представляет собой терапевтический индекс и он может быть выражен как отношение LD50/ED50. Предпочтительными являются соединения, имеющие высокий терапевтический индекс. Хотя могут быть использованы соединения, имеющие побочные токсические эффекты, однако, следует разработать такую систему доставки, которая позволяет осуществлять направленную доставку соединений в область поражения ткани в целях минимизации возможного повреждения неинфицированных клеток и, тем самым, устранить побочные эффекты.
Данные, полученные из анализов клеточной культуры и исследований на животных, могут быть использованы для определения диапазона доз лекарственного препарата, вводимого человеку. Дозы указанных соединений, предпочтительно, составляют в пределах концентраций в кровотоке, которые включают значения ED50 при небольшой токсичности или с отсутствием токсичности. Эти дозы могут варьироваться в этом диапазоне в зависимости от используемой лекарственной формы и способа ее введения. Для лечения и/или профилактики любого соединения, используемого в способе настоящего изобретения, терапевтически эффективная доза может быть определена, исходя из предварительного анализа клеточной культуры. Концентрация лекарственного средства в плазме крови варьируется в диапазоне, который включает величину IC50 (то есть концентрация исследуемого соединения, которое дает полумаксимальное ингибирование симптомов), определенную в данной клеточной культуре. Указанные данные могут быть использованы для более точного определения доз, используемых для введения человеку. Уровни в плазме могут быть определены, например, с помощью высокоразрешающей жидкостной хроматографии.
Кроме того, клетки и ткани могут быть генетически модифицированы для усиления экспрессии нужного продукта, такого как, например, инсулин, и/или для экспрессии нуклеотидных последовательностей и/или молекул, обеспечивающих доставку вышеперечисленных генных продуктов, например рибозима, антисмысловых молекул и тройных спиралей, которые могут оказывать ингибирующее действие на экспрессию и/или активность гена-мишени. Это может оказаться преимущественным при культивировании тканей, в которых специализированные стромальные клетки в данной среде могут играть конкретные структурные/функциональные роли, например глиальные клетки нервной ткани, клетки печени Купфера и т.п.
5.8.7. Стимуляция роста волос
Данная среда может быть кондиционирована, например, клетками волосяных сосочков человека. Предпочтительно, чтобы данная среда, кондиционированная такими клетками, была выращена в трех измерниях. Клетки волосяных сосочков представляют собой мезенхимные стволовые клетки, которые играют главную роль в образовании, росте и восстановлении волос (Matsuzaki et al., Wound Repair Regen, 6:524-530 (1998)). Кондиционированную среду, предпочтительно, концентрируют и используют в виде композиции для местного применения. Композиции кондиционированных сред могут быть приготовлены в виде препарата для местного применения с использованием агента, облегчающего проникновение данного соединения в кожу, например, ДМСО, и нанесены в виде местной аппликации для стимуляции роста волос.
Композиции настоящего изобретения, при их местном применении, стимулируют или восстанавливают рост волос благодаря присутствующим в них факторам роста и другим факторам, которые усиливают миграцию эпителиальных клеток в волосяные фолликулы. Помимо факторов роста, присутствующих в кондиционированных средах, могут быть использованы другие соединения, такие как миноксидил и антибиотики. В процессе роста волос происходит уменьшение подачи крови во время катагена (промежуточной фазы образования волосяного фолликула между фазой роста и фазой покоя) и телогена (фазы покоя). Биологически активные молекулы, происходящие из кондиционированной клеточной среды, могут быть определены и оптимизированы для их использования во время этих фаз роста волос с помощью анализов, известных специалистам, включая, например, анализ с применением модели облысения по мужскому типу у безхвостых макак, см., например, Brigham, P.a., A. Cappas & H.Uno, The Stumptailed Macaque as a Model for Androgenetic Alopecia: Effects of Topical Minoxidil Analyzed by Use of the Folliculogram, Clin Dermatol, 1988, 6(4): р.177-87; Diani, A.R. & C.J. Mills, Immunocytochemical Localization of Androgen Receptors in the Scalp of the Stumptail Macaque Monkey, a Model of Androgenetic Alopecia, J. Invest. Dermatol. 1994, 102(4): р.511-4; Holland, J.M. Animal Models of Alopecia, Clin Dermatol, 1988, 6(4): р.159-162; Pan H.J., et al., Evaluation of RU58841 as an Anti-Androgen in Prostate PC3 Cells and a Topical Anti-Alopecia Agent in the Bald Scalp of Stumptailed Macaques, Endocrine, 1998, 9(1): р.39-43; Rittmaster, R.S. et al., The Effects of N, N-diethyl-4-methyl-3-oxo-4-aza-5-alpha-androstane-17-beta-carboxamide, a 5-alpha-reductase Inhibitor and Antiandrogen, on the Development of Baldness in the Stumptail Macaque, J.Clin. Endocrinol Metab, 1987, 65 (1): р.188-93 (каждая из которых во всей свой полноте вводится в настоящее описание посредством ссылки). Другими моделями являются модели, используемые для измерения различия в пролиферации волосяных фолликулов для фолликулов, культивированных на лысых и волосистых участках головы, модели с использованием новорожденных крыс, а также модели гнездной алопеции у крыс, см., Neste D.V., The Growth of Human hair in Nude Mice, Dermatol Clin., 1996, 14(4): р.609-17; McElwee, K.J., E.M. Spiers, and R.F. Oliver, In Vivo Depletion of CD8+T Cells Restores Hair Growth in the DEBR Model for Alopecia Areata, Br.J.Dermatol, 1996, 135(2): р.211-7; Hussein, A.M., Protection Against Cytosine Arabinowide-Induced Alopecia by Minoxidil in a Rat Model, Int. J. Dermatol, 1995, 34(7): р.470-3; Oliver, R.F., et al., The DEBR Rat Model for Alopecia Areata, J. Invest. Dermatol. 1991, 96(5): р.978; Michie, H.J., et al., Immunobiological Studies on the Alopecic (DEBER) Rat. Br. J. Dermatol, 1990, 123(5): р.557-67 (каждая из которых во всей своей полноте вводится в настоящее описание посредством ссылки).
6. Примеры
6.1. Кондиционирование среды
Фибробласты кожи человека высевали на субстрат аппарата, описанного в патенте '766 и подробно описанного выше в Разделах 5.3, 5.4. и 5.6. Этот субстрат помещали в камере, сконструированной для облегчения трехмерного роста ткани на его поверхности и клетки культивировали в закрытой системе, культивированной в DMEM с высоким содержанием глюкозы (10% BCS с добавлением 2 мМ L-глутамина и 50 мг/мл аскорбиновой кислоты) при 37°С в 5% СО2-атмосфере с повышенной влажностью. Через 10 дней клеточную культуру удаляли и добавляли свежую среду. Клетки культивировали еще 4 дня, как описано выше. Затем полученную кондиционированную среду, экспонированную клеточной и тканевой культурой в течение четырех дней (дни 10-14), вынимали из отдельных камер и объединяли. Эту кондиционированную среду (приблизительно 5-10 литров/пул) разделяли на 200 мл-аликвоты, а затем подвергали 10-20-кратному концентрированию с использованием концентрирующего устройства, работающего при избыточном давлении и имеющего фильтр с отсечкой 10000 мол.масс. (Amicon Beverly, MA). Полученные 10-20 мл концентрированной кондиционированной среды разделяли на 1 мл-аликвоты и замораживали при -20°С для последующего анализа. 1х концентрацию кондиционированной среды получают, исходя из 10х кондиционированной среды, добавленной к основной среде в виде 10% (об/об) раствора. Аналогично, 1х концентрацию "среды" или "бессывороточной среды" получали, исходя из 10х среды (то есть основной среды) или 10х бессывороточной среды (основной бессывороточной среды), добавленной к основной среде в виде 10% (об/об) раствора, которые затем использовали в качестве контролей.
6.2. Пролиферирующая активность трехмерной кондиционированной среды
6.2.1. Экспонирование фибробластов и кератиноцитов кондиционированной средой
Кондиционированную среду, описанную в Разделе 6.1, оценивали на способность стимулировать пролиферацию человеческих фибробластов и кератиноцитов. Человеческие фибробласты и человеческие базальные кератиноциты засевали на 96-луночные планшеты (˜5000 клеток/лунку) и культивировали в среде DMEM с высоким содержанием глюкозы (10% BCS с добавлением 2 мМ L-глутамина и 1х антибиотика/противогрибкового агента), в которую добавляли 1х конечную концентрацию бессывороточной среды, питательной среды или трехмерной кондиционированной среды, описанной выше в Разделе 6.1. Эти культуры поддерживали при 37°С в 5% СО2-атмосфере с повышенной влажностью в течение 3 дней.
6.2.2. Клеточная пролиферация
Пролиферацию клеток оценивали при помощи коммерчески доступного анализа с использованием флуоресцентного красителя путем измерения содержания полной нуклеиновой кислоты как показатель пролиферации клеток (CyQuant Cell Proliferation Assay Kit, Molecular Probes, Eugene, Or). Все анализы проводили в соответствии с инструкциями производителей. Среду удаляли путем промокания и клетки лизировали в буфере для лизиса, содержащем зеленый флуоресцентный краситель, краситель CyQuant GR. Этот краситель обнаруживает сильное флуоресцентное усиление интенсивности при связывании с клеточными нуклеиновыми кислотами, и количество флуоресценции пропорционально количеству нуклеиновой кислоты, присутствующей в данном образце. Образцы инкубировали в течение 5 минут в отсутствии света и флуоресценцию образца определяли на аппарате для чтения микротитрационных планшетов, снабженном фильтрами, соответствующими максимальному возбуждению при ˜480 нм и излучению при ˜520 нм. Количество нуклеиновой кислоты в каждом образце вычисляли путем сравнения количества наблюдаемой флуоресценции в каждой лунке по стандартной кривой, построенной с использованием известных концентраций для ДНК телячьего тимуса в качестве стандарта.
Как показано на фиг.3, клетки, как фибробласты, так и кератиноциты, культивированные в среде, содержащей указанную кондиционированную среду, обнаруживали повышенную пролиферацию по сравнению с двумя контролями.
6.3. Модуляция отложения коллагена в тканях, продуцированного трехмерной кондиционированной средой
6.3.1. Применение для заживления ран
Действие трехмерной кондиционированной среды на получение и композицию трехмерных тканей оценивали путем измерения количества коллагена, секретированного во внеклеточный матрикс тканей, культивированных в присутствии бессывороточной среды, питательной среды или трехмерной кондиционированной среды.
Найлоновые носители разрезали лазером на квадраты размером 11 мм × 11 мм, промывали в 0,5М уксусной кислоте, интенсивно прополаскивали в FBS, и засевали вместе с клиническими фибробластами 12F в 8 пассажей (˜38000/см2). Культуры выращивали в среде DMEM (10% BCS с добавлением 2 мМ L-глутамина и 1х антибиотика/противогрибкового агента), в которую добавляли 1х конечную концентрацию бессывороточной среды, питательной среды или трехмерной кондиционированной среды, описанной выше в Разделе 6.1, при этом при каждой подпитке добавляли 50 мг/мл аскорбата. Затем добавляли сульфат меди до конечной концентрации 2,5 нг/мл, и высокое содержание кислорода (40%, примерно в два раза превышающее содержание кислорода в атмосфере) поддерживали при регулированном выделении газа в стандартном инкубаторе (n=3 или более). Культуры поддерживали при 37°С в 5% CO2-атмосфере с повышенной влажностью в течение 10 дней. Был также включен контроль без аскорбата.
6.3.2. Выделение коллагена
Коллаген выделяли и очищали почти до гомогенности из трехмерных тканевых культур, выращенных в присутствии базальной культуры, в которую добавляли 1х конечную концентрацию бессывороточной среды, питательной среды или трехмерной кондиционированной среды, описанной выше. Чистоту конечных препаратов образцов оценивали путем обработки образцов очищенного коллагена электрофорезом на градиентных ДСН-полиакриламидных гелях с визуализацией отдельных полос белка кумасси синим и определением количества специфичных для коллагена альфа-, бета- и гамма-полос по сравнению с общим белком (см. ниже). Методы очистки давали аналогичную картину во всех образцах.
Образцы промывали в PBS, а затем в стерильной воде, после чего промывали в течение 2-6 часов в 0,5М уксусной кислоте. Затем образцы гидролизовали в течение ночи в 1 мг/мл пепсина (Worthington, Inc.) в 0,012 н HCl при 4°С. Образцы осветляли путем центрифугирования при 13000 об/мин при 4°С. Коллаген осаждался в течение 30-60 минут при 4°С после добавления 5М NaCl до конечной концентрации 0,7М. Осажденный коллаген выделяли путем центрифугирования при 13000 об/мин при 4°С в течение 30-60 минут и ресуспендировали в 0,012н. HCl.
6.3.3. Анализ
Весь белок определяли с использованием коммерчески доступного набора для колориметрического анализа (Pierce, Inc. набор для анализа ВСА, ВСА assay kit) и эти анализы проводили в соответствии с инструкциями производителей. Коллагены бычьей кожи использовали в качестве стандарта (InVitrogen, Carlsbad, CA; Cohesion Technologies, Inc., Palo Alto, CA) для определения общего белка.
Затем образцы (10 мг) подвергали анализу с помощью электрофореза в ДСН-ПААГ на 3-8% градиентном геле. После этого образцы выделенного коллагена нагревали до 95°С в восстанавливающем буфере для образца. Гели окрашивали кумасси синим, обесцвечивали и подвергали компьютерному сканированию для визуализации.
Как показано на фиг.4, для трехмерных культур, по сравнению с контролем, наблюдалось статистически значимое (р<0,05) увеличение отложения коллагена, составляющее приблизительно 50%. Эта активность не может быть обусловлена присутствием лишь среды или сыворотки.
Такое повышенное отложение коллагена in vivo имеет ряд применений, включая заживление ран, обработку морщин и складок определенной формы, которые появляются с возрастом, а также способно стимулировать отложение матрикса в областях выступающей кости, восприимчивых к пролежням у парализованных или лежачих больных.
7. Противооксислительная активность
7.1. Обработка эпидермальных клеток кожи кондиционированной средой
Противокислительные агенты продемонстрировали способность к предохранению/предупреждению старения и озлокачествования клеток. Противоокислительную активность трехмерной кондиционированной среды измеряли на эпидермальных клетках кожи человека. Человеческие базальные кератиноциты (˜100000/лунку) культивировали в чашках Петри в присутствии среды MCDB153 (KGM, Cloneties, Inc.), в которую добавляли 1х трехмерную кондиционированную среду, питательную среду или бессывороточную контрольную среду, в течение 3 дней при 37°С в 5% СО2-атмосфере с повышенной влажностью. Эту среду удаляли из каждого образца, клетки выделяли из чашки путем инкубирования в присутствии трипсина (Sambrook et al., 1989, Molecular Cloning: A Laboratory Manual, 2nd Ed., Cold Spring Harbor Lab Press, Cold Spring Harbor, NY), а затем центрифугировали.
7.2. FACS-анализ
Выделенные клетки инкубировали в присутствии 1 мМ дигидрородамина-1,2,3 (Molecular Probes, Eugene, Or) при 37°С в течение 30 минут, а затем анализировали с помощью FACS-анализа (сортинга флуоресцентно-активированных клеток) с использованием аппарата FACSCAN Becton-Dickinson (Franklin Lakes, New Jersey) в соответствии с инструкциями производителей. Величина внутриклеточного окисления восстановленного дигидрородаминового красителя прямо пропорциональна величине детектируемой внутриклеточной флуоресценции данного красителя в окисленном состоянии.
7.3. Результаты
Кератиноциты человека, экспонированные кондиционированной средой настоящего изобретения, обнаруживали статистически значимое (р<0,0003) 50% снижение внутриклеточного окисления по сравнению с теми же клетками, инкубированными в присутствии бессывороточной среды или среды, содержащей сыворотку (см. фиг.5). Наблюдаемое различие, очевидно, не обусловлено сывороточными факторами или аскорбиновой кислотой, присутствующими в контрольных образцах. Поэтому местное введение среды, кондиционированной трехмерными культурами, может быть использовано в косметике для лечения или предохранения клеток от старения.
8. Испытание окклюзивного пластыря, в котором оцениваются in vivo-действие биологически сконструированного косметического питательного раствора на кожу человека
8.1. Экспериментальный протокол:
В эксперименте участвовали шесть взрослых женщин (30-60 лет), давших свое согласие на данный эксперимент и имеющих хорошее здоровье. Критериями исключения из эксперимента были чувствительность к белкам, кожные болезни, поражения кожи в тестируемой области, диабет, почечные, сердечно-сосудистые или иммунологические расстройства, использование противоспалительных средств, иммунодепрессантов, антигистаминных лекарственных средств или лекарственных средств местного применения, применение косметики и беременность. Испытуемые продукты наносили на тестируемые участки (2 участка, 3,8 см2) на правом или левом предплечье каждому индивидууму в соответствии с ротационной схемой для минимизации смещения положения или порядка расположения. Участок I соответствовал контролю с использованием носителя, а участок 2 представлял собой обработанный участок (то есть обработанный кондиционированной средой). Окклюзивные пластыри представляли собой хлопчатобумажные подушечки из нетканного материала Werbil, содержащие 0,2 мл носителя или состава для обработки. Эти пластыри наносили на кожу и закрепляли 3М окклюзивной пластиковой гипоаллергенной лентой. Окклюзивные пластыри ежедневно помещали на предплечья 3 женщин в течение 5 последовательных 24-часовых периодов. Остальным 3 женщинам ежедневно наносили пластыри в течение 12 последовательных 24-часовых периодов (обработка еще продолжается). В день после последнего нанесения пластыря из каждого участка брали биопсию. Этот протокол был одобрен IRB для исследовательской организации Калифорнийского научно-исследовательского института кожи (San Diego, Са.) в соответствии со Разделом 21 CFR (Свода федеральных правил США), Части 50 и 56.
8.2. Оценки
Были проведены обширные наблюдения для оценки степени лощения, шелушения, покрывания коркой, растрескивания, гиперпигментации и гипопигментации кожи. Раздражение оценивали визуально с использованием 5-бальной шкалы и проводили количественную оценку степени эритемы, отека, появления папул и пузырьков (>25% участка нанесения пластыря), и идентифицируемых реакций (>25% участка нанесения пластыря), то есть образования или отсутствия образования мокнущих, распространенных или отвердевших волдырей. Гистологическая оценка по Н & Е дипломированными патологами предусматривала определение параметров, описывающих толщину жизнеспособного эпидермиса, эпидермальную гиперплазию (акантоз), толщину гранулярного клеточного слоя, наличие воспалительного инфильтрата, фигур митоза, появление коллагена и эластичных волокон и сосудистой сети.
8.3. Результаты
Каких-либо неблагоприятных эффектов, индуцированных кондиционированной средой или контролем у 3 индивидуумов, прошедших курс 5-дневного лечения не наблюдалось. Средние оценки, проводимые ежедневно на раздражение кожи с использованием питательного раствора (0,3) и контролей (0,2), показали, что оба участка, в большинстве случаев, не обнаруживали видимой реакции или эритемы, либо обнаруживали легкую сплошную или пятнообразную эритему. Гистология (путем окрашивания коллагена трихромом) указывала на здоровую ткань по всем измеряемым параметрам. Следовательно, кондиционированная среда обладает благоприятным действием на кожу человека.
9. Модуляция поведения эндотелиальных клеток человека
Определяли действие кондиционированной среды и человеческого матрикса, продуцированного связанными с матриксом фибробластами, на ангиогенез и подвижность эндотелиальных клеток. Кондиционированную среду продуцировали путем пересева на трехмерную культуру фибробластов, описанную в настоящей заявке (в Разделах 5.3, 5.4 и 5.6) и либо концентрировали (10х), либо лиофилизовали. Внеклеточный матрикс человека физически удаляли из ткани после продуцирования.
9.1. Анализ на образование трубочек эндотелиальных клеток
Анализ на образование трубочек эндотелиальных клеток с использованием эндотелиальных клеток пупочной вены (HUVEC) проводили для оценки ангиогенеза. Совместное культивирование HUVEC с лиофилизованной кондиционированной средой приводило к увеличению образования трубочек по сравнению с негативным контролем (среда до кондиционирования), 4,9±9,31 мм и 0,00±0,00 мм, соответственно; концентрированная среда давала увеличение образования трубочек до 44,10±1,75 мм; а внеклеточный матрикс человека давал увеличение образования трубочек до 39,3±5,6 мм.
9.2. Анализ на заживление ран
Конфлюентный слой эндотелиальных клеток соскабливали и скорость закрытия полученной "раны" измеряли для оценки подвижности клеток. Анализ на "заживление раны" измеряли как скорость закрытия раны, выраженную в мм/час (миллиметров/час). Эндотелиальные клетки, обработанные лиофилизованной средой, обнаруживали скорость 25,59±12,907 мм/ч, а скорость при обработке концентрированной средой составляла 39,56±15,87 мм/ч. Внеклеточный матрикс человека не давал увеличения скорости по сравнению с негативным контролем (среда до кондиционированная), и скорости для внеклеточного матрикса человека и негативного контроля составляли 0,00 мм/ч и 27,96±10,01 мм/ч, соответственно.
Таким образом, как было проиллюстрировано по изменениям в ангиогенезе (анализ на образование трубочек) и в подвижности клеток (анализ на "заживление ран"), кондиционированная среда настоящего изобретения обладает способностью к модуляции поведения эндотелиальных клеток человека.
Объем настоящего изобретения не ограничивается описанными здесь конкретными вариантами его осуществления. Действительно, в настоящее изобретение могут быть внесены различные модификации, которые будут очевидны каждому специалисту из вышеприведенного описания изобретения и сопровождающего его графического материала. Указанные модификации входят в объем прилагаемой формулы изобретения.
В настоящем описании цитируются различные публикации, содержание которых во всей своей полноте вводится в настоящее описание посредством ссылки.
Реферат
Изобретение относится к области биотехнологии. Средство содержит кондиционированную культуральную среду, полученную при культивировании эукариотических клеток в трех измерениях. Способ получения средства предусматривает: а) получение кондиционированной клеточной среды культивирования, содержащей требуемые уровни внеклеточных продуктов, путем культивирования эукариотических клеток в трех измерениях в клеточной культуральной среде in vitro; b) отделение кондиционированной клеточной среды культивирования от клеток, использованных для кондиционирования указанной среды; и, в случае необходимости, с) объединение указанной кондиционированной клеточной среды культивирования с фармацевтически приемлемым носителем. Средство используют для стимуляции заживления ран или лечения ожогов, коррекции косметического дефекта, ингибирования старения кожи и стимуляции роста волос. Изобретение позволяет модулировать скорость роста и репродукции эукариотических клеток. 6 с. и 31 з.п. ф-лы, 2 табл., 5 ил.
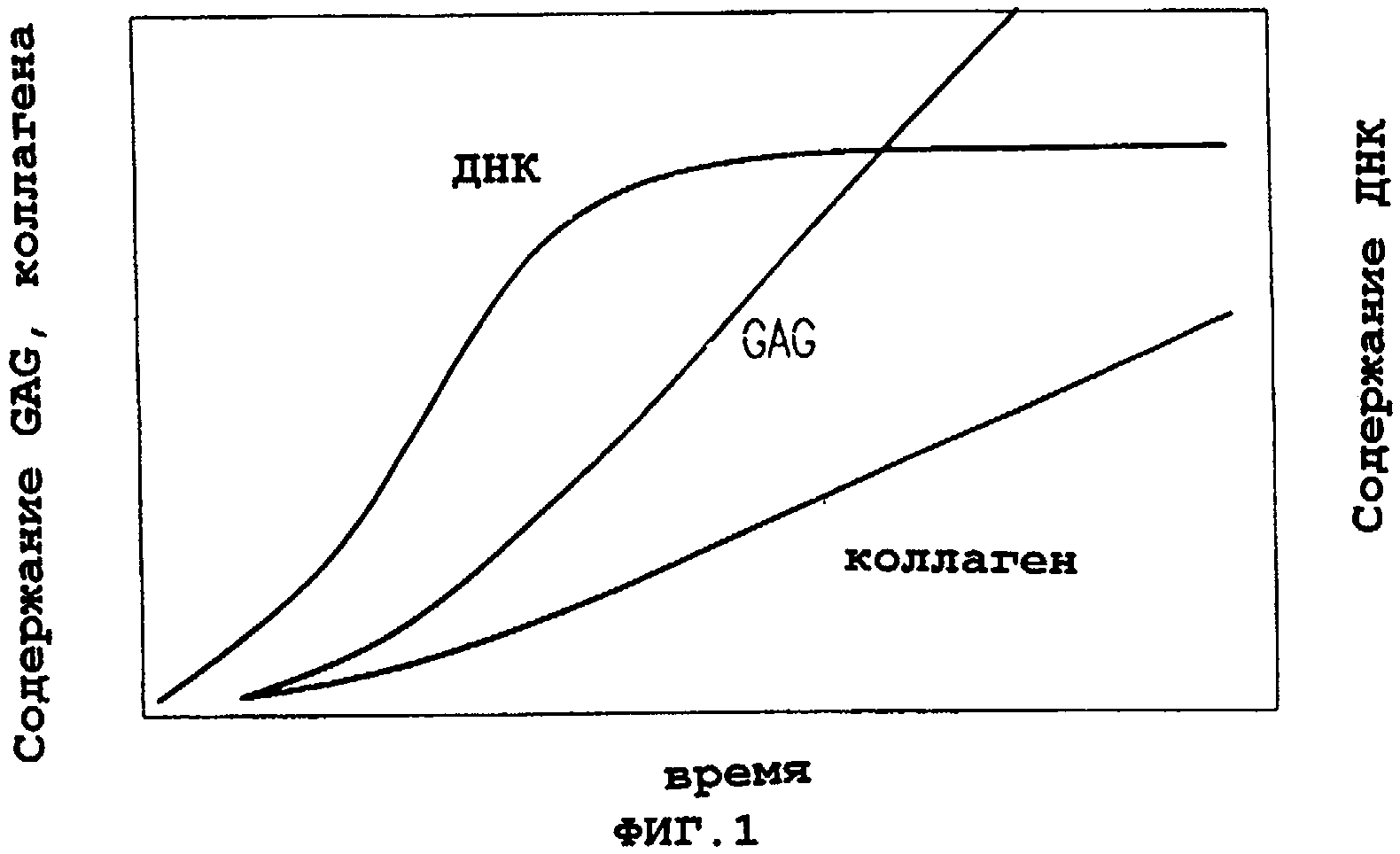

Комментарии