1
Изобретение относится к способу
получения новых фенилхинолинкарбо- новых кислот, прояв.пяющих противоопухолевую активность.
Целью изобретения является получение новых фенилхинолинкарбоновьгх
кислот, проявляющих усиленное противоопухолевое действие.
Пример 1. 2-(4-Циклогексил- фенил)-6-фтор-3-метилхинолин-4-кар- боновая кислота.
too г (0,61 моль) З-фторизатинаи 131 г (0,61 моль) 4-циклогексилпро-
пиофенона взвешивают в 1100 мл этанола и механическим образом перемешивают
с добавлением по каплям раствора 219 г (5,5 моль) КОН в 550 мл водь: . По завершении добавления смесь
нагревают 12 ч с обратным холодильником ., охлаждают, упаривая этанол
при пониженном давлении. Полученный твердый продукт растворяют в воде и
отмьшают этиловьи эфиром. Водный слой подкисляют НС1,. Полученный осадок
фильтруют и сушат. Перекристаллизацией из диметилформамида и воды получают 117 г целевого соединения
с т.пл. 316-323°С.
Пример 2. 2-(4-Бифенилил)-
-6-фтор-3-метилхинолин-4-карбоновая кислота.
18,9 г (0,09 моль) 4-фенилпропио- фенона и 20 г (0,09 моль) 5-фторизатина1
взвешивают в 360 мл этанола и механическим путем перемешивают с добавлением
по каплям раствора 33,2 г KOFi в 100 мл воды в течение 13 мин. Реакционную
смесь нагревают 12 ч с обратным холодипьником, охлаждают, этанол
упаривают при пониженном давлении. Полученный желтый твер,цьй продукт растворяют в воде и отмывают этиловым эфиром. Водный слой охлаждают до З С
и подкисляют ледяной уксусной кисло - той. Полученный желтый осадок фильт-
руют и сушат, Перекристаллизацией из 200 мл диметилформамида и 25 мл воды
получают 13,8 г целевого соединения с т.пл. 303- 306°С (с разложением) в
виде белого твердого продукта.
Примеры 3-27. Соединения,
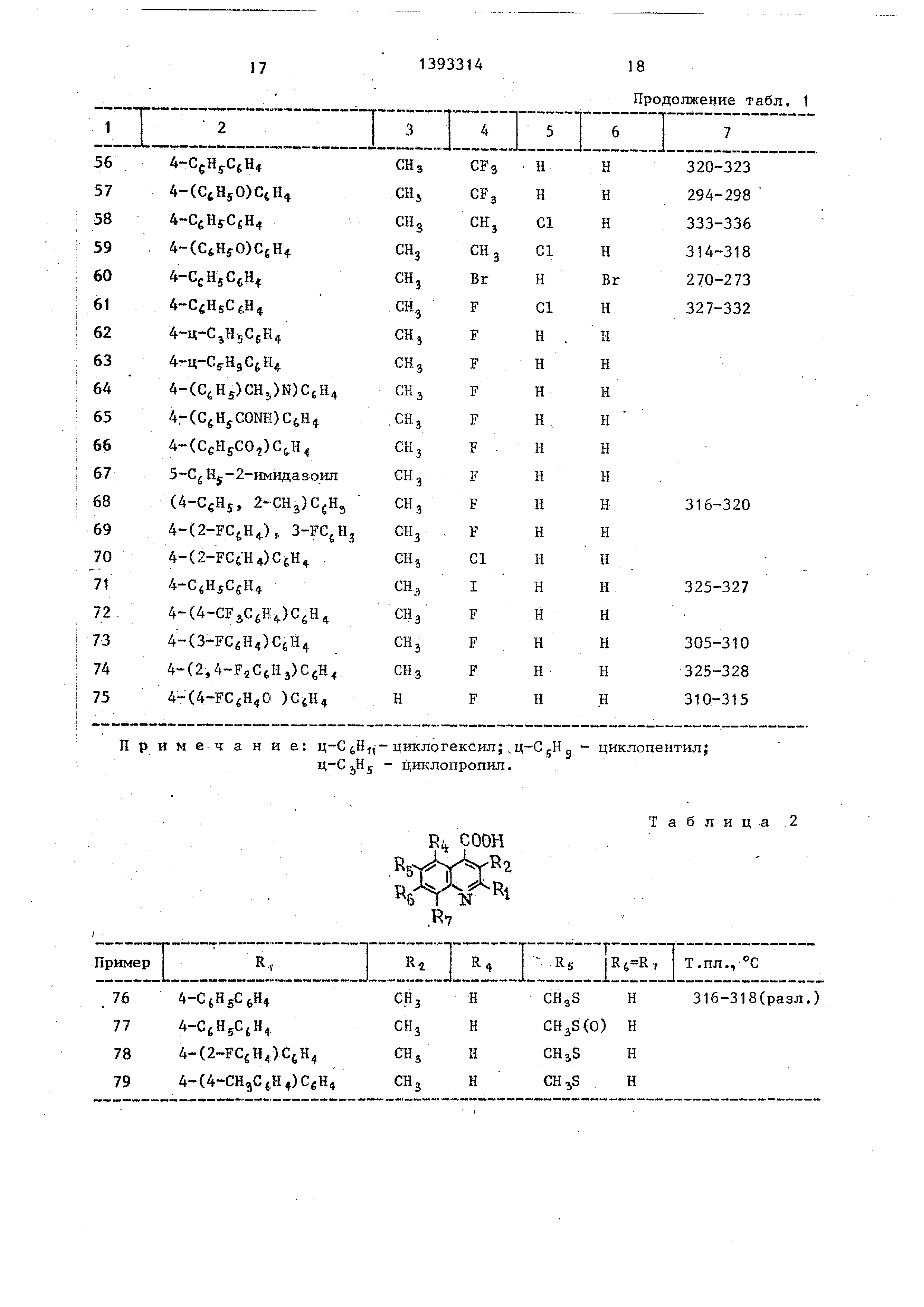
полученные аналогично, примерам 1 и 2, приведены в табл. 1.
Пример 28. 2-(2 -Фтор-1,1- -бифенил-4-ил)-6-фтор-3-метил-4-хи
нолинкарбоновая кислота.
72,6 (0,44 моль) 5-фторизатина- и
100 г (0,44 моль) 4-(2-фторфенил)про- пиофенона взвешивают в 720 мл этанола
и механическим образом перемешивают с добавлх ением по каплям в течение
15 мин раствора КОН (147, 7 г, 2,64 моль) в 300 мл воды. Реакционную смесь н.агревают
в течение 12 ч с обратным холодильником , охлаждают, этанол упари -
вают при пониженном давлении. Полученный тв.ердый продукт растворяют в
воде и отмывают этиловьм эфиром. Водный слой охлаждают до 3°С и подкисляют
ледяной уксусной кислотой. Полученный осадок фильтруют, дважды отмывают
этиловым эфиром по 300 мл и сушат . Перекристаллизацией из диметилформамида
и воды получают 83 г целевого соединения с т.пл. 315-317 С.
Примеры 29-75. Аналогично примерам 1,2, 28 получают соединения, приведенные в табл. 1.
Пример 76. 2-(4-Бифенил)-3-метил-6-метилтио-4-хинолинкарбоно- вая кислота.
2-(4-Бифенил)6-фтор-3-метнл-4- -хинолинкарбоновую кислоту - соединение
примера 2 - (7,2 г, 0,02 моль) и калийметилмеркаптида (6 г) растворяют в 100 мл диметилформамида и
нагревают до 130°С в течение 3 ч. Смесь охлаждают, растворитель упаривают
при пониженном давлении. Остаток растворяют в 250 мл воды, фильтруют , фильтрат подкисляют до рН 2.
Желтый осадок фильтруют и сушат. Порцию желтого осадка (1,8 г, 0,005 моль
взвешивают в ацетоне, содержащем 5 мл йодистого метила и 4 г карбоната калия, нагревая 24 ч с обратным
.холодильником. Реакционную смесь фильтруют и упаривают при пониженном
давлении. Остаток растворяют в этиловом эфире, отмьшают водой, сушат сул
фатом натрия и упаривают при пониженном давлении, получая твердый
продукт. Твердые продукты, полученные на отдельных прогонах этим путем (
по 6 г) соединяют и растворяют в 70 мл этанола и 30 мл воды, содер -
жащей 10 г КОН. Смесь нагревают 12 ч с обратным холодильником. Затем смес
охлаждают, упаривают при пониженном давлении, растворяют в 300 мл воды
и отмывают этиловым эфиром. Водный раствор подкисляют до рН 2 с помощью
НС1. Осадок собирают,отмьшают водой и горячим этанолом, получая 4,9 г
целевого соединения с т.пл. 316-318 С (с разложением).
Примеры 77-79. Аналогично примеру 76 получают соединения,приведенные в табл.2.
Пример ВО. 2-(4-Бифенил)- -5-хлор-6-фтор-3-метил-4-хинолинкар- боновая кислота.
4,0 г (0,02 моль) 4-хлор-5-фтори- затина, 1,46 г (0,02 моль) диэтил-
амина и 4,4 г (0,021 моль) 4-фенил- пропиофенона взвешивают в 100 мл
этанола, перемешивая в течение 12ч Осадок фильтруют, отмьгеают холодным
этанолом и сушат, получая 2,t г сырого аддукта с т.пл. 202-206 С. По -
следний растворяют в 75 мл тетрагид- рофурана и 30 мл концентрированной
НС1. Полученный раствор нагревают 24 ч с обратным холодильником, охлаждают
и разбавляют водой. Тетрагид рофуран упаривают при пониженном давлении. -Осадок фильтруют, отмьта-
ют эфиром и кипятят вместе с метанолом , получая 0,90 г целевой кисло0
5
0 5 Q
5
0
5
0
5
ты в виде кристаллического твердого
продукта с т.пл. 300-305°С.
Примеры 81-85. Аналогично
примеру 80 получают соединения приведенные в табл. 3.
Пример 86. 6-Фтор-З-метил- -2-(4-нитрофеноксифенил)-4-хинолин- карбоновая кислота.
2,0 г (0,0104 моль) 5-фторизатина, 0,77 г (0,0105 моль) диэтиламина и
2,82 г (0,0104 моль) 4-(4-нитрофенок- си)-пропиофенона взвешивают в 100 мл
этанола и 12 ч перемешивают при . Осадок фильтруют, отмьгеают толуолом
и сушат на воздухе, получая 3,0 г сырьевого продукта.
Сырьевой продукт, полученный из двух прогонов (5,0 г, 0,0108 моль),
соединяют в 180 мл тетрагидрофурана и 40 мл концентрированной НС1. Полученный
раствор 12 ч нагревают с обратным холодильником, охлаждают, растворитель упаривают при пониженном
давлении. Твердый остаток отмывают этиловым эфиром и сушат, получая 4,37 г целевой кислоты в виде
твердого продукта белого цвета с т.пл. 335-337°С.
Примеры 87-90. Аналогично примеру 86 получают соединения, приведенные в табл.3.
П р -и м е р 91. Натрий-2-(4-цик- логексилфенил)-6-фтор-3-метилхинолин- -4-карбоксилат.
Соединение примера 1 (10,0 г, 0,0275 моль) взвешивают в 400 мл
этанола и обрабатывают 1 н. NaOH (27,5 мл, 0,0275 моль). Смесь neper
мешивают до тех пор, пока раствор не станет прозрачным; этанол и воду
упаривают при пониженном давлении, получая 9,95 г натриевой соли в виде
твердого продукта белого цвета с т.пл. 350°С (с разложением).
Пример 92. Натрий-2-(4-бифе- нилил)-6-фтop-3-мeтилxинoлин-4-кapбоксилат .
Соединение примера 2 (3,57 г, 0,01 моль) растворяют в 500 мл этанола
, обрабатьшают 1 н. NaOH (10 мл) и нагревают с обратным холодильником
в течение 30 мин. Этанол и воду упаривают при пониженном давлении, получая
3,6 г натриевой соли в виде бледно-рыжего твердого продукта с т.пл. более 360°С.,
Пример ы 93-1f7. Аналогично ripwfepy 92 по/гучают соединения, приведенные
в табл. 4.
Пример 118. Натрий-2(2- -фтор-1,1 -бифеннл-4-ил)-6-фтop-3-
-мeтилxинoлин-4-кapбoкcилaт .
Соединение примера 28 (37,5 г,
О, 10 молъ) взвешивают в ЮОО мл этанола и обрабатывают 1 н. NaOH (100 м
0,10 моль). Эту смесь нагревают и перемешивают, пока она не станет прозрачной . Этанол и воду упаривают
при пониженном давлении, получая 39,6 г целевого соединения в виде белого твердого продукта с т.пл.
.
Примеры 119-163. Аналогично примеру 118 получают соединения,
приведенные в табл.4,
Пример 164,, Натрий-2-(4-
-бифенилил)-5-хлор-6-фтор-3 метил)- -хинолин-4-карбоксилат.
Соединение npi-гмера 81 (7,85 г, 0,02 моль) взвешивают в 150 мл воды
и обрабатывают 1 н. NaOH (19,9 мл, 0,0199 моль) с добавлением 150 мл
этанола. Смесь перемешивают до прозрачности и фильтруют в целях удаления
нерастворимых продуктов. Этанол и воду упаривают при пониженном давлении
, получая 8,1 г белой твердой натриевой соли с т.пл. вьше З60 с„
Примеры 165-191. Аналогично примеру 164 получают соединения, приведенные в табл.4.
Пример 192., 6-Хлор-2-(4 -ок- си-1, l -бифенил-4-шт)-3-метил-4-хино-
линкарбоновая кислота, -
Соединение примера 24 (4,0 г,
0,01 моль) добавляют по порциям в раствор бортрибромида (5,7 мл, 0,06 моль) в 90 мл хлороформа при
25°С в атмосфере аз ота. Эту суспензию; каштанового цвета 1 ч перемешивают
и выливают затем на влажный лед. Полученный желтьй осадок фильтруют,
отмьгоают хлороформом и сушат на воздухе . Твердый продукт растворяют 1 н.
NaOH, отмывают хлороформом и подкисляют ледяной уксусной кислотой. Выпавший желтый осадок фильтруют и
суиат на воздухе с получением целевого соединения в виде желтого твердого
продукта с т.пл. выше 360°С.
Примеры 193 и 194. Аналогично
примеру 192 получают соеди- И01П1Я, ;ггинеденные в табл.5.
с
0
5 0
5
5
,.
5
0
Как показали результаты ггропеден- ных различных биологических испытаний
, соединения, полученные согласно предлагаемому способу,обладают свойством
ингибирования не только развития трансплантированных опухоле.й у
мьш1ей, но также и развития опухолей, трансплантигрованных мышам от человека,
Опыт с применением меланотической меланомы В16.
Опыт проводится на мьштах ()
одного пола и весом минимум 18 г (самды) и Г/ г (самки), причем вес в
пределах диапазона 4 г в начале проведения опыта. Испытательную группу
составляют 9 и 10 мышей. Опухоль пересаживают на каждую подопытную мышь
путем подкожной инъекции 0,5 мл опухолевого гомогената, полученного гомогенизацией
1 г меланотической мела- HoMiii в Ю мл холодного физиологического раствора. Испытуемые соединения
вводятся внутрибрюшинно во взвешенном в оксипропилцеллюлозе вргде в
различных дозах один раз в сутки в течение девяти дней подряд, начиная
с первого дня после дня инокуляции опухоли (нулевой день). Контрольным
животным вводят путем инъекций только оксипропилцеллюлозный носитель.
Мышей взвешивают, количество оставшихся в живых регистрируют регулярно
в течение 60 дней. Затем рассчитывают средние сроки выживаемости и соотношение
средних сроков выживаемости обработанных (0) и контрольных (К)
животных. Средний срок вьокиваемости необработанных зараженных опухолью
мышей колеблется в пределах от 15 до 17 дней. Действенность лекарст- .
венных средств рассчитывается на основе срока выживания. Результаты приведены
в процентах (срок выживания О/К X 100%). Критерий действенности О/К 100 7/ 125%.
Результаты, полученные при применении соединения по примеру 1 и цис-
платина, сведены в табл.б.
Данные табл.6 показывают, что соединение
по примеру 1 оказывает действие против меланомы В1б у мышей.
Лимфоидное белокровие.
В этом эксперименте работали с
мышами CDiF-. Все животные весили минимум по 18 г причем к началу эксперимента
в пределах диапазона 4 г. Испытуемая группа состояла из 6 мьпией.
Опухоль трансплантир(}вали каждой
мыши путем внутрибрюшинной инъекции 0,1 мл разбавленной Ascites-жидкости,
содержащей 10 клеток, перенесенных от мьши с лейкемией L 1210. Испытуемые
соединения взвешивают в оксипро- пилцеллюлозе или физиологическом
растворе с ПАВ Tween 80 или разбавля - ют в физиологическом растворе и вводят
посредством внутрибрюшииной инъек- д изводимые 35-миллиметровые образф
ции в разных дозах один раз в сутки
в течение девяти дней подряд, начиная с первого дня после дня инокуляции опухоли (нулевого). Контрольным
мышам вводят инъекциями физиологичес- с кий раствор или оксипропилцеллюлозный
носитель. Мьш1ей взвешивают, выживших подсчитьгоают регулярно в течение
30 дней. Средний срок выживаемости
и соотношение среднего срока выживае- 2о различных концентрациях к другим йульмости
обработанных (О) и контрольньк (К) животных вычисляют. Средний срок
выживаемости необработанных заражен- ных опухолью животных колеблется в
пределах от 8 до 9 дней. Действенность лекарственного средства определяют на основе срока выживания.
Результат выражен в процентах (средний срок выживания: О/К 100%). Критерий действенности 125%.
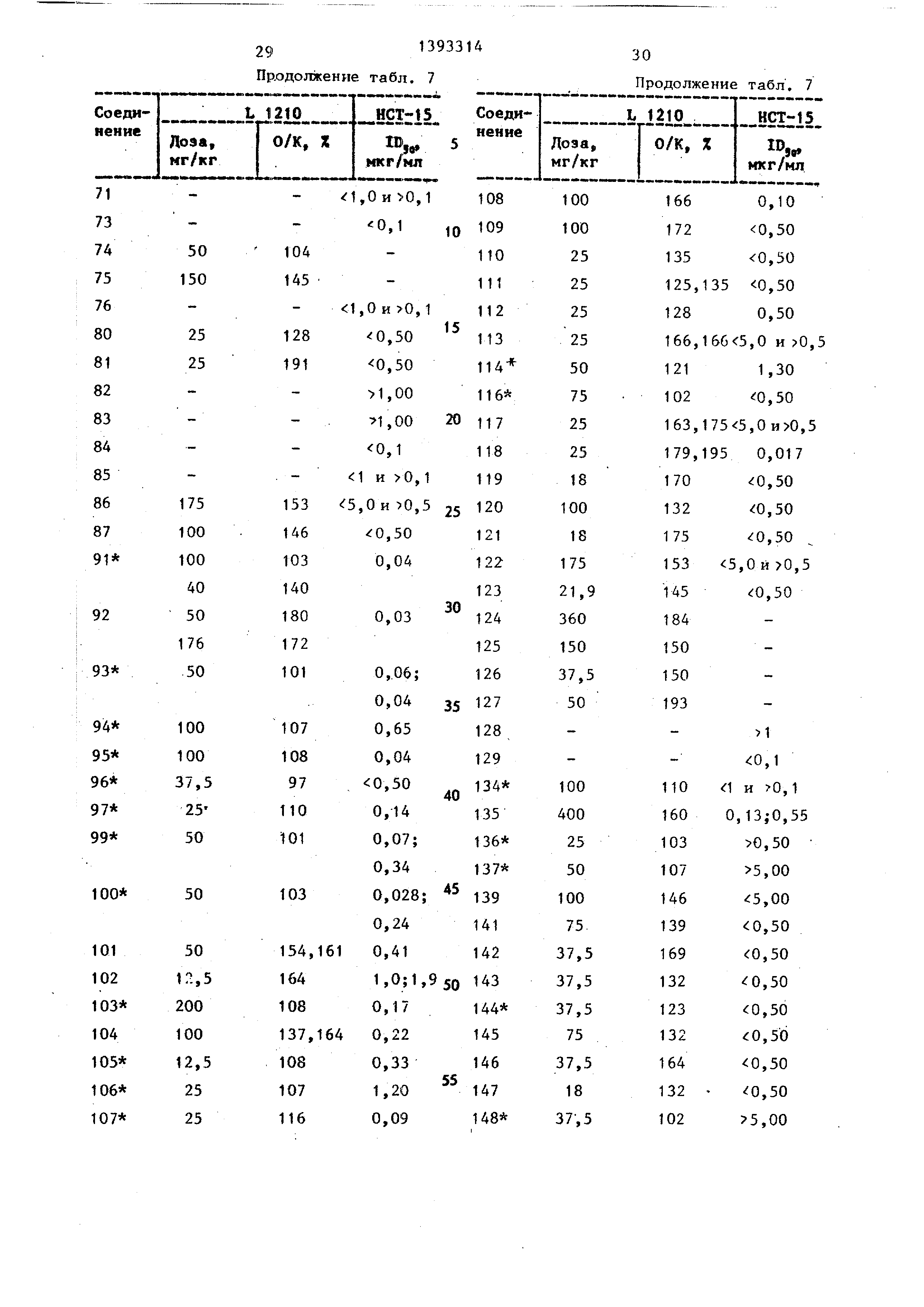
Результаты испытаний сведены в табл.7.
Данные табл.7 показывают, что соединения,полученные согласно предлагаемому способу,оказывают дей-
ствие против белокровия L 1210 у мьшгей.
Испытание на опухоли толстой кишки
человека в пробирке.
Соединения,полученные согласно
предлагаемому способу, также испытывают на их способность ингибиро-
вать развитие раковых клеток в тол- стой кишке человека в пробирке. Соединения
, ингибирующие развитие этих клеток, также ингибируют лейкемию L 1210 у мышей.
25
30
35
40
45
турам. На 4-й день обработанные и контрольные культуры собирают путем
обработки трипсином и определяют количество клеток. Количество дубликатов
контрольных клеток определяют-по количествам клеток в 1-й и 4-й дни.
Значение IDjp(концентрация соедине- ; ния,- необходимая для ингибирования
50% дубликатов) высчитывают по реакции дозы в виде кривой, которую
получают нанося количество клеток на логарифмическую бумагу типа log-
log относительно концентраций соединения . ,
Результаты испытаний сведены в
табл.7.
Данные табл. 7 показьшают, что соединения
оказывают ингибирующее действие на рост раковых клеток в толстой кишке человека.
Соединения примеров 1 и 91 также испытывались на действенность против
опухоли прямой кишки человека, пересаженной атимическим мьпиам. Эти
мыши отличаются недостаточным иммунитетом и вследствие этого не от
талкивают имплантированные опухоли человека.
Клетки рака толстой кишки, обозначенные НСТ-15, получают из образца
аденокарциномы толстой кишки чело- века, удаленной во время операции.
Клетки выращивают в среде 1640 института Roxoell Park Medical institute
(RPMI), в которую добавляют 10% термически дезактивированной сыво- ротки теленка, пенициллином
(100 ед/мл), стрептомицином 100 мкг/мл), гентамицином (20 мкг/мл)
фунгизоном (25 мкг/мл), 0,075% бикарбоната натрия, 10 мкмоль 4-(2-окси-
этш1)-1-пиперазинэтансульфоновой кислоты и 10 мкмоль 11-трис(оксиметил)-
-метилглицина. В целях определения эффективности испытуемых соединений
при ингибировании развития этих клеток проводят следующий опыт. Воспротканевой
культуры инокулируют клетками 1,5x10 НСТ-15 в 2 мл среды RPMI 16АО, описанной выше. В первый
день после инокуляции клетки собирают с пластин с. применением обработки
трипсинов (0,25%), подсчитывают количество клеток на пластине гемоцито-
метром в момент добавления соединений. Испытуемые соединения добавляют в
5
0
5
0
5
5
турам. На 4-й день обработанные и контрольные культуры собирают путем
обработки трипсином и определяют количество клеток. Количество дубликатов
контрольных клеток определяют-по количествам клеток в 1-й и 4-й дни.
Значение IDjp(концентрация соедине- ; ния,- необходимая для ингибирования
50% дубликатов) высчитывают по реакции дозы в виде кривой, которую
получают нанося количество клеток на логарифмическую бумагу типа log-
log относительно концентраций соединения . ,
Результаты испытаний сведены в
табл.7.
Данные табл. 7 показьшают, что соединения
оказывают ингибирующее действие на рост раковых клеток в толстой кишке человека.
Соединения примеров 1 и 91 также испытывались на действенность против
опухоли прямой кишки человека, пересаженной атимическим мьпиам. Эти
мыши отличаются недостаточным иммунитетом и вследствие этого не от
талкивают имплантированные опухоли человека.
Опухоль НСТ-15 прямой кишки человека .
Работают с подопытными швейцарскими
атимическими мьш1ами (NU/NU) весом 20-22 г к началу проведения испытания
. Испытуемая группа состоит из 12 мьш1ей - 7 самцов и 5 самок.
Линию клеток опухоли НСТ-15, полу- , ченную от пациента с аденокарционо-
мой толстой кишки, выдерживают в культуре . Опухоль трансплантируют каждои из подопытных мьшюй путем внут- рибрюишнной инъекции в бок 0,2 мл физиологического раствора, содержащего
10 НСТ-15 культуральных кле Ток. Опухоль начинает появляться в Течение 72 ч, обработку начинают
liiepes неделю после инокуляции опу- :|соли„
Испытуемые соединения, взвешенные
метоцеле (0,5% в воде) или растворенные в воде, впрыскивают внутрк-
|5рюшинно один раз в сутки в течение .) дней подряд, начиная с седьмого
дня после дня инокуляции опухоли, Зес тела и размеры опухоли замеряют
«ежесуточно. Размеры опухоли замеря- SOT двумерными кронциркулями. Вес опу
:)соли определяют согласно формуле
1 у w
мг.
де 1 - длина, мм; w - ширина опу
Коли , t-ГА ,
Вес (нетто) опухотш определяют Путем вычитания из веса опухоли в
момент оценки первоначально определенного веса опухоли в момент нача-
Па обра ботки (день седьмой). Эффек- гивность лекарственного средства оп
ределяют на основе ингибирования гвеличения веса-нетто оп холи: обра-
Зотанного (о) животного сравнительно с контрольным (к)„ Ингибирование
эоста опухоли (%) рассчитывают согласно формуле
Л-
Вес-нетто опухоли (О) Вес-нетто опухоли (К)
х100%.
Результаты испытания сведены в табл 8.
Данные табл. 8 показывают, что
соединения полученные согласно предлагаемому способу,, ингибируют рост
опухоли НСТ-15 толстой кишки человека в мышах. 5-Фторурацил, используемый
в качестве этгшона, токсичен в дозе 40 мг/кг и не оказьшает действия в дозе. 20 мг/кг (5-фторурацйл
иногда используют при лечении опухоли толстой кишки у человека, но это
средство не оказьшает существенного действия)..
В общей сложности опыты показали, что соединения,полученные согласно
предлагаемому способу, оказывают противоопухолевое действие на трансплантированные мьшам опухоли, включая лимфоидную лейкемию L1210 и мелано- . тическуто меланому В 16 у мышей. Соеди-
нения также оказывают действие про- тив опухоли толстой кишки человека
НСТ-15 в тканевых культурах и в чае переноса опухоли атимическим мышам.
10
Формула изобретения
Способ получения производных хи- нолинкарбоновых кислот общей форму™ I - Rti RS
O, i ls
Ry
где RI - группа
-( (0)R8
RIO
,o - i; to-c-R8
0
Rs
где X - 0, S или ,,
Rg - СНэСН2(СНз)СН, С5-С,р-алкил, Сз-С -циклоалкнл, группа
,W /-ry
или .
если R,- -(oVs(0)
TO R g дополнительно может означать С j-C 4-алкил j
Ri - водород, С ,-C з-алкокси, C -Cjалкилтио или С -С -алкил; Rj или CO,jR,i;
R, Rg, Rj, R7 - независимо друг от друга означают водород, фтор,
хлор, бром, йод, CHj, CFg или , причем,
по меньшей мере, два из радикалов
R45 5 4 Т
означают водороду
или -сн..
не
водород или С.,-С j-алкил;
RJlJиR,- независимо дрз г от друга
11139331412
RIJ- (СНг)г-4ЫК1.К,1;
W, Y и Z независимо друг от друга
водород, фтор, хлор,
бром, С -С -алкил, NOj,
С,-Су-алкокси или CFjj m О или 1,
или при условии, что
1)если R3-C02H, Rg - фенил, а R4,
RC, R7 водород, R 5 не может означать бром;
2)R, RJИ Rj не могут все означать
водород;
3)если RJ- CO CHxjCHxjNCCH j) , Rj - или R хлор, RJ не мо- jc
жет означать циклогексил;
Л) если Rg -циклогексил, а R-2 - во-О
дород, RS должен означать хлор где X - О, S, Rg- С -Сйалкил, или фтор, но RS и R, не могут оба С -С -циклоалкил,группа /-.
to
модействию со спиртом RjjOH в ра
ворителе, таком как тетрагидроф при температуре кипения реакцио смеси в присутствии основания,
кого как 4-диметиламинопиридин.
Приоритет по признакам:
22,07.83 при RT - группа Y Кй
(.0).
0)
30
означать хлор;20
5) если Rg - а R - водород , RS не может означать хлор,
и R7 не может означать бром, или их фармацевтически пpиeмлe мx солей
, или эфиров о т л и ч а ю щ и й- 2S с я тем, что соответственно замещенный
изатин подвергают взаимодействию с замещенным кетоном в растворителе , таком как этанол, в присутствии
водного раствора основания, такого как NaOH, NH.OH или КОН, при
температуре от 25°С до температуры кипения растворителя, затем подкисляют
реакционную смесь минеральной кислотой, такой как соляная, или органической
кислотой, такой как уксусная , и выделяют целевой продукт в свободном виде или в виде соли кар-
боновой кислоты, при этом хинолин- карбоновую кислоту общей формулы I
растворяют в протонном растворителе, таком как этанол, затем обрабатывают
гидроокисью металла или амином, таким как 1-аминобутанол, или лизином при температуре от комнатной до
температуры кипения растворителя, и получая в соответствующем случае
соль аминогруппы путем растворения амина в растворителе, таком как
этиловый эфир, и добавляя минеральную кислоту, такую как НС1, или выделяют
целевой продукт в виде эфира, при этом соль хинолинкарбоновой кислоты
общей формулы I подвергают взаимодействию с оксалилхлоридом в инертном растворителе, таком как
бензол, при температуре кипения реакционной смеси, образующийся гало-
генангидрид кислоты подвергают взаидополнительно Rg - Сз-С -алкил
рода (если R, - -xQ)-.) дород, Ci-Сз-алкил, Rj- COjH; ,; R, Rj, Rf, R, - водород,
хлор, бром, йод, , CFj, прич меньшей мере два из радикалов R R Р R 7 означают водород R э г
ДУ
; R ,Р и R,, - водород Iiл
40
Ci-Сз-алкил ; W, Уи Z - н симо друг от друга водород, фто
35 хлор, бром, С,-С5-алкш1, m О или при условии, что
1)если Ra - , R е- , а R и RY - водород, Rj не мож означать бром,
2)R, RS и Rj не могут все озн водород,
3)если Rg-циклогексил, а Rj -
род, Rf должен означать хлор фтор, но RS и RY не могут об начать хлор,
4)если Rg - , а R, - род, Rj не может означать х и RY не может означать бром;
30,04.84 при RT- группа
Rg; -@bOI 9;-XO)-S(O
45
50
55
,0 SiJU
о
где X - О, S или , Rg -
СН,,СН,г(СН j)CH, С5-С„-алкил, Cjциклоалкил , группа
модействию со спиртом RjjOH в растворителе , таком как тетрагидрофуран,
при температуре кипения реакционной . смеси в присутствии основания, такого как 4-диметиламинопиридин.
Приоритет по признакам: 22,07.83 при RT - группа Y Кй
О
(.0). 0)
дополнительно Rg - Сз-С -алкил углерода (если R, - -xQ)-.) 2 -водород , Ci-Сз-алкил, Rj- COjH; и
,; R, Rj, Rf, R, - водород, фтор, хлор, бром, йод, , CFj, причем по
меньшей мере два из радикалов R,, Ну, R Р R 7 означают водород R э группа ДУ
; R ,Р и R,, - водород Iiли
Ci-Сз-алкил ; W, Уи Z - независимо
друг от друга водород, фтор, хлор, бром, С,-С5-алкш1, m О или 1, или при условии, что
1)если Ra - , R е- , а R4, R и RY - водород, Rj не может означать бром,
2)R, RS и Rj не могут все означать водород,
3)если Rg-циклогексил, а Rj - водород , Rf должен означать хлор или
фтор, но RS и RY не могут оба означать хлор,I
4)если Rg - , а R, - водород
, Rj не может означать хлор, и RY не может означать бром; 30,04.84 при RT- группа
Rg; -@bOI 9;-XO)-S(OVB8;
,0 SiJULl g
о
где X - О, S или , Rg - СН,,СН,г(СН j)CH, С5-С„-алкил, циклоалкил, группа
или
13
если R, (0)mR8
то Rg дополнительно может означать
Сэ-С,-алкил, R - водород, f-an- кокси, С,-С з-алкилтио или С -Сз-алкил
Кз - или ,,,, R, Rj RgHR независшчо друг от друга водород, фтор, хлор, бром йод, СНзСРдИли
CHjCHj, причем, по меньшей мере два из радикалов R4s 59 с 7 озна . .
чают водородд R g - грушта
.W
или
СН,
R дЯ R.|, - независиi Z
МО друг от друга водород или С f-C 3алкил , RI - (СН/р .,,NR.,j,R,, W, f и
Н CQOH
sY Sr Y
щ
1393314
1.4
Z - независимо друг от друга водород, фтор, хлор, бром, 5--алкил5 N0,
С -С -алкокси или CFg, m О или 1, или при условии, что
1)если R3 - СО,Н, Rg - , а
R, R и R- - водород, то R не может означать бром,
2)R, R5 и Rj не могут все означать водород,
3)если Rj - COjCH CHsNCCHg), - CHjCHg или Rg - хлор, то Rg не может означать циклогексил,
4)если Rg циклогексил, а R - водород , .то R J должен означать
хлор или фтор, но Rg и RJ. не могут оба означать хлор,
5)если Rj 4-NH2C H, а R 2 - водород , то R j е может означать хлор и Ry не может означать бром.
Т а б л и ц а 1
Продолжение табл. 1
Продолжение табл. 1
Таблица 3
Ri СООН
21
1393314
22 Продолжение табл. 4
25
Лизин - H5NCH,CH,CH2CH,;CHCOiH
Ш;
1-Амяно-2-бутаиол - НjNCHCHGH СНз
ОН
139331А
26
Продолжение табл. 4
Таблица 5
29
Продолжение табл. 7
7
30
Продолжение табл. 7
Продолжение табл. 7


















Комментарии