Пиридилдиамидные комплексы переходных металлов, их получение и применение - RU2514405C2
Код документа: RU2514405C2
Чертежи


Описание
ПРИТЯЗАНИЕ НА ПРИОРИТЕТ
По настоящей заявке испрашивается приоритет по заявкам USSN 12/180132, поданной 25 июля 2008 г., и ЕР 081666190, поданной 15 октября 2008 г.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к пиридилдиамидным комплексам переходных металлов и промежуточным продуктам и способам, предпочтительно, но не исключительно предназначенным для получения таких пиридилдиамидных комплексов. Комплексы переходных металлов можно использовать в качестве катализаторов для полимеризации алкенов.
УРОВЕНЬ ТЕХНИКИ
Пиридиламины использовали для получения комплексов металлов группы 4, которые являются полезными содержащими переходные металлы компонентами для использования в полимеризации алкенов, см., например, US 2002/0142912, US 6900321 и US 6103657, где в комплексах использованы лиганды и в них лиганды бидентатно координированы с атомом переходного металла.
В WO 2005/095469 представлены каталитические соединения, в которых использованы тридентатные лиганды, связанные с двумя атомами азота (одним амидной группы и одним пиридильным) и с одним атомом кислорода.
В US 2004/0220050A1 и WO 2007/067965 раскрыты комплексы, в которых лиганд тридентатно координирован с донорами, двумя атомами азота (одним амидной группы и одним пиридильным) и с одним атомом углерода (арильного аниона).
Главной стадией активации этих комплексов является включение алкена в связь металл-арил предшественника катализатора (Froese, R. D. J. et al., J. Am. Chem. Soc. 2007, 129, 7831-7840) с образованием активного катализатора, т.е. 5-членного и 7-членного хелатных колец.
Все еще необходимы дополнительные пути синтеза с целью расширения ассортимента каталитических комплексов, которые можно получить, и расширения их рабочих характеристик для полимеризации алкенов. Рабочие характеристики могут меняться по количеству получаемого полимера в пересчете на количество катализатора (обычно называющемуся "активностью") при преобладающих условиях полимеризации; молекулярной массе и молекулярно-массовому распределению, получаемому при данной температуре; и распределению высших альфа-олефинов, выраженному с помощью степени стереорегулярного распределения.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к новым комплексам переходных металлов, содержащим тридентатные лиганды NNN. Лиганд можно образовать из нейтрального предшественника лиганда или образовать in situ в комплексе, как это будет описано ниже. Настоящее изобретение также относится к пиридилдиамидному комплексу переходного металла, описывающемуся общей формулой (I)

в которой
М обозначает металл группы 3, 4, 5, 6, 7, 8, 9, 10, 11 или 12;
Z обозначает -(R14)pC-C(R15)q-,
где R14 и R15 независимо выбраны из группы, включающей водород, гидрокарбилы (предпочтительно алкилы) и замещенные гидрокарбилы, и где соседние группы R14 и R15 могут быть связаны с образованием ароматического или насыщенного замещенного или незамещенного гидрокарбильного кольца, которое содержит 5, 6, 7 или 8 кольцевых атомов углерода и в котором заместители кольца могут связываться с образованием дополнительных колец,
р равно 1 или 2, и
q равно 1 или 2;
R1 и R11 независимо выбраны из группы, включающей гидрокарбилы (такие как алкилы, арилы), замещенные гидрокарбилы (такие как гетероарилы) и силильные группы;
R2 и R10 все независимо обозначают -E(R12)(R13)-, где Е обозначает углерод, кремний или германий, и каждый R12 и R13 независимо выбран из группы, включающей водород, гидрокарбилы (например, алкил и арил), замещенные гидрокарбилы (например, гетероарил), алкоксигруппу, силил, аминогруппу, арилоксигруппу, галоген и фосфиновую группу, R12 и R13 могут быть связаны с образованием насыщенного замещенного или незамещенного гидрокарбильного кольца, которое содержит 4, 5, 6 или 7 кольцевых атомов углерода и в котором заместители кольца могут связываться с образованием дополнительных колец, или R12 и R13 могут быть связаны с образованием насыщенного гетероциклического кольца или насыщенного замещенного гетероциклического кольца, в котором заместители кольца могут связываться с образованием дополнительных колец;
R3, R4 и R5 независимо выбраны из группы, включающей водород, гидрокарбилы (например, алкилы и арилы), замещенные гидрокарбилы (например, гетероарил), алкоксигруппу, арилоксигруппу, галоген, аминогруппу и силил, и где соседние группы R (R3 и R4 и/или R4 и R5) могут быть связаны с образованием замещенного или незамещенного гидрокарбильного или гетероциклического кольца, которое содержит 5, 6, 7 или 8 кольцевых атомов и в котором заместители кольца могут связываться с образованием дополнительных колец;
L обозначает анионную отщепляющуюся группу, причем группы L могут быть одинаковыми или разными и любые две группы L могут быть связаны с образованием дианионной отщепляющейся группы;
n равно 0, 1, 2, 3 или 4;
L' обозначает нейтральное основание Льюиса; и
w равно 0, 1, 2, 3 или 4.
Настоящее изобретение также относится к способу получения указанного выше комплекса, к способу получения промежуточных продуктов для указанного выше комплекса и к способам полимеризации олефинов с использованием указанного выше комплекса.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фиг.1 является иллюстрацией молекулярной структуры комплекса переходного металла С3, предлагаемого в настоящем изобретении, определенной с помощью рентгенографии монокристалла и изображенной с 50% термическими эллипсоидами. Совместно кристаллизующиеся молекулы эфира и атомы водорода для наглядности опущены.
Фиг.2 является иллюстрацией молекулярной структуры комплекса переходного металла С7, предлагаемого в настоящем изобретении, определенной с помощью рентгенографии монокристалла и изображенной с 50% термическими эллипсоидами. Совместно кристаллизующиеся молекулы гексана и атомы водорода для наглядности опущены.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В настоящем описании описаны комплексы переходных металлов. Термин используется для описания молекул, в которых дополнительный лиганд координирован с центральным атомом переходного металла. Лиганд является объемным и стабильно связан с переходным металлом, так чтобы обеспечивать его воздействие при использовании катализатора, например, при полимеризации. Лиганд может быть связан с переходным металлом с помощью ковалентной связи и/или электронодонорной координационной связи или связей промежуточных типов. Комплексы переходных металлов обычно активируют, чтобы они выполняли свою функцию полимеризации или олигомеризации, с помощью активатора, который предположительно образует катион в результате отщепления от металла анионной группы, часто называющейся отщепляющейся группой.
При использовании в настоящем изобретении в схеме нумерации для групп Периодической системы используются новые обозначения, описанные в публикации Chemical и Engineering News, 63(5), 27 (1985).
При использовании в настоящем изобретении Me обозначает метил, Et обозначает этил, t-Bu иtВи обозначают третичный бутил, iPr иiРr обозначают изопропил. Су обозначает циклогексил, ТГФ обозначает тетрагидрофуран, Вn обозначает бензил и Ph обозначает фенил.
Термин "замещенный" означает, что водород замещен гетероатомом или гидрокарбильной группой. Например, метилциклопентадиен замещен метильной группой.
Термины "гидрокарбильный радикал", "гидрокарбил" и "гидрокарбильная группа" в настоящем документе используются взаимозаменяемым образом. Аналогичным образом, термины "группа", "радикал" и "заместитель" в настоящем документе используются взаимозаменяемым образом. В настоящем описании "гидрокарбильный радикал" определяется как C1-С100-радикалы, которые могут быть линейными, разветвленными или циклическими, и если они являются циклическими, то они могут быть ароматическими или неароматическими.
Замещенные гидрокарбильные радикалы являются радикалами, в которых по меньшей мере один атом водорода гидрокарбильного радикала замещен по меньшей мере одной функциональной группой, такой как NR*2, OR*, SeR*, TeR*, PR*2, AsR*2, SbR*2, SR*, BR*2, SiR*3, GeR*3, SnR*3, PbR*3 и т.п., или в которых в гидрокарбильное кольцо включен по меньшей мере один гетероатом.
Термин "каталитическая система" определяется как пара комплекс/активатор. Если термин "каталитическая система" используется для описания такой пары до активации, то он означает неактивированный каталитический комплекс (прекатализатор) вместе с активатором и необязательно соактиватором. Если он используется для описания такой пары после активации, то он означает активированный комплекс вместе с активатором или другим нейтрализующим заряд фрагментом. Соединение переходного металла может быть нейтральным, как в прекатализаторе, или заряженной системой с противоионом, как в активированной каталитической системе.
Комплекс при использовании в настоящем изобретении часто означает предшественник катализатора, прекатализатор, катализатор, каталитическое соединение, соединение переходного металла или комплекс переходного металла. Эти термины используются взаимозаменяемым образом.
Поглотитель представляет собой соединение, которое обычно добавляют для облегчения полимеризации за счет поглощения примесей. Некоторые поглотители также могут выступать в качестве активаторов и их могут называть соактиваторами. Соактиватор, который не является поглотителем, также можно использовать вместе с активатором для образования активного катализатора. В некоторых вариантах осуществления соактиватор можно предварительно смешать с соединением переходного металла для образования алкилированного соединения переходного металла.
Некоординирующийся анион (НКА) означает анион, который не координируется с катионом металла катализатора или который координируется с катионом металла, но лишь слабо. Термин НКА также включает многокомпонентные содержащие НКА активаторы, такие как N,N-диметиланилинийтетракис(пентафторфенил)борат, которые содержат кислотную катионную группу и некоординирующийся анион. Термин НКА также включает нейтральные кислоты Льюиса, такие как трис(пентафторфенил)бор, который может взаимодействовать с катализатором с образованием активированных систем путем отщепления анионной группы. НКА координируется достаточно слабо, так что нейтральное основание Льюиса, такое как олефиново- или ацетиленовоненасыщенный мономер, может вытеснить его из каталитического центра. Можно использовать или включить в некоординирующийся анион любой металл или металлоид, которые образует совместимый слабокоординирующийся анион. Подходящие металлы включают, но не ограничиваются только ими, алюминий, золото и платину. Подходящие металлоиды включают, но не ограничиваются только ими, бор, алюминий, фосфор и кремний. Стехиометрический активатор может быть нейтральным или ионным. Термины ионный активатор и стехиометрический ионный активатор можно использовать взаимозаменяемым образом, аналогичным образом, термины нейтральный стехиометрический активатор и активатор - кислота Льюиса можно использовать взаимозаменяемым образом. Термин некоординирующийся анион включает нейтральные стехиометричеекие активаторы, ионные стехиометричеекие активаторы и активаторы - кислоты Льюиса.
Если указано, что полимер или олигомер включает олефин, то олефин, содержащийся в полимере или олигомере, представляет собой полимеризованную или олигомеризованную форму олефина. Олигомер определяется как композиции, содержащие 2-50 мономерных звеньев. Полимер определяется как композиции, содержащие 51 или большее количество мономерных звеньев.
Высший α-олефин определяется как α-олефин, содержащий 4 или большее количество атомов углерода.
Если не указано иное, все единицы молекулярных масс (например, Mw, Mn, Mz) выражены в г/моль.
Если не указано иное, все температуры плавления (Тm) соответствуют вторым положениям плавления по данным ДСК.
"Кольцевой атом углерода" представляет собой атом углерода, который является частью циклической кольцевой структуры. При этом определении бензильная группа содержит 6 кольцевых атомов углерода и пара-метилстирол также содержит 6 кольцевых атомов углерода,
Термин "арил" или "арильная группа" означает содержащее 6 атомов углерода ароматическое кольцо и его замещенные варианты, включая, но не ограничиваясь только ими, фенил, 2-метилфенил, ксилил, 4-бромксилил. Аналогичным образом, гетероарил означает арильную группу, в которой кольцевой атом углерода (или 2, или 3 кольцевых атома углерода) заменен на гетероатом, предпочтительно N, О или S.
Термин "кольцевой атом" означает атом, который является частью циклической кольцевой структуры. При этом определении бензильная группа содержит 6 кольцевых атомов и тетрагидрофуран содержит 5 кольцевых атомов.
Гетероциклическое кольцо означает кольцо, в кольцевой структуре содержащее гетероатом в отличие от гетероатома замещенного кольца, когда атом водорода, связанный с кольцевым атомом, заменяется на гетероатом. Например, тетрагидрофуран является гетероциклическим кольцом и 4-N,N-диметиламинофенил является кольцом, замещенным гетероатомом.
При использовании в настоящем изобретении термин "ароматический" также означает псевдоароматические гетероциклы, которые являются гетероциклическими заместителями, которые обладают свойствами и структурой (почти плоской), сходными с характеристиками ароматических гетероциклических лигандов, но не соответствуют определению ароматичности; аналогичным образом, термин "ароматический" также означает замещенные ароматические соединения.
Термин "непрерывная" означает систему, которая действует без перерывов или остановок. Например, непрерывный способ получения полимера будет таким, в котором реагенты непрерывно вводят в одну или большее количество реакций и полимерный продукт непрерывно выводят.
Полимеризация в растворе означает полимеризацию, при которой полимер растворяют в жидкой полимеризационной среде, такой как инертный растворитель, или мономер(ы), или их смеси. Полимеризация в растворе обычно является гомогенной. Гомогенная полимеризация означает полимеризацию, при которой полимер растворяют в полимеризационной среде. Такие системы предпочтительно не являются мутными, как это описано в публикации J. Vladimir Oliveira, С.Dariva and J. С.Pinto, Ind. Eng, Chem. Res. 29, 2000, 4627.
Полимеризация в блоке означает полимеризацию, при которой полимеризующиеся мономеры и/или сомономеры используют в качестве растворителя или разбавителя с использованием небольшого количества или без использования инертного растворителя в качестве растворителя или разбавителя. Небольшую часть инертного растворителя можно использовать в качестве носителя для катализатора и поглотителя. Блочная полимеризационная система содержит менее 25 мас.% инертного растворителя или разбавителя, предпочтительно менее 10 мас.%, предпочтительно менее 1 мас.%, предпочтительно 0 мас.%.
Первым объектом настоящего изобретения является пиридилдиамидный комплекс переходного металла (необязательно предназначенный для использования для полимеризации алкена), описывающийся общей формулой (I)
в которой

М обозначает металл группы 3, 4, 5, 6, 7, 8, 9, 10, 11 или 12 (предпочтительно металл группы 4, предпочтительно Ti, Zr или Hf);
Z обозначает -(R14)pC-C(R15)q-,
где R14 и R15 независимо выбраны из группы, включающей водород, гидрокарбилы и замещенные гидрокарбилы (предпочтительно водород и алкилы), и где соседние группы R14 и R15 могут быть связаны с образованием ароматического или насыщенного замещенного или незамещенного гидрокарбильного кольца, которое содержит 5, 6, 7 или 8 кольцевых атомов углерода и в котором заместители кольца могут связываться с образованием дополнительных колец, р равно 1 или 2, и q равно 1 или 2;
R1 и R11 независимо выбраны из группы, включающей гидрокарбилы, замещенные гидрокарбилы и силильные группы (предпочтительно алкил, арил, гетероарил и силильные группы);
R2 и R10 все независимо обозначают -E(R12)(R13)-, где Е обозначает углерод, кремний или германий, и каждый R12 и R13 независимо выбран из группы, включающей водород, гидрокарбил и замещенный гидрокарбил, алкоксигруппу, силил, аминогруппу, арилоксигруппу, галоген и фосфиновую группу (предпочтительно водород, алкил, арил, алкоксигруппу, силил, аминогруппу, арилоксигруппу, гетероарил, галоген и фосфиновую группу), R12 и R13 могут быть связаны с образованием насыщенного замещенного или незамещенного гидрокарбильного кольца, которое содержит 4, 5, 6 или 7 кольцевых атомов углерода и в котором заместители кольца могут связываться с образованием дополнительных колец, или R12 и R13 могут быть связаны с образованием насыщенного гетероциклического кольца или насыщенного замещенного гетероциклического кольца, в котором заместители кольца могут связываться с образованием дополнительных колец;
R3, R4 и R5 независимо выбраны из группы, включающей водород, гидрокарбилы, замещенные гидрокарбилы, алкоксигруппу, арилоксигруппу, галоген, аминогруппу и силил (предпочтительно водород, алкил, алкоксигруппу, арилоксигруппу, галоген, аминогруппу, силил и арил), и где соседние группы R (R3 и R4 и/или R4 и R5) могут быть связаны с образованием замещенного или незамещенного гидрокарбильного или гетероциклического кольца, которое содержит 5, 6, 7 или 8 кольцевых атомов и в котором заместители кольца могут связываться с образованием дополнительных колец;
L обозначает анионную отщепляющуюся группу, причем группы L могут быть одинаковыми или разными и любые две группы L могут быть связаны с образованием дианионной отщепляющейся группы;
n равно 0, 1, 2, 3 или 4;
L' обозначает нейтральное основание Льюиса; и
w равно 0, 1, 2, 3 или 4.
Предпочтительно, если группы R, указанные выше, и другие группы R, указанные ниже в настоящем изобретении, содержат до 30, предпочтительно не более 30 атомов углерода, более предпочтительно от 2 до 20 атомов углерода.
Предпочтительно, если М обозначает Ti, Zr или Hf и/или Z обозначает арильную группу, образующую мостик между NR11 и остальной частью комплекса через соседние атомы углерода фенильного кольца, и Е обозначает атом углерода, и комплексы на основе Zr или Hf являются особенно предпочтительными. Z может обозначать арильную группу и в этом случае 2 соседних атома углерода СС являются частью арильного кольца.
В предпочтительном варианте осуществления комплексы, предлагаемые в настоящем изобретении, описываются общей формулой IV

в которой R6, R7, R8 и R9 независимо выбраны из группы, включающей водород, гидрокарбилы, замещенные гидрокарбилы, алкоксигруппу, галоген, аминогруппу, силил и пары положений, и в которой соседние группы R (R6 и R7 и/или R7 и R8, и/или R8 и R9) могут быть связаны с образованием насыщенного замещенного или незамещенного гидрокарбильного или гетероциклического кольца, которое содержит 5, 6, 7 или 8 кольцевых атомов углерода и в котором заместители кольца могут связываться с образованием дополнительных колец; и М, L, L', w, n, R1, R2, R3, R4, R5, R10 и R11 являются такими, как определено выше.
В предпочтительном варианте осуществления R1 и R11 могут быть независимо выбраны из числа фенильных групп, которые содержат от 0 до 5 различных заместителей, которые включают F, Cl, Вr, I, СF3, NO2, алкоксигруппу, диалкиламиногруппу, арильные и алкильные группы, содержащие от 0 до 10 атомов углерода.
В предпочтительном варианте осуществления L может быть выбран из группы, включающей галоген, алкил, арил, алкоксигруппу, амидную группу, гидридную группу, феноксигруппу, гидроксигруппу, силил, аллил, алкенил и алкинил. Выбор отщепляющихся групп зависит от использующегося пути получения комплекса и может меняться при добавлении реакций, удовлетворяющих требованиям последующей методики активации при полимеризации. Например, алкил является предпочтительным при использовании некоординирующихся анионов, таких как N,N-диметиланилинийтетракис(пентафторфенил)-борат или трис(пентафторфенил)боран. В другом варианте осуществления 2 группы L могут быть связаны с образованием дианионной отщепляющейся группы, например, оксалата.
В другом варианте осуществления каждый L' независимо выбран из группы, включающей простые эфиры, простые тиоэфиры, амины, нитрилы, имины, пиридины и фосфины, предпочтительно простые эфиры.
Комплексы, описанные в настоящем изобретении, можно получить с помощью различных путей синтеза, которые все дают комплекс с тридентатно координированным пиридилдиамидным лигандом. Типичные структуры пиридилдиамидных комплексов переходных металлов приведены ниже на диаграмме 1.

Вторым объектом настоящего изобретения являются различные способы синтеза комплексов, соответствующих первому объекту, таких как приведенные выше. В некоторых из этих способов могут использоваться промежуточные продукты, которые сами по себе являются новыми и образуют дополнительный объект настоящего изобретения.
Первый путь синтеза основывается на формальном включении имина в связь металл-углерод орто-арильной группы отдельно синтезированного промежуточного пиридиламидного комплекса металла. Включение имина приводит к замене связи металл-углерод на связь металл-амид. Таким образом, исходные комплексы металл-лиганд, в которых лиганд координирован с металлом через донорные 2 атома азота и один атом углерода, называющиеся лигандами NNC и комплексами, коренным образом изменяются, так что теперь происходит координация через 3 донорных атома азота и образуются системы, называющиеся лигандами NNN и комплексами. Соединение, содержащее двойную связь углерод-азот, такое как имин R11N=C(R12)(R13), можно включать в связь металл-арил с образованием комплекса NNN с одним 5-членным и одним 7-членным хелатным кольцом. R11, R12 и R13 являются такими, как определено выше. Промежуточные пиридиламидные комплексы металлов (NNC) сами могут обладать каталитической активностью при полимеризации. В настоящем изобретении можно модифицировать характеристики таких промежуточных комплексов и обеспечить новые возможности в плане каталитических структур и характеристик полимеризации.
Например, NNN комплекс С5, приведенный выше на диаграмме 1, можно получить с использованием в качестве исходного вещества Hf-содержащего промежуточного комплекса NNC, называющегося Int-5, по методике, описанной в примере под названием "Синтез Int-5 с тридентатным лигандом N-N-C". Int-5 аналогичен некоторым комплексам, раскрытым в US 6900321.
В других более общих путях синтеза для получения комплексов, приведенных на диаграмме 1, можно использовать пиридилдиамины или содержащие щелочной или щелочноземельный металл производные вместо промежуточных комплексов NNC. В настоящем изобретении можно использовать имины, карбодиимиды, изоцианаты, изотиоцианаты или другие реагенты, содержащие двойные связи углерод-азот, и получить тридентатные лиганды NNN. Особый интерес представляет использование иминов, которые дадут тридентатные пиридилдиамидные донорные лиганды. Приведенное ниже уравнение V представляет общий пример получения комплекса NNN из комплекса NNC и реагента, содержащего двойную связь углерод-азот
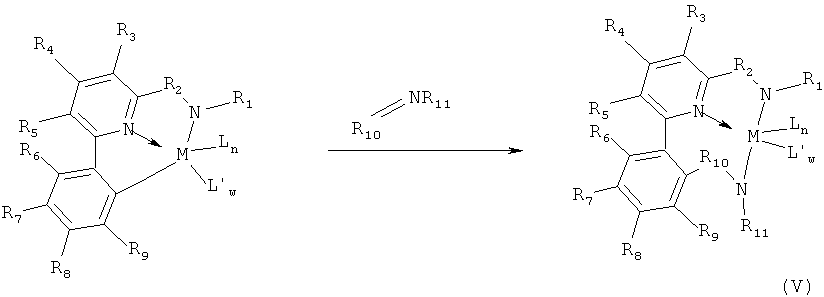
где М, L, L', w, n, R1, R2, R3, R4, R5, R6, R7, R8, R9, R10 и R11 являются такими, как определено выше.
Вторым путем синтеза является синтез подходящего нового нейтрального дополнительного предшественника лиганда NNN, который затем может координироваться с переходным металлом в комплексе NNN тридентатным образом. Этот путь отличается от первого пути синтеза тем, что в нем в качестве промежуточных продуктов не используются комплексы NNC. Одним вариантом этого пути является реакция нейтрального пиридилдиамина с подходящими металлоорганическими амидами или металлоорганическими реагентами. В альтернативном этому подходу варианте пиридилдиамин можно депротонировать с помощью литийорганического или магнийорганического реагента и затем эту пиридилдиамидную систему можно ввести в реакцию с галогенидом металла. Один пример первого подхода приведен в разделе, посвященном примерам, под названием "Синтез С7 с тридентатным лигандом N-N-N". В этом конкретном примере описана реакция пиридилдиамина L4 с металлоорганическим амидом Zr(NMe2)4 с образованием NNN комплекса С7.
Получение нейтральных лигандов NNN для использования во втором пути синтеза можно выполнить различными путями с использованием стандартных методик синтетической органической химии и некоторых новых промежуточных продуктов. Один общий путь синтеза, который можно использовать для получения предшественников пиридилдиаминовых лигандов, обладающих такими же заместителями (т.е. группы R являются такими же, как в соединении Е на диаграмме 1) аминов, приведен в верхней части диаграммы 1. На первой стадии имеющуюся в продаже (Sigma-Aldrich) бороновую кислоту А вводят в реакцию сочетания типа Судзуки с В и получают диальдегид С. При типичных условиях проведения реакции используют 1 экв. бороновой кислоты А, от 0,8 до 1,2 экв. соединения В, от 1,0 до 1,4 экв. Na2CO3, от 0,001 до 0,05 экв. подходящих катализаторов, таких как Рd(РРh3)4, и двухфазную смесь растворителей, содержащую примерно одинаковые объемы толуола и смеси 4:1 вода:метанол.
Диальдегид является новым соединением, которое можно использовать в качестве промежуточного продукта в других синтезах. Таким образом, настоящее изобретение также относится к новым соединениям, предназначенным для получения предшественников лигандов. Диальдегид описывается общей формулой

в которой R3-R9 являются такими, как определено выше.
Диальдегид С можно ввести в реакцию с арилом или алкиламином в присутствии кислотного катализатора и получить диимин D, как показано на схеме 1. Затем соединение D можно восстановить с помощью различных источников гидрид-иона и получить пиридилдиамин Е. Типичные условия проведения реакции, которые можно использовать, являются следующими. 1 мол. экв. диальдегида С объединяют с 2,0 экв. амина, от 0,00 до 0,05 экв. кислотного катализатора, такого как моногидрат п-толуолсульфоновой кислоты (Sigma-Aldrich), и толуолом или бензолом в качестве растворителя и получают смесь, которая содержит исходный диальдегид в концентрации от 0,05 до 1,0 М. Смесь кипятят с обратным холодильником, снабженным ловушкой Дина-Штарка для удаления образовавшейся воды путем азеотропной отгонки. После проводимого в течение 2-48 ч удаления летучих веществ получают диимин D. Диимин D можно восстановить в диамин Е по реакции растворов D в концентрации от 0,1 до 1,0 М в эфирных растворителях, таких как диэтиловый эфир или тетрагидрофуран, с количеством LiAlH4, составляющим от 0,3 до 1,4 мол. экв. Альтернативно, вместо LiAlH4 можно использовать NaBH4 в спирте или другие борогидридные восстановители.
Второй общий путь синтеза для получения нейтральных лигандов NNN приведен в нижней части диаграммы 1. Этот общий путь синтеза является особенно гибким, поскольку его можно использовать для получения несимметрично замещенных пиридилдиаминов, таких как соединение М на диаграмме 1, в котором R не совпадает с R". Последовательность реакций можно начать с образования имина F по реакции альдегида В с алкилом или ариламином. Обычно 1 мол. экв. альдегида В смешивают с 1 экв. амина в толуоле или бензоле с образованием раствора, в котором альдегид содержится в концентрации от 0,05 до 1,0 М В. Затем добавляют от 0,001 до 0,05 мол. экв. кислотного катализатора, такого как моногидрат п-толуолсульфоновой кислоты, и смесь кипятят с обратным холодильником, снабженным ловушкой Дина-Штарка для удаления образовавшейся воды. Затем продукт F можно ввести в реакцию с литийорганическим реагентом или реагентом Гриньяра и получить амин G. Альтернативно, соединение F можно восстановить с помощью источника гидрид-иона, такого как LiAlH4, и получить G'. Затем соединение G можно ввести в реакцию сочетания Судзуки с бороновой кислотой А при таких же условиях, как и описанные выше для получения соединения К.
В качестве промежуточного продукта для получения асимметрично замещенных предшественников лигандов можно использовать соединение, которое допускает последовательное аминирование. В соответствии с этим, настоящее изобретение также относится к новому соединению IX следующей структуры:

в которой R1, R2 и R3-R9 являются такими, как определено выше.
Затем альдегид К можно ввести в реакцию с первичными аминами и получить имин J. Условия проведения реакции являются такими же, как и описанные выше для получения соединения F. Соединение J можно восстановить в диамин L по реакции растворов D в концентрации от 0,1 до 1,0 М в эфирных растворителях, таких как диэтиловый эфир или тетрагидрофуран, с количеством LiАlН4, составляющим от 0,3 до 1,4 мол. экв. Альтернативно, вместо LiAlH4 можно использовать NaBH4 в спирте или другие борогидридные восстановители.
Схемы реакций получения дополнительных предшественников лигандов, рассмотренные выше, приведены ниже.
Схема 1. Два пути синтеза пиридилдиаминовых лигандов.
Путь для симметрично замещенных аминогрупп
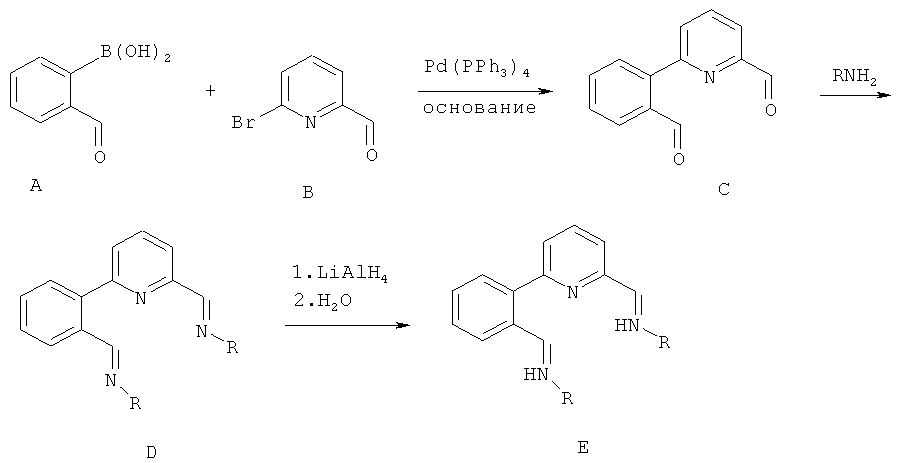
путь для несимметрично замещенных аминогрупп

где R, R', R" независимо обозначают гидрокарбил или замещенный гидрокарбил, предпочтительно алкильные группы.
Эти варианты способов синтеза могут привести к дополнительным предшественникам лигандов, указанным ниже, которые также можно использовать для получения комплексов, приведенных выше на диаграмме 1, по реакции с соответствующим металлоорганическим реагентом или металлоорганическим амидом или по реакции пиридилдиамидных производных, путем депротонирования с помощью литийорганических или магнийорганических реагентов и с солью переходного металла.
Диаграмма 2. Пиридилдиаминовые лиганды и их аббревиатуры

Поэтому в другом объекте настоящего изобретения можно получить различные дополнительные предшественники лигандов или промежуточные продукты, которые являются новыми и применимы в некоторых путях способа для получения дополнительных лигандов, рассмотренных выше. Этим объектом настоящего изобретения является пиридилдиамин, предназначенный для использования при получении комплекса переходного металла с соединением, которое описывается общей формулой (II)

в которой Z, R1-R5, R10 и R11 обладают указанными выше значениями.
Как и для самих комплексов переходных металлов, схема замещения может меняться в широких пределах с получением конечных комплексов переходного металла самых различных структур. Для предпочтительных комплексов дополнительные предшественники лигандов могут обладать структурой, в которой Z может обозначать арильную группу, приведенную в общей формуле (III)
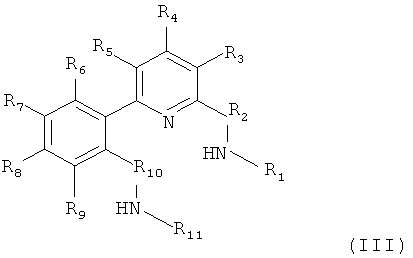
в которой R1-R11 независимо выбраны так, как указано выше.
Синтезированные комплексы можно использовать в качестве содержащих переходный металл компонентов для катализаторов, использующихся для полимеризации или олигомеризации алкенов. Эти комплексы можно использовать в комбинации с подходящими активаторами для полимеризации олефинов с получением таких полимеров, как полимеры на основе этилена или полимеры на основе пропилена, включая полимеризацию в системе этилен-октен. Они также могут быть активны при олигомеризации этилена и могут обладать высокой активностью.
В других вариантах осуществления предпочтительно, чтобы R1-R13 содержали до 30 и не более 30 атомов углерода, более предпочтительно от 2 до 20 атомов углерода. R1 и R11, замещенные по атому азота, предпочтительно выбраны из числа арильных групп, содержащих от 6 до 30 атомов углерода, более предпочтительно фенильных групп. Предпочтительно, чтобы R1 и R11 были выбраны из числа арильных или алкильных групп и чтобы R12-R15 независимо были выбраны из группы, включающей водород, алкильные и арильные группы, такие как фенил. Фенильные группы могут быть замещены алкилом. Алкильные заместители могут быть линейными алкилами, но включают и разветвленные алкилы.
Предпочтительно, если каждый R1 и R11 обозначает замещенную фенильную группу, в которой один или оба атома углерода, соседние с атомом углерода, связанным с атомом азота амидной группы, были замещены группой, содержащей от 1 до 10 атомов углерода. Некоторые конкретные примеры включают R1 и R11, выбранные из группы, включающей 2-метилфенил, 2-изопропилфенил, 2-этилфенил, 2,6-диметилфенил, мезитил, 2,6-диэтилфенил и 2,6-диизопропилфенил.
R2 предпочтительно выбран из числа фрагментов, в которых Е обозначает углерод, более предпочтительно фрагмент -C(R12)(R13)-, в котором Р12 обозначает водород и R13 обозначает арильную группу или бензильную группу (предпочтительно фенильное кольцо, присоединенное к атому С через алкиленовый фрагмент, такой как метилен). Фенильная группа может быть замещенной, как указано выше. Предпочтительно, если R3-R9 обозначают водород или алкил, содержащий от 1 до 4 атомов углерода. Предпочтительно, если 0, 1 или 2 группы R3-R9 являются алкильными заместителями.
В комплексе пиридилдиамид-металл I центральный атом металла координирован с тридентатным лигандом с двумя донорными амидными группами и одним донорным пиридилом. Центральным атомом металла М является переходный металл групп 3-12. Хотя при использовании в качестве катализатора в соответствии с современной теорией предпочтительно, чтобы М находился в четырехвалентном состоянии, можно получить соединения, в которых М находится в состояниях с меньшей валентностью и переходит в состояние с нормальной валентностью при получении каталитической системы путем взаимодействия с активатором. Предпочтительно, чтобы в дополнение к координации с пиридилдиамидным лигандом металл М также был координирован с n анионных лигандов, где n равно от 1 до 4. Типичными анионными донорами являются галоген или алкил, но можно использовать различные другие анионные группы, включая те, которые ковалентно связаны друг с другом с образованием молекул, которые можно рассматривать как дианионные, такие как оксалат. В некоторых комплексах с центральным металлом также могут координироваться до 3 нейтральных оснований Льюиса (L'), обычно простых эфиров. В предпочтительном варианте осуществления w равно 0, 1, 2 или 3.
Для стереорегулярных вариантов полимеризации и/или изменений характеристик полимеризации в случае изомерных структур Z предпочтительно обозначает арильную группу и R12 не совпадает с R13 и R14 не совпадает с R15. Предпочтительно, если R2 и R10 являются центрами хиральности. Предпочтительно, если 7-членное хелатное кольцо, образованное с помощью М-N-R10-C-C-C-N, приводит к образованию третьего хирального элемента вследствие конформации, которую приобрело большое кольцо, как это показано в твердофазных структурах, представленных на фиг.1 и 2. На это также указывают данные1Н-ЯМР для многих комплексов NNN, таких как С1, представленных в экспериментальном разделе. Таким образом доступны смеси диастереоизомеров комплексов, которые при использовании с активаторами для олигомеризации или полимеризации алкенов могут дать полиолефиновые продукты с более широкой полидисперсностью, чем типичные "одноцентровые" катализаторы, при использовании которых значения Мn/Мw обычно равны около 2. Предпочтительно, если Е обозначает углерод.
В связи с получением комплексов, содержащих аналогичные тридентатные системы лигандов NNC, описаны многие варианты и стадии синтеза, указанные выше. Эти подробности относятся к вариантам в рамках широких категорий, описанных ранее, и к отличиям от описанных ранее вариантом синтеза с использованием тридентатных конфигураций NNC.
В одном предпочтительном варианте осуществления Z определяется как арил, так что комплекс описывается формулой IV, и Е определяется как углерод, и М определяется как Zr и/или Hf и R1 и R11 являются арильными группами, каждая из которых содержит от 6 до 20 атомов углерода.
Предпочтительной методикой синтеза пиридилдиамидных комплексов является реакция нейтральных предшественников пиридилдиаминового лиганда с металлоорганическим амидом, включая Zr(NMe2)4, Zr(NEt2)4, Hf(NMe2)4 и Hf(NEt2)4. Другой предпочтительной методикой синтеза пиридилдиамидных комплексов является реакция нейтральных предшественников пиридилдиаминового лиганда с литийорганическим реагентом с образованием дилитиевого производного пиридилдиамида, затем реакция этих соединений с солью переходного металла, включая ZrCl4, НfCl4, ZrСl4(1,2-диметоксиэтан), HfCl4(1,2-диметоксиэтан), ZrСl4(тетрагидрофуран)2, НfСl4(тетрагидрофуран)2, ZrBn2Cl2(OEt2), HfBn2Cl2(OEt2). Другой предпочтительной методикой синтеза пиридилдиамидных комплексов является реакция нейтральных предшественников пиридилдиаминового лиганда с металлоорганическим реагентом, включая ZrBn4, ZrВn2Cl2(ОEt2), Zr(CH2SiMe3)4, Zr(CH2CMe3)4, HfBn4, HfBn2Cl2(OEt2), Hf(CH2SiMe3)4, Нf(СН2СМе3)4.
В другом варианте осуществления Z обозначает 5-членное кольцо (такое как замещенный или незамещенный циклопентадиен, "Ср"). В предпочтительном варианте осуществления Z обозначает ферроценильную группу, причем одно из колец Ср связывает R10 с пиридильным кольцом.
Активаторы
После синтеза комплексов каталитические системы можно получить путем их объединения с активатором по любой методике, известной из литературы, включая нанесение на подложку для использования в суспензионной или газофазной полимеризации. Каталитические системы также можно добавить или образовать при полимеризации в растворе или полимеризации в массе (в мономер). Каталитическая система обычно включает комплекс, описанный выше, и активатор, такой как алюмоксан или некоординирующийся анион. Активацию можно провести с использованием раствора алюмоксана, включая метилалюмоксан, который обозначают как МАО, а также модифицированный МАО, который обозначают как ММАО, содержащий высшие алкильные группы для улучшения растворимости. Особенно подходящий МАО можно приобрести у фирмы Albemarle в виде 10 мас.% раствора в толуоле. В каталитической системе, использующейся в настоящем изобретении, предпочтительно используют активатор, выбранный из группы, включающей алюмоксаны, такие как метилалюмоксан, модифицированный метилалюмоксан, этилалюмоксан, изобутилалюмоксан и т.п.
Если используют алюмоксан или модифицированный алюмоксан, то молярное отношение комплекс-активатор составляет примерно от 1:3000 до 10:1; альтернативно от 1:2000 до 10:1; альтернативно от 1:1000 до 10:1; альтернативно от 1:500 до 1:1; альтернативно от 1:300 до 1:1; альтернативно от 1:200 до 1:1; альтернативно от 1:100 до 1:1; альтернативно от 1:50 до 1:1; альтернативно от 1:10 до 1:1. Если активатором является алюмоксан (модифицированный или немодифицированный), то в некоторых вариантах осуществления выбирают максимальное количество активатора, составляющее 5000-кратный молярный избыток по сравнению с предшественником катализатора (в пересчете на содержащий металл каталитический центр). Предпочтительное молярное отношение комплекс-активатор составляет 1:1.
Активацию также можно провести с помощью некоординирующихся анионов, которые обозначают как НКА, такого типа, как описанные в ЕР 277003 А1 и ЕР 277004 А1. НКА можно добавить в виде ионной пары с использованием, например, [DMAH]+[НКА]-, где катион N,N-диметиланилиния (DMAH) реагирует с основной отщепляющейся группой комплекса переходного металла с образованием катиона комплекса переходного металла и [НКА]-. В предшественнике катионом альтернативно может быть тритил. Альтернативно, комплекс переходного металла можно ввести в реакцию с нейтральным предшественником НКА, таким как В(С6F5)3, который отщепляет от комплекса анионную группу с образованием активированной системы. Подходящие активаторы включают N,N-диметиланилинийтетракис(пентафторфенил)борат (т.е. [РhNMе2Н]В(С6F5)4) и N,N- диметиланилинийтетракис(гептафторнафтил)борат, где Ph обозначает фенил, и Me обозначает метил.
Дополнительные предпочтительные активаторы, применимые в настоящем изобретении, включают описанные в US 7247687 от столбца 169, строка 50 до столбца 174, строка 43, предпочтительно от столбца 172, строка 24 до столбца 173, строка 53.
Если используют НКА (такой как ионный или нейтральный стехиометрический активатор), то молярное отношение комплекс-активатор обычно составляет от 1:10 до 1:1; от 1:10 до 10:1; от 1:10 до 2:1; от 1:10 до 3:1; от 1:10 до 5:1; от 1:2 до 1,2:1; от 1:2 до 10:1; от 1:2 до 2:1; от 1:2 до 3:1; от 1:2 до 5:1; от 1:3 до 1,2:1; от 1:3 до 10:1; от 1:3 до 2:1; от 1:3 до 3:1; от 1:3 до 5:1; от 1:5 до 1:1; от 1:5 до 10:1; от 1:5 до 2:1; от 1:5 до 3:1; от 1:5 до 5:1; от 1:1 до 1:1,2.
Альтернативно, в каталитической системе, предлагаемой в настоящем изобретении, также можно использовать соактиватор. Молярное отношение комплекс-соактиватор составляет от 1:100 до 100:1; от 1:75 до 75:1; от 1:50 до 50:1; от 1:25 до 25:1; от 1:15 до 15:1; от 1:10 до 10:1; от 1:5 до 5:1, от 1:2 до 2:1; от 1:100 до 1:1; от 1:75 до 1:1; от 1:50 до 1:1; от 1:25 до 1:1; от 1:15 до 1:1; от 1:10 до 1:1; от 1:5 до 1:1; от 1:2 до 1:1; от 1:10 до 2:1.
Подложки
Комплексы, описанные в настоящем изобретении, можно наносить на подложку (с активатором или без него) по любой методике, эффективной для нанесения на подложку других координационных каталитических систем.
Эффективная означает что приготовленный таким образом катализатор можно использовать для олигомеризации или полимеризации олефина в гетерогенном процессе. Предшественник катализатора, активатор, при необходимости соактиватор, подходящий растворитель и подложку можно добавлять в любом порядке или одновременно. Обычно комплекс и активатор можно объединить в растворителе с образованием раствора. Затем добавляют подложку и смесь перемешивают в течение от 1 мин до 10 ч. Полный объем раствора может быть больше объема пор в подложке, но в некоторых вариантах осуществления полный объем раствора должен быть меньше необходимого для образования геля или взвеси (примерно от 90 до 400%, предпочтительно примерно 100-200% в пересчете на объем пор). После перемешивания оставшийся растворитель удаляют в вакууме, обычно при температуре окружающей среды и в течение 10-16 ч. Однако возможно большее или меньшее время и температура.
Комплекс также можно наносить на подложку без активатора; в этом случае активатор (и при необходимости соактиватор) добавляют в жидкую фазу при полимеризации. Кроме того, на одну подложку можно нанести два или большее количество разных комплексов. Аналогичным образом, на одну подложку можно нанести два или большее количество активаторов или активатор и соактиватор.
Подходящие подложки из твердых частиц обычно состоят из полимерных или тугоплавких оксидных материалов, каждый из которых предпочтительно является пористым. Предпочтительным для использования в настоящем изобретении является любой материал подложки, содержащий частицы со средним размером более 10 мкм. В различных вариантах осуществления выбирают пористый материал подложки, такой как, например, тальк, неорганические оксиды, неорганические хлориды, например хлорид магния, и смолообразные материалы подложки, такие как полистирол, полиолефин или полимерные системы, или любые другие органические материалы подложки и т.п. В некоторых вариантах осуществления выбирают неорганические оксидные материалы, так что материал подложки содержит оксиды металлов или металлоидов группы 2, 3, 4, 5, 13 или 14. В некоторых вариантах осуществления выбранные материалы подложки для катализатора включают диоксид кремния, оксид алюминия, алюмосиликат и их смеси. Другие неорганические оксиды можно использовать по отдельности или в комбинации с диоксидом кремния, оксидом алюминия или алюмосиликатом. Ими являются оксид магния, оксид титана, оксид циркония и т.п. В качестве подложки могут выступать кислоты Льюиса, такие как монтмориллонит и аналогичные глины. В этом случае подложка необязательно может выступать в качестве компонента активатора, однако также можно использовать дополнительный активатор.
Материал подложки можно предварительно обработать с помощью любого количества методик. Например, неорганические оксиды можно прокалить, химически обработать дегидроксилирующими реагентами, такими как алюминийалкилы и т.п., или обработать по обеим методикам.
Как указано выше, полимерные носители также пригодны для использования в настоящем изобретении, см., например, описания в WO 95/15815 и US 5427991. Раскрытые способы можно использовать с каталитическими комплексами, активаторами или каталитическими системами, предлагаемыми в настоящем изобретении, для их адсорбции или абсорбции на полимерных подложках, в особенности если они изготовлены из пористых частиц, или их можно химически связать с помощью функциональных групп, связанных с полимерными цепями или находящихся в них.
Пригодные для использования подложки обычно обладают площадью поверхности, равной 10-700 м2/г, объемом пор, равным 0,1-4,0 см3/г, и частицами со средним размером, равным 10-500 мкм. В некоторых вариантах осуществления используют площадь поверхности, равную 50-500 м2/г, объем пор, равный 0,5-3,5 см3/г, или частицы со средним размером, равным 20-200 мкм. В других вариантах осуществления используют площадь поверхности, равную 100-400 м2/г, объем пор, равный 0,8-3,0 см3/г, и частицы со средним размером, равным 30-100 мкм. Пригодные для использования подложки обычно обладают объемом пор, равным 10-1000 , альтернативно 50-500 

Каталитические комплексы, описанные в настоящем изобретении, обычно осаждают на подложку в количестве, составляющем 10-100 мкМ комплекса на 1 г твердой подложки; альтернативно 20-80 мкМ комплекса на 1 г твердой подложки или 40-60 мкМ комплекса на 1 г подложки. Но можно использовать более значительные или меньшие значения при условии, что полное количество твердого комплекса не превышает объема пор подложки.
Полимеризация
Каталитические комплексы, предлагаемые в настоящем изобретении, применимы для полимеризации ненасыщенных мономеров, для которых известно, что они обычно вступают в катализируемую металлоценом полимеризацию, такую как полимеризация в растворе, в суспензии, в газовой фазе и полимеризация при высоком давлении. Обычно для получения полимера вводят во взаимодействие один или большее количество комплексов, описанных в настоящем изобретении, один или большее количество активаторов и один или большее количество мономеров. Комплексы можно нанести на подложку и в этом случае они являются особенно подходящими для известных режимов работы с фиксированным слоем, подвижным слоем, псевдоожиженным слоем, в суспензии, растворе или в блоке в одном, последовательных или параллельных реакторах.
В настоящем изобретении можно использовать один или большее количество последовательных или параллельных реакторов. Комплексы, активатор и при необходимости соактиватор можно ввести в реактор в виде раствора или взвеси по отдельности, активировать в технологической линии непосредственно перед введением в реактор или предварительно активировать и перекачать в реактор в виде активированного раствора или взвеси. Полимеризацию можно провести в одном реакторе, когда мономер, сомономеры, катализатор/активатор/соактиватор, необязательно поглотитель и необязательно модификаторы непрерывно добавляют в один реактор или в последовательности реакторов, когда указанные выше компоненты добавляют в каждый из двух или большего количества соединенных последовательно реакторов. Каталитические компоненты можно добавить в первый из последовательных реакторов. Каталитический компонент также можно добавить в оба реактора, причем один компонент добавляют в первый реактор, а другой компонент в другие реакторы. В одном предпочтительном варианте осуществления, комплекс активируют в реакторе в присутствии олефина.
В особенно предпочтительном варианте осуществления способ полимеризации является непрерывным способом.
Способ полимеризации, использующийся в настоящем изобретении, обычно включает введение во взаимодействие одного или большего количества алкеновых мономеров с комплексами (и необязательно активатором), описанными в настоящем изобретении. Для задач настоящего изобретения алкены определяются как включающие мультиалкены (такие как диалкены) и алкены, содержащие только одну двойную связь. Полимеризация может быть гомогенной (полимеризация в растворе или в блоке) или гетерогенной (суспензионная - в жидком разбавителе или газофазная - в газообразном разбавителе). В случае гетерогенной, суспензионной или газофазной полимеризации комплекс и активатор могут находиться на подложке. В настоящем изобретении в качестве подложки применим диоксид кремния. При практическом осуществлении настоящего изобретения можно использовать реагенты-переносчики цепи (такие как водород или диэтилцинк).
Способы полимеризации, предлагаемые в настоящем изобретении, можно осуществлять при условиях, предпочтительно включающих температуру, равную от примерно 30 до примерно 200°С, предпочтительно от 60 до 195°С, предпочтительно от 75 до 190°С. Способ можно осуществлять при давлении, равном от 0,05 до 1500 МПа. В предпочтительном варианте осуществления давление равно от 1,7 до 30 МПа или в другом варианте осуществления предпочтительно при сверхкритических условиях давление равно от 15 до 1500 МПа.
Мономеры
Мономеры, применимые в настоящем изобретении, включают олефины, содержащие от 2 до 20 атомов углерода, альтернативно от 2 до 12 атомов углерода (предпочтительно этилен, пропилен, бутилен, пентен, гексен, гептен, октен, нонен, децен и додецен) и необязательно также полиены (такие как диены). Особенно предпочтительные мономеры включают этилен и смеси С2-С10-альфа-олефинов, такие как этилен-пропилен, этилен-гексен, этилен-октен, пропилен-гексен и т.п.
Комплексы, описанные в настоящем изобретении, также являются особенно эффективными для полимеризации этилена, по отдельности или в комбинации по меньшей мере с одним олефиновоненасыщенным мономером, таким как С3-С20-α-олефин и предпочтительно С3-С12-α-олефин. Аналогичным образом, комплексы, предлагаемые в настоящем изобретении, также являются особенно эффективными для полимеризации пропилена, по отдельности или в комбинации по меньшей мере с одним другим олефиновоненасыщенным мономером, таким как этилен или С4-С20-α-олефин и предпочтительно С4-С20-α-олефин. Примеры предпочтительных α-олефинов включают этилен, пропилен, бутен-1, пентен-1, гексен-1, гептен-1, октен-1, нонен-1, децен-1, додецен-1, 4-метилпентен-1, 3-метилпентен-1, 3, 5, 5-триметилгексен-1 и 5-этилнонен-1.
В некоторых вариантах осуществления смесь мономеров также может содержать один или большее количество диенов в количестве, составляющем до 10 мас.%, таком как от 0,00001 до 1,0 мас.%, например от 0,002 до 0,5 мас.%, таком как от 0,003 до 0,2 мас.%, в пересчете на смесь мономеров. Неограничивающие примеры применимых диенов включают циклопентадиен, норборнадиен, дициклопентадиен, 5-этилиден-2-норборнен, 5-винил-2-норборнен, 1,4-гексадиен, 1,5-гексадиен, 1,5-гептадиен, 1,6-гептадиен, 6-метил-1,6-гептадиен, 1,7-октадиен, 7-метил-1,7-октадиен, 1,9-декадиен, 1,9-метил-1,9-декадиен.
При использовании олефинов, которые приводят к короткоцепочечным разветвлениям, таких как пропилен, каталитические системы при подходящих условиях могут приводить к образованию стереорегулярных полимеров или полимеров, содержащих в цепи стереорегулярные последовательности.
Поглотители
В некоторых вариантах осуществления при использовании комплексов, описанных в настоящем изобретении, в особенности когда они закреплены на подложке, каталитическая система дополнительно содержит один или большее количество соединений-поглотителей. В настоящем изобретении термин соединение-поглотитель означает соединение, которое удаляет полярные примеси из реакционной среды. Эти примеси вредно влияют на активность и стабильность катализатора. Обычно соединение-поглотитель представляет собой металлоорганическое соединение, такое как металлоорганические соединения элементов группы 13, приведенные в патентах US 5153157, 5241025 и WO-A-91/09882, WO-A-94/03506, WO-A-93/14132 и приведенные в WO 95/07941. Типичные соединения включают триэтилалюминий, триэтилборан, триизобутилалюминий, метилалюмоксан, изобутилалюмоксан и три-н-октилалюминий. Эти соединения-поглотители, содержащие объемные или C6-С20-линейные гидрокарбильные заместители, присоединенные к центральному металлу или металлоиду, обычно сводят к минимуму неблагоприятные взаимодействия с активным катализатором. Примеры включают триэтилалюминий, но более предпочтительно объемные соединения, такие как триизобутилалюминий, триизопренилалюминий, и длинноцепочечные линейные алкилзамещенные соединения алюминия, такие как три-н-гексилалюминий, три-н-октилалюминий или три-н-додецилалюминий. Если в качестве активатора используют алюмоксан, то избыток по сравнению с количеством, необходимым для активации, будет поглощать примеси и могут не потребоваться дополнительные соединения-поглотители. Алюмоксаны также можно добавлять в поглощающих количествах вместе с другими активаторами, например метилалюмоксан, [Me2HNPh]+[B(pfp)4]- или В(рfр)3 (перфторфенил=pfp=С6F5).
В предпочтительном варианте осуществления два или большее количество комплексов объединяют с диэтилцинком в одном реакторе с мономером. Альтернативно, один или большее количество комплексов объединяют с другим катализатором (таким как металлоцен) и диэтилцинком в одном реакторе с мономером.
Полимерные продукты
Поскольку на молекулярную массу полимеров, полученных в настоящем изобретении, влияют условия в реакторе, включая температуру, концентрацию мономера и давление, наличие реагентов, обрывающих цепь, и т.п., гомополимерные и сополимерные продукты, полученные способом, предлагаемым в настоящем изобретении, могут обладать значением Mw, определенным с помощью ГПХ (гель-проникающая хроматография), равным от примерно 1000 до примерно 2000000 г/моль, альтернативно от примерно 30000 до примерно 600000 г/моль или альтернативно от примерно 100000 до примерно 500000 г/моль. В настоящем изобретении предпочтительными полимерными продуктами могут быть гомополимеры или сополимеры. В предпочтительном варианте осуществления сомономер(ы) содержится в количестве, составляющем до 50 мол.%, предпочтительно от 0,01 до 40 мол.%, предпочтительно от 1 до 30 мол.%, предпочтительно от 5 до 20 мол.%,
Конечное применение
Изделия, изготовленные с использованием полимеров, полученных в настоящем изобретении, могут включать, например, формованные изделия (такие как контейнеры и бутылки, например домашние контейнеры, промышленные химические контейнеры, бутылки для личной гигиены, медицинские контейнеры, топливные баки и емкости для хранения, игрушки, листы, трубы, шланги, пленки, нетканые материалы и т.п.). Следует понимать, что приведенный выше перечень областей применения является типичным и его не следует понимать как ограничивающий.
В другом варианте осуществления настоящее изобретение относится к:
1. Пиридилдиамидному комплексу переходного металла, предназначенному для использования для полимеризации алкена, описывающемуся общей формулой (I)

в которой
М обозначает металл группы 3, 4, 5, 6, 7, 8, 9, 10, 11 или 12;
Z обозначает -(R14)pC-C(R15)q-,
где R14 и R15 независимо выбраны из группы, включающей водород, гидрокарбилы (такие как алкилы) и замещенные гидрокарбилы, и где соседние группы R14 и R15 могут быть связаны с образованием ароматического или насыщенного замещенного или незамещенного гидрокарбильного кольца, которое содержит 5, 6, 7 или 8 кольцевых атомов углерода и в котором заместители кольца могут связываться с образованием дополнительных колец,
р равно 0, 1 или 2, и
q равно 0, 1 или 2;
R1 и R11 независимо выбраны из группы, включающей гидрокарбилы (такие как алкилы и арилы), замещенные гидрокарбилы (такие как гетероарилы) и силильные группы;
R2 и R10 все независимо обозначают -E(R12)(R13)-, где Е обозначает углерод, кремний или германий, и каждый R12 и R13 независимо выбран из группы, включающей водород, гидрокарбилы (такие как алкилы, арилы), алкоксигруппу, силил, аминогруппу, арилоксигруппу, замещенные гидрокарбилы (такие как гетероарил), галоген и фосфиновую группу, R12 и R13 могут быть связаны с образованием насыщенного замещенного или незамещенного гидрокарбильного кольца, которое содержит 4, 5, 6 или 7 кольцевых атомов углерода и в котором заместители кольца могут связываться с образованием дополнительных колец, или R12 и R13 могут быть связаны с образованием насыщенного гетероциклического кольца или насыщенного замещенного гетероциклического кольца, в котором заместители кольца могут связываться с образованием дополнительных колец;
R3, R4 и R5 независимо выбраны из группы, включающей водород, гидрокарбилы (такие как алкилы и арилы), замещенные гидрокарбилы, алкоксигруппу, арилоксигруппу, галоген, аминогруппу и силил, и где соседние группы R (R3 и R4 и/или R4 и R5) могут быть связаны с образованием замещенного или незамещенного гидрокарбильного или гетероциклического кольца, которое содержит 5, 6, 7 или 8 кольцевых атомов и в котором заместители кольца могут связываться с образованием дополнительных колец;
L обозначает анионную отщепляющуюся группу, причем группы L могут быть одинаковыми или разными и любые две группы L могут быть связаны с образованием дианионной отщепляющейся группы;
n равно 0, 1, 2, 3 или 4;
L' обозначает нейтральное основание Льюиса; и
w равно 0, 1, 2, 3 или 4.
2. Комплексу по параграфу 1, в котором М обозначает Ti, Zr или Hf и/или Z обозначает замещенную арильную группу, образующую мостик между NR11 и остальной частью комплекса с помощью цепи из трех соседних атомов, из которых два являются соседними атомами углерода замещенного фенильного кольца и третий ковалентно связан с одним из этих двух атомов углерода.
3. Комплексу по параграфу 1 или параграфу 2, в котором Z обозначает арильную группу, так что комплекс описывается общей формулой IV

в которой
R6, R7, R8 и R9 независимо выбраны из группы, включающей водород, гидрокарбилы (такие как алкилы и арилы), замещенные гидрокарбилы, алкоксигруппу, галоген, аминогруппу, силил и пары положений, и в которой соседние группы R (R6 и R7 и/или R7 и R8, и/или R8 и R9) могут быть связаны с образованием насыщенного замещенного или незамещенного гидрокарбильного или гетероциклического кольца, которое содержит 5, 6, 7 или 8 кольцевых атомов углерода и в котором заместители кольца могут связываться с образованием дополнительных колец; и М, L, L', w, n, R1, R2, R3, R4, R5, R10 и R11 являются такими, как определено в параграфе 1.
4. Комплексу по любому из предыдущих параграфов 1-3, в котором R1 и R3-R9 и/или R11-R15, указанные выше, содержат не более 30 атомов углерода, предпочтительно от 2 до 20 атомов углерода.
5. Комплексу по любому из предыдущих параграфов 1-4, в котором Е обозначает углерод и R1 и R11 независимо выбраны из числа фенильных групп, которые содержат от 0 до 5 различных заместителей, которые включают F, Cl, Вr, I, СF3, NO2, алкоксигруппу, диалкиламиногруппу, гидрокарбил (такой как алкил и арил) и замещенные гидрокарбилы (такие как гетероарил), содержащие от 0 до 10 атомов углерода.
6. Комплексу по любому из предыдущих параграфов 1-5, в котором L выбран или выбраны из группы, включающей галоген, алкил, арил, алкоксигруппу, амидную группу, гидридную группу, феноксигруппу, гидроксигруппу, силил, аллил, алкенил и алкинил; и L' выбран или выбраны из группы, включающей простые эфиры, простые тиоэфиры, амины, нитрилы, имины, пиридины и фосфины.
7. Способу получения пиридилдиамидного комплекса по любому из предыдущих параграфов 1-6, включающему формальное включение имина в связь металл-углерод орто-металированной арильной группы отдельно синтезированного промежуточного пиридиламидного комплекса металла, как это показано в уравнении V

в котором М, L, L', w, n, R1, R2, R3, R4, R5, R6, R7, R8, R9, R10 и R11 являются такими, как определено в параграфе 1 и 3.
8. Способу получения комплекса по любому из предыдущих параграфов 1-6, включающему взаимодействие пиридилдиамина с металлоорганическим амидом или металлоорганическими реагентами, как это показано в уравнении VI

в котором М, L, L', Z, w, n, R1, R2, R3, R4, R5, R10 и R11 являются такими, как определено в параграфе 1.
9. Способу получения комплекса по любому из предыдущих параграфов 1-6, в котором пиридилдиамин депротонируют с помощью литийорганического или магнийорганического реагента и затем этот пиридилдиамидный реагент вводят в реакцию с галогенидом металла, как это показано в уравнении VII

в котором М, L, L', Z, w, n, R1, R2, R3, R4, R5, R10 и R11 являются такими, как определено в параграфе 1.
10. Пиридилдиамину, предназначенному для использования для получения комплекса переходного металла, который описывается общей формулой (II)

в которой Z обозначает -(R14)pC-C(R15)q-,
где R14 и R15 независимо выбраны из группы, включающей водород гидрокарбилы (такие как алкилы) и замещенные гидрокарбилы, и где соседние группы R14 и R15 могут быть связаны с образованием ароматического или насыщенного замещенного или незамещенного гидрокарбильного кольца, которое содержит 5, 6, 7 или 8 кольцевых атомов углерода и в котором заместители кольца могут связываться с образованием дополнительных колец,
р равно 0, 1 или 2, и
q равно 0, 1 или 2;
R1 и R11 независимо выбраны из группы, включающей алкил, арил, гетероарил или силильные группы;
R2 и R10 все независимо обозначают -E(R12)(R13)-, где Е обозначает углерод, кремний или германий, и каждый R12 и Р13 независимо выбран из группы, включающей водород, гидрокарбилы (такие как алкилы и арилы), замещенные гидрокарбилы (такие как гетероарил), алкоксигруппу, силил, аминогруппу, арилоксигруппу, галоген и фосфиновую группу, R12 и R13 могут быть связаны с образованием насыщенного замещенного или незамещенного гидрокарбильного кольца, которое содержит 4, 5, 6 или 7 кольцевых атомов углерода и в котором заместители кольца могут связываться с образованием дополнительных колец, или R12 и R13 могут быть связаны с образованием насыщенного гетероциклического кольца или насыщенного замещенного гетероциклического кольца, в котором заместители кольца могут связываться с образованием дополнительных колец; и
R3, R4 и R5 независимо выбраны из группы, включающей водород, гидрокарбилы (такие как алкилы), замещенные гидрокарбилы, алкоксигруппу, арилоксигруппу, галоген, аминогруппу и силил, и где соседние группы R (R3 и R4 и/или R4 и R5) могут быть связаны с образованием замещенного или незамещенного гидрокарбильного или гетероциклического кольца, которое содержит 5, 6, 7 или 8 кольцевых атомов и в котором заместители кольца могут связываться с образованием дополнительных колец.
11. Соединению по параграфу 10, в котором Z обозначает арильную группу, описывающуюся общей формулой (III)

в которой R6, R7, R8 и R9 независимо выбраны из группы, включающей водород, гидрокарбилы (такие как алкилы), замещенные гидрокарбилы, алкоксигруппу, галоген, аминогруппу, силил и пары положений, и в которой соседние группы R (R6 и R7 и/или R7 и R8, и/или R8 и R9) могут быть связаны с образованием насыщенного замещенного или незамещенного гидрокарбильного или гетероциклического кольца, которое содержит 5, 6, 7 или 8 кольцевых атомов углерода и в котором заместители кольца могут связываться с образованием дополнительных колец; и
в которой R1, R2, R3, R4, R5, R10 и R11 являются такими, как определено в параграфе 1.
12. Производному пиридила общей формулы VIII

в которой R3, R4, R5, R6, R7, R8 и R9 независимо выбраны из группы, включающей водород, гидрокарбилы (такие как алкилы), замещенные гидрокарбилы алкоксигруппу, арилоксигруппу, галоген, аминогруппу и силил, и в которой соседние группы R (R3 и R4 и/или R4 и R5, и/или R6 и R7, и/или R7 и R8, и/или R8 и R9) могут быть связаны с образованием замещенного или незамещенного гидрокарбильного или гетероциклического кольца, которое содержит 5, 6, 7 или 8 кольцевых атомов и в котором заместители кольца могут связываться с образованием дополнительных колец.
13. Производному пиридила общей формулы (IX)

в которой
R1 независимо выбран из группы, включающей гидрокарбилы (такие как алкилы и арилы), замещенные гидрокарбилы (гетероарилы) и силильные группы, R2 обозначает -E(R12)(R13)-, где Е обозначает углерод, кремний или германий, каждый R12 и R13 независимо выбран из группы, включающей водород, гидрокарбилы (такие как алкилы и арилы), замещенные гидрокарбилы, алкоксигруппу, силил, аминогруппу, галоген и фосфиновую группу, R3, R4, R5, R6, R7, R8 и R9 независимо выбраны из группы, включающей водород, гидрокарбилы (такие как алкилы и арилы), замещенные гидрокарбилы, алкоксигруппу, арилоксигруппу, галоген, аминогруппу и силил, и в которой соседние группы R (R3 и R4 и/или R4 и R5, и/или R6 и R7, и/или R7 и R8, и/или R8 и R9) могут быть связаны с образованием замещенного или незамещенного гидрокарбильного или гетероциклического кольца, которое содержит 5, 6, 7 или 8 кольцевых атомов и в котором заместители кольца могут связываться с образованием дополнительных колец.
14. Каталитической системе, включающей комплекс по любому из параграфов 1-6 и активатор или сокатализатор, такой как алюмоксан или некоординирующийся анион.
15. Способу полимеризации, включающему взаимодействие алкенового мономера с катализатором по параграфу 14 с получением полиалкена.
ПРИМЕРЫ
Примеры синтеза предшественников лигандов
Синтез предшественника бидентатного лиганда N-N Int-1 (не соответствует настоящему изобретению)
Int-1 (структура приведена ниже) является промежуточным продуктом, использующимся для синтеза комплексов с тридентатным лигандом N-N-Cs. 2-Фенил-6-пиридинкарбоксальдегид (4,08 г, 22,3 ммоля) и 2,6-диизопропиланилин (3,95 г, 22,3 ммоля) смешивали с бензолом (125 мл). Затем добавляли моногидрат п-толуолсульфоновой кислоты (0,010 г, 0,05 ммоля) (кислота-катализатор на приведенной ниже схеме реакции). Смесь в течение 4 ч кипятили с обратным холодильником, снабженным ловушкой Дина-Штарка. Удаление летучих веществ при пониженном давлении при 40-50°С давало пиридилимин Int-1 в виде желтого кристаллического твердого вещества. Выход: 7,35 г, 96,2%.1H ЯМР (250 МГц, С6D6): δ 8,69 (1Н, s), 8,34 (1H, d), 8,14 (2H, d), 7,2-7,4 (8H, m), 3,27 (2H, септет), 1,25 (12Н, d). Общая схема реакции приведена ниже:

Синтез предшественника бидентатного лиганда N-N Int-2 (не соответствует настоящему изобретению)
Int-2 (структура приведена ниже) является промежуточным продуктом, использующимся для синтеза комплексов с тридентатным лигандом N-N-Cs. Тетрагидрофуран (10 мл) добавляли к 2,6-диизопропиланилину (0,454 г, 2,56 ммоля) и 3 

Примеры синтеза комплексов переходных металлов
Синтез Int-3 с тридентатным лигандом N-N-C (не соответствует настоящему изобретению)
Int-3 (структура приведена ниже) используют в качестве промежуточного продукта для получения комплексов N-N-N. Раствор ZrBn2Cl2(OEt2) (0,532 г, 1,27 ммоля) в бензоле (5 мл) в течение 30 с по каплям добавляли к раствору Int-2 (0,438 г, 1,27 ммоля) в бензоле (5 мл). Оранжевый раствор нагревали при 70°С в течение 2 ч и 45 мин. Затем черный раствор охлаждали до температуры окружающей среды (примерно 23°С). Раствор фильтровали и добавляли Et2O (1 мл). Концентрирование до 6 мл приводило к образованию кристаллического осадка. На следующий день добавляли еще Et2O (10 мл). Затем темное кристаллическое твердое вещество собирали на диске из пористого стекла и промывали с помощью Et2O (10 мл), затем сушили при пониженном давлении и получали продукт в виде серого твердого вещества. Выход: 40 г, 54%.1Н ЯМР (250 МГц, CD2Cl2): δ 8,00-7,68 (4Н, m), 7,37-7,15 (6Н, m), 5,15 (2H, m), 3,60 (4Н, q), 3,46 (1H, септет), 1,35 (6Н, d), 1,16 (6Н, d), 1,08 (6Н, t).

Синтез Int-4 с тридентатным лигандом N-N-C (не соответствует настоящему изобретению)
Int-4 (структура приведена ниже) используют в качестве промежуточного продукта для получения комплексов N-N-N. Диэтиловый эфир (15 мл) добавляли к ZrBn2Cl2(OEt2) (0,217 г, 0,519 ммоля) с образованием мутного желтого раствора. При -68°С по каплям добавляли раствор имина Int-1 (0,178 г, 0,519 ммоля) в Et2O (4 мл). Смеси в течение нескольких часов давали медленно нагреваться до температуры окружающей среды (примерно 23°С). После перемешивания в течение ночи образовывался темный раствор. Летучие вещества удаляли путем выпаривания и твердое вещество суспендировали в пентане. Серое твердое вещество собирали на фильтре из пористого стекла, промывали пентаном и затем сушили при пониженном давлении. Выход: 0,24 г, 61%.1Н ЯМР (250 МГц, С6D6): δ 8,22 (1Н, d), 6,5-7,3 (примерно 14Н, m), 5,88 (1H, d), 4,93 (1Н, dd), 4,32 (1Н, септет), 3,48 (1Н, dd), 3.32 (4H), 2,8-2,1 (2Н, m), 1,64 (3H, d), 1,32 (3H, d), 1,28 (3H, d), 1,21 (3H, d), 1,03 (6H, t).

Синтез Int-5 с тридентатным лигандом N-N-C (не соответствует настоящему изобретению)
Int-5 (структура приведена ниже) используют в качестве промежуточного продукта для получения комплексов N-N-N. Бензол (4 мл) добавляли к комбинации Int-2 (0,281 г, 0,815 ммоля) и HfBn2Cl2(OEt2)1,5 (0,442 г, 0,815 ммоля). Оранжевый раствор нагревали при 60°С в течение 75 мин. Затем летучие вещества выпаривали почти досуха. Затем добавляли дополнительное количество бензола (5 мл) и суспендированное твердое вещество собирали на диске из пористого стекла, промывали бензолом (5 мл) и сушили при пониженном давлении. Выход: 0,467 г, 86,0%.1H ЯМР (250 МГц, CD2Cl2): δ 8,00 (1Н, t), 7,94 (1Н, d), 7,81 (2H, d), 7,40-7,15 (6H, m), 5,40 (2H, s), 3,66 (4H, q), 3,50 (2H, септет), 1,33 (6H, d), 1,17 (6H, d), 1,04 (6H, t).

Синтез Int-6 с тридентатным лигандом N-N-C (не соответствует настоящему изобретению)
Int-6 (структура приведена ниже) используют в качестве промежуточного продукта для получения комплексов N-N-N. Бензол (10 мл) добавляли к HfBn2Cl2(OEt2)1,5 (0,585 г, 1,08 ммоля) и имину Int-1 (0,371 г, 1,08 ммоля) и получали темный раствор. Смесь нагревали при 65°С в течение 14 ч и затем выпаривали с получение остатка. Добавляли Et2O (15 мл) и суспендированный продукт собирали на фильтре из пористого стекла, промывали с помощью Et2O (5 мл) и сушили при пониженном давлении. Данные ЯМР показывали, что примерно 1,45 экв. эфира координировались и/или совместно кристаллизовались. Выход: 0,65 г, 76%.1Н ЯМР (250 МГц, CD2Cl2): δ 7,99 (1Н, d), 7,80 (2H, t), 7,69 (1Н, t), 7,50-7,20 (8H, m), 6,98-6,92 (2H, m), 6,21 (1Н, d), 5,09 (1Н, dd), 3,98 (1Н, септет), 3.52 (5,8Н, q), 3,33 (1Н, dd), 2,91 (1Н, септет), 2,72 (1Н, dd), 1,43 (3H, d), 1,28 (3H, d), 1,23 (3H, d), 1,19-1,10 (6H, m).

Синтез лиганда L4 (предлагается в настоящем изобретении)
Толуол (15 мл) добавляли к Int-5 (0,0881 г, 0,132 ммоля) и PhCH=N(2,5-Ме2-С6Н3) (0,0277 г, 0,132 ммоля). Суспензию нагревали при 90°С и получали прозрачный бледно-желтый раствор. Через 16 ч летучие вещества выпаривали и остаток растворяли в Et2O (10 мл). Затем добавляли воду (10 мл). Органические вещества разделяли, сушили над MgSO4 и выпаривали и получали диамин в виде вязкого масла.1H ЯМР (250 МГц, С6D6): δ 7,55-6,80 (16Н, m), 6,62 (1H, s), 6,49 (2H, m), 4,26 (2H, v br), 4,22 (2H, s), 3,45 (2H, септет), 2,03 (3Н, s), 1,89 (3Н, s), 1,20 (6H,d), 1,17 (6H,d).
Синтез C1 с тридентатным лигандом N-N-N (предлагается в настоящем изобретении)
Раствор Int-3 (0,101 г, 0,175 ммоля) в CH2Cl2 (6 мл) добавляли к PhCH=NPh (0,0317 г, 0,175 ммоля). Сосуд герметично закрывали и нагревали при 50°С в течение 15,5 ч. Летучие вещества удаляли и получали остаток, который экстрагировали с помощью Et20 (5 мл) и фильтровали. Концентрирование этого раствора до 1 мл давало чистый продукт в виде желтого кристаллического комка. Выход: 0,089 г, 69%. Данные Н ЯМР показывали, что закристаллизовавшийся продукт представляет собой смесь состава 4:1 конформационных диастереоизомеров и содержит 0,75 экв. совместно закристаллизовавшегося Et2O.1Н ЯМР (250 МГц, С6D6): δ 7,3-6,6 (перекрывающиеся пики арилов), 6,45 (1,25Н, br d), 6,14 (0,25Н, d), 5,67 (1H, s), 5,39 (0.22H, s), 4,68 (0,44H, АВ квартет, Δυ=186 Гц, J=20 Гц), 4,39 (2H, АВ квартет, Δυ=160 Гц, J=20 Гц), 3,75-3,60 (1,4Н, m), 3,26 (3Н, q, Et2O), 2,30 (1H, септет), 1,57 (1,62Н, dd), 1,50-1,44 (3,86Н, m), 1,33 (3.31H, d), 1,11 (5.59H, t), 0,96 (6,28H, d).
Синтез С2 с тридентатным лигандом N-N-N (предлагается в настоящем изобретении)
Раствор Int-5 (0,105 г, 0,158 ммоля) в CH2Cl2 (4 мл) добавляли к PhCH=NPh (0,0332 г, 0,183 ммоля). Сосуд герметично закрывали и нагревали при 60°С в течение 18 ч. Летучие вещества удаляли и получали остаток, который растворяли в EtsO (10 мл). Концентрирование этого раствора до 2 мл и выдерживание в течение ночи приводило к кристаллизации избытка имина. Маточный раствор сливали. К нему добавляли пентан (4 мл) для осаждения продукта в виде бледно-желтого твердого вещества. Это твердое вещество выделяли и сушили при пониженном давлении. Выход: 0,085 г, 65%. Данные Н ЯМР показывали, что продукт выделялся в виде смеси состава 2:1 конформационных диастереоизомеров и что содержались небольшие количества эфира (0,1 экв.) и пентана (0,7 экв.). Вследствие сложности спектра ЯМР приведены только некоторые (метилиден и метин) резонансы.1Н ЯМР (250 МГц, CD2Cl2): δ Содержащийся в большом количестве диастереоизомер: 5,71 (1Н, s), 4,63 (2Н, АВ квартет, Δυ=97 Гц, J=20 Гц), 3,31 (1Н, септет), 1,95 (1Н, септет); содержащийся в небольшом количестве диастереоизомер: 5,89 (1Н, s), 5,03 (2Н, АВ квартет, Δυ=221 Гц, J=20 Гц), 3,93 (1Н, септет), 3,31 (1Н, септет).
Синтез С3 с тридентатным лигандом N-N-N (предлагается в настоящем изобретении)
Раствор Int-3 (0,101 г, 0,175 ммоля) в CH2Cl2 (6 мл) добавляли к PhCH=NiPr (0,0269 г, 0,182 ммоля). Сосуд герметично закрывали и нагревали при 50°С в течение 15,5 ч. Летучие вещества удаляли и получали желто-оранжевое твердое вещество, которое экстрагировали с помощью Et2O (5 мл) и фильтровали. Концентрирование этого раствора до 1 мл давало чистый продукт в виде желтых кристаллов. Выход: 0,079 г, 65%. Данные Н ЯМР показывали, что закристаллизовавшийся продукт представляет собой в основном (>90%) один конформационный диастереоизомер и содержит 0,61 экв. совместно закристаллизовавшегося Et2O. Вследствие сложности спектра ЯМР приведены только некоторые (метилиден и метин) резонансы1Н ЯМР (250 МГц, С6D6): δ 5,33 (1Н, септет), 5,32 (1Н, s), 4,75 (2Н, АВ квартет, Δυ=152 Гц, J=21 Гц), 4,19 (1Н, септет), 3,76 (1Н, септет).
Синтез С4 с тридентатным лигандом N-N-N (предлагается в настоящем изобретении)
СН2Сl2 г (4 мл) добавляли к Int-3 (0,089 г, 0,15 ммоля) и PhCH=N(2,5-Me2-С6Н3) (0,032 г, 0,15 ммоля). Сосуд герметично закрывали и нагревали при 65°С в течение ночи. Летучие вещества выпаривали и остаток экстрагировали с помощью Et2O (5 мл) и фильтровали. Концентрирование раствора до 1,5 мл в течение ночи давало продукт С4 в виде кристаллического твердого вещества. Выход: 0,018 г, 16%. Данные Н ЯМР показывали, что продукт являлся сложной смесью конформационных диастереоизомеров. Реакция эфирного раствора выделенного продукта с водой приводила к образованию чистого диамина L4 (по данным1Н ЯМР спектроскопии).
Синтез С5 с тридентатным лигандом N-N-N (предлагается в настоящем изобретении)
Толуол (7 мл) и PhCH=N(2,5-Me2-C6H3) (0,0821 г, 0,392 ммоля) объединяли с образованием прозрачного желтого раствора. Затем этот раствор добавляли к твердому веществу Int-5 (0,261 г, 0,392 ммоля). Смесь нагревали при 90°С в течение ночи. Аликвоту реакционной смеси (примерно одну треть) фильтровали и выпаривали и получали С5 в виде белого твердого вещества. Выход: 0,114 г, 36,3%. Данные Н ЯМР раствора С5 в CD2Cl2 показывали, что продукт являлся сложной смесью конформационных диастереоизомеров. Остаток раствора в толуоле разбавляли водой (4 мл). Органические вещества экстрагировали с помощью Et2O (10 мл), отделяли и сушили над MgSO4. Фильтрование и выпаривание летучих веществ давали диамин L4 (по данным1Н ЯМР) в виде липкого остатка. Выход: 0,131 г, 60,3%.
Синтез С7 с тридентатным лигандом N-N-N (предлагается в настоящем изобретении)
Раствор лиганда L4 (79,5 мг, 0,144 ммоля) в толуоле (3 мл) добавляли к твердому веществу Zr(NMe2)4 (38,4 мг, 0,144 ммоля) и получали желтый раствор. Сосуд герметично закрывали и нагревали при 120°С в течение 1 ч. Летучие вещества удаляли и получали кристаллический остаток. Его кристаллизовали из смеси толуола (0,5 мл) и гексанов (4 мл) и получали продукт в виде бесцветных кристаллов. Выход: 70 мг, 67%. Данные1Н ЯМР показывали, что содержался один конформационный диастереоизомер.1Н ЯМР (250 МГц, CD2Cl2): δ 7,5-6,6 (18Н), 5,24 (1H, s), 4,93 (2H, АВ квартет, Δυ=146 Гц, J=20 Гц), 3,91 (1H, септет), 3,53 (1H, септет), 2,44 (3Н, s), 2,19 (6Н, s), 2,09 (3Н, s), 1,88 (6Н, s), 1,50 (3Н, d), 1,4-0,8 (18Н, перекрывающиеся мультиплеты и некоторое количество совместно закристаллизовавшихся гексанов). Идентичность продукта подтверждали с помощью рентгенографии монокристалла.
Синтез С8 с лигандом N-N-N (предлагается в настоящем изобретении) с помощью метатезиса соли
Бензол (4 мл) добавляли к комплексу Cl (111 мг, 0,147 ммоля) и получали суспензию. Затем в течение 2-3 мин по каплям добавляли раствор Me2Mg (0,94 мл, 0,163 ммоля) в Et2O. Через 30 мин летучие вещества выпаривали и остаток экстрагировали бензолом (4 мл). Раствор фильтровали и выпаривали при пониженном давлении и получали продукт в виде вспененного вещества. Выход: 93 мг, 98%. Данные1Н ЯМР показывали, что продукт представляет собой смесь состава 3:2 конформационных диастереоизомеров. Вследствие сложности спектра ЯМР приведены только некоторые резонансы для каждого диастереоизомера.1Н ЯМР (250 МГц, C6D6): δ Содержащийся в большом количестве диастереоизомер: 5,79 (1H, s), 4,49 (2H, АВ квартет, Δυ=155 Гц, J=20 Гц), 0,64 (3Н, s, Zr-Me),0,06 (3Н, s, Zr-Me); содержащийся в небольшом количестве диастереоизомер: 5,79 (1H, s), 4,89 (2H, АВ квартет, Δυ=134 Гц, J=20 Гц), 0,23 (3Н, s, Zr-Me), 0,16 (3Н, s, Zr-Me).
Примеры полимеризации
Общие методики полимеризации
Сополимеризацию этилен/1-октен проводили параллельно в реакторе высокого давления, как это описано в US 6306658; US 6455316; US 6489168; WO 00/09255 и публикации Murphy et al., J. Am. Chem. Soc., 2003, 125, стр.4306-4317, каждая из которых во всей ее полноте включена в настоящее изобретение в качестве ссылки. В каждый реакционный сосуд реактора, который содержал 48 отдельных реакционных сосудов, помещали предварительно взвешенный вставной стеклянный сосуд и одноразовую лопасть для перемешивания. Затем реактор закрывали и каждый сосуд отдельно нагревали при установленной температуре (обычно от 50 до 110°С) и герметизировали при заданном давлении этилена, равном 1,38 МПа (200 фунт-сила/дюйм). В каждый реакционный сосуд через клапан вводили 1-октен (100 мкл, 637 мкМ), затем количество толуола, достаточное до доведения до полного реакционного объема, включая последующие добавления, равного 5 мл. Затем добавляли три-н-октилалюминий в толуоле (100 мкл, 10 мМ в толуоле, 1 мкМ) в качестве сокатализатора/поглотилеля, если его использовали. Пиридиламидный катализатор Int-3 не соответствует настоящему изобретению; катализаторы С1, С3 и С8 предлагаются в настоящем изобретении.
Затем содержимое сосуда перемешивали при 800 об/мин. Затем в реакционную смесь в сосуде вводили раствор активатора (1,0 экв. 0,40 мМ диметиланилинийтетракис-пентафторфенилбората (dmah-HKA) в толуоле или 100-1000 мол. экв. метилалюмоксана (МАО) в толуоле) и 500 мкл толуола, затем раствор катализатора (0,40 мМ в толуоле, 20-40 нМ катализатора) в толуоле и еще аликвоту толуола (500 мкл). Количество эквивалентов определяли по количеству мол. экв. на количество молей переходного металла в каталитическом комплексе.
Затем реакции давали протекать, пока давление этилена в реакционной смеси не станет равным 20 фунт-сила/дюйм (давление этилена в каждом реакционном сосуде поддерживали при предварительно заданном значении с помощью компьютерного управления). Затем реакцию останавливали путем создания в сосуде давления с помощью сжатого воздуха. После завершения реакции полимеризации вставной стеклянный сосуд, содержащий полимерный продукт и растворитель, удаляли из секции высокого давления и перчаточного бокса с инертной атмосферой и летучие компоненты удаляли с помощью центрифуги Genevac HT-12 и вакуумного выпаривающего устройства Genevac VC3000D, работающего при повышенной температуре и пониженном давлении. Затем сосуд взвешивали для определения выхода полимерного продукта. Полученный полимер анализировали с помощью системы Rapid GPC (см. ниже) для определения молекулярной массы, с помощью ФС-ИК (инфракрасная Фурье-спектроскопия) (см. ниже) для определения степени включения сомономера и с помощью ДСК (см. ниже) для определения температуры плавления.
Для определения различных значений, связанных с молекулярной массой, с помощью ГПХ применяли высокотемпературную эксклюзионную хроматографию с использованием автоматизированной системы "Rapid GPC", как это описано в US 6491816; US 6491823; US 6475391; US 6461515; US 6436292; US 6406632; US 6175409; US 6454947; US 6260407 и US 6294388; каждый из которых во всей его полноте включен в настоящее изобретение в качестве ссылки. Этот прибор содержит последовательность их трех линейных колонок 30 см × 7,5 мм, каждая из которых содержит PLgel 10 мкм, Mix В. Систему ГПХ калибровали с помощью стандартов из полистирола в диапазоне 580-3390000 г/моль. Система действовала при скорости потока элюента, равной 2,0 мл/мин, и при температур печи, равной 165°С. В качестве элюента использовали 1,2,4-трихлорбензол. Образцы полимера растворяли в 1,2,4-трихлорбензоле при концентрации, равной 0,1-0,9 мг/мл. В систему инжектировали 250 мкл раствора полимера. За концентрацией полимера в элюенте следили с помощью испарительного детектора светорассеяния. Приведенные молекулярные массы являются относительными по отношению к стандартам из линейного полистирола.
Исследования с помощью дифференциальной сканирующей калориметрии (ДСК) проводили на приборе TA-Q100 для определения температуры плавления полимеров. Образцы предварительно отжигали при 220°С в течение 15 мин и затем им давали охлаждаться до комнатной температуры в течение ночи. Затем образцы нагревали до 220°С со скоростью 100°С /мин и после этого охлаждали со скоростью 50°С /мин. Значения температур плавления накапливали за период нагревания. Отношение количества 1-октена к количеству этилена, включенного в полимеры (мас.%), определяли с помощью быстрой ФС-ИК спектроскопии на приборе Bruker Equinox 55+IR в режиме отражения. Образцы готовили в виде тонких пленок по методике испарительного осаждения. Содержание 1-октена в мас.% получали по отношению высот пиков при 1378 и 4322 см-1. Эту методику калибровали с помощью набора сополимеров этилен/1-октен с известным диапазоном содержания 1-октена в мас.%.
Пример 1
Полимеризация смеси этилена и 1-октена с использованием Int-3 и С1.
Полимеризацию проводили параллельно в реакторе высокого давления, как это описано выше, со следующими особенностями. Активатор МАО (1000 экв. на 1 экв. катализатора) добавляли в виде 1 мас.% раствора в толуоле. Концентрации катализатора равнялись 0,00800 мМ (использовали 40 нМ катализатора). Поглотители на основе триалкилалюминия не использовали. Данные приведены в таблице 1. Катализатор С1 образуется по реакции PhCH=NPh с Int-3. Приведенные данные показывают, что С1 обладает большей активностью при образовании сополимеров этилен-октен, чем Int-3 при температурах от 50 до 100°С. Катализатор С1 также приводит к образованию полимера с меньшей молекулярной массой (чем Int-3), который обладает меньшими значениями Мw/Мn. Катализатор Int-3 не соответствует настоящему изобретению; катализатор С1 предлагается в настоящем изобретении.
Пример 2
Полимеризация смеси этилена и 1-октена с использованием Int-3 и С3.
Полимеризацию проводили параллельно в реакторе высокого давления, как это описано выше, со следующими особенностями. Активатор МАО (1000 экв. на 1 экв. катализатора) добавляли в виде 1 мас.% раствора в толуоле. Концентрации катализатора равнялись 0,00800 мМ (использовали 40 нМ катализатора). Поглотители на основе триалкилалюминия не использовали. Данные приведены в таблице 2. Катализатор С3 образуется по реакции PhCH=NiPr с катализатором Int-3. Данные показывают, что С3 обладает большей активностью при образовании сополимеров этилен-октен, чем Int-3 при 50°С, но менее активен при более высоких температурах. Катализатор Int-3 не соответствует настоящему изобретению; катализатор С3 предлагается в настоящем изобретении.
Пример 3
Полимеризация смеси этилена и 1-октена с использованием С8. Полимеризацию проводили параллельно в реакторе высокого давления, как это описано выше, со следующими особенностями. В качестве растворителя использовали изогексан. N,N-Диметиланилинийтетракис(пентафторфенил)борат, для которого использована аббревиатура dmah-HKA, активатор (1,0 экв. на 1 экв. катализатора) добавляли в виде 20 мМ раствора в толуоле. Концентрации катализатора равнялись 0,00400 мМ (использовали 20 нМ катализатора). Три-н-октилалюминий (0,100 мл 0,010 М раствора в изогексане) использовали в качестве поглотителя. Данные приведены в таблице 3. Приведенные данные показывают, что С8 с активатором с некоординирующимся анионом dmah-HKA является активным катализатором полимеризации смеси этилена с 1-октеном.
Пример 4
Полимеризация пропилена с использованием С1, С2, С3 и С5. Полимеризацию проводили параллельно в реакторе высокого давления, аналогично тому, как описано выше для полимеризации этилен-октен, со следующими особенностями. В качестве растворителя использовали изогексан. Пропилен (1,0 мл) использовали вместо 1-октена. Полный объем равнялся 5,10 мл. Активатор МАО (700 экв. на 1 экв. катализатора) добавляли в виде 1 мас.% раствора в толуоле. Концентрации катализатора равнялись 0,01600 мМ (использовали 80 нМ катализатора). Поглотители на основе триалкилалюминия не использовали. Реакциям давали протекать в течение 20 мин. Данные приведены в таблице 4. Приведенные данные показывают, что пиридилдиамидные комплексы С1, С2, С3 и С5 с активатором МАО являются активными катализаторами для полимеризации пропилена.
Все документы, описанные в настоящем изобретении, включены в настоящее изобретение в качестве ссылки, включая все документы о приоритете и/или методиках исследований, в той степени, в которой они не являются несогласующимися с настоящим текстом. Как ясно из приведенного выше общего описания и конкретных вариантов осуществления, хотя формы настоящего изобретения проиллюстрированы и описаны без отклонения от сущности и объема настоящего изобретения, в него можно внести различные модификации. В соответствии с этим не предполагается, что они ограничивают настоящее изобретение. Аналогичным образом, термин "содержащий" является синонимом термина "включающий".
Реферат
Изобретение относится к пиридилдиамидному комплексу переходного металла. Комплекс описывается общей формулой (IV)в которой М обозначает Ti, Zr или Hf; R, R, Rи Rозначают водород; Rи Rнезависимо выбраны из группы, включающей алкилы и фенильные группы, которые содержат от 0 до 5 различных заместителей, которые включают F, Cl, Br, I, CF, NO, алкоксигруппу, диалкиламиногруппу, гидрокарбил (такой как алкил и арил) и замещенные гидрокарбилы (такие как гетероарил), содержащие от 0 до 10 атомов углерода; Rи Rвсе независимо обозначают -E(R)(R)-, где Е обозначает углерод, и каждый Rи Rнезависимо выбран из группы, включающей водород и фенильные группы; R, Rи Rозначают водород; L обозначает анионную отщепляющуюся группу, причем группы L могут быть одинаковыми или разными и любые две группы L могут быть связаны с образованием дианионной отщепляющейся группы; n равно 0, 1, 2, 3 или 4; L' выбран из группы, включающей простые эфиры, простые тиоэфиры, амины, нитрилы, имины, пиридины и фосфины; и w равно 0, 1, 2, 3 или 4. Также предложены способы получения комплекса (варианты), пиридилдиамин для получения комплекса, каталитическая система и способ полимеризации. Изобретение позволяет получить новые пиридилдиамидные комплексы переходного металла, которые могут быть использованы для полимеризации алкенов. 7 н.п. ф-лы, 2 ил., 4 табл., 4 пр.
Формула

в которой:
М обозначает Ti, Zr или Hf;
R6, R7, R8 и R9 означают водород;
R1 и R11 независимо выбраны из группы, включающей алкилы и фенильные группы, которые содержат от 0 до 5 различных заместителей, которые включают F, Cl, Br, I, CF3, NO2, алкоксигруппу, диалкиламиногруппу, гидрокарбил (такой как алкил и арил) и замещенные гидрокарбилы (такие как гетероарил), содержащие от 0 до 10 атомов углерода;
R2 и R10 все независимо обозначают -E(R12)(R13)-, где Е обозначает углерод, и каждый R12 и R13 независимо выбран из группы, включающей водород и фенильные группы;
R3, R4 и R5 означают водород;
L обозначает анионную отщепляющуюся группу, причем группы L могут быть одинаковыми или разными и любые две группы L могут быть связаны с образованием дианионной отщепляющейся группы;
n равно 0, 1, 2, 3 или 4;
L' выбран из группы, включающей простые эфиры, простые тиоэфиры, амины, нитрилы, имины, пиридины и фосфины; и
w равно 0, 1, 2, 3 или 4.

в котором М, L, L', w, n, R1, R2, R3, R4, R5, R6, R7, R8, R9, R10 и R11 являются такими, как определено в п.1.

в котором М, L, L', w, n, R1, R2, R3, R4, R5, R10 и R11 являются такими, как определено в п.1, и Z представляет собой арильную группу.

в котором М, L, L', w, n, R1, R2, R3, R4, R5, R10 и R11 являются такими, как определено в п.1, и Z представляет собой арильную группу.

R6, R7, R8 и R9 означают водород;
R1 и R11 независимо выбраны из группы, включающей алкил и фенильные группы;
R2 и R10 все независимо обозначают -E(R12)(R13)-, где Е обозначает углерод, и каждый R12 и R13 независимо выбран из группы, включающей водород и фенильные группы; и
R3, R4 и R5 означают водород.

Комментарии