Новое соединение, выделенное из pseudolysimachion rotundum var. subintegrum, с высоким содержанием активного ингредиента, композиция, содержащая указанное соединение, для предотвращения или лечения аллергического заболевания, воспалительного заболевания, - RU2685732C2
Код документа: RU2685732C2
Чертежи












Описание
Область техники
Настоящее изобретение относится к новому соединению, выделенному из Pseudolysimachion rotundum var. subintegrum, композиции, содержащей указанное соединение, для предотвращения или лечения аллергического заболевания, воспалительного заболевания, астмы или хронической обструктивной болезни легких, и ее применению.
Уровень техники
Как правило, воспалительный ответ представляет собой нормальный ответ организма человека, связанный с отеком, болью и т.п., в тех случаях, когда в ткань или клетку проникает что-либо вызывающее определенные органические изменения в указанной ткани или клетке. Недавно было обнаружено, что в воспалительное заболевание вовлечены цитокины различных типов.
Аллергическая реакция может быть классифицирована на 4 категории, а именно, на реакции типа I, II, III и IV в соответствии с типами ответа, или на две категории, а именно, на аллергические реакции немедленного типа, такие как реакции типа I, II или III, и аллергические реакции замедленного типа, такие как реакции типа IV, в соответствии с периодами времени, проходящими с момента повторной сенсибилизации в результате воздействия аллергена до начала реакции.
К ним относится, например, аллергия I типа, задействующая антитела IgE и называемая аллергией по типу анафилаксии, вызывающая бронхиальную астму, атопические заболевания, такие как дерматит или гастроэнтерит и т.д., аллергический ринит, такой как поллиноз, аллергический конъюнктивит, пищевая аллергия и т.п.
Астма рассматривается как комплексный синдром дыхательных путей, который характеризуется различными клиническими симптомами, например, кашлем, диспноэ, вызываемыми нарушением проходимости дыхательных путей, острым или хроническим воспалением дыхательных путей, гиперреактивностью дыхательных путей (ГРП) и структурным ремоделированием, и может быть обратимой или необратимой. Чаще всего астма представляет собой аллергическое заболевание и характеризуется хроническим воспалением дыхательных путей и гиперреактивностью бронхов (Minoguchi K and Adachi М., Pathophysiology of asthma. В источнике: Cherniack NS, Altose MD, Homma I. editors. Rehabilitation of the patient with respiratory disease. New York: McGraw-Hill, 1999, pp97-104).
Астма может быть разделена на два типа, а именно на экзогенную астму и эндогенную астму. Экзогенная астма вызвана воздействием антигена и дает положительную реакцию при кожной пробе или в бронхопровокационном тесте на антиген. Обычный возраст ее начала постепенно снижается. В основном вызывается клещом домашней пыли Dermatophagoides и пыльцой, эпителием животных, грибами и т.д. Эндогенная астма вызвана инфекциями верхних дыхательных путей, физическими упражнениями, эмоциональной нестабильностью, изменением климатической влажности, и распространена у взрослых пациентов. Также могут быть детектированы посредством кожной пробы комплексы IgE-антиген экзогенной астмы за счет повышения уровней IgE в сыворотке.
Что касается патофизиологии, астму определяют по запускаемому Т-хелперами 2 (Th2) хроническому воспалению и различным воспалительным медиаторам, таким как цитокины, хемокины, сигнальные молекулы, молекулы адгезии и факторы роста из иммунных клеток и структурных клеток в дыхательных путях, вовлеченных в различные стадии астмы (Elias JA et al., J Clin Invest. 2003, 111, 291-297). Активированные воспалительные клетки, такие как эозинофилы, тучные клетки, альвеолярные макрофаги и т.д. в бронхах пациентов, страдающих астмой, высвобождают различные медиаторы воспаления, такие как цистеинил-лейкотриены, простагландины и т.д., и вовлечены в выраженное сужение бронхов (Maggi Е. et al., Immunotechnology 1998, 3, 233-244.; Pawankar R. et al., Curr. Opin. Allergy Clin. Immunol. 2001, 1, 3-6.; Barnes PJ et al., Phamacol. Rev. 1998, 50, 515-596).
Соответственно, поскольку воспроизводство различных цитокинов, вовлеченных в активацию воспалительных клеток, таких как ИЛ-4, ИЛ-5, ИЛ-13 и т.д., и IgE, и воспроизводство цистеинил-лейкотриенов, высвобождаемых воспалительными клетками, являются главными причинами воспаления, аллергической реакции и астмы, до настоящего времени проводились многочисленные исследования, направленные на разработку ингибирующих воспроизводство указанных компонентов агентов.
В целом, хроническая обструктивная болезнь легких (ХОБЛ) представляет собой одно из заболеваний легких, вызываемое аномальным воспалительным заболеванием легкого, приводящим к обструкции дыхательных путей. ХОБЛ вызывает диспноэ в результате затрудненности выдоха, демонстрирует характеристики, например, малую обратимость ограничения или обструкции дыхательных путей, прогрессирующее развитие с течением времени и т.д., отличные от общих характеристик астмы, и может подразделяться на эмфизему легких и хронический обструктивный бронхит (Barnes P.J., Pharmacol. Rev. 2004, 56, 515-548).
ХОБЛ была описан как один из факторов риска заболеваемости и смертности в результате заболеваний сердечно-сосудистой системы, а также как пятая по счету в мире основная причина смерти на 2001 год. Распространенность хронической обструктивной болезни легких согласно критериям Глобальной инициативы по хронической обструктивной болезни легких (GOLD) (отношение FEV1 (объем воздуха при форсированном выдохе за 1 секунду) к FVC (форсированной жизненной емкости легких), составляющее менее чем 0,7) составила 17,2% (25,8% для мужчин; 9,6% для женщин) среди корейцев в возрасте старше 45 лет (Kim, D. S. et al., Am. J. Respir. Crit. Care Med. 2005, 172, 842-847.; Sin, D.D. et al, Proc. Am. Thorac. Soc. 2005, 2, 8-11.; Buist A.S. et al., Lancet, 2007, 370, 741-750)
У большинства пациентов с ХОБЛ наблюдаются все три патологических механизма (хронический обструктивный бронхит, эмфизема и закупорка слизью), поскольку все они индуцируются курением, однако могут наблюдаться различные пропорции эмфиземы и обструктивного бронхита. В развитых странах наиболее распространенной причиной ХОБЛ является, безусловно, курение сигарет, однако существуют и некоторые другие факторы риска, в том числе загрязнение воздуха (в частности, загрязнение воздуха в помещениях в результате сжигания топлива), неудовлетворительное питание и воздействия, связанные с родом занятий. ХОБЛ характеризуется ускорением нормального снижения функции легких, происходящей с возрастом. Медленно прогрессирующее ограничение циркуляции воздуха приводит к ограничению физических возможностей и преждевременной смерти и достаточно выраженно отличается от различных вариантов обструкции дыхательных путей и симптомов при астме, тяжесть которых редко возрастает.
Сообщалось, что патофизиологическое действие и синдром ХОБЛ принципиально отличаются от характерных для астмы. Хотя и ХОБЛ, и астма включают воспаление дыхательных путей, существуют заметные различия в природе воспалительного процесса, касающиеся различий воспалительных клеток, медиаторов, ответа на воспаление, анатомического распределения и ответа на противовоспалительную терапию, например, (а) применительно к воспалительным клеткам, при возникновении астмы в основном задействованы тучные клетки, эозинофилы, клетки D4+ (Th2), макрофаги и т.д., тогда как при возникновении ХОБЛ в основном задействованы нейтрофилы, CD8+ (Тс) и т.д.; (b) применительно к медиаторам воспаления, при возникновении астмы в основном задействованы лейкотриены В, гистамин, ИЛ-4, ИЛ-5, ИЛ-13, эотаксин, RENTES, окислительный стресс и т.д. тогда как при возникновении ХОБЛ в основном задействованы ФНО-альфа, ИЛ-8, связанный с ростом онкоген-α (GRO-альфа) и т.д.; (с) применительно к воспалительному синдрому, при астме наблюдается иной воспалительный синдром за счет влияния на весь легочный тракт в раннем возрасте, например, ГРП (гиперреактивность дыхательных путей), отслоение эпителия, фиброз без вовлечения паренхимы, секреция слизи, относительно обратимая обструкция дыхательных путей, кашель, чихание, диспноэ и т.д., отличный от воспалительного синдрома при ХОБЛ, который обусловлен действием на периферические дыхательные пути у взрослых и при котором наблюдаются различные явления, такие как эпителиальная метаплазия, разрушение паренхимы, относительно необратимая обструкция дыхательных путей, хронический бронхит, эмфизема и т.д. (Barnes PJ., Chest 2000, 117, 10S-14S.; Saetta М. et al., Am. J. Respir. Crit. Care Med. 2001, 163, 1304-1309).
Гистопатологические исследования ХОБЛ указывают на преимущественное вовлечение периферических дыхательных путей (бронхиол) и паренхимы легких, тогда как при астме происходит воспаление всех дыхательных путей, однако паренхима легких не вовлечена. Наблюдается обструкция бронхиол с фиброзом и инфильтрацией макрофагами и Т-лимфоцитами. Наблюдается разрушение паренхимы легких, а также повышенное число макрофагов и CD8 (цитотоксических) Т-лимфоцитов (Saetta М. et al., Am. J. Respir. Crit. Care Med. 1998, 157, 822-826). Биопсия бронхов демонстрирует аналогичные изменения с инфильтрацией макрофагами и CDS-клетками и повышенное число нейтрофилов у пациентов с тяжелой ХОБЛ (Di Stefano A. et al., Am. J. Respir. Crit. Care Med. 1998, 158, 1277-1285).
В отличие от астмы, эозинофилы не выражены, за исключением периодов обострений или наличия у пациентов сопутствующей астмы (Fabbri L. et al., Thorax 1998, 53, 803-808.; Fabbri LM. et al., Am. J. Respir. Crit. Care Med. 2003, 167, 418-424).
Соответственно, терапевтический подход при хронической обструктивной болезни легких (ХОБЛ) будет отличаться от подхода при астме; однако предлагаемая в настоящем изобретении терапия направлена на неспецифическое лечение обоих заболеваний. Соответственно, специфические одобренные варианты противовоспалительной терапии для ХОБЛ отсутствовали, а доступные варианты противовоспалительной терапии изначально были разработаны для астмы. Задачи, возникающие при исследованиях ХОБЛ, многогранны; механизмы, лежащие в основе сложной и гетерогенной патологии указанного заболевания, требуют изучения; роль воспаления в прогрессировании заболевания должна быть подтверждена. (Hele D. et al., Expert. Opino. Invest. Drug, 2003, 12, 5-18.; Fox, J C. et al., Curr. Opin. Pharmacol. 2009, 9, 231-242).
Продолжается усовершенствование современной доступной терапии для лечения астмы в форме бета-агонистов длительного действия, более безопасных стероидов и вариантов комбинированной терапии; в случае ХОБЛ антихолинергики обеспечивают симптоматическое облегчение. Стероиды использовались для лечения обострений, однако к настоящему времени пока не было описано лечение, которое оказывало бы значимое влияние на прогрессивное снижение функции легких при ХОБЛ или при развитии астмы.
Соответственно, до настоящего времени проводилось множество исследований, направленных на разработку новых лекарственных средств, обладающих потенциалом для успешного специфического лечения аллергических заболеваний, воспалительных заболеваний, астмы или ХОБЛ.
Авторы настоящего изобретения сосредоточили усилия на разработке эффективного агента для лечения, получаемого из природных источников, отличающегося безопасностью и эффективностью, например, растительного или животного происхождения и т.д., отличающегося высокой терапевтической активностью в отношении аллергических заболеваний, воспалительных заболеваний, астмы или ХОБЛ; в итоге, впоследствии были получены неожиданные результаты, например, впервые обнаружена мощная противовоспалительная, противоаллергенная и противоастматическая активность экстракта Pseudolysimachion longifolium (патент Кореи №10-860080 В1 и US 2012/0183632 A1) и различных выделенных из него соединений, таких как верпрозид (6-O-3,4-дигидроксибензоилкаталпол), пикрозид II (6-O-4-гидрокси-3-метоксибензоилкаталпол), верминозид (6-O-3,4-дигидроксициннамоилкаталпол), 6-0-вератроилкаталпол (6-O-3,4-диметоксибензоилкаталпол), минекозид (6-0-3-гидрокси-4-метоксициннамоилкаталпол), каталпол и т.п. (Патентная публикация Кореи №10-2006-125499 А1); мощная противовоспалительная, противоаллергенная и противоастматическая активность нового очищенного экстракта, содержащего значительное количество активных ингредиентов, таких как производные каталпола из экстракта Pseudolysimachion rotundum var subintegrum (ATC2: патент Кореи №1476045 B1, АТС1: патент Кореи №1504651 В1); и направленная против ХОБЛ активность указанного экстракта (патент Кореи №1476095 В1).
Pseudolysimachion rotundum var subintegrum представляет собой многолетнее травянистое растение, распространенное в Корее, Китае, Японии, на о. Сахалине и в России.
На основании предшествующих исследований противовоспалительной, противоаллергенной и противоастматической активности экстракта Pseudolysimachion rotundum var subintegrum авторами настоящего изобретения была предпринята попытка разработки нового соединения, демонстрирующего противовоспалительную, противоаллергенную, противоастматическую и направленную против ХОБЛ активность, выделенного из экстракта Pseudolysimachion rotundum var subintegrum.
При этом в цитируемых выше опубликованных источниках, содержание которых включено в настоящий документ посредством ссылки, не было описано или раскрыто новое соединение, демонстрирующее противовоспалительную, противоаллергенную, противоастматическую и направленную против ХОБЛ активность, выделенное из экстракта Pseudolysimachion rotundum var subintegrum.
Соответственно, авторы настоящего изобретения обнаружили новое соединение, демонстрирующее противовоспалительную, противоаллергенную, противоастматическую и направленную против ХОБЛ активность, выделенное из экстракта Pseudolysimachion rotundum var subintegrum; указанное предложенное в настоящем изобретении соединение демонстрировало мощную противовоспалительную, противоаллергенную, противоастматическую и направленную против ХОБЛ активность, определенную путем применения различных тестов in vitro, например, (1) теста на цитотоксичность с использованием линий клеток НТ1080, Н292 и EL4, (2) теста ингибирования экспрессии MUC5AC (олигомерный слизе-/гелеобразующий муцин), индуцируемой ФНО-альфа, (3) люциферазного репортерного анализа NF-каппа B, (4) теста ингибирования активности ядерного транскрипционного фактора каппа B (NF-каппа В); (5) ингибирования экспрессии мРНК целевых генов, таких как ММР-9, MUC5AC и ИЛ-4 путем ингибирования активности NF-каппа B; (6) дозозависимого ингибирующего эффекта на воспроизводство MUC5AC посредством анализа воспроизводства белка MUC5AC; а также тестов in vivo, например, (7) эффекта, заключающегося в уменьшении числа воспалительных клеток, таких как эозинофилы, с применением модели на сенсибилизированных/стимулированных OVA (овальбумином) мышах, (8) теста ингибирования высвобождения IgE, воспалительных цитокинов, таких как ИЛ-4, ИЛ-5, ИЛ-13 и т.д. в жидкости бронхоальвеолярного лаважа и инфильтрации воспалительными клетками, а также подавления гиперреактивности дыхательных путей и гиперплазии бокаловидных клеток, (9) теста ингибирования с применением модели ХОБЛ на животных (мыши C57B/6N) пролиферации воспалительных клеток в жидкости бронхоальвеолярного лаважа, ингибирования воспроизводства АФК (активных форм кислорода) и активности эластазы нейтрофилов, эффекта снижения уровней ИЛ-6, ФНО-альфа и инфильтрирующих воспалительных клеток и т.п.
Краткое описание изобретения
Техническая задача
В настоящем изобретении предложено новое соединение (KS534), выделенное из экстракта Pseudolysimachion rotundum var subintegrum.
В настоящем изобретении также предложены фармацевтическая композиция и функциональный пищевой продукт, содержащие новое соединение (KS534), выделенное из экстракта Pseudolysimachion rotundum var subintegrum, в качестве активного ингредиента в количестве, эффективном для лечения и предотвращения аллергического заболевания, воспалительного заболевания, астмы или заболевания ХОБЛ.
В настоящем изобретении также предложено применение нового соединения (KS534), выделенного из экстракта Pseudolysimachion rotundum var subintegrum, для получения медикаментов, применяемых для лечения или предотвращения воспалительного заболевания, аллергического заболевания, астмы или ХОБЛ.
В настоящем изобретении также предложен способ лечения или предотвращения воспалительного заболевания, аллергического заболевания, астмы или ХОБЛ у млекопитающего или человека, включающий введение указанному млекопитающему или человеку эффективного количества нового соединения (KS534), выделенного из экстракта Pseudolysimachion rotundum var subintegrum, совместно с фармацевтически приемлемым носителем.
Техническое решение
В настоящем изобретении предложен (3R,5S,5aS,6R,7S,8R,8aS)-8-хлop-8a-гидрокси-5-(2-гидрокси-ацетокси)гексагидро-1Н-3,6-метанциклопента[е][1,3]диоксепин-7-ил-3,4-дигидроксибензоат (KS534), представленный приведенной ниже химической формулой (1), его изомер, фармацевтически приемлемая соль или сольваты:
[Химическая формула 1]
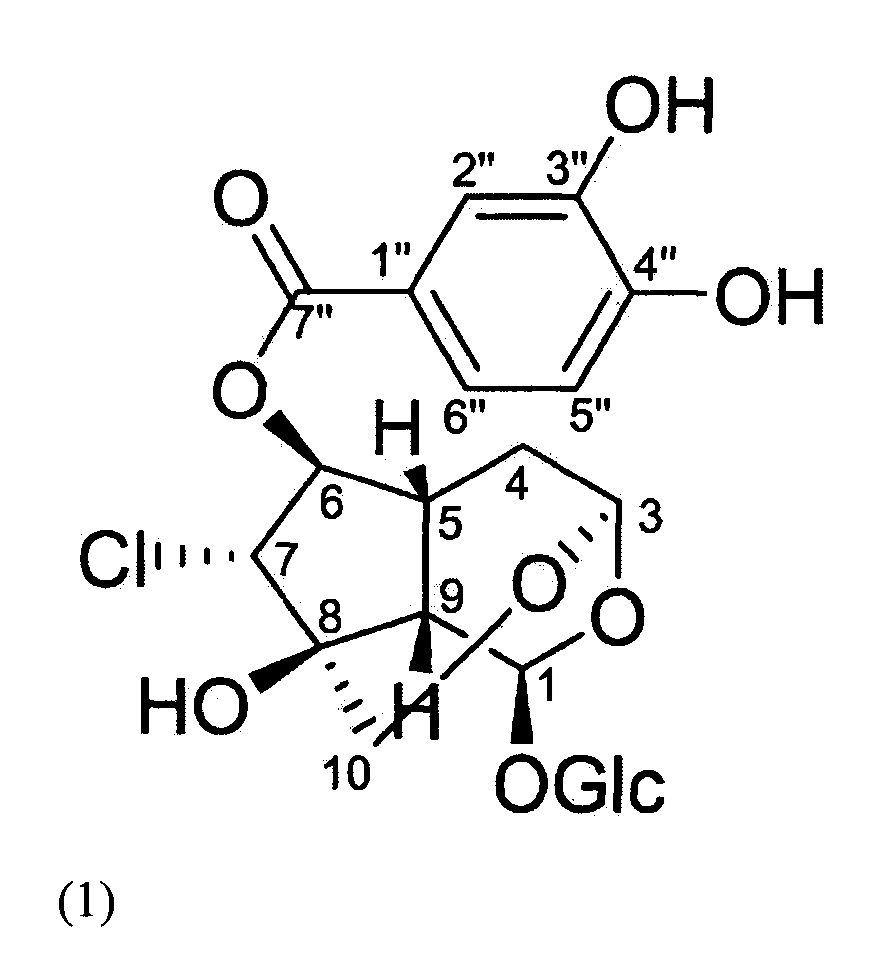
Предложенное в настоящем изобретении новое соединение может быть преобразовано в фармацевтически приемлемую соль и сольваты с применением стандартного хорошо известного в данной области техники способа. В случае солей подходит для применения и может быть получена с применением стандартного способа соль присоединения кислоты указанного соединения, образованная фармацевтически приемлемой свободной кислотой. Например, после растворения указанного соединения в избыточном количестве раствора кислоты, соли осаждают с использованием смешиваемого с водой органического растворителя, такого как метанол, этанол, ацетон или ацетонитрил, для получения соли присоединения кислоты, после чего смесь эквивалентного количества соединения и кислоты, разведенной водой или спиртом, например, простого монометилового эфира гликоля, может быть нагрета и затем высушена посредством испарения или профильтрован под пониженным давлением для получения высушенной солевой формы.
В качестве свободной кислоты в вышеописанном способе может применяться органическая кислота или неорганическая кислота. Например, в настоящем изобретении может применяться органическая кислота, такая как метансульфоновая кислота, n-толуолсульфоновая кислота, уксусная кислота, трифторуксусная кислота, лимонная кислота, малеиновая кислота, янтарная кислота, щавелевая кислота, бензойная кислота, молочная кислота, гликолевая кислота, глюконовая кислота, галактуроновая кислота, глутаминовая кислота, глутаровая кислота, глюкуроновая кислота, аспарагиновая кислота, аскорбиновая кислота, карбонильная кислота, ванилиновая кислота, бромоводородная кислота и т.п., и неорганическая кислота, такая как соляная кислота, фосфорная кислота, серная кислота, азотная кислота, винная кислота и т.п.
Кроме того, предложенные в настоящем изобретении соединения в форме фармацевтически приемлемых солей металлов могут быть получены с использованием основания. Соль щелочного металла или щелочноземельного металла указанного соединения может быть получена с применением стандартного способа, например, после растворения соединения в избыточном количестве раствора гидроксида щелочного металла или щелочноземельного металла, нерастворимые соли отфильтровывают и оставшийся фильтрат подвергают испарению и высушиванию для получения соли металла указанного соединения. В качестве соли металла согласно настоящему изобретению фармацевтически подходящими являются соли натрия, калия или кальция, а соответствующая соль серебра может быть получена путем проведения реакции соли щелочного металла или соли щелочноземельного металла с подходящей солью серебра, например, нитратом серебра.
Фармацевтически приемлемые соли указанного соединения включают все возможные кислые или основные соли указанных соединений, если в настоящем описании конкретным образом не указано иное. Например, фармацевтически приемлемые соли согласно настоящему изобретению включают соли с гидроксильными группами, например, натрия, кальция и калия; соль с аминогруппами, например, соль бромистого водорода, соль серной кислоты, сероводородную соль, фосфатную соль, гидрофосфатную соль, дигидрофосфатную соль, ацетатную соль, сукцинатную соль, цитратную соль, тартратную соль, лактатную соль, манделатную соль, метансульфонатную (мезилатную) соль и n-толуолсульфонатную (тозилатную) соль и т.д., которые могут быть получены с применением стандартного хорошо известного в данной области техники способа.
Они могут существовать в форме оптически отличных диастереомеров, поскольку указанные соединения имеют несимметричные центры, соответственно, соединения согласно настоящему изобретению включают все оптически активные изомеры, R- или S-стереоизомеры и их смеси. Настоящим изобретением также охвачены все варианты применения рацемической смеси, более чем одного оптически активного изомера или их смесей, а также все способы получения или выделения диастереоизомера, хорошо известные в данной области техники.
Соединения согласно настоящему изобретению могут быть выделены путем применения способа выделения или очищения, хорошо известного в данной области техники, например, хроматографии на колонке с силикагелем или рекристаллизации, например, с применением способа, раскрытого в патентной публикации Кореи №10-2006-125499; или химически синтезированы путем применения хорошо известных способов в данной области техники, исключительно иллюстративных и никоим образом не ограничивающих настоящее изобретение.
Предложенное в настоящем изобретении новое соединение (KS 534) может быть получено из Pseudolysimachion rotundum var subintegrum с применением следующей методики:
Например, новое соединение (KS 534) характеризуется получением посредством процесса добавления по меньшей мере одного экстрагирующего растворителя, выбранного из воды, низшего спирта С1-С4, такого как метанол, этанол, бутанол и т.д. или их смеси, предпочтительно, смеси воды и метанола, более предпочтительно, 10-100% (по массе) метанола в воде, с высушенным Pseudolysimachion rotundum var subintegrum на первом этапе; осуществление по меньшей мере одного способа экстракции, выбранного из рефлюкс-экстракции горячей водой, холодной водной экстракции, обработки ультразвуком или стандартной экстракции, предпочтительно холодной водной экстракции при температуре в диапазоне от 10 до 150°C, предпочтительно от 20 до 70°C, на протяжении периода в диапазоне от 30 минут до 72 часов, предпочтительно, от 1 до 48 часов, более предпочтительно, холодной водной экстракции при температуре в диапазоне от 10 до 60°C, предпочтительно от 20 до 50°С, на протяжении периода в диапазоне от 30 минут до 72 часов, предпочтительно, от 6 до 48 часов, многократно, и затем рефлюкс-экстракции при температуре в диапазоне от 40 до 120°С, предпочтительно от 60 до 90°С, на протяжении периода в диапазоне от 30 минут до 72 часов, предпочтительно, от 6 до 48 часов, многократно, для выделения первого экстракта на 2 этапе; осуществление способа фильтрации, концентрации под вакуумом и высушивания для выделения высушенного неочищенного экстракта на 3 этапе; и осуществление по меньшей мере одного способа очищения, выбранного из (i) распределительной хроматографии с обращенной фазой, (ii) колоночной флэш-хроматографии, (iii) колоночной хроматографии на RP С18, (iv) колоночной хроматографии с силикагелем, (v) ионообменной хроматографии или (iv) эксклюзионной хроматографии, с многократным проведением для выделения нового соединения (KS 534) согласно настоящему изобретению.
Термин «фармацевтически приемлемые носители или вспомогательные вещества» в настоящем документе включает фармацевтические добавки, неактивные ингредиенты, используемые для получения лекарственного средства. Они включают красители, вкусоароматические вещества, связывающие вещества, смягчающие вещества, наполнители, смазывающие вещества, консерванты и многие другие категории. Распространенные вспомогательные вещества включают кукурузный крахмал, лактозу, тальк, стеарат магния, сахарозу, желатин, стеарат кальция, диоксид кремния, шеллак и глазурь, хорошо известные в данной области техники (см. домашнюю страницу Управления по контролю пищевых продуктов и лекарственных средств: www.fda.gov или онлайн-ресурс информации о лекарственных средствах: www.drugs.com) или ранее опубликованные источники (например, Rowe, Raymond С et al., Handbook of Pharmaceutical Excipients, Pharmaceutical Press, 7th Edition, 2012)
Термин «предотвращать» в настоящем документе включает любое действие, ингибирующее или задерживающее возникновение определенного заболевания или расстройства, описанного в настоящем документе, путем введения предложенной в настоящем изобретении композиции; а термин «лечить» в настоящем документе включает любое действие, смягчающее или благоприятным образом изменяющее симптом, связанный с определенным заболеванием или расстройством, описанным в настоящем документе, путем введения предложенной в настоящем изобретении композиции.
Авторы настоящего изобретения обнаружили, что новое соединение (KS 534), которое может быть получено из Pseudolysimachion rotundum var subintegrum, демонстрировало мощную противовоспалительную, противоаллергенную, противоастматическую и направленную против ХОБЛ активность в различных тестах in vitro, например, (1) в тесте на цитотоксичность с использованием линий клеток НТ1080, Н292 и EL4, (2) в тесте ингибирования экспрессии MUC5AC (олигомерный слизе-/гелеобразующий муцин), индуцируемой ФНО-альфа, (3) в люциферазном репортерном анализе NF-каппа B, (4) в тесте ингибирования активности транскрипционного фактора NF-каппа B; (5) ингибирования экспрессии мРНК целевых генов, таких как ММР-9, MUC5АС и ИЛ-4 путем ингибирования активности NF-каппа B; (6) дозозависимого ингибирующего эффекта на воспроизводство MUC5AC посредством анализа воспроизводства белка MUC5AC; а также при тестировании in vivo, например, (7) эффекта, заключающегося в уменьшении числа воспалительных клеток, таких как эозинофилы, с применением модели на сенсибилизированных/стимулированных OVA (овальбумином) мышах, (8) в тесте ингибирования высвобождения IgE, воспалительных цитокинов, таких как ИЛ-4, ИЛ-5, ИЛ-13 и т.д. в жидкости бронхоальвеолярного лаважа, и инфильтрации воспалительными клетками, а также подавления гиперреактивности дыхательных путей и гиперплазии бокаловидных клеток, (9) в тесте ингибирования с применением модели ХОБЛ на животных (мыши C57B/6N) пролиферации воспалительных клеток в жидкости бронхоальвеолярного лаважа, ингибирования воспроизводства АФК (активных форм кислорода) и активности эластазы нейтрофилов, эффекта снижения уровня ИЛ-6, ФНО-альфа и инфильтрирующих воспалительных клеток и т.п.
Таким образом, в соответствии с другим аспектом настоящего изобретения, в настоящем изобретении предложена фармацевтическая композиция или функциональный пищевой продукт, содержащий(ая) в качестве активного ингредиента новое соединение (KS534), выделенное из экстракта Pseudolysimachion rotundum var subintegrum, в количестве, эффективном для лечения и предотвращения аллергического заболевания, воспалительного заболевания, астмы или заболевания ХОБЛ.
В настоящем изобретении предложена фармацевтическая композиция или функциональный пищевой продукт, содержащий(ая) новое соединение (KS534), выделенное из экстракта Pseudolysimachion rotundum var subintegrum, и фармацевтически приемлемые носители или вспомогательные вещества, для лечения или предотвращения аллергического заболевания, воспалительного заболевания, астмы или хронической обструктивной болезни легких (ХОБЛ).
В соответствии с другим аспектом настоящего изобретения, также предложено применение нового соединения (KS534), выделенного из экстракта Pseudolysimachion rotundum var subintegrum, для получения лекарственных средств, применяемых для лечения или предотвращения аллергического заболевания, воспалительного заболевания, астмы или хронической обструктивной болезни легких (ХОБЛ).
В соответствии с другим аспектом настоящего изобретения также предложено применение нового соединения (KS534), выделенного из экстракта Pseudolysimachion rotundum var subintegrum, и фармацевтически приемлемых носителей или вспомогательных веществ для получения лекарственных средств, применяемых для лечения или предотвращения аллергического заболевания, воспалительного заболевания, астмы или хронической обструктивной болезни легких (ХОБЛ).
В соответствии с другим аспектом настоящего изобретения также предложен способ лечения или предотвращения аллергического заболевания, воспалительного заболевания, астмы или хронической обструктивной болезни легких (ХОБЛ) у млекопитающего, отличающийся тем, что указанный способ включает введение терапевтически эффективного количества нового соединения (KS534), выделенного из экстракта Pseudolysimachion rotundum var subintegrum, млекопитающему, страдающему аллергическим заболеванием, воспалительным заболеванием, астмой или хронической обструктивной болезнью легких (ХОБЛ).
В соответствии с другим аспектом настоящего изобретения предложен также способ лечения или предотвращения аллергического заболевания, воспалительного заболевания, астмы или хронической обструктивной болезни легких (ХОБЛ) у млекопитающих, отличающийся тем, что указанный способ включает введение композиции, содержащей терапевтически эффективное количество нового соединения (KS534), выделенного из экстракта Pseudolysimachion rotundum var subintegrum, и фармацевтически приемлемых носителей или вспомогательных веществ млекопитающему, страдающему аллергическим заболеванием, воспалительным заболеванием, астмой или хронической обструктивной болезнью легких (ХОБЛ).
Предложенная в настоящем изобретении композиция для лечения и предотвращения аллергического заболевания, воспалительного заболевания, астмы или хронической обструктивной болезни легких (ХОБЛ), может содержать вышеуказанные соединения в количестве от 0,1~99%, предпочтительно, от 0,1~50% по массе от общей массы указанной композиции.
Композиция в соответствии с настоящим изобретением может быть представлена в форме фармацевтической композиции, содержащей фармацевтически приемлемые носители, адъюванты или разбавители, например, лактозу, декстрозу, сахарозу, сорбит, маннит, ксилит, эритрит, мальтит, крахмалы, гуммиарабик, альгинат, желатин, фосфат кальция, силикат кальция, целлюлозу, метилцеллюлозу, поливинилпирролидон, воду, метилгидроксибензоат, пропилгидроксибензоат, тальк, стеарат магния и минеральное масло. Указанные составы может дополнительно включать наполнители, антиагглютинирующие агенты, смазывающие агенты, смачивающие агенты, вкусоароматические агенты, эмульгаторы, консерванты и т.п. Композиции согласно настоящему изобретению могут быть введены в состав для обеспечения быстрого, продолжительного или отсроченного высвобождения активного ингредиента после его введения пациенту путем выполнения любых процедур, хорошо известных в данной области техники.
Например, композиции согласно настоящему изобретению могут быть растворены в маслах, пропиленгликоле или других растворителях, которые обычно используют для получения инъекционных составов. Подходящие примеры носителей включают физиологический солевой раствор, полиэтиленгликоль, этанол, растительные масла, изопропилмиристат, и т.п., однако не ограничиваются ими. В случае местного введения, экстракт согласно настоящему изобретению может быть представлен в форме мазей и кремов.
Фармацевтические составы, содержащие предложенную композицию, могут быть получены в любой форме, например, в виде лекарственной формы для перорального применения (порошок, таблетка, капсула, мягкая капсула, водный лекарственное средство, сироп, эликсиры, пилюли, порошок, саше, гранулы), или состава для местного применения (крем, мазь, лосьон, гель, бальзам, пластырь, паста, спрей, аэрозоль и т.п.), или инъекционного состава (раствор, суспензия, эмульсия).
Композиция согласно настоящему изобретению в составе фармацевтических лекарственных форм может применяться в форме ее фармацевтически приемлемой соли, и также может применяться по отдельности или в подходящем сочетании, а также в комбинации с другими фармацевтически активными соединениями.
Требуемая доза предложенного в настоящем изобретении экстракта или соединения варьируется в зависимости от состояния и массы тела субъекта, тяжести, формы лекарственного вещества, способа и периода введения, и может быть выбрана специалистами в данной области техники. При этом для получения требуемых эффектов, как правило, рекомендуется введение количества в диапазоне от 0,0001 до 1000 мг/кг, предпочтительно, от 0,001 до 100 мг/кг по массе в день предложенного в настоящем изобретении экстракта. Указанная доза может быть введена единоразово или разделена на несколько приемов в сутки.
Фармацевтическая композиция согласно настоящему изобретению может вводиться субъекту-животному, например, млекопитающим (крысам, мышам, домашним животным или человеку) различными способами. Включены все способы введения, например, введение может осуществляться перорально, ректально или путем внутривенной, внутримышечной, подкожной, внутрикожной, интратекальной, эпидуральной или интрацеребровентрикулярной инъекции.
В настоящем изобретении также предложены фармацевтическая композиция и функциональный пищевой продукт, содержащие новое соединение (KS534), выделенное из экстракта Pseudolysimachion rotundum var subintegrum в качестве активного ингредиента в количестве, эффективном для лечения и предотвращения аллергического заболевания, воспалительного заболевания, астмы или заболевания ХОБЛ.
В настоящем изобретении также предложено применение нового соединения (KS534), выделенного из экстракта Pseudolysimachion rotundum var subintegrum, для получения лекарственных средств, применяемых для лечения или предотвращения воспалительного заболевания, аллергического заболевания, астмы или ХОБЛ.
В настоящем изобретении также предложен способ лечения или предотвращения воспалительного заболевания, аллергического заболевания, астмы или ХОБЛ у млекопитающего или человека, включающий введение указанному млекопитающему или человеку эффективного количества нового соединения (KS534), выделенного из экстракта Pseudolysimachion rotundum var subintegrum, совместно с фармацевтически приемлемым носителем.
Предложенный в настоящем изобретении экстракт согласно настоящему изобретению также может применяться в качестве главного компонента или добавки и вспомогательного агента при получении различных функционального пищевого продукта и пищевого продукта лечебного назначения.
Соответственно, еще одна цель настоящего изобретения заключается в обеспечении функционального пищевого продукта, содержащего терапевтически эффективное количество нового соединения (KS534), выделенного из экстракта Pseudolysimachion rotundum var subintegrum, содержащего активные ингредиенты для предотвращения или облегчения аллергического заболевания, воспалительного заболевания, астмы или хронической обструктивной болезни легких (ХОБЛ).
Термин «функциональный пищевой продукт» в настоящем документе относится к функциональному продукту питания с повышенной функциональностью, например, физической функциональностью или физиологической функциональностью, за счет добавления экстракта согласно настоящему изобретению в стандартный пищевой продукт для предотвращения или ослабления целевых заболеваний у человека или млекопитающего.
Еще одна цель настоящего изобретения заключается в обеспечении пищевого продукта лечебного назначения, содержащего терапевтически эффективное количество нового соединения (KS534), выделенного из экстракта Pseudolysimachion rotundum var subintegrum, совместно с ситологически приемлемой добавкой для предотвращения или облегчения аллергического заболевания, воспалительного заболевания, астмы или хронической обструктивной болезни легких (ХОБЛ).
Термин «пищевой продукт лечебного назначения» в настоящем документе включает «пищевой продукт, содержащий экстракт или соединение(я) согласно настоящему изобретению, не демонстрирующий(ие) специфического направленного эффекта, однако демонстрирующий(ие) общенаправленный эффект в малых количествах в форме добавки или общего количества в форме порошка, гранул, капсул, пилюль, таблеток и т.п.
Термин «ситологически приемлемая добавка» в настоящем документе включает «любое вещество, предполагаемое применение которого приводит или может, как обоснованно ожидается, приводить, прямо или косвенно, к его включению в качестве компонента или другому влиянию на характеристики какого-либо пищевого продукта»; указанные добавки могут быть разделены на три группы в соответствии с происхождением, а именно: (1) химически синтезированная добавка, например, кетоны, глицин, цитрат калия, никотиновая кислота и т.д.; (2) природная добавка, такая как краситель на основе хурмы, экстракт лакрицы, кристаллическая целлюлоза, гуаровая камедь и т.д.; (3) смешанные добавки, такие как L-глутамат натрия, консерванты, красители из каменноугольной смолы и т.д., или различные категории в соответствии с функцией в продукте питания, например, загущающий агент, ускоритель созревания, отбеливающий агент, секвестрант, увлажнитель, антислеживающий агент, осветляющие агенты, отверждающий агент, эмульгатор, стабилизатор, загуститель, основания и кислоты, пенообразующие агенты, питательные вещества, красящий агент, вкусоароматический агент, подсластитель, консервирующий агент, антиоксидант и т.д., хорошо известные в данной области техники или из ранее опубликованных источников (см. «Общий стандарт Кодекса на пищевые добавки» (GSFA, Codex STAN 192-1995) на домашней интернет-странице GSFA: www.codexalimentarius.net/gsfaonline/index.html).
Если вещество добавляют в пищевой продукт для достижения конкретной цели в указанном пищевом продукте, его называют прямой добавкой; косвенные пищевые добавки представляют собой добавки, входящие в состав пищевого продукта в следовых количествах в результате упаковки, хранения или иных манипуляций.
Термин «пищевые продукты лечебного назначения или функциональные пищевые продукты» в настоящем документе могут относиться к пищевому продукту, лечебному напитку, биологически активной добавке и т.д., и могут быть представлены фармацевтической лекарственной формой, такой как порошок, гранулы, таблетки, суспензии, эмульсии, сироп, жевательные таблетки, капсулы, напиток и т.д.; или пищевым продуктом, например, хлебом, рисовыми хлебцами, сухофруктами, конфетами, шоколадом, жевательной резинкой, мороженым, молоком, например, маложирным молоком, молоком с гидролизованной лактозой, козьим молоком, переработанным молоком, молочным продуктом, таким как кисломолочный продукт, масло, концентрированное молоко, молочные сливки, молочный жир, натуральный сыр, плавленый сыр, сухое молоко, молочная сыворотка и т.д., готовым мясным продуктом, например, гамбургером, ветчиной, колбасой, беконом и т.д., готовым яичным продуктом, продуктом из рыбы, например, рыбными котлетами и т.д., лапшой, например, лапшой быстрого приготовления, высушенной лапшой, влажной лапшой, жареной лапшой, нежареной лапшой, желатинизированной сухой лапшой, приготовленной лапшой, замороженной лапшой, пастой и т.д., чайным продуктом, например, чайными пакетами, чайным экстрактом и т.д., оздоровительными напитками, такими как фруктовые напитки, растительные напитки, газированные прохладительные напитки, напитки на основе соевого молока, лактатный напиток, смешанный напиток, и т.д., приправами, такими как соевый соус, паста из соевых бобов, паста из красного перца, черная паста из соевых бобов (ферментированный продукт из соевых бобов, подкрашенных карамелью), чонгукчан (соевые бобы, естественным образом ферментированные В. subtillis), смешанная паста, уксус, соус, кетчуп, карри, заправка и т.д., маргарин, кулинарный жир, пицца и т.д., однако не ограничиваются перечисленными, для предотвращения или ослабления целевого заболевания.
Также вышеописанный экстракт или соединение может быть добавлен в пищевой продукт или напиток для предотвращения или ослабления целевого расстройства. Количество вышеописанного экстракта или соединения(ий) в пищевом продукте или напитке для функционального пищевого продукта или пищевого продукта лечебного назначения обычно может варьироваться от приблизительно 0,01 до 100% по массе относительно общей массы пищевого продукта в составе функционального пищевого продукта. В частности, хотя предпочтительно количество экстракта согласно настоящему изобретению в функциональном пищевом продукте, пищевом продукте лечебного назначения или специальном питательном продукте может варьироваться в соответствии с предусмотренным назначением каждого пищевого продукта, как правило, в качестве добавки предпочтительно используется количество экстракта или соединения(ий) согласно настоящему изобретению в диапазоне от приблизительно 0,01 до 5% для пищевого продукта, такого как лапша и т.п., от 40 до 100% для пищевого продукта лечебного назначения, на 100%) состава пищевого продукта.
При условии, что состав лечебного напитка согласно настоящему изобретению в качестве важнейшего компонента включает вышеописанный экстракт или соединение(ия) в указанной пропорции, какие-либо конкретные ограничения для других жидких компонентов отсутствуют, при этом указанный другой компонент может представлять собой какой-либо подсластитель или природный углевод и т.д., такой как входящие в стандартные напитки. Примером вышеупомянутого природного углевода является моносахарид, такой как глюкоза, фруктоза и т.д.; дисахарид, такой как мальтоза, сахароза и т.д.; стандартный сахар, такой как декстрин, циклодекстрин; и сахарный спирт, такой как ксилит и эритрит и т.п. В качестве отличного от вышеуказанных подсластителей может предпочтительно подходить для применения природный подсластитель, такой как тауматин, экстракт стевии, например, леваудиозид А, глицирризин и др., и синтетический подсластитель, такой как сахарин, аспартам и т.п. Количество вышеописанного природного углевода обычно варьируется от приблизительно 1 до 20 г, предпочтительно от 5 до 12 г на 100 мл предложенного состава напитка.
Отличные от вышеупомянутых компоненты композиции представлены различными питательными веществами, витамином, минеральным веществом или электролитом, синтетическим вкусоароматическим агентом, красящим агентом и улучшителем в случае сыра, шоколада и т.п., пектиновой кислотой и ее солью, альгиновой кислотой и ее солью, органической кислотой, защитный коллоидный клей, агент для контроля pH, стабилизатор, консервант, глицерин, спирт, агент для карбонизации, используемый при получении газированных напитков и т.п. Отличный от указанных выше компонент может быть представлен фруктовым соком для получения натурального фруктового сока, напитка на основе фруктового сока или овощей, при этом указанный компонент может применяться независимо или в составе комбинации. Соотношение компонентов не столь важно, однако обычно варьируется от приблизительно 0 до 20% по массе на 100% предложенной композиции. Примеры добавок к пище, содержащих вышеупомянутый экстракт или соединение, представлены различными пищевыми продуктами, напитками, жевательными резинками, витаминными комплексами, оздоровительными пищевыми продуктами и т.п.
Предложенный(ые) в настоящем изобретении экстракт или соединение(я) согласно настоящему изобретению нетоксичны и, соответственно, не вызывают нежелательных реакций; их применение безопасно.
Специалистам в данной области техники будет понятно, что могут быть осуществлены различные модификации и получены варианты композиций, применения и составов согласно настоящему изобретению без отступления от существа или объема настоящего изобретения.
Настоящее изобретение более конкретным образом описано в представленных ниже примерах. Тем не менее, следует понимать, что настоящее изобретение никоим образом не ограничивается указанными примерами.
Полезные эффекты настоящего изобретения
Согласно описанию предложенное в настоящем изобретении новое соединение (KS534), выделенное из экстракта Pseudolysimachion rotundum var subintegrum subintegrum, демонстрировало мощную противовоспалительную, противоаллергенную, противоастматическую и направленную против ХОБЛ активность путем применения различных тестов in vitro, например, (1) теста на цитотоксичность с использованием линий клеток НТ1080, Н292 и EL4, (2) теста ингибирования экспрессии MUC5AC (олигомерный слизе-/гелеобразующий муцин), индуцируемой ФНО-альфа, (3) люциферазного репортерного анализа NF-каппа B, (4) теста ингибирования активности транскрипционного фактора NF-каппа В; (5) ингибирования экспрессии мРНК целевых генов, таких как ММР-9, MUC5AC и ИЛ-4 путем ингибирования активности NF-каппа В; (6) дозозависимого ингибирующего эффекта на воспроизводство MUC5AC посредством анализа воспроизводства белка MUC5AC; а также тестов in vivo, например, (7) эффекта, заключающегося в уменьшении числа воспалительных клеток, таких как эозинофилы, с применением модели на сенсибилизированных/стимулированных OVA (овальбумином) мышах, (8) теста ингибирования высвобождения IgE, воспалительных цитокинов, таких как ИЛ-4, ИЛ-5, ИЛ-13 и т.д. в жидкости бронхоальвеолярного лаважа и инвазии воспалительных клеток, а также подавления гиперреактивности дыхательных путей и гиперплазии бокаловидных клеток, (9) теста ингибирования с применением модели ХОБЛ на животных (мыши C57B/6N) пролиферации воспалительных клеток в жидкости бронхоальвеолярного лаважа, ингибирования воспроизводства АФК (активных форм кислорода) и активности эластазы нейтрофилов, эффекта снижения уровней ИЛ-6, ФНО-альфа и инфильтрирующих воспалительных клеток, и т.п.
Краткое описание чертежей
Вышеуказанные и другие цели, признаки и другие преимущества настоящего изобретения будут более понятны после изучения приведенного ниже подробного описания в сочетании с прилагаемыми чертежами, где;
На фиг. 1 представлены результаты корреляционной спектроскопии (1Н-1Н COSY) и гетероядерной многоквантовой корреляционной спектроскопии (НМВС) соединения KS534;
На фиг. 2 показан эффект экспериментального образца на экспрессию мРНК MUC5AC по оценке с применением кПЦР-РВ;
На фиг. 3 показан ингибирующий эффект экспериментального образца на индуцированную ФНО-альфа активность NF-каппа В по оценке с применением люциферазного репортерного анализа (статистический анализ выполняли с применением t-критерия Стьюдента; Р - значение (**, <0,01) считали указывающим на статистическую значимость);
На фиг. 4 показан ингибирующий эффект экспериментального образца на уровень экспрессии белка MUC5AC по оценке с применением модифицированного способа ИФА ELISA (статистический анализ выполняли с применением t-критерия Стьюдента и Р-значение (**, <0,01 и ***, <0,001) считали указывающим на статистическую значимость);
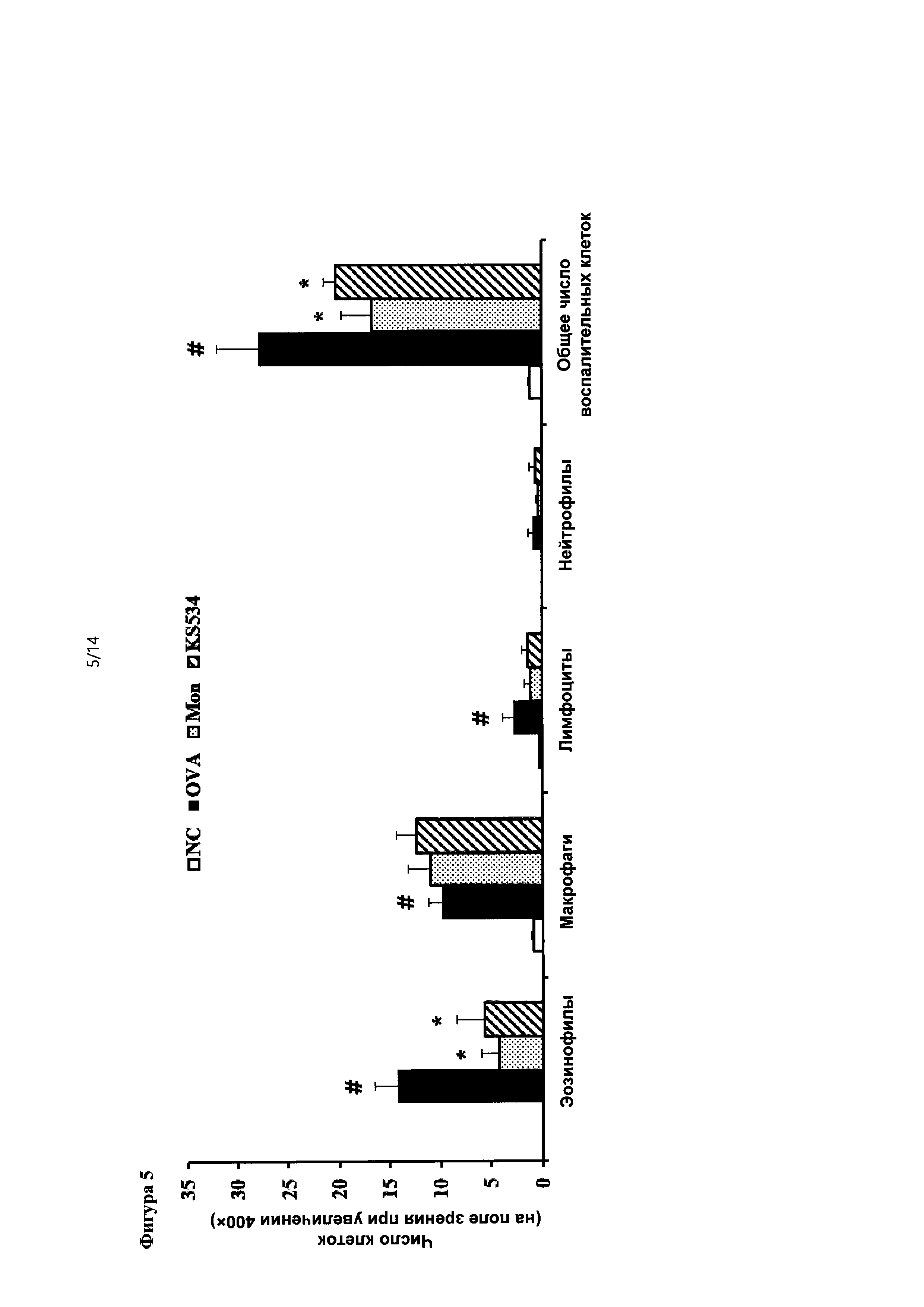
На фиг. 5 показан эффект предложенного в настоящем изобретении соединения на число воспалительных клеток в ЖБАЛ;
На фиг. 6 показан эффект предложенного в настоящем изобретении соединения на число воспалительных цитокинов в ЖБАЛ;
На фиг. 7 показан эффект предложенного в настоящем изобретении соединения на общее содержание IgE и уровень OVA-специфического IgE в сыворотке;
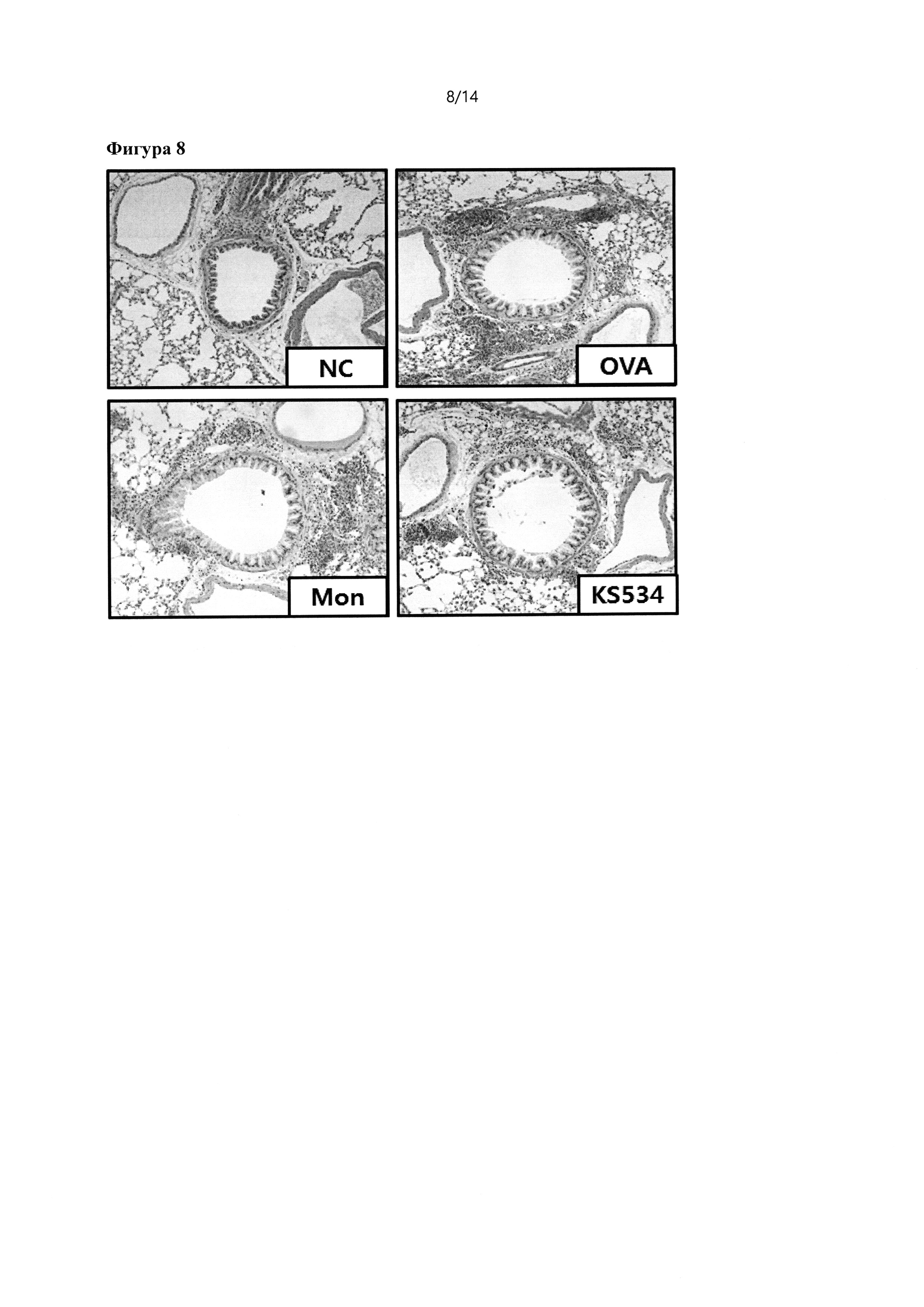
На фиг. 8 показан эффект предложенного в настоящем изобретении соединения на воспалительный ответ в клетках легочной ткани по оценке с применением гистологического исследования;
На фиг. 9 показан эффект предложенного в настоящем изобретении соединения на гиперсекрецию слизи в клетках легочной ткани по оценке с применением гистологического исследования;
На фиг. 10 показан эффект предложенного в настоящем изобретении соединения на количество воспалительных клеток в ЖБАЛ;
На фиг. 11 показан эффект предложенного в настоящем изобретении соединения на воспроизводство АФК в ЖБАЛ;
На фиг. 12 показан эффект предложенного в настоящем изобретении соединения на уровни содержимого ЖБАЛ и активность эластазы в ЖБАЛ;
На фиг. 13 представлен эффект предложенного в настоящем изобретении соединения на уровень ИЛ-6 и ФНО-альфа в ЖБАЛ;
На фиг. 14 показан эффект предложенного в настоящем изобретении соединения на воспалительный ответ в клетках легочной ткани по оценке с применением гистологического исследования;
Лучший вариант осуществления изобретения
Специалистам в данной области техники будет понятно, что могут быть осуществлены различные модификации и получены варианты композиций, применения и составов согласно настоящему изобретению без отступления от существа или объема настоящего изобретения.
Настоящее изобретение более конкретным образом описано в представленных ниже примерах. Тем не менее, следует понимать, что настоящее изобретение никоим образом не ограничивается указанными примерами.
ПРИМЕРЫ
Приведенные ниже сравнительный пример, примеры и экспериментальные примеры предназначены для дополнительной иллюстрации настоящего изобретения без ограничения его объема.
Сравнительный пример 1. Аналитический аппарат
Точку плавления определяли без коррекции с помощью аппарата для микроопределения точки плавления Кофлера (Kofler); оптическое вращение с применением поляриметра Jasco Р-1020; УФ-данные с применением спектрометра видимого и УФ-диапазона UV-VIS 2450; Фурье-ИК-спектры с применением Jasco FT/IR-4200; ЯМР-спектры с применением фурье-спектрометра для ЯМР Varian UNITY 400 МГц с применением ТМС в качестве внутреннего стандарта; масс-спектрометрию высокого разрешения с ионизацией электрораспылением (HRESIMS) с применением квадрупольного микромасс-спектрометра Waters Q-TOF Premier; ВЭЖХ-анализ в эксперименте проводили в системе ВЭЖХ Gilson с применением детектора видимого и УФ-диапазона UV/VIS-155 и насоса 305.
Пример 1. Получение нового соединения (KS 534) из Pseudolysimachion rotundum var subintegrum
1-1. Получение неочищенного экстракта
2,0 кг высушенного Pseudolysimachion rotundum var subintegrum (культивация: 244, Соимьян, Ымсон, провинция Чхунчхон-Пукто, Корея, в соответствии с надлежащей сельскохозяйственной практикой (GAP), KRIBB 0020697, банк растительных экстрактов Корейского исследовательского института биологических наук и биотехнологии (KRIBB), Тэджон, Корея) измельчали и смешивали с 10 л 40% этанола. Смесь перемешивали при комнатной температуре в течение 24 часов и троекратно экстрагировали путем рефлюкс-экстракции при 78°C в течение 12 часов для сбора фильтрата. Экстракт фильтровали через фильтровальную бумагу для удаления дебриса. Собранный фильтрат концентрировали с помощью ротационного испарителя (EYELA, N-2100, Япония) при 55-65°C под пониженным давлением и высушивали в аппарате для замораживания-высушивания с получением 198,7 г высушенного неочищенного экстракта
1-2. Получение очищенного экстракта
20 г высушенного неочищенного экстракта растворяли в смешанном растворителе (25% МеОН-вода) и подвергали дополнительному очищению с применением препаративной хроматографии с обращенной фазой (Zeoprep С18, 75 мкм, 200×250 мм, Zeochem, Луисвилль, США). Элюировавшие фракции (f1-f4) собирали и концентрировали под вакуумом. 5,0 г фракции f2 загружали на колонку RP С-18 (Zeoprep С18, 20×250 мм, 10 мкм, Zeochem, Луисвилль, США) для жидкостной хроматографии среднего давления (ЖХСД): и элюировали растворителем (раствор МеОН-вода = 2:8, 3:7, 4:6, 10:0) для выделения 5 субфракций, f2a, f2b, f2c, f2d и f2e.
1-3. Получение нового соединения KS534
0,8 г субфракции (f2c) подвергали полупрепаративной ВЭЖХ (Synergy Polar-RP 4 мкм, 21,2×250 мм, Phenomenex, Torrance, Калифорния, США, 22% MeCN в H2O) с получением светло-коричневого порошка нового иридоидного соединения (3R,5S,5aS,6R,7S,8R,8aS)-8-хлор-8а-гидрокси-5-(2-гидрокси-ацетокси)гексагидро-1Н-3,6-метанциклопента[е][1,3]диоксепин-7-ил-3,4-дигидроксибензоата (KS534; C22H26ClO13), демонстрировавшего физико-химические свойства:
[α]20D - 30,0° (с 0,2, МеОН).
Масс-спектрометрия высокого разрешения с ионизацией электроспреем (HRESIMS) (наблюдаемое отношение м/з: 533,1035 [М-Н]-): кластер квазимолекулярного иона 3:1
ИК-спектр: 3412 см-1 (гидроксильная группа); 1692 см-1, (карбонил α,β-ненасыщенного сложного эфира)
ЯМР-спектры1H и13С: таблица 1
1H-1Н COSY-спектр (фиг. 1)
NOESY-спектр (фиг. 1)
[Таблица 1]


Экспериментальный пример 1. Предварительное определение цитотоксичности.
Для определения цитотоксичности предложенного в настоящем изобретении соединения проводили следующий предварительный тест с применением способа, раскрытого в опубликованных источниках (Shiyama et al., Talanta, 1997, 44, 1299-1305.; Tominaga et al., Anal. Commun., 1999, 36, 47-50).
1-1. Получение линии клеток и культуры клеток
НТ1080 (CRL-12012), Н292 (CRL-1848) и клетки EL4 мыши (TIB-39) приобретали у компании «Американская коллекция типовых культур» (American Type Culture Collection).
Клетки НТ1080 (CRL-12012) и клетки EL4 мыши культивировали на среде DMEM (SB30243.01, модифицированная по способу Дульбекко среда Игла; DMEM, HyClone) с добавлением 10% ФБС (фетальная бычья сыворотка; Gibco) и антибиотика (100 единиц/мл пенициллина + 100 единиц/мл стрептомицина). Клетки Н292 культивировали в среде RPMI (SH30027.01, RPMI 1640, Gibco) с добавлением 10% ФБС и антибиотика. Клетки культивировали в условиях увлажненной атмосферы с 5% CO2 при 37°С. ФМА (Р8139, форбол-12-миристат-13-ацетат) приобретали у компании (Sigma Chemical Co., Сент-Луис, Миссури), а ФНО-α у компании (300-01А, PeproTech Inc., Нью-Джерси, США) для применения в эксперименте.
1-2. Оценка цитотоксичности в клетках Н292
Раковые клетки слизистой оболочки легкого человека линии Н292 суспендировали в среде RPMI с добавлением 10% ФБС, в концентрации 5×104 клеток/мл, и 100 мкл указанной суспензии инокулировали 96-лучночные планшеты для прикрепления клеток к планшетам в течение 12 часов. Их обрабатывали различными концентрациями экспериментального образца (соединения KS 534) и культивировали в течение 24 часов. По 10 мкл раствора ССК-8 смешивали с 90 мкл среды и добавляли в каждую лунку по 100 мкл указанного раствора. После проведения реакции на протяжении периода от 30 минут до 4 часов определяли поглощение в растворе при 570 нм. Жизнеспособность клеток рассчитывали в соответствии с приведенной ниже математической формулой 1 на основании данных группы отрицательного контроля, обработанной 0,2% ДМСО; результат представлен в таблице 2.
Математическая формула 1
Жизнеспособность клеток (%) = OD 570 нм (экспериментальная группа) / OD 570 нм (группа отрицательного контроля)×100
В результате, как показано в таблице 2, было подтверждено, что соединение KS 534 не проявляло цитотоксичности в клетках Н292 в концентрации менее 20 мкМ.

Экспериментальный пример 2. Ингибирование экспрессии MUC5AC.
Для определения ингибиторного эффекта на экспрессию MUC5AC, индуцируемую ФНО-альфа в клетках линии Н292, проводили следующий тест:
2-1. Определение уровня экспрессии мРНК
Выделение тотальной РНК, синтез кДНК и количественную ПЦР в реальном времени осуществляли с применением способа, раскрытого в опубликованных источниках (Kim et al., J. Cell. Biochem. 2008, 104, 1906-1917).
В целом, тотальную РНК выделяли с применением реагента Тризол (TRIzol, 155596-026, Life Technologies) и первую нить кДНК синтезировали с применением фермента (обратная транскриптаза Omniscript, 205113, Qiagen, Калифорния). Амплификацию путем количественной ПЦР в реальном времени выполняли с применением аппарата 1 (термоциклер S1000, Bio-rad, США) и аппарата 2 (2× мастер-микс Greenstar, Bioneer, Корея) в соответствии с инструкциями производителя.
2-2. Эффект на экспрессию MUC5AC
Для определения ингибиторного эффекта на экспрессию MUC5AC, индуцируемую ФНО-альфа в клетках линии Н292, проводили следующий тест.
Ингибиторный эффект соединения KS534 на экспрессию мРНК MUC5AC определяли для верификации терапевтической или профилактической активности в отношении воспалительного заболевания, такого как ХОБЛ.
В частности, воспроизводимый индуцированный ФНО-альфа уровень MUC5AC определяли посредством полимеразной цепной реакции в реальном времени (ПЦР в реальном времени), количественной полимеразной цепной реакции (кПЦР) и иммунологического анализа на MUC5AC. Клетками Н292 инокулировали 48-луночные планшеты в концентрации 2×104 клеток на лунку для прикрепления в течение 24 часов и культуральную среду заменяли на новую содержащую 0,1% ФБС для культивирования в течение 24 часов. Обрабатывали 10 мкМ KS-534 в течение 2 часов и 20 нг/мл ФНО-альфа с культивированием в течение 12 часов.
Тотальную РНК экстрагировали с применением Тризола В (Invitrogen) и синтезировали кДНК с применением набора для обратной транскрипции Omniscript (Qiagen, GmbH, Хильден, Германия) после количественного определения. Синтезированную кДНК смешивали с матрицей, праймерами для MUC5AC и GAPDH, как показано в таблице 3, соответственно, и проводили ПЦР с применением мастер-микса для ПЦР (PCR Master Mix, Bioneer, Корея) следующим образом: 5 минут при 94°C, 1 цикл для предварительной денатурации; 30 секунд при 95°C, 45 секунд при 60°C и 45 секунд при 72°C, 30 циклов для денатурации; 10 минут при 72°C, 1 цикл для конечной элонгации.

В результате было подтверждено, что количество MUC5AC увеличивалось в контрольной группе, получавшей лечение ФНО-альфа, а уровень экспрессии мРНК MUC5AC в экспериментальной группе, получавшей лечение 10 мкМ, снижался на 58,47% (показатель ингибирования KS-534 для экспрессии MUC5AC: 41,52%), как видно из таблицы 4 и на фиг. 2.
Соответственно, было подтверждено, что соединение KS-534 ингибирует генную экспрессию MUC5AC и подходит для лечения ХОБЛ.

Экспериментальный пример 3. Ингибирование активности NF-каппа В.
Для определения ингибиторного эффекта на активность NF-каппа B проводили следующий тест:
3-1. Люциферазный репортерный анализ NF-каппа B
Люциферазный репортерный анализ NF-каппа B выполняли с использованием следующей процедуры, раскрытой в опубликованных источниках (Pulin Che et al., Assay Drug Dev. Technol, 2012, 10, 61-68).
Для получения стабильных клеток для люциферазного репортерного анализа NF-каппа B элемент ответа NF-каппа B клонировали в вектор (pGL4.32вектор, Е849А, Promega) в соответствии с протоколом производителя и инфицировали им клетки (клетки Н292, CRL-1848, АТСС) с применением липофектамина 2000 (11668-019, Invitrogen). Инфицированные клетки отбирали с применением гигромицина (400 мкг/мл) в течение 2 недель; колонии клонировали индивидуальным образом и размножали. Клетки переносили в 96-луночные планшеты в концентрации 5×103 клеток/лунку в течение 24 часов. Предварительно обрабатывали экспериментальным образцом в заранее заданной концентрации, а также 20 нг/мл ФНО-альфа в течение 12 часов. Активность фермента люцифераза определяли с применением набора Е6110 (набор для люциферазного анализа OneGlo Luciferase Assay kit, Promega); в качестве основы для контроля использовали ДМСО.
3-2. Ингибиторный эффект на активацию транскрипционного фактора NF-каппа B
Сообщалось, что ФНО-альфа активирует транскрипционный фактор NF-каппа В, индуцируя экспрессию MUC5AC (Busse, P.J. et al., J. Allergy Clin. Immun., 2005, 116, 1256-1263.; Smirnova, M. G. et al, Cytokine. 2000, 12, 1732-1736).
На основании ингибиторного эффекта соединения KS-534 на экспрессию MUC5AC авторы настоящего изобретения провели исследования для подтверждения ингибирования активности транскрипционного фактора NF-каппа B в промоторе MUC5AC соединением KS-534.
Перед проведением описанного ниже эксперимента получали стабильно экспрессируемые клетки Н292, нормальные клетки эпителия бронхов человека, содержащие вектор с репортером люциферазы pGL4.32 (luc2P/NF-κB-RE/Hygro, Promega Company). Клетки суспендировали в содержащей 10% среде DMEM (Hyclone Company) в концентрации 5×104 клеток/мл и по 100 мкл суспензии клеток высевали на 96-луночные планшеты для прикрепления в течение 12 часов. Среду заменяли на новую содержащую 0,1%) ФБС среду для культивирования в течение 12 часов; обрабатывали 10 мкМ KS-534 в течение 2 часов. Обрабатывали 20 нг/мл ФНО-альфа и культивировали в течение 12 часов. Степень активации люциферазы определяли с применением системы люциферазного анализа One-glow (Promega Company). После удаления всей культуральной среды из лунок планшета, планшет двукратно промывали раствором ФСБ и добавляли в каждую лунку по 60 мкл пассивного буфера для лизиса (ПБЛ) для лизирования клеток в течение 30 минут. По 50 мкл раствора лизированных клеток переносили в новые 96-луночные планшеты и добавляли по 50 мкл реагента LAR II, содержащего субстрат люциферазы светлячков. Люминесценцию измеряли с помощью люминометра для микропланшетов LB 96V (компания EG&G Berthold) в течение 0,5 секунд; результат представлен в таблице 5 и на фиг. 3.

В результате было подтверждено, что в экспериментальной группе, получавшей 10 мкМ KS-534, наблюдался мощный ингибиторный эффект на активность, составлявшую 63,35% (показатель ингибирования KS-534 - 36,65%) относительно активности NF-каппа B, индуцируемой ФНО-альфа (100%).
Соответственно, было подтверждено, что соединение KS-534 значимо ингибировало активность транскрипционного фактора NF-каппа В.
Экспериментальный пример 4. Ингибирование воспроизводства белка MUC5AC.
Для определения ингибиторного эффекта на воспроизводство белка MUC5AC, проводили следующий тест с применением способа, раскрытого в опубликованных источниках (Sikder, MA. et al., Phytother. Res., 2014, 28, 62-68)
4-1. Эффект ингибирования воспроизводства белка MUC5AC
Для определения терапевтической активности в отношении воспалительного заболевания, такого как ХОБЛ, следующим образом определяли ингибиторный эффект на высвобождение MUC5AC:
Для иммунологического анализа воспроизводства MUC5AC, по 50 мкл собранного согласно экспериментальному примеру 3 супернатанта распределяли в 96-луночном планшете и высушивали в термостате при 50°С.
После промывания раствором ФСБ с 1% БСА добавляли антитело к MUC5AC (ab3649, Abcam Со.) для проведения реакции при комнатной температуре в течение 1 часа; затем добавляли вторичное антитело для проведения реакции в течение 1 часа. После повторного промывания добавляли раствор 3,3',5,5'-тетраметилбензидинпериксида (54827-17-7, Sigma-Aldrich) для проведения реакции в течение 20 минут. После остановки реакции добавлением раствора серной кислоты определяли поглощение с помощью ридера для микропланшетов VERSAmax (SMP500-14915, Molecular Devices, США) при 450 нм (Sikder, М.A. et al., Phytother. Res., 2014, 28, 62-68; Takeyama, K. et al. Proc. Natl. Acad. Sci. U.S.A., 1999, 96, 3081-3086). Результат представлен в таблице 6 и на фиг. 4.
В результате было подтверждено, что секретируемое количество MUC5AC в группе, получавшей ФНО-альфа, значимо увеличивалась, а в экспериментальной группе, получавшей лечение 2,5, 5 и 10 мкм KS-534, наблюдался мощный ингибиторный эффект, со снижением до 93,38, 78,27 и 64,77% (показатели ингибирования KS-534: 6,62, 21,73 и 35,23%) воспроизводства MUC5AC, относительно секретируемого количества MUC5AC в группе, получавшей ФНО-альфа (100%).

Экспериментальный пример 5. Противоастматическая активность в модели индуцированной астмы на животных.
Для определения противоастматической активности экспериментального образца в модели индуцированной астмы на животных проводили следующий тест с применением способа, раскрытого в опубликованных источниках (Shin, I. S. et al., Food Chem. Toxicol, 2013, 62, 506-513)
5-1. Сенсибилизация животных и стимуляция дыхательных путей
Свободных от специфической патогенной микрофлоры (СПФ) самок мышей BALB/c (с массой тела приблизительно 20 г) возрастом 6 недель, прошедших рутинный серологический скрининг на релевантные респираторные патогены, приобретали у компании Samtako Со. (Сеул, Корея) и акклиматизировали в экспериментальной среде в контролируемых условиях с температурой 22±2°С и относительной влажностью 55±15°С, при светотемновом цикле в течение 1 недели до эксперимента.
Вкратце, мышей сенсибилизировали путем внутрибрюшинной инъекции 20 мкг OVA (овальбумина; А5503, Sigma, Сент-Луис, Миссури), эмульгированного в 2 мг гидроксида алюминия (А8222, Sigma-Aldrich, Миссури, США) в 200 мкл ФСБ-буфера (pH 7,4), один раз в две недели. Мышей стимулировали введением OVA через дыхательные пути (1% в ФСБ) в течение 30 минут с применением ультразвукового небулайзера (NE-U12; Omron Corp., Токио, Япония) с 21-го по 23-й день после начальной сенсибилизации. Через 24 ч после введения антигена оценивали гиперреактивность дыхательных путей; через 48 ч после последней стимуляции мышей умерщвляли. Мышей умерщвляли введением сверхдозы пентобарбитала (50 мг/кг, Entobal®, Hanil, Корея) через 48 ч после последней стимуляции, и выполняли трахеотомию. После вливания 1,4 мл физиологического солевого раствора (ФСР) в легкие получали жидкость бронхоальвеолярного лаважа (ЖБАЛ) путем троекратной аспирации через канюлированную трахею.
Указанные группы разделяли на несколько групп, а именно: (а) нормальная контрольная группа (NC): группы, получавшие или не получавшие OVA; (b) группа с индуцированной астмой (OVA): группы, получавшие OVA для индуцирования астмы; и (с) группа сравнения: группы, получавшие лечение - положительная контрольная группа (М30, монтелукаст; 30 мг/кг, п/о, Sigma-Aldrich Co. Ltd., SML-0101 + OVA) и (d) получающая экспериментальный образец группа: группы, получавшие лечение соединением KS534 (30 мг/кг, п/о, Sigma-Aldrich Co. Ltd., SML-0101 + OVA).
Экспериментальная группа состояла из 7 мышей для каждой группы; экспериментальный образец в различной концентрации вводили мышам перорально с 21-го по 23-й день после первого введения OVA.
Все полученные в различных экспериментах результаты регистрировали как среднее ± SD (стандартное отклонение); сравнение между всеми группами осуществляли с применением однофакторного дисперсионного анализа ANOVA в программе SPSS 10.0. Статистическую значимость различий между всеми группами определяли в соответствии с апостериорным критерием Даннетта для множественных сравнений). Результат выражали через P-значения: значения <0,05 (*) считали соответствующими статистической значимости.
5-2. Выделение ЖБАЛ и определение числа иммуноцитов
Для определения уровня воспалительных клеток с применением центрифуги выделяли и хранили в холодильной камере супернатант жидкости бронхоальвеолярного лаважа (ЖБАЛ), полученного от каждой мыши.
ЖБАЛ наносили на предметное стекло и центрифугировали для фиксации клеток на стекле с применением цитоспиновой центрифуги (Cyto12.5 + clip5, Hanil Science Industrial, Корея). Клетки окрашивали реагентами Diff-Quick® (Sysmex, Кат. №38721, Швейцария) в соответствии с инструкциями производителя и подсчитывали число воспалительных клеток в каждом образец под микроскопом (×400).
Как показано на фиг. 5, общее число эозинофилов и воспалительных клеток в контрольной группе, которой ингаляционно вводили OVA, как в группе с индуцированной астмой (OVA), значимо увеличивалась по сравнению со значениями в не получающей OVA группе, как в нормальной контрольной группе (NC).
Общее число эозинофилов и воспалительных клеток в получавшей экспериментальный образец группе, в которой перорально вводили экспериментальный образец в различной концентрации, был значимо понижен.
5-3. Анализ уровня цитокинов в ЖБАЛ
Для подтверждения ингибирующего эффекта экспериментальных образцов на уровень цитокинов Th2 (ИЛ-4, ИЛ-5 и ИЛ-13) в жидкости бронхоальвеолярного лаважа (ЖБАЛ) определяли уровень цитокинов Th2 (ИЛ-4, ИЛ-5 и ИЛ-13) в жидкости бронхоальвеолярного лаважа (ЖБАЛ) с применением набора для ИФА ELISA (VersaMax, Molecular Devices, США) для проведения специфических реакций с каждым цитокином в соответствии с указаниями производителя.
Как показано на фиг. 6, уровень цитокинов Th2 (ИЛ-4, ИЛ-5 и ИЛ-13) в контрольной группе, получавшей OVA, как в группе с индуцированной астмой (OVA), значимо увеличивался по сравнению с уровнями в не получавшей OVA группе, как в нормальной контрольной группе (NC).
Повышенный уровень цитокинов Тh2 (ИЛ-4, ИЛ-5 и ИЛ-13) в группе положительного контроля, получавшей лечение монтелукастом (МО, 30 мг/кг), а также в получавшей экспериментальный образец группе, в которой перорально вводили экспериментальные образцы (KS534) в различных концентрациях, был значимо понижен.
5-4. Эффект в отношении уровней IgE и OVA-специфического IgE в сыворотке крови
Для подтверждения ингибирующего эффекта экспериментальных образцов полученных согласно описанию в разделе примеров, на уровень IgE и OVA-специфического IgE в сыворотке крови, проводили описанный ниже ИФА-тест ELISA с применением способа, раскрытого в опубликованных источниках (Kay, А.В., N. Engl. J. Med., 2001, 344, 30-37).
Сыворотку крови, выделенную из хвостовой вены согласно описанию выше, собирали для измерения уровня IgE и OVA-специфического IgE в сыворотке крови.
Указанную сыворотку крови добавляли в 96-луночные планшеты (планшет для ИФА ELISA, 2592, Costa, США) и покрывали 0,1 М буферным раствором NaHCO3 (pH 8,3), содержащим 20 мкг/мл OVA (Sigma, Миссури, США) при 4°C в течение 16 часов. После ингибирования неспецифической реакции с применением ФСБ, содержащего 1% бычий сывороточный альбумин (Р2007, Biosesang, Корея), сыворотку для тестирования разбавляли в пропорции 1:400 и проводили реакцию в течение 2 часов при комнатной температуре. После промывания ФСБ, содержащим 0,05% Tween 20, проводили реакцию сыворотки с разбавленным (×300) моноклональным антителом против IgE мыши (МСА419, Serotec, Оксфорд, Великобритания) в течение 2 часов и с разбавленным (×4000) конъюгированным с пероксидазой хрена поликлональным антителом козы против IgG крысы (432402, Biolegend, США) в течение 1 часа при комнатной температуре. После промывания раствор окрашивали субстратом 3,3',5,5'-тетраметилбензидином (432402, Biolegend Ins, США) и реакцию останавливали добавлением 2Н H2SO4 для определения поглощения с применением спектроскопии (Versamax, Molecular Devices, США) при 450 нм.
Как показано на фиг. 7, уровень IgE и OVA-специфического IgE в сыворотке крови в контрольной группе, получавшей OVA, как в группе с индуцированной астмой (OVA), значимо увеличивался, тогда как указанные уровни в группе положительного контроля, получавшей лечение монтелукастом (МО), а также в получавшей экспериментальный образец группе, в которой перорально вводили экспериментальные образцы (KS-534) в различных концентрациях, были значимо понижены.
5-4. Гистологическое исследование легких
Для подтверждения противоастматического эффекта экспериментальных образцов, получение которых описано в разделе примеров, проводили описанный ниже гистопатологический анализ бронхо-альвеолярной ткани с применением способа, раскрытого в опубликованных источниках (Kwak YG. et al., J. Clin. Invest., 2003, 111, 1083-1092).
Полученные легочные ткани мышей BALB/c, которым не проводили бронхоальвеолярный лаваж, фиксировали в течение 24 ч в 10% нейтральном буферном растворе формалина. После заливки в эпоксидную смолу получали срезы толщиной 4 мкм, ткань окрашивали раствором ГЭ (гематоксилин; Sigma MHS-16, и эозин, Sigma НТ110-I-32) для выявления воспаления легочной ткани, и периодной кислотой Schiff (PAS, IMEB Inc., США) для выявления секреции слизи в легочной ткани. Патологические изменения легочной ткани определяли посредством оптической микроскопии.
Как показано на фиг. 8, в контрольной группе, получавшей OVA, и в группе с индуцированной астмой (OVA) в бронхиолярном окружении обнаруживались многие воспалительные клетки, в том числе эозинофилы, и наблюдалась гиперплазия эпителиальных клеток, а также гипертрофия мышцы трахеи; тогда как в группе положительного контроля, получавшей лечение монтелукастом (МО, 30 мг/кг), а также в получающей экспериментальный образец группе, где перорально вводились экспериментальные образцы (KS 534) в различных концентрациях, инвазия воспалительных клеток значимо уменьшалась.
Как показано на фиг. 9, секреция слизи бокаловидными клетками бронхиального эпителия в легочной ткани резко повышалась в контрольной группе, получавшей OVA, как в группе с индуцированной астмой (OVA), тогда как секреция слизи бокаловидными бронхиальными эпителиальными клетками в легочной ткани значимо снижалась в группе положительного контроля, получавшей лечение монтелукастом (МО, 30 мг/кг) а также в получающей экспериментальный образец группе, где перорально вводились экспериментальные образцы (KS 534) в различных концентрациях.
В целом, предложенное в настоящем изобретении соединение KS534 может предотвращать или лечить различные заболевания, такие как астма, вызванная OVA. Предложенное в настоящем изобретении соединение KS534 эффективно ингибировало инфильтрацию воспалительными клетками, в том числе эозинофилию, воспроизводство ИЛ-4,5,13 Th2-типа, а также снижало уровень IgE и воспроизводство OVA-специфического IgE, что было подтверждено гистопатологическим анализом бронхоальвеолярной ткани.
Наконец, было подтверждено, что предложенное в настоящем изобретении соединение KS534 эффективно смягчало основные синдромы астмы, такие как эозинофилия, воспаление легких, гиперсекреция слизи, а также ингибировало иммунный ответ; соответственно, оно может подходить для применения в качестве мощного природного агента для лечения астмы, поскольку отличается эффективностью, аналогичной или эквивалентной стандартному доступному лекарственному средству монтелукасту.
Экспериментальный пример 6. Тестирование в модели на животных
Для определения направленного против ХОБЛ эффекта предложенных в настоящем изобретении соединений в модели ХОБЛ на животных проводили следующий тест с использованием мышей с индуцированной ХОБЛ согласно описанию в опубликованной источнике (Bhavsar, Т. et al., J. Chronic Obstr. Pulm. Dis., 2008, 3, 477-481).
6-1. Экспериментальное животное
Свободных от специфической патогенной микрофлоры самцов мышей C57BL/6N (приблизительно 22-24 г) возрастом 6 недель, прошедших рутинный серологический скрининг на релевантные респираторные патогены, приобретали у Koatech Со. (www.koatech.co.kr, Сеул, Корея) и содержали в условиях свободного доступа к пище (не содержащий антибиотиков корм от Samyang Oil & Feed Corp., Корея) и воде в помещении для разведения при контролируемых температуре (22±2°С) и влажности (55±15%) с 12-часовым светотемновым циклом, и позволяли акклиматизироваться к экспериментальным условиям в течение 1 недели.
6-2. Лекарственное средство и его введение
(1) Экспериментальный образец
2 вида экспериментальных образцов, а именно, KS534 (15 и 30 мг/кг), Даксас (основной ингредиент: Рофлумиласт, 10 мг/кг) растворяли в 0,5% карбоксиметилцеллюлозе натрия (С9481, Sigma-Aldrich, США) и использовали в качестве экспериментальных образцов.
(2) Введение
KS534 и рофлумиласт (ROF II-492, HETERO, Индия) вводили мышам перорально за 1 час до интратрахеального вливания (и/т).
6-3. Подготовка модели ХОБЛ на мышах
(1) Стандартная сигарета
Эталонные сигареты Кентукки 3R4F (Университет Калифорнии, США) применяли в качестве стандартных сигарет для получения сигаретного дыма. Сигарету, содержащую 9,4 мг смол, 11 мг ТРМ (общая масса частиц) и 12 мг монооксида углерода на штуку, использовали после доведения до температуры 22±1°C и влажности 60±2% после вскрытия упаковки в течение 48~72 ч.
(2) Процедура
Воздействие сигаретным дымом осуществляли с применением генератора сигаретного дыма (DBL Co. Ltd., www.dhbiolink.com, Корея). Мышей разделяли на пять групп: нормальные (NC), ХОБЛ (сигаретный дым с интраназальным закапыванием ЛПС), Rof (10 мг/кг рофлумиласта, перорально+сигаретный дым с интраназальным закапыванием ЛПС); и KS534-15 и 30 (15 мг/кг и 30 мг/кг KS534, перорально + сигаретный дым с закапыванием ЛПС, соответственно). Воздействие сигаретным дымом (одна затяжка в минуту, объем затяжки 35 мл в течение 2 с, каждые 60 секунд, 8 сигарет в день) осуществляли с применением генератора сигаретного дыма. Мышей подвергали воздействию сигаретного дыма в течение 1 часа в камере для обработки (50 см×30 см×30 см) в течение 3 дней. Рофлумиласт и пискрозид C вводили мышам через желудочный зонд за 1 ч до воздействия сигаретным дымом в течение 3 дней. ЛПС закапывали интраназально (10 мкг, растворенные в 50 мкл дистиллированной воды) под анестезией за 1 ч после последнего воздействия сигаретным дымом. После завершения эксперимента от каждой крысы получали кровь, ЖБАЛ и пневмоциты и собирали для тестирования.
6-4. Выделение ЖБАЛ и определение количества иммуноцитов
После завершения эксперимента крыс анестезировали Золетилом 50 (3VX9, Virbac, Франция, п/о), и извлекали кровь через хвостовые вены. Для выделения ЖБАЛ из легких бронх правого легкого лигировали шовным материалом и затем проводили трахеостомию. Внутривенный катетер (16 GA, 3S-Cath, Dukwoo, Корея) вводили в бронх, и бронх и катетер (16 GA, 3S-Cath, Dukwoo, Корея) фиксировали шовным материалом. Присоединяли инъектор, содержащий 1 мл ДФСБ 0,7 (забуференный фосфатом солевой раствор по Дульбекко, Invitrogen, США) и ДФСБ троекратно прогоняли для извлечения ЖБАЛ. Извлекали лигированное шовным материалом правое легкое, фиксировали 10% нейтральным раствором формалина, и оставшуюся ткань легкого сохраняли в холодильной камере при -70°С. Выделенный ЖБАЛ центрифугировали в течение 15 минут при 1500 об/мин для получения клеточного осадка, и супернатант сохраняли в холодильной камере при -70°С для анализа на цитокины. Клеточный осадок суспендировали в ДФСБ, и клетки присоединяли к предметным стеклам с применением цитоцентрифуги (CS03270047, Hanil, Корея). Выполняли окрашивание Diff-Quik (ZS1003, Sysmex, Япония) и исследовали клетки посредством оптической микроскопии (DM1000, Leica, Германия) для подсчета числа иммуноцитов в каждом экспериментальном образце.
Как показано на фиг.10, характерный повышенный уровень нейтрофилов в ЖБАЛ наблюдали в группе с индуцированной ХОБЛ. В получающей лекарственное средство контрольной группе, получающей лечение рофлумиластом, наблюдался пониженный приблизительно на 21,1% уровень нейтрофилов по сравнению с группой с индуцированной ХОБЛ. При этом в группах, получавших лечение 15 мг/кг и 30 мг/кг KS534, наблюдался значительно сниженный, на 26,3% и 25,7%, соответственно, уровень нейтрофилов по сравнению с группой с индуцированной ХОБЛ.
6-5. Эффект в отношении АФК и активности эластазы нейтрофилов в ЖБАЛ
Уровень АФК в полученном от мышей ЖБАЛ определяли с применением DCF-DA (дихлордигидрофлуоресцеиндиацетат, 35854, Sigma-Aldrich, США) и конечную концентрацию DCF-DA доводили до 20 мкМ в 200 мкл для инкубации в течение 30 минут. Флуоресценцию определяли аппаратным способом (Flexstation3, Molecular Device, США). Активность эластазы нейтрофилов в ЖБАЛ определяли с применением N-сукцинил-(Alа)3-п-нитроанилида (S4760, Sigma-Aldrich) в качестве субстрата, и инкубировали в течение 90 минут. Измеряли итоговое поглощение при 405 нм.
Как показано на фиг. 11, воспроизводство АФК (активных форм кислорода) в ЖБАЛ резко повышалось в группе с индуцированной ХОБЛ. При этом в получающей лекарственное средство контрольной группе, получающей лечение рофлумиластом, наблюдался пониженный приблизительно на 22,2% уровень АФК по сравнению с группой с индуцированной ХОБЛ; в группах, получавших лечение 15 мг/кг и 30 мг/кг KS534, наблюдался значительно сниженный уровень АФК, на 19,5% и 27,5%, по сравнению с группой с индуцированной ХОБЛ.
Как показано на фиг. 12, в группе с индуцированной ХОБЛ уровень белков в ЖБАЛ резко повышался. В получающей лекарственное средство контрольной группе, получающей лечение рофлумиластом, наблюдалось значимое снижение уровня белков по сравнению с группой с индуцированной ХОБЛ. В группах, получавших лечение 15 мг/кг и 30 мг/кг KS534, наблюдался значительно сниженный уровень белков: на 20,8% и 28,5% по сравнению с группой с индуцированной ХОБЛ.
Как показано на фиг. 12, в группе с индуцированной ХОБЛ активность фермента эластазы нейтрофилов в ЖБАЛ резко повышалась. Получающая лекарственное средство контрольная группа, получающая лечение рофлумиластом, демонстрировала значимое снижение активности фермента эластазы нейтрофилов по сравнению с группой с индуцированной ХОБЛ. В группах, получавших лечение 15 мг/кг и 30 мг/кг KS534, наблюдалось значительно сниженная активность фермента эластазы нейтрофилов по сравнению с группой с индуцированной ХОБЛ.
6-6. Анализ цитокинов в ЖБАЛ
Уровень ИЛ-6 (SM6000B, R&D System, США) и ФНО-альфа (555268, BD Bioscience, США)) в ЖБАЛ, полученном от мышей, определяли посредством твердофазного иммуноферментного анализа (ELISA). Анализ каждого цитокина выполняли в соответствии с инструкциями производителя, и поглощение определяли при 450 нм посредством ИФА ELISA Leader (VersaMax, Molecular Devices, США).
Как показано на фиг. 13, в группе с индуцированной ХОБЛ, уровень ИЛ-6 в ЖБАЛ резко повышался. В получающей лекарственное средство контрольной группе, получающей лечение рофлумиластом, наблюдалось значимое снижение уровня ИЛ-6 по сравнению с группой с индуцированной ХОБЛ; и в группах, получавших лечение 15 мг/кг и 30 мг/кг KS534, наблюдался пониженный уровень ИЛ-6: на 35,8% и 50,6% по сравнению с группой с индуцированной ХОБЛ. Уровень ФНО-альфа в ЖБАЛ резко повышался в группе с индуцированной ХОБЛ. В получающей лекарственное средство контрольной группе, получающей лечение рофлумиластом, наблюдалось значимое снижение уровня ФНО-альфа по сравнению с группой с индуцированной ХОБЛ; и в группах, получавших лечение 15 мг/кг и 30 мг/кг KS534, наблюдался пониженный уровень ФНО-альфа: на 18,3% и 27,6%) по сравнению с группой с индуцированной ХОБЛ.
Как показано на фиг. 14, в группе с индуцированной ХОБЛ значимо увеличивалась инвазия воспалительных клеток в бронхиолярные структуры, а также наблюдалась гиперплазия эпителиальных клеток и гипертрофия мышцы трахеи, тогда как в группе положительного контроля, получавшей лечение рофлумиластом, а также в получающей экспериментальный образец группе (30 мг/кг, KS534) при пероральном введении экспериментальных образцов (KS 534) в различных концентрациях, инвазия воспалительных клеток значимо уменьшалась.
В целом, в группе с индуцированной ХОБЛ значительно повышались уровни ИЛ-6 и ФНО-альфа в ЖБАЛ, число воспалительных клеток, а также уровни воспроизводства АФК и активность эластазы. При этом предложенное в настоящем изобретении соединение KS534 эффективно уменьшало число медиаторов воспаления, таких как нейтрофилы и воспалительные цитокины, например, ИЛ-6 и ФНО-альфа, что было подтверждено гистопатологическим анализом бронхо-альвеолярной ткани.
Наконец, было подтверждено, что предложенное в настоящем изобретении соединение KS534 эффективно ингибировало большинство патологических синдромов ХОБЛ по сравнению со стандартным доступным лекарственным средством (Рофлумиласт), использованном в группе положительного контроля, где не наблюдалось значимого снижения активности эластазы. Соответственно, предложенное в настоящем изобретении соединение KS534 может подходить для применения в качестве мощного природного агента для лечения ХОБЛ.
6-7. Статистика
Все полученные в различных экспериментах результаты анализировали с применением однофакторного дисперсионного анализа ANOVA, и статистическую значимость между соответствующими группами верифицировали в соответствии с критерием множественного сравнения Даннетта по результатам апостериорного сравнения.
Экспериментальный пример 7. Тест на острую токсичность при пероральном введении у крыс
Тест на острую токсичность выполняли путем введения предложенного в настоящем изобретении соединения СПФ-крысам линии Спрег-Доули возрастом 6 недель.
250 мг/кг, 500 мг/кг, 1000 мг/кг, 5000 мг/кг предложенных в настоящем изобретении экстракта и соединений вводили перорально в каждой группе, состоящей из 2 крыс и наблюдали за симптомами у крыс в течение 14 дней. После введения экстракта или соединений наблюдали за всеми клиническими изменениями, т.е. смертностью, клиническими признаками, изменением массы тела, и проводили анализ крови, например, гематологический тест и гематологический биохимический тест. Аномальные изменения органов брюшной полости и органов грудной клетки оценивали после аутопсии.
Каких-либо изменений смертности, клинических признаков, изменений массы тела и генерализованных данных в любой группе ни у самок, ни у самцов не наблюдалось. Кроме того, не наблюдалось какой-либо токсичности в экспериментальной группе, получавшей лечение 5000 мг/кг предложенного в настоящем изобретении экстракта или соединений.
Соответственно, было подтверждено, что предложенный в настоящем изобретении экстракт и соединения, полученные согласно настоящему изобретению, представляют собой эффективное и безопасное вещество с полулетальной дозой (LD50) более чем 5000 мг/кг при пероральном введении.
Варианты изобретения
Здесь и далее в настоящем документе описаны способы получения и виды вспомогательных веществ, однако настоящее изобретение не ограничивается ими. Репрезентативные примеры получения описаны ниже.
Получение состава для инъекций
Состав для инъекций получали путем растворения активного компонента, контроля показателей pH на уровне, составляющем приблизительно 7,5, с последующим заполнением всеми компонентами ампулы объемом 2 мл и стерилизации путем стандартного для составов для инъекций способа.
Получение порошка
Порошковый состав получали путем смешивания указанных выше компонентов и наполнения запечатанной упаковки.
Получение таблеток
Состав в виде таблеток получали путем смешивания указанных выше компонентов и таблетирования.
Получение капсул
Состав в виде таблеток получали путем смешивания указанных выше компонентов и наполнения желатиновых капсул с применением стандартного для желатиновых составов способа.
Получение жидкости
Жидкий состав получали путем растворения активного компонента с последующим наполнением всеми компонентами ампулу объемом 1000 мл и стерилизации с применением стандартного для жидких составов способа.
Получение функционального пищевого продукта
Вышеупомянутые смеси витаминов и минеральных веществ могут различным образом варьировать. Такие вариации не должны считаться отступлением от существа и объема настоящего изобретения.
Получение лечебного напитка
Лечебный напиток получали путем растворения активного компонента, смешивания, перемешивания при 85°C в течение 1 часа, фильтрации с последующим заполнением всеми компонентами ампулы объемом 1000 мл и стерилизации с применением стандартного для получения лечебного напитка способа.
Соответственно, очевидно, что варианты осуществления описанного изобретения могут различным образом варьировать. Такие вариации не должны считаться отступлением от существа и объема настоящего изобретения, и подразумевается, что все такие модификации, как будет очевидно специалисту в данной области техники, включены в объем приведенной ниже формулы изобретения.
Промышленная применимость
Согласно описанию настоящего изобретения, предложенное в настоящем изобретении соединение KS534 из экстракта Pseudolysimachion rotundum var subintegrum демонстрировало выраженную противовоспалительную, противоаллергенную, противоастматическую и направленную против ХОБЛ активность, что подтверждается в различных тестах in vitro, например, (1) теста на цитотоксичность с использованием линий клеток НТ1080, Н292 и EL4, (2) теста ингибирования экспрессии MUC5AC (олигомерный слизе-/гелеобразующий муцин), индуцируемой ФНО-альфа, (3) люциферазного репортерного анализа NF-каппа B, (4) теста ингибирования активности транскрипционного фактора NF-каппа B; (5) ингибирования экспрессии мРНК целевых генов, таких как ММР-9, MUC5AC и ИЛ-4 путем ингибирования активности NF-каппа B; (6) дозозависимого ингибирующего эффекта на воспроизводство MUC5AC посредством анализа воспроизводства белка MUC5AC; а также тестирования in vivo, например, (7) эффекта, заключающегося в уменьшении числа воспалительных клеток, таких как эозинофилы, с применением модели на сенсибилизированных/стимулированных OVA (овальбумином) мышах, (8) теста ингибирования высвобождения IgE, воспалительных цитокинов, таких как ИЛ-4, ИЛ-5, ИЛ-13 и т.д. в жидкости бронхоальвеолярного лаважа, и инвазии воспалительных клеток, а также подавления гиперреактивности дыхательных путей и гиперплазии бокаловидных клеток, (9) теста ингибирования с применением модели ХОБЛ на животных (мыши C57B/6N) пролиферации воспалительных клеток в жидкости бронхоальвеолярного лаважа, ингибирования воспроизводства АФК (активных форм кислорода) и активности эластазы нейтрофилов, эффекта снижения уровней ИЛ-6, ФНО-альфа и инфильтрирующих воспалительных клеток и т.п. Соответственно, оно может применяться в качестве терапевтического средства или функционального пищевого продукта для лечения и предотвращения аллергического заболевания, воспалительного заболевания, астмы или хронической обструктивной болезни легких (ХОБЛ).
Реферат
Изобретение относится к новому (3R,5S,5aS,6R,7S,8R,8aS)-8-хлор-8a-гидрокси-5-(((2S,3R,4S,5S,6R)-3,4,5-тригидрокси-6-(гидроксиметил)тетрагидро-2Н-пиран-2-ил)окси)-1Н-3,6-метанциклопента[е][1,3]диоксепин-7-ил-3,4-дигидроксибензоату (KS534), представленному химической формулой (1). Изобретение также относится к фармацевтической композиции и к функциональному пищевому продукту, содержащим терапевтически эффективное количество соединения (KS534), для лечения или предотвращения заболевания, вызванного повышенным продуцированием белка MUC5AC, повышенным уровнем эозинофилов, воспалением легких, гиперсекрецией слизи, иммунным ответом, повышенным уровнем ИЛ-6, ФНО-альфа в бронхоальвеолярном лаваже (БАЛ) или повышенным количеством воспалительных клеток. Технический результат – получено новое соединение и фармацевтическая композиция на его основе, которые могут найти применение в медицине для лечения аллергического заболевания, воспалительного заболевания, астмы или хронической обструктивной болезни легких (ХОБЛ). 6 н.п. ф-лы, 6 табл., 14 ил., 7 пр.
Формула
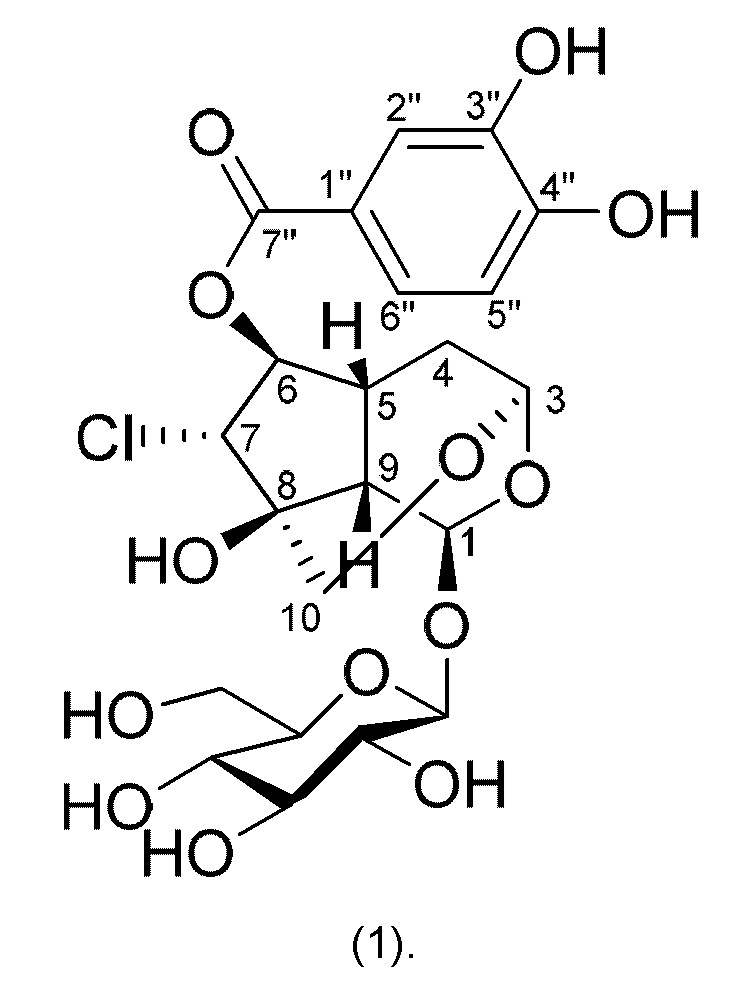

Комментарии