Производные пиперидина, способ их получения, фармацевтическая композиция на их основе и промежуточные вещества - RU2167865C2
Код документа: RU2167865C2
Чертежи





Описание
Изобретение относится к новым производным пиперидина, их получению и применению в качестве лекарственных средств. Изобретение относится прежде всего к новым производным пиперидина общей формулы I
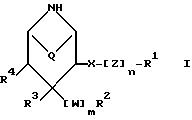
где R1 означает арил или гетероциклил;
R2 означает фенил, нафтил, аценафтил, циклогексил, пиридил, пиримидинил, пиразинил, оксопиридинил, диазинил, триазолил, тиенил, оксазолил, оксадиазолил, тиазолил, пирролил или фурил, каковые радикалы могут быть замещены 1-3 галогенами, гидроксигруппой, цианогруппой, трифторметилом, (низш. )алкилом, галоген-(низш.)алкилом, гидрокси-(низш.)алкилом, (низш.)алкокси-(низш. )алкилом, циано-(низш. )алкилом, карбокси-(низш. )алкилом, (низш. )алканоилокси-(низш. )алкилом, (низш. )алкоксикарбонилокси-(низш. )алкилом, (низш.)алкоксикарбонилом или (низш.)алкоксигруппами или (низш. )алкилендиоксигруппой и/или остатком L1-T1-L2T2-L3- T3-L4-T4-L5-U; L1, L2, L3, L4 и L5 независимо друг от друга представляют собой связь,
C1-8алкилен, C2-8алкенилен или C2-8алкинилен или отсутствуют;
Т1, Т2, Т3 и Т4 независимо друг от друга представляют собой
(а) связь или отсутствуют или представляют собой одну из групп
(б) -CH(OH)-
(в) -CH(OR6)-
(г) -CH(NR5R6)-
(д) -CO-
(е) -CR7R8-
(ж) -O- или -NR6-
(з) -S(O)0-2-
(и) -SO2NR6-
(к) -NR6SO2-
(л) -CONR6-
(м) -NR6CO-
(н) -O-CO-
(o) -CO-O-
(п) -O-CO-O-
(р) -O-CO-NR6-
(с) -N(R6)-CO-N(R6)-
(т) - N(R6)-CO-О-,
причем отходящие от (б), (г), (д) и (ж)-(т) связи ведут к C-атому смежной группы и этот C-атом является насыщенным, если связь отходит от гетероатома, и причем присутствуют не более двух групп (б)-(е), трех групп (ж)-(з) и одной группы (и)-(т);
R3 означает водород, гидрокси, (низш.)алкокси или (низш.)алкенилокси;
R4 означает водород, (низш.)алкил, (низш.)алкенил, (низш.)алкокси, гидрокси-(низш. )алкил, (низш. )алкокси-(низш. )алкил, бензил, оксо или группу R4a-Z1-X1-, где
R4a представляет собой
(а) Н-
(б) (низш.)алкил-
(в) (низш.)алкенил-
(г) гидрокси-(низш.)алкил-
(д) полигидрокси-(низш.)алкил-
(е) (низш.)алкил-O-(низш.)алкил-
(ж) арил-
(з) гетероциклил-
(и) арилалкил-
(к) гетероциклилалкил-
(л) арилоксиалкил-
(м) гетероциклилоксиалкил-
(н) (R5,R6)-N-(CH2)1-3-
(о) (R5R6)-N-
(п) (низш.)алкил- S(O)0-2-
(р) арил-S(O)0-2-
(с) гетероциклил-S(O)0-2-
(т) HO-SO3-, соответственно ее соли
(у) H2N-C(NH)-NH-
(ф) NC-,
а отходящие от (о)-(ф) связи ведут к C-атому смежной группы и этот C-атом является насыщенным, если связь отходит от гетероатома;
Z1 представляет собой
(а) связь, отсутствует или представляет собой одну из групп
(б) (низш.)алкилен-
(в) (низш.)алкенилен-
(г) -О-, - N(R11)-, -S(O)0-2-
(д) -CO-
(e) -O-CO-
(ж) -O-CO-O-
(з) -O-CO-N(R11)-
(и) -N(R11)-CO-O-
(к) -CO-N(R11)-
(л) -N(R11)-CO-
(м) -N(R11)-CO-N(R11 )-
(н) -CH(OR9)-,
а отходящие от (г) и (е)-(н) связи ведут к C-атому смежной группы и этот C-атом является насыщенным, если связь отходит от гетероатома;
X1 представляет собой
(а) связь, отсутствует или представляет собой одну из групп
(б) -O-
(в) -N(R11)-
(г) -S(O)0-2-
(д) -(CH2)1-3,
или R3 и R4 оба вместе представляют собой связь;
R5 и R6 означают водород, (низш.)алкил, (низш.)алкенил, арил-(низш. )алкил или ацил или вместе с N-атомом, с которым они связаны, представляют собой 5- или 6-членное гетероциклическое кольцо, которое может содержать дополнительный N-, О- либо S-атом или -SO- либо -SO2-группу, причем дополнительный N-атом необязательно может быть замещен (низш.)алкильными остатками;
R7 и R8 вместе с C-атомом, с которым они связаны, представляют собой 3-7-членное кольцо, которое может содержать один или два -О- либо -S- атома или -SO- либо -SO2- группы;
R9 означает водород, (низш.)алкил, ацил или арилалкил;
R10 означает карбоксиалкил, алкоксикарбонилалкил, алкил или водород;
R11 означает водород или (низш.)алкил;
U означает водород, (низш.)алкил, циклоалкил, циано, необязательно замещенный циклоалкил, арил или гетероциклил;
Q означает этилен или отсутствует;
X представляет собой связь, кислород, серу или группу -CH-R11, -CHOR9-, -О-CO, -CO- или C = NOR10, причем отходящая от атома кислорода или серы связь ведет к насыщенному C-атому группы Z либо к R1;
W означает кислород или серу;
Z означает (низш.)алкилен, (низш.)алкенилен, гидрокси-(низш.)алкилиден, -О-, -S-, -О-алк-, -S-алк-, -алк-О- или алк-S-, где алк обозначает (низш. )алкилен, и причем
а) если Z означает -О- или -S, X представляет собой -CH-R11- и либо R2 содержит заместитель L1-T1-L2-T2-L3-T3-L4- T4-L5-U, либо R4 представляет собой указанный выше заместитель, отличный от водорода,
б) если Z означает -О-алк- или -S-алк-, X представляет собой -CH-R11,
в) если X означает связь, Z представляет собой (низш.)алкенилен, -алк-О- или -алк-S-;
n означает 1, или, если X представляет собой -О-CO-, означает 0 или 1;
m означает 0 или 1,
и к фармацевтически применимым солям соединений I, за исключением соединения 4-(4-фторфенил)-3-(3,4- метилендиоксибензилокси) пиперидин и его гидрохлорида.
В контексте настоящего описания понятие "низший", соответственно сокращение "низш. ", обозначает группы с 1-6, предпочтительно 1-4 C-атомами. Примерами (низш. )алкильных и алкоксильных остатков являются метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, пентил, гексил, соответственно метокси, этокси, пропокси, изопропокси, бутокси, изобутокси, втор-бутокси и трет-бутокси. (Низш.)алкилендиоксиостатками являются предпочтительно метилендиокси, этилендиокси и пропилендиокси. В качестве примеров (низш. )алконоильных остатков можно назвать ацетил, пропионил и бутирил. Циклоалкил представляет собой насыщенные, циклические углеводородные остатки с 3-6 атомами углерода, т.е. циклопропил, цикло-бутил, циклопентил и циклогексил. C1-8алкиленовыми остатками являются, например, метилен, этилен, пропилен, 2-метилпропилен, тетра-, пента- и гексаметилен; C2-8алкенильными остатками являются, например, винилен и пропенилен; C2-8 алкинильными остатками являются, например, этинилен; ацильные остатки представляют собой алканоильные остатки, предпочтительно (низш.)алканоильные остатки, или ароильные остатки, такие как бензоил. Арил представляет собой одно- либо многоядерные ароматические остатки, которые могут быть одно- либо многократно замещены, такие, например, как фенил, замещенный фенил, нафтил, замещенный нафтил, тетрагидронафтил или замещенный тетрагидронафтил. Примерами заместителей в таких арильных остатках являются (низш.)алкил, трифторметил, нитро, амино, (низш.)алкенил, (низш.)алкокси, (низш.)алкилкарбонилокси, гидрокси, галоген, циано, карбамоил и (низш.)алкилендиокси, а также необязательно замещенный галогеном, (низш.)алкилом, (низш.)алкоксигруппой или дигидрокси-(низш. )алкиламинокарбонилом фенил, фенокси, фенилтио, фенил-(низш. )алкил или фенил-(низш.)алкокси. В качестве примеров других заместителей в арильных остатках можно назвать (низш.)алкоксикарбонилфенил, гидрокси-(низш. )алкилфенил, бензилокси, пиридилкарбониламино-(низш.)алкил, (низш. )алкенилокси, (низш. )алкокси-(низш. )алкокси, метоксибензилокси, гидроксибензилокси, фенэтилокси, метилендиоксибензилокси, диоксоланил-(низш. )алкокси, циклопропил-(низш. )алкокси, гидрокси-(низш.)алкокси, карбамоилокси-(низш.)алкокси, пиридилкарбамоилокси-(низш.)алкокси, бензилокси-(низш. )алкокси, а также необязательно замещенный галогеном, (низш.)алкилом, (низш. )алкоксигруппой или дигидрокси-(низш.)алкиламинокарбонилом пиридил, пиридилокси, пиридилтио, пиридиламино, пиридил-(низш. )алкил, пиридил-(низш. )алкокси, пиримидинил, пиримидинилокси, пиримидинилтио, пиримидиниламино, пиримидинил-(низш. )алкил, пиримидинил-(низш.)алкокси, тиенил, тиенил-(низш. )алкил, тиенил-(низш. )алкокси, фурил, фурил-(низш. )алкил, фурил-(низш. )алкокси.
Понятие гетероциклил обозначает моно- либо бициклические, насыщенные и ненасыщенные гетероциклические остатки с 1-4 атомами азота и/или 1-2 атомами серы либо кислорода, которые одно- либо многократно могут быть замещены прежде всего (в случае ненасыщенных гетероциклильных остатков) алкилом, гидроксигруппой, алкоксигруппой, нитрогруппой или галогеном либо заместителями, указанными выше для арильных остатков, или (в случае насыщенных гетероциклильных остатков) алкилом или алкоксигруппой. Примерами гетероциклильных остатков являются пиридил, тиенил, пиразинил, триазолил, имидазолил, бензтиазолил, фурил, пиримидинил, морфолинил, хиназолинил, хинолил, хиноксалинил, изохинолил, бензо[b] тиенил, изобензофуранил, бензимидазолил, 2-оксобензимидазолил или тиазолил. Примерами замещенных гетероциклильных остатков являются нитробензтиазолил, фенилтетразолил, фенилоксадиазолил, тиенилоксадиазолил, фуранилоксадиазолил, бензилоксадиазолил, фенилоксазолил. В качестве примеров насыщенных гетероциклильных остатков можно назвать диоксоланил, диоксанил, дитиоланил, дитианил, пирролидинил, пиперидинил, пиперазинил, 4-метилпиперазинил, морфолинил, тиоморфолинил, 2-гидроксиметилпирролидинил, З-гидроксипирролидинил, 3,4-дигидроксипирролидинил, 4-гидроксипиперидинил, 4-оксопиперидинил, 3, 5-диметилморфолинил, 4,4-диоксотиоморфолинил, 4-оксотиоморфолинил, 2,6-диметилморфолинил, 2-оксоимидазолидинил, 2-оксооксазолидинил, 2-оксопирролидинил, 2-оксо[1,3]оксазинил, 2-оксотетрагидропиримидинил и т.п.
В случае R1, R4a и R9 арильные, ароильные и гетероциклильные остатки дополнительно могут быть замещены еще и гетероциклилалкилом, гетероциклилалкоксигруппой, гетероциклилалкоксиалкилом, такими, например, как пиперидиноалкил, пиперидиноалкокси, пиперидиноалкоксиалкил, морфолиноалкил, морфолиноалкокси, морфолиноалкоксиалкил, пиперазиноалкил, пиперазиноалкокси, пиперазиноалкоксиалкил или N-метилпиперазиноалкил, N-метилпиперазиноалкокси, N-метилпиперазиноалкоксиалкил, а также алкиламиноалкилом, алкиламиноалкоксигруппой, алкиламиноалкоксиалкилом, моно- и полигидроксиалкилом, -алкоксигруппой, -алкоксиалкилом и -алкоксиалкоксигруппой, карбамоилалкилоксигруппой, (низш. )алкоксигруппой, амино-(низш.)алкоксигруппой, гидрокси-(низш. )алкоксигруппой или же остатком -O-CH2CH(OH)CH2NRx, где NRx представляет собой моно- либо ди(низш.)алкиламинный, пиперидиновый, морфолиновый, пиперазиновый или N-метилпиперазиновый остаток.
Примерами представленных NR5R6 5- и 6-членных гетероциклических колец являются пирролидинил, пиперидинил, пиперазинил, морфолинил, тиоморфолинил, 2-гидроксиметилпирролидинил, 3-гидроксипирролидинил, 3,4-дигидроксипирролидинил, 4-гидроксипиперидинил, 4-оксопиперидинил, 3, 5-диметилморфолинил, 4,4-диоксотиоморфолинил, 4-оксотиоморфолинил, 2,6-диметилморфолинил, 2-оксоимидазолидинил, 2-оксооксазолидинил, 2-оксопирролидинил, 2-оксо[1,3]оксазинил, 2-оксотетрагидропиримидинил и т.п. Примерами представленных CR7R8 3-7-членных колец являются циклопентил, циклогексил, циклогептил, 1,3-диоксоланил, 1,3-диоксанил, 1,3-дитиоланил и 1,3-дитианил.
Понятие полигидроксиалкил обозначает C1-C7алкильные остатки, которые могут быть замещены 2-6 гидроксигруппами, такими, например, как глицерил, арабитил, сорбитил и т.д.
Соединения формулы I имеют по крайней мере два асимметричных атома углерода и могут быть представлены поэтому в виде оптически чистых диастереомеров, смесей диастереомеров, диастереомерных рацематов, смесей диастереомерных рацематов или в виде мезосоединений. Изобретение включает все эти формы. Смеси диастереомеров, диастереомерные рацематы или смеси диастереомерных рацематов могут разделяться с помощью обычных методов, например посредством хроматографии на колонке, тонкослойной хроматографии, ЖХВР и т.п.
Предпочтительными соединениями согласно изобретению являются таковые общей формулы
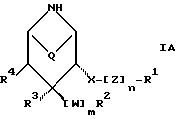
где R1-R4, Q, W, X и Z, n и m имеют значения, указанные выше.
Другая предпочтительная группа соединений формулы I включает соединения формулы

где R1 означает арил или гетероциклил;
R2 означает фенил, циклогексил, замещенный галогеном, гидроксигруппой, цианогруппой, трифторметилом, (низш.)алкилом, галоген-(низш.)алкилом, гидрокси-(низш. )алкилом, (низш.)алкокси-(низш.)алкилом, циано-(низш.)алкилом, карбокси-(низш. )алкилом, (низш. )алканоилокси-(низш. )алкилом, (низш. )алкоксикарбонилокси-(низш. )алкилом, (низш. )алкоксикарбонилом, (низш. )алкоксигруппой, (низш. )алкилендиоксигруппой либо остатком L1-T1-L2-T2-L3- T3-L4-T4-L5-U фенил или циклогексил; или нафтил либо аценафтил;
L1, L2, L3, L4 и L5 независимо друг от друга представляют собой связь, C1-8алкилен, C2-8алкенилен или C2-8алкинилен либо отсутствуют;
Т1, Т2, Т3 и Т4 независимо друг от друга представляют собой
(а) связь либо отсутствуют или представляют собой одну из групп
(б) -CH(ОН)-
(в) -CH(OR6)-
(г) -CH(NR5R6)-
(д) -CO-
(е) -CR7R8-
(ж) -O- или -NR6-
(з) -S(O)0-2-
(и) -SO2NR6-
(к) -NR6SO2-
(л) -CONR6-
(м) -NR6CO-
(н) -O-CO-
(o) -CO-O-
(п) -O-CO-O-
(p) -C-CO-NR6-,
причем отходящие от (б), (г), (д) и (ж)-(p) связи ведут к C-атому смежной группы и этот C-атом является насыщенным, если связь отходит от гетероатома, и причем присутствуют не более двух групп (б)-(е), трех групп (ж)-(з) и одной группы (и)-(p);
R3 означает водород, гидрокси, (низш.)алкокси или (низш.)алкенилокси;
R4 означает водород, (низш. )алкил, (низш. )алкенил, (низш.)алкокси, гидрокси-(низш.)алкил, (низш.)алкокси-(низш.)алкил или бензил;
R5 и R6 означают водород, (низш.)алкил или ацил или вместе с N-атомом, с которым они связаны, представляют собой 5- либо 6-членное гетероциклическое кольцо, которое может содержать дополнительный N-, О- или S-атом;
R7 и R8 вместе с атомом азота, с которым они связаны, представляют собой 3-7-членное кольцо, которое может содержать один либо два атома кислорода или серы;
U означает водород, (низш.)алкил, циклоалкил, циано, арил или гетероциклил;
Q означает этилен или отсутствует;
X означает кислород, серу или группу -CH2-, -CHOR9- или -OCO-, a R9 означает водород, (низш.)алкил, ацил или арилалкил;
W отсутствует либо может означать кислород или серу, если R3 является водородом;
Z означает (низш.)алкилен или отсутствует;
и фармацевтически применимые соли указанных соединений за исключением соединения 4-(4-фторфенил)-3-(3,4-метилендиоксибензилокси)пиперидин и его гидрохлорида.
К предпочтительным относятся далее соединения формул I и IA, в которых W отсутствует, и таковые, в которых Q отсутствует. X означает предпочтительно кислород, серу или -CO-; Z означает предпочтительно метилен.
Предпочтительными остатками R1 являются фенил, замещенный (низш. )алкилом, (низш. )алкенилом, (низш.)алкоксигруппой, (низш.)алкилтиогруппой, галогеном, гидроксигруппой, гидрокси-(низш.)алкоксигруппой, (низш.)алкокси- (низш. )алкоксигруппой, (низш. )алкилсульфинилом, (низш.)алкилсульфонилом, цианогруппой, трифторметилом, трифторметоксигруппой, карбоксигруппой, циклобутилметокси-(низш. )алкилом, (низш. )алкилендиоксигруппой, фенилом, феноксигруппой, (низш. )алкоксикарбонилфенилом, гидрокси-(низш. )алкилфенилом, 2,3-дигидроксипропиламинокарбонилфенилом, бензилоксигруппой, бензоилом, пиридил-(низш. )алкокси-(низш. )алкилом или никотиноиламино-(низш.)алкилом фенил.
Другими предпочтительными остатками R1 являются нафтил, замещенный гидроксигруппой, оксогруппой, (низш.)алкоксигруппой, (низш. )алкенилоксигруппой, (низш. )алкокси-(низш. )алкоксигруппой, ди-(низш. )алкиламиногруппой, 2,3-дигидроксипропоксигруппой, 2,3-дигидроксипропокси-(низш.)алкоксигруппой, 2, 3-диметоксипропоксигруппой, (низш. )алкоксикарбонил(низш.)алкоксигруппой, карбамоил-(низш.)алкоксигруппой, метоксибензилоксигруппой, гидроксибензилоксигруппой, фенэтилоксигруппой, метилендиоксибензилоксигруппой, диоксоланил-(низш. )алкоксигруппой, циклопропил-(низш. )алкоксигруппой, гидрокси-(низш.)алкоксигруппой, карбамоилокси-(низш.)алкоксигруппой, пиридилкарбамоилокси-(низш.)алкоксигруппой, морфолино-(низш.)алкоксигруппой, 3-морфолино-2-гидроксипропоксигруппой, N-метилпиразино-N-(низш.)алкоксигруппой, бензоилокси-(низш.)алкоксигруппой или пиколилоксигруппой нафтил; тетрагидронафтил либо замещенный метилом тетрагидронафтил, или инданил.
Также предпочтительны следующие остатки R1: пиридил, бензимидазолил, ди-(низш.)алкоксипиримидинил или 2- и 5-бензо[b]тиенил, 6- и 7-хинолил, 6- и 7-изохинолил, 6- и 7-тетрагидрохинолил, 6- и 7-тетрагидроизохинолинил, 6-хиноксалинил, 6- и 7-хиназолинил, а также замещенные гидроксигруппой, оксогруппой, (низш. )алкоксигруппой, (низш.)алкенилоксигруппой, (низш.)алкокси-(низш. )алкоксигруппой, ди-(низш.)алкиламиногруппой, 2,3-дигидроксипропоксигруппой, 2, 3-дигидроксипропокси-(низш. )алкоксигруппой, 2,3-диметоксипропоксигруппой, (низш.)алкоксикарбонил-(низш.)алкоксигруппой, карбамоил-(низш. )алкоксигруппой, метоксибензилоксигруппой, гидроксибензилоксигруппой, фенэтилоксигруппой, метилендиоксибензилоксигруппой, диоксоланил-(низш. )алкоксигруппой, циклопропил-(низш. )алкоксигруппой, гидрокси-(низш. )алкоксигруппой, карбамоилокси-(низш. )алкоксигруппой, пиридилкарбамоилокси-(низш.)алкоксигруппой, морфолино-(низш.)алкоксигруппой, 3-морфолино-2-гидроксипропоксигруппой, N-метилпиперазино-N- (низш.)алкоксигруппой, бензоилокси-(низш.)алкоксигруппой или пиколилоксигруппой 6- и 7-хинолил, 6- и 7-изохинолил, 6- и 7- тетрагидрохинолил, 6- и 7-тетрагидроизохинолинил, 6-хиноксалинил или 6- и 7-хиназолинил.
Предпочтительными остатками R2 являются фенил, замещенный галогеном, гидроксигруппой, цианогруппой, трифторметилом, (низш.)алкилом, галоген-(низш. )алкилом, гидрокси-(низш. )алкилом, (низш.)алкокси-(низш.)алкилом, циано-(низш.)алкилом, карбокси-(низш.)алкилом, (низш.)алканоилокси-(низш.)алкилом, (низш. )алкоксикарбонилокси-(низш.)алкилом, (низш.)алкоксикарбонилом, (низш. )алкоксигруппой или (низш.)алкилендиоксигруппой фенил.
Также к предпочтительным относятся следующие остатки R2: замещенный остатком L1-T1-L2 -T2-L3-T3-L4- T4-L5-U фенил, где L1 и L2 предпочтительно отсутствуют или означают C1-8алкилен, a L3 отсутствует и U означает водород, (низш. )алкил, цикло-(низш.)алкил, фенил, замещенный (низш.)алкилом, (низш. )алкоксигруппой, (низш. ) алкилтиогруппой, (низш.) алкилсульфинилом, (низш. )алкилендиоксигруппой, галогеном, бензоил-(низш. )алкилом, галоген-(низш. )алкилом, (низш.)алканоилоксигруппой или гидроксигруппой фенил; или нафтил; или пиридил, тиенил, пиразинил, триазолил, имидазолил, фенилоксадиазолил, тиенилоксадиазолил, фурилоксадиазолил, фенилоксазолил, бензтиазолил, фурил, пиримидинил, нитробензтиазолил, фенилтетразолил или морфолинил.
Для групп Т1-Т4 предпочтительны значения групп (а)-(в), (д)- (з), (н) и (о).
Примерами особенно предпочтительных остатков R2 являются фенил или фенил, замещенный 2-бензотиазолилтио-(низш. )алкилом, 2-бензилокси-3-метоксипропоксигруппой, 2-бензоилокси-3-метоксипропоксигруппой, 2,3-дигидроксипропоксигруппой, 2-гидрокси-3-бензиламинопропоксигруппой, 2-гидрокси-3-феноксипропоксигруппой, 2-гидрокси-3-фенилтиопропоксигруппой, 2-метокси-3-феноксипропоксигруппой, 2-метокси-3-бензилоксипропоксигруппой, 2-метил-3-фторфенилбутирилокси-(низш. )алкоксигруппой, 2-(низш.)алкенилокси-4-фенилбутилом, 3,4,5-триметоксифенилоксадиазолил-(низш.)алкоксигруппой, 6-нитро-2-бензотиазолилтио-(низш. )алкилом, бензамидо-(низш.)алкоксигруппой, бензамидо-(низш. )алкилом, бензоил-(низш.)алкоксигруппой и ее кеталями, бензоил-(низш. )алкилом и его кеталями, бензоил-(низш.)алкиламинокарбонил-(низш. )алкилом, бензоил-(низш. ) алкоксикарбонил-(низш. )алкилом, бензоил-(низш. )алкиламинокарбонилом, бензоилоксигруппой, бензоилокси-(низш. )алкилбензоилокси-(низш. )алкоксигруппой, бензоилокси-(низш.)алкоксигруппой, бензоилокси-(низш. )алкилом, бензтиазолилтио-(низш.)алкоксигруппой, бензтиазолилтио-(низш. )алкилом, бензилкарбамоил-(низш.)алкоксигруппой, бензилокси-(низш.)алкилкарбонилокси-(низш.)алкилом, бензилокси-(низш. )алкоксигруппой, бензилтио-(низш. )алкоксигруппой, карбамоилокси-(низш. )алкоксигруппой, карбамоилокси-(низш.)алкилом, карбокси-(низш. )алкоксигруппой, карбокси-(низш. )алкилом, цианогруппой, циано-(низш. )алкоксигруппой, циано-(низш. )алкилом, цианофенил-(низш.)алкоксигруппой, циклогексилкарбонилокси-(низш. )алкилом, циклопропилкарбонилокси-(низш. )алкилом, циклопропилоксибензилокси-(низш. )алкоксигруппой, диоксоланил-(низш. )алкоксигруппой, фурилоксадиазолил-(низш. )алкоксигруппой, фуроилокси-(низш. )алкоксигруппой, галогенфенокси-(низш. )алкилом, галогенбензоил-(низш. )алкоксигруппой, галогенбензоилокси-(низш.)алкилом, галогенбензоилокси-(низш.)алкокси группой, галогенбензилокси-(низш.)алкоксигруппой, галогеном, галоген-(низш. )алкилом, галогенфеноксигруппой, галогенфенилоксадиазолил-(низш. )алкоксигруппой, гидроксигруппой, гидроксибензоилокси-(низш. )алкилом, гидроксибензилокси-(низш.)алкоксигруппой, гидрокси-(низш.)алкокси группой, гидрокси-(низш. )алкилом, имидазолилкарбонилокси-(низш. )алкилом, метоксибензоил-(низш.)алкилом, метоксибензилокси-(низш.)алкоксигруппой, метилендиоксибензоил-(низш. )алкоксигруппой, морфолино-(низш. )алкоксигруппой, морфолинокарбонилокси-(низш. )алкоксигруппой, морфолинокарбонилокси-(низш. )алкилом, N-метиламинофенилкарбонилокси-(низш. )алкилом, N-метилбензиламино-(низш.)алкоксигруппой, N-метилпирролилкарбонилокси- (низш. )алкоксигруппой, N-(низш. )алкилбензамидо-(низш. )алкилом, нафтил-(низш. )алкоксигруппой, никотиноилокси-(низш.)алкоксигруппой, никотиноилокси-(низш. )алкилом, (низш. )алканоилбензоилокси-(низш.)алкилом, (низш.)алканоилокси-(низш.)алкоксигруппой, (низш.)алканоилокси-(низш.)алкилом, (низш. )алкенилбензилокси(низш. )алкоксигруппой, (низш.)алкенилоксигруппой, (низш. )алкенилоксибензилокси(низш. )алкокси группой, (низш.)алкоксигруппой, (низш. )алкоксибензоилокси-(низш. )алкилом, (низш. )алкоксикарбонилом, (низш. )алкокси(низш. )алкилом, (низш. )алкоксибензоиламино-(низш.)алкилом, (низш. )алкоксибензилкарбонилокси-(низш. )алкилом, (низш.)алкоксибензилокси-(низш. )алкоксигруппой, (низш. )алкоксибензилтио-(низш. )алкоксигруппой, (низш. )алкоксикарбонилом, (низш. )алкоксикарбонил-(низш. )алкоксигруппой, (низш. )алкоксикарбонил-(низш. )алкилом, (низш. )алкоксифенилоксадиазолил-(низш. )алкоксигруппой, (низш.)алкилом, (низш.)алкилбензилокси-(низш. )алкоксигруппой, (низш.)алкилендиоксигруппой, (низш. )алкилендиоксибензилокси-(низш.)алкоксигруппой, (низш. )алкилсульфонилбензоил-(низш. )алкоксигруппой, (низш.)алкилтиобензоилокси-(низш.)алкоксигруппой, (низш.)алкилтиобензилокси-(низш.)алкоксигруппой, бензоилоксибензил-(низш.)алкокси группой, гидроксибензил-(низш.)алкоксигруппой, (низш.)алкоксибензил-(низш.)алкоксигруппой, (низш. )алкоксибензилкарбонилоксиалкоксигруппой, феноксибензилокси-(низш. )алкоксигруппой, феноксикарбонил-(низш.)алкилом, фенокси-(низш. )алкенилоксигруппой, фенокси-(низш. )алкинилоксигруппой, фенил-(низш. )алканоиламино-(низш.)алкилом, фенил-(низш.)алкенилоксигруппой, фенил-(низш. )алкоксигруппой, фенокси-(низш.)алкилом, фенил- (низш.)алкиламинокарбонилом, фенокси-(низш.)алкилкарбонил-(низш.)алкоксигруппой, фенил-(низш. )алкиламинокарбонил-(низш.)алкилом, фениламинокарбонилокси-(низш. )алкоксигруппой, фениламинокарбонилокси-(низш.)алкилом, фенилгидрокси-(низш. )алкилом, фенилоксадиазолил-(низш.)алкоксигруппой, фенилоксадиазолил-(низш. )алкилом, фенилоксазолил-(низш.)алкоксигруппой, фенилокси-(низш. )алкоксигруппой, фенилсульфамоил-(низш. )алкилом, фенилсульфинил-(низш. )алкилом, фенилсульфонил-(низш. )алкоксигруппой, фенилсульфонил-(низш. )алкилом, фенилтетразолилтио-(низш.)алкилом, фенилтио-(низш.)алкоксигруппой, фенилтио-(низш. )алкилом, пиразинилкарбонилокси-(низш.)алкилом, пиридиламинокарбонилокси-(низш. )алкоксигруппой, пиридиламинокарбонилокси-(низш. )алкилом, пиридилкарбамоилоксигруппой, пиридил-(низш. )алкокси-(низш. )алкоксигруппой, пиридил-(низш. )алкокси-(низш.)алкилом, пиридилоксадиазолил-(низш.)алкоксигруппой, пиридилтио-(низш.)алкилом, пиримидинилокси-(низш. )алкоксигруппой, пиримидинилтио-(низш.)алкилом, теноилокси-(низш. )алкоксигруппой, теноилокси-(низш. )алкилом, тиенилоксадиазолил-(низш. )алкоксигруппой, триазолил-(низш. )алкоксигруппой, трифторметилбензилокси-(низш.)алкоксигруппой или трифторметилом.
Предпочтительными остатками R4 являются 2-оксоимидазолидин-1-ил-(низш. )алкил, 4-гидроксипиперидин-1-ил-(низш. )алкоксигруппа, 4-гидроксипиперидин-1-ил-(низш.)алкокси-(низш.)алкил, 4-метилпиперазин-1-ил-(низш. )алкоксигруппа, 4-метилпиперазин-1-ил-(низш.)алкокси-(низш.)алкил, 4-метилпиперазин-1-ил-(низш. ) алкилкарбамоилокси-(низш. )алкил, 1,2,4-триазолил-(низш. )алкил, амино, амино-(низш.)алкил, амино-(низш.)алкиламино, амино-(низш. )алкиламино-(низш. )алкил, амино-(низш.)алкоксигруппа, амино-(низш. )алкокси-(низш. )алкил, аминокарбонилокси-(низш.)алкил, бензилокси либо бензилокси, замещенный (низш.)алкилом, (низш.)алкенилом, (низш.)алкоксигруппой, трифторметоксигруппой, (низш. )алкилтиогруппой, гидроксигруппой или галогеном, бензилокси-(низш.)алкил либо бензилокси-(низш.)алкил, замещенный (низш. )алкилом, (низш.)алкенилом, (низш.)алкоксигруппой или галогеном, карбамоилокси-(низш. )алкил, циано-(низш. )алкил, ди-(низш. )алкиламино, ди-(низш. )алкиламино-(низш. )алкил, ди-(низш. )алкиламино-(низш. )алкил-(N-(низш. )алкил)амино-(низш.)алкил, ди-(низш.)алкиламино-(низш.)алкиламино, ди-(низш. )алкиламино-(низш. )алкиламино-(низш. )алкил, ди-(низш. )алкиламино-(низш. )алкокси, ди-(низш. )алкиламино-(низш. )алкокси-(низш. )алкил, дигидрокси-(низш. )алкокси, дигидрокси-(низш.)алкокси-(низш.)алкил, дигидрокси-(низш. )алкиламино, дигидрокси-(низш. )алкиламино-(низш. )алкил, гуанидинил-(низш. )алкокси-(низш. )алкил, гуанидинил-(низш. )алкил, гидрокси, гидрокси-(низш. )алкил, сульфоокси-(низш. )алкил, гидрокси-(низш.)алкокси, гидрокси-(низш. )алкокси-(низш. )алкил, морфолин-4-ил-(низш. )алкокси, морфолин-4-ил-(низш. )алкокси-(низш.)алкил, морфолин-4-ил-(низш.)алкилкарбамоилокси-(низш.)алкил, нафтилалкокси либо замещенный (низш.)алкоксигруппой нафтилалкокси, (низш. )алкокси, (низш. )алкокси-(низш. )алкокси, (низш.)алкокси-(низш.)алкокси-(низш.)алкил, (низш.)алкокси-(низш.)алкил, (низш.)алкил, (низш. )алкилсульфониламино-(низш. )алкил, фенокси-(низш. )алкил или замещенный (низш. )алкилом, (низш.)алкоксигруппой фенокси-(низш.)алкил, фенилтио-(низш. )алкил или замещенный (низш.)алкилом, (низш.)алкоксигруппой фенилтио-(низш. )алкил, пиперазин-4-ил-(низш.)алкокси, пиперазин-4-ил-(низш.)алкокси-(низш. )алкил, пиперидин-1-ил-(низш. )алкилкарбамоилокси-(низш.)алкил, пиперидин-4-ил-(низш. )алкокси, пиперидин-4-ил-(низш.)алкокси-(низш.)алкил, пиридил-(низш. )алкокси, пиридил-(низш. )алкокси-(низш. )алкил, пиридилтио-(низш. )алкил, пиримидинилокси-(низш. )алкил либо замещенный (низш.)алкоксигруппой пиримидинилокси-(низш. )алкил, тетразолил-(низш.)алкил, трифторметилсульфониламино-(низш.)алкил или водород.
К другим предпочтительным группам соединений формулы I относятся таковые, в которых R2 означает циклогексил или бензоилоксиметилциклогексил; таковые, в которых R2 означает нафтил, тетрагидронафтил или аценафтил; таковые, в которых R2 означает пиридил или оксопиридил либо замещенный 3-Н-2-тиоксобензтиозолилом, (низш.)алкоксифенил-(низш.)алкокси-(низш. )алкоксигруппой, фенил-(низш. )алкокси-(низш. )алкоксигруппой, фенил-(низш. )алкилом, циклогексил-(низш.)алкоксигруппой, фенокси-(низш.)алкилом или фенил-(низш.)алкокси-(низш.)алкилом пиридил или оксопиридил, или также таковые, в которых R2 означает пиримидинил либо пиримидинил, замещенный бензодиоксанил-(низш.)алкоксигруппой, бифенилилоксигруппой, бифенилил-(низш. )алкоксигруппой, циклогексил-(низш. )алкоксигруппой, циклогексилокси-(низш. )алкоксигруппой, галогенфенил-(низш. )алкоксигруппой, галогенфенилоксадиазолил-(низш. )алкоксигруппой, инданил-(низш. )алкоксигруппой, нафтил-(низш. )алкоксигруппой, фенил-(низш.)алкилом, N-(низш.)алкилфенил-(низш.)алкокси-(низш. )алкиламиногруппой, N-(низш. )алкилфенил-(низш. )алкиламиногруппой, (низш. )алкилтиогруппой, (низш.)алкоксигруппой, (низш.)алкоксифенил-(низш. )алкокси-(низш. )алкоксигруппой, (низш.)алкоксифенил-(низш.) алкиламиногруппой, (низш. )алкилфенил-(низш. ) алкиламиногруппой, галогенфенил-(низш. )алкиламиногруппой, галогенфенокси-(низш.)алкоксигруппой, (низш. )алкилпиридил-(низш.)алкоксигруппой, фенил-(низш.)алкокси-(низш. )алкоксигруппой, фенил-(низш. )алкокси-(низш.)алкилтиогруппой, фенил-(низш. )алкокси-(низш.)алкиламиногруппой, феноксифенил-(низш.)алкоксигруппой, феноксифеноксигруппой, фенил-(низш. )алкокси-(низш.)алкоксигруппой, фенилтио-(низш. )алкоксигруппой, фенилоксазолил-(низш.)алкоксигруппой, фенил-(низш. )алкинилоксигруппой, фенил-(низш.)алкенилоксигруппой, фенил-(низш. )алкиламиногруппой, фенилпиридил-(низш. )алкоксигруппой или фенилпиридил-(низш. )алкиламиногруппой, и, наконец, таковые, в которых R2 означает галогенбензоилокси-(низш.)алкилтриазолил, фенил-(низш.)алкокси-(низш. )алкилтриазолил или фенил-(низш.)алкокси-(низш.)алкокси-(низш. )алкилтриазолил.
Особенно предпочтительными являются следующие соединения:
4-[2-[7-[(3R, 4R)-4-[4-(3-бензилоксипропокси)фенил] пиперидин-3- илоксиметил] нафталин-2-илокси]этил] морфолин;
(R)-3-[7-[(ЗR, 4R)-4-[4-(3-бензилоксипропокси)фенил]пиперидин-3- илоксиметил] нафталин-2-илокси]пропан-1,2-диол;
(S)-3-[7-[(3R, 4R)-4-[4-(3- бензилоксипропокси)фенил] пиперидин-3-илоксиметил]нафталин-2- илокси] пропан-1,2-диол;
(R)-3-[2-[7-[(3R,4R)-4-[4-(3- бензилоксипропокси)фенил]пиперидин-3-илоксиметил]нафталин-2- илокси]этокси] пропан-1,2-диол;
(S)-3-[2-[7-[(3R, 4R)-4-[4-(3-бензилоксипропокси)фенил] пиперидин-3- илоксиметил] нафталин-2-илокси] этокси] пропан-1,2-диол;
1-[2-[7-[(3R, 4R)-4-[4-(3-бензилоксипропокси)фенил] пиперидин-3- илоксиметил] нафталин-2-илокси] этил]-4-метилпиперазин;
1-[(3R, 4S)-4-[4-(3-бензилоксипропокси)фенил]пиперидин-3-ил]-2-нафталин- 2-илэтанон;
(3R, 4S, 5S)-4-[4-(3-бензилоксипропокси)фенил] -3-(1,4- диметоксинафталин-2-илметокси)пиперидин-5-ол;
(3R,4R)-4-[4-(3-бензилоксипропокси)фенил]-3-[7-[(R)-2,3- дигидроксипропоксиметил] нафталин-2-илметокси] пиперидин;
(3R,4R)-4-[4-(3-бензилоксипропокси)фенил]-3-[7-[(S)-2, 3- дигидроксипропоксиметил] нафталин-2-илметокси] пиперидин;
(3R,4R)-4-[4-(3-бензилоксипропокси)фенил]-3-[6-[(R)-2,3- дигидроксипропоксиметил] нафталин-2-илметокси] пиперидин;
(3R, 4R)- 4-[4-(3-бензилоксипропокси)фенил]-3-[6-[(S)-2,3- дигидроксипропоксиметил] нафталин-2-илметокси] пиперидин;
4-[(3R,4S, 5S)-4-[4-(3-бензилоксипропокси)фенил]-3-(нафталин-2- илметокси) пиперидин-5-илокси] бутан-1-ол;
3-[(3R, 4S, 5S)-4- [4-(3-бензилоксипропокси)фенил] -3-(нафталин-2-илметокси)пиперидин-5-илокси]пропан-1-ол;
1-{ 2-[(3R,4R,5S)-4-[4-(3-бензилоксипропокси)фенил]-3-(нафталин-2- илметокси)пиперидин-5-илокси]этил}-4-метилпиперазин;
4-[2-(3R, 4R, 5S)-[4-[4-(3-бензилоксипропокси)фенил] -3-(нафталин-2- илметокси) пиперидин-5-илокси]этил]морфолин;
(3R,4S, 5S)-4-[4-(3-бензилоксипропокси)фенил]-3-(4-метоксибензилокси) пиперидин-5-ол;
(3R, 4S, 5S)-4-[4-(3-бензилоксипропокси)фенил] -3,5-бис(4-метоксибензилокси) пиперидин;
(3S, 4R, 5R)-4-[2-[4-[4-[(3-бензилоксипропокси)фенил]-5-(нафталин-2- илметокси)пиперидин-3-илметокси]этил]морфолин;
(3S,4R, 5R)-4-[4-(3-бензилоксипропокси)фенил]-3-метоксиметил-5- (нафталин-2-илметокси)пиперидин;
(3S, 4R, 5R)-4-[4-(3-бензилоксипропокси)фенил] -5-(нафталин-2- илметокси)пиперидин-3-илметиловый эфир [3-(4-метилпиперазин-1-ил) пропил] карбаминовой кислоты;
(3S,4R, 5R)-4-[4-[4-(3-бензилоксипропокси)фенил]-5-(нафталин-2-илметокси) пиперидин-3-илметилсульфанил] пиридин;
2-(4-циклогексилбутокси)-5-[(3R, 4R)-3-(1,4-диметоксинафталин-2-илметокси) пиперидин-4-ил]пиримидин;
(3'R, 4'R)-6-(3-циклогексилпропокси)-3'-(1,4- диметоксинафталин-2-илметокси)-1',2',3',4',5',6'- гексагидро-[3,4']бипиридин;
(3S, 4R, 5R)-[4-[4-(3-бензилоксипропокси)фенил] -5- (нафталин-2-илметокси)пиперидин-3-ил]метанол;
(3S, 4R, 5R)-N-[4-[4-(3-бензилоксипропокси)фенил] -5- (нафталин-2-илметокси)пиперидин-3-илметил]-N,N',N'- тpиметилэтaн-1,2-диaмин;
(3S, 4R, 5R)-[4-[4-(3- бензилоксипропокси)фенил]-5-(нафталин-2-илметокси)пиперидин-3- илметил]диэтиламин;
1-[(3R, 4S, 5S)-4-[4-(3-бензилоксипропокси)фенил] -5- (2-морфолин-4-илэтоксиметил)пиперидин-3-ил]-2-нафталин-2-илэтанон;
(3R, 4R)-3-(1,4-диметоксинафталин-2-илметокси)-4-[4-[3-(2- метоксифенокси)пропокси] фенил] пиперидин;
(3R, 4S, 5S)-4-[4-(3-бензилоксипропокси)фенил]-3,5-бис(3,4,5-триметоксибензилокси)пиперидин;
(3R, 4R, 5S)-4-[4-(3-бензилоксипропокси)фенил]-3-(нафталин-2-илметокси)- 5-[1,2, 4]триазол-1-илметилпиперидин;
(3R, 4R)-4-[4-[3-(2-метоксибензилокси)пропокси] фенил]-3- (хинолин-7-илметокси) пиперидин;
2-(7-{ (3R, 4R)-4-[4-(3- бензилоксипропокси)фенил] пиперидин-3-илоксиметил} нафталин-2- илметокси)этанол;
7-{ (3R, 4R)-4-[4-(3-бензилоксипропокси) фенил] пиперидин-3-илоксиметил} нафталин-2-илметил)диметиламин;
(3R,4R)-3-(4-бензилоксинафталин-2-илметокси)-4-(4-фторфенил) пиперидин;
(3'R, 4'R)-3'-(1, 4-диметоксинафталин-2-илметокси)-6- [3-(2-метоксибензилокси)пропокси]-1',2',3',4',5',6'- гексагидро[3,4']бипиридин;
(3R,4R)-3-(1, 4-диметоксинафталин-2-илметокси)-4-[4-[3- (2-метоксибензилокси)пропокси]фенил]пиперидин;
(3S, 4R, 5R)-1-[4-[4-(3-бензилоксипропокси)фенил] -5- (нафталин-2-илметокси)пиперидин-3-илметил]имидазолидин-2-он;
(3R, 4R)-4-[4-[3-(2-метоксибензилокси)пропокси]фенил]-3-(2- оксо-1,2-дигидрохинолин-7-илметокси)пиперидин;
(3R, 4R)-3-(изохинолин-7-илметокси)-4-[4-[3-(2- метоксибензилокси)пропокси]фенил]пиперидин;
(3R, 4R)-4-[4-[3-(2-метоксибензилокси)пропокси]фенил]-3-(1,2,3, 4- тетрагидрохинолин-7-илметокси)пиперидин;
1-[2-[7-[(3R,4R)-4-[4-[3-(2-метоксибензилокси)пропокси]пиперидин-3- илоксиметил]нафталин-2-илокси]этил]-4-метилпиперазин;
1-[2-[7-[(3R, 4S, 5S)-5-гидрокси-4-[4-[3-(2-метоксибензилокси)пропокси] пиперидин-3-илоксиметил]нафталин-2-илокси]этил]-4- метилпиперазин;
(3R,4S,5S)-3-(1, 4-диметоксинафталин-2-илметокси)-4-[4-[3-(2- метоксибензилокси)пропокси]фенил]пиперидин-5-ол;
(3R,4R,5S)-3-(1, 4-диметоксинафталин-2-илметокси)-4-{4-[3-(2- метоксибензилокси)пропокси]фенил}-5-(1Н-тетразол-5-илметил) пиперидин и
(3'S, 4'S)-3'-(1,4-диметоксинафталин-2-илметокси) -4-[3-(2-метоксибензилокси)пропокси]-1',2',3',4',5',6'- гексагидро[1,4']бипиридин-2-он.
Под понятием "фармацевтически применимые соли" имеются в виду соли, получаемые с помощью неорганических и органических кислот, таких как соляная кислота, бромистоводородная кислота, азотная кислота, серная кислота, фосфорная кислота, лимонная кислота, муравьиная кислота, малеиновая кислота, уксусная кислота, янтарная кислота, винная кислота, метансульфоновая кислота, п-толуолсульфоновая кислота и т.п.
Соединения формулы I могут быть получены согласно изобретению благодаря тому, что из соединения формулы II

в которой P1 представляет собой защитную группу, а остальные символы имеют значения, указанные в п.1 формулы изобретения, и необязательно содержащиеся в R1, R2 и R4 гидроксильные группы могут быть представлены в защищенном виде, защитную(ые) группу(ы) отщепляют, при необходимости в полученном таким путем соединении формулы I реакционноспособную группу функционально модифицируют и/или соединение формулы I переводят в фармацевтически применимую соль, при этом исключение составляет получение 4-(4-фторфенил)-3-(3,4- метилендиоксибензилокси)пиперидина и его гидрохлорида.
Отщепление защитной группы P1 и необязательно присутствующих гидроксильных защитных групп может осуществляться по известной технологии. Примерами защитных групп P1 являются обычные аминозащитные группы, такие как трет-бутоксикарбонил, бензилоксикарбонил, винилоксикарбонил, алкилсилилалкилоксикарбонил, такой как 2-(триметилсилил)этоксикарбонил, и трихлорэтоксикарбонил. Примерами гидроксильных защитных групп могут служить эфирозащитные группы, такие как тетрагидропиранил, аллил, 2-(триметилсилил)этоксиметил, тритил, трет-бутилдиметилсилил, или сложноэфирные защитные группы, такие как ацетил.
Отщепление этих защитных групп проводят путем кислотного либо основного гидролиза, путем гидрогенолиза, методами восстановления или с помощью кислот Льюиса. При кислотном гидролизе применяют предпочтительно раствор минеральной кислоты, такой как хлористоводородная кислота, бромистоводородная кислота, серная кислота, фосфорная кислота и т.п., в инертном растворителе либо в смеси растворителей. Пригодными для этих целей растворителями являются спирты, такие как метанол или этанол, простые эфиры, такие как тетрагидрофуран или диоксан, хлорированные углеводороды, такие как метиленхлорид, и.т.п. Для основного гидролиза могут применяться гидроксиды и карбонаты щелочных металлов, такие как гидроксид калия либо натрия или карбонат калия либо натрия, органические амины, такие как пиперидин, и т.п. Инертные органические растворители, указанные выше для кислотного гидролиза, могут использоваться в качестве агентов растворения. Температуру реакции при кислотном и основном гидролизе можно варьировать в интервале от 0oС до температуры дефлегмации, причем работают предпочтительно в диапазоне от 0oC до комнатной температуры. трет-Бутоксикарбонильный остаток целесообразно отщеплять с помощью соляной кислоты, хлористого водорода, трифторуксусной кислоты или муравьиной кислоты в присутствии либо при отсутствии инертного растворителя. Указанный трет-бутоксикарбонильный остаток можно также отщеплять с помощью безводного бромида цинка в присутствии инертного растворителя, предпочтительно метиленхлорида. Отщепление трихлорэтоксикарбонильной группы может осуществляться предпочтительно путем восстановления цинком в ледяной уксусной кислоте. Температура реакции может находиться в интервале от 0 до 40oC, причем предпочтительно работают при комнатной температуре. Отщепление 2-(триметилсилил)этоксикарбонильного остатка может осуществляться с помощью ионов фторида в присутствии инертного растворителя, такого как ацетонитрил, диметилсульфоксид, диметилформамид или тетрагидрофуран, предпочтительно с помощью фторида тетрабутиламмония в тетрагидрофуране, при температурах в интервале от 0oC до примерно комнатной температуры.
Соединения формулы II являются новыми и также являются предметом изобретения. Их получение подробнее поясняется на схемах 1-15, представленных в конце описания, и в примерах.
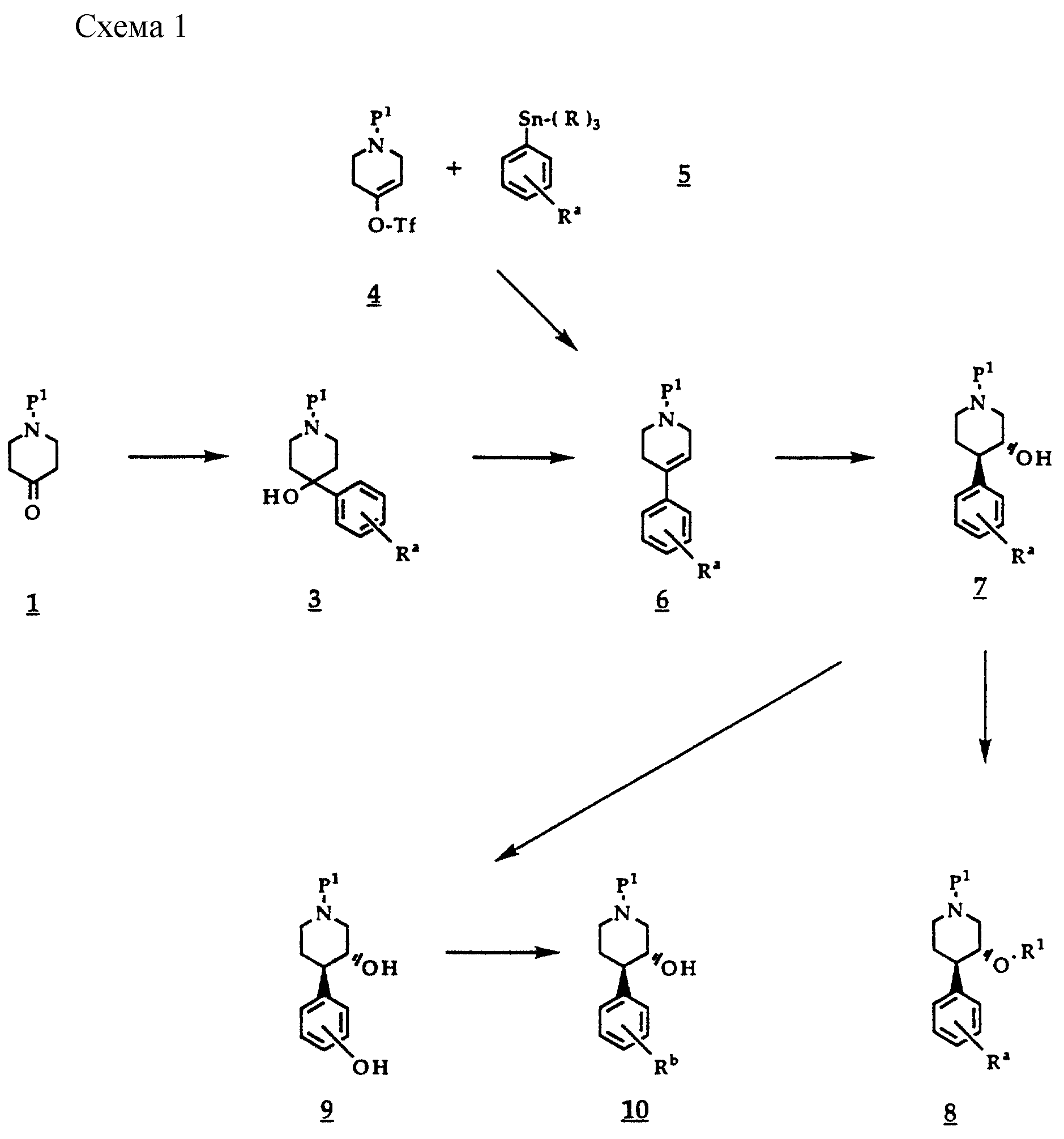
Согласно схеме 1 соединения общей формулы 3 могут быть получены осуществляемым по известной методике взаимодействием соединений общей формулы 1 с металлоорганическими производными, предпочтительно производными лития или магния, получаемыми из соединений общей формулы 2
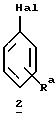
где Ra представляет собой водород или заместитель, который является инертным в условиях реакции или в котором реакционноспособные группы представлены в защищенном виде. Предпочтительно исходят из соединений 2, в которых Ra означает галоген, (низш.)алкокси или бензилокси, и используют эти заместители для построения другого требуемого заместителя на соответствующей последующей стадии осуществления реакции.
Взаимодействие с металлоорганическим соединением указанного типа осуществляют по известным методам, например в инертном в условиях реакции растворителе, таком как простой эфир, при температуре в интервале от -78 до +75oC. Таким путем в присутствии кислоты или каких-либо других отщепляющих воду реагентов, необязательно в присутствии основания, в органическом растворителе можно получить соединения общей формулы 6. В качестве кислот приемлемы среди прочих, например, соляная кислота, трифторуксусная кислота или п-толуолсульфоновая кислота, а в качестве отщепляющего воду реагента может применяться, например, фосфорокситрихлорид в пиридине. Температура реакции находится в диапазоне от 0 до 120oC, а в качестве растворителя могут использоваться, например, толуол, диметилформамид или спирты.
Получение соединений общей формулы 6 можно осуществлять также непосредственно, исходя из соединения общей формулы 4, в которой Tf представляет собой активирующую группу, такую как трифторметилсульфонил (трифлат), взаимодействием с металлоорганическим соединением, в частности с производным олова общей формулы 5, в которой R означает (низш.)алкил, например бутил, или с соответствующим производным арилборной кислоты с использованием пригодного для этих целей катализатора, такого, например, как тетракистрифенилфосфинпалладий, в инертном растворителе, таком как диоксан, диметоксиэтан или диметилформамид, при температурах в диапазоне от комнатной температуры до 150oC.
Соединения общей формулы 7 могут быть получены гидроборированием с последующей основной окислительной переработкой соединений общей формулы 6. Гидроборирование может осуществляться по известным методам, например, в инертном в условиях реакции растворителе, таком как простой эфир, например 1,2-диметоксиэтан, в диапазоне температур от 0 до 70oC и с помощью реагента, содержащего либо высвобождающего диборан, такого, например, как боран в тетрагидрофуране или смесь из борогидрида натрия и этерата боротрифторида. Образующиеся в качестве промежуточных продуктов карбобораны взаимодействием с основанием, например с гидроксидом калия, и с окислителем, например с пероксидом водорода, при температурах в интервале от комнатной температуры до 120oC могут переводиться во вторичные спирты общей формулы 7.
Соединения общей формулы 8, в которой Ra представляет собой галоген, циано, трифторметил, (низш. )алкил, (низш. )алкокси-(низш. )алкил, (низш. )алкокси или (низш.)алкилендиокси, могут быть получены из соединений 7 путем алкилирования соединением, отдающем остаток R1. Алкилирование вторичного спирта осуществляют по известным методам, например, в инертном в условиях реакции растворителе, таком как простой эфир, например тетрагидрофуран или 1,2-диметоксиэтан, или диметилформамид, с помощью образующего алкоголят основания, например гидрида натрия, при температуре в интервале от 0 до 40oC и с использованием галогенида, предпочтительно хлорида либо бромида, или эфира сульфоновой кислоты, например мезилата либо тозилата, в качестве соединения, отдающего R1. Соединения общей формулы 7, в которой Ra представляет собой (низш.)алкокси, за счет отщепления алкиларилового эфира могут переводиться в соединения общей формулы 9. Отщепление эфира осуществляют по известным методам, а именно предпочтительно исходя из соединений, где Ra означает метокси, алкилариловый эфир подвергают взаимодействию с минеральными кислотами, такими как бромистоводородная кислота либо иодистоводородная кислота, или предпочтительно с кислотами Льюиса, такими как трихлорид бора либо трибромид бора, в инертном в условиях реакции растворителе, таком, например, как галоидированный углеводород, при температуре в интервале от приблизительно -10oC до комнатной температуры.
Соединения общей формулы 9 могут служить исходными субстанциями для получения соединений общей формулы 10, в которой Rb представляет собой остаток -T1-L2-T2-L3-T3-L4-T4-U, где T1 представляет собой кислород, (н), (п) или (р), а другие заместители L2,3,4, T2,3,4 и U могут иметь значения, указанные выше. Присоединение остатка -L2-T2-L3-T3-L4-T4-U может осуществляться выборочно взаимодействием с несущим соответствующую уходящую группу производным вводимого остатка, причем требуемый остаток может быть также построен по стадийному механизму. Селективное присоединение к фенольному спирту осуществляют по известным методам алкилирования, соответственно ацилирования в присутствии основания, такого как карбонат калия. В качестве ацилирующих агентов приемлемы хлориды, бромиды, иодиды, тозилаты или мезилаты. Реакцию проводят в инертном в условиях реакции растворителе, например в простом эфире, таком как тетрагидрофуран, в ароматическом углеводороде, как, например, толуол, пиридин, ацетон или метилэтилкетон, при температуре в интервале от приблизительно 0 до 100oC. Пригодными для указанных целей ацилирующими агентами являются активированные производные, такие как необязательно активированные сложные эфиры, галогениды кислот, ангидриды кислот или смешанные ангидриды кислот. Реакцию осуществляют в инертном в условиях реакции растворителе, например в простом эфире, таком как тетрагидрофуран, в ароматическом углеводороде, таком как толуол, в хлорированном углеводороде, таком как метиленхлорид или хлороформ, и т.п. при температуре в интервале от 0 до 50oC.
Во вводимом остатке наряду с уходящей группой содержащиеся реактивные группы, такие как кето- или гидроксигруппы, представлены при этом в соответствующем защищенном виде, например в виде ацеталей, сложных эфиров, карбаматов, производных силила и т.п. После отщепления этих защитных групп может быть продолжено построение по стадийному механизму остатка -T1-L2-T2-L3-T3 -L4-T4-U. Содержащуюся в пиперидиновом кольце полученных таким путем соединений гидроксильную группу можно алкилировать аналогично тому, как это описано выше, для превращения соединений формулы 7 в соединения формулы 8.
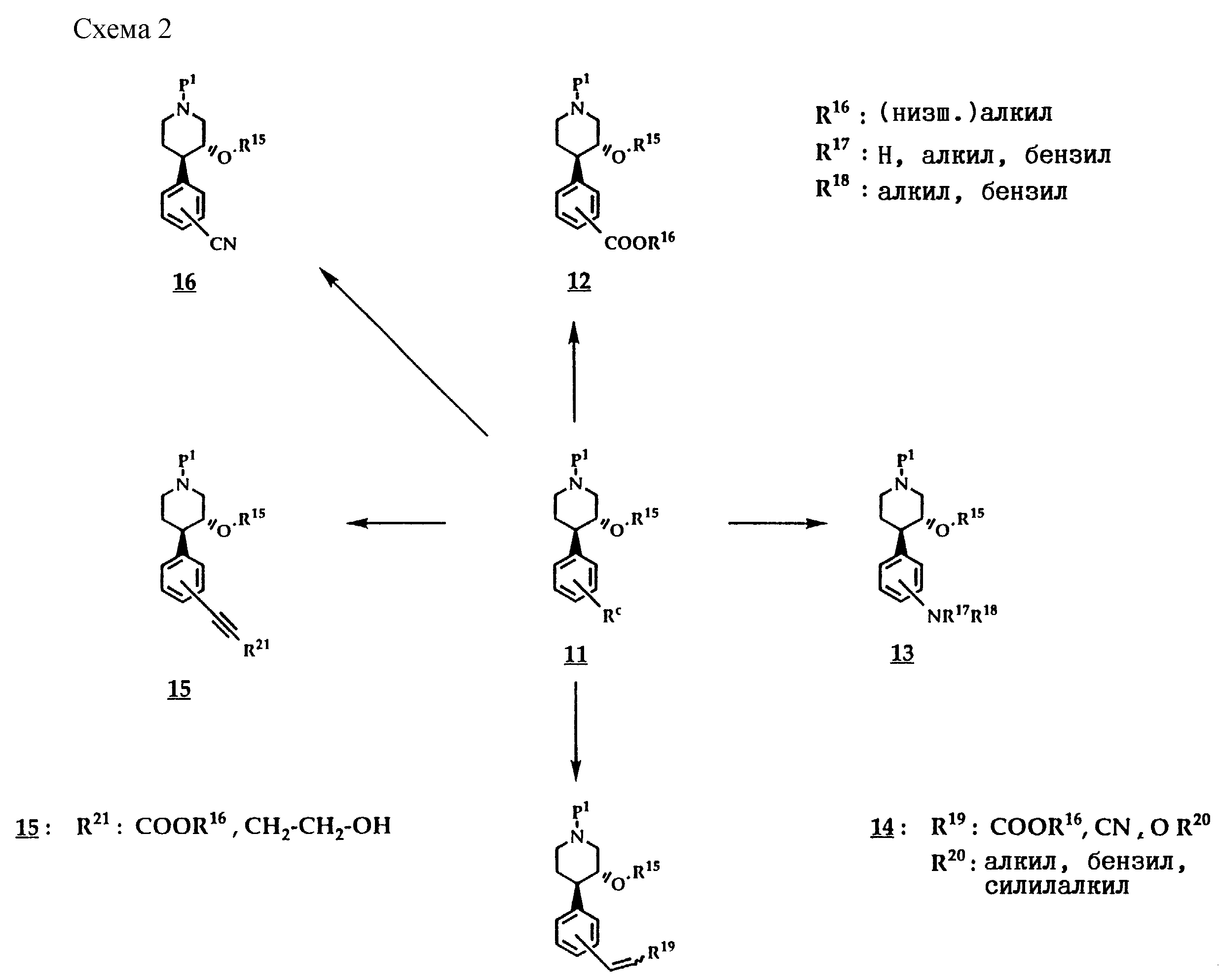
Согласно схеме 2 исходя из соединений общей формулы 11, в которой Rс представляет собой хлор, бром, иод, а также гидроксильную группу в виде активированного производного, как, например, трифлат, R15 означает водород или инертный в условиях реакции остаток R1, могут быть получены следующим путем соединения формул 12-16: по известной методике осуществляют катализированную палладием реакцию сочетания с моноксидом углерода, цианидами, аминами либо с соединениями общих формул
H2C = CH-R19 или
HC=C-R19
где R19 представляет собой -COOR16, -CN или -OR20. В качестве палладиевых катализаторов могут использоваться при этом полученные in situ комплексы, например PdCl2(CH3CN)2 или Pd(OAc)2 с 1,1'-бис(дифенилфосфино)ферроценом, 1, 3-бис(дифенилфосфино)пропаном или три(о-толил)фосфином. В полученных таким путем соединениях остатки -HC=CH-R19 или -C= C-R19 могут быть дериватизированы для дальнейшего построения по стадийному механизму остатка -L1-T1-L2-T2-L3-T3-L4- T4-U. Тройная связь C≡C может переводиться в двойную связь, а последняя может переводиться в одинарную связь. Цианогруппу можно переводить в амид, альдегид, кислоту, сложный эфир либо в амин. Соединения формулы 13, где R17, 18 означают бензил, могут быть дебензилированы, а образующиеся при этом вторичную, соответственно первичную аминогруппу также можно использовать для дальнейшей дериватизации. Все эти превращения и дериватизации, представленные на схемах 3-9, но не ограниченные ими, могут осуществляться по известным методам.
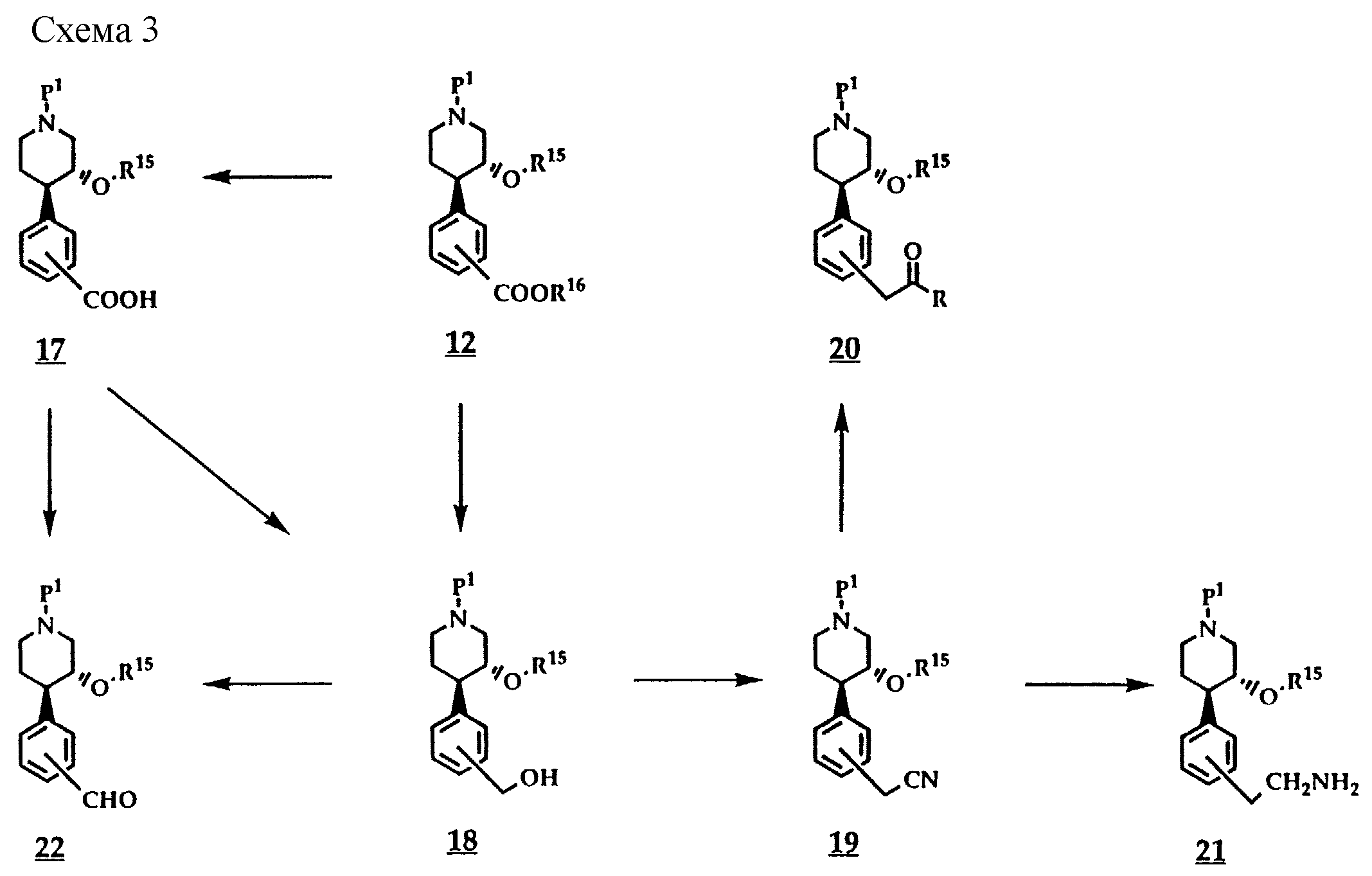
Согласно схеме 3 из соединений общей формулы 12, получаемых взаимодействием соединений общей формулы 11 с моноксидом углерода путем палладиевого катализа, могут быть получены соединения общих формул 17-22.
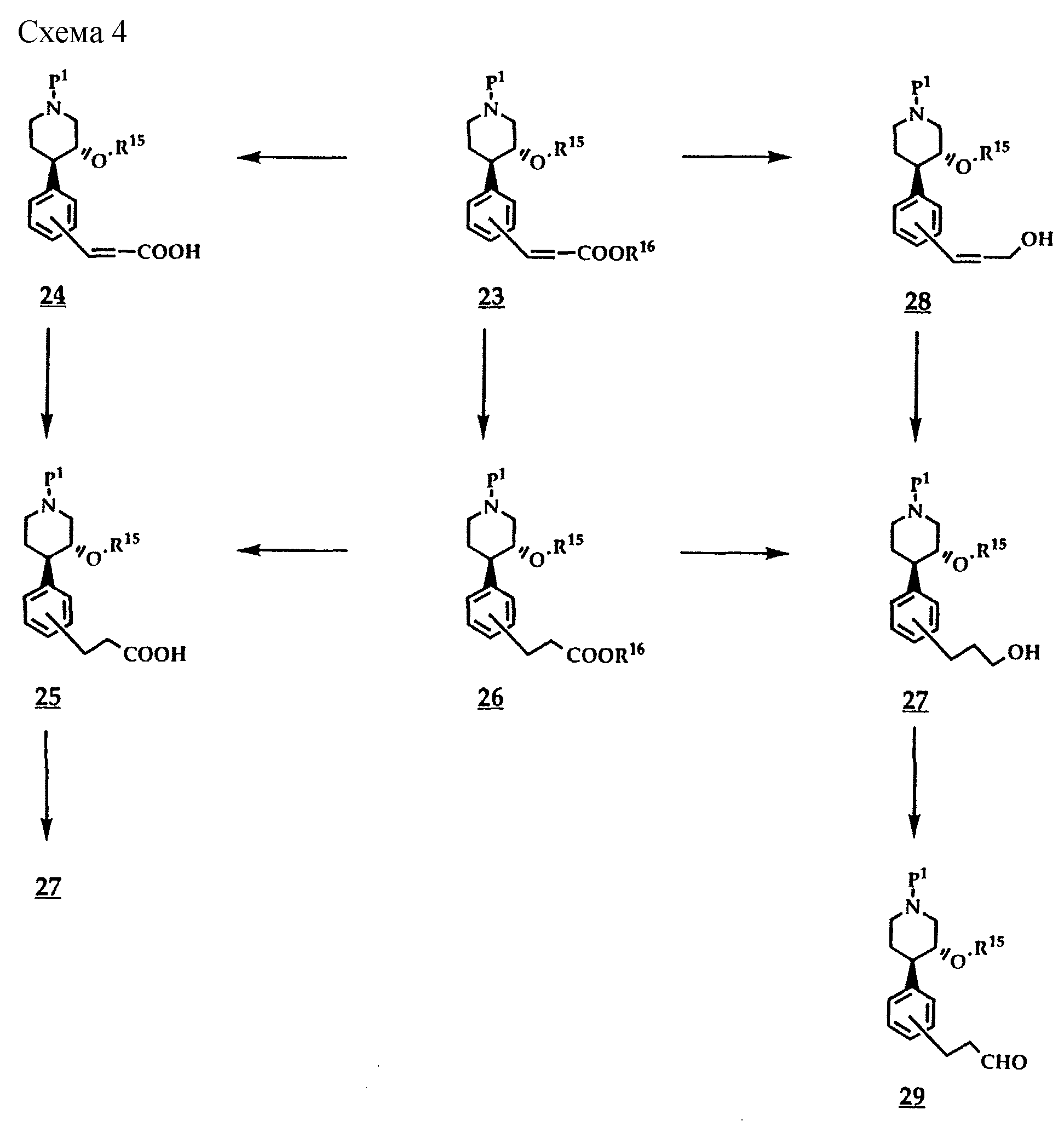
Согласно схеме 4 из соединений общей формулы 23, получаемых взаимодействием соединений общей формулы 11 с эфирами акриловой кислоты путем палладиевого катализа, могут быть получены соединения общих формул 24-29.
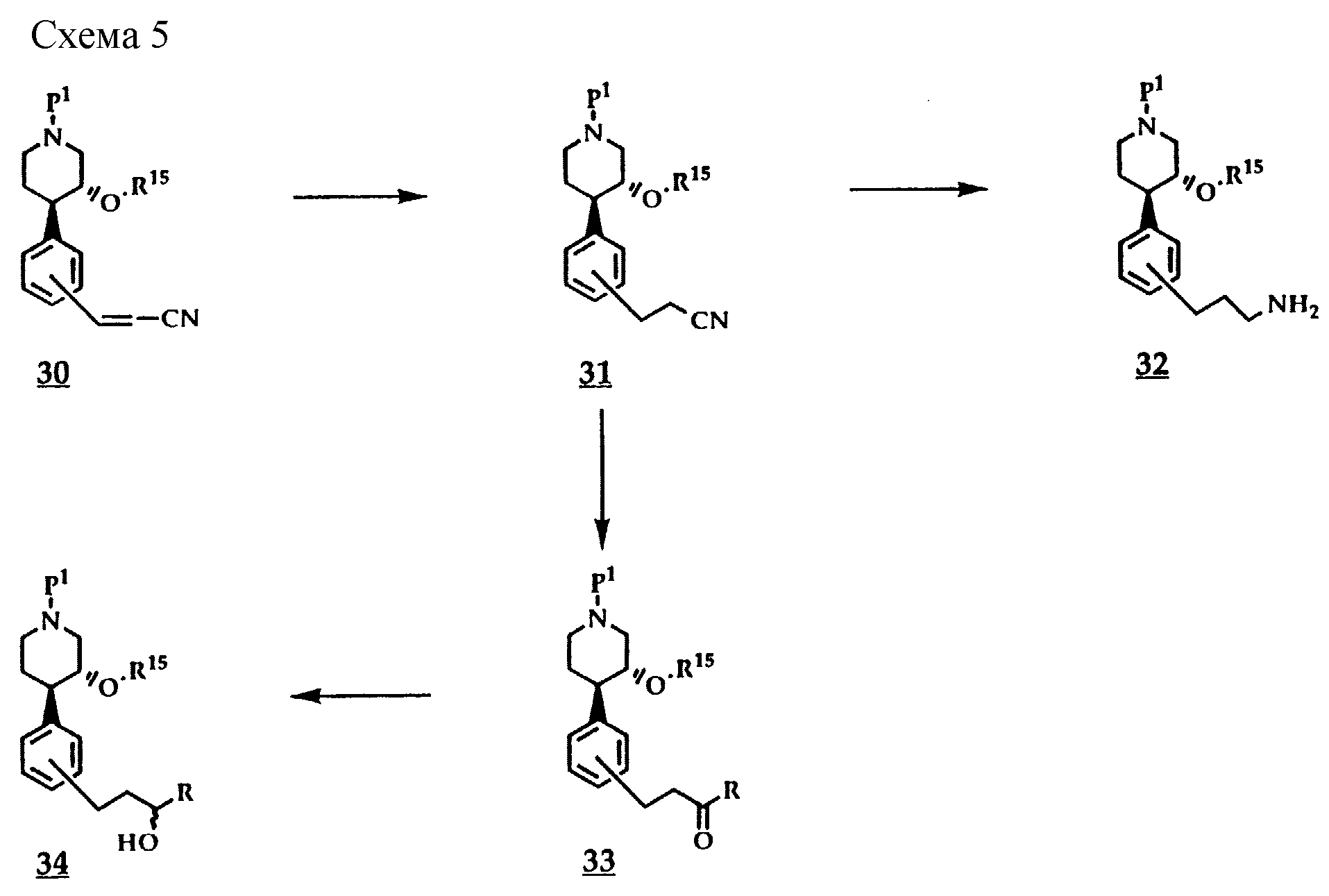
Согласно схеме 5 из соединений общей формулы 30, получаемых взаимодействием соединений общей формулы 11 с акрилнитрилом путем палладиевого катализа, могут быть получены соединения общих формул 31-34.
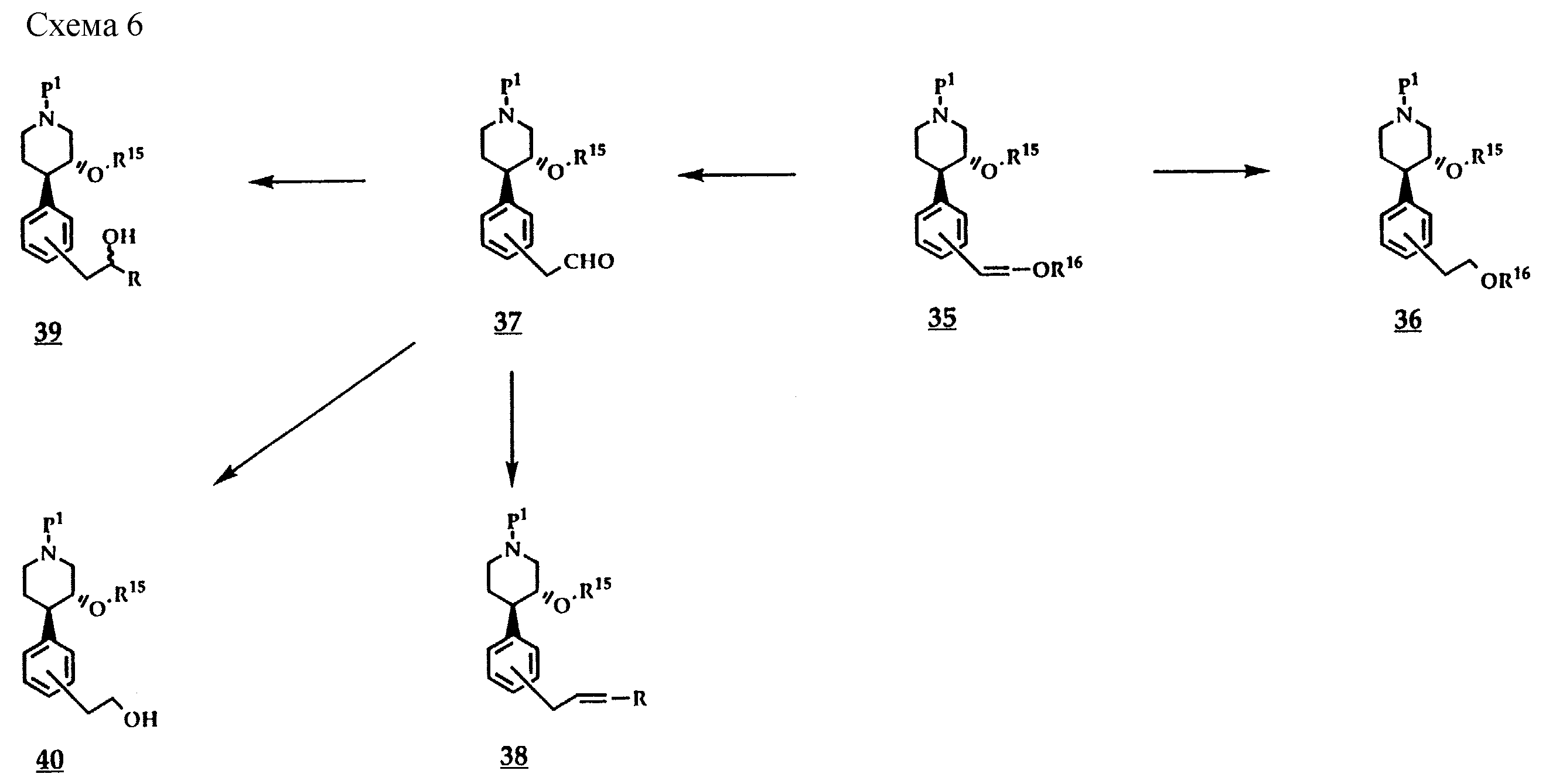
Согласно схеме 6 из соединений общей формулы 35, получаемых взаимодействимем соединений общей формулы 11 с виниловыми эфирами путем палладиевого катализа, могут быть получены соединения общих формул 36-40.
Пиперидоны общей формулы 41 по методике, аналогичной описанной для пиперидона 1, могут использоваться в качестве исходных веществ для синтеза производных пиперидина 1. Их можно получить по способу, аналогичному описанному A. H. Beckett и др. в Journal of Medicinal and Pharmaceutical Chemistry, том 1(1), стр. 37-58 (1959). Пиперидоны общей формулы 41 могут быть получены за счет внутримолекулярного замыкания кольца производного пропионовой кислоты общей формулы 42.

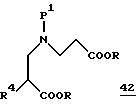
В приведенных формулах R4 имеет значения, указанные выше, либо представляет собой заместитель, который является инертным в условиях реакции или в котором реакционноспособные группы представлены в соответствующем защищенном виде. Предпочтительно R4 выбирают таким образом, чтобы при необходимости обеспечить возможность построения другого требуемого заместителя на соответствующей последующей стадии проведения реакции. P1 означает метил или бензил. Это замыкание кольца осуществляют в присутствии основания, такого, например, как алкоголят натрия, гидрид натрия или натриевая дисперсия в ксилоле. Последующее декарбалкоксилирование полученного таким путем соединения общей формулы 43 или 44
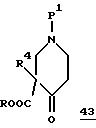

с использованием соляной кислоты приводит к соединениям общей формулы 41.
Производные общей формулы 43, в которых R4 означает аллил или бензил, также могут быть получены прямым путем C-алкилированием натриевой соли соединения общей формулы 45
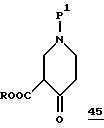
с помощью бромида аллилдиметиланилина, соответственно бромида бензилдиметиланилина по способу, аналогичному описанному A.H.Beckett и др. (см. выше).
Производные общей формулы 41, в которых R4 означает гидроксиметил, соответствующим образом защищенный по гидроксильной функции, также могут быть получены из соединения общей формулы 45 восстановлением до диола по способу, аналогичному описанному Е. Jaeger и J.H. Biel в Journ. Org. Chem. 30(3), стр. 740-744 (1965), введением соответствующей защитной группы для первичного спирта, как, например, тритил, и окислением вторичного спирта.
Далее могут быть получены производные общей формулы 46 гидроксиметилированием соединений общей формулы 6 по способу, аналогичному описанному К. Willcocks и др. в Journ. of Labelled Compounds and Radiopharmaceuticals, том XXXIII, N 8, стр. 783-794 (1993).

Соединения общей формулы II, в которой R3 означает водород, a W означает кислород или серу, могут быть получены исходя из соединений общей формулы 47
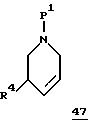
путем эпоксидирования. Соединения общей формулы 47 могут быть получены в свою очередь по способу, описанному М. Ferles и М. Jankovski в Coll. Czechoslov. Chem. Commun. , том 35, стр. 2802-2809 (1970). Эпоксидное кольцо может быть затем раскрыто взаимодействием с соответствующими тиофенолятами и фенолятами аналогично тому, как это описано R. Paioni в выложенной заявке Германии 2738477. Последующий синтез с получением соединений формулы II может осуществляться аналогично тому, как это описано выше.
Согласно схеме 7 могут быть получены соединения общей формулы 51 из соединений общей формулы 46 благодаря тому, что сначала двойную связь с использованием комплексных гидридов, например алюмогидрида лития, как это описано J. M. Lundbeck и др. в европейской патентной заявке ЕР 0374674, или дигидро-бис(2-метоксиэтокси)алюмината натрия, в инертном в условиях реакции растворителе, таком как тетрагидрофуран, диоксан или толуол, при температурах в интервале от комнатной температуры до 110oC восстанавливают или с использованием катализатора гидрируют водородом, в результате чего получают соединения общей формулы 48. Соединения общей формулы 48 по обычным способам окисления, например, с использованием оксалилхлорида и диметилсульфоксида, как это описано A.J. Mancuso и D. Swern в Synthesis 1981, 165, могут переводиться в соответствующие альдегиды общей формулы 49.
Реакция конденсации между альдегидами общей формулы 49 и соединениями Гриньяра или литиевыми соединениями, осуществляемая в инертных в условиях реакции растворителях, таких как простые эфиры, тетрагидрофуран или диоксан, при температурах в интервале от -80oC до комнатной температуры, приводит к соединениям общей формулы 50, которые могут переводиться по известным способам в соответствующие сложноэфирные и эфирные соединения общей формулы 51.
Согласно схеме 8 могут быть получены соединения общей формулы 54 благодаря тому, что бромированием соединений общей формулы 1 в инертном в условиях реакции растворителе, таком как хлороформ или метиленхлорид, и с использованием буферной соли, такой как гидрофосфат динатрия, при температурах в интервале от 0 до 50oC сначала образуют соединения общей формулы 52, которые подвергают взаимодействию с щелочно-металлической солью тиола в растворителе, таком как ацетон, ацетонитрил или диметилформамид, при температурах в интервале от комнатной температуры до 100oC с получением в результате соединений общей формулы 53. Реакцией конденсации между последними и соединениями Гриньяра или литиевыми соединениями, осуществляемой в инертных растворителях, таких как простые эфиры, тетрагидрофуран или диоксан, при температурах в интервале от -80oC до комнатной температуры, получают затем соединения общей формулы 54.
Согласно схеме 9 могут быть получены соединения общей формулы 56 путем дигидроксилирования соединений общей формулы 6 до соединений общей формулы 55. Алкилированием последних по уже описанным выше способам получают соединения общей формулы 56. Дигидроксилирование может осуществляться по известным методам, например, в инертном в условиях реакции растворителе, таком как ацетон или трет-бутанол, при температуре в интервале от 0 до 50oC, предпочтительно при комнатной температуре, с помощью гидроксилирующего реагента, как, например, смесь из тетроксида осмия и пероксид водорода.
Полученные согласно схемам 2-9 соединения могут в свою очередь использоваться в качестве исходного материала для последующего построения необязательно присутствующего в R2 заместителя -L1-T1-L2-T2 -L3-T3- L4-T4-U, указанного выше.
Кроме того, соединения общей формулы II с имеющимся этиленовым мостиком Q могут быть получены по способам, представленным на схемах 1-9, а также по способам, более подробно описанным выше и в примерах.
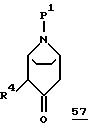
Используемые в качестве исходных веществ тропиноны общей формулы 57 могут быть получены, в частности, по способам, описанным М. Lounasmaa и C.J. Johansson в Tetrahedron Letters, N 29, стр. 2509 (1974) или Ö.Kovács и др. в Helv. Chim. Acta, том XXXVII, стр. 802 (1954).
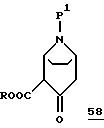
Производные общей формулы 57 могут быть получены из соединения общей формулы 58 аналогично способу, описанному Ö.Kovács и др. в Helv. Chim. Acta, том XXXVII, стр. 802 (1954), восстановлением до диола, введением соответствующей защитной группы для первичного спирта, как, например, тритил, и окислением вторичного спирта. При этом R4 имеет значения, указанные выше, либо представляет собой заместитель, который является инертным в условиях реакции или в котором реакционноспособные группы представлены в соответствующим образом защищенном виде, причем R4 выбирают таким образом, чтобы была обеспечена возможность построения при необходимости другого требуемого заместителя на соответствующей последующей стадии проведения реакции.
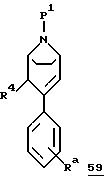
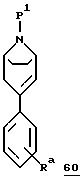
Далее могут быть получены производные общей формулы 59, в которых R4 означает гидроксиметил, гидроксиметилированием соединений общей формулы 60 по способу, аналогичному описанному К. Willcocks и др. в Journal of Labelled Compounds and Radiopharmaceuticals, том XXIII, N 8, стр. 783-794 (1993).
Кроме того, существует возможность получения производных общей формулы 57, состоящая в том, что исходя из соответственно замещенных производных ацетондикарбоновой кислоты, взаимодействием с сукциндиальдегидом и амином по способам, аналогичным известным из литературы, синтезируют соответствующее производное тропинона. Применяемые в качестве исходных веществ замещенные производные ацетондикарбоновой кислоты могут быть получены, например, по способам, описанным I. Ito и S.I. Nagai в Chem. Pharm. Bull. 22(9), стр. 2131 (1974) или Т. Arslan и S.A. Benner в Journ. Org. Chem. 58, стр. 2260 (1993).
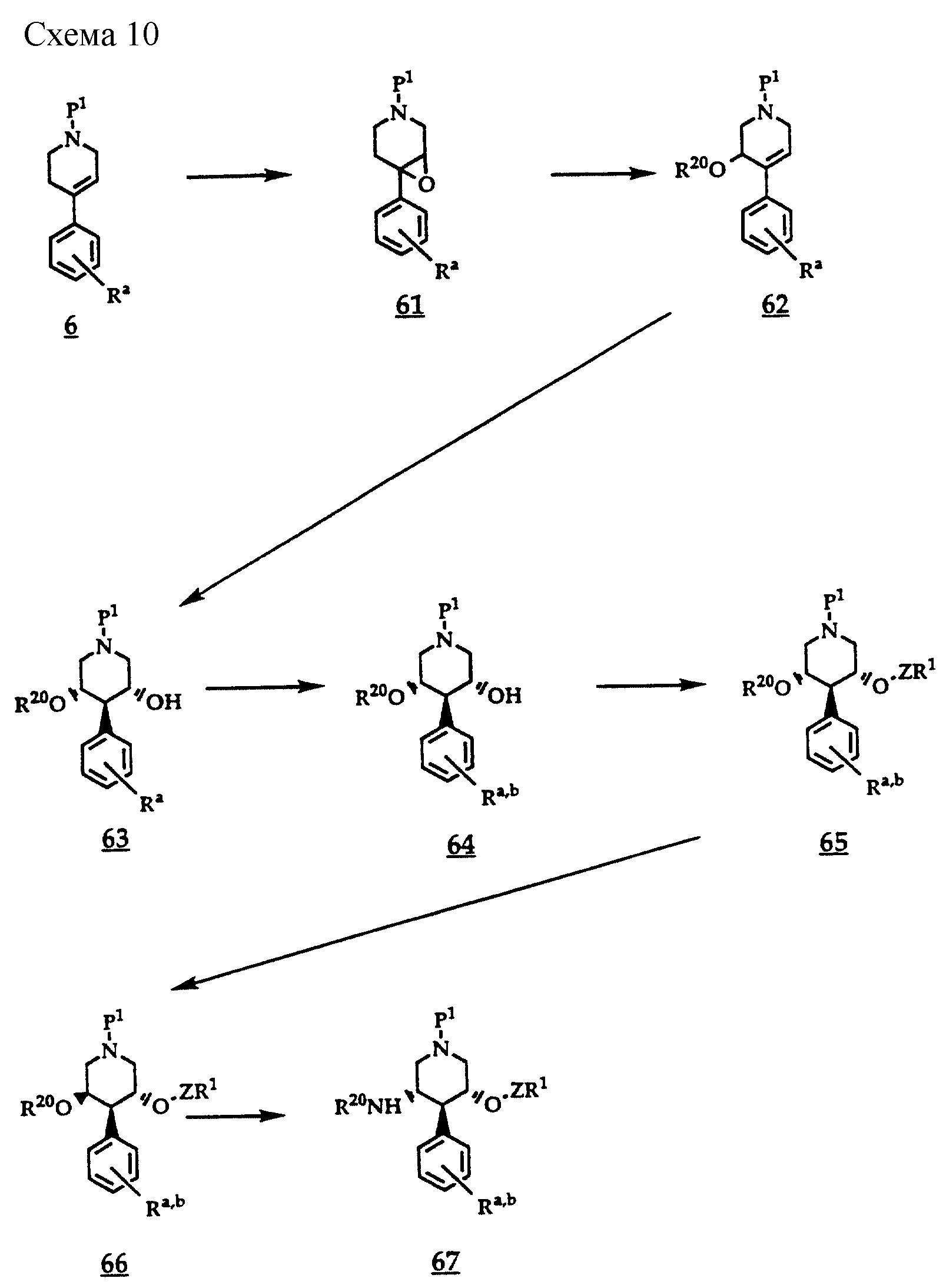
Один из возможных вариантов синтеза 4-арилпиперидинов, замещенных в положении 3 и 5 соответственно О-, соответственно N-атомами, представлен на схеме 10. Оксирановые соединения общей формулы 61 могут быть образованы из олефинов 6, например, через образующийся в качестве промежуточного продукта бромгидрин, который можно получить присоединением брома в водном диоксане. Бромгидриновое кольцо может быть затем замкнуто добавлением водного едкого натра с получением эпоксида 61. Обработке такого оксирана метиллитием, бутиллитием либо амидом лития в апротонных растворителях, таких как простые эфиры или тетрагидрофуран, при температурах в интервале от -80 до +60oC приводит к аллиловым спиртам 62, которые могут подвергаться дальнейшей переработке свободным ОН или после введения эфирной функции R20. В результате гидроборирования этих производных аллилового спирта 62, как это уже описывалось выше при получении соединений общей формулы 7, получают свободные либо монофункционализованные дигидроксипроизводные 63. Для структурной вариации остатков R20 (R4aZ1- или Н), -ZR1 и Ra в зависимости от требуемой целевой молекулы могут вводиться в различной последовательности остатки R20 и -ZR1, а остаток Ra может быть модифицирован в Rb, остаток общей формулы -T1-L2-T2-L3-T3-L4-T4-U. В зависимости от схемы построения может оказаться целесообразным предусмотреть для одной из обеих OH-функций на промежуточной стадии защитную группу и снова отщепить ее в ходе дальнейшего процесса или же остатки -ZR1 и R20 выбирать таким образом, чтобы обеспечить при необходимости построение какого-либо другого требуемого заместителя на соответствующей последующей стадии осуществления реакции. Исходя из моноэфирозащищенных производных 65, свободную OH-функцию, например, взаимодействием с муравьиной кислотой, трифенилфосфином и эфиром азодикарбоновой кислоты в инертном растворителе, таком, как тетрагидрофуран, согласно Mitsunobu [Synthesis 1981, 1], можно стереохимически инвертировать, получая при этом соединения общей формулы 66. Применение вместо муравьиной кислоты дифенилфосфорилазида в аналогичных условиях обеспечивает возможность исходя из соединений 66 повторной инверсией у того же центра вводить азидофункцию, которую, например, восстановлением трифенилфосфином/водой в тетрагидрофуране при температурах в интервале от комнатной температуры до 80oC [Synth. Commun. 17, 377 (1987)] , можно трансформировать в первичную аминофункцию. В результате получают соединения общей формулы 67, которые затем можно алкилировать или ацилировать.
Согласно схеме 11 известные из литературы производные коричной кислоты 68 могут подвергаться взаимодействию с моноамидами моноэфиров малоновой кислоты 69 в протонных растворителях, таких как этанол или метанол, либо в апротонных растворителях, таких как N,N-диметилформамид, диметилсульфоксид, тетрагидрофуран или ацетонитрил, с использованием оснований, как, например, трет-бутилат калия или гидрид натрия, при температурах в интервале от комнатной температуры до 130oC с получением в результате циклических имидов 70. Восстановлением этих имидов 70 с помощью гидридных восстановительных реагентов, таких как алюмогидрид лития, диизобутилалюмогидрид или дигидро-бис(2-метоксиэтокси)алюминат натрия, в апротонных растворителях, таких, как простые эфиры, тетрагидрофуран или диоксан, при температурах в интервале от комнатной температуры до 120oC получают моно- и диметанолы 71 пиперидина, для которых у азота пиперидина может быть предусмотрена соответствующая защитная группа. Моно- и дигидроксисоединения общей формулы 71 аналогичным путем, как это было описано выше для моно- и дигидроксисоединений 7, 10, 62, 63, 64, либо превращением в соответствующие бром-, хлор-, иодсодержащие соединения, эфиры арил- или алкилсульфокислот и последующим нуклеофильным замещением с использованием алкоголятов, фенолятов или тиофенолятов по обычной методике можно по стадийному механизму выборочно функционализовать. При этом ZR1, Z1R4a могут представлять собой заместители, имеющие значения, указанные в общей формуле I, либо представлять собой соответствующие предварительные стадии, которые в условиях реакции являются инертными или в которых реакционноспособные группы представлены в соответствующим образом защищенном виде, при этом указанные заместители предпочтительно выбирают таким образом, чтобы при необходимости обеспечить возможность построения другого требуемого заместителя на соответствующей последующей стадии осуществления реакции. Ra и Rb имеют соответственно указанные выше значения. С другой стороны, моногидроксисоединения 71, дигидроксисоединения 71 или производные 73 дигидроксисоединений 71, одна гидроксильная функция которых структурно модифицирована, путем окисления, например по Сверну (диметилсульфоксид, оксалилхлорид) [Journ. Org. Chem. 43, стр. 2480 (1978)] могут переводиться в альдегиды 74. Присоединением соединения Гриньяра или литиевого соединения, осуществляемым по известной методике в инертном растворителе, таком как тетрагидрофуран или 1,2-диметоксиэтан, при температурах в интервале от -78oC до комнатной температуры, получают затем спирты 76 (R9 является Н), которые можно при необходимости алкилировать, ацилировать или повторно окислять, например, по Сверну, и тем самым получить производные 76 (R9 не означает Н), соответственно кетоны 77. Исходя из дигидроксисоединений 71, за счет одновременного превращения обеих гидроксильных функций аналогично тому, как это описано выше, можно получить через диальдегиды 75 соединения общих формул 78 и 80. Трансформация альдегидов 74, 75 в кетоны 78, 80 может осуществляться также окислением в кислоту [например, хлоритом натрия, амидосульфокислотой и изопропенилацетатом в растворителе, таком как ацетон/вода, при температурах в интервале от 0oC до комнатной температуры согласно Journ. Am. Chem. Soc. 110, стр. 2242 (1988)], последующей реакцией сочетания между амидом и N-метил-N-метоксиамидами с использованием N, O-диметилгидроксиламина, осуществляемой по известным методам, а также их взаимодействием с литий- либо магнийорганическими соединениями в инертном растворителе, таком как тетрагидрофуран или 1, 2-диметоксиэтан, при температурах в интервале от -78oC до комнатной температуры, как это описано, например, в [Synthesis 1986, 944]. Кетоны 77 взаимодействием с необязательно замещенными производными гидроксиламина, осуществляемым в растворителе, таком как пиридин, в присутствии каталитических либо стехиометрических количеств сильной кислоты при температурах в интервале от комнатной температуры до 120oC, могут переводиться в оксимы 79, где R10 имеет значения, указанные в общей формуле I.
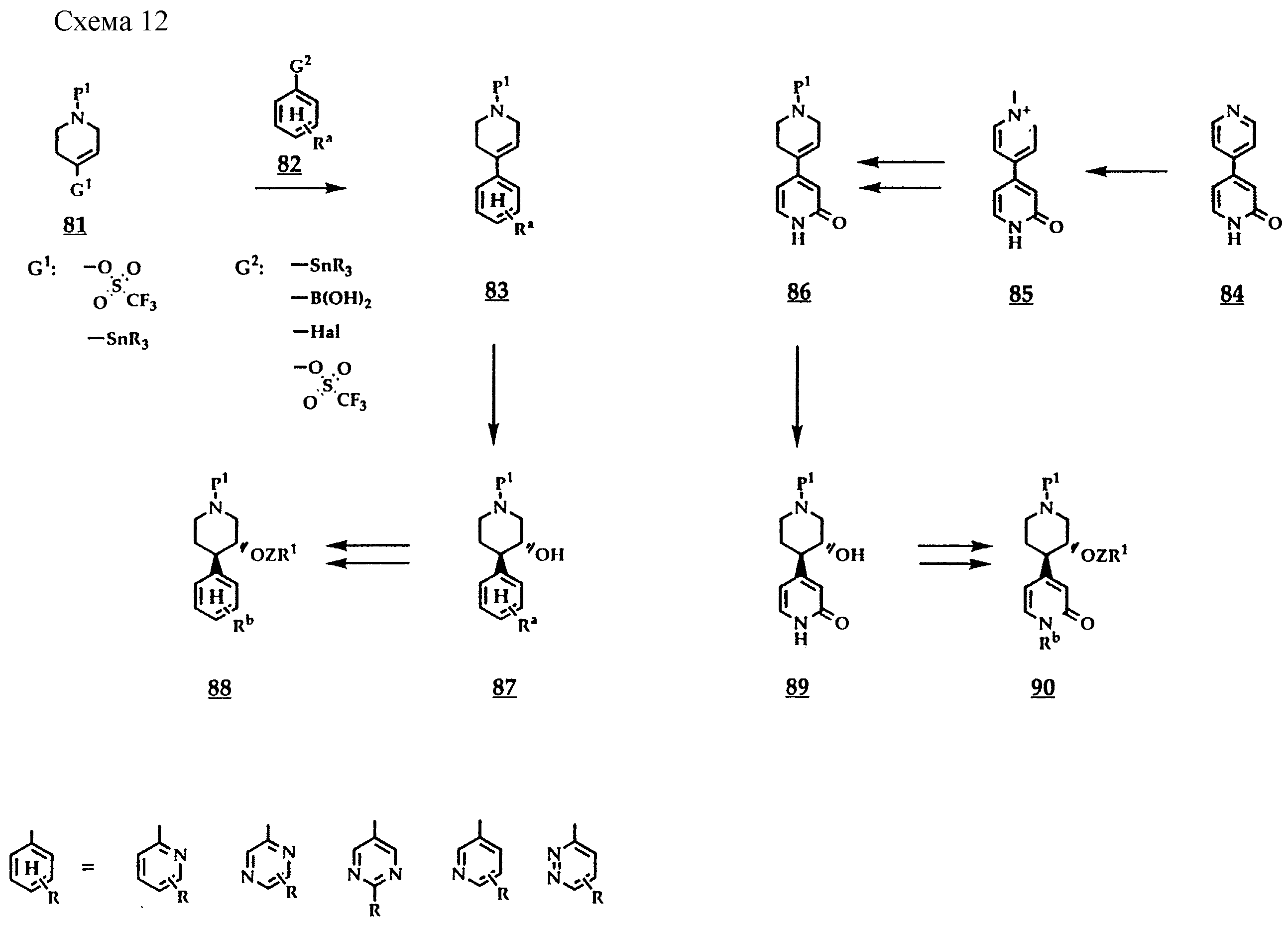
Согласно схеме 12 по стадийному механизму, например, как это описано ниже, могут быть построены соединения общих формул 88 и 90, содержащие гетероциклические заместители в положении 4 пиперидинового кольца.
Производные 4-гетероарил-1,2, 3,6-тетрагидропиридина 83 могут быть получены, например, из производных 1,2,3,6-тетрагидропиридина 81, активированных в виде енольного трифлата, реакцией конденсации с соответствующим образом функционализованными гетероароматическими соединениями 82, активированными, например, в виде соединений олова. Реакции сочетания такого типа проводят предпочтительно в инертном растворителе, таком как 1,2-диметоксиэтан, тетрагидрофуран или N,N-диметилформамид, с использованием катализатора, такого как тетракис(трифенилфосфин)палладий, при температурах до порядка 130oC. Вместо оловянных соединений в тех же целях при соблюдении идентичных условий реакции можно применять также аналогичные производные борной кислоты 82 либо аналогичное енольному трифлату 81 винилоловянное соединение 81, подвергая его взаимодействию с гетероциклическими галоидными соединениями или трифлатами 82; в обоих случаях реакции приводят к тем же самым продуктам. Производные 4-гетероарил-1,2,3, 6-тетрагидропиридина 86 могут быть получены также из пиридилгетероарилбиарильных производных типа 84 по известным методам: N-метилированием, частичным гидрированием метилированного пиридинового кольца с помощью соответствующего гидрирующего реагента, такого как борогидрид натрия, с последующим превращением N-метильной функции в соответствующую защитную группу путем диметилирующего карбамоилирования [аналогично, например, тому, как описано в Journ. Org. Chem. 49, 2081 (1984)].
Соединения общих формул 87 и 89 могут быть получены гидроборированием и последующей основной окислительной переработкой соединений общих формул 83 и 86. Гидроборирование можно осуществлять по известным методам, например, в инертном в условиях реакции растворителе, таком как простой эфир, например 1,2-диметоксиэтан, при температуре в интервале от приблизительно 0 до 70oC и с использованием содержащего либо высвобождающего диборан реагента, как, например, боран, в тетрагидрофуране, борандиметилсульфиде либо в смеси из борогидрида натрия и эфирата трифторида бора. Образующиеся в качестве промежуточных продуктов карбобораны взаимодействием с основаниями, например гидроксидом калия, и с окислителем, например пероксидом водорода, перборатом натрия или перкарбонатом натрия, с сочетанием основания и окислителя или же с N-оксидом триметиламина без добавок основания при температуре в интервале приблизительно от комнатной температуры до 120oC могут переводиться во вторичные спирты общих формул 87 и 89.
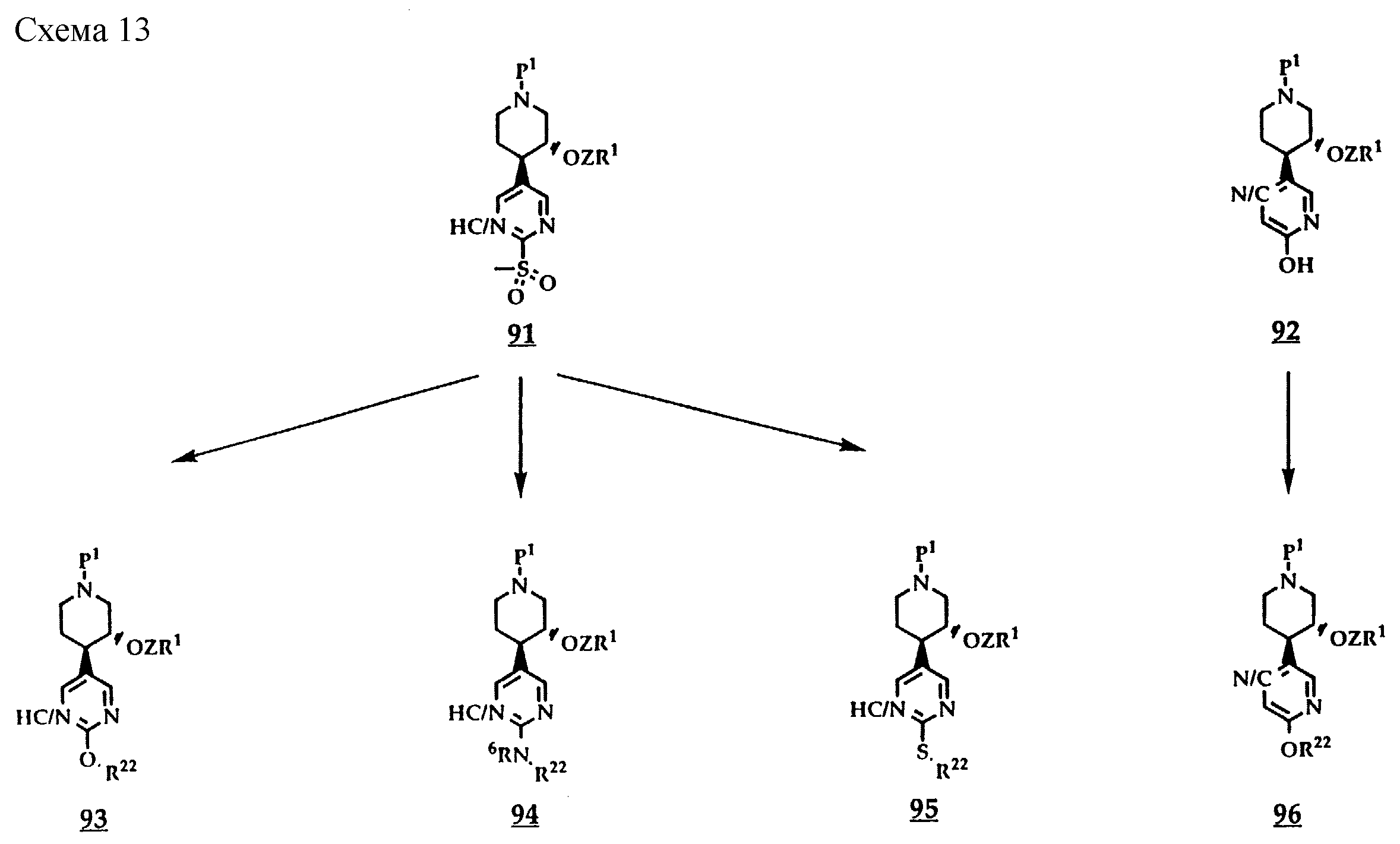
Соединения общих формул 88 и 90, где -ZR1 представляет собой заместитель, содержащий арил или гетероарильную функцию, могут быть получены из соединений общих формул 87 и 89 путем алкилирования соединением, отдающим остаток -ZR1. Алкилирование вторичного спирта осуществляют по известным методам, например, в инертном в условиях реакции растворителе, таком как простой эфир, например тетрагидрофуран или 1, 2-диметоксиэтан, или диметилформамид, с помощью образующего алкоголят основания, например гидрида натрия, при температуре в интервале от приблизительно 0 до 40oC и с использованием галогенида, предпочтительно хлорида либо бромида, или эфира сульфоновой кислоты, например мезилата или тозилата, в качестве соединения, отдающего -ZR1. Остаток Ra при этом может быть структурно модифицирован до проведения описанного выше алкилирования либо непосредственно после него. Реакции модифицирования остатка Ra в Rb, остаток общей формулы -T1-L2-T2-L3-T3-L4-Т4-U, включают обычные реакции трансформирования, такие как удаление и повторное введение функциональной группы, алкилирование и ацилирование спирта и аминофункций, окисление сульфидов до сульфоксидов и сульфонов, а также другие подобные реакции, подробно описанные в соответствующих публикациях. Примеры конкретных структурных превращений остатка Ra в остатки Rb представлены на схеме 13. 2-Метилсульфонилпиридин и производные пиридина 91, уже соответствующим образом замещенные в положении 3 пиперидина, могут подвергаться взаимодействию с алкоголятами, тиолятами и аминами в тетрагидрофуране, 1,2-диметоксиэтане, диметилформамиде или диметилсульфоксиде при температурах в интервале от комнатной температуры до приблизительно 150oC с получением в результате соответствующих замещенных гетероарильных соединений. Фенольные пиридин или производные пиразина 92, имеющие в положении 3 пиперидина OH- или OZR1-функциональную группу, благодаря применению основания и алкилирующего агента можно алкилировать по известным методам по фенольной O-функции, в ходе какового процесса одновременно могут образовываться соответственно различные незначительные количества продуктов N-алкилирования. Если же осуществлять взаимодействие со спиртом в присутствии трифенилфосфина и эфира азодикарбоновой кислоты в растворителе, таком как тетрагидрофуран или 1,2-диметоксиэтан, согласно Mitsunobu [Synthesis 1981, 1], то при этом образуются почти исключительно продукты O-алкилирования. В реакционных продуктах общих формул 93-96 тем самым -OR22, -R6NR22, -SR22 представляют собой каждый соответственно остаток -T1-L2-T2-L3-T3-L4-T4-U, где Т1 означает кислород, азот или серу.
Согласно схеме 14 соединения общих формул 104, 105, а также 108-110 могут быть получены из оксирановых соединений 98. Оксирановые соединения в свою очередь можно получить окислением соответствующих олефинов с помощью перкислот, таких как перуксусная кислота или пербензойная кислота, предпочтительно 3-хлорпербензойная кислота. Их можно подвергать взаимодействию с азидными анионами в протонных растворитилях, таких как этанол или метанол, либо в апротонных растворителях, таких как N,N-диметилформамид, ацетонитрил или диметилсульфоксид, с добавками либо без добавок кислот Льюиса, таких как перхлорат лития или сульфат магния, при температурах в интервале от 50 до 150oC с образованием различных количеств продуктов раскрытия эпоксидного кольца, имеющих азидную функцию в положении 3 и OH-функцию в положении 4 пиперидинового кольца, с получением в результате азидосоединений 101. Побочные изомерные соединения с азидной функцией в положении 3 пиперидинового кольца можно отделить, например, посредством хроматографии на силикагеле. После введения соответствующей эфирной функции в положении 3 азидосоединения реакцией конденсации с соответствующим ацетиленовым соединением 103, таким как, например, пропаргиловый спирт, в аполярном растворителе, таком как толуол или ксилол, при температурах в интервале от 60 до 160oC могут быть трансформированы в оба изомерных N-триазолильных соединения общих формул 104 и 105. Из обоих этих соединений после введения соответствующей боковой цепи у заместителя триазольного кольца путем осуществления обычных реакций модифицирования остатка Ra в Rb, таких как удаление и повторное введение функциональной группы, алкилирование и ацилирование спирта и аминофункций, окисление сульфидов до сульфоксидов и сульфонов, а также других подобных реакций, подробно описанных в соответствующих публикациях, и после отщепления защитной группы у азота пиперидинового кольца получают активные ингибиторы ренина.
Соединения общей формулы 106 могут быть синтезированы за счет нуклеофильного раскрытия оксиранового кольца общей формулы 98 с помощью полученного из замещенного пиридона аниона. Указанное нуклеофильное раскрытие может осуществляться по известным методам, например, в инертном в условиях реакции растворителе, как, например, ацетонитрил, 1,2-диметоксиэтан или N,N-диметилформамид, при температуре в интервале от приблизительно комнатной температуры до 120oC и с использованием катализатора, например хлорида аммония или перхлората лития, причем образующийся в различных количествах изомерный продукт раскрытия эпоксидного кольца целесообразно отделять посредством хроматографии на силикагеле. Соединения общей формулы 109 могут быть получены исходя из соединений общей формулы 98 следующим путем: сначала осуществляют нуклеофильное раскрытие оксиранового кольца с помощью ионов цианида, получая в результате соединения формулы 99. Указанное нуклеофильное раскрытие может осуществляться по известным методам, например, в инертном в условиях реакции растворителе, таком, например, как ацетонитрил, 1,2-диметоксиэтан или N,N-диметилформамид, при температуре в интервале от приблизительно комнатной температуры до 120oC и с использованием катализатора, например хлорида аммония, трифторацетата цинка или тетрафторбората лития, прежде всего перхлората лития, причем образующийся в различных количествах изомерный продукт раскрытия эпоксидного кольца целесообразно отделять посредством хроматографии на силикагеле. Соединения общей формулы 107 могут быть получены непосредственным присоединением аммиака либо через соответствующие тиоамиды общей формулы 100 из соединений общей формулы 99. Указанное присоединение может осуществляться по известным методам, например взаимодействием нитрила под давлением с аммиаком и хлоридом аммония или же взаимодействием сероводорода, предпочтительно в виде гидросульфида, с нитрилом с получением в результате тиоамида общей формулы 100. Этот последний в свою очередь, например, по способу, описанному в Helv. Chim. Acta, том 69, стр. 1224 (1986), алкилированием с помощью метилиодида или этилиодида можно переводить в соответствующее производное сульфония, аммонолиз которого, осуществляемый, например, хлоридом аммония, приводит к амидину общей формулы 107. Соединения общей формулы 109 могут быть получены за счет замыкания кольца амидина общей формулы 107 с помощью соответствующего малондиальдегида. Построение пиримидинового звена может осуществляться по известным методам, например взаимодействием амидина с диацеталем или енамином 2-замещенного малондиальдегида в инертном в условиях реакции растворителе, как, например, метанол, при температуре в интервале от приблизительно комнатной температуры до 120oC.
В зависимости от целевой молекулы исходя из соединений 106 и 109 можно сначала вводить -ZR1, а затем остаток Ra модифицировать в Rb или же можно применять схему построения в обратном порядке.
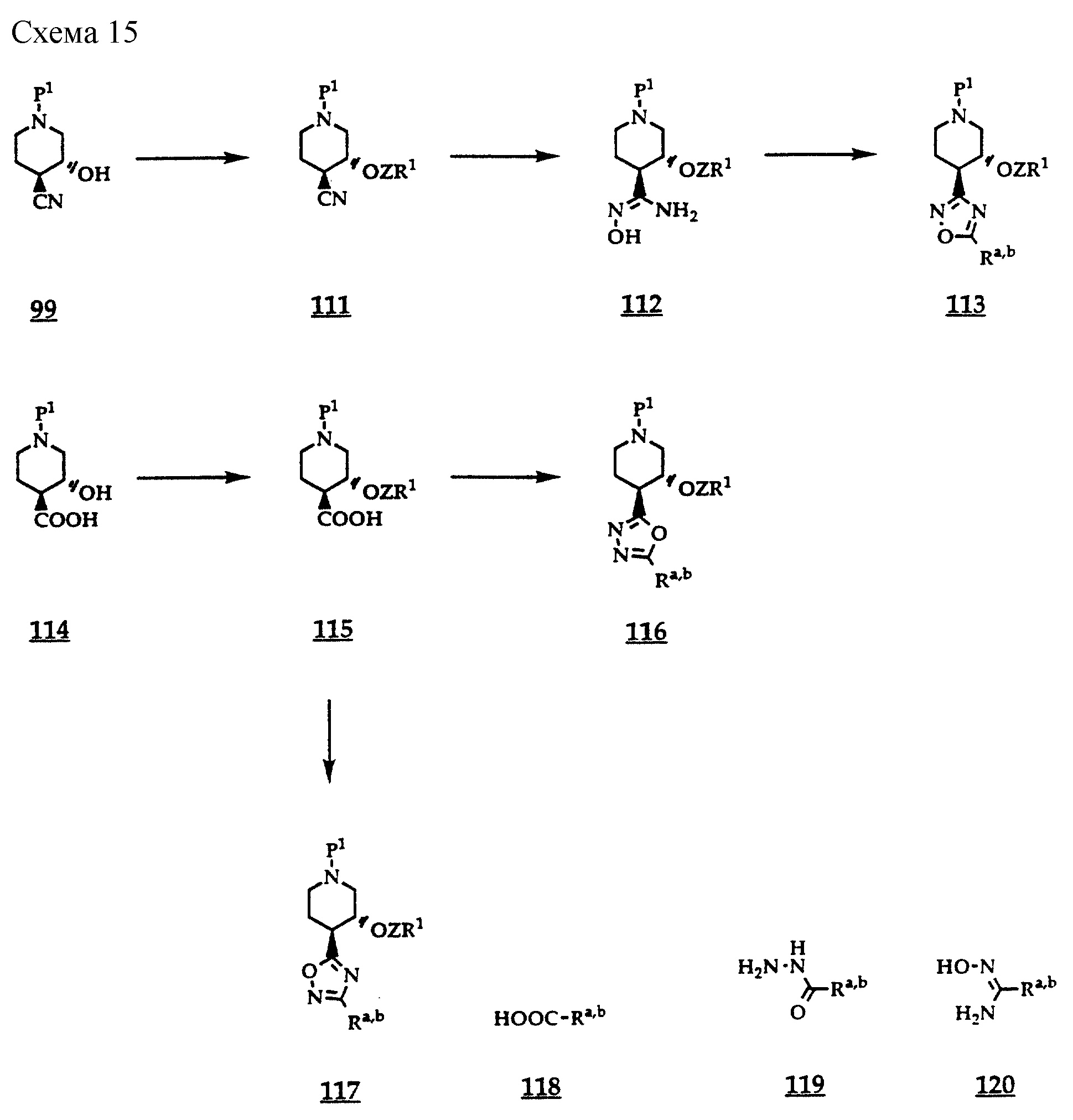
Согласно схеме 15 могут быть получены соединения общей формулы 113 из соединений общей формулы 99 благодаря тому, что сначала вторичный спирт алкилируют соединением, отдающим остаток - ZR1, причем при необходимости возможно дальнейшее построение требуемого заместителя на последующей стадии осуществления реакции. Алкилирование вторичного спирта проводят по известным способам, например, в инертном в условиях реакции растворителе, таком как простой эфир, например тетрагидрофуран либо 1,2-диметоксиэтан, или диметилформамид, с помощью образующего алкоголят основания, как, например, гидрид натрия, при температуре в интервале от приблизительно 0 до 40oC и с использованием галогенида, предпочтительно хлорида либо бромида, или эфира сульфоновой кислоты, например мезилата либо тозилата, в качестве соединения, отдающего -ZR1.
Взаимодействием соединений общей формулы 111 с гидроксиламином в присутствии основания, как, например, метилат натрия, предпочтительно при температурах в интервале от 40 до 100oC получают амидоксимы общей формулы 112. Соединения общей формулы 113 получают благодаря тому, что реакционноспособные функциональные производные карбоновой кислоты общей формулы 118 подвергают взаимодействию с амидоксимом формулы 112. Реакцию целесообразно осуществлять нагревом в течение нескольких часов до температуры в интервале от приблизительно 70 до 130oC в инертном растворителе, например в диметилформамиде. Образующийся в качестве промежуточного, нециклизованный продукт конденсации циклизуется спонтанно в данных условиях реакции. В качестве реакционноспособных функциональных производных карбоновой кислоты общей формулы 118 могут применяться соответствующие имидазолиды, которые можно получить по известным способам из соответствующих свободных карбоновых кислот, например, взаимодействием с 1,1'-карбонилдиимидазолом в инертном органическом растворителе, например в диметилформамиде. Кроме того, в качестве реакционноспособных функциональных производных карбоновой кислоты могут применяться также хлорангидриды карбоновых кислот, получить которые возможно из соответствующих свободных карбоновых кислот с помощью тионилхлорида или оксалилхлорида.
Согласно схеме 15 могут быть получены соединения общей формулы 116 из соединений общей формулы 114 благодаря тому, что сначала, как уже указывалось выше, алкилированием получают соединения общей формулы 115, которые затем переводят в реакционноспособные, функциональные производные карбоновой кислоты и подвергают взаимодействию с гидразидами общей формулы 119. Реакцию целесообразно проводить в диапазоне температур от комнатной температуры до 50oC в инертном органическом растворителе, например в диметилформамиде. Образующийся при этом нециклизованный продукт конденсации может быть выделен для последующей циклизации путем нагрева в течение нескольких часов с полифосфорной кислотой до температуры порядка 100oC с получением соединений общей формулы 116.
Согласно схеме 15 могут быть получены соединения общей формулы 117 из соединений общей формулы 115 благодаря тому, что реакционноспособные, функциональные производные карбоновой кислоты подвергают взаимодействию с амидоксимами общей формулы 120. Реакцию целесообразно осуществлять путем нагрева в течение нескольких часов до температуры в интервале от приблизительно 70 до 130oC в инертном растворителе, например в диметилформамиде. Образующийся в качестве промежуточного, нециклизованный продукт конденсации циклизуется спонтанно в данных условиях реакции.
Соединения общих формул 114, 118-120 относятся к общеизвестным классам соединений и поэтому доступны каждому специалисту без каких-либо проблем.
Еще одна возможность получить соединения общей формулы II, в которых R2 представляет собой 5-членный ароматический остаток, реализуется осуществлением их последовательного построения аналогично тому, как это представлено на схеме 12, с тем лишь отличием, что соответственно функционализованный 6-членный ароматический синтон 82 должен быть заменен на соответствующий 5-членный ароматический синтон.
Пиперидины общей формулы I могут быть представлены также в оптически чистой форме. Разделение на антиподы может осуществляться по известным методам либо предпочтительно на ранней стадии синтеза путем солеобразования с помощью оптически активной кислоты, как, например, (+)- либо (-)- миндальная кислота, и разделением диастереомерных солей фракционированной кристаллизацией, либо предпочтительно на одной из последующих стадий дериватизацией с помощью хирального структурного фрагмента, как, например, (+)- либо (-)-хлорангидрид камфановой кислоты, и разделением диастереомерных продуктов посредством хроматографии и/или кристаллизации и последующим расщеплением связи с хиральным вспомогательным агентом. Для определения абсолютной конфигурации полученного пиперидина чистые диастереомерные соли и производные могут подвергаться анализу с помощью обычных спектроскопических методов, причем рентгеновская спектроскопия на монокристаллах является наиболее приемлемым методом.
Соединения формулы I и их фармацевтически применимые соли обладают ингибирующим действием по отношению к природному ферменту ренину. Последний, проникая из почек в кровь, обусловливает там расщепление ангиотензиногена с образованием декапептида ангиотензина I, который затем в легких, почках и других органах расщепляется с образованием октапептида ангиотензина II. Ангиотензин II повышает кровяное давление как непосредственно, сужая кровеносные сосуды, так и косвенно, способствуя высвобождению удерживающего ионы натрия гормона альдостерона из надпочечников, что обусловливает увеличение объема внеклеточной жидкости. Это увеличение объясняется действием самого ангиотензина II или же образованного из него в качестве продукта расщепления гептапептида ангиотензина III. Ингибиторы ферментативной активности ренина способствуют снижению образования ангиотензина I и, как следствие, этого уменьшают количество образующегося ангиотензина II. Сниженная концентрация этого активного пептидного гормона является непосредственной причиной действия ингибиторов ренина, способствующего снижению кровяного давления.
Активность in vitro ингибиторов ренина, как это уже описано W. Fischli и др. в Hypertension, том 18(1), стр. 22-31 (1991) или в Hypertension, том 22(1), стр. 9-17 (1993), может быть подтверждена экспериментальным путем в ходе проведения описанных ниже опытов. Эти опыты проводятся по методике, аналогичной описанной D.T. Pals и др. в Hypertension, том 8, стр. 1105-1112 (1986) или J. Boger и др. в Journ. Med. Chem. 28, стр. 1779-1790 (1985) или J. F. Dellaria и др. в Journ. Med. Chem. 30, стр. 2137-2144 (1987) или T. Kokubu и др. в Biochem. Biophys. Res. Commun. 118, стр. 929-933 (1984).
Опыт in vitro с чистым ренином человека
Опыт проводят в трубках Эппендорфа. Инкубационная смесь состоит из (1) 100 мкл ренина человека в буфере А (0,1М раствор фосфата натрия, pH 7,4, содержащий 0,1% бычьего сывороточного альбумина, 0,1% азида натрия и 1 мМ этилендиаминтетрауксусную кислоту), что является достаточным для активности ренина, равной 2-3 нг ангиотензин I/мл/ч; (2) 145 мкл буфера А; (3) 30 мкл 10 мМ субстрата человеческого тетрадекарертид-ренина (hTD) в 10 мМ соляной кислоте; (4) 15 мкл диметилсульфоксида с ингибитором, соответственно без такового и (5) 10 мкл 0, 03-молярного раствора гидроксихинолинсульфата в воде.
Пробы инкубируют в течение 3 ч при 37oC, соответственно 4oC в трех параллельных опытах. 3атем используют две пробы по 100 мкл на каждую из экспериментальных трубок для определения продуцирования ангиотензина I посредством РИА (стандартный радиоиммуноанализ; набор твердофазных проб для клинических испытаний). Перекрестная реактивность используемых антител в РИА составляет: для ангиотензина I 100%, для ангиотензина II 0,0013%; для hTD (ангиотензин I-Val-Ile-His-Ser-OH) 0,09%. Продуцирование ангиотензина I определяется по разности между результатами опыта при 37oC и опыта при 4oC.
Параллельно проводят следующие контрольные опыты:
а) инкубация hTD-проб без ренина и без ингибиторов при 37 и 4oC. По разности между обоими показателями определяют основной показатель продуцирования ангиотензина I;
б) инкубация hTD-проб с ренином, однако без ингибиторов при 37 и 4oC. По разности между этими показателями определяют максимальный показатель продуцирования ангиотензина I.
Для каждой пробы из выявленного продуцирования ангиотензина I вычитают основной показатель продуцирования ангиотензина I. По разности между максимальным значением и основным значением определяют показатель степени максимального гидролиза субстрата (= 100%) под действием ренина.
Результаты представлены в качестве IC50-значений, обозначающих такую концентрацию ингибитора, при которой ферментативная активность подавляется на 50%. IC50-значения определяют по кривой линейной регрессии из построенного в логарифмическом масштабе графика Логита.
Полученные в описанном опыте результаты представлены в нижеследующей таблице.
Соединение - IC50-значения, мкмоль/л
А - 0,011
Б - 0,026
В - 0,070
Г - 0,040
Д - 0,041
Е - 0,057
Ж - 0,033
З - 0,073
И - 0,317
К - 0,017
Л - 2,600
М - 3,080
Н - 0,008
О - 0,012
П - 0,017
Р - 0,006
С - 0,005
Т - 0,003
У - 0,002
Ф - 0,005
Х - 0,024
Ц - 0,002
Ч - 0,002
Ш - 0,003
Щ - 0,003
Э - 0,001
АА - 0,001
ББ - 0,003
ВВ - 0,002
ГГ - 0,001
ДД - 0, 0004
ЕЕ - 0,0006
ЖЖ - 0,001
33 - 0,006
ИИ - 0,002
КК - 0,002
ЛЛ - 0,012
ММ - 0, 001
НН - 0,0005
ОО - 0,001
ПП - 0,006
РР - 0,002
СС - 0,002
ТТ - 0,270
УУ - 132
ФФ - 0,0005
XX - 0,0001
ЦЦ - 0,002
ЧЧ - 0,009
ШШ - 0,0008
ЩЩ - 0,0005
ЭЭ - 0,00003
А: гидрохлорид (3RS, 4RS)-2-[4-(3-нафталин-2- илметоксипиперидин-4-ил)фенокси]этилового эфира тиофен-2-карбоновой кислоты (пример 58-4);
Б: гидрохлорид (3RS, 4RS)-2-[4-(3-нафталин-2- илметоксипиперидин-4-ил)фенокси] этилового эфира 2-хлорбензойной кислоты (пример 54-2);
В: гидрохлорид (3RS, 4RS)-2-[4-[3-[4-(2- метоксибензилокси)нафталин-2-илметокси] пиперидин-4-ил]фенокси] этилового эфира бензойной кислоты (пример 55-2);
Г: (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил]-3-(2,3-дигидробензо [1,4] диоксин-6-илметокси)пиперидин (пример 86-53);
Д: трифторацетат (3RS, 4RS)-3-(нaфтaлин-2-илметoкcи)-4- [4-(3-фенил-[1,2, 4]оксадиазол-5-илметокси)фенил]пиперидина(пример 86-41);
Е: трифторацетат (3RS,4RS)-3-(нaфтaлин-2-илметoкcи)-4-[4-(3-фенилизоксазол-5-илметокси) фенил]пиперидина (пример 86-43);
Ж: (3RS, 4RS)-3-(нaфтaлин-2-илметoкcи)-4-[4-(3-фенилcульфaнилпpoпил) фенил]пиперидин(пример 86-19);
З: (3RS,4RS)-3-[4-[4-[2-(бензотиазол-2-илсульфанил)этил]фенил] пиперидин-3-илоксиметил]нафталин-1-ол (пример 86-23);
И: (3RS, 4RS,5SR)-3-(4-бензилоксинафталин-2-илметокси)-4-(4-фторфенил)- 5-пропилпиперидин (пример 64);
К: (3SR, 4RS,5RS)-4-(4-бензилoкcиметилфенил)-3-метoкcиметил-5- (нафталин-2-илметокси)пиперидин (пример 86-59);
Л: гидрохлорид (SR)- или (RS)-1-[(3RS, 4SR)-4-(4-фтopфенил)пипеpидин-3-ил]-2- нафталин-2-илэтилового эфира бензойной кислоты (пример 75б);
М: (1RS, 2RS, 3RS, 5SR)-2-(4-бензилоксинафталин-2-илметокси)-3-(4- фторфенил)-8-азабицикло[3.2.1]октан (пример 84д);
Н: (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил]-3-(нафталин-2- илметокси)пиперидин;
О: гидрохлорид 4-[2-[7-[(3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] пиперидин-3-илоксиметил] нафталин-2-илокси] этил]морфолина (1:2) (пример 90-07);
П: смесь (RS)- и (SR)-3-[7-[(3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] пиперидин-3- илоксиметил]нафталин-2-илокси]пропан-1,2-диола (пример 90-08);
Р: смесь гидрохлорида (RS)- и (SR)-3-[2-[7-[(3RS, 4RS)-4-[4- (3-бензилоксипропокси)фенил] пиперидин-3-илоксиметил] нафталин-2- илокси] этокси]пропан-1,2-диола (1:1) (пример 98);
С: гидрохлорид 1-[2-[7-[(3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] пиперидин-3-илоксиметил]нафталин-2-илокси]этил]-4-метилпиперазина (1:3) (пример 90-13);
Т: гидрохлорид 1-[(3RS, 4SR)-4-[4-(3- бензилоксипропокси)фенил]пиперидин-3-ил]-2-нафталин-2-илэтанона (1:1) (пример 100);
У: (3RS, 4SR, 5SR)-4-[4-(3- бензилоксипропокси)фенил]-3-(1, 4-диметоксинафталин-2-илметокси) пиперидин-5-ол (пример 109-04);
Ф: смесь (3RS,4RS)- и (3SR,4SR)-4- [4-(3-бензилоксипропокси)фенил]-3-[7-[(RS)-2,3 - дигидроксипропоксиметил] нафталин-2-илметокси] пиперидина (пример 106-02);
Х: смесь (3RS,4RS)- и (3SR,4SR)-4-[4-(3- бензилоксипропокси)фенил]-3-[6-[(RS)-2,3-дигидроксипропоксиметил] нафталин-2-илметокси] пиперидина (пример 106-01);
Ц: 4-[(3RS,4SR,5SR)-4-[4-(3-бензилоксипропокси)фенил]-3-(нафталин-2- илметокси)пиперидин-5-илокси]бутан-1-ол (пример 110-08);
Ч: 3-[(3RS, 4SR,5SR)-4-[4-(3-бензилоксипропокси)фенил]-3-(нафталин-2- илметокси)пиперидин-5-илокси]пропан-1-ол (пример 110-07);
Ш: 1-{2-[(3RS,4RS, 5SR)-4-[4-(3-бензилоксипропокси)фенил]-3- (нафталин-2-илметокси)пиперидин-5-илокси]этил}-4-метилпиперазин (пример 110-02);
Щ: 4-{2-[(3RS,4RS, 5SR)-4-[4-(3- бензилоксипропокси)фенил]-3-(нафталин-2-илметокси)пиперидин-5- илокси]этил}морфолин (пример 110-09);
Э: (3RS, 4SR, 5SR)-4-[4-(3-бензилоксипропокси)фенил]-3- (4-метоксибензилокси)пиперидин-5-ол (пример 109-28);
AA: (3R,4s,5S)-4-[4-(3-бензилоксипропокси)фенил]-3,5-бис (4-метоксибензилокси) пиперидин (пример 109-27);
ББ: (3SR,4RS,5RS)-4-[2-[4-[4-(3- бензилоксипропокси)фенил]-5-(нафталин-2-илметокси)пиперидин-3- илметокси]этил]морфолин(пример 149-04);
BB: (3SR,4RS, 5RS)-4-[4-(3-бензилоксипропокси)фенил]-3-метоксиметил- 5-(нафталин-2-илметокси)пиперидин (пример 148);
ГГ: (3SR,4RS, 5RS)-4-[4-(3-бензилоксипропокси)фенил]-5- (нафталин-2-илметокси)пиперидин-3-илметиловый эфир [3-(4-метилпиперазин-1-ил)пропил] карбаминовой кислоты (пример 150-01);
ДД: (3SR,4RS, 5RS)-4-[4-[4-(3-бензилоксипропокси)фенил]-5- (нафталин-2-илметокси)пиперидин-3-илметилсульфанил]пиридин (пример 149-02);
ЕЕ: 2-(4-циклогексилбутокси)-5-[(3RS,4RS)-3- (1, 4-диметоксинафталин-2-илметокси)пиперидин-4-ил] пиримидин (пример 139-03);
ЖЖ: (3'RS, 4'RS)-6-(3-циклогексилпропокси)-3'- (1,4-диметоксинафталин-2-илметокси)-1',2',3',4',5', 6'- гексагидро[3,4']бипиридин (пример 140-01);
33: гидрохлорид (3SR, 4RS, 5RS)-4-[4-(3-бензилоксипропокси)фенил] -5-(нафталин-2- илметокси)пиперидин-3-ил] метанола (пример 149-01);
ИИ: (3SR,4RS,5RS)-N-[4-[4-(3-бензилоксипропокси)фенил]-5-(нафталин- 2-илметокси)пиперидин-3-илметил] -N, N', N'-триметилэтан-1,2- диамин (пример 149-06);
КК: (3SR,4RS, 5RS)-[4-[4-(3-бензилоксипропокси)фенил]-5- (нафталин-2-илметокси)пиперидин-3-илметил]диэтиламин (пример 149-05);
ЛЛ: 1-[(3RS,4SR, 5SR)-4-[4-(3-бензилоксипропокси)фенил]-5- (2-морфолин-4-илэтоксиметил)пиперидин-3-ил]-2-нафталин-2-илэтанон (пример 101);
MM: (3RS, 4RS)-3-(1, 4-диметoкcинaфтaлин-2-илметoкcи)-4-[4-[3-(2- метоксифенокси)пропокси]фенил]пиперидин (пример 123-27);
НН: (3R, 4s,5S)-4-[4-(3-бензилоксипропокси)фенил]-3,5-бис(3,4, 5- триметоксибензилокси)пиперидин (пример 109-29);
ОО: гидрохлорид (3RS, 4RS, 5SR)-4-[4-(3-бензилоксипропокси)фенил] -3-(нафталин-2- илметокси)-5-[1,2,4] триазол-1-илметилпиперидина (пример 149-07);
ПП: (3RS,4RS)-4-[4-[3-(2-метоксибензилокси)пропокси]фенил]-3- (хинолин-7-илметокси)пиперидин (пример 120-07);
РР: 2-(7-{ (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] пиперидин-3-илоксиметил}нафталин-2-илметокси)этанол (пример 106-03);
СС: (7- {(3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил]пиперидин- 3-илоксиметил}нафталин-2-илметил)диметиламин (пример 106-03);
ТТ: (3R, 4R)-3-(4-бензилоксинафталин-2-илметокси)-4- (4-фторфенил)пиперидин (пример 154-06);
УУ: (3S, 4S)-3-(4-бензилоксинафталин-2-илметокси)-4-(4-фторфенил) пиперидин (пример 154-07);
ФФ: (3'RS,4'RS)-3'-(1,4-диметоксинафталин-2-илметокси)-6-[3- (2-метоксибензилокси)пропокси] -1', 2',3',4',5',6'-гексагидро- [3,4']бипиридин (пример 140-02);
XX: (3RS, 4RS)-3-(1,4- диметоксинафталин-2-илметокси)-4-[4-[3-(2-метоксибензилокси)пропокси] фенил]пиперидин (пример 123-32);
ЦЦ: (3SR,4RS, 5RS)-1-[4-[4-(3-бензилоксипропокси)фенил]-5- (нафталин-2-илметокси)пиперидин-3-илметил]имидазолидин-2-он (пример 149-08);
ЧЧ: (3RS,4RS)-4-[4-[3-(2-метоксибензилокси)пропокси] фенил]-3-(2-оксо-1,2-дигидрохинолин-7-илметокси)пиперидин (пример 120-10);
ШШ: (3RS, 4RS)-3-(изохинолин-7-илметокси)-4-[4- [3-(2-метоксибензилокси)пропокси]фенил]пиперидин (пример 120-11);
ЩЩ: (3RS, 4RS)-4-[4-[3-(2-метоксибензилокси)пропокси] фенил] -3-(1,2,3,4-тетрагидрохинолин-7-илметокси)пиперидин (пример 120-12);
ЭЭ: (3RS, 4SR, 5SR)-3-(1, 4-диметоксинафталин-2-илметокси)-4-[4- [3-(2-метоксибензилокси)пропокси]фенил]пиперидин-5-ол (пример 112-11).
Соединения формулы I, а также их фармацевтически применимые соли могут применяться в качестве лекарственных средств, например в виде фармацевтических препаратов. Фармацевтические препараты могут назначаться для энтерального введения, в частности орального, например, в форме таблеток, таблеток с лаковым покрытием, твердо- и мягкожелатиновых капсул, растворов, эмульсий или суспензий, для назального введения, например, в форме носовых аэрозолей, или для ректального введения, например, в форме суппозиториев. Препараты могут вводиться также парентерально, в частности внутримышечно или внутривенно, например, в форме растворов для инъекций.
Для изготовления таблеток, таблеток с лаковым покрытием, драже и твердожелатиновых капсул соединения формулы I и их фармацевтически применимые соли могут подвергаться совместной переработке с фармацевтически инертными неорганическими или органическими наполнителями. В качестве таковых, например, для таблеток, драже и твердожелатиновых капсул, можно использовать лактозу, кукурузный крахмал либо его производные, тальк, стеариновую кислоту либо ее соли и т.п.
В качестве инертных наполнителей для твердожелатиновых капсул пригодны среди прочих растительные масла, воски, жиры, полутвердые и жидкие полиолы и т.п.
Для приготовления растворов и сиропов в качестве инертных наполнителей могут использоваться, например, вода, полиолы, сахароза, инвертный сахар, глюкоза и т.п.
В качестве инертных наполнителей для растворов для инъекций приемлемы, например, вода, спирты, полиолы, глицерин, растительные масла, желчные кислоты, лецитин и т.п.
В качестве инертных наполнителей для суппозиториев можно использовать, например, природные или отвержденные масла, воски, жиры, полужидкие и жидкие полиолы и т.п.
Наряду с вышеуказанными инертными наполнителями фармацевтические препараты могут содержать также консерванты, агенты растворения, вещества, повышающие вязкость, стабилизаторы, смачиватели, эмульгаторы, сладкие вещества, красители, ароматизаторы, соли для изменения осмотического давления, буферы, средства для покрытия или антиоксиданты. В их состав могут входить также и другие ценные в терапевтическом отношении вещества.
Согласно изобретению соединения общей формулы I и их фармацевтически применимые соли могут применяться для лечения, соответственно предупреждения артериальной гипертонии и сердечной недостаточности, а также глаукомы, инфаркта миокарда, почечной недостаточности и рестеноза.
Соединения по изобретению могут применяться также в сочетании с одним или несколькими средствами, воздействующими на сердечно-сосудистую систему, например с α- и β--блокаторами, такими как фентоламин, феноксибензамин, празозин, теразозин, толазин, атенолол, метопролол, надолол, пропранолол, тимолол, картеолол и т.п.; с вазодилататорами, такими как гидралазин, миноксидил, диазоксид, нитропруссид, флосехинан и т. п. ; с антагонистами кальция, такими как амринон, бенциклан, дилтиазем, фендилин, флунаризин, никардипин, нимодипин, пергексилен, верапамил, галлопамил, нифедипин и т.п.; с ингибиторами ангиотензинконвертирующего фермента (АСЕ), такими как цилазаприл, каптоприл, эналаприл, лизиноприл и т.п.; с активаторами калия, такими как пинацидил; с антисеротонинергическими средствами, такими как кетансерин; с ингибиторами тромбоксансинтетазы; с антагонистами ангиотензина II; а также с диуретиками, такими как гидрохлоротиазид, хлоротиазид, ацетазоламид, амилорид, буметанид, бензтиазид, этакриновая кислота, фуросемид, индакринон, метолазон, спиронолактон, триамтерен, хлорталидон и т.п.; с симпатолитиками, такими как метилдопа, клонидин, гуанабенз, резерпин; а также с другими средствами, пригодными для лечения артериальной гипертонии, сердечной недостаточности или сосудистых заболеваний у человека и животных, связанных с диабетом либо заболеваниями почек, такими как острая или хроническая почечная недостаточность. Такие сочетания можно использовать раздельно или же в препаратах, содержащих несколько компонентов.
Дозировка может варьироваться в широких пределах и должна назначаться в каждом отдельном случае, естественно, с учетом индивидуальных особенностей пациента. В принципе при оральном введении можно рекомендовать для назначения взрослому пациенту (вес тела 70 кг) суточную дозу в пределах от приблизительно 3 мг до приблизительно 3 г, предпочтительно от приблизительно 10 мг до приблизительно 1 г, например, в общей сложности 300 мг, распределив суточную дозу предпочтительно на 1-3 разовые дозы, которые могут быть, например, равными, причем, однако, если окажется целесообразным, вполне допустимо превышение указанного верхнего предела. Дети же с учетом их возраста и веса тела получают обычно соответственно уменьшенную дозу.
Ниже изобретение поясняется на примерах, которые не ограничивают его объем. Все температуры указаны в градусах Цельсия. В примерах использованы следующие аббревиатуры:
BOC: трет-бутоксикарбонил
ДМЭ: диметоксиэтан
ДМФ: диметилформамид
ТБАФ: тетрабутиламмонийфторид
ЭДК: N-этил-N'-(3-диметиламинопропил)карбодиимид, гидрохлорид
ТГП: тетрагидропиранил
ТРОК: трихлорэтоксикарбонил
ТПТУ: тетрафторборат O-(1,2-дигидро-2-оксо-1-пиридил)-N, N,N',N'- тетраметилурония
ГБТУ: гексафторфосфат O-(1Н-бензотриазол-1-ил)- N,N,N',N'-тетраметилурония
СЭМ: 2-(триметилсилил)этоксиметил
Пример 1.
(а) Раствор 23,6 г (100 ммолей) 1,3-дибромбензола в 250 мл абсолютного эфира охлаждали до -75oC. В течение 45 мин по каплям добавляли раствор 62,5 мл (100 ммолей) н-бутиллития (1,6 М в гексане). Образовавшуюся суспензию перемешивали в течение 2,5 ч при -75oC. После этого в течение 30 мин при температуре в интервале от -70 до -75oC по каплям добавляли раствор 19,0 г (100 ммолей) 1-бензил-4-пиперидона в 100 мл абсолютного эфира и затем перемешивали в течение 2 ч. Далее смесь распределяли между простым эфиром и насыщенным раствором хлорида аммония, органическую фазу сушили над сульфатом магния и в завершение удаляли растворитель при пониженном давлении. Сырой продукт очищали хроматографией на силикагеле с использованием смеси 1:1 метиленхлорида и гексана в качестве элюента. Таким путем получили 28,3 г (82% от теории) 1-бензил-4-(3-бромфенил)пиперидин-4-ола в виде желтого масла; МС: 345, 347 (М)+.
(б) Раствор 28,2 г (81,4 ммоля) 4-(3-бромфенил)пиперидин-4-ола в 600 мл толуола смешивали с 30 г (157 ммолей) моногидрата п-толуолсульфокислоты
и в течение 4 ч нагревали с обратным холодильником с использованием насадки для отделения воды. Далее реакционную смесь охлаждали до комнатной температуры и с помощью 3 н. едкого натра значение pH устанавливали равным 10. 3атем сначала трижды экстрагировали 500 мл метиленхлорида. Объединенные органические фазы трижды промывали водой порциями по 200 мл, сушили над сульфатом магния и затем упаривали при пониженном давлении. Сырой продукт очищали хроматографией на силикагеле с использованием смеси 1:1 метиленхлорида и гексана в качестве элюента. Таким путем получили 9,5 г (36% от теории) 1-бензил-4-(3-бромфенил)-1,2,3,6-тетрагидропиридина в виде светло-желтого масла; МС: 327, 329 (М+Н)+.
(в) К суспензии из 9,5 г (28,9 ммоля) 1-бензил-4-(3-бромфенил)- 1,2,3,6-тетрагидропиридина в 65 мл абсолютного диметоксиэтана (ДМЭ) при комнатной температуре порциями добавляли 3,15 г (83,3 ммоля) борогидрида натрия. После этого при 15-20oC по каплям добавляли раствор из 17,7 мл (20,0 г, 140,9 ммоля) эфирата трифторида бора в 11 мл ДМЭ и в течение 2 ч перемешивали при комнатной температуре. 3атем при 20-25oC в течение 30 мин по каплям добавляли раствор 18,3 г (326 ммолей) гидроксида калия в 100 мл воды. Далее при 20-25oC в течение 30 мин по каплям добавляли 55 мл 30%-ного раствора перекиси водорода. Смесь перемешивали в течение 30 мин и затем в течение 3 ч нагревали с обратным холодильником. После охлаждения реакционной смеси выпавшую в осадок борную кислоту отфильтровывали. 3атем фильтрат распределяли между метиленхлоридом и водой, органическую фазу сушили над сульфатом магния и удаляли растворитель при пониженном давлении. Сырой продукт очищали хроматографией на силикагеле с использованием смеси 1:1 уксусного эфира и метиленхлорида в качестве элюента. Таким путем получили 6,3 г (63% от теории) (3RS, 4RS)-1-бензил-4-(3-бромфенил)пиперидин-3-ола в виде бесцветного масла; МС: 345, 347 (М)+.
(г) Раствор из 691 мг (2,00 ммоля) (3RS,4RS)-1-бензил-4-(3-бромфенил)пиперидин-3-ола в 3 мл абсолютного тетрагидрофурана смешивали с 163 мг (2,20 ммоля) карбоната лития и охлаждали до -50oC. К этой смеси при -50oC по каплям добавляли раствор 722 мг (4,00 ммоля) β- триметилсилилэтилового эфира хлормурвьиной кислоты [Synthesis 346 (1987)] в 4 мл толуола. Реакционную смесь нагревали до комнатной температуры и перемешивали в течение 24 ч. 3атем смесь распределяли между метиленхлоридом и водой, органическую фазу сушили над сульфатом магния и в завершение удаляли растворитель при пониженном давлении. Сырой продукт (0,8 г) очищали хроматографией на силикагеле с использованием метиленхлорида в качестве элюента. Таким путем получили 470 мг (43% от теории) 2-триметилсилилэтилового эфира (3RS,4RS)-4-(3-бромфенил)-3-(2- триметилсилилэтоксикарбонилокси) пиперидин-1-карбоновой кислоты в виде светло-желтого масла, которое использовали непосредственно на последующей стадии.
(д) Раствор из 470 мг (0,863 ммоля) 2-триметилсилилэтилового эфира (3RS, 4RS)-4-(3-бромфенил)-3-(2- триметилсилилэтоксикарбонилокси)пиперидин-1-карбоновой кислоты в 3 мл абсолютного тетрагидрофурана смешивали с 2,65 мл (2,91 ммоля) раствора тетрабутиламмонийфторида (1,1 М в ТГФ) и перемешивали в течение 2,5 ч при комнатной температуре. 3атем смесь распределяли между метиленхлоридом и насыщенным раствором карбоната натрия, органическую фазу сушили над сульфатом магния и в завершение удаляли растворитель при пониженном давлении. Сырой продукт (440 мг) очищали хроматографией на силикагеле с использованием смеси 6,5:1:0,1 метиленхлорида, MeOH и 25%-ного аммиака в качестве элюента. Таким путем получили 180 мг (81% от теории) (3RS,4RS)-4- (3-бромфенил)пиперидин-3-ола в виде светло-желтого масла; МС: 255, 257 (М)+.
(е) Раствор 180 мг (0,702 ммоля) (3RS,4RS)-4-(3- бромфенил)пиперидин-3-ола в 1 мл абсолютного диметилформамида при 0oC смешивали с 0,1 мл (73 мг, 0,72 ммоля) триэтиламина. К этой смеси при 0oC добавляли раствор 167 мг (76,5 ммоля) ди-трет-бутилдикарбоната в 0,5 мл диметилформамида. Смесь нагревали до комнатной температуры и перемешивали в течение 20 ч. Растворитель отгоняли при 50-55oC и при давлении 0,1 мм рт.ст. После этого полученный остаток распределяли между метиленхлоридом и водой, органическую фазу сушили над сульфатом магния и в завершение удаляли растворитель при пониженном давлении. Сырой продукт очищали хроматографией на силикагеле с использованием смеси 4:1 метиленхлорида и уксусного эфира в качестве элюента. Таким путем получили 220 мг (92% от теории) трет-бутилового эфира (3RS,4RS)-4-(3- бромфенил)-3-гидроксипиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 299, 301 (M-C4H8)+.
(ж) Раствор 168 мг (0,47 ммоля) трет-бутилового эфира (3RS,4RS)-4-(3- бромфенил)-3-гидроксипиперидин-1-карбоновой кислоты и 157 мг (0,71 ммоля) 2-бромметилнафталина в 2 мл диметилформамида смешивали с 28 мг (0,7 ммоля) гидрида натрия (60%-ная дисперсия в вазелиновом масле) и смесь перемешивали в течение 3 ч при комнатной температуре. 3атем реакционную смесь распределяли между уксусным эфиром и водой, органическую фазу сушили над сульфатом магния и в завершение удаляли растворитель при пониженном давлении. Сырой продукт очищали хроматографией на силикагеле с использованием смеси 1:4 уксусного эфира и гексана в качестве элюента. Таким путем получили 173 мг (74% от теории) трет-бутилового эфира (3RS, 4RS)-4-(3-бромфенил)-3-(нафталин-2-илметокси) пиперидин-1- карбоновой кислоты в виде светло-желтого масла; МС: 439, 441 (M-C4H8)+.
(з) Раствор 173 мг (0,35 ммоля) трет-бутилового эфира (3RS, 4RS)-4-(3-бромфенил)-3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в 6 мл метанола смешивали с 6 мл 2 н. раствора хлористого водорода в MeOH и перемешивали в течение 4 ч при 50oC. 3атем смесь распределяли между уксусным эфиром и 5%-ным раствором гидрокарбоната натрия, органическую фазу сушили над сульфатом магния и в завершение удаляли растворитель при пониженном давлении. Сырой продукт очищали хроматографией на силикагеле с использованием смеси 10: 1:0,1 метиленхлорида, MeOH и 25%-ного аммиака в качестве элюента. Таким путем получили 126 мг (91% от теории) (3RS, 4RS)-4-(3-бромфенил)-3-(нафталин-2- илметокси)пиперидина в виде светло-желтого масла; МС: 396, 398 (М+Н)+.
Пример 2.
Аналогично примеру 1(з) путем отщепления BOC-группы получали следующие соединения:
1) из трет-бутилового эфира (3RS,4RS)-3-(4-метоксибензилокси)-4-фенилпиперидин-1-карбоновой кислоты получили (3RS, 4RS)-3-(4- метоксибензилокси)-4-фенилпиперидин в виде светло-желтого масла; МС: 298 (М+Н)+;
2) из трет-бутилового эфира (3RS, 4RS)-4-(4-бромфенил)-3-(4-метоксибензилокси)пиперидин-1- карбоновой кислоты получили (3RS, 4RS)-4-(4-бромфенил)-3-(4- метоксибензилокси)пиперидин в виде бесцветного масла; МС: 376,378 (М+Н)+ ;
3) из трет-бутилового эфира (3RS,4RS)-3-(4- метоксибензилокси)-4-(3-трифторметилфенил)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-3-(4-метоксибензилокси)-4-(3- трифторметилфенил)пиперидин в виде бесцветного масла; МС: 366 (М+Н)+;
4) из трет-бутилового эфира (3RS, 4RS)-3-(4- метоксибензилокси)-4-п-толилпиперидин-1-карбоновой кислоты получили (3RS,4RS)-3-(4-метоксибензилокси)-4-п-толилпиперидин в виде бесцветного твердого вещества; МС: 312 (М+Н)+;
5) из трет-бутилового эфира (3RS,4RS)-3-(нафталин-2-илметокси)-4- фенилпиперидин-1-карбоновой кислоты получили (3RS,4RS)-3- (нафталин-2-илметокси)-4-фенилпиперидин в виде светло-желтого масла; МС: 318 (М+Н)+;
6) из трет-бутилового эфира (3RS,4RS)-4- (4-бpoмфенил)-3-(нaфтaлин-2-илметокси)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-(4-бромфенил)-3-(нафталин-2- илметокси)пиперидин в виде бесцветного твердого вещества; МС: 396, 398 (М+Н)+;
7) из трет-бутилового эфира (3RS, 4RS)-3-(нафталин-2- илметокси)-4-(3-трифторметилфенил)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-3-(нафталин-2-илметокси)-4-(3- трифторметилфенил)пиперидин в виде бесцветного масла; МС: 386 (М+Н)+;
8) из трет-бутилового эфира (3RS,4RS)-4-циклoгeкcил-3- (нaфтaлин-2-илметокси)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-циклогексил-3-(нафталин-2-илметокси)пиперидин в виде светло-желтого масла; МС: 324 (М+Н)+;
9) из трет-бутилового эфира (3RS, 4RS)-3-(нафталин-2-илметокси)-4-п-толилпиперидин-1-карбоновой кислоты получили (3RS,4RS)-3-(нафталин-2- илметокси)-4-п-толилпиперидин-1-карбоновой в виде бесцветного твердого вещества; МС: 332 (М+Н)+;
10) из трет-бутилового эфира (3RS,4RS)-4-нафталин-2-ил-3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4- нафталин-2-ил-3-(нафталин-2-илметокси)пиперидин в виде бесцветного масла; МС: 367 (М+Н)+;
11) из трет-бутилового эфира (3RS,4RS)-3- (нафталин-2-илметокси)-4-(5,6,7, 8-тетрагидронафталин-2- ил)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-3-(нафталин- 2-илметокси)-4-(5,6,7,8-тетрагидронафталин-2-ил)пиперидин в виде бесцветного масла; МС: 372 (М+Н)+;
12) из трет-бутилового эфира (3RS,4RS)-4-нафталин-1-ил-3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты получили (3RS,4RS)-4-нафталин-1-ил-3- (нафталин-2-илметокси) пиперидин в виде бесцветного твердого вещества; МС: 367 (М)+;
13) из трет-бутилового эфира (3RS, 4RS)-4-(3,4-диметоксифенил)-3- (нафталин-2-илметокси) пиперидин-1-карбоновой кислоты получили (3RS,4RS)-4-(3,4-диметоксифенил)-3- (нафталин-2-илметокси) пиперидин в виде бесцветной смолы; МС: 377 (М)+;
14) из трет-бутилового эфира (3RS, 4RS)-4-аценафтен-5-ил-3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4- аценафтен-5-ил-3-(нафталин-2-илметокси)пиперидин в виде бесцветного твердого вещества; МС: 394 (М+Н)+;
15) из трет-бутилового эфира (3RS,4RS)-4-(4-хлорфенил)-3-(3- феноксибензилокси)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-(4-хлорфенил)-3-(3-феноксибензилокси)пиперидин в виде бесцветного твердого вещества; МС: 394, 396 (М+Н)+;
16) из трет-бутилового эфира (3RS, 4SR)-3-(нафталин-2-илметокси)-4-фенилпиперидин-1-карбоновой кислоты получили гидрохлорид (3RS, 4SR)-3-(нафталин-2-илметокси)-4-фенилпиперидина в виде бесцветного порошка; МС: 318 (М+Н)+.
BOC-содержащие соединения, использованные в качестве исходных веществ, получали следующим образом.
Аналогично примеру 1(б)-(в) и (е)-(ж) получали следующие соединения.
(а) Из 4-фенилпиперидин-4-ола путем элиминирования получили 4-фенил-1,2,3,6-тетрагидропиридин в виде светло-желтого масла; МС: 159 (М)+. Последующим гидроборированием получили (3RS,4RS)-4-фенилпиперидин-3-ол в виде бесцветного твердого вещества; МС: 177 (М)+. Путем введения BOC-группы получили трет-бутиловый эфир (3RS, 4RS)-3-гидрокси-4-фенилпиперидин-1- карбоновой кислоты в виде бесцветного твердого вещества; МС: 277 (М)+. После алкилирования 4-метоксибензилбромидом получили трет-бутиловый эфир (3RS, 4RS)-3-(метоксибензилокси)-4- фенилпиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 340 (M-C4H9)+.
(б) Из 4-(4-бромфенил)пипиридин-4-ола путем элиминирования получили 4-(4-бромфенил)-1,2,3,6-тетрагидропиридин в виде светло-желтого твердого вещества; МС: 237, 239 (М)+. Последующим гидроборированием получили (3RS,4RS)-4-(4-бромфенил)пиперидин-3-ол в виде бесцветного твердого вещества; МС: 255, 257 (М)+. Путем введения BOC-группы получили трет-бутиловый эфир (3RS, 4RS)-4-(4-бромфенил)-3-гидроксипиперидин-1- карбоновой кислоты в виде бесцветного твердого вещества; МС: 299, 301 (M-C4H9)+. После алкилирования 4-метоксибензилбромидом получили трет-бутиловый эфир (3RS,4RS)-4-(4-бромфенил)-3-(4- метоксибензилокси)пиперидин-1-карбоновой кислоты в виде светло-желтого масла; МС: 418, 420 (M-C4H9)+.
(в) Из 4-(3- трифторметилфенил)пипиридин-4-ола путем элиминирования получили 4-(3-трифторметилфенил)-1,2,3,6-тетрагидропиридин в виде бесцветного твердого вещества; МС: 227 (М)+. Последующим гидроборированием получили (3RS, 4RS)-4-(3-трифторметилфенил)пиперидин-3-ол в виде бесцветного твердого вещества; МС: 245 (М)+. Путем введения BOC-группы получили трет-бутиловый эфир (3RS, 4RS)-3-гидрокси-4-(3- трифторметилфенил) пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 289 (M-C4H8)+. После алкилирования 4-метоксибензилбромидом получили трет-бутиловый эфир (3RS,4RS)-3-(4-метоксибензилокси)-4-(3- трифторметилфенил) пиперидин-1-карбоновой кислоты в виде светло-желтого масла; МС: 408 (M-C4H9)+.
(г) Из 1-бензил-4-(п-толил)пипиридин-4-ола путем элиминирования получили 1-бензил-4-(п-толил)-1,2,3,6-тетрагидропиридин в виде светло-желтого твердого вещества; МС: 263 (М)+. Последующим гидроборированием получили (3RS, 4RS)-1-бензил-4-(п-толил)пиперидин-3-ол в виде бесцветного твердого вещества; МС: 281 (М)+.
(д) Раствор 2,5 г (8,9 ммоля) (3RS,4RS)-1-бензил-4-(п-толил)пиперидин-3-ола в 100 мл метанола гидрировали при комнатной температуре и при давлении 5 бар в течение 18 ч с применением 10%-ного палладия на угле в качестве катализатора. Для последующей переработки катализатор отфильтровывали, промывали метанолом и полученный раствор упаривали при пониженном давлении. Остаток очищали хроматографией на силикагеле с использованием смеси 5:1:0,1 метиленхлорида, метанола и аммиака в качестве элюента. Таким путем получили 1,15 г (68% от теории) (3RS, 4RS)-4-(п-толил)пиперидин-3-ола в виде бесцветного твердого вещества; МС: 191 (М)+.
(е) Путем введения BOC-группы из (3RS,4RS)-4-(п-толил)пиперидин-3-ола получили трет-бутиловый эфир (3RS,4RS)-3-гидрокси-4-(п-толил)пиперидин-1- карбоновой кислоты в виде бесцветного твердого вещества; МС: 291 (М)+. После алкилирования 4-метоксибензилбромидом получили трет-бутиловый эфир (3RS, 4RS)-3-(4-метоксибензилокси)-4-(п-толил)пиперидин- 1-карбоновой кислоты в виде бесцветного масла; МС: 354 (M-C4H9)+.
Аналогично примеру 1(ж) получали следующие соединения.
(ж) Путем алкилирования трет-бутилового эфира (3RS,4RS)-3-гидрокси-4-фенилпиперидин-1-карбоновой кислоты 2-бромметилнафталином получили трет-бутиловый эфир (3RS,4RS)-3- (нафталин-2-илметокси)-4-фенилпиперидин-1-карбоновой кислоты в виде светло-желтого масла; МС: 417 (М)+.
(з) Путем алкилирования трет-бутилового эфира (3RS,4RS)-4-(4-бромфенил)-3- гидроксипиперидин-1-карбоновой кислоты 2-бромметилнафталином получили трет-бутиловый эфир (3RS, 4RS)-4-(4-бромфенил)-3-нафталин- 2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 495, 497 (М)+.
(и) Путем алкилирования трет-бутилового эфира (3RS,4RS)-3- гидрокси-4-(3-трифторметилфенил)пиперидин-1- карбоновой кислоты 2-бромметилнафталином получили трет-бутиловый эфир (3RS, 4RS)-3-(нафталин-2-илметокси)-4-(3- трифторметилфенил)пиперидин-1-карбоновой кислоты в виде светло-желтого масла; МС: 485 (М)+.
(к) Раствор 4,0 г (13,8 ммоля) трет-бутилового эфира (3RS,4RS)-3-гидрокси-4-фенилпиперидин-1- карбоновой кислоты в 100 мл метанола гидрировали при 100oC и при давлении 150 бар в течение 18 ч с применением 5%-ного родия на оксиде алюминия в качестве катализатора. Для последующей переработки катализатор отфильтровывали, промывали метанолом и полученный раствор упаривали при пониженном давлении. Остаток очищали хроматографией на силикагеле с использованием смеси 4: 1 гексана и уксусного эфира в качестве элюента. Таким путем получили 2,32 г (59% от теории) трет-бутилового эфира (3RS, 4RS)-4- циклогексил-3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 283 (М)+.
(л) Путем алкилирования трет-бутилового эфира (3RS,4RS)-4-циклогексил- 3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты 2- бромметилнафталином получили трет-бутиловый эфир (3RS, 4RS)-4- циклогексил-3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде светло-желтого масла; МС: 423 (М)+.
(м) Путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-(п- толил) пиперидин-1-карбоновой кислоты 2-бромметилнафталином получили трет-бутиловый эфир (3RS, 4RS)-3-(нафталин-2-илметокси)-4- п-толилпиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 431 (М)+.
Другие исходные вещества получали следующим образом.
(н) Из 2-бромнафталина и 1-бензил-4-пиперидона аналогично примеру 1(а) получили 1-бензил-4-нафталин-2-илпиперидин-4-ол в виде светло-желтого масла; МС: 317 (М)+. Путем элиминирования аналогично примеру 1(б) получили 1-бензил-4-нафталин-2-ил-1,2,3, 6-тетрагидропиридин в виде светло-коричневого масла; МС: 299 (М)+. Последующим отщеплением бензильной группы аналогично примеру 1(г) получили 2-триметилсилилэтиловый эфир 4- нафталин-2-ил-1, 2,3,6-тетрагидропиридин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 325 (M-C2H4)+. Обработкой тетрабутиламмонийфторидом в тетрагидрофуране аналогично примеру 1 (д) получили 4-нафталин-2-ил-1,2,3,6-тетрагидропиридин в виде бесцветного твердого вещества; МС: 209 (М)+. Последующим гидроборированием аналогично примеру 1(в) получили (3RS,4RS)-нафталин-2-ил-4-пиперидин-3-ол в виде бесцветного твердого вещества; МС: 227 (М)+. Путем введения BOC-группы аналогично примеру 1(е) получили трет-бутиловый эфир (3RS, 4RS)-3-гидрокси-4- нафталин-2-илпиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 327 (М)+. После алкилирования 2-бромметилнафталином аналогично способу, описанному в примере 1(ж), получили трет- бутиловый эфир (3RS, 4RS)-4-нафталин-2-ил-3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 467 (М)+.
(о) Аналогично примеру 2(д) каталитическим гидрированием (3RS,4RS)-1-бензил-4-нафталин-2-илпиперидин-3-ола получили (3RS,4RS)-4-(5,6,7,8-тетрагидронафталин-2-ил)пиперидин-3-ол в виде бесцветного твердого вещества; МС: 231 (М)+. Путем введения BOC-группы аналогично примеру 1(е) получили трет-бутиловый эфир (3RS, 4RS)-3-гидрокси-4-(5,6,7,8-тетрагидронафталин-2-ил) пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 331 (М)+. После алкилирования 2-бромметилнафталином аналогично способу, описанному в примере 1(ж), получили трет-бутиловый эфир (3RS, 4RS)- 3-(нафталин-2-илметокси)-4-(5,6,7,8-тетрагидронафталин-2-ил) пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 471 (М)+.
(п) Из 1-бензил-4-нафталин-1-ил-1, 2,3,6-тетрагидропиридина (ЕР-А-372776) путем гидроборирования аналогично примеру 1(в) получили (3RS,4RS)-1-бензил-4-нафталин-1-илпиперидин-3-ол в виде бесцветного твердого вещества; МС: 317 (М)+. Аналогично примеру 2(д) каталитическим гидрированием [10%-ный палладий на угле, этанол, 80oC, 24 ч, 50 бар, 21% от теории] удаляли бензильную группу. Полученный (3RS, 4RS)-4-нафталин-1-илпиперидин-3-ол представлял собой твердое вещество бежевого цвета; МС: 227 (М)+. Введением BOC-группы аналогично примеру 1(е) получили трет-бутиловый эфир (3RS, 4RS)-3-гидрокси-4-нафталин-1-илпиперидин-1- карбоновой кислоты в виде бесцветного твердого вещества; МС: 327 (М)+. После алкилирования 2-бромметилнафталином аналогично способу, описанному в примере 1(ж), получили трет-бутиловый эфир (3RS, 4RS)-4-нафталин-1-ил-3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты в виде бесцветного твердого вещества; МС: 467 (М)+.
(р) Из 1-бензил-4-(3,4-диметоксифенил)-1,2,3,6- тетрагидропиридина (JP 60146872) путем гидроборирования аналогично примеру 1(в) получили (3RS, 4RS)-1-бензил-(3, 4- диметоксифенил)пиперидин-3-ол в виде бесцветного твердого вещества; МС: 327 (М)+. Аналогично примеру 2(д) каталитическим гидрированием [10%-ный палладий на угле, метанол, комнатная температура, 18 ч, 5 бар, 81% от теории] удаляли бензильную группу. Полученный (3RS,4RS)-(3,4-диметоксифенил) пиперидин-3-ол представлял собой бесцветное твердое вещество; МС: 237 (М)+. Введением BOC-группы аналогично примеру 1(е) получили трет-бутиловый эфир (3RS, 4RS)-3-гидрокси-4-(3,4-диметоксифенил)пиперидин- 1-карбоновой кислоты в виде светло-желтого масла; МС: 337 (М)+. После алкилирования 2-бромметилнафталином аналогично способу, описанному в примере 1(ж), получили трет- бутиловый эфир (3RS,4RS)-4-(3,4-диметоксифенил)-3-(нафталин-2- илметокси) пиперидин-1-карбоновой кислоты в виде светло-желтого масла; МС: 477 (М)+.
(с) Из 5-бромаценафтена и 1-бензил-4- пиперидона аналогично примеру 1(а) получили 4-аценафтен-5-ил-1- бензилпиперидин-4-ол в виде желтого масла; МС: 343 (М)+. Путем элиминирования аналогично примеру 1(б) получили 4-аценафтен-5-ил-1- бензил-1,2,3,6-тетрагидропиридин в виде светло-коричневого масла; МС: 325 (М)+. Последующим гидроборированием аналогично примеру 1(в) получили (3RS,4RS)-1-бензилаценафтен-5-ил-4-пиперидин-3-ол в виде желтого масла; МС: 343 (М)+. Аналогично примеру 2(д) каталитическим гидрированием [10%-ный палладий на угле, метанол, комнатная температура, 18 ч, 5 бар, 95% от теории] удаляли бензильную группу. Полученный (3RS, 4RS)-4-аценафтен-5-илпиперидин- 3-ол представлял собой бесцветное твердое вещество; МС: 253 (М)+. Путем введения BOC-группы аналогично примеру 1(е) получили трет-бутиловый эфир (3RS, 4RS)-4-аценафтен-5-ил-3- гидроксипиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 353 (М)+. После алкилирования 2-бромметилнафталином аналогично способу, описанному в примере 1(ж), получили трет-бутиловый эфир (3RS,4RS)-4- аценафтен-5-ил-3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты в виде желтого твердого вещества; МС: 493 (М)+.
(т) Из 4- (4-хлорфенил)пипиридин-4-ола путем элиминирования аналогично примеру 1(б) получили 4-(4-хлорфенил)-1,2,3,6-тетрагидропиридин в виде светло-желтого твердого вещества; МС: 193, 195 (М)+. Последующим гидроборированием аналогично примеру 1(в) получили (3RS,4RS)-4-(4-хлорфенил)пиперидин-3-ол в виде бесцветного твердого вещества; МС: 211, 213 (М)+. Путем введения BOC-группы аналогично примеру 1(е) получили трет-бутиловый эфир (3RS, 4RS)-4- (4-хлорфенил)-3-гидроксипиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 255, 257 (М-C2H8)+. После алкилирования 4-феноксибензилхлоридом аналогично способу, описанному в примере 1(ж), получили трет-бутиловый эфир (3RS, 4RS)- 4-(4-хлорфенил)-3-(4-феноксибензилокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 437, 439 (M-C4H9)+.
(у) Путем введения BOC-группы из (3RS,4RS)-4-фенилпиперидин-3-ола [J.A. Gauthier и др. , US 4132710] получили трет-бутиловый эфир (3RS,4RS)-3-гидрокси-4-фенилпиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; tпл 134-134,5oC. Последующим алкилированием 2-бромметилнафталином получили трет-бутиловый эфир (3RS,4RS)-3-(нафталин-2-илметокси)-4-фенилпиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 417 (М)+.
Пример 3.
130 мг (0,31 ммоля) трет-бутилового эфира (3RS, 4RS)-4-(4- фторфенил)-3-(4-метоксибензилокси)пиперидин-1-карбоновой кислоты растворяли в 5 мл метанола, смешивали с 5 мл 2 н. раствора хлористого водорода в метаноле и полученную смесь перемешивали в течение 4 ч при 50oC. Далее смесь распределяли между уксусным эфиром и водным 5%-ным раствором гидрокарбоната натрия, органическую фазу сушили над сульфатом магния и в завершение удаляли растворитель при пониженном давлении. Сырой продукт очищали хроматографией на силикагеле с использованием смеси 10:1:0,1 метиленхлорида, метанола и аммиака в качестве элюента. Таким путем получили 76 мг (78% от теории) (3RS, 4RS)-4-(4- фторфенил)-3-(4-метоксибензилокси)пиперидина в виде бесцветного масла; МС: 316 (М+Н)+.
Использованный в качестве исходного продукта трет-бутиловый эфир (3RS, 4RS)-4-(4-фторфенил)-3-(4- метоксибензилокси)пиперидин-1-карбоновой кислоты получали следующим образом.
(а) 20,0 г (93,6 ммоля) гидрохлорида 4-(4- фторфенил)-1,2,3,6-тетрагидропиридина суспендировали в 160 мл абсолютного диметоксиэтана. 3атем при комнатной температуре порциями добавляли 10,6 г (280 ммолей) борогидрида натрия. После этого при 15-20oC по каплям добавляли раствор из 62 мл (500 ммолей) эфирата трифторида бора в 30 мл диметоксиэтана и в течение 2 ч перемешивали при комнатной температуре. 3атем при 20-25oC в течение 60 мин по каплям добавляли раствор 65 г (1,16 моля) гидроксида калия в 340 мл воды. Далее при 20-25oC в течение 30 мин по каплям добавляли 55 мл раствора перекиси водорода (30%-ного). Смесь перемешивали в течение 30 мин при комнатной температуре и затем в течение 3 ч нагревали с обратным холодильником. После охлаждения реакционной смеси выпавшую в осадок борную кислоту отфильтровывали. 3атем фильтрат распределяли между метиленхлоридом и водой, органическую фазу сушили над сульфатом магния и удаляли растворитель при пониженном давлении. Сырой продукт очищали хроматографией на силикагеле с использованием смеси 3:1:0,1 метиленхлорида, метанола и аммиака в качестве элюента. Таким путем получили 9,1 г (50% от теории) (3RS,4RS)-4-(4-фторфенил)пиперидин-3-ола в виде бесцветного масла; МС: 195 (М)+.
(б) 4,10 г (21,0 ммоль) (3RS, 4RS)-4-(4- фторфенил)пиперидин-3-ола растворяли в 35 мл абсолютного диметилформамида. К этому раствору при 0oC добавляли 3,2 мл (23,0 ммоля) триэтиламина с последующим добавлением по каплям раствора 5,04 г (23,1 ммоля) ди-трет-бутилдикарбоната в 15 мл диметилформамида. Смесь нагревали до комнатной температуры и перемешивали в течение 20 ч. Растворитель отгоняли при 50-55oC и при давлении 0,1 мм рт.ст. После этого полученный остаток распределяли между метиленхлоридом и водой, органическую фазу сушили над сульфатом магния и в завершение удаляли растворитель при пониженном давлении. Сырой продукт (7,09 г) очищали хроматографией на силикагеле с использованием смеси 2:3 уксусного эфира и гексана в качестве элюента. Таким путем получили 5,45 мг (88% от теории) трет-бутилового эфира (3RS, 4RS)-4-(4-фторфенил)-3- гидроксипиперидин-1-карбоновой кислоты; МС: 239 (M-C4H8)+.
(в) 200 мг (0,68 ммоля) трет-бутилового эфира (3RS,4RS)-4-(4-фтopфенил)- 3-гидроксипиперидин-1-карбоновой кислоты и 159 мг (1,01 ммоля) 4-метоксибензилхлорида растворяли в 3 мл диметилформамида. Добавляли 40 мг (1,01 ммоля) 60%-ной суспензии гидрида натрия и смесь перемешивали в течение 3 ч при комнатной температуре. 3атем реакционную смесь распределяли между уксусным эфиром и водой, органическую фазу сушили над сульфатом магния и в завершение удаляли растворитель при пониженном давлении. Сырой продукт очищали хроматографией на силикагеле с использованием смеси 1:3 уксусного эфира и гексана в качестве элюента. Таким путем получили 250 мг (90% от теории) трет-бутилового эфира (3RS, 4RS)-4-(4- фторфенил)-3-(4-метоксибензилокси)пиперидин-1-карбоновой кислоты в виде светло-желтого масла; МС: 358 (M-C4H9)+.
Пример 4.
Аналогично примеру 3 получали следующие соединения:
1) из трет-бутилового эфира (3RS,4RS)-4-(4-фторфенил)-3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-(4-фторфенил)-3-(нафталин-2-илметокси)пиперидин в виде бесцветного масла; МС: 336 (М+1)+;
2) из трет-бутилового эфира (3RS, 4RS)-3-(3-бензилоксибензилокси)-4-(4-фторфенил)пиперидин-1-карбоновой кислоты получили (3RS,4RS)-3-(3-бензилоксибензилокси)-4-(4-фторфенил) пиперидин в виде бесцветного твердого вещества; МС: 392 (М+1)+;
3) из трет-бутилового эфира (3RS,4RS)-4-(4-фторфенил)-3- (4-метоксихиназолин-2-илметокси)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-(4-фторфенил)-3-(4-метоксихиназолин-2- илметокси)пиперидин в виде бесцветного твердого вещества; МС: 368 (М+1)+;
4) из трет-бутилового эфира (3RS, 4RS)-3-(бензо[b]тиофен-5- илметокси)-4-(4-фторфенил)пиперидин-1-карбоновой кислоты получили (3RS, 4RS) -3-(бензо[b] тиофен-5-илметокси)-4-(4- фторфенил)пиперидин в виде бесцветного твердого вещества; МС: 342 (М+1)+;
5) из трет-бутилового эфира (3RS,4RS)-4-(4-фторфенил)-3- (индан-5-илметокси)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-(4-фторфенил)-3-(индан-5-илметокси)пиперидин в виде бесцветного твердого вещества; МС: 326 (М+1)+;
6) из трет-бутилового эфира (3RS,4RS)-4-(4-фторфенил)-3- (5,6,7, 8-тетрагидронафталин-2-илметокси)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-(4-фторфенил)-3-(5,6,7,8-тетрагидронафталин- 2-илметокси)пиперидин в виде бесцветного твердого вещества; МС: 340 (М+1)+;
7) из трет-бутилового эфира (3RS,4RS)-4-(4-фторфенил)- 3-(изохинолин-6-илметокси)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-(4-фторфенил)-3-(изохинолин-6-илметокси) пиперидин в виде бесцветного твердого вещества; МС: 337 (М+1)+.
Использованные в качестве исходных веществ BOC-производные получали аналогично описанному в примере 3(в) методу алкилирования следующим образом:
- из трет-бутилового эфира (3RS,4RS)-4-(4- фторфенил)-3-гидроксипиперидин-1-карбоновой кислоты получили трет- бутиловый эфир (3RS,4RS)-4-(4-фторфенил)-3-(нафталин-2-илметокси)пиперидинкарбоновой кислоты в виде светло-желтого масла; МС: 436 (М+1)+;
- из трет-бутилового эфира (3RS,4RS)-4-(4-фторфенил)-3-гидроксипиперидин-1-карбоновой кислоты и 3- бензилоксибензилхлорида [J. Med. Chem. 31(3), 606 (1988)] получили трет-бутиловый эфир (3RS, 4RS)-3-(3-бензилоксибензилокси)-4-(4- фторфенил)пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 492 (М+1)+;
- из трет-бутилового эфира (3RS, 4RS)-4-(4-фторфенил)-3-гидроксипиперидин-1-карбоновой кислоты и 2-бромметил-4-метоксихиназолина получили трет-бутиловый эфир (3RS, 4RS)-4-(4-фторфенил)-3-(4- метоксихиназолин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 492 (М+1)+;
- из трет-бутилового эфира (3RS, 4RS)-4-(4-фторфенил)-3-гидроксипиперидин-1-карбоновой кислоты и 5-бромметилбензо[b]тиофена [J. Med. Chem. 34(1), 65 (1991)] получили трет-бутиловый эфир (3RS, 4RS)-3-(бензо[b]тиофен-5-илметокси)-4-(4-фторфенил) пиперидин-1-карбоновой кислоты в виде светло-желтой смолы; МС: 442 (М+1)+;
- из трет-бутилового эфира (3RS, 4RS)-4-(4-фторфенил)-3- гидроксипиперидин-1-карбоновой кислоты и 5-хлорметилиндан [Recl. Trav. Chim. Pays-Bas 77, 792 (1988)] получили трет-бутиловый эфир (3RS, 4RS)-4-(4-фторфенил)-3-(индан-5-илметокси)пиперидин-1- карбоновой кислоты в виде бесцветного твердого вещества; МС: 426 (М+1)+;
- из трет-бутилового эфира (3RS, 4RS)-4-(4-фторфенил)-3- гидроксипиперидин-1-карбоновой кислоты и 4-хлорметил-1,2,3,4- тетрагидронафталина [J. Chem. Soc. 684 (1941)] получили трет-бутиловый эфир (3RS,4RS)-4-(4-фторфенил)-3-(5,6,7, 8- тетрагидронафталин-2-илметокси) пиперидин-1 -карбоновой кислоты в виде светло-желтой смолы; МС: 440 (М+1)+;
- из трет-бутилового эфира (3RS, 4RS)-4-(4-фторфенил)-3-гидроксипиперидин-1-карбоновой кислоты и гидробромида 6-бромметилизохинолина получили трет-бутиловый эфир (3RS, 4RS)-4-(4-фторфенил)-3-(изохинолин-6-илметокси)пиперидин-1-карбоновой кислоты в виде светло-желтой смолы; МС: 437 (М+1)+.
Указанные ниже соединения, использованные в качестве алкилирующих агентов, получали следующим образом.
2-Бромметил-4-метоксихиназолин.
(а) Аналогично методике, описанной для способа получения 6-бромметилхиноксалина [J. Het. Chem. 11, 595 (1974)] из 6-метилхиноксалина, бромированием 2-метил-4-метоксихиназолина [Reсl. Trav. Chim. Pays-Bas 76, 401 (1957)] N-бромсукцинимидом в четыреххлористом углероде получили 2-бромметил-4-метоксихиназолин в виде светло-желтого твердого вещества; МС: 252, 254 (М)+.
Гидробромид 6-бромметилизохинолина.
(б) Из изохинолин-6-карбоновой кислоты [J. Am. Chem. Soc. 61, 183 (1939)] этерификацией этанолом/серной кислотой получили этиловый эфир изохинолин-6-карбоновой кислоты в виде бесцветного твердого вещества; МС: 201 (М)+. Путем последующего восстановления получили 6-изохинолинметанол в виде желтого твердого вещества, которое непосредственно использовали на следующей стадии.
(в) Раствор 190 мг (1,19 ммоля) 6-изохинолинметанола в 1 мл ледяной уксусной кислоты смешивали с 2 мл 30%-ного HBr в ледяной уксусной кислоте и выдерживали в течение 45 мин при 70oC. Реакционную смесь охлаждали, смешивали с 20 мл диэтилового эфира и перемешивали при 0oC в течение 30 мин. Образовавшийся твердый продукт отфильтровывали, промывали диэтиловым эфиром и сушили в высоком вакууме. Таким путем получили гидробромид 6-бромметилизохинолина (73% от теории) в виде светло-коричневого твердого вещества; МС: 221, 223 (М)+.
Пример 5.
70 мг (0,141 ммоля) β- триметилсилилэтилового эфира (3RS,4RS)-4-(4- фторфенил)-3-(4- гидроксинафталин-2-илметокси) пиперидин-1-карбоновой кислоты растворяли в 1,0 мл раствора тетрабутиламмонийфторида (в растворе тетрагидрофурана) и перемешивали в течение 1 ч при комнатной температуре. 3атем смесь распределяли между метиленхлоридом и водным 5%-ным раствором гидрокарбоната натрия, после чего органическую фазу сушили над сульфатом магния и в завершение отгоняли растворитель при пониженном давлении. Сырой продукт (72 мг) очищали хроматографией на силикагеле с использованием смеси 10:1:0,1 метиленхлорида, метанола и аммиака в качестве элюента. Таким путем получили 41 мг (83% от теории) (3RS, 4RS)-4-(4- фторфенил)-3-(4-гидроксинафталин-2-илметокси)пиперидина в виде бесцветного твердого вещества; МС: 352 (М+Н)+.
Использованный в качестве исходного вещества β- триметилсилилэтиловый эфир (3RS, 4RS)-4-(4-фторфенил)-3-(4-гидроксинафталин-2-илметокси) пиперидин-1-карбоновой кислоты получали следующим образом.
(a) 17,87 г (82,64 ммоля) этилового эфира 4-гидроксинафталин-2-карбоновой кислоты [J. Agric. Chem. Soc. Japan 24, 313 (1950)] суспендировали в 900 мл метиленхлорида, суспензию охлаждали до 0-5oC и затем смешивали с 17,9 мл (91,02 ммоля) 2-(триметилсилил)этоксиметилхлорида (СЭМ-хлорида) и 28,3 мл (165,31 ммоля) N-этилдиизопропиламина. Желтый раствор нагревали до комнатной температуры и перемешивали в течение 2 ч. Растворитель отгоняли при пониженном давлении и сырой продукт без последующей переработки хроматографировали на силикагеле с использованием смеси 3:2 метиленхлорида и гексана в качестве элюента. Таким путем получили 15,81 г (99% от теории) этилового эфира 4-(2- триметилсилилэтоксиметокси)нафталин-2-карбоновой кислоты в виде светло-желтого масла; МС: 322, 324 (М)+.
(б) К суспензии из 3,29 г (86,69 ммоля) алюмогидрида лития в 230 мл диэтилового эфира при температуре в интервале от -5 до 0oC в атмосфере аргона в течение 90 мин по каплям добавляли раствор 28, 31 г (81,70 ммоля) этилового эфира 4-(2-триметилсилилэтоксиметокси)нафталин-2-карбоновой кислоты в 480 мл диэтилового эфира. Реакционную смесь нагревали до комнатной температуры и перемешивали в течение 2 ч. Для дальнейшей переработки смесь охлаждали до 0oC, смешивали, добавляя по каплям, с 25 мл уксусного эфира, а также 50 мл насыщенного раствора калийнатрийтартрата. Образовался слегка желтоватый раствор с белым осадком. Раствор нагревали до комнатной температуры и декантировали с осадка. Остаток трижды взмучивали в диэтиловом эфире и в каждом случае растворитель удаляли декантированием. Объединенные органические фазы промывали водой, сушили над сульфатом магния и в завершение удаляли растворитель при пониженном давлении. Сырой продукт (26,4 г) очищали хроматографией на силикагеле с использованием смеси 3:7 уксусного эфира и гексана. Таким путем получили 23,72 г (95% от теории) [4-(2-триметилсилилэтоксиметокси)нафталин-2-ил] метанола в виде светло-желтого масла; МС: 304 (М)+.
(в) 23,72 г (77,91 ммоля) [4-(2-триметилсилилэтоксиметокси)нафталин-2-ил] метанола растворяли в 350 мл четыреххлористого углерода, затем раствор охлаждали до 0oC. Далее добавляли 350 мл ацетонитрила и 26,54 г (101,2 ммоля) трифенилфосфина. Светло-желтый раствор перемешивали в течение 30 мин при 0oC, нагревали до комнатной температуры и вновь перемешивали в течение 2 ч. 3атем дополнительно добавляли 10,14 г (38,7 ммоля) трифенилфосфина и реакционную смесь перемешивали далее в течение 90 мин при комнатной температуре. После этого смесь распределяли между метиленхлоридом и водой, органическую фазу сушили над сульфатом магния и в завершение удаляли растворитель при пониженном давлении. Сырой продукт (26,4 г) очищали хроматографией на силикагеле с использованием смеси 3:7 уксусного эфира и гексана в качестве элюента. Таким путем получили 15,81 г (63% от теории) 2-хлорметил-4- ( β - триметилсилилэтоксиметокси)нафталина в виде светло-желтого масла; МС: 322, 324 (М)+.
(г) Раствор 4,00 г (20,5 ммоля) (3RS,4RS)-4-(4-фторфенил)пиперидин-3-ола в 150 мл этанола смешивали с 2,80 г (26,4 ммоля) карбоната натрия и нагревали до температуры дефлегмации. В течение 1 ч по каплям добавляли раствор 2,50 мл (21,1 ммоля) бензилбромида в 50 мл этанола и затем перемешивали в течение 2 ч при температуре дефлегмации. Бледно-коричневатую суспензию фильтровали и фильтрат концентрировали при пониженном давлении. После этого остаток распределяли между метиленхлоридом и водой, органическую фазу сушили над сульфатом магния и в завершение удаляли растворитель при пониженном давлении. Сырой продукт очищали хроматографией на силикагеле с использованием смеси 2:3 уксусного эфира и гексана в качестве элюента. Таким путем получили 4,34 г (74% от теории) (3RS,4RS)-1- бензил-4-(4-фторфенил)пиперидин-3-ола в виде бесцветного твердого вещества; МС: 285 (М)+.
(д) Аналогично примеру 1(ж) путем алкилирования (3RS,4RS)-1-бензил-4-(4-фторфенил) пиперидин-3-ола 2-хлорметил-4-( β- -триметилсилилэтоксиметокси) нафталином получили (3RS,4RS)-1-бензил-4-(4-фторфенил)-3-[4-(2- триметилсилилэтоксиметокси)нафталин-2-илметокси] пиперидин в виде светло-желтого масла; МС: 572 (М+Н)+.
(е) Аналогично примеру 1(г) путем отщепления бензильной группы с помощью (β- триметилсилилэтилового эфира хлормуравьиной кислоты из (3RS,4RS) -1-бензил-4-(4-фторфенил)-3-[4-(2-триметилсилилэтоксиметокси) нафталин-2-илметокси] пиперидина получили β- триметилсилилэтиловый эфир (3RS,4RS)-4-(4-фторфенил)-3-[4-(2-триметилсилилэтоксиметокси)нафталин- 2-илметокси] пиперидин-1-карбоновой кислоты в виде светло-желтого масла; МС: 626 (M+H)+.
(ж) 4,65 г (7,43 ммоля) β- триметилсилилэтилового эфира (3RS, 4RS)-4-(4-фторфенил)-3-[4-(2-триметилсилилэтоксиметокси)нафталин-2- илметокси] пиперидин-1-карбоновой кислоты растворяли в 40 мл метанола, смешивали с 2 н. раствором хлористого водорода в метаноле и перемешивали в течение 90 мин при 50oC. После этого смесь распределяли между метиленхлоридом и водным 5%-ным раствором гидрокарбоната натрия, органическую фазу сушили над сульфатом магния и в завершение удаляли растворитель при пониженном давлении. Сырой продукт (6,8 г) очищали хроматографией на силикагеле с использованием смеси 3: 7 уксусного эфира и гексана. Таким путем получили 2,93 г (80% от теории) β- триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)-3-(4- гидроксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 496 (M)+.
Пример 6.
Аналогично примеру 5 получали следующие соединения:
1) из β- триметилсилилэтилового эфира (3RS, 4RS)-4-(4-фторфенил)-3-(1-гидроксинафталин-2-илметокси)пиперидин-1- карбоновой кислоты получили 4-(4-фторфенил)-3-(1-гидроксинафталин-2- илметокси)пиперидин в виде светло-коричневого твердого вещества; МС: 351 (M)+;
2) из β- триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)-3-(5-гидроксинафталин-2-илметокси)пиперидин-1- карбоновой кислоты получили 4-(4-фторфенил)-3-(5-гидроксинафталин-2- илметокси)пиперидин в виде бесцветного твердого вещества; МС: 351 (M)+;
3) из β- триметилсилилэтилового эфира (3RS, 4RS)-4-(4-фторфенил)-3-(6-гидроксинафталин-2-илметокси)пиперидин-1- карбоновой кислоты получили 4-(4-фторфенил)-3-(6-гидроксинафталин-2- илметокси)пиперидин в виде бесцветного твердого вещества; МС: 351 (M)+;
4) из β- триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)-3-(7-гидроксинафталин-2-илметокси)пиперидин-1- карбоновой кислоты получили 4-(4-фторфенил)-3-(7-гидроксинафталин-2-илметокси)пиперидин в виде светло-коричневого твердого вещества; МС: 351 (M)+;
5) из β- триметилсилилэтилового эфира (3RS, 4RS)-4-(4-фторфенил)-3-(8-гидроксинафталин-2-илметокси)пиперидин-1- карбоновой кислоты получили 4-(4-фторфенил)-3-(8-гидроксинафталин-2- илметокси)пиперидин в виде светло-желтой смолы; МС: 352 (M+H)+.
Использованные в качестве исходных материалов β- триметилсилилэтилкарбаматы получали аналогично описанному в примере 5(а)-(е) способу следующим образом.
(а) Из метилового эфира 1-гидроксинафталин-2-карбоновой кислоты [J. Chem. Soc. 309 (1948)] путем введения защитной группы получили метиловый эфир 1-(2-триметилсилилэтоксиметокси)нафталин-2-карбоновой кислоты в виде светло-желтого масла; МС: 333 (M+H)+.
(б) Восстановлением метилового эфира 1-(2-триметилсилилэтоксиметокси)нафталин-2-карбоновой кислоты получили [1-(2-триметилсилилэтоксиметокси)нафталин-2-ил]метанол в виде светло-желтого масла; МС: 305 (M+H)+.
(в) Путем хлорирования [1-(2-триметилсилилэтоксиметокси)нафталин-2-ил] метанола получили 2-хлорметил-1-( β- триметилсилилэтоксиметокси)нафталин в виде бесцветного масла; МС: 322, 324 (M)+.
(г) Путем алкилирования (3RS,4RS)-1-бензил-4-(4-фторфенил)пиперидин-3-ола 2-хлорметил-1-( β- триметилсилилэтоксиметокси)нафталином получили (3RS, 4RS)-1-бензил-3-(4-фторфенил)-3-[1-(2- триметилсилилэтоксиметокси)нафталин-2-илметокси] пиперидин в виде светло-желтого масла; МС: 572 (M+H)+.
(д) Путем отщепления N-бензильной группы (3RS,4RS)-1-бензил-3-(4-фторфенил)-3-[1-(2- триметилсилилэтоксиметокси)нафталин-2-илметокси] пиперидина β- триметилсилилэтиловым эфиром хлормуравьиной кислоты получили β- триметилсилилэтиловый эфир (3RS, 4RS)-4-(4-фторфенил)-3-[1-(2- триметилсилилэтоксиметокси)нафталин-2-илметокси]пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 626 (M+H)+.
(е) Отщепление СЭМ-группы β- триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)-3-[1-(2-триметилсилилэтоксиметокси)нафталин-2- илметокси] пиперидин-1-карбоновой кислоты получили β- триметилсилилэтиловый эфир (3RS, 4RS)-4-(4-фторфенил)-3-(1-гидроксинафталин-2-илметокси)пиперидин-1- карбоновой кислоты в виде бесцветного масла; МС: 494 (M-H)- .
(ж) Из 5-гидроксинафталин-2-карбоновой кислоты [Bull. Soc. Chim. Fr., 857 (1953)] сначала путем этерификации метанолом/серной кислотой получили метиловый эфир 5-гидроксинафталин-2-карбоновой кислоты в виде светло-желтого твердого вещества; МС: 202 (M)+. Введением защитной группы получили метиловый эфир 5-(2-триметилсилилэтоксиметокси)нафталин-2-карбоновой кислоты в виде светло-желтого масла; МС: 333 (M+H)+.
(з) Восстановлением метилового эфира 5-(2-триметилсилилэтоксиметокси)нафталин-2-карбоновой кислоты получили [5-(2-триметилсилилэтоксиметокси)нафталин-2-ил]метанол в виде светло-желтого масла; МС: 305 (M+H)+.
(и) Хлорированием [5-(2-триметилсилилэтоксиметокси)нафталин-2-ил]метанола получили 2-хлорметил-5-( β- триметилсилилэтоксиметокси)нафталин в виде бесцветного масла; МС: 322, 324 (M)+ .
(к) Путем алкилирования (3RS,4RS)-1-бензил-4-(4-фторфенил)пиперидин-3-ола 2-хлорметил-5-( β- триметилсилилэтоксиметокси)нафталином получили (3RS, 4RS)-1-бензил-3-(4-фторфенил)пиперидин-3-[5-(2- триметилсилилэтоксиметокси)нафталин-2-илметокси] пиперидин в виде светло-желтого масла; МС: 572 (M+H)+.
(л) Отщеплением N-бензильной группы (3RS, 4RS)-1-бензил-3-(4-фторфенил)-3-[5-(2- триметилсилилэтоксиметокси)нафталин-2-илметокси]пиперидина β- триметилсилилэтиловым эфиром хлормуравьиной кислоты получили β- триметилсилилэтиловый эфир (3RS,4RS)-4-(4-фторфенил)-3-[5-(2- триметилсилилэтоксиметокси)нафталин-2-илметокси]пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 626 (M+H)+.
(м) Путем отщепления СЭМ-группы в β- триметилсилилэтиловом эфире (3RS, 4RS)-4-(4-фторфенил)-3-[5-(2- триметилсилилэтоксиметокси)нафталин-2-илметокси] пиперидин-1-карбоновой кислоты получили β- триметилсилилэтиловый эфир (3RS, 4RS)-4-(4-фторфенил)-3-(5-гидроксинафталин-2-илметокси)пиперидин-1- карбоновой кислоты в виде бесцветного масла; МС: 494 (M-H)-.
(н) Из этилового эфира 6-гидроксинафталин-2-карбоновой кислоты [J. Chem. Soc. 123 (1923)] путем введения защитной группы получили этиловый эфир 6-(2-триметилсилилэтоксиметокси)нафталин-2-карбоновой кислоты в виде светло-желтого масла; МС: 346 (M)+.
(о) Восстановлением этилового эфира 6-(2-триметилсилилэтоксиметокси)нафталин-2-карбоновой кислоты получили [6-(2-триметилсилилэтоксиметокси)нафталин-2-ил]метанол в виде бесцветного твердого вещества; МС: 304 (M)+.
(п) Путем хлорирования [6-(2-триметилсилилэтоксиметокси)нафталин-2-ил] метанола получили 6-хлорметил-2-( β- триметилсилилэтоксиметокси)нафталин в виде бесцветного масла; МС: 322, 324 (M)+.
(р) Путем алкилирования (3RS,4RS)-1-бензил-4-(4-фторфенил)пиперидин-3-ола 6-хлорметил-2-( β- триметилсилилэтоксиметокси)нафталином получили (3RS, 4RS)-1-бензил-3-(4-фторфенил)-3-[6-(2- триметилсилилэтоксиметокси)нафталин-2-илметокси] пиперидин в виде светло-желтого масла; МС: 572 (M+H)+.
(с) Путем отщепления N-бензильной группы (3RS,4RS)-1-бензил-3-(4-фторфенил)-3-[6-(2- триметилсилилэтоксиметокси)нафталин-2-илметокси] пиперидина β- триметилсилилэтиловым эфиром хлормуравьиной кислоты получили β- триметилсилилэтиловый эфир (3RS, 4RS)-4-(4-фторфенил)-3-[6-(2- триметилсилилэтоксиметокси)нафталин-2-илметокси]пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 626 (M+H)+.
(т) Отщепление СЭМ-группы β- триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)-3-[6-(2-триметилсилилэтоксиметокси)нафталин-2- илметокси] пиперидин-1-карбоновой кислоты получили β- триметилсилилэтиловый эфир (3RS, 4RS)-4-(4-фторфенил)-3-(6- гидроксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветной смолы; МС: 495 (M)+.
(у) Из 7-гидроксинафталин-2-карбоновой кислоты [Bull. Soc. Chim. Fr., 573 (1952)] сначала путем этерификации метанолом/серной кислотой получили метиловый эфир 7-гидроксинафталин-2-карбоновой кислоты в виде бесцветного твердого вещества; МС: 202 (M)+. Введением защитной группы получили метиловый эфир 7-(2-триметилсилилэтоксиметокси)нафталин-2-карбоновой кислоты в виде светло-желтого масла; МС: 332 (M+H)+.
(ф) Восстановлением метилового эфира 7-(2-триметилсилилэтоксиметокси)нафталин-2-карбоновой кислоты получили [7-(2-триметилсилилэтоксиметокси)нафталин-2-ил]метанол в виде светло-желтого масла; МС: 304 (M+H)+.
(х) Хлорированием [7-(2-триметилсилилэтоксиметокси)нафталин-2-ил]метанола получили 2-хлорметил-7-( β- триметилсилилэтоксиметокси)нафталин в виде светло-желтого масла; МС: 322, 324 (M)+.
(ц) Путем алкилирования (3RS,4RS)-1-бензил-4-(4-фторфенил)пиперидин-3-ола 2-хлорметил-7-( β- триметилсилилэтоксиметокси)нафталином получили (3RS, 4RS)-1-бензил-3-(4-фторфенил)пиперидин-3-[7-(2- триметилсилилэтоксиметокси)нафталин-2-илметокси] пиперидин в виде светло-желтого масла; МС: 572 (M+H)+.
(ч) Отщеплением N-бензильной группы (3RS, 4RS)-1-бензил-3-(4-фторфенил)-3-[7-(2- триметилсилилэтоксиметокси)нафталин-2-илметокси]пиперидина β- триметилсилилэтиловым эфиром хлормуравьиной кислоты получили β- триметилсилилэтиловый эфир (3RS,4RS)-4-(4-фторфенил)-3-[7-(2- триметилсилилэтоксиметокси)нафталин-2-илметокси]пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 626 (M+H)+.
(ш) Путем отщепления СЭМ-группы β- триметилсилилэтилового эфира (3RS, 4RS)-4-(4-фторфенил)-3-[7-(2-триметилсилилэтоксиметокси)нафталин-2- илметокси] пиперидин-1-карбоновой кислоты получили β- триметилсилилэтиловый эфир (3RS, 4RS)-4-(4-фторфенил)-3-(7- гидроксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде светло-желтого масла; МС: 495 (M)+.
(щ) Из 8-гидроксинафталин-2-карбоновой кислоты [Bull. Soc. Chim. Fr., 857 (1953)] сначала путем этерификации метанолом/серной кислотой получили метиловый эфир 8-гидроксинафталин-2-карбоновой кислоты в виде светло-желтого твердого вещества; МС: 202 карбоновой кислоты в виде светло-желтого масла; МС: 274 [M-(C2H4+CH2O)]+.
(э) Восстановлением метилового эфира 8-(2-триметилсилилэтоксиметокси)нафталин-2-карбоновой кислоты получили [8-(2-триметилсилилэтоксиметокси)нафталин-2-ил]метанол в виде бесцветного масла; МС: 304 (M)+.
(аа) Хлорированием [8-(2-триметилсилилэтоксиметокси)нафталин-2-ил] метанола получили 2-хлорметил-8-(2-триметилсилилэтоксиметокси)нафталин в виде светло-желтого масла; МС: 322, 324 (M)+.
(бб) Путем алкилирования (3RS,4RS)-1-бензил-4-(4-фторфенил)пиперидин-3-ола 2-хлорметил-8-(2-триметилсилилэтоксиметокси)нафталином получили (3RS, 4RS)-1-бензил-3-(4-фторфенил)пиперидин-3-[8-(2- триметилсилилэтоксиметокси)нафталин-2-илметокси] пиперидин в виде светло-желтого масла; МС: 572 (M+H)+.
(вв) Отщеплением N-бензильной группы (3RS,4RS)-1-бензил-3-(4-фторфенил)-3-[8-(2- триметилсилилэтоксиметокси)нафталин-2-илметокси]пиперидина β - триметилсилилэтиловым эфиром хлормуравьиной кислоты получили β- триметилсилилэтиловый эфир (3RS, 4RS)-4-(4-фторфенил)-3-[8-(2- триметилсилилэтоксиметокси)нафталин-2-илметокси]пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 626 (M+H)+.
(гг) Путем отщепления СЭМ-группы β- триметилсилилэтилового эфира (3RS, 4RS)-4-(4-фторфенил)-3-[8-(2- триметилсилилэтоксиметокси)нафталин-2-илметокси] пиперидин-1-карбоновой кислоты получили β - триметилсилилэтиловый эфир (3RS, 4RS)-4-(4-фторфенил)-3-(8-гидроксинафталин-2-илметокси)пиперидин-1- карбоновой кислоты в виде бесцветного масла; МС: 494 (M-H)-.
Пример 7.
Аналогично примеру 3, соответственно 5 получали следующие соединения.
1) (3RS,4RS)-4-(4-Фторфенил)-3-(3-гидроксинафталин-2- илметокси)пиперидин.
Аналогично примерам 3 и 5(ж) путем отщепления обеих защитных групп с помощью метанольной соляной кислоты из трет-бутилового эфира (3RS, 4RS)-4-(4-фторфенил)-3-[3-(2-триметилсилилэтоксиметокси)нафталин-2- илметокси] пиперидин-1-карбоновой кислоты получили (3RS,4RS)-4-(4-фторфенил)-3-(3-гидроксинафталин-2- илметокси)пиперидин в виде бесцветного твердого вещества; МС: 351 (M)+.
Использованный в качестве исходного вещества трет-бутиловый эфир (3RS, 4RS)-4-(4-фторфенил)-3-[3-(2-триметилсилилэтоксиметокси)нафталин-2- илметокси]пиперидин-1-карбоновой кислоты получали следующим образом.
(а) Аналогично примеру 5(а) путем введения защитной группы из метилового эфира из метилового эфира 3-гидроксинафталин-2-карбоновой кислоты получили метиловый эфир 3-(2-триметилсилилэтоксиметокси)нафталин-2-карбоновой кислоты в виде светло-желтого масла; МС: 274 [M-(C2H4+CH2O)]+.
(б) Аналогично примеру 5(б) восстановлением метилового эфира 3-(2-триметилсилилэтоксиметокси)нафталин-2-карбоновой кислоты получили [3-(2-триметилсилилэтоксиметокси)нафталин-2-ил]метанол в виде светло-желтого масла; МС: 304 (M)+.
(в) 400 мг (1,30 ммоля) [3-(2-триметилсилилэтоксиметокси)нафталин-2-ил] метанола и 462 мг (1,81 ммоля) четырехбромистого углерода растворяли в 5 мл абсолютного ацетонитрила и раствор охлаждали до 0oC. Далее при 0oC в течение 10 мин по каплям добавляли раствор 446 мг (1,68 ммоля) трифенилфосфина в 6 мл абсолютного ацетонитрила и перемешивание продолжали в течение 30 мин при 0oC. После этого растворитель отгоняли при пониженном давлении и сырой продукт без дальнейшей переработки очищали хроматографией на силикагеле с использованием смеси 2:3 метиленхлорида и гексана в качестве элюента. Таким путем получили 314 мг (65% от теории) 2-бромметил-3-(2-триметилсилилэтоксиметокси)нафталина в виде светло-желтого масла; МС: 366, 368 (M)+.
(г) Аналогично примеру 3(в) путем алкилирования трет-бутилового эфира (3RS,4RS)-4-(4-фторфенил)-3-гидроксипиперидин-1-карбоновой кислоты 2-бромметил-3-(2-триметилсилилэтоксиметокси)нафталином получили трет-бутиловый эфир (3RS,4RS)-4-(4-фторфенил)-3-[3-(2- триметилсилилэтоксиметокси)нафталин-2-илметокси] пиперидин-1-карбоновой кислоты в виде светло-желтого масла; МС: 523 [M-(C2 H4+CH2O)]+.
2) (3RS,4RS)-4-(4-Фторфенил)-3-(1-метоксинафталин-2- илметокси)пиперидин.
Аналогично примеру 3 путем отщепления защитной BOC-группы из трет-бутилового эфира (3RS, 4RS)-4-(4-фторфенил)-3-[1-метоксинафталин-2- илметокси] пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-(4-фторфенил)-3-(1-метоксинафталин-2-илметокси)пиперидин в виде светло-желтого масла; МС: 365 (M)+.
Использованный в качестве исходного вещества трет-бутиловый эфир (3RS, 4RS)-4-(4-фторфенил)-3-[1-метоксинафталин-2-илметокси] пиперидин-1- карбоновой кислоты получали следующим образом.
(д) Аналогично примеру 5(б) восстановлением метилового эфира 1-метоксинафталин-2-карбоновой кислоты [J. Chem. Soc. 121 (1922)] получили [1-метоксинафталин-2-ил]метанол в виде бесцветного твердого вещества; МС: 188 (M)+.
(е) Аналогично примеру 7(в) путем бромирования [1-метоксинафталин-2-ил] метанола получили 2-бромметил-1-метоксинафталин в виде бесцветного твердого вещества; МС: 250, 252 (M)+.
(ж) Аналогично примеру 3(в) путем алкилирования трет-бутилового эфира (3RS, 4RS)-4-(4-фторфенил)-3-гидроксипиперидин-1-карбоновой кислоты [пример 3(б)] 2-бромметил-1-метоксинафталином получили трет-бутиловый эфир (3RS, 4RS)-4-(4-фторфенил)-3-[1-метоксинафталин-2- илметокси] пиперидин-1-карбоновой кислоты в виде бесцветной смолы; МС: 465 (M)+.
3) (3RS, 4RS)-4-(4-Фторфенил)-3-(3-метоксинафталин-2- илметокси)пиперидин.
Аналогично примеру 3 путем отщепления защитной BOC-группы из трет-бутилового эфира (3RS, 4RS)-4-(4-фторфенил)-3-[3-метоксинафталин-2- илметокси] пиперидин-1-карбоновой кислоты получили (3RS,4RS)-4-(4-фторфенил)-3-(3-метоксинафталин-2-илметокси)пиперидин в виде светло-желтого масла; МС: 365 (M)+.
Использованный в качестве исходного вещества трет-бутиловый эфир (3RS, 4RS)-4-(4-фторфенил)-3-[3-метоксинафталин-2-илметокси] пиперидин-1- карбоновой кислоты получали следующим образом.
(з) Аналогично примеру 5(б) восстановлением метилового эфира 3-метоксинафталин-2-карбоновой кислоты [J. Chem. Soc. 2351 (1951)] получили [3-метоксинафталин-2-ил] метанол в виде бесцветного твердого вещества; МС: 188 (M)+.
(и) Аналогично примеру 7(в) путем бромирования [3-метоксинафталин-2-ил] метанола получили 2-бромметил-3-метоксинафталин в виде бесцветного твердого вещества; МС: 250, 252 (M)+.
(к) Аналогично примеру 3(в) путем алкилирования трет-бутилового эфира (3RS, 4RS)-4-(4-фторфенил)-3-гидроксипиперидин-1-карбоновой кислоты [пример 3(б)] 2-бромметил-3-метоксинафталином получили трет-бутиловый эфир (3RS, 4RS)-4-(4-фторфенил)-3-[3-метоксинафталин-2- илметокси] пиперидин-1-карбоновой кислоты в виде бесцветной смолы; МС: 465 (M)+.
Пример 8.
(а) К 1,49 г магниевой стружки, предварительно покрытой тетрагидрофураном, по каплям добавляли раствор 12,06 г (60 ммолей) 5-бромбензо[1,3]диоксола в 30 мл абсолютного тетрагидрофурана с последующим добавлением 11,35 г (60 ммолей) 1-бензил-4-пиперидона. Реакционную смесь перемешивали в течение 1 ч при 50oC, а затем сливали на лед и раствор хлорида аммония. Образовавшийся 4-бензо[1,3]диоксол-5-ил-1-бензилпиперидин-4-ол после экстрагирования уксусным эфиром кристаллизовался при концентрировании раствора. Таким путем получили 10,85 г (58% от теории) белых кристаллов; tпл 144oC.
(б) Аналогично примеру 2(д) путем каталитического гидрирования при нормальном давлении в течение 4 ч из 4-бензо[1,3]диоксол-5-ил-1-бензилпиперидин-4-ола получили 4-бензо[1,3]диоксол-5-илпиперидин-4-ол в виде бесцветного твердого вещества с количественным выходом; МС: 221 (M)+.
(в) Аналогично примеру 1(б) путем элиминирования из 4-бензо[1,3]диоксол-5-илпиперидин-4-ола получили 4-бензо[1,3] диоксол-5-ил-1,2,3,6-тетрагидропиридин в виде окрашенного в бежевый цвет твердого вещества; МС: 203 (M)+.
(г) Аналогично примеру 1(е) путем введения BOC-группы из 4-бензо[1, 3]диоксол-5-ил-1,2,3,6-тетрагидропиридина получили трет-бутиловый эфир 4-бензо[1,3] диоксол-5-ил-3,6-дигидро-2H-пиридин-1-карбоновой кислоты в виде бесцветного масла; МС: 304 (M+H)+.
(д) Аналогично примеру 1(в) путем гидроборирования трет-бутилового эфира 4-бензо[1,3]диоксол-5-ил-3,6-дигидро-2H- пиридин-1-карбоновой кислоты получили (3RS,4RS)-4-бензо[1, 3]диоксол-5-ил-3-гидроксипиперидин-1-карбоновой кислоты в виде белых кристаллов; tпл 112oC.
(е) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS, 4RS)-4-бензо[1,3]диоксол-5-ил-3-гидроксипиперидин-1-карбоновой кислоты 2-бромнафталином получили после кристаллизации из гексана трет-бутиловый эфир (3RS,4RS)-4-бензо[1, 3]диоксол-5-ил-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты в виде белых кристаллов; tпл 128-129oC.
(ж) Раствор 190 мг (0,41 ммоля) трет-бутилового эфира (3RS,4RS)-4-бензо[1,3] диоксол-5-ил-3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты в смеси из 5 мл метанола и 25%-ной водной соляной кислоты нагревали с обратным холодильником в течение 1 ч. Затем растворитель отгоняли при пониженном давлении. После перекристаллизации остатка из смеси метанола с простым эфиром получили 130 мг (73% от теории) гидрохлорида (3RS,4RS)-4-(1, 3-бензодиоксол-5-ил)-3-нафталин-2-илметоксипиперидина в виде белого порошка; МС: 362 (M+H)+.
Пример 9.
Аналогично примеру 8(ж) путем отщепления BOC-группы с помощью кислоты получали следующие соединения:
1) из трет-бутилового эфира (3RS,4RS)-4-фенил-3-(2-{[(пиридин-3- карбонил)амино] метил} бензилокси)пиперидин-1-карбоновой кислоты получили гидрохлорид (3RS,4RS)-2-(4-фенилпиперидин-3- илоксиметил)бензиламида пиридин-3-карбоновой кислоты в виде окрашенного в бежевый цвет порошка; МС: 402 (M+H)+;
2) из трет-бутилового эфира (3RS,4RS)-4-бензо[1,3]диоксол-5-ил- 3-(2-карбамоилбензилокси)пиперидин-1-карбоновой кислоты получили гидрохлорид (3RS, 4RS)-2-(4-бензо[1,3] диоксол-5-илпиперидин-3- илоксиметил)бензоамида в виде белого порошка; МС: 355 (M+H)+.
Использованные в качестве исходных веществ BOC-производные получали следующим путем.
(а) Аналогично примеру 1(ж) алкилированием трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-фенилпиперидин-1-карбоновой кислоты [пример 2(а)] 2-бромметилбензонитрилом получили трет-бутиловый эфир (3RS,4RS)-3-(2-цианбензилокси)-4-фенилпиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 393 (M+H)+.
(б) Аналогично способу, описанному у H.C. Brown и др. в Synthesis 1981, 605, с использованием 0,3 мл боран-диметилсульфидного комплекса восстанавливали 528 мг (1,35 ммоля) трет-бутилового эфира (3RS, 4RS)-3-(2-цианбензилокси)-4-фенилпиперидин-1-карбоновой кислоты. Таким путем получили 480 мг (90% от теории) трет-бутилового эфира (3RS,4RS)-3-(2-аминометилбензилокси)-4-фенилпиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 397 (M+H)+.
(в) Раствор 150 мг (0,38 ммоля) трет-бутилового эфира (3RS, 4RS)-3-(2-аминометилбензилокси)-4-фенилпиперидин-1-карбоновой кислоты в 2 мл метиленхлорида смешивали с 229 мг (2,26 ммоля) триэтиламина, 139 мг ((1,05 ммоля) никотиновой кислоты, 216 мг (1,13 ммоля) ЭДК и 10 мг (0,08 ммоля) 4-диметиламинопиридина и перемешивали в течение 24 ч при комнатной температуре. Затем реакционный раствор разбавляли метиленхлоридом и промывали насыщенным раствором гидрокарбоната натрия. Органическую фазу отделяли, сушили над сульфатом натрия и упаривали при пониженном давлении. Остаток хроматографировали на силикагеле с использованием уксусного эфира в качестве элюента. Таким путем получили 100 мг (53% от теории) трет-бутилового эфира (3RS,4RS)-4-фенил-3-(2-{[(пиридин-3- карбонил)амино]метил}бензилокси)пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 502 (M+H)+.
(г) Аналогично примеру 1(ж) алкилированием трет-бутилового эфира (3RS, 4RS)-4-бензо[1,3] диоксол-5-ил-3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты [пример 8(е)] 2-бромметилбензонитрилом получили трет-бутиловый эфир (3RS, 4RS)-4-бензо[1, 3]диоксол-5-ил-3-(2- цианбензилокси)пиперидин-1-карбоновой кислоты в виде бесцветных кристаллов; МС: 455 (M+H)+.
(д) К раствору 236 мг (0,54 ммоля) трет-бутилового эфира (3RS,4RS)-4-бензо[1,3]диоксол-5-ил-3-(2-цианбензилокси)пиперидин-1- карбоновой кислоты в 5 мл метанола добавляли 0,5 мл перекиси водорода (33%-ной) и 0,2 мл 2 н. едкого натра. Реакционный раствор нагревали с обратным холодильником в течение 2 ч. Затем снова в тех же количествах добавляли перекись водорода и едкий натр и перемешивание раствора продолжали в течение 2 ч. После этого раствор охлаждали и упаривали при пониженном давлении. Остаток очищали хроматографией на силикагеле с использованием смеси 9:1 метиленхлорида и простого эфира в качестве элюента. Таким путем получили 140 мг (57% от теории) трет-бутилового эфира (3RS, 4RS)-4-бензо[1,3]диоксол-5-ил-3-(2- карбамоилбензилокси)пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 455 (M)+.
Пример 10.
(а) Аналогично примеру 1(ж) алкилированием трет-бутилового эфира (3RS, 4RS)-4-(4-фторфенил)-3-гидроксипиперидин-1-карбоновой кислоты 6-хлорметил-2, 3-дигидробензо[1,4] диоксином [британский патент 566732 (1943)] получили трет-бутиловый эфир (3RS, 4RS)-3-(2,3-дигидробензо[1,4] диоксин-6-илметокси)-4-(4- фторфенил)пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 444 (M+H)+.
(б) Раствор 280 мг (0,63 ммоля) трет-бутилового эфира (3RS,4RS)-3-(2,3-дигидробензо[1,4] диоксин-6-илметокси)-4-(4- фторфенил)пиперидин-1-карбоновой кислоты в 5 мл безводного метиленхлорида смешивали с 808 мг (1,89 ммоля) безводного бромида цинка и смесь перемешивали в течение 5 ч при комнатной температуре. Затем растворитель отгоняли при пониженном давлении, остаток растворяли в 10 мл метанола, смешивали с 2 мл 2 н. едкого натра и отделяли твердое вещество. Фильтрат упаривали при пониженном давлении и остаток распределяли между метиленхлоридом и водой. Органическую фазу отделяли и упаривали при пониженном давлении. Таким путем получили 220 мг (98% от теории) (3RS, 4RS)-3-(2, 3-дигидробензо[1,4] диоксин-6-илметокси)-4-(4- фторфенил)пиперидина
в виде твердого вещества желтоватого цвета; МС: 344 (M+H)+.
Пример 11.
Аналогично примеру 10(б) из трет-бутилового эфира (3RS,4RS)-3-(бензо[b] фуран-5-илметокси)-4-(4-фторфенил)пиперидин-1- карбоновой кислоты получили (3RS, 4RS)-3-(бензо[b]фуран-5-илметокси)-4-(4-фторфенил)пиперидин в виде бесцветного твердого вещества; МС: 326 (M+1)+.
Использованный в качестве исходного соединения трет-бутиловый эфир (3RS, 4RS)-3-(бензо[b] фуран-5-илметокси)-4-(4-фторфенил)пиперидин-1- карбоновой кислоты получили аналогично способу, описанному в примере 1(ж), путем алкилирования трет-бутилового эфира (3RS,4RS)-4-(4-фторфенил)-3-гидроксипиперидин-1-карбоновой кислоты 5-бромметилбензо[b] фураном в виде бесцветного твердого вещества; МС: 426 (M+H)+.
Использованный в качестве алкилирующего агента 5-бромметилбензо[b]фуран получали следующим путем.
Аналогично описанному в литературе способу получения 5-бромметилбензо[b] тиофена из 5-метилбензо[b] тиофена [J. Med. Chem. 34(1), 65 (1991)] путем бромирования 5-метилбензо[b] фурана [Synth. Commun. 19, 257 (1989)] N-бромсукцинимидом в четыреххлористом углероде получили 5-бромметилбензо[b]фуран в виде светло-желтого твердого вещества; МС: 210, 212 (M)+.
Пример 12.
(а) Аналогично примеру 1(в) путем гидроборирования с помощью борана в тетрагидрофуране из 4-(4-хлорфенил)-1-метил-1,2,3,6-тетрагидропиридина [патент США 3320265] получили (3RS,4RS)-4-(4-хлорфенил)-1-метилпиперидин-3-ол, который после перекристаллизации из смеси метиленхлорида с гексаном представлял собой бесцветные кристаллы с tпл 99-100oC.
(б) К суспензии 0,264 г (5 ммолей) гидрида натрия (50%-ная дисперсия в вазелиновом масле) в 8 мл тетрагидрофурана по каплям добавляли раствор из 1,12 г (5 ммолей) (3RS,4RS)-4-(4-хлорфенил)-1-метилпиперидин-3-ола в 5 мл тетрагидрофурана и перемешивали в течение 60 мин при 50oC. Затем реакционную смесь охлаждали до комнатной температуры и смешивали с 1,10 г (5 ммолей) 2-бромметилнафталина в 5 мл тетрагидрофурана. После выдержки в течение 2 ч при 50oC реакционный раствор сливали на 60 мл ледяной воды и трижды экстрагировали уксусным эфиром порциями по 25 мл. Органическую фазу промывали насыщенным раствором поваренной соли, сушили над сульфатом магния, фильтровали и упаривали. Остаток хроматографировали на силикагеле с использованием смеси 95: 5 метиленхлорида и метанола в качестве элюента. Таким путем получили 0,53 г (28% от теории) (3RS, 4RS)-4-(4-хлорфенил)-1-метил-3-(нафталин-2-илметокси)пиперидина в виде светло-желтого масла; МС: 366 (M)+.
(в) Раствор 0,526 г (1,43 ммоля) (3RS, 4RS)-4-(4-хлорфенил)-1-метил-3-(нафталин-2-илметокси)пиперидина в 12 мл толуола смешивали с 100 мг карбоната калия и нагревали до 100oC. Затем к этой смеси добавляли 0,423 г (0,288 мл, 2 ммоля) 2,2,2-трихлорэтилового эфира хлормуравьиной кислоты и перемешивали в течение 12 ч при 100oC. Реакционный раствор упаривали, растворяли в 50 мл уксусного эфира и промывали 20 мл воды и 20 мл насыщенного раствора гидрокарбоната натрия. После сушки над сульфатом магния, фильтрования и упаривания получили бесцветное масло, которое хроматографировали на силикагеле с использованием смеси 3:2 гексана и уксусного эфира в качестве элюента. Таким путем получили 0,426 г (57% от теории) 2,2,2-трихлорэтилового эфира 4-(4-хлорфенил)-3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; Rf 0,31 (силикагель, гексан/уксусный эфир в соотношении 3:2).
(г) Суспензию 0,420 г (0,8 ммоля) 2,2,2-трихлорэтилового эфира 4-(4-хлорфенил)-3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты и 300 мг цинка в 10 мл уксусной кислоты перемешивали в течение 12 ч при комнатной температуре. Реакционный раствор разбавляли 40 мл воды и четырежды экстрагировали 30 мл метиленхлорида. Органическую фазу дважды промывали 1 н. едким натром порциями по 40 мл, сушили над сульфатом натрия, фильтровали и упаривали. Остаток хроматографировали на силикагеле с использованием смеси 9:1 метиленхлорида и метанола в качестве элюента. Таким путем получили 0,210 г (74% от теории) (3RS, 4RS)-4-(4-хлорфенил)-3-(нафталин-2-илметокси)пиперидина [МС: 210 (M-C11H9)+], который с помощью раствора хлористого водорода в метаноле переводили в гидрохлорид с tпл 159-161oC (разложение).
Пример 13.
Аналогично примеру 12(б)-(г) путем алкилирования и последующего отщепления N-метильной группы получали следующие соединения:
1) из (3RS,4RS)-4-(4-хлорфенил)-1-метилпиперидин-3-ола и 1-бромметилнафталина получили (3RS,4RS)-4-(4-хлорфенил)-3-(нафталин-1-илметокси)пиперидин [МС: 210 (M-C11H9)+], который с помощью раствора хлористого водорода в этаноле переводили в гидрохлорид с tпл 210-213oC (разложение);
2) из (3RS,4RS)-4-(4-хлорфенил)-1-метилпиперидин-3-ола и 1-бромметил-4-трет-бутилбензола получили (3RS, 4RS)-4-(4-трет-бутилбензилокси)-4-(4-хлорфенил)пиперидин [МС: 358 (M)+], который с помощью раствора хлористого водорода в этаноле переводили в гидрохлорид с tпл 164-166oC (разложение);
3) из (3RS, 4RS)-4-(4-хлорфенил)-1-метилпиперидин-3-ола и 5-хлорметилбензо[1,3] диоксола получили (3RS,4RS)-3-(бензо[1,3]диоксол-5-илметокси-4-(4-хлорфенил)пиперидин [МС: 210 (M-C8H7O2)+], который с помощью метансульфокислоты в смеси диоксана и воды и последующей лиофилизацией переводили в соответствующий метансульфонат, Rf 0,45 (силикагель, метиленхлорид/метанол в соотношении 9:1);
4) из (3RS,4RS)-4-(4-хлорфенил)-1-метилпиперидин-3-ола и 1,2-дихлор-4-хлорметилбензола получили (3RS,4RS)-4-(4-хлорфенил)-3-(3,4-дихлорбензилокси)пиперидин [МС: 370 (M)+], который с помощью раствора хлористого водорода в этаноле переводили в гидрохлорид с tпл 156-158oC (разложение);
5) из (3RS, 4RS)-4-(4-хлорфенил)-1-метилпиперидин-3-ола и 2,4-дихлор-4-хлорметилбензола получили (3RS,4RS)-4-(4-хлорфенил)-3-(2,4-дихлорбензилокси)пиперидин с tпл 83-84oC; МС: 370 (M)+;
6) из (3RS,4RS)-4-(4-хлорфенил)-1-метилпиперидин-3-ола и 1-хлор-4-хлорметилбензола получили (3RS,4RS)-3-(4-хлорбензилокси)-4-(4-хлорфенил)пиперидин [МС: 210 (M-C7 H6Cl)+], который с помощью раствора хлористого водорода в этаноле переводили в гидрохлорид с tпл 128-130oC (разложение);
7) из (3RS, 4RS)-4-(4-хлорфенил)-1-метилпиперидин-3-ола и 1-хлор-4-хлорметил-3-метоксибензола получили (3RS, 4RS)-4-(4-хлорфенил)-3-(2-метоксибензилокси)пиперидин [МС: 332 (M)+] , который с помощью раствора хлористого водорода в этаноле переводили в гидрохлорид с tпл 116-118oC (разложение);
8) из (3RS,4RS)-4-(4-хлорфенил)-1-метилпиперидин-3-ола и 1-хлор-2-хлорметилбензола получили (3RS,4RS)-3-(2-хлорбензилокси)-4-(4-хлорфенил)пиперидин [МС: 210 (M-C7H6Cl)+], который с помощью раствора хлористого водорода в этаноле переводили в гидрохлорид с tпл 145-147oC (разложение);
9) из (3RS,4RS)-4-(4-хлорфенил)-1-метилпиперидин-3-ола и 4-хлорметилбифенила получили (3RS, 4RS)-3-(бифенил-4-илметокси)-4-(4-хлорфенил)пиперидин [МС: 210 (M-C13H11)+], который с помощью раствора хлористого водорода в этаноле переводили в гидрохлорид с tпл 177-178oC (разложение);
10) из (3RS,4RS)-4-(4-хлорфенил)-1-метилпиперидин-3-ола и 2-хлорметилхинолина получили (3RS, 4RS)-2-[4-(4-хлорфенил)пиперидин-3-илоксиметил]хинолин [МС: 353 (M)+] с tпл 109-110oC (разложение);
11) из (3RS, 4RS)-4-(4-хлорфенил)-1-метилпиперидин-3-ола и 2-хлорметилбензофурана [J. Am. Chem. Soc. 73, 4400 (1951)] получили (3RS,4RS)-3-(бензофуран-2-илметокси)-4-(4-хлорфенил)пиперидин [МС: 341 (M)+ ], который с помощью раствора хлористого водорода в этаноле переводили в гидрохлорид с tпл 144-146oC (разложение);
12) из (3RS, 4RS)-4-(4-хлорфенил)-1-метилпиперидин-3-ола и 2-хлорметилбензо[b] тиофена [J. Am. Chem. Soc. 71, 2856 (1949)] получили (3RS,4RS)-3-(бензо[b] тиофен-2-илметокси)-4-(4-хлорфенил)пиперидин [МС: 210 (M-C8H7S)+], который с помощью раствора хлористого водорода в этаноле переводили в гидрохлорид с tпл 141-144oC (разложение);
13) из (3RS, 4RS)-4-(4-хлорфенил)-1-метилпиперидин-3-ола и метилового эфира 4'-бромметилбифенил-2-карбоновой кислоты [J. Med. Chem. 34, 2525 (1991)] получили метиловый эфир (3RS, 4RS)-4'-[4-(4- хлорфенил)пиперидин-3-илоксиметил] бифенил-2-карбоновой кислоты [МС: 436 (M)+], который с помощью соляной кислоты в этаноле переводили в гидрохлорид с tпл 95-99oC (разложение);
14) из (3RS,4RS)-4-(4-хлорфенил)-1-метилпиперидин-3-ола и 3-хлорметилпиридина [J. Am. Chem. Soc. 77, 1054 (1955)] получили (3RS, 4RS)-3-[4-(4-хлорфенил)пиперидин-3-илоксиметил] пиридин [МС: 303 (M)+], который с помощью раствора хлористого водорода в этаноле переводили в дигидрохлорид с tпл 78-81o C (разложение);
15) из (3RS,4RS)-4-(4-хлорфенил)-1-метилпиперидин-3-ола и 6-хлорметил-1,1,4,4-тетраметил-1,2,3,4-тетрагидронафталина получили (3RS, 4RS)-4-(4-хлорфенил)-3-(5,5,8, 8-тетраметил-5,6,7,8- тетрагидронафталин-2-илметокси)пиперидин [МС: 412 (M)+], который с помощью раствора хлористого водорода в этаноле переводили в гидрохлорид с tпл 118-121oC (разложение);
16) из (3RS, 4RS)-4-(3-хлорфенил)-1-метилпиперидин-3-ола [патент США 4132710 (1976)] и 4-метоксибензилхлорида получили (3RS, 4RS)-3-(4-метоксибензилокси)-4-(3-хлорфенил)пиперидин, МС: 332 (M)+.
Пример 14.
Аналогично способу, описанному в примере 1(д), путем отщепления 2-триметилсилилэтоксикарбонильной группы с помощью тетрабутиламмонийфторида в тетрагидрофуране получали следующие соединения:
1) из β- триметилсилилэтилового эфира (3RS, 4RS)-4-(4-фторфенил)-3-(4-метоксинафталин-2-илметокси)пиперидин-1- карбоновой кислоты получили (3RS, 4RS)-4-(4-фторфенил)-3-(4-метоксинафталин-2-илметокси)пиперидин в виде бесцветного твердого вещества; МС: 365 (M)+;
2) из β- триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)-3-(5-метоксинафталин-2-илметокси)пиперидин- 1-карбоновой кислоты получили (3RS, 4RS)-4-(4-фторфенил)-3-(5-метоксинафталин-2-илметокси)пиперидин в виде бесцветного твердого вещества; МС: 365 (M)+;
3) из β- триметилсилилэтилового эфира (3RS, 4RS)-4-(4-фторфенил)-3-(6-метоксинафталин-2-илметокси)пиперидин- 1-карбоновой кислоты получили (3RS, 4RS)-4-(4-фторфенил)-3-(6-метоксинафталин-2-илметокси)пиперидин в виде бесцветного твердого вещества; МС: 365 (M)+;
4) из β- триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)-3-(7-метоксинафталин-2-илметокси)пиперидин- 1-карбоновой кислоты получили (3RS, 4RS)-4-(4-фторфенил)-3-(7-метоксинафталин-2-илметокси)пиперидин в виде бесцветного твердого вещества; МС: 365 (M)+;
5) из β- триметилсилилэтилового эфира (3RS, 4RS)-4-(4-фторфенил)-3-(8-метоксинафталин-2-илметокси)пиперидин- 1-карбоновой кислоты получили (3RS, 4RS)-4-(4-фторфенил)-3-(8-метоксинафталин-2-илметокси)пиперидин в виде бесцветной смолы; МС: 366 (M)+;
6) из β- триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)-3-[4-(пиридин-2-илметокси)нафталин-2- илметокси] пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-(4-фторфенил)-3-[4-(пиридин-2-илметокси)нафталин-2- илметокси]пиперидин в виде бесцветного твердого вещества; МС: 442 (M)+;
7) из β- триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)-3-[4-(пиридин-3-илметокси)нафталин-2- илметокси] пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-(4-фторфенил)-3-[4-(пиридин-3-илметокси)нафталин-2- илметокси]пиперидин в виде бесцветного твердого вещества; МС: 443 (M+H)+;
8) из β- триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)-3-[4-(пиридин-4-илметокси)нафталин-2- илметокси] пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-(4-фторфенил)-3-[4-(пиридин-4-илметокси)нафталин-2- илметокси]пиперидин в виде бесцветного твердого вещества; МС: 442 (M)+;
9) из β- триметилсилилэтилового эфира (3RS,4RS)-3-(4-аллилоксинафталин-2-илметокси)-4-(4-фторфенил)пиперидин- 1-карбоновой кислоты получили (3RS, 4RS)-3-(4-аллилоксинафталин-2-илметокси)-4-(4-фторфенил)пиперидин в виде бесцветного твердого вещества; МС: 391 (M)+;
10) из β- триметилсилилэтилового эфира (3RS,4RS)-3-(6-аллилоксинафталин-2-илметокси)-4-(4-фторфенил)пиперидин- 1-карбоновой кислоты получили (3RS, 4RS)-3-(6-аллилоксинафталин-2-илметокси)-4-(4- фторфенил)пиперидин в виде бесцветного твердого вещества; МС: 391 (M)+;
11) из β - триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)-3-(4-изобутоксинафталин-2-илметокси)пиперидин- 1-карбоновой кислоты получили (3RS, 4RS)-4-(4-фторфенил)-3-(4- изобутилоксинафталин-2-илметокси)пиперидин в виде бесцветного твердого вещества; МС: 407 (M)+;
12) из β- триметилсилилэтилового эфира (3RS, 4RS)-3-(1-бензилоксинафталин-2-илметокси)-4-(4-фторфенил)пиперидин- 1-карбоновой кислоты получили (3RS, 4RS)-3-(1-бензилоксинафталин-2- илметокси)-4-(4-фторфенил)пиперидин в виде светло-желтого масла; МС: 441 (M)+;
13) из β- триметилсилилэтилового эфира (3RS,4RS)-3-(4-бензилоксинафталин-2-илметокси)-4-(4-фторфенил)пиперидин- 1-карбоновой кислоты получили (3RS, 4RS)-3-(4-бензилоксинафталин-2- илметокси)-4-(4-фторфенил)пиперидин в виде бесцветного твердого вещества; МС: 441 (M)+;
14) из β- триметилсилилэтилового эфира (3RS, 4RS)-3-(5-бензилоксинафталин-2-илметокси)-4-(4-фторфенил)пиперидин- 1-карбоновой кислоты получили (3RS, 4RS)-3-(5-бензилоксинафталин-2- илметокси)-4-(4-фторфенил)пиперидин в виде светло-желтого масла; МС: 442 (M+H)+;
15) из β- триметилсилилэтилового эфира (3RS,4RS)-3-(7-бензилоксинафталин-2-илметокси)-4-(4-фторфенил)пиперидин- 1-карбоновой кислоты получили (3RS, 4RS)-3-(7-бензилоксинафталин-2- илметокси)-4-(4-фторфенил)пиперидин в виде бесцветного твердого вещества; МС: 441 (M)+;
16) из β- триметилсилилэтилового эфира (3RS, 4RS)-3-(8-бензилоксинафталин-2-илметокси)-4-(4-фторфенил)пиперидин- 1-карбоновой кислоты получили (3RS, 4RS)-3-(8-бензилоксинафталин-2- илметокси)-4-(4-фторфенил)пиперидин в виде светло-желтой смолы; МС: 442 (M+H)+;
17) из β- триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)-3-[4-(2-метоксиэтокси)нафталин-2- илметокси] пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-(4-фторфенил)-3-[4-(2-метоксиэтокси)нафталин-2- илметокси]пиперидин в виде бесцветного твердого вещества; МС: 410 (M+H)+;
18) из β - триметилсилилэтилового эфира 4-(4-фторфенил)-3-[4-(3-метоксипропокси)нафталин-2- илметокси] пиперидин-1-карбоновой кислоты получили 4-(4-фторфенил)-3-[4-(3-метоксипропокси)нафталин-2- илметокси] пиперидин в виде светло-желтого твердого вещества; МС: 424 (M+H)+;
19) из β- триметилсилилэтилового эфира (3RS, 4RS)-3-(4-бутоксинафталин-2-илметокси)-4-(4-фторфенил)пиперидин- 1-карбоновой кислоты получили (3RS, 4RS)-3-(4-бутоксинафталин-2-илметокси)-4-(4-фторфенил)пиперидин в ввде бесцветного твердого вещества; МС: 408 (M+H)+;
20) из β- триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)-3-[4-(2-метоксибензилокси)нафталин-2- илметокси] пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-(4-фторфенил)-3-[4-(2-метоксибензилокси)нафталин-2- илметокси]пиперидин в виде бесцветной смолы; МС: 472 (M+H)+;
21) из β - триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)-3-[4-(3-метоксибензилокси)нафталин-2- илметокси] пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-(4-фторфенил)-3-[4-(3-метоксибензилокси)нафталин-2- илметокси]пиперидин в виде бесцветного твердого вещества; МС: 471 (M)+;
22) из β-триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)-3-[4-(4-метоксибензилокси)нафталин-2- илметокси] пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-(4-фторфенил)-3-[4-(4-метоксибензилокси)нафталин-2- илметокси]пиперидин в виде бесцветного масла; МС: 471 (M)+;
23) из β- триметилсилилэтилового эфира (3RS, 4RS)-4-(4-фторфенил)-3-(1-фенэтилоксинафталин-2- илметокси)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-(4-фторфенил)-3-(1-фенэтилоксинафталин-2- илметокси)пиперидин в виде светло-желтого масла; МС: 456 (M+H)+;
24) из β- триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)-3-(4-фенэтилоксинафталин-2- илметокси)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-(4-фторфенил)-3-(4-фенэтилоксинафталин-2- илметокси)пиперидин в виде светло-желтого масла; МС: 456 (M+H)+;
25) из β- триметилсилилэтилового эфира (3RS, 4RS)-3-[4-(2-[1,3]диоксолан-2-илэтокси)нафталин-2-илметокси] - 4-(4-фторфенил)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-3-[4-(2-[1,3]диоксолан-2-илэтокси)нафталин-2-илметокси] - 4-(4-фторфенил)пиперидин в виде светло-желтого масла; МС: 451 (M)+;
26) из β- триметилсилилэтилового эфира (3RS,4RS)-3-[1-(2-[1, 3]диоксолан-2-илэтокси)нафталин-2-илметокси] - 4-(4-фторфенил)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-3-[1-(2-[1,3]диоксолан-2-илэтокси)нафталин-2-илметокси] - 4-(4-фторфенил)пиперидин в виде светло-желтого масла; МС: 452 (M+H)+;
27) из β- триметилсилилэтилового эфира (3RS,4RS)-3-[4-(бензо[1,3]диоксол-5-илэтокси)нафталин-2-илметокси] - 4-(4-фторфенил)пиперидин-1-карбоновой кислоты получили (3RS,4RS)-3-[4-(бензо[1,3]диоксол-5-илэтокси)нафталин-2-илметокси]- 4-(4-фторфенил)пиперидин в виде бесцветной смолы; МС: 485 (M)+;
28) из β- триметилсилилэтилового эфира (3RS,4RS)-3-[4-(2-циклопропилэтокси)нафталин-2-илметокси] -4-(4- фторфенил)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-3-[4-(2-циклопропилэтокси)нафталин-2-илметокси] -4-(4- фторфенил)пиперидин в виде бесцветного твердого вещества; МС: 419 (M)+;
29) из β- триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)-3-[4-(2-гидроксиэтокси)нафталин-2- илметокси] пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-(4-фторфенил)-3-[4-(2-гидроксиэтокси)нафталин-2- илметокси]пиперидин в виде бесцветного твердого вещества; МС: 395 (M)+.
Использованные в качестве исходных веществ соединения получали следующим путем.
(а) 99 мг (0,20 ммоля) β- триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)-3-(4-гидроксинафталин-2-илметокси)пиперидин- 1-карбоновой кислоты растворяли в 1 мл диметилформамида, смешивали с 69 мг (0,50 ммоля) безводного карбоната калия и 19 мкл (43 мг, 0,30 ммоля) метилиодида и перемешивали в течение 4 ч при комнатной температуре. После этого смесь распределяли между метиленхлоридом и водой, органическую фазу сушили над сульфатом магния и в завершение удаляли растворитель при пониженном давлении. Сырой продукт очищали хроматографией на силикагеле с использованием смеси 4:1 гексана и метиленхлорида в качестве элюента. Таким путем получили 85 мг (83% от теории) β- триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)-3-(4- метоксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде светло-желтого масла; МС: 509 (M)+.
Аналогично описанному выше способу получали следующие соединения:
- из β- триметилсилилэтилового эфира (3RS, 4RS)-4-(4-фторфенил)-3-(5-гидроксинафталин-2-илметокси)пиперидин- 1-карбоновой кислоты и метилиодида получили β- триметилсилилэтиловый эфир (3RS, 4RS)-4-(4-фторфенил)-3-(5-метоксинафталин-2-илметокси)пиперидин- 1-карбоновой кислоты, который без очистки использовали на следующей стадии;
- из β- триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)-3-(6- гидроксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты и метилиодида получили β- триметилсилилэтиловый эфир (3RS, 4RS)-4-(4-фторфенил)-3-(6-метоксинафталин-2-илметокси)пиперидин-1- карбоновой кислоты в виде светло-желтого масла; МС: 509 (M)+;
- из β- триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)-3-(7-гидроксинафталин-2-илметокси)пиперидин- 1-карбоновой кислоты и метилиодида получили β- триметилсилилэтиловый эфир (3RS, 4RS)-4-(4-фторфенил)-3-(7-метоксинафталин-2- илметокси)пиперидин-1-карбоновой кислоты, который без очистки использовали на следующей стадии;
- из β- триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)- 3-(8-гидроксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты и метилиодида получили β- триметилсилилэтиловый эфир (3RS, 4RS)-4-(4-фторфенил)-3-(8-метоксинафталин-2-илметокси)пиперидин- 1-карбоновой кислоты, который без очистки использовали на следующей стадии;
- из β- триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)- 3-(4-гидроксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты и 2-пиридилметилхлорида получили β- триметилсилилэтиловый эфир (3RS, 4RS)-4-(4-фторфенил)-3-[4-(пиридин-2-илметокси)нафталин-2- илметокси]пиперидин-1-карбоновой кислоты в виде светло-желтого масла; МС: 587 (M)+;
- из β - триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)-3-(4-гидроксинафталин-2-илметокси)пиперидин- 1-карбоновой кислоты и 3-пиридилметилхлорида получили β- триметилсилилэтиловый эфир (3RS, 4RS)-4-(4-фторфенил)-3-[4-(пиридин-3- илметокси)нафталин-2-илметокси]пиперидин-1-карбоновой кислоты, который без очистки использовали на следующей стадии;
- из β - триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)-3-(4-гидроксинафталин-2-илметокси)пиперидин- 1-карбоновой кислоты и 4-пиридилметилхлорида получили β- триметилсилилэтиловый эфир (3RS, 4RS)-4-(4-фторфенил)-3-[4-(пиридин-4-илметокси)нафталин-2- илметокси]пиперидин-1-карбоновой кислоты в виде светло-желтого масла; МС: 587 (M)+;
- из β - триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)- 3-(4-гидроксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты и аллилбромида получили β- триметилсилилэтиловый эфир (3RS, 4RS)-3-(4-аллилоксинафталин-2-илметокси)-4-(4-фторфенил)пиперидин- 1-карбоновой кислоты, который без очистки использовали на следующей стадии;
- из β- триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)-3-(6-гидроксинафталин-2-илметокси)пиперидин- 1-карбоновой кислоты и аллилбромида получили β- триметилсилилэтиловый эфир (3RS, 4RS)-3-(6-аллилоксинафталин-2- илметокси)-4-(4-фторфенил)пиперидин-1-карбоновой кислоты, который без очистки использовали на следующей стадии;
- из β- триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)- 3-(4-гидроксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты и изобутилбромида получили β- триметилсилилэтиловый эфир (3RS, 4RS)-4-(4-фторфенил)-3-(4-изобутоксинафталин-2- илметокси)пиперидин-1-карбоновой кислоты, который без очистки использовали на следующей стадии;
- из β- триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)- 3-(1-гидроксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты и бензилбромида получили β- триметилсилилэтиловый эфир (3RS, 4RS)-4-(4-фторфенил)-3-(1-бензилоксинафталин-2- илметокси)пиперидин-1-карбоновой кислоты, который без очистки использовали на следующей стадии;
- из β- триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)- 3-(4-гидроксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты и бензилбромида получили
- из β- триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)-3-(7-гидроксинафталин-2-илметокси)пиперидин- 1-карбоновой кислоты и бензилбромида получили β - триметилсилилэтиловый эфир (3RS,4RS)-3-(7-бензилоксинафталин-2- илметокси)-4-(4-фторфенил)пиперидин-1-карбоновой кислоты в виде светло-желтого масла; МС: 585 (M)+;
- из β- триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)-3-(5-гидроксинафталин-2-илметокси)пиперидин- 1-карбоновой кислоты и бензилбромида получили β- триметилсилилэтиловый эфир (3RS, 4RS)-3-(5-бензилоксинафталин-2- илметокси)-4-(4-фторфенил)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 586 (M)+;
- из β- триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)- 3-(8-гидроксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты и бензилбромида получили β- триметилсилилэтиловый эфир (3RS, 4RS)-3-(8-бензилоксинафталин-2-илметокси)-4-(4-фторфенил)пиперидин- 1-карбоновой кислоты, который без очистки использовали на следующей стадии;
- из β- триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)- 3-(4-гидроксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты и 2-метоксиэтилбромида получили β- триметилсиланилэтиловый эфир (3RS, 4RS)-4-(4-фторфенил)-3-[4-(2-метоксиэтокси)нафталин-2- илметокси] пиперидин-1-карбоновой кислоты, который без очистки использовали на следующей стадии;
- из β - триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)- 3-(4-гидроксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты и 3-метоксипропилхлорида [J. Org. Chem. 16, 704 (1951)] получили 2-триметилсиланилэтиловый эфир (3RS,4RS)-4-(4-фторфенил)-3-[4-(3- метоксипропокси)нафталин-2-илметокси] пиперидин-1-карбоновой кислоты, который без очистки использовали на следующей стадии;
- из β- триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)- 3-(4-гидроксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты и бутилбромида получили 2-триметилсиланилэтиловый эфир (3RS,4RS)-3-(4-бутилнафталин-2-илметокси)-4-(4-фторфенил)пиперидин-1- карбоновой кислоты, который без очистки использовали на следующей стадии;
- из β - триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)- 3-(4-гидроксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты и 2-метоксибензилхлорида получили 2-триметилсиланилэтиловый эфир (3RS, 4RS)-4-(4-фторфенил)-3-[4-(2-метоксибензилокси)нафталин-2- илметокси]пиперидин-1-карбоновой кислоты, который без очистки использовали на следующей стадии;
- из β - триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)- 3-(4-гидроксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты и 3-метоксибензилхлорида получили 2-триметилсиланилэтиловый эфир (3RS, 4RS)-4-(4-фторфенил)-3-[4-(3-метоксибензилокси)нафталин-2- илметокси]пиперидин-1-карбоновой кислоты в виде светло-желтого масла; МС: 615 (M)+;
- из β - триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)- 3-(4-гидроксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты и 4-метоксибензилхлорида получили 2-триметилсиланилэтиловый эфир (3RS, 4RS)-4-(4-фторфенил)-3-[4-(4-метоксибензилокси)нафталин-2- илметокси]пиперидин-1-карбоновой кислоты в виде светло-желтого масла; МС: 616 (M+H)+;
- из β - триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)- 3-(4-гидроксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты и фенэтилбромида получили β- триметилсилилэтиловый эфир (3RS, 4RS)-4-(4-фторфенил)-3-(4-фенэтилоксинафталин-2- илметокси)пиперидин-1-карбоновой кислоты, который без очистки использовали на следующей стадии;
- из β- триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)- 3-(1-гидроксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты и фенэтилбромида получили 2-триметилсиланилэтиловый эфир
(3RS, 4RS)-4-(4-фторфенил)-3-(1- фенэтилоксинафталин-2- илметокси)пиперидин-1-карбоновой кислоты в виде светло-желтого масла; МС: 600 (M+H)+;
- из β - триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)- 3-(4-гидроксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты и 2-(2-бромэтил)-1,3-диоксолана получили 2-триметилсиланилэтиловый эфир (3RS, 4RS)-3-[4-(2-[1,3] диоксолан-2-илэтокси)нафталин-2-илметокси] - 4-(4-фторфенил)пиперидин-1-карбоновой кислоты, который без очистки использовали на следующей стадии;
- из β - триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)- 3-(1-гидроксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты и 2-(2-бромэтил)-1,3-диоксолана получили β- триметилсилилэтиловый эфир (3RS,4RS)-3-[1-(2-[1,3]диоксолан-2-илэтокси)нафталин-2-илметокси]- 4-(4-фторфенил)пиперидин-1-карбоновой кислоты, который без очистки использовали на следующей стадии;
- из β - триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)- 3-(4-гидроксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты и 3,4-метилендиоксибензилхлорида получили β- триметилсилилэтиловый эфир (3RS,4RS)-3-[4-(бензо[1,3]диоксол-5-илметокси)нафталин-2- илметокси]-4-(4-фторфенил)пиперидин-1-карбоновой кислоты, который без очистки использовали на следующей стадии;
- из β- триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)- 3-(4-гидроксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты и 2-циклопропилэтилхлорида [Justus Liebigs Ann. Chem. 759, 132 (1972)] получили β- триметилсилилэтиловый эфир (3RS,4RS)-3-[4-(2-циклопропилэтокси)нафталин-2-илметокси] -4-(4- фторфенил)пиперидин-1-карбоновой кислоты в виде окрашенного в светло-розовый цвет масла; МС: 564 (M+H)+;
- из β- триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)- 3-(4-гидроксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты и 2-(2-бромэтокси)тетрагидропирана получили смесь β- триметилсиланилэтилового эфира (3RS, 4RS)-4-(4-фторфенил)-3-{ 4-[2-[(RS)- и (SR)-тетрагидропиран-2-илокси]этокси] нафталин-2-илметокси} пиперидин- 1-карбоновой кислоты в виде бесцветного масла; МС: 624 (M+H)+.
Последующим отщеплением защитной ТГП-группы с помощью 1 М раствора хлористого водорода в метаноле (10 мин, комнатная температура) получили β- триметилсилилэтиловый эфир (3RS,4RS)-4-(4-фторфенил)-3-[4-(2-гидроксиэтокси)нафталин-2- илметокси] пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 540 (M+H)+.
Пример 15.
(а) Раствор из 63 мг (0,116 ммоля) β- триметилсилилэтилового эфира (3RS, 4RS)-4-(4-фторфенил)-3-[4-(2-гидроксиэтокси)нафталин-2- илметокси] пиперидин-1-карбоновой кислоты в 2 мл метиленхлорида смешивали с 38 мг (0,58 ммоля) цианата натрия. К этой суспензии при 0o C добавляли 44 мкл (67 мг, 0,58 ммоля) трифторуксусной кислоты и реакционную смесь перемешивали в течение 2 ч при комнатной температуре. После этого смесь распределяли между метиленхлоридом и 5%-ным раствором гидрокарбоната натрия, органическую фазу сушили над сульфатом магния и в завершение удаляли растворитель при пониженном давлении. Полученный сырой β- триметилсилилэтиловый эфир (3RS, 4RS)-3-[4-(2-карбамоилоксиэтокси)нафталин-2-илметокси] -4-(4- фторфенил)пиперидин-1-карбоновой кислоты без последующей очистки и определения характеристик использовали на следующей стадии.
(б) Из сырого β- триметилсилилэтилового эфира (3RS,4RS)-3-[4-(2-карбамоилоксиэтокси)нафталин-2-илметокси] -4-(4- фторфенил)пиперидин-1-карбоновой кислоты аналогично описанному в примере 1(д) способу путем отщепления защитной группы с помощью тетрабутиламмонийфторида в тетрагидрофуране получили (3RS, 4RS)-3-[4-(2-карбамоилоксиэтокси)нафталин-2-илметокси] -4-(4- фторфенил)пиперидин в виде светло-желтого масла; МС: 438 (M)+.
Пример 16.
Аналогично примеру 1(д) отщеплением защитной группы с помощью тетрабутиламмонийфторида в тетрагидрофуране получали следующие соединения:
1) из β- триметилсилилэтилового эфира 4-(4-фторфенил)-3-[4-[2-(пиридин-2-илкарбамоилокси)этокси] нафталин-2- илметокси]пиперидин-1-карбоновой кислоты получили 4-(4-фторфенил)-3-[4-[2-(пиридин-2- илкарбамоилокси)этокси] нафталин-2-илметокси]пиперидин в виде бесцветного твердого вещества; МС: 395 [M-(PyNCO)]+;
2) из β- триметилсилилэтилового эфира (3RS,4RS)-3-[4-(2-бензоилоксиэтокси)нафталин-2-илметокси] -4-(4- фторфенил)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-3-[4-(2-бензоилоксиэтокси)нафталин-2-илметокси] -4-(4- фторфенил)пиперидин в виде бесцветной смолы; МС: 500 (M+H)+.
Использованные в качестве исходных веществ β- триметилсилилэтилкарбаматы получали следующим путем.
(а) Раствор из 54 мг (0,10 ммоля) β- триметилсилилэтилового эфира (3RS, 4RS)-4-(4-фторфенил)-3-[4-(2-гидроксиэтокси)нафталин-2- илметокси] пиперидин-1-карбоновой кислоты в 5 мл толуола смешивали с 30 мг (0,20 ммоля) 2-пиридилкарбонилазида [Monatsh. Chem. 33, 397 (1912)] и 5 мг 4-диметиламинопиридина. Раствор нагревали с обратным холодильником в течение 2 ч в атмосфере аргона. Смесь охлаждали и растворитель удаляли при пониженном давлении. Остаток распределяли между метиленхлоридом и насыщенным раствором поваренной соли, органическую фазу сушили над сульфатом магния и в завершение удаляли растворитель при пониженном давлении. Сырой продукт (103 мг) хроматографировали на силикагеле с использованием смеси 1:2 уксусного эфира и гексана в качестве элюента. Таким путем получили 65 мг (99% от теории) β- триметилсилилэтилового эфира (3RS, 4RS)-4-(4-фторфенил)-3-[4-[2-(пиридин-2-илкарбамоилокси)этокси] нафталин-2-илметокси] пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 660 (M+H)+.
(б) Раствор из 108 мг (0,20 ммоля) β- триметилсилилэтилового эфира (3RS, 4RS)-4-(4-фторфенил)-3-[4-(2-гидроксиэтокси)нафталин-2- илметокси] пиперидин-1-карбоновой кислоты в 2 мл метиленхлорида смешивали с 56 мкл (41 мг, 0,40 ммоля) триэтиламина. К этой смеси добавляли 36 мкл (42 мг, 0,30 ммоля) бензоилхлорида. Реакционную смесь перемешивали в течение 6 ч при комнатной температуре и в течение 1 ч при 50oC. Затем смесь распределяли между метиленхлоридом и 5%-ным раствором гидрокарбоната натрия, органическую фазу сушили над сульфатом магния и в завершение удаляли растворитель при пониженном давлении. Сырой β- триметилсилилэтиловый эфир (3RS,4RS)-3-[4-(2-бензоилоксиэтокси)нафталин- 2-илметокси]-4-(4-фторфенил)пиперидин-1-карбоновой кислоты использовали непосредственно на последующей стадии.
Пример 17.
Аналогично примеру 5 получали следующие соединения.
Работали аналогично примеру 5(а)-(г) следующим образом.
(а) Из метилового эфира салициловой кислоты путем введения СЭМ-группы получили метиловый эфир 2-(2-триметилсилилэтоксиметокси)бензойной кислоты в виде бесцветного масла; МС: 224 [M-(C2H4+CH2O)]+.
(б) Восстановлением метилового эфира 2-(2-триметилсилилэтоксиметокси)бензойной кислоты получили [2-(2-триметилсилилэтоксиметокси)фенил]метанол в виде светло-желтого масла; МС: 226 [M-(C2H4)]+.
(в) Хлорированием [2-(2-триметилсилилэтоксиметокси)фенил] метанола получили 1-хлорметил-2-(2-триметилсилилэтоксиметокси)бензол в виде бесцветного масла; МС: 214, 216 [M-(C2H4+CH2O)]+.
(г) Путем алкилирования β- триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)-3-(4-гидроксинафталин-2-илметокси)пиперидин- 1-карбоновой кислоты [пример 5(ж)] 1-хлорметил-2-(2-триметилсилилэтоксиметокси)бензолом получили β- триметилсилилэтиловый эфир (3RS,4RS)-4-(4-фторфенил)-3-[4-[2-(2- триметилсилилэтоксиметокси)бензилокси] нафталин-2-илметокси] пиперидин- 1-карбоновой кислоты в виде бесцветного масла; МС: 749 (M+NH4)+.
(д) Из β- триметилсилилэтилового эфира (3RS, 4RS)-4-(4-фторфенил)-3-[4-[2-(2-триметилсилилэтоксиметокси) бензилокси] нафталин-2-илметокси] пиперидин-1-карбоновой кислоты аналогично описанному в примере 5 способу путем расщепления β - триметилсилилэтилкарбамата тетрабутиламмонийфторидом в тетрагидрофуране получили (3RS, 4RS)-4-(4-фторфенил)-3-[4-[2-(2- триметилсилилэтоксиметокси)бензилокси] нафталин-2-илметокси]пиперидин в виде окрашенного в розовый цвет масла; МС: 588 (M+H)+.
(е) Отщеплением СЭМ-группы (3RS, 4RS)-4-(4-фторфенил)-3-[4-[2-(2- триметилсилилэтоксиметокси)бензилокси]нафталин-2-илметокси]пиперидина с помощью 2 н. раствора хлористого водорода в метаноле аналогично описанному в примере 5(ж) способу получили (3RS,4RS)-4-(4-фторфенил)-3-[4-[2-гидроксибензилокси] нафталин-2- илметокси]пиперидин в виде бесцветной смолы; МС: 458 (M+H)+.
Пример 18.
Аналогично примеру 12(г) путем расщепления 2,2,2-трихлорэтилкарбамата получали следующие соединения:
1) из 2,2,2-трихлорэтилового эфира (3RS, 4RS)-4-(2-фторфенил)- 3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты получили (3RS,4RS)-4-(2-фторфенил)-3-(нафталин-2-илметокси)пиперидин в виде светло-желтого масла; МС: 336 (M+H)+;
2) из 2,2,2-трихлорэтилового эфира (3RS, 4RS)-4-(3-фторфенил)- 3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-(3-фторфенил)-3-(нафталин-2-илметокси)пиперидин в виде светло-желтого масла; МС: 336 (M+H)+;
3) из 2,2,2-трихлорэтилового эфира (3RS, 4RS)-3-(нафталин-2-илметокси)-4-[3-(2,2,2- трихлорэтоксикарбонилокси)фенил]пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-(3-гидроксифенил)-3-(нафталин-2-илметокси)пиперидин в виде бежевого твердого вещества; МС: 333 (M)+.
Использованные в качестве исходных веществ 2,2,2-трихлорэтилкарбаматы получали следующим путем.
(а) Аналогично примеру 1(а)-(в) работали следующим образом.
Из 2-бромфторбензола и 1-бензил-4-пиперидона получили 1-бензил-4-(2-фторфенил)пиперидин-4-ол в виде желтого масла; МС: 285 (M)+. Последующим элиминированием получили 1-бензил-4-(2-фторфенил)-1,2,3,6-тетрагидропиридин в виде светло-желтого масла; МС: 267 (M)+. В результате последующего гидроборирования получили (3RS, 4RS)-1-бензил-4-(2-фторфенил)пиперидин-3-ол в виде бесцветного твердого вещества; МС: 285 (M)+.
(б) Аналогично примеру 1(ж) путем алкилирования (3RS, 4RS)-1-бензил-4-(2-фторфенил)пиперидин-3-ола 2-бромметилнафталином получили (3RS,4RS)-1-бензил-4-(2-фторфенил)-3-(нафталин-2-илметокси)пиперидин в виде желтого масла; МС: 284 (M-C11H9)+. Отщеплением бензильной защитной группы с помощью 2,2,2- трихлорэтилового эфира хлормуравьиной кислоты аналогично примеру 12(в) получили 2,2,2-трихлорэтиловый эфир (3RS, 4RS)-4-(2-фторфенил)-3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде желтого масла; МС: 509 (M)+.
(в) Аналогично примеру 1(а)-(в) работали следующим образом.
Из 3-бромфторбензола и 1-бензил-4-пиперидона получили 1-бензил-4-(3-фторфенил)пиперидин-4-ол в виде бесцветного твердого вещества; МС: 285 (M)+. Последующим элиминированием получили 1-бензил-4-(3-фторфенил)-1,2,3,6-тетрагидропиридин в виде светло-желтого масла; МС: 267 (M)+. В результате последующего гидроборирования получили (3RS, 4RS)-1-бензил-4-(3-фторфенил)пиперидин-3-ол в виде бесцветного масла; МС: 285 (M)+.
(г) Аналогично примеру 1(ж) путем алкилирования (3RS, 4RS)-1-бензил-4-(3-фторфенил)пиперидин-3-ола 2-бромметилнафталином получили (3RS,4RS)-1-бензил-4-(3-фторфенил)-3-(нафталин-2-илметокси)пиперидин в виде бесцветного масла; МС: 426 (M+H)+. Отщеплением бензильной защитной группы с помощью 2,2,2-трихлорэтилового эфира хлормуравьиной кислоты аналогично примеру 12(в) получили 2,2,2-трихлорэтиловый эфир (3RS, 4RS)-4-(3-фторфенил)-3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде желтого масла; МС: 510 (M+H)+.
(д) Аналогично примеру 1(а)-(в) работали следующим образом.
Из 3-бензилоксииодбензола [J. Chem. Soc. 2857 (1932)] и 1-бензил-4-пиперидона получили 1-бензил-4-(3-бензилоксифенил)пиперидин-4-ол в виде светло-желтого масла; МС: 373 (M)+. Последующим элиминированием получили 1-бензил-4-(3-бензилоксифенил)-1,2,3,6-тетрагидропиридин в виде бесцветного твердого вещества; МС: 355 (M)+. В результате последующего гидроборирования получили (3RS, 4RS)-1-бензил-4-(3-бензилоксифенил)пиперидин-3-ол в виде бесцветного твердого вещества; МС: 373 (M)+.
(е) Аналогично примеру 1(ж) путем алкилирования (3RS,4RS)-1-бензил-4-(3-бензилоксифенил)пиперидин-3-ола 2-бромметилнафталином получили (3RS, 4RS)-1-бензил-4-(3-бензилоксифенил)-3-(нафталин-2-илметокси)пиперидин в виде бесцветной смолы; МС: 514 (M+H)+.
(ж) Раствор из 250 мг (0,487 ммоля) (3RS,4RS)-1-бензил-4-(3-бензилоксифенил)-3-(нафталин-2-илметокси)пиперидина в 1,1 мл метиленхлорида смешивали при комнатной температуре с 247 мкл (236 мг, 1,946 ммоля, 4 экв.) N,N-диметиланилина и 195 мг (1,46 ммоля, 3,0 экв.) трихлорида алюминия и перемешивали в течение 2,5 ч при комнатной температуре. После этого смесь распределяли между метиленхлоридом и 5%-ным раствором гидрокарбоната натрия, органическую фазу сушили над сульфатом магния и в завершение удаляли растворитель при пониженном давлении. Сырой продукт очищали хроматографией на силикагеле с использованием смеси 4:1 метиленхлорида и гексана в качестве элюента. Таким путем получили 65 мг (32% от теории) (3RS, 4RS)-1-бензил-4-(3-гидроксифенил)-3-(нафталин- 2-илметокси)пиперидин в виде окрашенного в бежевый цвет твердого вещества; МС: 423 (M)+.
(з) Аналогично примеру 12(в) отщеплением бензильной защитной группы с помощью 2,2,2-трихлорэтилового эфира хлормуравьиной кислоты получили 2,2,2-трихлорэтиловый эфир (3RS, 4RS)-3-(нафталин-2-илметокси)- 4-[3-(2,2, 2-трихлорэтоксикарбонилокси)фенил] пиперидин-1-карбоновой кислоты, который в сыром виде использовали непосредственно на следующей стадии.
Пример 19.
Аналогично описанному в примере 2(д) способу путем каталитического гидрирования (3RS, 4RS)-1-бензил-4-(3-фторфенил)пиперидин-3-ола получили (3RS, 4RS)-4-(3-фторфенил)пиперидин-3-ол в виде бесцветного твердого вещества; МС: 196 (M+H)+. Введением BOC-группы аналогично примеру 1(е) получили трет-бутиловый эфир (3RS,4RS)-4-(3-фторфенил)-3-гидроксипиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 296 (M+H)+. Путем последующего алкилирования 4-бензилокси-2-хлорметилнафталином аналогично описанному в примере 1(ж) способу получили трет-бутиловый эфир (3RS, 4RS)-3-(4-бензилоксинафталин-2-илметокси)-4-(3- фторфенил)пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 541 (M)+. В результате отщепления BOC-группы с помощью раствора хлористого водорода в метаноле аналогично описанному в примере 1(з) способу получили (3RS,4RS)-3-(4-бензилоксинафталин-2-илметокси)-4-(3- фторфенил)пиперидин, который представлял собой бесцветное твердое вещество; МС: 442 (M+H)+.
Использованный в качестве исходного вещества 4-бензилокси-2-хлорметилнафталин получали следующим путем:
(а) Аналогично примеру 14(а) путем алкилирования этилового эфира 4-гидроксинафталин-2-карбоновой кислоты [J. Agric. Chem. Soc. Japan 24, 313 (1950)] бензилбромидом получили этиловый эфир 4-бензилоксинафталин-2-карбоновой кислоты в виде бесцветного твердого вещества; МС: 216 (M)+.
(б) Восстановлением этилового эфира 4-бензилоксинафталин-2-карбоновой кислоты аналогично примеру 5(б) получили (4-бензилоксинафталин-2-ил)метанол в виде бесцветного твердого вещества; МС: 264 (M)+.
(в) Хлорированием (4-бензилоксинафталин-2-ил)метанола с помощью четыреххлористого углерода аналогично примеру 7(в) получили 4-бензилокси-2-хлорметилнафталин в виде бесцветного твердого вещества; МС: 282 (M)+ .
Пример 20.
Аналогично примеру 1(з) путем отщепления BOC-группы с помощью раствора хлористого водорода в метаноле получали следующие соединения:
1) из трет-бутилового эфира (3RS,4RS)-4-(4-цианфенил)-3-(нафталин- 2-илметокси)-4-(3-фторфенил)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-(4-цианфенил)-3-(нафталин-2-илметокси)-4-(3-фторфенил)пиперидин в виде светло-желтого твердого вещества; МС: 342 (M+H)+;
2) из трет-бутилового эфира (3RS, 4RS)-4-[4-(фенилсульфониламинометил)фенил] -3-(нафталин-2- илметокси)-4-(3-фторфенил)пиперидин-1-карбоновой кислоты получили (3RS,4RS)-4-[4-(фенилсульфониламинометил)фенил] -3-(нафталин-2- илметокси)-4-(3-фторфенил)пиперидин в виде бесцветного твердого вещества; МС: 485 (M-H)+;
3) из трет-бутилового эфира (3RS, 4RS)-4-[4-(4-метоксибензоиламино)метил] фенил-3-(нафталин-2- илметокси)-4-(3-фторфенил)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-[4-(4-метоксибензоиламино)метил]фенил- 3-(нафталин-2-илметокси)-4-(3-фторфенил)пиперидин в виде бесцветной смолы; МС: 481 (M+H)+;
4) из трет-бутилового эфира (3RS, 4RS)-3-(нафталин-2-илметокси)- 4-[4-(фенилацетиламинометил)фенил] пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-3-(нафталин-2-илметокси)-4-[4-(фенилацетиламинометил) фенил]пиперидин в виде бесцветной смолы; МС: 465 (M+H)+;
5) из трет-бутилового эфира (3RS,4RS)-4-[4-(бензоиламинометил)фенил]-3-[4-(2- триметилсилилэтоксиметокси)нафталин-2-илметокси] пиперидин-1-карбоновой кислоты путем одновременного отщепления BOC- и СЭМ-групп аналогично примеру 3 и 5(ж) получили (3RS, 4RS)-4-[4-(бензоиламинометил)фенил]- 3-(4-гидроксинафталин-2-илметокси)пиперидин в виде окрашенного в слегка оранжевый цвет твердого вещества; МС: 467 (M+H)+.
Использованные в качестве исходных веществ BOC-содержащие соединения получали следующим образом:
(а) Суспензию из 20 мг (0,30 ммоля) порошка активированного цинка, 76 мг (1,17 ммоля) цианида калия, 52 мг (0,20 ммоля) трифенилфосфина и 74 мг (0,10 ммоля) дибромида бис(трифенилфосфин)никеля (II) в 2 мл ацетонитрила выдерживали при температуре 60oC в атмосфере аргона в течение 5 мин. К этой суспензии добавляли 356 мг (1,00 ммоль) трет-бутилового эфира (3RS,4RS)-4-(4-бромфенил)-3-гидроксипиперидин-1-карбоновой кислоты в твердом виде. Суспензию зеленого цвета перемешивали в атмосфере аргона в течение 20 ч при 60oC. Образовавшуюся темно-коричневую суспензию фильтровали через Speedex и нерастворившийся материал промывали метиленхлоридом. Фильтрат распределяли между метиленхлоридом и 5%-ным раствором гидрокарбоната натрия, органическую фазу сушили над сульфатом магния и в завершение удаляли растворитель при пониженном давлении. Сырой продукт (416 мг) очищали хроматографией на силикагеле с использованием смеси 1:1 уксусного эфира и гексана в качестве элюента. Таким путем получили 168 мг (56% от теории) трет-бутилового эфира (3RS, 4RS)-4-(4-цианфенил)-3-гидроксипиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 302 (M)+.
(б) Аналогично описанному в примере 1(ж) способу путем алкилирования трет-бутилового эфира (3RS,4RS)-4-(4-цианфенил)-3-гидроксипиперидин-1-карбоновой кислоты 2-бромметилнафталином получили трет-бутиловый эфир (3RS, 4RS)-4-(4-цианфенил)-3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде светло-желтой смолы; МС: 443 (M+H)+.
(в) Раствор из 133 мг (0,301 ммоля) трет-бутилового эфира (3RS,4RS)-4-(4-цианфенил)-3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в 0,5 мл тетрагидрофурана смешивали с 1,5 мл (1,5 ммоля) 1М раствора комплекса боран-тетрагидрофуран в тетрагидрофуране и нагревали с обратным холодильником в атмосфере аргона в течение 6 ч. Реакционную смесь распределяли между метиленхлоридом и водой, органическую фазу сушили над сульфатом магния и в завершение удаляли растворитель при пониженном давлении. Сырой продукт (163 мг) очищали хроматографией на силикагеле с использованием смеси 14:1:0,1 метиленхлорида, метанола и 25%-ного раствора аммиака в качестве элюента. Таким путем получили 106 мг (79% от теории) трет-бутилового эфира (3RS,4RS)-4-(4-аминометилфенил)-3-(нафталин-2-илметокси)пиперидин- 1-карбоновой кислоты в виде бесцветной смолы; МС: 447 (M+H)+.
(г) Раствор из 47 мг (0,105 ммоля) трет-бутилового эфира (3RS,4RS)-4-(4-аминометилфенил)-3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты в 2 мл метиленхлорида смешивали с 18 мкл (12,7 мг, 0,126 ммоля, 1,2 экв.) триэтиламина и охлаждали до 0oC. Затем по каплям добавляли 15 мкл (20,4 мг, 0,116 ммоля, 1,1 экв. ) бензолсульфохлорида, смесь нагревали до комнатной температуры, после чего ее перемешивали в течение 1 ч. Реакционную смесь распределяли между метиленхлоридом и 5%-ным раствором гидрокарбоната натрия, органическую фазу сушили над сульфатом магния и в завершение удаляли растворитель при пониженном давлении. Таким путем получили 47 мг сырого трет-бутилового эфира (3RS, 4RS)-4-[4-(фенилсульфониламинометил)фенил] -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты, который без последующей очистки и определения характеристик использовали на следующей стадии.
(д) Аналогично описанному в разделе (г) способу из трет-бутилового эфира (3RS, 4RS)-4-(4-аминометилфенил)-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты путем ацилирования п-анизоилхлоридом получили сырой трет-бутиловый эфир (3RS,4RS)-4-[4-(4-метоксибензоиламино)метил]фенил-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты, который без последующей очистки и определения характеристик использовали на следующей стадии.
(е) Аналогично описанному в разделе (г) способу из трет-бутилового эфира (3RS, 4RS)-4-(4-аминометилфенил)-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты путем ацилирования хлорангидридом фенилуксусной кислоты получили сырой трет-бутиловый эфир (3RS,4RS)-3-(нафталин-2-илметокси)-4-[4-(фенилацетиламинометил) фенил] пиперидин-1-карбоновой кислоты, который без последующей очистки и определения характеристик использовали на следующей стадии.
(ж) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS, 4RS)-4-(4-цианфенил)-3-гидроксипиперидин-1-карбоновой кислоты 2-хлорметил-4-(-(β-- триметилсилилэтоксиметокси)нафталином получили трет-бутиловый эфир (3RS, 4RS)-4-(4-цианфенил)-3-[4-(2- триметилсилилэтоксиметокси)нафталин-2-илметокси]пиперидин-1-карбоновой кислоты в виде светло-желтого масла; МС: 530 [M-(C2H4+CH2O)]+.
(з) Аналогично описанному в разделе (в) способу восстановлением нитрильной группы из трет-бутилового эфира (3RS, 4RS)-4-(4-цианфенил)-3-[4-(2-триметилсилилэтоксиметокси)нафталин- 2-илметокси] пиперидин-1-карбоновой кислоты получили трет-бутиловый эфир (3RS, 4RS)-4-(4-аминометилфенил)-3-[4-(2- триметилсилилэтоксиметокси)нафталин-2-илметокси] пиперидин-1-карбоновой кислоты в виде светло-желтого масла; МС: 593 (M+H)+.
(и) Аналогично описанному в разделе (г) способу из трет-бутилового эфира (3RS,4RS)-4-(4-аминометилфенил)-3-[4-(2- триметилсилилэтоксиметокси)нафталин-2-илметокси] пиперидин-1-карбоновой кислоты путем ацилирования бензоилхлоридом получили сырой трет-бутиловый эфир (3RS, 4RS)-4-[4-(бензоиламинометил)фенил] -3-[4-(2- триметилсилилэтоксиметокси)нафталин-2-илметокси] пиперидин-1-карбоновой кислоты, который без последующей очистки и определения характеристик использовали на следующей стадии.
Пример 21.
Аналогично примеру 1(з) путем отщепления BOC-группы с помощью раствора хлористого водорода в метаноле получали следующие соединения:
1) из трет-бутилового эфира (3RS,4RS)-4-(4-хлорфенил)-4-гидрокси-3-(4-метоксибензилокси)пиперидин- 1-карбоновой кислоты получили (3RS,4RS)-4-(4-хлорфенил)-4-гидрокси- 3-(4-метоксибензилокси)пиперидин в виде бесцветного твердого вещества; МС: 348 (M+H)+;
2) из трет-бутилового эфира (3RS,4RS)-4-(4-хлорфенил)-4-гидрокси- 3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты получили (3RS,4RS)-4-(4-хлорфенил)-4-гидрокси-3-(нафталин-2-илметокси)пиперидин в виде бесцветного твердого вещества; МС: 226, 228 [M-(C11H9)]+.
Использованные в качестве исходных веществ соединения получали следующим образом:
(а) Раствор из 3,0 г (15,5 ммоля) 4-(4-хлорфенил)-1,2,3,6-тетрагидропиридина в 20 мл абсолютного диметилформамида смешивали с 2,37 мл (1,72 г, 17,0 ммоля) триэтиламина и охлаждали до 0oC. По каплям при 0oC добавляли раствор из 3,7 г (17,0 ммоля) ди-трет-бутилдикарбоната в 8 мл абсолютного диметилформамида. Смесь нагревали до комнатной температуры и перемешивали в течение 20 ч. Растворитель отгоняли при 50-55oC и давлении 0,1 мм рт. ст. Затем полученный остаток распределяли между метиленхлоридом и водой, органическую фазу сушили над сульфатом магния и в завершение удаляли растворитель при пониженном давлении. Сырой продукт (5,0 г) очищали хроматографией на силикагеле с использованием смеси 95:5 метиленхлорида и уксусного эфира в качестве элюента. Таким путем получили 4,5 г (99% от теории) трет-бутилового эфира 4-(4-хлорфенил)-1,2,3,6-тетрагидропиридин-1-карбоновой кислоты в виде бесцветного масла; МС: 236, 238 [M-(C4H9)]+ .
(б) Раствор из 2,5 г (8,5 ммоля) трет-бутилового эфира 4-(4-хлорфенил)-1,2,3,6-тетрагидропиридин-1-карбоновой кислоты в 20 мл ацетона смешивали с 0,425 мл (0,0085 ммоля, 0,01 экв.) раствора тетроксида осмия (0,02 М в трет-бутаноле) и 8,6 мл раствора (30%-ного в воде) перекиси водорода и смесь перемешивали в течение 18 ч при комнатной температуре. Смесь распределяли между уксусным эфиром и водой, органическую фазу промывали 10%-ным раствором бисульфита натрия и водой, сушили над сульфатом магния и в завершение удаляли растворитель при пониженном давлении. Сырой продукт (2,2 г) очищали хроматографией на силикагеле с использованием смеси 3:1 метиленхлорида и уксусного эфира в качестве элюента. Таким путем получили 544 мг (20% от теории) трет-бутилового эфира (3RS, 4RS)-4-(4-хлорфенил)-3,4-дигидроксипиперидин-1-карбоновой кислоты в виде бесцветной смолы; МС: 270, 272 [M-(C4H9)]+.
(в) К суспензии 16 мг (0,4 ммоля) гидрида натрия (60%-ная дисперсия в вазелиновом масле) в 3 мл диметилсульфоксида по каплям добавляли раствор из 128 мг (0,392 ммоля) трет-бутилового эфира (3RS,4RS)-4-(4-хлорфенил)-3, 4-дигидроксипиперидин-1-карбоновой кислоты в 1,5 мл диметилсульфоксида. Через 15 мин при комнатной температуре в течение 10 мин по каплям добавляли раствор из 61 мг (0,39 ммоля) п-метоксибензилхлорида в 1 мл диметилсульфоксида и смесь перемешивали в течение 18 ч. Затем реакционную смесь распределяли между уксусным эфиром и водой, органическую фазу сушили над сульфатом магния и в завершение удаляли растворитель при пониженном давлении. Сырой продукт (200 мг) очищали хроматографией на силикагеле с использованием смеси 3: 1 гексана и уксусного эфира в качестве элюента. Таким путем (наряду с исходным материалом и бисалкилированным продуктом) получили 63 мг (38% от теории) трет-бутилового эфира (3RS, 4RS)-4-(4-хлорфенил)-4-гидрокси-3-(4- метоксибензилокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 448, 450 (M+H)+.
(г) Аналогично описанному в разделе (в) способу путем алкилирования трет-бутилового эфира (3RS,4RS)-4-(4-хлорфенил)-3, 4-дигидроксипиперидин-1-карбоновой кислоты 2-бромметилнафталином получили трет-бутиловый эфир (3RS, 4RS)-4-(4-хлорфенил)-4-гидрокси-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты в виде светло-желтого масла; МС: 411, 413 [M-(C4H8)]+.
Пример 22.
(а) К охлажденному до -70oC раствору из 112,5 г (0,48 моля) 1, 4-дибромбензола в 1200 мл диэтилового эфира в течение 45 мин по каплям добавляли 400 мл 1,2 М раствора н-BuLi в гексане таким образом, чтобы температура не повышалась выше -60oC. По завершении добавления смесь перемешивали в течение 2,5 ч при -70oC. После этого в течение одного часа при температуре в интервале от -70 до -65oC по каплям добавляли раствор из 90,84 г (0,48 моля) 1-бензил-4-пиперидона в 300 мл простого эфира. По окончании этого добавления смесь перемешивали в течение 2 ч при -70oC. Для дальнейшей переработки холодную реакционную смесь сливали на 1200 мл 15%-ного раствора хлорида аммония, смесь переносили в делительную воронку и отделяли органическую фазу. Водную фазу дважды экстрагировали простым эфиром, после чего объединенные органические фазы дважды экстрагировали водой и насыщенным раствором хлорида натрия. После этого органическую фазу сушили над сульфатом магния и упаривали при пониженном давлении, при этом сырой продукт выпадал в осадок в виде желтоватого твердого вещества. Для очистки этот продукт растворяли в горячем метиленхлориде, раствор смешивали с гексаном до начала помутнения и при перемешивании охлаждали до комнатной температуры. Образовавшийся осадок подвергали вакуум-фильтрации и сушили. Таким путем получили 121,65 г (73% от теории) 1-бензил-4-(4-бромфенил)пиперидин-4-ола в виде желтоватого твердого вещества; tпл 106oC, МС: 346,348 (M+H)+.
(б) Смесь из 121,6 г (0,35 моля) 1-бензил-4-(4-бромфенил)пиперидин-4-ола и 121,6 г (0,64 моля) моногидрата п-толуолсульфокислоты в 1200 мл толуола в течение 4,5 ч нагревали с обратным холодильником с использованием насадки для отделения воды. Далее реакционную смесь охлаждали до комнатной температуры и с помощью 3 н. едкого натра значение pH устанавливали равным 10. После этого экстрагировали метиленхлоридом порциями сначала 2000 мл, а затем 500 мл. Объединенные органические фазы дважды промывали водой порциями по 1000 мл, сушили над сульфатом магния и затем упаривали при пониженном давлении. Таким путем получили 109,1 г (99% от теории) 1-бензил-4-(4-бромфенил)-1,2,3, 6-тетрагидропиридина в виде желтоватого твердого вещества; МС: 328, 330 (M+H)+.
(в) К раствору из 51,1 г (0,156 моля) 1-бензил-4-(4-бромфенил)-1,2,3,6-тетрагидропиридина в 350 мл диметоксиэтана добавляли 16,9 г (83,3 ммоля) борогидрида натрия и реакционную смесь перемешивали при комнатной температуре в течение 15 мин. После этого при 25-30oC в течение 30 мин по каплям добавляли 95,2 мл эфирата трифторида бора, а затем реакционную смесь перемешивали в течение 2 ч при комнатной температуре. Далее в указанной последовательности по каплям медленно добавляли сначала раствор 98,4 г гидроксида калия в 530 мл воды, а затем в течение 15 мин 80,7 мл 30%-ного раствора перекиси водорода. После этого смесь в течение 2 ч кипятили с обратным холодильником. Для последующей переработки охлажденную реакционную смесь фильтровали через дикалит, а затем эту смесь промывали метиленхлоридом. Полученный раствор смешивали с 700 мл метиленхлорида, органическую фазу отделяли и затем водную фазу экстрагировали 300 мл метиленхлорида. Объединенные органические фазы дважды промывали водой порциями по 200 мл, сушили над сульфатом магния и упаривали при пониженном давлении. Кристаллизацией сырого продукта из ацетона получили 31 г (57% от теории) (3RS,4RS)-1-бензил-4-(4-бромфенил)пиперидин-3-ола в виде бесцветных кристаллов; tпл 125-129o C.
(г) В трубку Шленка в атмосфере аргона загружали 74,9 мг (0,29 ммоля) PdCl2(CH3CN)2, 168,0 мг (0,303 ммоля) 1,1'-бис(дифенилфосфино)ферроцена и 10 мл метанола (перегнанного в атмосфере аргона) и реакционную смесь перемешивали в течение 30 мин при комнатной температуре. Суспензию красно-коричневого цвета в атмосфере аргона переносили в 185-миллилитровый стальной автоклав, снабженный стеклянной вставкой. После этого добавляли 10,0 г (29 ммолей) (3RS, 4RS)-1-бензил-4-(4-бромфенил)пиперидин-3-ола (предварительно обработанного активированным углем), 60 мл метанола и 6 мл (43 ммоля) триэтиламина. Автоклав закрывали, с помощью монооксида углерода создавали в нем давление 15 бар и реакционную смесь перемешивали при 110oC в течение 20 ч при постоянном давлении. После охлаждения автоклава и сброса давления газа реакционную смесь оранжевого цвета упаривали при пониженном давлении. Твердый, окрашенный в оранжевый цвет остаток растворяли в 20 мл метиленхлорида. Раствор дважды промывали 5%-ным раствором карбоната натрия порциями по 100 мл, соответственно 100 мл воды, а затем упаривали при пониженном давлении. Желто-коричневый твердый остаток очищали хроматографией на силикагеле с использованием смеси 1:1 уксусного эфира и гексана в качестве элюента. Таким путем получили 7,74 г (82% от теории) метилового эфира (3RS,4RS)-4-(1-бензил-3-гидроксипиперидин-4-ил)бензойной кислоты в виде белого твердого вещества; tпл 103-104oC, МС: 326 (M+H)+.
(д) Раствор из 5,0 г (15,3 ммоля) метилового эфира (3RS,4RS)-4-(1-бензил-3-гидроксипиперидин-4-ил)бензойной кислоты в 50 мл тетрагидрофурана смешивали при комнатной температуре с 720 мг (32,9 ммоля) борогидрида лития. Далее реакционную смесь в течение 15 ч выдерживали при 60oC. Для дальнейшей переработки реакционную смесь при охлаждении льдом смешивали с 20 мл воды, а затем дважды экстрагировали путем встряхивания уксусным эфиром, используя порции по 50 мл. Органические фазы объединяли, сушили над сульфатом натрия и упаривали при пониженном давлении. Полученный сырой (3RS, 4RS)-1-бензил-4-(4-гидроксиметилфенил)пиперидин-3-ол (Rf 0,23, SiO2, метиленхлорд:метанол: аммиак = 95:5:0,1) без последующей очистки использовали на следующей стадии.
(е) Раствор из 2,0 г (6,72 ммоля) (3RS,4RS)-1-бензил-4-(4-гидроксиметилфенил)пиперидин-3-ола в 100 мл этанола гидрировали в течение 4 ч в присутствии 1,0 г палладия на угле (20%-ного) при комнатной температуре и давлении 3 бар. Для дальнейшей переработки катализатор удаляли вакуум-фильтрацией через дикалит и остаток дважды промывали этанолом, используя порции по 50 мл. Этанольный раствор упаривали при пониженном давлении и остаток хроматографировали на силикагеле с использованием смеси 65:10:1 метиленхлорида, метанола и аммиака в качестве элюента. Таким путем получили 1,1 г (79% от теории) (3RS,4RS)-4-(4-гидроксиметилфенил)пиперидин-3-ол в виде бесцветного твердого вещества; МС: 207 (M)+.
(ж) Раствор 1,10 г (5,31 ммоля) (3RS, 4RS)-4-(4-гидроксиметилфенил)пиперидин-3-ола в 20 мл диметилформамида смешивали при 0oC с 0,59 г (5,82 ммоля) триэтиламина и 1,22 г (5,57 ммоля) ди-трет-бутилдикарбоната и перемешивали в течение 15 ч при комнатной температуре. Затем диметилформамид отгоняли в вакууме, создаваемом масляным насосом, и остаток очищали хроматографией на силикагеле с использованием смеси 98:2 метиленхлорида и метанола в качестве элюента. Таким путем получили 1,51 г (92% от теории) трет-бутилового эфира (3RS,4RS)-3-гидрокси-4-(4-гидроксиметилфенил)пиперидин-1-карбоновой кислоты в виде бесцветной пены; МС: 233 (M-C4H10O)+.
(з) Раствор из 1,50 г (5,14 ммоля) трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-(4-гидроксиметилфенил)пиперидин-1-карбоновой кислоты, 1,73 г (6,16 ммоля) трифенилхлорметана и 674 мг (6,68 ммоля) триэтиламина в 20 мл метиленхлорида перемешивали в течение 5 ч при комнатной температуре. Для дальнейшей переработки реакционную смесь промывали 10 мл воды и 10 мл насыщенного раствора гидрокарбоната натрия, органическую фазу сушили над сульфатом натрия и упаривали при пониженном давлении. Сырой продукт хроматографировали на силикагеле с использованием смеси 95:5 толуола и уксусного эфира в качестве элюента. Таким путем получили 2,08 г (77,5% от теории) трет-бутилового эфира (3RS,4RS)-3-гидрокси-4-(4-тритилоксиметилфенил)пиперидин-1-карбоновой кислоты в виде бесцветной пены; МС: 567 (M+NH4)+.
(и) К раствору из 2, 08 г (3,78 ммоля) трет-бутилового эфира (3RS,4RS)-3-гидрокси-4-(4-тритилоксиметилфенил)пиперидин-1-карбоновой кислоты и 1,0 г (4,54 ммоля) 2-бромметилнафталина в 30 мл диметилформамида добавляли 290 мг (6,05 ммоля) гидрида натрия (50%-ная дисперсия в вазелиновом масле) и реакционную смесь перемешивали в течение 2 ч при комнатной температуре. Для дальнейшей переработки реакционную смесь упаривали в вакууме, создаваемом масляным насосом, остаток распределяли между 100 мл насыщенного раствора хлорида аммония и 100 мл уксусного эфира, а затем отделенную водную фазу дважды экстрагировали путем встряхивания уксусным эфиром, используя порции по 50 мл. Объединенные уксусноэфирные экстракты сушили над сульфатом натрия и упаривали при пониженном давлении. Сырой продукт очищали хроматографией на силикагеле с использованием смеси 4:1 метиленхлорида и гексана в качестве элюента. Таким путем получили 2,27 г (87% от теории) трет-бутилового эфира (3RS, 4RS)-3-нафталин-2-илметокси-4-(4-тритилоксиметилфенил)пиперидин- 1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 707 (M+NH4)+.
(к) Раствор из 1,07 г (1,48 ммоля) трет-бутилового эфира (3RS,4RS)-3-нафталин-2-илметокси-4-(4-тритилоксиметилфенил)пиперидин- 1-карбоновой кислоты в 15 мл метиленхлорида смешивали при комнатной температуре с 2 мл 2 н. хлористого водорода в метаноле и перемешивали в течение 15 мин при комнатной температуре. Далее раствор сливали в 30 мл насыщенного раствора карбоната натрия и эту смесь дважды экстрагировали путем встряхивания уксусным эфиром, используя порции по 50 мл. Объединенные органические фазы сушили над сульфатом натрия и упаривали при пониженном давлении. Сырой продукт очищали хроматографией на силикагеле с использованием смеси 99:1 метиленхлорида и метанола в качестве элюента. Таким путем получили 580 мг (82% от теории) трет-бутилового эфира (3RS, 4RS)-4-(4-гидроксиметилфенил)-3-(нафталин-2-илметокси)пиперидин- 1-карбоновой кислоты в виде бесцветного масла; МС: 447 (M)+.
(л) К раствору из 45 мг (0,1 ммоля) трет-бутилового эфира (3RS,4RS)-4-(4-гидроксиметилфенил)-3-(нафталин-2-илметокси)пиперидин- 1-карбоновой кислоты, 12 мг (0,12 ммоля) триэтиламина и 12 мг (0,1 ммоля) хлорангидрида пивалиновой кислоты в 5 мл метиленхлорида перемешивали при комнатной температуре в течение 15 ч. Для дальнейшей переработки реакционную смесь разбавляли 10 мл метиленхлорида, затем промывали 5 мл воды, сушили над сульфатом натрия и упаривали при пониженном давлении. Остаток хроматографировали на силикагеле с использованием смеси 4:1 гексана и уксусного эфира в качестве элюента. Таким путем получили 39 мг (73% от теории) трет-бутилового эфира (3RS,4RS)-4-[4-(2,2-диметилпропионилоксиметил)фенил]- 3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 549 (M+NH4)+.
(м) Раствор из 35 мг (0,07 ммоля) трет-бутилового эфира (3RS,4RS)-4-[4-(2,2-диметилпропионилоксиметил)фенил]-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты в 2 мл 2 М хлористого водорода в метаноле перемешивали в течение 4,5 ч при комнатной температуре. Далее реакционный раствор упаривали при пониженном давлении. Остаток растворяли в диэтиловом эфире, при этом часть (15 мг, 49% от теории) гидрохлорида (3RS,4RS)-4-(3-нафталин-2-илметоксипиперидин-4-ил)бензилового эфира 2,2-диметилпропионовой кислоты получали в форме белых кристаллов; МС: 432 (M+H)+ .
Пример 23.
Раствор из 1,10 г (1,59 ммоля) трет-бутилового эфира (3RS,4RS)-3-нафталин-2-илметокси-4-(4-тритилоксиметилфенил)пиперидин- 1-карбоновой кислоты в 50 мл метанола смешивали при комнатной температуре с 30 мл 2 М раствора хлористого водорода в метаноле и перемешивали в течение 4 ч при комнатной температуре. Далее реакционный раствор упаривали при пониженном давлении и остаток распределяли между 30 мл насыщенного раствора карбоната натрия и 50 мл уксусного эфира. Водную фазу еще раз экстрагировали путем встряхивания 50 мл уксусного эфира, после чего органические фазы объединяли, сушили над сульфатом натрия и упаривали при пониженном давлении. Сырой продукт очищали хроматографией на силикагеле с использованием смеси 90:10 метиленхлорида и метанола в качестве элюента. Таким путем получили 462 мг (83% от теории) (3RS, 4RS)-[4-[3-(нафталин-2-илметокси)пиперидин-4-ил] фенил]метанола в виде бесцветного твердого вещества; МС: 348 (M+H)+.
Пример 24.
Аналогично примеру 22(м) путем отщепления BOC-группы с помощью кислоты получали следующие соединения:
1) из трет-бутилового эфира (3RS,4RS)-4-(4-бензоилоксиметилфенил)- 3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты получили (3RS,4RS)-4-[3-(нафталин-2-илметокси)пиперидин-4-ил] бензиловый эфир бензойной кислоты в виде бесцветной пены; МС: 452 (M+H)+;
2) из трет-бутилового эфира (3RS, 4RS)-4-[4-(3-метоксибензоилоксиметил)фенил] -3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты получили гидрохлорид (3RS, 4RS)-4-(3-нафталин-2-илметоксипиперидин-4-ил)бензилового эфира 3-метоксибензойной кислоты в виде бесцветного твердого вещества; МС: 482 (M+H)+;
3) из трет-бутилового эфира (3RS,4RS)-4-[4-(3,5-диметоксибензоилоксиметил)фенил] -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты получили гидрохлорид (3RS, 4RS)-4-(3-нафталин-2-илметоксипиперидин-4-ил)бензилового эфира 3,5-диметоксибензойной кислоты в виде бесцветного твердого вещества; МС: 512 (M+H)+;
4) из трет-бутилового эфира (3RS,4RS)-4-(4-циклогексанкарбонилоксиметилфенил)-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты с применением трифторуксусной кислоты в метиленхлориде получили трифторацетат (3RS, 4RS)-4-[3-(нафталин-2-илметокси)пиперидин-4-ил] бензилового эфира циклогексанкарбоновой кислоты в виде бесцветного твердого вещества; МС: 458 (M+H)+;
5) из трет-бутилового эфира (3RS,4RS)-[4-(2-хлорбензоилоксиметил)фенил] -3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты с применением трифторуксусной кислоты в метиленхлориде получили трифторацетат (4RS, 3RS)-4-(3-нафталин-2-илметоксипиперидин-4-ил)бензилового эфира 2-хлорбензойной кислоты в виде бесцветного твердого вещества; МС: 486 (M+H)+;
6) из трет-бутилового эфира (3RS,4RS)-4-(4-метоксикарбонилоксиметилфенил)-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты получили гидрохлорид (3RS,4RS)-4-(нафталин-2-илметоксипиперидин-4-ил)бензилового эфира и метилового эфира угольной кислоты в виде бесцветного масла; МС: 406 (M+H)+;
7) из (3RS,4RS)-4-(1-трет-бутоксикарбонил-3-нафталин-2- илметоксипиперидин-4-ил)бензилового эфира пиридин-4-карбоновой кислоты получили гидрохлорид (3RS,4RS)-4-[3-(нафталин-2- илметокси)пиперидин-4-ил]бензилового эфира пиридин-4-карбоновой кислоты в виде желтоватого масла; МС: 453 (M+H)+;
8) из (3RS, 4RS)-4-[1-трет-бутоксикарбонил-3-(нафталин-2- илметокси)пиперидин-4-ил] бензилового эфира пиразин-2-карбоновой кислоты получили гидрохлорид (3RS, 4RS)-4-(3-нафталин-2- илметоксипиперидин-4-ил)бензилового эфира пиразин-2-карбоновой кислоты в виде бесцветного твердого вещества; МС: 454 (M+H)+;
9) из трет-бутилового эфира (3RS, 4RS)-4-[4-(2-хлорбензоилоксиметил)фенил] -3-(1- метоксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты с применением трифторуксусной кислоты в метиленхлориде получили трифторацетат (3RS, 4RS)-4-[3-(1-метоксинафталин-2-илметокси)пиперидин- 4-ил]бензилового эфира 2-хлорбензойной кислоты в виде бесцветного твердого вещества; МС: 516 (M+H)+;
10) из трет-бутилового эфира (3RS,4RS)-4-[4-(4-гидроксибензоилоксиметил)фенил] -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты с применением трифторуксусной кислоты в метиленхлориде получили трифторацетат (3RS, 4RS)-4-(3-нафталин-2-илметоксипиперидин-4-ил)бензилового эфира 4-гидроксибензойной кислоты в виде желтоватого твердого вещества; МС: 468 (M+H)+;
11) из трет-бутилового эфира (3RS,4RS)-3-(нафталин-2-илметокси)-4-[4-(пиридин-2- илкарбамоилоксиметил)фенил] пиперидин-1-карбоновой кислоты получили гидрохлорид (3RS, 4RS)-4-[3-(нафталин-2-илметокси)пиперидин-4-ил] бензилового эфира пиридин-2-илкарбаминовой кислоты в виде бесцветной пены; Rf 0,15 (SiO2, метиленхлорид:метанол:аммиак = 90:10:0, 1);
12) из трет-бутилового эфира (3RS,4RS)-4-[4-(3-гидроксипропенил) фенил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-[4-(3-метоксипропенил)фенил] -3-(нафталин-2- илметокси)пиперидин в виде желтого масла; МС: 388 (M+H)+;
13) из трет-бутилового эфира (3RS, 4RS)-4-[4-(3-бензоилоксипропенил)фенил] -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-[4-(3-бензоилоксипропенил)фенил] -3-(нафталин-2- илметокси)пиперидин в виде желтого масла; МС: 478 (M+H)+;
14) из трет-бутилового эфира (3RS, 4RS)-4-[4-[3-(2-хлорбензоилокси)пропил] фенил] -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты получили 3-[4-[3-(нафталин-2-илметокси)пиперидин-4-ил]фенил]пропиловый эфир (3RS, 4RS)-2-хлорбензойной кислоты в виде желтоватого масла; МС: 514, 516 (M+H)+.
Исходные субстанции получали аналогично описанному в примере 22(л) способу следующим путем.
(а) Из трет-бутилового эфира (3RS, 4RS)-4-(4-гидроксиметилфенил)-3-(нафталин-2-илметокси)пиперидин- 1-карбоновой кислоты и бензоилхлорида получили трет-бутиловый эфир (3RS, 4RS)-4-(4-бензоилоксиметилфенил)-3-нафталин-2-илметокси)пиперидин- 1-карбоновой кислоты в виде бесцветного масла; МС: 552 (M+H)+.
(б) Из трет-бутилового эфира (3RS, 4RS)-4-(4-гидроксиметилфенил)-3-(нафталин-2-илметокси)пиперидин- 1-карбоновой кислоты и 3-метоксибензоилхлорида получили трет-бутиловый эфир (3RS,4RS)-4-[4-(3-метоксибензоилоксиметил)фенил] - 3-нафталин-2-илметоксипиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 582 (M+H)+.
(в) Из трет-бутилового эфира (3RS, 4RS)-4-(4-гидроксиметилфенил)- 3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты и 3,5-диметоксибензоилхлорида получили трет-бутиловый эфир (3RS,4RS)-4-[4-(3, 5-диметоксибензоилоксиметил)фенил]-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 612 (M+H)+.
(г) Из трет-бутилового эфира (3RS, 4RS)-4-(4-гидроксиметилфенил)-3-(нафталин-2-илметокси)пиперидин- 1-карбоновой кислоты и хлорангидрида циклогексанкарбоновой кислоты получили трет-бутиловый эфир (3RS, 4RS)-4-(4-циклогексанкарбонилоксиметилфенил)-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 558 (M+H)+.
(д) Из трет-бутилового эфира (3RS,4RS)-4-(4-гидроксиметилфенил)- 3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты и 2-хлорбензоилхлорида получили трет-бутиловый эфир (3RS, 4RS)-[4-(2-хлорбензоилоксиметил)фенил]-3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 586 (M+H)+.
(е) Из трет-бутилового эфира (3RS, 4RS)-4-(4-гидроксиметилфенил)-3-(нафталин-2-илметокси)пиперидин- 1-карбоновой кислоты и метилового эфира хлормуравьиной кислоты получили трет-бутиловый эфир (3RS, 4RS)-4-(4-метоксикарбонилоксиметилфенил)- 3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла.
(ж) Раствор из 60 мг (0,13 ммоля) трет-бутилового эфира (3RS, 4RS)-4-(4-гидроксиметилфенил)-3-(нафталин-2-илметокси)пиперидин- 1-карбоновой кислоты, 16 мг (0,13 ммоля) изоникотиновой кислоты, 34 мг (0,26 ммоля) этилдиизопропиламина и 58 мг (0,13 ммоля) гексафторфосфата бензотриазол-1-илокситрис(диметиламино)фосфония (БОФ) в 5 мл ацетонитрила перемешивали в течение 2 ч при комнатной температуре. Далее реакционную смесь упаривали при пониженном давлении и остаток без дополнительной переработки хроматографировали на силикагеле с использованием смеси 3:1 гексана и уксусного эфира в качестве элюента. Таким путем получили 15 мг (21% от теории) (3RS,4RS)-4-(1-трет-бутоксикарбонил-3-нафталин-2-илметоксипиперидин-4- ил)бензилового эфира пиридин-4-карбоновой кислоты в виде бесцветного твердого вещества; МС: 552 (M)+.
(з) Аналогично описанной в разделе (ж) методике путем реакции конденсации трет-бутилового эфира (3RS,4RS)-4-(4-гидроксиметилфенил)- 3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты и пиразинкарбоновой кислоты с применением 1,1-карбонилдиимидазола в качестве агента конденсации получили 4-[1-трет-бутоксикарбонил-3-(нафталин-2-илметокси)пиперидин-4-ил] бензиловый эфир (3RS, 4RS)-пиразин-2-карбоновой кислоты; МС: 554 (M+H)+.
Аналогично примеру 22(и)-(л) работали следующим образом.
(и) В результате алкилирования метилового эфира (3RS,4RS)-4-(1-бензил-3-гидроксипиперидин-4-ил)бензойной кислоты 2-бромметил-1-метоксинафталином получили трет-бутиловый эфир (3RS, 4RS)-3-(1-метоксинафталин-2-илметокси)-4-(4- тритилоксиметилфенил)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 720 (M+H)+.
(к) Путем отщепления тритильной группы из трет-бутилового эфира (3RS, 4RS)-3-(1-метоксинафталин-2-илметокси)-4-(4- тритилоксиметилфенил)пиперидин-1-карбоновой кислоты получили трет-бутиловый эфир (3RS, 4RS)-4-(4-гидроксиметилфенил)-3-(1- метоксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 478 (M+H)+.
(л) Ацилированием трет-бутилового эфира (3RS,4RS)-4-(4-гидроксиметилфенил)-3-(1-метоксинафталин-2- илметокси)пиперидин-1-карбоновой кислоты 2-хлорбензоилхлоридом получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(2-хлорбензоилоксиметил)фенил] - 3-(1-метоксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 615 (M+H)+.
(м) Аналогично описанной в разделе (ж) методике путем реакции конденсации трет-бутилового эфира (3RS, 4RS)-4-(4-гидроксиметилфенил)- 3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты и 4-(2-триметилсиланилэтоксиметокси)бензойной кислоты с применением гидрохлорида N-этил-N'-(3-диметиламинопропил)карбодиимида (ЭДК) в качестве агента конденсации получили трет-бутиловый эфир (3RS, 4RS)-3-(нафталин-2-илметокси)-4-{ 4-[4-(2- триметилсиланилэтоксиметокси)бензоилоксиметил] фенил} пиперидин-1-карбоновой кислоты; МС: 715 (M+NH4)+.
4-(2-Триметилсиланилэтоксиметокси)бензойную кислоту получили аналогично примеру 5(а) взаимодействием метилового эфира 4-гидроксибензойной кислоты с 2-(триметилсилил)этоксиметилхлоридом и последующим основным омылением сложного эфира в виде бесцветного твердого вещества.
(н) Раствор из 57 мг (0,13 ммоля) трет-бутилового эфира (3RS, 4RS)-4-(4-гидроксиметилфенил)-3-(нафталин-2-илметокси)пиперидин- 1-карбоновой кислоты, 20 мг (0,14 ммоля) пиридин-2-карбонилазида [H. Saikachi и T. Kitgawa, Chem. Pharm. Bull. 25(7), 1651-1657 (1977)] и 3 мг 4-диметиламинопиридина в 3 мл толуола выдерживали в течение 3 ч при 90oC. Затем толуол выпаривали при пониженном давлении, остаток растворяли в 15 мл метиленхлорида и раствор промывали 5 мл воды. После этого органическую фазу сушили над сульфатом натрия и упаривали при пониженном давлении. К маслянистому остатку добавляли смесь простого эфира и гексана, что приводило к кристаллизации продукта. Таким путем получили 64 мг (88% от теории) трет-бутилового эфира (3RS, 4RS)-3-(нафталин-2-илметокси)-4-[4-(пиридин-2- илкарбамоилоксиметил)фенил] пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 568 (M+H)+.
(о) В трубку Шленка в атмосфере аргона загружали 25,6 мг (0,114 ммоля) Pd(OAc)2, 69,6 мг (0,229 ммоля) три(о-толил)фосфина и 20 мл ДМФ (перегнанного в атмосфере аргона) и реакционную смесь перемешивали в течение 15 мин при комнатной температуре. В 200-миллилитровую колбу для сульфирования в атмосфере аргона и при перемешивании загружали 8,15 г (22,9 ммоля) трет-бутилового эфира (3RS,4RS)-4-(4-бромфенил)-3-гидроксипиперидин-1-карбоновой кислоты [пример 25(в)], 100 мл ДМФ, 3,73 мл (34,3 ммоля) этилового эфира акриловой кислоты, 2,25 г (27,5 ммоля) ацетата натрия и желтого раствора катализатора. Реакционную смесь перемешивали при 120oC в течение 6 ч. С целью обеспечить полноту реакции через 5 ч добавляли раствор 5,1 мг Pd(OAc)2 и 14,3 мг три(о-толил)фосфина в 5 мл ДМФ. Темную реакционную смесь упаривали на ротационном испарителе. Серый твердый остаток растворяли в простом эфире и мутный раствор трижды промывали водой, сушили над сульфатом натрия и упаривали при пониженном давлении. Желтый твердый остаток хроматографировали на 250 г силикагеля с использованием смеси 2:1 гексана и уксусного эфира в качестве элюента. После кристаллизации из уксусного эфира получили 6,66 г (77% от теории) трет-бутилового эфира (3RS, 4RS)-4-[4-(2-этоксикарбонилвинил)фенил] -3-гидроксипиперидин-1- карбоновой кислоты в виде бесцветных кристаллов; МС: 376 (M+H)+.
(п) Алкилированием трет-бутилового эфира (3RS,4RS)-4-[4-(2-этоксикарбонилвинил)фенил] -3-гидроксипиперидин-1- карбоновой кислоты 2-бромметилнафталином аналогично описанному в примере 22(и) способу получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(2-этоксикарбонилвинил)фенил]-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты в виде светло-желтой смолы; МС: 516 (M+H)+.
(р) К раствору из 698 мг (1,35 ммоля) трет-бутилового эфира (3RS,4RS)-4-[4-(2-этоксикарбонилвинил)фенил] -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты в 15 мл толуола при -50oC по каплям добавляли 5 мл (5 ммолей) раствора диизобутилалюминийгидрида (ДИБАГ) (1 М в гексане) и смесь перемешивали при -50oC в течение 30 мин. Далее реакционную смесь при -50oC смешивали с 10 мл этанола, добавляя его по каплям, и нагревали до комнатной температуры. Для дальнейшей переработки реакционную смесь при охлаждении льдом смешивали с 20 мл воды и 20 мл насыщенного раствора калийнатрийтартрата, а затем трижды экстрагировали путем встряхивания уксусным эфиром, используя порции по 50 мл. Органические фазы объединяли, сушили над сульфатом натрия и упаривали при пониженном давлении. Сырой продукт хроматографировали на силикагеле с использованием смеси 6:4 гексана и уксусного эфира в качестве элюента. Таким путем получили 354 мг (55% от теории) трет-бутилового эфира (3RS, 4RS)-4-[4-(3-гидроксипропенил)фенил] -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 474 (M+H)+.
(с) Ацилированием трет-бутилового эфира (3RS,4RS)-4-[4-(3-гидроксипропенил)фенил] -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты бензоилхлоридом аналогично описанному в примере 22(л) способу получили трет-бутиловый эфир (3RS,4RS)-4-[4-(3-бензоилоксипропенил)фенил]-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты в виде бесцветной смолы; МС: 578 (M+H)+.
(т) Раствор из 2,0 г (5,35 ммоля) трет-бутилового эфира (3RS,4RS)-4-[4-(2-этоксикарбонилвинил)фенил]-3-гидроксипиперидин-1- карбоновой кислоты в 100 мл этанола смешивали с 200 мг палладия на угле (тип E101R) и гидрировали при комнатной температуре в течение 1 ч. Далее катализатор отфильтровывали и затем промывали этанолом. Фильтрат упаривали при пониженном давлении и светло-серый остаток (1,97 г) объединяли с остатками, полученными в результате гидрирования трех других смесей (всего 3,08 г). Сырой продукт очищали хроматографией на силикагеле с использованием смеси 2:1 гексана и уксусного эфира в качестве элюента, а затем кристаллизовали из уксусного эфира/гексана. Таким путем получили 2,67 г (87% от теории) трет-бутилового эфира (3RS, 4RS)-4-[4-(2-этоксикарбонилэтил)фенил]-3- гидроксипиперидин-1-карбоновой кислоты в виде бесцветных кристаллов; МС: 378 (M+H)+.
(у) Аналогично описанному в примере 22(и) способу путем алкилирования трет-бутилового эфира (3RS,4RS)-4-[4-(2-этоксикарбонилэтил)фенил]-3-гидроксипиперидин-1- карбоновой кислоты 2-бромметилнафталином получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(2-этоксикарбонилэтил)фенил]-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты; МС: 518 (M+H)+.
(ф) Аналогично описанному в примере 22(д) способу путем восстановления трет-бутилового эфира (3RS, 4RS)-4-[4-(2-этоксикарбонилэтил)фенил] -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты с помощью борогидрида лития получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(3-гидроксипропил)фенил]- 3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 476 (M+H)+.
(х) В результате ацилирования трет-бутилового эфира (3RS,4RS)-4-[4-(3-гидроксипропил)фенил] -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты 2-хлорбензоилхлоридом аналогично описанному в примере 22(л) способу получили трет-бутиловый эфир (3RS,4RS)-4-[4-[3-(2-хлорбензоилокси)пропил] фенил] -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного аморфного твердого вещества; МС: 614,6, 616 (M+H)+.
Пример 25.
(а) Смесь из 1,0 г (2,9 ммоля) (3RS,4RS)-1-бензил-4-(4-бромфенил)пиперидин-3-ола [пример 22(в)], 1,36 мл (10,2 ммоля) 2,2, 2-трихлорэтилового эфира хлормуравьиной кислоты и 0,90 г (12,6 ммоля) карбоната лития в 20 мл толуола в течение 18 ч выдерживали при 105oC. Для дальнейшей переработки охлажденную реакционную смесь сливали на 20 мл ледяной воды, а затем трижды экстрагировали уксусным эфиром порциями по 25 мл. Объединенные органические фазы сушили над сульфатом натрия и упаривали при пониженном давлении. Полученный сырой продукт очищали хроматографией на силикагеле с использованием смеси 2:3 метиленхлорида и гексана в качестве элюента. Таким путем получили 1,3 г (76% от теории) 2,2, 2-трихлорэтилового эфира (3RS,4RS)-4-(4-бромфенил)-3-(2,2,2- трихлорэтоксикарбонилокси)пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; Rf 0,17 (SiO2, метиленхлорид: гексан = 1:1), МС: 622, 624, 626 (M+NH4)+.
(б) Смесь из 1,3 г (2,1 ммоля) 2,2,2-трихлорэтилового эфира (3RS,4RS)-4-(4-бромфенил)-3-(2,2, 2-трихлорэтоксикарбонилокси)пиперидин- 1-карбоновой кислоты и 1,54 г активированного цинка в 20 мл ледяной уксусной кислоты перемешивали в течение 5 ч при комнатной температуре. Для дальнейшей переработки цинк отфильтровывали, остаток промывали ледяной уксусной кислотой и в завершение раствор упаривали досуха при пониженном давлении. Остаток распределяли между 20 мл насыщенного раствора карбоната натрия и 30 мл уксусного эфира, после чего отделенную водную фазу дважды экстрагировали путем встряхивания уксусным эфиром, используя порции по 30 мл. Объединенные органические фазы сушили над сульфатом натрия и упаривали при пониженном давлении. Путем кристаллизации остатка с использованием смеси 1:2 уксусного эфира и гексана получили 250 мг (46% от теории) (3RS, 4RS)-4-(4-бромфенил)пиперидин-3-ола в виде бесцветного твердого вещества; МС: 255, 257 (M)+. Маточный раствор очищали хроматографией на силикагеле с использованием смеси 4: 1 метиленхлорида и метанола в качестве элюента. Таким путем получили дополнительно 101 мг (18% от теории) продукта.
(в) Раствор из 351 мг (1,37 ммоля) (3RS,4RS)-4-(4-бромфенил)пиперидин-3-ола в 12 мл диметилформамида смешивали с 139 мг (1,37 ммоля) триэтиламина и 300 мг (1,37 ммоля) ди-трет-бутилдикарбоната и перемешивали в течение 15 ч при комнатной температуре. Затем диметилформамид отгоняли в вакууме, создаваемом масляным насосом, и остаток кристаллизовали из смеси 1:1 простого эфира и гексана. Таким путем получили 318 мг (65% от теории) трет-бутилового эфира (3RS, 4RS)-4-(4-бромфенил)-3-гидроксипиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 299, 301 (M-C4H8)+. В результате хроматографии маточного раствора на силикагеле с использованием смеси 98:2 метиленхлорида и метанола в качестве элюента дополнительно получили 96 мг (19% от теории) продукта.
(г) Аналогично примеру 22(г) карбонилированием трет-бутилового эфира (3RS, 4RS)-4-(4-бромфенил)-3-гидроксипиперидин-1-карбоновой кислоты с применением PdCl2(CH3CN)2 и 1,3-бис(дифенилфосфин)пропана в качестве катализатора в присутствии триэтиламина под давлением моноксида углерода 10 бар и температуре 100oC в течение 40 ч получили трет-бутиловый эфир (3RS, 4RS)-3-гидрокси-4-(4-метоксикарбонилфенил)пиперидин-1-карбоновой кислоты в виде белых кристаллов; tпл 145,5-146oC, МС: 279 (M-C4H8)+.
(д) Аналогично примеру 22(и) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-(4-метоксикарбонилфенил)пиперидин-1- карбоновой кислоты 2-бромметилнафталином получили трет-бутиловый эфир (3RS,4RS)-4-(4-метоксикарбонилфенил)-3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 476 (M+H)+.
(е) Аналогично примеру 22(м) после отщепления BOC-группы из трет-бутилового эфира (3RS,4RS)-4-(4-метоксикарбонилфенил)-3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты получили гидрохлорид метилового эфира (3RS, 4RS)-4-(3-нафталин-2-илметоксипиперидин-4-ил)бензойной кислоты в виде бесцветного твердого вещества; МС: 344 (M-OCH3)+.
Пример 26.
Аналогично примеру 22(м) путем отщепления BOC-группы получали следующие соединения.
1) из трет-бутилового эфира (3RS, 4RS)-3-(4-бензилоксинафталин-2- илметокси)-4-(3-гидроксиметилфенил)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-[3-[3-(4-бензилоксинафталин-2-илметокси)пиперидин-4- ил]фенил]метанол в виде бесцветного аморфного порошка; МС: 454 (M+H)+;
2) из трет-бутилового эфира (3RS,4RS)-4-(3-бензоилоксиметилфенил)-3- нафталин-2-илметоксипиперидин-1-карбоновой кислоты получили гидрохлорид (3RS, 4RS)-3-(3-нафталин-2-илметоксипиперидин-4-ил)бензилового эфира бензойной кислоты в виде бесцветного твердого вещества; МС: 452 (M+H)+.
Использованные в качестве исходных веществ BOC-производные получали следующим путем:
(а) Аналогично примеру 22(а)-(г) исходя из 3-бромфениллития и 1-бензил-4-пиперидона получили метиловый эфир (3RS,4RS)-3-(1-бензил-3-гидроксипиперидин-4-ил)бензойной кислоты в виде светло-желтой смолы; МС: 325 (M)+.
(б) Аналогично примеру 2(д) путем каталитического гидрирования метилового эфира (3RS,4RS)-3-(1-бензил-3-гидроксипиперидин-4-ил)бензойной кислоты отщепляли бензильную группу. Полученный сырой метиловый эфир (3RS, 4RS)-3-(3-гидроксипиперидин-4-ил)бензойной кислоты без последующей очистки и определения характеристик аналогично примеру 22(ж) подвергали взаимодействию с ди-трет-бутилдикарбонатом с получением трет-бутилового эфира (3RS,4RS)-3-гидрокси-4-(3- метоксикарбонилфенил)пиперидин-1-карбоновой кислоты; МС: 304 (M-OCH3)+.
(в) Аналогично примеру 22(и) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-(3-метоксикарбонилфенил)пиперидин-1-карбоновой кислоты 1-бензилокси-3-хлорметилнафталином получили трет-бутиловый эфир (3RS, 4RS)-3-(4-бензилоксинафталин-2-илметокси)-4-(3- метоксикарбонилфенил)пиперидин-1-карбоновой кислоты в виде светло-желтого аморфного порошка; МС: 582 (M+H)+.
(г) Аналогично примеру 22(д) путем восстановления трет-бутилового эфира (3RS, 4RS)-3-(4-бензилоксинафталин-2-илметокси)- 4-(3-метоксикарбонилфенил)пиперидин-1-карбоновой кислоты с помощью борогидрида лития получили трет-бутиловый эфир (3RS, 4RS)-3-(4-бензилоксинафталин-2-илметокси)-4-(3- гидроксиметилфенил)пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 554 (M+H)+.
(д) Аналогично примеру 22(и) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-(3-метоксикарбонилфенил)пиперидин-1-карбоновой кислоты 2-бромметилнафталином получили трет-бутиловый эфир (3RS,4RS)-4-(3-метоксикарбонилфенил)-3-нафталин-2-илметоксипиперидин- 1-карбоновой кислоты в виде бесцветного масла; МС: 493 (M+NH4)+.
(е) Аналогично примеру 22(д) путем восстановления трет-бутилового эфира (3RS, 4RS)-4-(3-метоксикарбонилфенил)-3-нафталин- 2-илметоксипиперидин-1-карбоновой кислоты с помощью боргидрида лития получили трет-бутиловый эфир (3RS, 4RS)-4-(3-гидроксиметилфенил)- 3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 448 (M+H)+.
(ж) Аналогично примеру 22(л) путем ацилирования трет-бутилового эфира (3RS, 4RS)-4-(3-гидроксиметилфенил)-3-(нафталин-2-илметокси)пиперидин- 1-карбоновой кислоты бензоилхлоридом получили трет-бутиловый эфир (3RS, 4RS)-4-(3-бензоилоксиметилфенил)-3-нафталин-2-илметоксипиперидин- 1-карбоновой кислоты в виде бесцветного масла; МС: 569 (M+NH4)+.
Пример 27.
Аналогично примеру 22(м) путем отщепления BOC-группы получали следующие соединения.
1) из трет-бутилового эфира (3RS, 4RS)-3-(4-бензилоксинафталин-2-илметокси)-4-(3- метоксикарбонилфенил)пиперидин-1-карбоновой кислоты получили метиловый эфир (3RS,4RS)-3-[3-(4-бензилоксинафталин-2- илметокси)пиперидин-4-ил] бензойной кислоты в виде бесцветного аморфного порошка; МС: 482 (M+H)+;
2) из трет-бутилового эфира (3RS,4RS)-4-(3-метоксикарбонилфенил)-3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты получили метиловый эфир (3RS,4RS)-3-[3-(нафталин-2-илметокси)пиперидин-4-ил]бензойной кислоты в виде бесцветного масла; МС: 376 (M+H)+.
Пример 28.
Из 57 мг сырого трет-бутилового эфира (3RS,4RS)-3-(4-бензилоксинафталин-2-илметокси)-4-(3- фторметилфенил)пиперидин-1-карбоновой кислоты аналогично примеру 22 путем отщепления BOC-группы получили (3RS, 4RS)-3-(4-бензилоксинафталин-2-илметокси)-4-(3- фторметилфенил)пиперидин в виде светло-желтой смолы; МС: 456 (M+H)+.
Использованный в качестве исходного вещества трет-бутиловый эфир (3RS, 4RS)-3-(4-бензилоксинафталин-2-илметокси)-4-(3- фторметилфенил)пиперидин-1-карбоновой кислоты получали следующим путем.
Раствор из 18 мг (0,106 ммоля) диэтиламиносератрифторида (ДАСТ) в 1 мл метиленхлорида охлаждали до -65oC, а затем в течение 3 мин при температуре в интервале от -60 до -65oC по каплям добавляли раствор из 56 мг (0,101 ммоля) трет-бутилового эфира (3RS,4RS)-3-(4-бензилоксинафталин-2-илметокси)-4-(3- гидроксиметилфенил)пиперидин-1-карбоновой кислоты в 1 мл метиленхлорида. Образовавшийся желтый раствор нагревали до комнатной температуры, после чего перемешивали в течение 1 ч. Далее смесь распределяли между метиленхлоридом и 5%-ным раствором гидрокарбоната натрия, органическую фазу сушили над сульфатом магния и в завершение удаляли растворитель при пониженном давлении. Таким путем получили 57 мг сырого трет-бутилового эфира (3RS, 4RS)-3-(4-бензилоксинафталин-2-илметокси)-4-(3- фторметилфенил)пиперидин-1-карбоновой кислоты, который без последующей очистки и определения характеристик использовали на следующей стадии.
Пример 29.
(а) Аналогично примеру 22(а) исходя из 1-бензил-4-пиперидона и рац.-2-[2-(4-бромфенил)этокси] тетрагидропирана получили (RS)-1-бензил-4-[4-[2-(тетрагидропиран-2-илокси)этил] фенил] пиперидин-4-ол в виде желтого масла; МС: 396 (M+H)+.
(б) Раствор из 78 г (197 ммолей) (RS)-1-бензил-4-[4-[2-(тетрагидропиран-2-илокси)этил] фенил] пиперидин-4-ола в 400 мл метанола смешивали с 470 мл 2 н. соляной кислоты и перемешивали в течение 5 ч при комнатной температуре. Для дальнейшей переработки реакционный раствор сливали на 1500 мл насыщенного раствора гидрокарбоната натрия, после чего трижды экстрагировали уксусным эфиром порциями по 1000 мл. Объединенные органические фазы сушили над сульфатом натрия и упаривали при пониженном давлении. Сырую субстанцию очищали экспресс-хроматографией на силикагеле с использованием смеси 95: 5 метиленхлорида и метанола в качестве элюента. Таким путем получили 51,6 г (84% от теории) 1-бензил-4-[4-(2-гидроксиэтил)фенил]пиперидин-4-ола в виде желтоватого твердого вещества; МС: 312 (M+H)+.
(в) Аналогично примеру 22(б) реакцией элиминирования из 1-бензил-4-[4-(2-гидроксиэтил)фенил]пиперидин-4-ола с помощью п-толуолсульфокислоты получили 2-[4-(1-бензил-1,2,3, 6-тетрагидропиридин-4-ил)фенил]этанол в виде бесцветного масла; МС: 293 (M)+.
(г) Аналогично примеру 22(в) из 2-[4-(1-бензил-1,2,3,6-тетрагидропиридин-4-ил)фенил] этанола с помощью гидроборирования получили (3RS,4RS)-1-бензил-4-[4-(2-гидроксиэтил)фенил] пиперидин-3-ол в виде бесцветного масла; МС: 311 (M)+.
(д) Аналогично примеру 2(д) и примеру 22(ж) путем каталитического гидрирования (3RS,4RS)-1-бензил-4-[4-(2-гидроксиэтил)фенил]пиперидин-3-ола получили (3RS,4RS)-4-[4-(2-гидроксиэтил)фенил]пиперидин-3-ол, который без последующей очистки и определения характеристик подвергали взаимодействию с ди-трет-бутилдикарбонатом с получением трет-бутилового эфира (3RS,4RS)-3-гидрокси-4-[4-(2-гидроксиэтил)фенил]пиперидин-1-карбоновой кислоты; бесцветное масло, МС: 322 (M+H)+.
(е) Аналогично примеру 22(з) путем введения тритильной группы из трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-[4-(2-гидроксиэтил)фенил] пиперидин-1-карбоновой кислоты получили трет-бутиловый эфир (3RS,4RS)-3-гидрокси-4-[4-(2-тритилоксиэтил)фенил] пиперидин-1-карбоновой кислоты в виде бесцветной пены; МС: 581 (M+NH4)+.
(ж) Аналогично примеру 22(и) путем алкилирования 2-бромметилнафталином из трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-[4-(2-тритилоксиэтил)фенил] пиперидин-1-карбоновой кислоты получили трет-бутиловый эфир (3RS,4RS)-3-(нафталин-2- илметокси)-4-[4-(2-тритилоксиэтил)фенил]пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 721 (M+H)+.
(з) Аналогично примеру 22(к) из трет-бутилового эфира (3RS,4RS)-3-(нафталин-2-илметокси)-4-[4-(2-тритилоксиэтил)фенил] пиперидин- 1-карбоновой кислоты путем отщепления тритильной группы получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(2-гидроксиэтил)фенил] -3-нафталин- 2-илметоксипиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 462 (M+H)+.
(и) Аналогично примеру 22(л) путем ацилирования трет-бутилового эфира (3RS, 4RS)-4-[4-(2-гидроксиэтил)фенил] -3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты хлорангидридом циклопропанкарбоновой кислоты получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(2-циклопропилкарбонилоксиэтил)фенил]-3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 572 (M+H)+.
(к) Аналогично примеру 22(м) путем отщепления BOC-группы с помощью трифторуксусной кислоты в метиленхлориде из трет-бутилового эфира (3RS,4RS)-4-[4-(2-циклопропилкарбонилоксиэтил)фенил] -3-нафталин- 2-илметоксипиперидин-1-карбоновой кислоты получили трифторацетат (3RS,4RS)-2-[4-(3-нафталин-2-илметоксипиперидин-4-ил)фенил] этилового эфира циклопропанкарбоновой кислоты в виде белого твердого вещества; МС: 430(M+H)+.
Пример 30.
Аналогично примеру 23 путем одновременного отщепления BOC-группы и тритильной группы получали следующее соединение:
- из трет-бутилового эфира (3RS,4RS)-3-(нафталин-2-илметокси)- 4-[4-(2-тритилоксиэтил)фенил] пиперидин-1-карбоновой кислоты получили гидрохлорид (3RS, 4RS)-2-{4-[3-(нафталин-2-илметокси)пиперидин-4- ил]фенил}этанола в виде белого порошка; МС: 362 (M+H)+.
Пример 31.
Аналогично примеру 22(м) путем отщепления BOC-группы с помощью кислоты получали следующие соединения:
1) из трет-бутилового эфира (3RS, 4RS)-4-[4-(2-бензоилоксиэтил)фенил]-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты получили гидрохлорид (3RS, 4RS)-2-[4-(3-нафталин-2-илметоксипиперидин-4-ил)фенил] этилового эфира бензойной кислоты в виде белого твердого вещества; МС: 466 (M+H)+;
2) из трет-бутилового эфира (3RS, 4RS)-4-{ 4-[2-(3-метоксибензоилокси)этил] фенил} -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты получили гидрохлорид (3RS, 4RS)-2-[4-(3-нафталин-2-илметоксипиперидин-4-ил)фенил] этилового эфира 3-метоксибензойной кислоты в виде бесцветного масла; МС: 496 (M+H)+;
3) из трет-бутилового эфира (3RS, 4RS)-4-{ 4-[2-(2-метоксибензоилокси)этил] фенил} -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты получили гидрохлорид (3RS, 4RS)-2-[4-(3-нафталин-2-илметоксипиперидин-4-ил)фенил] этилового эфира 2-метоксибензойной кислоты в виде бесцветного твердого вещества; МС: 496 (M+H)+;
4) из трет-бутилового эфира (3RS, 4RS)-4-[4-(2-бензилоксиацетоксиэтил)фенил] -3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты получили гидрохлорид (3RS, 4RS)-2-[4-(3-нафталин-2-илметоксипиперидин-4-ил)фенил] этилового эфира бензилоксиуксусной кислоты в виде бесцветного твердого вещества; МС: 510 (M+H)+;
5) из трет-бутилового эфира (3RS,4RS)-4-[4-[2-[(4-метоксифенил)ацетокси] этил] фенил] -3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты с применением трифторуксусной кислоты в метиленхлориде получили трифторацетат (3RS, 4RS)-2-[4-(3-нафталин-2-илметоксипиперидин-4-ил)фенил]этилового эфира (4-метоксифенил)уксусной кислоты в виде бесцветного твердого вещества; МС: 510 (M+H)+;
6) из трет-бутилового эфира (3RS,4RS)-4-[4-(2-циклогексилкарбонилоксиэтил)фенил] -3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты с применением трифторуксусной кислоты в метиленхлориде получили трифторацетат (3RS, 4RS)-2-[4-(3-нафталин-2-илметоксипиперидин-4-ил)фенил]этилового эфира циклогексанкарбоновой кислоты в виде бесцветного твердого вещества; МС: 472 (M+H)+;
7) из трет-бутилового эфира (3RS, 4RS)-4-{4-[2-(2,6-дихлорбензоилокси)этил] фенил} -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты с применением трифторуксусной кислоты в метиленхлориде получили трифторацетат (3RS, 4RS)-2-[4-(3-нафталин-2-илметоксипиперидин-4-ил)фенил] этилового эфира 2,6-дихлорбензойной кислоты в виде бесцветного твердого вещества; МС: 534 (M+H)+;
8) из трет-бутилового эфира (3RS,4RS)-4-[4-[2-(2,6-диметоксибензоилокси)этил] фенил] -3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты с применением трифторуксусной кислоты в метиленхлориде получили трифторацетат (3RS, 4RS)-2-[4-(3-нафталин-2-илметоксипиперидин-4-ил)фенил] этилового эфира 2,6-диметоксибензойной кислоты в виде бесцветного твердого вещества; МС: 526 (M+H)+;
9) из трет-бутилового эфира (3RS,4RS)-[4-[4-[2-(2-ацетоксибензоилокси)этил] фенил] -3-нафталин-2- илметоксипиперидин] -1-карбоновой кислоты с применением трифторуксусной кислоты в метиленхлориде получили трифторацетат (3RS, 4RS)-2-[4-(3-нафталин-2-илметоксипиперидин-4-ил)фенил] этилового эфира 2-ацетоксибензойной кислоты в виде бесцветного твердого вещества; МС: 524 (M+H)+;
10) из трет-бутилового эфира (3RS,4RS)-[4-[2-(2-хлорбензоилокси)этил] фенил] -3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты с применением трифторуксусной кислоты в метиленхлориде получили трифторацетат (3RS,4RS)-2-[4-(3-нафталин-2-илметоксипиперидин-4- ил)фенил] этилового эфира 2-хлорбензойной кислоты в виде бесцветного твердого вещества; МС: 500 (M+H)+;
11) из трет-бутилового эфира (3RS,4RS)-3-нафталин-2-илметокси-4-[4-(2-пиридин-2- илкарбамоилоксиэтил)фенил]пиперидин-1-карбоновой кислоты получили гидрохлорид (3RS, 4RS)-2-[4-(3-нафталин-2-илметоксипиперидин-4- ил)фенил] этилового эфира пиридин-2-илкарбаминовой кислоты в виде бесцветной пены; МС: 482 (M+H)+;
12) из трет-бутилового эфира (3RS,4RS)-3-нафталин-2-илметокси- 4-[4-(2-фенилкарбамоилоксиэтил)фенил] пиперидин-1-карбоновой кислоты получили гидрохлорид (3RS, 4RS)-2-[4-(3-нафталин-2-илметоксипиперидин- 4-ил)фенил] этилового эфира фенилкарбаминовой кислоты в виде бесцветного твердого вещества; МС: 598 (M+H)+;
13) из трет-бутилового эфира (3RS,4RS)-3-нафталин-2-илметокси- 4-[4-(2-пиридин-3-илкарбонилоксиэтил)фенил] пиперидин-1-карбоновой кислоты получили гидрохлорид (3RS, 4RS)-2-[4-(3-нафталин-2-илметоксипиперидин-4-ил)фенил] этилового эфира пиридин-3-карбоновой кислоты в виде бесцветного твердого вещества; МС: 467 (M+H)+;
14) из 2-{4-[1-трет-бутоксикарбонил-3-(нафталин-2- илметокси)пиперидин-4-ил]фенил)этилового эфира (3RS,4RS)-пиридин-2-карбоновой кислоты получили (3RS, 4RS)-2-[4-(3-нафталин-2-илметоксипиперидин-4-ил)фенил] этиловый эфир пиридин-2-карбоновой кислоты в виде бесцветного масла; МС: 467 (M+H)+;
15) из трет-бутилового эфира (3RS, 4RS)-3-нафталин-2-илметокси-4-[4-(2-тиофен-3- илкарбонилоксиэтил)фенил]пиперидин-1-карбоновой кислоты с применением трифторуксусной кислоты в метиленхлориде получили трифторацетат (3RS, 4RS)-2-[4-(3-нафталин-2-илметоксипиперидин-4-ил)фенил]этилового эфира тиофен-3-карбоновой кислоты в виде бесцветного твердого вещества; МС: 472 (M+H)+;
16) из трет-бутилового эфира (3RS,4RS)-3-нафталин-2-илметокси-4-[4-(2-тиофен-3- илацетоксиэтил)фенил]пиперидин-1-карбоновой кислоты с применением трифторуксусной кислоты в метиленхлориде получили трифторацетат (3RS,4RS)-2-[4-(3-нафталин-2-илметоксипиперидин-4- ил)фенил] этилового эфира тиофен-2-илуксусной кислоты в виде бесцветного твердого вещества; МС: 486 (M+H)+;
17) из трет-бутилового эфира (3RS,4RS)-4-[4-(2-имидазол-2-илкарбонилоксиэтил)фенил] -3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты с применением трифторуксусной кислоты в метиленхлориде получили трифторацетат (3RS, 4RS)-2-[4-(3-нафталин-2-илметоксипиперидин-4-ил)фенил] этилового эфира имидазол-2-карбоновой кислоты в виде бесцветного твердого вещества; МС: 456 (M+H)+;
18) из трет-бутилового эфира (3RS,4RS)-4-[4-(2-бензоилоксиэтил)фенил-3-(4-бензилоксинафталин-2- илметокси)пиперидин-1-карбоновой кислоты получили гидрохлорид (3RS, 4RS)-2-[4-(3-(4-бензилоксинафталин-2-илметокси)пиперидин-4- ил)фенил] этилового эфира бензойной кислоты в виде желтоватого твердого вещества; МС: 572 (M+H)+.
Следующие субстанции получали аналогично описанному в примере 22(л) способу:
(а) из трет-бутилового эфира (3RS,4RS)-4-[4-(2-гидроксиэтил)фенил]-3-нафталин-2-илметоксипиперидин- 1-карбоновой кислоты и бензоилхлорида получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(2-бензоилоксиэтил)фенил] -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 583 (M+NH4)+;
(б) из трет-бутилового эфира (3RS,4RS)-4-[4-(2-гидроксиэтил)фенил]- 3-нафталин-2-илметоксипиперидин-1-карбоновой кислоты и 3-метоксибензоилхлорида получили трет-бутиловый эфир (3RS,4RS)-4-{4-[2-(3-метоксибензоилокси)этил] фенил} -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 593 (M+H)+;
(в) из трет-бутилового эфира (3RS,4RS)-4-[4-(2-гидроксиэтил)фенил]-3-нафталин-2-илметоксипиперидин- 1-карбоновой кислоты и 2-метоксибензоилхлорида получили трет-бутиловый эфир (3RS, 4RS)-4-{4-[2-(2-метоксибензоилокси)этил] фенил} - 3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; Rf 0,35 (SiO2, гексан:уксусный эфир = 2:1);
(г) из трет-бутилового эфира (3RS,4RS)-4-[4-(2-гидроксиэтил)фенил]-3-нафталин-2-илметоксипиперидин- 1-карбоновой кислоты и бензилоксиацетилхлорида получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(2-бензилоксиацетоксиэтил)фенил] -3- нафталин-2-илметоксипиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 627 (M+NH4)+;
(д) из трет-бутилового эфира (3RS,4RS)-4-[4-(2-гидроксиэтил)фенил]- 3-нафталин-2-илметоксипиперидин-1-карбоновой кислоты и 4-метоксифенилацетилхлорида получили трет-бутиловый эфир (3RS, 4RS)-4-[4-[2-[(4-метоксифенил)ацетокси] этил] фенил] -3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 627 (M+NH4)+;
(е) из трет-бутилового эфира (3RS,4RS)-4-[4-(2-гидроксиэтил)фенил]-3-нафталин-2-илметоксипиперидин- 1-карбоновой кислоты и хлорангидрида циклогексанкарбоновой кислоты получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(2-циклогексилкарбонилоксиэтил)фенил] -3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 572 (M+H)+;
(ж) из трет-бутилового эфира (3RS,4RS)-4-[4-(2-гидроксиэтил)фенил]-3-нафталин-2-илметоксипиперидин- 1-карбоновой кислоты и 2,6-дихлорбензоилхлорида получили трет-бутиловый эфир (3RS,4RS)-4-{4-[2-(2,6-дихлорбензоилокси)этил] фенил} - 3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 651 (M+NH4)+;
(з) из трет-бутилового эфира (3RS, 4RS)-4-[4-(2-гидроксиэтил)фенил]- 3-нафталин-2-илметоксипиперидин-1-карбоновой кислоты и 2,6-диметоксибензоилхлорида получили трет-бутиловый эфир (3RS,4RS)-4-[4-[2-(2,6-диметоксибензоилокси)этил] фенил] -3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты в виде бесцветного аморфного твердого вещства; МС: 643 (M+NH4)+;
(и) из трет-бутилового эфира (3RS, 4RS)-4-[4-(2-гидроксиэтил)фенил]-3-нафталин-2-илметоксипиперидин- 1-карбоновой кислоты и хлорангидрида O-ацетилсалициловой кислоты получили трет-бутиловый эфир (3RS, 4RS)-[4-[4-[2-(2-ацетоксибензоилокси)этил] фенил] -3-нафталин-2- илметоксипиперидин]-1-карбоновой кислоты в виде бесцветного масла; МС: 641 (M+NH4)+;
(к) из трет-бутилового эфира (3RS,4RS)-4-[4-(2-гидроксиэтил)фенил]- 3-нафталин-2-илметоксипиперидин-1-карбоновой кислоты и 2-хлорбензоилхлорида получили трет-бутиловый эфир (3RS, 4RS)-4-[4-[2-(2-хлорбензоилокси)этил]фенил] -3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 617 (M+NH4)+.
(л) Аналогично примеру 24(н) взаимодействием трет-бутилового эфира (3RS, 4RS)-4-[4-(2-гидроксиэтил)фенил] -3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты с пиридин-2-карбонилазидом получили трет-бутиловый эфир (3RS, 4RS)-3-нафталин-2-илметокси-4-[4-(2- пиридин-2-илкарбамоилоксиэтил)фенил]пиперидин-1-карбоновой кислоты в виде бесцветных кристаллов; МС: 582 (M+H)+.
(м) Аналогично примеру 24(н) взаимодействием трет-бутилового эфира (3RS, 4RS)-4-[4-(2-гидроксиэтил)фенил] -3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты с фенилизоцианатом получили трет-бутиловый эфир (3RS,4RS)-3-нафталин-2-илметокси-4-[4-(2- фенилкарбамоилоксиэтил)фенил]пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 481(M+H)+.
(н) Аналогично примеру 24(ж) путем реакции конденсации трет-бутилового эфира (3RS, 4RS)-4-[4-(2-гидроксиэтил)фенил]-3-нафталин- 2-илметоксипиперидин-1-карбоновой кислоты и никотиновой кислоты получили трет-бутиловый эфир (3RS, 4RS)-3-нафталин-2-илметокси-4-[4-(2-пиридин-3- илкарбонилоксиэтил)фенил] пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 567 (M+H)+.
(о) Аналогично примеру 24(ж) путем реакции конденсации трет-бутилового эфира (3RS, 4RS)-4-[4-(2-гидроксиэтил)фенил]-3- нафталин-2-илметоксипиперидин-1-карбоновой кислоты и пиридин-2-карбоновой кислоты с применением 1,1-карбонилдиимидазола в качестве агента конденсации получили 2-{4-[1-трет-бутоксикарбонил-3-(нафталин-2-илметокси)пиперидин-4- ил] фенил} этиловый эфир (3RS, 4RS)-пиридин-2-карбоновой кислоты в виде бесцветного масла; МС: 567 (M+H)+.
(п) Аналогично примеру 24(ж) путем реакции конденсации трет-бутилового эфира (3RS, 4RS)-4-[4-(2-гидроксиэтил)фенил]-3- нафталин-2-илметоксипиперидин-1-карбоновой кислоты и тиофен-3-карбоновой кислоты с применением 1,1-карбонилдиимидазола в качестве агента конденсации получили трет-бутиловый эфир (3RS,4RS)-3-нафталин-2-илметокси-4-[4-(2-тиофен-3- илкарбонилоксиэтил)фенил] пиперидин-1-карбоновой кислоты в виде белых кристаллов; МС: 572 (M+H)+.
(р) Аналогично примеру 24(ж) путем реакции конденсации трет-бутилового эфира (3RS, 4RS)-4-[4-(2-гидроксиэтил)фенил]-3- нафталин-2-илметоксипиперидин-1-карбоновой кислоты и тиофенуксусной кислоты с применением 1,1-карбонилдиимидазола в качестве агента конденсации получили трет-бутиловый эфир (3RS, 4RS)-3-нафталин-2-илметокси-4-[4-(2-тиофен-3- илацетоксиэтил)фенил] пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 603 (M+NH4)+.
(с) Аналогично примеру 24(ж) путем реакции конденсации трет-бутилового эфира (3RS, 4RS)-4-[4-(2-гидроксиэтил)фенил]-3- нафталин-2-илметоксипиперидин-1-карбоновой кислоты и имидазол-2-карбоновой кислоты с применением 1,1-карбонилдиимидазола в качестве агента конденсации получили трет-бутиловый эфир (3RS,4RS)-4-[4-(2-имидазол-2-илкарбонилоксиэтил)фенил]-3- нафталин-2-илметоксипиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 556 (M+H)+.
Аналогично примеру 22(и)-(л) работали следующим образом.
(т) Алкилированием трет-бутилового эфира (3RS,4RS)-3-гидрокси-4-[4-(2-тритилоксиэтил)фенил] пиперидин-1-карбоновой кислоты 1-бензилокси-3-хлорметилнафталином получили трет-бутиловый эфир (3RS,4RS)-3-(4-бензилоксинафталин-2-илметокси)-4-[4-(2- тритилоксиэтил)фенил] пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 827 (M+NH4)+.
(у) В результате отщепления тритильной группы из трет-бутилового эфира (3RS, 4RS)-3-(4-бензилоксинафталин-2-илметокси)-4-[4-(2- тритилоксиэтил)фенил] пиперидин-1-карбоновой кислоты получили трет-бутиловый эфир (3RS, 4RS)-3-(4-бензилоксинафталин-2-илметокси)- 4-[4-(2-гидроксиэтил)фенил]пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 568 (M+H)+.
(ф) Путем ацилирования трет-бутилового эфира (3RS,4RS)-3-(4-бензилоксинафталин-2-илметокси)-4-[4-(2- гидроксиэтил)фенил] пиперидин-1-карбоновой кислоты бензоилхлоридом получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(2-бензоилоксиэтил)фенил- 3-(4-бензилоксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 689 (M+NH4)+.
Пример 32.
Аналогично примеру 22(м) путем отщепления BOC-группы с помощью кислоты получали следующие соединения:
1) из трет-бутилового эфира (3RS, 4RS)-3-(нафталин-2-илметокси)- 4-[4-(нафталин-2-илметоксиметил)фенил] пиперидин-1-карбоновой кислоты получили гидрохлорид (3RS, 4RS)-3-нафталин-2-илметокси-4-(4-нафталин-2- илметоксиметилфенил)пиперидина в виде бесцветного твердого вещества; МС: 488 (M+H)+;
2) из трет-бутилового эфира (3RS, 4RS)-4-[4-(4-метоксифеноксиметил)фенил] -3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты получили (3RS,4RS)-4-[4-(4-метоксифеноксиметил)фенил] -3-нафталин-2- илметоксипиперидин в виде желтой пены; МС: 454 (M+H)+;
3) из трет-бутилового эфира (3RS,4RS)-3-(1-метоксинафталин-2- илметокси)-4-[4-(2-феноксиэтил)фенил] пиперидин-1-карбоновой кислоты с применением трифторуксусной кислоты в метиленхлориде получили трифторацетат (3RS,4RS)-3-(1-метоксинафталин-2-илметокси)-4-[4-(2- феноксиэтил)фенил] пиперидина в виде бесцветного масла; МС: 468 (M+H)+;
4) из трет-бутилового эфира (3RS,4RS)-4-[4-(2-метоксиэтил)фенил]- 3-нафталин-2-илметоксипиперидин-1-карбоновой кислоты получили (3RS,4RS)-4-[4-(2-метоксиэтил)фенил] -3-нафталин-2-илметоксипиперидин в виде бесцветного твердого вещества; МС: 376 (M+H)+.
Использованные в качестве исходных субстанций BOC-производные получали следующим путем.
(а) Аналогично примеру 22(и) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-(4-гидроксиметилфенил)пиперидин-1-карбоновой кислоты 2-бромметилнафталином получили трет-бутиловый эфир (3RS,4RS)-3-(нафталин-2-илметокси)-4-[4-(нафталин-2- илметоксиметил)фенил] пиперидин-1-карбоновой кислоты в виде бесцветного масла; Rf 0,31 (SiO2, гексан:уксусный эфир = 2: 1).
(б) Раствор из 200 мг (0,45 ммоля) трет-бутилового эфира (3RS,4RS)-4-(4-гидроксиметилфенил)-3-(нафталин-2-илметокси)пиперидин- 1-карбоновой кислоты в 10 мл тетрагидрофурана последовательно смешивали с 143 мг (0,58 ммоля) трифенилфосфина, 94 мг (0,58 ммоля) диэтилового эфира азодикарбоновой кислоты и 166 мг (1,35 ммоля) гидрохинонмонометилового эфира и реакционную смесь перемешивали в течение 15 ч при комнатной температуре. Для дальнейшей переработки реакционную смесь разбавляли 20 мл метиленхлорида и экстрагировали путем встряхивания 20 мл насыщенного раствора карбоната натрия. Органическую фазу сушили над сульфатом натрия и упаривали при пониженном давлении. Сырой продукт очищали хроматографией на силикагеле с использованием метиленхлорида в качестве элюента. Таким путем получили 245 мг бесцветного масла, которое наряду с трет-бутиловым эфиром (3RS,4RS)-4-[4-(4-метоксифеноксиметил)фенил] -3- нафталин-2-илметоксипиперидин-1-карбоновой кислоты [Rf 0,08 (SiO2, метиленхлорид)] содержало также трет-бутиловый эфир (3RS, 4RS)-4-(4-гидроксиметилфенил)-3-(нафталин-2-илметокси)пиперидин- 1-карбоновой кислоты.
Аналогично примеру 22(и)-(к) работали следующим образом.
(в) Путем алкилирования трет-бутилового эфира (3RS,4RS)-3-гидрокси-4-[4-(2-тритилоксиэтил)фенил] пиперидин-1-карбоновой кислоты 2-бромметил-1-метоксинафталином получили трет-бутиловый эфир (3RS, 4RS)-3-(1-метоксинафталин-2-илметокси)-4-[4-(2- тритилоксиэтил)фенил] пиперидин-1-карбоновой кислоты, из которого после отщепления тритильной группы получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(2-гидроксиэтил)фенил] -3-(1-метоксинафталин-2- илметокси)пиперидин-1-карбоновой кислоты, а после взаимодействия с фенолом аналогично описанному в разделе (б) способу получили трет-бутиловый эфир (3RS, 4RS)-3-(1-метоксинафталин-2-илметокси)- 4-[4-(2-феноксиэтил)фенил]пиперидин-1-карбоновой кислоты в виде бесцветного масла; Rf 0,34 (SiO2, гексан:уксусный эфир = 2:1).
(г) Аналогично примеру 22(и) путем алкилирования трет-бутилового эфира (3RS, 4RS)-4-[4-(2-гидроксиэтил)фенил] -3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты метилиодидом получили трет-бутиловый эфир (3RS,4RS)-4-[4-(2-метоксиэтил)фенил] -3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 493 (M+NH4)+.
Пример 33.
Аналогично примеру 22(м) путем отщепления BOC-группы с помощью кислоты получали следующие соединения:
1) из трет-бутилового эфира (3RS, 4RS)-3-нафталин-2-илметокси- 4-[4-(2-фенилсульфанилэтил)фенил]пиперидин-1-карбоновой кислоты получили гидрохлорид (3RS, 4RS)-3-нафталин-2-илметокси-4-[4-(2- фенилсульфанилэтил)фенил]пиперидина в виде белых кристаллов; МС: 454 (M+H)+;
2) из смеси трет-бутилового эфира (3RS,4RS)-3-нафталин-2-илметокси-4-[4-[(RS)- и -[(SR)-2-фенилсульфинилэтил]фенил]пиперидин-1-карбоновой кислоты получили смесь (3RS,4RS)-3-нафталин-2-илметокси-4-[4-[(RS)- и -[(SR)-2-фенилсульфинилэтил] фенил] пиперидина в виде бесцветного аморфного твердого вещества; МС: 470 (M+H)+;
3) из трет-бутилового эфира (3RS,4RS)-3-нафталин-2-илметокси- 4-[4-(2-фенилсульфонилэтил)фенил]пиперидин-1-карбоновой кислоты получили гидрохлорид (3RS, 4RS)-3-нафталин-2-илметокси-4-[4-(2- фенилсульфонилэтил)фенил]пиперидина в виде белых кристаллов; МС: 486 (M+H)+;
4) из трет-бутилового эфира (3RS, 4RS)-4-[4-(2-бензотиазол-2-илсульфанилэтил)фенил] -3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-[4-(2-бензотиазол-2-илсульфанилэтил)фенил] -3-нафталин-2- илметоксипиперидин в виде бесцветной пены; МС: 511 (M+H)+;
5) из трет-бутилового эфира (3RS, 4RS)-4-[4-(бензотиазол-2- илсульфанилметил)фенил]-3-нафталин-2-илметоксипиперидин-1-карбоновой кислоты получили (3RS,4RS)-2-[4-(3-нафталин-2-илметоксипиперидин-4- ил)бензилсульфанил]бензотиазол в виде желтой пены; МС: 497 (M+H)+;
6) из трет-бутилового эфира (3RS,4RS)-3-нафталин-2-илметокси-4-[4-(1-фенил-1H-тетразол-5- илсульфанилметил)фенил] пиперидин-1-карбоновой кислоты получили гидрохлорид (3RS, 4RS)-3-нафталин-2-илметокси-4-[4-(1-фенил-1H- тетразол-5-илсульфанилметил)фенил] пиперидина в виде бесцветного масла; МС: 508 (M+H)+;
7) из трет-бутилового эфира (3RS,4RS)-3-(нафталин-2-илметокси)- 4-[4-(2-феноксиэтил)фенил] пиперидин-1-карбоновой кислоты получили (3RS,4RS)-3-(нафталин-2-илметокси)-4-[4-(2-феноксиэтил)фенил]пиперидин в виде желтоватой пены; МС: 438 (M+H)+.
Использованные в качестве исходных субстанций BOC-производные получали следующим путем.
(а) Смесь из 200 мг (0,43 ммоля) трет-бутилового эфира (3RS,4RS)-4-[4-(2-гидроксиэтил)фенил] -3-нафталин-2-илметоксипиперидин- 1-карбоновой кислоты, 263 мг (1,29 ммоля) трибутилфосфина и 284 мг (1,29 ммоля) дифенилсульфида в 1 мл пиридина перемешивали при комнатной температуре в течение 18 ч. Далее реакционную смесь упаривали при пониженном давлении и остаток без дальнейшей переработки непосредственно хроматографировали на силикагеле с использованием метиленхлорида в качестве элюента. Таким путем получили трет-бутиловый эфир (3RS, 4RS)-3-нафталин-2-илметокси-4-[4-(2- фенилсульфанилэтил)фенил] пиперидин-1-карбоновой кислоты в виде бесцветного масла с количественным выходом; МС: 554 (M+H)+.
(б) К раствору из 128 мг (0,23 ммоля) трет-бутилового эфира (3RS, 4RS)-3-нафталин-2-илметокси-4-[4-(2-фенилсульфанилэтил)фенил] пиперидин-1-карбоновой кислоты в 10 мл метиленхлорида при комнатной температуре очень медленно по каплям добавляли раствор 216 мг (0,23 ммоля) тетрабутиламмонийоксона. Через 6 ч реакционный раствор упаривали при пониженном давлении и сырой продукт для отделения уже образовавшегося сульфона хроматографировали на силикагеле с использованием смеси 2:1 гексана и уксусного эфира в качестве элюента. Таким путем получили 100 мг (76% от теории) смеси трет-бутилового эфира (3RS, 4RS)-3-нафталин-2-илметокси-4-[4-[(RS)- и -[(SR)-2-фенилсульфинилэтил] фенил] пиперидин-1-карбоновой кислоты в виде бесцветного масла, которое постепенно кристаллизовалось; МС: 570 (M+H)+.
(в) Аналогично описанной в разделе (б) методике исходя из трет-бутилового эфира (3RS, 4RS)-3-нафталин-2-илметокси-4-[4-(2- фенилсульфанилэтил)фенил] пиперидин-1-карбоновой кислоты с применением избытка тетрабутиламмонийоксона получили трет-бутиловый эфир (3RS,4RS)-3-нафталин-2-илметокси-4-[4-(2-фенилсульфонилэтил)фенил] пиперидин-1-карбоновой кислоты в виде бесцветной пены; МС: 603 (M+NH4)+.
(г) Аналогично описанной в разделе (б) методике взаимодействием трет-бутилового эфира (3RS, 4RS)-4-[4-(2-гидроксиэтил)фенил] -3- нафталин-2-илметоксипиперидин-1-карбоновой кислоты с бис(бензотиазол-2-ил)дисульфидом получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(2-бензотиазол-2-илсульфанилэтил)фенил] -3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты в виде желтоватого твердого вещества; МС: 611 (M+H)+.
(д) Аналогично описанной в разделе (б) методике взаимодействием трет-бутилового эфира (3RS, 4RS)-4-(4-гидроксиметилфенил)-3-(нафталин- 2-илметокси)пиперидин-1-карбоновой кислоты с бензотиазол-2-илдисульфидом получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(бензотиазол-2-илсульфанилметил)фенил]-3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты в виде желтоватой пены; МС: 597 (M+H)+.
(е) Аналогично описанной в разделе (б) методике взаимодействием трет-бутилового эфира (3RS, 4RS)-4-(4-гидроксиметилфенил)-3-(нафталин- 2-илметокси)пиперидин-1-карбоновой кислоты с бис(1-фенил-1H-тетразол-5-ил)дисульфидом получили трет-бутиловый эфир (3RS,4RS)-3-нафталин-2-илметокси-4-[4-(1-фенил-1H-тетразол-5- илсульфанилметил)фенил] пиперидин-1-карбоновой кислоты в виде бесцветной пены; МС: 630 (M+Na)+.
(ж) Аналогично примеру 32(б) из трет-бутилового эфира (3RS,4RS)-4-[4-(2-гидроксиэтил)фенил]-3-нафталин-2-илметоксипиперидин- 1-карбоновой кислоты получили трет-бутиловый эфир (3RS, 4RS)-3-(нафталин-2-илметокси)-4-[4-(2-феноксиэтил)фенил] пиперидин- 1-карбоновой кислоты в виде бесцветного масла; МС: 555 (M+NH4)+.
Пример 34.
(а) К раствору из 100 мг (0,22 ммоля) трет-бутилового эфира (3RS,4RS)-4-(4-гидроксиметилфенил)-3-(нафталин-2-илметокси)пиперидин- 1-карбоновой кислоты в 10 мл тетрагидрофурана добавляли 68 мг (0,66 ммоля) триэтиламина, а затем при 0oC по каплям добавляли 25 мг (0,26 ммоля) хлорангидрида метансульфокислоты. Реакционную смесь перемешивали в течение 90 мин при комнатной температуре, после чего добавляли 38 мг (0,33 ммоля) 2-меркаптопиримидина и перемешивание продолжали еще в течение 18 ч при комнатной температуре. Для дальнейшей переработки реакционную смесь упаривали при пониженном давлении, остаток растворяли в 20 мл метиленхлорида, а затем экстрагировали путем встряхивания 10 мл воды. Органическую фазу сушили над сульфатом натрия и в завершение упаривали при пониженном давлении. Сырой продукт очищали хроматографией на силикагеле с использованием смеси 5:1 гексана и уксусного эфира в качестве элюента. Таким путем получили 100 мг (82% от теории) трет-бутилового эфира (3RS, 4RS)-3-нафталин-2-илметокси-4-[4-(пиримидин-2- илсульфанилметил)фенил]пиперидин-1-карбоновой кислоты в виде желтоватого масла; МС: 542 (M+H)+.
(б) Аналогично примеру 22(м) путем отщепления BOC-группы получили (3RS, 4RS)-2-[4-(3-нафталин-2-илметоксипиперидин-4- ил)бензилсульфанил]пиримидин в виде желтой пены; МС: 442 (M+H)+.
Пример 35.
Аналогично примеру 22(м) путем отщепления BOC-группы с помощью кислоты получали следующие соединения:
1) из трет-бутилового эфира (3RS, 4RS)-3-нафталин-2-илметокси- 4-[4-(6-нитробензотиазол-2-илсульфанилметил)фенил] пиперидин-1-карбоновой кислоты получили гидрохлорид (3RS, 4RS)-2-[4-(3-нафталин-2- илметоксипиперидин-4-ил)бензилсульфанил] -6-нитробензотиазола в виде желтоватой пены; МС: 542 (M+H)+;
2) из трет-бутилового эфира (3RS, 4RS)-4-[4-(2-цианэтил)фенил]-3- нафталин-2-илметоксипиперидин-1-карбоновой кислоты с применением трифторуксусной кислоты в метиленхлориде получили трифторацетат (3RS, 4RS)-3-{4-[3-(нафталин-2-илметокси)пиперидин-4-ил] фенил} пропионитрила в виде белого порошка; МС: 371 (M+H)+.
Использованные в качестве исходных веществ BOC-производные получали следующим путем.
(а) Аналогично примеру 34(а) взаимодействием трет-бутилового эфира (3RS, 4RS)-4-(4-гидроксиметилфенил)-3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты с 6-нитро-2-меркаптобензотиазолом через образовавшийся in situ мезилат получили трет-бутиловый эфир (3RS,4RS)-3-нафталин-2-илметокси-4-[4-(6- нитробензотиазол-2-илсульфанилметил)фенил] пиперидин-1-карбоновой кислоты в виде желтого твердого вещества; МС: 642 (M+H)+.
(б) Аналогично примеру 34(а) взаимодействием трет-бутилового эфира (3RS, 4RS)-4-[4-(2-гидроксиэтил)фенил] -3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты с цианидом калия в диметилформамиде через соответствующий мезилат получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(2-цианэтил)фенил]-3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты в виде белого порошка; МС: 471 (M+H)+.
Пример 36.
(а) К раствору из 5,0 г (10,83 ммоля) трет-бутилового эфира (3RS,4RS)-4-[4-(2-гидроксиэтил)фенил] -3-нафталин-2-илметоксипиперидин- 1-карбоновой кислоты в 500 мл бензола добавляли 6,95 г (44 ммоля) измельченного в тонкий порошок перманганата калия, растворенного в смеси из 100 мл воды и 100 мл ледяной уксусной кислоты, а также 0,73 г (2 ммоля) тетрабутиламмонийиодида. Реакционную смесь интенсивно перемешивали в течение 48 ч. Для дальнейшей переработки разделяли фазы. Органическую фазу промывали 100 мл насыщенного раствора тиосульфата натрия. Водную фазу обесцвечивали путем добавления насыщенного раствора тиосульфата натрия, а затем дважды экстрагировали путем встряхивания уксусным эфиром, используя порции по 100 мл, и 100 мл метиленхлорида. Органические фазы объединяли, сушили над сульфатом натрия и упаривали при пониженном давлении. Сырой материал очищали хроматографией на силикагеле с использованием смеси 9:1 метиленхлорида и метанола в качестве элюента, при этом колонку предварительно подготавливали промывкой смеси 90: 10: 0,1 метиленхлорида, метанола и аммиака. Таким путем получили 2,6 г (50% от теории) (3RS, 4RS)-[4-(1-трет-бутоксикарбонил-3-нафталин-2- илметоксипиперидин-4-ил)фенил] уксусной кислоты в виде бесцветного аморфного твердого вещества; МС: 476 (M+H)+.
(б) Раствор из 150 мг (0,32 ммоля) (3RS,4RS)-[4-(1-трет- бутоксикарбонил-3-нафталин-2-илметоксипиперидин-4-ил)фенил] уксусной кислоты и 55 мг (0,32 ммоля) 2-амино-1-фенилэтанона в 5 мл диметилформамида последовательно смешивали с 44,6 мкл (0,32 ммоля) триэтиламина и 96 мг (0,32 ммоля) тетрафторбората O-(1,2-дигидро-2-оксо-1-пиридил)-N,N,N',N'-тетраметилурония (ТПТУ) и перемешивали в течение 18 ч при комнатной температуре. Для дальнейшей переработки реакционную смесь упаривали в вакууме, создаваемом масляным насосом, остаток растворяли в 20 мл метиленхлорида и промывали 5 мл воды. Органическую фазу сушили над сульфатом натрия и упаривали при пониженном давлении. Сырой материал очищали хроматографией на силикагеле с использованием смеси 95: 5 метиленхлорида и метанола в качестве элюента. Таким путем получили 120 мг (64% от теории) трет-бутилового эфира (3RS,4RS)-3-(нафталин-2-илметокси)-4-{ 4-[(2-оксо-2- фенилэтилкарбамоил)метил] фенил} пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 615 (M+Na)+.
(в) Аналогично примеру 22(м) исходя из трет-бутилового эфира (3RS, 4RS)-3-(нафталин-2-илметокси)-4-{ 4-[(2-оксо-2- фенилэтилкарбамоил)метил] фенил} пиперидин-1-карбоновой кислоты путем отщепления BOC-группы с помощью трифторуксусной кислоты в метиленхлориде получили трифторацетат (3RS,4RS)-2-{ 4-[3-(нафталин-2-илметокси)пиперидин-4-ил] фенил} -N-(2- оксо-2-фенилэтил)ацетамида в виде белого порошка; МС: 493 (M+H)+.
Пример 37.
Аналогично примеру 36(б)-(в) получали следующие соединения.
1) Из (3RS,4RS)-[4-(1-трет-бутоксикарбонил-3-нафталин-2- илметоксипиперидин-4-ил)фенил]уксусной кислоты и 3-амино-1-фенилпропан-1-она [H. Zinner и G. Brossmann, J. Prakt. Chem. 5, 91 (1958)] получили трет-бутиловый эфир (3RS, 4RS)-3-(нафталин-2-илметокси)-4-{ 4-[(3-оксо-3- фенилпропилкарбамоил)метил] фенил} пиперидин-1-карбоновой кислоты, МС: 607 (M+H)+, из которого после отщепления BOC-группы получили трифторацетат (3RS, 4RS)-2-[4-[3-(нафталин-2- илметокси)пиперидин-4-ил]фенил]-N-(3-оксо-3-фенилпропил)ацетамида в виде белого порошка; МС: 507 (M+H)+.
2) Из (3RS,4RS)-[4-(1-трет-бутоксикарбонил-3-нафталин-2- илметоксипиперидин-4-ил)фенил]уксусной кислоты и 2-гидрокси-1-фенилэтанона с использованием 1,1-карбонилдиимидазола в качестве агента конденсации получили трет-бутиловый эфир (3RS,4RS)-3-(нафталин-2-илметокси)-4-[4-(2-оксо-2- фенилэтоксикарбонилметил)фенил] пиперидин-1-карбоновой кислоты, из которого после отщепления BOC-группы получили трифторацетат 2-оксо-2-фенилэтилового эфира (3RS, 4RS)-[4-[3-(нафталин-2-илметокси)пиперидин-4-ил] фенил] уксусной кислоты в виде белого порошка; МС: 494 (M+H)+.
3) Из (3RS, 4RS)-[4-(1-трет-бутоксикарбонил-3-нафталин-2- илметоксипиперидин-4-ил)фенил] уксусной кислоты и фенола с использованием 1,1-карбонилдиимидазола в качестве агента конденсации получили трет-бутиловый эфир (3RS,4RS)-3-(нафталин-2-илметокси)-4-(4- феноксикарбонилметилфенил)пиперидин-1-карбоновой кислоты, из которого после отщепления BOC-группы получили трифторацетат фенилового эфира (3RS,4RS)-[4-(3-нафталин-2-илметоксипиперидин-4-ил)фенил] уксусной кислоты в виде белых кристаллов; МС: 452 (M+H)+.
Пример 38.
(а) Раствор из 100 мг (0,21 ммоля) (3RS,4RS)-[4-(1-трет-бутоксикарбонил-3-нафталин-2-илметоксипиперидин-4- ил)фенил] уксусной кислоты в 5 мл диметилформамида смешивали с 50 мг (0,31 ммоля) 1,1-карбонилдиимидазола и перемешивали в течение одного часа при 50oC. Далее смесь охлаждали до комнатной температуры, добавляли раствор 43 мг (0,33 ммоля) бензамидоксима в 2 мл диметилформамида и перемешивали в течение одного часа при 50oC. Для дальнейшей переработки охлаждали до комнатной температуры и диметилформамид отгоняли в вакууме, создаваемом масляным насосом. Остаток хроматографировали на силикагеле с использованием смеси 98:2:0,1 метиленхлорида, метанола и аммиака в качестве элюента. Таким путем получили 90 мг (72% от теории) бензамидоксимового эфира в виде бесцветной пены; МС: 594 (M+Na)+; Rf 0,68 (SiO2, метиленхлорид:метанол:аммиак = 95:5:0,1).
(б) Раствор из 90 мг (0,15 ммоля) бензамидоксимового эфира в 10 мл диметилформамида выдерживали в течение 18 ч при 130oC. Для дальнейшей переработки раствор упаривали при пониженном давлении и остаток хроматографировали на силикагеле с использованием смеси 4:1 гексана и уксусного эфира в качестве элюента. Таким путем получили 63 мг (72% от теории) трет-бутилового эфира (3RS, 4RS)-3-(нафталин-2-илметокси)-4-[4-(3-фенил[1,2,4]оксадиазол-5- илметил)фенил] пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 592 (M+NH4)+.
(в) Аналогично примеру 22(м) исходя из трет-бутилового эфира (3RS, 4RS)-3-(нафталин-2-илметокси)-4-[4-(3-фенил[1,2,4] оксадиазол-5- илметил)фенил]пиперидин-1-карбоновой кислоты путем отщепления BOC-группы с помощью трифторуксусной кислоты в метиленхлориде получили трифторацетат (3RS, 4RS)-3-(3-нафталин-2-илметокси)-4-[4-(3- фенил[1,2,4] оксадиазол-5-илметил)фенил]пиперидина в виде белого порошка; МС: 476 (M+H)+.
Пример 39.
(а) Раствор из 100 мг (0,21 ммоля) (3RS,4RS)-[4-(1-трет- бутоксикарбонил-3-нафталин-2-илметоксипиперидин-4-ил)фенил] уксусной кислоты в 5 мл метиленхлорида смешивали с 1 мл раствора диазометана в простом эфире, а затем перемешивали в течение 2 ч при комнатной температуре. Реакционную смесь упаривали при пониженном давлении и полученный таким путем с количественным выходом трет-бутиловый эфир (3RS,4RS)-4-(4-метоксикарбонилметилфенил)-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты [Rf 0,5 (SiO2 , гексан: уксусный эфир = 2:1)] без последующей очистки и определения характеристик использовали на следующей стадии.
(б) Раствор из 102 мг (0,21 ммоля) трет-бутилового эфира (3RS, 4RS)-4-(4-метоксикарбонилметилфенил)-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты в 0,5 мл гидразингидрата выдерживали при 120oC в течение 18 ч. Для дальнейшей переработки реакционную смесь охлаждали до комнатной температуры, смешивали с 3 мл ледяной воды и дважды экстрагировали метиленхлоридом порциями по 5 мл. Объединенные органические фазы сушили над сульфатом натрия и упаривали при пониженном давлении. Таким путем получили 63 мг (63% от теории) трет-бутилового эфира (3RS,4RS)-4-(4-гидразинкарбонилметилфенил)- 3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветной пены; Rf 0,22 (SiO2, метиленхлорид:метанол:аммиак = 95:5:0,1).
(в) Смесь из 60 мг (0,12 ммоля) трет-бутилового эфира (3RS, 4RS)-4-(4-гидразинкарбонилметилфенил)-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты и 27,7 мкл (0,12 ммоля) триэтилортобензоата в 5 мл этанола кипятили с обратным холодильником в течение 18 ч. После охлаждения смесь упаривали при пониженном давлении и остаток хроматографировали на силикагеле с использованием смеси 2:1 гексана и уксусного эфира в качестве элюента. Таким путем получили 30 мг (44% от теории) трет-бутилового эфира (3RS,4RS)-3-(нафталин-2-илметокси)-4-[4-(5-фенил[1,3,4] оксадиазол-2- илметил)фенил]пиперидин-1-карбоновой кислоты в виде бесцветной пены; МС: 575 (M+Na)+.
(г) Аналогично примеру 22(м) исходя из трет-бутилового эфира (3RS, 4RS)-3-(нафталин-2-илметокси)-4-[4-(5-фенил[1,3,4] оксадиазол-2- илметил)фенил]пиперидин-1-карбоновой кислоты путем отщепления BOC-группы с помощью трифторуксусной кислоты в метиленхлориде получили трифторацетат (3RS, 4RS)-3-нафталин-2-илметокси-4-[4-(5- фенил[1,3,4]оксадиазол-2-илметил)фенил] пиперидина в виде белого порошка; МС: 476 (M+H)+.
Пример 40.
(а) К раствору из 80 мг (0,17 ммоля) трет-бутилового эфира (3RS,4RS)-4-[4-(2-цианэтил)фенил] -3-нафталин-2-илметоксипиперидин-1- карбоновой кислоты (пример 35) в 10 мл толуола с помощью шприца добавляли 70 мг (0,51 ммоля) фенилмагнийхлорида. Реакционную смесь кипятили с обратным холодильником в течение 3 ч, после чего охлаждали до комнатной температуры и гидролизовали 4 мл 1 н. соляной кислоты. Далее смесь перемешивали в течение 1 ч при 80oC, затем охлаждали до комнатной температуры и дважды экстрагировали уксусным эфиром. Объединенные органические фазы сушили над сульфатом натрия и упаривали при пониженном давлении. Остаток хроматографировали на силикагеле с использованием смеси 90:10:0,1 метиленхлорида, метанола и аммиака в качестве элюента. Полученную смесь из (3RS,4RS)-3-[4-(3-нафталин-2-илметоксипиперидин-4-ил)фенил] -1- фенилпропан-1-она и (3RS, 4RS)-3-{4-[3-(нафталин-2-илметокси)пиперидин- 4-ил] фенил} пропионовой кислоты аналогично примеру 1(е) переводили в соответствующее BOC-производное и затем хроматографировали на силикагеле с использованием смеси 2:1 гексана и уксусного эфира в качестве элюента. Таким путем получили 13 мг (14% от теории) трет-бутилового эфира (3RS, 4RS)-3-(нафталин-2-илметокси)-4-[4-(3-оксо- 3-фенилпропил)фенил]пиперидин-1-карбоновой кислоты в виде бесцветной пены; Rf 0,38 (гексан:уксусный эфир = 2:1).
(б) Аналогично примеру 22(м) исходя из трет-бутилового эфира (3RS, 4RS)-3-(нафталин-2-илметокси)-4-[4-(3-оксо-3- фенилпропил)фенил]пиперидин-1-карбоновой кислоты путем отщепления BOC-группы с помощью трифторуксусной кислоты в метиленхлориде получили трифторацетат (3RS,4RS)-3-[4-(3-нафталин-2-илметоксипиперидин- 4-ил)фенил] -1-фенилпропан-1-она в виде белого порошка; МС: 450 (M+H)+.
Пример 41.
(а) Раствор из 60 мг (0,13 ммоля) трет-бутилового эфира (3RS,4RS)-4-(3-метоксикарбонилфенил)-3-нафталин-2-илметоксипиперидин- 1-карбоновой кислоты [пример 26(е)] и 0,26 мл (0,26 ммоля) 1 н. едкого натра в 2 мл метанола перемешивали в течение 18 ч при 30oC. Для дальнейшей переработки реакционную смесь нейтрализовали 1 н. соляной кислотой и дважды экстрагировали путем встряхивания метиленхлоридом, используя порции по 10 мл. Органические фазы объединяли, сушили над сульфатом натрия и упаривали при пониженном давлении. Остаток кристаллизовали из смеси гексана и диэтилового эфира. Таким путем получили 45 мг (75% от теории) (3RS,4RS)-3-(1-трет-бутоксикарбонил-3- нафталин-2-илметоксипиперидин-4-ил)бензойной кислоты в виде бесцветных кристаллов; МС: 462 (M+H)+.
(б) Аналогично примеру 36(б) из (3RS,4RS)-3-(1-трет-бутоксикарбонил-3-нафталин-2- илметоксипиперидин-4-ил)бензойной кислоты реакцией конденсации с бензиламином с применением 1,1-карбонилдиимидазола в качестве агента конденсации получили трет-бутиловый эфир (3RS, 4RS)-4-(3-бензилкарбамоилфенил)-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 551 (M+H)+.
(в) Аналогично примеру 22(м) путем отщепления BOC-группы из трет-бутилового эфира (3RS, 4RS)-4-(3-бензилкарбамоилфенил)- 3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты получили гидрохлорид (3RS,4RS)-N-бензил-3-(3-нафталин-2-илметоксипиперидин-4- ил)бензамида в виде белого порошка; МС: 451 (M+H)+.
Пример 42.
Аналогично примеру 22(м) путем отщепления BOC-группы с применением трифторуксусной кислоты в метиленхлориде получали следующие соединения:
1) из трет-бутилового эфира (3RS,4RS)-4-(4-бензилкарбамоилфенил)- 3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-N-бензил-4-[3-(нафталин-2-илметокси)пиперидин-4-ил] бензамид в виде белого порошка; МС: 453 (M+H)+;
2) из трет-бутилового эфира (3RS, 4RS)-3-(нафталин-2-илметокси)-4-[4-(3-оксо-3- фенилпропилкарбамоил)фенил] пиперидин-1-карбоновой кислоты получили трифторацетат (3RS, 4RS)-4-[3-(нафталин-2-илметокси)пиперидин-4- ил]-N-(3-оксо-3-фенилпропил)бензамида в виде белого порошка; МС: 493 (M+H)+;
3) из трет-бутилового эфира (3RS, 4RS)-3-(нaфтaлин-2-илметокси)-4-[4-(2-оксо-2- фенилэтилкарбамоил)фенил]пиперидин-1-карбоновой кислоты получили трифторацетат (3RS, 4RS)-4-[3-(нафталин-2-илметокси)пиперидин-4-ил]- N-(2-оксо-2-фенилэтил)бензамида в виде белого порошка; МС: 479 (M+H)+.
Использованные в качестве исходных веществ BOC-производные получали следующим путем.
(а) Аналогично примеру 41(б) путем щелочного омыления трет-бутилового эфира (3RS, 4RS)-4-(4-метоксикарбонилфенил)-3- нафталин-2-илметоксипиперидин-1-карбоновой кислоты получили (3RS,4RS)-4-(1-трет-бутоксикарбонил-3-нафталин-2- илметоксипиперидин-4-ил)безойную кислоту в виде бесцветного твердого вещества; МС: 461 (M)+.
(б) Аналогично примеру 36(б) из (3RS,4RS)-4-(1-трет-бутоксикарбонил-3-нафталин-2-илметоксипиперидин-4- ил)бензойной кислоты реакцией конденсации с бензиламином получили трет-бутиловый эфир (3RS,4RS)-4-(4-бензилкарбамоилфенил)-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты в виде бесцветной пены; МС: 551 (M+H)+.
(в) Аналогично примеру 36(б) из (3RS,4RS)-4-(1-трет-бутоксикарбонил-3-нафталин-2-илметоксипиперидин-4- ил)бензойной кислоты реакцией конденсации с 3-амино-1-фенилпропан-1-оном получили трет-бутиловый эфир (3RS, 4RS)-3-(нафталин-2-илметокси)-4-[4-(3-оксо-3- фенилпропилкарбамоил)фенил]пиперидин-1-карбоновой кислоты в виде бесцветной пены; МС: 593 (M+H)+.
(г) Аналогично примеру 36(б) из (3RS,4RS)-4-(1-трет-бутоксикарбонил-3-нафталин-2-илметоксипиперидин-4- ил)бензойной кислоты реакцией конденсации с 2-амино-1-фенилэтаноном получили трет-бутиловый эфир (3RS,4RS)-3-(нафталин-2-илметокси)-4-[4-(2- оксо-2-фенилэтилкарбамоил)фенил]пиперидин-1-карбоновой кислоты в виде бесцветной пены; МС: 579 (M+H)+.
Пример 43.
(а) Раствор из 1,0 г (3 ммоля) трет-бутилового эфира (3RS,4RS)-3-гидрокси-4-(4-метоксикарбонилфенил)пиперидин-1-карбоновой кислоты в 100 мл метанола смешивали с 100 мг родия (5%-ного) на оксиде алюминия и гидрировали в течение 5 ч при 50oC под давлением водорода 10 бар. После этого реакционную смесь фильтровали через 30 г дикалита, фильтровальное вспомогательное вещество затем промывали 200 мл метанола и полученный раствор упаривали при пониженном давлении. Таким путем с количественным выходом получили смесь 2:1 или 1: 2 трет-бутилового эфира (3RS,4RS)-3-гидрокси-4-(транс- и -(цис-4-метоксикарбонилциклогексил)пиперидин-4-карбоновой кислоты в виде бесцветного твердого вещества; МС: 342 (M+H)+.
Аналогично примеру 22(д) и (з)-(м) работали следующим образом.
(б) Путем восстановления с помощью борогидрида лития из смеси 2:1 или 1: 2 трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-(транс- и -(цис-4-метоксикарбонилциклогексил)пиперидин-4-карбоновой кислоты получили смесь 2:1 или 1: 2 трет-бутилового эфира (3RS,4RS)-цис- и -транс-3-гидрокси-4-(4-гидроксиметилциклогексил)пиперидин-1-карбоновой кислоты в виде бесцветной пены; МС: 314 (M+H)+.
(в) Введением тритильной группы из смеси 2:1 или 1:2 трет-бутилового эфира (3RS,4RS)-цис- и -транс-3-гидрокси-4-(4-гидроксиметилциклогексил)пиперидин-1-карбоновой кислоты получили смесь 2:1 или 1:2 трет-бутилового эфира (3RS,4RS)-цис- и -транс-3-гидрокси-4-(4-тритилоксиметилциклогексил) пиперидин-1-карбоновой кислоты в виде бесцветной пены; МС: 573 (M+H)+.
(г) В результате алкилирования 2-бромметилнафталином исходя из смеси 2:1 или 1: 2 трет-бутилового эфира (3RS,4RS)-цис- и -транс-3-гидрокси-4-(4-тритилоксиметилциклогексил)пиперидин-1-карбоновой кислоты получили смесь 2:1 или 1: 2 трет-бутилового эфира (3RS,4RS)-цис- и -транс-3-нафталин-2-илметокси-4-(4- тритилоксиметилциклогексил)пиперидин-1-карбоновой кислоты в виде бесцветной пены; МС: 713 (M+H)+.
(д) Из смеси 2: 1 или 1:2 трет-бутилового эфира (3RS,4RS)-цис- и -транс-3-нафталин-2-илметокси-4-(4-тритилоксиметилциклогексил)пиперидин- 1-карбоновой кислоты путем отщепления тритильной группы с помощью хлористого водорода в метаноле получили смесь 2:1 или 1:2 трет-бутилового эфира (3RS, 4RS)-цис- и -транс-3-нафталин-2-илметокси-4-(4-гидроксиметилциклогексил)пиперидин- 1-карбоновой кислоты в виде бесцветной пены; МС: 453 (M+H)+.
(е) Путем ацилирования смеси 2:1 или 1:2 трет-бутилового эфира (3RS, 4RS)-цис- и -транс-3-нафталин-2-илметокси-4-(4- гидроксиметилциклогексил)пиперидин-1-карбоновой кислоты бензоилхлоридом получили смесь 2:1 или 1: 2 трет-бутилового эфира (3RS,4RS)-цис- и -транс-4-(4-бензоилоксиметилциклогексил)-3- нафталин-2-илметоксипиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 558 (M+H)+.
(ж) Путем отщепления BOC-группы с помощью хлористого водорода в метаноле из смеси 2:1 или 1:2 трет-бутилового эфира (3RS,4RS)-цис- и -транс-4-(4-бензоилоксиметилциклогексил)-3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты получили смесь 2:1 или 1:2 (3RS,4RS)-цис- и -транс-4-(3-нафталин-2-илметоксипиперидин-4- ил)циклогексилметилового эфира бензойной кислоты в виде бесцветной пены; МС: 458 (M+H)+.
Пример 44.
Аналогично примеру 22(а)-(в) работали следующим образом.
(а) Из 1-бензилпиперидона и 4-иоданизола получили 1-бензил-4-(4-метоксифенил)пиперидин-4-ол в виде бесцветного твердого вещества; МС: 298 (M+H)+.
(б) Из 1-бензил-4-(4-метоксифенил)пиперидин-4-ола путем элиминирования получили 1-бензил-4-(4-метоксифенил)-1,2,3,6-тетрагидропиридин в виде бежевого твердого вещества; МС: 280 (M+H)+.
(в) Гидроборированием 1-бензил-4-(4-метоксифенил)-1,2,3, 6-тетрагидропиридина получили (3RS,4RS)-1-бензил-4-(4-метоксифенил)пиперидин-3-ол в виде бесцветных кристаллов; МС: 297 (M)+.
(г) К раствору из 7,38 г (24,82 ммоля) (3RS, 4RS)-1-бензил-4-(4-метоксифенил)пиперидин-3-ола в 248 мл метиленхлорида в течение 10 мин при 3-7oC по каплям добавляли 49,6 мл (49,6 ммоля, 2 экв.) примерно 1 М раствора трибромида бора в метиленхлориде. Эту суспензию перемешивали в течение 3 ч при комнатной температуре. Далее реакционную смесь сливали на 750 мл смеси льда/воды, с помощью 2 н. едкого натра значение pH устанавливали на 8 и трижды экстрагировали метиленхлоридом порциями по 500 мл. Органические фазы промывали небольшим количеством воды, сушили над сульфатом магния, упаривали при пониженном давлении и сушили в высоком вакууме. Таким путем получили 6,42 г (3RS, 4RS)-1-бензил-4-(4-гидроксифенил)пиперидин-3-ола в виде белой пены; МС: 283 (M)+.
(д) Раствор из 3,0 г (10,6 ммоля) (3RS, 4RS)-1-бензил-4-(4-гидроксифенил)пиперидин-3-ола в 75 мл этилметилкетона последовательно смешивали с 10,84 г (42,4 ммоля, 4,8 экв.) рац.-2-(2-иодэтокси)тетрагидропирана и 5,25 г (53 ммоля, 5 экв.) карбоната калия. Эту смесь перемешивали в течение 25 ч при 95oC. Далее смесь концентрировали до объема в несколько миллилитров, сливали на 200 мл смеси льда/воды и трижды экстрагировали метиленхлоридом порциями по 300 мл. Объединенные органические фазы один раз промывали небольшим количеством воды, сушили над сульфатом магния, упаривали при пониженном давлении и сушили в высоком вакууме. Полученный таким путем сырой продукт (11,81 г) разделяли на силикагеле с использованием смеси 99:1 метиленхлорида и метанола в качестве элюента с получением в результате 3,2 г (73% от теории) смеси (3RS,4RS)-1-бензил-4-[4-[2-[(RS)- и -[(SR)-тетрагидропиран-2-илокси] этокси] фенил]пиперидин-3-ола в виде бесцветного масла; Rf 0,55 (SiO2, метиленхлорид:метанол = 9:1).
(е) Аналогично примеру 22(и) путем алкилирования смеси (3RS,4RS)-1-бензил-4-[4-[2-[(RS)- и -[(SR)-тетрагидропиран-2-илокси] этокси]фенил]пиперидин-3-ола 2-бромметилнафталином получили смесь (3RS, 4RS)-1-бензил-3-(нафталин-2-илметокси)-4-[4-[2-[(RS)- и -[(SR)-тетрагидропиран-2-илокси] этокси]фенил]пиперидина в виде бесцветного масла; Rf 0,46 (SiO2, метиленхлорид:уксусный эфир = 1:1).
(ж) Аналогично примеру 25(а) путем отщепления бензильной группы с помощью 2,2,2-трихлорэтилового эфира хлормуравьиной кислоты и карбоната калия получили смесь 2,2,2-трихлорэтилового эфира (3RS,4RS)-3-(нафталин-2-илметокси)-4-[4-[2-[(RS)- и -[(SR)-тетрагидропиран-2-илокси]этокси]фенил]пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 653,3, 655 (M+H)+.
(з) Раствор из 500 мг (0,785 ммоля) смеси 2,2,2-трихлорэтилового эфира (3RS, 4RS)-3-(нафталин-2-илметокси)-4-[4-[2-[(RS)- и -[(SR)-тетрагидропиран-2-илокси] этокси] фенил] пиперидин-1-карбоновой кислоты в 10 мл метанола смешивали с 1 мл воды и 1,120 г (5,888 ммоля) моногидрата п-толуолсульфокислоты. Эту суспензию перемешивали в течение 1,5 ч при комнатной температуре, затем концентрировали при пониженном давлении до половины объема и четырежды экстрагировали метиленхлоридом в противотоке воды. Органические фазы по одному разу промывали насыщенным раствором гидрокарбоната натрия и насыщенным раствором хлорида натрия, сушили над сульфатом магния, упаривали при пониженном давлении и сушили в высоком вакууме. Сырой продукт (465 мг) разделяли на силикагеле с использованием смеси 9:1 метиленхлорида и метанола в качестве элюента. Таким путем получили 344 мг (79% от теории) 2,2,2-трихлорэтилового эфира (3RS, 4RS)-4-[4-(2-гидроксиэтокси] фенил] - 3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного аморфного порошка; МС: 569,3, 571 (M+NH4)+.
(и) Аналогично примеру 24(н) из 2,2,2-трихлорэтилового эфира (3RS, 4RS)-4-[4-(2-гидроксиэтокси] фенил] -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты и пиридин-2-карбонилазида получили 2,2,2-трихлорэтиловый эфир (3RS,4RS)-3-(нафталин-2-илметокси)-4-[4-(2-пиридин-2- илкарбамоилоксиэтокси)фенил] пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 672,2, 674 (M+H)+.
(к) Аналогично примеру 25(6) путем обработки 2,2,2-трихлорэтилового эфира (3RS, 4RS)-3-(нафталин-2-илметокси)- 4-[4-(2-пиридин-2-илкарбамоилоксиэтокси)фенил]пиперидин-1-карбоновой кислоты цинком в ледяной уксусной кислоте получили (3RS, 4RS)-2-[4-[3-(нафталин-2-илметокси)пиперидин-4-ил] фенокси] этиловый эфир пиридин-2-илкарбаминовой кислоты в виде бесцветного твердого вещества; МС: 498 (M+H)+.
Пример 45.
Аналогично примеру 25(б) получали следующие соединения:
1) из 2,2,2-трихлорэтилового эфира (3RS,4RS)-4-[4-(2-карбамоилоксиэтокси)фенил] -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты получили (3RS,4RS)-2-[4-[3-(нафталин-2-илметокси)пиперидин-4-ил]фенокси]этиловый эфир карбаминовой кислоты в виде бесцветного масла; МС: 421 (M+H)+;
2) из 2,2,2-трихлорэтилового эфира (3RS,4RS)-4-[4-[2-(морфолин-4-илкарбонилокси)этокси] фенил] -3-(нафталин- 2-илметокси)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-2-[4-[3-(нафталин-2-илметокси)пиперидин-4-ил] фенокси] этиловый эфир морфолин-4-карбоновой кислоты в виде бесцветного масла; МС: 491 (M+H)+;
3) из 2,2, 2-трихлорэтилового эфира (3RS, 4RS)-4-(4-метоксифенил)-3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты получили (3RS,4RS)-4-(4-метоксифенил)-3 -(нафталин-2-илметокси)пиперидин в виде бесцветного масла; МС: 348 (M+H)+;
4) из смеси 2,2,2-трихлорэтилового эфира (3RS,4RS)-3-(нафталин-2-илметокси)-4-[4-[2-[(RS)- и -[(SR)-тетрагидропиран-2-илокси]этокси]фенил]пиперидин-1-карбоновой кислоты с одновременным отщеплением ТГП-группы получили (3RS,4RS)-2-[4-[3-(нафталин-2-илметокси)пиперидин-4-ил]фенокси]этанол в виде бесцветного аморфного твердого вещества; МС: 378 (M+H)+.
Использованные в качестве исходных веществ производные получали следующим образом.
(а) Аналогично примеру 24(н) из 2,2,2-трихлорэтилового эфира (3RS, 4RS)-4-[4-(2-гидроксиэтокси)фенил] -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты и изоцианата натрия получили 2,2,2-трихлорэтиловый эфир (3RS, 4RS)-4-[4-(2-карбамоилоксиэтокси)фенил] - 3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; Rf 0,28 (SiO2, метиленхлорид:ацетон = 1:1).
(б) Раствор из 250 мг (0,56 ммоля) 2,2,2-трихлорэтилового эфира (3RS, 4RS)-4-[4-(2-гидроксиэтокси)фенил] -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты в 20 мл толуола последовательно смешивали с 250 мл (2,8 ммоля, 5,0 экв.) морфолин-4-карбонилхлорида, 375 мг (3,08 ммоля, 5,5 экв.) 4-диметиламинопиридина и 20 мкл (0,075 ммоля, 0,13 экв.) диацетата дибутилолова. Эту смесь кипятили с обратным холодильником в течение 64 ч. В ходе протекания реакции дополнительно добавляли 125 мл (1,40 ммоля, 5,0 экв.) морфолин-4-карбонилхлорида и 188 мг (1,56 ммоля, 2,3 экв.) 4-диметиламинопиридина и кипячение с обратным холодильником продолжали в течение 24 ч. Далее охлажденную до комнатной температуры реакционную смесь сливали на 100 мл смеси льда/воды, перемешивали в течение 5 мин и трижды экстрагировали метиленхлоридом. Органические фазы по одному разу промывали водой и насыщенным раствором хлорида натрия, сушили над сульфатом магния, упаривали при пониженном давлении и сушили в высоком вакууме. Сырой продукт (546 мг) разделяли на силикагеле с использованием смеси 9:1 гексана и ацетона в качестве элюента. Таким путем получили 42 мг (14% от теории) 2,2, 2-трихлорэтилового эфира (3RS, 4RS)-4-[4-[2-(морфолин-4-илкарбонилокси)этокси]фенил]- 3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 665,3, 667 (M+H)+ .
(в) Аналогично примеру 12(б) путем алкилирования (3RS,4RS)-1-бензил-4-(4-метоксифенил)пиперидин-3-ола [пример 44(в)] 2-бромметилнафталином получили (3RS, 4RS)-1-бензил-4-(4-метоксифенил)-3-(нафталин-2-илметокси)пиперидин в виде окрашенного в бежевый цвет твердого вещества; МС: 437 (M)+. Последующим взаимодействием с 2,2,2-трихлорэтиловым эфиром хлормуравьиной кислоты получили 2,2,2-трихлорэтиловый эфир (3RS, 4RS)-4-(4-метоксифенил)-3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде желтоватого масла; МС: 539, 541 (M+NH4)+.
Пример 46.
(а) Аналогично примеру 2(д) путем сопровождаемого гидрогенолизом отщепления бензильной группы из (3RS, 4RS)-1-бензил-4-(4-гидроксифенил)пиперидин-3-ола [пример 44(г)] получили (3RS, 4RS)-4-(4-гидроксифенил)пиперидин-3-ол в виде бесцветного твердого вещества; МС: 194 (M+H)+.
(б) Аналогично примеру 22(ж) из (3RS,4RS)-4-(4-гидроксифенил)пиперидин-3-ола путем введения BOC-группы получили трет-бутиловый эфир (3RS, 4RS)-3-гидрокси-4-(4-гидроксифенил)пиперидин-1-карбоновой кислоты в виде бесцветной пены; МС: 237 (M-C4H8)+.
(в) Смесь 4,5 г (15,3 ммоля) трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-(4-гидроксифенил)пиперидин-1-карбоновой кислоты, 20,8 г (91,8 ммоля, 6,0 экв. ) 2-(3-хлорпропил)-2-фенил[1,3] диоксолана [J. Med. Chem. 34, 12 (1991)] , 14,6 г (105,5 ммоля, 6,9 экв.) карбоната калия и 2,0 г (0,012 ммоля, 0,078 экв. ) иодида калия перемешивали при температуре бани 100oC в течение 60 ч в закрытом, рассчитанном на работу под давлением сосуде. Реакционную смесь сливали на смесь льда/воды и трижды экстрагировали уксусным эфиром. Органические фазы по одному разу промывали водой и насыщенным раствором хлорида натрия, сушили над сульфатом магния, концентрировали при пониженном давлении и сушили в высоком вакууме. Желтое масло (25,72 г) разделяли на силикагеле с использованием
изменяющегося от 4 : 1 до 1 : 1 градиента смеси гексана и уксусного эфира в качестве элюента. Таким путем получили 5,34 г (72% от теории) третбутилового эфира (3RS, 4RS)-3-гидрокси-4-[4-[3-(2-фенил-[1,3]диоксолан-2-ил)пропокси] фенил]пиперидин-1-карбоновой кислоты в виде белых кристаллов; МС: 484 (М + Н)+.
(г) Аналогично примеру 22(и) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-[4-[3-(2-фенил-[1,3] диоксолан-2-ил)пропокси]фенил] пиперидин-1-карбоновой кислоты 2-бромметилнафталином получили трет-бутиловый эфир (3RS, 4RS)-3-(нафталин-2-илметокси)-4-[4-3-(2-фенил-[1,3]диоксолан-2-ил)пропокси]фенил]пиперидин-1-карбоновой кислоты в виде белых кристаллов; МС: 624 (М + Н)+.
(д) Раствор из 193 мг (0,31 ммоля) в 3 мл тетрагидрофурана и 3 мл 2н. соляной кислоты перемешивали в течение 12 ч при комнатной температуре и в течение 24 ч при 50oC. Далее реакционную смесь сливали на смесь 1 : 1 воды и насыщенного раствора гидрокарбоната натрия и трижды экстрагировали уксусным эфиром. Бесцветное масло (165 мг) разделяли на силикагеле с использованием смеси 9 : 1 метиленхлорида и метанола (экстр. в противотоке 5 об.% конц. NH4OH. Таким путем получили 127,4 мг (82% от теории) (3RS, 4RS)-4-[4-(3-нафталин-2-илметоксипиперидин-4-ил)фенокси] -1-фенилбутан-1-она в виде бесцветного масла; МС: 502 (М + Na)+.
Пример 47
Аналогично примеру 46(г)-(д), соответственно 3(в)-(д) получали следующие соединения:
1) Из трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-[4-(3-(2-фенил-[1,3] диоксолан-2-ил)пропокси] фенил] пиперидин-1-карбоновой кислоты путем алкилирования 5-брометилбензо[b]тиофеном в виде бледно-желтой смолы получили трет-бутиловый эфир (3RS, 4RS)-3-(бензо[b]тиофен-5-илметокси)-4-{4-[3-(2-фенил-[1,3] диоксолан-2-ил)пропокси] фенил}пиперидин-1-карбоновой кислоты; МС: 630 (M + H)+. В результате последующего отщепления ВОС- и ацетальной групп получили (3RS, 4RS)-4-[4-[3-(бензо[b]тиофен-5-илметокси)пиперидин-4-ил]фенокси]-1-фенилбутан-1-он в виде бесцветной смолы; МС: 486 (М + Н)+.
2) Из трет-бутилового эфира (3RS,4RS)-3-гидрокси-4- [4-[3-(2-фенил[1,3] диоксолан-2-ил)пропокси] фенил] пиперидин- 1-карбоновой кислоты путем алкилирования 5-(хлорметил)инданом в виде бледно-желтой смолы получили трет-бутиловый эфир (3RS,4RS)-3- (индан-5-илметокси)-4-{4-[3-(2-фенил[1,3]диоксолан-2- ил)пропокси] фенил}пиперидин-1-карбоновой кислоты; МС: 614 (М+Н)+. В результате последующего отщепления BOC- и ацетальной групп получили (3RS, 4RS)-4-[4- [3-(индан-5-илметокси)пиперидин-4-ил]фенокси]-1-фенилбутан-1-он в виде бесцветной смолы; МС: 470 (М+Н)+.
3) Из трет-бутилового эфира (3RS,4RS)-3-гидрокси-4-[4- [3-(2-фенил[1,3] диоксолан-2-ил)пропокси] фенил] пиперидин-1 -карбоновой кислоты путем алкилирования 3-хлорметил-1-(2- триметилсиланилэтоксиметокси) нафталином в виде бесцветной смолы получили трет-бутиловый эфир (3RS,4RS)-4-[4-[3-(2-фенил- [1,3] диоксолан-2-ил)пропокси] фенил] -3-[4-(2- триметилсиланилэтоксиметокси)нафталин-2-илметокси] пиперидин-1- карбоновой кислоты; МС: 770 (М+Н)+. В результате последующего отщепления BOC- и обеих ацетальных групп получили (3RS, 4RS)-4-[4-[3-(4-гидроксинафталин-2-илметокси)пиперидин-4-ил] фенокси] -1-фенилбутан-1-он в виде бесцветной смолы; Rf0,17 (SiO2, метиленхлорид:метанол = 9:1, экстракция в противотоке 5%-ного аммиака).
4) Из трет-бутилового эфира (3RS, 4RS)-3-гидpoкcи-4-(4- гидpoкcифенил)пиперидин-1-карбоновой кислоты путем алкилирования 1-бром-4-(2-бромэтил) бензолом аналогично примеру 46(в) получили трет-бутиловый эфир (3RS,4RS)-4-[4-[2-(4-бромфенокси)этокси] фенил] -3-гидроксипиперидин-1-карбоновой кислоты в виде бесцветной смолы. В результате последующего алкилирования 2-бромметилнафталином получили трет-бутиловый эфир (3RS,4RS)-4-[4-[2-(4-бромфенокси)этокси] фенил] -3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты, из которого отщеплением BOC-группы получили (3RS,4RS)-4-[4- [2-(4-бромфенокси)этокси] фенил] -3-(нафталин-2-илметокси)пиперидин в виде бесцветной смолы; МС: 532, 534 (М+Н)+.
5) Из трет-бутилового эфира (3RS, 4RS)-3-гидpoкcи-4-(4- гидpoкcифенил)пиперидин-1-карбоновой кислоты путем алкилирования 2-бромметил-5- фенил-[1,3,4] оксадиазолом аналогично примеру 44(д) получили трет-бутиловый эфир (3RS, 4RS)-3-гидрокси-4-[4-(5-фенил-[1,3,4] оксадиазол-2-илметокси)фенил]пиперидин-1-карбоновой кислоты в виде желтоватого аморфного твердого вещества. В результате последующего алкилирования 2-бромметилнафталином получили трет- бутиловый эфир (3RS,4RS)-3-(нафталин-2-илметокси)-4-[4-(5-фенил- [1,3,4] оксадиазол-2-илметок-си)фенил]пиперидин-1-карбоновой кислоты, из которого отщеплением BOC-группы получили (3RS,4RS)-3- (нафталин-2-илметокси)-4-[4-(5-фенил[1,3,4] оксадиазол-2- илметокси)фенил] пиперидин в виде бесцветного твердого вещества; МС: 492 (M+Н)+.
6) Из трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4- (4-гидроксифенил)пиперидин-1-карбоновой кислоты путем алкилирования β- бромфенетолом аналогично примеру 46 (в) получили трет-бутиловый эфир (3RS,4RS)-3-гидрокси-4-[4-(2-феноксиэтокси) фенил] пиперидин-1-карбоновой кислоты; МС: 414 (М+Н)+. В результате последующего алкилирования 2-бромметилнафталином получили трет-бутиловый эфир (3RS,4RS)-3-(нафталин-2-илметокси)-4- [4-(2-феноксиэтокси)фенил]пиперидин-1-карбоновой кислоты [МС: 554 (М+Н)+], из которого отщеплением BOC-группы получили (3RS, 4RS)-3-(нафталин-2-илметокси)-4-[4-(2-феноксиэтокси)фенил] пиперидин; МС: 454 (М+Н)+.
7) Из трет-бутилового эфира (3RS,4RS)-3-гидрокси-4-[4-(2- феноксиэтокси)фенил] пиперидин-1-карбоновой кислоты путем алкилирования 3-хлорметил-1-(2- триметилсиланилэтоксиметокси)нафталином получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(2-феноксиэтокси)фенил]-3-[4-(2- триметилсиланилэтоксиметокси) нафталин-2-илметокси] пиперидин -1-карбоновой кислоты; МС: 700 (М+Н)+. В результате последующего отщепления BOC- и ацетальной групп получили (3RS, 4RS)-3-{ 4-[4-(2-феноксиэтокси)фенил]пиперидин-3-илоксиметил} нафталин-1-ол; МС: 470 (М+Н)+.
Пример 48.
К раствору из 44 мг (0,074 ммоля) (3RS,4RS)-4-[4-[3-(4-гидроксинафталин-2-илметокси)пиперидин-4-ил] фенокси]-1-фенилбутан-1-она в 1,5 мл диоксана с помощью шприца добавляли раствор 18,7 мг (0,494 ммоля, 6,7 экв.) борогидрида натрия в 0,35 мл воды. Эту смесь перемешивали в течение 1,5 ч при комнатной температуре. Далее реакционный раствор смешивали с равным объемным количеством ледяной воды и значение pH смеси устанавливали равным 1 с помощью 2 н. соляной кислоты. После перемешивания в течение 5-10 мин при комнатной температуре значение pH устанавливали равным 9 с помощью концентрированного аммиака и водный раствор трижды экстрагировали метиленхлоридом, используя каждый раз объемный эквивалент. Объединенные органические фазы сушили над сульфатом магния, концентрировали при пониженном давлении и при 45oC и сушили в высоком вакууме. Коричневатое твердое вещество (40,1 мг) разделяли на силикагеле с использованием смеси 9:1 метиленхлорида и метанола в качестве элюента (экстр. в противотоке 5 об.% конц. водн. NH3). Таким путем получили 13 мг (35% от теории) (3RS,4RS)-3-[4-[4- (4-гидрокси-4-фенилбутокси)фенил] пиперидин-4-илоксиметил] нафталин-1-ола (конфигурация в бутанольной части неизвестна) в виде бесцветного масла; МС: 498 (М+Н)+.
Пример 49.
Аналогично примеру 48 путем восстановления кетонов получили следующие спирты:
1) из (3RS,4RS)-4-[4-[3-(индан-5-илметокси)пиперидин-4-ил]фенокси] -1-фенилбутан-1-она получили смесь 2:1 или 1:2 (RS)- и (SR)-4-[4- [(3RS, 4RS)-3-(индан-5-илметокси)пиперидин-4-ил] фенокси] -1- фенилбутан-1-ола в виде бесцветной смолы; МС: 472 (М+Н)+;
2) из (3RS, 4RS)-4-[4-[3-(бензо[b] тиофен-5-илметокси) пиперидин-4-ил] фенокси] -1-фенилбутан-1-она получили смесь (RS)- и (SR)-4-[4-[(3RS,4RS)-3-(бензо[b] тиофен-5-илметокси) пиперидин-4-ил] фенокси]-1-фенилбутан-1-ола в виде бесцветной смолы; МС: 488 (М+Н)+;
3) из (3RS,4RS)-4-[4-(3-нафталин-2-илметоксипиперидин-4-ил) фенокси]-1-фенилбутан-1-она получили 4-[4-[(3RS,4RS)-3-нaфтaлин-2- илметоксипиперидин-4-ил] фенокси]-1-фенилбутан-1-ол (конфигурация в бутанольной части неизвестна) в виде бесцветной смолы; МС: 482 (М+Н)+.
Пример 50.
(а) Аналогично примеру 22(ж) путем введения BOC-группы из (3RS,4RS)-4-[4-(3-нафталин-2-илметоксипиперидин-4-ил)фенокси] -1- фенилбутан-1-она получили трет-бутиловый эфир (3RS, 4RS)-3- (нафталин-2-илметокси)-4-[4-(4-оксо-4-фенилбутокси)фенил] пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 580 (М+Н)+.
(б) Восстановлением трет-бутилового эфира (3RS,4RS)-3-(нафталин-2-илметокси)-4-[4-(4-оксо-4-фенилбутокси) фенил] пиперидин-1-карбоновой кислоты аналогично примеру 48 получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(4- гидрокси-4-фенилбутокси)фенил] -3-нафталин-2-илметоксипиперидин -1-карбоновой кислоты (конфигурация в бутокси-части неизвестна) в виде бесцветного твердого вещества; МС: 582 (М+Н)+.
(в) В результате алкилирования трет-бутилового эфира (3RS,4RS)-4-[4-(4-гидрокси-4-фенилбутокси)фенил] -3-нафталин- 2-илметоксипиперидин-1-карбоновой кислоты метилиодидом аналогично примеру 22(и) получили трет-бутиловый эфир (3RS,4RS)-4- [4-(4-метокси-4-фенилбутокси)фенил]- 3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты (конфигурация в бутокси-части неизвестна) в виде бесцветного масла; Rf 0,61 (SiO2, гексан:уксусный эфир = 2: 1).
(г) Аналогично примеру 22(м) путем отщепления BOC-группы из трет-бутилового эфира (3RS, 4RS)-4- [4-(4-метокси-4-фенилбутокси)фенил]-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-[4- (4-метокси-4-фенилбутокси)фенил]-3-(нафталин-2-илметокси) пиперидин (конфигурация в бутокси-части неизвестна) в виде бесцветной смолы; МС: 496 (М+Н)+.
Пример 51.
Раствор из 30 мг (0,052 ммоля) трет-бутилового эфира (3RS, 4RS)-4-[4-(4-гидрокси-4-фенилбутокси)фенил] -3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты (конфигурация в бутокси-части неизвестна), 25,5 мкл (0,186 ммоля, 3,6 экв.) триэтиламина и 1,7 мл метиленхлорида последовательно смешивали с 21,6 мкл (0,186 ммоля, 3,6 экв.) бензоилхлорида и 2 мг (0,016 ммоля) 4-диметиламинопиридина. Этот реакционный раствор перемешивали в течение 10 ч при комнатной температуре, затем сливали на 5 мл воды и трижды экстрагировали уксусным эфиром порциями по 10 мл. Объединенные органические фазы сушили над сульфатом магния, упаривали при пониженном давлении и сушили в высоком вакууме. Бледно-желтую смолу (62 мг) растворяли в 1 мл метанола, повторно концентрировали и сушили в высоком вакууме. Полученный сырой продукт без последующей очистки и определения характеристик аналогично описанному в примере 22(м) способу подвергали взаимодействию с хлористым водородом в метаноле. Коричнево-желтую смолу (56 мг) разделяли на силикагеле с использованием смеси 95:5 метиленхлорида и метанола в качестве элюента (экстракция в противотоке 5 об.% конц. аммиака). Таким путем получили 15 мг (50% от теории) 4-[4-[(3RS, 4RS)-3-нафталин-2-илметоксипиперидин-4- ил]фенокси]-1-фенилбутилового эфира бензойной кислоты (конфигурация в бутокси-части неизвестна) в виде бесцветной смолы; МС: 586 (М+Н)+.
Пример 52.
Смесь из 600 мг (0,962 ммоля) трет-бутилового эфира (3RS,4RS)-3-(нафталин-2-илметокси)-4-{4-[3-(2-фенил- [1,3]диоксолан-2-ил)пропокси]фенил} пиперидин-1-карбоновой кислоты в 3,0 мл метиленхлорида и 433 мг (1,92 ммоля, 2,0 экв. ) бромида цинка перемешивали в течение 4 ч при комнатной температуре. Реакционную смесь сливали на воду и трижды экстрагировали уксусным эфиром. Органические фазы по одному разу промывали водой и насыщенным раствором хлорида натрия, сушили над сульфатом магния, упаривали при пониженном давлении и сушили в высоком вакууме. Аморфный бледно-желтый сырой продукт разделяли на силикагеле с использованием смеси 95:5:0,1 метиленхлорида, метанола и аммиака. Таким путем получили 355 мг (71% от теории) (3RS, 4RS)-3-(нафталин-2-илметокси)-4- [4-[3-(2-фенил[1,3] диоксолан-2-ил)пропокси]фенил]пиперидина в виде бесцветной смолы; МС: 524 (М+Н)+.
Пример 53.
(а) Аналогично примеру 44(д)-(е) путем алкилирования трет-бутилового эфира (3RS,4RS)-3-гидрокси-4-(4-гидроксифенил) пиперидин-1-карбоновой кислоты 2-(2-иодэтокси)тетрагидропираном получили смесь трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-[4-[2-[(RS)- и -[(SR)-тетрагидропиран-2- илокси]этокси]фенил] пиперидин-1-карбоновой кислоты в виде желтого масла: Rf 0,45 (SiO2, гексан:уксусный эфир = 1:1).
(б) Аналогично примеру 22(и) путем алкилирования смеси трет- бутилового эфира (3RS, 4RS)-3-гидрокси-4-[4-[2-[(RS)- и -[(SR)- тетрагидропиран-2-илокси]этокси]фенил]пиперидин-1-карбоновой кислоты 2-бромметилнафталином получили смесь трет-бутилового эфира (3RS,4RS)-3-(нафталин-2-илметокси)-4-[4-[2-[(RS)- и - [(SR)-тетрагидропиран-2-илокси] этокси] фенил] пиперидин-1- карбоновой кислоты в виде бесцветного твердого вещества; МС: 579 (М+Н)+.
(в) Раствор из 1,99 г (3,54 ммоля) смеси трет-бутилового эфира (3RS, 4RS)-3-(нафталин-2-илметокси)-4-[4-[2-[(RS)- и - [(SR)-тетрагидропиран-2-илокси] этокси] фенил] пиперидин-1- карбоновой кислоты в 11,3 мл метанола смешивали с 11,3 мл 2 н. хлористого водорода в метаноле и перемешивали в течение 5 мин при комнатной температуре. Реакционную смесь сливали на 200 мл смеси льда и насыщенного раствора гидрокарбоната натрия и трижды экстрагировали уксусным эфиром. Органические фазы промывали насыщенным раствором хлорида натрия, сушили над сульфатом магния, упаривали при пониженном давлении и сушили в высоком вакууме. Желтую смолу (1,80 г) перекристаллизовывали из гексана. Таким путем получили 950 мг (56% от теории) трет-бутилового эфира (3RS, 4RS)-4-[4-(2-гидроксиэтокси)фенил] -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 478 (М+Н)+.
(г) Аналогично примеру 22 (л) в результате ацилирования трет-бутилового эфира (3RS, 4RS)-4-[4-(2-гидроксиэтокси)фенил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты 4-хлорбензоилхлоридом получили трет-бутиловый эфир (3RS, 4RS)-4-[4- [2-(4-хлорбензоилокси)этокси]фенил]-3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 616 (М+Н)+.
(д) Аналогично примеру 22(м) путем отщепления BOC-группы из трет-бутилового эфира (3RS, 4RS)-4-[4-[2-(4-хлорбензоилокси)этокси] фенил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты получили гидрохлорид (3RS, 4RS)-2- [4-(3-нафталин-2-илметоксипиперидин-4- -ил)фенокси] этилового эфира 4-хлорбензойной кислоты в виде бесцветного твердого вещества; МС: 516 (М+Н)+.
Пример 54.
Аналогично примеру 22(м) путем отщепления BOC-группы с помощью кислоты получили следующие соединения:
1) из трет-бутилового эфира (3RS, 4RS)-4-[4-[2-(4-метоксибензоилокси)этокси] фенил] -3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты получили гидрохлорид (3RS, 4RS)-2-[4-[3-(нафталин-2-илметокси)пиперидин-4- ил] фенокси] этилового эфира 4-метоксибензойной кислоты в виде бесцветного твердого вещества; МС: 512 (М+Н)+;
2) из трет-бутилового эфира (3RS,4RS)-4-[4-[2-(2-хлорбензоилокси)этокси] фенил] -3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты получили гидрохлорид (3RS, 4RS)-2-[4-(3-нафталин-2- илметоксипиперидин-4-ил)фенокси] этилового эфира 2-хлорбензойной кислоты в виде бесцветного твердого вещества; МС: 516 (М+Н)+;
3) из трет-бутилового эфира (3RS,4RS)-4-[4-(2-бeнзoилoкcиэтoкcи)фенил] -3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-2-[4-[3-(нафталин-2-илокси)пиперидин-4-ил] фенокси] этиловый эфир бензойной кислоты в виде бесцветного аморфного твердого вещества; МС: 340 (M-нафтилметил)+;
4) из трет-бутилового эфира (3RS,4RS)-4-[4-[2-(2-бензоилоксиметилбензоилокси)этокси] фенил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты получили гидрохлорид (3RS, 4RS)-2-[4-[3-(нафталин-2-илметокси)пиперидин-4-ил] фенокси] этилового эфира 2-бензоилоксиметилбензойной кислоты в виде бесцветного твердого вещества; МС: 616 (М+Н)+;
5) из трет-бутилового эфира (3RS,4RS)-3- (нaфтaлин-2-илмeтoкcи)-4-[4-(2-фенилсульфанилэтокси)фенил] пиперидин-1-карбоновой кислоты получили гидрохлорид (3RS, 4RS)-3- (нaфтaлин-2-илмeтoкcи)-4-[4-(2-фенилсульфанилэтокси)фенил] пиперидина в виде бесцветного твердого вещества; МС: 470 (М+Н)+;
6) из трет-бутилового эфира (3RS, 4RS)-3-(нaфтaлин-2-илмeтoкcи) -4-[4-(2-фенилсульфонилэтокси)фенил] пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-3-нафталин-2-илметокси-4-[4-(2- фенилсульфонилэтокси)фенил] пиперидин в виде желтоватой пены; МС: 502 (М+Н)+;
7) из трет-бутилового эфира (3RS,4RS)-4-[4-(2- бензоиламиноэтокси)фенил] -3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты получили (3RS, 4RS)-N-[2-[4-[3-(нафталин-2- илокси)пиперидин-4-ил] фенокси] этилбензамид в виде бесцветного аморфного твердого вещества; МС: 481 (М+Н)+;
8) из трет-бутилового эфира (3RS,4RS)-3-нафталин-2-илметокси-4-[4-(2-[1,2,4] триазол-1- илэтокси)фенил] пиперидин-1-карбоновой кислоты получили гидрохлорид (3RS, 4RS)-3-(нафталин-2-илметокси)-4-[4-(2-[1,2,4] триазол-1-илэтокси)фенил]пиперидина в виде белого порошка; МС: 428 (М)+;
9) из трет-бутилового эфира (3RS,4RS)-4-[4-(2- бензилоксиэтокси)фенил] -3-(нафталин-2-илметокси)пиперидин- 1-карбоновой кислоты получили (3RS, 4RS)-4-[4-(2- бензилоксиэтокси)фенил]-3-(нафталин-2-илметокси)пиперидин; МС: 468 (М+Н)+.
Использованные в качестве исходных веществ BOC- производные получали следующим образом.
(а) Раствор из 150 мг (0,314 ммоля) трет-бутилового эфира (3RS,4RS)-4-[4-(2-гидроксиэтокси] фенил]-3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты, 3,7 мг (0,031 ммоля, 0,1 экв.) 4- диметиламинопиридина, 65,9 мг (0,375 ммоля, 1,2 экв.) 4- метоксибензоилхлорида и 51,7 мкл триэтиламина в 10 мл метиленхлорида перемешивали в течение 15 ч при комнатной температуре. Реакционную смесь сливали на 50 мл смеси льда/воды и трижды экстрагировали уксусным эфиром. Органические фазы по одному разу промывали водой и насыщенным раствором хлорида натрия, сушили над сульфатом магния, упаривали при пониженном давлении и сушили в высоком вакууме. Сырой продукт (208 мг) разделяли на силикагеле с использованием смеси 95:5 гексана и ацетона в качестве элюента. Таким путем получили 104 мг (51% от теории) трет-бутилового эфира (3RS, 4RS)-4-[4-[2-(4-метоксибензоилокси)этокси] фенил] -3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 612 (М+Н)+.
(б) Аналогично примеру 22(л) в результате ацилирования трет-бутилового эфира (3RS, 4RS)-4-[4-(2-гидроксиэтокси)фенил] -3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты 2- хлорбензоилхлоридом получили трет-бутиловый эфир (3RS, 4RS)-4-[4- [2-(2-хлорбензоилокси)этокси] фенил] -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты в виде желтого масла; МС: 616 (М+Н)+.
(в) Аналогично примеру 22(л) в результате ацилирования трет-бутилового эфира (3RS, 4RS)-4-[4-(2-гидроксиэтокси)фенил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты бензоилхлоридом получили трет-бутиловый эфир (3RS, 4RS)-4- [4-(2-бензоилоксиэтокси)фенил] -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного аморфного твердого вещества; Rf 0,61 (SiO2, гексан:ацетон = 95:5).
(г) Аналогично примеру 22(л) в результате ацилирования трет-бутилового эфира (3RS,4RS)-4-[4-(2-гидроксиэтокси)фенил]-3- (нафталин-2-илметокси) пиперидин-1-карбоновой кислоты 2- хлоркарбонилбензиловым эфиром бензойной кислоты получили трет- бутиловый эфир (3RS,4RS)-4-[4-[2-(2- бензоилоксиметилбензоилокси)этокси]фенил]-3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 716 (М+Н)+.
(д) Аналогично примеру 33(а) из трет-бутилового эфира (3RS,4RS)-4-[4-(2-гидроксиэтокси)фенил] -3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты и дифенилсульфида получили трет-бутиловый эфир (3RS, 4RS)-3-(нафталин-2-илметокси)-4- [4-(2-фенилсульфанилэтокси)фенил] пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 570 (М+Н)+.
(е) Аналогично примеру 33(в) путем окисления трет-бутилового эфира (3RS, 4RS)-3-(нафталин-2-илметокси)-4- [4-(2-фенилсульфанилэтокси)фенил] пиперидин-1-карбоновой кислоты получили трет-бутиловый эфир (3RS, 4RS)-3-(нафталин-2-илметокси)-4- [4-(2-фенилсульфонилэтокси)фенил] пиперидин-1-карбоновой кислоты в виде бесцветной пены; МС: 619 (M+NH4)+.
(ж) Раствор из 478 мг (1,00 ммоль) трет-бутилового эфира (3RS, 4RS)-4-[4-(2-гидроксиэтокси)фенил]-3-(нафталин-2-илметокси) пиперидин-1- карбоновой кислоты и 93 мл мезилхлорида в 5 мл пиридина перемешивали в течение 2 ч при комнатной температуре. Далее реакционный раствор сливали на 50 мл смеси льда/воды и трижды экстрагировали метиленхлоридом. Органические фазы дважды промывали водой, сушили над сульфатом магния, упаривали при пониженном давлении и сушили в высоком вакууме. Таким путем получили 569 мг сырого трет-бутилового эфира (3RS,4RS)-4-[4-(2- метилсульфонилоксиэтокси)фенил]-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты, который без дальнейшей очистки и определения характеристик использовали на следующей стадии.
(з) Смесь из 569 мг сырого трет-бутилового эфира (3RS,4RS)-4- [4-(2-метилсульфонилоксиэтокси)фенил] -3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты и 650 мг азида натрия в 20 мл диметилсульфоксида перемешивали в течение 3,5 ч при 80oC. Далее реакционный раствор сливали на 50 мл смеси льда/воды и трижды экстрагировали уксусным эфиром. Органические фазы промывали водой, сушили над сульфатом магния, упаривали при пониженном давлении и сушили в высоком вакууме. Желтое масло (670 мг) разделяли на силикагеле с использованием смеси 9:1 гексана и уксусного эфира в качестве элюента. Таким путем получили 271 мг (54% от теории по обеим стадиям) трет-бутилового эфира (3RS, 4RS)- 4-[4-(2-азидоэтокси)фенил]-3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты в виде бесцветного твердого вещества; МС: 503 (М+Н)+.
(и) Смесь из 115,9 мг (0,231 ммоля) трет-бутилового эфира (3RS,4RS)-4-[4-(2-азидоэтокси)фенил] -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты, 87,4 мг (0,330 ммоля, 1,43 экв.)трифенилфосфина и 6,1 мкл (6,1 мг, 0,339 ммоля, 1,47 экв.) деионизованной воды перемешивали в течение 4 ч при комнатной температуре. Далее добавляли 3 мл уксусной кислоты и перемешивали в течение 17 ч при комнатной температуре. Эту реакционную смесь сливали на смесь льда/воды, с помощью насыщенного раствора гидрокарбоната натрия создавали щелочную среду и трижды экстрагировали уксусным эфиром. Органические фазы по одному разу промывали водой и насыщенным раствором хлорида натрия, сушили над сульфатом магния, упаривали при пониженном давлении и сушили в высоком вакууме. Таким путем получили 192,3 мг сырого трет-бутилового эфира (3RS, 4RS)-4- [4-(2-аминоэтокси)фенил]-3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты, который без дальнейшей очистки использовали в следующей реакции; Rf 0,10 (SiO2, метиленхлорид:ацетон = 95:5 + 0,1% аммиака).
(к) Раствор из 192,4 мг сырого трет-бутилового эфира (3RS,4RS) -4-[4-(2-аминоэтокси)фенил] -3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты в 3 мл метиленхлорида смешивали при 0oC с 51,7 мл триэтиламина и 64,9 мг (0,462 ммоля, 2,0 экв.) бензоилхлорида и перемешивали сначала в течение 0,75 ч при 0oC, а затем в течение 3 ч при комнатной температуре. Далее реакционную смесь сливали на смесь льда/воды, с помощью насыщенного раствора гидрокарбоната натрия создавали щелочную среду и трижды экстрагировали уксусным эфиром. Органические фазы по одному разу промывали водой и насыщенным раствором хлорида натрия, сушили над сульфатом магния, упаривали при пониженном давлении и сушили в высоком вакууме. Бесцветное масло разделяли на силикагеле с использованием смеси 95:5 метиленхлорида и ацетона в качестве элюента. Таким путем получили 44,9 мг (33% от теории) трет-бутилового эфира (3RS, 4RS)-4-[4-(2-бензоиламиноэтокси)фенил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бледно-желтого масла; МС: 581 (М+Н)+.
(л) Раствор из 110 мг (0, 2 ммоля) сырого трет-бутилового эфира (3RS, 4RS)-4-[4-(2-метилсульфонилоксиэтокси) фенил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в 5 мл диметилформамида смешивали с 70 мг (1,0 ммоль) натриевой соли 1,2,4-триазола и реакционную смесь выдерживали при 100oC в течение 6 ч. Далее смесь охлаждали до комнатной температуры и диметилформамид отгоняли в вакууме, создаваемом масляным насосом. Остаток растворяли в 10 мл метиленхлорида, промывали 2 мл воды, органическую фазу сушили над сульфатом натрия и упаривали при пониженном давлении. Остаток хроматографировали на силикагеле с использованием смеси 95:5:0,1 метиленхлорида, метанола и аммиака в качестве элюента. Таким путем получили 90 мг (85% от теории) трет-бутилового эфира (3RS, 4RS)-3-нафталин-2-илметокси-4-[4-(2- [1,2,4] триазол-1-илэтокси)фенил] пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 529 (М+Н)+.
(м) Аналогично примеру 3(в) путем алкилирования трет-бутилового эфира (3RS,4RS)-4-[4-(2-гидроксиэтокси]фенил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты бензилбромидом получили трет-бутиловый эфир (3RS, 4RS)-4- [4-(2-бензилоксиэтокси)фенил] -3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты; МС: 568 (М+Н)+.
Пример 55.
Аналогично примеру 22(м) получали следующие соединения:
1) из трет-бутилового эфира (3RS,4RS)-4-[4-[2-(2- хлорметилбензоилокси)этокси] фенил]-3- [4-(2-триметилсиланилэтоксиметокси)нафталин- 2-илметокси] пиперидин-1-карбоновой кислоты в результате одновременного отщепления BOC- и ацетальной групп получили (3RS,4RS)-2-{4-[3-(4-гидроксинафталин-2-илметокси)пиперидин-4-ил] фенокси} этиловый эфир 2-хлорметилбензойной кислоты в виде бесцветного масла;
2) из трет-бутилового эфира (3RS,4RS)-4-[4-(2- бeнзoилoкcиэтoкcи)фенил] -3-[4-(2-метоксибензилокси)нафталин-2- илметокси]пиперидин-1-карбоновой кислоты получили гидрохлорид (3RS,4RS)-2-[4-[3-[4-(2-метоксибензилокси)нафталин-2-илметокси] пиперидин-4-ил] фенокси] этилового эфира бензойной кислоты в виде бесцветного твердого вещества; МС: 618 (М+Н)+;
3) из трет-бутилового эфира (3RS, 4RS)-4-[4-(2-бeнзилoкcиэтoкcи)фенил]-3-(4-бензилоксинафталин- 2-илметокси)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-[4-(2-бензилоксиэтокси)фенил] -3-(4- бензилоксинафталин-2-илметокси)пиперидин; МС: 574 (М+Н)+.
Использованные в качестве исходных веществ BOC-производные получали следующим путем:
(а) Аналогично примеру 44(д) путем алкилирования смеси трет-бутилового эфира (3RS,4RS)-3-гидрокси-4-[4-[2-[(RS)- и -[(SR)-тетрагидропиран-2-илокси] этокси] фенил] пиперидин-1 -карбоновой кислоты 2-хлорметил-1-(2-триметилсиланилэтоксиметокси) нафталином получили смесь трет-бутилового эфира (3RS, 4RS)-4-[4-[2-[(RS)- и [(SR)-тетрагидропиран-2-ил] этокси]фенил] -3-[4-(2-триметилсиланилэтоксиметокси)нафталин- 2-илметокси] пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 725 (M+NH4)+.
(б) Аналогично примеру 53(в) из смеси трет-бутилового эфира (3RS,4RS)-4-[4-[2-[(RS)- и -[(SR)-тетрагидропиран-2-ил]этокси] фенил]-3-[4-(2-триметилсиланилэтоксиметокси)нафталин-2-илметокси] пиперидин-1-карбоновой кислоты получили трет-бутиловый эфир (3RS,4RS)-4-[4-(2-гидроксиэтокси)фенил]-3-[4-(2- триметилсиланилэтоксиметокси)нафталин-2-илметокси] пиперидин-1- карбоновой кислоты в виде бесцветного твердого вещества; МС: 624 (М+Н)+.
(в) Аналогично примеру 22(л) в результате ацилирования трет-бутилового эфира (3RS, 4RS)-4-[4-(2-гидроксиэтокси)фенил] -3- [4-(2-триметилсиланилэтоксиметокси)нафталин-2-илметокси] пиперидин-1-карбоновой кислоты 2-хлорметилбензоилхлоридом получили трет-бутиловый эфир (3RS, 4RS)-4-[4-[2-(2- хлорметилбензоилокси)этокси]фенил]-3-[4-(2- триметилсиланилэтоксиметокси)нафталин-2-илметокси] пиперидин-1- карбоновой кислоты в виде бесцветного твердого вещества; МС: 776 (М+Н)+.
(г) 200 мг (0,28 ммоля) смеси трет-бутилового эфира (3RS,4RS)-4-[4-[2-[(RS)- и -[(SR)-тетрагидропиран-2-ил] этокси] фенил]-3-[4-(2-триметилсиланилэтоксиметокси)нафталин-2 - илметокси] пиперидин-1-карбоновой кислоты растворяли в 7,6 мл 0,1 М хлористого водорода в метаноле и перемешивали в течение 2 ч при комнатной температуре. Далее повторно добавляли 0,36 мл 2 М хлористого водорода в метаноле и перемешивание продолжали в течение 2 ч при комнатной температуре. Этот реакционный раствор сливали на полунасыщенный раствор гидрокарбоната натрия и трижды экстрагировали уксусным эфиром. Органические фазы по одному разу промывали водой и насыщенным раствором хлорида натрия, сушили над сульфатом магния, упаривали при пониженном давлении и сушили в высоком вакууме. Желтоватое масло (204 мг) разделяли на силикагеле с использованием смеси 1: 1 гексана и уксусного эфира (экстракция в противотоке концентрированного аммиака). Таким путем получили 111 мг (80% от теории) трет-бутилового эфира (3RS,4RS)-4-[4-(2- гидроксиэтокси)фенил]-3-(4-гидроксинафталин-2- илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; Rf 0,26 (SiO2, гексан:уксусный эфир = 1:1).
(д) Аналогично примеру 44(д) путем алкилирования трет-бутилового эфира (3RS, 4RS)-4-[4-(2-гидроксиэтокси)фенил] -3-(4-гидроксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты 2-метоксибензилхлоридом получили трет-бутиловый эфир (3RS, 4RS)-4- [4-(2-гидроксиэтокси)фенил]-3-[4-(2-метоксибензилокси)нафталин-2 -илметокси] пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 652 (М+K)+.
(е) Аналогично примеру 22(л) в результате ацилирования трет-бутилового эфира (3RS, 4RS)-4-[4-(2-гидроксиэтокси)фенил] -3- [4-(2-метоксибензилокси)нафталин-2-илметокси] пиперидин-1-карбоновой кислоты бензоилхлоридом получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(2-бензоилоксиэтокси)фенил] - 3-[4-(2-метоксибензилокси)нафталин-2-илметокси] пиперидин-1- карбоновой кислоты в виде бесцветного масла; МС: 736 (М+Н)+.
(ж) Аналогично примеру 1(ж) в результате двукратного алкилирования трет-бутилового эфира (3RS,4RS)-4- [4-(2-гидроксиэтокси)фенил]-3-(4-гидроксинафталин-2-илметокси) пиперидин-1-карбоновой кислоты бензилбромидом получили трет-бутиловый эфир (3RS,4RS)-4-[4-(2-бензилоксиэтокси)фенил] -3-(4-бензилоксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты.
Пример 56.
Аналогично примеру 22(м) путем одновременного отщепления BOC- и СЭМ-групп с помощью кислоты получили следующие соединения:
1) из трет-бутилового эфира (3RS, 4RS)-3-(нaфтaлин-2-илмeтoкcи)-4-[4-[2-[4- (2-триметилсиланилэтоксиметокси)бензоилокси] этокси]фенил]пиперидин- 1-карбоновой кислоты получили гидрохлорид (3RS, 4RS)-2-[4-(3- нафталин-2-илметокси-4-ил)фенокси] этилового эфира 4- гидроксибензойной кислоты в виде бесцветного твердого вещества; МС: 498 (М+Н)+;
2) из трет-бутилового эфира (3RS,4RS)-4-[4-(2- бензилоксиэтокси)фенил] -3-(4-гидроксинафталин-2-илметокси) пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-3-[4-[4-(2- бензилоксиэтокси)фенил]пиперидин-3-илоксиметил]нафталин-1-ол; МС: 484 (М+Н)+.
Использованные в качестве исходных веществ BOC-производные получали следующим путем.
(а) Аналогично примеру 22(м) с применением гидрохлорида N-этил-N'-(3-диметиламинопропил)карбодиимида (ЭДК) в качестве агента конденсации из трет-бутилового эфира (3RS,4RS)-4-[4-(2- гидроксиэтокси)фенил]-3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты и 4-(2-триметилсиланилэтоксиметокси)бензойной кислоты получили трет-бутиловый эфир (3RS, 4RS)-3-(нафталин-2- илметокси)-4-[4-[2-[4-(2-триметилсиланилэтоксиметокси) бензоилокси] этокси]фенил]пиперидин-1-карбоновой кислоты в виде бесцветного аморфного твердого вещества; МС: 728 (М+Н)+.
(б) Аналогично примеру 1(ж) в результате алкилирования трет-бутилового эфира (3RS, 4RS)-4-[4-(2-гидроксиэтокси)фенил] -3- [4-(2-триметилсиланилэтоксиметокси)нафталин-2-илметокси] пиперидин-1-карбоновой кислоты бензилбромидом получили трет- бутиловый эфир (3RS, 4RS)-4-[4-(2-бензилоксиэтокси)фенил]-3-(4- гидроксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты.
Пример 57.
(а) Аналогично примеру 44(д) путем алкилирования трет- бутилового эфира (3RS,4RS)-3-гидрокси-4-(4-гидроксифенил) пиперидин-1-карбоновой кислоты рац. -2-(3- бромпропокси)тетрагидропираном получили смесь трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-[4-[3-[(RS)- и -[(SR)- тетрагидропиран-2-илокси] пропокси] фенил] пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; Rf 0,23 (SiO2, гексан:уксусный эфир = 4:1).
(б) В результате алкилирования смеси трет-бутилового эфира (3RS,4RS)-3-гидрокси-4-[4-[3-[(RS)- и - [(SR)-тетрагидропиран-2-илокси]пропокси]фенил] пиперидин-1- карбоновой кислоты 2-бромметилнафталином аналогично описанному в примере 22(и) способу получили смесь трет-бутилового эфира (3RS,4RS)-3-(нафталин-2-илметокси)-4-[4-[3-[(RS)- и -[(SR)- тетрагидропиран-2-илокси] пропокси]фенил] пиперидин-1-карбоновой кислоты в виде желтого масла; Rf 0,35 (SiО2, гексан:ацетон = 4:1).
(в) Раствор из 5,22 г сырой смеси трет-бутилового эфира (3RS,4RS)-3-(нафталин-2-илметокси)-4-[4-[3-[(RS)- и -[(SR)- тетрагидропиран-2-илокси] пропокси] фенил]пиперидин-1-карбоновой кислоты в 30 мл тетрагидрофурана и 30 мл 2 н. соляной кислоты перемешивали в течение 14 ч при комнатной температуре и в течение 2 ч при 40oC. После этого тетрагидрофуран отгоняли при пониженном давлении, а оставшуюся водную фазу трижды экстрагировали метиленхлоридом. Органическую фазу сушили над сульфатом магния, а затем отгоняли при пониженном давлении. Образовавшееся желтое масло (2,9 г) хроматографировали на силикагеле с использованием смеси 9:1 метиленхлорида и уксусного эфира в качестве элюента. Таким путем получили 1,08 г (34% от теории по двум стадиям) трет-бутилового эфира (3RS, 4RS)-4-[4-(3-гидроксипропокси)фенил] -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты в виде белого аморфного твердого вещества; МС: 491 (М)+.
(г) Взаимодействием трет-бутилового эфира (3RS,4RS)-4-[4-(3-гидроксипропокси)фенил] -3-(нафталин -2-илметокси)пиперидин-1-карбоновой кислоты с мезилхлоридом аналогично описанному в примере 54(з) способу получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(3-метилсульфонилоксипропокси)фенил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде желтого масла; Rf 0,50 (SiO2, гексан:уксусный эфир = 1:1).
(д) Раствор из 850 мг сырого трет-бутилового эфира (3RS,4RS)-4-[4-(3-метилсульфонилоксипропокси)фенил] -3-(нафталин -2-илметокси)пиперидин-1-карбоновой кислоты в 6,1 мл (48,98 ммоля, 32,4 экв.) 33%-ного раствора метиламина в этаноле перемешивали в течение 14 ч при комнатной температуре. Затем раствор упаривали при пониженном давлении. Желтый твердый продукт (932 мг) хроматографировали на силикагеле с использованием смеси 90:10:0,1 метиленхлорида, метанола и аммиака в качестве элюента. Таким путем получили 610 мг (80% от теории по двум стадиям) трет-бутилового эфира (3RS,4RS)-4-[4-(3-метиламинопропокси)фенил]-3-(нафталин- 2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 505 (М+Н)+.
(е) Путем ацилирования трет-бутилового эфира (3RS,4RS)-4- [4-(3-метиламинопропокси)фенил] -3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты бензоилхлоридом аналогично описанному в примере 22 (л) способу получили трет-бутиловый эфир (3RS,4RS)-4-[4-[3-(бензоилметиламино) пропокси]фенил]-3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 609 (М+Н)+.
(ж) Аналогично описанному в примере 22(м) способу из трет-бутилового эфира (3RS, 4RS)-4-[4-[3- (бензоилметиламино)пропокси]фенил]-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты путем отщепления BOC- группы получили (3RS, 4RS)-N-метил-N-[3-[4-[3-(нафталин-2- илокси)пиперидин-4-ил]фенокси]пропил] бензамид в виде бесцветного твердого вещества; МС: 509 (М+Н)+.
Пример 58.
Аналогично описанному в примере 8(ж) способу путем отщепления BOC-группы с помощью соляной кислоты в метаноле получали следующие соединения:
1) из 2-[4-[1-трет-бутоксикарбонил-3-(нафталин-2-илметокси) пиперидин-4-ил]фенокси] этилового эфира (3RS,4RS)-никотиновой кислоты получили гидрохлорид (3RS, 4RS)-2-[4-(3-нафталин-2- илметоксипиперидин-4-ил)фенокси] этилового эфира пиридин-3- карбоновой кислоты в виде бесцветного твердого вещества; МС: 483 (М+Н)+;
2) из трет-бутилового эфира (3RS,4RS)-4-{4-[2-(бензо[1,3] диоксол-5-карбонилокси)этокси] фенил} -3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты получили гидрохлорид (3RS, 4RS)-2-[4-(3-нaфтaлин-2-илметоксипиперидин-4-ил)фенокси] этилового эфира 1,3-бензодиоксол-5-карбоновой кислоты в виде бесцветного твердого вещества; МС: 526 (М+Н)+;
3) из трет-бутилового эфира (3RS,4RS)-3-(нaфтaлин-2-илмeтoкcи)-4-{4-[2-(тиофен-3-карбонилокси) этокси] фенил}пиперидин-1-карбоновой кислоты получили гидрохлорид (3RS, 4RS)-2-[4-(3-нафталин-2-илметоксипиперидин-4-ил)фенокси] этилового эфира тиофен-3-карбоновой кислоты в виде бесцветного твердого вещества; МС: 488 (М+Н)+;
4) из трет-бутилового эфира (3RS,4RS)-3-(нaфтaлин-2- илмeтoкcи)-4-[4-[2-(тиофен-2-карбонилокси)этокси]фенил] пиперидин-1-карбоновой кислоты получили гидрохлорид (3RS, 4RS)-2- [4-(3-нафталин-2-илметоксипиперидин-4-ил)фенокси] этилового эфира тиофен-2-карбоновой кислоты в виде бесцветного твердого вещества; МС: 488 (М+Н)+;
5) из трет-бутилового эфира 4-[4-[2-(фуран-3- карбонилокси)этокси]фенил] -3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты получили гидрохлорид 2-[(3RS, 4RS)-4-[3- (нафталин-2-илметокси)пиперидин-4-ил]фенокси] этилового эфира фуран-3-карбоновой кислоты в виде бесцветного твердого вещества; МС: 472 (М+Н)+;
6) из трет-бутилового эфира 4-[4-[2-(фуран-2- карбонилокси)этокси]фенил] -3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты получили гидрохлорид 2-[(3RS, 4RS)-4-[3- (нафталин-2-илметокси)пиперидин-4-ил]фенокси] этилового эфира фуран-2-карбоновой кислоты в виде бесцветного твердого вещества; МС: 472 (М+Н)+;
7) из смеси трет-бутилового эфира (3RS,4RS)-4-[4-[2-[(RS)- и (SR)-метоксифенилацетокси] этокси] фенил]-3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты получили смесь гидробромида (3RS, 4RS)-2-[4-(2-нафталин-2-илметоксипиперидин-4-ил)фенокси] этилового эфира (RS)- и (SR)-метoкcифенилукcуcнoй кислоты в виде коричневатого твердого вещества; МС: 526 (М+Н)+;
8) из трет-бутилового эфира (3RS,4RS)-4- [4-[2-(2-метилсульфанилбензоилокси)этокси]фенил]-3-(нафталин- 2-илметокси)пиперидин-1-карбоновой кислоты получили гидрохлорид (3RS, 4RS)-2-[4-(3-нaфтaлин-2-илметoксипиперидин-4-ил)фенокси] этилового эфира 2-метилсульфанилбензойной кислоты в виде окрашенного в бежевый цвет твердого вещества; МС: 528 (М+Н)+;
9) из трет-бутилового эфира (3RS,4RS)-4-{4-[2-[(RS)- и (SR)-2-метилсульфинилбензоилокси] этокси] фенил} -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты получили гидрохлорид (3RS, 4RS)-2-[4-(2-нафталин-2-илметоксипиперидин- 4-ил)фенокси] этилового эфира (RS)- и (SR)-2-метилcульфинилбензoйнoй кислоты в виде бесцветного твердого вещества; МС: 544 (М+Н)+.
Использованные в качестве исходных субстанций BOC-производные получали аналогично примеру 24(м) с применением гидрохлорида N-этил-N'-(3-диметиламинопропил)карбодиимида (ЭДК) в качестве агента конденсации следующим образом.
(а) Из трет-бутилового эфира (3RS,4RS)-4-[4-(2- гидроксиэтокси)фенил]-3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты и пиридин-3-карбоновой кислоты получили 2-[4- [1-трет-бутоксикарбонил-3-(нафталин-2-илметокси)пиперидин-4- ил]фенокси] этилового эфира (3RS,4RS)-никотиновой кислоты в виде бесцветного твердого вещества; МС: 481 (М-C4H9COO)+.
(б) Из трет-бутилового эфира (3RS,4RS)-4-[4-(2-гидроксиэтокси) фенил]-3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты и пиперониловой кислоты получили трет-бутиловый эфир (3RS,4RS)-4- {4-[2-(бензо[1,3]диоксол-5-карбонилокси)этокси] фенил} -3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 626 (М+Н)+.
(в) Из трет-бутилового эфира (3RS,4RS)-4-[4-(2-гидроксиэтокси)фенил]-3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты и тиофен-3- карбоновой кислоты получили трет-бутиловый эфир (3RS,4RS)-3- (нафталин-2-илметокси)-4-{ 4-[2-(тиофен-3-карбонилокси)этокси] фенил}пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 587 (М)+.
(г) Из трет-бутилового эфира (3RS,4RS)-4- [4-(2-гидроксиэтокси)фенил]-3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты и тиофен-2-карбоновой кислоты получили трет- бутиловый эфир (3RS,4RS)-3-(нафталин-2-илметокси)-4-[4-[2- (тиофен-2-карбонилокси)этокси] фенил]пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 588 (М+Н)+.
(д) Из трет-бутилового эфира (3RS,4RS)-4-[4-(2-гидроксиэтокси)фенил]-3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты и фуран-3-карбоновой кислоты получили трет-бутиловый эфир 4-[4-[2-(фуран-3-карбонилокси) этокси] фенил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 572 (М+Н)+.
(е) Из трет-бутилового эфира (3RS,4RS)-4-[4-(2-гидроксиэтокси) фенил]-3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты и фуран-2-карбоновой кислоты получили трет-бутиловый эфир 4-[4-[2-(фуран-2-карбонилокси)этокси] фенил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 572 (М+Н)+.
(ж) Из трет-бутилового эфира (3RS,4RS)-4-[4-(2- гидроксиэтокси)фенил]-3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты и (RS)--α--метоксифенилуксусной кислоты получили смесь трет-бутилового эфира (3RS, 4RS)-4-[4-[2-[(RS)- и (SR)- метоксифенилацетокси]этокси]фенил]-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 648 (М+Na)+.
(з) Из трет-бутилового эфира (3RS,4RS)-4-[4- (2-гидроксиэтокси)фенил]-3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты и 2-метилсульфанилбензойной кислоты получили трет-бутиловый эфир (3RS,4RS)-4-[4-[2-(2- метилсульфанилбензоилокси)этокси] фенил] -3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 628 (М+Н)+.
(и) К раствору из 250 мг (0,4 ммоля) трет-бутилового эфира (3RS,4RS)-4-[4-[2-(2- метилсульфанилбензоилокси)этокси] фенил] -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты в 25 мл метанола добавляли раствор 170 мг (0,8 ммоля) метапериодата натрия в 2 мл воды. Полученную реакционную смесь перемешивали в течение 8 ч при 50oC. После этого растворитель отгоняли при пониженном давлении, остаток распределяли между уксусным эфиром и водой, органическую фазу сушили над сульфатом натрия и упаривали при пониженном давлении. Таким путем получили 230 мг (90% от теории) сырого трет- бутилового эфира (3RS, 4RS)-4-{ 4-[2-[(RS)- и (SR)-2- метилсульфинилбензоилокси] этокси]фенил}-3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 644 (М+Н)+.
Пример 59
Аналогично примеру 22(м) способу путем отщепления BOC-группы получали следующие соединения:
1) из трет-бутилового эфира (3RS, 4RS)-4-[4-(3-морфолин-4- илпропокси)фенил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-[4-(3-морфолин-4-илпропокси)фенил] -3-(нафталин-2-илметокси)пиперидин в виде бесцветного твердого вещества; МС: 461 (М+Н)+;
2) из трет-бутилового эфира (3RS,4RS)-4-[4-[3-(2, 2- диметилпропионилокси)пропокси]фенил]-3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты получили (3RS,4RS)-3-[4-(3- нафталин-2-илметоксипиперидин-4-ил)фенокси] пропиловый эфир 2, 2- диметилпропионовой кислоты в виде бесцветного аморфного твердого вещества; МС: 476 (М+Н)+;
3) из трет-бутилового эфира (3RS, 4RS)- 4-[4-(3-бензоилоксипропокси)фенил] -3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты получили гидрохлорид (3RS, 4RS)-3- [4-(3-нафталин-2-илметоксипиперидин-4-ил)фенокси] пропилового эфира бензойной кислоты в виде бесцветного твердого вещества; МС: 496 (М+Н)+;
4) из трет-бутилового эфира (3RS, 4RS)-4-(4- бензилоксифенил)-3-(нафталин-2-илокси)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-(4-бензилоксифенил)-3-(нафталин-2- илокси)пиперидин в виде бесцветного аморфного твердого вещества; МС: 424 (М+Н)+;
5) из трет-бутилового эфира (3RS, 4RS)-3-(2- метоксибензилокси)-4-[4-(нафталин-2-илметокси)фенил] пиперидин-1- карбоновой кислоты получили гидрохлорид (3RS, 4RS)-3-(2- метоксибензилокси)-4-(4-нафталин-2-илметоксифенил)пиперидина в виде бесцветного твердого вещества; МС: 454 (М+Н)+.
Использованные в качестве исходных веществ BOC-производные получали следующим образом:
(а) Раствор из 200 мг (0,35 ммоля) трет-бутилового эфира (3RS,4RS)-4-[4-(3-метилсульфонилоксипропокси)фенил]-3-(нафталин- 2-илметокси)пиперидин-1-карбоновой кислоты в 1 мл уксусного эфира смешивали с 60 мкл морфолина и кипятили с обратным холодильником в течение 3 ч. Далее реакционный раствор разбавляли 5 мл уксусного эфира и дважды экстрагировали насыщенным раствором гидрокарбоната натрия порциями по 1 мл. Органические фазы сушили над сульфатом магния, упаривали при пониженном давлении и сушили в высоком вакууме. Бесцветное масло (169 мг) хроматографировали на силикагеле с использованием уксусного эфира в качестве элюента. Таким путем получили 142 мг трет-бутилового эфира (3RS,4RS)-4-[4- (3-морфолин-4-илпропокси)фенил] -3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты в виде белых кристаллов; МС: 561 (М+Н)+.
(б) Аналогично примеру 22(л) в результате ацилирования трет-бутилового эфира (3RS, 4RS)-4-[4-(3- гидроксипропокси)фенил]-3-(нафталин-2-илметокси) пиперидин-1- карбоновой кислоты хлорангидридом пивалиновой кислоты получили трет-бутиловый эфир (3RS,4RS)-4-[4-[3-(2, 2-диметилпропионилокси) пропокси] фенил] -3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты в виде бесцветного масла; МС: 576 (М+Н)+.
(в) Аналогично примеру 22(л) в результате ацилирования трет- бутилового эфира (3RS, 4RS)-4-[4-(3-гидроксипропокси)фенил] -3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты бензоилхлоридом получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(3- бeнзoилoкcипpoпoкcи)фенил]-3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты в виде бесцветного масла; Rf 0,84 (SiO2, гексан:уксусный эфир = 1:1).
(г) Смесь из 1,0 г (3,41 ммоля) трет-бутилового эфира (3RS,4RS)-3-гидрокси-4-(4-гидроксифенил)пиперидин-1-карбоновой кислоты, 471 мг (34,1 ммоля, 10 экв.) карбоната калия и 607 мл (5,11 ммоля, 1,5 экв.) бензилбромида в 30 мл диметилформамида перемешивали в течение 2 ч при комнатной температуре и в течение 15 ч при 80oC. Далее повторно добавляли 471 мг (34,1 ммоля, 10 экв.) карбоната калия и 607 мл (5,11 ммоля, 1,5 экв.) бензилбромида и перемешивание продолжали в течение 6 ч при 80oC. Охлажденную до комнатной температуры реакционную смесь сливали на 300 мл смеси льда/воды и трижды экстрагировали 250 мл уксусного эфира. Органические фазы по одному разу промывали водой и насыщенным раствором хлорида натрия, сушили над сульфатом магния, упаривали при пониженном давлении и сушили в высоком вакууме. Желтое масло (1,82 г) разделяли на силикагеле с использованием изменявшегося от 4:1 до 3:2 градиента смеси гексана и уксусного эфира в качестве элюента. Таким путем получили 620 мг (72% от теории) трет-бутилового эфира (3RS,4RS)-4-(4-бензилоксифенил)-3-гидроксипиперидин-1-карбоновой кислоты, из которого после перекристаллизации из смеси метиленхлорида и гексана было получено 361 мг (28% от теории) продукта в виде белых кристаллов; МС: 383 (М)+.
(д) Аналогично примеру 22(и) путем алкилирования трет- бутилового эфира (3RS, 4RS)-4-(4-бензилоксифенил)-3- гидроксипиперидин-1-карбоновой кислоты 2-бромметилнафталином получили трет-бутиловый эфир (3RS,4RS)-4-(4-бензилоксифенил)-3- (нафталин-2-илокси) пиперидин-1-карбоновой кислоты в виде бесцветного аморфного твердого вещества; МС: 523 (М)+.
(е) Аналогично описанному в примере 14 способу путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-(4- гидроксифенил)пиперидин-1-карбоновой кислоты 2-бромметилнафталином в присутствии карбоната калия получили трет-бутиловый эфир (3RS, 4RS)-3-гидрокси-4-[4-(нафталин-2-илметокси)фенил] пиперидин-1- карбоновой кислоты в виде бесцветного твердого вещества; МС: 434 (М+Н)+.
(ж) Аналогично описанному в примере 3(в) способу путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-[4- (нафталин-2-илметокси)фенил] пиперидин-1-карбоновой кислоты 2- метоксибензилхлоридом получили трет-бутиловый эфир (3RS, 4RS)-3-(2- метоксибензилокси)-4-[4-(нафталин-2-илметокси)фенил] пиперидин-1- карбоновой кислоты в виде бесцветного твердого вещества; МС: 554 (М+Н)+.
Пример 60.
Аналогично примеру 25(б) отщеплением 2,2,2-трихлорэтилкарбамата путем обработки цинком в ледяной уксусной кислоте получали следующие соединения:
1) из 2,2, 2-трихлорэтилового эфира (3RS,4RS)-4-[4-(3-карбамоилоксипропокси)фенил] -3-(нафталин -2-илметокси)пиперидин-1-карбоновой кислоты получили 3-{ 4-[3-(нафталин-2-илметокси)пиперидин-4-ил] фенокси}пропиловый эфир (3RS,4RS)-карбаминовой кислоты в виде бесцветного твердого вещества; МС: 435 (М+Н)+;
2) из 2,2,2- трихлорэтилового эфира (3RS, 4RS)-3-(нафталин-2-илметокси)-4-{ 4-[3-(пиридин-2- илкарбамоилокси)пропокси]фенил}пиперидин-1- карбоновой кислоты получили 3-{4-[3-(нафталин-2-илметокси) пиперидин-4-ил]фенокси}пропиловый эфир (3RS, 4RS)-пиридин-2- илкарбаминовой кислоты в виде бесцветного масла; МС: 512 (М+Н)+;
3) из 2,2,2-трихлорэтилового эфира (3RS, 4RS)-3- (нафталин-2-илметокси)-4-[3-(2-пиридин-2- илкарбамоилоксиэтокси)фенил] пиперидин-1-карбоновой кислоты получили (3RS,4RS)-2-[3-[3-(нафталин-2-илметокси)пиперидин-4-ил] фенокси] этиловый эфир пиридин-2-илкарбаминовой кислоты в виде бесцветного масла; МС: 498 (М+Н)+;
4) из 2,2,2-трихлорэтилового эфира (3RS,4RS)-4-[3-(2-карбамоилоксиэтокси)фенил] -3-(нафталин- 2-илметокси)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-2- [3-[3-(нафталин-2-илметокси)пиперидин-4-ил]фенокси] этиловый эфир карбаминовой кислоты в виде бесцветного аморфного твердого вещества; МС: 421 (М+Н)+;
5) из смеси 2,2,2-трихлорэтилового эфира (3RS,4RS)-3-(нафталин-2-илметокси)-4-[3-[2-[(RS)- и - [(SR)-тетрагидропиран-2-илокси]этокси]фенил]пиперидин-1- карбоновой кислоты при одновременном отщеплении ТГП-группы получили (3RS, 4RS)-2-[3-[3-(нафталин-2-илметокси)пиперидин-4-ил] фенокси] этанол в виде бесцветного аморфного твердого вещества; МС: 378 (М+Н)+;
6) из 2,2,2-трихлорэтилового эфира (3RS,4RS)-4- [3-(2-бензоилоксиэтокси)фенил] -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты получили (3RS,4RS)-2-[3- (3-нафталин-2-илметоксипиперидин-4-ил)фенокси] этиловый эфир бензойной кислоты в виде бесцветного аморфного твердого вещества; МС: 482 (М+Н)+;
7) из 2,2,2-трихлорэтилового эфира (3RS,4RS)-3- (нaфтaлин-2-илметокси)-4-{ 3-[3-(пиридин-2- илкарбамоилокси)пропокси] фенил}пиперидин-1-карбоновой кислоты получили 3-{ 3-[3-(нафталин-2-илметокси)пиперидин-4-ил] фенокси} пропиловый эфир (3RS,4RS)-пиридин-2-илкарбаминовой кислоты в виде бесцветного аморфного твердого вещества; МС: 512 (М+Н)+;
8) из 2,2,2-трихлорэтилового эфира (3RS,4RS)-4-[3-(4- бензоилоксибутокси)фенил]-3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-[3-[3-(нафталин-2-илокси)пиперидин- 4-ил] фенокси] бутиловый эфир бензойной кислоты в виде бесцветного аморфного твердого вещества; МС: 510 (М+Н)+.
Использованные в качестве исходных веществ 2,2,2- трихлорэтилкарбаматы получали следующим путем.
Аналогично примеру 22(а)-(в) работали следующим образом.
(а) Из 1-бензил-4-пиперидона и 3-иоданизола получили 1-бензил-4-(3-метоксифенил)пиперидин-4-ол в виде бесцветного твердого вещества; Rf 0,18 (SiO2 метиленхлорид:уксусный эфир = 1:1). Последующим элиминированием с помощью п-толуолсульфокислоты получили 1-бензил- 4-(3-метоксифенил)-1,2,3,6-тетрагидропиридин в виде бесцветного твердого вещества; МС: 279 (М)+. Затем на следующей стадии гидроборирования был получен 1-бензил-4-(3-метоксифенил)пиперидин- 3-ол в виде бесцветного порошка; МС: 297 (М)+.
Далее аналогично примеру 44(г)-(и) работали следующим образом.
(б) Путем расщепления простого метилового эфира с помощью трибромида бора в метиленхлориде из 1-бензил-4-(3-метоксифенил)пиперидин-3-ола получили (3RS, 4RS)-1-бензил-4-(3-гидроксифенил)пиперидин-3-ол в виде светло-желтого твердого вещества; МС: 283 (М)+. В результате алкилирования рац.-2-(2-иодэтокси)тетрагидропираном в присутствии карбоната калия получили смесь (3RS, 4RS)-1-бензил-4-[3-[2-[(RS)- и -[(SR)-тетрагидропиран-2-илокси]этокси]фенил] пиперидин-3-ола в виде бесцветного масла; МС: 410 (M-H)+. Аналогично примеру 22(и) при последующем алкилировании 2-бромметилнафталином получили смесь (3RS,4RS)-1-бензил-3-(нафталин-2-илметокси)-4-[3-[2-[(RS)- и -[(SR)-тетрагидропиран-2-илокси] этокси] фенил]пиперидин в виде бесцветного масла; МС: 552 (М)+. Затем аналогично примеру 25(а) отщеплением бензильной группы с помощью 2,2,2-трихлорэтилового эфира хлормуравьиной кислоты и карбоната калия получили смесь 2,2,2-трихлорэтилового эфира (3RS,4RS)-3-(нафталин-2-илметокси)-4- [3-[2-[(RS)- и - [(SR)-тетрагидропиран-2-илокси]этокси]фенил] пиперидин-1-карбоновой кислоты; Rf 0,60 (SiO2, метиленхлорид:уксусный эфир = 2: 1). Последующим отщеплением ТГП- группы с помощью п-толуолсульфокислоты получили 2,2,2-трихлорэтиловый эфир (3RS, 4RS)-4-[3-(2-гидроксиэтокси)фенил]-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты. В завершение аналогично примеру 24(н) взаимодействием с пиридин-2-карбонилазидом получили 2,2, 2-трихлорэтиловый эфир (3RS, 4RS)-3-(нафталин-2-илметокси)-4-[3-(2-пиридин-2-илкарбамоилоксиэтокси)фенил] пиперидин-1-карбоновой кислоты; Rf 0,45 (SiO2, метиленхлорид:уксусный эфир = 9:1).
(в) Аналогично примеру 44(д) путем алкилирования (3RS,4RS)-1-бензил-4-(4-гидроксифенил)пиперидин-3-ола рац. -2-(3-бромпропокси)тетрагидропираном получили (3RS, 4RS)-1-бензил-4-{4-[3-[(RS)- и (SR)-тетрагидропиран-2-илокси] пропокси]фенил}пиперидин-3-ола в виде бесцветного твердого вещества; МС: 426 (М+Н)+. При последующем алкилировании 2-бромметилнафталином аналогично описанному в примере 12(б) способу получили (3RS,4RS)-1-бензил-3- (нафталин-2-илметокси)-4-{4-[3-[(RS)- и (SR)-тетрагидропиран-2- илокси]пропокси]фенил}пиперидин в виде бесцветного твердого вещества; МС: 566 (М)+. Далее взаимодействием с 2,2,2- трихлорэтиловым эфиром хлормуравьиной кислоты аналогично примеру 12(в) был получен 2,2,2-трихлорэтиловый эфир (3RS,4RS)-3- (нафталин-2-илметокси)-4-{4-[3-[(RS)- и (SR)-тетрагидропиран-2- илокси]пропокси] фенил}пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 672 (M+Na)+ . Отщеплением ТГП-группы с помощью п-толуолсульфокислоты аналогично примеру 44(з) 2,2,2-трихлорэтиловый эфир (3RS,4RS)-4-[4-(3-гидроксипропокси) фенил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 583 (M+HN4)+. В завершение аналогично примеру 24(н) взаимодействием с изоцианатом натрия получили 2,2,2-трихлорэтиловый эфир (3RS,4RS)-4-[4-(3-карбамоилоксипропокси)фенил]-3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 609 (М+Н)+.
(г) Аналогично примеру 24(н) взаимодействием 2,2,2-трихлорэтилового эфира (3RS, 4RS)-4- [4-(3-гидроксипропокси)фенил]-3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты с пиридин-2-карбонилазидом получили 2,2, 2-трихлорэтиловый эфир (3RS, 4RS)-3-(нафталин-2-илметокси)-4- { 4- [3-(пиридин-2-илкарбамоилокси)пропокси] фенил} пиперидин-1- карбоновой кислоты в виде бесцветного твердого вещества.
(д) Аналогично примеру 24(н) взаимодействием 2,2,2-трихлорэтилового эфира (3RS, 4RS)-4-[3-(2-гидроксиэтокси)фенил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты с изоцианатом натрия получили 2,2,2- трихлорэтиловый эфир (3RS,4RS)-4-[3-(2- карбамоилоксиэтокси)фенил]-3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты в виде бесцветного твердого вещества; Rf 0,40 (SiO2, метиленхлорид:метанол = 9:1).
(е) Аналогично примеру 22(л) в результате ацилирования 2,2,2-трихлорэтилового эфира (3RS, 4RS)-4- [3-(2-гидроксиэтокси)фенил]-3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты бензоилхлоридом получили 2,2,2- трихлорэтиловый эфир (3RS, 4RS)-4-[3-(2-бензоилоксиэтокси)фенил] - 3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла.
(ж) Аналогично примеру 14 путем алкилирования (3RS,4RS)-1-бензил-4-(3-гидроксифенил)пиперидин-3-ола рац. -2- (3-бромпропокси)тетрагидропираном в присутствии карбоната калия получили смесь диастереомерных рацематов (3RS, 4RS)-1-бензил-4-{ 3- [3-(тетрагидропиран-2-илокси)пропокси]фенил}пиперидин-3-ола в виде бесцветного масла; Rf 0,38 (гексан:ацетон = 1:1). При последующем алкилировании 2-бромметилнафталином аналогично примеру 12(б) получили смесь диастереомерных рацематов (3RS, 4RS)- 1-бeнзил-3-(нaфтaлин-2-илмeтoкcи)-4-{ 3-[3-(тетрагидропиран-2- илокси)пропокси] фенил} пиперидин в виде бесцветного масла; МС: 566 (М+Н)+. Далее взаимодействием с 2,2, 2-трихлорэтиловым эфиром хлормуравьиной кислоты аналогично примеру 12(в) была получена смесь диастереомерных рацематов 2,2,2-трихлорэтилового эфира (3RS,4RS)-3-(нафталин-2-илметокси)-4-{ 3-[3-(тетрагидропиран-2- илокси)пропокси] фенил} пиперидин-1-карбоновой кислоты, которую без дальнейшей очистки и определения характеристик подвергали взаимодействию аналогично примеру 53 (в) с п-толуолсульфокислотой с получением 2,2,2-трихлорэтилового эфира (3RS,4RS)-4-[3-(3- гидроксипропокси)фенил] -3-(нафталин-2-илметокси) пиперидин-1- карбоновой кислоты. В завершение аналогично примеру 24(н) взаимодействием с пиридин-2-карбонилазидом получили 2,2,2- трихлорэтиловый эфир (3RS,4RS)-3-(нaфтaлин-2-илмeтoкcи)-4-{ 3-[3- (пиридин-2-илкарбамоилокси)пропокси]фенил} пиперидин-1-карбоновой кислоты в виде бесцветного масла; Rf 0,55 (метиленхлорид:уксусный эфир = 1:1).
(з) Аналогично примеру 14 путем алкилирования (3RS,4RS)-1-бензил-4-(3-гидроксифенил) пиперидин-3-ола рац.-2-(4- бромбутокси)тетрагидропираном [S. W. Baldwin и др., J. Org. Chem. 1985, 50, 4432-4439] и далее по описанной в разделе (ж) методике получили 2,2,2-трихлорэтиловый эфир (3RS, 4RS)-4-[3-(4- гидроксибутокси)фенил] -3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты в виде бесцветного твердого вещества; Rf 0,50 (метиленхлорид:уксусный эфир = 9:1). В результате последующего ацилирования бензоилхлоридом аналогично примеру 22(л) получили 2,2,2-трихлорэтиловый эфир (3RS,4RS)-4-[3-(4- бензоилоксибутокси)фенил] -3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты в виде бесцветного твердого вещества; Rf 0,85 (SiO2, метиленхлорид:уксусный эфир = 95:5).
Пример 61.
Аналогично описанному в примере 10(6) способу путем отщепления BOC-группы с помощью бромида цинка в метиленхлориде получали следующие соединения:
1) из трет-бутилового эфира (3RS, 4RS)-3-(нафталин-2-илметокси)-4-[4-(2-оксо-2-фенилэтокси)фенил] пиперидин-1-карбоновой кислоты получили гидробромид (3RS, 4RS)-2-[4- [3-(нафталин-2-илокси)пиперидин-4-ил]фенокси]-1-фенилэтанона в виде бесцветного твердого вещества; МС: 452 (М+Н)+;
2) из трет-бутилового эфира (3RS,4RS)-4-[4-(2-бензоилоксиэтокси) фенил] -3-(2-метоксибензилокси)пиперидин-1-карбоновой кислоты получили гидробромид (3RS, 4RS)-2-[4-[3-(2-метоксибензилокси)пиперидин-4- ил] фенокси] этилового эфира бензойной кислоты в виде окрашенного в бежевый цвет твердого вещества; МС: 462 (М+Н)+;
3) из трет-бутилового эфира (3RS,4RS)-4-[4-([1,3]диоксолан-2-илметокси)фенил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-(4-[1,3] диоксолан-2-илметоксифенил)-3- (нафталин-2-илметокси)пиперидин в виде желтоватого твердого вещества; МС: 420 (М+Н)+.
Использованные в качестве исходных веществ BOC-производные получали следующим образом:
(а) Аналогично описанному в примере 14 способу путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-(4- гидроксифенил)пиперидин-1-карбоновой кислоты аллилбромидом в присутствии карбоната калия получили трет-бутиловый эфир (3RS, 4RS) -4-(4-аллилоксифенил)-3-гидроксипиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; tпл 113oC (гексан).
(б) Аналогично описанному в примере 3(в) способу путем алкилирования трет-бутилового эфира (3RS,4RS)-4-(4-аллилоксифенил) -3-гидроксипиперидин-1-карбоновой кислоты 2-бромметилнафталином получили трет-бутиловый эфир (3RS, 4RS)-4-(4-аллилоксифенил)-3- (нафталин-2-илметокси) пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 474 (М+Н)+.
(в) Смесь из 400 мг (0,8 ммоля) трет-бутилового эфира (3RS,4RS)-4-(4-аллилоксифенил)-3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты, 0,2 мл триэтиламина, 0,5 мл воды и 78 мг трис(трифенилфосфин)родий(I)хлорида в 10 мл этанола перемешивали в течение 1 ч при нагреве с обратным холодильником. Частично образовавшийся трет-бутиловый эфир (3RS,4RS)-4-(4-гидроксифенил)-3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты (30% от теории), МС: 434 (М+Н)+, отделяли хроматографией и использовали на следующей стадии.
(г) Аналогично описанному в примере 14 способу путем алкилирования трет-бутилового эфира (3RS, 4RS)-4-(4-гидроксифенил)-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты фенацилбромидом в присутствии карбоната калия получили трет-бутиловый эфир (3RS, 4RS)-3-(нафталин-2-илметокси)-4-[4-(2-оксо-2- фенилэтокси)фенил] пиперидин-1-карбоновой кислоты в виде желтоватого твердого вещества; МС: 551 (М+Н)+.
(д) Аналогично описанному в примере 3(в) способу путем алкилирования смеси трет-бутилового эфира (3RS,4RS)-3-гидрокси-4- [4-[2-[(RS)- и -[(SR)-тетрагидропиран-2-илокси] этокси] фенил] пиперидин-1-карбоновой кислоты [пример 53 (а)] 2-метоксибензилхлоридом получили трет-бутиловый эфир (3RS, 4RS)-3-(2-метоксибензилокси)-4-{ 4-[2-[(RS)- и -[(SR)-тетрагидропиран-2-илокси]этокси]фенил}пиперидин- 1-карбоновой кислоты в виде бесцветного масла.
(е) Аналогично описанному в примере 53 (в) способу путем расщепления простого ТГП-эфира из трет-бутилового эфира (3RS,4RS)- 3-(2-метоксибензилокси)-4-{ 4-[2-[(RS)- и - [(SR)- тетрагидропиран-2-илокси]этокси]фенил}пиперидин-1-карбоновой кислоты получили трет-бутиловый эфир (3RS,4RS)-4-[4-(2- гидроксиэтокси)фенил] -3-(2-метоксибензилокси)пиперидин-1- карбоновой кислоты.
(ж) Аналогично описанному в примере 22(л) способу в результате ацилирования трет-бутилового эфира (3RS, 4RS)- 4-[4-(2-гидроксиэтокси)фенил]-3-(2-метоксибензилокси)пиперидин-1- карбоновой кислоты получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(2- бензоилоксиэтокси)фенил] -3-(2-метоксибензилокси)пиперидин-1- карбоновой кислоты в виде бесцветной вязкой жидкости; МС: 562 (М+ Н)+.
(з) Аналогично описанному в примере 14 способу путем алкилирования трет-бутилового эфира (3RS,4RS)-3-гидрокси-4- (4-гидроксифенил) пиперидин-1-карбоновой кислоты 2-бромметил-1,3- диоксоланом в присутствии карбоната калия получили трет-бутиловый эфир (3RS,4RS)-4-[4-([1,3]диоксолан-2-илметокси)фенил] -3- гидроксипиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; tпл 136-137oC (гексан).
(и) Аналогично описанному в примере 3(в) способу путем алкилирования смеси трет-бутилового эфира (3RS, 4RS)-4-[4-([1,3] диоксолан-2-илметокси)фенил] -3- гидроксипиперидин-1-карбоновой кислоты 2-бромметилнафталином получили трет-бутиловый эфир (3RS, 4RS)-4-[4-([1,3] диоксолан-2- илметокси)фенил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 520 (М+Н)+.
Пример 62.
Раствор из 210 мг (0,425 ммоля) трет-бутилового эфира (3RS,4RS, 5SR)-4-(4-хлорфенил)-3-нафталин-2-илметокси-5- пропилпиперидин-1-карбоновой кислоты в 18 мл метанола смешивали с 12 мл 1 н. соляной кислоты и перемешивали при 50oC в течение ночи. Далее раствор упаривали при пониженном давлении, остаток растворяли в теплом толуоле и снова упаривали, при этом продукт начинал выпадать в осадок. Таким путем получили 153 мг (84% от теории) гидрохлорида (3RS, 4RS,5SR)-4-(4-xлopфeнил)-3-нaфтaлин- -2-илметокси-5-пропилпиперидина в виде бесцветного твердого вещества; МС: 252 (M-нафтилметил)+.
Использованный в качестве исходного соединения трет- бутиловый эфир (3RS, 4RS,5SR)-4-(4-хлорфенил)-3-нафталин-2- илметокси-5-пропилпиперидин-1-карбоновой кислоты получали следующим образом:
(а) Аналогично описанному у A. Ziering и др. в J. Org. Chem. 22, 1521-1528 (1957) способу получения пиперидин-4-онов из соответствующих эфиров акриловых кислот взаимодействием с метиламином либо бензиламином, реакцией с этиловым либо метиловым эфиром акриловой кислоты, циклизацией и последующего декарбалкоксилирования, исходя из этилового эфира 2-пропилакриловой кислоты и метиламина, получили (3RS)-1-метил-3-пропилпиперидин-4-он в виде бесцветного масла; Rf 0,38 (SiO2, метиленхлорид:метанол = 95:5).
(б) К охлажденному до -78oC раствору из 25,68 г (134 ммоля) 1-бром-4-хлорбензола в 250 мл трет-бутилметилового эфира в течение 30 мин по каплям добавляли 83,8 мл (134 ммоля) н-BuLi (1,6 н. в гексане). Далее по окончании добавления смесь перемешивали в течение 1 ч при -78oC. Затем при температуре в интервале от -70 до -65oC по каплям добавляли раствор из 10,41 г (67,05 ммоля) (3RS)-1-метил-3-пропилпиперидин-4-она в 100 мл трет-бутилметилового эфира. По окончании этого добавления смесь перемешивали при -78oC в течение 2 ч. Для дальнейшей переработки реакционную смесь сливали на лед, смесь переносили в делительную воронку и отделяли органическую фазу. Водную фазу экстрагировали уксусным эфиром, после чего объединенные органические фазы сушили над сульфатом натрия и упаривали при пониженном давлении. Для очистки сырой продукт хроматографировали на силикагеле с использованием смеси 95:5: 0,1 метиленхлорида, метанола и аммиака в качестве элюента. Таким путем получили 15,9 г (88% от теории) (3RS,4RS)- и (3RS,4RS)-4-(4- хлорфенил)-1-метил-3-пропилпиперидин-4-ола в виде бесцветного твердого вещества; МС: 267 (М)+.
(в) Раствор из 13,68 г (51,06 ммоля) (3RS, 4RS)- и (3RS,4SR)-4-(4-хлорфенил)-1-метил-3-пропилпиперидин-4-ола в 67 мл трифторуксусной кислоты кипятили с обратным холодильником в течение 18 ч. После этого реакционный раствор упаривали при пониженном давлении. Остаток распределяли между насыщенным раствором карбоната натрия и простым эфиром, затем отделенную водную фазу экстрагировали простым эфиром и в завершение объединенные органические фазы сушили над сульфатом натрия и упаривали при пониженном давлении. Для очистки и разделения изомерных олефинов сырой продукт хроматографировали на силикагеле с использованием смеси 96:4 метиленхлорида и метанола в качестве элюента. Таким путем в каждом случае в виде желтоватого масла получили 9,71 г (76% от теории) (RS)-4-(4-хлорфенил)-1-метил-3-пропил-1,2,3, 6- тетрагидропиридина [МС: 249 (М)+] и 1,74 г 4-(4-хлорфенил)-1- метил-5-пропил-1,2,3,6-тетрагидропиридина; МС: 248 (M-H)+.
(г) К суспензии из 9,7 г (39 ммолей) (RS)-4-(4-хлорфенил)-1-метил-3-пропил-1,2,3,6-тетрагидропиридина в 80 мл 1,2-диметоксиэтана с помощью шпателя добавляли 2,23 г (60 ммолей) борoгидрида натрия таким образом, чтобы температура не превышала 35oC. Далее в течение 45 мин по каплям добавляли 13,2 мл эфирата трифторида бора, растворенного в 15 мл 1,2-диметоксиэтана, а затем реакционную смесь перемешивали в течение 2 ч при комнатной температуре. После этого последовательно сначала при 30oC медленно по каплям добавляли раствор 15,65 г (277 ммолей) гидроксида калия, растворенного в 60 мл воды, а затем в течение 15 мин добавляли 11,22 мл 30%-ного раствора перекиси водорода, при этом температура поднималась до 40oC. Далее смесь кипятили с обратным холодильником в течение 2,5 ч. Для дальнейшей переработки охлажденную реакционную смесь фильтровали через дикалит, после чего его промывали уксусным эфиром. Полученный раствор смешивали с уксусным эфиром и водой, органическую фазу отделяли, а водную фазу затем экстрагировали 100 мл уксусного эфира. Объединенные органические фазы сушили над сульфатом натрия и упаривали при пониженном давлении. Для очистки сырой продукт хроматографировали на силикагеле с использованием смеси 95:5 метиленхлорида и метанола в качестве элюента. Таким путем получили 8,64 г (73% от теории) (3RS,4RS, 5SR)-4-(4-хлорфенил)-1-метил-5-пропилпиперидин-3- ола в виде бесцветного твердого вещества; МС: 267 (М)+.
(д) Смесь из 7,19 г (26,85 ммоля) (3RS,4RS, 5SR)-4-(4- хлорфенил)-1-метил-5-пропилпиперидин-З-ола, 5,96 г (80,7 ммоля) карбоната лития и 14,22 г (67,1 ммоля) 2,2,2-трихлорэтилового эфира хлормуравьиной кислоты в 200 мл толуола перемешивали в течение 8 ч при 105oC. Для дальнейшей переработки охлажденную реакционную смесь смешивали с водным раствором карбоната натрия и уксусным эфиром. Органическую фазу отделяли, сушили над сульфатом натрия и упаривали при пониженном давлении. Для очистки сырой продукт хроматографировали на силикагеле с использованием смеси 1:1 метиленхлорида и гексана в качестве элюента. Таким путем получили 13,05 г (80% от теории) 2,2,2-трихлорэтилового эфира (3RS,4RS,5SR)-4-(4-хлорфенил)-3-пропил-5-(2,2,2- трихлорэтоксикарбонилокси) пиперидин-1-карбоновой кислоты в виде желтоватого масла; МС: 621 (М+NH4)+.
(е) Смесь из 13,05 г (21,6 ммоля) 2,2,2-трихлорэтилового эфира (3RS,4RS, 5SR)-4-(4-хлорфенил)-3-пропил-5-(2,2,2- трихлорэтоксикарбонилокси) пиперидин-1- карбоновой кислоты и 14,5 г цинка в 200 мл ледяной уксусной кислоты в течение 15 ч обрабатывали в ультразвуковой ванне. Далее с целью обеспечить полноту реакции дополнительно добавляли 5 г цинка и оставляли для обработки в ультразвуковой ванне еще на 5 ч. Для дальнейшей переработки цинк отфильтровывали через вакуум-фильтр, после чего остаток промывали ледяной уксусной кислотой и раствор упаривали досуха при пониженном давлении. Остаток распределяли между 1 н. NaOH и уксусным эфиром, а отделенную водную фазу затем еще раз экстрагировали уксусным эфиром и в завершение объединенные органические фазы упаривали при пониженном давлении. После этого сырой продукт кристаллизовали из диэтилового эфира, в результате чего получили 3,0 г (55% от теории) (3RS,4RS, 5SR)-4-(4- хлорфенил)-5-пропилпиперидин-3-ола в виде бесцветных кристаллов; МС: 253 (М)+. Для очистки маточный раствор хроматографировали на силикагеле с использованием смеси 90:10:0,1 метиленхлорида, метанола и аммиака в качестве элюента. Таким путем дополнительно получили 1,1 г (20% от теории) (3RS,4RS,5SR)-4-(4-хлорфенил)-5- пропилпиперидин-3-ола.
(ж) Раствор из 3,05 г (12,0 ммолей) (3RS,4RS,5SR)-4-(4-хлорфенил)-5-пропилпиперидин-3-ола в 20 мл диметилформамида смешивали при 0oC с 1,34 г (13,2 ммоля) триэтиламина и 3,02 г (13,8 ммоля) ди- трет-бутилдикарбоната и перемешивали в течение 15 ч при комнатной температуре. Далее диметилформамид отгоняли в вакууме, создаваемом масляным насосом, и для очистки остаток хроматографировали на силикагеле с использованием смеси 99:1 метиленхлорида и метанола в качестве элюента. Таким путем получили 3,92 г (92% от теории) трет-бутилового эфира (3RS, 4RS, 5SR)-4-(4-хлорфенил)-3-гидрокси-5- пропилпиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 297 (M-C4H8)+.
(з) К раствору из 200 мг (0,56 ммоля) трет-бутилового эфира (3RS,4RS, 5SR)-4-(4-хлорфенил)-3-гидрокси-5- пропилпиперидин-1-карбоновой кислоты и 188 мг (0,85 ммоля) 2- бромметилнафталина в 10 мл диметилформамида добавляли 37 мг (0,85 ммоля) гидрида натрия (55%-ная дисперсия в вазелиновом масле) и реакционную смесь перемешивали в течение 5 ч при комнатной температуре. Для дальнейшей переработки реакционную смесь упаривали в вакууме, создаваемом масляным насосом, остаток распределяли между водой и простым эфиром, после чего отделенную водную фазу пять раз экстрагировали путем встряхивания простым эфиром, используя порции по 50 мл. Объединенные эфирные экстракты промывали насыщенным раствором хлорида натрия, сушили над сульфатом натрия и упаривали при пониженном давлении. Для очистки сырой продукт хроматографировали на силикагеле с использованием смеси 96:4 толуола и уксусного эфира в качестве элюента. Таким путем получили 215 мг (77% от теории) трет-бутилового эфира (3RS,4RS, 5SR)-4-(4-хлорфенил)-3-нафталин-2-илметокси-5- пропилпиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 494 (М+Н)+.
Пример 63.
Аналогично примеру 62 получали следующие соединения:
1) из трет-бутилового эфира (3RS,4RS,5SR)-4- (4-хлорфенил)-3-(4-метоксибензилокси)-5-пропилпиперидин-1- карбоновой кислоты получили (3RS,4RS, 5SR)-4-(4-хлорфенил)-3-(4- метоксибензилокси)-5-пропилпиперидин в виде желтоватого масла; МС: 252 (M-метоксибензил)+;
2) из трет-бутилового эфира (3RS,4RS, 5SR)-4-(4-хлорфенил)-3-(1-этил-1H-бензимидазол-2- илметокси)-5-пропилпиперидин-1-карбоновой кислоты получили (3RS, 4RS, 5SR)-4-(4-хлорфенил)-3-(1-этил-1H- бензимидазол-2-илметокси)-5-пропилпиперидин в виде бесцветного твердого вещества; МС: 412 (М+Н)+.
Использованные в качестве исходных субстанций BOC-производные получали следующим путем.
Аналогично примеру 62(з) путем алкилирования трет-бутилового эфира (3RS, 4RS, 5SR)-4-(4-хлорфенил)-3-гидрокси-5- пропилпиперидин-1-карбоновой кислоты 4-метоксибензилхлоридом получили трет-бутиловый эфир (3RS,4RS, 5SR)-4-(4-хлорфенил)-3- (4-метоксибензилокси)-5-пропилпиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 416 (M-C4H9)+.
Аналогично примеру 62(з) путем алкилирования трет-бутилового эфира (3RS, 4RS, 5SR)-4-(4-хлорфенил)-3-гидрокси-5-пропилпиперидин-1- карбоновой кислоты 2-хлорметил-1-этил-1H-бензоимидазолом [Acta Pol. Pharm. 1977, 34(4), 359-369] получили трет-бутиловый эфир (3RS,4RS,5SR)-4-(4-хлорфенил)-3-(1-этил-1H-бензимидазол-2- илметокси)-5-пропилпиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 495 (М+Н)+.
Пример 64.
Аналогично примeру 5 путем обработки 2-триметилсиланилэтилового эфира (3RS, 4RS, 5SR)-3-(4-бензилоксинафталин-2-илметокси) -4-(4-фторфенил)-5-пропилпиперидин-1-карбоновой кислоты раствором тетрабутиламмонийфторида получили (3RS, 4RS,5SR)-3-(4- бензилоксинафталин-2-илметокси)-4-(4-фторфенил)-5-пропилпиперидин в виде бесцветного твердого вещества; МС: 484 (М+Н)+.
Использованный в качестве исходной субстанции 2- триметилсиланилэтиловый эфир (3RS, 4RS, 5SR)-3-(4- бензилоксинафталин-2-илметокси)-4-(4-фторфенил)-5-пропилпиперидин- 1-карбоновой кислоты получали следующим путем.
(а) Аналогично примеру 62(а)-(г) исходя из (RS)-1-бензил-3-пропилпиперидин-4-она[ МС: 231 (М)+] и 1-бром-4-фторбензола получили (3RS,4RS,5SR)-1-бeнзил-4-(4-фтopфeнил)-5-пpoпилпипepидин-3-oл в виде бесцветного твердого вещества; МС: 327 (М)+.
(б) Аналогично примеру 62(з) путем алкилирования (3RS,4RS,5SR)-1-бензил-4-(4-фторфенил)-5-пропилпиперидин-3-ола 1- бензилокси-3-хлорметилнафталином получили (3RS, 4RS, 5SR)-1-бензил- 3-(4-бензилоксинафталин-2-илметокси)-4-(4-фторфенил)-5- пропилпиперидин в виде желтой смолы; МС (ISP): 574 (М+Н)+.
(в) Аналогично примеру 1(г) взаимодействием (3RS,4RS,5SR)-1-бензил-3-(4-бензилоксинафталин-2-илметокси) -4-(4-фторфенил)-5-пропилпиперидина с β- -триметилсилилэтиловым эфиром хлормуравьиной кислоты [Synthesis 346 (1987)] получили 2-триметилсиланилэтиловыйэфир (3RS, 4RS,5SR)-3-(4- бензилоксинафталин-2-илметокси)-4-(4-фторфенил)-5- пропилпиперидин-1-карбоновой кислоты в виде светло-желтого сиропа; МС: 628 (М+Н)+.
Использованный в качестве исходного соединения 1-бензилокси-3-хлорметилнафталин получали следующим путем.
(а) Аналогично примеру 14(а) путем алкилирования этилового эфира 4-гидроксинафталин-2-карбоновой кислоты [J. Agric. Chem. Soc. Japan 24, 313 (1950)] бензилбромидом получили этиловый эфир 4- бензилоксинафталин-2-карбоновой кислоты в виде практически бесцветного твердого вещества; Rf 0,53 (SiO2, гексан:уксусный эфир = 4:1).
(б) В результате восстановления этилового эфира 4- бензилоксинафталин-2-карбоновой кислоты аналогично примеру 7(б) был получен (4-бензилоксинафталин-2-ил)метанол в виде бесцветного твердого вещества; Rf 0,42 (SiO2, гексан:уксусный эфир = 2:1).
(в) Хлорированием (4-бензилоксинафталин-2-ил)метанола аналогично примеру 7 (в) получили 1-бензилокси-3-хлорметилнафталин в виде бесцветного твердого вещества; МС: 282 (М)+.
Пример 65.
Аналогично примеру 62 получали следующие соединения:
1) из трет-бутилового эфира (3RS,4RS, 5SR)-4-(4-хлорфенил)-5-изопропил-3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты получили гидрохлорид (3RS,4RS,5SR)-4-(4-хлорфенил)-5-изопропил-3-(нафталин-2- илметокси)пиперидина в виде бесцветного твердого вещества; МС: 394 (М+Н)+;
2) из трет-бутилового эфира (3RS,4RS,5SR)-4-(4-бромфенил)-5- изобутил-3-нафталин-2-илметоксипиперидин-1-карбоновой кислоты получили гидрохлорид (3RS,4RS,5SR)-4-(4-бромфенил)-5-изобутил- 3-нафталин-2-илметоксипиперидина в виде бесцветного твердого вещества; МС: 310 (M-нафтилметил)+;
3) из трет-бутилового эфира (3RS,4RS,5SR)-4- (4-фторфенил)-5-метил-3-нафталин-2-илметоксипиперидин-1-карбоновой кислоты получили гидрохлорид (3RS, 4RS, 5SR)-4-(4-фторфенил) -5-метил-3-нафталин-2-илметоксипиперидина в виде бесцветного твердого вещества; Rf 0,37 (SiO2, метиленхлорид:метанол: аммиак = 95:5:0,1);
4) из трет-бутилового эфира (3RS,4RS,5SR)-5-бензил-4-(4-фторфенил)-3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты получили гидрохлорид (3RS, 4RS,5SR)-5-бензил-4-(4-фторфенил)-3 - нафталин-2-илметоксипиперидина в виде бесцветного твердого вещества; МС: 426 (М+Н)+.
Использованные в качестве исходных субстанций BOC-производные получали следующим путем.
Аналогично примеру 62(а)-(з) работали следующим образом.
(а) Исходя из этилового эфира 2-изопропилакриловой кислоты и метиламина получили (3RS)-1-метил-3-изопропилпиперидин-4-он в виде бесцветного масла; МС: 155 (М)+. Взаимодействием с 1-бром-4- хлорбензолом получили (3RS,4RS)- и (3RS,4SR)-4-(4-хлорфенил)-3- изопропил-1-метилпиперидин-4-ол в виде бесцветного твердого вещества; МС: 267 (М)+. Далее элиминированием с помощью трифторуксусной кислоты с последующим хроматографическим разделением получили оба изомерных олефина, в каждом случае в виде бесцветного масла, а именно (RS)-4-(4-хлорфенил)-3-изопропил-1- метил-1,2,3,6-тетрагидропиридин [МС: 249 (М)+] и 4-(4-хлорфенил)-5-изопропил-1-метил-1,2,3,6-тетрагидропиридин. Гидроборированием (RS)-4-(4-хлорфенил)-3-изопропил-1-метил-1,2,3,6- тетрагидропиридина получили (3RS, 4RS,5SR)-4-(4-хлорфенил)-5- изопропил-1-метилпиперидин-3-ол в виде бесцветного твердого вещества; МС: 267 (М)+. В результате последующего взаимодействия с 2,2,2-трихлорэтиловым эфиром хлормуравьиной кислоты получили 2,2,2-трихлорэтиловый эфир (3SR,4RS, 5RS)-4-(4- хлорфенил)-3-изопропил-5-(2,2,2-трихлорэтоксикарбонилокси) пиперидин-1-карбоновой кислоты в виде желтоватого масла; МС: 619, 621, 623, 625 (M+NH4)+. Отщеплением ТРОК-группы с помощью цинка в ледяной уксусной кислоте получили (3RS, 4RS,5SR)-4-(4- хлорфенил)-5-изопропилпиперидин-3-ол в виде бесцветного твердого вещества; МС: 253 (М)+. Из этого продукта путем введения BOC-группы получили трет-бутиловый эфир (3RS,4RS,5SR)-4-(4-хлорфенил) -3-гидрокси-5-изопропилпиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 297 (M-C4H8)+. В завершение алкилированием 2-бромметилнафталином получили трет-бутиловый эфир (3RS,4RS, 5SR)-4-(4-хлорфенил)-5-изопропил-3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 437 (M-C4H8)+.
Аналогично примеру 62(а)-(з) работали следующим образом.
(б) Исходя из метилового эфира 2-изобутилакриловой кислоты и бензиламина получили (3RS)-1-бензил-3-изoбутилпипepидин-4-oн в виде желтоватого масла; МС: 245 (М)+. Взаимодействием с 1,4-дибромбензолом с последующим элиминированием с помощью трифторуксусной кислоты, а также хроматографическим разделением получили оба изомерных олефина, в каждом случае в виде коричневатого масла, а именно (RS)-1-бензил-4-(4-бромфенил)-3- изобутил-1,2,3,6-тетрагидропиридин [МС: 383 (М)+] и 1-бензил-4-(4-бромфенил)-5-изобутил-1,2,3,6-тетрагидропиридин. Далее гидроборированием (RS)-1-бензил-4-(4-бромфенил)-3-изобутил- 1,2,3,6-тетрагидропиридина получили (3RS,4RS, 5SR)-1-бензил-4-(4- бромфенил)-5-изобутил-1-метилпиперидин-3-ол в виде бесцветного твердого вещества; МС: 401 (М)+. В результате последующего взаимодействия с 2,2,2-трихлорэтиловым эфиром хлормуравьиной кислоты получили 2,2,2-трихлорэтиловый эфир (3RS, 4RS, 5SR)-4-(4- бромфенил-5-изобутил-3-(2,2,2-трихлорэтоксикарбонилокси) пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; Rf 0,25 (SiO2, метиленхлорид:гексан = 1:1). Отщеплением ТРОК-группы с помощью цинка в ледяной уксусной кислоте получили (3RS,4RS, 5SR)-4-(4-бромфенил)-5-изобутилпиперидин-3-ол в виде бесцветного твердого вещества; МС: 311 (М)+. Из этого продукта путем введения BOC-группы получили трет-бутиловый эфир (3RS, 4RS, 5SR)-4-(4-бромфенил)-3- гидрокси-5-изобутилпиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 412 (М+Н)+. В завершение алкилированием 2-бромметилнафталином получили трет-бутиловый эфир (3RS,4RS,5SR)-4-(4-бромфенил)-5-изобутил-3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты в виде бесцветной пены; МС: 552 (М+Н)+.
Аналогично примеру 62(б)-(г) работали следующим образом.
(в) Из (RS)-1-бензил-3-метилпиперидин-4-она и 1-бром-4- фторбензола получили (3RS, 4RS)- и (3RS, 4SR)-1-бензил-4-(4- фторфенил)-3-метилпиперидин-4-ол в виде бесцветного твердого вещества; МС: 299 (М)+. Путем элиминирования с помощью трифторуксусной кислоты и хроматографического разделения получили оба изомерных олефина, в каждом случае в виде коричневатого масла, а именно (RS)-1-бензил-4-(4-фторфенил)-3-метил-1,2,3,6- тетрагидропиридин [МС: 281 (М)+] и 1-бензил-4-(4-фторфенил)-5- метил-1,2,3,6-тетрагидропиридин; МС: 281 (М)+. Последующим гидроборированием (RS)-1-бензил-4-(4-фторфенил)-3-метил-1,2,3,6- тетрагидропиридина получили (3RS, 4RS, 5SR)-1-бензил-4-(4- фторфенил)-5-метилпиперидин-3-ол в виде бесцветного твердого вещества; МС: 299 (М)+.
(г) Раствор из 600 мг (2 ммоля) (3RS,4RS, 5SR)-1-бензил-4- (4-фторфенил)-5-метилпиперидин-3-ола в 20 мл метанола гидрировали в присутствии 60 мг палладия на угле (10%-ного) при комнатной температуре и нормальном давлении. Для дальнейшей переработки катализатор отфильтровывали, затем его отделяли путем перемешивания в теплом метаноле и снова отфильтровывали. Объединенные метанольные растворы упаривали при пониженном давлении. Полученный сырой продукт (410 мг) без дальнейшей очистки использовали на следующей стадии. Взятую из этого продукта для анализа пробу перекристаллизовывали из простого эфира/гексана. Таким путем получили гидрохлорид (3RS,4RS,5SR)-4-(4-фторфенил)-5-метилпиперидин-3-ола в виде бесцветных кристаллов; МС: 209 (М)+.
(д) Путем введения защитной BOC-группы из гидрохлорида (3RS,4RS,5SR)-4-(4-фторфенил)-5-метилпиперидин-3-ола получили трет-бутиловый эфир (3RS, 4RS, 5SR)-4-(4-фторфенил)-3- гидрокси-5-метилпиперидин- 1-карбоновой кислоты в виде бесцветного масла; МС: 253 (M-C4H8)+. В завершение алкилированием 2-бромметилнафталином получили трет-бутиловый эфир (3RS,4RS,5SR) -4-(4-фторфенил)-5-метил-3-нафталин-2-илметоксипиперидин-1- карбоновой кислоты в виде бесцветного твердого вещества; МС: 393 (M-C4H8)+.
Аналогично примеру 62(а)-(г) и (ж)-(з) работали следующим образом.
(а) Исходя из этилового эфира 2-бензилакриловой кислоты и бензиламина получили (3RS)-1,3-дибензилпиперидин-4-он в виде желтоватого масла; МС: 279 (М)+. Взаимодействием с 1-бром-4-фторбензолом получили (3RS,4RS)- и (3RS, 4SR)-1,3-дибензил-4-(4-фторфенил)пиперидин-4-ол в виде бесцветного твердого вещества; МС: 375 (М)+. Путем элиминирования с помощью трифторуксусной кислоты с последующим хроматографическим разделением получили оба изомерных олефина, а именно (RS)-1, 3-дибензил-4-(4-фторфенил)-1,2,3,6-тетрагидропиридин в виде желтого твердого вещества [МС: 357 (М)+] и 1,5-дибензил-4- (4-фторфенил)-1,2,3,6-тетрагидропиридин. Последующим гидроборированием (RS)-1,3-дибензил-4-(4-фторфенил) -1,2,3,6-тетрагидропиридина получили (3RS, 4RS, 5SR)-1,5-дибензил-4-(4-фторфенил)пиперидин-3-ол в виде бесцветного твердого вещества; МС: 375 (М)+. В результате отщепления бензильной группы с помощью каталитического гидрирования аналогично описанному выше примеру получили (3RS, 4RS, 5SR)-5- бензил-4-(4-фторфенил)пиперидин-3-ол в виде бесцветного твердого вещества; МС: 285 (М)+. Путем введения BOC-группы из этого продукта получили трет-бутиловый эфир (3RS,4RS,5SR)-3-бензил-4-(4- фторфенил)-5-гидроксипиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 329 (M-C4H8)+. В завершение алкилированием 2-бромметилнафталином получили трет-бутиловый эфир (3RS, 4RS, 5SR)-5-бензил-4-(4-фторфенил)-3 -(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветной пены; Rf 0,32 (SiO2, толуол:уксусный эфир = 95:5).
Пример 66.
Аналогично описанному у A. Mann и др. в Synth. Comm. 19(18), 3139-3142 (1989) способу 40 мг (0,08 ммоля) трет-бутилового эфира (3SR,4RS, 5RS)-4-(4-хлорфенил)-3-(1-этилпропил)-5-(нафталин-2- илметокси)пиперидинкарбоновой кислоты растворяли в 5 мл сухого метиленхлорида и смешивали с 35 мг (0,16 ммоля) безводного бромида цинка. Реакционную смесь перемешивали в течение 5 ч при комнатной температуре. Для дальнейшей переработки реакционную смесь упаривали при пониженном давлении и полученный сырой продукт очищали хроматографей на силикагеле с использованием смеси 90:10:0,1 метиленхлорида, метанола и аммиака в качестве элюента. Таким путем получили 28 мг (86% от теории) (3SR, 4RS, 5RS)-4-(4- хлорфенил)-3-(1-этилпропил)-5-(нафталин-2-илметокси)пиперидина в виде бесцветного масла; МС: 422 (М+Н)+.
Использованный в качестве исходной субстанции трет-бутиловый эфир (3SR, 4RS,5RS)-4-(4-хлорфенил)-3-(1-этилпропил)-5- (нафталин-2-илметокси)пиперидинкарбоновой кислоты получали аналогично примеру 62(а)-(з) следующим образом.
Исходя из метилового эфира 2-(1-этилпропил)акриловой кислоты и метиламина получили (3RS)-3-(1-этилпропил)-1-метилпиперидин-4-он в виде бесцветного масла; МС: 183 (М)+. Взаимодействием с 1-бром-4-хлорбензолом из этого продукта получили (3RS,4RS)- и (3RS,4SR)-4-(4-хлорфенил)-3-(1-этилпропил)-1-метилпиперидин-4-ол в виде бесцветного твердого вещества; МС: 295 (М)+. Далее элиминированием с помощью трифторуксусной кислоты и хроматографическим разделением получили оба изомерных олефина, в каждом случае в виде бесцветного масла, а именно (RS)-4-(4-хлорфенил)-3-(1-этилпропил)-1-метил-1,2,3,6- тетрагидропиридин [МС: 277 (М)+] и 4-(4-хлорфенил)-5-(1- этилпропил)-1-метил-1,2,3,6-тетрагидропиридин. Последующим гидроборированием (RS)-4-(4-хлорфенил)-3-(1-этилпропил)-1-метил- 1,2,3,6-тетрагидропиридина получили (3RS,4RS,5SR)-4-(4-хлорфенил)- 5-(1-этилпропил)-1-метилпиперидин-3-ол в виде бесцветного твердого вещества; МС: 296 (М+Н)+. В результате последующего взаимодействия с 2,2,2-трихлорэтиловым эфиром хлормуравьиной кислоты получили 2,2,2-трихлорэтиловый эфир (3SR, 4RS, 5RS)-4-(4- хлорфенил)-3-(1-этилпропил)-5-(2,2,2- трихлорэтоксикарбонилокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 653 (M+Na)+. Отщеплением ТРОК-группы с помощью цинка в ледяной уксусной кислоте получили (3RS,4RS,5SR)-4- (4-хлорфенил)- 5-(1-этилпропил)пиперидин-3-ол в виде бесцветного твердого вещества; МС: 281 (М)+. Из этого продукта путем введения защитной BOC-группы получили трет-бутиловый эфир (3SR,4RS,5RS)-4- (4-хлорфенил)-3-(1-этилпропил)-5-гидроксипиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 325 (M-C4H8 )+. В завершение алкилированием 2-бромметилнафталином получили трет-бутиловый эфир (3SR, 4RS, 5RS) -4-(4-хлорфенил)-3-(1-этилпропил) -5-(нафталин-2-илметокси)пиперидинкарбоновой кислоты; Rf 0,41 (SiO2, толуол: уксусный эфир = 95:5).
Пример 67.
Аналогично примеру 66 из трет-бутилового эфира (3SR,4RS,5RS) -4-(4-хлорфенил)-3- изопропил-5-(4-метоксибензилокси)пиперидинкарбоновой кислоты получили трет-бутиловый эфир (3SR,4RS,5RS)-4-(4-хлорфенил)-3- изопропил-5-(4-метоксибензилокси)пиперидин в виде бесцветного масла; Rf 0,21 (SiO2, метиленхлорид:метанол:аммиак = 95:5:0,1).
Использованный в качестве исходной субстанции трет-бутиловый эфир (3SR, 4RS, 5RS)-4-(4-хлорфенил)-3-изопропил-5-(4- метоксибензилокси)пиперидинкарбоновой кислоты получали аналогично примеру 62(з) путем алкилирования трет-бутилового эфира (3RS,4RS, 5SR)-4-(4-хлорфенил)-3-гидрокси-5-изопропилпиперидин-1- карбоновой кислоты (пример 65) 4-метоксибензилхлоридом; Rf 0,39 (SiO2, толуол:уксусный эфир = 9:1).
Пример 68.
Раствор из 60 мг (0,11 ммоля) трет-бутилового эфира (3RS,4RS,5SR)-4-(4-бромфенил)-5-метоксиметил-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты в 5 мл метиленхлорида смешивали с 2 мл 2 н. хлористого водорода в метаноле и перемешивали в течение 2 ч при комнатной температуре. Для дальнейшей переработки реакционную смесь упаривали при пониженном давлении. Остаток перекристаллизовывали из диэтилового эфира, в результате чего получили 53 мг (98% от теории) гидрохлорида (3RS,4RS, 5SR)-4-(4-бромфенил)-5- метоксиметил-3-нафталин-2-илметоксипиперидина в виде бесцветного твердого вещества; МС: 442 (М+Н)+.
Использованный в качестве исходной субстанции трет-бутиловый эфир (3RS, 4RS, 5SR)-4-(4-бромфенил)-5-метоксиметил-3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты получали следующим образом.
(а) Раствор из 7,45 г (33,7 ммоля) (3RS,4RS)-1-бензил-3- гидроксиметилпиперидин-4-ола и (3SR, 4RS)-1-бензил-3- гидроксиметилпиперидин-4-ола [Е. Jaeger и J.H. Biel, J. Org. Chem. 30(3), 740-744 (1965)], 10,89 г (39,6 ммоля) трет- бутилдифенилхлорсилана, 3,44 г (50,5 ммоля) имидазола и 0,2 г (1,6 ммоля) 4-диметиламинопиридина в 80 мл диметилформамида перемешивали в присутствии молекулярного сита
(б) Раствор из 2,45 г (19, 33 ммоля) оксалилхлорида в 60 мл метиленхлорида охлаждали до -70oC, после чего, добавляя по каплям, смешивали с 3,02 г (38,66 ммоля) диметилсульфоксида и затем перемешивали в течение 5 мин при -70oC. К этой смеси по каплям добавляли раствор из 8,08 г (17,6 ммоля) смеси (3RS, 4RS)- и (3RS,4SR)-1-бензил-3-(трет-бутилдифенилсиланилоксиметил) пиперидин-4-ола в 15 мл метиленхлорида, после чего перемешивали в течение 15 мин. Далее при -70oC по каплям добавляли 8,86 г (87,6 ммоля) триэтиламина. После нагрева смеси до комнатной температуры (приблизительно в течение 15 мин) ее гидролизовали в ледяной воде, а затем трижды экстрагировали метиленхлоридом порциями по 200 мл. Объединенные органические фазы сушили над сульфатом натрия и упаривали при пониженном давлении. Для очистки сырой продукт хроматографировали на силикагеле с использованием метиленхлорида в качестве элюента. Таким путем получили 6,5 г (81% от теории) (3RS)-1-бензил-3-(трет- бутилдифенилсиланилоксиметил)пиперидин-4-она в виде бесцветного масла; МС: 458 (М+Н)+.
(в) Аналогично примеру 62(б) из (3RS)-1- бензил-3-(трет-бутилдифенилсиланилоксиметил)пиперидин-4-она и 1,4-дибромбензола получили (3RS,4RS)- и/или (3RS, 4SR)-1-бензил-4- (4-бромфенил)-3-(трет-бутилдифенилсиланилоксиметил)пиперидин-4- ола в виде бесцветной пены; МС: 616 (М+Н)+.
(г) Аналогично примеру 62(в) путем элиминирования третичного спирта и одновременного отщепления силильной группы с помощью трифторуксусной кислоты из (3RS, 4RS)- и/или (3RS, 4SR)-1-бензил-4-(4-бромфенил)-3-(трет- бутилдифенилсиланилоксиметил)пиперидин-4-ола получили (3RS)-[1- бензил-4-(4-бромфенил)-1,2,3,6-тетрагидропиридин-3-ил] метанол в виде бесцветного твердого вещества; МС: 360 (М+Н)+.
(д) Аналогично примеру 62(г) путем гидроборирования (3RS)-[1-бензил-4-(4-бромфенил)-1,2,3,6-тетрагидропиридин-3-ил] метанола получили смесь (3RS, 4RS, 5SR)-1-бензил-4-(4-бромфенил)-5- гидроксиметилпиперидин-3-ола и (3RS, 4RS)- и/или (3RS,4SR)-1- бeнзил-4-(4-бpoмфeнил)-3-гидpoкcимeтилпиперидин-4-ола в виде бесцветной пены.
(е) Аналогично примеру 62(д) путем обработки указанной выше смеси 2,2,2-трихлорэтиловым эфиром хлормуравьиной кислоты получили смесь 2,2,2-трихлорэтилового эфира (3RS, 4RS, 5SR)- 4-(4-бромфенил)-3-(2,2, 2-трихлорэтоксикарбонилокси)-5-(2,2,2- трихлорэтоксикарбонилоксиметил)пиперидин-1-карбоновой кислоты и 2,2,2-трихлорэтилового эфира (3RS,4RS)-и/или (3RS, 4SR)-4-(4- бромфенил)-4-(2,2, 2-трихлорэтоксикарбонилокси)-3-(2,2,2- трихлорэтоксикарбонилоксиметил)пиперидин-1-карбоновой кислоты в виде бесцветной пены.
(ж) Аналогично примеру 62(е) в результате взаимодействия указанной выше смеси с цинком в ледяной уксусной кислоте получили смесь 4:1 (3RS,4RS, 5RS)-4-(4-бромфенил)-5- гидроксиметилпиперидин-3-ола и (3RS, 4RS)- и/или (3RS, 4SR)-4-(4- бромфенил)-3-гидроксиметилпиперидин-4-ола в виде бесцветной пены.
(з) Аналогично примеру 62(ж) путем введения BOC-группы и последующего хроматографического разделения смеси получили трет- бутиловый эфир (3RS,4RS, 5SR)-4-(4-бромфенил)-3-гидрокси-5- гидроксиметилпиперидин-1-карбоновой кислоты в виде бесцветной пены [МС: 386 (М+Н)+] и трет-бутиловый эфир (3RS, 4RS)- и/или (3RS,4SR)-4-(4-бромфенил)-4-гидрокси-3-гидроксиметилпиперидин- 1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 386 (М+Н)+.
(и) Раствор из 735 мг (1,91 ммоля) трет-бутилового эфира (3RS,4RS, 5SR)-4-(4-бромфенил)-3-гидрокси-5- гидроксиметилпиперидин-1-карбоновой кислоты, 766 мг (2,75 ммоля) трифенилхлорметана и 324 мг (3,20 ммоля) триэтиламина в 8 мл метиленхлорида перемешивали в течение 15 ч при комнатной температуре. Для дальнейшей переработки реакционную смесь упаривали при пониженном давлении и сырой продукт непосредственно хроматографировали на силикагеле с использованием метиленхлорида в качестве элюента. Таким путем получили 1,01 г (84,5% от теории) трет-бутилового эфира (3RS,4RS, 5SR)-4-(4-бромфенил)-3- гидрокси-5-тритилоксиметилпиперидин-1-карбоновой кислоты в виде бесцветной пены; МС: 646 (M+NH4)+.
(к) Аналогично примеру 62(з) путем алкилирования трет-бутилового эфира (3RS, 4RS, 5SR)-4-(4- бромфенил)-3-гидрокси-5-тритилоксиметилпиперидин-1-карбоновой кислоты 2-бромметилнафталином получили трет-бутиловый эфир (3RS, 4RS, 5SR)-4-(4-бромфенил)-3-нафталин-2-илметокси-5- тритилоксиметилпиперидин-1-карбоновой кислоты в виде бесцветной пены; МС: 785 (M+NH4)+.
(л) Раствор из 990 мг (1, 29 ммоля) трет-бутилового эфира (3RS,4RS, 5SR)-4-(4-бромфенил)-3-нафталин-2-илметокси-5- тритилоксиметилпиперидин-1-карбоновой кислоты и 4 мл 2 н. хлористого водорода/метанола в 5 мл метиленхлорида перемешивали в течение 45 мин при комнатной температуре. Для дальнейшей переработки реакционный раствор сливали в 40 мл насыщенного раствора карбоната натрия, а затем дважды экстрагировали метиленхлоридом порциями по 40 мл. Объединенные органические фазы сушили над сульфатом натрия и упаривали при пониженном давлении. Очистку и разделение полученных продуктов осуществляли хроматографией на силикагеле сначала с использованием смеси 98:2 метиленхлорида и метанола в качестве элюента. При этом получили 360 мг (54% от теории) трет-бутилового эфира (3RS,4RS, 5SR)-4-(4-бромфенил)-5-гидроксиметил-3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 528 (М+Н)+. Затем при использовании смеси 90: 10: 1 метиленхлорида, метанола и аммиака получили (3SR,4RS,5RS)-4-[(4-бромфенил)-5-нафталин-2-илметоксипиперидин- 3-ил] метанол в виде бесцветного твердого вещества; МС: 426 (М+Н)+.
(м) Аналогично примеру 62(з) путем алкилирования (3SR,4RS,5RS)-4-[(4-бромфенил)-5-нафталин-2-илметоксипиперидин- 3-ил] метанола метилиодидом получили трет-бутиловый эфир (3RS,4RS, 5SR)-4-(4-бромфенил)-5-метоксиметил-3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 540 (М+Н)+.
Пример 69.
а) Раствор из 32,5 г (163 ммоля) трет-бутилового 4-оксопиперидин-1-карбоновой кислоты в 200 мл хлороформа смешивали с 24,0 г (168 ммолей) динатрийгидрофосфата и охлаждали до 5oC. Далее в течение 1 ч по каплям добавляли раствор из 27,9 г (175 ммолей) брома в 75 мл хлороформа, после чего реакционную смесь нагревали до комнатной температуры и перемешивали в течение 18 ч. Реакционную смесь обрабатывали с одновременной эктракцией ледяной водой и метиленхлоридом, органическую фазу сушили над сульфатом магния, фильтровали и растворитель отгоняли в вакууме, создаваемом водоструйным насосом. Сырой продукт (38 г) хроматографировали на силикагеле с использованием метиленхлорида и уксусного эфира в качестве элюента. Полученный при этом продукт перекристаллизовывали из уксусного эфира и н-гексана. Таким путем получили 19,1 г (42% от теории) трет-бутилового эфира 3-бром-4-оксопиперидин-1-карбоновой кислоты в виде светло-желтого твердого вещества; МС: 277, 279 (М)+ .
(б) Раствор из 2,78 г (10 ммолей) трет-бутилового эфира 3-бром-4- оксопиперидин-1-карбоновой кислоты и 2,09 г (12 ммолей) 2-меркаптометилнафталина в 100 мл абсолютного ацетонитрила смешивали с 13,8 г (100 ммолей) безводного карбоната калия, а затем перемешивали в течение 18 ч при комнатной температуре. Реакционную смесь фильтровали, фильтрат сливали на ледяную воду и с помощью концентрированной соляной кислоты значение pH устанавливали равным 2-3; водную фазу трижды экстрагировали уксусным эфиром порциями по 200 мл, органическую фазу один раз промывали 200 мл воды, сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Сырой продукт (5,5 г) хроматографировали на силикагеле с использованием гексана и уксусного эфира в качестве элюента. Полученный при этом продукт перекристаллизовывали из уксусного эфира и гексана. Таким путем получили 2,27 г (61% от теории) трет-бутилового эфира (3RS) -3-(нафталин-2-илметилтио)-4-оксопиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 371 (М)+.
(в) 0,31 г (12,8 мг-атом) магниевой стружки суспендировали в атмосфере аргона в 5 мл абсолютного тетрагидрофурана, после чего при нагревании с обратным холодильником подвергали взаимодействию с раствором из 1,75 г (10 ммолей) 4-бромфторбензола в 10 мл тетрагидрофурана. По завершении реакции при комнатной температуре по каплям добавляли раствор из 1,86 г (5 ммолей) трет-бутилового эфира (3RS)-3-(нафталин-2-илметилтио)-4-оксопиперидин-1-карбоновой кислоты в 10 мл тетрагидрофурана и затем перемешивали в течение 4 ч. После гидролиза 10 мл воды реакционную смесь обрабатывали с одновременной экстракцией уксусным эфиром. Органическую фазу сушили над сульфатом магния, фильтровали и растворитель отгоняли в вакууме, создаваемом водоструйным насосом. Сырой продукт (2,6 г) хроматографировали на силикагеле с использованием гексана и уксусного эфира в качестве элюента. Таким путем получили 1,45 г (62% от теории) трет-бутилового эфира (3RS,4SR или 3RS, 4RS)-4-(4- фторфенил)-4-гидрокси-3-(нафталин-2-илметилтио)пиперидин-1- карбоновой кислоты в виде бесцветного твердого вещества [МС: 468 (М+Н)+] и 0,37 г (16% от теории) трет-бутилового эфира (3RS,4RS или 3RS,4SR)-4-(4-фторфенил)-4-гидрокси-3-(нафталин-2-илметилтио) пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 468 (М+Н)+.
(г) Раствор из 0,23 г (0,5 ммоля) трет-бутилового эфира (3RS,4SR или 3RS, 4RS)-4-(4-фторфенил)-4-гидрокси-3-(нафталин- 2-илметилтио)пиперидин-1-карбоновой кислоты в 5 мл абсолютного метанола смешивали с 1 мл соляной кислоты в метаноле (1,4-молярный раствор) и затем перемешивали в течение 3 ч при 50oC. После отгонки растворителя в вакууме, создаваемом водоструйным насосом, продукт перекристаллизовывали из метанола. При этом получили 0,18 г (89% от теории) гидрохлорида (3RS,4SR или 3RS,4RS)-4-(4-фторфенил)-4- гидрокси-3-(нафталин-2-илметилтио)пиперидина в виде светло- желтого твердого вещества; МС: 368 (М+Н)+.
Пример 70.
Раствор из 0,23 г (0,5 ммоля) трет-бутилового эфира (3RS,4RS или 3RS, 4SR)-4-(4-фторфенил)-4-гидрокси-3-(нафталин-2-илметилтио) пиперидин-1-карбоновой кислоты [пример 69(в)] в 5 мл абсолютного метанола смешивали с 1 мл соляной кислоты в метаноле (1,4-молярный раствор) и затем перемешивали в течение 3 ч при 50oC. После отгонки растворителя в вакууме, создаваемом водоструйным насосом, остаток распределяли между метиленхлоридом и водой, нейтрализовали насыщенным раствором бикарбоната натрия и экстрагировали; органическую фазу сушили над сульфатом магния, фильтровали и концентрировали. Сырой продукт (0,15 г) хроматографировали на силикагеле с использованием метиленхлорида и метанола в качестве элюента. При этом получили 0,041 г (22% от теории) (3RS,4RS или 3RS,4SR)-4-(4-фторфенил)-4-метокси-3-(нафталин-2- илметилтио)пиперидина в виде желтого масла [МС: 381 (М)+] и 0,067 г (37% от теории) (3RS, 4RS или 3RS,4SR)-4-(4-фторфенил)-4- гидрокси-3-(нафталин-2-илметилтио)пиперидина в виде светло-желтого твердого вещества; МС: 367 (М)+.
Пример 71.
(а) 2,33 г (10,0 ммолей) бензилового эфира рац.-3-аза-7-оксабицикло[4,1,0] гептан-3-карбоновой кислоты [S. V. D'Andrea и др., J. Org. Chem. (1991), 56(9), 3133-3137] и 1,88 г (20,0 ммолей, 2 экв.) фенола растворяли в 30 мл ацетонитрила и при комнатной температуре смешивали с 10,0 мл 2 н. едкого натра. Этот раствор перемешивали в течение 5 ч при 95oC. Далее охлажденный до комнатной температуры раствор смешивали с 60 мл воды и трижды экстрагировали метиленхлоридом. Органические фазы промывали 100 мл 2 н. едкого натра и дважды водой, сушили над сульфатом магния, упаривали при пониженном давлении и сушили в высоком вакууме. Сырой продукт (3,05 г) разделяли на силикагеле с использованием смеси 7:3 гексана и уксусного эфира в качестве элюента. Таким путем получили 2,06 г (63% от теории) бензилового эфира (3RS, 4RS)-3-гидрокси-4-феноксипиперидин- 1-карбоновой кислоты в виде бесцветного масла; МС: 327 (М)+.
(б) Дисперсию 262 мг (6,0 ммолей, 2 экв.) гидрида натрия (60%-ная дисперсия в вазелиновом масле) в 40 мл диметилсульфоксида смешивали с раствором из 982 мг (3,0 ммоля, 1 экв.) бензилового эфира (3RS,4RS)-3-гидрокси-4-феноксипиперидин-1-карбоновой кислоты в 67 мл диметилсульфоксида. Эту смесь перемешивали в течение 2 ч при 40oC, затем охлаждали до комнатной температуры, смешивали, добавляя по каплям, с раствором из 1326 мг (6,0 ммолей, 2 экв.) 2- бромметилнафталина в 40 мл диметилсульфоксида и перемешивали в течение 4 ч при комнатной температуре. Смесь сливали на 1 л смеси льда/воды, перемешивали в течение 10 мин и трижды экстрагировали диэтиловым эфиром. Органические фазы по одному разу промывали водой и насыщенным раствором хлорида натрия, сушили над сульфатом магния, упаривали при пониженном давлении и сушили в высоком вакууме. Бледно-желтое масло (1,75 г) разделяли на силикагеле с использованием смеси 4:1 гексана и уксусного эфира в качестве элюента. Таким путем получили 647 мг (46% от теории) бензилового эфира (3RS, 4RS)-3-(нaфтaлин-2-илмeтoкcи)-4-феноксипиперидин-1- карбоновой кислоты в виде аморфного твердого вещества; МС:476(М- бензил)+.
(в) 30 мг (0,065 ммоля) бензилового эфира (3RS,4RS)-3- (нафталин-2-илметокси)-4-феноксипиперидин-1-карбоновой кислоты растворяли в 1,6 мл тетрагидрофурана, охлаждали до 0oC и последовательно в течение 25 мин смешивали с раствором из 95 мл (0,32 ммоля, ок. 5 экв.) 70%-ного раствора дигидробис(2- метоксиэтокси)алюмината натрия (ДМАН) в толуоле и 1,6 мл тетрагидрофурана. Этот реакционный раствор перемешивали в течение 2,5 ч при 0oC. Далее сливали на смесь насыщенного раствора калийнатрийтартрата и льда и четырежды экстрагировали метиленхлоридом порциями по 50 мл. Органические фазы дважды промывали водой, упаривали при пониженном давлении и сушили в высоком вакууме. Смолу оранжевого цвета разделяли на силикагеле с использованием смеси 95:5 метиленхлорида и метанола в качестве элюента. Таким путем получили 10 мг (47% от теории) (3RS,4RS)-3- (нафталин-2-илметокси)-4-феноксипиперидина в виде бесцветного аморфного твердого вещества; Rf 0,38 (SiO2, метиленхлорид: метанол = 9:1).
Пример 72.
Аналогично примеру 71 путем отщепления бензилоксикарбонильной группы получали следующие соединения:
1) из бензилового эфира (3RS,4RS)-4-(4-бромфенокси)-3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-(4-бромфенокси)-3-(нафталин-2-илметокси)пиперидин в виде бесцветного аморфного твердого вещества; МС: 412,4, 414 (М+Н)+;
2) из бензилового эфира (3RS, 4RS)-4-(4-хлорфенилсульфанил)-3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты получили (3RS,4RS)-4-(4-хлорфенилсульфанил)-3-(нафталин-2-илметокси) пиперидин в виде бесцветного аморфного твердого вещества; МС: 384 (М+Н)+.
Использованные в качестве исходных веществ производные получали следующим образом.
(а) Аналогично примеру 71(а)-(б) из бензилового эфира рац.-3-аза-7-оксабицикло[4,1,0] гептан-3-карбоновой кислоты взаимодействием с 4-бромфенолом получили бензиловый эфир (3RS,4RS)-4-(4-бромфенокси)-3-гидроксипиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества [Rf 0,40 (SiO2, метиленхлорид:уксусный эфир = 2:1)], алкилированием которого 2-бромметилнафталином получили бензиловый эфир (3RS, 4RS)- 4-(4-бромфенокси)-3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 454, 456 (М- бензил)+.
(б) Смесь из 2,33 г (10,0 ммолей) бензилового эфира рац.-3-аза-7-оксабицикло[4,1,0] гептан-3-карбоновой кислоты, 2,89 г (20,0 ммолей, 2 экв.) п-хлортиофенола и 10,0 мл 2 н. едкого натра в 20,5 мл ацетонитрила кипятили с обратным холодильником в течение 4 ч. Далее охлажденный до комнатной температуры раствор смешивали с 25 мл воды и трижды экстрагировали метиленхлоридом. Органические фазы один раз промывали 1 н. едким натром и дважды водой, сушили над сульфатом магния, упаривали при пониженном давлении и сушили в высоком вакууме. Сырой продукт (3,55 г) разделяли на силикагеле с использованием смеси 9:1 метиленхлорида и уксусного эфира в качестве элюента. Таким путем получили 1,89 г (46% от теории) бензилового эфира (3RS,4RS)-4-(4-хлорфенилсульфанил)-3- гидроксипиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества [МС: 377 (М)+] и 169 мг (4%) бензилового эфира (3RS, 4SR)-4-(4-хлорфенилсульфанил)-3-гидроксипиперидин-1- карбоновой кислоты.
(в) Аналогично примеру 71(б) из бензилового эфира (3RS,4RS)-4-(4-хлорфенилсульфанил)-3-гидроксипиперидин-1- карбоновой кислоты путем алкилирования 2-бромметилнафталином получили бензиловый эфир (3RS, 4RS)-4-(4-хлорфенилсульфанил)-3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 518 (М+Н)+.
Пример 73.
а) Раствор из 5,0 г (16,9 ммолей) трет-бутилового эфира (3RS,4RS)-4-(4-фторфенил)-3-гидроксипиперидин-1-карбоновой кислоты в 50 мл метиленхлорида смешивали с 240 мг (1,96 ммоля) 4- диметиламинопиридина и 4,2 мл (29 ммолей) триэтиламина и охлаждали до 0oC. Далее порциями добавляли 4,65 г (24,4 ммоля) 2- нафтоилхлорида и реакционную смесь перемешивали в течение 18 ч при комнатной температуре. Непосредственно после этого реакционную смесь смешивали с ледяной водой и экстрагировали метиленхлоридом. Объединенные метиленхлоридные фазы сушили над сульфатом магния, фильтровали и растворитель отгоняли в вакууме, создаваемом водоструйным насосом. Сырой продукт хроматографировали на силикагеле с использованием метиленхлорида в качестве элюента. Полученную при этом содержащую продукт фракцию перекристаллизовывали из простого эфира и н-гексана. Таким путем получили 7,4 г (97% от теории) трет-бутилового эфира (3RS, 4RS)-4- (4-фторфенил)-3-(нафталин-2-илкарбонилокси)пиперидин-1- карбоновой кислоты в виде бесцветного твердого вещества; МС: 450 (М+Н)+.
б) Раствор из 2,7 мл (24,6 ммоля) четыреххлористого титана в 18 мл метиленхлорида в атмосфере аргона и в условиях, исключающих наличие влаги, по каплям добавляли при 0oC к 30 мл тетрагидрофурана, при этом образовывалась желтая суспензия. После нагрева до комнатной температуры добавляли 15 мл (95 ммолей) тетраметилэтилендиамина и реакционную смесь перемешивали в течение 10 мин. Затем добавляли 3,6 г (55 ммолей) цинковой пыли и перемешивание продолжали в течение 30 мин при комнатной температуре. После этого по каплям добавляли раствор из 2,1 мл (30 ммолей) дибромметана и 2,7 г (6,0 ммолей) трет-бутилового эфира (3RS, 4RS)-4-(4-фторфенил)-3-(нафталин-2- илкарбонилокси)пиперидин-1-карбоновой кислоты в 30 мл тетрагидрофурана таким образом, чтобы температура не поднималась выше 36oC. Далее реакционную смесь перемешивали в течение 60 ч при комнатной температуре, затем сливали на насыщенный раствор хлорида аммония и экстрагировали простым эфиром. Объединенные эфирные фазы сушили над сульфатом магния, концентрировали и остаток хроматографировали на силикагеле с использованием смеси 99:1 метиленхлорида и триэтиламина в качестве элюента. В результате получили 1,23 г (46% от теории) трет-бутилового эфира (3RS, 4RS)-4- (4-фторфенил)-3-(1-нафталин-2-илвинилокси) пиперидин-1-карбоновой кислоты в виде бесцветного аморфного твердого вещества; МС: 448 (М+Н)+.
в) Раствор из 70 мг (0,156 ммоля) трет-бутилового эфира (3RS,4RS)-4-(4-фторфенил)-3-(1-нафталин-2-илвинилокси) пиперидин-1-карбоновой кислоты в 10 мл тетрагидрофурана смешивали с 0,2 мл триэтиламина и 100 мг палладия на угле и гидрировали в атмосфере водорода при комнатной температуре и нормальном давлении. Далее реакционную смесь фильтровали на целлюлозном нутч- фильтре с размером пор 0,8 мкм и растворитель выпаривали в вакууме, создаваемом водоструйным насосом. Таким путем получили 68,4 мг (97% от теории) смеси трет-бутилового эфира (3RS,4RS)-4- (4-фторфенил)-3-[(RS)- и -[(SR)-1-нафталин-2-илэтокси] пиперидин-1- карбоновой кислоты в виде бесцветного аморфного твердого вещества; МС: 450 (М+Н)+.
г) 69 мг (0,153 ммоля) смеси трет-бутилового эфира (3RS,4RS)-4-(4-фторфенил)-3-[(RS)- и -[(SR)-1-нафталин- 2-илэтокси]пиперидин-1-карбоновой кислоты растворяли в 2 мл метиленхлорида, смешивали с 104 мг (0,46 ммоля) безводного бромида цинка и перемешивали в течение 2,5 ч при комнатной температуре. После этого реакционную смесь сливали на водный раствор карбоната натрия и экстрагировали метиленхлоридом. Объединенные метиленхлоридные фазы сушили над сульфатом магния, концентрировали и полученный при этом остаток хроматографировали на силикагеле с использованием смеси 9:1 метиленхлорида и метанола в качестве элюента. В результате получили 22,1 мг (41% от теории) (3RS, 4RS)- 4-(4-фторфенил)-3-[(RS)- или -[(SR)-1-нафталин-2-илэтокси] пиперидина в виде аморфного желтоватого твердого вещества [MС: 350 (М+Н)+] и 13,6 мг (25% от теории) (3RS,4RS)-4-(4-фторфенил)-3- [(SR)- или -[(RS)-1-нафталин-2-илэтокси] пиперидина в виде бесцветного твердого вещества, МС: 350 (М+Н)+.
Пример 74.
а) К раствору из 10,0 г (46,8 ммоля) гидрохлорида 4-(4-фторфенил)- 1,2,3,6-тетрагидропиридина в 400 мл этанола добавляли 13,8 г (100 ммолей) карбоната калия и затем реакционную смесь нагревали до температуры дефлегмации. В течение 1 ч по каплям добавляли раствор из 5,8 мл (49 ммолей) бензилбромида в 100 мл этанола и затем перемешивали еще в течение 1 ч при этой температуре. Реакционную смесь охлаждали до комнатной температуры и фильтровали, фильтрат экстрагировали водой и уксусным эфиром и в завершение органические фазы сушили над сульфатом магния. После упаривания в вакууме, создаваемом водоструйным насосом, полученный сырой продукт хроматографировали на силикагеле гексаном и уксусным эфиром в качестве элюента. Таким путем получили 8,90 г (71% от теории) 1-бензил-4- (4-фторфенил)-1,2,3,6-тетрагидропиридина; МС: 267 (М)+.
б) 4,5 г (16,8 ммолей) 1-бензил-4-(4-фторфенил) -1,2,3,6-тетрагидропиридина суспендировали в 55 мл воды, затем добавлением 70 мл концентрированной соляной кислоты частично растворяли, добавляли 1,36 г (45,3 ммоля) параформальдегида и перемешивали в течение 5 ч при 100oC. После охлаждения до комнатной температуры значение pH устанавливали равным 5-6 с помощью едкого натра и продукт дважды экстрагировали 100 мл уксусного эфира. Органические фазы один раз промывали 100 мл воды, сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный таким образом сырой продукт хроматографировали на силикагеле гексаном и уксусным эфиром в качестве элюента. Таким путем получили 3,91 г (78% от теории) (RS)-[1-бензил-4-(4-фторфенил)-1,2,3,6-тетрагидропиридин-3-ил] метанола; МС: 297 (М)+.
в) К раствору из 17,4 г (58,5 ммоля) (RS)-[1-бензил-4-(4- фторфенил)-1,2,3,6-тетрагидропиридин-3-ил] метанола в 580 мл абсолютного толуола в атмосфере аргона при комнатной температуре и при перемешивании по каплям добавляли 58 мл (203 ммоля) дигидробис(2-метоксиэтокси)алюмината натрия (70%-ный раствор в толуоле). Далее смесь перемешивали в течение 4 ч при 80oC. К реакционной смеси при комнатной температуре по каплям добавляли 100 мл воды, а затем обрабатывали с одновременной экстракцией водой и уксусным эфиром. Сырой продукт хроматографировали на силикагеле гексаном и уксусным эфиром в качестве элюента. Таким путем получили 3,90 г (44% от теории) (3RS, 4SR)-[1-бензил-4-(4- фторфенил)пиперидин-3-ил] метанола; МС: 300 (М+Н)+.
г) 6,86 г (22,9 ммоля) (3RS, 4SR)-[1-бензил-4-(4-фторфенил)пиперидин-3-ил] метанола в 70 мл метанола при комнатной температуре гидрировали с добавлением 1,5 г палладия на угле (10%-ный). После отфильтровывания катализатора растворитель отгоняли в вакууме, создаваемом водоструйным насосом. Таким путем получили 4,79 г (100% от теории) (3RS,4SR)-[4-(4-фтopфeнил)пипеpидин-3-ил] метанола; МС: 210 (М+Н)+.
д) К раствору из 4,89 г (23,4 ммоля) (3RS,4SR)-[4-(4- фторфенил)пиперидин-3-ил] метанола в 60 мл диоксана добавляли 4,20 г (50 ммолей) гидрокарбоната натрия и 20 мл воды, затем порциями добавляли 6,10 г (28 ммолей) ди-трет-бутилдикарбоната и перемешивали в течение 4 ч при комнатной температуре. Реакционную смесь сливали на ледяную воду и продукт дважды экстрагировали 200 мл уксусного эфира; органические фазы один раз промывали 300 мл воды, сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный при этом сырой продукт хроматографировали на силикагеле с использованием метиленхлорида и метанола в качестве элюента. Таким путем получили 7,03 г (97% от теории) трет-бутилового эфира (3RS, 4SR)-4-(4- фторфенил)-3-гидроксиметилпиперидин-1-карбоновой кислоты; МС: 309 (М+Н)+.
е) К раствору из 2,34 мл (27,3 ммоля) оксалилхлорида в 250 мл метиленхлорида в атмосфере аргона при -70oC по каплям добавляли 3,28 мл (46,2 ммоля) диметилсульфоксида. По истечении 30 мин по каплям добавляли 6,50 г (21 ммоль) трет-бутилового эфира (3RS, 4SR)-4-(4- фторфенил)-3-гидроксиметилпиперидин-1-карбоновой кислоты, растворенного в 75 мл метиленхлорида, и перемешивали в течение 2 ч при -70oC. Далее по каплям добавляли 7,25 мл (52,5 ммоля) триэтиламина. Реакционную смесь в течение 3 ч нагревали до комнатной температуры, после чего экстрагировали водой и метиленхлоридом. После сушки над сульфатом магния и упаривания в вакууме, создаваемом водоструйным насосом, сырой продукт очищали перекристаллизацией из н-гексана. Таким путем получили 5,51 г (85% от теории) трет-бутилового эфира (3RS, 4SR)-4-(4-фторфенил)-3- формилпиперидин-1-карбоновой кислоты; МС: 279 (M-CO)+.
ж) В атмосфере аргона при 0oC предварительно загружали 28,0 мл (54 ммоля) гексабутилдистаннана в 150 мл тетрагидрофурана. После этого по каплям добавляли 31,3 мл (50 ммолей) раствора н-бутиллития (1,6 М в н-гексане). Через 30 мин по каплям добавляли раствор из 11,1 г (50 ммолей) 2-бромметилнафталина в 50 мл тетрагидрофурана, а затем перемешивали при комнатной температуре. По истечении 2 ч растворитель отгоняли в вакууме, создаваемом водоструйным насосом, и остаток хроматографировали на силикагеле с использованием гексана и уксусного эфира в качестве элюента. Таким путем получили 16,8 г (78% от теории) трибутилнафталин-2-илметилстаннана; МС: 432 (М+Н)+ .
з) 16,8 г (38,9 ммоля) трибутилнафталин-2-илметилстаннана растворяли в 150 мл тетрагидрофурана в атмосфере аргона. После этого при -78oC по каплям добавляли 12,5 мл (20 ммолей) раствора н-бутиллития (1,6 М в н-гексане). Через 30 мин при -78oC по каплям добавляли раствор из 4,80 г (15,6 ммоля) трет-бутилового эфира (3RS, 4SR)-4-(4-фторфенил)-3-формилпиперидин-1-карбоновой кислоты в 70 мл тетрагидрофурана, а затем реакционную смесь перемешивали в течение 2 ч. Далее в течение 2 ч нагревали до комнатной температуры и перемешивание продолжали еще в течение 18 ч. После отгонки растворителя в вакууме, создаваемом водоструйным насосом, реакционную смесь распределяли между водой и метиленхлоридом, органическую фазу сушили над сульфатом магния и концентрировали. Сырой продукт хроматографировали на силикагеле с использованием гексана и уксусного эфира в качестве элюента. Таким путем получили 5,50 г (78% от теории) смеси трет-бутилового эфира (3RS,4SR)-4-(4-фторфенил)-3- [(RS)- и -[(SR)-1-гидрокси-2-нафталин-2-илэтил]пиперидин-1- карбоновой кислоты; МС: 450 (М+Н)+.
и) 0,45 г (1 ммоль) смеси трет-бутилового эфира (3RS,4SR)-4-(4-фторфенил)-3-[(RS)- и -[(SR)-1-гидрокси-2-нафталин-2-илэтил]пиперидин-1-карбоновой кислоты растворяли в 10 мл метанола. К раствору добавляли 2,0 мл (2, 8 ммоля) HCl в метаноле и реакционную смесь перемешивали в течение 1 ч при 50oC. После отгонки растворителя в вакууме, создаваемом водоструйным насосом, остаток перекристаллизовывали из метанола и простого эфира. Таким путем получили 0,16 г (42% от теории) смеси гидрохлорида (RS)- и (SR)-1-[(3RS, 4SR)-4-(4- фторфенил)пиперидин-3-ил] -2-нафталин-2-илэтанола в виде бесцветных кристаллов; МС: 350 (М+Н)+.
Пример 75.
а) 0,45 г (1 ммоль) смеси трет-бутилового эфира (3RS,4SR)-4-(4-фторфенил)-3-[(RS)- и -[(SR)-1-гидрокси-2-нафталин-2-илэтил]пиперидин-1-карбоновой кислоты растворяли в атмосфере аргона в 5 мл диметилформамида, а затем последовательно смешивали с 0,16 г (1,2 ммоля) 4- диметиламинопиридина и 0,14 мл (1,2 ммоля) бензоилхлорида и перемешивали в течение 16 ч при комнатной температуре. Далее реакционную смесь обрабатывали с одновременной экстракцией ледяной водой и метиленхлоридом. Полученный при этом сырой продукт хроматографировали на силикагеле с использованием гексана и уксусного эфира в качестве элюента. Таким путем получили 0,27 г (49% от теории) трет-бутилового эфира (3RS, 4SR)-3-[(RS)- или - [(SR)-1-бензоилокси-2-нафталин-2-илэтил] -4-(4-фторфенил) пиперидин-1-карбоновой кислоты [МС: 554 (М+Н)+] и 0,19 г (34% от теории) трет-бутилового эфира (3RS,4SR)-3-[(SR)- или -[(RS)-1- бензоилокси-2-нафталин-2-илэтил]-4-(4-фторфенил) пиперидин-1- карбоновой кислоты; МС: 554 (М+Н)+.
б) 0,15 г (0,27 ммоля) трет-бутилового эфира (3RS,4SR)-3-[(SR)- или -[(RS)-1-бензoилoкcи-2-нaфтaлин-2-илэтил] -4-(4-фторфенил) пиперидин-1-карбоновой кислоты перемешивали в 10 мл метанола с добавкой 1,0 мл (1,4 ммоля) HCl в метаноле в течение 1 ч при 50oC. После отгонки растворителя в вакууме, создаваемом водоструйным насосом, и последующей сушки в высоком вакууме получили 0,12 г (91% от теории) гидрохлорида (SR)- или (RS)-1-[(3RS,4SR)-4-(4-фтopфенил)пипеpидин- 3-ил] -2-нaфтaлин-2-илэтилoвoгo эфира бензойной кислоты (в соотношении 1:1) в виде бесцветной пены; МС: 454 (М+Н)+.
Пример 76.
0,25 г (0,45 ммоля) трет-бутилового эфира (3RS,4SR)-3-[(RS)- или - [(SR)-1-бензоилокси-2-нафталин-2-илэтил] -4-(4-фторфенил) пиперидин-1-карбоновой кислоты подвергали аналогично примеру 75 (б) взаимодействию с 1,2 мл (1,68 ммоля) HCl в метаноле. При этом получили 0,21 г (95% от теории) гидрохлорида (RS)- или (SR)-1- [(3RS, 4SR)-4-(4-фторфенил)пиперидин-3-ил]-2-нафталин-2-илэтилового эфира бензойной кислоты (в соотношении 1:1) в виде бесцветной пены; МС: 454 (М+Н)+.
Пример 77.
а) 0,45 г (1 ммоль) смеси трет-бутилового эфира (3RS,4SR)-4-(4-фторфенил)-3-[(RS)- и -[(SR)-1- гидрокси-2-нафталин-2-илэтил]пиперидин-1-карбоновой кислоты подвергали аналогично примеру 75(а) взаимодействию с 0,09 мл (1,26 ммоля) ацетилхлорида и 0,16 г (1,3 ммоля) диметиламинопиридина. При этом получили 0,38 г (77% от теории) смеси трет-бутилового эфира (3RS, 4SR)-3-[(RS)- и -[(SR)-1- ацетилокси-2-нафталин-2-илэтил]-4-(4-фторфенил) пиперидин-1- карбоновой кислоты, которую использовали непосредственно на следующей стадии.
б) 0,15 г (0,31 ммоля) смеси трет-бутилового эфира (3RS,4SR)-3-[(RS)- и -[(SR)-1-aцeтилoкcи-2-нaфтaлин-2-илэтил] -4-(4-фторфенил)пиперидин-1-карбоновой кислоты смешивали в 10 мл метиленхлорида с 0,5 мл (6,5 ммоля) трифторуксуcной кислоты и перемешивали в течение 16 ч при комнатной температуре. После отгонки растворителя в вакууме, создаваемом водоструйным насосом, и последующей сушки в высоком вакууме получили 0,15 г (96% от теории) смеси трифторацетата (RS)- или (SR)-1-[(3RS,4SR)-4-(4- фтоpфенил)пиперидин-3-ил]-2-нафталин-2-илэтилового эфира уксусной кислоты (в соотношении 1:1) в виде бесцветной пены; МС: 392 (М+Н)+.
Пример 78.
a) 0,45 г (1 ммоль) смеси трет-бутилового эфира (3RS,4SR)-4-(4-фторфенил)-3-[(SR)- и -[(SR)-1-гидрокси-2-нафталин- 2-илэтил]пиперидин-1-карбоновой кислоты растворяли в атмосфере аргона в 10 мл диметилформамида, а затем при комнатной температуре и при перемешивании добавляли 0,07 г (1, 6 ммоля) дисперсии гидрида натрия (55%-ная в минеральном масле). По истечении 1 ч по каплям добавляли 0,14 мл (1,2 ммоля) бензилбромида и реакционную смесь перемешивали в течение 18 ч при комнатной температуре. Далее обрабатывали с одновременной экстракцией ледяной водой и метиленхлоридом. Полученный при этом сырой продукт хроматографировали на силикагеле с использованием гексана и уксусного эфира в качестве элюента. Таким путем получили 0,21 г (39% от теории) трет-бутилового эфира (3RS,4SR)-3-[(RS)- или -[(SR)-1-бензилокси-2-нафталин-2-илэтил]-4-(4- фторфенил)пиперидин-1-карбоновой кислоты [МС: 540 (М+Н)+] и 0,17 г (31% от теории) трет-бутилового эфира (3RS,4SR)-3-[(SR)- или - [(RS)-1-бензилокси-2-нафталин-2-илэтил]-4-(4-фторфенил) пиперидин-1-карбоновой кислоты, МС: 540 (М+Н)+.
б) 0,12 г (0,22 ммоля) трет-бутилового эфира (3RS,4SR)-3-[(RS)- или -[(SR)-1-бензилокси-2-нафталин-2-илэтил] -4-(4-фторфенил) пиперидин-1-карбоновой кислоты подвергали аналогично примеру 75(б) взаимодействию с 1,0 мл (1,40 ммоля) HCl в метаноле. При этом получили 0,10 г (95% от теории) гидрохлорида [(3RS, 4SR)-3-[(RS)- или -[(SR)-1-бeнзилoкcи-2-нaфтaлин-2-илэтил] -4-(4- фторфенил)пиперидина (в соотношении 1:1) в виде бесцветной пены; МС: 440 (М+Н)+.
Пример 79.
0,16 г (0,3 ммоля) трет-бутилового эфира (3RS,4SR)-3-[(SR)- или -[(RS)-1-бензилокси-2-нафталин-2-илэтил] -4-(4-фторфенил) пиперидин-1-карбоновой кислоты подвергали аналогично примеру 75(б) взаимодействию с 1,0 мл (1,40 ммоля) HCl в метаноле. После отгонки растворителя в вакууме, создаваемом водоструйным насосом, остаток перекристаллизовывали из метанола и диэтилового эфира. При этом получили 0,085 г (60% от теории) гидрохлорида (3RS, 4SR)-3-[(SR)- или -[(RS)-1-бензилокси-2-нафталин-2- илэтил] -4-(4-фторфенил)пиперидина (в соотношении 1:1) в виде белого твердого вещества; МС: 440 (М+Н)+.
Пример 80.
а) 0,45 г (1 ммоль) смеси трет-бутилового эфира (3RS,4SR)-4-(4-фторфенил)-3-[(RS)- и -[(SR)-1-гидрокси-2-нафталин-2-илэтил]пиперидин-1-карбоновой кислоты растворяли в атмосфере аргона в 10 мл диметилформамида, а затем при комнатной температуре и при перемешивании добавляли 0,07 г (1,6 ммоля) дисперсии гидрида натрия (55%-ная в минеральном масле). По истечении 1 ч добавляли 0,27 г (1,2 ммоля) 2-(бромметил)нафталина и реакционную смесь перемешивали в течение 72 ч при комнатной температуре. Далее экстрагировали ледяной водой и уксусным эфиром, органическую фазу сушили над сульфатом магния и в завершение упаривали в вакууме, создаваемом водоструйным насосом. Полученный при этом сырой продукт хроматографировали на силикагеле с использованием гексана и уксусного эфира в качестве элюента. Таким путем получили 0,19 г (32% от теории) трет-бутилового эфира (3RS,4SR)-4-(4-фтopфенил)-3-[(SR)- или (RS)-2-нафталин-2-ил-1-(нафталин-2-илметокси)этил] пиперидин- 1-карбоновой кислоты, который использовали непосредственно на следующей стадии, и 0,09 г (15% от теории) трет-бутилового эфира (3RS, 4SR)-4-(4-фторфенил)-3-[(RS)-или (SR)- 2-нaфтaлин-2-ил-1- (нафталин-2-илметокси)этил] пиперидин-1-карбоновой кислоты, который также использовали непосредственно на следующей стадии.
б) 0,19 г (0,32 ммоля) трет-бутилового эфира (3RS,4SR)-4-(4-фторфенил)-3-[(SR)- или (RS)-2-нaфтaлин-2-ил-1- (нaфтaлин-2-илметoкси)этил]пиперидин-1-карбоновой кислоты подвергали аналогично примеру 75 (б) взаимодействию с 1,0 мл (1,40 ммоля) HCl в метаноле. Реакционный раствор сливали на ледяную воду, нейтрализовали насыщенным раствором гидрокарбоната натрия, после чего продукт дважды экстрагировали 50 мл метиленхлорида. Органические фазы сушили над сульфатом магния, фильтровали и растворитель отгоняли в вакууме, создаваемом водоструйным насосом. Полученный при этом сырой продукт хроматографировали на силикагеле с использованием метиленхлорида и метанола в качестве элюента.
Таким путем получили 0,028 г (18% от теории) (3RS,4SR)-4-(4- фторфенил)-3-[(SR)- или (RS)-2-нафталин-2-ил-1-(нафталин-2- илметокси)этил] пиперидина в виде аморфного бесцветного твердого вещества; МС: 490 (М+Н)+.
Пример 81.
0,09 г (0,15 ммоля) трет-бутилового эфира (3RS,4SR)-4-(4-фторфенил)-3-[(RS)- или (SR)-2- нафталин-2-ил-1-(нафталин-2-илметокси)этил]пиперидин-1-карбоновой кислоты подвергали аналогично примеру 75 (б) взаимодействию с 1,0 мл (1,40 ммоля) HCl в метаноле. Реакционный раствор сливали на ледяную воду, нейтрализовали насыщенным раствором гидрокарбоната натрия, после чего продукт дважды экстрагировали 50 мл метиленхлорида. Органические фазы сушили над сульфатом магния, фильтровали и растворитель отгоняли в вакууме, создаваемом водоструйным насосом. Полученный при этом сырой продукт хроматографировали на силикагеле с использованием метиленхлорида и метанола в качестве элюента. Таким путем получили 0,036 г (49% от теории) (3RS,4SR)-4-(4-фторфенил)-3-[(RS)- или (SR)-2-нафталин-2- ил-1-(нафталин-2-илметокси) этил] пиперидина в виде аморфного бесцветного твердого вещества; МС: 490 (М+Н)+.
Пример 82.
(а) К суспензии из 0,206 г (4,3 ммоля) гидрида натрия (50%-ная дисперсия в вазелиновом масле) в 6 мл тетрагидрофурана по каплям добавляли раствор из 1,08 г (4,3 ммоля) (1RS,2RS,3RS, 5SR)-3-(4-хлорфенил)-8-метил-8-азабицикло [3,2,1] октан-2-ола [J. Org. Chem. 35, 802, (1970)] в 5 мл тетрагидрофурана и перемешивали в течение 60 мин при 50oC. Далее охлаждали до комнатной температуры и смешивали с 0,95 г (4,3 ммоля) 2-бромметилнафталина в 5 мл тетрагидрофурана. По истечении 2 ч выдержки при 50oC реакционный раствор сливали на 60 мл ледяной воды и трижды экстрагировали 25 мл этилового эфира уксусной кислоты. Органические фазы промывали насыщенным раствором поваренной соли, сушили над сульфатом магния, фильтровали и упаривали. Остаток хроматографировали на силикагеле с использованием смеси 95:5 метиленхлорида и метанола в качестве элюента, в результате чего получили 1,04 г (62% от теории) (1RS,2RS,3RS, 5SR)-3-(4-хлорфенил)-8-метил-2-(нафталин-2- илметокси)-8-азабицикло[3,2,1] октана в виде светло-желтого масла; Rf 0,43 (силикагель, метиленхлорид:метанол = 95:5); МС: 392 (М)+ .
(б) Раствор из 1,02 г (2,6 ммоля) (1RS,2RS,3RS,5SR)-3-(4- хлорфенил)-8-метил-2-(нафталин-2-илметокси)-8-азабицикло [3,2,1] октана в 40 мл толуола смешивали с 150 мг карбоната калия и нагревали до 100oC. Далее добавляли 0,635 г (0,400 мл, 3 ммоля) 2,2,2-трихлорэтилового эфира хлормуравьиной кислоты и перемешивали в течение 12 ч при 100oC. Реакционный раствор упаривали при пониженном давлении, остаток растворяли в 70 мл уксусного эфира и промывали 30 мл воды и 30 мл насыщенного раствора гидрокарбоната натрия. После сушки над сульфатом магния, фильтрации и упаривания получили бесцветное масло, которое хроматографировали на силикагеле с использованием смеси 3:2 гексана и уксусного эфира. Таким путем получили 1,14 г (79% от теории) 2,2,2-трихлорэтилового эфира (1RS, 2RS,3RS,5SR)-3-(4-хлорфенил)-2-(нафталин-2-илметокси)- 8-азабицикло[3,2,1]октан-8-карбоновой кислоты в виде бесцветного масла; Rf 0,38 (силикагель, гексан:уксусный эфир = 3:2).
(в) Суспензию 1,14 г (2,06 ммоля) 2,2,2-трихлорэтилового эфира (1RS,2RS, 3RS, 5SR)-3-(4-хлорфенил)-2-(нафталин-2-илметокси)-8- азабицикло[3,2,1] октан-8-карбоновой кислоты и 400 мг цинка в 10 мл уксусной кислоты перемешивали в течение 12 ч при комнатной температуре. Реакционный раствор разбавляли 50 мл воды и четырежды экстрагировали 40 мл метиленхлорида. Органические фазы дважды промывали 50 мл 1 н. едкого натра, сушили над сульфатом натрия, фильтровали и упаривали. Остаток хроматографировали на силикагеле с использованием смеси 9:1 метиленхлорида и метанола в качестве элюента. Таким путем получили 0,480 г (61% от теории) (1RS,2RS,3RS,5SR)-3-(4-хлорфенил)-2-(нафталин-2-илметокси)-8- азабицикло [3,2,1] октана с tпл 184-185oC; МС: 379 (М+Н)+.
Пример 83.
Аналогично примеру 82(а)-(в) получали следующие соединения:
1) из (1RS, 2RS, 3RS, 5SR)-3-(4-хлорфенил)-8-метил-8- азабицикло[3,2,1] октан-2-ола и 4-хлорметилбифенила получили (1RS,2RS,3RS,5SR)-2-(бифенил-4-илметокси)-3-(4-хлорфенил)-8- азабицикло [3,2,1] октан[МС: 236 (М-C13H11)+], который с помощью хлористого водорода в этаноле переводили в гидрохлорид с tпл 175-177oC (разлож.);
2) из (1RS, 2RS, 3RS, 5SR)-3-(4-хлорфенил)-8-метил-8- азабицикло[3,2,1] октан-2-ола и 3,4-дихлор-1-хлорметилбензола получили (1RS,2RS,3RS,5SR)-3-(4-хлорфенил)-2-(3,4- дихлорбензилокси)-8-азабицикло [3,2,1] октан [МС: 236 (M- C7H5Cl2)+], который с помощью хлористого водорода в этаноле переводили в гидрохлорид с tпл 211-213oC;
3) из (1RS, 2RS, 3RS,5SR)-3-(4-хлорфенил)-8-метил-8-азабицикло [3,2,1] октан-2-ола и 1-хлорметил-4-метоксибензола получили (1RS,2RS,3RS,5SR)-3-(4-хлорфенил)-2-(4-метоксибензилокси)-8- азабицикло [3,2,1] октан [МС: 358 (М+Н)+] , который с помощью метансульфокислоты в диоксане/воде с последующей лиофилизацией переводили в соответствующий метансульфонат; Rf 0,26 (силикагель, метиленхлорид:метанол:аммиак = 200:10:1);
4) из (1RS,2RS,3RS,5SR)-3-(4-хлорфенил)-8-метил-8-азабицикло [3,2,1]октан-2-ола и 3-хлорметилбензо[b] тиофена [J. Am. Chem. Soc. 71, 2856 (1949)] получили (1RS, 2RS, 3RS, 5SR)-2-(бензо[b] тиофен-2-илметокси)-3-(4-хлорфенил)-8-азабицикло[3,2,1] октан [МС: 236 (M-C8H7S)+], который с помощью хлористого водорода в этаноле переводили в гидрохлорид с tпл 196-198oC (разлож. );
5) из (1RS,2RS,3RS,5SR)-3-(4-хлорфенил)-8-метил-8-азабицикло[3,2,1] октан-2-ола и метилового эфира 4'-бромметилбифенил-2-карбоновой кислоты [J. Med. Chem. 34, 2525 (1991)] получили метиловый эфир (1RS,2RS,3RS,5SR)-4'-[3-(4-хлорфенил)-8-азабицикло [3,2,1] окт-2-илоксиметил]бифенил-2-карбоновой кислоты [МС: 236 (M-C15H13О2)+] , который с помощью хлористого водорода в этаноле переводили в гидрохлорид с tпл 101-103oC (разлож.);
6) из (1RS, 2RS, 3RS,5SR)-3-(4-хлорфенил)-8-метил-8- азабицикло[3,2,1] октан-2-ола и 6-хлорметил-1,1,4,4-тетраметил- 1,2,3, 4-тетрагидронафталина получили (1RS,2RS,3RS,5SR)-3-(4-хлорфенил)-2- (5,5,8,8-тетраметил-5,6,7,8-тетрагидронафталин-2-илметокси)-8- азабицикло[3,2,1] октан [МС: 437 (М)+], который с помощью хлористого водорода в этаноле переводили в гидрохлорид с tпл 87-90oC (разлож.).
Пример 84.
(а) Аналогично описанному в примере 12 (в) способу осуществляли отщепление N-метильной группы путем взаимодействия 2,2,2-трихлорэтилового эфира хлормуравьиной кислоты с (1RS,2RS,3RS,5SR)-3-(4-фторфенил)-8-метил-8- азабицикло[3,2,1] октан-2-олом, который был получен аналогично 4- хлорфенильному производному [J. Org. Chem. 35, 802, (1970)]. При этом получили 2,2,2-трихлорэтиловый эфир (1RS,2RS,3RS,5RS)-3-(4- фторфенил)-2-(2,2, 2-трихлорэтоксикарбонилокси)-8- азабицикло[3,2,1]октан-8-карбоновой кислоты в виде желтоватого твердого вещества; МС: 587, 589, 591, 593 (M+NH4)+.
(б) Путем отщепления 2,2,2-трихлорэтилкарбамата и 2,2,2-трихлорэтилкарбоната аналогично примеру 12(г) из 2,2,2-трихлорэтилового эфира (1RS,2RS, 3RS, 5RS)-3-(4-фторфенил)-2- (2,2,2-трихлорэтоксикарбонилокси) -8-азабицикло[3,2,1] октан-8-карбоновой кислоты получили (1RS,2RS,3RS,5RS)-3-(4-фторфенил)-8-азабицикло[3,2,1] октан-2-ола в виде бесцветного твердого вещества; МС: 221 (М)+.
(в) Аналогично описанному в примере 1(е) способу путем введения BOC-группы из (1RS,2RS,3RS,5RS)-3-(4-фторфенил)-8-азабицикло[3,2,1] октан-2-ола получили трет-бутиловый эфир (1RS,2RS,3RS, 5RS)-3-(4-фторфенил)-2-гидрокси-8- азабицикло[3,2,1] октан-8-карбоновой кислоты в виде бесцветной пены; МС: 265 (M-C4H9)+.
(г) Алкилированием трет-бутилового эфира (1RS,2RS,3RS,5RS)-3-(4-фторфенил)-2-гидрокси-8-азабицикло [3,2,1] октан-8-карбоновой кислоты 1-бензилокси-3- хлорметилнафталином (пример 19) аналогично описанному в примере 1(ж) способу получили трет-бутиловый эфир (1RS,2RS,3RS,5SR)-2-(4- бензилоксинафталин-2-илметокси)-3-(4-фторфенил)-8-азабицикло [3,2,1]октан-8-карбоновой кислоты в виде бесцветного твердого вещества; МС: 568 (М+Н)+.
(д) В результате отщепления BOC-группы с помощью хлористого водорода в этаноле аналогично описанному в примере 22(м) способу получили (1RS,2RS,3RS, 5SR)-2-(4-бензилоксинафталин-2-илметокси) -3-(4-фторфенил)-8-азабицикло[3,2,1] октан в виде окрашенного в бежевый цвет твердого вещества; МС: 468 (М+Н)+.
Пример 85.
Раствор из 0,330 г (0,71 ммоля) метилового эфира (1RS,2RS,3RS,5SR)-4'-[3-(4-хлорфенил)-8- азабицикло[3,2,1]окт-2-илоксиметил]бифенил-2-карбоновой кислоты в 10 мл простого эфира медленно по каплям добавляли к суспензии 33 мг алюмогидрида лития в 5 мл простого эфира и перемешивали в течение 4 ч при комнатной температуре. После добавления водного простого эфира, а затем воды фазы разделяли, органическую фазу промывали насыщенным раствором поваренной соли, сушили над сульфатом натрия, фильтровали и упаривали. Остаток хроматографировали на силикагеле с использованием смеси 140:10:1 метиленхлорида, метанола и аммиака в качестве элюента. Таким путем получили 0,210 г (68% от теории) (1RS, 2RS,3RS,5SR)-[4'-[3-(4- хлорфенил)-8-азабицикло[3,2,1]окт-2-илоксиметил] бифенил-2-ил] метанола в виде бесцветной пены; Rf 0,18 (SiO2, метиленхлорид:метанол:аммиак = 140:10:1); МС: 434 (М+Н)+.
Пример 86.
Путем отщепления BOC-группы получали следующие соединения:
1) из трет-бутилового эфира (3RS,4RS)-3- (нафталин-2-илметокси)-4-(4-проп-2-инилоксифенил)пиперидин-1- карбоновой кислоты с использованием трифторуксусной кислоты получили трифторацетат (3RS,4RS)-3-(нафталин-2-илметокси)-4-[4-(проп-2- инилокси)фенил] пиперидина в виде бесцветного твердого вещества; tпл 186oC (разлож.);
2) из трет-бутилового эфира (3RS,4RS)-4-(4-аллилоксифенил)-3-(нафталин-2-илметокси)пиперидин- 1-карбоновой кислоты с использованием соляной кислоты в метаноле получили (3RS,4RS)-4-(4-аллилоксифенил)-3- нафталин-2-илметоксипиперидин в виде светло-желтого масла; МС: 374 (М+Н)+;
3) из смеси трет-бутилового эфира (3RS,4RS)- и (3SR, 4SR)-4-[4-[(RS)-2,2-диметил[1,3] диоксолан-4-илметокси] фенил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты с использованием соляной кислоты в метаноле с одновременным отщеплением изопропилиденовой группы получили смесь (RS)- и (SR)-3-[(3RS, 4RS)-4-[3-(нафталин-2-илметокси)пиперидин-4- ил]фенокси]пропан-1,2-диола в виде желтоватого твердого вещества; МС: 408 (М+Н)+;
4) из смеси трет-бутилового эфира (3RS,4RS)- и (3SR,4SR)-4-[4-[(RS)-2-гидрокси-3-феноксипропокси] фенил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты с использованием трифторуксусной кислоты получили смесь трифторацетата (RS)- и (SR)-1-[4-[(3RS,4RS)-3-(нaфтaлин-2-илметoкси) пиперидин-4-ил] фенокси] -3-феноксипропан-2-ола в виде белого твердого вещества; МС: 484 (М+Н)+;
5) из смеси трет-бутилового эфира (3RS,4RS)- и (3SR,4SR)-4-[4-[(RS)-2-бензилокси-3-метоксипропокси] фенил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты с использованием трифторуксусной кислоты получили смесь трифторацетата (RS)- и (SR)-4-[(3RS,4RS)-4-(2-бензилокси-3-метоксипропокси) фенил] -3-(нафталин-2-илметокси)пиперидина в виде белого твердого вещества; tпл 138-139oC;
6) из смеси трет-бутилового эфира (3RS,4RS)- и (3SR,4SR)- 4-[4-[(RS)-2-гидрокси-3-фенилсульфанилпропокси] фенил] -3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты с использованием трифторуксусной кислоты получили смесь трифторацетата (RS)- и (SR)-1-[(3RS, 4RS)-4-[3-(нафталин-2- илоксиметил)пиперидин-4-ил]фенокси]-3-фенилсульфанилпропан-2- ола в виде белого твердого вещества; МС: 500 (М+Н)+;
7) из смеси трет-бутилового эфира (3RS,4RS)- и (3SR,4SR)-4-[4-[(RS)-2 метокси-3-феноксипропокси] фенил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты с использованием трифторуксусной кислоты получили смесь трифторацетата (3RS,4RS)-4-[4-[(RS)- и -[(SR)-2-метокси-3- феноксипропокси] фенил] -3-(нафталин-2-илметокси)пиперидина в виде белого твердого вещества; МС: 498 (М+Н)+;
8) из смеси трет-бутилового эфира (3RS,4RS)- и (3SR,4SR)-4-[4-[(RS)-2-бензоилокси-3-метоксипропокси] фенил]-3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты с использованием трифторуксусной кислоты получили смесь трифторацетата 1-метоксиметил-2-[4-[(3RS, 4RS)-3-(нафталин-2-илметокси)пиперидин- 4-ил]фенокси] этилового эфира (RS)- и (SR)-бензойной кислоты в виде белого твердого вещества; МС: 526 (М+Н)+;
9) из смеси трет-бутилового эфира (3RS,4RS)-4-[4-[(RS)- и -[(SR)-(3-бензилокси-2-метоксипропокси] фенил] -3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты получили смесь трифторацетата (3RS,4RS)-4-[4-[(RS)- и -[(SR)-(3- бензилокси-2-метоксипропокси]фенил]-3-(нафталин-2-илметокси) пиперидина в виде белого твердого вещества; МС: 512 (М+Н)+;
10) из трет-бутилового эфира (3RS,4RS)-3-(нафталин-2-илметокси)-4-{4-[2-(пиридин -3-илметокси)этокси]фенил}пиперидин-1-карбоновой кислоты с использованием хлористого водорода в метаноле получили (3RS,4RS)-3-(2-[4-[3-(нафталин-2-илметокси)пиперидин-4-ил] фенокси] этоксиметил)пиридин в виде бесцветной смолы; МС: 469 (М+ Н)+;
11) из трет-бутилового эфира (3RS, 4RS)-4-{4-[2-(пиpидин- 3-илметокси)этокси]фенил}-3-[4-(2- триметилсиланилэтоксиметокси)нафталин-2-илметокси] пиперидин-1- карбоновой кислоты с использованием хлористого водорода в метаноле с одновременным отщеплением СЭМ-группы получили (3RS,4RS)-3-(4- [4-[2-(пиридин-3-илметокси)этокси]фенил]пиперидин-3-илоксиметил)нафталин-1-ол в виде бесцветной смолы; МС: 485 (М+Н)+;
12) из трет-бутилового эфира (3RS,4RS)-3-(нaфтaлин-2- илмeтoкcи)-4-{4-[2-(пиридин-4-илметокси)этокси] фенил} пиперидин- 1-карбоновой кислоты с использованием хлористого водорода в метаноле получили (3RS,4RS)-4-(2-{4-[3-(нафталин-2- илметокси)пиперидин-4-ил] фенокси} этоксиметил)пиридин в виде бесцветной смолы; МС: 469 (М+Н)+;
13) из трет-бутилового эфира (3RS,4RS)-3-(нафталин-2-илметокси)-4-{4-[2-(пиридин-2- илметокси)этокси] фенил}пиперидин-1-карбоновой кислоты с использованием хлористого водорода в метаноле получили (3RS, 4RS)- 2-(2- {4-[3-(нафталин-2-илметокси)пиперидин-4-ил] фенокси} этоксиметил)пиридин в виде бесцветной смолы; МС: 469 (М+Н)+;
14) из трет-бутилового эфира (3RS, 4RS)-4-[4-(3- бензилоксипропокси)фенил] -3-(нафталин-2-илметокси)пиперидин- 1-карбоновой кислоты с использованием хлористого водорода в метаноле получили (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(нафталин-2- илметокси)пиперидин в виде бесцветной смолы; МС: 482 (М+Н)+;
15) из трет-бутилового эфира (3RS, 4RS)-3-(нафталин-2- илметокси)-4-[4-[3-(пиридин-2-илметокси)пропокси]фенил] пиперидин-1-карбоновой кислоты с использованием хлористого водорода в метаноле получили (3RS, 4RS)-2-(3-{4-[3-(нафталин-2-илметокси) пиперидин-4-ил] фенокси}пропоксиметил)пиридин в виде бесцветного твердого вещества; МС: 483 (М+Н)+;
16) из трет-бутилового эфира (3RS,4RS)- 3-(нафталин-2-илметокси)-4-[4-[3-(пиридин-2-илметокси)пропил] фенил]пиперидин-1-карбоновой кислоты с использованием хлористого водорода в метаноле получили (3RS, 4RS)-2-[3-[4-[3-(нафталин-2- илметокси)пиперидин-4-ил] фенил] пропоксиметил] пиридин в виде бесцветного аморфного твердого вещества; МС: 467 (М+Н)+;
17) из трет-бутилового эфира (3RS,4RS)-4-[4-[3-(бензилметиламино)пропокси] фенил] -3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты с использованием хлористого водорода в метаноле получили (3RS, 4RS)-бензилметил-(3-{ 4-[3-(нафталин-2-илметокси) пиперидин-4-ил] фенокси}пропил)амин в виде бесцветного твердого вещества; МС: 495 (М+Н)+;
18) из трет-бутилового эфира (3RS, 4RS)- 4-[4-[3-(бензотиазол-2-илсульфонил)пропокси] фенил] -3-(1- метоксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты с использованием хлористого водорода в метаноле получили (3RS, 4RS)- 2-[3-[4-[3-(1-метоксинафталин-2-илметокси)пиперидин-4-ил] фенокси]пропилсульфонил]бензотиазол в виде бесцветной пены; МС: 571 (М+Н)+;
19) из трет-бутилового эфира (3RS,4RS)-3-(нафталин-2- илметокси)-4-[4-(3-фенилсульфанилпропил)фенил] пиперидин-1- карбоновой кислоты с использованием хлористого водорода в метаноле получили (3RS, 4RS)-3-(нафталин-2-илметокси)-4-[4-(3- фенилсульфанилпропил)фенил] пиперидин в виде белого твердого вещества; МС: 468 (М+Н)+;
20) из трет-бутилового эфира (3RS, 4RS)-4-{4-[3-(бензотиазол-2-илсульфанил)пропил] фенил)-3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты с использованием хлористого водорода в метаноле получили (3RS,4RS)- 2-(3-{ 4-[3-(нафталин-2-илметокси)пиперидин-4-ил]фенил} пропилсульфанил)бензотиазол в виде белого твердого вещества; МС: 525 (М+Н)+;
21) из трет-бутилового эфира (3RS, 4RS)-4-{4-[2- (пиримидин-2-илсульфанил)этил] фенил}-3-[4-(2- триметилсиланилэтоксиметокси)нафталин-2-илметокси] пиперидин-1- карбоновой кислоты с использованием хлористого водорода в метаноле с одновременным отщеплением СЭМ-группы получили (3RS,4RS)-3-[4- [4-[2-(пиримидин-2-илсульфанил)этил] фенил] пиперидин-3- илоксиметил]нафталин-1-ол в виде бесцветной пены; МС: 472 (М+Н)+;
22) из трет-бутилового эфира (3RS, 4RS)-4-{4-[2-(пиридин-2-илсульфанил)этил] фенил}-3-[4-(2- триметилсиланилэтоксиметокси)нафталин-2-илметокси] пиперидин-1- карбоновой кислоты с использованием хлористого водорода в метаноле с одновременным отщеплением СЭМ-группы получили (3RS,4RS)-3-(4- {4-[2-(пиридин-2-илсульфанил)этил] фенил}пиперидин-3-илоксиметил)нафталин-1-ол; МС: 471 (М+Н)+;
23) из трет-бутилового эфира (3RS,4RS)-4-[4-[2-(бензотиазол-2-илсульфанил)этил] фенил] -3- [4-(2-триметилсиланилэтоксиметокси)нафталин-2- илметокси] пиперидин-1-карбоновой кислоты с использованием хлористого водорода в метаноле с одновременным отщеплением СЭМ- группы получили (3RS,4RS)-3-[4-[4-[2-(бензотиазол-2- илсульфанил)этил] фенил] пиперидин-3-илоксиметил]нафталин-1-ол в виде бесцветного твердого вещества; МС: 527 (М+Н)+;
24) из трет-бутилового эфира (3RS, 4RS)-3-(нафталин-2-илметокси)-4-[4-(пиридин-3-илметоксиметил) фенил]пиперидин-1-карбоновой кислоты с использованием хлористого водорода в метаноле получили (3RS, 4RS)-3-[4-[3- (нафталин-2-илметокси)пиперидин-4-ил] бензилоксиметил] пиридин в виде бесцветной пены; МС: 438 (М+Н)+;
25) из смеси трет-бутилового эфира (3RS, 4RS)-4-(4-{2-[(RS)- и (SR)-2-(4-фторфенил)-3-метилбутирилокси] этокси} фенил] -3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты с использованием бромида цинка в метиленхлориде получили смесь гидробромида (3RS,4RS)-2-[4-(3- нафталин-2-илметоксипиперидин-4-ил)фенокси] этилового эфира (RS)- и (SR)-2-(4-фторфенил)-3-метилмасляной кислоты в виде белого твердого вещества; МС: 556 (М+Н)+;
26) из трет-бутилового эфира (3RS,4RS)-4-[4-[2-(1-метил-1H-пиррол-2-карбонилокси)этокси] фенил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты с использованием бромида цинка в метиленхлориде получили гидробромид (3RS, 4RS)-[4-[3-(нафталин-2-илметокси)пиперидин-4-ил] фенокси] этилового эфира 1-метил-1H-пиррол-2-карбоновой кислоты в виде бежевого твердого вещества; МС: 485 (М+Н)+;
27) из трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензоилоксипропил)фенил] -3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты с использованием хлористого водорода в метаноле получили 3-{ 4-[3- (нафталин-2-илметокси)пиперидин-4-ил] фенил} пропиловый эфир (3RS,4RS)-бензойной кислоты в виде желтого сиропа; МС: 480 (М+Н)+;
28) из трет-бутилового эфира (3RS,4RS)-4-{4-[3-(3- метоксибензоилокси)пропил] фенил)-3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты с использованием хлористого водорода в метаноле получили 3-{4-[3-(нафталин-2- илметокси)пиперидин-4-ил]фенил}пропиловый эфир (3RS,4RS)-3- метоксибензойной кислоты в виде желтого твердого вещества; МС: 510 (М+Н)+;
29) из трет-бутилового эфира (3RS,4RS)-4-[4-(3- метоксибензоилоксиметил)фенил]-3-[1-(2- триметилсиланилэтоксиметокси)нафталин-2-илметокси]пиперидин-1- карбоновой кислоты с использованием хлористого водорода в метаноле с одновременным отщеплением СЭМ-группы получили (3RS,4RS)-4-[3- (1-гидроксинафталин-2-илметокси)пиперидин-4-ил] бензиловый эфир 3- метоксибензойной кислоты в виде бесцветной пены; МС: 498 (М+Н)+;
30) из трет-бутилового эфира (3RS,4RS)-4-(4- этоксикарбонилметоксифенил)-3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты с использованием трифторуксусной кислоты получили трифторацетат этилового эфира (3RS, 4RS)-[4-[3- (нафталин-2-илметокси)пиперидин-4-ил]фенокси] уксусной кислоты в виде белого твердого вещества; МС: 420 (М+Н)+;
31) из трет-бутилового эфира (3RS,4RS)-4-[4-(бензилкарбамоилметокси)фенил] - 3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты с использованием трифторуксусной кислоты получили трифторацетат (3RS,4RS)-N-бензил-2-[4-[3-(нафталин-2-илметокси)пиперидин-4- ил]фенокси]ацетамида в виде белого твердого вещества; tпл 185oC;
32) из трет-бутилового эфира (3RS,4RS)-3-(нафталин-2-илметокси)-4-[4- (пиридин-2-илкарбамоилокси)фенил] пиперидин-1-карбоновой кислоты с использованием трифторуксусной кислоты получили трифторацетат (3RS,4RS)-[4-[3-(нафталин-2-илметокси)пиперидин-4-ил] -3-фенилового эфира пиридин-2-илкарбаминовой кислоты в виде белого твердого вещества; tпл 158oC;
33) из трет-бутилового эфира (3RS,4RS)-4-(4-карбоксиметоксифенил)-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты [пример 86(дд)] с использованием трифторуксусной кислоты получили трифторацетат (3RS,4RS)-[4-[3-(нафталин-2-илметокси)пиперидин-4-ил] фенокси] уксусной кислоты в виде белого твердого вещества; tпл 183-184oC;
34) из трет-бутилового эфира (3RS,4RS)-3-(нaфтaлин-2-илметoкcи)-4-[4-(2-оксо-3-феноксипропокси) фенил]пиперидин-1-карбоновой кислоты с использованием трифторуксусной кислоты получили трифторацетат (3RS, 4RS)-1-[4- [3-(нафталин-2-илметокси)пиперидин-4-ил] фенокси] -3-феноксипропан-2-она в виде белого твердого вещества; tпл 145-146oC;
35) из трет-бутилового эфира (3RS, 4RS)- 4-[4-(2-этоксикарбонилэтил)фенил] -3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты [пример 24(у)] с использованием бромида цинка в метиленхлориде получили этиловый эфир (3RS, 4RS)-3- {4-[3-(нафталин-2-илметокси)пиперидин-4-ил]фенил}пропионовой кислоты в виде желтоватого сиропа; МС: 418 (М+Н)+;
36) из смеси трет-бутилового эфира (3RS, 4RS)-4-[4-[(RS)- и - [(SR)-2-гидрокси-2-фенилэтил] фенил] -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты с использованием хлористого водорода в метаноле получили смесь гидрохлорида (RS)- и (SR)-2-[4-[(3RS,4RS)-3-нафталин-2-илметоксипиперидин-4-ил] фенил]этанола; МС: 438 (М+Н)+;
37) из трет-бутилового эфира (3RS,4RS)-4-(4-фторфенил)-3-(2-{ [(пиридин-2-карбонил)амино] метил} бензилокси)пиперидин-1-карбоновой кислоты с использованием хлористого водорода в метаноле получили дигидрохлорид (3RS, 4RS)-2- [4-(4-фторфенил)пиперидин-3-илоксиметил]бензилбромида пиридин-2-карбоновой кислоты в виде белого твердого вещества; МС: 420 (М+Н)+;
38) из трет-бутилового эфира (3RS,4RS)-3-(3-бензоилбензилокси)-4-(4-фторфенил)пиперидин-1- карбоновой кислоты с использованием хлористого водорода в метаноле получили гидрохлорид (3RS, 4RS)-[3-[4-(4-фторфенил)пиперидин-3- илоксиметил] фенил] фенилметанона в виде белого аморфного твердого вещества; МС: 390 (М+Н)+;
39) из трет-бутилового эфира (3RS, 4RS)-3-(нафталин-2-илметокси)-4-[4-[2-(5-фенил[1,2,4] оксадиазол-3-ил)этил]фенил]пиперидин-1-карбоновой кислоты с использованием хлористого водорода в метаноле получили (3RS, 4RS)- 3-(нафталин-2-илметокси)-4-[4-[2-(5-фенил[1,2,4] оксадиазол-3- ил)этил]фенил] пиперидина в виде белого твердого вещества; МС: 490 (М+Н)+;
40) из трет-бутилового эфира (3RS,4RS)-3-(нафталин- 2-илметокси)-4-[4-[2-(3-фенил[1,2,4]оксадиазол-5-ил)этил] фенил]пиперидин-1-карбоновой кислоты с использованием хлористого водорода в метаноле получили (3RS, 4RS)-3-(нафталин-2-илметокси)-4- [4-[2-(3-фенил[1,2,4] оксадиазол-5-ил)этил]фенил] пиперидина в виде белого твердого вещества; МС: 490 (М+Н)+;
41) из трет-бутилового эфира (3RS,4RS)-3-(нафталин-2-илметокси)-4-[4-(3-фенил-[1,2,4] оксадиазол-5-илметокси)фенил]пиперидин-1-карбоновой кислоты с использованием трифторуксусной кислоты получили трифторацетат (3RS, 4RS)-3-(нафталин-2-илметокси)-4-[4-(3-фенил-[1,2,4] оксадиазол-5- илметокси)фенил] пиперидина в виде белого твердого вещества; tпл 195-196oC;
42) из трет-бутилового эфира (3RS,4RS)-3-(нафталин-2-илметокси)-4-[4-(3-пиридин-З-ил-[1,2,4] оксадиазол-5-илметокси)фенил]пиперидин-1-карбоновой кислоты с использованием трифторуксусной кислоты получили трифторацетат (3RS, 4RS)-3-(5-[4-[3-(нафталин-2-илметокси)пиперидин-4- ил]феноксиметил]-[1,2,4] оксадиазол-3-ил) пиридина в виде белого твердого вещества; МС: 493 (М+Н)+;
43) из трет-бутилового эфира (3RS,4RS)-3-(нафталин-2-илметокси)-4-[4-(3-фенилизоксазол- 5-илметокси)фенил] пиперидин-1-карбоновой кислоты с использованием трифторуксусной кислоты получили трифторацетат (3RS,4RS)-3- (нафталин-2-илметокси)-4-[4-(3-фенилизоксазол-5-илметокси)фенил] пиперидина в виде белого твердого вещества; МС: 491 (М+Н)+;
44) из трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(3-метоксибензилокси)пиперидин-1-карбоновой кислоты с использованием хлористого водорода в метаноле получили гидрохлорид (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(3- метоксибензилокси)пиперидина в виде бесцветного масла; МС: 462 (М+Н)+;
45) из трет-бутилового эфира (3RS, 4RS)-4-[4-(3- бензилоксипропокси)фенил]-3-[3-(2- триметилсиланилэтоксиметокси)бензилокси]пиперидин-1-карбоновой кислоты с использованием хлористого водорода в метаноле с одновременным отщеплением СЭМ-группы получили (3RS,4RS)-3-{4-[4- (3-бензилоксипропокси)фенил] пиперидин-3-илоксиметил}фенол в виде бесцветного масла; МС: 448 (М+Н)+;
46) из трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(3-хлор-4- метоксибензилокси)пиперидин-1-карбоновой кислоты с использованием бромида цинка в метиленхлориде получили гидробромид (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(З-хлор-4- метоксибензилокси)пиперидина в виде бесцветного масла; МС: 497 (М+Н)+;
47) из трет-бутилового эфира (3RS, 4RS)-4-[4-(3- бензилоксипропокси)фенил] -3-(3,4-дихлорбензилокси)пиперидин-1- карбоновой кислоты с использованием хлористого водорода в метаноле получили гидрохлорид (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил]-3-(3,4- дихлорбензилокси)пиперидина в виде бесцветного масла; МС: 500 (М)+;
48) из трет-бутилового эфира (3RS, 4RS)-4-[4-(3- бензилоксипропокси)фенил] -3-(2,5-дихлорбензилокси)пиперидин-1- карбоновой кислоты с использованием хлористого водорода в метаноле получили гидрохлорид (3RS, 4RS)-4-[4-(3-бензилокрипропокси)фенил] - 3-(2,5-дихлорбензилокси)пиперидина в виде бесцветного масла; МС: 500 (М)+;
49) из трет-бутилового эфира (3RS, 4RS)-3-бензилоксипропокси-4-[4-(3-бензилоксипропокси)фенил] пиперидин-1-карбоновой кислоты с использованием бромида цинка в метиленхлориде получили гидробромид (3RS, 4RS)-3-бензилокси-4-[4-(3-бензилоксипропокси)фенил] пиперидина в виде бесцветного твердого вещества; МС: 432 (М+Н)+;
50) из трет-бутилового эфира (3RS, 4RS)-4-[4-(3- бензилоксипропокси)фенил] -3-(2,5-диметилбензилокси)пиперидин-1- карбоновой кислоты с использованием бромида цинка в метиленхлориде получили гидробромид (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(2,5-диметилбензилокси)пиперидина в виде бесцветного масла; МС: 460 (М+Н)+;
51) из трет-бутилового эфира (3RS, 4RS)-4-[4-(3- бензилоксипропокси)фенил]-3-(4-этилбензилокси)пиперидин-1- карбоновой кислоты с использованием бромида цинка в метиленхлориде получили (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(4- этилбензилокси)пиперидин в виде бесцветного масла; МС: 460 (М+Н)+;
52) из смеси трет-бутилового эфира (3RS,4RS)-4-[4-(3- бензилоксипропокси)фенил]-3-(3- и 4-винилбензилокси)пиперидин-1- карбоновой кислоты с использованием бромида цинка в метиленхлориде получили смесь гидробромида (3RS, 4RS)-4-[4-(3- бензилоксипропокси)фенил]-3-(3- и 4-винилбензилокси)пиперидина в виде бесцветного твердого вещества; МС: 458 (М+Н)+;
53) из трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(2, 3-дигидробензо [1,4]диоксин-6-илметокси)пиперидин-1-карбоновой кислоты с использованием бромида цинка в метиленхлориде получили (3RS,4RS)-4- [4-(3-бензилоксипропокси)фенил]-3-(2,3-
дигидробензо[1,4] диоксин-6-илметокси)пиперидин в виде бесцветной смолы; МС: 490 (М+Н)+;
54) из трет-бутилового эфира (RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(5,6,7, 8- тетрагидронафталин-2-илметокси)пиперидин-1-карбоновой кислоты с использованием бромида цинка в метиленхлориде получили (3RS,4RS)- 4-[4-(3-бензилоксипропокси)фенил] -3-(5,6,7, 8-тетрагидронафталин- 2-илметокси)пиперидин в виде бесцветной смолы; МС: 486 (М+Н)+;
55) из трет-бутилового эфира (3RS, 4RS)-4-[4-(3- бензилоксипропокси)фенил]-3-[4-(2- триметилсиланилэтоксиметокси)нафталин-2-илметокси]пиперидин-1- карбоновой кислоты с использованием хлористого водорода в метаноле с одновременным отщеплением СЭМ-группы получили (3RS,4RS)-3-{4-[4- (3-бензилоксипропокси)фенил]пиперидин-3-илоксиметил} нафталин-1-ол в виде бесцветной смолы; МС: 498 (М+Н)+;
56) из трет-бутилового эфира (3RS,4RS)-4-[4-(4-бензилоксибутокси)фенил]- 3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты с использованием хлористого водорода в метаноле получили (3RS, 4RS)- 4-[4-(4-бензилоксибутокси)фенил] -3-(нафталин-2- илметокси)пиперидин в виде бесцветного масла; МС: 496 (М+Н)+;
57) из трет-бутилового эфира (3SR,4RS, 5RS)-4-[4-(2- хлорбензоилоксиметил)фенил] -3-метоксиметил-5-(нафталин-2- илметокси)пиперазин-1-карбоновой кислоты с использованием хлористого водорода в метаноле получили 4-[3-метоксиметил-5- (нафталин-2-илметокси)пиперидин-4-ил] бензиловый эфир (3SR,4RS, 5RS)-2-xлopбeнзoйнoй кислоты в виде бесцветной пены; МС: 530 (М+Н)+;
58) из трет-бутилового эфира (3SR, 4RS,5RS)-4-(4- мeтoкcикapбoнилфенил)-3-метоксиметил-5-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты с использованием хлористого водорода в метаноле получили метиловый эфир (3SR,4RS,5RS)-4-[3- мeтoкcиметил-5-нaфтaлин-2-илметoкcипипepидин-4-ил]бензойной кислоты в виде бесцветного твердого вещества; МС: 420 (М+Н)+;
59) из трет-бутилового эфира (3SR, 4RS,5RS)-4-(4- бензилоксиметилфенил)-3-метоксиметил-5-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты с использованием хлористого водорода в метаноле получили (3SR, 4RS,5RS)-4-(4- бензилоксиметилфенил)-3-метоксиметил-5-(нафталин-2- илметокси)пиперидин в виде бесцветной пены; МС: 482 (М+Н)+;
60) из трет-бутилового эфира (1RS,2RS,3RS, 5SR)-3-[4-(2-бензилоксипропоксиметил)фенил] -2-(нафталин-2-илметокси)-8-азабицикло [3,2,1] октан-8-карбоновой кислоты с использованием хлористого водорода в метаноле получили (1RS, 2RS, 3RS, 5SR)-2-(нафталин-2- илметокси)-3-[4-(3-феноксипропоксиметил)фенил] -8- азабицикло[3,2,1] октан в виде бесцветного масла; МС: 508 (М+Н)+.
Использованные в качестве исходных веществ BOC-производные получали следующим путем.
(а) Аналогично примеру 44(д) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-(4-гидроксифенил) пиперидин-1-карбоновой кислоты [пример 46 (б)] пропаргилбромидом в присутствии карбоната калия в ацетоне получили трет-бутиловый эфир (3RS,4RS)-3-гидрокси-4-(4-проп-2-инилоксифенил) пиперидин-1-карбоновой кислоты, алкилированием которого 2-бромметилнафталином аналогично примеру 1(ж) получили трет-бутиловый эфир (3RS, 4RS)-3-(нафталин-2-илметокси)-4-(4-проп- 2-инилоксифенил)пиперидин-1-карбоновой кислоты в виде светло-желтого твердого вещества; МС: 472 (М+Н)+.
(б) Аналогично примеру 44(д) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-(4-гидроксифенил) пиперидин-1-карбоновой кислоты [пример 46(б)] аллилбромидом в присутствии карбоната калия в ацетоне получили трет-бутиловый эфир (3RS,4RS)-3-гидрокси-4-(4-аллилоксифенил)пиперидин-1-карбоновой кислоты, алкилированием которого 2-бромметилнафталином аналогично примеру 1(ж) получили трет-бутиловый эфир (3RS, 4RS)-4-(4-аллилоксифенил)-3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты в виде бесцветной смолы; МС: 474 (М+Н)+.
(в) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-(4- гидроксифенил)пиперидин-1-карбоновой кислоты [пример 46(б)] (RS)-2,2-диметил[1,3]диоксолан-4- илметиловым эфиром метансульфокислоты в присутствии гидрида натрия получили смесь трет-бутилового эфира (3RS, 4RS)- и (3SR,4SR)-4-[4- [(RS)-2,2-диметил[1,3]диоксолан-4-илметокси]фенил]-3- гидроксипиперидин-1-карбоновой кислоты, алкилированием которой 2- бромметилнафталином аналогично примеру 1(ж) получили смесь трет- бутилового эфира (3RS, 4RS)- и (3SR,4SR)-4-[4-[(RS)-2,2-диметил[1,3]диоксолан-4-илметокси]фенил]-3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты в виде белого твердого вещества; МС: 547 (М)+.
(г) Аналогично примеру 1(ж) путем алкилирования трет- бутилового эфира (3RS, 4RS)-3-гидрокси-4-(4-гидроксифенил) пиперидин-1-карбоновой кислоты [пример 46 (б)] (RS)-2,3- эпoкcипpoпил-п-тoлуoлcульфoнaтoм в присутствии гидрида натрия получили смесь трет-бутилового эфира (3RS, 4RS)- и (3SR, 4SR)-3- гидрокси-4-[(RS)-4-oкcиpaнилметoкcифенил] пипеpидин-1-карбоновой кислоты, алкилированием которой 2-бромметилнафталином аналогично примеру 1(ж) получили смесь трет-бутилового эфира (3RS, 4RS)- и (3SR,4SR)-3-(нафталин-2-илметокси)-4-[(RS)-4- oкcиpaнилметoкcифенил] пиперидин-1-карбоновой кислоты. В результате последующего раскрытия эпоксидного кольца фенолятом калия аналогично примеру 71(а) получили смесь трет-бутилового эфира (3RS, 4RS)- и (3SR,4SR)-4-[4-[(RS)-2-гидрокси-3-феноксипропокси] фенил]-3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде белого твердого вещества; МС: 584 (М+Н)+.
(д) Раскрытием эпоксидного кольца из смеси трет-бутилового эфира (3RS, 4RS)- и (3SR, 4SR)-3-(нафталин-2- илметокси)-4-[(RS)-4-оксиранилметоксифенил] пиперидин-1-карбоновой кислоты [пример 86(г)] метилатом натрия в N,N-диметилформамиде получили смесь трет-бутилового эфира (3RS,4RS)- и (3SR,4SR) -4- [4-[(RS)-2-гидрокси-3-метоксипропокси] фенил] -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты, алкилированием которой бензилбромидом аналогично примеру 1(ж) получили смесь трет- бутилового эфира (3RS,4RS)- и (3SR, 4SR)-4-[4-[(RS)-бензилокси-3-метоксипропокси] фенил]-3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты в виде бесцветной смолы; МС: 612 (М+Н)+ .
(е) Раскрытием эпоксидного кольца из смеси трет-бутилового эфира (3RS, 4RS)- и (3RS,4SR)-3-(нафталин-2-илметокси)-4-[(RS)-4-oксиранилметоксифенил] пиперидин-1-карбоновой кислоты [пример 86(г)] тиофенолятом натрия аналогично примеру 71(а) получили смесь трет-бутилового эфира (3RS,4RS)- и (3SR,4SR)-4-[4-[(RS)-2- гидрокси-3-фенилсульфанилпропокси] фенил] -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты в виде белого твердого вещества; МС: 600 (М+Н)+.
(ж) Алкилированием смеси трет-бутилового эфира (3RS,4RS)- и (3SR, 4SR)-4-[4-[(RS)-2-гидрокси-3-феноксипропокси] фенил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты [пример 86(г)] метилиодидом аналогично примеру 1(ж) получили смесь трет-бутилового эфира (3RS,4RS)- и (3SR,4SR)-4-[4-[(RS) -2-метокси-3-феноксипропокси] фенил] -3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты в виде бесцветной смолы; МС: 598 (М+Н)+.
(з) Аналогично примеру 22(л) путем бензоилирования смеси трет-бутилового эфира (3RS,4RS)- и (3SR,4SR)-4-[4-[(RS)-2-гидрокси-3-метоксипропокси]фенил] -3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты [пример 86(д)] получили смесь трет-бутилового эфира (3RS,4RS)- и (3SR,4SR)-4-[4-[(RS)-2-бензоилокси-3-метоксипропокси] фенил]-3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветной смолы; МС: 626 (М+Н)+.
(и) Раскрытием эпоксидного кольца из смеси трет-бутилового эфира (3RS, 4RS)- и (3SR, 4SR)-3- (нaфтaлин-2-илметoкcи)-4-[(RS)-4-оксиранилметоксифенил] пиперидин- 1-карбоновой кислоты [пример 86(г)] бензилатом натрия в N,N- диметилформамиде получили смесь трет-бутилового эфира (3RS, 4RS)- и (3SR, 4SR)-4-[4-[(RS)-3-бензилокси-2-гидроксипропокси] фенил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты, алкилированием которой метилиодидом аналогично примеру 1(ж) получили смесь трет-бутилового эфира (3RS,4RS)- и (3SR, 4SR)-4-[4- [(RS)-3-бензилокси-2-метоксипропокси]фенил]-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты в виде бесцветной смолы; МС: 612 (М+Н)+.
(к) Аналогично примеру 1(ж) алкилированием трет-бутилового эфира (3RS, 4RS)-4-[4-(2-гидроксиэтокси)фенил] -3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты [пример 53(в)] 3-xлорметилпиридином получили трет-бутиловый эфир (3RS, 4RS)-3- (нафталин-2-илметокси)-4-{ 4-[2-(пиридин-3-илметокси)этокси] фенил}пиперидин-1-карбоновой кислоты; МС: 569 (M+H)+.
(л) Аналогично примеру 1(ж) алкилированием трет-бутилового эфира (3RS, 4RS)-4-[4-(2-гидроксиэтокси)фенил] -3-[4-(2- триметилсиланилэтоксиметокси)нафталин-2-илметокси] пиперидин-1- карбоновой кислоты [пример 55(б)] 3-хлорметилпиридином получили трет-бутиловый эфир (3RS, 4RS)-4-{ 4-[2-(пиридин-3- илметокси)этокси] фенил} -3-[4-(2-триметилсиланилэтоксиметокси)нафталин-2- илметокси]пиперидин-1-карбоновой кислоты.
(м) Аналогично примеру 1(ж) алкилированием трет-бутилового эфира (3RS, 4RS)-4-[4-(2-гидроксиэтокси)фенил] -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты [пример 53(в)] 4-хлорметилпиридином получили трет-бутиловый эфир (3RS, 4RS)-3- (нaфтaлин-2-илметoкcи)-4-{4-[2-(пиридин-4-илметокси)этокси]фенил}пиперидин-1-карбоновой кислоты в виде бесцветного масла.
(н) Аналогично примеру 1(ж) алкилированием трет-бутилового эфира (3RS, 4RS)-4-[4-(2-гидроксиэтокси)фенил] -3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты [пример 53(в)] 2-хлорметилпиридином получили трет-бутиловый эфир (3RS, 4RS)-3- (нaфтaлин-2-илметoкcи)-4-{4-[2-(пиридин-2-илметокси)этокси] фенил}пиперидин-1-карбоновой кислоты в виде бесцветного масла.
(о) Аналогично примеру 44(д) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-(4-гидроксифенил)пиперидин-1- карбоновой кислоты [пример 46(б)] бензил-3-бромпропиловым эфиром в присутствии карбоната калия в бутан-2-оне получили трет-бутиловый эфир (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3- гидроксипиперидин-1-карбоновой кислоты, алкилированием которого 2-бромметилнафталином аналогично примеру 1(ж) получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(3- бензилоксипропокси)фенил]-3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 582 (M+H)+.
(п) Аналогично примеру 1(ж) алкилированием трет-бутилового эфира (3RS, 4RS)-4-[4-(3-гидроксипропокси)фенил] -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты [пример 57(в)] 2- хлорметилпиридином получили трет-бутиловый эфир (3RS, 4RS)-3- (нафталин-2-илметокси)-4-[4-[3-(пиридин-2-илметокси)пропокси] фенил]пиперидин-1-карбоновой кислоты в виде бесцветной смолы; МС: 583 (М+Н)+.
(р) Аналогично примеру 1(ж) алкилированием трет-бутилового эфира (3RS, 4RS)-4-[4-(3-гидроксипропил)фенил] -3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты [пример 24(ф)] 2-хлорметилпиридином получили трет-бутиловый эфир (3RS,4RS)-3-(нафталин-2-илметокси)-4-[4-[3-(пиридин-2- илметокси)пропил] фенил] пиперидин-1-карбоновой кислоты в виде бесцветного аморфного твердого вещества, которое без дальнейшей очистки и определения характеристик использовали на следующей стадии.
(с) Аналогично примеру 44(д) путем алкилирования трет-бутилового эфира (3RS, 4RS)-4-[4-(3-метиламинопропокси)фенил] -3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты [пример 57(д)] бензилбромидом получили трет-бутиловый эфир (3RS,4RS)-4-[4- [3-(бензилметиламино) пропокси] фенил] -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 595 (М+Н)+.
(т) Аналогично примеру 1(ж) путем алкилирования смеси трет-бутилового эфира (3RS, 4RS)- и (3SR,4SR)-3-гидрокси-4-[4-[3-[(RS)-тетрагидропиран-2-илокси] пропокси]фенил]пиперидин-1-карбоновой кислоты [пример 57(а)] 1-метокси-2-бромметилнафталином [пример 7(е)] получили смесь трет-бутилового эфира (3RS, 4RS)- и (3SR,4SR)-3-(1-метoкcинaфтaлин-2- илметокси)-4-[4-[3-[(RS)-тетрагидропиран-2-илокси] пропокси] фенил]пиперидин-1-карбоновой кислоты. В результате отщепления ТГП-группы с помощью пиридиний(толуол-4-сульфоната) в этаноле аналогично примеру 53(в) получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(3-гидроксипропокси)фенил] -3-(1-метоксинафталин-2- илметокси)пиперидин-1-карбоновой кислоты, в результате взаимодействия которого с бис(бензотиазол-2- ил)дисульфидом аналогично примеру 33 (а) получили трет-бутиловый эфир (3RS,4RS)-4-[4-[3-(бензотиазол-2-илсульфонил)пропокси]фенил] -3- (1-метоксинафталин-2- илметокси)пиперидин-1-карбоновой кислоты в виде бесцветной жидкости; МС: 671 (М+Н)+.
(у) Аналогично примеру 33(а) взаимодействием трет-бутилового эфира (3RS, 4RS)-4-[4-(3- гидроксипропил)фенил]-3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты [пример 24(ф)] с дифенилдисульфидом получили трет-бутиловый эфир (3RS,4RS)-3-(нaфтaлин-2-илмeтoкcи)-4-[4-(3- фенилсульфанилпропил)фенил] пиперидин-1-карбоновой кислоты в виде бесцветного аморфного твердого вещества; МС: 568 (М+Н)+.
(ф) Аналогично примеру 33(а) взаимодействием трет-бутилового эфира (3RS, 4RS)-4-[4-(3-гидроксипропил)фенил] -3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты [пример 24(ф)] с бис(бензотиазол- 2-ил)дисульфидом получили трет-бутиловый эфир (3RS,4RS)-4-{4-[3- (бензотиазол-2-илсульфанил)пропил]фенил} -3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты, который без дальнейшей очистки и определения характеристик использовали на следующей стадии.
(х)(α) Аналогично примеру 1(ж) алкилированием трет-бутилового эфира (3RS, 4RS)-3-гидpoкcи-4-[4-(2-тритилоксиэтил)фенил] пиперидин-1-карбоновой кислоты [пример 24(ф)] 3-хлорметил-1-(2- триметилсиланилэтоксиметокси)нафталином [пример 5(в)] получили трет-бутиловый эфир (3RS,4RS)-3-[4-(2- триметилсиланилэтоксиметокси)нафталин-2-илметокси] -4- [4-(2-тритилоксиэтил)фенил]пиперидин-1-карбоновой кислоты.
(β) Селективное отщепление тритильной группы осуществляли аналогично способу Е. Krainer и др. , опубликованному в Tetrahedron Letters 1993, 1713-1716, смешивая раствор из 780 мг (0,92 ммоля) трет-бутилового эфира (3RS, 4RS)-3-[4-(2- триметилсиланилэтоксиметокси)нафталин-2-илметокси] -4-[4-(2- тритилоксиэтил)фенил]пиперидин-1-карбоновой кислоты в 15 мл метиленхлорида с раствором из 436 мг (3,68 ммоля) трифторуксусной кислоты и 803 мг (3,68 ммоля) ангидрида трифторуксусной кислоты в 2 мл метиленхлорида. По истечении 30 с реакционную смесь охлаждали до 0oC и смешивали с 4 мл триэтиламина. По истечении 5 мин добавляли 10 мл метанола и смесь перемешивали в течение 10 мин. Далее промывали насыщенным раствором гидрокарбоната натрия, после чего водную фазу экстрагировали 10 мл метиленхлорида. Объединенные органические фазы сушили над сульфатом натрия и затем упаривали при пониженном давлении. Сырой продукт хроматографировали на силикагеле с использованием смеси 4:1 гексана и уксусного эфира в качестве элюента. Таким путем получили 553 мг трет-бутилового эфира (3RS,4RS)-4-[4-(2-гидроксиэтил)фенил]-3-[4-(2- триметилсиланилэтоксиметокси)нафталин-2-илметокси] пиперидин -1-карбоновой кислоты в виде бесцветного масла.
(γ) Аналогично примеру 34 из трет-бутилового эфира (3RS,4RS)-4-[4-(2- гидроксиэтил)фенил] -3-[4-(2- триметилсиланилэтоксиметокси)нафталин-2-илметокси] пиперидин-1- карбоновой кислоты через соответствующий мезилат путем взаимодействия с 2-меркаптопиримидином получили трет-бутиловый эфир (3RS, 4RS)-4-{ 4-[2-(пиримидин-2-илсульфанил)этил] фенил}-3-[4- (2-триметилсиланилэтоксиметокси)нафталин-2-илметокси] пиперидин-1 -карбоновой кислоты в виде бесцветного масла, которое без дальнейшей очистки и определения характеристик использовали на следующей стадии.
(ц) Аналогично примеру 33(а) из трет-бутилового эфира (3RS,4RS)-4-[4-(2-гидроксиэтил)фенил] -3-[4-(2- триметилсиланилэтоксиметокси)нафталин-2-илметокси]пиперидин-1- карбоновой кислоты путем взаимодействия с 2,2'-дитиопиридином получили трет-бутиловый эфир (3RS,4RS)-4-{4-[2-(пиридин-2- илсульфанил)этил] фенил} -3-[4-(2- триметилсиланилэтоксиметокси)нафталин-2-илметокси] пиперидин-1- карбоновой кислоты в виде бесцветного масла, которое без дальнейшей очистки и определения характеристик использовали на следующей стадии.
(ч) Аналогично примеру 33(а) из трет-бутилового эфира (3RS, 4RS)-4-[4-(2-гидроксиэтил)фенил] -3-[4-(2- триметилсиланилэтоксиметокси)нафталин-2-илметокси]пиперидин-1- карбоновой кислоты путем взаимодействия с бис(бензотиазол-2- ил)дисульфидом получили трет-бутиловый эфир (3RS,4RS)-4-[4-[2- (бензотиазол-2-илсульфанил)этил] фенил] -3-[4-(2-триметилсиланилэтоксиметокси)нафталин-2-илметокси] пиперидин-1-карбоновой кислоты в виде бесцветной пены; МС: 757 (М+Н)+.
(ш) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS, 4RS)-4-(4-гидроксиметилфенил)-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты [пример 22(к)] 3-хлорметилпиридином получили трет-бутиловый эфир (3RS, 4RS)-3- (нафталин-2-илметокси)-4-[4-(пиридин-3-илметоксиметил)фенил] пиперидин- 1-карбоновой кислоты в виде бесцветного масла; МС: 539 (М+Н)+.
(щ) Аналогично примеру 9(в) этерификацией трет-бутилового эфира (3RS, 4RS)-4-[4-(2- гидроксиэтокси)фенил]-3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты [пример 53(в)] (RS)-2-(4-фторфенил)-3- метилмасляной кислотой (патент Германии 2365555) в присутствии ЭДК получили смесь трет-бутилового эфира (3RS,4RS)- и (3SR,4SR)-4- (4-[2-[(RS)-2-(4-фторфенил)-3-метилбутирилокси]этокси] фенил)-3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 656 (М+Н)+.
(э) Аналогично примеру 9(в) этерификацией трет-бутилового эфира (3RS, 4RS)-4-[4-(2-гидроксиэтокси)фенил] -3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты [пример 53(в)] 1-метилпиррол-2- карбоновой кислотой в присутствии ЭДК получили трет-бутиловый эфир (3RS,4RS)-4-[4-[2-(1-метил-1Н-пиррол-2-карбонилокси)этокси] фенил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 585 (М+Н)+.
(аа) Аналогично примеру 22(л) путем ацилирования трет-бутилового эфира (3RS,4RS)-4-[4-(3- гидроксипропил)фенил]-3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты [пример 24(ф)] бензоилхлоридом получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(3-бензоилоксипропил)фенил]-3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 580 (М+Н)+.
(бб) Аналогично примеру 22(л) путем ацилирования трет-бутилового эфира (3RS,4RS)- 4-[4-(3-гидроксипропил)фенил]-3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты [пример 24(ф)] 3-метоксибензоилхлоридом получили трет-бутиловый эфир (3RS,4RS)-4-{4-[3-(3-метоксибензоилокси) пропил] фенил} -3-(нафталин-2-илметокси)пиперидин-1 -карбоновой кислоты в виде бесцветного аморфного твердого вещества; МС: 610 (М + Н)+.
(вв) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-(4- тритилоксиметилфенил)пиперидин-1-карбоновой кислоты [пример 22(3)] 2-хлорметил-1-(2-триметилсиланилэтоксиметокси)нафталином [пример 6(в)] получили трет-бутиловый эфир (3RS,4RS)-3-[1-(2- триметилсиланилэтоксиметокси)нафталин-2-илметокси] -4-(4- тритилоксиметилфенил)пиперидин-1-карбоновой кислоты. Селективным отщеплением тритильной группы аналогично примеру 86(х)(β) получили трет-бутиловый эфир (3RS, 4RS)-4-(4-гидроксиметилфенил)-3-[1- (2-триметилсиланилэтоксиметокси)нафталин-2-илметокси] пиперидин-1-карбоновой кислоты, в результате ацилирования которого 3-метоксибензоилхлоридом аналогично примеру 22 (л) был получен трет-бутиловый эфир (3RS,4RS)-4-[4-(3- метоксибензоилоксиметил)фенил]-3-[1-(2-триметилсиланилэтоксиметокси) нафталин-2-илметокси]пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 745 (М+NH4)+.
(гг) Аналогично примеру 44(д) путем алкилирования трет-бутилового эфира (3RS, 4RS)-4-(4-гидроксифенил)-3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты [пример 61(в)] этиловым эфиром бромуксусной кислоты получили трет-бутиловый эфир (3RS, 4RS)-4-(4- этоксикарбонилметоксифенил)-3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты в виде бесцветного твердого вещества; МС: 520 (М+Н)+.
(дд) Омылением трет-бутилового эфира (3RS,4RS)-4-(4- этоксикарбонилметоксифенил)-3-(нафталин-2-илметокси)пиперидин- 1-карбоновой кислоты [пример 86(гг)] с помощью 1 н. едкого натра в метаноле получили трет-бутиловый эфир (3RS, 4RS)-4-(4- карбоксиметоксифенил)-3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты, из которого реакцией конденсации с бензиламином в присутствии ГБТУ аналогично примеру 36(б) был получен трет-бутиловый эфир (3RS, 4RS)-4-[4-(бензилкарбамоилметокси) фенил]-3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде желтоватого твердого вещества; МС: 598 (М+NH4)+.
(ее) Аналогично примеру 24(н) взаимодействием трет-бутилового эфира (3RS, 5RS)-4-(4-гидроксифенил)-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты с 2-пиридилизоцианатом получили трет-бутиловый эфир (3RS, 4RS)-3-(нафталин-2-илметокси)-4-[4-(пиридин-2- илкарбамоилокси)фенил] пиперидин-1-карбоновой кислоты в виде белого твердого вещества; МС: 554 (М+Н)+.
(жж) Аналогично примеру 68(б) путем окисления по Сверну (Swern) из смеси трет-бутилового эфира (3RS,4RS)- и (3SR,4SR)-4-[4-[(RS)-2-гидрокси-3- феноксипропокси] фенил] -3-(нафталин-2-илметокси)пиперидин -1-карбоновой кислоты получили трет-бутиловый эфир (3RS,4RS)-3- (нафталин-2-илметокси)-4-[4-(2-оксо-3-феноксипропокси)фенил] пиперидин-1-карбоновой кислоты в виде белого твердого вещества; МС: 582 (М+Н)+.
(зз) (α) К раствору из 0,270 г (0,58 ммоля) трет-бутилового эфира (3RS, 4RS)-4-[4-(2-гидроксиэтил)фенил] -3-нафталин-2- илметоксипиперидин-1-карбоновой кислоты [пример 29(з)] в 10 мл метиленхлорида в атмосфере аргона при перемешивании и при комнатной температуре добавляли раствор из 5 мг (0,04 ммоля) бромида калия и 20 мг (0,24 ммоля) гидрокарбоната натрия в 10 мл воды. Реакционную смесь охлаждали до 0oC и смешивали с 2 мг (0,01 ммоля) 2,2,6,6-тетраметил-1-пиперидинилоксилом (ТЕМПО). Далее при непрерывном перемешивании в реакционную смесь добавляли впрыскиванием 1 мл (0,658 ммоля) жавельевой воды (раствор гипохлорита натрия). По окончании добавления реакционную смесь перемешивали при 0oC в течение примерно 30 мин. Для дальнейшей переработки добавляли 20 мл смеси 1:1 метиленхлорида и воды и реакционную смесь промывали 10 мл насыщенного раствора хлорида натрия, после чего водную фазу экстрагировали 10 мл метиленхлорида. Объединенные органические фазы сушили над сульфатом натрия и упаривали при пониженном давлении. Сырой продукт очищали экспресс-хроматографией на силикагеле с использованием смеси 2:1 гексана и уксусного эфира в качестве элюента. Таким путем получили 200 мг (75% от теории) трет-бутилового эфира (3RS, 4RS)-3-(нaфтaлин-2-илметoкcи)-4-[4-(2- оксоэтил)фенил]пиперидин-1-карбоновой кислоты в виде пены; МС: 460 (М+Н)+.
(β) Аналогично примеру 40(а) по реакции Гриньяра из трет-бутилового эфира (3RS, 4RS)-3-(нафталин-2-илметокси)-4-[4-(2- оксоэтил)фенил] пиперидин-1-карбоновой кислоты взаимодействием с фенилмагнийхлоридом получили смесь трет-бутилового эфира (3RS, 4RS)-4-[4-[(RS)- и -[(RS)-2-гидрокси-2-фенилэтил] фенил]-3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла.
(ии) Аналогично примеру 9 (а)-(в) путем алкилирования трет-бутилового эфира (3RS, 4RS)-4-(4-фторфенил)-3- гидроксипиперидин-1-карбоновой кислоты [пример 3(б)] 2-бромметилбензонитрилом получили трет-бутиловый эфир (3RS, 4RS)-3- (2-циaнбензилoкcи)-4-(4-фтopфенил)пипеpидин-1-карбоновой кислоты, в результате восстановления которого боран-дисульфидным комплексом был получен трет-бутиловый эфир (3RS, 4RS)-3-(2- аминометилбензилокси)-4-(4-фторфенил)пиперидин-1-карбоновой кислоты. Последующим ацилированием пиридин-2-карбоновой кислотой в присутствии ЭДК получили трет-бутиловый эфир (3RS, 4RS)-4-(4- фторфенил)-3-(2-{[(пиридин-2-карбонил)амино]метил}бензилокси)пиперидин -1-карбоновой кислоты в виде белого твердого вещества.
(кк) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS, 4RS)-4-(4-фторфенил)-3-гидроксипиперидин-1- карбоновой кислоты [пример 3(б)] (3-бромметилфенил)фенилметаноном [J. Med. Chem. 1984, 27(12), 1682-1690] получили трет-бутиловый эфир (3RS,4RS)-3-(3-бензоилбензилокси)-4-(4-фторфенил)пиперидин-1- карбоновой кислоты в виде желтоватой жидкости; МС: 490 (М+Н)+.
(лл) (α) Раствор из 470 мг (1,0 ммоль) трет-бутилового эфира (3RS, 4RS)-4-[4-(2-цианэтил)фенил] -3-нафталин-2-илметоксипиперидин- 1-карбоновой кислоты [пример 35(б)] и 348 мг (5,0 ммолей) гидрохлорида гидроксиламина в 6 мл 1М раствора метилата натрия в метаноле перемешивали в течение 5 ч при 65oC. Для дальнейшей переработки смесь распределяли между 40 мл уксусного эфира и 40 мл воды, после чего отделяли органическую фазу. Водную фазу дважды экстрагировали уксусным эфиром порциями по 40 мл. Объединенные органические фазы сушили над сульфатом магния и в завершение растворитель отгоняли при пониженном давлении. Сырой продукт (550 мг) очищали хроматографией на силикагеле с использованием смеси 20:1:0,1 метиленхлорида, метанола и 25%-ного раствора аммиака в качестве элюента. Таким путем получили 501 мг (99% от теории) трет-бутилового эфира (3RS,4RS)-4-{4-[2-(N- гидроксикарбамидоил)этил] фенил} -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты в виде желтого масла, которое использовали непосредственно на следующей стадии.
(β) Аналогично примеру 38 из трет-бутилового эфира (3RS,4RS)-4-{4-[2-(N-гидроксикарбамидоил)этил] фенил} -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты реакцией конденсации с бензойной кислотой в присутствии ЭДК с последующей циклизацией получили трет-бутиловый эфир (3RS, 4RS)-3-(нафталин-2-илметокси)-4- [4-[2-(5-фенил-[1,2,4] оксадиазол-3-ил)этил]фенил] пиперидин-1- карбоновой кислоты; МС: 590 (М+Н)+.
(мм) Щелочным омылением трет-бутилового эфира (3RS,4RS)-4-[4-(2-этоксикарбонилэтил)фенил] -3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты [пример 24(у)] с помощью водного едкого натра в тетрагидрофуране получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(2-карбоксиэтил)фенил] -3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты, из которого реакцией конденсации с N-гидроксибензамидином в присутствии ЭДК аналогично примеру 38 был получен соответствующий N-гидроксибензамидиновый эфир, из которого в результате циклизации получили трет-бутиловый эфир (3RS, 4RS)-3-(нафталин-2-илметокси)-4- [4-[2-(3-фенил-[1,2,4] оксадиазол-5-ил)этил] фенил] пиперидин-1- карбоновой кислоты в виде желтоватого аморфного твердого вещества; МС: 590 (М+Н)+.
(нн) Омылением трет-бутилового эфира (3RS,4RS)- 4-(4-этоксикарбонилметоксифенил)-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты [пример 86(гг)] с помощью 1 н. едкого натра в метаноле получили трет-бутиловый эфир (3RS, 4RS) -4-(4-карбоксиметоксифенил)-3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты, из которого реакцией конденсации с N-гидроксибензамидином в присутствии ГБТУ аналогично примеру 38 был получен соответствующий N-гидроксибензамидиновый эфир, из которого в результате циклизации получили трет-бутиловый эфир (3RS, 4RS)- 3-(нафталин-2-илметокси)-4-[4-(3-фенил-[1,2,4] оксадиазол-5-илметокси) фенил]пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 592 (М+Н)+.
(оо) Аналогично примеру 38 из трет-бутилового эфира (3RS,4RS)-4-(4-карбоксиметоксифенил)-3- (нафталин-2-илметокси)пиперидин-1-карбоновои кислоты [пример 86(нн)] реакцией конденсации с 3-пиридинамидоксимом в присутствии ГБТУ и последующей циклизацией получили трет-бутиловый эфир (3RS,4RS)-3-(нафталин-2-илметокси)-4-[4-(3-пиридин-3-ил[1,2,4] оксадиазол-5-илметокси)фенил] пиперидин-1-карбоновой кислоты в виде желтоватого твердого вещества; МС: 593 (М+Н)+.
(пп) Аналогично примеру 44(д) путем алкилирования трет-бутилового эфира (3RS, 4RS)-4-(4-гидроксифенил)-3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты [пример 61(в)] мезилатом 5-гидроксиметил-3-фенил-4,5-дигидроизоксазола, который был получен общеизвестным способом, получили трет-бутиловый эфир (3RS, 4RS)-3-(нaфтaлин-2-илмeтoкcи)-4-[4-(3-фенилизоксазол-5- илметокси)фенил] пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 591 (М+Н)+.
Указанные ниже ВОС-производные получали аналогично примеру 1(ж) из трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил]-3-гидроксипиперидин- 1-карбоновой кислоты [пример 86(о)] путем его алкилирования следующим путем:
(рр) алкилированием 3-метоксибензилхлоридом получили трет-бутиловый эфир (3RS, 4RS)-4-[4- (3-бензилоксипропокси)фенил]-3-(3-метоксибензилокси)пиперидин- 1-карбоновой кислоты в виде бесцветного масла; МС: 579 (M+NH4)+;
(cc) алкилированием 1-хлорметил-3-(2-триметилсиланилэтоксиметокси) бензолом получили трет-бутиловый эфир (3RS,4RS)-4-[4-(3- бензилоксипропокси)фенил]-3-[3-(2-триметилсиланилэтоксиметокси)бензилокси] пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 695 (M+H)+
[использованный в качестве алкилирующего агента 1-хлорметил-3-(2-триметилсиланилэтоксиметокси)бензол был получен аналогично примеру 5(а)-(г), при этом путем введения СЭМ-группы из метилового эфира 3-гидроксибензойной кислоты получили метиловый эфир 3-(2-триметилсиланилэтоксиметокси)бензойной кислоты. В результате последующего восстановления алюмогидридом лития получили [3-(2- триметилсиланилэтоксиметокси)фенил] метанол, из которого хлорированием получили 1-хлорметил-3-(2- триметилсиланилэтоксиметокси) бензол в виде бесцветного масла; МС: 272 (М)+];
(тт) алкилированием 3-хлор-4-метоксибензилхлоридом получили трет-бутиловый эфир (3RS,4RS)-4-[4-(3- бензилоксипропокси)фенил]-3-(3-хлор-4- метоксибензилокси)пиперидин-1-карбоновой кислоты, который без дальнейшей очистки и определения характеристик использовали на следующей стадии;
(уу) алкилированием 3,4-дихлорбензилхлоридом получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(3- бензилоксипропокси)фенил] -3-(3, 4-дихлорбензилокси)пиперидин-1- карбоновой кислоты, который без дальнейшей очистки и определения характеристик использовали на следующей стадии;
(фф) алкилированием 2, 5-дихлорбензилхлоридом получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(2,5- дихлорбензилокси)пиперидин-1-карбоновой кислоты, который без дальнейшей очистки и определения характеристик использовали на следующей стадии;
(хх) алкилированием бензилхлоридом получили трет-бутиловый эфир (3RS, 4RS)-3-бензилокси-4-[4-(3- бензилоксипропокси)фенил] пиперидин-1-карбоновой кислоты, который без дальнейшей очистки и определения характеристик использовали на следующей стадии;
(цц) алкилированием 2,5-диметилбензилхлоридом получили трет-бутиловый эфир (3RS,4RS)-4- [4-(3- бензилоксипропокси)фенил]-3-(2,5-диметилбензилокси) пиперидин-1- карбоновой кислоты, который без дальнейшей очистки и определения характеристик использовали на следующей стадии;
(чч) алкилированием 4-этилбензилхлоридом получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(4-этилбензилокси) пиперидин-1-карбоновой кислоты, который без дальнейшей очистки и определения характеристик использовали на следующей стадии;
(шш) алкилированием смесью 3- и 4-винилбензилхлорида получили трет-бутиловый эфир (3RS,4RS)-4-[4-(3- бензилоксипропокси)фенил]-3-(3- и 4-винилбензилокси)пиперидин-1- карбоновой кислоты, который без дальнейшей очистки и определения характеристик использовали на следующей стадии;
(щщ) алкилированием 6-хлорметил-2,3-дигидробензо[1,4]диоксином получили трет-бутиловый эфир (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(2,3-дигидробензо[1,4] диоксин-6-илметокси) пиперидин-1- карбоновой кислоты в виде бесцветной смолы; МС: 607 (М+NH4)+;
(ээ) алкилированием 6-хлорметил-1,2,3,4-тетрагидронафталином получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(3-бензилоксипропокси) фенил] -3-(5,6,7,8-тетрагидронафталин-2-илметокси) пиперидин-1- карбоновой кислоты в виде бесцветной смолы; МС: 603 (М+NH4 )+;
(ааа) алкилированием 3-хлорметил-1-(2-триметилсиланилэтоксиметокси) нафталином [пример 5(в)] получили трет-бутиловый эфир (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-[4-(2- триметилсиланилэтоксиметокси)нафталин-2-илметокси]пиперидин-1- карбоновой кислоты в виде бесцветной смолы; МС: 745 (M+NH4)+.
(ббб) Аналогично примеру 44(д) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-(4-гидроксифенил) пиперидин-1-карбоновой кислоты [пример 46(б)] 2-(4-хлорбутокси)тетрагидро-2Н- пираном получили смесь трет-бутилового эфира (3RS,4RS)- и (3SR,4SR)-3-гидрокси-4-[4-[4-[(RS)-тетрагидропиран-2-илокси] бутокси]фенил]пиперидин-1-карбоновой кислоты, алкилированием которой 2-бромметилнафталином аналогично примеру 1(ж) получили смесь трет-бутилового эфира (3RS,4RS)- и (3SR,4SR)-3-(нафталин-2- илметокси)-4-[4-[4-[(RS)-тетрагидропиран-2-илокси] бутокси] фенил]пиперидин-1-карбоновой кислоты. В результате отщепления ТГП-группы с помощью хлористого водорода в метаноле аналогично примеру 53(в) был получен трет-бутиловый эфир (3RS, 4RS)-4-[4- (4-гидроксибутокси)фенил]-3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты, алкилированием которого бензилбромидом аналогично примеру 1(ж) получили трет-бутиловый эфир (3RS, 4RS)-4- [4-(4-бензилоксибутокси)фенил]-3-
(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 613 (M+NH4)+.
(ввв) Аналогично примеру 22(г) из трет-бутилового эфира (3RS,4RS,5RS)-4-(4-бромфенил)-5- метоксиметил-3-нафталин-2-илметоксипиперидин-1-карбоновой кислоты [пример 68(м)] путем катализируемого палладием карбонилирования с помощью моноксида углерода в метаноле получили трет-бутиловый эфир (3RS,4RS, 5RS)-4-(4-метоксикарбонилфенил)-3-метоксиметил-5- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты, в результате восстановления которого борoгидридом лития аналогично примеру 22(д) был получен трет-бутиловый эфир (3SR, 4RS, 5RS)-4-(4- гидроксиметилфенил)-3-метоксиметил-5-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты. Последующим алкилированием 2-хлорбензоил-хлоридом аналогично примеру 22(л) получили трет-бутиловый эфир (3SR, 4RS, 5RS)-4-[4-(2-хлорбензоилоксиметил)фенил] -3-метоксиметил-5-(нафталин-2-илметокси)пиперазин-1-карбоновой кислоты в виде бесцветной пены; МС: 630 (М+Н)+.
(ггг) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3SR, 4RS, 5RS)-4-(4-гидроксиметилфенил)-3-метоксиметил-5- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты бензилбромидом получили трет-бутиловый эфир (3SR,4RS,5RS)-4-(4- бензилоксиметилфенил)-3-метоксиметил-5-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 582 (М+Н)+.
(ддд) Аналогично примеру 12(в)-(г) осуществляли отщепление N-метильной группы (1RS, 2RS, 3RS, 5SR)-3-(4-бpoмфeнил)-8- метил-8-азабицикло[3,2,1]октан-2-ола, который был получен аналогично 4-хлорфенильному производному [J. Org. Chem. 35, 802 (1970)], при этом сначала взаимодействием с 2,2,2-трихлорэтиловым эфиром хлормуравьиной кислоты был синтезирован 2,2, 2- трихлорэтиловый эфир (1RS,2RS,3RS,5SR)-3-(4-бромфенил)-2-(2,2,2- трихлорэтоксикарбонилокси)-8-азабицикло[3,2,1] октан-8- карбоновой кислоты, а затем взаимодействием с цинком в ледяной уксусной кислоте был получен (1RS,2RS,3RS, 5SR)-3-(4-бpoмфeнил)-8- азабицикло[3,2,1] октан-2-ол. Последующим введением ВОС-группы аналогично примеру 1(е) получили трет-бутиловый эфир (1RS,2RS, 3RS, 5SR)-3-(4-бромфенил)-2-гидрокси-8- азабицикло[3,2,1]октан-8-карбоновой кислоты, из которого путем катализируемого палладием карбонилирования с помощью моноксида углерода в метаноле аналогично примеру 22(г) получили трет-бутиловый эфир (1RS,2RS,3RS,5SR)-2-гидрокси-3-(4-метоксикарбонил-фенил)-8- азабицикло[3,2,1]октан-8-карбоновой кислоты. В результате последующего восстановления борoгидридом лития аналогично примеру 22(д) 8-азабицикло[3,2,1] октан-8-карбоновой кислоты, из которого взаимодействием с тритилхлоридом аналогично примеру 22(з) получили трет-бутиловый эфир (1RS,2RS,3RS, 5SR)-2-гидрокси-3-(4- тритилоксиметилфенил)-8-азабицикло[3,2,1] октан-8-карбоновой кислоты. Путем последующего взаимодействия с 2-бромметилнафталином аналогично примеру 1(ж) получили трет-бутиловый эфир (1RS,2RS,3RS, 5RS)-2-(нафталин-2-илметокси)-3-(4-тритилоксиметилфенил)- 8-азабицикло [3,2,1] октан-8-карбоновой кислоты. Аналогично примеру 86(х) (β) отщеплением тритильной группы с помощью смеси трифторуксусной кислоты и ангидрида трифторуксусной кислоты получили трет-бутиловый эфир (1RS,2RS,3RS,5SR)-3-(4- гидроксиметилфенил)-2-(нафталин-2-илметокси)-8-азабицикло [3,2,1] октан-8-карбоновой кислоты, из которого алкилированием бензил-3-бромпропиловым эфиром аналогично примеру 44(д) получили трет-бутиловый эфир (1RS,2RS,3RS, 5SR)-3-[4-(2-бензилоксипропоксиметил) фенил] -2-(нафталин-2-илметокси)-8-азабицикло [3,2,1] октан-8-карбоновой кислоты в виде бесцветного масла.
Пример 87.
Аналогично примеру 73(г) путем отщепления BOC-группы с помощью безводного бромида цинка получали следующие соединения:
1) из трет-бутилового эфира (3RS,4RS)-3-(нафталин-2-карбонилокси)-4- [4-(2-феноксиэтокси)фенил] пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-[4-(2-феноксиэтокси)фенил] пиперидин-3-иловый эфир нафталин-2-карбоновой кислоты в виде бесцветного твердого вещества; МС: 468 (М+Н)+;
2) из смеси трет-бутилового эфира (3RS,4RS)-4-(4- фторфенил)-3-[(RS)- и (SR) -2-гидрокси-1-нафталин-2-илэтокси] пиперидин-1-карбоновой кислоты получили смесь (RS)- и (SR)-2- [(3RS, 4RS)-4-(4-фторфенил)пиперидин-3-илокси] -2-нафталин-2- илэтанола в виде бесцветного аморфного твердого вещества; МС: 366 (М+Н)+.
Использованные в качестве, исходных субстанций BOC-производные получали следующим образом:
(а) К раствору из 5,50 г (13,3 ммоля) трет-бутилового эфира (3RS,4RS)-3-гидрокси-4-[4-(2- феноксиэтокси)фенил] пиперидин-1-карбоновой кислоты (пример 47.6) в 50 мл метиленхорида добавляли 250 мг 4-диметиламинопиридина и 2,5 мл триэтиламина, а затем при охлаждении льдом добавляли 2,77 г (14,5 ммоля) 2-нафтоилхлорида в твердом виде. Далее реакционную смесь перемешивали в течение 20 ч при комнатной температуре, реакционный раствор распределяли между водой и метиленхлоридом, объединенные метиленхлоридные фазы сушили над сульфатом магния, концентрировали и полученный в результате остаток хроматографировали на силикагеле с использованием смеси метиленхлорид/простой эфир (95:5). Таким путем получили 7,3 г (97% от теории) трет-бутилового эфира (3RS, 4RS)-3-(нафталин-2- карбонилокси)-4-[4-(2-феноксиэтокси)фенил] пиперидин-1-карбоновой кислоты в виде бесцветного аморфного твердого вещества; МС: 568 (М + Н)+.
(б) 255 мг (0,57 ммоля) трет-бутилового эфира (3RS,4RS)-4- (4-фторфенил)-3-(1-нафталин-2-илвинилокси)пиперидин-1-карбоновой кислоты [пример 73(б)] в атмосфере аргона и условиях, исключающих наличие влаги, растворяли в 3 мл тетрагидрофурана, при 0oC смешивали последовательно с 50 мг триэтиламина и с 0,11 мл (около 1,1 ммоля) боран-диметилсульфидного комплекса и перемешивали в течение 30 мин при комнатной температуре. Далее снова при охлаждении льдом последовательно добавляли 1,5 мл 50%-ного раствора КОН в воде и 1,5 мл 30%-ного раствора перекиси водорода в воде и реакционную смесь нагревали с обратным холодильником в течение 1,5 ч. 3атем реакционный раствор распределяли между водой и метиленхлоридом, объединенные метиленхлоридные фазы сушили над сульфатом магния, концентрировали и полученный в результате остаток хроматографировали на силикагеле с использованием смеси гексан/уксусный эфир (1:1). Таким путем получили 30 мг (11% от теории) смеси трет-бутилового эфира (3RS,4RS)-4-(4-фторфенил)-3-[(RS)- и (RS)-2- гидрокси-1-нафталин-2-илэтокси] пиперидин-1-карбоновой кислоты в виде бесцветного аморфного твердого вещества; МС: 466 (М+Н)+.
Пример 88.
(а) 25,23 г (91 ммоль) трет-бутилового эфира 4-(4- фторфенил)-1,2,3,6-тетрагидропиридин-1-карбоновой кислоты [получен из 4-(4-фторфенил)-1,2,3,6-тетрагидропиридина и ди-трет- бутилдикарбоната аналогично примеру 1(е)] суспендировали в 200 мл 1,2-диметоксиэтана, к полученной суспензии при 20o C добавляли 5,1 г (135 ммолей) борогидрида натрия, а затем при 20oC по каплям в течение 45 мин при периодическом охлаждении добавляли раствор из 22,85 мл (182 ммоля) эфирата трифторида бора в 35 мл 1,2-диметоксиэтана. Далее смесь перемешивали при комнатной температуре в течение 2,5 ч, после чего при интенсивном перемешивании и при комнатной температуре в течение 1 ч по каплям добавляли раствор из 82 г (1,26 ммоля) гидроксида калия (86%-ный) в 430 мл дистиллированной воды. Далее при комнатной температуре в течение 30 мин по каплям добавляли 69,3 мл (0,68 ммоля) перекиси водорода (30%-ная), а затем перемешивали в течение 3 ч при нагревании с обратным холодильником. После охлаждения до комнатной температуры смесь сливали на ледяную воду, продукт трижды экстрагировали уксусным эфиром порциями по 200 мл, органические фазы дважды промывали дистиллированной водой порциями по 300 мл, затем сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. После сушки в течение 90 мин в высоком вакууме при комнатной температуре получили 24,4 г (91% от теории) трет-бутилового эфира (3RS, 4RS)-4-(4-фторфенил)-3- гидроксипиперидин-1-карбоновой кислоты в виде бесцветных кристаллов; МС: 296 (М+Н)+.
(б) 39,2 г (0,2 моля) 3-метилбензофенона и 38,4 г (0,24 моля) брома перемешивали в 1 л четырххлористого углерода при нагревании с обратным холодильником в течение 8 ч. После отгонки растворителя в вакууме, создаваемом водоструйным насосом, полученный в результате сырой продукт хроматографировали на 500 г силикагеля с использованием гексана и метиленхлорида. Очищенный таким образом продукт перекристаллизовывали из н-гексана. Таким путем получили 21, 76 г (40% от теории) (3-бромметилфенил)фенилметанона в виде бесцветных кристаллов; МС: 274, 276 (М+Н)+.
(в) 0,29 г (1 ммоль) трет-бутилового эфира (3RS, 4RS)-4-(4-фторфенил)-3-гидроксипиперидин-1- карбоновой кислоты и 0,30 г (1,1 ммоля) (3-бромметилфенил)фенилметанона растворяли в атмосфере аргона при комнатной температуре в 10 мл диметилформамида, затем с добавлением 0,25 г (1,5 ммоля) иодида калия смешивали с 0,056 г (1,3 ммоля) дисперсии гидрида натрия (55%-ная в минеральном масле) и перемешивали в течение 18 ч при комнатной температуре. Реакционную смесь сливали на ледяную воду, продукт трижды экстрагировали метиленхлоридом, органические фазы дважды промывали дистиллированной водой, затем сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием метиленхлорида и метанола. Таким путем получили 0, 42 г (86% от теории) трет-бутилового эфира (3RS, 4RS)-3-(3-бензоилбензилокси)-4-(4-фторфенил)пиперидин-1- карбоновой кислоты в виде бесцветного масла; МС: 490 (М+Н)+.
(г) Аналогично примеру 22(м) из трет-бутилового эфира (3RS,4RS)-3-(3-бензоилбензилокси)-4-(4-фторфенил)пиперидин-1-карбоновой кислоты путем отщепления ВОС-группы с помощью хлористого водорода в метаноле получили гидрохлорид 1-[3-[(3RS,4RS)-4-(4- фторфенил)пиперидин-3-илоксиметил]фенил]фенилметанона (1:1) в виде бесцветных кристаллов; МС: 390 (М+Н)+.
Пример 89.
Аналогично примеру 73(г) путем отщепления BOC-группы с помощью безводного бромида цинка получали следующие соединения:
1) из трет-бутилового эфира (E)-(3RS, 4RS)-4-(4-фторфенил)-3-(3-фенилаллилокси)пиперидин- 1-карбоновой кислоты получили (E)-(3RS,4RS)-4-(4-фторфенил)-3-(3- фенилаллилокси)пиперидин в виде светло-желтого масла; МС: 312 (М+Н)+;
2) из трет-бутилового эфира (3R, 4s, 5S)-4-[4-(3- бензилоксипропокси)фенил] -3,5-бис-(4,5-диметоксипиримидин-2 -илоксиметил)пиперидин-1-карбоновой кислоты получили 2-{(3R,4s, 5S)-4-[4-(3-бензилоксипропокси)фенил]-5-(4,5- диметоксипиримидин-2-оксиметил)пиперидин-3-илметокси}-4,5- диметоксипиримидин в виде светло-желтой смолы; МС: 662 (М+Н)+;
3) из трет-бутилового эфира (3R,4s,5S)-4-[4-(3-бензилоксипропокси) фенил] -3,5-бис-(4-метоксифеноксиметил)пиперидин-1-карбоновой кислоты получили (3R, 4s, 5S)-4-[4-(3-бензилоксипропокси)фенил] - 3, 5-бис(4-метоксифеноксиметил)пиперидин в виде светло-желтого масла; МС: 598 (М+Н)+;
4) из трет-бутилового эфира (3R,4s,5S)-4-[4-(3-бензилоксипропокси)фенил] - 3, 5-бис-п-толилсульфанилметилпиперидин-1-карбоновой кислоты получили (3R, 4s, 5S)-4-[4-(3-бензилоксипропокси)фенил] -3,5-бис- п-толилсульфанилметилпиперидин в виде светло-желтого масла; МС: 598 (М+Н)+;
5) из трет-бутилового эфира (3RS, 4RS)-4-[4-[3-(2- метоксибензилокси)пропокси] фенил] -3-{7-[2-(4-метилпиперазин-1- ил)этокси]нафталин-2-илметокси]пиперидин-1-карбоновой кислоты получили 1-[2-[7-[(3RS,4RS)-4-[4-[3-(2- метоксибензилокси)пропокси] пиперидин-3-илоксиметил]нафталин-2- илокси]этил] -4-метилпипеpaзин в виде аморфного бесцветного вещества; МС: 654 (М+Н)+.
Использованные в качестве исходных субстанций BOC-производные получали следующим образом.
(а) 1,48 г (5 ммолей) трет-бутилового эфира (3RS,4RS)-4-(4-фторфенил)-3- гидроксипиперидин-1-карбоновой кислоты [пример 88(а)] и 1,08 г (5, 5 ммоля) 3-бром-1-фенилпропена растворяли в атмосфере аргона при комнатной температуре в 10 мл диметилформамида, затем с добавлением 1,25 г (7,5 ммоля) иодида калия смешивали с 0,284 г (6,5 ммоля) дисперсии гидрида натрия (55%-ная в минеральном масле) и перемешивали в течение 18 ч при комнатной температуре. Реакционную смесь сливали на ледяную воду, продукт трижды экстрагировали метиленхлоридом, органические фазы дважды промывали дистиллированной водой, сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием метиленхлорида и метанола. Таким путем получили 1,01 г (49% от теории) трет-бутилового эфира (Е)-(3RS, 4RS)-4-(4-фторфенил)-3-(3- фенилаллилокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 412 (М+Н)+.
(б) 0,49 г (1 ммоль) трет-бутилового эфира (3R,4s, 5S)-4-[4-(3-бензилоксипропокси) фенил] -3,5-бисгидроксиметилпиперидин-1-карбоновой кислоты [пример 101 (е)] и 0,45 г (2 ммоля) 4,5-диметокси-2-метилсульфанилпиримидина [полученного путем окисления м-хлорпербензойной кислотой аналогично примеру 129(в)] загружали в атмосфере аргона при 5oC в 5 мл диметилформамида, при перемешивании смешивали с 0,10 г (2,2 ммоля) дисперсии гидрида натрия (55%-ная в минеральном масле) и перемешивали в течение 2 ч при комнатной температуре. После этого реакционную смесь сливали на ледяную воду, продукт трижды экстрагировали метиленхлоридом, органические фазы дважды промывали дистиллированной водой, сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием метиленхлорида и метанола. Таким путем получили 0,47 г (61% от теории) трет-бутилового эфира (3R,4s,5S)- 4-[4-(3-бензилоксипропокси)фенил]-3,5-бис-(4, 5- диметоксипиримидин-2-илоксиметил)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 762 (М+Н)+.
(в) (α) 2,91 г (6 ммолей) трет-бутилового эфира (3R,4s, 5S)-4-[4-(3-бензилоксипропокси) фенил]-3,5-бис-гидроксиметилпиперидин-1-карбоновой кислоты [пример 101(е)] и 1,93 мл (24 ммоля) пиридина загружали в атмосфере аргона при 5oC в 30 мл ацетонитрила, при перемешивании порциями добавляли 8,00 г (18 ммолей) трифенилфосфиндибромида и затем перемешивали при комнатной температуре. По истечении 90 мин реакционную смесь сливали на ледяную воду, продукт трижды экстрагировали уксусным эфиром, органические фазы дважды промывали дистиллированной водой, сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием н-гексана и уксусного эфира. Таким путем получили 2,81 г (77% от теории) трет-бутилового эфира (3R, 4s,5S)-4-[4-(3-бензилоксипропокси)фенил]- 3,5-бис-бромметилпиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 610 (М+Н)+.
(в) (β) 0,30 г (0,5 ммоля) трет-бутилового эфира (3R,4s,5S)-4-[4-(3-бензилоксипропокси)фенил] - 3,5-бисбромметилпиперидин-1-карбоновой кислоты и 0,19 г (1,5 ммоля) монометилового эфира гидрохинона с добавлением 0,69 г (5 ммолей) безводного карбоната калия перемешивали в течение 18 ч в атмосфере аргона при нагревании с обратным холодильником в 15 мл ацетонитрила. После охлаждения до комнатной температуры реакционную смесь сливали на ледяную воду, продукт трижды экстрагировали метиленхлоридом, органические фазы дважды промывали дистиллированной водой, затем сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием метиленхлорида и метанола. Таким путем получили 0, 15 г (43% от теории) трет-бутилового эфира (3R, 4s, 5S)-4-[4-(3-бензилоксипропокси)фенил] -3,5-бис(4- метоксифеноксиметил)пиперидин-1-карбоновой кислоты в виде светло-желтых кристаллов; МС: 698 (М+Н)+.
(г) Аналогично примеру 89(в)(β) из трет-бутилового эфира (3R,4s,5S)-4-[4-(3-бензилоксипропокси)фенил] -3,5-бис бромметилпиперидин-1-карбоновой кислоты и 4-метилтиофенола получили трет-бутиловый эфир (3R,4s,5S)-4-[4-(3- бензилоксипропокси)фенил] -3,5-бис-п-толилсульфанил метилпиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 698 (М+Н)+.
(д) Аналогично примеру 95(а) из трет-бутилового эфира (3RS,4RS)-3-гидрокси-4-[4-[3-(2-метоксибензилокси)пропокси] фенил] пиперидин-1-карбоновой кислоты [пример 120(ж) (α)] и 2-хлорметил-7-(2- триметилсиланилэтоксиметокси)нафталина [пример 6(х)] получили трет-бутиловый эфир (3RS,4RS)-4-[4-[3-(2- метоксибензилокси)пропокси] фенил]-3-[7-(2- триметилсиланилэтоксиметокси)нафталин-2-илметокси] пиперидин-1- карбоновой кислоты в виде светло-желтого масла; МС: 758 (М+Н)+. Далее трет-бутиловый эфир (3RS, 4RS)-4-[4-[3-(2- метоксибензилокси)пропокси] фенил]-3-[7-(2- триметилсиланилэтоксиметокси)нафталин-2-илметокси]пиперидин-1- карбоновой кислоты аналогично примеру 95(б) путем отщепления СЭМ-защитной группы превращали в трет-бутиловый эфир (3RS,4RS)-4-[4-[3-(2-метоксибензилокси)пропокси]фенил]-3- (7-гидроксинафталин-2- илметокси)пиперидин-1-карбоновой кислоты [желтое масло; МС: 628 (М+Н)+], из которого путем алкилирования гидрохлоридом 1-(2- хлорэтил)-4-метилпиперазина [Chim. Ther. 4, 283, (1969)] аналогично примеру 90(о) получили трет-бутиловый эфир (3RS, 4RS)-4-[4-[3-(2-метоксибензилокси)пропокси]фенил] -3-[7-[2-(4- метилпиперазин-1-ил)этокси] нафталин-2-илметокси] пиперидин-1- карбоновой кислоты в виде светло-коричневого масла; МС: 754 (М+Н)+.
Пример 90.
Аналогично примеру 22(м) путем отщепления BOC-группы с помощью хлористого водорода в метаноле получали следующие соединения:
1) из смеси трет-бутилового эфира (3RS,4SR)-4-(4-фтopфенил)-3-[(RS)- и -[(SR)-1-[4-(2-морфолин-4-илэтокси)бензоилокси] -2-нафталин-2-илэтил]пиперидин-1-карбоновой кислоты получили смесь трет-бутилового эфира (RS)- и (SR)-1-[(3RS, 4SR)-4-(4-фтopфенил)пипеpидин-3-ил] -2-нафталин-2-илэтилового эфира 4-(2-морфолин-4-илэтокси)бензойной кислоты в виде бесцветного масла; МС: 583 (М+Н)+;
2) из трет-бутилового эфира (3RS,4SR)-4-(4-фтopфенил)-3-(нaфтaлин-2-илацетил)пиперидин-1- карбоновой кислоты получили гидрохлорид 1-[(3RS, 4SR)-4-(4- фторфенил)пиперидин-3-ил] -2-нафталин-2-илэтанона (1:1) в виде бесцветных кристаллов; МС: 348 (М+Н)+;
3) из смеси трет-бутилового эфира (Е)- и (Z)-(3RS, 4SR)-3- (1-карбоксиметоксиимино-2-нафталин-2-илэтил)-4-(4-фторфенил)пиперидин-1- карбоновой кислоты получили смесь 3:1 метилового эфира (Е)- и (Z)- [1-[(3RS,4SR)-4-(4-фтopфенил)пипеpидин-3-ил] -2-нафталин-2-илэтилиденаминоокси] уксусной кислоты в виде желтого масла; МС: 435 (М+Н)+;
4) из трет-бутилового эфира (3RS,4RS)-3-[2-(3Н- бензоимидазол-5-илокси)этокси] -4-[4-(3-бензилоксипропокси)фенил]пиперидин- 1-карбоновой кислоты получили 6-[2-[(3RS,4RS)- 4-[4-(3-бензилоксипропокси)фенил]пиперидин-3-илокси]этокси]-1H- бензоимидазол в виде желтого масла; МС: 502 (М+Н)+;
5) из трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3- [2-(2-оксо-2,3-дигидро-1Н-бензоимидазол-5-илокси)этокси] пиперидин-1-карбоновой кислоты получили 5-[2-[(3RS, 4RS)-4-[4- (3-бензилоксипропокси)фенил] пиперидин-3-илокси] этокси] -1,3- дигидробензоимидазол-2-он в виде желтых кристаллов; МС: 518 (М+Н)+;
6) из трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-[2-(3,4-динитрофенокси)этокси] пиперидин-1- карбоновой кислоты [пример 94(г)] получили (3RS, 4RS)-4-[4-(3- бензилоксипропокси)фенил]-3-[2-(3,4-динитрофенокси)этокси] пиперидин в виде аморфной желтой пены; МС: 552 (М+Н)+;
7) из трет-бутилового эфира (3RS, 4RS)-4-[4-(3-бензилоксипропокси) фенил] -3-[7-(2-морфолин-4-илэтокси)нафталин-2- илметокси] пиперидин-1-карбоновой кислоты получили гидрохлорид 4-[2-[7-[(3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] пиперидин-3-илоксиметил] нафталин-2-илокси]этил]морфолина (1:2) в виде бежевых кристаллов; МС: 611 (М+Н)+;
8) из смеси трет-бутилового эфира (3RS,4RS)- и (3SR, 4SR)-4-[4-(3-бензилоксипропокси)фенил] -3- [7-[(RS)-2,2-диметил-[1,3]диоксолан-4-илметокси] нафталин-2- илметокси]пиперидин-1-карбоновой кислоты получили смесь (RS)- и (SR)-3-[7-[(3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] пиперидин- 3-илоксиметил] нафталин-2-илокси] пропан-1,2-диола в виде бесцветного масла; МС: 572 (М+Н)+;
9) из трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипокси)фенил] -3-[6-(2-триметилсиланилэтоксиметокси)нафталин-2-илметокси] пиперидин-1- карбоновой кислоты [пример 97(а)] получили гидрохлорид 6-[(3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] пиперидин-3- илоксиметил] нафталин-2-ола (1:1) в виде бесцветных кристаллов; МС: 498 (М+Н)+;
10) из смеси трет-бутилового эфира [3RS,4RS]- и [3SR,4SR]-4- [4-(3-бензилоксипропокси)фенил] -3-[6-[(RS)-2,2-диметил- [1,3] диоксолан-4-илметокси]нафталин-2-илметокси]пиперидин-1- карбоновой кислоты при одновременном отщеплении диоксолановой защитной группы получили смесь гидрохлорида (RS)- и (SR)-3-[6- [(3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил]пиперидин-3- илоксиметил] нафталин-2-илокси] пропан-1,2-диола (1: 1) в виде светло-коричневых кристаллов; МС: 572 (М+Н)+;
11) из смеси трет-бутилового эфира (3RS,4RS)- и (3SR,4SR)-4-[4-(3-бензилоксипропокси)фенил] -3-[6-[2-[(RS)-2,2-диметил- [1,3] диоксолан-4-илметокси] этокси]нафталин-2-илметокси] пиперидин-1-карбоновой кислоты при одновременном отщеплении диоксолановой защитной группы получили смесь гидрохлорида [RS] - и [SR]-3-[2-[6-[(3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] пиперидин-3-илоксиметил] нафталин-2-илокси] этокси] пропан-1,2- диола (1:1) в виде бесцветных кристаллов; МС: 616 (М+Н)+;
12) из смеси трет-бутилового эфира (3RS,4RS)-4-[4- (3-бензилоксипропокси)фенил] -3-[(RS)- и -[(SR)-1-гидрокси-2-нафталин-2- илэтил]пиперидин-1-карбоновой кислоты [пример 100(б)] получили смесь гидрохлорида (RS)- и (SR)-1-[(3RS, 4SR)-4-[4-(3- бензилoкcипpoпoкcи)фенил]пипеpидин-3-ил]-2-нафталин-2-илэтанола (1:1) в виде бежевых кристаллов; МС: 496 (М+Н)+;
13) из трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-[7-[2-(4-метилпиперазин-1-ил)этокси]нафталин-2-илметокси] пиперидин-1-карбоновой кислоты получили гидрохлорид 1-[2-[7-[(3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] пиперидин-3- илоксиметил]нафталин-2-илокси]этил]-4-метилпиперазина (1:3) в виде бесцветных кристаллов; МС: 624 (М+Н)+;
14) из смеси трет-бутилового эфира (Е)- и (Z)-(3RS,4SR)-4-[4-(3-бензилоксипропокси) фенил] -3-(1-метоксикарбонилметоксиимино-2-нафталин-2-илэтил)пиперидин- 1-карбоновой кислоты получили смесь метилового эфира (Е)- и (Z)-(1-[(3RS,4SR)-4-[4-(3-бензилоксипропокси)фенил] пиперидин-3-ил]-2-нафталин-2-илэтилиденаминоокси] уксусной кислоты в виде светло-желтого масла; МС: 581 (М+Н)+;
15) из трет-бутилового эфира (3R, 4s, 5S)-4-[4-(3-бензилоксипропокси)фенил]-3,5-бис(2- морфолин-4-илэтоксиметил)пиперидин-1-карбоновой кислоты [пример 101(ж)] получили (3R,4s, 5R)-4-[4-(3-бензилоксипропокси)фенил]-3,5- бис-(2-морфолин-4-илэтоксиметил)пиперидин в виде желтого масла; МС: 612 (М+Н)+.
Использованные в качестве исходных субстанций BOC-производные получали следующим образом.
(а) 0,45 г (1 ммоль) смеси трет-бутилового эфира (3RS,4SR)-4-(4-фторфенил)-3-[(RS)- и -[(SR)-1-гидрокси-2-нафталин-2-илэтил]пиперидин-1-карбоновой кислоты [пример 74(з)] и 0,28 г (1,1 ммоля) 4-(2-морфолин-4- илэтокси)бензойной кислоты (получена путем алкилирования метилового эфира 4-гидроксибензойной кислоты 4-(2- хлорэтил)морфолином в диметилформамиде в присутствии карбоната калия при 100oC с последующим основным омылением) растворяли в 15 мл метиленхлорида в атмосфере аргона, затем добавляли 0,23 г (1,2 ммоля) гидрохлорида N-этил-N'-(3-диметиламинопропил)карбодиимида и 0,04 г (0,33 ммоля) 4-диметиламинопиридина и перемешивали в течение 70 ч при комнатной температуре. После отгонки растворителя в вакууме, создаваемом водоструйным насосом, сырой продукт хроматографировали на силикагеле с использованием н-гексана, метиленхлорида и метанола. Таким путем получили 0,54 г (79% от теории) смеси трет-бутилового эфира (3RS,4SR)-4-(4-фторфенил)-3- [(RS)- и -[(SR)-1-[4-(2-морфолин-4-илэтокси)бензоилокси]-2- нафталин-2-илэтил]пиперидин-1-карбоновой кислоты в виде светло-желтого масла; МС: 683 (М+Н)+.
(б) Аналогично примеру 74(е) из смеси трет-бутилового эфира (3RS,4SR)-4-(4-фторфенил)-3-[(RS)- и - [(SR)-1-гидрокси-2-нафталин-2-илэтил]пиперидин-1-карбоновой кислоты [пример 74(з)] путем окисления диметилсульфоксидом/оксалилхлоридом в метиленхлориде получили трет-бутиловый эфир (3RS, 4SR)-4-(4-фторфенил)-3-(нафталин-2- илацетил)пиперидин-1-карбоновой кислоты в виде желтого масла; МС: 447 (М)+.
(в) 0,22 г (0,5 ммоля) трет-бутилового эфира (3RS, 4SR)-4-(4- фторфенил)-3-(нафталин-2-илаицетил)пиперидин-1-карбоновой кислоты и 0,11 г (1 ммоль) гидрохлорида аминооксиуксусной кислоты (1:0,5) [Organic Synthesis Collect. , т. III, 172 (1955)] перемешивали в течение 18 ч в атмосфере аргона при 60oC в 2 мл пиридина. 3атем реакционную смесь сливали на ледяную воду, продукт трижды экстрагировали уксусным эфиром, органические фазы дважды промывали дистиллированной водой, сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием метиленхлорида и метанола. Таким путем получили 0,24 г (92% от теории) смеси трет-бутилового эфира (Е)- и (Z)-(3RS, 4SR)-3-(1-карбоксиметоксиимино-2-нафталин-2- илэтил)-4-(4-фторфенил)пиперидин-1-карбоновой кислоты в виде светло-желтого масла; МС: 521 (М+Н)+.
(г) 0,55 г (0,93 ммоля) трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-[2-(3,4-диаминофенокси)этокси]пиперидин-1-карбоновой кислоты [пример 94(д)] перемешивали в течение 1 ч в атмосфере аргона при 50oC в 5 мл триэтилового эфира ортомуравьиной кислоты. Реакционную смесь сливали на ледяную воду, продукт трижды экстрагировали метиленхлоридом, органические фазы дважды промывали дистиллированной водой, сушили над карбонатом калия, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием метиленхлорида и метанола. Таким путем получили 0,38 г (68% от теории) смеси трет-бутилового эфира 3-[2- (3Н-бензоимидазол-5-илокси)этокси] -4-[(3RS, 4RS)-4-(3- бензилоксипропокси)фенил]пиперидин-1-карбоновой кислоты в виде светло-коричневого масла; МС: 602 (М+Н)+.
(д) 0,60 г (1,0 ммоль) трет-бутилового эфира (3RS, 4RS)-4-[4-(3-бензилоксипропокси) фенил] -3-[2-(3,4-диаминофенокси)этокси]пиперидин-1-карбоновой кислоты [пример 94(д)], перемешивая, растворяли в атмосфере аргона при комнатной температуре в 5 мл диметилформамида, а затем добавляли 0,18 г (1,1 ммоля) 1,1'-карбонилдиимидазола. По истечении 1 ч реакционную смесь сливали на ледяную воду, продукт трижды экстрагировали метиленхлоридом, органические фазы дважды промывали дистиллированной водой, затем сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием метиленхлорида и метанола. Таким путем получили 0,46 г (74% от теории) трет-бутилового эфира (3RS,4RS)-4- [4-(3-бензилоксипропокси)фенил] -3-[2-(оксо-2,3-дигидро-1Н- бензоимидазол-5-илокси)этокси] пиперидин-1-карбоновой кислоты в виде желтого масла; МС: 618 (М+Н)+.
(ж) 0,30 г (0,5 ммоля) трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3- (7-гидроксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты [пример 95(б)] и 0,13 г (0,7 ммоля) гидрохлорида 4-(2-хлорэтил)морфолина перемешивали в течение 18 ч в атмосфере аргона при 60oC в 15 мл диметилформамида с добавлением 0,69 г (5 ммолей) карбоната калия (безводного). Реакционную смесь сливали на ледяную воду, продукт трижды экстрагировали метиленхлоридом, органические фазы дважды промывали дистиллированной водой, затем сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием метиленхлорида и метанола. Таким путем получили 0,32г (90% от теории)трет-бутилового эфира (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил]-3- [7-(2-морфолин-4-илэтокси)нафталин-2- илметокси]пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 711 (М+Н)+.
(з) 0,33 г (0,54 ммоля) трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(7- гидроксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты [пример 95(б)] и 0,20 г (0,70 ммоля) γ- тозилата D,L- α,β- изопропилиденглицерина перемешивали в течение 3 ч в атмосфере аргона при нагревании с обратным холодильником в 15 мл диметилформамида с добавлением 0,69 г (5 ммолей) карбоната калия (безводного). После этого реакционную смесь сливали на ледяную воду, продукт трижды экстрагировали метиленхлоридом, органические фазы дважды промывали дистиллированной водой, затем сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием метиленхлорида и метанола. Таким путем получили 0,32 г (83% от теории) смеси трет-бутилового эфира (3RS,4RS)- и (3SR, 4SR)-4-[4- (3-бензилоксипропокси)фенил]-3-[7-[(RS)-2,2-диметил[1, 3]диоксолан-4- илметокси] нафталин-2-илметокси] пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 712 (М+Н)+.
(л) Аналогично примеру 90(з) из трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(6-гидроксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты [пример 97(б)] получили смесь трет-бутилового эфира [3RS, 4RS] - и [3SR, 4SR]-4- [4-(3-бензилоксипропокси)фенил]-3-[6-[(RS)-2,2-диметил-[1,3] диоксолан-4-илметокси] нафталин-2-илметокси]пиперидин-1- карбоновой кислоты в виде бесцветных кристаллов; МС: 712 (М+Н)+ .
(м) Аналогично примеру 90(ж) из трет-бутилового эфира (3RS,4RS)-4- [4-(3-бензилоксипропокси)фенил] -3-(6-гидроксинафталин-2- илметокси)пиперидин-1-карбоновой кислоты [пример 97(б)] и (RS)-2-(2,2-диметил-[1,3] диоксолан-4-илметокси)этилового эфира толуол-4-сульфокислоты [пример 98(а)] получили смесь трет-бутилового эфира (3RS,4RS)- и (3SR, 4SR)-4-[4-(3- бензилоксипропокси)фенил]-3-[6-[2-[(RS)-2,2-диметил[1,3]диоксолан-4-илметокси]этокси]нафталин-2-илметокси] пиперидин-1-карбоновой кислоты в виде бесцветных кристаллов; МС: 773 (М+Н)+.
(о) 0,30 г (0,5 ммоля) трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(7-гидроксинафталин- 2-илметокси)пиперидин-1-карбоновой кислоты [пример 95(б)] и 0,47 г (2 ммоля) гидрохлорида 1-(2-хлорэтил)-4-метилпиперазина (1: 2) [Chim. Ther. 4, 283, (1969)] растворяли в атмосфере аргона при комнатной температуре в 5 мл диметилформамида, а затем с добавлением 0,05 г (0,3 ммоля) иодида калия и 0,22 г (5 ммолей) дисперсии гидрида натрия (55%-ная в минеральном масле) перемешивали в течение 3 ч при 100oC. Реакционную смесь сливали на ледяную воду, продукт трижды экстрагировали метиленхлоридом, органические фазы дважды промывали дистиллированной водой, затем сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием метиленхлорида и метанола. Таким путем получили 0,20 г (55% от теории) трет-бутилового эфира (3RS, 4RS)-4- [4-(3- бензилоксипропокси)фенил]-3-[7-[2-(4-метилпиперазин-1-ил)этокси] нафталин-2-илметокси] пиперидин-1-карбоновой кислоты в виде светло-коричневого масла; МС: 724 (М+Н)+.
(п) Аналогично примеру 102(а) из трет-бутилового эфира (3RS,4RS)-4-[4-(3- бензилоксипропокси)фенил]-3-(нафталин-2-илацетил)пиперидин -1-карбоновой кислоты [пример 100(в)] и гидрохлорида метилового эфира аминооксиуксусной кислоты [J. Med. Chem. 28, 1447, (1985)] получили смесь трет-бутилового эфира (Е)- и (Z)-(3RS, 4SR)-4-[4-(3- бензилоксипропокси)фенил]-3-(1-метоксикарбонилметоксиимино-2- нафталин-2-илэтил)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 698 (M+NH4)+.
Пример 91.
(а) 0,90 г (2 ммоля) смеси трет-бутилового эфира (3RS,4SR)-4-(4-фторфенил)-3- [(RS)- и -[(SR)-1-гидрокси-2-нафталин-2-илэтил]пиперидин-1- карбоновой кислоты [пример 74(3)] и 0,55 г (2,2 ммоля) 4-(2-морфолин-4-илэтокси)бензойной кислоты (получена путем алкилирования метилового эфира 4-гидроксибензойной кислоты 4-(2-хлорэтил)морфолином в диметилформамиде в присутствии карбоната калия при 100oC с последующим основным омылением) растворяли в 30 мл тетрагидрофурана в атмосфере аргона, затем после добавления 0,66 г (2,5 ммоля) трифенилфосфина по каплям при 5oC добавляли 0,44 мл (2,8 ммоля) диэтилазодикарбоксилата, после чего перемешивали в течение 18 ч при комнатной температуре. После отгонки растворителя в вакууме, создаваемом водоструйным насосом, сырой продукт хроматографировали на силикагеле с использованием н-гексана и уксусного эфира. Таким путем получили 0,31 г (23% от теории) трет-бутилового эфира (Е)-(3RS, 4SR)-4-(4-фторфенил)-3-(2- нафталин-2-илвинил)пиперидин-1-карбоновой кислоты в виде светло-желтой смолы; МС: 432 (М+Н)+.
(б) Аналогично примеру 22(м) путем отщепления BOC-группы с помощью хлористого водорода в метаноле из трет-бутилового эфира (Е)-(3RS,4SR)-4-(4-фторфенил)-3-(2-нафталин- 2-илвинил) пиперидин-1-карбоновой кислоты получили (E) - (3RS, 4SR)-4-(4-фторфенил)-3-(2-нафталин-2- илвинил)пиперидин в виде светло-желтого масла; МС: 331 (М)+.
(в) 0,060 г (0,18 ммоля) (Е)-(3RS, 4SR)-4-(4-фторфенил)-3-(2-нафталин- 2-илвинил) пиперидина гидрировали при нормальных условиях в 3 мл метанола с добавлением 30 мг палладия на угле (10%-ного). После отфильтровывания катализатора растворитель отгоняли в вакууме, создаваемом водоструйным насосом. Таким путем получили 0,055 г (92% от теории) (3RS,4SR)-4-(4-фторфенил)-3-(2-нафталин-2- илэтил)пиперидина в виде светло-желтого масла; МС: 334 (М+Н)+.
Пример 92.
(а) 2,95 г (10 ммолей) трет-бутилового эфира (3RS,4RS)- 4-(4-фторфенил)-3-гидроксипиперидин-1-карбоновой кислоты [пример 88(а)] и 3,82 г (11 ммолей) трет-бутилового эфира 4'-бромметилбифенил-2-карбоновой кислоты [J. Med. Chem. 34, 2525, (1991)] растворяли в атмосфере аргона при комнатной температуре в 100 мл диметилформамида, после чего сначала добавляли 2,49 г (15 ммолей) иодида калия, а затем 0,57 г (13 ммолей) дисперсии гидрида натрия (55%-ная в минеральном масле). По окончании перемешивания, длившегося в течение 4 ч при комнатной температуре, реакционную смесь сливали на ледяную воду, продукт трижды экстрагировали метиленхлоридом, органические фазы дважды промывали дистиллированной водой, затем сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием н-гексана и уксусного эфира. Таким путем получили 5,08 г (90% от теории) трет-бутилового эфира (3RS,4RS)-3-(2'-тpет-бутoкcикapбoнилбифенил-4-илметокси)-4-(4- фторфенил)пиперидин-1-карбоновой кислоты в виде аморфной бесцветной пены.
(б) 2,25 г (4 ммоля) трет-бутилового эфира (3RS,4RS)-3-(2'-трет-бутоксикарбонилбифенил-4-илметокси)-4- (4-фторфенил)пиперидин-1-карбоновой кислоты перемешивали в течение 18 ч при нагревании с обратным холодильником в 50 мл монометилового эфира этиленгликоля с добавлением 8 мл (36 ммолей) едкого натра (14%-ного). После отгонки растворителя в вакууме, создаваемом водоструйным насосом, остаток растворяли в ледяной воде, после чего значение pH с помощью 2 н. соляной кислоты устанавливали равным 3 и продукт трижды экстрагировали метиленхлоридом, органические фазы дважды промывали дистиллированной водой, затем сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием метиленхлорида и метанола. Таким путем получили 1,66 г (82% от теории) трет-бутилового эфира (3RS, 4RS)-3-(2'-карбоксибифенил-4-илметокси)-4-(4- фторфенил)пиперидин-1-карбоновой кислоты в виде аморфной бесцветной пены; МС: 504 (M-H)-.
(в) 0,51 г (1 ммоль) трет-бутилового эфира (3RS,4RS)-3-(2'-карбоксибифенил-4-илметокси)-4- (4-фторфенил)пиперидин-1-карбоновой кислоты и 0,18 г (1 ммоль) 2-хлор-4,6-диметокси-1,3,5-триазина растворяли в атмосфере аргона в смеси из 3,5 мл диметилформамида и 5 мл ацетонитрила, затем при 0oC по каплям добавляли 0,22 мл (2 ммоля) N-метилморфолина и перемешивали в течение 2 ч при 0oC. Далее по каплям добавляли раствор из 0,08 мл (1 ммоль) (RS)-3-амино-1,2-пропандиола в 6 мл ацетонитрила, после чего перемешивали в течение 18 ч при комнатной температуре. Реакционную смесь сливали на ледяную воду, продукт трижды экстрагировали метиленхлоридом, органические фазы дважды промывали дистиллированной водой, затем сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием метиленхлорида и метанола. Таким путем получили 0,29 г (50% от теории) смеси трет-бутилового эфира (3RS,4RS)- и (3SR,4SR)-3-[2'-[(RS)-(2,3- дигидроксипропил)карбамоил] бифенил-4-илметокси] -4-(4- фторфенил)пиперидин-1-карбоновой кислоты в виде аморфной бесцветной пены; МС: 579 (М+Н)+.
(г) Аналогично примеру 22(м) из смеси трет-бутилового эфира (3RS,4RS)- и (3SR, 4SR)-3-[2'-[(RS)- (2,3-дигидроксипропил)карбамоил]бифенил-4-илметокси] -4-(4- фторфенил)пиперидин-1-карбоновой кислоты путем отщепления BOC-защитной группы с помощью хлористого водорода в метаноле получили смесь гидрохлорида (RS)- и (RS)-2,3-дигидроксипропил)амида 4'-[(3RS,4RS)-4-(4-фторфенил)пиперидин-3-илоксиметил] бифенил-2- карбоновой кислоты (1: 1) в виде аморфной бесцветной пены; МС: 479 (М+Н)+.
Пример 93.
0, 050 г (0,12 ммоля) смеси 3:1 метилового эфира (Е)- и (Z)-[l- [(3RS, 4SR)-4-(4- фторфенил)пиперидин-3-ил] -2-нафталин-2-илэтилиденаминоокси] уксусной кислоты [пример 90.03] перемешивали в течение 18 ч при 50oC в 3 мл метанола с добавлением 1,0 мл 1 н. едкого натра. После охлаждения до комнатной температуры по каплям добавляли 1,0 мл 1 н. соляной кислоты, а затем концентрировали в вакууме, создаваемом водоструйным насосом. Остаток суспендировали в этаноле, затем фильтровали, к фильтрату добавляли 0,025 мл (0,3 ммоля) соляной кислоты (37%-ной) и снова концентрировали в вакууме, создаваемом водоструйным насосом. Далее полученный остаток сушили в течение 2 ч в высоком вакууме при комнатной температуре. Таким путем получили 0,040 г (73% от теории) смеси гидрохлорида (Е)- и (Z)- (3RS,4SR)-(1-[4-(4-фторфенил)пиперидин-3-ил]-2-нафталин-2- илэтилиденаминоокси)уксусной кислоты (1: 1) в виде аморфной светло-желтой пены; МС: 421 (М+Н)+.
Пример 94.
(а) 4,30 г (9,7 ммоля) трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-гидроксипиперидин-1-карбоновой кислоты [пример 86(о] загружали в 215 мл тетрагидрофурана в атмосфере аргона при 0oC и при перемешивании добавляли 1,23 г (28,1 ммоля) дисперсии гидрида натрия (55%-ная в минеральном масле). По истечении 30 мин по каплям добавляли раствор из 1,86 мл (12,7 ммоля) трет-бутилового эфира бромуксусной кислоты в 10 мл тетрагидрофурана и нагревали до комнатной температуры. Реакционную смесь сливали на ледяную воду, продукт трижды экстрагировали уксусным эфиром, органические фазы дважды промывали дистиллированной водой, затем сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием метиленхлорида и метанола. Таким путем получили 4,77 г (88% от теории) трет-бутилового эфира (3RS, 4RS)-4-[4-(3- бензилоксипропокси)фенил] -3-трет-бутоксикарбонилметоксипиперидин- 1-карбоновой кислоты в виде желтого масла; МС: 556 (М+Н)+.
(б) 0,36 г (16,5 ммоля) борогидрида лития загружали в атмосфере аргона при комнатной температуре в 55 мл тетрагидрофурана и при перемешивании по каплям добавляли раствор из 4,58 г (8,24 ммоля) трет-бутилового эфира (3RS, 4RS)-4-[4-(3- бензилоксипропокси)фенил] -3-трет-бутоксикарбонилметоксипиперидин-1- карбоновой кислоты в 55 мл тетрагидрофурана и затем нагревали с обратным холодильником. По истечении 4 ч реакционную смесь сливали на ледяную воду, значение pH с помощью соляной кислоты (2 н.) устанавливали равным 3, а затем продукт трижды экстрагировали уксусным эфиром. Далее органические фазы дважды промывали дистиллированной водой, сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Таким путем получили 3,95 г (99% от теории) трет-бутилового эфира (3RS, 4RS)-4-[4-(3- бензилоксипропокси)фенил] -3-(2-гидроксиэтокси)пиперидин-1- карбоновой кислоты в виде желтого масла; МС: 486 (М+Н)+.
(в) 5,56 г (13,2 ммоля) трифенилфосфиндибромида растворяли в атмосфере аргона в 20 мл ацетонитрила, а затем при 0oC по каплям добавляли 1,06 мл (13,2 ммоля) пиридина; этот раствор при 0oC по каплям добавляли к раствору из 3,95 г (8,1 ммоля) трет-бутилового эфира (3RS,4RS)-4- [4-(3-бензилоксипропокси)фенил] -3-(2-гидроксиэтокси) пиперидин-1-карбоновой кислоты в 20 мл ацетонитрила, после чего перемешивали в течение 18 ч при комнатной температуре. Реакционную смесь сливали на ледяную воду, продукт трижды экстрагировали уксусным эфиром, органические фазы дважды промывали дистиллированной водой, затем сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием н-гексана и уксусного эфира. Таким путем получили 3,14 г (71% от теории) трет-бутилового эфира (3RS,4RS)-4-[4-(3- бензилоксипропокси)фенил]-3-(2-бромэтокси)пиперидин-1-карбоновой кислоты в виде желтого масла; МС: 548, 550 (М+Н)+.
(г) 3,14 г (5,72 ммоля) трет-бутилового эфира (3RS,4RS)-4- [4-(3-бензилоксипропокси)фенил] -3-(2-бромэтокси)пиперидин-1- карбоновой кислоты и 2,53 г (13,76 ммоля) 3,4-динитрофенола перемешивали в течение 22 ч в атмосфере аргона при нагревании с обратным холодильником в 230 мл ацетонитрила с добавлением 7,9 г (57,2 ммоля) карбоната калия (безводного). После отгонки растворителя в вакууме, создаваемом водоструйным насосом, остаток сливали на ледяную воду и продукт трижды экстрагировали метиленхлоридом, органические фазы дважды промывали дистиллированной водой, затем сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием н-гексана и уксусного эфира. Таким путем получили 2,57 г (69% от теории) трет-бутилового эфира (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил]-3-[2-(3,4- динитрофенокси)этокси]пиперидин-1-карбоновой кислоты в виде коричневого масла; МС: 652 (М+Н)+.
(д) 1,63 г (2,5 ммоля) трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил]-3- [2-(3,4-динитрофенокси)этокси]пиперидин-1-карбоновой кислоты гидрировали при нормальных условиях в течение 2 ч в 80 мл уксусного эфира с добавлением 0,50 г оксида платины. Катализатор отфильтровывали через подушку из дикалита и растворитель отгоняли в вакууме, создаваемом водоструйным насосом. Таким путем получили 1,44 г (97% от теории) трет-бутилового эфира (3RS, 4RS)-4-[4-(3- бензилоксипропокси)фенил]-3-[2-(3,4-диаминофенокси)этокси] пиперидин-1-карбоновой кислоты в виде фиолетового масла; МС: 592 (М+Н)+.
(е) Аналогично примеру 22(м) из трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-[2-(3,4- диаминофенокси)этокси]пиперидин-1-карбоновой кислоты путем отщепления BOC-защитной группы с помощью хлористого водорода в метаноле получили гидрохлорид 4-[2-[(3RS,4RS)-4-[4-(3- бензилоксипропокси)фенил] пиперидин-3-илокси] этокси] бензол-1,2- диамина (1:3) в виде светло-фиолетовых кристаллов; МС: 492 (М+Н)+.
Пример 95.
(a) 4,37 г (9,9 ммоля) трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси) фенил] - 3 - гидроксипиперидин-1 -карбоновой кислоты [пример 86(о)] и 3,20 г (9,9 ммоля) 2-хлорметил-7-(2-триметилсиланилэтоксиметокси) нафталина [пример 6(х)] растворяли в 35 мл диметилформамида в атмосфере аргона, а затем добавляли 0,46 г (10,5 ммоля) дисперсии гидрида натрия (55%-ная в минеральном масле). Далее перемешивали в течение 18 ч при комнатной температуре. Реакционную смесь сливали на ледяную воду, продукт трижды экстрагировали метиленхлоридом, органические фазы дважды промывали дистиллированной водой, затем сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием метиленхлорида и метанола. Таким путем получили 7,15 г (99% от теории) трет-бутилового эфира (3RS, 4RS)-4-[4-(3- бензилоксипропокси)фенил] -3-[7-(2- триметилсиланилэтоксиметокси)нафталин-2-илметокси] пиперидин-1- карбоновой кислоты в виде светло-желтого масла; МС: 728 (М+Н)+ .
(б) 6,72 г (9,23 ммоля) трет-бутилового эфира (3RS,4RS)-4-[4-(3- бензилоксипропокси)фенил]-3-[7-(2-триметилсиланилэтоксиметокси) нафталин-2-илметокси] пиперидин-1-карбоновой кислоты загружали при 0oC в 140 мл абс. метанола, затем по каплям при температуре максимально 5oC добавляли 2,8 мл (19,4 ммоля) соляной кислоты в метаноле (7,0-молярный раствор) и после этого нагревали до комнатной температуры. По истечении 90 мин реакционную смесь сливали на ледяной раствор гидрокарбоната калия и продукт трижды экстрагировали метиленхлоридом, органические фазы один раз промывали дистиллированной водой, затем сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием метиленхлорида и метанола. Таким путем получили 4,92 г (89% от теории) трет-бутилового эфира (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] -3- (7-гидроксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде желтого масла; МС: 598 (М+Н)+.
(в) Аналогично примеру 22(м) из трет-бутилового эфира (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(7- гидроксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты путем отщепления BOC-защитной группы с помощью хлористого водорода в метаноле получили гидрохлорид 7-[(3RS,4RS)-4-[4-(3- бензилоксипропокси)фенил]пиперидин-3-илоксиметил]нафталин-2-ола (1:1) в виде аморфной бежевой пены; МС: 498 (М+Н)+.
Пример 96.
(а) 0,33 г (0,54 ммоля) трет-бутилового эфира (3RS,4RS)-4-[4-(3- бензилоксипропокси)фенил] -3-(7-гидроксинафталин-2- илметокси) пиперидин-1-карбоновой кислоты [пример 95(б)] и 0,27 г (0,7 ммоля) 2,3;4,5-ди-O-изопропилиден-1-O-(4-метилфенилсульфонил) -D-арабинитола [Liebigs Ann. Chem. 1992, 1131] перемешивали в течение 2 ч в атмосфере аргона при нагревании с обратным холодильником в 15 мл диметилформамида с добавлением 0,69 г (5 ммолей) карбоната калия (безводного). Реакционную смесь сливали на ледяную воду, продукт трижды экстрагировали метиленхлоридом, органические фазы дважды промывали дистиллированной водой, затем сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием метиленхлорида и метанола. Таким путем получили 0,34 г (78% от теории) смеси 1:1 трет-бутилового эфира (3R,4R)- и (3S,4S)-4-[4- (3-бензилоксипропокси)фенил] -3-[7-[(4S, 4'R, 5R)-2,2,2',2'- тетраметил-[4,4']] би [[1,3] диоксолан-5-илметокси] нафталин-2- илметокси]пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 829 (M+NH4)+.
(б) 0,10 г (0,12 ммоля) смеси 1:1 трет-бутилового эфира (3R,4R)- и (3S, 4S)-4-[4-(3- бензилоксипропокси)фенил] -3-[7-[(4S,4'R,5R)-2,2,2',2'- тетраметил-[4,4'] би[[1, 3]диоксолан-5-илметокси]нафталин- 2-илметокси]пиперидин-1-карбоновой кислоты растворяли в 5 мл абс. этанола, затем добавляли 1 мл соляной кислоты в этаноле (5,6-молярный раствор) и перемешивали в течение 90 ч при 50oC в атмосфере аргона. После отгонки растворителя в вакууме, создаваемом водоструйным насосом, остаток сушили в течение 3 ч в высоком вакууме при 50oC над пятиокисью фосфора. Таким путем получили 0,07 г (87% от теории) смеси 1:1 гидрохлорида (2R,3R,4R)-5-[7-[(3R,4R)- и (3S,4S)-4-[4-(3- бензилоксипропокси)фенил] пиперидин-3-илоксиметил] нафталин-2- илокси] пентан-1,2,3,4-тетраола (1:1) в виде светло-желтых кристаллов; МС: 632 (М+Н)+.
Пример 97.
(а) 4,77 г (10,8 ммоля) трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] - 3-гидроксипиперидин-1-карбоновой кислоты [пример 86(o)] и 3,49 г (10,8 ммоля) 2-хлорметил-6-(2-триметилсиланилэтоксиметокси) нафталина [пример 6(п)] растворяли при комнатной температуре в атмосфере аргона в 35 мл диметилформамида, а затем добавляли 0,50 г (11,5 ммоля) дисперсии гидрида натрия (55%-ная в минеральном масле) и перемешивали в течение 18 ч при комнатной температуре. Реакционную смесь сливали на ледяную воду, продукт трижды экстрагировали метиленхлоридом, органические фазы дважды промывали дистиллированной водой, затем сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием н-гексана и метиленхлорида. Таким путем получили 6,74 г (83% от теории) трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-[6-(2- триметилсиланилэтоксиметокси)нафталин-2-илметокси] пиперидин-1- карбоновой кислоты в виде светло-желтого масла; МС: 728 (М+Н)+.
(б) Аналогично примеру 95(б) из трет-бутилового эфира (3RS, 4RS)-4- [4-(3-бензилоксипропокси)фенил] -3-[6-(2-триметилсиланилэтоксиметокси) нафталин-2-илметокси] пиперидин-1-карбоновой кислоты получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил]-3-(6-гидроксинафталин-2- илметокси)пиперидин-1-карбоновой кислоты в виде аморфной бесцветной пены; МС: 598 (М+Н)+.
(в) Аналогично примеру 90(ж) из трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(6-гидроксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(3- бензилоксипропокси)фенил] -3-[6-(2-морфолин-4- илэтокси)нафталин-2-илметокси] пиперидин-1-карбоновой кислоты в виде светло-желтого масла; МС: 711 (М+Н)+.
(г) Аналогично примеру 22(м) из трет-бутилового эфира (3RS,4RS)-4-[4-(3- бензилоксипропокси)фенил]-3-[6-(2-морфолин-4-илэтокси) нафталин-2-илметокси] пиперидин-1-карбоновой кислоты путем отщепления BOC-защитной группы с помощью хлористого водорода в метаноле получили гидрохлорид 4-[2-[6-[(3RS, 4RS)-4-[4-(3- бензилоксипропокси)фенил] пиперидин-3-илоксиметил]нафталин-2- илокси]этил]морфолина (1:2) в виде бесцветных кристаллов; МС: 611 (М+Н)+.
Пример 98.
(а) 4,10 г (21,5 ммоля) п-толуолсульфохлорида загружали в атмосфере аргона при 5oC в 20 мл абс. пиридина, добавляли 0,06 г (0,5 ммоля) 4-диметиламинопиридина и при перемешивании по каплям добавляли раствор из 3,58 г (20,3 ммоля) (RS)-2-[(2,2-диметил-1,3-диоксолан-4-ил)метокси] этанола [J. Chem. Soc. 1965, 2968] в 20 мл абс. пиридина. По окончании перемешивания, длившегося в течение 6 ч при комнатной температуре, реакционную смесь сливали на ледяную воду, продукт трижды экстрагировали метиленхлоридом, органические фазы дважды промывали дистиллированной водой, затем сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием метиленхлорида и метанола. Таким путем получили 1,72 г (26% от теории) (RS)-2-(2,2-диметил[1, 3]диоксолан-4-илметокси)этилового эфира толуол-4-сульфокислоты в виде бесцветного масла; МС: 315 (M-CH3)+.
(б) Аналогично примеру 90(ж) из (RS)-2-(2,2-диметил[1, 3]диоксолан-4-илметокси)этилового эфира толуол-4-сульфокислоты и трет-бутилового эфира (3RS, 4RS)-4- [4-(3-бензилоксипропокси)фенил] -3-(7-гидроксинафталин-2- илметокси)пиперидин-1-карбоновой кислоты [пример 95(б] получили смесь трет-бутилового эфира (3RS,4RS)- и (3SR,4SR)-4-[4-(3- бензилоксипропокси)фенил]-3-[7-[2-[(RS)-2,2-диметил[1,3] диоксолан-4-илметокси]этокси]нафталин-2-илметокси] пиперидин- 1-карбоновой кислоты в виде бесцветных кристаллов; МС: 773 (М+NH4)+.
(в) Аналогично примеру 22(м) из смеси трет-бутилового эфира (3RS,4RS)- и (3SR, 4SR)-4-[4-(3-бензилоксипропокси)фенил]-3-[7-[2- [(RS)-2,2-диметил[1,3] диоксолан-4-илметокси] этокси] нафталин-2- илметокси]пиперидин-1-карбоновой кислоты путем отщепления BOC-защитной группы с помощью хлористого водорода в метаноле получили смесь гидрохлорида (RS)- и (SR)-3-[2-[7-[(3RS,4RS)-4-[4-(3- бензилоксипропокси)фенил] пиперидин-3-илоксиметил] нафталин-2- илокси] этокси]пропан-1, 2-диола (1:1) в виде аморфной бежевой пены; МС: 616 (М+Н)+.
Пример 99.
(а) 9,92 г (227,4 ммоля) дисперсии гидрида натрия (55%-ная в минеральном масле) загружали в атмосфере аргона при 5oC в 220 мл абс. тетрагидрофурана, затем в течение 1 ч при 5oC по каплям добавляли раствор из 68,3 мл (341,1 ммоля) триэтилового эфира фосфонуксусной кислоты в 220 мл абс. тетрагидрофурана, после чего перемешивали в течение 1 ч при комнатной температуре. Далее снова при 5oC в течение 30 мин по каплям добавляли раствор из 24,1 г (113,7 ммоля) 4-бензилоксибензальдегида в 220 мл тетрагидрофурана и затем перемешивали при 5oC в течение 2 ч. Реакционную смесь смешивали с 300 мл ледяной воды и растворитель отгоняли в вакууме, создаваемом водоструйным насосом; водную суспензию продукта трижды экстрагировали уксусным эфиром, органические фазы дважды промывали дистиллированной водой, затем сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием н-гексана и уксусного эфира. Таким путем получили 30,8 г (96% от теории) этилового эфира (Е)-3-(4- бензилоксифенил)акриловой кислоты в виде бесцветного твердого вещества; МС: 282 (М)+.
(б) 17,85 г (136,1 ммоля) моноамида моноэтилового эфира малоновой кислоты смешивали в атмосфере аргона в 350 мл абс. этанола с 15,3 г (136,1 ммоля) трет-бутилата калия, затем при перемешивании и при комнатной температуре добавляли 19,2 г (68,1 ммоля) этилового эфира (Е)-3-(4-бензилоксифенил)акриловой кислоты и перемешивали в течение 1 ч при нагревании с обратным холодильником. После охлаждения до 10oC по каплям добавляли 15,4 мл (269,7 ммоля) ледяной уксусной кислоты. Реакционную смесь сливали на ледяную воду, продукт трижды экстрагировали метиленхлоридом, органические фазы дважды промывали дистиллированной водой, затем сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием метиленхлорида и метанола. Таким путем получили 17,2 г (69% от теории) этилового эфира (3RS,4SR)-4-(4-бензилоксифенил)-2,6-диоксопиперидин-3-карбоновой кислоты в виде бесцветного твердого вещества; МС: 367 (М)+.
(в) 4,33 г (114,2 ммоля) алюмогидрида лития суспендировали в атмосфере аргона в 200 мл тетрагидрофурана, затем при комнатной температуре по каплям добавляли раствор из 18,31 г (49,8 ммоля) этилового эфира (3RS,4SR)-4-(4-бензилоксифенил)-2,6-диоксопиперидин-3-карбоновой кислоты в 200 мл тетрагидрофурана, после чего перемешивали в течение 2 ч при нагревании с обратным холодильником. К реакционной смеси при 5-10oC осторожно по каплям добавляли 100 мл дистиллированной воды и образовавшийся при этом осадок отфильтровывали. Далее фильтрат трижды экстрагировали уксусным эфиром, органические фазы дважды промывали дистиллированной водой, сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт перекристаллизовывали из метиленхлорида и н-гексана. Таким путем получили 11,14 г (75% от теории) (3RS, 4SR)-[4-(4- бензилоксифенил)пиперидин-3-ил] метанола в виде бесцветных кристаллов; МС: 297 (М)+.
(г) 11,14 г (37,5 ммоля) (3RS,4SR)-[4-(4- бензилоксифенил)пиперидин-3-ил] метанола растворяли в атмосфере аргона в 140 мл диоксана, затем при комнатной температуре добавляли раствор из 6,72 г (80 ммолей) гидрокарбоната натрия в 45 мл воды и порциями добавляли 9,78 г (44,8 ммоля) ди-трет-бутилдикарбоната. По окончании перемешивания, длившегося в течение 18 ч при комнатной температуре, реакционную смесь трижды экстрагировали уксусным эфиром, органические фазы дважды промывали дистиллированной водой, затем сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием метиленхлорида и метанола. Таким путем получили 13,38 г (90% от теории) трет-бутилового эфира (3RS,4SR)-4-(4-бензилоксифенил)-3- гидроксиметилпиперидин-1-карбоновой кислоты в виде аморфной бесцветной пены; МС: 398 (М+Н)+.
(д) 3,92 мл (45,6 ммоля) оксалилхлорида загружали в атмосфере аргона при -70oC в 400 мл метиленхлорида, затем по каплям добавляли 5,48 мл (77,2 ммоля) диметилсульфоксида и перемешивали в течение 30 мин. Далее при -70oC по каплям добавляли раствор из 13,95 г (35,1 ммоля) трет-бутилового эфира (3RS, 4SR)-4-(4-бензилоксифенил)-3- гидроксиметилпиперидин-1-карбоновой кислоты в 200 мл метиленхлорида, после чего перемешивали при этой температуре в течение 2 ч. После этого к реакционной смеси по каплям добавляли 12,2 мл (87,7 ммоля) триэтиламина и затем нагревали до комнатной температуры. По окончании перемешивания, длившегося в течение 18 ч при этой температуре, смесь сливали на ледяную воду и продукт трижды экстрагировали метиленхлоридом, органические фазы дважды промывали дистиллированной водой, затем сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт перекристаллизовывали из н-гексана. Таким путем получили 11,31 г (81% от теории) трет-бутилового эфира (3RS, 4SR)-4-(4- бензилоксифенил)-3-формилпиперидин-1-карбоновой кислоты в виде бесцветных кристаллов; МС: 395 (М+Н)+.
(е) 11,04 г (25,6 ммоля) трибутилнафталин-2-илметилстаннана [пример 74(ж)] загружали при -70oC в атмосфере аргона в 100 мл тетрагидрофурана, а затем по каплям добавляли 12,0 мл (19,2 ммоля) раствора н-бутиллития (1, 6 молярный раствор в н-гексане). По окончании перемешивания, длившегося в течение 30 мин при этой температуре, по каплям добавляли раствор из 5,94 г (15 ммолей) трет-бутилового эфира (3RS, 4SR)-4-(4-бензилоксифенил)-3-формилпиперидин-1-карбоновой кислоты в 45 мл тетрагидрофурана и перемешивание продолжали еще в течение 1 ч при -70oC. Далее нагревали до комнатной температуры и по истечении 18 ч сливали на ледяную воду, продукт трижды экстрагировали уксусным эфиром, органические фазы дважды промывали дистиллированной водой, затем сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием н-гексана и уксусного эфира. Таким путем получили 6, 88 г (85% от теории) смеси трет-бутилового эфира (3RS,4SR)-4-(4-бензилоксифенил)-3-[(RS)- и -[(SR)-1-гидрокси-2-нафталин-2-илэтил]пиперидин-1-карбоновой кислоты в виде желтых кристаллов; МС: 538 (М+Н)+.
(ж) Аналогично примеру 22(м) из смеси трет-бутилового эфира (3RS,4SR)-4-(4- бензилоксифенил)-3-[(RS)- и -[(SR)-1-гидрокси-2-нафталин-2- илэтил] пиперидин-1-карбоновой кислоты путем отщепления BOC-защитной группы с помощью хлористого водорода в метаноле получили смесь гидрохлорида (RS)- и (SR)-1-[(3RS, 4SR)-4-(4- бензилoкcифенил)пипеpидин-3-ил] -2-нафталин-2-илэтанола (1:1) в виде бежевых кристаллов; МС: 438 (М+Н)+.
Пример 100.
(а) 6,36 г (11,8 ммоля) смеси трет-бутилового эфира (3RS,4SR)-4-(4- бензилоксифенил)-3-[(RS)- и -[(SR)-1-гидpoкcи-2-нaфтaлин-2- илэтил]пиперидин-1-карбоновой кислоты [пример 99(е)] гидрировали в нормальных условиях в течение 4 ч в 50 мл метанола с добавлением 2,0 г палладия на угле (10%-ного). После отфильтровывания катализатора через подушку из дикалита и отгонки растворителя в вакууме, создаваемом водоструйным насосом, получили 4,97 г (94% от теории) смеси трет-бутилового эфира (3RS,4SR)-4-(4-гидроксифенил)- 3-[(RS)- и -(SR)-1-гидрокси-2-нафталин-2-илэтил]пиперидин-1- карбоновой кислоты в виде аморфной светло-серой пены; МС: 448 (М+Н)+.
(б) 3,97 г (8,9 ммоля) смеси трет-бутилового эфира (3RS,4SR)-4-(4-гидроксифенил)-3-[(RS)- и -[SR)-1-гидрокси-2- нафталин-2-илэтил] пиперидин-1-карбоновой кислоты загружали в атмосфере аргона при комнатной температуре в 60 мл метилэтилкетона, далее добавляли 4,90 г (35,5 ммоля) карбоната калия (безводного) и 4,54 мл (27,7 ммоля) бензил-3-бромпропилового эфира, а затем перемешивали в течение 8 ч при нагревании с обратным холодильником. После охлаждения до комнатной температуры реакционную смесь сливали на ледяную воду и продукт трижды экстрагировали уксусным эфиром, органические фазы дважды промывали дистиллированной водой, затем сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием метиленхлорида и метанола. Таким путем получили 5,13 г (97% от теории) смеси трет-бутилового эфира (3RS, 4SR)-4-[4-(3-бензилоксипропокси)фенил] -3-[(RS)- и -[(SR)-1- гидрокси-2-нафталин-2-илэтил]пиперидин-1-карбоновой кислоты в виде аморфной желтой пены; МС: 596 (М+Н)+.
(в) Аналогично примеру 99(д) из смеси трет-бутилового эфира (3RS,4SR)-4-[4-(3- бензилоксипропокси)фенил] -3-[(RS)- и -[(SR)-1-гидрокси-2- нафталин-2-илэтил] пиперидин-1-карбоновой кислоты с помощью оксалилхлорида и диметилсульфоксида получили трет-бутиловый эфир (3RS,4SR)-4-[4-(3-бензилоксипропокси)фенил] -3-(нафталин-2-илацетил) пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 594 (М+Н)+.
(г) Аналогично примеру 22(м) из трет-бутилового эфира (3RS,4SR)-4-[4-(3-бензилоксипропокси)фенил] -3-(нафталин-2- илацетил)пиперидин-1-карбоновой кислоты путем отщепления BOC-защитной группы с помощью хлористого водорода в метаноле получили гидрохлорид 1-[(3RS, 4SR)-4-[4-(3- бензилоксипропокси)фенил]пиперидин-3-ил]-2-нафталин-2-илэтанона (1:1) в виде бесцветных кристаллов; МС: 494 (М+Н)+.
Пример 101.
(а) 10,66 г (50,2 ммоля) 4-бензилоксибензальдегида и 8,54 мл (56,2 ммоля) диэтилового эфира малоновой кислоты перемешивали в течение 18 ч в атмосфере аргона при нагревании с обратным холодильником в 100 мл толуола с добавлением 10,15 г молекулярного сита

(6) 6, 42 г (48,9 ммоля) моноамида моноэтилового эфира малоновой кислоты смешивали в атмосфере аргона в 115 мл абс. этанола с 5,49 г (48,9 ммоля) трет-бутилата калия, затем при перемешивании и при комнатной температуре добавляли 17,35 г (48,9 ммоля) диэтилового эфира 2-(4-бензилоксибензилиден) малоновой кислоты и перемешивали в течение 2 ч при нагревании с обратным холодильником. После охлаждения до 10oC по каплям добавляли 13,0 мл (227 ммолей) ледяной уксусной кислоты. Реакционную смесь сливали на ледяную воду, продукт трижды экстрагировали метиленхлоридом, органические фазы дважды промывали дистиллированной водой, затем сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием метиленхлорида и н-гексана. Таким путем получили 16,76 г (78% от теории) диэтилового эфира (3R,4s,5S)-4-(4-бензилоксифенил)-2,6-диоксопиперидин-3,5- дикарбоновой кислоты в виде бесцветного твердого вещества; МС: 439 (М)+.
(в) 3,83 г (100,9 ммоля) алюмогидрида лития суспендировали в атмосфере аргона в 200 мл тетрагидрофурана, затем при комнатной температуре по каплям добавляли раствор из 18,37 г (41,8 ммоля) диэтилового эфира (3R,4s,5S)-4-(4-бензилоксифенил)-2,6- диоксопиперидин-3,5-дикарбоновой кислоты в 200 мл тетрагидрофурана, после чего перемешивали в течение 1 ч при нагревании с обратным холодильником. Далее к реакционной смеси при 5-10oC осторожно по каплям добавляли 25 мл дистиллированной воды. После фильтрации реакционной смеси растворитель отгоняли в вакууме, создаваемом водоструйным насосом. Таким путем получили 11,04 г (81% от теории) (3R,4s, 5S)-[4-(4-бензилоксифенил)-5- гидроксиметилпиперидин-3-ил] метанола в виде бесцветных кристаллов; МС: 328 (М+Н)+.
(г) 8,10 г (24,7 ммоля) (3R,4s, 5S)- [4-(4-бензилоксифенил)-5-гидроксиметилпиперидин-3-ил] метанола растворяли в атмосфере аргона в 100 мл диоксана, затем при комнатной температуре добавляли раствор из 4,44 г (52,8 ммоля) гидрокарбоната натрия в 34 мл воды, а затем порциями добавляли 6,46 г (29,6 ммоля) ди-трет-бутилдикарбоната. По окончании перемешивания, длившегося в течение 66 ч при комнатной температуре, реакционную смесь трижды экстрагировали уксусным эфиром, органические фазы дважды промывали дистиллированной водой, затем сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием метиленхлорида и метанола. Таким путем получили 8,10 г (77% от теории) трет-бутилового эфира (3R,4s,5S)-4-(4-бензилоксифенил)- 3,5-бисгидроксиметилпиперидин-1-карбоновой кислоты в виде аморфной бесцветной пены; МС: 428 (М+Н)+.
(д) 7,46 г (17, 5 ммоля) трет-бутилового эфира (3R,4s,5S)-4-(4-бензилоксифенил)-3,5- бисгидроксиметилпиперидин-1-карбоновой кислоты гидрировали в нормальных условиях в течение 2 ч в 250 мл метанола с добавлением 1,5 г палладия на угле (10%-ного). После этого катализатор отфильтровывали через подушку из дикалита и растворитель отгоняли в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием метиленхлорида и метанола. Таким путем получили 6,07 г (99% от теории) трет-бутилового эфира (3R,4s,5S)-3, 5-бисгидроксиметил-4-(4-гидроксифенил)пиперидин-1-карбоновой кислоты в виде аморфной бесцветной пены; МС: 338 (М+Н)+.
(е) 6,77 г (20 ммолей) трет-бутилового эфира (3R,4s, 5S)-3,5- бисгидроксиметил-4-(4-гидроксифенил)пиперидин-1-карбоновой кислоты загружали в атмосфере аргона при комнатной температуре в 90 мл метилэтилкетона. Далее добавляли 11,05 г (80 ммолей) карбоната калия (безводного) и 10,25 мл (58 ммоля) бензил-3-бромпропилового эфира, а затем перемешивали в течение 18 ч при нагревании с обратным холодильником. После охлаждения до комнатной температуры реакционную смесь сливали на ледяную воду и продукт трижды экстрагировали уксусным эфиром, органические фазы дважды промывали дистиллированной водой, затем сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием метиленхлорида и метанола. Таким путем получили 7,95 г (82% от теории) трет-бутилового эфира (3R, 4s, 5S)-4-[4-(3- бензилоксипропокси)фенил]-3,5-бисгидроксиметилпиперидин-1-карбоновой кислоты в виде аморфной бесцветной пены; МС: 486 (М+Н)+.
(ж) 1,51 г (33,2 ммоля) дисперсии гидрида натрия (55%-ная в минеральном масле) и 2,94 г (15,9 ммоля) гидрохлорида 4-(2-хлорэтил)морфолина растворяли в атмосфере аргона при комнатной температуре в 25 мл диметилформамида, далее при перемешивании добавляли раствор из 7,33 г (15,1 ммоля) трет-бутилового эфира (3R, 4s, 5S)-4-[4-(3-бензилоксипропокси)фенил]- 3, 5-бисгидроксиметилпиперидин-1-карбоновой кислоты в 50 мл диметилформамида и 0,1 г (0,6 ммоля) иодида калия. Реакционную смесь перемешивали в течение 9 ч при 100oC. После охлаждения до комнатной температуры реакционную смесь сливали на ледяную воду и продукт трижды экстрагировали метиленхлоридом, органические фазы дважды промывали дистиллированной водой, затем сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием метиленхлорида и метанола. Таким путем получили 0,29 г (3% от теории) трет-бутилового эфира (3R,4s,5S)-4-[4-(3- бензилоксипропокси)фенил] -3,5-бис(2-морфолин-4- илэтоксиметил)пиперидин-1-карбоновой кислоты в виде светло-коричневого масла [МС: 712 (М+Н)+] и 2,37 г (26% от теории) трет-бутилового эфира (3RS, 4RS, 5SR)-4-[4-(3- бензилоксипропокси)фенил]-3-гидроксиметил-5-(2-морфолин-4- илэтоксиметил)пиперидин-1-карбоновой кислоты в виде светло-коричневого масла; МС: 599 (М+Н)+.
(з) Аналогично примеру 74(е) из трет-бутилового эфира (3RS,4RS,5SR)-4-[4-(3- бензилоксипропокси)фенил] -3-гидроксиметил-5-(2-морфолин-4- илэтоксиметил)пиперидин-1-карбоновой кислоты путем окисления диметилсульфоксидом/оксалилхлоридом в метиленхлориде получили трет-бутиловый эфир (3RS,4SR, 5SR)-4-[4-(3- бензилоксипропокси)фенил] -3-формил-5-(2-морфолин-4- илэтоксиметил)пиперидин-1-карбоновой кислоты в виде желтого масла; МС: 597 (М+Н)+.
(и) 1,20 г (0,05 г-атом) магниевой стружки загружали в атмосфере аргона при комнатной температуре в 15 мл абс. простого эфира, добавляли 1 кристалл иода и 5 капель 1,2-дибромметана и нагревали до температуры дефлегмации. После начала реакции (обесцвечивание) в течение 30 мин по каплям добавляли раствор из 1,77 г (10,0 ммолей) 2-(хлорметил)нафталина в 10 мл абс. простого эфира. По окончании добавления давали остыть до комнатной температуры и по истечении 1 ч по каплям добавляли раствор из 0,70 г (1,17 ммоля) трет-бутилового эфира (3RS,4SR,5SR)-4-[4-(3-бензилоксипропокси)фенил] -3-формил-5-(2-морфолин-4-илэтоксиметил)пиперидин-1-карбоновой кислоты в 15 мл абс. простого эфира. 3атем перемешивали в течение 18 ч при комнатной температуре. После добавления по каплям при охлаждении льдом 3 мл воды реакционную смесь сливали на ледяную воду, продукт трижды экстрагировали простым эфиром, органические фазы дважды промывали дистиллированной водой, затем сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием метиленхлорида и метанола. Таким путем получили 0,77 г (89% от теории) смеси трет-бутилового эфира (3RS,4SR,5SR)-4-[4-(3-бензилоксипропокси)фенил] -3-[(RS)- и -[SR)-1-гидрокси-2- нафталин-2-илэтил] -5-(2-морфолин-4-илэтоксиметил)пиперидин-1- карбоновой кислоты; МС: 739 (М+Н)+.
(л) Аналогично примеру 74(е) из 0,74 г (1 ммоль) смеси трет-бутилового эфира (3RS, 4SR,5SR)-4-[4- (3-бензилоксипропокси)фенил]-3-[(RS)- и -[(SR)-1-гидрокси-2- нафталин-2-илэтил]-5-(2-морфолин-4-илэтоксиметил)пиперидин-1- карбоновой кислоты путем окисления диметилсульфоксидом/оксалилхлоридом в метиленхлориде получили 0,15 г (20% от теории) трет-бутилового эфира (3RS, 4SR, 5SR)-4-[4-(3-бензилоксипропокси)фенил] -5-(2-морфолин-4- илэтоксиметил)-3-(нафталин-2-илацетил)пиперидин-1-карбоновой кислоты в виде светло-желтого масла; МС: 737 (М+Н)+.
(м) Аналогично примеру 73(г) из трет-бутилового эфира (3RS,4SR,5SR)-4-[4-(3- бензилоксипропокси)фенил]-5-(2-морфолин-4-илэтоксиметил)-3- (нафталин-2-илацетил)пиперидин-1-карбоновой кислоты путем отщепления BOC-защитной группы с помощью безводного бромида цинка в метиленхлориде получили 1-[(3RS, 4SR, 5SR)-4-[4-(3- бензилоксипропокси)фенил] -5-(2-морфолин-4-илэтоксиметил)пиперидин-3-ил]- 2-нафталин-2-илэтанона в виде желтого масла; МС: 637 (М+Н)+.
Пример 102.
(a) 0,30 г (0,5 ммоля) трет-бутилового эфира (3RS,4SR)-4-[4-(3-бензилоксипропокси)фенил] -3-(нафталин-2- илацетил)пиперидин-1-карбоновой кислоты [пример 100(в)] и 0,071 г (0,5 ммоля) гидрохлорида 3-(аминоокси)пропионовой кислоты [J. Am. Chem. Soc. 77, 2345, (1955)] перемешивали в течение 18 ч в атмосфере аргона при 60oC в 3 мл пиридина. Далее реакционную смесь сливали на ледяную воду, значение pH с помощью разбавленной соляной кислоты устанавливали равным 3, затем продукт трижды экстрагировали уксусным эфиром, органические фазы дважды промывали дистиллированной водой, сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием метиленхлорида и метанола. Таким путем получили 0,018 г (5% от теории) смеси трет-бутилового эфира (Е)- и (Z)-(3RS,4SR)-4-[4-(3-бензилоксипропокси)фенил] -3-[1-(2- карбоксиэтоксиимино)-2-нафталин-2-илэтил] пиперидин-1- карбоновой кислоты в виде светло-желтого масла [МС: 681 (М+Н)+] и 0, 21 г (69% от теории) смеси трет-бутилового эфира (Е)- и (Z) - (3RS, 4SR)-4-[4-(3-бензилоксипропокси)фенил]-3-(1- гидроксиимино-2-нафталин-2-илэтил)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 609 (М+Н)+.
(б) Аналогично примеру 22(м) из смеси трет-бутилового эфира (Е)- и (Z) - (3RS, 4SR)-4- [4-(3-бензилоксипропокси)фенил]-3-[1-(2-карбоксиэтоксиимино)-2- нафталин-2-илэтил]пиперидин-1-карбоновой кислоты путем отщепления BOC-защитной группы с помощью хлористого водорода в диоксане получили смесь (Е)- и (Z)-3-(1-[(3RS, 4SR)-4-[4-(3- бензилоксипропокси)фенил] пиперидин-3-ил]-2-нафталин-2- илэтилиденаминоокси)пропионовой кислоты в виде аморфной бежевой пены [МС: 581 (М+Н)+] и из смеси трет-бутилового эфира (Е)- и (Z)-(3RS, 4SR)-4-[4-(3-бензилоксипропокси)фенил] -3-(1- гидроксиимино-2-нафталин-2-илэтил)пиперидин-1- карбоновой кислоты путем отщепления BOC-защитной группы с помощью хлористого водорода в метаноле получили смесь (Е)- и (Z)-1- [(3RS, 4SR)-4-[4-(3-бензилоксипропокси)фенил] пиперидин-3-ил] -2- нафталин-2-илэтаноноксима в виде бесцветного твердого вещества; МС: 509 (М+Н)+.
Пример 103.
0,15 г (0,22 ммоля) смеси трет-бутилового эфира (Е)- и (Z)-(3RS,4SR)-4-[4-(3- бензилоксипропокси)фенил] -3-(1-метоксикарбонилметоксиимино-2- нафталин-2-илэтил)пиперидин-1-карбоновой кислоты [пример 90(п)] растворяли в 10 мл метанола, смешивали с 3,1-молярным раствором соляной кислоты в метаноле (4 ммоля) и реакционную смесь перемешивали в течение 7 ч при комнатной температуре. После добавления 1 мл (9 ммолей) едкого натра (28%-ного) при 5oC реакционную смесь перемешивали в течение 18 ч при комнатной температуре. Путем добавления по каплям 0,7 мл (8,75 ммоля) соляной кислоты (37%-ной) значение pH реакционного раствора устанавливали равным 1, фильтровали и растворитель отгоняли в высоком вакууме. Остаток суспендировали в 5 мл абс. этанола, фильтровали и фильтрат концентрировали. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием метиленхлорида, метанола и раствора аммиака (25%-ного). Таким путем получили 0,059 г (47% от теории) смеси (Е)- и (Z)-(1-[(3RS,4SR)-4-[4-(3- бензилоксипропокси)фенил] пиперидин-3-ил]-2-нафталин-2- илэтилиденаминоокси)уксусной кислоты в виде аморфной бежевой пены; МС: 567 (М+Н)+.
Пример 104.
Указанные ниже соединения получали благодаря тому, что аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси) фенил] -3-гидроксипиперидин-1-карбоновой кислоты [пример 86(о)] синтезировали соответствующие BOC-производные, которые без дальнейшей очистки и определения характеристик использовали в реакции отщепления BOC-группы с помощью хлористого водорода в метаноле аналогично примеру 22(м) либо с помощью бромида цинка в метиленхлориде аналогично примеру 10(б):
1) путем алкилирования 4-трифторметилбензилбромидом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(4- трифторметилбензилокси) пиперидина в виде бесцветного масла; МС: 500 (М+Н)+;
2) путем алкилирования 4-фторбензилбромидом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] - 3-(4-фторбензилокси)пиперидина в виде бесцветного масла; МС: 450 (М+Н)+;
3) путем алкилирования 2-хлорбензилбромидом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3- (2-хлорбензилокси)пиперидина в виде бесцветного масла; МС: 466 (М+Н)+;
4) путем алкилирования 4-бромбензилбромидом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(4- бромбензилокси)пиперидина в виде бесцветного масла; МС: 510 (М+Н)+;
5) путем алкилирования 3-бромбензилбромидом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(3-бромбензилокси)пиперидина в виде бесцветного масла; МС: 511 (М+Н)+;
6) путем алкилирования 4-иодбензилбромидом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(4-иодбензилокси)пиперидина в виде бесцветного масла; МС: 558 (М+Н)+;
7) путем алкилирования 2-трифторметилбензилбромидом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(2-трифторметилбензилокси) пиперидина в виде бесцветного масла; МС: 500 (М+Н)+;
8) путем алкилирования 3,5-диметилбензилбромидом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS,4RS)-4-[4-(3- бензилоксипропокси)фенил]-3-(3,5-диметилбензилокси)пиперидина в виде бесцветного масла; МС: 460 (М+Н)+;
9) путем алкилирования 2,4-диметилбензилхлоридом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил]-3-(2,4 - диметилбензилокси)пиперидина в виде бесцветного масла; МС: 460 (М+Н)+;
10) путем алкилирования 4-метилбензилбромидом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(4- метилбензилокси)пиперидина в виде бесцветного масла; МС: 446 (М+Н)+;
11) путем алкилирования 4-изопропилбензилхлоридом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(4-изопропилбензилокси)пиперидина в виде бесцветного масла; МС: 474 (М+Н)+;
12) путем алкилирования 4-трет-бутилбензилбромидом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(4-трет-бутилбензилокси)пиперидина в виде бесцветного масла; МС: 488 (М+Н)+;
13) путем алкилирования 2-метоксибензилхлоридом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(2-метоксибензилокси)пиперидина в виде бесцветного масла; МС: 462 (М+Н)+;
14) путем алкилирования 2-фторбензилбромидом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3- (2-фторбензилокси) пиперидина в виде бесцветного масла; МС: 450 (М+Н)+;
15) путем алкилирования 2-фтор-6-трифторметилбензилбромидом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS, 4RS)-4- [4-(3-бензилоксипропокси)фенил]-3-(2-фтор-6- трифторметилбензилокси)пиперидина в виде бесцветного масла; МС: 518 (М+Н)+;
16) путем алкилирования 2-бром-5-фторбензилбромидом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] - 3-(2-бром-5-фторбензилокси)пиперидина в виде бесцветного масла; МС: 528 (М+Н)+;
17) путем алкилирования 4-фтор-3-трифторметилбензилбромидом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(4-фтор-3-трифторметилбензилокси)пиперидина в виде бесцветного масла; МС: 518 (М+Н)+;
18) путем алкилирования 3,5-дитрифторметилбензилбромидом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] -3- (3, 5-бистрифторметилбензилокси) пиперидина в виде бесцветного масла; МС: 568 (М+Н)+;
19) путем алкилирования 2-фтор-3-метилбензилбромидом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил]-3-(2-фтор-3- метилбензилокси)пиперидина в виде бесцветного масла; МС: 464 (М+Н)+;
20) путем алкилирования 2-фтор-4- трифторметилбензилбромидом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS, 4RS)-4- [4-(3-бензилоксипропокси)фенил]-3-(2-фтор-4- трифторметилбензилокси)пиперидина в виде желтого масла; МС: 518 (М+Н)+;
21) путем алкилирования 2-фтор-5- трифторметилбензилбромидом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS, 4RS)-4- [4-(3-бензилоксипропокси)фенил]-3-(2-фтор-5- трифторметилбензилокси)пиперидина в виде желтоватого масла; МС: 518 (М+Н)+;
22) путем алкилирования 4-фтор-2- трифторметилбензилбромидом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS, 4RS)-4- [4-(3-бензилоксипропокси)фенил]-3-(4-фтор-2- трифторметилбензилокси)пиперидина в виде бесцветного масла; МС: 518 (М+Н)+;
23) путем алкилирования 3, 5-дихлорбензилхлоридом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] - 3-(3,5-дихлорбензилокси)пиперидина в виде бесцветного масла; МС: 500 (М+Н)+;
24) путем алкилирования 2,4-дихлорбензилхлоридом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] - 3-(2,4-дихлорбензилокси)пиперидина в виде бесцветного масла; МС: 500 (М+Н)+;
25) путем алкилирования 2-бромбензилхлоридом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(2-бромбензилокси) пиперидина в виде бесцветного масла; МС: 510 (М)+;
26) путем алкилирования 2,6-дихлорбензилхлоридом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS, 4RS)-4-[4-(3-бензилoкcипpoпoкcи)фенил] - 3-(2,6-диxлopбензилoкси)пиперидина в виде бесцветного масла; МС: 500 (М+Н)+;
27) путем алкилирования 3-фторбензилхлоридом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(3-фторбензилокси)пиперидина в виде бесцветного масла; МС: 450 (М+Н)+;
28) путем алкилирования 6-хлор-2-фторбензилхлоридом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(2-хлор-6-фторбензилокси)пиперидина в виде бесцветного масла; МС: 484 (М)+;
29) путем алкилирования 2-иодбензилхлоридом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(2-иодбензилокси)пиперидина в виде бесцветного масла; МС: 558 (М+Н)+;
30) путем алкилирования 3,4-дифторбензилбромидом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] - 3-(3,4-дифторбензилокси)пиперидина в виде бесцветного масла; МС: 468 (М+Н)+;
31) путем алкилирования 2,3-дифторбензилбромидом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] - 3-(2,3-дифторбензилокси) пиперидина в виде бесцветного масла; МС: 468 (М+Н)+;
32) путем алкилирования 2,5-дифторбензилбромидом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS, 4RS)-4- [4-(3-бензилоксипропокси)фенил] -3-(2,5-дифторбензилокси)пиперидина в виде бесцветного масла; МС: 468 (М+Н)+;
33) путем алкилирования 2,6-дифторбензилхлоридом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(2,6-дифторбензилокси)пиперидина в виде бесцветного масла; МС: 468 (М+Н)+;
34) путем алкилирования 2,4-дифторбензилбромидом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(2,4-дифторбензилокси)пиперидина в виде бесцветного масла; МС: 468 (М+Н)+;
35) путем алкилирования 3,5-дифторбензилбромидом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(3,5-дифторбензилокси)пиперидина в виде бесцветного масла; МС: 468 (М+Н)+;
36) путем алкилирования метиловым эфиром 4-бромметилбензойной кислоты, омыления метилового эфира во время водной обработки и последующего отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид 4-{ (3RS,4RS)- 4-[4-(3-бензилоксипропокси)фенил]пиперидина-3- илоксиметил}бензойной кислоты в виде бесцветного масла; МС: 476 (М+Н)+;
37) путем алкилирования 1-бромметил-4- трифторметоксибензолом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS, 4RS)-4- [4-(3-бензилоксипропокси)фенил]-3-(4-трифторметоксибензилокси) пиперидина в виде бесцветного масла; МС: 516 (М+Н)+;
38) путем алкилирования 3-бромметилбензонитрилом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид 3-{(3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] пиперидин-3- илоксиметил}бензонитрила в виде бесцветного масла; МС: 457 (М+Н)+;
39) путем алкилирования 4-бром-2-фторбензилбромидом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(4-бром-2-фторбензилокси)пиперидина в виде бесцветного масла; МС: 529 (М+Н)+;
40) путем алкилирования 3-хлорбензилбромидом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(3-хлорбензилокси)пиперидина в виде бесцветного масла; МС: 466 (М+Н)+;
41) путем алкилирования 3-хлор-2-фторбензилбромидом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил]- 3-(3-хлор-2-фторбензилокси)пиперидина в виде бесцветного масла; МС: 484 (М+Н)+;
42) путем алкилирования 3, 5-дибромбензилбромидом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] - 3-(3,5-дибромбензилокси)пиперидина в виде бесцветного масла; МС: 590 (М+Н)+;
43) путем алкилирования 2,5-диметоксибензилхлоридом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(2,5-диметоксибензилокси)пиперидина в виде бесцветного масла; МС: 492 (М+Н)+;
44) путем алкилирования 2-метилбензилхлоридом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(2- метилбензилокси)пиперидин в виде бесцветного масла; МС: 446 (М+Н)+;
45) путем алкилирования 3-бромметилпиридином и отщепления BOC-группы с помощью бромида цинка в метиленхлориде получили 3-[(3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] пиперидин-3-илоксиметил] пиридин в виде бесцветного масла; Rf 0,08 (SiO2, метиленхлорид:метанол = 98:2, экстракция в противотоке 5 об.% насыщенного аммиака);
46) путем алкилирования 4-метилтиобензилхлоридом [J. Org. Chem. (1988), 53(3), 561-569] и отщепления BOC-группы с помощью бромида цинка в метиленхлориде получили гидрохлорид (3RS,4RS)-4-[4-(3-бензилоксипропокси) фенил] -3-(4-метилсульфанилбензилокси)пиперидина в виде бесцветного масла; МС: 478 (М+Н)+;
47) путем алкилирования 5-хлорметилбензо[1,3]диоксолом и отщепления BOC-группы с помощью бромида цинка в метиленхлориде получили гидробромид (3RS, 4RS)-3- (бензо[1,3] диоксол-5-илметокси)-4-[4-(3-бензилоксипропокси)фенил] пиперидина в виде бесцветного масла; МС: 476 (М+Н)+;
48) путем алкилирования 4-метоксибензилхлоридом и отщепления BOC-группы с помощью бромида цинка в метиленхлориде получили (3RS,4RS)-4-[4- (3-бензилоксипропокси)фенил] -3-(4-метоксибензилокси)пиперидин в виде бесцветного масла; МС: 462 (М+Н)+;
49) путем алкилирования 3,4,5-триметоксибензилхлоридом и отщепления BOC-группы с помощью бромида цинка в метиленхлориде получили (3RS,4RS)-4-[4-(3- бензилоксипропокси)фенил] -3-(3,4, 5-триметоксибензилокси) пиперидин в виде бесцветного масла; МС: 522 (М+Н)+;
50) путем алкилирования 4-метокси-3-метилбензилхлоридом и отщепления BOC-группы с помощью бромида цинка в метиленхлориде получили (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(4-метокси-3-метилбензилокси) пиперидин в виде бесцветного масла; МС: 476 (М+Н)+;
51) путем алкилирования 3,5-диметоксибензилхлоридом и отщепления BOC-группы с помощью бромида цинка в метиленхлориде получили (3RS,4RS)-4- [4-(3-бензилоксипропокси)фенил] -3-(3,5-диметоксибензилокси) пиперидин в виде бесцветного масла; МС: 492 (М+Н)+;
52) путем алкилирования 2,3,5,6-тетраметилбензилхлоридом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил]-3-(2,3,5,6-тетраметилбензилокси) пиперидина в виде бесцветного масла; МС: 488 (М+Н)+;
53) путем алкилирования 3-метилбензилбромидом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(3-метилбензилокси) пиперидина в виде бесцветного масла; МС: 446 (М+Н)+;
54) путем алкилирования 4-хлорбензилхлоридом и отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3- (4-хлорбензилокси) пиперидина в виде бесцветного масла; МС: 466 (М+Н)+.
Пример 105.
Указанные ниже соединения получали благодаря тому, что аналогично примеру 12(б) путем взаимодействия соответствующих бензилбромидов с 3 эквивалентами соответствующих алкоголятов синтезировали соответствующие BOC-производные, которые без дальнейшей очистки и определения характеристик использовали в реакции отщепления BOC-группы с помощью хлористого водорода в метаноле аналогично примеру 22(м) либо с помощью бромида цинка в метиленхлориде аналогично примеру 10(б):
1) взаимодействием трет-бутилового эфира (3RS,4RS)-4-[4-(3- бензилоксипропокси)фенил] -3-(3-бромметилбензилокси)пиперидин-1- карбоновой кислоты с этанолом и отщеплением BOC-группы с помощью бромида цинка в метиленхлориде получили (3RS, 4RS)-4-[4-(3- бензилоксипропокси)фенил]-3-(3-этоксиметилбензилокси)пиперидин [МС: 490 (М+Н)+] и [3-[(3RS,4RS)-4-[4-(3- бензилоксипропокси)фенил]пиперидин-3-илоксиметил]фенил]метанола [МС: 479 (M+NH4)+] в каждом случае в виде бесцветного масла;
2) взаимодействием трет-бутилового эфира (3RS,4RS)-4-[4-(3- бензилоксипропокси)фенил] -3-(3-бромметилбензилокси) пиперидин-1-карбоновой кислоты с циклобутилметанолом и отщеплением BOC-группы с помощью хлористого водорода в метаноле получили (3RS, 4RS)-4-[4- (3-бензилоксипропокси)фенил]-3-(3-циклобутилметоксиметилбензилокси) пиперидин в виде бесцветного масла; МС: 530 (М+Н)+;
3) взаимодействием трет-бутилового эфира (3RS,4RS)-4-[4- (3-бензилоксипропокси)фенил] -3-(3-бромметилбензилокси)пиперидин-1- карбоновой кислоты с 3-фенилпропан-1-олом и отщеплением BOC-группы с помощью хлористого водорода в метаноле получили (3RS,4RS)-4-[4- (3-бензилоксипропокси)фенил]-3-[3-(3-фенилпропоксиметил)бензилокси] пиперидин в виде бесцветного масла; МС: 580 (М+Н)+;
4) взаимодействием трет-бутилового эфира (3RS,4RS)-4-[4-(3- бензилоксипропокси)фенил] -3-(3-бромметилбензилокси) пиперидин-1-карбоновой кислоты с 3,3-диметилбутан-1-олом и отщеплением BOC-группы с помощью хлористого водорода в метаноле получили (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил]-3-[3-(3,3- диметилбутоксиметил)бензилокси] пиперидин в виде бесцветного масла; МС: 546 (M+Н)+;
5) взаимодействием трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил]-3-(3- бромметилбензилокси)пиперидин-1-карбоновой кислоты с пиридин-3- илметанолом и отщеплением BOC-группы с помощью хлористого водорода в метаноле получили 3-[3-[(3RS,4RS)-4-[4-(3- бензилоксипропокси)фенил] пиперидин-3-илоксиметил] бензилоксиметил] пиридин в виде бесцветного масла; МС: 553 (М+Н)+;
6) взаимодействием трет-бутилового эфира (3RS,4RS)-4-[4-(3- бензилоксипропокси)фенил]-3-(3-бромметилбензилокси)пиперидин-1- карбоновой кислоты с пиридин-4-илметанолом и отщеплением BOC-группы с помощью хлористого водорода в метаноле получили 4-[3- [(3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил]пиперидин-3- илоксиметил] бензилоксиметил] пиридин в виде бесцветного масла; МС: 553 (М+Н)+;
7) взаимодействием трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил]-3-(3- бромметилбензилокси)пиперидин-1-карбоновой кислоты с 2-пиридин- 2-илэтанолом и отщеплением BOC-группы с помощью хлористого водорода в метаноле получили 2-[2-[3-[(3RS,4RS)-4-[4-(3- бензилоксипропокси)фенил]пиперидин-3-илоксиметил]бензилокси] этил]пиридин в виде бесцветного масла; МС: 567 (М+Н)+;
8) взаимодействием трет-бутилового эфира (3RS,4RS)-4-[4-(3- бензилоксипропокси)фенил] -3-(4-бромметилбензилокси) пиперидин-1- карбоновой кислоты с циклобутилметанолом и отщеплением BOC-группы с помощью хлористого водорода в метаноле получили (3RS,4RS)-4-[4- (3-бензилоксипропокси)фенил]-3-(4-циклобутилметоксиметилбензилокси) пиперидин в виде бесцветного масла; МС: 530 (М+Н)+;
9) взаимодействием трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] - 3-(4-бромметилбензилокси)пиперидин-1- карбоновой кислоты с 3-фенилпропан-1-олом и отщеплением BOC-группы с помощью хлористого водорода в метаноле получили (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил]-3-[4-(3- фенилпропоксиметил)бензилокси] пиперидин в виде бесцветного масла; МС: 580 (М+Н)+;
10) взаимодействием трет-бутилового эфира (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил]-3-(4- бромметилбензилокси)пиперидин-1-карбоновой кислоты с 3,3-диметилбутан-1-олом и отщеплением BOC-группы с помощью хлористого водорода в метаноле получили (3RS,4RS)-4-[4-(3-бензилоксипропокси) фенил]-3-[4-(3,3-диметилбутоксиметил)бензилокси] пиперидин в виде бесцветного масла; МС: 546 (М+Н)+;
11) взаимодействием трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(4-бромметилбензилокси)пиперидин-1-карбоновой кислоты с пиридин-3-илметанолом и отщеплением BOC-группы с помощью хлористого водорода в метаноле получили 3-[4-[(3RS,4RS)-4-[4- (3-бензилоксипропокси)фенил]пиперидин-3-илоксиметил] бензилоксиметил]пиридин в виде бесцветного масла; МС: 553 (М+Н)+;
12) взаимодействием трет-бутилового эфира (3RS,4RS)-4-[4-(3- бензилоксипропокси)фенил]-3-(4-бромметилбензилокси)пиперидин-1- карбоновой кислоты с пиридин-4-илметанолом и отщеплением BOC-группы с помощью хлористого водорода в метаноле получили 4-[4- [(3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил]пиперидин-3- илоксиметил] бензилоксиметил] пиридин в виде бесцветного масла; МС: 553 (М+Н)+;
13) взаимодействием трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил]-3-(4- бромметилбензилокси)пиперидин-1-карбоновой кислоты с 2-пиридин-2- илэтанолом и отщеплением BOC-группы с помощью хлористого водорода в метаноле получили 2-[2-[4-[(3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] пиперидин-3-илоксиметил]бензилокси]этил]пиридин в виде бесцветного масла; МС: 567 (М+Н)+;
14) взаимодействием трет-бутилового эфира (3RS,4RS)-4-[4-(3- бензилоксипропокси)фенил] -3-(2-бромметилбензилокси) пиперидин-1- карбоновой кислоты с 3-фенилпропан-1-олом и отщеплением BOC-группы с помощью хлористого водорода в метаноле получили (3RS,4RS)-4-[4- (3-бензилоксипропокси)фенил]-3-[2-(3- фенилпропоксиметил)бензилокcи] пиперидин в виде бесцветного масла; МС: 580 (М+Н)+;
15) взаимодействием трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил]-3-(2- бромметилбензилокси)пиперидин-1-карбоновой кислоты с 3,3-диметилбутан-1-олом и отщеплением BOC-группы с помощью хлористого водорода в метаноле получили (3RS,4RS)-4-[4-(3- бензилоксипропокси)фенил]-3-[2-(3, 3- диметилбутоксиметил)бензилокси]пиперидин в виде бесцветного масла; МС: 546 (М+Н)+;
16) взаимодействием трет-бутилового эфира (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил]-3-(2- бромметилбензилокси)пиперидин-1-карбоновой кислоты с пиридин-3- илметанолом и отщеплением BOC-группы с помощью хлористого водорода в метаноле получили 3-[2-[(3RS,4RS)-4-[4-(3- бензилоксипропокси)фенил] пиперидин-3-илоксиметил] бензилоксиметил]пиридин в виде бесцветного масла; МС: 553 (М+Н)+;
17) взаимодействием трет-бутилового эфира (3RS,4RS)-4-[4-(3- бензилоксипропокси)фенил]-3-(2-бромметилбензилокси)пиперидин-1- карбоновой кислоты с пиридин-4-илметанолом и отщеплением BOC-группы с помощью хлористого водорода в метаноле получили 4-[2- [(3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил]пиперидин-3- илоксиметил] бензилоксиметил] пиридин в виде бесцветного масла; МС: 553 (М+Н)+;
18) взаимодействием трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил]-3-(2- бромметилбензилокси)пиперидин-1-карбоновой кислоты с 2-пиридин-2- илэтанолом и отщеплением BOC-группы с помощью хлористого водорода в метаноле получили 2-[2-[2-[(3RS,4RS)-4-[4-(3- бензилоксипропокси)фенил]пиперидин-3-илоксиметил] бензилокси] этил]пиридин в виде бесцветного масла; МС: 567 (М+Н)+;
19) взаимодействием трет-бутилового эфира (3RS,4RS)-4-[4-(3- бензилоксипропокси)фенил]-3-(2-бромметилбензилокси)пиперидин-1- карбоновой кислоты с циклобутилметанолом и отщеплением BOC-группы с помощью хлористого водорода в метаноле получили (3RS,4RS)-4-[4- (3-бензилоксипропокси)фенил]-3-(2- циклобутилметоксиметилбензилокси)пиперидин в виде бесцветного масла; МС: 530 (М+Н)+.
Использованные в качестве исходных веществ бензилбромиды получали путем алкилирования трет-бутилового эфира (3RS, 4RS)-4-[4- (3-бензилоксипропокси)фенил] -3-гидроксипиперидин-1-карбоновой кислоты [пример 86(о] соответствующим бисбромметилбензолом аналогично примеру 1(ж), но с применением 4 эквивалентов дибромида и путем осторожного гидролиза реакционного раствора ледяным раствором бикарбоната натрия:
(а) алкилированием 1,3- бисбромметилбензолом получили трет-бутиловый эфир (3RS, 4RS)-4-[4- (3-бензилоксипропокси)фенил]-3-(3-бромметилбензилокси)пиперидин-1- карбоновой кислоты в виде бесцветной смолы; МС: 624, 626 (М+Н)+;
(б) алкилированием 1, 4-бисбромметилбензолом получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(4- бромметилбензилокси)пиперидин-1-карбоновой кислоты в виде желтоватого масла; МС: 643, 645 (M+NH4)+;
(в) алкилированием 1,2- бисбромметилбензолом получили трет-бутиловый эфир (3RS, 4RS)-4-[4- (3-бензилоксипропокси)фенил]-3-(2-бромметилбензилокси)пиперидин-1- карбоновой кислоты в виде бесцветного масла; МС: 624, 626 (М+Н)+.
Пример 106.
Указанные ниже соединения получали благодаря тому, что аналогично примеру 1(ж) путем взаимодействия соответствующих бензилбромидов с 3 эквивалентами соответствующих алкоголятов синтезировали соответствующие BOC-производные, которые, если не указано иное, без дальнейшей очистки и определения характеристик использовали в реакции отщепления BOC-группы с помощью хлористого водорода в метаноле аналогично примеру 22(м).
1) Взаимодействием трет-бутилового эфира (3RS,4RS)-4-[4-(3- бензилоксипропокси)фенил] -3-(6-бромметилнафталин-2-илметокси)пиперидин-1- карбоновой кислоты с (RS)-(2,2-диметил[1,3]диоксолан-4-ил)метанолом с последующим одновременным отщеплением BOC- и диоксолановой групп получили смесь (3RS,4RS)- и (3SR, 4SR)-4-[4-(3-бензилоксипропокси)фенил]-3-[6-[(RS)- 2,3-дигидроксипропоксиметил] нафталин-2-илметокси] пиперидина в виде бесцветного масла; МС: 586 (М+Н)+.
2) Взаимодействием трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил]-3- (7-бромметилнафталин-2-илметокси)пиперидин-1-карбоновой кислоты с (RS)-(2,2-диметил[1, 3]диоксолан-4-ил)метанолом с последующим одновременным отщеплением BOC- и диоксолановой групп получили смесь (3RS,4RS)- и (3SR, 4SR)-4-[4-(3-бензилоксипропокси)фенил]-3- [7-[(RS)-2, 3-дигидроксипропоксиметил] нафталин-2-илметокси] пиперидина в виде бесцветного масла; МС: 586 (М+Н)+.
3) Взаимодействием трет-бутилового эфира (3RS, 4RS)-4-[4-(3- бензилоксипропокси)фенил]-3-(7-бромметилнафталин-2-илметокси) пиперидин-1-карбоновой кислоты с рац.-2-[(тетрагидро-2Н-пиран-2- ил)окси]-1-этанолом получили смесь трет-бутилового эфира (3RS, 4RS)- и (3SR, 4SR)-4-[4-(3-бензилоксипропокси)фенил] -3-{ 7- [2-[(RS)-тетрагидропиран-2-илокси]этоксиметил]нафталин-2- илметокси} пиперидин-1-карбоновой кислоты [бесцветное масло, МС: 740 (М+Н)+] и трет-бутиловый эфир (3RS,4RS)-4-[4-(3- бензилоксипропокси)фенил]-3-(7-диметиламинометилнафталин-2- илметокси)пиперидин-1-карбоновой кислоты [побочный продукт, бесцветное масло, МС: 639 (М)+]. В результате одновременного отщепления BOC- и тетрагидропиранильной групп основного продукта был получен 2-(7-{(3RS, 4RS)-4-[4-(3- бензилоксипропокси)фенил]пиперидин-3-илоксиметил} нафталин-2- илметокси)этанол в виде бесцветного масла; МС: 556 (М+Н)+. Отщеплением BOC-группы побочного продукта получили (7-{(3RS,4RS)- 4-[4-(3-бензилоксипропокси)фенил]пиперидин-3-илоксиметил}нафталин-2-илметил) диметиламин в виде бесцветного масла; МС: 539 (М+Н)+.
4) Взаимодействием смеси трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3- (8-бромметилнафталин-2-илметокси)пиперидин-1-карбоновой кислоты и трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси) фенил] -3-(7-бромметилнафталин-1-илметокси)пиперидин-1- карбоновой кислоты с (RS)-(2,2-диметил[1,3] диоксолан-4- ил) метанолом с последующим одновременным отщеплением BOC- и диоксолановой групп получили смесь (3RS, 4RS)- и (3SR,4SR)-4-[4-(3- бензилоксипропокси)фенил]-3-[8-[(RS)-2,3-дигидроксипропоксиметил] нафталин-2-илметокси] пиперидина и (3RS,4RS)- и (3SR, 4SR)-4-[4- (3-бензилоксипропокси)фенил] -3-[7-[(RS)- 2,3-дигидроксипропоксиметил] нафталин-1-илметокси] пиперидина в виде бесцветного масла; МС: 586 (М+Н)+.
Использованные в качестве исходных веществ нафтилметилбромиды получали путем алкилирования трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси) фенил] -3-гидроксипиперидин-1-карбоновой кислоты [пример 86(о)] соответствующим бисбромметилнафталином аналогично примеру 1(ж), но с применением 4 эквивалентов дибромида и путем осторожного гидролиза реакционного раствора ледяным раствором бикарбоната натрия:
(а) алкилированием 2,6-бисбромметилнафталином [J. Chem. Soc. (1961), 3741-3748] получили трет-бутиловый эфир (3RS,4RS)-4- [4-(3-бензилоксипропокси)фенил] -3-(6-бромметилнафталин-2- илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 675 (М+Н)+;
(б) алкилированием 2,7-бисбромметилнафталином [J. Am. Chem. Soc. (1979), 4259-4267] получили трет-бутиловый эфир (3RS,4RS)-4-[4-(3-бензилоксипропокси) фенил] -3-(7-бромметилнафталин-2-илметокси)пиперидин-1- карбоновой кислоты в виде бесцветного масла; МС: 675 (М+Н)+;
(в) алкилированием 1,7-бисбромметилнафталином [Chem. Ber. 91, 1981 (1958)] получили смесь трет-бутилового эфира (3RS, 4RS)-4-[4-(3- бензилоксипропокси)фенил]-3-(8-бромметилнафталин-2-илметокси) пиперидин-1-карбоновой кислоты и трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси) фенил] -3-(7- бромметилнафталин-1-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 675 (М+Н)+.
Пример 107.
Указанные ниже соединения получали благодаря тому, что аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS,4RS)-4-[4-(3- гидроксипропокси)фенил] -3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты [пример 57 (в)] синтезировали соответствующие BOC-производные, которые без дальнейшей очистки и определения характеристик использовали в реакции отщепления BOC-группы с помощью хлористого водорода в метаноле аналогично примеру 22(м):
1) алкилированием 4-фторбензилбромидом и отщеплением BOC-группы получили гидрохлорид (3RS, 4RS)-4-{ 4- [3- (4- фторбензилокси)пропокси]фенил}-3-(нафталин-2- илметокси)пиперидина в виде бесцветного масла; МС: 500 (М+Н)+;
2) алкилированием 2-хлорбензилбромидом и отщеплением BOC-группы получили (3RS, 4RS)-4-{ 4-[3-(2-хлорбензилокси)пропокси] фенил} - 3-(нафталин-2-илметокси)пиперидин в виде бесцветного масла; МС: 516 (М)+;
3) алкилированием 2,3,4,5,6-пентафторбензилбромидом и отщеплением BOC-группы получили (3RS, 4RS)-3-(нафталин-2-илметокси)-4-{ 4- [3-(2,3,4,5,6-пентафторбензилокси)пропокси] фенил} пиперидин в виде бесцветного масла; МС: 572 (М+Н)+;
4) алкилированием 4- бромбензилбромидом и отщеплением BOC-группы получили гидрохлорид (3RS, 4RS)-4-{ 4-[3-(4-бромбензилокси)пропокси] фенил}-3- (нафталин-2-илметокси)пиперидина в виде бесцветного масла; МС: 560 (М)+;
5) алкилированием 3-бромбензилбромидом и отщеплением BOC-группы получили гидрохлорид (3RS, 4RS)-4-{ 4-[3-(3- бромбензилокси)пропокси] фенил} -3-(нафталин-2- илметокси)пиперидина в виде бесцветного масла; МС: 560 (М+Н)+;
6) алкилированием 4-иодбензилбромидом и отщеплением BOC-группы получили гидрохлорид (3RS, 4RS)-4-{ 4- [3-(4- иодбензилокси)пропокси] фенил} -3-(нафталин-2-илметокси)пиперидина в виде бесцветного масла; МС: 608 (М+Н)+;
7) алкилированием 2-трифторметилбензилбромидом и отщеплением BOC-группы получили гидрохлорид (3RS, 4RS)-3-(нaфтaлин-2-илметoкcи)-4-{4-[3-(2- трифторметилбензилокси)пропокси] фенил}пиперидина в виде бесцветного масла; МС: 550 (М+Н)+;
8) алкилированием 3-трифторметилбензилбромидом и отщеплением BOC-группы получили гидрохлорид (3RS, 4RS)-3-(нафталин- 2-илметокси)-4-{4-[3-(3-трифторметилбензилокси)пропокси] фенил} пиперидина в виде бесцветного масла; МС: 550 (М+Н)+;
9) алкилированием 4-трифторметилбензилбромидом и отщеплением BOC-группы получили гидрохлорид (3RS, 4RS)-3-(нафталин-2-илметокси)-4- {4-[3-(4-трифторметилбензилокси)пропокси] фенил} пиперидина в виде бесцветного масла; МС: 550 (М+Н)+;
10) алкилированием 2-фторбензилбромидом и отщеплением BOC-группы получили (3RS,4RS)-4-{4-[3-(2-фторбензилокси)пропокси]фенил}-3-(нафталин-2- илметокси)пиперидин в виде бесцветного масла; МС: 500 (М+Н)+;
11) алкилированием 2-метилбензилхлоридом и отщеплением BOC-группы получили гидрохлорид (3RS,4RS)-4-{4-[3-(2-метилбензилокси)пропокси]фенил} -3-(нафталин-2-илметокси)пиперидина в виде бесцветного масла; МС: 496 (М+Н)+;
12) алкилированием 3,5-диметилбензилбромидом и отщеплением BOC-группы получили гидрохлорид (3RS, 4RS)-4-{ 4-[3-(3, 5-диметилбензилокси)пропокси] фенил} -3-(нафталин-2-илметокси)пиперидина в виде бесцветного масла; МС: 510 (М+Н)+;
13) алкилированием 3-метоксибензилхлоридом и отщеплением BOC-группы получили гидрохлорид (3RS,4RS)-4-{4-[3- (3-метоксибензилокси)пропокси]фенил} -3-(нафталин-2- илметокси)пиперидина в виде бесцветного масла; МС: 512 (М+Н)+;
14) алкилированием 4-изопропилбензилхлоридом и отщеплением BOC-группы получили гидрохлорид (3RS, 4RS)-4-{ 4-[3-(4-изопропилбензилокси) пропокси] фенил} -3-(нафталин-2-илметокси)пиперидина в виде бесцветного масла; МС: 524 (М+Н)+;
15) алкилированием 2,4-диметилбензилхлоридом и отщеплением BOC-группы получили гидрохлорид (3RS, 4RS)-4-{ 4-[3-(2, 4-диметилбензилокси)пропокси] фенил} -3-(нафталин-2-илметокси)пиперидина в виде бесцветного масла; МС: 510 (М+Н)+;
16) алкилированием 4-метилбензилбромидом и отщеплением BOC-группы получили гидрохлорид (3RS,4RS)-4-{4-[3-(4- метилбензилокси)пропокси]фенил}-3-(нафталин-2- илметокси)пиперидина в виде бесцветного масла; МС: 496 (М+Н)+;
17) алкилированием 4-трет-бутилбензилбромидом и отщеплением BOC-группы получили гидрохлорид (3RS, 4RS)-4-{ 4-[3-(4-трет-бутилбензилокси)пропокси] фенил} -3-(нафталин-2-илметокси)пиперидина в виде бесцветного масла; МС: 538 (М+Н)+;
18) алкилированием 2,3,5,6-тетраметилбензилхлоридом и отщеплением BOC-группы получили гидрохлорид (3RS, 4RS)-3-(нафталин-2-илметокси)-4-{4-[3-(2,3,5,6- тетраметилбензилокси)пропокси]фенил}пиперидина в виде бесцветного масла; МС: 538 (М+Н)+;
19) алкилированием 3, 5-дихлорбензилхлоридом и отщеплением BOC-группы получили гидрохлорид (3RS,4RS)-4-{4-[3-(3,5-дихлорбензилокси)пропокси]фенил} -3- (нафталин-2-илметокси)пиперидина в виде бесцветного масла; МС: 550 (М+Н)+;
20) алкилированием 2,4-дихлорбензилхлоридом и отщеплением BOC-группы получили гидрохлорид (3RS,4RS)-4-{4-[3- (2,4-дихлорбензилокси)пропокси]фенил} -3-(нафталин-2- илметокси)пиперидина в виде бесцветного масла; МС: 550 (М+Н)+;
21) алкилированием 2,6-дихлорбензилхлоридом и отщеплением BOC-группы получили гидрохлорид (3RS,4RS)-4-{4-[3-(2,6-дихлорбензилокси)пропокси] фенил} -3-(нафталин-2-илметокси)пиперидина в виде бесцветного масла; МС: 550 (М+Н)+;
22) алкилированием 2, 5-дихлорбензилхлоридом и отщеплением BOC-группы получили гидрохлорид (3RS,4RS)-4-{4-[3-(2,5-дихлорбензилокси)пропокси]фенил-} -3- (нафталин-2-илметокси)пиперидина в виде бесцветного масла; МС: 550 (М+Н)+;
23) алкилированием 2-хлор-6-фторбензилхлоридом и отщеплением BOC-группы получили гидрохлорид (3RS,4RS)-4-{4-[3-(2- хлор-6-фторбензилокси)пропокси] фенил}-3-(нафталин-2- илметокси)пиперидина в виде бесцветного масла; МС: 534 (М+Н)+;
24) алкилированием 2-иодбензилхлоридом и отщеплением BOC-группы получили гидрохлорид (3RS, 4RS)-4-{ 4-[3-(2- иодбензилокси)пропокси] фенил} -3-(нафталин-2-илметокси)пиперидина в виде бесцветного масла; МС: 608 (М+Н)+;
25) алкилированием 2-бромбензилхлоридом и отщеплением BOC-группы получили гидрохлорид (3RS, 4RS)-4-{ 4-[3-(2-бромбензилокси)пропокси] фенил}-3- (нафталин-2-илметокси)пиперидина в виде бесцветного масла; МС: 560 (М+Н)+;
26) алкилированием 4-хлорбензилхлоридом и отщеплением BOC-группы получили гидрохлорид (3RS, 4RS)-4-{4-[3-(4- хлорбензилокси)пропокси]фенил}-3-(нафталин-2- илметокси)пиперидина в виде бесцветного масла; МС: 517 (М+Н)+;
27) алкилированием 4-метилтиобензилхлоридом [J. Org. Chem. (1988), 53(3), 561-569] и отщеплением BOC-группы получили гидрохлорид (3RS,4RS)-4-{ 4-[3-(4-метилсульфанилбензилокси)пропокси] фенил} - 3-(нафталин-2-илметокси) пиперидина в виде бесцветного масла; МС: 528 (М+Н)+;
28) алкилированием смесью 3- и 4-винилбензилхлоридa и отщеплением BOC-группы получили смесь гидрохлорида (3RS, 4RS)-3- (нaфтaлин-2-илметокси)-4-{ 4-[3-(3- и 4-винилбензилокси)пропокси] фенил}пиперидина в виде бесцветного масла; МС: 508 (М+Н)+;
29) алкилированием 4- метоксибензилхлоридом и отщеплением BOC-группы получили гидрохлорид (3RS,4RS)-4-{4-[3-(4-метоксибензилокси)пропокси] фенил} -3-(нафталин-2-илметокси)пиперидина в виде бесцветного масла; МС: 512 (М+Н)+;
30) алкилированием 2,4-диметоксибензилхлоридом и отщеплением BOC-группы получили гидрохлорид (3RS, 4RS)-4-{4-[3-(2,4-диметоксибензилокси)пропокси] фенил} -3-(нафталин-2-илметокси)пиперидина в виде бесцветного масла; МС: 542 (М+Н)+;
31) алкилированием 3,4,5-триметоксибензилхлоридом и отщеплением BOC-группы получили гидрохлорид (3RS,4RS)-3-(нaфтaлин-2-илметoкcи)-4-{4-[3-(3,4,5- триметоксибензилокси)пропокси] фенил} пиперидина в виде бесцветного масла; МС: 572 (М+Н)+;
32) алкилированием 5-хлорметилбензо[1,3]диоксолом и отщеплением BOC-группы получили гидрохлорид (3RS,4RS)-4-{4-[3- (бензо[1,3]диоксол-5-илметокси)пропокси] фенил} -3-(нафталин-2- илметокси)пиперидина в виде бесцветного масла; МС: 526 (М+Н)+;
33) алкилированием 3-хлор-4-метоксибензилхлоридом и отщеплением BOC-группы получили гидрохлорид (3RS, 4RS)-4-{4-[3-(3-хлор-4-метоксибензилокси) пропокси]фенил}-3-(нафталин-2-илметокси)пиперидина в виде бесцветного масла; МС: 546 (М+Н)+;
34) алкилированием 3-метилбензилбромидом и отщеплением BOC-группы получили гидрохлорид (3RS, 4RS)-4-{ 4-[3-(3-метилбензилокси)пропокси] фенил}-3- (нафталин-2-илметокси)пиперидина в виде бесцветного масла; МС: 496 (М+Н)+;
35) алкилированием 3-фторбензилхлоридом и отщеплением BOC-группы получили гидрохлорид (3RS, 4RS)-4-{4-[3-(3- фторбензилокси)пропокси]фенил}-3-(нафталин-2-илметокси)пиперидина в виде бесцветного масла; МС: 500 (М+Н)+;
36) алкилированием 2-метоксибензилхлоридом и отщеплением BOC-группы получили (3RS, 4RS)-4-{ 4-[3-(2-метоксибензилокси)пропокси] фенил} -3-(нафталин-2-илметокси)пиперидин в виде бесцветного масла; МС: 512 (М+Н)+;
37) алкилированием 2,5-диметилбензилхлоридом и отщеплением BOC-группы получили гидрохлорид (3RS, 4RS)-4-{ 4-[3-(2,5-диметилбензилокси) пропокси] фенил} -3-(нафталин-2-илметокси)пиперидина в виде бесцветного масла; МС: 510 (М+Н)+;
38) алкилированием 4-этилбензилхлоридом и отщеплением BOC-группы получили гидрохлорид (3RS, 4RS)-4-{ 4-[3-(4-этилбензилокси)пропокси] фенил}-3- (нафталин-2-илметокси)пиперидина в виде бесцветного масла; МС: 510 (М+Н)+.
Пример 108.
Указанные ниже соединения получали благодаря тому, что аналогично примеру 44(д) путем алкилирования трет-бутилового эфира (3RS,4RS)-4-{4-[3-(2-гидроксибензилокси)пропокси] фенил} -3-(нафталин-2- илметокси) пиперидин-1-карбоновой кислоты синтезировали соответствующие BOC-производные, которые без дальнейшей очистки и определения характеристик использовали в реакции отщепления BOC-группы с помощью бромида цинка в метиленхлориде аналогично примеру 10(б):
1) алкилированием 1-бромпропаном и отщеплением BOC-группы получили гидробромид (3RS, 4RS)-4-{ 4-[3-(2- пропоксибензилокси)пропокси] фенил)-3-(нафталин-2- илметокси)пиперидина в виде бесцветного масла; МС: 540 (М+Н)+;
2) алкилированием 1-бромбутаном и отщеплением BOC-группы получили гидробромид (3RS, 4RS)-4-{ 4-[3-(2-бутоксибензилокси)пропокси] фенил} -3-(нафталин-2-илметокси)пиперидина в виде бесцветного масла; МС: 554 (М+Н)+;
3) алкилированием бромметилциклопропаном и отщеплением BOC-группы получили гидробромид (3RS,4RS)-4-{4-[3-(2-циклопропилметоксибензилокси)пропокси] фенил} -3-(нафталин-2-илметокси)пиперидина в виде бесцветного масла; МС: 552 (М+Н)+;
4) алкилированием этилиодидом и отщеплением BOC-группы получили гидробромид (3RS, 4RS)-4-{4- [3-(2-этоксибензилокси)пропокси] фенил}-3-(нафталин-2-илметокси)пиперидина в виде бесцветного масла; МС: 526 (М+Н)+;
5) алкилированием бромметилциклобутаном и отщеплением BOC-группы получили гидробромид (3RS, 4RS)-4-{4-[3- (2-циклобутилметоксибензилокси)пропокси] фенил}-3-(нафталин-2- илметокси)пиперидина в виде бесцветного масла; МС: 566 (М+Н)+;
6) алкилированием изобутилбромидом и отщеплением BOC-группы получили гидробромид (3RS, 4RS)-4-{ 4-[3-(2-изобутоксибензилокси)пропокси] фенил}-3-(нафталин-2-илметокси)пиперидина в виде бесцветного масла; МС: 554 (М+Н)+;
7) алкилированием бензилбромидом и отщеплением BOC-группы получили гидробромид (3RS, 4RS)-4-{ 4-[3- (2-бензилоксибензилокси)пропокси] фенил}-3-(нафталин-2- илметокси)пиперидина в виде бесцветного масла; МС: 588 (М+Н)+;
8) алкилированием 4-бром-1-бутеном и отщеплением BOC-группы получили гидробромид (3RS, 4RS)-4-{4-[3-(2-бут-3- енилоксибензилокси)пропокси]фенил} -3-(нафталин-2- илметокси)пиперидина в виде бесцветного масла; МС: 552 (М+Н)+;
9) алкилированием аллилбромидом и отщеплением BOC-группы получили гидробромид (3RS, 4RS)-4-{ 4-[3-(2-аллилоксибензилокси)пропокси] фенил} -3-(нафталин-2-илметокси)пиперидина в виде бесцветного масла; МС: 538 (М+Н)+;
10) алкилированием бромциклопропаном и отщеплением BOC-группы получили гидробромид (3RS,4RS)-4-{4-[3- (2-циклопропилоксибензилокси)пропокси]фенил} -3-(нафталин-2- илметокси)пиперидина в виде бесцветного масла; МС: 538 (М+Н)+.
Использованный в качестве исходной субстанции трет-бутиловый эфир (3RS, 4RS)-4-{ 4-[3-(2-гидроксибензилокси)пропокси] фенил}-3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты получали следующим образом:
(а) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS, 4RS)-4-[4-(3-гидроксипропокси)фенил]-3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты [пример 57(в)] 1-хлорметил-2-(2-триметилсилилэтоксиметокси) бензолом [пример 17(в)] трет-бутиловый эфир (3RS, 4RS)-3-(нафталин-2-илметокси)- 4-(4-{ 3-[2-(2-триметилсиланилэтоксиметокси)бензилокси] пропокси} фенил) пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 746 (M+NH4)+.
(б) Раствор из 50 мг (0,069 ммоля) трет-бутилового эфира (3RS,4RS)-3-(нафталин-2- илметокси)-4-(4- { 3- [2-(2-триметилсиланилэтоксиметокси)бензилокси] пропокси} фенил)пиперидин-1-карбоновой кислоты в 0,5 мл метанола охлаждали в атмосфере аргона до 0oC и смешивали с 69 мкл (0,138 ммоля) 2 н. раствора хлористого водорода в метаноле. После этого давали нагреться до комнатной температуры, а затем перемешивали в течение 1 ч. Для дальнейшей переработки реакционный раствор смешивали со смесью 95:5 метиленхлорида и метанола (экстракция в противотоке 5 об.% насыщенного аммиака) и упаривали досуха при пониженном давлении. Остаток очищали хроматографией на силикагеле с использованием смеси 3:1 гексана и уксусного эфира в качестве элюента. Таким путем получили 33,1 мг (81% от теории) трет-бутилового эфира (3RS, 4RS)-4-{4-[3-(2- гидроксибензилокси)пропокси]фенил}-3 (нафталин-2- илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 598 (М+Н)+.
Пример 109.
Путем отщепления BOC-группы с помощью хлористого водорода в метаноле аналогично примеру 22(м) или с помощью бромида цинка в метиленхлориде аналогично примеру 10(б) получали следующие соединения:
1) из трет-бутилового эфира (3R,4s,5S)-4-[4-(3-бензилоксипропокси)фенил] -3, 5-бис(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты с помощью хлористого водорода в метаноле получили гидрохлорид (3R,4s,5S)-4-[4-(3- бензилоксипропокси)фенил] -3,5-бис(нафталин-2-илметокси) пиперидина в виде бесцветного твердого вещества; МС: 638 (М+Н)+;
2) из трет-бутилового эфира (3RS,4SR, 5SR)-4-[4-(3- бензилоксипропокси)фенил]-5-гидрокси-3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты с помощью хлористого водорода в метаноле получили (3RS,4SR,5SR)-4-[4-(3- бензилоксипропокси) фенил] -3-(нафталин-2-илметокси)пиперидин-5-ол в виде бесцветного масла; МС: 498 (М+Н)+;
3) из трет-бутилового эфира (3R,4s,5S)-4-[4-(3-бензилоксипропокси)фенил] -3, 5-бис(1,4- диметоксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3R,4s,5S)-4-[4-(3-бензилоксипропокси)фенил]-3,5-бис (1, 4- диметоксинафталин-2-илметокси)пиперидин в виде бесцветного воска; МС: 758 (М+Н)+;
4) из трет-бутилового эфира (3RS,4SR,5SP)-4-[4- (3-бензилоксипропокси)фенил] -3-(1, 4-диметоксинафталин-2- илметокси)-5-гидроксипиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS, 4SR, 5SR)-4-[4-(3- бензилоксипропокси)фенил]-3-(1, 4-диметоксинафталин-2- илметокси)пиперидин-5-ол в виде бесцветного масла; МС: 558 (М+Н)+;
5) из трет-бутилового эфира (3R, 4s, 5S)-4-[4-(3- бензилоксипропокси)фенил] -3, 5-бис(2,4-дихлорбензилокси)пиперидин-1- карбоновой кислоты с помощью хлористого водорода в метаноле получили гидрохлорид (3R,4s,5S)-4- [4-(3-бензилоксипропокси)фенил] -3,5-бис(2, 4- дихлорбензилокси)пиперидина в виде бесцветного твердого вещества; МС: 676 (М+Н)+;
6) из трет-бутилового эфира (3RS,4SR,5SR)-4-[4- (3-бензилоксипропокси)фенил]-3-(2, 4-дихлорбензилокси)-5- гидроксипиперидин-1-карбоновой кислоты с помощью хлористого водорода в метаноле получили гидрохлорид (3RS,4SR, 5SR)-4-[4-(3- бензилоксипропокси)фенил]-3-(2, 4-дихлорбензилокси)пиперидин-5- ола в виде бесцветного масла; МС: 516 (М+Н)+;
7) из трет-бутилового эфира (3R,4s,5S)-4-[4-(3-бензилоксипропокси)фенил] -3,5-бис (2, 5-дифторбензилокси)пиперидин-1-карбоновой кислоты с помощью хлористого водорода в метаноле получили гидрохлорид (3R,4s,5S)-4- [4-(3-бензилоксипропокси)фенил] -3,5-бис(2,5-дифторбензилокси) пиперидина в виде бесцветного масла; МС: 610 (М+Н)+;
8) из трет-бутилового эфира (3RS,4SR,5SR)-4-[4-(3-бензилоксипропокси) фенил] -3-(2, 5-дифторбензилокси)-5-гидроксипиперидин-1-карбоновой кислоты с помощью хлористого водорода в метаноле получили гидрохлорид (3RS,4SR,5SR)-4- [4-(3-бензилоксипропокси)фенил] -3-(2, 5-дифторбензилокси)пиперидин-5-ола в виде бесцветного масла; МС: 484 (М+Н)+;
9) из трет-бутилового эфира (3R,4s,5S)-4-[4-(3-бензилоксипропокси)фенил] -3, 5-бис(4-карбоксибензилокси)пиперидин-1-карбоновой кислоты с помощью хлористого водорода в метаноле получили гидрохлорид (3R,4s,5S)-4- [4-(3-бензилоксипропокси)фенил] -3,5-бис(4-карбоксибензилокси) пиперидина в виде бесцветного масла; Rf 0,63 (SiO2, метиленхлорид:метанол = 95:5, экстракция в противотоке 5 об.%-ного насыщенного водного раствора аммиака);
10) из трет-бутилового эфира (3RS,4SR,5SR)-4-[4-(3-бензилоксипропокси) фенил] -3-(4-карбоксибензилокси)-5-гидроксипиперидин-1- карбоновой кислоты с помощью хлористого водорода в метаноле получили гидрохлорид 4-{4-(3RS,4SR, 5SR)-4-[4-(3- бензилоксипропокси)фенил]-5-гидроксипиперидин-3- илоксиметил] бензойной кислоты в виде бесцветного масла; Rf 0,30 (SiO2, метиленхлорид: метанол = 9: 1, экстракция в противотоке 5 об.%-ного насыщенного водного раствора аммиака);
11) из трет-бутилового эфира (3R, 4s, 5S)-4-[4-(3-бензилоксипропокси)фенил] 3,5-бис(2, 4-дифторбензилокси)пиперидин-1-карбоновой кислоты с помощью хлористого водорода в метаноле получили гидрохлорид (3R,4s,5S)-4-[4-(3-бензилоксипропокси)фенил] -3,5-бис (2,4- дифторбензилокси)пиперидина в виде бесцветного масла; МС: 610 (М+Н)+;
12) из трет-бутилового эфира (3RS,4SR,5SR)-4-[4-(3- бензилоксипропокси)фенил]-3-(2, 4-дифторбензилокси)-5- гидроксипиперидин-1- карбоновой кислоты с помощью хлористого водорода в метаноле получили гидрохлорид (3RS,4SR, 5SR)-4-[4-(3- бензилоксипропокси)фенил]-3-(2, 4-дифторбензилокси)пиперидин-5-ола в виде бесцветного масла; Rf 0,28 (SiO2, метиленхлорид:метанол = 9:1, экстракция в противотоке 5 об.%-ного насыщенного водного раствора аммиака);
13) из трет-бутилового эфира (3R, 4s, 5S)-4-[4- (3-бензилоксипропокси)фенил]-3,5-бис(4-хлорбензилокси)пиперидин- 1-карбоновой кислоты с помощью хлористого водорода в метаноле получили гидрохлорид (3R,4s,5S)-4-[4-(3-бензилоксипропокси)фенил] -3,5-бис(4-хлорбензилокси)пиперидина в виде бесцветного масла; МС: 606 (М+Н)+;
14) из трет-бутилового эфира (3RS,4SR,5SR)-4-[4- (3-бензилоксипропокси)фенил] -3-(4-хлорбензилокси)-5- гидроксипиперидин-1-карбоновой кислоты с помощью хлористого водорода в метаноле получили гидрохлорид (3RS,4SR,5SR)-4-[4-(3- бензилоксипропокси)фенил] -3-(4-хлорбензилокси)пиперидин-5-ола в виде бесцветного твердого вещества; МС: 482 (М+Н)+;
15) из трет-бутилового эфира (3R, 4s,5S)-4-[4-(3-бензилоксипропокси) фенил]-3,5-бис(3,4-дихлорбензилокси)пиперидин-1-карбоновой кислоты с помощью хлористого водорода в метаноле получили гидрохлорид (3R,4s, 5S)-4-[4-(3-бензилоксипропокси)фенил] -3,5 бис(3,4 - дихлорбензилокси) пиперидина в виде бесцветного твердого вещества; МС: 676 (М+Н)+;
16) из трет-бутилового эфира (3RS, 4SR,5SR)-4-[4-(3- бензилоксипропокси)фенил]-3-(3,4-дихлорбензилокси)-5-гидроксипиперидин-1- карбоновой кислоты с помощью хлористого водорода в метаноле получили гидрохлорид (3RS,4SR, 5SR)-4-[4-(3- бензилоксипропокси)фенил]-3-(3,4-дихлорбензилокси)пиперидин-5- ола в виде бесцветного твердого вещества; МС: 516 (М+Н)+;
17) из трет-бутилового эфира (3R, 4s, 5S)-4-[4-(3-бензилоксипропокси) фенил]-3,5-бис(3,5-дихлорбензилокси)пиперидин-1-карбоновой кислоты с
помощью хлористого водорода в метаноле получили гидрохлорид (3R,4s, 5S)-4-[4-(3-бензилоксипропокси)фенил]-3,5-бис(3,5- дихлорбензилокси)пиперидина в виде бесцветного масла; МС: 676 (М+Н)+;
18) из трет-бутилового эфира (3RS,4SR, 5SR)-4-[4-(3- бензилоксипропокси)фенил]-3-(3,5-дихлорбензилокси)-5- гидроксипиперидин-1-карбоновой кислоты с помощью хлористого водорода в метаноле получили гидрохлорид (3RS,4SR, 5SR)-4-[4-(3- бензилоксипропокси)фенил]-3-(3,5-дихлорбензилокси)пиперидин-5-ола в виде бесцветного масла; МС: 516 (М+Н)+;
19) из трет-бутилового эфира (3R, 4s, 5S)-4-[4-(3-бензилоксипропокси)фенил] - 3,5-бис(3-хлор-2-фторбензилокси)пиперидин-1-карбоновой кислоты с помощью хлористого водорода в метаноле получили (3R,4s,5S)-4-[4- (3-бензилоксипропокси)фенил] -3,5-бис(3-хлор-2-фторбензилокси) пиперидин в виде бесцветного масла; МС: 642 (М+Н)+;
20) из трет-бутилового эфира (3RS,4SR,5SR)-4-[4-(3-бензилоксипропокси)фенил] -3-(3-хлор-2-фторбензилокси)-5- гидроксипиперидин-1-карбоновой кислоты с помощью хлористого водорода в метаноле получили гидрохлорид (3RS, 4SR, 5SR)-4-[4-(3-бензилоксипропокси)фенил] - 3-(3-хлор-2-фторбензилокси)пиперидин-5-ола в виде бесцветного масла; МС: 500 (М+Н)+;
21) из трет-бутилового эфира (3R, 4s, 5S)-4-[4-(3-бензилоксипропокси)фенил] - 3, 5-бис(хинолин-7-илметокси)пиперидин-1-карбоновой кислоты с помощью хлористого водорода в метаноле получили гидрохлорид (3R,4s,5S)-4-[4- (3-бензилоксипропокси)фенил] -3,5-бис(хинолин-7-илметокси) пиперидина в виде бесцветного масла; МС: 640 (М + Н)+;
22) из трет-бутилового эфира (3RS,4SR,5SR)-4-[4-(3-бензилоксипропокси) фенил] -5-гидрокси-3-(хинолин-7-илметокси)пиперидин-1-карбоновой кислоты с помощью хлористого водорода в метаноле получили гидрохлорид (3RS,4SR,5SR)-4-[4-(3-бензилоксипропокси)фенил] -3-(хинолин-7-илметокси)пиперидин-5-ола в виде бесцветного масла; МС: 499 (М+Н)+;
23) из трет-бутилового эфира (3R, 4s, 5S)-4-[4-(3- бензилоксипропокси)фенил] -3, 5-бис(4-этилбензилокси)пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3R,4s,5S)-4-[4-(3- бензилоксипропокси)фенил] -3,5-бис(4-этилбензилокси)пиперидин в виде бесцветного масла; МС: 594 (М+Н)+;
24) из трет-бутилового эфира (3RS,4SR,5SR)-4-[4-(3- бензилоксипропокси)фенил] -3-(4-этилбензилокси)-5-гидроксипиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS,4SR,5SR)-4-[4-(3-бензилоксипропокси)фенил] -3-(4-этилбензилокси)пиперидин- 5-ол в виде бесцветного масла; МС: 476 (М + Н)+;
25) из трет-бутилового эфира (3R, 4s, 5S)-4-[4-(3-бензилоксипропокси)фенил] - 3,5-бис(4-винилбензилокси)пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3R,4s,5S)-4-[4-(3-бензилоксипропокси)фенил] - 3,5-бис(4-винилбензилокси)пиперидин в виде бесцветного масла; МС: 590 (М+Н)+;
26) из трет-бутилового эфира (3RS,4SR, 5SR)-4-[4-(3-бензилоксипропокси) фенил] -5-гидрокси -3-(4-винилбензилокси)пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS,4SR, 5SR)-4- [4-(3-бензилоксипропокси)фенил]-3-(4-винилбензилокси)пиперидин-5-ол в виде бесцветного масла; МС: 474 (М+Н)+;
27) из трет-бутилового эфира (3R, 4s, 5S)-4-[4-(3-бензилоксипропокси)фенил] - 3,5-бис(4-метоксибензилокси)пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3R,4s,5S)-4-[4- (3-бензилоксипропокси)фенил] -3, 5-бис(4-метоксибензилокси)пиперидин в виде бесцветного масла; МС: 598 (М+Н)+;
28) из трет-бутилового эфира (3RS,4SR,5SR)-4-[4-(3- бензилоксипропокси)фенил] -5-гидрокси-3-(4-метоксибензилокси) пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS,4SR,5SR)-4-[4-(3-бензилоксипропокси) фенил] -3-(4-метоксибензилокси)пиперидин-5-ол в виде бесцветного масла; МС: 478 (М+Н)+;
29) из трет-бутилового эфира (3R, 4s, 5S)-4-[4-(3-бензилоксипропокси)фенил]-3,5-бис(3,4, 5- триметоксибензилокси)пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3R,4s,5S)-4-[4-(3- бензилоксипропокси)фенил] -3,5-бис(3,4,5-триметоксибензилокси)пиперидин в виде бесцветного масла; МС: 718 (М+Н)+;
30) из трет-бутилового эфира (3RS,4SR,5SR)-4-[4-(3- бензилоксипропокси)фенил] -5-гидрокси-3-(3,4, 5-триметоксибензилокси)пиперидин- 1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS,4SR,5SR)-4-[4-(3-бензилоксипропокси)фенил] -3-(3,4,5-триметоксибензилокси)пиперидин-5-ол в виде бесцветного масла; МС: 538 (М+Н)+;
31) из трет-бутилового эфира (3R, 4s, 5S)-4-[4-(3-бензилоксипропокси)фенил] -3,5-бис (3, 5-диметоксибензилокси)пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3R,4s,5S)-4-[4-(3-бензилоксипропокси) фенил] -3,5-бис(3,5-диметоксибензилокси)пиперидин в виде бесцветного масла; МС: 658 (М+Н)+;
32) из трет-бутилового эфира (3RS,4SR,5SR)-4-[4-(3-бензилоксипропокси) фенил] -3-(3, 5-диметоксибензилокси)-5-гидроксипиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS,4SR,5SR)-4-[4-(3-бензилоксипропокси)фенил] -3- (3, 5-диметоксибензилокси)пиперидин-5-ол в виде бесцветного масла; МС: 508 (М+Н)+;
33) из трет-бутилового эфира (3R, 4s, 5S)-4-[4-(3-бензилоксипропокси)фенил] - 3, 5-бис(4-трифторметоксибензилокси) пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3R,4s,5S)-4-[4-(3- бензилоксипропокси)фенил] -3,5-бис(4-трифторметоксибензилокси) пиперидин в виде бесцветного масла; МС: 706 (М+Н)+;
34) из трет-бутилового эфира (3RS,4SR,5SR)-4-[4-(3-бензилоксипропокси) фенил] -5-гидрокси-3-(4-трифторметоксибензилокси)пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS,4SR,5SR)-4-[4-(3-бензилоксипропокси)фенил] -3-(4- трифторметокси-бензилокси)пиперидин-5-ол в виде бесцветного масла; МС: 532 (М+Н)+;
35) из трет-бутилового эфира (3R,4s,5S)-4-[4-(3- бензилоксипропокси) фенил] -3, 5-бис(4-метилсульфанилбензилокси)пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3R,4s,5S)-4-[4-(3- бензилоксипропокси)фенил] -3,5-бис(4-метилсульфанилбензилокси) пиперидин в виде бесцветного масла; МС: 630 (М+Н)+;
36) из трет-бутилового эфира (3RS,4SR,5SR)-4-[4-(3-бензилоксипропокси)фенил] -5-гидрокси-3-(4- метилсульфанилбензилокси)пиперидин-1- карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS,4SR,5SR)-4-[4-(3-бензилоксипропокси)фенил] -3-(4- метилсульфанилбензилокси)пиперидин-5-ол в виде бесцветного масла; МС: 494 (М+Н)+;
37) из трет-бутилового эфира (3R, 4s, 5S)-4-[4-(3-бензилоксипропокси)фенил] - 3, 5-бис(4-изопропилбензилокси)пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3R,4s,5S)-4-[4-(3- бензилоксипропокси)фенил] -3,5-бис(4-изопропилбензилокси)пиперидин в виде бесцветного масла; МС: 622 (М + Н)+;
38) из трет-бутилового эфира (3RS,4SR,5SR)-4-[4-(3-бензилоксипропокси) фенил] -5-гидрокси-3-(4-изопропилбензилокси)пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS,4SR,5SR)-4- [4-(3-бензилоксипропокси)фенил] -3-(4-изопропилбензилокси)пиперидин-5-ол в виде бесцветного масла; МС: 490 (М+Н)+;
39) из трет-бутилового эфира (3R, 4s, 5S)-4-[4-(3- бензилоксипропокси)фенил]-3, 5-бис(3-хлор-4-метоксибензилокси) пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3R,4s,5S)-4-[4-(3- бензилоксипропокси)фенил] -3, 5-бис(3-хлор-4-метоксибензилокси)пиперидин в виде бесцветного масла; МС: 666 (М+Н)+;
40) из трет-бутилового эфира (3RS,4SR,5SR)-4-[4-(3-бензилоксипропокси)фенил] -3-(3-хлор-4-метоксибензилокси)- 5-гидроксипиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS,4SR,5SR)-4-[4-(3-бензилоксипропокси)фенил] -3- (3-хлор-4-метоксибензилокси)пиперидин-5-ол в виде бесцветного масла; МС: 512 (М+Н)+;
41) из трет-бутилового эфира (3R, 4s, 5S)-4-[4-(3-бензилоксипропокси)фенил] - 3, 5-бис(4-метокси-3-метилбензилокси)пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3R,4s,5S)-4-[4-(3- бензилоксипропокси)фенил] -3, 5-бис(4-метокси-3-метилбензилок- си)пиперидин в виде бесцветного масла; МС: 626 (М+Н)+;
42) из трет-бутилового эфира (3RS,4SR,5SR)-4-[4-(3-бензилоксипропокси)фенил] -5-гидрокси-3-(4-метокси-3- метилбензилокси)пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS,4SR,5SR)-4-[4-(3-бензилоксипропокси)фенил] -3-(4-метокси-3-метилбензилокси) пиперидин-5-ол в виде бесцветного масла; МС: 492 (М+Н)+.
Использованные в качестве исходных соединений BOC-производные получали следующим путем.
Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3R, 4s,5S)-4-[4-(3-бензилоксипропокси)фенил]-3,5-дигидроксипиперидин-1- карбоновой кислоты с использованием одного эквивалента бензильного галогенида примерно в равных количествах получили непрореагировавший исходной материал, а также соответствующие моно- и диалкилированные BOC-производные. Эти смеси затем разделяли с помощью хроматографии:
(а) алкилированием 2-бромметилнафталином получили трет-бутиловый эфир (3R, 4s, 5S)-4-[4-(3-бензилоксипропокси)фенил]-3,5-бис(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты [МС: 739 (М+Н)+] и трет-бутиловый эфир (3RS, 4SR, 5SR)-4-[4-(3-бензилоксипропокси)фенил] -5-гидрокси-3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты [МС: 598 (М+Н)+] в каждом случае в виде бесцветного твердого вещества;
(б) алкилированием 2-хлорметил-1,4-диметоксинафталином [J. Org. Chem. (1983), 48(19), 3265-3268] получили трет-бутиловый эфир (3R,4s,5S)-4-[4-(3-бензилоксипропокси)фенил] -3,5-бис(1,4- диметоксинафталин-2-илметокси)-пиперидин-1-карбоновой кислоты [МС: 876 (М+Н)+] в виде бесцветной пены и трет-бутиловый эфир (3RS,4SR,5SR)-4-[4-(3-бензилоксипропокси)фенил]-3-(1,4- диметоксинафталин-2-илметокси)-5-гидроксипиперидин-1-карбоновой кислоты [МС: 659 (М+Н)+] в виде бесцветного масла;
(в) алкилированием 2,4-дихлорбензилхлоридом получили трет-бутиловый эфир (3R, 4s, 5S)-4-[4-(3-бензилоксипропокси)фенил] -3,5-бис(2,4-дихлорбензилокси)пиперидин-1-карбоновой кислоты, Rf 0,83 (SiO2, метиленхлорид:этиловый эфир уксусной кислоты = 8:2), и трет-бутиловый эфир (3RS,4SR,5SR)-4- [4-(3-бензилоксипропокси)фенил]-3-(2, 4-дихлорбензилокси)-5-гидроксипиперидин-1- карбоновой кислоты, Rf 0,30 (SiO2, метиленхлорид:этиловый эфир уксусной кислоты = 8:2), в каждом случае в виде бесцветного масла;
(г) алкилированием 2,5-дифторбензилбромидом получили трет- бутиловый эфир (3R, 4s, 5S)-4-[4-(3-бензилоксипропокси)фенил]-3,5- бис(2,5-дифторбензилокси)пиперидин-1-карбоновой кислоты [МС: 727 (M+NH4)+] и трет-бутиловый эфир (3RS, 4SR, 5SR)-4-[4-(3- бензилоксипропокси)фенил]-3-(2,5-дифторбензилокси)-5-гидроксипиперидин-1- карбоновой кислоты, Rf 0,26 (SiO2, метиленхлорид: этиловый эфир уксусной кислоты = 8:2), в каждом случае в виде бесцветного масла;
(д) алкилированием метиловым эфиром 4-бромметилбензойной кислоты и омылением метилового эфира во время водной обработки получили трет-бутиловый эфир (3R, 4s, 5S)-4-[4-(3-бензилоксипропокси)фенил] -3,5-бис(4-карбоксибензилокси)пиперидин-1-карбоновой кислоты, Rf 0,18 (SiO2, метиленхлорид:метанол = 9: 1), и трет-бутиловый эфир (3RS, 4SR,5SR)-4-[4-(3-бензилоксипропокси)фенил] -3-(4-карбоксибензилокси)-5-гидроксипиперидин-1-карбоновой кислоты, Rf 0,42 (SiO2, метиленхлорид:метанол = 9:1), в каждом случае в виде бесцветного масла;
(е) алкилированием 2,4-дифторбензилбромидом получили трет-бутиловый эфир (3R, 4s, 5S)-4-[4-(3-бензилоксипропокси)фенил] -3,5-бис(2,4- дифторбензилокси)пиперидин-1-карбоновой кислоты [МС: 727 (M+NH4)+] и трет-бутиловый эфир (3RS,4SR, 5SR)-4-[4-(3- бензилоксипропокси)фенил]-3-(2,4-дифторбензилокси)-5- гидроксипиперидин-1-карбоновой кислоты, Rf 0,24 (SiO2, метиленхлорид:этиловый эфир уксусной кислоты = 8:2), в каждом случае в виде бесцветного масла;
(ж) алкилированием 4-хлорбензилхлоридом получили трет-бутиловый эфир (3R, 4s, 5S)-4-[4-(3-бензилоксипропокси)фенил] -3, 5-бис(4-хлорбензилокси)пиперидин-1-карбоновой кислоты [МС: 724 (M+NH4)+] и трет-бутиловый эфир (3RS, 4SR, 5SR)-4- [4-(3-бензилоксипропокси)фенил]-3-(4-хлорбензилокси)-5-гидроксипиперидин-1- карбоновой кислоты [МС: 582 (М + Н)+] в каждом случае в виде бесцветного масла;
(з) алкилированием 3,4-дихлорбензилхлоридом получили трет-бутиловый эфир (3R, 4s, 5S)-4-[4-(3-бензилоксипропокси)фенил] -3,5-бис(3,4-дихлорбензилокси)пиперидин-1-карбоновой кислоты [МС: 793 (M+NH4)+] и трет-бутиловый эфир (3RS, 4SR, 5SR)-4- [4-(3-бензилоксипропокси)фенил] -3- (3,4-дихлорбензилокси)-5-гидроксипиперидин-1-карбоновой кислоты, Rf 0,55 (SiO2, метиленхлорид: этиловый эфир уксусной кислоты = 8:2), в каждом случае в виде бесцветного масла;
(и) алкилированием 3,5-дихлорбензилхлоридом получили трет- бутиловый эфир (3R, 4s, 5S)-4-[4-(3-бензилоксипропокси)фенил]-3,5- бис(3,5-дихлорбензилокси)пиперидин-1-карбоновой кислоты [МС: 793 (M+NH4)+] и трет-бутиловый эфир (3RS, 4SR, 5SR)-4-[4-(3- бензилоксипропокси)фенил]-3-(3,5-дихлорбензилокси)-5- гидроксипиперидин-1-карбоновой кислоты [МС: 634 (М + NH4)+] в каждом случае в виде бесцветного масла;
(к) алкилированием 3-хлор-2-фторбензилбромидом получили трет-бутиловый эфир (3R, 4s, 5S)-4-[4-(3-бензилоксипропокси)фенил] -3,5-бис(3-хлор-2-фторбензилокси)пиперидин-1-карбоновой кислоты [МС: 760 (M+NH4)+] и трет-бутиловый эфир (3RS, 4SR,5SR)-4-[4-(3-бензилоксипропокси)фенил]-3-(3-хлор-2-фторбензилокси)-5- гидроксипиперидин-1-карбоновой кислоты, Rf 0, 54 (SiO2, метиленхлорид: этиловый эфир уксусной кислоты = 8:2), в каждом случае в виде бесцветного масла;
(л) алкилированием гидробромидом 7-бромметилхинолина [J. Am. Chem. Soc. 77, 1054 (1955)] с применением соответственно в большем количестве гидрида натрия получили трет-бутиловый эфир (3R,4s,5S)-4-[4-(3-бензилоксипропокси)фенил] -3, 5-бис(хинолин-7-илметокси)пиперидин-1-карбоновой кислоты [МС: 740 (М+Н)+] и трет-бутиловый эфир (3RS,4SR,5SR)-4- [4-(3-бензилоксипропокси)фенил] -5-гидрокси-3- (хинолин-7-илметокси)пиперидин-1-карбоновой кислоты [МС: 599 (М+Н)+, Rf 0,35 (SiO2, метиленхлорид:этиловый эфир уксусной кислоты = 2:3)] в каждом случае в виде бесцветного масла;
(м) алкилированием 4-этилбензилхлоридом получили трет-бутиловый эфир (3R, 4s, 5S)-4-[4-(3-бензилоксипропокси)фенил] -3, 5-бис(4-этилбензилокси)пиперидин-1-карбоновой кислоты [МС: 711 (M+NH4)+] и трет-бутиловый эфир (3RS, 4SR, 5SR)-4-[4-(3- бензилоксипропокси)фенил] -3-(4-этилбензилокси)-5- гидроксипиперидин-1-карбоновой кислоты, Rf 0,30 (SiO2, метиленхлорид:этиловый эфир уксусной кислоты = 8:2), в каждом случае в виде бесцветного масла;
(н) алкилированием 4-винилбензилхлоридом получили трет- бутиловый эфир (3R, 4s, 5S)-4-[4-(3-бeнзилoкcипpoпoкcи)фенил] -3,5- бис(4-винилбензилокси)пиперидин-1-карбоновой кислоты [МС: 707 (M+NH4)+] и трет-бутиловый эфир (3RS, 4SR, 5SR)-4-[4-(3- бензилоксипропокси)фенил]-5-гидрокси-3-(4-винилбензилокси)пиперидин-1- карбоновой кислоты, Rf 0,30 (SiO2, метиленхлорид:этиловый эфир уксусной кислоты = 8:2), в каждом случае в виде бесцветного масла;
(о) алкилированием 4-метоксибензилхлоридом получили трет-бутиловый эфир (3R, 4s, 5S)-4-[4-(3-бензилоксипропокси)фенил] -3,5-бис(4-метоксибензилокси) пиперидин-1-карбоновой кислоты [МС: 715 (M+NH4)+] и трет-бутиловый эфир (3RS, 4SR, 5SR)-4- [4-(3-бензилоксипропокси)фенил] -5-гидрокси- 3-(4-метоксибензилокси)пиперидин-1-карбоновой кислоты [МС: 595 (М + NH4)+] в каждом случае в виде бесцветного масла;
(п) алкилированием 3,4,5-триметоксибензилхлоридом получили трет- бутиловый эфир (3R, 4s, 5S)-4-[4-(3-бензилоксипропокси)фенил]-3,5- бис(3,4,5-триметоксибензилокси)пиперидин-1-карбоновой кислоты [МС: 835 (M+NH4)+] и трет-бутиловый эфир (3RS,4SR,5SR)-4-[4-(3-бензилоксипропокси)фенил]-5-гидрокси-3-(3,4,5- триметоксибензилокси)пиперидин-1-карбоновой кислоты [МС: 655 (M+NH4)+] в каждом случае в виде бесцветного масла;
(р) алкилированием 3,5-диметоксибензилхлоридом получили трет-бутиловый эфир (3R, 4s, 5S)-4-[4-(3-бензилоксипропокси)фенил] -3,5-бис(3,5-диметоксибензилокси)пиперидин-1-карбоновой кислоты [МС: 775 (M+NH4)+] и трет-бутиловый эфир (3RS,4SR, 5SR)-4-[4-(3-бензилоксипропокси)фенил] -3-(3,5-диметоксибензилокси)-5-гидроксипиперидин-1-карбоновой кислоты [МС: 625 (М + NH4)+] в каждом случае в виде бесцветного масла;
(с) алкилированием 4-трифторметоксибензилбромидом получили трет-бутиловый эфир (3R,4s,5S)-4-[4-(3-бензилоксипропокси)фенил]- 3,5-бис(4-трифторметоксибензилокси)пиперидин-1-карбоновой кислоты [МС: 823 (M+NH4)+] и трет-бутиловый эфир (3RS, 4SR,5SR)-4-[4-(3- бензилоксипропокси)фенил]-5-гидрокси-3-(4-трифторметоксибензилокси)пиперидин-1- карбоновой кислоты, Rf 0,32 (SiO2, метиленхлорид:этиловый эфир уксусной кислоты = 8:2), в каждом случае в виде бесцветного масла;
(т) алкилированием 4-метилтиобензилхлоридом [J. Org. Chem. (1988), 53(3), 561-569] получили трет-бутиловый эфир (3R,4s,5S)-4-[4-(3-бензилоксипропокси)фенил]-3,5-бис(4- метилсульфанилбензилокси)пиперидин-1-карбоновой кислоты, [МС: 747 (M+NH4 )+] и трет-бутиловый эфир (3RS,4SR,5SR)-4- [4-(3-бензилоксипропокси)фенил]-5-гидрокси-3-(4- метилсульфанилбензилокси)пиперидин-1-карбоновой кислоты [МС: 611 (М + NH4)+ ] в каждом случае в виде бесцветного масла;
(у) алкилированием 4-изопропилбензилхлоридом получили трет-бутиловый эфир (3R, 4s,5S)-4-[4-(3-бензилоксипропокси)фенил] -3, 5-бис(4-изопропилбензилокси)пиперидин-1-карбоновой кислоты [МС: 739 (M+NH4)+] и трет-бутиловый эфир (3RS,4SR, 5SR)-4-[4-(3-бензилоксипропокси)фенил]-5-гидрокси-3-(4- изопропилбензилокси)пиперидин-1-карбоновой кислоты [МС: 607 (М + NH4)+] в каждом случае в виде бесцветного масла;
(ф) алкилированием 3-хлор-4-метоксибензилхлоридом получили трет- бутиловый эфир (3R,4s,5S)-4-[4-(3-бензилоксипропокси)фенил]-3,5- бис(3-хлор-4-метоксибензилокси)пиперидин-1-карбоновой кислоты [МС: 784 (M+NH4)+] и трет-бутиловый эфир (3RS,4SR,5SR)-4-[4-(3-бензилоксипропокси)фенил]-3-(3-хлор-4- метоксибензилокси)-5-гидроксипиперидин-1-карбоновой кислоты [МС: 630 (М + NH4)+] в каждом случае в виде бесцветного масла;
(х) алкилированием 4-метокси-3-метилбензилхлоридом получили трет-бутиловый эфир (3R, 4s, 5S)-4-[4-(3-бензилоксипропокси)фенил] -3,5-бис(4-метокси-3-метилбензилокси)пиперидин-1-карбоновой кислоты [МС: 743 (M+NH4)+] и трет-бутиловый эфир (3RS, 4SR, 5SR)-4-[4-(3-бензилоксипропокси)фенил] -5-гидрокси-3-(4-метокси-3-метилбензилокси)пиперидин-1-карбоновой кислоты [МС: 609 (М + NH4)+] в каждом случае в виде бесцветного масла.
Использованный в качестве исходного соединения трет-бутиловый эфир (3R, 4s, 5S)-4-[4-(3-бензилоксипропокси)фенил] -3,5-дигидроксипиперидин-1-карбоновой кислоты получали следующим путем.
(α) 50,0 г (179 ммолей) 1-бензил-4-(4-метоксифенил)-1,2,3,6- тетрагидропиридина [пример 44(6)] растворяли в 500 мл тетрагидрофурана, при комнатной температуре смешивали с 36,3 мл (322 ммоля) 48%-ной водной бромистоводородной кислоты и затем реакционную смесь концентрировали на ротационном испарителе. Образовавшийся в результате остаток дважды взмучивали в 500 мл толуола и снова концентрировали, затем растворяли в 1500 мл диоксана и 1200 мл воды, смешивали с 51,6 г (501 ммоль) бромида натрия и 9,3 мл (181 ммоль) брома и перемешивали в течение 2 ч при комнатной температуре. Полученный в результате окрашенный в оранжевый цвет раствор далее охлаждали до 0oC и при температуре в интервале от 5 до 10oC смешивали с 1240 мл 2 н. едкого натра и перемешивание продолжали еще в течение 2 ч при комнатной температуре. После этого реакционную смесь трижды экстрагировали 2 л этилового эфира уксусной кислоты, объединенные органические фазы промывали водой, сушили над сульфатом магния и упаривали на ротационном испарителе при температуре максимально 40oC. Таким путем получили 53,64 г (ок. 100% от теории) (1RS,6RS)-3-бензил-6- (4-метоксифенил)-7-окса-3-азабицикло[4,1,0]гептана в виде коричневого твердого вещества; МС: 295 (М)+.
(β) 53,44 г (179 ммолей) (1RS, 6RS)-3-бензил-6-(4-метоксифенил)-7-окса-3- азабицикло[4,1,0] гептана суспендировали в 980 мл простого эфира и эту суспензию в атмосфере аргона и в условиях, исключающих наличие влаги, при комнатной добавляли по каплям к 226 мл 1,6 М раствора метиллития в диэтиловом эфире (362 ммоля). Далее реакционную смесь в течение 1 ч нагревали с обратным холодильником. После охлаждения до комнатной температуры смесь сливали на 1,5 л насыщенного раствора гидрокарбоната натрия и дважды экстрагировали 1,5 л этилового эфира уксусной кислоты, объединенные этилацетатные фазы промывали водой, сушили над сульфатом магния и упаривали на ротационном испарителе при температуре максимально 40oC. Таким путем получили 52,8 г (ок. 100% от теории) (RS)-1-бензил-4-(4- метоксифенил)-1,2,3, 6-тетрагидропиридин-3-ола в виде коричневого масла; МС: 296 (M+H)+.
(γ) 52,6 г (178 ммоля) (RS)-1-бензил-4-(4-метоксифенил)- 1,2,3,6-тетрагидропиридин-3-ола растворяли в 300 мл N,N- диметилформамида, смешивали, добавляя порциями, с 25 г (около 600 ммолей) дисперсии гидрида натрия в вазелиновом масле (55-65%-ной) и реакционную смесь выдерживали в течение 1 ч в атмосфере аргона при 50oC. После охлаждения до 5oC медленно смешивали с 23 мл (285 ммолей) этилиодида и перемешивали в течение 1 ч без охлаждения. Далее реакционную смесь сливали на 2 л ледяной воды и трижды экстрагировали 1 л этилового эфира уксусной кислоты. Объединенные этилацетатные фазы затем промывали водой, сушили над сульфатом магния и упаривали на ротационном испарителе при температуре максимально 40oC. Полученный в результате остаток хроматографировали на силикагеле с использованием гексана/этилового эфира уксусной кислоты (5:1). Таким путем получили 42,51 г (74% от теории) (RS)-1-бензил-3-этокси-4-(4- метоксифенил)-1,2,3,6-тетрагидропиридина в виде окрашенного в оранжевый цвет масла; МС: 324 (М)+.
(δ) 42,3 г (131 ммоль) (RS)-1-бензил-3-этокси-4-(4-метоксифенил)-1,2,3,6-тетрагидропиридина растворяли в 500 мл 1,2-диметоксиэтана, смешивали с 7,45 г (196 ммоля) борогидрида натрия, при охлаждении при температуре максимально 28oC смешивали с раствором из 44,3 мл (353 ммоля) эфирата трифторида бора в 44,3 мл 1,2-диметоксиэтана и реакционную смесь перемешивали в течение 2 ч при комнатной температуре. Далее при охлаждении при температуре максимально 35oC последовательно добавляли по каплям сначала 4,1 н. раствор гидроксида калия, а затем 33,9 мл 30%-ного раствора перекиси водорода и реакционную смесь в течение 3 ч нагревали с обратным холодильником. После охлаждения до комнатной температуры реакционный раствор сливали на 2 л воды и дважды экстрагировали метиленхлоридом порциями по 1 л. Объединенные метиленхлоридные фазы промывали водой, сушили над сульфатом магния и упаривали на ротационном испарителе при температуре максимально 40oC. Полученный в результате остаток хроматографировали на силикагеле с использованием гексана/этилового эфира уксусной кислоты (сначала в соотношении 4:1 с последующим ступенчатым повышением доли этилового эфира уксусной кислоты до соотношения 1: 1). Таким путем получили 22,1 г (49% от теории) (3RS,4RS,5SR)-5- этокси-1-бензил-3-гидрокси-4-(4-метоксифенил)пиперидина в виде желтоватого масла; МС: 342 (М+Н)+.
(ε) 52,39 г (153,4 ммоля) (3RS,4RS,5SR)-5-этокси-1-бензил-3-гидрокси-4-(4- метоксифенил)пиперидина растворяли в 525 мл метиленхлорида и при температуре максимально 40oC смешивали с 306 мл (1 М раствора трибромида бора в метиленхлориде, после чего реакционную смесь перемешивали в течение 4 ч при комнатной температуре. Далее смесь охлаждали до 5oC и отфильтровывали образовавшиеся кристаллы. Последние затем, растворенные в метиленхлориде/метаноле (8: 2, экстракция в противотоке 5 об.% конц. водного аммиака), хроматографировали на силикагеле с использованием той же смеси растворителей. Таким путем получили 34,18 г (74% от теории) (3R,4s,5S)-1-бензил-4-(4-гидроксифенил)пиперидин-3,5-диола в виде аморфного бесцветного твердого вещества; МС: 300 (М+Н)+.
(ζ) 33,98 г (113,5 ммоля) (3R,4s,5S)-1-бензил-4-(4-гидроксифенил)пиперидин-3,5-диола растворяли в 1,7 л метанола, смешивали с 5,1 г палладия на угле (10%-ного) и гидрировали до полного завершения реакции при комнатной температуре и нормальном давлении. Далее реакционную смесь фильтровали через силикагель и концентрировали в вакууме, создаваемом водоструйным насосом. Таким путем получили 22,56 г (95% от теории) (3R,4s,5S)-4-(4- гидроксифенил)пиперидин-3,5-диола в виде аморфного бесцветного твердого вещества; МС: 209 (М)+.
(η) 22,36 г (106 ммолей) (3R,4s,5S)-4-(4-гидроксифенил)пиперидин-3,5- диола растворяли в 559 мл диоксана и 186 мл воды, смешивали с 18,85 г (224 ммоля) гидрокарбоната натрия и 25,65 г (117,5 ммоля) ди-трет- бутилдикарбоната и перемешивали в течение 2 ч при комнатной температуре. Далее реакционную смесь сливали на 1,5 л ледяной воды и дважды экстрагировали 1,5 л этилового эфира уксусной кислоты. Объединенные этилацетатные фазы сушили над сульфатом магния и упаривали на ротационном испарителе при температуре максимально 50oC. Полученный в результате остаток хроматографировали на силикагеле с использованием метиленхлорида/метанола (95:5). Таким путем получили 15,79 г (48% от теории) трет- бутилового эфира (3R,4s,5S)-3, 5-дигидрокси-4-(4- гидроксифенил)пиперидин-1-карбоновой кислоты в виде бесцветных кристаллов; МС: 310 (М+Н)+.
(θ) 15,59 г (50,4 ммоля) трет-бутилового эфира (3R,4s, 5S)-3,5-дигидрокси-4-(4- гидроксифенил)пиперидин-1-карбоновой кислоты растворяли в 510 мл метилэтилкетона, последовательно смешивали сначала с 28 г (201 ммоль) карбоната калия, а затем 34,7 г (151 ммоль) бензил-3-бромпропилового эфира и реакционную смесь в течение 24 ч нагревали с обратным холодильником. После охлаждения до комнатной температуры смесь сливали на 800 мл ледяной воды и дважды экстрагировали 500 мл этилового эфира уксусной кислоты, объединенные этилацетатные фазы промывали водой, сушили над сульфатом магния и упаривали на ротационном испарителе при температуре максимально 40oC. Полученный в результате остаток хроматографировали на силикагеле с использованием метиленхлорида/этилового эфира уксусной кислоты (7:3). Таким путем получили 20,5 г (89% от теории) трет-бутилового эфира (3R,4s,5S)-4-[4-(3-бензилоксипропокси)фенил] -3,5- дигидроксипиперидин-1-карбоновой кислоты в виде аморфного бесцветного твердого вещества; МС: 458 (М+Н)+.
Пример 110.
Путем отщепления BOC-группы с помощью хлористого водорода в метаноле аналогично примеру 22(м) или с помощью бромида цинка в метиленхлориде аналогично примеру 10(б) получали следующие соединения:
1) из трет-бутилового эфира (3RS,4SR,5SR)-4-[4-(3- бензилоксипропокси)фенил]-5-этокси-3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS,4SR,5SR)-4-[4-(3- бензилоксипропокси)фенил] -5-этокси-3-(нафталин-2-илметокси)- пиперидин в виде бесцветного масла; МС: 526 (М + Н)+;
2) из трет-бутилового эфира (3RS,4RS,5SR)-4-[4-(3-бензилоксипропокси) фенил]-5-[2-(4-метилпиперазин-1-ил)этокси]-3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты с помощью хлористого водорода в метаноле получили 1-{ 2-[(3RS, 4RS, 5SR)-4-[4-(3- бензилоксипропокси)фенил] -3-(нафталин-2-илметокси)пиперидин-5- илокси] этил} -4-метилпиперазин в виде бесцветного масла; МС: 624 (М+Н)+;
3) из трет-бутилового эфира (3RS,4SR,5SR)-4-[4-(3- бензилоксипропокси)фенил]-3-(нафталин-2-илметокси)-5- пропоксипиперидин-1-карбоновой кислоты с помощью хлористого водорода в метаноле получили (3RS,4SR,5SR)-4-[4-(3- бензилоксипропокси)фенил] -3-(нафталин-2-илметокси)-5- пропоксипиперидин в виде бесцветного масла; МС: 540 (М+Н)+;
4) из трет-бутилового эфира (3RS, 4SR,5SR)-4-[4-(3-бензилоксипропокси)фенил] -5-бутокси-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты с помощью хлористого водорода в метаноле получили (3RS,4SR,5SR)-4-[4-(3-бензилоксипропокси)фенил] -5-бутокси-3-(нафталин-2-илметокси)пиперидин в виде бесцветного масла; МС: 554 (М+Н)+;
5) из трет-бутилового эфира (3RS,4SR,5SR)-4-[4-(3-бензилоксипропокси) фенил] -5-метокси-3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты с помощью хлористого водорода в метаноле получили (3RS,4SR, 5SR)-4- [4-(3-бензилоксипропокси)фенил]-5-метокси-3-(нафталин-2-илметокси)пиперидин в виде бесцветного масла; МС: 512 (М+Н)+;
6) из смеси трет-бутилового эфира (3RS,4RS, 5SR)- и (3SR,4SR,5RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(нафталин-2-илметокси)-5- [2-[(RS)-тетрагидропиран-2-илокси] этокси] пиперидин-1-карбоновой кислоты с помощью хлористого водорода в метаноле с одновременным отщеплением тетрагидропиранильного остатка получили 2-[(3RS, 4RS, 5SR)-4-[4-(3- бензилоксипропокси)фенил]-3-(нафталин-2-илметокси)пиперидин-5-илокси]этанол в виде бесцветного масла; МС: 542 (М+Н)+;
7) из смеси трет-бутилового эфира (3RS,4SR,5SR)- и (3SR,4RS,5RS)-4-[4-(3-бензилоксипропокси)фенил] - 3-(нафталин-2-илметокси)-5-[3-[(RS)-тетрагидропиран-2-илокси] пропокси]пиперидин-1-карбоновой кислоты с помощью хлористого водорода в метаноле с одновременным отщеплением тетрагидропиранильного остатка получили 3-[(3RS, 4SR, 5SR)-4-[4-(3- бензилоксипропокси)фенил] -3-(нафталин-2-илметокси)пиперидин-5- илокси] пропан-1-ол в виде бесцветного масла; МС: 556 (М+Н)+;
8) из смеси трет-бутилового эфира (3RS,4SR,5SR)- и (3SR,4RS,5RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(нафталин-2-илметокси)-5-[4-[(RS)-тетрагидропиран-2-илокси] бутокси]пиперидин-1-карбоновой кислоты с помощью хлористого водорода в метаноле с одновременным отщеплением тетрагидропиранильного остатка получили 4-[(3RS, 4SR, 5SR)-4- [4-(3-бензилоксипропокси)фенил]-3-(нафталин-2-илметокси)пиперидин-5-илокси] бутан-1-ол в виде бесцветного масла; МС: 570 (М+Н)+;
9) из трет-бутилового эфира (3RS, 4RS,5SR)-4-[4-(3-бензилоксипропокси) фенил]-5-(2-морфолин-4-илэтокси)-3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты с помощью хлористого водорода в метаноле получили 4-{2-[(3RS, 4RS, 5SR)-4-[4-(3-бензилоксипропокси)фенил]-3-(нафталин-2-илметокси) пиперидин-5-илокси] этил} морфолин в виде бесцветного масла; МС: 611 (М+Н)+;
10) из трет-бутилового эфира (3RS,4RS)-3-(нафталин-2-илметокси)-4-(4-{3- [2-(2-триметилсиланилэтоксиметокси)бензилокси] пропокси} фенил)пиперидин-1- карбоновой кислоты [пример 108(б)] с помощью хлористого водорода в метаноле с одновременным отщеплением 2-триметилсиланилэтоксиметоксильного остатка получили 2-(3-{ 4-[(3RS,4RS)-3-(нафталин-2-илметокси)пиперидин-4- ил]фенокси} пропоксиметил)фенол в виде бесцветного масла; МС: 579 (М+Н)+.
Аналогично примеру 1(ж), но при реакционной температуре 50oC и с применением большого избытка гидрида натрия и алкилирующего агента использованные в качестве исходных соединений BOC-производные получали из трет-бутилового эфира (3RS,4SR,5SR)-4- [4-(3-бензилоксипропокси)фенил]-5-гидрокси-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты [пример 109(а)] следующим путем:
(а) алкилированием этилбромидом получили трет-бутиловый эфир (3RS,4SR, 5SR)-4-[4-(3-бензилоксипропокси)фенил] -5-этокси-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 626 (М+Н)+;
(б) алкилированием 1-(2-хлорэтил)-4-метилпиперазином [Austr. J. Chem. 9 (1956), 89] получили трет-бутиловый эфир (3RS,4RS,5SR)-4-[4-(3-бензилоксипропокси)фенил] -5-[2-(4-метилпиперазин-1-ил) этокси]-3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 724 (М+Н)+;
(в) алкилированием н-пропилбромидом получили трет-бутиловый эфир (3RS, 4SR, 5SR)-4-[4-(3-бензилоксипропокси)фенил] -3- (нафталин-2-илметокси)-5-пропоксипиперидин-1-карбоновой кислоты в виде желтоватого масла; МС: 640 (М+Н)+;
(г) алкилированием н-бутилбромидом получили трет-бутиловый эфир (3RS, 4SR, 5SR)-4-[4-(3-бензилоксипропокси)фенил]-5-бутокси-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты в виде желтоватого масла; МС: 654 (М+Н)+;
(д) алкилированием метилиодидом получили трет-бутиловый эфир (3RS,4SR, 5SR)-4-[4-(3-бензилоксипропокси)фенил] -5-метокси-3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде желтоватого масла; МС: 612 (М+Н)+;
(е) алкилированием рац.-2-(2-бромэтокси)тетрагидропираном J. Amer. Chem. Soc. 70, 4187 (1948)] получили смесь трет-бутилового эфира (3RS,4RS,5SR)- и (3SR, 4SR,5RS)-4-[4-(3-бензилоксипропокси)фенил]-3- (нафталин-2-илметокси)-5-[2-[(RS)-тетрагидропиран-2-илокси]этокси] - пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 743 (M+NH4 )+;
(ж) алкилированием рац. -2-(3-бромпропокси)тетрагидропираном J. Chem. Soc. 1955, 1770] получили смесь трет-бутилового эфира (3RS,4SR,5SR)- и (3SR, 4RS, 5RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(нафталин-2-илметокси)-5-[3-[(RS)-тетрагидропиран-2-илокси] пропокси] пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 740 (М+Н)+;
(з) алкилированием рац.-2-(4-бромбутокси)тетрагидропираном [S.W. Baldwin и др. , J. Org. Chem. 1985, 50, 4432-4439] получили смесь трет-бутилового эфира (3RS,4SR,5SR)- и (3SR,4RS, 5RS)-4-[4-(3- бензилоксипропокси)фенил]-3-(нафталин-2-илметокси)-5-[4-[(RS)- тетрагидропиран-2-илокси]бутокси]пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 771 (M+NH4)+;
(и) алкилированием 4-(2-хлорэтил)морфолином получили трет-бутиловый эфир (3RS, 4RS, 5SR)-4-[4-(3-бензилоксипропокси)фенил] -5-(2-морфолин-4- илэтокси)-3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 711 (М+Н)+.
Пример 111.
Путем отщепления BOC-группы и одновременно, если таковая имеется, тетрагидропиранильной защитной группы с помощью хлористого водорода в метаноле аналогично примеру 22(м) либо путем отщепления BOC-группы с помощью бромида цинка в метиленхлориде аналогично примеру 10(6) получали следующие соединения:
1) из трет-бутилового эфира (3RS,4SR,5RS)-4-[4-(3-бензилоксипропокси) фенил] -5-гидрокси-3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS,4SR,5RS)-4- [4-(3-бензилоксипропокси)фенил] -3-(нафталин-2-илметокси)пиперидин- 5-ол в виде бесцветного твердого вещества; МС: 499 (М + Н)+;
2) из трет-бутилового эфира (RS)-4-[4-(3-бензилоксипропокси)фенил]-3- (нафталин-2-илметокси)-3,6-дигидро-2Н-пиридин-1-карбоновой кислоты с помощью хлористого водорода в метаноле получили (RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(нафталин-2-илметокси)-1,2,3,6-тетрагидропиридин в виде бесцветного масла; МС: 480 (М+Н)+;
3) из трет-бутилового эфира (3RS,4SR, 5SR)-5-амино-4-[4-(3- бензилоксипропокси)фенил]-3-(нафталин-2-илметокси) пиперидин -1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS,4SR, 5SR)-4-[4-(3-бензилоксипропокси)фенил] -3-(нафталин-2- илметокси)пиперидин-5-иламин в виде бесцветного твердого вещества; МС: 497 (М+Н)+;
4) из смеси трет-бутилового эфира (3RS,4RS,5SR)- и (3SR,4SR,5RS)-4-[4- (3-бензилоксипропокси)фенил] -3-(хинолин-7-илметокси)-5-[2-[(RS)-тетрагидропиран- 2-илокси]этокси]пиперидин-1-карбоновой кислоты получили 2-[4-(3RS, 4RS, 5RS)-4- [4-(3-бензилоксипропокси)фенил]-3-(хинолин-7-илметокси)пиперидин-5- илокси] этанол в виде бесцветного масла; МС: 543 (М+Н)+;
5) из смеси трет-бутилового эфира (3RS, 4SR,5SR)- и (3SR,4RS,5RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(хинолин-7-илметокси)-5- [3-[(RS)- тетрагидропиран-2-илокси] пропокси]пиперидин-1-карбоновой кислоты получили 3-[4-(3RS, 4SR, 5SR)-4-[4-(3-бензилоксипропокси)фенил] -3-(хинолин-7-илметокси)пиперидин-5-илокси]пропан-1-ол в виде бесцветного масла; МС: 557 (М+Н)+;
6) из смеси трет-бутилового эфира (3RS,4SR,5SR)- и (3SR,4RS,5RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(хинолин-7-илметокси)-5- [4-[(RS)-тетрагидропиран-2-илокси] бутокси]пиперидин-1-карбоновой кислоты получили 4-[4-(3RS, 4SR, 5SR)-4-[4-(3-бензилоксипропокси)фенил]-3- (хинолин-7-илметокси)пиперидин-5-илокси]бутан-1-ол в виде бесцветного масла; МС: 571 (М+Н)+.
Использованные в качестве исходных соединений BOC-производные получали следующим путем.
(а) Раствор из 850 мг (1,422 ммоля) трет-бутилового эфира (3RS,4SR,5SR)- 4-[4-(3-бензилоксипропокси)фенил] -5-гидрокси-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты [пример 109(а)] и 1,884 г (7,11 ммоля) трифенилфосфина в 170 мл сухого тетрагидрофурана смешивали при одновременном перемешивании с 274 мкл (7,11 ммоля) сухой муравьиной кислоты и раствором из 1,238 г (7,11 ммоля) диэтилазодикарбоксилата в 42,5 мл тетрагидрофурана. Далее реакционную смесь перемешивали в течение 90 ч при комнатной температуре. Затем смесь упаривали при пониженном давлении и при температуре 40oС, остаток смешивали с раствором из 42,5 мл метанола и 464 мг (7,11 ммоля) гидроксида калия и перемешивали в течение 3 ч при комнатной температуре. После этого раствор смешивали с 500 мл деионизованной воды и смесь четырежды экстрагировали метиленхлоридом порциями по 200 мл. Объединенные органические фазы сушили над сульфатом натрия, упаривали при пониженном давлении и температуре 40oC и остаток сушили в высоком вакууме. Белый кристаллический остаток (4,2 г) хроматографировали на силикагеле с использованием смеси 4:1 метиленхлорида и этилового эфира уксусной кислоты в качестве элюента. Таким путем получили 560 мг (66% от теории) трет-бутилового эфира (3RS,4SR, 5RS)-4-[4-(3-бензилоксипропокси)фенил] -5- гидрокси-3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 598 (М + Н)+.
(б) Раствор из 560 мг (0,937 ммоля) трет-бутилового эфира (3RS,4SR, 5RS)-4-[4-(3-бензилоксипропокси)фенил] -5-гидрокси-3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты и 273 мг (1,031 ммоля) трифенилфосфина в 20 мл сухого тетрагидрофурана смешивали при одновременном перемешивании с 160,2 мкл (1,031 ммоля) диэтилазодикарбоксилата, а по истечении 10 мин - с раствором из 319,8 мкл (1,405 ммоля) дифенилфосфорилазида в 2 мл тетрагидрофурана. Эту смесь перемешивали в течение 72 ч при комнатной температуре, затем упаривали при пониженном давлении и при температуре 40oC и сушили в высоком вакууме. Желтый маслянистый остаток хроматографировали на силикагеле с использованием смеси 4:1 н-гексана и этилового эфира уксусной кислоты в качестве элюента. Таким путем получили 210 мг (36% от теории) трет-бутилового эфира (3RS, 4SR, 5SR)-5-азидо-4-[4-(3-бензилоксипропокси)фенил] -3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты в виде бесцветного масла; МС: 623 (М+Н)+. В качестве дополнительного продукта получили 180 мг (33,1% от теории) трет-бутилового эфира (RS)-4-[4-(3-бензилоксипропокси)фенил] -3- (нафталин-2-илметокси)-3, 6-дигидро-2Н-пиридин-1-карбоновой кислоты также в виде бесцветного масла; МС: 580 (М + Н)+.
(в) Раствор из 50 мг (0,0803 ммоля) трет-бутилового эфира (3RS,4SR, 5SR)-5-азидо-4-[4-(3-бензилоксипропокси)фенил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в 0,36 мл сухого тетрагидрофурана смешивали при одновременном перемешивании с 21 мг (0,0793 ммоля) трифенилфосфина, растворенного в 0,36 мл сухого тетрагидрофурана. Далее смесь перемешивали в течение 4 ч при комнатной температуре (примерно 50%-ное превращение), а затем вновь смешивали с 10,6 мг (0,040 ммоля) трифенилфосфина, после чего перемешивание продолжали в течение последующих 24 ч при комнатной температуре. Затем смешивали с деионизованной водой и перемешивали в течение 1 ч при комнатной температуре. После этого упаривали при пониженном давлении и при температуре 40oC, остаток растворяли в 40 мл простого эфира и экстрагировали в противотоке воды. Органическую фазу сушили на сульфатом натрия и фильтрат упаривали. Бесцветный маслянистый остаток (110 мг) хроматографировали на силикагеле с использованием смеси 4:1 н-гексана и этилового эфира уксусной кислоты в качестве элюента. Таким путем получили 30 мг (63% от теории) трет-бутилового эфира (3RS, 4SR, 5SR)-5-амино-4-[4-(3-бензилоксипропокси)фенил] - 3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 597 (М+Н)+.
Аналогично примеру 1(ж), но при реакционной температуре 50oC из трет-бутилового эфира (3RS,4SR, 5SR)-4- [4-(3-бензилоксипропокси)фенил]-5-гидрокси-3-(хинолин-7-илметокси) пиперидин-1-карбоновой кислоты [пример 109(л)] получали указанные ниже BOC-производные следующим путем:
(г) алкилированием рац. -2-(2-бромэтокси)тетрагидропираном [J. Amer. Chem. Soc. 70, 4187 (1948)] получили смесь трет-бутилового эфира (3RS,4RS, 5SR)- и (3SR, 4SR, 5RS)-4-[4-(3-бензилоксипропокси)фенил]-3- (хинолин-7-илметокси)-5-[2-[(RS)-тетрагидропиран-2-илокси] этокси]пиперидин-1- карбоновой кислоты в виде бесцветного масла; МС: 727 (М+Н)+;
(д) алкилированием рац. -2-(3-бромпропокси)тетрагидропираном [J. Chem. Soc. 1955, 1770] получили смесь трет-бутилового эфира (3RS,4SR,5SR)- и (3SR, 4RS, 5RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(хинолин-7-илметокси)-5-[3-[(RS)-тетрагидропиран-2-илокси] пропокси] пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 741 (М+Н)+;
(е) алкилированием рац.-2-(4-бромбутокси)тетрагидропираном [S.W. Baldwin и др. , J. Org. Chem. 1985, 50, 4432-4439] получили смесь трет-бутилового эфира (3RS,4SR,5SR)- и (3SR,4RS, 5RS)-4-[4-(3- бензилоксипропокси)фенил]-3-(хинолин-7-илметокси)-5-[4-[(RS)- тетрагидропирин-2-илокси]бутокси]пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 755 (М+Н)+.
Пример 112.
Путем отщепления ВОС-группы с помощью бромида цинка в метиленхлориде аналогично примеру 10(б) получали следующие соединения:
1) из трет-бутилового эфира (3R,4s,5S)-3,5-бис(4- метоксибензилокси)-4-{ 4-[3-(2-метоксибензилокси)пропокси] фенил}пиперидин-1-карбоновой кислоты получили (3R, 4s, 5S)-4-[4- [3-(2-метоксибензилокси)пропокси] фенил] -3,5-бис(нафталин-2- илметокси)пиперидин в виде бесцветного масла; МС: 628 (М+Н)+;
2) из трет-бутилового эфира (3RS,4SR, 5SR)-5-гидрокси-3-(4- метоксибензилокси)-4-{4-[3-(2-метоксибензилокси)пропокси] фенил}пиперидин-1-карбоновой кислоты получили (3RS,4SR, 5SR)-3- (4-метоксибензилокси)-4-{4-[3-(2-метоксибензилокси)пропокси] фенил} пиперидин-5-ол в виде бесцветного масла; МС: 508 (М + Н)+;
3) из трет-бутилового эфира (3R,4s, 5S)-4-[4-[3-(2-метоксибензилокси) пропокси] фенил] -3,5-бис(пиридин-2-илметокси)пиперидин-1-карбоновой кислоты получили (3R, 4s, 5S)-2-[5-(пиридин-2-илметокси)-4-[4- [3-(2-метоксибензилокси) пропокси] фенил] пиперидин-3-илоксиметил] пиридин в виде бесцветного масла; МС: 570 (М + Н)+;
4) из трет-бутилового эфира (3RS,4SR, 5SR)-5-гидрокси- 4-{4-[3-(2-метоксибензилокси)пропокси] фенил}-3-(пиридин-2- илметокси)пиперидин-1-карбоновой кислоты получили (3RS,4SR,5SR)- 4-[4-[3-(2-метоксибензилокси)пропокси]фенил] -3-(пиридин-2- илметокси)пиперидин-5-ол в виде бесцветного масла; МС: 479 (М+Н)+;
5) из трет-бутилового эфира (3R, 4s,5S)-4-[4-[3-(2- метоксибензилокси)пропокси] фенил] -3, 5-бис(пиридин-3- илметокси)пиперидин-1-карбоновой кислоты получили (3R, 4s,5S)- 3-[5-(пиридин-3-илметокси)-4-[4-[3-(2-метоксибензилокси)пропокси] фенил] пиперидин-3-илоксиметил]пиридин в виде бесцветного масла; МС: 570 (М + Н)+;
6) из трет-бутилового эфира (3RS,4SR,5SR)-5-гидpoкcи-4-{4-[3-(2- метоксибензилокси)пропокси] фенил} -3-(пиридин-3-илметокси)пиперидин-1- карбоновой кислоты получили (3RS,4SR,5SR)-4-[4-[3-(2-метоксибензилокси)пропокси]фенил] -3- (пиридин-3-илметокси)пиперидин-5-ол в виде бесцветного масла; МС: 479 (М+Н)+;
7) из трет-бутилового эфира (3R, 4s,5S)-4-[4-[3-(2- метоксибензилокси)пропокси] фенил] -3,5-бис(пиридин-4-илметокси) пиперидин-1-карбоновой кислоты получили (3R, 4s,5S)-4-[5-(пиридин-4-илметокси)-4- [4-[3-(2-метоксибензилокси)пропокси] фенил] пиперидин-3- илоксиметил] пиридин в виде бесцветного масла; МС: 570 (М+Н)+;
8) из трет-бутилового эфира (3RS,4SR,5SR)-5-гидрокси-4-{4-[3-(2- метоксибензилокси)пропокси] фенил} -3-(пиридин-4-илметокси) пиперидин-1-карбоновой кислоты получили (3RS,4SR, 5SR)-4-[4-[3- (2-метоксибензилокси)пропокси] фенил] -3-(пиридин-4- илметокси)пиперидин-5-ол в виде бесцветного масла; МС: 479 (М+Н)+;
9) из трет-бутилового эфира (3RS,4SR, 5SR)-5-гидрокси-4-[4-[3- (2-метоксибензилокси)пропокси] фенил]-3-[7-[2-(4-метилпиперазин-1-ил)этокси] нафталин-2-илметокси] пиперидин-1-карбоновой кислоты получили 1-[2- [7-[(3RS, 4SR, 5SR)-5-гидрокси-4-[4-[3-(2-метоксибензилокси)пропокси] фенил] пиперидин-3-илоксиметил] нафталин-2-илокси]этил]-4-метилпиперазин в виде аморфного бесцветного твердого вещества; МС: 670 (М+Н)+ ;
10) из трет-бутилового эфира (3R,4s,5S)-3,5-бис(1,4-диметоксинафталин-2-илметокси)-4-[4-[3- (2-метоксибензилокси)пропокси] фенил]пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3R,4s, 5S)-3,5-бис(1,4-диметоксинафталин-2-илметокси)-4- [4-[3-(2-метоксибензилокси)пропокси]фенил]пиперидин в виде бесцветного воска; МС: 788 (М+Н)+;
11) из трет-бутилового эфира (3RS,4SR,5SR)-3-(1,4-диметоксинафталин-2- илметокси)-5-гидрокси-4-[4-[3-(2-метоксибензилокси)пропокси]фенил}пиперидин-1- карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS, 4SR,5SR)-3-(1,4-диметоксинафталин-2-илметокси)-4-[4- [3-(2-метоксибензилокси)пропокси] фенил] пиперидин-5-ол в виде бесцветного масла; МС: 588 (М+Н)+ .
Использованные в качестве исходных соединений BOC-производные получали следующим путем.
(α) Аналогично примеру 44(д) алкилированием трет-бутилового эфира (3R, 4s, 5S)-3,5-дигидрокси-4-(4-гидроксифенил)пиперидин-1-карбоновой кислоты [пример 109(η) ] 2-метоксибензил-3-хлорпропиловым эфиром [пример 120(ж)] получили трет-бутиловый эфир (3R,4s,5S)-3, 5- дигидрокси-4-{4-[3-(2-метоксибензилокси)пропокси] фенил} пиперидин-1-карбоновой кислоты в виде аморфного бесцветного твердого вещества; МС: 505 (М + NH4)+.
(β) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3R, 4s, 5S)-3,5-дигидpoкcи-4-{4-[3-(2-метоксибензилокси)пропокси] фенил}пиперидин-1-карбоновой кислоты с использованием одного эквивалента бензильного галогенида примерно в равных количествах получили непрореагировавший исходный материал, а также соответствующие моно- и диалкилированные BOC-производные. Эти смеси затем разделяли с помощью хроматографии:
(а) алкилированием 4-метоксибензилхлоридом получили трет-бутиловый эфир (3R, 4s, 5S)-3,5-бис(4-метоксибензилокси)-4-{ 4- [3-(2-метоксибензилокси)пропокси] фенил} пиперидин-1-карбоновой кислоты [МС: 746 (M+NH4)]+ и трет-бутиловый эфир (3RS,4SR, 5SR)-5-гидрокси-3-(4-метоксибензилокси)-4-{4- [3-(2-метоксибензилокси)пропокси] фенил} пиперидин-1-карбоновой кислоты [МС: 626 (М + NH4)+] в каждом случае в виде аморфного бесцветного твердого вещества;
(б) алкилированием гидрохлоридом 2-хлорметилпиридина и соответствующим избытком основания получили трет-бутиловый эфир (3R,4s, 5S)-4-[4-[3-(2-метоксибензилокси)пропокси] фенил] -3,5-бис(пиридин-2-илметокси)пиперидин-1-карбоновой кислоты [МС: 670 (М+Н)+] и трет-бутиловый эфир (3RS,4SR,5SR)-5-гидрокси-4- { 4-[3-(2-метоксибензилокси)пропокси] фенил}-3-(пиридин-2-илметокси)пиперидин- 1-карбоновой кислоты [МС: 579 (М+Н)+] в каждом случае в виде аморфного бесцветного твердого вещества;
(в) алкилированием гидрохлоридом 3-хлорметилпиридина и соответствующим избытком основания получили трет-бутиловый эфир (3R,4s,5S)-4-[4-[3-(2-метоксибензилокси)пропокси] фенил] -3, 5-бис(пиридин-3- илметокси)пиперидин-1-карбоновой кислоты [МС: 670 (М+Н)+] и трет-бутиловый эфир (3RS,4SR,5SR)-5-гидрокси-4-{ 4-[3-(2-метоксибензилокси)пропокси] фенил} -3- (пиридин-3-илметокси)пиперидин-1-карбоновой кислоты [МС: 579 (М+Н)+] в каждом случае в виде аморфного бесцветного твердого вещества;
(г) алкилированием гидрохлоридом 4-хлорметилпиридина и соответствующим избытком основания получили трет-бутиловый эфир (3R,4s,5S)-4-[4-[3-(2-метоксибензилокси)пропокси] фенил] -3,5- бис(пиридин-4-илметокси)пиперидин-1-карбоновой кислоты [МС: 670 (М+Н)+] и трет-бутиловый эфир (3RS,4SR,5SR)-5-гидрокси-4-{ 4- [3-(2-метоксибензилокси)пропокси]фенил}-3-(пиридин-4- илметокси)пиперидин-1-карбоновой кислоты [МС: 579 (М+Н)+] в каждом случае в виде аморфного бесцветного твердого вещества.
(д) Алкилированием трет-бутилового эфира (3R,4s,5S)-3,5-дигидрокси-4-{ 4-[3-(2-метоксибензилокси)пропокси] фенил} пиперидин-1-карбоновой кислоты [пример 112 (α) ] 2-хлорметил-7-(2-триметилсиланилэтоксиметокси)нафталином[пример 6(х)] получили трет-бутиловый эфир (3RS,4SR,5SR)-5-гидрокси-4-[4- [3-(2-метоксибензилокси)пропокси] фенил]-3-[7-(2-триметилсиланилэтоксиметокси) нафталин-2-илметокси] пиперидин-1-карбоновой кислоты в виде светло-желтого масла; МС: 774 (М+Н)+. Этот продукт далее аналогично примеру 95(б) путем отщепления СЭМ-защитной группы превращали в трет-бутиловый эфир (3RS,4SR,5SR)-5-гидрокси-4-[4-[3-(2- метоксибензилокси)пропокси] фенил] -3-(7-гидроксинафталин-2-илметокси) пиперидин-1-карбоновой кислоты [желтое масло; МС: 644 (М+Н)+], алкилированием которого гидрохлоридом 1-(2-хлорэтил)-4-метилпиперазина [Chim. Ther. 4, 283 (1969)] аналогично примеру 90(o) получили трет-бутиловый эфир (3RS,4SR,5SR)-5-гидрокси-4-[4-[3-(2-метоксибензилокси)пропокси] фенил] -3- [7-[2-(4-метилпиперазин-1-ил)этокси] нафталин-2-илметокси] пиперидин-1- карбоновой кислоты в виде светло-коричневого масла; МС: 770 (М+Н)+.
(е) Алкилированием трет-бутилового эфира (3R,4s,5S)-3, 5-дигидрокси-4-{ 4-[3-(2-метоксибензилокси)пропокси] фенил} пиперидин-1-карбоновой кислоты [пример 112 (α) ] 2-хлорметил-1,4-диметоксинафталином [J. Org. Chem. (1983), 48(19), 3265-3268] получили трет-бутиловый эфир (3R,4s,5S)-3,5-бис(1,4-диметоксинафталин-2-илметокси)-4-[4-[3- (2-метоксибензилокси)пропокси] фенил] пиперидин-1-карбоновой кислоты [МС: 906 (М+Н)+] в виде бесцветной пены и трет-бутиловый эфир (3RS,4SR,5SR)-3-(1,4- диметоксинафталин-2-илметокси)-5-гидрокси-4-{ 4-[3-(2-метоксибензилокси) пропокси]фенил}пиперидин-1-карбоновой кислоты [МС: 705 (M+NH4)+] в виде бесцветного масла.
Пример 113.
Путем отщепления BOC-группы с помощью бромида цинка в метиленхлориде аналогично примеру 10(б) получали следующие соединения:
1) из трет-бутилового эфира (3RS,4SR,5SR)-4-[4-(3- бензилоксипропокси)фенил]-5-гидрокси-3-(4- гидроксибензилокси)пиперидин-1-карбоновой кислоты получили (3RS, 4SR,5SR)-4-[4-(3-бензилоксипропокси)фенил]-3- (гидроксибензилокси)пиперидин-5-ол в виде бесцветного масла; МС: 464 (М+Н)+;
2) из трет-бутилового эфира (3R,4s, 5S)-4-[4-(3-бензилоксипропокси)фенил] - 3,5-бис(4-гидроксибензилокси)пиперидин-1-карбоновой кислоты получили 4-[(3R,4s,5S)-5-(4-гидроксибензилокси)-4-[4-(3-бензилоксипропокси)фенил] пиперидин-3-илоксиметил] фенол в виде бесцветного масла; МС: 570 (М+Н)+.
Использованные в качестве исходных соединений BOC-производные получали следующим путем.
(а) (α) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3R, 4s, 5S)-4-[4-(3-бензилоксипропокси)фенил] -3,5-дигидроксипиперидин-1-карбоновой кислоты [пример 109 (θ) ] 1-хлорметил-4-(2-триметилсиланилэтоксиметокси)бензолом получили трет-бутиловый эфир (3RS,4SR,5SR)-4-[4-(3-бензилоксипропокси)фенил] -5-гидрокси-3-[4-(2-триметилсиланилэтоксиметокси)бензилокси] пиперидин-1-карбоновой кислоты [Rf 0,33 (SiO2, н-гексан: этиловый эфир уксусной кислоты = 2:1)] и трет-бутиловый эфир (3R,4s,5S)-4-[4-(3-бензилоксипропокси)фенил] -3,5-бис[4-(2- триметилсиланилэтоксиметокси)бензилокси]пиперидин-1-карбоновой кислоты [Rf 0,64 (SiO2, н-гексан:этиловый эфир уксусной кислоты = 2:1)] в каждом случае в виде аморфного бесцветного твердого вещества.
(a) (β) Раствор из 2,16 г (3,113 ммоля) трет-бутилового эфира (3RS,4SR, 5SR)-4-[4-(3-бензилоксипропокси)фенил] -5-гидрокси- 3-[4-(2-триметилсиланилэтоксиметокси)бензилокси] пиперидин-1- карбоновой кислоты в 50 мл метанола смешивали с 2,02 мл (4,046 ммоля) безводного 2 М раствора хлористого водорода в метаноле и перемешивали в течение 2 ч при комнатной температуре. Далее смешивали с 100 мл смеси 95:5 метиленхлорида и метанола (экстракция в противотоке 5 об.% насыщенного водного раствора аммиака) и раствор упаривали на ротационном испарителе при 30oC. Белое твердое вещество (2,17 г) затем хроматографировали на силикагеле с использованием смеси 4:1 метиленхлорида и этилового эфира уксусной кислоты в качестве элюента. Таким путем получили 780 мг (45% от теории) трет- бутилового эфира (3RS,4SR,5SR)-4-[4-(3-бензилоксипропокси)фенил] -5- гидрокси-3-(4-гидроксибензилокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 581 (M+NH4)+.
(б) Раствор из 1,1 г (1,18 ммоля) трет-бутилового эфира (3R,4s,5S)-4- [4-(3-бензилоксипропокси)фенил] -3,5-бис[4-(2-триметилсиланилэтоксиметокси) бензилокси] пиперидин-1-карбоновой кислоты в 20 мл метанола смешивали с 1,30 мл (2,60 ммоля) безводного 2М раствора хлористого водорода в метаноле и перемешивали в течение 70 мин при комнатной температуре. Далее смешивали с 50 мл смеси 95: 5 метиленхлорида и метанола (экстракция в противотоке 5 об.% насыщенного водного раствора аммиака) и раствор упаривали на ротационном испарителе при 30oC. Белое твердое вещество (920 мг) затем хроматографировали на силикагеле с использованием смеси 4:1 метиленхлорида и этилового эфира уксусной кислоты в качестве элюента. Таким путем получили 300 мг (38% от теории) трет-бутилового эфира (3R, 4s, 5S)-4-[4-(3- бензилоксипропокси)фенил] -3,5-бис(4-гидроксибензилокси)пиперидин- 1-карбоновой кислоты в виде бесцветного масла; Rf 0,26 (SiO2, н-гексан:этиловый эфир уксусной кислоты = 1:1).
Использованный в качестве алкилирующего агента 1-хлорметил-4-(2- триметилсиланилэтоксиметокси) бензол получали благодаря тому, что аналогично примеру 5(а)-(в) метиловый эфир 4-гидроксибензойной кислоты путем введения СЭМ-группы превращали в метиловый эфир 4- (2-триметилсиланилэтоксиметокси)бензойной кислоты. Последующим восстановлением алюмогидридом лития был получен [4-(2- триметилсиланилэтоксиметокси)фенил] метанол, хлорированием которого получили 1-хлорметил- 4-(2-триметилсиланилэтоксиметокси)бензол в виде бесцветного масла; МС: 272 (М)+ .
Пример 114.
Аналогично примеру 1(д) путем отщепления СЭМ-группы с помощью тетрабутиламмонийфторида в тетрагидрофуране получали следующие соединения:
1) из 2-триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)-3-[4-(2-морфолин-4-илэтокси)нафталин-2-илметокси] пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-(4-фторфенил)-3-[4-(2-морфолин-4-илэтокси) нафталин-2-илметокси]пиперидин-1 в виде бесцветного твердого вещества; МС: 465 (М)+;
2) из 2-триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)-3- [8-(3-метоксипропокси)нафталин-2-илметокси] пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-(4-фторфенил)-3-[8-(3-метоксипропокси)нафталин-2- илметокси]пиперидин в виде бесцветного твердого вещества; МС: 424 (М)+;
3) из 2-триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)-3-[5- (3-метоксипропокси)нафталин-2-илметокси] пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-(4-фторфенил)-3-[5-(3- метоксипропокси)нафталин-2-илметокси]пиперидин в виде бесцветного твердого вещества; МС: 424 (М)+;
4) из 2-триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)-3-[7-(3-метоксипропокси)нафталин-2-илметокси] пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-(4-фтopфeнил)-3-[7-(3- метоксипропокси)нафталин-2-илметокси] пиперидин в виде бесцветного твердого вещества; МС: 424 (М)+.
Использованные в качестве исходных субстанций СЭМ-производные получали следующим путем:
(а) из 2-триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)-3-(4-гидроксинафталин-2-илметокси) пиперидин-1-карбоновой кислоты [пример 5(ж)] и гидрохлорида 4-(2-хлорэтил)морфолина получили 2-триметилсилил-этиловый эфир (3RS, 4RS)-4- (4-фтopфeнил)-3-[4-(2-мopфoлин-4- илэтокси)нафталин-2-илметокси]пиперидин-1-карбоновой кислоты в виде желтого масла; МС: 609 (М)+;
(б) из 2-триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)-3- (8-гидроксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты [пример 6(гг)] и 1-хлор-3-метоксипропана получили 2- триметилсилилэтиловый эфир (3RS,4RS)-4-(4-фторфенил)-3-[8-(3- метоксипропокси) нафталин-2-илметокси]пиперидин-1-карбоновой кислоты в виде светло-желтого масла; МС: 568 (М)+;
(в) из 2-триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)-3-(5 - гидроксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты [пример 6(м)] и 1-хлор-3-метоксипропана получили 2- триметилсилилэтиловый эфир (3RS,4RS)-4-(4-фторфенил)-3-[5-(3- метоксипропокси)нафталин-2-илметокси]пиперидин-1-карбоновой кислоты в виде бесцветной смолы, который без дальнейшей очистки и определения характеристик использовали в последующей реакции;
(г) из 2-триметилсилилэтилового эфира (3RS, 4RS)-4-(4-фторфенил)-3-(7-гидроксинафталин-2-илметокси) пиперидин-1-карбоновой кислоты [пример 6(ш)] и 1-хлор-3-метоксипропана получили 2- триметилсилилэтиловый эфир (3RS, 4RS)-4-(4-фторфенил)-3-[7-(3- метоксипропокси)нафталин-2-илметокси]пиперидин-1-карбоновой кислоты в виде бесцветной смолы, который без дальнейшей очистки и определения характеристик использовали в последующей реакции.
Пример 115.
Аналогично примеру 5 получали (3RS,4RS)-4-(4-фтopфeнил)-3-[4-[3- гидроксибензилокси]нафталин-2-илметокси]пиперидин, работая следующим образом.
(а) Аналогично примеру 5(а)-(г) сначала из этилового эфира 3-гидроксибензойной кислоты путем введения СЭМ-группы получили этиловый эфир 3-(2-триметилсилилэтоксиметокси)бензойной кислоты в виде бесцветного масла; МС: 238 [M-(C2H4+CH2O)]+. В результате последующего восстановления получили [3-(2-триметилсилилэтоксиметокси)фенил] метанол, МС: 196 [M-(C2H4+CH2O)]+, в виде бесцветного масла, хлорированием которого получили 1-хлорметил-3-(2-триметилсилилэтоксиметокси) бензол в виде бесцветного масла; МС: 214, 216 [М-(C2H4+CH2O)]+. Последующим алкилированием 2-триметилсилилэтилового эфира (3RS, 4RS)-4-(4-фторфенил)-3-(4-гидроксинафталин-2-илметокси) пиперидин-1-карбоновой кислоты [пример 5(ж)] 1-хлорметил-3-(2-триметилсилилэтоксиметокси)бензолом получили 2-триметилсилилэтиловый эфир (3RS,4RS)-4-(4-фторфенил)-3-[4- [3-(2-триметилсилилэтоксиметокси)бензилокси] нафталин-2-илметокси] пиперидин-1-карбоновой кислоты в виде светло-желтого масла; МС: 749 (M+NH4)+.
(б) Из 2-триметилсилилэтилового эфира (3RS,4RS)-4-(4-фторфенил)-3-[4- [3-(2-триметилсилилэтоксиметокси)бензилокси] нафталин-2-илметокси] пиперидин-1- карбоновой кислоты аналогично описанному в примере 1(д) способу путем отщепления 2-триметилсилилэтилкарбамата с помощью тетрабутиламмонийфторида в тетрагидрофуране получили (3RS, 4RS)-4-(4-фторфенил)-3-[4-[3-(2-триметилсилилэтоксиметокси)бензилокси] нафталин-2-илметокси]пиперидин [МС: 588 (М+Н)+] в виде светло-желтого масла, из которого отщеплением СЭМ-группы с помощью 2 н. раствора хлористого водорода в метаноле аналогично описанному в примере 5(ж) способу был получен (3RS,4RS)-4-(4-фторфенил)-3-[4- [3-гидроксибензилокси] нафталин-2-илметокси] пиперидин в виде бесцветного твердого вещества; МС: 458 (М+Н)+.
Пример 116.
Аналогично примеру 10(б) путем отщепления BOC-группы с помощью бромида цинка в метиленхлориде получили следующее соединение:
- из трет-бутилового эфира (3RS,4RS)-3-(нaфтaлин-2-илмeтoкcи)-4-[4-[2-(5-фенил-[1,3,4] оксадиазол-2-ил)этил]фенил]пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS,4RS)-3-(нафталин-2-илметокси)-4-[4-[2-(5-фенил [1,3,4] оксадиазол-2-ил)этил] фенил]пиперидин в виде бесцветного твердого вещества; МС: 490 (М+Н)+.
Использованное в качестве исходной субстанции BOC-производное получали следующим путем.
(а) Из трет-бутилового эфира (3RS, 4RS)-4-[4-(2-карбоксиэтил)фенил]-3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты [пример 86(мм)] реакцией конденсации с гидразидом бензойной кислоты в присутствии ЭДК аналогично примеру 38 был получен трет-бутиловый эфир (3RS,4RS)-4- [4-[3-(N'-бензоилгидразин)-3-оксопропил] фенил] -3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты в виде бесцветной смолы; МС: 608 (М+Н)+.
(б) Раствор из 106 мг (0,174 ммоля) трет-бутилового эфира (3RS,4RS)-4-[4-[3-(N'-бензоилгидразин)-3-оксопропил] фенил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в 1,5 мл гексаметилдисилазана смешивали с 39 мкл (0,039 ммоля) 1 М раствора тетрабутиламмонийфторида в тетрагидрофуране и нагревали с обратным холодильником в течение 20 ч. Для дальнейшей переработки реакционную смесь смешивали с 50 мл смеси 1:1 метиленхлорида и воды, затем отделяли органическую фазу, а водную фазу дважды экстрагировали метиленхлоридом порциями по 25 мл. Объединенные органические фазы сушили над сульфатом натрия и упаривали при пониженном давлении. Сырой продукт очищали хроматографией быстрого разрешения на силикагеле с использованием смеси 7:3 гексана и уксусного эфира в качестве элюента. Таким путем получили 70 мг (68% от теории) трет-бутилового эфира (3RS,4RS)-3-(нафталин-2- илметокси)-4-[4-[2-(5-фенил[1,3,4] оксадиазол-2-ил)этил] фенил] пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 590 (М+Н)+.
Пример 117.
Аналогично примеру 22(м) путем отщепления BOC-группы с помощью хлористого водорода в метаноле получили следующее соединение:
- из трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропил)фенил]-3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты получили (3RS,4RS)-4- [4-(3-бензилоксипропил)фенил] -3-(нафталин-2-илметокси)пиперидин в виде бесцветного аморфного твердого вещества; МС: 467 (М+Н)+.
Использованное в качестве исходной субстанции BOC-производное получали следующим путем.
Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS, 4RS)-4-[4-(3-гидроксипропил)фенил] -3-(нафталин-2- илметокси) пиперидин-1-карбоновой кислоты [пример 24(ф)] бензилбромидом получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(3- бензилоксипропил)фенил] -3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты в виде бесцветного аморфного твердого вещества, который без определения характеристик использовали на следующей стадии.
Пример 118.
Путем отщепления BOC-группы с помощью хлористого водорода в метаноле аналогично примеру 22(м) получали следующие соединения:
1) из трет-бутилового эфира (3RS,4RS)-3-(нафталин-2-илметокси)-4-[4- (2-феноксиэтоксиметил)фенил] пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-3-(нафталин-2-илметокси)-4-[4-(2- феноксиэтоксиметил)фенил]пиперидин в виде светло-желтого масла; МС: 468 (М+Н)+;
2) из трет-бутилового эфира (3RS,4RS)-3-(нафталин-2-илметокси)-4-[4- (3-феноксипропоксиметил)фенил] пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-3-(нафталин-2-илметокси)-4-[4-(3-феноксипропоксиметил)фенил] пиперидин в виде бесцветной пены; МС: 482 (М+Н)+;
3) из трет-бутилового эфира (3RS, 4RS)-4-[4-(3-бензилоксипропоксиметил) фенил]-3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-[4-(3-бензилоксипропоксиметил)фенил] -3-(нафталин-2-илметокси)пиперидин в виде светло-желтого масла; МС: 496 (М+Н)+;
4) из трет-бутилового эфира (3RS,4RS)-4-[4-[3-(4-фторфенокси)пропоксиметил] фенил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты получили (3RS,4RS)-4-[4-[3-(4-фторфенокси)пропоксиметил]фенил]-3-(нафталин-2- илметокси)пиперидин в виде светло-желтого масла; МС: 500 (М+Н)+.
Использованные в качестве исходных веществ BOC-производные получали путем алкилирования трет-бутилового эфира (3RS,4RS)-4-(4- гидроксиметилфенил)-3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты [пример 22(к)] аналогично примеру 1(ж) следующим образом:
(а) алкилированием β-бромфенетолом получили трет-бутиловый эфир (3RS, 4RS)-3-(нафталин-2-илметокси)-4-[4-(2-феноксиэтоксиметил)фенил] пиперидин-1-карбоновой кислоты в виде бесцветной смолы, который без определения характеристик использовали в последующей реакции;
(б) алкилированием 3-феноксипропилбромидом получили трет-бутиловый эфир (3RS,4RS)-3-(нафталин-2-илметокси)-4-[4-(3-феноксипропоксиметил)фенил] пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 582 (М+Н)+;
(в) алкилированием бензил-3-бромпропиловым эфиром получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(3-бензилоксипропоксиметил)фенил]-3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветной смолы; МС: 596 (М+Н)+;
(г) алкилированием 1-(3-хлорпропокси)-4-фторбензолом получили трет-бутиловый эфир (3RS, 4RS)-4-[4-[3-(4-фторфенокси)пропоксиметил] фенил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветной смолы; МС: 600 (М+Н)+.
Пример 119.
Путем отщепления BOC-группы с помощью хлористого водорода в метаноле аналогично примеру 22(м) либо с помощью бромида цинка в метиленхлориде аналогично примеру 10(б) получали следующие соединения:
1) из трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси) фенил] -3-(8-гидроксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты с помощью хлористого водорода в метаноле получили (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил]-3-(8-гидроксинафталин-2-илметокси) пиперидин в виде бесцветного твердого вещества; МС: 498 (М+Н)+;
2) из трет-бутилового эфира (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил]- 3-[8-(3-метоксиэтокси)нафталин-2-илметокси] пиперидин-1-карбоновой кислоты с помощью хлористого водорода в метаноле получили (3RS, 4RS)-4- [4-(3-бензилоксипропокси)фенил] -3-[8-(3-метоксиэтокси)нафталин-2-илметокси] пиперидин в виде светло-желтого масла; МС: 556 (М+Н)+;
3) из трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил]- 3-[8-(3-метоксипропокси)нафталин-2-илметокси] пиперидин-1-карбоновой кислоты с помощью хлористого водорода в метаноле получили (3RS, 4RS)-4-[4-(3- бензилоксипропокси)фенил] -3-[8-(3-метоксипропокси)нафталин-2- илметокси] пиперидин в виде светло-желтого масла; МС: 570 (М+Н)+;
4) из трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил]- 3-(8-метоксикарбонилметоксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты с помощью хлористого водорода в метаноле получили (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(8-метоксикарбонилметоксинафталин- 2-илметокси)пиперидин в виде бесцветного твердого вещества; МС: 570 (М+Н)+;
5) из трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил]- 3-(8-карбамоилметоксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS, 4RS)-4-[4-(3-бeнзилoкcипpoпoкcи)фeнил] -3-(8-карбамоилметоксинафталин-2- илметокси)пиперидин в виде бесцветной пены; МС: 555 (М+Н)+.
Использованные в качестве исходных веществ BOC-производные получали аналогично примерам 1 и 5 путем алкилирования трет-бутилового эфира (3RS, 4RS)-4-[4-(3- бензилоксипропокси)фенил] -3-(8-гидpoкcинaфтaлин-2-илметокси) пиперидин-1-карбоновой кислоты следующим образом:
(а) алкилированием 2-метоксиэтилбромидом получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил]-3-[8-(3- метоксиэтокси)нафталин-2-илметокси] пиперидин-1-карбоновой кислоты в виде бесцветной смолы, который без определения характеристик использовали в последующей реакции;
(б) алкилированием 1-хлор-3-метоксипропаном получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил]-3-[8-(3-метоксипропокси)нафталин-2- илметокси]пиперидин-1-карбоновой кислоты в виде светло-желтой смолы, который без определения характеристик использовали в последующей реакции;
(в) алкилированием метиловым эфиром бромуксусной кислоты получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил]-3- (8-метоксикарбонилметоксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 670 (М + Н)+;
(г) алкилированием иодацетамидом получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(8-карбамоилметоксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде светло-желтой смолы, который без определения характеристик использовали в последующей реакции.
Использованный в качестве исходного вещества трет-бутиловый эфир (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] - 3-(8-гидроксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты получали аналогично примерам 1, 5 и 6 следующим образом.
(а) Путем алкилирования трет-бутилового эфира (3RS,4RS)-4-[4-(3- бензилоксипропокси)фенил]-3-гидроксипиперидин-1-карбоновой кислоты [пример 86(о)] 2-хлорметил-8-(2-триметилсилилэтоксиметокси)нафталином [пример 6(аа)] получили трет-бутиловый эфир (3RS,4RS)-4-[4-(3-бензилоксипропокси) фенил]-3-[8-(2-триметилсиланилэтоксиметокси)нафталин-2-илметокси]пиперидин-1- карбоновой кислоты в виде светло-желтого масла; МС: 728 (М + Н)+.
(б) Раствор из 552 мг трет-бутилового эфира (3RS,4RS)-4-[4-(3- бензилоксипропокси)фенил] -3-[8-(2-триметилсиланилэтоксиметокси)нафталин-2- илметокси] пиперидин-1 карбоновой кислоты в 4 мл метанола смешивали с 4 мл 2 н. раствора хлористого водорода в метаноле и перемешивали в течение 45 мин при комнатной температуре. Смесь для дальнейшей переработки распределяли между 50 мл уксусного эфира и 50 мл водного 5%-ного раствора гидрокарбоната натрия и затем отделяли органическую фазу. Водную фазу трижды экстрагировали уксусным эфиром порциями по 25 мл. Объединенные уксусноэфирные фазы сушили над сульфатом магния и в завершение отгоняли растворитель при пониженном давлении. Сырой продукт (538 мг) очищали хроматографией на силикагеле с использованием смеси 1:2 уксусного эфира и гексана в качестве элюента. Таким путем получили 348 мг (77% от теории) трет-бутилового эфира (3RS,4RS)-4-[4-(3- бензилоксипропокси)фенил] -3-(8-гидроксинафталин-2-илметокси) пиперидин-1-карбоновой кислоты в виде бесцветной пены; МС: 598 (М + Н)+.
Пример 120.
Путем отщепления BOC-группы с помощью хлористого водорода в метаноле аналогично примеру 22(м) или с помощью бромида цинка в метиленхлориде аналогично примеру 10(б) получали следующие соединения:
1) из трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил]- 3-(хинолин-7-илметокси)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4- [4-(3-бензилоксипропокси)фенил]-3-(хинолин-7-илметокси)пиперидин в виде бесцветного масла; МС: 483 (М+Н)+;
2) из трет-бутилового эфира (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил]- 3-(1,2,3,4-тетрагидрохинолин-7-илметокси)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] -3- (1,2,3, 4-тетрагидрохинолин-7-илметокси)пиперидин в виде светло- желтой смолы; МС: 487 (М+Н)+;
3) из иодида (3RS, 4RS)-7-[4-[4-(3-бензилоксипропокси)фенил] -1-трет- бутоксикарбонилпиперидин-3-илоксиметил] -1-метилхинолиния получили хлорид (3RS, 4RS)-7-[4-[4-(3-бензилоксипропокси)фенил]пиперидин-3- илоксиметил]-1-метилхинолиния в виде бесцветного твердого вещества; МС: 497 (М)+;
4) из трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(1-метил-1,2,3,4-тетрагидрохинолин-7-илметокси)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил]-3-(1-метил-1,2,3,4-тетрагидрохинолин-7-илметокси)пиперидин в виде светло-желтого масла; МС: 501 (М+Н)+;
5) из трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(изохинолин-6-илметокси) пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(изохинолин-6-илметокси) пиперидин в виде светло-желтой смолы; МС: 483 (М+Н)+;
6) из трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(2-метил- 1,2, 3,4-тетрагидроизохинолин-6-илметокси)пиперидин- 1-карбоновой кислоты получили (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил]-3 -(2-метил-1,2,3,4-тетрагидроизохинолин-6-илметокси)пиперидин в виде светло-желтого масла; МС: 501 (М+Н)+;
7) из трет-бутилового эфира (3RS, 4RS)-4-[4-[3-(2-метоксибензилокси) пропокси] фенил]-3-(хинолин-7-илметокси)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-[4-[3-(2-метоксибензилокси)пропокси] фенил]-3-(хинолин-7- илметокси)пиперидин в виде светло-желтой смолы; МС: 513 (М+Н)+;
8) из трет-бутилового эфира (3RS,4RS)-3-(1Н-бензимидазол-5-илметокси)-4- [4-(3-бензилоксипропокси)фенил] пиперидин-1-карбоновой кислоты с помощью хлористого водорода в метаноле получили (3RS, 4RS)-3-(1Н-бензимидазол-5-илметокси)-4-[4-(3- бензилоксипропокси)фенил] пиперидин в виде бесцветной смолы; МС: 472 (М + Н)+;
9) из трет-бутилового эфира (3RS, 4RS)-4-[4-[3-(2- метоксибензилокси)пропокси] фенил]-3-(1-оксихинолин-7- илметокси)пиперидин-1-карбоновой кислоты с помощью хлористого водорода в метаноле получили (3RS, 4RS)-4-[4-[3-(2- метоксибензилокси)пропокси]фенил]-3-(1-оксихинолин-7-илметокси)пиперидин в виде бесцветного твердого вещества; МС: 529 (М+Н)+;
10) из трет-бутилового эфира (3RS, 4RS)-4-[4-[3-(2- метоксибензилокси)пропокси] фенил]-3-(2-оксо-1,2-дигидрохинолин- 7-илметокси) пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS, 4RS)-4-[4-[3-(2- метоксибензилокси)пропокси] фенил]-3-(2-оксо-1,2- дигидрохинолин-7-илметокси)пиперидин в виде бесцветного твердого вещества; МС: 529 (М+Н)+;
11) из трет-бутилового эфира (3RS,4RS)-3- (изохинолин-7-илметокси)-4-[4-[3-(2-метоксибензилокси)пропокси] фенил]пиперидин-1-карбоновой кислоты с помощью хлористого водорода в метаноле получили (3RS, 4RS)-3-(изохинолин-7-илметокси)- 4-[4-[3-(2-метоксибензилокси)пропокси] фенил] пиперидин в виде светло-желтого масла; МС: 513 (М+Н)+;
12) из трет-бутилового эфира (3RS, 4RS)-4-[4-[3-(2-метоксибензилокси)пропокси] фенил] -3- (1,2,3,4-тетрагидрохинолин-7-илметокси)пиперидин-1-карбоновой кислоты с помощью хлористого водорода в метаноле получили (3RS, 4RS)-4-[4-[3-(2-метоксибензилокси)пропокси] фенил] -3- (1,2,3,4-тетрагидрохинолин-7-илметокси)пиперидин в виде светло- желтого сиропа; МС: 517 (М+Н)+;
13) из трет-бутилового эфира (3RS, 4RS)-4-[4-[3-(2-метоксибензилокси)пропокси]фенил]-3- (хиноксалин-6-илметокси)пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS, 4RS)-4-[4-[3-(2- метоксибензилокси)пропокси] фенил] -3-(хиноксалин-6-илметок си)пиперидин в виде желтого масла; МС: 514 (М+Н)+.
Использованные в качестве исходных веществ BOC-производные получали аналогично примерам 1 и 5 следующим образом.
(а) Путем алкилирования трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3- гидроксипиперидин-1-карбоновой кислоты [пример 86(о)] гидробромидом 7-бромметилхинолина [J. Am. Chem. Soc. 77, 1054, (1955)] аналогично примеру 1(ж) получили трет-бутиловый эфир (3RS, 4RS)-4- [4-(3-бензилоксипропокси)фенил] -3-(хинолин-7-илметокси) пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 583 (М+Н)+.
(б) Раствор из 116 мг (0,20 ммоля) трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3- (хинолин-7-илметокси)пиперидин-1-карбоновой кислоты в 1,5 мл метанола смешивали с 24 мг (0,1 ммоля) гексагидрата хлорида никеля(II) и 30 мг (0,8 ммоля) борогидрида натрия. Суспензию темной окраски перемешивали в течение 1 ч при 0oC, а затем в течение еще 1 ч при комнатной температуре. Смесь для дальнейшей переработки распределяли между 20 мл простого эфира и 5 мл водного насыщенного раствора хлорида аммония и затем отделяли органическую фазу. Водную фазу трижды экстрагировали простым эфиром порциями по 20 мл. Объединенные эфирные фазы сушили над сульфатом магния и в завершение отгоняли растворитель при пониженном давлении. Сырой продукт (150 мг) очищали хроматографией на силикагеле с использованием смеси 1:1 уксусного эфира и гексана в качестве элюента. Таким путем получили 70 мг (60% от теории) трет- бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3- (1,2,3, 4-тетрагидрохинолин- 7-илметокси)пиперидин-1-карбоновой кислоты в виде светло-желтой смолы; МС: 587 (М+Н)+.
(в) Раствор из 146 мг (0,25 ммоля) трет-бутилового эфира (3RS, 4RS)-4- [4-(3-бензилоксипропокси)фенил] -3-(хинолин-7-илметокси)пиперидин-1- карбоновой кислоты в 0,5 мл абсолютного хлороформа смешивали с 40 мкл (0,6 ммоля) метилиодида и нагревали с обратным холодильником в течение 3 ч. Далее дополнительно добавляли 40 мкл метилиодида и смесь выдерживали при температуре дефлегмации в течение ночи. После отгонки растворителя при пониженном давлении получили сырой иодид (3RS,4RS)-7-[4-[4-(3-бензилоксипропокси)фенил]-1-трет- бутоксикарбонилпиперидин-3-илоксиметил]-1-метилхинолиния, который без определения характеристик использовали в последующей реакции.
(г) Раствор из 91 мг (0,125 ммоля) сырого иодида (3RS,4RS)-7-[4- [4-(3-бензилоксипропокси)фенил]-1-трет-бутоксикарбонилпиперидин- 3-илоксиметил] -1-метилхинолиния в 1 мл метанола смешивали при 0oC с 47 мг (0,125 ммоля) борогидрида натрия, затем нагревали до комнатной температуры и перемешивали в течение 2 ч при комнатной температуре. Смесь для дальнейшей переработки распределяли между 50 мл уксусного эфира и 50 мл водного 5%-ного раствора гидрокарбоната натрия и затем отделяли органическую фазу. Водную фазу трижды экстрагировали уксусным эфиром порциями по 25 мл. Объединенные уксусноэфирные фазы сушили над сульфатом магния и в завершение отгоняли растворитель при пониженном давлении. Сырой трет-бутиловый эфир (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] - 3-(1-метил-1,2,3,4-тетрагидрохинолин-7-илметокси)пиперидин- 1-карбоновой кислоты без определения характеристик использовали в последующей реакции.
(д) Путем алкилирования трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-гидроксипиперидин- 1-карбоновой кислоты [пример 86(o)] гидробромидом 6- бромметилизохинолина (пример 4) аналогично примеру 1(ж) получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] - 3-(изохинолин-6-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 583 (М+Н)+.
(е) Аналогично описанной выше методике путем алкилирования трет-бутилового эфира (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил]- 3-(изохинолин-6-илметокси)пиперидин-1-карбоновой кислоты метилиодидом в хлороформе с последующим восстановлением борогидридом натрия в метаноле получили трет-бутиловый эфир (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил]-3-(2-метил-1,2,3,4- тетрагидроизохинолин-6-илметокси)пиперидин-1-карбоновой кислоты, который в виде сырого продукта без дальнейшего определения характеристик использовали в последующей реакции.
(ж) (α) Раствор из 5,2 г (17,7 ммоля) трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-(4-гидроксифенил)пиперидин-1-карбоновой кислоты [пример 46(б)] и 3,37 мл (3,8 г, 17,7 ммоля) 2-метоксибензил-3-хлорпропилового эфира в 18 мл абсолютного ДМФ смешивали с 3,7 г (26,9 ммоля) безводного карбоната калия и перемешивали в течение 60 ч при 120oC. Для дальнейшей переработки реакционную смесь распределяли между 250 мл воды и 250 мл уксусного эфира. Органическую фазу отделяли, а водную фазу трижды экстрагировали уксусным эфиром порциями по 100 мл. Объединенные органические фазы дважды промывали водой порциями по 100 мл и в завершение отгоняли растворитель при пониженном давлении. Сырой продукт кристаллизовали обработкой простым эфиром. Таким путем получили 7,3 г (88% от теории) трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-[4-[3-(2-метоксибензилокси)пропокси] фенил] пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 472 (М+Н)+.
(β) Последующим алкилированием трет-бутилового эфира (3RS,4RS)-3 -гидрокси-4-[4-[3-(2-метоксибензилокси)пропокси]фенил]пиперидин-1-карбоновой кислоты гидробромидом 7-бромметилхинолина [J. Am. Chem. Soc. 77, 1054, (1955)] аналогично примеру 1(ж) получили трет-бутиловый эфир (3RS,4RS)-4-[4-[3-(2-метоксибензилокси)пропокси] фенил] -3-(хинолин-7-илметокси) пиперидин-1-карбоновой кислоты в виде светло-желтой смолы; МС: 613 (М+Н)+.
Использованный в качестве алкилирующего агента 2-метоксибензил-3-хлорпропиловый эфир получали следующим образом.
Раствор из 24,6 г (0,157 ммоля) 2-метоксибензилхлорида и 26 мл (29,4 г, 0,311 ммоля) 3-хлор-1-пропанола в 150 мл абсолютного ДМФ при 10oC смешивали, добавляя порциями, в течение 2,5 ч с 8,4 г (0,196 ммоля) дисперсии гидрида натрия (55%-ная в вазелиновом масле) и перемешивали в течение 1 ч при комнатной температуре. Далее при комнатной температуре дополнительно добавляли 1,0 г (0,023 ммоля) дисперсии гидрида натрия и смесь продолжали перемешивать еще в течение 3 ч. Для дальнейшей переработки реакционную смесь распределяли между 500 мл воды и 500 мл уксусного эфира. Органическую фазу отделяли. Водную фазу четырежды экстрагировали уксусным эфиром порциями по 250 мл. Объединенные органические фазы дважды промывали водой порциями по 250 мл и в завершение отгоняли растворитель при пониженном давлении. Сырой продукт (44 г) очищали хроматографией на силикагеле с использованием смеси 1:2 метиленхлорида и гексана в качестве элюента. Таким путем получили 25,0 г (74% от теории) 2- метоксибензил-3-хлорпропилового эфира в виде бесцветного масла; МС: 214, 216 (М)+.
(з) (α) Раствор из 2,15 г (14,50 ммоля) (1Н-бензимидазол-5-ил)метанола [патент Германии 2813523] в 55 мл абсолютного ДМФ смешивали с безводным карбонатом калия и 3,15 мл (2,96 г, 16,02 ммоля) добавляемого по каплям СЭМ-хлорида. По истечении 3 ч выдержки при комнатной температуре реакционную смесь фильтровали и основное количество ДМФ отгоняли при в высоком вакууме. Остаток для дальнейшей переработки распределяли между 60 мл уксусного эфира и 60 мл воды, после чего отделяли органическую фазу. Водную фазу дважды экстрагировали уксусным эфиром порциями по 60 мл. Объединенные органические фазы сушили над сульфатом магния и в завершение отгоняли растворитель при пониженном давлении. Сырой продукт (4,57 г) очищали хроматографией на силикагеле с использованием смеси 14:1:0,1 метиленхлорида, метанола и 28%-ного раствора аммиака в качестве элюента. Таким путем получили 1,26 г (31% от теории) смеси 1:2 или 2:1 [3-(2-триметилсилилэтоксиметил)-3Н-бензимидазол-5-ил] метанола и [1-(2-триметилсилилэтоксиметил)-1Н-бензимидазол-5-ил]метанола в виде окрашенного в оранжевый цвет масла; МС: 278 (М)+.
(β) Аналогично примеру 5(в) осуществляли хлорирование смеси 1:2 или 2:1 [3- (2-триметилсилилэтоксиметил)-3H-бензимидазол-5-ил] метанола и [1-(2-триметилсилилэтоксиметил)-1Н-бензимидазол-5-ил] метанола, в результате которого получили смесь 1:2 или 2:1 6- хлорметил-1-(2-триметилсилилэтоксиметил)-1Н-бензимидазола и 5- хлорметил-1-(2-триметилсилилэтоксиметил)-1Н-бензимидазола в виде светло-желтого масла; МС: 296, 298 (М)+.
(γ) Путем алкилирования трет-бутилового эфира (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил]-3-гидроксипиперидин-1-карбоновой кислоты [пример 86(о)] смесью 1: 2 или 2:1 6-хлорметил-1-(2-триметилсилилэтоксиметил)-1Н-бензимидазола и 5-хлорметил-1-(2-триметилсилилэтоксиметил)-1Н-бензимидазола получили смесь 2: 1 или 1:2 трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-[1-(2-триметилсилилэтоксиметил)- 1Н-бензимидазол-5-илметокси] пиперидин-1-карбоновой кислоты и трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-[3-(2- триметилсиланилэтоксиметил)-3H-бензимидазол-5-илметокси]пиперидин -1-карбоновой кислоты в виде желтого масла; МС: 702 (М+Н)+.
(δ) Раствор из 328 мг (0,467 ммоля) смеси 2:1 или 1:2 трет-бутилового эфира (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-[1-(2-триметилсилилэтоксиметил)-1Н-бензимидазол-5-илметокси] пиперидин-1-карбоновой кислоты и трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил]-3-[3-(2-триметилсиланилэтоксиметил) - 3H-бензимидазол-5-илметокси]пиперидин-1-карбоновой кислоты в 14 мл абсолютного тетрагидрофурана смешивали с 3,5 мл 1,1 М раствора тетрабутиламмонийфторида в тетрагидрофуране и выдерживали в течение 2 ч при температуре дефлегмации. Реакционную смесь для дальнейшей переработки распределяли между 50 мл уксусного эфира и 50 мл раствора гидрокарбоната натрия (5%-ного), после чего отделяли органическую фазу. Водную фазу дважды экстрагировали уксусным эфиром порциями по 50 мл. Объединенные органические фазы дважды промывали водой порциями по 25 мл, сушили над сульфатом магния и в завершение отгоняли растворитель при пониженном давлении. Сырой продукт (280 мг) очищали хроматографией на силикагеле с использованием смеси 14:1:0,1 метиленхлорида, метанола и 28%-ного раствора аммиака в качестве элюента. Таким путем получили 176 мг (66% от теории) трет-бутилового эфира (3RS, 4RS)-3-(1H-бензимидазол-5- илметокси)-4-[4-(3-бензилоксипропокси)фенил] пиперидин-1- карбоновой кислоты в виде желтого масла; МС: 572 (М + Н)+.
(и) К раствору из 459 мг (0, 75 ммоля) трет-бутилового эфира (3RS,4RS)-4-[4-[3-(2-метоксибензилокси)пропокси] фенил] -3-(хинолин-7-илметокси)пиперидин-1-карбоновой кислоты в 30 мл хлороформа при 0oC по каплям добавляли раствор из 240 мг (около 0,82 ммоля) 60-70%-ной хлорпербензойной кислоты в 15 мл хлороформа. Реакционную смесь перемешивали в течение 2,5 ч при комнатной температуре, а затем для дальнейшей переработки распределяли между 50 мл хлороформа и 50 мл 10%-ного раствора карбоната калия. Органическую фазу отделяли, а водную фазу трижды экстрагировали хлороформом порциями по 25 мл. Объединенные органические фазы дважды промывали водой порциями по 25 мл, сушили над сульфатом магния и в завершение отгоняли растворитель при пониженном давлении. Сырой продукт очищали хроматографией на силикагеле с использованием смеси 19: 1 метиленхлорида и метанола в качестве элюента. Таким путем получили 450 мг (96% от теории) трет-бутилового эфира (3RS,4RS)-4-[4-[3- (2-метоксибензилокси)пропокси] фенил] -3-(1-оксихинолин-7- илметокси)пиперидин-1-карбоновой кислоты в виде светло-желтой смолы; МС: 629 (М+Н)+.
(к) Раствор из 50 мг (0,080 ммоля) трет-бутилового эфира (3RS, 4RS)-4-[4-[3-(2-метоксибензилокси)пропокси] фенил] -3-(1-оксихинолин-7-илметокси)пиперидин-1-карбоновой кислоты в 0,5 мл хлороформа смешивали с 17 мг (0,088 ммоля) тозилхлорида и 0,5 мл 10%-ного раствора карбоната калия и интенсивно перемешивали в течение 3 ч при комнатной температуре. Реакционную смесь для дальнейшей переработки распределяли между 20 мл уксусного эфира и 50 мл воды, затем отделяли органическую фазу, а водную фазу трижды экстрагировали уксусным эфиром порциями по 20 мл. Объединенные органические фазы дважды промывали водой порциями по 25 мл, сушили над сульфатом магния и в завершение отгоняли растворитель при пониженном давлении. Сырой продукт (60 мг) очищали хроматографией на силикагеле с использованием смеси 2:1 уксусного эфира и гексана в качестве элюента. Таким путем получили 37 мг (74% от теории) трет-бутилового эфира (3RS, 4RS)-4-[4-[3-(2-метоксибензилокси)пропокси] фенил] -3-(2-оксо-1,2-дигидрохинолин-7-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества, который без определения характеристик непосредственно использовали в последующей реакции.
(л) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-[4-[3-(2-метоксибензилокси) пропокси]фенил]пиперидин-1-карбоновой кислоты [пример 120(ж) (α)] 7-бромметилизохинолином (WO 93/19059) получили трет-бутиловый эфир (3RS,4RS)-3-(изохинолин-7-илметокси)-4-[4-[3-(2- метоксибензилокси)пропокси] фенил] пиперидин-1-карбоновой кислоты в виде светло-желтой смолы; МС: 613 (М+Н)+.
(м) Аналогично примеру 120(б) путем восстановления трет-бутилового эфира (3RS, 4RS)-4-[4-[3-(2-метоксибензилокси)пропокси] фенил]- 3-(хинолин-7-илметокси)пиперидин-1-карбоновой кислоты [пример 120(ж)(β)] с помощью гексагидрата хлорида никеля(II) и борoгидрида натрия получили трет-бутиловый эфир (3RS, 4RS)-4-[4-[3-(2- метоксибензилокси)пропокси] фенил]-3-(1,2,3, 4-тетрагидрохинолин- 7-илметокси)пиперидин-1-карбоновой кислоты в виде светло-желтого сиропа, который без дальнейшей очистки и определения характеристик использовали в последующей реакции.
(н) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-[4-[3-(2-метоксибензилокси)пропокси] фенил]пиперидин-1-карбоновой кислоты [пример 120(ж)(α)] 6-бромметилхиноксалином [J. Heterocycl. Chem. 11, 595 (1974)] получили трет-бутиловый эфир (3RS,4RS)-4-[4- [3-(2-метоксибензилокси)пропокси] фенил] -3-(хиноксалин-6-илметокси) пиперидин-1-карбоновой кислоты в виде светло-желтого масла; МС: 614 (М+Н)+.
Пример 121.
Путем отщепления BOC-группы получали следующие соединения:
1) из смеси трет-бутилового эфира (3RS,4RS)- и (3SR,4SR)-4-[4-[(RS)-3-бензилокси-2-метоксипропокси] фенил] -3-(1- метоксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили смесь (3RS, 4RS)-4-[4-[(RS)- и -[(SR)- 3-бензилокси-2-метоксипропокси] фенил] -3-(1-метоксинафталин-2- илметокси) пиперидина в виде желтого масла; МС: 542 (М+Н)+;
2) из смеси трет-бутилового эфира (3RS,4RS)- и (3SR,4SR)-4-[4-[(RS)-2-бензилокси-3-феноксипропокси] фенил]-3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты с помощью трифторуксусной кислоты в метиленхлориде получили смесь трифторацетата (3RS,4RS)-4-[4-[(RS)- и-[(SR)-2-бензилокси-3-феноксипропокси] фенил] -3-(нафталин-2-илметокси) пиперидина в виде белого твердого вещества; МС: 574 (М+Н)+;
3) из смеси трет-бутилового эфира (3RS,4RS)- и (3SR,4SR)-4-[4-[(RS)-2-гидрокси-3-(4- метилфенилсульфониламино)пропокси] фенил]-3-(нафталин-2- илметокси) пиперидин-1-карбоновой кислоты с помощью трифторуксусной кислоты в метиленхлориде получили смесь трифторацетата N-[(RS)- и -[(SR)-2-гидрокси-3-[(3RS, 4RS)-4-[3- (нафталин-2-илметокси)пиперидин-4-ил]фенокси]пропил]-4- метилбензолсульфонамида в виде белого твердого вещества; МС: 561 (М+Н)+;
4) из смеси трет-бутилового эфира (3RS,4RS)- и (3SR,4SR)-4-[4-[(RS)-2-аллилокси-4-фенилбутокси] фенил] -3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты с помощью трифторуксусной кислоты в метиленхлориде получили смесь трифторацетата (3RS, 4RS)-4-[4-[(RS)- и -[(SR)-2-аллилокси-4- фенилбутокси]фенил]-3-(нафталин-2-илметокси)пиперидина в виде белого твердого вещества; МС: 522 (М+Н)+.
Использованные в качестве исходных соединений BOC-производные получали следующим образом:
(а) Аналогично примеру 1(ж) путем алкилирования смеси трет-бутилового эфира (3RS,4RS)- и (3SR,4SR)-3-гидрокси-4-[(RS)- 4-оксиранилметоксифенил]пиперидин-1-карбоновой кислоты [пример 86(г)] 1-метокси-2-бромметилнафталином [пример 7(е)] получили смесь трет-бутилового эфира (3RS,4RS)- и (3SR, 4SR)-3-(1- метоксинафталин-2-илметокси)-4-[(RS)-4-оксиранилметоксифенил] пиперидин-1-карбоновой кислоты. В результате последующего раскрытия эпоксидного кольца с помощью бензилата натрия в N, N- диметилформамиде была получена смесь трет-бутилового эфира (3RS,4RS)- и (3SR,4SR)-4-[4-[(RS)-3-бензилокси-2-гидроксипропокси] фенил] -3- (1-метоксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты, из которой алкилированием метилиодидом аналогично примеру 1(ж) получили смесь трет-бутилового эфира (3RS,4RS)- и (3SR,4SR)-4-[4-[(RS)-3- бензилокси-2-метоксипропокси] фенил]-3-(1-метоксинафталин-2 -илметокси) пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 628 (М+Н)+.
(б) Аналогично примеру 1(ж) путем алкилирования смеси трет-бутилового эфира (3RS,4RS)- и (3SR,4SR)- 4-[4-[(RS)-2-гидрокси-3-феноксипропокси]фенил] -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты [пример 86(г)] бензилбромидом получили смесь трет-бутилового эфира (3RS,4RS)- и (3SR,4SR)-4-[4-[(RS)-2-бензилокси-3-феноксипропокси] фенил] -3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде твердого вещества; МС: 674 (М + Н)+.
(в) Из смеси трет-бутилового эфира (3RS,4RS)- и (3SR,4SR)-3-(нафталин-2-илметокси)-4-[(RS)- 4- оксиранилметоксифенил]пиперидин-1-карбоновой кислоты [пример 86(г)] раскрытием эпоксидного кольца с помощью калиевой соли толуол-4-сульфонамида аналогично примеру 71(а) получили смесь трет-бутилового эфира (3RS, 4RS)- и (3SR, 4SR)-4-[4-[(RS)-2- гидрокси-3-(4-метилфенилсульфониламино)пропокси] фенил] -3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде белого твердого вещества; МС: 661 (М+Н)+.
(г) Из смеси трет-бутилового эфира (3RS,4RS)- и (3SR,4SR)-3-(нафталин-2-илметокси)-4-[(RS)-4-oкcиpaнилмeтoкcифeнил] пиперидин-1-карбоновой кислоты [пример 86 (г)] раскрытием эпоксидного кольца с помощью бензилмагнийхлорида в тетрагидрофуране получили смесь трет-бутилового эфира (3RS,4RS)- и (3SR, 4SR)-4-[4-[(RS)-2-гидрокси-4-фенилбутокси] фенил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты, из которой путем алкилирования аллилбромидом аналогично примеру 1(ж) была получена смесь трет-бутилового эфира (3RS, 4RS)- и (3SR, 4SR)-4-[4- [(RS)-2-аллилокси-4-фенилбутокси] фенил] -3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 621 (М+Н)+.
Пример 122.
Путем отщепления BOC-группы получали следующие соединения:
1) из трет-бутилового эфира (3RS,4RS)-3-(нафталин-2- илметокси)-4-[4-(3-фенилпропокси)фенил] пиперидин-1-карбоновой кислоты с помощью трифторуксусной кислоты в метиленхлориде получили трифторацетат (3RS, 4RS)-3-(нафталин-2-илметокси)-4- [4-(3-фенилпропокси)фенил] пиперидина в виде бесцветного твердого вещества; МС: 452 (М + Н)+;
2) из трет-бутилового эфира (3RS,4RS)-3-(нафталин-2-илметокси)-4-[4- (4-фенилбутокси)фенил] пиперидин-1-карбоновой кислоты с помощью трифторуксусной кислоты в метиленхлориде получили трифторацетат (3RS,4RS)-3-(нафталин-2-илметокси)-4-[4-(4-фенилбутокси)фенил] пиперидина в виде бесцветного твердого вещества; МС: 466 (М+Н)+ ;
3) из трет- бутилового эфира (3RS,4RS)-3-(нaфтaлин-2-илмeтoкcи)-4-[4- (5-фенилпентилокси)фенил] пиперидин-1-карбоновой кислоты с помощью трифторуксусной кислоты в метиленхлориде получили трифторацетат (3RS, 4RS)-3-(нафталин-2-илметокси)-4-[4-(5-фенилпентилокси)фенил] пиперидина в виде бесцветного твердого вещества; МС: 480 (М+Н)+;
4) из трет-бутилового эфира (Е)-(3RS,4RS)-3-(нафталин-2-илметокси)-4- [4-(3-фенилаллилокси)фенил] пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (Е)-(3RS, 4RS)-3-(нафталин-2- илметокси)-4-[4-(3-фенилаллилокси)фенил] пиперидин в виде бесцветного твердого вещества; МС: 450 (М+Н)+;
5) из трет-бутилового эфира (Е)-(3RS,4RS)-3-(1, 4-диметоксинафталин-2-илметокси)-4- [4-(3-фенилаллилокси)фенил] пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (Е)-(3RS,4RS)-3-(1, 4-диметоксинафталин- 2-илметокси)-4-[4-(3-фенилаллилокси)фенил] пиперидин в виде бежевого твердого вещества; МС: 510 (М+Н)+;
6) из трет-бутилового эфира (Е)-(3RS, 4RS)-3-(4-метилсульфанилбензилокси)-4-[4-(3-фенилаллилокси)фенил] пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (Е)-(3RS, 4RS)-3-(4- метилсульфанилбензилокси)-4-[4-(3-фенилаллилокси)фенил] пиперидин в виде желтоватого масла; МС: 446 (М+Н)+;
7) из трет-бутилового эфира (Е)-(3RS,4RS)-3-(1, 4- диметоксинафталин-2-илметокси)-4-[4-(4 -фенилбут-3-енилокси) фенил]пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (E)-(3RS,4RS)-3-(1, 4-диметоксинафталин-2- илметокси)-4-[4-(4-фенилбут-3-енилокси)фенил]пиперидин в виде бежевого твердого вещества; МС: 524 (М+Н)+;
8) из трет-бутилового эфира (3RS, 4RS)-4-[4-(3-цианбензилокси)фенил]-3-[1-(2-метоксиэтокси) нафталин-2-илметокси] пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS,4RS)-3-[4-[3-[1-(2-метоксиэтокси) нафталин-2-илметокси]пиперидин-4-ил]феноксиметил]бензонитрил в виде вязкого светло-желтого масла; МС: 523 (М+Н)+;
9) из трет-бутилового эфира (3RS,4RS)-3-(1, 4-диметоксинафталин-2- илметокси)-4-[4-(4-фенилбутокси)фенил]пиперидин-1-карбоновой кислоты с помощью бромида цинка получили (3RS,4RS)-3-(1, 4-диметоксинафталин-2- илметокси)-4-[4-(4-фенилбутокси)фенил] пиперидин в виде бежевого твердого вещества; МС: 526 (М+Н)+.
Использованные в качестве исходных соединений BOC-производные получали следующим образом.
(а) Аналогично примеру 44(д) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-(4-гидроксифенил)пиперидин-1-карбоновой кислоты [пример 46(б)] 1-бром-3-фенилпропаном в присутствии карбоната калия получили трет-бутиловый эфир (3RS,4RS)-3-гидрокси-4-[4-(3-фенилпропокси)фенил]пиперидин-1- карбоновой кислоты, из которого алкилированием аналогично примеру 1(ж) 2-бромметилнафталином был получен трет-бутиловый эфир (3RS,4RS)-3-(нафталин-2-илметокси)-4-[4-(3-фенилпропокси)фенил] пиперидин-1- карбоновой кислоты в виде бесцветного твердого вещества; МС: 551 (М)+.
(б) Аналогично примеру 44(д) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-(4-гидроксифенил) пиперидин-1-карбоновой кислоты [пример 46(б)] мезилатом 4-фенилбутанола, который был получен общеизвестным способом, в присутствии карбоната калия получили трет-бутиловый эфир (3RS, 4RS)-3-гидрокси-4-[4-(4-фенилбутокси)фенил] пиперидин-1-карбоновой кислоты, из которого алкилированием аналогично примеру 1(ж) 2-бромметилнафталином был получен трет-бутиловый эфир (3RS, 4RS)-3-(нафталин-2-илметокси)-4-[4-(4-фенилбутокси)фенил] пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 566 (М+Н)+.
(в) Аналогично примеру 44(д) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-(4-гидроксифенил) пиперидин-1-карбоновой кислоты [пример 46(б)] мезилатом 5-фенилпентанола, который был получен общеизвестным способом, в присутствии карбоната калия в ДМФ получили трет-бутиловый эфир (3RS, 4RS)-3-гидрокси-4-[4-(5-фенилпентилокси)фенил] пиперидин-1-карбоновой кислоты, из которого алкилированием аналогично примеру 1(ж) 2-бромметилнафталином был получен трет-бутиловый эфир (3RS,4RS)-3-(нафталин-2-илметокси)-4-[4-(5-фенилпентилокси)фенил] пиперидин-1- карбоновой кислоты в виде бесцветного твердого вещества; МС: 580 (М+Н)+.
(г) Аналогично примеру 44(д) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-(4-гидроксифенил) пиперидин-1-карбоновой кислоты [пример 46(б)] циннамилбромидом в присутствии карбоната калия в ацетоне получили трет-бутиловый эфир (Е)-(3RS, 4RS)-3-гидрокси-4-[4-(3-фенилаллилокси)фенил] пиперидин-1-карбоновой кислоты, из которого алкилированием аналогично примеру 1(ж) 2- бромметилнафталином был получен трет-бутиловый эфир (E)-(3RS, 4RS)- 3-(нафталин-2-илметокси)-4-[4-(3-фенилаллилокси)фенил] пиперидин-1- карбоновой кислоты в виде бесцветного твердого вещества; МС: 550 (М+Н)+.
(д) Алкилированием трет-бутилового эфира (Е)-(3RS,4RS)-3-гидрокси-4- [4-(3-фенилаллилокси)фенил]пиперидин-1-карбоновой кислоты аналогично примеру 1(ж) 2-хлорметил-1,4-диметоксинафталином [J. Org. Chem. (1983), 48(19), 3265-3268] получили трет-бутиловый эфир (E)-(3RS,4RS)-3-(1, 4-диметоксинафталин-2-илметокси)-4- [4-(3-фенилаллилокси)фенил] пиперидин-1-карбоновой кислоты в виде желтоватого твердого вещества; МС: 610 (М+Н)+.
(е) Алкилированием трет-бутилового эфира (Е)-(3RS,4RS)-3-гидрокси-4- [4-(3-фенилаллилокси)фенил]пиперидин-1-карбоновой кислоты аналогично примеру 1(ж) 4-метилтиобензилхлоридом [J. Org. Chem. (1988), 53(3), 561-569] получили трет-бутиловый эфир (Е)-(3RS,4RS)-3-(4- метилсульфанилбензилокси)-4-[4-(3-фенилаллилокси)фенил] пиперидин-1-карбоновой кислоты в виде желтоватого твердого вещества; МС: 546 (М+Н)+ .
(ж) Аналогично примеру 44(д) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-(4-гидроксифенил)пиперидин-1-карбоновой кислоты [пример 46(б)] мезилатом (Е)-4-фенил-3-бутен-1-ола получили трет-бутиловый эфир (Е)-(3RS, 4RS)-3-гидрокси-4-[4-(4-фенилбут-3-енилокси)фенил] пиперидин-1-карбоновой кислоты, из которого алкилированием аналогично примеру 1(ж) 2-хлорметил-1,4-диметоксинафталином был получен трет-бутиловый эфир (Е)-(3RS, 4RS)-3-(1,4-диметоксинафталин-2-илметокси)- 4-[4-(4-фенилбут-3-енилокси)фенил] пиперидин-1-карбоновой кислоты в виде вязкого светло-желтого масла; МС: 624 (М+Н)+.
Использованный в качестве алкилирующего агента (Е)-4-фенилбут-3-ениловый эфир получали следующим образом.
(α) Раствор из 3,24 г (20 ммолей) (Е)-стирилуксусной кислоты в 20 мл метанола, 2 мл триметилортоформиата и 192 мг (2 ммоля) метансульфокислоты перемешивали в атмосфере аргона в течение 1 ч при 50oC. Для дальнейшей переработки нейтрализовали 2 ммолями метилата натрия и в завершение отгоняли растворитель при пониженном давлении. Таким путем с количественным выходом получили метиловый эфир (Е)-4-фенилбут-3-еновой кислоты в виде бесцветной жидкости.
(β) Аналогично примеру 5(б) восстановлением метилового эфира (Е)-4-фенилбут-3-еновой кислоты с помощью алюмогидрида лития в тетрагидрофуране получили (Е)-4-фенилбут-3-ен-1-ол, который аналогично способу, описанному для получения (Z)-изомера в J. Chem. Soc. Perk. Trans. 1 (1988), (6), 1517-1519, превращали в (Е)-4-фенилбут-3-ениловый эфир метансульфокислоты.
(з) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS, 4RS)-4-(4-аллилоксифенил)-3-гидроксипиперидин-1-карбоновой кислоты [пример 86(б)] 2-хлорметил-1-(2-метоксиэтокси)нафталином получили трет-бутиловый эфир (3RS, 4RS)-4-(4-аллилоксифенил)-3-[1- (2-метоксиэтокси)нафталин-2-илметокси] пиперидин-1-карбоновой кислоты, из которого после отщепления аллильной группы с помощью бис(трифенилфосфин)палладий(II)диацетата аналогично примеру 152(д) был получен трет-бутиловый эфир (3RS,4RS)-4-(4-гидроксифенил)-3- [1-(2-метоксиэтокси)нафталин-2-илметокси] пиперидин-1-карбоновой кислоты, алкилированием которого аналогично примеру 44(д) 3-бромметилбензонитрилом получили трет-бутиловый эфир (3RS,4RS)-4-[4-(3-цианбензилокси)фенил]-3-[1-(2- метоксиэтокси)нафталин-2-илметокси] пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 623 (М+Н)+.
Использованный в качестве алкилирующего агента 2-хлорметил-1-(2-метоксиэтокси) нафталин получали следующим образом.
Путем алкилирования метилового эфира 1-гидроксинафталин-2-карбоновой кислоты аналогично примеру 1(ж) 2-бромэтилметиловым эфиром получили метиловый эфир 1-(2-метоксиэтокси)нафталин-2-карбоновой кислоты, который последовательно аналогично примеру 5(б)-(в) сначала превращали в [1- (2-метоксиэтокси)нафталин-2-ил] метанол, а затем в 2-хлорметил-1-(2-метоксиэтокси)нафталин, который был получен в виде бежевого твердого вещества; МС: 250 (М)+.
(и) Аналогично примеру 1(ж) алкилированием трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-[4-(4-фенилбутокси)фенил] пиперидин-1-карбоновой кислоты [пример 122(б)] 2-хлорметил-1,4-диметоксинафталином [J. Org. Chem. (1983), 48(19), 3265-3268] получили трет-бутиловый эфир (3RS,4RS)-3-(1, 4-диметоксинафталин-2-илметокси)-4-[4-(4- фенилбутокси)фенил] пиперидин-1-карбоновой кислоты в виде бесцветного вязкого масла; МС: 626 (М + Н)+.
Пример 123.
Отщеплением BOC-группы получали следующие соединения:
1) из трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил]- 3-(1, 4-диметоксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили гидробромид (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -(1, 4- диметоксинафталин-2-илметокси)пиперидина в виде бежевого твердого вещества; МС: 542 (М+Н)+;
2) из трет-бутилового эфира (3RS,4RS)-3-(1, 4-диметоксинафталин-2-илметокси)-4-{ 4-[3-(тиофен- 2-илметокси)пропокси]фенил}пиперидин-1- карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS,4RS)-3-{ 1, 4-диметоксинафталин-2-илметокси} -4-[4- [3-(тиофен-2-илметокси)пропокси] фенил]пиперидин в виде бежевого твердого вещества; МС: 548 (М+Н)+;
3) из трет-бутилового эфира (3RS,4RS)-3-(4-метилсульфанилбензилокси)-4- [4-[3-(тиофен-2-илметокси)пропокси] фенил] пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS, 4RS)-3-(4-метилсульфанилбензилокси)-4-[4-[3-(тиофен-2-илметокси) пропокси] фенил] пиперидин в виде желтоватой смолы; МС: 484 (М + Н)+;
4) из трет-бутилового эфира (3RS, 4RS)-4-[4-(3-бензилсульфанилпропокси) фенил]-3-(1,4-диметоксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS, 4RS)-4-[4-(3-бензилсульфанилпропокси)фенил] -3-(1,4 -диметоксинафталин-2-илметокси)пиперидин в виде желтого твердого вещества; МС: 558 (М+Н)+;
5) из трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилсульфанилпропокси) фенил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты с помощью трифторуксусной кислоты в метиленхлориде получили трифторацетат (3RS, 4RS)-4-[4-(3-бензилсульфанилпропокси)фенил]-3-(нафталин-2-илметокси) пиперидина в виде бесцветного твердого вещества; МС: 498 (М+Н)+;
6) из трет-бутилового эфира (3RS, 4RS)-3-(нафталин-2-илметокси)-4- [4-(2-фенэтилоксиэтокси)фенил] пиперидин-1-карбоновой кислоты с помощью трифторуксусной кислоты в метиленхлориде получили трифторацетат (3RS, 4RS)-3-(нафталин-2-илметокси)-4-[4-(2- фенэтилоксиэтокси)фенил] пиперидина в виде бесцветного твердого вещества; МС: 482 (М+Н)+;
7) из трет-бутилового эфира (3RS, 4RS)-3-(4-метилсульфанилбензилокси)-4- [4-(2-фенэтилоксиэтокси)фенил] пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили гидробромид (3RS, 4RS)-3- (4-метилсульфанилбензилокси)-4-[4-(2-фенэтилоксиэтокси)фенил] пиперидина в виде светло-желтого твердого вещества; МС: 478 (М+Н)+;
8) из трет-бутилового эфира (3RS, 4RS)-3-(1,4-диметоксинафталин-2- илметокси)-4-[4-(2-фенэтилоксиэтокси)фенил]пиперидин-1-карбоновой кислоты получили бутиловый эфир (3'RS, 4'RS)-3'-(нафталин-2-илметокси)-5- [(RS)- и -[(SR)-тетрагидропиран-2-илоксиметил] -3', 4',5',6'- тетрагидро-2'H-[2,4']бипиридин-1'-карбоновой кислоты в виде желтого масла; МС: 533 (М+Н)+.
(ε) Раствор из 102 мг (0,19 ммоля) смеси 1:1 трет-бутилового эфира (3'RS, 4'RS)-3'-(нафталин-2-илметокси)-5-[(RS)- и -[(SR)-тетрагидропиран-2-илоксиметил] -3', 4', 5', 6'-тетрагидро-2'H- [2,4'] бипиридин-1'-карбоновой кислоты растворяли в 2 мл метанола и охлаждали до -15oC. В течение 2 мин при температуре в интервале от -10 до -15oC по каплям добавляли 2 н. раствор хлористого водорода в метаноле. Смесь нагревали до комнатной температуры, после чего перемешивали в течение 30 мин, а затем для дальнейшей переработки распределяли между 25 мл уксусного эфира и 25 мл водного 5%-ного раствора гидрокарбоната натрия. Органическую фазу отделяли, а водную фазу трижды экстрагировали уксусным эфиром порциями по 10 мл. Объединенные уксусноэфирные фазы сушили над сульфатом магния и в завершение упаривали при пониженном давлении. Сырой продукт (96 мг) очищали хроматографией на силикагеле с использованием смеси 1:1 уксусного эфира и метиленхлорида в качестве элюента. Таким путем получили 78 мг (92% от теории) трет-бутилового эфира (3'RS, 4'RS)-5-гидроксиметил-3'-(нафталин-2-илметокси)-3', 4', 5', 6'-тетрагидро- 2'H-[2,4'] бипиридин-1'-карбоновой кислоты в виде светло-желтого масла; МС: 449 (М+Н)+.
(ζ) Раствор из 70 мг (0,156 ммоля) трет-бутилового эфира (3'RS,4'RS)-5-гидроксиметил-3'-(нафталин-2-илметокси)-3',4',5', 6'-тетрагидро-2'H-[2, 4'] бипиридин-1'-карбоновой кислоты в 2 мл абсолютного ДМФ охлаждали до -10oC и смешивали с 26 мкл (19 мг, 0,187 ммоля) триэтиламина. При температуре в интервале от -10 до -15oC добавляли 13 мкл (20 мг, 0,172 ммоля) метансульфохлорида и 2 мг N,N-диметиламинопиридина (ДМАП) и после этого перемешивали в течение 1 ч при 0oC. Для дальнейшей переработки смесь распределяли между 25 мл уксусного эфира и 25 мл водного 5%-ного раствора хлорида аммония и отделяли органическую фазу. Водную фазу трижды экстрагировали уксусным эфиром порциями по 10 мл. Объединенные уксусноэфирные фазы сушили над сульфатом магния и получили трет-бутиловый эфир (3RS,4RS)-3-(1,4-диметоксинафталин-2-илметокси)-4-[4-(4-феноксибут-2-инилокси)фенил] пиперидин-1-карбоновой кислоты в виде желтого вязкого масла; МС: 478 (М+Н)+;
15) из трет-бутилового эфира (3RS,4RS)-3-(1,4-диметоксинафталин-2- илметокси)-4-[4-(4-феноксибут-2-инилокси)фенил] пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS,4RS)-3-(1,4-диметоксинафталин-2-илметокси)-4- [4-(4-феноксибут-2-инилокси)фенил] пиперидин в виде коричневого твердого вещества; МС: 538 (М+Н)+;
16) из трет-бутилового эфира (Е)-(3RS,4RS)-3-(нафталин-2-илметокси)-4- [4-(4-феноксибут-2-енилокси)фенил] пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (E)-(3RS,4RS)-3-(нафталин-2- илметокси)-4-[4-(4-феноксибут-2-енилокси)фенил] пиперидин в виде бесцветного твердого вещества; МС: 480 (М+Н)+;
17) из трет-бутилового эфира (Z)-(3RS,4RS)-3-(нaфтaлин-2-илмeтoкcи)-4- [4-(4-феноксибут-2-енилокси)фенил] пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (Z)-(3RS,4RS)-3- (нафталин-2-илметокси)-4-[4-(4-феноксибут-2-енилокси)фенил] пиперидин в виде светло-желтого твердого вещества; МС: 480 (М+Н)+;
18) из трет-бутилового эфира (3RS,4RS)-3-(4,8-диметоксинафталин-2-илметокси)-4-{ 4-[3-(тиофен-2-илметокси) пропокси]фенил}пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS, 4RS)-3-(4,8-диметоксинафталин-2- илметокси)-4-[4-[3-(тиофен-2-илметокси)пропокси] фенил]пиперидин в виде бежевого твердого вещества; МС: 548 (М+Н)+;
19) из трет-бутилового эфира (3RS,4RS)-3-(7-гидроксинафталин-2- илметокси)-4-{ 4-[3-(тиофен-2-илметокси)пропокси] фенил} пиперидин-1-карбоновой кислоты с помощью хлористого водорода в метаноле получили (3RS, 4RS)-7-[4-[4-[3-(тиофен-2- илметокси)пропокси] фенил] пиперидин-3-илоксиметил] нафталин-2-ол в виде бесцветного твердого вещества; МС: 504 (М+Н)+;
20) из трет-бутилового эфира (3RS,4RS)-3-[8-метокси-4-(3- метоксипропокси)нафталин-2-илметокси]-4-{4-[3-(тиофен-2- илметокси)пропокси]фенил}пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS, 4RS)-3-[8-метокси-4-(3-метоксипропокси)нафталин- 2-илметокси] -4-[4-[3-(тиофен-2-илметокси)пропокси] фенил] пиперидин в виде бежевого твердого вещества; МС: 606 (М+Н)+;
21) из смеси трет-бутилового эфира (3RS,4RS)- и (3SR,4SR)-3-[7-[(RS)-2,3-диметоксипропокси] нафталин-2-илметокси] -4- { 4-[3-(тиофен-2-илметокси)пропокси] фенил} пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили смесь (3RS,4RS)- и (3SR,4SR)-3-[7-[(RS)-2,3-диметоксипропокси] нафталин-2-илметокси] - 4-[4-[3-(тиофен-2-илметокси)пропокси] фенил]пиперидина в виде желтого вязкого масла; МС: 606 (М+Н)+;
22) из смеси трет-бутилового эфира (3RS,4RS)- и (3SR,4SR)-3-[1-[(RS)-2,3-диметоксипропокси] нафталин-2-илметокси] -4- { 4-[3-(тиофен-2-илметокси)пропокси] фенил} пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили смесь (3RS,4RS)- и (3SR,4SR)-3-[1-[(RS)-2,3-диметоксипропокси] нaфтaлин-2-илмeтoкcи] - 4-[4-[3-(тиофен-2-илметокси)пропокси] фенил] пиперидина в виде желтого вязкого масла; МС: 606 (М+Н)+;
23) из трет-бутилового эфира (3RS,4RS)-3-(1, 4-диметоксинафталин-2- илметокси)-4-{ 4-[3-(тиофен-3-илметокси)пропокси] фенил}пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS,4RS)-3-(1, 4-диметоксинафталин-2-илметокси)-4-[4-[3-(тиофен-3- илметокси)пропокси] фенил] пиперидин в виде коричневого твердого вещества; МС: 548 (М+Н)+;
24) из трет-бутилового эфира (3RS,4RS)-3-(7-гидpoкcинaфтaлин-2-илметокси)- 4-{ 4-[3-(тиофен-3-илметокси)пропокси] фенил}пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS, 4RS)-7-[4-[4-[3-(тиофен- 3-илметокси)пропокси] фенил] пиперидин-3-илоксиметил] нафталин-2-ол в виде коричневого твердого вещества; МС: 504 (М+Н)+;
25) из трет-бутилового эфира (3RS,4RS)-3-[8- метокси-4-(3-метоксипропокси)нафталин-2-илметокси] -4-{4-[3- (тиофен-3-илметокси)пропокси]фенил}пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS, 4RS)-3-[8-метокси-4-(3-метоксипропокси)нафталин- 2-илметокси]-4-[4-[3-(тиофен-3-илметокси)пропокси]фенил]пиперидин в виде желтоватого вязкого масла; МС: 606 (М + Н)+;
26) из трет-бутилового эфира (3RS,4RS)-3-(1,4-диметоксинафталин-2- илметокси)-4-[4-(3-феноксипропокси)фенил] пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS, 4RS)-3-(1,4-диметоксинафталин-2-илметокси)-4-[4-(3-феноксипропокси)фенил] пиперидин в виде желтого вязкого масла; МС: 528 (М+Н)+;
27) из трет-бутилового эфира (3RS, 4RS)-3-(1,4-диметоксинафталин-2- илметокси)-4-{4-[3-(2-метоксифенокси)пропокси]фенил}пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS,4RS)-3-(1, 4-диметоксинафталин-2-илметокси)-4-[4-[3-(2- метоксифенокси)пропокси] фенил]пиперидин в виде светло-коричневого твердого вещества; МС: 558 (М+Н)+;
28) из трет-бутилового эфира (3RS,4RS)-3-(1,4-диметоксинафталин-2- илметокси)-4-{ 4-[3-(3-метоксифенокси)пропокси] фенил} пиперидин- 1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS,4RS)-3-(1, 4-диметоксинафталин-2-илметокси)-4- [4-[3-(3-метоксифенокси)пропокси] фенил]пиперидин в виде желтого вязкого масла; МС: 558 (М+Н)+;
29) из трет-бутилового эфира (3RS, 4RS)-4-{4-[3-(2-хлорфенокси) пропокси] фенил} -3-(1,4-диметоксинафталин-2-илметокси) пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS, 4RS)-4-[4-[3-(2-хлорфенокси)пропокси] фенил]-3-(1,4-диметоксинафталин-2-илметокси)пиперидин в виде желтого полутвердого продукта; МС: 562 (М+Н)+;
30) из трет-бутилового эфира (3RS,4RS)-3-(1,4-диметоксинафталин-2- илметокси)-4-{ 4-[3-(2-метоксифенилсульфанил)пропокси] фенил}пиперидин-1- карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS, 4RS)-3-(1,4-диметоксинафталин-2-илметокси)-4-[4-[3-(2- метоксифенилсульфанил)пропокси]фенил]пиперидин в виде желтого вязкого масла; МС: 574 (М+Н)+;
31) из трет-бутилового эфира (3RS,4RS)-4-[4-(3-бензилсульфанилпропокси) фенил]-3-(4,8-диметоксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS, 4RS)-4-[4-(3-бензилсульфанилпропокси)фенил] -3-(4,8-диметоксинафталин-2-илметокси)пиперидин в виде бесцветного твердого вещества; МС: 558 (М+Н)+;
32) из трет-бутилового эфира (3RS,4RS)-3-(1,4-диметоксинафталин-2- илметокси)-4-[4-[3-(2-метоксибензилокси)пропокси] фенил]пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS,4RS) -3-(1, 4-диметоксинафталин-2-илметокси)-4-[4-[3-(2-метоксибензилокси)пропокси] фенил]пиперидин в виде желтого сиропа; МС: 572 (М+Н)+;
33) из смеси 1:1 трет-бутилового эфира (3R, 4R)- и (3S,4S)-3-[7-[(R)-2-гидрокси-3-морфолин-4-илпропокси]нафталин-2-илметокси]-4- {4-[3-(тиофен-2-илметокси)пропокси] фенил}пиперидин-1-карбоновой кислоты с помощью хлористого водорода в метаноле получили смесь 1:1 дигидрохлорида (R)-1-морфолин-4-ил-3-[(3R, 4R)- и -[(3S,4S)-7- [4-[4-[3-(тиофен-2-илметокси)пропокси]фенил]пиперидин-3- илоксиметил] нафталин-2-илокси] пропан-2-ола в виде бежевого твердого вещества; МС: 647 (М+Н)+;
34) из трет-бутилового эфира (3RS,4RS)-3-(1,4-диметоксинафталин-2- илметокси)-4-[4-(2-фенэтилоксиэтокси)фенил] пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS,4RS)-3-(1,4- диметоксинафталин-2-илметокси)-4-[4-(2-фенэтилоксиэтокси)фенил] пиперидин, который далее окисляли следующим образом.
К раствору из 118 г (0,22 ммоля) (3RS,4RS)-3-(1,4-диметоксинафталин-2-илметокси)-4-[4-(2-фенэтилоксиэтокси) фенил]пиперидина в 10 мл ацетонитрила при комнатной температуре по каплям добавляли раствор из 240 мг аммонийнитрата церия (IV) в 1 мл воды. Реакционный раствор перемешивали в течение 15 мин при комнатной температуре, а затем упаривали при пониженном давлении. Остаток распределяли между метиленхлоридом и водой, органическую фазу сушили и упаривали при пониженном давлении. Сырой продукт очищали хроматографией на силикагеле с использованием смеси 9:1 метиленхлорида и метанола в качестве элюента. Таким путем получили 95 мг (85% от теории) (3RS,4RS)-2-[4-[4-(2-(фенэтилоксиэтокси)фенил] пиперидин-3-илоксиметил] [1,4] нафтохинона в виде красного твердого вещества; МС: 512 (М+Н)+.
Использованные в качестве исходных субстанций BOC-производные получали следующим образом.
(а) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-гидроксипиперидин-1- карбоновой кислоты [пример 86(o)] 2-хлорметил-1,4-диметоксинафталином [J. Org. Chem. (1983), 48(19), 3265-3268] получили трет-бутиловый эфир (3RS,4RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(1,4- диметоксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 642 (М+Н)+.
(б) Аналогично примеру 1(ж) путем алкилирования (RS)-2-(3- бромпропокси)тетрагидропирана 2-гидроксиметилтиофеном в ДМФ получили (RS)-2-[3-(тиофен-2-илметокси)пропокси] тетрагидропиран, из которого после отщепления ТГП-группы аналогично примеру 53(в) получили 3-(тиофен-2-илметокси)пропан-1-ол. Путем последующего превращения в мезилат известным из литературы методом и осуществленного с его помощью алкилирования аналогично примеру 44(д) трет-бутилового эфира (3RS,4RS)-3-гидрокси-4-(4- гидроксифенил)пиперидин-1-карбоновой кислоты [пример 46(б)] получили трет-бутиловый эфир (3RS, 4RS)-3-гидpoкcи-4-[4-[3-(тиофен-2- илметокси)пропокси]фенил]пиперидин-1-карбоновой кислоты. Алкилированием 2-хлорметил-1,4-диметоксинафталином аналогично примеру 1(ж) был получен трет-бутиловый эфир (3RS,4RS)-3-(1,4-диметоксинафталин-2-илметокси)-4- { 4-[3-(тиофен-2-илметокси)пропокси] фенил} пиперидин-1-карбоновой кислоты в виде светло-желтой смолы; МС: 648 (М+Н)+.
(в) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-[4-[3-(тиофен-2-илметокси)пропокси] фенил] пиперидин-1- карбоновой кислоты 4-метилтиобензилхлоридом [J. Org. Chem. (1988), 53(3), 561-569] получили трет-бутиловый эфир (3RS, 4RS)-3-(4-метилсульфанилбензилокси)-4-[4-[3-(тиофен-2-илметокси)пропокси] фенил]пиперидин-1-карбоновой кислоты в виде желтоватого масла; МС: 584 (М+Н)+.
(г) Аналогично примеру 44(д) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-(4-гидроксифенил)пиперидин-1- карбоновой кислоты [пример 46(б)] (3-бромпропилсульфанилметил)бензолом [J. Org. Chem. (1986), 51, 846-850] в присутствии карбоната калия получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(3-бензилсульфанилпропокси)фенил] - 3-гидроксипиперидин-1-карбоновой кислоты, из которого алкилированием 2-хлорметил-1,4-диметоксинафталином аналогично примеру 1(ж) был получен трет-бутиловый эфир (3RS, 4RS)-4-[4-(3-бензилсульфанилпропокси)фенил] - 3-(1, 4-диметоксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде светло-желтого масла; МС: 584 (М+Н)+.
(д) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS, 4RS)-4-[4-(3- бензилсульфанилпропокси) фенил] -3-гидроксипиперидин-1-карбоновой кислоты 2-бромметилнафталином получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(3-бензилсульфанилпропокси)фенил] - 3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветной смолы; МС: 598 (М+Н)+.
(е) Аналогично примеру 44(д) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-(4-гидроксифенил) пиперидин-1-карбоновой кислоты [пример 46(б)] мезилатом 2- фенэтилоксиэтанола [J. Med. Chem. (1983), 26(11), 1570-1576], полученным известным из литературы способом, в присутствии карбоната калия получили трет-бутиловый эфир (3RS,4RS)-3-гидрокси-4- [4-(2-фенэтилоксиэтокси)фенил] пиперидин-1-карбоновой кислоты, из которого алкилированием аналогично примеру 1(ж) был получен трет-бутиловый эфир (3RS, 4RS)-3-(нaфтaлин-2-илмeтoкcи)-4-[4-(2- фенэтилоксиэтокси)фенил] пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 582 (М+Н)+ .
(ж) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS,4RS)-3-гидрокси-4-[4-(2-фенэтилоксиэтокси)фенил] пиперидин-1-карбоновой кислоты 4-метилтиобензилхлоридом [J. Org. Chem. (1988), 53(3), 561-569] получили трет-бутиловый эфир (3RS,4RS)-3-(4-мeтилcульфaнилбeнзилокси)- 4-[4-(2-фенэтилоксиэтокси)фенил]пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 578 (М+Н)+.
(з) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS,4RS)-3-гидрокси-4-[4-(2-фенэтилоксиэтокси)фенил] пиперидин-1-карбоновой кислоты 2-хлорметил-1,4-диметоксинафталином получили трет-бутиловый эфир (3RS, 4RS)-3-(1,4-диметоксинафталин-2- илметокси)-4-[4-(2-фенэтилоксиэтокси)фенил] пиперидин-1-карбоновой кислоты в виде желтого твердого вещества; МС: 642 (М + Н)+.
(и) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS, 4RS)-4-[4-(2-гидроксиэтокси)фенил] -3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты [пример 53(в)] 2-хлорпиримидином получили трет-бутиловый эфир (3RS, 4RS)-3-(нафталин-2-илметокси)-4-[4-[2- (пиримидин-2-илокси)этокси]фенил]пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 556 (М + Н)+.
(к) Аналогично примеру 44(д) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-(4-гидроксифенил) пиперидин-1-карбоновой кислоты [пример 46(б)] мезилатом 3-феноксипропанола, полученным известным из литературы способом, получили трет-бутиловый эфир (3RS,4RS)-3-гидрокси-4-[4- (3-феноксипропокси)фенил] пиперидин-1-карбоновой кислоты, из которого алкилированием 2-бромметилнафталином аналогично примеру 1(ж) был получен трет-бутиловый эфир (3RS, 4RS)-3-(нафталин-2-илметокси) -4-[4-(3-феноксипропокси)фенил] пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 568 (М+Н)+.
(л) Аналогично примеру 44(д) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-(4-гидроксифенил) пиперидин-1-карбоновой кислоты [пример 46(б)] (Е)-(4-бромбут-2-енилокси)бензолом получили трет-бутиловый эфир (E)-(3RS,4RS)-3-гидpoкcи-4-[4-(4-фeнoкcибут-2-енилокси)фенил]пиперидин-1- карбоновой кислоты. Последующим гидрированием в присутствии палладия на угле аналогично примеру 73(в) получили трет-бутиловый эфир (3RS,4RS)-3-гидрокси-4-[4- (4-феноксибутокси)фенил] пиперидин-1-карбоновой кислоты, из которого алкилированием 2-бромметилнафталином аналогично примеру 1(ж) был получен трет-бутиловый эфир (3RS, 4RS)-3-(нафталин-2-илметокси)-4-[4-(4-феноксибутокси)фенил] пиперидин- 1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 582 (М + Н)+.
Использованный в качестве алкилирующего агента (Е)-(4-бромбут-2-енилокси) бензол был получен аналогично примеру 44(д) путем алкилирования фенола 1,4-дибром-2-бутеном.
(м) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-[4-(4-феноксибутокси)фенил] пиперидин-1-карбоновой кислоты 2-хлорметил-1,4-диметоксинафталином получили трет-бутиловый эфир (3RS, 4RS)-3-(1,4-диметоксинафталин- 2-илметокси)-4-[4-(4-феноксибутокси)фенил]пиперидин-1-карбоновой кислоты в виде светло-желтого твердого вещества; МС: 642 (М + Н)+.
(н) Аналогично примеру 44(д) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-(4-гидроксифенил) пиперидин-1-карбоновой кислоты [пример 46(б)] мезилатом 3-фенилтиопропанола, который был получен известным из литературы способом, получили трет-бутиловый эфир (3RS, 4RS)-3-гидрокси-4-[4-(3-фенилсульфанилпропокси) фенил] пиперидин-1-карбоновой кислоты, из которого алкилированием аналогично примеру 1(ж) 2-хлорметил-1,4-диметоксинафталином был получен трет-бутиловый эфир (3RS,4RS)-3-(1,4-диметоксинафталин-2- илметокси)-4-[4-(3-фенилсульфанилпропокси)фенил] пиперидин-1- карбоновой кислоты в виде желтого вязкого масла; МС: 644 (М+Н)+.
(о) Аналогично примеру 44(д) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-(4-гидроксифенил) пиперидин-1-карбоновой кислоты [пример 46(б)] 4-феноксибут-2-иниловым эфиром метансульфокислоты получили трет-бутиловый эфир (3RS, 4RS)-3-гидрокси-4-[4-(4-феноксибут-2-инилокси)фенил] пиперидин-1-карбоновой кислоты, из которого алкилированием 2-бромметилнафталином был получен трет-бутиловый эфир (3RS,4RS)-3- (нафталин-2-илметокси)-4-[4-(4-феноксибут-2-инилокси)фенил] пиперидин-1- карбоновой кислоты в виде светло-желтого вязкого масла; МС: 578 (М+Н)+.
Использованный в качестве алкилирующего агента 4-феноксибут- 2-иниловый эфир метансульфокислоты получали аналогично примеру 44(д) путем алкилирования фенола димезилатом 2-бутан-1,4-диола, который был получен известным из литературы способом.
(п) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-[4-(4, -феноксибут-2-инилокси) фенил] пиперидин-1-карбоновой кислоты 2-хлорметил-1,4-диметоксинафталином получили трет-бутиловый эфир (3RS,4RS)-3-(1,4-диметоксинафталин-2- илметокси)-4- [4-(4-феноксибут-2-инилокси)фенил] пиперидин-1- карбоновой кислоты в виде светло-желтого твердого вещества; МС: 638 (М+Н)+.
(р) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (Е)-(3RS, 4RS)-3-гидрокси-4-[4-(4-феноксибут-2-енилокси) фенил]пиперидин-1-карбоновой кислоты [пример 123(л)] 2- бромметилнафталином получили трет-бутиловый эфир (Е)-(3RS, 4RS)-3- (нафталин-2-илметокси)-4-[4-(4-феноксибут-2-енилокси)фенил]пиперидин-1- карбоновой кислоты в виде бесцветного твердого вещества; МС: 580 (М+Н)+.
(с) Аналогично примеру 44(д) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-(4-гидроксифенил) пиперидин-1-карбоновой кислоты [пример 46(б)] (Z)-4-феноксибут-2-ениловым эфиром метансульфокислоты получили трет-бутиловый эфир (Z)-(3RS,4RS)-3-гидрокси-4-[4-(4-феноксибут-2- енилокси)фенил] пиперидин-1-карбоновой кислоты, из которого алкилированием 2-бромметилнафталином был получен трет-бутиловый эфир (Z)-(3RS, 4RS)-3-(нафталин-2-илметокси)-4-[4-(4- феноксибут-2-енилокси)фенил] пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 580 (М+Н)+.
Использованный в качестве алкилирующего агента (Z)-4-феноксибут-2-ениловый эфир метансульфокислоты получали аналогично примеру 44(д) путем алкилирования фенола (Z)-4-мeтилcульфoнилoкcибут-2-eнилoвым эфиром метансульфокислоты, который был получен известным из литературы способом из (Z)-2-бутен-1,4-диола.
(т) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-[4-[3-(тиофен-2-илметокси)пропокси] фенил] пиперидин-1-карбоновой кислоты [пример 123(б)] 2-хлорметил-4,8-диметоксинафталином получили трет-бутиловый эфир (3RS,4RS)-3-(4, 8-диметоксинафталин-2-илметокси)-4-{ 4-[3-(тиофен-2- илметокси)пропокси] фенил} пиперидин-1-карбоновой кислоты в виде бежевого твердого вещества; МС: 648 (М+Н)+.
Использованный в качестве алкилирующего агента 2-хлорметил-4,8-диметоксинафталин получали следующим образом.
(α) Аналогично примеру 5(б) восстановлением метилового эфира 4, 8-диметоксинафталин-2- карбоновой кислоты (J. Chem. Soc. 1959, 1024) с помощью алюмогидрида лития получили (4,8-диметоксинафталин-2-ил) метанол [МС: 218 (М)+] в виде бесцветного твердого вещества.
(β) К охлажденному до -10oC раствору из 7,7 г (35,3 ммоля) (4,8-диметоксинафталин-2-ил)метанола и 4,4 г (38,8 ммоля) триэтиламина в 50 мл метиленхлорида по каплям добавляли раствор из 3,92 г хлорангидрида метансульфокислоты в 20 мл метиленхлорида. Реакционную смесь перемешивали в течение 18 ч при комнатной температуре. Для дальнейшей переработки смесь экстрагировали путем встряхивания с 50 мл ледяного раствора гидрокарбоната натрия, водную фазу отделяли и экстрагировали 25 мл метиленхлорида. Объединенные органические фазы сушили над сульфатом натрия, а затем упаривали при пониженном давлении. Остаток очищали фильтрацией через слой силикагеля с использованием метиленхлорида в качестве элюента. Таким путем получили 7,2 г 2-хлорметил-4, 8-диметоксинафталина в виде бежевого твердого вещества; МС: 296 (М)+.
(у) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-[4-[3-(тиофен-2-илметокси)пропокси]фенил]пиперидин-1-карбоновой кислоты [пример 123(б)] 2-хлорметил-7-( β-триметилсилилэтоксиметокси)нафталином [пример 6(х)] получили трет-бутиловый эфир (3RS,4RS)-4-{4-[3-(тиофен-2-илметокси)пропокси]фенил}-3-[7-(2-триметилсиланилэтоксиметокси)нафталин-2-илметокси]пиперидин-1-карбоновой кислоты в виде бесцветного вязкого масла [МС: 734 (М+Н)+], из которого отщеплением СЭМ-группы с помощью хлористого водорода в метаноле получили трет-бутиловый эфир (3RS, 4RS)-3-(7-гидроксинафталин-2- илметокси)-4-{4-[3-(тиофен-2-илметокси)пропокси] фенил} пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 604 (М+Н)+.
(ф) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS,4RS)-3-гидрокси-4-[4-[3-(тиофен-2-илметокси)пропокси] фенил] пиперидин-1-карбоновой кислоты [пример 123(б)] 3-хлорметил-5-метокси-1-(3-метоксипропокси)нафталином получили трет-бутиловый эфир (3RS,4RS)-3-[8-метокси-4-(3-метоксипропокси)нафталин-2- илметокси] -4-{ 4-[3-(тиофен-2-илметокси)пропокси] фенил} пиперидин-1-карбоновой кислоты в виде светло-желтого вязкого масла; МС: 706 (М + Н)+.
Использованный в качестве алкилирующего агента 3-хлорметил-5- метокси-1-(3-метоксипропокси)нафталин получали следующим образом.
Аналогично примеру 44(д) путем алкилирования метилового эфира 4- гидрокси-8-метоксинафталин-2-карбоновой кислоты [Justus Liebigs Ann. Chem. (1967), 702, 94-100] мезилатом 3-метоксибутан-1-ола, полученным известным из литературы способом, получили этиловый эфир 8-метокси-4-(3-метоксипропокси)нафталин-2-карбоновой кислоты, восстановлением которого алюмогидридом лития аналогично примеру 5(б) был получен [8-метокси-4-(3-метоксипропокси)нафталин-2-ил] метанол. Последующим хлорированием аналогично примеру 123(т) (β) получили 3-хлорметил-5-метокси-1-(3-метоксипропокси)нафталин в виде светло-желтой жидкости; МС: 276 (М)+.
(х) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS,4RS)-3-гидрокси-4-[4-[3-(тиофен-2-илметокси)пропокси]фенил]пиперидин-1- карбоновой кислоты [пример 123(б)] (RS)-2-хлорметил-7-(2,3-диметоксипропокси)нафталином получили смесь трет-бутилового эфира (3RS,4RS)- и (3SR, 4SR)-3-[7- [(RS)-2,3-димeтoкcипpoпoкcи] нaфтaлин-2-илмeтoкcи] -4-{ 4-[3- (тиофен-2-илметокси)пропокси] фенил)пиперидин-1-карбоновой кислоты в виде бесцветного вязкого масла; МС: 706 (М + Н)+.
Использованный в качестве алкилирующего агента (RS)-2-хлорметил-7-(2,3-диметоксипропокси)нафталин получали следующим образом.
Аналогично примеру 44(д) путем алкилирования этилового эфира 7- гидроксинафталин-2-карбоновой кислоты (ЕРА 61800) мезилатом (RS)- 2,3-диметоксипропан-1-ола (J. Chem. Soc. C, 1966, 415-419), полученным известным из литературы методом, получили метиловый эфир (RS)-7-(2, 3-диметоксипропокси)нафталин-2-карбоновой кислоты, восстановлением которого алюмогидридом лития аналогично примеру 5(б) был получен (RS)-[7-(2,3-диметоксипропокси) нафталин-2-ил] метанол. Последующим хлорированием аналогично примеру 123(т)(β) получили (RS)-2-хлорметил-7-(2,3-диметоксипропокси)нафталин в виде бесцветного твердого вещества; МС: 294 (М)+.
(ц) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-[4- [3-(тиофен-2-илметокси)пропокси] фенил] пиперидин-1-карбоновой кислоты [пример 123(б)] (RS)-2-хлорметил-1-(2,3-диметоксипропокси)нафталином получили смесь трет-бутилового эфира (3RS,4RS)- и (3SR, 4SR)-3-[1- [(RS)-2,3-диметоксипропокси] нафталин-2-илметокси] -4-{ 4- [3-(тиофен-2-илметокси)пропокси] фенил}пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 706 (М + Н)+.
Использованный в качестве алкилирующего агента (RS)-2- хлорметил-1-(2,3-диметоксипропокси)нафталин получали следующим образом.
Аналогично примеру 44(д) путем алкилирования метилового эфира 1-гидроксинафталин-2-карбоновой кислоты мезилатом (RS)-2,3- диметоксипропан-1-ола (J. Chem. Soc. С, 1966, 415-419), полученным известным из литературы методом, получили метиловый эфир (RS)-1-(2,3-диметоксипропокси)нафталин-2-карбоновой кислоты, восстановлением которого алюмогидридом лития аналогично примеру 5(б) был получен (RS)-[1-(2,3-диметоксипропокси)нафталин-2-ил] метанол. Последующим хлорированием аналогично примеру 123(т)(β) получили (RS)-2-хлорметил-1-(2,3-диметоксипропокси) нафталин в виде бесцветного вязкого масла; МС: 294 (М)+.
(ч) Аналогично примеру 1(ж) путем алкилирования (RS)-2-(3- бромпропокси)тетрагидропирана 3-гидроксиметилтиофеном в ДМФ получили (RS)-2-[3-(тиофен-3-илметокси)пропокси] тетрагидропиран, из которого после отщепления ТГП-группы аналогично примеру 53(в) получили 3-(тиофен-3-илметокси)пропан-1-ол. Путем последующего превращения в мезилат по известным из литературы методам и осуществленного с его помощью алкилирования аналогично примеру 44(д) трет-бутилового эфира (3RS, 4RS)-3-гидрокси -4-(4- гидроксифенил)пиперидин-1-карбоновой кислоты [пример 46(б)] получили трет-бутиловый эфир (3RS, 4RS)-3-гидрокси-4- [4-[3-(тиофен-3-илметокси)пропокси] фенил] пиперидин -1- карбоновой кислоты. Алкилированием 2-хлорметил-1,4- диметоксинафталином аналогично примеру 1(ж) был получен трет- бутиловый эфир (3RS, 4RS)-3-(1,4-диметоксинафталин-2-илметокси)-4- { 4-[3-(тиофен-3-илметокси)пропокси] фенил} пиперидин-1-карбоновой кислоты в виде светло-желтого твердого вещества; МС: 648 (М+Н)+ .
(ш) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-[4-[3-(тиофен-3-илметокси)пропокси] фенил] пиперидин-1-карбоновой кислоты 2-аллилокси-7-хлорметилнафталином получили трет-бутиловый эфир (3RS, 4RS)-3-(7-аллилоксинафталин-2-илметокси)-4- { 4-[3-(тиофен-3-илметокси)пропокси] фенил} пиперидин-1-карбоновой кислоты, из которого после отщепления аллильной группы с помощью бис(трифенилфосфин)палладий(II)диацетата аналогично примеру 152(д) получили трет-бутиловый эфир (3RS, 4RS)-3-(7-гидроксинафталин-2- илметокси)-4-{4-[3-(тиофен-3-илметокси)пропокси] фенил} пиперидин-1-карбоновой кислоты в виде желтоватого вязкого масла; МС: 604 (М+Н)+.
Использованный в качестве алкилирующего агента 2-аллилокси-7-хлорметилнафталин получали следующим образом.
Аналогично примеру 44(д) путем алкилирования этилового эфира 7-гидроксинафталин-2-карбоновой кислоты (ЕРА 61800) аллилбромидом получили метиловый эфир 7-аллилоксинафталин-2-карбоновой кислоты, восстановлением которого алюмогидридом лития аналогично примеру 5(б) был получен (7-аллилоксинафталин-2-ил)метанол. Последующим хлорированием аналогично примеру 123(т) (β) получили 2-аллилокси-7- хлорметилнафталин в виде бесцветного твердого вещества; МС: 232 (М)+.
(щ) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS,4RS)-3-гидрокси-4-[4-[3-(тиофен-3-илметокси)пропокси]фенил]пиперидин-1- карбоновой кислоты 3-хлорметил-5-метокси-1-(3-метоксипропокси)нафталином [пример 123(ф)] получили трет-бутиловый эфир (3RS, 4RS)-3- [8-метокси-4-(3-метоксипропокси)нафталин-2-илметокси]-4- {4-[3-(тиофен-3-илметокси)пропокси] фенил} пиперидин-1-карбоновой кислоты в виде светло-желтого вязкого масла; МС: 723 (M+NH4 )+.
(э) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-[4-(3-феноксипропокси)фенил] пиперидин-1-карбоновой кислоты [пример 123(к)] 2-хлорметил-1,4-диметоксинафталином получили трет-бутиловый эфир (3RS, 4RS)-3-(1,4-диметоксинафталин-2-илметокси)- 4-[4-(3-феноксипропокси)фенил] пиперидин-1-карбоновой кислоты в виде вязкого желтого масла; МС: 628 (М + Н)+.
(аа) Аналогично примеру 44(д) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-(4-гидроксифенил) пиперидин-1-карбоновой кислоты [пример 46(б)] 1-(3-бромпропокси)-2-метоксибензолом получили трет-бутиловый эфир (3RS, 4RS)-3-гидрокси-4-{ 4-[3-(2-метоксифенокси)пропокси]фенил} пиперидин-1-карбоновой кислоты, из которого последующим алкилированием 2-хлорметил-1,4-диметоксинафталином был получен трет-бутиловый эфир (3RS,4RS)-3-(1,4-диметоксинафталин-2- илметокси)-4-{ 4-[3-(2-метоксифенокси)пропокси] фенил} пиперидин- 1-карбоновой кислоты в виде светло-желтого твердого вещества; МС: 657 (М)+.
Использованный в качестве алкилирующего агента 1-(3- бромпропокси)-2-метоксибензол был получен аналогично примеру 44(д) алкилированием 2-метоксифенола 1,3-дибромпропаном в виде бесцветной жидкости; МС: 244, 246 (М)+.
(бб) Аналогично примеру 44(д) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-(4-гидроксифенил) пиперидин-1-карбоновой кислоты [пример 46(б)] 1-(3-бромпропокси)-3-метоксибензолом получили трет-бутиловый эфир (3RS, 4RS)-3-гидpoкcи-4-{4-[3-(3-метоксифенокси)пропокси] фенил} пиперидин-1-карбоновой кислоты, из которого последующим алкилированием 2-хлорметил-1,4-диметоксинафталином был получен трет-бутиловый эфир (3RS,4RS)-3-(1,4-диметоксинафталин-2- илметокси)-4-{ 4-[3-(3-метоксифенокси)пропокси] фенил} пиперидин- 1-карбоновой кислоты в виде светло-желтого твердого вещества; МС: 658 (М+Н)+.
Использованный в качестве алкилирующего агента 1-(3-бромпропокси)-3- метоксибензол был получен аналогично примеру 44(д) алкилированием 3-метоксифенола 1,3-дибромпропаном в виде бесцветной жидкости; МС: 244, 246 (М)+.
(вв) Аналогично примеру 44(д) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-(4-гидроксифенил) пиперидин-1-карбоновой кислоты [пример 46(б)] 1-(3-бромпропокси)-2-хлорбензолом получили трет-бутиловый эфир (3RS, 4RS)-4-{4-[3-(2-хлорфенокси)пропокси]фенил}-3-гидроксипиперидин-1- карбоновой кислоты, из которого последующим алкилированием 2-хлорметил-1,4-диметоксинафталином был получен трет-бутиловый эфир (3RS,4RS)-4-{4-[3-(2-хлорфенокси)пропокси] фенил} -3-(1, 4-диметоксинафталин- 2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного вязкого масла; МС: 662 (М+Н)+.
Использованный в качестве алкилирующего агента 1-(3-бромпропокси)-2-хлорбензол был получен аналогично примеру 44(д) алкилированием 2-хлорфенола 1,3-дибромпропаном в виде бесцветной жидкости; МС: 248 (М)+.
(гг) Аналогично примеру 44(д) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-(4-гидроксифенил) пиперидин-1-карбоновой кислоты [пример 46(б)] 3-(2-метоксифенилсульфанил)пропиловым эфиром метансульфокислоты получили трет-бутиловый эфир (3RS,4RS)- 3-гидрокси-4-{4-[3-(2- метоксифенилсульфанил)пропокси] фенил}пиперидин-1-карбоновой кислоты, из которого последующим алкилированием 2-хлорметил-1,4-диметоксинафталином был получен трет-бутиловый эфир (3RS, 4RS)-3-(1,4-диметоксинафталин-2-илметокси)-4-{4- [3-(2-метоксифенилсульфанил)пропокси] фенил}пиперидин-1-карбоновой кислоты в виде светло-желтого вязкого масла: МС: 674 (М+Н)+.
Использованный в качестве алкилирующего агента 3-(2-метоксифенилсульфанил) пропиловый эфир метансульфокислоты получали следующим образом.
(α) Аналогично примеру 44(д) алкилированием 2-метокситиофенола (RS)-2-(3-бромпропокси)тетрагидропираном получили (RS)-2-[3-(2- метоксифенилсульфанил)пропокси]тетрагидропиран.
(β) Раствор из 9,5 г (33,6 ммоля) (RS)-2-[3-(2-метоксифенилсульфанил) пропокси]тетрагидропирана и 1,0 г (4 ммоля) пиридиний(толуол-4-сульфоната) в 100 мл метанола нагревали с обратным холодильником в течение 2 ч. Для дальнейшей переработки растворитель отгоняли при пониженном давлении, а затем остаток распределяли между уксусным эфиром и насыщенным раствором гидрокарбоната натрия. Органическую фазу далее сушили над сульфатом натрия и упаривали при пониженном давлении. Таким путем получили с количественным выходом 3-(2- метоксифенилсульфанил)пропан-1-ол в виде желтоватой жидкости; МС: 198 (М)+. В результате осуществлявшегося общеизвестным способом взаимодействия с мезилхлоридом получили 3-(2- метоксифенилсульфанил)пропиловый эфир метансульфокислоты в виде светло-желтой жидкости; МС: 276 (М)+.
(дд) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS, 4RS)-4-[4-(3-бензилсульфанилпропокси)фенил] -3- гидроксипиперидин-1-карбоновой кислоты [пример 123(г)] 3-хлорметил-1,5-диметоксинафталином [пример 123(т)] получили трет-бутиловый эфир (3RS,4RS)-4-[4-(3-бензилсульфанилпропокси)фенил] -3-(4,8-диметоксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде желтого вязкого масла; МС: 658 (М+Н)+.
(ее) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-[4-[3- (2-метоксибензилокси)пропокси]фенил]пиперидин-1-карбоновой кислоты 2-хлорметил-1, 4-диметоксинафталином получили трет-бутиловый эфир (3RS, 4RS)-3-(1,4-диметоксинафталин-2-илметокси)-4-[4- [3-(2-метоксибензилокси)пропокси] фенил] пиперидин-1-карбоновой кислоты в виде светло-желтого сиропа; МС: 689 (M+NH4)+.
(жж) Аналогично примеру 1(ж) путем алкилирования трет- бутилового эфира (3RS, 4RS)-3-(7-гидроксинафталин-2-илметокси)-4-{ 4- [3-(тиофен-2-илметокси)пропокси] фенил} пиперидин-1-карбоновой кислоты [пример 123(у)] (R)-оксиранилметиловым эфиром толуол-4- сульфокислоты получили смесь 1:1 трет-бутилового эфира (3R,4R)- и (3S, 4S)-3-[(R)-7-оксиранилметоксинафталин-2-илметокси] -4-{ 4- [3-(тиофен-2-илметокси)пропокси]фенил}пиперидин-1-карбоновой кислоты [МС: 660 (М+Н)+] в виде желтоватого вязкого масла. Последующим раскрытием эпоксидного кольца аналогично примеру 71(а) с помощью морфолина получили смесь 1: 1 трет-бутилового эфира (3R,4R)- и (3S, 4S)-3-[7-[(R)-2-гидрокси-3-морфолин-4- илпропокси]нафталин-2-илметокси]-4-{4- [3-(тиофен-2- илметокси)пропокси] фенил} пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 747 (М+Н)+.
Пример 124.
Путем отщепления BOC-группы получали следующие соединения:
1) из трет-бутилового эфира (3RS, 4RS)-4-{4-[3-(2-метоксифенил)[1,2,4] оксадиазол-5-илметокси] фенил} -3-(4-метилсульфанилбензилокси)пиперидин-1- карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS, 4RS)-4-[4-[3-(2-метоксифенил)[1,2,4] оксадиазол-5-илметокси] фенил]-3-(4-метилсульфанилбензилокси)пиперидин в виде бесцветного масла; МС: 518 (М+Н)+;
2) из трет-бутилового эфира (3RS,4RS)-3-(4-метансульфонилбензилокси)-4- { 4-[3-(2-метоксифенил)[1,2,4] оксадиазол-5-илметокси] фенил} пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS, 4RS)-4-[4-[3-(2-метоксифенил)[1,2,4] оксадиазол-5-илметокси] фенил]-3-(4-метилсульфонилбензилокси)пиперидин в виде бежевого твердого вещества; МС: 550 (М+Н)+;
3) из смеси трет-бутилового эфира (3RS,4RS)-3-[4-[(RS)- и -[(SR)-2,3-диметоксипропокси] -8-метоксинафталин-2-илметокси] -4- { 4-[3-(2-метоксифенил)[1,2,4] оксадиазол-5-илметокси] фенил} пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили смесь (3RS,4RS)-3-[4-[(RS)- и -[(SR)-2,3-диметоксипропокси] -8-метоксинафталин-2-илметокси] -4-[4- [3-(2-метоксифенил)[1,2,4] оксадиазол-5-илметокси] фенил] пиперидина в виде бежевого твердого вещества; МС: 670 (М+Н)+;
4) из трет-бутилового эфира (3RS,4RS)-3-(1, 4-димeтoкcинaфтaлин-2-илметокси)- 4-[4-[3-(2-метоксифенил)[1,2,4] оксадиазол-5-илметокси] фенил]пиперидин-1- карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS, 4RS)-3-(1, 4-диметоксинафталин-2-илметокси)- 4-[4-[3-(2-метоксифенил)[1,2,4]оксадиазол-5-илметокси]фенил]пиперидин в виде бежевого твердого вещества; МС: 582 (М+Н)+;
5) из трет-бутилового эфира (3RS,4RS)-3-(1,4-диметоксинафталин-2- илметокси)-4-{ 4-[3-(3,4,5-триметоксифенил)[1,2,4] оксадиазол-5-илметокси] фенил} пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS, 4RS)-3-(1,4-диметоксинафталин-2-илметокси)-4- [4-[3-(3,4,5-триметоксифенил)[1,2,4] оксадиазол-5-илметокси] фенил]пиперидин в виде бежевого твердого вещества; МС: 642 (М+Н)+;
6) из трет-бутилового эфира (3RS,4RS)-3-(4-метилсульфанилбензилокси)-4-[4-(3-тиофен-2-ил[1,2,4] оксадиазол-5-илметокси)фенил] пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS,4RS)-3-(4-метилсульфанилбензилокси)-4-[4-(3-тиофен-2-ил[1,2,4] оксадиазол-5-илметокси)фенил]пиперидин в виде светло-желтого вязкого масла; МС: 494 (М+Н)+;
7) из трет-бутилового эфира (3RS,4RS)-3-(1,4-диметоксинафталин-2- илметокси)-4-[4-(3-тиофен-2-ил[1,2,4] оксадиазол-5-илметокси)фенил] пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS, 4RS)-3-(1,4-диметоксинафталин-2-илметокси)-4- [4-(3-тиофен-2-ил-[1,2,4]оксадиазол-5-илметокси)фенил] пиперидин в виде бежевого твердого вещества; МС: 558 (М+Н)

8) из трет-бутилового эфира (3RS,4RS)-3-[1-(2-метоксиэтоксиметокси) нафталин-2-илметокси]-4-[4-(3-тиофен-2-ил[1,2,4]оксадиазол-5-илметокси) фенил] пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде при одновременном отщеплении МЭМ-группы получили (3RS,4RS)-2-[4-[4-(3-тиофен-2-ил[1,2,4] оксадиазол-5-илметокси)фенил] пиперидин-3-илоксиметил]нафталин-1-ол в виде коричневого твердого вещества; МС: 514 (М+Н)+;
9) из трет-бутилового эфира (3RS,4RS)-3-[1-(2-метоксиэтокси)нафталин-2- илметокси] -4-[4-(3-тиофен-2-ил[1,2,4] оксадиазол-5-илметокси)фенил] пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили гидробромид (3RS,4RS)-3-[1-(2-метоксиэтокси)нафталин-2-илметокси]-4-[4-(3-тиофен-2-ил[1,2,4] оксадиазол-5-илметокси)фенил] пиперидина в виде бесцветного твердого вещества; МС: 572 (М+Н)+;
10) из трет-бутилового эфира (3RS,4RS)-3-(нафталин-2-илметокси)-4-[4- (3-тиофен-2-ил[1,2,4] оксадиазол-5-илметокси)фенил] пиперидин-1-карбоновой кислоты с помощью трифторуксусной кислоты в метиленхлориде получили трифторацетат (3RS,4RS)-3-(нафталин-2-илметокси)-4-[4-(3-тиофен-2-ил[1,2,4]оксадиазол-5-илметокси)фенил] пиперидина в виде бесцветного твердого вещества; МС: 498 (М+Н)+;
11) из трет-бутилового эфира (3RS,4RS)-4-[4-(3-фуран-2-ил[1,2,4]оксадиазол-5-илметокси)фенил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты с помощью трифторуксусной кислоты в метиленхлориде получили трифторацетат (3RS, 4RS)-4-[4-(3-фуран-2-ил-[1,2,4] оксадиазол-5-илметокси)фенил]-3-(нафталин-2-илметокси)пиперидина в виде бесцветного твердого вещества; МС: 482 (М+Н)+;
12) из трет-бутилового эфира (3RS, 4RS)-4-[4-[3-(2-xлopфeнил)[1,2,4]оксадиазол-5-илметокси] фенил] -3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты с помощью трифторуксусной кислоты в метиленхлориде получили трифторацетат (3RS, 4RS)-4-[4-[3-(2- хлорфенил)[1,2,4]оксадиазол-5-илметокси]фенил] -3-(нафталин-2- илметокси)пиперидина в виде бесцветного твердого вещества; МС: 526 (М+Н)+;
13) из трет-бутилового эфира (3RS,4RS)-3-(1,4-димeтoкcинaфтaлин-2- илметокси)-4-[4-(2-фенилоксазол-5-илметокси)фенил]пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS, 4RS)-3-(1,4-диметоксинафталин-2-илметокси)-4- [4-(2-фенилоксазол-5-илметокси)фенил]пиперидин в виде бесцветного твердого вещества; МС: 551 (М+Н)+;
14) из трет-бутилового эфира (3RS,4RS)-3-(1,4-димeтoкcинaфтaлин-2- илметокси)-4-[4-(2-фенилтиазол-5-илметокси) фенил] пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили [3RS,4RS]-3-(1, 4-диметоксинафталин-2-илметокси)-4-[4-(2-фенилтиазол-5-илметокси)фенил] пиперидин в виде бежевого твердого вещества; МС: 567 (М+Н)+;
15) из трет-бутилового эфира (3RS, 4RS)-3-[1-(2-метоксиэтокси)нафталин-2- илметокси] -4-[4-(3-фенилизоксазол-5-илметокси)фенил] пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS, 4RS)-3-[1-(2-метоксиэтокси)нафталин-2-илметокси] -4- [4-(3-фенилизоксазол-5-илметокси)фенил]пиперидин в виде бесцветного твердого вещества; МС: 565 (М+Н)+;
16) из трет-бутилового эфира (3RS,4RS)-3-(1,4-диметоксинафталин-2- илметокси)-4-[4-(3-фенилизоксазол-5-илметокси)фенил]пиперидин-1-карбоновой кислоты с помощью бромида цинка в метиленхлориде получили (3RS, 4RS)-3-(1,4-диметоксинафталин-2-илметокси)-4-[4-(3-фенилизоксазол-5- илметокси)фенил] пиперидин в виде бесцветного твердого вещества; МС: 551 (М+Н)+;
17) из трет-бутилового эфира (3RS,4RS)-3-(1-метоксинафталин-2-илметокси)- 4-[4-(3-фенилизоксазол-5-илметокси)фенил]пиперидин-1-карбоновой кислоты с помощью трифторуксусной кислоты в метиленхлориде получили трифторацетат (3RS, 4RS)-3-(1-метоксинафталин-2-илметокси)-4 -[4-(3-фенилизоксазол-5-илметокси)фенил] пиперидина в виде бесцветного твердого вещества; МС: 521 (М+Н)+.
Использованные в качестве исходных субстанций BOC-производные получали следующим образом.
(а) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS, 4RS)-4-(4-аллилоксифенил)-3-гидроксипиперидин-1- карбоновой кислоты [пример 86(б)] 4-метилтиобензилхлоридом [J. Org. Chem. (1988), 53(3), 561-569] получили трет-бутиловый эфир (3RS, 4RS)-4-(4-аллилоксифенил)-3-(4-метилсульфанилбензилокси) пиперидин-1-карбоновой кислоты, из которого после отщепления аллильной группы с помощью бис(трифенилфосфин)палладий(II)диацетата аналогично примеру 152(д) был получен трет-бутиловый эфир (3RS, 4RS)-4-(4-гидроксифенил)-3-(4-метилсульфанилбензилокси)пиперидин- 1-карбоновой кислоты. Последующим алкилированием 5-бромметил-3-(2-метоксифенил)[1, 2,4] оксадиазолом аналогично примеру 44(д) получили трет-бутиловый эфир (3RS, 4RS)-4-{ 4-[3-(2- метоксифенил)[1,2,4] оксадиазол-5-илметокси] фенил} -3-(4- метилсульфанилбензилокси)пиперидин-1-карбоновой кислоты в виде светло-желтого вязкого масла; МС: 618 (М+Н)+.
(б) Аналогично примеру 152(в) путем окисления трет-бутилового эфира (3RS, 4RS)-4-{4-[3-(2-метоксифенил)[1,2,4]оксадиазол-5-илметокси] фенил}-3-(4-метилсульфанилбензилокси)пиперидин-1-карбоновой кислоты м-хлорпербензойной кислотой получили трет-бутиловый эфир (3RS,4RS)- 3-(4-метансульфонилбензилокси)-4-{4-[3-(2-метоксифенил)[1,2,4]оксадиазол-5-илметокси] фенил} пиперидин-1-карбоновой кислоты в виде бежевого твердого вещества; МС: 650 (М + Н)+.
(в) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS, 4RS)-4-(4-аллилоксифенил)-3-гидроксипиперидин-1-карбоновой кислоты [пример 86(б)] (RS)-3-хлорметил-1-(2,3-диметоксипропокси)-5- метоксинафталином получили смесь трет-бутилового эфира (3RS,4RS)- 4-(4-aллилoкcифeнил)-3-[4-[(RS)- и -[(SR)-2, 3-диметоксипропокси]- 8-метоксинафталин-2-илметокси] пиперидин-1-карбоновой кислоты, из которого после отщепления аллильной группы с помощью бис(трифенилфосфин)палладий(II)диацетата аналогично примеру 152(д) была получена смесь трет-бутилового эфира (3RS,4RS)-3-[4-[(RS)- и -[(SR)-2,3-диметоксипропокси]-8-метоксинафталин-2-илметокси]-4-(4- гидроксифенил) пиперидин-1-карбоновой кислоты. Последующим алкилированием 5-бромметил-3-(2-метоксифенил)[1,2,4] оксадиазолом аналогично примеру 44(д) получили смесь трет-бутилового эфира (3RS,4RS)-3-[4-[(RS)- и -[(SR)-2,3-диметоксипропокси] -8- метоксинафталин-2-илметокси] -4-{ 4-[3-(2-метоксифенил)[1,2,4] оксадиазол-5-илметокси] фенил}пиперидин-1-карбоновой кислоты в виде бежевого твердого вещества; МС: 770 (М+Н)+.
Использованный в качестве алкилирующего агента (RS)-3-хлорметил-1-(2,3-диметоксипропокси)-5-метоксинафталин получали следующим образом.
Этиловый эфир 4-ацетокси-8-метоксинафталин-2-карбоновой кислоты [Chem. Pharm. Bull. 19(6), 1245-1256 (1971)] омыляли с помощью водного карбоната калия в этаноле до этилового эфира 4-гидрокси-8- метоксинафталин-2-карбоновой кислоты, который в присутствии карбоната калия в метиленхлориде алкилировали (RS)-2,3-диметоксипропиловым эфиром метансульфокислоты, который был получен известным из литературы способом из (RS)-2,3-диметоксипропан-1-ола [J. Chem. Soc. (1931), 450], до этилового эфира (RS)-4-(2,3-диметоксипропокси)-8-метоксинафталин-2- карбоновой кислоты. Последующим восстановлением с помощью алюмогидрида лития аналогично примеру 5(б) был получен (RS)-[4-(2,3- диметоксипропокси)-8-метоксинафталин-2-ил]метанол, который аналогично примеру 5(в) переводили в (RS)-3-хлорметил-1-(2,3- диметоксипропокси)-5-метоксинафталин; МС: 324 (М)+.
(г) Алкилированием трет-бутилового эфира (3RS,4RS)-3-(1, 4- диметоксинафталин-2-илметокси)-4-(4-гидроксифенил)пиперидин-1- карбоновой кислоты [пример 152(д)] 5-бромметил-3-(2-метоксифенил)[1,2,4]оксадиазолом аналогично примеру 44(д) получили трет- бутиловый эфир (3RS,4RS)-3-(1,4-диметоксинафталин-2-илметокси)-4- [4-[3-(2-метоксифенил)[1,2,4] оксадиазол-5-илметокси] фенил] пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 682 (М+Н)+.
(д) Алкилированием трет-бутилового эфира (3RS,4RS)-3-(1,4- диметоксинафталин-2-илметокси)-4-(4-гидроксифенил)пиперидин-1-карбоновой кислоты [пример 152(д)] 5-бромметил-3-(3,4,5-триметоксифенил)[1,2,4]оксадиазолом аналогично примеру 44(д) получили трет-бутиловый эфир (3RS,4RS)-3-(1,4- диметоксинафталин-2-илметокси)-4-{ 4-[3-(3,4,5-триметоксифенил) [1,2, 4]оксадиазол-5-илметокси]фенил}пиперидий-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 742 (М + Н)+.
(е) Алкилированием трет-бутилового эфира (3RS, 4RS)-4-(4-гидроксифенил)-3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты [пример 61(в)] 5-бромметил-3-(2-хлорфенил)[1,2,4] оксадиазолом аналогично примеру 44(д) получили трет-бутиловый эфир (3RS,4RS)-4-[4-[3-(2-хлорфенил)-[1,2,4] оксадиазол-5-илметокси]фенил]-3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде желтого твердого вещества; МС: 626 (М+Н)+.
(ж) Алкилированием трет-бутилового эфира (3RS, 4RS)-4-(4-гидроксифенил)-3-(4-метилсульфанилбензилокси)пиперидин-1- карбоновой кислоты 5-бромметил-3-тиофен-2-ил[1,2,4] оксадиазолом аналогично примеру 44(д) получили трет-бутиловый эфир (3RS,4RS)-3-(4- метилсульфанилбензилокси)- 4-[4-(3-тиофен-2-ил[1,2,4] оксадиазол-5-илметокси)фенил]пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 594 (М + Н)+.
(з) Алкилированием трет-бутилового эфира (3RS,4RS)-3-(1, 4-диметоксинафталин-2-илметокси)-4-(4-гидроксифенил)пиперидин-1- карбоновой кислоты [пример 152(д)] 5-бромметил-3-тиофен-2-ил[1,2,4] оксадиазолом аналогичнр примеру 44(д) получили трет-бутиловый эфир (3RS,4RS)-3-(1,4- диметоксинафталин-2-илметокси)-4-[4-(3-тиофен-2-ил[1,2,4]оксадиазол-5- илметокси)фенил]пиперидин-1-карбоновой кислоты в виде бесцветного вязкого масла; МС: 658 (М+Н)+.
(и) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS, 4RS)-4-(4-аллилоксифенил)-3-гидроксипиперидин-1-карбоновой кислоты [пример 86(б)] 2-хлорметил-1-(2-метоксиэтоксиметокси)нафталином получили трет-бутиловый эфир (3RS,4RS)-4-(4-aллилoкcифeнил)-3-[1- (2-метоксиэтоксиметокси) нафталин-2-илметокси] пиперидин-1- карбоновой кислоты, из которого путем отщепления аллильной группы с помощью бис(трифенилфосфин)палладий(II)диацетата аналогично примеру 152(д) был получен трет-бутиловый эфир (3RS, 4RS)-4-(4- гидpoкcифeнил)-3-[1-(2-метоксиэтоксиметокси) нафталин -2- илметокси] пиперидин -1-карбоновой кислоты. Последующим алкилированием 5-бромметил-3-тиофен-2-ил[1,2,4]оксадиазолом аналогично примеру 44(д) получили трет-бутиловый эфир (3RS,4RS)-3- [1-(2-метоксиэтоксиметокси)нафталин-2-илметокси] -4-[4-(3-тиофен- 2-ил[1,2,4] оксадиазол-5-илметокси)фенил]пиперидин-1- карбоновой кислоты в виде бесцветного вязкого масла; МС: 702 (М+Н)+.
Использованный в качестве алкилирующего агента 2-хлорметил-1-(2- метоксиэтоксиметокси)нафталин получали следующим образом.
(α) Раствор из 2,3 г (11,4 ммоля) метилового эфира 1-гидроксинафталин-2- карбоновой кислоты в 15 мл сухого тетрагидрофурана смешивали с 0,51 г (17 ммолей) гидрида натрия (80%-ного), а затем при охлаждении льдом по каплям добавляли 2,13 г 2-метоксиэтоксиметилхлорида. По истечении 3 ч выдержки при комнатной температуре раствор экстрагировали путем встряхивания c водным раствором гидрокарбоната натрия, органическую фазу отделяли, сушили над сульфатом натрия и упаривали при пониженном давлении.
Сырой продукт очищали хроматографией на силикагеле с использованием смеси 9: 1 метиленхлорида и простого эфира в качестве элюента. Таким путем наряду с 1,55 г исходного материала получили 1,2 г метилового эфира 1-(2-метоксиэтоксиметокси)нафталин-2-карбоновой кислоты; МС: 290 (М)+.
(β) Аналогично примеру 5(б)-(в) из метилового эфира 1-(2- метоксиэтоксиметокси) нафталин-2-карбоновой кислоты восстановлением с помощью алюмогидрида лития получили [1-(2- метоксиэтоксиметокси)нафталин-2-ил] метанол, который затем переводили в 2-хлорметил-1-(2-метоксиэтоксиметокси)нафталин; МС: 280 (М)+.
(к) Алкилированием трет-бутилового эфира (3RS, 4RS)-4-(4- гидроксифенил)-3-[1-(2-метоксиэтокси)нафталин-2-илметокси] пиперидин-1-карбоновой кислоты [пример 122(з)] 5-бромметил-3- тиофен-2-ил[1,2,4]оксадиазолом аналогично примеру 44(д) получили трет-бутиловый эфир (3RS,4RS)-3-[1-(2-метоксиэтокси)нафталин-2- илметокси] -4-[4-(3-тиофен-2-ил[1,2,4]оксадиазол-5- илметокси)фенил] пиперидин-1-карбоновой кислоты в виде бесцветного вязкого масла; МС: 672 (М+Н)+.
(л) Алкилированием трет-бутилового эфира (3RS,4RS)-4-(4-гидроксифенил)- 3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты [пример 61(в)] 5- бромметил-3-тиофен-2-ил[1,2,4]оксадиазолом аналогично примеру 44(д) получили трет-бутиловый эфир (3RS,4RS)-3-(нафталин-2- илметокси)-4-[4-(3-тиофен-2-ил[1,2, 4]оксадиазол-5- илметокси)фенил]пиперидин-1-карбоновой кислоты в виде бесцветного вязкого масла; МС: 597 (М+Н)+.
(м) Алкилированием трет-бутилового эфира (3RS, 4RS)-4-(4-гидроксифенил)- 3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты [пример 61(в)] 5-бромметил-3-фуран-2-ил[1,2,4] оксадиазолом аналогично примеру 44(д) получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(3-фуран-2-ил- [1,2,4]оксадиазол-5-илметокси)фенил]-3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты в виде бесцветного твердого вещества; МС: 582 (М+Н)+.
(н) Алкилированием трет-бутилового эфира (3RS,4RS)-3-(1,4- диметоксинафталин-2-илметокси)-4-(4-гидроксифенил)пиперидин-1-карбоновой кислоты [пример 152(д)] 4-хлорметил-2-фенолоксазолом [Arch. Pharmazie (1971), 425] аналогично примеру 44(д) получили трет-бутиловый эфир (3RS,4RS)-3-(1,4-диметоксинафталин-2-илметокси)-4- [4-(2-фенилоксазол-5-илметокси)фенил] пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 651 (М+Н)+.
(о) Алкилированием трет-бутилового эфира (3RS,4RS)-3- (1,4-диметоксинафталин-2-илметокси)-4-(4-гидроксифенил)пиперидин -1-карбоновой кислоты [пример 152(д)]4-хлорметил-2-фенилтиазолом [Chem.Ber.(1961), 2887] аналогично примеру 44(д) получили трет-бутиловый эфир (3RS,4RS)-3-(1, 4-диметоксинафталин-2-илметокси)-4- [4-(2-фенилтиазол-5-илметокси)фенил]пиперидин-1-карбоновой кислоты в виде светло-желтого твердого вещества; МС: 667 (М+Н)+.
(п) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS, 4RS)-4-(4-аллилоксифенил)-3-гидроксипиперидин-1-карбоновой кислоты [пример 86(б)] 2-хлорметил-1-(2-метоксиэтокси)нафталином [пример 122(з)] получили трет-бутиловый эфир (3RS,4RS)-4-(4- aллилoкcифeнил)-3-[1-(2-метоксиэтокси)нафталин-2-илметокси] пиперидин-1-карбоновой кислоты, из которого путем отщепления аллильной группы с помощью бис(трифенил-фосфин)палладий(II)диацетата аналогично примеру 152(д) был получен трет-бутиловый эфир (3RS,4RS)-4-(4-гидpoкcифeнил)-3-[1-(2-метоксиэтокси)нафталин-2- илметокси] пиперидин-1-карбоновой кислоты. Последующим алкилированием 3-фенилизоксазол-5-илметиловым эфиром метансульфокислоты аналогично примеру 44(д) получили трет-бутиловый эфир (3RS, 4RS)-3-[1- (2-метоксиэтокси)нафталин-2-илметокси]-4-[4-(3-фенилизоксазол-5- илметокси)фенил]пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 665 (М+Н)+.
(р) Аналогично примеру 44(д) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-гидрокси-4-(4-гидроксифенил) пиперидин-1-карбоновой кислоты [пример 46(б)] 3-фенилизоксазол-5-илметиловым эфиром метансульфокислоты был получен трет-бутиловый эфир (3RS,4RS)-3- гидрокси-4-[4-(3-фенилизоксазол-5-илметокси)фенил]пиперидин-1-карбоновой кислоты, последующим алкилированием которого 2-хлорметил-1,4-диметоксинафталином [J. Org.Chem. (1983), 48(19), 3265-3268] получили трет-бутиловый эфир (3RS,4RS)-3-(1, 4-диметоксинафталин-2-илметокси)-4-[4-(3- фенилизоксазол-5-илметокси)фенил]пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 651 (М+Н)+.
(с) Алкилированием трет-бутилового эфира (3RS,4RS)-3-гидрокси-4-[4-(3-фенилизоксазол-5-илметокси)фенил] пиперидин-1-карбоновой кислоты 1-метокси-2-бромметилнафталином [пример 7(е)] аналогично примеру 1(ж) получили трет-бутиловый эфир (3RS,4RS)-3-(1-метоксинафталин-2-илметокси)-4- [4-(3-фенилизоксазол-5-илметокси)фенил] пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 621 (М+Н)+.
Использованные в качестве алкилирующих агентов замещенные 5-бромметил[1,2,4]оксадиазолы, а именно:
- 5-бромметил-3-(2-метоксифенил)[1,2, 4]оксадиазол,
- 5-бромметил-3-(3,4,5-триметоксифенил)[1,2,4]оксадиазол,
- 5-бромметил-3-(2-хлорфенил)[1,2,4]оксадиазол,
- 5-бромметил-3-тиофен-2-ил[1,2,4]оксадиазол и
- 5-бромметил-3-фуран-2-ил[1,2,4]оксадиазол,
получали аналогично описанному в J.Med.Chem. (1986, 26, 2174-2183) способу.
Использованный в качестве алкилирующего агента 3- фенилизоксазол-5-илметиловый эфир метансульфокислоты синтезировали следующим образом.
(α) К раствору из 1,21 г бензальдегидоксима в 10 мл метиленхлорида при -30oC добавляли 1,47 г (11 ммолей) N-хлорсукцинимида. По истечении 2 ч по каплям добавляли раствор из 1,0 г триэтиламина и 1, 4 г (RS)-тетрагидро-2-(2-пропинилокси)-2H- пирана в 5 мл метиленхлорида. Реакционную смесь перемешивали в течение 5 ч при комнатной температуре, затем отгоняли растворитель и сырой продукт очищали хроматографией на силикагеле с использованием метиленхлорида в качестве элюента. Таким путем получили 1,8 г (RS)-3-фенил-5-(тетрагидропиран-2- илоксиметил)изоксазола в виде бесцветной жидкости; МС: 259 (М)+.
(β) Последующее отщепление ТГП-группы осуществляли аналогично примеру 53(в). Полученный в результате (3-фенилизоксазол-5-ил) метанол превращали известным из литературы способом в 3-фенилизоксазол-5-илметиловый эфир метансульфокислоты, который был получен в виде бесцветного твердого вещества; МС: 253 (М)+.
Пример 125.
(а) Суспензию из 13,32 г (0,1 моля) (Е)-3-(4- пиридил)-2-пропеналя [Tetrahedron Letters 26, 6447 (1985)] и 19,92 r (0,1 моля) 2-(фенилсульфонил)ацетамида [Synthesis 1987, 56] в 300 мл этанола при перемешивании и при комнатной температуре смешивали в течение 15 мин, добавляя по каплям, с 20 мл раствора Тритона В (40%-ного в метаноле), а затем перемешивали в течение 16 ч при комнатной температуре и в течение 90 мин при нагревании с обратным холодильником. После охлаждения смешивали с 100 мл ледяной уксусной кислоты, после чего в течение 2,5 ч нагревали с обратным холодильником. Далее концентрировали в вакууме, создаваемом водоструйным насосом, смешивали с 200 мл воды, а затем с 16,4 г (0,2 моля) ацетата натрия и снова концентрировали. Остаток растворяли в метиленхлориде, фильтровали, фильтрат концентрировали и полученный в результате остаток перекристаллизовывали из изопропанола. Таким путем получили 3,9 г (23% от теории) 1H-[4,4'] бипиридин-2-она в виде бледно-желтых кристаллов; tпл 263-265oC.
(б) К суспензии из 9,0 г (52,3 ммоля) 1H-[4,4']бипиридин-2-она в 150 мл N,N-диметилформамида добавляли 15 мл метилиодида и реакционную смесь перемешивали в течение 20 ч при комнатной температуре. Далее по каплям добавляли 300 мл простого эфира и образовавшийся при этом осадок отфильтровывали, промывали простым эфиром и сушили в высоком вакууме. Таким путем получили 15,8 г (96% от теории) иодида 1-метил-4-(2-оксо-1,2-дигидропиридин-4-ил)пиридиния в виде бледно-желтых кристаллов; tпл 264-266oC.
(в) 5,3 г (16,9 ммоля) иодида 1-метил-4-(2-оксо-1,2-дигидропиридин- 4-ил)пиридиния взмучивали в 100 мл метанола и в атмосфере аргона при комнатной температуре смешивали, добавляя порциями, с 1,1 г (29 ммолей) борогидрида натрия. После этого реакционную смесь в течение 5 ч нагревали с обратным холодильником, а затем концентрировали в вакууме, создаваемом водоструйным насосом. Полученный при этом остаток распределяли между насыщенным раствором поваренной соли и метиленхлоридом/метанолом (9:1), объединенные метиленхлоридные фазы сушили над сульфатом магния и концентрировали. Перекристаллизацией остатка из метанола/уксусного эфира получили в результате 2,7 г (84% от теории) 1'-метил- 1',2',3',6'-тетрагидро-1H-[4,4']бипиридин-2-она в виде бледно-желтых кристаллов; tпл 250-252oC.
(г) 0,88 г (4,6 ммоля) 1'-метил-1',2',3',6'-тетрагидро-1H-[4,4']бипиридин-2-она, 180 мг (2,4 ммоля) карбоната лития и 2 г молекулярного сита
(д) 0,50 г (1, 8 ммоля) трет-бутилового эфира 2'-оксо-1',2',3,6-тетрагидро-2H-[4,4']бипиридин-1-карбоновой кислоты, 0,50 г (2,5 ммоля) (2-бромэтокси) бензола и 0,35 г (2,5 ммоля) карбоната калия выдерживали, нагревая, в течение 20 ч в 6 мл ацетонитрила при 75oC. Далее реакционную смесь концентрировали в вакууме, создаваемом водоструйным насосом, затем распределяли между водой и метиленхлоридом, объединенные метиленхлоридные фазы сушили над сульфатом магния, концентрировали и полученный в результате остаток хроматографировали на силикагеле с использованием метиленхлорида/уксусного эфира (1: 1). Таким путем получили 0,41 г (58% от теории) трет-бутилового эфира 2'-оксо-1'-(2-феноксиэтил)- 1', 2',3,6-тетрагидро-2H-[4,4']бипиридин-1-карбоновой кислоты в виде аморфного желтоватого твердого вещества; МС: 397 (М+Н)+.
(е) 0,20 г (0,5 ммоля) трет-бутилового эфира 2'-оксо-1'-(2-феноксиэтил)-1', 2', 3,6-тетрагидро-2Н-[4,4']бипиридин- 1-карбоновой кислоты растворяли в 5 мл 1,2-диметоксиэтана, смешивали с 1,5 мл 1-молярного раствора борана в тетрагидрофуране и перемешивали в течение 48 ч при комнатной температуре. Далее дополнительно добавляли 1,0 мл 1-молярного раствора борана в тетрагидрофуране и перемешивание продолжали в течение 60 ч при комнатной температуре. После этого при охлаждении льдом добавляли сначала 2,5 мл 50%-ного раствора КОН в воде, а затем 2,5 мл 30%-ного раствора перекиси водорода в воде и реакционную смесь нагревали с обратным холодильником в течение 2 ч. Затем реакционный раствор распределяли между водой и метиленхлоридом, объединенные метиленхлоридные фазы сушили над сульфатом магния, концентрировали и полученный в результате остаток хроматографировали на силикагеле с использованием метиленхлорида/метанола (95:5). Таким путем получили 23 мг (11% от теории) трет-бутилового эфира (3RS,4RS)-3-гидрокси-2'-оксо- 1'-(2-феноксиэтил)-3,4,5,6,1', 2'-гексагидро-2H- [4, 4']бипиридин-1-карбоновой кислоты в виде аморфного желтоватого твердого вещества; МС: 414 (М)+.
(ж) Раствор из 21 мг (0,051 ммоля) трет-бутилового эфира (3RS, 4RS)-3-гидрокси-2'-оксо-1'-(2-феноксиэтил)-3,4,5,6,1', 2'- гексагидро-2H-[4,4']бипиридин-1-карбоновой кислоты и 15 мг (0,068 ммоля) 2-бромметилнафталина в 0,5 мл диметилформамида смешивали с 4,0 мг (0, 083 ммоля) гидрида натрия (50%-ная дисперсия в вазелиновом масле) и смесь перемешивали в течение 0,5 ч при комнатной температуре. Далее реакционную смесь распределяли между простым эфиром и водой, объединенные эфирные фазы сушили над сульфатом магния и концентрировали в вакууме, создаваемом водоструйным насосом. Сырой продукт хроматографировали на силикагеле с использованием метиленхлорида/метанола (95:5). Таким путем получили 20 мг (71% от теории) трет-бутилового эфира (3'RS,4'RS)-3'-(нафталин-2- илметокси)-1-(2-феноксиэтил)-1',2',3', 4', 5', 6'-гексагидро- 1H-[4, 4']бипиридин-2-он-1'-карбоновой кислоты в виде аморфного желтоватого твердого вещества; МС: 555 (М+Н)+.
(з) 20 мг (0,036 ммоля) трет-бутилового эфира (3'RS, 4'RS) -3'-(нафталин-2-илметокси)-1-(2-феноксиэтил)-1', 2',3',4',5',6'- гексагидро-1H-[4,4']бипиридин-2-он-1'-карбоновой кислоты растворяли в 3 мл метиленхлорида, смешивали с 40 мг (0,18 ммоля) безводного бромида цинка и перемешивали в течение 3 ч при комнатной температуре. Далее реакционную смесь сливали на водный раствор карбоната натрия и экстрагировали метиленхлоридом. Объединенные метиленхлоридные фазы сушили над сульфатом магния, концентрировали и полученный в результате остаток хроматографировали на силикагеле с использованием смеси 9:1 метиленхлорида и метанола в качестве элюента. Таким путем получили 5,8 мг (35% от теории) (3'RS,4'RS)-3'-(нафталин-2- илметокси)-1-(2-феноксиэтил)-1',2',3',4',5',6'-гексагидро- 1H-[4,4']бипиридин-2-она в виде аморфного бесцветного твердого вещества; МС: 455 (М+Н)+.
Пример 126.
(а) 41 г (0,173 моля) 2,5-дибромпиридина и 20,1 г (0,173 ммоля) 3-фенил-1-пропина в атмосфере аргона и условиях, исключающих наличие влаги, растворяли в 450 мл триэтиламина, при охлаждении льдом смешивали с 740 мг (3,88 ммоля) иодида меди(I) и 2,7 г (3,88 ммоля) дихлорида бис(трифенилфосфин)палладия и перемешивали в течение 1 ч при 0-5oC, а затем в течение 1 ч при комнатной температуре. Далее реакционный раствор сливали на ледяную воду и экстрагировали метиленхлоридом, объединенные метиленхлоридные фазы сушили над сульфатом магния, концентрировали и полученный в результате остаток хроматографировали на силикагеле один раз с использованием метиленхлорида и один раз с использованием гексана/этилового эфира уксусной кислоты (9: 1). Таким путем получили 27 г (57% от теории) 5-бром-2-(3-фенилпроп-1-инил) пиридина в виде бесцветного твердого вещества; МС: 271, 273 (М)+.
(б) 17 г (0,062 моля) 5-бром-2-(3-фенилпроп-1-инил)пиридина растворяли в 300 мл этанола, смешивали с 150 мг оксида платины и гидрировали в течение 1 ч в атмосфере водорода. Далее реакционную смесь фильтровали через целлюлозный фильтр с размером пор 0,8 мкм и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате остаток хроматографировали на силикагеле с использованием метиленхлорида. Таким путем получили 5,2 г (30% от теории) 5-бром-2-(3-фенилпропил)пиридина в виде желтоватого масла; МС: 171, 173 (М-винилбензол)+.
(в) К 21,5 мл (0,152 моля) диизопропиламина, растворенного в 145 мл тетрагидрофурана, в атмосфере аргона и в условиях, исключающих наличие влаги, по каплям добавляли 1,6-молярный раствор н-бутиллития в гексане (около 0,16 моля) таким образом, чтобы температура не поднималась выше -70oC. Далее в течение 45 мин по каплям добавляли 29 г (0,145 моля) трет-бутилового эфира 4-пиперидон- 1-карбоновой кислоты, растворенного в 145 мл тетрагидрофурана, поддерживая при этом температуру ниже -70oC. После перемешивания, продолжавшегося в течение 10 мин при той же температуре, в течение 30 мин по каплям добавляли раствор из 56 г (0,157 моля) N-фенилбис(трифторметансульфонамида) в 145 мл тетрагидрофурана таким образом, чтобы температура не поднималась выше -70oC. После этого реакционной смеси давали нагреться до комнатной температуры и перемешивали при этой температуре еще в течение 3 ч. В завершение реакционный раствор концентрировали при 40oC в вакууме, создаваемом водоструйным насосом, и полученный в результате остаток хроматографировали на основном оксиде алюминия с использованием гексана/этилового эфира уксусной кислоты (9:1). Таким путем получили 41 г (85% от теории) трет-бутилового эфира 4-трифторметилсульфонилокси-3,6-дигидро-2H-пиридин-1- карбоновой кислоты в виде бесцветного масла; МС: 332 (М+Н)+.
(г) 1,05 г (3, 8 ммоля) 5-бром-2-(3-фенилпропил)пиридина, 1,12 мл (5,4 ммоля) гексаметилдистаннана, 100 мг (0,086 ммоля) тетракис(трифенилфосфин)палладия, 3 г молекулярного сита

(д) 0,93 г (2,6 ммоля) 2-(3-фенилпропил)-5-триметилстаннилпиридина, 0,9 г (2,7 ммоля) трет-бутилового эфира 4-трифторметилсульфонилокси-3,6-дигидро-2Н-пиридин-1-карбоновой кислоты, 0,345 г (8,0 ммолей) хлорида лития, 100 мг (0,086 ммоля) тетракис(трифенилфосфин)палладия, 3 г молекулярного сита
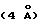
(е) 0,587 г (1, 55 ммоля) трет-бутилового эфира 6-(3-фенилпропил)- 3', 6'-дигидро-2'H-[3,4'] бипиридин-1'-карбоновой кислоты растворяли в 8 мл 1,2-диметоксиэтана, смешивали с 6 мл 1-молярного раствора борана в тетрагидрофуране и перемешивали в течение 4 ч при 60-65oC в колбе, закрытой тефлоновой пробкой. Далее дополнительно добавляли 3 мл 1-молярного раствора борана в тетрагидрофуране, а через 24 ч добавляли еще 2,2 мл 1-молярного раствора борана в тетрагидрофуране и перемешивали в общей сложности в течение 48 ч при 60-65oC. После этого при охлаждении льдом добавляли сначала 7,0 мл 50%-ного раствора КОН в воде, а затем 6,0 мл 30%-ного раствора перекиси водорода в воде и реакционную смесь нагревали с обратным холодильником в течение 2 ч. Затем реакционный раствор распределяли между водой и метиленхлоридом, объединенные метиленхлоридные фазы сушили над сульфатом магния, концентрировали и полученный в результате остаток хроматографировали на силикагеле с использованием простого эфира/метанола (99:1). Таким путем получили 211 мг (34% от теории) трет-бутилового эфира (3'RS,4'RS)-3'-гидрокси-6-(3- фенилпропил)-3',4',5',6'-тетрагидро-2'H-[3,4']бипиридин-1'- карбоновой кислоты в виде аморфного бесцветного твердого вещества; МС: 397 (М+Н)+.
(ж) Аналогично примеру 125(ж) из трет-бутилового эфира (3'RS,4'RS)-3'-гидрокси-6-(3-фенилпропил)-3', 4',5',6' -тетрагидро-2'H-[3,4']бипиридин-1'-карбоновой кислоты и 2-бромметилнафталина получили трет-бутиловый эфир (3'RS, 4'RS)-3'-(нафталин-2-илметокси)-6-(3-фенилпропил)-3', 4',5', 6'-тетрагидро-2'H-[3,4']бипиридин-1'-карбоновой кислоты в виде аморфного бесцветного твердого вещества; МС: 537 (М+Н)+.
(з) Аналогично примеру 125(з) из трет-бутилового эфира (3'RS, 4'RS)-3'-(нафталин-2-илметокси)-6-(3-фенилпропил)-3', 4', 5', 6'-тетрагидро-2'H-[3,4'] бипиридин-1'-карбоновой кислоты путем отщепления ВОС-группы с помощью безводного бромида цинка получили (3'RS,4'RS)-3'-(нафталин-2-илметокси)-6-(3- фенилпропил)-1',2',3',4',5',6'-гексагидро[3,4']бипиридин в виде аморфной бесцветной пены; МС: 437 (М+Н)+.
Пример 127.
(а) 1,24 г (5,7 ммоля) 5-бром-2-(3-гидроксипропил)пиридина [J.Org.Chem. 53, 386 (1988)] растворяли в 4 мл N,N-диметилформамида, смешивали сначала с 0,7 мл (5,9 ммоля) бензилбромида, а затем с 285 мг (около 5,9 ммоля) дисперсии гидрида натрия (примерно 50%-ная в минеральном масле) и перемешивали в атмосфере аргона в течение 90 мин при комнатной температуре. Затем реакционный раствор распределяли между водой и метиленхлоридом, объединенные метиленхлоридные фазы сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате остаток хроматографировали на силикагеле с использованием простого эфира/метиленхлорида (5: 95). Таким путем получили 1,57 г (90% от теории) 2-(3-бензилоксипропил)-5- бромпиридина в виде желтоватого масла.
(б) 1,57 г (5,10 ммоля) 2-(3-бензилоксипропил)-5-бромпиридина, 1,6 мл (7,5 ммоля) гексаметилдистаннана, 150 мг (0,129 ммоля) тетракис(трифенилфосфин)палладия, 3 г молекулярного сита

(в) 1,43 г (3,66 ммоля) 2-(3-бензилоксипропил)- 5-триметилстаннанилпиридина, 1, 32 г (4,00 ммоля) трет-бутилового эфира 4-трифторметилсульфонилокси-3,6-дигидро-2H-пиридин-1-карбоновой кислоты [пример 126(в)], 0,477 г (11,3 ммоля) хлорида лития, 150 мг (0,129 ммоля) тетракис(трифенилфосфин)палладия, 3 г молекулярного сита

(г) 0,115 г (0, 28 ммоля) трет-бутилового эфира 6-(3-бензилоксипропил)-3',6'-дигидро-2'H-[3,4']бипиридинил-1'- карбоновой кислоты растворяли в 1 мл 1,2-диметоксиэтана, смешивали с 1 мл 1-молярного раствора борана в тетрагидрофуране и перемешивали в течение 96 ч при комнатной температуре. После этого при охлаждении льдом добавляли сначала 1,0 мл 50%-ного раствора КОН в воде, а затем 1,0 мл 30%-ного раствора перекиси водорода в воде и реакционную смесь нагревали с обратным холодильником в течение 2 ч. Затем реакционный раствор распределяли между водой и метиленхлоридом, объединенные метиленхлоридные фазы сушили над сульфатом магния и концентрировали. Таким путем получили 105 мг (88% от теории) трет- бутилового эфира (3'RS,4'RS)-6-(3-бензилоксипропил)-3'- гидрокси-3', 4', 5', 6'-тетрагидро-2'Н-[3, 4']бипиридин-1'- карбоновой кислоты в виде желтоватого масла, который использовали непосредственно на следующей стадии.
(д) Аналогично примеру 125(ж) из трет-бутилового эфира (3'RS, 4'RS)-6-(3-бензилоксипропил)-3'-гидрокси-3', 4', 5',6'-тетрагидро- 2'H-[3,4']бипиридин-1-карбоновой кислоты и 2-бромметилнафталина получили трет-бутиловый эфир (3'RS, 4'RS)-6-(3-бензилоксипропил)-3'-(нафталин-2-илметокси)-3', 4',5',6'-тетрагидро-2'H-[3,4']бипиридин-1'-карбоновой кислоты в виде бесцветного масла; МС: 568 (М+Н)+.
(е) Аналогично примеру 125(з) из трет-бутилового эфира (3'RS,4'RS)- 6-(3-бензилоксипропил)-3'-(нафталин-2-илметокси)-3', 4',5',6'- тетрагидро-2'Н- [3,4'] бипиридин-1'-карбоновой кислоты путем отщепления ВОС-группы с помощью безводного бромида цинка получили (3'RS,4'RS)-6-(3-бензилоксипропил)-3'-(нафталин-2-илметокси)-1', 2', 3', 4',5',6'-гексагидро[3,4']бипиридин в виде бесцветного масла; МС: 467 (М+Н)+.
Пример 128.
(а) К 104 мл (1,0 моль) бензилового спирта, растворенного в 175 мл N, N-диметилформамида, при температуре максимально 30oC порциями добавляли 19 г дисперсии гидрида натрия (50%-ная в масле, 0,38 моля) и затем перемешивали в течение 2 ч при комнатной температуре. После этого в течение 10 мин по каплям добавляли 46,4 г (0, 183 моля) 5-бром-2-(2-триметилсилил)этинилпиридина [J.Org.Chem. 53, 386 (1988)] в 50 мл N,N-диметилформамида и перемешивали в течение 2 ч при комнатной температуре. Далее реакционную смесь сливали на 1000 мл насыщенного раствора гидрокарбоната натрия и экстрагировали простым эфиром. Объединенные эфирные фазы промывали насыщенным раствором поваренной соли, сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате остаток хроматографировали на силикагеле с использованием метиленхлорида/простого эфира (99:1). Таким путем получили 19,5 г (37% от теории) (Е)-2-(2- бензилоксивинил)-5-бромпиридина в виде желтоватого твердого вещества.
(б) 17,5 г (0,0603 моля) (Е)-2-(2-бензилоксивинил)-5-бромпиридина растворяли в 650 мл толуола, смешивали примерно с 3 г никеля Ренея (влажный, промытый метанолом и толуолом) и перемешивали в течение 72 ч в атмосфере водорода при комнатной температуре. В течение этого времени дополнительно трижды добавляли такое же количество никеля Ренея. Далее фильтровали через подушку из дикалита, концентрировали в вакууме, создаваемом водоструйным насосом, и остаток хроматографировали на силикагеле с использованием метиленхлорида/простого эфира (95: 5). Таким путем получили 13,2 г (75,4% от теории) 2-(2-бензилоксиэтил)-5-бромпиридина в виде красноватой пены; МС: 292, 294 (М+Н)+.
(в) Аналогично примеру 127(б)-(г) из 2-(2-бензилоксиэтил)- 5-бромпиридина через 2-(2-бензилоксиэтил)-5-триметилстаннанилпиридин [желтоватое масло, МС: 362 (M-CH3)+], а также трет- бутиловый эфир 4-трифторметилсульфонилокси-3,6-дигидро-2Н-пиридин- 1-карбоновой кислоты и трет-бутиловый эфир 6-(2-бензилоксиэтил)- 3', 6'-дигидро-2'H-[3, 4']бипиридин-1'-карбоновой кислоты [бесцветное масло, МС: 395 (М+Н)+] получили трет-бутиловый эфир (3'RS, 4'RS)-6-(2-бензилоксиэтил)-3'-гидрокси-3', 4', 5', 6'- тетрагидро-2'Н-[3,4'] бипиридин-1'-карбоновой кислоты в виде бесцветного твердого вещества; МС: 413 (М+Н)+.
(г) Аналогично примеру 125(ж) из трет-бутилового эфира (3'RS, 4'RS)-6-(2- бензилоксиэтил)-3'-гидрокси-3', 4', 5',6'-тетрагидро-2'H- [3,4'] бипиридин-1'-карбоновой кислоты и 2-бромметилнафталина получили трет-бутиловый эфир (3'RS, 4'RS)-6-(2-бензилоксиэтил)- 3'-(нафталин-2-илметокси)-3',4',5',6'-тетрагидро-2'H- [3,4']бипиридин-1'-карбоновой кислоты в виде аморфного бесцветного твердого вещества; МС: 553 (М+Н)+.
(д) Аналогично примеру 125(з) из трет-бутилового эфира (3'RS,4'RS)-6-(2- бензилоксиэтил)-3'-(нафталин-2-илметокси)-3',4',5',6'- тетрагидро-2'H-[3,4'] бипиридин-1'-карбоновой кислоты путем отщепления BOC-группы с помощью безводного бромида цинка получили (3'RS, 4'RS)-6-(2-бензилоксиэтил)-3'-(нафталин-2-илметокси)- 1', 2',3',4',5',6'-гексагидро[3,4']бипиридин в виде бежевого резинообразного вещества; МС: 453 (М+Н)+.
Пример 129.
(а) Аналогично примеру 127(б)-(г) из 5-бром-2- метилсульфанилпиримидина [J.Chem.Soc. 1953, 3129] через 2-метилсульфанил-5-триметилстаннанилпиримидин [желтоватое масло] , а также трет-бутиловый эфир 4-трифторметилсульфонилокси-3,6-дигидро- 2Н-пиридин-1-карбоновой кислоты и трет-бутиловый эфир 4-(2- метилсульфанилпиримидин-5-ил)-3,6-дигидро-2Н-пиридин-1-карбоновой кислоты [желтоватое масло, МС: 308 (М+Н)+] . получили трет-бутиловый эфир (3RS, 4RS)-3-гидрокси-4-(2-метилсульфанил- пиримидин-5-ил)пиперидин-1-карбоновой кислоты в виде аморфного желтоватого твердого вещества; МС: 326 (М+Н)+.
(б) Аналогично примеру 125(ж) из трет-бутилового эфира (3RS,4RS)-3-гидрокси-4-(2-метилсульфанилпиримидин-5-ил)пиперидин- 1-карбоновой кислоты и 2-бромметилнафталина получили трет-бутиловый эфир (3RS, 4RS)- 4-(2-метилсульфанилпиримидин-5-ил)-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты в виде аморфного желтоватого твердого вещества; МС: 466 (М+Н)+
(в) 0,138 г (0,296 ммоля) трет-бутилового эфира (3RS,4RS)-4- (2-метилсульфанилпиримидин-5-ил)-3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты растворяли в 5 мл метиленхлорида, смешивали с 0,113 г (около 0, 46 ммоля) м-хлорпербензойной кислоты (примерно 70%-ной), перемешивали в течение 3 ч при комнатной температуре, смешивали с дополнительными 0,050 г (около 0,20 ммоля) м-хлорпербензойной кислоты и перемешивание продолжали еще в течение 16 ч. Далее реакционную смесь распределяли между метиленхлоридом и насыщенным содовым раствором, объединенные метиленхлоридные фазы сушили над сульфатом магния, фильтровали и коцентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате остаток перекристаллизовывали из простого эфира. Таким путем получили 0,102 г (69% от теории) трет-бутилового эфира (3RS, 4RS)-4-(2-метилсульфонилпиримидин-5- ил)-3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 498 (М+Н)+.
(г) 0,027 г (0,24 ммоля) трет-бутилата калия предварительно загружали в 1 мл тетрагидрофурана и при 0oC по каплям добавляли 0,038 г (0,22 ммоля) 3-бензилоксипропанола, растворенного в 0,5 мл тетрагидрофурана. По окончании перемешивания, длившегося в течение 15 мин при 0oC, при той же температуре по каплям добавляли 0,098 г (0,20 ммоля) трет-бутилового эфира (3RS,4RS)-4-(2- метилсульфонилпиримидин-5-ил)-3-(нафталин-2-илметокси)пиперидин- 1-карбоновой кислоты, растворенного в 1 мл тетрагидрофурана, и реакционную смесь перемешивали в течение 18 ч при комнатной температуре. Далее смесь сливали на ледяную воду и экстрагировали простым эфиром. Объединенные эфирные фазы промывали насыщенным раствором поваренной соли, сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате остаток хроматографировали на силикагеле с использованием метиленхлорида/метанола (95:5). Таким путем получили 0,076 г (66% от теории) трет-бутилового эфира (3RS,4RS)-4-[2-(3-бензилоксипропокси)пиримидин-5-ил] -3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 585 (М+Н)+.
(д) Аналогично примеру 125(з) из трет-бутилового эфира (3RS,4RS)-4-[2-(3-бензилоксипропокси)пиримидин-5-ил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты путем отщепления BOC-группы с помощью безводного бромида цинка получили 2-(3-бензилоксипропокси)-5-[(3RS, 4RS)-3-(нафталин-2- илметокси)пиперидин-4-ил] пиримидин в виде желтоватого резинообразного вещества; МС: 485 (М+Н)+.
Пример 130.
(а) 0,90 г (2,18 ммоля) трет-бутилового эфира (3'RS, 4'RS)-6-(2-бензилоксиэтил)-3'-гидрокси-3', 4', 5',6'-тетрагидро- 2'H-[3,4']бипиридин-1'-карбоновой кислоты [пример 128(в)] , растворенного в 15 мл тетрагидрофурана, смешивали с 0,3 мл уксусной кислоты и 250 мг палладия на угле (10%-ного) и реакционную смесь перемешивали в течение 14 дней в атмосфере водорода. Далее фильтровали через целлюлозный фильтр с размером пор 0,8 мкм и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный при этом остаток распределяли между метиленхлоридом и насыщенным содовым раствором, объединенные метиленхлоридные фазы сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт в завершение хроматографировали на силикагеле с использованием метиленхлорида/метанола (95:5). Таким путем получили 0,555 г (80% от теории) трет-бутилового эфира (3'RS,4'RS)-3'-гидрокси-6-(2-гидроксиэтил)-3',4',5',6'-тетрагидро-2'H-[3, 4']бипиридин-1'-карбоновой кислоты в виде бесцветного резинообразного вещества; МС: 323 (М+Н)+.
(б) 0,46 г (1,43 ммоля) трет-бутилового эфира (3'RS, 4'RS)-3'-гидрокси-6-(2-гидроксиэтил)-3',4',5',6'- тетрагидро-2'H-[3,4']бипиридин-1'-карбоновой кислоты, 0,18 г (1,5 ммоля) 4-диметиламинопиридина и 0,32 мл (2,2 ммоля) триэтиламина предварительно загружали в 5 мл метиленхлорида и смешивали с 0,55 г (1,7 ммоля) бромтрифенилметана. По окончании перемешивания, длившегося в течение 16 ч при комнатной температуре, дополнительно
добавляли 0,32 мл (2,2 ммоля) триэтиламина и 0,50 г (1,5 ммоля) бромтрифенилметана и перемешивание продолжали еще в течение 1 ч при комнатной температуре. После этого реакционную смесь распределяли между метиленхлоридом и насыщенным содовым раствором, объединенные метиленхлоридные фазы сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате остаток хроматографировали на силикагеле с использованием метиленхлорида/метанола (95: 5). Таким путем получили 0,67 г (83% от теории) трет-бутилового эфира (3'RS, 4'RS)-3'-гидрокси-6-(2- тритилоксиэтил)-3', 4', 5',6'-тетрагидро-2'H-[3,4']бипиридин- 1'-карбоновой кислоты в виде бесцветной пены; МС: 566 (М+Н)+.
(в) Аналогично примеру 125(ж) из трет-бутилового эфира (3'RS, 4'RS)-3'-гидрокси-6-(2-тритилоксиэтил)-3', 4', 5',6'-тетрагидро-2'H- [3,4']бипиридин-1'-карбоновой кислоты и 2-бромметилнафталина получили трет-бутиловый эфир (3'RS, 4'RS)-3'-(нафталин-2- илметокси)-6-(2-тритилоксиэтил)-3', 4',5', 6'-тетрагидро-2'H-[3,4'] бипиридин-1'-карбоновой кислоты в виде аморфного бесцветного твердого вещества; МС: 706 (М+Н)+.
(г) 0,35 г (0,50 ммоля) трет-бутилового эфира (3'RS,4'RS)-3'- (нафталин-2-илметокси)-6-(2-тритилоксиэтил)-3', 4', 5', 6'-тетрагидро- 2'Н-[3,4'] бипиридин-1'-карбоновой кислоты растворяли в 8 мл метиленхлорида, затем при комнатной температуре быстро смешивали с раствором из 240 мг трифторуксусной кислоты и 440 мг ангидрида трифторуксусной кислоты в 2 мл метиленхлорида и реакционную смесь перемешивали в течение 50 с. После этого при охлаждении льдом добавляли 2,2 мл триэтиламина, а затем 3 мл метанола и перемешивали в течение 10 мин без охлаждения. Далее реакционную смесь распределяли между метиленхлоридом и насыщенным содовым раствором, объединенные метиленхлоридные фазы сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате остаток хроматографировали на силикагеле с использованием метиленхлорида/метанола (95: 5). Таким путем получили 0,189 г (82% от теории) трет-бутилового эфира (3'RS, 4'RS)-6-(2-гидpoкcиэтил)-3'-(нафталин-2-илметокси)-3', 4', 5',6'-тетрагидро-2'H-[3,4']бипиридин-1'- карбоновой кислоты в виде аморфного оранжевого твердого вещества; МС: 463 (М+Н)+.
(д) 0,060 г (0,129 ммоля) трет-бутилового эфира (3'RS,4'RS)-6-(2-гидроксиэтил)-3'-(нафталин-2- илметокси)-3', 4',5',6'-тетрагидро-2'H-[3, 4']бипиридин-1'- карбоновой кислоты и 0,022 г (0,129 ммоля) 2-хлорбензотиазола растворяли в 0,5 мл N, N-диметилформамида и смешивали с 0,008 г гидрида натрия (примерно 50%-ного в минеральном масле, около 0,17 ммоля) и реакционную смесь перемешивали в течение 4,5 ч при комнатной температуре. После этого смешивали с ледяной водой и экстрагировали простым эфиром. Объединенные эфирные фазы сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате остаток хроматографировали на силикагеле с использованием метиленхлорида/простого эфира (1: 1). Таким путем получили 0,053 г (70% от теории) трет-бутилового эфира (3'RS,4'RS)-3'-(нaфтaлин- 2-илметокси)-6-винил-3',4', 5',6'-тетрагидро-2'H-[3,4'] бипиридин-1'-карбоновой кислоты в виде аморфного бесцветного твердого вещества; МС: 446 (М+Н)+.
(е) 0,041 г (0,091 ммоля) трет-бутилового эфира (3'RS, 4'RS)-3'- (нафталин-2-илметокси)-6-винил-3', 4', 5', 6'-тетрагидро-2'H- [3,4']бипиридин-1'- карбоновой кислоты и 0,054 г (0,32 ммоля) 2-меркаптобензотиазола растворяли в 0,5 мл ацетонитрила, смешивали с 0,2 мл (0,12 ммоля) 0,6 М раствора метилата натрия в метаноле и перемешивали в течение 3,5 ч при 80oC. После этого реакционную смесь концентрировали и остаток хроматографировали на силикагеле с использованием этилового эфира уксусной кислоты/гексана (3: 2). Таким путем получили 0,040 г (72% от теории) трет-бутилового эфира (3'RS, 4'RS)-3'-(нафталин-2-илметокси)-6-[2-(2-тиоксобензотиазол-3-ил) этил] -3', 4', 5', 6'-тетрагидро-2'H-[3,4'] бипиридин-1'-карбоновой кислоты в виде аморфного желтоватого твердого вещества; МС: 612 (М+Н)+.
(ж) Аналогично примеру 125(з) из трет-бутилового эфира (3'RS,4'RS) -3'-(нафталин-2-илметокси)-6-[2-(2-тиоксобензотиазол-3-ил)этил] - 3', 4',5', 6'-тетрагидро-2'H-[3,4'] бипиридин-1'-карбоновой кислоты путем отщепления -BOC-группы с помощью безводного бромида цинка получили 3-[2-[(3'RS,4'RS)-3'-(нафталин-2-илметокси)- 1', 2',3',4',5', 6'-гексагидро-[3,4'] бипиридин-6-ил] этил] - 3Н-бензотиазол-2-тион в виде аморфного бесцветного твердого вещества; МС: 512 (М+Н)+.
Пример 131.
(а) 0,15 г (0,56 ммоля) 5-бромметил-3-(2-хлорфенил)[1,2,4]оксадиазола [пример 124], 0,21 г карбоната калия и 0,15 г гидрокарбоната натрия перемешивали в течение 42 ч при 65oC в смеси из 4,5 мл тетрагидрофурана и 1,0 мл воды. После этого реакционный раствор охлаждали, разбавляли водой и экстрагировали простым эфиром. Объединенные эфирные фазы сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате остаток хроматографировали на силикагеле с использованием метиленхлорида/простого эфира (9: 1). Таким путем получили 0,041 г (35% от теории) [3-(2-хлорфенил)[1,2,4]оксадиазол-5-ил] метанола в виде бесцветного твердого вещества; МС: 210 (М)+.
(б) 0,040 г (0,19 ммоля) [3-(2-хлорфенил)[1,2,4]оксадиазол-5-ил] метанола и 0,094 г (0,19 ммоля) трет-бутилового эфира (3RS,4RS)-4-(2- метилсульфонилпиримидин-5-ил)-3-(нафталин-2-илметокси)пиперидин- 1-карбоновой кислоты [пример 129(в)] растворяли в 0,5 мл N,N-диметилформамида, при охлаждении льдом смешивали с 0,0095 г гидрида натрия (примерно 50%-ного в минеральном масле, около 0,20 ммоля) и реакционную смесь перемешивали в течение 1 ч при комнатной температуре. После этого смешивали с ледяной водой и экстрагировали простым эфиром. Объединенные эфирные фазы сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате остаток хроматографировали на силикагеле с использованием простого эфира. Таким путем получили 0,112 г (94% от теории) трет-бутилового эфира (3RS,4RS)-4-[2- [3-(2-хлорфенил)[1,2,4]оксадиазол-5- илметокси] пиримидин-5-ил] -3-(нафталин-2-илметокси) пиперидин-1- карбоновой кислоты в виде аморфного резинообразного вещества красноватого цвета; МС: 628 (М+Н)+.
(в) Аналогично примеру 125(з) из трет-бутилового эфира (3RS,4RS)- 4-[2-[3-(2-хлорфенил)[1,2,4] оксадиазол-5-илметокси] пиримидин-5-ил] -3- (нафталин-2-илметокси) пиперидин-1-карбоновой кислоты путем отщепления BOC-группы с помощью безводного бромида цинка получили 2-[3-(2-хлорфенил)-[1,2,4] оксадиазол-5-илметокси] -5-[(3RS, 4RS)- 3-(нафталин-2-илметокси)пиперидин-4-ил] пиримидин в виде аморфного желтоватого твердого вещества; МС: 528 (М+Н)+.
Пример 132.
(а) 2,3 г (10 ммолей) 3-бензилокси-1-бромпропана и 0,76 г (10 ммолей) тиомочевины нагревали с обратным холодильником в 5,0 мл этанола в течение 3,5 ч. После этого охлаждали до комнатной температуры, смешивали с 0,6 г (15 ммолей) гидроксида натрия в 6,0 мл воды и далее перемешивали в течение 3 ч в атмосфере аргона. Затем подкисляли разбавленной соляной кислотой и экстрагировали простым эфиром. Объединенные эфирные фазы сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате остаток хроматографировали на силикагеле с использованием гексана/метиленхлорида (1:1). Таким путем получили 1,5 г (83% от теории) 3-бензилоксипропан-1-тиола в виде бесцветной жидкости.
(б) Аналогично примеру 131(б) из 3-бензилоксипропан-1-тиола и трет-бутилового эфира (3RS,4RS)-4-(2-метилсульфонилпиримидин-5-ил)- 3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты [пример 129(в)] получили трет-бутиловый эфир (3RS,4RS)-4-[2-(3-бензилоксипропилсульфанил)пиримидин-5-ил] -3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде розово-красного твердого вещества; МС: 600 (М+Н)+.
(в) Аналогично примеру 125(з) из трет-бутилового эфира (3RS,4RS)-4-[2-(3-бензилоксипропилсульфанил)пиримидин-5-ил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты путем отщепления BOC-группы с помощью безводного бромида цинка получили 2-(3-бензилоксипропилсульфанил)-5-[(3RS, 4RS)-3-(нафталин-2- илметокси)пиперидин-4-ил] пиримидин в виде аморфного бесцветного твердого вещества; МС: 500 (М+Н)+.
Пример 133.
(а) 0,50 г (2,2 ммоля) 3-бензилокси-1-бромпропана смешивали с 2,5 мл 30%-ного раствора метиламина в этаноле и перемешивали в течение 10 ч при 60oC в закрытом сосуде. После этого смешивали с ледяной водой и экстрагировали простым эфиром. Объединенные эфирные фазы сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате остаток хроматографировали на силикагеле с использованием метиленхлорида/метанола (9: 1). Таким путем получили 0,16 г (41% от теории) (3-бензилоксипропил)метиламина в виде бесцветного масла.
(б) 0,15 г (0,84 ммоля) (3-бензилоксипропил)метиламина и 0,060 г (0,112 ммоля) трет-бутилового эфира (3RS, 4RS)-4-(2- метилсульфонилпиримидин-5-ил)-3-(нафталин-2-илметокси) пиперидин- 1-карбоновой кислоты [пример 129(в)] перемешивали в атмосфере аргона в течение 18 ч при 80oC в 1,5 мл триэтиламина. После этого смешивали с ледяной водой и экстрагировали простым эфиром. Объединенные эфирные фазы сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате остаток хроматографировали на силикагеле с использованием метиленхлорида/этилового эфира уксусной кислоты (1:1). Таким путем получили 0,070 г (97% от теории) трет- бутилового эфира (3RS, 4RS)-4-[2-[(3-бензилоксипропил)метиламино] пиримидин-5-ил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде коричневатого резинообразного вещества; МС: 598 (М+Н)+.
(в) Аналогично примеру 125(з) из трет-бутилового эфира (3RS,4RS)-4-[2-[(3-бензилоксипропил)метиламино] пиримидин-5-ил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты путем отщепления BOC-группы с помощью безводного бромида цинка получили (3- бензилоксипропил)метил-[5-[(3RS, 4RS)-3-(нафталин-2-илметокси) пиперидин-4-ил] пиримидин-2-ил] амин в виде аморфного бесцветного твердого вещества; МС: 498 (М+Н)+.
Пример 134.
(а) 1,15 г (5,0 ммолей) 3-бензилокси-1-бромпропана и 1,02 г (5,5 ммоля) фталимида калия перемешивали в течение 2 ч при 70-80oC в 10 мл N,N-диметилформамида. После этого смешивали с ледяной водой и образовавшийся при этом осадок отфильтровывали, промывали водой и сушили над пятиокисью фосфора в вакууме, создаваемом водоструйным насосом. Таким путем получили 1,4 г (95% от теории) 2-(3-бензилоксипропил)изоиндол-1,3- диона в виде бесцветного твердого вещества.
(б) 1,4 г (4,7 ммоля) 2-(3-бензилоксипропил)изоиндол-1,3-диона и 0,9 мл моногидрата гидразина перемешивали в течение 2 ч в атмосфере аргона при 100oC в 10 мл абсолютного этанола. После охлаждения смешивали с простым эфиром, фильтровали и фильтрат концентрировали. Таким путем получили 0,75 г (96% от теории) 3-бензилоксипропиламина в виде светло-желтого масла.
(в) Аналогично примеру 133(б) из 3-бензилоксипропиламина и трет-бутилового эфира (3RS, 4RS)-4-(2-метилсульфонилпиримидин-5-ил)-3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты [пример 129(в)] получили трет-бутиловый эфир (3RS, 4RS)-4-[2-(3-бензилоксипропиламино)пиримидин-5-ил] -3- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде коричневатого резинообразного вещества; МС: 583 (М+Н)+.
(г) Аналогично примеру 125(з) из трет-бутилового эфира (3RS,4RS)-4-[2-(3-бензилоксипропиламино)пиримидин-5-ил]-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты путем отщепления BOC-группы с помощью безводного бромида цинка получили (3-бензилоксипропил)- {5-[(3RS,4RS)-3-(нафталин-2-илметокси)пиперидин-4-ил] пиримидин-2- ил} амин в виде коричневатого резинообразного вещества; МС: 483 (М+Н)+.
Пример 135.
Аналогично примеру 125(з) путем отщепления BOC-группы с помощью безводного бромида цинка получали следующие соединения:
1) из трет-бутилового эфира (3RS, 4RS)-4-(2-метилсульфанилпиримидин- 5-ил)-3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты [пример 129(б)] получили 2-метилсульфанил-5- [(3RS,4RS)-3-(нафталин-2-илметокси)пиперидин-4-ил] пиримидин в виде аморфного желтоватого твердого вещества; МС: 366 (М+Н)+;
2) из трет-бутилового эфира (3'RS, 4'RS)-6-(3-бензилоксипропил)- 3'-(нафталин-2-илметокси)-1-окси-3', 4',5',6'-тетрагидро-2'Н- [3,4']бипиридин-1'-карбоновой кислоты получили (3'RS, 4'RS)-6-(3- бензилоксипропил)-3'-(нафталин-2-илметокси)- 1',2',3',4',5',6'-гексагидро[3,4'] бипиридин-1-оксид в виде бесцветного масла; МС: 483 (М+Н)+;
3) из трет-бутилового эфира (3'RS,4'RS)-3'-(нафталин-2- илметокси)-6-(3-фенилпропил)-1-окси-3', 4', 5',6'-тетрагидро- 2'H-[3,4']бипиридин-1'-карбоновой кислоты получили (3'RS, 4'RS)-3'-(нафталин-2-илметокси)-6-(3-фенилпропил)-1', 2', 3', 4', 5', 6'-гексагидро[3,4'] бипиридин-1-оксид в виде аморфного желтоватого твердого вещества; МС: 453 (М+Н)+;
4) из трет-бутилового эфира (3RS,4RS)-3-(нaфтaлин-2-илмeтoкcи)- 4-[2-(4-фенилбутиламино)пиримидин-5-ил] пиперидин-1-карбоновой кислоты получили [5-[(3RS, 4RS)-3-(нaфтaлин-2-илмeтoкcи)пипepидин- 4-ил]пиримидин-2-ил]-(4-фенилбутил)амин в виде аморфного красноватого твердого вещества; МС: 467 (М+Н)+;
5) из трет-бутилового эфира (3RS,4RS)-4-{2-[метил (4-фенилбутил)амино] пиримидин-5-ил} -3-(нафталин-2-илметокси)пиперидин- 1-карбоновой кислоты получили метил{ 5-[(3RS, 4RS)-3-(нaфтaлин-2- илмeтoкси)пиперидин-4-ил]пиримидин-2-ил} -(4-фенилбутил)амин в виде аморфного бесцветного твердого вещества; МС: 481 (М+Н)+.
Использованные в качестве исходных субстанций BOC-производные получали следующим путем:
(б) 0,074 г (0,13 ммоля) трет-бутилового эфира (3'RS,4'RS)-6-(3-бензилоксипропил)-3'-(нафталин-2- илметокси)-3', 4', 5', 6'-тетрагидро-2'H-[3,4'] бипиридин-1'- карбоновой кислоты [пример 127(д)] растворяли в 1,5 мл метиленхлорида, смешивали с 0,046 г (около 0,19 ммоля) м-хлорпербензойной кислоты (примерно 70%-ной) и перемешивали при комнатной температуре в течение 30 мин. После этого реакционную смесь распределяли между метиленхлоридом и насыщенным содовым раствором, объединенные метиленхлоридные фазы сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате остаток хроматографировали на силикагеле с использованием метиленхлорида/метанола (95:5). Таким путем получили 0,032 г (42% от теории) трет-бутилового эфира (3'RS,4'RS)-6-(3-бензилоксипропил)-3'-(нафталин-2-илметокси)-1-окси- 3',4',5',6'-тетрагидро-2'H-[3,4'] бипиридин-1'-карбоновой кислоты в виде аморфного бесцветного твердого вещества; МС: 584 (М+Н)+.
(в) Аналогично примеру 135(б) из трет-бутилового эфира (3'RS, 4'RS)-3'-(нафталин-2-илметокси)-6-(3-фенилпропил)- 3',4',5',6'-тетрагидро-2'H-[3,4'] бипиридин-1'-карбоновой кислоты [пример 126(ж)] получили трет-бутиловый эфир (3'RS, 4'RS) -3'-(нафталин-2-илметокси)-6-(3-фенилпропил)-1-окси- 3',4',5', 6'-тетрагидро-2'H-[3,4'] бипиридин-1'-карбоновой кислоты в виде бесцветного масла; МС: 553 (М+Н)+.
(г) Аналогично примеру 135(б) из трет-бутилового эфира (3RS,4RS)-4-(2-метилсульфонилпиримидин-5-ил)-3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты и 4-фенилбутиламина получили трет-бутиловый эфир (3RS,4RS)-3-(нафталин-2-илметокси)-4-[2-(4- фенилбутиламино)пиримидин-5-ил] пиперидин-1-карбоновой кислоты в виде аморфного бесцветного твердого вещества; МС: 568 (М+Н)+.
(д) 0,058 г (0,10 ммоля) трет-бутилового эфира (3RS,4RS)-3- (нафталин-2-илметокси)-4-[2-(4-фенилбутиламино)пиримидин-5-ил] пиперидин-1-карбоновой кислоты растворяли в 1,0 мл N,N- диметилформамида, при 0oC смешивали сначала с 0,08 мл (1,3 ммоля) метилиодида, а затем с 0,010 г (около 0,2 ммоля) дисперсии гидрида натрия (примерно 50 %-ной в минеральном масле) и перемешивали в течение 90 мин при комнатной температуре в атмосфере аргона. После этого реакционный раствор распределяли между водой и простым эфиром, объединенные эфирные фазы сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате остаток хроматографировали на силикагеле с использованием гексана/этилового эфира уксусной кислоты (1:1). Таким путем получили 0,021 г (35% от теории) трет-бутилового эфира (3RS,4RS)-4-{2-[метил(4-фенилбутил)амино] пиримидин-5-ил} -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде аморфного бесцветного твердого вещества; МС: 582 (М+Н)+.
Пример 136.
(а) Раствор из 40 мг (0,080 ммоля) трет-бутилового эфира (3RS, 4RS)-4-(2-метилсульфонилпиримидин-5-ил)-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты [пример 129(в)] в 1,1 мл 2 M хлористого водорода в метаноле перемешивали в течение 5 ч при комнатной температуре. Далее реакционный раствор распределяли между насыщенным раствором карбоната натрия и метиленхлоридом, объединенные метиленхлоридные фазы сушили над сульфатом магния и концентрировали. Таким путем получили 33 мг (95% от теории) гидрохлорида 2-метилсульфонил-5- [(3RS, 4RS)-3-(нафталин-2-илметокси)пиперидин-4-ил] пиримидина в виде бесцветного твердого вещества; МС: 398 (М+Н)+.
(б) Взаимодействием гидрохлорида 2-метилсульфонил-5-[(3RS, 4RS)- 3-(нафталин-2-илметокси)пиперидин-4-ил] пиримидина со спиртами аналогично примеру 131(б), но с применением 2 эквивалентов гидрида натрия получали следующие соединения:
1) взаимодействием с (Е)-3-фенил-2-пропен-1-олом получили (Е)-5-[(3RS, 4RS)-3-(нафталин-2-илметокси)пиперидин-4-ил] -2-(3- фенилаллилокси)пиримидин в виде аморфного желтоватого твердого вещества; МС: 452 (М+Н)+;
2) взаимодействием с (Е)-2-метил-3-фенил-2-пропен-1-олом получили (Е)-2-(2-метил-3-фенилаллилокси)-5-[(3RS,4RS)-3-(нафталин-2- илметокси)пиперидин-4-ил] пиримидин в виде аморфного желтоватого твердого вещества; МС: 466 (М+Н)+.
Пример 137.
Взаимодействием трет-бутилового эфира (3RS,4RS)-4-(2-метилсульфонилпиримидин-5- ил)-3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты [пример 129(в)] со спиртами и фенолами аналогично примеру 131(б) с последующим отщеплением BOC-группы с помощью 2 M хлористого водорода в метаноле аналогично примеру 136(а) получали следующие соединения:
1) взаимодействием с 3-гидроксибифенилом получили 2-(бифенил-3- илокси)-5-[(3RS, 4RS)-3-(нафталин-2-илметокси)пиперидин-4-ил] пиримидин в виде аморфного бесцветного твердого вещества; МС: 488 (М+Н)+;
2) взаимодействием с 3-феноксибензиловым спиртом получили 5-[(3RS, 4RS)-3-(нафталин-2-илметокси)пиперидин-4-ил] -2-(3-феноксибензилокси)пиримидин в виде аморфного коричневатого твердого вещества; МС: 519 (М+Н)+;
3) взаимодействием с 4-феноксифенолом получили 5- [(3RS, 4RS)-3-(нафталин-2-илметокси)пиперидин-4-ил]-2-(3- феноксифенокси) пиримидин в виде аморфного коричневатого твердого вещества [МС: 504 (М+Н)+], а также 2-метокси-5-[(3RS, 4RS)-3- (нафталин-2-илметокси)пиперидин-4-ил] пиримидин в виде аморфного коричневатого резинообразного вещества; МС: 349 (М+Н)+;
4) взаимодействием с 4-гидроксибифенилом получили 2-(бифенил- 4-илокси)-5-[(3RS, 4RS)-3-(нафталин-2-илметокси)пиперидин-4-ил] пиримидин в виде аморфного бесцветного твердого вещества; МС: 488 (М+Н)+;
5) взаимодействием с 3-фенил-2-пропин-1-олом получили 5-[(3RS,4RS)-3-(нафталин-2-илметокси)пиперидин-4-ил]-2-(3- фенилпроп-2-инилокси)пиримидин в виде аморфного коричневатого твердого вещества; МС: 451 (М+Н)+;
6) взаимодействием с 2-гидроксиметил-2,3-дигидробензо[1,4] диоксином получили 2-(RS и SR)-(2,3-дигидробензо[1,4] диоксин-2-илметокси)-5-(3RS, 4RS)-3-(нафталин-2-илметокси)пиперидин-4-ил] пиримидин в виде бесцветного твердого вещества; МС: 484 (М+Н)+;
7) взаимодействием с 4-бифенилэтанолом [Chemische Berichte 85, 897 (1952)] получили 2-(2-бифенил-4-илэтокси)-5-[(ЗRS, 4RS)-3-(нaфтaлин-2- илметокси)пиперидин-4-ил] пиримидин в виде аморфного желтоватого резинообразного вещества; МС: 517 (М+Н)+;
8) взаимодействием с 4-феноксибензиловым спиртом получили 5-[(3RS, 4RS)-3-(нафталин-2-илметокси)пиперидин-4-ил] -1-(4-феноксибензил)-1Н-пиримидин-2-он в виде аморфного бесцветного твердого вещества; МС: 518 (М+Н)+;
9) взаимодействием с 4-бифенилметанолом получили 2-(бифенил-4- илметокси)-5-[(3RS,4RS)-3-(нафталин-2-илметокси)пиперидин-4-ил] пиримидин в виде желтоватого резинообразного вещества; МС: 503 (М+Н)+;
10) взаимодействием с [1-(4-хлорфенил)циклопентил] метанолом получили 2-[[1-(4-хлорфенил)циклопентил] метокси] -5- [(3RS,4RS)-3-(нафталин-2- илметокси)пиперидин-4-ил] пиримидин в виде бесцветного твердого вещества; МС: 528 (М+Н)+;
11) взаимодействием с 2-нафталинметанолом получили 2-(нафталин- 2-илметокси)-5-[(3RS, 4RS)-3-(нафталин-2-илметокси)пиперидин-4-ил] пиримидин в виде аморфного желтоватого твердого вещества; МС: 476 (М+Н)+;
12) взаимодействием с 2-нафталинэтанолом получили 2- (нафталин-2-илэтокси)-5-[(3RS,4RS)-3-(нафталин-2- илметокси)пиперидин-4-ил] пиримидин в виде аморфного коричневатого твердого вещества; МС: 490 (М+Н)+;
13) взаимодействием с 2-(4-бромфенил)этанолом получили 2-[2- (4-бромфенил)этокси]-5-[(3RS,4RS)-3-(нaфтaлин-2-илмeтoкcи)пипepидин-4-ил] пиримидин в виде аморфного коричневатого твердого вещества; МС: 518, 520 (М+Н)+;
14) взаимодействием с 2-(2-хлорфенокси)этанолом получили 2-[2-(2-хлорфенокси)этокси] -5- [(3RS, 4RS)-3-(нафталин-2-илметокси)пиперидин-4-ил]пиримидин в виде аморфного коричневатого твердого вещества; МС: 490 (М+Н)+;
15) взаимодействием с 2- бензилоксиэтанолом получили 2-(2-бензилоксиэтокси)-5-[(3RS, 4RS)-3-(нафталин-2-илметокси)пиперидин- 4-ил] пиримидин в виде аморфного желтоватого твердого вещества; МС: 470 (М+Н)+;
16) взаимодействием с 3-циклогексилпропанолом получили 2-(3- циклогексилпропокси)-5-[(3RS, 4RS)-3-(нафталин-2-илметокси)пиперидин-4-ил] пиримидин в виде аморфного коричневатого твердого вещества; МС: 461 (М+Н)+;
17) взаимодействием с 3-(6-метилпиридин-2-ил)пропанолом получили 2-[3-(6-метилпиридин-2-ил)пропокси]-5-[(3RS,4RS)-3-(нафталин-2-илметокси) пиперидин-4-ил]пиримидин в виде аморфного коричневатого твердого вещества; МС: 469 (М+Н)+;
18) взаимодействием с 2-циклогексилоксиэтанолом получили 2-(2-циклогексилоксиэтокси)-5-[(3RS, 4RS)-3-(нафталин-2- илметокси)пиперидин- 4-ил]пиримидин в виде аморфного желтоватого твердого вещества; МС: 462 (М+Н)+;
19) взаимодействием с 2-(фенилтио)этанолом получили 5-[(3RS,4RS)- 3-(нафталин-2-илметокси)пиперидин-4-ил]-2-(2-фенилсульфанилэтокси) пиримидин в виде аморфного желтоватого твердого вещества; МС: 472 (М+Н)+;
20) взаимодействием с 2-(5-метил-2-фенилоксазол-4-ил)этанолом (был приобретен у фирмы "Maybridge Chemical Company") получили 2-[2-(5- метил-2-фенилоксазол-4-ил)этокси]-5-[(3RS, 4RS)-3-(нафталин-2- илметокси)пиперидин-4-ил] пиримидин в виде аморфного коричневатого твердого вещества; МС: 522 (М+Н)+;
21) взаимодействием с 2-циклогексилэтанолом получили 2- (2-циклогексилэтокси)-5-[(3RS, 4RS)-3-(нафталин-2-илметокси) пиперидин-4-ил] пиримидин в виде аморфного бесцветного твердого вещества; МС: 447 (М+Н)+;
22) взаимодействием с (RS)-4-(2-гидроксиэтил)-5-метил-2-фенил-2,4- дигидропиразол-3-оном (был приобретен у фирмы "Maybridge Chemical Company") получили смесь (RS)- и (SR)-5-метил-4-[2-[5-[(3RS, 4RS)-3- (нафталин-2-илметокси)пиперидин-4-ил] пиримидин-2-илокси]этил]- 2-фенил-2,4-дигидропиразол-3-он в виде аморфного бесцветного твердого вещества; МС: 536 (М+Н)+.
Пример 138.
0,045 г (0,082 ммоля) трет-бутилового эфира (3'RS,4'RS)-3'- (нафталин-2-илметокси)-6-(3-фенилпропил)-1-окси-3', 4', 5', 6'-тетрагидро- 2'H-[3,4'] бипиридин-1'-карбоновой кислоты [пример 135(в)] растворяли в 1,5 мл N,N-диметилформамида, смешивали 0,10 мл (0,8 ммоля) ангидрида трифторуксусной кислоты и перемешивали в течение 2 ч при комнатной температуре. После этого реакционную смесь распределяли между метиленхлоридом и насыщенным раствором бикарбоната, объединенные метиленхлоридные фазы сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате остаток хроматографировали на силикагеле с использованием метиленхлорида/метанола (95:5). Таким путем получили 0,019 г (52% от теории) (3'RS, 4'RS)-3'-(нафталин-2-илметокси)-6-(3- фенилпропил)-1',2', 3', 4', 5',6'-гексагидро-[3,4']бипиридин- 4-ола в виде аморфного бесцветного твердого вещества; МС: 453 (М+Н)+.
Пример 139.
Взаимодействием трет-бутилового эфира (3RS,4RS)-3-(1,4-диметоксинафталин-2-илметокси)-4-(2- метилсульфонилпиримидин-5-ил)пиперидин-1-карбоновой кислоты со спиртами аналогично примеру 131(6) с последующим отщеплением BOC- группы с помощью безводного бромида цинка в метиленхлориде аналогично примеру 125(з) получали следующие соединения:
1) взаимодействием с 3-фенил-2-пропин-1-олом получили 5-[(3RS,4RS)-3-(1,4-диметоксинафталин-2-илметокси)пиперидин-4-ил] - 2-(3-фенилпроп-2-инилокси)пиримидин в виде аморфного желтоватого твердого вещества; МС: 510 (М+Н)+;
2) взаимодействием с 3-циклогексилпропанолом получили 2-(3-циклогексилпропокси)-5-[(3RS,4RS)-3-(1, 4-диметоксинафталин-2- илметокси)пиперидин-4-ил] -2-(3-фенилпроп-2-инилокси)пиримидин в виде аморфного коричневатого твердого вещества; МС: 521 (М+Н)+;
3) взаимодействием с 4-циклогексилбутанолом получили 2-(4-циклогексилбутокси)-5-[(3RS, 4RS)-3-[1,4-диметоксинафталин-2- илметокси)пиперидин-4-ил] пиримидин в виде аморфного желтоватого твердого вещества; МС: 535 (М+Н)+;
4) взаимодействием с 2-индан-2-илэтанолом [J. Am. Chem.Soc. 87, 1297 (1965)] получили 5-[(3RS, 4RS)-3-(1,4-димeтoкcинaфтaлин-2-илмeтoкси) пиперидин-4-ил] -2-(2-индан-2-илэтокси)пиримидин в виде аморфного желтоватого твердого вещества; МС: 540 (М+Н)+;
5) взаимодействием с 3-(2-метоксибензилокси)пропан-1-олом (полученным путем алкилирования пропиленгликоля в большом избытке 2-метоксибензилхлоридом с применением гидрида натрия в N,N-диметилформамиде) получили 5-[(3RS, 4RS)-3-(1, 4-димeтoкcинaфтaлин-2-илмeтoкси)пиперидин-4-ил] - 2- [3-(2-метоксибензилокси)пропокси]пиримидин в виде аморфного бесцветного твердого вещества; МС: 574 (М+Н)+;
6) взаимодействием с (Е)-4-фенилбут-3-ен-1-олом [пример 122((β))] получили 5-[(3RS,4RS)-3-(1,4-диметоксинафталин- 2-илметокси)пиперидин-4-ил]-2-[(Е)-4-фенилбут-3-енилокси] пиримидин в виде аморфного бесцветного твердого вещества; МС: 526 (М+Н)+;
7) взаимодействием с 2-(5-фенилпиридин-2-ил)этанолом [пример 139(β)] получили 5-[(3RS,4RS)-3-(1, 4-диметоксинафталин- 2-илметокси)пиперидин-4-ил]-2-[2-(5-фенилпиридин-3-ил)этокси] пиримидин в виде аморфного бесцветного твердого вещества; МС: 576 (М+Н)+;
8) взаимодействием с 5-фенил-4-пентин-1-олом получили 5-[(3RS,4RS)- 3-(1,4-диметоксинафталин-2-илметокси)пиперидин-4-ил]-2-(5-фенилпент-4- инилокси)пиримидин в виде аморфного оранжевого твердого вещества; МС: 537 (М+Н)+.
Взаимодействием трет-бутилового эфира (3RS,4RS)-3-(1,4- диметоксинафталин-2-илметокси)-4-(2-метилсульфонилпиримидин-5- ил)пиперидин-1-карбоновой кислоты с аминами аналогично примеру 133(б) с последующим отщеплением BOC-группы с помощью безводного бромида цинка в метиленхлориде аналогично примеру 125(з) получали следующие соединения:
9) взаимодействием с 4-фенилбутиламином получили {5-[(3RS,4RS)- 3-(1,4-диметоксинафталин-2-илметокси)пиперидин-4-ил] пиримидин-2-ил} -(4-фенилбутил)амии в виде аморфного оранжевого твердого вещества; МС: 527 (М+Н)+;
10) взаимодействием с 2-(5-фенилпиридин-2-ил)этиламином [пример 139(δ) ] получили {5-[(3RS,4RS)-3-(1,4-диметоксинафталин-2- илметокси)пиперидин-4-ил] пиримидин-2-ил}-[2-(5-фенилпиридин-2- ил)этил] амин в виде аморфного бесцветного твердого вещества; МС: 576 (М+Н)+;
11) взаимодействием с 3-метоксибензиламином получили {5-[(3RS,4RS)-3-(1,4-диметоксинафталин-2-илметокси)пиперидин- 4-ил]пиримидин-2-ил}-(3-метоксибензил)амин в виде аморфного бесцветного твердого вещества; МС: 514 (М)+;
12) взаимодействием с 4-метоксибензиламином получили {5-[(3RS,4RS)- 3-(1,4-диметоксинафталин-2-илметокси)пиперидин-4-ил] пиримидин-2- ил}- (4-метоксибензил)амин в виде аморфного желтоватого твердого вещества; МС: 514(М)+;
13) взаимодействием с 3-бромбензиламином получили (3-бромбензил)-{5-[(3RS, 4RS)-3-(1,4-диметоксинафталин -2-илметокси)пиперидин-4-ил]пиримидин-2-ил}амин в виде аморфного бесцветного твердого вещества; МС: 562,564 (М)+;
14) взаимодействием с 3-метилбензиламином получили {5-[(3RS,4RS)-3-(1,4-диметоксинафталин-2-илметокси)пиперидин-4 - ил]пиримидин-2-ил}-(3-метилбензил)амин в виде аморфного бесцветного твердого вещества; МС: 499 (М+Н)+;
15) взаимодействием с 4-бромбензиламином получили (4-бромбензил)- {5-[(3RS, 4RS)-3-(1,4-диметоксинафталин-2-илметокси)пиперидин-4-ил] пиримидин-2-ил} амин в виде аморфного бесцветного твердого вещества; МС: 563, 565 (М+Н)+.
Использованный в качестве исходного материала трет-бутиловый эфир (3RS, 4RS)-3-(1, 4-диметоксинафталин-2-илметокси)-4-(2-метилсульфонилпиримидин-5-ил)пиперидин-1-карбоновой кислоты получали следующим образом:
(а) Аналогично примеру 125(ж) из трет-бутилового эфира (3RS,4RS)-3-гидрокси-4-(2-метилсульфанилпиримидин-5-ил)пиперидин-1- карбоновой кислоты [пример 129(а)] и 2-хлорметил-1,4-диметоксинафталина [J.Amer.Chem.Soc. 64, 2657 (1942)] получили трет-бутиловый эфир (3RS,4RS)-3-(1,4-диметоксинафталин- 2-илметокси)-4-(2-метилсульфанилпиримидин-5-ил)пиперидин-1-карбоновой кислоты в виде аморфного бесцветного твердого вещества; МС: 527 (М+Н)+.
(б) Аналогично примеру 129(в) из трет-бутилового эфира (3RS,4RS)-3-(1,4-диметоксинафталин-2-илметокси)-4-(2- метилсульфанилпиримидин-5-ил)пиперидин-1-карбоновой кислоты путем окисления м-хлорпербензойной кислотой получили трет- бутиловый эфир (3RS,4RS)-3-(1,4-диметоксинафталин-2-илметокси)-4- (2-метилсульфонилпиримидин-5-ил)пиперидин-1-карбоновой кислоты в виде аморфного бесцветного твердого вещества; МС: 558 (М+Н)+.
Использованные в качестве агентов конденсации 2-(5- фенилпиридин-2-ил)этанол и 2-(5-фенилпиридин-2-ил)этиламин получали следующим образом.
(α) 1,16 г (4 ммоля) 2-(2-бензилоксиэтил)-5-бромпиридина [пример 128(б)] , 139 мг (1,13 ммоля) тетракис(трифенилфосфин) палладия и 537 мг (8,2 ммоля) фенилборной кислоты растворяли в небольшом количестве этанола и одной порцией добавляли к 80 мл толуола. После этого добавляли 1,87 г (17,6 ммоля) карбоната натрия в 4,4 мл воды и реакционную смесь в течение 7,5 ч нагревали в атмосфере аргона и с обратным холодильником. После охлаждения реакционный раствор концентрировали в вакууме, создаваемом водоструйным насосом, и распределяли между метиленхлоридом и водой. Объединенные метиленхлоридные фазы сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Затем полученный в результате остаток хроматографировали на силикагеле с использованием метиленхлорида/простого эфира (93:7). Таким путем получили 1,005 г (87% от теории) 2-(2-бензилоксиэтил)-5- фенилпиридина в виде бесцветного твердого вещества; Rf 0,08 (SiO2, метиленхлорид: простой эфир = 93:7).
(β) 1,0 г (3,5 ммоля) 2-(2-бензилоксиэтил)-5-фенилпиридина растворяли в 1 мл ледяной уксусной кислоты, смешивали с 1,8 мл (6,7 ммоля) бромистоводородной кислоты в ледяной уксусной кислоте (30%-ной) и реакционную смесь перемешивали в течение 18 ч при комнатной температуре. После этого добавляли ледяную воду, дважды экстрагировали гексаном, гексановые фазы отбрасывали, в водной фазе с помощью раствора карбоната натрия создавали щелочную среду и трижды экстрагировали простым эфиром. Объединенные эфирные фазы сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате 2-(5-фенилпиридин-2-ил)этиловый эфир уксусной кислоты затем растворяли в 12 мл ацетонитрила, смешивали с 5 мл воды и 4 мл 2 н. едкого натра и перемешивали в течение 2,5 ч при комнатной температуре. После этого добавляли водный раствор хлорида аммония и экстрагировали метиленхлоридом. Объединенные метиленхлоридные фазы сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате остаток далее хроматографировали на силикагеле с использованием метиленхлорида/простого эфира (1:1). Таким путем получили 0,656 г (94% от теории) 2-(5-фенилпиридин-2- ил)этанола в виде бесцветного твердого вещества; Rf 0,09 (SiO2, метиленхлорид: простой эфир = 1:1).
(γ) 0,473 г (2,4 ммоля) 2-(5-фенилпиридин-2-ил)этанола, 0,420 г (2,85 ммоля) фталимида и 0,747 г (2,85 ммоля) трифенилфосфина растворяли в 10 мл тетрагидрофурана и после этого реакционную смесь при -5oC в атмосфере аргона смешивали с 0,47 мл (3,0 ммоля) диэтилового эфира азодикарбоновой кислоты, перемешивали далее в течение 20 мин при -5oC, а затем в течение 18 ч при комнатной температуре. После этого реакционную смесь концентрировали в вакууме, создаваемом водоструйным насосом и остаток хроматографировали на силикагеле с использованием метиленхлорида/метанола (98:2). Таким путем получили 0,657 г (83% от теории) 2-[2-(5-фенилпиридин-2-ил)этил]изоиндол-1,3- диона в виде бесцветного твердого вещества; Rf = 0,38 (SiO2, гексан: этиловый эфир уксусной кислоты = 1:1).
(δ) 0,657 г (2,0 ммоля) 2-[2-(5-фенилпиридин-2- ил)этил]изоиндол-1,3-диона, 0,5 мл гидразингидрата и 5 мл этанола в течение 3,5 ч нагревали с обратным холодильником в атмосфере аргона. После этого разбавляли 5 мл этанола и 20 мл простого эфира, фильтровали и фильтрат концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате остаток в завершение хроматографировали на силикагеле с использованием метиленхлорида/метанола/конц. водного аммиака (89:10:1). Таким путем получили 0,250 г (63% от теории) 2-(5-фенилпиридин-2- ил)этиламина в виде желтоватого аморфного твердого вещества; Rf 0,17 (SiO2, метиленхлорид/метанол/конц. водный аммиак = 89:10:1).
Пример 140.
Взаимодействием трет-бутилового эфира (3'RS, 4'RS)-3'-(1,4-диметоксинафталин-2-илметокси)-6- метилсульфонил-3', 4', 5',6'-тетрагидро-2'H-[3,4'] бипиридин-1'-карбоновой кислоты со спиртами аналогично примеру 129 (г) с последующим отщеплением BOC-группы с помощью безводного бромида цинка в метиленхлориде аналогично примеру 125(з) получали следующие соединения:
1) взаимодействием с 3-циклогексилпропанолом получили (3'RS,4'RS)-6-(3-циклогексилпропокси)-3'-(1,4-диметоксинафталин-2- илметокси)-1',2',3',4', 5', 6'-гексагидро[3,4'] бипиридин в виде бесцветного твердого вещества; МС: 519 (М+Н)+;
2) взаимодействием с 3-(2-метоксибензилокси)пропан-1-олом (полученным путем алкилирования пропиленгликоля в большом избытке 2-метоксибензилхлоридом с применением гидрида натрия в N,N-диметилформамиде) получили (3'RS, 4'RS)-3'-(1,4-диметоксинафталин-2-илметокси)-6-[3- (2-метоксибензилокси)пропокси] -1', 2', 3',4',5',6'-гексагидро[3,4']бипиридин в виде аморфного бесцветного твердого вещества; МС: 573 (М+Н)+;
3) взаимодействием с 4-циклогексилбутанолом получили (3'RS,4'RS)-6-(4-циклогексилбутокси)-3'-(1, 4-диметоксинафталин-2- илметокси)-1',2',3',4',5', 6'-гексагидро[3,4'] бипиридин в виде аморфного бесцветного масла; МС: 533 (М+Н)+.
Использованный в качестве исходного материала трет-бутиловый эфир (3'RS, 4'RS)-3'-(1,4-диметоксинафталин-2-илметокси)-6-метилсульфонил- 3', 4', 5', 6'-тетрагидро-2'H-[3,4'] бипиридин-1'-карбоновой кислоты получали следующим образом.
(а) Аналогично примеру 127(б)-(в) из 2-метилсульфанил-5- бромпиридина [Tetrahedron 41, 1373 (1985)] через 2-метилсульфанил-5- триметилстаннанилпиридин [бесцветно масло, МС: 289 (М)+], а также трет-бутиловый эфир 4-трифторметилсульфонилокси-3,6 -дигидро-2Н-пиридин-1-карбоновой кислоты получили трет-бутиловый эфир 6-метилсульфанил-3',6'-дигидро-2'H-[3, 4']бипиридин-1'-карбоновой кислоты в виде желтоватого твердого вещества; МС: 307 (М+Н)+.
(б) 1,5 г (4,9 ммоля) трет-бутилового эфира 6-метилсульфанил-3',6'-дигидро-2'H-[3, 4'] бипиридин-1'-карбоновой кислоты растворяли в 15 мл 1,2-диметоксиэтана, при 3-4oC смешивали с 8,8 мл 1-молярного раствора борана в тетрагидрофуране и далее перемешивали в течение 4 ч при комнатной температуре. После этого при охлаждении льдом добавляли 15 мл воды, а затем порциями 3,5 г (22,3 ммоля) твердого перкарбоната натрия и реакционную смесь выдерживали в течение 1 ч при 50oC. Далее реакционный раствор распределяли между водой и метиленхлоридом, объединенные метиленхлоридные фазы промывали раствором пиросульфита натрия и водой, сушили над сульфатом магния, фильтровали и концентрировали. Полученный в результате остаток в завершение хроматографировали на силикагеле с использованием гексана/этилового эфира уксусной кислоты (1: 1). Таким путем получили 330 мг (21% от теории) трет-бутилового эфира (3'RS, 4'RS)-3'-гидрокси-6-метилсульфанил - 3',4',5',6'-тетрагидро-2'H-[3,4'] бипиридин-1'-карбоновой кислоты в виде бесцветного аморфного твердого вещества; МС: 324 (М)+.
(в) Аналогично примеру 125(ж) из трет-бутилового эфира (3'RS,4'RS)-3'-гидрокси-6-метилсульфанил-3', 4', 5',6'-тетрагидро-2'Н-[3,4'] бипиридин-1'-карбоновой кислоты путем алкилирования 2-хлорметил-1,4-диметоксинафталином [J. Amer. Chem. Soc. 64, 2657 (1942)] получили трет-бутиловый эфир (3'RS, 4'RS)-3'-(1, 4-диметоксинафталин-2-илметокси)-6- метилсульфанил-3', 4', 5', 6'-тетрагидро-2'H-[3,4'] бипиридин- 1'-карбоновой кислоты в виде бесцветного твердого вещества; МС: 526 (М+Н)+.
(г) Аналогично примеру 129(в) из трет-бутилового эфира (3'RS,4'RS)-3'-(1,4-диметоксинафталин-2-илметокси)-6- метилсульфанил-3', 4', 5', 6'-тетрагидро-2'H-[3,4'] бипиридин- 1'-карбоновой кислоты путем окисления м-хлорпербензойной кислотой получили трет-бутиловый эфир (3'RS,4'RS)-3'-(1,4 - диметоксинафталин-2-илметокси)-6-метилсульфонил-3', 4', 5', 6'-тетрагидро-2'Н-[3,4'] бипиридин-1'-карбоновой кислоты в виде аморфного бесцветного твердого вещества; МС: 557 (М+Н)+.
Пример 141.
(а) 50,0 г (0,6 моля) 1,2,5, 6-тетрагидропиридина и 135,3 г (0,6 моля) ди-трет-бутилдикарбората в течение 3 ч перемешивали при комнатной температуре с добавкой 166,0 г (1,2 моля) карбоната калия (безводного) в 1250 мл воды (деионизованной)/диоксана. Смесь сливали на ледяную воду, продукт трижды экстрагировали уксусным эфиром порциями по 300 мл, органические фазы дважды промывали дистиллированной водой порциями по 500 мл, затем сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием гексана и уксусного эфира. После сушки в высоком вакууме в течение 3 ч при комнатной температуре получили 109,4 г (99% от теории) трет-бутилового эфира 3,6- дигидро-2Н-пиридин-1-карбоновой кислоты в виде светло-желтого масла; МС: 183 (М)+.
(б) 127,0 г (0,6 моля) м-хлорпербензойной кислоты растворяли в атмосфере аргона в 1,5 л метиленхлорида, затем при 5oC в течение 1 ч по каплам добавляли раствор из 108 г (0,59 моля) трет-бутилового эфира 3,6-дигидро-2H-пиридин-1- карбоновой кислоты в 500 мл метиленхлорида и после этого перемешивали при комнатной температуре в течение ночи. Смесь сливали на ледяную воду, с помощью раствора карбоната калия значение pH устанавливали более 8 и после разделения фаз дважды экстрагировали метиленхлоридом порциями по 500 мл; органические фазы дважды промывали водой до получения нейтральной среды, затем сушили над сульфатом магния, фильтровали и растворитель отгоняли в вакууме, создаваемом водоструйным насосом. Сырой продукт хроматографировали на силикагеле с использованием гексана и уксусного эфира. Таким путем получили 86,64 г (74% от теории) трет-бутилового эфира (1RS,6RS)-7-окса-3-азабицикло[4,1,0] гептан- 3-карбоновой кислоты в виде светло-желтого масла; МС: 199 (М)+.
(в) 19,9 г (100 ммолей) трет-бутилового эфира (1RS,6SR)-7-окca-3- азабицикло[4,1, 0]гептан-3-карбоновой кислоты и 32,5 г (500 ммолей) азида натрия в течение 3 ч перемешивали при нагревании с обратным холодильником с добавкой 39,1 г (250 ммолей) дигидрата сульфата магния в 500 мл абс. метанола. После этого смесь охлаждали до 10oC, фильтровали и растворитель отгоняли в вакууме, создаваемом водоструйным насосом. Остаток растворяли в 300 мл метиленхлорида, снова фильтровали и отгоняли растворитель в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием н-гексана и уксусного эфира. Таким путем получили 15,86 г (66% от теории) трет-бутилового эфира (3RS,4RS)-4-азидо-3-гидроксипиперидин-1- карбоновой кислоты в виде бесцветных кристаллов; МС: 242 (М)+.
(г) 15,4 г (63,5 ммоля) трет-бутилового эфира (3RS,4RS)-4-азидо-3-гидроксипиперидин-1-карбоновой кислоты и 15,5 г (69,9 ммоля) 2-бромметилнафталина предварительно загружали в атмосфере аргона при 5oC в 200 мл диметилформамида. После этого при внешнем охлаждении одной порцией добавляли 3,33 г (76,2 ммоля) дисперсии гидрида натрия (55%-ной в минеральном масле), а затем перемешивали в течение ночи при комнатной температуре. Смесь сливали на ледяную воду, продукт трижды экстрагировали уксусным эфиром порциями по 200 мл, органические фазы дважды промывали водой порциями по 300 мл, затем сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием н-гексана и уксусного эфира. Таким путем получили 23,18 г (95% от теории) трет-бутилового эфира (3RS,4RS)-4-азидо-3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде светло-желтого масла; МС: 383 (М+Н)+.
(д) 3,20 г (8,37 ммоля) трет-бутилового эфира (3RS,4RS)-4-азидо-3-(нафталин- 2-илметокси)пиперидин-1-карбоновой кислоты и 9,87 мл (176,3 ммоля) пропаргилового спирта в течение 5 ч перемешивали при нагревании с обратным холодильником в 80 мл толуола. После отгонки растворителя в вакууме, создаваемом водоструйным насосом, сырой продукт хроматографировали на силикагеле с использованием метиленхлорида и метанола. Таким путем получили 1,47 г (40% от теории) трет- бутилового эфира (3RS,4RS)-4-(4-гидроксиметил-[1,2,3] триазол-1- ил)-3-(нафталин-2-илметокси)-4-пиперидин-1-карбоновой кислоты в виде бесцветных кристаллов [МС: 439 (М+Н)+] и 0,81 г (22% от теории) трет-бутилового эфира (3RS, 4RS)-4-(5-гидроксиметил[1,2,3]триазол-1-ил)-3-(нафталин-2-илметокси)-4-пиперидин-1- карбоновой кислоты в виде бесцветных кристаллов; МС: 439 (М+Н)+.
(е) 0,22 г (0,5 ммоля) трет-бутилового эфира (3RS,4RS)-4-(4- гидроксиметил-[1,2,3] триазол-1-ил)-3-(нафталин-2-илметокси)-4- пиперидин-1-карбоновой кислоты и 0,064 мл (0,5 ммоля) о-хлорбензоилхлорида предварительно загружали в атмосфере аргона при комнатной температуре в 10 мл метиленхлорида. После этого сначала при перемешивании добавляли 0,41 мл (3 ммоля) триэтиламина, а затем 0,025 г (0,2 ммоля) 4-диметиламинопиридина и перемешивали в течение 18 ч при комнатной температуре. После отгонки растворителя в вакууме, создаваемом водоструйным насосом, сырой продукт хроматографировали на силикагеле с использованием метиленхлорида и метанола. Таким путем получили 0,14 г (49% от теории) трет-бутилового эфира (3RS, 4RS)-4-[4-(2- хлорбензоилоксиметил)[1,2, 3]триазол-1-ил]-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты в виде бесцветной смолы; МС: 577 (М+Н)+.
(ж) Аналогично примеру 136(а) из трет-бутилового эфира (3RS,4RS)-4-[4-(2-хлорбензоилоксиметил)[1,2,3] триазол-1-ил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты путем отщепления BOC-группы с помощью хлористого водорода в метаноле получили гидрохлорид 1-[(3RS, 4RS)-3-(нафталин-2- илметокси)пиперидин-4-ил] -1H-[1,2,3] триазол-4-илметилового эфира 2-хлорбензойной кислоты (1:1) в виде бесцветных кристаллов; МС: 477 (М+Н)+.
Пример 142.
Аналогично примеру 136(а) путем отщепления BOC-группы с помощью хлористого водорода в метаноле получали следующие соединения:
1) из трет-бутилового эфира (3RS,4RS)-4-(5-бензилоксиметил[1,2,3]триазол-1-ил)-3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты получили (3RS,4RS)-4-(5- бензилоксиметил[1,2, 3]триазол-1-ил)-3-(нафталин-2- илметокси)пиперидин в виде светло-желтого масла; МС: 429 (М+Н)+;
2) из трет-бутилового эфира (3RS,4RS)-4-(4-бензилоксиметил [1,2, 3]триазол-1-ил)-3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты получили гидрохлорид (3RS, 4RS)-4-(4- бензилоксиметил[1,2,3] триазол-1-ил)-3-(нафталин-2- илметокси)пиперидина (1: 1) в виде бесцветных кристаллов; МС: 429 (М+Н)+;
3) из трет-бутилового эфира (3RS,4RS)-4-[5-(3- бензилоксипропоксиметил)[1,2,3] триазол-1-ил] -3-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-[5-(3-бензилоксипропоксиметил)-[1,2,3] триазол-1-ил] -3- (нафталин-2-илметокси)пиперидин в виде бесцветного масла; МС: 487 (М+Н)+;
4) из трет-бутилового эфира (3RS, 4RS)-4-[4-(3-бензилоксипропоксиметил)[1,2,3] триазол-1-ил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты получили (3RS,4RS)-4-[4-(3-бензилоксипропоксиметил)[1,2,3]триазол-1-ил] -3-(нафталин-2-илметокси)пиперидин в виде бесцветного масла; МС: 487 (М+Н)+.
Использованные в качестве исходных субстанций BOC-производные получали следующим образом.
(а) 0,22 г (0,5 ммоля) трет-бутилового эфира (3RS,4RS)-4-(5- гидроксиметил[1,2, 3]триазол-1-ил)-3-(нафталин-2-илметокси)-4- пиперидин-1-карбоновой кислоты [пример 141(д)] и 0,09 мл (0,75 ммоля) бензилбромида при 5oC предварительно загружали в атмосфере аргона в 5 мл диметилформамида, затем одной порцией добавляли 0,044 г (1 ммоль) дисперсии гидрида натрия (55%-ной в минеральном масле) и перемешивали в течение 18 ч при комнатной температуре. После этого смесь сливали на ледяную воду, продукт трижды экстрагировали уксусным эфиром порциями по 30 мл, органические фазы дважды промывали дистиллированной водой порциями по 25 мл, сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием метиленхлорида и метанола. Таким путем получили 0,24 г (91% от теории) трет-бутилового эфира (3RS, 4RS)-4-(5-бензилоксиметил[1,2,3]триазол-1-ил)-3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты в виде светло-желтого масла; МС: 529 (М+Н)+.
(б) Аналогично примеру 142(а) из трет-бутилового эфира (3RS,4RS)- 4-(4-гидроксиметил[1,2,3] триазол-1-ил)-3-(нафталин-2- илметокси)-4-пиперидин-1-карбоновой кислоты [пример 141(д)] получили трет-бутиловый эфир (3RS, 4RS)-4-(4-бензилоксиметил[1,2,3] триазол-1-ил)-3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты в виде желтого масла; МС: 529 (М+Н)+.
(в) 0,22 г (0,5 ммоля) трет-бутилового эфира (3RS,4RS)-4-(5-гидроксиметил[1,2,3]триазол-1-ил)-3-(нафталин- 2-илметокси)-4-пиперидин-1-карбоновой кислоты [пример 141(д)] и 0,13 мл (0,75 ммоля) 3-бензилоксипропилбромида при 5oC предварительно загружали в атмосфере аргона в 5 мл диметилформамида, после чего одной порцией добавляли сначала 0,17 г (1 ммоль) иодида калия, а затем 0,044 г (1 ммоль) дисперсии гидрида натрия (55%-ной в минеральном масле) и далее перемешивали в течение 72 ч при комнатной температуре. После этого смесь сливали на ледяную воду, продукт трижды экстрагировали уксусным эфиром порциями по 30 мл, органические фазы дважды промывали дистиллированной водой порциями по 25 мл, сушили над сульфатом магния, фильтровали и концентрировали в вакууме, создаваемом водоструйным насосом. Полученный в результате сырой продукт хроматографировали на силикагеле с использованием метиленхлорида и метанола. Таким путем получили 0, 27 г (92% от теории) трет- бутилового эфира (3RS,4RS)-4-[5-(3-бензилоксипропоксиметил)[1,2,3]триазол-1-ил] -3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты в виде светло-желтого масла; МС: 586 (М)+.
(г) Аналогично примеру 142(в) из трет-бутилового эфира (3RS,4RS)-4-(4-гидроксиметил[1,2,3] триазол-1-ил)-3-(нафталин-2- илметокси)-4-пиперидин-1-карбоновой кислоты [пример 141(д)] получили трет-бутиловый эфир (3RS,4RS)-4-[4-(3-бензилоксипропоксиметил)[1,2,3] триазол-1-ил] -3-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты в виде светло-желтого масла; МС: 586 (М+Н)+.
Пример 143.
Аналогично примеру 136(а) путем отщепления BOC-группы с помощью хлористого водорода в метаноле получали следующие соединения:
1) из трет-бутилового эфира (3'RS,4'RS)-3'- (нафталин-2-илметокси)-3', 4', 5', 6'-тетрагидро-2'Н-[2,4'] бипиридин- 1-карбоновой кислоты получили (3'RS, 4'RS)-3'- (нафталин-2-илметокси)-1',2',3',4',5',6'-гексагидро- [2,4'] бипиридин в виде светло-желтого масла; МС: 319 (М+Н)+;
2) из трет-бутилового эфира (3'RS, 4'RS)-3'-(нафталин-2-илметокси)- 3', 4',5',6'-тетрагидро-2'Н-[3,4']бипиридин-1-карбоновой кислоты получили (3'RS, 4'RS)-3'-(нафталин-2-илметокси)-1',2',3',4',5',6'-гексагидро-[3,4']бипиридин в виде желтого масла; МС: 319 (М+Н)+.
Использованные в качестве исходных субстанций BOC-производные получали следующим образом.
(а)(α) Раствор из 662 мг (2,0 ммоля) трет-бутилового эфира 4-трифторметилсульфонилокси-3,6-дигидро-2H-пиридин-1- карбоновой кислоты [пример 126(в)], 884 мг (2,4 ммоля) (был приобретен у фирмы "Maybridge Chemical Company") и 254 мг (6,0 ммолей) безводного хлорида лития в 30 мл абсолютного ДМФ продували аргоном, после этого смешивали с тетракис(трифенилфосфин)палладием(IV) и затем в течение 3 ч перемешивали в атмосфере аргона при нагревании с обратным холодильником. Для дальнейшей переработки реакционную смесь сливали в 25 мл 10%-ного раствора аммиака и затем интенсивно перемешивали в течение 5 мин. Светло-желтый раствор смешивали с 100 мл метиленхлорида, после чего перемешивали в течение 5 мин. Органическую фазу отделяли, а водную фазу трижды промывали метиленхлоридом порциями по 25 мл. Объединенные органические фазы дважды промывали водой порциями по 25 мл, сушили над сульфатом магния и в завершение отгоняли растворитель при пониженном давлении. Сырой продукт очищали хроматографией быстрого разрешения на силикагеле с использованием смеси 2:1 гексана и уксусного эфира в качестве элюента. Таким путем получили 354 мг (68% от теории) трет-бутилового эфира 3', 6'-дигидро-2'H-[2, 4']бипиридин-1'- карбоновой кислоты в виде желтого масла; МС: 261 (М+Н)+.
(β) Раствор из 1,30 г (5,0 ммолей) трет-бутилового эфира 3',6'-дигидро-2'H-[2,4'] бипиридин-1'-карбоновой кислоты в 15 мл абсолютного тетрагидрофурана при 0oC в атмосфере аргона смешивали, добавляя по каплям, с 1,0 мл (801 мг, 10,0 ммолей) боран-диметилсульфидного комплекса (95%-ного) в диметилсульфиде. Смесь нагревали до кипения таким образом, что происходила медленная отгонка растворителя (примерно 1 капля в минуту). По истечении 3 ч при 0oC по каплям добавляли 3 мл 2 н. раствора гидроксида натрия и 2 мл раствора перекиси водорода (30%-ной). Смесь перемешивали в течение 6 ч при 50oC, затем охлаждали до комнатной температуры и для дальнейшей переработки при интенсивном перемешивании сливали на смесь из 200 мл простого эфира, 200 мл воды и 25 мл раствора пиросульфита натрия (10%-ного). Органическую фазу отделяли, а водную фазу трижды экстрагировали простым эфиром порциями по 50 мл. Объединенные органические фазы дважды промывали водой порциями по 25 мл, сушили над сульфатом магния и в завершение отгоняли растворитель при пониженном давлении. Сырой продукт очищали хроматографией быстрого разрешения на силикагеле с использованием смеси 1:1 гексана и уксусного эфира в качестве элюента. Таким путем получили 354 мг (24% от теории) трет-бутилового эфира (3'RS, 4'RS)-3'-гидрокси- 3', 4', 5',6'-тетрагидро-2'H-[2,4']бипиридин-1'-карбоновой кислоты в виде желтого масла; МС: 279 (М+Н)+.
(γ) Аналогично примеру 125(ж) путем алкилирования трет-бутилового эфира (3'RS, 4'RS)-3'-гидрокси-3', 4', 5', 6'-тетрагидро-2'H- [2,4']бипиридин-1'-карбоновой кислоты 2-бромметилнафталином получили трет-бутиловый эфир (3'RS, 4'RS)-3'-(нафталин-2- илметокси)-3', 4', 5',6'-тетрагидро-2'H-[2,4']бипиридин-1- карбоновой кислоты в виде бесцветной смолы; МС: 419 (М+Н)+.
(б) (α) Раствор из 16,7 г (106 ммоля) 3-бромпиридина в 200 мл трет-бутилметилового эфира охлаждали до -75oC. К этому раствору в течение 45 мин по каплям добавляли раствор из 66 мл (106 ммолей) н-бутиллития (1,6 М в гексане) и затем перемешивали при -75oC в течение 1 ч. Далее при температуре в интервале от -70 до -75oC по каплям добавляли раствор из 10,0 г (52,8 ммоля) 1- бензил-4-пиперидона в 50 мл трет-бутилметилового эфира, а затем перемешивали в течение 2 ч. Затем смеси давали нагреться до комнатной температуры. После этого гидролизовали 50 мл воды и экстрагировали 100 мл уксусного эфира. Органическую фазу сушили над сульфатом магния и в завершение концентрировали выпариванием растворителя при пониженном давлении, при этом продукт начинал выпадать в осадок. Из упаренного маточного раствора путем кристаллизации из смеси уксусного эфира и гексана выделяли дополнительные 1,9 г, получив в общей сложности 8,4 г (60% от теории) 1'-бензил-2',3',5',6'-тетрагидро-1'H-[3,4'] бипиридин-4'-ола в виде бесцветного твердого вещества; МС: 268 (М+Н)+.
(β) Дисперсию из 4,52 г (16,8 ммоля) 1'-бензил-2', 3',5',6'- тетрагидро-1'H-[3,4'] бипиридин-4'-ола и 18 г (71 ммоль) дисульфата калия в 35 мл декалина перемешивали в течение 30 мин при 190oC. После охлаждения до комнатной температуры реакционную смесь растворяли в воде и дважды экстрагировали толуолом порциями по 50 мл. Далее в водной фазе с помощью едкого натра создавали щелочную среду и экстрагировали уксусным эфиром. Уксусноэфирную фазу затем сушили над сульфатом натрия и упаривали при пониженном давлении. Сырой продукт очищали хроматографией на силикагеле с использованием смеси 98:2:0,1 метиленхлорида, метанола и аммиака в качестве элюента. Таким путем получили 4,03 г (61% от теории) 1'-бензил-1',2',3',6'- тетрагидро-3,4'-бипиридина в виде желтоватого масла; МС: 250 (М)+.
(γ ) Аналогично примеру 126(е) путем гидроборирования 1'-бензил-1',2',3', 6'-тетрагидро-3,4'-бипиридина получили (3'RS,4'RS)-1'-бензил-1',2',3',4',5', 6'-гексагидро[3,4']бипиридинил-3'-ол в виде желтоватого масла; МС: 268 (М)+. Последующим отщеплением бензильной группы с помощью каталитического гидрирования в присутствии палладия на угле (10%-ного) при комнатной температуре и при нормальном давлении в метаноле в течение 18 ч получили (3'RS,4'RS)- 1', 2', 3', 4', 5', 6'-гексагидро[3,4'] бипиридинил-3'-ол, из которого после взаимодействия с ди-трет-бутилдикарбонатом аналогично примеру 141(а) получили трет-бутиловый эфир (3'RS,4'RS)-3'-гидрокси-3',4',5',6'-тетрагидро-2'H- [3,4'] бипиридинил-1'-карбоновой кислоты в виде желтоватого масла; МС: 279 (М+Н)+. Путем последующего алкилирования 2-бромметилнафталином аналогично примеру 125(ж) получили трет-бутиловый эфир (3'RS,4'RS)-3'-(нафталин-2-илметокси)-3', 4', 5', 6'-тетрагидро-2'H-[3,4']бипиридин-1-карбоновой кислоты, который в неочищенном виде использовали в реакции отщепления BOC-группы с помощью хлористого водорода в метаноле.
Пример 144.
Путем отщепления BOC-группы получали следующие соединения:
1) из трет-бутилового эфира (3'RS,4'RS)-6-(3- бензилоксипропокси)-3'-(нафталин-2-илметокси)-3', 4', 5',6'- тетрагидро-2'H-[3,4']бипиридир-1'-карбоновой кислоты с помощью бромида цинка в метиленхлориде аналогично примеру 125(з) получили (3'RS,4'RS)-6-(3-бензилоксипропокси)-3'-(нафталин-2- илметокси)-1',2',3',4',5',6'-гексагидро[3,4']бипиридин в виде бесцветного твердого вещества; МС: 483 (М+Н)+;
2) из трет-бутилового эфира (3'RS,4'RS)-5-(2-бензилоксиэтоксиметил)- 3'-(нафталин-2-илметокси)-3',4',5',6'-тетрагидро-2'H-[2, 4']бипиридин-1'- карбоновой кислоты с помощью хлористого водорода в метаноле аналогично примеру 136(а) получили (3'RS, 4'RS)-5-(2- бензилоксиэтоксиметил)-3'-(нафталин-2-илметокси)- 1',2',3',4',5', 6'-гексагидро[2,4']бипиридин в виде светло- желтого масла; МС: 483 (М+Н)+.
Использованные в качестве исходных веществ BOC-производные получали следующим образом.
(а)(α) Раствор из 10,62 г (40,2 ммоля) 2-бензил-5-бромпиридина [J.Org. Chem. 60, 1408 (1995)] и 10,0 мл (15,8 г, 48,2 ммоля) гексаметилдистаннана в 100 мл абсолютного диоксана продували аргоном и смешивали с 2,32 г (2,0 ммоля) тетракис(трифенилфосфин)палладия(IV). Смесь в течение 15 ч кипятили с обратным холодильником. Темный раствор для дальнейшей переработки фильтровали через Speedex и растворитель отгоняли при пониженном давлении. Остаток растворяли в 300 мл метиленхлорида, дважды промывали водой порциями по 100 мл, сушили над сульфатом магния и в завершение отгоняли растворитель при пониженном давлении. Сырой продукт очищали хроматографией быстрого разрешения на силикагеле с использованием смеси 3:1 гексана и метиленхлорида в качестве элюента. Таким путем получили 10,4 г (74% от теории) 2- бензилокси-5-триметилстаннилпиридина в виде бесцветного масла; МС: 349 (М+Н)+.
(β) Аналогично описанной выше методике путем катализируемой палладием реакции сочетания 2-бензилокси-5- триметилстаннилпиридина с трет-бутиловым эфиром 4-трифторметилсульфонилокси-3,6-дигидро-2Н-пиридин-1-карбоновой кислоты [пример 126(в)] получили трет-бутиловый эфир 6- бензилокси-3',6'-дигидро-2H-[3,4']бипиридин-1'-карбоновой кислоты в виде бесцветного твердого вещества; МС: 367 (М+Н)+.
(γ) Раствор из 0,75 г (2,04 ммоля) трет-бутилового эфира 6-бензилокси-3', 6'-дигидро-2H-[3,4'] бипиридин-1'-карбоновой кислоты в 3 мл абсолютного тетрагидрофурана при 0oC в атмосфере аргона смешивали, добавляя по каплям, с 0,42 мл (4,20 ммоля) боран-диметилсульфидного комплекса (95%-ного) в диметилсульфиде. Смесь нагревали до 60oC, одновременно пропуская слабый поток аргона. По истечении 1,5 ч при 0oC по каплям добавляли 3 мл тетрагидрофурана и 2 мл воды. Далее порциями добавляли 740 мг (4,71 ммоля) перкарбоната натрия, смесь нагревали до комнатной температуры и затем выдерживали в течение 1 ч при 60oC. После этого охлаждали до комнатной температуры и для дальнейшей переработки при интенсивном перемешивании сливали на смесь из 100 мл простого эфира, 100 мл воды и 10 мл 10%-ного раствора пиросульфита натрия. Органическую фазу отделяли, а водную фазу трижды экстрагировали простым эфиром порциями по 25 мл. Объединенные органические фазы дважды промывали водой порциями по 10 мл, сушили над сульфатом магния и в завершение отгоняли растворитель при пониженном давлении. Сырой продукт (0,9 г) очищали хроматографией быстрого разрешения на силикагеле с использованием смеси 4:1 метиленхлорида и уксусного эфира в качестве элюента. Таким путем получили 0,630 г (80% от теории) смеси 4:1 трет-бутилового эфира (3'RS,4'RS)-6-бензилокси-3'- гидрокси-3', 4', 5',6'-тетрагидро-2'H-[3,4']бипиридин-1'- карбоновой кислоты и трет-бутилового эфира 6-бензилокси-4'- гидрокси-3',4',5', 6'-тетрагидро-2'H-[3,4'] бипиридин-1'- карбоновой кислоты в виде бесцветного твердого вещества; МС: 385 (М+Н)+.
(δ) Раствор из 256 мг (0,67 ммоля) смеси 4:1 трет- бутилового эфира (3'RS, 4'RS)-6-бензилокси-3'-гидрокси- 3',4',5', 6'-тетрагидро-2'H-[3,4']бипиридин-1'-карбоновой кислоты и трет-бутилового эфира 6-бензилокси-4'-гидрокси- 3',4',5',6'-тетрагидро-2'H-[3,4']бипиридин-1'-карбоновой кислоты в 6 мл абсолютного метанола смешивали с 40 мг палладия на угле (10%-ного) и гидрировали в течение 6 ч при нормальном давлении. После отфильтровывания катализатора и последующей отгонки растворителя при пониженном давлении получили смесь 4:1 трет-бутилового эфира (3'RS,4'RS)-3'-гидрокси-6-оксо-1,6,3', 4',5',6'-гексагидро-2'H-[3,4'] бипиридин-1'-карбоновой кислоты и трет-бутилового эфира 4'-гидрокси-6- оксо-1,6,3',4',5', 6'-гексагидро-2'H-[3,4']бипиридин-1'-карбоновой кислоты в виде бесцветного твердого вещества; МС: 295 (М+Н)+.
(ε) Раствор из 74 мг (0,25 ммоля) смеси 4:1 трет- бутилового эфира (3'RS, 4'RS)-3'-гидрокси-6-оксо- 1,6,3',4',5',6'-гексагидро-2'H-[3,4']бипиридин-1'- карбоновой кислоты и трет-бутилового эфира 4'-гидрокси-6-оксо- 1,6,3',4',5', 6'-гексагидро-2'Н-[3,4']бипиридин-1'- карбоновой кислоты, 99 мг (0,375 ммоля) трифенилфосфина и 52 мг (0,312 ммоля) 3-бензилокси-1-пропанола в 5 мл абсолютного тетрагидрофурана смешивали, добавляя порциями, с 69 мг (0,30 ммоля) ди-трет- бутилового эфира азодикарбоновой кислоты и перемешивали в течение 6 ч при комнатной температуре. Далее реакционную смесь смешивали с 0,25 мл метанола и для дальнейшей переработки при интенсивном перемешивании сливали в 10 мл метиленхлорида и 10 мл воды. Органическую фазу отделяли, а водную фазу трижды экстрагировали метиленхлоридом порциями по 10 мл. Объединенные органические фазы дважды промывали водой порциями по 10 мл, сушили над сульфатом магния и в завершение отгоняли растворитель при пониженном давлении. Сырой продукт (280 мг) очищали хроматографией быстрого разрешения на силикагеле с использованием смеси 4:1 метиленхлорида и уксусного эфира в качестве элюента. Таким путем получили 37 мг (34% от теории) смеси 4: 1 трет-бутилового эфира (3'RS,4'RS)-6- (3-бензилоксипропокси)-3'-гидрокси-3',4',5',6'-тетрагидро- 2'H- [3,4']бипиридин-1'-карбоновой кислоты и трет-бутилового эфира 6-(3-бензилоксипропокси)-4'-гидрокси-3',4',5', 6'- тетрагидро-2'H-[3,4']бипиридин-1'-карбоновой кислоты в виде бесцветного масла; МС: 443 (М+Н)+ .
(ζ) Аналогично примеру 125(ж) путем алкилирования смеси 4:1 трет-бутилового эфира (3'RS,4'RS)-6-(3-бензилоксипропокси)-3'- гидрокси-3',4',5',6'-тетрагидро-2'H-[3,4'] бипиридин-1'- карбоновой кислоты и трет-бутилового эфира 6-(3-бензилоксипропокси) -4'-гидрокси-3', 4',5',6'-тетрагидро-2'H-[3,4']бипиридин-1'-карбоновой кислоты 2-бромметилнафталином и последующего разделения изомеров получили трет-бутиловый эфир (3'RS, 4'RS)-6-(3-бензилоксипропокси)-3'- (нафталин-2-илметокси)-3', 4',5',6'-тетрагидро-2'H-[3,4']бипиридин-1'- карбоновой кислоты в виде бесцветного масла; МС: 583 (М+Н)+.
(б)(α) Сначала при 0oC получали раствор из 54 мл (86 ммолей) метиллития (1,6 М в эфире) в 100 мл абсолютного тетрагидрофурана. После этого при 0oC в течение 30 мин по каплям добавляли раствор из 20 мл (96,8 ммоля) гексаметилдистаннана в 100 мл абсолютного тетрагидрофурана, а затем перемешивали в течение 30 мин при 0oC. Светло-желтый раствор охлаждали
до -78oC. К этому раствору при -78oC в течение 45 мин по каплям добавляли раствор из 14,2 г (71,3 ммоля) N-трет- бутоксикарбонил-4-пиперидона в 80 мл абсолютного тетрагидрофурана. По истечении 4 ч выдержки при -78oC по каплям добавляли 60 мл насыщенного раствора калий-натрийтартрата и смесь нагревали до комнатной температуры. Органическую фазу отделяли, а водную фазу трижды экстрагировали простым эфиром порциями по 200 мл. Объединенные органические фазы дважды промывали насыщенным раствором хлорида аммония порциями по 100 мл и дважды насыщенным раствором поваренной соли порциями по 100 мл, сушили над сульфатом магния и в завершение отгоняли растворитель при пониженном давлении. Полученное желтое масло (23,1 г) растворяли в 250 мл метиленхлорида, смешивали с 25,6 мл (183,9 ммоля) триэтиламина и охлаждали до 0oC. После этого в течение 1 ч при 0oC по каплям добавляли раствор из 9,82 мл (18,4 ммоля) метансульфохлорида в 90 мл метиленхлорида и затем перемешивали в течение 1 ч. После этого при 0oC в течение 30 мин по каплям добавляли 28,3 мл (190,3 ммоля) 1,8-диазабицикло[5,4, 0]ундец-7-ена (ДБУ). Красный раствор перемешивали в течение 15 ч при комнатной температуре. Для дальнейшей переработки смесь при интенсивном перемешивании смешивали с 200 мл воды. Органическую фазу отделяли, а водную фазу трижды экстрагировали метиленхлоридом порциями по 100 мл. Объединенные органические фазы дважды промывали насыщенным раствором поваренной соли порциями по 100 мл, сушили над сульфатом магния и в завершение отгоняли растворитель при пониженном давлении. Сырой продукт (21,4 г) очищали хроматографией быстрого разрешения на силикагеле с использованием метиленхлорида в качестве элюента. Таким путем получили 12,9 г (37,2 ммоля, 52% от теории) трет-бутилового эфира 4-триметилстаннил-3,6-2Н-пиридин-1- карбоновой кислоты в виде желтого масла; МС: 348 (М+Н)+ .
(β) Аналогично описанной выше методике путем катализируемой палладием реакции сочетания 4-триметилстаннил-3,6-2H-пиридин-1- карбоновой кислоты с рац. -2-хлор-5-[(тетрагидро-2H-пиран-2- илокси)метил] пиридина [ЕР 475273] получили трет-бутиловый эфир (RS)-5- (тетрагидропиран-2-илоксиметил)-3', 6'-дигидро-2'H- [2,4']бипиридин-1'-карбоновой кислоты в виде желтого масла; МС: 375 (М+Н)+.
(γ) Раствор из 2,56 г (6,84 ммоля) трет-бутилового эфира (RS)-5-(тетрагидропиран-2-илоксиметил) -3',6'-дигидро-2'H-[2,4'] бипиридин-1'-карбоновой кислоты в 10 мл абсолютного тетрагидрофурана при 0oC в атмосфере аргона смешивали, добавляя по каплям, с 1,40 мл (1,12 г, 14,0 ммолей) боран-диметилсульфидного комплекса (95%-ного) в диметилсульфиде. Смесь нагревали до 50oC, одновременно пропуская слабый поток аргона. По истечении 45 мин добавляли 10 мл тетрагидрофурана, охлаждали до 0o C и порциями добавляли 1,58 г (21,0 ммоля) N-оксида триметиламина в твердом виде, при этом температуру поддерживали на уровне 5-10oC. Смесь нагревали до комнатной температуры, в течение 1 ч нагревали с обратным холодильником, смешивали с 10 мл метанола, а затем еще в течение 1 ч нагревали с обратным холодильником. Смесь охлаждали до комнатной температуры и для дальнейшей переработки при интенсивном перемешивании сливали на смесь из 200 мл метиленхлорида, 200 мл воды и 10 мл 2 н. раствора гидроксида натрия. Органическую фазу отделяли, а водную фазу трижды экстрагировали метиленхлоридом порциями по 50 мл. Объединенные органические фазы дважды промывали раствором пиросульфита натрия (10%-ного) порциями по 50 мл (при этом путем добавления 2 н. раствора гидроксида натрия значение pH устанавливали примерно равным 9) и дважды - водой порциями по 25 мл, затем сушили над сульфатом магния и в завершение упаривали при пониженном давлении. Сырой продукт (2,59 г) очищали хроматографией быстрого разрешения на силикагеле с использованием метиленхлорида и уксусного эфира в качестве элюента. Таким путем получили 0,280 г (10% от теории) смеси 1:1 трет-бутилового эфира (3'RS,4'RS)-3'- гидрокси-5-[(RS)- и -[(SR)-тетрагидропиран-2-илоксиметил] - 3', 4', 5',6'-тетрагидро-2'H-[2,4']бипиридин-1'-карбоновой кислоты в виде светло-желтого масла; МС: 393 (М+Н)+ .
(δ) Аналогично примеру 125(ж) путем алкилирования смеси 1:1 трет-бутилового эфира (3'RS,4'RS)-3'-гидрокси-5-[(RS)- и -[(RS)-тетрагидропиран-2-илоксиметил] -3', 4', 5', 6'-тетрагидро-2'H- [2,4'] бипиридин-1'-карбоновой кислоты 2-бромметилнафталином получили смесь 1: 1 трет- бутилового эфира (3'RS, 4'RS)-3'-(нафталин-2-илметокси)-5- [(RS)- и -[(SR)-тетрагидропиран-2-илоксиметил] -3', 4', 5', 6'-тетрагидро-2'H-[2,4'] бипиридин-1'-карбоновой кислоты в виде желтого масла; МС: 533 (М+Н)+.
(ε) Раствор из 102 мг (0,19 ммоля) смеси 1:1 трет-бутилового эфира (3'RS, 4'RS)-3'-(нафталин-2-илметокси)-5-[(RS)- и -[(RS)- тетрагидропиран-2-илоксиметил] -3', 4', 5', 6'-тетрагидро-2'H- [2,4']бипиридин-1'-карбоновой кислоты растворяли в 2 мл метанола и охлаждали до -15oC. В течение 2 мин при температуре в интервале от -10 до -15oC по каплям добавляли 2 н. раствор хлористого водорода в метаноле. Смесь нагревали до комнатной температуры, после чего перемешивали в течение 30 мин, а затем для дальнейшей переработки распределяли между 25 мл уксусного эфира и 25 мл водного 5%-ного раствора гидрокарбоната натрия. Органическую фазу отделяли, а водную фазу трижды экстрагировали уксусным эфиром порциями по 10 мл. Объединенные уксусноэфирные фазы сушили над сульфатом магния и в завершение упаривали при пониженном давлении. Сырой продукт (96 мг) очищали хроматографией на силикагеле с использованием смеси 1:1 уксусного эфира и метиленхлорида в качестве элюента. Таким путем получили 78 мг (92% от теории) трет-бутилового эфира (3'RS, 4'RS)-5-гидроксиметил-3'-(нафталин-2-илметокси)- 3', 4', 5',6'-тетрагидро-2'H-[2,4'] бипиридин-1'-карбоновой кислоты в виде светло-желтого масла; МС: 449 (М+Н)+.
(ζ) Раствор из 70 мг (0,156 ммоля) трет-бутилового эфира (3'RS,4'RS)-5-гидроксиметил-3'-(нафталин-2-илметокси)-3', 4',5',6'-тетрагидро-2'H-[2, 4'] бипиридин-1'-карбоновой кислоты в 2 мл абсолютного ДМФ охлаждали до -10oC и смешивали с 26 мкл (19 мг, 0,187 ммоля) триэтиламина. При температуре в интервале от -10 до -15oC добавляли 13 мкл (20 мг, 0,172 ммоля) метансульфохлорида и 2 мг N,N-диметиламинопиридина (ДМАП) и после этого перемешивали в течение 1 ч при 0oC. Для дальнейшей переработки смесь распределяли между 25 мл уксусного эфира и 25 мл водного 5%-ного раствора хлорида аммония и отделяли органическую фазу. Водную фазу трижды экстрагировали уксусным эфиром порциями по 10 мл. Объединенные уксусноэфирные фазы сушили над сульфатом магния и в завершение упаривали при пониженном давлении. Сырой продукт очищали хроматографией на силикагеле с использованием смеси 1:1 уксусного эфира и гексана в качестве элюента. Таким путем получили 22 мг (35% от теории) трет-бутилового эфира (3'RS,4'RS)-5- хлорметил-3'-(нафталин-2-илметокси)-3', 4', 5', 6'-тетрагидро- 2'H-[2,4'] бипиридин-1'-карбоновой кислоты в виде светло-желтого масла; МС: 467, 469 (М+Н)+.
(η) Раствор из 22 мг (0,047 ммоля) трет-бутилового эфира (3'RS, 4'RS)-5-хлорметил-3'-(нафталин-2-илметокси)-3', 4', 5', 6'- тетрагидро-2'H-[2,4'] бипиридин-1'-карбоновой кислоты в 0,5 мл ДМФ смешивали с 67 мкл (72 мг, 0,47 ммоля) 2-бензилоксиэтанола и 19 мг (0,47 ммоля) гидрида натрия (60%-ная дисперсия в масле) и после этого перемешивали в течение 2 ч при комнатной температуре. Смесь для дальнейшей переработки распределяли между 15 мл уксусного эфира и 15 мл водного 5%-ного раствора хлорида аммония и затем отделяли органическую фазу. Водную фазу трижды экстрагировали уксусным эфиром порциями по 5 мл. Объединенные уксусноэфирные фазы сушили над сульфатом магния и в завершение отгоняли растворитель при пониженном давлении. Сырой трет-бутиловый эфир (3'RS, 4'RS) -5- (2-бензилоксиэтоксиметил)-3'-(нафталин-2-илметокси)- 3', 4',5',6'-тетрагидро-2'H-[2, 4']бипиридин-1'-карбоновой кислоты без дальнейшей очистки и определения характеристик использовали на следующей стадии.
Пример 145.
(а) Раствор из 10,8 г (54,3 ммоля) трет-бутилового эфира (1RS,6SR)-7-окса-3- азабицикло[4,1,0] гептан-3-карбоновой кислоты [пример 141(б)] в 250 мл ацетонитрила смешивали с 7,98 г (162,9 ммоля) порошкообразного цианида натрия и 17,3 г (162,9 ммоля) перхлората лития и реакционную смесь в течение 24 ч перемешивали в атмосфере аргона при 95oC. Для дальнейшей переработки коричневатый раствор охлаждали, смешивали с 150 мл уксусного эфира и фильтровали через декалит. Фильтрат промывали 100 мл воды и разделяли фазы. Значение pH водной фазы устанавливали на 5 и трижды экстрагировали путем встряхивания уксусным эфиром, используя порции по 60 мл. Объединенные органические фазы сушили над сульфатом натрия и упаривали при пониженном давлении. Сырой продукт очищали хроматографией на силикагеле с использованием смеси 4:1 гексана и уксусного эфира в качестве элюента. Таким путем получили 9,9 г (80,5% от теории) смеси 4:1 трет-бутилового эфира (3RS,4RS)-4-циано-3- гидроксипиперидин-1-карбоновой кислоты и трет-бутилового эфира (3RS,4RS)-3-циано-4-гидроксипиперидин-1-карбоновой кислоты в виде бесцветных кристаллов; МС: 227 (М+Н)+.
(б) Раствор из 5,8 г (25,6 ммоля) смеси 4:1 трет-бутилового эфира (3RS, 4RS)-4-циано-3-гидроксипиперидин-1-карбоновой кислоты и трет-бутилового эфира (3RS,4RS)-3-циано-4-гидроксипиперидин-1-карбоновой кислоты в 50 мл N, N-диметилформамида перемешивали в атмосфере аргона в течение 4 ч при комнатной температуре с 1,8 мг (38,4 ммоля) моногидрата гидросульфида натрия и 2,05 г (38,4 ммоля) хлорида аммония. Для дальнейшей переработки реакционную смесь упаривали при пониженном давлении и остаток растворяли в 150 мл метиленхлорида. Полученный раствор дважды промывали водой порциями по 10 мл, органическую фазу отделяли, сушили над сульфатом натрия и затем упаривали при пониженном давлении. Для очистки и разделения смеси изомеров остаток хроматографировали на силикагеле с использованием смеси 95:5:0,1 метиленхлорида, метанола и аммиака в качестве элюента. Таким путем получили 3,48 г (52% от теории) трет-бутилового эфира (3RS,4SR)-3-гидрокси-4-тиокарбамоилпиперидин-1-карбоновой кислоты [Rf 0,37, силикагель, метиленхлорид/метанол/аммиак в объемном соотношении 90:10:0,1; МС: 260 (М)+], а также 1,2 г смеси 4:1 трет-бутилового эфира (3RS,4SR)-3-гидрокси-4-тиокарбамоилпиперидин- 1-карбоновой кислоты и трет-бутилового эфира (3RS,4RS)-4-гидрокси-3-тиокарбамоилпиперидин-1-карбоновой кислоты, в каждом случае в виде бесцветного масла.
(в) К раствору из 1,88 г (7,22 ммоля) трет-бутилового эфира (3RS,4SR)-3-гидрокси-4-тиокарбамоилпиперидин-1-карбоновой кислоты в 5 мл ацетона при комнатной температуре добавляли 4 мл метилиодида. После перемешивания в течение 14 ч при комнатной температуре продукт выпадал в осадок. Добавляли 10 мл простого эфира и реакционную смесь перемешивали в течение 30 мин. После отфильтровывания и сушки получили 2,76 г (98% от теории) иодида (3RS, 4SR)-[амино(1- трет-бутоксикарбонил-3-гидроксипиперидин-4- ил)метилен] метилсульфония в виде бесцветных кристаллов; Rf 0,22 (силикагель, метиленхлорид/метанол/аммиак в объемном соотношении 95:5:0,1).
(г) Раствор из 2,76 г (7,09 ммоля) иодида (3RS,4SR)-[амино(1-трет-бутоксикарбонил-3-гидроксипиперидин-4- ил)метилен] метилсульфония в 15 мл метанола смешивали с 0,41 г (3,55 ммоля) карбоната аммония и перемешивали в течение 18 ч при комнатной температуре. Для дальнейшей переработки реакционную смесь упаривали при пониженном давлении. Таким путем получили 2, 5 г (95% от теории) иодида трет-бутилового эфира (3RS,4RS)-4- карбамимидоил-3-гидроксипиперидин-1-карбоновой кислоты в виде бесцветной пены.
Раствор из 715 мг (1,92 ммоля) иодида трет- бутилового эфира (3RS, 4RS)-4-карбамимидоил-3-гидроксипиперидин-1- карбоновой кислоты в 20 мл метанола перемешивали в течение 1 ч при комнатной температуре с 321 мг (1,92 ммоля) ацетата серебра. Выпавший в осадок иодид серебра отфильтровывали и промывали 20 мл метанола. Полученный светло-желтый фильтрат упаривали при пониженном давлении. Таким путем получили 538 мг (92% от теории) ацетата трет-бутилового эфира (3RS, 4RS)-4- карбамимидоил-3-гидроксипиперидин-1-карбоновой кислоты в виде бесцветной пены.
(д) Раствор из 372 мг (1 ммоль) ацетата трет- бутилового эфира (3RS, 4RS)-4-карбамимидоил-3-гидроксипиперидин-1- карбоновой кислоты в 10 мл метанола смешивали с 1 мл 1 н. раствора метилата натрия и перемешивали при комнатной температуре. Далее добавляли 205 мг (1 ммоль) 2-бензилокси-3-диметиламиноакролеина (ЕРА 0477901) и раствор в течение 18 ч нагревали с обратным холодильником. Для дальнейшей переработки реакционную смесь упаривали при пониженном давлении, остаток растворяли в 20 мл метиленхлорида и промывали 5 мл воды. Органическую фазу отделяли, сушили над сульфатом натрия и в завершение упаривали при пониженном давлении. Остаток очищали хроматографией на силикагеле с использованием смеси 1:4 метиленхлорида и уксусного эфира в качестве элюента. Таким путем получили 106 мг (27% от теории) трет-бутилового эфира (3RS, 4RS)-4-(5-бензилоксипиримидин-2-ил)-3- гидроксипиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 386 (М+Н)+.
(е) Раствор из 110 мг (0,29 ммоля) трет-бутилового эфира (3RS,4RS)-4-(5-бензилоксипиримидин-2-ил)-3-гидроксипиперидин-1- карбоновой кислоты в 5 мл метанола смешивали с 20 мг палладия (5%-ного) на угле и гидрировали в течение 12 ч при комнатной температуре. Для дальнейшей переработки катализатор отфильтровывали и промывали 20 мл метанола. Метанольный раствор упаривали при пониженном давлении и образовавшееся масло кристаллизовали добавлением простого эфира. Таким путем получили 80 мг (93% от теории) трет-бутилового эфира (3RS,4RS)-3- гидрокси-4-(5-гидроксипиримидин-2-ил)пиперидин-1-карбоновой кислоты в виде бесцветных легко расплывающихся кристаллов; МС: 296 (М+Н)+.
(ж) Смесь из 65 мг (0,22 ммоля) трет-бутилового эфира (3RS,4RS)-3-гидрокси-4-(5-гидроксипиримидин-2-ил)пиперидин-1- карбоновой кислоты, 90 мг (0,66 ммоля) карбоната калия и 151,2 мг (0,66 ммоля) (3-бромпропоксиметил)бензола в 10 мл метилэтилкетона перемешивали в атмосфере аргона в течение 48 ч при 80oC. Для дальнейшей переработки реакционную смесь упаривали при пониженном давлении, остаток растворяли в метиленхлориде и раствор непосредственно хроматографировали на силикагеле с использованием смеси 1:4 метиленхлорида и уксусного эфира в качестве элюента. Таким путем получили 40 мг (41% от теории) трет-бутилового эфира (3RS,4RS)-4-[5-(3-бензилоксипропокси)пиримидин-2-ил]-3- гидроксипиперидин-1-карбоновой кислоты в виде пены; Rf0,43 (силикагель, метиленхлорид/уксусный эфир в объемном соотношении 1:4).
(з) Раствор из 40 мг (0,09 ммоля) трет-бутилового эфира (3RS, 4RS)-4-[5-(3-бензилоксипропокси)пиримидин-2-ил] -3- гидроксипиперидин-1 -карбоновой кислоты и 23 мг (0,1 ммоля) 2-бромметилнафталина в 5 мл N,N-диметилформамида смешивали с 5 мг (0,1 ммоля) гидрида натрия (50%-ная дисперсия в масле) и перемешивали в течение 18 ч при комнатной температуре. Для дальнейшей переработки реакционную смесь упаривали при пониженном давлении, полученный остаток растворяли в 3 мл метиленхлорида и раствор непосредственно хроматографировали на силикагеле с использованием смеси 2:1 гексана и уксусного эфира в качестве элюента. Таким путем получили 40 мг (76% от теории) трет- бутилового эфира (3RS,4RS)-4-[5-(3-бензилоксипропокси) пиримидин-2-ил]-3-(нафталин-2-илметокси)пиперидин- 1-карбоновой кислоты в виде масла; МС: 584 (М+Н)+.
(и) Раствор из 40 мг (0,07 ммоля) трет-бутилового эфира (3RS,4RS)-4-[5-(3-бензилоксипропокси)пиримидин-2-ил]-3-(нафталин- 2-илметокси)пиперидин-1-карбоновой кислоты и 0,1 мл трифторуксусной кислоты в 1 мл метиленхлорида перемешивали в течение 2 ч при комнатной температуре. После этого раствор упаривали, остаток растворяли в 1 мл уксусного эфира и кристаллизовали добавлением гексана. Таким путем получили 25 мг (60% от теории) трифторацетата (3RS, 4RS)-5-(3-бензилоксипропокси)-2-[3-(нафталин-2-илметокси) пиперидин-4-ил] пиримидина в виде бесцветных кристаллов; МС: 484 (М+Н)+.
Пример 146.
(а) Аналогично примеру 145(а) путем раскрытия эпоксидного кольца с помощью 4-бензилокси-2(1H)-пиридона [Chem. Pharm. Bull. 22, 763-770 (1974)] из трет-бутилового эфира (1RS,6SR)-7-окса-3- азабицикло[4,1,0]гептан-3-карбоновой кислоты [пример 141(б)] получили смесь 1:1 трет-бутилового эфира (3'RS, 4'RS)-4- бензилокси-4'-гидрокси-2-оксо-3',4',5', 6'-тетрагидро-2H,2'H- [1,3'] бипиридин-1'-карбоновой кислоты и трет-бутилового эфира (3'RS,4'RS)-4-бензилокси-3'-гидрокси-2-оксо-3', 4',5',6'- тетрагидро-2H,2'H-[1,4']бипиридин-1'-карбоновой кислоты в виде бесцветных кристаллов; МС: 401 (М+Н)+.
(б) Аналогично примеру 145(е) из смеси 1:1 трет-бутилового эфира (3'RS, 4'RS)-4-бензилокси-4'-гидрокси-2-оксо-3', 4',5', 6'-тетрагидро- 2H,2'H-[1,3'] бипиридин-1'-карбоновой кислоты и трет-бутилового эфира (3'RS,4'RS)-4-бензилокси-3'-гидрокси-2-оксо-3', 4', 5', 6'- тетрагидро-2H,2'H- [1,4']бипиридин-1'-карбоновой кислоты путем каталитического гидрирования получили смесь 1: 1 трет-бутилового эфира (3'RS,4'RS)-4,3'-дигидрокси-2-оксо-3',4',5',6'- тетрагидро-2H, 2'H-[1,4'] бипиридин-1'-карбоновой кислоты и трет- бутилового эфира (3'RS, 4'RS)-4,4'-дигидрокси-2-оксо- 3',4',5',6'-тетрагидро-2H,2'H-[1,3'] бипиридин-1'-карбоновой кислоты в виде бесцветной пены; МС: 311 (М+H)+.
(в) Аналогично примеру 145(ж) из смеси 1:1 трет-бутилового эфира (3'RS, 4'RS)-4,3'-дигидрокси-2-оксо-3', 4', 5', 6'- тетрагидро-2H,2'H-[1,4']бипиридин-1'-карбоновой кислоты и трет- бутилового эфира (3'RS, 4'RS) -4,4'-дигидрокси-2-оксо-3', 4',5',6'-тетрагидро-2H,2'H- [1,3'] бипиридин-1'- карбоновой кислоты в присутствии карбоната калия получили смесь трет-бутилового эфира (3'RS, 4'RS)-4-(3-бензилоксипропокси) - 3'-гидрокси-2-оксо-3',4',5',6'-тетрагидро-2H,2'H- [1,4'] бипиридин-1'-карбоновой кислоты и трет-бутилового эфира (3'RS, 4'RS)-4-(3-бензилоксипропокси)-4'-гидрокси-2- оксо -3',4',5',6'-тетрагидро-2H, 2'H-[1,3']бипиридин-1'- карбоновой кислоты в виде бесцветного масла; МС: 459 (М+Н)+.
(г) Аналогично примеру 145(з) из смеси трет-бутилового эфира (3'RS, 4'RS)-4-(3-бензилоксипропокси)-3'-гидрокси-2-оксо-3',4',5',6'-тетрагидро-2H, 2'H-[1,4'] бипиридин-1'-карбоновой кислоты и трет-бутилового эфира (3'RS, 4'RS)-4-(3- бензилоксипропокси)-4'-гидрокси-2-оксо-3', 4', 5',6'- тетрагидро-2H, 2'H-[1,3'] бипиридин-1'-карбоновой кислоты путем алкилирования 2-бромметилнафталином и после хроматографического разделения обоих изомеров на силикагеле с использованием смеси 1:4 метиленхлорида и уксусного эфира в качестве элюента получили трет- бутиловый эфир (3'RS, 4'RS)-4-(3-бензилоксипропокси)-4'- (нафталин-2-илметокси)-2-оксо-3',4',5',6'-тетрагидро-2H,2'H- [1,3'] бипиридин-1'-карбоновой кислоты (Rf0,64, SiO2, метиленхлорид/уксусный эфир в объемном соотношении 1:4) и трет- бутиловый эфир (3'RS,4'RS)-4-(3-бензилоксипропокси)-3'- (нафталин-2-илметокси)-2-оксо-3',4',5',6'-тетрагидро-2H, 2'H-[1,4'] бипиридин-1'-карбоновой кислоты, МС: 599 (М+Н)+ (Rf 0,44, SiO2, метиленхлорид/уксусный эфир в объемном соотношении 1:4), в каждом случае в виде желтоватого масла.
(д) Аналогично примеру 145(и) из трет-бутилового эфира (3'RS,4'RS)-4-(3-бензилоксипропокси)-3'-(нафталин-2-илметокси)-2-оксо- 3', 4', 5',6'-тетрагидро-2H, 2'H-[1,4']бипиридин-1'-карбоновой кислоты путем отщепления BOC-группы с помощью трифторуксусной кислоты получили трифторацетат (3'RS, 4'RS)-4-(3-бензилоксипропокси) - 3'-(нафталин-2-илметокси- 1',2',3',4',5', 6'-гексагидро-[1,4'] бипиридин-2-она в виде бесцветного твердого вещества; МС: 499 (М+Н)+.
Пример 147.
Аналогично примеру 22(м) путем отщепления BOC-группы с помощью хлористого водорода в метаноле получали следующие соединения:
1) из трет-бутилового эфира (1RS,2RS,3RS,5SR)-3-[4-(2-бензилоксиэтоксиметил)фенил] -2-(нафталин-2-илметокси)-8-азабицикло[3,2,1] октан-8-карбоновой кислоты получили (1RS, 2RS, 3RS, 5SR)-3-[4-(2- бензилоксиэтоксиметил)фенил]-2-(нафталин-2-илметокси)-8- азабицикло[3,2,1]октан в виде бесцветного масла; Rf 0,15 (силикагель, метиленхлорид/метанол/аммиак = 95:5:0,1);
2) из трет-бутилового эфира (1RS,2RS,3RS,5SR)-2-(нафталин-2-илметокси)- 3-[4-(2-феноксиэтоксиметил)фенил] -8-азабицикло[3,2,1] октан-8- карбоновой кислоты получили (1RS, 2RS, 3RS,5SR)-2-(нафталин-2- илметокси)-3-[4-(2-феноксиэтоксиметил)фенил] -8- азабицикло[3,2,1]октан в виде желтого масла; Rf 0,21 (силикагель, метиленхлорид/метанол/аммиак = 95:5:0,1);
3) из трет-бутилового эфира (1RS,2RS,3RS,5SR)-3-(4-бензилоксиметилфенил)-2-(нафталин-2- илметокси)-8-азабицикло[3,2,1]октан-8-карбоновой кислоты +BOC получили гидрохлорид (1RS,2RS,3RS,5SR)-3-(4-бензилоксиметилфенил)-2-(нафталин-2-илметокси)-8-азабицикло[3,2,1] октана в виде бесцветного масла; МС: 464 (М+Н)+;
4) из трет-бутилового эфира (1RS,2RS,3RS,5SR)-2-(нафталин-2-илметокси)-3-(4- фенилсульфанилметилфенил)-8-азабицикло[3,2,1] октан-8-карбоновой кислоты получили гидрохлорид (1RS,2RS,3RS, 5SR)-2-(нафталин-2- илметокси)-3-(4-фенилсульфанилметилфенил)-8-азабицикло[3,2,1] октана в виде бесцветного масла; МС: 566 (М+Н)+;
5) из трет-бутилового эфира (1RS,2RS,3RS, 5SR)-3-[4-(2-хлорбензоилоксиметил)фенил] -2-(нафталин-2-илметокси)-8-азабицикло[3,2,1]октан-8-карбоновой кислоты +BOC получили (1RS,2RS,3RS,5SR)-3-[2- (нaфтaлин-2-илметокси)-8-азабицикло [3.2.1] окт-3-ил] бензиловый эфир 2-хлорбензойной кислоты в виде желтоватой пены; МС: 512 (М+Н)+.
Использованные в качестве исходных соединений BOC- производные получали следующим образом.
(а) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (1RS,2RS,3RS,5SR)-3-(4-гидроксиметилфенил)-2-(нафталин-2-илметокси)- 8-азабицикло[3,2, 1]октан-8-карбоновой кислоты [пример 86(ддд)] 2-(бензилокси)этилиодидом [Helv. Chim. Acta, т. 71 (1988), 2039] получили трет-бутиловый эфир (1RS,2RS,3RS,5SR)-3-[4-(2- бензилоксиэтоксиметил)фенил] -2-(нафталин-2-илметокси)-8- азабицикло[3,2,1] октан-8-карбоновой кислоты в виде бесцветного масла; МС: 625 (М+Н)+.
(б) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (1RS, 2RS, 3RS, 5SR)-3-(4- гидроксиметилфенил)-2-(нафталин-2-илметокси)-8-азабицикло[3,2,1]октан-8-карбоновой кислоты [пример 86(ддд)] феноксиэтилбромидом получили трет-бутиловый эфир (1RS,2RS,3RS,5SR)-2-(нафталин-2- илметокси)-3-[4-(2-феноксиэтоксиметил)фенил] -8-азабицикло[3,2,1]октан-8-карбоновой кислоты в виде бесцветного масла; МС: 611 (M+NH4)+.
(в) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (1RS, 2RS, 3RS, 5SR)-3-(4-гидроксиметилфенил)- 2-(нафталин-2-илметокси)-8-азабицикло[3,2,1] октан-8-карбоновой кислоты [пример 86(ддд)] бензилбромидом получили трет-бутиловый эфир (1RS,2RS,3RS,5SR)-3-(4-гидроксиметилфенил)-2-(нафталин-2- илметокси)-8-азабицикло[3,2,1] октан-8-карбоновой кислоты +BOC, который в неочищенном виде использовали в реакции отщепления BOC-группы.
(г) Аналогично примеру 33(а) взаимодействием трет- бутилового эфира (1RS, 2RS, 3RS, 5SR)-3-(4-гидроксиметилфенил)-2- (нафталин-2-илметокси)-8-азабицикло[3,2,1] октан-8-карбоновой кислоты [пример 86(ддд)] с дифенилсульфидом в присутствии трибутилфосфина получили трет-бутиловый эфир (1RS,2RS, 3RS, 5SR)-2- (нафталин-2-илметокси)-3-(4-фенилсульфанилметилфенил)-8- азабицикло[3,2,1] октан-8-карбоновой кислоты в виде бесцветного масла; МС: 566 (М+Н)+.
(д) Аналогично примеру 22(л) путем этерификации трет-бутилового эфира (1RS,2RS,3RS,5SR)-3-(4- гидроксиметилфенил)-2-(нафталин-2-илметокси)-8- азабицикло[3,2,1]октан-8-карбоновой кислоты [пример 86(ддд)] 2- хлорбензоилхлоридом трет-бутиловый эфир (1RS, 2RS, 3RS, 5SR)-3-[4-(2-хлорбензоилоксиметил)фенил] -2- (нафталин-2-илметокси)-8-азабицикло[3,2,1]октан-8-карбоновой кислоты +BOC в виде бесцветного масла, который в неочищенном виде использовали в реакции отщепления BOC-группы.
Пример 148.
Аналогично примеру 22(м) из трет-бутилового эфира (3SR,4RS, 5RS)-4-[4-(3-бензилоксипропокси) фенил] -3-метоксиметил-5-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты путем отщепления BOC-группы с помощью хлористого водорода в метаноле получили (3SR,4RS, 5RS)-4-[4-(3-бензилоксипропокси)фенил] -3-метоксиметил-5-(нафталин-2-илметокси) пиперидин в виде аморфного бесцветного твердого вещества; МС: 526 (М+Н)+.
Использованный в качестве исходного соединения трет-бутиловый эфир (3SR, 4RS, 5RS)-4- [4-(3-бензилоксипропокси)фенил] -3-метоксиметил-5-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты синтезировали следующим образом.
(а) Аналогично примеру 68(а)-(б) сначала защищали первичную гидроксильную функцию (3RS,4RS)- и (3SR,4RS)-1-бензил-3- гидроксиметилпиперидин-4-ола [Е. Jaeger и J.H. Biel, J. Org. Chem. 30(3), 740-744 (1965)], используя вместо трет- бутилдифенилхлорсилана аналогично примеру 22(з) трифенилхлорметан в пиридине с получением таким путем (3RS,4RS)- и (3SR, 4RS)-1- бензил-3-тритилоксиметилпиперидин-4-ола. В результате последующего окисления оксалилхлоридом в диметилсульфоксиде был получен (RS)-1 -бeнзил-3-тpитилoкcимeтилпипepидин-4-oн в виде бесцветной пены; МС: 462 (М+Н)+. Последующим взаимодействием с 4-иоданизолом аналогично примеру 62(б) получили смесь (3RS, 4RS)- и (3RS, 4SR)-1-бензил-4-(4-метоксифенил)-3-тритилоксиметилпиперидин-4-ола в виде бесцветного твердого вещества; МС: 570 (М+Н)+.
(б) К раствору из 8,36 г (14,6 ммоля) смеси (3RS, 4RS)- и (3RS,4SR)-1-бензил-4-(4-метоксифенил)-3-тритилоксиметилпиперидин-4-ола в 20 мл сухого пиридина в течение 20 мин по каплям добавляли раствор из 5,5 мл (58,7 ммоля) хлорокиси фосфора в 20 мл сухого пиридина, реакционную смесь перемешивали в течение 20 ч при 60oC. Темно-красную реакционную смесь охлаждали и упаривали при пониженном давлении. Остаток растворяли в метиленхлориде и смешивали с насыщенным раствором карбоната натрия. Органическую фазу отделяли, сушили над сульфатом натрия и упаривали при пониженном давлении. Остаток хроматографировали на силикагеле с использованием смеси 20:1 толуола и уксусного эфира в качестве элюента. Таким путем получили 6,1 г (75% от теории) (RS)-1-бензил-4-(4-метоксифенил)-3- тритилоксиметил-1,2,3,6-тетрагидропиридина в виде бесцветного твердого вещества; МС: 552 (М+Н)+.
(в) Аналогично примеру 62(г) путем гидроборирования (RS)-1-бензил-4-(4-метоксифенил)-3- тритилоксиметил-1,2,3, 6-тетрагидропиридина боран-тетрагидрофураном и последующего окисления с помощью перкарбоната натрия получили (3RS, 4RS,5SR)-1-бензил-4-(4-метоксифенил)-5-тритилоксиметил пиперидин-3-ол в виде бесцветной пены; МС: 570 (М+Н)+.
(г) Аналогично примеру 44 (г) путем одновременного расщепления метокси- и тритилоксигруппы с помощью трибромида бора в метиленхлориде из (3RS,4RS, 5SR)-1-бензил-4-(4-метоксифенил)-5- тритилоксиметилпиперидин-3-ола получили гидробромид (3RS, 4RS, 5SR)- 1-бензил-5-гидроксиметил-4-(4-гидроксифенил)пиперидин-3-ола в виде белого твердого вещества; МС: 314 (М+Н)+.
(д) Аналогично примеру 2(д) путем каталитического гидрирования при атмосферном давлении с использованием в качестве катализатора палладия (10%-ного) на угле в метаноле из гидробромида (3RS,4RS,5SR)-1-бензил-5-гидроксиметил-4-(4-гидроксифенил)пиперидин-3-ола получили гидробромид (3RS,4RS, 5SR)-5-гидроксиметил-4-(4-гидроксифенил)пиперидин-3-ола в виде бесцветной пены; МС: 224 (М+Н)+.
(е) Аналогично примеру 1(е) взаимодействием гидробромида (3RS,4RS, 5SR)-5-гидроксиметил-4-(4- гидроксифенил)пиперидин-3-ола с ди-трет-бутилдикарбонатом получили трет-бутиловый эфир (3RS,4RS,5SR)-3-гидрокси-5-гидроксиметил-4-(4- гидроксифенил) пиперидин-1-карбоновой кислоты в виде бесцветной пены.
(ж) Аналогично примеру 44(д) путем алкилирования трет- бутилового эфира (3RS, 4RS, 5SR)-3-гидрокси-5-гидроксиметил-4-(4- гидроксифенил)пиперидин-1-карбоновой кислоты бензил-3- бромпропиловым эфиром в присутствии карбоната калия в бутан-2-оне получили трет-бутиловый эфир (3RS,4RS, 5SR)-4-[4-(3- бензилоксипропокси)фенил] -3-гидрокси-5-гидроксиметилпиперидин- 1-карбоновой кислоты в виде бесцветного масла; МС: 472 (М+Н)+.
(з) Аналогично примеру 22(з) взаимодействием трет-бутилового эфира (3RS, 4RS, 5SR)-4-[4-(3-бензилоксипропокси)фенил] -З-гидрокси-5- гидроксиметилпиперидин-1-карбоновой кислоты с трифенилхлорметаном в пиридине получили трет-бутиловый эфир (3RS,4RS,5SR)-4-[4-(3- бензилоксипропокси)фенил]-3-гидрокси-5-тритилоксиметилпиперидин- 1-карбоновой кислоты [МС: 731 (M+NH4)+] в виде бесцветной пены, алкилированием которого 2-бромметилнафталином аналогично примеру 62(3) получили трет-бутиловый эфир (3RS,4RS,5SR)-4-[4-(3-бензилоксипропокси)фенил] -3-(нафталин-2- илметокси)-5-тритилоксиметилпиперидин-1-карбоновой кислоты [МС: 871 (M+NH4)+] в виде бесцветной пены. В результате последующего селективного отщепления тритильной группы с помощью смеси трифторуксусной кислоты и ангидрида трифторуксусной кислоты в метиленхлориде аналогично примеру 86(х) был получен трет-бутиловый эфир (3SR,4RS, 5RS)-4-[4-(3-бензилоксипропокси)фенил] -3-гидроксиметил-5-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 612 (М+Н)+. Путем последующего алкилирования метилиодидом аналогично примеру 62(з) получили трет- бутиловый эфир (3SR,4RS,5RS)-4- [4-(3-бензилоксипропокси)фенил] -3-метоксиметил-5- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 626 (М+Н)+.
Пример 149.
Аналогично примеру 22(м) путем отщепления BOC-группы с помощью хлористого водорода в метаноле получали следующие соединения:
1) из трет-бутилового эфира (3SR,4RS,5RS)-4-[4-(3- бензилоксипропокси)фенил] -3-гидроксиметил-5-(нафталин-2- илметокси) пиперидин-1- карбоновой кислоты [пример 148(з)] получили гидрохлорид (3SR,4RS,5RS)-4-[4-(3-бензилоксипропокси)фенил] -5-(нафталин-2 -илметокси)пиперидин-3-ил] метанола в виде бесцветного твердого вещества; МС: 512 (М+Н)+;
2) из трет-бутилового эфира (3RS, 4RS,5SR)-4-[4-(3-бензилоксипропокси)фенил]-3-(нафталин -2-илметокси)-5-(пиридин-4-илсульфанилметил)пиперидин- 1-карбоновой кислоты получили гидрохлорид (3SR,4RS,5RS)-4-[4- [4-(3-бензилоксипропокси)фенил] -5-(нафталин-2-илметокси)пиперидин- 3-илметилсульфанил] пиридина в виде бесцветного твердого вещества; МС: 605 (М+Н)+;
3) из трет-бутилового эфира (3RS,4RS, 5SR)-4-[4-(3- бензилоксипропокси)фенил] -3-(нафталин-2-илметокси)-5- фенилсульфанилметилпиперидин-1-карбоновой кислоты получили гидрохлорид (3RS,4RS,5SR)-4-[4-(3-бензилоксипропокси)фенил] -3- (нафталин-2-илметокси)-5-фенилсульфанилметилпиперидина в виде бесцветного масла; МС: 604 (М+Н)+;
4) из трет-бутилового эфира (3SR, 4RS, 5RS)-4-[4-(3-бензилоксипропокси)фенил]-3-(2-морфолин-4- илэтоксиметил)-5-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты получили (3SR, 4RS,5RS)-4-[2-[4-[4-(3-бензилоксипропокси) фенил] -5-(нафталин-2-илметокси)пиперидин-3-илметокси] этил] морфолин в виде бесцветного масла; МС: 625 (М+Н)+;
5) из трет-бутилового эфира (3RS, 4RS, 5RS)-4-[4-(3-бензилоксипропокси)фенил] -3 -диэтиламинометил-5-(нафталин-2-илметокси)пиперидин-1 -карбоновой кислоты получили (3SR,4RS, 5RS)-[4-[4-(3- бензилоксипропокси)фенил]-5-(нафталин-2-илметокси)пиперидин-3- илметил] диэтиламин в виде желтоватого масла; МС: 567 (М+Н)+;
6) из трет-бутилового эфира (3RS,4RS,5RS)-4-[4- (3-бензилоксипропокси)фенил] -3-[[(2-диметиламиноэтил)метиламино] метил] -5-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты получили (3SR, 4RS, 5RS)-N-[4-[4-(3-бензилоксипропокси) фенил] -5-(нафталин-2-илметокси)пиперидин-3-илметил]-N, N',N'-триметилэтан- 1,2-диамин в виде желтоватого масла; МС: 596 (М+Н)+;
7) из трет-бутилового эфира (3RS, 4RS,5SR)-4-[4-(3-бензилоксипропокси)фенил] - 3-(нафталин-2-илметокси)-5-[1,2,4] триазол-1-илметилпиперидин- 1-карбоновой кислоты получили гидрохлорид (3RS,4RS, 5SR)-4-[4- (3-бензилоксипропокси)фенил] -3-(нафталин-2-илметокси)-5- [1,2,4] триазол-1-илметилпиперидина в виде бесцветного твердого вещества; МС: 563 (М+Н)+;
8) из трет-бутилового эфира (3RS, 4RS,5RS)-4-[4-(3-бензилоксипропокси)фенил]-3-(нафталин-2- илметокси)-5-(2-оксоимидазолидин-1-илметил)пиперидин-1- карбоновой кислоты получили (3SR,4RS,5RS)-1-[4-[4-(3 - бензилоксипропокси)фенил] -5-(нафталин-2-илметокси)пиперидин- 3-илметил] имидазолидин-2-он в виде бесцветного твердого вещества; МС: 580 (М+Н)+;
9) из триметиламмониевой соли трет-бутилового эфира (3SR,4RS,5RS)-4-[4-(3-бензилоксипропокси)фенил] -3- (нафталин-2-илметокси)-5-сульфооксиметилпиперидин-1-карбоновой кислоты получили моно-(3SR,4RS, 5RS)-[4-[4-(3-бензилоксипропокси)фенил] -5-(нафталин-2-илметокси)пиперидин-3-илметиловый] эфир серной кислоты в виде бесцветного твердого вещества; МС: 590 (M-H)-.
Использованные в качестве исходных соединений BOC-производные получали следующим образом.
(а) Аналогично примеру 33(a) взаимодействием трет-бутилового эфира (3SR, 4RS, 5RS)-4-[4-(3-бензилоксипропокси)фенил]-3- гидроксиметил-5-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты [пример 148(з)] с 4,4'-дитиопиридином в присутствии трибутилфосфина получили трет-бутиловый эфир (3RS,4RS, 5SR)-4-[4- (3-бензилоксипропокси)фенил]-3-(нафталин-2-илметокси)-5-(пиридин- 4-илсульфанилметил)пиперидин-1-карбоновой кислоты в виде желтой, полутвердой субстанции; МС: 705 (М+Н)+.
(б) Аналогично примеру 33(a) взаимодействием трет-бутилового эфира (3SR, 4RS, 5RS)-4-[4-(3- бензилоксипропокси)фенил]-3-гидроксиметил-5-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты [пример 148(з)] с дифенилдисульфидом в присутствии трибутилфосфина получили трет- бутиловый эфир (3RS,4RS, 5SR)-4-[4-(3-бензилоксипропокси)фенил] -3- (нафталин-2-илметокси)-5-фенилсульфанилметилпиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 721 (М+NH4 )+.
(в) Аналогично примеру 1(ж) путем алкилирования трет- бутилового эфира (3SR, 4RS, 5RS)-4-[4-(3-бензилоксипропокси) фенил] -3-гидроксиметил-5-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты [пример 148(з)] 4-(2-хлорэтил)морфолином получили трет- бутиловый эфир (3SR,4RS,5RS)-4-[4-(3-бензилоксипропокси)фенил] -3- (2-морфолин-4-илэтоксиметил)-5-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты в виде бесцветного масла; МС: 725 (М+Н)+.
(г) По известному из литературы методу взаимодействием трет-бутилового эфира (3SR, 4RS,5RS)-4-[4-(3-бензилоксипропокси) фенил]-3-гидроксиметил-5-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты [пример 148(з)] с мезилхлоридом получили трет-бутиловый эфир (3SR,4RS,5RS)-4-[4-(3-бензилоксипропокси)фенил]-3- метансульфонилоксиметил-5-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты [МС: 707 (M+NH4)+] в виде бесцветного твердого вещества. Последующим взаимодействием с диэтиламином в ацетонитриле при 50oC аналогично примеру 34 получили трет- бутиловый эфир (3RS,4RS, 5RS)-4-[4-(3-бензилоксипропокси)фенил] - 3-диэтиламиноме-тил-5-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде коричневой пены; МС: 667 (М+Н)+.
(д) Взаимодействием трет-бутилового эфира (3SR,4RS,5RS)-4-[4-(3- бензилоксипропокси) фенил] -3-метансульфонилоксиметил-5-(нафталин- 2-илметокси) пиперидин-1-карбоновой кислоты с N,N, N'- триметилэтилендиамином при 100oC аналогично примеру 34 получили трет-бутиловый эфир (3RS,4RS,5RS)-4-[4-(3-бензилоксипропокси)фенил] - 3-[[(2-диметиламиноэтил)метиламино] метил] -5-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 696 (М+Н)+.
(е) Раствор из 22 мг (0,32 ммоля) 1,2,4-триазола в 5 мл ДМФ охлаждали до 0oC и смешивали с 15 мг (0,29 ммоля) гидрида натрия (50%-ная дисперсия в вазелиновом масле). Далее давали нагреться до комнатной температуры и перемешивание продолжали в течение 1 ч. К этому раствору добавляли 70 мг (0,105 ммоля) трет-бутилового эфира (3SR,4RS,5RS)-4-[4-(3-бензилоксипропокси)фенил] -3-метансульфонилоксиметил-5-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты. Реакционную смесь выдерживали при 100oC в течение 24 ч. Для дальнейшей переработки реакционную смесь упаривали при пониженном давлении, остаток распределяли между водой и метиленхлоридом, органическую фазу отделяли, сушили над сульфатом натрия и упаривали. Сырой продукт (70 мг) очищали хроматографией на силикагеле с использованием смеси 98:2 метиленхлорида и метанола в качестве элюента. Таким путем получили 52 мг (77% от теории) трет-бутилового эфира (3RS,4RS,5SR)-4-[4- (3-бензилоксипропокси)фенил]-3-(нафталин-2-илметокси)-5-[1,2,4] триазол-1-илметилпиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 663 (М+Н)+.
(ж) Аналогично примеру 149(е) взаимодействием трет-бутилового эфира (3SR, 4RS, 5RS)-4-[4-(3-бензилоксипропокси)фенил] -3- метансульфонилоксиметил-5-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты с имидазолидин-2-оном получили трет-бутиловый эфир (3RS,4RS, 5RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(нафталин- 2-илметокси)-5-(2-оксоимидазолидин-1-илметил)пиперидин-1- карбоновой кислоты в виде желтоватого масла.
(з) Раствор из 100 мг (0, 136 ммоля) трет-бутилового эфира (3SR,4RS, 5RS)-4-[4-(3-бензилоксипропокси)фенил] -3-гидроксиметил-5- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты [пример 148(з)] в 10 мл сухого пиридина смешивали с 78 мг (0,43 ммоля) комплекса трехокись серы-триметиламин и перемешивали в течение 36 ч при комнатной температуре. Для дальнейшей переработки реакционную смесь упаривали при пониженном давлении и сырой продукт непосредственно очищали с помощью хроматографии быстрого разрешения с использованием смеси 9:1 метиленхлорида и метанола в качестве элюента. Таким путем получили 102 мг триметиламмониевой соли трет- бутилового эфира (3SR,4RS, 5RS)-4-[4-(3-бензилоксипропокси)фенил] -3-(нафталин-2-илметокси)-5-сульфооксиметилпиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 690 (М+Н)+.
Пример 150.
Аналогично примеру 10(б) путем отщепления BOC-группы с помощью бромида цинка в метиленхлориде получали следующие соединения:
1) из трет-бутилового эфира (3SR,4RS,5RS)-4-[4-(3- бензилоксипропокси)фенил] -3-[3-(4-метилпиперазин-1- ил)пропилкарбамоилоксиметил] -5- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты получили-(3SR, 4RS, 5RS)-4-[4-(3-бензилоксипропокси)фенил] -5- (нафталин-2-илметокси)пиперидин-3-илметиловый эфир [3-(4- метилпиперазин-1-ил)пропил]карбаминовой кислоты в виде бесцветного твердого вещества; МС: 695 (М+Н)+;
2) из трет-бутилового эфира (3SR,4RS, 5RS)-4-[4- (3-бензилоксипропокси)фенил] -3-(2-морфолин-4-илэтилкарбамоилоксиметил) -5-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты получили (3SR,4RS,5RS)-4-[4-(3-бензилоксипропокси)фенил] -5-(нафталин-2- илметокси)пиперидин-3-илметиловый эфир (2-морфолин-4- илэтил)карбаминовой кислоты в виде бесцветного масла; МС: 668 (М+Н)+;
3) из трет-бутилового эфира (3SR,4RS,5RS)-4-[4-(3- бензилоксипропокси)фенил] -3-карбамоилоксиметил-5-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты получили (3SR,4RS, 5RS)-4- [4-(3-бензилоксипропокси)фенил]-5-(нафталин-2-илметокси)пиперидин-3- илметиловый эфир карбаминовой кислоты в виде бесцветного твердого вещества; МС: 555 (М+Н)+.
Использованные в качестве исходных соединений BOC-производные получали следующим образом.
(а) Смесь из 90 мг (0,15 ммоля) трет-бутилового эфира (3SR,4RS, 5RS)-4-[4-(3-бензилоксипропокси)фенил] -3-гидроксиметил-5- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты [пример 148(з)] и 60 мг (0,75 ммоля) карбоната лития в 10 мл сухого тетрагидрофурана охлаждали до 0oC. К этой смеси при охлаждении льдом по каплям добавляли раствор из 0,90 мл (1,6 ммоля) фосгена в толуоле (1,93 н.). С целью полного завершения реакции перемешивали в течение ночи при комнатной температуре. Для удаления избыточного фосгена реакционную смесь упаривали при пониженном давлении и полученный сырой эфир хлормуравьиной кислоты растворяли в 10 мл тетрагидрофурана. Эту смесь смешивали с 58 мг (0,38 ммоля) 1-(3-аминопропил)-4-метилпиперазина и затем перемешивали в течение 3 ч при комнатной температуре. Для дальнейшей переработки реакционную смесь разбавляли 40 мл метиленхлорида, а затем экстрагировали 20 мл воды. Органическую фазу сушили над сульфатом натрия и в завершение упаривали при пониженном давлении. Остаток очищали хроматографией на силикагеле с использованием смеси 95:5:0,1 метиленхлорида, метанола и аммиака в качестве элюента. Таким путем получили 85 мг (73% от теории) трет-бутилового эфира (3SR,4RS, 5RS)-4-[4-(3- бензилоксипропокси)фенил]-3-[3-(4-метилпиперазин-1-ил) пропилкарбамоилоксиметил] -5-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 795 (М+Н)+.
(б) Аналогично примеру 150(а) из трет-бутилового эфира (3SR,4RS,5RS)-4-[4-(3-бензилоксипропокси)фенил] - 3-гидроксиметил-5-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты [пример 148(з)] синтезировали соответствующий эфир хлормуравьиной кислоты, из которого взаимодействием с 4-(2- аминоэтил)морфолином получили трет-бутиловый эфир (3SR,4RS,5RS)-4- [4-(3- бензилоксипропокси) фенил] -3-(2-морфолин-4- илэтилкарбамоилоксиметил)-5-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты в виде бесцветного твердого вещества; МС: 768 (М+Н)+.
(в) Аналогично примеру 150(а) из трет-бутилового эфира (3SR,4RS,5RS)-4-[4-(3-бензилоксипропокси)фенил] -3- гидроксиметил-5-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты [пример 148(з)] синтезировали соответствующий эфир хлормуравьиной кислоты, из которого взаимодействием с раствором аммиака в тетрагидрофуране получили трет-бутиловый эфир (3SR,4RS,5RS)-4-[4-(3-бензилоксипропокси)фенил] -3- карбамоилоксиметил-5-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного твердого вещества; МС: 672 (М+Н)+.
Пример 151.
Аналогично примеру 22(м) путем отщепления BOC-группы с помощью хлористого водорода в метаноле получали следующие соединения:
1) из трет-бутилового эфира (3RS, 4RS)-4-[4-(2- бензилоксиэтоксиметил)фенил] -3-(нафталин-2-илметокси)пиперидин- 1-карбоновой кислоты получили (3RS, 4RS)-4-[4-(2- бензилоксиэтоксиметил)фенил] -3-(нафталин-2-илметокси)пиперидин в виде бесцветной пены; МС: 482 (М+Н)+;
2) из трет-бутилового эфира (3SR,4RS, 5RS)-4-[4-(2-бензилоксиэтоксиметил)фенил] -3- гидроксиметил-5-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты получили (3SR, 4RS,5RS)-[4-[4-(2-бензилоксиэтоксиметил) фенил]-5-(нафталин-2-илметокси)пиперидин-3-ил] метанол в виде бесцветного масла; МС: 512 (М+Н)+;
3) из трет-бутилового эфира (3SR,4RS, 5RS)-4-[4-(2-бензилоксиэтоксиметил)фенил] -3- метоксиметил-5-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты получили (3SR,4RS, 5RS)-4-[4-(2- бензилоксиэтоксиметил)фенил]-3-метоксиметил-5-(нафталин-2- илметокси)пиперидин в виде бесцветного масла; МС: 526 (М+Н)+;
4) из трет-бутилового эфира (3RS,4RS, 5SR)-4-[4-(2-бензилоксиэтоксиметил)фенил]-3- (нафталин-2-илметокси)-5-(пиридин-3-илметоксиметил)пиперидин-1- карбоновой кислоты получили (3SR,4RS,5RS)-3-[4-[4- (2-бензилоксиэтоксиметил)фенил] -5-(нафталин-2-илметокси)пиперидин-3- илметоксиметил]пиридин в виде бесцветного масла; МС: 603 (М+Н)+;
5) из трет-бутилового эфира (3SR,4RS, 5RS)-4-[4-(2-бензилоксиэтоксиметил)фенил] -3-(2- метоксиэтоксиметил)-5-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты получили (3SR, 4RS, 5RS)-4-[4-(2- бензилоксиэтоксиметил)фенил] -3-(2-метоксиэтоксиметил)-5- (нафталин-2-илметокси)пиперидин в виде бесцветного масла; МС: 570 (М+Н)+;
6) из смеси трет-бутилового эфира (3RS,4RS,5SR)- и (3SR,4SR, 5RS)-4-[4-(2-бензилоксиэтоксиметил)фенил] -3-(нафталин-2- илметокси)-5-[3-[(RS)-тетрагидропиран-2-илокси] пропоксиметил] пиперидин-1-карбоновой кислоты при одновременном отщеплении ТГП- группы получили (3SR,4RS,5RS)-3-[4-[4-(2-бензилоксиэтоксиметил)фенил] -5-(нафталин-2-илметокси)пиперидин-3-илметокси] пропан-1-ол в виде бесцветного масла; МС: 570 (М+Н)+;
7) из трет-бутилового эфира (3SR,4RS,5RS)-3-метоксиметил-4-{4- [(метилфенилкарбамоилокси)метил] фенил}-5-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты получили (3SR,4RS, 5RS)-4-[3- метоксиметил-5-(нафталин-2-илметокси)пиперидин-4-ил] бензиловый эфир метилфенилкарбаминовой кислоты в виде бесцветного масла; МС: 525 (М+Н)+;
8) из трет-бутилового эфира (3SR,4RS,5RS)-4-[4- [(бензилметилкарбамоилокси)метил] фенил]-3-метоксиметил-5- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты получили (3SR,4RS, 5RS)-4-[3-метоксиметил-5- (нафталин- 2-илметокси)пиперидин-4-ил] бензиловый эфир бензилметилкарбаминовой кислоты в виде бесцветного масла; МС: 539 (М+Н)+.
Использованные в качестве исходных веществ BOC-производные получали следующим образом.
(а) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS, 4RS)-4-(4-гидроксиметилфенил)-3-(нафталин-2-илметокси) пиперидин-1-карбоновой кислоты [пример 22(к)] 2-(бензилокси)этилиодидом [Helv.Chim. Acta, т. 71 (1988), 2039] получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(2-бензилоксиэтоксиметил) фенил] -3-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветной пены; МС: 599 (M+NH4)+.
(б) Аналогично примеру 22(г) из (3RS,4RS,5SR)-1-бензил-4- (4-бромфенил)-5-гидроксиметилпиперидин-3-ола [пример 68(д)] путем катализируемого палладием карбонилирования с помощью моноксида углерода в метаноле получили метиловый эфир (3RS,4RS,5SR)-4-(1-бензил-3-гидрокси-5-гидроксиметилпиперидин-4- ил)бензойной кислоты, из которого гидрогенолизом в присутствии палладия (5%-ного) на угле при атмосферном давлении в метаноле аналогично примеру 2(д) получили метиловый эфир 4-(3-гидрокси-5- гидроксиметилпиперидин-4-ил)бензойной кислоты. Последующим введением BOC-группы аналогично примеру 1(е) получили трет- бутиловый эфир (3RS,4RS,5SR)-3-гидрокси-5-гидроксиметил-4-(4- метоксикарбонилфенил)пиперидин-1-карбоновой кислоты, из которого взаимодействием с трифенилхлорметаном аналогично примеру 68(и) получили трет-бутиловый эфир (3RS,4RS,5SR)-3-гидрокси-4-(4- метоксикарбонилфенил)-5-тритилоксиметилпиперидин-1-карбоновой кислоты. В результате дальнейшего алкилирования с помощью 2- бромметилнафталина аналогично примеру 1(ж) был получен трет- бутиловый эфир (3RS,4RS,5SR)-4-(4-метоксикарбонилфенил)-3- (нафталин-2-илметокси)-5-тритилоксиметилпиперидин-1-карбоновой кислоты, из которого восстановлением борoгидридом лития аналогично примеру 22(д) получили трет-бутиловый эфир (ЗRS,4RS, 5SR)-4-(4- гидpoкcимeтилфeнил)-3-(нафталин-2-илметокси)-5- тритилоксиметилпиперидин-1-карбоновой кислоты в виде бесцветной пены; МС: 737 (M+NH4)+. Путем последующего алкилирования 2-(бензилокси)этилиодидом [Helv. Chim. Acta, т. 71 (1988), 2039] аналогично примеру 1(ж) получили трет-бутиловый эфир (3RS,4RS,5SR)-4-[4-(2-бензилоксиэтоксиметил)фенил] -3-(нафталин- 2-илметокси)-5-тритилоксиметилпиперидин-1-карбоновой кислоты, из которого после отщепления тритильной группы с помощью смеси трифторуксусной кислоты и ангидрида трифторуксусной кислоты в метиленхлориде аналогично примеру 86(х) был получен трет-бутиловый эфир (3SR, 4RS, 5RS)-4-[4-(2-бензилоксиэтоксиметил)фенил]-3-гидроксиметил-5-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 629 (M+NH4)+.
(в) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3SR, 4RS, 5RS)-4-[4-(2-бензилоксиэтоксиметил)фенил] -3-гидроксиметил-5-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты метилиодидом получили трет-бутиловый эфир (3SR,4RS, 5RS)-4-[4-(2-бензилоксиэтоксиметил)фенил] -3-метоксиметил-5-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 643 (M+NH4)+.
(г) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3SR, 4RS, 5RS)-4-[4-(2-бензилоксиэтоксиметил)фенил] -3- гидроксиметил-5-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты 3-(хлорметил)пиридином получили трет-бутиловый эфир (3RS, 4RS, 5SR)-4-[4-(2-бензилоксиэтоксиметил)фенил]-3-(нафталин- 2-илметокси)-5-(пиридин-3-илметоксиметил)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 703 (М+Н)+.
(д) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3SR, 4RS, 5RS)-4-[4-(2-бензилоксиэтоксиметил)фенил] -3- гидроксиметил-5-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты 2-метоксиэтилбромидом получили трет-бутиловый эфир (3SR, 4RS, 5RS)-4-[4-(2-бензилоксиэтоксиметил)фенил] -3-(2- метоксиэтоксиметил)-5-(нафталин-2-илметокси)пиперидин-1- карбоновой кислоты в виде бесцветного масла; МС: 687 (M+NH4)+.
(е) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3SR, 4RS, 5RS)-4-[4-(2-бензилоксиэтоксиметил)фенил] -3- гидроксиметил-5-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты рац.-2-(3-бромпропокси) тетрагидро-2H-пираном [J.Org.Chem. 53, (1988), 25, 5903-5908] получили смесь трет-бутилового эфира (3RS, 4RS,5SR)- и (3SR,4RS,5RS)-4-[4-(2-бензилоксиэтоксиметил)фенил] -3-(нафталин- 2-илметокси)-5-[3-[(RS)-тетрагидропиран-2-илокси] пропоксиметил] пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 771 (M+NH4)+.
(ж) Аналогично примеру 24(н) в результате взаимодействия трет-бутилового эфира (3RS, 4RS,5SR)-4-(4-гидроксиметилфенил)-3- (нафталин-2-илметокси)-5-тритилоксиметилпиперидин-1-карбоновой кислоты с фенилизоцианатом был получен трет-бутиловый эфир (3RS,4RS,5SR)-3- (нафталин-2-илметокси)-4-(4-фенилкарбамоилоксиметилфенил)-5- тритилоксиметилпиперидин-1-карбоновой кислоты, из которого после отщепления тритильной группы с помощью смеси трифторуксусной кислоты и ангидрида трифторуксусной кислоты в метиленхлориде аналогично примеру 86(х) получили трет-бутиловый эфир (3SR,4RS, 5RS)-3-гидроксиметил-5-(нафталин-2-илметокси)-4-(4- фенилкарбамоилоксиметилфенил)пиперидин-1-карбоновой кислоты. Путем последующего алкилирования метилиодидом аналогично примеру 1(ж) получили трет-бутиловый эфир (3SR,4RS,5RS)-3-метоксиметил-4- { 4-[(метилфенилкарбамоилокси)метил]фенил)-5-(нафталин-2- илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 642 (M+NH4)+.
(з) Аналогично примеру 24(н) в результате взаимодействия трет-бутилового эфира (3RS, 4RS, 5SR)-4- (4-гидроксиметилфенил)-3-(нафталин-2-илметокси)-5- тритилоксиметилпиперидин-1-карбоновой кислоты с бензилизоцианатом был получен трет-бутиловый эфир (3RS,4RS, 5SR)-4-(4- бензилкарбамоилоксиметилфенил)-3-(нафталин-2-илметокси)-5- тритилоксиметилпиперидин-1-карбоновой кислоты, из которого после отщепления тритильной группы с помощью смеси трифторуксусной кислоты и ангидрида трифторуксусной кислоты в метиленхлориде аналогично примеру 86(х) получили трет-бутиловый эфир (3SR,4RS, 5RS)-4-(4-бензилкарбамоилоксиметилфенил)-3- гидроксиметил-5-(нафталин-2-илметокси)пиперидин-1-карбоновой кислоты. Путем последующего алкилирования метилиодидом аналогично примеру 1(ж) получили трет-бутиловый эфир (3SR,4RS, 5RS)-4-[4- [(бензилметилкарбамоилокси)метил] фенил] -3-метоксиметил-5- (нафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 656 (M+NH4)+.
Пример 152.
Путем отщепления BOC-группы с помощью бромида цинка в метиленхлориде получали следующие соединения:
1) из трет-бутилового эфира (3RS,4RS)-4-(4-фторфенил)-3-(4- метилсульфанилбензилокси)пиперидин-1-карбоновой кислоты получили (3RS,4RS)-4-(4-фторфенил)-3-(4-метилсульфанилбензилокси) пиперидин в виде желтоватого масла; МС: 332 (М+Н)+;
2) из смеси трет-бутилового эфира (3RS,4RS)- и (3SR,4SR)-4- (4-фторфенил)-3-[(RS)-4-метансульфинилбензилокси)пиперидин-1-карбоновой кислоты получили смесь (3RS, 4RS)- и (3SR,4SR)-4-(4-фторфенил)-3-[(RS)- 4-метилсульфинилбензилокси)пиперидина в виде желтоватого масла; МС: 348 (М+Н)+;
3) из трет-бутилового эфира (3RS,4RS)-4-(4-фторфенил)-3-(4-метилсульфонилбензилокси) пиперидин-1-карбоновой кислоты получили гидробромид (3RS, 4RS)-4-(4-фторфенил)-3-(4-метилсульфонилбензилокси)пиперидина в виде желтоватого твердого вещества; МС: 364 (М+Н)+;
4) из трет-бутилового эфира (3RS,4RS)-3-(1,4-диметоксинафталин-2- илметокси)-4-(4-гидроксифенил)пиперидин-1-карбоновой кислоты получили (3RS, 4RS)-4-[3-(1,4-диметоксинафталин-2-илметокси)пиперидин-4-ил] фенол в виде бесцветного твердого вещества; МС: 394 (М+Н)+;
5) из трет-бутилового эфира (3RS,4RS)-4-[4-(3-циaнoбeнзилoкcи) фeнил-] -3-(1,4-диметоксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты с помощью бромида цинка получили (3RS,4RS)-3-[4-[3-(1, 4- димeтoкcинaфтaлин-2-илметокси)пиперидин-4-ил] феноксиметил] бензонитрил в виде бесцветного твердого вещества; МС: 509 (М+Н)+.
Использованные в качестве исходных соединений BOC-производные получали следующим образом.
(а) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS, 4RS)-4-(4-фторфенил)-3-гидроксипиперидин-1-карбоновой кислоты [пример 3(б)] 4-метилтиобензилхлоридом [J.Org.Chem. (1988), 53(3), 561-569] получили трет-бутиловый эфир (3RS, 4RS)-4-(4-фторфенил)-3-(4-метилсульфанилбензилокси) пиперидин-1-карбоновой кислоты в виде бесцветного масла; МС: 432 (М+Н)+.
(б) Аналогично примеру 58(и) путем окисления трет-бутилового эфира (3RS, 4RS)-4-(4-фторфенил)-3-(4-метилсульфанилбензилокси) пиперидин-1-карбоновой кислоты с помощью метапериодата натрия получили смесь трет-бутилового эфира (3RS, 4RS)- и (3SR, 4SR)-4-(4- фторфенил)-3-[(RS)-4-метансульфинилбензилокси)пиперидин-1- карбоновой кислоты в виде желтоватого масла; МС: 448 (М+Н)+.
(в) К раствору из 115 мг (0,27 ммоля) трет-бутилового эфира (3RS,4RS)-4-(4-фторфенил)-3-(4-метилсульфанилбензилокси) пиперидин-1-карбоновой кислоты в 2 мл метиленхлорида добавляли 126 мг (0,586 ммоля) м-хлорпербензойной кислоты (80%-ной). Реакционный раствор перемешивали в течение 2 ч при комнатной температуре, а затем нейтрализовали карбонатом калия в метаноле. Далее раствор разбавляли метиленхлоридом. После этого перерабатывали обычным образом и полученный сырой продукт очищали хроматографией на силикагеле с использованием смеси 4:1 метиленхлорида и простого эфира в качестве элюента. Таким путем получили 105 мг (85% от теории) трет-бутилового эфира (3RS, 4RS)-4-(4-фторфенил)-3-(4- метилсульфонилбензилокси) пиперидин-1-карбоновой кислоты в виде бесцветного вязкого масла; МС: 464 (М+Н)+.
(г) (α) Аналогично примеру 1(ж) путем алкилирования трет-бутилового эфира (3RS,4RS)- 4-(4-аллилоксифенил)-3-гидроксипиперидин-1-карбоновой кислоты [пример 86(б)] 2-хлорметил-1, 4-диметоксинафталином [J.Org.Chem. (1983), 48(19), 3265-3268] получили трет-бутиловый эфир (3RS,4RS)- 4-(4-аллилоксифенил)-3-(1,4-диметоксинафталин-2-илметокси) пиперидин-1-карбоновой кислоты в виде светло-желтого твердого вещества; МС: 534 (М+Н)+.
(β) Раствор из 315 мг (0,59 ммоля) трет-бутилового эфира (3RS,4RS)-4-(4-аллилоксифенил)-3-(1, 4-диметоксинафталин-2- илметокси)пиперидин-1-карбоновой кислоты, 44 мг (0,059 ммоля) бис(трифенилфосфин)палладий(II)диацетата и 132 мг (1,18 ммоля) 1,4-диазабицикло[2,2,2] октана в 10 мл 95%-ного этанола в течение 2 ч нагревали с обратным холодильником в атмосфере аргона. Далее реакционную смесь охлаждали до 0-5oC и смешивали с 0,6 мл 1 н. соляной кислоты. После этого растворитель отгоняли при пониженном давлении и остаток распределяли между уксусным эфиром и водой. После экстракции и сушки органической фазы над сульфатом натрия упаривали при пониженном давлении. Остаток очищали на силикагеле с использованием смеси 9:1 метиленхлорида и простого эфира в качестве элюента. Таким путем получили 265 мг (91% от теории) трет-бутилового эфира (3RS, 4RS)-3-(1, 4-диметоксинафталин-2- илметокси)-4-(4-гидроксифенил)пиперидин-1-карбоновой кислоты в виде желтоватой пены; МС: 494 (М+Н)+.
(д) Аналогично примеру 44(д) путем алкилирования трет-бутилового эфира (3RS, 4RS)-3-(1,4-диметоксинафталин-2-илметокси)-4-(4-гидроксифенил) пиперидин-1-карбоновой кислоты 3-бромметилбензонитрилом получили трет-бутиловый эфир (3RS, 4RS)-4-[4-(3-цианобензилокси)фенил]-3-(1,4- диметоксинафталин-2-илметокси)пиперидин-1-карбоновой кислоты в виде бежевого твердого вещества; МС: 609 (М+Н)+.
Пример 153.
Раствор из 736 мг (1,28 ммоля) (3R,4R)-4-(4-бромфенил)-3-(нафталин-2-илметокси)-1- [(1S,4R)-4,7,7-триметил-3-оксо-2-оксабицикло[2,2,1]гептан-1-карбонил] пиперидина в 32 мл абсолютного тетрагидрофурана охлаждали до -70oC. После этого по каплям добавляли раствор из 1,86 мл (6,5 ммоля) дигидробис(2-метоксиэтокси)алюмината натрия (70%-ного в толуоле, примерно 3,5 М) в 32 мл тетрагидрофурана. Смесь нагревали до -40oC, затем в течение 8 ч перемешивали при -40oC, после этого охлаждали до -78oC и смешивали, добавляя по каплям, с раствором из 0,5 мл ледяной уксусной кислоты в 10 мл тетрагидрофурана. Для дальнейшей переработки реакционную смесь распределяли между 200 мл уксусного эфира и 200 мл водного 5%-ного раствора гидрокарбоната натрия. Органическую фазу отделяли, а водную фазу трижды экстрагировали уксусным эфиром порциями по 50 мл. Объединенные органические фазы сушили над сульфатом магния и в завершение отгоняли растворитель при пониженном давлении. Сырой продукт (800 мг) очищали хроматографией на силикагеле с использованием смеси 9:1 метиленхлорида и метанола в качестве элюента. Таким путем получили 344 мг (68% от теории) (3R, 4R)-4-(4-бромфенил)-3-(нафталин-2- илметокси)пиперидина в виде бесцветного твердого вещества; МС: 396, 398 (М+Н)+.
Использованное в качестве исходной субстанции производное камфановой кислоты получали следующим образом.
Раствор из 1,98 г (5,00 ммоля) (3RS,4RS)-4-(4-бромфенил)-3-(нафталин-2-илметокси) пиперидина [пример 2.6] в 20 мл метиленхлорида охлаждали до 0oC и смешивали с 0,84 мл (0,61 г, 6,0 ммолей) триэтиламина. После этого в атмосфере аргона при 0oC по каплям добавляли раствор из 1,19 г (5,5 ммоля) хлорангидрида (-)-(1S,4R)-камфановой кислоты в 20 мл метиленхлорида и далее перемешивали в течение 30 мин при 0oC, а затем в течение 2 ч при комнатной температуре. Для дальнейшей переработки реакционную смесь распределяли между 200 мл метиленхлорида и 200 мл ледяной воды. Органическую фазу отделяли, а водную фазу трижды экстрагировали уксусным эфиром порциями по 50 мл. Объединенные органические фазы сушили над сульфатом магния и в завершение отгоняли растворитель при пониженном давлении. Сырую смесь изомеров (2,89 г) разделяли хроматографией на силикагеле с использованием смеси 2:3 уксусного эфира и гексана в качестве элюента. Таким путем получили 1,14 г (40% от теории) (3R, 4R)-4-(4-бромфенил)-3-(нафталин-2-илметокси)- 1-[(1S, 4R)-4,7, 7-триметил-3-оксо-2-оксабицикло[2,2,1] гептан-1- карбонил] пиперидина [МС: 575, 577 (М)+] и 1,01 г (35% от теории) (3S,4S)-4-(4-бромфенил)-3-(нафталин-2-илметокси)-1-[(1S, 4R)-4,7, 7- триметил-3-оксо-2-оксабицикло [2.2.1] гептан-1-карбонил] пиперидина [МС: 575, 577 (М)+], в каждом случае в виде бесцветного твердого вещества.
Пример 154.
Аналогично предыдущему примеру путем восстановительного отщепления камфанильного остатка получали следующие соединения:
1) из (3S, 4S)-4-(4-бромфенил)-3-(нафталин-2- илметокси)-1-[(1S,4R)-4,7,7-триметил-3-оксо-2-оксабицикло[2,2,1] гептан-1-карбонил] пиперидина получили (3S,4S)-4-(4-бромфенил)-3-(нафталин-2-илметокси) пиперидин в виде бесцветного твердого вещества; МС: 396, 398 (М+Н)+;
2) из (3R, 4R)-4-(4-хлорфенил)-3-(4-метоксибензилокси)-1- [(1S, 4R)-4,7,7-триметил-3-оксо-2-оксабицикло[2,2,1] гептан-1- карбонил] пиперидина получили (3R, 4R)-4-(4-хлорфенил)-3-(4- метоксибензилокси) пиперидин в виде бесцветного твердого вещества; МС: 332, 334 (М+Н)+;
3) из (3S, 4S)-4-(4-хлорфенил)-3-(4-метоксибензилокси)-1- [(1S, 4R)-4,7,7-триметил-3-оксо-2-оксабицикло[2,2,1] гептан-1-карбонил] пиперидина получили (3S, 4S)-4-(4-хлорфенил)-3-(4-метоксибензилокси) пиперидин в виде бесцветного твердого вещества; МС: 332, 334 (М+Н)+;
4) из (3R, 4R)-4-нафталин-1-ил-3-(нафталин-2-илметокси)-1- [(1S,4R)-4,7,7-триметил-3-оксо-2-оксабицикло[2,2,1] гептан-1-карбонил] пиперидина получили (3R, 4R)-4-нафталин-1-ил-3-(нафталин-2-илметокси) пиперидин в виде бесцветного твердого вещества; МС: 368 (М+Н)+;
5) из (3S, 4S)-4-нафталин-1-ил-3-(нафталин-2-илметокси)-1- [(1S,4R)-4,7,7-триметил-3-оксо-2-оксабицикло[2,2,1] гептан-1-карбонил] пиперидина получили (3S, 4S)-4-нафталин -1-ил-3-(нафталин-2-илметокси) пиперидин в виде бесцветного твердого вещества; МС: 368 (М+Н)+;
6) из (3R,4R)-3-(4-бензилоксинафталин-2-илметокси)-4- (4-фторфенил)-1-[(1S, 4R)-4,7,7-триметил-3-оксо-2-оксабицикло[2, 2,1]гептан-1-карбонил] пиперидина получили (3R,4R)-3-(4- бензилоксинафталин-2-илметокси)-4-(4-фторфенил)пиперидин в виде бесцветного твердого вещества; МС: 441 (М)+;
7) из (3S,4S)-3-(4-бензилоксинафталин-2-илметокси)-4-(4-фторфенил) -1-[(1S,4R)-4,7,7-триметил-3-оксо-2-оксабицикло[2,2,1]гептан-1-карбонил] пиперидина получили (3S, 4S)-3-(4-бензилоксинафталин-2-илметокси)- 4-(4-фторфенил)пиперидин в виде бесцветного твердого вещества; МС: 441 (М)+.
Аналогично предыдущему примеру путем ацилирования хлорангидридом (-)-камфановой кислоты получали следующие производные:
(а) из (3RS,4RS)-4-(4-хлорфенил)-3-(4-метоксибензилокси)пиперидина [был синтезирован аналогично методике, описанной в примерах 1 и 2 для (3RS, 4RS)-3-(4-метоксибензилокси)-4-п-толилпиперидина (пример 2.4)] получили (3R, 4R)-4-(4-хлорфенил)-3-(4-метоксибензилокси)-1- [(1S, 4R)-4,7, 7-триметил-3-оксо-2-оксабицикло[2,2,1]гептан-1- карбонил] пиперидин [MC: 511, 513 (М)+] и (3S, 4S)-4-(4- хлорфенил)-3-(4-метоксибензилокси)-1-[(1S, 4R)-4,7, 7-триметил-3- оксо-2-оксабицикло[2,2,1] гептан-1-карбонил] пиперидин [MC: 511, 513 (M)+] в каждом случае в виде бесцветного твердого вещества;
(б) из (3RS, 4RS)-4-нафталин-1-ил-3-(нафталин-2-илметокси) пиперидина (пример 2.12) получили (3R,4R)-4-нафталин-1-ил-3-(нафталин-2-илметокси)-1- [(1S, 4R)-4,7,7-триметил-3-оксо-2-оксабицикло[2,2,1] гептан-1-карбонил] пиперидин [MC: 547 (M)+] и (3S,4S)-4-нaфтaлин-1-ил-3-(нaфтaлин-2-илметокси)-1- [(1S, 4R)-4,7,7-триметил-3-оксо-2-оксабицикло[2,2,1] гептан-1-карбонил] пиперидин [MC: 547 (M)+] в каждом случае в виде бесцветной пены;
(в) из (3RS, 4RS)-3-(4-бензилоксинафталин-2-илметокси)-4-(4-фторфенил) пиперидина (пример 14.13) получили (3R, 4R)-3-(4-бензилоксинафталин-2-илметокси)-4-(4-фторфенил)-1- [(1S, 4R)-4,7,7-триметил-3-оксо-2-оксабицикло[2,2,1] гептан-1-карбонил] пиперидин [MC: 621 (M)+], и (3S, 4S)-3-(4- бензилоксинафталин-2-илметокси)-4-(4-фторфенил)-1-[(1S, 4R)- 4,7,7-триметил-3-оксо-2-оксабицикло[2,2,1] гептан-1-карбонил] пиперидин [MC: 621 (M)+] в каждом случае в виде бесцветной пены.
Пример А.
Водная суспензия для орального применения.
Состав:
Соединение формулы I, например (3RS, 4RS)-4-[4-(3- бензилоксипропокси)фенил]-3-(нафталин-2-илметокси) пиперидин микронизированный - 5,0 г
Полисорбат 80 - 0,3 г
Гидроксипропилметилцеллюлоза - 1,0 г
Вкусовая добавка - q.s.
Метилпарабен - 0,2 г
Пропиленпарабен - 0,04 г
Вода - до 100,0 мл
Пример Б.
Таблетки.
Состав:
1) Соединение формулы I, например (3RS,4RS)-4-[4- (3-бензилоксипропокси)фенил]-3-(нафталин-2-илметокси) пиперидин - 200 мг
2) Молочный сахар безводный - 160 мг
3) Гидроксипропилметилцеллюлоза - 18 мг
4) Натрийкарбоксиметилцеллюлоза - 20 мг
5) Стеарат магния - 2 мг
Масса таблетки - 400 мг
Приготовление. Компоненты 1) и 2) интенсивно перемешивают. Смесь затем увлажняют водным раствором компонента 3) и месят, образовавшуюся массу гранулируют, сушат и просеивают. Гранулят смешивают с компонентами 4) и 5) и прессуют в таблетки соответствующего размера.
Пример В.
Капсулы.
Состав:
1) Соединение формулы I, например (3RS,4RS)-4-[4- (3-бензилоксипропокси)фенил]-3-(нафталин-2-илметокси) пиперидин - 200 мг
2) Молочный сахар безводный - 160 мг
3) Гидроксипропилметилцеллюлоза - 18 мг
4) Натрийкарбоксиметилцеллюлоза - 20 мг
5) Стеарат магния - 2 мг
Масса для заполнения капсулы. - 400 мг
Приготовление. Компоненты 1) и 2) интенсивно перемешивают. Смесь затем увлажняют водным раствором компонента 3) и месят, образовавшуюся массу гранулируют, сушат и просеивают. Гранулят смешивают с компонентами 4) и 5) и смесью заполняют капсулы соответствующего размера.
Пример Г.
Раствор для инъекций.
Состав:
Соединение формулы I, например гидрохлорид 4-[2-[7- [(3RS, 4RS)-4-[4-(3-бензилоксипропокси)фенил]пиперидин-3- илоксиметил]нафталин-2-илокси]этил] морфолина (1:2) - 3 мг
D-Маннит, свободный от пирогена - 10 мг
Вода для инъекций - До 1,0 мл
Приготовление. Действующее вещество и маннит растворяют в газированной азотом воде и далее стерилизуют одним из известных способов.
Пример Д.
Раствор для инъекций в виде смешанного мицеллярного раствора.
Состав:
Соединение формулы I, например (3RS, 4RS)-4-[4-(3- бензилоксипропокси)фенил]-3-(нафталин-2-илметокси)пиперидин - 2,0 мг
Гликохолат натрия - 98,5 мг
Соевый лецитин - 158,2 мг
Na-Дигидрофосфат - 1,8мг
Ди-Na-гидpoфocфaт - 9,5 мг
Вода для инъекций - До 1,0 мл
Приготовление. Соединение формулы I, Na-гликохолат, а также соевый лецитин растворяют в необходимом количестве этанола (либо адекватного летучего растворителя). Растворитель выпаривают при пониженном давлении и слабом нагревании. Полученный остаток с помощью забуференной водной фазы переводят в раствор. Этот раствор обрабатывают далее по известным методам.
Реферат
Изобретение относится к новым производным пиперидина ф-лы (I), где R1 - арил, гетероциклил, R2 - фенил, нафтил, аценафтил, циклогексил, пиридил, пиримидинил, пиразинил, оксопиридинил, диазинил, триазолил, тиенил, оксазолил, оксадиазолил, тиазолил, пирролил или фурил, которые могут быть замещены галогеном, гидрокси, циано, CF3, алкилом, R3-H, гидрокси, алкокси, алкенилокси, R4-Н, алкил, алкенил, алкокси, бензил, оксо, Q - этилен или отсутствует, Х - связь, кислород, сера, W - кислород или сера, Z - алкилен, алкенилен, -О, -S; n = 1, m = 0 или 1. Соединения формулы (I) обладают ингибирующей по отношению к ренину активностью и могут найти применение в медицине. Описываются промежуточные соединения ф-лы (II, где R1 обозначает защитную группу, а остальные символы имеют значения, указанные для соединений ф-лы (I). 5 н.п. ф-лы, 19 з.п. ф-лы. 1 табл.
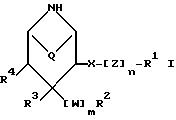
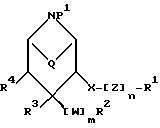
Формула

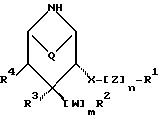

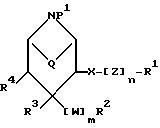
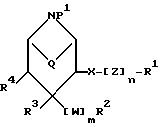

Комментарии