Карбоксамидные соединения и их применение в качестве ингибиторов кальпаина - RU2540856C2
Код документа: RU2540856C2
Описание
Настоящее изобретение относится к новым карбоксамидным соединениям и их применению для производства лекарственного средства. Карбоксамидные соединения являются ингибиторами кальпаина (кальций-зависимых цистеинпротеаз). Следовательно, изобретение также относится к применению таких карбоксамидных соединений для лечения расстройства, ассоциированного с повышенной активностью кальпаина.
Кальпаины представляют собой внутриклеточные, протеолитические ферменты из группы цистеинпротеаз и обнаружены во многих клетках. Фермент кальпаин активируется повышенными концентрациями кальция, при этом существует различие между кальпаином I или μ-кальпаином, который активируется микромолярными концентрациями ионов кальция, и кальпаином II или m-кальпаином, который активируется миллимолярными концентрациями ионов кальция. Кроме того, в настоящее время также утверждается существование кальпаиновых изоферментов (M.E. Saez et al., Drug Discovery Today 2006, 11 (19/20), pp. 917-923; K. Suzuki et al., Biol. Chem. Hoppe-Seyler 1995, 376 (9), pp. 523-529).
Кальпаины играют важную роль в различных физиологических процессах. Такие процессы включают расщепление различных регуляторных белков, таких как протеинкиназа C, белков цитоскелета, таких как MAP 2 и спектрин, и мышечных белков, деградацию белков при ревматоидном артрите, белков при активации тромбоцитов, метаболизме нейропептидов, белков при митозе и других процессах, которые перечислены в публикациях: M.J. Barrett et al., Life Sci. 1991, 48, pp. 1659-69; K. Wang et al., Trends in Pharmacol. Sci. 1994, 15, pp. 412-419.
Повышенные уровни кальпаина были обнаружены при различных патофизиологических процессах, например: при ишемиях сердца (например, инфаркте миокарда), почек, легкого, печени или центральной нервной системы (например, при ударе), при воспалениях, мышечных дистрофиях, катаракте глаз, диабете, расстройствах у ВИЧ-инфицированных, травмах центральной нервной системы (например, при травме головного мозга), при болезнях Альцгеймера, Гентингтона, Паркинсона, рассеянном склерозе и т.д. (см. выше публикацию K.K. Wang) и инфекционных заболеваниях, таких как малярия (I.M. Medana et al., Neuropath. and Appl. Neurobiol. 2007, 33, pp. 179-192). Считается, что существует связь между указанными заболеваниями и обычными или персистентно повышенными внутриклеточными уровнями кальция. Она приводит к кальций-зависимым процессам, которые становятся гиперактивированными и долгое время не поддаются обычному физиологическому контролю. Соответствующая гиперактивация кальпаинов также может инициировать патофизиологические процессы.
По этой причине было утверждено, что ингибиторы кальпаина могут применяться для лечения таких заболеваний. Данный постулат был подтвержден рядом исследований. Так в публикациях Seung-Chyul Hong et al., Stroke 1994, 25 (3), pp. 663-669 и R.T. Bartus et al., Neurological Res. 1995, 17, pp. 249-258 показано, что ингибитор кальпаина обладает нейропротективным эффектом при острых нейродегенеративных нарушениях или ишемиях, которые происходят в результате церебрального удара. В публикации K.E. Saatman et al., Proc. Natl. Acad. Sci. USA 1996, 93, pp. 3428-3433 описано, что после экспериментальной травмы головного мозга ингибитор кальпаина также улучшал излечение от функциональных нарушений памяти и нейромоторных нарушений. В публикации C.L. Edelstein et al., Proc. Natl. Acad. Sci. USA 1995, 92, pp. 7662-6, обнаружено, что ингибитор кальпаина обладает защитным эффектом при гипоксическом повреждении почек. В публикации Yoshida, Ken Ischi et al., Jap. Circ. J., 1995, 59 (1), pp. 40-48 отмечено, что ингибитор кальпаина обладал благоприятными эффектами после сердечного нарушения, которое было вызвано ишемией или реперфузией. Ингибитор кальпаина BDA-410 замедлял развитие малярийной инфекции при моделировании патогенеза малярии на мышах, как показано в публикации X. Li et al., Mol. Biochem. Parasitol., 2007, 155 (1), pp. 26-32.
Более современные исследования на кальпастатин-трансгенных животных показали, что экспрессия природного ингибитора кальпаина в значительной степени ослабляет патофизиологические эффекты активированного кальпаина при экспериментальном гломерулонефрите, как показано в публикации J. Peltier et al., J. Am. Soc. Nephrol. 2006, 17, pp. 3415-3423; при сердечно-сосудистом ремоделировании при гипертензии, индуцированной ангиотензином II, при нарушенной синаптической трансмиссии при конгенитальном миастеническом синдроме медленных каналов, как показано в публикации J.S. Groshong et al., J. Clin. Invest. 2007, 117 (10), pp. 2903-2912; при эксайтотоксичной фрагментации ДНК через митохондриальные пути, как показано в публикации J. Takano et al., J. Biol. Chem. 2005, 280 (16), pp. 16175-16184; и при некротических процессах в дистрофичных мышцах, как показано в публикации M.J. Spencer et al., Hum. Mol. Gen. 2002, 11 (21), pp. 2645-2655.
В последние годы было показано, что как функция, так и метаболизм ряда важных белков, вовлеченных в развитие болезни Альцгеймера, модулируются кальпаином. Различные внешние воздействия, например, такие как эксайтотоксины, оксидативный стресс или иное действие амилоидного белка, приводят к гиперактивации кальпаина в нервной клетке, вызывая в виде каскада дисрегуляцию CNS-специфической киназы cdk5 и последующее гиперфосфорилирование так называемого тау-белка. Принимая во внимание, что фактическое назначение тау-белка заключается в стабилизации микротрубочек и, следовательно, цитоскелета, фосфорилированный тау-белок больше не способен выполнять указанную функцию; происходит коллапс цитоскелета, аксональный транспорт вещества нарушается и поэтому в результате нервная клетка деградирует (G. Patrick et al., Nature 1999, 402, pp. 615-622; E.A. Monaco et al., Curr. Alzheimer Res. 2004, 1 (1), pp. 33-38). Накопление фосфорилированного тау-белка дополнительно приводит к образованию так называемых нейрофибриллярных клубков (NFT), которые вместе с хорошо известными амилоидными бляшками, представляют собой патологический отличительный признак болезни Альцгеймера. Аналогичные изменения тау-белка, обычно определяемые как важный отличительный признак таупатий, также наблюдаются при других (нейро)дегенеративных расстройствах, например, таких как расстройства, сопровождающие удар, при воспалениях головного мозга, паркинсонизме, нормотензивной гидроцефалии и болезни Крейцфельдта-Якоба.
Вовлеченность кальпаина в нейродегенеративные процессы была продемонстрирована на трансгенных мышах с помощью кальпастатина, специфического и природного ингибитора кальпаинов (Higuchi et al.; J. Biol. Chem. 2005, 280 (15), pp. 15229-15237). С помощью ингибитора кальпаина можно было заметно уменьшить клинические симптомы острого аутоиммунного энцефаломиелита при моделировании рассеянного склероза на мышах (F. Mokhtarian et al.; J. Neuroimmunology 2006, 180, pp. 135-146). Дополнительно было показано, что ингибиторы кальпаина, с одной стороны, блокируют Aβ-индуцированную дегенерацию нейронов (Park et al.; J. Neurosci. 2005, 25, pp. 5365-5375) и, кроме того, уменьшают высвобождение предшественника β-амилоидного белка (β-APP) (J. Higaki et al., Neuron 1995, 14, pp. 651-659). При таком уровне техники ингибиторы кальпаина, обладающие достаточной доступностью для ЦНС, представляют собой новую терапевтическую основу для лечения в общем случае нейродегенеративных расстройств, а также, в частности, болезни Альцгеймера.
Аналогичным образом ингибиторы кальпаина ингибируют высвобождение интерлейкина-1α (N. Watanabe et al., Cytokine 1994, 6(6), pp. 597-601). Дополнительно было обнаружено, что ингибиторы кальпаина проявляют цитотоксические эффекты в отношении клеток опухоли (E. Shiba et al. 20th Meeting Int. Ass. Breast Cancer Res., Sendai Jp., 1994, 25-28. Sept., Int. J. Oncol. S(Suppl), 1994, 381).
Совсем недавно была показана вовлеченность кальпаина в расстройства ВИЧ-инфицированных. Так было продемонстрировано, что ВИЧ-индуцированная нейротоксичность опосредована кальпаином (O'Donnell et al., J. Neurosci. 2006, 26 (3), pp. 981-990). Также была показана вовлеченность кальпаина в репликацию вируса ВИЧ (Teranishi et al.; Biochem. Biophys. Res. Comm. 2003, 303 (3), pp. 940-946).
Современные исследования свидетельствуют о том, что кальпаин играет роль в так называемой ноцицепции, восприятии боли. Ингибиторы кальпаина показали определенно благоприятный эффект на различных доклинических релевантных моделях боли, например, при термически индуцированной гипералгезии у крыс (Kunz et al., Pain 2004, 110, pp. 409-418), при невропатии, индуцированной таксолом (Wang et al.; Brain 2004, 127, pp. 671-679), и при острых и хронических воспалительных процессах (Cuzzocrea et al., American Journal of Pathology 2000, 157 (6), pp. 2065-2079).
В последнее время также была показана вовлеченность кальпаина в развитие заболеваний почек, таких как хронические болезни почек, например, диабетическая нефропатия. Так, Y. Shi et al. на животных моделях продемонстрировали, что природный ингибитор кальпаина кальпастатин подавляется во время почечной ишемии/реперфузии (Am. J. Physiol. Renal Physiol. 2000, 279, pp. 509-517). Более того, в публикации A. Dnyanmote et al. Toxicology and Applied Pharmacology 2006, 215, pp. 146-157 на модели острой почечной недостаточности показано, что ингибирование кальпаина посредством сверхэкспрессии кальпастатина уменьшает развитие DCVC-индуцированного повреждения почек. Кроме того, Peltier et al. на экспериментальном гломерулонефрите продемонстрировали, что активация и секреция кальпаина промотирует гломерулярное повреждение (J. Am. Soc. Nephrol. 2006, 17, pp. 3415-3423). Также было показано, что ингибиторы кальпаина уменьшают почечную дисфункцию и повреждение, вызванное почечной ишемией-реперфузией, и поэтому могут применяться для повышения толерантности почек против почечного повреждения, связанного с сосудистой хирургией на аорте или трансплантацией почек (P. Chatterjee et al., Biochem. Pharmacol. 2005, 7, pp. 1121-1131).
Кроме того, возможные применения ингибиторов кальпаина подробно описаны в публикациях: M.E. Saez et al., Drug Discovery Today 2006, 11 (19/20), pp. 917-923; N.O. Carragher, Curr. Pharm. Design 2006, 12, pp. 615-638; K.K. Wang et al., Drugs of the Future 1998, 23 (7), pp. 741-749; и Trends in Pharmacol. Sci. 1994, 15, pp. 412-419.
Что касается ингибиторов кальпаина, описанных к настоящему времени, делается общее различие между необратимо и обратимо действующими ингибиторами и пептидными и непептидными ингибиторами.
Необратимо действующие ингибиторы обычно представляют собой алкилирующие вещества. Их недостаток заключается в том, что они, прежде всего, взаимодействуют неселективно и/или нестабильны в организме. Поэтому соответствующие ингибиторы часто проявляют нежелательные побочные эффекты, такие как токсичность, и, следовательно, их применение заметно ограничено. Необратимо действующие ингибиторы включают, например, эпоксиды, такие как E64, α-галогенкетоны и дисульфиды.
Большое число известных обратимо действующих ингибиторов кальпаина представляет собой пептидные альдегиды, которые, в частности, получают из ди- или трипептидов, например, такие как Z-Val-Phe-H (MDL 28170). Также описаны производные и пролекарства, по своей структуре производные альдегидов, особенно соответствующие ацетали и гемиацетали (например, гидрокситетрагидрофураны, гидроксиоксазолиндины, гидроксиморфолины и т.п.), а также имины или гидразоны. Однако в физиологических условиях пептидные альдегиды и родственные им соединения обычно имеют недостаток, который связан с их химической активностью, они часто нестабильны, быстро метаболизируются и склонны к неспецифическим реакциям, которые также могут вызывать токсические эффекты (J.A. Fehrentz и B. Castro, Synthesis 1983, pp. 676-78).
В последние годы описан ряд непептидных карбоксамидов, содержащих функциональную β-кетогруппу в аминном фрагменте и ингибирующих кальпаин. Так, в патентной заявке WO-98/16512 описаны производные 3-амино-2-оксокарбоновой кислоты, аминогруппа которых амидирована с использованием соединения 4-пиперидинкарбоновой кислоты. В патентной заявке WO-99/17775 описаны аналогичные соединения, которые амидированы с использованием хинолинкарбоновой кислоты. В патентных заявках WO-98/25883, WO-98/25899 и WO-99/54294 описаны производные 3-амино-2-оксокарбоновой кислоты, аминогруппа которых амидирована с использованием замещенной бензойной кислоты. В патентной заявке WO-99/61423 описаны производные 3-амино-2-оксокарбоновой кислоты, аминогруппа которых амидирована с использованием ароматической карбоновой кислоты, несущей тетрагидрохинолиновый/изохинолиновый остаток и 2,3-дигидроиндольный/изоиндольный остаток. Подобные соединения, в которых остаток ароматической карбоновой кислоты несет гетероциклоалкильный радикал или (гетеро)арильный радикал, который необязательно присоединен посредством линкера, описаны в патентных заявках WO-99/54320, WO-99/54310, WO-99/54304 и WO-99/54305. Также в патентной заявке WO-08/080969 описаны никотинамиды производных 3-амино-2-оксокарбоновой кислоты, которые в положении 2 пиридинового кольца присоединены к замещенному пиразолу посредством атома азота. В патентной заявке WO-03/080182 описано применение указанных выше амидов для лечения легочных заболеваний. Приведенные в указанной ссылке непептидные ингибиторы кальпаина также имеют ряд недостатков, в частности низкую селективность или отсутствие селективности в отношении родственных цистеинпротеаз, таких как различные катепсины, также вероятно приводящих к нежелательным побочным эффектам.
В патентных заявках WO-07/016589 и WO-08/106130 описаны производные 2-оксокарбоновых кислот, несущие 2-пирролидинкарбоксиламидогруппу, N-ацилированную в положении 3. Также описано их применение для лечения инфекций вируса гепатита С.
Таким образом, настоящее изобретение основано на обеспечении соединений, которые ингибируют кальпаин, в частности селективно ингибируют кальпаин даже при низких сывороточных концентрациях. В частности, подразумевается, что соединения демонстрируют высокую селективность в отношении ингибирования кальпаина, то есть ингибируют отнюдь не все другие цистеинпротеазы, например катепсин, или ингибируют их только при более высоких концентрациях.
Указанная цель и дополнительные цели достигаются с помощью карбоксамидных соединений общей формулы I, описанной ниже, их таутомеров и их фармацевтически приемлемых солей:

где

R1 представляет собой атом водорода, С1-С10алкил, С2-С10алкенил, С2-С10алкинил, где три последних указанных радикала могут быть частично или полностью галогенированы и/или могут содержать 1, 2 или 3 заместителя R1a,
C3-C7циклоалкил, C3-C7циклоалкил-С1-С4алкил, где группа CH2 в циклоалкильном фрагменте двух последних указанных радикалов может быть заменена O, NH или S, или два соседних атома С могут образовывать двойную связь, где циклоалкильный фрагмент может дополнительно содержать 1, 2, 3 или 4 радикала R1b,
арил, гетарил, арил-С1-С6алкил, арил-С2-С6алкенил, гетарил-С1-С4алкил или гетарил-С2-С6алкенил, где арил и гетарил в шести последних указанных радикалах могут быть незамещенными или могут нести 1, 2, 3 или 4 одинаковых или различных радикала R1c; где
R1a независимо один от другого выбран из OH, SH, COOH, CN, OCH2COOH, C1-C6алкокси, C1-C6галогеналкокси, C3-C7циклоалкилокси, C1-C6алкилтио, C1-C6галогеналкилтио, COORa1, CONRa2Ra3, SO2NRa2Ra3, -NRa2-SO2-Ra4, NRa2-CO-Ra5, SO2-Ra4 и NRa6Ra7;
R1b независимо один от другого выбран из OH, SH, COOH, CN, OCH2COOH, галогена, фенила, который необязательно содержит 1, 2 или 3 заместителя R1d,
С1-С6алкила, C1-C6алкокси, C1-C6алкилтио, где алкильные фрагменты в трех последних указанных заместителях могут быть частично или полностью галогенированы и/или содержать 1, 2 или 3 заместителя R1a,
COORb1, CONRb2Rb3, SO2NRb2Rb3, NRb2-SO2-Rb4, NRb2-CO-Rb5, SO2-Rb4 и NRb6Rb7,
кроме того, два радикала R1b вместе могут образовывать С1-С4алкиленовую группу, или два радикала R1b, связанные с соседними атомами С циклоалкила, могут также образовывать вместе с атомами углерода, к которым они присоединены, бензольное кольцо;
R1c независимо один от другого выбран из OH, SH, галогена, NO2, NH2, CN, COOH, OCH2COOH, C1-C6алкила, C1-C6алкокси, C1-C6алкокси-C1-C4алкила, C1-C6алкилтио, где алкильные фрагменты в последних четырех указанных заместителях могут быть частично или полностью галогенированы и/или могут содержать 1, 2 или 3 заместителя R1a,
C3-C7циклоалкила, C3-C7циклоалкил-C1-C4алкила, C3-C7циклоалкилокси, где циклоалкильный фрагмент в трех последних указанных радикалах может содержать 1, 2, 3 или 4 радикала R1b, и где 1 или 2 группы CH2 в циклоалкильном фрагменте могут быть заменены O, NH или S,
арила, гетарила, O-арила, O-CH2-арила, где три последних указанных радикала являются незамещенными в арильном фрагменте или могут нести 1, 2, 3 или 4 радикала R1d,
COORc1, CONRc2Rc3, SO2NRc2Rc3, NRc2-SO2-Rc4, NRc2-CO-Rc5, SO2-Rc4,
-(СН2)р-NRc6Rc7, где р равно 0, 1, 2, 3, 4, 5 или 6, и
О-(СН2)q-NRc6Rc7, где q равно 2, 3, 4, 5 или 6, где
Ra1, Rb1 и Rc1 независимо друг от друга представляют собой H, C1-C6алкил, C1-C6галогеналкил, C1-C6алкил, который содержит 1, 2 или 3 заместителя R1a, или C2-C6алкенил, C2-C6алкинил, C3-C7циклоалкил, C3-C7циклоалкил-C1-C4алкил, C3-C7гетероциклоалкил-C1-C4алкил, C1-C6алкокси-C1-C4алкил, арил, арил-C1-C4алкил, гетарил или гетарил-C1-C4алкил, где арил и гетарил в последних четырех указанных радикалах являются незамещенными или содержат 1, 2 или 3 заместителя R1d;
Ra2, Rb2 и Rc2 независимо друг от друга представляют собой H, C1-C6алкил, C1-C6галогеналкил, C1-C6алкил, который содержит 1, 2 или 3 заместителя R1a, или C2-C6алкенил, C2-C6алкинил, С3-С7циклоалкил, С3-С7циклоалкил-C1-C4алкил, С3-С7гетероциклоалкил-C1-C4алкил, C1-C6алкокси-C1-C4алкил, арил, арил-C1-C4алкил, гетарил или гетарил-C1-C4алкил, где арил и гетарил в последних четырех указанных радикалах являются незамещенными или содержат 1, 2 или 3 заместителя R1d; и
Ra3, Rb3 и Rc3 независимо друг от друга представляют собой H, C1-C6алкил, C1-C6галогеналкил, C1-C6алкил, который содержит 1, 2 или 3 заместителя R1a, или C2-C6алкенил, C2-C6алкинил, С3-С7циклоалкил, С3-С7циклоалкил-C1-C4алкил, С3-С7гетероциклоалкил-C1-C4алкил, C1-C6алкокси-C1-C4алкил, арил, арил-C1-C4алкил, гетарил или гетарил-C1-C4алкил, где арил и гетарил в последних четырех указанных радикалах являются незамещенными или содержат 1, 2 или 3 заместителя R1d, или
два радикала Ra2 и Ra3, или Rb2, или Rc2 и Rc3 образуют вместе с атомом N 3-7-членный, необязательно замещенный азотный гетероцикл, который необязательно может дополнительно содержать 1, 2 или 3 различных или одинаковых гетероатома, выбранных из группы O, N, S, в качестве членов кольца;
Ra4, Rb4 и Rc4 независимо друг от друга представляют собой C1-C6алкил, C1-C6галогеналкил, C1-C6алкил, который содержит 1, 2 или 3 заместителя R1a, или C2-C6алкенил, C2-C6алкинил, С3-С7циклоалкил, С3-С7циклоалкил-C1-C4алкил, С3-С7гетероциклоалкил-C1-C4алкил, C1-C6алкокси-C1-C4алкил, арил, арил-C1-C4алкил, гетарил или гетарил-C1-C4алкил, где арил и гетарил в последних четырех указанных радикалах являются незамещенными или содержат 1, 2 или 3 заместителя R1d; и
Ra5, Rb5 и Rc5 независимо друг от друга имеют одно из значений, указанных для Ra1, Rb1 и Rc1;
Ra6, Rb6 и Rc6 независимо друг от друга представляют собой H, C1-C6алкил, C1-C6алкокси, C1-C6галогеналкил, C1-C6алкил, который содержит 1, 2 или 3 заместителя R1a, или C2-C6алкенил, C2-C6алкинил, С3-С7циклоалкил, С3-С7циклоалкил-C1-C4алкил, С3-С7гетероциклоалкил-C1-C4алкил, C1-C6алкокси-C1-C4алкил, CO-C1-C6алкил, CO-O-C1-C6алкил, SO2-C1-C6алкил, арил, гетарил, O-арил, OCH2-арил, арил-C1-C4алкил, гетарил-C1-C4алкил, CO-арил, CO-гетарил, CO-(арил-C1-C4алкил), CO-(гетарил-C1-C4алкил), CO-O-арил, CO-О-гетарил, CO-O-(арил-C1-C4алкил), CO-O-(гетарил-C1-C4алкил), SO2-арил, SO2-гетарил, SO2-(арил-C1-C4алкил) или SO2-(гетарил-C1-C4алкил), где арил и гетарил в последних восемнадцати указанных радикалах являются незамещенными или содержат 1, 2 или 3 заместителя R1d; и
Ra7, Rb7 и Rc7 независимо друг от друга представляют собой H, С1-С6алкил, С1-С6галогеналкил, С1-С6алкил, который содержит 1, 2 или 3 заместителя R1a, или C2-C6алкенил, C2-C6алкинил, С3-С7циклоалкил, С3-С7циклоалкил-C1-C4алкил, С3-С7гетероциклоалкил-C1-C4алкил, C1-C6алкокси-C1-C4алкил, арил, арил-C1-C4алкил, гетарил или гетарил-C1-C4алкил, где арил и гетарил в последних четырех указанных радикалах являются незамещенными или содержат 1, 2 или 3 заместителя R1d; или
два радикала Ra6 и Ra7, или Rb6 и Rb7, или Rc6 и Rc7 образуют вместе с атомом N 3-7-членный, необязательно замещенный азотный гетероцикл, который необязательно содержит дополнительно 1, 2 или 3 различных или одинаковых гетероатома, выбранных из группы O, N и S, в качестве членов кольца;
или два радикала R1b или R1c, связанных с соседними атомами С, образуют вместе с атомами С, к которым они присоединены, 4-, 5-, 6- или 7-членный, необязательно замещенный карбоцикл или необязательно замещенный гетероцикл, который содержит 1, 2 или 3 различных или одинаковых гетероатома, выбранных из группы O, N и S, в качестве членов кольца;
R1d выбран из галогена, OH, SH, NO2, COOH, C(O)NH2, CHO, CN, NH2, OCH2COOH, С1-С6алкила, С1-С6галогеналкила, С1-С6алкокси, С1-С6галогеналкокси, С1-С6алкилтио, С1-С6галогеналкилтио, CO-С1-С6алкила, CO-O-С1-С6алкила, NH-С1-С6алкила, NHCHO, NH-C(O)С1-С6алкила и SO2-С1-С6алкила; или два радикала R1d, связанные с соседними атомами углерода, вместе могут образовывать фрагмент -О-Alk"-О-, где Alk" представляет собой линейный C1-C2алкандиил, который является незамещенным, или где 1 или 2 атома водорода могут быть заменены фтором, хлором или метилом, например, Alk" представляет собой CH2, CF2, CHF, CHCH3 или C(CH3)2, в частности CH2;
R2 представляет собой С3-С7циклоалкил, где группа CH2 в циклоалкильном фрагменте может быть заменена O, NH или S, или два соседних атома С могут образовывать двойную связь, где циклоалкильный фрагмент может дополнительно содержать 1, 2, 3 или 4 радикала R2a, арил или гетарил, где арил и гетарил может быть незамещенным или может нести 1, 2, 3 или 4 одинаковых или различных радикала R2b; где
R2a имеет одно из значений, указанных для R1b, и
R2b имеет одно из значений, указанных для R1c;
R3a и R3b независимо друг от друга представляют собой гидрокси или C1-C4алкокси, или вместе с атомом углерода, к которому они присоединены, представляют собой C=O или C=NR3; или
R3a и R3b вместе образуют фрагмент S-Alk-S, O-Alk-S или O-Alk-O, где Alk представляет собой линейный C2-C5алкандиил, который может быть незамещенным или замещен 1, 2, 3 или 4 радикалами, выбранными из C1-C4алкила или галогена;
R3 представляет собой H, C1-C6алкил, C1-C6алкокси, C2-C6алкенил, C3-C6циклоалкил, C3-C6циклоалкил-C1-C4алкил, C2-C6алкенилокси, C3-C6циклоалкилокси или C3-C6циклоалкил-C1-C4алкилокси;
R4 отсутствует или означает атом водорода;
A представляет собой C=O, S(=O) или S(=O)2;
Q представляет собой одинарную связь или фрагмент Alk'-Z, где Z связан с R2 и выбран из одинарной связи, O, S, S(=O), S(=O)2 и NRq, где Rq выбран из атома водорода, C1-C4алкила и C1-C4галогеналкила; Alk' представляет собой линейный C1-C3алкандиил, где 1, 2 или 3 атома водорода могут быть замещены C1-C4алкилом, C1-C4галогеналкилом или галогеном;
X представляет собой атом водорода или радикал формул: C(=O)-O-Rx1, C(=O)-NRx2Rx3, C(=O)-N(Rx4)-(C1-C6алкилен)-NRx2Rx3 или C(=O)-N(Rx4)NRx2Rx3, где
Rx1 представляет собой атом водорода, C1-C6алкил, C1-C6галогеналкил, C1-C6алкил, который содержит 1, 2 или 3 заместителя Rxa, или C2-C6алкенил, C2-C6алкинил, С3-С7циклоалкил, С3-С7циклоалкил-C1-C4алкил, С3-С7гетероциклоалкил-C1-C4алкил, C1-C6алкокси-C1-C4алкил, где алкил, алкенил, алкокси, алкинил, циклоалкил, гетероциклоалкил в последних шести указанных радикалах являются незамещенными или содержат 1, 2 или 3 заместителя Rxa, или арил, арил-C1-C4алкил, гетарил или гетарил-C1-C4алкил, где арил и гетарил в последних 4 указанных радикалах являются незамещенными или содержат 1, 2 или 3 заместителя Rxd,
Rx2 представляет собой H, OH, CN, C1-C6алкил, C1-C6галогеналкил, C1-C6алкил, который содержит 1, 2 или 3 заместителя Rxa, или C2-C6алкенил, C2-C6алкинил, С3-С7циклоалкил, С3-С7циклоалкил-C1-C4алкил, С3-С7гетероциклоалкил-C1-C4алкил, С1-С6алкокси-C1-C4алкил, CO-С1-С6алкил, CO-O-С1-С6алкил, SO2-С1-С6алкил, O-С1-С6алкил, где алкил, алкокси, алкенил, алкинил, циклоалкил, гетероциклоалкил в последних десяти указанных радикалах являются незамещенными или содержат 1, 2 или 3 заместителя Rxa,
арил, O-арил, O-CH2-арил, гетарил, O-CH2-гетарил, арил-C1-C4алкил, гетарил-C1-C4алкил, CO-арил, CO-гетарил, CO-(арил-C1-C4алкил), CO-(гетарил-C1-C4алкил), CO-O-арил, CO-O-гетарил, CO-O-(арил-C1-C4алкил), CO-O-(гетарил-C1-C4алкил), SO2-арил, SO2-гетарил, SO2-(арил-C1-C4алкил) или SO2-(гетарил-C1-C4алкил), где арил и гетарил в последних девятнадцати указанных радикалах являются незамещенными или содержат 1, 2 или 3 заместителя Rxd, и
Rx3 представляет собой H, С1-С6алкил, С1-С6галогеналкил, С1-С6алкил, который содержит 1, 2 или 3 заместителя Rxa, или C2-C6алкенил, C2-C6алкинил, С3-С7циклоалкил, С3-С7циклоалкил-C1-C4алкил, С3-С7гетероциклоалкил-C1-C4алкил, С1-С6алкокси-C1-C4алкил, где алкил, алкенил, алкокси, алкинил, циклоалкил, гетероциклоалкил в последних шести указанных радикалах являются незамещенными или содержат 1, 2 или 3 заместителя Rxa,
арил, арил-C1-C4алкил, гетарил или гетарил-C1-C4алкил, где арил и гетарил в последних четырех указанных радикалах являются незамещенными или содержат 1, 2 или 3 заместителя Rxd, или
два радикала Rx2 и Rx3 образуют вместе с атомом N 3-7-членный азотный гетероцикл, который необязательно может дополнительно содержать 1, 2 или 3 различных или одинаковых гетероатома, выбранных из группы O, N, S, в качестве членов кольца, и который может содержать 1, 2 или 3 заместителя Rxb;
Rx4 представляет собой H, OH, CN, С1-С6алкил, С1-С6галогеналкил, С1-С6алкил, который содержит 1, 2 или 3 заместителя Rxa, или C2-C6алкенил, C2-C6алкинил, С3-С7циклоалкил, С3-С7циклоалкил-C1-C4алкил, С3-С7гетероциклоалкил-C1-C4алкил, С1-С6алкокси-C1-C4алкил, CO-С1-С6алкил, CO-O-С1-С6алкил, SO2-С1-С6алкил, где алкил, алкенил, алкокси, алкинил, циклоалкил, гетероциклоалкил в последних девяти указанных радикалах являются незамещенными или содержат 1, 2 или 3 заместителя Rxa;
арил, O-арил, O-CH2-арил, гетарил, арил-C1-C4алкил, гетарил-C1-C4алкил, CO-арил, CO-гетарил, CO-(арил-C1-C4алкил), CO-(гетарил-C1-C4алкил), CO-O-арил, CO-O-гетарил, CO-O-(арил-C1-C4алкил), CO-O-(гетарил-C1-C4алкил), SO2-арил, SO2-гетарил, SO2-(арил-C1-C4алкил) или SO2-(гетарил-C1-C4алкил), где арил и гетарил в последних восемнадцати указанных радикалах являются незамещенными или содержат 1, 2 или 3 заместителя Rxd, и
где Rxa имеет одно из значений, указанных для R1a, Rxb имеет одно из значений, указанных для R1b, и Rxd имеет одно из значений, указанных для R1d;
Y представляет собой CH2, CH2-CH2, CH2-CH2-CH2, N(Ry#)-CH2 или N(Ry#)-CH2-CH2 или, если R4 отсутствует, фрагмент CH=CH-CH=, где в шести указанных выше фрагментах 1 или 2 атома водорода могут быть замещены радикалом Ry;
Ry независимо один от другого выбран из атома водорода, OH, SH, галогена, NO2, NH2, CN, CF3, CHF2, CH2F, О-CF3, О-CHF2, О-CH2F, COOH, OCH2COOH, С1-С6алкила, С1-С6алкокси, С1-С6алкокси-C1-C4алкила, С1-С6алкилтио, где последние четыре указанных радикала могут быть частично или полностью галогенированы и/или содержать 1, 2 или 3 заместителя Rya;
C3-C7циклоалкила, С3-С7циклоалкил-C1-C4алкила, С3-С7циклоалкил-O, где циклоалкильный фрагмент в последних трех указанных радикалах может содержать 1, 2, 3 или 4 радикала Ryb, и где 1 или 2 группы CH2 в циклоалкильном фрагменте могут быть заменены O, NH или S;
арила, гетарила, O-арила, CH2-арила, O-CH2-арила, где последние четыре указанных радикала являются незамещенными в арильном фрагменте или могут нести 1, 2, 3 или 4 радикала Ryd;
COORy1, CONRy2Ry3, SO2NRy2Ry3, -NH-SO2-Ry4, NH-CО-Ry5, SO2-Ry4, -(CH2)p-NRy6Ry7, где p равно 0, 1, 2, 3, 4, 5 или 6, и O-(CH2)q-NRy6Ry7, где q равно 2, 3, 4, 5 или 6; где
Rya имеет одно из значений, указанных для R1a,
Ryb имеет одно из значений, указанных для R1b,
Ryd имеет одно из значений, указанных для R1d,
Ryl имеет одно из значений, указанных для Rc1,
Ry2 имеет одно из значений, указанных для Rc2,
Ry3 имеет одно из значений, указанных для Rc3,
Ry4 имеет одно из значений, указанных для Rc4,
Ry5 имеет одно из значений, указанных для Rc5,
Ry6 имеет одно из значений, указанных для Rc6, и
Ry7 имеет одно из значений, указанных для Rc7;
Ry# независимо один от другого выбран из атома водорода, NH2, CN, CF3, CHF2, CH2F, О-CF3, О-CHF2, О-CH2F, OCH2COOH, С1-С6алкила, С1-С6алкокси, С1-С6алкокси-C1-C4алкила, С1-С6алкилтио, где последние четыре указанных радикала могут быть частично или полностью галогенированы и/или содержать 1, 2 или 3 заместителя Rya;
С3-С7циклоалкила, С3-С7циклоалкил-C1-C4алкила, С3-С7циклоалкил-O, где циклоалкильный фрагмент в последних трех указанных радикалах может содержать 1, 2, 3 или 4 радикала Ryb, и где 1 или 2 группы CH2 в циклоалкильном фрагменте могут быть заменены O, NH или S;
арила, гетарила, O-арила, CH2-арила, O-CH2-арила, где последние 4 указанных радикала являются незамещенными в арильном фрагменте или могут нести 1, 2, 3 или 4 радикала Ryd,
COORy1, CONRy2Ry3, SO2NRy2Ry3, -NH-SO2-Ry4, NH-CО-Ry5, SO2-Ry4, -(CH2)p-NRy6Ry7, где p равно 0, 1, 2, 3, 4, 5 или 6, и O-(CH2)q-NRy6Ry7, где q равно 2, 3, 4, 5 или 6.
Следовательно, настоящее изобретение относится к карбоксамидным соединениям общей формулы I, их таутомерам и фармацевтически приемлемым солям карбоксамидных соединений I.
Карбоксамидные соединения формулы I настоящего изобретения, их соли и их таутомеры эффективно ингибируют кальпаин даже при низких концентрациях. Они дополнительно характеризуются высокой селективностью в отношении ингибирования кальпаина по сравнению с другими цистеинпротеазами, такими как катепсин B, катепсин K, катепсин L и катепсин S.
Следовательно, карбоксамидные соединения формулы I настоящего изобретения, их соли и их таутомеры особенно подходят для лечения расстройств и состояний у живых существ, особенно у человека, которые ассоциированы с повышенной активностью кальпаина.
Следовательно, изобретение также относится к применению карбоксамидных соединений формулы I, их таутомеров и их фармацевтически приемлемых солей для производства лекарственного средства, в частности лекарственного средства, которое подходит для лечения расстройства или состояния, которое ассоциировано с повышенной активностью кальпаина.
Изобретение дополнительно относится к лекарственному средству, в частности к лекарственному средству, которое подходит для лечения расстройства или состояния, которое ассоциировано с повышенной активностью кальпаина. Лекарственное средство содержит по меньшей мере одно карбоксамидное соединение формулы I, как описано в настоящем описании, таутомер или фармацевтически приемлемую соль соединения I.
Карбоксамидные соединения формулы I могут находиться в форме β-кетосоединений, то есть радикалы R3a и R3b в соединениях формулы I образуют вместе с атомом углерода, к которому они присоединены, карбонильную группу, как показано в формуле на схеме A слева. Соединения настоящего изобретения также могут находиться в форме гидрата, то есть каждый из радикалов R3a и R3b представляет собой OH, как показано в формуле на схеме A справа. R1, R2, R4, Q, X, A и Y на схеме A имеют указанные выше значения.
Схема A

В присутствии воды, особенно в физиологических условиях, в смеси обычно присутствует как β-кетоформа, так и гидратная форма.
Когда в следующих формулах и описаниях указана только β-кетоформа, если не указано иное, подразумевается, что она включает также гидрат и его смеси с β-кетоформой. В качестве ингибитора кальпаина в равной степени подходят гидраты и β-кетоформы.
Карбоксамидные соединения формулы I настоящего изобретения также способны образовывать таутомеры, когда R3a и R3b образуют карбонильную группу вместе с атомом углерода, к которому они присоединены. Таутомеры в равной степени подходят в качестве ингибиторов кальпаина. Конкретные примеры таутомеров, которые можно привести, представляют собой соединения формулы I-T:

R1, R2, R4, Q, A, X и Y в формуле I-T имеют указанные выше значения.
Карбоксамидные соединения формулы I настоящего изобретения также могут образовывать гемиацетали, гемикетали, ацетали или кетали с алканолами или имины с первичными аминами или аммиаком. Такие соединения являются в равной степени подходящими в качестве ингибитора кальпаина, поскольку они представляют собой пролекарства соединений I, где CR3aR3b представляет собой карбонильную группу (то есть C=O) или C(OH)2. Соответственно, согласно настоящему изобретению также могут использоваться соединения, где один или оба радикала R3a и R3b представляют собой радикал, производный от алканола и особенно C1-C4алкокси.
Используемый в настоящем описании термин "пролекарство" относится к соединению, которое в условиях метаболизма подвергается преобразованию в соединение формулы I. Наряду с указанными выше гемиацеталями, гемикеталями, ацеталями и кеталями пролекарства соединений I включают соединения формулы I, где R3a и R3b вместе образуют группу O-Alk-O, S-Alk-O или S-Alk-S, где Alk представляет собой линейный C2-C5алкандиил, который может быть незамещенным или замещен 1, 2, 3 или 4 радикалами, выбранными из C1-C4алкила или атомов галогена, примерами таких групп являются O(CH2)2O, O(CH2)5O, O(CH2)4O, S(CH2)2O, S(CH2)5O, S(CH2)4О и т.д. Дополнительно пролекарства соединений I включают соединения формулы I, где R3a и R3b вместе с атомом углерода образуют группу C=NR3, где R3 выбран из H, C1-C6алкила, C1-C6алкокси, C2-C6алкенила, C3-C6циклоалкила, C3-C6циклоалкил-C1-C4алкила, C2-C6алкенилокси, C3-C6циклоалкилокси, C3-C6циклоалкил-C1-C4алкилокси. В условиях метаболизма указанные выше пролекарства подвергаются преобразованию в соответствующие β-кетосоединения формулы I (CR3aR3b представляет собой C=O) или в их гидраты (CR3aR3b представляет собой C(OH)2). Аналогично, соединения, в которых R3a и R3b представляют собой C1-C4алкокси, могут быть использованы в качестве пролекарств.
В равной степени возможно применение фармацевтически приемлемых солей карбоксамидных соединений формулы I, их таутомеров или их пролекарств, особенно кислотно-аддитивных солей с физиологически переносимыми органическими или неорганическими кислотами. Примерами подходящих физиологически переносимых органических и неорганических кислот являются хлористоводородная кислота, бромистоводородная кислота, фосфорная кислота, азотная кислота, серная кислота, органические сульфоновые кислоты, содержащие 1-12 атомов углерода, например C1-C4алкилсульфоновые кислоты, такие как метансульфоновая кислота, циклоалифатические сульфоновые кислоты, такие как S-(+)-10-камфорсульфоновые кислоты, и ароматические сульфоновые кислоты, такие как бензолсульфоновая кислота и толуолсульфоновая кислота, ди- и трикарбоновые кислоты и гидроксикарбоновые кислоты, содержащие 2-10 атомов углерода, такие как щавелевая кислота, малоновая кислота, малеиновая кислота, фумаровая кислота, слизевая (муциновая) кислота, молочная кислота, винная кислота, лимонная кислота, гликолевая кислота и адипиновая кислота, а также цис- и транс-коричная кислота, фуран-2-карбоновая кислота и бензойная кислота. Кроме того, подходящие кислоты описаны в публикации: "Fortschritte der Arzneimittelforschung", том 10, pp. 224 и далее, Birkhauser Verlag, Basel и Stuttgart, 1966. Физиологически переносимые соли соединений формулы I могут находиться в форме моно-, ди-, три- или тетрасолей, означающей, что они могут содержать 1, 2, 3 или 4 молекулы указанной выше кислоты на одну молекулу формулы I. Молекулы кислоты могут находиться в форме кислоты или в виде аниона.
Соединения настоящего изобретения могут находиться в форме смеси диастереомеров или смеси диастереомеров, которая обогащена одним из двух диастереомеров, или в форме по существу диастереомерно чистых соединений (диастереомерный избыток de >90%). Предпочтительно соединения находятся в форме по существу диастереомерно чистых соединений (диастереомерный избыток de >90%). Кроме того, соединения настоящего изобретения I могут находиться в форме смеси энантиомеров (например, в виде рацемической смеси), смеси энантиомеров, которая обогащена одним из двух энантиомеров, или в форме по существу энантиомерно чистых соединений (энантиомерный избыток >90%). Однако соединения настоящего изобретения часто склонны к эпимеризации в зависимости от конфигурации атома углерода, который несет радикал R1, так что часто образуются смеси относительно такого атома углерода, или соединения, которые проявляют одинаковую конфигурацию относительно такого атома C, в физиологических условиях образуют смеси. Однако, что касается других стереоцентров и существования связанных с этим явлением энантиомеров и диастереомеров, предпочтительно использовать энантиомерно чистые или диастереомерно чистые соединения. В частности, соединения формулы I, где

В контексте настоящего описания, если не указано иное, термины "алкил", "алкокси", "алкилтио", "галогеналкил", "галогеналкокси", "галогеналкилтио", "алкенил", "алкинил", "алкилен" и их производные радикалы всегда включают как неразветвленный, так и разветвленный "алкил", "алкокси", "алкилтио", "галогеналкил", "галогеналкокси", "галогеналкилтио", "алкенил", "алкинил" и "алкилен" соответственно.
Префикс Cn-Cm- указывает на соответствующее число атомов углерода в структурном углеводородном элементе. Если не указано иное, галогенированные заместители предпочтительно содержат от одного до пяти одинаковых или различных атомов галогена, в частности атомов фтора или атомов хлора. C0алкилен или (CH2)0 или аналогичные обозначения в контексте описания означают, если не указано иное, одинарную связь.
Термин "галоген" в каждом случае означает фтор, бром, хлор или йод, в частности фтор, хлор или бром.
Примерами других обозначений являются:
алкил и алкильные фрагменты, например, в алкокси, алкилтио, арилалкиле, гетарилалкиле, циклоалкилалкиле или алкоксиалкиле: насыщенные углеводородные радикалы с прямой или разветвленной цепью, содержащие один или несколько атомов С, например 1-4, 1-6 или 1-10 атомов углерода, например С1-С6алкил, такой как метил, этил, пропил, 1-метилэтил, бутил, 1-метилпропил, 2-метилпропил, 1,1-диметилэтил, пентил, 1-метилбутил, 2-метилбутил, 3-метилбутил, 2,2-диметилпропил, 1-этилпропил, гексил, 1,1-диметилпропил, 1,2-диметилпропил, 1-метилпентил, 2-метилпентил, 3-метилпентил, 4-метилпентил, 1,1-диметилбутил, 1,2-диметилбутил, 1,3-диметилбутил, 2,2-диметилбутил, 2,3-диметилбутил, 3,3-диметилбутил, 1-этилбутил, 2-этилбутил, 1,1,2-триметилпропил, 1,2,2-триметилпропил, 1-этил-1-метилпропил, 1-этил-2-метилпропил. В одном из вариантов осуществления изобретения алкил означает небольшие алкильные группы, такие как C1-C4алкил. В еще одном варианте осуществления изобретения алкил означает более большие алкильные группы, такие как С5-С10алкил;
галогеналкил: алкильный радикал, обычно содержащий 1-6 или 1-4 атома C, как указано выше, атомы водорода которого частично или полностью заменены атомами галогена, такими как фтор, хлор, бром и/или йод, например, хлорметил, дихлорметил, трихлорметил, фторметил, дифторметил, трифторметил, хлорфторметил, дихлорфторметил, хлордифторметил, 2-фторэтил, 2-хлорэтил, 2-бромэтил, 2-йодэтил, 2,2-дифторэтил, 2,2,2-трифторэтил, 2-хлор-2-фторэтил, 2-хлор-2,2-дифторэтил, 2,2-дихлор-2-фторэтил, 2,2,2-трихлорэтил, пентафторэтил, 2-фторпропил, 3-фторпропил, 2,2-дифторпропил, 2,3-дифторпропил, 2-хлорпропил, 3-хлорпропил, 2,3-дихлорпропил, 2-бромпропил, 3-бромпропил, 3,3,3-трифторпропил, 3,3,3-трихлорпропил, 2,2,3,3,3-пентафторпропил, гептафторпропил, 1-(фторметил)-2-фторэтил, 1-(хлорметил)-2-хлорэтил, 1-(бромметил)-2-бромэтил, 4-фторбутил, 4-хлорбутил, 4-бромбутил и нонафторбутил;
циклоалкил и циклоалкильные фрагменты, например, в циклоалкокси или циклоалкил-С1-С6алкиле: моноциклические, насыщенные углеводородные группы, содержащие три или более атомов C, например 3, 4, 5, 6 или 7 углеродных членов кольца, такие как циклопропил, циклобутил, циклопентил, циклогексил;
алкенил и алкенильные фрагменты, например, в арил(C2-C6)алкениле: мононенасыщенные углеводородные радикалы с прямой или разветвленной цепью, содержащие два или более атомов C, например, 2-4, 2-6 или 2-10 атомов углерода и одну двойную связь в любом положении, например, C2-C6алкенил, такой как этенил, 1-пропенил, 2-пропенил, 1-метилэтенил, 1-бутенил, 2-бутенил, 3-бутенил, 1-метил-1-пропенил, 2-метил-1-пропенил, 1-метил-2-пропенил, 2-метил-2-пропенил, 1-пентенил, 2-пентенил, 3-пентенил, 4-пентенил, 1-метил-1-бутенил, 2-метил-1-бутенил, 3-метил-1-бутенил, 1-метил-2-бутенил, 2-метил-2-бутенил, 3-метил-2-бутенил, 1-метил-3-бутенил, 2-метил-3-бутенил, 3-метил-3-бутенил, 1,1-диметил-2-пропенил, 1,2-диметил-1-пропенил, 1,2-диметил-2-пропенил, 1-этил-1-пропенил, 1-этил-2-пропенил, 1-гексенил, 2-гексенил, 3-гексенил, 4-гексенил, 5-гексенил, 1-метил-1-пентенил, 2-метил-1-пентенил, 3-метил-1-пентенил, 4-метил-1-пентенил, 1-метил-2-пентенил, 2-метил-2-пентенил, 3-метил-2-пентенил, 4-метил-2-пентенил, 1-метил-3-пентенил, 2-метил-3-пентенил, 3-метил-3-пентенил, 4-метил-3-пентенил, 1-метил-4-пентенил, 2-метил-4-пентенил, 3-метил-4-пентенил, 4-метил-4-пентенил, 1,1-диметил-2-бутенил, 1,1-диметил-3-бутенил, 1,2-диметил-1-бутенил, 1,2-диметил-2-бутенил, 1,2-диметил-3-бутенил, 1,3-диметил-1-бутенил, 1,3-диметил-2-бутенил, 1,3-диметил-3-бутенил, 2,2-диметил-3-бутенил, 2,3-диметил-1-бутенил, 2,3-диметил-2-бутенил, 2,3-диметил-3-бутенил, 3,3-диметил-1-бутенил, 3,3-диметил-2-бутенил, 1-этил-1-бутенил, 1-этил-2-бутенил, 1-этил-3-бутенил, 2-этил-1-бутенил, 2-этил-2-бутенил, 2-этил-3-бутенил, 1,1,2-триметил-2-пропенил, 1-этил-1-метил-2-пропенил, 1-этил-2-метил-1-пропенил, 1-этил-2-метил-2-пропенил;
алкинил: углеводородные группы с прямой или разветвленной цепью, содержащие два или более атомов C, например, 2-4, 2-6 или 2-10 атомов углерода и одну или две тройных связи в любом положении, но не в соседних положениях, например, C2-C6алкинил, такой как этинил, 1-пропинил, 2-пропинил, 1-бутинил, 2-бутинил, 3-бутинил, 1-метил-2-пропинил, 1-пентинил, 2-пентинил, 3-пентинил, 4-пентинил, 1-метил-2-бутинил, 1-метил-3-бутинил, 2-метил-3-бутинил, 3-метил-1-бутинил, 1,1-диметил-2-пропинил, 1-этил-2-пропинил, 1-гексинил, 2-гексинил, 3-гексинил, 4-гексинил, 5-гексинил, 1-метил-2-пентинил, 1-метил-3-пентинил, 1-метил-4-пентинил, 2-метил-3-пентинил, 2-метил-4-пентинил, 3-метил-1-пентинил, 3-метил-4-пентинил, 4-метил-1-пентинил, 4-метил-2-пентинил, 1,1-диметил-2-бутинил, 1,1-диметил-3-бутинил, 1,2-диметил-3-бутинил, 2,2-диметил-3-бутинил, 3,3-диметил-1-бутинил, 1-этил-2-бутинил, 1-этил-3-бутинил, 2-этил-3-бутинил, 1-этил-1-метил-2-пропинил;
алкокси или алкокси-фрагменты, например, в алкоксиалкиле: алкил, как описано выше, содержащий предпочтительно 1-6 или 1-4 атома C, который присоединен через посредство атома O, например, метокси, этокси, н-пропокси, 1-метилэтокси, бутокси, 1-метилпропокси, 2-метилпропокси или 1,1-диметилэтокси, пентокси, 1-метилбутокси, 2-метилбутокси, 3-метилбутокси, 1,1-диметилпропокси, 1,2-диметилпропокси, 2,2-диметилпропокси, 1-этилпропокси, гексокси, 1-метилпентокси, 2-метилпентокси, 3-метилпентокси, 4-метилпентокси, 1,1-диметилбутокси, 1,2-диметилбутокси, 1,3-диметилбутокси, 2,2-диметилбутокси, 2,3-диметилбутокси, 3,3-диметилбутокси, 1-этилбутокси, 2-этилбутокси, 1,1,2-триметилпропокси, 1,2,2-триметилпропокси, 1-этил-1-метилпропокси или 1-этил-2-метилпропокси;
галогеналкокси: алкоксигруппа, как описано выше, в которой атомы водорода таких групп частично или полностью заменены атомами галогена, то есть, например, С1-С6галогеналкокси, такой как хлорметокси, дихлорметокси, трихлорметокси, фторметокси, дифторметокси, трифторметокси, хлорфторметокси, дихлорфторметокси, хлордифторметокси, 2-фторэтокси, 2-хлорэтокси, 2-бромэтокси, 2-йодэтокси, 2,2-дифторэтокси, 2,2,2-трифторэтокси, 2-хлор-2-фторэтокси, 2-хлор-2,2-дифторэтокси, 2,2-дихлор-2-фторэтокси, 2,2,2-трихлорэтокси, пентафторэтокси, 2-фторпропокси, 3-фторпропокси, 2,2-дифторпропокси, 2,3-дифторпропокси, 2-хлорпропокси, 3-хлорпропокси, 2,3-дихлорпропокси, 2-бромпропокси, 3-бромпропокси, 3,3,3-трифторпропокси, 3,3,3-трихлорпропокси, 2,2,3,3,3-пентафторпропокси, гептафторпропокси, 1-(фторметил)-2-фторэтокси, 1-(хлорметил)-2-хлорэтокси, 1-(бромметил)-2-бромэтокси, 4-фторбутокси, 4-хлорбутокси, 4-бромбутокси, нонафторбутокси, 5-фтор-1-пентокси, 5-хлор-1-пентокси, 5-бром-1-пентокси, 5-йод-1-пентокси, 5,5,5-трихлор-1-пентокси, ундекафторпентокси, 6-фтор-1-гексокси, 6-хлор-1-гексокси, 6-бром-1-гексокси, 6-йод-1-гексокси, 6,6,6-трихлор-1-гексокси или додекафторгексокси, в частности, хлорметокси, фторметокси, дифторметокси, трифторметокси, 2-фторэтокси, 2-хлорэтокси или 2,2,2-трифторэтокси;
алкоксиалкил: алкильный радикал, обычно содержащий 1-4 атома C, где один атом водорода заменен алкокси-радикалом, содержащим обычно 1-6 или 1-4 атома C. Примерами такого радикала являются CH2-OCH3, CH2-OC2H5, н-пропоксиметил, CH2-OCH(CH3)2, н-бутоксиметил, (1-метилпропокси)метил, (2-метилпропокси)метил, CH2-OC(CH3)3, 2-(метокси)этил, 2-(этокси)этил, 2-(н-пропокси)этил, 2-(1-метилэтокси)этил, 2-(н-бутокси)этил, 2-(1-метилпропокси)этил, 2-(2-метилпропокси)этил, 2-(1,1-диметилэтокси)этил, 2-(метокси)пропил, 2-(этокси)пропил, 2-(н-пропокси)пропил, 2-(1-метилэтокси)пропил, 2-(н-бутокси)пропил, 2-(1-метилпропокси)пропил, 2-(2-метилпропокси)пропил, 2-(1,1-диметилэтокси)пропил, 3-(метокси)пропил, 3-(этокси)пропил, 3-(н-пропокси)пропил, 3-(1-метилэтокси)пропил, 3-(н-бутокси)пропил, 3-(1-метилпропокси)пропил, 3-(2-метилпропокси)пропил, 3-(1,1-диметилэтокси)пропил, 2-(метокси)бутил, 2-(этокси)бутил, 2-(н-пропокси)бутил, 2-(1-метилэтокси)бутил, 2-(н-бутокси)бутил, 2-(1-метилпропокси)бутил, 2-(2-метилпропокси)бутил, 2-(1,1-диметилэтокси)бутил, 3-(метокси)бутил, 3-(этокси)бутил, 3-(н-пропокси)бутил, 3-(1-метилэтокси)бутил, 3-(н-бутокси)бутил, 3-(1-метилпропокси)бутил, 3-(2-метилпропокси)бутил, 3-(1,1-диметилэтокси)бутил, 4-(метокси)бутил, 4-(этокси)бутил, 4-(н-пропокси)бутил, 4-(1-метилэтокси)бутил, 4-(н-бутокси)бутил, 4-(1-метилпропокси)бутил, 4-(2-метилпропокси)бутил, 4-(1,1-диметилэтокси)бутил и т.д.;
алкилтио: алкил, как описано выше, предпочтительно содержащий 1-6 или 1-4 атома C, который присоединен через посредство атома S, например, метилтио, этилтио, н-пропилтио и т.п.;
галогеналкилтио: галогеналкил, как описано выше, предпочтительно содержащий 1-6 или 1-4 атома C, который присоединен через посредство атома S, например, фторметилтио, дифторметилтио, трифторметилтио, 2-фторэтилтио, 2,2-дифторэтилтио, 2,2,2-трифторэтилтио, пентафторэтилтио, 2-фторпропилтио, 3-фторпропилтио, 2,2-дифторпропилтио, 2,3-дифторпропилтио и гептафторпропилтио;
арил: моно-, би- или трициклический ароматический углеводородный радикал, такой как фенил или нафтил, особенно фенил;
гетероциклил: гетероциклический радикал, который может быть насыщенным или частично ненасыщенным, и который обычно содержит 3, 4, 5, 6, 7 или 8 атомов кольца, где обычно 1, 2, 3 или 4, в частности 1, 2 или 3 атома кольца представляют собой гетероатомы, такие как N, S или O, кроме атомов углерода в качестве членов кольца.
Примеры насыщенных гетероциклов, в частности, представляют собой:
гетероциклоалкил: то есть насыщенный гетероциклический радикал, который обычно содержит 3, 4, 5, 6 или 7 атомов кольца, где обычно 1, 2 или 3 атома кольца, кроме атомов углерода, представляют собой гетероатомы, такие как N, S или O, в качестве членов кольца. Такие радикалы включают, например:
C-связанные 3-4-членные насыщенные кольца, такие как 2-оксиранил, 2-оксетанил, 3-оксетанил, 2-азиридинил, 3-тиетанил, 1-азетидинил, 2-азетидинил;
C-связанные 5-членные насыщенные кольца, такие как
тетрагидрофуран-2-ил, тетрагидрофуран-3-ил,
тетрагидротиен-2-ил, тетрагидротиен-3-ил,
тетрагидропиррол-2-ил, тетрагидропиррол-3-ил,
тетрагидропиразол-3-ил, тетрагидропиразол-4-ил,
тетрагидроизоксазол-3-ил, тетрагидроизоксазол-4-ил,
тетрагидроизоксазол-5-ил, 1,2-оксатиолан-3-ил,
1,2-оксатиолан-4-ил, 1,2-оксатиолан-5-ил,
тетрагидроизотиазол-3-ил, тетрагидроизотиазол-4-ил,
тетрагидроизотиазол-5-ил, 1,2-дитиолан-3-ил, 1,2-дитиолан-4-ил,
тетрагидроимидазол-2-ил, тетрагидроимидазол-4-ил,
тетрагидрооксазол-2-ил, тетрагидрооксазол-4-ил,
тетрагидрооксазол-5-ил, тетрагидротиазол-2-ил,
тетрагидротиазол-4-ил, тетрагидротиазол-5-ил,
1,3-диоксолан-2-ил, 1,3-диоксолан-4-ил, 1,3-оксатиолан-2-ил,
1,3-оксатиолан-4-ил, 1,3-оксатиолан-5-ил, 1,3-дитиолан-2-ил,
1,3-дитиолан-4-ил, 1,3,2-диоксатиолан-4-ил;
C-связанные 6-членные насыщенные кольца, такие как:
тетрагидропиран-2-ил, тетрагидропиран-3-ил,
тетрагидропиран-4-ил, пиперидин-2-ил, пиперидин-3-ил,
пиперидин-4-ил, тетрагидротиопиран-2-ил,
тетрагидротиопиран-3-ил, тетрагидротиопиран-4-ил,
1,3-диоксан-2-ил, 1,3-диоксан-4-ил, 1,3-диоксан-5-ил,
1,4-диоксан-2-ил, 1,3-дитиан-2-ил, 1,3-дитиан-4-ил,
1,3-дитиан-5-ил, 1,4-дитиан-2-ил, 1,3-оксатиан-2-ил,
1,3-оксатиан-4-ил, 1,3-оксатиан-5-ил, 1,3-оксатиан-6-ил,
1,4-оксатиан-2-ил, 1,4-оксатиан-3-ил, 1,2-дитиан-3-ил,
1,2-дитиан-4-ил, гексагидропиримидин-2-ил,
гексагидропиримидин-4-ил, гексагидропиримидин-5-ил,
гексагидропиразин-2-ил, гексагидропиридазин-3-ил,
гексагидропиридазин-4-ил, тетрагидро-1,3-оксазин-2-ил,
тетрагидро-1,3-оксазин-4-ил, тетрагидро-1,3-оксазин-5-ил,
тетрагидро-1,3-оксазин-6-ил, тетрагидро-1,3-тиазин-2-ил,
тетрагидро-1,3-тиазин-4-ил, тетрагидро-1,3-тиазин-5-ил,
тетрагидро-1,3-тиазин-6-ил, тетрагидро-1,4-тиазин-2-ил,
тетрагидро-1,4-тиазин-3-ил, тетрагидро-1,4-оксазин-2-ил,
тетрагидро-1,4-оксазин-3-ил, тетрагидро-1,2-оксазин-3-ил,
тетрагидро-1,2-оксазин-4-ил, тетрагидро-1,2-оксазин-5-ил,
тетрагидро-1,2-оксазин-6-ил;
N-связанные 5-членные насыщенные кольца, такие как:
тетрагидропиррол-1-ил, тетрагидропиразол-1-ил,
тетрагидроизоксазол-2-ил, тетрагидроизотиазол-2-ил,
тетрагидроимидазол-1-ил, тетрагидрооксазол-3-ил,
тетрагидротиазол-3-ил;
N-связанные 6-членные насыщенные кольца, такие как:
пиперидин-1-ил, гексагидропиримидин-1-ил,
гексагидропиразин-1-ил, гексагидропиридазин-1-ил,
тетрагидро-1,3-оксазин-3-ил, тетрагидро-1,3-тиазин-3-ил,
тетрагидро-1,4-тиазин-4-ил, тетрагидро-1,4-оксазин-4-ил,
тетрагидро-1,2-оксазин-2-ил.
Ненасыщенные гетероциклические радикалы, которые обычно содержат 4, 5, 6 или 7 атомов кольца, где обычно 1, 2 или 3 из атомов кольца, кроме атомов углерода, представляют собой гетероатомы, такие как N, S или O, в качестве членов кольца. Такие радикалы включают, например:
C-связанные 5-членные, частично ненасыщенные кольца, такие как:
2,3-дигидрофуран-2-ил, 2,3-дигидрофуран-3-ил,
2,5-дигидрофуран-2-ил, 2,5-дигидрофуран-3-ил,
4,5-дигидрофуран-2-ил, 4,5-дигидрофуран-3-ил,
2,3-дигидротиен-2-ил, 2,3-дигидротиен-3-ил,
2,5-дигидротиен-2-ил, 2,5-дигидротиен-3-ил,
4,5-дигидротиен-2-ил, 4,5-дигидротиен-3-ил,
2,3-дигидро-1H-пиррол-2-ил, 2,3-дигидро-1H-пиррол-3-ил,
2,5-дигидро-1H-пиррол-2-ил, 2,5-дигидро-1H-пиррол-3-ил,
4,5-дигидро-1H-пиррол-2-ил, 4,5-дигидро-1H-пиррол-3-ил,
3,4-дигидро-2H-пиррол-2-ил, 3,4-дигидро-2H-пиррол-3-ил,
3,4-дигидро-5H-пиррол-2-ил, 3,4-дигидро-5H-пиррол-3-ил,
4,5-дигидро-1H-пиразол-3-ил, 4,5-дигидро-1H-пиразол-4-ил,
4,5-дигидро-1H-пиразол-5-ил, 2,5-дигидро-1H-пиразол-3-ил,
2,5-дигидро-1H-пиразол-4-ил, 2,5-дигидро-1H-пиразол-5-ил,
4,5-дигидроизоксазол-3-ил, 4,5-дигидроизоксазол-4-ил,
4,5-дигидроизоксазол-5-ил, 2,5-дигидроизоксазол-3-ил,
2,5-дигидроизоксазол-4-ил, 2,5-дигидроизоксазол-5-ил,
2,3-дигидроизоксазол-3-ил, 2,3-дигидроизоксазол-4-ил,
2,3-дигидроизоксазол-5-ил, 4,5-дигидроизотиазол-3-ил,
4,5-дигидроизотиазол-4-ил, 4,5-дигидроизотиазол-5-ил,
2,5-дигидроизотиазол-3-ил, 2,5-дигидроизотиазол-4-ил,
2,5-дигидроизотиазол-5-ил, 2,3-дигидроизотиазол-3-ил,
2,3-дигидроизотиазол-4-ил, 2,3-дигидроизотиазол-5-ил,
4,5-дигидро-1H-имидазол-2-ил, 4,5-дигидро-1H-имидазол-4-ил,
4,5-дигидро-1H-имидазол-5-ил, 2,5-дигидро-1H-имидазол-2-ил,
2,5-дигидро-1H-имидазол-4-ил, 2,5-дигидро-1H-имидазол-5-ил,
2,3-дигидро-1H-имидазол-2-ил, 2,3-дигидро-1H-имидазол-4-ил,
4,5-дигидрооксазол-2-ил, 4,5-дигидрооксазол-4-ил,
4,5-дигидрооксазол-5-ил, 2,5-дигидрооксазол-2-ил,
2,5-дигидрооксазол-4-ил, 2,5-дигидрооксазол-5-ил,
2,3-дигидрооксазол-2-ил, 2,3-дигидрооксазол-4-ил,
2,3-дигидрооксазол-5-ил, 4,5-дигидротиазол-2-ил,
4,5-дигидротиазол-4-ил, 4,5-дигидротиазол-5-ил,
2,5-дигидротиазол-2-ил, 2,5-дигидротиазол-4-ил,
2,5-дигидротиазол-5-ил, 2,3-дигидротиазол-2-ил,
2,3-дигидротиазол-4-ил, 2,3-дигидротиазол-5-ил,
1,3-диоксол-2-ил, 1,3-диоксол-4-ил, 1,3-дитиол-2-ил,
1,3-дитиол-4-ил, 1,3-оксатиол-2-ил, 1,3-оксатиол-4-ил,
1,3-оксатиол-5-ил.
C-связанные 6-членные, частично ненасыщенные кольца, такие как:
2H-3,4-дигидропиран-6-ил, 2H-3,4-дигидропиран-5-ил,
2H-3,4-дигидропиран-4-ил, 2H-3,4-дигидропиран-3-ил,
2H-3,4-дигидропиран-2-ил, 2H-3,4-дигидротиопиран-6-ил,
2H-3,4-дигидротиопиран-5-ил, 2H-3,4-дигидротиопиран-4-ил,
2H-3,4-дигидротиопиран-3-ил, 2H-3,4-дигидротиопиран-2-ил,
1,2,3,4-тетрагидропиридин-6-ил, 1,2,3,4-тетрагидропиридин-5-ил,
1,2,3,4-тетрагидропиридин-4-ил, 1,2,3,4-тетрагидропиридин-3-ил,
1,2,3,4-тетрагидропиридин-2-ил, 2H-5,6-дигидропиран-2-ил,
2H-5,6-дигидропиран-3-ил, 2H-5,6-дигидропиран-4-ил,
2H-5,6-дигидропиран-5-ил, 2H-5,6-дигидропиран-6-ил,
2H-5,6-дигидротиопиран-2-ил, 2H-5,6-дигидротиопиран-3-ил,
2H-5,6-дигидротиопиран-4-ил, 2H-5,6-дигидротиопиран-5-ил,
2H-5,6-дигидротиопиран-6-ил, 1,2,5,6-тетрагидропиридин-2-ил,
1,2,5,6-тетрагидропиридин-3-ил, 1,2,5,6-тетрагидропиридин-4-ил,
1,2,5,6-тетрагидропиридин-5-ил, 1,2,5,6-тетрагидропиридин-6-ил,
2,3,4,5-тетрагидропиридин-2-ил, 2,3,4,5-тетрагидропиридин-3-ил,
2,3,4,5-тетрагидропиридин-4-ил, 2,3,4,5-тетрагидропиридин-5-ил,
2,3,4,5-тетрагидропиридин-6-ил, 4H-пиран-2-ил, 4H-пиран-3-ил,
4H-пиран-4-ил, 4H-тиопиран-2-ил, 4H-тиопиран-3-ил,
4H-тиопиран-4-ил, 1,4-дигидропиридин-2-ил,
1,4-дигидропиридин-3-ил, 1,4-дигидропиридин-4-ил, 2H-пиран-2-ил,
2H-пиран-3-ил, 2H-пиран-4-ил, 2H-пиран-5-ил, 2H-пиран-6-ил,
2H-тиопиран-2-ил, 2H-тиопиран-3-ил, 2H-тиопиран-4-ил,
2H-тиопиран-5-ил, 2H-тиопиран-6-ил, 1,2-дигидропиридин-2-ил,
1,2-дигидропиридин-3-ил, 1,2-дигидропиридин-4-ил,
1,2-дигидропиридин-5-ил, 1,2-дигидропиридин-6-ил,
3,4-дигидропиридин-2-ил, 3,4-дигидропиридин-3-ил,
3,4-дигидропиридин-4-ил, 3,4-дигидропиридин-5-ил,
3,4-дигидропиридин-6-ил, 2,5-дигидропиридин-2-ил,
2,5-дигидропиридин-3-ил, 2,5-дигидропиридин-4-ил,
2,5-дигидропиридин-5-ил, 2,5-дигидропиридин-6-ил,
2,3-дигидропиридин-2-ил, 2,3-дигидропиридин-3-ил,
2,3-дигидропиридин-4-ил, 2,3-дигидропиридин-5-ил,
2,3-дигидропиридин-6-ил, 2H-5,6-дигидро-1,2-оксазин-3-ил,
2H-5,6-дигидро-1,2-оксазин-4-ил,
2H-5,6-дигидро-1,2-оксазин-5-ил,
2H-5,6-дигидро-1,2-оксазин-6-ил, 2H-5,6-дигидро-1,2-тиазин-3-ил,
2H-5,6-дигидро-1,2-тиазин-4-ил, 2H-5,6-дигидро-1,2-тиазин-5-ил,
2H-5,6-дигидро-1,2-тиазин-6-ил, 4H-5,6-дигидро-1,2-оксазин-3-ил,
4H-5,6-дигидро-1,2-оксазин-4-ил,
4H-5,6-дигидро-1,2-оксазин-5-ил,
4H-5,6-дигидро-1,2-оксазин-6-ил, 4H-5,6-дигидро-1,2-тиазин-3-ил,
4H-5,6-дигидро-1,2-тиазин-4-ил, 4H-5,6-дигидро-1,2-тиазин-5-ил,
4H-5,6-дигидро-1,2-тиазин-6-ил, 2H-3,6-дигидро-1,2-оксазин-3-ил,
2H-3,6-дигидро-1,2-оксазин-4-ил,
2H-3,6-дигидро-1,2-оксазин-5-ил,
2H-3,6-дигидро-1,2-оксазин-6-ил, 2H-3,6-дигидро-1,2-тиазин-3-ил,
2H-3,6-дигидро-1,2-тиазин-4-ил, 2H-3,6-дигидро-1,2-тиазин-5-ил,
2H-3,6-дигидро-1,2-тиазин-6-ил, 2H-3,4-дигидро-1,2-оксазин-3-ил,
2H-3,4-дигидро-1,2-оксазин-4-ил,
2H-3,4-дигидро-1,2-оксазин-5-ил,
2H-3,4-дигидро-1,2-оксазин-6-ил, 2H-3,4-дигидро-1,2-тиазин-3-ил,
2H-3,4-дигидро-1,2-тиазин-4-ил, 2H-3,4-дигидро-1,2-тиазин-5-ил,
2H-3,4-дигидро-1,2-тиазин-6-ил,
2,3,4,5-тетрагидропиридазин-3-ил,
2,3,4,5-тетрагидропиридазин-4-ил,
2,3,4,5-тетрагидропиридазин-5-ил,
2,3,4,5-тетрагидропиридазин-6-ил,
3,4,5,6-тетрагидропиридазин-3-ил,
3,4,5,6-тетрагидропиридазин-4-ил,
1,2,5,6-тетрагидропиридазин-3-ил,
1,2,5,6-тетрагидропиридазин-4-ил,
1,2,5,6-тетрагидропиридазин-5-ил,
1,2,5,6-тетрагидропиридазин-6-ил,
1,2,3,6-тетрагидропиридазин-3-ил,
1,2,3,6-тетрагидропиридазин-4-ил,
4H-5,6-дигидро-1,3-оксазин-2-ил,
4H-5,6-дигидро-1,3-оксазин-4-ил,
4H-5,6-дигидро-1,3-оксазин-5-ил,
4H-5,6-дигидро-1,3-оксазин-6-ил, 4H-5,6-дигидро-1,3-тиазин-2-ил,
4H-5,6-дигидро-1,3-тиазин-4-ил, 4H-5,6-дигидро-1,3-тиазин-5-ил,
4H-5,6-дигидро-1,3-тиазин-6-ил,
3,4,5-6-тетрагидропиримидин-2-ил,
3,4,5,6-тетрагидропиримидин-4-ил,
3,4,5,6-тетрагидропиримидин-5-ил,
3,4,5,6-тетрагидропиримидин-6-ил,
1,2,3,4-тетрагидропиразин-2-ил, 1,2,3,4-тетрагидропиразин-5-ил,
1,2,3,4-тетрагидропиримидин-2-ил,
1,2,3,4-тетрагидропиримидин-4-ил,
1,2,3,4-тетрагидропиримидин-5-ил,
1,2,3,4-тетрагидропиримидин-6-ил, 2,3-дигидро-1,4-тиазин-2-ил,
2,3-дигидро-1,4-тиазин-3-ил, 2,3-дигидро-1,4-тиазин-5-ил,
2,3-дигидро-1,4-тиазин-6-ил, 2H-1,3-оксазин-2-ил,
2H-1,3-оксазин-4-ил, 2H-1,3-оксазин-5-ил, 2H-1,3-оксазин-6-ил,
2H-1,3-тиазин-2-ил, 2H-1,3-тиазин-4-ил, 2H-1,3-тиазин-5-ил,
2H-1,3-тиазин-6-ил, 4H-1,3-оксазин-2-ил, 4H-1,3-оксазин-4-ил,
4H-1,3-оксазин-5-ил, 4H-1,3-оксазин-6-ил, 4H-1,3-тиазин-2-ил,
4H-1,3-тиазин-4-ил, 4H-1,3-тиазин-5-ил, 4H-1,3-тиазин-6-ил,
6H-1,3-оксазин-2-ил, 6H-1,3-оксазин-4-ил, 6H-1,3-оксазин-5-ил,
6H-1,3-оксазин-6-ил, 6H-1,3-тиазин-2-ил, 6H-1,3-оксазин-4-ил,
6H-1,3-оксазин-5-ил, 6H-1,3-тиазин-6-ил, 2H-1,4-оксазин-2-ил,
2H-1,4-оксазин-3-ил, 2H-1,4-оксазин-5-ил, 2H-1,4-оксазин-6-ил,
2H-1,4-тиазин-2-ил, 2H-1,4-тиазин-3-ил, 2H-1,4-тиазин-5-ил,
2H-1,4-тиазин-6-ил, 4H-1,4-оксазин-2-ил, 4H-1,4-оксазин-3-ил,
4H-1,4-тиазин-2-ил, 4H-1,4-тиазин-3-ил,
1,4-дигидропиридазин-3-ил, 1,4-дигидропиридазин-4-ил,
1,4-дигидропиридазин-5-ил, 1,4-дигидропиридазин-6-ил,
1,4-дигидропиразин-2-ил, 1,2-дигидропиразин-2-ил,
1,2-дигидропиразин-3-ил, 1,2-дигидропиразин-5-ил,
1,2-дигидропиразин-6-ил, 1,4-дигидропиримидин-2-ил,
1,4-дигидропиримидин-4-ил, 1,4-дигидропиримидин-5-ил,
1,4-дигидропиримидин-6-ил, 3,4-дигидропиримидин-2-ил,
3,4-дигидропиримидин-4-ил, 3,4-дигидропиримидин-5-ил или
3,4-дигидропиримидин-6-ил.
N-связанные 5-членные, частично ненасыщенные кольца, такие как:
2,3-дигидро-1H-пиррол-1-ил, 2,5-дигидро-1H-пиррол-1-ил,
4,5-дигидро-1H-пиразол-1-ил, 2,5-дигидро-1H-пиразол-1-ил,
2,3-дигидро-1H-пиразол-1-ил, 2,5-дигидроизоксазол-2-ил,
2,3-дигидроизоксазол-2-ил, 2,5-дигидроизотиазол-2-ил,
2,3-дигидроизоксазол-2-ил, 4,5-дигидро-1H-имидазол-1-ил,
2,5-дигидро-1H-имидазол-1-ил, 2,3-дигидро-1H-имидазол-1-ил,
2,3-дигидрооксазол-3-ил, 2,3-дигидротиазол-3-ил.
N-связанные 6-членные, частично ненасыщенные кольца, такие как:
1,2,3,4-тетрагидропиридин-1-ил, 1,2,5,6-тетрагидропиридин-1-ил,
1,4-дигидропиридин-1-ил, 1,2-дигидропиридин-1-ил,
2H-5,6-дигидро-1,2-оксазин-2-ил, 2H-5,6-дигидро-1,2-тиазин-2-ил,
2H-3,6-дигидро-1,2-оксазин-2-ил, 2H-3,6-дигидро-1,2-тиазин-2-ил,
2H-3,4-дигидро-1,2-оксазин-2-ил, 2H-3,4-дигидро-1,2-тиазин-2-ил,
2,3,4,5-тетрагидропиридазин-2-ил,
1,2,5,6-тетрагидропиридазин-1-ил,
1,2,5,6-тетрагидропиридазин-2-ил,
1,2,3,6-тетрагидропиридазин-1-ил,
3,4,5,6-тетрагидропиримидин-3-ил,
1,2,3,4-тетрагидропиразин-1-ил,
1,2,3,4-тетрагидропиримидин-1-ил,
1,2,3,4-тетрагидропиримидин-3-ил, 2,3-дигидро-1,4-тиазин-4-ил,
2H-1,2-оксазин-2-ил, 2H-1,2-тиазин-2-ил, 4H-1,4-оксазин-4-ил,
4H-1,4-тиазин-4-ил, 1,4-дигидропиридазин-1-ил,
1,4-дигидропиразин-1-ил, 1,2-дигидропиразин-1-ил,
1,4-дигидропиримидин-1-ил или 3 ,4-дигидропиримидин-3-ил;
гетарил: 5- или 6-членный ароматический гетероциклический радикал, который обычно содержит 1, 2, 3 или 4 атома азота или гетероатом, выбранный из атомов кислорода и серы, и необязательно 1, 2 или 3 атома азота в качестве членов кольца, кроме атомов углерода в качестве членов кольца, например:
C-связанные 5-членные гетероароматические радикалы, содержащие 1, 2, 3 или 4 атома азота или гетероатом, выбранный из атомов кислорода и серы, и, если целесообразно, содержащие 1, 2 или 3 атома азота в качестве членов кольца, такие как:
2-фурил, 3-фурил, 2-тиенил, 3-тиенил, пиррол-2-ил, пиррол-3-ил, пиразол-3-ил, пиразол-4-ил, изоксазол-3-ил, изоксазол-4-ил, изоксазол-5-ил, изотиазол-3-ил, изотиазол-4-ил, изотиазол-5-ил, имидазол-2-ил, имидазол-4-ил, оксазол-2-ил, оксазол-4-ил, оксазол-5-ил, тиазол-2-ил, тиазол-4-ил, тиазол-5-ил, 1,2,3-оксадиазол-4-ил, 1,2,3-оксадиазол-5-ил, 1,2,4-оксадиазол-3-ил, l,2,4-оксадиазол-5-ил, 1,3,4-оксадиазол-2-ил, 1,2,3-тиадиазол-4-ил, 1,2,3-тиадиазол-5-ил, 1,2,4-тиадиазол-3-ил, 1,2,4-тиадиазол-5-ил, 1,3,4-тиадиазолил-2-ил, 1,2,3-триазол-4-ил, 1,2,4-триазол-3-ил, тетразол-5-ил;
C-связанные 6-членные гетероароматические радикалы, содержащие 1, 2, 3 или 4 атома азота в качестве членов кольца, такие как:
пиридин-2-ил, пиридин-3-ил, пиридин-4-ил, пиридазин-3-ил, пиридазин-4-ил, пиримидин-2-ил, пиримидин-4-ил, пиримидин-5-ил, пиразин-2-ил, 1,3,5-триазин-2-ил, 1,2,4-триазин-3-ил, 1,2,4-триазин-5-ил, 1,2,4-триазин-6-ил, 1,2,4,5-тетразин-3-ил;
N-связанные 5-членные гетероароматические радикалы, содержащие 1, 2, 3 или 4 атома азота в качестве членов кольца, такие как:
пиррол-1-ил, пиразол-1-ил, имидазол-1-ил, 1,2,3-триазол-1-ил, 1,2,4-триазол-1-ил, тетразол-1-ил.
Гетероциклил также включает бициклические гетероциклы, которые содержат одно из указанных выше 5- или 6-членных гетероциклических колец и дополнительно конденсированный с ним насыщенный, ненасыщенный или ароматический карбоцикл, например, бензольное, циклогексановое, циклогексеновое или циклогексадиеновое кольцо, или дополнительно конденсированное с ним 5- или 6-членное гетероциклическое кольцо, где последнее также может быть насыщенным, ненасыщенным или ароматическим. Они включают, например, хинолинил, изохинолинил, индолил, индолизинил, изоиндолил, индазолил, бензофурил, бензотиенил, бензо[b]тиазолил, бензоксазолил, бензтиазолил и бензимидазолил. Примеры 5-6-членных гетероароматических соединений, содержащих конденсированное бензольное кольцо, включают дигидроиндолил, дигидроиндолизинил, дигидроизоиндолил, дигидрохинолинил, дигидроизохинолинил, хроменил и хроманил;
арилалкил: арильный радикал, как описано выше, который присоединен через посредство алкиленовой группы, в частности, через посредство метиленовой, 1,1-этиленовой или 1,2-этиленовой группы, например, бензил, 1-фенилэтил и 2-фенилэтил;
арилалкенил: арильный радикал, как описано выше, который присоединен через посредство алкениленовой группы, в частности через посредство 1,1-этенильной, 1,2-этенильной или 1,3-пропенильной группы, например, 2-фенилэтен-1-ил и 1-фенилэтен-1-ил;
циклоалкокси: циклоалкильный радикал, как описано выше, который присоединен через посредство атома кислорода, например, циклопропилокси, циклобутилокси, циклопентилокси или циклогексилокси;
циклоалкилалкил: циклоалкильный радикал, как описано выше, который присоединен через посредство алкиленовой группы, в частности через посредство метиленовой, 1,1-этиленовой или 1,2-этиленовой группы, например, циклопропилметил, циклобутилметил, циклопентилметил или циклогексилметил;
гетероциклилалкил и гетарилалкил: гетероциклильный или гетарильный радикал, как описано выше, который присоединен через посредство алкиленовой группы, в частности, через посредство метиленовой, 1,1-этиленовой или 1,2-этиленовой группы.
Выражение "необязательно замещенный" в контексте настоящего изобретения означает, что соответствующий фрагмент является замещенным или содержит 1, 2 или 3 заместителя (в частности, 1 заместитель), которые выбраны из галогена, C1-C4алкила, OH, SH, CN, CF3, О-CF3, COOH, О-CH2-COOH, C1-C6алкокси, C1-C6алкилтио, С3-С7циклоалкила, COO-C1-C6алкила, CONH2, CONH-C1-C6алкила, SO2NH-C1-C6алкила, CON-(C1-C6алкила)2, SO2N-(C1-C6алкила)2, NH-SO2-C1-C6алкила, NH-CO-C1-C6алкила, SO2-C1-C6алкила, O-фенила, O-CH2-фенила, CONH-фенила, SO2NH-фенила, CONH-гетарила, SO2NH-гетарила, SO2-фенила, NH-SO2-фенила, NH-CO-фенила, NH-SO2-гетарила и NH-CO-гетарила, где фенил и гетарил в последних 11 указанных радикалах являются незамещенными или могут содержать 1, 2 или 3 заместителя, которые выбраны из атома галогена, C1-C4алкила, C1-C4галогеналкила, C1-C4алкокси и C1-C4галогеналкокси.
В связи с использованием указанных соединений в качестве ингибиторов кальпаина, переменные параметры R1, R2, R4, Q, A, Y и X предпочтительно имеют следующие значения (при рассмотрении их как независимо, так и в комбинации друг с другом), где указанные параметры представляют определенные варианты осуществления соединений формулы I:
R1 представляет собой С1-С10алкил, предпочтительно С3-С10алкил, который может быть частично или полностью галогенирован и/или содержать 1, 2 или 3 заместителя R1a; в частности, незамещенный С1-С10алкил, особенно незамещенный С3-С10алкил или С3-С10алкил, который частично или полностью галогенирован и/или содержит 1, 2 или 3 заместителя R1a;
С3-С7циклоалкил-С1-С4алкил, особенно С3-С7циклоалкилметил, 1-(С3-С7циклоалкил)этил или 2-(С3-С7циклоалкил)этил, где циклоалкильный фрагмент может содержать 1, 2, 3 или 4 радикала R1b, более конкретно, циклогексилметил;
фенил-С1-С4алкил и гетарил-С1-С4алкил, в частности, бензил, 1-фенилэтил, 2-фенилэтил, гетарилметил, 1-гетарилэтил, 2-гетарилэтил, такие как тиенилметил, пиридинилметил, где фенил и гетарил в последних указанных радикалах могут быть незамещенными или могут нести 1, 2, 3 или 4 одинаковых или различных радикала R1c.
Предпочтительными среди таких соединений являются соединения общей формулы I, где R1 представляет собой С3-С10алкил, который является незамещенным или может быть частично или полностью галогенирован и/или содержит 1, 2 или 3 заместителя R1a, в частности, С3-С10алкил и наиболее предпочтительно C3-C8алкил.
Аналогично, предпочтительными среди таких соединений являются соединения общей формулы I, где R1 представляет собой фенил-С1-С4алкил или гетарил-С1-С4алкил, где фенил и гетарил в двух последних указанных радикалах являются незамещенными или несут 1, 2, 3 или 4 одинаковых или различных радикала R1c. В гетарил-С1-С4алкиле гетарильный фрагмент предпочтительно представляет собой пиридил или тиенил.
В конкретном предпочтительном варианте осуществления R1 представляет собой фенил-C1-C4алкил и наиболее предпочтительно бензил, где фенильное кольцо в фенил-C1-C4алкиле или бензиле является незамещенным или несет 1, 2, 3 или 4 одинаковых или различных радикала R1c.
В связи с этим R1a, R1b и R1c, когда присутствуют, имеют указанные выше значения. В частности:
R1a представляет собой С1-С4алкокси или С1-С4галогеналкокси;
R1b представляет собой атом галогена, С1-С4алкил, С1-С4галогеналкил, С1-С4алкокси или С1-С4галогеналкокси; и
R1c представляет собой атом галогена, С1-С4алкил, С1-С4галогеналкил, OH, SH, CN, COOH, О-CH2-COOH, C1-C6алкокси, С1-С4галогеналкокси, C1-C6алкилтио, С3-С7циклоалкил, COO-C1-C6алкил, CONH2, CONH-C1-C6алкил, SO2NH-C1-C6алкил, CON-(C1-C6алкил)2, SO2N-(C1-C6алкил)2, NH-SO2-C1-C6алкил, NH-CO-C1-C6алкил, SO2-C1-C6алкил,
O-фенил, O-CH2-фенил, CONH-фенил, SO2NH-фенил, CONH-гетарил, SO2NH-гетарил, SO2-фенил, NH-SO2-фенил, NH-CO-фенил, NH-SO2-гетарил, NH-CO-гетарил, где фенил и гетарил в последних 11 указанных радикалах являются незамещенными или могут содержать 1, 2 или 3 заместителя, которые выбраны из атома галогена, C1-C4алкила, C1-C4галогеналкила, C1-C4алкокси и C1-C4галогеналкокси,
-(CH2)p-NRc6Rc7, где p равно 0, 1, 2, 3, 4, 5 или 6, в частности 0, и -O-(CH2)q-NRc6Rc7, где q равно 2, 3, 4, 5 или 6, в частности 2, где Rc6, Rc7 независимо друг от друга представляют собой атом водорода или С1-С6алкил, или вместе с атомом азота, к которому они присоединены, представляют собой морфолиновый, пиперидиновый, пирролидиновый, азетидиновый или пиперазиновый остаток, где пять последних указанных радикалов являются незамещенными или могут нести 1, 2, 3 или 4 радикала, выбранных из C1-C4алкила, C1-C4галогеналкила, C1-C4алкокси или C1-C4галогеналкокси. R1c, в частности, представляет собой атом галогена, C1-C4алкил, C1-C4галогеналкил, особенно C1-C2фторалкил, такой как CF3, CHF2, CH2F, в частности, CF3, C1-C4алкокси или C1-C4галогеналкокси, особенно C1-C2фторалкокси, такой как O-CF3, О-CHF2 или О-CH2F, в частности, OCF3.
R2, в частности, представляет собой:
арил или гетарил, где арил и гетарил в двух последних указанных радикалах может быть незамещенным или может нести 1, 2, 3 или 4 одинаковых или различных радикала R2b.
Предпочтительными среди таких соединений являются соединения общей формулы I, где R2 выбран из арила и гетарила, в частности, из фенила, нафтила, тиенила и пиридила, и наиболее предпочтительно из фенила и нафтила, где арил и гетарил (или фенил, нафтил, тиенил и пиридил) могут быть незамещенными или могут нести 1, 2, 3 или 4, в частности 1 или 2, одинаковых или различных радикала R2b.
В связи с этим R2b, когда присутствует, имеет указанные выше значения. В частности:
R2b представляет собой атом галогена, C1-C4алкил, OH, SH, CN, CF3, О-CF3, COOH, О-CH2-COOH, С1-С6алкокси, С1-С6алкилтио, С3-С7циклоалкил, COO-С1-С6алкил, CONH2, CONH-С1-С6алкил, SO2NH-С1-С6алкил, CON-(С1-С6алкил)2, SO2N-(С1-С6алкил)2, NH-SO2-С1-С6алкил, NH-CO-С1-С6алкил, SO2-С1-С6алкил, O-фенил, O-CH2-фенил, CONH-фенил, SO2NH-фенил, CONH-гетарил, SO2NH-гетарил, SO2-фенил, NH-SO2-фенил, NH-CO-фенил, NH-SO2-гетарил, NH-CO-гетарил, где фенил и гетарил в 11 последних указанных радикалах являются незамещенными или могут содержать 1, 2 или 3 заместителя, которые выбраны из атома галогена, C1-C4алкила, C1-C4галогеналкила, C1-C4алкокси и C1-C4галогеналкокси,
-(CH2)p-NRc6Rc7, где p равно 0, 1, 2, 3, 4, 5 или 6, в частности, 0, и -O-(CH2)q-NRc6Rc7, где q равно 2, 3, 4, 5 или 6, в частности 2, где Rc6, Rc7 независимо друг от друга представляют собой атом водорода или С1-С6алкил, или вместе с атомом азота, к которому они присоединены, представляют собой морфолиновый, пиперидиновый, пирролидиновый, азетидиновый или пиперазиновый остаток, где пять последних указанных радикалов являются незамещенными или могут нести 1, 2, 3 или 4 радикала, выбранных из C1-C4алкила, C1-C4галогеналкила, C1-C4алкокси или C1-C4галогеналкокси.
R3a, R3b, в частности, представляют собой OH, или группа CR3aR3b представляет собой карбонильную группу, где последнее наиболее предпочтительно.
Q представляет собой одинарную связь или фрагмент Alk'-Z, где Z связан с R2 и предпочтительно выбран из одинарной связи, O, S и NRq, где Rq выбран из атома водорода, C1-C4алкила и C1-C4галогеналкила; и Alk' предпочтительно представляет собой линейный C1-C3алкандиил.
Особое предпочтение отдается соединениям формулы I, где Q представляет собой одинарную связь, CH2 или CH2-CH2 и, в частности, CH2 или CH2-CH2.
Х представляет собой радикал C(=O)-NRx2Rx3, где Rx2 и Rx3 имеют одно из указанных выше значений. Предпочтительными среди таких соединений являются соединения, в которых:
Rx2 представляет собой H, OH, CN, С1-С6алкил, С1-С6галогеналкил, С1-С6алкил, который содержит 1, 2 или 3 заместителя Rxa, или C2-C6алкенил, C2-C6алкинил, С3-С7циклоалкил, С3-С7циклоалкил-C1-C4алкил, С3-С7гетероциклоалкил-C1-C4алкил, С1-С6алкокси-C1-C4алкил, арил, гетарил, арил-C1-C4алкил или гетарил-C1-C4алкил, где арил и гетарил в четырех последних указанных радикалах являются незамещенными или содержат 1, 2 или 3 заместителя Rxd. В частности, Rx2 представляет собой атом водорода, С1-С6алкил, С1-С6галогеналкил, С1-С6алкил, который содержит 1 или 2 заместителя Rxa, С3-С7циклоалкил-C1-C4алкил, С3-С7гетероциклоалкил-C1-C4алкил, арил, гетарил, арил-C1-C4алкил или гетарил-C1-C4алкил;
Rx3 представляет собой H, С1-С6алкил, С1-С6галогеналкил или С1-С6алкил, который содержит 1, 2 или 3 заместителя Rxa. В частности, Rx3 представляет собой атом водорода, С1-С6алкил, С1-С6галогеналкил, С1-С6алкил, который содержит 1 или 2 заместителя Rxa. Более конкретно Rx3 предпочтительно представляет собой водород.
Соединения формулы I, которые также являются предпочтительными, представляют собой такие соединения, где группа NRx2Rx3 представляет собой азотный гетероцикл следующих формул:

где Rx5 представляет собой атом водорода или имеет значение, указанное для Rxb. В частности, Rx5 представляет собой С1-С6алкил, С1-С6галогеналкил, С1-С6алкил, который содержит 1, 2 или 3 заместителя Rxa, или С1-С6алкокси-С1-С4алкил, или COO-С1-С6алкил, CONH2, CONH-С1-С6алкил, SO2NH-С1-С6алкил, CON-(С1-С6алкил)2, SO2N-(С1-С6алкил)2, NH-SO2-С1-С6алкил, CONH-фенил, SO2NH-фенил, CONH-гетарил, SO2NH-гетарил, где фенил и гетарил в четырех последних указанных радикалах являются незамещенными или могут содержать 1, 2 или 3 заместителя, которые выбраны из атома галогена, С1-С4алкила, С1-С4галогеналкила, С1-С4алкокси и С1-С4галогеналкокси. В частности, Rx5 представляет собой атом водорода или С1-С4алкил. В данном варианте осуществления группа NRx2Rx3предпочтительно представляет собой морфолин-4-ил.
В особенно предпочтительном варианте осуществления изобретения X представляет собой C(O)-NH2.
В еще одном особенно предпочтительном варианте осуществления изобретения X представляет собой C(O)-NHRx22, где Rx22 предпочтительно выбран из С1-С4алкила, С1-С4алкокси-С1-С4алкила, гидрокси-С1-С4алкила, гидрокси-С1-С4алкокси, фенила, где фенил является незамещенным или замещен одним, двумя или тремя радикалами Rxd; фенил-С1-С4алкила, где фенильный фрагмент фенил-С1-С4алкила является незамещенным или замещен одним, двумя или тремя радикалами Rxd; гетарила, С3-С7циклоалкила и С3-С7циклоалкил-С1-С4алкила. В еще одном особенно предпочтительном варианте осуществления изобретения X представляет собой C(O)-NHRx22, где Rx22 представляет собой С3-С7гетероциклоалкил-С1-С4алкил или гетарил-С1-С4алкил, где гетероциклил представляет собой 5-, 6- или 7-членный гетероциклический радикал, который содержит в качестве членов кольца 1 или 2 гетероатома, выбранных из O, S и N, и гетарил представляет собой 5- или 6-членный гетероароматический радикал, который содержит в качестве членов кольца 1 или 2 гетероатома, выбранных из O, S и N, и где гетарильный фрагмент гетарил-С1-С4алкила является незамещенным или замещен одним, двумя или тремя радикалами Rxd. Предпочтительными примерами С3-С7гетероциклоалкил-С1-С4алкила являются тетрагидрофуран-2-илметил или тетрагидрофуран-2-илэтил. Предпочтительными примерами гетарил-С1-С4алкила являются пиридин-2-илметил, пиридин-3-илметил, пиридин-4-илметил, пиридин-2-илэтил, пиридин-3-илэтил, пиридин-4-илэтил, пиридин-2-илпропил, пиридин-3-илпропил, пиридин-4-илпропил, тиофен-2-илметил, тиофен-2-илэтил, фуран-2-илметил, фуран-2-илэтил, оксазол-2-илметил, оксазол-2-илэтил, тиазол-5-илметил, тиазол-2-илметил, тиазол-5-илэтил, тиазол-2-илэтил, тиазол-4-илметил, тиазол-4-илметил, бензотиазол-2-илметил или бензотиазол-2-илэтил.
В частности, Rx22 представляет собой С1-С4алкил, C3-C6циклоалкил, гетероциклоалкил-С1-С4алкил, фенил, фенил-С1-С4алкил или гетарил-С1-С4алкил, где фенил и гетарил в трех последних указанных радикалах являются незамещенными или содержат 1, 2 или 3 заместителя Rxd, гетарил представляет собой 5- или 6-членный гетероароматический радикал, который содержит в качестве членов кольца 1 или 2 гетероатома, выбранных из O, S и N, и гетероциклил представляет собой 5-, 6- или 7-членный гетероциклический радикал, который содержит в качестве членов кольца 1 или 2 гетероатома, выбранных из O, S и N. Rxdпредпочтительно представляет собой атом галогена, такой как атом хлора или фтора, С1-С4галогеналкил, особенно С1-С2фторалкил, такой как трифторметил, или С1-С4алкил, такой как метил или этил, или два радикала Rxd, связанные с соседними атомами С, вместе образуют фрагмент -О-CH2-O-.
Особенно предпочтительными являются соединения формулы I, где Rx22 представляет собой метил, этил, циклопропил, циклобутил, циклогексил, бензил, 2-хлорбензил, 4-трифторметилбензил, 1,3-бензодиоксол-5-илметил, 2-фенилэтил, 3-фенилпропил, пиридин-2-илметил, пиридин-2-илэтил, пиридин-2-илпропил, пиридин-4-илметил, тиофен-2-илметил, фуран-2-илметил, оксазол-2-илметил, тиазол-5-илметил, тиазол-2-илметил, бензотиазол-2-илметил, оксазол-2-илметил или тетрагидрофуран-2-ил.
В еще одном варианте осуществления изобретения X представляет собой C(=O)-N(Rx4)NRx2Rx3, где Rx4 предпочтительно представляет собой атом водорода или С1-С6алкил, в частности атом водорода. В таком варианте осуществления Rx3 предпочтительно представляет собой атом водорода. Rx2 предпочтительно представляет собой CO-арил, в частности бензоил, или арил-C1-C4алкил, в частности бензил.
В еще одном варианте осуществления изобретения X представляет собой атом водорода.
В еще одном варианте осуществления изобретения X представляет собой C(O)ORx1, где Rx1 имеет указанные выше значения. В частности, Rx1 представляет собой С1-С6алкил, С1-С6галогеналкил, С1-С6алкил, который содержит 1, 2 или 3 заместителя Rxa, или С3-С7циклоалкил, С3-С7циклоалкил-C1-C4алкил, С3-С7гетероциклоалкил-C1-C4алкил, C1-C6алкокси-C1-C4алкил, арил, гетарил, арил-C1-C4алкил или гетарил-C1-C4алкил, где арил и гетарил в четырех последних указанных радикалах являются незамещенными или содержат 1, 2 или 3 заместителя Rxd.
В связи с этим, Rxa имеет указанные выше значения и, в частности, представляет собой OH, C1-C4алкокси или C1-C4галогеналкокси. В связи с этим, Rxd имеет указанные выше значения и предпочтительно представляет собой F, Cl, OH, COOH, C(O)NH2, CN, NH2, OCH2COOH, C1-C4алкил, C1-C4галогеналкил, C1-C4алкокси, C1-C4галогеналкокси, C1-C4алкилтио, C1-C4галогеналкилтио, CO-C1-C4алкил, CO-O-C1-C4алкил, NH-C1-C4алкил, NH-C(O)C1-C4алкил или SO2-C1-C4алкил.
"А" выбран из C=O, S(=О) и S(=О)2.
В предпочтительном варианте осуществления изобретения "А" представляет собой C=O.
R4 представляет собой атом водорода. В предпочтительном варианте осуществления изобретения атом углерода, несущий радикал R4, имеет преимущественно R-конфигурацию.
В еще одном предпочтительном варианте осуществления изобретения R4 отсутствует.
"Y" представляет собой фрагмент CH2-CH2, CH2CH2CH2, N(Ry#)-CH2 или N(Ry#)-CH2-CH2 или, если R4 отсутствует, представляет собой фрагмент CH=CH-CH=, каждый из которых может содержать 1 или 2 атома водорода, замененные радикалом Ry, где радикалы Ry, которые могут быть одинаковыми или различными, и радикал Ry# имеют одно из указанных выше значений.
В предпочтительном варианте осуществления изобретения "Y" представляет собой фрагмент CH2-CH2 или CH2CH2CH2, и особенно предпочтительно фрагмент CH2-CH2, каждый из которых может содержать 1 или 2 атома водорода, замененных радикалом Ry, где
радикалы Ry могут быть одинаковыми или различными, каждый из которых имеет одно из указанных выше значений.
В еще одном предпочтительном варианте осуществления изобретения "Y" представляет собой фрагмент N(Ry#)-CH2 или N(Ry#)-CH2-CH2, каждый из которых может содержать 1 или 2 атома водорода, замененных радикалом Ry, где радикалы Ry, которые могут быть одинаковыми или различными, и радикал Ry# имеют одно из указанных выше значений. Предпочтительно N(Ry#)-CH2 и N(Ry#)-CH2-CH2, соответственно, присоединяются к переменному параметру "А" через посредство атома азота.
В предпочтительном варианте осуществления изобретения "Y" представляет собой фрагмент CH=CH-CH=, который может содержать 1 или 2 атома водорода, замененных радикалом Ry, где радикалы Ry могут быть одинаковыми или различными, и каждый имеет одно из указанных выше значений.
Циклический радикал формулы I, который включает переменный параметр "Y", предпочтительно содержит 0, 1 или 2 одинаковых или различных заместителя Ry, отличающихся от атома водорода, и более предпочтительно 0 или 1 заместитель Ry, отличающийся от атома водорода. В частности, предпочтительными являются соединения формулы I, где все заместители Ry представляют собой атом водорода.
Когда присутствует заместитель Ry, который отличается от атома водорода, его предпочтительно выбирают из OH, F, Cl, NH2, CN, CF3, CHF2, О-CF3, О-CHF2, О-CH2F, С1-С6алкила, С3-С7циклоалкила, С1-С6алкиламино, С1-С6-диалкиламино, пирролидинила, пиперидинила, морфолинила, имидазолила, C1-C4алкокси, C1-C4алкокси-C1-C4алкила, CONRy2Ry3, SO2NRy2Ry3, NH-SO2-Ry4, -(CH2)p-NRy6Ry7, NH-CO-Ry5, где p равно 0, 1, 2, 3, 4 или 5, и где Ry2, Ry3, Ry4, Ry5, Ry6, Ry7 имеют указанные выше значения, предпочтительно значения, указанные ниже в качестве предпочтительных, и в частности, представляют собой H и С1-С6алкил, фенил, бензил и O-бензил, где фенильное кольцо в трех последних указанных группах может содержать 1, 2 или 3 заместителя, выбранных из атома галогена, OH, SH, NO2, COOH, C(O)NH2, CHO, CN, NH2, OCH2COOH, С1-С6алкила, С1-С6галогеналкила, С1-С6алкокси, С1-С6галогеналкокси, С1-С6алкилтио, С1-С6галогеналкилтио, CO-С1-С6алкила, CO-O-С1-С6алкила, NH-С1-С6алкила, NHCHO, NH-C(O)С1-С6алкила и SO2-С1-С6алкила.
В частности, Ry, который отличается от атома водорода, представляет собой OH, F, Cl, NH2, CN, CF3, CHF2, О-CF3, О-CHF2, О-CH2F, С1-С6алкил, С3-С7циклоалкил, С1-С6алкиламино, С1-С6-диалкиламино, пирролидинил, пиперидинил, морфолинил, имидазолил, C1-C4алкокси, C1-C4алкокси-C1-C4алкил, CONH-С1-С6алкил, SO2N(С1-С6алкил)2, NH-SO2-С1-С6алкил, NH-CO-С1-С6алкил, (CH2)p-N(С1-С6алкил)2, где p равно 2, 3 или 4.
Ry, который отличается от атома водорода, особенно предпочтительно представляет собой F, Cl, CN, CF3, CHF2, О-CF3, О-CHF2, О-CH2F или C1-C3алкил.
Когда присутствует заместитель Ry#, который отличается от атома водорода, его предпочтительно выбирают из NH2, CN, CF3, CHF2, О-CF3, О-CHF2, О-CH2F, С1-С6алкила, С3-С7циклоалкила, С1-С6алкиламино, С1-С6-диалкиламино, пирролидинила, пиперидинила, морфолинила, имидазолила, C1-C4алкокси, C1-C4алкокси-C1-C4алкила, CONRy2Ry3, SO2NRy2Ry3, NH-SO2-Ry4, -(CH2)p-NRy6Ry7, NH-CО-Ry5, где p равно 0, 1, 2, 3, 4 или 5, и где Ry2, Ry3, Ry4, Ry5, Ry6, Ry7 имеют указанные выше значения, предпочтительно значения, указанные ниже в качестве предпочтительных, и в частности, представляют собой H и С1-С6алкил, фенил, бензил и O-бензил, где фенильное кольцо в трех последних указанных группах может содержать 1, 2 или 3 заместителя, выбранных из атома галогена, OH, SH, NO2, COOH, C(O)NH2, CHO, CN, NH2, OCH2COOH, С1-С6алкила, С1-С6галогеналкила, С1-С6алкокси, С1-С6галогеналкокси, С1-С6алкилтио, С1-С6галогеналкилтио, CO-С1-С6алкила, CO-O-С1-С6алкила, NH-С1-С6алкила, NHCHO, NH-C(O)С1-С6алкила и SO2-С1-С6алкила.
В частности, Ry#, который отличается от атома водорода, представляет собой NH2, CN, CF3, CHF2, О-CF3, О-CHF2, О-CH2F, С1-С6алкил, C3-C7циклоалкил, С1-С6алкиламино, С1-С6-диалкиламино, пирролидинил, пиперидинил, морфолинил, имидазолил, C1-C4алкокси, C1-C4алкокси-C1-C4алкил, CONH-С1-С6алкил, SO2N(С1-С6алкил)2, NH-SO2-С1-С6алкил, NH-CO-С1-С6алкил, (CH2)p-N(С1-С6алкил)2, где p равно 2, 3 или 4.
Ry#, который отличается от атома водорода, особенно предпочтительно представляет собой CF3, CHF2 или C1-C3алкил.
Более предпочтительными являются соединения формулы I, где:
"Y" представляет собой фрагмент CH2-CH2 или CH2-CH2-CH2, каждый из которых необязательно содержит 1 или 2 атома H, замененных одинаковыми или различными радикалами Ry;
Q представляет собой одинарную связь, фрагмент CH2 или CH2-CH2;
"A" представляет собой C=O;
R1 представляет собой фенил-C1-C4алкил, который является незамещенным или несет 1, 2, 3 или 4 одинаковых или различных радикала R1c;
R2 представляет собой фенил или нафтил, где фенил и нафтил могут быть незамещенными или замещены 1 или 2 одинаковыми или различными радикалами R2b,
"X" представляет собой CONH2 или CONHRx22, и
каждый из R3a и R3bпредставляет собой OH, или группа CR3aR3bпредставляет собой карбонильную группу.
Также более предпочтительными являются соединения формулы I, где:
"Y" представляет собой фрагмент CH2-CH2 или CH2-CH2-CH2, каждый из которых необязательно содержит 1 или 2 атома H, замененных одинаковыми или различными радикалами Ry;
Q представляет собой одинарную связь, фрагмент CH2 или CH2-CH2;
"A" представляет собой C=O;
R1 представляет собой C3-C8алкил;
R2 представляет собой фенил или нафтил, где фенил и нафтил могут быть незамещенными или замещены 1 или 2 одинаковыми или различными радикалами R2b,
"X" представляет собой CONH2 или CONHRx22, и
каждый из R3a и R3b представляет собой OH, или группа CR3aR3b представляет собой карбонильную группу.
Также более предпочтительными являются соединения формулы I, где:
"Y" представляет собой фрагмент CH2-CH2 или CH2-CH2-CH2, каждый из которых необязательно содержит 1 или 2 атома H, замененных одинаковыми или различными радикалами Ry;
Q представляет собой одинарную связь, фрагмент CH2 или CH2-CH2;
"A" представляет собой C=O;
R1 представляет собой фенил-C1-C4алкил, который является незамещенным или несет 1, 2, 3 или 4 одинаковых или различных радикала R1c;
R2 представляет собой фенил или нафтил, где фенил и нафтил могут быть незамещенными или замещены 1 или 2 одинаковыми или различными радикалами R2b,
"X" представляет собой C(=O)-N(Rx4)NRx2Rx3, и
каждый из R3a и R3b представляет собой OH, или группа CR3aR3b представляет собой карбонильную группу.
Также более предпочтительными являются соединения формулы I, где:
"Y" представляет собой фрагмент CH2-CH2 или CH2-CH2-CH2, каждый из которых необязательно содержит 1 или 2 атома H, замененных одинаковыми или различными радикалами Ry;
Q представляет собой одинарную связь, фрагмент CH2 или CH2-CH2;
"A" представляет собой C=O;
R1 представляет собой C3-C8алкил;
R2 представляет собой фенил или нафтил, где фенил и нафтил могут быть незамещенными или замещены 1 или 2 одинаковыми или различными радикалами R2b;
"X" представляет собой C(=O)-N(Rx4)NRx2Rx3, и
каждый из R3a и R3b представляет собой OH, или группа CR3aR3b представляет собой карбонильную группу.
Также более предпочтительными являются соединения формулы I, где:
"Y" представляет собой фрагмент N(Ry#)-CH2 или N(Ry#)-CH2-CH2, каждый из которых необязательно содержит 1 или 2 атома H, замененных одинаковыми или различными радикалами Ry;
Q представляет собой одинарную связь, фрагмент CH2 или CH2-CH2;
"A" представляет собой C=O;
R1 представляет собой фенил-C1-C4алкил, который является незамещенным или несет 1, 2, 3 или 4 одинаковых или различных радикала R1c;
R2 представляет собой фенил или нафтил, где фенил и нафтил могут быть незамещенными или замещены 1 или 2 одинаковыми или различными радикалами R2b;
"X" представляет собой CONH2 или CONHRx22, и
каждый из R3a и R3b представляет собой OH, или группа CR3aR3b представляет собой карбонильную группу.
Также более предпочтительными являются соединения формулы I, где:
"Y" представляет собой фрагмент N(Ry#)-CH2 или N(Ry#)-CH2-CH2, каждый из которых необязательно содержит 1 или 2 атома H, замененных одинаковыми или различными радикалами Ry, где N(Ry#)-CH2 и N(Ry#)-CH2-CH2, соответственно, предпочтительно связаны с переменным параметром "A" через посредство атома азота;
Q представляет собой одинарную связь, фрагмент CH2 или CH2-CH2;
"A" представляет собой C=O;
R1 представляет собой C3-C8алкил;
R2 представляет собой фенил или нафтил, где фенил и нафтил могут быть незамещенными или замещены 1 или 2 одинаковыми или различными радикалами R2b;
"X" представляет собой CONH2 или CONHRx22, и
каждый из R3a и R3b представляет собой OH, или группа CR3aR3b представляет собой карбонильную группу.
Также более предпочтительными являются соединения формулы I, где:
"Y" представляет собой фрагмент CH=CH-CH=, необязательно содержащий 1 или 2 атома H, замененных одинаковыми или различными радикалами Ry;
Q представляет собой одинарную связь, фрагмент CH2 или CH2-CH2;
"A" представляет собой C=O;
R1 представляет собой фенил-C1-C4алкил, который является незамещенным или несет 1, 2, 3 или 4 одинаковых или различных радикала R1c;
R2 представляет собой фенил или нафтил, где фенил и нафтил могут быть незамещенными или замещены 1 или 2 одинаковыми или различными радикалами R2b;
"X" представляет собой CONH2 или CONHRx22, и
каждый из R3a и R3b представляет собой OH, или группа CR3aR3b представляет собой карбонильную группу.
Также более предпочтительными являются соединения формулы I, где:
"Y" представляет собой фрагмент CH=CH-CH=, необязательно содержащий 1 или 2 атома H, замененных одинаковыми или различными радикалами Ry;
Q представляет собой одинарную связь, фрагмент CH2 или CH2-CH2;
"A" представляет собой C=O;
R1 представляет собой C3-C8алкил;
R2 представляет собой фенил или нафтил, где фенил и нафтил могут быть незамещенными или замещены 1 или 2 одинаковыми или различными радикалами R2b;
"X" представляет собой CONH2 или CONHRx22, и
каждый из R3a и R3b представляет собой OH, или группа CR3aR3b представляет собой карбонильную группу.
В других случаях радикалы Rya, Ryb Ryd, Ra1, Rb1, Rc1, Ry1, Ra2, Rb2, Rc2, Ry2, Rа3, Rb3, Rc3, Ry3, Ra4, Rb4, Rc4, Ry4, Ra5, Rb5, Rc5, Ry5, Ra6, Rb6, Rc6, Ry6, Ra7, Rb7, Rc7 и Ry7, если не указано иное, независимо друг от друга предпочтительно имеют одно из следующих значений:
Rya: C1-C4алкокси или C1-C4галогеналкокси;
Ryb: атом галогена, C1-C4алкил, C1-C4галогеналкил, C1-C4алкокси или C1-C4галогеналкокси;
Ryd: F, Cl, OH, COOH, C(O)NH2, CN, NH2, OCH2COOH, C1-C4алкил, C1-C4галогеналкил, C1-C4алкокси, C1-C4галогеналкокси, C1-C4алкилтио, C1-C4галогеналкилтио, CO-C1-C4алкил, CO-O-C1-C4алкил, NH-C1-C4алкил, NH-C(O)C1-C4алкил или SO2-C1-C4алкил;
Ra1, Rb1, Rc1, Ry1 независимо друг от друга: атом водорода, C1-C6алкил, C1-C6галогеналкил, фенил, бензил, гетарил и гетарилметил, где фенил и гетарил в четырех последних указанных радикалах являются незамещенными или содержат 1, 2 или 3 заместителя, которые выбраны из атома галогена, C1-C4алкила, C1-C4галогеналкила, C1-C4алкокси и C1-C4галогеналкокси;
Ra2, Rb2, Rc2, Ry2 независимо друг от друга: атом водорода, С1-С6алкил, фенил, бензил, гетарил и гетарилметил, где фенил и гетарил в четырех последних указанных радикалах являются незамещенными или содержат 1, 2 или 3 заместителя, которые выбраны из атома галогена, C1-C4алкила, C1-C4галогеналкила, C1-C4алкокси и C1-C4галогеналкокси;
Ra3, Rb3, Rc3, Ry3 независимо друг от друга: атом водорода или C1-C6алкил;
или Ra2 с Ra3(и аналогичным образом Rb2 с Rb3, Rc2 с Rc3 и Ry2 с Ry3) вместе с атомом азота, к которому они присоединены, представляют собой морфолиновый, пиперидиновый, пирролидиновый, азетидиновый или пиперазиновый остаток, где пять последних указанных радикала являются незамещенными или могут нести 1, 2, 3 или 4 радикала, выбранных из C1-C4алкила, C1-C4галогеналкила, C1-C4алкокси или C1-C4галогеналкокси;
Ra4, Rb4, Rc4, Ry4 независимо друг от друга: С1-С6алкил, фенил, бензил, гетарил и гетарилметил, где фенил и гетарил в четырех последних указанных радикалах являются незамещенными или содержат 1, 2 или 3 заместителя, которые выбраны из атома галогена, C1-C4алкила, C1-C4галогеналкила, C1-C4алкокси и C1-C4галогеналкокси;
Ra5, Rb5, Rc5, Ry5 независимо друг от друга: атом водорода, С1-С6алкил, фенил, бензил, гетарил и гетарилметил, где фенил и гетарил в четырех последних указанных радикалах являются незамещенными или содержат 1, 2 или 3 заместителя, которые выбраны из атома галогена, C1-C4алкила, C1-C4галогеналкила, C1-C4алкокси и C1-C4галогеналкокси;
Ra6, Rb6, Rc6, Ry6 независимо друг от друга: атом водорода, С1-С6алкил, фенил, бензил, гетарил и гетарилметил, где фенил и гетарил в четырех последних указанных радикалах являются незамещенными или содержат 1, 2 или 3 заместителя, которые выбраны из атома галогена, C1-C4алкила, C1-C4галогеналкила, C1-C4алкокси и C1-C4галогеналкокси;
Ra7, Rb7, Rc7, Ry7 независимо друг от друга: атом водорода или C1-C6алкил;
или Ra6 с Ra7 (и аналогичным образом Rb6 с Rb7, Rc6 с Rc7 и Ry6 с Ry7) вместе с атомом азота, к которому они присоединены, представляют собой морфолиновый, пиперидиновый, пирролидиновый, азетидиновый или пиперазиновый остаток, где пять последних указанных радикалов являются незамещенными или могут нести 1, 2, 3 или 4 радикала, выбранных из C1-C4алкила, C1-C4галогеналкила, C1-C4алкокси или C1-C4галогеналкокси.
Предпочтительными среди карбоксамидных соединений формулы I настоящего изобретения являются такие соединения, которые соответствуют общей формуле Ia:

где X, Y, R1, R3a, R3b, R4 и R2b имеют указанные выше значения, в частности, значения, указанные в качестве предпочтительных, и "r" равно целому числу от 0 до 4, предпочтительно от 0 до 2, и в частности, от 0 до 1. В формуле Ia переменный параметр Y предпочтительно представляет собой фрагмент CH2-CH2, CH2-CH2-CH2, N(Ry#)-CH2, N(Ry#)-CH2-CH2 или CH=CH-CH=, каждый из которых необязательно содержит 1 или 2 (предпочтительно 1) атома H, замененных одинаковыми или различными радикалами Ry. Также предпочтительными являются таутомеры соединений Ia, их фармацевтически приемлемые соли и их таутомеры.
Также предпочтительными среди карбоксамидных соединений формулы I настоящего изобретения являются такие соединения, которые соответствуют общей формуле Ib:

где X, Y, R1, R3a, R3b, R4 и R2b имеют указанные выше значения, в частности, значения, указанные в качестве предпочтительных, и "r" равно целому числу от 0 до 4, предпочтительно от 0 до 2 и, в частности, от 0 до 1. В формуле Ib переменный параметр Y предпочтительно представляет собой фрагмент CH2-CH2, CH2-CH2-CH2, N(Ry#)-CH2, N(Ry#)-CH2-CH2 или CH=CH-CH=, каждый из которых необязательно содержит 1 или 2 (предпочтительно 1) атома H, замененных одинаковыми или различными радикалами Ry. Также предпочтительными являются таутомеры соединений Ib, их фармацевтически приемлемые соли и их таутомеры.
Также предпочтительными среди карбоксамидных соединений формулы I настоящего изобретения являются такие соединения, которые соответствуют общей формуле I-A:

где X, Q, R1, R2, R3a, R3b и Ry имеют указанные выше значения, в частности, значения, указанные в качестве предпочтительных; переменный параметр "n" равен 0, 1 или 2, предпочтительно 0 или 1, и переменный параметр "q" равен 2 или 3, предпочтительно 2. В формуле I-A "Q" предпочтительно представляет собой одинарную связь, фрагмент CH2 или CH2-CH2 и особенно предпочтительно фрагмент CH2 или CH2-CH2. Переменный параметр R2 предпочтительно представляет собой фенил, который является незамещенным или несет 1-4, предпочтительно 1-2 одинаковых или различных радикала R2b. В предпочтительных соединениях формулы I-A атом углерода, отмеченный звездочкой, преимущественно имеет R-конфигурацию. Также предпочтительными являются таутомеры I-A, их фармацевтически приемлемые соли и их таутомеры.
В соединениях формулы I-A атом углерода, отмеченный звездочкой (*), является центром хиральности. Поэтому с учетом такого центра хиральности соединения I-A могут иметь R-конфигурацию или S-конфигурацию. Смеси стереоизомеров I-A, содержащие практически равные количества соединений, в которых такой центр имеет R-конфигурацию, и соединений, в которых такой центр имеет S-конфигурацию, обозначаются как rac-соединения, в то время как соединения, где в значительной степени доминирует одна конфигурация, обозначаются как R-соединение и S-соединение, соответственно.
Предпочтительные примеры соединений формулы I-A включают:
rac-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-бензил-5-оксопирролидин-2-карбоксамид,
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-бензил-5-оксопирролидин-2-карбоксамид,
(2S)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-бензил-5-оксопирролидин-2-карбоксамид,
rac-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(3-хлорбензил)-5-оксопирролидин-2-карбоксамид,
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(3-хлорбензил)-5-оксопирролидин-2-карбоксамид,
(2S)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(3-хлорбензил)-5-оксопирролидин-2-карбоксамид,
rac-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(4-фторбензил)-5-оксопирролидин-2-карбоксамид,
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(4-фторбензил)-5-оксопирролидин-2-карбоксамид,
(2S)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(4-фторбензил)-5-оксопирролидин-2-карбоксамид,
rac-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(3-метоксибензил)-5-оксопирролидин-2-карбоксамид,
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(3-метоксибензил)-5-оксопирролидин-2-карбоксамид,
(2S)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(3-метоксибензил)-5-оксопирролидин-2-карбоксамид,
rac-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(3-трифторметилбензил)-5-оксопирролидин-2-карбоксамид,
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(3-трифторметилбензил)-5-оксопирролидин-2-карбоксамид,
(2S)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(3-трифторметилбензил)-5-оксопирролидин-2-карбоксамид,
rac-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(3-фторбензил)-5-оксопирролидин-2-карбоксамид,
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(3-фторбензил)-5-оксопирролидин-2-карбоксамид,
(2S)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(3-фторбензил)-5-оксопирролидин-2-карбоксамид,
rac-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-[2-(трифторметокси)бензил]пирролидин-2-карбоксамид,
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-[2-(трифторметокси)бензил]пирролидин-2-карбоксамид,
(2S)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-[2-(трифторметокси)бензил]пирролидин-2-карбоксамид,
rac-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(нафталин-1-илметил)-5-оксопирролидин-2-карбоксамид,
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(нафталин-1-илметил)-5-оксопирролидин-2-карбоксамид,
(2S)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(нафталин-1-илметил)-5-оксопирролидин-2-карбоксамид,
rac-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(нафталин-2-илметил)-5-оксопирролидин-2-карбоксамид,
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(нафталин-2-илметил)-5-оксопирролидин-2-карбоксамид,
(2S)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(нафталин-2-илметил)-5-оксопирролидин-2-карбоксамид,
rac-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-[3-(трифторметокси)бензил]пирролидин-2-карбоксамид,
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-[3-(трифторметокси)бензил]пирролидин-2-карбоксамид,
(2S)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-[3-(трифторметокси)бензил]пирролидин-2-карбоксамид,
rac-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-бензил-6-оксопиперидин-2-карбоксамид,
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-бензил-6-оксопиперидин-2-карбоксамид,
(2S)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-бензил-6-оксопиперидин-2-карбоксамид,
rac-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-фенилпирролидин-2-карбоксамид,
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-фенилпирролидин-2-карбоксамид,
(2S)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-фенилпирролидин-2-карбоксамид,
rac-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(3-цианобензил)-5-оксопирролидин-2-карбоксамид,
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(3-цианобензил)-5-оксопирролидин-2-карбоксамид,
(2S)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(3-цианобензил)-5-оксопирролидин-2-карбоксамид,
rac-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-[2-(трифторметил)бензил]пирролидин-2-карбоксамид,
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-[2-(трифторметил)бензил]пирролидин-2-карбоксамид,
(2S)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-[2-(трифторметил)бензил]пирролидин-2-карбоксамид,
(2RS,4S)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-бензил-4-метил-5-оксопирролидин-2-карбоксамид,
(2R,4S)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-бензил-4-метил-5-оксопирролидин-2-карбоксамид,
(2S,4S)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-бензил-4-метил-5-оксопирролидин-2-карбоксамид,
rac-1-бензил-N-{3,4-диоксо-1-фенил-4-[(пиридин-2-илметил)амино]бутан-2-ил}-5-оксопирролидин-2-карбоксамид,
(2R)-1-бензил-N-{3,4-диоксо-1-фенил-4-[(пиридин-2-илметил)амино]бутан-2-ил}-5-оксопирролидин-2-карбоксамид,
(2S)-1-бензил-N-{3,4-диоксо-1-фенил-4-[(пиридин-2-илметил)амино]бутан-2-ил}-5-оксопирролидин-2-карбоксамид,
rac-1-бензил-N-[4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил]-5-оксопирролидин-2-карбоксамид,
(2R)-1-бензил-N-[4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил]-5-оксопирролидин-2-карбоксамид,
(2S)-1-бензил-N-[4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил]-5-оксопирролидин-2-карбоксамид,
rac-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(3,5-диметоксибензил)-5-оксопирролидин-2-карбоксамид,
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(3,5-диметоксибензил)-5-оксопирролидин-2-карбоксамид,
(2S)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(3,5-диметоксибензил)-5-оксопирролидин-2-карбоксамид,
rac-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(пиридин-4-илметил)пирролидин-2-карбоксамид,
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(пиридин-4-илметил)пирролидин-2-карбоксамид,
(2S)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(пиридин-4-илметил)пирролидин-2-карбоксамид,
rac-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(3,5-дифторбензил)-5-оксопирролидин-2-карбоксамид,
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(3,5-дифторбензил)-5-оксопирролидин-2-карбоксамид,
(2S)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(3,5-дифторбензил)-5-оксопирролидин-2-карбоксамид,
rac-1-бензил-N-(4-(метиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2R)-1-бензил-N-(4-(метиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2S)-1-бензил-N-(4-(метиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
rac-1-бензил-N-(3,4-диоксо-1-фенил-4-(пропиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2R)-1-бензил-N-(3,4-диоксо-1-фенил-4-(пропиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2S)-1-бензил-N-(3,4-диоксо-1-фенил-4-(пропиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
rac-1-бензил-N-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2R)-1-бензил-N-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2S)-1-бензил-N-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
rac-1-бензил-N-(4-(изобутиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2R)-1-бензил-N-(4-(изобутиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2S)-1-бензил-N-(4-(изобутиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
rac-1-бензил-N-(4-(циклобутиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2R)-1-бензил-N-(4-(циклобутиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2S)-1-бензил-N-(4-(циклобутиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
rac-1-бензил-N-(4-(метоксиамино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2R)-1-бензил-N-(4-(метоксиамино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2S)-1-бензил-N-(4-(метоксиамино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
rac-1-бензил-N-(3,4-диоксо-1-фенил-4-(2-(пиридин-2-ил)этиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2R)-1-бензил-N-(3,4-диоксо-1-фенил-4-(2-(пиридин-2-ил)этиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2S)-1-бензил-N-(3,4-диоксо-1-фенил-4-(2-(пиридин-2-ил)этиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
rac-1-бензил-N-(3,4-диоксо-1-фенил-4-(3-(пиридин-2-ил)пропиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2R)-1-бензил-N-(3,4-диоксо-1-фенил-4-(3-(пиридин-2-ил)пропиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2S)-1-бензил-N-(3,4-диоксо-1-фенил-4-(3-(пиридин-2-ил)пропиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
rac-1-бензил-N-(3,4-диоксо-1-фенил-4-(3-фенилпропиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2R)-1-бензил-N-(3,4-диоксо-1-фенил-4-(3-фенилпропиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2S)-1-бензил-N-(3,4-диоксо-1-фенил-4-(3-фенилпропиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
rac-1-бензил-N-(4-(этил(метил)амино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2R)-1-бензил-N-(4-(этил(метил)амино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2S)-1-бензил-N-(4-(этил(метил)амино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
rac-1-бензил-N-(4-(2-хлорбензиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2R)-1-бензил-N-(4-(2-хлорбензиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2S)-1-бензил-N-(4-(2-хлорбензиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
rac-N-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамид,
(2R)-N-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамид,
(2S)-N-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамид,
rac-N-(4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамид,
(2R)-N-(4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамид,
(2S)-N-(4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамид,
rac-N-(4-(бензиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамид,
(2R)-N-(4-(бензиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамид,
(2S)-N-(4-(бензиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамид,
rac-N-(4-(изопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамид,
(2R)-N-(4-(изопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамид,
(2S)-N-(4-(изопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамид,
rac-N-(3,4-диоксо-1-фенил-4-(2-(пиридин-2-ил)этиламино)бутан-2-ил)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамид,
(2R)-N-(3,4-диоксо-1-фенил-4-(2-(пиридин-2-ил)этиламино)бутан-2-ил)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамид,
(2S)-N-(3,4-диоксо-1-фенил-4-(2-(пиридин-2-ил)этиламино)бутан-2-ил)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамид,
rac-N-(3,4-диоксо-1-фенил-4-(3-(пиридин-2-ил)пропиламино)бутан-2-ил)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамид,
(2R)-N-(3,4-диоксо-1-фенил-4-(3-(пиридин-2-ил)пропиламино)бутан-2-ил)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамид,
(2S)-N-(3,4-диоксо-1-фенил-4-(3-(пиридин-2-ил)пропиламино)бутан-2-ил)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамид,
rac-N-(4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-(2-метокси-6-(трифторметил)бензил)-5-оксопирролидин-2-карбоксамид,
(2R)-N-(4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-(2-метокси-6-(трифторметил)бензил)-5-оксопирролидин-2-карбоксамид,
(2S)-N-(4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-(2-метокси-6-(трифторметил)бензил)-5-оксопирролидин-2-карбоксамид,
rac-N-(3,4-диоксо-1-фенил-4-(пиридин-2-илметиламино)бутан-2-ил)-1-(2-метокси-6-(трифторметил)бензил)-5-оксопирролидин-2-карбоксамид,
(2R)-N-(3,4-диоксо-1-фенил-4-(пиридин-2-илметиламино)бутан-2-ил)-1-(2-метокси-6-(трифторметил)бензил)-5-оксопирролидин-2-карбоксамид,
(2S)-N-(3,4-диоксо-1-фенил-4-(пиридин-2-илметиламино)бутан-2-ил)-1-(2-метокси-6-(трифторметил)бензил)-5-оксопирролидин-2-карбоксамид,
rac-N-(4-(бензиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-(2-метокси-6-(трифторметил)бензил)-5-оксопирролидин-2-карбоксамид,
(2R)-N-(4-(бензиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-(2-метокси-6-(трифторметил)бензил)-5-оксопирролидин-2-карбоксамид,
(2S)-N-(4-(бензиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-(2-метокси-6-(трифторметил)бензил)-5-оксопирролидин-2-карбоксамид,
rac-N-(3,4-диоксо-1-фенил-4-(2-(пиридин-2-ил)этиламино)бутан-2-ил)-5-оксо-1-(2-(трифторметокси)бензил)пирролидин-2-карбоксамид,
(2R)-N-(3,4-диоксо-1-фенил-4-(2-(пиридин-2-ил)этиламино)бутан-2-ил)-5-оксо-1-(2-(трифторметокси)бензил)пирролидин-2-карбоксамид,
(2S)-N-(3,4-диоксо-1-фенил-4-(2-(пиридин-2-ил)этиламино)бутан-2-ил)-5-оксо-1-(2-(трифторметокси)бензил)пирролидин-2-карбоксамид,
rac-1-(2-хлорбензил)-N-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2R)-1-(2-хлорбензил)-N-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2S)-1-(2-хлорбензил)-N-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
rac-1-(2-хлорбензил)-N-(4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2R)-1-(2-хлорбензил)-N-(4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2S)-1-(2-хлорбензил)-N-(4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
rac-N-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-(2,6-дифторбензил)-5-оксопирролидин-2-карбоксамид,
(2R)-N-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-(2,6-дифторбензил)-5-оксопирролидин-2-карбоксамид,
(2S)-N-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-(2,6-дифторбензил)-5-оксопирролидин-2-карбоксамид,
rac-1-(2,6-дифторбензил)-N-(4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2R)-1-(2,6-дифторбензил)-N-(4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2S)-1-(2,6-дифторбензил)-N-(4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
rac-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-[2-метокси-6-(трифторметил)бензил]пирролидин-2-карбоксамид,
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-[2-метокси-6-(трифторметил)бензил]пирролидин-2-карбоксамид,
(2S)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-[2-метокси-6-(трифторметил)бензил]пирролидин-2-карбоксамид,
rac-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(2,6-дифторбензил)пирролидин-2-карбоксамид,
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(2,6-дифторбензил)пирролидин-2-карбоксамид,
(2S)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(2,6-дифторбензил)пирролидин-2-карбоксамид,
rac-1-бензил-N-(3,4-диоксо-1-фенил-4-(2-фенилэтиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2R)-1-бензил-N-(3,4-диоксо-1-фенил-4-(2-фенилэтиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2S)-1-бензил-N-(3,4-диоксо-1-фенил-4-(2-фенилэтиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
rac-1-бензил-N-(3,4-диоксо-1-фенил-4-(тиазол-5-илметиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2R)-1-бензил-N-(3,4-диоксо-1-фенил-4-(тиазол-5-илметиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2S)-1-бензил-N-(3,4-диоксо-1-фенил-4-(тиазол-5-илметиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
rac-N-(4-(бензо[d]тиазол-2-илметиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-бензил-5-оксопирролидин-2-карбоксамид,
(2R)-N-(4-(бензо[d]тиазол-2-илметиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-бензил-5-оксопирролидин-2-карбоксамид,
(2S)-N-(4-(бензо[d]тиазол-2-илметиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-бензил-5-оксопирролидин-2-карбоксамид,
rac-1-бензил-N-(4-морфолино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2R)-1-бензил-N-(4-морфолино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2S)-1-бензил-N-(4-морфолино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
rac-N-(4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(4-(трифторметил)бензил)пирролидин-2-карбоксамид,
(2R)-N-(4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(4-(трифторметил)бензил)пирролидин-2-карбоксамид,
(2S)-N-(4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(4-(трифторметил)бензил)пирролидин-2-карбоксамид,
rac-1-бензил-N-(4-(циклогексиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2R)-1-бензил-N-(4-(циклогексиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2S)-1-бензил-N-(4-(циклогексиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
rac-N-(4-(2-бензоилгидразинил)-3,4-диоксо-1-фенилбутан-2-ил)-1-бензил-5-оксопирролидин-2-карбоксамид,
(2R)-N-(4-(2-бензоилгидразинил)-3,4-диоксо-1-фенилбутан-2-ил)-1-бензил-5-оксопирролидин-2-карбоксамид,
(2S)-N-(4-(2-бензоилгидразинил)-3,4-диоксо-1-фенилбутан-2-ил)-1-бензил-5-оксопирролидин-2-карбоксамид,
rac-N-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(4-(трифторметил)бензил)пирролидин-2-карбоксамид,
(2R)-N-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(4-(трифторметил)бензил)пирролидин-2-карбоксамид,
(2S)-N-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(4-(трифторметил)бензил)пирролидин-2-карбоксамид,
rac-1-бензил-N-(3,4-диоксо-1-фенил-4-(тиазол-2-илметиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2R)-1-бензил-N-(3,4-диоксо-1-фенил-4-(тиазол-2-илметиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2S)-1-бензил-N-(3,4-диоксо-1-фенил-4-(тиазол-2-илметиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
rac-1-бензил-N-(3,4-диоксо-1-фенил-4-(тиофен-2-илметиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2R)-1-бензил-N-(3,4-диоксо-1-фенил-4-(тиофен-2-илметиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2S)-1-бензил-N-(3,4-диоксо-1-фенил-4-(тиофен-2-илметиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
rac-N-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-(2,6-дихлорбензил)-5-оксопирролидин-2-карбоксамид,
(2R)-N-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-(2,6-дихлорбензил)-5-оксопирролидин-2-карбоксамид,
(2S)-N-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-(2,6-дихлорбензил)-5-оксопирролидин-2-карбоксамид,
rac-1-(2,6-дихлорбензил)-N-(4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2R)-1-(2,6-дихлорбензил)-N-(4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2S)-1-(2,6-дихлорбензил)-N-(4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
rac-1-бензил-N-(3,4-диоксо-1-фенил-4-(пиридин-4-илметиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2R)-1-бензил-N-(3,4-диоксо-1-фенил-4-(пиридин-4-илметиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2S)-1-бензил-N-(3,4-диоксо-1-фенил-4-(пиридин-4-илметиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
rac-1-бензил-N-(4-(оксазол-2-илметиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2R)-1-бензил-N-(4-(оксазол-2-илметиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2S)-1-бензил-N-(4-(оксазол-2-илметиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
rac-1-бензил-N-(3,4-диоксо-1-фенил-4-(фениламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2R)-1-бензил-N-(3,4-диоксо-1-фенил-4-(фениламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(S)-1-бензил-N-(3,4-диоксо-1-фенил-4-(фениламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
rac-N-(4-(бензо[d][1,3]диоксол-5-илметиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-бензил-5-оксопирролидин-2-карбоксамид,
(2R)-N-(4-(бензо[d][1,3]диоксол-5-илметиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-бензил-5-оксопирролидин-2-карбоксамид,
(2S)-N-(4-(бензо[d][1,3]диоксол-5-илметиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-бензил-5-оксопирролидин-2-карбоксамид,
rac-1-бензил-N-(4-(4-фторбензиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2R)-1-бензил-N-(4-(4-фторбензиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2S)-1-бензил-N-(4-(4-фторбензиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
rac-1-бензил-N-(3,4-диоксо-1-фенил-4-(4-(трифторметил)бензиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2R)-1-бензил-N-(3,4-диоксо-1-фенил-4-(4-(трифторметил)бензиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2S)-1-бензил-N-(3,4-диоксо-1-фенил-4-(4-(трифторметил)бензиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
rac-1-бензил-N-(3,4-диоксо-1-фенил-4-(((R)-тетрагидрофуран-2-ил)метиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2R)-1-бензил-N-(3,4-диоксо-1-фенил-4-(((R)-тетрагидрофуран-2-ил)метиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2S)-1-бензил-N-(3,4-диоксо-1-фенил-4-(((R)-тетрагидрофуран-2-ил)метиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
rac-1-бензил-N-(3,4-диоксо-1-фенил-4-(((S)-тетрагидрофуран-2-ил)метиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2R)-1-бензил-N-(3,4-диоксо-1-фенил-4-(((S)-тетрагидрофуран-2-ил)метиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2S)-1-бензил-N-(3,4-диоксо-1-фенил-4-(((S)-тетрагидрофуран-2-ил)метиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
rac-1-бензил-N-(3,4-диоксо-1-фенил-4-(2-(тиофен-3-ил)этиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2R)-1-бензил-N-(3,4-диоксо-1-фенил-4-(2-(тиофен-3-ил)этиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2S)-1-бензил-N-(3,4-диоксо-1-фенил-4-(2-(тиофен-3-ил)этиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид,
rac-1-бензил-N-(4-(фуран-2-илметиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2R)-1-бензил-N-(4-(фуран-2-илметиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2S)-1-бензил-N-(4-(фуран-2-илметиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
rac-1-бензил-N-(4-(2-бензилгидразинил)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2R)-1-бензил-N-(4-(2-бензилгидразинил)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
(2S)-1-бензил-N-(4-(2-бензилгидразинил)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид,
rac-N-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-(2-метокси-6-(трифторметил)бензил)-5-оксопирролидин-2-карбоксамид,
(2R)-N-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-(2-метокси-6-(трифторметил)бензил)-5-оксопирролидин-2-карбоксамид и
(2S)-N-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-(2-метокси-6-(трифторметил)бензил)-5-оксопирролидин-2-карбоксамид.
Также предпочтительными среди карбоксамидных соединений формулы I настоящего изобретения являются такие соединения, которые соответствуют общей формуле I-B:

где X, Q, R1, R2, R3a, R3b, Ry и Ry# имеют указанные выше значения, в частности значения, указанные в качестве предпочтительных, переменный параметр "n" равен 0, 1 или 2, предпочтительно 0 или 1, и переменный параметр "s" равен 1 или 2, предпочтительно 1. В формуле I-В Q предпочтительно представляет собой одинарную связь, фрагмент CH2 или CH2-CH2 и особенно предпочтительно фрагмент CH2 или CH2-CH2. Переменный параметр R2 предпочтительно представляет собой фенил, которое является незамещенным или несет 1-4, предпочтительно 1-2 одинаковых или различных радикалов R2b. В предпочтительных соединениях формулы I-B атом углерода, отмеченный звездочкой, преимущественно имеет R-конфигурацию. Также предпочтительными являются таутомеры I-B, их фармацевтически приемлемые соли и их таутомеры.
В соединениях формулы I-B атом углерода, отмеченный звездочкой (*), является центром хиральности. Поэтому с учетом такого центра хиральности соединения I-B могут иметь R-конфигурацию или S-конфигурацию. Смеси стереоизомеров I-B, содержащие практически равные количества соединений, в которых такой центр имеет R-конфигурацию, и соединений, в которых такой центр имеет S-конфигурацию, обозначаются как rac-соединения, в то время как соединения, где в значительной степени доминирует одна конфигурация, обозначаются как R-соединение и S-соединение, соответственно.
Предпочтительные примеры соединений формулы I-B включают:
rac-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-3-бензил-1-метил-2-оксоимидазолидин-4-карбоксамид,
(4R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-3-бензил-1-метил-2-оксоимидазолидин-4-карбоксамид,
(4S)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-3-бензил-1-метил-2-оксоимидазолидин-4-карбоксамид.
Также предпочтительными среди карбоксамидных соединений формулы I настоящего изобретения являются такие соединения, которые соответствуют общей формуле I-С:

где X, Q, R1, R2, R3a, R3b и Ry имеют указанные выше значения, в частности значения, указанные в качестве предпочтительных, переменный параметр "n" равен 0, 1 или 2 и предпочтительно 0 или 1. В формуле I-С Q предпочтительно представляет собой одинарную связь, фрагмент CH2 или CH2-CH2 и особенно предпочтительно фрагмент CH2 или CH2-CH2. Переменный параметр R2 предпочтительно представляет собой фенил, который является незамещенным или несет 1-4, предпочтительно 1-2 одинаковых или различных радикала R2b. Также предпочтительными являются таутомеры I-С, их фармацевтически приемлемые соли и их таутомеры.
Предпочтительные примеры соединений формулы I-С включают:
N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-бензил-6-оксо-1,6-дигидропиридин-2-карбоксамид.
Предпочтительные примеры соединений формулы I, где Y представляет собой CH2-CH2, A представляет собой SO2, и Q представляет собой CH2, включают:
1,1-диоксид N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-2-бензилизотиазолидин-3-карбоксамида,
1,1-диоксид (3R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-2-бензилизотиазолидин-3-карбоксамида и
1,1-диоксид (3S)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-2-бензилизотиазолидин-3-карбоксамида.
В свою очередь предпочтительными среди карбоксамидных соединений формулы I-А настоящего изобретения являются соединения, которые соответствуют общим формулам Ia-А, Ia-В или Ia-С:


где n, q, s, r, Ry, Ry#, R2b, X, R1, R3a и R3b имеют указанные выше значения, в частности значения, указанные в качестве предпочтительных.
В свою очередь предпочтительными среди карбоксамидных соединений формулы I-В настоящего изобретения являются соединения, которые соответствуют общим формулам Ib-А, Ib-В или Ib-С
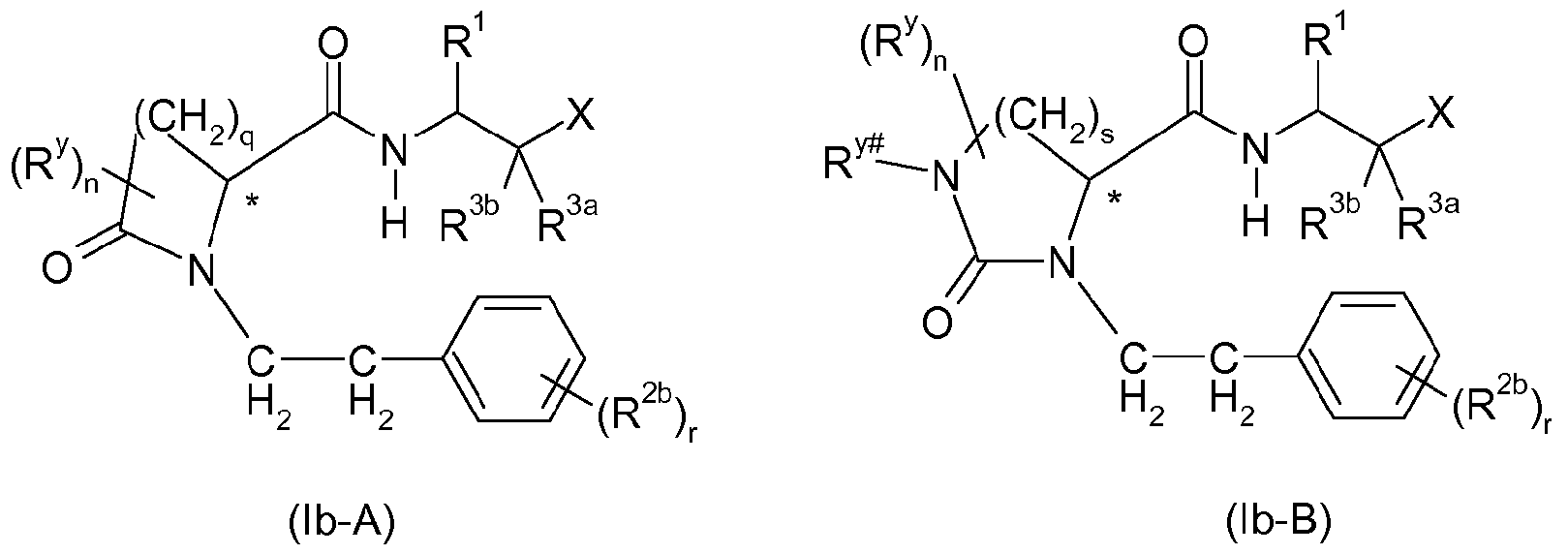

где n, q, r, s, Ry, Ry#, R2b, X, R1, R3a и R3b имеют указанные выше значения, в частности, значения, указанные в качестве предпочтительных.
Соединения общих формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', которые указаны ниже в таблицах 1-228, и в которых CR3aR3b представляет собой карбонильную функциональную группу или группу C(OH)2, и их таутомеры, пролекарства и фармацевтически приемлемые соли, сами по себе представляют предпочтительные варианты осуществления настоящего изобретения. Формулы I-А'.rac, I-А".rac, I-B'.rac и I-B".rac обозначают карбоксамидные соединения I-A и I-B, которые преимущественно имеют R/S-конфигурацию на атоме углерода, отмеченном звездочкой, что проиллюстрировано с помощью ломаных линий. С другой стороны, формулы I-А'.R, I-A"R, I-B'.R и I-B".R обозначают карбоксамидные соединения I-A и I-B, которые имеют преимущественно R-конфигурацию на соответствующем атоме углерода, что проиллюстрировано с помощью штриховых клинообразных линий. Звездочка указывает на стереоцентр. Значения R1 и R2, указанные ниже в таблице A, представляют варианты осуществления изобретения, которые независимо друг от друга также являются предпочтительными, особенно в комбинации.




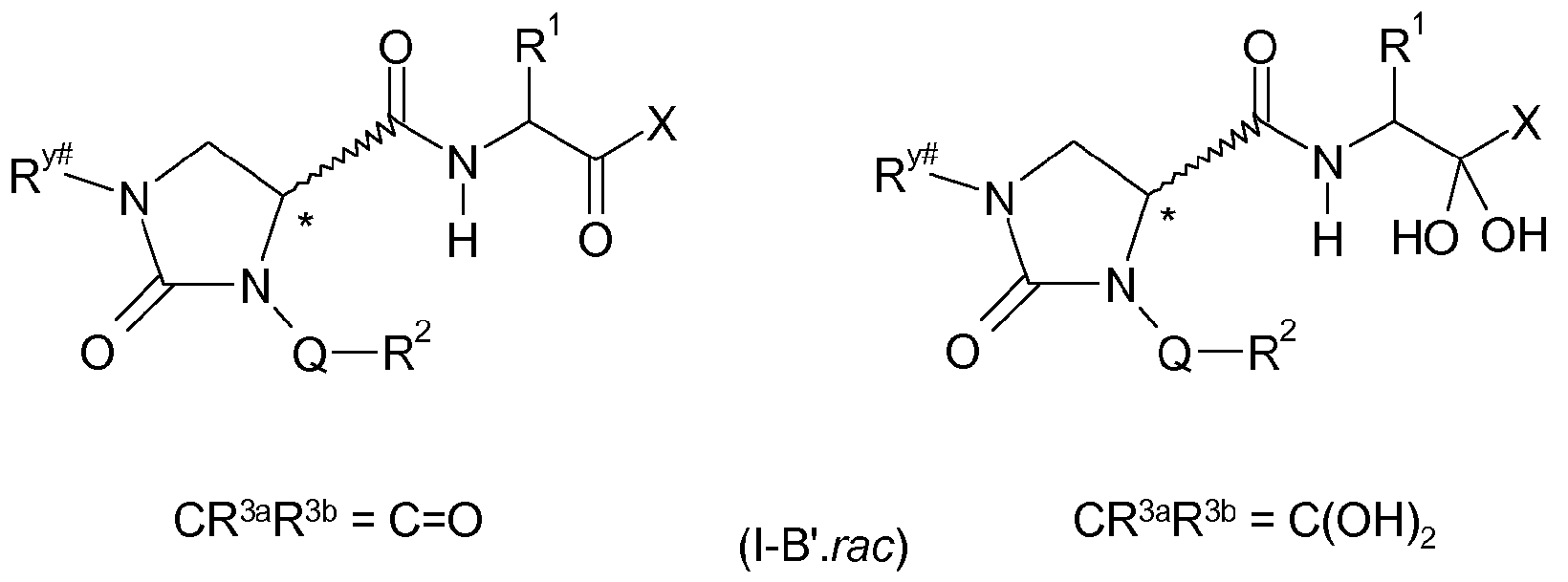





Таблица 1
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой карбамоил, Ry' и Ry#, соответственно, представляет собой атом водорода, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 2
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, X представляет собой карбамоил, Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой одинарную связь, и комбинация R1и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 3
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, X представляет собой карбамоил, Ry' и Ry#, соответственно, представляет собой CN, Q представляет собой одинарную связь, и комбинация R1 и R2для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 4
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой карбамоил, Ry' представляет собой Cl, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 5
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой карбамоил, Ry' представляет собой F, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 6
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой -C(O)NHCH3, Ry' и Ry#, соответственно, представляет собой атом водорода, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 7
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой -C(O)NHCH3, Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 8
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой -C(O)NHCH3, Ry' и Ry#, соответственно, представляет собой CN, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 9
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой -C(O)NHCH3, Ry' представляет собой Cl, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 10
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой -C(O)NHCH3, Ry' представляет собой F, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 11
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой карбамоил, Ry' и Ry#, соответственно, представляет собой водород, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 12
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой карбамоил, Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 13
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой карбамоил, Ry' и Ry#, соответственно, представляет собой CN, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 14
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой карбамоил, Ry' представляет собой Cl, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 15
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой карбамоил, Ry' представляет собой F, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 16
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой -C(O)NHCH3, Ry' и Ry#, соответственно, представляет собой атом водорода, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 17
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой -C(O)NHCH3, Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 18
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой -C(O)NHCH3, Ry' и Ry#, соответственно, представляет собой CN, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 19
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой -C(O)NHCH3, Ry' представляет собой Cl, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 20
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой -C(O)NHCH3, Ry' представляет собой F, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 21
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой карбамоил, Ry' и Ry#, соответственно, представляет собой атом водорода, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 22
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой карбамоил, Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 23
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой карбамоил, Ry' и Ry#, соответственно, представляет собой CN, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 24
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой карбамоил, Ry' представляет собой Cl, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 25
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой карбамоил, Ry' представляет собой F, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 26
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой -C(O)NHCH3, Ry' и Ry#, соответственно, представляет собой атом водорода, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 27
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой -C(O)NHCH3, Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 28
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой -C(O)NHCH3, Ry' и Ry#, соответственно, представляет собой CN, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 29
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой -C(O)NHCH3, Ry' представляет собой Cl, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 30
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой -C(O)NHCH3, Ry' представляет собой F, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 31
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой карбамоил, Ry' и Ry#, соответственно, представляет собой атом водорода, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 32
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой карбамоил, Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 33
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой карбамоил, Ry' и Ry#, соответственно, представляет собой CN, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 34
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой карбамоил, Ry' представляет собой Cl, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 35
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой карбамоил, Ry' представляет собой F, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 36
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой -C(O)NHCH3, Ry' и Ry#, соответственно, представляет собой атом водорода, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 37
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой -C(O)NHCH3, Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 38
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой -C(O)NHCH3, Ry' и Ry#, соответственно, представляет собой CN, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 39
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой -C(O)NHCH3, Ry' представляет собой Cl, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 40
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой -C(O)NHCH3, Ry' представляет собой F, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 41
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой карбамоил, Ry' и Ry#, соответственно, представляет собой атом водорода, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 42
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой карбамоил, Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 43
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой карбамоил, Ry' и Ry#, соответственно, представляет собой CN, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 44
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой карбамоил, Ry' представляет собой Cl, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 45
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой карбамоил, Ry' представляет собой F, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 46
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой -C(O)NHCH3, Ry' и Ry#, соответственно, представляет собой атом водорода, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 47
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой -C(O)NHCH3, Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 48
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой -C(O)NHCH3, Ry' и Ry#, соответственно, представляет собой CN, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 49
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой -C(O)NHCH3, Ry' представляет собой Cl, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 50
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой -C(O)NHCH3, Ry' представляет собой F, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 51
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой карбамоил, Ry' и Ry#, соответственно, представляет собой атом водорода, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 52
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой карбамоил, Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 53
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой карбамоил, Ry' и Ry#, соответственно, представляет собой CN, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 54
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой карбамоил, Ry' представляет собой Cl, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 55
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой карбамоил, Ry' представляет собой F, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 56
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой -C(O)NHCH3, Ry' и Ry#, соответственно, представляет собой атом водорода, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 57
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой -C(O)NHCH3, Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 58
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой -C(O)NHCH3, Ry' и Ry#, соответственно, представляет собой CN, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 59
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой -C(O)NHCH3, Ry'представляет собой Cl, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 60
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой -C(O)NHCH3, Ry' представляет собой F, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 61
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой -C(O)NH-циклопропил, Ry' и Ry#, соответственно, представляет собой атом водорода, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 62
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой -C(O)NH-циклопропил, Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 63
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой -C(O)NH-циклопропил, Ry' и Ry#, соответственно, представляет собой CN, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 64
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой -C(O)-NH-циклопропил, Ry' представляет собой Cl, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 65
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой -C(O)NH-циклопропил, Ry' представляет собой F, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 66
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой -C(O)NH-циклопропил, Ry' и Ry#, соответственно, представляет собой атом водорода, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 67
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой -C(O)NH-циклопропил, Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 68
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой -C(O)NH-циклопропил, Ry' и Ry#, соответственно, представляет собой CN, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 69
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой -С(O)NH-циклопропил, Ry' представляет собой Cl, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 70
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой -C(O)NH-циклопропил, Ry' представляет собой F, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 71
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой -C(O)NH-циклопропил, Ry' и Ry#, соответственно, представляет собой атом водорода, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 72
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой -C(O)NH-циклопропил, Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 73
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой -C(O)NH-циклопропил, Ry' и Ry#, соответственно, представляет собой CN, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 74
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой -C(O)NH-циклопропил, Ry' представляет собой Cl, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 75
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой -C(O)NH-циклопропил, Ry' представляет собой F, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 76
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой -C(O)NH-циклопропил, Ry' и Ry#, соответственно, представляет собой атом водорода, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 77
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой -C(O)NH-циклопропил, Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 78
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой -C(O)NH-циклопропил, Ry' и Ry#, соответственно, представляет собой CN, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 79
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой -C(O)NH-циклопропил, Ry' представляет собой Cl, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 80
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой -C(O)NH-циклопропил, Ry' представляет собой F, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 81
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой -C(O)NH-циклопропил, Ry' и Ry#, соответственно, представляет собой атом водорода, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 82
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой -C(O)NH-циклопропил, Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 83
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой -C(O)NH-циклопропил, Ry' и Ry#, соответственно, представляет собой CN, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 84
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой -C(O)NH-циклопропил, Ry' представляет собой Cl, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 85
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой -C(O)NH-циклопропил, Ry' представляет собой F, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 86
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH-циклопропил, Ry' и Ry#, соответственно, представляет собой атом водорода, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 87
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH-циклопропил, Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 88
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH-циклопропил, Ry' и Ry#, соответственно, представляет собой CN, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 89
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH-циклопропил, Ry' представляет собой Cl, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 90
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH-циклопропил, Ry' представляет собой F, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 91
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(бензил), Ry'и Ry#, соответственно, представляет собой атом водорода, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 92
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(бензил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 93
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(бензил), Ry' и Ry#, соответственно, представляет собой CN, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 94
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(бензил), Ry' представляет собой Cl, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 95
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(бензил), Ry' представляет собой F, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 96
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(бензил), Ry' и Ry#, соответственно, представляет собой атом водорода, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 97
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(бензил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 98
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(бензил), Ry' и Ry#, соответственно, представляет собой CN, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 99
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(бензил), Ry' представляет собой Cl, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 100
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(бензил), Ry' представляет собой F, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 101
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(бензил), Ry' и Ry#, соответственно, представляет собой атом водорода, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 102
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(бензил), Ry'и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 103
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(бензил), Ry' и Ry#, соответственно, представляет собой CN, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 104
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(бензил), Ry' представляет собой Cl, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 105
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(бензил), Ry' представляет собой F, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 106
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(бензил), Ry' и Ry#, соответственно, представляет собой атом водорода, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 107
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(бензил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 108
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(бензил), Ry' и Ry#, соответственно, представляет собой CN, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 109
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(бензил), Ry' представляет собой Cl, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 110
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(бензил), Ry' представляет собой F, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 111
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(бензил), Ry' и Ry#, соответственно, представляет собой атом водорода, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 112
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(бензил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 113
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(бензил), Ry' и Ry#, соответственно, представляет собой CN, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 114
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(бензил), Ry' представляет собой Cl, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 115
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(бензил), Ry' представляет собой F, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 116
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(бензил), Ry' и Ry#, соответственно, представляет собой атом водорода, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 117
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(бензил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 118
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(бензил), Ry' и Ry#, соответственно, представляет собой CN, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 119
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(бензил), Ry' представляет собой Cl, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 120
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(бензил), Ry' представляет собой F, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 121
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(О)NH(4-трифторметилбензил), Ry'и Ry#, соответственно, представляет собой атом водорода, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 122
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(О)NH(4-трифторметилбензил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 123
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(4-трифторметилбензил), Ry' и Ry#, соответственно, представляет собой CN, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 124
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(4-трифторметилбензил), Ry' представляет собой Cl, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 125
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(4-трифторметилбензил), Ry' представляет собой F, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 126
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(О)NH(4-трифторметилбензил), Ry' и Ry#, соответственно, представляет собой атом водорода, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 127
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(4-трифторметилбензил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 128
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(О)NH(4-трифторметилбензил), Ry' и Ry#, соответственно, представляет собой CN, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 129
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(4-трифторметилбензил), Ry' представляет собой Cl, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 130
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(4-трифторметилбензил), Ry' представляет собой F, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 131
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(О)NH(4-трифторметилбензил), Ry' и Ry#, соответственно, представляет собой атом водорода, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 132
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(4-трифторметилбензил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 133
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(О)NH(4-трифторметилбензил), Ry' и Ry#, соответственно, представляет собой CN, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 134
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(4-трифторметилбензил), Ry' представляет собой Cl, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 135
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(4-трифторметилбензил), Ry' представляет собой F, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 136
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(О)NH(4-трифторметилбензил), Ry' и Ry#, соответственно, представляет собой атом водорода, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 137
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(4-трифторметилбензил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 138
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(4-трифторметилбензил), Ry' и Ry#, соответственно, представляет собой CN, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 139
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(4-трифторметилбензил), Ry' представляет собой Cl, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 140
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(4-трифторметилбензил), Ry' представляет собой F, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 141
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(О)NH(4-трифторметилбензил), Ry' и Ry#, соответственно, представляет собой атом водорода, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 142
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(4-трифторметилбензил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 143
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(О)NH(4-трифторметилбензил), Ry' и Ry#, соответственно, представляет собой CN, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 144
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(4-трифторметилбензил), Ry' представляет собой Cl, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 145
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(4-трифторметилбензил), Ry' представляет собой F, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 146
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(О)NH(4-трифторметилбензил), Ry' и Ry#, соответственно, представляет собой атом водорода, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 147
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(4-трифторметилбензил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 148
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(4-трифторметилбензил), Ry' и Ry#, соответственно, представляет собой CN, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 149
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(4-трифторметилбензил), Ry' представляет собой Cl, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 150
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(4-трифторметилбензил), Ry' представляет собой F, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 151
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(пиридин-4-илметил), Ry' и Ry#, соответственно, представляет собой атом водорода, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 152
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(пиридин-4-илметил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 153
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(пиридин-4-илметил), Ry' и Ry#, соответственно, представляет собой CN, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 154
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(пиридин-4-илметил), Ry' представляет собой Cl, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 155
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(пиридин-4-илметил), Ry' представляет собой F, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 156
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(пиридин-4-илметил), Ry' и Ry#, соответственно, представляет собой атом водорода, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 157
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(пиридин-4-илметил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 158
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(пиридин-4-илметил), Ry' и Ry#, соответственно, представляет собой CN, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 159
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(пиридин-4-илметил), Ry' представляет собой Cl, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 160
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(пиридин-4-илметил), Ry' представляет собой F, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 161
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(пиридин-4-илметил), Ry' и Ry#, соответственно, представляет собой атом водорода, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 162
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(пиридин-4-илметил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 163
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(пиридин-4-илметил), Ry' и Ry#, соответственно, представляет собой CN, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 164
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(пиридин-4-илметил), Ry' представляет собой Cl, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 165
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(пиридин-4-илметил), Ry' представляет собой F, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 166
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(пиридин-4-илметил), Ry' и Ry#, соответственно, представляет собой атом водорода, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы А.
Таблица 167
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(пиридин-4-илметил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 168
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(пиридин-4-илметил), Ry' и Ry#, соответственно, представляет собой CN, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 169
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(пиридин-4-илметил), Ry' представляет собой Cl, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 170
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(пиридин-4-илметил), Ry' представляет собой F, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 171
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(пиридин-4-илметил), Ry' и Ry#, соответственно, представляет собой атом водорода, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 172
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(пиридин-4-илметил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 173
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(пиридин-4-илметил), Ry' и Ry#, соответственно, представляет собой CN, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 174
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(пиридин-4-илметил), Ry' представляет собой Cl, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 175
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(пиридин-4-илметил), Ry' представляет собой F, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 176
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(пиридин-4-илметил), Ry' и Ry#, соответственно, представляет собой атом водорода, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 177
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(пиридин-4-илметил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 178
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(пиридин-4-илметил), Ry' и Ry#, соответственно, представляет собой CN, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 179
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(пиридин-4-илметил), Ry' представляет собой Cl, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 180
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(пиридин-4-илметил), Ry' представляет собой F, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 181
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(фенилпропил), Ry' и Ry#, соответственно, представляет собой H, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 182
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(фенилпропил), Ry' и Ry#, соответственно, представляет собой H, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 183
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(фенилпропил), Ry' и Ry#, соответственно, представляет собой H, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 184
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(фенилпропил), Ry' и Ry#, соответственно, представляет собой H, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 185
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(фенилпропил), Ry' и Ry#, соответственно, представляет собой H, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 186
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(фенилпропил), Ry' и Ry#, соответственно, представляет собой H, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 187
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(фенилпропил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 188
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(фенилпропил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 189
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(фенилпропил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 190
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(фенилпропил), Ry'и Ry#, соответственно, представляет собой CH3, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 191
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(фенилпропил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 192
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(фенилпропил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 193
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(пиридин-2-илпропил), Ry' и Ry#, соответственно, представляет собой H, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 194
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(пиридин-2-илпропил), Ry' и Ry#, соответственно, представляет собой H, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 195
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(пиридин-2-илпропил), Ry' и Ry#, соответственно, представляет собой H, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 196
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(пиридин-2-илпропил), Ry' и Ry#, соответственно, представляет собой H, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 197
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(пиридин-2-илпропил), Ry' и Ry#, соответственно, представляет собой H, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 198
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(пиридин-2-илпропил), Ry' и Ry#, соответственно, представляет собой H, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 199
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(пиридин-2-илпропил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 200
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(пиридин-2-илпропил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 201
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(пиридин-2-илпропил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 202
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(пиридин-2-илпропил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 203
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(пиридин-2-илпропил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 204
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(пиридин-2-илпропил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 205
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(пиридин-3-илпропил), Ry' и Ry#, соответственно, представляет собой H, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 206
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(пиридин-3-илпропил), Ry' и Ry#, соответственно, представляет собой H, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 207
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(пиридин-3-илпропил), Ry' и Ry#, соответственно, представляет собой H, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 208
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(пиридин-3-илпропил), Ry' и Ry#, соответственно, представляет собой H, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 209
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(пиридин-3-илпропил), Ry' и Ry#, соответственно, представляет собой H, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 210
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(пиридин-3-илпропил), Ry' и Ry#, соответственно, представляет собой H, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 211
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(пиридин-3-илпропил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 212
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(пиридин-3-илпропил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 213
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(пиридин-3-илпропил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 214
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(пиридин-3-илпропил), Ry'и Ry#, соответственно, представляет собой CH3, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 215
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(пиридин-3-илпропил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 216
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(пиридин-3-илпропил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 217
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(пиридин-4-илпропил), Ry' и Ry#, соответственно, представляет собой H, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 218
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(пиридин-4-илпропил), Ry' и Ry#, соответственно, представляет собой H, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 219
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(пиридин-4-илпропил), Ry' и Ry#, соответственно, представляет собой H, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 220
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(пиридин-4-илпропил), Ry' и Ry#, соответственно, представляет собой H, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 221
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(пиридин-4-илпропил), Ry' и Ry#, соответственно, представляет собой H, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 222
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(пиридин-4-илпропил), Ry' и Ry#, соответственно, представляет собой H, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 223
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(пиридин-4-илпропил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 224
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(пиридин-4-илпропил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 225
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C=O, Х представляет собой C(O)NH(пиридин-4-илпропил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 226
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(пиридин-4-илпропил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой одинарную связь, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 227
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(пиридин-4-илпропил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Таблица 228
Соединения формул I-А'.rac, I-А'.R, I-А".rac, I-А".R, I-В'.rac, I-В'.R, I-В".rac, I-В".R и I-С', где группа C(R3aR3b) представляет собой C(OH)2, Х представляет собой C(O)NH(пиридин-4-илпропил), Ry' и Ry#, соответственно, представляет собой CH3, Q представляет собой CH2-CH2, и комбинация R1 и R2 для соединения в каждом случае соответствует одной строке таблицы A.
Соединения общей формулы I настоящего изобретения и необходимые исходные вещества, используемые для их получения, могут быть получены по аналогии с известными способами органической химии, которые описаны в стандартных работах по органической химии, например, в публикациях: Houben-Weyl "Methoden der Organischen Chemie", Thieme-Verlag Stuttgart; Jerry March "Advanced Organic Chemistry", 5-е издание, Wiley & Sons и в процитированной в указанной публикации литературе; и R. Larock, "Comprehensive Organic Transformations", 2-е издание, Weinheim 1999 и в процитированной в указанной публикации литературе. Соединения общей формулы I настоящего изобретения предпочтительно получают способами, описанными ниже и/или в экспериментальном разделе.
В дальнейшем переменные параметры R1, R2, Q, и X имеют указанные выше значения, и переменный параметр W означает дирадикал:

где R4, Y и A имеют указанные в настоящем описании значения, и где (*) указывает на место присоединения к Q, в то время как (#) указывает на место присоединения к карбонильной группе.
Соединения формулы I могут быть получены аналогично схемам и способам, описанным в патентных заявках WO 99/54305 и WO 2008/080969.
Схема 1
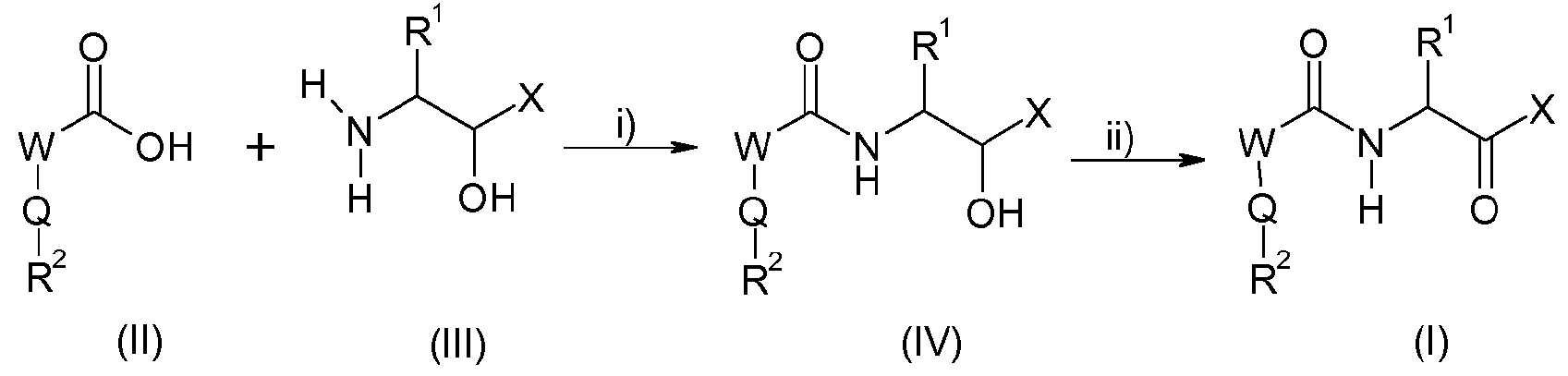
Как показано на схеме 1, на первой стадии i) карбоновую кислоту II преобразовывают взаимодействием с аминоспиртом III в соответствующий гидроксиамид IV. В связи с этим, обычно используют общепринятые способы сочетания пептидов, как описано, например, у R.C. Larock, в Comprehensive Organic Transformations, VCH Publisher, 1989, pp. 972-976, или Houben-Weyl, в Methoden der organischen Chemie, 4-е издание, E5, глава V. Может быть предпочтительным сначала активировать карбоновую кислоту II. С этой целью, например, карбоновую кислоту II подвергают взаимодействию с карбодиимидом, таким как дициклогексилкарбодиимид (DCC) или 1-этил-3-(3-диметиламинопропил)карбодиимид (EDC), в присутствии гидроксибензотриазола (HOBt), нитрофенола, пентафторфенола, 2,4,5-трихлорфенола или N-гидроксисукцинимида для получения активированного сложного эфира IIа. Альтернативой использованию дициклогексилкарбодиимида (DCC) или 1-этил-3-(3-диметиламинопропил)карбодиимида (EDC) является использование гексафторфосфата 2-(7-аза-1H-бензотриазол-1-ил)-1,1,3,3-тетраметилурония (HATU). Кроме того, может быть предпочтительным получение активированного сложного эфира IIа в присутствии основания, например, в присутствии третичного амина. Активированный сложный эфир IIа затем подвергают взаимодействию с аминоспиртом формулы III или его гидрогалоидной солью, получая при этом гидроксиамид IV. Обычно реакцию проводят в безводных инертных растворителях, таких как хлорированные углеводороды, например, дихлорметан или дихлорэтан, простые эфиры, например, тетрагидрофуран или 1,4-диоксан, или карбоксамиды, например, N,N-диметилформамид, N,N-диметилацетамид или N-метилпирролидон. Стадию i) обычно осуществляют при температурах в диапазоне от -20°C до +25°C.
Затем на второй стадии ii) гидроксиамидное соединение IV подвергают окислению до карбоксамидного соединения I. Подходящими для этого являются различные общепринятые реакции окисления (см. R.C. Larock, Comprehensive Organic Transformations, VCH Publisher, 1989, pp. 604 и далее), например, такие как окисление по Сверну и реакции окисления, аналогичные окислению по Сверну (T.T. Tidwell, Synthesis 1990, pp. 857-870), или реакция окисления Пфицнера-Моффатта. Подходящими окислителями являются диметилсульфоксид (ДМСО) в комбинации с дициклогексилкарбодиимидом или 1-этил-3-(3-диметиламинопропил)карбодиимидом, диметилсульфоксид в комбинации с комплексом пиридин-SO3 или диметилсульфоксид в комбинации с оксалилхлоридом, гипохлорид натрия/TEMPO (S.L. Harbenson et al., J. Med. Chem. 1994, 37, 2918-2929) и реагенты на основе гипервалентного йода типа 2-йодоксибензойной кислоты (IBX) (J. Org. Chem. 1995, 60, 7272), реагент Десс-Мартина (J. Org. Chem. 1983, 48, 4155) или IBX на полимерной подложке (H.S Jang, Tetrahedron Lett. 2007, 48, 3731-3734). В зависимости от используемого окислителя окисление гидроксиамидного соединения IV проводят при температурах от -50 до +25°C.
Если аминоспирты III коммерчески недоступны, их можно получить способами, описанными в литературе (для производных аминогидроксикарбоновых кислот см., например, S.L. Harbenson et al., J. Med. Chem. 1994, 37, 2918-2929 или J.P. Burkhardt et al., Tetrahedron Lett. 1988, 29, 3433-3436), или способами и методиками, описанными в патентной заявке WO 2008/08969.
Карбоновая кислота II может быть получена согласно схеме 2 путем гидролиза сложного эфира V карбоновой кислоты с кислотами или основаниями в общепринятых условиях. Гидролиз предпочтительно происходит с основаниями, такими как гидроксиды щелочных металлов или щелочноземельных металлов, например, гидроксид лития, гидроксид натрия или гидроксид калия, в водной среде или в смеси воды и органических растворителей, например, спиртов, таких как метанол или этанол, простых эфиров, таких как тетрагидрофуран или диоксан, при комнатной температуре или повышенной температуре, такой как 25-100°C.
Схема 2

На схеме 2 R2, Q и W имеют указанные выше значения. В формуле V R' представляет собой, например, алкил, арил или арилалкил, предпочтительно С1-С6алкил или бензил.
В общем случае карбоновые кислоты формулы II или сложные эфиры формулы V коммерчески доступны или могут быть получены с применением стандартных реакций замыкания кольца или общих способов алкилирования или арилирования с использованием подходящих исходных веществ, как изображено на схемах 3, 5 и 6.
Схема 3

На схеме 3 T представляет собой атом водорода или переменный параметр R', значения которого указаны выше, и LG обозначает уходящую группу, такую как атом галогена, если "A" представляет собой CO, SO или SO2, или, если "A" представляет собой CO, OH, OR", О(C)O)R'", атом галогена или N-имидазол (R", например, представляет собой активируемую группу активного сложного эфира, как описано ниже, и R”', например, представляет собой алкил, арил или арилалкил). В том случае, когда A-LG представляет собой CO-OH, сначала можно предпочтительно активировать карбоновую кислоту VI с применением стандартных способов. С этой целью, карбоновую кислоту VI, например, подвергают взаимодействию с карбодиимидом, таким как дициклогексилкарбодиимид (DCC) или 1-этил-3-(3-диметиламинопропил)карбодиимид (EDC), в присутствии гидроксибензотриазола (HOBt), нитрофенола, пентафторфенола, 2,4,5-трихлорфенола или N-гидроксисукцинимида, получая при этом активированный сложный эфир VIa, который обычно циклизуется до требуемого соединения V. Конкретные реакции циклизации описаны, например, H. McAlonan et al., в Tetrahedron Asymmetry 1995, 6(1), 239-244; S. Marchalin et al., в Synthetic Communications 1998, 28(19), 3619-3624; B. Debnathet et al., в Internet Electronic Journal of Molecular Design 2005, 4(6), 393-412; S. Samanta et al., в Bioorganic & Medicinal Chemistry 2004, 12(6), 1413-1423; K. Srikanth et al., в Bioorganic & Medicinal Chemistry 2002, 10(7), 2119-2131; и D. Goswamiet et al., в Pharmazie 2001, 56(5), 366-371.
Соединения формулы VI', где Q представляет собой фрагмент Alk'-Z, значения которого указаны выше, и Y представляет собой CH2-CH2, CH2-CH2-CH2 или CH=CH-CH=, могут быть получены согласно синтезу, изображенному на схеме 4.
Схема 4

На схеме 4 PG представляет собой подходящую защитную группу, и Q' обозначает фрагмент Alk'-Z с Alk', представляющим собой Alk минус метиленовая группа. Как показано на схеме 4, производное 2-аминокарбоновой кислоты VII преобразовывают восстановительным аминированием с альдегидом VIII до вторичного амина VI' с использованием восстановителя, такого как NaBH4. Реакцию можно осуществлять в виде одностадийного процесса или, альтернативно, в виде двух отдельных стадий путем образования на начальной стадии основания Шиффа продуктов VII и VIII с последующим восстановлением. Подходящие исходные вещества формулы VII, такие как глутаминовая кислота, могут быть либо куплены, либо получены общеизвестными способами.
Альтернативно, можно получить сложный эфир карбоновой кислоты формулы V, где Q представляет собой фрагмент Alk'-Z, значения которого указаны выше, как отмечено на схеме 5, путем алкилирования аминогруппы соединения-предшественника IX с применением стандартных способов.
Схема 5

На схеме 5 переменный параметр LG' обозначает уходящую группу, такую как галоген, тозилат или трифлат. В общем случае, необходимо присутствие органического или неорганического основания, такого как триэтиламин, DIPEA, KOtBu, K2CO3, Cs2CO3 или NaH. В качестве примера сложный эфир V с заместителем Q-R2, представляющим собой бензил, может быть получен путем взаимодействия соответствующего вторичного амина IX с бензилбромидом X в присутствии карбоната калия в ДМФА при комнатной температуре. Конкретные способы преобразования соединения-предшественника IX, например, описаны в публикациях: T. Simandan et al., Synth Commun 1996, 26(9), 1827; P. Cauliez et al., J. Heterocyclic Chem. 1991, 28(4), 1143-1146; R. F. Menezes et al., Tetrahedron Lett. 1989, 30(25), 3295-3298; T. Itoh et al., Tetrahedron 2003, 59(19), 3527-3536 и Tetrahedron 2001, 57(34), 7277-7289.
Соединения формулы V, где Q представляет собой одинарную связь, и R2 представляет собой арил или гетарил, в дальнейшем обозначаемые как соединения формулы V', могут быть получены с применением реакции связывания C-N, катализируемой переходным металлом, с использованием сложного эфира IX' и (гет)арильного соединения X', как изображено на схеме 6.
Схема 6

На схеме 6 LG" обозначает уходящую группу типа атома галогена или трифлата, которые, как известно, способны замещаться в реакциях, катализируемых переходными металлами. Переменный параметр V обозначает необходимую дополнительную группу и обычно представляет собой атом водорода. Подходящими катализаторами для таких реакций являются, например, комплексы палладия, содержащие Pd(0) или Pd(II) и фосфиновый лиганд, такой как 4,5-бис(дифенилфосфино)-9,9-диметилксантен (Xantphos), которые описаны, например, Guram et al., в Angew. Chem. Int. Ed. Eng. 1995, 34, 1348. Альтернативно, для осуществления катализа таких реакций также можно использовать комплексы Cu(I), такие как Cu(1,10-фенантролин)(PPh3)Br, которые известны, например, из публикации Gujadhur et al., Org. Lett. 2001, 2, 4315. Кроме катализатора реакции согласно схеме 3 обычно также включают основание, такое как трет-бутоксилат калия или карбонат цезия, и обычно осуществляются при повышенных температурах.
Соединения формулы I, в которых X представляет собой -C(O)N(Rx4)-(C1-C6алкилен)-NRx2Rx3 или -C(O)N(Rx4)NRx2Rx3, где Rx2, Rx3 и Rx4 имеют указанные выше значения, дополнительно могут быть получены путем взаимодействия соединений формулы I, где X представляет собой COOH, с гидразиновыми соединениями формулы NH(Rx4)NRx2Rx3 или диаминами формулы NH(Rx4)-(C1-C6алкилен)-NRx2Rx3. Реакцию можно осуществлять с применением способов, аналогично описанным для реакции связывания на стадии i) схемы 1.
Альтернативно, соединения формулы I, в которых X представляет собой -C(O)-NRx2Rx3, -C(O)-N(Rx4)-(C1-C6алкилен)-NRx2Rx3 или -C(O)-N(Rx4)-NRx2Rx3, также могут быть получены согласно схеме 7.
Схема 7

Как показано на схеме 7, на первой стадии i) сложный эфир карбоновой кислоты формулы IVa (R"", например, представляет собой алкил, арил или арилалкил, предпочтительно С1-С6алкил или бензил), полученный согласно схеме 1, подвергают гидролизу до соответствующей карбоновой кислоты IVb, которую на стадии ii) подвергают взаимодействию с амином HNRx2Rx3, HN(Rx4)-(C1-C6алкилен)-NRx2Rx3 или HN(Rx4)-NRx2Rx3 до получения амидов общей формулы IV с применением общепринятых способов связывания, как описано выше. Заключительное окисление (стадия iii) осуществляют, как отмечено выше.
Кроме того, имидазолидиноновые производные формул V, IX или IX', где Y представляет собой фрагмент N(Ry#)-CH2 или N(Ry#)-CH2-CH2 могут быть, например, получены путем взаимодействия соответствующих соединений-предшественников, производных 2,3-диаминопропионовой кислоты или 2,4-диаминомасляной кислоты, с фосгеном или эквивалентным ему соединением в присутствии основания, такого как триэтиламин. Заместитель Ry#, отличающийся от атома водорода, можно вводить либо до, либо после такой реакции замыкания кольца с применением общепризнанных стандартных методик. Подходящие исходные вещества для такого пути синтеза соединений VI' и VI кроме указанных диаминокислотных соединений-предшественников также представляют собой их производные, содержащие две разные аминозащитные группы или только одну аминозащитную группу.
Согласно одному из аспектов изобретения атом водорода, присоединенный к атому углерода, несущему радикал R1, соединения I заменяется атомом дейтерия, как показано ниже в формуле I-D. R1, R2, R3a, R3b, R4, A, Y, Q и X в формуле I-D имеют указанные выше значения.

Соединения формулы I-D могут быть получены способом, аналогично описанному F. Maltais et al., в J. Med. Chem. 2009, 52 (24), 7993-8001 (DOI 10.1021/jm901023f). Степень дейтерирования в указанном положении обычно превышает 80%, предпочтительно превышает 90% и, в частности, превышает 95%. Дейтерированные соединения формулы I-D часто показывают заметно более высокую стабильность против рацемизации, чем их аналоги формулы I, вероятно, вследствие кинетического изотопного эффекта (см. F. Maltais et al., J. Med. Chem. 2009, 52 (24), 7993-8001).
Реакционные смеси обрабатывают общепринятыми способами, например, путем смешивания с водой, разделения фаз и, где необходимо, проводят очистку неочищенных продуктов с помощью хроматографии. Промежуточные продукты и конечные продукты в некоторых случаях приводят к образованию бесцветных или бледно-коричневатых, вязких масел, которые отделяют от летучих веществ или очищают при пониженном давлении и умеренно повышенной температуре. Если промежуточные продукты и конечные продукты получают в виде твердых веществ, очистку можно также осуществлять с помощью перекристаллизации или гидролитического разложения.
Если индивидуальные соединения I не образуются описанными выше способами, они могут быть получены путем дериватизации других соединений I.
Соединения настоящего изобретения проявляют крайне низкие значения Ki в отношении ингибирования кальпаина и поэтому позволяют эффективно ингибировать кальпаин, особенно кальпаин I, при низких сывороточных уровнях. Соединения настоящего изобретения обычно имеют значения Ki в отношении ингибирования кальпаина in vitro <600 нМ, в частности, <100 нМ и, в частности, <50 нМ. Следовательно, соединения настоящего изобретения особенно подходят для лечения расстройств, ассоциированных с повышенной активностью кальпаина.
Кроме того, соединения настоящего изобретения являются селективными ингибиторами кальпаина, то есть ингибирование других цистеинпротеаз, таких как катепсин B, катепсин K, катепсин L или катепсин S, происходит только при концентрациях, которые являются заметно более высокими, чем концентрации, необходимые для ингибирования кальпаина. Соответственно, соединения настоящего изобретения должны демонстрировать определенно меньше побочных эффектов, чем соединения прототипа, которые являются относительно неселективными в отношении ингибирования кальпаина, а также ингибируют другие цистеинпротеазы.
Соответственно, предпочтительные соединения настоящего изобретения обладают селективностью в отношении ингибирования катепсина B, выраженной в форме отношения константы Ki для ингибирования катепсина B к константе Ki для ингибирования кальпаина, >5, предпочтительно >10 и, в частности, >30.
Соответственно, предпочтительные соединения настоящего изобретения обладают селективностью в отношении ингибирования катепсина K, выраженной в форме отношения константы Ki для ингибирования катепсина K к константе Ki для ингибирования кальпаина, >5, предпочтительно >10 и, в частности, >30.
Соответственно, предпочтительные соединения настоящего изобретения обладают селективностью в отношении ингибирования катепсина L, выраженной в форме отношения константы Ki для ингибирования катепсина L к константе Ki для ингибирования кальпаина, >5, предпочтительно >10 и, в частности, >30.
Соответственно, предпочтительные соединения настоящего изобретения обладают селективностью в отношении ингибирования катепсина S, выраженной в форме отношения константы Ki для ингибирования катепсина S к константе Ki для ингибирования кальпаина, >10, предпочтительно >30 и, в частности, >100.
Кроме того, соединения согласно настоящему изобретению отличаются улучшенной стабильностью в цитозоле клеток человеческого организма, которая вносит заметный вклад в их общую хорошую метаболическую стабильность. Стабильность в цитозоле можно измерить, например, путем инкубирования раствора соединения настоящего изобретения с цитозолем печени конкретных видов (например, крысы, собаки, обезьяны или человека) и определения времени полужизни соединения в данных условиях. Из более длительного времени полужизни можно сделать заключение, что метаболическая стабильность соединения улучшается. Стабильность в присутствии цитозоля печени человека представляет особый интерес, поскольку это дает возможность прогнозировать метаболическую деградацию соединения в печени человека. Следовательно, есть основания полагать, что соединения с повышенной стабильностью в цитозоле в печени подвергаются деградации с меньшими скоростями. Более медленная метаболическая деградация в печени, в свою очередь, может приводить к более высоким и/или более длительно сохраняющимся концентрациям (эффективным уровням) соединения в организме, так что период полувыведения соединений настоящего изобретения увеличивается. Повышенные и/или более длительно сохраняющиеся эффективные уровни могут приводить к лучшей эффективности соединения при лечении или профилактике различных кальпаин-зависимых заболеваний. Улучшенная метаболическая стабильность может дополнительно приводить к повышенной биодоступности после перорального введения, поскольку после поглощения в кишечном тракте соединение подвергается меньшей метаболической деградации в печени (именуемой эффектом первого прохождения). Поскольку концентрация (эффективный уровень) соединения увеличивается, повышенная биодоступность после перорального введения может приводить к лучшей эффективности соединения после перорального введения.
Соответственно, благодаря своей улучшенной стабильности в цитозоле соединения настоящего изобретения остаются в цитозоле в течение продолжительного периода времени, то есть обладают пониженным клиренсом соединения из цитозоля и, следовательно, должны демонстрировать улучшенную фармакокинетику в организме человека.
Соответственно, предпочтительные соединения настоящего изобретения обладают клиренсом соединения из цитозоля печени человека ≤30 мкл/мин/мг, в частности, ≤15 мкл/мин/мг.
Улучшенная стабильность в цитозоле соединений согласно настоящему изобретению, прежде всего, вероятно, обусловлена их пониженной чувствительностью к воздействию альдо-кеторедуктаз (AKR), которые опосредуют метаболическую деградацию соединений, содержащих карбонильную группу, в цитозоле печени человека и обезьян. Поэтому AKR-катализируемое восстановление кетоамидов формулы I должно быть менее выражено, чем восстановление менее стабильных кетоамидов. Следовательно, отношение концентрации исходного соединения, то есть кетоамида формулы I, к концентрации метаболита, то есть возникающей гидроксиамидной формы кетоамида, является критерием стабильности соединений настоящего изобретения.
Соответственно, для предпочтительных соединений настоящего изобретения после пребывания в гепатоцитах человека в течение 4 часов отношение концентрации гидроксиамидного метаболита к концентрации соответствующего им исходного соединения формулы I составляет ≤5, в частности, ≤2 и конкретно ≤0,5.
Благодаря их ингибирующему действию на кальпаин и их селективности в отношении кальпаина по сравнению с другими цистеинпротеазами соединения настоящего изобретения формулы I, их таутомеры и их фармацевтически приемлемые соли особенно подходят для лечения расстройства или состояния, которое ассоциировано с повышенной активностью кальпаина и которое описано, например, в предшествующем уровне техники, процитированном в начале.
Расстройства, ассоциированные с повышенной активностью кальпаина, в частности, представляют собой нейродегенеративные расстройства, особенно нейродегенеративные расстройства, возникающие в результате хронической недостаточности питания головного мозга, ишемии (удара) или травмы, такой как травма головного мозга, и нейродегенеративные расстройства типа болезни Альцгеймера, болезни Паркинсона, амиотрофического бокового склероза и болезни Гентингтона, а также рассеянный склероз и ассоциированное с ним поражение нервной системы, особенно поражение зрительного нерва (неврит зрительного нерва) и нервов, которые регулируют движение глаза. Соответственно предпочтительные варианты осуществления изобретения относятся к лечению нейродегенеративных расстройств, особенно указанных выше нейродегенеративных расстройств человека, и к применению соединений формулы I настоящего изобретения, их таутомеров и их фармацевтически приемлемых солей для производства лекарственного средства для лечения таких расстройств.
Расстройства, ассоциированные с повышенной активностью кальпаина, также включают эпилепсию. Соответственно, предпочтительные варианты осуществления изобретения относятся к лечению эпилепсии у человека и к применению соединений формулы I настоящего изобретения, их таутомеров и их фармацевтически приемлемых солей для производства лекарственного средства для лечения эпилепсии.
Расстройства или состояния, ассоциированные с повышенной активностью кальпаина, также включают боль и болезненные состояния. Соответственно предпочтительные варианты осуществления изобретения относятся к лечению боли и болезненных состояний у млекопитающих, особенно у человека, и к применению соединений формулы I настоящего изобретения, их таутомеров и их фармацевтически приемлемых солей для производства лекарственного средства для лечения боли и болезненных состояний.
Расстройства или состояния, ассоциированные с повышенной активностью кальпаина, также включают поражение сердца вследствие сердечных ишемий, поражение почек вследствие почечных ишемий, повреждение скелетных мышц, мышечные дистрофии, повреждение, происходящее из-за пролиферации гладкомышечных клеток, коронароспазмов, спазмов сосудов головного мозга, макулярной дегенерации, катаракты глаз или рестеноза кровеносных сосудов вследствие ангиопластики. Соответственно, предпочтительные варианты осуществления изобретения относятся к лечению заболеваний или состояний, ассоциированных с поражением сердца вследствие сердечных ишемий, поражением почек вследствие почечных ишемий, повреждением скелетных мышц, с мышечными дистрофиями, повреждением, происходящим в результате пролиферации гладкомышечных клеток, коронароспазмов, спазмов сосудов головного мозга, макулярной дегенерации, катаракты глаз или рестеноза кровеносных сосудов вследствие ангиопластики у млекопитающих, особенно у человека, и к применению соединений формулы I настоящего изобретения, их таутомеров и их фармацевтически приемлемых солей для производства лекарственного средства для лечения таких расстройств.
Дополнительно было обнаружено, что ингибирование кальпаина приводит к цитотоксическим эффектам в отношении опухолевых клеток. Соответственно, соединения настоящего изобретения подходят для химиотерапии опухолей и их метастазов. Следовательно, предпочтительные варианты осуществления изобретения относятся к применению соединений формулы I настоящего изобретения, их таутомеров и их фармацевтически приемлемых солей для терапии опухолей и метастазов и к применению данных соединений для производства лекарственного средства для терапии опухолей и метастазов.
Дополнительно было обнаружено, что различные нарушения, ассоциированные с расстройствами ВИЧ-инфицированных, особенно повреждение нервов (ВИЧ-индуцированная нейротоксичность), опосредуются кальпаином и, следовательно, ингибирование кальпаина дает возможность лечить или облегчать такие нарушения. Соответственно, соединения формулы I настоящего изобретения, их таутомеры и их фармацевтически приемлемые соли подходят для лечения ВИЧ-инфицированных пациентов. Следовательно, предпочтительные варианты осуществления изобретения относятся к применению соединений формулы I настоящего изобретения, их таутомеров и их фармацевтически приемлемых солей для лечения ВИЧ-инфицированных пациентов, особенно для лечения таких нарушений, которые вызваны ВИЧ-индуцированной нейротоксичностью, и к применению данных соединений для производства лекарственного средства для лечения ВИЧ-пациентов.
Дополнительно было обнаружено, что с помощью ингибиторов кальпаина можно уменьшить или полностью ингибировать высвобождение интерлейкина-I, TNF или β-амилоидных пептидов (Aβ или Aβ-пептидов). Соответственно, с помощью соединений формулы I настоящего изобретения, их таутомеров и их фармацевтически приемлемых солей можно лечить нарушения или расстройства, ассоциированные с повышенным уровнем интерлейкина-I, TNF или Aβ. Следовательно, предпочтительные варианты осуществления изобретения относятся к применению соединений формулы I настоящего изобретения, их таутомеров, их пролекарств и их фармацевтически приемлемых солей для лечения нарушений или расстройств, ассоциированных с повышенным уровнем интерлейкина-I, TNF или Aβ, таких как ревматизм, ревматоидный артрит, и к применению данных соединений для производства лекарственного средства для лечения таких нарушений или расстройств.
Соединения общей формулы (I) также характеризуются, в частности, хорошей метаболической стабильностью. Метаболическую стабильность соединения можно измерить, например, путем инкубирования раствора такого соединения с микросомами печени конкретных видов (например, крысы, собаки или человека) и определения времени полужизни соединения в данных условиях (RS Obach, Curr Opin Drug Discov Devel. 2001, 4, 36-44). На основании более длительного времени полужизни можно сделать заключение, что метаболическая стабильность соединения улучшается. Стабильность в присутствии микросом печени человека представляет особый интерес, поскольку дает возможность прогнозировать метаболическую деградацию соединения в печени человека. Следовательно, соединения с повышенной метаболической стабильностью, вероятно, деградируют в печени также более медленно (измеряют в испытании с микросомами печени). Более медленная метаболическая деградация в печени может приводить к более высоким и/или длительно сохраняющимся концентрациям (эффективным уровням) соединения в организме, так что период полувыведения соединений настоящего изобретения увеличивается. Повышенные и/или длительно сохраняющиеся эффективные уровни могут приводить к лучшей эффективности соединения при лечении или профилактике различных кальпаин-зависимых заболеваний. Улучшенная метаболическая стабильность может дополнительно приводить к повышенной биодоступности после перорального введения, поскольку соединение после поглощения в кишечном тракте подвергается меньшей метаболической деградации в печени (именуемой эффектом первого прохождения). Повышенная биодоступность после перорального введения может приводить к лучшей эффективности соединения после перорального введения, поскольку концентрация (эффективный уровень) соединения увеличивается.
Соединения формулы I настоящего изобретения дополнительно характеризуются проявлением повышенной фармакологической активности по сравнению с карбоксамидными соединениями формулы I, описанными в предшествующем уровне техники, у пациентов или в релевантных животных моделях, давая возможность прогностических предположений для применения при лечении.
Настоящее изобретение также относится к фармацевтическим композициям (то есть лекарственным средствам), которые содержат по меньшей мере одно соединение формулы I настоящего изобретения или его таутомер или фармацевтически приемлемую соль и, где необходимо, один или несколько подходящих носителей лекарственного средства.
Носители лекарственного средства выбирают в соответствии с фармацевтической формой и требуемым способом введения.
Соединения общей формулы I настоящего изобретения, их таутомеры и фармацевтически приемлемые соли таких соединений можно использовать для производства фармацевтических композиций для перорального, подъязычного, подкожного, внутримышечного, внутривенного, местного, внутритрахеального, интраназального, трансдермального или ректального введения и вводить животным или человеку в виде единичных дозированных форм в смеси с общепринятыми фармацевтическими носителями для профилактики или лечения перечисленных выше нарушений или заболеваний.
Подходящие единичные дозированные формы включают формы для перорального введения, такие как таблетки, желатиновые капсулы, порошки, гранулы и растворы или суспензии для перорального приема, формы для подъязычного, трансбуккального, внутритрахеального или интраназального введения, аэрозоли, импланты, формы для подкожного, внутримышечного или внутривенного введения и формы для ректального введения.
Соединения настоящего изобретения можно использовать в кремах, мазях или лосьонах для местного введения.
Чтобы достичь требуемого профилактического или терапевтического эффекта, доза основного активного ингредиента может варьироваться от 0,01 до 50 мг на кг массы тела в день.
Каждая единичная доза может содержать от 0,05 до 5000 мг, предпочтительно 1-1000 мг активного ингредиента в комбинации с фармацевтическим носителем. Такую единичную дозу можно вводить 1-5 раз в день таким образом, чтобы вводимая суточная доза составляла от 0,5 до 25000 мг, предпочтительно 1-5000 мг.
Если твердую композицию получают в форме таблеток, основной ингредиент смешивают с фармацевтическим носителем, таким как желатин, крахмал, лактоза, стеарат магния, тальк, диоксид кремния или т.п.
Таблетки могут быть покрыты сахарозой, производным целлюлозы или другим подходящим веществом или могут быть обработаны иным способом для того, чтобы они могли демонстрировать пролонгированную или замедленную активность, и для того, чтобы непрерывно происходило высвобождение заданного количества основного активного ингредиента.
Препарат в форме желатиновых капсул получают путем смешивания активного ингредиента с наполнителем и наполнения полученной смесью мягких или жестких желатиновых капсул.
Препарат в форме сиропа или эликсира или препарат для введения в форме капель может содержать активные ингредиенты вместе с подсластителем, который предпочтительно не содержит калорий, метилпарабеном или пропилпарабеном в качестве антисептиков, корригентом вкуса и запаха и подходящим красителем.
Диспергируемые в воде порошки или гранулы могут содержать активные ингредиенты, смешанные с диспергаторами, увлажняющими средствами или суспендирующими средствами, такими как поливинилпирролидоны, и подсластителями или улучшителями вкуса.
Ректальное введение обеспечивают путем применения суппозиториев, которые получают со связующими, которые плавятся при ректальной температуре, например, с кокосовым маслом или полиэтиленгликолями. Парентеральное введение осуществляют путем использования водных суспензий, изотонических солевых растворов или стерильных растворов для инъекций, которые содержат фармакологически приемлемые диспергаторы и/или увлажняющие средства, например пропиленгликоль или полиэтиленгликоль.
Основной активный ингредиент также может быть приготовлен в виде микрокапсул или липосом/центросом, если дополнен одним или несколькими подходящими носителями или добавками.
Кроме соединений общей формулы I, их таутомеров или их фармацевтически приемлемых солей композиции настоящего изобретения могут дополнительно содержать основные активные ингредиенты, которые могут быть благоприятны для лечения указанных выше нарушений или заболеваний.
Поэтому настоящее изобретение дополнительно относится к фармацевтическим композициям, в которых несколько основных активных ингредиентов присутствует вместе, где по меньшей мере один из таких ингредиентов представляет собой соединение настоящего изобретения.
Соединения настоящего изобретения также включают такие соединения, в которых один или несколько атомов заменены их стабильными, нерадиоактивными изотопами, например, атом водорода замещен дейтерием.
Стабильные изотопы (например, дейтерий,13C,15N,18O) являются нерадиоактивными изотопами, которые содержат один дополнительный нейтрон и которые обычно представляют собой широко распространенный изотоп соответствующего атома. Дейтерированные соединения применяют в фармацевтическом исследовании, чтобы изучать метаболическое поведение соединений in vivo путем определения механизма действия и метаболического пути недейтерированного исходного соединения (Blake et al., J. Pharm. Sci. 64, 3, 367-391 (1975)). Такие метаболические исследования важны для создания безопасных, эффективных терапевтических лекарственных средств, либо потому что активное соединение вводят пациенту in vivo, либо потому что метаболиты, образующиеся из исходного соединения, оказываются токсичными или канцерогенными (Foster et al., Advances in Drug Research т.14, pp. 2-36, Academic press, London, 1985; Kato et al., J. Labelled Comp. Radiopharmaceut., 36(10):927-932 (1995); Kushner et al., Can. J. Physiol.Pharmacol., 77, 79-88 (1999).
Включение тяжелого атома, в частности замена водорода дейтерием, может приводить к изотопному эффекту, который может изменять фармакокинетику лекарственного средства. Такой эффект обычно является незначительным, если метка находится в метаболически инертных положениях молекулы.
Введение в лекарственное средство метки в виде стабильного изотопа может изменять его физико-химические свойства, такие как pKa и жирорастворимость. Такие изменения могут влиять на поведение лекарственного средства на разных стадиях во время его прохождения через организм. Поглощение, распределение, метаболизм или выведение могут меняться. Поглощение и распределение представляют собой процессы, которые, прежде всего, зависят от молекулярного размера и липофильности вещества. Такие эффекты и изменения могут влиять на фармакодинамический ответ молекулы лекарственного средства, если изотопная замена влияет на область, вовлеченную во взаимодействие лиганд-рецептор.
Метаболизм лекарственного средства может приводить к большому изотопному эффекту, если разрыв химической связи с атомом дейтерия является стадией, лимитирующей скорость процесса. В то время как некоторые из физических свойств молекулы, меченной стабильным изотопом, отличаются от физических свойств немеченой молекулы, химические и биологические свойства являются теми же самыми, с одним важным исключением: благодаря более высокой массе тяжелого изотопа любая связь, в которую вовлечен тяжелый изотоп и другой атом, будет более сильной, чем та же самая связь между легким изотопом и этим атомом. Благодаря "кинетическому изотопному эффекту" при любой реакции, в которой разрыв такой связи является стадией, лимитирующей скорость процесса, реакция будет протекать более медленно для молекулы с тяжелым изотопом. Реакция, в которую вовлечен разрыв связи C-D, может быть на 700 процентов более медленной, чем аналогичная реакция, в которую вовлечен разрыв связи C-H. Если связь C-D не вовлечена в какую-либо из стадий, приводящих к метаболиту, какого-либо влияния на поведение лекарственного средства может не существовать. Если атом дейтерия расположен на участке, вовлеченном в метаболизм лекарственного средства, изотопный эффект будет наблюдаться только если разрыв связи C-D является стадией, лимитирующей скорость процесса. Имеются экспериментальные данные о том, что во всех случаях, когда происходит расщепление алифатической связи C-H, обычно путем окисления, катализируемого оксидазой со смешанной функцией, замена водорода дейтерием будет приводить к доступному для наблюдения изотопному эффекту. Также важно понимать, что включение атома дейтерия в участок, вовлеченный в метаболизм, замедляет скорость метаболизма до той точки, где другой метаболит, образующийся в результате воздействия на атом углерода, не замещенный атомом дейтерия, становится главным путем процесса выведения, называемого "метаболическим переключением".
В некоторых случаях дейтериевые индикаторы, такие как лекарственные средства и дозы, меченные дейтерием, тысячи миллиграммов дейтерированной воды также многократно применяют на здоровых людях всех возрастов, включая новорожденных и беременных женщин, без чрезвычайных инцидентов (например, Pons G. и Rey E., Pediatrics 1999 104:633; Coward W.A. et al., Lancet 1979 7:13; Schwarcz H.P., Control. Clin. Trials 1984 5(4 Suppl): 573; Rodewald L.E. et al., J. Pediatr. 1989 114:885; Butte N.F. et al., Br. J. Nutr. 1991 65:3; MacLennan A.H. et al., Am. J. Obstet Gynecol. 1981 139:948). Поэтому очевидно, что любое высвобождение дейтерия, например, во время метаболизма соединений согласно настоящему изобретению не предполагает угрозы здоровью.
Процентное содержание (по массе) водорода в организме млекопитающего (приблизительно 9%) и распространенность дейтерия в природе (приблизительно 0,015%) указывают на то, что организм человека массой 70 кг обычно содержит фактически грамм дейтерия. Кроме того, замена приблизительно до 15% обычного водорода дейтерием была предпринята и поддерживалась в течение периода времени от нескольких дней до недель у млекопитающих, включая грызунов и собак, с минимально наблюдаемыми побочными эффектами (Czajka D.M. и Finkel A.J., Ann. N. Y. Acad. Sci. 1960 84:770; Thomson J.F., Ann. New York Acad. Sci 1960 84:736; Czakja D.M. et al., Am. J. Physiol. 1961 201:357). Более высокие концентрации дейтерия, обычно превышающие 20%, могут быть токсичными для животных. Однако не было обнаружено, что кратковременная замена водорода дейтерием в жидкостях человеческого организма вплоть до 15%-23% служит причиной токсичности (Blagojevic N. et al. в "Dosimetry & Treatment Planning for Neutron Capture Therapy", Zamenhof R., Solares G. и Harling O. Eds. 1994. Advanced Medical Publishing, Madison Wis. стр.125-134; Diabetes Metab. 23:251 (1997)).
Увеличение количества дейтерия, присутствующего в соединении, выше, чем его распространенность в природе, называется обогащением или обогащение дейтерием. Примеры процента обогащения включают приблизительно от 0,5, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 12, 16, 21, 25, 29, 33, 37, 42, 46, 50, 54, 58, 63, 67, 71, 75, 79, 84, 88, 92, 96 до приблизительно 100% моль.
Атомы водорода, присутствующие в конкретном органическом соединении, обладают разной способностью к замене атомами дейтерия. Некоторые атомы водорода способны легко обмениваться в физиологических условиях и в случае замещения атомами дейтерия предполагается, что они без труда будут обмениваться на протоны после введения пациенту. Некоторые атомы водорода можно обменивать на атомы дейтерия под действием дейтериевой кислоты, такой как D2SO4/D2O. Альтернативно, атомы дейтерия можно включать в состав различных комбинаций во время синтеза соединений настоящего изобретения. Некоторые атомы водорода не способны легко обмениваться на атомы дейтерия. Однако атомы дейтерия могут быть включены в оставшиеся положения путем использования исходных дейтерированных веществ или дейтерированных промежуточных продуктов во время создания соединений настоящего изобретения.
Дейтерированные соединения и соединения, обогащенные дейтерием, настоящего изобретения могут быть получены с применением известных способов, описанных в литературе. Такие способы можно осуществить, используя соответствующие дейтерированные реагенты и/или промежуточные продукты и необязательно реагенты и/или промежуточные продукты, содержащие другие изотопы, для синтеза описанных в данном описании соединений, или прибегая к применению стандартных протоколов синтеза, известных в данной области, для введения изотопов в химическую структуру. Соответствующие методики и промежуточные продукты описаны, например в публикациях: Lizondo, J. et al., Drugs Fut, 21(11), 1116 (1996); Brickner S.J. et al., J. Med. Chem., 39(3), 673 (1996); Mallesham B. et al., Org. Lett., 5(7), 963 (2003); в публикациях РСТ WO1997010223, WO2005099353, WO1995007271, WO2006008754; в патентах США 7538189; 7534814; 7531685; 7528131; 7521421; 7514068; 7511013; и в патентных заявках США №№ 20090137457; 20090131485; 20090131363; 20090118238; 20090111840; 20090105338; 20090105307; 20090105147; 20090093422; 20090088416; 20090082471; описанные в них способы включены в настоящее описание посредством ссылки.
Следующие примеры иллюстрируют изобретение без его ограничения. В зависимости от способа проведения реакции и обработки соединения общей формулы I получают в виде смесей карбонильной формы и соответствующих гидратов. Преобразование в чистые карбонильные соединения обычно происходит путем обработки веществ с помощью HCl в инертном растворителе.
Примеры получения
I. Получение структурных элементов общей формулы II
Следующие структурные элементы II коммерчески доступны:
(R)-1-бензил-5-оксопирролидин-2-карбоновая кислота и (S)-1-бензил-5-оксопирролидин-2-карбоновая кислота.
Пример A
(R)-1-(3-метоксибензил)-5-оксопирролидин-2-карбоновая кислота
К раствору (R)-2-аминопентандиовой кислоты (степень чистоты 99%; 1000 мг, 6,37 ммоль) в 6,37 мл 2н раствора NaOH (13,46 ммоль) добавляли 3-метоксибензальдегид (0,827 мл; 925 мг, 6,37 ммоль) в 1,8 мл этанола и перемешивали полученную смесь в течение ночи при комнатной температуре, давая возможность образоваться имину. Последующее добавление NaBH4 (309 мг; 8,07 ммоль) приводило к немного экзотермической реакции (повышение температуры приблизительно до 40°C), и завершали реакцию путем перемешивания при комнатной температуре. Затем смесь разбавляли водой и дважды экстрагировали простым метил-трет-бутиловым эфиром (MTBE). Водный слой подкисляли до pH 3 с использованием концентрированной HCl. Полученный осадок затем отфильтровывали, дважды промывали водой и сушили при пониженном давлении. (R)-2-(3-Метоксибензиламино)пентандиовую кислоту (1,075 г, 4,02 ммоль; выход: 60%), полученную в виде белого твердого вещества, подвергали циклизации путем нагревания в этаноле при кипячении с обратным холодильником в течение 3 часов. Растворитель выпаривали при пониженном давлении, с получением требуемого продукта, (R)-1-(3-метоксибензил)-5-оксопирролидин-2-карбоновой кислоты (1,06 г; выход: 100%), в виде белого твердого вещества.
ESI-МС [M+H]+=250,1
Соединения примеров B-Q могут быть получены способом, аналогично описанному выше получению примера A.
Пример B
(R)-1-(3-хлорбензил)-5-оксопирролидин-2-карбоновая кислота
ESI-МС [M+H]+=254,1, 256,2.
Пример C
(R)-1-(4-фторбензил)-5-оксопирролидин-2-карбоновая кислота
ESI-МС [M+H]+=238,1.
Пример D
(R)-1-(3,5-дифторбензил)-5-оксопирролидин-2-карбоновая кислота
ESI-МС [M+H]+=256,1.
Пример E
(R)-1-(3-трифторметилбензил)-5-оксопирролидин-2-карбоновая кислота
ESI-МС [M+H]+=288,1.
Пример F
(R)-1-(3-фторбензил)-5-оксопирролидин-2-карбоновая кислота
ESI-МС [M+H]+=238,1.
Пример G
(R)-1-(2-трифторметоксибензил)-5-оксопирролидин-2-карбоновая кислота
ESI-МС [M+H]+=304,1.
Пример H
(R)-1-(3-трифторметоксибензил)-5-оксопирролидин-2-карбоновая кислота
ESI-МС [M+H]+=304,1.
Пример I
(R)-1-нафталин-1-илметил-5-оксопирролидин-2-карбоновая кислота
ESI-МС [M+H]+=270,1.
Пример J
(R)-1-нафталин-2-илметил-5-оксопирролидин-2-карбоновая кислота
ESI-МС [M+H]+=270,1.
Пример K
(R)-5-оксо-1-пиридин-4-илметилпирролидин-2-карбоновая кислота
ESI-МС [M+H]+=221,1.
Пример L
(R)-1-(3,5-диметоксибензил)-5-оксопирролидин-2-карбоновая кислота
ESI-МС [M+H]+=280,1.
Пример M
(R)-1-бензил-6-оксопиперидин-2-карбоновая кислота
ESI-МС [M+H]+=234,1.
Пример N
(R)-5-оксо-1-(2-(трифторметокси)бензил)пирролидин-2-карбоновая кислота
ESI-МС [M+H]+=304,1.
Пример O
(R)-1-(2-хлорбензил)-5-оксопирролидин-2-карбоновая кислота
ESI-МС [M+H]+=254,1.
Пример P
(R)-1-(2-метокси-6-(трифторметил)бензил)-5-оксопирролидин-2-карбоновая кислота
ESI-МС [M+H]+=318,1.
Пример Q
(R)-1-(2,6-дифторбензил)-5-оксопирролидин-2-карбоновая кислота
ESI-МС [M+H]+=256,1.
Пример R
(R)-5-оксо-1-(2-трифторметилбензил)пирролидин-2-карбоновая кислота
К раствору (R)-этил-5-оксопирролидин-2-карбоксилата (этиловый эфир D-пироглутаминовой кислоты; степень чистоты 99%; 1403 мг, 8,84 ммоль) в 20 мл ДМФА добавляли 1-(бромметил)-2-(трифторметил)бензол (степень чистоты 96%; 2200 мг, 8,84 ммоль), K2CO3 (3660 мг, 26,5 ммоль) и небольшое количество каждого из KI и 18-краун-6 и нагревали смесь при 80°C в течение 6 часов. Затем смесь выливали в воду и экстрагировали три раза MTBE. Органический слой промывали насыщенным раствором соли, сушили над MgSO4 и удаляли растворитель при пониженном давлении. Хроматография на силикагеле с использованием дихлорметана и смеси дихлорметан/MeOH (99:1) приводила к этиловому эфиру (R)-5-оксо-1-(2-трифторметилбензил)пирролидин-2-карбоновой кислоты (410 мг, ESI-МС [M+H]+=316,1; выход: 12%), который подвергали гидролизу до соответствующего карбоксилата путем перемешивания в течение ночи при комнатной температуре в растворе, содержащем 15 мл этанола и 1,56 мл 2н раствора NaOH (водн.). Выпаривание растворителя с последующим добавлением к остатку воды, экстракция этилацетатом, последующее подкисление водного слоя до pH 3 с использованием концентрированной HCl, экстракция дихлорметаном, сушка объединенных органических слоев над MgSO4 и удаление растворителя при пониженном давлении приводили к требуемому продукту в виде белой пены.
ESI-МС [M+H]+=288,1.
Пример S
(R)-1-(3-цианобензил)-5-оксопирролидин-2-карбоновая кислота
Указанное в заголовке соединение получали способом, аналогично описанному выше получению примера R.
ESI-МС [M+H]+=245,1.
Пример T
(R)-5-оксо-1-фенилпирролидин-2-карбоновая кислота
Смесь (R)-этил-5-оксопирролидин-2-карбоксилата (2760 мг, 17,56 ммоль), бромбензола (2,034 мл, 3030 мг, 19,32 ммоль), Pd2(dba)3 (402 мг, 0,439 ммоль), Cs2CO3 (8580 мг, 26,3 ммоль) и 4,5-бис(дифенилфосфино)-9,9-диметилксантена (ксантфос (Xantphos), 254 мг, 0,439 ммоль) в 70 мл диоксана перемешивали в атмосфере азота при 100°C в течение 6 часов. С учетом того, что реакция проходила только частично, после указанного времени дополнительно добавляли Pd2(dba)3 (402 мг, 0,439 ммоль), Cs2CO3 (2860 мг, 8,77 ммоль) и ксантфос (254 мг, 0,439 ммоль) и продолжали перемешивание при 100°C в течение дополнительных 6 часов. Реакционную смесь фильтровали через короткую колонку с целитом, затем удаляли растворитель при пониженном давлении и оставшийся остаток помещали в этилацетат, последовательно промывали насыщенным водным раствором NaHCO3 и водным раствором лимонной кислоты (каждый по 3 раза), затем водой и насыщенным раствором соли. Органический слой сушили над Na2SO4, растворитель выпаривали при пониженном давлении и полученный остаток очищали колоночной хроматографией на силикагеле с использованием дихлорметана, получая при этом (R)-этил-5-оксо-1-фенилпирролидин-2-карбоксилат в виде коричневого масла (715 мг, 3.07 ммоль; выход: 17%; ESI-МС [M+H]+=234,1). Гидролиз сложного эфира до соответствующего карбоксилата обеспечивали путем перемешивания при комнатной температуре в течение ночи в растворе, содержащем 4 мл этанола и 1,84 мл 2н раствора NaOH (водн.). Последующее выпаривание растворителя с последующим добавлением воды, экстракция MTBE (3×), подкисление водного слоя до pH 3 с использованием концентрированной HCl, экстракция дихлорметаном (3×), промывание объединенных органических слоев насыщенным раствором соли, сушка над MgSO4 и удаление растворителя при пониженном давлении приводили к указанному в заголовке соединению в виде бледно-коричневого порошка (0,5 г; выход: 79%).
ESI-МС [M+H]+=206,1.
Пример U
(R)-3-бензил-1-метил-2-оксоимидазолидин-4-карбоновая кислота
К раствору (R)-бензил-1-метил-2-оксоимидазолидин-4-карбоксилата (1000 мг, 4,27 ммоль) в 11 мл ДМФА добавляли гидрид натрия (129 мг, 5,12 ммоль), тем самым вызывая слегка экзотермическую реакцию (повышение температуры приблизительно до 27°C) и образование мутного раствора. После перемешивания в течение 1 часа при комнатной температуре добавляли (бромметил)бензол (0,609 мл, 876 мг, 5,12 ммоль), снова вызывая слегка экзотермическую реакцию (повышение температуры приблизительно 29°C). После перемешивания в течение ночи реакционную смесь выливали в воду и три раза экстрагировали этилацетатом. Объединенные органические слои промывали последовательно 10%-ным раствором лимонной кислоты, дважды насыщенным раствором NaHCO3 и насыщенным раствором соли, сушили над Na2SO4 и затем удаляли растворитель при пониженном давлении. Колоночная хроматография на силикагеле с использованием дихлорметана и смеси дихлорметан/метанол 98/2 давала (R)-бензил-3-бензил-1-метил-2-оксоимидазолидин-4-карбоксилат (425 мг, 1,38 ммоль, выход: 31%, ESI-МС [M+H]+=325,1), который преобразовывали в соответствующий карбоксилат путем перемешивания в течение ночи при комнатной температуре в смеси, состоящей из 2,7 мл ТГФ и 1,44 мл 2н раствора NaOH. К реакционной смеси добавляли воду с последующей экстракцией MTBE. Затем водный слой подкисляли до pH 3 с преобразовывали 2M раствора HCl и экстрагировали три раза дихлорметаном. Затем объединенные органические слои промывали насыщенным раствором соли, сушили над Na2SO4 и удаляли растворитель при пониженном давлении. Указанное в заголовке соединение получали в виде бесцветного масла, которое затвердевало с течением времени (245 мг, выход: 75%).
ESI-МС [M+H]+=235,1.
Пример V
(2R,4S)-1-бензил-4-метил-5-оксопирролидин-2-карбоновая кислота
К раствору (R)-1-бензил-5-оксопирролидин-2-карбоновой кислоты (1000 мг, 4,56 ммоль) в 55 мл ТГФ 10,03 мл медленно при -10°C добавляли 1M раствор бис(триметилсилил)амида лития в ТГФ (10.03 ммоль) и продолжали перемешивание при такой температуре в течение 1 часа. Затем добавляли раствор йодметана (0,284 мл, 647 мг, 4,56 ммоль) в 9 мл ТГФ (слегка экзотермическая реакция) и завершали реакцию путем перемешивания в течение ночи при комнатной температуре. Реакционную смесь коричневого цвета подкисляли с преобразовывали 2M HCl, экстрагировали три раза этилацетатом. Затем объединенные органические слои промывали насыщенным раствором соли, сушили над Na2SO4 и выпаривали растворитель при пониженном давлении. Указанное в заголовке соединение получали в виде коричневого масла, которое подвергали взаимодействию на следующей стадии без дополнительной очистки (890 мг неочищенного вещества, выход: 84%).
ESI-МС [M+H]+=234,1.
Пример W
2-бензил-1,1-диоксоизотиазолидин-3-карбоновая кислота
К раствору 1,1-диоксоизотиазолидин-3-карбоновой кислоты (степень чистоты 97%; 1040 мг, 6,11 ммоль) в 15 мл ДМФА добавляли (бромметил)бензол (степень чистоты 98%; 1,85 мл, 2660 мг, 15,27 ммоль) и K2CO3 (2350 мг, 18,3 ммоль) и перемешивали смесь в течение ночи при комнатной температуре. Затем реакционную смесь выливали в воду и три раза экстрагировали MTBE. Объединенные органические слои промывали насыщенным раствором соли, сушили над MgSO4 и удаляли растворитель при пониженном давлении. Хроматография на силикагеле с использованием дихлорметана приводила к бензиловому эфиру 2-бензил-1,1-диоксоизотиазолидин-3-карбоновой кислоты (1000 мг, 2,9 ммоль; выход: 47%; ESI-МС [M+H]+=346,1). Гидролиз сложного эфира до соответствующего карбоксилата обеспечивали путем перемешивания в течение ночи при комнатной температуре в растворе, содержащем 20 мл этанола и 2,46 мл 2н NaOH, с последующим нагреванием до 50°C в течение 2 часов. Выпаривание растворителя с последующим добавлением воды, экстракция этилацетатом, последующее удаление воды при пониженном давлении и обработка изопропанолом приводили в результате к выделению натриевой соли указанного в заголовке соединения (880 мг; содержит немного NaOH) в виде белого аморфного порошка.
ESI-МС [M+H]+=256,0.
Пример X
1-бензил-6-оксо-1,6-дигидропиридин-2-карбоновая кислота
К суспензии 6-гидроксипиколиновой кислоты (2500 мг, 17,97 ммоль) в 37,75 мл ДМФА добавляли (бромметил)бензол (6450 мг, 37,7 ммоль) и Cs2CO3 (12300 мг, 37,7 ммоль). Смесь перемешивали в течение ночи при комнатной температуре (тонкослойная хроматография указывала на практически полное превращение с образованием двух продуктов, вероятно, O- и N-алкилирования). Реакционную смесь выливали в воду и трижды экстрагировали этилацетатом. Объединенные органические слои последовательно промывали насыщенным водным раствором NaHCO3 (2×), водой, 10%-ным раствором лимонной кислоты (2×) и насыщенным раствором соли, сушили над Na2SO4 и удаляли растворитель при пониженном давлении. Колоночная хроматография на силикагеле с использованием смеси дихлорметан/гептан (3:1) с последующим использованием дихлорметана и смеси дихлорметан/MeOH (99:1) приводила к бензиловому эфиру 6-бензилоксипиридин-2-карбоновой кислоты (3030 мг, 9,41 ммоль, выход: 53%; ESI-МС [M+H]+=320,1) и бензиловому эфиру 1-бензил-6-оксо-1,6-дигидропиридин-2-карбоновой кислоты (содержащему незначительные примеси; 1920 мг, 6,01 ммоль, выход: 34%; ESI-МС [M+H]+=320,1). Последнее соединение подвергали гидролизу до соответствующего карбоксилата путем перемешивания в растворе, содержащем 10,3 мл этанола и 5,17 мл 2н водного раствора NaOH, при комнатной температуре в течение 3 часов. К реакционной смеси добавляли воду с последующей экстракцией этилацетатом (3×). Водный слой подкисляли до pH 3 2M раствором HCl и затем трижды экстрагировали дихлорметаном. Объединенные органические слои промывали насыщенным раствором соли и сушили над Na2SO4. Затем растворитель удаляли при пониженном давлении, с получением указанного в заголовке продукта в виде бледно-коричневого порошка (1230 мг, выход: 89%).
ESI-МС [M+H]+=230,1.
Соединения примеров Y и Z могут быть получены способом, аналогично описанному выше получению примера A.
Пример Y
(R)-5-оксо-1-(4-(трифторметил)бензил)пирролидин-2-карбоновая кислота
ESI-МС [M+H]+=493,2.
Пример Z
(R)-1-(2,6-дихлорбензил)-5-оксопирролидин-2-карбоновая кислота
ESI-МС [M+H]+=493,2.
II. Получение соединений общей формулы I
Пример 1
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-бензил-5-оксопирролидин-2-карбоксамид
1.1 (2R)-N-(4-амино-3-гидрокси-4-оксо-1-фенилбутан-2-ил)-1-бензил-5-оксопирролидин-2-карбоксамид
К раствору (R)-1-бензил-5-оксопирролидин-2-карбоновой кислоты (475 мг, 2,167 ммоль) в смеси, содержащей 15 мл ТГФ и 0,5 мл ДМФА, при 5°C последовательно добавляли 1-гидроксибензотриазол (365 мг, 2,383 ммоль), 3-амино-2-гидрокси-4-фенилбутанамид (421 мг, 2,167 ммоль), гидрохлорид N-(3-диметиламинопропил)-N'-этилкарбодиимида (EDC; 457 мг, 2,383 ммоль) и DIPEA (0,416 мл; 308 мг, 2,383 ммоль). После перемешивания в течение ночи при комнатной температуре растворитель выпаривали при пониженном давлении, к оставшемуся остатку добавляли воду и после перемешивания в течение 30 минут приблизительно при 5°C осадок отфильтровывали. Сушка при пониженном давлении давала указанное в заголовке соединение в виде не совсем белого порошка (786 мг; выход: 92%), которое без дополнительной очистки использовали на следующей стадии. ESI-МС [M+H]+=396,2. ВЭЖХ-анализ показал, что соединение выделялось в виде смеси диастереомеров.
1.2 (2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-бензил-5-оксопирролидин-2-карбоксамид
К раствору (2R)-N-(4-амино-3-гидрокси-4-оксо-1-фенилбутан-2-ил)-1-бензил-5-оксопирролидин-2-карбоксамида (400 мг, 1,012 ммоль) в 8 мл сухого диметилсульфоксида (ДМСО) добавляли EDC (1543 мг, 8,05 ммоль) и 2,2-дихлоруксусную кислоту (0,446 мл; 696 мг, 5,4 ммоль), получая слегка экзотермическую реакцию (40°C). После перемешивания в течение ночи при комнатной температуре добавляли этилацетат и воду, образовавшийся осадок отфильтровывали и оставшийся органический слой концентрировали досуха при пониженном давлении. Осадок и полученный остаток объединяли и после добавления воды и перемешивания приблизительно при 5°C в течение 30 минут образовавшийся осадок отфильтровывали и сушили при пониженном давлении. Указанное в заголовке соединение получали в виде не совсем белого порошка (243 мг, выход: 61%).
ESI-МС [M+H]+=394,2;
1H-ЯМР (400 МГц ДМСО), δ [м.д.]: 8,62 (д, 1H), 8,09 и 8,11 (2c, 1H), 7,85 (c, 1H), 7,18-7,34 (м, 8H), 7,12 (д, 1H), 7,01 (д, 1H), 5,15-5,26 (м, 1H), 4,83 и 4,74 (2д, 1H), 3,84-3,88 (м, 1H), 3,48 и 3,34 (2д, 1H частичное перекрывание сигналом воды), 3,15-3,21 (м, 1H), 2,71-2,78 (м, 1H), 2,18-2,32 (м, 2H), 1,98-2,15 (м, 1H), 1,67-1,74 и 1,48-1,55 (2м, 1H);
1H-ЯМР-анализ показал отношение диастереомерных конфигураций приблизительно 1:1.
Соединения следующих примеров получали способом, аналогично способу получения примера 1.
Пример 2
(2S)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-бензил-5-оксопирролидин-2-карбоксамид
Связывание (S)-1-бензил-5-оксопирролидин-2-карбоновой кислоты с 3-амино-2-гидрокси-4-фенилбутанамидом с последующим окислением полученного промежуточного гидроксиамида до соответствующего кетоамида.
1H-ЯМР (400 МГц, ДМСО), δ [м.д.]: 8,61 (д, 1H), 8,08 и 8,10 (2c, 1H), 7,84 (c, 1H), 7,18-7,34 (м, 8H), 7,12 (д, 1H), 7,01 (д, 1H), 5,15-5,26 (м, 1H), 4,83 и 4,74 (2д, 1H), 3,84-3,88 (м, 1H), 3,48 и 3,35 (2д, 1H частичное перекрывание сигналом воды), 3,15-3,21 (м, 1H), 2,71-2,78 (м, 1H), 2,18-2,32 (м, 2H), 1,98-2,15 (м, 1H), 1,67-1,74 и 1,48-1,55 (2м, 1H);
ESI-МС [M+H]+=394,2.
Пример 3
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(3-хлорбензил)-5-оксопирролидин-2-карбоксамид
Связывание (R)-1-(3-хлорбензил)-5-оксопирролидин-2-карбоновой кислоты с 3-амино-2-гидрокси-4-фенилбутанамидом и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=428,2, 430,2.
Пример 4
N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-бензил-6-оксо-1,6-дигидропиридин-2-карбоксамид
Связывание 1-бензил-6-оксо-1,6-дигидропиридин-2-карбоновой кислоты с 3-амино-2-гидрокси-4-фенилбутанамидом и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
1H-ЯМР (400 МГц, ДМСО), δ [м.д.]: 9,32 (д, 1H), 8,09 (c, 1H), 7,83 (c, 1H), 7,45 (дд, 1H), 7,16-7,28 (м, 10H), 6,50 (д, 1H), 6,17 (д, 1H), 5,32-5,36 (м, 1H), 5,08 и 4,98 (2д, 2H), 3,19 и 2,74 (2дд, 2H);
ESI-МС [M+H]+=404,2.
Пример 5
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(4-фторбензил)-5-оксопирролидин-2-карбоксамид
Связывание (R)-1-(4-фторбензил)-5-оксопирролидин-2-карбоновой кислоты с 3-амино-2-гидрокси-4-фенилбутанамидом и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
1H-ЯМР (400 МГц, ДМСО), δ [м.д.]: 8,63 (д, 1H), 8,09 и 8,11 (2c, 1H), 7,84 и 7,85 (2c, 1H), 7,01-7,32 (м, 9H), 5,15-5,23 (м, 1H), 4,77 и 4,67 (2д, 1H), 3,87 и 3,83 (2д, 1H), 3,51 и 3,36 (2д, 1H частичное перекрывание сигналом воды), 3,15-3,21 (м, 1H), 2,70-2,77 (м, 1H), 2,17-2,33 (м, 2H), 1,98-2,15 (м, 1H), 1,66-1,74 и 1,47-1,56 (2м, 1H);
ESI-МС [M+H]+=412,2.
Пример 6
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(3-метоксибензил)-5-оксопирролидин-2-карбоксамид
Связывание (R)-1-(3-метоксибензил)-5-оксопирролидин-2-карбоновой кислоты с 3-амино-2-гидрокси-4-фенилбутанамидом и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=424,2.
Пример 7
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(3-трифторметилбензил)-5-оксопирролидин-2-карбоксамид
Связывание (R)-1-(3-трифторметилбензил)-5-оксопирролидин-2-карбоновой кислоты с 3-амино-2-гидрокси-4-фенилбутанамидом и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=462,2.
Пример 8
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(3-фторбензил)-5-оксопирролидин-2-карбоксамид
Связывание (R)-1-(3-фторбензил)-5-оксопирролидин-2-карбоновой кислоты с 3-амино-2-гидрокси-4-фенилбутанамидом и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=412,1.
Пример 9
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-[2-(трифторметокси)бензил]пирролидин-2-карбоксамид
Связывание (R)-1-(2-трифторметоксибензил)-5-оксопирролидин-2-карбоновой кислоты с 3-амино-2-гидрокси-4-фенилбутанамидом и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=478,1.
Пример 10
1,1-диоксид N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-2-бензилизотиазолидин-3-карбоксамида
Связывание натриевой соли 2-бензил-1,1-диоксоизотиазолидин-3-карбоновой кислоты с 3-амино-2-гидрокси-4-фенилбутанамидом и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=430,1.
Пример 11
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(нафталин-1-илметил)-5-оксопирролидин-2-карбоксамид
Связывание (R)-1-нафталин-1-илметил-5-оксопирролидин-2-карбоновой кислоты с 3-амино-2-гидрокси-4-фенилбутанамидом и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=444,2.
Пример 12
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(нафталин-2-илметил)-5-оксопирролидин-2-карбоксамид
Связывание (R)-1-нафталин-2-илметил-5-оксопирролидин-2-карбоновой кислоты с 3-амино-2-гидрокси-4-фенилбутанамидом и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=444,2.
Пример 13
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-[3-(трифторметокси)бензил]пирролидин-2-карбоксамид
Связывание (R)-1-(3-трифторметоксибензил)-5-оксопирролидин-2-карбоновой кислоты с 3-амино-2-гидрокси-4-фенилбутанамидом и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=478,1.
Пример 14
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-бензил-6-оксопиперидин-2-карбоксамид
Связывание (R)-1-бензил-6-оксопиперидин-2-карбоновой кислоты с 3-амино-2-гидрокси-4-фенилбутанамидом и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=408,2.
Пример 15
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-фенилпирролидин-2-карбоксамид
Связывание (R)-5-оксо-1-фенилпирролидин-2-карбоновой кислоты с 3-амино-2-гидрокси-4-фенилбутанамидом и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=380,2.
Пример 16
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(3-цианобензил)-5-оксопирролидин-2-карбоксамид
Связывание (R)-1-(3-цианобензил)-5-оксопирролидин-2-карбоновой кислоты с 3-амино-2-гидрокси-4-фенилбутанамидом и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=419,1.
Пример 17
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-[2-(трифторметил)бензил]пирролидин-2-карбоксамид
Связывание (R)-5-оксо-1-(2-трифторметилбензил)пирролидин-2-карбоновой кислоты с 3-амино-2-гидрокси-4-фенилбутанамидом и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=462,1.
Пример 18
(4R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-3-бензил-1-метил-2-оксоимидазолидин-4-карбоксамид
Связывание (R)-3-бензил-1-метил-2-оксоимидазолидин-4-карбоновой кислоты с 3-амино-2-гидрокси-4-фенилбутанамидом и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=409,2.
Пример 19
(2R,4S)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-бензил-4-метил-5-оксопирролидин-2-карбоксамид
Связывание (2R,4S)-1-бензил-4-метил-5-оксопирролидин-2-карбоновой кислоты с 3-амино-2-гидрокси-4-фенилбутанамидом и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=408,1.
Пример 20
(2R)-1-бензил-N-{3,4-диоксо-1-фенил-4-[(пиридин-2-илметил)амино]бутан-2-ил}-5-оксопирролидин-2-карбоксамид
20.1 Этил 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутаноат
К раствору (R)-1-бензил-5-оксопирролидин-2-карбоновой кислоты (2440 мг, 11,13 ммоль) в смеси, содержащей 24 мл ТГФ и 4 мл ДМФА, последовательно добавляли при 5°C 1-гидроксибензотриазол (1875 мг, 12,24 ммоль), этил-3-амино-2-гидрокси-4-фенилбутаноат (2485 мг, 11,13 ммоль; получение описано в патентной заявке WO 98/25883, пример 8a на стр. 24), EDC (2347 мг, 12,24 ммоль) и DIPEA (6,41 мл; 4750 мг, 36,7 ммоль). После перемешивания в течение ночи при комнатной температуре реакционную смесь концентрировали при пониженном давлении, добавляли воду и трижды экстрагировали полученную смесь этилацетатом. Органический слой последовательно промывали насыщенным водным раствором NaHCO3 (2×), водным 10%-ным раствором лимонной кислоты (3×) и насыщенным раствором соли, сушили над Na2SO4 и затем удаляли растворитель при пониженном давлении. Указанное в заголовке соединение получали в виде желтого масла (4550 мг, выход: 96%), которое использовали без дополнительной очистки на следующей стадии.
ESI-МС [M+H]+=425,2.
20.2 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановая кислота
Этил 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутаноат (4550 мг неочищенного вещества с предыдущей стадии 22,1; макс. 10,72 ммоль), растворенный в 13 мл этанола, обрабатывали 6,43 мл 2н водного раствора NaOH при комнатной температуре в течение ночи. Затем для завершения реакции смесь нагревали до 50°C в течение 2 часов. Добавляли воду с последующей экстракцией MTBE (3×). Водный слой подкисляли до pH 3 с использованием 2M раствора HCl и трижды экстрагировали дихлорметаном. Затем объединенные дихлорметановые слои последовательно промывали водой и насыщенным раствором соли, сушили над Na2SO4 и удаляли растворитель при пониженном давлении. Указанное в заголовке соединение получали в виде бледно-коричневого порошка (2450 мг, выход: 58%).
ESI-МС [M+H]+=397,2.
20.3 (2R)-1-бензил-N-(3-гидрокси-4-оксо-1-фенил-4-(пиридин-2-илметиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид
3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановую кислоту (300 мг, 0,757 ммоль) и пиридин-2-илметанамин (94 мкл, 98 мг, 0,908 ммоль) растворяли в 13 мл дихлорметана и охлаждали до 5°C. При данной температуре последовательно добавляли гидрат 1-гидроксибензотриазола (127 мг, 0,832 ммоль), EDC (160 мг, 0,832 ммоль) и триэтиламин (1,58 мл, 127 мг, 1135 ммоль). После перемешивания в течение ночи при комнатной температуре реакционную смесь концентрировали при пониженном давлении, добавляли воду и трижды экстрагировали смесь этилацетатом. Объединенные органические слои последовательно промывали насыщенным водным раствором NaHCO3 и насыщенным раствором соли, сушили над Na2SO4 и удаляли растворитель при пониженном давлении. Колоночная хроматография на силикагеле с использованием смеси дихлорметан/MeOH (97/3), с последующим использованием смеси дихлорметан/MeOH (95/5), давала указанное в заголовке соединение (125 мг, выход: 34%) в виде белого порошка.
ESI-МС [M+H]+=487,2.
20.4 (2R)-1-бензил-N-{3,4-диоксо-1-фенил-4-[(пиридин-2-илметил)амино]бутан-2-ил}-5-оксопирролидин-2-карбоксамид
(2R)-1-бензил-N-(3-гидрокси-4-оксо-1-фенил-4-(пиридин-2-илметиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид преобразовывали в соответствующий кетоамид, как описано для стадии 1.2 примера 1.
ESI-МС [M+H]+=485,2.
Пример 21
(2R)-1-бензил-N-[4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил]-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с этиламином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=422,2.
Пример 22
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(3,5-диметоксибензил)-5-оксопирролидин-2-карбоксамид
Связывание (R)-1-(3,5-диметоксибензил)-5-оксопирролидин-2-карбоновой кислоты с 3-амино-2-гидрокси-4-фенилбутанамидом и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=454,2;
1H-ЯМР (400 МГц, ДМСО), δ [м.д.]: 8,60-8,57 (м, 1H), 8,03 (д, 1H, J=9,0 Гц), 7,12 (д, 1H, J=4,8 Гц), 7,29-7,18 (м, 5H), 6,39-6,22 (м, 3H), 5,22-5,17 (м, 1H), 4,75 (д, 0,5H, J=15,2 Гц), 4,70 (д, 0,5H, J=14,8 Гц), 3,94-3,89 (м, 1H), 3,40 (д, 0,5H, J=15,2 Гц), 3,31-2,26 (д, 0,5H, скрыт под пиком растворителя), 3,19-3,14 (м, 1H), 3,81-2,66 (м, 1H), 2,32-1,99 (м, 3H), 1,74-1,69 (м, 0,5H), 1,55-1,50 (м, 0,5H).
1H-ЯМР-анализ указывал на отношение диастереомерных конфигураций приблизительно 1:1.
Пример 23
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(пиридин-4-илметил)пирролидин-2-карбоксамид
Связывание (R)-5-оксо-1-пиридин-4-илметилпирролидин-2-карбоновой кислоты с 3-амино-2-гидрокси-4-фенилбутанамидом и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида с использованием реагента Десс-Мартина.
ESI-МС [M+H]+=395,1.
Пример 24
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(3,5-дифторбензил)-5-оксопирролидин-2-карбоксамид
Связывание (R)-1-(3,5-дифторбензил)-5-оксопирролидин-2-карбоновой кислоты с 3-амино-2-гидрокси-4-фенилбутанамидом и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=430,2;
1H-ЯМР (500 МГц, ДМСО), δ [м.д.]: 8,66-8,63 (м, 1H), 8,07 (д, 1H, J=5,0 Гц), 7,82 (c, 1H), 7,28-7,11 (м, 6H), 6,87 (c, 0,5H), 6,86 (c, 0,5H), 6,79 (c, 0,5H), 6,78 (c, 0,5H), 5,22-5,19 (м, 1H), 4,77 (д, 0,5H, J=20,0 Гц), 4,77 (д, 0,5H, J=20,0 Гц), 3,99-3,96 (м, 1H), 3,62 (д, 0,5H, J=15,0 Гц), 3,47 (д, 0,5H, J=15,0 Гц), 3,20-3,16 (м, 1H), 2,78-2,75 (м, 1H), 2,31-2,11 (м, 3H), 1,76 (м, 0,5H), 1,56 (м, 0,5H).
1H-ЯМР-анализ указывал на отношение диастереомерных конфигураций приблизительно 1:1.
Следующие соединения примеров 25-35 получали способом, аналогично синтезу (2R)-1-бензил-N-(3-гидрокси-4-оксо-1-фенил-4-(пиридин-2-илметиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамида (пример 20.3) с последующим окислением до соответствующего кетоамида, как описано на стадии 1.2 примера 1.
Пример 25
(2R)-1-бензил-N-(4-(метиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с метиламином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=408,2.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~1,5:1: δ [м.д.]: 8,71-8,68 (м, 1H), 8,65-8,63 (м, 1H), 7,36-7,03 (м, 10H), 5,26-5,19 (м, 1H), 4,86 (д, 0,6H), 4,76 (д, 0,4H), 3,92-3,88 (м, 1H), 3,52 (д, 0,6H), 3,37 (д, 0,4H), 3,24-3,15 (м, 1H), 2,80-2,75 (м, 1H), 2,72-2,70 (м, 3H), 2,31-2,22 (м, 2H), 2,15-2,05 (м, 1H), 1,75-1,72 (м, 0,4H), 1,58-1,53 (м, 0,6H).
Пример 26
(2R)-1-бензил-N-(3,4-диоксо-1-фенил-4-(пропиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с пропиламином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=436,2.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~2:1: δ [м.д.]: 8,83-8,81 (м, 1H), 8,69-8,67 (м, 1H), 7,37-7,04 (м, 10H), 5,29-5,22 (м, 1H), 4,86 (д, 0,7H), 4,77 (д, 0,3H), 3,93-3,91 (м, 1H), 3,53 (д, 1H), 3,23-3,13 (м, 3H), 2,82-2,77 (м, 1H), 2,29-2,23 (м, 2H), 2,12-2,06 (м, 1H), 1,57-1,49 (м, 3H), 0,98-0,86 (м, 3H).
Пример 27
(2R)-1-бензил-N-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с циклопропиламином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=434,2.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~1:1: δ [м.д.]: 8,86-8,83 (м, 1H), 8,69-8,67 (м, 1H), 7,36-7,04 (м, 10H), 5,26-5,18 (м, 1H), 4,86 (д, 0,5H), 4,77 (д, 0,5H), 3,91-3,89 (м, 1H), 3,52 (д, 0,5H), 3,39-3,35 (д, 0,5H, скрыт под сигналом растворителя), 3,23-3,19 (м, 1H), 2,84-2,74 (м, 2H), 2,33-2,21 (м, 2H), 2,17-2,01 (м, 1H), 1,76-1,70 (м, 0,5H), 1,59-1,52 (м, 0,5H), 0,72-0,59 (м, 4H).
Пример 28
(2R)-1-бензил-N-(4-(изобутиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с изобутиламином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=450,2.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~1:1: δ [м.д.]: 8,81-8,78 (м, 1H), 8,68-8,67 (м, 1H), 7,33-7,03 (м, 10H), 5,30-5,22 (м, 1H), 4,86 (д, 0,5H), 4,76 (д, 0,5H), 3,92-3,91 (м, 1H), 3,26-3,16 (м, 1H), 3,08-2,94 (м, 2H), 2,86-2,74 (м, 1H), 2,36-2,05 (м, 3,5H), 1,88-1,70 (м, 2H), 1,52-1,61 (м, 0,5H), 0,95-0,83 (м, 6H).
Пример 29
(2R)-1-бензил-N-(4-(циклобутиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с циклобутиламином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=448,2.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~2:1: δ [м.д.]: 9,05-9,03 (м, 1H), 8,70-8,68 (м, 1H), 7,36-7,03 (м, 10H), 5,21-5,15 (м, 1H), 4,85 (д, 0,7H), 4,75 (д, 0,3H), 4,31-4,25 (м, 1H), 3,91-3,88 (м, 1H), 3,50 (д, 0,7H), 3,38-3,33 (д, 0,3H, скрыт под сигналом растворителя), 3,21-3,17 (м, 1H), 2,79-2,74 (м, 1H), 2,29-2,04 (м, 6H), 1,72-1,53 (м, 4H).
Пример 30
(2R)-1-бензил-N-(4-(метоксиамино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с O-метилгидроксиламином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида с использованием 2-йодоксибензойной кислоты (IBX):
IBX (293 мг, 0,472 ммоль) добавляли к раствору (2R)-1-бензил-N-(3-гидрокси-4-(метоксиамино)-4-оксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамида (143 мг, 0,337 ммоль) в ДМСО (5 мл). После перемешивания в течение 2 часов добавляли еще IBX (105 мг, 0,169 ммоль) и продолжали перемешивание в течение ночи. Добавляли насыщенный водный раствор NaHCO3 и разбавляли реакционную смесь водой и DCM. Органические слой отделяли и экстрагировали водный слой DCM. Объединенные органические слои промывали водой и сушили (MgSO4). Полученный неочищенный продукт растворяли в минимальном количестве DCM и добавляли простой диэтиловый эфир. Образовавшийся осадок выделяли и сушили в вакууме. Указанное в заголовке соединение получали в виде бесцветного твердого вещества (12 мг, 8%).
ESI-МС [M+H]+=424,2.
1H-ЯМР (500 МГц, ДМСО) (отдельные диастереомеры, абсолютная конфигурация не определена: δ [м.д.]: 8,24-8,22 (м, 1H), 7,31-7,22 (м, 9H), 7,02-7,00 (м, 2H), 5,52-5,47 (м, 1H), 4,74-4,70 (м, 1H), 3,95-3,93 (м, 1H), 3,65 (c, 3H), 2,70-2,44 (м, 2H, скрыт под сигналом растворителя), 2,36-2,09 (м, 4H), 1,79-1,72 (м, 1H).
Пример 31
(2R)-1-бензил-N-(3,4-диоксо-1-фенил-4-(2-(пиридин-2-ил)этиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с 2-(пиридин-2-ил)этанамином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=499,2.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~1:1: δ [м.д.]: 8,84-8,79 (м, 1H), 8,59-8,56 (м, 1H), 8,47-8,46 (м, 1H), 7,69-7,65 (м, 1H), 7,31-7,19 (м, 10H), 7,12-7,10 (м, 1H), 7,01-6,99 (м, 1H), 5,27-5,18 (м, 1H), 4,82 (д, 0,5H), 4,73 (д, 0,5H), 3,89-3,86 (м, 1H), 3,56-3,47 (м, 3H), 3,15-3,11 (м, 1H), 2,96-2,92 (м, 2H), 2,74-2,69 (м, 1H), 2,30-2,19 (м, 2H), 2,11-2,01 (м, 1H), 1,72-1,70 (м, 0,5H), 1,55-1,51 (м, 0,5H).
Пример 32
(2R)-1-бензил-N-(3,4-диоксо-1-фенил-4-(3-(пиридин-2-ил)пропиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с 3-(пиридин-2-ил)пропан-1-амином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=513,2.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~1:1: δ [м.д.]: 8,84-8,79 (м, 1H), 8,59-8,56 (м, 1H), 8,47-8,46 (м, 1H), 7,69-7,65 (м, 1H), 7,31-7,19 (м, 10H), 7,12-7,10 (м, 1H), 7,01-6,99 (м, 1H), 5,27-5,18 (м, 1H), 4,82 (д, 0,5H), 4,73 (д, 0,5H), 3,89-3,86 (м, 1H), 3,56-3,47 (м, 3H), 3,15-3,11 (м, 1H), 2,96-2,92 (м, 2H), 2,74-2,69 (м, 1H), 2,30-2,19 (м, 2H), 2,11-2,01 (м, 1H), 1,72-1,70 (м, 0,5H), 1,55-1,51 (м, 0,5H).
Пример 33
(2R)-1-бензил-N-(3,4-диоксо-1-фенил-4-(3-фенилпропиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с 3-фенилпропан-1-амином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=512,3.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~4:3: δ [м.д.]: 8,84-8,79 (м, 1H), 8,61-8,59 (м, 1H), 8,45-8,43 (м, 1H), 7,67-7,63 (м, 1H), 7,31-7,14 (м, 10H), 7,11 (д, 1H), 7,00 (д, 1H), 5,27-5,18 (м, 1H), 4,82 (д, 0,6H), 4,73 (д, 0,4H), 3,89-3,86 (м, 1H), 3,50 (д, 0,6H), 3,35 (д, 0,4H), 3,21-3,16 (м, 3H), 2,78-2,70 (м, 3H), 2,29-1,99 (м, 3H), 1,91-1,84 (м, 2H), 1,73-1,68 (м, 0,4H), 1,55-1,49 (м, 0,6H), 2,64-1,53 (м, 2H), 2,33-2,05 (м, 3Н), 1,84-1,71 (м, 2,4H), 1,59-1,54 (м, 0,6H).
Пример 34
(2R)-1-бензил-N-(4-(этил(метил)амино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с N-метилэтанамином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=436,2.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~2:1: δ [м.д.]: 8,82-8,79 (м, 1H), 7,35-7,22 (м, 8H), 7,10-7,08 (м, 1,5H), 7,01-7,00 (м, 0,5H), 4,90-4,87 (м, 1H), 4,82-4,75 (м, 1H), 3,86-3,84 (м, 1H), 3,44-3,19 (м, 4H), 2,99-2,87 (м, 4H), 2,37-2,17 (м, 2H), 2,14-2,04 (м, 1H), 1,67-1,60 (м, 0,3H), 1,53-1,43 (м, 0,6H), 1,16-1,05 (м, 3H).
Пример 35
(2R)-1-бензил-N-(4-(2-хлорбензиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с (2-хлорфенил)метанамином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=518,2.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~1:1: δ [м.д.]: 9,36 (ушир.с, 1H), 8,76-8,75 (м, 1H), 7,47-7,05 (м, 14H), 5,29-5,19 (м, 1H), 4,89-4,86 (м, 0,5H), 4,78-4,75 (м, 0,5H), 3,92 (ушир.с, 1H), 3,57-3,52 (д, 0,5H), 3,38-3,32 (0,5H скрыт под сигналом растворителя), 3,25-3,23 (м, 1H), 2,87-2,83 (м, 1H), 2,53-2,51 (м, 1H), 2,35-2,05 (м, 4H), 1,76-1,71 (м, 0,5H), 1,58-1,55 (м, 0,5H).
Пример 36
(2R)-N-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамид
36.1 2-гидрокси-3-((R)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамидо)-4-фенилбутановая кислота
Указанное в заголовке соединение получали способом, аналогично синтезу этил-3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутаноата с последующим гидролизом сложного эфира, обеспечивающим 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановую кислоту, как описано на стадиях 20.1 и 20.2 примера 20.
ESI-МС [M+H]+=465,1.
36.2 (2R)-N-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамид
Связывание 2-гидрокси-3-((R)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамидо)-4-фенилбутановой кислоты с циклопропиламином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=502,2.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~3:1: δ [м.д.]: 8,78-8,77 (м, 1H), 8,60-8,57 (м, 1H), 7,76-7,50 (м, 4H), 7,35-7,18 (м, 5H), 5,27-5,22 (м, 1H), 4,99-4,90 (м, 1H), 4,00-3,98 (м, 1H), 3,90-3,81 (м, 1H), 3,20-3,16 (м, 1H), 2,82-2,69 (м, 2H), 2,35-2,15 (м, 3H), 1,84-1,80 (м, 0,3H), 1,62-1,55 (м, 0,7H), 0,70-0,61 (м, 4H).
Пример 37
(2R)-N-(4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамид
Связывание 2-гидрокси-3-((R)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамидо)-4-фенилбутановой кислоты с этиламином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=490,2.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~2:1: δ [м.д.]: 8,74-8,72 (м, 1H), 8,60-8,57 (м, 1H), 7,75-7,50 (м, 4H), 7,34-7,17 (м, 5H), 5,28-5,24 (м, 1H), 4,98-4,90 (м, 1H), 4,00-3,99 (м, 1H), 3,88 (д, 0,7H), 3,83 (д, 0,3H), 3,20-3,16 (м, 3H), 2,79-2,70 (м, 1H), 2,34-2,13 (м, 3H), 1,84-1,80 (0,3H), 1,60-1,56 (м, 0,7H), 1,10-1,06 (м, 3H).
Пример 38
(2R)-N-(4-(бензиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамид
Связывание 2-гидрокси-3-((R)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамидо)-4-фенилбутановой кислоты с фенилметанамином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=552,2.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~3:2: δ [м.д.]: 9,26-9,25 (м, 1H), 8,64-8,60 (м, 1H), 7,75-7,48 (м, 3H), 7,35-7,16 (м, 11H), 5,27-5,21 (м, 1H), 4,94 (т, 1H), 4,37-4,34 (м, 2H), 4,01-4,00 (м, 1H), 3,89-3,81 (м, 1H), 3,21-3,14 (м, 1H), 2,83-2,72 (м, 1H), 2,36-2,13 (м, 3H), 1,81-1,77 (0,4H), 1,61-1,54 (м, 0,6H).
Пример 39
(2R)-N-(4-(изопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамид
Связывание 2-гидрокси-3-((R)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамидо)-4-фенилбутановой кислоты с пропан-2-амином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=504,2.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~1:1: δ [м.д.]: 8,64-8,60 (м, 2H), 7,77-7,49 (м, 3H), 7,35-7,18 (м, 6H), 5,30-5,23 (м, 1H), 4,99-4,91 (м, 1H), 4,02-3,80 (м, 3H), 3,19-3,16 (м, 1H), 3,79-3,70 (м, 1H), 2,35-2,26 (м, 3H), 1,85-1,81 (0,5H), 1,59-1,55 (м, 0,5H), 1,15-1,12 (м, 6H).
Пример 40
(2R)-N-(3,4-диоксо-1-фенил-4-(2-(пиридин-2-ил)этиламино)бутан-2-ил)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамид
Связывание 2-гидрокси-3-((R)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамидо)-4-фенилбутановой кислоты с 2-(пиридин-2-ил)этанамином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=567,2.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~1:1: δ [м.д.]: 8,84-8,81 (м, 1H), 8,58-8,54 (м, 1H), 8,51-8,50 (м, 1H), 7,74-7,59 (м, 3H), 7,53-7,48 (м, 1H), 7,34-7,15 (м, 8H), 5,28-5,24 (м, 1H), 4,97-4,90 (м, 1H), 4,00-3,97 (м, 1H), 3,89 (д, 0,7H), 3,83 (д, 0,3H), 3,60-3,46 (м, 2H), 3,15-3,09 (м, 1H), 2,98-2,95 (м, 2H), 2,76-2,65 (м, 1H), 2,34-2,13 (м, 3H), 1,84-1,80 (м, 0,3H), 1,60-1,55 (м, 0,7H).
Пример 41
(2R)-N-(3,4-диоксо-1-фенил-4-(3-(пиридин-2-ил)пропиламино)бутан-2-ил)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамид
Связывание 2-гидрокси-3-((R)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамидо)-4-фенилбутановой кислоты с 3-(пиридин-2-ил)пропан-1-амином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=581,2.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~1:1: δ [м.д.]: 8,84-8,83 (м, 1H), 8,61-8,58 (м, 1H), 8,48-8,47 (м, 1H), 7,74-7,58 (м, 3H), 7,52-7,48 (м, 1H), 7,34-7,17 (м, 8H), 5,28-5,25 (м, 1H), 4,98-4,90 (м, 1H), 4,01-3,99 (м, 1H), 3,90 (д, 0,6H), 3,83 (д, 0,4H), 3,23-3,13 (м, 2H), 2,80-2,70 (м, 3H), 2,54-2,52 (м, 1H), 2,33-2,15 (м, 3H), 1,93-1,80 (м, 2,4H), 1,60-1,56 (м, 0,6H).
Пример 42
(2R)-N-(4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-(2-метокси-6-(трифторметил)бензил)-5-оксопирролидин-2-карбоксамид
42.1 2-гидрокси-3-((R)-1-(2-метокси-6-(трифторметил)бензил)-5-оксопирролидин-2-карбоксамидо)-4-фенилбутановая кислота
Указанное в заголовке соединение получали способом, аналогично синтезу этил-3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутаноата с последующим гидролизом сложного эфира, обеспечивающим 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановую кислоту, как описано на стадиях 20.1 и 20.2 примера 20.
ESI-МС [M+H]+=495,2.
42.2 (2R)-N-(4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-(2-метокси-6-(трифторметил)бензил)-5-оксопирролидин-2-карбоксамид
Связывание 2-гидрокси-3-((R)-1-(2-метокси-6-(трифторметил)бензил)-5-оксопирролидин-2-карбоксамидо)-4-фенилбутановой кислоты с этиламином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=520,2.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~1:1: δ [м.д.]: 8,79-8,70 (м, 1H), 8,32-8,31 (м, 1H), 7,52-7,46 (м, 1H), 7,33-7,16 (м, 7H), 5,45-5,41 (м, 0,5H), 5,20-5,17 (м, 0,5H), 4,93-4,86 (м, 1H), 3,99-3,95 (м, 1H), 3,71 (c, 2H), 3,40 (c, 3H), 3,23-3,13 (м, 2H), 2,76-2,70 (м, 1H), 2,15-2,11 (м, 1H), 2,04-1,96 (м, 1,5H), 1,89-1,80 (м, 1H), 1,41-1,37 (м, 0,5H), 1,11-1,04 (м, 3H).
Пример 43
(2R)-N-(3,4-диоксо-1-фенил-4-(пиридин-2-илметиламино)бутан-2-ил)-1-(2-метокси-6-(трифторметил)бензил)-5-оксопирролидин-2-карбоксамид
Связывание 2-гидрокси-3-((R)-1-(2-метокси-6-(трифторметил)бензил)-5-оксопирролидин-2-карбоксамидо)-4-фенилбутановой кислоты с пиридин-2-илметанамином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=583,2.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~3:4: δ [м.д.]: 9,32-9,22 (м, 1H), 8,53-8,51 (м, 1H), 8,37-8,33 (м, 1H), 7,80-7,74 (м, 1H), 7,53-7,47 (м, 1H), 7,35-7,19 (м, 9H), 5,47-5,41 (м, 0,5H), 5,24-5,19 (м, 0,5H), 4,95-4,87 (м, 1H), 4,50-4,45 (м, 2H), 3,99 (д, 1H), 3,73 (c, 3H), 3,26-3,15 (м, 1H), 2,82-2,61 (м, 1H), 2,18-1,91 (м, 3H), 1,90-1,77 (м, 1H), 1,45-1,39 (м, 1H).
Пример 44
(2R)-N-(4-(бензиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-(2-метокси-6-(трифторметил)бензил)-5-оксопирролидин-2-карбоксамид
Связывание 2-гидрокси-3-((R)-1-(2-метокси-6-(трифторметил)бензил)-5-оксопирролидин-2-карбоксамидо)-4-фенилбутановой кислоты с фенилметанамином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=582,3.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~1:1: δ [м.д.]: 9,39-9,31 (м, 1H), 8,40-8,36 (м, 1H), 7,53-7,48 (м, 1H), 7,37-7,19 (м, 12H), 5,46-5,43 (м, 0,5H), 5,22-5,18 (м, 0,5H), 4,95-4,88 (м, 1H), 4,39-4,35 (м, 2H), 4,99 (д, 1H), 3,72 (c, 3H), 3,41-3,38 (м, 1H, скрыт под сигналом растворителя), 3,22-3,16 (м, 1H), 2,81-2,76 (м, 1H), 2,14-2,11 (м, 1H), 2,04-1,96 (м, 1,5H), 1,87-1,77 (м, 1H), 1,41-1,40 (м, 0,5H).
Пример 45
(2R)-N-(3,4-диоксо-1-фенил-4-(2-(пиридин-2-ил)этиламино)бутан-2-ил)-5-оксо-1-(2-(трифторметокси)бензил)пирролидин-2-карбоксамид
45.1 2-гидрокси-3-((R)-5-оксо-1-(2-(трифторметокси)бензил)пирролидин-2-карбоксамидо)-4-фенилбутановая кислота
Указанное в заголовке соединение получали способом, аналогично синтезу этил-3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутаноата с последующим гидролизом сложного эфира, обеспечивающим 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановую кислоту, как описано на стадиях 20.1 и 20.2 примера 20.
ESI-МС [M+H]+=481,1.
45.2 (2R)-N-(3,4-диоксо-1-фенил-4-(2-(пиридин-2-ил)этиламино)бутан-2-ил)-5-оксо-1-(2-(трифторметокси)бензил)пирролидин-2-карбоксамид
Связывание 2-гидрокси-3-((R)-5-оксо-1-(2-(трифторметокси)бензил)пирролидин-2-карбоксамидо)-4-фенилбутановой кислоты с 2-(пиридин-2-ил)этанамином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=583,2.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~3:2: δ [м.д.]: 8,86-8,84 (м, 1H), 8,59-8,57 (м, 1H), 8,50-8,49 (м, 1H), 7,72-7,69 (м, 1H), 7,46-7,12 (м, 11H), 5,29-5,25 (м, 1H), 4,89-4,82 (м, 1H), 3,93-3,86 (м, 1H), 3,72 (д, 0,6H), 3,65 (д, 0,4H), 3,60-3,49 (м, 2H), 3,17-3,12 (м, 1H), 3,01-2,91 (м, 2H), 2,76-2,70 (м, 1H), 2,33-2,07 (м, 3H), 1,79-1,74 (м, 0,4H), 1,59-1,53 (м, 0,6H).
Пример 46
(2R)-1-(2-хлорбензил)-N-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид
46.1 3-((R)-1-(2-хлорбензил)-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановая кислота
Указанное в заголовке соединение получали способом, аналогично синтезу этил-3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутаноата с последующим гидролизом сложного эфира, обеспечивающим 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановую кислоту, как описано на стадиях 20.1 и 20.2 примера 20.
ESI-МС [M+H]+=431,1.
46.2 (2R)-1-(2-хлорбензил)-N-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-(2-хлорбензил)-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с циклопропиламином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=468,2.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~3:2: δ [м.д.]: 8,85-8,84 (м, 1H), 8,67-8,66 (м, 1H), 7,48-7,11 (м, 9H), 5,27-5,21 (м, 1H), 4,86-4,78 (м, 1H), 3,99-3,96 (м, 1H), 3,79 (д, 0,6H), 3,70 (д, 0,4H), 3,22-3,19 (м, 1H), 2,82-2,74 (м, 2H), 2,33-2,12 (м, 3H), 1,80-1,76 (м, 0,4H), 1,60-1,56 (м, 0,6H), 0,71-0,55 (м, 4H).
Пример 47
(2R)-1-(2-хлорбензил)-N-(4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-(2-хлорбензил)-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с этиламином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=456,2.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~1:1: δ [м.д.]: 8,81-8,79 (м, 1H), 8,67-8,64 (м, 1H), 7,49-7,09 (м, 9H), 5,26-5,24 (м, 1H), 4,83 (д, 0,5H), 4,78 (д, 0,5H), 4,02-3,98 (м, 1H), 3,81-3,35 (м, 2H, скрыт под сигналом растворителя), 3,23-3,17 (м, 2H), 2,79-2,73 (м, 1H), 2,32-2,11 (м, 3H), 1,79-1,76 (м, 0,5H), 1,59-1,55 (м, 0,5H), 1,10-1,07 (м, 3H).
Пример 48
(2R)-N-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-(2,6-дифторбензил)-5-оксопирролидин-2-карбоксамид
48.1 3-((R)-1-(2,6-дифторбензил)-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановая кислота
Указанное в заголовке соединение получали способом, аналогично синтезу этил-3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутаноата с последующим гидролизом сложного эфира, обеспечивающим 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановую кислоту, как описано на стадиях 20.1 и 20.2 примера 20.
ESI-МС [M+H]+=433,1
48.2 (2R)-N-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-(2,6-дифторбензил)-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-(2,6-дифторбензил)-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с циклопропиламином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=470,2.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~3:2: δ [м.д.]: 8,85-8,81 (м, 1H), 8,64-8,60 (м, 1H), 7,43-6,98 (м, 8H), 5,28-5,19 (м, 1H), 4,86-4,76 (м, 1H), 3,97-3,80 (м, 2H), 3,24-3,16 (м, 1H), 2,81-2,72 (м, 2H), 2,25-2,00 (м, 3H), 1,77-1,73 (м, 0,6H), 1,50-1,46 (м, 0,4H), 0,70-0,55 (м, 4H).
Пример 49
(2R)-1-(2,6-дифторбензил)-N-(4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-(2,6-дифторбензил)-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с этиламином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=458,2.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~1:1: δ [м.д.]: 8,82-8,77 (м, 1H), 8,64-8,60 (м, 1H), 7,42-6,99 (м, 8H), 5,30-5,19 (м, 1H), 4,84 (д, 0,5H), 4,78 (д, 0,5H), 3,97-3,92 (м, 1H), 3,84-3,81 (м, 1H), 3,23-3,15 (м, 3H), 2,82-2,73 (м, 1H), 2,24-2,00 (м, 3H), 1,77-1,35 (м, 0,5H), 1,49-1,46 (м, 0,5H), 1,14-1,04 (м, 3H).
Пример 50
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-[2-метокси-6-(трифторметил)бензил]пирролидин-2-карбоксамид
Связывание (R)-5-оксо-1-(2-метокси-6-трифторметилбензил)пирролидин-2-карбоновой кислоты с 3-амино-2-гидрокси-4-фенилбутанамидом и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=492,1.
Пример 51
(2R)-N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(2,6-дифторбензил)пирролидин-2-карбоксамид
Связывание (R)-5-оксо-1-(2,6-дифторбензил)пирролидин-2-карбоновой кислоты с 3-амино-2-гидрокси-4-фенилбутанамидом и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
ESI-МС [M+H]+=430,1.
Пример 52
(2R)-1-бензил-N-(3,4-диоксо-1-фенил-4-(тиазол-5-илметиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с C-тиазол-5-илметиламином (5-тиазолметиламином) и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида описанным выше способом.
ESI-МС [M+H]+=491,1.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~5:3: δ [м.д.]: 9,47-9,46 (м, 1H), 9,00 (c, 1H), 8,71-8,70 (м, 1H), 7,81 (c, 1H), 7,34-7,04 (м, 10H), 5,30-5,21 (м, 1H), 5,87-5,75 (м, 1H), 5,65-4,48 (м, 2H), 3,91-3,90 (м, 1H), 3,54-3,20 (м, 2H), 2,83-2,79 (м, 1H), 2,33-2,01 (м, 3H), 1,74-1,69 (м, 0,3H), 1,57-1,51 (м, 0,5H).
Пример 53
(2R)-N-(4-(бензо[d]тиазол-2-илметиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-бензил-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с гидрохлоридом бензо[d]тиазол-2-илметанамина и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида описанным выше способом.
ESI-МС [M+H]+=541,2.
1H-ЯМР (500 МГц, ДМСО), один диастереомер: δ [м.д.]: 9,77-9,74(м, 1H), 8,74-8,73 (м, 1H), 8,08 (д, 1H), 7,98 (д, 1H), 7,55-7,08 (м, 12H), 5,27-5,22 (м, 1H), 4,88-4,79 (м, 2H), 3,93 (м, 1H), 3,57-3,54 (м, 1H), 3,32-3,22 (м, 1H), 2,88-2,83 (м, 1H), 2,28-2,05 (м, 3H), 1,59-1,56 (м, 1H).
Пример 54
(2R)-1-бензил-N-(4-морфолино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с морфолином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида описанным выше способом.
ESI-МС [M+H]+=464,2.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~1:2: δ [м.д.]: 8,89-8,88 (м, 1H), 7,34-7,03 (м, 10H), 4,92-4,79 (м, 2H), 3,87-3,86 (м, 1H), 3,63-3,26 (м, 10H), 2,98-2,93 (м, 1H), 2,33-2,11 (м, 3H), 1,72-1,60 (м, 0,3H), 1,57-1,50 (м, 0,6H).
Пример 55
(2R)-N-(4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(4-(трифторметил)бензил)пирролидин-2-карбоксамид
55.1 2-гидрокси-3-((R)-5-оксо-1-(4-(трифторметил)бензил)пирролидин-2-карбоксамидо)-4-фенилбутановая кислота
Указанное в заголовке соединение получали способом, аналогично получению этил-3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутаноата, описанному в примере 20.1, с последующим гидролизом сложного эфира, обеспечивающим 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановую кислоту, описанную в примере 20.2.
ESI-МС [M+H]+=504,2.
55.2 (2R)-N-(4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(4-(трифторметил)бензил)пирролидин-2-карбоксамид
Связывание 2-гидрокси-3-((R)-5-оксо-1-(4-(трифторметил)бензил)пирролидин-2-карбоксамидо)-4-фенилбутановой кислоты с этиламином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида описанным выше способом.
ESI-МС [M+H]+=490,2.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~1:1: δ [м.д.]: 8,80-8,79 (м, 1H), 8,68-8,67 (м, 1H), 7,72-7,65 (м, 2H), 7,40-7,25 (м, 7H), 5,28-5,23 (м, 1H), 4,91-4,88 (м, 0,5H), 4,79-4,76 (м, 0,5H), 3,95-3,94 (м, 1H), 3,71-3,68 (м, 1H), 3,55-3,52 (м, 1H), 3,25-3,14 (м, 2H), 2,79-2,74 (м, 1H), 2,38-2,05 (м, 3H), 1,83-1,72 (м, 0,5H), 1,65-1,56 (м, 0,5H), 1,14-1,05 (м, 3H).
Пример 56
(2R)-1-бензил-N-(4-(циклогексиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с циклогексиламином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида описанным выше способом.
ESI-МС [M+H]+=476,2.
1H-ЯМР (400 МГц, ДМСО), смесь диастереомеров ~4:3: δ [м.д.]: 8,64-8,57 (м, 2H), 7,36-7,05 (м, 8H), 7,16-7,14 (м, 1H), 7,05-7,03 (м, 1H), 5,31-5,21 (м, 1H), 4,86 (д, 0,6H), 4,77 (д, 0,4H), 3,93-3,89 (м, 1H), 3,63-3,51 (м, 1,5H), 3,40-3,32 (м, 0,5H), 3,23-3,17 (м, 1H), 2,82-2,76 (м, 1H), 2,36-2,02 (м, 3H), 1,74-1,59 (м, 6H), 1,37-1,27 (м, 5H).
Пример 57
(2R)-N-(4-(2-бензоилгидразинил)-3,4-диоксо-1-фенилбутан-2-ил)-1-бензил-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с бензоилгидразином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида описанным выше способом.
ESI-МС [M+H]+=513,2.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~1:1: δ [м.д.]: 10,86 (д, 1H), 10,59 (д, 1H), 8,70-8,67 (м, 1H), 7,92-7,91 (м, 2H), 7,1-7,09 (м, 13H), 5,34-5,24 (м, 1H), 4,87 (д, 0,5H), 4,78 (д, 0,5H), 3,94-3,93 (м, 1H), 3,58 (д, 1H), 3,44-3,28 (д, 1H, скрыт под сигналом растворителя), 2,87-2,82 (м, 1H), 2,40-2,33 (м, 3H), 1,83-1,77 (м, 0,5H), 1,66-1,59 (м, 0,5H).
Пример 58
(2R)-N-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(4-(трифторметил)бензил)пирролидин-2-карбоксамид
Связывание 2-гидрокси-3-((R)-5-оксо-1-(4-(трифторметил)бензил)пирролидин-2-карбоксамидо)-4-фенилбутановой кислоты с циклопропанамином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида описанным выше способом.
ESI-МС [M+H]+=502,2.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~2:1: δ [м.д.]: 8,84-8,83 (м, 1H), 8,69-8,67 (м, 1H), 7,71-7,65 (м, 2H), 7,40-7,23 (м, 7H), 5,23-5,20 (м, 1H), 4,89 (д, 0,6H), 4,77 (д, 0,3H), 3,95-3,92 (м, 1H), 3,70-3,52 (м, 1H), 3,22-3,19 (м, 1H), 2,82-2,74 (м, 2H), 2,34-2,09 (м, 3H), 1,79-1,74 (м, 0,3H), 1,60-1,56 (м, 0,6H), 0,70-0,62 (м, 4H).
Пример 59
(2R)-1-бензил-N-(3,4-диоксо-1-фенил-4-(тиазол-2-илметиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с 2-аминометилтиазолом и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида описанным выше способом.
ESI-МС [M+H]+=491,2.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~5:3: δ [м.д.]: 9,64-9,64 (м, 1H), 8,73-8,72 (м, 1H), 7,76-7,66 (м, 2H), 7,3-7,05 (м, 10H), 5,31-5,24 (м, 1H), 4,89-4,57 (м, 3H), 3,93-3,92 (м, 1H), 3,55 (д, 1H), 3,24 (д, 1H), 2,86-2,82 (м, 1H), 2,33-1,98 (м, 3H), 1,77-1,72 (м, 0,4H), 1,58-1,57 (м, 0,7H).
Пример 60
(2R)-1-бензил-N-(3,4-диоксо-1-фенил-4-(тиофен-2-илметиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с 2-тиофенметиламином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида описанным выше способом.
ESI-МС [M+H]+=490,2.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~2:1: δ [м.д.]: 9,44-9,42 (м, 1H), 8,72-8,69 (м, 1H), 7,44-6,98 (м, 13H), 5,32-5,22 (м, 1H), 4,91-4,75 (м, 1H), 4,54 (c, 2H), 3,94-3,92 (м, 1H), 3,57-3,41 (м, 1H), 3,27-3,21 (м, 1H), 2,85-2,79 (м, 1H), 2,36-2,02 (м, 3H), 1,81-1,69 (м, 0,3H), 1,63-1,49 (м, 0,6H).
Пример 61
(2R)-N-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-(2,6-дихлорбензил)-5-оксопирролидин-2-карбоксамид
61.1 3-((R)-1-(2,6-дихлорбензил)-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановая кислота
Указанное в заголовке соединение получали способом, аналогично получению этил-3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутаноата, описанному в примере 20.1, с последующим гидролизом сложного эфира, обеспечивающим 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановую кислоту, описанную в примере 20.2.
ESI-МС [M+H]+=492,1.
61.2 (2R)-N-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-(2,6-дихлорбензил)-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-(2,6-дихлорбензил)-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с циклопропанамином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида описанным выше способом.
ESI-МС [M+H]+=502,1.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~1:1: δ [м.д.]: 8,85-8,81 (м, 1H), 8,53-8,49 (м, 1H), 7,47-7,23 (м, 8H), 5,38-5,33 (м, 0,5H), 5,23-5,21 (м, 0,5H), 5,00-4,92 (м, 1H), 4,11-4,08 (м, 1H), 3,80-3,75 (м, 1H), 3,22-3,16 (м, 1H), 2,82-2,72 (м, 2H), 2,22-1,92 (м, 3H), 1,81-1,78 (м, 0,5H), 1,47-1,43 (м, 0,5H), 0,73-0,63 (м, 4H).
Пример 62
(2R)-1-(2,6-дихлорбензил)-N-(4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-(2,6-дихлорбензил)-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с этиламином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида описанным выше способом.
ESI-МС [M+H]+=490,1.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~1:1: δ [м.д.]: 8,82-8,79 (м, 1H), 8,54-8,49 (м, 1H), 7,47-7,24 (м, 8H), 5,38 (с, 0,5H), 5,23 (с, 0,5H), 5,01-4,92 (м, 1H), 4,11-4,05 (м, 1H), 3,81-3,76 (м, 1H), 3,22-3,17 (м, 3H), 2,75 (c, 1H), 2,21-1,93 (м, 3H), 1,81-1,79 (м, 0,5H), 1,44-1,43 (м, 0,5H), 1,22-1,09 (м, 3H).
Пример 63
(2R)-1-бензил-N-(3,4-диоксо-1-фенил-4-(пиридин-4-илметиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с 4-(аминометил)пиридином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида описанным выше способом.
ESI-МС [M+H]+=485,2.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~4:1: δ [м.д.]: 9,41-9,40 (м, 1H), 8,75-8,74 (м, 1H), 8,52-8,51 (м, 2H), 7,33-7,04 (м, 12H), 5,28-5,21 (м, 1H), 4,86 (д, 0,2H), 4,76 (д, 0,8H), 4,40 (c, 2H), 3,92-3,90 (м, 1H), 3,55-3,52 (м, 1H), 2,23-3,21 (м, 1H), 2,87-2,82 (м, 1H), 2,31-2,02 (м, 3H), 1,74-1,69 (м, 0,2H), 1,56-1,55 (м, 0,8H).
Пример 64
(2R)-1-бензил-N-(4-(оксазол-2-илметиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с оксазол-2-илметиламином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида описанным выше способом.
ESI-МС [M+H]+=475,2.
Пример 65
(2R)-1-бензил-N-(3,4-диоксо-1-фенил-4-(фениламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с анилином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида описанным выше способом.
ESI-МС [M+H]+=470,2.
1H-ЯМР (500 МГц, ДМСО, смесь диастереомеров ~1:1: δ [м.д.]: 10,70 (c, 1H), 8,83 (д, 1H), 7,84 (c, 2H), 7,40-6,99 (м, 13H), 5,28-5,27 (м, 1H), 4,87 (c, 0,5H), 4,75 (д, 0,5H), 3,92-3,90 (м, 1H), 3,55-3,29 (м, 2H), 2,92-2,87 (м, 1H), 2,33-2,02 (м, 3H), 1,76-1,71 (м, 0,5H), 1,58-1,55 (м, 0,5H).
Пример 66
(2R)-N-(4-(бензо[d][1,3]диоксол-5-илметиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-бензил-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с 3,4-метилендиоксибензиламином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида описанным выше способом.
ESI-МС [M+H]+=528,3.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~1:1: δ [м.д.]: 9,27 (д, 1H), 8,72-8,6 (м, 1H), 7,32-6,78 (м, 13H), 6,00 (2×c, 2H), 5,29-2,18 (м, 1H), 4,85 (д, 0,5H), 4,75 (д, 0,5H), 4,33-4,31 (м, 2H), 3,91-3,89 (м, 1H), 3,56 (д, 0,5H), 3,38-3,35 (м, 0,5H, скрыт под сигналом растворителя), 3,23-3,20 (м, 1H), 2,84-2,79 (м, 1H), 2,29-2,04 (м, 3H), 1,73-1,68 (м, 0,5H), 1,55-1,51 (м, 0,5H).
Пример 67
(2R)-1-бензил-N-(4-(4-фторбензиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с 4-фторбензиламином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида описанным выше способом.
ESI-МС [M+H]+=502,2.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~3:2: δ [м.д.]: 9,36-9,35 (м, 1H), 8,72 (c, 1H), 7,34-7,04 (м, 14H), 5,29-5,22 (м, 1H), 4,86 (д, 0,6H), 4,76 (д, 0,4H), 4,36 (c, 2H), 3,92-3,90 (м, 1H), 3,55-3,52 (м, 1H), 3,24-3,21 (м, 1H), 2,85-2,80 (м, 1H), 2,33-2,05 (м, 3H), 1,74-1,69 (м, 0,4H), 1,55-1,53 (м, 0,6H).
Пример 68
(2R)-1-бензил-N-(3,4-диоксо-1-фенил-4-(4-(трифторметил)бензиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с 4-(трифторметил)бензиламином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида описанным выше способом.
ESI-МС [M+H]+=552,3.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~1:1: δ [м.д.]: 9,44-9,42 (м, 1H), 8,74-8,72 (м, 1H), 7,72-7,71 (м, 2H), 7,53-7,50 (2H), 7,33-7,03 (м, 10H), 5,28-5,18 (м, 1H), 4,86 (д, 0,5H), 4,75 (д, 0,5H), 4,46-4,45 (м, 2H), 3,91-3,89 (м, 1H), 3,54-3,51 (м, 1H), 3,24-3,21 (м, 1H), 2,85-2,81 (м, 1H), 2,29-2,02 (м, 3H), 1,72-1,67 (м, 0,5H), 1,57-1,48 (м, 0,5H).
Пример 69
(2R)-1-бензил-N-(3,4-диоксо-1-фенил-4-(((R)-тетрагидрофуран-2-ил)метиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с (R)-(-)-тетрагидрофурфуриламином с использованием гексафторфосфата 2-(7-аза-1H-бензотриазол-1-ил)-1,1,3,3-тетраметилурония (HATU) и N,N-диизопропилэтиламина (DIPEA) с последующим окислением полученного промежуточного гидроксиамида до соответствующего кетоамида описанным выше способом.
ESI-МС [M+H]+=478,2.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~1:1: δ [м.д.]: 8,77-8,65 (м, 2H), 7,37-7,04 (м, 10H), 5,33-5,23 (м, 1H), 4,86 (д, 0,5H), 4,77 (д, 0,5H), 3,97-3,90 (м, 2H), 3,80-3,75 (м, 1H), 3,66-3,60 (м, 1H), 3,54 (д, 0,5H), 3,36-3,35 (м, 0,5H, скрыт под сигналом растворителя), 3,27-3,18 (м, 3H), 2,82-2,76 (м, 1H), 2,34-2,16 (м, 2H), 2,18-2,04 (м, 1H), 1,92-1,72 (м, 3H), 1,61-1,56 (м, 2H).
Пример 70
(2R)-1-бензил-N-(3,4-диоксо-1-фенил-4-(((S)-тетрагидрофуран-2-ил)метиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с (S)-(+)-тетрагидрофурфуриламином с использованием HATU и DIPEA с последующим окислением полученного промежуточного гидроксиамида до соответствующего кетоамида описанным выше способом.
ESI-МС [M+H]+=478,2.
1H-ЯМР (500 МГц, ДМСО), только один диастереомер: δ [м.д.]: 8,75-8,66 (м, 2H), 7,37-7,15 (м, 10H), 5,26-5,22 (м, 1H), 4,86 (д, 1H), 3,98-3,90 (м, 2H), 3,80-3,76 (м, 1H), 3,66-3,62 (м, 1H), 3,53 (д, 1H), 3,33-3,16 (м, 3H), 2,81-2,76 (м, 1H), 2,27-2,23 (м, 2H), 2,12-2,02 (м, 1H), 1,93-1,78 (м, 3H), 1,61-1,52 (м, 2H).
Пример 71
(2R)-1-бензил-N-(3,4-диоксо-1-фенил-4-(2-(тиофен-3-ил)этиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с гидрохлоридом 2-(тиофен-3-ил)этанамина с использованием HATU и DIPEA с последующим окислением полученного промежуточного гидроксиамида до соответствующего кетоамида описанным выше способом.
ESI-МС [M+H]+=504,2.
1H-ЯМР (500 МГц, ДМСО), только один диастереомер: (абсолютная конфигурация не определена): δ [м.д.]: 8,90 (c, 1H), 8,67 (c, 1H), 7,47-7,04 (м, 13H), 5,27 (м, 1H), 4,89,4,86 (м, 1H), 3,94-3,93 (м, 1H), 3,56-3,42 (м, 3H, скрыт под сигналом растворителя), 3,19-3,17 (м, 1H), 2,86-2,75 (м, 3H), 2,31-2,06 (м, 3H), 1,58-1,57 (м, 1H).
Пример 72
(2R)-1-бензил-N-(4-(фуран-2-илметиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с фуран-2-илметанамином с использованием HATU и DIPEA с последующим окислением полученного промежуточного гидроксиамида до соответствующего кетоамида описанным выше способом.
ESI-МС [M+H]+=474,2.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~3:1: δ [м.д.]: 9,26 (д, 1H), 8,70 (д, 1H), 7,59 (c, 1H), 7,35-7,04 (м, 10H), 6,41 (c, 1H), 6,28 (c, 1H), 5,27-5,21 (м, 1H), 4,86 (д, 0,7H), 4,76 (д, 0,3H), 4,42-4,32 (м, 2H), 3,91-3,89 (м, 1H), 3,53 (д, 1H), 3,23-3,20 (м, 1H), 2,83-2,78 (м, 1H), 2,31-2,01 (м, 3H), 1,74-1,69 (м, 0,3H), 1,55-1,54 (м, 0,7H).
Пример 73
(2R)-1-бензил-N-(4-(2-бензилгидразинил)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид·трифторуксусной кислоты
73.1 (2R)-1-бензил-N-(4-(2-бензилгидразинил)-3-гидрокси-4-оксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с дигидрохлоридом бензилгидразина аналогично стадии 1.1 примера 1 обеспечивает соответствующий гидроксиамид.
ESI-МС [M+H]+=501,3.
73.2 трет-бутил-1-бензил-2-(3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутаноил)гидразинкарбоксилат
К смеси (2R)-1-бензил-N-(4-(2-бензилгидразинил)-3-гидрокси-4-оксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамида (300 мг, 0,599 ммоль) в трет-BuOH (6 мл) добавляли NaOH (1M в воде, 2 мл, 2 ммоль) и ди-трет-бутилдикарбонат (Boс2O) (144 мг, 0,659 ммоль). После перемешивания в течение ночи добавляли воду (20 мл) и экстрагировали смесь EtOAc. Объединенные органические слои промывали насыщенным водным раствором NaHCO3, водой и сушили (MgSO4). Очистка колоночной флэш-хроматографией (градиент 1-10% MeOH в DCM) давала указанное в заголовке соединение (130 мг, 36%).
ESI-МС [M+Na]+=623,3, [M-Boc+H]+=501,2.
73.3 трет-бутил-1-бензил-2-(3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-оксо-4-фенилбутаноил)гидразинкарбоксилат
К раствору трет-бутил-1-бензил-2-(3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутаноил)гидразинкарбоксилата (130 мг, 0,216 ммоль) в ДМСО (3 мл) добавляли IBX (189 мг, 0,303 ммоль, 45% масс.). После перемешивания в течение ночи добавляли насыщенный водный раствор NaHCO3 (15 мл) и воду (15 мл). Смесь экстрагировали EtOAc, объединенные органические слои промывали насыщенным водным раствором NaHCO3, водой и сушили (MgSO4). Очистка колоночной флэш-хроматографией (градиент 1-10% MeOH в DCM) давала указанное в заголовке соединение (110 мг, 85%).
ESI-МС [M+Na]+=621,3, [M-Boc+H]+=499,2.
73.4 (2R)-1-бензил-N-(4-(2-бензилгидразинил)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамид·трифторуксусная кислота
К раствору трет-бутил-1-бензил-2-(3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-оксо-4-фенилбутаноил)гидразинкарбоксилата (110 мг, 0,184 ммоль) в DCM (2 мл) добавляли трифторуксусную кислоту (TFA) (0,2 мл, 2,60 ммоль). После перемешивания в течение 4 часов растворитель удаляли в вакууме и полученный остаток растирали в простом диэтиловом эфире, с получением указанного в заголовке соединения (48 мг, 43%).
ESI-МС [M+H]+=499,2.
Пример 74
(2R)-N-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-(2-метокси-6-(трифторметил)бензил)-5-оксопирролидин-2-карбоксамид
74.1 Этил-3-(трет-бутоксикарбониламино)-2-гидрокси-4-фенилбутаноат
К суспензии 4-этокси-3-гидрокси-4-оксо-1-фенилбутан-2-аминийхлорида (4,7 г, 18,10 ммоль) в ТГФ (50 мл) при 10°C добавляли Et3N (6 мл, 43,00 ммоль). Добавляли раствор ди-трет-бутилдикарбоната (4,2 г, 19,24 ммоль) в ТГФ (30 мл) около 10 минут при 10°C. Реакционной смеси давали нагреться до комнатной температуры и перемешивали в течение ночи. Растворитель удаляли в вакууме, и остаток экстрагировали DCM. Объединенные органические слои промывали насыщенным водным раствором NaCl и сушили над MgSO4. Очистка колоночной флэш-хроматографией (DCM/MeOH) давала указанное в заголовке соединение (4,5 г, 77%).
ESI-МС [M+H]+=224,1.
74.2 Трет-бутил-4-(циклопропиламино)-3-гидрокси-4-оксо-1-фенилбутан-2-илкарбамат
К смеси 3-(трет-бутоксикарбониламино)-2-гидрокси-4-фенилбутановой кислоты (10,6 г, 35,9 ммоль) и циклопропиламина (3,3 мл, 47,6 ммоль) в DCM (300 мл) при 5°Cдобавляли EDC (8,3 г, 43,3 ммоль), HOBT (6,6 г, 43,1 ммоль) и Et3N (7 мл, 50,2 ммоль). Реакционной смеси давали нагреться до комнатной температуры и перемешивали в течение ночи. После охлаждения до 5°C добавляли еще циклопропиламин (2 мл, 28,5 ммоль), EDC (5 г, 26,1 ммоль), HOBT (4 г, 26,1 ммоль) и Et3N (3,5 мл, 25,1 ммоль), смеси давали нагреться до комнатной температуры и продолжали перемешивание в течение ночи. Добавляли DCM (300 мл) с последующим промыванием 0,5M водным раствором HCl, насыщенным раствором соли и сушкой с помощью MgSO4. Неочищенный продукт перекристаллизовывали из простого метил-трет-бутилового эфира, полученные кристаллы промывали н-пентаном и сушили, с получением указанного в заголовке соединения (10,2 г, 85%).
ESI-МС [M-Boc+H]+=231,1.
74.3 Гидрохлорид 3-амино-N-циклопропил-2-гидрокси-4-фенилбутанамида
К раствору трет-бутил-4-(циклопропиламино)-3-гидрокси-4-оксо-1-фенилбутан-2-илкарбамата (7,5 г, 22,43 ммоль) в DCM (130 мл) по каплям добавляли раствор HCl (4M в диоксане, 16 мл, 64,00 ммоль). После перемешивания в течение 5 часов дополнительно добавляли раствор HCl (4M в диоксане, 5 мл, 20,00 ммоль) и продолжали перемешивание в течение ночи. Растворитель выпаривали в вакууме и добавляли простой метил-трет-бутиловый эфир (200 мл). Полученный осадок отфильтровывали, промывали простым метил-трет-бутиловым эфиром и н-пентаном и сушили, с получением указанного в заголовке соединения (5,8 г, 96%).
ESI-МС [M+H]+=236,1.
74.4 (2R)-N-(4-(циклопропиламино)-3-гидрокси-4-оксо-1-фенилбутан-2-ил)-1-(2-метокси-6-(трифторметил)бензил)-5-оксопирролидин-2-карбоксамид
К смеси (R)-1-(2-метокси-6-(трифторметил)бензил)-5-оксопирролидин-2-карбоновой кислоты (234 мг, 0,74 ммоль) и гидрохлорида 3-амино-N-циклопропил-2-гидрокси-4-фенилбутанамида (200 мг, 0,74 ммоль) в DCM (50 мл) добавляли DIPEA (0,8 мл, 4,58 ммоль). После перемешивания в течение 10 минут добавляли HATU (337 мг, 0,89 ммоль) и продолжали перемешивание в течение ночи. Реакционную смесь разбавляли DCM и добавляли воду. Органический слой отделяли и экстрагировали водный слой DCM. Объединенные органические слои промывали насыщенным водным раствором NaHCO3, насыщенным водным раствором NaCl и сушили над MgSO4. При удалении растворителя в вакууме получали указанное в заголовке соединение (498 мг, 95%, степень чистоты около 75%).
ESI-МС [M+H]+=534,3.
74.5 (2R)-N-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-(2-метокси-6-(трифторметил)бензил)-5-оксопирролидин-2-карбоксамид
(2R)-N-(4-(циклопропиламино)-3-гидрокси-4-оксо-1-фенилбутан-2-ил)-1-(2-метокси-6-(трифторметил)бензил)-5-оксопирролидин-2-карбоксамид (498 мг, 95%, степень чистоты около 75%) подвергали окислению до соответствующего кетоамида, как описано на стадии 1.2 примера 1.
ESI-МС [M+H]+=532,2.
1H-ЯМР (500 МГц, ДМСО), смесь диастереомеров ~1:1: δ [м.д.]: 8,87-8,80 (м, 1H), 8,35-8,32 (м, 1H), 7,53-7,48 (м, 1H), 7,35-7,18 (м, 7H), 5,46-5,42 (м, 0,5H), 5,20-5,16 (м, 0,5H), 4,96-4,88 (м, 1H), 4,01-3,96 (м, 1H), 3,72 (c, 3H), 3,22-3,16 (м, 1H), 2,84-2,71 (м, 2H), 2,16-1,81 (м, 4H), 1,42-1,19 (м, 1H), 0,72-0,62 (м, 4H).
Пример 75
(2R)-1-бензил-N-(3,4-диоксо-1-фенил-4-(2-фенилэтиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамид
Связывание 3-((R)-1-бензил-5-оксопирролидин-2-карбоксамидо)-2-гидрокси-4-фенилбутановой кислоты с 2-фенилэтил-1-амином и окисление полученного промежуточного гидроксиамида до соответствующего кетоамида.
Биологическое исследование ингибирования кальпаина и катепсинов
Использовали следующие растворы и буферы:
HBS (на 40 мл): 800 мкл 1M HEPES; 2,16 мл 100 мМ KCl; 4,8 мл 1M NaCl; 3,59 мл 5% раствора глюкозы; 60 мкл 1M MgSO4; 400 мкл 100 мМ пирувата Na, 28,19 мл воды; рН 7,2-7,5;
лизирующий буфер (на 20 мл): 400 мкл 1M Tris рН 8,2; 2,74 мл 1М NaCl; 520 мкл 0,5M EDTA; 2 мл 10% тритона X-100; 0,8 мл (=1:25) CompletePlus (1 таблетка/2 мл H2O); 200 мкл 100 мМ Pefabloc; 13,34 мл воды, рН 8,2;
TBST (10×) (на 11): 100 мМ Tris (12,1 г); 1,5М NaCl (87 г); 1% Tween 20 (10 г); доведенный до рН 8.
I. Ингибирование фермента in vitro
Испытание блокады соответствующих ферментативных активностей осуществляли с помощью кинетических флуоресцентных анализов (возбуждение 390 нм, излучение 460 нм).
Значения кажущихся Ki рассчитывали из экспериментально определенных значений IC50по уравнению Ченга-Пруссова в предположении обратимого конкурентного ингибирования фермента. Значения Km субстратов, используемых в условиях анализа, указанных выше, составляли: 90 мкМ (Z-Phe-Arg-AMC, катепсин B), 10 мкМ (Z-Gly-Pro-Arg-AMC, катепсин K), 2 мкМ (Z-Phe-Arg-AMC, катепсин L) и 30 мкМ (Z-Val-Val-Arg-AMC, катепсин S).
Указанные значения Ki представляют собой усредненные константы ингибирования, рассчитанные на основе 2-4 независимых графиков доза-эффект.
Применяли следующие анализы:
1. Кальпаин I:
20 нМ кальпаин-I - выделен из эритроцитов человека (Calbiochem #208713), 100 мкМ Suc-Leu-Tyr-AMC (Bachem #1-1355) в виде субстрата в буфере с 62 мМ имидазола, 0,3 мМ CaCl2, 0,10% CHAPS, 0,05% BSA, 1 мМ DTT при рН 7,3 и комнатной температуре.
2. Катепсин B:
0,25 нМ катепсин B - выделен из печени человека (Calbiochem #219362), 100 мкМ Z-Phe-Arg-AMC (Bachem #1-1160) в виде субстрата 50 мМ MES, 2 мМ EDTA, 0,05% Brij 35, 2,5 мМ L-цистеина, pH 6,0, комнатная температура.
3. Катепсин K:
3 нМ катепсин K - активирован из рекомбинантного человеческого прокатепсина K, выделенного из E. coli (Calbiochem #342001), 10 мкМ Z-Gly-Pro-Arg-AMC (Biomol #P-142) в виде субстрата в 50 мМ MES, 2 мМ EDTA, 0,05% Brij 35, 2,5 мМ L-цистеина, рН 6,0, комнатная температура.
4. Катепсин L:
1 нМ катепсин L - выделен из печени человека (Calbiochem #219402), 2 мкМ Z-Phe-Arg-AMC (Bachem #1-1160) в виде субстрата в 50 мМ MES, 2 мМ EDTA, 0,05% Brij 35, 2,5 мМ L-цистеина, рН 6,0, комнатная температура.
5. Катепсин S:
0,5 нМ рекомбинантный человеческий катепсин S - выделен из E. coli (Calbiochem #219343), 20 мкМ Z-Val-Val-Arg-AMC (Bachem #1-1540) в виде субстрата в 50 мМ MES, 2 мМ EDTA, 0,05% Brij 35, 2,5 мМ L-цистеина, pH 6,0, комнатная температура.
Результаты определения in vitro указаны в таблице 1. В таблице 1 использованы следующие сокращения:
В колонке "активность кальпаина" +++ обозначает Ki кальпаина (Ki(кальпаин)) <50 нМ; ++ означает 50 нМ ≤Ki(кальпаин) <100 нМ; и + означает 100 нМ ≤Ki(кальпаин)<600 нМ.
Колонка "Сел. кат. B" показывает отношение Ki(катепсин B)/Ki(кальпаин). В связи с этим +++ означает, что отношение Ki(катепсин B)/Ki(кальпаин) >30; ++ означает 10 Колонка "Сел. кат. K" показывает отношение Ki(катепсин K)/Ki(кальпаин). В связи с этим +++ означает, что отношение Ki(катепсин K)/Ki(кальпаин)>30; ++ означает 10 Колонка "Сел. кат. L" показывает отношение Ki(катепсин L)/Ki(кальпаин). В связи с этим +++ означает, что отношение Ki(катепсин L)/Ki(кальпаин)>30; ++ означает 10 Колонка "Сел. кат.S" показывает отношение Ki(катепсин S)/Ki(кальпаин). В связи с этим +++ означает, что отношение Ki(катепсин S)/Ki(кальпаин)>100; ++ означает 30
II. Анализ спектрина в клетках molt-4 для определения ингибирования клеточного кальпаина Схема и методика анализа описаны в публикации Chatterjee; BMC 1998, 6, pp. 509-522; значения EC50 рассчитывали из процента деградации спектрина в зависимости от дозы. Условия культивирования клеток: клетки molt-4 поддерживали в среде RPMI 1640+GlutamaxTM I (Gibco) с 10% FCS и 50 мкг/мл гентамицина при 37°C, 5% CO2 и рассевали 1:15 дважды в неделю. Препарат клеток molt-4: клетки отмывали, считали и при концентрации 2×107 клеток/мл помещали в буфер HBS. Разведение веществ-ингибиторов: все ингибиторы растворяли при концентрации 10-2М в ДМСО. Затем сток-раствор разводили 1:15 в ДМСО (=6,67×10-4М). Затем разведенный (1:15) сток-раствор разводили в ДМСО в соотношении 1:4 в две стадии (=1,67×10-4М и 4,17×10-5М). Затем полученные три раствора дополнительно разводили 1:50 в буфере HBS, с получением растворов с концентрацией 1,33×10-5М, 3,36×10-6М и 8,34×10-7М. Испытуемая смесь: 106 клеток каждой смеси (см. выше) вводили в 1,5 миллилитровую эппендорфовскую пробирку. В каждом случае к ним добавляли по 150 мкл разведенных веществ (конечные концентрации: 10-5М; 2,5×100-6М и 6,25×10-7М) и тщательно перемешивали. В качестве контрольных образцов использовали отрицательный контроль и положительный контроль. В этом случае первоначально на клетки пипеткой наносили только по 150 мкл буфера HBS. Все смеси инкубировали при 37°C, 5% CO2 в инкубаторе в течение 10 мин. Затем, за исключением отрицательного контроля, в каждом случае добавляли CaCl2 (конечная концентрация 5 мМ) и иономицин (конечная концентрация 5 мкМ), тщательно перемешивали и инкубировали при 37°C, 5% CO2 в инкубаторе в течение 30 минут. Затем центрифугировали при 700 g в течение 5 минут. Супернатанты сливали и клеточные осадки помещали в 20 мкл лизирующего буфера. Затем смеси на 30-60 минут помещали на лед и центрифугировали при 15000 g в течение 15 минут. Супернатанты удаляли и помещали в новые эппендорфовские пробирки. Затем в них проводили определение белка, например, путем анализа MicroBC A (Pierce). ДСН-ПААГ-электрофорез: 10 мкг суммарного белка из каждой смеси помещали в новую эппендорфовскую пробирку, и после добавления с помощью пипетки в тот же объем 2× стандартного буфера для электрофоретических образцов Tris-глицин-SDS (Invitrogen) и 1/10 объема 1М DTT тщательно перемешивали и нагревали при 95°C в течение 15 минут. Растворы в течение короткого времени центрифугировали и наносили на 6% ДСН-гель (Invitrogen). Гель-электрофорез проводили при 100V с 1× Tris-глициновым буфером Лэммли (Biomol) до тех пор, пока нижняя полоса маркера не достигала основания геля. Вестерн-блоттинг: гель удаляли из аппарата и подвергали блоттингу на нитроцеллюлозу в 1× Tris-глициновом буфере для переноса (Invitrogen)+20% метанола при 1,5 А/см2 в камере FastBlot (Biometra) в течение 30 минут. Нитроцеллюлозный фильтр удаляли, быстро промывали в TBST-буфере и блокировали в смеси TBST/5% молочный порошок в течение 1 часа при КТ (комнатной температуре). Затем блокированную нитроцеллюлозу инкубировали с анти-спектрином Ab (Chemicon) (1:10000 в смеси TBST/5% молочный порошок) при комнатной температуре в течение 3 часов или при 4°C в течение ночи. Нитроцеллюлозу промывали 3× в TBST-буфере. Затем инкубировали с антимышиным IgG-антителом (POD) (Sigma) (1:10000 в смеси TBST/5% молочный порошок) при комнатной температуре в течение 1 часа. Затем нитроцеллюлозу промывали 5× в TBST-буфере. На следующей стадии 5 мл полученного раствора субстрата для хемилюминесценции SuperSignal® West Pico (Pierce) помещали на фильтр и инкубировали в течение 5 минут. Затем нитроцеллюлозу забирали из раствора, осторожно промокали насухо и вставляли в кассету с пленкой (Tropix) для проявления. Для записи данных и количественного определения ECL (QuantityOne) использовали систему анализа цифрового изображения (VersaDoc, Biorad) и из полученных данных рассчитывали процент деградации спектрина. Для нанесения данных по проценту деградации спектрина как функции от дозы на сигмоидальный график доза-эффект использовали программу Graph-pad prism (в качестве верхней точки устанавливается 100% и нижней - 0%), и рассчитывали EC 50%. III. Анализ для определения клиренса соединений формулы I из цитозоля В результате сравнения данные, измеренные на цитозоле печени человека, отличались от данных, полученных на цитозоле печени яванских макак. 0,5 мкМ тестируемого соединения инкубировали с 1 мг/мл цитозоля печени человека, а также с цитозолем печени макаки, при 37°C в 0,5M фосфатном буфере при pH 7,5 при перемешивании (коммерческие источники: цитозоль печени самки яванской макаки от компании Tebu bio, цитозоль печени человека от компании BDgentest). В каждом случае брали аликвоты по 65 мкл спустя 0, 5, 10 и 15 минут и переносили в лунки луночного планшета, которые немедленно заполняли 130 мкл этанола, чтобы остановить реакцию. До проведения анализа в системе ЖХ/МС/МС (использовали биосистемы SCIEX 4000) образцы хранили в замороженном состоянии. Считываемые параметры представляли собой потерю исходных соединений, из которой рассчитывали время полужизни (T1/2). Исходя из этих данных, рассчитывали следующие параметры: клиренс из цитозоля (cytCL), нормированный (пересчитанный) клиренс (CLs) и прогнозируемый клиренс (CLp) с применением следующих уравнений: 1) cytCL=(ln 2/T1/2)×[цитозольный белок]×1000 2) CLs=cytCL×[цитозольный выход]/1000000×60 3) CLp=(CLs+печеночный поток плазмы)/печеночный поток плазмы/CLs. Чтобы оценить стабильность испытуемых соединений, диапазоны клиренса корректировали в соответствии с печеночным потоком плазмы для разных видов согласно следующей схеме: Стабильные = от 0 до приблизительно 1/3 печеночного потока плазмы; умеренно стабильные = приблизительно от 1/3 до приблизительно 2/3 печеночного потока плазмы; нестабильные = более 2/3 печеночного потока плазмы. На основании такой коррекции для оценки стабильности испытуемых соединений в цитозоле были определены следующие ограничительные интервалы:




Данные cytCL, полученные таким путем, для соединений настоящего изобретения приведены выше в таблице 1.
Реферат
Изобретение относится к новым карбоксамидным соединениям формулы, приведенной ниже, их таутомерам и фармацевтически приемлемым солям, где значения R, R, R, R, R, Q, Y, A и X приведены в пункте 1 формулы. Соединения являются ингибиторами клеточного кальпаина (кальций-зависимых цистеинпротеаз), что позволяет использовать их для лечения ряда расстройств, связанных с повышенной активностью кальпаина. 2 н. и 31 з.п. ф-лы, 2 табл., 75 пр., 7 ил.
Формула

где

R1 представляет собой фенил, фенил-С1-С6алкил, C1-С10алкил или С3-С7циклоалкил-С1-С4алкил, где группа СН2 в циклоалкильном фрагменте последний указанный радикал может быть замещен NH, где циклоалкильный фрагмент может дополнительно содержать 1 радикал Rlb, где
Rlb представляет собой COORbl, где Rbl представляет собой фенил-С1-Сбалкил,
R2 представляет собой арил или 6-членный гетарил, содержащий 1 атом азота, где арил и гетарил может быть незамещенным или может нести 1 или 2 одинаковых или различных радикала R2b; где
R2b выбирают из галоген, CN, С1-С6алкил, С1-С6алкокси, C1-С6алкокси-С1-С6алкил, где алкильные фрагменты в последних трех заместителях частично или полностью являются галоген-замещенными и/или содержат 1 заместитель Rla, где Rla представляет собой NRa6Ra7, где Ra6 и Ra7 вместе с атомом N образуют 6-членный азотный гетероцикл, который необязательно содержит дополнительно О, в качестве дополнительного гетероатома;
R3a и R3b вместе с атомом углерода, к которому они присоединены, представляют собой С=O; или
R4 означает атом водорода;
А представляет собой С=O или S(=O)2;
Q представляет собой одинарную связь или фрагмент Alk′-Z, где Ζ связан с R2 представляет собой одинарную связь;
Аlk′ представляет собой линейный С1-С3алкандиил, где 1, 2 или 3 атома водорода могут быть заменены С1-С4алкилом;
X представляет собой С(=O) -NRx2Rx3, С(=O)-Ν(Rx4)-(С1-С6алкилен)-NRx2Rx3 или С(=O)-Ν(Rx4)NRx2Rx3, где
Rx2 представляет собой Η, С1-С6алкил, С1-С6алкокси-С1-С6алкил, С3-С7циклоалкил, С3-С7циклоалкил-С1-С4алкил, С3-С7гетероциклоалкил-С1-С4алкил, где 1 или 2 кольцевых атома представляют собой N, S или О, помимо атомов углерода, в качестве атомов кольца, O-С1-С6алкил,
фенил, фенил-С1-С4алкил, СО-фенил, СО-(фенил-С1-С4алкил), где фенил в последних четырех указанных радикалах является незамещенным или содержат 1 или 2 заместителя, выбранных из галогена, C1-С6-алкила, С1-С6-галогеналкила, C1-С6-алкокси и C1-C6-галогеналкокси или два заместителя вместе с фенильным кольцом образуют бензо[b]-1,3-диоксольный радикал, 5- или 6-членный гетарил, содержащий 1 или 2 атома азота или 1 гетероатом, выбранный из О и S, и необязательно 1 атом азота, в качестве кольцевых атомов, 5- или 6-членный гетарил-С1-С4-алкил, где гетарил содержит 1 или 2 атома азота или 1 гетероатом, выбранный из О и S, и необязательно 1 атом азота, в качестве кольцевых атомов, или представляет собой бензо[d]тиазол, и
Rx3 представляет собой Н, С1-С6алкил, С1-С6алкокси-С1-С6алкил, С3-С7циклоалкил, С3-С7циклоалкил-C1-С4алкил, С3-С7гетероциклоалкил-C1-С4алкил, где 1 или 2 атома кольца представляют собой N, S или О, помимо атомов углерода, в качестве атомов кольца, O-С1-С6-алкил, фенил, фенил-С1-С4алкил, СО-фенил, СО-(фенил-С1-С4алкил), где фенил в последних четырех указанных радикалах является незамещенным или содержат 1 или 2 заместителя, выбранных из галогена, C1-С6-алкила, C1-С6-галогеналкила, C1-С6-алкокси и С1-С6-галогеналкокси или два заместителя вместе с фенильным кольцом образуют бензо[b]-1,3-диоксольный радикал, 5- или 6-членный гетарил, содержащий 1 или 2 атома азота или 1 гетероатом, выбранный из О и S, и необязательно 1 атом азота, в качестве кольцевых атомов, 5- или 6-членный гетарил-С1-С4-алкил, где гетарил содержит 1 или 2 атома азота или 1 гетероатом, выбранный из О и S, и необязательно 1 атом азота, в качестве кольцевых атомов, или представляет собой бензо[d]тиазол,
или два радикала Rx2 и Rx3 образуют вместе с атомом N 6-членный азотный гетероцикл, который необязательно может содержать О, дополнительно в качестве гетероатома;
Rx4 представляет собой Η или С1-С6алкил;
Υ представляет собой СН2-СН2, СН2-СН2-СН2, N (Ry#)-СН2 или N (Ry#)-СН2-СН2, где в четырех вышеуказанных фрагментах 1 атом водорода может быть заменен радикалом Ry;
Ry представляет собой С1-С6алкил
Ry# независимо один от другого выбран из атома водорода, или С1-С6алкила;
и его таутомеры и их фармацевтически приемлемые соли.
Rx2 представляет собой Н, С1-С6алкил, С3-С7циклоалкил, С3-С7циклоалкил-С1-С4алкил, С3-С7гетероциклоалкил-С1-С4алкил, фенил, C1-С6алкокси-С1-С4алкил, гетарил, фенил-С1-С4алкил или гетарил-С1-С4алкил, где фенил и фенильное кольцо в фенил-С3-С4алкиле является незамещенным или содержит 1 или 2 заместителя, выбранных из галогена, С1-С6-алкила, С1-С6-галогеналкила, С1-С6-алкокси и C1-C6-галогеналкокси или два заместителя, вместе с фенильным кольцом, образуют бензо[b]-1,3-диоксольный радикал, и
Rx3 представляет собой Н, С1-С6алкил, или
NRx2Rx3 представляет собой азотный гетероцикл следующей формулы:

гетарил, фенил-С1-С4алкил или гетарил-С1-С4алкил, где фенил и фенильное кольцо в фенил-Сх-С4алкиле является незамещенным или содержит 1 или 2 заместителя, выбранных из галогена, C1-C6-алкила, С1-С6-галогеналкила, C1-С6-алкокси и С1-С6-галогеналкокси или два заместителя, вместе с фенильным кольцом, образуют бензо[b]-1,3-диоксольный радикал.


где X, Y, R1, R2b, R3a, R3b и R4 имеют указанные выше значения, и где r равно 0, 1 или 2, его таутомеры и его фармацевтически приемлемые соли.

где X, Q, R1, R2, R3a, R3b и Ry имеют указанные выше значения, n равно 0 или 1, q равно 2 или 3, и звездочкой (*) отмечен центр хиральности, его таутомеры и его фармацевтически приемлемые соли.

где X, Q, R1, R2, R3a, R3b, Ry и Ry# имеют указанные выше значения, n равно 0 или 1, s равно 1 или 2, и звездочкой (*) отмечен центр хиральности, его таутомеры и его фармацевтически приемлемые соли.
С3-С10алкила и
фенил-С1-С4алкила.
N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-бензил-5-оксопирролидин-2-карбоксамида,
N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(3-хлорбензил)-5-оксопирролидин-2-карбоксамида,
N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(4-фторбензил)-5-оксопирролидин-2-карбоксамида,
N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(3-метоксибензил)-5-оксопирролидин-2-карбоксамида,
N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(3-трифторметилбензил)-5-оксопирролидин-2-карбоксамида,
N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(3-фторбензил)-5-оксопирролидин-2-карбоксамида,
N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-[2-(трифторметокси)бензил]пирролидин-2-карбоксамида,
Ν-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(нафталин-1-илметил)-5-оксопирролидин-2-карбоксамида,
Ν-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(нафталин-2-илметил)-5-оксопирролидин-2 -карбоксамида,
Ν-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-[3-(трифторметокси)бензил]пирролидин-2-карбоксамида,
Ν-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-бензил-6-оксопиперидин-2-карбоксамида,
N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-фенилпирролидин-2-карбоксамида,
Ν-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(3-цианобензил)-5-оксопирролидин-2-карбоксамида,
N-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-[2-(трифторметил)бензил]пирролидин-2-карбоксамида,
Ν-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-бензил-4-метил-5-оксопирролидин-2-карбоксамида,
1-бензил-N-{3,4-диоксо-1-фенил-4-[(пиридин-2-илметил)амино]бутан-2-ил}-5-оксопирролидин-2-карбоксамида,
1-бензил-N-[4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил]-5-оксопирролидин-2-карбоксамида,
Ν-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(3,5-диметоксибензил)-5-оксопирролидин-2-карбоксамида,
Ν-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(пиридин-4-илметил)пирролидин-2-карбоксамида,
Ν-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-1-(3,5-дифторбензил)-5-оксопирролидин-2-карбоксамида,
1-бензил-N-(4-(метиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамида,
1-бензил-N-(3,4-диоксо-1-фенил-4-(пропиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамида,
1-бензил-N-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамида,
1-бензил-N-(4-(изобутиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамида,
1-бензил-N-(4-(циклобутиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамида,
1-бензил-N-(4-(метоксиамино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамида,
1-бензил-N-(3,4-диоксо-1-фенил-4-(2-(пиридин-2-ил)этиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамида,
1-бензил-N-(3,4-диоксо-1-фенил-4-(3-(пиридин-2-ил)пропиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамида,
1-бензил-N-(3,4-диоксо-1-фенил-4-(3-фенилпропиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамида,
1-бензил-N-(4-(этил(метил)амино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамида,
1-бензил-N-(4-(2-хлорбензиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамида,
N-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамида,
N-(4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамида,
N-(4-(бензиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамида,
Ν-(4-(изопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамида,
Ν-(3,4-диоксо-1-фенил-4-(2-(пиридин-2-ил)этиламино)бутан-2-ил)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамида,
Ν-(3,4-диоксо-1-фенил-4-(3-(пиридин-2-ил)пропиламино)бутан-2-ил)-5-оксо-1-(2-(трифторметил)бензил)пирролидин-2-карбоксамида,
Ν-(4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-(2-метокси-6-(трифторметил)бензил)-5-оксопирролидин-2-карбоксамида,
Ν-(3,4-диоксо-1-фенил-4-(пиридин-2-илметиламино)бутан-2-ил)-1-(2-метокси-6-(трифторметил)бензил)-5-оксопирролидин-2-карбоксамида,
Ν-(4-(бензиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-(2-метокси-6-(трифторметил)бензил)-5-оксопирролидин-2-карбоксамида,
Ν-(3,4-диоксо-1-фенил-4-(2-(пиридин-2-ил)этиламино)бутан-2-ил)-5-оксо-1-(2-(трифторметокси)бензил)пирролидин-2-карбоксамида,
1-(2-хлорбензил)-Ν-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамида,
1-(2-хлорбензил)-Ν-(4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамида,
Ν-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-(2,6-дифторбензил)-5-оксопирролидин-2 -карбоксамида,
1-(2,6-дифторбензил)-Ν-(4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамида,
Ν-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-[2-метокси-6-(трифторметил)бензил]пирролидин-2-карбоксамида,
Ν-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(2,6-дифторбензил)пирролидин-2-карбоксамида,
1-бензил-N-(3,4-диоксо-1-фенил-4-(2-фенилэтиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамида,
Ν-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-3-бензил-1-метил-2-оксоимидазолидин-4-карбоксамида,
1,1-диоксида Ν-(4-амино-3,4-диоксо-1-фенилбутан-2-ил)-2-бензилизотиазолидин-3-карбоксамида и
их таутомеров и их фармацевтически приемлемых солей.
1-бензил-N-(3,4-диоксо-1-фенил-4-(тиазол-5-илметиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамида,
Ν-(4-(бензо[d]тиазол-2-илметиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-бензил-5-оксопирролидин-2-карбоксамида,
1-бензил-N-(4-морфолино-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамида,
N-(4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(4-(трифторметил)бензил)пирролидин-2-карбоксамида,
1-бензил-N-(4-(циклогексиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамида,
N-(4-(2-бензоилгидразинил)-3,4-диоксо-1-фенилбутан-2-ил)-1-бензил-5-оксопирролидин-2-карбоксамида,
N-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксо-1-(4-(трифторметил)бензил)пирролидин-2-карбоксамида,
1-бензил-N-(3,4-диоксо-1-фенил-4-(тиазол-2-илметиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамида,
1-бензил-N-(3,4-диоксо-1-фенил-4-(тиофен-2-илметиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамида,
Ν-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-(2,6-дихлорбензил)-5-оксопирролидин-2-карбоксамида,
1-(2,б-дихлорбензил)-Ν-(4-(этиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамида,
1-бензил-N-(3,4-диоксо-1-фенил-4-(пиридин-4-илметиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамида,
1-бензил-N-(4-(оксазол-2-илметиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамида,
1-бензил-N-(3,4-диоксо-1-фенил-4-(фениламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамида,
N-(4-(бензо[d][1,3]диоксол-5-илметиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-бензил-5-оксопирролидин-2-карбоксамида,
1-бензил-N-(4-(4-фторбензиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2 -карбоксамида,
1-бензил-N-(3,4-диоксо-1-фенил-4-(4-(трифторметил)бензиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамида,
1-бензил-N-(3,4-диоксо-1-фенил-4-(((R)-тетрагидрофуран-2-ил)метиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамида,
1-бензил-N-(3,4-диоксо-1-фенил-4-(((S)-тетрагидрофуран-2-ил)метиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамида,
1-бензил-N-(3,4-диоксо-1-фенил-4-(2-(тиофен-3-ил)этиламино)бутан-2-ил)-5-оксопирролидин-2-карбоксамида,
1-бензил-N-(4-(фуран-2-илметиламино)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамида,
1-бензил-N-(4-(2-бензилгидразинил)-3,4-диоксо-1-фенилбутан-2-ил)-5-оксопирролидин-2-карбоксамида,
Ν-(4-(циклопропиламино)-3,4-диоксо-1-фенилбутан-2-ил)-1-(2-метокси-6-(трифторметил)бензил)-5-оксопирролидин-2-карбоксамида
и их таутомеров и их фармацевтически приемлемых солей.

Комментарии