Би-арил-мета-пиримидиновые ингибиторы киназы - RU2448959C2
Код документа: RU2448959C2
Описание
Текст описания приведен в факсимильном виде.






































































































Реферат
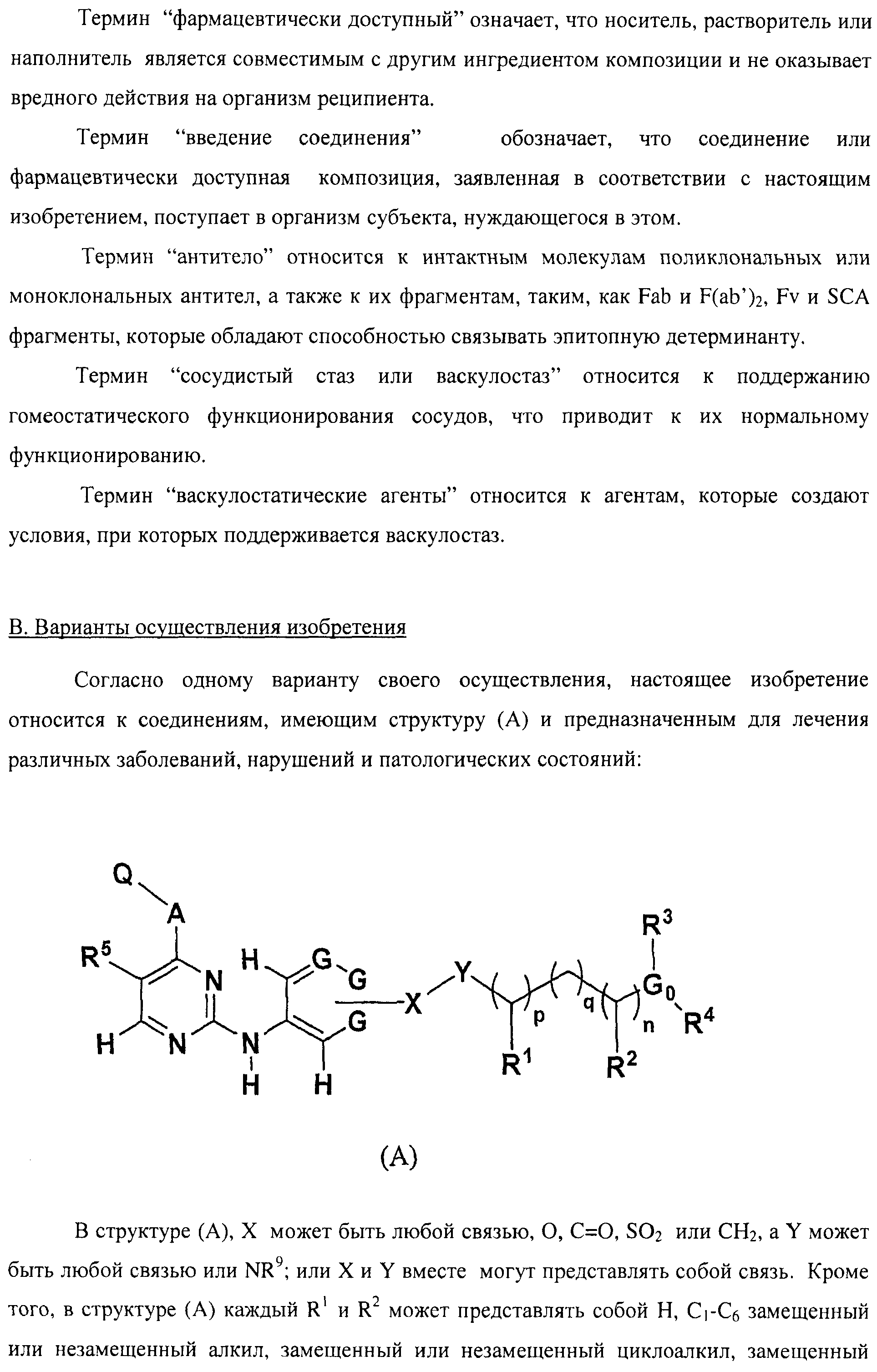
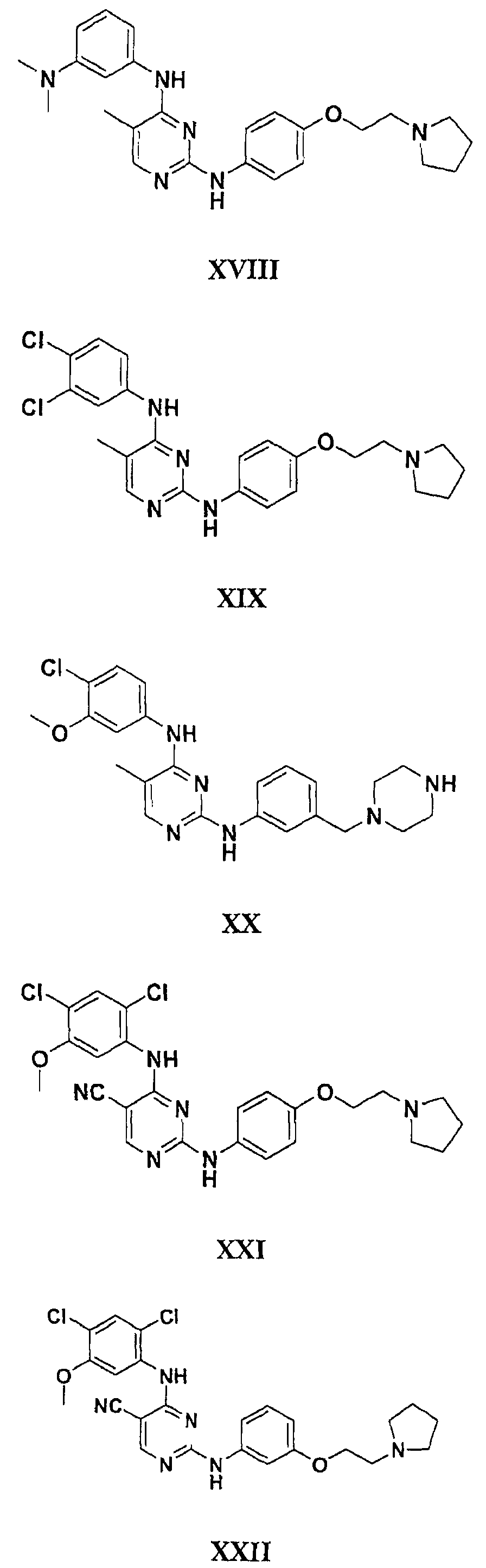
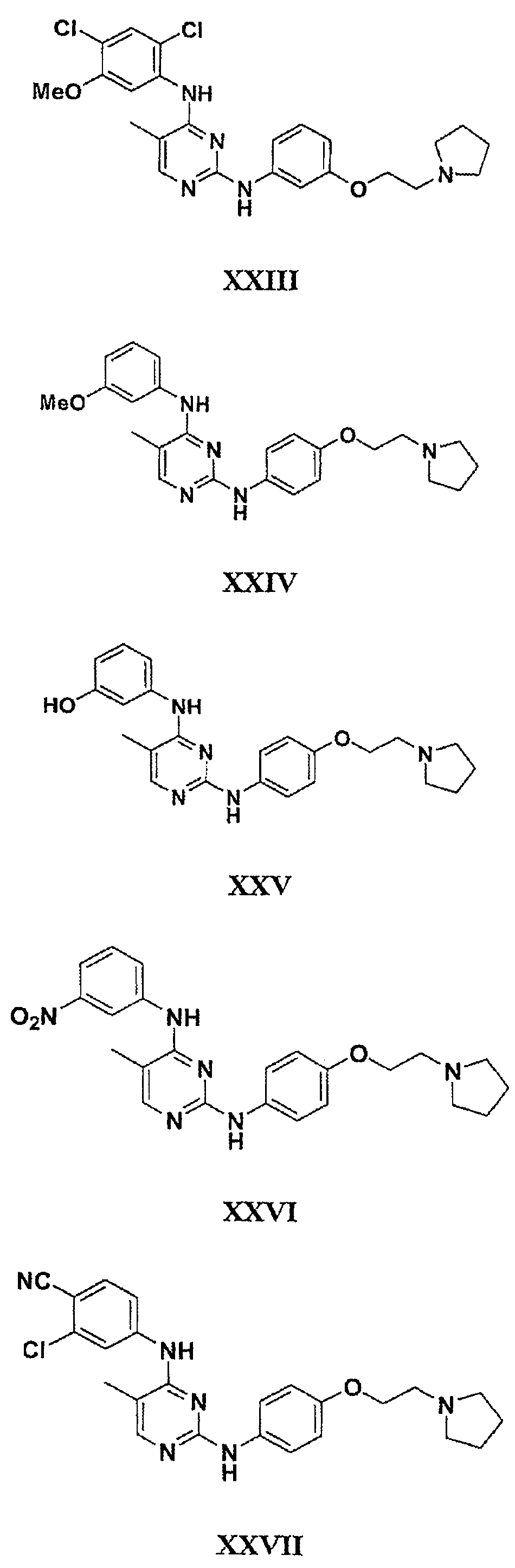
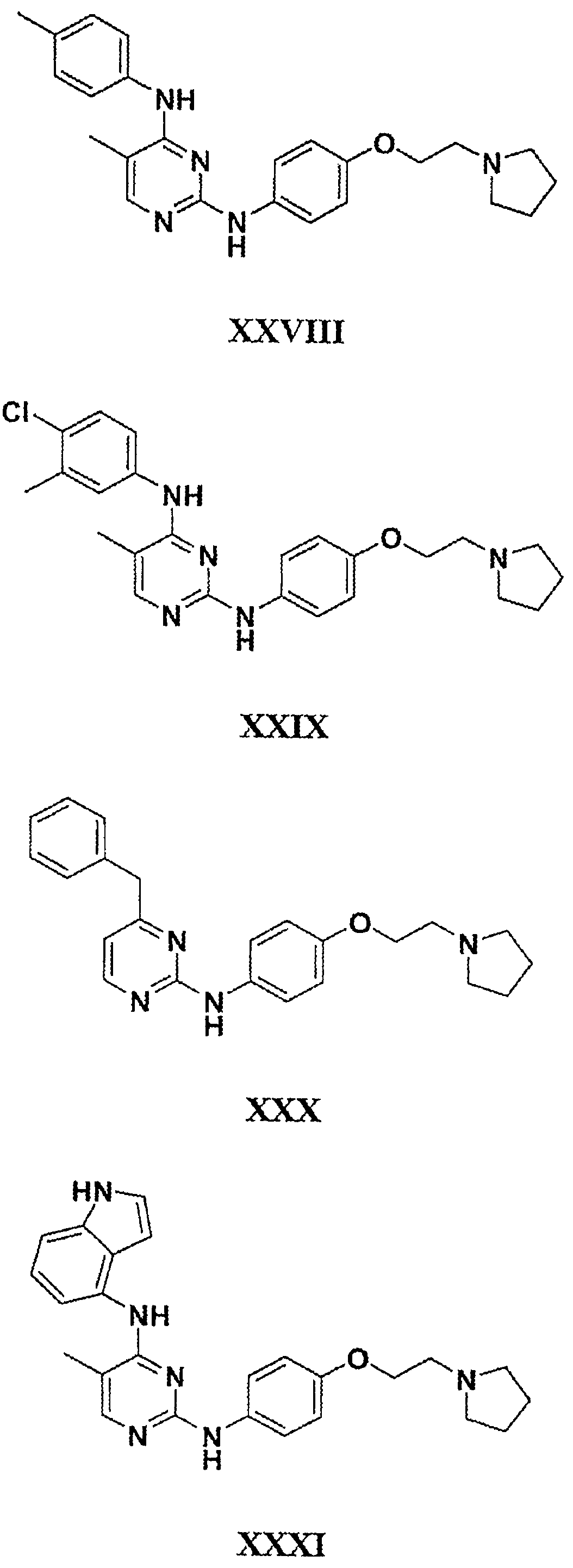
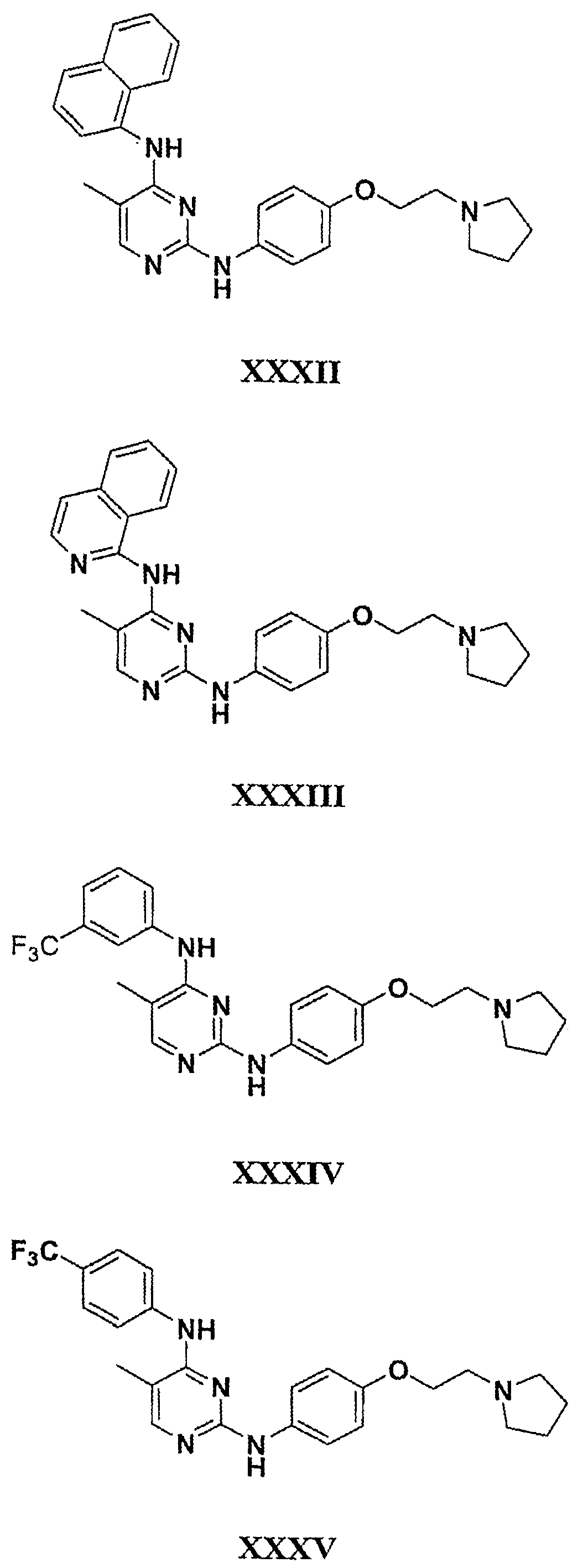
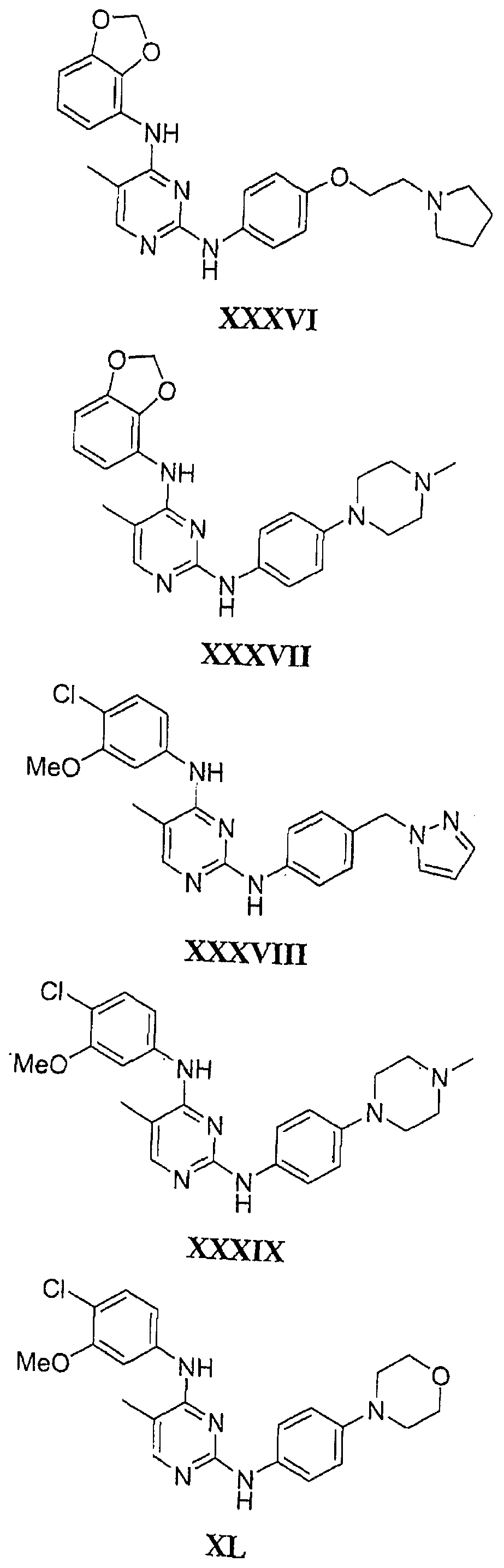
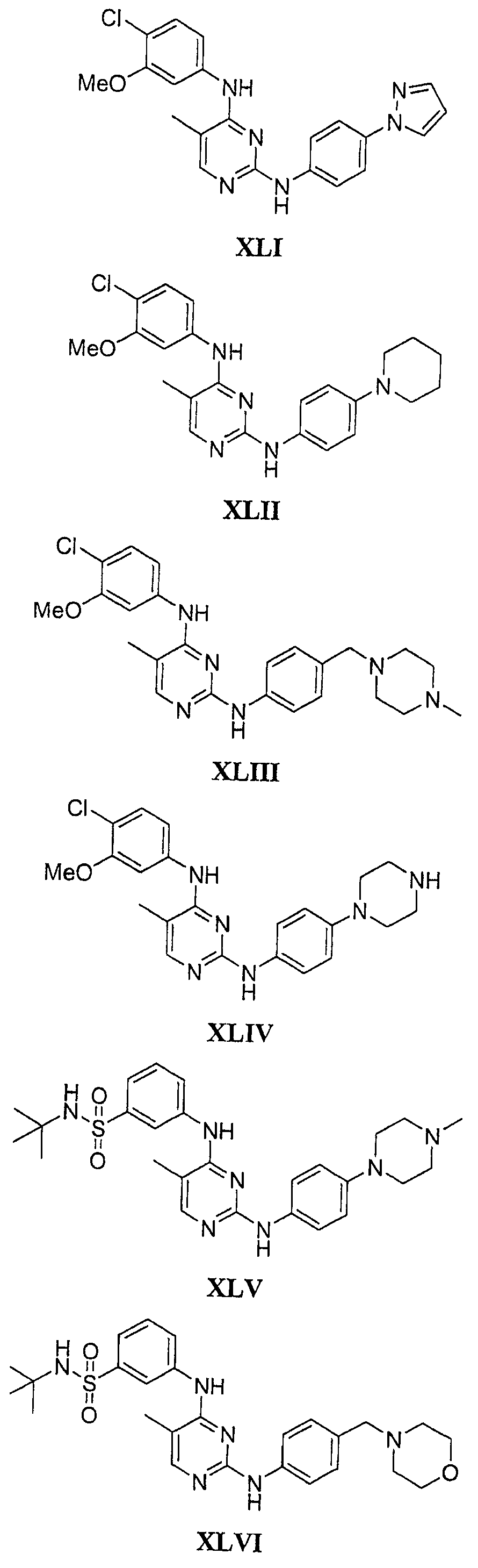
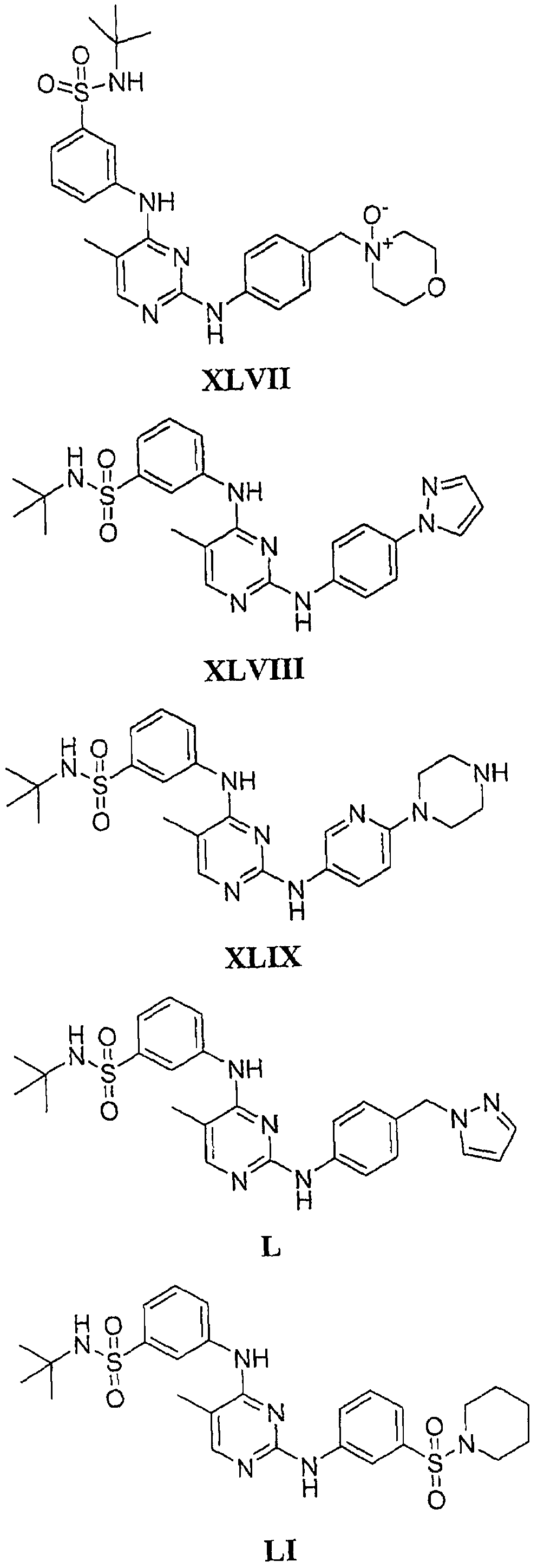
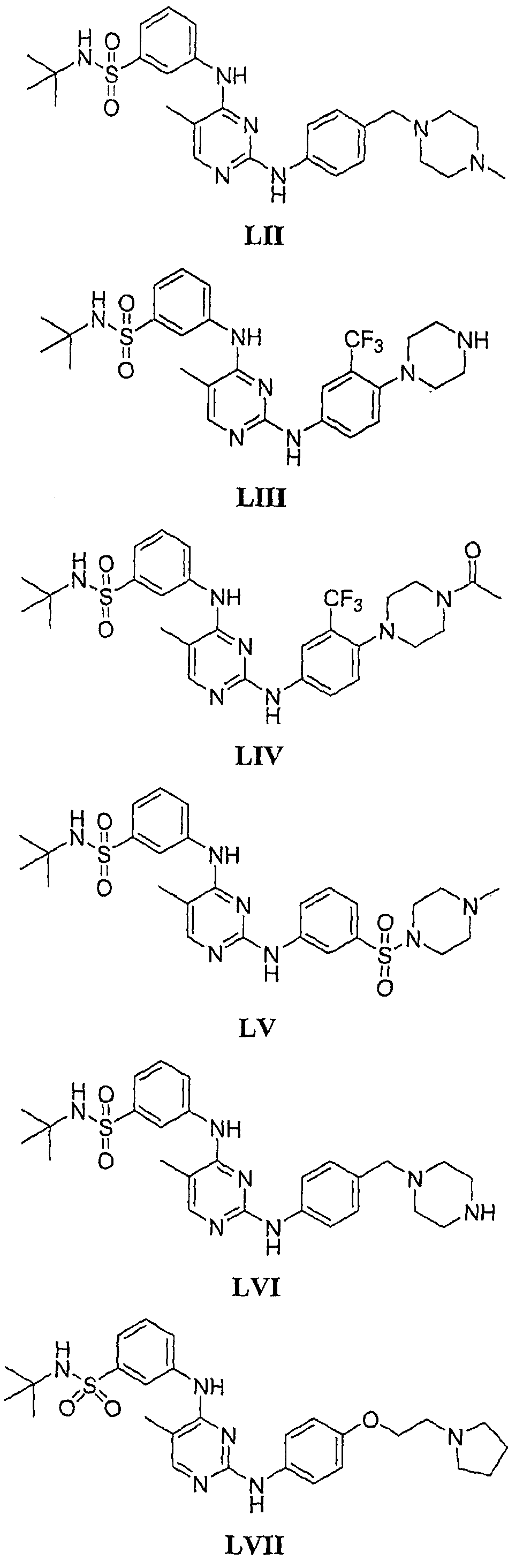
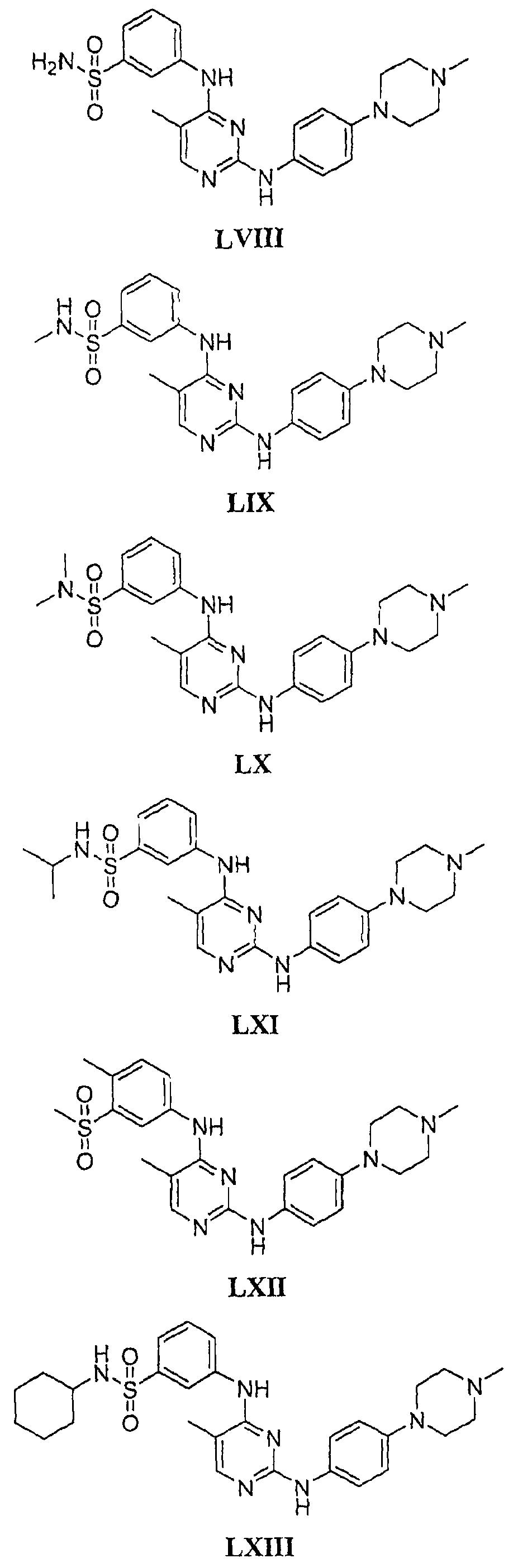
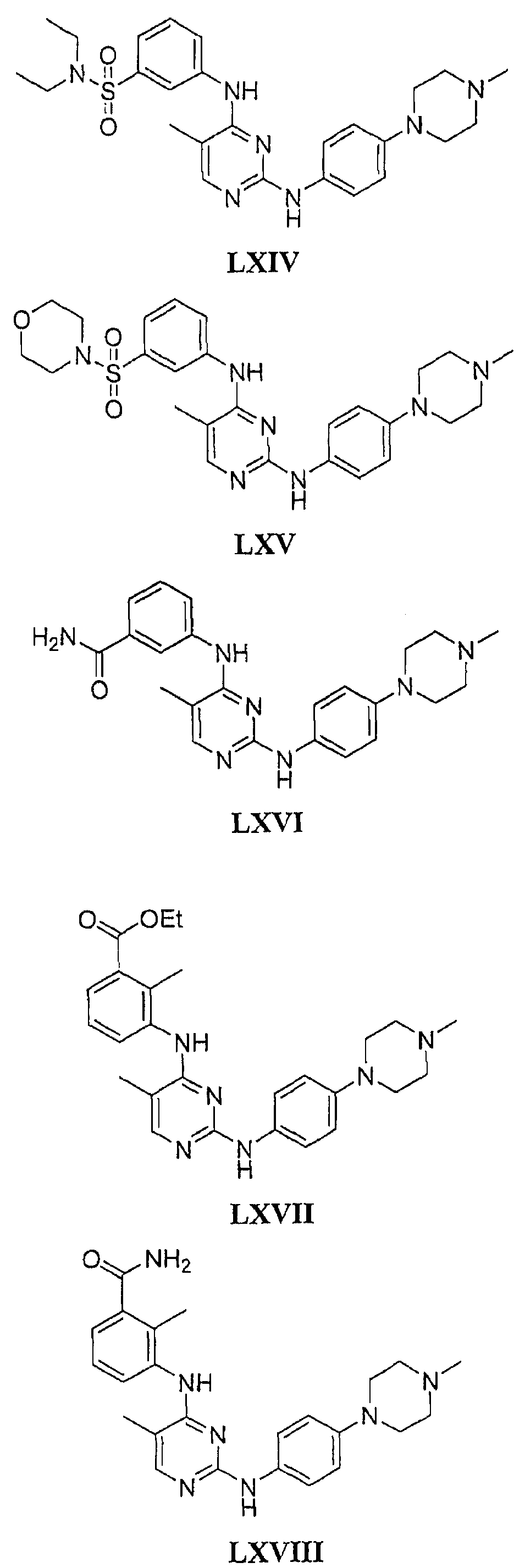
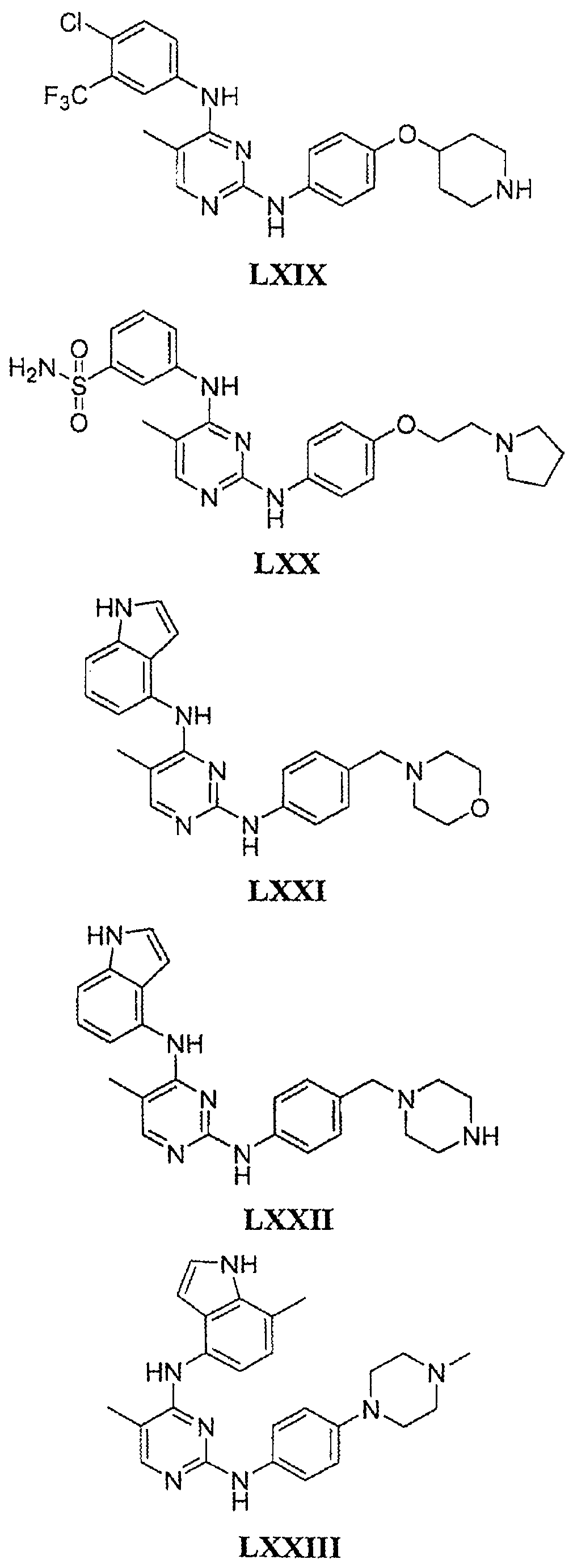
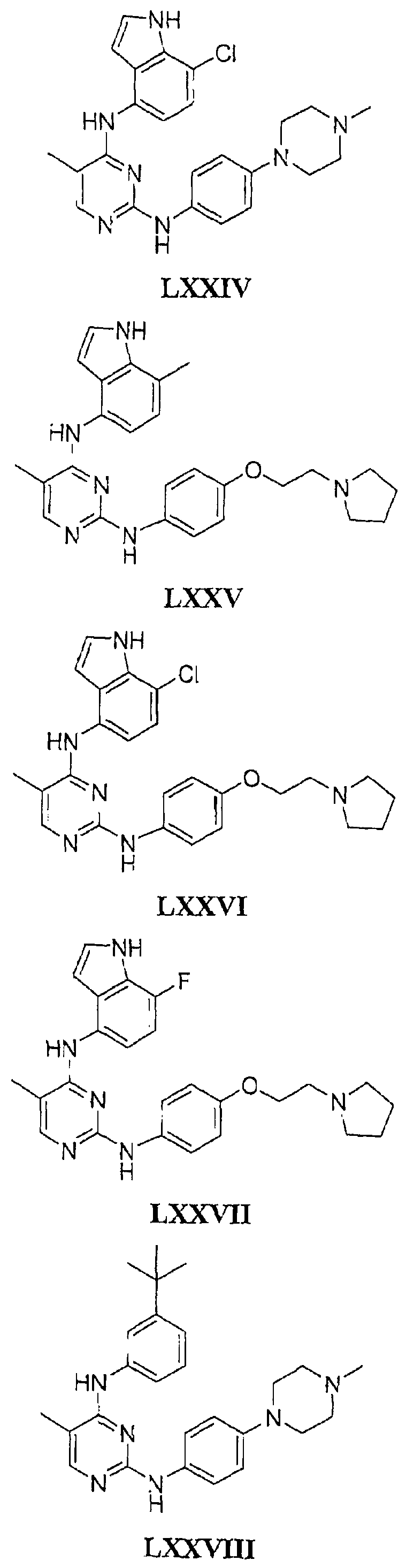
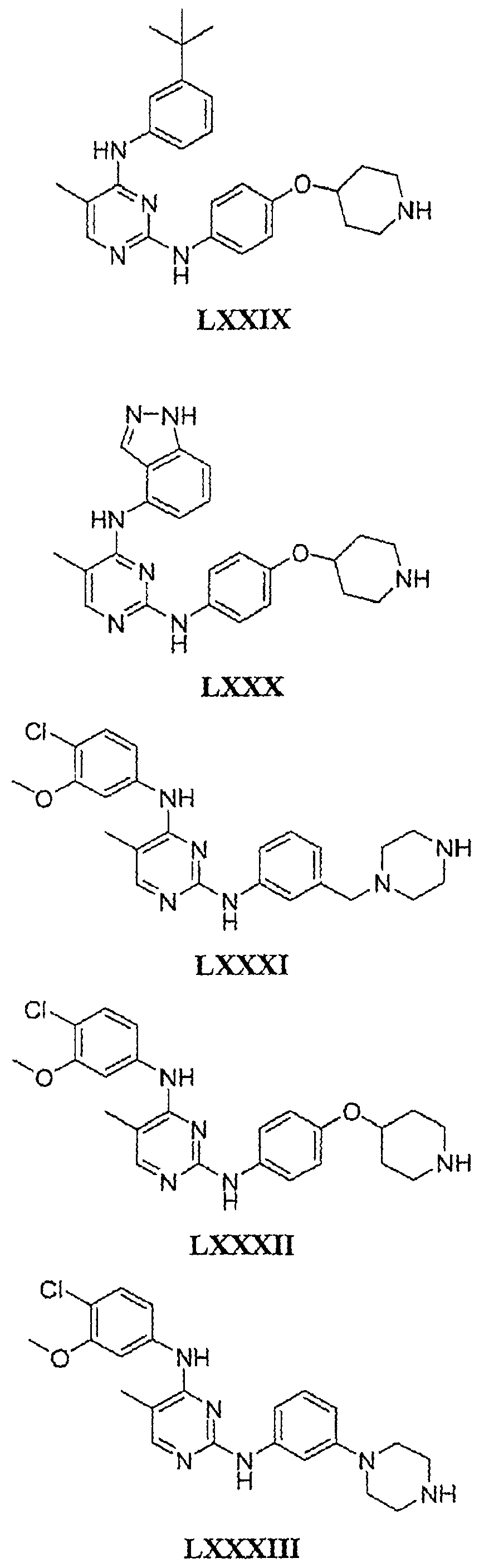
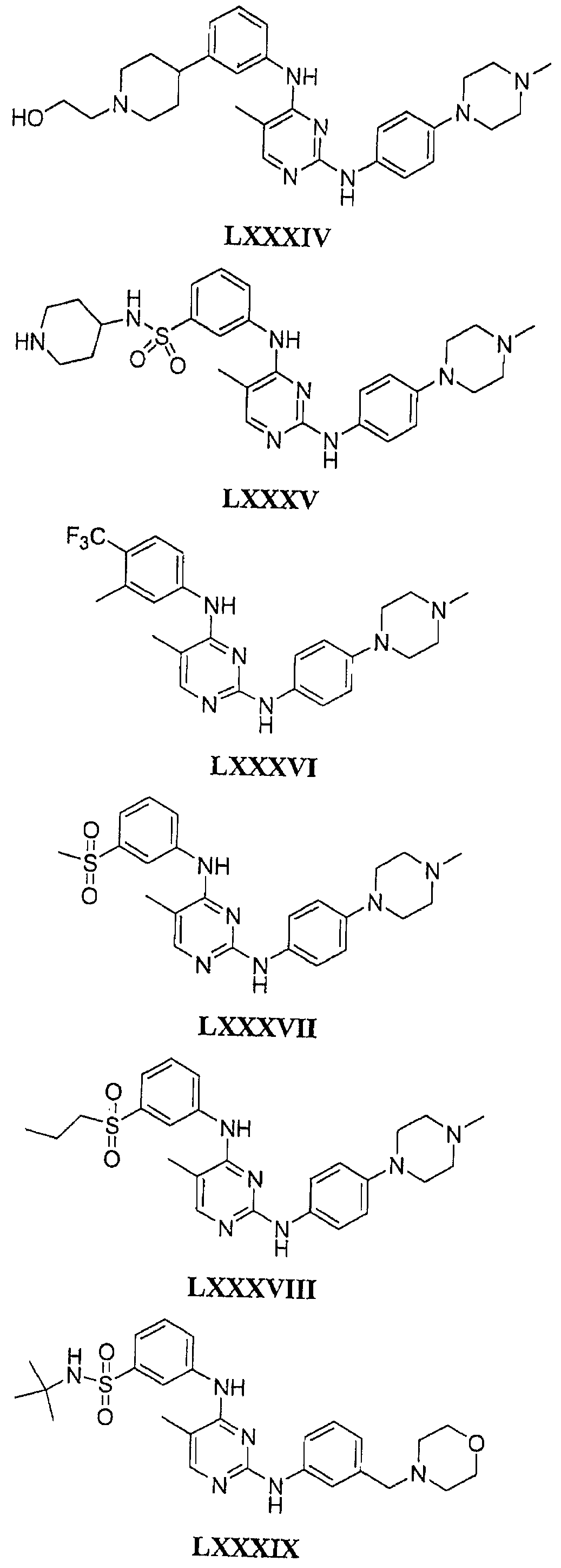
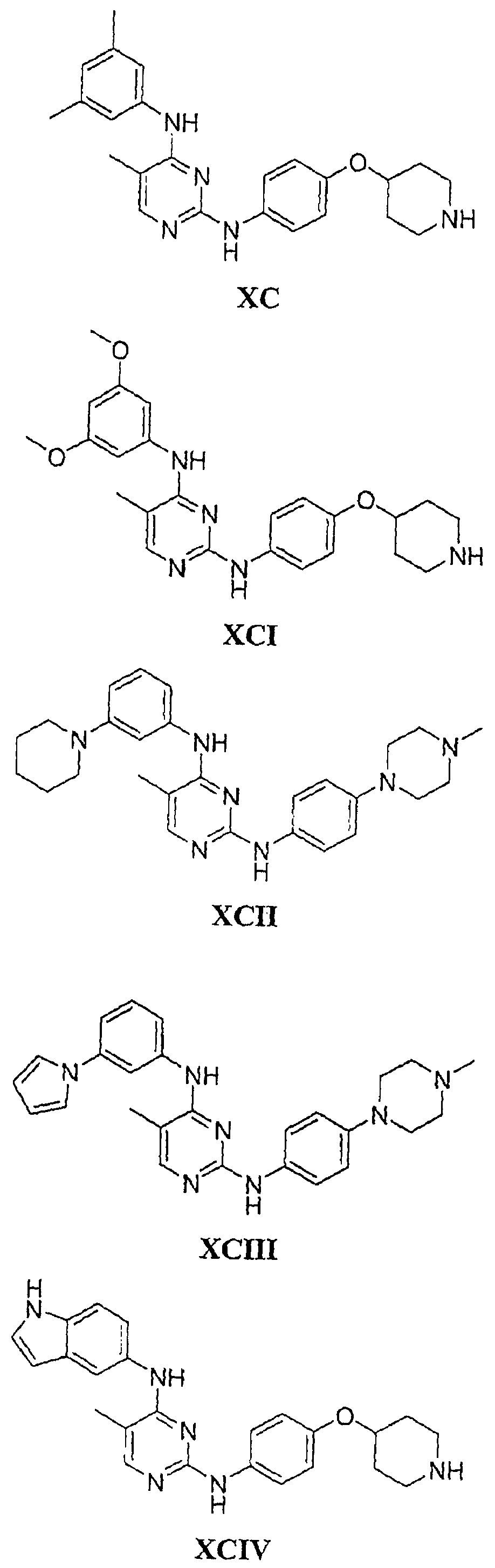
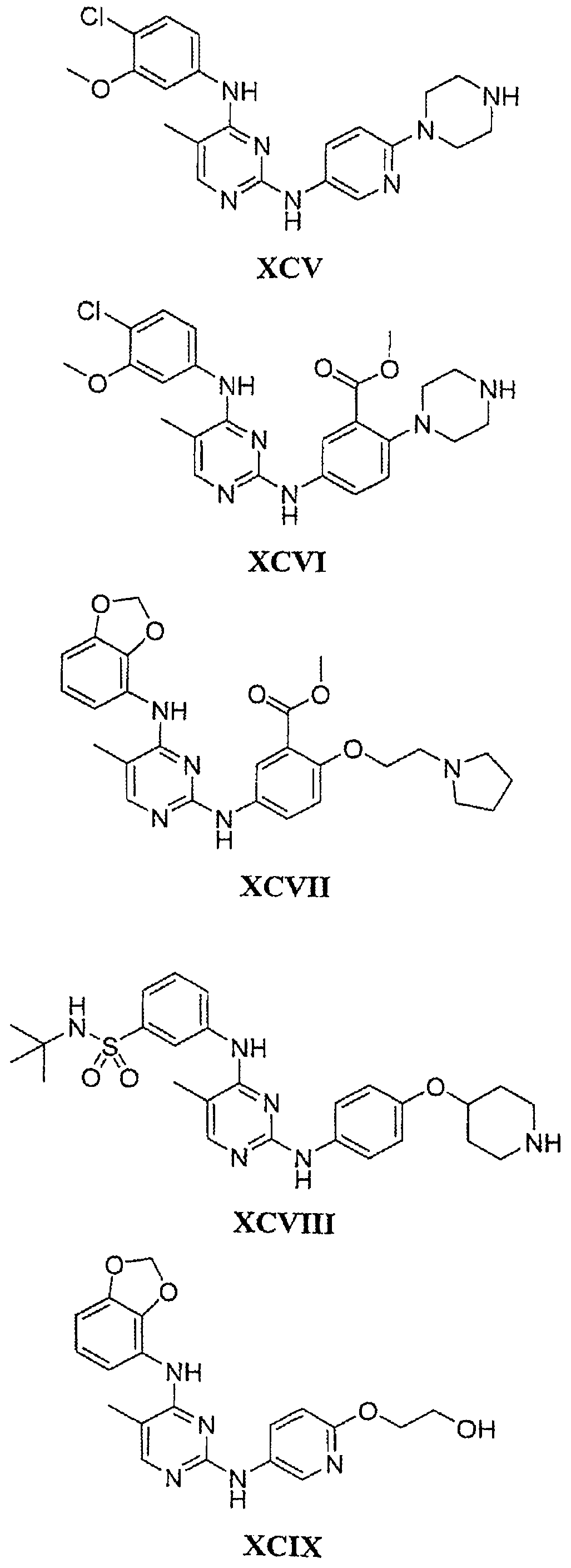
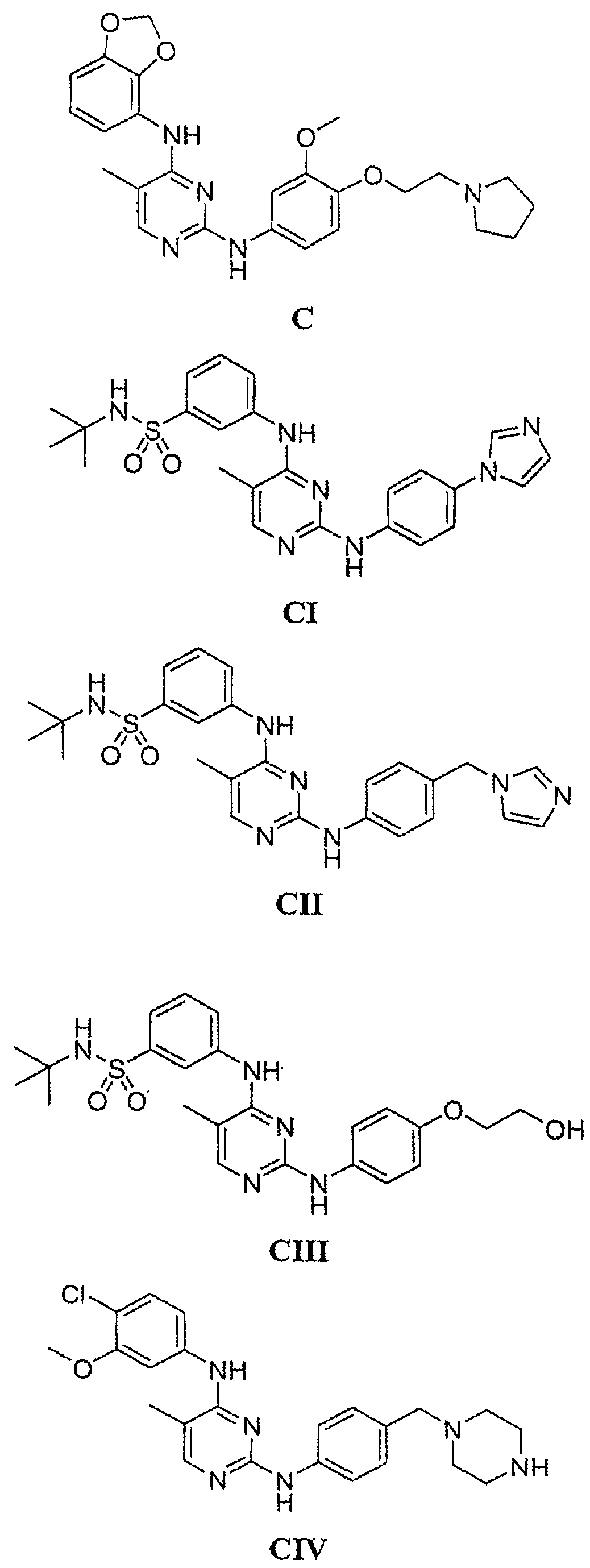
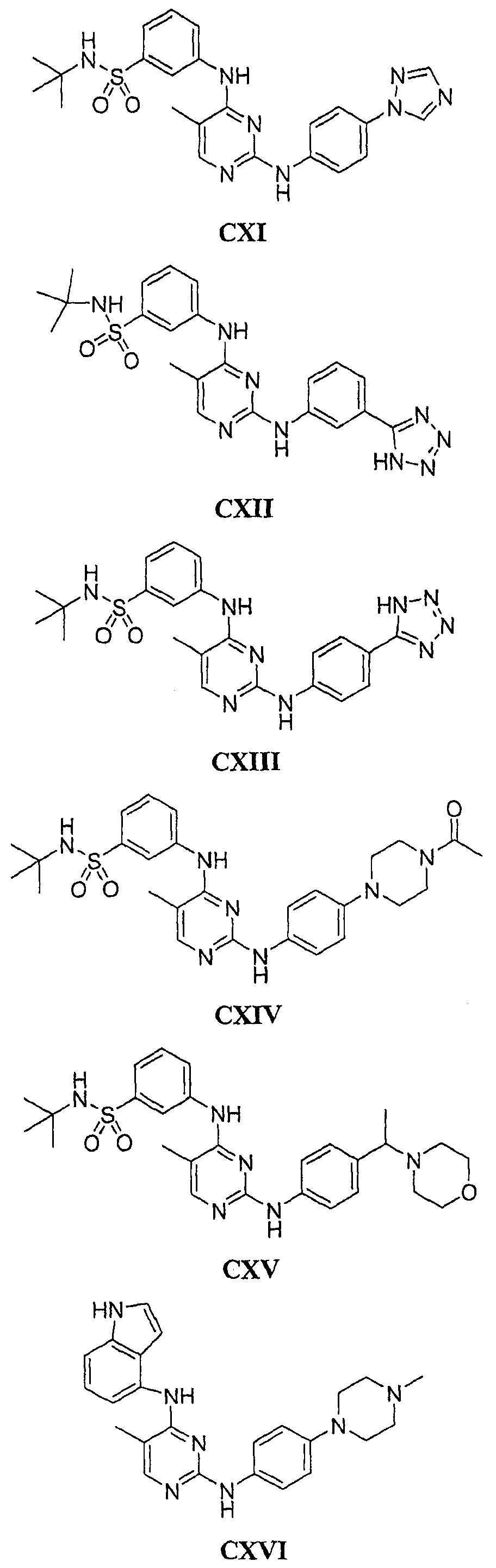
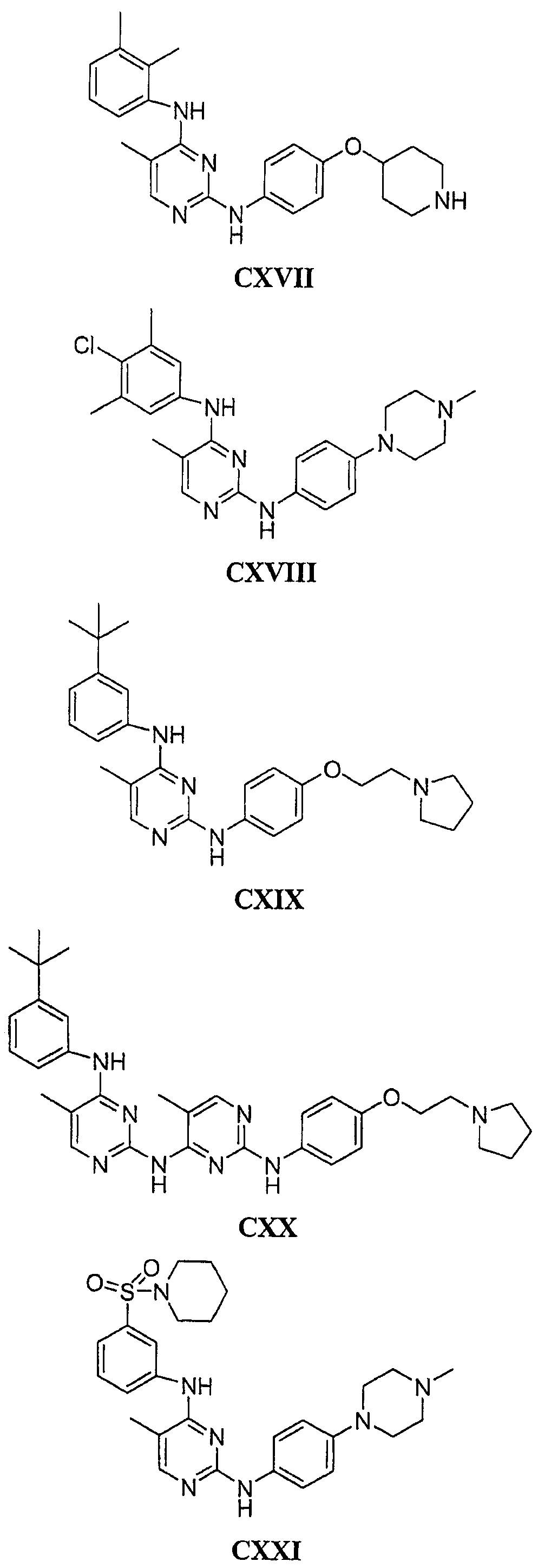
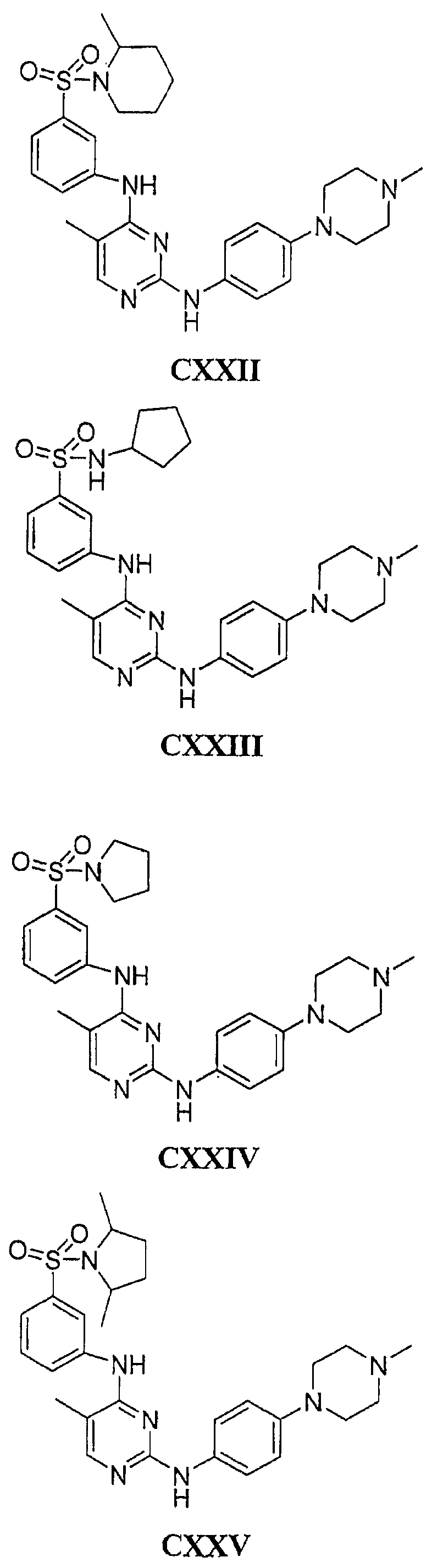
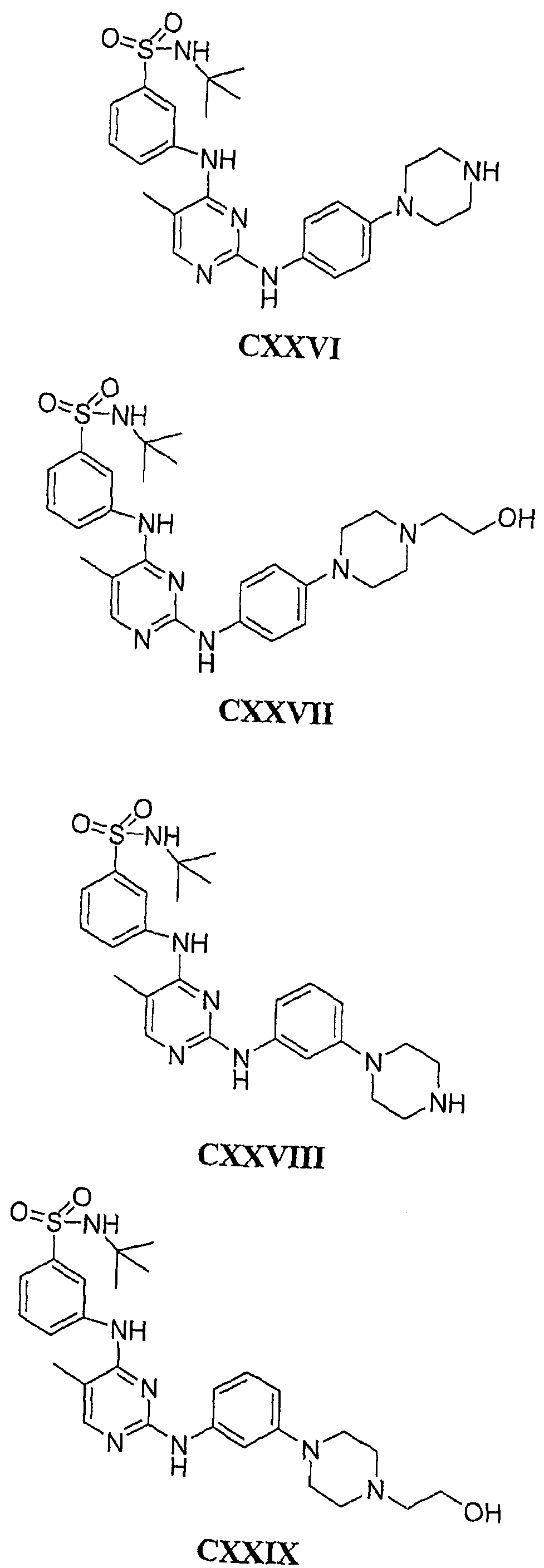
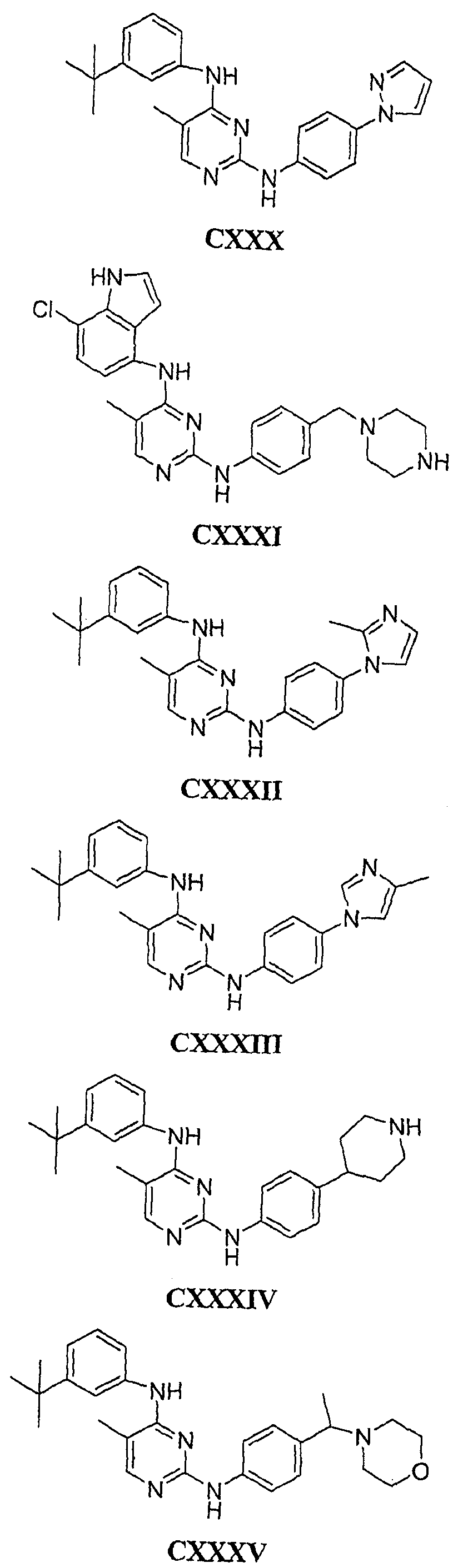
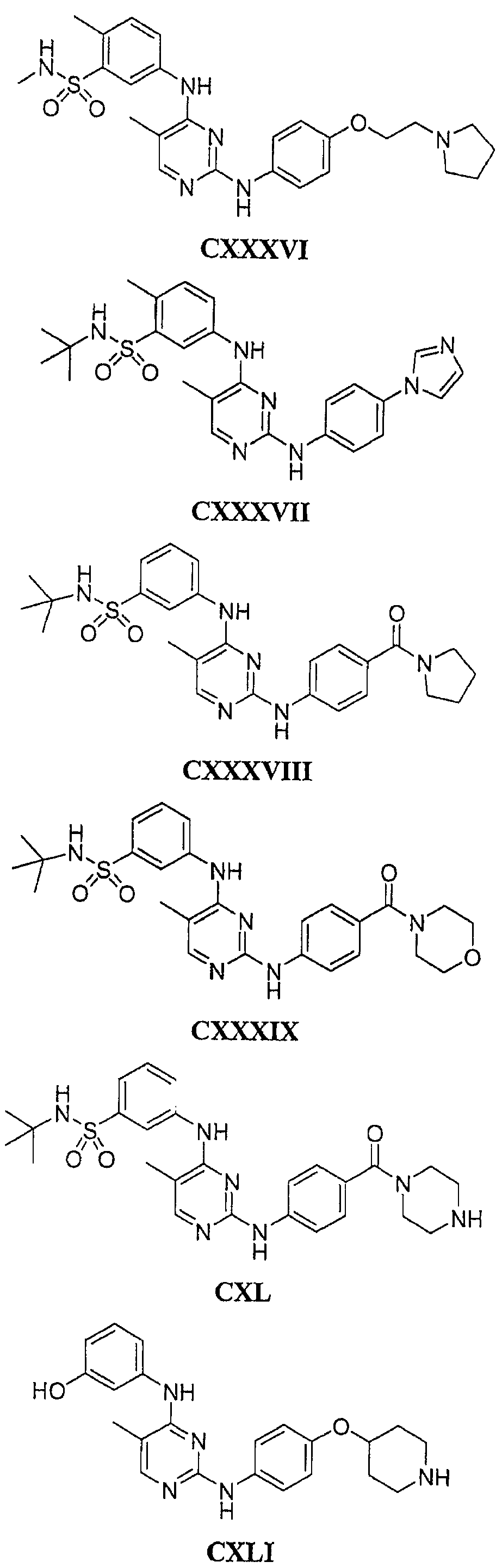
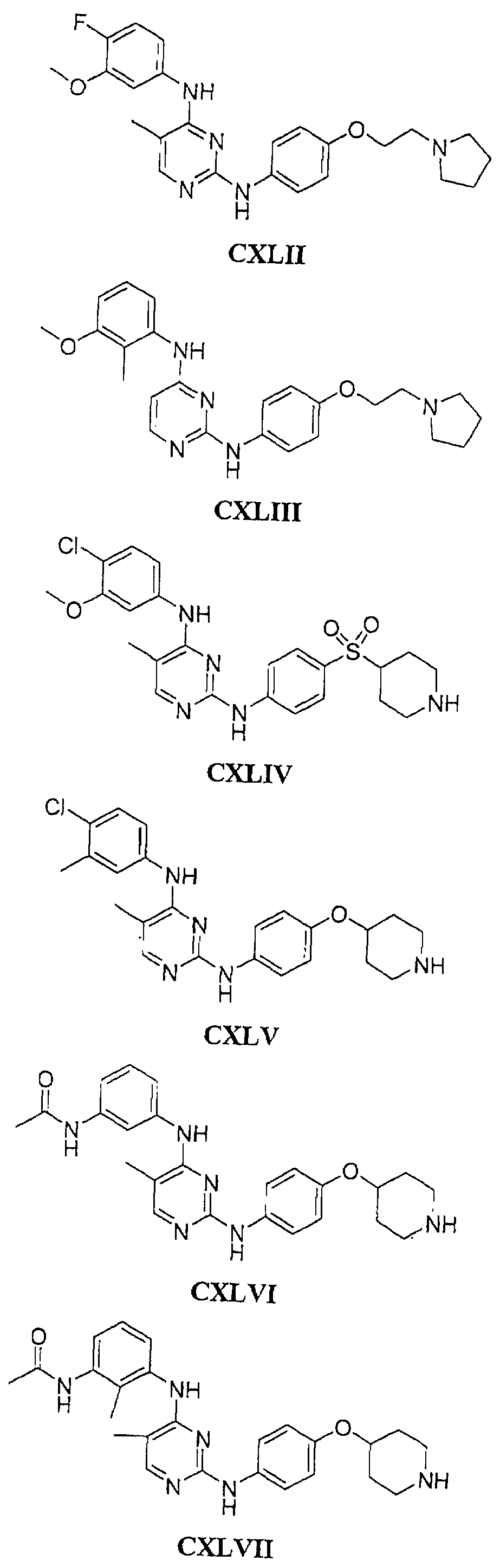
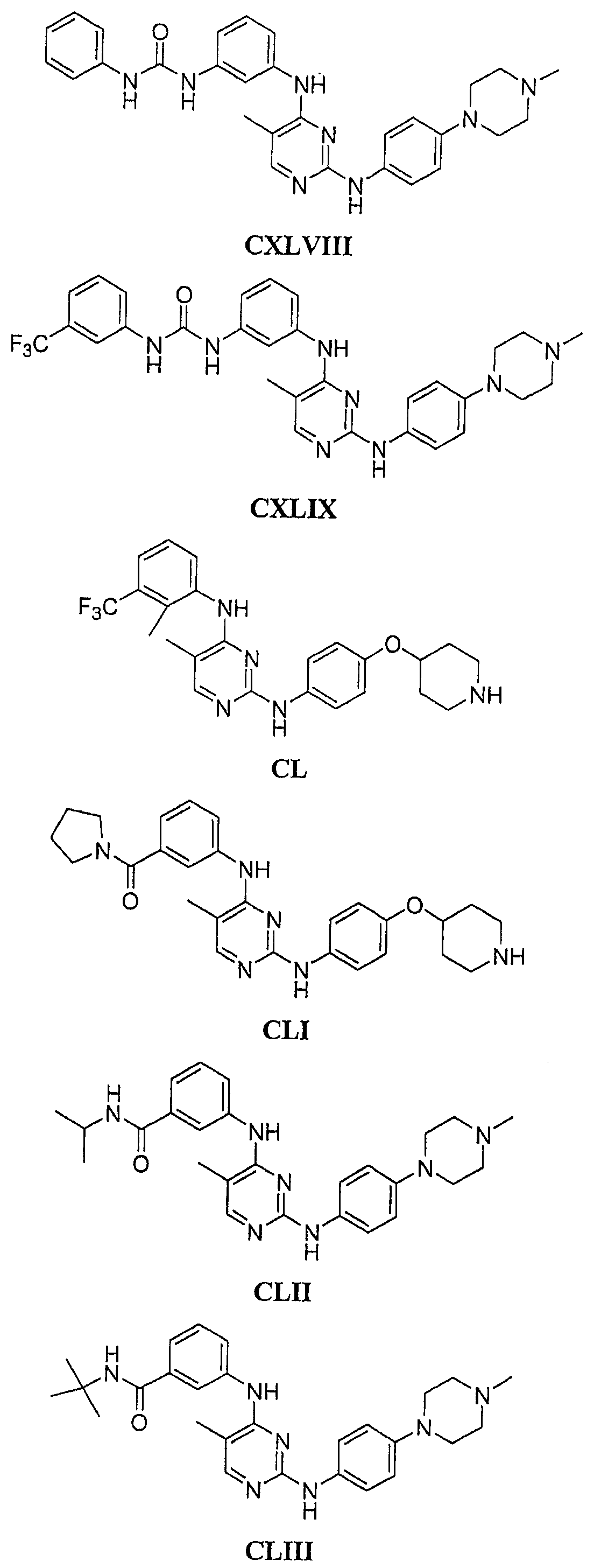
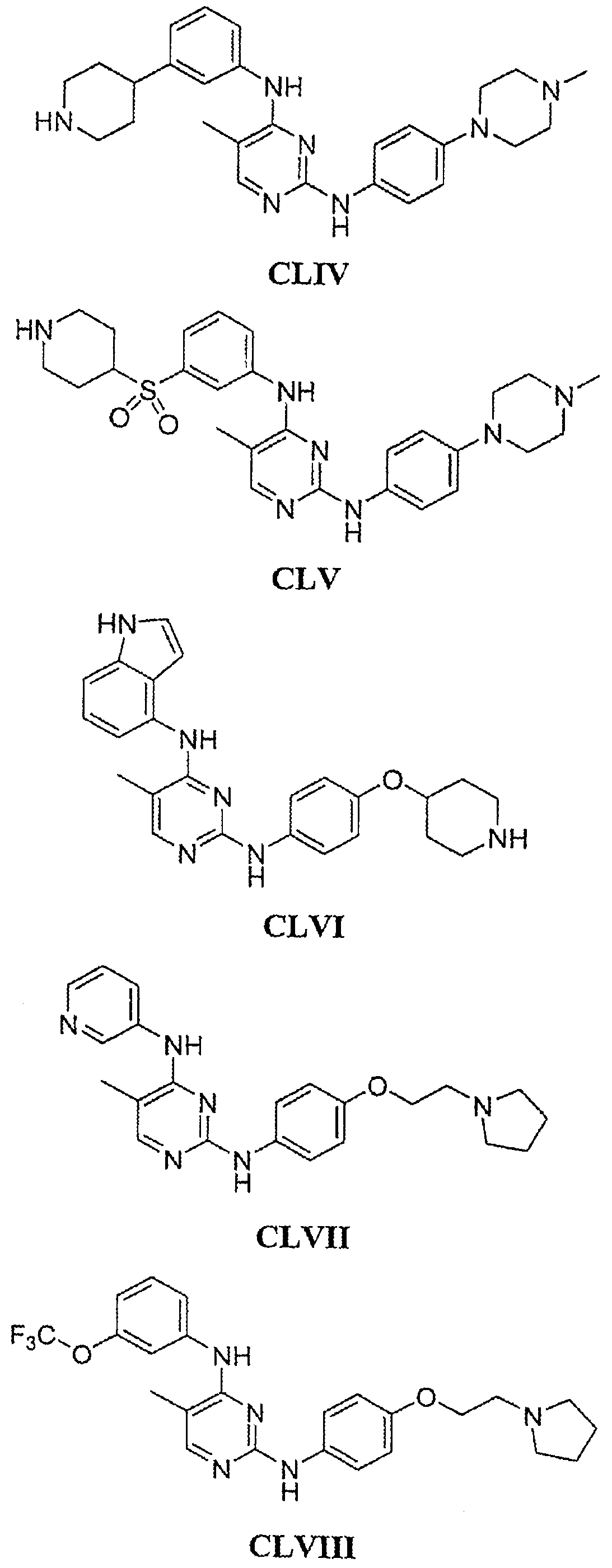
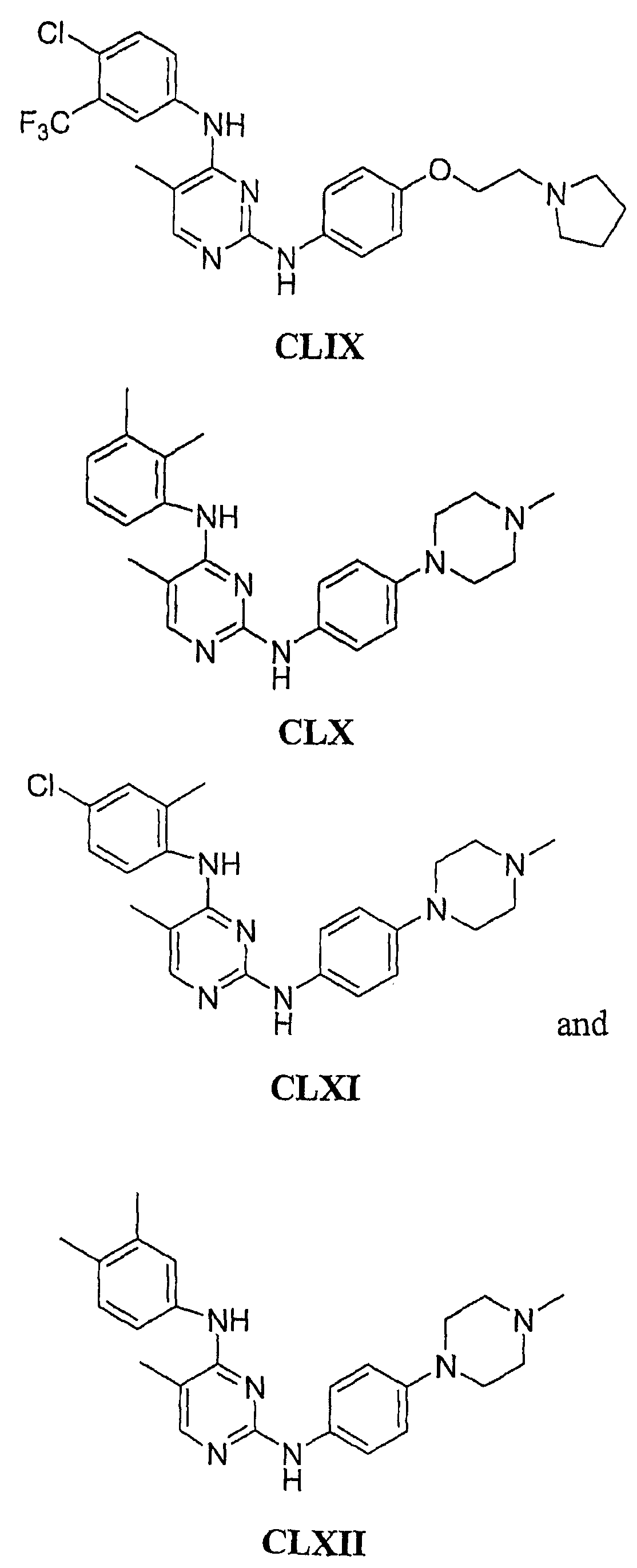
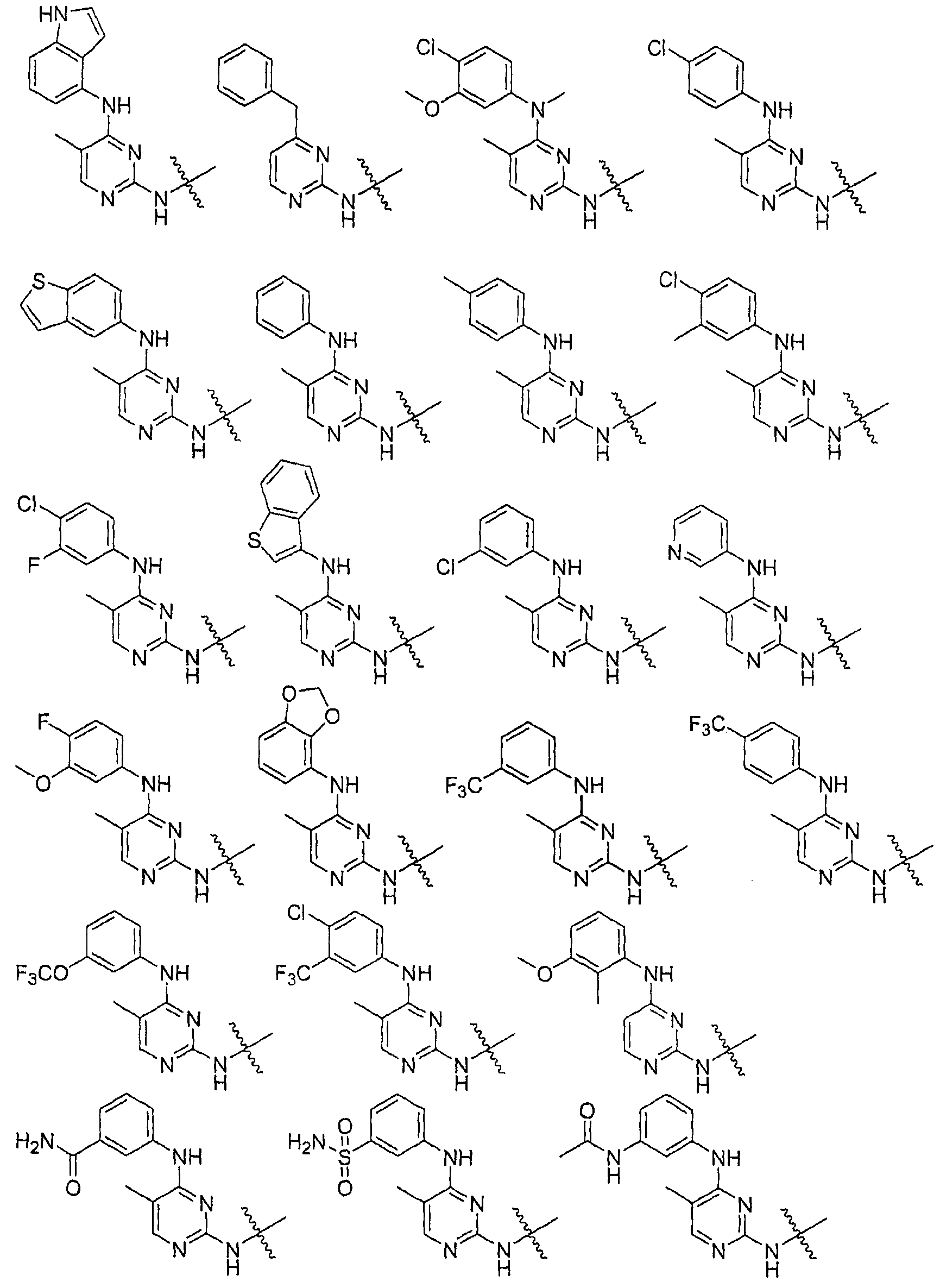
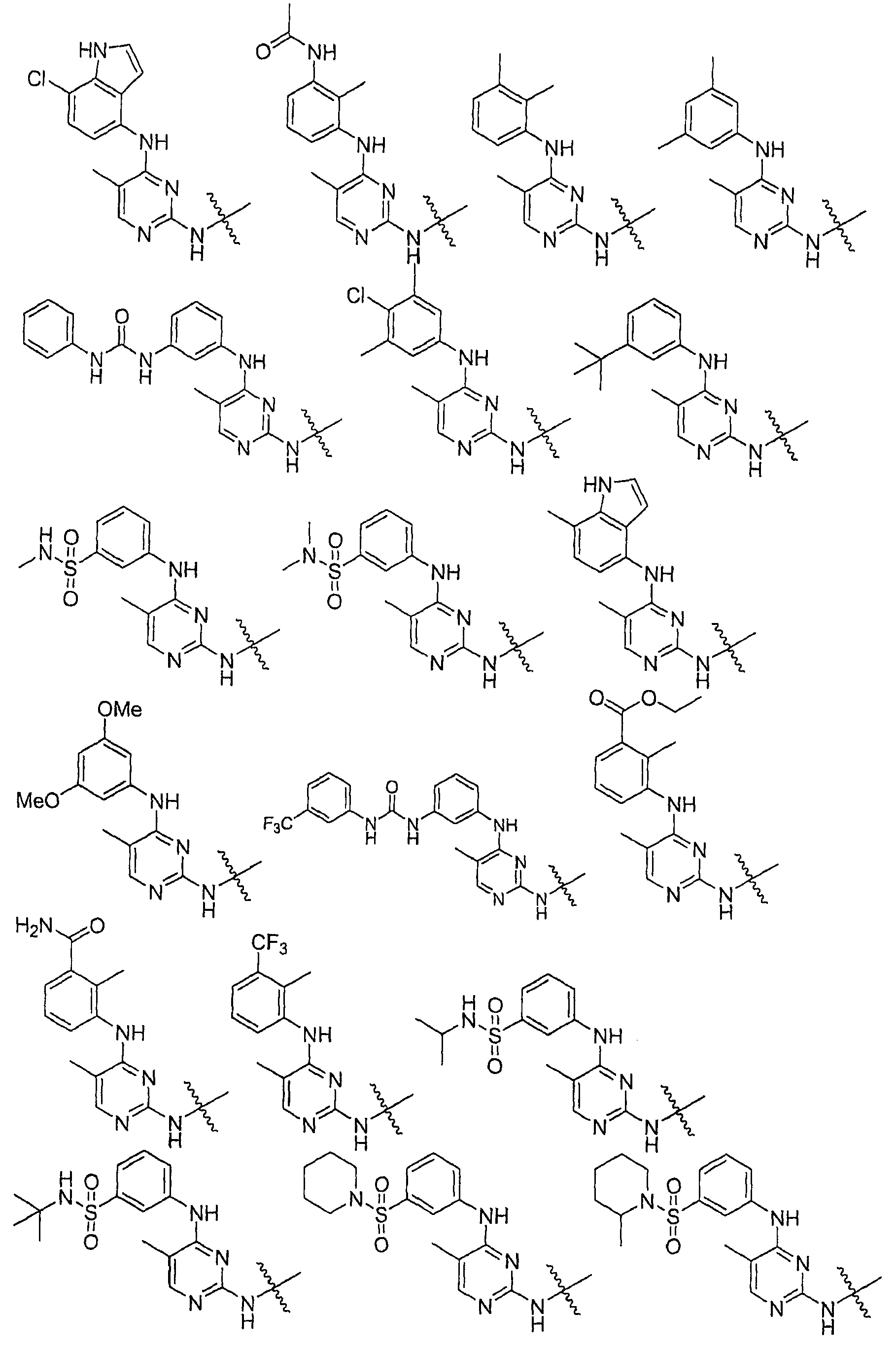
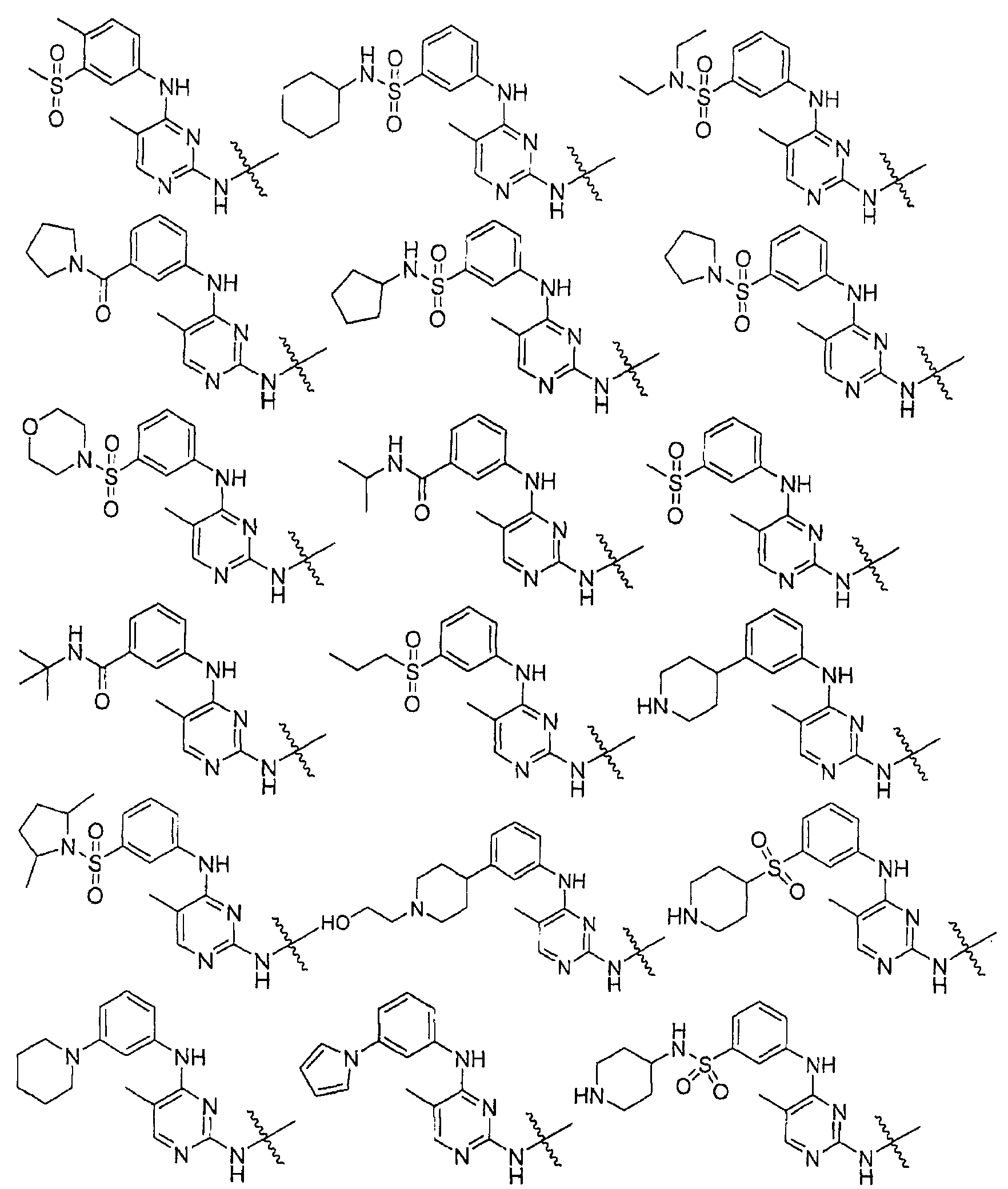
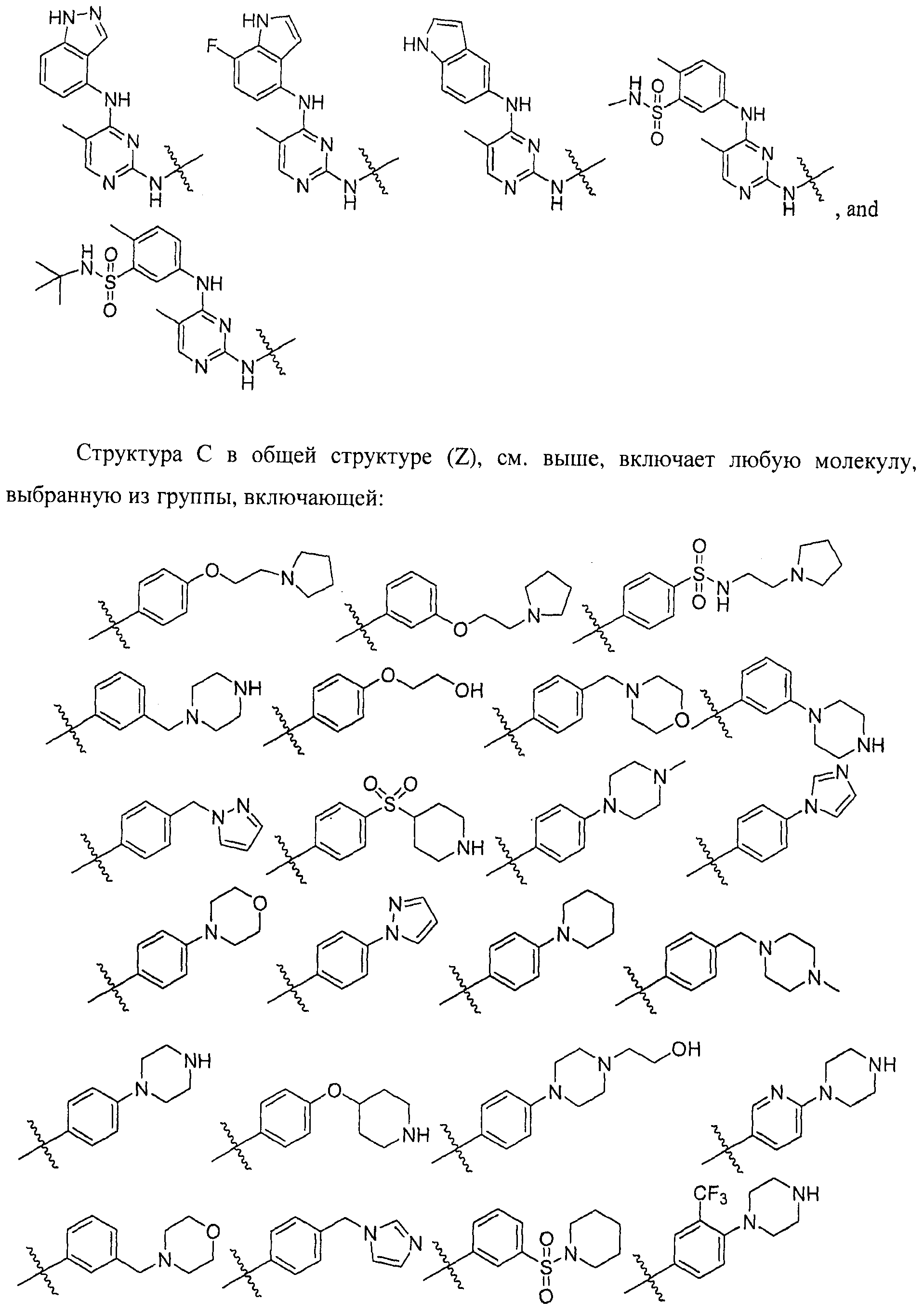
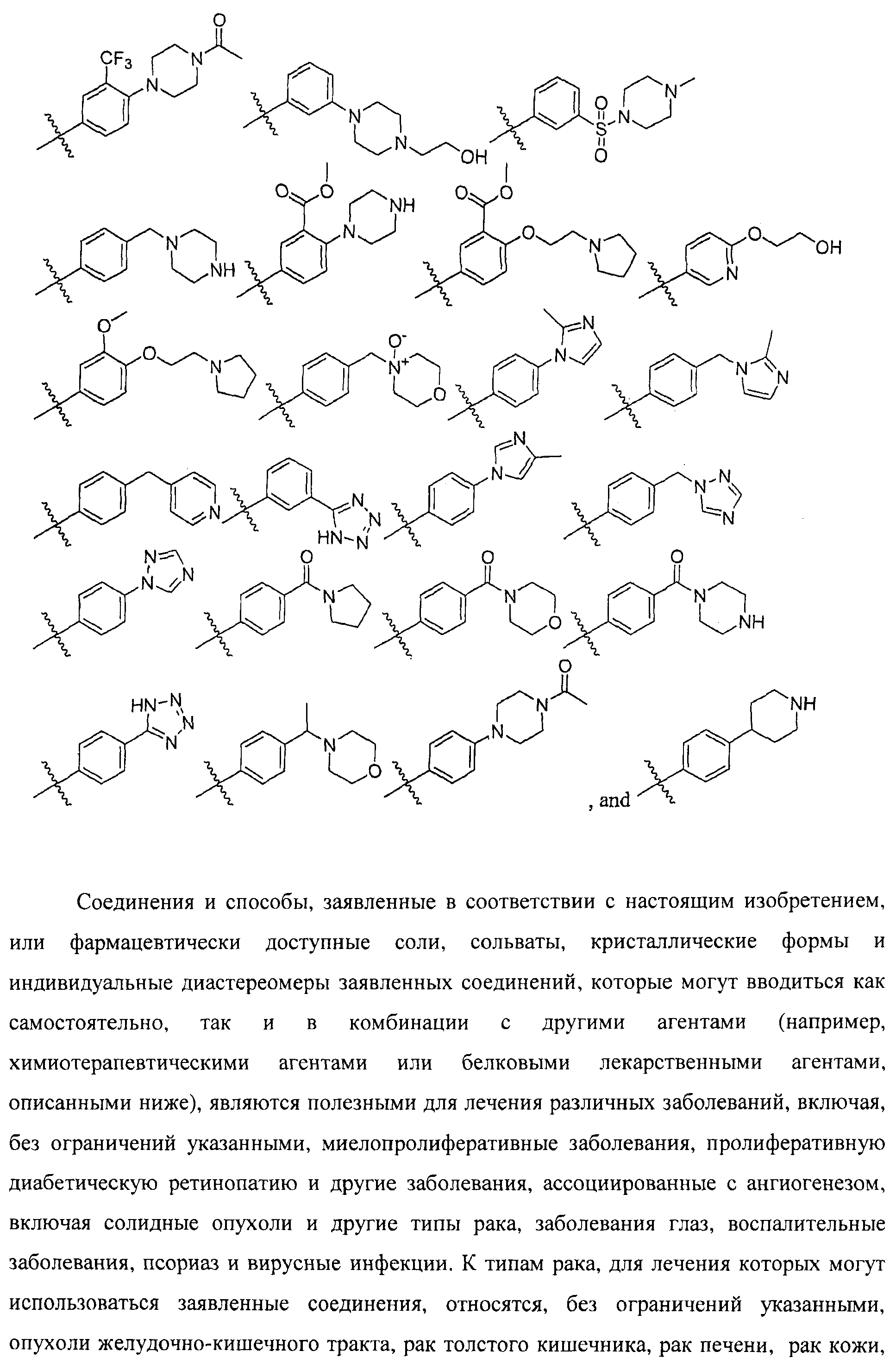
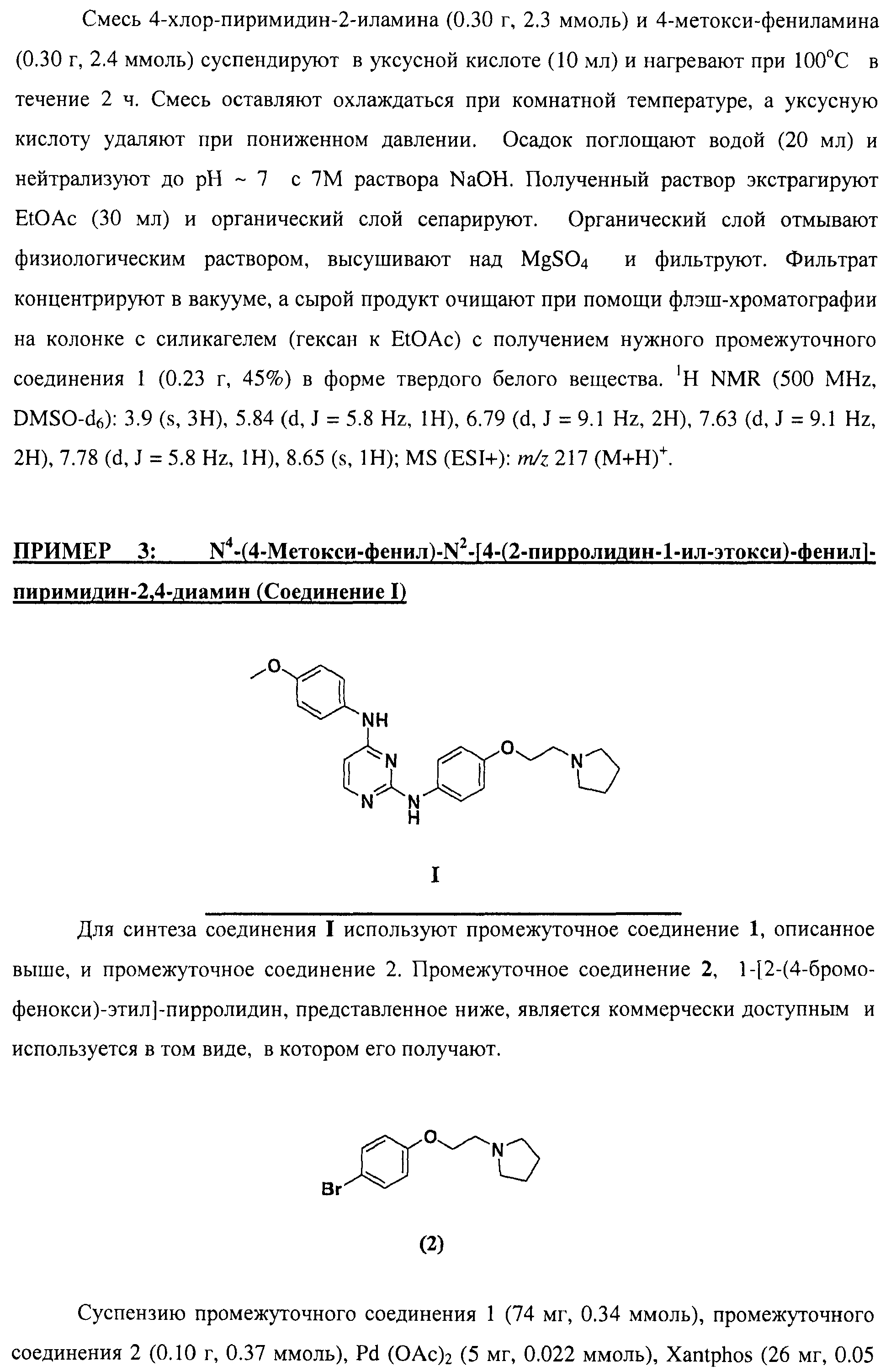
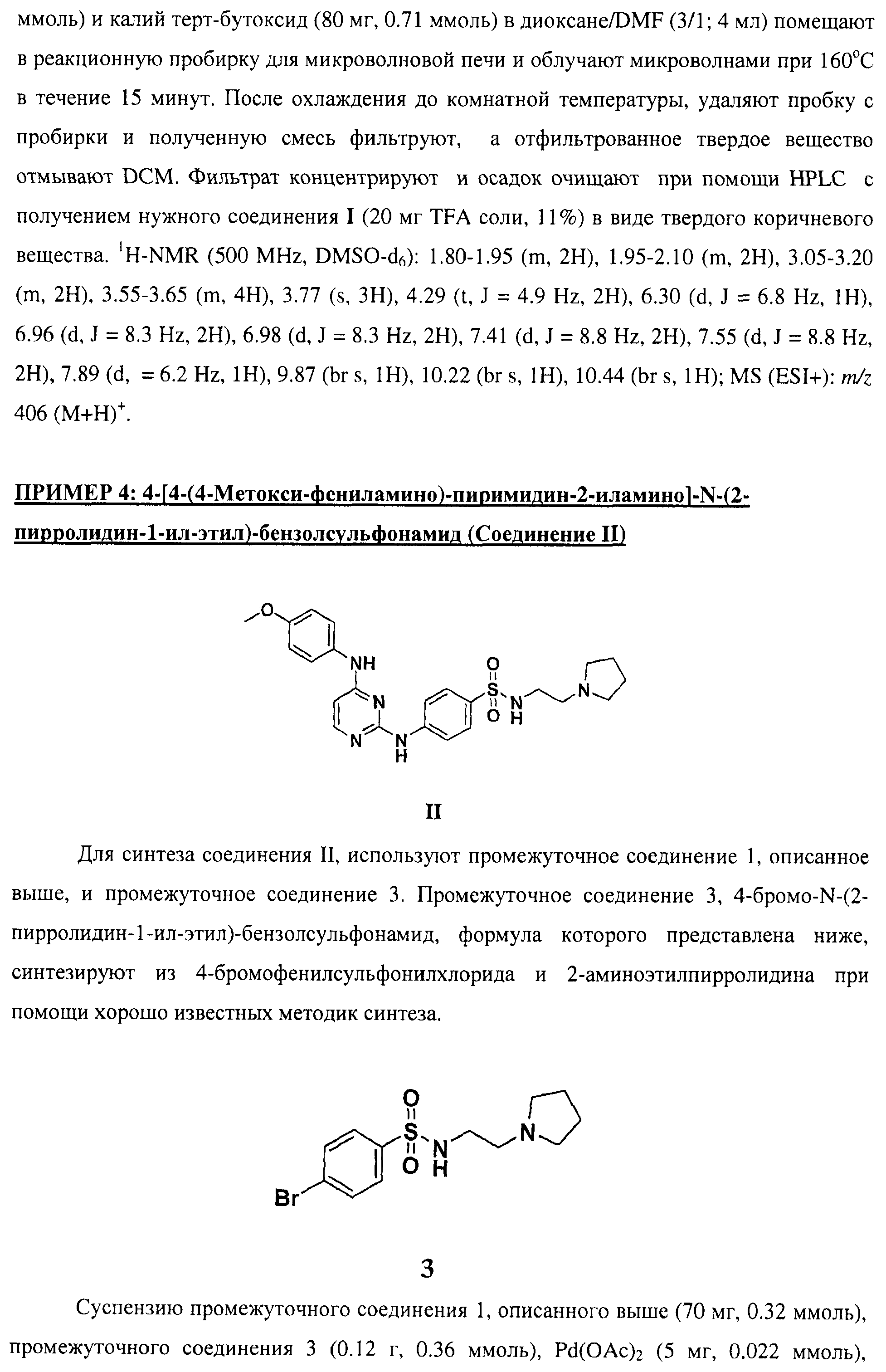
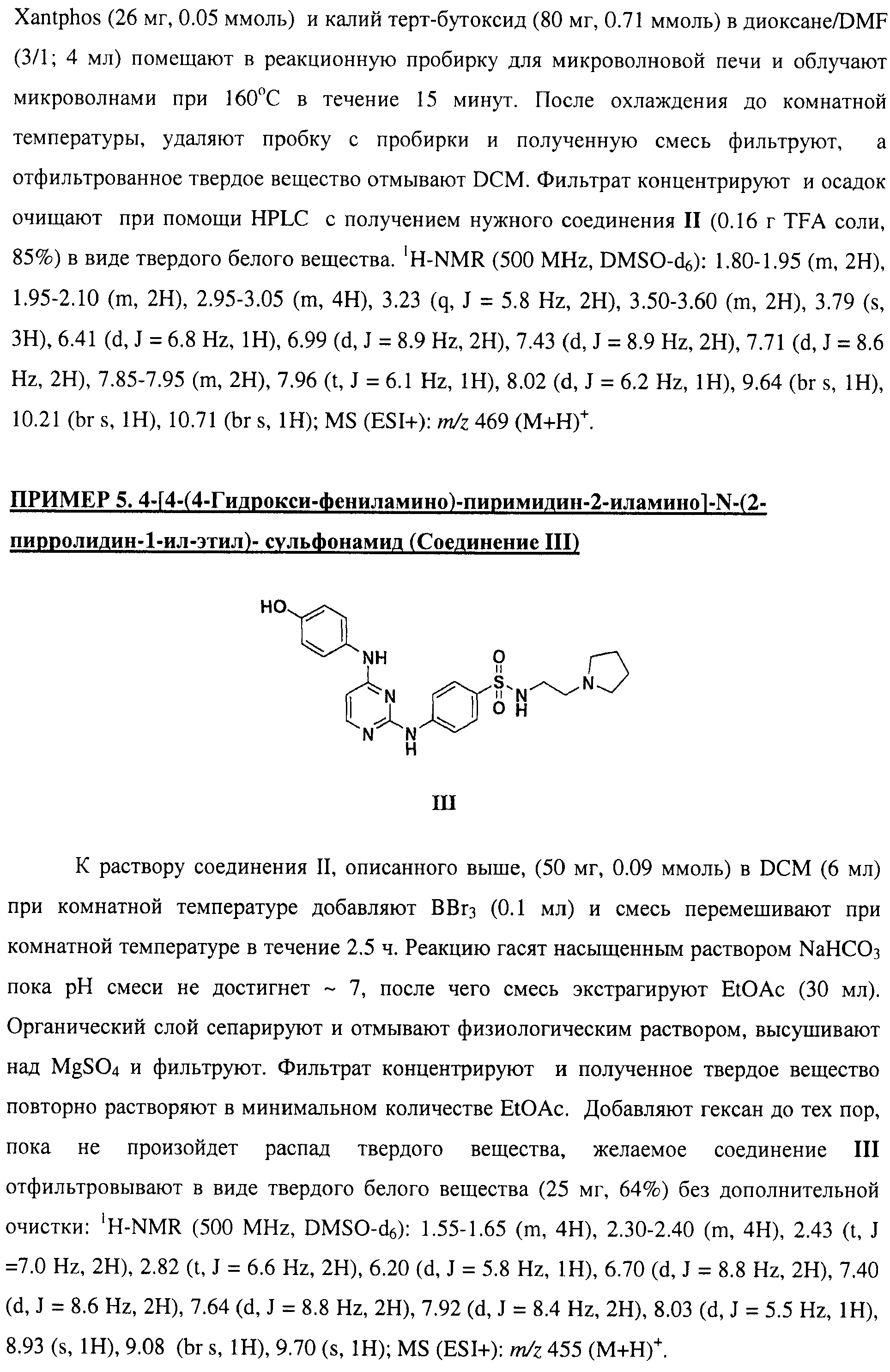
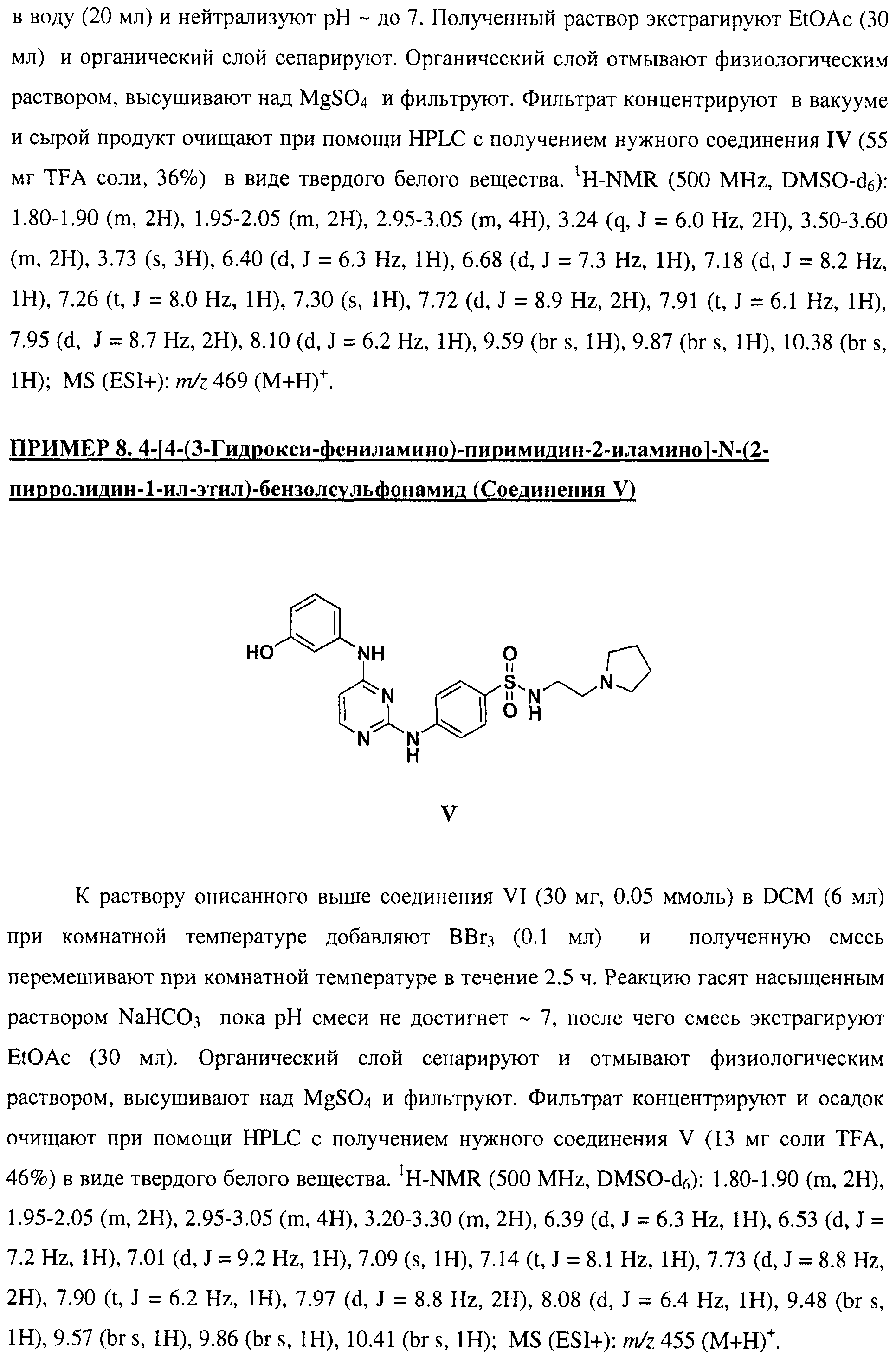
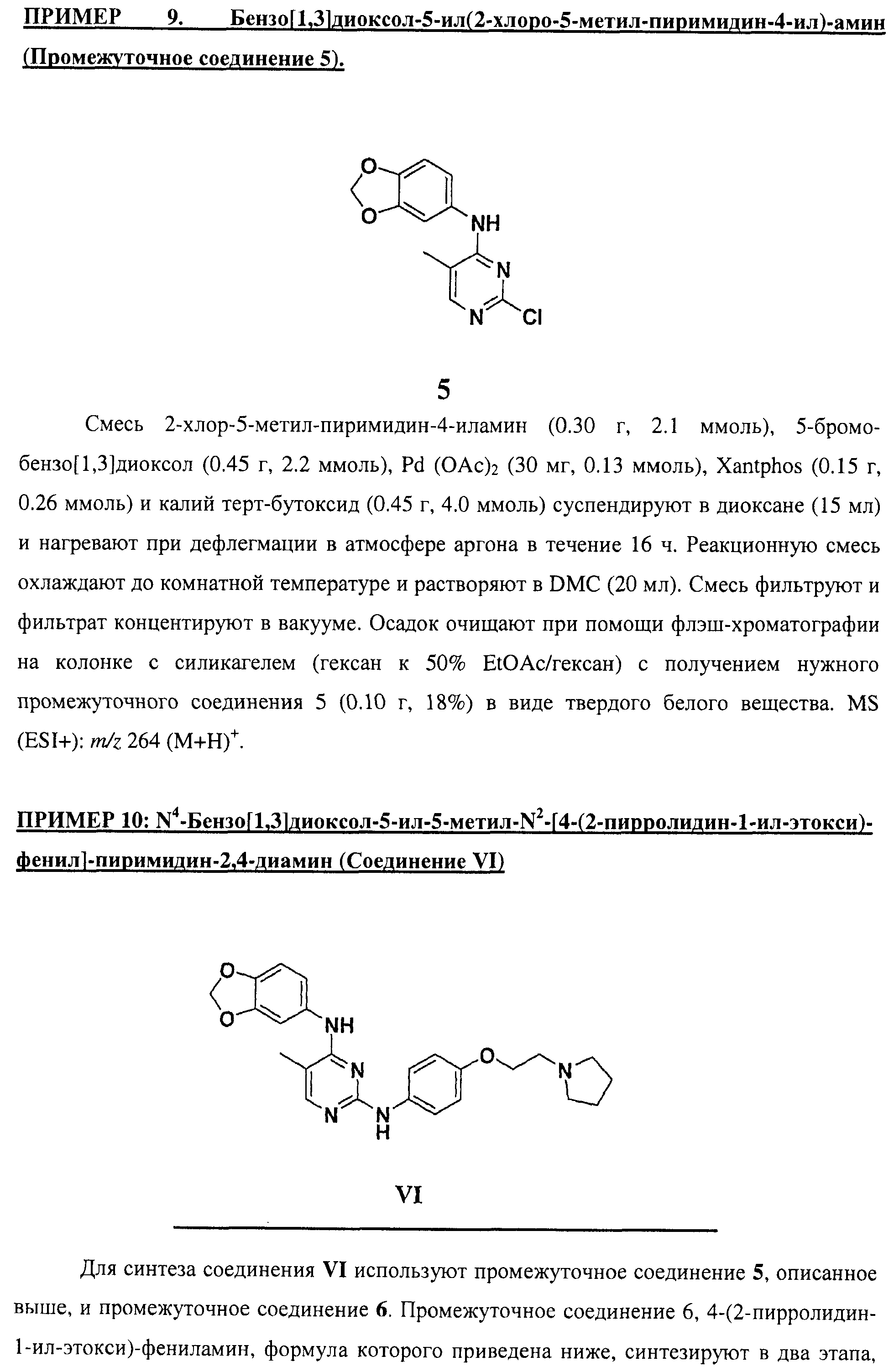
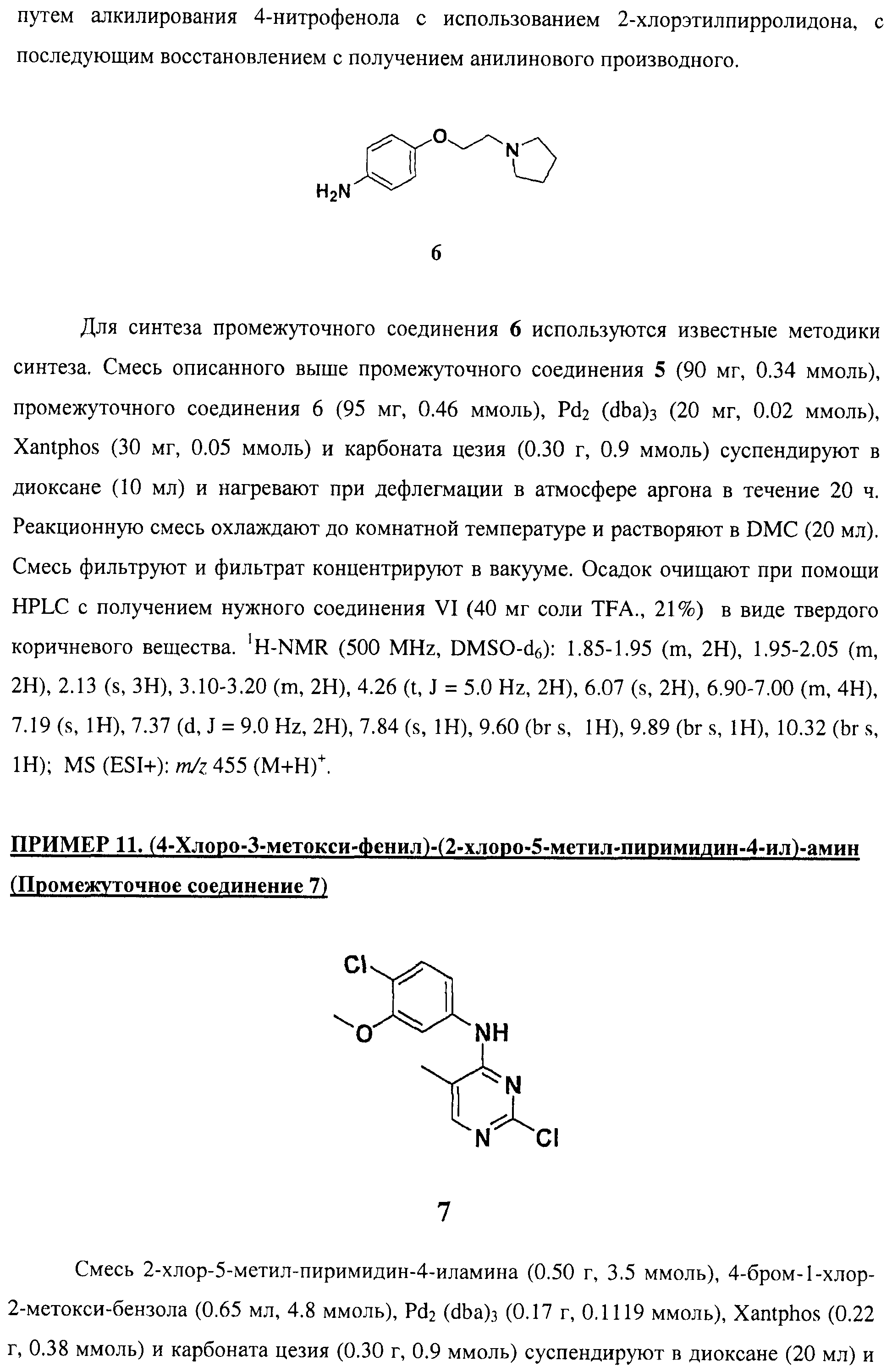
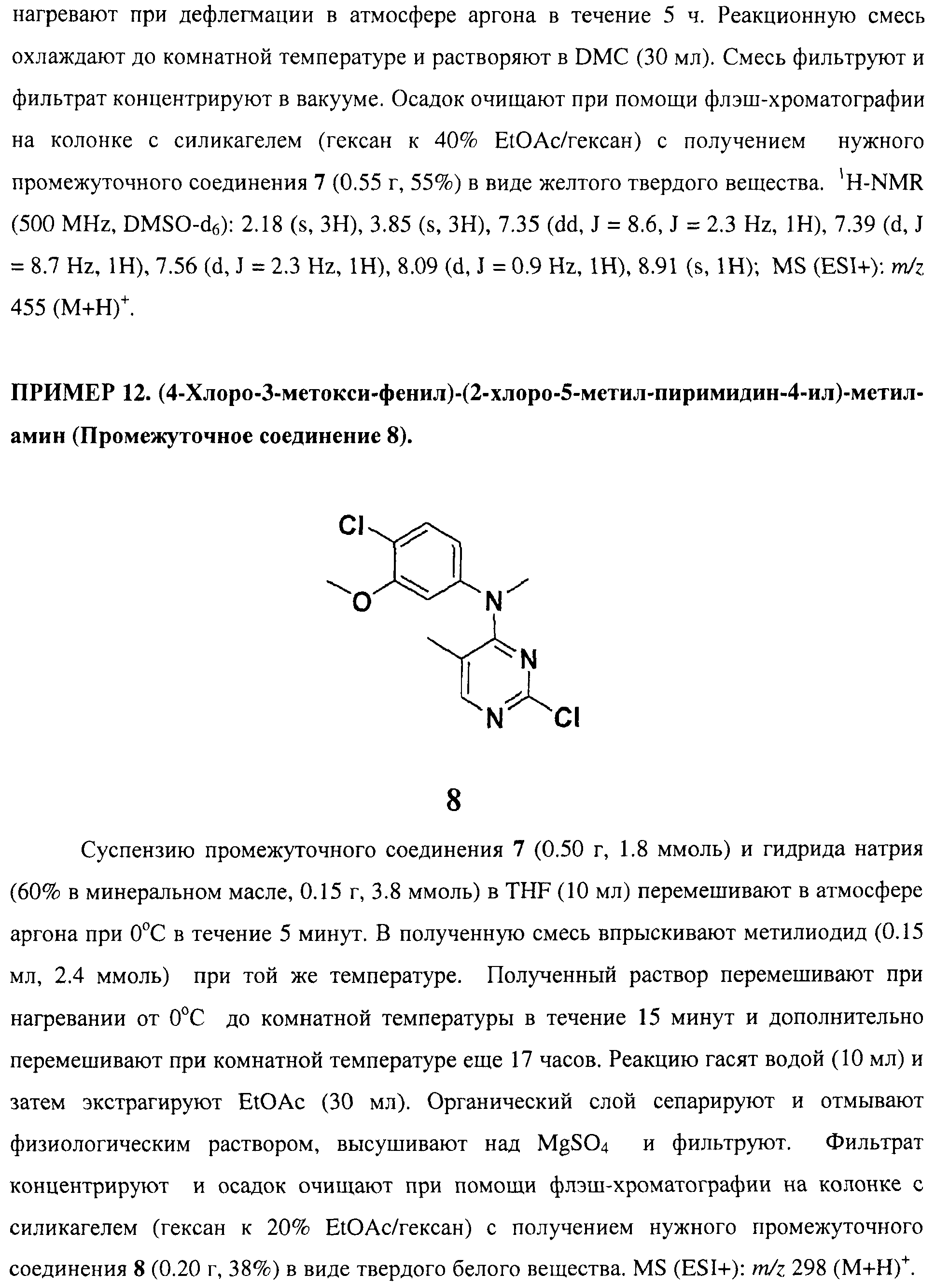
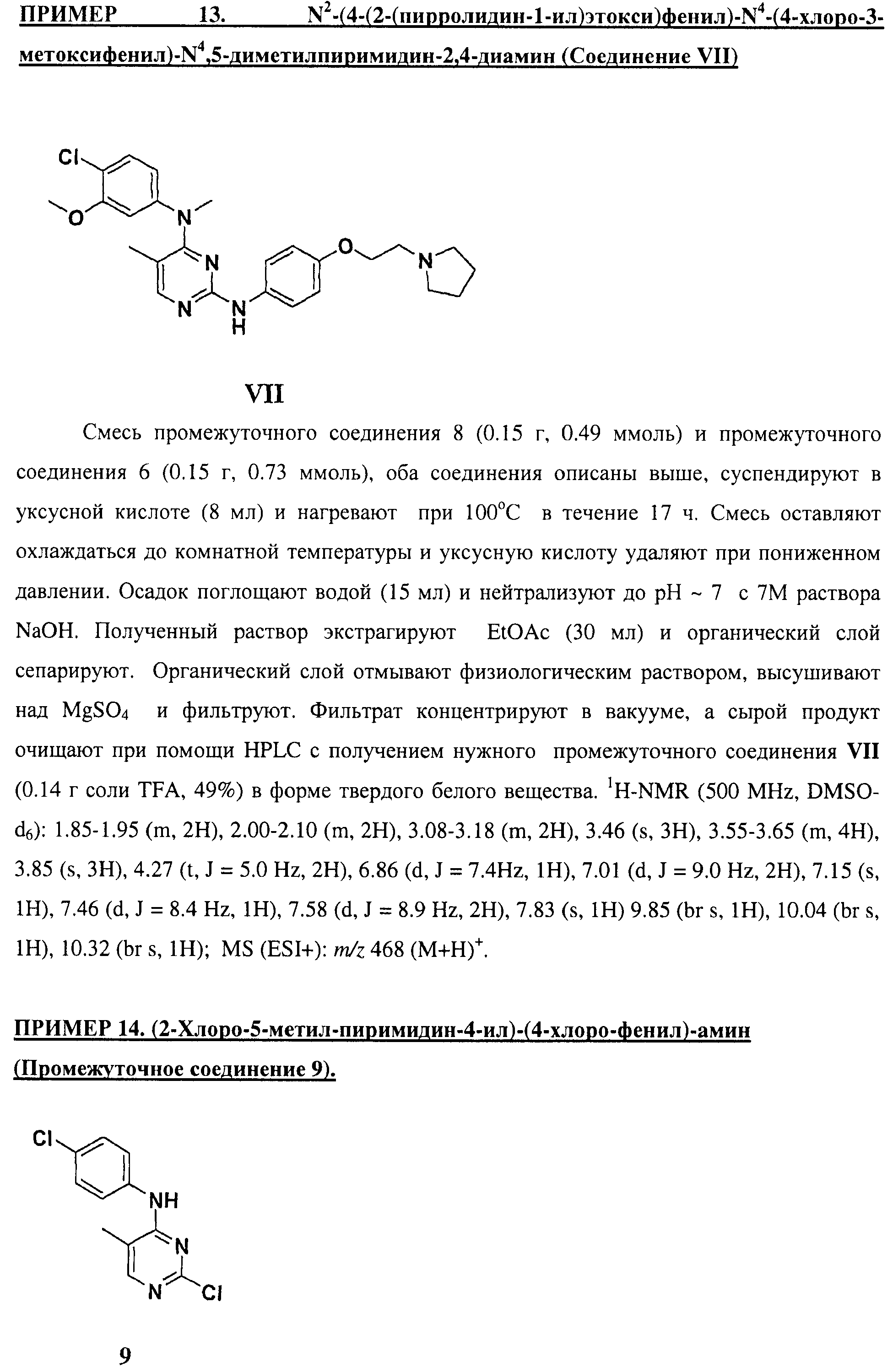
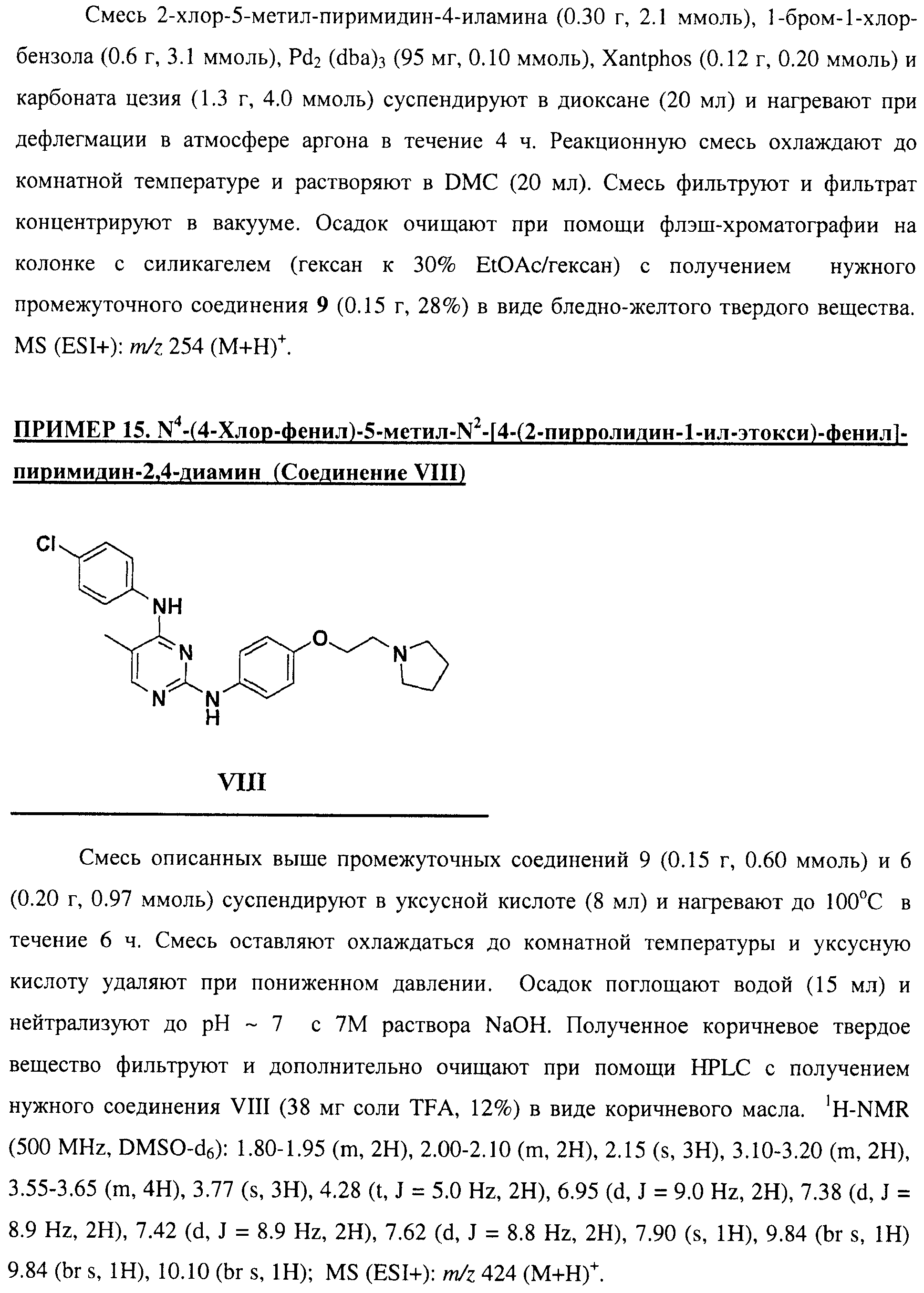
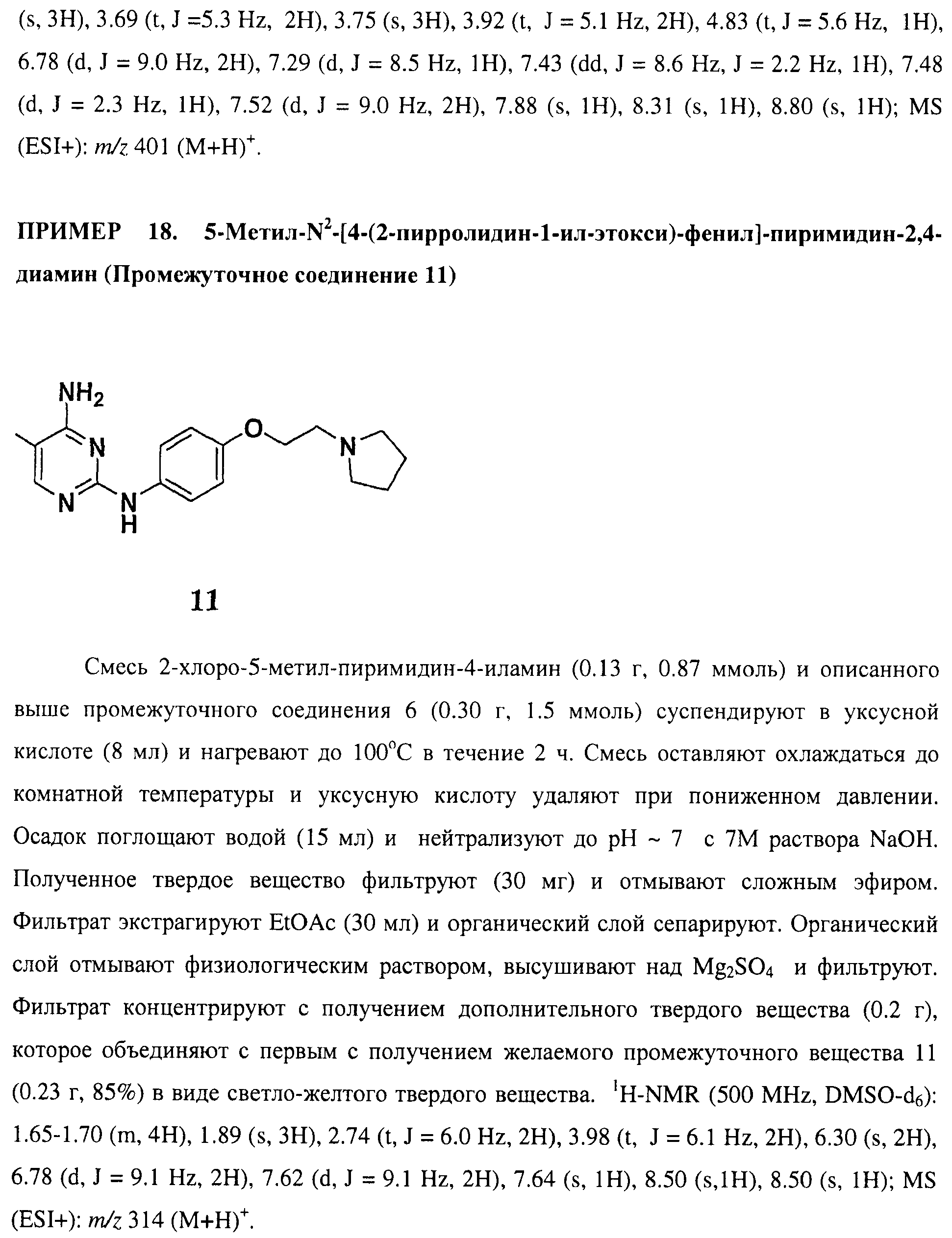
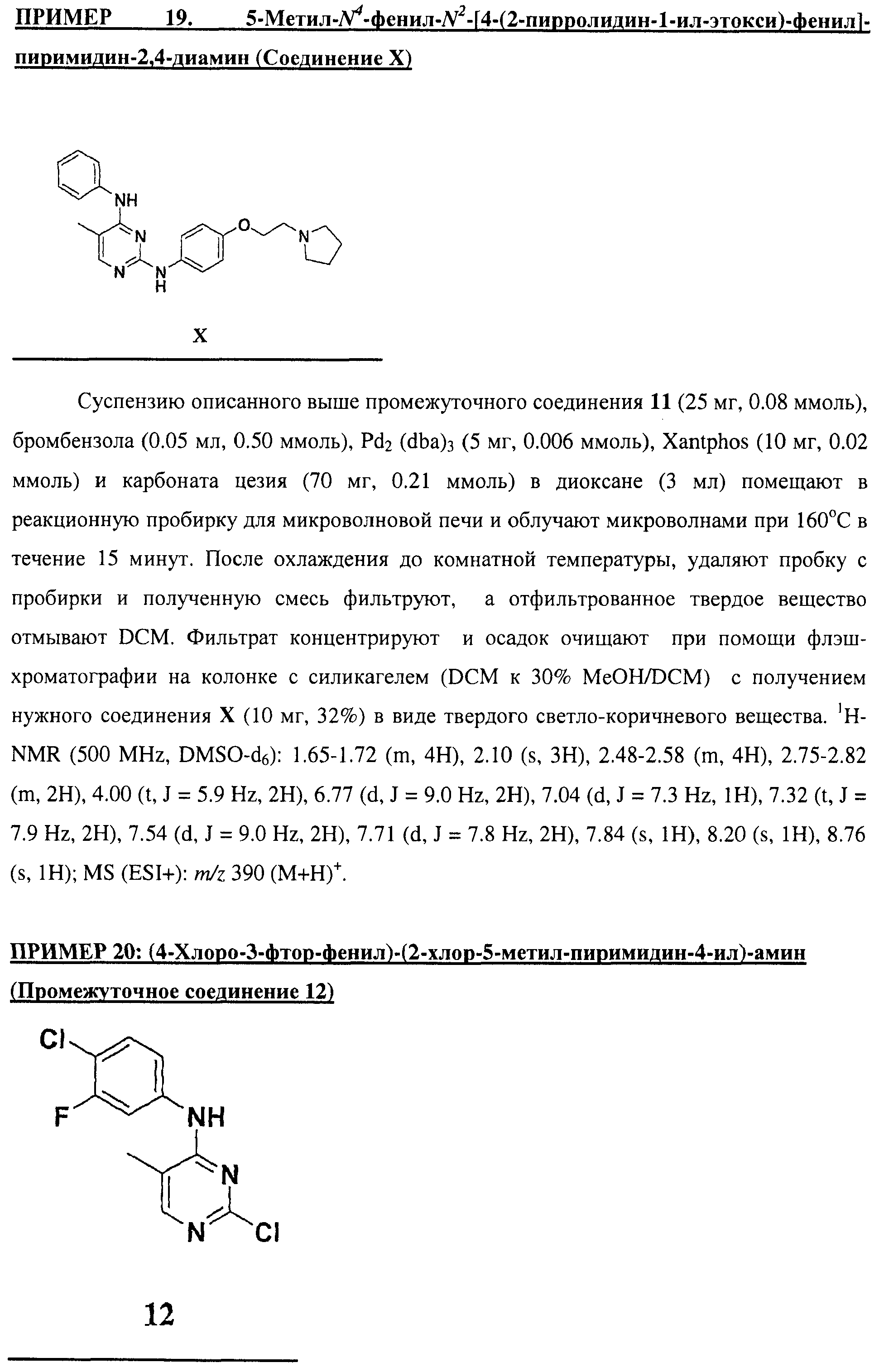
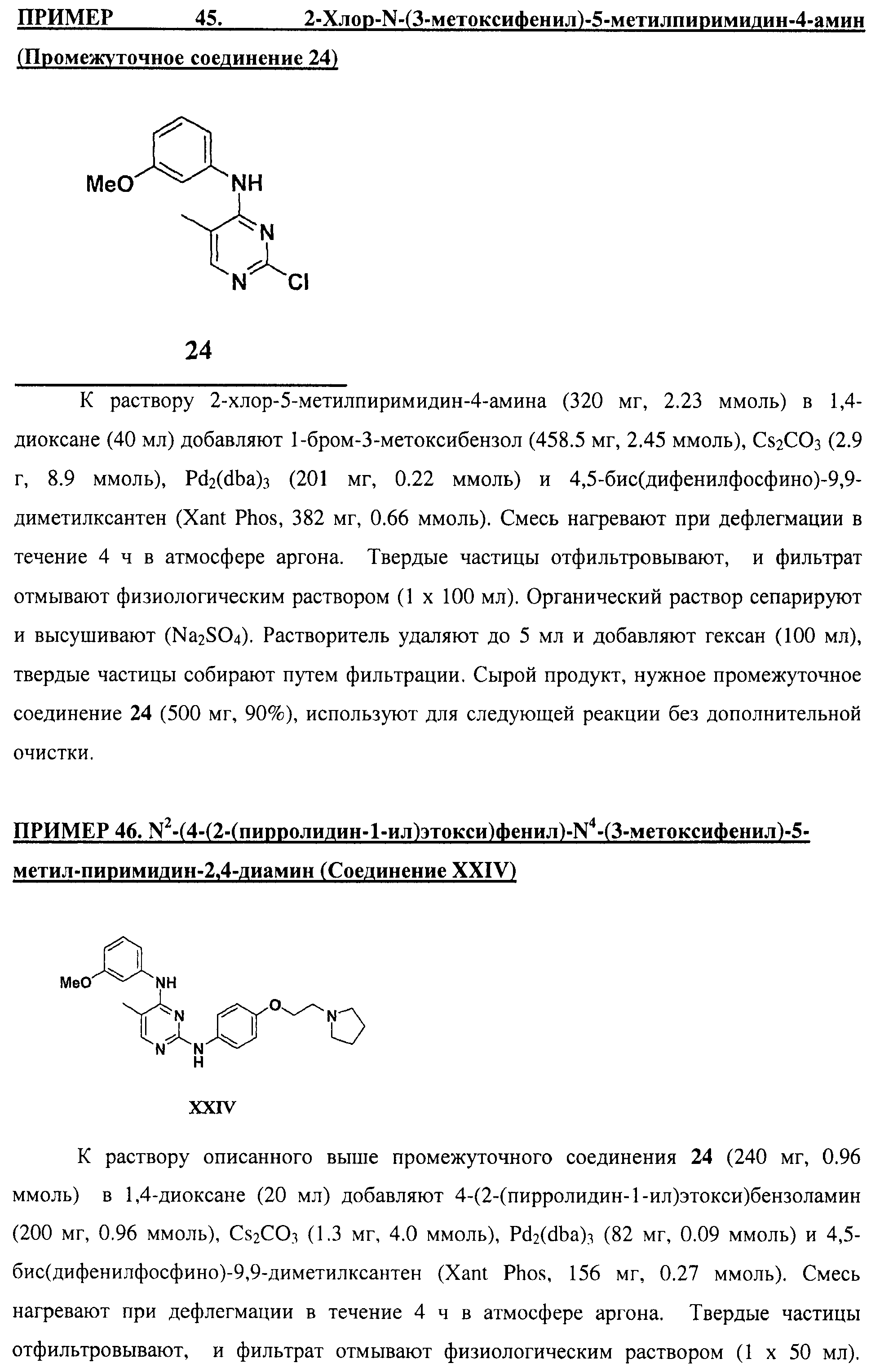
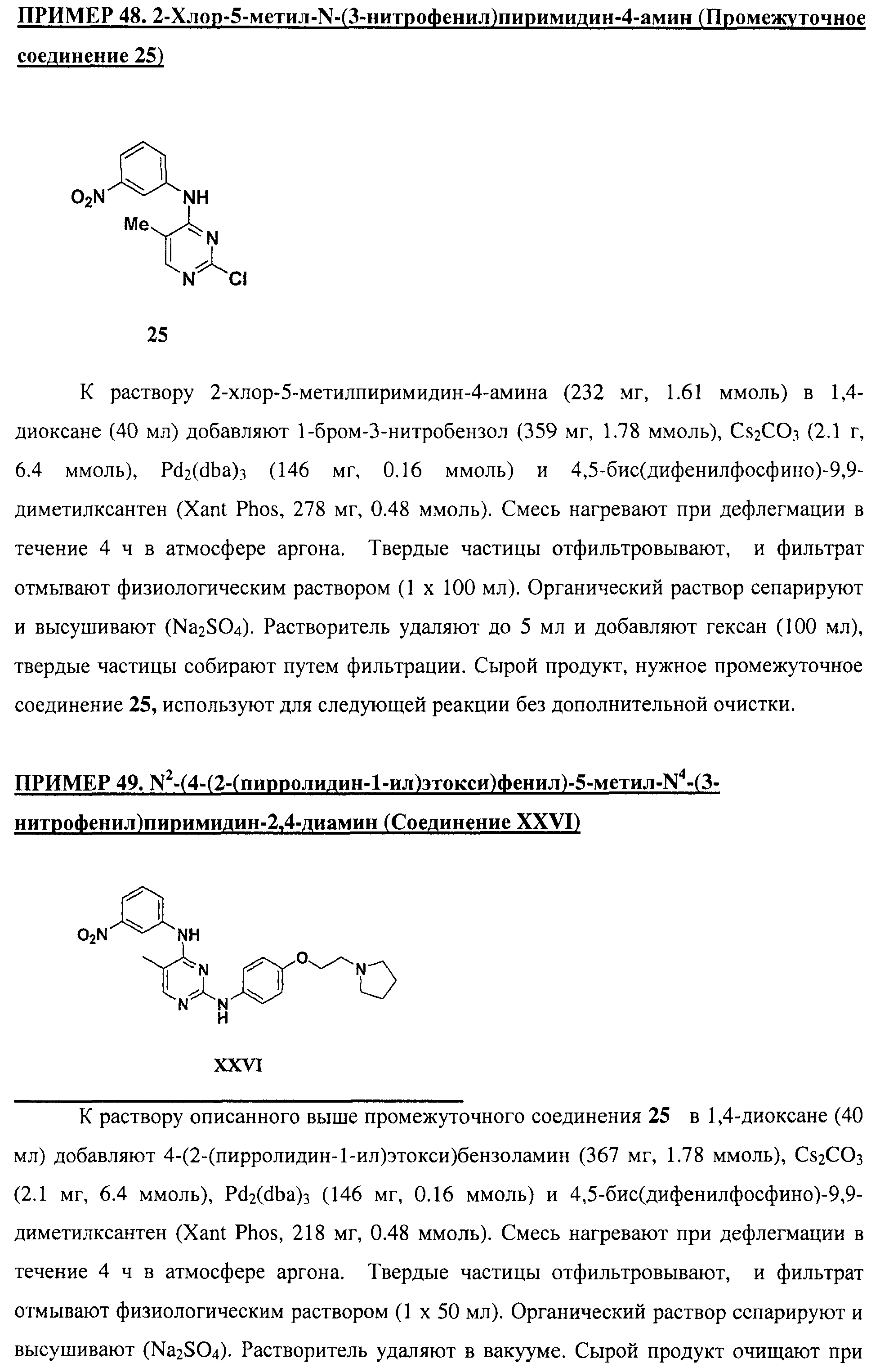
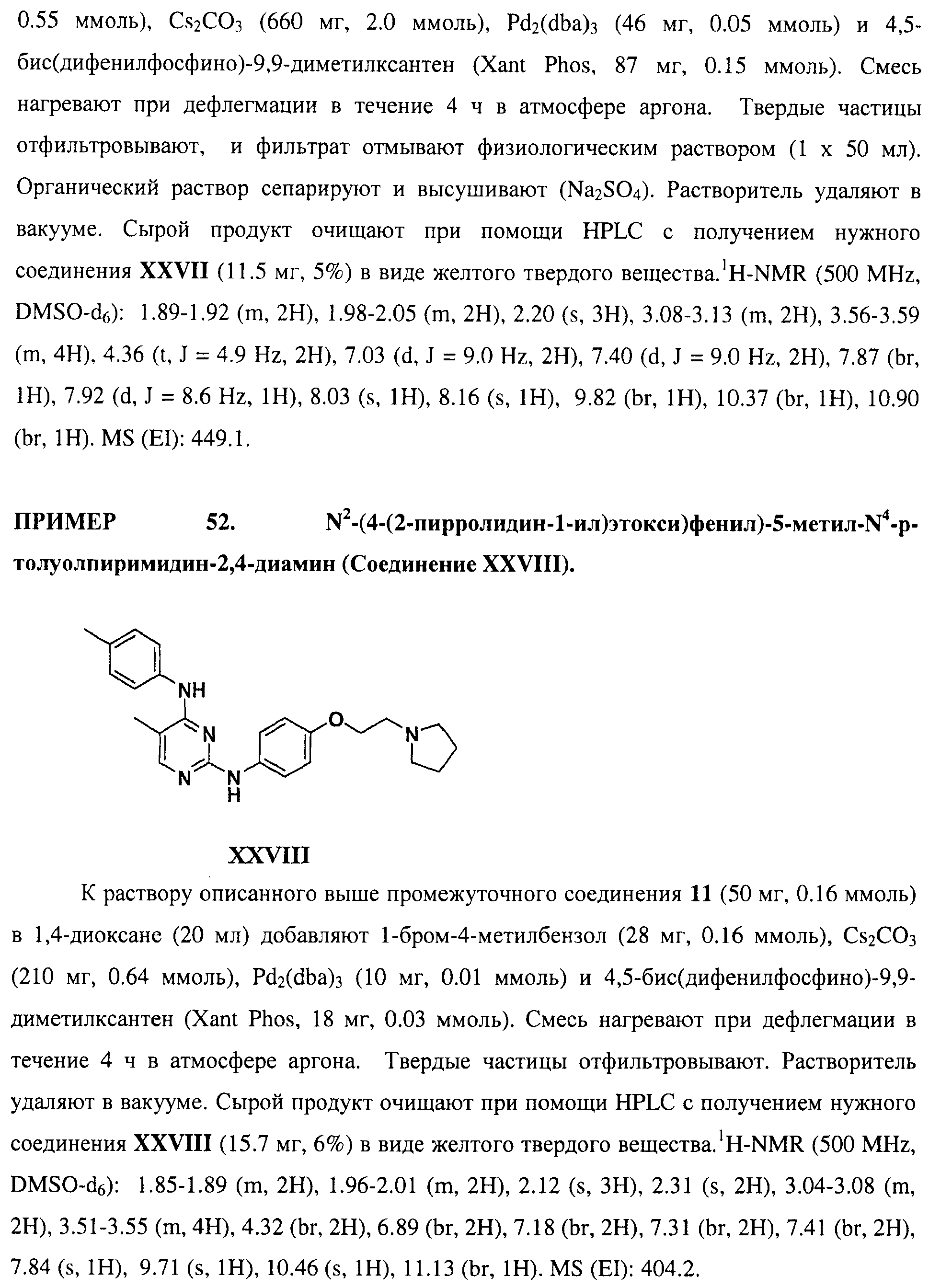
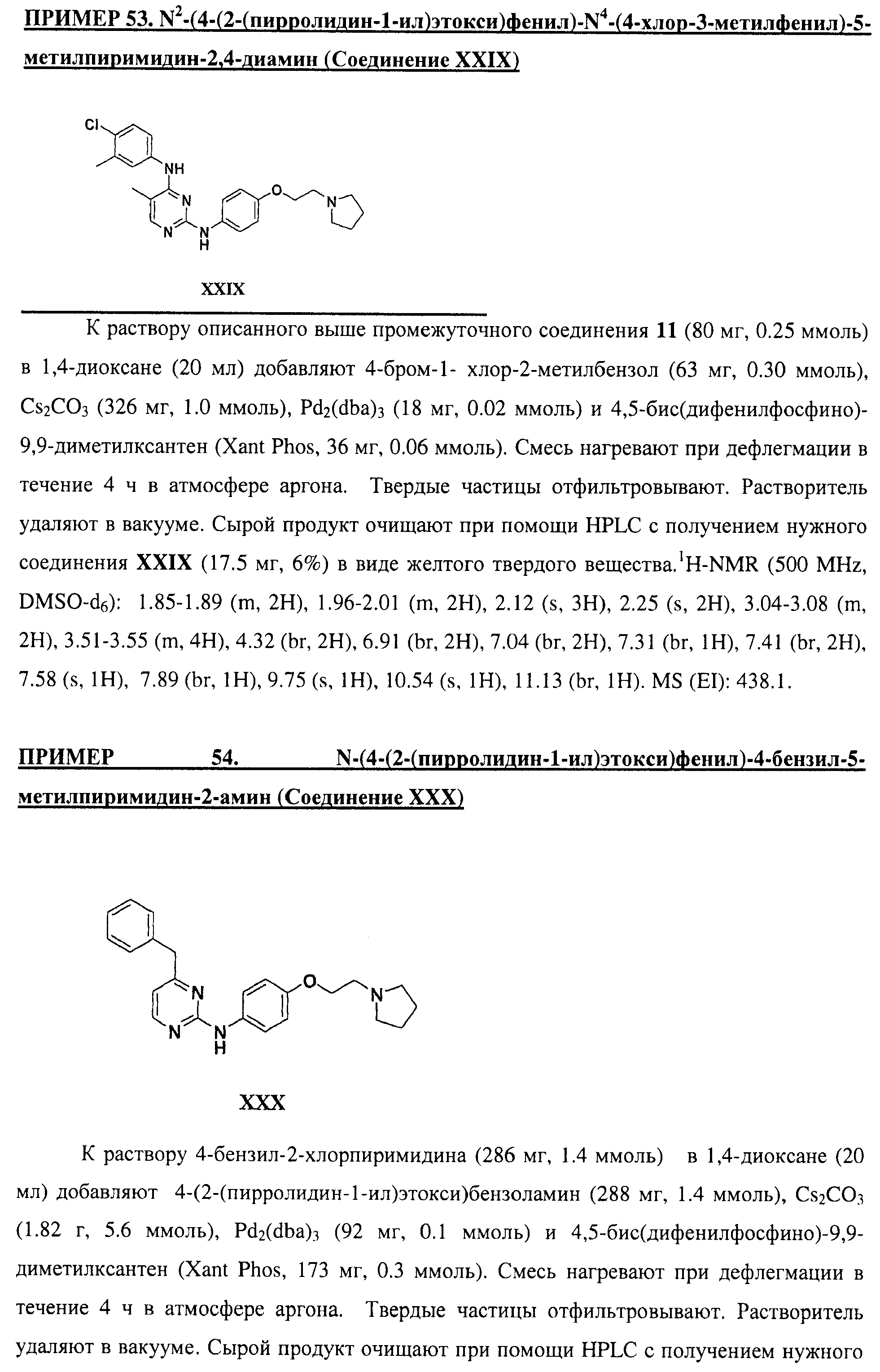
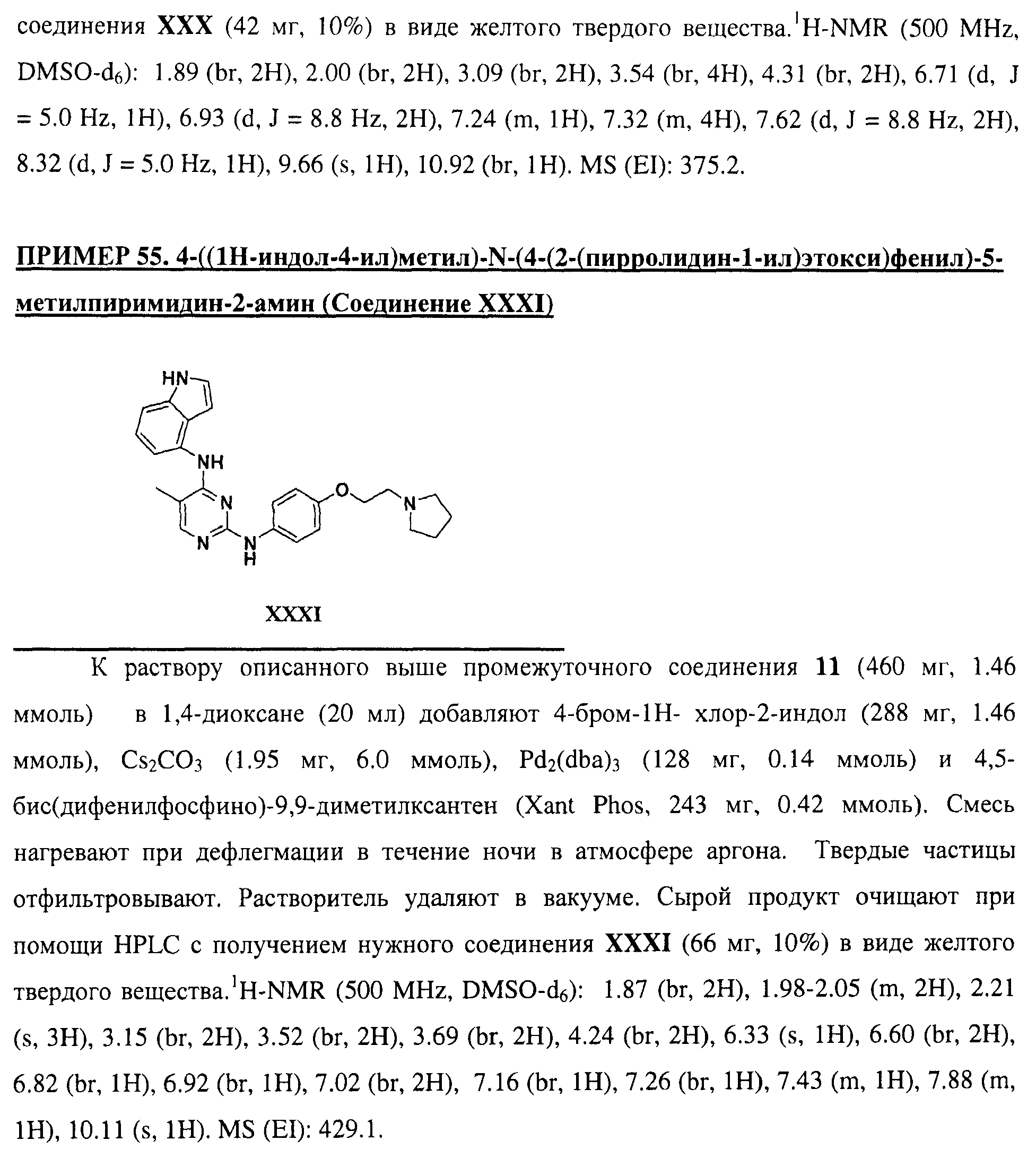
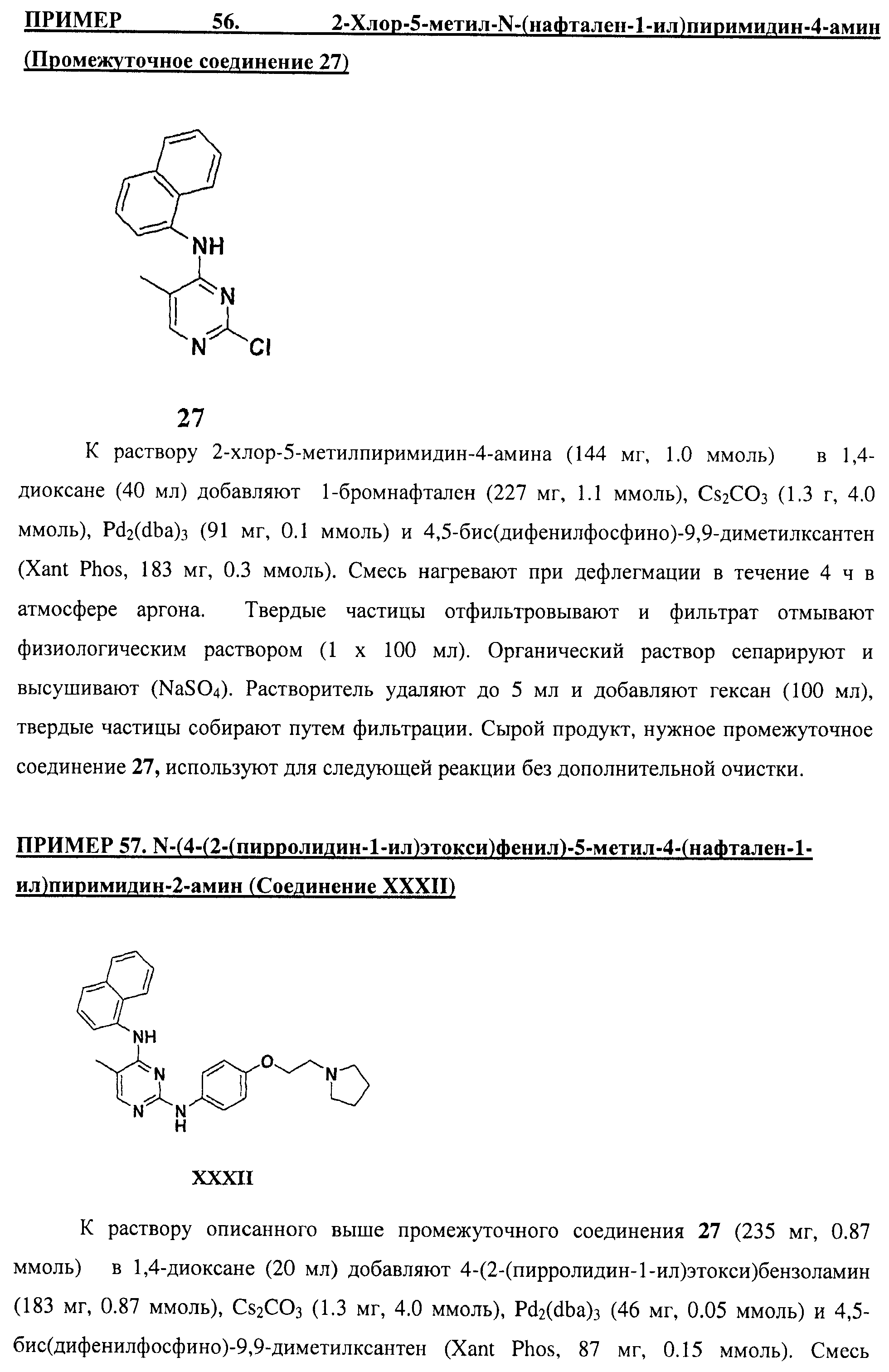
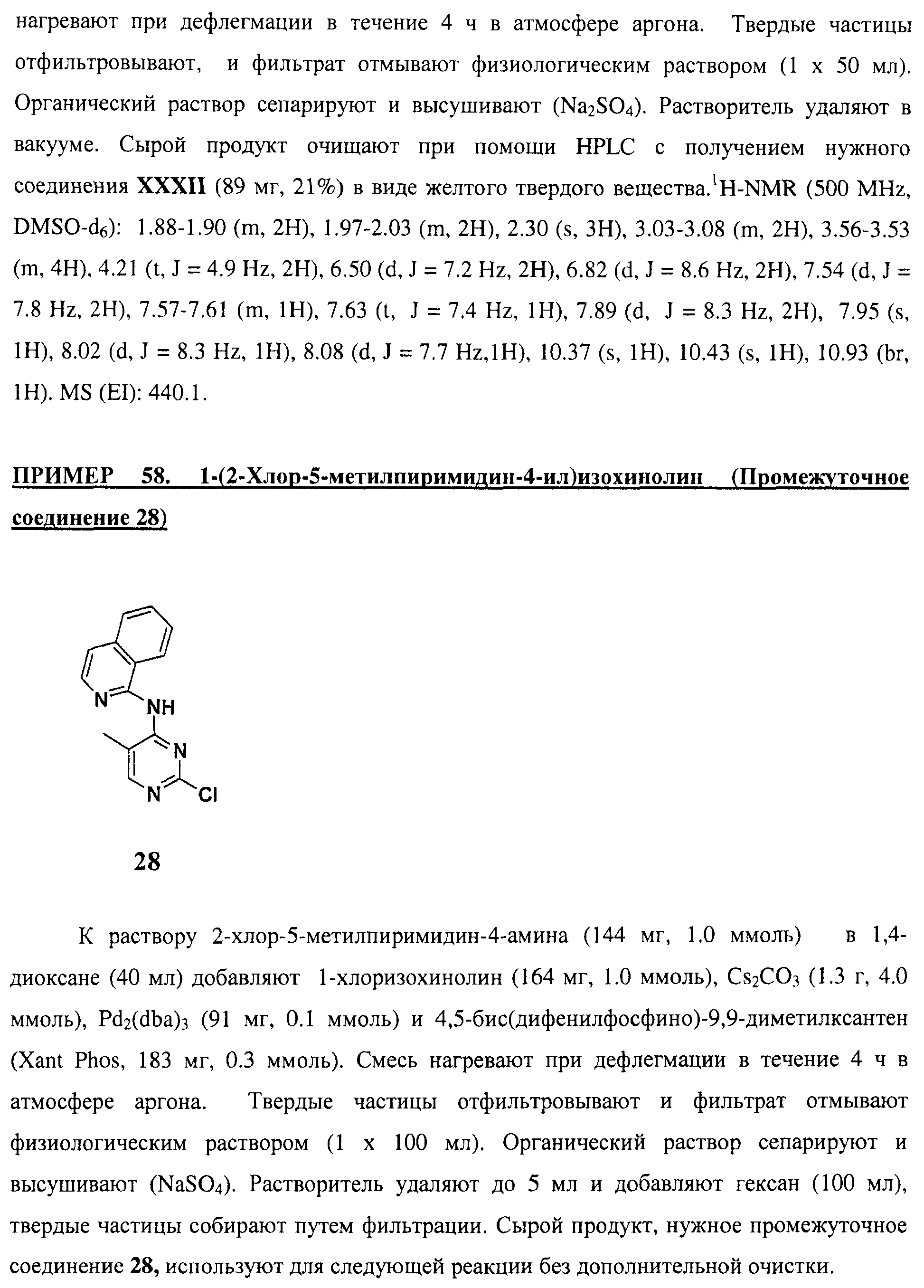
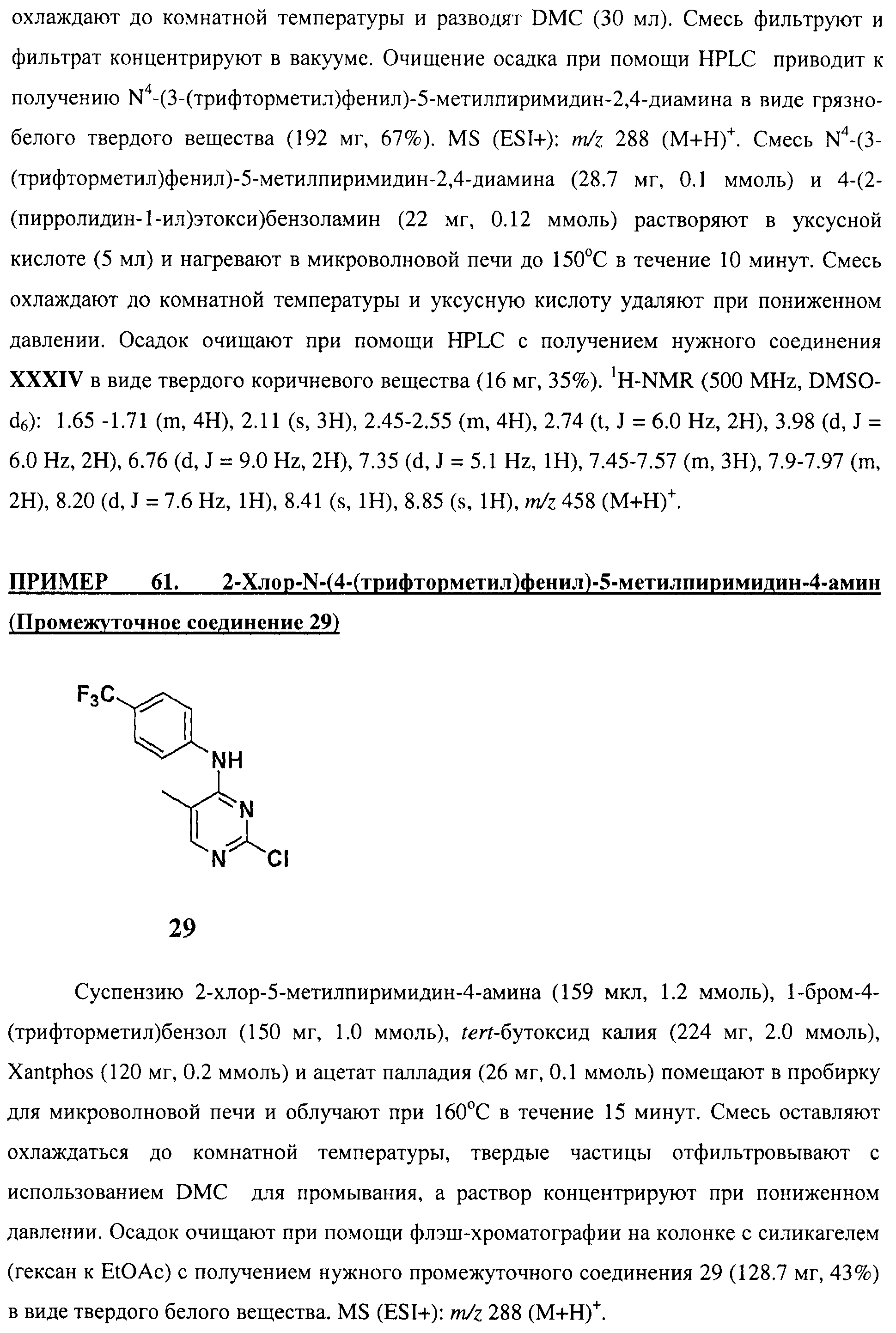
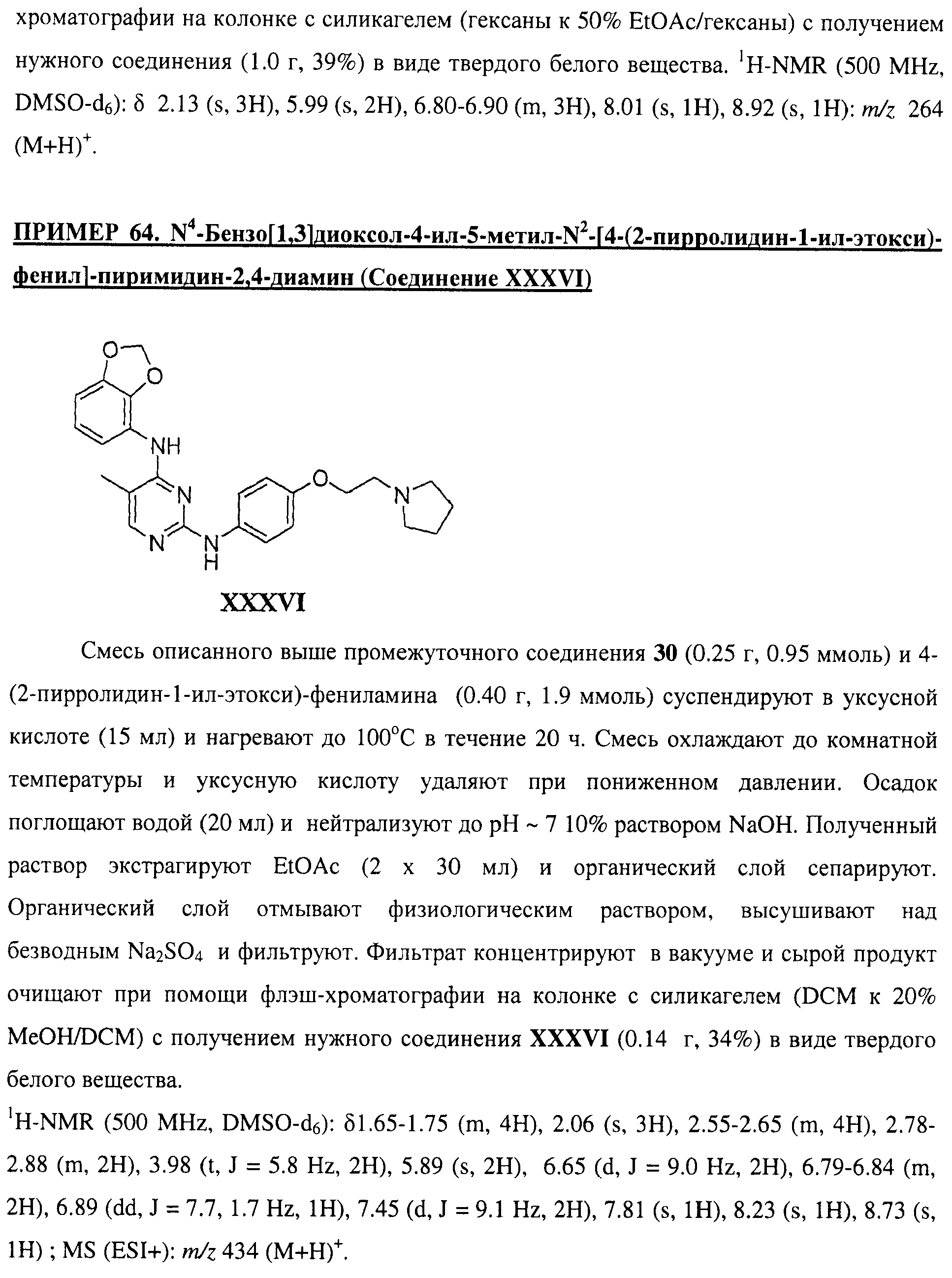
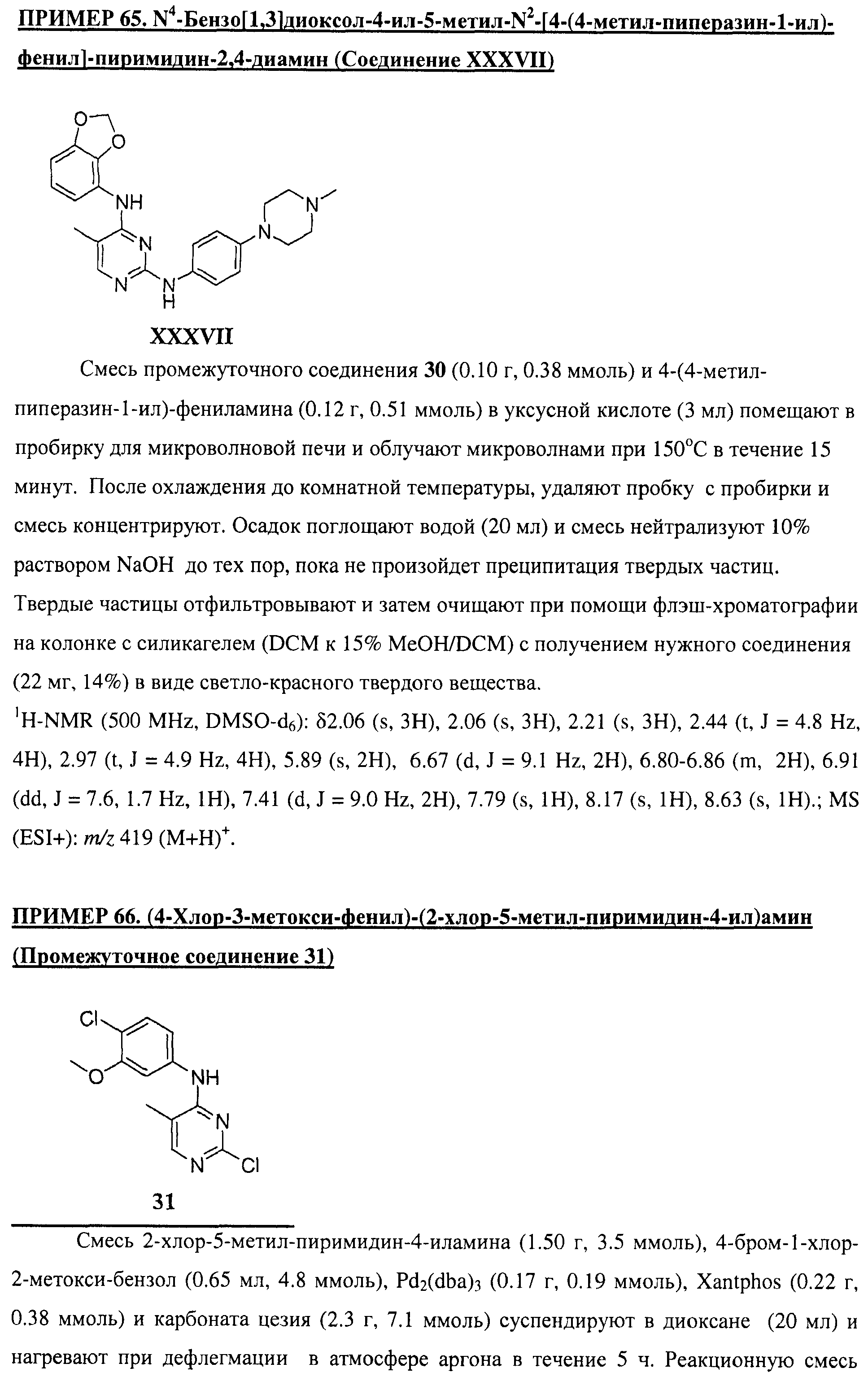
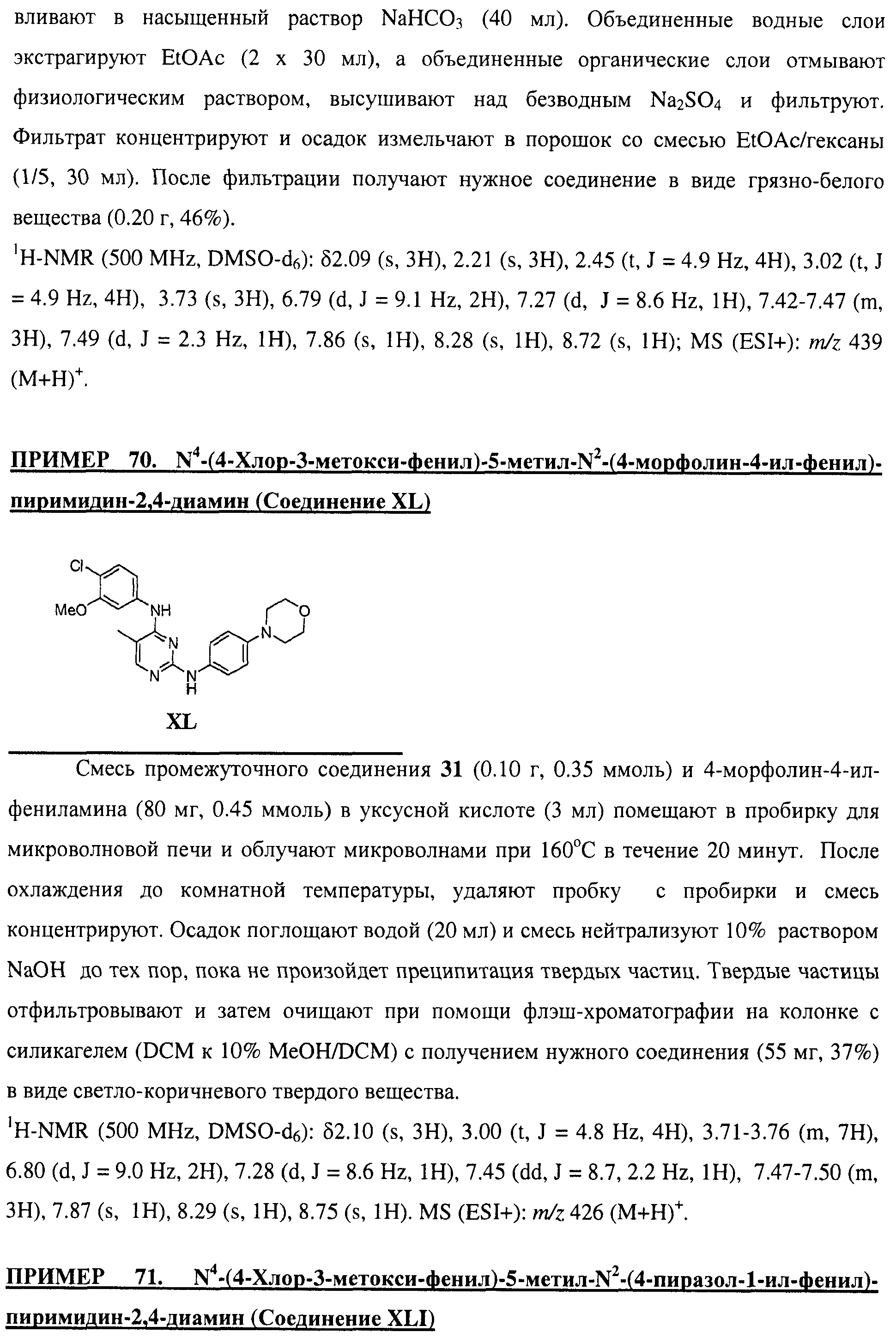
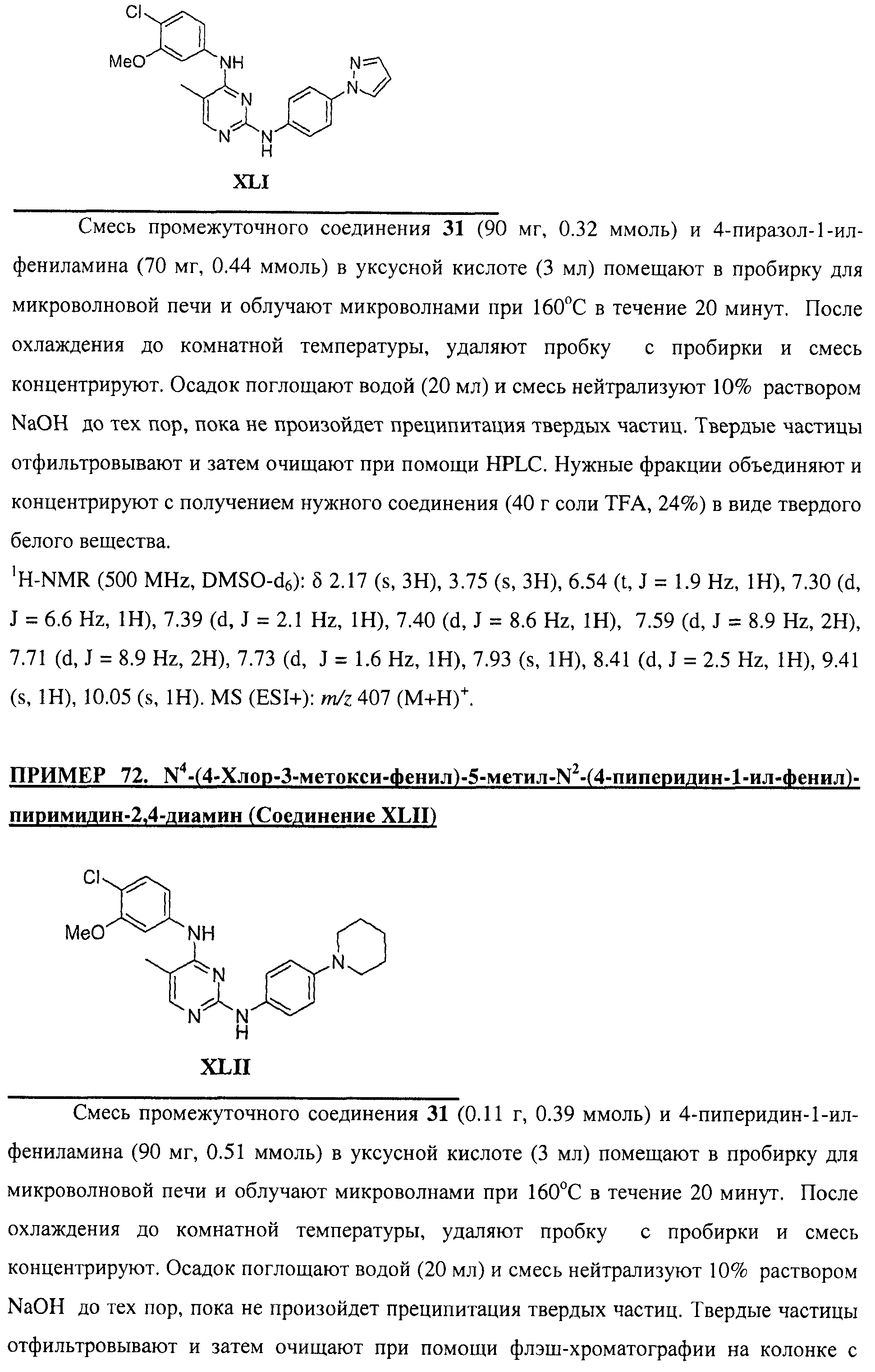
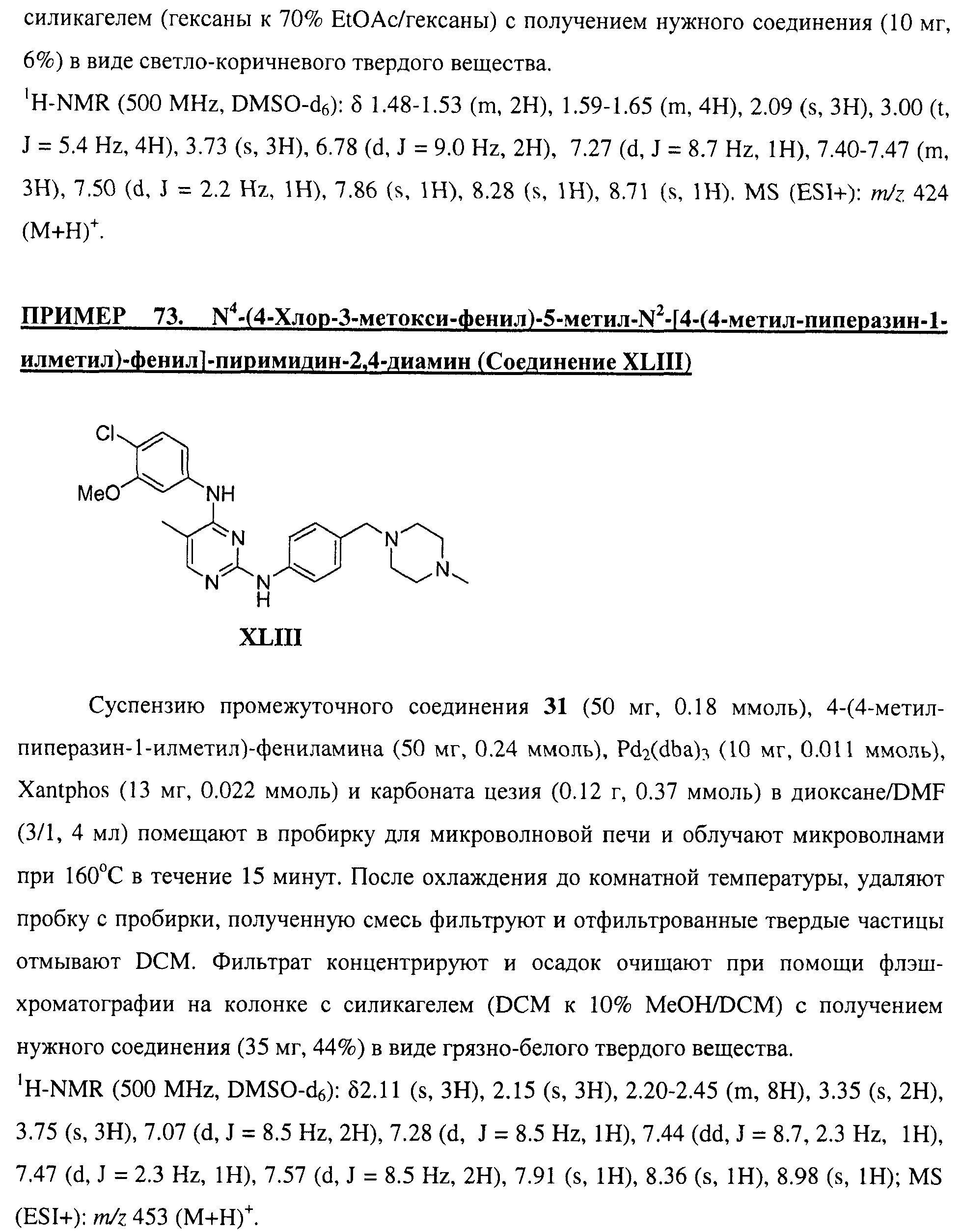
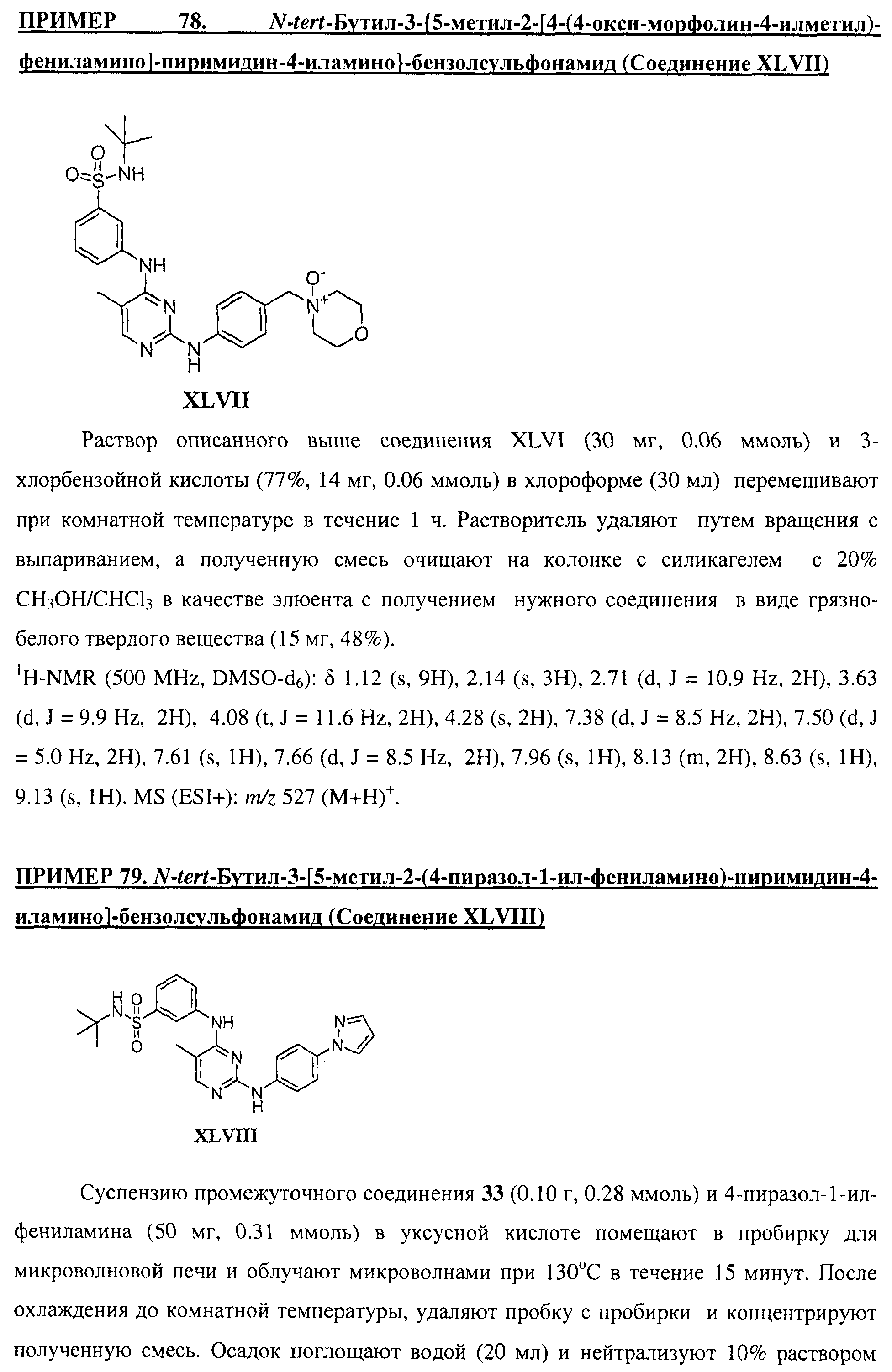
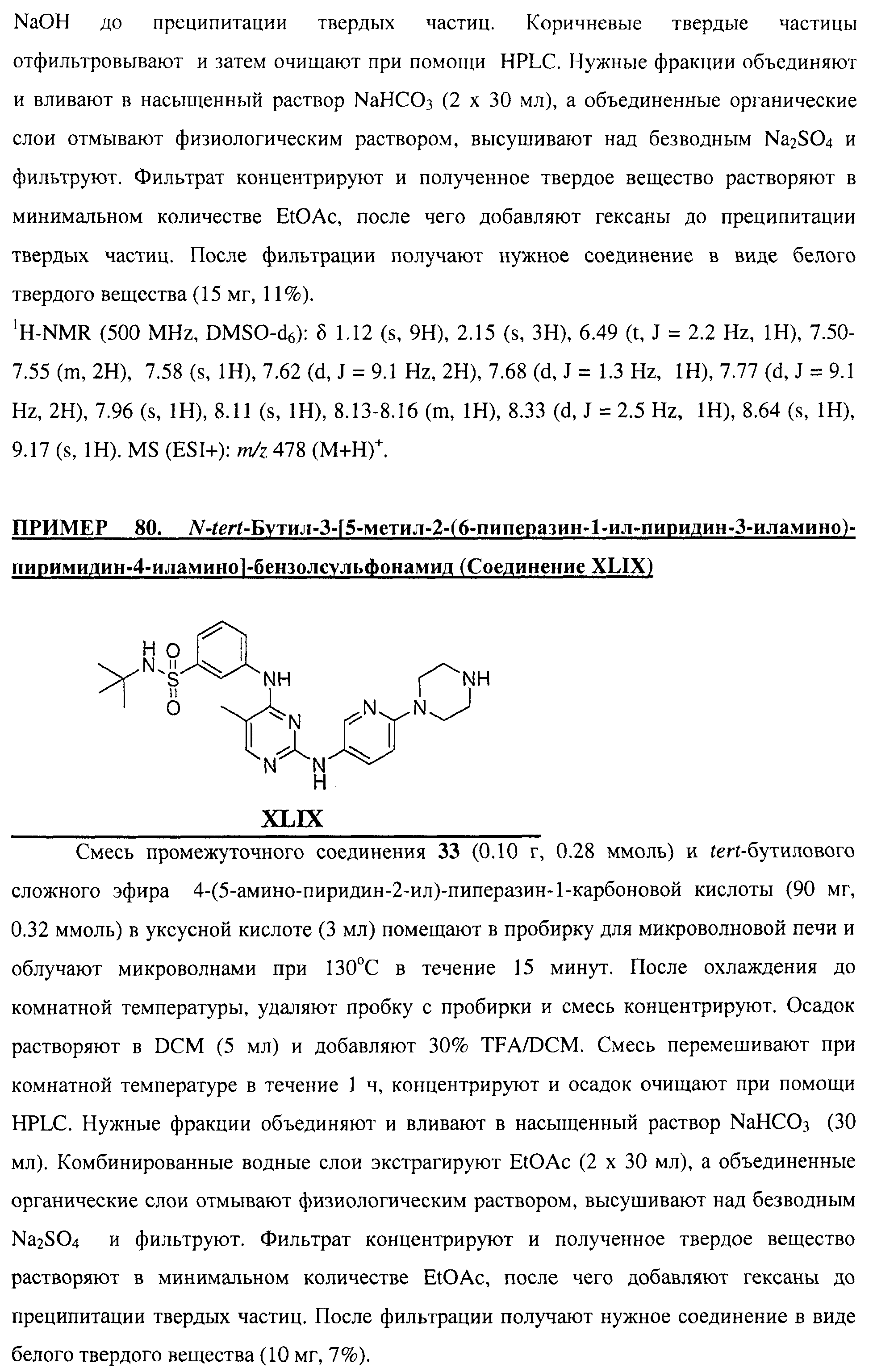
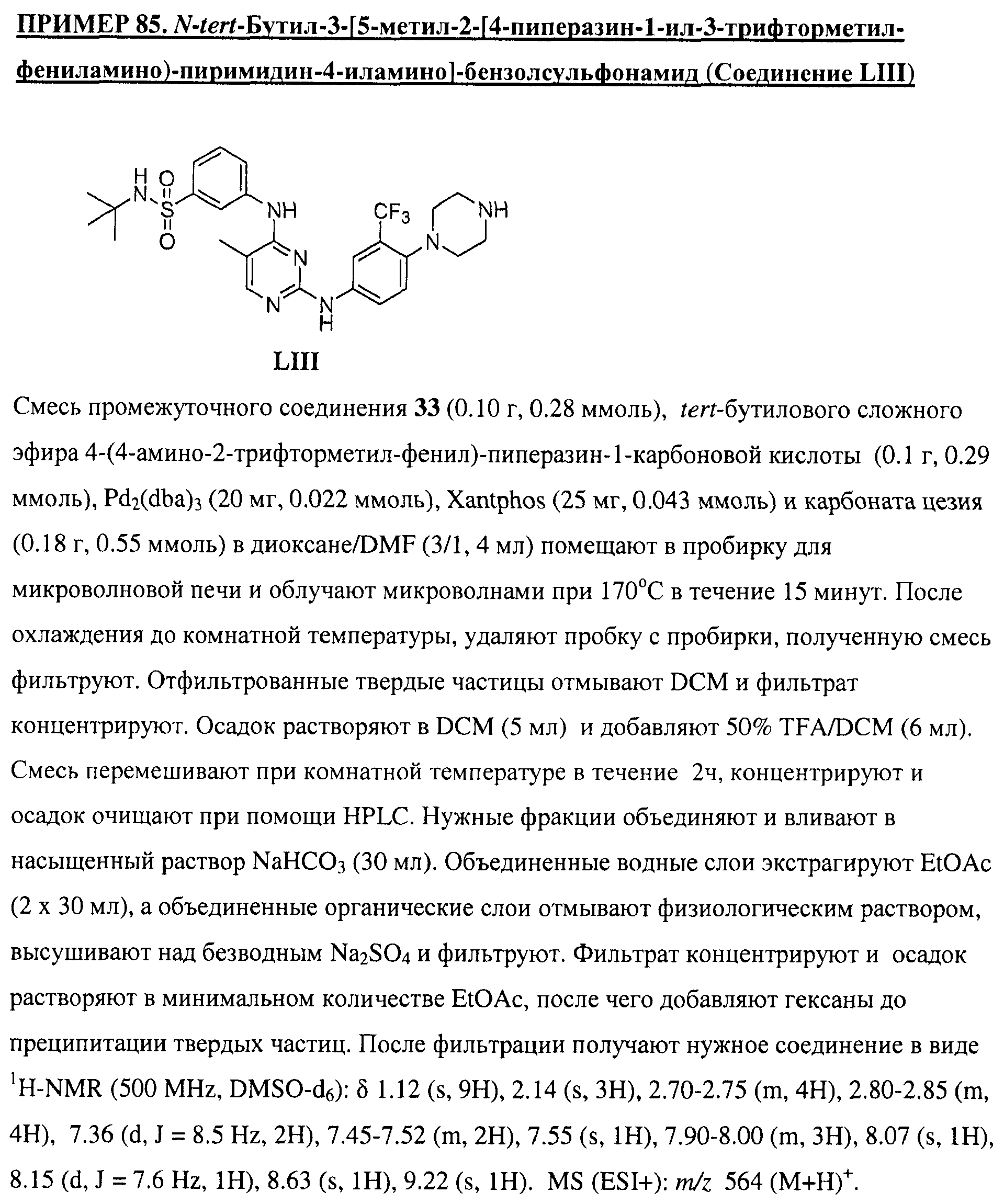
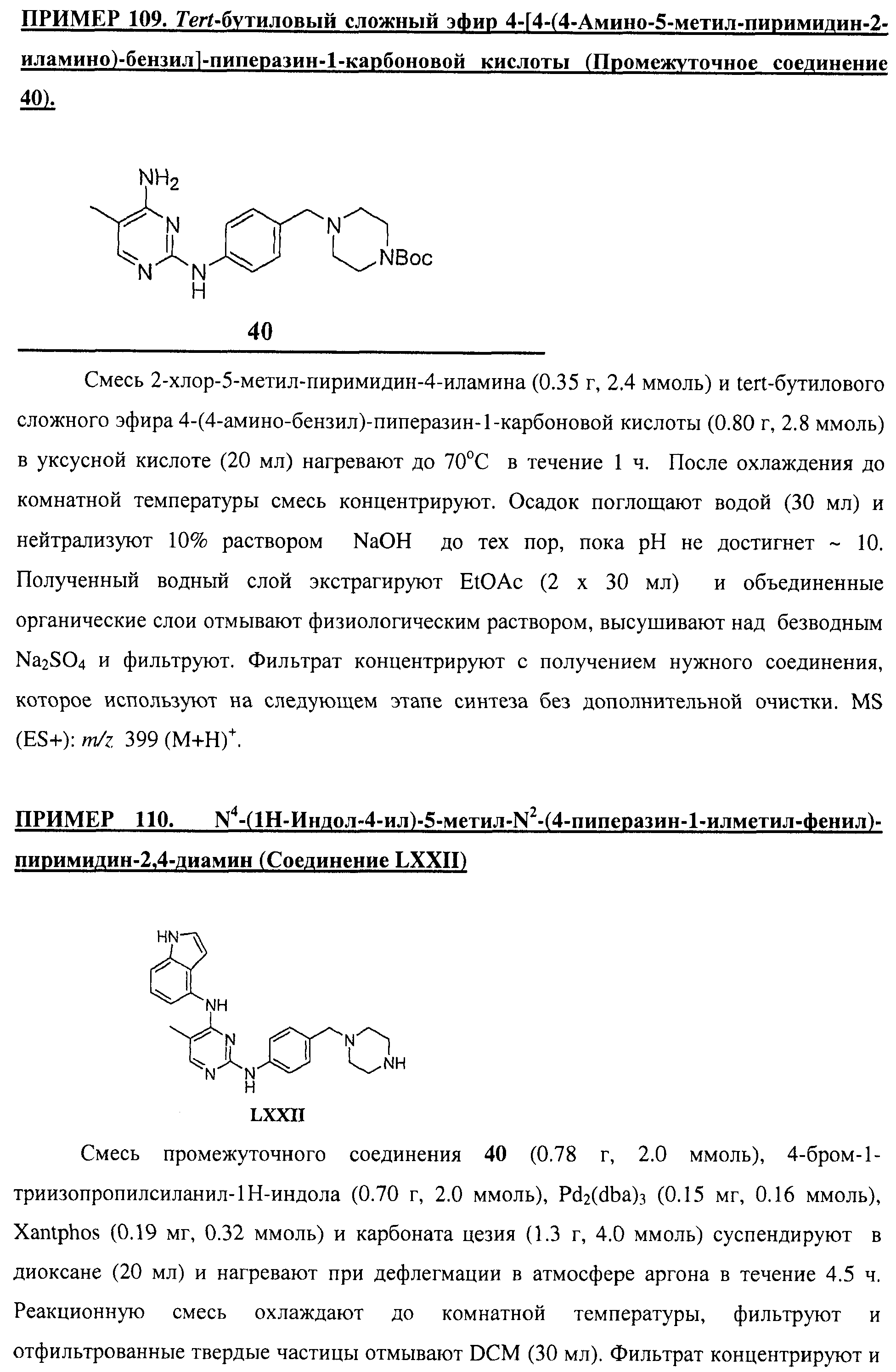
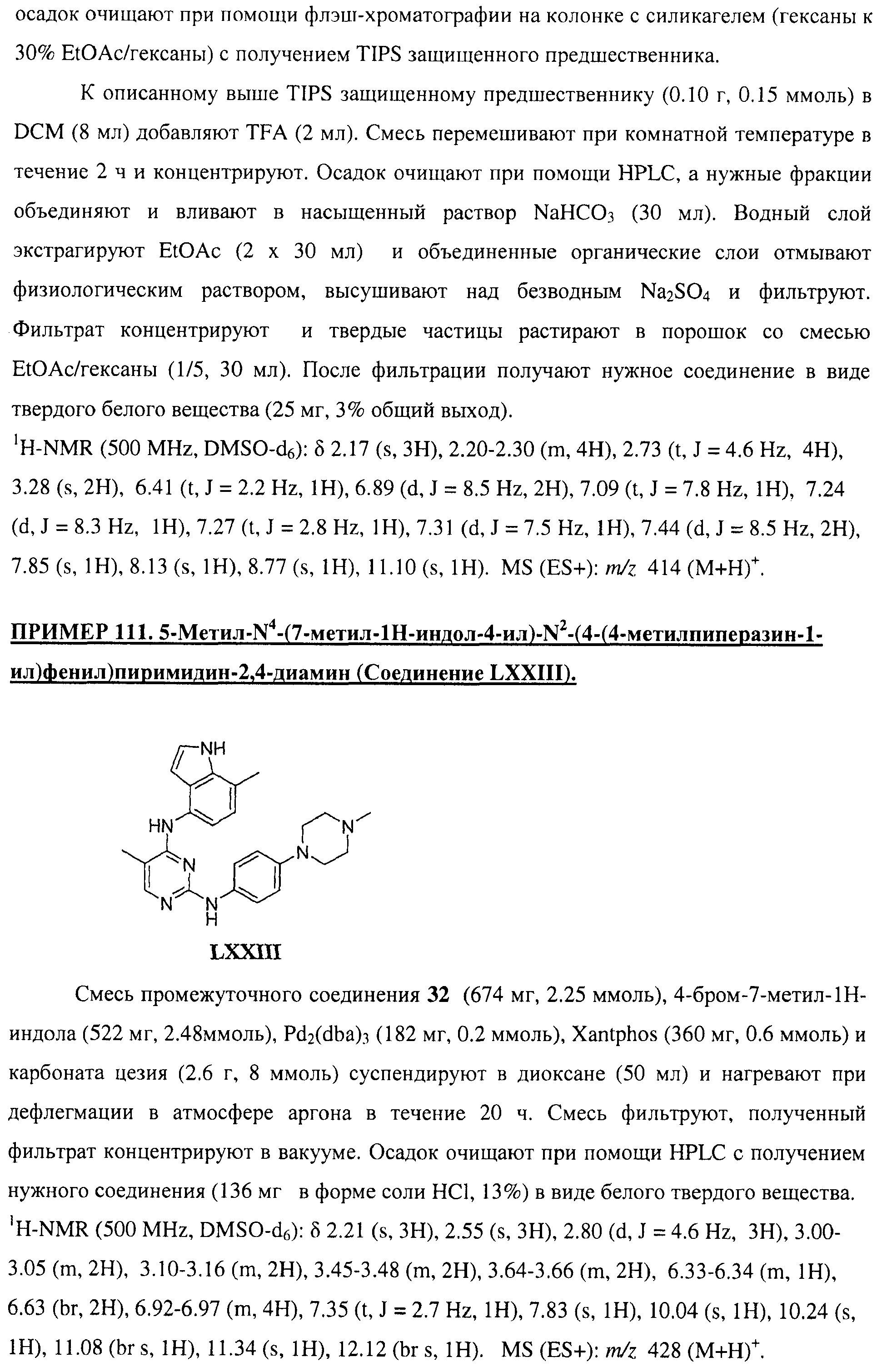
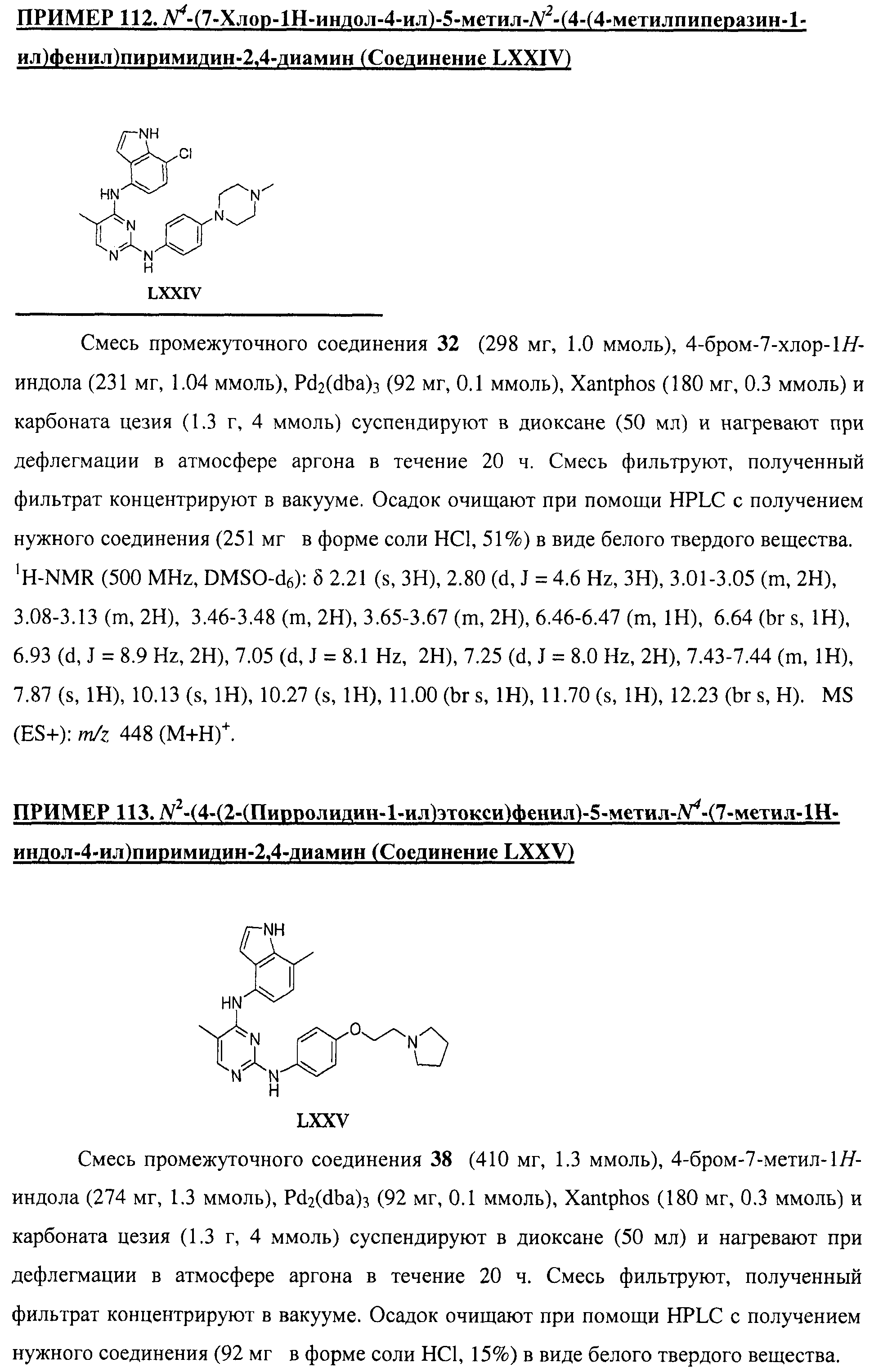
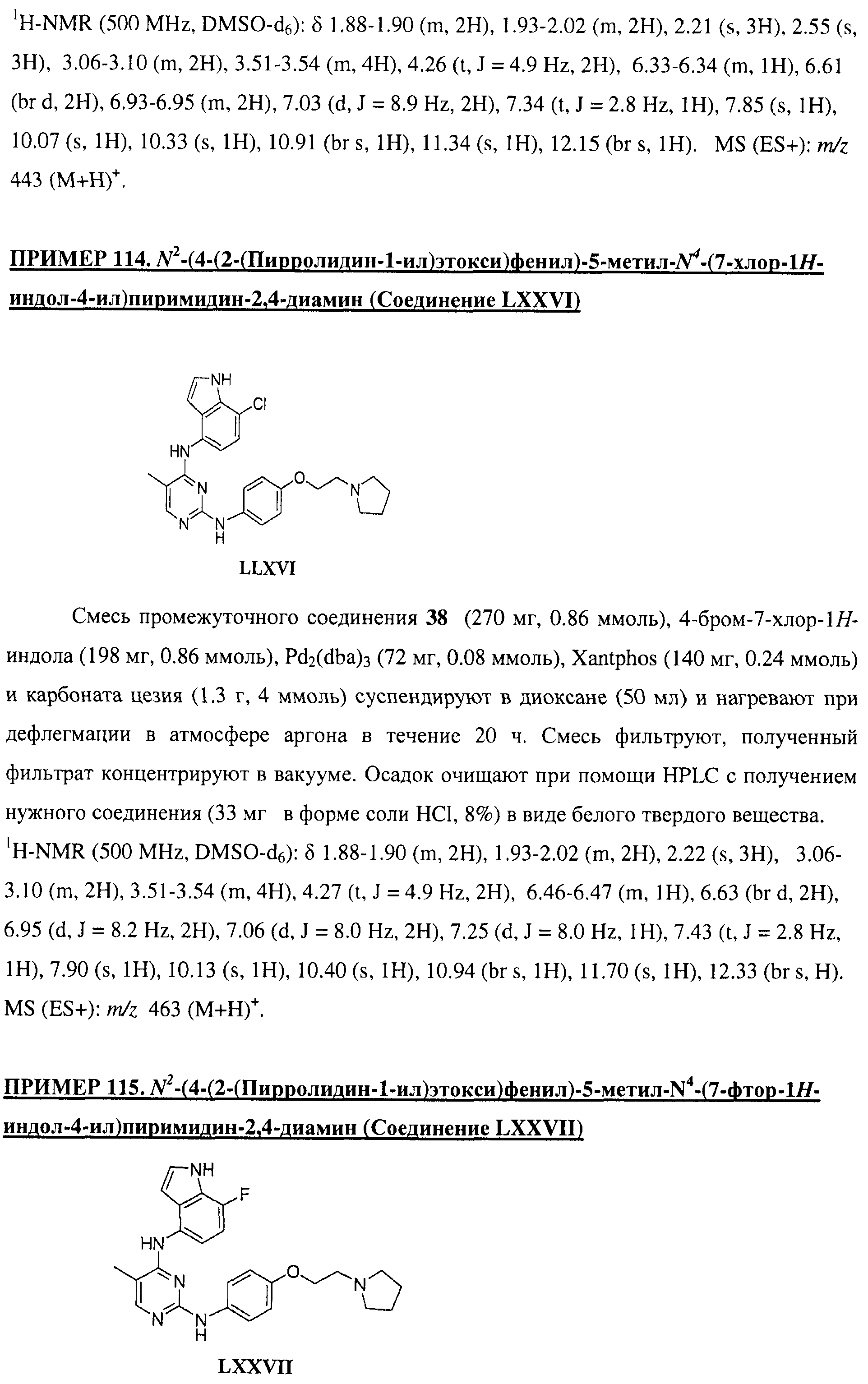
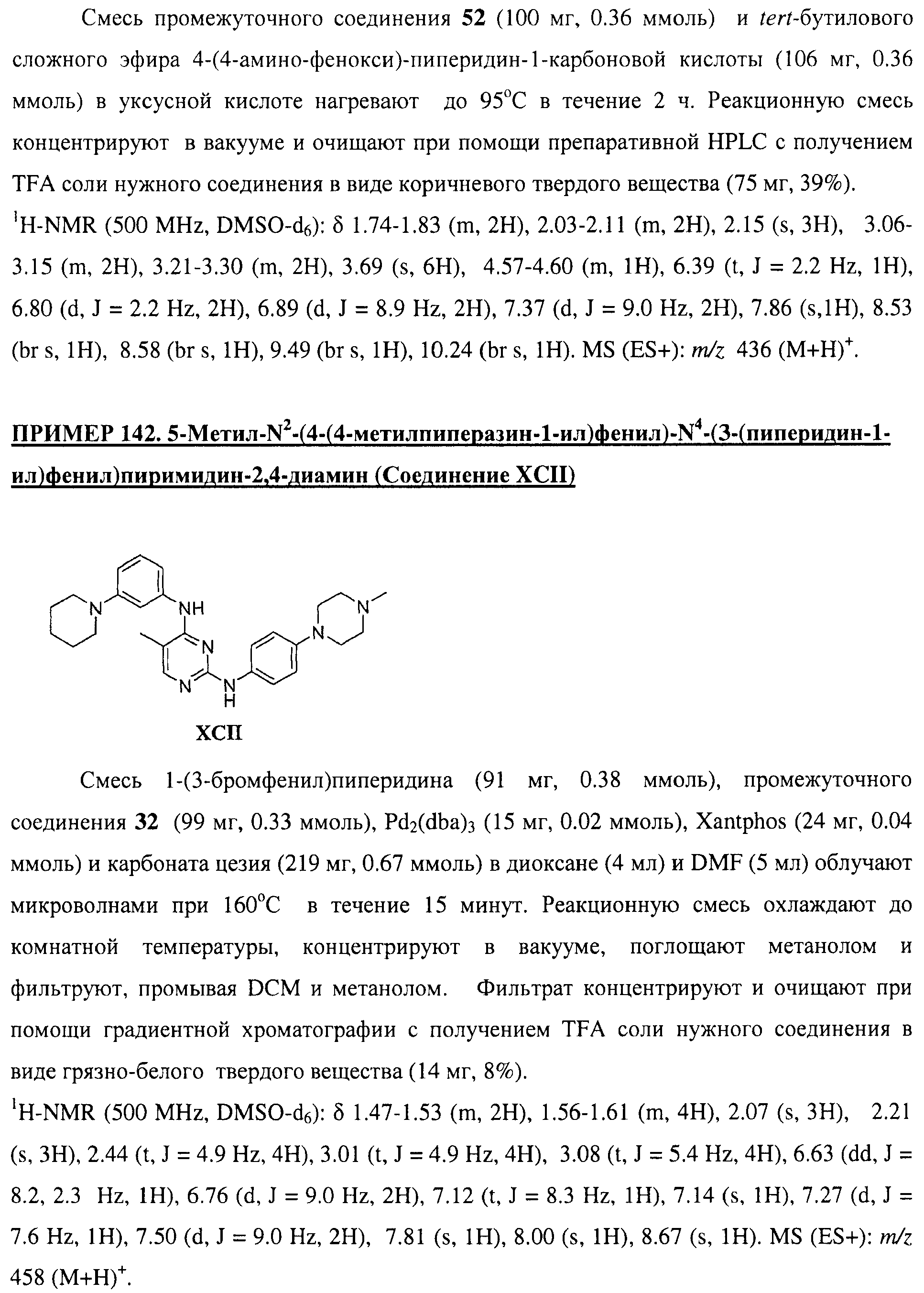
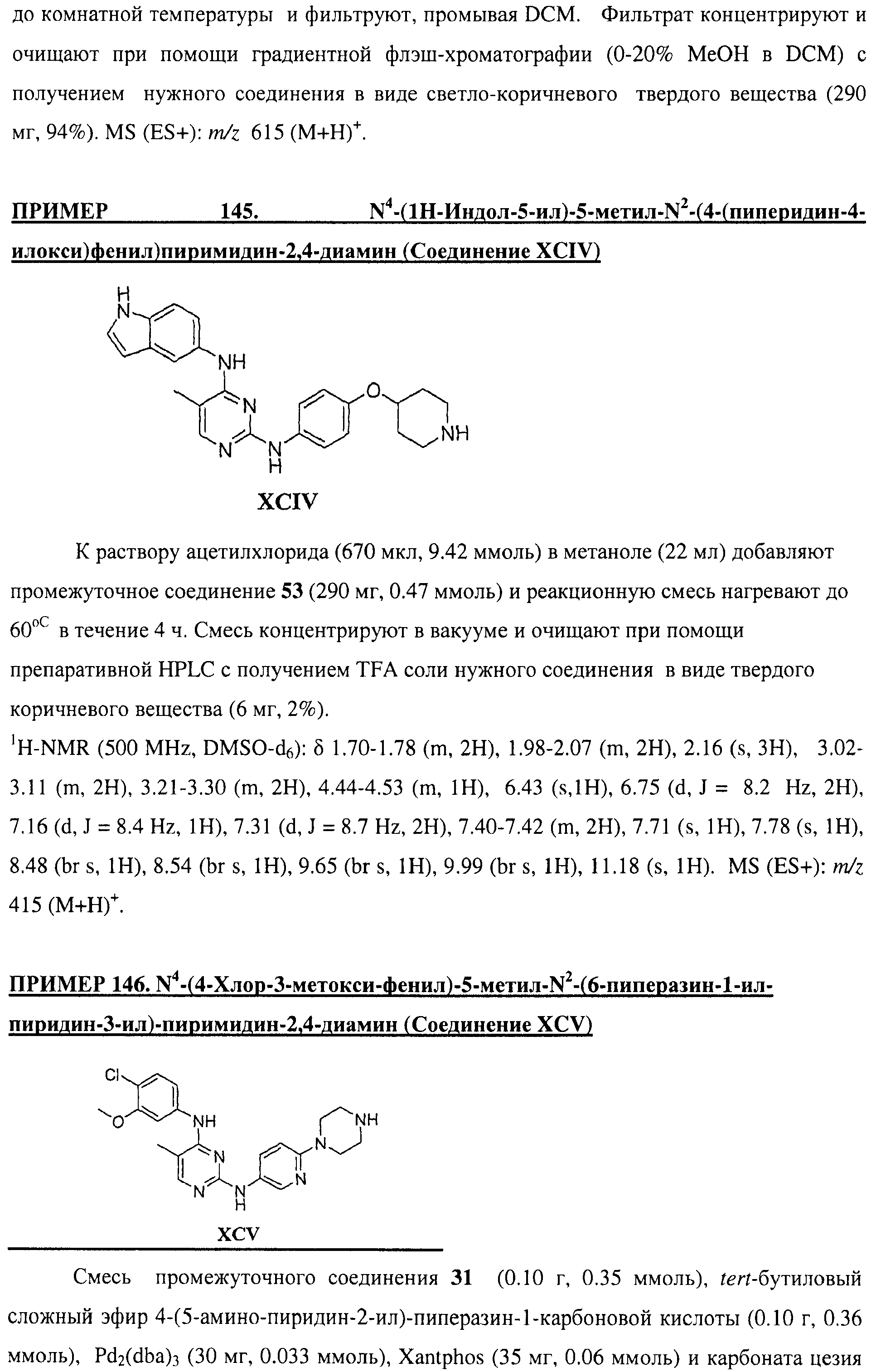
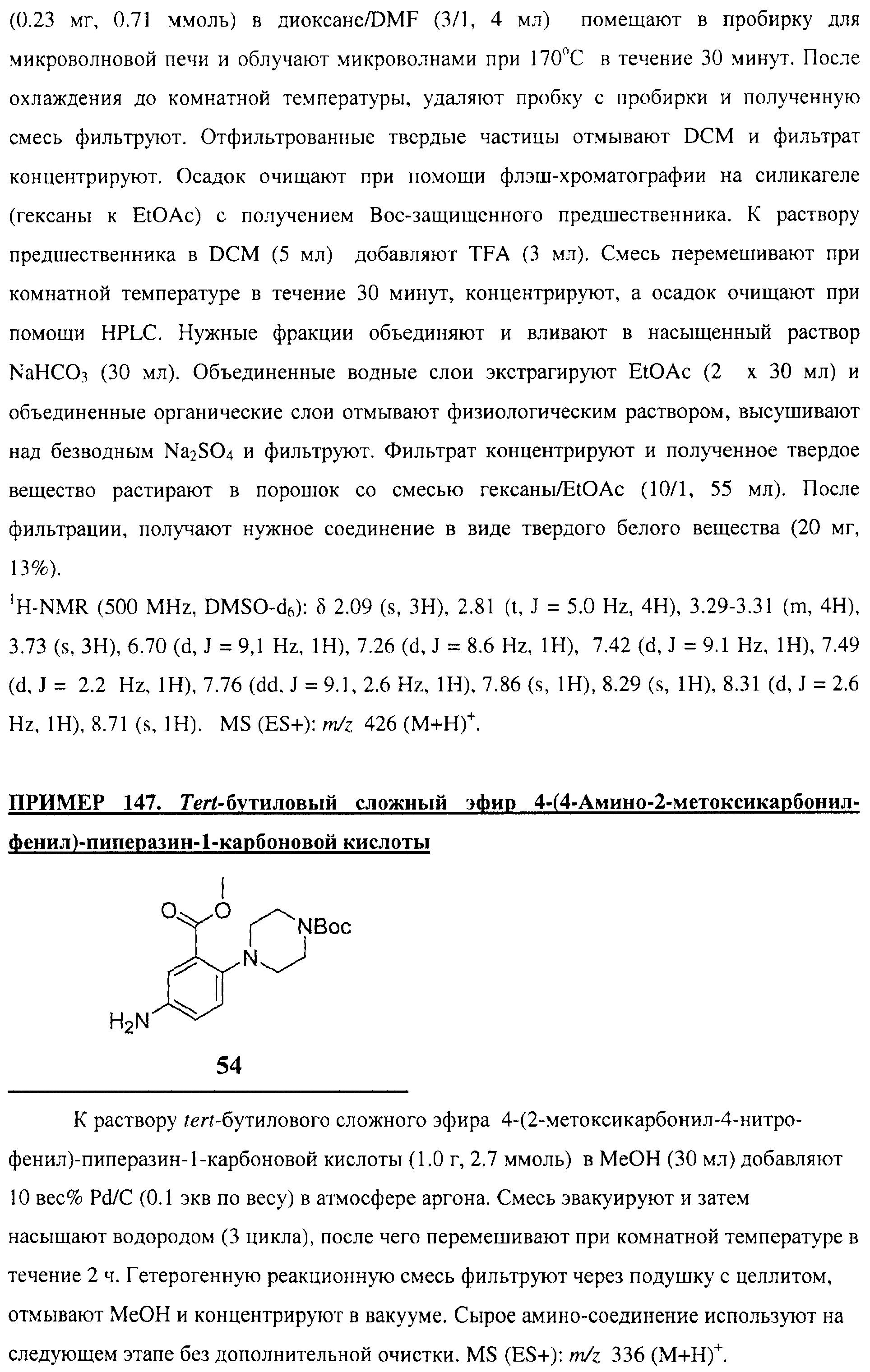
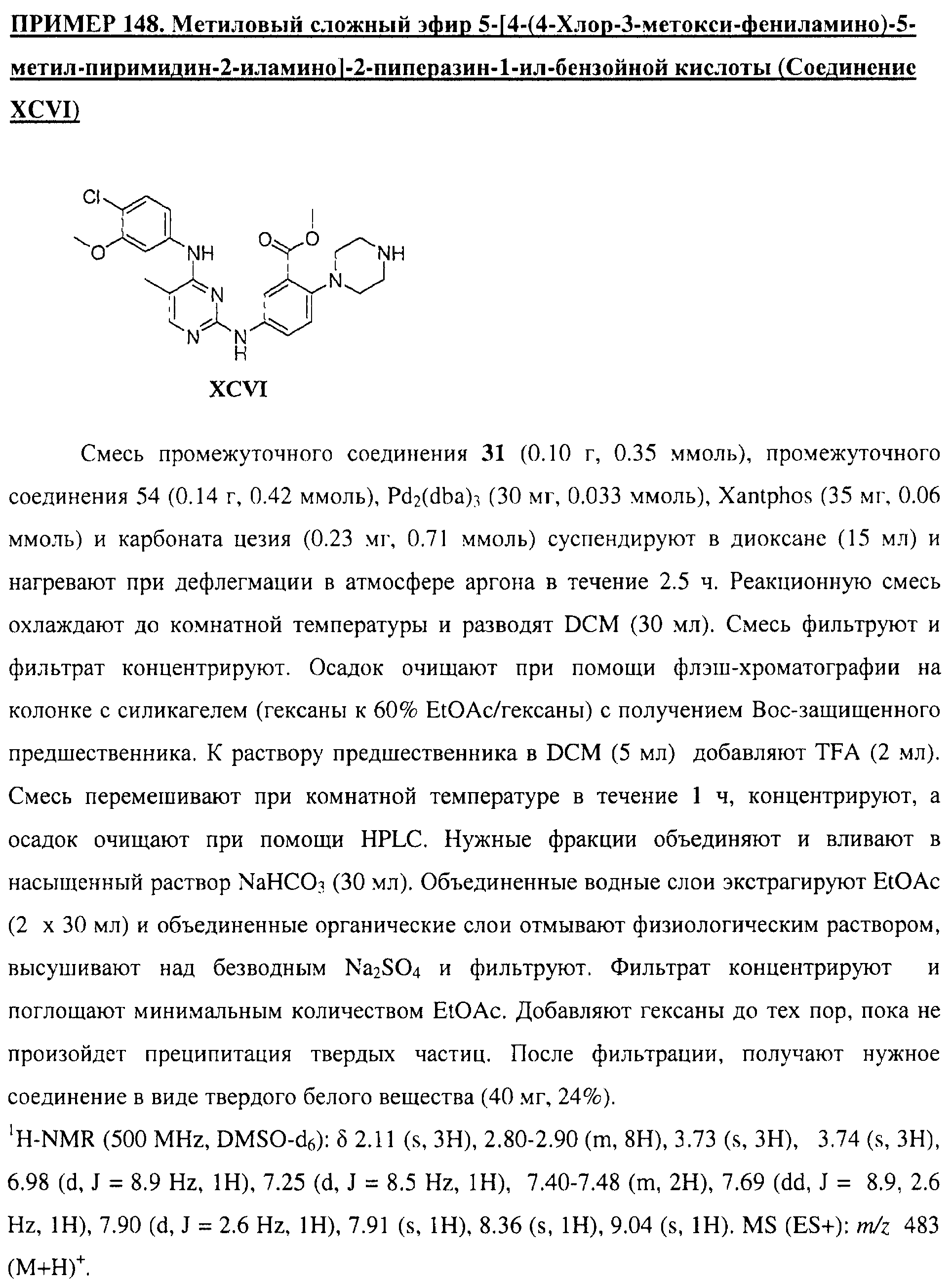
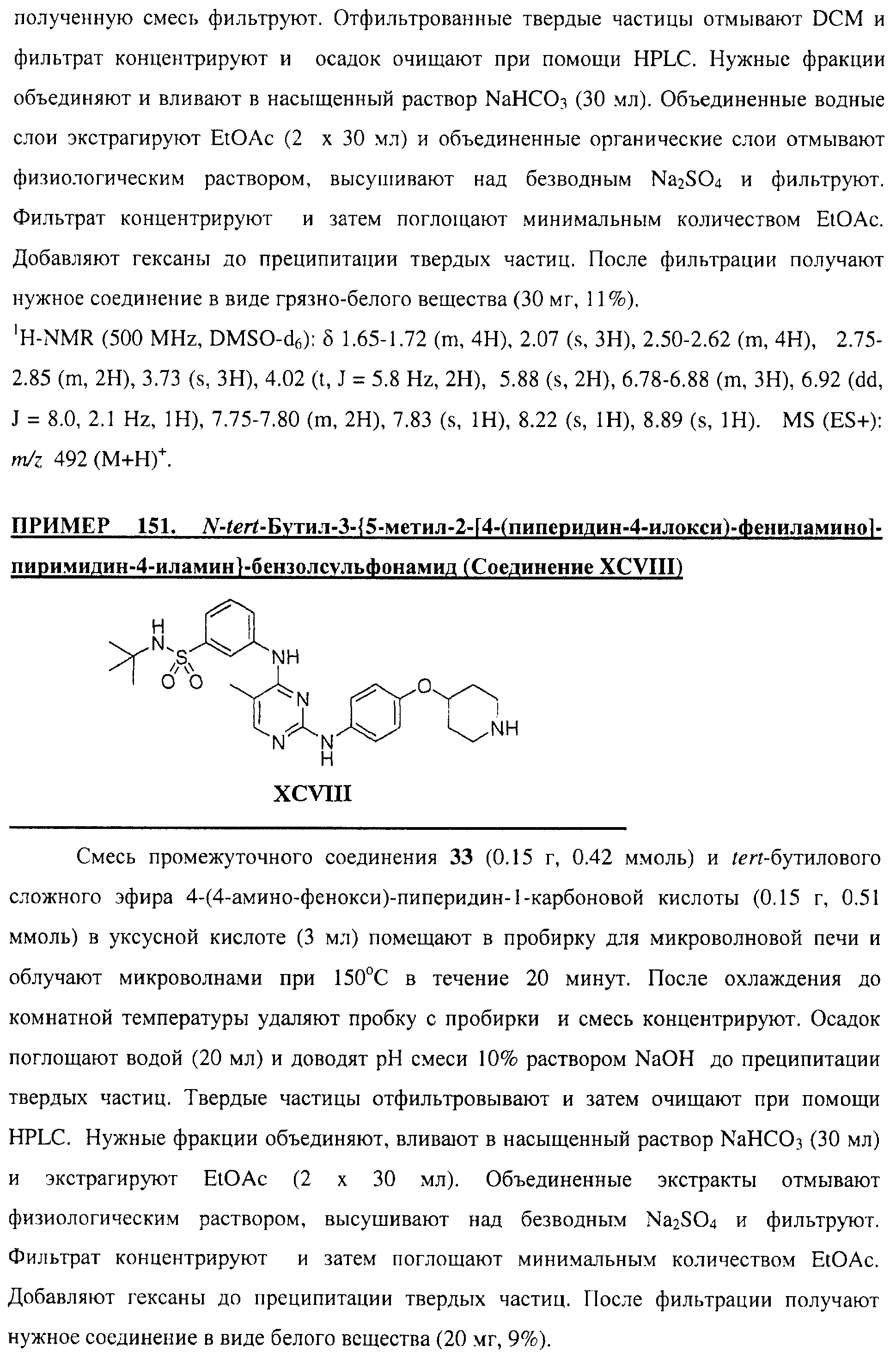
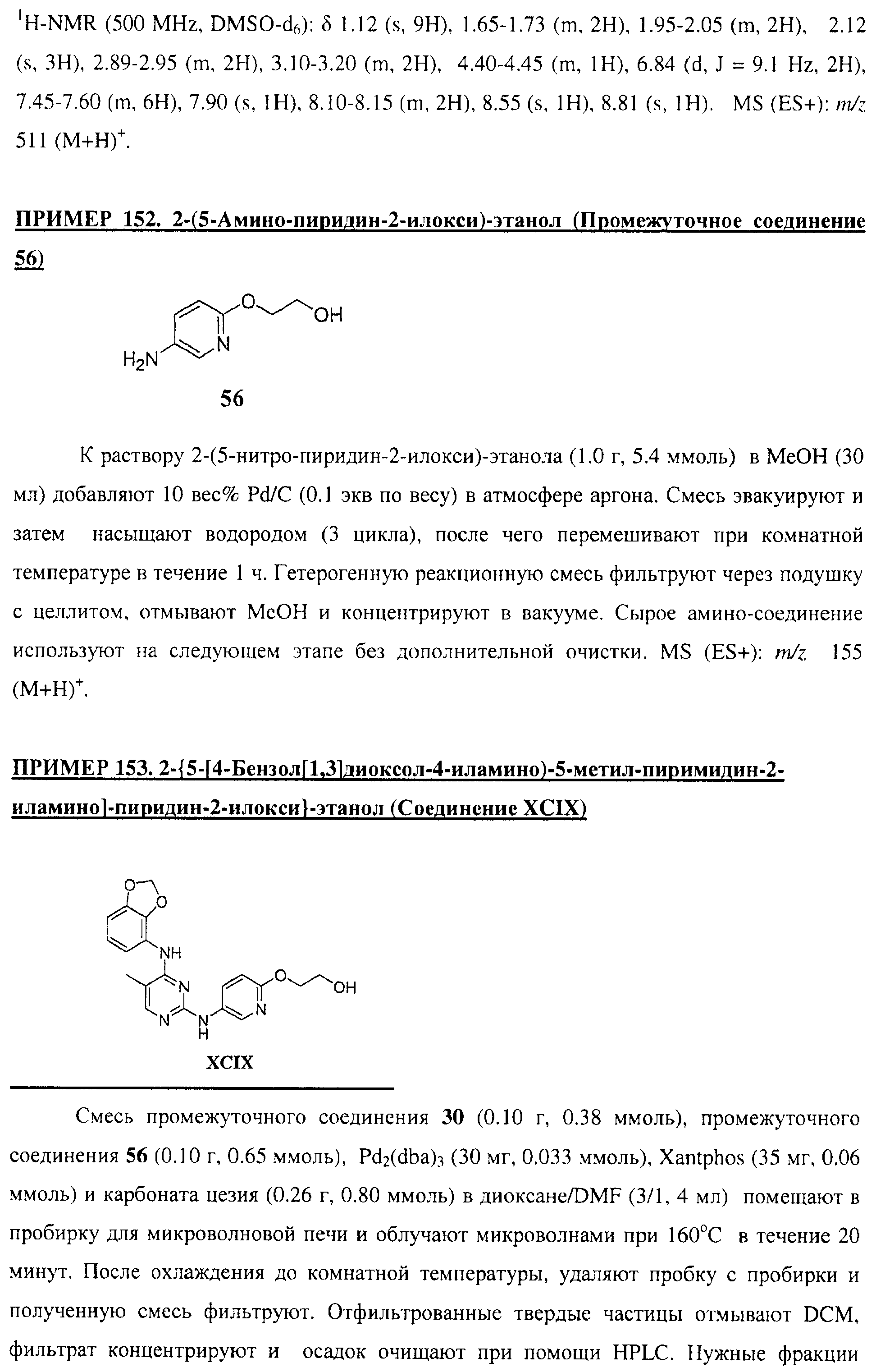
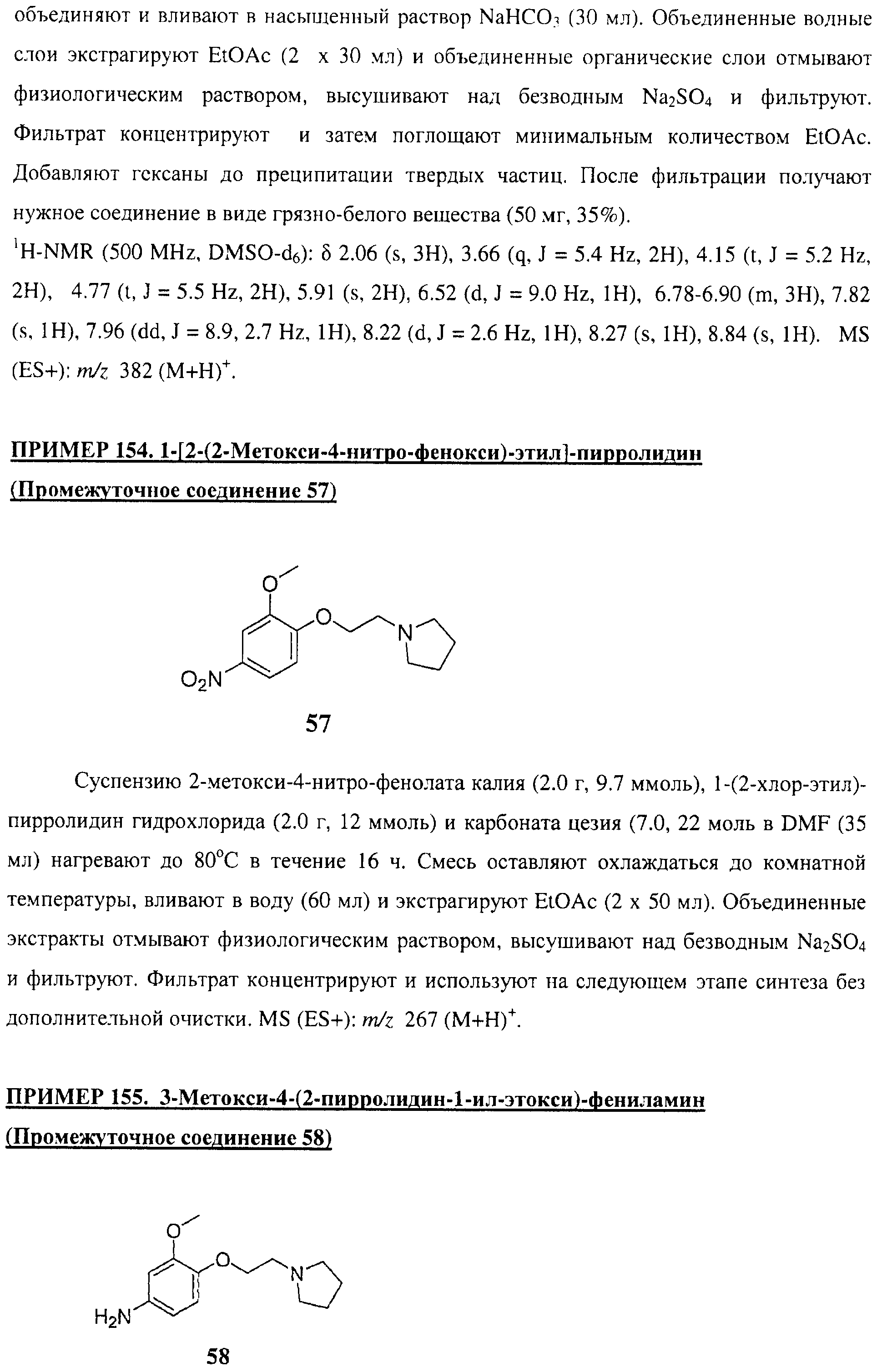
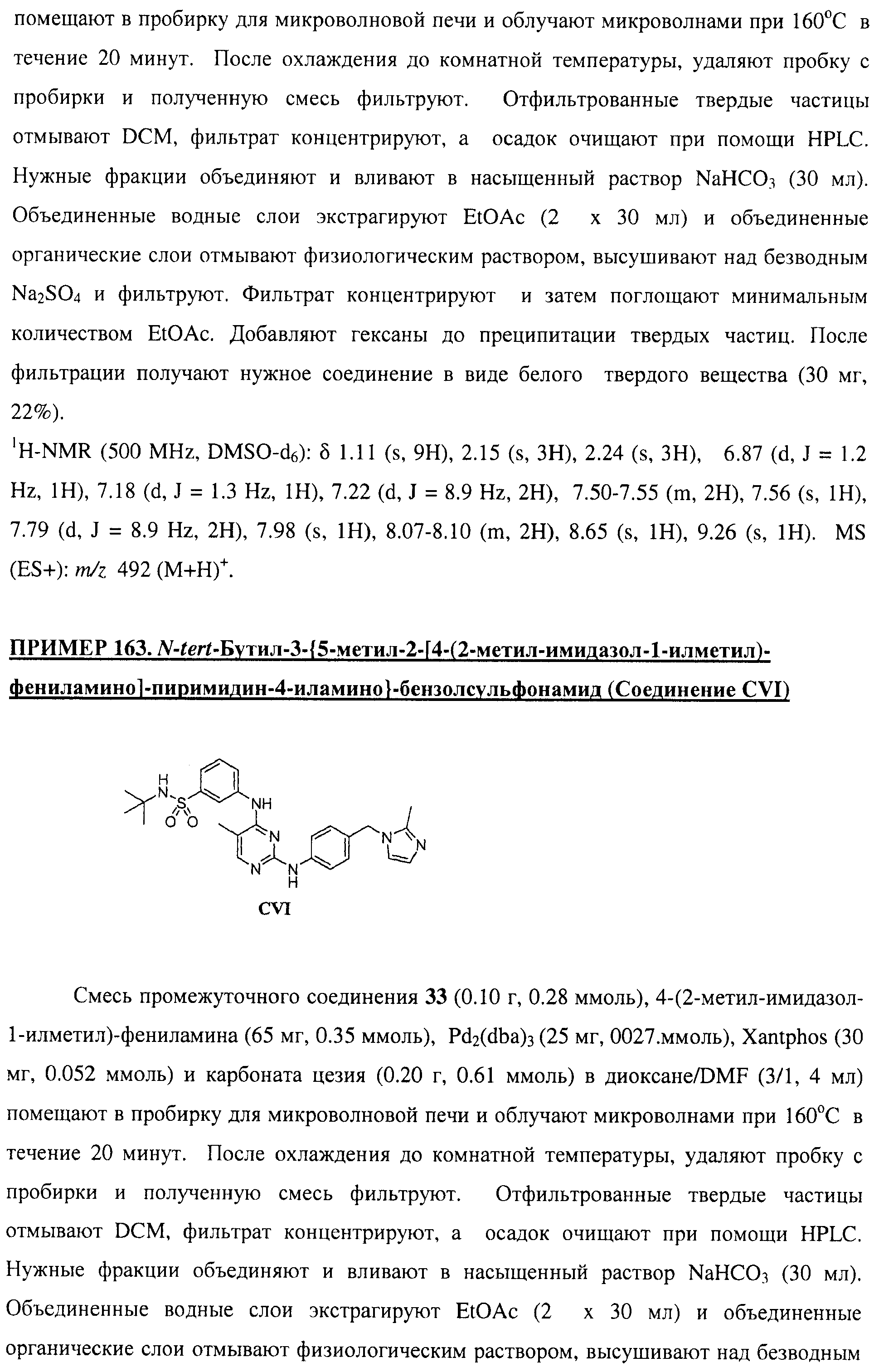
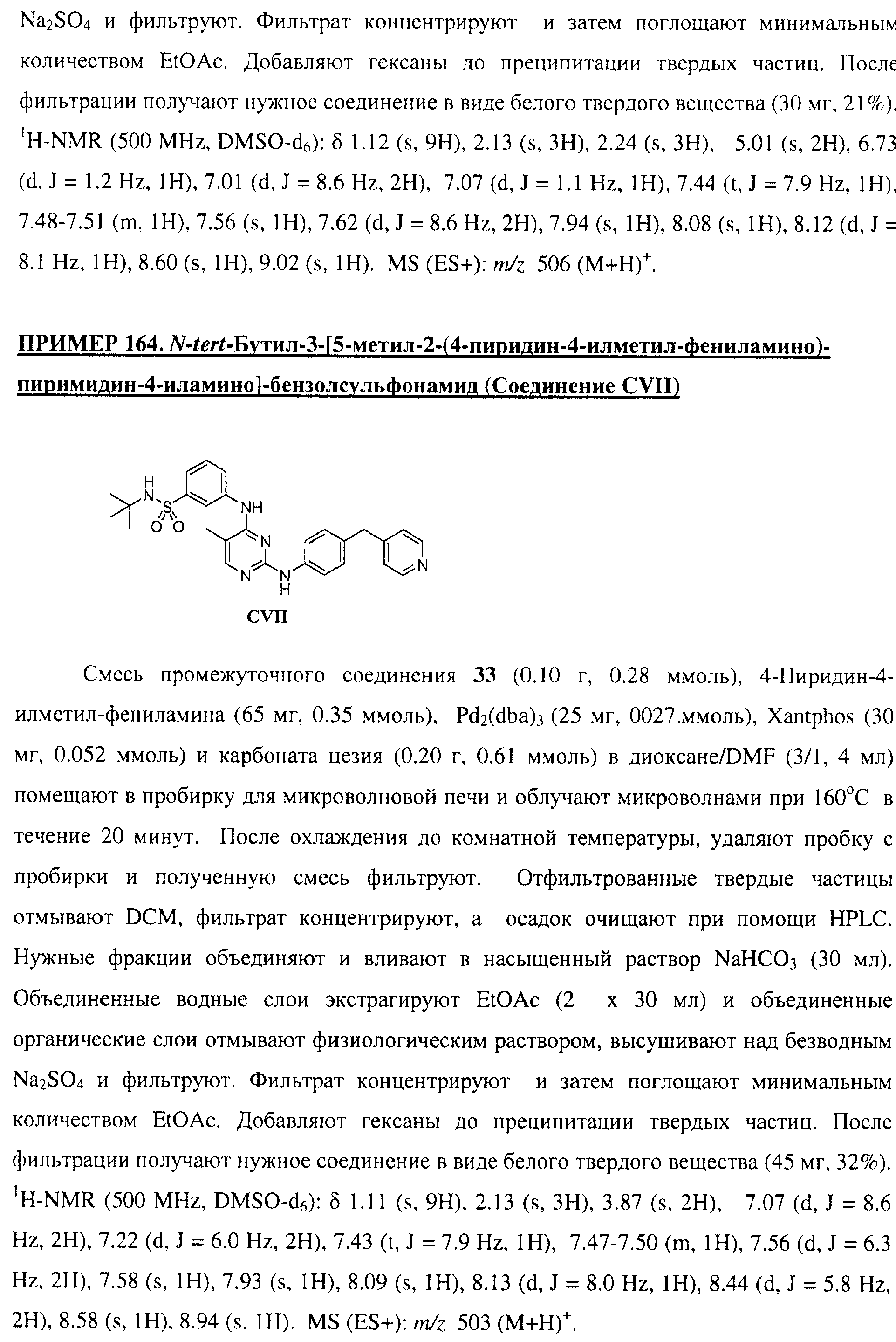
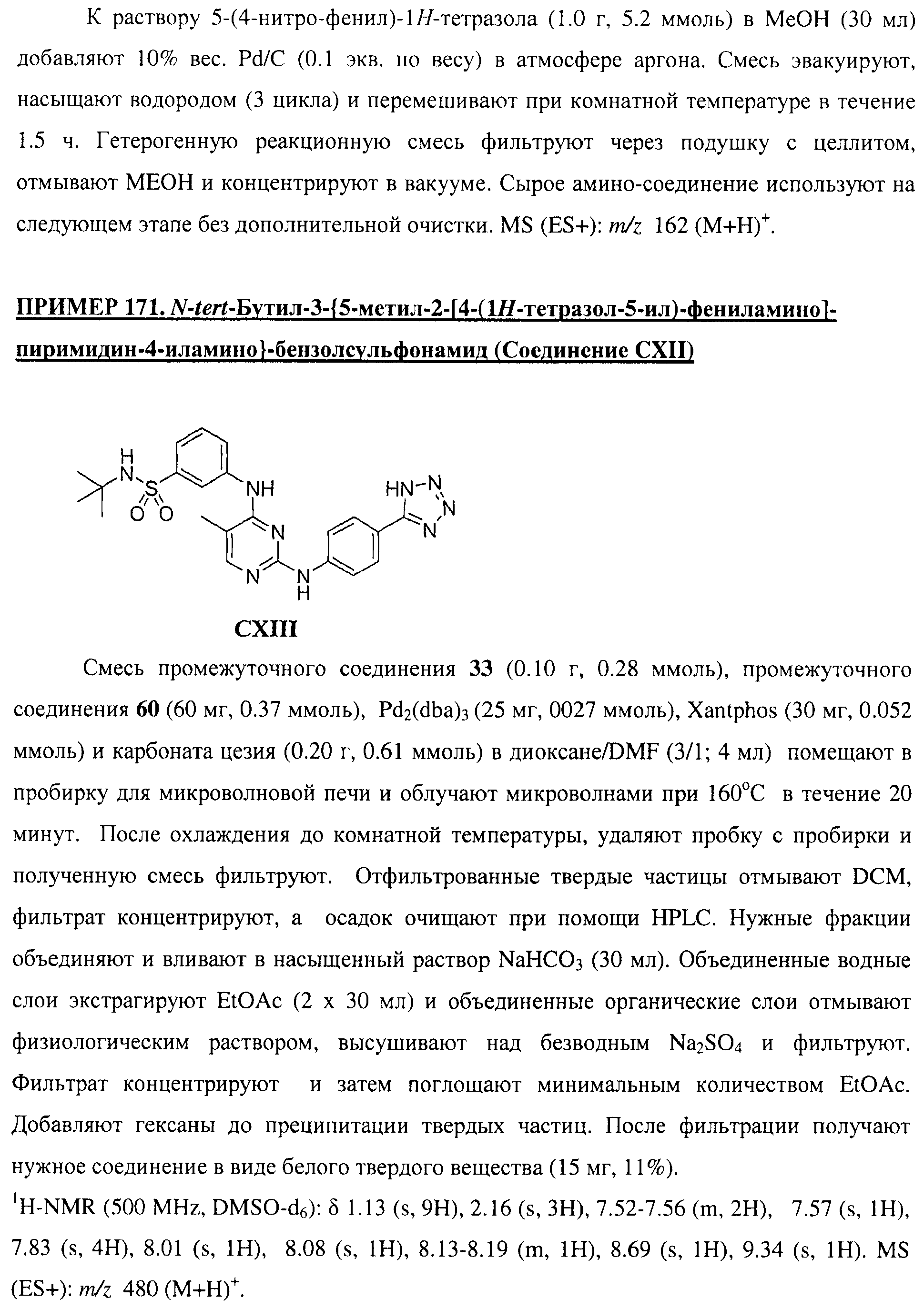
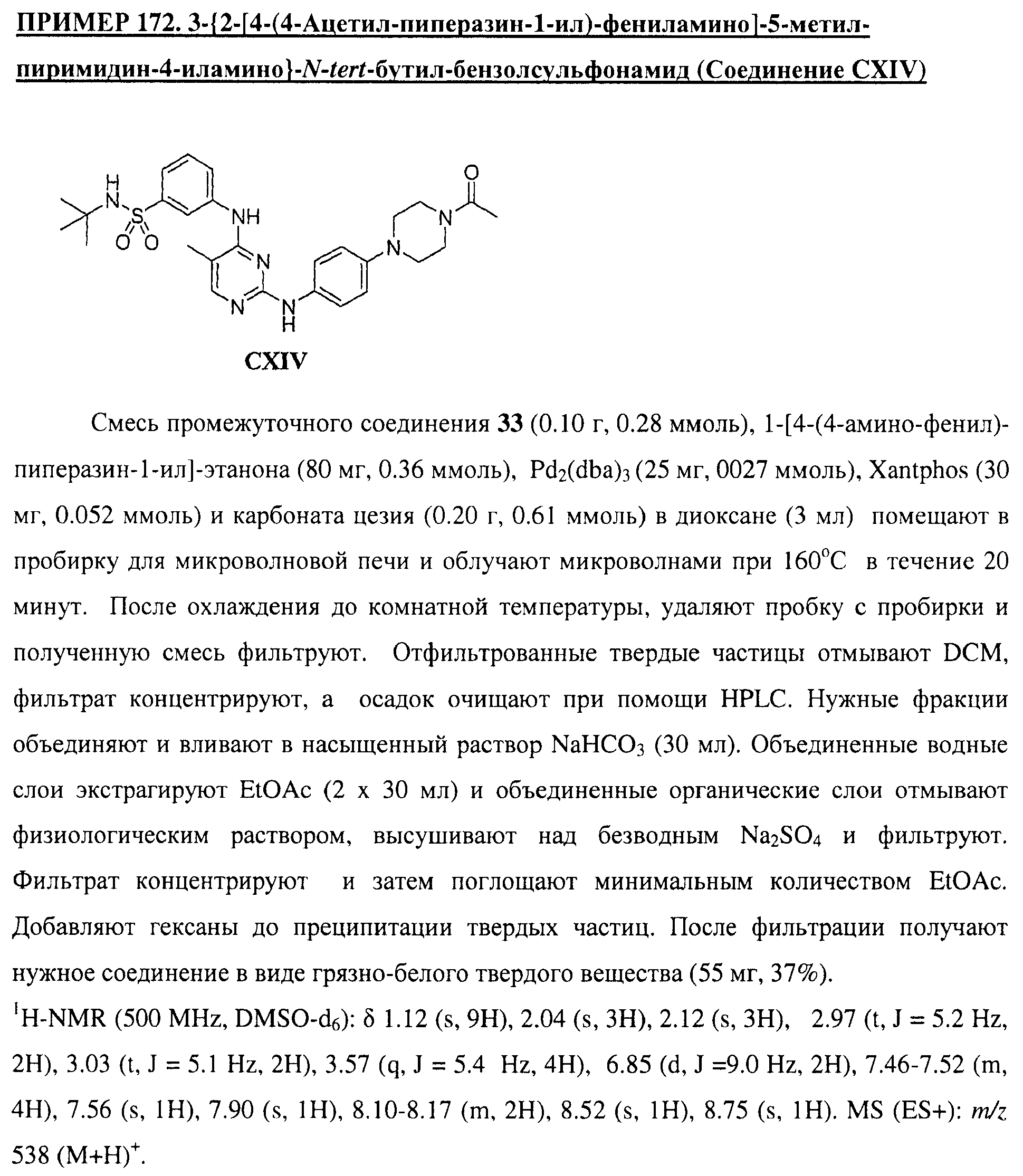
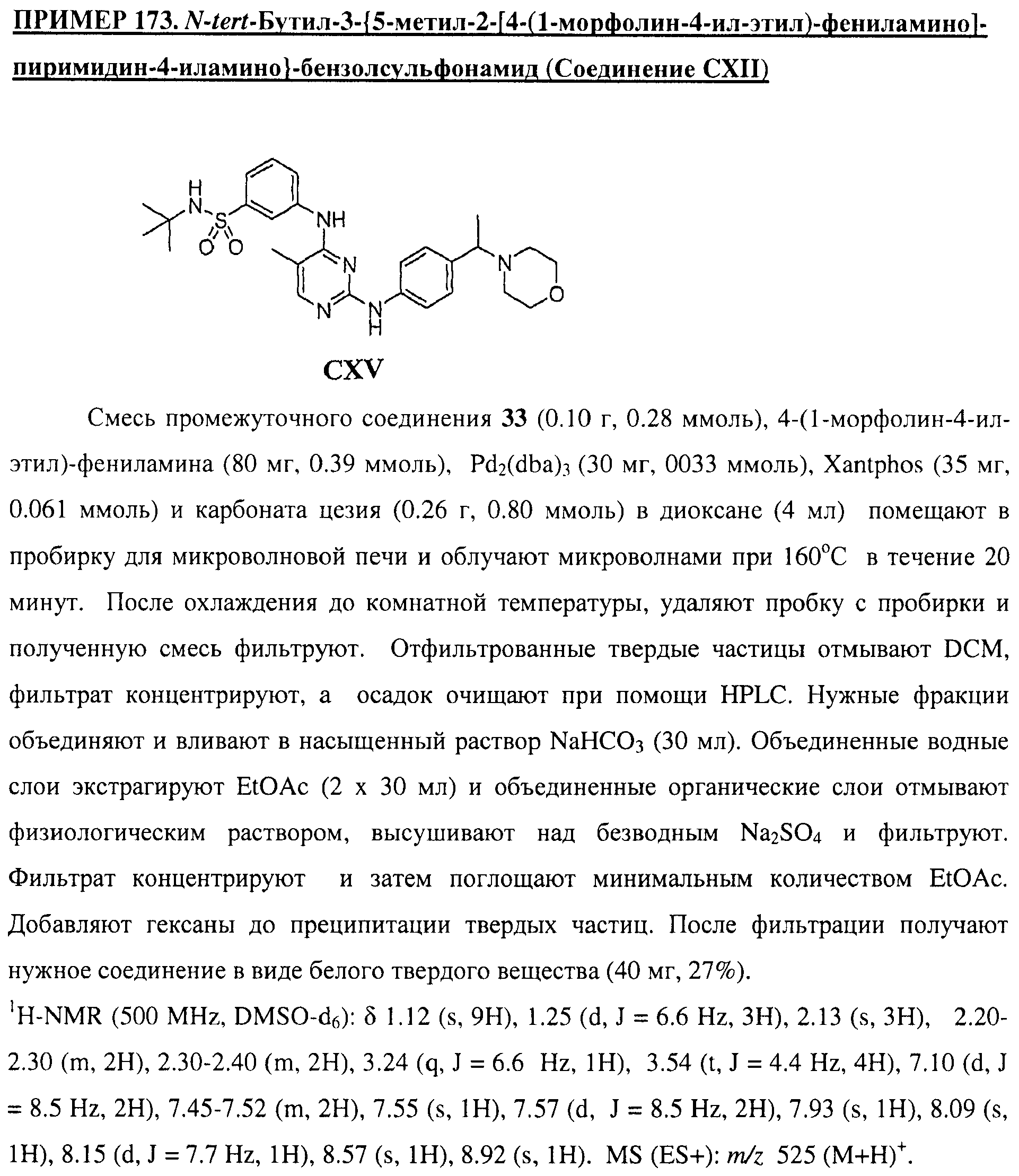
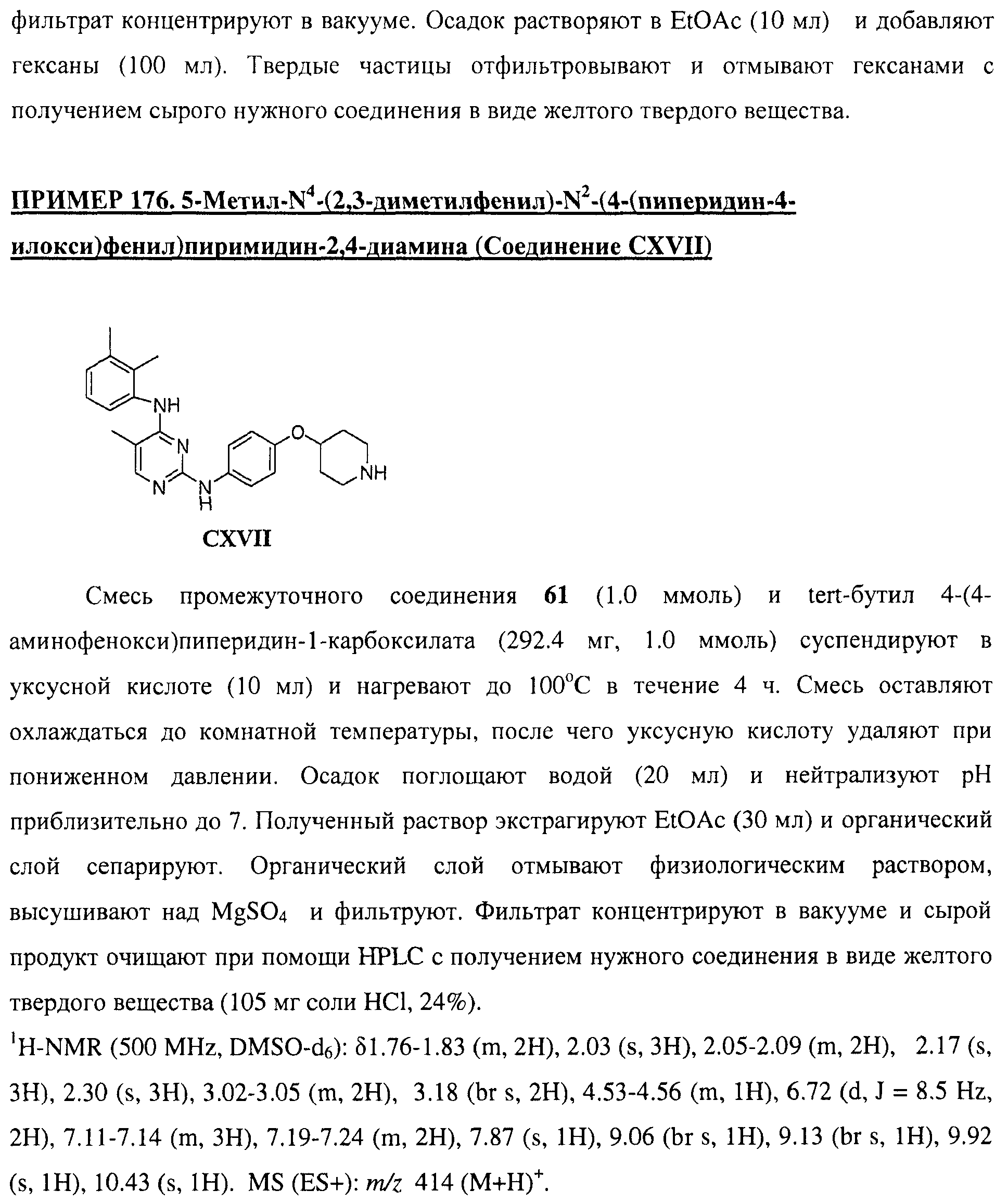
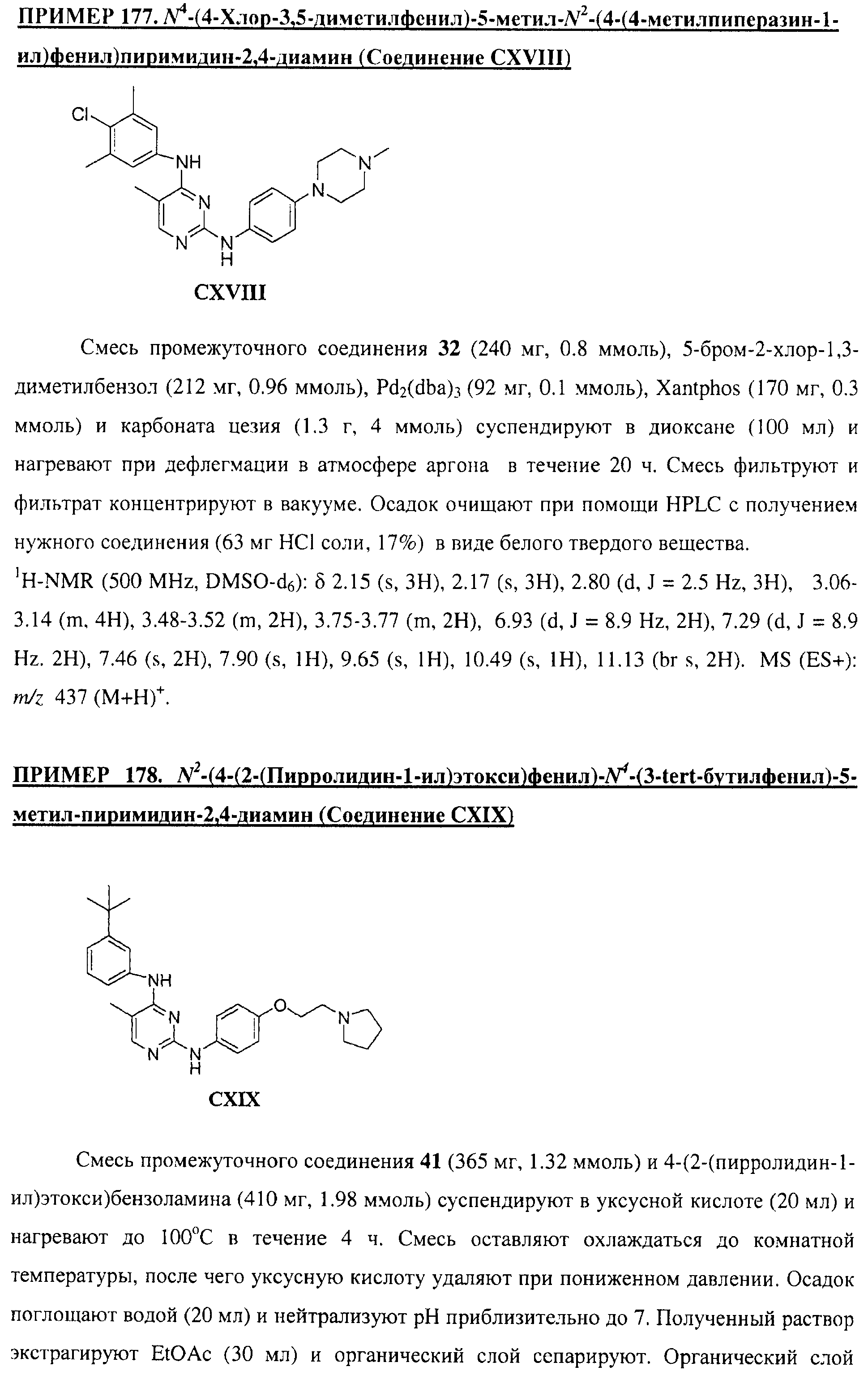
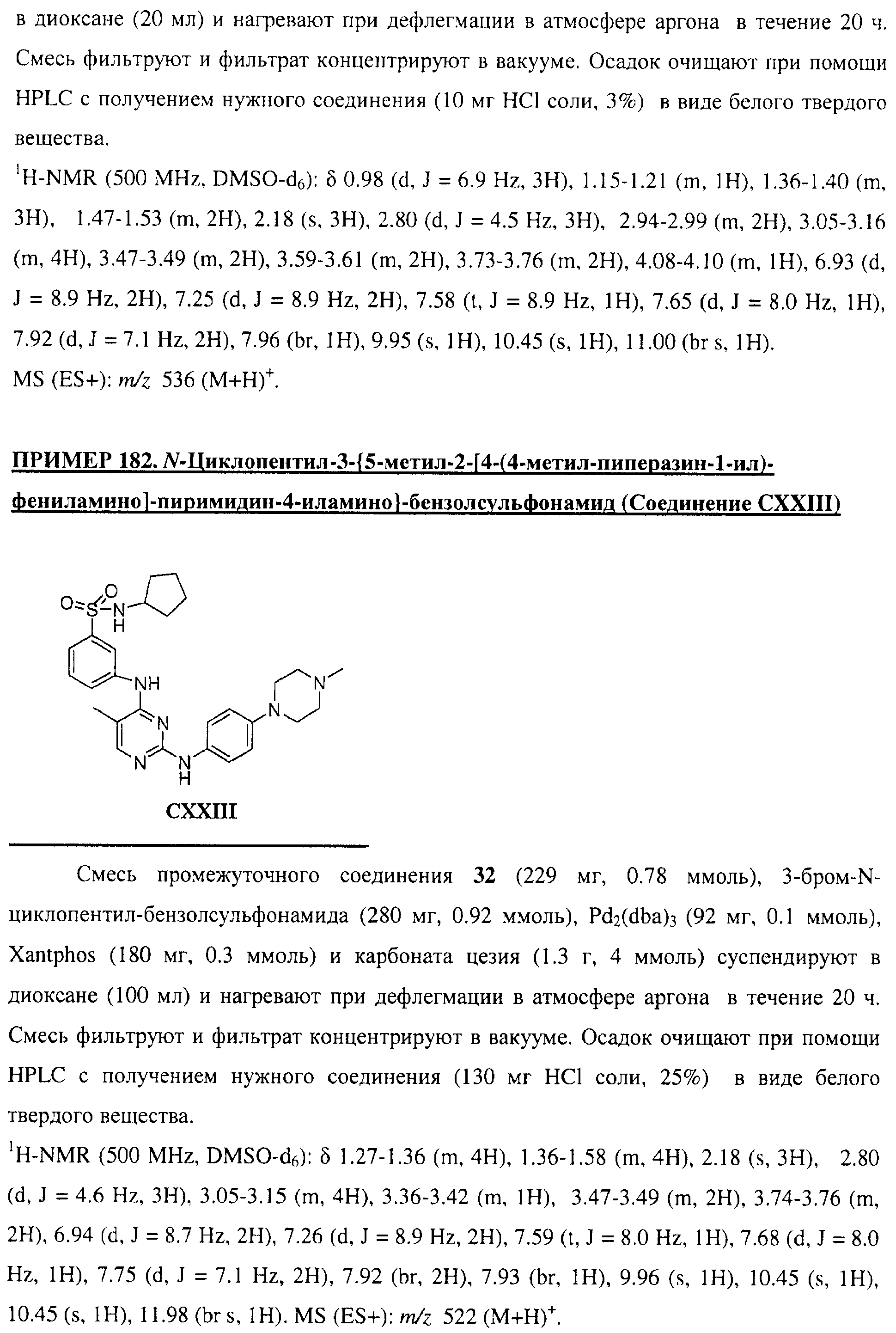
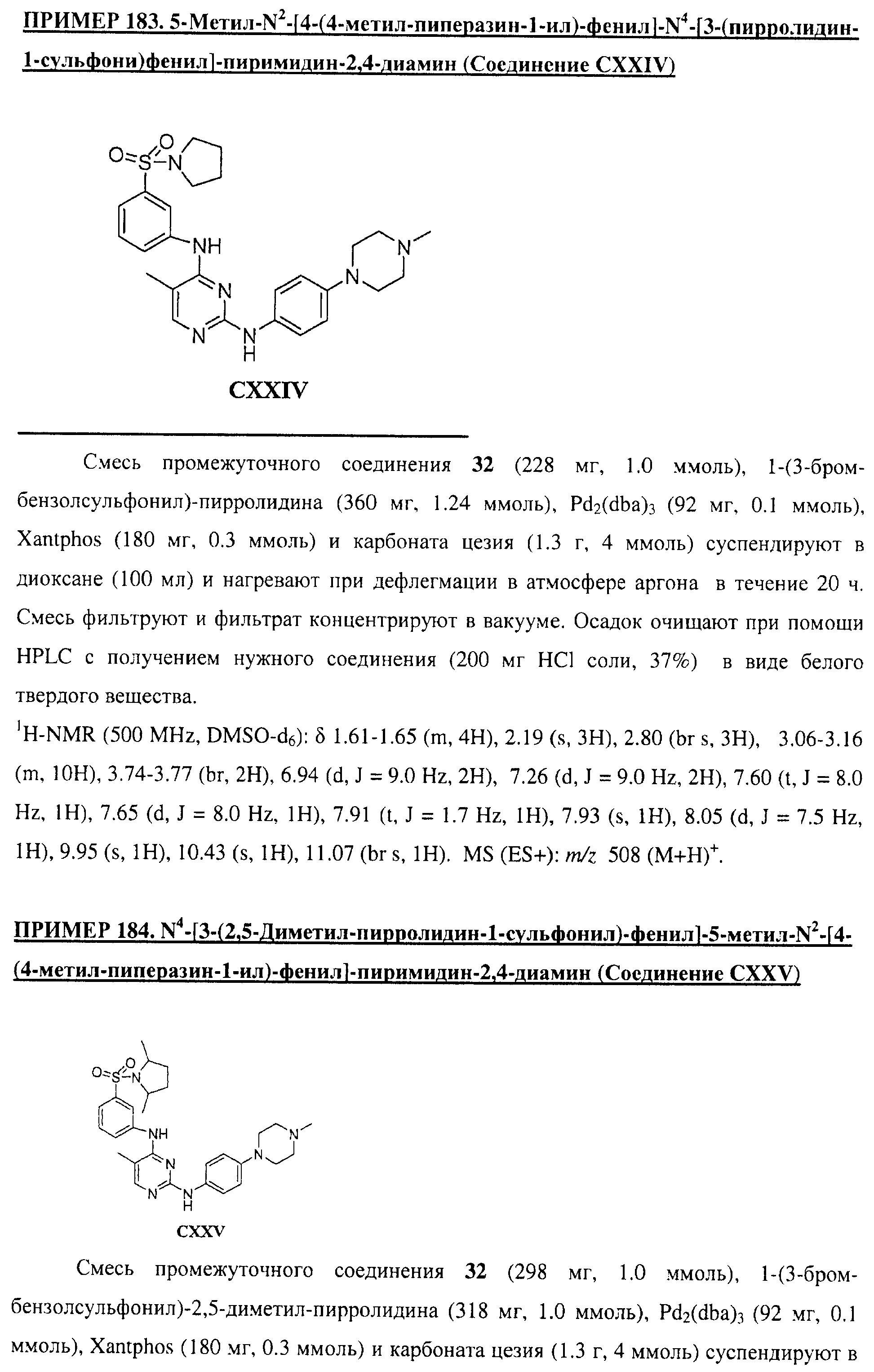
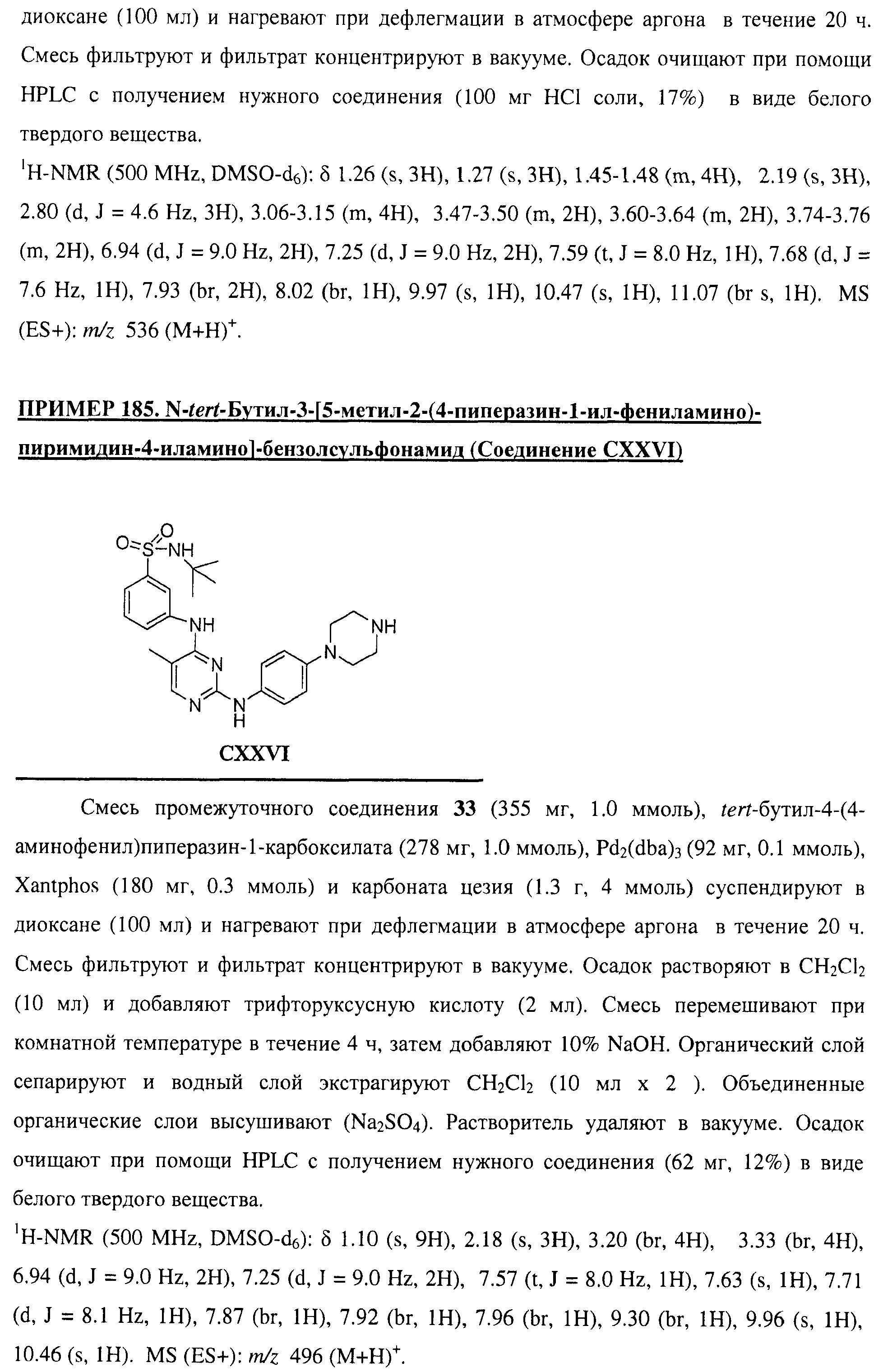
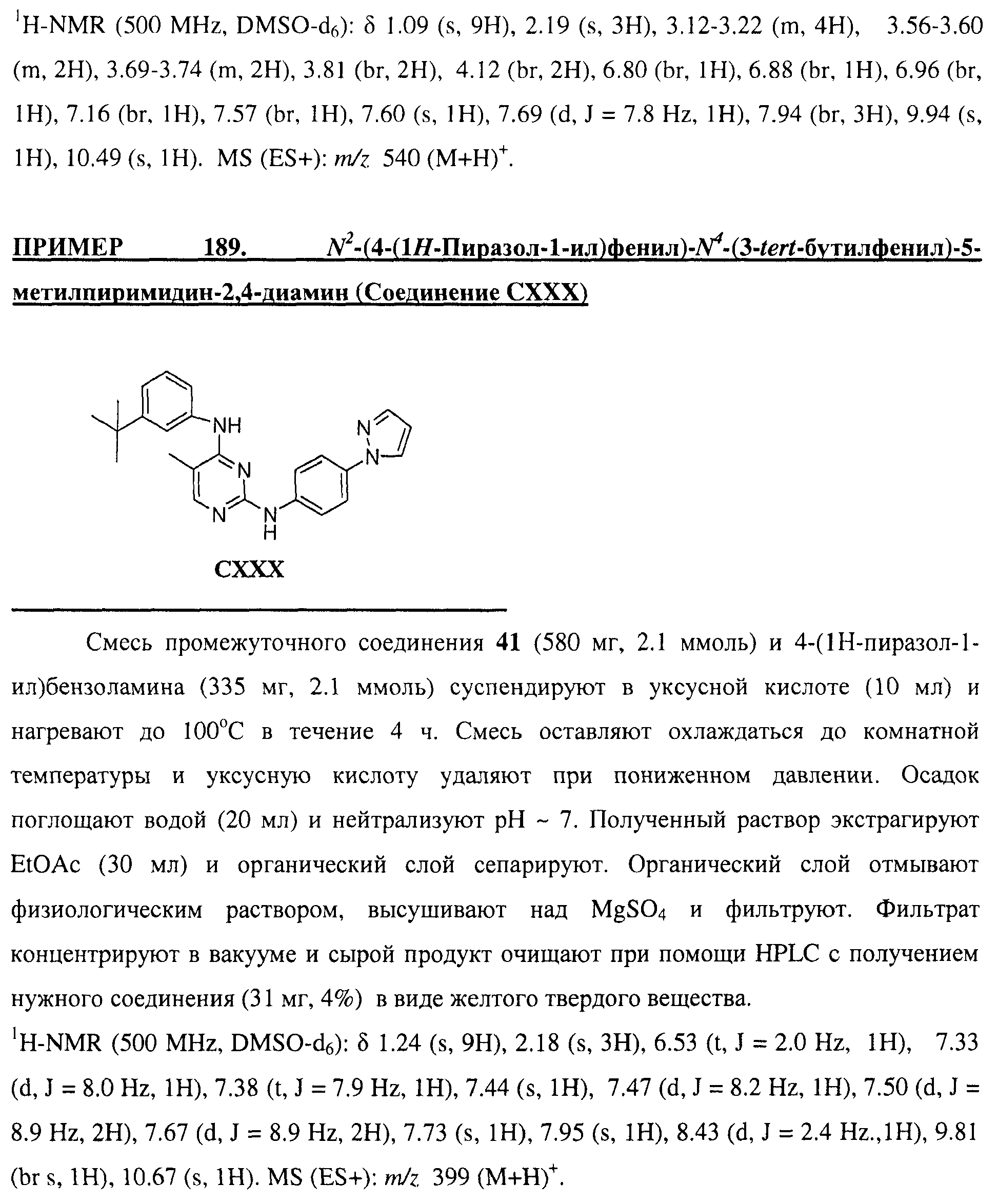
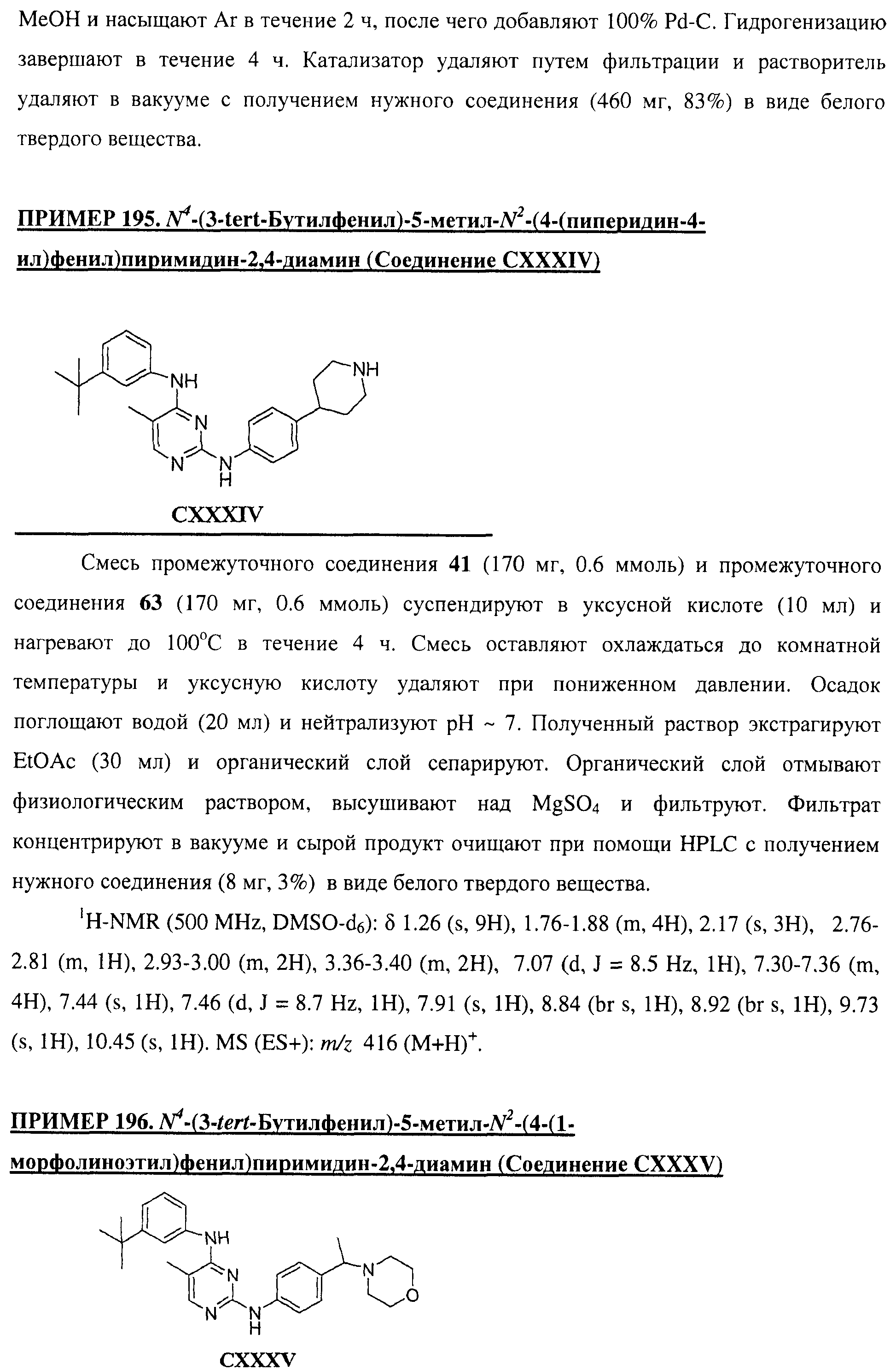
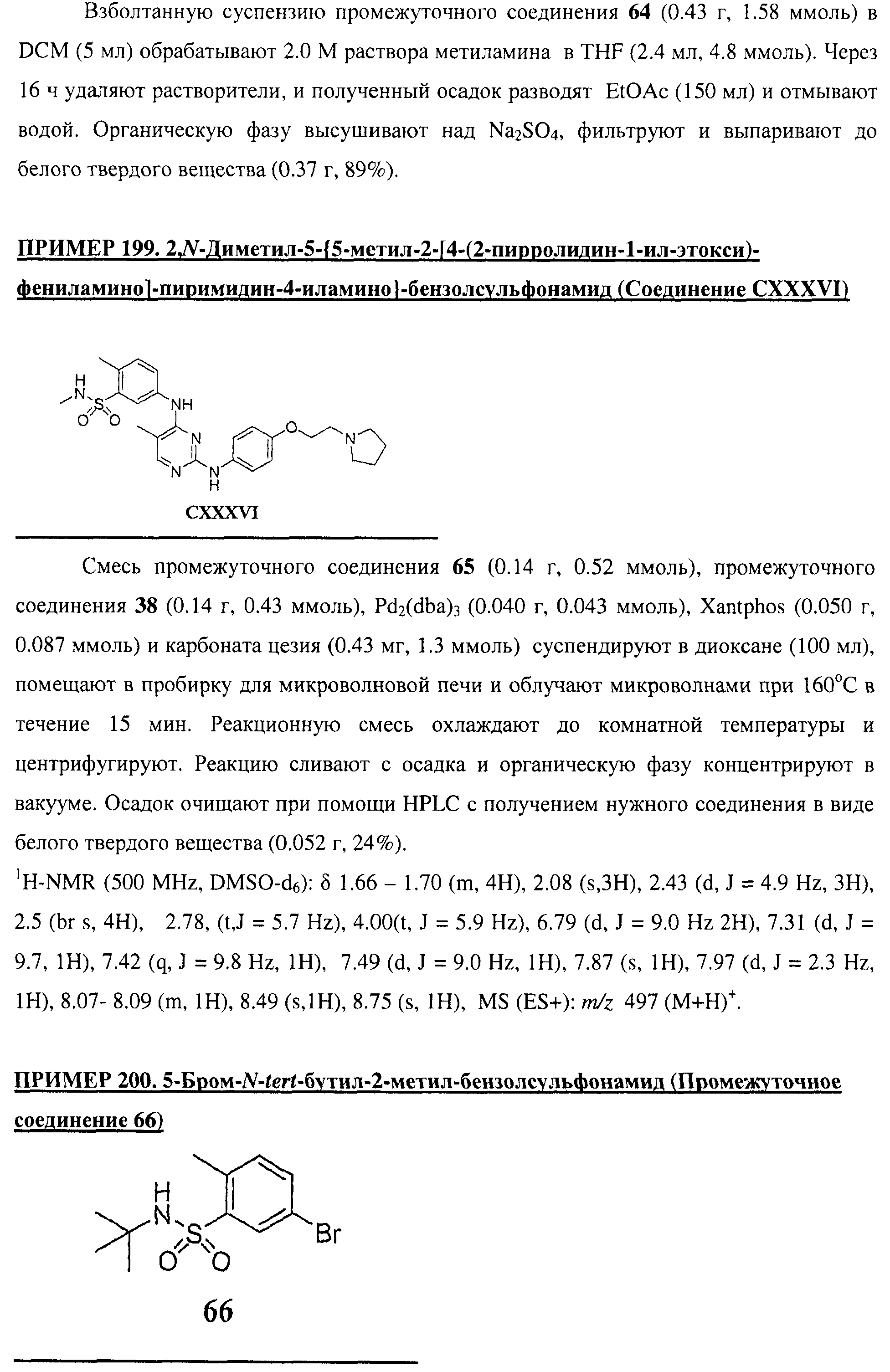
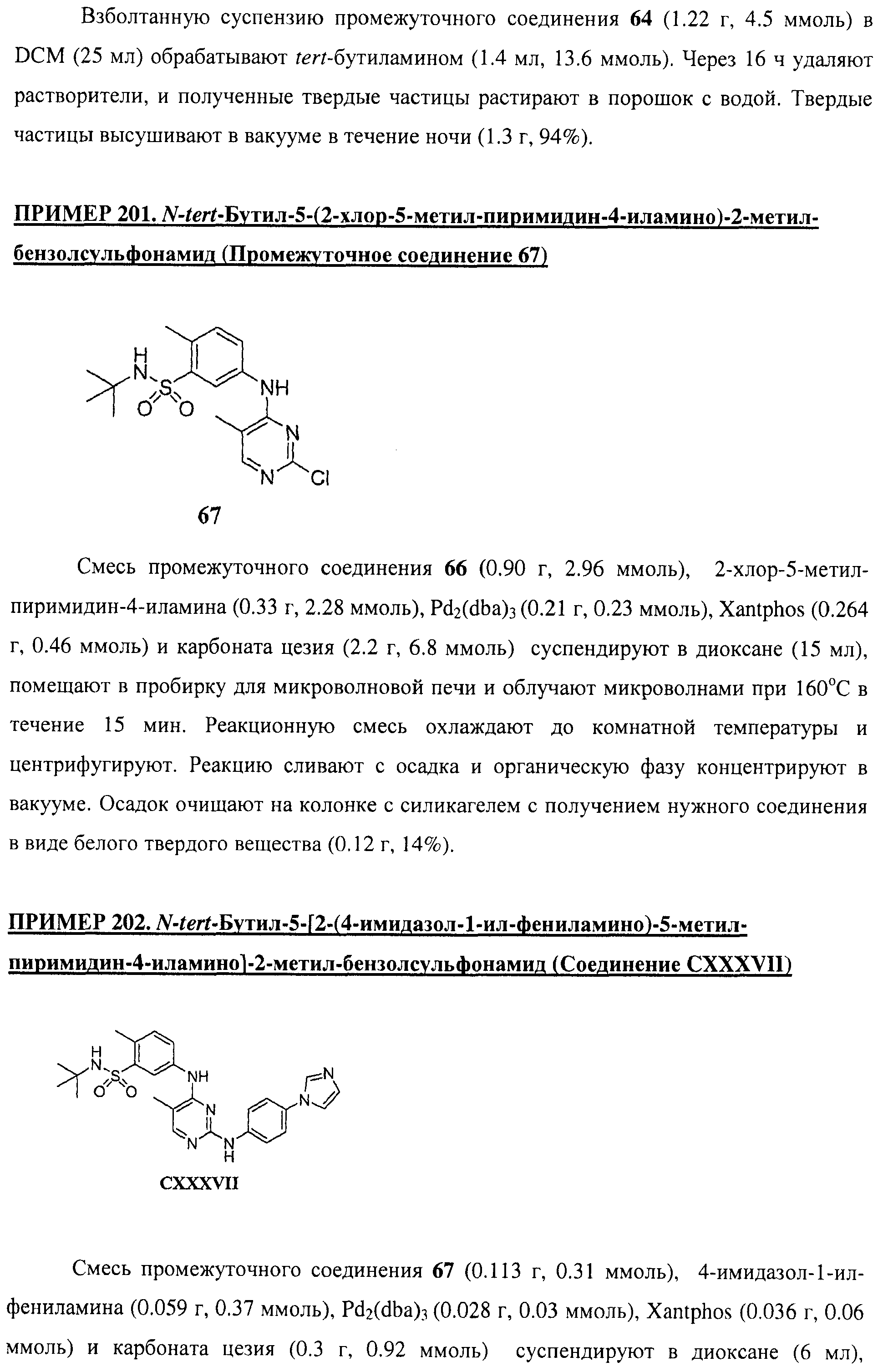
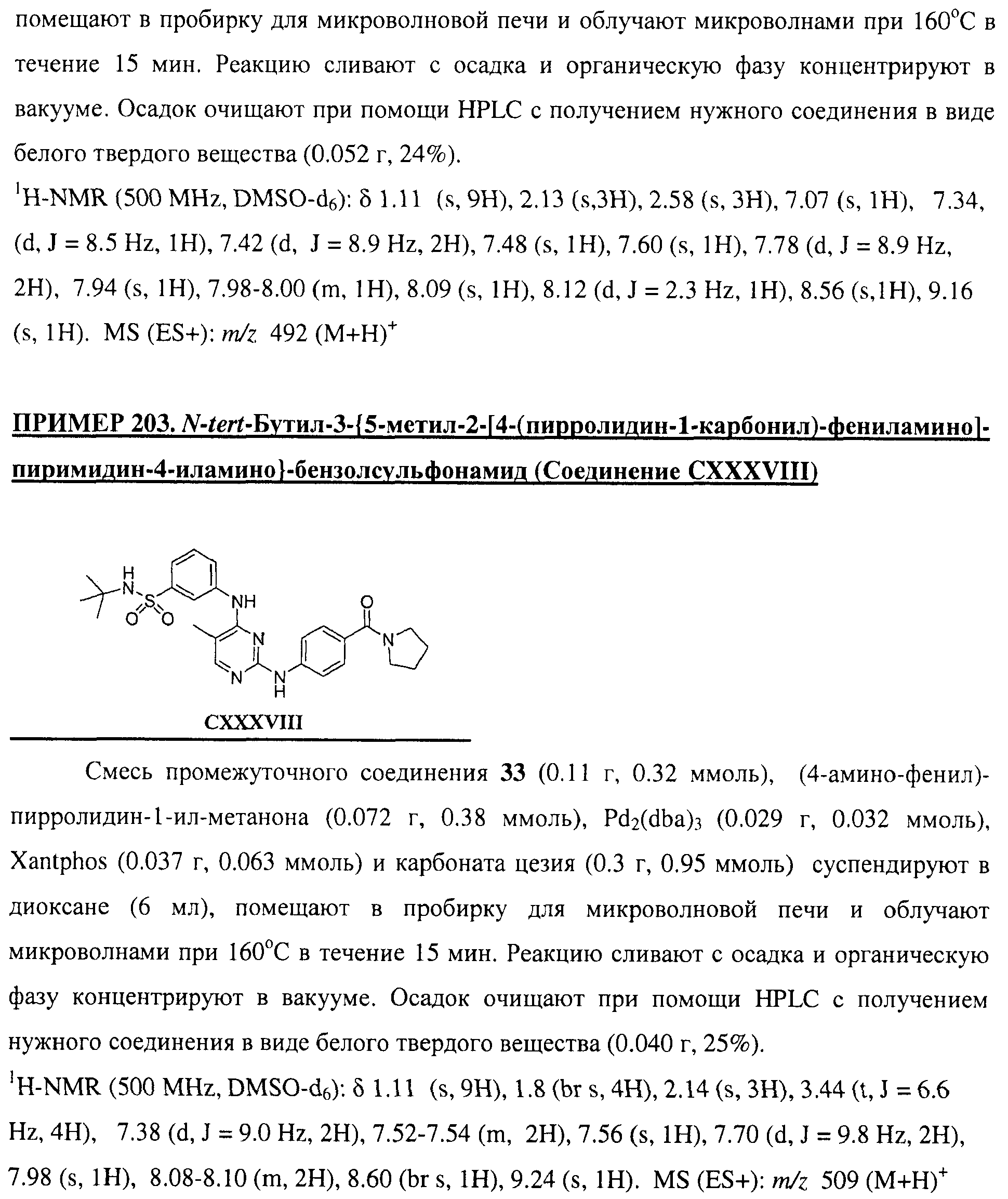
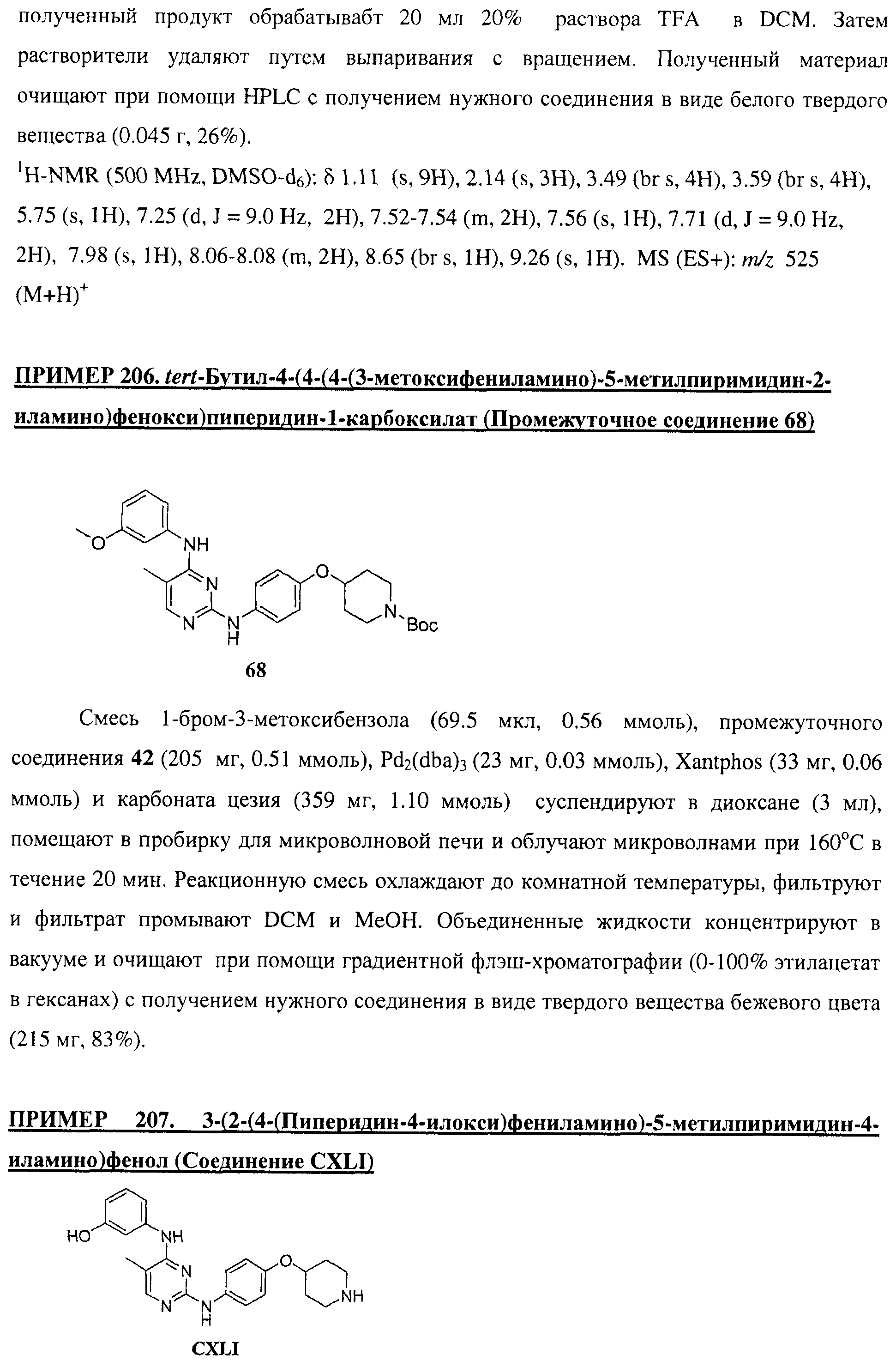
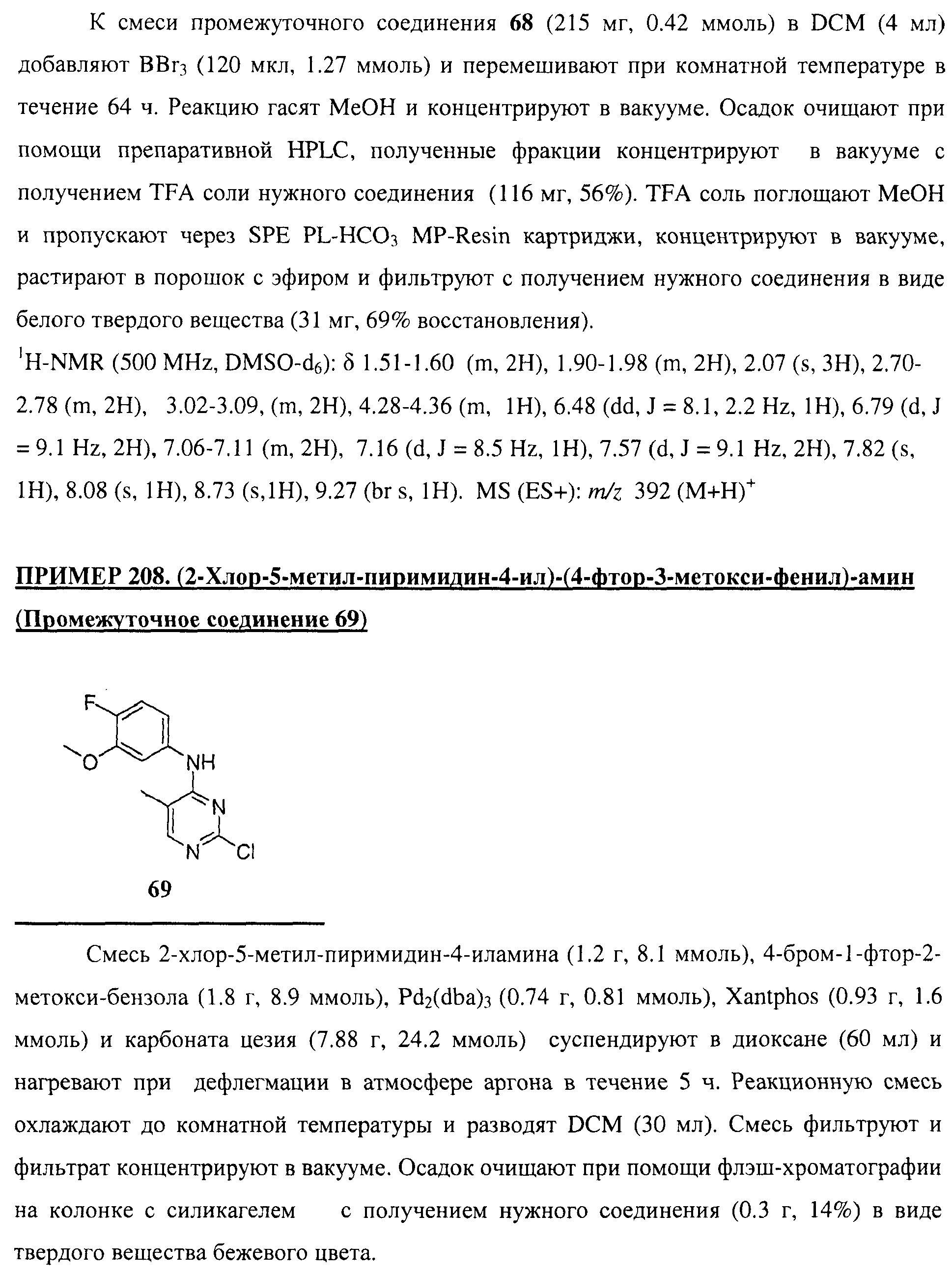
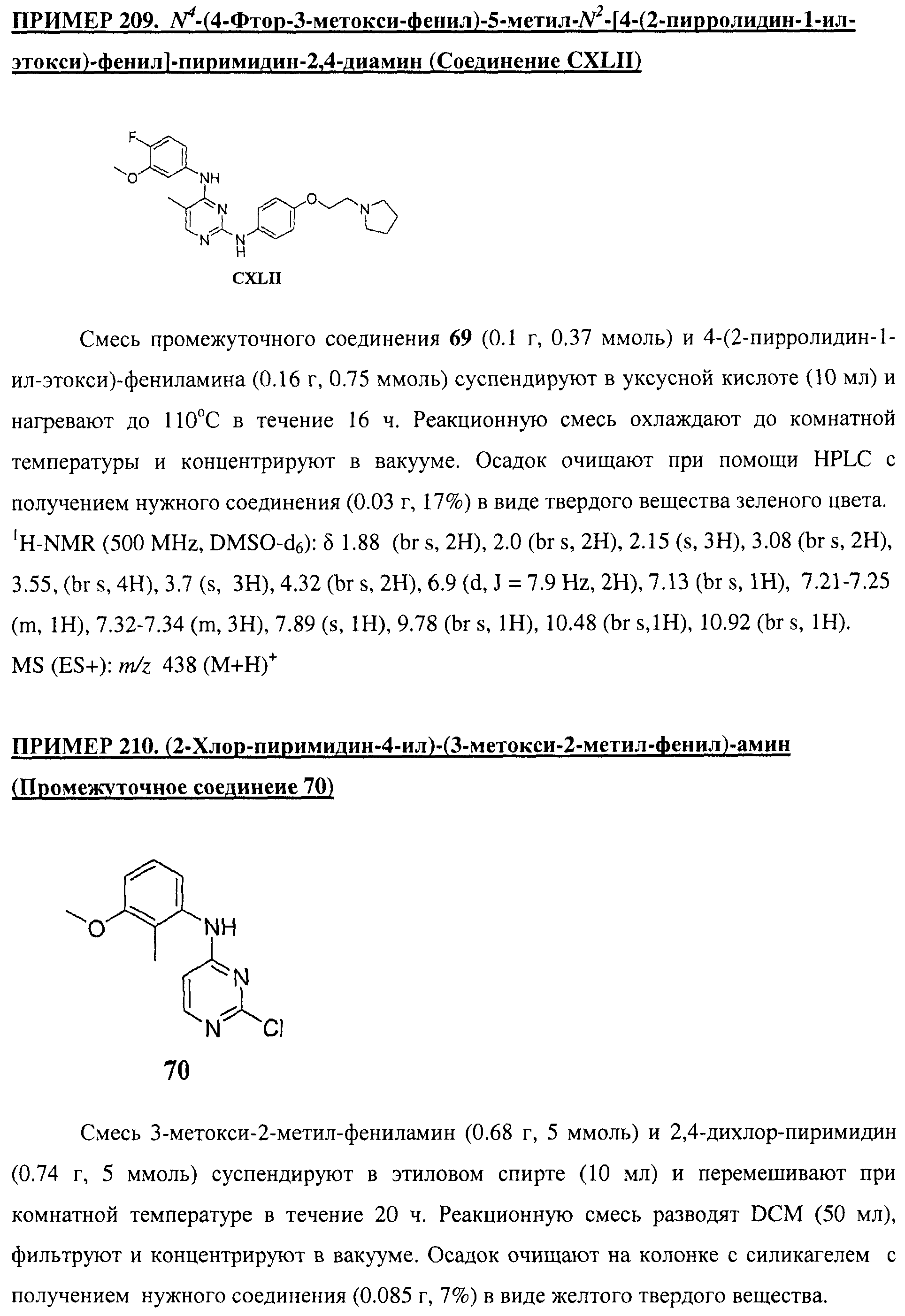
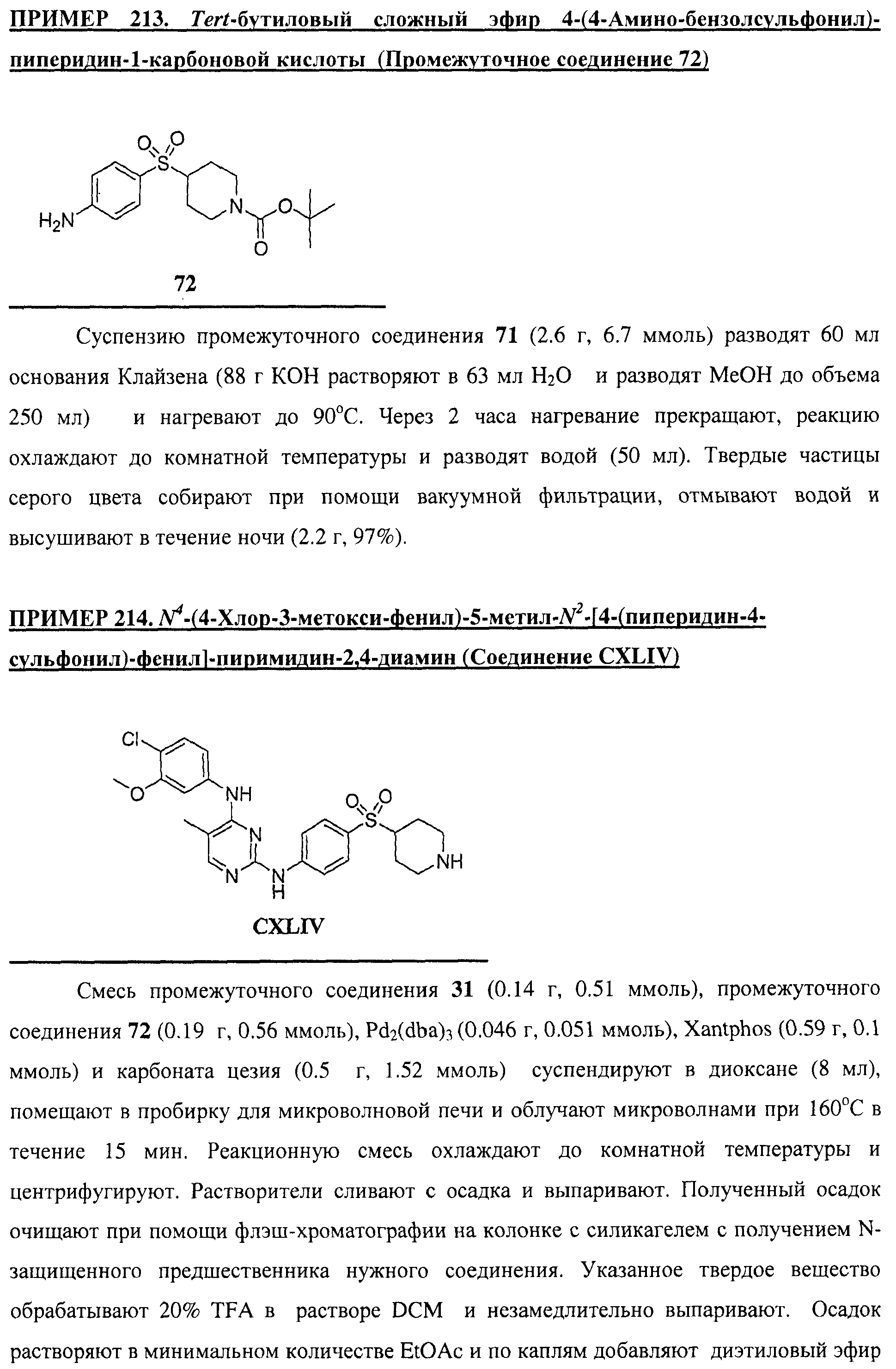
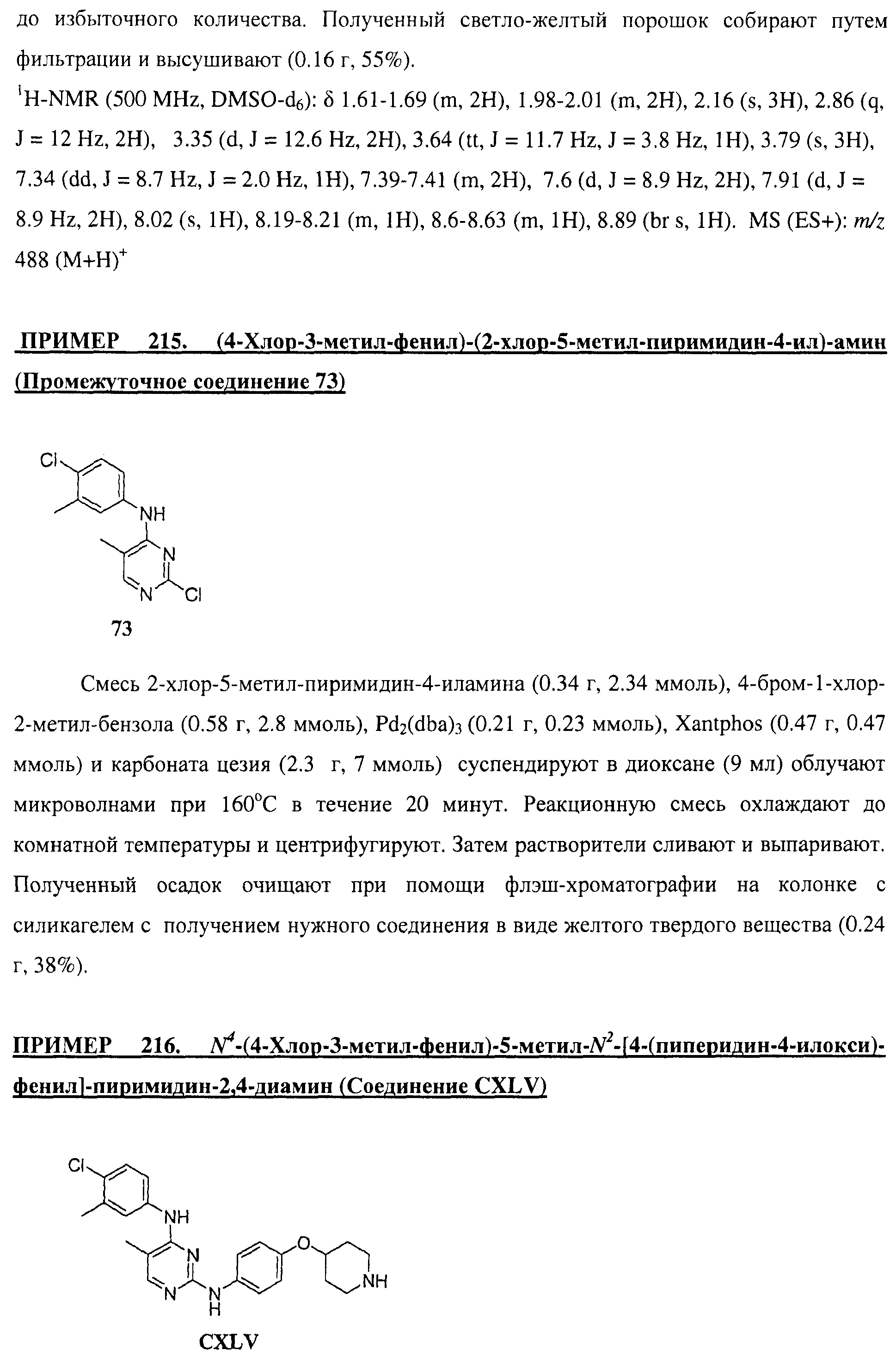
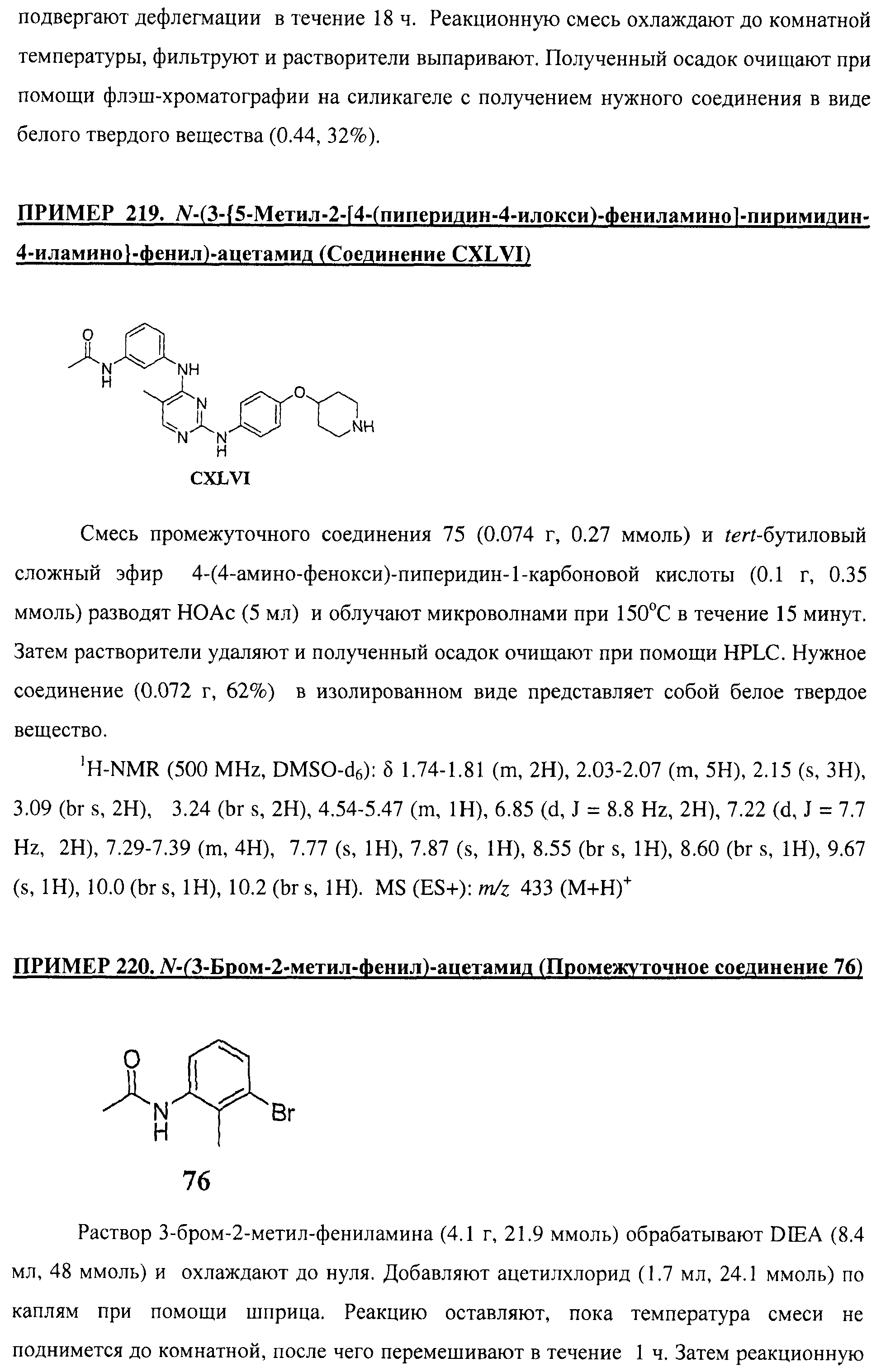
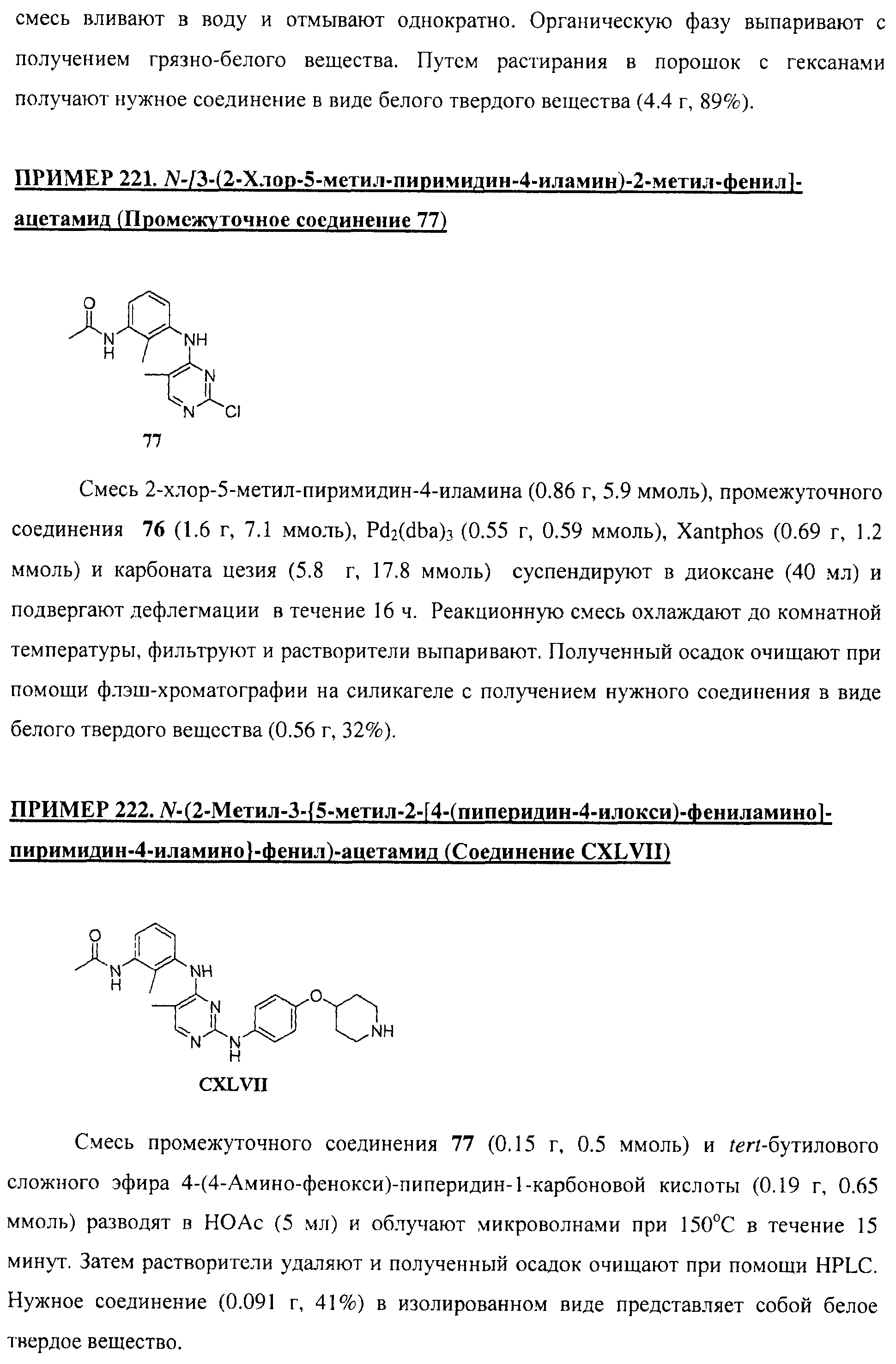
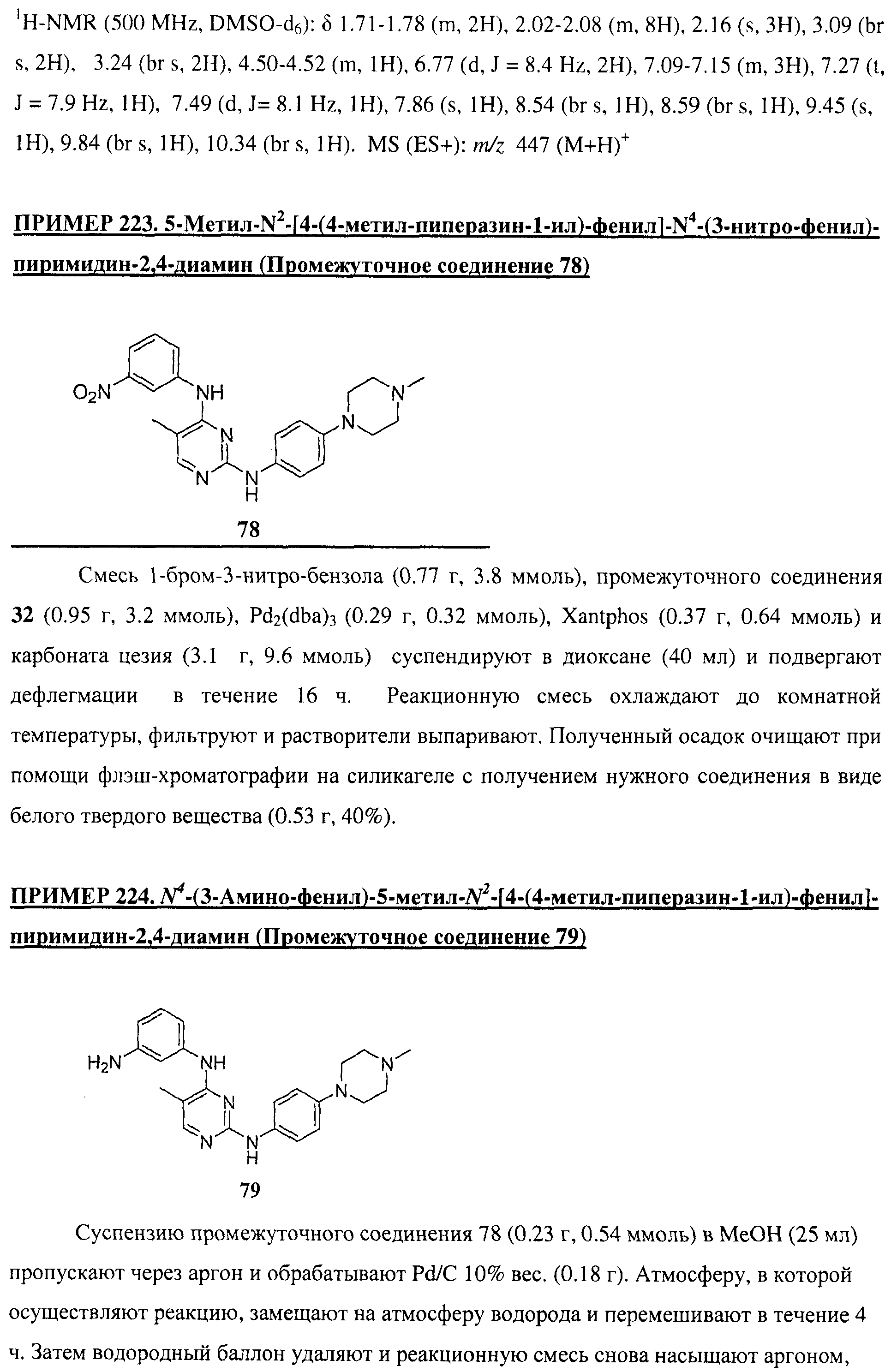
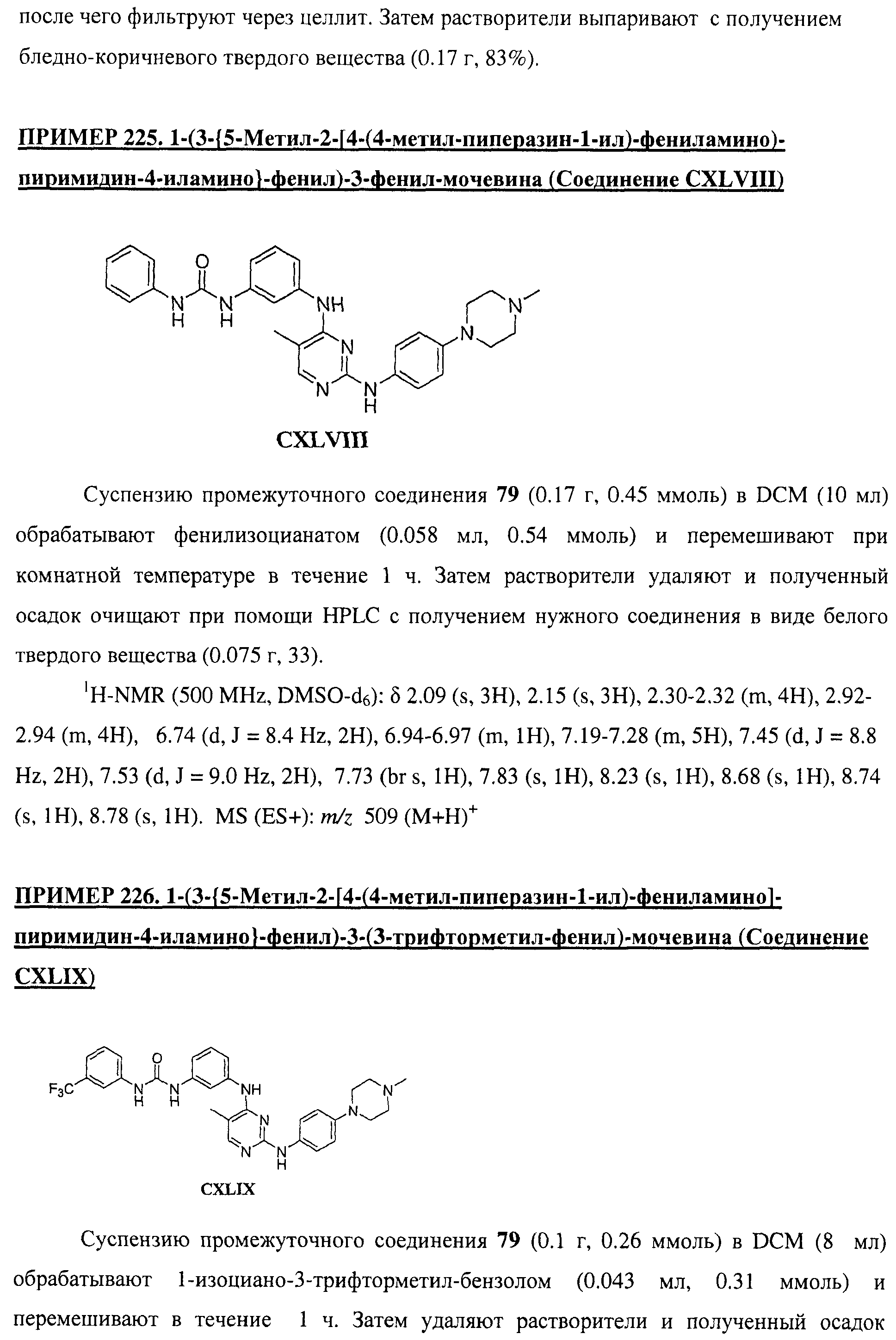
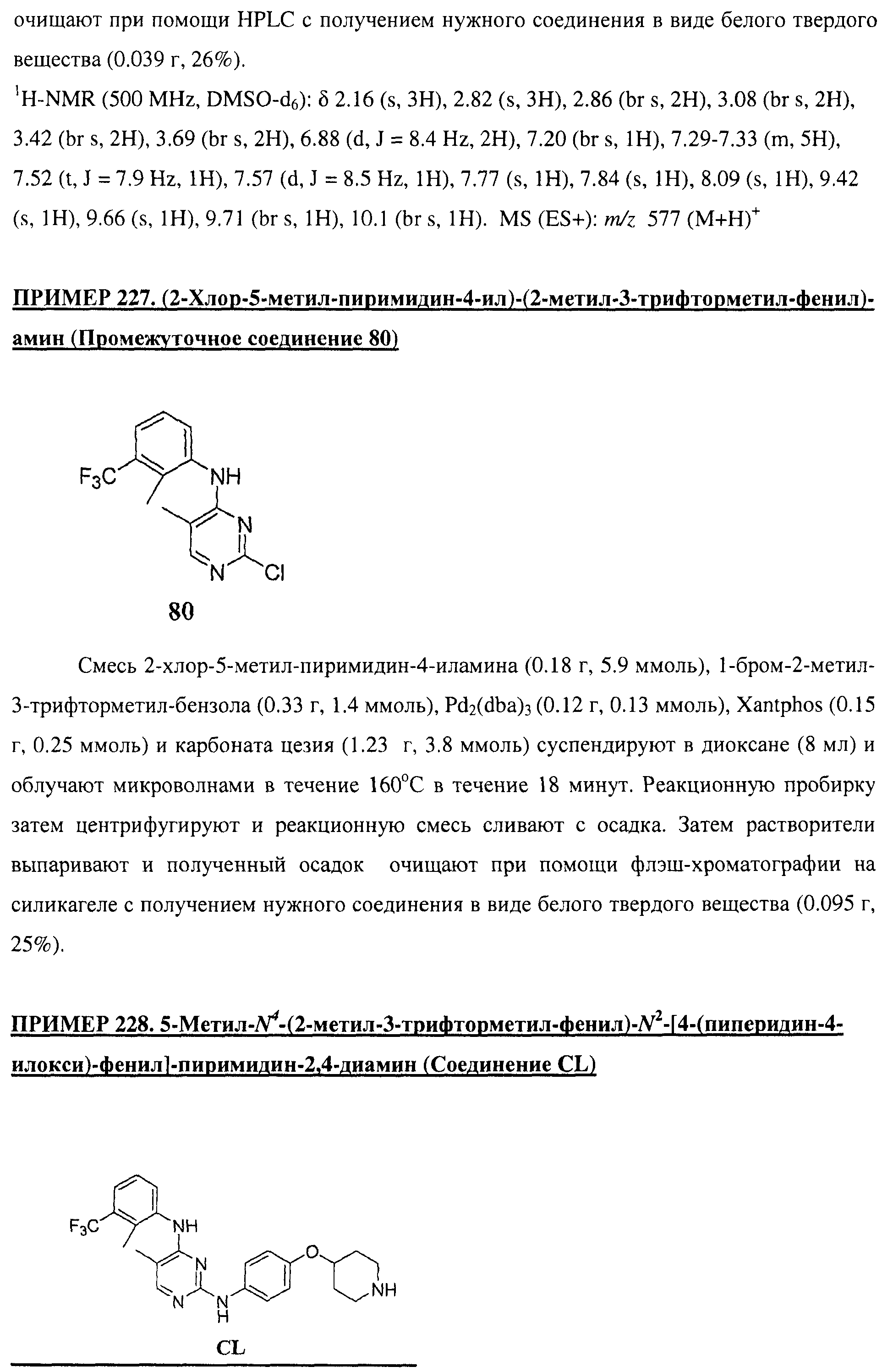
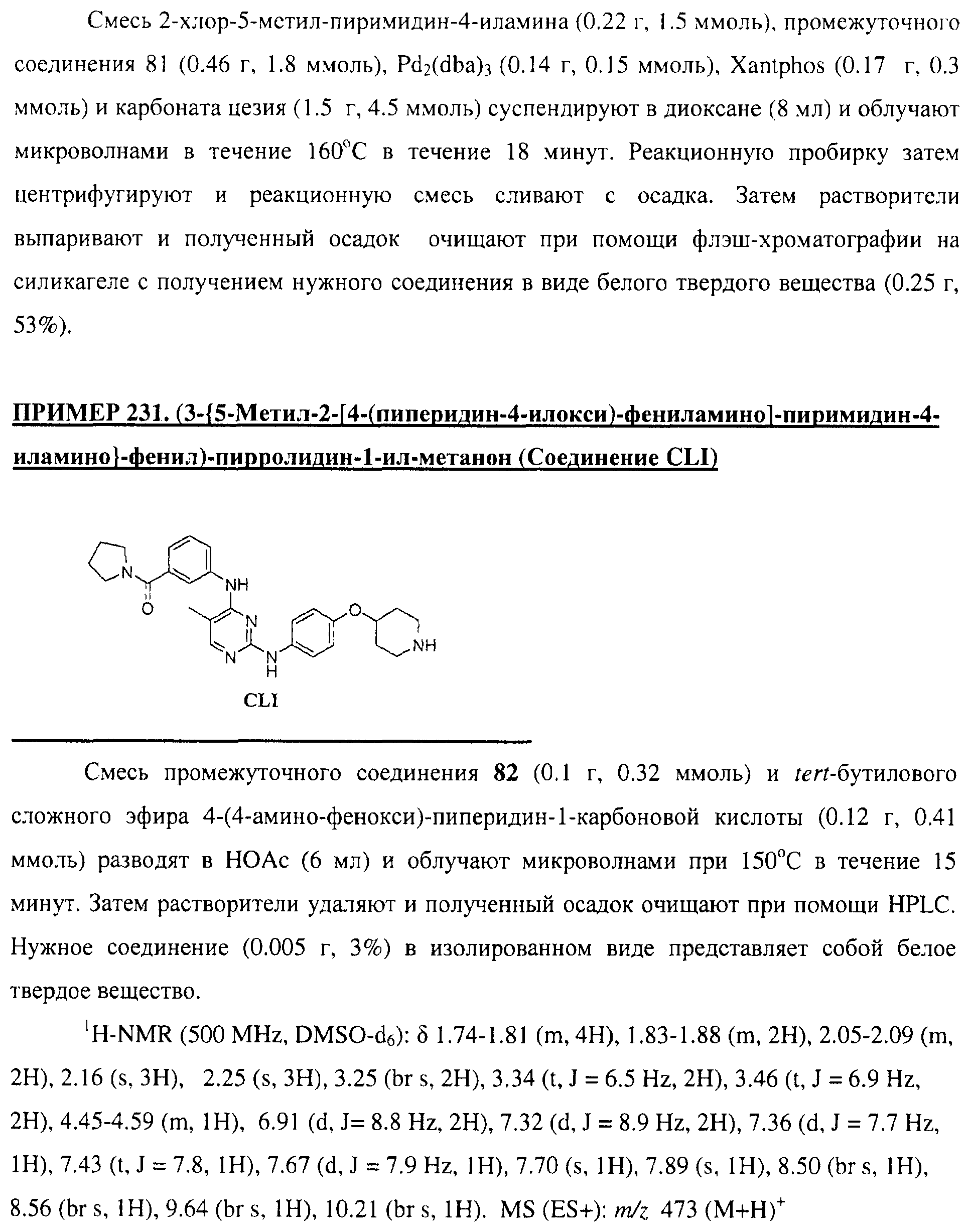
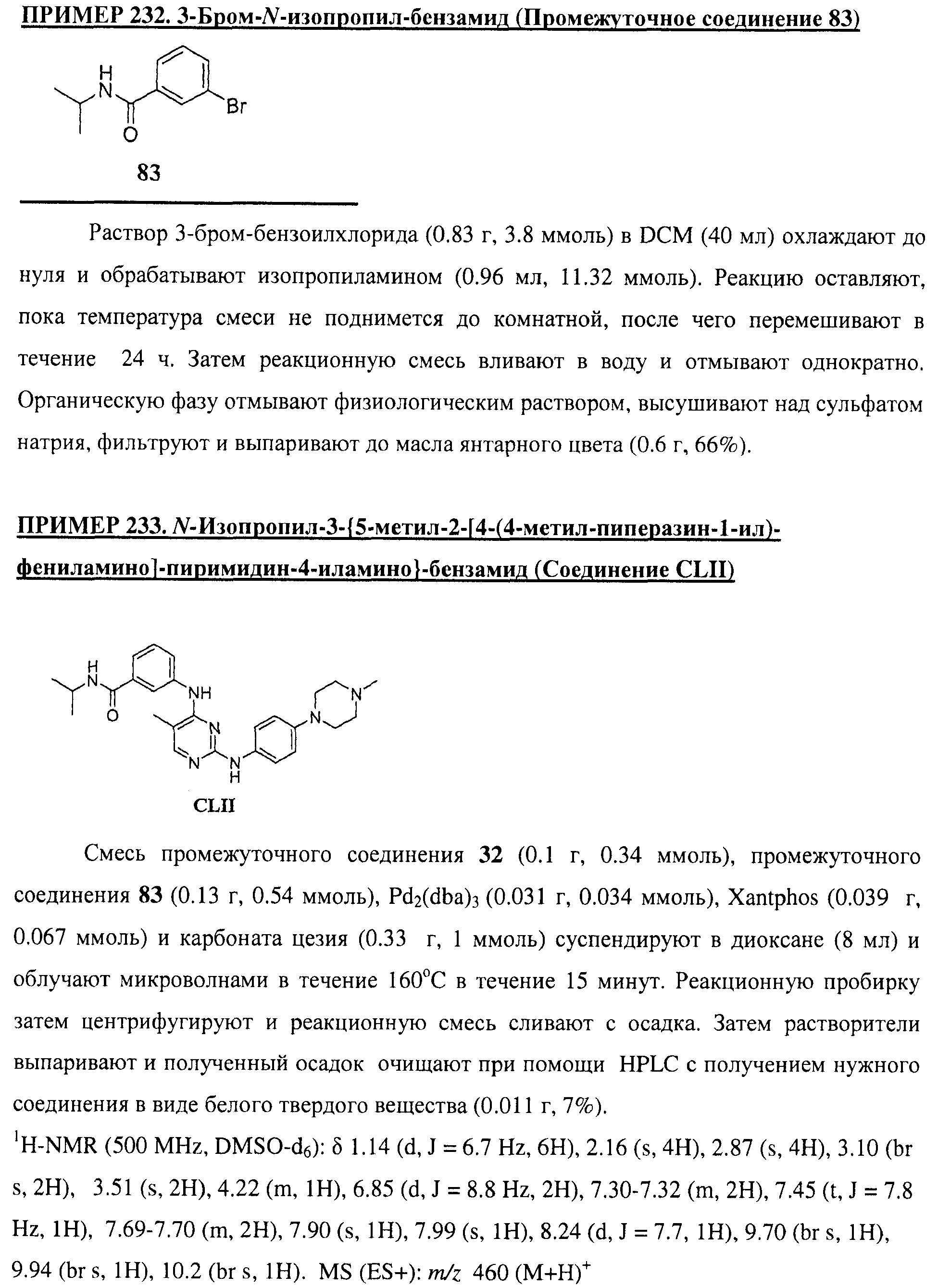
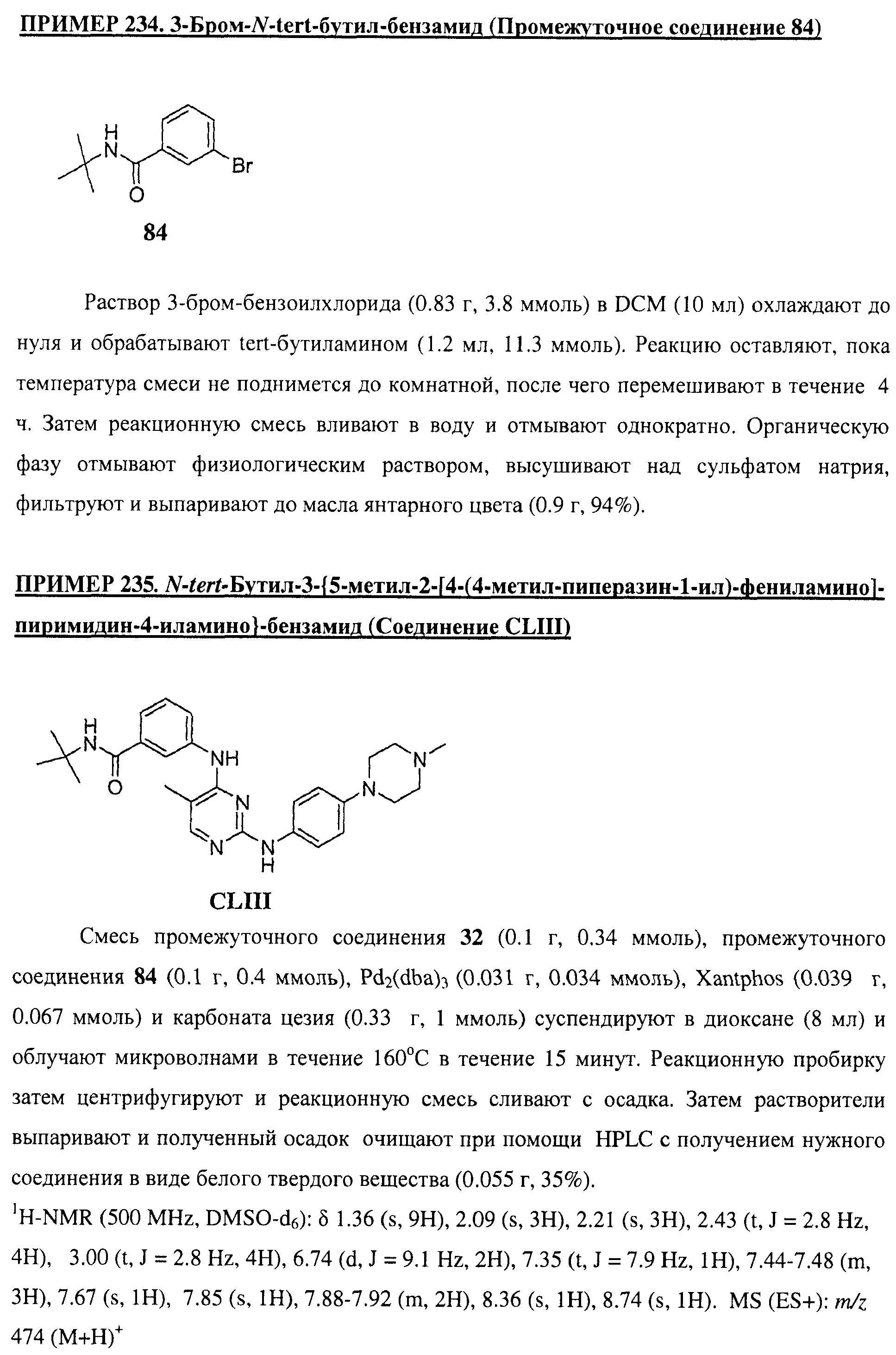
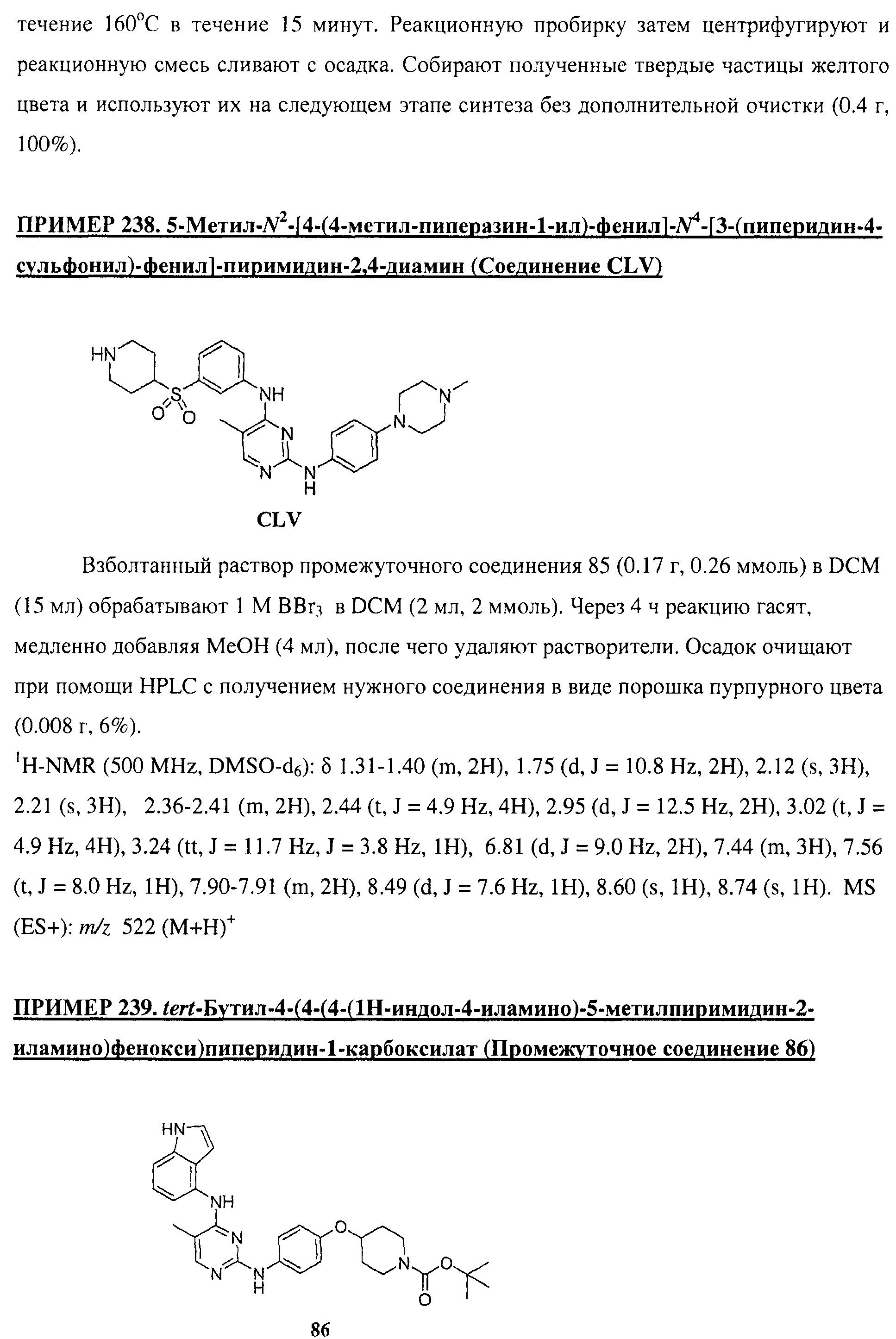
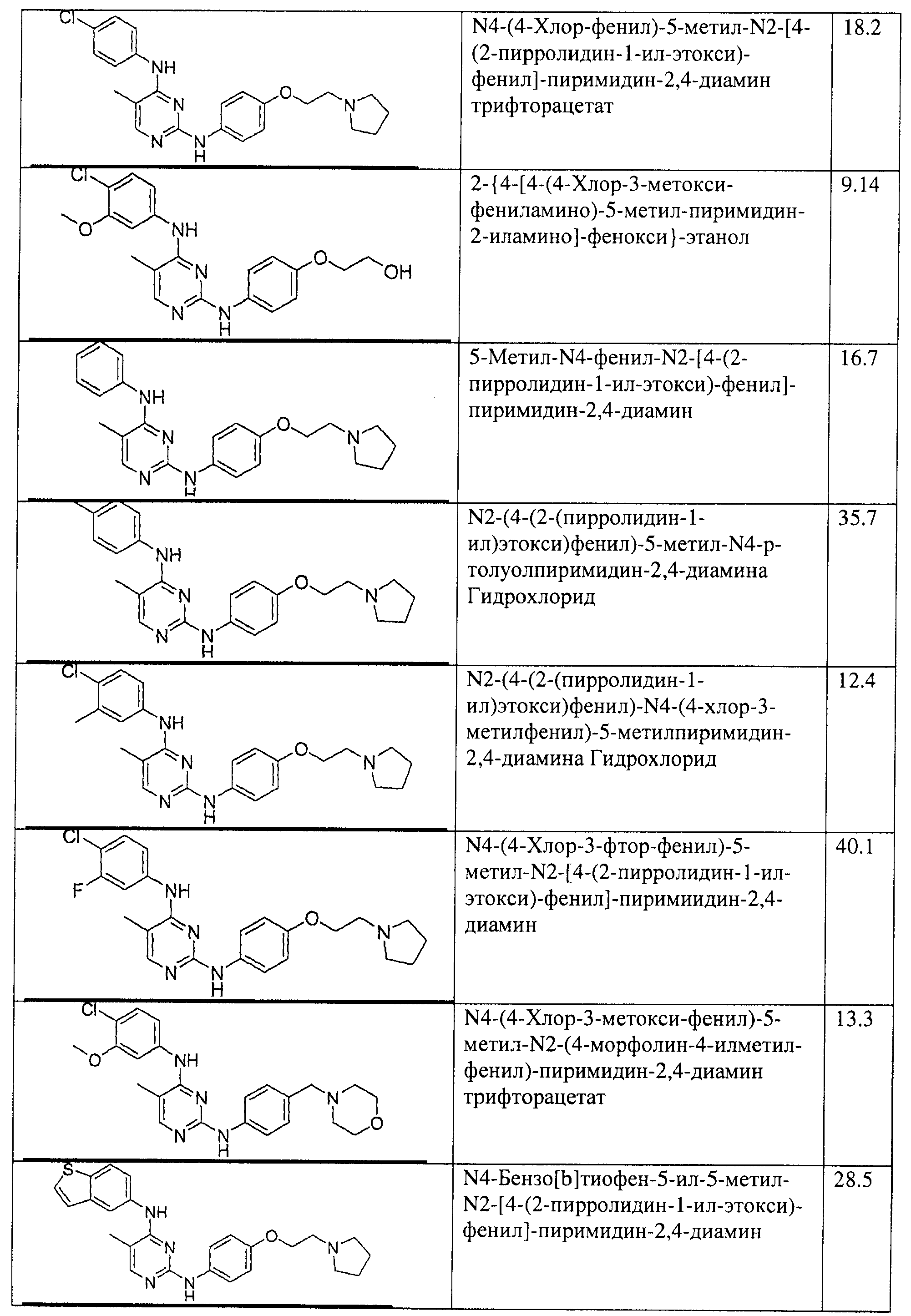
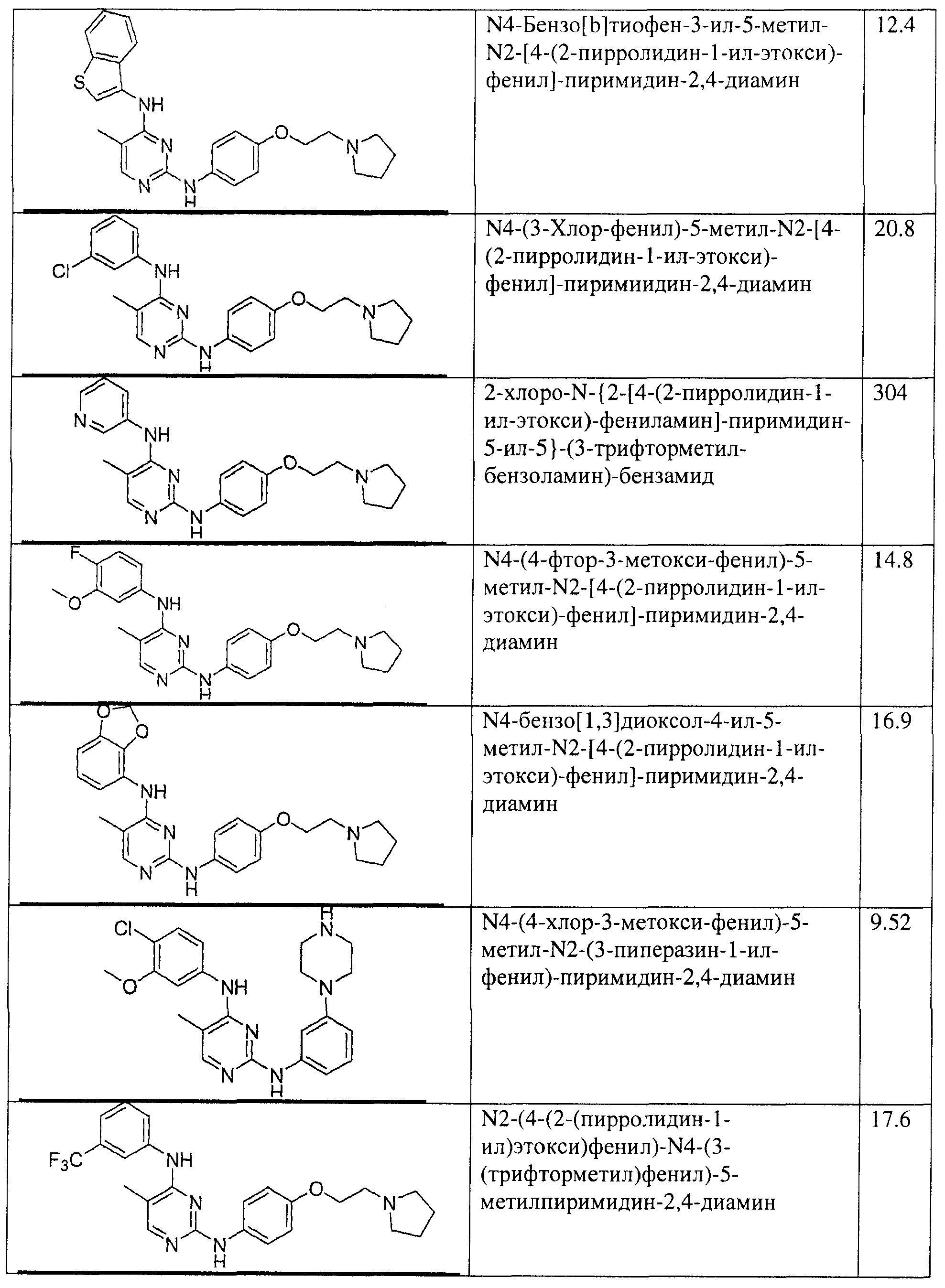
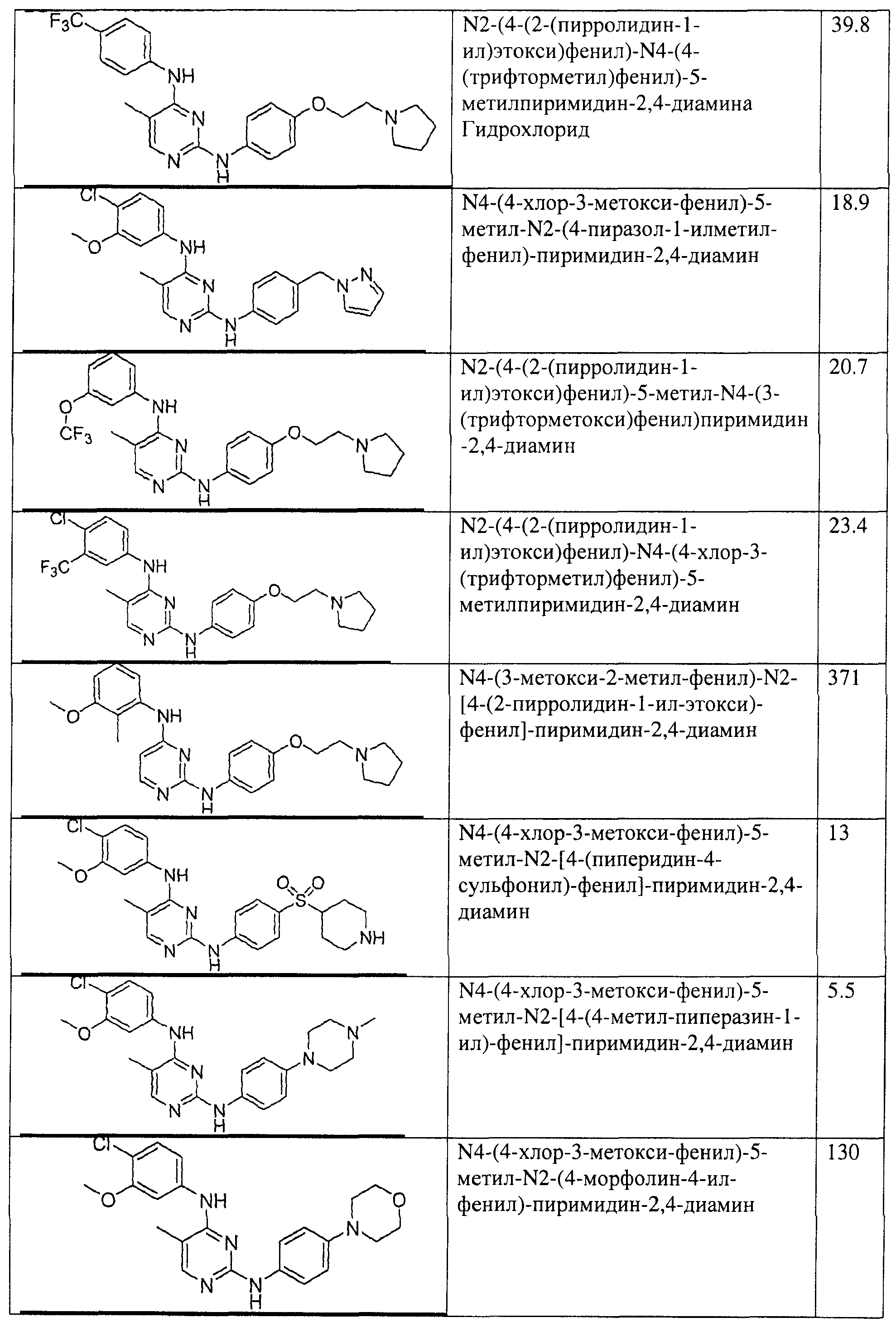
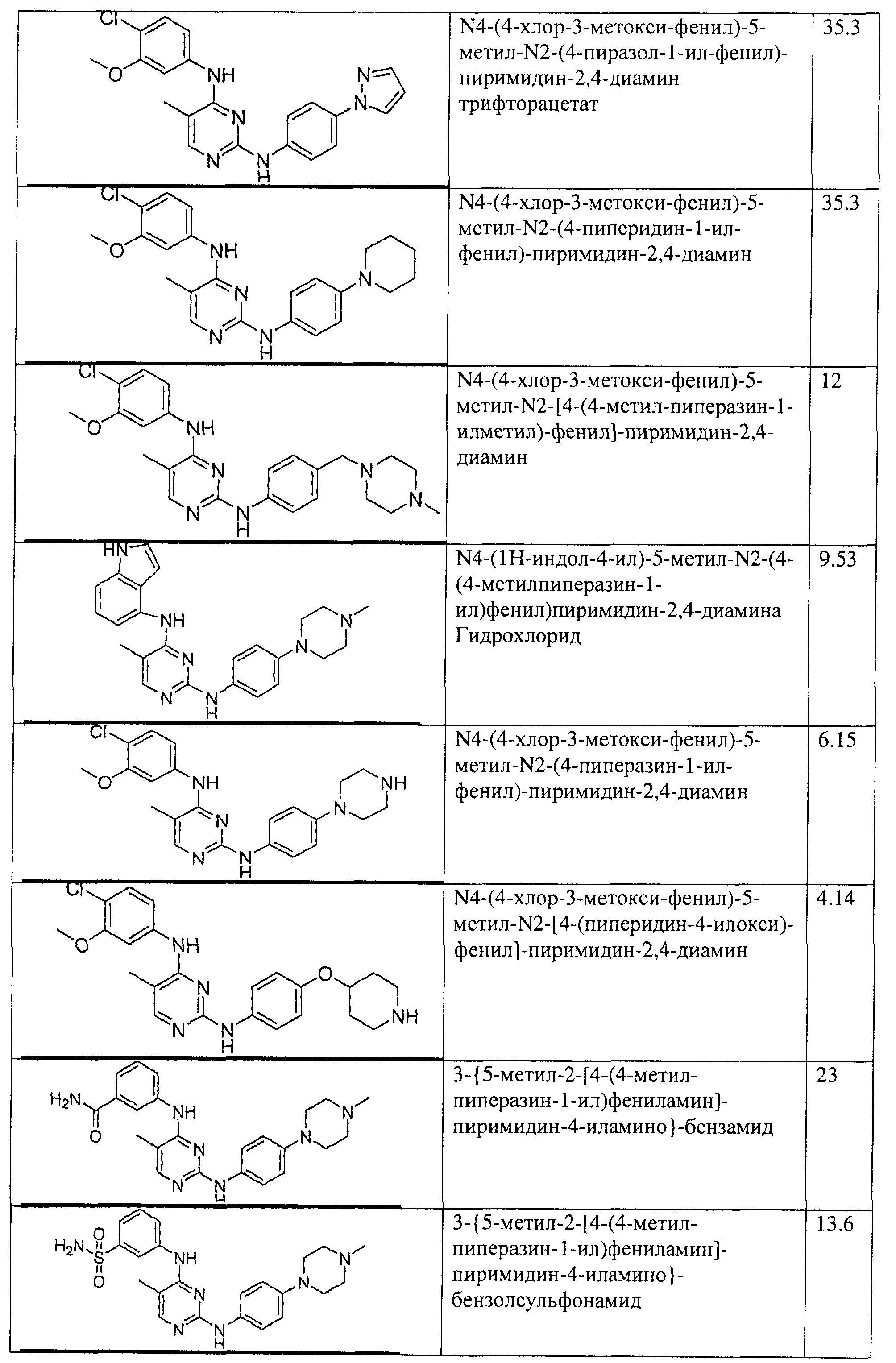
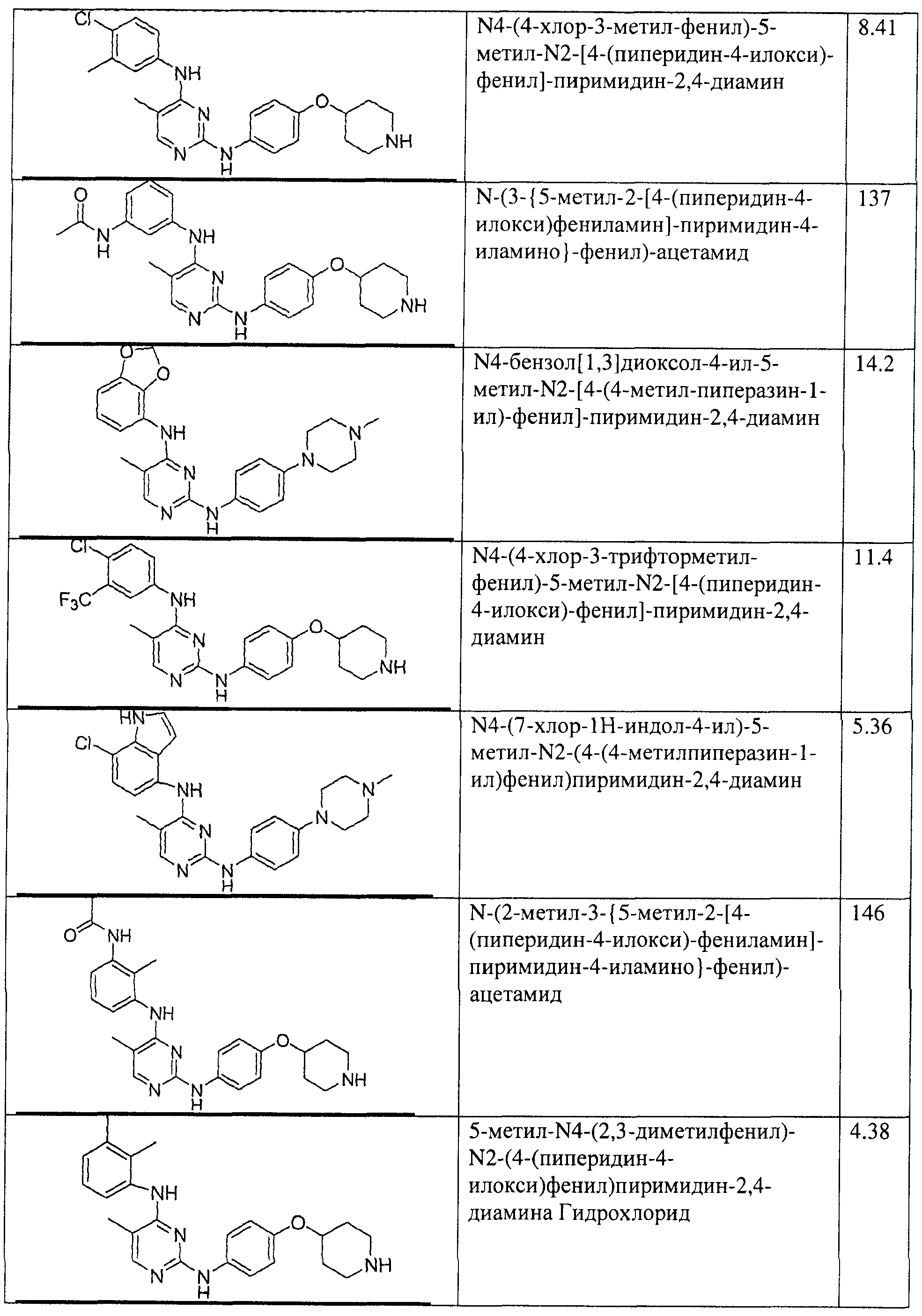
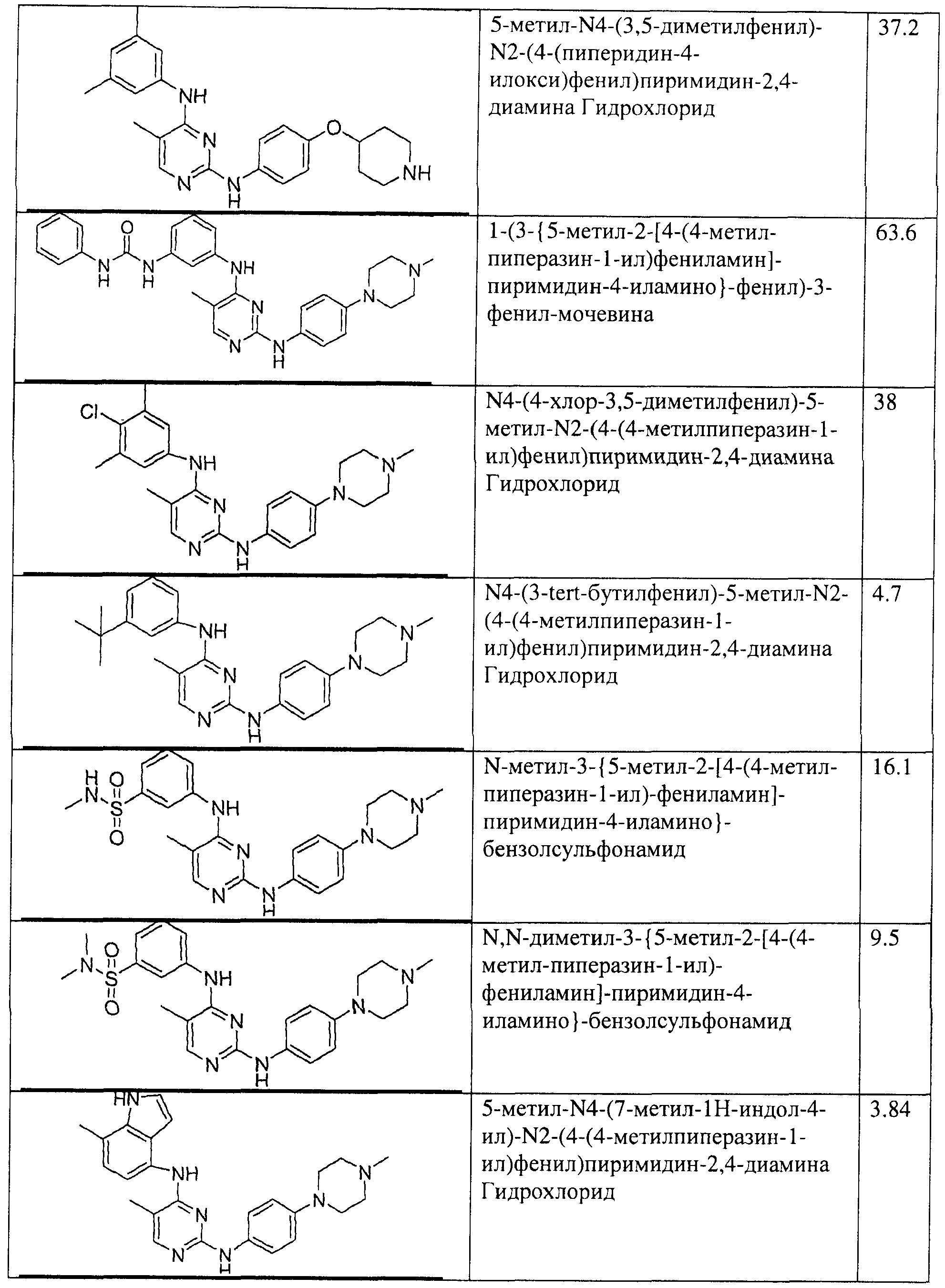
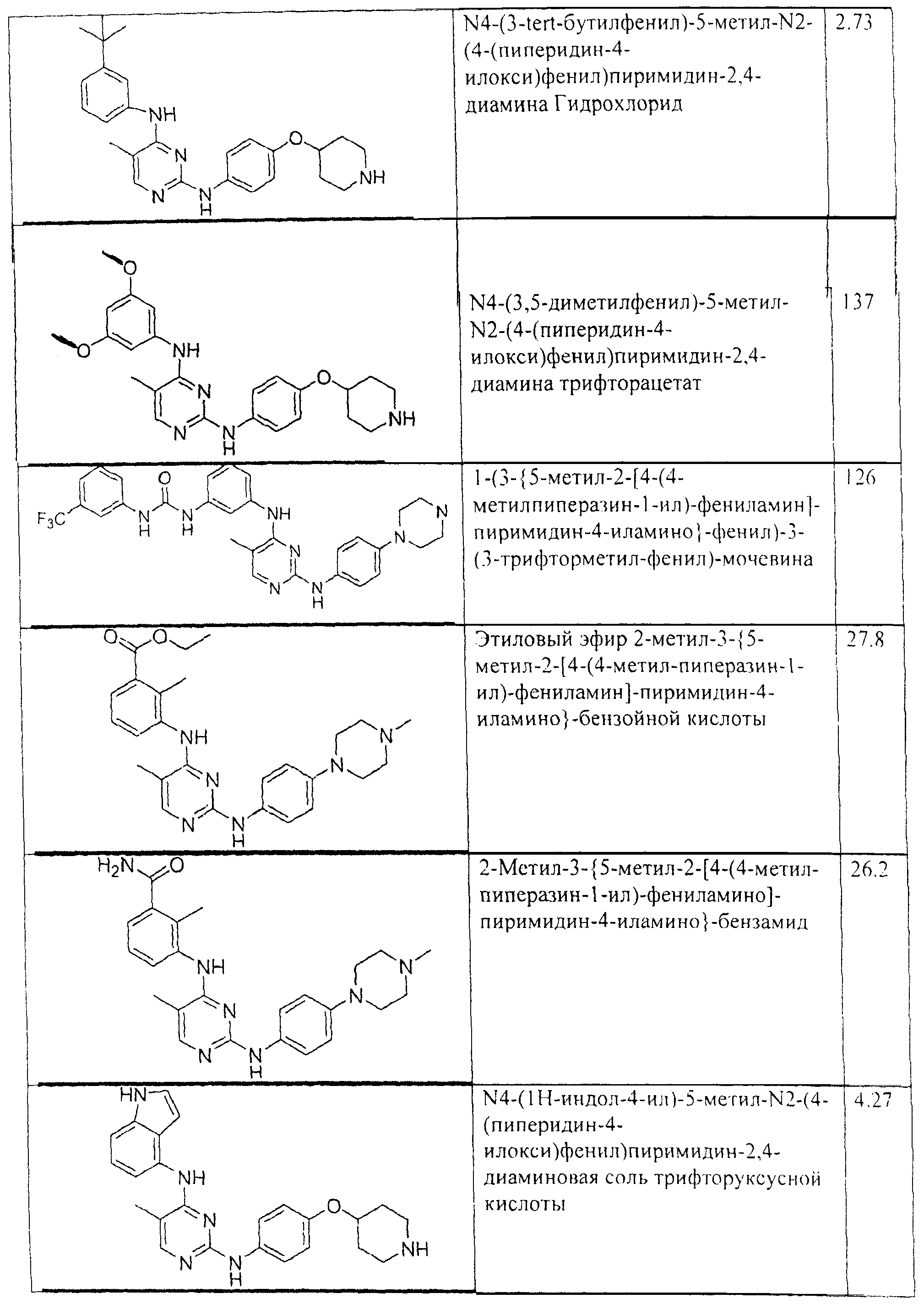
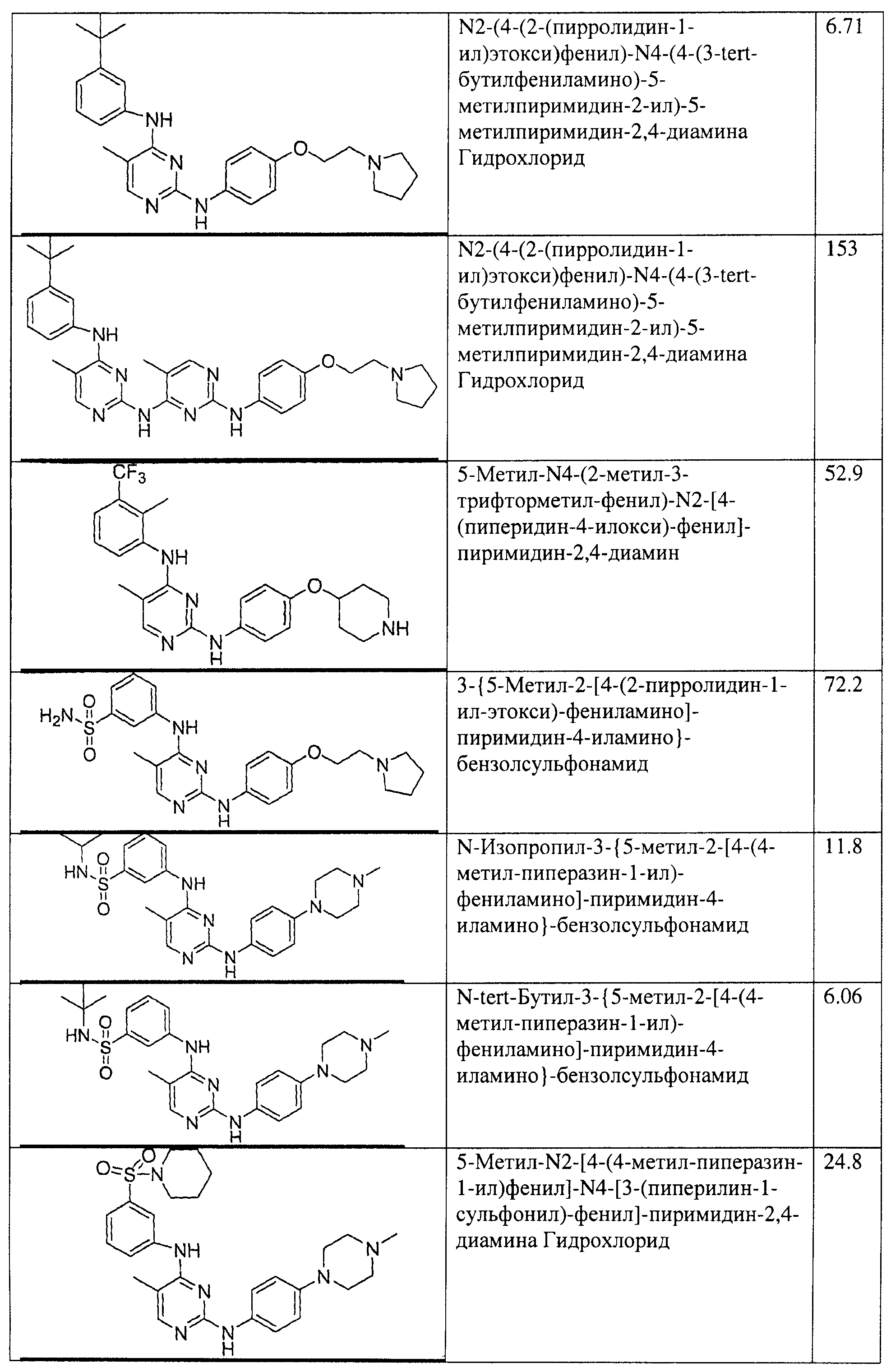
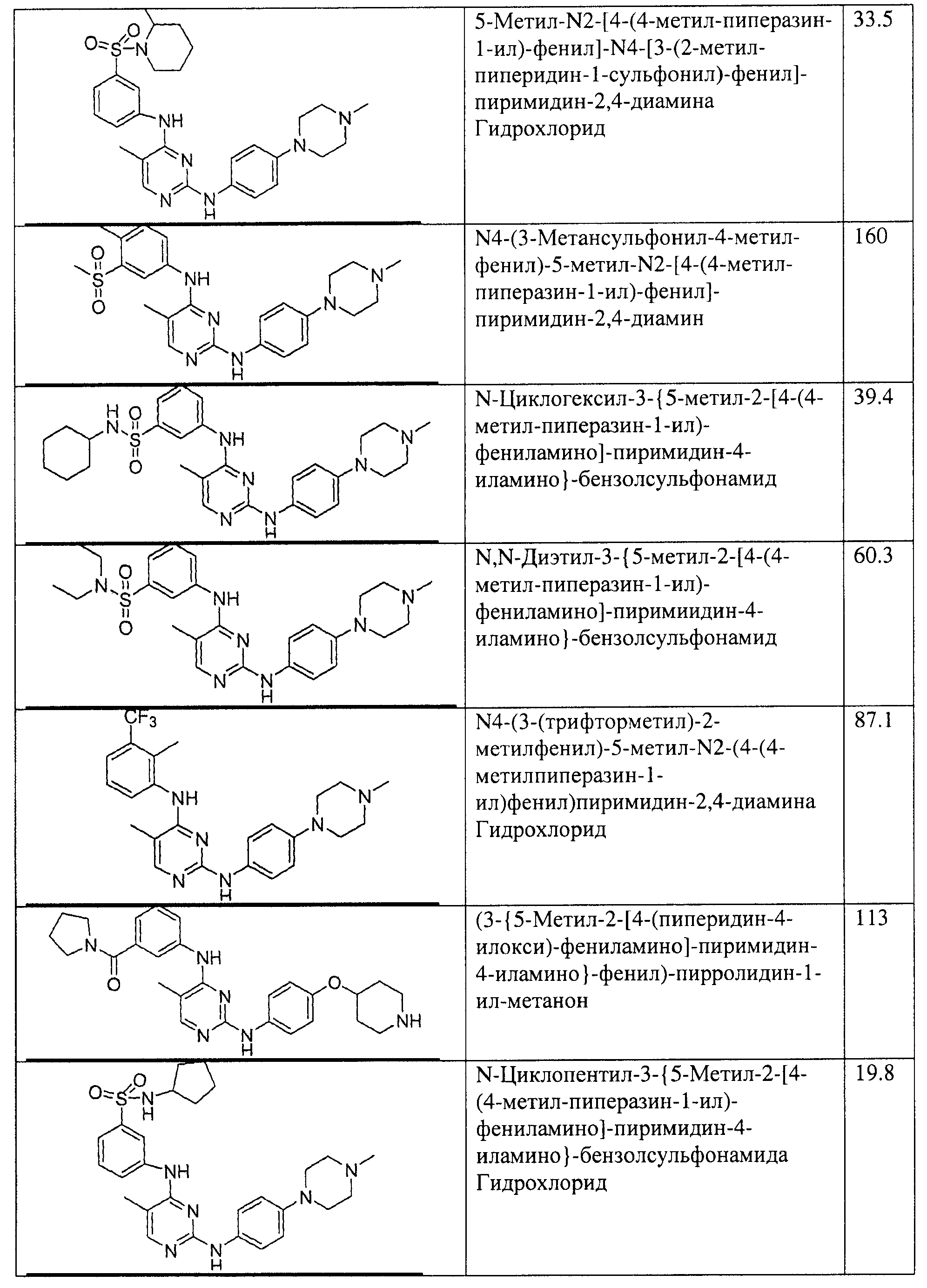
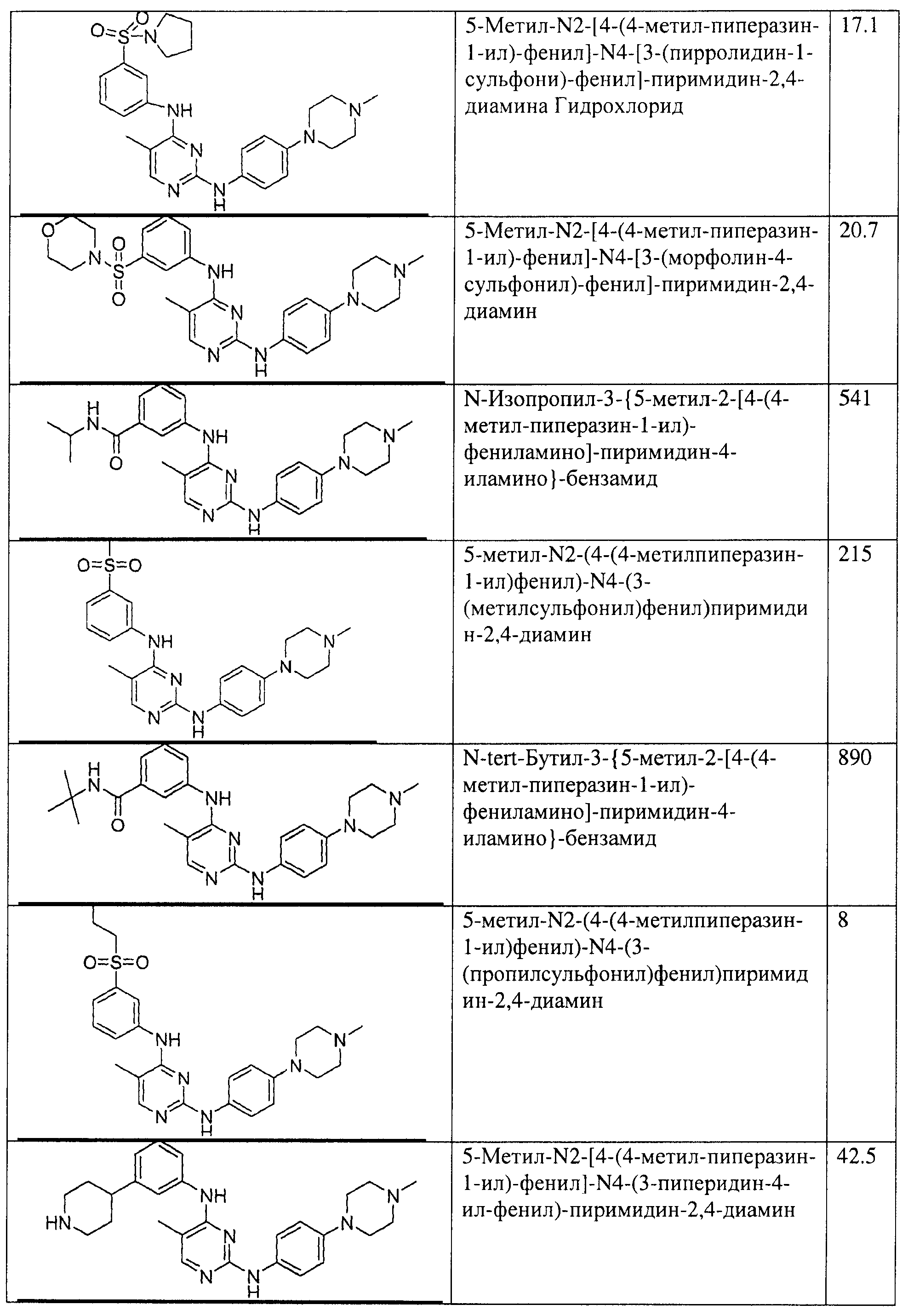
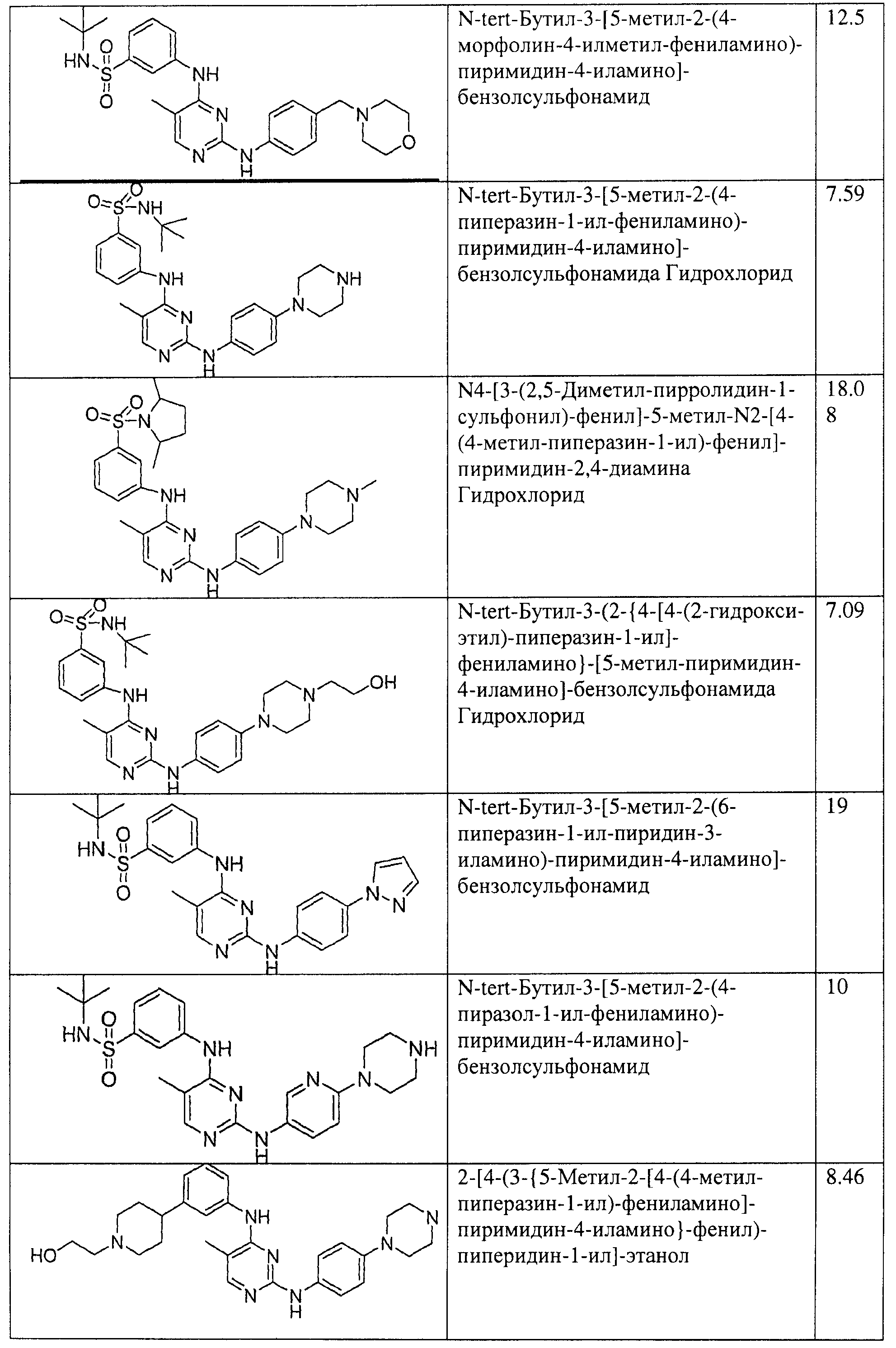
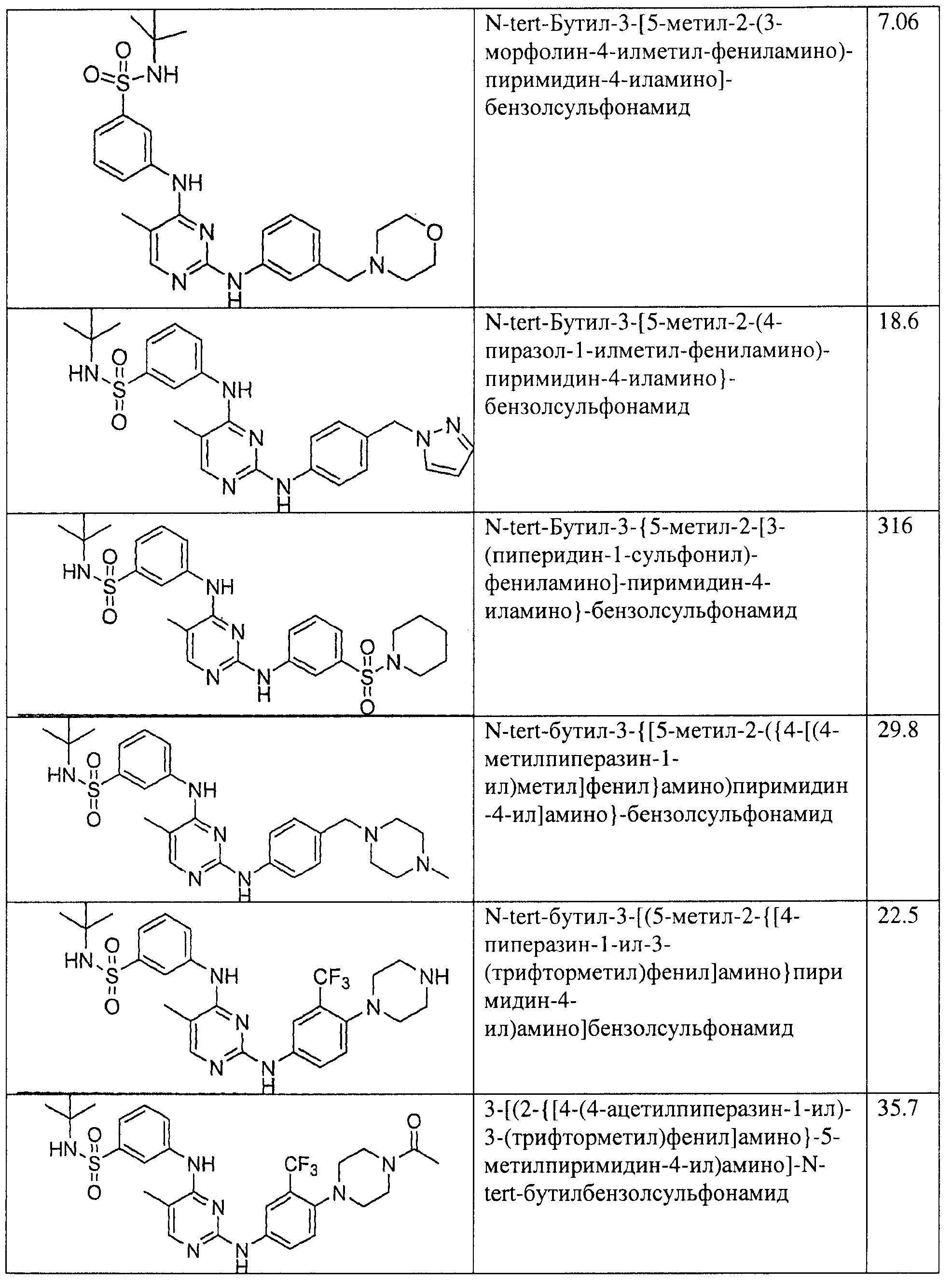
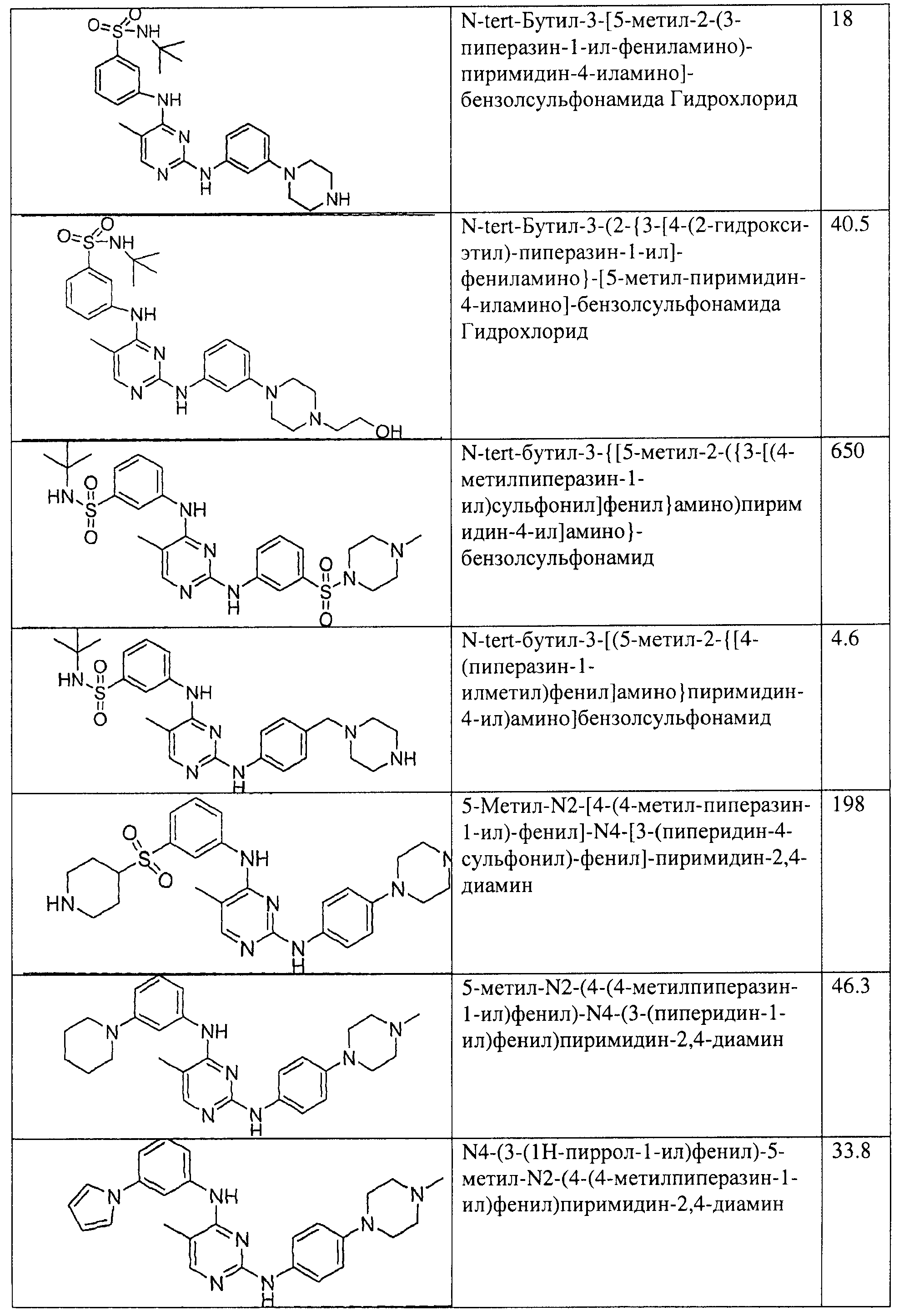
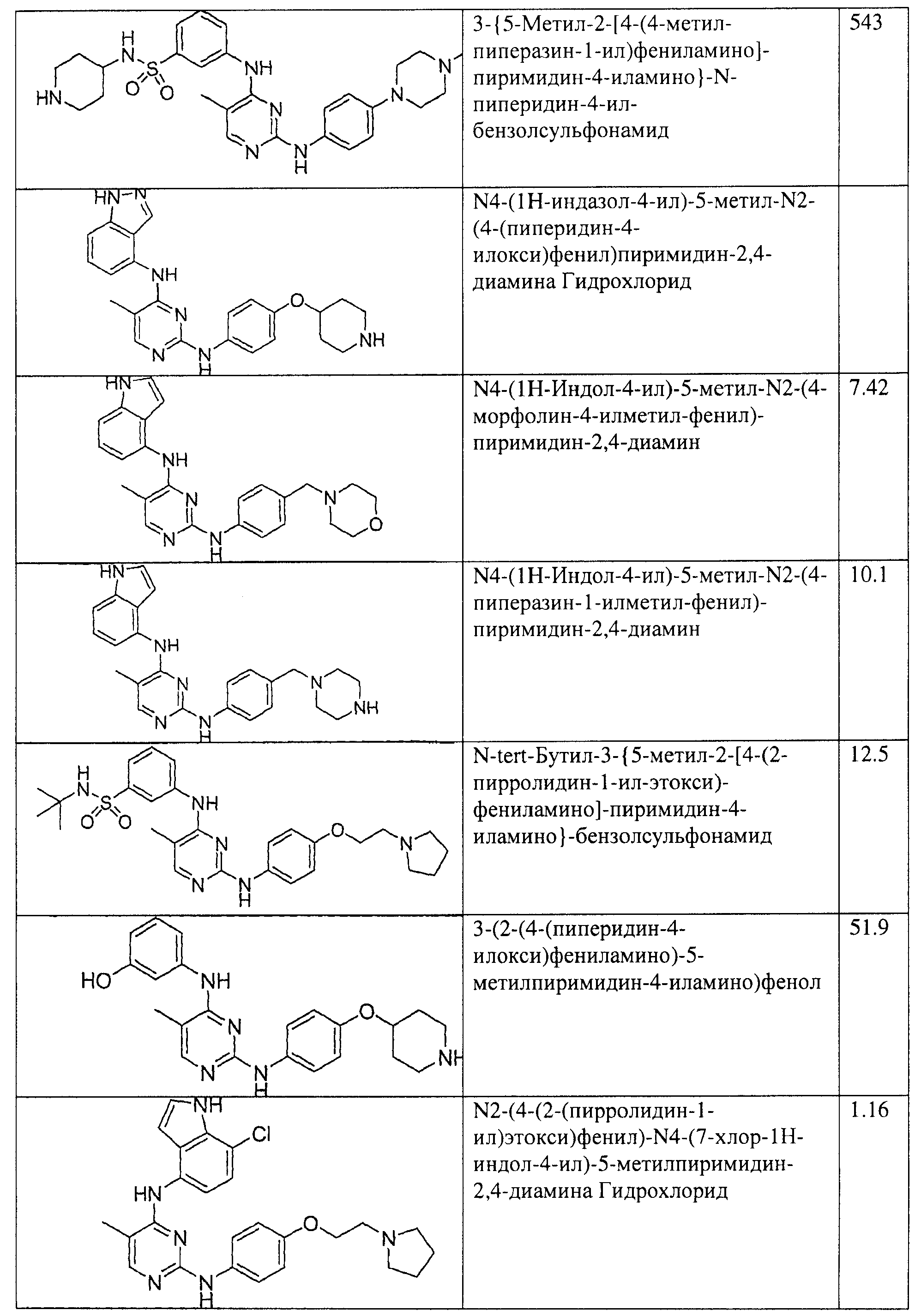
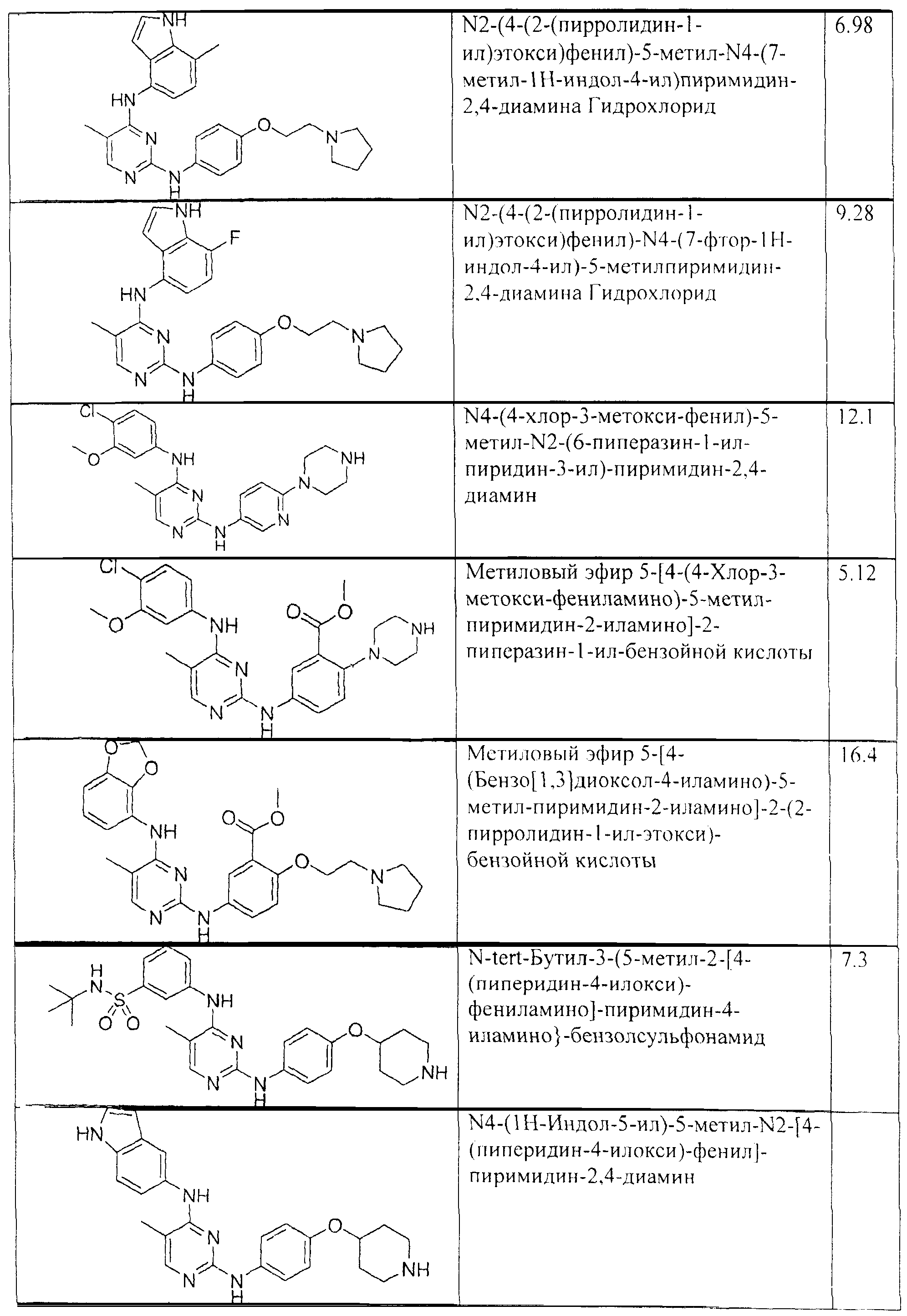
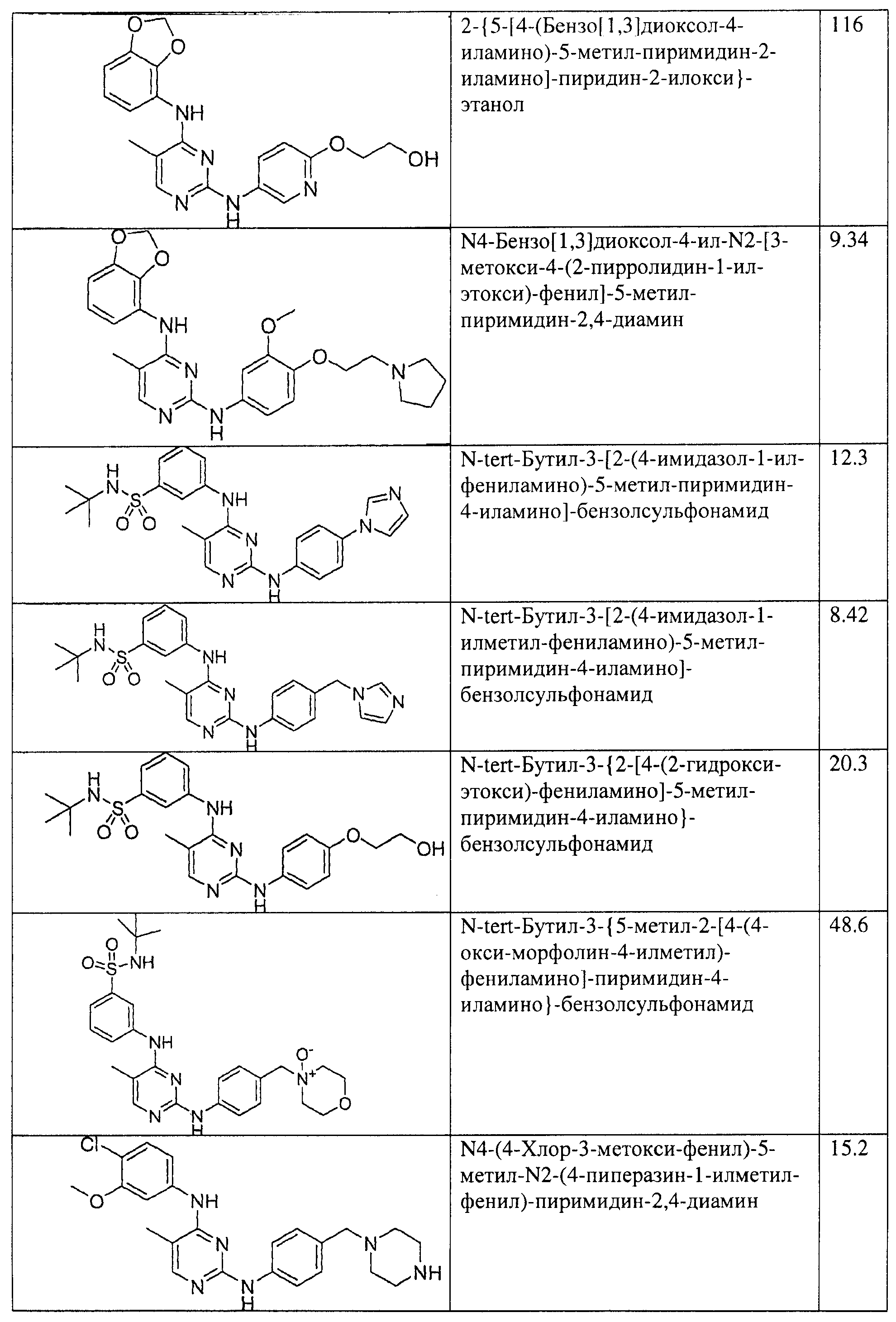
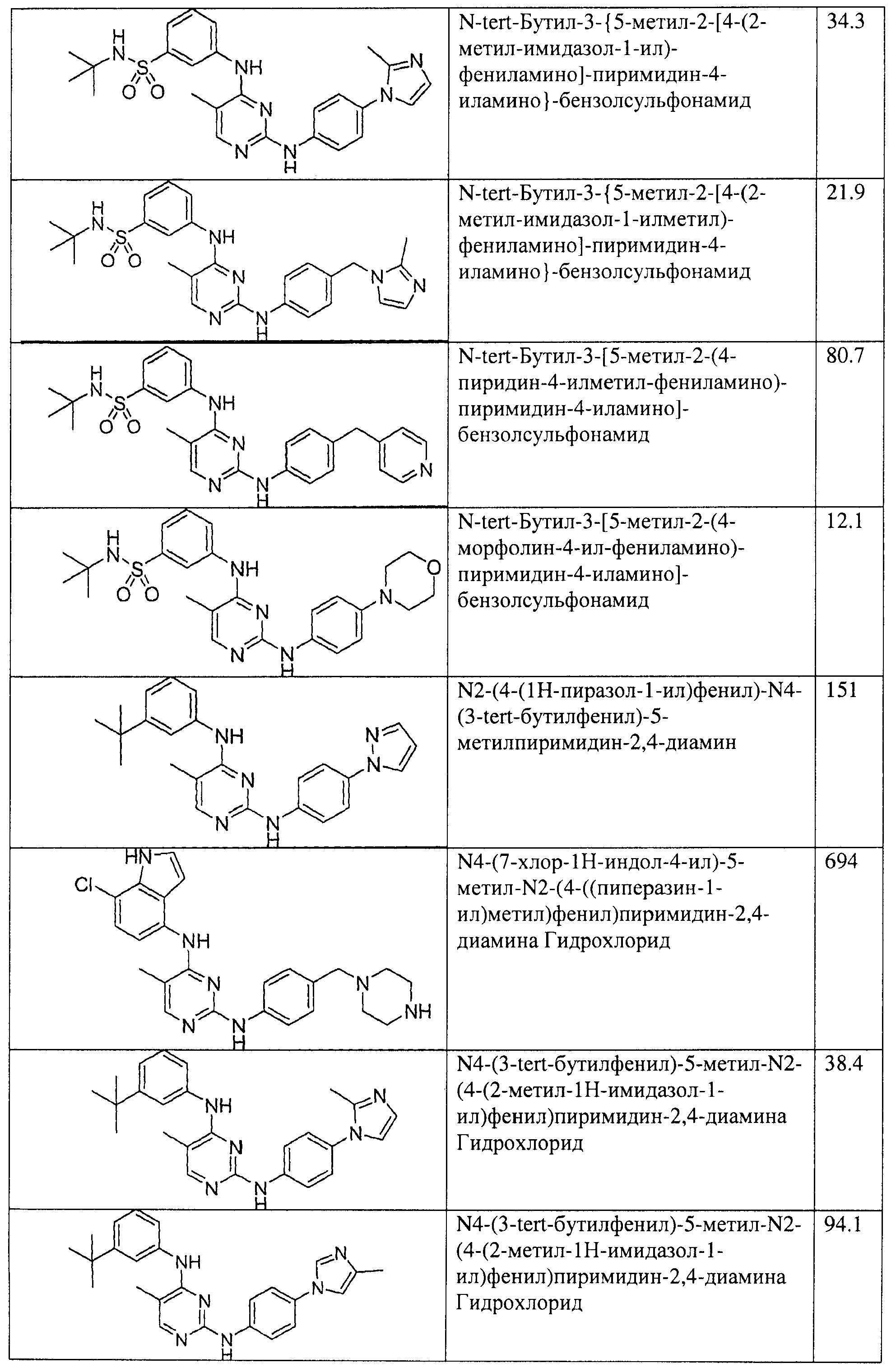
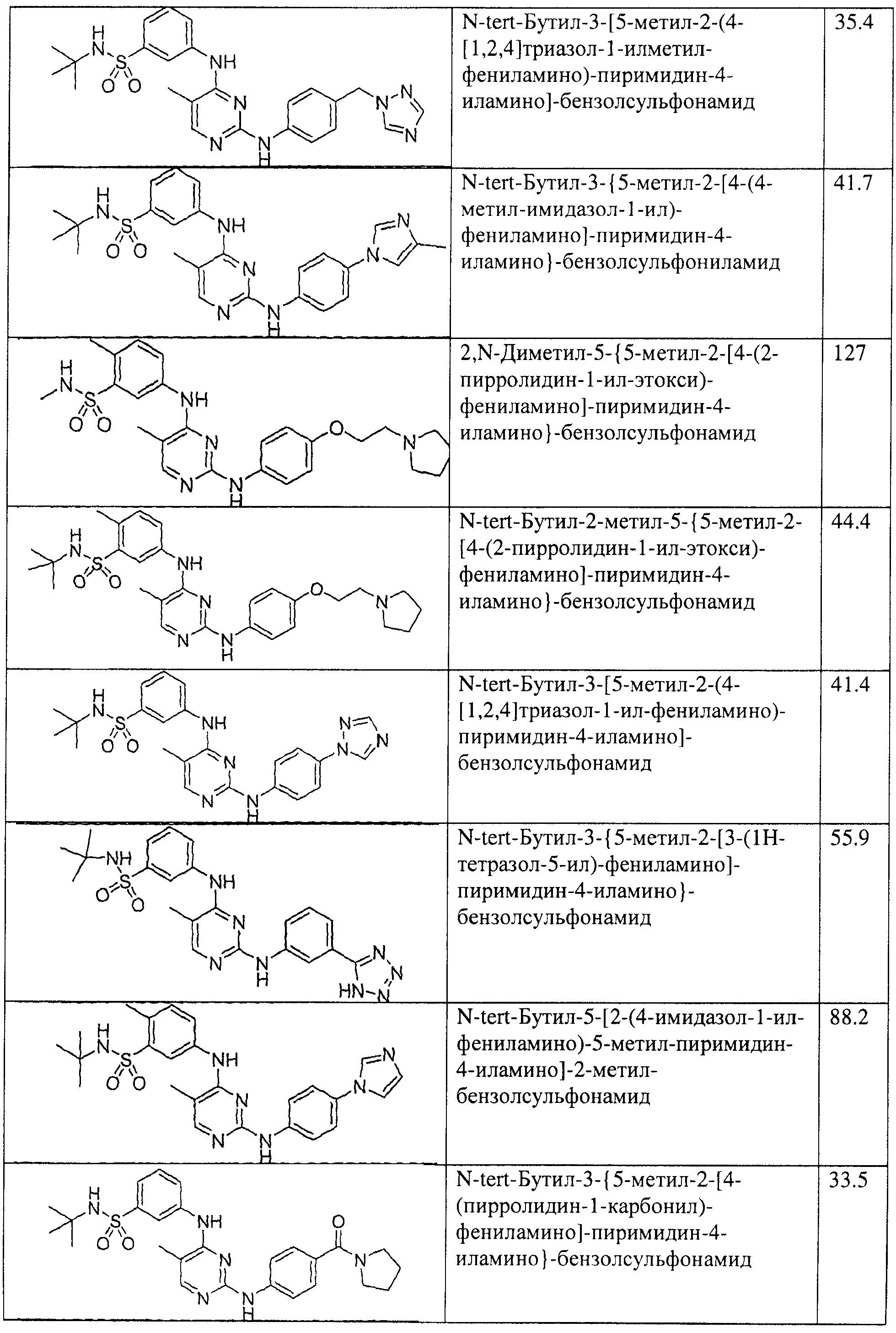
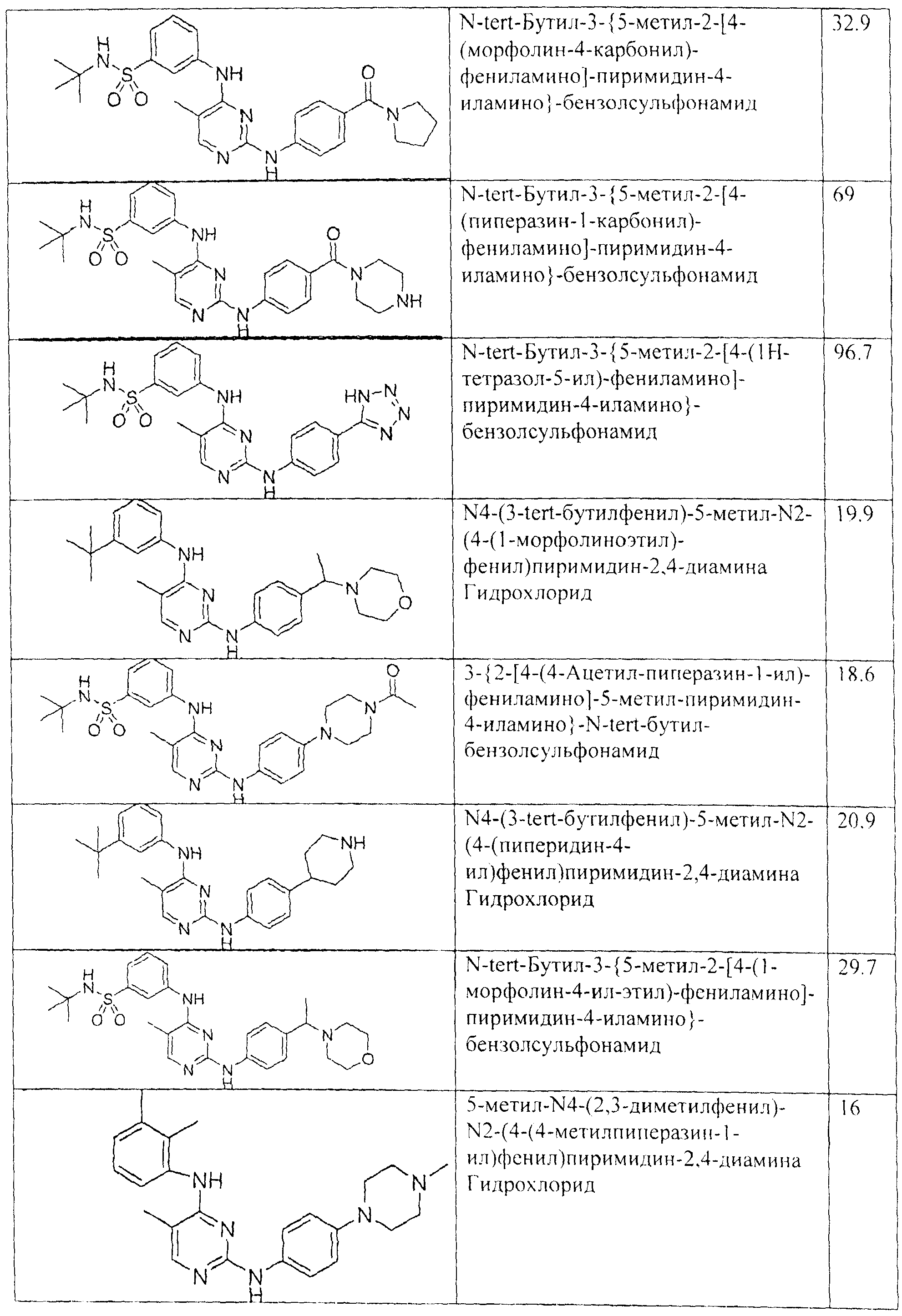
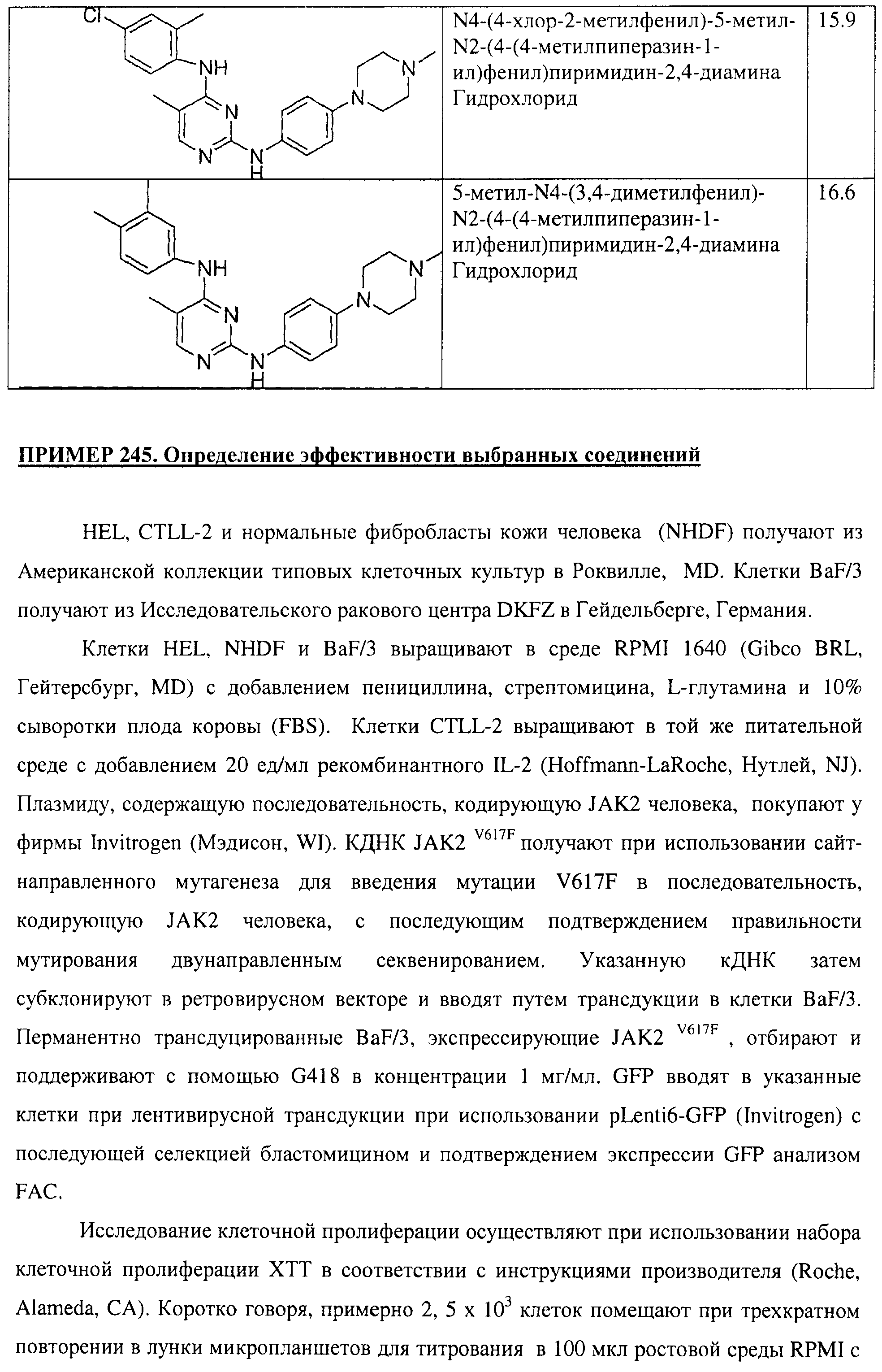
Настоящее соединение относится к новым би-арил-мета-пиримидинам, соответствующим структуре (А) и их фармацевтически приемлемым солям. Соединения обладают ингибирующей активностью в отношении семейства JAK киназ, в частности JAK2 киназ, и могут быть использованы при лечении миелопролиферативного заболевания, которое является следствием генных или белковых слияний, в результате повышения функции киназы из семейства JAK киназ в клеточной передаче сигнала, а также при лечении истинной полицитемии, первичной тромбоцитопении, миелоидного фиброза с миелоидной метаплазией, пролиферативной диабетической ретинопатии, рака или заболевания глаз. В структуре (А): ! ! Х выбран из группы, состоящей из связи О и СН2, a Y представляет собой связь; или Х и Y вместе могут представлять собой связь; каждый R1 и R2 независимо друг от друга выбран из группы, состоящей из Н и незамещенного С1-С6алкила; каждый из р, q, r, n, m независимо друг от друга представляет собой целое число 0 или 1; Go выбран из группы, состоящей из N и СН; каждый G представляет собой независимо СН, N, CR6 или С, когда связан с X, при условии, что не более, чем две группы G представляют собой N, и каждый R6 не зависит от другого R6; R5 представляет собой метил, ! Значения других радикалов указаны в формуле изобретения. 11 н. и 55 з.п. ! ф-лы, 3 табл., 246 пр.
Формула
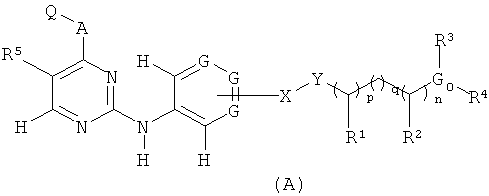
где Х выбран из группы, состоящей из связи О, и СН2, a Y представляет собой связь; или Х и Y вместе могут представлять собой связь;
каждый R1 и R2 независимо друг от друга выбран из группы, состоящей из Н и незамещенного C1-С6алкила;
каждый из р, q, r, n, m независимо друг от друга представляет собой целое число 0 или 1;
G0 выбран из группы, состоящей из N и СН;
при условии, что если G0 означает N, тогда:
каждый R3 и R4 независимо друг от друга выбран из группы, состоящей из C1-С6алкила; или R3 и R4, взятые вместе с G0 могут образовывать гетероароматическую или гетероциклическую 5-6-членную кольцевую систему, содержащую 1-4 атома азота и необязательно один атом кислорода в цикле;
при условии, что если G0=CH, тогда:
каждый R3 и R4 независимо друг от друга выбран из группы, состоящей из Н, незамещенного С1-С6гидроксиалкила,
или R3 и R4 вместе могут образовывать остаток, выбранный из группы, состоящей из (CHR9)r-NR9-(CHR9)m, где каждый r и m независимо друг от друга представляют собой целое число 1 или 2;
каждый G представляет собой независимо СН, N, CR6 или С, когда связан с X, при условии, что не более чем две группы G представляют собой N, и каждый R6 не зависит от другого R6;
R5 представляет собой метил;
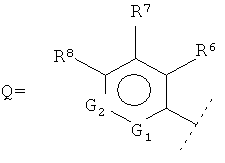
каждый из R6, R7 и R8 независимо друг от друга выбран из группы, состоящей из Н, незамещенного C1-С6гидроксиалкила, C1-С6гидроксиалкила, замещенного С1-С6алкилом, 5-6-членного гетероарила, содержащего 1-2 атома, выбранных из атома азота и атома кислорода, присоединенного через атом углерода или гетероатом, галогена, CF3, -OCF3, SO2-гетероцикла, SO2N(С1-С6алкила)Н, SO2N(С1-С6алкила) (С1-С6алкила), SO2NH(С3-С6циклоалкила), SO2NH-гетероцикла, (SO2N(C1-C6разветвленного алкила)Н, NH2, NH(C1-C6алкила), N(С1-С6алкила) (C1-С6алкила), NO2, CN, CONH2, CONH(С1-С6алкила), CON(С1-С6алкила) (C1-С6алкила), СО(С1-С6алкила), СО-гетероцикла, СООН, СОО(С1-С6алкила) и NHCO-(С1-С6алкила), где каждый из указанных гетероциклических остатков выбирают из 5-6-членного азотсодержащего гетероцикла, и HNCONH-арила; или
каждый из R6 и R7, взятые вместе, или R7 и R8, взятые вместе, или R6 и R8, взятые вместе, образуют остаток, независимо выбранный из группы, состоящей из -HN-СН=СН-, -HN-N=CH-, -O(СН2)O-, -СН=СН-CH=СН-, -N=CH-CH=CH-, -CH=N-CH=CH- и -S-CH=CH-;
при этом замещенный гетероарил или гетероцикл имеют один заместитель, выбранный из группы, состоящей из C1-С6ацила, и замещенный алкил имеет один заместитель, выбранный из группы, состоящей из 5-6-членного азотсодержащего гетероцикла;
А выбран из группы, состоящей из NH и СН2;
G1 выбран из группы, состоящей из CH и N;
G2 выбран из группы, состоящей из CR7 и N, при этом каждая R7 группа не зависит от другой R7 группы;
или их фармацевтически приемлемая соль.
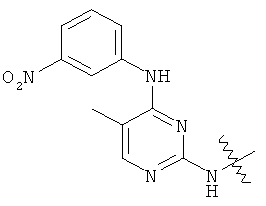

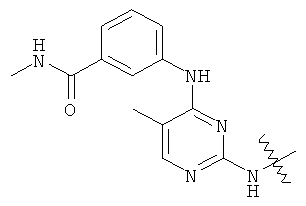
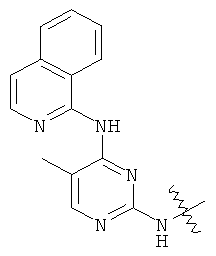
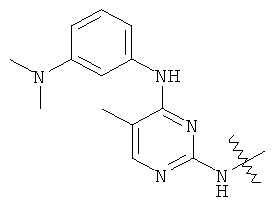
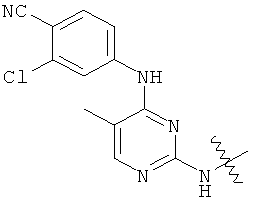
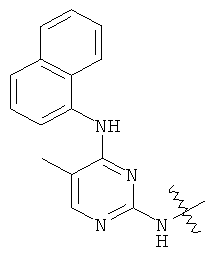
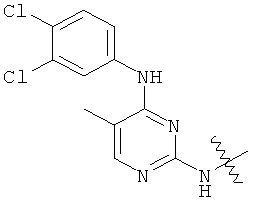
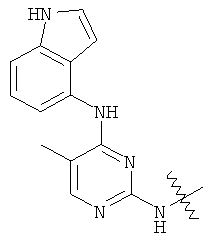
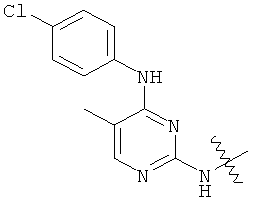
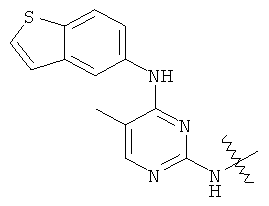
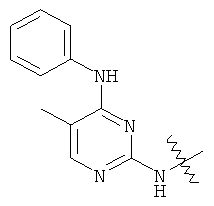
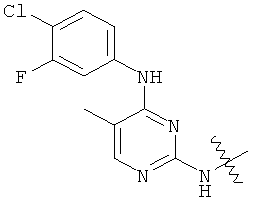
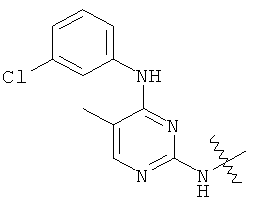
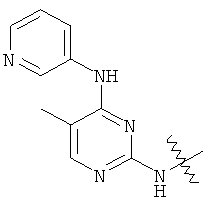
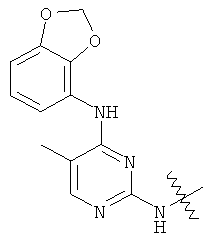
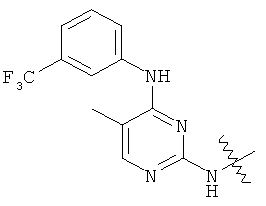
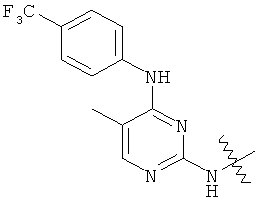
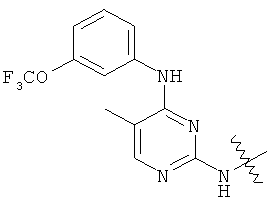
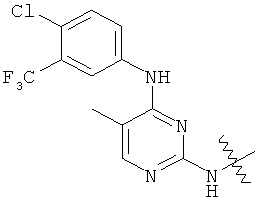
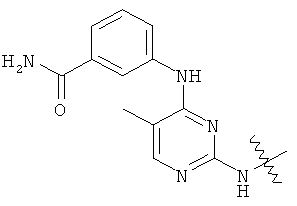
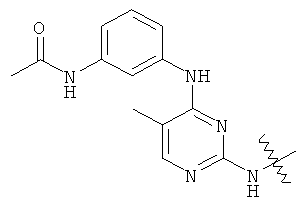
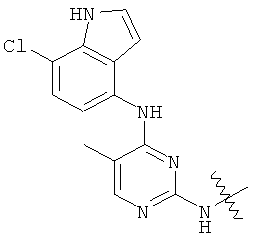
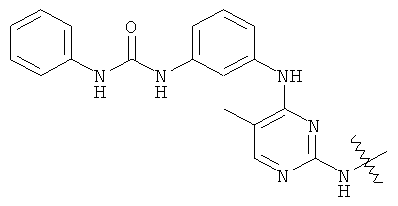
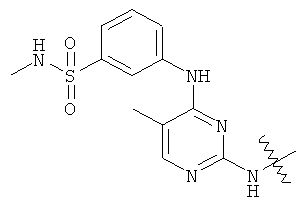
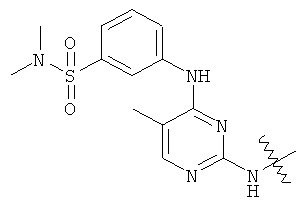
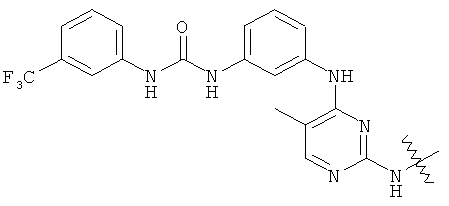
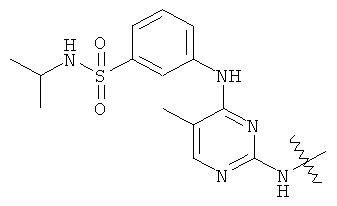
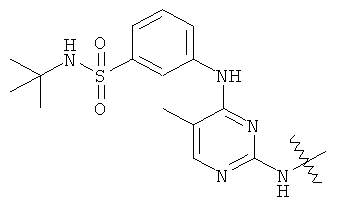
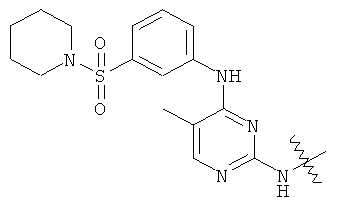
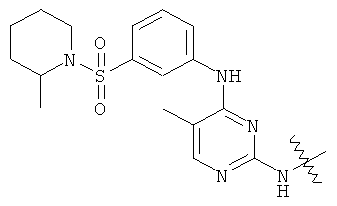
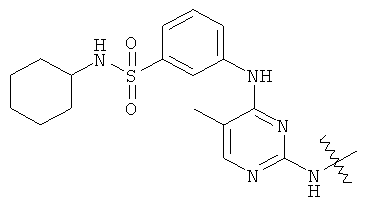
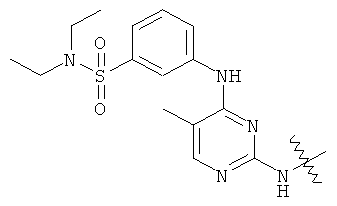
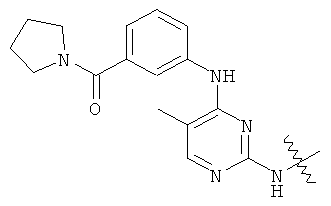
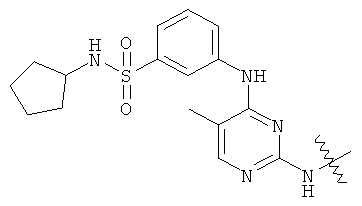
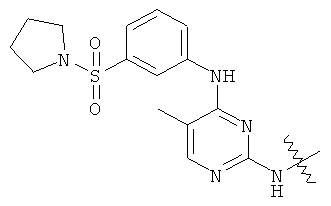
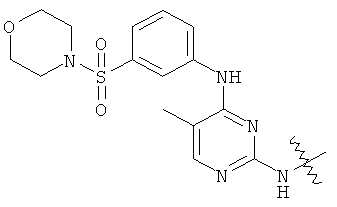
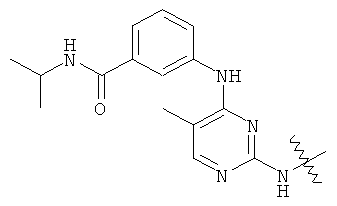
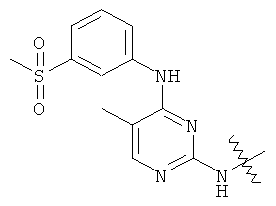
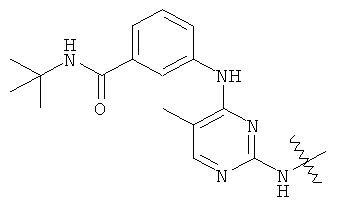
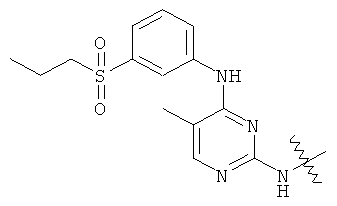
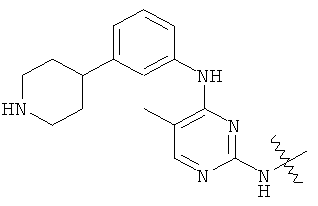
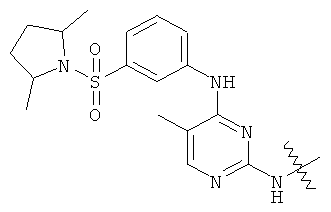
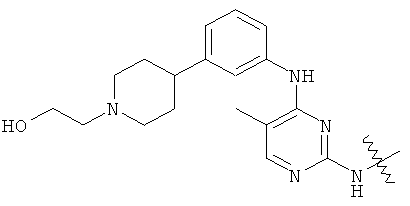
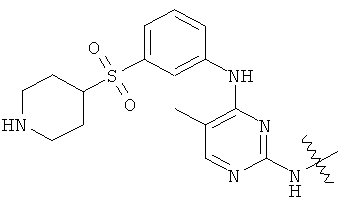
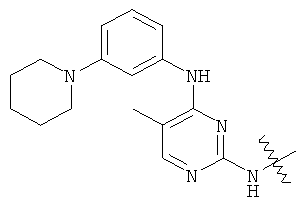
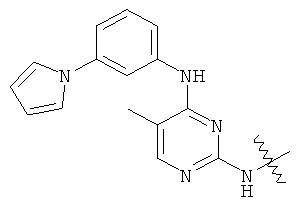
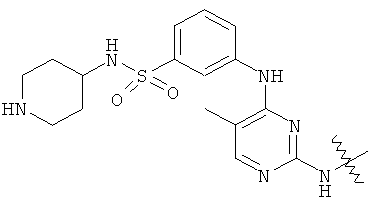

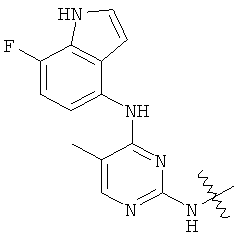
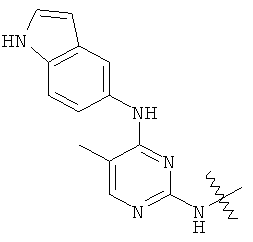
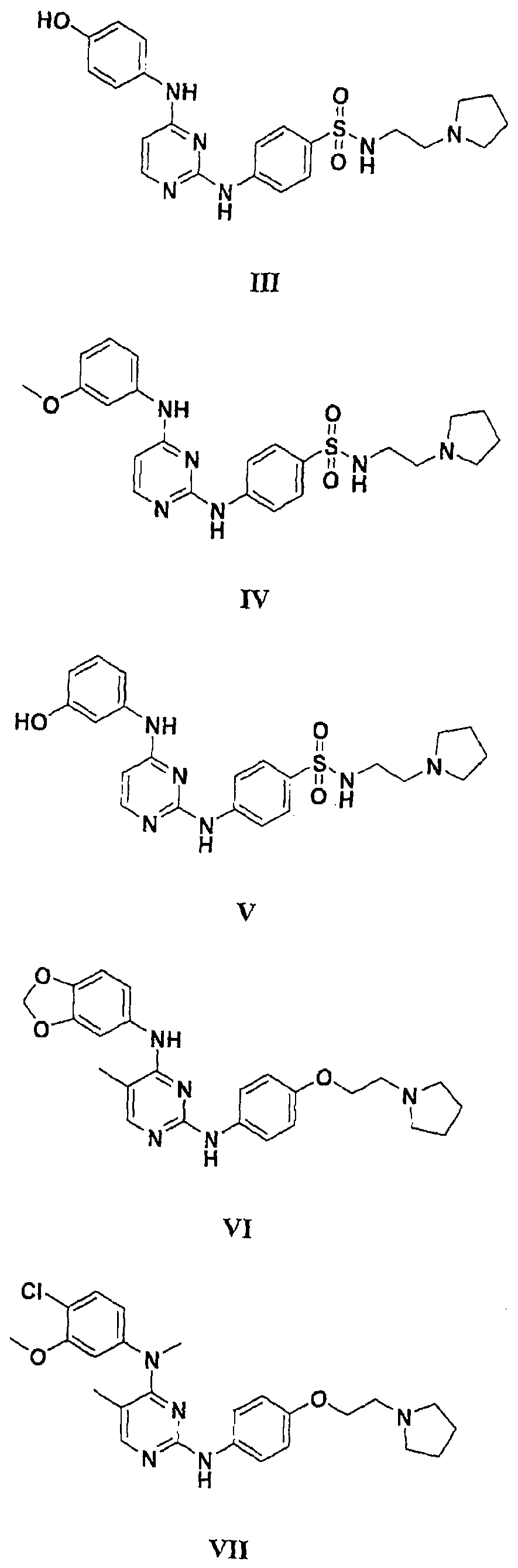
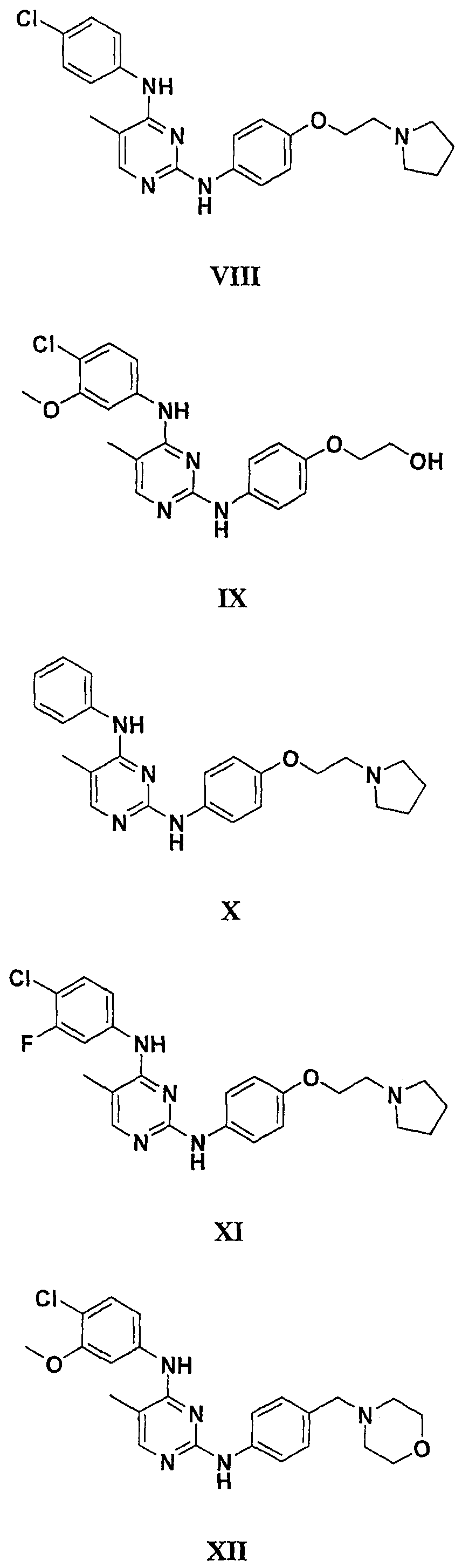
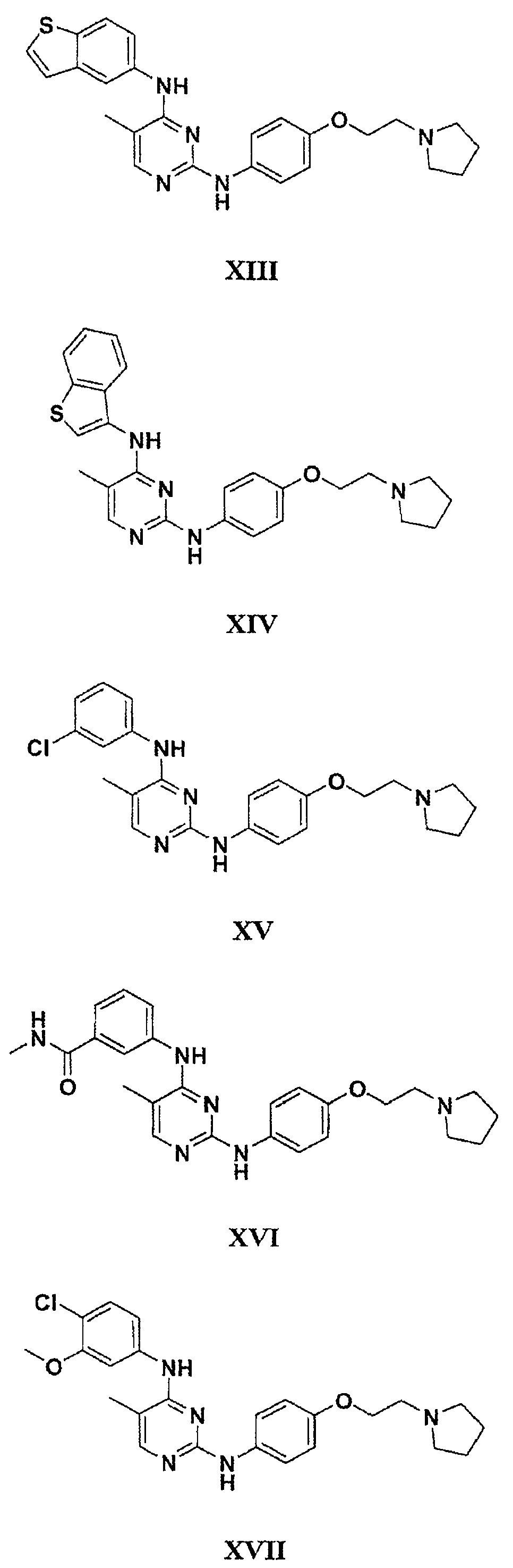
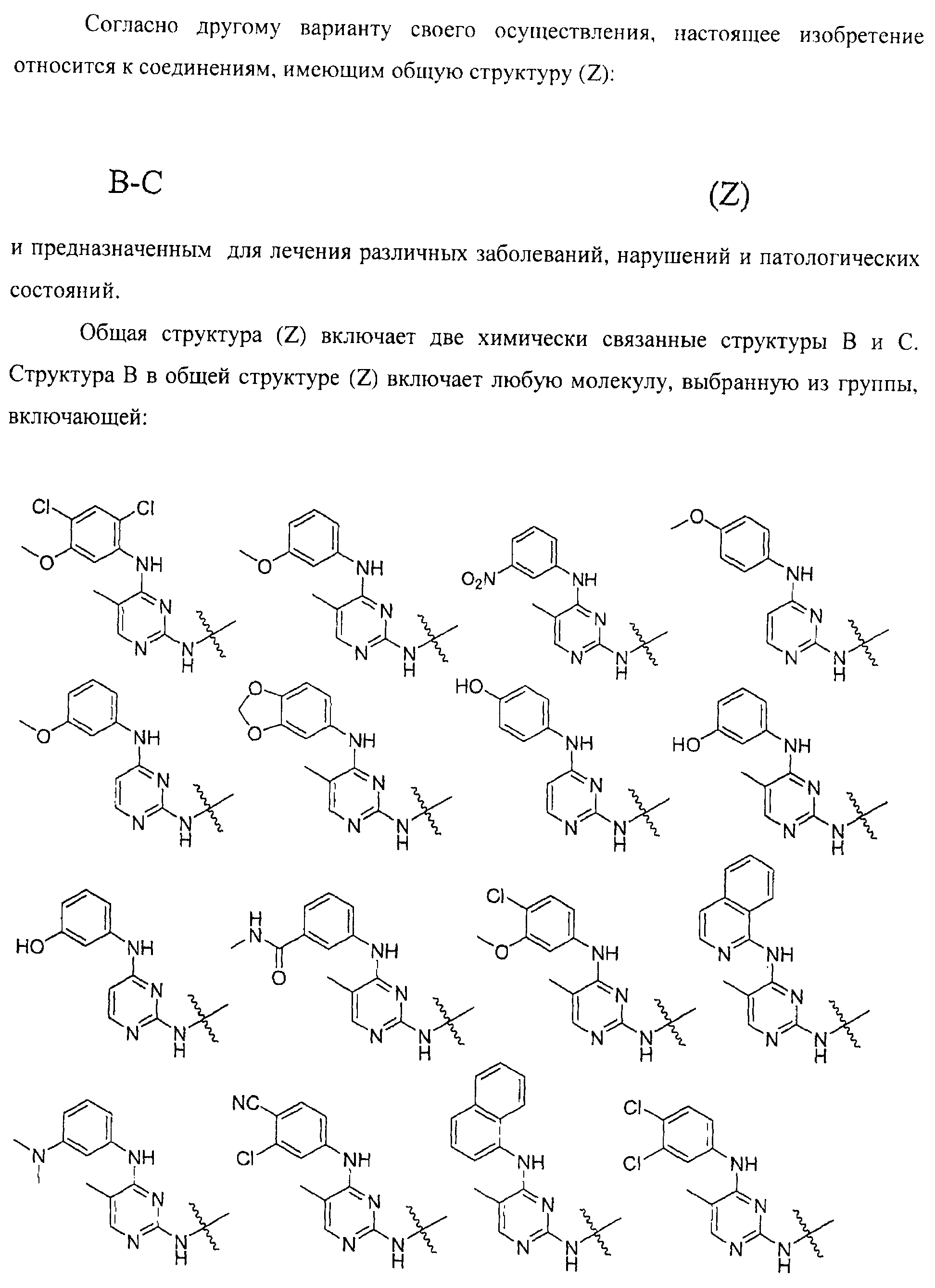
а второй остаток выбран из группы, включающей:
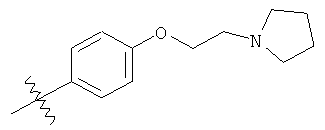
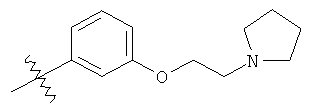
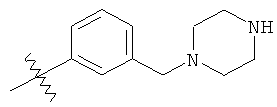
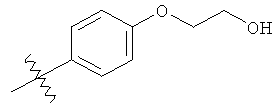
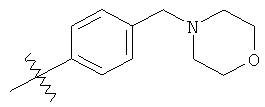
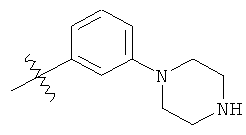
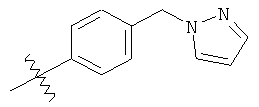
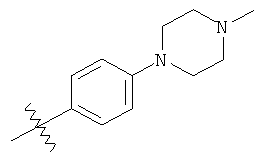
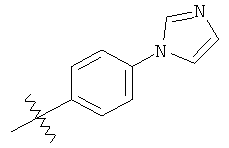
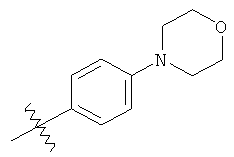
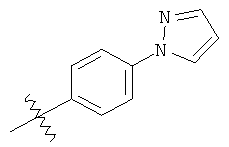
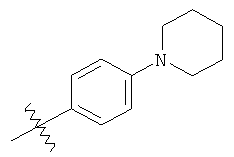
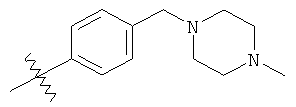
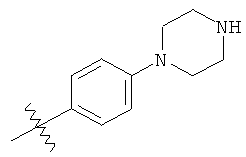
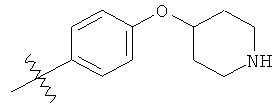
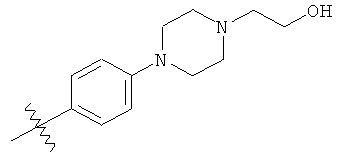
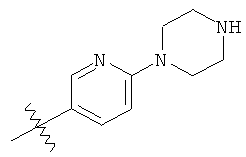
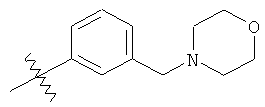
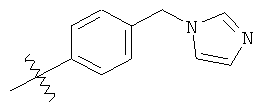
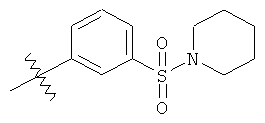
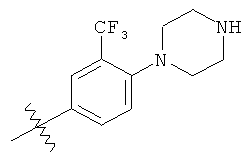
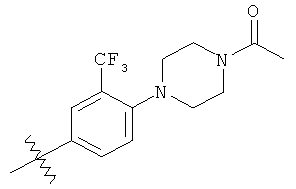
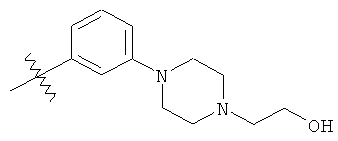
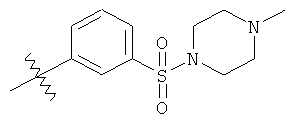
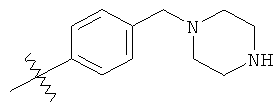
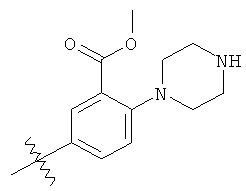
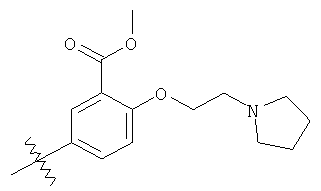
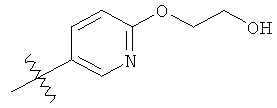
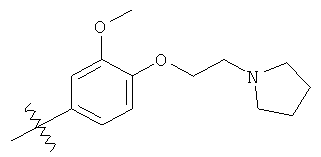
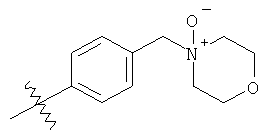
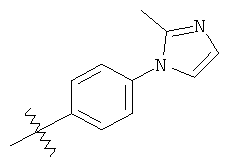
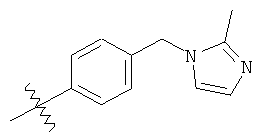
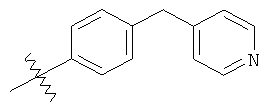
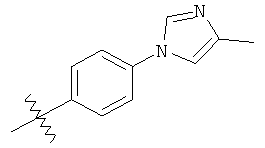
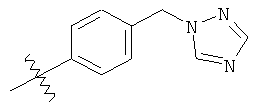
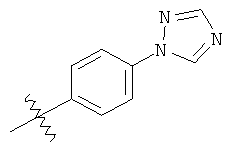
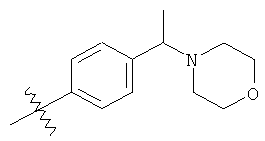
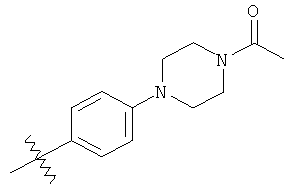
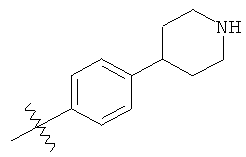
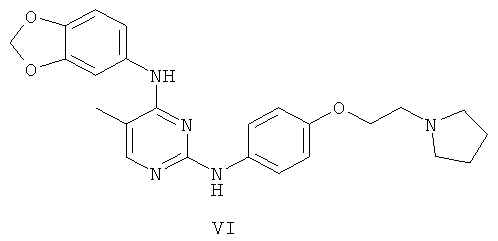
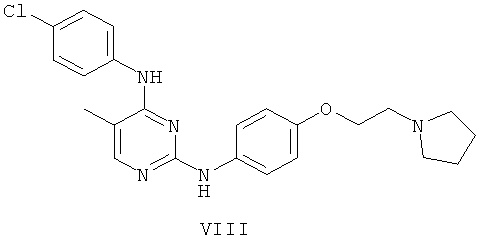
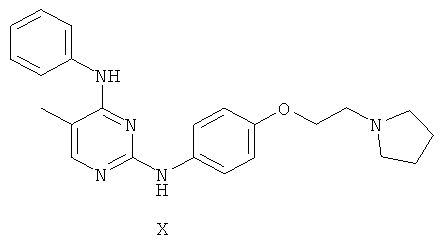
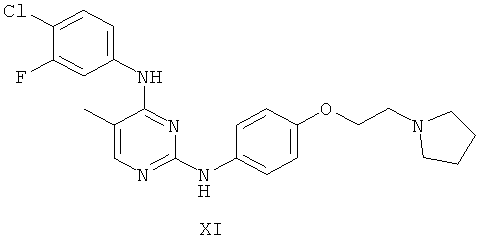
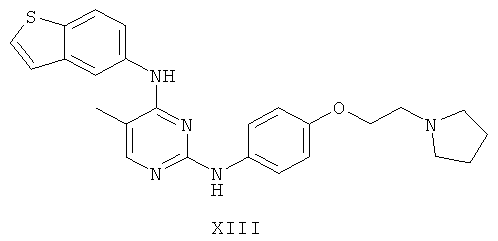
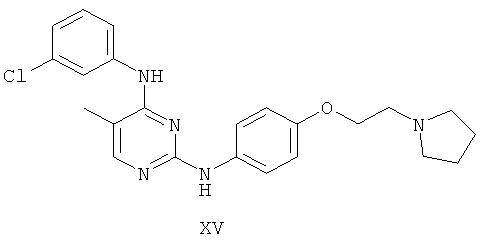
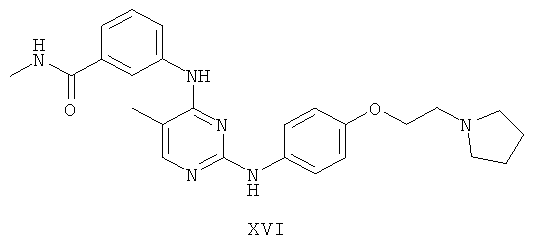
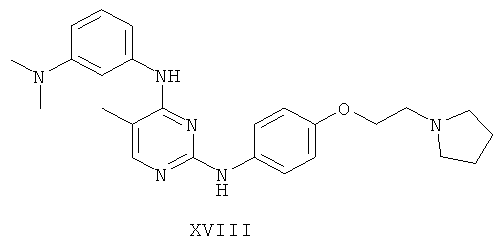
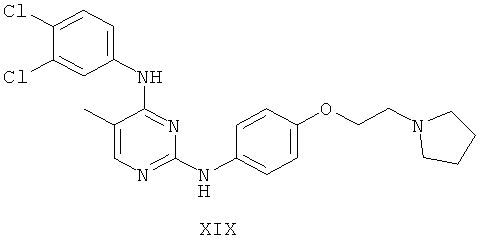
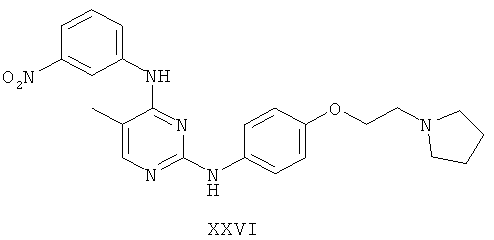
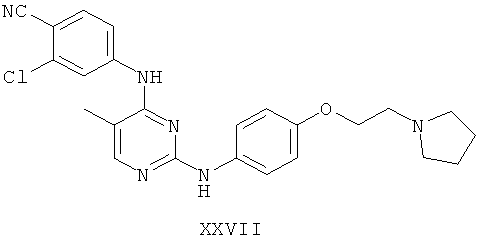
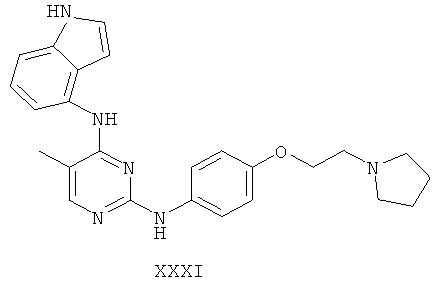
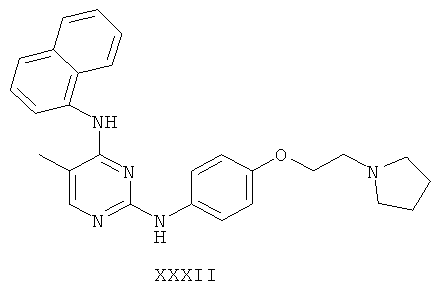
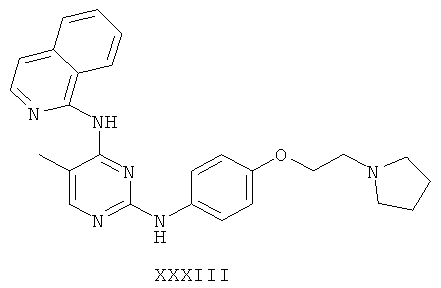
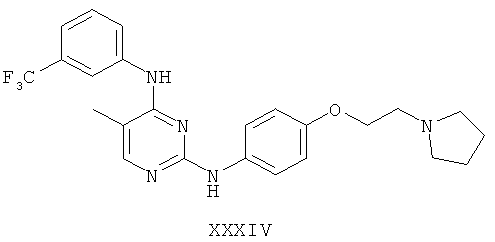
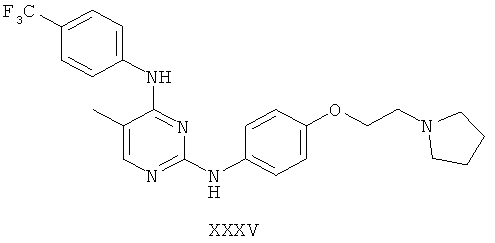
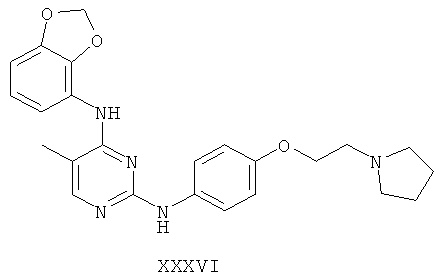

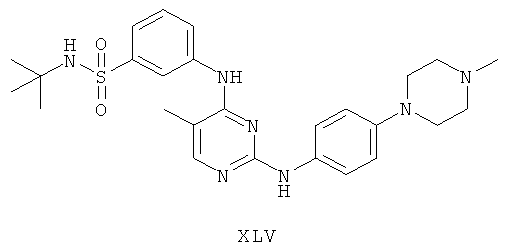
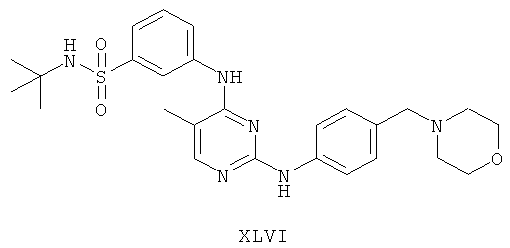
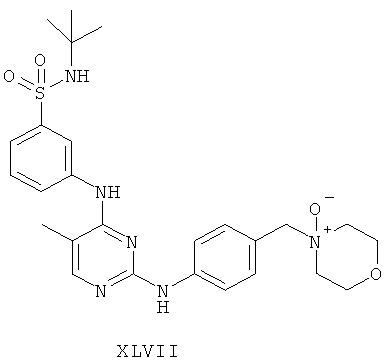
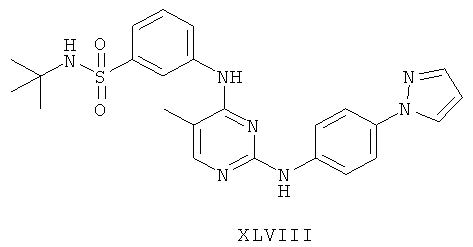
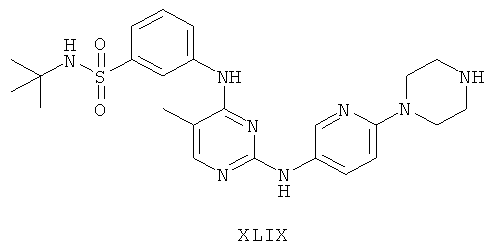
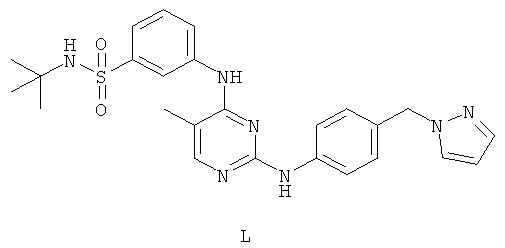
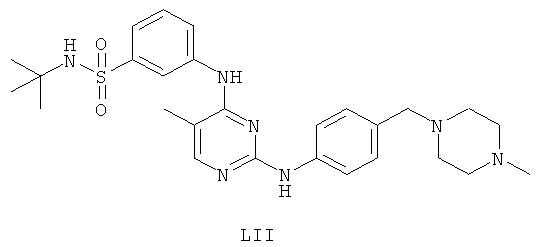
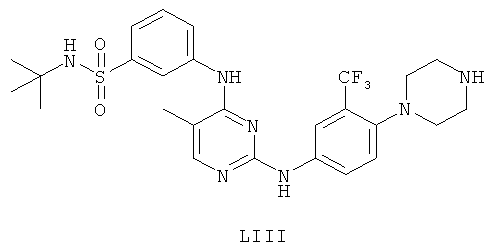
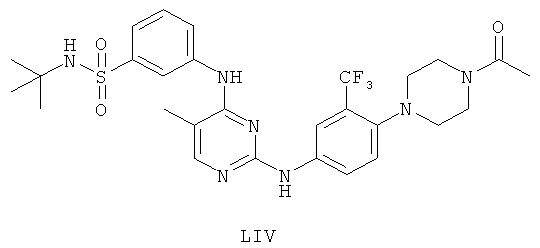
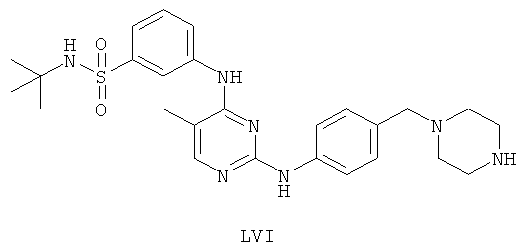
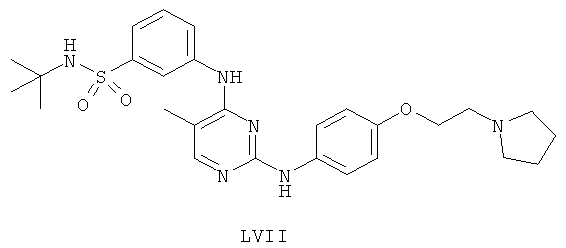
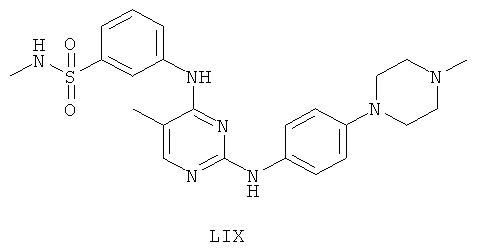
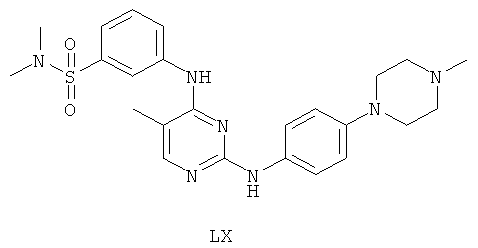
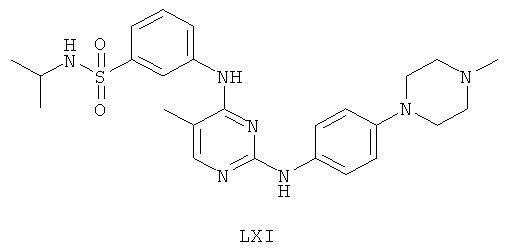
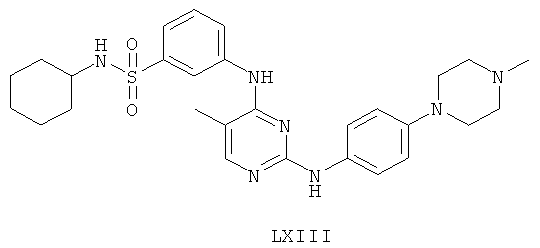
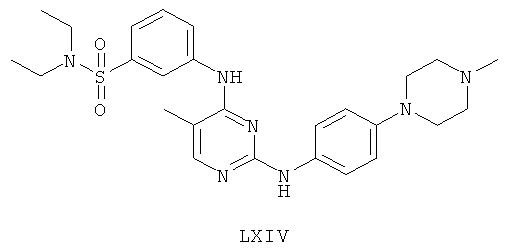
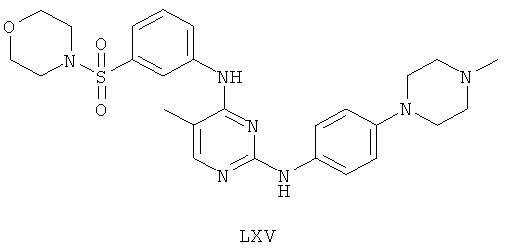
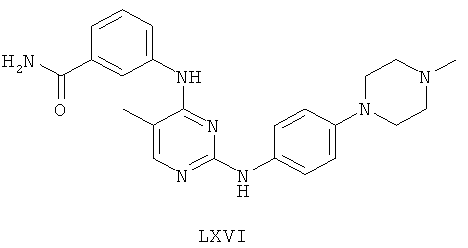
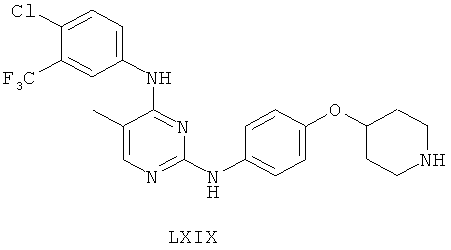
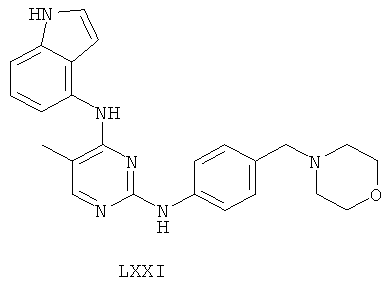
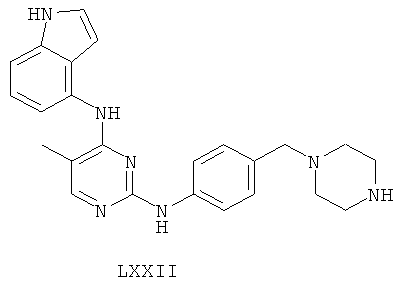

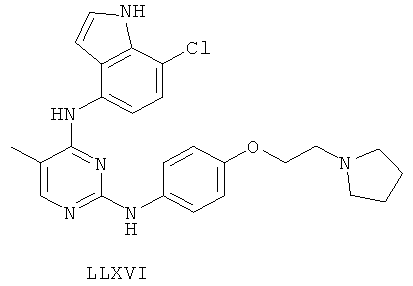
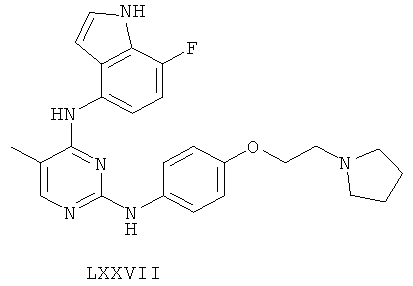
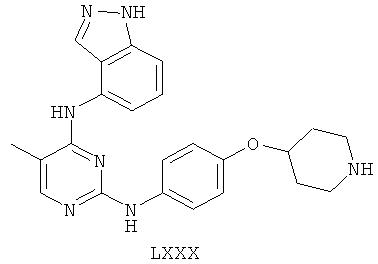
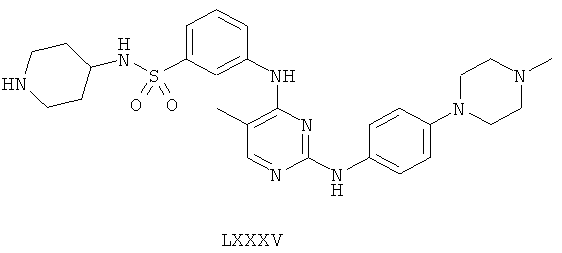
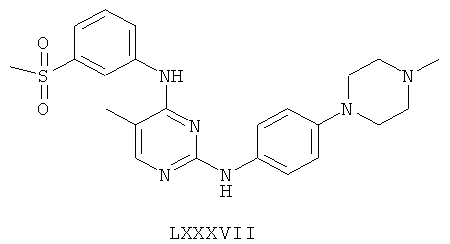
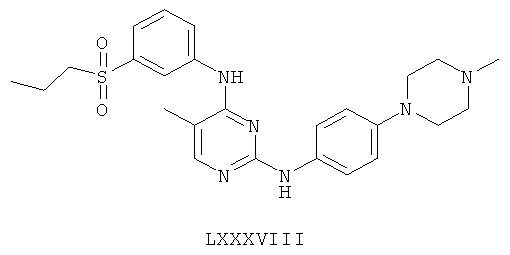
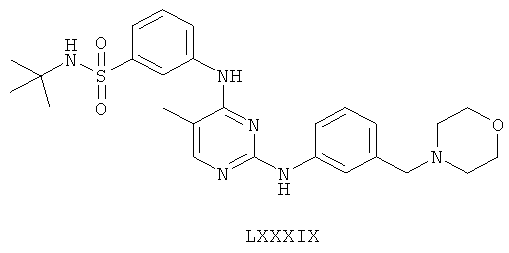
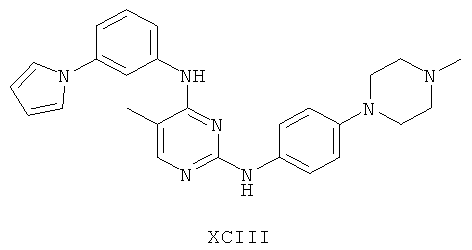
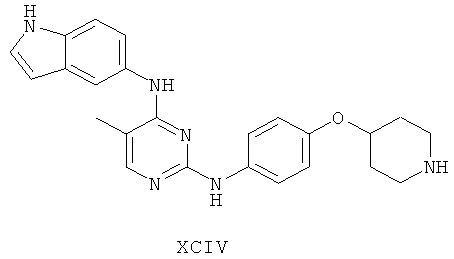
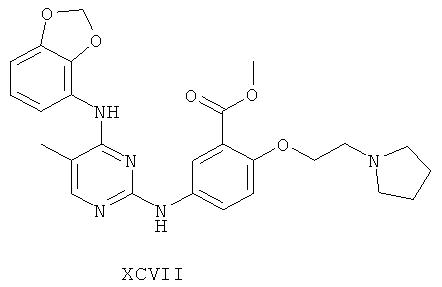
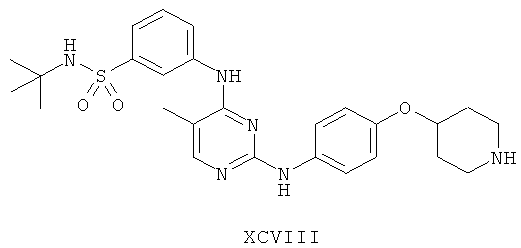
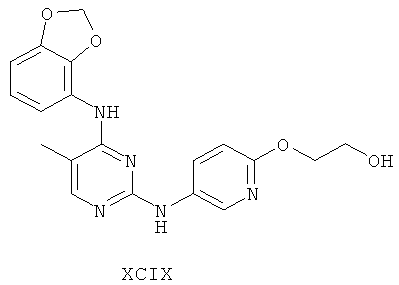
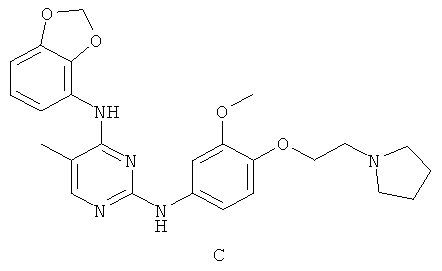
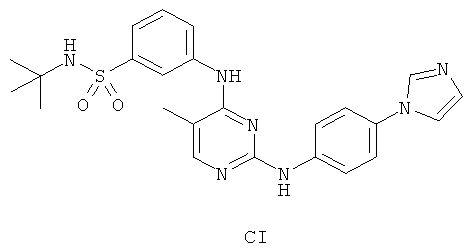
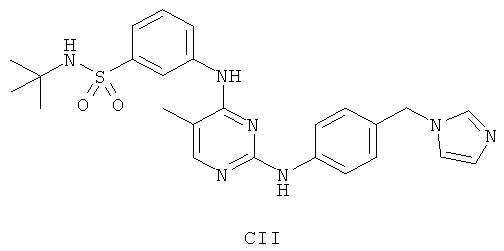
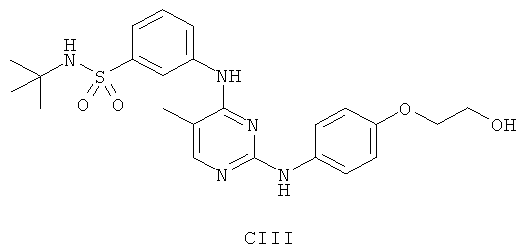
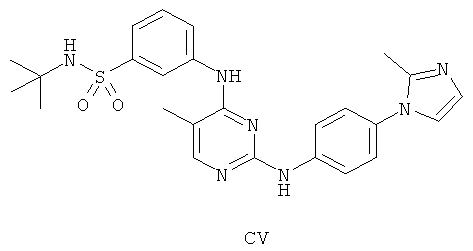
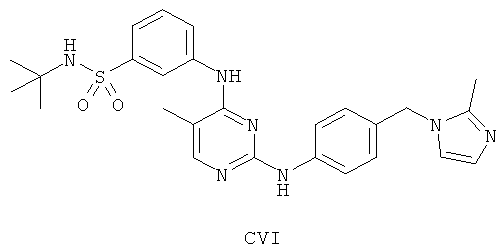
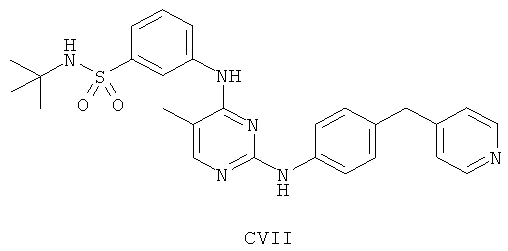
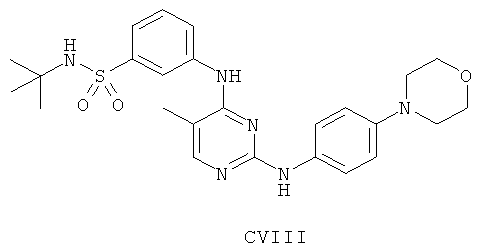
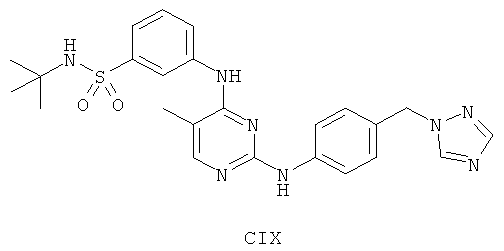
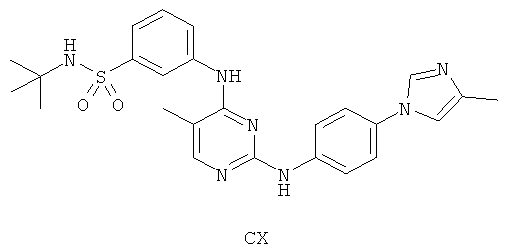
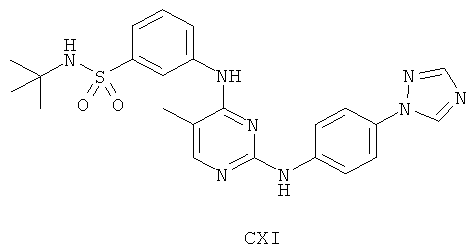
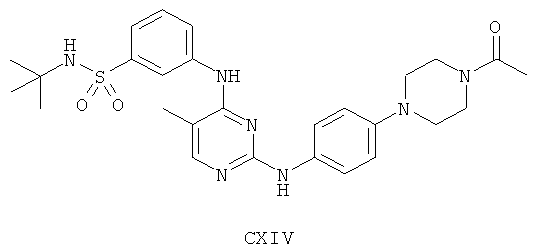
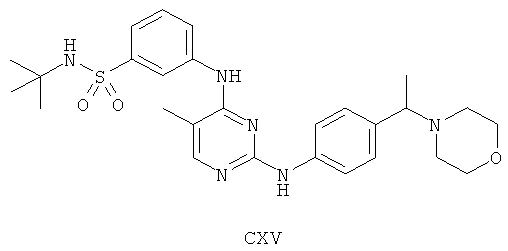
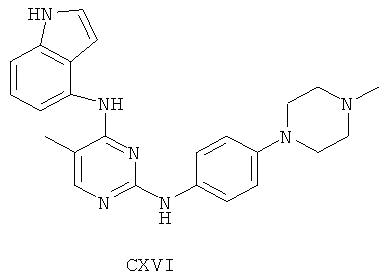
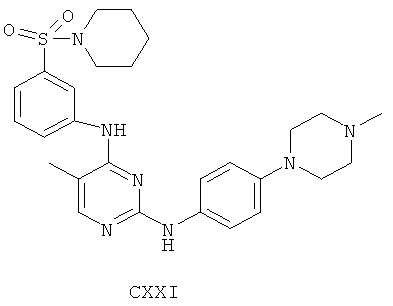
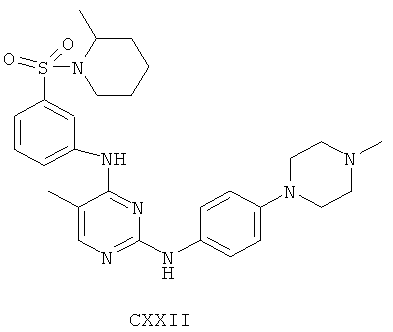
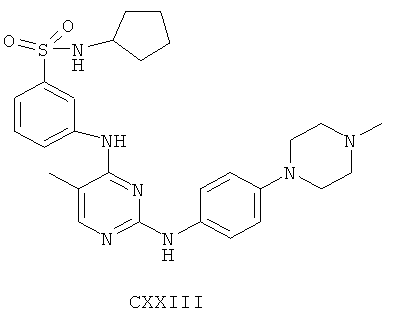
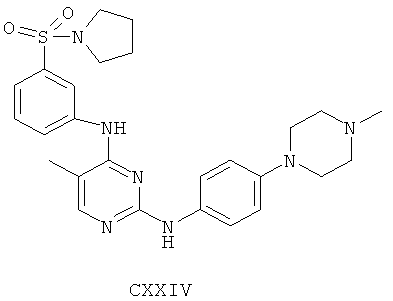
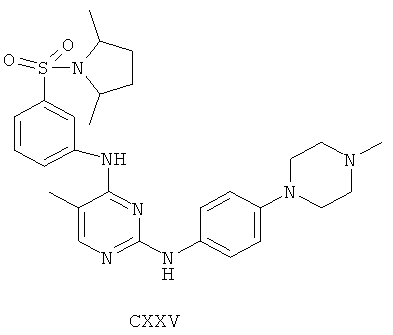
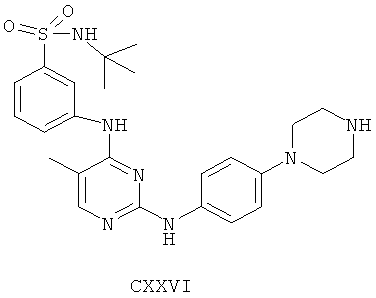
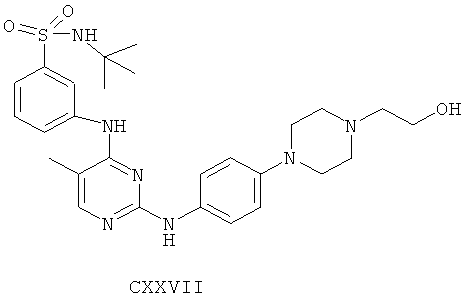
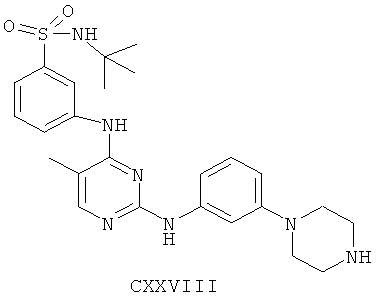
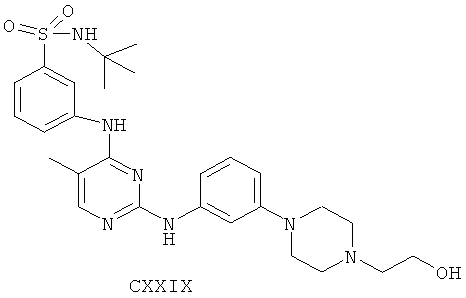
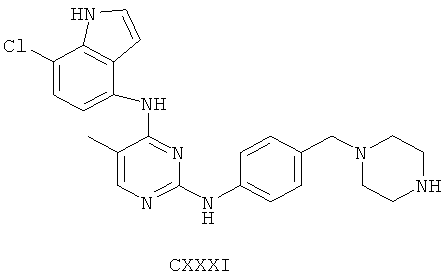
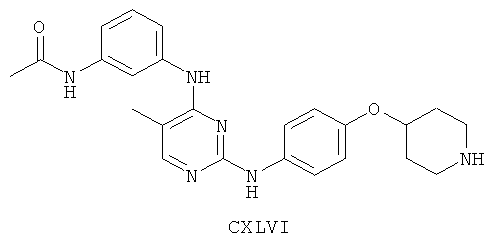
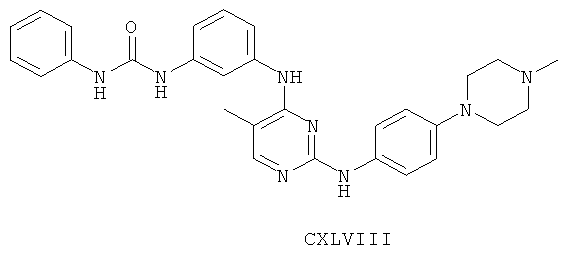
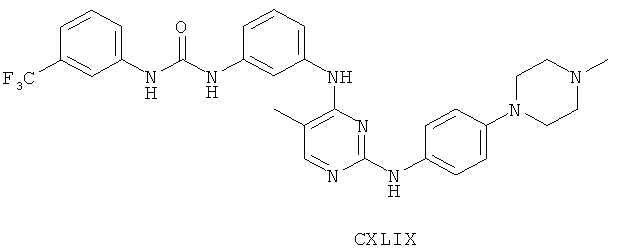
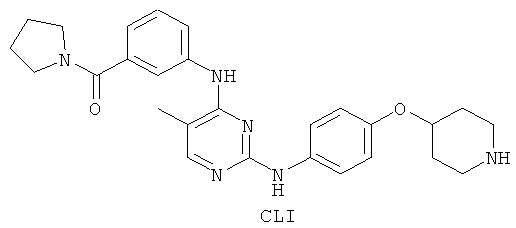
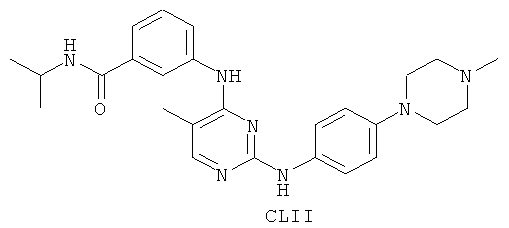
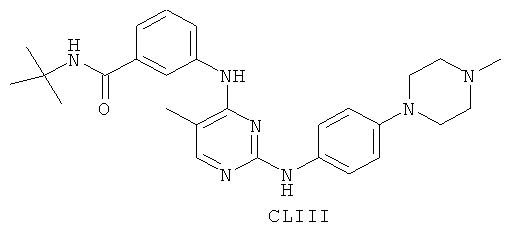
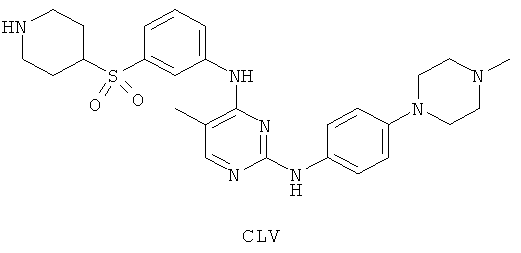
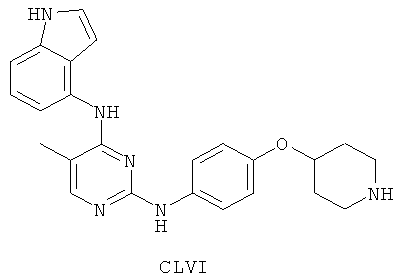
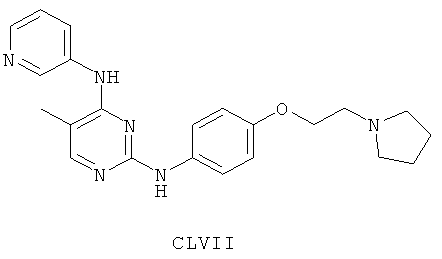
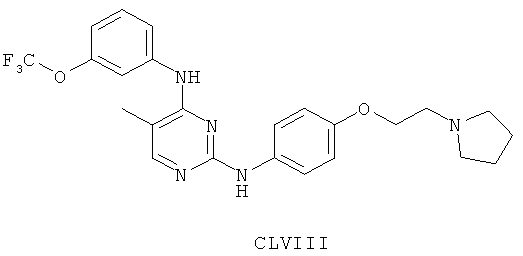
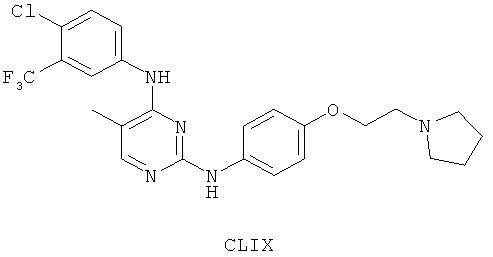
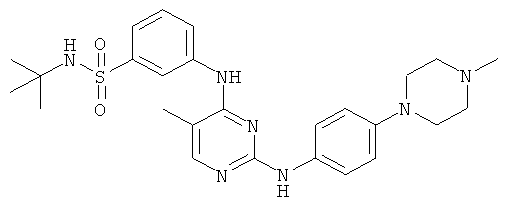
или его фармацевтически приемлемая соль.
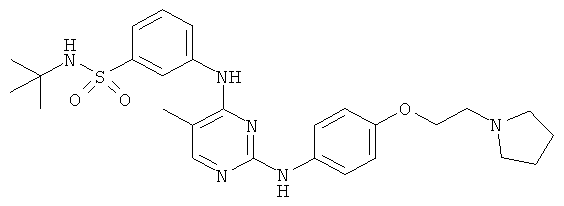
или его фармацевтически приемлемая соль.
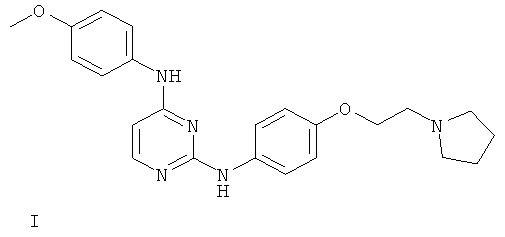
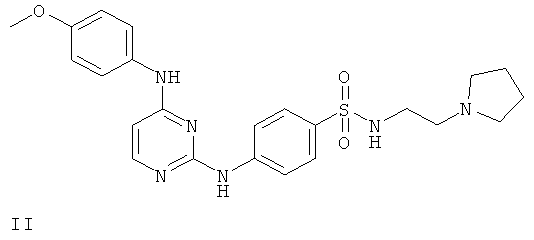
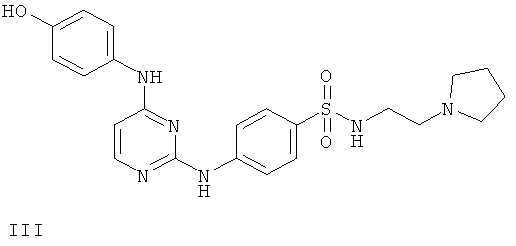
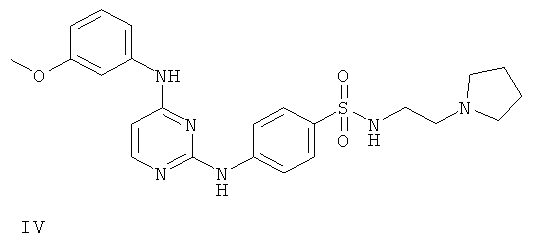
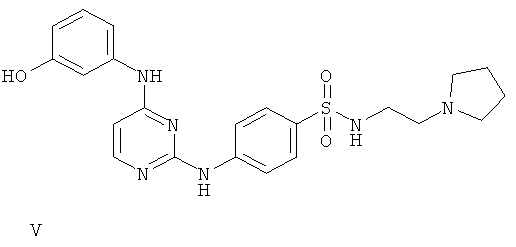
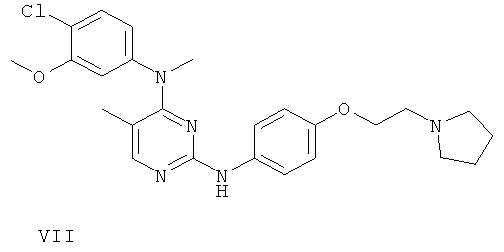
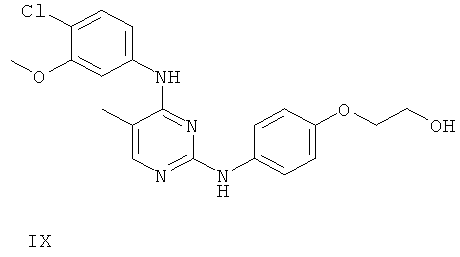
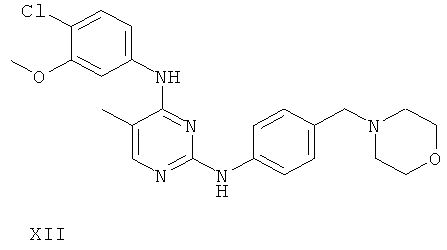
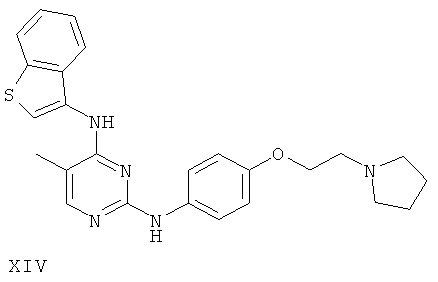
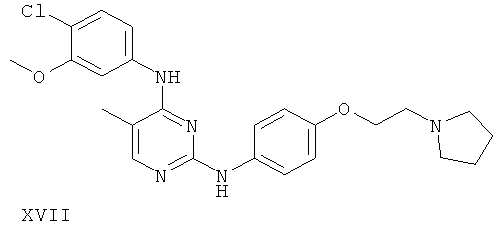
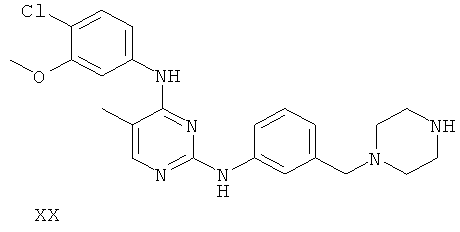
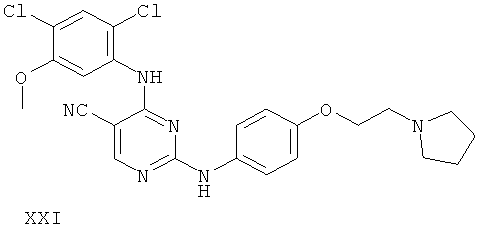
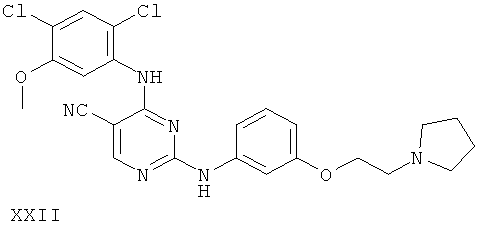
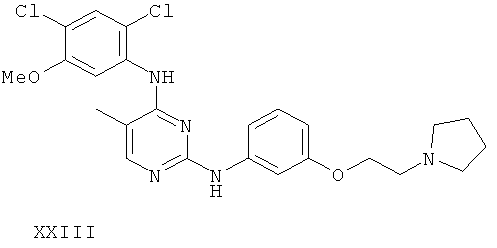
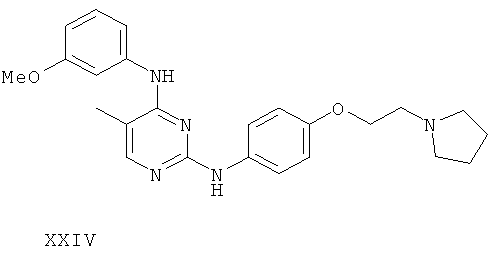
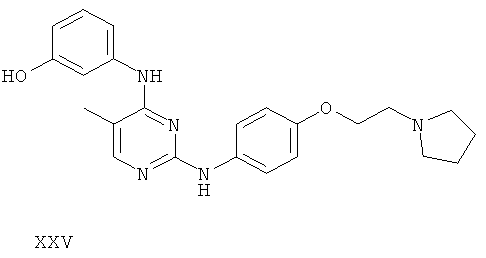
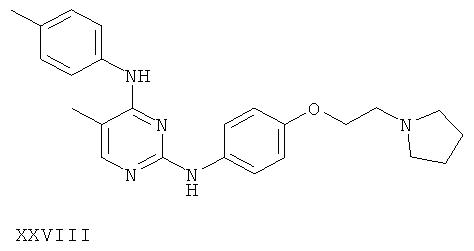
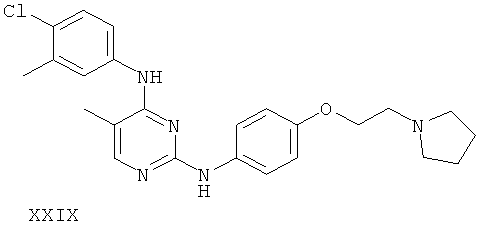
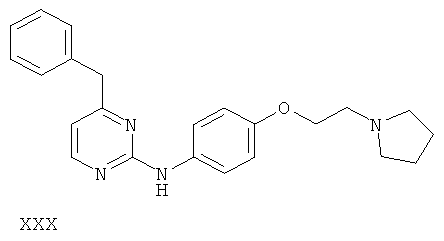
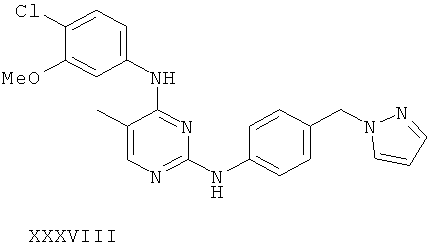
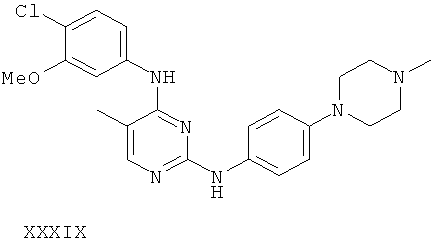

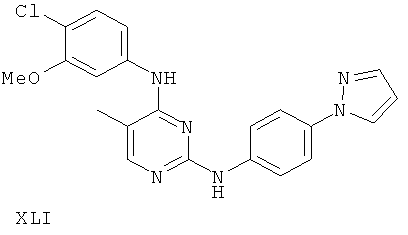
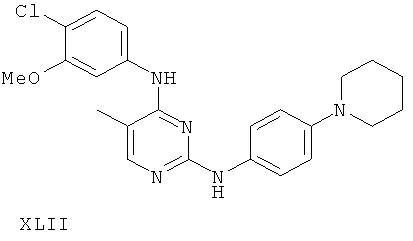
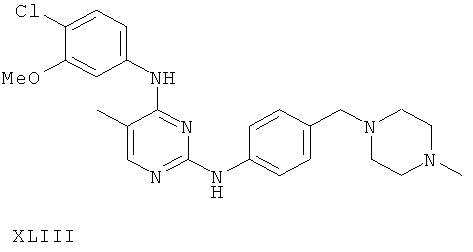
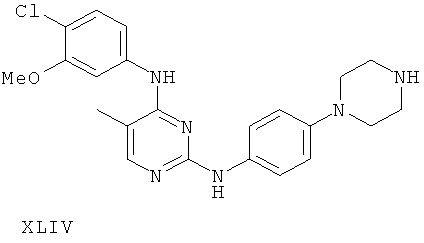
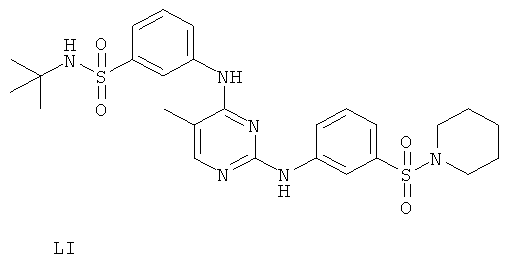
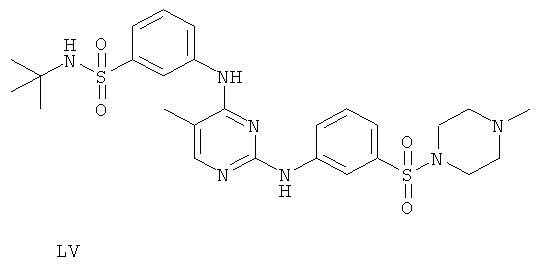
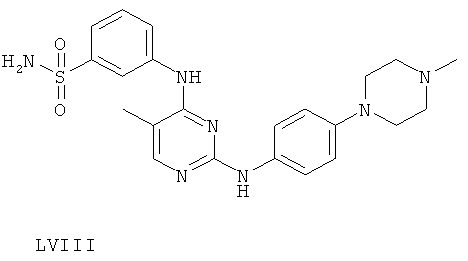
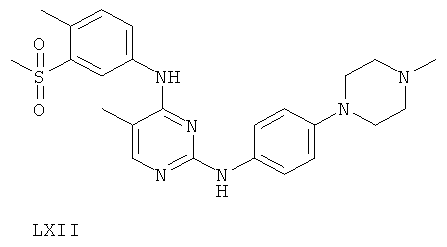
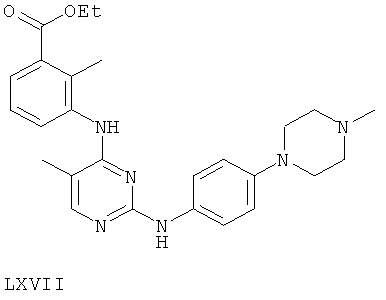
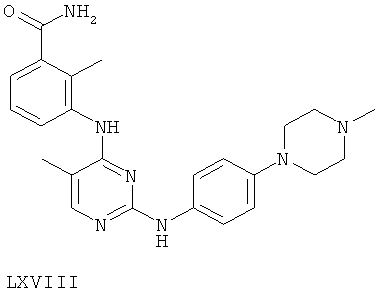
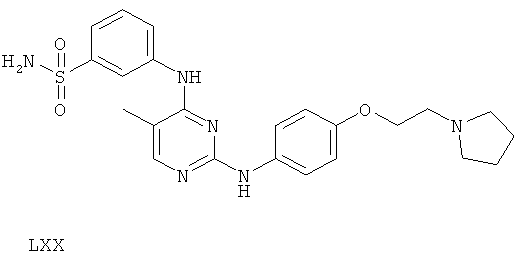
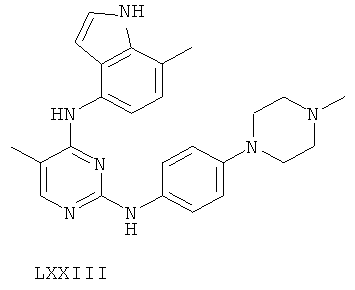
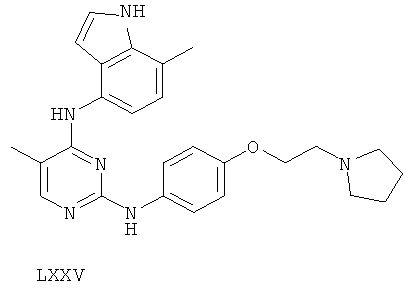
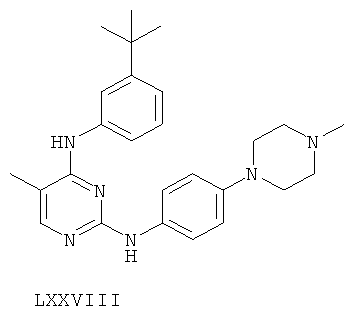
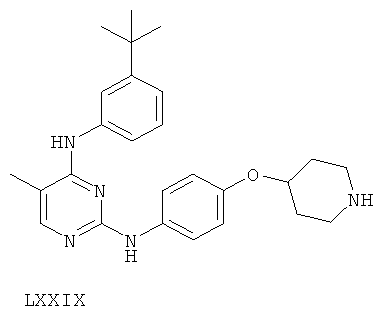
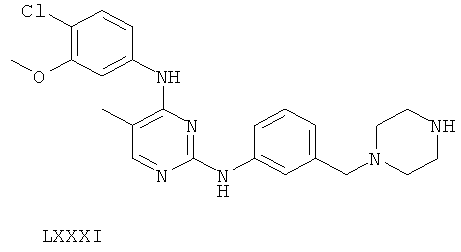
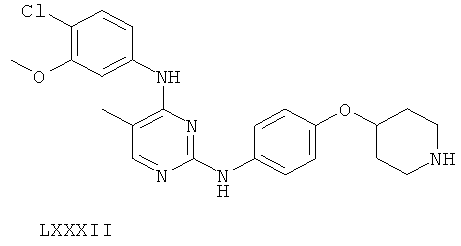
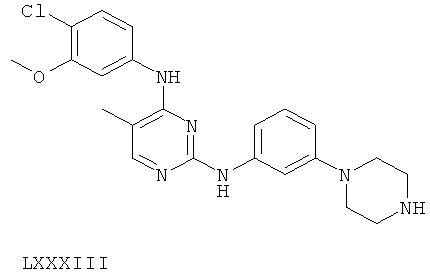
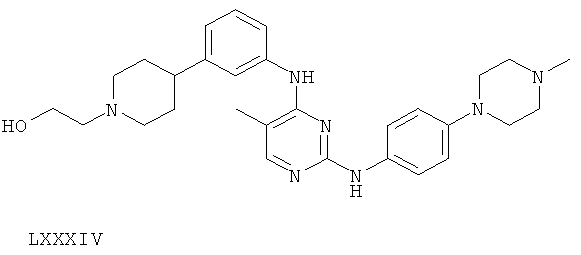
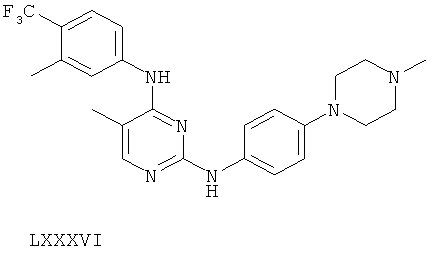
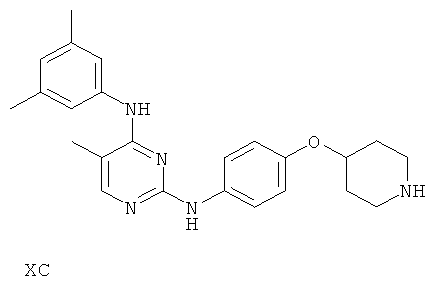
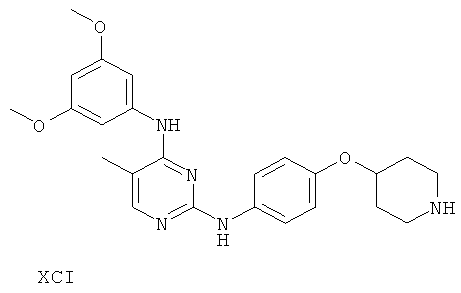
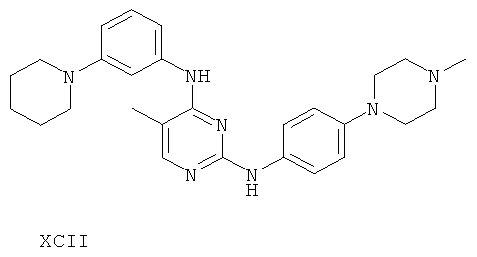
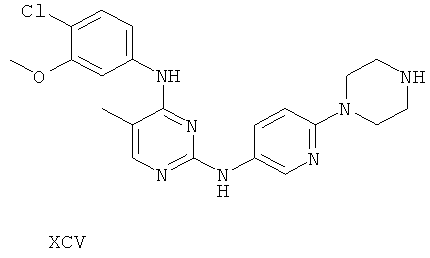
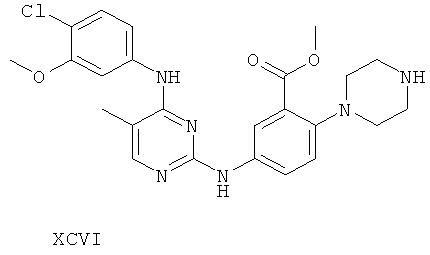
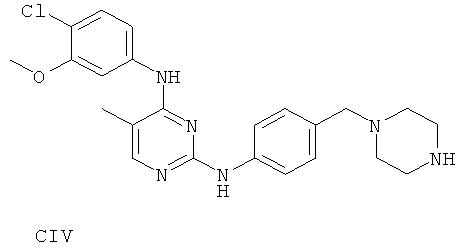
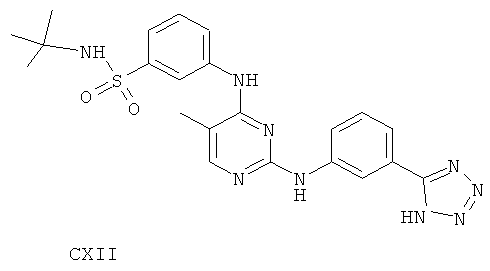
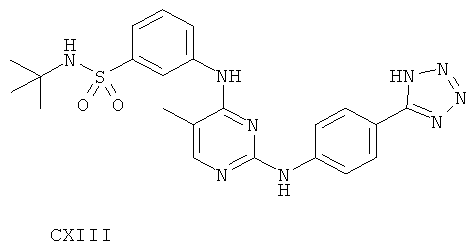
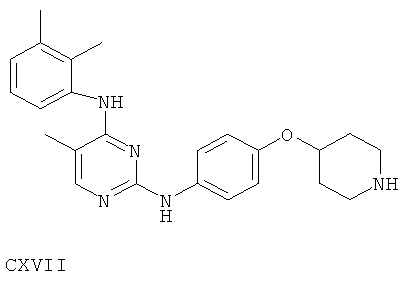
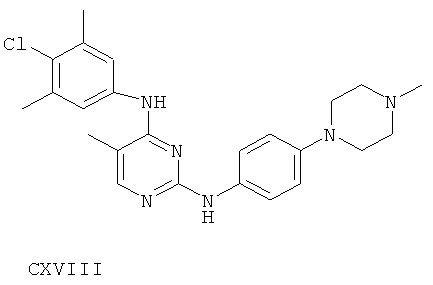
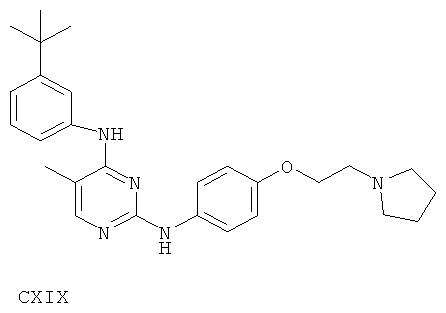
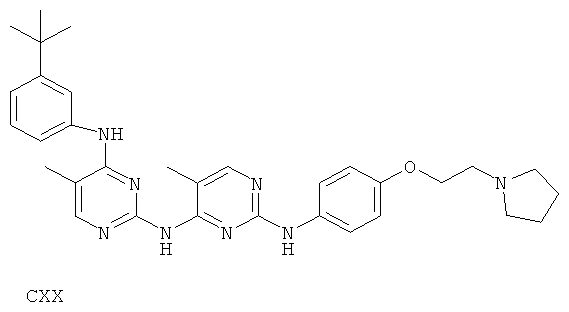
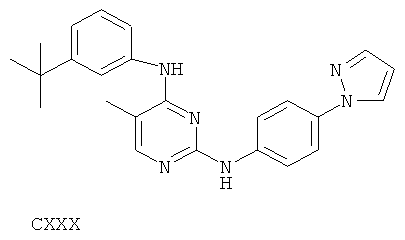
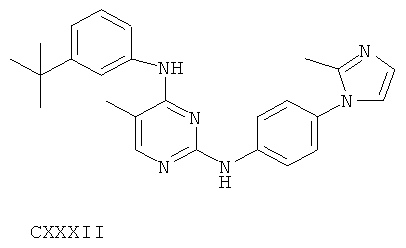
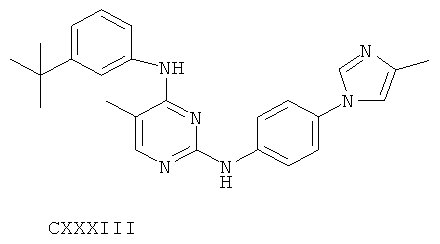
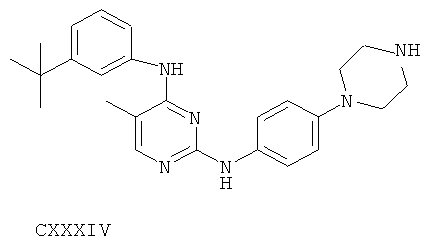
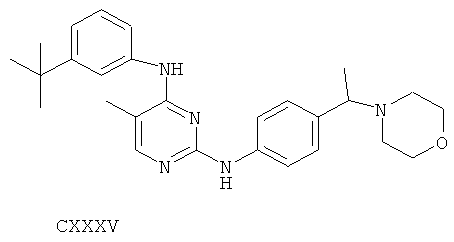
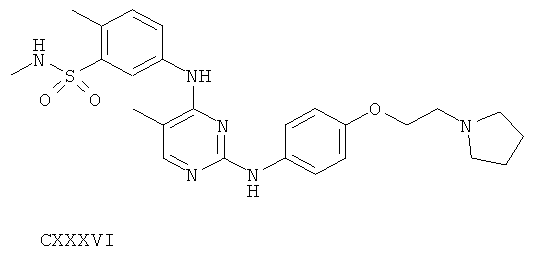
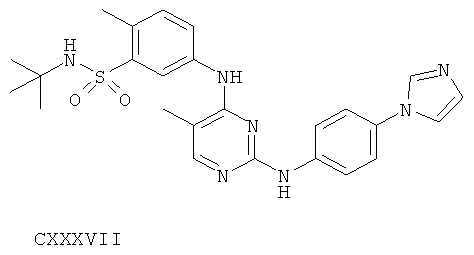
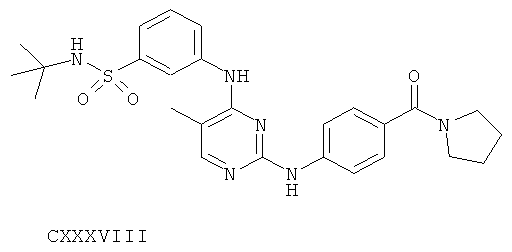
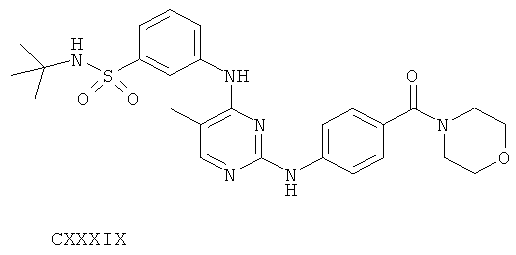
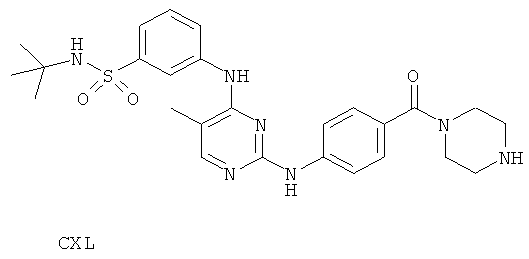
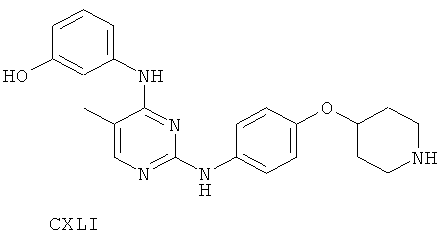
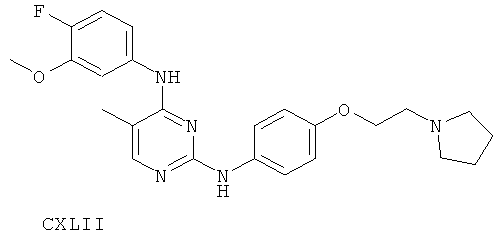
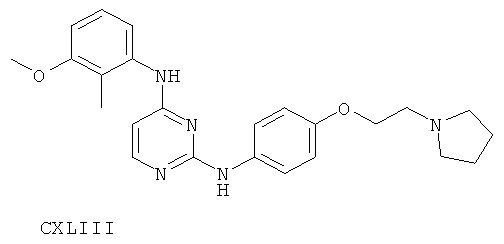
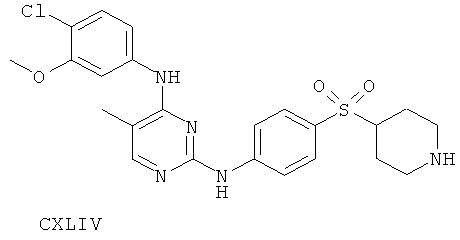
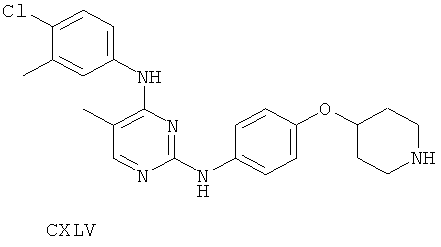
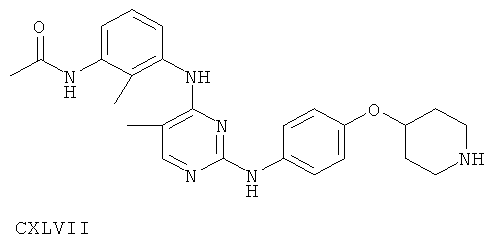
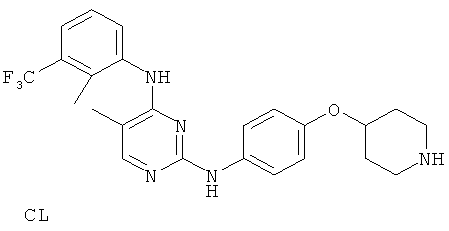
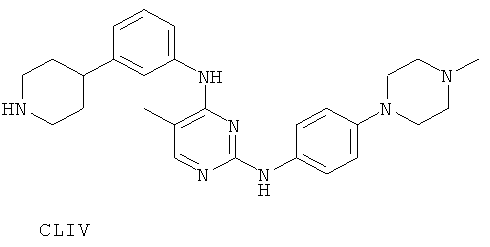
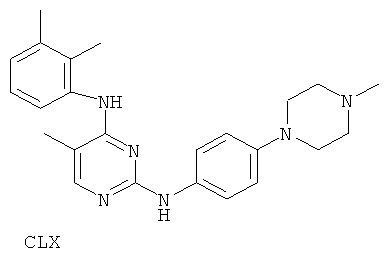
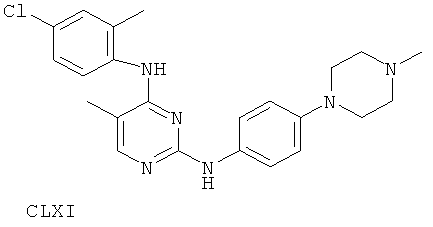
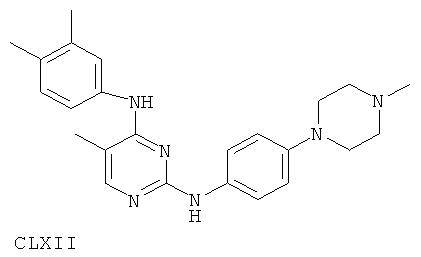

или его фармацевтически приемлемой соли.

или его фармацевтически приемлемой соли.

или его фармацевтически приемлемой соли.

или его фармацевтически приемлемой соли.

или его фармацевтически приемлемой соли.

или его фармацевтически приемлемой соли.

или его фармацевтически приемлемой соли.

или его фармацевтически приемлемой соли.

или его фармацевтически приемлемой соли.

или его фармацевтически приемлемой соли.

или его фармацевтически приемлемой соли.

или его фармацевтически приемлемой соли.

или его фармацевтически приемлемой соли.

или его фармацевтически приемлемой соли.

или его фармацевтически приемлемую соль.

или его фармацевтически приемлемую соль.

или его фармацевтически приемлемую соль.

или его фармацевтически приемлемую соль.

или его фармацевтическую соль.

или его фармацевтически приемлемую соль.

или его фармацевтически приемлемую соль.

или его фармацевтически приемлемую соль.

или его фармацевтически приемлемую соль.

или его фармацевтически приемлемую соль.
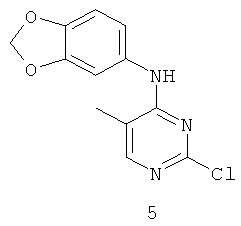
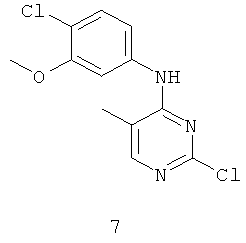
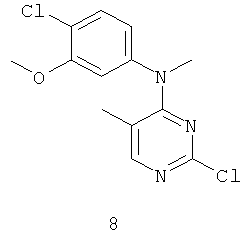
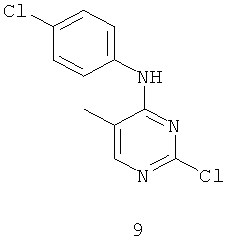
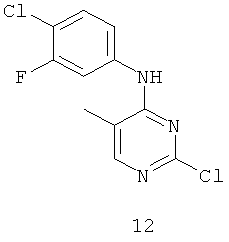
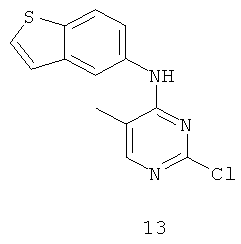
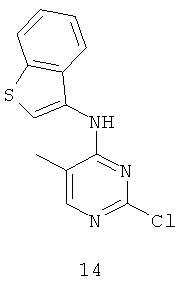
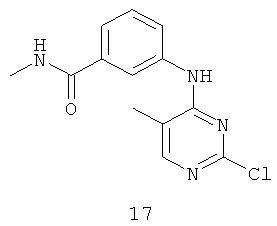
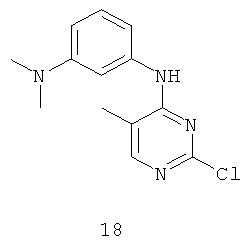
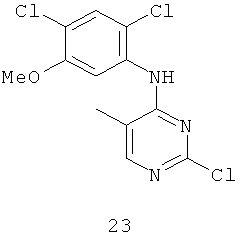
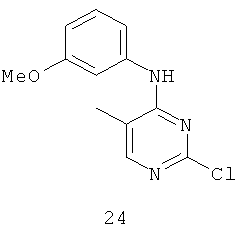
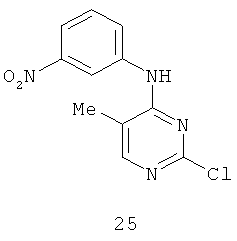
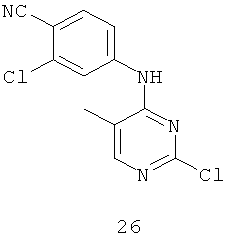
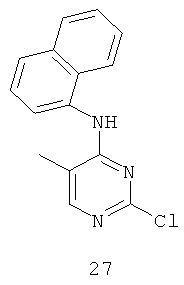
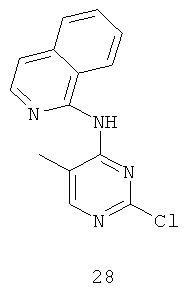
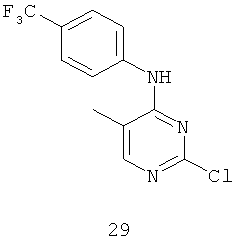
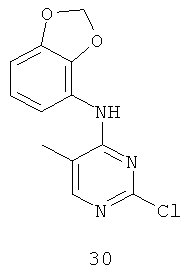
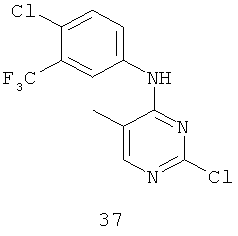
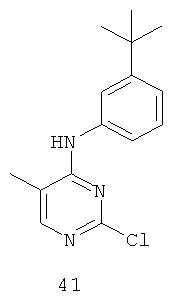
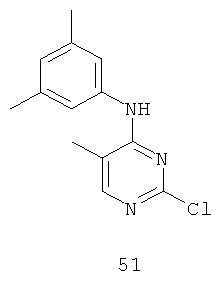
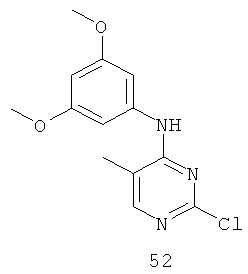
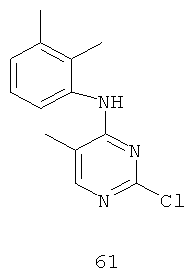
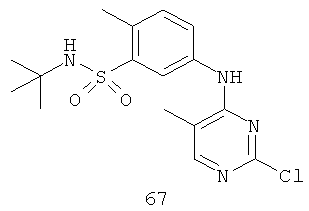
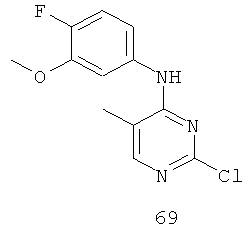
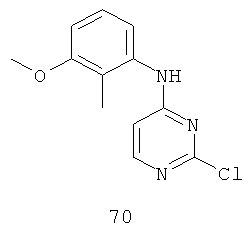
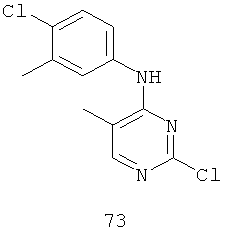
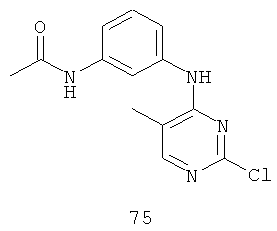
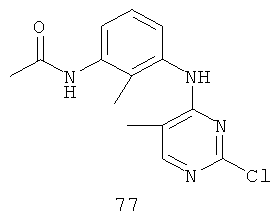
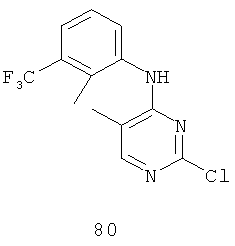
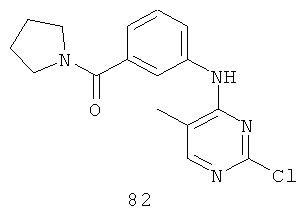
Документы, цитированные в отчёте о поиске
Циклические ингибиторы протеинтирозинкиназ

Комментарии