Способ получения производных сульфониламида - SU405204A3
Код документа: SU405204A3
Описание
1
Изобретение относится к способу получения новых производных сульфониламида, обладающих ценными фармакологическими свойствами.
Известно взаимодействие 2-замеш,енных 4,5дигидроимидазолов с бензолсульфохлоридом в щелочном растворе, которое приводит к расщеплению имидазолинового кольца с образованием 1,2-дибензолсульфамидоэтанов.
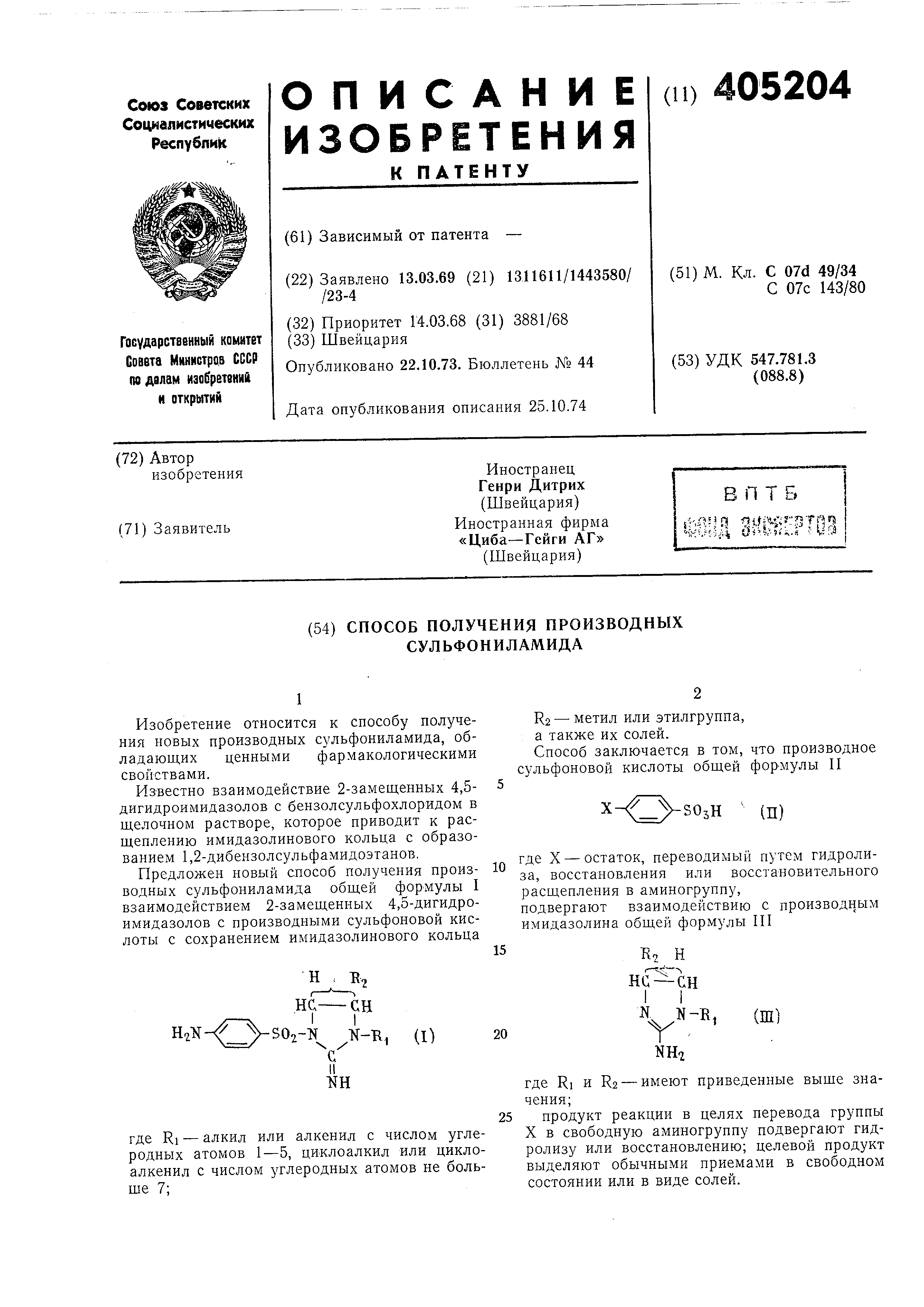
Предложен новый способ получения производных сульфониламида общей формулы I взаимодействием 2-замещенных 4,5-дигидроимидазолов с производными сульфоновой кислоты с сохранением имидазолинового кольца
где RI - алкил или алкенил с числом углеродных атомов 1-5, циклоалкил или циклоалкенил с числом углеродных атомов не больше 7;
R2 - метил или этилгруппа, а также их солей.
Способ заключается в том, что производное сульфоновой кислоты общей форМулы И
(П)
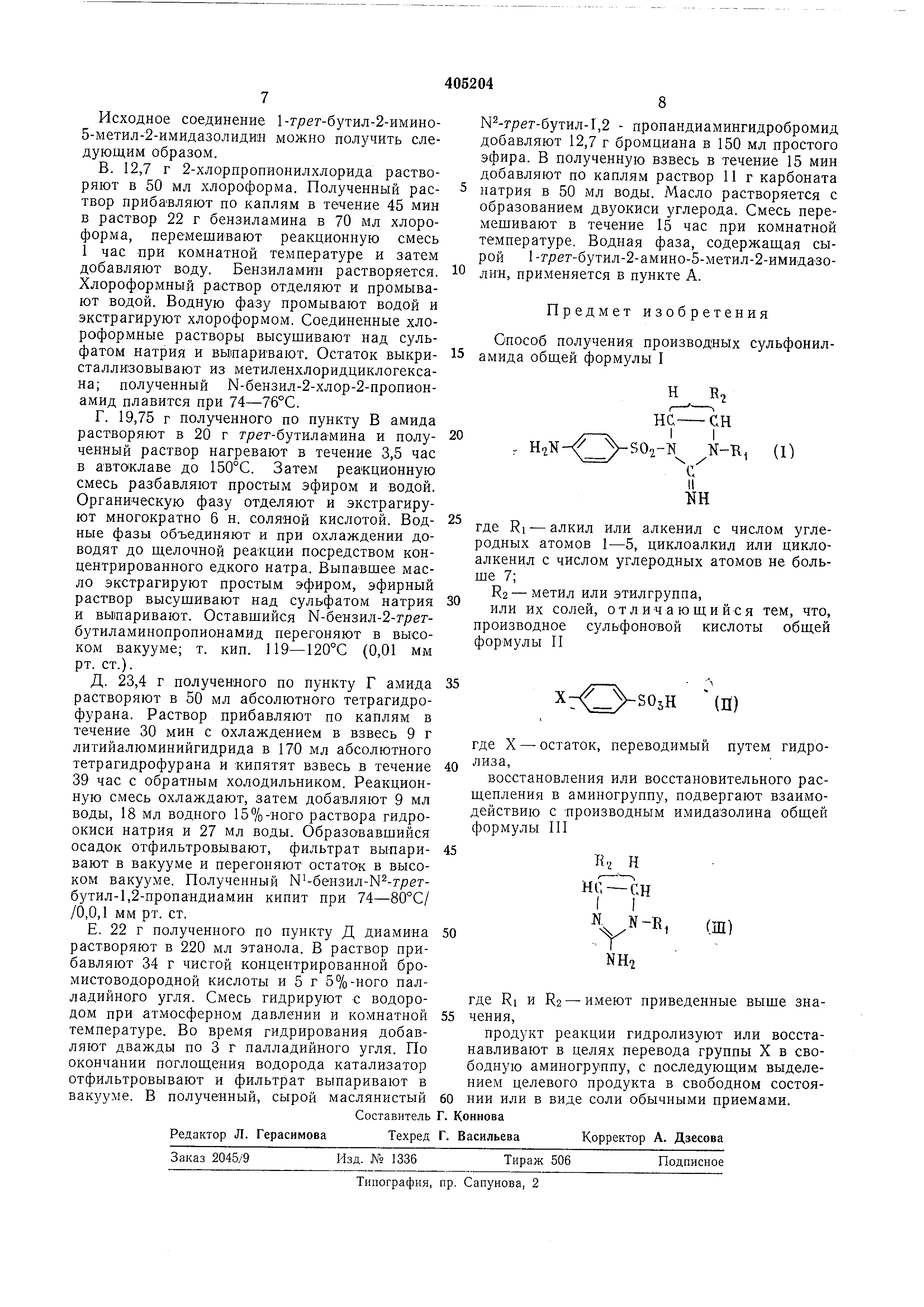
где X - остаток, переводимый путем гидролиза , восстановления или восстановительного расщепления в аминогруппу, подвергают взаимодействию с производным имидазолина общей формулы П1
R7 Н
YH-B.
(Ш)
20
NH
где RI и R2 - имеют приведенные выще значения;
продукт реакции в целях перевода группы X в свободную аминогруппу подвергают гидролизу или восстановлению; целевой продукт выделяют обычными приемами в свободном состоянии или в виде солей.
В соединениях общей структурной формулы I RI может быть в качестве низших алкильных групп, например метиловой, этиловой, пропилоБОЙ, изопропиловой, бутиловой, вторбутиловой , г/йет-бутиловой, изобутиловой, пеитиловой , изопентиловой, 2,2-диметилпроииловой 1-метилбутиловой, 1-этилпропиловой, 1,2диметилпропиловой групиой и в качестве алкениловой группы, например аллиловой , 1-, 2- или З-бутен-1-иловой, 2метилпропеииловой , металлиловой, или 3или 4-пентен-1-иловой группой. Далее Ri может быть, например, в качестве циклоалкиловой группы, циклопропиловой, циклопропилметиловой , 2-циклопропилэтиловой, 3циклопропилпропиловой , циклобутиловой, циклобутиЛМетиловой , 2-циклобутилэтиловой, 3циклобутилпропиловой , циклопентиловой, 1метилциклопентиловой , 2-метилциклопентиловой , 3-метилциклопентиловой, 1-этилциклопентиловой , 2-этилциклопентиловой, 3-этилциклопентиловой , циклопентилметиловой, 2-метилциклопентилметиловой , 3-метилциклопентилметиловой , циклогексиловой, 1-метилциклогексиловой , 2-метилциклогексиловой, 3-метилциклогексиловой , 4-метилциклогексиловой, циклогексилметиловой или циклогептиловой группой и в качестве циклоалкиленовой группы может быть 2-циклопентен-1-иловой, 2-метил2-циклопентен-1 -иловой, З-метил-2-циклопентен-1-иловой , 2-этил-2-циклопентен-1-иловой, З-этил-2-циклопентен-1 -иловой, 3-циклопентен1-иловой , 2-метил-3-циклопентен-1-иловой, 3метил-3-циклопентен-1 -иловой, 2-этил-З-циклопентен-1 -иловой, 3-этил-З-циклопентен-1 -иловой , 2-циклогексен-1-иловой, 1-метил-2-циклогексен-1 -иловой, 2-метил-2-циклогексен-1 -иловой , 3-метил-2-циклогексеН-1-иловой, 4-метил2-циклогексен-1-иловой , З-циклогексен-1-иловой , 1-метил-3-циклогексен-1-иловой, 2-метил3-циклогексен-1-иловой , 3-метил-З-циклогексен-1 -иловой, 4-метил-З-циклогексен-1 -иловой, 2- или З-циклопентен-1-илметиловой, 2-, 3- или 4-циклогексен- 1-илметиловой, 2-циклогептен-1иловой , З-циклогептен-1-иловой или 4-циклогептен-1-иловой группой.
Реакцию проводят преимущественно в присутствии смещивающегося или несмешивающегося с водой инертного органического растворителя в присутствии воды или без нее. Такими растворителями являются, например, углеводороды, как бензол, толуол или ксилол, эфиры, например простой эфир, диоксан или тетрагидрофуран, хлорированные углеводороды , метиленхлорид, и низшие кетоны, как ацетон или метилэтилкетон. Целесообразно добавлять в реакционную смесь или раствор связывающее кислоты вещество. Такими являются , например, неорганические основания или соли, можно использовать также органические основания, например пиридин, триметил- или триэтиламино-Ы,Ы-диизопропилэтиламин или коллидин, которые могут быть использованы в избытке также и в качестве растворителей.
Переводимыми путем гидролиза в свободную аминогруппу остатками X - являются, например, ациламиновые остатки, например ацетамидогруппа, низшие алкоксикарбониламиновые остатки, например этоксикарбониламиновая группа, арилоксикарбониламиновые остатки, как феноксикарбониламиновый остаток , или арилметоксикарбониламиновые остатки , каК бензилоксикарбониламиновый остаток , или остатки соответствующих производных тиоуглекислоты.
Примером переводимого путем восстановле}шя в аминогрЗ-пиу остатка X является нитрогруппа , а примерами остатков, переводимых
в аминогруппу путем восстановительного расщепления , являются фенилазо- или л-диметиламинофенилазогруппы . Восстановление этих остатков проводится каталитически, например при помощи водорода в присутствии никеля
Ренея, палладиевого или платинового угля, в инертном растворителе, например этаноле. Имеются еще и другие общеизвестные способы восстаковлепия, например восстановление нитрогрупп или восстановительное расщеплеиие азогрупп железом в уксусной или соляной кислотах.
Полученные по способу согласно изобретению соединения общей структурной формулы I переводятся затем по желанию в их соли
при помощи неорганических и органических кислот. Получают эти соли, например, введением в реакцию соединений общей структурной формулы I с эквивалентным количеством кислоты в подходящем водноорганическом или
органическом растворителе, например метаноле , этаноле, диэтиловом простом эфире, хлороформе или метиленхлориде. Пример 1. А. В раствор 13,2 г бромциана в 220 мл
простого эфира добавляют 31 г сырого Nг/ ег-бутил - 1,2 - пропаидиаминдигидробромида . К полученной смеси добавляют по частям в течение 5 мин раствор 11,4 г карбоната натрия в 88 мл воды. Полученную взвесь перемещивают в течение 15 час при комнатной температуре и оставляют стоять два дня. Отделяют водный слой, содержащий 1-грег-бутил-2-амино-4-метил-2-ИМидазолин , от эфирного раствора и разбавляют водную фазу водой
для растворения выпавшего натрийбромида. В водный раствор добавляют 23,8 г N-ацетилсульфанилилхлорида в 220 мл ацетона и затем раствор 8,8 г гидроокиси натрия в 44 мл воды. Смесь кипятят в течение 30 мин с обратным холодильником, охлаждают, отфильтровывают выпавший сырой продукт и перекристаллизовывают из смеси хлороформ-этанол . Получают 4-(2-имино-3-трет-бутил-5-метилимидазолин-1-Илсульфонил )-ацетанилид с
I. пл. 238-240°С.
Б. 35,2 г полученного по пункту А ацетанилида растворяют в 180 мл 8 н. этаноловой соляной КИСЛОТЫ; раствор оставляют стоять в течение двух дней при комнатной температуре . Реакционную смесь выпаривают и остаток растворяют в воде. Раствор отфильтровывают и доводят едким натром до щелочной реакции. Выпавшие кристаллы отфильтровывают , промьгвают водой и перекристаллизовывают из смеси ацетон-метанол; получают 1сульфанилил-2-имино-З-трег-бутил-5 - метилимидазолидик с т. пл. 145-146°С.
Исходный продукт пункта А можно получить следующим образом.
В. 16,35 г К-трет-бутил-2-хлорпроционамида и 25,0 г бензиламина нагревают в течение 3,5 час до 150-170°С. Из первоначально гомогенного раствора выпадают кристаллы. Реакционную смесь охлаждают и добавляют 150 мл 2 н. едкого натра и хлороформ. Органическую фазу отделяют, промывают водой, высушивают и выпаривают. Остаток перегоняют . После головного отгона бензиламина получают Ы-грет-бутил-2-бензиламинопропионамид с т. кип. 123-125°С (0,03 мм рт. ст.). Гидрохлорид плавится при 158-162°С.
Г. Во взвесь 9,0 г литийалюминийгидрида в 200 мл абсолютного тетрагидрофурана в течение 15 мин добавляют по каплям раствор 23,4 г полученного по пункту А амида в 80 мл абсолютного тетрагидрофурана. Затем взвесь кипятят в течение 38 час с обратным холодильником . Реакционную смесь охлаждают, разрушают избыточный литийалюмияийгидрид при охлаждении этилацетатом, затем водой и метанолом и выпаривают взвесь. Серый остаток дважды экстрагируют в течение 30 мин кипящим хлороформом и отфильтровывают. Соединенные хлороформные растворы высушивают над сульф|атом натрия и выпаривают. Оставшееся масло перегоняют. N-rper-бутилМ -бензил-1 ,2-пропандиамин дистилирует при 72-86°С (0,005 мм рт. ст.).
Д. К 22,0 г полученного по пункту Г амина в 440 мл дестиллированного этанола добавляются 34,0 г 48%-ного чистого бромистого водорода и 8,8 г 5%-ного палладийного угля, затем гидрируют при комнатной температуре и нормальном давлении. После поглощения 95% вычисленного водорода добавляют еще 8,8 г 5%,-ного палладийного угля и продолжают гидрировать. После 17 час реакционная смесь поглощает 98% водорода.
Катализатор отфильтровывают, последовательно промывают этанолом и выпаривают фильтрат. Остаток Н-грег-бутил-1,2-пропандиаминдигидробромид , используют в качестве сырого продукта.
Пример 2.
А. Аналогично примеру 1 А и Б получают следующий конечный продукт.
Из Ы-бутил-1,2-пропаНдиамина и бромциана 1-бутил-2-амино-4-метил-2-имидазолидингидробромида (сырой продукт), который с Nацетилсульфанилилхлоридом дает 4- (2-иминоЗ-бутил-5-метилимидазолидин - 1 - илсульфонил )-ацетанилид с т. пл. 243-244°С, гидролизом получают 1-сульфанилил-2-имино-3-бутил-5-метилимидазолидин с т. пл. 125- 126°С.
Исходный продукт получают следующим образом.
Б. В раст-вор 16,1 г бутиламина в 50 мл хлороформа добавляют по каплям в течение
30 мин при достаточном охлаждении льдом 12,7 г 2-хлорпропионилхлорида в 20 мл хлороформа . Полученный раствор оставляют стоять при комнатной температуре Б течение 15 час, затем многократно промывают водой
и отделяют органическую фазу. Последнюю высущивают над сульфатом натрия и выпаривают . Остается сырой Ы-бутил-2-хлорпропионамид .
В. Аналогично примеру 1 В и Д получают
продукт, исходя из сырого амида через межпродукты N-бyтил-2-бeнзиЛvnмииoпpoпиoнaмид с т. кип. 151-154°С (0,005 мм рт. ст.) и Nбутил-№-бензил-1 ,2-пропандиамин с т. кип. 98-104 С (0,04 мм рт. ст.) Ы-бутил-1,2-пропандиамин .
Пример 3.
А. Аналогично примеру 1 А и Б получают следующий конечный продукт.
Из М-бутил-1,2-бутандиамина (сырой продукт ) с бромцианом получают 1-бутил-2-амино-4-этил-2-имидазолиндигидробромид (сырой продукт), который дает с N-ацетилсульфанилилхлоридом 4- (2-имино-3-бутил-5-этилимидазолидин-1-илсульфонил )-ацетанилид (сырье) с т. пл. 107-11 ГС, который гидролизуется в 1 -сульфанилил-2-имино-3-бутил-5-этилимидазолидин с т. пл. 161-163°С.
Исходное соединение пункта А получают следующим образом.
Б. Аналогично примерам 2, Б и 1, В и Д получают продукт, исходя из 2-хлорбутирилхлорида , через промежуточные продукты Nбутил-2-хлорбутирамид (сырье), Ы-бутил-2бензиламинобутирамид (сырье) и М-бутил-№бензил-1 ,2-бутандиамин (сырье) Ы-бутил-1,2бутандиамин . Пример 4.
А. 23,6 г (0,1 моль) 1-т эег-бутил-2-амино-5метил-2-имидазолингидробромида растворяют в 100 мл воды, затем добавляют 21,8 г (0,1 моль) N-ацетилсульфанилхлорида в 200 мл ацетона. Затем в течение 10 мин
добавляют по каплям раствор 10,0 г гидроокиси натрия в 40 мл воды и полученную взвесь кипятят в течение 45 мин с обратным холодильником . Реакционную смесь охлаждают и выпаривают ацетон в вакууме. В остаток добавляют воду и выпавщее масло поглощают метиленхлоридом. Раствор высушивают над сульфатом натрия и выпаривают. Остаток выкристаллизовывают из метанола. Получают 4-(2-имино-3-т/7ет-бутил-4 - метилимидазолидин-1-ил )-ацетанилид с т. пл. 178-180°С.
Б. Полученный по пункту А продукт реакции гидролизуют аналогично примеру 1, Б в 1 -сульфанил-2-имино-3-грег-бутил-4-метилимидазолидин с т. пл. 178-180°С (из изопропанола ).


Реферат

Формула


Комментарии