Компонеты катализатора для полимеризации олефинов - RU2631426C2
Код документа: RU2631426C2
Описание
КОМПОНЕТЫ КАТАЛИЗАТОРА ДЛЯ ПОЛИМЕРИЗАЦИИ ОЛЕФИНОВ
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТНИЕ
Настоящее изобретение относится к области химии. В частности, оно относится к компонентам катализатора для полимеризации олефинов, в частности пропилена, включающее в себя основной носитель дигалогенид Mg, на котором держатся атомы Ti и донор электронов, выбранный из особого класса производных меркаптоспиртов. Настоящее изобретение далее относится к катализаторам, полученным из указанных компонентов и способам их использования для полимеризации олефинов, в частности пропилена.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Компоненты катализатора для стереоспецифической полимеризации олефинов широко известны в отрасли техники, к которой относится данное изобретение. Что касается полимеризации пропилена, то наиболее распространенное семейство катализаторов относится к типу Циглера-Натта и, как правило, содержит твердый компонент катализатора, представленный дигалогенидом магния, на котором удерживается соединение титана и внутреннее электронодонорное соединение, используемое в комбинации с алкилалюминиевым соединением. Однако для более высокой кристалличности полимера, необходим внешний донор (например алкоксисилан), дающий более высокую стереорегулярность. Один из предпочтительных классов внутренних доноров представлен эфирами фталиевой кислоты, причем наиболее часто используется диизобутилфталат. Фталаты используются в качестве внутренних доноров в комбинации с алкилалкоксисиланами, в качестве внешнего донора. Данная система катализатора дает хорошие характеристики в отношении активности, стереорегулярности и нерастворимости в ксилоле.
Одной из проблем, связанных с использованием данной каталитической системы, являются недавно выявленные медицинские проблемы фталатов, связанными с их использованием, а некоторые из соединений этого типа были классифицированы как источник серьезных проблем для здоровья.
Исследовательская деятельность направлялась на обнаружение альтернативных классов внутренних доноров, используемых при по дготовке компонентов катализатора, для полимеризации пропилена.
Внутренние доноры, описанные в Патенте США 7388061 и патентной заявке WO2010/078494, относятся к эфирам алифатических или ароматических диолов. Обе ссылки не описывают возможные варианты этих структур. Кроме того и в связи с тем, что их базовая структура представляет собой диол, трудно образовать многофункциональные производные с различными функциональными группами (сложный эфир/эфир, сложный эфир/карбамат и т.д.), поскольку два атома кислорода базовой структуры диола имеют одинаковую химическую активность.
Заявитель с удивлением обнаружил, что определенный класс доноров на основе меркаптановых производных пригоден для образования широкого ряда молекул с одинаковыми или различными функциональными группами, которые, при использовании их в качестве внутренних доноров, образуют катализаторы, показывающие превосходный баланс химической активности и стереоспецифичности.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩЕСТВА ИЗОБРЕТЕНИЯ
Соответственно предлагается компонент катализатора для полимеризации олефинов, содержащий Mg, Ti и электронодонорное соединение с формулой (I)

(I)
В котором X и Y выбираются из групп R1, –OR1 и –NR2, а В представляет собой кислород или серу, S представляет собой серу, R1 выбирается из углеводородных групп C1-C15, необязательно содержащих гетероатом, выбранный из галогена, P, S, N, O и Si, которые могут быть сплавлены с образованием одного или нескольких циклов, R представляет собой водород или R1, а А представляет собой двухвалентную мостиковую группу с длиной цепи между двумя мостиковыми связями равную 1-10 атомам.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В случае циклических структур, действующих в качестве мостиковых групп, термин "длина цепи" относится к самой короткой последовательности атомов, соединяющих два атома серы или кислорода/серы в формуле (I). В предпочтительном варианте осуществления изобретения мостиковая группа имеет формулу -(ZR2m)n-, в которой Z независимо выбирается из C, Si, Ge, O, N, S или P, группы R2, равные или отличающиеся друг от друга, представляют собой водород или углеводородные радикалы C1-C20, необязательно содержащие гетероатом, выбранный из галогена, P, S, N, O и Si, которые могут быть сплавлены с образованием одного или нескольких циклов, m представляет собой число, равное валентности Z, а n–целое число от 1 до 10. Предпочтительно, чтобы в мостиковой группе, имеющей формулу -(ZR2m)n-, атомы O, S, и N непосредственно не связывались с S или O в формуле (I), то есть не являлись концевыми атомами мостиковой группы. Предпочтительно выбирать Z из С и Si. В более предпочтительном варианте осуществления изобретения Z представляет собой углерод.
В конкретном варианте осуществления изобретения указанная двухвалентная мостиковая группа выбирается из группы, состоящей из алифатических, алициклических и ароматических двухвалентных радикалов, необязательно замещенных углеводородными группами C1-C15 и/или гетероатомами, выбранными из галогена, Р, S, N, O и Si, с длиной цепи мостиковой группы от 1 до 6 атомов и особенно от 1 до 4 атомов.
В конкретном предпочтительном варианте осуществления мостиковая группа представляет собой алифатическую или алициклическую мостиковую группу с длиной цепи в 2-3 атома углерода. Среди данного класса, конкретными предпочтительными мостиковыми группами являются группы с формулой –(CR3p)s-, в которой R3представляет собой независимый водород или углеводородные радикалы C1-C20, необязательно замещенные гетероатомами, выбранными из галогена, Р, S, N, O и Si, которые могут быть сплавлены вместе с образованием одного или более циклов, р представляет собой число, равное валентности углерода, а s представляет собой число от 1 до 6, предпочтительно от 1 до 4. Примерами мостиковых групп являются метилиды, этан-1,2-диил, бутан-2,3-диил, пентан-2,4-диил, 2,2-диизобутилпропан-1,3-диил, циклогексан-1,2-диил, циклопентан-1,2-диил.
Особенно предпочтительным подклассом является соединение с формулой (II), ниже
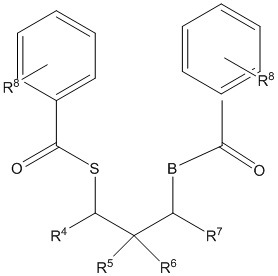
(II)
в котором В представляет собой серу или кислород, где группы R4-R7, равные или отличающиеся друг от друга, представляют собой водород или углеводородные радикалы C1-C15, необязательно содержащие гетероатом, выбранный из галогена, P, S, N и Si, а группы R8,, равные или отличающиеся друг от друга, выбираются из углеводородных групп C1-C15, которые необязательно имеют связи, образующие цикл, а n–целое число от 0 до 5.
Предпочтительно В является серой, R4 и R7 выбираются из алкильных групп C1-C10 и более предпочтительно из алкильных групп C1-C5, в частности метила, группы R5 и R6 выбираются из водорода или алкильных групп C1-C10 и более предпочтительно из водорода. Группы R8 независимо выбираются из алкильных групп C1-C10 и более предпочтительно из алкильных групп C1-C5. Среди них особенно предпочтительными являются метил, этил, n-пропил и n-бутил. Число n может меняться от 0 до 5 включительно, предпочтительно от 1 до 3, и более предпочтительно равно 1. При n=1, заместитель R8 предпочтительно находится в позиции 4 бензоатного кольца.
Другим классом предпочтительной мостиковой группы является класс, основанный на циклических ароматических группах, которые через кольцевые атомы углерода могут связать два атома серы или серы/кислорода в формуле (I). Среди них особенно предпочтительными являются фенильные группы, необязательно замещенные атомами галогена или алкильными радикалами C1-C20, соединяющие атомы кислорода в позиции 1,2 или 1,3 или 1,4, и нафталиновые группы, необязательно замещенные, соединяющие кислородные группы в позиции 1,2 или 2,3 или 1,8.
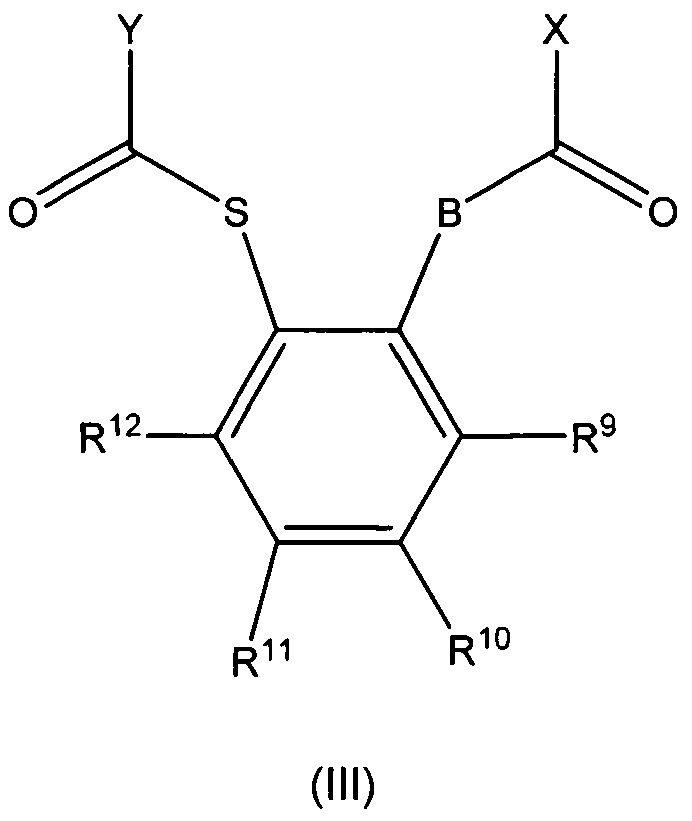
Среди них особенно предпочтительной является структура формулы (III), ниже

(III)
в которой X, Y и B имеют значение, указанное в пункте 1, а R9-R12 независимо выбираются из водорода, галогенов или углеводородных групп, необязательно замещаемых гетероатомами, выбранными из галогенов P, S, N, O и Si.
Предпочтительными структурами формулы (III) являются структуры, в которых группы R9, R11 и/или R12 являются алкильными группами C1-C5. Особенно предпочтительными структурами являются структуры, в которых R9 и/или R12 являются первичной алкильной группой, особенно метильной, а R11 представляет собой третичную алкильную группу, особенно трет-бутил.
Конкретными примерами являются группы: 1,2-фенилен, 3-метил-1,2-фенилен, 4-хлор-1,2-фенилен, 4-трет-бутил-1,2-фенилен, 3,6-диметил-1,2-фенилен, 3,5-диметил-1,2-фенилен, 5-трет-бутил-3-метил-1,2-фенилен, 3,5-диизопропил-1,2-фенилен, нафталин-1,8-диил, нафталин-1,2-диил, нафталин-2,3-диил.
Предпочтительно в формулах (I) и (III), B представляет собой кислород. Кроме того, в указанных формулах группы R1 предпочтительно выбираются из алкильных групп C1-C1 и арильных или алкиларильных групп C6-C15. Среди алкильных групп предпочтительными являются линейные алкильные группы C1-C5, такие как метил, этил и пропил, хотя предпочтительными арильными или алкиларильными группами являются фенильные группы, предпочтительно замещенные галогеном и/или алкильными группами C1-C5.
Предпочтительными возможными комбинациями между группами X и Y в формулах (I) и (III) являются комбинации, в которых В представляет собой О, X представляет собой R1, Y выбирается из группы, содержащей R1, -OR1 и -NR2, в которой R1 и R имеют значения, описанные выше. В предпочтительном варианте осуществления изобретения обе группы X и Y выбираются из групп R1, в частности из арильных или алкиларильных групп C6-C15. Другой предпочтительной комбинацией является комбинация, в которой В представляет собой О, X представляет собой -OR1, Y выбирается из -NR2 и -OR1. В соответствии с другим предпочтительным вариантом осуществления изобретения В представляет собой О, X представляет собой группу -R1, выбранную из арильных или алкиларильных групп С6-С15, a Y представляет собой группу -OR1, в которой R1 выбирается из алкильной группы С1-С10.
В группах -NR2 радикалы R предпочтительно выбираются из алкильных групп C1-С10, более предпочтительно из линейных алкильных групп С1-С5, таких как метил, этил и пропил.
Предпочтительно, чтобы конечный объем электронодонорного соединения в твердом компоненте катализатора составлял от 1 до 25 вес. %, предпочтительно от 3 до 20 вес. %.
Неограничивающими примерами структур с формулами (I) и (II), являются: 2-тиобензоил-4-трет-бутил-3,6-диметилфенилбензоат, 2-тиобензоил-4-трет-бутил-6-метилфенилбензоат, 4-трет-бутил-2-3-тиохлорбензоил-3,6-диметилфенил-3-хлоробензоат, 4-трет-бутил-2-3-тиохлорбензоил-6-метилфенил-3-хлоробензоат, 4-трет-бутил-2-дитиоэтилкарбамоил-3,6-диметилфенилбензоат, 4-трет-бутил-2-дитиоэтилкарбамоил-6-метилфенилбензоат, 4-трет-бутил-2-дитиоэтилкарбамоил-3,6-диетилфенилбензоат, 4-трет-бутил-2-дитиоэтилкарбамоил-6-метилфенилбензоат, 4-трет-бутил-2-метил-6-4-тиопропилбензоил-фенил-4-пропилбензоат, 4-трет-бутил-3,6-диметил-2-4-тиопропилбензоил-фенил-4-пропилбензоат, S-3-трет-бутил-6-диоксиэтилкарбамоил-2,5-диметилфенилтиобензоат, S-3-трет-бутил-6-диоксиметилкарбамоил-2,5-диметилфенилтиобензоат, S-5-трет-бутил-2-диоксиэтилкарбамоил-3-метилфенилтиобензоат, S-5-трет-бутил-2-диоксиметилкарбамоил-3-метилфенилтиобензоат, 4-трет-бутил-2-дитиоэтилкарбамоил-3,6-диметилфенилдиэтилкарбаминат, 4-трет-бутил-2-дитиоэтилкарбамоил-6-метилфенилдиэтилкарбаминат, 4-трет-бутил-2-дитиоэтилкарбамоил-3,6-диметилфенилдиметилкарбаминат,4-трет-бутил-2-дитиоэтилкарбамоил-6-метилфенилдиметилкарбаминат, 4-трет-бутил-2-тиоэтоксикарбонил-3,6-диметилфенилэтилкарбонат, 4-трет-бутил-2-тиоэтоксикарбонил-6-метилфенилэтилкарбонат, S,S'-4-трет-бутил-3,6-диметил-1,2-фенилендитиобензоат, S,S'-4-трет-бутил-3-метил-1,2-фенилендитиобензоат, S-3-трет-бутил-6-дитиоэтилкарбамоил-2,5-диметилфенилтиобензоат, S-3-трет-бутил-6-дитиоэтилкарбамоил-2-метилфенилтиобензоат, S-3-трет-бутил-6-тиоэтоксикарбонил-2,5-диметилфенилтиобензоат, S-3-трет-бутил-6-тиоэтоксикарбонил-2-метилфенилтиобензоат, S-4-трет-бутил-2-тиодиэтилкарбамоил-3,6-диметилфенилтиобензоат, S-4-трет-бутил-2-тиодиэтилкарбамоил-3-метилфенилтиобензоат, S-4-трет-бутил-2-тиоэтоксикарбонил-3,6-диметилфенилтиобензоат, S-4-трет-бутил-2-тиоэтоксикарбонил-3-метилфенилтиобензоат, S,S'-4-трет-бутил-3,6-диметил-1,2-фенилен-O,O'-диэтилдитиокарбонат, S,S'-4-трет-бутил-3,6-диметил-1,2-фенилен-бис-диэтилтиокарбамат, S,S'-4-трет-бутил-3-метил-1,2-фенилен-O,O'-диэтилдитиокарбонат, S,S'-4-трет-бутил-3-метил-1,2-фенилен-бис-диэтилтиокарбамат, S-3-трет-бутил-6-тиоэтоксикарбонил-2,5-диметилфенил-диэтилтиокарбамат, S-3-трет-бутил-6-тиоэтоксикарбонил-2-метилфенил-диэтилтиокарбамат, S-4-трет-бутил-2-тиэтоксикарбонил-3,6-диметилфенил-диэтилтиокарбамат, S-4-трет-бутил-2-тиоэтоксикарбонил-3-метилфенил-диэтилтиокарбамат, S,S'-4-трет-бутил-3,6-диметил-1,2-фенилен-бис-4-пропилтиобензоат, S,S'-4-трет-бутил-3,6-диметил-1,2-фенилен-бис-3-хлоротиобензоат, 4-тиодиэтилкарбамоил-пентан-2-ил-бензоат, 4-тиоэтоксикарбонил-пентан-2-ил-бензоат, 4-тиобензоил-пентан-2-ил-бензоат, S,S'-пентан-2,4-диил-дитиобензоат, S-4-оксидиэтилкарбамоил-пентан-2-ил-тиобензоат, S-4-тиодиэтилкарбамоил-пентан-2-ил-тиобензоат, S-4-оксиэтоксикарбонил-пентан-2-ил-тиобензоат, S-4-тиоэтоксикарбонил-пентан-2-ил-тиобензоат, 4-тиодиэтилкарбамоил-пентан-2-ил-диэтилкарбамат, 4-тиоэтоксикарбонил-пентан-2-ил-диэтилкарбамат, 4-тиоэтоксикарбонил-пентан-2-ил-этилкарбонат, O,O'-диэтил-S,S'-пентан-2,4-диил-дитиокарбонат, S,S'-пентан-2,4-диил-бис-диэтилтиокарбамат, S-4-оксиэтоксикарбонил-пентан-2-ил-диэтилтиокарбамат, S-4-тиоэтоксикарбонил-пентан-2-ил-диэтилтиокарбамат, 4-тио-3-хлоробензоил-пентан-2-ил-3-хлоробензоат, 4-тиодиэтилкарбамоил-пентан-2-ил-3-хлоробензоат, 4-тиоэтоксикарбонил-пентан-2-ил-3-хлоробензоат, S,S'-пентан-2,4-диил-бис-3-хлоротиобензоат, S-4-оксидиэтилкарбамоил-пентан-2-ил-3-хлоротиобензоат, S-4-тиодиэтилкарбамоил-пентан-2-ил-3-хлоротиобензоат, S-4-оксиэтоксикарбонил-пентан-2-ил-3-хлоротиобензоат, S-4-тиоэтоксикарбонил-пентан-2-ил-3-хлоротиобензоат, 4-тиодиэтилкарбамоил-пентан-2-ил-диэтилкарбамат, 4-тиоэтоксикарбонил-пентан-2-ил-диэтилкарбамат, 4-тиоэтоксикарбонил-пентан-2-ил-этилкарбонат, O,O'-диэтил-S,S'-пентан-2,4-диил-дитиокарбонат, S,S'-пентан-2,4-диил-бис-диэтилтиокарбамат, S-4-оксиэтоксикарбонил-пентан-2-ил-диэтилтиокарбамат, S-4-тиоэтоксикарбонил-пентан-2-ил-диэтилтиокарбамат, 4-тио-4-пропилбензоил-пентан-2-ил-4-пропилбензоат, 4-дитиоэтилкарбамоил-пентан-2-ил-4-пропилбензоат, 4-тиоэтоксикарбонил-пентан-2-ил-4-пропилбензоат, S,S'-пентан-2,4-диил-бис-4-пропилтиобензоат, S-4-диоксиэтилкарбамоил-пентан-2-ил-4-пропилтиобензоат, S-4-дитиоэтилкарбамоил-пентан-2-ил-4-пропилтиобензоат, S-4-оксиэтоксикарбонил-пентан-2-ил-4-пропилтиобензоат, S-4-тиоэтоксикарбонил-пентан-2-ил-4-пропилтиобензоат, 4-тиодиэтилкарбамоил-пентан-2-ил-диэтилкарбамат, 4-тиоэтоксикарбонил-пентан-2-ил-диэтилкарбамат, 4-тиоэтоксикарбонил-пентан-2-ил-этилкарбонат, O,O'-диэтил- S,S'-пентан-2,4-диил-дитиокарбонат, S,S'-пентан-2,4-диил-бис-диэтилтиокарбамат, S-4-оксиэтоксикарбонил-пентан-2-ил-диэтилтиокарбамат, S-4-тиоэтоксикарбонил-пентан-2-ил-диэтилтиокарбамат, 2-тиодиэтилкарбамоил-циклогексилбензоат, 2-тиоэтоксикарбонил-циклогексилбензоат, 2-тиобензоил-циклогексилбензоат, S,S'-циклогексан -1,2-диил-дитиобензоат, S-2-оксидиэтилкарбамоил-циклогексилтиобензоат, S-2-тиодиэтилкарбамоил-циклогексил-тиобензоат, S-2-оксиэтоксикарбонил-циклогексилтиобензоат, S-2-тиоэтоксикарбонил-циклогексилтиобензоат, 2-тиодиэтилкарбамоил-циклогексил-диэтилкарбамат, 2-тиоэтоксикарбонил-циклогексил-диэтилкарбамат, 2-тиоэтоксикарбонил-циклогексил-этилкарбонат, S,S'-циклогексан-1,2-диил-O,O'-диэтил-дитиокарбонат, S,S'-циклогексан-1,2-диил-бис-диэтилтиокарбамат, S-2-оксиэтоксикарбонил-циклогексил-диэтилтиокарбамат, S-2-тиоэтоксикарбонил-циклогексил-диэтилтиокарбамат, 2-тио-3-хлоробензоил-циклогексил-3-хлоробензоат, 2-дитиоэтилкарбамоил-циклогексил-3-хлоробензоат, 2-тиоэтоксикарбонил-циклогексил-3-хлоробензоат, S,S'-циклогексан-1,2-диил-бис-3-хлоротиобензоат, S-2-диоксиэтилкарбамоил-циклогексил-3-хлоротиобензоат, S-2-дитиоэтилкарбамоил-циклогексил-3-хлоротиобензоат, S-2-оксиэтоксикарбонил-циклогексил-3-хлоротиобензоат, S-2-тиоэтоксикарбонил-циклогексил-3-хлоротиобензоат, 2-дитиоэтилкарбамоил-циклогексил- диэтилкарбамат, 2-тиоэтоксикарбонил-циклогексил-диэтилкарбамат, 2-тиоэтоксикарбонил-циклогексил-этилкарбонат, S,S'-циклогексан-1,2-диил-O,O'-диэтил-дитиокарбонат, S,S'-циклогексан-1,2-диил-бис-диэтилтиокарбамат, S-2-оксиэтоксикарбонил-циклогексил-диэтилтиокарбамат, S-2-тиоэтоксикарбонил-циклогексил-диэтилтиокарбамат, 2-4-тиопропилбензоил-циклогексил-4-пропилбензоат, 2-дитиоэтилкарбамоил-циклогексил-4-пропилбензоат, 2-тиоэтоксикарбонил-циклогексил-4-пропилбензоат, S,S'-циклогексан-1,2-диил-бис-4-пропилтиобензоат, S-2-диоксиэтилкарбамоил-циклогексил-4-пропилтиобензоат, S-2-дитиоэтилкарбамоил-циклогексил-4-пропилтиобензоат, S-2-оксиэтоксикарбонил-циклогексил-4-пропилтиобензоат, S-2-тиоэтоксикарбонил-циклогексил-4-пропилтиобензоат, 2-дитиоэтилкарбамоил-циклогексил-диэтилкарбамат, 2-тиоэтоксикарбонил-циклогексил-диэтилкарбамат, 2-тиоэтоксикарбонил-циклогексил-этилкарбонат, S,S'-циклогексан-1,2-диил-O,O'-диэтил-дитиокарбонат, S,S'-циклогексан-1,2-диил-бис-диэтилтиокарбамат, S-2-оксиэтоксикарбонил-циклогексил-диэтилтиокарбамат, S-2-тиоэтоксикарбонил-циклогексил-диэтилтиокарбамат, 8-дитиоэтилкарбамоил-нафталин-1-ил-бензоат, 8-тиоэтоксикарбонил-нафталин-1-ил-бензоат, 8-тиобензоил-нафталин-1-ил-бензоат, S,S'-нафталин-1,8-диил-дитиобензоат, S-8-диоксиэтилкарбамоил-нафталин-1-ил-тиобензоат, S-8-дитиоэтилкарбамоил-нафталин-1-ил-тиобензоат, S-8-оксиэтоксикарбонил-нафталин-1-ил-тиобензоат, S-8-тиоэтоксикарбонил-нафталин-1-ил-тиобензоат, 8-дитиоэтилкарбамоил-нафталин-1-ил-диэтилкарбамат, 8-тиоэтоксикарбонил-нафталин-1-ил-диэтилкарбамат, 8-тиоэтоксикарбонил-нафталин-1-ил-этилкарбонат, O,O'-диэтил-S,S'-нафталин-1,8-диил-дитиокарбонат, S,S'-нафталин-1,8-диил-бис-диэтилтиокарбамат, S-8-оксиэтоксикарбонил-нафталин-1-ил-диэтилтиокарбамат, S-8-тиоэтоксикарбонил-нафталин-1-ил-диэтилтиокарбамат, 8-3-тиохлоробензоил-нафталин-1-ил-3-хлоробензоат, 8-дитиоэтилкарбамоил-нафталин-1-ил-3-хлоробензоат, 8-тиоэтоксикарбонил-нафталин-1-ил-3-хлоробензоат, S,S'-нафталин-1,8-диил-бис-3-хлоротиобензоат, S-8-диоксиэтилкарбамоил-нафталин-1-ил-3-хлоротиобензоат, S-8-дитиоэтилкарбамоил-нафталин-1-ил3-хлоротиобензоат, S-8-оксиэтоксикарбонил-нафталин-1-ил-3-хлоротиобензоат, S-8-тиоэтоксикарбонил-нафталин-1-ил-3-хлоротиобензоат, 8-дитиоэтилкарбамоил-нафталин-1-ил-диэтилкарбамат, 8-тиоэтоксикарбонил-нафталин-1-ил-диэтилкарбамат, 8-тиоэтоксикарбонил-нафталин-1-ил-этилкарбонат, O,O'-диэтил-S,S'-нафталин-1,8-диил-дитиокарбонат, S,S'-нафталин-1,8-диил-бис-диэтилтиокарбамат, S-8-оксиэтоксикарбонил-нафталин-1-ил-диэтилтиокарбамат, S-8-тиоэтоксикарбонил-нафталин-1-ил-диэтилтиокарбамат, 8-4-тиопропилбензоил-нафталин-1-ил-4-пропилбензоат, 8-дитиоэтилкарбамоил-нафталин-1-ил-4-пропилбензоат, 8-тиоэтоксикарбонил-нафталин-1-ил-4-пропилбензоат, S,S'-нафталин-1,8-диил-бис-4-пропилтиобензоат, S-8-диоксиэтилкарбамоил-нафталин-1-ил-4-пропилтиобензоат, S-8-дитиоэтилкарбамоил-нафталин-1-ил-4-пропилтиобензоат, S-8-оксиэтоксикарбонил-нафталин-1-ил-4-пропилтиобензоат, S-8-тиоэтоксикарбонил-нафталин-1-ил-4-пропилтиобензоат, 8-дитиоэтилкарбамоил-нафталин-1-ил-диэтилкарбамат, 8-тиоэтоксикарбонил-нафталин-1-ил-диэтилкарбамат, 8-тиоэтоксикарбонил-нафталин-1-ил-этилкарбонат, O,O'-диэтил-S,S'-нафталин-1,8-диил-дитиокарбонат, S,S'-нафталин-1,8-диил-бис-диэтилтиокарбамат, S-8-оксиэтоксикарбонил-нафталин-1-ил-диэтилтиокарбамат, S-8-тиоэтоксикарбонил-нафталин-1-ил-диэтилтиокарбамат, 9-дитиолэтилкарбамоил-метил-9H-флуорен-9-ил-метилбензоат, 9-тиоэтоксикарбонил-метил-9H-флуорен-9-ил-метилбензоат, 9-тиобензоил-метил-9H-флуорен-9-ил-метилбензоат, S,S'-9H-флуорен-9,9-диил-бис-метилeн-дитиобензоат, S-9-диоксиэтилкарбамоил-метил-9H-флуорен-9-ил-метилтиобензоат, S-9-дитиоэтилкарбамоил-метил-9H-флуорен-9-ил-метилтиобензоат, S-9-оксиэтоксикарбонил-метил-9H-флуорен-9-ил-метилтиобензоат, S-9-тиоэтоксикарбонил-метил-9H-флуорен-9-ил-метилтиобензоат, 9-дитиолэтилкарбамоил-метил-9H-флуорен-9-ил-метил-диэтилкарбамат, 9-тиоэтоксикарбонил-метил-9H-флуорен-9-ил-метил- диэтилкарбамат, 9-тиоэтоксикарбонил-метил-9H-флуорен-9-ил-метил- этилкарбонат, S,S'-9H-флуорен-9,9-диил-бис-метил-O,O'-диэтил- дитиокарбонат, S,S'-9H-флуорен-9,9-диил-бис-метил-бис-диэтилтиокарбамат, S-9-оксиэтоксикарбонил-метил-9H-флуорен-9-ил-метил-диэтил-тиокарбамат, S-9-тиоэтоксикарбонил-метил-9H-флуорен-9-ил-метил-диэтил-тиокарбамат
Как объяснено выше, компоненты катализатора содержат, дополнительно к указанным выше донорам электронов, Ti, Mg и галоген. В частности компоненты катализатора содержат соединение титана, имеющее, по меньшей мере, связь Ti-галоген и вышеупомянутые электронодонорные соединения на носителе из галогенида Mg. Галогенидом магния предпочтительно является MgCl2 в активной форме, который широко известен из патентной литературы в качестве носителя для катализаторов Циглера-Натта. Патенты США 4298718 и США 4495338 первыми описали использование указанных соединений в катализе Циглера-Натта. Как известно из этих патентов, дигалогениды магния в активной форме, используемые в качестве носителя или соносителя в компонентах катализаторов для полимеризации олефинов, характеризуются рентгеновскими спектрами, в которых наиболее интенсивная линия дифракции, появляющаяся в спектре неактивного галогенида, уменьшается по интенсивности и замещается галогенной группой, максимум интенсивности которой, смещается в сторону более низких углов по отношению к наиболее интенсивной линии.
Предпочтительными соединениями титана, используемыми в компоненте катализатора по настоящему изобретению, являются TiCl4 and TiCl3, кроме того, могут быть использованы Ti-галоалкоголяты формулы Ti(OR)m-yXy, где m представляет собой валентность титана, у представляет собой число от 1 до m-1, Х представляет собой галоген, а R представляет собой углеводородный радикал, содержащий от 1 до 10 атомов углерода.
В конкретном варианте осуществления изобретения количество атомов Ti составляет более 2,5 вес.%, более предпочтительно более 3,0 вес.% и особенно от 3,0 до 8 вес.% по отношению к общей массе указанного компонента катализатора.
Получение твердого каталитического компонента может быть осуществлено различными способами. Один способ включает в себя реакцию между алкоголятами магния или алкоголятами хлора (в частности алкоголяты хлора получают в соответствии с патентом США 4220554) и избыточным TiCl4 в присутствии электронодонорных соединений при температуре от около 80 до 120°С.
В соответствии с предпочтительным способом твердый компонент катализатора может быть получен реакцией титанового соединения формулы Ti(OR)m-yXy, где m представляет собой валентность титана, y представляет собой число от 1 до m, предпочтительно TiCl4, с хлоридом магния, являющегося производным аддукта формулы MgCl2⋅pROH, где р представляет собой число от 0,1 до 6, предпочтительно от 2 до 3,5, а R представляет собой углеводородный радикал, содержащий 1-18 атомов углерода. Аддукты сферической формы получают путем смешивания спирта и хлорида магния в присутствии инертного углеводорода, несмешиваемого с аддуктом, в режиме перемешивания при температуре плавления аддукта (100-130°C). Эмульсия затем быстро охлаждается, вызывая отверждение аддукта в виде сферических частиц. Примеры сферических аддуктов, полученных в соответствии с данным способом, описываются в патенте США 4399054 и патенте США 4469648. Полученный таким образом аддукт может непосредственно вступать в реакцию с соединением Ti или быть предварительно подвергнут термическому контролируемому удалению спирта (80-130°C), чтобы получить аддукт, в котором число молей спирта обычно меньше 3, предпочтительно от 0,1 до 2,5. Реакция с соединением Ti может проводиться при суспендировании аддукта (деалкоголированного или как такового) с холодным TiCl4 (обычно 0°C). Смесь нагревают до 80-130°С и выдерживают при этой температуре в течение 0,5-2 часов. Обработка TiCl4 может проводиться один или несколько раз. Электронодонорное соединение на основе меркаптановой производной предпочтительно добавляют в процессе обработки соединением TiCl4. Приготовление компонентов катализатора сферической формы описываются, например, в европейских заявках на патент EP-A-395083, EP-A-553805, EP-A-553806, EPA601525 и WO98/44009.
Твердые компоненты катализатора, полученные в соответствии с описанным выше способом, показывают удельную поверхность частиц (по методу БЭТ) обычно равную от 20 до 500 м2/г, предпочтительно от 50 до 400 м2/г, а полную пористость (по методу БЭТ) выше 0,2 см3/г, предпочтительно от 0,2 до 0,6 см3/г. Пористость (по ртутному способу), являющаяся результатом пор радиусом до 10000Å, обычно составляет от 0,3 до 1,5 см3/г, предпочтительно от 0,45 до 1см3/г. Твердый компонент катализатора имеет средний размер частиц от 5 до 120 мкм и более предпочтительно от 10 до 100 мкм.
В любой из этих способов получения может быть добавлено желательное электронодонорное соединение как таковое или, как вариант, оно может быть получено на месте с использованием соответствующего предшественника, способного к преобразованию в желательное электронодонорное соединение с помощью, например, известных химических реакций.
Независимо от используемого способа получения конечный объем электронодонорного соединения формулы (I) таков, что его мольное отношение к атомам Ti составляет от 0,01 до 2, предпочтительно от 0,05 до 1,2.
Твердые компоненты катализатора, согласно настоящему изобретению превращаются в катализаторы для полимеризации олефинов путем их реакции с алюминийорганическими соединениями в соответствии с известными способами.
В частности, целью настоящего изобретения является катализатор полимеризации олефинов CH2=CHR, в которой R представляет собой водород или углеводородный радикал с 1-12 атомами углерода, включающий продукт, полученный реакцией:
(i) твердого компонента катализатора, как описано выше, и
(ii) алкилалюминиевого соединения и, необязательно,
(iii) внешнего электронодонорного соединения.
Алкилалюминиевое соединение (ii) предпочтительно выбирается из группы, включающей триалкилалюминевые соединения, например триэтилалюминий, триизобутилалюминий, три-n-бутилалюминий, три-n-гексилалюминий, n-гексилалюминий, три-n-октилалюминий. Можно также использовать алкилалюминийгалогениды, алкилалюминийгидриды или алкилалюминийсесквихлориды, такие как AlEt2Cl и Al2Et3Cl3, возможно в смеси с указанными выше триалкилалюминиевыми соединениями.
Подходящие внешние электронодонорные соединения включают в себя соединения кремния, простые эфиры, сложные эфиры, амины, гетероциклические соединения и, в частности, 2,2,6,6-тетраметилпиперидины и кетоны.
Другим классом предпочтительных внешних электронодонорных соединений являются соединения кремния, имеющие формулу (R7)a(R8)bSi(OR9)c, где a и b представляют собой целые числа от 0 до 2, c представляет собой целое число от 1 до 4, а сумма (a+b+c) равна 4, а R7, R8 и R9 представляют собой алкильные, циклоалкильные или арильные радикалы, содержащие от 1 до 18 атомов углерода, необязательно содержащие гетероатомы. Особенно предпочтительными являются соединения кремния, в которых a=1, b=1, c=2, по меньшей мере, один из радикалов R7 и R8 выбирается из разветвленных алкильных, циклоалкильных или арильных групп, содержащих от 3 до 10 атомов углерода, необязательно содержащих гетероатомы, а R9 представляет собой алкильную группу C1-C10, в частности, метил. Примерами таких предпочтительных соединений кремния являются: метилциклогексил-диметоксисилан (С донор), дифенил-диметоксисилан, метил-трет-бутил-диметоксисилан, дициклопентил-диметоксисилан (D донор), диизопропил-диметоксисилан, 2-этилпиперидинил-трет-бутил-диметоксисилан, 2-этилпиперидинил-тексил-диметоксисилан, 3,3,3-трифторо-n-пропил-2-этилпиперидинил-диметоксисилан, метил-3,3,3-трифторо-n-пропил-диметоксисилан, N,N-диэтиламинотриэтоксисилан. Кроме того, также предпочтительными являются соединения кремния, в которых а равно 0, с равно 3, R8 представляет собой разветвленную алкильную или циклоалкильную группу, необязательно содержащую гетероатомы, а R9 представляет собой метил. Примерами таких предпочтительных соединений кремния являются циклогексилтриметоксисилан, трет-бутил-триметоксисилан и тексилтриметоксисилан.
Электронодонорное соединение (iii) используется в таком количестве, чтобы получить молярное соотношение между алюминийорганическим соединением и указанным электронодонорным соединением (iii) в пределах от 0,1 до 500, предпочтительно от 1 до 300 и более предпочтительно от 3 до 100.
Таким образом, оно представляет собой еще один вариант осуществления настоящего изобретения, а именно способ (со) полимеризации олефинов CH2=CHR, в котором R представляет собой водород или нециклический углеводородный остаток различной степени насыщенности с 1-12 атомами углерода, осуществляемый в присутствии катализатора, содержащего продукт реакции между:
(i) твердым компонентом катализатора, содержащего Mg, Ti и электронодонорное соединение с формулой (I), как описано выше;
(ii) алкилалюминиевым соединением и,
(ii) необязательно, электронодонорным соединением (внешний донор).
Процесс полимеризации может быть проведен в соответствии с известными способами, например как суспензионная полимеризация с использованием в качестве разбавителя инертного углеводородного растворителя или как объемная полимеризация с использованием жидкого мономера (например, пропилена) в качестве реакционной среды. Кроме того, можно проводить газофазную полимеризацию в одном или нескольких реакторах с псевдоожиженным или механически перемешиваемым слоем.
Полимеризацию обычно проводится при температуре от 20 до 120°С, предпочтительно от 40 до 80°С. При газофазной полимеризации рабочее давление, как правило, составляет от 0,5 до 5 МПа, предпочтительно от 1 до 4 МПа. При объемной полимеризации рабочее давление обычно составляет от 1 до 8 МПа, предпочтительно от 1,5 до 5 МПа.
Следующие примеры приводятся для иллюстрации изобретения, не ограничивая его.
ПРИМЕРЫ
ХАРАКТЕРИСТИКИ
Определение X.I.
2,5 г полимера и 250 мл о-ксилола помещали в круглодонную колбу, снабженную холодильником и дефлегматором, и держали в атмосфере азота. Полученную смесь нагревали до 135°С и подвергали перемешиванию в течение приблизительно 60 минут. Конечный раствор охлаждали до 25°С при непрерывном перемешивании, а нерастворимый полимер отфильтровывали. Фильтрат упаривали в потоке азота при 140°С до получения постоянного веса. Содержание указанной и растворимой в ксилоле фракции выражалось как процент от первоначальных 2,5 г, а затем по разности, как X.I. %.
Содержание доноров.
Содержание донора электронов определялось с помощью газовой хроматографии. Твердый компонент растворяли в кислой воде. Раствор экстрагировали этилацетатом, добавляли внутренний эталон, а образец органической фазы анализировали в газовом хроматографе с целью определения числа доноров, присутствующих на исходном каталитическом соединении.
Скорость течения расплава (MFR)
Индекс расплава MIL полимера определялся согласно ISO 1133 (230°C, 2,16 кг).
Пример 1. Синтез 2-тиобензоил-4-трет-бутил-3,6-диметилфенилбензоата
Первая стадия Синтез 4-трет-бутил-2-меркапто-3,6 диметилфенола
Реакция проводится в атмосфере аргона. 4-трет-бутил-2,5-диметилфенол (20 г, 0,11 моль) растворяют в 120 мл толуола, содержащего 0,37 г серы. Раствор S2Cl2 объемом 4,9 мл (0,062 моль) в 50 мл толуола медленно добавляют через капельную воронку при непрерывном активном перемешивании с такой скоростью, чтобы температура реакции не превышала 30°С. По завершении раствор греют при 75°С в течение 1 ч и охлаждают до комнатной температуры. Реакционную смесь концентрируют при низком вакууме до объема остатка около 60 мл. Полученную суспензию медленно добавляют к суспензии из 5,38 г (0,14 моль) LiAlH4 в раствор Et2O объемом 180 мл.
Реакционную смесь нагревают с обратным холодильником в течение 6 часов, перемешивают в течение ночи и осторожно обрабатывают 5% HCl. Органический раствор отделяют, водный слой экстрагируют Et2O несколько раз. Комбинированную органическую фазу сушат над MgSO4, упаривают и остаток кристаллизуют гептаном. Выход 5,76 г (49%).
Вторая стадия Синтез 2-тиобензоил-4-трет-бутил-3,6-диметилфенилбензоата
Раствор 4-трет-бутил-2-меркапто-3,6-диметилфенол (10 г, 0,048 моль) в толуоле (290 мл) последовательно обрабатывают хлористым бензоилом (11,8 мл, 0,10 моль) и Et3N (20,0 мл) при 0°С. После 16 часов перемешивания при комнатной температуре раствор выливают в водный раствор HCl и разбавляют толуолом (100 мл). Органический слой последовательно промывают водой, 2% водным раствором NaOH, водой, сушат над MgSO4, упаривают и полученное масло перекристаллизовывают из 95% EtOH (50 мл). Выход 15,5 г (78%).
Пример 2. Синетез 4-трет-бутил-2-тиоэтоксикарбонил-6-метилфенил-этилкарбоната
Первая стадия. Синтез 4-трет-бутил-2-меркапто-6-метилфенола
Реакция проводится в атмосфере аргона. 4-трет-бутил-2-метилфенол (90 г, 0,5 моль) растворяют в 250 мл толуола, содержащего 0,5 г серы. Раствор S2Cl2 объемом 22 мл (0,55 моль) в 100 мл толуола медленно добавляют через капельную воронку при непрерывном активном перемешивании с такой скоростью, чтобы температура реакции не превышала 30°С. Затем раствор греют при 75°С в течение 1 часа и охлаждают до комнатной температуры. Толуол удаляют при низком вакууме, а остаток растворяют в 200 мл Et2O. Полученный раствор медленно добавляют к суспензии из 24 г (0,63 моль) LiAlH4 в 600 мл Et2O.
Реакционную смесь нагревают с обратным холодильником в течение 6 часов, перемешивают в течение ночи и осторожно обрабатывают 5% HCl. Органический раствор отделяют, водный слой экстрагируют Et2O несколько раз. Комбинированную органическую фазу сушат над MgSO4, упаривают и перегоняют. Выход 50,1 г (47%).
Вторая стадия. Синетез 4-трет-бутил-2-тиоэтоксикарбонил-6-метилфенил-этилкарбоната
Раствор 4-трет-бутил-2-меркапто-6-метилфенола (7,88 г, 0,0342 моль) в толуоле (150 мл) последовательно обрабатывают пиридином (12 мл) и этилхлорформиатом (7,19 мл, 0,0752 моль) при перемешивании и охлаждении (0°С). После перемешивания при комнатной температуре в течение 16 часов реакционную смесь обрабатывают водой и разбавляют толуолом (100 мл). Органический слой последовательно промывают водным раствором HCl и водой, сушат над MgSO4, упаривают и перегоняют в вакууме (165°С/0,5 мм рт.ст.). Выход 8,9 г (73%).
Пример 3. Синетез 4-трет-бутил-2-тиоэтоксикарбонил-3,6-диметилфенил-этилкарбоната
Процедура та же, что и в Примере 2, за исключением того, что вместо 4-трет-бутил-2-меркапто-6-метилфенола используется 4-трет-бутил-2-меркапто-3,6-диметилфенол. После перегонки выход равен 73%.
Пример 4. Одностадийный синтез 4-трет-бутил-2-дитиоэтилкарбамоил-6-метилфенил-3-хлоробензоата
Раствор 4-трет-бутил-2-меркапто-6-метилфенола (9,82 г, 0,05 моль) в пиридине (40 мл) обрабатывают в течение 30 мин с диэтилкарбамоилхлоридом (7,0 г, 0,05 моль) при перемешивании и охлаждении (-30°С). После перемешивания при комнатной температуре в течение 16 часов реакционную смесь обрабатывают 3-хлорангидридом хлорбензойной кислоты (9,1 г, 0,05 моль) при перемешивании и охлаждении (0°С). После перемешивания при комнатной температуре в течение дополнительных 16 часов реакционную смесь выливают в смесь воды со льдом, содержащую 80 мл концентрированной HCl. Затем его экстрагируют CH2Cl2 и органическую фазу последовательно промывают водным раствором HCl, водой, 5% раствором NaOH, водой и сушат над MgSO4 и концентрируют. Продукт очищают хроматографией на колонках с нейтральным Al2O3 и с использованием смеси толуола/гексана (1/2) в качестве элюента. Выход 10,0 г (46%).
Пример 5. Одностадийный синтез 4-трет-бутил-2-дитиометилкарбамоил-6-метилфенил-3-хлоробензоата
Процедура та же, что и в Примере 4, за исключением того, что вместо диэтилкарбамоилхлорида используется диметилкарбамоилхлорид. Выход 72%.
Пример 6. Одностадийный синтез S-5-трет-бутил-2-оксиэтоксикарбонил-3-метилфенил-дитиометилкарбамината
Процедура та же, что и в Примере 4, за исключением того, что вместо 3-хлорангидрида хлорбензойной кислоты используется этилхлорформиат. Выход 59%.
Пример 7. Одностадийный синтез S-5-трет-бутил-2-оксиэтоксикарбонил-3-метилфенил-дитиоетилкарбамината
Процедура та же, что и в Примере 6, за исключением того, что вместо диметилкарбамоилхлорида используется диэтилкарбамоилхлорид. Выход 57%.
Пример 8. Одностадийный синтез 4-трет-бутил-2-тиоэтоксикарбонил-3,6-диметилфенил-3-хлоробензоата
Раствор 4-трет-бутил-2-меркапто-6-метилфенола (9,0 г, 0,043 моль) и пиридина (16 мл) в толуоле (160 мл) подвергают 3-х часовой обработке раствором этилхлорформиата (4,64 г, 0,043 моль) в толуоле (30 мл) при перемешивании и охлаждении (0°С). После перемешивания при комнатной температуре в течение 16 часов реакционную смесь обрабатывают 3-хлорангидридом хлорбензойной кислоты (7,53 г, 0,043 моль) при перемешивании и охлаждении (0°С). После 16 часов перемешивания при комнатной температуре раствор, взбалтывая, выливают в водный раствор HCl и разбавляют толуолом (100 мл). Органический слой последовательно промывают водой, 2% водным раствором NaOH, водой, сушат над MgSO4, упаривают и полученное масло перекристаллизовывают из петролейного эфира. Выход 11,6 г (64%).
Пример 9. Одностадийный синтез 4-трет-бутил-2-тиоэтоксикарбонил-3,6-диметилфенилбензоата
Процедура та же, что и в Примере 8, за исключением того, что вместо 3-хлорангидрида хлорбензойной кислоты используется хлористый бензоил. Выход после кристаллизации из гептана 54%.
Пример 10. Одностадийный синтез 4-трет-бутил-2-тиоэтоксикарбонил-3,6-диметилфенил-4-метилбензоата
Процедура та же, что и в Примере 8, за исключением того, что вместо 3-хлорангидрида хлорбензойной кислоты используется 4-метилбензоилхлорид. Выход после кристаллизации из петролейного эфира составляет 56%.
Пример 11. Одностадийный синтез 4-трет-бутил-2-тиоэтоксикарбонил-6-метилфенил-3-хлоробензоата
Процедура та же, что и в Примере 8, за исключением того, что вместо 4-трет-бутил-2-меркапто-3,6-диметилфенола используется 4-трет-бутил-2-меркапто-6-метилфенол. Выход после кристаллизации из петролейного эфира составляет 46%.
Пример 12. Одностадийный синтез 4-трет-бутил-2-тиоэтоксикарбонил-6-метилфенилбензоата
Процедура та же, что и в Примере 9, за исключением того, что вместо 4-трет-бутил-2-меркапто-3,6-диметилфенола используется 4-трет-бутил-2-меркапто-6-метилфенол. Выход после кристаллизации из смеси петролейного эфира/CHCl3(в соотношении около 1/1) составляет 34%.
Пример 13. Одностадийный синтез 4-трет-бутил-2-тиоэтоксикарбонил-6-метилфенил-4-метилбензоата
Процедура та же, что и в Примере 10, за исключением того, что вместо 4-трет-бутил-2-меркапто-3,6-диметилфенола используется 4-трет-бутил-2-меркапто-6-метилфенол. Выход после кристаллизации из петролейного эфира составляет 38%.
Пример 14. Одностадийный синтез 4-трет-бутил-2-тиоэтоксикарбонил-3,6-диметилфенил-фуран-2-карбоксилата
Процедура та же, что и в Примере 11, за исключением того, что вместо 3-хлорангидрида хлорбензойной кислоты используется 2-фуроилхлорид. Выход после кристаллизации из петролейного эфира и EtOH составляет 56%.
Пример 15. Одностадийный синтез 4-трет-бутил-2-тиоэтоксикарбонил-6-метилфенил-диэтилкарбамината
Раствор 4-трет-бутил-2-меркапто-6-метилфенола (18,83 г, 0,096 моль) и пиридина (27 мл) в толуоле (350 мл) подвергают 4-х часовой обработке раствором этилхлорформиата (9,15 мл, 0,097 моль) в толуоле (50 мл) при перемешивании и охлаждении (0°С). После перемешивания при комнатной температуре в течение 16 часов смесь обрабатывали раствором диэтилкарбамоилхлорида (20 мл, 0,158 моль) и Et3N (20 мл) при перемешивании и охлаждении (0°С). После 48 часов перемешивания при комнатной температуре, производилось быстрое охлаждение водным раствором HCl и разбавление толуолом (100 мл). Органический слой промывали водой, сушили над MgSO4, упаривали и полученный остаток перегоняли в вакууме (180-182°С/0,3 мм рт.ст.). Выход 8,4 г (24%).
Пример 16. Синтез S-5-циклогексил-2-оксиэтоксикарбонил-3-метилфенил-дитиометилкарбамината
Первая стадия: Синтез 4-циклогексил-2-меркапто-6-метилфенола
Раствор S2Cl2 (20 мл, 0,25 моль) в толуоле (250 мл) обрабатывали раствором 4-циклогексил-2-метилфенола (47,6 г, 0,25 моль) в толуоле (250 мл) при перемешивании. После добавления раствор перемешивали еще 2 часа. Растворитель выпаривали в вакууме, остаток растворяли в 95% EtOH (400 мл), а затем добавляли порошок цинка (50 г, 0,79 моль) с последующим добавлением каплями концентрированной НСl (190 мл) при 0°С и перемешивании. После добавления смесь перемешивали еще 2 часа. Реакционную смесь выливали в воду (900 мл) и экстрагировали CH2Cl2 несколько раз. Комбинированную органическую фазу сушили над MgSO4, упаривали и остаток перегоняли в вакууме (133-136°С/0,5 мм рт.ст.). Выход 26,7 г (48%).
Вторая стадия Синтез S-5-циклогексил-2-оксиэтоксикарбонил-3-метилфенил-дитиометилкарбамината
Раствор 4-циклогексил-2-меркапто-6-метилфенола (16,68, 0,075 моль) и пиридина (19 мл) в толуоле (180 мл) обрабатывали в течение 30 минут диметилкарбамоилхлоридом (8,47 г, 0,082 моль) при перемешивании и охлаждение (0°С). После перемешивания при комнатной температуре в течение 16 часов реакционную смесь обрабатывали этилхлорформиатом (9,77 мл, 0,09 моль) при перемешивании и охлаждении (0°С). После перемешивания при комнатной температуре в течение дополнительных 16 часов реакционную смесь выливали в смесь воды со льдом, содержащую 30 мл концентрированной HCl. Затем ее экстрагировали CH2Cl2, органическую фазу промывали последовательно водным раствором HCl и водой, сушили над MgSO4, упаривали и остаток перегоняли в вакууме (212-215°С / 0,4 мм рт.ст.). Выход 11,4 г (42%)
Пример 17. Синтез син S,S'-пентана-2,4-диил-дитиобензоата
Первая стадия: Синтез син-пентана-2,4-диил-бис-4-метилбензолсульфоната
В реакционный сосуд объемом 250 мл загружают син-2,4-пентандиола (10 г, 95,1 ммоль) и пиридина (70 г). Смесь охлаждают до -10°С и медленно добавляют p-толуолсульфонилхлорид (40,3 г, 2,2 экв). Смесь оставляют перемешиваться при комнатной температуре в течение 15 часов. Этилацетат (100 мл) добавляется к реакционной смеси и полученный органический слой промывается насыщенным водным раствором NH4Cl и насыщенным водным раствором NaCl, затем сушится над MgSO4, фильтруется и концентрируется на ротационном испарителе с получением твердого сырого продукта желтого цвета.
Вторая стадия: Синтез син S,S'-пентана-2,4-диил-дитиобензоата
В реакционный сосуд объемом 100 мл загружают син-пентан-2,4-диил-бис-4-метилбензолсульфонат (5,6 г, 13,4 ммоль), тиобензойную карбонодитионовую кислоту (4,13 г, 2 экв), NaHCO3 (2,28 г, 2 экв) и диметилформамид (25 мл). Смесь оставляют перемешиваться при 80°С в течение 2 часов. Красный раствор разбавляют этилацетатом (50 мл) и полученный раствор промывают насыщенным водным раствором NaHCO3 и насыщенным водным раствором NaCl. Органический слой сушат над MgSO4, фильтруют и концентрируют на ротационном испарителе с получением сырого продукта в виде масла красного цвета. Он очищается на хроматографе (SiO2) циклогексан/этилацетатом в соотношении 40/1. Выход: 2 г (43,3%).
Пример 18. Синтез S,S'-пентана-2,4-диил-бис-4-тиопропилбензоата
Первая стадия: Синтез S,S'-пентана-2,4-диил-дитиоэтаната
В реакционный сосуд объемом 250 мл загружают смесь пентан-2,4-диил-бис-4-метилбензолсульфоната (19 г, 45,6 ммоль), тиоацетата калия (15,78 г, 3 экв) и диметилформамид (70 мл). Смесь оставляют перемешиваться температуре окружающей среды в течение 12 часов. Красный раствор разбавляют этилацетатом (200 мл) и полученный раствор промывают насыщенным водным раствором NaHCO3 и насыщенным водным раствором NaCl. Органическую фазу сушат над MgSO4, фильтруют и концентрируют на ротационном испарителе с получением сырого продукта в виде масла красного цвета. Его очищают перегонкой. Выход: 8,1 г (80%)–желтое масло. Вторая стадия: Синтез S,S'-пентана-2,4-диил-бис-4-тиопропилбензоата
В реакционный сосуд объемом 100 мл загружают S,S'-пентан-2,4-диил- дитиоэтаната (5 г, 22,5 ммоль) и метанол (50 мл). Затем медленно добавляют метилат натрия (2,57 г, 2,1 экв) при комнатной температуре. Смесь перемешивают в течение 2 часов. Метанол удаляют перегонкой и полученное масло оранжевого цвета разбавляют пиридином (50 мл). Смесь охлаждают до 0°С, медленно добавляют 4-n-пропил-бензоилхлорид (11,08 г, 2,7 экв) и перемешивают в течение 12 часов. Пиридин удаляют перегонкой, а полученное масло разбавляют этилацетатом (100 мл). Полученный раствор промывают насыщенным водным раствором NaHCO3 и насыщенным водным раствором NaCl. Органический фазу сушат над MgSO4, фильтруют и концентрируют на ротационном испарителе с получением сырого продукта в виде масла желтого цвета. Он очищается на хроматографе (SiO2) циклогексан/этилацетатом в соотношении 60/1. Выход: 4,4 г (45,6%).
Процедура подготовки твердого компонента катализатора с использованием доноров из примеров 1-17.
В круглодонную колбу объемом 500 мл, снабженную механической мешалкой, холодильником и термометром загружали 250 мл TiCl4 при комнатной температуре в атмосфере азота. После охлаждения до 0°C и при перемешивании, в колбу последовательно добавляли внутренний донор и 10,0 г сферического аддукта (полученного согласно вышеприведенного описания). Объем добавляемого внутреннего донора выдерживался для получения молярного соотношения Mg/донор равного 6. Температуру повышали до 100°С и выдерживали в течение 2 часов. Затем перемешивание прекращали, твердому продукту давали возможность осесть, а надосадочную жидкость сливали через сифон при 100°С. После удаления надосадочной жидкости дополнительно добавляли первичный TiCl4 для достижения начального объема жидкости. Смесь нагревали при 120°С и выдерживали при этой температуре в течение 1 часа. Перемешивание прекращали и давали осесть твердому осадку,а надосадочную жидкость сливали через сифон.
Твердое вещество промывали безводным гексаном шесть раз (6 х 100 мл) с понижением температуры до 60°С и один раз (100 мл) при комнатной температуре. Полученное твердое вещество затем сушили в вакууме и подвергали анализу.
Процедура подготовки твердого компонента катализатора с использованием доноров из примера 18.
В круглодонную колбу объемом 500 мл, снабженную механической мешалкой, холодильником и термометром загружали 250 мл TiCl4 при комнатной температуре в атмосфере азота. После охлаждения до 0°C и при перемешивании в колбу последовательно добавляли этилбензоат и 10,0 г сферического аддукта (полученного согласно вышеприведенному описанию). Объем добавляемого этилбензоата выдерживался для получения молярного соотношения Mg/EB равного 4. Температуру повышали до 100°С и выдерживали в течение 2 часов. Затем перемешивание прекращали, твердому продукту давали возможность осесть, а надосадочную жидкость сливали через сифон при 100°С. После удаления надосадочной жидкости дополнительно добавляли первичный TiCl4 для достижения начального объема жидкости, с последующим добавлением внутреннего донора с молярным соотношением Mg/донор равным 6. Смесь нагревали при 120°С и выдерживали при этой температуре в течение 1 часа. Перемешивание прекращали и давали осесть твердому осадку, а надосадочную жидкость сливали через сифон. Дополнительно повторялась горячая обработка при 120°С в течение 1 часа. Перемешивание прекращали и давали осесть твердому осадку, а надосадочную жидкость сливали через сифон.
Твердое вещество промывали безводным гексаном шесть раз (6 х 100 мл) с понижением температуры до 60°С и один раз (100 мл) при комнатной температуре. Полученное твердое вещество затем сушили в вакууме и подвергали анализу.
Общий способ полимеризации пропилена
Стальной автоклав объемом 4 литра, снабженный мешалкой, манометром, термометром, системой подачи катализатора, линиями подачи мономера и термостатическим кожухом, продували потоком азота при 70°С в течение одного часа. Затем, при 30°С и в потоке пропилена, последовательно загружали 75 мл безводного гексана, 0,76 г AlEt3, 0,076 г дициклопентил-диметоксисилана (D донора) и 0,006 ÷ 0,010 г твердого компонента катализатора. Автоклав закрывали и впоследствии добавляли 2,0 л водорода. Затем при перемешивании подавали 1,2 кг жидкого пропилена. Температуру повышали до 70°С в течение пяти минут и проводили полимеризацию при этой температуре в течение двух часов. В конце полимеризации не прореагировавший пропилен удаляли, полимер извлекали и сушили при 70°С в вакууме в течение трех часов. Затем полимер взвешивали и фракционировали о-ксилолом, чтобы определить объем фракции (X.I.), нерастворимой в ксилоле.


Реферат
Изобретение относится к твердому компоненту катализатора, к катализатору и к способу (со)полимеризации олефинов в присутствии указанного катализатора. Твердый компонент катализатора содержит Mg, Ti, Cl и электронодонорное соединение с формулой (I), в котором X и Y выбираются из R, -ORи -NR, а В представляет собой кислород или серу, S представляет собой серу, Rвыбирается из углеводородных групп С-С, необязательно содержащих гетероатом, выбранный из галогена и О, которые могут быть соединены с образованием одного или нескольких циклов, R представляет собой водород или R, а А представляет собой двухвалентную мостиковую группу с длиной цепи между двумя мостиковыми связями, равную 1-10 атомам, и имеет формулу -(ZR)-, где Z независимо выбирается из С, группы R, равные или отличающиеся друг от друга, представляют собой водород или углеводородные радикалы С-С, которые могут быть соединены с образованием одного или нескольких циклов, m представляет собой число, равное валентности Z, а n - целое число от 1 до 10. Катализатор полимеризации содержит продукт реакции между твердым компонентом катализатора и алкилалюминиевым соединением; и необязательно внешним электронодонорным соединением. Технический результат – превосходный баланс химической активности и стереоспецифичности. 3 н. и 11 з.п. ф-лы, 1 табл., 18 пр.формула (I):
Формула


Документы, цитированные в отчёте о поиске
Твердый каталитический компонент для полимеризации олефинов, содержащий его катализатор и его применение

Комментарии