Конверсия с1-3 оксигенатных соединений до с4-оксигенатных соединений, опосредованная кристаллическим микропористым материалом - RU2710598C2
Код документа: RU2710598C2
Чертежи


Описание
Избирательное и высокопродуктивное получение С4 оксигенатных соединений, например, С4 сахаров, таких как эритроза, треоза и эритрулоза, может оказаться ценным для их применения в химической промышленности для получения, например: С4 полиолов; метилвинилгликолята или продуктов, получаемых из них; 2-гидрокси-4-метоксибутановой кислоты или ее солей или сложных эфиров, таких как метил 2-гидрокси-4-метоксибутаноат.
Известные способы получения С4 оксигенатных соединений включают альдольную самоконденсацию гликолевого альдегида. Наблюдалось, что альдольные конденсации не являются селективными для получения С4 оксигенатных соединений; наблюдается смесь продуктов по мере того, как С4 продукт продолжает взаимодействовать с образованием оксигенатных соединений с большим количеством атомов углерода. Для контроля селективности взаимодействия для С4 оксигенатных соединений требуется образование комплексов С4-оксигенатных соединений и силиката или бората, или применение С4-оксигенатных селективных катализаторов.
Пример применения силикатного комплекса для селективного образования С4 оксигенатных соединений включает альдольную конденсацию гликолевого альдегида в присутствии водного силиката натрия; Science (2010) 327, стр. 984-986. В ходе взаимодействия образуется комплекс силикат-С4-сахар, что в свою очередь контролирует селективность взаимодействия. Дополнительный пример включает конденсацию гликолевого альдегида в присутствии боратного буферного раствора. Получают высокий выход (86%) С4 оксигенатных соединений (С4 сахаров); J. Am. Chem. Soc. (2011) 133, стр. 9457-9468.
Пример С4-оксигенатного селективного катализатора включает получение С4 оксигенатных соединений альдольной конденсацией гликолевого альдегида в присутствии гомохирального дипептидного катализатора. Выход продуктов С4 оксигенатных соединений составлял вплоть до 63%; PNAS (2006) 103, стр. 12712-12717. Альтернативно можно применять цинк-пролиновый катализатор. Общий выход продуктов С4-сахаров составлял приблизительно 51%. С6-сахара образовывались с выходом, равным приблизительно 30%; Org. Biomol. Chem. (2005) 3, стр. 1850-1855.
Альтернативное получение С4 оксигенатных соединений из гликолевого альдегида включает предложенную промежуточную тетрозу, полуфабрикат в получении 2-гидрокси-4-метоксибутаноата (С4) и метилвинилгликолята (С4). Взаимодействие протекает в присутствии катализатора цеотипа. Материалом цеотипа являлся Sn-BEA, кольцевая пористая двенадцатичленная структура; Green Chemistry (2012) 14, стр. 702-706.
Альтернативный материал цеотипа, такой как пористый структурированный цеотип с десятичленным кольцом (например, Sn-MFI или Ti-MFI), можно применять для изомеризации С2 оксигенатных соединений. Подобный цеотип был применен для изомеризации глиоксаля до гликолевой кислоты. Выход гликолевой кислоты составлял приблизительно 90%; Green Chemistry (2014) 16, стр. 1176-1 186.
Цель настоящего изобретения заключается в предоставлении способа получения С4 оксигенатных соединений из композиции, содержащей С1-3 оксигенатные соединения, где способ является селективным для получения С4 оксигенатных соединений, и продукт получают с высокими выходами.
Раскрытие изобретения
В настоящее время обнаружено, что гликолевый альдегид можно селективно преобразовывать в С4 оксигенатные соединения в присутствии кристаллического микропористого материала, содержащего структуру с небольшим и средним размером пор. Взаимодействие протекает с высоким выходом. Кроме того, возможно, чтобы взаимодействие протекало в присутствии дополнительных соединений с селективным образованием желательных С4 оксигенатных соединений.
Дополнительно изобретение определяется способом получения С4 оксигенатных соединений из композиции, содержащей С1-3 оксигенатные соединения, где способ осуществляют в присутствии кристаллического микропористого материала, содержащего структуру с небольшим и средним размером пор.
С4 оксигенатные соединения могут быть известны как С4 сахара или оксигенатные соединения с длиной углеродной цепи из четырех атомов углерода. Молекулярной формулой С4 оксигенатных соединений может быть С4Н8О4. С4 оксигенатные соединения можно также описать как тетрозы. С4 оксигенатные соединения выбирают из одной или более группы, состоящей из треозы, эритрозы и эритрулозы.
В одном варианте выполнения изобретения композиции, содержащие С1-3 оксигенатные соединения, содержат одно или более оксигенатных соединений, выбираемых из группы, состоящей из С1 оксигенатных соединений, С2 оксигенатных соединений и С3 оксигенатных соединений. С1, С2 и С3 оксигенатные соединения означают соединения, которые обладают длиной углеродной цепи из одного, двух или трех атомов углерода соответственно. Молекулярными формулами С1-3 оксигенатных соединений являются формулы, выбираемые из одной или более из группы, состоящей из: СН2О; С2Н4О2; С2Н2О2; C3H6O2 и С3Н4О2. Предпочтительно композицией, содержащей С1-3 оксигенатные соединения, является композиция, содержащая одно или более соединений, выбираемых из группы, состоящей из формальдегида, глиоксаля, гликолевого альдегида, пирувальдегида и ацетола. Во втором варианте выполнения предпочтительно композицией, содержащей С1-3 оксигенатные соединения, является композиция, содержащая одно или более С2 оксигенатных соединений, выбираемых из группы, состоящей из гликолевого альдегида (2-гидроксиацетальдегида) и глиоксаля. Гликолевым ангидридом является соединение с длиной углеродной цепи из двух атомов углерода, также известного как С2 оксигенатное соединение или С2 сахар.
Композиция, содержащая С1-3 оксигенатные соединения, может находиться в форме раствора, где растворитель выбирают из группы, состоящей из воды, метанола и смеси воды и метанола. Например, композиция, содержащая С1-3 оксигенатные соединения, может быть водным или метанольным раствором гликолевого альдегида или водным или метанольным раствором композиции, содержащей одно или более соединений, выбираемых из группы, состоящей из формальдегида, глиоксаля. гликолевого альдегида, пирувальдегида и анетола.
Композиции, содержащие С1-3 оксигенатные соединения, получают пиролизом биомассы или пиролизом одного или более оксигенатных соединений, выбираемых из группы, состоящей из С5 оксигенатных соединений, С6 оксигенатных соединений и сахарозы. С5 оксигенатные соединения и С6 оксигенатные соединения означают одно или более соединений, выбираемых из группы, состоящей из глюкозы, фруктозы, ксилозы и их изомеров. Типичные реакции пиролиза представлены в US 7094932 В2 и РСТ/ЕР2014/053587.
Кристаллический микропористый материал включает цеолитные материалы и материалы цеотипа. Цеолитными материалами являются кристаллические алюмосиликаты с микропористой кристаллической структурой согласно Corma и др., Chem. Rev. 1995, 95 стр. 559-614. Атомы алюминия цеолитного материала могут быть частично или полностью замещены металлом (атомами металла), таким как цирконий (Zr), титан (Ti) и олово (Sn), эти материалы известны как материалы цеотипа.
Кристаллический микропористый материал, содержащий структуру с малым размером пор, означает кристаллический микропористый материал, содержащий кольцевую пористую восьмичленную структуру; кристаллический микропористый материал, содержащий структуру со средним размером пор, означает кристаллический микропористый материал, содержащий кольцевую пористую десятичленную структуру. Примеры кристаллических микропористых материалов со структурой с небольшим или средним размером пор представлены в Chem. Rev. 1995, 95 стр. 559-614 и включают структуры, такие как LTA, СНА, MFI (ZSM-5), MEL, МТТ, MWW, TON, HEU, AEL, AFO, MWW и FER.
Кристаллический микропористый материал со структурой ВЕА содержит огромную кольцевую пористую двадцатичленную структуру (Chem. Rev. 1995, 95 стр. 559-614), и не рассматривается в качестве признака настоящего изобретения.
Примеры материалов цеотипа со средним размером пор включают структуры, такие как Sn-MFI, Ti-MFI и Zr-MFI. Примером материала цеотипа с небольшим размером пор является Sn-LTA.
Можно считать, что кристаллические микропористые материалы, содержащие структуру с небольшим или средним размером пор, ведут себя как катализатор.
Выход в процентах С4 оксигенатных соединений, полученных способом согласно настоящему изобретению, равен или более чем 20%, равен или более чем 24%, равен или более чем 27%, равен или более чем 30%, равен или более чем 35%.
Содержание металла (атомов металлов) в кристаллическом микропористом материале, содержащем структуру с небольшим или средним размером пор, составляет от 0,1 до 15 мас. %, от 0,5 до 5,0 мас. %, от 0,5 до 1,5 мас. %.
Процесс можно осуществлять в растворителе, где растворитель можно выбирать из одного или более из группы, состоящей из воды, спирта или смеси воды и спирта (воды и спирта). Спирт можно выбирать из одного или более из группы, состоящей из метанола и этанола.
Процесс можно осуществлять при температуре от 25 до 150°С, от 50 до 120°С, и от 70 до 100°С.
С4 оксигенатные соединения, полученные посредством настоящего изобретения, можно преобразовать в С4-полиолы гидрированием. Подобные реакции гидрирования можно проводить в присутствии нанесенного на металл катализатора, где металлом является, например, металлы медь, никель, молибден, кобальт, железо, хром, цинк и платина. В предпочтительном варианте выполнения металлический катализатор выбирают из группы, состоящей из палладия и рутения, нанесенного на углерод или никель Ренея. Типичные условия реакции гидрирования раскрыты в US 6300494 В1 и US 4487980 В1. Примеры дополнительных подходящих металлических катализаторов и условия реакций для применения в реакциях гидрирования раскрыты в Ullmann's Encyclopaedia of Industrial Chemistry: Hydrogenation and Dehydrogenation.
C4 оксигенатные соединения, полученные способом согласно настоящему изобретению, можно преобразовать в метилвинилгликолят и 2-гидрокси-4-метоксибутановую кислоту или ее соли или ее сложные эфиры. Science (2010) 328, стр. 602-605 и Green Chemistry (2012) 14, стр. 702-706 раскрывают соответствующие процедуры синтезов. Кроме того, из С4 оксигенатных соединений можно получить α-гидрокси-γ-бутиролактон при таких же условиях или условиях, описанных в ACS Catal., 2013, 3 (8), стр. 1786-1800.
Соединение метилвинилгликолят может далее взаимодействовать с образованием аналогов α-гидроксиметинонина, пример этой трансформации раскрыт в WO 98/32735.
Аналоги α-гидроксиметинонина включают соединения, выбираемые из группы, состоящей из 2-гидрокси-4-(С1-5алкилтио)бутановой кислоты, ее солей и ее сложных эфиров.
С1-5алкилтио означает алкилтиол, выбираемый из группы, состоящей из метантиола, этантиола, пропантиола с прямой или разветвленной цепью, бутантиола с прямой или разветвленной цепью и пентантиола с прямой или разветвленной цепью.
Сложные С1-8 алкильные эфиры означают сложные эфиры, содержащие алкильную группу, выбираемую из группы, состоящей из метила, этила, пропила, бутила, изопропила, изобутила, пентила, гексила, гептила, октила и 2-этилгексила.
В одном варианте выполнения изобретения аналог α-гидроксиметинонина представляет собой 2-гидрокси-4-(метилтио)бутановую кислоту.
Во втором варианте выполнения изобретения аналог α-гидроксиметинонина выбирают из группы, состоящей из сложного метилового эфира 2-гидрокси-4-(метилтио)бутановой кислоты, сложного этилового эфира 2-гидрокси-4-(метилтио)бутановой кислоты, сложного пропилового эфира 2-гидрокси-4-(метилтио)бутановой кислоты, сложного бутилового эфира 2-гидрокси-4-(метилтио)бутановой кислоты, сложного изопропилового эфира 2-гидрокси-4-(метилтио)бутановой кислоты, сложного пентилового эфира 2-гидрокси-4-(метилтио)бутановой кислоты, сложного гексилового эфира 2-гидрокси-4-(метилтио)бутановой кислоты, сложного гептилового эфира 2-гидрокси-4-(метилтио)бутановой кислоты, сложного октилового эфира 2-гидрокси-4-(метилтио)бутановой кислоты и сложного 2-этилгексилового эфира 2-гидрокси-4-(метилтио)бутановой кислоты.
С4 оксигенатные соединения, полученные процессом согласно настоящему изобретению, можно преобразовать в бутандиолы, как описано в ChemSusChem (2012) 5,стр. 1991-1999.
Процесс получения С4 оксигенатных соединений из С1-3 оксигенатных соединений можно также осуществлять одновременно с реакцией гидрирования С4 оксигенатных соединений с образованием С4 полиолов. Следовательно, реакции можно проводить в одну стадию, т.е. 'однореакторная реакция. 'Одностадийная' или 'однореакторная' реакция означает, что кристаллический микропористый материал для конверсии гликолевого альдегида в С4 оксигенатные соединения и металлический катализатор для гидрирования С4 оксигенатных соединений присутствуют в реакционном сосуде одновременно. Реакция обрывается в случае присутствия гидрированного продукта (С4 полиолов).
С4 полиол означает С4 оксигенатные соединения, которые содержат соединения с длиной цепи в четыре атома углерода, и каждый атом углерода связан с спиртовой (ОН) функциональной группой. С4 полиолы могут быть также известны как сахарные спирты, содержащие четыре атома углерода, и имеют молекулярную формулу С4Н10О4. С4 полиолы представляют собой соединения, выбираемые из одного или более из группы, состоящей из эритрита и треита. Эритрит и треит включают все стереоизомеры, такие как D- и L-треит. Эритрит можно применять в качестве пищевых продуктов, подсластителя и для получения бутандиолов. ChemSusChem (2012) 5, стр. 1991-1999 иллюстрирует получение бутандиолов из эритрита.
Пример 1:
Получение кристаллического микропористого материала (Sn-MFI, Ti-MFI, Sn-BEA и Sn-LTA):
Sn-MFI:
200 Sn-MFI (Si/Sn=200) получают согласно способу, описанному Mal и др. (Mal, N.K.; Ramaswamy, V.; Rajamohanan, P.R.; Ramaswamy, A.V. Sn-MFI molecular sieves: Synthesis methods, 29Si liquid and solid MAS-NMR, 119Sn static and MAS NMR studies. Microporous Mater., 1997, 12, 331-340). Согласно этой процедуре NH4F (5,35 г) растворяют в деминерализованной воде (25,0 г). При быстром перемешивании добавляют раствор SnCl4.5H2O (0,25 г) в Н2О (10,0 г). После этого медленно добавляют бромид тетрапропиламмония [TPABr (9,8 г)] в Н2О (56,0 г). В смеси растворяют белую сажу (8,6 г). Смесь перемешивают в течение 3 часов, и затем гель перемещают в футерованный тефлоном автоклав и кристаллизуют при 200°С в течение 6 дней. Затем продукт фильтруют отсасыванием с помощью обильного количества воды и высушивают в течение ночи при 80°С. Извлеченный порошок прокаливают при 550°С (2°С/мин) в течение 6 часов. 400Sn-MFI (Si/Sn=400) получают, следуя такой же процедуре, но регулируя количество SnCl4.5H2O.
Sn-MFI (Альтернативное получение):
200 Sn-MFI (Si/Sn=200) можно получить из ZSM-5 (Zeochem, ZEOcat ® PZ-2 100Н). ZSM-5 обрабатывают в условиях пара при 450°С в течение 6 ч, промывают кислотой с помощью HCl 1 М при 100°С в течение 16 ч и промывают обильным количеством воды. Твердый осадок высушивают при 120°С в течение 16 ч. пропитывают водным раствором SnCl2 и прокаливают при 550°С (2°С/мин) в течение 6 ч.
Ti-MFI:
200 Ti-MFI (Si/Ti=200) получают согласно модификации способа, описанного Mal и др. (Mal, N.K.; Ramaswamy, V.; Rajamohanan, P.R.; Ramaswamy, A.V. Sn-MFI molecular sieves: Synthesis methods, 29Si liquid and solid MAS-NMR, 119Sn static and MAS NMR studies. Microporous Mater., 1997, 12, 331-340). Согласно этой процедуре в деминерализованной воде (25,0 г) растворяют NH4F (5,35 г). В условиях быстрого перемешивания добавляют раствор этоксида Ti (IV) (0,17 г) в Н2О (3,5 г) и Н2О2 (6,5 г). После этого медленно добавляют раствор бромида тетрапропиламмония [TPABr (9,8 г)] в Н2О (56,0 г). В смеси растворяют белую сажу (8,6 г). Смесь перемешивают в течение 20 часов, и затем гель перемещают в футерованный тефлоном автоклав и кристаллизуют при 200°С в течение 6 дней. Затем продукт фильтруют отсасыванием с помощью обильного количества воды и высушивают в течение ночи при 80°С. Извлеченный порошок прокаливают при 550°С (2°С/мин) в течение 6 часов.
Sn-BEA:
Sn-BEA получали согласно способу, описанному в ЕР 2184270 В1.
Sn-LTA:
125 Sn-LTA (Si/Sn=125) можно получить из цеолита LTA (Sigma-Aldrich, молекулярные сита, 4

Получение С4 оксигенатных соединений из гликолевого альдегида:
Пример 2:
Кристаллический микропористый материал (0,15 г), полученный согласно Примеру 1, димер гликолевого альдегида [SAFC, 0,25 г] и деионизированную воду (5 г) добавляют в склянку емкостью 20 мл (трубку высокого давления Асе) и нагревают при 80°С в условиях интенсивного перемешивания (600 об/мин). Образцы взаимодействия берут при выбранных временах (0,5-24 ч). Анализ жидких образцов после фильтрации осуществляют с применением HPLC Agilent 1200, оснащенного колонной BIORAD Amminex НРХ-87Н, при 65°С и 0,004 М раствора H2SO4 в воде при 0,6 мл мин-1.


Пример 3:
Композиции, содержащие С1-3 оксигенатные соединения, можно получить пиролизом биомассы или С5-6 сахаров (С5-6 оксигенатных соединений), таких как глюкоза, сахароза, фруктоза или ксилоза. Типичные реакции пиролиза представлены в US 7094932 В2 и РСТ/ЕР2014/053587. С1-3 оксигенатные соединения содержат 5 мас. % или более гликолевого альдегида, таком как между 5 мас. % и 65 мас. %.
Композицию, содержащую С1-3 оксигенатные соединения, полученные в результате пиролиза глюкозы согласно US 7094932 В2, разбавляют в воде с получением 5 г раствора, содержащего 8 мас. % гликолевого альдегида. В смесь добавляют кристаллический микропористый материал (0,15 г), полученный согласно Примеру 1, в склянке емкостью 20 мл (трубке высокого давления Асе), и реакцию нагревают при 80°С в условиях интенсивного перемешивания (600 об/мин). Образцы взаимодействия берут при выбранных временах (0,5-24 ч). Анализ жидких образцов после фильтрации осуществляют, как ранее объяснено.

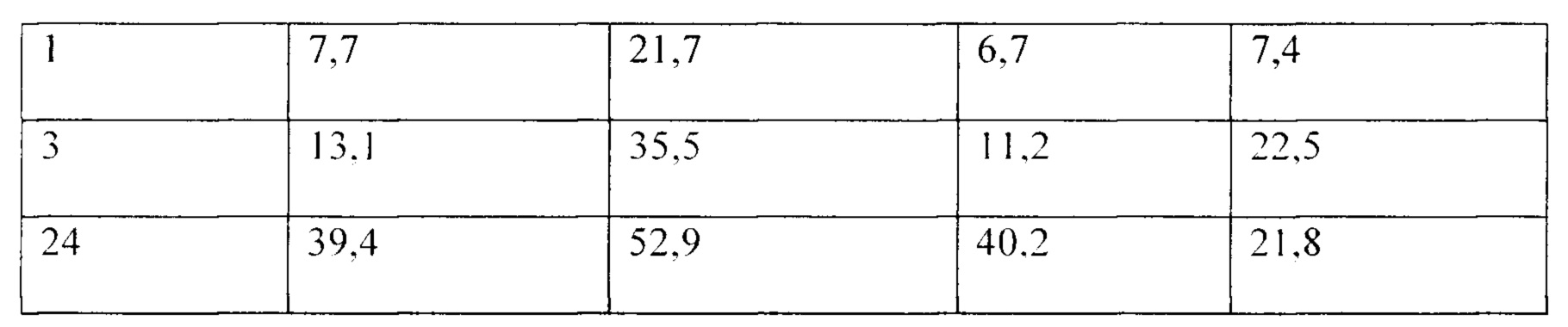
Пример 4:
Гидрирование С4 оксигенатных соединений осуществляют в автоклавном реакторе при давлениях Н2 30-90 бар. Реакцию осуществляют добавлением композиции, содержащей С4 оксигенатные соединения (15 г), полученные согласно Примеру 2 или 3, в автоклав Parr (50 мл) вместе с катализатором Ru/C (0,2 г; 5% на активированном угле от Aldrich). Реактор нагревают при 80°С и перемешивают со скоростью 500 об/мин в течение 3 ч.
Пример 5:
Сопутствующая конверсия гликолевого альдегида до С4 оксигенатных соединений и последующее гидрирование, ('однореакторная' или 'одностадийная' конверсия и гидрирование).
В автоклав Parr емкостью 50 мл добавляют димер гликолевого альдегида (SAFC, 0,25 г), Sn-MFI (0,1 г), полученный согласно Примеру 1, катализатор Ru/C (0,075 г; 5% на активированном угле от Aldrich) и воду (15 г). Первую реакцию конденсации осуществляют при 80°С в воздушной атмосфере. После 3 ч реакции в автоклаве повышают давление с помощью водорода при 90 бар и дают возможность взаимодействию протекать в течение 3 ч. После стадии конденсации и гидрирования получают образцы продуктов и анализируют после фильтрации в HPLC, как ранее объяснено.
Альтернативно винилгликолевую кислоту или метилвинилгликолят (MVG) можно получить взаимодействием композиции, содержащей С4 оксигенатные соединения, полученные согласно Примеру 1 или 2, с катализатором Sn-BEA в воде или метаноле соответственно Green Chemistry (2012) 14, стр. 702-706.
Фигура 1: Выход в процентах С4 оксигенатных соединений, полученных согласно Примеру 2, относительно времени. Показаны различные кристаллические микропористые материалы. Кристаллические микропористые материалы представляют собой:
Квадраты: 200Sn-MFI;
Круги: Ti-MFI;
Треугольники: Sn-BEA.
Фигура 2: Выход в процентах С4 оксигенатных соединений, полученных согласно Примеру 3, относительно времени. Показаны различные кристаллические микропористые материалы. Кристаллические микропористые материалы представляют собой:
Квадраты: 200Sn-MFI;
Круги: Ti-MFI;
Треугольники: Sn-BEA.
Реферат
Изобретение относится к способу получения одного или более Соксигенатных соединений, выбранных из треозы, эритрозы и эритрулозы, и может быть использовано в химической промышленности. В предложенном способе получают одно или более указанных Соксигенатных соединений из композиции, содержащей Cоксигенатные соединения, которые подвергают взаимодействию в присутствии растворителя и кристаллического микропористого материала, содержащего материал цеотипа, выбранного из группы, состоящей из структур СНА, LTA, MFI, MEL, МТТ, MWW, TON, HEU, AEL, AFO и FER, где кристаллический микропористый материал содержит металл, выбранный из одного или более из группы, состоящей из циркония, алюминия, олова или титана. Предложен новый эффективный способ получения ценных Соксигенатных соединений с улучшенной селективностью. 11 з.п. ф-лы, 5 пр., 2 табл., 2 ил.
Формула
Документы, цитированные в отчёте о поиске
Применение эритрита и d-тагатозы в диетических напитках и пищевых продуктах или в напитках и пищевых продуктах пониженной калорийности

Комментарии