Новые тиосоединения и способ их получения - RU2509762C2
Код документа: RU2509762C2
Чертежи




Описание
Область техники
Настоящее изобретение относится к тиосоединениям, полученным в результате проведения реакции между продуктом алкилирования, полученным из п-крезола и дициклопентадиена, с меркаптаном и параформальдегидом.
Уровень техники
В настоящее время для предотвращения окислительной деструкции полимеров используют антиоксиданты на фенольной, аминовой, фосфитной основе и на основе сложного тиоэфира. Данные антиоксиданты могут быть использованы индивидуально или в комбинации и им свойственны свои собственные ограничения. Как правило, несмотря на первоначальную демонстрацию антиоксидантами на фенольной основе хорошей термостойкости, их использование ограничено вследствие наличия для них тенденции к окрашиванию после окисления. Антиоксиданты на аминовой основе демонстрируют превосходные эксплуатационные характеристики, но у них имеется собственная окраска. А антиоксиданты на фосфитной основе не только подвержены гидролизу при контакте с водой, но также и разложению во время вулканизации для синтеза резины. Антиоксиданты на основе сложного тиоэфира не полностью проявляют свои эксплуатационные характеристики при их индивидуальном использовании и нуждаются в других первичных антиоксидантах.
Несмотря на демонстрацию 2,6-ди-трет-бутил-4-метилфенолом (БГТ), который обычно добавляют к полимерам, хорошей термостойкости в качестве первичного антиоксиданта, он является летучим вследствие своей низкой молекулярной массы. В результате эксплуатационные характеристики термостойких добавок ухудшаются и может иметь место серьезное изменение окраски. В частности, как известно, БГТ оказывает неблагоприятное воздействие на печень и может вызвать появление аллергий и новообразований.
Вследствие существования проблемы в виде загрязнения окружающей среды летучим БГТ в промышленности существует спрос на полимерные продукты, свободные от БГТ. В соответствии с этим существует настоятельная потребность в разработке антиоксиданта, не вредного для людей и менее летучего при одновременном наличии у него способности предотвращать окисление полимеров и сохранять их физические свойства.
Несмотря на использование в качестве заменителей БГТ продуктов 1076 (октадецил-3-(3,5-ди-трет-бутил-4-гидроксифенил)пропионат), 1010 (пентаэритритилтетракис[3-(3,5-ди-трет-бутил-4-гидроксифенил)пропионат]) и тому подобного, они требуют добавления вторичных антиоксидантов, поскольку они ограничены по эксплуатационным характеристикам в качестве первичных антиоксидантов и по физическим свойствам.
Краткое изложение изобретения
Техническая проблема
Изобретатели настоящего изобретения приложили усилия к разработке многофункционального фенольного антиоксиданта, демонстрирующего улучшенное антиоксидантное действие и способного заменить 2,6-ди-трет-бутил-4-метилфенол (БГТ). Как было установлено, в результате новое тиосоединение может оказаться подходящим для использования в качестве как первичных, так и вторичных антиоксидантов в результате добавления меркаптана к олигомерам, полученным из п-крезола и дициклопентадиена и использующимся для увеличения молекулярной массы в целях разрешения проблемы с летучестью.
В соответствии с этим настоящее изобретение относится к предложению новых тиосоединений и способа их получения.
Решение проблемы
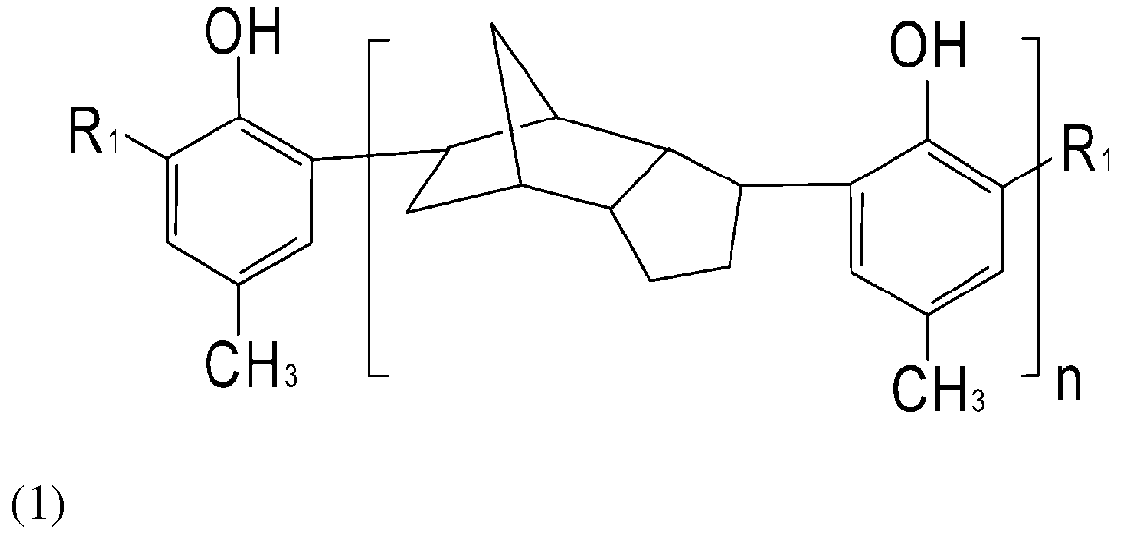
В одном аспекте настоящее изобретение относится к тиосоединению химической формулы 1:

где R1 представляет собой -CH2SR2, R2 представляет собой линейную, разветвленную или циклическую алкильную группу С5-С16 или ароматическую группу С6-С16; а n представляет собой вещественное число, удовлетворяющее выражению 1≤n≤20.
В еще одном аспекте настоящее изобретение относится к способу получения тиосоединения, включающему: проведение реакции между п-крезолом и дициклопентадиеном для получения продукта алкилирования химической формулы 2 и проведение реакции между продуктом алкилирования химической формулы 2, меркаптаном химической формулы R2SH и параформальдегидом для получения тиосоединения химической формулы 1:

где n представляет собой вещественное число, удовлетворяющее выражению 1≤n≤20; и
где R1 представляет собой -CH2SR2, где R2 представляет собой линейную, разветвленную или циклическую алкильную группу С5-С16 или ароматическую группу С6-С16; а n представляет собой вещественное число, удовлетворяющее выражению 1≤n≤20.
В еще одном аспекте настоящее изобретение относится к антиоксиданту, включающему данное тиосоединение в качестве эффективного ингредиента.
Выгодные эффекты от изобретения
В отличие от коммерчески доступных антиоксидантов, таких как 2,6-ди-трет-бутил-4-метилфенол (БГТ), являющихся вредными для организма человека вследствие высокой летучести, новые тиосоединения по настоящему изобретению, которые характеризуются низкой летучестью вследствие своей высокой молекулярной массы, не оказывают какого-либо вредного воздействия на организм человека. Кроме того, при наличии у них превосходных эксплуатационных характеристик они пригодны для замены существующих антиоксидантов.
Другие признаки и аспекты будут очевидны после ознакомления со следующими далее подробным описанием изобретения, чертежами и формулой изобретения.
Краткое описание чертежей
Представленные выше и другие цели, признаки и преимущества настоящего изобретения станут очевидными после ознакомления со следующим далее описанием предпочтительных вариантов осуществления, приведенным в сочетании с прилагаемыми чертежами, в числе которых:
Фиг.1 демонстрирует спектры масс-спектроскопии (МС) для измерения молекулярной массы (А: пример синтеза 1; В, С: пример 1);
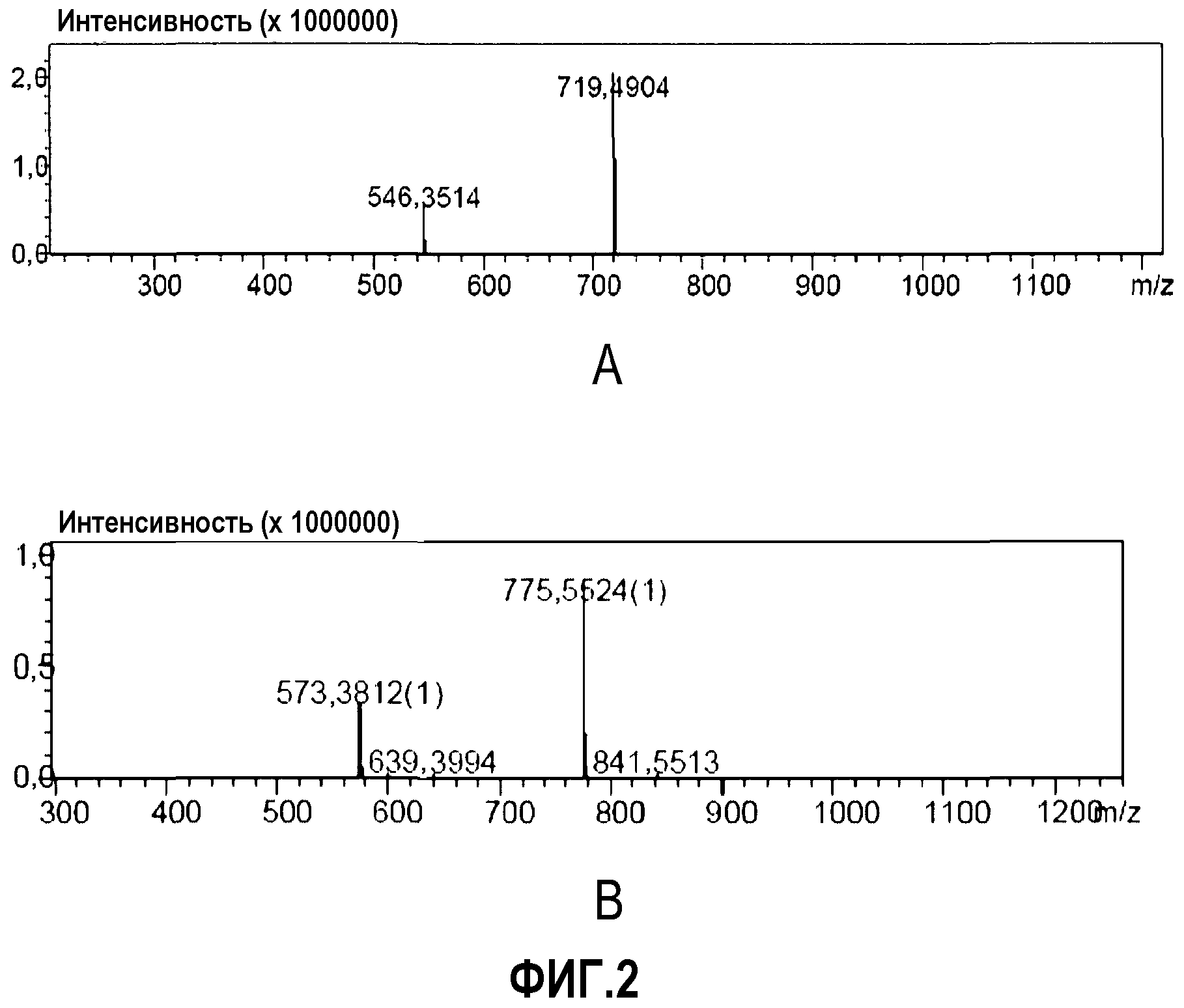
Фиг.2 демонстрирует спектры МС для измерения молекулярной массы (А: пример 3; В: пример 4);
Фиг.3 демонстрирует спектры гельпроникающей хроматографии (ГПХ) для измерения среднечисловой молекулярной массы у продуктов алкилирования, полученных в примере синтеза 1;
Фиг.4 демонстрирует спектры ГПХ для измерения среднечисловой молекулярной массы у октилтиосоединений, полученных в примере 1;
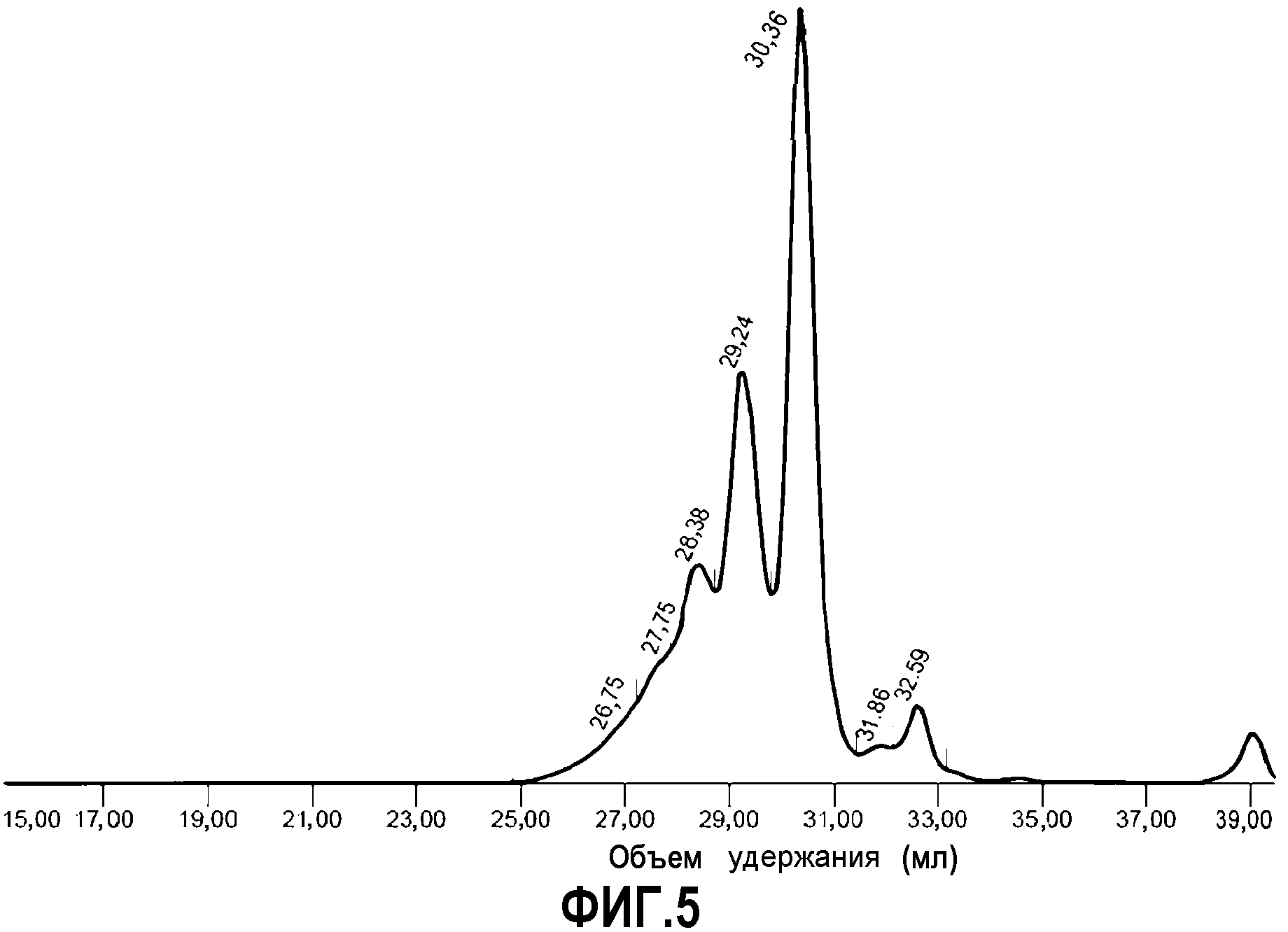
Фиг.5 демонстрирует спектры ГПХ для измерения среднечисловой молекулярной массы у деканилтиосоединений, полученных в примере 1; и
Фиг.6 демонстрирует спектры ГПХ для измерения среднечисловой молекулярной массы у додеканилтиосоединений, полученных в примере 1.
Осуществление изобретения
Преимущества, признаки и аспекты настоящего изобретения станут очевидными после ознакомления со следующим далее описанием вариантов осуществления при обращении к прилагаемым чертежам, что представлено ниже в настоящем документе. Однако настоящее изобретение может быть реализовано в различных формах и не должно восприниматься как ограниченное вариантами осуществления, представленными в настоящем документе. Вместо этого данные варианты осуществления представлены для обеспечения доскональности и полноты данного описания изобретения и будут полностью передавать специалистам в соответствующей области техники объем настоящего изобретения. Терминология, использующаяся в настоящем документе, имеет целью только описание конкретных вариантов осуществления и не подразумевает ограничения примеров вариантов осуществления. В соответствии с использованием в настоящем документе формы единственного числа «один», «некий» и «данный» предполагают также и включение форм множественного числа, если только контекст не будет ясно указывать на другое. Кроме того, необходимо понимать, что термины «включает» и/или «включающий» в случае использования в данном описании изобретения будут указывать на присутствие указанных признаков, целых чисел, стадий, операций, элементов и/или компонентов, но не исключают и присутствия или добавления одного или нескольких других признаков, целых чисел, стадий, операций, элементов, компонентов и/или их групп.
Ниже в настоящем документе настоящее изобретение будет описываться более подробно.
Настоящее изобретение относится к тиосоединению химической формулы 1:
(Химическая формула 1)
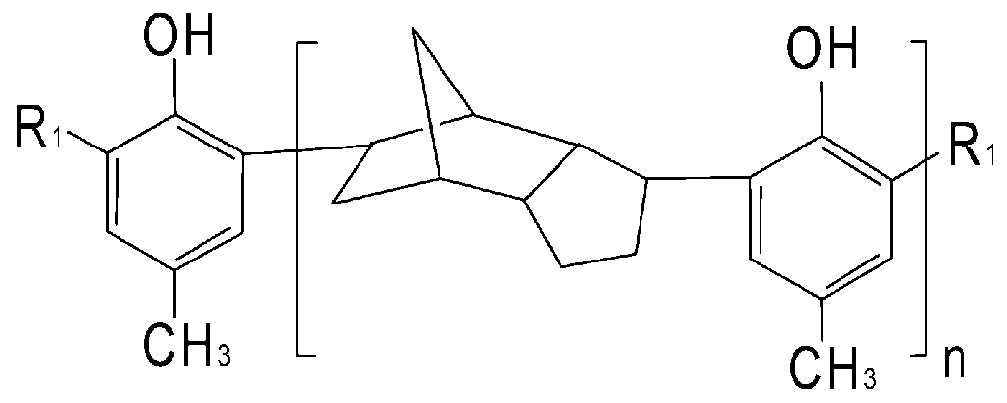
где R1 представляет собой -CH2SR2, R2 представляет собой линейную, разветвленную или циклическую алкильную группу С5-С16 или ароматическую группу С6-С16; а n представляет собой вещественное число, удовлетворяющее выражению 1≤n≤20. Предпочтительно R2 представляет собой линейную, разветвленную или циклическую алкильную группу С6-С16, более предпочтительно - линейную или разветвленную алкильную группу С8-С12. И предпочтительно n представляет собой вещественное число, удовлетворяющее выражению 1≤n≤12, более предпочтительно - вещественное число, удовлетворяющее выражению 1≤n≤6.
Предпочтительно тиосоединение по настоящему изобретению имеет среднечисловую молекулярную массу (Mn) в диапазоне от 400 до 5000, более предпочтительно от 400 до 3000. В случае среднечисловой молекулярной массы тиосоединения по настоящему изобретению, меньшей чем 400, соединение может оказаться летучим. Между тем, в случае превышения среднечисловой молекулярной массой 5000 желательного тиосоединения не может быть получено. Поэтому предпочтительно выдерживать описанный выше диапазон средней молекулярной массы.
Тиосоединение по настоящему изобретению получают в две стадии: первая стадия представляет собой проведение реакции между п-крезолом и дициклопентадиеном для получения продукта алкилирования химической формулы 2; а вторая стадия представляет собой реакцию между продуктом алкилирования химической формулы 2, меркаптаном химической формулы R2SH и параформальдегидом для получения тиосоединения химической формулы 1:

где n представляет собой вещественное число, удовлетворяющее выражению 1≤n≤20; и

где R1 представляет собой -CH2SR2, R2 представляет собой линейную, разветвленную или циклическую алкильную группу С5-С16 или ароматическую группу С6-С16; а n представляет собой вещественное число, удовлетворяющее выражению 1≤n≤20.
На первой стадии получения продукта алкилирования п-крезол вводят в реакцию с дициклопентадиеном по механизму алкилирования Фриделя-Крафтса для получения продукта алкилирования химической формулы 2. Предпочтительно п-крезол используют с эквивалентом в диапазоне от 1 до 10, более предпочтительно с эквивалентом в диапазоне от 2 до 5, в расчете на 1 эквивалент дициклопентадиена. Вне вышеупомянутого диапазона эксплуатационные характеристики могут оказаться плохими. Поэтому предпочитается выдерживать вышеупомянутый диапазон.
Реакцию первой стадии проводят в присутствии кислотного катализатора. Предпочтительно кислотный катализатор представляет собой один или несколько галогенидов (галогенид) металлов, выбранных из AlCl3, AlBr3, AlI3, TiCl4, SnCl4, FeCl3, ZnCl2 и ZrCl4; одну или несколько неорганических кислот (кислоту), выбранных из H2SO4, H3PO4 и HF; и катализатора на основе кислоты Льюиса, такого как BF3. Предпочтительно кислотный катализатор используют в количестве в диапазоне от 0,1 до 5% (масс.) в расчете на совокупную массу п-крезола и дициклопентадиена. В случае использования кислотного катализатора в количестве, меньшем чем 0,1% (масс.), потребуется чрезмерно продолжительное время реакции. Между тем, в случае использования его в количестве, большем чем 5% (масс.), может быть получено множество побочных продуктов. Поэтому предпочтительно выдерживать вышеупомянутый диапазон.
Предпочтительно реакцию первой стадии проводят при температуре в диапазоне от 25 до 160°С в течение периода времени продолжительностью от 1 до 10 часов, более предпочтительно при температуре в диапазоне от 80 до 150°С в течение периода времени продолжительностью от 2 до 8 часов. В случае проведения реакции при температуре, меньшей чем 25°С, реакция не может быть проведена плавно, что приводит к неполноте прохождения реакции. Между тем, в случае проведения реакции при температуре, большей чем 160°С, реакция может протекать хорошо, но приведет к получению множества побочных продуктов, что таким образом уменьшает экономическую эффективность. Кроме того, в случае проведения реакции в течение менее 1 часа реакция может пройти неполностью. Между тем, в случае проведения реакции в течение более 10 часов может быть ухудшена экономическая эффективность.
Первая стадия может дополнительно включать процесс концентрирования продуктов алкилирования при температуре в диапазоне от 100 до 200°С при давлении в диапазоне от 1 до 50 мм ртутного столба.
На второй стадии получения тиосоединений меркаптан химической формулы R2SH может быть использован с эквивалентом в диапазоне от 2 до 4, предпочтительно с эквивалентом в диапазоне от 2 до 3 в расчете на 1 эквивалент продукта алкилирования. В дополнение к этому, параформальдегид может быть использован с эквивалентом в диапазоне от 2 до 4, предпочтительно с эквивалентом в диапазоне от 2 до 3 в расчете на 1 эквивалент продукта алкилирования. В случае добавляемого количества меркаптана и параформальдегида, меньшего чем 2 эквивалента, соответственно, может быть получена смесь из монотиосоединения и дитиосоединения. А в случае превышения им 4 эквивалентов будет получено множество побочных продуктов и после этого для очистки может потребоваться сложный технологический процесс. R2 меркаптана может представлять собой линейную, разветвленную, циклическую или ароматическую алкильную группу С6-С16, предпочтительно линейную или разветвленную алкильную группу С6-С16, более предпочтительно ту, которая содержит от 8 до 12 атомов углерода. В случае содержания в R2 менее 6 атомов углерода меркаптан R2SH, отделившийся от тиосоединений в результате разложения, легко может вызвать появление интенсивного запаха. Между тем, в случае содержания в нем более 16 атомов углерода может ухудшиться реакционная способность продуктов алкилирования. Конкретные примеры меркаптана включают октилмеркаптан, децилмеркаптан, додецилмеркаптан, бензилмеркаптан, тиофенол и тому подобное.
Реакцию второй стадии проводят в присутствии основного катализатора или смеси катализаторов из основного катализатора и кислотного катализатора. На основный катализатор каких-либо конкретных ограничений не накладывают, но предпочтительным является катализатор на основе амина. Как правило, могут быть использованы один или несколько основных катализаторов, выбранных из пиперидина, пирролидина, пиперазина, диметиламина, диэтиламина и бензилметиламина. Основный катализатор может быть использован с эквивалентом в диапазоне от 0,1 до 0,6, предпочтительно с эквивалентом в диапазоне от 0,2 до 0,5 в расчете на 1 эквивалент продуктов алкилирования. В случае использования основного катализатора в количестве, меньшем чем 0,1 эквивалента, может увеличиться время реакции. Между тем, в случае использования его в количестве, большем чем 0,6 эквивалента, время реакции уменьшится, но будет получено множество побочных продуктов. Поэтому предпочтительно выдерживать вышеупомянутый диапазон.
В случае смеси катализаторов из основания и кислоты кислотным катализатором могут быть один или несколько кислотных катализаторов, выбранных из органической и неорганической кислоты. Как правило, органической кислотой может быть алифатическая или ароматическая органическая кислота, имеющая одну или несколько функциональных групп (группу), выбранных из карбоксилата, сульфата и фосфата; или алифатическая органическая кислота или ароматическая органическая кислота, имеющие одну или несколько функциональных групп (группу), выбранных из групп алкила, алкенила, арила, гидроксила, тиола, простого эфира, сложного эфира, кетона и альдегида, и в то же самое время одну или несколько функциональных групп (группу), выбранных из карбоксилата, сульфата и фосфата. Кроме того, неорганическая кислота может быть одной или несколькими гетерогенными кислотами, выбранными из серной кислоты, фосфорной кислоты и двух и более оксикислот. В качестве сложных неорганических кислот могут быть использованы гетерогенные кислоты, которые наносят на глину, катионообменную смолу и тому подобное. В смеси катализаторов кислотный катализатор может быть использован с эквивалентом в диапазоне от 0,1 до 0,9, предпочтительно с эквивалентом в диапазоне от 0,4 до 0,8 в расчете на 1 эквивалент основного катализатора. В случае использования его в количестве, меньшем чем 0,1 эквивалента, действие кислоты больше уже может и не проявиться. Между тем, в случае использования его в количестве, большем чем 0,9 эквивалента, это может ухудшить действие основного катализатора. Поэтому предпочтительно выдерживать вышеупомянутый диапазон.
На второй стадии к растворителю реакции добавляют продукты алкилирования химической формулы 2, меркаптан химической формулы R2SH, параформальдегид и основный катализатор или смесь катализаторов и проводят реакцию. Реакцию проводят в растворителе реакции, который может представлять собой толуол или смесь из воды и толуола с соотношением между количествами компонентов смеси 1:10-100, предпочтительно 1:30-70, в расчете на массу. Растворитель реакции может быть использован в количестве в диапазоне от 50 до 200 массовых частей, более предпочтительно от 80 до 150 массовых частей, в расчете на 100 частей совокупной массы реагентов, включающих продукт алкилирования химической формулы 2, меркаптан химической формулы R2SH, параформальдегид и основный катализатор или смесь катализаторов. В случае использования растворителя реакции в количестве, меньшем чем 50 массовых частей, перемешивание может оказаться затруднительным. Между тем, в случае использования его в количестве, большем чем 200 массовых частей, может иметь место неполное прохождение реакции или может уменьшиться скорость реакции. Поэтому предпочтительно выдерживать вышеупомянутый диапазон.
На второй стадии реакция может быть проведена при температуре в диапазоне от 50 до 150°С в течение периода времени продолжительностью от 1 до 6 часов, более предпочтительно при температуре в диапазоне от 90 до 120°С в течение периода времени продолжительностью от 2 до 4 часов. В случае проведения реакции при температуре, меньшей чем 50°С, может иметь место неполное прохождение реакции. Между тем, в случае повышения температуры до значения выше 150°С реакция может протекать хорошо и изменения окраски не возникнет, но способ может оказаться неэффективным по затратам. Кроме того, в случае проведения реакции в течение менее 1 часа может иметь место неполное прохождение реакции. Между тем, в случае проведения реакции в течение более 6 часов может ухудшиться экономическая эффективность, хотя изменение окраски и будет предотвращено.
ПРИМЕРЫ
Далее будут описываться примеры и эксперименты. Следующие далее примеры и эксперименты представлены только в иллюстративных целях и не предназначены для ограничения объема данного описания изобретения.
Пример синтеза 1
Получение продукта алкилирования
п-Крезол (324 г) и раствор BF3-эфир (эфират трехфтористого бора, 5,5 г) перемешивали и нагревали до 90°С. После медленного добавления дициклопентадиена (132 г) в течение 1 часа с последующим проведением реакции в течение 3 часов получающийся в результате реакционный раствор концентрировали при 190°С при давлении 15 мм ртутного столба для получения продуктов алкилирования (300 г).
Пример 1
Получение октилтиосоединений химической формулы 1-1
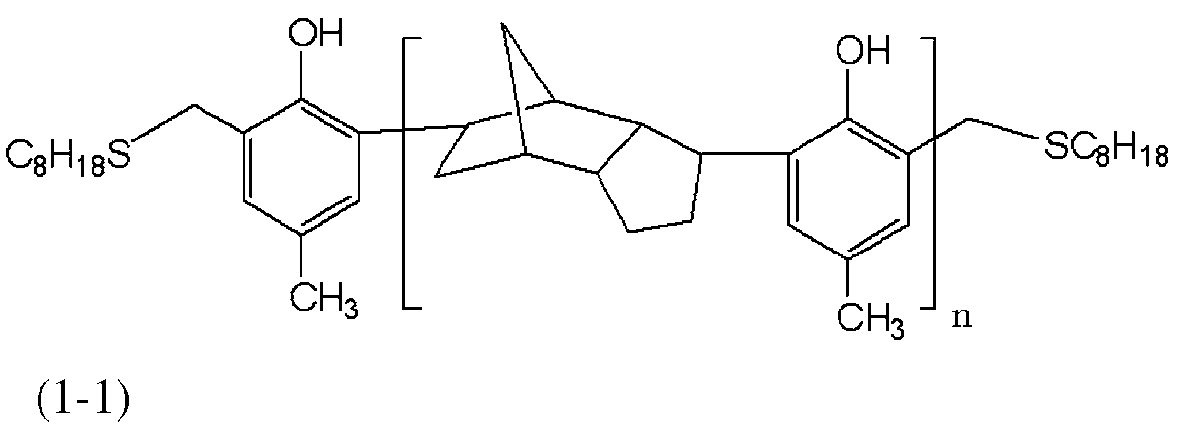
Продукты алкилирования (1 эквивалент), полученные в примере синтеза 1, растворяли в толуоле в том же самом количестве. Затем после добавления параформальдегида (2 эквивалента), октилмеркаптана (2 эквивалента) и диметиламина (0,2 эквивалента) реакцию проводили при 100°С в течение 3 часов. Органический слой, отделенный от продукта реакции, концентрировали при пониженном давлении для получения октилтиосоединений в виде светло-коричневой жидкости. Степень превращения и степень чистоты измеряли по методу ВЭЖХ. Результат представлен в таблице 1.
Пример 2
Октилтиосоединения получали тем же самым образом, что и в примере 1, за исключением использования смеси катализаторов из диэтиламина и уксусной кислоты вместо основного катализатора диметиламина. Результат также представлен в таблице 1.
Пример 3
Получение децилтиосоединения химической формулы 3-1

Децилтиосоединения получали тем же самым образом, что и в примере 1, за исключением использования децилмеркаптана вместо октилмеркаптана и использования смеси катализаторов из пиперидина и фосфорной кислоты вместо основного катализатора диметиламина. Результат также представлен в таблице 1.
Пример 4
Получение додецилтиосоединения химической формулы 4-1

Додецилтиосоединения получали тем же самым образом, что и в примере 1, за исключением использования додецилмеркаптана вместо октилмеркаптана и использования смеси катализаторов из пиперидина и пропановой кислоты вместо основного катализатора диметиламина. Результат также представлен в таблице 1.
Пример испытания 1
Анализ
Тиосоединения, полученные в примере синтеза 1, примере 1, примере 3 и примере 4, анализировали следующим далее образом.
1) Элементный анализ
Для проведения элементного анализа на углерод, водород, кислород и серу использовали анализатор Flash EA 1112 Series CHNS-O (Thermo Electron Co.). Газообразная среда, использованная для проведения элементного анализа, представляла собой воздух, газообразный водород (99,999%), газообразный гелий (99,9999%) и высокочистый газообразный кислород (Flex Air). Левую камеру сгорания выставляли на 900°С, а правую камеру сгорания выставляли на 680°С. Температуру печи устанавливали равной 50°С. Скорость течения газа устанавливали равной 130 мл/мин для газообразного носителя (Не), 250 мл/мин для газообразного кислорода и 100 мл/мин для газа сравнения (Не). ББОТ (2,5-бис(5-трет-бутилбензоксазол-2-ил)тиофен) использовали в качестве стандартного образца для получения количественных характеристик. Результат представлен в таблице 2.
2) Измерение молекулярной массы
Для измерения молекулярной массы соединений использовали прибор LCMS-IT-TOF (Shimadzu Co.). Использующийся газ для соударений представлял собой газообразный аргон, а в качестве газа-распылителя использовали газообразный азот (99,5% и более). Использовали колонку для жидкостной хроматографии Shiseido Capcell Pak C18 UG120 (2,0 мм, внутренний диаметр × 250 мм). В качестве подвижной фазы перепускали 100%-ный ацетонитрил при скорости течения 0,2 мл/мин. В качестве режима ионизации выбрали химическую ионизацию при атмосферном давлении, а скорость течения газа-распылителя устанавливали равной 2,0 л/мин. Температуру для зонда химической ионизации при атмосферном давлении устанавливали равной 400°С, а для искривленной линии десольватации - равной 200°С. Результат анализа получали при использовании программы решения для ЖХ/МС. Молекулярную формулу идентифицировали при использовании устройства прогноза формулы. Результат представлен в таблице 3, а спектры МС продемонстрированы на фиг.1.
Анализ пиков жидкостной хроматографии (ЖХ) выявил равенство значения n 1 или 2 в примере 1. Однако значение n составляло только 1 для примера синтеза 1 и примеров 3 и 4. Для разрешения данной проблемы среднечисловую молекулярную массу (Mn) и уровень содержания тиосоединений, состоящих из нескольких олигомеров, анализировали по методу гельпроникающей хроматографии (ГПХ).
3) Измерение среднечисловой молекулярной массы (Mn) по методу ГПХ
Для метода ГПХ использовали детектор TDA302 (Viscotek Co.) и насос LC-20AD (Shimadzu Co.). Использовали две колонки OligoPore (30 см, размер пор 5 мкм, Polymer Laboratories Co.) и колонки G2500HHR и G2000HHR (Tosoh Co.). Выбрали детектор показателя преломления (ПП). В качестве растворителя использовали тетрагидрофуран (ТГФ). Скорость течения составляла 1 мл/мин. Среднечисловую молекулярную массу (Mn) вычисляли при использовании полистирола в качестве стандартного образца. Результат представлен в таблице 4, а спектры ГПХ продемонстрированы на фиг.3-6.
Пики от 1 до 5 являются пиками тиосоединений, включающих п-крезол и дициклопентадиен с молярным соотношением 2:1, в то время как пик 6 является пиком тиосоединений, которые включают п-крезол и дициклопентадиен с молярным соотношением 1:1, или тиосоединений, которые включают только п-крезол.
Пример получения 1
Получение синтетического каучука
Для получения синтетического каучука к 100 г бутадиенового каучука (Kumho KBR 01, вязкость по Муни для сырого каучука = 45, уровень содержания цис-звеньев ≥94%), полученного в соответствии с обычным способом, добавляли 0,2 г октилтиосоединений, полученных в примере 1.
Сравнительный пример получения 1
Для получения синтетического каучука к 100 г бутадиенового каучука (Kumho KBR 01, вязкость по Муни для сырого каучука = 45, уровень содержания цис-звеньев ≥94%), полученного в соответствии с обычным способом, добавляли 0,4 г 2,6-ди-трет-бутил-4-метилфенола (БГТ) - существующего антиоксиданта.
Пример испытания 2
Из растворов синтетического каучука, полученных в примере получения 1 и сравнительном примере получения 1, под действием водяного пара отгоняли низкокипящие соединения для получения каучуковой крошки, которую после этого высушивали на вальцах при 110°С для получения высушенных синтетических каучуков. Высушенные синтетические каучуки подвергали термическому старению при 130ºС в течение 60 минут, а после этого проводили измерение вязкости по Муни при 100°С с использованием прибора Mooney MV 2000 (Alpha Technology). Результат представлен в таблице 5. В таблице 5 выражение «ML1+4, 100°C» обозначает измерение вязкости по Муни при 100°С в течение 4 часов после предварительного нагревания в течение 1 минуты.
Как продемонстрировано в таблице 5, пример получения 1 продемонстрировал меньшее изменение вязкости по Муни (ВМ), несмотря на использование антиоксиданта в половинном количестве в сопоставлении с тем, что имеет место в сравнительном примере получения 1. Поэтому она демонстрирует наличие у тиосоединений по настоящему изобретению в 2 раза и более лучшего действия антиоксиданта в сопоставлении с тем, что имеет место для БГТ, который представляет собой коммерчески доступный антиоксидант.
Применимость в промышленности
Как это описывалось выше, тиосоединения по настоящему изобретению представляют собой подходящие для использования антиоксиданты универсального действия, исполняющие функцию как первичного, так и вторичного антиоксидантов, при одновременном решении проблемы с летучестью благодаря увеличению молекулярной массы. Поэтому они могут быть использованы в качестве антиоксиданта для каучуков и смол.
Несмотря на описание настоящего изобретения при обращении к конкретным вариантам осуществления, специалистам в соответствующей области техники должна быть очевидна возможность внесения различных изменений и модификаций без отклонения от сущности и объема изобретения, определенного в следующей далее формуле изобретения.
Реферат
Изобретение относится к новым тиосоединениям, которые могут быть использованы как антиоксиданты для каучуков, и способу их получения. Новое тиосоединение получают в результате осуществления реакции между продуктом алкилирования, полученным из п-крезола и дициклопентадиена, с меркаптаном и параформальдегидом. В отличие от существующих антиоксидантов, таких как 2,6-ди-трет-бутил-4-метилфенол (БГТ), являющихся вредными для организма человека вследствие высокой летучести, новые тиосоединения по настоящему изобретению характеризуются низкой летучестью и не оказывают какого-либо вредного воздействия на организм человека. 3 н. и 12 з.п. ф-лы, 6 ил., 5 табл., 2 пр.
Формула
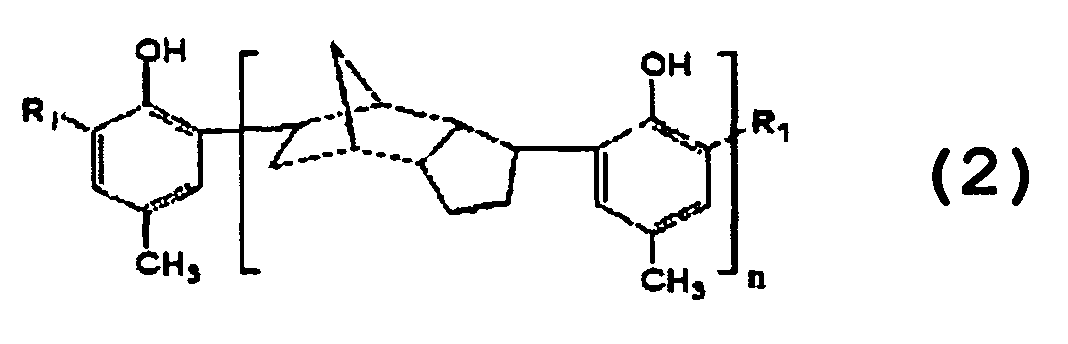
где R1 представляет собой -CH2SR2, где R2 представляет собой линейную или разветвленную алкильную группу C5-C16; a n представляет собой вещественное число, удовлетворяющее выражению 1≤n≤20.
осуществление реакции между п-крезолом и дициклопентадиеном для получения продукта алкилирования химической формулы 1
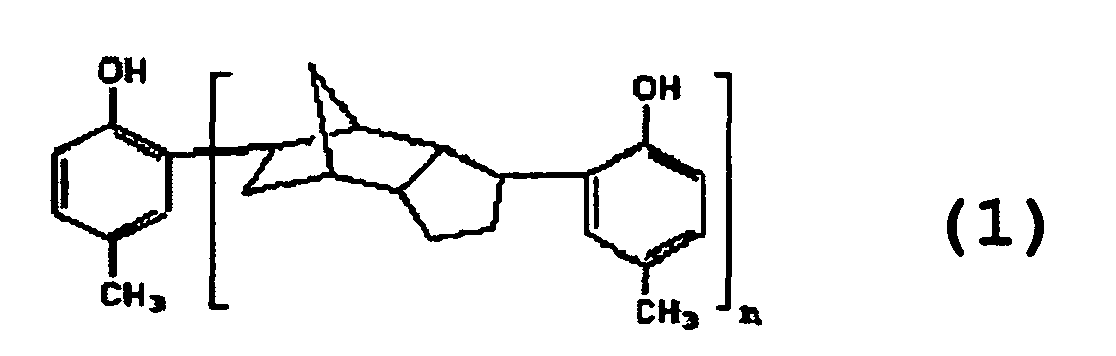
и осуществление реакции между продуктом алкилирования химической формулы 1, меркаптаном химической формулы R2SH и параформальдегидом для получения тиосоединения химической формулы 2:
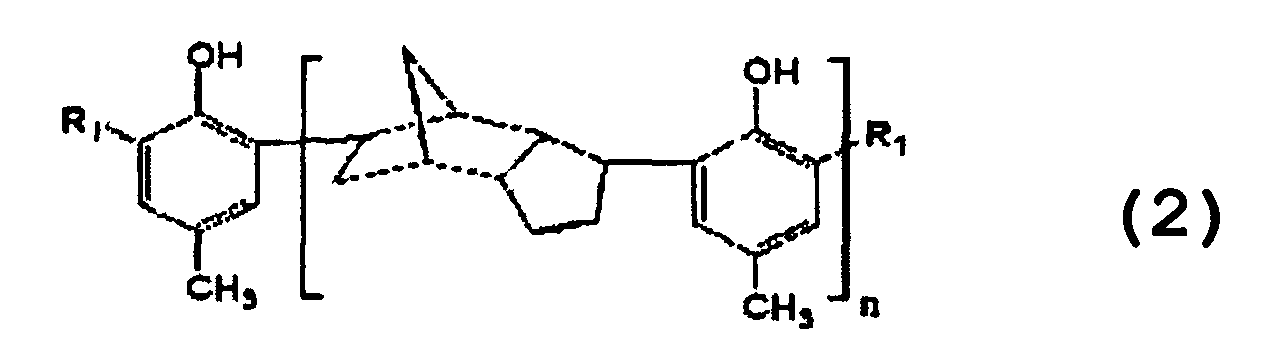
где n представляет собой вещественное число, удовлетворяющее выражению 1≤n≤20; и
где R1 представляет собой -CH2SR2, где R2 представляет собой линейную или разветвленную алкильную группу C5-C16; a n представляет собой вещественное число, удовлетворяющее выражению 1≤n≤20.
одного или нескольких галогенидов (галогенида) металлов, выбранных из AlCl3, AlBr3, AlI3, TiCl4, SnCl4, FeCl3, ZnCl2 и ZrCl4;
одной или нескольких неорганических кислот (кислоты), выбранных из H2SO4, H3PO4 и HF; И BF3.
алифатическую органическую кислоту или ароматическую органическую кислоту, имеющие одну или несколько функциональных групп (группу), выбранных из карбоксилата, сульфата и фосфата; или
алифатическую органическую кислоту или ароматическую органическую кислоту, имеющие в структуре одного соединения одну или несколько функциональных групп (группу), выбранных из групп алкила, алкенила, арила, гидроксила, тиола, простого эфира, сложного эфира, амида, кетона и альдегида, и одну или несколько функциональных групп (группу), выбранных из карбоксилата, сульфата и фосфата.

Комментарии