Производные сульфонамида - RU2059615C1
Код документа: RU2059615C1
Чертежи



Описание
Изобретение относится к новым производным сульфонамида, способу их получения и лекарственным композициям, содержащим указанные соединения в качестве активного ингредиента.
Используемые в настоящее время для лечения рака химиотерапевтические средства представляют собой вещества различной природы, например, алкилирующие агенты, такие, как циклофосфамиды; антиметаболиты, такие, как метотрексат и фтороурацил; антибиотики, такие, как адримицин, митомицин и блеомицин; вещества растительного происхождения, такие, как винкристин, и этопсид, и металлические комплексы, такие, как цисплатин.
Производные 4-аминобензолсульфонамида (патент Японии N 3093/1968), производные 2-сульфаниламид/хиноксалина (патент Японии N 426/1987), и производные m= AMSA [см. I. Med. Chem 18, 1110 (1975)] известны как активные противоопухолевые соединения, имеющие сульфонамидную группу.
Большинство из указанных соединений обладают низкой эффективностью при лечении опухолей человека, особенно, твердых опухолей с медленным ростом, таких, как рак легких, или рак прямой кишки, и кроме того, они вызывают серьезные побочные реакции. В связи с вышеуказанным, разработка новых лекарственных средств, обладающих низкой токсичностью и хорошей противоопухолевой активностью, остается актуальной до настоящего времени.
Целью настоящего изобретения является получение новых производных сульфонамида, обладающих прекрасной противоопухолевой активностью и при этом низкой токсичностью. Другой целью настоящего изобретения является разработка способа получения указанных соединений, а также изготовления лекарственных препаратов, содержащих указанные соединения в качестве активного ингредиента.
В процессе интенсивных исследований, проводимых авторами настоящего изобретения в целях получения противоопухолевых соединений, обладающих низкой токсичностью, было обнаружено, что описанные ниже сульфонамидные производные обладают прекрасной противоопухолевой активностью и при этом низкой токсичностью. И на основе этого открытия было разработано настоящее изобретение.
Таким образом, настоящее изобретение относится к сульфонамидным производным общей формулы (I) или их фармакологически приемлемым солям.


(I) где R1 низший алкил, низший алкокси, амино-;
R2 водород, низший алкил;
R3 и R4 различные и каждый представляет собой атом галогена, низший алкокси- или оба являются водородами;
A означаетN- илиCH-;
B представляет собой группу формулы N- или

E представляет собой группу формулы
-

E представляет собой пиридил, пиримидинил или фенил, который может быть замещен низшим алкилокси, гидроксилом, низшим алкилом, галогеном, (низший) алкилокси (низшей) алкилокси группой, фенилкарбонилокси, фосфорилокси, глюкопирано- зилокси, низшим алкилоксикарбонилом, диметиламинокарбонилокси, аминоацетилокси, аминобензоилокси, фенокси; или их фармокологически приемлемые соли; за исключением случаев когда:
1. R1 является низший алкил, амино;
R2 водород; А и В группаCН-;
E фенил, который может быть замещен гидроксилом, галогеном, низшей алкилокси, низшим алкилом, фенилкарбонилокси, низшим алкилоксикарбонилом, диметиламинокарбонилокси, аминобензоилокси;
2. R2 низший алкил, А и В каждыйCH-;
E группа формулы
-

E представляет фенил, который может быть замещен низшим алкилокси, гидроксилом, низшим алкилом, галогеном, фенилкарбонилокси, низшим алкилоксикарбонилом, диметиламинокарбонилом, аминобензоилокси группой, или их фармакологически приемлемые соли.
Низшие алкильные группы, представленные R1, R2, R5 и R6 и заместителем Е [cм. формулу (I)] являются прямыми или разветвленными алкильными группами, имеющими 1-6 атомов углерода, например, такими, как метил, этил н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, н-пентил (амил), изопентил, неопентил, трет-пентил, 1-метилбутил, 2-метилбутил, 1,2-диметилпропил, н-гексил, изогексил, 1-метилпентил, 2-метилпентил, 3-метилпентил, 1,1-диметилбутил, 1,2-диметилбутил, 2,2-диметилбутил, 1,3-диметилбутил, 2,3-диметилбутил, 3,3-диметилбутил, 1-этилбутил, 2-этилбутил, 1,1,2-триметилпропил, 1,2,2-триметилпропил, 1-этил-1-метилпропил и 1-этил-2-метилпропил. Среди них предпочтительными являются метил, этил, пропил и изопропил, и наиболее предпочтительными являются метильная и этильная группы.
Низшие алкокси-группы, представленные R1, R3 и R6 являются группами, происходящими от описанных выше алкильных групп, такими, как метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси и т-бутокси- группы. Среди них наиболее предпочтительными являются метокси и этокси-группы.
Атомами галогена являются атомы фтора, хлора и брома.
Сульфонамидные производные, представленные вышеуказанной формулой (I), могут образовывать соль с кислотой или основанием. Соли соединений (I) также входят в объем настоящего изобретения. Примерами таких солей с неорганическими кислотами являются гидрохлорид, гидробромид и сульфат, а с органическими кислотами ацетат, лактат, сукцинат, фумарат, малеат, цитрат, бензоат, метансульфонат и n-толуолсульфонат. Примерами основных солей являются неорганические соли, такие, как соли натрия, калия и кальция; и органические соли, такие, как триэтиламин, аргинин и лизин.
Само собой разумеется, что гидраты указанных соединений и их оптические изомеры, если они существуют, также входят в объем настоящего изобретения. Соединения настоящего изобретения обладают сильной противоопухолевой активностью. Соединения настоящего изобретения, которые обладают противоопухолевой активностью в процессе метаболизма, например, после их окисления, гидролиза или конъюгации in vivo, также входят в объем настоящего изобретения.
Соединения
настоящего изобретения формулы (I) могут быть получены различными
способами. Из них наиболее типичными являются следующие способы:
(1) Сульфоновую кислоту общей формулы (II) или ее реактивное
производное
R

(II) где R является атомом водорода, атомом галогена, или низшим алкилом, низшим алкокси защищенным гидроксилом, нитро, фенокси, циано, ацетилом или защищенной амино-группой, подвергают реакции взаимодействия с соединением общей формулы III
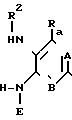

(III) где R2, A, B и E определены выше, а R
Реакционноспособные производные сульфоновых кислот (II) представляют собой известные, часто используемые соединения, такие, как сульфонилгалид, сульфонилангидрид и N-сульфонилимидазолид. Из них наиболее предпочтительным является сульфонилгалид. Указанную реакцию осуществляют с использованием стехиометрически эквимолярных количеств. И хотя в этой реакции могут быть использованы практически любые растворители, однако, желательно, чтобы исходные материалы были растворимыми в этих растворителях и чтобы эти растворители не вступали легко в реакцию с исходными материалами. Такими растворителями, например, могут быть пиридин, тетрагидрофуран, диоксан, бензол, простой эфир, метиленхлорид, диметилформамид и смеси двух или нескольких из указанных растворителей. Если в процессе реакции высвобождается кислота, как в случае использования сульфонилгалида, то реакцию желательно проводить в присутствии соответствующего связывающего кислоту агента. Поэтому, использование основного растворителя, такого, как пиридин, особенно предпочтительно. Если используется нейтральный растворитель, то может быть добавлено основание, например, такое, как карбонат щелочного металла или органический третичный амин. Само собой разумеется, что растворители, которые могут быть использованы в описываемой реакции, не ограничиваются указанными выше примерами. Реакция, как правило, протекает при комнатной температуре, но по желанию, может быть осуществлена при охлаждении или нагревании. Реакционное время обычно варьируется от 10 мин до 20 ч, и зависит от используемых исходных материалов и реакционной температуры.
Если в полученном сульфонамидном производном (I) аминогидроксильная или карбоксильная группа является защищенной, то она может быть разблокирована обычным способом удаления защитных групп, например, путем обработки кислотой, щелочной обработки или каталитического восстановления, по желанию, с получением соединения (I), имеющего свободную, амино или карбоксильную группу.
(2) Соединение общей формулы (IV)


(IV) где R
X-Y (V) где Х является группой, способной к связыванию с атомом кислорода гидроксильной группы, а Y является удаляемой группой, или с ангидридом неорганической кислоты или органической кислоты, который реагирует с гидроксильной группой.
Соединение X-Y представляет собой реакционноспособные производные ароматических и алифатических кислот, ароматических и алифатических карбоновых кислот, аминокислот, которые могут быть защищенными, фосфорной кислоты, которая может быть защищенной; серной кислоты, которая может быть защищенной; карбаминовой кислоты, которая может быть замещенной низшей алкильной группой; и сахаридов, которые могут быть защищенными. Примерами указанных соединений являются n-метоксибензолсульфонилхлорид, метансульфонилхлорид, о-хлорбензоилхлорид, ацетилхлорид, N-(т-бутоксикарбониламиноацетил) имидазол, оксихлорид фосфора, хлоросульфоновая кислота, N,N-диметилкарбамоилхлорид, и 1,2,3,4-тетра-о-ацетил-D-глюкуронат. Примерами ангидридов являются ангидриды неорганических кислот, например, пентаоксид дифосфора и триоксид серы, а также ангидриды органических кислот, например, N-карбоксиангидриды (NCA) α -аминокислот и ангидрид изатоновой кислоты.
И хотя в указанной реакции могут быть использованы практически любые растворители, однако, желательно, чтобы исходные материалы были растворимыми в этих растворителях, и чтобы эти растворители не вступали легко в реакцию с исходными материалами. Такими растворителями являются, например, пиридин, тетрагидрофуран, диоксан, бензол, простой эфир, метиленхлорид, диметилформамид и смесь двух или нескольких из указанных растворителей. Если используются жидкие исходные соединения, такие, как оксихлорид фосфора, то реакцию проводят в отсутствии растворителя.
(3) Соединение общей формулы (VI)

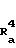
(VI) где R
R
(4) Соединение общей формулы (VII):
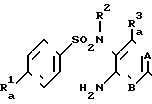

(VII) где R
R11-Z, (VIII) где R11 определен выше, а Z является карбоксильной группой или ее реактивным производным, или, когда R11 является низшей алкиламино-группой, то (VII) реагирует с низшим алкилизоцианатом.
Реакционноспособными производными карбоновых кислот, используемыми в настоящем изобретении, могут быть, например, галоидангидриды, ангидриды кислоты, активные амидные соединения и активные сложные эфиры.
Примерами используемых галоидангидридов являются хлорангидриды и бромангидриды. Примерами используемых ангидридов кислоты являются смешанные ангидриды моноалкилкарбоновой кислоты, смешанные ангидриды кислоты, содержащие алифатические карбоновые кислоты (таких, как уксусная кислота, пивалиновая кислота, валериановая кислота, изовалериановая кислота трихлоруксусная кислота), смешанные ангидриды карбоновых кислот (таких, как бензойная кислота) и симметрические ангидриды кислот. Примерами активных амидных соединений, используемых в настоящем изобретении, являются амиды кислот с имидазолом, пиразолом, 4-замещенным имидазолом, диметилпиразолом, триазолом, тетразолом и бензотиазолом. Активные сложные эфиры выбирают из группы, содержащей сложный метиловый эфир, метоксиметиловый эфир, цианометиловый эфир, пропаргиловый эфир, 4-нитрофениловый эфир, 2,4-динитрофениловый эфир, трихлорфениловый эфир, 2,4-динитрофениловый эфир, пентахлорфениловый эфир, метасульфонилфениловый эфир, фенилазофениловый эфир и эфиры с 1-гидрокси-1Н-2-пиридоном, N-гидроксисукцимидом, N-гидроксифталимидом или 1-гидроксибензотриазолом.
Карбоновые кислоты (VIII) могут взаимодействовать с амином (VII) в присутствии конденсирующего агента, такого, как N, N'-дициклогенсилкарбомид (DCC), или N-циклогенсил-N'-морфолиноэтилкарбодиимид.
Если R11 является аминогруппой, замещенной низшей алкильной группой, то амин (VII) может реагировать с низшим алкилизоцианатом. Если R11 является амино-группой, то амин (VII) может реагировать с щелочно-металлической солью циановой кислоты.
Эти реакции могут быть осуществлены в присутствии основания, такого, как органический третичный амин (например, триэтиламин, N,N-диметиланилин или пиридин), карбонат щелочного металла, или бикарбонат щелочного металла или, по желанию, кислоты. Реакцию осуществляют при использовании стехиометрически эквимолярных количеств реагентов. И хотя в реакции могут быть использованы практически любые растворители, однако, желательно, чтобы исходные материалы были растворимыми в этих растворителях, и чтобы эти растворители не вступали легко в реакцию с исходными материалами. Такими растворителями являются, например, пиридин, тетрагидрофуран, диоксан, бензол, простой эфир, метиленхлорид, диметилформамид и смесь двух или нескольких из указанных растворителей. Если используется реагент, трудно растворимый в органическом растворителе, например, такой, как цианат, то реакция может быть осуществлена в водных условиях. Растворители, которые могут быть использованы в настоящем изобретении, не ограничиваются вышеуказанными примерами. Реакционная температура также не является критической. Обычно используют комнатную температуру, но, если необходимо, реакция может быть осуществлена при охлаждении или нагревании. Реакционное время составляет от 5 мин до 20 ч и зависит от исходных соединений и реакционной температуры. Если продукт имеет защищенную гидроксильную или амино-группу, то он может быть подвергнут обработке по удалению защитных групп, например, кислотной обработке, щелочной обработке или каталитическому восстановлению с получением соединения (I), имеющего свободную гидроксильную или амино-группу. Если продукт имеет нитро-группу, то эта группа может быть превращена в амино-группу путем восстановления нитро-групп с использованием стандартного способа, например, каталитического восстановления в присутствии катализатора, такого, как палладированный уголь, или с использованием цинковой пудры и соляной кислоты.
Ниже приводится описание способа получения исходных
соединений (IX),
используемых в настоящем изобретении


(IX) где R
Способ получения 1.
[химическая формула 20]






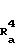
Соединения общей формулы (XII) могут быть синтезированы различными способами, описанными, например, в публикациях I.Med. Chem, 21, стр. 965, I. Org. Chem. 28, стр. 3 114, I. Chem. Soc. Perkin I, 1974, 1611, 1974, 1970 и 1979, 135, Helv. Chim. Acta, 61, стр. 2 452 или аналогичными способами. То есть, они могут быть получены с помощью реакции соединения общей формулы (X) с соединением общей формулы (XI) в отсутствие или в присутствии органического растворителя, такого, как диметилформамид, этанол или диоксан, при комнатной температуре или при нагревании.
Если необходимо удалить образованный таким образом галогенводород, то в качестве связующего кислоты добавляют органические основание, такое, как триэтиламин или пиридин или карбонат щелочного металла; либо реакцию проводят с использованием, по крайней мере, двух эквивалентов соединения (XI) на эквивалент соединения (Х). Если продукт (XII) на своем ароматическом кольце имеет высоко реакционноспособный атом галогена, то может быть проведена еще одна реакция с алкоксидом или амином для превращения в другое соединение. Соединение общей формулы (IX) может быть получено путем восстановления соединения (XII), полученного описанным выше способом, используемым для восстановления нитро-групп. В предпочтительном варианте процесса восстановления, каталитическое восстановление проводят в присутствии катализатора палладированного угля или с использованием цинкового порошка и уксусной кислоты. Каталитическое восстановление обычно проводят в органическом растворителе, таком, как метанол, тетрагидрофуран или диметилформамид, при атмосферном или повышенном давлении.
Способ получения 2

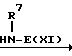

Соединения, представленные общей формулой (IX) могут быть синтезированы, например, способом, описанным в I. Org Chem 24, cтр 1314, или I. Heterocycl. Chem, 20, с. 1339, или способом аналогичным этим способам. То есть, они могут быть получены с помощью реакции соединения общей формулы (XIII) с соединением общей формулы (XI) в присутствии кислотного катализатора, такого, как соляная кислота или серная кислота, в растворителе, таком, как вода, этанол или диэтиленгликоль. Для повышения скорости реакции, реакционную смесь предпочтительно нагревать.
Способ получения 3.



Соединения, представленные формулой (IX), могут быть синтезированы, например, способом, описанным в I.Chem Soc. (C) 1970, c. 1355 или аналогичным способом. То есть, они могут быть получены с помощью реакции общей формулы (XIV) с соединением общей формулы (XV) в отсутствие или присутствии органического растворителя, такого, как диметилформамид или диоксан, при комнатной температуре или при нагревании.
Способ получения 4


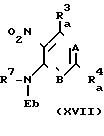

Eb представляет собой Е, определенное выше, в котором по крайней мере один является защищенной гидроксильной группой.
Соединения, представленные общей формулой (XVII) могут быть получены с помощью реакции соединения общей формулы (XVI) с соединением общей формулы: X-Y (V), где Х и Y определены выше, или с использованием ангидрида неорганической или органической кислоты, способной вступать в реакцию с гидроксильной группой. Реакционные условия варьируются в зависимости от вида X-Y (V) и ангидрида. Реакционным растворителем является предпочтительно инертный растворитель, который не вступает в реакцию с указанными соединениями, например, такой, как диметилформид, тетрагидрофуран или диоксан. Для увеличения скорости реакции к реакционной системе может быть добавлено основание, такое, как гидрид натрия, карбонат калия или триэтиламин, или может быть повышена температура реакции. Если R7 является атомом водорода, то перед осуществлением реакции c X-Y (V) иногда бывает желательно защитить его стандартной амино-защитной группой, такой, как бензилоксикарбонильная группа, а после завершения реакции защитная группа может быть удалена. Соединения, представленные общей формулой (XVIII), могут быть получены путем восстановления соединений (XVII), полученных в соответствии с вышеупомянутым способом восстановления нитро-групп.
Способ получения 5
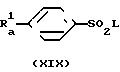




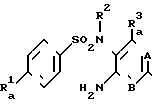

Соединения, представленные общей формулой (VII), могут быть получены путем восстановления соединения общей формулы (XIX) с использование соединения общей формулы (ХХ). Реакционные условия зависят от используемых соединений. Предпочтительно, на 1 эквивалент сульфонилгалида (XIX) использовать 2-4 эквивалента соединения (XX). В качестве реакционного растворителя предпочтительно использовать тетрагидрофуран, диоксан, пиридин, диметилформамид или т. п. Реакция также может быть осуществлена в водных условиях. Обычно, реакцию проводят при комнатной температуре, однако, если необходимо, она может быть проведена при охлаждении или при нагревании.
Если соединения настоящего изобретения используются в качестве лекарственных средств, они могут быть введены перорально или перентально. Вводимая доза варьируется в зависимости от симптомов, возраста, пола, веса, и чувствительности пациента; метода введения, времени и интервала введения; свойств, состава и типа препарата; и вида активного ингредиента.
Указанная доза обычно составляет от 10 до 6000 мг, предпочтительно, около 50-4000 мг, и наиболее предпочтительно 100-3000 мг в день для взрослого человека. Эта доза может быть введена частями от 1 до 3 раз в день.
При получении твердого препарата для перорального введения, к активному ингредиенту может быть добавлен наполнитель, и если необходимо, связующее вещество, дезинтегратор, замасливатель, окрашивающее вещество, модификатор, и т. п. при этом указанный препарат может быть изготовлен в виде таблеток; таблеток, покрытых оболочкой; гранул; мелких гранул, порошка или капсул.
Примерами наполнителей являются лактоза, кукурузный крахмал, белый сахар, глюкоза, сорбит, кристаллическая целлюлоза и диоксид кремния. Примерами связующих являются поливиниловый спирт, поливиниловый эфир, этилцеллюлоза, метилцеллюлоза, акация, трагакант, желатин, шеллак, гидроксипропилцеллюлоза, гидроксипропилметилцеллюлоза, цитрат кальция, декстрин и пектин. Примерами замасливателей являются стеарат магния, тальк, полиэтиленгликоль, кремнозем и отвержденные растительные масла. В препараты могут быть также добавлены окрашивающие агенты. Примерами модификаторов являются порошок какао, метанол, ароматические порошки, эфирное масло из перечной мяты, борнеол и молотая корица. Эти таблетки и гранулы могут быть покрыты сахаром, желатином и т.п.
При получении препаратов для инъекций, к активному ингредиенту могут быть добавлены рН-модификатор, буфер, суспендирующий агент, солюбилизатор, стабилизатор, изотонизирующий агент, консервант и т.п. при этом указанный препарат может быть изготовлен в виде форм для внутривенных, подкожных или внутримышечных инъекций. Если необходимо, указанные препараты могут быть лиофилизованы.
Примерами суспендирующих агентов являются метилцеллюлоза, полисорбат 80, гидроксиэтилцеллюлоза, акация, порошок трагаканта, натрийсодержащаяя карбоксиметилцеллюлоза и полиоксиэтиленсорбитанмонолаурат.
Примерами солюбилизаторов являются полиоксиэтиленотвержденное касторовое масло, полисорбит 80, никотинамид, полиоксиэтиленсорбитанмонолаурат, макрогель и этиловые сложные эфиры жирных кислот касторового масла.
Примерами стабилизаторов являются сульфит натрия, метасульфит натрия и простой эфир. Примерами консервантов являются метил n-гидроксибензоат, этил n-гидроксибензоат, сорбиновая кислота, фенол, крезол и хлорокрезол.
Осуществление настоящего изобретения.
Экспериментальный пример 1.
In vitro противоопухолевый тест на КВ-клетках (клетки из носоглокти человека):
1,25 х 103 (0,1 мл) КВ-клеток, суспендированных
в среде RPM1 1640 (продукт Nissui Seiyaku Co. Ltd), содержащий 20% околоплодной сыворотки теленка, пенициллин (100 ед/мл), стрептомицин (100 мкг/мл), меркаптоэтанол (5 х 10-5 М) и пируват
натрия (1 мМ), помещали в каждую лунку 96-луночной планшеты для микротитрования, и культивировали в инкубаторе, содержащем 5% двуокись углерода, в течение 1 дня при 37оС.
Соединение настоящего изобретения растворяли в диметилсульфоксиде и получали 20 мг/мл раствор, который разводили до концентрации 100 мкг/мл культуральной жидкостью, содержащей 0,1% околоплодную сыворотку теленка в среду RPM1 1640. Эта концентрация была максимальной и ее подвергали двухкратному серийному разведению культуральной средой RPM1 1640 с 0,1% околоплодной сывороткой теленка, содержащей диметилсульфоксид. Этот раствор добавляли к КВ-клеткам в каждую лунку с вышеописанной культурой в количестве 0,1 мл, и культивировали в инкубаторе, содержащем 5% диоксида кремния, в течение 3 дней при 37оС.
После завершения культивирования, в каждую лунку добавляли 0,05 мл МТТ-(3-(465-диметилтиазол-2-ил)-2,5-дифенилтет-разолия бромид)-раствор (3,3 мг/мл), и культивировали еще 1 ч. Затем из каждой лунки удаляли надосадочную жидкость путем отсасывания, а образовавшийся таким образом формазан растворяли в 0,1 мл диметилсульфоксида. Затем определяли оптическую плотность при 540 нм с помощью считывающего устройства, используя в качестве показателя число жизнеспособных клеток. Процент ингибирования рассчитывали по приведенной ниже формуле, а затем определяли концентрацию испытуемого соединения, требуемого для 50% ингибирования (IC50).
[Численная формула 1]
Процент ингибирования (%) (С-Т)/C х
100
Т
оптическое поглощение лунки, содержащей испытуемые соединения,
С оптическое поглощение лунки, не содержащей испытуемого соединения,
IC50 величины,
определенные таким
образом, представлены в табл. 2.
Сравнительные соединения приведены в табл. 1.
Экспериментальный пример 2.
In vivo противоопухолевый
тест на прямой
кишке 38 (рак прямой кишки мыши):
Около 75 мг прямой кишки 38 подкожно трансплантировали с боковой стороны каждой мыши BDF1 (самка, 7 недель). Соединение настоящего
изобретения
суспендировали в 0,5% метилцеллюлозы и вводили перорально один раз в день, начиная со следующего дня и продолжая в течение 8 дней. Контрольная группа состояла из 10 мышей, а испытуемая
группа состояла
из 6 мышей.
Через 21 день после трансплантации, опухоли вырезали и взвешивали. Степень ингибирования опухолевого роста испытуемой
группы по отношению к контрольной
группе определяли
по следующей формуле:
[Численная формула 2]
Степень ингибирования роста опухоли (%) (С-Т)/С х 100
Т средний вес опухоли в группе мышей, которым вводили
испытуемое соединение,
С средний вес опухоли в контрольной группе.
Результаты экспериментов представлены в табл. 3.
Экспериментальный пример 3: Тест на токсичность.
Группе из 5 мышей BDF1 (самки, 7 недель) вводили один раз 0,5% суспензию соединения примера 3, 4 или 6 в метилцеллюлозе, и в течение 7 дней после введения наблюдали за жизнеспособностью обработанных мышей. Ни одна мышь не погибла даже при введении 1651 мг/кг соединения.
Как видно из приведенных выше экспериментальных примеров, соединения настоящего изобретения обладают прекрасным противоопухолевым действием. Кроме того, соединения настоящего изобретения являются в высокой степени безвредным лекарственным средством и поэтому могут быть с успехом использованы для лечения злокачественных опухолей, т.е. в качестве противоопухолевого средства.
П р и м е р ы.
Приведенные примеры получения иллюстрируют способы получения исходных соединений для синтеза соединений настоящего изобретения, а следующие ниже примеры иллюстрируют типичные соединения настоящего изобретения, однако при этом указанные примеры не должны рассматриваться как некие ограничения возможных вариантов осуществления настоящего изобретения.
Пример получения 1.
2-Анилино-3-нитропиридин:
[химическая формула 25]

Смесь 11,21 г (70 мМ) 2-хлоро-3-нитропиридина и 19,56 г (210 мМ) анилина нагревали, размешивая, при 100оС в течение 1 ч. Реакционную смесь охлаждали до комнатной температуры и растворяли в этилацетате. Раствор промывали водным раствором лимонной кислоты, а затем водой. После осушки сульфатом магния, растворитель отгоняли при пониженном давлении, а остаток перекристаллизовывали из смеси этилацетата и н-гексана, в результате чего получали 13,7 целевого соединения.
Т.пл. 73-74оС
FAB масс-спектрометрия (m/z): 216 ([M+H]+)
1Н-ЯМР
(CDCl3) δ (ppm): 6,84 (1Н, дд, I=8,4, 4,4 Гц), 7,18-7,22 (1Н, м); 7,
37-7,43 (2Н, м), 7,62-7,68 (2Н, м), 8,49 (1Н, дд, I=4,4, 2,0 Гц), 8,53 (1Н, дд, I=8,4, 2,0 Гц), 10,12 (1Н, шир.
с)
Элементный анализ для C11H9N3 ·O2:
Вычислено: С 61,39; Н 4,22; N19,53
Найдено: C 61,49; H 4,34; N 19,23
Пример получения 2.
3-Амино-2-анилинопиридин
[химическая формула
26]

6,8 г (31,6 мМ) соединения, полученного в примере получения 1, растворяли в смеси 40 мл тетрагидрофурана и 6 мл метанола. После чего к раствору добавляли палладированный уголь в целях осуществления гидрогенизации при комнатной температуре и атмосферном давлении. Затем палладированный угол отгоняли фильтрацией при пониженном давлении, а остаток перекристаллизировали из смеси этилацетата и н-гексана, в результате чего получали 5,5 г целевого соединения.
Т.пл.
143-144оС
FAB масс-спектроскопия FAB-MC (m/z):186 ([M+H]+)
1
Н-ЯМР (DMCO-d6) δ (ppm): 4,95-5,10 (2Н, шир), 6,61 (1Н, дд, I=7,2, 4,8
Гц), 6,80-6,86 (1Н, м), 6,90 (1Н, дд, I=7,2, 1,6 Гц), 7,18-7,24 (2Н, м), 7,49 (1Н, дд, I=4,8, 1,6 Гц), 7,60-7,
65 (2Н, м); 7,69 (1Н, с).
Элементный анализ для С11Н11N3:
Вычислено: C 71,33; H 5,99; N 22,69
Найдено: C 71,49; H 6,04; N 22,59
Пример получения 3.
4-[(3-Нитро-2-пиридил)амино]фенол
[химическая формула 27]
HO
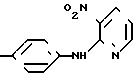
8,17 г (50 мМ) 2-хлоро-3-нитропиридина и 16,70 г (150 мМ) n-аминофенола добавляли к 50 мл диметилформамида, и полученную смесь размешивали 40 мин при 100оС. Растворитель отгоняли при пониженном давлении и обрабатывали способом, описанным в примере получения 1, после чего продукт перекристаллизовывали из этанола и получали 9,4 г целевого соединения.
Т.пл. 143-144оС
FAB-MC (m/z): 231 (M+)
1H-ЯМР (CDCl3) δ (ppm): 5,23 (1Н, с); 6,79 (1Н, дд, I=4,8, 8,4
Гц), 6,84 (2Н, д, I= 8,8 Гц), 7,41 (2Н, д, I=8,8 Гц), 8,44 (1Н, дд, I=1,6, 4,8 Гц), 8,52 (1Н, дд, I=1,6, 8,4
Гц), 9,94 (1Н, шир. с).
Элементный анализ для C11H9
N3O3:
Вычислено: C 57,14; H 3,92; N 18,18
Найдено: C 57,15; H 3,97; N
18,14
Пример получения 4.
4-[(3-Амино-2-пиридил)амино]фенол
[химическая формула 28]
HO

9,25 г (40 мМ) соединения, полученного в примере получения 3, каталитически восстанавливали и обрабатывали способом, аналогичным описанному в примере получения 2, после чего продукт перекристаллизовывали из метанола и получали 7,8 г целевого соединения.
Т.пл. 205-207оС
FAB-MC (m/z): 202 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 4,94 (2Н, шир. с); 6,50 (1Н, дд, I=4,8, 7,6 Гц); 6,
66 (2Н, д, I=8,8 Гц); 6,82 (1Н, дд, I=1,6, 7,6 Гц); 7,38 (1Н, с); 7,39 (2Н, д, I=8,8 Гц); 7,40 (1Н,
дд, I=1,6, 4,8 Гц), 8,85 (1Н, с).
Элементный анализ для C11H11
N3O:
Вычислено: C 65,66; H 5,51; N 20,88
Найдено: C 65,85; H 5,51; N 20,
84
Пример получения 5.
3-[(3-Нитро-2-пиридил)амино]фенол
[химическая формула 29]

Т.пл. 148-149оС (перекристаллизован из этанола)
FAB-MC (m/z): 232 ([M+H]+)
1Н-ЯМР (CDCl3) δ (ppm): 5,31 (1Н, шир. с); 6,65 (1Н, дд, I=8,0, 2,4 Гц), 6,85 (1Н, дд, I=8,4, 4,8 Гц), 7,08 (1Н, дд, I=8,0, 2,4 Гц), 7,24 (1Н, т, I= 8,0 Гц), 7,37 (1Н, т, I=2,4 Гц), 8,49 (1Н, дд, I=4,8, 1,6 Гц), 8,54 (1Н, дд, I=8,4, 1,6 Гц), 10,11 (1Н, шир. с).
Элементный анализ для C11H9N3O3:
Вычислено: С 57,14; H 3,92; N 18,17
Найдено:
C 57,33; H 4,03; N 18,18
Пример получения 6.
3-[(3-Амино-2-пиридил)амино]фенол
[химическая формула 30]

Т. пл. постепенное разложение наблюдается при 198оС (после перекристаллизации из этанола);
FAB-MC (m/z): 202 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 5,04 (2Н, с); 6, 24-6,28 (1Н, м); 6,60 (1Н, дд, I= 7,6, 4,8 Гц), 6,89 (1Н, дд, I=7,6, 1,6 Гц), 6,97-6,99 (2Н, м); 7,23 (1Н, шир. с), 7,50 (1Н, дд, I=4,8, 1,6 Гц); 7,57 (1Н, с); 9,10 (1Н, с).
Элементный анализ для C11H11N3O:
Вычислено: C 65,66; H 5,51; N 20,88
Найдено: C 65,
92; H 5,58; N 20,86
Пример получения 7.
2-[(4-Метоксиметилоксифенил)амино]-3-нитропиридин
[химическая формула 31]
CH3OCH2O

8,4 г (54,8 мМ) 4-метоксиметилоксианилина и 7,5 г (49 мМ) 2-хлоро-3-нитропиридина растворяли в 35 мл диметилформамида. После чего к раствору добавляли 7,6 г (55 мМ) безводного карбоната калия. Полученный в результате раствор нагревали, размешивали, при 100оС в течение 4 ч. Затем реакционную жидкость охлаждали до комнатной температуры, а нерастворившееся вещество, образованное таким образом, удаляли путем фильтрации. Растворитель отгоняли при пониженном давлении, а остаток растворяли в этилацетате. Раствор промывали водным раствором лимонной кислоты, а затем водой. После осушки сульфатом магния, растворитель отгоняли при пониженном давлении, а остаток перекристаллизовывали из этанола, в результате чего получали целевое соединение.
Т.пл. 80-81оС
FAB-MC (m/z): 275 (M+)
1Н-ЯМР (CDCl3) δ (ppm): 3,50 (3H, c); 5,19 (2H, с); 6,79 (1Н, дд,
I=4,4, 8,4 Гц); 7,08 (2Н, д, I=8,8 Гц); 7,50 (2Н, д, I=8,8 Гц); 8,45 (1Н, дд, I= 1,6; 4,4 Гц); 8,51 (1Н, дд, I=1,6, 8,4 Гц), 9,99 (1Н,
шир. с).
Элементный анализ для C13
H13N3O4:
Вычислено: C 56,73; H 4,76; M 15,27
Найдено: C 57,06; H 4,83; N 15,02
Пример получения 8
2-[N-бензилоксикарбонил-N-(4-метокс- иметилоксифенил)-амино]-3-нитропиридин
[химическая формула 32]
CH3OCH2O

4,0 г (14,5 мМ) соединения, полученного в примере получения 7, растворяли в 70 мл диметилформамида. Затем к раствору добавляли 720 г (18 мМ) 60% гидрида натрия. И перемешивая при комнатной температуре, к раствору по капле добавляли 3,2 мл (22,4 мМ) бензилхлороформата. После перемешивания в течение ночи при комнатной температуре, растворитель отгоняли при пониженном давлении. Затем к остатку добавляли этилацетат и воду, и слой этилацетата отделяли. Выделенный слой промывали водой, а затем осушали, концентрировали, и очищали с помощью колоночной хроматографии на силикагеле, в результате чего получали 4,5 г маслянистого целевого соединения.
1Н-ЯМР (CDCl3) δ (ppm): 3,47 (3Н, с); 5, 17 (4Н, с+с); 7,06 (2Н, д, I=8,8 Гц); 7,22-7,26 (2Н, м); 7,29-7,33 (4Н, м); 7,37 (2Н, д, I=8,8 Гц); 8,29 (1Н, д, I=8,0 Гц); 8,56 (1Н, д, I=4,4 Гц).
Пример получения 9.
4-[N-бензилоксикарбонил-N-(3-нитро-2-пиридил)амино]фенол
[химическая формула 33]
HO

500 мг (1,22 мМ) соединения, полученного в примере получения 8, растворяли в смеси 6 мл тетрагидрофурана и 1 мл воды. К полученному раствору добавляли 2 мл конц. соляной кислоты. После этого смесь размешивали в течение ночи при комнатной температуре, а растворитель отгоняли при пониженном давлении. К остатку добавляли этилацетат и насыщенный водный раствор бикарбоната натрия, и образовавшийся таким образом слой этилацетата отделяли. Выделенный слой промывали водой (осушали сульфатом магния) и концентрировали, в результате чего получали 445 мг целевого соединения.
1 Н-ЯМР (DMCO-d6) δ (ppm): 5,11 (2H, c); 6,77 (2H, д, I=8,8 Гц); 7,18-7,24 (4Н, м); 7,31-7,34 (3Н, м); 7,58 (1Н, дд, I=4,8, 8,0 Гц); 8,51 (1Н, дд, I=1,6, 8,0 Гц); 8,66 (1Н, дд, I=1,6 4,8 Гц); 9,64 (1Н, с).
Пример получения 10.
4-[[(3-Амино-2-пиридил)амино]фенил] трет-бутокси-карбонил-аминоацетат
[химическая формула
34]
(CH3)3COCONHCH2COO

440 мг (1,2 мМ) соединения, полученного в примере получения 9, 250 мг (1,43 мМ) N-(трет-бутоксикарбонил)-глицина и 25 г (0,2 мМ) 4-диметиламинопиридина растворяли в 10 мл пиридина. 290 мг (1,41 мМ) 1,3-дициклогексилкарбодиимида добавляли к полученному раствору. После размешивания в течение ночи при комнатной температуре, растворитель отгоняли при пониженном давлении. К остатку добавляли этилацетат, нерастворенное вещество удаляли путем фильтрации, а растворитель отгоняли при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле, и полученное соединение каталитически восстанавливали в присутствии палладированного угля стандартным способом. Затем катализатор удаляли с последующей концентрацией, а остаток очищали с помощью колоночной хроматографии на силикагеле, в результате чего получали 236 мг целевого соединения.
1Н-ЯМР (DMCO-d6) δ (ppm): 1,41 (9H, c); 3,93 (2Н, д, I=6,0 Гц); 5,05 (2Н, шир. с); 6,62 (1Н, дд, I=4,8, 7,2 Гц); 6,90 (1Н, дд, I=1, 6, 7,2 Гц); 6,96 (2Н, д, I=9,2 Гц); 7,37 (1Н, шир. т, I=6,4 Гц); 7,49 (1Н, дд, I=1,6, 4,8 Гц); 7,64 (2Н, д, I=9,2 Гц), 7,79 (1Н, с).
Пример получения 11.
4-[[3-(4-Метоксибензолсульфонамидо)-2-пиридил] амино]фенил-2,3,4,6-тетра -0-ацетил- β -D-глюкопиранозид
[химическая формула 35]

3,753 г (10,10 мМ) соединения, полученного в примере 6, и 3,959 г (10,14 мМ) β -D-глюкозы пентаацетата суспендировали в 200 мл 1, 2-дихлорэтана. К полученной суспензии, размешивая и охлаждая льдом в атмосфере азота, по капле добавляли 30 мл 1,0 М раствора тетрахлорида олова в дихлорметане. После перемешивания в течение 2 часов при охлаждении льдом, а затем в течение 4 дней при комнатной температуре, реакционную смесь добавляли в воду со льдом, содержащую 16 г бикарбоната натрия. Органический растворитель отгоняли при пониженном давлении. К остатку добавляли этилацетат, а образованное нерастворившееся вещество удаляли путем фильтрации. Слой этилацетата отделяли, промывали водой, осушали, концентрировали и очищали с помощью колоночной хроматографии на силикагеле, в результате чего получали 2,47 г целевого соединения.
1Н-ЯМР (CDCl3) δ (ppm): 2,04 (3Н, с), 2,05 (3Н, с); 2, 08 (3Н, с); 2,10 (3Н, с); 3,08-3,86 (1Н, м); 3,84 (3Н, с); 4,17 (1Н, дд, I=12,4, 2,4 Гц); 4,30 (1Н, дд, I=12,4, 5,6 Гц); 4,99 (1Н, д, I=7,6 Гц); 5,16 (1Н, т, I=9,6 Гц); 5,23-5,32 (2Н, м); 6,37 (1Н, шир. с); 6,54 (1Н, дд, I=4,8, 7,6 Гц); 6,84 (1Н, дд, I= 1,6, 7,6 Гц); 6,92 (2Н, д, I=8,8 Гц); 6,94 (2H, д, I=8,8 Гц); 7,32 (1Н, шир. с); 7,38 (2Н, д, I=8,8 Гц); 7,69 (2Н, д, I=8,8 Гц); 8,07 (1Н, дд, I=1,6, 4,8 Гц).
Пример получения 12.
N-(2-аминофенил)-4-метоксибензолсул- ьфонамид
[химическая формула 36]

33,1 г (0,3 М) 1,2-фенилендиамина растворяли в 200 мл диоксана. К этому раствору, размешивая, добавляли раствор 20,87 г (0,1 М) 4-метоксибензолсульфонилхлорида в 110 мл диоксана. Полученную смесь размешивали при комнатной температуре в течение ночи. К этой смеси добавляли 12,1 г (0,12 М). После концентрации с последующим добавлением водного раствора лимонной кислоты и этилацетата, органический слой отделяли, концентрировали и очищали с помощью колоночной хроматографии на силикагеле, в результате чего получали 27,1 г целевого соединения.
Т.пл. 141-142оС (после перекристаллизации из этанола);
FAB-MC (m/z): 279 ([M+H]+)
1Н-ЯМР (DMCO-d6)
δ (ppm): 3,81 (3Н, с); 4,91 (2Н, шир. с); 6,37 (1Н, тд, I= 1,6, 7,2, 8,0 Гц); 6,60 (1Н, дд, I=1,6, 8,0 Гц); 6,66 (1Н, дд, I=1,6, 8,0 Гц), 6,86 (1Н, тд, I=1,6, 7,2, 8,0 ГЦ), 7,03 (2Н, д, I=8,8
Гц), 7,61 (2Н, д, I=8,8 Гц), 9,07 (1Н, шир. с).
Элементный анализ для C13H14N2O3S:
Вычислено: C 56,10; H 5,07; N 10,07
Найдено: C 55,98; H 5,03; N 10,00
Пример получения 13.
N-(2-аминофенил)-4-нитробензолсуль-фонамид:
[химическая формула 37]

Целевое соединение было получено способом, аналогичным способу в примере получения 12.
Т.пл. 190-191оС
(перекристаллизовано из бензола)
FAB-MC (m/z): 294 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 4,90 (2Н, шир. с); 6,42 (1Н, дт, I=1,6, 8,0 Гц); 6,61
(1Н,
дд, I=1,6, 8,0 Гц); 6,71 (1Н, дд, I=1,6, 8,0 Гц); 6,91 (1Н, дт, I=1,6, 8,0 Гц); 7,91 (2Н, д, I=8,8 Гц); 8,36 (2Н, д, I=8,8 Гц).
Элементный анализ для C12H11
N3O4S:
Вычислено: C 49,14; H 3,78; N 14,33
Найдено: С 49, 38; H 3,82; N 14,13
Пример получения 14.
N-(2-амино-3-метилфенил)-4-метокси-бензолсульфонамид
[химическая формула 38]
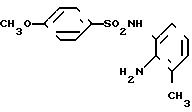
Целевое соединение было получено способом, аналогичным способу, описанному в примере получения 12.
Т.пл. 177-178оС (перекристаллизовано из этанола)
FAB-MC
(m/z):293
([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 2,03 (3Н, с); 3,81 (3Н, с); 4,75 (2Н, шир. с); 6,30 (1Н, т, I=7,6 Гц); 6,44 (1Н, дд, I=1,2, 7,6 Гц); 6,79
(1Н, дд,
I=1,2, 7,6 Гц); 7,04 (2Н, д, I=8,8 Гц); 7,61 (2Н, д, I=8,8 Гц).
Элементный анализ для C14H16N2O3S:
Вычислено: C 57,52; H
5,52; N 9,
58
Найдено: C 57,76; H 5,51; N 9,57
П р и м е р 1.
N-(2-анилино-3-пиридил)-n-толуолсуль- фонамид
[химическая формула 39]

3,7 г (20 мМ) соединения, полученного в примере получения 2, растворяли в 30 мл пиридина. К этому раствору, перемешивая при комнатной температуре, по частям добавляли 30 мл раствора 3,81 г (20 мМ) n-толуолсульфонилхлорида в тетрагидро- фуране. После размешивания в течение ночи, раствор отгоняли при пониженном давлении, а остаток растворяли в этилацетате. Раствор промывали водой и осушали сульфатом магния. Растворитель отгоняли при пониженном давлении, остаток перекристаллизовывали из этанола и получали 5,2 г целевого соединения.
Т.пл. 164-165оC
FAB-MC (m/z): 340 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 2,23 (3Н,
с); 6,73 (1Н, дд, I=4,8,
7,6 Гц); 6,86-6,92 (1Н, м); 7,18-7,24 (2Н, м); 7,24 (2Н, д, I=8,0 Гц); 7,27 (1Н, дд, I= 7,6, 1,6 Гц); 7,36-7,42 (2Н, м); 7,54 (2Н, д, I=8,0 Гц); 7,86 (1Н, с); 7,99 (1Н, дд,
I=4,8, 1,6 Гц); 9,62 (1Н,
с).
Элементный анализ для C18H17N3O2S:
Вычислено: С 63,70; H 5,05; N 12,38
Найдено: C 63,77; H
5,11; N 12,28
П р
и м е р 2.
N-(2-анилино-3-пиридил)-4-этилбензолсульфонамид
[химическая формула 40]

3,11 г (16,8 мМ) соединения, полученного в примере получения 2, подвергали реакции взаимодействия с 3,43 г (16,8 мМ) n-этилбензолсульфонилхлорида и продукт обрабатывали способом, описанным в примере 1, в результате чего получали 0,5 г целевого соединения.
Т.пл. 138-139оС (после
перекристаллизации из этанола)
FAB-MC (m/z): 354 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 1,02 (3Н, т); 2,50 (2Н, кв.); 6,72 (1Н, дд, I= 5,2, 8,0
Гц); 6,83-6,89 (1Н, м); 7,14-7,20 (2Н, м); 7,24 (2Н, д, I=8,4 Гц); 7,29
(1Н, дд, I= 8,0, 1,8 Гц); 7,32-7,37 (2Н, м); 7,54 (2Н, д, I=8,4 Гц); 7,80 (1Н, с); 7,97 (1Н, дд, I=5,2, 1,8 Гц); 9,60 (1Н,
с).
Элементный анализ для C19H19N3O2S:
Вычислено: C 64,57; H 5,42; N 11,89
Найдено: C 64,89; H 5,33; N 12,00
П
р и м е р 3.
N-(2-анилино-3-пиридил)-4-метоксибен- золсульфонамид
[химическая формула 41]
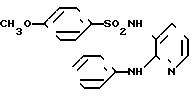
1,39 г (7,5 мМ) соединения, полученного в примере получения 2, подвергали реакции с 1,55 г (7,5 мМ) n-метоксибензолсульфонилхлорида и полученный продукт обрабатывали способом, описанным в примере 1, в результате чего получали 2,6 г целевого соединения.
Т.пл. 172-173оС (после перекристаллизации из этанола)
FAB-MC
(m/z): 356 ([M+H]+)
1
Н-ЯМР (DMCO-d6) δ (ppm): 3,68 (3Н, с); 6,71 (1Н, дд, I=7,6, 5,0 Гц); 6,84-6,90 (1Н, м); 6,92 (2Н, д, I=9,2 Гц); 7,15-7,22 (2Н, м);
7,25 (1Н, дд, I= 7,6, 1,2 Гц); 7,36-7,42 (2Н, м); 7,
57 (2Н, д, I=9,2 Гц); 7,86 (1Н, с); 7,97 (1Н, дд, I=5,0, 1,2 Гц); 9,51 (1Н, с).
Элементный анализ для C18H17
N3O3S:
Вычислено: C 60,
83; H 4,82; N 11,82
Найдено: C 61,02; H 4,69; N 11,86
П р и м е р 4.
4-Метокси-N-[2-[(4-метоксифенил)ами-но]-3-пиридил]бензол-сульфонамид
[химическая формула 42]

Целевое соединение получали способом, описанным в примере 1.
Т.пл. 145-147оС (после перекристаллизации из этанола)
FAB-MC (m/z): 386 ([M+H]+
)
1Н-ЯМР (CDCl3) δ (ppm): 3,79 (3Н, с); 3,85 (3Н, с); 6,16 (1Н, шир. с);
6,52 (1Н, дд, I= 4,8, 7,6 Гц); 6,85 (3Н, д, I=8,8 Гц); 6,93 (2Н, д, I=8,8 Гц); 7,12 (1Н,
шир. с); 7,32 (2Н, д, I=8,8 Гц); 7,69 (2Н, д, I=8,8 Гц); 8,07 (1Н, дд, I=1,6, 4,8 Гц).
Элементный анализ для C19H19N3O4S:
Вычислено: C 59,21; H 4,97; N 10,90
Найдено: C 59,26; H 5,05; N 10,75
П р и м е р 5.
4-Метокси-N-[2-[(4-метоксиметилоксифе- нил)амино] -3-пиридил]
бензолсульфонамид
[химическая формула 43]

Целевое соединение было получено способом, описанным в примере 1.
Т.пл. 118-119оС (после перекристаллизации из этанола)
FAB-MC (m/z): 416 ([M+H]+)
1Н-ЯМР (CDCl3)
δ (ppm): 3,48 (3Н, с); 3,83 (3Н, с); 5,13 (2Н, с); 6,45 (1Н, шир. с); 6,52 (1Н, дд, I=4,4, 7,6 Гц); 6,87 (1Н,
дд, I=1,6, 7,6 Гц); 6,92 (2Н, д, I=8,8 Гц); 6,97 (2Н, д, I=8,8 Гц); 7,16 (1H,
шир.c); 7,31 (2H, д, τ8,8 Гц); 7,69 (2Н, д, I=8,8 Гц); 8,07 (1Н, д).
Элементный анализ для C20H21N3O5S:
Вычислено: C 57,82;
H 5,09; N 10,11
Найдено: C 57,93; H 5,02; N 9,84
П р и м е р 6.
N-[2-[(4-гидроксифенил)амино]-3-пири-дил]-4-метоксибензолсульфонамид
[химическая формула 44]

1,01 г (5 мМ) соединения, полученного в примере получения 4, подвергали реакции с 1,05 г (5 мМ) n-метоксибензолсульфонилхлорида, и полученный продукт обрабатывали способом, аналогичным описанному в примере 1, в результате чего получали целевое соединение.
Т.пл. 178-179оС (после перекристаллизации из этанола)
FAB-MC (m/z): 372 ([M+H]+
)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,75 (3Н, с); 6,60 (1Н, дд, I=4,8, 7,6 Гц);
6,63 (2Н, д, I=8,8 Гц); 6,98 (2Н, д, I=8,8 Гц); 7,14 (2Н, д, I=8,8 Гц); 7,18 (1Н, дд, I= 1,
6, 7,6 Гц); 7,58 (1Н, шир. с); 7,60 (2Н, д, I=8,8 Гц); 7,88 (1Н, дд, I=1,6, 4,8 Гц); 8,97 (1Н, с); 9,44 (1Н,
с).
Элементный анализ для С18H17N3O4S:
Вычислено: C 58,21; H 4,61; N 11,31
Найдено: C 58,40; H 4,67; N 11,38
2,
0 г целевого соединения растворяли в 50 мл тетрагидрофурана. К этому раствору добавляли 0,5
мл конц. соляной кислоты, и полученный раствор концентрировали досуха. Остаток перекристаллизовывали из
метанола и получали 1,9 г гидрохлорида целевого соединения.
Т.пл. постепенное разложение наблюдалось при 225оС.
Элементный анализ для C18H17N3O4S x xHCl
Вычислено: C 53,01; H 4,45; N 10,30
Найдено: C 52,97; H 4,33; N 10,19
П р и м е р 7.
4-Метокси-N-[2-[(4-пиридил)амино]-3- пиридил]бензолсульфонамид
[химическая формула 45]

Целевое соединение получали способом, описанным в примере 1.
Т.пл. 172-173оС
(после перекристаллизации из этилацетата)
FAB-MC (m/z): 357 ([M+H]+
)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,67 (3Н, с); 6,86-6,91 (3Н, м); 7,37 (1Н, дд,
I= 1,6, 7,6 Гц); 7,48 (2Н, д, I=5,6 Гц); 7,54 (2Н, д, I=9,2 Гц); 8,04 (1Н, дд, I=1,6, 4,
8 Гц); 8,26 (2Н, д, I=5,6 Гц); 8,59 (1Н, шир. с).
Элементный анализ для C17H16N4O3S:
Вычислено: C 57,29; H 4,53; N 15,72
Найдено: С 57,37; H 4,56; N 15,66
П р и м е р 8.
4-Метокси-N-[2-[(4-метилфенил)амино]-3-пиридил]бензол-сульфонамид
[химическая формула 46]

Целевое соединение получали способом, описанным в примере 1.
Т.пл. 188-189оС
(после перекристаллизации из этанола)
FAB-MC (m/z): 370 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 2,21 (3Н, с); 3,69 (3Н, с); 6,66 (1Н, дд, I= 6,4, 2,
4 Гц); 6,92 (2Н, д, I=7,2 Гц); 6,99 (2Н, д, I=7,6 Гц); 7,21 (1Н, дд, I= 6,4, 1,6 Гц); 7,
27 (2Н, д, I=7,2 Гц); 7,56 (2Н, д, I=7,6 Гц); 7,75 (1Н, с); 7,93 (1Н, дд, I=2,4, 1,6 Гц); 9,48 (1Н, шир. с).
Элементный анализ для C19H19N3O3S:
Вычислено: C 61,77; H 5,18; N 11,38
Найдено: C 61,82; H 5,21; N 11,30
П р и м е
р 9. N-[2-[(2-фторфторофенил)амино]-3-пи-ридил]-4-метоксибензолсульфонамид
[химическая формула 47]

Целевое соединение получали способом, аналогичным описанному в примере 1.
Т.пл. 148-150оС (после перекристаллизации из этанола)
FAB-MC (m/z): 374
([M+H]+)
1Н-ЯМР (DMCO-d6) δ
(ppm): 3,72 (3Н, с); 6,76 (1Н, дд, I=7,6, 4,8 Гц); 6, 90-6,98 (3Н, м); 7,05 (1Н, тд, I=8,0, 0,8 Гц); 7,13-7,20 (2Н, м); 7,
57 (2Н, д, I=8,8 Гц); 7,82 (1Н, д, I=2,8 Гц); 7,95 (1Н, т, I=8,0 Гц); 8,01 (1Н,
дд, I=4,8, 1,6 Гц); 9,76 (1Н, с).
Элементный анализ для C18H16FN3
O3S:
Вычислено: C 57,90; H 4,32; N 11,25
Найдено: C 57,
93; H 4,57; N 10,98
П р и м е р 10.
N-[2-[(3-фторофенил)амино]-3-пиридил]-4-метоксибензол-сульфонамид
[химическая формула 48]

Целевое соединение получали способом, описанным в примере 1.
Т.пл. 180-181оС (после
перекристаллизации из этанола)
FAB-MC (m/z): 374 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,69 (3Н, с); 6,67 (1Н, тд, I=8,4); 6,81 (1Н, дд, I= 7,6, 4,
8 Гц); 6,92 (2Н, д, I=8,8 Гц); 7,09 (1Н, дд, I=8,4, 2,0 Гц); 7,22 (1Н, дт, I=8,
4, 6,8 Гц); 7,31 (1Н, дд, I=7,6, 1,6 Гц); 7,49 (1Н, дт, I= 2,0, 12,4 Гц). 7,56 (2Н, д, I=8,8 Гц); 8,05 (1Н, дд, I=4,8, 1,
6 Гц); 8,12 (1Н, с); 9,52 (1Н, шир. с).
Элементный анализ для
C18H16FN3O3S:
Вычислено: C 57,90; H 4,32; N 11,25
Найдено:
С 57,89; Н 4,42; N 11,16
П р и м е р 11.
N-[2-[(4-фторфенил)амино]-3-пиридил]-4-метоксибензол-сульфонамид
[химическая формула 49]
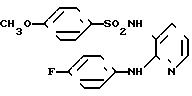
Целевое соединение получали способом, описанным в примере 1.
Т.пл. 196-197оС (после
перекристаллизации из этанола)
FAB-MC (m/z): 374 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,71 (3H, c); 6,72 (1H, дд, I=4,8, 7,6 Гц); 6,95 (2Н, д, I=
8,8 Гц); 7,04 (2Н, т, I=8,8 Гц); 7,25 (1Н, дд, I=1,6, 7,6 Гц); 7,42 (2Н, м); 7,
58 (2Н, д, I=8,8 Гц); 7,95 (1Н, шир. с); 7,98 (1Н, дд, I=1,6, 4,8 Гц); 9,48 (1Н, шир. с).
Элементный
анализ для C18H16FN3O3S:
Вычислено: C 57,90; H 4,32; N 11,25
Найдено: C 57,83; H 4,32; N 11,21
П р и м е р 12.
N-(2-анилино-3-пиридил)бензолсульфо- намид
[химическая формула 50]
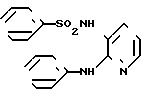
Целевое соединение было получено способом, описанным в примере 1.
Т.пл.
148-150оС (после перекристаллизации из метанола)
FAB-MC (m/z): 326 ([M+H]+)1
Н-ЯМР (DMCO-d6) δ (ppm): 6,73 (1H, дд, I= 7,6, 4,8 Гц); 6,87-6,
93 (1H, м); 7,18-7,24 (2Н, м); 7,25 (1Н, дд, I=7,6, 1,6 Гц); 7,41-7,47 (2Н, м); 7,74-7,51 (2Н, м); 7,51-7,57 (1Н, м); 7,
67-7,72 (2Н, м); 7,90 (1Н, с); 7,99 (1Н, дд, I=4,8, 1,6 Гц); 9,73 (1Н, с).
Элементный анализ для С17H15N3O2S:
Вычислено: C 62,75;
H 4,65; N 12,91
Найдено: С 63,03; H 4,74; N 12,67
П р и м е
р 13. 4-Метокси-N-[2-[(3-метоксифенил)ами-но]-3-пиридил]бензол-сульфонамид
[химическая формула 51]

Целевое соединение получали способом, описанным в примере 1.
Т.пл. 161-162оС
(после перекристаллизации из этанола)
FAB-MC (m/z): 386 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,67, 3,70 (3Н х 2); 6,47 (1Н, дд, I=8,0, 2,0 Гц); 6,
73 (1Н, дд, I=8,0, 4,8 Гц); 6,93 (2Н, д, I=8,8 Гц); 6,97 (1Н, дд, I= 8,0,
2,0 Гц); 7,10 (1Н, т, I=8,0 Гц); 7,13 (1Н, т, I=2,0 Гц); 7,29 (1Н, дд, I= 8,0, 1,6 Гц); 7,59 (2Н, д, I=8,8 Гц); 7,89 (1Н, с);
8,01 (1Н, дд, I=4,8, 1,6 Гц); 9,55 (1Н, с).
Элементный
анализ для C19H19N3O4S:
Вычислено: С 59,21; H 4,97; N 10,90
Найдено: C 59,14; H 4,96; N 10,74
П р и м е р 14.
4-Гидрокси-N-[2-[(4-гидроксифенил)ами- но]-3-пиридил]бензолсульфонамид
[химическая формула 52]

Соединение, полученное в примере 4, растворяли в диметилформамиде, и к этому раствору добавляли пять эквивалентов метантиолат натрия. Полученный раствор нагревали при 100оС и после обработки получали целевое соединение.
Т. пл. 252-257оС (разл. ) (после
перекристаллизации из смеси этанола и воды)
FAB-MC (m/z): 358 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 6,60 (1Н, дд, I=7,6, 4,8 Гц); 6,65 (2Н, д, I=
8,8 Гц); 6,81 (2Н, д, I=8,8 Гц); 7,14 (1Н, дд, I=7,6, 1,6 Гц); 7,19 (2Н, д, I= 8,8 Гц); 7,52
(2H, д, I=8,8 Гц); 7,61 (1Н, с); 7,87 (1Н, дд, I=4,8, 1,6 Гц); 9,01 (1Н, с); 9,39 (1Н, с); 10,42 (1Н,
с).
П р и м е р 15.
N-[2-[(3,4-диметоксифенил)амино]
-3-пи- ридил]-4-метокси-бензолсульфонамид
[химическая формула 53]
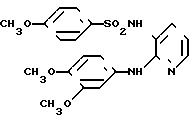
Целевое соединение было получено способом, описанным в примере 1.
Т. пл. 126-127оС (после
перекристаллизации из этанола)
FAB-MC (m/z): 415 (M+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,72, 3,73 (3Н х 3); 6,66 (1Н, дд, I=8,0, 3,6 Гц); 6,81 (1Н, д, I=8,8 Гц);
6,96-6,98 (3Н, м); 7,02 (1Н, с); 7,21 (1Н, дд, I= 8,0, 1,2 Гц); 7,60 (2Н, д, I=8,0 Гц); 7,73 (1Н,
с); 7,95 (1Н, дд, I=3,6, 1,2 Гц); 9,45 (1Н, шир. с).
Элементный анализ для C20H21N3O5S:
Вычислено: C 57,82; H 5,10; N 10,12
Найдено: C 57,73; H 5,10; N 10,07
П р и м е р 16.
4-Метокси-N-[(2-[(2-метоксифенил)ами- но]-3-пиридил]бензолсульфонамид
[химическая формула 54]
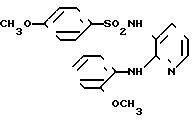
Целевое соединение было получено способом, описанным в примере 1.
Т.пл. 159-160оС (после перекристаллизации из этанола)
FAB-MC (m/z): 386 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,78 (3Н, с); 3,89 (3Н, с); 6,69 (1Н, дд,
I= 7,6, 4,8 Гц); 6,87-6,90 (2Н, м); 6,96-7,01 (2Н, м); 7,05 (2Н, д, I=8,8 Гц); 7,66
(2Н, д, I= 8,8 Гц); 8,08 (1Н, дд, I=4,8, 1,6 Гц); 8,10 (1Н, с); 8,40 (1Н, дд, I=6,4, 2,8 Гц); 9,78 (1Н, с).
Элементный анализ для C19H19N3O4
S:
Вычислено: C 59,21; H 4,97; N 10,90
Найдено: C 59,16; H 5,01; N 10,96
П р и м е р
17. 4-Метокси-N-[2-[(3-метоксифенил)ами-но]-3-пиридил]бензолсульфонамид
[химическая формула 55]

Целевое соединение получали способом, описанным в примере 1.
Т. пл. 147-148оС (после перекристаллизация из этанола)
FAB-MC (m/z): 370 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 2,26 (3Н, с);
3,71 (3Н, с); 6,71-6,73 (2Н, м); 6,95 (2Н, д, I=7,6 Гц); 7,09 (1Н, т, I=7,6 Гц); 7,16 (1Н, с); 7,25-7,27 (2Н, м);
7,59 (2Н, д, I=7,6 Гц); 7,90 (1Н, с); 8,00 (1Н, дд, I=2,8, 1,6 Гц); 9,53 (1Н, шир.
с).
Элементный анализ для C19H19N3O3S:
Вычислено: C 61,71; H 5,18; N 11,38
Найдено: C 61,79; H 5,18; N 11,46
П р
и м е р 18.
4-Метокси-N-[2-[(2-метилфенил)амино]-3-пиридил]бензолсульфонамид
[химическая формула 56]

Целевое соединение получали способом, описанным в примере 1.
Т.пл. 147-148оС (после перекристаллизации из этанола)
FAB-MC
(m/z): 370 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 2,06 (3Н, с);
3,77 (3Н, с); 6,65 (1Н, дд, I= 7,6, 4,8 Гц); 6,92 (1Н, т, I= 7,6 Гц); 7,03 (2Н, д, I=8,8 Гц);
7,09 (1Н, т, I= 7,6 Гц); 7,11-7,15 (2Н, м); 7,53 (1Н, с); 7,55 (1Н, д, I=7,6 Гц); 7,63 (2Н, д, I=8,8 Гц);
7,91 (1H, дд, l=4,8, 1,6 Гц); 9,67 (1Н, с).
Элементный анализ для C19H19N3O3S:
Вычислено: C 61,77; H 5,18; N 11,38
Найдено: C 61,80; H 5,17; N 11,40
П р и м е р 19.
N-(2-анилино-3-пиридил)-4- гидроксибензолсульфонамид
[химическая формула 57]

Целевое соединение путем обработки соединения примера 3 способом, описанным в примере 14.
Т.пл. 226-228оС (после перекристаллизации из метанола)
FAB-MC (m/z): 342
([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 6,71 (1Н, дд, I=7,6, 4,8 Гц); 6,79 (2Н, д,
I= 8,8 Гц); 6,88-6,94 (1Н, м); 7,21 (1Н, дд, I=7,6, 1,6 Гц); 7,21-7,27 (2Н,
м); 7,46-7,51 (2Н, м); 7,52 (2Н, д, I=8,8 Гц); 7,92 (1Н, с); 7,97 (1Н, дд, I= 4,8, 1,6 Гц); 9,50 (1Н, с); 10,40 (1H,
c).
П р и м е р 20.
N-(2-анилино-3-пиридил)-4-нитробен- золсульфонамид
[химическая формула 58]

Целевое соединение получали способом, описанным в примере 1.
Т.пл. 191-192оС (после перекристаллизации из
этанола)
FAB-MC (m/z): ([M+H]+)
1
Н-ЯМР (DMCO-d6) δ (ppm): 6,80-6,83 (2Н, м); 7,12 (2Н, т, I=8,4 Гц); 7,25 (2Н, д, I= 8,4 Гц); 7,40 (1Н, дд,
I=1,6, 7,6 Гц); 7,83 (3Н, д, I=8,8 Гц); 8,07 (1Н, шир. с); 8,19 (2Н, д, I=8,
8 Гц); 9,91 (1Н, шир. с).
Элементный анализ для C17H14N4O4
S:
Вычислено: C 55,13; H 3,81; N 15,13
Найдено: C 55,17; H 3,97;
N 14,77
П р и м е р 21.
4-Амино-N-(2-анилино-3-пиридил)бен-золсульфонамид
[химическая формула 59]

Целевое соединение было получено путем каталитического восстановления соединения, полученного в примере 20, в присутствии палладированного угля стандартным способом.
Т.пл. 228-230оС (после перекристаллизации из этанола)
FAB-MC
(m/z): 341 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm);
5,99 (2Н, шир. с); 6,50 (2Н, д, I=8,8 Гц); 6,70 (1Н, дд, I=4,4, 7,6 Гц); 6,91 (1Н, тд, I=0,8, 7,2 Гц); 7,
18 (1Н, дд, I= 1,6, 7,6 Гц); 7,24 (2Н, т, I=7,6 Гц); 7,33 (2Н, д, I=8,8 Гц); 7,53 (2Н, дт, I=1,
2, 7,6 Гц); 7,95 (2Н, шир. с); 9,31 (1Н, с).
Элементный анализ для C17H16N4O2S:
Вычислено: C 59,98; H 4,74; N 16,46
Найдено: C 60,08; H 4,67; N 16,23
П р и м е р 22.
N-(2-анилино-3-пиридил)-3,
4-диметоксибензолсульфонамид
[химическая формула 60]

Целевое соединение получали способом, описанным в примере 1.
Т.пл. 171-172оС (после
перекристаллизации из этанола)
FAB-MC (m/z): 386 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,64 (3Н, с); 3,69 (3Н, с); 6,75 (1Н, дд, I= 4,8, 7,6 Гц);
6,88 (1Н, т, I=7,6 Гц); 6,93 (1Н, д, I=8,8 Гц); 7,10 (1Н, д, I= 2,0 Гц); 7,17-7,22 (3Н, м); 7,32 (1Н, д, I=7,6 Гц);
7,39 (2Н, д, I=8,0 Гц); 7,89 (1Н, шир. с); 8,00 (1Н, д, I=4,8 Гц); 9,48 (1Н, шир.
с).
Элементный анализ для C19H19N3O4S:
Вычислено: C 59,21; H 4,97; N 10,90
Найдено: C 59,22; H 4,91; N 10,63
П р
и м е р 23.
4-Гидрокси-N-[2-[(4-метоксифенил)ами- но]-3-пиридил]бензолсульфонамид
[химическая формула 61]

Целевое соединение получали способом, описанным в примере 14.
Т.пл. 214-216оС (после перекристаллизации из смеси этанола и воды).
FAB-MC (m/z): 372 ([M+H]+)
1Н-ЯМР (DCMO-d6) δ
(ppm): 3,71 (3Н, с); 6,63 (1Н, дд, I=7,6, 4,8 Гц); 6,80 (2Н, д, I= 8,8 Гц); 6,82 (2Н, д, I=8,
8 Гц); 7,16 (1Н, дд, I=7,6, 1,6 Гц); 7,35 (2Н, д, I=8,8 Гц); 7,51 (2Н, д, I=8,8 Гц); 7,75 (1Н, с); 7,90
(1Н, дд, I=4,8, 1,6 Гц); 9,41 (1Н, с); 10,42 (1Н, с).
Элементный анализ для
C18H17N3O4S:
Вычислено: C 58,21; H 4,61; N 11,31
Найдено: C 58,21; H 4,74; N 11,01
П р и м е р 24.
N-(2-анилино-3-пиридил)-4-хлоробен- золсульфонамид
[химическая формула 62]

Целевое соединение получали способом, описанным в примере 1.
Т.пл. 186-188оС (после
перекристаллизации из этанола)
FAB-MC (m/z): 360 ([M+H]+)
1H-ЯMР (DMCO-d6) δ (ppm): 6,77 (1Н, дд, I=7,6, 4,8 Гц); 6,90 (1Н, дт, I= 7,6, 0,8
Гц); 7,22 (2Н, т, I=7,6 Гц); 7,30 (1Н, дд, I=7,6, 1,2 Гц); 7,38 (2Н, дд, I= 7,6, 0,8 Гц); 7,51
(2Н, д, I=8,4 Гц); 7,64 (2Н, д, I=8,4 Гц); 7,89 (1Н, с); 8,02 (1Н, дд, I=4,8, 1,2 Гц); 9,76 (1Н, шир.
с).
Элементный анализ для C17H14ClN3O2
S:
Вычислено: C 56,74; H 3,92; N 11,68
Найдено: C 56,79; H 4,03; N 11,67
П р и м е р 25.
N-(2-анилино-3-пиридил)-3-хлоробен- золсульфонамид
[химическая формула 63]

Целевое соединение получали способом, описанным в примере 1.
Т.пл. 143-144оС (после перекристаллизации из этанола)
FAB-MC
(m/z): 360 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 6,77 (1Н, дд,
I=7,6, 4,8 Гц); 6,91 (1Н, дт, I= 7,6, 1,2 Гц); 7,21 (2Н, т, I=7,6 Гц); 7,32 (1Н, дд, I=7,6,
1,6 Гц); 7,41 (2Н, дд, I= 7,6, 1,2 Гц); 7,46 (1Н, т, I=8,0 Гц); 7,54-7,61 (2Н, м); 7,68 (1Н, шир. с); 7,92
(1Н, шир. с); 8,04 (1Н, дд, I=4,8, 1,6 Гц); 9,80 (1Н, шир. с).
Элементный
анализ для C17H14ClN3O2S:
Вычислено: C 56,74; H 3,92; N
11,68
Найдено: C 56,73; H 4,09; S 11,68
П р и м е р 26.
N-(2-анилино-3-пиридил)-3-метилбензолсульфонамид
[химическая формула 64]

Целевое соединение получали способом, описанным в примере 1.
Т.пл. 161-162оС
(после перекристаллизации из этанола)
FAB-MC (m/z): 340 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 2,22 (3Н, с); 6,74 (1Н, дд, I=7,6, 4,8 Гц); 6,90 (1Н,
дт, I= 7,2, 1,2 Гц); 7,21 (2Н, т, I=7,2 Гц); 7,27-7,35 (3Н, м); 7,42 (2Н, дд, I=7,2, 1,2 Гц); 7,
45 (1Н, тд, I=7,2, 2,0 Гц); 7,52 (1Н, шир. с); 7,92 (1Н, с); 8,00 (1Н, дд, I=4,8, 1,2 Гц); 9,68 (1Н,
шир. с).
Элементный анализ для C18H17N3O2S:
Вычислено: C 63,70; H 5,05; N 12,38
Найдено: C 63,81; H 5,16; N 12,43
П р и м е р 27.
N-(2-анилино-3-пиридил)-4-этоксибензолсульфонамид
[химическая формула 65]

Целевое соединение получали способом, описанным в примере 1.
Т.пл. 161-162оC (после перекристаллизации из этанола)
FAB-MC
(m/z): 370 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 1,26 (3Н, т,
I=7,0 Гц); 3,94 (2Н, кв. I=7,0 Гц); 6,74 (1Н, дд, I=7,6, 4,8 Гц); 6,89 (1Н, тт, I=7,2, 0,8
Гц); 6,92 (2Н, д, I= 8,8 Гц); 7,21 (2Н, т, I=7,2 Гц); 7,27 (1Н, дд, I=7,6, 1,6 Гц); 7,42 (2Н, дд, I=7,2, 0,8
Гц); 7,57 (2Н, д, I=8,8 Гц); 7,88 (1Н, с); 7,99 (1Н, дд, I=4,8, 1,6 Гц); 9,53 (1Н, шир.
с).
Элементный анализ для C19H19N3O3S:
Вычислено: C 61,77; H 5,18; N 11,37
Найдено: C 61,72; H 5,31; N 11,43
П р
и м е р 28.
4-Ацетиламино-N-(2-анилино-3-пири- дил)бензолсульфонамид
[химическая
формула 66]

Целевое соединение получали способом, описанным в примере 1.
Т.пл. 234-236оС (после перекристаллизации из метанола)
FAB-MC
(m/z): 383 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 2,04 (3Н, с); 6,72 (1Н,
дд, I=7,6, 4,8 Гц); 6,90 (1Н, тт, I=8,0, 1,2 Гц); 7,19-7,24 (3Н, м); 7,45 (2Н, дд,
I=8,0, 1,2 Гц); 7,60 (2Н, д, I=9,2 Гц); 7,65 (2Н, д, I=9,2 Гц); 7,91 (1Н, с); 7,98 (1Н, дд, I=4,8, 1,6 Гц); 9,60 (1Н,
шир. с); 10,23 (1Н, шир. с).
Элементный анализ для C19
H18N4O3S:
Вычислено: C 59,67; H 4,74; N 14,65
Найдено: C 59,69; H
4,82; N 14,38
П р и м е р 29.
N-(2-анилино-3-пиридил)-4-феноксибе- нзолсульфонамид
[химическая формула 67]

Целевое соединение получали способом, описанным в примере 1.
Т.пл. 164-166оС (после перекристаллизации из
этанола)
FAB-MC (m/z): 418 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 6,78 (1Н, дд, I=7,6, 4,8 Гц); 6,84 (2Н, дд, I= 7,6, 1,2 Гц); 6,91-6,96 (3Н, м);
7,19-7,27 (3Н, м); 7,36-7,40 (3Н, м); 7,44 (2Н, дд, I=7,6, 1,2 Гц); 7,
62 (2Н, д, I=9,2 Гц); 7,85 (1Н, с); 8,02 (1Н, дд, I=4,8, 1,6 Гц); 9,62 (1Н, шир. с).
Элементный анализ для C23H19N3O3S:
Вычислено:
C 66,17; H 4,59; N 10,06
Найдено: C 66,15; H 4,68; N 10,04
П р и м е р 30.
N-(2-анилино-3-пиридил)-4-цианобен-золсульфонамид
[химическая формула 68]

Целевое соединение получали способом, описанным в примере 1.
Т.пл. 155-157оС (после перекристаллизации из метанола)
FAB-MC (m/z): 351 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 6,80 (1Н, дд, I=7,6, 4,8 Гц); 6,90 (1Н, т,
I= 7,6 Гц); 7,20 (2Н, т, I=7,6 Гц); 7,31 (2Н, д, I=7,6 Гц); 7,36 (1Н, дд, I= 7,6, 1,6 Гц); 7,76 (2Н, д,
I=7,6 Гц); 7,86-7.89 (3Н, м); 8,05 (1Н, шир.); 9,90 (1Н, шир. с).
Элементный
анализ для C18H14N4O2S:
Вычислено: C 61,70; H 4,03;
N 15,99
Найдено: C 61,73; H 4,14; N 15,75
П р и м е р 31.
N-(2-анилино-3-пиридил)-2,4-диметок-сибензолсульфонамид
[химическая формула 69]

Целевое соединение получали способом, описанным в примере 1.
Т.пл. 176-178оС
(после перекристаллизации из этанола)
FAB-MC (m/z): 386 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,76 (3Н, с); 3,81 (3Н, с); 6,53 (1Н, дд, I= 8,8, 2,4 Гц); 6,
59 (1Н, д, I=2,4 Гц); 6,69 (1Н, дд, I=7,6, 4,8 Гц); 6,92 (1Н, т, I= 7,6 Гц); 7,25 (2Н, т, I=7,6
Гц); 7,33 (1Н, дд, I=7,6, 1,6 Гц); 7,50 (2Н, д, I= 7,6 Гц); 7,55 (1Н, д, I=8,8 Гц); 7,92 (1Н, дд, I=4,8,
1,6 Гц); 8,07 (1Н, с).
Элементный анализ для C19H19N3O4S:
Вычислено: C59,21; H 4,97; N 10,90
Найдено: C 59,19; H 5,04;
N 10,91
П р и м е р 32.
N-(2-анилино-3-пиридил)-2-хлоробен- золсульфонамид
[химическая формула 70]
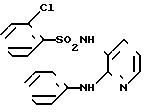
Целевое соединение получали способом, описанным в примере 1.
Т.пл. 140-141оС (после перекристаллизации из
толуола)
FAB-MC (m/z): 360 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 6,72 (1Н, дд, I=7,6, 4,8 Гц); 6,93 (1Н, т, I= 7,6 Гц); 7,25 (2Н, т, I=7,6 Гц); 7,
31 (1Н, дд, I=7,6, 1,6 Гц); 7,42-7,46 (1Н, м); 7,49 (2Н, д, I=7,6 Гц);
7,56-7,59 (2Н, м); 7,87 (1Н, д, I=7,6 Гц); 7,95-8,01 (2Н, м); 10,14 (1Н, шир. с).
Элементный анализ для C17H14ClN3O2S:
Вычислено:
C 56,74; H 3,92; N 11,68
Найдено: C 56,86; H 4,06; N 11,62
П р и м е р 23.
4-Ацетил-N-(2-анилино-3-пиридил)бен-золсульфонамид
[химическая формула 71]

Целевое соединение получали способом, описанным в примере 1.
Т.пл. 171-173оС (после перекристаллизации из этанола)
FAB-MC (m/z): 368 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 2,46 (3Н, с); 6,78 (1Н, дд, I=7,6, 4,8 Гц);
6,85 (1Н, т, I= 7,6 Гц); 7,15 (2Н, т. I=7,6 Гц); 7,31 (2Н, дд, I=7,6, 1,2 Гц); 7,35 (1Н, дд, I=7,6, 1,6
Гц); 7,74 (2Н, д, I=8,4 Гц); 7,85 (1Н, с); 7,94 (2Н, д, I=8.4 Гц); 9,03 (1Н, дд, I=4,8, 1,6 Гц);
9,83 (1Н, шир. с).
Элементный анализ для C19H17N3
O3S:
Вычислено: C 62,11; H 4,66; N 11,44
Найдено: C 62,31; H 4,78; N 11,
19
П р и м е р 34.
N-[2-[(3-гидроксифенил)амино]-3-пири-дил]-4-метоксибензолсульфонамид
[химическая формула 72]

4,0 г (19,9 мМ) соединения, полученного в примере получения 6, подвергали взаимодействию с 4,11 г (19,9 мМ) п-метоксибензолсульфонилхлорида, после чего продукт обрабатывали способом, описанным в примере 1, в результате чего получали 5,0 г целевого соединения.
Т.пл. 181-182оС (после перекристаллизации из толуола)
FAB-MC
(m/z): 372 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,72 (2Н, с); 6,31 (1Н, дд, I=8,0, 2,0 Гц); 6,72 (1Н, дд, I= 7,6, 4,8 Гц); 6,79 (1Н, д, I=8,0 Гц); 6,96
(2Н, д, I=8,8 Гц); 6,98
(1Н, т, I=8,0 Гц); 7,02 (1Н, т, I=2,0 Гц); 7,25 (1Н, дд, I=7,6, 1,6 Гц); 7,59 (2Н, д, I=8,8 Гц); 7,77 (1Н, с); 7,99 (1Н, дд, I=4,8, 1,6 Гц); 9,18 (1Н, с); 9,56 (1Н, шир. с).
Элементный анализ для C18H17N3OL3S:
Вычислено: C 58,21; H 4,61; N 11,31
Найдено: C 58,26; H 4,67; N 10,99
П р и м е
р 35.
N-[2-[(4-этоксифенил)амино]-3-пиридил] 4-метоксибензолсульфонамид
[химическая формула 73]
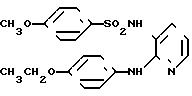
Целевое соединение получали способом, описанным в примере 1.
Т.пл. 144-146оС (после перекристаллизации из этанола)
FAB-MC
(m/z): 400 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 1,31 (3Н, т, I=2,8 Гц); 3,73 (3Н, с); 3,97 (2Н, кв. I=2,8 Гц); 6,65 (1Н, дд, I=4,8, 7,6 Гц); 6,80 (2Н, д,
I=8,8 Гц); 6,98 (2Н,
д, I= 8,8 Гц); 7,21 (2Н, дд, I=1,6, 7,6 Гц); 7,28 (2Н, д, I=8,8 Гц); 7,60 (2Н, д, I=8,8 Гц); 7,72 (1Н, шир. с); 7,92 (1Н, дд, I=1,6, 4,8 Гц); 9,47 (1Н, шир. с).
Элементный анализ для
C20H21N3O4S:
Вычислено: C 60,13; H 5,30; N 10,52
Найдено: C 60,02; H 5,27; N 10,21
П р и м е р 36.
N-[2-[(4-гидрокси-3-метилфенил)амино]-3-пиридил]-4-метоксибензолсульфонамид
[химическая формула 74]

Целевое соединение получали способом, описанным в примере 1.
Т.пл. 89-91оС (после перекристаллизации из толуола)
FAB-MC (m/z): 386 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 2,07 (3Н, с); 3,75 (3Н, с); 6,60 (1Н, дд, I= 4,8, 7,6 Гц); 6,63 (1Н, д, I=8,4 Гц); 6,93 (1Н, д, I=2,8 Гц); 6,98-7,03 (3Н, м); 7,
18 (1Н, дд, I=1,6, 7,6 Гц); 7,50 (1Н, шир. с); 7,60 (2Н, д, I=8,8 Гц); 7,88 (1Н, дд, I=1,6, 4,8 Гц); 8,87 (1Н, с); 9,44 (1Н, шир. с).
Элементный анализ для C19H19
N3O4S:
Вычислено: C 59,21; H 4,97; N 10,90
Найдено: C 58,97; H 5,06; N 10,53
П р и м е р 37.
Этил-4-[[3-(4-метоксибензолсульфона-мидо)-2-пиридил]амино]-бензоат
[химическая формула 75]

Целевое соединение получали способом, описанным в примере 1.
Т.пл. 172-173оС (после перекристаллизации из этанола)
FAB-MC (m/z): 428 ([M+H]+
)
1Н-ЯМР (DMCO-d6) δ (ppm): 1,31 (3Н, т, I=3,2 Гц); 3,63 (3Н, с); 4,27 (2Н, кв. I=3,2 Гц); 6,88 (2Н, д, I=8,8 Гц); 6,88 (1Н, дд, I=4,8, 7,6 Гц); 7,38 (1Н, дд, I= 1,
6, 7,
6 Гц); 7,51 (2Н, д, I=8,8 Гц); 7,54 (2Н, д, I=8,8 Гц); 7,80 (2Н, д, I=8,8 Гц); 8,10 (1Н, дд, I=1,6, 4,8 Гц); 8,34 (1Н, шир. с); 9,58 (1Н, шир. с).
Элементный анализ для C21
H21N3O3S:
Вычислено: C 59,00; H 4,95; N 9,83
Найдено: C 59,98; H 4,91; N 9,63
П р и м е р 38.
4-Метокси-N-[2-[(4-метилтиофенил)ами- но]-3-пиридил]-бензолсульфонамид
[химическая формула 76]

Целевое соединение получали способом, аналогичным описанному в примере 1.
Т.пл. 148-149оС (после перекристаллизации из этанола)
FAB-MC (m/z): 402
([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 2,43 (3Н, с); 3,70 (3Н, с); 6,73 (1Н, дд, I= 4,8, 7,6 Гц); 6,94 (2Н, д, I=8,8 Гц); 7,17 (2Н, д, I=8,8 Гц); 7,26 (1Н,
дд, I= 1,6, 7,6 Гц); 7,39 (2Н, д, I=8,8 Гц); 7,57 (2Н, д, I=8,8 Гц); 7,93 (1Н, шир. с); 7,98 (1Н, дд, I=1,6, 4,8 Гц); 9,51 (1Н, шир. с).
Элементный анализ для С19H19N3O3S:
Вычислено: C 56,84; H 4,77; N 10,47
Найдено: C 56,90; H 4,77; N 10,24
П р и м е р 39.
4-[[3-(4-Метоксибензолсульфонамидо)-2-пиридил]амино]фенилсульфат калия
[химическая формула 77]

2,0 г (5,38 мМ) соединения примера 6 растворяли в 20 мл пиридина. К раствору при -15 -10оС по капле добавляли 800 мг (6,87 мМ) хлоросульфоновой кислоты 95% Затем температуру медленно повышали до комнатной температуры и смесь размешивали в течение 3 дней. Для доведения рН до 8-9 к реакционной смеси добавляли 1н водный карбонат калия. Растворитель отгоняли при пониженном давлении. К остатку добавляли воду и этилацетат, и образовавшийся водный слой отделяли, концентрировали, очищали с помощью колоночной хроматографии на силикагеле, и осаждали метанолом/дихлорметаном, в результате чего получали 1,58 г целевого соединения.
Т.пл. 165-166оС
FAB-MC (m/z): 528 ([M+H]+)
1Н-ЯМР (DMCO-d6)
δ
(ppm): 3,73 (3Н, с); 6,68 (1Н, дд, I=4,8, 8,0 Гц); 6,98 (2Н, д, I=8,8 Гц); 7,02 (2Н, д, I=8,4 Гц); 7,25-7,27 (3Н, м); 7,61 (2Н, д, I=8,8 Гц); 7,83 (1Н, с); 7,94 (1Н, дд, I=1,2, 4,8 Гц); 9,55
(1Н,
с).
Элементный анализ для C18H16N3O7S2K x x3/2H2O:
Вычислено: C 41,85; H 3,71; N 8,13
Найдено: C 41,
88; H 3,41; N 8,08
П р и м е р 40.
4-Метокси-N-[2-[(4-феноксифенил)ами- но]-3-пиридил]бензол-сульфонамид
[химическая формула 78]

Целевое соединение получали способом, описанным в примере 1.
Т.пл. 174-176оС
(после
перекристаллизации из этанола)
FAB-MC (m/z): 448 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,75 (3Н, с), 6,72 (1Н, дд, I=4,8, 7,6 Гц), 6,92
(2Н, д,
I=8,8 Гц); 6,91-6,97 (2Н, м); 6,96 (2Н, д, I=8,8 Гц), 7,05-7,10 (1Н, м), 7,27 (1Н, дд, I=1,6, 7,6 Гц), 7,32-7,40 (2Н, м), 7,43 (2Н, д, I=8,8 Гц), 7,59 (2Н, д, I=8,8 Гц), 7,92 (1Н, шир. с), 7,
98 (1Н,
дд, I=1,6, 4,8 Гц), 9,44 (1Н, шир. с).
Элементный анализ для C24H21N3O4S:
Вычислено: C 64,41; H 4,73; N 9,39
Найдено: C
64,71; H 4,96; N 9,30
П р и м ер 41.
4-[[3-(4-Метоксибензолсульфонамидо)-2-пиридил]амино]бензойная кислота.
[химическая формула 79]

Целевое соединение получали путем щелочного гидролиза соединения примера 37, осуществляемого стандартным способом.
Т.пл. 238-250оС (после перекристаллизации из этанола)
FAB-MC (m/z): 400 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ
(ppm): 3,64 (3Н, с), 6,87 (1Н, дд, I=4,8, 7,6 Гц), 6,89 (2Н, д, I= 8,8 Гц), 7,37 (1Н, дд, I=1,6, 7,6 Гц), 7,49 (2Н, д, I=8,8 Гц), 7,54 (2Н, д, I=8,8 Гц), 7,78 (2Н, д, I=8,8 Гц), 8,09 (1Н, дд, I=1,6,
4,
8 Гц), 8,29 (1Н, шир. с), 9,58 (1Н, шир. с), 12,44 (1Н, шир.).
Элементный анализ для C19H17N3O5S:
Вычислено: C 57,13; H 4,29; N
10,
52
Найдено: C 57,10; H 4,42; N 10,35
П р и м е р 42.
N-[2-[(4-Хлорфенил)амино]-3-пиридил]-4-метоксибензолсульфонамид
[химическая формула 80]

Целевое соединение получали способом, описанным в примере 1.
Т.пл. 205-207оС
(разл.) (после перекристаллизации из этанола)
FAB-MC (m/z): 390 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,70 (3Н, с), 6,78 (1Н, дд, I=7,6,
4,8 Гц),
6,93 (2Н, д, I=8,8 Гц), 7,24 (2Н, д, I=8,8 Гц), 7,30 (1Н, дд, I=7,6, 20 Гц), 7,45 (2Н, д, I= 8,8 Гц), 7,56 (2Н, д, I=8,8 Гц), 8,02 (1Н, дд, I=4,8, 2,0 Гц), 8,05 (1Н, с), 9,51 (1Н, шир.
с).
Элементный анализ для C18H16ClN3O3S:
Вычислено: C 55,46; H 4,14; N 10,78
Найдено: C 55,44; H 4,32; N 10,71
П
р и м е
43.
N-[-2-[(2-гидроксифенил)амино]-3-пири- дил]-4-метоксибензолсульфонамид
[химическая формула 81]
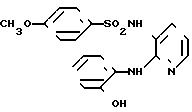
Целевое соединение получали способом, описанным в примере 1.
Т.пл. 154-155оС (после перекристаллизации из толуола)
FAB-MC
(m/z): 372 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,81 (3Н, с), 6,63 (1Н, дд, I=8,0, 5,2 Гц), 6,72-6,79 (2Н, м), 6,82-6,86 (2Н, м), 7,07 (2Н, д, I=8,8 Гц),
7,66 (2Н, д, I= 8,8 Гц), 8,05 (1Н, дд, I=5,2, 1,6 Гц), 8,15 (1Н, с), 8,29 (1Н, дд, I=7,6, 2,0 Гц), 9,70 (1Н, с), 9,94 (1Н, с).
Элементный анализ для С18H17N3O4S:
Вычислено: C 58,22, H 4,61, N 11,32
Найдено: C 58,39, H 4,60, N 11,20
П р и м е р 44.
N-(2-анилино-3-пиридил)-2,4,
6-триме- тилбензолсульфонамид
[химическая формула 82]

Целевое соединение получали способом, описанным в примере 1.
Т.пл. 140-142оС (после перекристаллизации из этанола)
FAB-MC (m/z): 368 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 2,16 (3Н, с), 2,41 (6Н, с), 6,70 (1Н, дд, I= 7,6, 4,8 Гц), 6,89-6,94 (3Н, м), 7,08 (1Н, дд, I=7,6, 1,6 Гц), 7,24 (2Н, т, I= 7,6 Гц), 7,43 (2Н, д, I=7,6 Гц), 7,89 (1Н, с), 8,
01
(1Н дд, I=4,8, 1,6 Гц), 9,58 (1Н, с).
Элементный анализ для C20H21N3O2S:
Вычислено: C 65,37, H 5,76, N 11,43
Найдено:
C
65,45, H 5,67, N 11,34
П р и м е р 45.
N-(2-анилино-3-пиридил)-4хлоро-2,5-ди- метилбензолсульфонамид
[химическая формула 83]
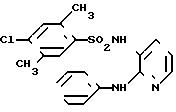
Целевое соединение получали способом, описанным в примере 1.
Т.пл. 153-154оС (после
перекристаллизации из
этанола)
FAB-MC (m/z): 388 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 2,20 (3Н, с), 2,41 (3Н, с), 6,75 (1Н, дд, I= 7,6, 4,8 Гц),
6,91 (1Н, т, I=7,6 Гц),
7,23 (2Н, т, I=7,6 Гц), 7,26 (1Н, дд, I= 7,6, 1,6 Гц), 7,33 (1Н, с), 7,38 (2Н, д, I=7,6 Гц), 7,63 (1Н, с), 7,93 (1Н, с), 8,02 (1Н, дд, I=4,8, 1,6 Гц), 9,76 (1Н, с).
Элементный анализ
для C19H18 ClN3O2S:
Вычислено: C 58,83, H 4,68, N 10,83
Найдено: C 58,97, H 4,64, N 10,85
П р и м е
р 46.
4-Метокси-N-[2-[(2-метокси-5-пиридил)амино]-3-пиридил] бензолсульфонамид
[химическая формула 84]
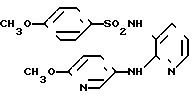
Целевое соединение получали способом, описанным в примере 1.
Т.пл. 159-160оС (после перекристаллизации из этанола)
FAB-MC
(m/z): 387 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,73 (3Н, с), 3,81 (3Н, с), 6,68-6,73 (2Н, м), 6,98 (2Н, д, I= 8,8 Гц), 7,25 (1Н, дд, I=7,6, 1,2 Гц), 7,
60 (2Н, д, I=8,8 Гц), 7,
72 (1Н, дд, I=8,8 Гц), 7,90 (1Н, с), 7,93 (1Н, дд, I=4,8, 1,2 Гц), 8,13 (1Н, д, I=2,8 Гц), 9,44 (1Н, шир. с).
Элементный анализ для C18H18N4O4S:
Вычислено: C 55,95; H 4,69; N 14,50
Найдено: C 55,95, H 4,72, N 14,46
П р и м е р 47.
N-(4-анилино-6-метокси-5-пиримидил)-4-метоксибензолсульфонамид
[химическая формула 85]
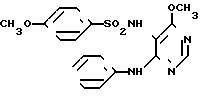
Целевое соединение получали способом, описанным в примере 1.
Т.пл. 159-160оС (после перекристаллизации из этанола)
FAB-MC (m/z): 387 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,38 (3Н, с), 3,80 (3Н, с), 7,01-7,07 (3Н, м), 7,30 (2Н, т, I=8,0 Гц), 7,57 (2Н, дд, I=8,0, 0,8 Гц), 7,6 (2Н, д, I=8,8 Гц), 8,20 (1Н, с); 8,
33 (1Н, с); 9,29 (1Н, с).
Элементный анализ для C18H18N4O4S:
Вычислено: C 55,95, H 4,70, N 14,50
Найдено: C 55,90, H 4,
71,
N 14,49
П р и м е р 48.
N-(4-анилино-6-хлоро-5-пиримидил)-4-метоксибензолсульфонамид
[химическая формула 86]
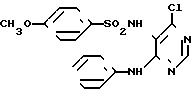
Целевое соединение получали способом, описанным в примере 1.
Т.пл. 174-175оС (перекристаллизовано из этанола)
FAB-MC (m/z): 391 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,75 (3H, c); 7,03 (2Н, д, I=8,8 Гц); 7,09 (1Н, т, I=7,6 Гц); 7,32 (2Н, т, I=7,6 Гц); 7,46
(2Н, д, I=7,6 Гц); 7,65 (2Н, д, I=8,8 Гц); 8,29 (1Н, с); 8,63 (1Н, с); 9,74 (1Н, шир. с).
Элементный анализ для C17H15N4O3SCl:
Вычислено: C 52,24, H 3,87, N 14,33
Найдено: C 52,29, H 3,85, N 14,27
П р и м е р 49. N-(2-анилино-6-диметиламино-3-пири-дил)-4-метокси-бензолсульфонамид
[химическая
формула
87]
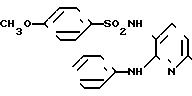

Целевое соединение получали способом, описанным в примере 1.
Т.пл.152-153oC (перекристаллизовано из смеси этилацетата и гексана)
FAB-MC (m/z): 399
([M+H]+)
1Н-ЯМР (CDCl3) δ (ppm): 3,04 (6Н, с); 3,83 (3Н, с); 5,71 (1Н, д, I=8,8 Гц); 5,75 (1Н, с); 6,59 (1Н, д, I=8,8 Гц); 6,91-6,96 (3Н, м); 7,24-7,28
(3Н, м); 7,
53 (2Н, д, I=7,6 Гц); 7,72 (2Н, д, I=9,2 Гц).
Элементный анализ для C20H22N4O3S:
Вычислено: C 60,28, H 5,56, N 14,
06
Найдено: C 60,21, H 5,47, N 13,92
П р и м е р 50.
N-(2-анилино-6-хлоро-3-пиридил)-4-метоксибензолсульфонамид
[химическая формула 88]


Целевое соединение получали способом, описанным в примере 1.
Т.пл. 206-208оС (перекристаллизовано из этанола)
FAB-MC (m/z): 390 ([M+H]+)
1Н-ЯМР
(DMCO-d6)
δ (ppm): 3,71 (3H, c); 6,79 (1H, д I=8,0 Гц); 6,93-6,99 (3Н, м); 7,26 (3Н, т, I=8,0 Гц); 7,38 (2Н, д, I=8,0 Гц); 7,61 (2Н, д, I=9,2 Гц); 8,15 (1Н, с); 9,56 (1Н, с).
Элементный
анализ для C18H16ClN3O3S:
Вычислено: C 55,46, H 4,14, N 10,78
Найдено: C 55,49, H 4,04, N 10,62
П р и м е
р 51.
N-(4-анилино-3-пиридил)-4-метоксибен- золсульфонамид
[химическая формула 89]

Целевое соединение получали способом, аналогичным описанному в примере 1.
Т.пл. 201-202оС (перекристаллизовано из этанола)
FAB-MC (m/z): 356
([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,75 (3Н, с); 6,92 (1Н, д, I=6,4 Гц); 6,95 (2Н, д, I=8,8 Гц); 7,13-7,20 (3Н, м); 7,39 (2Н, т, I=8,0 Гц); 7,67 (2Н, д,
I=8,8 Гц); 7,78 (1Н, с); 7,
82 (1Н, д, I= 5,6 Гц).
Элементный анализ для C18H17N3O3S:
Вычислено: C 60,83, H 4,82, N 11,82
Найдено: C 60,78, H 4,77, N
11,84
П р и м е р 52.
N-[2-[(4-Диметилкарбамоилоксифенил)амино] -3-пиридил] -4 -метоксибензолсульфонамид
[химическая формула 90]

Целевое соединение получали способом, описанным в примере 1.
Т.пл. 202-203оС (перекристаллизовано
из этанола)
FAB-MC (m/z): 443 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 2,90 (3Н, с); 3,03 (3Н, с); 3,72 (3Н, с); 6,72
(1Н, дд, I= 7,6, 4,8 Гц); 6,96
(2Н, д, I=8,8 Гц); 6,97 (2Н, д, I=8,8 Гц); 7,26 (1Н, дд, I= 7,6, 1,6 Гц); 7,41 (2Н, д, I=8,8 Гц); 7,60 (2Н, д, I=8,8 Гц); 7,94 (1Н, с); 7,97 (1Н, дд, I=4,8, 1,6 Гц); 9,
52 (1Н, шир. с).
Элементный анализ для C21H22N4O5S:
Вычислено: C 57,00, H 5,01, N 12,66
Найдено: C 57,35, H 4,98, N 12,
55
П р и м е р 53.
N-(4-анилино-5-пиримидил)-4-метокси- бензолсульфонамид
[химическая формула 91)

Целевое соединение получали путем каталитического восстановления соединения примера 48 в присутствии палладированного угля стандартным способом.
Т.пл. 189-190оС
(перекристаллизовано из этанола)
FAB-MC (m/z): 357 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,73 (3Н, с); 7,01 (2Н, д,
I=8,8 Гц); 7,05 (1Н, т, I=8,0
Гц); 7,30 (2Н, т, I=8,0 Гц); 7,50 (2Н, д, I=6,0 Гц); 7,64 (2Н, д, I=8,8 Гц); 7,87 (1Н, с); 8,40 (1Н, с); 8,57 (1Н, шир. с).
Элементный анализ для C17H16N4O3S:
Вычислено: C 57,29, H 4,53, N 15,72
Найдено: C 57,25, H 4,68, N 15,36
П р и м е р 54.
N-(2-анилино-6-метокси-3-пиридил)-4-метоксибензолсульфонамид
[химическая формула 92]

Целевое соединение получали способом, описанным в примере 1.
Т.пл. 187-188оС
(перекристаллизовано из этанола)
FAB-MC (m/z): 386 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,70 (3Н, с); 3,77 (3Н, с); 6,11 (1Н, д, I=8,0 Гц); 6,89
(1Н, т, I=7,6 Гц); 6,95 (2Н, д, I=9,2 Гц); 7,07 (1Н, д, I=8,0 Гц); 7,22 (2Н, т, I=7,6 Гц); 7,43 (2Н, д, I=7,6 Гц); 7,52 (2Н, д, I=9,2 Гц); 7,83 (1Н, шир. с); 9,23 (1Н, шир. с).
Элементный анализ для C19H19N3O4S:
Вычислено: C 59, 21, H 4,97, N 10,90
Найдено: C 59,32, H 4,97, N 10,76
П р и м е р 55.
N-(4,5-дианилино-5-пиримидил)-4-ме- токсибензолсульфонамид
[химическая формула 93]

Целевое соединение получали способом, описанным в примере 1.
Т.пл. 149-151оС (перекристаллизовано из смеси дихлорметана и н-гексана)
FAB-MC (m/z): 448
([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,53 (3Н, с); 6,82 (2Н, д, I=8,8 Гц); 6,96 (2Н, т, I=7,6 Гц); 7,23 (4Н, т, I=7,6 Гц); 7,40 (4Н, д, I=7,6 Гц); 7,62
(2Н, д, I=8,8 Гц); 8,05 (2Н, с); 8,11 (1Н, с); 8,90 (1Н, с).
Элементный анализ для C23H21N5O3S:
Вычислено: C 61,73, H 4,73, N 15,
05
Найдено: C 61,91, H 4,72, N 15,74
П р и м е р 56.
4-Метокси-N-[2-(метоксифенил)амино-3-пиридил]бензолсульфонамид
[химическая формула 94]

Целевое соединение получали способом, описанным в примере 1.
Т.пл. 80-81оС
(перекристаллизовано из диизопропилового эфира)
FAB-MC (m/z): 370 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,01 (3Н, с); 3,82 (3Н, с); 6,46-6,51 (2Н,
м); 6,78-6,84 (1Н, м); 7,04 (2Н, д, I=8,8 Гц; 7,11-7,17 (2Н, м); 7,17 (1Н, дд, I= 4,8, 8,0 Гц); 7,65 (1Н, дд, I=1,6, 8,0 Гц); 7,68 (2Н, д, I=8,8 Гц); 8,14 (1Н, дд, I=1,6, 4,8 Гц); 9,30 (1Н, шир.
с).
Элементный анализ C19H19N3O3S:
Вычислено: C 61,77, H 5,18, N 11,38
Найдено: С 61,85, H 5,28, N 11,36
П р и
м
е р 57.
4-Метокси-N-[2-[(2-пиримидил)амино]фенил]-бензолсульфонамид
[химическая формула 95]
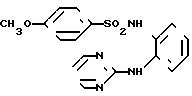
Целевое соединение получали способом, описанным в примере 1.
Т.пл. 193-195оС (перекристаллизовано из этанола)
FAB-MC (m/z):
357 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,70 (3Н, с); 6,79-6,83 (3Н, м); 6,96 (1Н, дт, I= 1,6, 8,4 Гц); 7,01 (1Н, дд, I=1,6, 8,4 Гц); 7,19 (1Н, дт, I=1,
6,
8,4 Гц); 7,47 (2Н, д, I=8,8 Гц); 7,87 (1Н, дд, I=1,6, 8,4 Гц); 8,38 (2Н, дд, I=1,6, 4,8 Гц); 8,54 (1Н, шир. с); 9,53 (1H, шир.c).
Элементный анализ для C17H16
N4O3S:
Вычислено: C 57,29, H 4,53, N 15,72
Найдено: C 57,18, H 4,57, N 15,80
П р и м е р 58.
N-(2-анилинофенил)-4-метоксибензол-сульфонамид
[химическая формула 96]

Целевое соединение получали способом, описанным в примере 1.
Т.пл. 140-142оС (перекристаллизовано из этанола)
FAB-MC (m/z): 345 (M+)
1Н-ЯМР
(DMCO-d6) δ (ppm): 3,69 (3Н, с); 6,66-6,72 (2Н, м); 6,81 (2Н, д, I= 8,8 Гц); 6,76-6,87 (2Н, м); 7,04-7,17 (5Н, м); 7,24 (1Н, шир. с); 7,52 (2Н, д, I=8,8 Гц); 9,30 (1Н, шир. с).
Элементный анализ для C19H18N2O3S:
Вычислено: C 64,39, H 5,12, N 7,90
Найдено: C 64,49, H 5,17, N 7,77
П р и м е р
59.
N-[2-[(4-Безоилоксифенил)амино]-3-пи- ридил]-4-метоксибензолсульфонамид
[химическая формула 97]

Целевое соединение получали способом, описанным в примере 1.
Т.пл. 208-210оС (перекристаллизовано из метанола)
FAB-MC
(m/z): 476 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,73 (3Н, с); 6,75 (1Н, д, I=4,8, 7,6 Гц); 6,98 (2Н, д, I= 8,8 Гц); 7,13 (2Н, д, I=8,8 Гц); 7,28 (1Н, дд,
I=1,6, 7,6 Гц); 7,51 (2Н, д, I= 8,8 Гц); 7,61 (2Н, д, I=8,8 Гц); 7,58-7,65 (2Н, м); 7,72-7,78 (1Н, м); 8,00 (1Н, дд, I= 1,6, 4,8 Гц); 8,04 (1Н, шир. с); 8,11-8,16 (2Н, м); 9,54 (1Н, шир. с).
Элементный анализ для C25H21N3O5S:
Вычислено: C 63,15, H 4,45, N 8,84
Найдено: C 62,95, H 4,57, N 8,76
П р и м е р 60.
N-[2-[[4-(трет-бутоксикарбониламино-ацетилокси)фенил]-амино]-3-пиридил] 4-метоксибензолсульфонамид
[химическая формула 98]
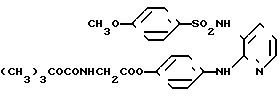
Целевое соединение получали способом, описанным в примере 1.
1Н-ЯМР (CDCl3) δ (ppm): 1,47 (9Н, с); 3,82 (3Н, с); 4, 18 (2Н, д, I=5,6 Гц); 5,17 (1Н, шир. с); 6,58 (2Н, дд, I=7,6, 4,8 Гц); 6,89 (1Н, дд, I=7,6, 1,6 Гц); 6,90 (2Н, д, I=8,8 Гц); 7,00 (2Н, д, I=8,8 Гц); 7,35 (1Н, шир. с); 7,47 (2Н, д, I= 8,8 Гц); 7,68 (2Н, д, I=8,8 Гц); 8,10 (1Н, дд, I=4,8, 1,6 Гц).
П р и м е р 61
N-[2-[[4-(аминоацетилокси)фенил] ами-но] -3-пиридил] -4- метоксибензолсульфонамида дигидрохлорид
[химическая формула 99]

272 мг (0,515 мМ) соединения примера 60 добавляли к 10 мл тетрагидрофурана. К смеси добавляли 2 мл конц. соляной кислоты и размешивали 3 часа при комнатной температуре. Растворитель отгоняли при комнатной температуре. Растворитель отгоняли при пониженном давлении, а остаток перекристаллизовывали из этанола и получали в результате 159 г целевого соединения.
Т.пл. 196-199оС (разл.)
FAB-MC (m/z): 429 ([M+H]+
)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,71 (3Н, с); 4,08-4,11 (2Н, м); 6,78 (1Н, дд, I= 4,8, 7,6 Гц); 6,94 (2Н, д, I=8,8 Гц); 7,04 (2Н, д, I=8,8 Гц); 7,32 (1Н, дд,
I=1,6, 7,
6 Гц); 7,48-7,51 (2Н, м); 7,61 (2Н, д, I=8,8 Гц); 7,97 (1Н, дд, I=1,6, 4,8 Гц); 8,48 (3Н, шир. с); 9,84 (1Н, шир. с).
Элементный анализ для C20H20N4
O5S x x2HCl·1/2H2O:
Вычислено: C 47,07, H 4,54, N 10,98
Найдено: C 47,38, H 4,45, N 10,78
П р и м е р 62.
4-Метокси-N-[2-[(4-метоксифенил)ами-но]-3-пиридил]-N-метилбензолсульфона- мид
[химическая формула 100]

500 мг (1,3 мМ) соединения примера 4 растворяли в 5 мл диметилформамида. К раствору добавляли 60 мг (1,5 мМ) гидрида натрия (60%). Полученный раствор размешивали при комнатной температуре в течение 30 минут, а затем к раствору добавляли метилиодид.
После размешивания в течение ночи, растворитель отгоняли при пониженном давлении. Остаток растворяли в этилацетате, и раствор промывали водой. После осушки сульфатом магния, концентрировании и очистки с помощью колоночной хроматографии на силикагеле, получали 290 мг целевого соединения.
FAB-MC (m/z): 400 ([M+H]+)
1Н-ЯМР (СDCl3) δ (ppm): 3,15 (3Н, с); 3,80 (3Н, с); 3,88 (3Н, с); 6,50 (1Н, дд, I= 4,8, 7,6 Гц);
6,67 (1Н, дд, I=1,6, 7,6 Гц); 6,89 (2Н, д, I=8,8 Гц); 6,98 (2Н, д, I=8,8 Гц); 7,29 (1Н, шир. с); 7,47 (2Н, д, I=8,8 Гц); 7,65 (2Н, д, I=8,8 Гц); 8,09 (1Н, дд, I=1,6, 4,8 Гц).
Элементный анализ для C20H21N3O4S:
Вычислено: C 60,14, H 5,30, N 10,52
Найдено: C 60,08, H 5,39, N 10,29
П р и м е р 63.
N-[2-[[4-(2-аминобензилокси)фенил] ами- но] -3-пиридил] -4 -метоксибензолсульфонамид
[химическая формула 101]

500 мг (1,35 мМ) соединения примера 6; 260 мг (1,59 мМ) ангидрида изатоевой кислоты; и 170 мг (1,39 мМ) 4-диметиламинопиридина растворяли в 5 мл диметилформамида, и полученный раствор размешивали при 80оС в течение 5 часов. Растворитель отгоняли при пониженном давлении и к остатку добавляли этилацетат. Образовавшийся таким образом осадок перекристаллизовывали из этанола и получали 500 мг целевого соединения.
Т.пл. 221-225оС (разл.)
FAB-MC (m/z): 491 ([M+H]+)
1
Н-ЯМР (DMCO-d6) δ (ppm): 3,74 (3H, с); 6,60 (1Н, тд, I=1,6, 8,4 Гц); 6,73 (2Н, шир. с); 6,74 (1Н, дд, I=4,8, 8,0 Гц); 6,83 (1Н, дд, I=0,8, 8,4 Гц); 6,98 (2Н, д, I=8,8 Гц); 7,08 (2Н,
д, I=9,2 Гц); 7,27 (1Н, дд, I=2,0, 8,0 Гц); 7,33 (1Н, тд, I=1,6, 7,2 Гц); 7,49 (1Н, д, I=9,2 Гц); 7,61 (2Н, д, I= 8,8 Гц); 7,92 (1Н, дд, I=1,6, 8,4 Гц); 7,99 (1Н, дд, I=2,0, 4,8 Гц); 8,02 (1Н, с); 9,
60 (1Н, шир. с).
Элементный анализ для C25H22N4O5S:
Вычислено: C 61,21, H 4,52, N 11,42
Найдено: C 60,98, H 4,52, N 11,
24
П р и м е р 64.
4-[[3-(4-Метоксибензолсульфонамидо)-2-пиридил] амино] фенил (первичный кислый фосфат)
[химическая формула 102]

7,44 г (20 мМ) соединения примера 6 суспендировали в 100 мл оксихлорида фосфора, и полученную суспензию нагревали в сосуде с обратным холодильником, в результате чего получали гомогенный раствор. Оксихлорид фосфора отгоняли при пониженном давлении, к остатку добавляли диизопропиловый эфир, а образовавшееся твердое вещество удаляли фильтрацией и суспендировали в 100 мл тетрагидрофуране. К суспензии добавляли, охлаждая при этом льдом, 50 мл воды и размешивали до тех пора пока не получали гомогенный раствор. Затем растворитель отгоняли при пониженном давлении, к остатку добавляли 100 мл метанола и 100 мл воды, и полученный раствор концентрировали при пониженном давлении до тех пор, пока не образовывалось нерастворимое вещество. Это вещество удаляли, а остаток опять концентрировали при пониженном давлении, полученный осадок отделяли путем фильтрации и получали 4,27 г целевого соединения.
Т.пл. 215-216оС
FAB-MC (m/z): 452 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,73 (3Н, с); 6,70 (1Н, дд, I=7,6, 4,8 Гц); 6,98 (2Н,
д, I= 8,8 Гц); 7,02 (2Н, д, I=8,8 Гц); 7,24 (1Н, дд, I=7,6, 1,6 Гц); 7,35 (2Н, д, I=8,8 Гц); 7,60 (2H, д, l=8,8 Гц); 7,88 (1Н, с); 7,95 (1Н, дд, I=4,8, 1,6 Гц); 9,50 (1Н, шир. с).
Элементный анализ для C18H18N3O7PS:
Вычислено: C 47,90, H 4,03, N 9,31
Найдено: C 47,72, H 4.00, N 9,39
П р и м е р 65.
3-[[3-(4-Метоксибензолсульфонамидо)-2-пиридин]амино]фенил монофосфат
[химическая формула 103]

120 мг целевого соединения получали путем реакции взаимодействия 1,00 г (2,7 мМ) соединения примера 34 с 10 мл оксихлорид фосфора, и полученный продукт обрабатывали способом, описанным в примере 64.
Т.пл. 166-168оС
FAB-MC (m/z): 452 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ
(ppm):
3,70 (3Н, с); 6,73 (1Н, д, I=7,6 Гц) 6,77 (1Н, дд, I= 7,6, 4,8 Гц); 6,95 (2Н, д, I=8,8 Гц); 7,15 (1Н, т, I=7,6 Гц); 7,21 (1Н, д, I=7,6 Гц); 7,30 (1Н, дд, I=7,6, 1,6 Гц); 7,37 (1Н, с); 7,59 (2Н,
д, I=8,
8 Гц); 8,01 (1Н, дд, I=4,8, 1,6 Гц); 8,10 (1Н, с); 9,61 (1Н, шир. с).
Элементный анализ для C18H18N3O7PS x xH2O:
Вычислено: C 46,06, H 4,29, N 8,95
Найдено: C 46,16, H 4,13, N 8,83
П р и м е р 66.
4-Метокси-N-[2-[[4-(4-метоксибензолсу- льфонилокси)фенил]-амино]-3-пиридил]
бензолсульфонамид
[химическая формула 104]

Соединение, полученное в примере получения 4, подвергали реакции взаимодействия с 4-метоксибензолсульфонилхлоридом в эквивалентном отношении 1:2, в результате чего получали целевое соединение.
Т.пл. 122-123оС (перекристаллизовано из этанола)
FAB-MC (m/z): 542 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,71 (3Н, с); 3,88 (3Н, с); 6,76 (1Н, дд, I= 7,6,
4,8 Гц); 6,84 (2Н, д, I=8,8 Гц); 6,94 (2Н, д, I=8,8 Гц); 7,17 (2Н, д, I= 8,8 Гц); 7,25 (1Н, дд, I=7,6, 1,2 Гц); 7,42 (2Н, д,
I=8,8 Гц); 7,56 (2Н, д, I= 8,8 Гц); 7,76 (2Н, д, I=8,8 Гц); 7,98 (1Н, дд,
I=4,8, 1,2 Гц); 8,06 (1Н, с); 9,51 (1Н, шир. с).
Элементный анализ для C25H23N3O7S3:
Вычислено: C 55,40, H 4,28, N 7,
76
Найдено: C 55,57, H 4,26, N 7,61
П р и м е р 67.
N-[2-[(4-гидроксифенил)амино]фенил]-4-метоксибензолсульфонамид
[химическая формула 105]
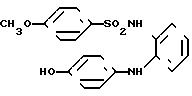
Целевое соединение получали способом, описанным в примере 1.
Т.пл. 163-164оС
(перекристаллизовано из этанола)
FAB-MC (m/z): 370 (M+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,76 (3Н, с); 6,58-6,67 (5Н, м); 6,77 (1Н, шир. с); 6,80 (1Н,
дд, I=1,6, 8,0 Гц); 6,90-7,00 (4Н, м); 7,56 (2Н, д, I=8,8 Гц); 9,05 (1Н, с); 9,23 (1Н,
шир. с).
Элементный анализ для C19H18N2O4S:
Вычислено: C 61,61, H 4,90, N 7,56
Найдено: C 61,86, H 4,90, N 7,39
П р и м е р 68.
4-Метокси-N-[2-[(4-пивалоилоксифенил) амино] -3-пиридил]-бензолсульфона-мид
[химическая формула 106]
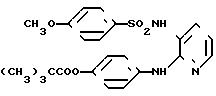
Целевое соединение получали способом, описанным в примере 1.
Т.пл. 188-189оС (перекристаллизовано из толуола)
FAB-MC (m/z): 456 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 1,30 (9Н,
с); 3,72 (3Н, с); 6,73 (1Н, дд, I= 7,6,4,8 Гц); 6,94 (2Н, д, I=8,8 Гц); 6,97 (2Н,
д, I=8,8 Гц); 7,25 (1Н, дд, I= 7,6, 1,6 Гц); 7,45 (2Н, д, I=8,8 Гц); 7,60 (2Н, д, I=8,8 Гц); 7,97-8,00 (2Н, м); 9,52
(1Н, шир. с).
Элементный анализ для C23H25
N3O5S:
Вычислено: C 60,64, H 5,53, N 9,22
Найдено: C 60,57, H 5,43, N 8,95
П р и м е р 69.
4-Метокси-N-[2-[(4-пиридил)амино]фе-нил]бензолсульфонамид
[химическая формула 107]
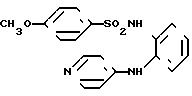
Целевое соединение получали способом, описанным в примере 1.
Т.пл. 185-187оС (перекристаллизовано из этанола)
FAB-MC (m/z):
356 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,67 (3Н, с); 6,45 (2Н, д, I=6,0 Гц); 6,73 (2Н, д, I= 8,8 Гц); 7,07 (1Н, дт, I=7,6, 1,2 Гц); 7,16 (1Н, дт, I=7,6,
1,2 Гц); 7,22 (1Н, дд, I=7,6, 1,2
Гц); 7,28 (1Н, дд, I=7,6, 1,2 Гц); 7,45 (2Н, д, I=8,8 Гц); 7,90 (1Н, шир. с); 8,05 (2Н, д, I=6,0 Гц).
Элементный анализ для C18H17N3O3
S:
Вычислено: C 60,83, H 4,82, N 11,82
Найдено: C 61,08, H 4,86, N 11,87
П р и м е р 70.
N-[2-(4-Метоксибензолсульфонамидо)фенил]-2-метилникотинамид
[химическая формула 108]

0,97 г (7 мМ) 2-метилникотиновой кислоты суспендировали в 4,5 мл дихлорметана. К раствору добавляли 1,33 г (16,8 мМ) пиридина, а затем 1,05 г (8,4 мМ) тионилхлорида. Полученную смесь размешивали при комнатной температуре в течение 30 мин, а затем к этой смеси добавляли раствор 1,77 г (6,36 мМ) соединения, полученного в примере получения 12, в 7 мл дихлорметана. Затем раствор размешивали в течение ночи, после чего к нему добавляли раствор бикарбоната натрия, и полученный продукт экстрагировали дихлорметаном. Раствор концентрировали, и к концентрату добавляли этанол, а образовавшиеся при этом кристаллы выделяли путем фильтрации и перекристаллизовывали из этанола, в результате чего получали 0,80 г целевого соединения.
Т.пл. 148-149оС
FAB-MC (m/z): 398
([M+H]+)
1
Н-ЯМР (DMCO-d6) δ (ppm): 2,56 (3Н, с); 3,80 (3Н, с); 7,02 (2Н, д, I=8,8 Гц); 7,08 (1Н, дд, I=2,0, 8,4 Гц); 7,11 (1H, дт, I=1,6, 4,4 Гц); 7,
18-7,27 (1Н, м); 7,37 (1Н, дд, I=4,8, 7,6
Гц); 7,57 (2Н, д, I=8,8 Гц); 7,71-7,84 (2Н, м); 8,58 (1Н, дд, I=1,6, 4,8 Гц); 9,37 (1Н, шир. с); 9,60 (1Н, шир. с).
Элементный анализ для
C20H19N3
O4S:
Вычислено: C 60,44, H 4,82, N 10,57
Найдено: C 60,37, H 4,90, N 10,41
П р и м е р 71.
N-[2-(4-метоксибензолсульфонамидо)
фенил]-4-метилникотинамид
[химическая формула 109]

Целевое соединение получали способом, описанным в примере 70.
Т.пл. 199-200оС (перекристаллизовано из метанола)
FAB-MC (m/z): 398 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 2,58 (3Н, с); 3,81 (3Н, с); 7,00-7,07 (3Н, м); 7,09-7,18 (1Н, м); 7,19-7,27 (1Н, м); 7,62 (2Н, д, I=8,4 Гц); 7,74-7,80 (1Н, м); 7,82 (1Н, д, I=5,6 Гц);
8,80 (1Н, д, I=5,6 Гц);
8,87 (1Н, с); 9,62 (1Н, шир. с); 10,16 (1Н, шир. с).
П р и м е р 72
N-[2-(4-Метоксибензолсульфонамидо)фенил]-3-метилизоникотинамид
[химическая формула 110]

Целевое соединение получали способом, описанным в примере 70
Т.пл. 194-195оС (перекристаллизовано из этанола)
FAB-MC (m/z): 398 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 2,36 (3Н, с); 3,81 (3Н, с); 7, 03 (2Н, д, I=8,8 Гц); 7,07 (1Н, дд, I=1,6, 8,0 Гц); 7,12 (1Н, дт, I=1,6, 8,0 Гц); 7,20-7,27 (1Н, м); 7,36 (1Н, д, I=4,8 Гц); 7,58 (2Н, д, I=8,8 Гц); 7,76-7,83 (1Н, м); 8,55-8,61 (2Н, м); 9,39 (1Н, шир. с); 9,65 (1Н, шир. с).
Элементный анализ для C20H19N3O4S:
Вычислено: C 60,44, H 4,82, N 10,57
Найдено: C 60,29, H 4,
83, N 10,49
П
р и м е р 73.
4-[[3-(4-Метоксибензолсульфонамидо)-2-пиридил] амино] фенил β-D-глюкопиранозид
[химическая формула 111]

637 г (0,908 мМ) соединения, полученного в примере получения 11, растворяли в смеси 7 мл 1 н гидроксида натрия и 20 мл этанола, и полученный раствор нагревали в колбе с обратным холодильником в течение 3 часов. После охлаждения к раствору добавляли 4 мл 1 н соляной кислоты, и полученную смесь концентрировали. К концентрату добавляли этилацетат и воду, и образованный таким образом слой этилацетата отделяли, осушали, концентрировали и очищали с помощью колоночной хроматографии на силикагеле, в результате чего получали 270 мг целевого соединения.
1Н-ЯМР (DMCO-d6+D2O) δ (ppm): 3,15-3,33 (4Н, м); 3,49 (1Н, дд, I=5,6, 11,6 Гц); 3,70-3,73 (4Н, с+дд); 4,75 (1Н, д, I=7,6 Гц); 6,68 (1Н, дд, I=4,8, 8,0 Гц); 6,93 (2Н, д, I=9,2 Гц); 6,97 (2Н, д, I=9,2 Гц); 7,23 (1Н, дд, I=2,0 7,6 Гц); 7,29 (2Н, д, I= 9,2 Гц); 7,60 (2Н, д, I=9,2 Гц); 7,95 (1Н, дд, I= 2,0, 4,8 Гц).
П р и м е р 74.
4-[[3-(4-Метоксибензолсульфонамидо)-2-пиридил] амино] фенил β-D-глюкопиранозид-уронат
[химическая формула
112]

Целевое соединение получали способом, аналогичным способу, описанному в примере получения 11 и в примере 73.
1Н-ЯМР (DMCO-d6+D2O) δ (ppm): 3,27 (1Н, т, I=8,8 Гц); 3,42 (1Н, т, I=8,8 Гц); 3,71 (3Н, с); 3,86 (1Н, д, I=9,6 Гц); 4,92 (1Н, д, I=7,6 Гц); 6,70 (1Н, дд, I= 5,2, 7,6 Гц); 6,90 (2Н, д, I=8,8 Гц); 6,96 (2Н, д, I=8,8 Гц); 7,25 (1Н, дд, I= 1,6, 7,6 Гц); 7,29 (2Н, д, I=8,8 Гц); 7,59 (2Н, д, I=8,8 Гц); 7,95 (1Н, дд, I=1, 6, 5,2 Гц).
П р и м е р 75.
4-Метокси-N-[2-[(3,4,5-триметоксифе- нил)амино] -3-пиридил]бензолсульфонамид
[химическая формула 113]

Целевое соединение получали способом, описанным в примере 1.
FAB-MC (m/z): 445 (M+)
1
Н-ЯМР (DMCO-d6) δ (ppm): 3,61 (3Н, с); 3,71 (3Н, с); 3,74 (6Н, с); 6,72 (1Н, дд, I=4,8, 7,6 Гц); 6,80 (2Н, с+с); 6,98 (2Н, д, I=8,8 Гц); 7,24 (1Н, дд,
I=1,6, 7,6 Гц); 7,59 (2Н, д,
I=8,8 Гц); 7,81 (1Н, шир. с); 8,00 (1Н, дд, I=1,6, 4,8 Гц); 9,47 (1Н, шир. с).
Элементный анализ для C21H23N3O6
S:
Вычислено: C 56,
62, H 5,20, N 9,43
Найдено: C 56,42, H 5,22, N 9,14
П р и м е р 76.
4-Метокси-N-[2-[(2-пиридил)амино]фенил]бензолсульфонамид
[химическая формула 114]

Целевое соединение получали способом, описанным в примере 1.
Т.пл. 113-116оС (перекристаллизовано из циклогексана).
FAB-MC (m/z): 356 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,70
(3Н, с); 6,53-6,59 (1Н, м);
6,70-6,75 (1Н, м); 6,71 (2Н, д, I=8,8 Гц); 6,95 (1Н, дт, I=1,2, 8,0 Гц); 7,11 (1Н, дд, I= 1,2, 8,0 Гц); 7,14 (1Н, дт, I=1,6, 8,0 Гц); 7,41-7,52 (3Н, м); 7,61-7,66 (1Н, м);
8,05 (1Н, дд, I=1,2, 4,8
Гц); 8,06 (1Н, шир. с); 9,59 (1Н, шир. с).
Элементный анализ для С18H17N3O3S:
Вычислено: C 60,83, H 4,82,
N 11,82
Найдено: C 61,11, H 4,82, N 11,85
П р и м е р 77.
N-(2-анилино-4-фторофенил)-4-метокси- бензолсульфонамид
[химическая формула 115]


Целевое соединение получали способом, описанным в примере 1.
Т.пл. 173-174оС (перекристаллизовано из этанола).
FAB-MC (m/z): 372 (M+)
1Н-ЯМР
(DMCO-d6)
δ (ppm): 3,69 (3Н, с); 6,57 (1Н, дт, I=2,8, 8,8 Гц); 6,73-6,91 (6Н, м); 7,00 (1Н, дд, I=6,4, 8,8 Гц); 7,19 (2Н, т, I=7,6 Гц); 7,37 (1Н, шир. с); 7,50 (2Н, д, I=8,8 Гц); 9,
33 (1Н, шир. с).
Элементный анализ для C19H17FN2O3S:
Вычислено: C 61,28, H 4,60, N 7,52
Найдено: C 61,39, H 4,62, N 7,
25
П р и м е
р 78.
N-[2-[(4-Хлорoфенил)амино]фенил]-4-ме- токсибензол сульфонамид
[химическая формула 116]
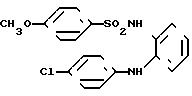
Целевое соединение получали способом, описанным в примере 1.
FAB-MC (m/z): 388 (M+)
Т.пл. 127-128оС
(перекристаллизовано из этанола)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,69 (3Н, с); 6,61 (2Н, д, I=8,8 Гц); 6,77 (2Н, д, I= 9,2 Гц); 6,88-6,94 (1Н, м); 7,07-7,14 (4Н,
м); 7,
18 (1Н, дд, I= 1,2, 8,0 Гц); 7,36 (1Н, шир. с); 7,47 (2Н, д, I=9,2 Гц); 9,28 (1Н, шир. с).
Элементный анализ для C19H17ClN2O3S:
Вычислено: С 58,68, Н 4,41, N 7,20
Найдено: C 58,85, H 4,39, N 7,04
П р и м е р 79.
N-[2-[(3-Гидроксифенил)амино]фенил]-4-метоксибензолсульфонамид
[химическая формула 117]

Целевое соединение получали способом, аналогичным описанному в примере 1.
Т.пл. 165-166оС (перекристаллизовано из этанола)
FAB-MC (m/z): 370 (M+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,71
(3Н, с); 6,12-6,17 (2Н, с); 6,19-6,24 (1Н, м); 6,79-6,86 (3Н, м); 6,91 (1Н, т, I=8,4 Гц); 7,07 (1Н, дт, I=1,2, 8,0 Гц); 7,08 (1Н, дд, I=1,2, 8,0 Гц); 7,13 (1Н, дд, I=1,2, 8,0 Гц); 7,14 (1Н, шир. с);
7,
52 (2Н, д, I=8,8 Гц); 9,16 (1Н, с), 9,28 (1Н, шир. с).
Элементный анализ для C19H18N2O4S:
Вычислено: C 61,61, H 4,90, N 7,56
Найдено: C 61,62, H 4,91, N 7,42
П р и м е р 80.
4-Бензилокси-N-[2-(4-метоксибензолсу- льфонамидо)фенил]-бензамид
[химическая формула 118]

Целевое соединение получали способом, описанным в примере 70.
Т.пл. 148-149оС
(перекристаллизовано из этанола)
FAB-MC (m/z): 489 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,74 (3Н, с); 5,23 (2Н, с); 6,89 (2Н, д, I=8,8 Гц); 7,07
(1Н, дд, I=2,0, 8,0 Гц); 7,10 (1Н, дт, I=1,2, 8,0 Гц); 7,17 (2Н, д, I=8,8 Гц); 7,23 (1Н, дт. I=2,0, 8,0 Гц); 7,33-7,39 (1Н, м); 7,42 (2Н, т, I= 7,6 Гц); 7,47-7,52 (4Н, м); 7,74 (1Н, дд, I=1,2, 8,0
Гц);
7,81 (2Н, д, I= 8,8 Гц); 9,44 (1Н, шир. с); 9,47 (1Н, шир. с).
Элементный анализ для C27H24N2O5S:
Вычислено: C 66,38, H 4,95,
N 5,
73
Найдено: C 66,34, H 4,92, N 5,73
П р и м е р 81.
4-Гидрокси-N-[2-(4-метоксибензолсуль- фонамидо)фенил]бензамид
[химическая формула 119]

Целевое соединение получали путем каталитического восстановления соединения, полученного в примере 80, в соответствии со стандартной процедурой.
Т.пл.205-207оС (перекристаллизовано из этилацетата)
FAB-MC (m/z): 399 ([M+H]+)
1Н-ЯМР
(DMCO-d6) δ (ppm): 3,76 (3Н, с); 6,89 (2Н, д, I=8,8 Гц); 6,91 (2Н, д, I= 8,8 Гц); 7,04 (1Н, дд, I=1,6, 8,0 Гц); 7,09 (1Н, дт, I=1,6, 8,0 Гц); 7,20-7,25 (1Н, м); 7,50 (2Н, д, I=8,8
Гц); 7,68-7,76 (3Н, м); 9,38 (1Н, с); 9,47 (1Н, с); 10,20 (1Н, с).
Элементный анализ для C20H18N2O5S:
Вычислено: C 60,29, H 4,55,
N 7,03
Найдено: C 60,38, H 4,58, N 6,75
П р и м е р 82.
4-Фторо-N-[2-(4-метоксибензолсульфо- намидо)фенил]бензамид
[химическая формула 120]

Целевое соединение получали способом, описанным в примере 70.
Т.пл. 169-170оС
(перекристаллизовано из этанола)
FAB-MC (m/z): 401 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,75 (3Н, с); 6,90 (2Н, д); 7,07-7,16 (2Н, м); 7,19-7,26
(1Н, м); 7,39 (2Н, т, I=8,8 Гц); 7,50 (2Н, д, I=8,8 Гц); 7,66-7,73 (1Н, м); 7,91 (2Н, дд, I=5,6, 8,8 Гц); 9,38 (1Н, шир. с); 9,54 (1Н, шир. с).
Элементный анализ для C20
H17FN2O4S:
Вычислено: C 59,99; H 4,28; N 7,00
Найдено: C 60,00; H 4,31; N 6,70
П р и м е р 83.
3-Гидрокси-N-[2-(4-метоксибензолсуль- фонамидо)фенил]бензамид
[химическая формула 121]
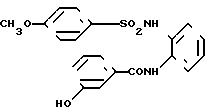
Целевое соединение получали способом, описанным в примере 81.
Т.пл.
191-192оС (перекристаллизовано из этанола)
FAB-MC (m/z): 399 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,77 (3Н, с); 6,92 (2Н, д, I=8,8 Гц); 6,99-7,06 (2Н, м); 7,09 (1Н, дм, I=1,6, 8,0 Гц); 7,20-7,27 (3Н, м); 7,34 (1Н, т, I= 8,0 Гц); 7,51 (2Н, т,
I=8,8 Гц); 7,75-7,81 (1Н, м); 9,46 (1Н, с); 9,51 (1Н, с); 9,81 (1Н, с).
Элементный анализ для C20H18N2O5S:
Вычислено: C 60,29; H
4,
55; N 7,03
Найдено: C 60,41; H 4,55; N 6,71
П р и м е р 84.
N-[2-(4-Метоксибензолсульфонамидо)фенил]-2-тиофенкарбоксамид).
[химическая формула
122]

Целевое соединение получали способом, описанным в примере 70.
Т. пл.
136-137оС (перекристаллизовано из этанола) FAB-MC (m/z): 389 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,75 (3Н, с); 6,85 (2Н, д, I=8,8 Гц); 7,05-7,
13 (2Н, м); 7,17-7,26 (2Н, м); 7,49 (2Н, д, I=8,8 Гц); 7,60-7,70 (1Н, м); 7,77 (1Н, дд, I=1,6, 4,0 Гц); 7,87 (1Н, дд, I=1,6, 5,2 Гц); 9,50 (2Н, шир. с).
Элементный анализ для C18H16N2O4S:
Вычислено: C 55,65; H 4,15; N 7,21
Найдено: C 55,80; H 4,27; N 7,24
П р и м е р 85.
N-[2-(4-Метоксибензолсульфонамидо)фенил]-2-фуранкарбоксамид
[химическая формула 123]

Целевое соединение получали способом, описанным в примере 70.
Т.пл. 158-159оС (перекристаллизовано из этанола)
FAB-MC (m/z): 373 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,76 (3Н, с); 6,73 (1Н, дд, I=1,6, 3,6 Гц); 6,91 (2Н, д, I=8,8 Гц); 6,98 (1Н, дд, I=8,0 Гц); 7,08 (1Н, дт, I=1,6, 8,0 Гц); 7,21 (1Н, дд, I=0,8, 3,6
Гц); 7,24 (1Н, дт, I=1,6, 8,0 Гц); 7,53 (2Н, д, I= 8,8 Гц); 7,84 (1Н, дд, I=1,6, 8,0 Гц); 7,99 (1Н, дд, I=0,8, 1,6 Гц); 9,42 (1Н, шир. с); 9,62 (1Н, шир. с).
Элементный анализ для
C18H16N2O5S:
Вычислено: С 58,05; H 4,33; N 7,52
Найдено: С 58,08; H 4,39; N 7,44
П р и м е р 86.
N-[2-(4-Метоксибензолсульфонамидо)фенил]-2-пиридинкарбоксамид
[химическая формула 124]

Целевое соединение получали способом, аналогичным описанному в примере 70.
Т.пл. 174-175оС (перекристаллизовано из этанола)
FAB-MC (m/z): 384 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,75 (3Н, с); 6,82 (1Н, дд, I=1,6, 8,0 Гц); 6,92 (2Н, д, I=8,8 Гц); 7,03 (1Н, дт, I=1,6, 8,0 Гц); 7,30 (1Н, дт, I=1,6, 8,0 Гц);
7,57 (2Н, д, I=8,8 Гц); 7,70 (1Н, тд, I=1,6, 4,8, 7,6 Гц); 8,08 (1Н, дт, I= 1,6, 7,6 Гц); 8,12-8,17 (1Н, м); 8,24 (1Н, дд, I=1,6, 7,6 Гц); 8,77 (1Н, дд, I=1,6, 4,8 Гц); 9,73 (1Н, шир. с); 10,67 (1Н,
шир. с).
Элементный анализ для C19H17N3O4S:
Вычислено: С 59,52; H 4,47; N 10,96
Найдено: C 59,73; H 4,54; N 10,92
П р и м е р 87.
N-[2-(4-Метоксибензолсульфонамидо)фенил]никотамид
[химическая формула 125]

Целевое соединение получали способом, описанным в примере 70.
Т.пл. 179-180оС (перекристаллизовано из этанола)
FAB-MC
(m/z): 384 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,74 (3Н, с); 6,89 (2Н, д, I=8,8 Гц); 7,12-7,19 (2Н, м); 7,19-7,27 (1Н, м); 7,51 (2Н, д, I=8,8 Гц); 7,59
(1Н, дд, I= 4,8, 8,0 Гц); 7,63-7,71 (1Н, м); 8,17 (1Н, дд, I=1,2, 8,0 Гц); 8,79 (1Н, дд, I=1,2, 4,8 Гц); 8,99 (1Н, д, I=1,2 Гц); 9,49 (1Н, шир. с); 9,68 (1Н, шир. с. ).
Элементный
анализ для C19H17N3O4S:
Вычислено: C 59,52; H 4,47; N 10,96
Найдено: C 59,61; H 4,57; N 10,84
П р и м е р 88.
N-[2-(4-Метоксибензолсульфонамидо)фенил]изоникотинамид
[химическая формула 126]

Целевое соединение получали способом, описанным в примере 70.
Т.пл. 162-163оС (перекристаллизовано из этанола)
FAB-MC (m/z): 384 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,75 (3Н, с); 6,90 (2Н, д, I=8,8 Гц); 7,11-7,27 (3Н, м); 7,53 (2Н, д, I=8,8 Гц); 7,64-7,71 (1Н, т); 7,75 (2Н, д, I=4,8 Гц); 8,81 (2Н, д, I=4,8 Гц); 9,
52 (1Н, шир. с); 9,73 (1Н, шир. с).
Элементный анализ для C19H17N3O4S:
Вычислено: C 59,52; H 4,47; N 10,96
Найдено: C 59,
59; H 4,52; N 10,96
П р и м е р 89.
4-Фторо-N-[2-(4-метоксибензолсульфо- намидо)-6-метилфенил]-бензамид
[химическая формула 127]

Целевое соединение получали способом, описанным в примере 70.
Т.пл. 204-206оС (перекристаллизовано
из этанола)
FAB-MC (m/z): 415 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 2,10 (3Н, с); 3,80 (3Н, с); 6,97 (2Н, д, I=8,8 Гц); 7,00-7,12 (3Н, м); 7,37
(2Н, т, I=8,8 Гц); 7,65 (2Н, д, I=8,8 Гц); 8,03 (2Н, дд, I=5,6, 8,8 Гц); 9,46 (1Н, шир. с); 9,48 (1Н, шир. с).
Элементный анализ для C21H19FN2O4S:
Вычислено: C 60,86; H 4,62; N 6,76
Найдено: C 60,74; H 4,56; N 6,65
П р и м е р 90.
N-[2-(4-метоксибензолсульфонамидо)-6-метилфенил]никотинамид
[химическая формула 128]
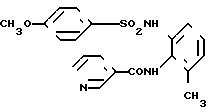
Целевое состояние получали способом, описанным в примере 70.
Т.пл. 207-209оС (перекристаллизовано из этанола)
FAB-MC (m/z): 398 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 2,11 (3Н,
с); 3,79 (3Н, с); 6,98 (2Н, д, I=8,8 Гц); 7,02 (1Н, дд, I=1,6, 7,6 Гц); 7,05-7,14 (2Н, м); 7,58 (1Н, дд, I=4,8, 8,8 Гц); 7,66 (2Н, д, I=8,8
Гц); 8,29 (1Н, дт, I=1,6, 8,0 Гц); 8,77 (1Н, дд, I=1,6, 4,8
Гц); 9,13 (1Н, д, I=1,6 Гц); 9,53 (1Н, шир.); 9,64 (1Н, шир. с).
Элементный анализ для C20H19N3O4S:
Вычислено: C 60,44; H 4,82; N
10,57
Найдено: C 60,55; H 4,90; N 10,53
П р и м е р 91.
N-[2-(4-Метоксибензперсульфонамидо)-6-метилфенил]изоникотинамид
[химическая формула 129]

Целевое соединение получали способом, описанным в примере 70.
Т.пл. 213-217оС (перекристаллизовано из этанола)
FAB-MC (m/z): 398 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 2,10 (3Н, с); 3,80 (3Н, с); 6,99 (2Н, д, I=8,8
Гц); 7,02 (1Н, дд, I=1,6, 7,6 Гц); 7,04-7,14 (2Н, м); 7,67 (2Н, д, I=8,8 Гц); 7,87 (2Н, дд, I=1,6,
8,4 Гц); 8,80 (2Н, дд, I=1,6, 8,4 Гц); 9,56 (1Н, шир. с); 9,53 (1Н, шир. с).
Элементный анализ для C20H19N3O4S:
Вычислено: C 60,
44; H 4,82; N 10,57
Найдено: C 60,60; H 4,85; N 10,53
П р и м е р 92.
N-[2-(4-метоксибензолсульфонамидо)-6-метилфенил]-2-пиридинкарбоксамид
[химическая формула 130]

Целевое соединение получали способом, описанным в примере 70.
Т.пл. 180-182оС (перекристаллизовано из этанола)
FAB-MC (m/z): 398 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 2,12 (3Н, с); 3,78 (3Н, с); 6,90 (2Н, д, I=8,8
Гц); 6,93 (1Н, т, I=4,8 Гц); 7,11 (2Н, д, I=4,8 Гц); 7,54 (2Н, д, I=8,8 Гц); 7,65-7,72 (1Н,
м); 8,03-8,08 (2Н, м); 8,75 (1Н, дд, I=1,2, 5,2 Гц); 9,53 (1Н, шир. с); 10,11 (1Н, шир. с).
Элементный анализ для C20H19N3O4S:
Вычислено: C 60,44; H 4,82; N 10,57
Найдено: C 60,43; H 4,92; N 10,45
П р и м е р 93.
N-[2-(4-Метоксибензолсульфонамидо)фенил]-2-нитробензамид
[химическая
формула 131]
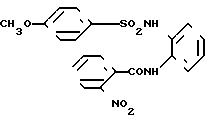
Целевое соединение получали способом, описанным в примере 70.
Т.пл. 168-170оС (перекристаллизовано из этанола)
FAB-MC (m/z): 428 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,80 (3Н, с); 7,05 (2Н, д, I=8,
8 Гц); 7,07-7,16 (2Н, м); 7,19-7,26 (1Н, м); 7,62 (2Н, д, I=8,8 Гц); 7,66 (1Н, д, I=8,0 Гц); 7,73 (1Н, д,
I=8,0 Гц); 7,79 (1Н, т, I=8,0 Гц); 7,92 (1Н, т, I=8,0 Гц); 8,16 (1Н, д, I=8,0 Гц); 9,23 (1Н,
шир. с); 9,93 (1Н, шир. с).
Элементный анализ для C20H17N3O6S:
Вычислено: C 56,20; H 4,01; N 9,83
Найдено: C 56,21; H 4,
05; N 9,77
П р и м е р 94.
2-Хлоро-4-фторо-N-[2-(4-метоксибензо- лсульфонамидо)фенил]-бензамид
[химическая формула 132]

Целевое соединение получали способом, описанным в примере 70.
Т.пл. 160-162оС (перекристаллизовано из
этанола)
FAB-MC (m/z): 435 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,81 (3Н, с); 6,97-7,18 (4Н, м); 7,19-7,28 (1Н, м); 7,34-7,44 (1Н, м); 7,51-7,64
(4Н, м); 6,74-7,82 (1Н, м); 9,33 (1Н, шир. с); 9,69 (1Н,
с).
Элементный анализ для C20H16ClN2O4S:
Вычислено: C 55,24; H 3,71; N 6,
44
Найдено: C 55,42; H 3,90; N 6,20
П
р и м е р 95.
N-[2-(4-Метоксибензолсульфонамидо)фенил]-2-метилбензамид
[химическая формула 133]
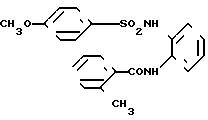
Целевое соединение получали способом, описанным в примере 70.
Т.пл. 129-130оС
(перекристаллизовано из этанола)
FAB-MC
(m/z): 397 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 2,38 (3Н, с); 3,81 (3Н, с); 7,03 (2Н, д, I=8,8 Гц); 7,07
(1Н, дд, I=2,0, 8,0 Гц); 7,10 (1Н, дд, I=1,2, 8,
0 Гц); 7,19-7,27 (1Н, м); 7,27-7,39 (3Н, м); 7,42 (1Н, дт, I=2,0, 7,2 Гц); 7,56 (2Н, д, I=8,8 Гц); 7,80-7,87 (1Н, м); 9,40 (1Н, шир. с); 9,46 (1Н, шир.
с).
Элементный анализ для
C21H20N2O4S:
Вычислено: C 63,62; H 5,09; N 7,07
Найдено: C 63,64; H 5,09; N 7,03
П р и
м е р 96.
2-Хлорo-N-[2-(4-метоксибензолсульфо- намидо)фенил]никотинамид
[химическая формула 134]

Целевое соединение получали способом, описанным в примере 70.
Т.пл. 133-135оС (перекристаллизовано из этанола)
FAB-MC
(m/z): 418 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,81 (3Н, с); 7,04 (2Н, д, I=8,8 Гц); 7,07-7,15 (2Н, м); 7,18-7,22 (1Н, м); 7,60 (2Н, д, I=8,8 Гц); 7,61
(1Н, дд, I= 4,8, 7,6 Гц); 7,78 (1Н, д,
I=7,6 Гц); 7,98 (1Н, дд, I=2,0, 7,6 Гц); 8,56 (1Н, дд, I=2,0, 4,8 Гц); 9,29 (1Н, шир. с); 9,87 (1Н, с).
Элементный анализ для C19
H16ClN3O4
S:
Вычислено: C 54,61; H 3,86; N 10,06
Найдено: C 54,71; H 3,87; N 9,90
П р и м е р 97.
4-Фторо-N-[2-(4-метоксибензолсульфо- намидо)фенил]бензотиоамид
[химическая формула 135]
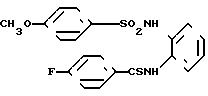
Смесь 549 мг (1,371 мМ) соединения, полученного в примере 82; 333 мг (0,823 мМ) реагента Ловессона и 10 мл толуола нагревали при 100оС. После концентрирования остаток очищали с помощью колоночной хроматографии на силикагеле, в результате чего получали 506 мг целевого соединения.
Т.пл. 155-156оС (после перекристаллизации из н-бутанола)
FAB-MC (m/z): 417 ([M+H]+)
1Н-ЯМР
(DMCO-d6) δ (ppm): 3,80 (3Н, с); 7,02 (2Н, д, I=8,8 Гц); 7,10-7,25 (3Н, м); 7,33 (2Н, т, I=8,8 Гц); 7,47-7,58 (1Н, м);
7,63 (2Н, д, I=8,8 Гц); 7,98 (2Н, дд, I=5,6, 8,8 Гц); 9,45 (1Н,
шир); 11,13 (1Н, шир).
Элементный анализ для С20H17FN2O3S2:
Вычислено: C 57,68; H 4,11; N 6,73
Найдено: C 57,
63; H 4,12; N 6,58
П р и м е р 98.
N-[5-фторо-2-(4-метоксибензолсульфо-намидо)фенил]бензамид
[химическая формула 136]
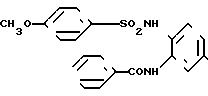

Целевое соединение получали способом, описанным в примере 70.
Т.пл. 153-154оС (после перекристаллизации из этанола)
FAB-MC
(m/z): 401 ([M+H]+)
1Н-ЯМР (DMCO-d6)
δ (ppm): 3,75 (3Н, с); 6,88 (2Н, д, I=8,8 Гц);6,94 (1Н, дт, I= 3,2, 8,8 Гц); 7,00 (1Н, дд, I=6,0, 8,8 Гц); 7,47 (2Н,
д, I=8,8 Гц); 7,55 (2Н, т, I=7,6 Гц); 7,59-7,66 (1Н, м); 7,74-7,83 (3Н, м);
9,45 (1Н, шир. с); 9,55 (1Н, шир. с).
Элементный анализ для C20H17FN2
O4S:
Вычислено: C 59,55; H 4,28; N 7,00
Найдено: C
59,97; H 4,32; N 6,79
П р и м е р 99.
4-Фторо-N-[2-(4-нитробензолсульфона- мидо)фенил]бензамид
[химическая формула 137]

Целевое соединение получали из соединения, полученного в примере получения 13, способом, описанным в примере 70.
Т.пл. 265-266оС (после перекристаллизации из
этилацетата)
FAB-MC (m/z): 416 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 7,21 (1Н, дт, I=1,6,
8,0 Гц); 7,25 (1Н, дд, I= 2,0, 8,0 Гц); 7,30 (1Н, дт,
I=2,0, 8,0 Гц); 7,35 (2Н, т, I=8,8 Гц); 7,55-7,60 (1Н, м); 7,76 (2Н, д, I=8,8 Гц); 7,83 (2Н, дд, I=5,6, 8,8 Гц); 8,22 (2Н, д, I=8,8 Гц); 9,42 (1Н,
с); 9,89 (1Н, с).
Элементный анализ
для C19H19FN3O5S:
Вычислено: C 54,94; H 3,40; N 10,12
Найдено: C 54,90; H 3,36; N 9,
93
П р и м е р 100.
2-Хлоро-6-метил-N-[2-(4-метоксибензо- лсульфонамидо)фенил] изоникотинамид
[химическая формула 138]

Целевое соединение получали способом, описанным в примере 1.
Т.пл. 150-151оС (после перекристаллизации из
этанола)
FAB-MC (m/z): 432 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 2,58 (3Н, с); 3,76 (3Н, с); 6,90 (2Н, д, I=8,8 Гц); 7,15-7,26 (3Н, м); 7,52 (2Н,
д, I=8,8 Гц); 7,54-7,63 (3Н, м); 9,44 (1Н, шир.
с); 9,73 (1Н, шир. с).
Элементный анализ для C20H18ClN3O4S:
Вычислено: C 55,62; H
4,20; N 9,73
Найдено: C 55,80; H 4,26;
N 9,75
П р и м е р 101.
N-[2-(4-метоксибензолсульфонамидо)фенил]ацетамид
[химическая формула 139]

Целевое соединение получали способом, описанным в примере 70.
Т.пл. 160-161оС
(перекристаллизовано из этанола)
FAB-MC
(m/z): 321 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 1,96 (3Н, с); 3,80 (3Н, с); 6,99-7,17 (5Н, м); 7,48 (1Н,
д, I=8,0 Гц); 7,53 (2Н, д, I=8,8 Гц); 9,23 (2Н,
шир. с).
Элементный анализ для C15H16N2O4S:
Вычислено: C 56,24; H 5,03; N 8,75
Найдено: C 56,26; H 5,03; N 8,72
П р и м е р 102.
N-[2-(4-Метоксибензолсульфонамидо)фенил]формамид
[химическая формула 140]
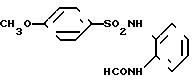
Целевое соединение получали способом, описанным в примере 70.
Т.пл. 143-144оС (перекристаллизовано
из этанола)
FAB-MC
(m/z): 307 ([M+H]+)
Элементный анализ для C14H14N2O4S:
Вычислено: C 54,89; H 4,61; N 9,14
Найдено: C 55,05; H 4,65; N
9,09
П р и м е р 103.
N-[2-[(Этоксикарбонил)амино]фенил]-4-метоксибензолсульфонамид
[химическая формула 141]

Целевое соединение получали способом, описанным в примере 70.
Т.пл. 118-119оС
(перекристаллизовано из этанола)
FAB-MC (m/z): 351 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 1,22 (3Н, т, I=7,2 Гц); 3,79 (3Н, с); 4,03 (2Н, кв. I=7,2
Гц); 6,98-7,03 (4Н, м); 7,17 (1Н, т,
I=8,0 Гц); 7,52 (2Н, д, I=8,8 Гц); 7,57 (1Н, д, I=8,0 Гц); 8,43 (1Н, с); 9,35 (1Н, с).
Элементный анализ для С16H18N2O5S:
Вычислено: C 54,84; H 5,18; N 7,99
Найдено: C 54,78; H 5,19; N 7,86
П р и м е р 104.
N-[2-[(Этиламинокарбонил)амино]фен-ил]-4-метоксибензолсульфонамид
[химическая формула 142]

Целевое соединение получали с помощью реакции соединения, полученного в примере получения 12, с этилизоцианатом с последующей обработкой продукта стандартным способом.
Т.пл. 152-154оС (перекристаллизовано из этанола)
FAB-MC (m/z): 350 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 1,08 (3Н, т, I=7,2 Гц); 3,10
(2Н, дкв. I=5,6, 7,2 Гц); 3,82 (3Н, с); 6,61 (1Н, дд, I=1,6, 8,0 Гц);
6,77 (1Н, дт, I=1,2, 8,0 Гц); 6,89 (1Н, т, I=5,6 Гц); 7,04 (2Н, д, I=8,8 Гц); 7,05-7,12 (1Н, м); 7,57 (2Н, д, I= 8,8 Гц); 7,78
(1Н, дд, I=1,2, 8,4 Гц); 7,94 (1Н, с); 9,41 (1Н, с).
Элементный анализ для C16H19N3O4S:
Вычислено: С 55,00; H 5,48; N 12,03
Найдено: C 55,08; H 5,47; N 11,88
П р и м е р 105.
N-[3-(4-Метоксибензолсульфонамидо)-2-пиридил]-2-метилбензамид
[химическая формула 143]
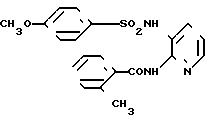
Целевое соединение получали способом, описанным в примере 70.
Т.пл. 160-162оС
(перекристаллизовано из этанола)
FAB-MC (m/z): 398 ([M+H]+
)
1Н-ЯМР (DMCO-d6) δ (ppm): 2,37 (3Н, с); 3,81 (3Н, с); 7,05 (2Н, д, I=8,8 Гц); 7,
22-7,23 (4Н, м); 7,36-7,43 (1Н, м); 7,59 (2Н, д, I=8,8 Гц); 7,71 (1Н, дд, I= 1,6,
8,0 Гц); 8,25 (1Н, дд, I=1,6, 4,8 Гц); 9,24 (1Н, шир. с); 10,47 (1Н, шир. с).
Элементный анализ для
C20H19N3O4S:
Вычислено: C 60,
44; H 4,82; N 10,57
Найдено: C 60,53; H 4,84; N 10,67
П р и м е р 106.
N-[2-(4-Аминобензолсульфонамидо)фе- нил]-4-фторобензамид
[химическая формула 144]

Целевое соединение получали путем восстановления соединения, полученного в примере 99, с использованием цинка/соляной кислоты.
Т.пл. 203-205оС (перекристаллизовано из
этанола)
FAB-MC (m/z): 386 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 5,98 (2Н, шир. с); 6,45 (2Н, д, I=8,8 Гц); 7,05 (1Н, дд, I=1,6, 8,0 Гц); 7,09
(1Н, дт, I=1,6, 8,0 Гц); 7,20 (1Н, дт, I= 1,6, 8,0 Гц); 7,23 (2Н, д, I=8,8 Гц); 7,39 (2Н, т, I=8,
8 Гц); 7,74-7,80 (1Н, м); 7,93 (2Н, дд, I=5,6, 8,8 Гц); 9,20 (1Н, шир. с); 9,63 (1Н, шир. с).
Элементный анализ для С19H16FN3O3S:
Вычислено: C 59,21; H 4,18; N 10,90
Найдено: C 59,36; H 4,21; N 10,80
П р и м е р
107.
N-[2-(4-Хлоробензолсульфонамидо)фе-нил]бензамид
[химическая формула
145]
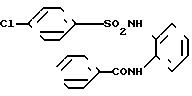
Целевое соединение получали способом, описанным в примере 70.
Т.пл.
191-192оС (перекристаллизовано из этанола)
FAB-MC (m/z): 387 ([M+H]+
)
1Н-ЯМР (DMCO-d6) δ (ppm): 7,13-7,20 (2Н, м); 7,24-7,30 (1Н, м);
7,42 (2Н, д, I=8,8 Гц); 7,54 (2Н, д, I=8,8 Гц); 7,55 (2Н, т, I=8,8 Гц); 7,60-7,66 (1Н, м); 7,
68-7,72 (1Н, м); 7,78-7,83 (2Н, м); 9,52 (1Н, с); 9,71 (1Н, с).
Элементный анализ для
C19H15ClN2O3S:
Вычислено: С 58,99; H 3,91;
N 7,24
Найдено: C 59,25; H 4,02; N 7,29
П р и м е р 108.
N-[2-(3,
4-Диметоксибензолсульфонами- до)фенил]бензамид
[химическая формула 146]

Целевое соединение получали способом, описанным в примере 70.
Т.пл. 183-184оС
(перекристаллизовано из этанола)
FAB-MC (m/z): 413 ([M+H]+)
1
Н-ЯМР (DMCO-d6) δ (ppm): 3,53 (3Н, с); 3.75 (3Н, с); 6,90 (1Н, д, I=8,4 Гц); 6,95
(1Н, д, I=2,0 Гц); 7,13 (1Н, дд, I=2,0, 8,4 Гц); 7,13-7,18 (2Н, м); 7,23-7,29 (1Н, м); 7,54 (2Н, т,
I=7,6 Гц); 7,59- 7,65 (1Н, м); 7,71-7,76 (1Н, м); 7,76-7,82 (2Н, м); 9,43 (1Н, шир. с); 9,53 (1Н,
шир. с).
Элементный анализ для C21H20N2O5
S:
Вычислено: C 61,15; H 4,89; N 6,79
Найдено: C 61,16; H 4,90; N 6,82
П р и м е р 109.
N-[2-(4-Метоксибензолсульфонамидо)фенил]бензамид
[химическая формула 147]

Целевое соединение получали способом, описанным в примере 70.
Т.пл. 167-168оС (перекристаллизовано из этанола)
FAB-MC
(m/z): 383 ([M+H]+)
1Н-ЯМР (DMCO-d6) δ (ppm): 3,75 (3Н, с); 6,91
(2Н, д, I=8,8 Гц); 7,08 (1Н, дд, I=1,6, 8,0 Гц); 7,12 (1Н, дт, I=1,6, 8,0 Гц); 7,24
(1Н, дт, I=1,6, 8,0 Гц); 7,51 (2Н, д, I=8,8 Гц); 7,52-7,59 (2Н, м); 7,60-7,66 (1Н, м); 7,76 (1Н, дд, I= 1,6, 8,0 Гц);
7,81-7,86 (2Н, м); 9,50 (1Н, шир. с); 9,55 (1Н, шир. с).
Элементный анализ для C20H18N2O4S:
Вычислено: C 62,81; H 4,74; N 7,33
Найдено: C 63,06; H 4,77; N 7,32
П р и м е р 110.
4-Этокси-N-[2-((4-гидроксифенил)ами-но) -3-пиридил]бензолсульфонамид
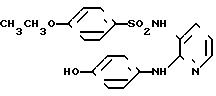
Получали целевое соединение.
Т.пл. 194-195оС (перекристаллизовывали из этанола)
FAB-MC (m/z): 386
([M+H]+)
Элементный анализ для C19H19N3O3S:
Вычислено: C 59,21; H 4,97; N 10,90
Найдено: C 59,12; H 4,93; N 10,66
1Н-ЯМР (DMCO-d6) δ (ppm): 1,27 (3Н, т, I=7,2 Гц);
3,98 (2Н, кв. I=7,2 Гц); 6,59 (1Н, дд, I=4,8, 7,6 Гц); 6,61 (2Н, д, I=8,8 Гц); 6,95 (2Н, д, I= 9,2 Гц); 7,12 (2Н, д, I=8,8 Гц);
7,17 (1Н, дд, I=1,6, 7,6 Гц); 7,55 (1Н, шир. с); 7,56 (2Н, д, I=9,2
Гц); 7,87 (1Н, дд, I=1,6, 4,8 Гц); 8,97 (1Н, с); 9,41 (1Н, шир. с).
Реферат
Использование: в медицине. Сущность: продукт - производные сульфонамида

Формула

где R1 низший алкил, низший алкокси, амино-;
R2 водород, низший алкил;
R3 и R4 различные и каждый представляет собой галоген, низший алкокси- или оба водород;
A означает N илиCH-;
B группаN- или

ε группа формулы

где Q кислород или сера, R6 водород, низший алкил, низший алкокси, низший алкиламино, 2-фурил, фенил, который может быть замещен низшим алкилом, гидрокси, галогеном, или R6 пиридил, который может быть замещен низшим алкилом, галогеном; пиридил, пиримидинил или фенил, который может быть замещен низшим алкилокси, гидроксилом, низшим алкилом, галогеном, (низшей)алкилокси(низшей)алкилоксигруппой, фенилкарбонилокси, фосфорилокси, глюкопиранозилокси, низшим алкилоксикарбонилом, диметиламинокарбонилокси, аминоацетилокси, аминобензоилокси, фенокси, или их фармакологически приемлемые соли, за исключением случаев, когда а) R1 низший алкил, амино, R2 водород, А и В группа -CH-; ε фенил, который может быть замещен гидроксилом, галогеном, низшей алкилокси, низшим алкилом, фенилкарбонилокси, низшим алкилоксикарбонилом, диметитиламинокарбонилокси, аминобензоилокси, б) R2 низший алкил, А и В каждыйCH-,
e группа формулы

где R6 низший алкил, низший алкиламино, или ε фенил, который может быть замещен низшим алкокси, гидроксилом, низшим алкилом, галогеном, фенилкарбонилокси, низшим алкилоксикарбонилом, диметиламинокарбонилом, аминобензоилоксигруппой,
или их фармакологически приемлемые соли.
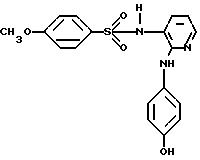


или фармакологически приемлемые соли.
20.08.90 при R1 низший алкил, низший алкилокси, амино, R2 водород, низший алкил, R3 и R4 оба водород. A CH-, B N-, ε фенил, который может быть замещен низшим алкокси, низшим алкилом, гидрокси, галогеном, низшей алкилоксинизшей алкилоксигруппой или пиридил, или их фармакологически приемлемые соли.

где R5 водород, R3 и R4 одинаковые или различные - галоген, низший алкокси, ε фенил замещенный низшим алкоксикарбонилом, фенокси, диметиламинокарбонилокси, фенилкарбонилокси, аминоацетилокси, аминобензоилокси, фосфорилокси или пиримидинил.

где Q кислород или сера, R6 водород, низший алкил, низший алкокси, низший алкиламино, фурил, или ε фенил, который может быть замещен низшим алкилом, галогеном, гидрокси, глюкопиранозилокси, или пиридил, замещенный низшим алкилом, В группа

где R5 низший алкил.

Комментарии