Способ получения серосодержащих производных имидазола и промежуточные продукты - RU2135475C1
Код документа: RU2135475C1
Описание
Настоящее изобретение относится к способу получения серосодержащих производных имидазола и к новым полученным промежуточным продуктам.
Предметом настоящего изобретения
является способ получения
продуктов формулы (I):
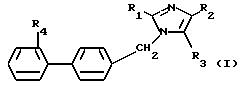
в которой R1 представляет собой такие радикалы, как алкильный, алкенильный, алкинильный, алкилтионильный, каждый из которых может быть линейным или разветвленным и включает не более 10 атомов углерода, или же циклоалкильный радикал, включающий от 3 до 7 атомов углерода, причем все указанные радикалы могут быть замещены,
R2 и R3, одинаковые или различные, выбраны среди:
а) атома водорода, галогенных атомов, радикалов, таких как гидроксильный, меркапто, формильный, ацильный, карбоксильный, свободный или превращенный в соль или в сложный эфир, нитрильный, цианильный, и -PO3 (R)2, где R представляет собой атом водорода, алкильный или фенильный радикал с возможностью замещения:
б) радикалов -(CH2)m1S(O)m2-X-R10, котором m1 принимает целочисленное значение от 0 до 4, m2 принимает целочисленное значение от 0 до 2, a X представляет собой простую связь или радикалы -NH-, -NH- CO-, -NH-CO-O-, -N= CH-N-R13, -NH-CO-NH-, а R10 и R13, одинаковые или различные, представляют собой атом водорода, линейный или разветвленный алкильный или алкенильный радикал, включающий не более 6 атомов углерода, или же циклоалкильный радикал, включающий от 3 до 6 атомов углерода, фенильный или бензильный радикал с возможностью замещения, или же такие радикалы, как пиридильный, нитропиридильный, пиримидильный, тетразолильный, диазолильный, пиперидинильный, алкилпиперидинильный, тиазолильный, алкилтиазолильный, тетрагидрофуранильный, метилтетрагидрофуранильный;
в) алкильного, алкенильного, алкоксильного и алкилтионильного радикалов, в котором атом серы может быть моно или диокисленным, причем каждый из вышеуказанных радикалов, линейных или разветвленных, включающих не более 6 атомов углерода, может быть разорван одним или несколькими гетероатомами, выбранными среди атомов серы, кислорода или азота, с возможностью замещения;
г) фенильного, бензоильного и фенилтионильного радикалов, в котором атом серы может быть моно или диокисленным, причем указанные радикалы могут быть замещенными;
д) радикалов
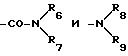
в которых: или R6 и R7 или R8 и R9, одинаковые или различные, выбраны среди:
атома водорода,
аминокислот,
алкильного и алкенильного радикалов, включающих не более 6 атомов углерода, с возможностью замещения,
фенильного, бензильного и фенетильного радикалов, с возможностью замещения,
радикала -(CH2)m1-S(O)m2-X-R10, как определено выше,
или R6 и R7 или R8 и R8 соответственно образуют с атомом азота, с которым они связаны, моноциклический радикал, содержащий 5, 6 или 7 атомов, или радикал, состоящий из одинаковых или различных конденсированных циклов, содержащий от 8 до 14 атомов, причем они могут включать один или несколько других гетероатомов, выбранных среди атомов кислорода, азота и серы, и могут быть замещены одним или несколькими радикалами, выбранными среди галогенных атомов, таких радикалов, как гидроксильный, нитрильный, алкильный и алкоксильный, включающих не более 6 атомов углерода, аминный, который может быть замещен одним или двумя одинаковыми или различными алкильными радикалами, включающими не более 6 атомов углерода, и фенильный,
или R8 и R9, одинаковые или различные, представляют собой ацильный радикал, или один из R8 или R9 представляет собой карбамоильный, алкоксикарбонильный или бензилоксикарбонильный радикал, или R8 и R9 образуют вместе с атомом азота, с которым они связаны, радикал фталимидо или сукцинимидо,
е) радикала -S-S-R12, в котором R12 имеет значения, определенные для R2 или R3 в пунктах с а) по д), за исключением аминного и алкоксильного радикалов, причем следует иметь ввиду, что хотя бы один из R2 и R3 представляет собой алкоксильный радикал с возможным замещением или радикал -(CH2)m1-S(O)m2-X-R10, как определено выше, R4 выбран среди радикала -(CH2)m1-S(O)m2-X-R10, как определено выше, галогенного атома, нитрильного радикала, радикалов -(CH2)m1-COOR14, -(CH2 )m1-CONHR14, -(CH2)m1-CN, в которых m1 имеет вышеуказанное значение, -SO2-NH-SO2-R14, -NH-SO2-R14, -PO3R14, -NH-SO2-CF3 и
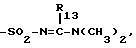
-SO2NHSO2R14, -SO2NHPO(R14 )2, -CONHPO(R14)2, -SO2NHCN, -SO2NHCOR14, -SO2NHSO2NR14R15, -SO2NHSO2 N(CH2CH2)2Y, -NHSO2NHSO2R14, -NHSO2NHPO(R14)2,
-NHSO2R14, -NR14COCO2H, -SO2NHCO2R14 в которых R13 имеет вышеуказанное значение, a R14 и R15, одинаковые или различные, представляют собой атом водорода, алкильный радикал, включающий не более 6 атомов углерода, или циклоалкильный радикал, включающий от 3 до 6 атомов углерода, с возможностью замещения, a Y представляет собой атом кислорода или серы, причем все радикалы: алкильный, алкенильный, циклоалкильный, алкилтионильный, фенилтионильный, алкоксильный, фенильный, бензильный могут быть замещены одним или несколькими радикалами, выбранными среди галогенных атомов, гидроксильного, нитрильного радикала, алкильного, алкенильного и алкоксильного радикалов, включающих не более 4 атомов углерода, трифторметильного, цианильного, аминного, моно и диалкиламинного, карбоксильного, свободного, превращенного в соль или в сложный эфир, галоалкильного, алкилтионильного, галоалкилтионильного, галоалкоксильного, фенильного, пиридильного, бензильного, фенетильного, бензоильного, феноксильного, бензилоксильного, фенилтионильного, карбамоильного, ацильного, ацилоксильного и тетразолильного, причем указанные продукты формулы (I) могут иметь любые возможные изомерные рацемические, энантиомерные и диастереоизомерные формы, а также аддитивных солей с неорганическими и органическими кислотами или с неорганическими и органическими основаниями вышеуказанных продуктов формулы (I), причем отличительной особенностью является то, что соединение формулы (А):
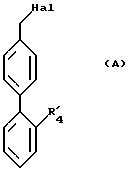
в которой Hal представляет собой галогенный атом, a R'4 имеет значение, указанное выше для R4, в которой возможные функциональные группы могут быть защищены, вводится в реакцию с окислителем для получения соединения формулы (В):
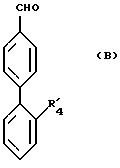
в которой R'4 имеет вышеуказанное значение и который вводят в реакцию с соединением формулы (II):
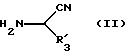
в которой R'3 имеет значение, указанное выше для R3, и в которой возможные функциональные группы могут быть защищены, для получения продукта формулы (С):
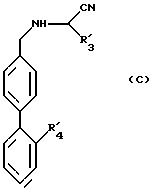
в которой R'3 и R'4 имеют вышеуказанные значения, который вводят в реакцию с соединением формулы (III):
R'1-CO-Hal (III)
в которой R'1 имеет значение, указанное выше для R1, и в которой возможные функциональные группы могут быть защищены, a Hal представляет собой галоген, для получения продукта формулы (D):
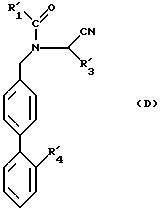
в которой R'1, R'3 и R'4 имеют указанные выше значения, который подвергается реакции присоединения на радикале CN с помощью реактива, способного ввести заменитель R'2, причем R'2 имеет значение, указанное выше для R2, в котором возможные функциональные группы могут быть защищены, для получения продукта формулы (Е):
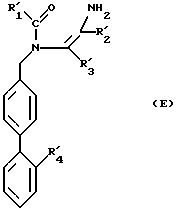
в которой R'1, R'2, R'3 и R'4 имеют указанные выше значения, который при необходимости подвергается реакции замещения атома кислорода атомом серы для получения продукта формулы (L):
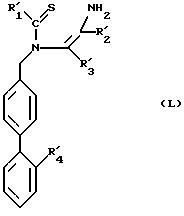
в которой R'1, R'2, R'3 и R'4 имеют указанные выше значения, продукт формулы (Е) или продукт, формулы (L) подвергают реакции циклизации для получения продукта формулы (I'):
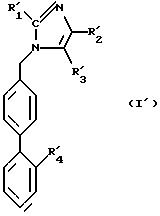
в которой R'1, R'2, R'3 и R'4 имеют указанные выше значения, причем следует иметь в виду, что продукты формул (D), (Е) и (L) в ходе вышеописанного способа и продукты формулы (I') могут подвергаться при желании и в случае необходимости одной или нескольким из нижеследующих реакций в произвольном порядке:
а) реакции превращения в сложный эфир кислой функциональной группы,
б) реакции омыления сложноэфирной функциональной группы,
в) реакции превращения функциональной цианогруппы в кислую функциональную группу,
г) реакции восстановления функциональной карбоксигруппы в спиртовую функциональную группу,
д) реакции превращения функциональной алкоксигруппы в гидроксильную функциональную группу,
е) реакции окисления группы, включающей атом серы, в соответствующий сульфоксид или сульфон,
ж) реакции превращения спиртовой или сульфонной функциональной группы в соответствующую альдегидную или кислую функциональную группу,
з) реакции превращения функциональной нитрильной группы в тетразольную функциональную группу,
и) реакции превращения формильного радикала в карбамоильный,
к) реакции превращения карбамоильного радикала в нитрильный,
л) реакции превращения радикала
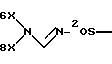
в радикал
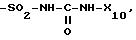
а) реакции выделения защитных групп, которые могут быть включены в защищенные функциональные группы,
6) реакции превращения в соответствующую соль неорганической или органической кислотой или основанием,
в) реакции раздвоения рацемических форм на раздвоенные продукты, причем указанные полученные таким образом продукты формулы (I) могут иметь любые возможные изомерные рацемические, энантиомерные и диастереоизомерные формы.
В радикале -(CH2 )m1-S(O)m2-X-R10, как определено выше, когда ml отличается от 0, радикал (CH2)m1 имеет значения алкиленных радикалов, таких как, например, метилен, этилен, н-пропилен или н-бутилен, и, в частности, когда m1 имеет значение 0, 1 или 2, радикал -(CH2)m1 - представляет собой соответственно простую связь, метиленный или этиленный радикал.
Среди значений -S(O)m2-X-R10
можно назвать, например, причем этот перечень не будет исчерпывающим, такие радикалы, как: -SO2-NH2, -SO2-NH-СН3, -SO2-NH-CF3, -SO2-NH-C6H5, -SO2-NH-CH2-C6H5, -CH2-SO2-NH2, -CH2-SO2-NH-C6H5, -SO2-NH-CO-NH-CH3, -SO2-NH-CO-NH-C6H5,
-SO2-NH-CO-NH-CF3, -SO2-NH-CO-NH-CH2-C6
H5, -SO2-NH-CO-NH-D, где D представляет собой радикал, такой как фенильный,
пиридинный или пиримидинный,
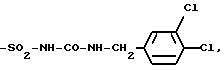
-SO2-NH-CO-NH-CH2-CH2-CH3, -SO2-NH-CO-NH-CH=CH-CH3,
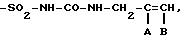
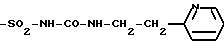
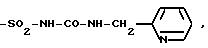
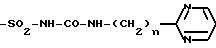
где n = 1 или 2.
В продуктах формулы (I), а также в нижеследующем :
термин
линейный или разветвленный алкильный радикал означает, в первую очередь, такие радикалы, как метильный, этильный,
пропильный, изопропильный, бутильный, изобутильный, втор-бутильный и трет-бутильный,
но может также означать радикалы пентильный или гексильный и, в частности, изопентильный и изогексильный;
термин линейный или разветвленный алкенильный радикал означает, в первую очередь,
такие радикалы, как винильный, аллильный, 1-пропенильный, бутенильный и, в частности, 1-бутенильный или пентенильный;
термин линейный или разветвленный алкинильный радикал означает, в первую
очередь, радикалы этинильный, пропинильный, бутинильный, линейный или разветвленный.
Среди алкильных радикалов, разорванных одним или несколькими гетероатомами, можно назвать такие радикалы, как метоксиметильный, метоксиэтоксиметильный, пропилтиопропильный, пропилоксипропильный, пропилтиоэтильный, метилтиометильный.
термин галогенный атом означает, в первую
очередь, атом хлора или брома, однако он может также представлять атом фтора или иода;
термин линейный или
разветвленный алкоксильный радикал означает, в первую очередь, такие радикалы, как
метоксильный, этоксильный, пропоксильный или изопропоксильный, однако он может также представлять собой линейный,
вторичный или третичный бутоксильный радикал;
термин ацильный радикал
означает, в первую очередь, радикал, включающий от 1 до 6 атомов углерода, как, например, такие радикалы, как формильный,
ацетильный, пропионильный, бутирильный или бензоильный, однако он может также
представлять собой радикалы, такие как пентаноильный, гексаноильный, акрилоильный, кротоноильный или карбамоильный;
термин амино, замещенный одним или двумя алкильными радикалами, означает, в
первую очередь, радикалы, в которых алкильный радикал (алкильные радикалы) выбран (выбраны) среди алкильных радикалов,
как определено выше, как, например, для моноалкиламино, метиламинный или
этиламинный радикал, или, например, для диалкиламино - диметиламинный или же метилэтиламинный;
термин ацилоксильный
радикал означает, например, радикал, в котором ацильный радикал имеет
указанные выше значения и означает, в первую очередь, такие радикалы, как формилоксильный, ацетилоксильный, пропионилоксильный,
бутирилоксильный или бензоилоксильный;
термин циклоалкильный
радикал означает, в первую очередь, такие радикалы, как циклопропильный, циклобутильный, циклопентильный или циклогексильный;
термины моноциклический радикал и радикал, состоящий из
конденсированных циклов, означают насыщенные или ненасыщенные радикалы;
термин моноциклический радикал означает насыщенные
радикалы, например, пирролидинильный, имидазолидинильный,
пиразолидинильный, пиперидильный, пиперазинильный, морфолинильный, тиоморфолинильный, азепинильный радикалы, или ненасыщенные радикалы,
например, пираннильный, пирролильный, имидазолильный,
пиразолильный, пиридильный, пиразинильный, пиримидинильный, пиридазинильный, тиазолильный, тиадиазолильный, оксазолильный, фуразаннильный,
пирролинильный, такой как δ-2-пирролинильный,
имидазолинильный, такой как δ-2-имидазолинильный, пиразолинильный, такой как δ-3- пиразолинильный, а также изомеры положения
гетероатома (гетеро-атомов), которые могут быть включены в
указанные радикалы, такие как, например, изотиазолильный или изоксазолильный радикалы;
термин радикал, состоящий из
конденсированных циклов, означает насыщенные радикалы, например, 1-окса
спиро [4,5] децильный, тетрагидропирран-2-спироциклогексильный, циклогексанспиро-2'- (тетрагидрофуранильный) или 1,10-диаза
антр-4-ильный радикалы, или ненасыщенные радикалы, например, бензотиенильный,
нафто [2,3-b] тиенильный, инденильный, индолизинильный, изоиндолильный, 3H-индолильный, индолильный, индазолильный,
пуринильный, хинолизинильный, бензопирролильный, бензимидазолильный, изохинолинный,
хинолильный, фталазинильный, нафтиридинильный, хиноксалинильный, хиназолинильный, циннолинильный, птеридинильный,
карбазолильный, β-карболинильный, акридинильный, феназинильный, индолинильный,
изоиндолинильный или же конденсированные полициклические системы, состоящие из гетероциклических моноциклов,
таких как, например, определенные выше, например: фуро[2,3-b]пиррол или тиено[2,3-b] фурам;
термин галоалкильный радикал означает, в первую очередь, радикалы, в которых алкильный радикал
соответствует определенному выше и замещается одним или несколькими галогенными атомами, как
определено выше, как, например, бромэтил, трифторметил, трифторэтил или же пентафторэтил;
термин
алкилтионильный радикал означает, в первую очередь, радикалы, в которых алкильный радикал
соответствует определенному выше, как, например, метилтио или этилтио;
термин галоалкилтионильный
радикал означает, в первую очередь, радикалы, в которых алкильный радикал соответствует
определенному выше и замещен одним или несколькими галогенными атомами, как определено выше, как, например,
бромэтилтио, трифторметилтио, трифторэтилтио или же пентафторэтилтио;
термин
галоалкоксильный радикал означает, в первую очередь, радикалы, в которых алкоксильный радикал соответствует
определенному выше и замещен одним или несколькими галогенными атомами, как определено выше,
как, например, бромэтокси, трифторметокси, трифторэтокси или же пентафторэтокси;
термин
карбамоильный радикал также означает карбамоильные радикалы, замещенные, например, низшей
N-моноалкилкарбамоильной группой, такой как N-метилкарбамоил, N-этилкарбамоил, низшей карбамоильной группой N,
N-диалкил, такой как N,N-диметилкарбамоил, N,N-диэтилкарбамоил, карбамоильной группой
N-(низший гидроксиалкил), такой как N-(гидроксиметил) карбамоил, N-(гидроксиэтил) карбамоил, низшей
карбамоилалкильной группой, такой как карбамоилметил, карбамоилэтил;
термин фенильный
радикал, защищенный алкилтионильным радикалом, представляет, например, бензилтионильный радикал.
В продуктах формулы (I), а также в нижеследующем, алкильный, алкенильный, циклоалкильный и фенильный радикалы, которые могут представлять или включать R1, R2, R3 и R4, могут принимать значения, указанные выше для данных радикалов, и могут или не могут замещаться одним или несколькими одинаковыми или различными заменителями, как определено выше для указанных радикалов.
Таким образом, R2 и R3 могут, например,
представлять собой радикалы, такие как алкилтионильный, фенилтионильный, алкилсульфинильный,
фенилсульфинильный, алкилсульфонильный или арилсульфонильный, но также и циклоалкилтионильный радикал, как,
например, циклогексилтио:
термины алкилтионильный, алкилсульфинильный и
алкилсульфонильный радикалы означают радикалы, в которых линейный или разветвленный алкильный радикал может иметь,
например, значения, указанные выше для алкильного радикала; таким образом, эти
радикалы означают, в первую очередь, радикалы метилтио, гидроксиметилтио, этилтио, аминоэтилтио, метилсульфинил,
этилсульфинил; метилсульфонил, этилсульфонил, но могут также представлять собой
радикалы пропилтио, изопропилтио, бутилтио, втор-бутилтио, трет-бутилтио, изопентилтио или изогексилтио, или же радикалы,
в которых радикал тио оксидирован в радикал сульфинил или сульфонил.
В зависимости от значений m1, m2 и R10 в радикале -(CH2)m1-S(O)m2 -X-R10, R2 и R3 могут также представлять следующие радикалы: фенилтио, пиридилтио или пиримидилтио, имидазолилтио, N-метилимидазолилтио, или же радикалы, в которых радикал тио оксидирован в радикал сульфинил или сульфонил, как, например, в фенилсульфиниле или в фенилсульфониле.
В качестве примеров замещенных алкильных радикалов, можно назвать радикалы, замещенные одним или несколькими фенильными радикалами, например бензильный, дифенилметильный, трифенилметильный радикалы, и радикалы, замещенные пиридильным радикалом, например пиридилметильный радикал, причем следует учитывать, что в вышеуказанном неисчерпывающем перечне примеров радикалов алкильный радикал может быть безразлично представлен такими радикалами, как этильный, пропильный или бутильный, такими как, например, в фенэтильном радикале.
В качестве примеров замещенных алкенильных радикалов, можно назвать радикалы, замещенные одним или несколькими фенильными или пиридильными радикалами, как указано в вышеприведенных примерах, в которых алкильный радикал замещен алкенильным радикалом, например, фенилвинильный или фенилаллильный радикалы.
Вышеуказанные карбамоильный и аминный
радикалы, в частности радикалы
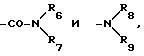
означают радикалы, в которых с атомом азота связаны два радикала, одинаковых или различных, выбранных среди атома водорода для получения аминного радикала; алкильные радикалы, определенные выше для получения моноалкильных или диалкиламинных радикалов, в которых линейные или разветвленные алкильные радикалы включают от 1 до 6 атомов углерода, в частности, метильный, этильный, изопропильный, метоксиметильный, метоксиэтильный, этоксиэтильный радикалы; фенильный, бензильный, фенетильные радикалы, с возможностью замещения для получения, например фениламинного или бензиламинного радикала.
Среди замещенных карбамоильных радикалов можно назвать в качестве замещенного карбамоильного радикала такие группы, как низшая N-моноалкилкарбамоильная группа, например, N-метилкарбамоил, N-этилкарбамоил; низшая N, N-диалкилкарбамоильная группа, например, N,N-диметилкарбамоил, N,N-диэтилкарбамоил; (низшая гидроксиалкильная) N-карбамоильная группа, например, N-(гидроксиметил)карбамоил, N-(гидроксиэтил)карбамоил; низшая карбамоилалкильная группа, например, карбамоилметил, карбамоилэтил; фенилкарбамоил; пиридилкарбамоил: бензил-карбамоил; N-метил N-фенилкарбамоил; пиридилметилкарбамоил.
Термин аминокислота означает, в первую очередь, остаток, производный от одной из природных аминокислот, таких как α- аминоуксусная кислота, аминопропионовая кислота, α- аминоизовалериановая кислота, α - аминоизокапроновая кислота, α- амино β- метил β- этилпропионовая кислота, β- фенил α - аминопропионовая кислота и, в первую очередь, α-пирролидинкарбоновая кислота или другая природная аминокислота, известная специалистам.
Среди радикалов -(CH2)m1-X-R10, которые могут быть представлены R6,
R7, R8 или R9 можно назвать,
в частности, радикалы -NH-SO2-CH3,
-NH-SO2-C6H5, -NH-SO2-CF3
, -NH-CH2-SO2-NH-C6H5, -CO-NH-SO2-C6H5,
-CO-NH-SO2-CH3,
-CO-NH-SO2-CH2
-C6H5.
Гетероцикл, который может быть образован R6 и R7 или R7 и R9, предпочтительно насыщен.
Он может быть замещен уже указанными ранее заменителями, в частности, одним или несколькими радикалами, выбранными среди атомов хлора и фтора, такими радикалами, как метильный, этильный, изопропильный, трет-бутильный, метоксильный, этоксильный, пропоксильный, бензоильный, метоксикарбонильный, этоксикарбонильный; в качестве примера можно назвать такие радикалы, как метилпиперазинильный, этилпиперазинильный, пропилпиперазинильный, фенилпиперазинильный или бензилпиперазинильный радикалы; при этом в двух последних радикалах фенильный и бензильный радикалы могут быть замещены, как указано ранее, как, например, в хлорфениле или трифторфениле.
Ацильные радикалы, которые могут быть представлены R8 и R9, могут быть выбраны, в частности, среди таких радикалов, как ацетильный, пропионильный, бутирильный, пентаноильный и карбамоильный.
В тех случаях, когда R8 или R9 представляет собой алкоксикарбонильный радикал, этим радикалом в первую очередь является трет-бутилоксикарбонильный.
Карбоксильный радикал
(карбоксильные радикалы) продуктов формулы (I) могут быть превращены в соль или в
сложный эфир различными группами, известными специалистам, среди которых можно, в качестве примера, назвать:
среди солеобразующих соединений: минеральные основания, такие как, например, соль
натрия, калия, лития, кальция, магния или аммиака, или органические основания, такие как, например, метиламин,
пропиламин, триметиламин, диэтиламин, триэтиламин, N,N-диметилэтаноламин, трис
(гидроксиметил) аминометан, этаноламин, пиридин, пиколин, дициклогексиламин, морфолин, бензиламин, прокаин, лизин,
аргинин, гистидин, N-метилглюкамин,
среди этерифицирующих соединений:
алкильные радикалы для образования алкоксикарбонильных групп, такие как, например, метоксикарбонил, этоксикарбонил,
трет-бутоксикарбонил или бензилоксикарбонил, причем указанные алкильные радикалы
могут быть замещены радикалами, выбранными, например, среди галогенных атомов, таких радикалов, как гидроксильный,
алкоксильный, ацильный, ацилоксильный, алкилтионильный, аминный или арильный, как,
например, в хлорметильной, гидроксипропильной, метоксиметильной, пропионилоксиметильной, метилтиометильной,
диметиламиноэтильной, бензильной или фенетильной группах.
Аддитивными солями с неорганическими или органическими кислотами продуктов формулы (I) могут быть, например, соли, образованные с бромистым водородом, йодистым водородом, хлористоводородной, азотной, серной, фосфорной, пропионовой, уксусной, муравьиной, бензойной, малеиновой, фумаровой, янтарной, винной, лимонной, щавелевой, глиоксиловой, аспаргиновой, аскорбиновой кислотами, с алкилмоносульфокислотами, такими как, например, метансульфокислота, этансульфокислота, пропансульфокислота, с алкилдисульфокислотами, такими как, например, метандисульфокислота α- этандисульфокислота и β - этандисульфокислота, с арилмоносульфокислотами, такими как бензолсульфокислота, и с арилдисульфокислотами.
Когда R2 и R3 представляют собой оба алкилтионильную или фенилтионильную серосодержащую группу, которая может быть окислена, причем R2 и R3 могут быть одинаковыми или различными, предпочтительными продуктами изобретения являются, в частности, продукты формулы (I), в которых указанные серосодержащие группы обладают той же степенью окисления.
Среди предпочтительных продуктов изобретения находятся, в частности, продукты формулы (I), в которых один из R2 и R3 представляет собой серосодержащую группу, которая может быть окислена, как указано выше, а второй из R2 и R3 представляет собой такой радикал, как алкильный, алкоксильный, карбоксильный, свободный, превращенный в соль или в сложный эфир, или фенильный с возможностью замещения одним или несколькими заменителями, как указано выше.
Среди предпочтительных продуктов изобретения находятся, в первую очередь, продукты формулы (I), в которых R2 представляет собой серосодержащий радикал.
R2 и/или R3 могут, в частности, представлять собой такие радикалы, как алкилтионильный или алкенилтионильный, которые могут быть замещены одним или несколькими радикалами, выбранными среди радикалов, таких как формильный, гидроксильный, алкоксильный, ацилоксильный, карбоксильный, свободный, превращенный в соль или в сложный эфир, аминный, замещенный аминный, карбамоильный, замещенный карбамоильный, алкилтионильный, фенилтионильный, пиридинильный, пиримидинильный, фенильный.
Среди заместителей, которые могут
содержать радикалы R2 и R3, аминный и карбамоильный радикалы могут, в частности, быть замещены одним
или двумя алкильными радикалами и вышеперечисленными аминокислотами
Замещенный аминный и карбамоильный радикалы, которые могут содержать радикалы R2 и R3, могут также
составлять гетероцикл наподобие вышеперечисленных.
R2 и R3 могут также представлять алкилтионильные радикалы, замещенные одним или несколькими галогенными атомами, такими как хлор и фтор. В качестве примера можно назвать радикалы -S-CF3, -S-CHF2, -S-CH2F, -S-CF2-CHF2, -S-CF2-CHFCl.
Таким образом, R2 и R3 могут представлять
следующие радикалы, в которых n, n1 и n2, одинаковые или различные, имеют значения от 0 до 2:
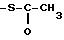
-S-(CH2)n1-S-(CH2)n2-X4;
-S-(CH2 )n-X4;
-S-(CH2)n1-NH-(CH2)n2-X4;
-S-CH=CH-(CH2)n-X4;
-S-(CH2)n1-CH=CH-(CH2)n2 -X4;
где X4 представляет собой H, OH, циклогексил, пиридил, фенил, CHO, CO-OH, NH2 или
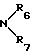
Радикалы R2 и R3 могут также представлять, в частности, следующие радикалы: -COOH; -CO2X5; -SX5; -NH2; -C≡N; -OME; -OEt; -CH=СH-CO-OH; тетразолил;
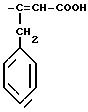
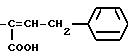
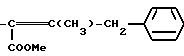
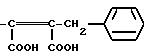
во всех их изомерных и цис-транс-изомерных формах,
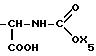
-NH-CH2-COO-X2
-NH-COO-X2
где X2 представляет собой алкильный или арильный радикал.
Радикалы R2 и R3 могут, в частности, представлять собой радикал:
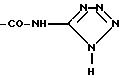
Таким образом, продукты формулы (I) представляют, в частности, продукты, в которых R2 и R3 имеют указанные выше значения и, в первую очередь, продукты, в которых R2 представляет собой алкилтионильный радикал, который может быть замещен, как указано выше, или алкоксильный радикал, такой как, например, метоксильный, a R3 представляет собой карбоксильный радикал, свободный или превращенный в соль или в сложный эфир, или амидированный радикал, такой как, в частности, -COOH, -COO метил, -COO этил, -CONH2 или
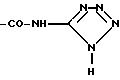
Среди предпочтительных значений R4 можно назвать, в частности, цианильный радикал, радикал -(CH2)m1-SO2-X-R10, как указано выше, и, в частности, нижеперечисленные радикалы:
-SO2 -NH-CO-NH-CH2-CH = CH2, -SO2-NH-СО-NH-СН2-CH2-CH3,
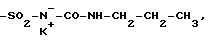
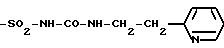
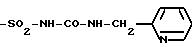
Предметом настоящего изобретения также является метод получения продуктов формулы (I), отвечающий формуле (Ia):
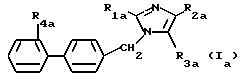
в которой:
R2a представляет собой линейный или разветвленный алкильный или алкенильный радикал, включающий не более 4 атомов углерода,
R2a и R3a, одинаковые или различные, выбраны среди :
а) атома водорода, радикалов, таких как меркапто, формильный, карбоксильный, свободный или превращенный в соль или в сложный эфир, галогенного атома, гидроксильного, цианильного, нитрильного, ацильного радикалов;
б) радикалов, таких как алкильный, алкенильный, алкоксильный, алкилтионильный, в котором атом серы может быть моно или диокисленным, причем каждый из вышеуказанных радикалов может быть линейным или разветвленным и включает не более 6 атомов углерода, таких радикалов как фенильный, бензоильный, фенилтионильный, в котором атом серы может быть моно или диокисленным, причем все перечисленные радикалы могут быть замещены одним или несколькими одинаковыми или различными радикалами, выбранными среди:
галогенных атомов,
таких радикалов, как гидроксильный, трифторметильный, цианильный, нитрильный, формильный, алкильный и алкоксильный, включающий не более 4 атомов углерода, фенильный и карбоксильный, свободный, превращенный в соль или в сложный эфир,
в) радикалов
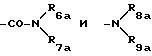
в которых:
или R6a, R7a, R8a и R9a одинаковые или различные, выбраны среди атома водорода, аминокислот, алкильных радикалов, причем указанные радикалы включают не более 6 атомов углерода, фенильного, бензильного, фенетильного радикалов,
или R6a и R7a и R8a и R9a соответственно образуют с атомом азота, с которым они связаны, гетероциклический радикал, причем эти одинаковые или различные радикалы выбраны среди таких радикалов, как имидазолильный, пирролильный, пирролинильный, пирролидинильный, пиридильный, пиперидинильный, пиримидинильный, пиридазинильный, пиразинильный, пиперазинильный, фенилпиперазинильный, пиперидильный, оксазолильный, морфолинильный и тиоморфолинильный, азепинный, индолильный, причем перечисленные радикалы могут быть замещены одним или несколькими одинаковыми или различными радикалами, выбранными среди галогенных атомов, радикалов, таких как гидроксильный, нитрильный, алкильный и алкоксильный, причем указанные радикалы включают не более 6 атомов углерода и фенила,
R4a представляет собой радикал, такой как цианильный, карбоксильный, свободный, превращенный в соль или в сложный эфир, радикал -(CH2)p-SO2-Xa-R10a, в котором p имеет значения 0 и 1, Xa представляет собой радикалы -NH- -NH-CO- -NH-CO-O-,
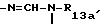
Предметом настоящего изобретения также является метод получения продуктов формулы (I), отвечающий формуле (1b):
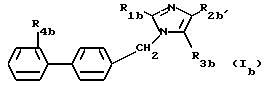
в которой
R1b представляет собой алкильный радикал, включающий не более 4 атомов углерода,
R3b представляет собой атом водорода, формильный, ацилоксильный, алкильный или алкоксильный радикал с возможностью замещения и карбоксильный радикал, свободный, превращенный в соль или в сложный эфир алкильным радикалом,
R2b представляет собой такой радикал, как фенилтионильный, фенилсульфонильный, фенилсульфинильный, алкилтионильный, алкилсульфонильный или алкилсульфинильный, с возможностью замещения, как во всех радикалах, которые могут быть представлены R2b и R3b, алкильный, алкоксильный радикалы, включающие не более 6 атомов углерода, а фенильные радикалы могут быть замещены одним или несколькими радикалами, выбранными среди галогенных атомов и таких радикалов, как гидроксильный, трифторметильный, ацилоксильный, карбоксильный, свободный, превращенный в соль или в сложный эфир, фенильный, пиридильный, тетразолильный, алкильный и алкоксильный, включающие не более 4 атомов углерода, причем они сами могут быть замещены алкоксильным радикалом, включающим не более 4 атомов углерода,
R4b представляет собой такой радикал, как цианильный, карбоксильный, свободный, превращенный в соль или в сложный эфир, радикал -SO2-Xb-R10b, в котором Xb представляет собой радикал -NH-, -NH-CO-, -NH-CO-O-
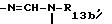
одинаковые или различные, представляют собой атом водорода, метильный, этильный, пропильный, винильный, аллильный, пиридильный, фенильный, бензильный, нитропиридильный, пиримидильный, тетразолильный, диазолильный, пиперидинильный, алкилпиперидинильный, тиазолильный, алкилтиазолильный, тетрагидрофуранильный, метилтетрагидрофуранильный, причем вышеуказанные продукты формулы (Ib) могут иметь любые возможные изомерные рацемические, энантиомерные и диастереоизомерные формы, а также добавляемые соли с неорганическими и органическими кислотами или с неорганическими и органическими основаниями вышеуказанных продуктов формулы (Ib), причем отличительной особенностью является то, что для их получения, как описано выше, используют продукты формул (А), (II), (III) и реактив, способный ввести радикал R'2, в которых R'1, R'2, R'3 и R'4 имеют значения, указанные выше соответственно для R1b, R2b, R3b и R4b, в которых функциональные группы могут быть защищены.
Предметом настоящего изобретения является, в первую очередь, вышеуказанный метод получения продуктов формулы (I), отвечающий формуле
(Id):
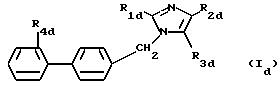
в которой:
R1d представляет собой алкильный радикал, включающий не более 4 атомов углерода,
R3d представляет собой радикал:
карбоксильный, свободный или превращенный в соль или в сложный эфир линейным или разветвленным алкильным радикалом, включающим не более 4 атомов углерода, формильный, ацилоксильный, алкильный, включающий не более 4 атомов углерода, с возможностью замещения гидроксильным радикалом,
R2d представляет собой радикал:
фенилтионильный, фенилсульфонильный, фенилсульфинильный, алкилтионильный, алкилсульфонильный или алкилсульфинильный, в котором алкильный радикал включает не более 4 атомов углерода,
R4d представляет собой радикал -SO2-NH2, -SO2-NH-CO-O-R10d, -SO2-N=CH-NR13d или -SO2-NH-CO-NH-R10d, в котором R10d и R13d, одинаковые или различные, выбраны среди атома углерода, метильного, этильного,
Предметом настоящего изобретения является, в первую очередь, вышеуказанный метод, отличающийся тем, что используется продукт формулы (А), в которой R'4 представляет собой радикал -SO2-NH2, -SO2-NH-CO-O-R10d, -SO2-N= CH-NR13d или -SO2-NH-CO-NH-R10d, в котором R10d и R13d, одинаковые или различные, выбраны среди атома углерода, метильного, этильного,
продукт формулы (II), в которой R'3 представляет собой радикал, такой как карбоксильный, свободный, превращенный в соль или в сложный эфир линейным или разветвленным алкильным радикалом, включающим не более 4 атомов углерода, формильный, ацилоксильный или алкильный, включающий не более 4 атомов углерода, с возможностью замещения гидроксильным радикалом,
продукт формулы (III), в которой R'1 представляет собой алкильный радикал, включающий не более 4 атомов углерода, и реактив, способный ввести заменитель R'2, в котором R'2 представляет собой радикал, такой как фенилтионильный, фенилсульфонильный, фенилсульфинильный, алкилтионильный, алкилсульфонильный или алкилсульфинильный, в которых алкильный радикал включает не более 4 атомов углерода, а функциональные группы могут быть замещены.
Предметом
настоящего изобретения является, в первую очередь, вышеуказанный метод, отличающийся тем, что использованию подлежит продукт формулы (А), в которой R'4 представляет собой радикал
продукт формулы (II), в которой R'3 представляет собой алкоксильный или карбоксильный радикал, свободный, превращенный в соль или в сложный эфир, продукт формулы (III), в которой R'1 представляет собой алкильный радикал, включающий не более 4 атомов углерода, и реактив, способный ввести заменитель R'2, в котором R'2 представляет собой радикал, такой как алкилтионильный или фенилтионильный, с возможностью окисления в форме сульфоксида или сульфона, причем указанные алкоксильный, алкилтионильный и фенилтионильный радикалы могут быть замещены одним или несколькими радикалами, выбранными среди галогенных атомов, алкильного или алкоксильного радикалов, включающих не более 4 атомов углерода, трифторметильного, аминного, моно или диалкиламинного, цианильного, фенильного, гидроксильного, карбоксильного, свободного, превращенного в соль или в сложный эфир, ацильного и ацилоксильного радикалов.
Таким образом предметом настоящего изобретения также является вышеописанный метод, отличающийся тем, что
соединение формулы (А1):
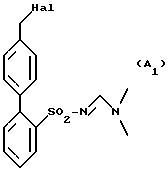
в которой Hal представляет собой галогенный атом, вводится в реакцию с окислителем для получения соединения формулы (В1):
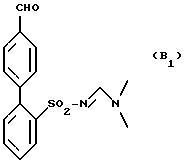
которое вводят в реакцию с соединением формулы (II):
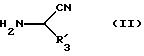
в которой R'3 имеет вышеуказанное значение, для получения продукта формулы (С1):
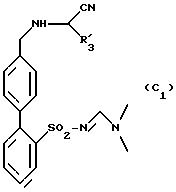
в которой R'3 имеет вышеуказанное значение, который вводят в реакцию с соединением формулы (III):
R'1-CO-Hal
в которой R'1 и Hal имеют вышеуказанное значение, для получения продукта формулы (D1):
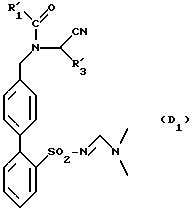
в которой R'1 и R'3 имеют указанные выше значения, который либо подвергают реакции присоединения на радикале CN с помощью реактива, способного ввести заменитель R'2, как определено выше, для получения продукта формулы (E1):
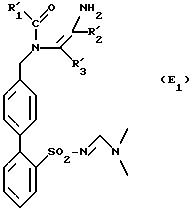
в которой R'1, R'2 и R'3 имеют указанные выше значения, который при необходимости подвергается реакции замещения атома кислорода атомом серы для получения продукта формулы (L1):
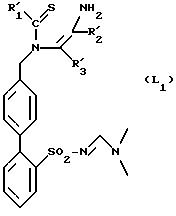
в которой R'1, R'2 и R'3 имеют указанные выше значения, который при желании и в случае необходимости превращают в продукт формулы (L2):
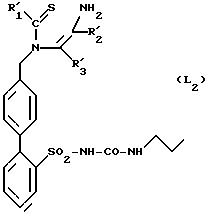
в которой R'1, R'2 и R'3 имеют указанные выше значения, продукт формулы (E1), (L1) или (L2), который подвергают реакции циклизации для получения продукта формулы (I'1 ) или (I'2):
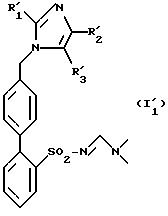
или
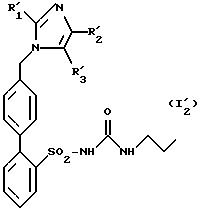
в которой R'1, R'2 и R'3 имеют указанные выше значения, с превращением, в случае необходимости, продукта формулы (I'1) в продукт формулы (I'2), как указано выше,
либо подвергают продукт формулы (D1) реакции присоединения на радикале
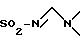
для получения продукта формулы (D2):
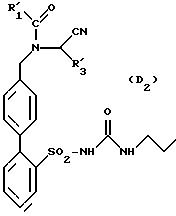
в которой R'1 и R'3 имеют указанные выше значения,
который подвергают реакции присоединения на радикале CN, как указано выше, для получения продукта формулы (E2):
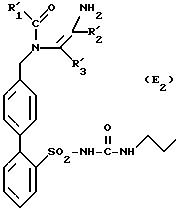
в которой R'1, R'2 и R'3 имеют указанные выше значения, который подвергают реакции циклизации для получения продукта формулы (I'2), как указано выше.
Предметом
настоящего изобретения, в частности, является вышеописанный метод получения продуктов формулы (I), отвечающих следующим формулам:
- 2-бутил 1-[[2'-карбокси(1,1'-6ифенил)-4-ил]метил]
4- (фенилтио) 1Н-имидазол-5-карбоновая кислота,
- 2-бутил 1-[[2'-карбокси(1,1'-бифенил)-4-ил]метил] 4- (метилтио) 1Н-имидазол-5-карбоновая кислота,
- 4'-[[2-бутил
4-(этилтио)5-(гидроксиметил) 1Н-имидазол-1-ил] метил] (1,1'-бифенил)-2-карбоновая кислота,
- 2-бутил 1-[[2'-карбокси(1,1'-бифенил)-4-ил]метил] 4- (этилсульфонил) 1Н-имидазол-5-карбоновая
кислота,
- 2-бутил 1-[[2'-карбокси(1,1'-бифенил)-4-ил]метил] 4- (этилсульфинил) 1Н-имидазол-5-карбоновая кислота,
- 2-бутил 1-[[2'-карбокси(1,1'-бифенил)-4-ил]метил] 4- (этилтио)
1Н-имидазол-5-карбоновая кислота,
- 2-бутил 1-[[2'-карбокси(1,1'-бифенил)-4-ил]метил] 4- (фенилсульфонил) 1Н-имидазол-5-карбоновая кислота,
- 2-бутил 1-[[2'-карбокси(1,
1'-бифенил)-4-ил]метил] 4- (фенилсульфинил) 1Н-имидазол-5-карбоновая кислота,
- 2-бутил 1-[[2'-тетразолил(1,1'-бифенил)-4-ил] метил] 4- (метилтио) 1Н-имидазол-5-карбоновая кислота,
- 2-бутил 4-(метилтио)1-[[2'-((((пропиламино)карбонил) амино)сульфонил)(1,1'-бифенил)-4-ил]метил]-1Н-имидазол 5- карбоксилат этила,
- 2-бутил 4-(метилтио)1-[[2'-((((пропиламино)карбонил)
амино)сульфонил)(1,1'-бифенил)-4-ил] метил]-1Н-имидазол 5- карбоновая кислота,
- 2-бутил 4-(метилтио)1-[[2'-((((пропиламино)карбонил) амино)сульфонил)(1,1'-бифенил)-4-ил] метил] -1Н-имидазол
5- карбоновая кислота, дикалиевая соль.
В предпочтительных условиях внедрения настоящего изобретения продукт формулы (В) может быть получен путем окисления галогенида формулы (А), например с помощью гексаметилентетрамина в 50- процентной уксусной кислоте или с помощью N-оксид N-метилморфолина в растворителе, таком как, например, дихлорметан, дихлорэтан или же толуол.
Продукт формулы (А) таков, что Hal представляет собой, в первую очередь, атом брома, но может также представлять собой атом хлора или иода.
Реакция соединения формулы (В) с
соединением (II) может осуществляться путем восстановительного аминирования, выполняемого в два этапа:
Первым этапом является образование имина продукта формулы (В) путем добавления продукта
формулы (II) к альдегидной функциональной группе продукта формулы (В) в растворителе, таком как, например, дихлорметан, дихлорэтан или тетрагидрофуран, желательно в условиях кислого катализа,
например,
в присутствии амберлиста H+ или же уксусной кислоты.
Вторым этапом является восстановление полученного таким образом имина с помощью восстановителя, такого как, например, NaBH3CN или NaBH(OAc)3 (предварительно полученного на основе боргидрида натрия и уксусной кислоты).
Продукт формулы (С) превращается в продукт формулы (D) с помощью ацилирующего средства, например, кислого галогенида, такого как, в частности, хлористый бутирил или хлористый валерил, в присутствии карбоната натрия или калия, пиридина или триэтиламина, в растворителе, таком как, например, ацетон, тетрагидрофуран, дихлорметан или дихлорэтан.
Продукт формулы (D) превращается в продукт формулы (E) путем добавления радикала R'2 к цианильной функциональной группе; указанное аминирование может производиться в растворителе, таком как, например, спирт, такой как метиловый или этиловый, в результате реакции соединения R'2-SH с цианильной функциональной группой в растворителе, таком как, например, толуол, тетрагидрофуран или дихлорэтан.
В случае если R'2 представляет собой радикал, включающий атом серы, реакцией продукта формулы (D) для получения соответствующего продукта формулы (E) является реакция тиоаминирования, выполняемая воздействием соединения формулы R10-SH, в которой R10 представляет собой остаток радикала R'2, как указано выше, в частности линейный или разветвленный алкильный радикал, включающий не более 4 атомов углерода, или фенильный радикал, причем указанные радикалы могут быть замещены, как указано выше.
Тиоаминирование может выполняться, например, путем барботирования вышеуказанного соединения формулы R10-SH в растворителе, например, в спирте, таком как этиловый или метиловый, или же в дихлорэтане, дихлорметане, толуоле, тетрагидрофуране, в присутствии основания, например, триэтиламина.
Тиоаминирование может также выполняться с использованием реактива R10SNa или R10SK с теми же растворителями, что и указанные для соединения R10SH.
Реакция замещения атома кислорода атомом серы для получения продукта формулы (L) может выполняться, например, с помощью реактива Лоусона.
Реакция циклизации продукта формулы (E) в продукт формулы (I') может выполняться, например, либо путем кислого катализа с использованием, например, амберлиста H+, n-толуолсульфокислоты или серной кислоты, в растворителе, таком как, например, толуол, этилацетат, дихлорметан, дихлорэтан, либо с использованием пентахлорида в пиридине или диметиламинопиридине, либо же в диметилсульфоне.
Различные функциональные группы, которые могут входить в некоторые соединения определенных выше реакций могут, при необходимости, быть защищены: речь идет, например, о таких радикалах, как гидроксильный, ацильный, свободный карбоксильный или же аминный и моноалкиламинный, которые могут быть защищены соответствующими защитными группами.
Перечень различных используемых защитных групп приводится, например, во французском патенте BF 2 499 995.
Ниже приводится неисчерпывающий перечень примеров защиты функциональных
групп:
гидроксильные группы
могут быть защищены, например, алкильными радикалами, такими как, например, трет-бутильный, триметилсилильный, трет-бутилдиметилсилильный, метоксиметильный,
тетрагидропиранильный, бензильный или
ацетильный,
аминные группы могут быть защищены, например, такими радикалами, как ацетильный, тритильный, бензильный, трет-бутоксикарбонильный, фталимидо
или другими радикалами, известными в
химии пептидов,
ацильные группы, такие как формильная группа, могут быть защищены, например, в виде
циклических или нециклических кеталей, таких как
диметил или диэтилкеталь или
диоксикетальный этилен,
кислые центры описанных выше продуктов могут, при желании, быть аминированы первичным или вторичным амином, например в метиленхлориде в
присутствии, например,
хлоргидрата 1-этил-3- (диметиламинопропил)карбодиимида при комнатной температуре,
кислые центры могут быть защищены, например, в виде сложных эфиров, полученных с
помощью легкорасщепляемых
сложных эфиров, таких как бензиловые или трет-бутиловые сложные эфиры, или же сложных эфиров, широко известных в химии пептидов.
Как и в случае продуктов формулы (I'), продукты формул (D) и (E) могут подвергаться в рамках вышеописанного метода различным вышеуказанным реакциям, касающимся, в частности, заменителя R'4, как указано выше.
Таким образом продукт формулы (E1) может быть превращен в продукт формулы (E2) до продолжения синтеза, как это указано выше в отношении превращения продукта формулы (D1) в продукт (D2).
В зависимости от значений R'1, R'2, R'3 и R'4, продукты формул (I'), (I'1) или (I'2), как определено выше, являются или не являются продуктами формулы (I).
Реакции, которым могут подвергаться продукты вышеуказанных формул (D), (Е) и (I'), могут осуществляться при желании и в случае необходимости, например, как описано ниже.
а) В отношении возможных карбоксильных функциональных групп описанные выше продукты могут при желании явиться предметом реакции превращения в соль с помощью неорганического или органического основания или же реакции превращения в сложный эфир, причем указанные реакции превращения в сложный эфир или в соль могут выполняться с использованием обычных методов, хорошо известных специалистам.
б) Возможные превращения сложноэфирных групп в кислую функциональную группу могут, при желании, выполняться в общепринятых у специалистов условиях, в частности, методом кислого или щелочного гидролиза с использованием, например, едкого натра или едкого кали в спиртовой среде, как, например, в метаноле или же с использованием хлористоводородной или серной кислоты.
в) Возможные цианильные функциональные группы вышеописанных продуктов могут при желании быть превращены в кислую функциональную группу в общепринятых у специалистов условиях, в частности, методом двойного гидролиза в кислой среде, как, например, в смеси серной кислоты, ледяной уксусной кислоты и воды, причем указанные три компонента используются, как правило, в равных пропорциях, или же в кипящей смеси едкого натра, этанола и воды.
г) Возможные функциональные карбоксигруппы, свободные или превращенные в сложный эфир, описанных выше продуктов могут, при желании, быть превращены в спиртовую функциональную группу общеизвестными у специалистов методами: для функциональных карбоксигрупп, превращенных в сложный эфир, можно использовать, в частности, гидрид лития и алюминия в растворителе, таком как, например, тетрагидрофуран или же диоксан или этиловый эфир.
Для свободных функциональных карбоксигрупп можно использовать, в частности, гидрид бора.
д) Возможные функциональные алкоксигруппы, в частности такие, как метокси, описанных выше продуктов могут, при желании, быть превращены в гидроксильную функциональную группу в общепринятых у специалистов условиях, например трибромидом бора в таком растворителе, как, например, метиленхлорид, бромгидратом или хлоргидратом пиридина или же бромистым водородом или хлористоводородной кислотой в воде или в уксусной кислоте в состоянии кипения.
е) Возможные функциональные группы, включающие атом серы, описанных выше продуктов могут, при желании, быть превращены в соответствующую сульфоксидную или сульфонную группу в общепринятых у специалистов условиях, такими надкислотами, как, например, надуксусная или метахлорнадбензойная кислоты, или же озоном, оксоном, периодатом натрия в растворителе, таком как, например, метиленхлорид или диоксан, при комнатной температуре.
Для получения сульфоксидной функциональной группы может использоваться эквимолярная смесь продукта, включающего алкилтионильную или арилтионильную группу, и реактива, такого как, в частности, надкислота.
Для получения сульфонной функциональной группы может использоваться смесь продукта, включающего алкилтионильную или арилтионильную группу с избытком реактива, такого как, в частности, надкислота.
ж) Возможные спиртовые функциональные группы вышеописанных продуктов могут быть превращены, при желании, в альдегидную или кислую функциональную группу путем окисления в общепринятых у специалистов условиях, например, путем воздействия окисью марганца для получения альдегидов или реактива Джонса для доступа к кислотам.
з) Возможные
нитрильные функциональные группы описанных выше продуктов могут, при желании, быть превращены в тетразол в общепринятых у специалистов условиях, например
циклическим добавлением азидида металла,
например, азидида триалкила олова, в нитрильную функциональную группу, как в методе, описанном в следующей статье:
J. Organometallic Chemistry, 33,
337 (1971), С. Козима и др.
и) Реакции превращения формильного радикала в карбамоильный радикал и карбамоильного радикала в нитрильный радикал выполняются в общепринятых у специалистов условиях.
Кроме того, продукты формулы (I') подвергаются, при необходимости, указанным ниже реакциям.
Выделение защитных групп может производиться в общепринятых у специалистов условиях, в частности, путем кислого гидролиза, выполняемого с использованием такой кислоты, как хлористоводородная кислота, бензолсульфокислота или паратолуолсульфокислота, муравьиная или трифторуксусная кислота или же путем каталитической гидрогенизации. Группа фталимидо может быть выделена гидразином.
Превращение в соль выполняется с помощью неорганической или органической кислоты с использованием методов, хорошо известных специалистам.
Разделения рацемических форм для получения оптически активных форм продуктов формулы (I) осуществляется общепринятыми у специалистов методами.
Продукты формулы (I) известны и описаны, в частности, в патентных заявках ЕЭС N 0 465 368 и 0 503 162.
Продукты формулы (I), полученные в соответствии с вышеописанным методом, а также их добавляемые соли с кислотами обладают любопытными фармакологическими свойствами.
Продукты обладают антагонистическими свойствами для рецептора к ангиотензину II и являются, таким образом, ингибиторами действия ангиотензина II, в частности сосудосуживающего действия, а также трофического действия на уровне миоцитов.
Указанные свойства оправдывают употребление в качестве медикаментов продуктов формулы (I), полученных в соответствии с вышеописанным методом, причем указанные продукты формулы (I) могут иметь любые изомерные рацемические или оптически активные формы, а также добавляемые соли с приемлемыми с фармацевтической точки зрения неорганическими или органическими кислотами указанных продуктов формулы (I).
Продукты формулы (I), полученные в соответствии с вышеописанным методом, а также их добавляемые соли с приемлемыми с фармацевтической точки зрения неорганическими или органическими кислотами могут использоваться, в частности, в качестве медикаментов при лечении артериальной гипертонии, сердечной недостаточности, почечной недостаточности и для предупреждения рецидива стеноза ангиопластики.
Они могут также использоваться при лечении некоторых желудочно-кишечных и гинекологических нарушений и, в частности, для релаксации на уровне матки, в виде фармацевтических составов, включающих, в качестве действующего начала, как минимум один из определенных выше медикаментов.
Указанные фармацевтические составы могут применяться внутрь, ректальным путем, парентеральным путем или локально, нанесением на кожу или на слизистые оболочки.
Указанные составы могут быть твердыми или жидкими и иметь любую фармацевтическую форму, широко применяемую при лечении человека, как, например, простые или дражевидные таблетки, капсулы, гранулы, суппозитории, препараты для инъекций, мази, кремы, гели и препараты в аэрозольной упаковке; они производятся обычными методами. Действующее начало вводится в основы, обычно используемые при изготовлении фармацевтических составов, такие как тальк, аравийская камедь, лактоза, амидон, стеарат магния, какао-масло, водные или безводные связующие, жиры животного или растительного происхождения, производные парафина, гликоли, различные увлажняющие, диспергирующие или эмульсионные агенты, консерванты.
Обычно применяемые дозы могут, в зависимости от используемого препарата, от особенностей больного и от заболевания, составлять от 1 до 100 мг в день для взрослых при приеме внутрь.
Некоторые исходные продукты формулы (А) известны и могут быть приготовлены, например, как описано в патенте ЕЭС ЕР 0 503 162.
Продукты формулы (II) встречаются в торговой сети или могут быть получены как описано в патентной заявке ЕЭС N 0 465 368.
Продукты формулы (III) встречаются в торговой сети или могут быть легко получены из кислоты или соответствующего производного.
Предметом настоящего изобретения также являются, в качестве новых промышленных продуктов, соединения формул (В), (С), (D), (D1), (D2), (Е), (E1), (E2), (L), (L1) и (L2 ).
Приводимые далее примеры иллюстрируют изобретение, вместе с тем не ограничивая его.
Пример 1: 2-бутил 4-(метилтио) 1-[[2'-((((пропиламино) карбонил)амино)сульфонил)
1,1'(бифенил) 4-ил]метил]1Н- имидазол 5-карбоновая кислота дикалиевая соль
Этап А:
N-[(диметиламино)метилен] 4'-формил(1,1'-бифенил) 2-сульфонамид
Для начала вводят 10 г
N-[(диметиламино)метилен] 4-бромметил (1,1'-6ифенил) 2-сульфонамида, 8,14 г гексаметилентетрамина и 80
мл 50-процентной уксусной кислоты и взбалтывают в течение 1 ч при температуре +120oC.
После добавления 220 мл воды реакционную смесь нейтрализуют с помощью насыщенного раствора бикарбоната
натрия, экстрагируют с использованием дихлорметана, высушивают и выпаривают, в результате чего
получают 7,99 г искомого продукта.
SM MH+ 317
Спектр ЯМР: CDCl3
2,71 и 2,77 (2S, 6H
7,17 (S,
7,15 до 7,91 (система AB, 6H, ароматич.)
10, 11 (
Этап Б: аминоцианоацетат этил моно(4-метилбензолсульфоната)
50 г (E) циано(гидроксиимино)этилацетата вводят в 440 мл воды и 340 мл раствора бисульфата натрия, добавляют 150 г гидросульфита натрия и взбалтывают примерно в течение 30 мин. при температуре около +350oC.
Затем раствор насыщают путем добавления хлорида натрия, экстрагируют с использованием метиленхлорида и доводят до сухого состояния.
Остаток забирают в эфире: добавляют 44 г паратолуолсульфокислоты в 110 мл этанола, 740 мл эфира, удаляют растворители и в результате получают 35 г искомого продукта (tпл = 128-130oC).
Этап В: циано-[[[2'-[[[(диметиламино)метилен]амино] сульфонил] (1,1'(бифенил)
4-ил]метил]амино]этилацетат
Раствор 13 г аминоцианоацетат этил моно(4- метилбенэолсульфоната), полученного на
вышеописанном Этапе Б, 1 г амберлиста 15- (H+) и 12,3
продукта, полученного на Этапе А в дихлорметане, взбалтывают при температуре кипения примерно в течение 7 ч. Затем
указанный раствор охлаждают и добавляют во взвесь, содержащую 3,1 г боргидрида натрия,
14,2 мл ледяной уксусной кислоты и 60 мл дихлорметана при температуре +10oC.
Полученный таким образом раствор взбалтывают примерно в течение 18 ч. Затем добавляют 200 мл воды и фильтруют полученный осадок. Органическую фазу промывают водой, высушивают и концентрируют в вакууме. После очистки методом хроматографии на двуокиси кремния (элюент : дихлорметан-этилацетат (85 : 15)) получают 9 r искомого продукта в виде вязкой субстанции.
Rf (дихлорметан-этилацетат (85 : 15)) = 0,20.
Инфракрасный спектр (CHCl3)
3340 (-NH-) 1754 (C=O) 1628 (N=CH-N) 1344, 1148 (SO2).
Спектр ЯМР
CDCl3
1,37 (t, J= 7,
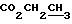
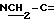
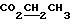
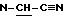
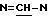
Этап Г:
циано-[[[2'-[[[(диметиламино)метилен]амино]сульфонил] (1,1'(бифенил)
4-ил]метил](1-оксопентил)амино]этилацетат
К раствору 11,1 г циано-[[[2'-[[[(диметиламино)метилен] амино]сульфонил] (1,
1'(бифенил) 4-ил] метил] амино] этилацетат, полученного на вышеописанном
Этапе В, в 200 мл сухого ацетона добавляют 5,53 г K2CO3 и 3,33 мл хлорида валерила. Раствор взбалтывают в
течение 20 ч при комнатной температуре, фильтруют и доводят до сухого
состояния. После очистки методом хроматографии на двуокиси кремния (элюант : дихлорметан-этилацетат (85 : 15)) получают 11,6 г
белого твердого вещества.
Rf
(дихлорметан-этилацетат (85 : 15)) = 0,24
Этап Д: 3-амино 2-[[[2'-[[[(диметиламино)метилен] амино] сульфонил] (1,1'(бифенил) 4-ил]
метил] (1-оксопентил)амино] 3-(метилтио) 2-пропеноат
этила
Для начала вводят 250 мг циано-[[[2'-[[[(диметиламино) метилен]амино] сульфонил] (1,1'(бифенил) 4-ил]
метил](1- оксопентил)амино]этилацетата, полученного на вышеописанном Этапе Г, 2,5
мл этанола и 7 мкл триэтиламина, охлаждают до -5oC и барботируют метантиол в течение 10 мин. Затем
взбалтывают в течение 1 ч при температуре -5oC, дают температуре подняться до
уровня комнатной и взбалтывают еще в течение 48 ч. Затем барботируют азот в течение 1 ч при комнатной
температуре и удаляют растворители при пониженном давлении. После хроматографии на двуокиси
кремния (элюант : дихлорметан-этилацетат (80 : 20)) получают 0,91 г искомого продукта.
Этап
E: 2-бутил 4-(метилтио) 1-[[2'-[[[(диметиламино) метилен]амино]сульфонил](1,
1'(бифенил)4-ил]метил] 1Н-имидазол 5-карбоксилат этила
Для начала вводят 50 мг 3-амино 2-[[[2'-[[[(диметиламино)
метилен]амино] сульфонил)(1,1'(бифенил)4-ил] метил] (1- тиопентил)амино]
3-(метилтио)2-пропеноата этила, полученного на вышеописанном Этапе Д, 500 мкл толуола и каталитическое количество амберлиста
15. Затем нагревают при температуре кипения в течение 20 ч, фильтруют
амберлист, промывают, удаляют растворители при пониженном давлении и в результате получают 0,20 г искомого продукта.
Этап Ж: 2-бутил 4-(метилтио)1-[[2'-[[[амино]сульфонил] (1,
1'(бифенил)4-ил]метил] 1Н-имидазол 5-карбоксилат этила
Раствор 43,5 г 2-бутил 4-(метилтио) 1-[[2'-[[1(диметиламино)
метилен] амино] сульфонил] (1,1'(бифенил)4-ил]метил] 1Н-имидаэол
5-карбоксилат этила, полученного на вышеописанном Этапе E, в 800 мл метанола, 400 мл концентрированной хлористоводородной кислоты
доводят за 3 ч до температуры кипения. Затем метанол выпаривают, pH
оставшейся фазы доводят до уровня pH 5-6 путем добавления 6 н. едкого натра. После этого три раза экстрагируют с использованием
эфира (400 мл), высушивают на Na2SO4 и выпаривают
растворитель. Таким образом получают 37,5 г сырого продукта, который сгущают в смеси 50 мл этанола и 500 мл простого
изопропилового эфира, после чего фильтруют. В результате получают 31,4 г искомого
белого твердого продукта (tпл = 127-129oC).
Этап 3: 2-бутил
4-(метилтио)1-[[2'-[[[(пропиламино)карбонил] амино] сульфонил](1,1'(бифенил)4-ил]метил]1Н-имидазол
5- карбоксилат этила
В среде инертного газа доводят до кипения раствор 10 г 2-бутил
4-(метилтио) 1-[[2'-[[[амино]сульфонил](1,1'(бифенил)4-ил] метил] 1Н-имидазол 5-карбоксилата этила,
полученного на вышеописанном Этапе Ж, 5,6 г карбоната калия (предварительно измельченного и
высушенного при пониженном давлении при температуре + 100oC в течение 2 ч. в 70 мл диметилэфира
этиленгликоля. По истечении 1 ч добавляют 4 мл н-пропилизоцианата и продолжают нагревать еще
в течение 30 мин. Затем температуре дают опуститься до уровня комнатной и выпаривают растворитель. После
этого к остатку добавляют 100 мл воды и доводят pH до уровня pH 5-6 путем добавления 1 н.
хлористоводородной кислоты. Продукт кристаллизуется. Затем выполняют рекристаллизацию из 50 мл этилацетата и
получают 10,1 г искомого продукта.
Этап И: 2-бутил 4-(метилтио)
1-[[2'-[[[(пропиламино)карбонил] амино]сульфонил] 1,1'(бифенил)4-ил] метил]1Н-имидазол 5-карбоновая кислота дикалиевая
соль
При температуре 0oC к раствору 2 г 2-бутил
4-(метилтио)1- [[2'-[[[(пропиламино)карбонил] амино] сульфонил](1,1'(бифенил) 4-ил]метил]1Н-имидазол 5-карбоксилата этила,
полученного на вышеописанном
Этапе 3, в 40 мл этанола добавляют 2,3
мл 6 н. раствора едкого кали. Затем температуре дают подняться до уровня комнатной. По истечении 72 ч осадок
центрифугируют и промывают с использованием 4 мл этанола, а затем 4 мл этилацетата. Таким
образом после высушивания получают 2,04 г целевого продукта (tпл > 260oC).
Химический состав для C26H30K2O5
S2;
% расчетный: С 50,30; H 4,87; N 9,02; S 10,33;
%полученный: С 50,5; H 4,9; N 9,
0; S 10,3.
Пример 2: 2-бутил 4-(метилтио) 1-[[2'-[[[(пропиламино)
карбонил]амино] сульфонил] 1,1'(бифенил)4-ил] метил]1Н-имидазол 5-карбоновая кислота дикалиевая соль
1)
Циано-[[[2'-[[[(диметиламино)метилен] амино] сульфонил] (1,
1'-бифенил)4-ил]метил]амино]этилацетат
2 г аминоцианоацетат этил моно(4-метилбензолсульфоната), полученного на Этапе Б Примера 1,
смешивают с 1,9 г N-((диметиламино)метилен]4'-формил (1,
1'-бифенил)2-сульфонамида, полученного на Этапе А Примера 1, и взбалтывают в дихлорметане в течение 3 ч при температуре +35oC, после
чего добавляют 0,396 г цианоборгидрида натрия и
взбалтывают раствор в течение 18 ч при комнатной температуре. Затем реакционную смесь фильтруют, промывают водой и выпаривают. Таким образом после
хроматографии на двуокиси кремния (элюант :
дихлорметан-этилацетат (85 : 15)) получают 770 мг искомого продукта, идентичного продукту, полученному на Этапе В Примера 1.
2) Операции выполняют как в Примере 1, заменив продукт, полученный на Этапе В Примера 1, продуктом, полученным в вышеописанном п. 1), в результате чего получают целевой продукт: 2-бутил 4-(метилтио)1-[[2'-[[[пропиламино)карбонил] амино] сульфонил]1, 1'(бифенил)4-ил]метил] 1Н-имидазол 5-карбоновую кислоту дикалиевую соль.
Пример 3: 2-бутил 4-(метилтио)
1-[(2'-(((пропиламино) карбонил)амино)сульфонил)1,1'(бифенил)4-ил]метил]
1Н-имидазол 5-карбоновая кислота дикалиевая соль
Этап А: [[[2'-(аминосульфонил)(1,1'-бифенил)4-ил] метил]
(1- оксопентил)амино]цианоацетат этила
При температуре +100oC
взбалтывают в течение 30 мин. 1,0 г циано-[([2'-[[[(диметиламино) метилен] амино]сульфонил] (1,1'(бифенил)4-ил]метил]
(1-оксопентил)амино] этилацетата, полученного на Этапе Г Примера 1, в 20 мл
диметилэфира этиленгликоля и 10 мл концентрированной хлористоводородной кислоты. После охлаждения до комнатной температуры
pH раствора доводят до уровня pH ≈ 6 путем добавления 6 н. едкого
натра. Затем раствор экстрагируют с использованием этилацетата. Органические фазы промывают водой, насыщенной хлоридом натрия,
и высушивают. После очистки методом хроматографии на двуокиси кремния
(элюант : этилацетат-гептан (4 : 1)) получают 320 мг искомого продукта.
Этап Б: Получение
циано-[[[2'-[[[(пропиламино)карбонил] амино]сульфонал] (1,
1'-бифенил)4-ил]метил](1-оксопентил)амино] этилацетата
7,2 г [[[2'-(аминосульфонил)(1,1'-бифенил)4-ил] метил] (1- оксопентил)амино]
цианоацетат этила, полученного на вышеописанном Этапе А, 6,
5 г безводного карбоната калия и 1,48 мл н-пропилизоцианата взбалтывают в течение 2 ч 30 мин. при температуре кипения в 180 мл ацетона.
После охлаждения раствор обрабатывают 2 н. хлористоводородной
кислотой. Полученный остаток растворяют в водной смеси дихлорметана. После экстрагирования с использованием метиленхлорида, высушивания и
удаления растворителей при пониженном давлении продукт
подвергают рекристаллизации из этилацетата и получают, таким образом, 6,5 г твердого белого искомого продукта.
Rf (SiO2, этилацетат = 0,48.
МР 131-133oC.
Этап В: 3-амино 2-[[[2'-[[[(пропиламино)карбонил] амино] сульфонил] (1,1'-бифенил)4-ил] метил]
(1-оксопентил)амино] 3- (метилтио) 2-пропеноат этила
Раствор 8,5 г циано-[[[(2'-[[[(пропиламино)карбонил]амино] сульфонил] (1,1'-бифенил)4-ил] метил] (1-оксопентил)амино] этилацетата,
полученного на вышеописанном Этапе Б, и 2,4 мл триэтиламина в 100 мл
дихлорметана насыщают метантиолом, выполняя продувку через взбалтываемый и охлажденный до -20oC раствор. Затем
температуре дают подняться и выдерживают раствор в течение 48 ч под
воздействием азота при давлении 10 баров и температуре +40oC. После концентрации остаток очищают методом хроматографии
на двуокиси кремния (элюант : дихлорметан-MeOH (20: 1)). В результате
получают 8,0 г искомого продукта.
Rf (SiO2, дихлорметан-MeOH (20 : 1)) = 0,39
Этап Г: 2-бутил 4-(метилтио)1-[[2'-[[[(пропиламино) карбонил] амино] (1,
1'-бифенил)4-ил]метил]1Н-имидазол 5-карбоксилат этила
180 мг пентахлорида фосфора взвешивают в 16 мл дихлорметана в
среде аргона. Затем охлаждают до температуры -78oC и добавляют
230 мг диметиламинопиридина, растворенного в 10 мл безводного дихлорметана, и взбалтывают в течение еще 10 мин. Затем при
температуре -78oC добавляют раствор 500 мг 3-амино
2-[[[2'- [[[(пропиламино)карбонил] амино] сульфонил](1,1'-бифенил) 4-ил] метил](1-оксопентил)амино] 3-(метилтио) 2-пропеноата этила,
полученного на вышеописанном Этапе В, в 25 мл дихлорметана и
взбалтывают при комнатной температуре в течение 18 ч. Осадок фильтруют, промывают водой и высушивают. После хроматографии на двуокиси
кремния (элюант : дихлорметан-MeOH (20: 1)) получают 330 мг сырого
продукта, который подвергают кристаллизации из смеси этилацетата и н-гептана, в результате чего получают 270 мг белого твердого
вещества (tпл = 127-129oC).
Rf (SiO2, этилацетат / н-гептан (4 : 1)) = 0,42
Этап Д: 2-бутил 4-(метилтио)
1-[[2'-[[[(пропиламино)карбонил] амино]сульфонил](1,1'-бифенил)4-ил]метил] 1Н-имидазол
5-карбоновая кислота
Раствор 130 мг 2-бутил 4-(метилтио) 1-[[2'-[[[(пропиламино) карбонил]амино]
сульфонил](1,1'-бифенил)4-ил]метил] 1Н- имидазол 5-карбоксилата этила в 10 мл метанола и 3,1
мл 2 н. едкого натра взбалтывают в течение 18 ч при комнатной температуре. Затем метанол выпаривают, а
оставшийся водный раствор подкисляют до pH ≈6 путем добавления 2 н. хлористоводородной
кислоты. Осадок фильтруют, промывают водой и высушивают при пониженном давлении. В результате получают
115 мг искомого продукта (tпл = 109-111oC).
Этап Е:
2-бутил 4-(метилтио) 1-[[2'-[[[(пропиламино) карбонил]амино]сульфонил](1,1'-бифенил)4-ил]метил]1Н-имидазол
5-карбоновая кислота дикалиевая соль
Путем превращения в соль 2-бутил
4-(метилтио)1-[[2'- [[[(пропиламино)карбонил]амино]сульфонил](1,1'-бифенил)4-ил] метил] 1Н-имидазол 5-карбоновой кислоты,
полученной на вышеописанном Этапе Д, с использованием водного раствора едкого
кали, указанного в Примере 1, получают целевой продукт.
Пример 4: 2-бутил
4-(метилтио)1-[[2'-[[[(пропиламино) карбонил]амино]сульфонил] 1,1'(бифенил)4-ил] метил] 1Н-имидазол
5-карбоновая кислота дикалиевая соль
1) Циано-[[[2'-[[[(диметиламино)метилен] амино]
сульфонил] (1,1'-бифенил)4-ил]метил](1-оксопентил)амино]этилацетат
200 мг 3-амино
2-[[[2'-[[[(пропиламино)карбонил] амино] сульфонил] (1,1'-бифенил)4-ил] метил] (1-оксопентил)амино]
3- (метилтио)2-пропеноата этила, полученного на Этапе В Примера 3, растворяют в 5 мл диметилэфира
этиленгликоля и 1 мл концентрированной серной кислоты, которую добавляют при комнатной температуре.
После взбалтывания в течение 1 ч добавляют воды, одновременно охлаждая с помощью ледяной ванны.
Затем выполняют экстрагирование с использованием дихлорметана, промывают органические фазы, высушивают
и выпаривают растворитель при пониженном давлении. В результате получают 180 мг сырого продукта,
который подвергают кристаллизации с использованием этилацетата и получают 140 мг целевого продукта
(tпл = 130-132oC).
2) Синтез продолжают как в Примере 3, заменив продукт, полученный на Этапе Г Примера 3, продуктом, полученным в вышеописанном п. 1), в результате чего получают целевой продукт.
Пример 5: 2-бутил
4-(метилтио)1-[[2'-[[[пропиламино) карбонил]амино] сульфонил] 1,1'(бифенил)4-ил] метил] 1Н-имидазол 5-карбоновая кислота
дикалиевая соль
Этап А: циано-[[[2'-[[[(пропиламино)карбонил]амино]
сульфонил](1,1'-бифенил)4-ил]метил]амино]этилацетат
Раствор 2 г формил (1,1'-бифенил) 2-[2'-[[(пропиламино)
карбонил]амино] сульфонила] , полученного, как указано на Этапе А Примера 1, на
основе соответствующего сульфонамидного производного и 1,83 г цианоаминоацетата этила, полученного, как указано в
патентной заявке ЕЭС N 0 465 368, в 40 мл дихлорметана подвергают взбалтыванию в
течение 6 ч при температуре +35oC. При температуре +10oC указанный раствор добавляют к взвеси,
содержащей 11,55 ммолей боргидрида натрия, 2 мл ледяной уксусной кислоты и 30 мл
дихлорметана. Полученный таким образом раствор взбалтывают в течение 16 ч. После этого добавляют воды, экстрагируют
органическую фазу, промывают и высушивают, после чего выпаривают растворители при
пониженном давлении и хроматографируют на двуокиси кремния (элюант : дихлорметан-MeOH (30: 1)). В результате получают
1,8 г искомого продукта.
Rf (SiO2,
дихлорметан - MeOH (20 : 1)) = 0,39
Этап Б: циано-[[[2'-[[[(пропиламино)карбонил]амино] сульфонил](1,
1'-бифенил)4-ил]метил](1-оксопентил)амино] этилацетат
1,7 г
циано-[[2'-[[[(пропиламино)карбонил]амино]сульфонил] (1,1'-бифенил)4-ил] метил] амино] этилацетата, полученного на вышеописанном
Этапе А, растворяют в 50 мл ацетона и добавляют 0,79 г K2
CO3 и 0,45 мл хлористого валерила. Полученную таким образом смесь взбалтывают в течение 6 ч при комнатной температуре.
Нерастворимую фракцию фильтруют и фильтрат доводят до сухого состояния,
который очищают методом хроматографии на двуокиси кремния (элюант : дихлорметан-этилацетат (4 : 1)), в результате чего получают
295 мг искомого продукта.
Rf (SiO2, дихлорметан-этилацетат (4:1)) = 0,30.
Синтез продолжают как указано на Этапах В, Г, Д и Е Примера 3 для получения целевого продукта.
Пример 6: 2-бутил
4-(метилтио) 1-[[2'-((((пропиламино) карбонил)амино)сульфонил) 1,1'(бифенил)4-ил]метил] 1Н-имидазол 5-карбоновая кислота дикалиевая
соль
Этап А: 3-амино 2-[[[2'-[[[(пропиламино)карбонил]
амино] сульфонил] (1,1'-бифенил)4-ил]метил](1-тиопентил)амино]3- (метилтио) 2-пропеноат этила
Раствор 1 г 3-амино
2-[[[2'-[[[(пропиламино)карбонил]амино] сульфонил] (1,1'-бифенил)4-ил] метил]
(1-оксопентил)амино] 3-(метилтио) 2-пропеноата этила, полученного на Этапе В Примера 3, и 342 мг реактива Лоусона в 10 мл
безводного диметилэфира этиленгликоля взбалтывают при комнатной температуре в
течение 2-х суток. Затем раствор концентрируют при пониженном давлении, а остаток забирают в смеси дихлорметана и воды (1
: 1), После экстрагирования и промывки водой, высушивания и удаления
растворителей оставшуюся вязкую жидкость очищают и получают 506 мг искомого продукта.
Rf (SiO2, этилацетат - н-гептан (4:1)) = 0,45.
Этап Б:
2-бутил 4-(метилтио) 1-[[2'-[[[(пропиламино) карбонил]амино] сульфонил](1,1'-бифенил)4-ил]метил] 1H-имидазол 5-карбоксилат
этила
Раствор 150 мг 3-амино 2-[[[2'-[[[(пропиламино)карбонил]
амино]сульфонил] (1,1'-бифенил)4-ил] метил](1-тиопентил)амино] 3-(метилтио) 2-пропеноата этила, полученного на вышеописанном
Этапе А, 34 мкл и 24 мкл диметилсульфона в 5 мл дихлорметана взбалтывают в
течение 15 ч при температуре кипения. После охлаждения до комнатной температуры раствор промывают насыщенным раствором
хлорида натрия и выпаривают досуха при пониженном давлении. После хроматографии
на двуокиси кремния (элюант : этилацетат-н-гептан (2 : 1)) получают 35 мг искомого продукта.
Выполнение синтеза продолжают затем как указано на Этапах Д и Е Примера 3 для получения целевого продукта.
Реферат
Изобретение относится к новому способу получения серосодержащих
производных имидазола формулы I
R4-C6H4-C6H4-CH2-NC4R, R2R3,
отличающийся тем, что
соединение формулы (A)
Hal-C6H4-C6H4R'4
вводят в реакцию с окислителем для получения соединения формулы (B)
CHO-C6H4-C6H4-R41,
которое затем вводят в реакцию с соединением формулы (II)
H2N-CH(CN)-R31,
где возможные функциональные группы могут быть защищены для
получения соединения формулы (С)
R31-CH(CN)-NH-CH2-C6H4-C6H4-R41,
которое вводят в реакцию с соединением формулы (III)
R11-CO-Hal
для получения соединения формулы (D)
R31
-CH(CN)-N(COR1CH2-C6H4C6H4-R41,
которое подвергается реакции присоединения на радикале CN с
помощью реактива, способного ввести заместитель R21, в котором возможные функциональные
группы могут быть защищены для получения соединения формулы (Е)
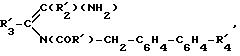
которое при необходимости подвергается реакции замещения атома кислорода атомом серы для получения соединения формулы (L)
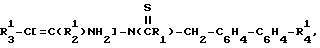
после чего соединение формулы (Е) и соединение формулы (L) подвергают реакции циклизации для получения соединения формулы (I). Все значения радикалов указаны в п. 1 формулы изобретения. Описаны также новые промежуточные продукты. Соединения формулы (I) обладают антагонистическими свойствами для рецептора к ангиотензину II и являются ингибиторами действия ангиотензина II. 6 c. и 1 з.п. ф-лы.
Формула
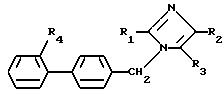
в которой R1 представляет собой алкильный радикал, включающий не более 4 атомов углерода;
R3 представляет собой радикал, такой, как карбоксильный, свободный или превращенный в соль или в сложный эфир, в котором линейный или разветвленный алкильный радикал включает не более 4 атомов углерода;
R2 представляет собой алкилтионильный радикал, в котором алкильный радикал включает не более 4 атомов углерода;
R4 представляет собой такой радикал, как -SO2 - NH - CO- NHR10, -SO2-NH2, -SO2N = CHNR13, в котором R10 и R13, одинаковые или различные, выбраны из метила, этила, н-пропила, отличающийся тем, что соединение формулы A
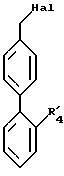
в котором R41 имеет вышеуказанные значения для R4, а HaL представляет собой атом галогена, вводят в реакцию с окислителем для получения соединения формулы B
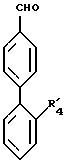
в которой R41 имеет вышеуказанное значение, и которое вводят в реакцию с соединением формулы II
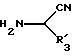
в которой R31 имеет значение, указанное выше для R3 и в которой возможные функциональные группы могут быть защищены для получения соединения формулы C
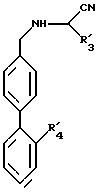
в которой R31 и R41 имеют вышеуказанные значения, и которое вводят в реакцию с соединением формулы III
R11 - CO - HaL,
в которой R11 имеет значение, указанное выше для R1, HaL представляет собой атом галогена, для получения соединения формулы D
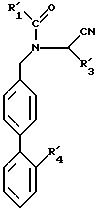
в которой R11, R31 и R41 имеют указанные выше значения, которые подвергаются реакции присоединения на радикале CN с помощью реактива, способного ввести заместитель R21, причем R21 имеет значение, указанное выше для R2, в котором возможные функциональные группы могут быть защищены, для получения соединения формулы E
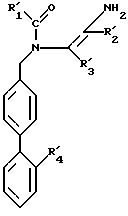
в которой R11, R21, R31 и R41 имеют указанные выше значения, которые при необходимости подвергаются реакции замещения атома кислорода атомом серы для получения соединения формулы L
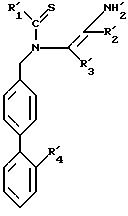
в которой R11, R21, R31 и R41 имеют указанные выше значения, после чего соединение формулы E или соединение формулы L подвергают реакции циклизации для получения соединения формулы I, в которой R1, R2, R3, R4 имеют указанные выше значения.
2-бутил-4-(метилтио)-[[21-(((пропиламино)карбонил)-амино)сульфонил)(1,11-бифенил)-4-ил]метил]-1H-имидазол-5-карбоксилат этила;
2-бутил-4-(метилтио)-[[21 -((((пропиламино)карбонил)-амино)сульфонил)(1,11 -бифенил)-4-ил]метил]-1H-имидазол-5-карбоновая кислота;
2-бутил-4-(метилтио)-[[21 -(((пропиламино)карбонил)-амино)сульфонил)(1,11-бифенил)-4-ил] метил] -1H-имидазол-5-карбоновая кислота, дикалиевая соль.
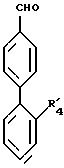
в которой R41 имеет значения, указанные для R4 в п.1, в которых функциональные группы защищены в качестве промежуточных соединений синтеза продуктов формулы 1.
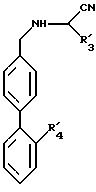
в которой R31 имеет значения, указанные для R3 в п.1, в которых функциональные группы защищены, и R41 имеет указанное в п.3 значение, в качестве промежуточных соединений синтеза продуктов формулы 1.
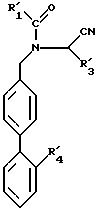
в которой R11 имеет значения, указанные для R1 в п.1, в которых функциональные группы защищены, R31 и R41 имеют указанные в п.4 значения, в качестве промежуточных соединений синтеза продуктов формулы 1.
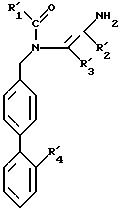
в которой R21 имеет значения, указанные для R2 по п.1, в которых функциональные группы могут быть защищены, R11, R31 и R41 имеют указанные в п.5 значения, в качестве промежуточных соединений синтеза продуктов формулы 1.
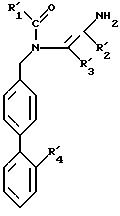
в которой R11, R21, R31 и R41 имеют указанные в п.6 значения, в качестве промежуточных соединений синтеза продуктов формулы 1.

Комментарии