Перфторалкансульфонат калия и способ его получения - RU2379286C2
Код документа: RU2379286C2
Чертежи

Описание
ОБЛАСТЬ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к перфторалкансульфонату калия, представленному общей формулой: CnF2n+1SO3K, в которой n представляет собой целое число от 1 до 3, и к способу его получения, который подходит в качестве исходного вещества при получении перфторалкансульфоновой кислоты, представленной общей формулой CnF2n+1SO3H, в которой n представляет собой целое число от 1 до 3, которая применима, например, в качестве синтетического катализатора при изготовлении фармацевтических препаратов.
Данная заявка на изобретение заявляет приоритет заявки на патент
Японии № 2005-288008, поданной 30 сентября 2005 года, содержание которой включено в данное описание ссылкой.
УРОВЕНЬ ТЕХНИКИ
В качестве способа получения перфторалкансульфоновой кислоты, представленной общей формулой CnF2n+1SO3H, в которой n представляет собой целое число от 1 до 3, известен способ, описанный в патенте США № 2732398 (патентный документ 1). Вкратце, перфторалкансульфоновую кислоту получают способом, в котором алкансульфонилгалогенид, содержащий от 1 до 3 атомов углерода, используют в качестве исходного вещества и подвергают реакции электрохимического фторирования во фтористом водороде, таким образом замещая атомы водорода алкильной части молекулы алкиленсульфонилгалогенида фтором (электрохимическое фторирование), получая перфторалкансульфонилфторид, и затем осуществляют взаимодействие перфторалкансульфонилфторида с щелочным раствором, чтобы превратить перфторалкансульфонилфторид в его соль со щелочным металлом, и далее соль щелочного металла подвергают реакции кислотного расщепления, используя серную кислоту.
Однако в вышеуказанном способе необходимо собирать при низких температурах газообразный перфторалкансульфонилфторид, полученный в стадии электрохимического фторирования. Более того, необходимо осуществить взаимодействие полученного в результате перфторалкансульфонилфторида со щелочью при высоких температурах и при высоких давлениях. По указанным причинам данный способ имеет трудности, например, при непрерывном производстве и является проблематичным при промышленном осуществлении.
В качестве улучшенного способа получения описанного выше процесса, нерассмотренная заявка на патент Японии № S64-61452 (патентный документ 2) описывает способ, в котором газ, полученный в результате электрохимического фторирования, абсорбируют, в то же время превращая в соль калия, посредством увеличения контакта между полученным газом и водным раствором гидроксида калия для взаимодействия полученного газа с водным раствором при обычном давлении. Данный способ отличается тем, что перфторалкансульфонат калия кристаллизуют из абсорбировавшего газ раствора посредством концентрирования абсорбировавшего газ раствора или добавления щелочи к абсорбировавшему газ раствору и затем подвергают фильтрованию и фильтрат направляют на повторную переработку в стадию абсорбции газа.
Однако в данном способе кристаллизацию перфторалкансульфоната калия осуществляют при условиях, когда гидроксид калия и фторид калия, который получается в виде побочного продукта в реакции, присутствуют в своем растворенном состоянии в абсорбировавшем газ растворе. В результате кристаллы перфторалкансульфоната калия имеют тенденцию быть загрязненными гидроксидом калия и фторидом калия, которые трудно удалить промывкой водой после фильтрования, поскольку они заключены внутри кристаллов. Следовательно, не просто снизить содержание данных примесей до достаточной степени.
Например, в случае когда перфторалкансульфонат калия содержит фторид калия в высоких количествах, в качестве побочного продукта получают фтористый водород, когда перфторалкансульфоновую кислоту получают, подвергая перфторалкансульфонат калия реакции кислотного расщепления, и он приводит к коррозии материалов реактора, таких как облицовка стеклом, приводя к серьезным промышленным проблемам.
Кроме того, в случае когда перфторалкансульфонат калия содержит гидроксид калия в высоких количествах, в качестве побочного продукта получают воду, когда перфторалкансульфоновую кислоту получают, подвергая перфторалкансульфонат калия реакции кислотного расщепления посредством добавления к нему концентрированной серной кислоты или аналогичного, и это приводит к образованию из воды и перфторалкансульфоновой кислоты гидрата или гидратов, имеющих высокую температуру плавления, приводя к проблеме закупоривания трубопроводов в течение перегонки перфторалкансульфоновой кислоты при пониженном давлении.
Более того, технологические стадии становятся сложными, поскольку фильтрат после фильтрования перфторалкансульфоната калия в данном способе содержит значительные количества перфторалкансульфоната калия, который является целевым продуктом, и остающегося в нем непрореагировавшего гидроксида калия, и требуется направить его на рециркуляцию и повторное использование в стадию абсорбции газа.
Кроме вышеописанных способов существует альтернативный способ, патент Японии № 3294323 (патентный документ 3), который описывает способ, по которому в качестве исходного вещества используют метансульфонилгалогенид и его подвергают электрохимическому фторированию в безводном фтористом водороде с тем, чтобы получить трифторметансульфонилфторид, и затем трифторметансульфонилфторид промывают водой для удаления кислотных газов и осуществляют его взаимодействие с водным раствором или суспензией гидроксида лития для удаления фторида лития, образующегося в качестве побочного продукта, чтобы таким образом получить трифторметансульфонат лития. Трифторметансульфонат лития можно подвергнуть реакции кислотного расщепления с тем, чтобы получить перфторалкансульфоновую кислоту. Однако в данном способе в качестве щелочного абсорбирующего раствора используют водный раствор гидроксида лития, и в качестве побочного продукта образуется фторид лития, который плохо растворим в воде, в результате приводя к проблеме осаждения внутри аппаратуры и закупориванию трубопроводов.
Кроме того, в любом описанном выше способе до настоящего времени в стадии электрохимического фторирования было трудно избежать получения в качестве побочных продуктов фторалканов и сульфонилдифторида вследствие разложения в реакции электрохимического фторирования. Глобальное потепление недавно поставило проблемы, и фторалканы, получаемые реакцией разложения, которая является побочной реакцией в электрохимическом фторировании, являются классом тепличных газов, которые представляют собой ключевые компоненты глобального потепления и группой соединений, которые имеют наиболее высокие потенциалы среди известных в настоящее время тепличных газов, причем их потенциалы глобального потепления в несколько тысяч раз выше значения для диоксида углерода. Данные фторалканы не абсорбируются в кислотном или щелочном водном растворе, делая трудной их последующую обработку, и, следовательно, требуется снижение их доли. Предшествующие описанные выше технологии получения не принимают во внимание подавление образования фторалканов в качестве побочных продуктов.
Кроме того, сульфонилдифторид, получаемый в качестве побочного продукта в реакции разложения, образует сульфат калия при поглощении в водном растворе гидроксида калия, который имеет относительно низкую растворимость в воде и, таким образом, имеет тенденцию выпадать в осадок внутри аппарата в стадии абсорбции газа, приводя к проблеме закупоривания трубопроводов.
Более того, поскольку реакция разложения усиливается, содержание сульфата калия в получающемся в результате кристаллическом перфторалкансульфонате калия увеличивается. В случае когда такой перфторалкансульфонат калия используют в качестве исходного вещества для осуществления реакции кислотного расщепления для синтеза перфторалкансульфоновой кислоты, реакционный остаток после отгонки перфторалкансульфоновой кислоты при пониженном давлении затвердевает и делает обработку затруднительной.
Патентный документ 1 - Патент США № 2732398.
Патентный документ 2 - Нерассмотренная заявка на патент Японии, первая публикация №S64-61452.
Патентный документ 3 - Патент Японии № 3294323.
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
ЗАДАЧИ, РЕШАЕМЫЕ ИЗОБРЕТЕНИЕМ
Настоящее изобретение решило вышеуказанные проблемы предшествующих способов и предлагает перфторалкансульфонат калия и способ его получения, который подходит в качестве исходного вещества для промышленного производства перфторалкансульфоновой кислоты.
Конкретно, настоящее изобретение предлагает перфторалкансульфонат калия, который используют в качестве исходного вещества при промышленном производстве перфторалкансульфоновой кислоты, и содержит пониженные количества примесей, таких как хлорид-ионы, фторид-ионы, сульфат-ионы и гидроксид калия, и способы получения такого перфторалкансульфоната калия, которые уменьшают образование парниковых газов, образующихся в результате реакции разложения в стадии электрохимического фторирования, не повышают вероятность закупоривания трубопроводов в стадии абсорбции газа и обеспечивают намного более простые технологические стадии.
Процентное содержание в следующем ниже описании представляет собой массовые проценты, если не указано иным образом.
СРЕДСТВА РЕШЕНИЯ ЗАДАЧ
Первый аспект способа получения перфторалкансульфоната калия по настоящему изобретению включает: электрохимическое фторирование в безводном фтористом водороде алкансульфонилгалогенидного соединения, представленного общей формулой: CnH2n+1SO2X, в которой n представляет собой целое число от 1 до 3 и X представляет собой Cl или F, чтобы таким образом получить газ, содержащий в качестве основного компонента перфторалкансульфонилфторид, представленный общей формулой: CnF2n+1SO2F, в которой n представляет собой целое число от 1 до 3 (стадия электрохимического фторирования); взаимодействие полученного газа с водным раствором гидроксида калия, чтобы таким образом получить абсорбировавший газ раствор, содержащий перфторалкансульфонат калия, представленный общей формулой: CnF2n+1SO3K, в которой n представляет собой целое число от 1 до 3 (стадия абсорбции газа); удаление фторида калия, гидроксида калия и сульфата калия, которые представляют собой примеси, содержащиеся в абсорбировавшем газ растворе (стадия очистки); и концентрирование и сушку водного раствора, из которого удалены примеси, чтобы таким образом получить перфторалкансульфонат калия, представленный общей формулой: CnF2n+1SO3K, в которой n представляет собой целое число от 1 до 3 (стадия концентрирования и сбора).
В описанном выше первом аспекте в качестве исходного вещества для электрохимического фторирования можно использовать алкансульфонилфторидное соединение, представленное общей формулой: CnH2n+1SO2F, в которой n представляет собой целое число от 1 до 3.
В стадии электрохимического фторирования скорость разложения продукта, перфторалкансульфонилфторида, можно контролировать до менее чем 3%, поддерживая концентрацию протонов в реакционном растворе для электрохимического фторирования в диапазоне от 150 до 1500 ч./млн.
В стадии электрохимического фторирования скорость разложения в реакции электрохимического фторирования можно контролировать до менее чем 3%, удерживая температуру реакции от 0°C до 18°C и плотность тока от 1 до 3 А/дм2 и поддерживая концентрацию протонов в реакционном растворе в диапазоне от 150 до 1500 ч./млн.
В стадии абсорбции газа может быть получен содержащий перфторалкансульфонат калия абсорбировавший газ раствор, который имеет концентрацию гидроксида калия менее чем 1%.
В стадии абсорбции газа абсорбировавший газ раствор, содержащий перфторалкансульфонат калия, можно получить контактом водного раствора гидроксида калия при отношении жидкости к газу, равном 10 или более относительно количества вводимого полученного газа.
В стадии абсорбции газа можно использовать водный раствор гидроксида калия, имеющий начальную концентрацию гидроксида калия 10% или более, и абсорбцию газа осуществляют, пока концентрация гидроксида калия не достигнет менее 1%.
В стадии очистки к абсорбировавшему газ раствору можно добавить гидроксид щелочного металла или гидроксид щелочноземельного металла, чтобы позволить ему взаимодействовать с фторидом калия, содержащимся в абсорбировавшем газ растворе, с тем, чтобы образовать осадок фторида и гидроксид калия, и далее можно добавить серную кислоту, чтобы осадить гидроксид калия из раствора в виде сульфата калия, данные осадки можно удалить фильтрованием и фильтрат можно подвергнуть концентрированию и сушке, получая перфторалкансульфонат калия.
В стадии очистки к абсорбировавшему газ раствору можно добавить гидроксид щелочного металла или гидроксид щелочноземельного металла, чтобы позволить ему взаимодействовать с фторидом калия, содержащимся в абсорбировавшем газ растворе, с тем, чтобы образовать осадок фторида и гидроксид калия, и далее можно добавить перфторалкансульфоновую кислоту, чтобы превратить гидроксид калия в растворе в перфторалкансульфонат калия, осадок можно удалить фильтрованием, и в стадии концентрирования и сбора фильтрат можно подвергнуть концентрированию и сушке, получая перфторалкансульфонат калия.
В стадии очистки к абсорбировавшему газ раствору можно добавить гидроксид щелочного металла или гидроксид щелочноземельного металла, чтобы позволить ему взаимодействовать с фторидом калия, содержащимся в абсорбировавшем газ растворе, с тем, чтобы образовать осадок фторида и гидроксид калия, и остаток реакционного раствора, образовавшийся при получении перфторалкансульфоновой кислоты реакцией кислотного расщепления, можно далее добавить для нейтрализации гидроксида калия в растворе, и затем осадок можно удалить фильтрованием, и в стадии концентрирования и сбора фильтрат можно подвергнуть концентрированию и сушке, получая перфторалкансульфонат калия.
В стадии очистки к абсорбировавшему газ раствору можно добавить сульфат алюминия, чтобы позволить ему взаимодействовать с фторидом калия и гидроксидом калия, содержащимися в абсорбировавшем газ растворе, с тем, чтобы образовать осадок фторида, сульфата калия или их двойной соли, осадок можно отфильтровать и в стадии концентрирования и сбора фильтрат можно подвергнуть концентрированию и сушке, получая перфторалкансульфонат калия.
Второй аспект способа получения перфторалкансульфоната калия по настоящему изобретению включает: электрохимическое фторирование в безводном фтористом водороде алкансульфонилгалогенидного соединения, представленного общей формулой: CnH2n+1SO2X, в которой n представляет собой целое число от 1 до 3 и X представляет собой Cl или F, чтобы таким образом получить газ, содержащий в качестве основного компонента перфторалкансульфонилфторид, представленный общей формулой: CnF2n+1SO2F, в которой n представляет собой целое число от 1 до 3, и использование полученного газа для получения перфторалкансульфоната калия, где в электрохимическом фторировании концентрацию протонов в реакционном растворе поддерживают в диапазоне от 150 до 1500 ч./млн, чтобы подавить образование побочных продуктов.
В описанном выше втором аспекте алкансульфонилфторидное соединение, представленное общей формулой: CnH2n+1SO2F, в которой n представляет собой целое число от 1 до 3, можно использовать в качестве исходного вещества для электрохимического фторирования.
В стадии электрохимического фторирования скорость разложения в реакции электрохимического фторирования можно контролировать до менее чем 3%, поддерживая концентрацию протонов в реакционном растворе в диапазоне от 150 до 1500 ч./млн.
В стадии электрохимического фторирования скорость разложения в реакции электрохимического фторирования можно контролировать до менее чем 3%, удерживая температуру реакции в диапазоне от 0°C до 18°C и плотность тока от 1 до 3 А/дм2 и поддерживая концентрацию протонов в реакционном растворе в диапазоне от 150 до 1500 ч./млн.
Первый аспект перфторалкансульфоната калия по настоящему изобретению представляет собой перфторалкансульфонат калия, полученный вышеуказанными способами получения и имеющий содержание хлорид-ионов менее чем 50 ч./млн.
Второй аспект перфторалкансульфоната калия по настоящему изобретению представляет собой перфторалкансульфонат калия, полученный вышеуказанными способами получения и имеющий содержание фторид-ионов менее чем 300 ч./млн.
Третий аспект перфторалкансульфоната калия по настоящему изобретению представляет собой перфторалкансульфонат калия, полученный вышеуказанными способами получения и имеющий содержание сульфат-ионов менее чем 3%.
Четвертый аспект перфторалкансульфоната калия по настоящему изобретению представляет собой перфторалкансульфонат калия, полученный вышеуказанными способами получения и имеющий содержание гидроксида калия менее чем 1%.
Пятый аспект перфторалкансульфоната калия по настоящему изобретению представляет собой перфторалкансульфонат калия, полученный вышеуказанными способами получения и имеющий чистоту 95% или более.
ЭФФЕКТЫ ИЗОБРЕТЕНИЯ
В способах получения по настоящему изобретению, поскольку газу, получающемуся в электрохимическом фторировании, дают возможность абсорбироваться в водном растворе гидроксида калия, пока концентрация гидроксида калия в абсорбирующем газ растворе не достигнет менее чем 1%, когда газ абсорбируется в водном растворе гидроксида калия, концентрация щелочи в абсорбирующем газ растворе значительно снижается. Соответственно, рециркуляция и повторная переработка абсорбирующего газ раствора не требуются, и технологические стадии упрощаются, делая способы получения по настоящему изобретению промышленно удобными.
В настоящем изобретении, поскольку электрохимическое фторирование проводят, в то же время контролируя скорость разложения до менее чем 3%, образование фторалканов и сульфонилдифторида является крайне низким, возможность загрязнения окружающей среды и глобального потепления снижается, и никакого закупоривания трубопроводов не происходит в стадии абсорбции газа.
Согласно способам получения по настоящему изобретению можно получить высокочистый перфторалкансульфонат калия, который имеет чистоту 95% или более и содержание хлорид-ионов менее 50 ч./млн, фторид-ионов менее чем 300 ч./млн и сульфат-ионов менее чем 3%.
В случае когда перфторалкансульфонат калия по настоящему изобретению применяют в качестве исходного вещества для получения перфторалкансульфоновой кислоты, поскольку содержание фторид-ионов достаточно снижено, фтористый водород образуется в качестве побочного продукта в меньших количествах, и никакой коррозии материалов аппаратуры, таких как облицовка стеклом, не происходит. Кроме того, из-за низкого содержания гидроксида калия не увеличивается возможность того, что перфторалкансульфоновая кислота образует гидрат или гидраты и произойдет закупоривание трубопровода. Помимо этого из-за низкого содержания сульфата калия реакционный раствор после отгонки продукта не затвердевает, позволяя с легкостью осуществить переработку.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
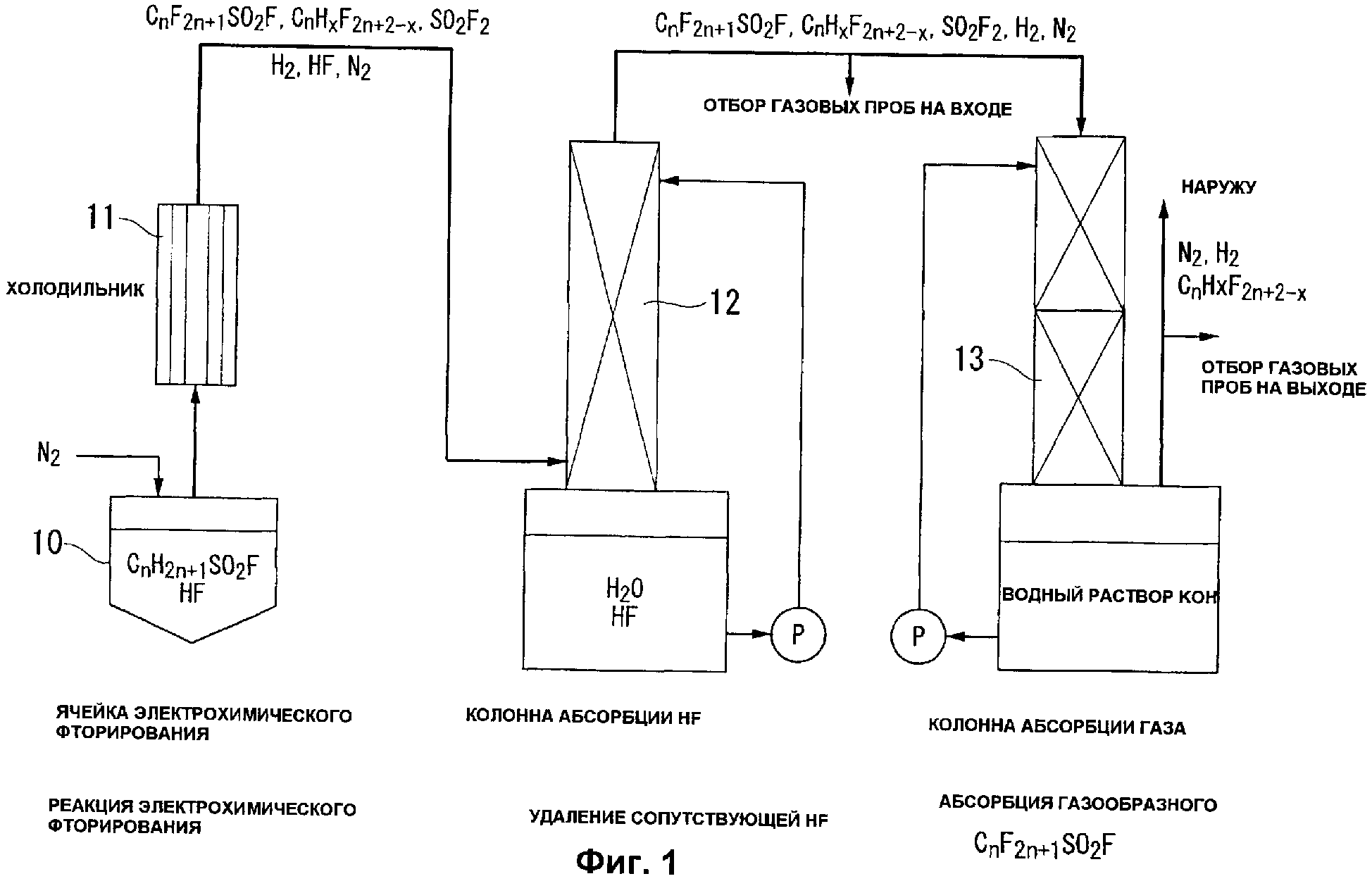
Фиг.1 представляет собой технологическую схему стадий электрохимического фторирования и абсорбции газа.
Фиг.2 представляет собой технологическую схему стадий очистки и концентрирования и сбора.
КРАТКОЕ ОПИСАНИЕ НОМЕРОВ ПОЗИЦИЙ
ЛУЧШИЙ РЕЖИМ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Организация настоящего изобретения теперь объясняется со ссылкой на чертежи.
Исходное вещество
В способах получения по вариантам осуществления настоящего изобретения алкансульфонилгалогенидные соединения, представленные общей формулой CnH2n+1SO2X, в которой n представляет собой целое число от 1 до 3 и X представляет собой Cl или F, можно использовать в качестве исходного вещества для электрохимического фторирования. В особенности при использовании алкансульфонилфторида содержание хлорид-ионов в конечном получаемом перфторалкансульфонате калия можно снизить до менее чем 50 ч./млн, что делает способы получения по настоящему изобретению более предпочтительными. С другой стороны, в случае когда в качестве исходного вещества для электрохимического фторирования используют алкансульфонилхлорид, содержание хлорид-ионов в конечном получаемом перфторалкансульфонате калия возрастает и ведет к тенденции примешивания хлорид-ионов к конечному желаемому продукту, и возможность снижения качества возрастает, когда такой перфторалкансульфонат калия подвергают кислотному расщеплению для получения перфторалкансульфоновой кислоты. Алкансульфонилфторид можно легко получить, подвергая алкансульфонилхлорид замещению на фтор, при использовании фторида калия или аналогичное, как показано в следующей ниже формуле:
CnH2n+1SO2Cl + KF → CnH2n+1SO2F + KCl
Стадия электрохимического фторирования
Рекомендуется использовать в качестве исходного вещества алкансульфонилгалогенид, предпочтительно алкансульфонилфторид, и загружать его в ячейку электрохимического фторирования с фтористым водородом для осуществления электрохимического фторирования при атмосфере газообразного азота при обычном давлении. В стадии электрохимического фторирования алкильную часть молекулы алкансульфонилгалогенида, представленного
общей формулой CnH2n+1SO2X, в которой n представляет собой целое число от 1 до 3 и X представляет собой Cl или F, замещают фтором, получая перфторалкансульфонилфторид, представленный общей формулой CnF2n+1SO2F, в которой n представляет собой целое число от 1 до 3, как показано в формуле, описанной ниже. В качестве побочной реакции разложение исходного вещества, промежуточных продуктов и
получаемого CnF2n+1SO2F вызывает образование фторалканов, таких как тетрафторметан (CF4), и сульфонилдифторида (SO2F2).
Основная реакция: CnH2n+1SO2F + (2n+1)HF → CnF2n+1SO2F↑ + (2n+1)H2↑
Побочная реакция: CnH2n+1SO2F + HF → CnHxF2n+2-xSO2F2 и аналогичная, в которой n представляет собой целое число от 1 до 3 и x представляет собой целое число от 0 до 2n+2.
Каждый перфторалкансульфонилфторид, полученный таким образом, имеет низкую температуру кипения, составляющую, например, -21°C (n=1), 0°C (n=2) и 40°C (n=3), и таким образом выбрасывается в виде газа из ячейки электрохимического фторирования наружу вместе с водородом, получающимся в качестве побочного продукта, продуктами разложения, такими как фторалканы и сульфонилдифторид, замещающим газом, представляющим собой азот, и растворителем электрохимического фторирования, представляющим собой фтористый водород.
В вышеуказанном электрохимическом фторировании предпочтительно проводить электрохимическое фторирование, в то же время поддерживая концентрацию протонов в реакционном растворе в диапазоне от 150 до 1500 ч./млн. Поддерживая концентрацию протонов в реакционном растворе в диапазоне от 150 до 1500 ч./млн, можно контролировать скорость разложения в реакции электрохимического фторирования до менее чем 3% и снизить образование побочных продуктов.
Концентрация протонов в реакционном растворе представляет собой величину, показывающую массовую концентрацию протонов (водородов), которыми обладает исходное вещество и промежуточные продукты (соединения, в которых остаются один или несколько водородов их алкильной части молекулы) в реакционном растворе, и ее можно определить, проведя анализ ядерным магнитным резонансом (1Н-ЯМР) реакционного раствора, применяя внешний стандарт.
Скорость разложения относится к сфере реакции или реакций разложения, которая(ые) является(ются) побочной реакцией при электрохимическом фторировании. Конкретно, скорость разложения выражается отношением образовавшегося количества побочного продукта, сульфонилдифторида (SO2F2), к сумме образовавшихся количеств основного продукта, перфторалкансульфонилфторида, и побочного продукта, сульфонилдифторида. Данные количества могут быть установлены, например, по площади пика каждого из данных компонентов на хроматограмме в газохроматографическом анализе полученного газа электрохимического фторирования.
Скорость разложения (%) = [образовавшееся количество SO2F2]/([образовавшееся количество CnF2n+1SO2F] + [образовавшееся количество SO2F2]) × 100
В приведенном уравнении каждое из данных количеств дается по площади пика в газохроматографическом анализе.
Авторы настоящей заявки обнаружили, что существует корреляция между концентрацией протонов и скоростью разложения и что можно контролировать скорость разложения до менее чем 3%, поддерживая концентрацию протонов в реакционном растворе в диапазоне от 150 до 1500 ч./млн в диапазоне температур реакции от 0°C до 18°C и плотность тока в диапазоне от 1 до 3 А/дм2.
Контролируя скорость разложения до менее чем 3%, можно снизить образование фторалканов и можно внести вклад в предотвращение глобального потепления. Кроме того, в то же время, поскольку образование сульфонилдифторида снижают, можно подавить образование сульфата калия в качестве побочного продукта, который получают в результате реакции сульфонилдифторида с гидроксидом калия в стадии абсорбции газа.
Стадия абсорбции газа
Полученный газ, выгружаемый из ячейки электрохимического фторирования в стадии электрохимического фторирования, проходит через холодильник при температуре от 0 до -40°C; таким образом, ожижают сопутствующий фтористый водород и его возвращают в ячейку электрохимического фторирования. Поскольку полученный газ, выгружаемый на выходе холодильника, содержит фтористый водород, который не был ожижен в холодильнике, полученный газ, предпочтительно, промывают посредством контакта газ-жидкость с орошением водой или низкоконцентрированным водным щелочным раствором, чтобы удалить фтористый водород, и затем направляют в колонну абсорбции газа, где полученный газ контактирует с щелочным раствором. В качестве щелочного раствора используют водный раствор гидроксида калия и осуществляют контакт газ-жидкость между описанным выше полученным газом и водным раствором гидроксида калия, так что перфторалкансульфонилфторид, содержащийся в полученном газе, абсорбируется в водном растворе гидроксида калия.
В стадии абсорбции газа, как показано в описанной ниже формуле, перфторалкансульфонилфторид, который является основным компонентом, содержащимся в полученном газе электрохимического фторирования, взаимодействует с гидроксидом калия и образует перфторалкансульфонат калия, который растворяется и абсорбируется в растворе. С другой стороны, фторалканы, которые являются побочными продуктами, содержащимися в полученном газе электрохимического фторирования, не абсорбируются в водном растворе гидроксида калия и, таким образом, сбрасываются наружу. Кроме того, сульфонилдифторид
(SO2F2), который является побочным продуктом, также содержащимся в полученном газе электрохимического фторирования, абсорбируется в водном растворе гидроксида калия и дает сульфат калия и фторид калия:
Основная реакция: CnF2n+1SO2F + 2KOH → CnF2n+1SO3K + KF + H2O
Побочная реакция: SO2F2 + 4KOH → K2SO4↓ + 2KF + 2H2O
В случае высоких скоростей разложения в стадии электрохимического фторирования в качестве побочного продукта образуются значительные количества сульфонилдифторида, и сульфонилдифторид взаимодействует с гидроксидом калия в абсорбировавшем газ растворе, и это приводит к образованию значительных количеств сульфата калия. Это ведет к расходованию больших количеств гидроксида калия, а также к увеличению содержания сульфата калия в кристаллах перфторалкансульфоната калия. Более того, сульфат калия имеет относительно низкую растворимость в воде (7,35 г/100 г (0°C) и 24,1 г/100 г (100°C)), а также обладает дополнительно сниженной растворимостью и имеет тенденцию осаждаться вследствие эффекта высаливания, когда перфторалкансульфонат калия также присутствует в растворе. Следовательно, данная проблема является причиной того, что при увеличении количества сульфата калия в абсорбировавшем газ растворе, осаждением сульфата калия вызывается закупоривание трубопроводов, через которые идет циркуляция раствора в стадии абсорбции газа.
В стадии абсорбции газа рекомендуется использовать водный раствор гидроксида калия, имеющий концентрацию 10% или более, и полученному газу дают возможность абсорбироваться данным раствором, пока концентрация гидроксида калия не достигнет величины менее 1%. В данном случае рекомендуется поддерживать температуру водного раствора гидроксида калия (абсорбирующий раствор) в диапазоне от 40 до 90°C, предпочтительно от 50 до 80°C, регулировать скорость потока циркуляции и сделать контакт газ-жидкость таким, чтобы отношение жидкости к газу количеств водного раствора гидроксида калия и вводимого полученного газа составляло 10 или более. Регулируя отношение жидкости к газу до 10 или более в описанном выше температурном диапазоне, можно продолжать абсорбцию газа, в то же время поддерживая скорость абсорбции газа от 95 до 100%, пока концентрация гидроксида калия не достигнет величины менее 1%.
В случае когда стадию абсорбции начинают при концентрации гидроксида калия 10% или более и продолжают, пока концентрация гидроксида калия не достигнет менее чем 1%, концентрация перфторалкансульфоната калия в абсорбировавшем газ растворе увеличивается, и содержание сульфата калия можно снизить эффектом его высаливания, что делает способы получения по настоящему изобретению выгодными. Даже в случае использования водного раствора гидроксида калия с такой высокой концентрацией можно предотвратить закупоривание трубопроводов из-за осаждения сульфата калия, если скорость разложения в реакции электрохимического фторирования контролируют до менее 3%. Однако когда концентрация гидроксида калия составляет 40% или более, вязкость водного раствора увеличивается, приводя к трудностям при обращении. Поэтому подходящим является, чтобы концентрация водного раствора гидроксида калия составляла от 10 до 40%.
Скорость абсорбции газа дается описанной ниже формулой, в которой количества перфторалкансульфонилфторида (CnF2n+1SO2F) и N2 даны по их площадям пиков на хроматограмме газохроматографического анализа газов с входа и выхода колонны абсорбции газа:
Скорость абсорбции газа (%) = [1 - (массовое соотношение CnF2n+1SO2F)×(массовое соотношение N2)]×100, в которой массовое соотношение CnF2n+1SO2F = количество CnF2n+1SO2F на выходе/количество CnF2n+1SO2F на входе и
массовое соотношение N2 = количество N2 на входе/количество N2 на выходе.
Стадия очистки
Стадия очистки представляет собой стадию, в которой удаляют фторид калия, который получается в качестве побочного продукта в основной реакции в указанной выше стадии абсорбции газа, сульфат калия и фторид калия, которые образуются в побочных реакциях, и гидроксида калия, который не израсходовался в стадии абсорбции газа. В качестве таких методов можно указать: (A) метод, по которому абсорбировавший газ раствор обрабатывают гидроксидом щелочного металла или гидроксидом щелочноземельного металла и затем нейтрализуют кислотой, и метод (B), по которому абсорбировавший газ раствор обрабатывают сульфатом алюминия.
(A) Метод, в котором используют гидроксид щелочного металла или гидроксид щелочноземельного металла, имеет первую стадию добавления любого из данных гидроксидов к описанному выше абсорбировавшему газ раствору с образованием умеренно нерастворимого фторидного осадка и гидроксида калия по реакции с фторидом калия, растворенным в абсорбировавшем газ растворе (1 стадия), и вторую стадию последовательного добавления серной кислоты либо после фильтрования осадка сразу, либо без фильтрования для взаимодействия с растворенным гидроксидом калия с получением осадка сульфата калия (2 стадия), и затем осадок(ки) отфильтровывают.
В качестве примера гидроксидов щелочного металла или гидроксидов щелочноземельного металла подходит гидроксид кальция. Гидроксид кальция добавляют к абсорбировавшему газ раствору, получая осадок фторида кальция (1 стадия), и далее добавляют серную кислоту, получая осадок сульфата калия (2 стадия), и затем данные осадки отфильтровывают. Фильтрование можно провести раздельно в каждой из 1 и 2 стадиях.
1 стадия: 2KF + Ca(OH)2 → CaF2↓ + 2KOH
2 стадия: 2KOH + H2SO4 → K2SO4↓ + 2H2O
В 1 стадии вместо гидроксида кальция можно использовать гидроксид лития. В данном случае образуется осадок фторида лития, как показано в описанной ниже формуле, и он имеет лучшую фильтруемость по сравнению с вышеописанным осадком фторида кальция, приводя к более легкому фильтрованию. С другой стороны, поскольку фторид кальция имеет более низкую растворимость в воде, чем фторид лития, фторид кальция имеет преимущество, состоящее в том, что количество фторид-ионов можно уменьшить до более низкого уровня.
1 стадия: KF + LiOH → LiF↓ + KOH
Гидроксид щелочного металла или гидроксид щелочноземельного металла добавляют при молярном отношении от 0,5 до 2,5, предпочтительно от 0,5 до 1,0, относительно фторида калия, растворенного в абсорбировавшем газ растворе, и смесь нагревают до температуры от 50 до 90°C и перемешивают от 1 до 4 часов, давая возможность осаждения фторида калия в растворе. В данном случае количество растворенных фторид-ионов в абсорбировавшем газ растворе, которые присутствуют в количестве более 10000 ч./млн, можно уменьшить в большей степени, так что содержание фторид-ионов в виде содержания фторид-иона в кристаллическом перфторалкансульфонате калия можно уменьшить до менее чем 300 ч./млн.
Рекомендуется, чтобы во 2 стадии серную кислоту, имеющую концентрацию от 50 до 100%, медленно добавляли к раствору, который был обработан в первой стадии, при нагревании от 20 до 90°C и перемешивании и добавление серной кислоты прекращали, когда значение рН становится нейтральным, и затем перемешивание продолжали в течение дополнительного времени от 1 до 4 часов.
Во 2 стадии вместо серной кислоты можно использовать перфторалкансульфоновую кислоту. В данном случае, как показано в описанной ниже формуле, гидроксид калия в растворе взаимодействует с перфторалкансульфоновой кислотой и образует перфторалкансульфонат калия. Поэтому содержание сульфата калия снижается до крайне низкой степени по сравнению с нейтрализацией серной кислотой, и концентрированием и сушкой можно получить высокочистый перфторалкансульфонат калия, имеющий содержание сульфат-ионов менее чем 1%.
2 стадия: KOH + CnF2n+1SO3H → CnF2n+1SO3K + H2O
Кроме того, в качестве кислоты, которую можно использовать для нейтрализации во 2 стадии, можно использовать реакционный остаток, который получили после добавления серной кислоты к перфторалкансульфонату калия для осуществления кислотного расщепления для получения перфторалкансульфоновой кислоты и удаления перфторалкансульфоновой кислоты перегонкой. Данный остаток содержит перфторалкансульфоновую кислоту, которая не была удалена перегонкой, и сульфат калия, который является побочным продуктом реакции, а также серную кислоту, которую используют в избытке в реакции кислотного расщепления и, таким образом, серная кислота и перфторалкансульфоновая кислота, которые обычно сбрасывают, могут быть эффективно использованы, что делает способы получения по настоящему изобретению предпочтительными.
Кроме того, во 2 стадии посредством удаления сульфата калия в абсорбировавшем газ растворе настолько полно, насколько возможно, количество сульфат-ионов, которое содержится в кристаллическом перфторалкансульфонате калия, полученном из абсорбировавшего газ раствора, можно понизить. Для осуществления этого, как уже было описано выше, например, концентрацию перфторалкансульфоната калия в абсорбировавшем газ растворе увеличивают с тем, чтобы осадить сульфат калия посредством эффекта высаливания.
Для того чтобы увеличить концентрацию перфторалкансульфоната калия в абсорбировавшем газ растворе, предпочтительно, как уже указывалось, чтобы в стадии абсорбции газа начальная концентрация водного раствора гидроксида калия, который используют в качестве абсорбирующего газ раствора, составляла 10% или более, а концентрация гидроксида калия в конце составляла менее 1% и дополнительно скорость разложения в реакции электрохимического фторирования была 3% или менее. Поэтому концентрацию перфторалкансульфоната калия в абсорбировавшем газ растворе во 2 стадии очистки увеличивают, так что содержание сульфат-ионов в кристаллическом перфторалкансульфонате калия можно снизить до менее чем 3%.
В стадии абсорбции газа, когда абсорбцию газа осуществляют при начальной концентрации гидроксида калия менее чем 10%, концентрация перфторалкансульфоната калия в абсорбировавшем газ растворе снижается и эффект высаливания ослабевает. Вследствие этого концентрация сульфата калия становится относительно высокой. В данном случае можно снизить содержание сульфата калия, концентрируя абсорбировавший газ раствор во 2 стадии очистки, чтобы увеличить концентрацию перфторалкансульфоната калия, но данный способ не является предпочтительным из-за снижения производительности и увеличения технологических стадий.
В случае использования перфторалкансульфоната калия с содержанием сульфат-иона менее чем 3% реакционный раствор не затвердевает после отгонки продукта вслед за реакцией без использования серной кислоты в большом избытке при получении перфторалкансульфоновой кислоты реакцией кислотного расщепления, позволяя осуществить процесс с легкостью.
(B) В методе очистки, использующем сульфат алюминия, фторид калия и гидроксид калия, растворенные в абсорбировавшем газ растворе, реагируют с сульфатом алюминия, и фторид алюминия, сульфат калия или их двойная соль образуется и выпадает в осадок. Поэтому данные соли следует отфильтровывать.
Рекомендуется добавлять сульфат алюминия при молярном отношении от 0,1 до 1,0, предпочтительно от 0,1 до 0,3, относительно суммы количеств фторида калия и гидроксида калия, растворенных в абсорбировавшем газ растворе, смесь нагревают до температуры от 50 до 90°C и перемешивают от 1 до 4 часов и затем охлаждают до температуры от 0 до 10°C, оставляя смесь выстаиваться от 1 до 10 часов.
Данным методом можно понизить содержание растворенных фторид-ионов в абсорбировавшем газ растворе в большей степени, чем в методе (A), так что можно снизить содержание фторид-ионов в кристаллическом перфторалкансульфонате калия до менее чем 300 ч./млн. Кроме того, поскольку данная обработка не дает какую-либо щелочь в качестве побочного продукта, данная обработка не требует стадии нейтрализации, в которой используют кислоту [2 стадия в методе (A)], что также делает возможным упрощение технологических стадий.
Стадия концентрирования и сбора
Можно собрать кристаллический перфторалкансульфонат калия, имеющий чистоту 95% или более, концентрированием и сушкой раствора, содержащего перфторалкансульфонат калия, в котором количества фторид-ионов, сульфат-ионов и гидроксида калия были снижены технологическими стадиями, описанными выше.
Для концентрирования и сушки раствора применимы процедуры, которые обычно используют. Особенно предпочтительны методы, которыми концентрирование и сушку осуществляют при пониженном давлении с перемешиванием. В таких методах полученный кристаллический перфторалкансульфонат калия имеет низкое содержание воды, представляет собой тонкий порошок, и это приводит к легкости в обращении.
Стадия кислотного расщепления
Перфторалкансульфоновую кислоту можно получить, добавляя серную кислоту к перфторалкансульфонату калия для протекания кислотного расщепления, как показано в формуле, описанной ниже. Реакцию, как правило, проводят при обычном давлении при температуре в диапазоне от 100 до 180°C, перемешивая от 1 до 20 часов, посредством добавления серной кислоты при молярном отношении от 1 до 10, предпочтительно от 2 до 5, относительно перфторалкансульфоната калия. После завершения взаимодействия полученную в результате перфторалкансульфоновую кислоту перегоняют при пониженном давлении; таким образом можно получить желаемый продукт.
Основная реакция: 2CnF2n+1SO3K + H2SO4 → 2CnF2n+1SO3H + K2SO4
В стадии кислотного расщепления в случае, когда перфторалкансульфонат калия, который используют в качестве исходного вещества, имеет высокое содержание фторид-ионов, в больших количествах образуется фтористый водород, как показано в побочной реакции, описанной ниже, и он приводит к коррозии материалов аппаратуры, таких как облицовка стеклом. Кроме того, в случае когда содержание гидроксида калия является высоким, гидроксид калия взаимодействует с серной кислотой и дает воду, и далее вода образует сольват или сольваты с перфторалкансульфоновой кислотой. Сольват(ы) имеет высокую температуру плавления и увеличивает возможность закупоривания трубопроводов в течение перегонки желаемого продукта при пониженном давлении. Более того, в случае когда исходное вещество имеет высокое содержание сульфата калия, реакционный раствор затвердевает после отгонки продукта, следующей за реакцией кислотного расщепления, что делает его обработку трудной.
Побочная реакция: 2KF + H2SO4 → 2HF + K2SO4
Технологическая схема способов получения, описанных выше, показана на фиг.1 и 2, хотя способ получения по настоящему изобретению не ограничивается иллюстрируемыми вариантами осуществления. Фиг.1 показывает стадии электрохимического фторирования и абсорбции газа. Алкансульфонилфторид (CnH2n+1SO2F) и фтористый водород помещают в ячейку электрохимического фторирования 10, обеспечивается атмосфера азота, и проводят электрохимическое фторирование, в течение которого температуру реакции контролируют в диапазоне от 0 до 18°C, концентрацию протонов в реакционном растворе контролируют
до 150-1500 ч./млн и скорость разложения поддерживают при менее чем 3%. Полученный газ направляют через холодильник 11 в колонну поглощения HF 12 для осуществления контакта газ-жидкость с водой или низкоконцентрированным водным щелочным раствором. Проводят орошение водой или низкоконцентрированным водным щелочным раствором с верхней части колонны абсорбции HF 12, и полученный газ промывается. Промытый полученный газ направляют в колонну абсорбции газа 13. Проводят орошение водным раствором гидроксида калия с верхней части колонны абсорбции газа 13, и основной продукт в полученном газе взаимодействует с гидроксидом калия посредством контакта газ-жидкость и дает перфторалкансульфонат калия (CnF2n+1SO3K), который абсорбируется в водном растворе гидроксида калия. С другой стороны, фторалканы, газообразный азот и газообразный водород, которые сопутствуют полученному газу, не абсорбируются в водном растворе гидроксида калия и сбрасываются наружу.
Фиг.2 показывает технологические стадии очистки, концентрирования и сушки абсорбировавшего газ раствора, содержащего перфторалкансульфонат калия (CnF2n+1SO3K), и сбор перфторалкансульфоната калия. В резервуаре с механическим перемешиванием 20 абсорбировавший газ раствор обрабатывают гидроксидом кальция. После обработки жидкость, содержащую осадок, направляют на фильтр 21 и твердое вещество и жидкость разделяют и затем фильтрат возвращают в резервуар с механическим перемешиванием 20. После этого для обработки добавляют серную кислоту. После обработки жидкость, содержащую осадок, направляют на фильтр 21 и твердое вещество и жидкость разделяют, после чего фильтрат направляют в концентратор и сушильное устройство 22 и кристаллическую перфторалкансульфоновую кислоту, сконцентрированную нагреванием и сушкой при пониженном давлении, выгружают из нижней части. Выпаренную воду, содержащую другие компоненты, направляют через холодильник 23 в емкость сбора воды 24.
ПРИМЕРЫ
Примеры настоящего изобретения будут иллюстрированы ниже.
Пример 1
Использовали железную ячейку электрохимического фторирования, оборудованную дефлегматором, температура которого установлена при -30°С, и внутрь ячейки электрохимического фторирования помещали никелевые электроды, имеющие площади поверхности анода и катода 378 дм2. В ячейку электрохимического фторирования загружали безводный фтористый водород (84,8 кг, 4240 моль) и исходное вещество, метансульфонилфторид (1,73 кг, 17,6 моль), так что концентрация протонов в реакционном растворе составляла примерно 600 ч./млн, и осуществляли циркуляцию раствора для получения реакционного раствора.
Электрохимическое фторирование проводили при постоянном токе 800 А, в то же время поддерживая температуру от 8 до 12°С посредством циркуляции реакционного раствора через внешний холодильник. В течение электрохимического фторирования в ячейку электрохимического фторирования подавали метансульфонилфторид и безводный фтористый водород, по мере необходимости, для пополнения реакционного раствора, так что концентрацию протонов в реакционном растворе поддерживали в диапазоне от 150 до 1500 ч./млн.
Полученный газ, содержащий трифторметансульфонилфторид, полученный электрохимическим фторированием, вводили в колонну абсорбции HF. В колонне абсорбции HF при комнатной температуре осуществляли циркуляцию подвергнутой ионному обмену воды и ее подвергали контакту в противотоке с полученным газом для удаления сопутствующего фтористого водорода.
Затем полученный газ, из которого был удален фтористый водород, вводили в колонну абсорбции газа. В колонну абсорбции газа заранее загружали 214 кг 24% водного раствора гидроксида калия и осуществляли циркуляцию водного раствора гидроксида калия со скоростью 11 м3/ч внутри колонны абсорбции газа, в то же время регулируя температуру водного раствора до 60°С с тем, чтобы дать возможность взаимодействия между трифторметансульфонилфторидом и гидроксидом калия.
Когда ток останавливали через 92,5 часа после начала электрохимического фторирования, внутри колонны абсорбции газа собирали 268 кг реакционного раствора (в дальнейшем называемого абсорбировавшего газ раствора). Данный раствор представлял собой бесцветный и прозрачный раствор. Титриметрический анализ данного раствора показал, что концентрация гидроксида калия составляла 0,9%.
В данном фторировании концентрация протонов в реакционном растворе внутри ячейки электрохимического фторирования изменялась от 400 до 800 ч./млн, общее количество исходного вещества, поданного в реакцию электрохимического фторирования, составляло 41,4 кг (422,0 моль), напряжение изменялось от 5,5 до 5,7 В, скорость расщепления составляла 1,8% или менее, отношение жидкости к газу в реакции абсорбции газа составляло 12,7 и скорость абсорбции газа составляла 96% или более.
Пример 2
Абсорбировавший газ раствор, полученный в примере 1, помещали в реакционный сосуд, облицованный фторуглеродным полимером (ПТФЭ). К данному абсорбировавшему газ раствору добавляли 26,2 кг (353,7 моль) порошкообразного гидроксида кальция и смесь нагревали до 70°С при перемешивании.
После того как температура повысилась, перемешивание продолжали в течение 2 часов для превращения растворенного фторида калия во фторид кальция. Двумя часами позднее перемешивание прекращали и смесь оставляли выдерживаться в течение ночи, позволяя осадиться фториду кальция. Затем данный водный раствор сливали и фторид кальция удаляли фильтрованием.
К полученному в результате фильтрату добавляли 75% серную кислоту, пока величина рН не достигала диапазона от 7,0 до 7,5 (добавленное количество: 27,8 кг (212,3 моль)), и при перемешивании проводили нейтрализацию. При этом температура раствора повышалась до 70°С вследствие выделения тепла при нейтрализации. Перемешивание продолжали в течение 1 часа, чтобы завершить реакцию нейтрализации. Через один час перемешивание прекращали и образовавшемуся сульфату калия давали возможность осадиться при выдерживании. Сульфат калия удаляли фильтрованием.
Бесцветный и прозрачный водный раствор трифторметансульфоната калия (219 кг), полученный данным фильтрованием, подвергали концентрированию и сушке, получая 53,6 кг трифторметансульфоната калия. Анализ продукта ионной хроматографией показал, что чистота трифторметансульфоната калия составляла 97,2%, содержание сульфат-ионов составляло 1,5%, содержание фторид-ионов составляло 120 ч./млн, содержание хлорид-ионов составляло 16 ч./млн и гидроксид калия отсутствовал.
Пример 3
Вместо добавления к абсорбировавшему газ раствору в примере 2 порошкообразного гидроксида кальция к абсорбировавшему газ раствору (267 кг) добавляли сульфат алюминия (21,8 кг, 63,7 моль) и смесь нагревали до 70°С при перемешивании.
После того как температура повысилась, перемешивание продолжали в течение 2 часов, после чего перемешивание прекращали и смесь оставляли выдерживаться при 5°С в течение ночи для осаждения твердого вещества. Затем данный водный раствор сливали и осадок удаляли фильтрованием.
Бесцветный и прозрачный водный раствор трифторметансульфоната калия (225 кг), полученный данным фильтрованием, подвергали концентрированию и сушке, получая 51,1 кг трифторметансульфоната калия. Анализ продукта показал, что чистота трифторметансульфоната калия составляла 95,9%, содержание сульфат-ионов составляло 2,3%, содержание фторид-ионов составляло 246 ч./млн, содержание хлорид-ионов составляло 12 ч./млн и гидроксид калия отсутствовал.
Пример 4
Вместо добавления 75% серной кислоты к фильтрату, из которого в примере 2 фильтрованием удалили фторид кальция, добавляли трифторметансульфоновую кислоту (добавленное количество: 63,8 кг), пока величина рН не достигала диапазона от 7,0 до 7,5, и проводили нейтрализацию. Перемешивание продолжали в течение 1 часа, чтобы завершить реакцию нейтрализации. Через один час перемешивание останавливали и нерастворимое вещество удаляли фильтрованием.
Бесцветный и прозрачный водный раствор трифторметансульфоната калия (219 кг), полученный данным фильтрованием, подвергали концентрированию и сушке, получая 119,8 кг трифторметансульфоната калия. Анализ продукта показал, что чистота трифторметансульфоната калия составляла 98,5%, содержание сульфат-ионов составляло 0,8%, содержание фторид-ионов составляло 180 ч./млн, содержание хлорид-ионов составляло 16 ч./млн и гидроксид калия отсутствовал.
ПРИМЕРЫ СРАВНЕНИЯ
Примеры сравнения 1-3
Электрохимическое фторирование в примере 1 осуществляли, поддерживая концентрацию протонов в реакционном растворе в диапазоне от 9000 до 11200 ч./млн (пример сравнения 1), от 5000 до 7050 ч./млн (пример сравнения 2) и от 3400 до 4650 ч./млн (пример сравнения 3). Скорости разложения для данных примеров сравнения составляли от 11,3 до 15,5%, от 8,3 до 12,0% и от 6,8 до 7,6% соответственно, и тетрафторметан и сульфонилдифторид в качестве побочных продуктов получали в больших количествах.
Пример 5
Использовали железную ячейку электрохимического фторирования, оборудованную дефлегматором, температура которого установлена при -20°С, и внутрь ячейки электрохимического фторирования помещали никелевые электроды, имеющие площади поверхности анода и катода 67 дм2. В ячейку электрохимического фторирования загружали безводный фтористый водород (11,81 кг, 590 моль) и исходное вещество, этансульфонилфторид (0,24 кг, 2,1 моль), так что концентрация протонов в реакционном растворе составляла примерно 600 ч./млн, и осуществляли циркуляцию раствора для получения реакционного раствора.
Электрохимическое фторирование проводили при постоянном токе 100 А, в то же время поддерживая температуру от 8 до 12°С посредством циркуляции реакционного раствора через внешний холодильник. В течение электрохимического фторирования в ячейку электрохимического фторирования подавали этансульфонилфторид и безводный фтористый водород, по мере необходимости, для пополнения реакционного раствора, так что концентрацию протонов в реакционном растворе поддерживали в диапазоне от 150 до 1500 ч./млн.
Полученный газ, содержащий перфторэтансульфонилфторид, полученный электрохимическим фторированием, вводили в колонну абсорбции HF. В колонне абсорбции HF при комнатной температуре осуществляли циркуляцию подвергнутой ионному обмену воды и ее подвергали контакту в противотоке с полученным газом для удаления сопутствующего фтористого водорода.
Затем полученный газ, из которого был удален фтористый водород, вводили в колонну абсорбции газа. В колонну абсорбции газа заранее загружали 48,0 кг 20% водного раствора гидроксида калия и осуществляли циркуляцию водного раствора гидроксида калия со скоростью 2 м3/ч внутри колонны абсорбции газа, в то же время регулируя температуру водного раствора до 60°С с тем, чтобы дать возможность взаимодействия между перфторэтансульфонилфторидом и гидроксидом калия.
Когда ток останавливали через 300 часов после начала электрохимического фторирования, внутри колонны абсорбции газа собирали 58,9 кг реакционного раствора (абсорбировавшего газ раствора). Данный раствор представлял собой бесцветный и прозрачный раствор. Титриметрический анализ данного раствора показал, что концентрация гидроксида калия составляла 0,2%.
В данном фторировании концентрация протонов в реакционном растворе изменялась от 550 до 780 ч./млн, общее количество исходного вещества, поданного в реакцию электрохимического фторирования, составляло 13,4 кг (119,5 моль), напряжение изменялось от 5,1 до 5,4 В, скорость разложения составляла 2,7% или менее, отношение жидкости к газу в реакции абсорбции газа составляло 27,0 и скорость абсорбции газа составляла 96% или более.
Пример 6
Абсорбировавший газ раствор, полученный в примере 5, помещали в реакционный сосуд, облицованный фторуглеродным полимером (ПТФЭ). К данному абсорбировавшему газ раствору добавляли 5,15 кг (69,6 моль) порошкообразного гидроксида кальция и смесь нагревали до 70°С при перемешивании.
После того как температура повысилась, перемешивание продолжали в течение 2 часов, после чего перемешивание останавливали и смесь оставляли выдерживаться в течение ночи, позволяя осадиться твердому веществу. Затем данный водный раствор сливали и фторид кальция удаляли фильтрованием.
К полученному в результате фильтрату добавляли 75% серную кислоту, пока величина рН не достигала диапазона от 7,0 до 7,5 (добавленное количество: 4,86 кг (37,2 моль)), и при перемешивании проводили нейтрализацию. Перемешивание продолжали в течение 1 часа, чтобы завершить реакцию нейтрализации. Через один час перемешивание прекращали и образовавшемуся сульфату калия давали возможность осадиться при выдерживании. Сульфат калия удаляли фильтрованием.
Полученный бесцветный и прозрачный водный раствор перфторэтансульфоната калия (45,6 кг) подвергали концентрированию и сушке, получая 14,3 кг перфторэтансульфоната калия. Анализ продукта ионной хроматографией показал, что чистота перфторэтансульфоната калия составляла 96,2%, содержание сульфат-ионов составляло 2,1%, содержание фторид-ионов составляло 240 ч./млн, содержание хлорид-ионов составляло 25 ч./млн и гидроксид калия отсутствовал.
Пример 7
Использовали железную ячейку электрохимического фторирования, оборудованную дефлегматором, температура которого установлена при -20°С, и внутрь ячейки электрохимического фторирования помещали никелевые электроды, имеющие площади поверхности анода и катода 67 дм2. В ячейку электрохимического фторирования загружали безводный фтористый водород (11,81 кг, 590 моль) и исходное вещество, 1-пропансульфонилфторид (0,24 кг, 1,90 моль), так что концентрация протонов в реакционном растворе составляла примерно 600 ч./млн, и осуществляли циркуляцию раствора для получения реакционного раствора.
Электрохимическое фторирование проводили при постоянном токе 100 А, в то же время поддерживая температуру от 8 до 12°С посредством циркуляции реакционного раствора через внешний холодильник. В течение электрохимического фторирования в ячейку электрохимического фторирования подавали 1-пропансульфонилфторид и безводный фтористый водород, по мере необходимости, для пополнения реакционного раствора, так что концентрацию протонов в реакционном растворе поддерживали в диапазоне от 150 до 1500 ч./млн.
Полученный газ, содержащий 1-перфторпропансульфонилфторид, полученный электрохимическим фторированием, вводили в колонну абсорбции HF. В колонне абсорбции HF при комнатной температуре осуществляли циркуляцию подвергнутой ионному обмену воды и ее подвергали контакту в противотоке с полученным газом для удаления сопутствующего фтористого водорода.
Затем полученный газ, из которого был удален фтористый водород, вводили в колонну абсорбции газа. В колонну абсорбции газа заранее загружали 48,0 кг 20% водного раствора гидроксида калия и осуществляли циркуляцию водного раствора гидроксида калия со скоростью 2 м3/ч внутри колонны абсорбции газа, в то же время регулируя температуру водного раствора до 60°С с тем, чтобы дать возможность взаимодействия между 1-перфторпропансульфонилфторидом и гидроксидом калия.
Когда ток останавливали через 300 часов после начала электрохимического фторирования, внутри колонны абсорбции газа собирали 58,5 кг реакционного раствора (абсорбировавшего газ раствора). Данный раствор представлял собой бесцветный и прозрачный раствор. Титриметрический анализ данного раствора показал, что концентрация гидроксида калия составляла 0,4%.
В данном фторировании концентрация протонов в реакционном растворе изменялась от 520 до 850 ч./млн, общее количество исходного вещества, поданного в реакцию электрохимического фторирования, составляло 15,2 кг (120,5 моль), напряжение изменялось от 5,2 до 6,2 В, скорость расщепления составляла 2,8% или менее, отношение жидкости к газу в реакции абсорбции газа составляло 27,9 и скорость абсорбции газа составляла 97% или более.
Пример 8
Абсорбировавший газ раствор, полученный в примере 7, помещали в реакционный сосуд, облицованный фторуглеродным полимером (ПТФЭ). К данному абсорбировавшему газ раствору добавляли 3,84 кг (51,9 моль) порошкообразного гидроксида кальция и смесь нагревали до 70°С при перемешивании.
После того как температура повысилась, перемешивание продолжали в течение 2 часов, после чего перемешивание останавливали и смесь оставляли выдерживаться в течение ночи, позволяя осадиться твердому веществу. Затем данный водный раствор сливали и твердое вещество удаляли фильтрованием.
К полученному в результате фильтрату добавляли 75% серную кислоту, пока величина рН не достигала диапазона от 7,0 до 7,5 (добавленное количество: 4,74 кг (36,3 моль)), и при перемешивании проводили нейтрализацию. Перемешивание продолжали в течение 1 часа, чтобы завершить реакцию нейтрализации. Через один час перемешивание прекращали и образовавшемуся сульфату калия давали возможность осадиться при выдерживании. Сульфат калия удаляли фильтрованием.
Полученный бесцветный и прозрачный водный раствор 1-перфторпропансульфоната калия (46,2 кг) подвергали концентрированию и сушке, получая 14,8 кг 1-перфторпропансульфоната калия. Анализ продукта ионной хроматографией показал, что чистота 1-перфторпропансульфоната калия составляла 95,8%, содержание сульфат-ионов составляло 2,3%, содержание фторид-ионов составляло 220 ч./млн, содержание хлорид-ионов составляло 10 ч./млн и гидроксид калия отсутствовал.
Пример 9
Вместо добавления 75% серной кислоты к фильтрату, из которого в примере 2 фильтрованием удалили фторид кальция, добавляли реакционный остаток способа получения трифторметансульфоновой кислоты кислотным расщеплением (содержащий 72% серной кислоты, 2% трифторметансульфоновой кислоты и 26% сульфата калия) к 267 кг абсорбировавшего газ раствора, пока величина рН не достигала диапазона от 7,0 до 7,5 (добавленное количество: 28,7 кг), и проводили нейтрализацию. Перемешивание продолжали в течение 1 часа, чтобы завершить реакцию нейтрализации. Через один час перемешивание останавливали и нерастворимое вещество удаляли фильтрованием.
Бесцветный и прозрачный водный раствор трифторметансульфоната калия (211 кг), полученный данным фильтрованием, подвергали концентрированию и сушке, получая 54,5 кг трифторметансульфоната калия. Анализ полученного в результате продукта показал, что чистота трифторметансульфоната калия составляла 97,6%, содержание сульфат-ионов составляло 1,3%, содержание фторид-ионов составляло 130 ч./млн, содержание хлорид-ионов составляло 14 ч./млн и гидроксид калия отсутствовал.
Пример 10
В течение реакции электрохимического фторирования в примере 1 брали примерно 5 г образца реакционного раствора, осторожно выливали в примерно 25 г смеси льда и воды и разбавляли. В данный раствор по каплям добавляли 48% водный раствор гидроксида калия и проводили нейтрализацию. Затем перемешивание продолжали в течение 20 минут, чтобы завершить реакцию нейтрализации.
Точно взвешивали примерно 5 г нейтрализованного раствора. В качестве внутреннего стандарта точно взвесили 0,015 г 1,4-диоксана, смешали с аликвотой и провели анализ аликвоты методом ядерного магнитного резонанса (1Н-ЯМР). Рассчитали, что концентрация протонов в реакционном растворе составляла 480 ч./млн, исходя из относительной интегральной интенсивности протонов в реакционном растворе (от 1,0 до 3,0 м.д.) к интегральной интенсивности 1,4-диоксана (примерно 3,7 м.д.).
ПРИМЕНИМОСТЬ В ПРОМЫШЛЕННОСТИ
Способ по настоящему изобретению подходяще применим к способам получения перфторалкансульфоната калия, и можно добиться упрощения технологических стадий, снижения вероятности загрязнения окружающей среды и глобального потепления и подавления закупоривания трубопроводов. Кроме того, перфторалкансульфонат калия по настоящему изобретению можно подходяще применить в качестве исходного вещества для перфторалкансульфоновой кислоты, которая применима в качестве синтетических катализаторов при производстве фармацевтических препаратов и позволяет предотвратить коррозию материалов аппаратуры, таких как облицовка стеклом, подавить закупоривание трубопроводов и упростить переработку.
Реферат
Заявлен способ получения перфторалкансульфоната калия, включающий стадию электрохимического фторирования, в которой алкансульфонилгалогенидное соединение подвергают электрохимическому фторированию в безводном фтористом водороде, таким образом получая газ, содержащий перфторалкансульфонилфторид в качестве основного компонента; стадию абсорбции газа, в которой осуществляют взаимодействие полученного газа с водным раствором гидроксида калия, чтобы таким образом получить абсорбировавший газ раствор, содержащий перфторалкансульфонат калия; стадию очистки, в которой удаляют примеси, такие как фторид калия, гидроксид калия и сульфат калия, и стадию концентрирования и сбора, в которой водный раствор, из которого удалены примеси, концентрируют и сушат. Концентрация протонов в реакционном растворе предпочтительно поддерживается в диапазоне от 150 до 1500 ч./млн для подавления образования побочных продуктов. 2 н. и 13 з.п. ф-лы, 2 ил.
Формула
электрохимическое фторирование в безводном фтористом водороде алкансульфонилгалогенидного соединения, представленного общей формулой
CnH2n+1SO2X,
в которой n представляет собой целое число от 1 до 3;
Х представляет собой Cl или F,
чтобы таким образом получить газ, содержащий в качестве основного компонента перфторалкансульфонилфторид, представленный общей формулой
CnF2n+1SO2F,
в которой n представляет собой целое число от 1 до 3, (стадия электрохимического фторирования);
взаимодействие полученного газа с водным раствором гидроксида калия, чтобы таким образом получить абсорбировавший газ раствор, содержащий перфторалкансульфонат калия, представленный общей формулой
CnF2n+1SO3K,
в которой n представляет собой целое число от 1 до 3, (стадия абсорбции газа);
удаление фторида калия, гидроксида калия и сульфата калия, которые представляют собой примеси, содержащиеся в абсорбировавшем газ растворе, (стадия очистки); и
концентрирование и сушку водного раствора, из которого удалены примеси, чтобы таким образом получить перфторалкансульфонат калия, представленный общей формулой
CnF2n+1SO3K,
в которой n представляет собой целое число от 1 до 3, (стадия концентрирования и сбора).
CnH2n+1SO2F,
в которой n представляет собой целое число от 1 до 3,
используют в качестве исходного вещества для электрохимического фторирования.
в стадии концентрирования и сбора фильтрат подвергают концентрированию и сушке, получая перфторалкансульфонат калия.
электрохимическое фторирование в безводном фтористом водороде алкансульфонилгалогенидного соединения, представленного общей формулой:
CnH2n+1SO2X,
в которой n представляет собой целое число от 1 до 3;
Х представляет собой Cl или F,
чтобы таким образом получить газ, содержащий в качестве основного компонента перфторалкансульфонилфторид, представленный общей формулой
CnF2n+1SO2F,
в которой n представляет собой целое число от 1 до 3,
и использование полученного газа для получения перфторалкансульфоната калия, где в электрохимическом фторировании концентрацию протонов в реакционном растворе поддерживают в диапазоне от 150 до 1500 ч./млн. чтобы подавить образование побочных продуктов.

Комментарии