Фторсодержащие бензоилгуанидины, способ их получения, фармацевтическая композиция и способ ее получения - RU2159230C2
Код документа: RU2159230C2
Чертежи
Описание
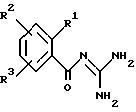
Изобретение относится к фторсодержащим бензоилгуанинам формулы (I)

где R1 - обозначает H, F, Cl, Br, I, A, CN, NO2, CnFmH2n+1-mOp алкинил с 2-4 C-атомами или -X-R4;
R2 обозначает CnFmH2n+1-mOp ;
R3 обозначает H, A, F, Br, Cl, I, CnFmH2n+1-mOp, SOq -R6, SO2NR4R5, Гет, OR6, SR6, S-Гет или NR7-Гет;
R4 и R5 каждый независимо друг от друга обозначают H или A или, однако, вместе также обозначают алкилен с 4-5 C-атомами, причем одна CH2-группа также может быть заменена на O, S, NH или NA;
R6 обозначает Ph или A;
R7 обозначает H или A;
A обозначает алкил с 1-6 C-атомами;
X обозначает O, S или NR7;
Ph обозначает незамещенный или одно-, двух- или трехкратно замещенный с помощью A, OA, NR4, R5, F, Cl, Br, I или CnFmH2n+1-mOp фенил;
Гет обозначает одно- или двухъядерный, насыщенный, ненасыщенный или ароматический гетероциклический остаток с 1-4 атомами N-, O- и/или S, который незамещен или может быть одно-, двух- или трехкратно замещен с помощью F, Cl, Br, CnFmH2n+1-mOp, A, X-R4, NO2, CN и/или карбонильного кислорода и через N или C связан с бензоильной системой;
m = 1, 2, 3, 4, 5, 6 или 7, самое большее, однако, 2n + 1;
n = 1, 2 или 3;
p = 0 или 1;
q = 1 или 2;
при условии, что R1 может обозначать H только тогда, когда R3 обозначает SOq-R6 или SO2NR4R5;
а также к их физиологически приемлемым солям.
В основу изобретения положена задача нахождения соединений с ценными свойствами, в частности таких, которые можно применять для приготовления лекарственных средств.
Найдено, что соединения формулы (I) и их физиологически приемлемые соли при хорошей совместимости обладают ценными фармакологическими свойствами.
В случае новых соединений речь идет об ингибиторах клеточного Na+/H+ - антипорта, т. е. о биологически активных веществах, которые ингибируют механизм обмена Na+/H+ в клетках (Deising et al., Med. Klin. 87, 378-384 (1992)) и которые, таким образом, представляют собой антиаритмические средства, в особенности пригодные для лечения аритмий, которые наступают как следствие недостатка кислорода.
Самым известным биологически активным веществом из группы ацилгуанидинов является амилорид. Это вещество, однако, обладает в первую очередь снижающим кровяное давление и салуретическим действием, что, в частности, нежелательно при лечении нарушений сердечного ритма, в то время как антиаритмические свойства выражены только очень слабо.
Сверх того структурно подобные соединения известны, например, из европейского патента EP-0416499.
Предлагаемые в изобретении вещества настоящей заявки обладают хорошим кардиозащитным действием и поэтому особенно пригодны для лечения инфаркта, для профилактики инфаркта и для лечения стенокардии. Далее вещества противодействуют всем патoлогическим гипоксическим и ишемическим повреждениям, так что можно лечить вызываемые ими первичные или вторичные заболевания. Биологически активные вещества также хорошо пригодны для профилактических применений.
Из защитных воздействий этих веществ при патологических гипоксических или ишемических ситуациях вытекают дальнейшие возможности применения при хирургических вмешательствах для защиты на время менее снабжаемых (например, кровью) органов, при трансплантациях органов для защиты извлекаемых органов, при ангиопластических вмешательствах в сосуды и сердце, при ишемиях нервной системы, при терапии шоковых состояний и для профилактического препятствования эссенциальной гипертонии.
Далее соединения также можно использовать в качестве терапевтических средств при обусловленных пролифераций клеток заболеваниях, как артериосклероз, диабетические поздние осложнения, опухолевые заболевания, фибротические заболевания, в особенности легких, печени и почек, а также гипертрофии и гиперплазии органов. Сверх того, вещества пригодны для диагностики с целью распознавания заболеваний, которые сопровождаются повышенной активностью Na+/H+ - антипорта, например в эритроцитах, тромбоцитах или лейкоцитах.
Воздействия соединений можно определять с помощью самих по себе известных методов, которые указываются, например, N. Escobales and J. Figueroa, J. Membrane Biol, 120, 41-49 (1001) или L. Counillon, W. Scholz, H.J. Lang and J. Pouyssegur, Mol. Pharmacol. 44, 1041-1045 (1993).
В качестве подопытных животных пригодны, например, мыши, крысы, морские свинки, собаки, кошки, обезьяны или свиньи.
Поэтому соединения можно применять в качестве биологически активных веществ лекарственных средств в медицине и ветеринарии. Далее они могут найти применение в качестве промежуточных продуктов для получения других биологически активных веществ лекарственных средств.
В указанных формулах A обозначает линейную или разветвленную алкильную группу с 1-6, предпочтительно 1-4, в особенности 1,2 или 3 C-атомами, в частности предпочтительно метил, далее предпочтительно этил, пропил, изоприл, бутил, изобутил, далее предпочтительно втор.бутил, трет.бутил, пентил, изопентил (3-метил-бутил), гексил или изогексил (4-метил-пентил).
R1 обозначает предпочтительно H, особенно предпочтительно A, Cl, Br или, однако, CnFmH2n+1-mOp, причем CnFmH2n+1-mOp предпочтительно представляет собой CF3, C2F5 или частично фторированный алкил с 1-4 C-атомами.
R2 обозначает предпочтительно F, Cl, Br или, однако, CnFmH2n+1-m Op, причем CnFmH2n+1-mOp предпочтительно представляет собой OCF3, OCH2F, OCHF2, CF2, C2 F5 или частично фторированный алкил с 1-4 C-атомами, как, например, CH2F, CHF2, C2HF4, C2H2F3, C2 H3F2, C2H4F.
R3 предпочтительно представляет собой H3C-SO2- или H2N-SO2-, далее, однако, также предпочтительно обозначает водород. Один из обоих остатков R2 и R3 предпочтительно находится в 4-положении, в то время как другой находится в 3- или 5-положении бензоильной группы. Особенно предпочтительно, однако, расположение, при котором остаток R2 находится в пара-положении к амидной группе. Если остаток R3 обозначает A-SO2-, то он предпочтительно находится в мета-положении. Особенно предпочтительна также бензоильная группа, которая в положении 3 содержит метилсульфонильный остаток, а в положении 6 - актильную группу, предпочтительно метильную или этильную группу.
R4 и R5 предпочтительно обозначают H или A.
В случае если R4 и R5 вместе обозначают алкилен, то алкиленовая группа предпочтительно является неразветвленной, в частности, предпочтительно представляет собой -(CH2)k-, причем "k"=4 или 5; однако также предпочтительно она обозначает -(CH2)2-O-(CH2)2-, -(CH2)2-NH-(CH2)2-, -(CH2)2 -NA-(CH2)2-, -CH2-O-(CH2)2-, -CH2-NH-(CH2)2- или -CH2-NA-(CH2)2-, соответственно -CO-(CH2)3-, -CO-(CH2)4- или -CH2 -CO-(CH2)2-.
Ph обозначает предпочтительно незамещенный или однократно замещенный с помощью Cl, Br, A, OA, NH2, NHA, NA или CF3 фенил.
R6 предпочтительно обозначает A, в частности метил, или, однако, предпочтительно также незамещенный фенил.
Остаток X обозначает предпочтительно O или NH.
Гет предпочтительно представляет собой 2- или 3-фурил; 2- или 3- тиенил; 1-, 2- или 3-пирролил; 1-, 2-, 4- или 5-имидазолил; 1-, 3-, 4- или 5-пиразолил; 2-, 4- или 5-оксазолил; 3-, 4- или 5-изоксазолил; 2-, 4- или 5-тиазолил; 3-, 4- или 5-изотиазолил; 2-, 3- или 4-пиридил; 2-, 4-, 5- или 6-пиримидинил; далее предпочтительно 1,2,3-триазол-1-4- или -5-ил; 1,2,4-триазол-1-, -3- или -5-ил; 1- или 5-тетразолил; 1,2,3-оксадиазол-4- или -5-ил; 1,2,4-оксадиазол-3- или -5-ил; 1, 3,4-тиадиазол-2- или -5-ил; 1,2,4-тиадиазол-3- или -5-ил; 1,2,3-тиадиазол-4- или -5-ил; 2-, 3-, 4-, 5- или 6-2H-тиопиранил; 2-, 3- или 4-4H-тиопиранил; 3-или 4- пиридазинил; 2-, 3-, 4-, 5-, 6- или 7-бензофурил; 2-, 3-, 4-, 5-, 6- или 7-бензотиенил; 1-, 2-, 3-, 4-, 5-, 6- или 7-индонил; 1-, 2-, 4- или 5-бензимидазолил; 1-, 3-, 4 , 5-, 6- или 7-бензопиразолил; 2-, 4-, 5-, 6- или 7-бензоксазолил; 3-, 4-, 5-, 6- или 7-бензизоксазолил; 2-, 4-, 5-, 6- или 7-бензтиазолил; 2-, 4-, 5-, 6- или 7-бензизотиазолил; 4-, 5-, 6- или 7-бенз-3,1,3-оксадиазолил; 2-, 3-, 4-, 5-, 6-, 7- или 8-хинолинил; 1-, 3-, 4-, 5-, 6-, 7- или 8-изохинолинил; 1-, 2-, 3-, 4- или 9-карбазолил; 1-, 2-, 3-, 4-, 5-, 6-, 7-, 8- или 9-акридинил, 3-, 4-, 5-, 6-, 7- или 8-циннолинил; 2-, 4-, 5-, 6-, 7- или 8-хиназолинил. Гетероциклические остатки могут быть также частично или полностью гидрированы. Гет, следовательно, также может обозначать, например, 2,3-дигидро-2-, -3-, -4-или -5-фурил; 2,5-дигидро-2-, -3-, -4- или -5-фурил; тетрагидро-2- или -3-фурил; 1,3-диоксолан-4-ил; тетрагидро-2- или -3-тиенил; 2, 3-дигидро-1-, -2-, -3-, -4- или -5- пирролил; 2,5-дигидро-1-, -2-, -3-, -4- или -5-пирролил; 1-, 2- или 3-пирролидинил; тетрагидро-1-, -2- или -4-имидазолил; 2,3-дигидро-1-, -2-, -3-, -4- или -5-пиразолил; тетрагидро-1-, -3- или -4-пиразолил; 1,4-дигидро-1-, -2-, -3- или -4-пиридил; 1,2,3, 4-тетрагидро-1-, -2-, -3-, -4-, -5- или -6-пиридил; 1,2,3,6-тетрагидро-1-, -2-, -3-, -4-, -5- или -6-пиридил; 1-, 2-, 3- или 4-пиперидинил; 2-, 3- или 4-морфолинил; тетрагидро-2-, -3- или -4-пиранил; 1,4-диоксанил; 1,3-диоксан-2-, -4- или -5-ил; гексагидро-1-, -3- или -4-пиридазинил; гексагидро-1-, -2-, -4- или -5-пиримиданил; 1-, 2- или 3-пиперазинил; 1,2,3,4-тетрагидро-1-, -2-, -3-, -4-, -5-, -6-, -7- или -8-хинолинил; 1,2,3,4-тетрагидро-1-, -2-, -3-, -4-, -5-, -6-, -7- или -8-изохинолинил.
Для всего изобретения действует то, что все без исключения остатки, как, например, Гет, Ph или CnFmH2n+1-mOp, которые встречаются многократно, независимо друг от друга могут быть одинаковыми или разными.
Соответственно
этому предметом изобретения являются в особенности те соединения формулы (I), в
которых по меньшей мере один из указанных остатков имеет одно из вышеуказанных предпочтительных значений. Некоторые
предпочтительные группы соединений могут быть выражены нижеследующими формулами (Iа)
- (Iз), которые соответствуют формуле (I) и где подробнее не указанные остатки имеют указанное в случае формулы
(I) значение, где, однако,
в Ia: R1 обозначает H и R3
обозначает -SO2-CH3-, -SO2-NH2 или водород;
в Iб: R1 обозначает H, метил или этил и R2 обозначает CF3, OCH2F, OCHF2, CF3, C2F5 или частично фторированный алкил с 1-4
C-атомами, как, например, CH2F, CHF2, C2HF4,
C2H2F3, C2H3F3, C2H4F;
в Iв: один из остатков R2 или R3 обозначает Cn
FmH2n+1-mOp, а другой обозначает водород, CF3Cl или Br;
в
Iг: R1 обозначает метил, этил, F, Cl или Br и R2 и/или R3
обозначает CnFmH2n+1-mOp;
в Iд: оба остатка R2 и R3, независимо друг от друга, обозначают CnFmH2n+1-mOp;
в Ie: R1 обозначает метил, этил, F, Cl, Br; R2
обозначает CnFmH2n+1-mOp и R3 обозначает
водород;
в Iж: остаток CnFmH2n+1-mOp находится в
пара-положении к гуанидинкарбонильной группе и R1 обозначает метил, этил, F, Cl или Br;
в Iз: R1 обозначает NO2 или CN и R3 обозначает CnFmH2n+1-mOp.
Предметом изобретения далее
является способ получения соединений формулы (I) по п.1 формулы изобретения, а также их солей,
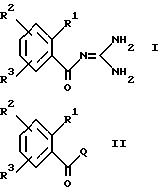
отличающийся тем, что соединение формулы (II)

где R1, R2 и R3 имеют вышеуказанные значения и
Q обозначает Cl, Br, OA, O-CO-A, O-CO-Ph, OH или другую реакционноспособную, этерифицированную до сложноэфирной, OH-группу, соответственно, легко нуклеофильно замещаемую удаляемую группу,
вводят во взаимодействие с гуанидином;
или бензоилгуанидин формулы (III)
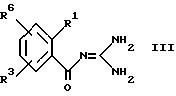
где R1 и R3 имеют вышеуказанные значения и
R6 обозначает Br, Cl, F, I или другие нуклеофильно замещаемую группу,
вводят во взаимодействие с соединением формулы (IV):
CnFmH2n+1-mOp-L, (IV)
где n, m и p имеют указанные значения, а L обозначает H, (CH3)3-Si, CO2K или CO2Na, катион щелочного металла, NH4+, Ag+ или Cu+;
или обычно соответствующее формуле (I) соединение, которое, однако, вместо одного или нескольких атомов водорода содержит одну или несколько восстанавливаемых групп и/или одну или несколько дополнительных C-C- и/или C-N-связей, обрабатывают восстановителем;
или обычно соответствующее формуле (I) соединение, которое, однако, вместо одного или нескольких атомов водорода содержит одну или несколько сольволизируемых групп, обрабатывают сольволизирующим средством;
и/или полученное основание формулы (I) путем обработки кислотой превращают в его соль.
Соединения формулы (I), впрочем, получают само по себе известными способами, которые описываются в литературе (например, в стандартных работах, как Губен-Вейл, Методы органической химии, изд. Georg-Thieme, Штутгарт; Органические реакции John Wiley and Sons Inc., Нью-Йорк; а также в вышеуказанной патентной заявке), а именно при реакционных условиях, которые известны и пригодны для указанных взаимодействий. При этом также можно применять само по себе известные, здесь подробнее не упомянутые варианты.
Исходные вещества в желательном случае также можно получать in situ, таким образом, что их не выделяют из реакционной смеси, а тотчас вводят во взаимодействие далее до получения соединений формулы (I).
Предпочтительно соединения формулы (I) получают тем, что активированное производное карбоновой кислоты формулы (II), причем О особенно предпочтительно обозначает Cl или -O-CH3, вводят во взаимодействие с гуанидином. Особенно пригодны варианты реакций, в случае которых свободную карбоновую кислоту формулы (II) (Q=OH) самим по себе известным образом превращают в соответствующее активированное производное и его затем прямо, без промежуточного выделения, вводят во взаимодействие с гуанидином. Способы, при которых промежуточное выделение ненужно, представляют собой, например, активирование с помощью карбонилдимидазола, дициклогексилкарбодиимида или вариант Mykaiyama (Angew. Chem. 91, 788-812 (1979)).
Карбоновые кислоты формулы (II) получают путем нуклеофильного ароматического замещения исходя из пригодных производных бензойной кислоты путем введения их во взаимодействие с соответствующими соединениями формулы (IV). Взаимодействие осуществляют по аналогии с реакцией соединений формул (III) и (IV). Оно описывается ниже.
Особенно пригодными соединениями формулы (IV) является, например, соли щелочных металлов частично или полностью фторированных алканкарбоновых кислот.
Взаимодействие реакционноспособного производного карбоновой кислоты формулы (II) с гуанидином осуществляют само по себе известным образом, предпочтительно в протонном или апротонном, полярном или неполярном, инертном органическом растворителе.
Пригодные растворители указываются ниже для взаимодействия соединений формул (III) и (IV). Особенно предпочтительными растворителями являются, однако, метанол, ТГФ, диметоксиэтан, диоксан или приготовляемые из них смеси, а также вода. В качестве температуры реакции пригодны, например, температуры от 20oC до температуры кипения растворителя. Время реакции составляет от 5 мин до 12 ч. При реакции можно целесообразно использовать улавливатель кислоты. Для этой цели пригодны любые виды оснований, которые сами не мешают реакции. Особенно пригодно, однако, применение неорганических оснований, как карбонат калия, или органических оснований, как триэтиламин или пиридин, или, однако, избыток гуанидина.
Соединения формулы (I) по п.1 формулы изобретения далее можно получать тем, что бензоилгуанидин формулы (III) вводят во взаимодействие с соединением формулы (IV). Исходные вещества формулы (III) можно получать простым образом путем взаимодействия соответствующим образом замещенных бензойных кислот или производимых от них реакционноспособных производных кислот, как, например, галоидангидриды кислот, сложные эфиры или ангидриды кислот, с гуанидином, при реакционных условиях, которые само по себе известны и общеприняты для получения амидов. Особенно пригодны опять такие варианты реакции, которые указаны выше для взаимодействия соединения формулы (II) с гуанидином.
Соединение формулы (IV), точно так же, как и способы их получения, само по себе известно. Если они не известны, то их можно получать самими по себе известными способами.
Получение соединения формулы (II), а также взаимодействие соединения формулы (III) с соединением формулы (IV) осуществляют самим по себе известным образом, предпочтительно в протонном или апротонном, полярном инертном органическом растворителе.
При получении соединения формулы (II) в случае взаимодействия соединения формулы (II) с гуанидином или в случае взаимодействия соединения формулы (III) с соединением формулы (IV) также целесообразно работать в присутствии основания или с избытком основного компонента. В качестве оснований предпочтительно пригодны, например, гидроксиды, карбонаты, алкоголяты щелочных или щелочноземельных металлов или органические основания, как триэтиламин или пиридин, которые также можно применять в избытке и тогда они могут служить одновременно растворителем.
В качестве инертных растворителей пригодны, в частности, спирты, как метанол, этанол, изопропанол, н-бутанол или трет.бутанол; простые эфиры, как диэтиловый эфир, диизопропиловый эфир, тетрагидрофуран (ТГФ) или диоксан; простые гликолевые эфиры, как простой этиленгликольмонометиловый или моноэтиловый эфир (метилгликоль или этилгликоль), простой этиленгликольдиметиловый эфир (диглим); кетоны, как ацетон или бутанон; нитрилы, как ацетонитрил; нитросоединения, как нитрометан или нитробензол; сложные эфиры, как этилацетат; амиды, как гексаметилтриамид фосфорной кислоты; сульфоксиды, как диметилсульфоксид (ДМСО); хлорированные углеводороды, как дихлорметан, хлороформ, трихлорэтилен, 1,2-дихлорэтан или тетрахлорид углерода; углеводороды, как бензол, толуол или ксилол. Далее пригодны смеси этих растворителей друг с другом.
Особенно предпочтительный вариант работы состоит в том, что избыток соединения формулы (IV) в форме триметилсилилоксипроизводного непосредственно без добавки растворителей вводят во взаимодействие с бензоилгуанидином формулы (III) при температурах 100-400oC, особенно предпочтительно при 100-200oC. Точно так же соединение формулы (IV), предпочтительно калиевую или натриевую соль, или соответствующую соль карбоновой кислоты, в присутствии C вводят во взаимодействие с бензоилгуанидином формулы (III) или пригодным предшественником, например сложным эфиром.
Далее в соединении формулы (I) один или несколько остатков R1, R2 и/или Гет можно превращать в другие остатки R1, R2 и/или Гет.
Например, H-атом путем галогенирования можно заменять на атом галогена или путем нитрования можно заменять нитро-группой и/или нитро-группу можно восстанавливать до амино-группы и/или амино- или гидроксильную группу можно ацилировать или алкилировать и/или бензильный остаток можно отщеплять гидрогенолитически (например, с помощью H2 в присутствии катализатора, как Pd, или с помощью формиата аммония в метаноле).
Нитрование протекает в обычных условиях, например с помощью смеси из концентрированной HNO3 и концентрированной H2SO4 при температурах 0-30oC.
Аналогичное имеет значение для галогенирования, которое можно осуществлять, например, с помощью элементного хлора или брома в одном из обычных инертных растворителей при температурах примерно 0-30oC.
Первичную или вторичную амино-группу и/или OH-группу путем обработки с помощью алкилирующих средств можно превращать в соответствующую вторичную или третичную амино-группу и/или алкокси-группу. В качестве алкилирующих средств пригодны, например, соединения формул A-Cl, A-Br или A-I или соответствующие сложные эфиры серной кислоты или сульфокислоты, как метилхлорид, метил бромид, метилиодид, диметилсульфат, метил-п-толуолсульфонат. Далее, можно вводить, например, одну или две метильные группы с помощью формальдегида в присутствии муравьиной кислоты. Алкилирование целесообразно осуществлять в присутствии или в отсутствие одного из указанных инертных растворителей, например, как ДМФ, при температурах примерно 0-120oC, причем также можно добавлять катализатор, предпочтительно основание, как трет.бутилат калия или NaH.
Основание формулы (I) с помощью кислоты можно переводить в соответствующую соль присоединения кислоты. Для этого превращения применяют кислоты, которые дают физиологически приемлемые соли. Так, можно применять неорганические кислоты, например, серную кислоту; азотную кислоту; галогенводородные кислоты, как соляная кислота или бромоводородная кислота; фосфорные кислоты, как ортофосфорная кислота; сульфаминовую кислоту; далее, органические кислоты, в особенности алифатические, алициклические, аралифатические, ароматические или гетероциклические одно- или многоосновные карбоновые, сульфоновые или серные кислоты, например, как муравьиная кислота, уксусная кислота, пропионовая кислота, пивалиновая кислота, диэтилуксусная кислота, малоновая кислота, янтарная кислота, пимелиновая кислота, фумаровая кислота, малеиновая кислота, молочная кислота, винная кислота, яблочная кислота, бензойная кислота, салициловая кислота, 2- или 3-фенилпропионовая кислота, лимонная кислота глюконовая кислота, аскорбиновая кислота, никотиновая кислота, изоникотиновая кислота, метан- или этансульфокислота, этандисульфокислота, 2-гидрокси-этансульфокислота, бензосульфокислота, п-толуолсульфокислота, нафталинмоно- и дисульфокислоты, лаурилсерная кислота.
Соединения формулы (I) и их физиологически приемлемые соли можно применять для приготовления фармацевтических композиций, в частности нехимическим путем. При этом их вместе по меньшей мере с одним твердым, жидким и/или полужидким носителем или вспомогательным веществом и в случае необходимости в комбинации с одним или несколькими другими биологически активными веществами можно доводить до пригодной дозировочной формы.
Предметом изобретения далее являются средства, в частности, фармацевтические композиции, содержащие по меньшей мере одно соединение формулы (I) и/или одну из его физиологически приемлемых солей.
Эти композиции можно применять в качестве лекарственных средств в медицине и ветеринарии. В качестве носителей применяют органические или неорганические вещества, которые пригодны для кишечного (например, орального), парентерального или топического применения и не реагируют с новыми соединениями, например, как вода, растительные масла, бензиловые спирты, полиэтиленгликоли, глицерин-триацетат, желатина, углеводы, как лактоза или крахмал, стеарат магния, тальк, ланолин, вазелин. Для орального применения служат в частности таблетки, драже, капсулы, сиропы, соки или капли; для ректального применения служат свечи; для парентерального применения служат растворы, предпочтительно масляные или водные растворы, далее, суспензии, эмульсии или имплантаты; для топического применения служат мази, кремы, пасты, лосьоны, гели, пульверизуемые препараты, пены, аэрозоли, растворы (например, растворы в спиртах, как этанол или изопропанол, в ацетонитриле, ДМФ, диметилацетонитриле, 1,2- -пропандиоле или их смесях друг с другом и/или с водой) или порошки. Новые соединения можно также лиофилизировать и полученные лиофилизаты применять, например, для приготовления препаратов для инъекции.
В частности, для топического применения применяют также липосомальные композиции. Указанные композиции могут быть стерилизованы и/или могут содержать вспомогательные вещества, как придающие скользкость (например, таблеткам) вещества, консерванты, стабилизаторы и/или смачиватели, эмульгаторы, соли для влияния на осмотическое давление, буферные вещества, красители, вкусовые вещества и/или ароматические вещества. Если желательно, они могут содержать также одно или несколько других биологически активных веществ, например, один или несколько витаминов.
Соединения формулы (I) и их физиологически приемлемые соли можно вводить людям или животным, в частности, млекопитающим, как обезьяны, собаки, кошки, крысы или мыши, и применять при терапии организма человека или животного, а также при борьбе с заболеваниями, в особенности при лечении и/или профилактике нарушений сердечно-сосудистой системы. Поэтому они пригодны для лечения аритмий, в частности когда они возникают вследствие недостатка кислорода, стенокардии, инфарктов, ишемий нервной системы, как, например, инсульт или отек мозга, шоковых состояний и для профилактики.
Вещества далее можно использовать в качестве терапевтических средств при заболеваниях, при которых играют роль пролиферации клеток, как артериосклероз, диабетические поздние осложнения, опухолевые заболевания, фиброзы, а также гипертрофии и гиперплазии органов.
При этом предлагаемые согласно изобретению вещества, как правило, вводят по аналогии с известными антиаритмическими средствами, например, как априндин, предпочтительно в дозировках примерно 0,01-5 мг, в особенности 0,02-0,5 мг, на дозировочную единицу. Суточная доза предпочтительно составляет примерно 0,0001-0,1, в частности 0,0003-0,01 мг/кг веса тела. Специальная доза для каждого определенного пациента, однако, зависит от самых различных факторов, например, от эффективности используемого специального соединения, от возраста, веса тела, общего состояния здоровья, пола, от стоимости, от момента и пути введения, от скорости выделения, комбинации лекарственных средств и тяжести соответствующего заболевания, которое имеет значение для терапии. Предпочтительно оральное введение.
В нижеследующих примерах выражение "обычная обработка" обозначает: добавляют, если требуется, воду; экстрагируют с помощью органического растворителя, как этилацетат; фазы разделяют; органическую фазу сушат над сульфатом натрия, отфильтровывают, выпаривают и очищают путем хроматографии и/или кристаллизации.
Пример 1. Раствор из 0,5 г 2-метил-4-фенокси-5-трифторметилбензойной кислоты (получают путем взаимодействия метилового эфира 2- метил-4-фенокси-5-бромбензойной кислоты с трифторацетатом калия в присутствии CuI и тетраметиламмонийхлорида и последующего омыления) и 300 мг карбонилдиимидазола в 15 мл ТГФ перемешивают в течение 2 ч при комнатной температуре и этот раствор затем добавляют к 383 мг гуанидина. Перемешивают следующие 2 ч. После обычной обработки получают N-диамино-метилен-2-метил-4-фенокси-5- трифторметил-бензамид.
Аналогичным образом, путем взаимодействия гуанидина
с 2-метил-5-дифторметокси-бензойной кислотой получают
N- диамино-метилен-2-метил-5-дифторметокси-бензамид;
с 2-метил-5-(2,2,2-трифторэтокси)бензойной кислотой получают
N-диаминометилен-2-метил-5-(2,2,2-трифторэтокси)бензамид;
с
3-метилсульфонил-4-(пентафторэтил)-бензойной кислотой получают N-диаминометилен-3-метилсульфонил-4-(пентафторэтил) бензамид;
с 3-метилсульфонил-4-трифторметокси-бензойной кислотой получают
N-диаминометилен-3-метилсульфонил-4-трифторметокси-бензамид;
с 3-метилсульфонил-4-дифторметокси-бензойной кислотой
получают N-диаминометилен-3-метилсульфонил-4-дифторметокси-бензамид;
с 3-метилсульфонил-4-фторметокси-бензойной кислотой получают N-диаминометилен-3-метилсульфонил-4-фторметокси-бензамид;
с 2-метил-4-пентафторэтил-5-метилсульфонил-бензойной кислотой получают
N-диаминометилен-2-метил-4-пентафторэтил-5-метилсульфонил-бензамид;
с
2-метил-4-трифторметокси-5-метилсульфонил-бензойной кислотой получают
N-диаминометилен-2-метил-4-трифторметокси-5-метил-сульфонил- бензамид;
с
2-метил-4-дифторметокси-5-мстилсульфонил-бензойной кислотой получают
N-лиаминометилен-2-метил-4-дифторметокси-5-метилсульфонил- бензамид;
с 2-метил-4-фторметокси-5-метилсульфонил-бензойной
кислотой получают
N-диаминометилен-2-метил-4-фторметокси-5-метилсульфонил-бензамид;
с 3-метилсульфонил-4-(1,6-дигидро-6-оксо-3-пиридазинилокси)- 6-трифторметил-бензойной кислотой получают
N-диаминометилен-3- метилсульфонил-4-(1,6-дигидро-6-оксо-3-пиридазинилокси)-6-три- фторметил-бензамид.
Пример 2. К раствору из 928 мг гуанидина в 15 мл метанола добавляют 1,1 г метилового эфира 3-метилсульфонил-4-трифторметил- бензойной кислоты (т.пл. 146-147oC; получают путем взаимодействия метилового эфира 3-метилсульфонил-4-бром-бензойной кислоты с трифторацетатом калия в присутствии CuI и тетраметиламмонийиодида в толуоле). Перемешивают 45 мин при 50oC, после удаления растворителя и обычной обработки получают N-диамино-метилен-3-метилсульфонил-4-трифторметил-бензамид, т.пл. 233-234oC. После обработки с помощью разбавленного водного раствора HCl, сушки вымораживанием из вышеполученного соединения получают соответствующий гидрохлорид.
Аналогичным образом, путем взаимодействия гуанидина
с метиловым эфиром 2-метил-4-трифторметил-5-метилсульфонил- бензойной
кислоты (т. пл.
135-136oC) получают N-диаминометилен-2- метил-4-трифторметил-5-метилсульфонил-бензамид, т.пл. 212-213oC (основание), гидрохлорид;
с метиловым эфиром 2,
5-бил-(2,2,
2-трифторэтокси)бензойной кислоты получают N-диаминометилен-2,5-бис-(2,2,2-трифторэтокси)бонзамид- гидрохлорид;
с метиловым эфиром 2-метил-бром-5-трифторметокси-бензойной кислоты
получают
N-диаминометилен-2-метил-4-бром-6-трифторметоксибензамид- гидрохлорид;
с метиловым эфиром 2-этил-4-бром-5-трифторметокси-бензойной кислоты получают
N-диаминометилен-2-этил-4-бром-5-трифторметокси-бензамид- гидрохлорид;
с метиловым эфиром 2,4-дибром-5-трифторметокси-бензойной кислоты получают N-диаминометилен-2,
4-дибром-5-трифторметокси-бензамид-гидрохлорид;
с метиловым эфиром 2-изопропил-4-бром-5-трифторметокси- бензой-ной кислоты получают
N-диаминометилен-2-изопропил-4- бром-5-трифторметокси-бензамид-гидрохлорид;
с метиловым эфиром 2-изопропил-4-хлор-5-трифторметокси- бензойной кислоты получают
N-диаминометилен-2-изопропил-4-хлор-5- трифторметокси-бензамид-гидрохлорид;
с метиловым эфиром 2-метил-4-хлор-5-трифторметокси- бензойной кислоты получают
N-диаминометилен-2-метил-4-хлор-5- трифторметокси-бензамид-гидрохлорид;
с метиловым эфиром 2-метил-4-циантрифторметокси-бензоной кислоты получают
N-диаминометилен-2-метил-4-циан-5-трифторметокси- бензамид-гидрохлорид;
с метиловым эфиром 2-нитро-4-хлор-5-трифторметокси-бензойной кислоты получают
N-диаминометилен-2-нитро-4-хлор-5-трифторметокси- бензамид-гидрохлорид;
с метиловым эфиром 2-нитро-4-бром-5-трифторметокcи- бензойной кислоты получают
N-диаминометилен-2-нитро-4-бром-5- трифторметокси-бензамид-гидрохлорид;
с метиловым эфиром 2,5-бис-(трифторметокси)-4-бромбензойной кислоты получают N-диаминометилен-2,
5-бис-(трифторметокси)-4-бром- бензамид-гидрохлорид;
с метиловым эфиром 2,5-бис-(трифторметокси)-4-хлор-бенэойной кислоты получают N-диаминометилен-2,
5-бис-(трифторметокси)-4-хлор- бензамид-гидрохлорид;
с метиловым эфиром 2,5-бис-(трифторметокси)-4-циан-бензойной кислоты получают N-диаминометилен-2,
5-бис-(трифторметокси)-4-циан- бензамид-гидрохлорид;
с метиловым эфиром 2-хлор-5-трифторметил-бензойной кислоты получают N-диаминометилен-2-хлор-5-трифторметил-бензамид- гидрохлорид; т.пл.
205oC;
с метиловым эфиром 2,5-бис- (трифторметил)бензойной кислоты получают N-диаминометилен-2,5- бис-(трифторметил)-бензамид-гидрохлорид, т.пл. 232oC;
с
метиловым эфиром 2,4-бис-(трифторметил)-бензойной кислоты получают N-диаминометилен-2,4-бис-(трифторметил)-бензамид гидрохлорид, т.пл. 179oC;
с метиловым эфиром 2,
3-бис-(трифторметил)-бензойной кислоты получают N-диаминометилен-2,3-бис-(трифторметил)- бензамид-гидрохлорид;
с метиловым эфиром 2-метил-4-бром-5- трифторметил-бензойной кислоты получают
N-диаминометилен-2-метил- 4-бром-5-трифторметил-бензамид-гидрохлорид;
с метиловым эфиром 2- этил-4-бром-5-трифторметил-бензойной кислоты получают
N- диаминометилен-2-этил-4-бром-5-трифторметил-бензамид-гидрохлорид;
с метиловым эфиром 2,4-дибром-5-трифторметил-бензойной кислоты получают N-диаминометилен-2,
4-дибром-5-трифторметил-бензамид- гидрохлорид;
с метиловым эфиром 2-изопропил-4-бром-5-трифторметил- бензойной кислоты получают
N-диаминометилен-2-изопропил-4-бром-5- трифторметил-бензамид-гидрохлорид;
с метиловым эфиром 2- изопропил-4-хлор-5-трифторметил-бензойной кислоты получают
N- диаминометилен-2-изопропил-4-хлор-5-трифторметил-бензамид- гидрохлорид;
с метиловым эфиром 2-метил-4-хлор-5-трифторметил-бензойной кислоты получают
N-диаминометилен-2-метил-4-хлор-5- трифторметил-бензамид-гидрохлорид;
с метиловым эфиром 2-метил-4- циан-5-трифторметил-бензойной кислоты получают
N- диаминометилен-2-метил-4-циан-5-трифторметил-бензамид- гидрохлорид;
с метиловым эфиром 2-нитро-4-хлор-5-трифторметил- бензойной кислоты получают
N-диаминометилен-2-нитро-4-хлор-5- трифторметил-бензамид-гидрохлорид;
с метиловым эфиром 2-нитро-4- бром-5-трифторметил-бензойной кислоты получают
N-диаминометилен-2- нитро-4-бром-5-трифторметил-бензамид-гидрохлорид;
с метиловым эфиром 2,5-бис-(трифторметил)-4-бром-бензойной кислоты получают N- диаминометилен-2,
5-бис-(трифторметил)-4-бром-бензамид- гидрохлорид;
с метиловым эфиром 2,5-бис-(трифторметил)-4-хлор- бензойной кислоты получают N-диаминометилен-2,
5-бис- (трифторметил)-4-хлор-бензамид-гидрохлорид;
с метиловым эфиром 2,5-бис-(трифторметил)-4-циан-бензойной кислоты получают N- диаминометилен-2,
5-бис-(трифторметил)-4-циан-бензамид- гидрохлорид;
Пример 3. Аналогично примеру 2, путем взаимодействия гуанидина
с метиловым эфиром 2-нитро-5- трифторметил-бензойной кислоты
получают N-диаминометилен-2- нитро-5-трифторметил-бензамид-гидрохлорид;
с метиловым эфиром 2-метил-5-трифторметил-бензойной кислоты получают
N-диаминометилен-2-метил-5-трифторметил- бензамид-гидрохлорид;
с метиловым эфиром 2-этил-5-трифторметил- бензойной кислоты получают
N-диаминометилен-2-этил-5- трифторметил-бензамид-гидрохлорид;
с метиловым эфиром 2-бутил-5- трифторметил-бензойной кислоты получают
N-диаминометилен-2-бутил- 5-трифторметил-бензамид-гидрохлорид;
с метиловым эфиром 2-трет.- бутил-5-трифторметил-бензойной кислоты получают
N-диаминометилен- 2-трет.-бутил-5-трифторметил-бензамид-гидрохлорид;
с метиловым эфиром 2-пропил-5-трифторметил-бензойной кислоты получают
N- диаминометилен-2-пропил-5-трифторметил-бензамид-гидрохлорид;
с метиловым эфиром 2-изопропил-5-трифторметил-бензойной кислоты получают
N-диаминометилен-2-изопропил-5-трифторметил- бензамид-гидрохлорид;
с метиловым эфиром 2-фтор-5-трифторметил- бензойной кислоты получают
N-диаминометилен-2-фтор-5-трифторметил- бензамид-гидрохлорид;
с метиловым эфиром 2-фтор-3-трифторметил-бензойной кислоты получают N-диаминометилен-2-фтор-3-трифторметил-бензамид- гидрохлорид;
с метиловым эфиром 2-фтор-4-трифторметил-бензойной кислоты получают N-диаминометилен-2-фтор-4-трифторметил-бензамид- гидрохлорид.
Пример 4. Аналогично примеру 2, путем
взаимодействия гуанидина
с метиловым эфиром 2-нитро-5- трифторметокси-бензойной кислоты получают N-диаминометилен-2- нитро-5-трифторметокси-бензамид-гидрохлорид;
с метиловым эфиром
2-метил-5-трифторметокси-бензойной кислоты получают N- диаминометилен-2-метил-5-трифторметокси-бензамид-гидрохлорид;
с метиловым эфиром 2-этил-5-трифторметокси-бензойной кислоты получают
N-диаминометилен-2-этил-5-трифторметокси-бензамид-гидрохлорид;
с метиловым эфиром 2-бутил-5-трифторметокси-бензойной кислоты получают
N-диаминометилен-2-бутил-5-трифторметокси- бензамид-гидрохлорид;
с метиловым эфиром 2-трет. бутил-5- трифторметокси-бензойной кислоты получают N-диаминометилен-2-трет.
бутил-5-трифторметокси-бензамид-гидрохлорид;
с метиловым эфиром 2-пропил-5-трифторметокси-бензойной кислоты получают N- диаминометилен-2-пропил-5-трифторметокси-бензамид-гидрохлорид;
с метиловым эфиром 2-изопропил-5-трифторметокси-бензойной кислоты получают N-диаминометилен-2-изопропил-5-трифторметокси-бензамид- гидрохлорид;
с метиловым эфиром
2-фтор-5трифторметокси-бензойной кислоты получают N-диаминометилен-2-фтор-5-трифторметокси- бензамид-гидрохлорид;
с метиловым эфиром 2-фтор-3-трифторметокси-бензойной кислоты получают
N-диаминометилен-2-фтор-3-трифторметокси-бензамид- гидрохлорид;
с метиловым эфиром 2-фтор-4-трифторметокси- бензойной кислоты получают
N-диаминометилен-2-фтор-4- трифторметокси-бензамид-гидрохлорид.
Пример 5. Аналогично примеру 2, путем взаимодействия гуанидина
с метиловым эфиром 2,
4- диметил-5-трифторметил-бензойной кислоты получают N- диаминометилен-2,4-диметил-5-трифторметил-бензамид-гидрохлорид;
с метиловым эфиром 2-метил-4-изопропил-5-трифторметил-бензойной
кислоты
получают N-диаминометилен-2-метил-4-изопропил-5-три- фторметил-бензамид-гидрохлорид;
с метиловым эфиром 2-этил-4-метил- 5-трифторметил-бензойной кислоты получают
N-диаминометилен-2-этил- 4-метил-5-трифторметил-бензамид-гидрохлорид;
с метиловым эфиром 2-бутил-4-трет.бутил-5-трифторметил-бензойной кислоты получают
N-диаминометилен-2-бутил-4-трет.бутил-5-трифторметил-бензамид- гидрохлорид;
с метиловым эфиром 2,4-бис-(трет.бутил)-5- трифторметил-бензойной кислоты получают N-диаминометилен-2,
4- бис-(трет.
бутил)-5-трифторметил-бонзамид-гидрохлорид;
с метиловым эфиром 2-пропил-4-этил-5-трифторметил-бензойной кислоты получают
N-диаминометилен-2-пропил-4-этил-5-трифторметил- бензамид-гидрохлорид;
с метиловым эфиром 2,4-диизопропил-5- трифторметил-бензойной кислоты получают N-диаминометилен-2,
4- диизопропил-5-трифторметил- бензамид-гидрохлорид;
с метиловым эфиром
2-фтор-3- трифторметил-4-метил-бензойной кислоты получают
N-диаминометилен- 2-фтор-3-трифторметил-4-метил-бензамид-гидрохлорид.
Hижеследующие примеры относятся к фармацевтическим композициям.
Пример А. Пузырьки с препаратом для инъекции.
В растворе из 100 г биологически активного вещества формулы (I) и 5 г вторичного кислого фосфата натрия в 3 л дважды перегнанной воды с помощью 2н соляной кислоты устанавливают pH=6,5, раствор стерильно фильтруют, разливают в пузырьки для препаратов для инъекций, лиофилизируют в стерильных условиях и стерильно закрывают. Каждый стеклянный пузырек с препаратом для инъекции содержит 5 мг биологически активного вещества.
Пример Б. Свечи.
Расплавляют смесь 20 г биологически активного вещества формулы (I) со 100 г соевого лецитина и 1400 г масла какао, разливают в формы и оставляют охлаждаться. Каждая свеча содержит 20 мг биологически активного вещества.
Пример В. Раствор.
Готовят раствор из 1 г биологически активного вещества формулы (I), 9,38 г NaH2PO4 • 2H2O, 28,48 г Na2 HPO4•12H2O и 0,1 г бензальконийхлорида в 940 мл дважды перегнанной воды. Устанавливают pH=6,8, доливают до общего объема 1 л и стерилизуют путем облучения. Этот раствор можно применять, например, в форме глазных капель.
Пример Г. Мазь.
500 мг биологически активного вещества формулы (I) смешивают с 99,5 г вазелина в асептических условиях.
Пример Д. Таблетки.
Смесь из 1 кг биологически активного вещества формулы (I), 4 кг лактозы, 1,2 кг картофельного крахмала, 0,2 кг талька и 0,1 кг стеарата магния обычным образом прессуют в таблетки, таким образом, что каждая таблетка содержит 10 мг биологически активного вещества.
Пример Е. Драже.
Аналогично примеру Д прессуют таблетки, на которые затем обычным образом наносят покрытие из сахарозы, картофельного крахмала, талька, траганта и красителя.
Пример Ж. Капсулы.
2 кг биологически активного вещества формулы (I) обычным образом вносят в твердые желатиновые капсулы, так, что каждая капсула содержит 20 мг биологически активного вещества.
Пример 3. Ампулы.
Раствор из 1 кг биологически активного вещества формулы (I) в 60 л дважды перегнанной воды стерильно фильтруют, разливают в ампулы, лиофилизируют в стерильных условиях и стерильно закрывают. Каждая ампула содержит 10 мг биологически активного вещества.
Фармакологические данные
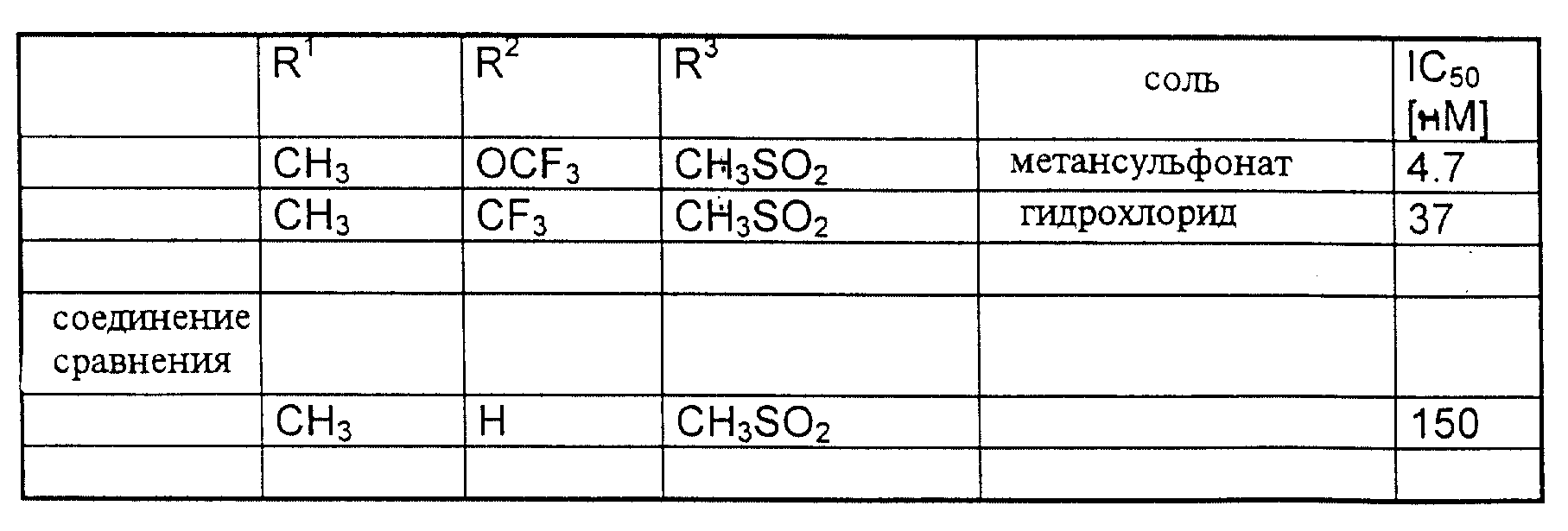
Изучали ингибирующую активность некоторых характерных соединений
общей формулы (I)
Ингибирующую активность в отношении Na+-поглощения, зависимого от Na+/H+-обмена, определяли также и для соединения сравнения, известного из EP 0556673, пример 20.
Приведенные в таблице данные подтверждают, что предлагаемые соединения формулы (I) характеризуются величиной IC50, превышающей в 4-30 раз известный уровень. Поскольку величина IC50 в наномолях соответствует 50%-ному ингибированию Na+/H+-обмена, можно сделать вывод, что соединения формулы (I) по изобретению обладают ингибирующей активностью в отношении зависимого от Na+/H+-обмена поглощения Na+, в 4-30 раз большей, чем соединение сравнения.
Реферат
Описываются новые фторсодержащие гуанидины формулы I, где R1 - H, F, Cl, Br, J, A, CN, NO2, CnFmH2n+1Op, алкинил или X-R4 ; R2 - Cn FmH2n+1O; R3 - H, A, F, Cl, Br, J, Cn FmH2n+1Op, SOq-R6, SO2NR4R5, OR6, SR6, которые получают взаимодействием соединения формулы II с гуанидином. Соединения обладают ингибирующей активностью в отношении клеточного Na+/H+ - антипорта и могут использоваться в медицине, например как антиаритмические средства. Описан также фармацевтическая композиция, включающая соединение формулы I, и способ ее получения. 4 с. и 3 з.п. ф-лы, 1 табл.
Формула
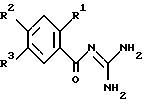
где R1 - H, F, Cl, Br, J, A, CN, NO2, CnFmH2n+1-m Op, алкинил с 2 - 4 C-атомами или - X-R4;
R2 - CnFmH2n+1-mOp;
R3 - H, A, F, Cl, Br, J, CnFmH2n+1-mOp, SOq-R6, SO2NR4R5, OR6, SR6, где
R4 и R5 каждый независимо друг от друга - H или A или вместе обозначают алкилен с 4 - 5 атомами,
R6 - Ph или A,
R7 - H или A,
A - алкил с 1 - 6 C-атомами,
X - O, S или NR7,
Ph - фенил, незамещенный или одно-, двух- или трехкратно замещенный группами A, OA, NR4R5, F, Cl, Br, J или CnFm H2n+1-mOp,
m = 1, 2, 3, 4, 5, 6 или 7, при этом самое большее 2n + 1,
n = 1, 2 или 3,
p = 0 или 1,
q = 1 или 2, при условии, что R1 может обозначать H только тогда, когда R3 - SOq-R6 или SO2NR4R5,
а также их физиологически приемлемые соли.

где R1, R2 и R3 имеют указанные в п.1 значения;
Q - F, Cl, Br, OA, O-CO-Ph, OH или другую реакционноспособную, этерифицированную до сложноэфирной OH-группу или легко нуклеофильно замещаемую удаляемую группу,
вводят во взаимодействие с гуанидином и в случае необходимости соединение формулы (I) переводят в одну из его солей.

Комментарии