К двухзамещенной сопи калия (О,48 мог ля) добавляют фосген в количестве 0,5 мо
|Пя в 12,5%-ном бензольном растворе при охлаждении льдом и при помешивании. Обра Ьующуюся
суспензию перемешивают при ком 1натной температуре в течение 24 час в беаводшлх
условиях, а затем подвергают фипьтрованию . Остаток хлористого калия промыПример 4. Синтез арилсульфэнил
(изоцианатов. 16,5 г (0,13 моля) оксалипхлорида {хлорагашдрида щавелевой кислоты) вводят
один раз в охлажденную льдом суспензию арилсульфонамида (0,1 моля) в ЮО мп бе
водного хлорбензола. Смеси дают нагреться до комнатной температу Л, после чего ее
нагревают с обратным холодильником и перемешивают в течение 24 час. Суспензию |вают эфиром (3 X 1ОО мп), а фильтрат и ;промывную жидкость концентрируют под ва куумом
. Полученное желтовато-оранжевое 1масло отличается высокой чистотой. Инфра красный
спектр показывает изотиоцианатную полосу при 4,9-5,4 мкм. В табл. 3 пред1ставлегаы
резултаты двух синтезов. Таблица 3 охлаждают и фильтруют под вакуумом через
инфузорную землю (диатомит). Фильтрат ociвобождают от содержащегося в нем растворителя
под вакуумом, а остаток перегоняют под вакуумом для получения продукта. Про|дукт
идентифицируют с помощью инфракрас;ной полосы при 4,5 мкм, являюш.ейся xapaj терной для изоцианата.
В-табл. 4 представлены результаты четырех таких синтезов.
f
Реакция проводилась с 0,0475 моля сульфонамида и О, Об моля оксалилхлорида. Продукты быстро распадаются при высокой температуре.
Пример 5. Синтез алканоил- или ароилизотиоцианатов.
Соответствующий алканоил- или ароилхлорид (0,25 моля) вводят в бейзольную
суспензию тиоцианата свинца (97 г, 0,3 мо- лосы при 5,8 - 5,9 мкм, характерной для
ля) и смесь нагревают с обратным холодиль- группы. В табл, 5 представлены резульником и перемешивают в течение 24 час, шести таких синтезов.
8
Таблица 4
а затем фильтруют под вакуумом через диатомит (инфузорную землю). Фильтрат
концентрируют под вакуумом. Инфракрасный спектр этих материалов показывает наличие
изоцианатных полос при 4,8-5,2 мкм и поТаблица 5 Реакция вначале проводилась в этилендихлоридном растворе, который в дальнейшем бып
заменен на хлорбензол для осуществления теплового разложения полупродукта (промежуточного соединения при температуре около 148°),
Пример 6. Синтез алканоил- или ароилзоцианатов,
К раствору амида соответствующей киспоты в этилендихпориде по каплям вводят
оксалилхлорид. Образовавшийся раствор нагПродукт разложения остается твердым до 225°. Другая проба показывает полный распад
при хранении в предварительно нагретой до 130° ванне.
Пример 7. Получение монодиалкиЛфосфонотиоурейда
.
В раствор желаемого 0-фенилендиамина (1 моль) в сухом фосфоноизотиопианате
Элементный анализ.
Вычислено,%: С 43,6; 47,11; Н 5,99;
6,70; N 13,85; 12,78.
Найдено, %: С 43,10; 47,25;Н 6,12; 6,45; N 13,71; 12,78.
Пример 8. Получение 1-(3-диалкилфосфонотиоуреидо )-2-( 3-алкил- или арил-
сульфонилуреидо) бензольных соединений.
К суспензии в фосфоноизотиоцианате или
другом растворителе соответствующего моиодиалкилфосфонотиоуреида быстро по каплям
добавляют арилсульфонилизоцианат. В ходе протекающей при этом слегка экзотермической
реакции смесь переходит в раствор . Его выдерживают при комнатной температуре
на протяжении указанного в табл. 8 времени реакции и при этом образуется
осадок. Продукт выделяют путем фильтрования под вакуумом и идентифицируют метода536
(300 мл) по каплям и при охлаждении льдом вводят арил- или алкилфосфоноизотиоцианат
(1 моль). После перемешивания суспензии в течение 24 час продукт выделяют фильтрованием
. Результаты приведены в табл.7.
Таблица 7
ми элементного анализа и .крг::..ого спектра.
В табл. 8 представлен :. гччэультаты ILIRCти таких синтезов.
Пример 9. Получение бензольных оединений 1-{3-диалкилфосг/. Тгтозрс го)2-{3-алканоил
или ароилурекдо,,
Монодиалкилфосфонотиоуреид, получаемый
аналогично примеру 7, и ароилизоцианат подвергают взаимодействию при комнатной температуре
. Продукт выделяют фильтрованием под вакуумом и идентифицируют методами
элементного анализа и инфракрасного спектра .
В табл. 9 представлены результаты двух таких синтезов.
Пример 10. Получение монодиал60 килфосфоноурейдов. ревают с обратным холодильником и перемешивают в течение 24 час, а затем концентрируют
под вакуумом. Остаточное масло отгоняют под вакуумом. В табл. 6 представлены результаты двух
таких синтезов. Таблица 6
11
12
с ю
0
15
Диэтилфосфоноизоцианат (10 г, 0,О5575
моля) в 5 МП фосфоноизотиоцианата по каплям вводят в охлажденный льдом раствор
0- j eнилeвдиaминa (6,03 г, 0,05575 моля) в 25 мл фосфоноизотиоцианата. Суспензию
перемешивают при комнатной температуре в течение 72 час, а затем подвергают фильтрованию
под вакуумом. При этом получают 12,5 г продукта (76%-ный выход) с т.пя.
137-14ОО (легкое разложение). Соединение идентифицируют по инфракрасному спектру и элементному анализу.
Пример 11. Получе1ше 1,3-диалкилфосфоноуреид-2- ( 3-алканоил или ароил или
алкилсульфонил или арилсульфонилуреидо- или тиоуреидэ) бензола.
Монодиалкилфосфоноуреид, получаемый по примеру 10, суспендируют в фосфоноизотиоцианате
, а затем вводят соответствующий алканоил, - ароил, - алкилсульфонил или
арилсульфонилизоцианат- или изотиоцианат . При этом происходит образование раствора
, при слабой экзотермии, а затем получается суспензия, которая перемешивается
Пример 13. Получение бензольных соединений 1-( 3-диалкилфосфэнотиоуреид)-2-
( 3-алканоил или ароилтиоуреидо).
В суспензию соответствующего монодиалкилфосфонотиоуреида
в сухом фосфоноизотиоцианате по каплям при комнатной температуре
вводят желаемый ацил- или ароилизотиоцианат (см. табл. 12).
Вслед за образующимся мгновенно раствором (слабая экзотермия) образуется осадок
. Реакцию осуществляют при комнатной температуре в течение указанного промежутка
времени. Продукт выделяют отфильтровыванием суспензии под вакуумом.
В табл. 12 представлены результаты семи таких синтезов.
16
при комнатной температуре. Суспензию фильтруют
под вакуумом, а продукт идентифицируют методами элементного анализа и инфракрасного
спектра. Каждое из соединений имеет карбонильную полосу .фосфономочевины при 5,9-6 мкм.
В табл. 1О представлены результаты пяти таких процессов.
П р к м е р 12. Получение бензольных соединений 1-( 3-диалкилфосфонотиоуреидо)-2-
( 3-алкилсульфонилтиоуреидо).
К суспензии соответствующего монодиалкилфосфонотиоуреида
(0,2 моля) в сухом фосфоноизотиоцианате (4ОО мл) по каплям при комнатной температуре добавляют жела
емый арил- или алкилсульфонилизотиоцианат (0,3 мопя). Во время перемешивания раствора
за время, указанное в табл. 11, температуру поддерживают не выше 35°. Продукт
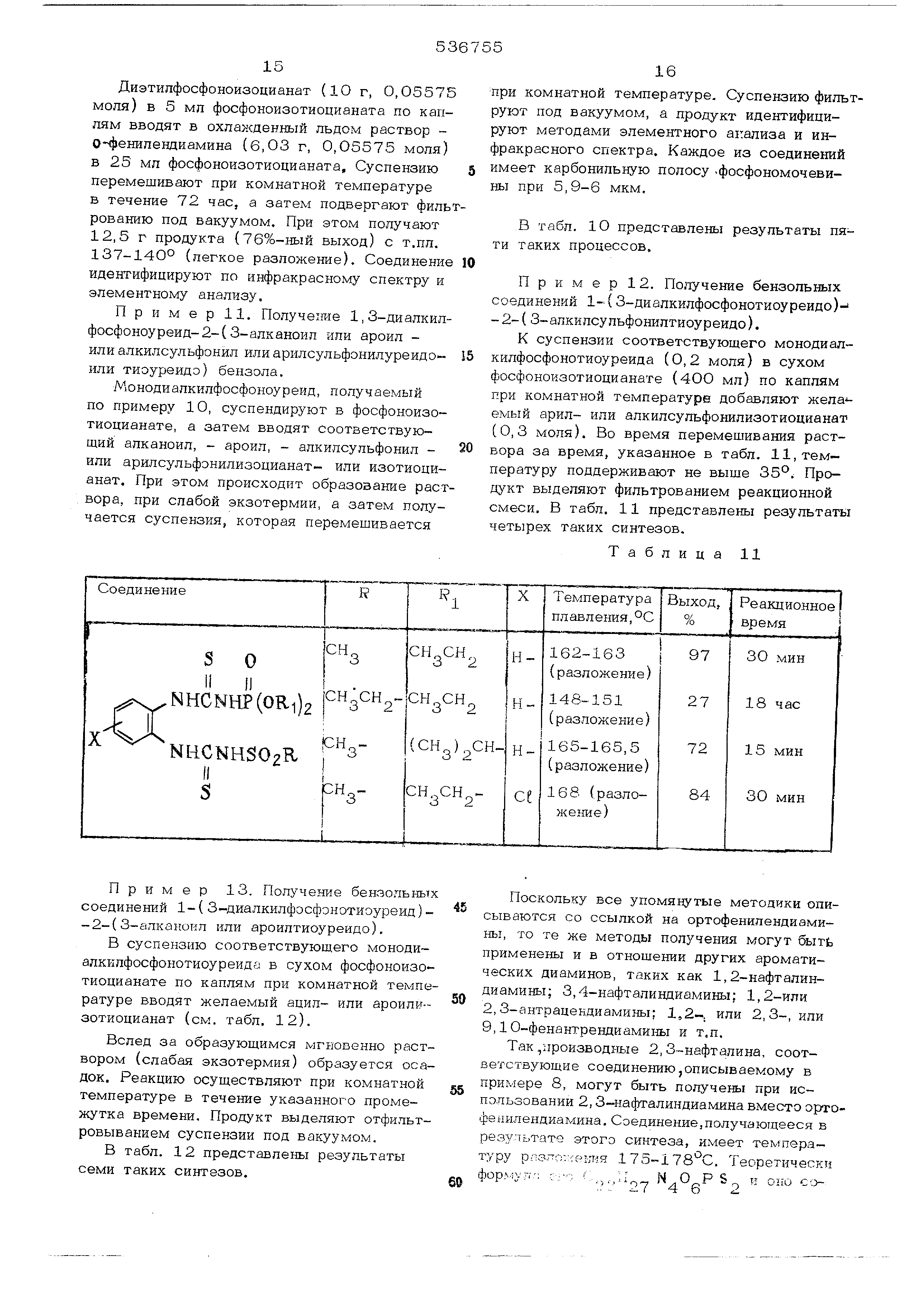
выделяют фильтрованием реакционной смеси. В табл. 11 представлены результаты четырех таких синтезов.
Таблица 11
Поскольку все упомянутые методики описываются
со ссылкой на ортофенилендиамины , то те же методы получения могут быть
применены и в отношении других ароматических диаминов, таких как 1,2-нафталиндиамины;
3,4-нафталиндиамины; 1,2-или 2.3-антрацендиамины; 1,2-. или 2,3-, или 9,10-фенантрендиамины и т.п.
Так,производные 2,3 нафталина, соответствующие соединению,описываемому в
примере 8, могут быть получены при использовании 2,3-нафталиндиамина вместо ортофенилендиамина
. Соединение, полу чающееся в реззльтате этого синтеза, имеет температуру
рлз,гтп-.:-;ршя 175-178С. Теоретически
форЛС-:
Н . 5„ и оно 2
17
держит 50,17% углерода, 4,94% водорода и 10,18% азота. Полученное соединение
имеет 50,61% углерода, 5,ОЗ% водорода и 10,3% азота.
Производное 2,3-нафталина, соответствующее соединению, описываемому в примере
7, может быть получено с использованием вместо ортофенилендиамина 2,3-нафталиндиамина
. Соединение, получающееся в результате этого синтеза, имеет температуру рафложения
148-151°С и формулу С
N S Теоретически это соединение
содержит 50,98% углерода; 5,78% водоро18
да, 11,89% азота. Найдено, что соединение
содержит 50,79% углерода; 11,79% азота. Это соединение обладает эффективной антигельминтной активностью.
Используя 9,10-фенантрендиамин вместо ортофенилендиамина, получают производное
9, Ю-фенантрена. Соединение, получающееся в результате этого синтеза, имеет температуру
разложения 175-177°С и формулу
С рН . Теоретически это соединение
содержит 56,56% углерода, 5,50% водорода, 10,42% азота и 7, 68% фосфора.
Найдено, что соединение содержит 56,55% углерода; 5,41% водорода; 10,13% азота
и 7,4% фосфора.
21
Формула изобретения
Способ получения фосфорипированной арипенмочевины
или тиомочевины общей формулыOR ,
NHC-NH-P
/ив
А; I
NHK.3
где А - незамещенный или замещенный
.арипен;
Т и - одновалентный алифатический или ароматический радикал с 1-18 углеродвыми атомами;
22
Т J - водород, низщий алкил или
г-С- N HR - группа;
Х ХиХ. кислород или сера;
j - низший алкилсульфонил, аллилсульфонил , незамещенный или замещенный
фенилсульфонил, низший алканоил или незамещенный или замещенный бензоил, отличающийся
тем, что соответствующий арилендиамин подвергают взаимодействию с изотио- или изоцианатофосфатом, с
последующим выделением продукта или обработкой его изоцианатом общей формулы Х.С N -1,
и К имеют указанные значения.













Комментарии