Способ получения ароматических эфиров циановой кислоты - SU591138A3
Код документа: SU591138A3
Описание
(54) СПОШБ ПОЛУЧЕНИЯ АРОМАТИЧЕСКИХ ЭФИРОВ
ЦИАНОВОЙ КИСЛОТЫ
ся во взаимодействии производных фенола с хлористым цианом примольном соотношении хлористого циана и произвооного фенола от 1,1:1 до 5:1 ь присутствии от 1,05 до 1,5 моль водной щелочи на 1 моль фенольного гидроксила и третичного амина при температуре 0-10 С в среде не смешивалощегося с водой органического растворителя. Наличие двух несмешивающйхся фаз, вод ной и органической, приводит к тому, что
процесс протекает на границе разрела водной и органической фаз, причем в водной фазе находятся фенолят и избыток щелочи, в органической - хлористый циан, а добавка третичного амина распределена между обейми фазами.
Процесс npoBOHSFT при интенсивном перемешивании (60О-1200 обор./мин) с добав кой иебольщих количеств поверхностно-активных веществ в сочетании с эмульгатором
При таком проведении процесса в воршом растворе, в основном, подавляется | np6t/ ная реакция омыления галоидного циана (степень омыления ниже 20%).
В качестве не смешивающихся с водой раствЬрителей можно применять углеводороды или. .хлоруглеводороды,
В случае использования алифатических хлоруглеводородов реакционную смесь можно легко эмульгировать путем простого перемешивания , и, кроме того, при этом упрощается; вы деление целевых эфиров циановой кислоты, растворимых в хлоруглеводородах.
Способ можно проводить путем диспергирования водного раствора фенолята в избытке раствора галоидного циана в органическом рестэорителе. Однако можно подавать лишь часть галоидного циава в орга«нической фазе в начале реакции, а другуто, часть ( в жидком или газообразном состоянии ) во время реакции. В последнем случае следует избегать избытка водного раствора фенолята.
Получаемая дисперсия из водного раствора неорганической соли и раствора образовавшегося ароматического эфира циановой кислоты в инертном растворителе легко раз деляется на органическую и водную фазы После заверещения реакции. Аром ический эфир циановой кислоты можно выделять из органической фазы путем промывки водой с последующей отгонкой раствррителя.
Предлагаемый способ можно проводить периодически или непрерывно.
П р и м,е р 1. В аппарате с мешалкой емкостью 1 л, снабжегаом плоскими лопастями (лопасть 10 см ), растворы 20 г хлористого циана в 40О г различных орга нических растворителей охлаждают до 5 С ;И.затем в раствор добавляют 0,1 г
триэтиламина. Затем каплями добавляют охлажденный до 5 С раствор 2О г бисфенола А, 7,3 г гидроокиси натрия и 500 мл дистиллированной воды. Реагенты перемешивают в течение 30 мйн при постоянной подаче азота в качестве защитного газа. Температуру реакционной смеси поддерживают 5 С путем наружного охлаждения, а рН эмульсии - около 5-6.
После завершения добавления и перемещивания эмульсию подают в делительную воронку, где эмульсию разделяют на органическую и водную фазу в течение 5-10 мин в зависимости от того, имеет ли органический растворитель более низкую (толуол) или или более вьюокую (метиленхлорид) плотность, чем водная фаза Органическая фаза, которая содержит образовавшийся сложный эфир циановой кислоты и органический растворитель, представляет собой верхний (в случае толуола) или нижний (в случае метиленхлорида) слой. Органическую фазу отделеяют от водной путем спуска, три раза промывают 200 мл дистиллировайг ной воды и снова отделяют от воднрй фазы,, затем растворитель удаляют из органической путем перегонки при температуре .ниже 65 С и давлении примерно 10О мм рт.ст.
Оставшийся расплав кристалл из .
Результаты трех опытов приведены в. табл.1.:
Выход 2,2 бис-(4-«ианатофенш1)-пропана
составляет 24,S г (100% от теории).
Если проводить реакцию в присутствий О,3 г амульгатрра .(см. табл.1, опыт 2)J: то после переработки получают 24 г (98,5% от теории) 2,2-6ис-( 4-аианатофенил)-пропана; содержание 30%, что соответствует чистоте 99,4 %,.
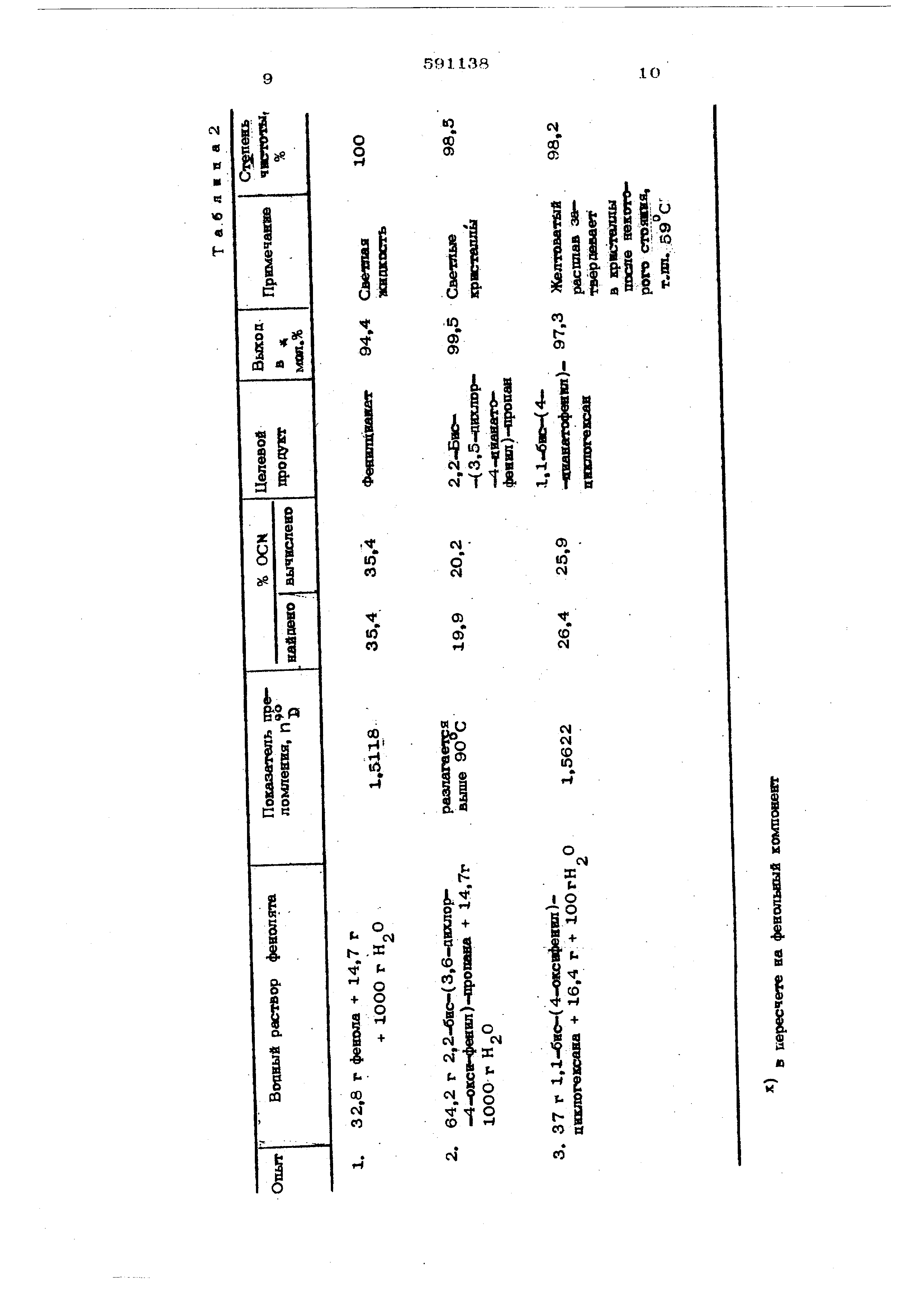
Пример 2. В аппарате с мешалкой емкостью 1 л, снабженном плоскими Гпопастями (лопасть 10 см }, растворы 4Ог хлористого циана в 80О мл метиленхлорида охлаждают до 5 С и в каждый раствор аобавляют О,2 г триэтиламина. Затем при nof даче азота в качестве инертного газа и пе ремешивании при 60О обор./мин, в течёвие 30 мин добавляют охлажденные до 5 С pfH створы перечисленных в табл. 2 ..
При этом температуру поддерживают при 5 С путем наружного охлажоения.
Реакционные смеси перерабатывают по примеру 1.
П р и м е р 3. В водоохлаждаемом аппйратё с м щалкой и с боковым переливом 1840 г/ч раствора хлористого циана в метилевхлориде (5% хлористого циана, 0,05%; Триэтиламина) непрерывво тщательно перемешивают с 1О54 г/ч ВОДНО1Ч) раствора бисфенолята натрия (3,8% бисфеврла А,
1,4% гидроокиси натрия, О,05% триэтиламина ). Для зешершевия реакции смесь пропускают еще через два воооохлаждаемых аппарата с переливом. Обшее время пре6ы- шнвя составляет примерно 15 мин. Затем реакциоввую смесь собирают в стеклянном сосуде, где она разделяется на | две хшдкве , фазы. Органическую фазу перерабатывают аналогично примеру 1.
Получают 2,2-внс-(4-«нанатофеннл)пропан с т.пл. 82 С н с показателем пр9|1Ьмлення П.р 1,5385.
Выход 99%; степень чистоты 100%. . irp им 4, В вопоохлаждаемсм аппЙ| ате с мешалкой, снабженном боковым пе релнвом, 475 г/ч раствора хлорнстого циана в ;метнленхлпрнае, (5% ХЛОРИСТОГОпя на 0,05% трнэтиламинд эмульг 1фу|сп,с lOS4r/4
водного раствора бнсфенолята натрия (3,8% бисфенола А, 1.,1% No ОН, О,05% триэтнламина ).
Получаемую смесь последовательно пропускают через два атгпарата с переливом для завершения реакции. Обшее время пребывания , составляет примерно 15 мин. Затем смесь подают в стеклянный сосуд, где она разделяется на две жидкие фазы.
Органическую фазу перерабатывают аналогично примеру 1.
Полученный 2,2-6ис-114-Ч1нанатофенил)пропан плавится при .
Выход 99%.
ПocлaJпepeкptIcтaллнзaдиa продукт имеет т.пл. 82 С и П 1,5385 (чнстота 10О%).
Выход 98% q переёчефе на примененный бисфенол А.
О
r.
m «
N
00
Oi





Реферат

Формула


Комментарии