Способ уменьшения молекулярной массы полипропилена - RU2298563C2
Код документа: RU2298563C2
Описание
Настоящее изобретение относится к новым гидроксиламиновым сложным эфирам и к способным полимеризоваться композициям, включающим эти гидроксиламиновые сложные эфиры и этиленово-ненасыщенный мономер или олигомер. Далее изобретение относится к применению гидроксиламиновых сложных эфиров в качестве инициаторов полимеризации и к применению гидроксиламиновых сложных эфиров для регулируемой деструкции полипропилена и для регулируемого увеличения молекулярной массы или сшивания полиэтилена.
Свободно-радикальная полимеризация относится к самым важным методам создания относительно длинной углеродной цепи. Ее применяют в технологии получения имеющих важное промышленное значение полимеров, таких, как полистирол, ПВХ, полиакрилаты, полиметакрилаты, ПАН (полиакрилонатрил) и другие полимеры. За техническими подробностями можно обратиться к до сих пор актуальной по данной теме общепризнанной работе G.Odian, Principles of Polymerization, McGraw-Hill New York 1970, а также к работам Н.-G.Elias, Makromolekule, издание 6-е, том I, Wiley-VCH, DE-Weinheim 1999, ISBN 3-527-29872-Х; K.Hatada, T.Kitayama, O.Vogl, Macromolecular Design of Polymeric Materials, Marcel Dekker New York 1997, ISBN 0-8247-9465-6; M.K.Mishra, Y.Yagci, Handbook of Radical Vinyl Polymerization, Marcel Dekker New York 1998, ISBN 0-8247-9464-8.
Процессы свободно-радикальной полимеризации начинают с использованием инициаторов. Инициаторами, которые стали общепринятыми в промышленной технологии, являются азосоединения, диалкилпероксиды, диацилпероксиды, гидропероксиды, термически нестойкие С-С-димеры, окислительно-восстановительные системы и фотоинициаторы.
Несмотря на их широкое применение, эти инициаторы обладают различными недостатками. Так, например, пероксиды отличаются исключительной легковоспламеняемостью и поддерживают горение. Вещества других классов являются потенциально взрывоопасными, вследствие чего их использование, хранение и транспортировка связаны с соблюдением дорогостоящих мер предосторожности.
Таким образом, существует естественная потребность в создании эффективных инициаторов, приемлемых для использования в промышленной технологии, которым свойственен удовлетворительный профиль безопасности в процессах свободно-радикальной полимеризации. В ЕР-А 735052 описан способ получения термопластичных полимеров, обладающих низкой полидисперсностью, который включает процессы свободно-радикальной полимеризации, проводимые добавлением в мономеры обычных инициаторов свободно-радикальной полимеризации в сочетании со стабильными свободными радикалами в качестве регуляторов полимеризации. В WO 98/30601 описаны нитроксильные радикалы (соединения >N-O•) на основе имидазолидинонов, дериватизированные из алкоксиаминов, и их применение в качестве инициаторов полимеризации. Аналогичным образом в WO 98/44008 описаны нитроксилы на основе морфолинонов, пиперазинонов и пмперазиндионов. В WO 00/07981 описаны ациклические алкоксиамины и их применение в качестве инициаторов полимеризации. В опубликованной заявке на патент Германии 19949352.9 описаны другие 5- и 6-членные гетероциклические алкоксиамины, которые замещены в одном или обоих α-положениях и благодаря размерам этих заместителей проявляют пространственную затрудненность.
Несмотря на такие предлагаемые возможности, которые в данной области техники являются типичными выбираемыми вариантами, для улучшения процессов свободно-радикальной полимеризации все еще сохраняется потребность в создании новых инициаторов полимеризации, которые можно безопасно применять и которые позволяют регулировать реакцию.
Было установлено, что особенно приемлемыми инициаторами полимеризации являются ациклические и циклические гидроксиламины разного строения, если их этерифицируют ацильными радикалами.
По изобретению предлагаются соединения
а) формулы:

где Ra обозначает ацильный радикал, выбранный из группы, включающей -С(=O)-Н, -С(=O)-С1-С19алкил, -С(=O)-С2-С19алкенил, -С(=O)-С2-С4алкенил-С6-С10арил, -С(=O)-С6-С10 арил, -С(=O)-O-С1-С6алкил, -С(=O)-O-С6-С10арил, -С(=O)-NH-С1-С6алкил, -С(=O)-NH-С6-С10арил и -С(=O)-N(С1-С6алкил)2;
R1-R4 каждый обозначает C1-С6алкил;
R5 и R6 каждый независимо друг от друга обозначает водородный атом, С1-С6алкил или С6-С10арил; или R5 и R6 совместно обозначают атом кислорода;
Q обозначает прямую связь или двухвалентный радикал -(CR7R8)- или -(CR7R8-CR9R10)-, где
R7, R8, R9 и R10 каждый независимо друг от друга обозначает водородный атом или C1-С6алкил; а
Z1 обозначает атом кислорода или двухвалентный радикал -NR11-, где R11 обозначает водородный атом, C1-С6алкил, С6-С10арил или ацильный радикал Ra, имеющий одно из вышеуказанных значений; или
б) формулы Ia, где
Ra обозначает ацильный радикал, выбранный из группы, включающей -Р(=O)-С1-С19алкил, -Р(=O)2-С1-С19алкил, -Р(=O)-С6-С10арил, -Р=O(-С1-С19алкил)2, -Р=O(-С6-С10арил)2 , -Р(=O)-O-С1-С6алкил, -Р(=O)-O-С6-С10арил, -Р=O(-O-С1-С6алкил)2, -Р=O(-O-С6-С10арил)2, -Р(-O-С1-С6алкил)2 и -Р(-O-С6-С10арил)2;
R1-R4 каждый обозначает C1-С6алкил;
R5 и R6 каждый независимо друг от друга обозначает водородный атом, C1-С6алкил или С6-С10арил; или
R5 и R6 совместно обозначают атом кислорода;
Q обозначает прямую связь или двухвалентный радикал -(CR7R8)- или -(CR7R8 -CR9R10)-, где
R7, R8, R9 и R10 каждый независимо друг от друга обозначает водородный атом или C1-С6алкил; а
Z1 обозначает атом кислорода или двухвалентный радикал -NR11- или -(CR12R13)-, где
R11 обозначает водородный атом, C1-С6алкил или С6-С10арил или независимо друг от друга
один из радикалов R12 и R13 представляет собой водородный атом или С1-С6алкил, а другой представляет собой C1-С6алкил, C1-С6алкокси, С6-С10арилокси, ацилоксирадикал, выбранный из группы, включающей -O-С(=O)-Н, -O-С(=O)-С1-С19алкил, -O-C(=O)-C1-C54алкенил, -O-С(=O)-С6-С10арил, -O-С(=O)-С1-С36алкенил-С6-С10арил, -O-С(=O)-O-С1-С19алкил, -O-С(=O)-O-С6-С10арил, -O-С(=O)-NH-С1 -С6алкил, -O-С(=O)-NH-С6-С10арил и -O-С(=O)-N(С1-С6алкил)2, C1-С6алкиламино-, ди-С1-С6 алкиламино-, С6-С10ариламино-, ациламиногруппу, выбранную из ряда, включающего -NH-С(=O)-Н, -NH-C(=O)-C1-C19аалкил, -NH-С(=O)-С1-С54 алкенил, -NH-С(=O)-С6- С10арил, -NH-С(=O)-С1-С36алкенил-С6-С10арил, -NH-С(=O)-O-С1-С19алкил, -NH-C(=O)-O-C6-C10арил, -NH-C(=O)-NH-C1-C6алкил, -NH-C(=O)-NH-C6-С10арил и -NH-С(=O)-N(С1-С6алкил)2, диациламиногруппу, выбранную из ряда, включающего -N[-С(=O)-С1-С19алкил]2 и -N[-С(=O)-С6-С10арил]2, или N-ацил-N-С1-С6 алкиламиногруппу; или
оба радикала R12 и R13 совместно обозначают оксогруппу; или
в) формулы:

Ra обозначает ацильный радикал, выбранный из группы, включающей -С(=O)-Н, -С(=O)-С1-С19 алкил, -С(=O)-С2-С19алкенил, -С(=O)-С2-С4алкенил-С6-С10арил, -С(=O)-С6-С10арил, -С(=O)-O-С1-С6алкил, -С(=O)-O-С6-С10арил, -С(=O)-NH-С1-С6алкил, -С(=O)-NH-С6-С10арил и -С(=O)-N(С1-С6алкил)2;
R1-R4 каждый обозначает C1-С6алкил;
А обозначает заместитель в фенильных кольцах; а
m обозначает ноль или целое число от одного до четырех; или
г) формулы:

Ra обозначает ацильный радикал, выбранный из группы, включающей -С(=O)-Н, -С(=O)-С1-С19алкил, -С(=O)-С2-С19алкенил, -С(=O)-С2-С4 алкенил-С6-С10арил, -С(=O)-С6-С10арил, -С(=O)-O-С1-С6алкил, -С(=O)-O-С6-С10арил, -С(=O)-NH-С1-С6алкил,-С(=O)-NH-С6-С10арил,-С(=O)-N(С1-С6алкил)2, -Р(=O)-С1-С19алкил, -Р(O)2-С1-С19 алкил, -Р(=O)-С6-С10арил, -P=O(-C1- С19алкил)2, -Р=O(-С6-С10арил)2, -Р(=O)-O-С1-С6алкил, -Р(=O)-O-С6-С10арил, -Р=O(-O-С1-С6алкил)2, -Р=O(-O-С6-С10арил)2, -Р(-O-С1-С6алкил)2 и -Р(-O-С6-С10арил)2;
Rb имеет такие же значения, как указанные для Ra, или обозначает карбамоил, С1-С6алкилкарбамоил или ди-С1-С6алкилкарбамоил;
Rc и Rd каждый независимо друг от друга обозначает водородный атом, С1-С6алкил или С6-С10арил; а
R1-R3 каждый независимо друг от друга обозначает С1-С6алкил или С6-С10арил.
Эти соединения приемлемы в качестве инициаторов полимеризации, в особенности для использования в процессах полимеризации, поскольку их применение позволяет получать особенно чистые полимеры и сополимеры.
Понятие "полимер" охватывает олигомеры, соолигомеры, полимеры и сополимеры, например статистические блок-, полиблок-, звездообразные и градиентные сополимеры.
Еще одним ценным свойством новых соединений в промышленной технологии является их приемлемость для применения в качестве добавок в процессах уменьшения молекулярной массы полимеров, в частности полипропиленов, и в процессах достижения регулируемого увеличения молекулярной массы или сшивания полиэтилена.
Использованные в описании изобретения понятия и выражения имеют следующие предпочтительные значения.
В варианте а) С1-С19алкил в гидроксиламиновых сложных эфирах (Ia) представляет собой, например, С1 -С6алкил, в частности метил, этил, н-пропил или изопропил, или н-, втор или трет-бутил, или прямоцепочечный или разветвленный пентил, или гексил, или С7-С19алкил, например прямоцепочечный или разветвленный гептил, октил, изооктил, нонил, трет-нонил, децил или ундецил, или прямоцепочечный С11-С19алкил, который совместно с радикалом -(С=O)- образует С14-С20алканоил, содержащий четное число атомов С, например лауроил (12С), миристоил (14С), пальмитоил (16С) или стеароил (18С).
С6 -С10арил представляет собой, например, карбоциклический моноарил или диарил, предпочтительно моноарил, например фенил, который может быть монозамещенным или дизамещенным приемлемыми заместителями, например С1-С4алкилом, в частности метилом, этилом или трет-бутилом, С1-С4алкокси, например метокси или этокси, или атомом галогена, например атомом хлора. В случае дизамещения предпочтительны 2- и 6-положения.
Ацильный радикал Ra, выбранный из группы, включающей -С(=O)-Н, -С(=O)-С1-С19алкил, -С(=O)-С2-С19алкенил, -С(=O)-С2-С4алкенил-С6-С10арил, -С(=O)-С6-С10арил, -С(=O)-O-С1-С6 алкил, -С(=O)-O-С6-С10арил, -C(=O)-NH-С1-С6алкил, -С(=O)-NH-С6-С10арил и -С(=O)-N(С1-С6алкил)2, может быть замещенным по свободным валентностям приемлемыми заместителями, например атомом фтора или хлора, а предпочтительно представляет собой формил, ацетил, трифторацетил, пивалоил, акрилоил, метакрилоил, олеоил, циннамоил, бензоил, 2,6-ксилоил, трет-бутоксикарбонил, этилкарбамоил или фенилкарбамоил.
С1-С6алкил в качестве значения R1-R4 в предпочтительном варианте представляет собой С1-С4алкил, в частности С1-С2алкил, например метил или этил.
В предпочтительных вариантах каждый из R1-R4 обозначает метил или этил. По другому варианту от одного до трех заместителей R1-R4 являются этилами. При этом остальными заместителями являются метилы.
R5 и R6 каждый в предпочтительном варианте обозначает водородный атом. В предпочтительном варианте каждый из С1-С6алкила и С6-С10арила в качестве значения R5 и R6 представляет собой метил или фенил.
R5 и R6 каждый в предпочтительном варианте обозначает атом кислорода, когда Z обозначает двухвалентный радикал -NR11- (R11 обозначает Н или С1-С4алкил). Q при этом обозначает прямую связь (пятичленное кольцо) или двухвалентный радикал -(CR7R8)- (шестичленное кольцо).
R7, R8, R9 и R10 в двухвалентных радикалах -(CR7R8)- или -(CR7R8-CR9R10)- каждый в предпочтительном варианте обозначает водородный атом, но может также представлять собой С1-С4алкил, как указанный выше, например метил.
R11 в двухвалентном радикале -NR11- обозначает водородный атом, С1-С6алкил, как указанный выше, в частности метил или трет-бутил, арил, например фенил, или ацильный радикал Ra, как указанный выше, в частности формил, ацетил, трифторацетил, пивалоил, бензоил, 2,6-ксилоил, трет-бутоксикарбонил, этилкарбамоил или фенилкарбамоил.
В варианте б) значения ацильного радикала Ra в гидроксиламиновом сложном эфире (Ia) выбирают из группы, включающей -Р(=O)-С1-С19алкил, -Р(=O)2-С1-С19алкил, -Р(=O)-С6-С10арил, -Р=O(-С1-С19алкил)2, -Р=O(-С6-С10арил)2, -Р(=O)-O-С1-С6алкил, -Р(=O)-O-С6-С10арил, -Р=O(-O-С1-С6алкил)2, -Р=O(-O-С6-С10арил)2, -Р(-O-С1-С6алкил)2 и -Р(-O-С6-С10арил)2 . С1-С19алкил и С6-С10арил имеют такие же значения, как указанные выше в разделе а), например метил или фенил.
R1-R4 имеют такие же значения, как указанные выше в разделе а).
Аналогичным образом R5, R6, Q, R7, R8, R9 и R10 имеют такие же значения, как указанные выше в разделе а).
Z1 как в варианте б), так и в варианте а) может быть атомом кислорода или двухвалентным радикалом -NR11-. По-другому в варианте б) Z1 может также представлять собой двухвалентный радикал -(CR12R13)- где один из радикалов R12 и R13 представляет собой водородный атом или С1-С6алкил, а другой представляет собой С1-С6алкил, С1-С6алкокси, например метокси, этокси или н-пропокси, С6 -С10арилокси, ацилоксирадикал, выбранный из группы, включающей -O-С(=O)-Н, -O-С(=O)-С1-С19алкил, -O-С(=O)-С1-С54алкенил, -O-С(=O)-С1 -С10арил, -O-С(=O)-С1-С36алкенил-С6-С10арил, -O-С(=O)-O-С1-С6алкил, -О-С(=О)-О-С6-С10арил, -O-С(=O)-NH-С1-С6алкил, -O-С(=O)-NH-С6-С10арил и -O-С(=O)-N(С1-С6алкил)2, С1-С6алкиламино-, ди-С1-С6алкиламино-, С6-С10ариламино-, ациламинорадикал, выбранный из группы, включающей -NH-С(=O)-Н, -NH-С(=O)-С1-С19алкил, -NH-С(=O)-С1-С54алкенил, -NH-С(=O)-С6-С10арил, -NH-С(=O)-С1-С36алкенил-С6-С10арил, -NH-C(=O)-O-С1-С19алкил, -NH-С(=O)-O-С6-С10арил, -NH-С(=O)-NH-С1-С6алкил, -NH-С(=O)-NH-С6-С10арил и - NH-С(=O)-N(С1-С6алкил)2, диациламинорадикал, выбранный из группы, включающей -N[-C(=O)-С1-С19алкил]2 и -N[-C(=O)-С6-С10арил]2, или N-ацил-N-С1 -С6алкиламинорадикал.
Примерами ацилокси являются формилокси, ацетокси, трифторацетокси, пивалоилокси, бензоилокси, 2,6-ксилоилокси, трет-бутоксикарбонилокси, этилкарбамоилокси или фенилкарбамоилокси.
Примерами -O-С(=O)-С1-С54алкенила или -O-С(=O)-С1-С36алкенил-С6-С10арила являются кислотные группы, дериватизированные из ненасыщенных димерных или тримерных кислот, содержащих большое число атомов С, например формул:
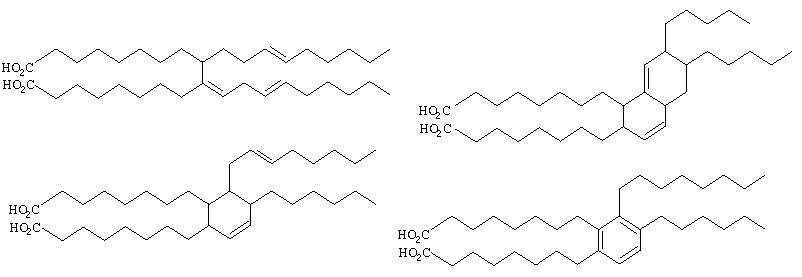
Примерами ациламинорадикала служат ацетиламино-, пивалоиламино- и трет-бутоксикарбониламинорадикалы.
Примерами диациламинорадикала служат N-ацетил-N-пивалоиламино- и диацетиламинорадикалы.
В варианте в) ацильный радикал Ra в гидроксиламиновом сложном эфире (Ib) выбирают из группы, включающей -С(=O)-Н, -С(=O)-С1-С19алкил, -С(=O)-С2-С19алкенил, -С(=O)-С2-С4алкенил-С6-С10арил, -С(=O)-С6-С10арил, -С(=O)-O-С1-С6алкил, -С(=O)-O-С6-С10арил, -С(=O)-NH-С1-С6алкил, -С(=O)-NH-С6-С10арил и -С(=O)-N(С1-С6алкил)2. Эти значения соответствуют определению ацильного радикала Ra в варианте а). Ацильный радикал Ra может быть замещенным по его свободным валентностям подходящими заместителями, например атомом фтора или хлора, а в предпочтительном варианте он представляет собой формил, ацетил, трифторацетил, пивалоил, бензоил, 2, 6-диметилбензоил, трет-бутоксикарбонил, этилкарбамоил или фенилкарбамоил.
С1-С6алкил в качестве R1-R4 имеет такие же значения, как в варианте а), предпочтительно С1-С4алкил, в частности метил или этил.
Предпочтительное фенильное кольцо не замещено (m обозначает 0). Когда фенильное кольцо замещено, подходящими заместителями А у фенильного кольца являются, в частности, функциональные группы, выбранные из ряда, включающего амино-, С1-С4алкиламино-, например метиламино- или этиламино-, С1-С4-диалкиламино-, например диметиламино- и диэтиламиногруппу, гидрокси, оксогруппу, тио, -NO2, карбокси и атом галогена, или представляют собой заместители, выбранные из ряда, включающего С1-С20алкил, как указанный выше, и С2-С20алкенил, например винил или аллил.
Вариант г) охватывает ациклические гидроксиламиновые сложные эфиры (Ic), где Ra обозначает ацильный радикал, выбранный из группы, включающей -С(=O)-Н, -С(=O)-С1-С19алкил, -С(=O)-С2-С19алкенил, -С(=O)-С2-С4алкенил-С6-С10арил, -С(=O)-С6-С10арил, -С(=O)-O-С1-С6 алкил, -С(=O)-O-С6-С10арил, -С(=O)-NH-С1-С6алкил, -С(=O)-NH-С6-С10арил и -С(=O)-N(С1-С6алкил)2. Эти значения соответствуют определениям ацильного радикала Ra в варианте а). В предпочтительном варианте Ra обозначает ацильный радикал, выбранный из группы, включающей -Р(=O)-С1-С19алкил, -Р(=O)2-С1-С19алкил, -Р(=O)-С6-С10арил, -Р=O(-С1-С19алкил)2, -Р=O(-С6 -С10арил)2, -Р(=O)-O-С1-С6алкил, -Р(=O)-O-С6-С10арил, -Р=O(-O-С1-С6алкил)2, -Р=O(-O-С6 -С10арил)2, -Р(-O-С1-С6алкил)2и -Р(-O-С6-С10арил)2. Эти значения соответствуют определениям ацильного радикала Ra с фосфорсодержащими ацильными группами в варианте б).
Rc и Rd, а также С1-С6алкильные или С6-С10арильные группы R1-R3представляют собой, например, метил, этил, н-пропил или изопропил, н-бутил, изобутил, трет-бутил, фенил или нафтил.
По предпочтительному варианту выполнения изобретения предлагаются соединения
а) формулы Ia, где
Ra обозначает ацильный радикал, выбранный из группы, включающей -С(=O)-С1-С19алкил, -С(=O)-С2-С19алкенил, -С(=O)-С2-С4алкенил-С6-С10арил, -С(=O)-С6-С10арил, -С(=O)-O-С1 -С6алкил, -С(=O)-NH-С1-С6алкил, -С(=O)- NH-С6-С10арил и -С(=O)-N(С1-С6алкил)2;
R1 -R4 каждый обозначает С1-С2алкил;
R5 и R6 каждый независимо друг от друга обозначает водородный атом или С1-С6алкил или R5 и R6 совместно обозначают атом кислорода;
Q обозначает одинарную связь или двухвалентный радикал -(CR7R8)- или -(CR7R8-CR9R10)-, где
R7, R8, R9 и R10 каждый обозначает водородный атом; а Z1 обозначает атом кислорода или двухвалентный радикал -NR11-, где R11 обозначает водородный атом, С1-С6алкил или С6-С10арил; или
б) формулы Ia, где
Ra обозначает ацильный радикал, выбранный из группы, включающей -Р(=O)-С1-С19алкил, -Р(=O)2-С1-С19алкил, -Р(=O)-С6-С10арил, -Р=O(-С1-С19алкил)2и -Р=O(-С6-С10арил)2;
R1-R4 каждый обозначает С1-С2алкил;
R5 и R6 каждый независимо друг от друга обозначает водородный атом, С1-С6алкил или R5 и R6 совместно обозначают атом кислорода;
Q обозначает одинарную связь или двухвалентный радикал -(CR7R8)- или -(CR7R8-CR9R10)-, где
R7, R8, R9 и R10 каждый обозначает водородный атом; а
Z1 обозначает атом кислорода или двухвалентный радикал -NR11- или -(CR12R13)-, где
R11 обозначает водородный атом, С1-С6алкил или С6-С10арил или независимо друг от друга
один из радикалов R12 и R13 представляет собой водородный атом, а другой представляет собой ацилоксирадикал, выбранный из группы, включающей -O-С(=O)-С1-С19алкил, -O-С(=O)-С6-С10арил, -O-С(=O)-O-С1-С6алкил, -O-С(=O)-O-С6-С10арил, -O-С(=O)-NH-С1-С6алкил, -O-С(=O)-NH-С6-С10арил и -O-С(=O)- N(С1-С6алкил)2; или в)
в) формулы Ib, где
Ra обозначает ацильный радикал, выбранный из группы, включающей -С(=O)-С1-С19алкил, -С(=O)-С6-С10арил, -С(=O)-O-С1-С6алкил, -C(=O)-NH-С1-С6алкил, -С(=O)-NH-С6-С10арил и -С(=O)-N(С1-С6алкил)2;
R1-R4 каждый обозначает С1-С2алкил; а
m обозначает ноль; или
г) формулы Ic, где
Ra обозначает ацильный радикал, выбранный из группы, включающей -С(=O)-С1-С19алкил, -С(=O)-С6-С10арил, -С(=O)-O-С1-С6алкил, -C(=O)-NH-С1-С6алкил, -С(=O)-NH-С6-С10арил и -С(=O)-N(С1-С6алкил)2, -P(=O)-С1-С19алкил, -Р(=O)2-С1-С19алкил, -Р(=O)-С6-С10арил, -Р=O(-С1-С19алкил)2, -Р=O(-С6-С10арил)2, -Р(=O)-O-С1-С6алкил, -Р(=O)-O-С6-С10арил, -Р=O(-O-С1-С6алкил)2, -Р=O(-O-С6-С10арил)2, -Р(-O-С1-С6алкил)2 и -Р(-O-С6-С10арил)2;
Rb имеет такие же значения, как указанные для Ra, или обозначает карбамоил, С1-С6алкилкарбамоил или ди-С1-С6алкилкарбамоил;
Rc и Rd каждый независимо друг от друга обозначает водородный атом, С1-С6алкил или С6-С10арил; a R1-R3 каждый обозначает С1-С2алкил или С6-С10арил.
В особенно предпочтительном варианте выполнения изобретения предлагаются соединения
а) формулы Ia, где
Ra обозначает ацильный радикал, выбранный из группы, включающей -С(=O)-С1-С19алкил, бензоил и -С(=O)-O-С1-С6алкил;
R1-R4 каждый обозначает С1-С2алкил;
R3 и R6 каждый независимо друг от друга обозначает водородный атом или метил или R5 и R6 совместно обозначают атом кислорода;
Q обозначает прямую связь или двухвалентный радикал -(CR7R8)- или -(CR7R8-CR9R10)-, где
R7, R8, R9 и R10 каждый обозначает водородный атом; а
Z1 обозначает атом кислорода или двухвалентный радикал -NR11-, где
R11 обозначает водородный атом, С1-С6алкил или С6-С10арил; или б) формулы Ia, где
Ra обозначает ацильный радикал, выбранный из группы, включающей -Р(=O)2-С1-С19алкил, -Р=O(-С1-С19алкил)2 и -Р=O(-С6-С10арил)2; R1-R4 каждый обозначает С1-С2алкил;
R5 и R6 каждый независимо друг от друга обозначает водородный атом, С1-С6алкил или R5 и R6 совместно обозначают атом кислорода;
Q обозначает прямую связь или двухвалентный радикал -(CR7R8)- или -(CR7R8-CR9R10)-, где
R7, R8, R9 и R10 каждый обозначает водородный атом; а
Z1 обозначает атом кислорода или двухвалентный радикал -NR11- или -(CR12R13)-, где
R11 обозначает водородный атом, С1-С6алкил или С6-С10арил или независимо друг от друга
один из радикалов R12 и R11 представляет собой водородный атом, а другой представляет собой ацилоксирадикал, выбранный из группы, включающей -O-С(=O)-С1-С19алкил, бензоил, -O-С(=O)-O-С1-С6алкил и бензилоксикарбонилокси; или
в) формулы Ib, где
Ra обозначает ацильный радикал, выбранный из группы, включающей -С(=O)-С1-С19алкил, бензоил и -С(=O)-O-С1-С6алкил;
R1-R4 каждый обозначает С1-С2алкил; а
m обозначает ноль; или
г) формулы Ic, где
Ra обозначает ацильный радикал, выбранный из группы, включающей -С(=O)-С1-С19алкил, бензоил, -С(=O)-O-С1-С6алкил, -Р(=O)2-С1 -С19алкил, -Р=O(-С1-С19алкил)2 и -Р=O(-С6-С10арил)2;
Rb имеет такие же значения, как указанные для Ra, или обозначает карбамоил, С1-С6алкилкарбамоил или ди-С1-С6алкилкарбамоил;
Rc и Rd каждый независимо друг от друга обозначает водородный атом, С1-С6алкил или С6-С10арил; а
R1-R3 каждый независимо друг от друга обозначает С1-С2алкил или С6-С10арил.
Представленные выше соединения в соответствии с вариантами от а) до г) являются новыми; их можно получать по методам, которые известны. Эти соединения представлены как вспомогательные вещества для полимеризации или инициаторы полимеризации в способных полимеризоваться композициях, которые включают по меньшей мере по одному этиленово-ненасыщенному способному полимеризоваться мономеру или олигомеру и соединение в соответствии с одним из вышеописанных вариантов от а) до г).
Таким образом, по изобретению далее предлагается композиция, включающая
А) по меньшей мере один этиленово-ненасыщенный способный полимеризоваться мономер или олигомер и
Б) по меньшей мере одно из представленных выше соединений от а) до г).
Приемлемые этиленово-ненасыщенные мономеры или олигомеры можно полимеризовать таким путем, который известен, с применением методов свободно-радикальной полимеризации.
Мономеры, приемлемые для свободно-радикальной полимеризации, представляют собой, например, этиленово-ненасыщенные способные полимеризоваться мономеры, выбранные из группы, включающей алкены, сопряженные диены, стиролы, акролеин, винилацетат, винилпирролидон, винилимидазол, малеиновый ангидрид, акриловую кислоту, производные акриловой кислоты, винилгалогениды и винилиденгалогениды.
Примерами алкенов и сопряженных алкенов служат этилен, изопрен, 1,3-бутадиен и α-С5-С18алкены.
Подходящие стиролы могут быть замещенными в фенильном радикале одним-тремя заместителями, выбранными из группы, включающей гидрокси, С1-С4алкокси, например метокси или этокси, атомы галогена, например атом хлора, аминогруппу и С1-С4алкил, например метил или этил.
Подходящие производные акриловой кислоты выбирают, например, из группы, включающей С1-С4алкилакриловые кислоты, амиды, нитрилы, ангидриды и соли акриловой кислоты и С1-С4алкилакриловых кислот, С1-С24алкилакрилаты и С1-С24алкил-С1-С4алкилакрилаты.
Особенно предпочтительными производными акриловой кислоты являются метакриловая кислота и ее соли, акриловый ангидрид и метакриловый ангидрид, С1-С24алкилакрилаты и -метакрилаты, моно- и ди-С1-С4алкиламино-С2-С4алкилакрилаты и -метакрилаты, гидрокси-С2-С4алкилакрилаты и -метакрилаты, (С1-С4алкил)3силилокси-С2-С4 алкилакрилаты и -метакрилаты, (С1-С4алкил)3силил-С2-С4алкилакрилаты и -метакрилаты, гетероциклил-С2-С4алкилакрилаты и метакрилаты, акриловые и метакриловые эфиры, содержащие группы поли-С2-С4алкиленгликолевых эфиров, которые в свою очередь могут быть этерифицированы замещенными С1 -С24алкоксигруппами, акриламиды и метакриламиды, моно- и ди-С1-С4алкиламиды акриловой и метакриловой кислот, амино-С2-С4алкиламиды акриловой и метакриловой кислот и акрилонитрил.
Приемлемыми солями акриловой кислоты или метакриловой кислоты являются, например, (С1-С4алкил)4аммониевые или (С1-С4алкил)3NH-соли, например тетраметиламмониевая, тетраэтиламмониевая, триметиламмониевая или триэтиламмониевая соль, триметил-2-гидроксиэтиламмониевая или триэтил-2-гидроксиэтиламмониевая соль, диметил-2-гидроксиэтиламмониевая или диэтил-2-гидроксиэтиламмониевая соль.
Приемлемыми С1-С24алкилакрилатами и метакрилатами являются эти последние, этерифицированные, например, метилом, этилом, н-бутилом, изобутилом, трет-бутилом, 2-этилгексилом, изоборнилом, изодецилом, лаурилом, миристилом, стеарилом или бегенилом.
Примерами моно- и ди-С1-С4алкиламино-С2-С4алкилакрилатов и -метакрилатов служат 2-монометиламиноэтилакрилат и -метакрилат, 2-диметиламиноэтилакрилат и -метакрилат и соответствующие 2-моноэтиламиноэтиловый и 2-диэтиламиноэтиловый эфиры, а также 2-трет-бутиламиноэтилакрилат и -метакрилат.
Примерами гидрокси-С2-С4алкилакрилатов и -метакрилатов служат 2-гидроксиэтилакрилат и -метакрилат (ГЭА, ГЭМА), а также 2-гидроксипропилакрилат и -метакрилат (ГПА, ГПМА).
Примерами силилокси-С2-С4алкилакрилатов и -метакрилатов служат 2-триметилсилилоксиэтилакрилат и -метакрилат (ТМС-ГЭА, ТМС-ГЭМА). Примерами (С1-С4алкил)3силил-С2-С4алкилакрилатов и -метакрилатов являются 2-триметилсилилэтилакрилат и -метакрилат, а также 3-триметилсилил-н-пропилакрилат и -метакрилат.
Акриловые и -метакриловые эфиры, содержащие группы поли-С2-С4алкиленгликолевых эфиров, которые могут быть в свою очередь этерифицированными замещенными С1-С24алкоксигруппами, отвечают формуле:

где R1 и R2 каждый независимо друг от друга обозначает водородный атом или метил, а R3 обозначает С1-С24алкил, например метил, этил, н-пропил или изопропил, н-бутил, изобутил или трет-бутил, н-пентил или неопентил, лаурил, миристил или стеарил, или арил-С1-С24алкил, например бензил или фенил-н-нонил, или, кроме того, С1-С24алкиларил или С1-С24алкиларил-С1-С24алкил.
Примерами гетероциклил-С2-С4алкилакрилатов и -метакрилатов являются 2-(N-морфолинил, -2-пиридил, -1-имидазолил, -2-оксо-1-пирролидинил, -4-метилпиперидин-1-ил или -2-оксоимидазолидин-1-ил)этилакрилат и -метакрилат.
Примерами вышеупомянутых моно- и ди-С1 -С4алкиламидов акриловой кислоты и метакриловой кислоты, ди-С1-С4алкиламино-С2-С4алкиламидов акриловой кислоты и метакриловой кислоты и амино-С2-С4алкиламидов акриловой кислоты и метакриловой кислоты являются N,N-диметилакриламид, N,N-диметил(мет)акриламид, 2-(N,N-диметиламиноэтил)акриламид, 2-(N, N-диметиламиноэтил)метакриламид, 2-аминоэтилакриламид и 2-аминоэтилметакриламид.
Вышеупомянутые производные акриловой кислоты содержатся в способной полимеризоваться композиции в качестве мономеров или в смеси с акриловой кислотой.
В такой композиции компонент Б) содержится относительно компонента А) в количестве от 0,01 до 30 мольных%, предпочтительно от 0,05 до 10 мольных %, особенно предпочтительно от 0,1 до 1,0 мольных %.
Предпочтительная композиция в соответствии с изобретением представляет собой композицию, включающую
А) по меньшей мере один этиленово-ненасыщенный способный полимеризоваться мономер или олигомер, выбранный из группы, включающей мономерные и олигомерные алкены, стиролы, сопряженные диены, акролеин, винилацетат, винилпирролидон, винилимидазол, малеиновый ангидрид, акриловую кислоту, С1-С4алкилакриловые кислоты, амиды, нитрилы, ангидриды и соли акриловой кислоты и С1-С4алкилакриловых кислот, С1-С24алкилакрилаты, С1-С24алкил-С1-С4алкилакрилаты, винилгалогениды и винилиденгалогениды; и
Б) по меньшей мере одно из вышеупомянутых соединений от а) до г).
Вышеописанные композиции могут дополнительно включать обычные добавки, которые по другому варианту можно также вводить после полимеризации. Такие добавки можно вводить в небольших количествах, например поглотители УФ-лучей или светостабилизаторы, например соединения, выбранные из группы, включающей гидроксифенилбензотриазолы, гидроксифенилбензофеноны, оксальамиды и гидроксифенил-симм. триазины. Особенно подходящими светостабилизаторами являются те, которые выбирают из группы, включающей пространственно затрудненные амины (ЗАСС, затрудненные аминовые светостабилизаторы), например типа 2-(2-гидроксифенил)-1,3,5-триазина и 2-гидроксифенил-2Н-бензотриазола. Примерами светостабилизаторов 2-(2-гидроксифенил)-1,3,5-триазинового типа служат соединения, известные из патентной литературы, в частности из US 4619956, ЕР-А 434608, US 5198498, US 5322868, US 5369140, US 5298067, WO 94/18278, ЕР-А 704437, GB-A 2297091 или WO 96/28431.
Композиции могут дополнительно включать другие обычные добавки, например наполнители, такие, как карбонат кальция, силикаты, стекло и материалы из стекловолокна, тальк, каолин, слюда, сульфат бария, оксиды и гидроксиды металлов, углеродная сажа, графит, измельченная древесина и измельченные или волокнистые материалы из других природных продуктов, синтетические волокна, пластификаторы, смазки, эмульгаторы, пигменты, флуидизаторы, катализаторы, оптические отбеливатели, антипирены, антистатики и газообразователи.
Вышеупомянутые полимеры могут содержаться в композиции в концентрациях от примерно 0,01 до 99,0 мас.%, предпочтительно от 0,1 до 95 мас.%, в частности от 1,0 до 90,0 мас.%, преимущественно от 5,0 до 80,0 мас.%, в пересчете на содержание мономера в композиции.
Кроме того, по изобретению дополнительно предлагается способ получения вышеописанного олигомера, соолигомера, полимера или сополимера свободно-радикальной полимеризацией с использованием либо вышеописанных новых соединений в соответствии с вариантами от а) до г), либо известных гидроксиламинов, у которых гидроксильную группу этерифицируют указанными ацильными радикалами Ra.
По предпочтительному варианту предлагается способ получения олигомера, соолигомера, полимера или сополимера свободно-радикальной полимеризацией, характеризующийся тем, что на композицию, включающую
α) по меньшей мере один этиленово-ненасыщенный способный полимеризоваться мономер или олигомер и
β) одно из вышеупомянутых новых соединений от а) до г), воздействуют реакционными условиями свободно-радикальной полимеризации.
Подобным же образом по изобретению предлагается способ получения олигомера, соолигомера, полимера или сополимера свободно-радикальной полимеризацией, характеризующийся тем, что на композицию, включающую
α) этиленово-ненасыщенный способный полимеризоваться мономер или олигомер и
β) по меньшей мере одно соединение формулы 1а, где
Ra обозначает ацильный радикал, выбранный из группы, включающей -С(=O)-Н, -С(=O)-С1-С19алкил, -(C(=О)С2-С19алкенил, -С(=O)-С2-С4 алкенил-С6-С10арил, -С(=O)-С6-С10арил, -С(=O)-O-С1-С6алкил, -С(=O)-O-С6-С10арил, -С(=O)-NH-С1-С6алкил, -С(=O)-NH-С6-С10арил, -С(=O)-N(С1-С6алкил)2, -Р(=O)-С1-С19алкил, -Р(=O)2-С1-С19алкил, -Р(=O)-С6-С10арил, -Р=O(-С1-С19алкил)2, -Р=O(-С1-С10арил)2, -Р(=O)-O-С1-С6 алкил, -Р(=O)-O-С6-С10арил, -P=O(-O-С1-С6алкил)2, -Р=O(-O-С6-С10арил)2, -Р(-O-С1-С6 алкил)2 и -Р(-O-С6-С10арил)2;
R1-R4 каждый обозначает С1-С6алкил;
R5 и R6 каждый независимо друг от друга обозначает водородный атом, С1-С6алкил или С6-С10арил или R5 и R6 совместно обозначают атом кислорода;
Q обозначает прямую связь или двухвалентный радикал -(CR7R8)- или -(CR7R8-CR9R10)-, где
R7, R8, R9 и R10 каждый независимо друг от друга обозначает водородный атом или С1-С6алкил; а
Z1 обозначает атом кислорода или двухвалентный радикал -NR11- или -(CR12R13)-, где
R11 обозначает водородный атом, С1-С6 алкил, С6-С10арил или ацильный радикал Ra, имеющий вышеуказанные значения; или независимо друг от друга R12 и R13 каждый обозначает водородный атом или С1-С6алкил; или один из радикалов R12 и R13 представляет собой водородный атом или С1-С6алкил, а другой представляет собой С1-С6алкил, С1-С6алкокси, арилокси, ацилоксирадикал, выбранный из группы, включающей -O-С(=O)-Н, -O-С(=O)-С1-С19алкил, -O-С(=O)-С1-С54алкенил, -O-С(=O)-С6-С10арил, -O-С(=O)-С1-С36алкенил-С6-С10арил, -O-С(=O)-O-С1-С6алкил, -O-С(=O)-O-С6-С10арил, -O-С(=O)-NH-С1-С6алкил, -O-С(=O)-NH-С6-С10арил и -O-С(=O)-N(С1-С6алкил)2, С1-С6алкиламино-, ди-С1-С6алкиламино-, С6-С10ариламино-, ациламинорадикал, выбранный из группы, включающей -NH-C(=O)-H, -NH-С(=O)-С1-С19алкил, -NH-С(=O)-С1-С54алкенил, -NH-С(=O)-С6-С10арил, -NH-C(=O)-С1-С36алкенил-С6 -С10арил, -NH-С(=O)-O-С1-С19алкил, -NH-С(=O)-O-С6-С10арил, -NH-C(=O)-NH-С1-С6алкил, -NH-C(=O)-NH-С6-С10арил и -NH-С(=O)-N(С1-С6алкил)2, диациламинорадикал, выбранный из группы, включающей -N[-C(=O)-С1-С19алкил]2, -N[-C(=O)-С6-С10арил]2, -N[-С(=O)-С1-С6алкилен-С(=O)-], -N[-С(=O)-С2-С6алкенилен-С(=O)-] и фталимидный радикал, или N-ацил-N-С1 -С6алкиламинорадикал;
или оба радикала R12 и R13 совместно обозначают оксогруппу; или формулы Ib, где
Ra обозначает ацильный радикал, выбранный из группы, включающей -С(=O)-Н, -С(=O)-С1-С19алкил, -С(=O)-С6-С10арил, -С(=O)-O-С1-С6алкил, -С(=O)-O-С6 -С10арил, -С(=O)-NH-С1-С6алкил, -С(=O)-NH-С6-С10арил и -C(=O)-N(С1-С6алкил)2;
R1 -R4 каждый обозначает С1-С6алкил;
А обозначает заместитель в фенильном кольце; а m обозначает целое число от одного до четырех; или формулы Ic, где
Ra обозначает ацильный радикал, выбранный из группы, включающей -С(=O)-Н, -С(=O)-С1-С19алкил, -С(=O)-С2-С19алкенил, -С(=O)-С2-С4алкенил-С6-С10 арил, -С(=O)-С6-С10арил, -С(=O)-O-С1-С6алкил, -С(=O)-O-С6-С10арил, -С(=O)-NH-С1-С6алкил, -С(=O)-NH-С6-С10арил, -С(=O)-N(С1-С6алкил)2, -Р(=O)-С1-С19алкил, -Р(=O)2-С1-С19алкил, -Р(=O)-С6-С10арил, -Р=O(-С1-С19алкил)2, -Р=O(-С6-С10арил)2, -Р(=O)-O-С1-С6алкил, -Р(=O)-O-С6-С10арил, -P=O(-O-С1-С6алкил)2, -Р=O(-O-С6-С10арил)2, -Р(-O-С1-С6алкил)2 и -Р(-O-С6-С10арил)2;
Rb обозначает водородный атом, карбамоил, С1-С6алкилкарбамоил, ди-С1-С6алкилкарбамоил или имеет значения, указанные для Ra;
Rc и Rd каждый независимо друг от друга обозначает водородный атом, С1-С20алкил или С6-С10арил; а
R1-R3 каждый независимо друг от друга обозначает водородный атом, С1-С6алкил или С6-С10арил;
воздействуют реакционными условиями свободно-радикальной полимеризации.
В гидроксиламиновых сложных эфирах (Ia) диациламинорадикал в качестве значения R12 или R13 представляет собой, например, -N[-С(=O)-С1-С6алкилен-С(=O)-], например частной формулы:

или -N[-С(=O)-С2-С6алкенилен-С(=O)-], например частной формулы:
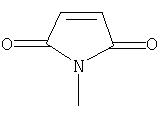
или фталимидную группу:

Свободно-радикальную полимеризацию проводят диссоциацией вышеуказанных инициаторов путем их обработки ультразвуком, нагреванием или воздействием электромагнитного излучения в диапазоне от γ-лучей до микроволн. В предпочтительном варианте инициатор подвергают диссоциациации термическим путем, предпочтительно при температуре от 50°С до 160°С, в частности от 80°С до 150°С. После завершения стадии полимеризации реакционной смеси можно дать остыть до температуры ниже 60°С, предпочтительно до комнатной температуры.
В другом варианте осуществления способа полимеризацию проводят в присутствии источника интенсивного излучения энергии, испускающего лучи в ближней инфракрасной области (БИО) при длинах волн примерно от 800 до 1200 нм. Такие источники излучения технически доступны на фирме AdPhos (см. www.adphos.de). Высокая тепловая энергия таких источников излучения особенно приемлема для приготовления термоотверждаемых лаков (преимущественно порошковые покрытия или клеи) в присутствии вышеуказанных инициаторов полимеризации. Дополнительными компонентами в этих лаках являются те, которые обычно используют при получении прозрачных или пигментированных покрытий.
Процесс полимеризации можно проводить в присутствии воды или органического растворителя, или их смесей. В реакционную смесь можно добавлять дополнительные сорастворители или поверхностно-активные вещества, например гликоли или аммониевые соли карбоновых кислот. Вышеупомянутые мономеры или олигомеры могут содержаться в реакционной смеси в концентрации от 1,0 до 99,9 мас.%, предпочтительно от 5,0 до 99,9 мас.%, особенно предпочтительно от 50,0 до 99,9 мас.%, в пересчете на содержание мономерных звеньев в получаемом полимере. Подходящими органическими растворителями являются алканы (гексан, гептан, октан, изооктан), углеводороды (бензол, толуол, ксилол), галоидированные углеводороды (хлорбензол), алканолы (метанол, этанол, этиленгликоль, этиленгликольмонометиловый эфир), сложные эфиры (этилацетат), простые эфиры (диэтиловый эфир, дибутиловый эфир, этиленгликольдиметиловый эфир, тетрагидрофуран) и их смеси.
Когда в качестве растворителя используют воду, в реакционную смесь можно добавлять смешивающийся с водой или гидрофильный растворитель. Необходимо принять меры предосторожности для гарантии того, чтобы во время реакции полимеризации реакционная смесь оставалась в виде единой гомогенной фазы, и не происходило образования осадка или разделения фаз. Подходящие сорастворители могут быть выбраны из группы, включающей алифатические спирты, гликоли, простые эфиры, гликолевые простые эфиры, пирролидины, N-алкилпирролидиноны, полиэтиленгликоли, полипропиленгликоли, амиды, карбоновые кислоты и их соли, сложные эфиры, органические сульфиды, сульфоксиды, сульфоны, производные спиртов, производные неполных эфиров многоатомных спиртов, например бутилкарбитол или целлозольв, аминоспирты, кетоны, их производные и смеси, например метанол, этанол, пропанол, диоксан, этиленгликоль, пропиленгликоль, диэтиленгликоль, глицерин, дипропиленгликоль, тетрагидрофуран или другие водорастворимые или смешивающиеся с водой растворители или их смеси.
Гидрофильные мономеры, полимеры и сополимеры могут быть выделены из реакционной смеси с использованием обычных методов, например перегонкой, осаждением, экстракцией, изменением значения pH или по другим обычным методам разделения.
Полимеры, которые могут быть получены согласно способу по изобретению, могут обладать среднечисленной молекулярной массой от 1000 до 400000 г/моль, предпочтительно от 2000 до 250000 г/моль и особенно предпочтительно от 2000 до 200000 г/моль. Среднечисленную молекулярную массу можно определить гельпроникающей хроматографией (ГПХ), масс-спектрометрией с лазерной десорбцией/ионизацией с использованием вспомогательной матрицы (MALDI-MC) или, когда инициатор несет группу, которой он отличается от мономеров, ЯМР-спектроскопией или по другим обычным методам.
Таким образом, по изобретению предлагается также получение новых олигомеров, соолигомеров, полимеров или сополимеров, например статистических блок-, полиблок-, звездообразных и градиентных сополимеров.
Полимеры, которые могут быть получены согласно способу по изобретению, и композиции по настоящему изобретению могут быть использованы для самых разнообразных целей в технологии переработки, например в качестве клеев, вспомогательных веществ в составе моющих средств для стирки белья, синтетических моющих средств, диспергаторов, эмульгаторов, поверхностно-активных веществ, пеногасителей, усилителей адгезии, ингибиторов коррозии, средств для улучшения вязкости, смазок, добавок, улучшающих текучесть, загустителей, сшивающих агентов, в качестве добавок для обработки воды, материалов для электронных приборов, в красках и лаках, покрытиях, типографских красках, фотографических проявителях, суперабсорбентах, косметических средствах, консервантах или в качестве биоцидов или модификаторов и вспомогательных добавок для асфальта, текстильных материалов, керамики и дерева.
По изобретению предлагается, кроме того, приемлемый для универсального применения уникальный способ снижения молекулярной массы полипропилена, пропиленовых сополимеров или смесей на основе полипропилена с использованием либо вышеописанных новых соединений, либо известных гидроксиламиновых сложных эфиров, у которых гидроксильную группу этерифицируют указанными ацильными радикалами Ra.
Регулируемое приготовление полиолефиновых материалов (полимеров таких типов, которые обладают разными молекулярными массами, вязкостями расплава, плотностями, значениями молекулярно-массового распределения и т.д.) по обычным методам компаундирования, например экструзией или литьем под давлением, является методом, который применяют производители полимеров и переработчики каучуков/составители смесей.
Достижение целевых параметров, например вязкости расплава, осуществлением этой стадии переработки полимера решительно зависит от регулируемой реакционной способности и типа воздействия используемых добавок.
Применение инициаторов свободных радикалов для модификации вязкости расплава (реологических свойств) полиолефинов является общеизвестным методом. То, приводит ли его осуществление к уменьшению молекулярной массы (к деструкции) или увеличению молекулярной массы (к сшиванию), зависит прежде всего от химического строения полиолефина.
Обычно результатом взаимодействия полимера полипропиленового типа с инициатором свободных радикалов во время процесса переработки полимера является деструкция полимера, тогда как полимеры полиэтиленового типа проявляют тенденцию к сшиванию. Примерами, которые при этом можно упомянуть, служат продукты полиэтиленовых типов, которые могут быть получены посредством катализаторов фирмы "Филлипс" (ПЭНП, полиэтилен низкой плотности) или металлоценовых катализаторов (ЛПЭНП, линейный полиэтилен низкой плотности). Исключениями являются продукты полиэтиленовых типов, получаемые по технологии Циглера, которые проявляют аналогичную тенденцию к деструкции цепи, когда их перерабатывают в присутствии источников свободных радикалов.
В случае сополимеров и тройных сополимеров или сополимерных смесей высокое содержание пропиленовых звеньев обуславливает поведение, аналогичное поведению полипропилена, тогда как следствием высокого содержания этиленовых звеньев является поведение, аналогичное поведению полиэтилена. Если вышеупомянутые сополимеры и тройные сополимеры или сополимерные смеси включают некоторые количества звеньев полиненасыщенных олефинов, то со снижением концентрации свободных двойных связей возможность сшивания уменьшается.
Регулируемая деструкция полипропилена (ПП) с получением продукта, обладающего уменьшенной молекулярной массой и более узким молекулярно-массовым распределением, является методом, имеющим важное промышленное значение для получения полипропилена с "регулируемыми реологическими свойствами" (ПП-РР). Хотя ПП конкретных сортов ("реакторных сортов") могут быть получены оптимизацией процесса синтеза или каталитических систем (металлоценовый катализатор, катализатор Циглера), ПП стандартных сортов часто модифицируют технологией переработки путем осуществления стадии переработки после синтеза.
Известные процессы деструкции протекают либо термически, в частности при температурах, превышающих 280°С, либо в присутствии источников свободных радикалов. В технологии переработки инициируемый свободными радикалами процесс проводят в экструдерах или машинах для литья под давлением при температурах выше 180°С. Используемые источники свободных радикалов представляют собой органические пероксиды, которые добавляют на стадии переработки в разбавленном виде (продукт РР Mastermix, разбавленный маслом, стабилизированный на неорганических носителях) или непосредственно в виде жидкости. В данных условиях переработки пероксид распадается на свободные радикалы, которые инициируют реакции расщепления цепей и образуют полимеры, обладающие целевыми реологическими свойствами (вязкостями расплава). Деструкцию ПП с образованием продукта, обладающего уменьшенной молекулярной массой [повышенной скоростью растекания расплава (СРР)], обычно называют процессом понижения вязкости или легкого крекинга для понижения вязкости.
Продукты сортов ПП-РР используют главным образом в технологии волокон и технологии литья под давлением, в которых непременным условием для экономичной переработки являются низкие значения вязкости расплава. Современным требованием в технологии переработки является широкий диапазон вязкостей расплава или молекулярных масс.
Другим параметром, который, в дополнение к молекулярной массе, влияет на технологические свойства полимера, является молекулярно-массовое распределение (ММР). В то время как полимеры тех сортов, которым свойственны широкие ММР, проявляют улучшенные ориентационные свойства полимерных цепей при низких скоростях вытяжки в процессах прядения волокон, в случаях высоких скоростей вытяжки и широких ММР наблюдается противоположный эффект. По этой причине при высоких скоростях вытяжки для достижения улучшенной непрерывности в процессе прядения существенное значение имеют узкие ММР.
Применение пероксидов является недостатком, поскольку из-за того, что их температура разложения как правило ниже обычной температуры переработки полимеров, доступное "технологическое температурное окно" оказывается довольно узким. Кроме того, во время хранения пероксидов, в обращении с ними и при переработке следует соблюдать жесткие правила безопасности. Еще одним недостатком пероксидов является невозможность избежать разложения при приготовлении их смесей с расплавами полимеров.
Помимо пероксидов известны также другие источники свободных радикалов, например вещества, образующие С-радикалы, на основе кумениловых систем, но их можно применять только при температурах выше 280°С. В WO 97/49737 описан способ уменьшения молекулярной массы полимеров при температурах выше 280°С с использованием NOR-3ACC соединений, содержащих группу:

где G обозначает водородный атом или метил, каждый из G1 и G2 обозначает водородный атом или метил или они совместно обозначают оксогруппу. Эти известные NOR-3ACC соединения вызывают заметную деструкцию полимера только при температурах выше 280°С. Поскольку большинство полимеров перерабатывают при температуре, которая ниже этой температуры, при 160-280°С, существует настоятельная потребность в соединениях, которые соответственно могут быть использованы при более низких температурах.
Таким образом, одним из объектов изобретения являются соединения, которые приемлемы для процессов получения ПП-РР и применение которых разрешает проблемы, связанные с неблагоприятными высокими технологическими температурами и использованием пероксидов, например проблемы безопасности.
Было установлено, что ациклические и циклические гидроксиламины различного строения особенно приемлемы для использования в качестве инициаторов свободных радикалов, если их этерифицируют ацильными радикалами по группам >NO-H.
По изобретению также предлагается способ уменьшения молекулярной массы полипропилена, пропиленовых сополимеров или полипропиленовых смесей, характеризующийся тем, что по меньшей мере один гидроксиламиновый сложный эфир или полимер гидроксиламинового сложного эфира формулы:

где Ra′ обозначает моноацильный или диацильный радикал;
R1-R4 каждый обозначает С1-С6алкил; а
R5 и R6 каждый независимо друг от друга обозначает водородный атом, С1-С6алкил или С6-С10арил или R5 и R6 совместно обозначают атом кислорода, добавляют к полипропилену, пропиленовому сополимеру или полипропиленовой смеси, подвергаемой деструкции, и смесь нагревают.
Предпочтение отдают способу с использованием соединений (I), у которых Ra обозначает С2-С18алканоил или С3-С6 алкеноил.
Моноацильным радикалом Ra′ может быть, например, ацильный радикал, дериватизированный из одноосновной органической кислоты, содержащей С радикалы и кислотную группу, например один из вышеупомянутых ацильных радикалов частных формул -С(=O)-Н, -С(=O)-С1-С19алкил, -С(=O)-С2-С19алкенил, -С(=O)-С2 -С4алкенил-С6-С10арил, -С(=O)-С6-С10арил, -С(=O)-O-С1-С6алкил, -С(=O)-O-С6-С10арил, -С(=O)-NH-С1-С6алкил, -С(=O)-NH-С6-С10арил и -С(=O)-N(С1-С6алкил)2.
Когда Ra′ обозначает моноацильный радикал, гидроксиламиновые сложные эфиры (I) характеризуются мономерными или димерными структурами. Таким образом, димерные структуры обладают подходящими двухвалентными заместителями в 4-м положении, а они в свою очередь замещены в концевом положении соединениями (I) посредством их 4-го положения (α,ω-замещение).
Понятие "гидроксиламиновый сложный эфир" охватывает как мономерные, так и олигомерные соединения, а также полимеры, образованные соединениями формулы I.
Диацильным радикалом Ra′ может быть, например, диацильный радикал, дериватизированный из одноосновной органической кислоты, содержащей С радикалы и две кислотные группы, например диацильный радикал, дериватизированный из алифатической, ароматической или циклоалифатической дикарбоновой кислоты.
Подходящие алифатические дикарбоновые кислоты содержат от 2 до 40 атомов С каждая, например щавелевая кислота, малоновая кислота, диметилмалоновая кислота, янтарная кислота, пимелиновая кислота, адипиновая кислота, триметиладипиновая кислота, себациновая кислота, азелаиновая кислота и димерные кислоты (продукты димеризации ненасыщенных алифатических карбоновых кислот, таких, как олеиновая кислота), алкилированные малоновая и янтарная кислоты, например октадецилянтарная кислота.
Приемлемыми циклоалифатическими дикарбоновыми кислотами являются, например, 1,3-циклобутандикарбоновая кислота, 1,3-циклопентандикарбоновая кислота, 1,3- и 1,4-циклогександикарбоновые кислоты, 1,3- и 1, 4-(дикарбоксиметил)циклогексановые или 4,4′-дициклогексилдикарбоновая кислоты.
Подходящими ароматическими дикарбоновыми кислотами являются, например, терефталевая кислота, изофталевая кислота, о-фталевая кислота, а также 1,3-, 1,4-, 2,6- или 2,7-нафталиндикарбоновые кислоты, 4,4′-дифенилдикарбоновая кислота, бис(4-карбоксифенил)сульфон, 4,4′ -бензофенондикарбоновая кислота, 1,1,3-триметил-5-карбокси-3-(п-карбоксилфенил)индан, бис-4-карбоксифениловый эфир, бис(п-карбоксифенил)метан или бис(п-карбоксифенил)этан.
Предпочтение отдают ароматическим дикарбоновым кислотам, в частности терефталевой кислоте, изофталевой кислоте и 2,6-нафталиндикарбоновой кислоте.
Другими подходящими дикарбоновыми кислотами являются те, которые содержат группы -CO-NH-. Они представлены в DE-A 2414349. Также приемлемы дикарбоновые кислоты, содержащие N-гетероциклические кольца, например те, которые дериватизированы из карбоксиалкилированных, карбоксифенилированных или карбоксилбензилированных моноамин-симм.триазиндикарбоновых кислот (см. DE-A 2121184 и 2533675), моногидантоины и бисгидантоины, галоидированные или негалоидированные бензимидазолы и парабановая кислота. Карбоксиалкильные группы могут содержать от 3 до 20 атомов С каждая.
Когда Ra′ обозначает диацильный радикал и подходящая функциональная группа, например гидроксильная или аминогруппа, содержится в 4-м положении, соединения формулы I обладают полимерными структурами, например сложные полиэфиры, полиэфирамиды, полиуретаны, поликарбонаты или полиимидные эфиры.
Способ имеет особенно важное значение, когда используют соединения (I), относящиеся к ряду, включающему пространственно затрудненные аминовые производные, например соединения формулы:
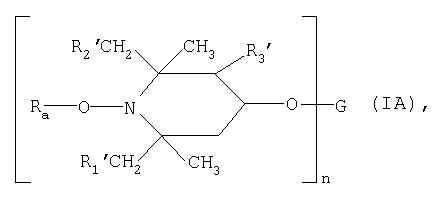
где n обозначает целое число от 1 до 4, Ra обозначает ацил, каждый из R1′, R2′ и R3′ независимо друг от друга обозначает водородный атом или метил; а
G имеет следующие значения:
когда n обозначает 1, водородный атом, С1-С18алкил, который может прерываться одним или несколькими атомами кислорода, 2-цианоэтил, бензил, глицидил, одновалентный радикал алифатической, циклоалифатической, аралифатической ненасыщенной или ароматической карбоновой кислоты, карбаминовой кислоты или фосфорсодержащей кислоты или одновалентный силильный радикал, предпочтительно ацильный радикал алифатической карбоновой кислоты, содержащей от 2 до 18 атомов С, циклоалифатической карбоновой кислоты, содержащей от 7 до 15 атомов С, α,β-ненасыщенной карбоновой кислоты, содержащей от 3 до 5 атомов С, или ароматической карбоновой кислоты, содержащей от 7 до 15 атомов С, где карбоновая кислота может быть замещенной в алифатической, циклоалифатической или ароматической части 1-3 группами -COOZ1, где Z1 обозначает водородный атом, С1-С20алкил, С3-С12алкенил, С5-С7циклоалкил, фенил или бензил; или
когда n обозначает 2, С2-С12алкилен, С2-С12 алкенилен, ксилилен, двухвалентная кислотная группа алифатической, циклоалифатической, аралифатической или ароматической дикарбоновой кислоты, дикарбаминовой кислоты или фосфорсодержащей кислоты или двухвалентный силильный радикал, предпочтительно ацильный радикал алифатической дикарбоновой кислоты, содержащей от 2 до 36 атомов С, циклоалифатической или ароматической дикарбоновой кислоты, содержащей от 8 до 14 атомов С, или алифатической, циклоалифатической или ароматической дикарбаминовой кислоты, содержащей от 8 до 14 атомов С, где дикарбоновая кислота может быть замещенной в алифатической, циклоалифатической или ароматической части 1 или 2 группами -COOZ1, где Z1 имеет указанные выше значения; или
когда n обозначает 3, трехвалентная кислотная группа алифатической, циклоалифатической или ароматической трикарбоновой кислоты, где эта группа может быть замещенной в алифатической, циклоалифатической или ароматической части группой -COOZ1, где Z1 имеет вышеуказанные значения, или трехвалентная кислотная группа ароматической трикарбаминовой кислоты или фосфорсодержащей кислоты, или трехвалентный силильный радикал; или
когда n обозначает 4, четырехвалентная кислотная группа алифатической, циклоалифатической или ароматической тетракарбоновой кислоты.
G, определенный как С1-С18алкил, может, например, иметь значения, указанные выше для алкила, и может, кроме того, представлять собой, например, н-тридецил, н-тетрадецил, н-гексадецил или н-октадецил.
Одновалентным ацильным радикалом карбоновой кислоты в качестве G может быть, например, ацильный радикал уксусной кислоты, гексеновой кислоты, стеариновой кислоты, акриловой кислоты, метакриловой кислоты, бензойной кислоты или β-(3,5-дитрет-бутил-4-гидроксифенил)пропионовой кислоты, предпочтительно ацильный радикал стеариновой кислоты, акриловой кислоты или метакриловой кислоты.
Одновалентным силильным радикалом G может быть, например, радикал - (CnH2n)-Si(Z′)2Z′′, где n обозначает целое число от 2 до 5, а каждый из Z′ и Z′′ независимо друг от друга обозначает С1-С4алкил или С1-С4алкокси.
Двухвалентной кислотной группой дикарбоновой кислоты в качестве G может быть, например, кислотная группа малоновой кислоты, янтарной кислоты, глутаровой кислоты, адипиновой кислоты, субериновой кислоты, себациновой кислоты, малеиновой кислоты, итаконовой кислоты, фталевой кислоты, дибутилмалоновой кислоты, дибензилмалоновой кислоты, бутил(3,5-дитрет-бутил-4-гидроксибензил)малоновой кислоты или бициклогептендикарбоновой кислоты.
Трехвалентным радикалом трикарбоновой кислоты в качестве G может быть, например, кислотная группа тримеллитовой кислоты, лимонной кислоты или нитрилтриуксусной кислоты.
Четырехвалентным радикалом тетракарбоновой кислоты в качестве G может быть, например, четырехвалентная кислотная группа бутан-1,2,3,4-тетракарбоновой кислоты или пиромеллитовой кислоты.
Двухвалентным радикалом дикарбаминовой кислоты в качестве G может быть, например, гексаметилендикарбаминовая кислотная группа или 2,4-толуилендикарбаминовая кислотная группа.
Предпочтительными соединениями являются соединения (IA), у которых n обозначает 1 или 2, каждый из R1′, R2′ и R3′ обозначает водородный атом, Ra обозначает С2-С18алканоил или С3-С6алкеноил, а G обозначает ацильный радикал алифатической монокарбоновой кислоты, содержащей от 12 до 18 атомов С, или диацильный радикал алифатической дикарбоновой кислоты, содержащей от 4 до 12 атомов С.
Другими затрудненными аминовыми производными являются соединения формулы:
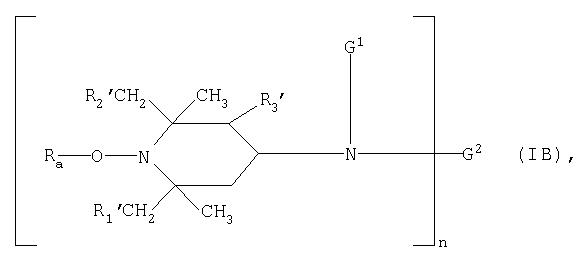
где n обозначает 1 или 2, a Ra, R1 ′, R2′ и R3′ имеют значения, указанные в описании формулы IA;
G1 обозначает водородный атом, С1-С12алкил, С2-С5гидроксиалкил, С5-С7циклоалкил, С7-С8аралкил, С2-С18алканоил, С3-С5алкеноил или бензоил, или группу:

где Ra, R1′, R2 ′ и R3′ имеют такие же значения, как указанные выше; а
G2 имеет следующие значения:
когда n обозначает 1, водородный атом, С1-С18алкил, С3-С8алкенил, С5-С7циклоалкил, С1-С4алкил, который в качестве заместителя несет гидроксильную, цианогруппу, алкоксикарбонил или карбамидную группу, глицидил или группу -CH2-CH(OH)-Z или CONH-Z, где Z обозначает водородный атом, метил или фенил; или
когда n обозначает 2, С2-С12алкилен, С6-С12арилен, ксилилен или -CH2CH(OH)-CH2-, или группа -CH2-CH(OH)-CH2-O-D-O-, где D обозначает С2-С10алкилен, С6-С15арилен или С6-С12циклоалкилен;
или, при условии, что G1 не обозначает алканоила, алкеноила или бензоила, G2 может также обозначать 1-оксо-С2-С12алкилен, двухвалентный радикал алифатической, циклоалифатической или ароматической дикарбоновой кислоты или дикарбаминовой кислоты, или группу -СО-;
или, когда n обозначает 1, G1 и G2 могут совместно обозначать двухвалентный радикал алифатической, циклоалифатической или ароматической 1,2-дикарбоновой кислоты или 1,3-дикарбоновой кислоты.
С1-С12алкильные и С1-С18алкильные заместители имеют такие же значения, как указанные выше в описании формулы (IA).
Предпочтительный С5-С7циклоалкил представляет собой циклогексил.
Предпочтительная С7-С8аралкильная группа G1 представляет собой 2-фенилэтил или бензил.
Предпочтительная С2-С5гидроксиалкильная группа G1 представляет собой 2-гидроксиэтил или 2- или 3-гидроксипропил.
С2-С18алканоильной группой G1 может быть, например, пропионил, бутирил, октаноил, додеканоил, гексадеканоил, октадеканоил, предпочтительно ацетил.
Предпочтительная С3-С5алкеноильная группа G1 представляет собой акрилоил.
С2-С8алкенильной группой G2 может быть, например, аллил, металлил, 2-бутенил, 2-пентенил, 2-гексенил или 2-октенил.
Гидрокси-, циано-, алкоксикарбонил- или карбамидозамещенной С1-С4алкильной группой G2 может быть, например, 2-гидроксиэтил, 2-гидроксипропил, 2-цианоэтил, метоксикарбонилметил, 2-этоксикарбонилэтил, 2-аминокарбонилпропил или 2-(диметиламинокарбонил)этил.
С2-С12алкиленовой группой G2 может быть, например, этилен, пропилен, 2,2-диметилпропилен, тетраметилен, гексаметилен, октаметилен, декаметилен или додекаметилен.
С6-С15ариленовой группой G2 может быть, например, о-, м- или п-фенилен, 1,4-нафтилен или 4,4′-дифенилен.
Предпочтительная С6-С12циклоалкиленовая группа G2 представляет собой циклогексилен.
Другими пространственно затрудненными аминовыми производными являются соединения формулы:
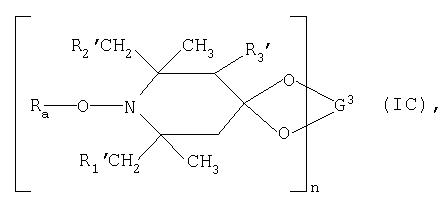
где n обозначает 1 или 2, a Ra, R1′, R2′ и R3′ имеют значения, указанные в описании формулы IA; а
G3 обозначает С2-С8алкилен, С2-С8гидроксиалкилен или С4-С22ацилоксиалкилен, когда n обозначает 1, или обозначает группу (-СН2)2С(СН2-)2, когда n обозначает 2.
С2-С8алкиленовой или С2-С8гидроксиалкиленовой группой G3 может быть, например, этилен, 1-метилэтилен, пропилен, 2-этилпропилен или 2-этил-2-гидроксиметилпропилен.
С4-С22 -ацилоксиалкиленовой группой G3 может быть, например, 2-этил-2-ацетоксиметилпропилен.
Кроме того, пространственно затрудненными аминовыми производными являются соединения формул:


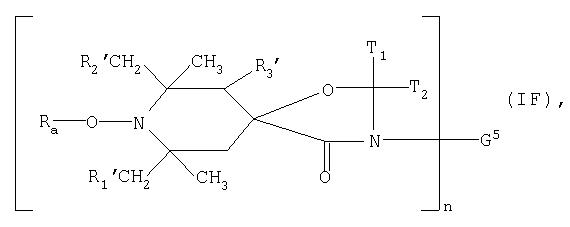
где n обозначает 1 или 2, a Ra, R1′, R2′ и R3′ имеют значения, указанные в описании формулы IA;
G4 обозначает водородный атом, С1-С12алкил, аллил, бензил, глицидил или С2-С6алкоксиалкил; а
G5 имеет следующие значения: когда n обозначает 1, водородный атом, С1-С12алкил, С3-С5алкенил, С7-С9аралкил, С5-С7циклоалкил, С2-С4гидроксиалкил, С2-С6 алкоксиалкил, С6-С10арил, глицидил или группу -(CH2)p-COO-Q или -(СН2)p-O-CO-Q, где p обозначает 1 или 2, a Q обозначает С1 -С4алкил или фенил; или
когда n обозначает 2, С2-С12алкилен, С4-С12алкенилен, С6-С12арилен, группу -CH2-CH(OH)-CH2-O-D-O-CH2-CH(OH)-CH2-, где D обозначает С2- С10алкилен, С6-С15арилен или С6-С12 циклоалкилен, или группу -CH2CH(OZ′)CH2-(OCH2-CH(OZ′)CH2)2-, где Z′ обозначает водородный атом, С1-С18 алкил, аллил, бензил, С2-С12алканоил или бензоил;
Т1 и Т2 каждый независимо друг от друга обозначает водородный атом, С1-С18алкил, С6-С10арил или С7-С9аралкил, каждый из которых может быть замещенным атомом галогена или С1-С4алкилом, или
Т1 и Т2 совместно с углеродным атомом, который с ними связан, образуют С5-С14циклоалкановое кольцо.
Заместителями С1 -С12алкила служат, например, метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, трет-бутил, н-гексил, н-октил, 2-этилгексил, н-нонил, н-децил, н-ундецил или н-додецил.
Заместителями, определенными как С1-С18алкилы, могут быть, например, вышеупомянутые группы или, например, н-тридецил, н-тетрадецил, н-гексадецил или н-октадецил.
С2-С6алкоксиалкил представляет собой, например, метоксиметил, этоксиметил, пропоксиметил, трет-бутоксиметил, 2-этоксиэтил, 2- или 3-этокси-н-пропил, 2-н-бутоксиэтил, 2-трет-бутоксиэтил, 2-изопропоксиэтил, 2- или 3-н-пропокси-н-пропил.
С3-С5алкенильной группой G5 может быть, например, 1-пропенил, аллил, металлил, 2-бутенил или 2-пентенил.
С7-С9аралкильные группы G5, Т1 и Т2 каждая в предпочтительном варианте представляет собой 2-фенетил или бензил. Когда Т1 и Т2 совместно с углеродным атомом образуют циклоалкановое кольцо, этим кольцом может быть, например, циклопентановое, циклогексановое, циклооктановое или циклододекановое кольцо.
С2-С4гидроксиалкильной группой G5 может быть, например, 2-гидроксиэтил, 2- или 3-гидрокси-н-пропил или 2-, 3- или 4-гидрокси-н-бутил.
С6-С10арильные группы G5, Т1 и Т2 каждая в предпочтительном варианте представляет собой фенил или α - или β-нафтил, каждый из которых может быть замещенным атомом галогена или С1-С4алкилом.
С2-С12алкиленовой группой G5 может быть, например, этилен, пропилен, 2,2-диметилпропилен, тетраметилен, гексаметилен, октаметилен, декаметилен или додекаметилен.
С4-С12алкениленовая группа G5 в предпочтительном варианте представляет собой 2-бутенилен, 2-пентенилен или 3-гексенилен.
С6-С12ариленовой группой G5 может быть, например, о-, м- или п-фенилен, 1,4-нафтилен или 4,4′-дифенилен.
С2-С12алканоильной группой Z′ в предпочтительном варианте является, например, ацетил, а может также быть пропионил, бутирил, н-октаноил или н-додеканоил.
С2-С10алкиленовые, С6-С15ариленовые и С6-С12циклоалкиленовые группы D являются такими, как представленные в описании формулы IB.
Дополнительные пространственно затрудненные аминовые производные представляют собой соединения формулы:

где n обозначает 1 или 2, а G6 обозначает группу:

или
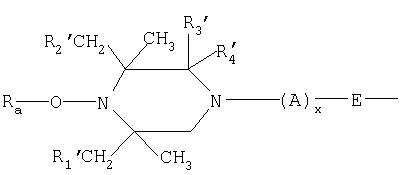
где Ra, R1′, R2′ и R3′ имеют значения, указанные в описании формулы IA, а каждый из R3′ и R4′ обозначает водородный атом или метил или совместно они образуют заместитель =O;
Е обозначает -О- или -NG1-, где G′ имеет значения, указанные в описании формулы IB;
А обозначает С2-С6алкилен или -(СН2)3-O-, а x обозначает либо 0, либо 1;
G1 в предпочтительном варианте представляет собой водородный атом, С1-С12алкил, С2-С5гидроксиалкил или С5-С7 циклоалкил;
G7 имеет такие же значения, как у G6, или обозначает одну из групп -NG9G10, -OG11, -NHCH2OG11 и -N(CH2OG11)2;
когда n обозначает 1, G8 имеет такие значения, как у G6 или G7; a
когда n обозначает 2, G8 обозначает группу -Е-В-Е-, где В обозначает С2-С8алкилен или С2-С8алкилен, прерываемый 1 или 2 группами -NG9-, а G9 обозначает С1-С12алкил, циклогексил, бензил или С1-С4гидроксиалкил, или группу:
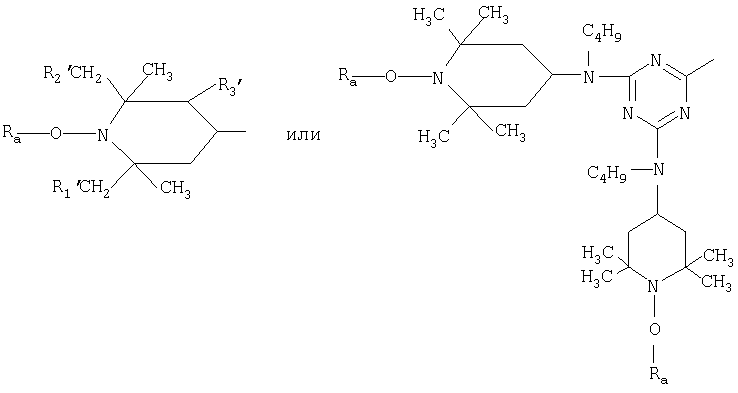
G10 обозначает С1-С12алкил, циклогексил, бензил или С1-С4гидроксиалкил, G11 обозначает водородный атом, С1-С12алкил или фенил; а
G9 и G10 совместно обозначают, например, С4-С5алкилен, С4-С5оксаалкилен, например тетраметилен, пентаметилен или 3-оксапентаметилен, или соответствующий С4-С5тиаалкилен, например группу

С1-С12алкил представляет собой, например, метил, этил, н-пропил, н-бутил, втор-бутил, трет-бутил, н-гексил, н-октил, 2-этилгексил, н-нонил, н-децил, н-ундецил или н-додецил.
С1-С4гидроксиалкил представляет собой, например, 2-гидроксиэтил, 2- или 3-гидроксипропил, или 2-, 3- или 4-гидрокси-н-бутил.
С2-С6алкиленовой группой А может быть, например, этилен, пропилен, 2,2-диметилпропилен, тетраметилен или гексаметилен.
Сложные полиэфиры (I) представляют собой, например, соединения формулы:

где n обозначает целое число больше двух, R1′, R2′ и R3′ имеют значения, указанные в описании формулы IA; а В обозначает двухвалентный заместитель, например С1-С12алкилен, в частности метилен, этилен, пропилен, 2,2-диметилпропилен или тетраметилен, гексаметилен, октаметилен, декаметилен или додекаметилен, С6-С15арилен, например группу:
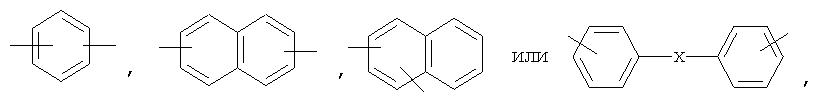
где Х обозначает двухвалентный заместитель, например С1-С12алкилен, как указанный выше, -О-, -(С=O)-, -S- или -S(=O)2-.
Сложные полиэфиры соединений формулы I могут также быть, например, сополимерами сложных полиэфиров (IH), у которых группа:

частично замещена приемлемыми диолами, которые дериватизируют, например, из алифатических, циклоалифатических или ароматических диолов.
Алифатические диолы могут содержать от 2 до 12 атомов С каждый, циклоалифатические диолы могут содержать от 5 до 8 атомов С каждый, а каждый из ароматических диолов может содержать от 6 до 15 атомов С.
Можно также использовать полиоксиалкиленгликоли, молекулярная масса которых находится в интервале от 150 до 40000.
Ароматические диолы представляют собой соединения, у каждого из которых две гидроксильные группы связаны с ароматическим углеводородным радикалом или с разными ароматическими углеводородными радикалами.
Сложным полиэфирам можно также придать разветвленность за счет небольших количеств, например от 0,1 до 3 мольных % в пересчете на имеющиеся дикарбоновые кислоты, больше чем бифункциональных мономеров [например, пентаэритрит, тримеллитовая кислота, 1,3,5-три(гидроксифенил)бензол, 2,4-дигидроксибензойная кислота или 2-(4-гидроксифенил)-2-(2,4-дигидроксифенил)пропан].
Подходящими алифатическими диолами являются линейные и разветвленные алифатические гликоли, в частности те, каждый из которых содержит в молекуле от 2 до 12, предпочтительно от 2 до 6, атомов С, например этиленгликоль, 1,2- и 1, 3-пропиленгликоли, 1,2-, 1,3-, 2,3- и 1,4-бутандиолы, пентилгликоль, неопентилгликоль, 1,6-гександиол, 1,12-додекандиол.
Приемлемым циклоалифатическим диолом является, например, 1, 4-дигидроксициклогексан. Другими подходящими диолами являются, например, 1,4-бис(гидроксиметил)циклогексан, ароматическоалифатические диолы, такие, как п-ксилиленгликоль и 2,5-дихлор-п-ксилиленгликоль, 2,2-(β-гидроксиэтоксифенил)пропан, а также полиоксиалкиленгликоли, такие, как диэтиленгликоль,триэтиленгликоль, полиэтиленгликоль и полипропиленгликоль. Предпочтительные алкилендиолы являются линейными и содержат, в частности, от 2 до 4 атомов С каждый.
Предпочтительные диолы представляют собой алкилендиолы, 1,4-дигидроксициклогексан и 1,4-бис(гидроксиметил)циклогексан. Особое предпочтение отдают этиленгликолю, 1,4-бутандиолу и 1,2-и 1,3-пропиленгликолю.
Кроме этого, подходящими алифатическими диолами являются (β-гидроксиалкилированные, в частности β-гидроксиэтилированные, бисфенолы, такие, как 2,2-бис[4′-(β-гидроксиэтокси)фенил]пропан.
Еще одна группа подходящих алифатических диолов включает гетероциклические диолы, описанные в DE-A 1812003, 2342432, 2342372 и 2453326. Примерами служат N,N′-бис(β-гидроксиэтил)-5,5-диметилгидантоин, N,N′-бис(β-гидроксипропил)-5, 5-диметилгидантоин, метиленбис[N-(β-гидроксиэтил)-5-метил-5-этилгидантоин], метиленбис[N-(β-гидроксиэтил)-5,5-диметилгидантоин], N,N′-бис(β-гидроксиэтил)бензимидазолон, N, N′-бис(β-гидроксиэтил)(тетрахлор)бензимидазолон и N,N′-бис(β-гидроксиэтил)(тетрабром)бензимидазолон.
Приемлемые ароматические диолы представляют собой бисфенолы, содержащие по одному ароматическому звену, в частности диолы, содержащие по два ароматических звена, которые на каждом ароматическом звене несут гидроксильную группу. Понятие "ароматические звенья" следует воспринимать как означающее ароматические углеводородные радикалы, такие, как фенилен и нафтилен. Не считая, например, гидрохинона, резорцина и 1,5-, 2,6- и 2,7-дигидроксинафталинов, можно особо упомянуть бисфенолы, которые могут быть представлены следующими формулами:
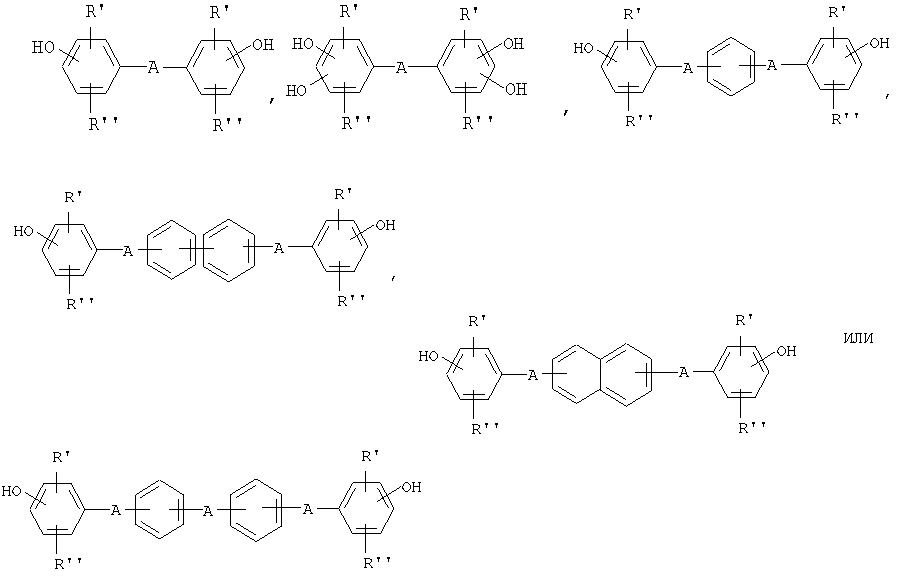
гидроксильные группы могут находиться в м-положении, но преимущественно в п-положении; каждый из R′ и R′′ в этих формулах может обозначать алкил, содержащий от 1 до 6 атомов С, атом галогена, такого, как хлор и бром, а преимущественно водородный атом. А может обозначать прямую связь или -О-, -S-, -S(=O)2-, -С(=O)-, -[Р(=O)С1-С20 алкил]-, замещенный или незамещенный алкилиден, циклоалкилиден или алкилен.
Примерами замещенного или незамещенного алкилидена служат этилиден, 1,1-и 2,2-пропилиден, 2,2-бутилиден, 1, 1-изобутилиден, пентилиден, гексилиден, гептилиден, октилиден, дихлорэтилиден, трихлорэтилиден.
Примерами замещенного или незамещенного алкилена служат метилен, этилен, фенилметилен, дифенилметилен и метилфенилметилен. Примерами циклоалкилидена являются циклопентилиден, циклогексилиден, циклогептилиден и циклооктилиден.
Примерами бисфенолов являются бис-п-гидроксифениловый эфир или тиоэфир, бис(п-гидроксифенил)сульфон, бис(п-гидроксифенил)метан, 2,2′-бис(4-гидроксифенил)дифенил, фенилгидрохинон, 1,2-бис(п-гидроксифенил)этан, 1-фенилбис(п-гидроксифенил)метан, дифенилбис(п-гидроксифенил)метан, дифенилбис(п-гидроксифенил)этан, бис(3,5-диметил-4-гидроксифенил)сульфон, бис(3,5-диметил-4-гидроксифенил)-п-диизопропилбензол, бис(3,5-диметил-4-гидроксифенил)-м-диизопропилбензол, 2,2-бис(3′,5′-диметил-4′-гидроксифенил)пропан, 1,1- и 2,2-бис(п-гидроксифенил)бутаны, 2,2-бис(п-гидроксифенил)гексафторпропан, 1,1-дихлор- и 1,1,1-трихлор-2,2-бис(п-гидроксифенил)этаны, 1,1-бис(п-гидроксифенил)циклопентан, а преимущественно 2,2-бис(п-гидроксифенил)пропан (бисфенол А) и 1,1-бис(п-гидроксифенил)циклогексан (бисфенол С).
Полиэфирамиды соединений формулы I представляют собой, например, соединения формулы:
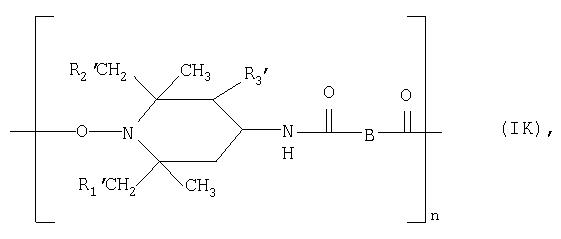
где n обозначает число больше двух, R1′, R2′ и R3′ имеют значения, указанные в описании формулы IA, а В представляет собой двухвалентный заместитель, имеющий значения, указанные в описании формулы IH.
Полиэфирамиды соединений формулы I также включают, например, сополимеры, у которых группа:

частично замещена вышеупомянутыми диолами или приемлемыми диаминами, дериватизированными, например, посредством вышеупомянутых алифатических, циклоалифатических или ароматических диолов путем замещения гидроксильных групп аминогруппами.
Полиуретаны соединений формулы I представляют собой, например, соединения формулы:

где n обозначает целое число больше двух, R1′, R2′ и R3′ имеют значения, указанные в описании формулы IA, а В обозначает двухвалентный заместитель, имеющий значения, указанные в описании формулы IH.
Полиуретаны соединений формулы I также включают, например, сополимеры, у которых группа
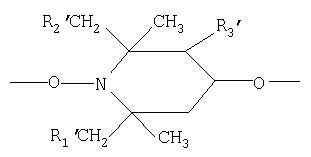
частично замещена приемлемыми диолами, например вышеупомянутыми диолами, или диаминами, дериватизированными, например, из вышеупомянутых алифатических, циклоалифатических или ароматических диолов путем замещения гидроксильных групп аминогруппами.
Полиуретаны могут быть получены по методу, который известен, реакцией вышеупомянутых циклических гидроксиламинов, содержащих гидроксильную группу в 4-м положении, с дикарбоновыми кислотами, у которых карбоксильные группы замещены изоцианатными группами.
Поликарбонаты соединений формулы I представляют собой, например, соединения формулы:
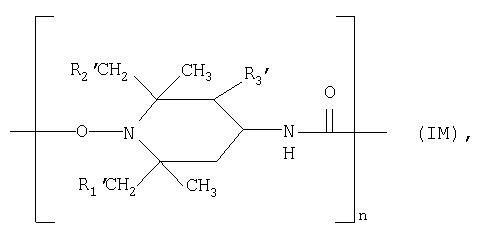
где n обозначает целое число больше двух, a R1′, R2′ и R3′ имеют значения, указанные в описании формулы IA.
Поликарбонаты могут быть получены по методу, который известен, реакцией вышеупомянутых циклических гидроксиламинов, содержащих гидроксильную группу в 4-м положении, с фосгеном или эфиром угольной кислоты, например с диэтилкарбонатом или дифенилкарбонатом.
Полиуретаны соединений формулы I также включают, например, сополимеры, у которых группа

частично замещена приемлемыми диолами, например вышеупомянутыми диолами.
Полиимидоэфиры соединений формулы I представляют собой, например, соединения формулы:
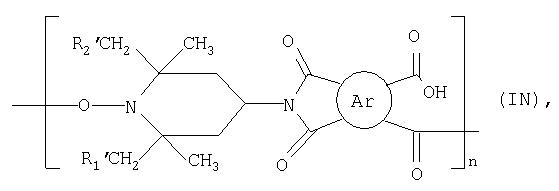
где n обозначает целое число больше двух, a R1′, R2′ и R3′ имеют значения, указанные в описании формулы IA. Ароматическое связывающее звено

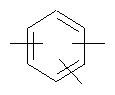
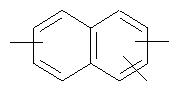
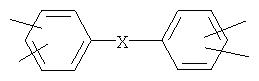
По изобретению предлагается, в частности, способ уменьшения молекулярной массы полипропилена, пропиленовых сополимеров или полипропиленовых смесей, характеризующийся тем, что в полипропилен, полипропиленовый сополимер или полипропиленовую смесь, которую необходимо деструктировать, добавляют по меньшей мере одно соединение формулы Ia, где
Ra обозначает ацильный радикал, выбранный из группы, включающей -С(=O)-Н, -С(=O)-С1-С19алкил, -С(=O)-С2-С19алкенил, -С(=O)-С2-С4алкенил-С6-С10арил, -С(=O)-С6-С10арил, -С(O)-O-С1-С6алкил, -С(=O)-O-С6-С10арил, -С(=O)-NH-С1-С6алкил,-С(=O)-NH-С6-С10арил,-С(=O)-N(С1-С6алкил)2, -Р(=O)-С1-С19алкил, -Р(=O)2-С1-С19алкил, -Р(=O)-С6-С10арил, -P=O(-C1-С19 алкил)2, -Р=O(-С6-С10арил)2, -Р(=O)-O-С1-С6алкил, -Р(=O)-O-С6-С10арил, -Р=O(-O-С1-С6 алкил)2, -Р=O(-O-С6-С10арил)2, -Р(-O-С1-С6алкил)2 и -Р(-O-С6-С10арил)2;
R1 -R4 каждый обозначает С1-С6алкил;
R5 и R6 каждый независимо друг от друга обозначает водородный атом, С1-С6 алкил или С6-С10арил; или
R5 и R6 совместно обозначают атом кислорода;
Q обозначает прямую связь или двухвалентный радикал -(CR7R8)- или -(CR7R8-CR9R10)-, где
R7, R8, R9 и R10 каждый независимо друг от друга обозначает водородный атом или С1-С6алкил; а
Z1 обозначает атом кислорода или двухвалентный радикал -NR11- или -(CR12R13)-, где
R11 обозначает водородный атом, С1-С6алкил, С6-С10арил или ацильный радикал Ra, как указанный выше; или независимо друг от друга
R12 и R13 каждый обозначает водородный атом или С1-С6алкил, или один из радикалов R12 и R13 представляет собой водородный атом или С1-С6алкил, а другой представляет собой С1-С6алкил, С1-С6алкокси, С6-С10арилокси, ацилоксирадикал, выбранный из группы, включающей -O-С(=O)-Н, -O-С(=O)-С1-С19алкил, -O-С(=O)-С1-С54алкенил, -O-С(=O)-С6-С10арил, -O-С(=O)-С1-С36алкенил-С6-С10арил, -O-C(=O)-O-С1-С6алкил, -O-С(=O)-O-С6-С10арил, -O-С(=O)-NH-С1-С6алкил, -O-С(=O)-NH-С6-С10арил и -O-С(=O)-N(С1-С6алкил)2, С1-С6алкиламино-, ди-С1-С6алкиламино-, С6-С10ариламино-, ациламиновый радикал, выбранный из группы, включающей -NH-C(=O)-H, NH-С(=O)-С1-С19алкил, -NH-С(=O)-С1-С54алкенил, -NH-С(=O)-С6-С10арил, -NH-С(=О)-С1-С36алкенил-С6-С10арил, -NH-C(=O)-O-С1-С19алкил, -NH-С(=O)-O-С6-С10арил, -NH-С(=O)-NH-С1-С6алкил, -NH-С(=O)-NH-С6-С10арил и -NH-С(=O)-N(С1-С6алкил)2, диациламиновый радикал, выбранный из группы, включающей -N[-С(=O)-С1-С19алкил]2, -N[-С(=O)-C6-C10арил]2,-N[-С(=O)-С1-С6алкилен-С(=O)-], -N[-С(=O)-С2-С6алкенилен-С(=O)-] и фталимидный радикал, или N-ацил-N-С1-С6алкиламиновый радикал;
или оба радикала R12 и R13 совместно образуют оксогруппу; или соединение формулы Ib, где
Ra обозначает ацильный радикал, выбранный из группы, включающей -С(=O)-Н, -С(=O)-С1-С19алкил, -С(=O)-С2-С19алкенил, -С(=O)-С2-С4алкенил-С6-С10арил, -С(=O)-С6-С10 арил, -С(=O)-O-С1-С6алкил, -С(=O)-O-С6-С10арил, -С(=O)-NH-С1-С6алкил, -С(=O)-NH-С6-С10арил и -С(=O)-N(С1-С6алкил)2; R1-R4 каждый обозначает С1-С6алкил;
А обозначают заместители в фенильных кольцах; а
m обозначает целое число от одного до четырех; или соединение формулы Ic, где
Ra обозначает ацильный радикал, выбранный из группы, включающей -С(=O)-Н, -С(=O)-С1 -С19алкил, -С(=O)-С2-С19алкенил, -С(=O)-С2-С4алкенил-С6-С10арил, -С(=O)-С6-С10арил, -С(=O)-O-С1-С6алкил, -С(=O)-O-С6-С10арил, -С(=O)-NH-С1-С6алкил, -С(=O)-NH-С6-С10арил, -С(=O)-N(С1-С6 алкил)2, -Р(=O)-С1-С19алкил, -P(=O)2-C1-C19алкил, -Р(=O)-С6-С10арил, -P=O(-C1-С19 алкил)2, -Р=O(-С6-С10арил)2, -Р(=O)-O-С1-С6алкил, -Р(=O)-O-С6-С10арил, -Р=O(-O-С1-С6 алкил)2, -Р=O(-O-С6-С10арил)2, -Р(-O-С1-С6алкил)2 и -Р(-O-С6-С10арил)2;
Rb обозначает водородный атом, карбамоил, С1-С6алкилкарбамоил или ди-С1-С6алкилкарбамоил или имеет такие же значения, как указанные для Ra; Rc и Rd каждый независимо друг от друга обозначает водородный атом, С1-С20алкил или С6-С10арил; а
R1-R3 каждый обозначает С1-С6алкил или С6-С10арил; или соединение формулы:

где n обозначает два;
Х обозначает прямую связь или одновалентный радикал С1-С18алкиленового мостика;
R1-R4 каждый обозначает С1-С6алкил;
R5 и R6 каждый независимо друг от друга обозначает водородный атом, С1-С6алкил или С6-С10арил; или
R5 и R6 совместно обозначают атом кислорода;
Q обозначает прямую связь или двухвалентный радикал -(CR7R8)- или -(CR7R8-CR9R10)-, где
R7, R8, R9 и R10 каждый независимо друг от друга обозначает водородный атом или C1-С6алкил; а
Z1 обозначает атом кислорода или двухвалентный радикал -NR11- или -(CR12R13)-, где
R11 обозначает водородный атом, С6-С10арил или C1-С6алкил, или независимо друг от друга
один из радикалов R12 и R13 представляет собой водородный атом или С1-С6алкил, а другой представляет собой С1-С6алкил, С1-С6алкокси, С6-С10арилокси, ацилоксирадикал, выбранный из группы, включающей -O-С(=O)-Н, -O-С(=O)-С1-С19алкил, -O-С(=O)-С1-С54алкенил, -O-С(=O)-С6-С10арил, -O-С(=O)-С1-С36алкенил-С6-С10арил, -O-С(=O)-O-С1-С6алкил, -O- С(=O)-O-С6-С10арил, -О-С(=О)-NH-С1-С6алкил, -O-С(=O)-NH-С6-С10арил и -O-C(=O)-N(С1-С6алкил)2, С1-С6алкиламино-, ди-С1-С6алкиламино-, С6-С10ариламино-, ациламиновый радикал, выбранный из группы, включающий -NH-C(=O)-H, -NH-С(=O)-С1-С19алкил, -NH-C(=O)-С1-С54алкенил, -NH-С(=O)-С6-С10арил, -NH-С(=O)-С1-С36алкенил-С6-С10арил, -NH-C(=O)-O-С1-С19алкил, -NH-C(=O)-O-С6-С10арил,-NH-C(=O)-NH-С1 -С6алкил, -NH-С(=O)-NH-С6-С10арил и -NH-С(=O)-N(С1-С6алкил)2, диациламиновый радикал, выбранный из группы, включающей -N[-C(=O)-С1-С19алкил]2, -N[-С(=O)-С6-С10арил]2, -N[-С(=O)-С1-С6алкилен-С(=O)-], -N[-C(=O)-С2-С6 алкенилен-C(=O)-] и фталимидный радикал, или N-ацил-N-С1-С6алкиламиновый радикал;
или оба радикала R12 и R13 совместно обозначают оксогруппу; или соединение формулы:

где n обозначает два;
Ra обозначает ацильный радикал, выбранный из группы, включающей -С(=O)-Н, -С(=O)-С1-С19алкил, -С(=O)-С2-С19алкенил, -С(=O)-С2-С4 алкенил-С6-С10арил, -С(=O)-С6-С10арил, -С(=O)-O-С1-С6алкил, -С(=O)-O-С6-С10арил, -С(=O)-NH-С1-С6алкил, -С(=O)-NH-С6-С10арил и -С(=O)-N(С1-С6алкил)2;
Х обозначает прямую связь или одновалентный радикал С1 -С18алкиленового мостика; R1-R4 каждый обозначает C1-С6алкил; R5 и R6 каждый независимо друг от друга обозначает водородный атом, C1-С6алкил или С6-С10арил; или R5 и R6 совместно обозначают атом кислорода; а
Q обозначает прямую связь или двухвалентный радикал -(CR7R8)- или -(CR7R8-CR9R10)-, где
R7, R8, R9 и R10 каждый независимо друг от друга обозначает водородный атом или С1-С6алкил; и смесь нагревают.
Формула Id) отображает бициклические соединения, две половины каждого из которых соединены двухвалентным мостиком X. Когда Х обозначает прямую связь, бициклическое соединение отвечает формуле

Это соединение представляет собой гидроксиламиновый диэфир щавелевой кислоты. Когда Х обозначает одновалентный радикал С1 -С18алкиленового мостика, бициклическое соединение представляет собой гидроксиламиновый диэфир малоновой кислоты, янтарной кислоты или более высшей дикарбоновой кислоты.
R1-R4 имеют такие же значения, как указанные выше.
Аналогичным образом R5, R6, Q, R7, R8, R9 и R10 имеют такие же значения, как указанные выше.
Z1 может быть атомом кислорода или двухвалентным радикалом -NR11- или -(CR12R13)-, где
R11 обозначает водородный атом, арил или С1-С6алкил, или независимо друг от друга
один из радикалов R12 и R13 представляет собой водородный атом или С1-С6алкил, а другой представляет собой С1-С6алкил, С1-С6алкокси, С6-С10 арилокси, ацилоксирадикал, выбранный из группы, включающей -O-С(=O)-Н, -O-С(=O)-С1-С19алкил, -O-C(=O)-С1-С54алкенил, -O-С(=O)-С6-С10 арил, -O- С(=O)-С1-С36алкенил-С6-С10арил,-O-С(=O)-O-С1-С19алкил, -O-С(=O)-O-С6-С10арил, -O-С(=O)-NH-С1 -С6алкил, -О-С(=О)-NH-С6-С10арил и -O-С(=O)-N(С1-С6алкил)2, С1-С6алкиламино-, ди-С1-С6 алкиламино-, С6-С10ариламино-, ациламиновый радикал, выбранный из группы, включающей -NH-C(=O)-H, -NH-С(=O)-С1-С19алкил, -NH-С(=O)-С1-С54алкенил, -NH-С(=O)-С6-С10арил, -NH-С(=O)-С1-С36алкенил-С6-С10арил, -NH-C(=O)-O-С1-С19алкил, -NH-С(=O)-O-С6-С10арил, -NH-С(=O)-NH-С1-С6алкил, -NH-С(=O)-NH-С6-С10арил и -NH-C(=O)-N(С1-С6алкил)2, диациламиновый радикал, выбранный из группы, включающей -N[-С(=O)-С1-С19алкил]2,-N[-С(=O)-С6-С10арил]2,-N[-С(=O)-С1-С6алкилен-С(=O)-], -N[-C(=O)-С2-С6алкенилен-C(=O)-] и фталимидный радикал, или N-ацил-N-С1-С6алкиламиновый радикал, как указанный выше; или оба радикала R12 и R13 совместно обозначают оксогруппу.
Добавление пропиленового полимера можно производить во всех обычных смесительных устройствах, в которых полимер плавят и смешивают с добавками. Подходящими устройствами являются те, которые известны специалистам в данной области техники. Ими служат преимущественно смесители, пластикаторы и экструдеры.
В предпочтительном варианте предлагаемый способ осуществляют в экструдере введением добавки во время переработки.
Особенно предпочтительными перерабатывающими устройствами являются одночервячные экструдеры, двухчервячные экструдеры с противовращением и с вращением в одном направлении, экструдеры с планетарными системами шнеков, экструдеры с кольцевыми нагревательными элементами и шнековая месильная машина. Можно также применять машины, оборудованные по меньшей мере одной секцией для удаления газов, к которой может быть подключена система создания вакуума.
Подходящие экструдеры и пластикаторы описаны, например, в работе Handbuch der Kunststoffextrusion, том 1, Grundlagen, под редакцией F.Hensen, W.Knappe, H.Potente, 1989, cc.3-7, ISBN: 3-446-14339-4 (том 2, Extrusionsanlagen 1986, ISBN 3-446-] 4329-7).
Так, например, длина шнека составляет от 1 до 60 диаметров шнека, предпочтительно от 35 до 48 диаметров шнека. Предпочтительная скорость вращения шнека равна от 10 до 600 оборотов в минуту (об/мин), очень часто предпочтительно от 25 до 300 об/мин.
Максимальная производительность зависит от диаметра шнека, скорости вращения и выталкивающего усилия. Способ по настоящему изобретению можно также осуществлять при производительности, которая ниже максимальной, варьированием упомянутых параметров или применением взвешивающих устройств, подающих дозированные количества.
Если добавляют множество компонентов, их можно предварительно смешивать или добавлять индивидуально.
Полимеры необходимо подвергать воздействию повышенной температуры в течение периода времени, достаточного для того, чтобы вызвать необходимую деструкцию. Температура обычно превышает температуру размягчения полимеров.
В предпочтительном варианте осуществления способа по настоящему изобретению температура находится в интервале ниже 280°С, в частности от примерно 160 до 280°С. В особенно предпочтительном варианте осуществления способа температура находится в интервале от примерно 200 до 270°С.
Период времени, необходимый для деструкции, можно варьировать в зависимости от температуры, количества деструктируемого материала и типа, например, применяемого экструдера. Обычно он составляет от примерно 10 с до 20 мин, в частности от 20 с до 10 мин.
Вышеописанные гидроксиламиновые сложные эфиры (I) приемлемы для уменьшения молекулярной массы полипропилена, пропиленовых сополимеров и полипропиленовых смесей во время компаундирования, когда они вызывают деструкцию полимерных цепей подобно пероксидам, которые обычно используют в данной области техники.
В процессе уменьшения молекулярной массы (в процессе деструкции) вышеописанные гидроксиламиновые сложные эфиры (I) содержатся в концентрациях от примерно 0,001 до 5,0 мас.%, в частности от 0,01 до 2,0 мас.%, а особенно предпочтительно от 0,02 до 1,0 мас.%, в пересчете на количество полимеров, которые необходимо деструктировать. Гидроксиламиновые сложные эфиры (I) можно добавлять в подвергаемый деструкции полимер в виде индивидуальных соединений или в виде смесей.
К подвергаемым деструкции полимерам полипропиленового типа можно отнести пропиленовые гомополимеры, пропиленовые сополимеры и полипропиленовые смеси. Пропиленовые сополимеры могут включать различные количества сомономерных звеньев, достигающие 90%, предпочтительно до 50%. Примерами сомономеров служат олефины такие, как 1-олефины, например этилен, 1-бутен, 1-пентен, 1-гексен, 1-гептен или 1-октен, изобутилен, циклоолефины, например циклопентен, циклогексен, норборнен или этилиденнорборнен, диены, такие, как бутадиен, изопрен, 1,4-гексадиен, циклопентадиен, дициклопентадиен и норборнадиен, а также производные акриловой кислоты и ненасыщенные ангидриды карбоновых кислот, такие, как малеиновый ангидрид.
Полипропиленовые смеси, которые могут быть использованы, представляют собой смеси полипропилена с полиолефинами. Примерами являются смеси полипропилена с полиэтиленом, выбранным из группы, включающей полиэтилен высокой плотности (ПЭВП), полиэтилен высокой плотности с высокой молекулярной массой (ПЭВП-ВММ), полиэтилен высокой плотности со сверхвысокой молекулярной массой (ПЭВП-СВММ), полиэтилен средней плотности (ПЭСП), полиэтилен низкой плотности (ПЭНП), линейный полиэтилен низкой плотности (ЛПЭНП), разветвленный полиэтилен низкой плотности (РПЭНП) и этилен-пропилен-диеновые тройные сополимеры (ЭПДМ), содержащие небольшие количества диеновых звеньев.
В то время как иногда летучие продукты разложения (дым) пероксидов могут вызвать обесцвечивание или появление запаха у деструктированных полимеров, в случае полимеров, деструктированных с использованием гидроксиламиновых сложных эфиров (I), обесцвечивание и запах оказываются очень слабо выраженными.
Введение в полимеры можно осуществлять, например, подмешиванием в полимеры вышеописанных гидроксиламиновых сложных эфиров (I) или их смесей и, если необходимо, других добавок с применением методов, которые обычны для технологии переработки.
По другому варианту их введение можно также производить при температурах, которые еще не вызывают разложения полимеров (латентный компаунд). В дальнейшем полимеры, приготовленные таким путем, можно нагревать во второй раз и подвергать воздействию повышенной температуры в течение периода времени, достаточного для того, чтобы происходила целевая деструкция полимера.
NOR-соединения (I) можно также добавлять в подвергаемые деструкции полимеры в форме маточной смеси, в которой эти соединения содержатся, в частности, в концентрации от примерно 1 до 25 мас.%. Такая маточная смесь (концентрат) может быть приготовлена при температурах, которые еще не вызывают разложения соединений по настоящему изобретению.
В результате получают продукт, который определяется конкретными дозированными количествами и который можно компаундировать с другими добавками. В дальнейшем такую маточную смесь можно компаундировать с подвергаемым деструкции полимером при температуре, превышающей температуру разложения гидроксиламинового сложного эфира (I).
Таким образом, по настоящему изобретению далее предлагается концентрат, в котором соединения по изобретению содержатся в концентрации от 1 до 25 мас.% и который можно добавлять в подвергаемый деструкции полимер. Следовательно, целевой продукт можно получать осуществлением эффективного двухстадийного способа.
В конкретном варианте в подвергаемые деструкции полимеры вводят
приемлемые добавки, например кислые земли, в частности типа Fulcat®, цеолитов, гидроталькитов или солей металлов, например Ca, Fe, Zn или Cu.
Было установлено, что деструктирующему действию способствуют оксиды, гидроксиды и карбонаты металлов в состоянии окисления II. Таким образом, предпочтение отдают композициям, которые, кроме вышеописанных NOR-соединений (I), дополнительно включают от 0,1 до 10 част. соли металла на часть NOR-соединения (I). Конкретно предпочтение отдают концентрациям от 0,5 до 10 част. соли металла, выбранной из группы, включающей СаО, СаСО3, ZnO, ZnCO3, MgO, MgCO3 и Mg(OH)2, на часть NOR-соединения (I).
Помимо гидроксиламиновых сложных эфиров в полимере могут также содержаться другие соединения, например светостабилизаторы типа 2-(2-гидроксифенил)-1,3,5-триазина, которые известны из патентной литературы, например US 4619956, ЕР-А 434608, US 5198498, US 5322868, US 5369140, US 5298067, WO 94/18278, ЕР-А 704437, GB-A 2297091 или WO 96/28431.
Ниже приведены примеры других добавок.
1. Антиоксиданты
1.1. Алкилированные монофенолы, например 2,6-дитрет-бутил-4-метилфенол, 2-бутил-4,6-диметилфенол, 2,6-дитрет-бутил-4-этилфенол, 2,6-дитрет-бутил-4-н-бутилфенол, 2,6-дитрет-бутил-4-изобутилфенол, 2, 6-дициклопентил-4-метилфенол, 2-(α-метилциклогексил)-4,6-диметилфенол, 2,6-диоктадецил-4-метилфенол, 2,4,6-трициклогексилфенол, 2,6-дитрет-бутил-4-метоксиметилфенол, нонилфенолы, у которых могут быть линейные или разветвленные боковые цепи, например 2,6-динонил-4-метилфенол, 2,4-диметил-6-(1′-метилундец-1′-ил)фенол, 2,4-диметил-6-(1′-метилгептадец-1′-ил)фенол, 2,4-диметил-6-(1′-метилтридец-1′-ил)фенол и их смеси.
1.2. Алкилтиометилфенолы. например 2,4-диоктилтиометил-6-трет-бутилфенол, 2,4-диоктилтиометил-6-метилфенол, 2, 4-диоктилтиометил-6-этилфенол, 2,6-дидодецилтиометил-4-нонилфенол.
1.3. Гидрохиноны и алкилированные гидрохиноны. например 2,6-дитрет-бутил-4-метоксифенол, 2,5-дитрет-бутилгидрохинон, 2,5-дитрет-амилгидрохинон, 2,6-дифенил-4-октадецилоксифенол, 2,6-дитрет-бутилгидрохинон, 2,5-дитрет-бутил-4-гидроксианизол, 3,5-дитрет-бутил-4-гидроксианизол, 3,5-дитрет-бутил-4-гидроксифенилстеарат, бис(3,5-дитрет-бутил-4-гидроксифенил)адипат.
1.4. Токоферолы, например α-, β-, γ- и δ-токоферолы.
1.5. Гидроксилированные тиодифениловые простые эфиры. например бис(3-трет-бутил-5-метил-2-гидроксифенил)тиоэфир, бис(5-октил-2-гидроксифенил)тиоэфир, бис(5-трет-бутил-2-метил-4-гидроксифенил)тиоэфир, бис(5-трет-бутил-3-метил-4-гидроксифенил)тиоэфир, бис(2,5-дивтор-амил-4-гидроксифенил)тиоэфир, бис(2,6-диметил-4-гидроксифенил)дисульфид.
1.6. Алкилиденбисфенолы, например 2,2′ -метиленбис(6-трет-бутил-4-метилфенол), 2,2′-метиленбис(6-трет-бутил-4-этилфенол), 2,2′-метиленбис[4-метил-6-(α-метилциклогексил)фенол], 2,2′ -метиленбис(4-метил-6-циклогексилфенол), 2,2′-метиленбис(6-нонил-4-метилфенол), 2,2′-метиленбис(4,6-дитрет-бутилфенол), 2,2′-этилиденбис(4,6-дитрет-бутилфенол), 2,2′ -этилиденбис(6-трет-бутил-4-изобутилфенол), 2,2′-метиленбис[6-(α-метилбензил)-4-нонилфенол], 2,2′-метиленбис[6-(α,α-диметилбензил)-4-нонилфенол], 4,4′ -метиленбис(2,6-дитрет-бутилфенол), 4,4′-метиленбис(6-трет-бутил-2-метилфенол), 1,1-бис(5-трет-бутил-4-гидрокси-2-метилфенил)бутан, 2,6-бис(3-трет-бутил-5-метил-2-гидроксибензил)-4-метилфенол, 1,1,3-трис(5-трет-бутил-4-гидрокси-2-метилфенил)бутан, 1,1-бис(5-трет-бутил-4-гидрокси-2-метилфенил)-3-н-додецилмеркаптобутан, этиленгликольбис[3,3-бис(3′-трет-бутил-4′ -гидроксифенил)бутират], бис(3-трет-бутил-4-гидрокси-5-метилфенил)дициклопентадиен, бис[2-(3′-трет-бутил-2′-гидрокси-5′-метилбензил)-6-трет-бутил-4-метилфенил]терефталат, 1, 1-бис(3,5-диметил-2-гидроксифенил)бутан, 2,2-бис(3,5-дитрет-бутил-4-гидроксифенил)пропан, 2,2-бис(5-трет-бутил-4-гидрокси-2-метилфенил)-4-н-додецилмеркаптобутан, 1,1,5, 5-тетра(5-трет-бутил-4-гидрокси-2-метилфенил)пентан.
1.7. О-, N- и S-бензиловые соединения, например бис(3,5-дитрет-бутил-4-гидроксибензил)эфир, октадецил-4-гидрокси-3, 5-диметилбензилмеркаптоацетат, тридецил-4-гидрокси-3,5-дитрет-бутилбензилмеркаптоацетат, трис(3,5-дитрет-бутил-4-гидроксибензил)амин, бис(4-трет-бутил-3-гидрокси-2,6-диметилбензил)дитиотерефталат, бис(3,5-дитрет-бутил-4-гидроксибензил)сульфид, изооктил-3,5-дитрет-бутил-4-гидроксибензилмеркаптоацетат.
1.8. Гидроксибензилированные малонаты, например диоктадецил-2,2-бис(3, 5-дитрет-бутил-2-гидроксибензил)малонат, диоктадецил-2-(3-трет-бутил-4-гидрокси-5-метилбензил)малонат, дидодецилмеркаптоэтил-2,2-бис(3,5-дитрет-бутил-4-гидроксибензил)малонат, ди[4-(1,1,3, 3-тетраметилбутил)фенил]-2,2-бис(3,5-дитрет-бутил-4-гидроксибензил)малонат.
1.9. Ароматические гидроксибензиловые соединения, например 1,3,5-трис(3,5-дитрет-бутил-4-гидроксибензил)-2,4, 6-триметилбензол, 1,4-бис(3,5-дитрет-бутил-4-гидроксибензил)-2,3,5,6-тетраметилбензол, 2,4,6-трис(3,5-дитрет-бутил-4-гидроксибензил)фенол.
1.10. Триазиновые соединения, например 2, 4-бисоктилмеркапто-6-(3,5-дитрет-бутил-4-гидроксианилино)-1,3,5-триазин, 2-октилмеркапто-4,6-бис(3,5-дитрет-бутил-4-гидроксианилино)-1,3,5-триазин, 2-октилмеркапто-4,6-бис(3, 5-дитрет-бутил-4-гидроксифенокси)-1,3,5-триазин, 2,4,6-трис(3,5-дитрет-бутил-4-гидроксифенокси)-1,2,3-триазин,
1,3,5-трис(3,5-дитрет-бутил-4-гидроксибензил)изоцианурат, 1,3, 5-трис(4-трет-бутил-3-гидрокси-2,6-диметилбензил)изоцианурат, 2,4,6-трис(3,5-дитрет-бутил-4-гидроксифенилэтил)-1,3,5-триазин, 1,3,5-трис(3,5-дитрет-бутил-4-гидроксифенилпропионил)гексагидро-1,3, 5-триазин, 1,3,5-трис(3,5-дициклогексил-4-гидроксибензил)изоцианурат.
1.11. Ациламинофенолы, например анилид 4-гидроксилауриновой кислоты, анилид 4-гидроксистеариновой кислоты, октил-N-(3,5-дитрет-бутил-4-гидроксифенил)карбамат.
1.12. Эфиры β-(3,5-дитрет-бутил-4-гидроксифенил)пропионовой кислоты и одно- и многоатомных спиртов, например метанола, этанола, н-октанола, изооктанола, октадеканола, 1,6-гександиола, 1,9-нонандиола, этиленгликоля, 1,2-пропандиола, неопентилгликоля, тиодиэтиленгликоля, диэтиленгликоля, триэтиленгликоля, пентаэритрита, трис(гидроксиэтил)изоцианурата, N,N′-бис(гидроксиэтил)оксамида, 3-тиаундеканола, 3-тиапентадеканола, триметилгександиола, триметилолпропана, 4-гидроксиметил-1-фосфа-2,6, 7-триоксабицикло[2.2.2]октана.
1.13. Эфиры β-(5-трет-бутил-4-гидрокси-3-метилфенил)пропионовой кислоты и одно- и многоатомных спиртов, например метанола, этанола, н-октанола, изооктанола, октадеканола, 1,6-гександиола, 1,9-нонандиола, этиленгликоля, 1,2-пропандиола, неопентилгликоля, тиодиэтиленгликоля, диэтиленгликоля, триэтиленгликоля, пентаэритрита, трис(гидроксиэтил)изоцианурата, N,N′-бис(гидроксиэтил)оксамида, 3-тиаундеканола, 3-тиапентадеканола, триметилгександиола, триметилолпропана, 4-гидроксиметил-1-фосфа-2,6, 7-триоксабицикло[2.2.2]октана.
1.14. Эфиры β-(3,5-дициклогексил-4-гидроксифенил)пропионовой кислоты и одно- и многоатомных спиртов, например метанола, этанола, октанола, октадеканола, 1,6-гександиола, 1,9-нонандиола, этиленгликоля, 1,2-пропандиола, неопентилгликоля, тиодиэтиленгликоля, диэтиленгликоля, триэтиленгликоля, пентаэритрита, трис(гидроксиэтил)изоцианурата, N, N′-бис(гидроксиэтил)оксамида, 3-тиаундеканола, 3-тиапентадеканола, триметилгександиола, триметилолпропана, 4-гидроксиметил-1-фосфа-2,6,7-триоксабицикло[2.2.2]октана.
1.15. Эфиры 3.5-дитрет-бутил-4-гидроксифенилуксусной кислоты и одно- и многоатомных спиртов, например метанола, этанола, октанола, октадеканола, 1,6-гександиола, 1,9-нонандиола, этиленгликоля, 1,2-пропандиола, неопентилгликоля, тиодиэтиленгликоля, диэтиленгликоля, триэтиленгликоля, пентаэритрита, трис(гидроксиэтил)изоцианурата, N,N′-бис(гидроксиэтил)оксамида, 3-тиаундеканола, 3-тиапентадеканола, триметилгександиола, триметилолпропана, 4-гидроксиметил-1-фосфа-2,6,7-триоксабицикло[2.2.2]октана.
1.16. Амиды β-(3,5-дитрет-бутил-4-гидроксифенил)пропионовой кислоты, например N,N′-бис(3,5-дитрет-бутил-4-гидроксифенилпропионил)гексаметилендиамид,
N,N′-бис(3,5-дитрет-бутил-4-гидроксифенилпропионил)триметилендиамид, N,N′-бис(3, 5-дитрет-бутил-4-гидроксифенилпропионил)гидразид, N,N′-бис[2-(3-[3,5-дитрет-бутил-4-гидроксифенил]пропионилокси)этил]оксамид (продукт Naugard® XL-1, фирма Uniroyal).
1.17. Аскорбиновая кислота (витамин С)
1.18. Аминовые антиоксиданты. например N,N′-диизопропил-п-фенилендиамин, N,N′-дивтор-бутил-п-фенилендиамин, N,N′ -бис(1,4-диметилпентил)-п-фенилендиамин, N,N′-бис(1-этил-3-метилпентил)-п-фенилендиамин, N,N′-бис(1-метилгептил)-п-фенилендиамин, N,N′-дициклогексил-п-фенилендиамин, N,N′ -дифенил-п-фенилендиамин, N,N′-ди(2-нафтил)-п-фенилендиамин, N-изопропил-N′-фенил-п-фенилендиамин, N-(1,3-диметилбутил)-N′-фенил-п-фенилендиамин, N-(1-метилгептил)-N′ -фенил-п-фенилендиамин, N-циклогексил-N′-фенил-п-фенилендиамин, 4-(п-толуолсульфонамидо)дифениламин, N,N′-диметил-N,N′-дивтор-бутил-п-фенилендиамин, дифениламин, N-аллилдифениламин, 4-изопропоксидифениламин, N-фенил-1 -нафтиламин, N-(4-трет-октилфенил)-1-нафтиламин, N-фенил-2-нафтиламин, октилированный дифениламин, например п,п′-дитрет-октилдифениламин, 4-н-бутиламинофенол, 4-бутириламинофенол, 4-нонаноиламинофенол, 4-додеканоиламинофенол, 4-октадеканоиламинофенол, ди(4-метоксифенил)амин, 2,6-дитрет-бутил-4-диметиламинометилфенол, 2,4′ -диаминодифенилметан, 4,4′-диаминодифенилметан, N,N,N′,N′-тетраметил-4,4′-диаминодифенилметан, 1,2-ди[(2-метилфенил)амино]этан, 1,2-бис(фениламино)пропан, (о-толил)дигуанид, ди[4-(1′,3′-диметилбутил)фенил]амин, трет-октилированный N-фенил-1-нафтиламин, смесь моноалкилированных и диалкилированных трет-бутил/трет-октилдифениламинов, смесь моноалкилированных и диалкилированных нонилдифениламинов, смесь моноалкилированных и диалкилированных додецилдифениламинов, смесь моноалкилированных и диалкилированных изопропил/изогексилдифениламинов, смеси моноалкилированных и диалкилированных трет-бутилдифениламинов, 2,3-дигидро-3,3-диметил-4Н-1,4-бензотиазин, фенотиазин, смесь моноалкилированных и диалкилированных трет-бутил/трет-октилфенотиазинов, смесь моноалкилированных и диалкилированных трет-октилфенотиазинов, N-аллилфенотиазин, N,N,N′,N′-тетрафенил-1,4-диаминобут-2-ен, N,N-бис(2,2,6,6-тетраметилпиперид-4-ил)гексаметилендиамин, бис(2,2,6,6-тетраметилпиперид-4-ил)себацат, 2,2,6,6-тетраметилпиперидин-4-он, 2,2,6,6-тетраметилпиперидин-4-ол.
2. Поглотители УФ-лучей и светостабилизаторы
2.1. 2-(2′-гидроксифенил)бензотриазолы, 2-(2′-гидрокси-5′-метилфенил)-бензотриазол, например 2-(3′,5′-дитрет-бутил-2′-гидроксифенил)бензотриазол, 2-(5′ -трет-бутил-2′-гидроксифенил)бензотриазол, 2-(2′-гидрокси-5′-(1,1,3,3-тетраметилбутил)фенил)бензотриазол, 2-(3′,5′-дитрет-бутил-2′ -гидроксифенил)-5-хлорбензотриазол, 2-(3′-трет-бутил-2′-гидрокси-5′-метилфенил)-5-хлорбензотриазол, 2-(3′-втор-бутил-5′-трет-бутил-2′ -гидроксифенил)бензотриазол, 2-(2′-гидрокси-4′-октоксифенил)бензотриазол, 2-(3′,5′-дитрет-амил-2′-гидроксифенил)бензотриазол, 2-(3′,5′-бис(α, α-диметилбензил)-2′-гидроксифенил)бензотриазол, 2-(3′-трет-бутил-2′-гидрокси-5′-(2-октилоксикарбонилэтил)фенил)-5-хлорбензотриазол, 2-(3′-трет-бутил-5′ -[2-(2-этилгексилокси)карбонилэтил]-2′-гидроксифенил)-5-хлорбензотриазол, 2-(3′-трет-бутил-2′-гидрокси-5′-(2-метоксикарбонилэтил)фенил)-5-хлорбензотриазол, 2-(3′ -трет-бутил-2′-гидрокси-5′-(2-метоксикарбонилэтил)фенил)бензотриазол, 2-(3′-трет-бутил-2′-гидрокси-5′-(2-октилоксикарбонилэтил)фенил)бензотриазол, 2-(3′ -трет-бутил-5′-[2-(2-этилгексилокси)карбонилэтил]-2′-гидроксифенил)бензотриазол, 2-(3′-додецил-2′-гидрокси-5′-метилфенил)бензотриазол, 2-(3′ -трет-бутил-2′-гидрокси-5′-(2-изооктилоксикарбонилэтил)фенил)бензотриазол, 2,2'-метиленбис[4-(1,1,3,3-тетраметилбутил)-6-бензотриазол-2-илфенол]; продукт переэтерификации 2-[3′ -трет-бутил-5′-(2-метоксикарбонилэтил)-2′-гидроксифенил]бензотриазола полиэтиленгликолем 300; [R-СН2СН2-СОО-СН2СН2-]2-, где R обозначает 3′-трет-бутил-4′-гидрокси-5′-2H-бензотриазол-2-илфенил, 2-[2′-гидрокси-3′-(α,α- диметилбензил)-5′-(1,1,3, 3-тетраметилбутил)фенил]бензотриазол; 2-[2′-гидрокси-3′-(1,1,3,3-тетраметилбутил)-5′-(α,α-диметилбензил)фенил]бензотриазол.
2.2. 2-гидроксибензофеноны. например 4-гидрокси-, 4-метокси-, 4-октилокси-, 4-децилокси-, 4-додецилокси-, 4-бензилокси-, 4,2′,4′-тригидрокси- и 2′-гидрокси-4,4′ -диметоксипроизводные.
2.3. Эфиры замещенных и незамещенных бензойных кислот, например 4-трет-бутилфенилсалицилат, фенилсалицилат, октилфенилсалицилат, дибензоилрезорцин, бис(4-трет-бутилбензоил)резорцин, бензоилрезорцин, 2,4-дитрет-бутилфенил-3,5-дитрет-бутил-4-гидроксибензоат, гексадецил-3,5-дитрет-бутил-4-гидроксибензоат, октадецил-3,5-дитрет-бутил-4-гидроксибензоат, 2-метил-4,6-дитрет-бутилфенил-3,5-дитрет-бутил-4-гидроксибензоат.
2.4. Акрилаты. например этил- и изооктил-α-циано-β,β-дифенилакрилат, метил-α -карбометоксициннамат, метил или бутил-α-циано-β-метил-п-метоксициннамат, метил-α-карбометокси-п-метоксициннамат и N-(β-карбометокси-β-циановинил)-2-метилиндолин.
2.5. Соединения никеля, например никелевые комплексы бис[5-(1,1,3,3-тетраметилбутил)-2-гидроксифенил]тиоэфира, такие, как, например, комплекс с соотношением 1:1 или 1:2, совместно или без дополнительных лигандов, таких, как н-бутиламин, триэтаноламин и N-циклогексилдиэтаноламин, дибутилдитиокарбамат никеля, никелевые соли моноалкил-4-гидрокси-3,5-дитрет-бутилбензилфосфонатов, например метилового или этилового эфира, никелевые комплексы кетоксимов, например 2-гидрокси-4-метилфенилундецилкетоксима, никелевые комплексы 1-фенил-4-лауроил-5-гидроксипиразола совместно или без дополнительных лигандов.
2.6. Пространственно затрудненные амины, например бис(2,2,6,6-тетраметилпиперидин-4-ил)себацат, бис(2,2,6,6-тетраметилпиперидин-4-ил)сукцинат, бис(1,2,2,6, 6-пентаметилпиперидин-4-ил)себацат, бис(1-октилокси-2,2,6,6-тетраметилпиперидин-4-ил)себацат, бис(1,2,2,6,6-пентаметилпиперидил)-н-бутил-3,5-дитрет-бутил-4-гидроксибензилмалонат, продукт реакции конденсации 1-(2-гидроксиэтил)-2,2,6,6-тетраметил-4-гидроксипиперидина и янтарной кислоты, линейные или циклические продукты реакции конденсации N,N′-бис(2,2,6, 6-тетраметил-4-пиперидил)гексаметилендиамина и 4-трет-октиламино-2,6-дихлор-1,3,5-симм.триазина, трис(2,2,6,6-тетраметил-4-пиперидил)нитрилтриацетат, тетракис(2,2,6,6-тетраметил-4-пиперидил)-1,2,3, 4-бутантетраоат, 1,1′-(1,2-этандиил)-бис(3,3,5,5-тетраметилпиперазинон), 4-бензоил-2,2,6,6-тетраметилпиперидин, 4-стеарилокси-2,2,6,6-тетраметилпиперидин, бис(1,2,2,6, 6-пентаметилпиперидил)-2-н-бутил-2-(2-гидрокси-3,5-дитрет-бутилбензил)малонат, 3-н-октил-7,7,9,9-тетраметил-1,3,8-триазаспиро[4.5]декан-2,4-дион, бис(1-октилокси-2,2,6,6-тетраметилпиперидил)-себацат, бис(1-октилокси-2,2,6,6-тетраметилпиперидил)сукцинат, линейные или циклические продукты реакции конденсации N,′N′-бис(2,2,6,6-тетраметил-4-пиперидил)гексаметилендиамина и 4-морфолино-2, 6-дихлор-1,3,5-триазина, продукт реакции конденсации 2-хлор-4,6-ди(4-н-бутиламино-2,2,6,6-тетраметилпиперидил)-1,3,5-триазина и 1,2-бис(3-аминопропиламино)этана, продукт реакции конденсации 2-хлор-4, 6-ди(4-н-бутиламино-1,2,2,6,6-пентаметилпиперидил)-1,3,5-триазина и 1,2-бис(3-аминопропиламино)этана, 8-ацетил-3-додецил-7,7,9,9-тетраметил-1,3,8-триазаспиро[4.5]декан-2,4-дион, 3-додецил-1-(2,2,6, 6-тетраметил-4-пиперидил)пирролидин-2,5-дион, 3-додецил-1-(1,2,2,6,6-пентаметил-4-пиперидил)пирролидин-2,5-дион, смесь 4-гексадецилокси 4-стеарилокси-2,2,6,6-тетраметилпиперидинов, продукт реакции конденсации N,N′-бис(2,2,6,6-тетраметил-4-пиперидил)гексаметилендиамина и 4-циклогексиламино-2,6-дихлор-1,3,5-триазина, продукт реакции конденсации 1,2-бис(3-аминопропиламино)этана и 2,4, 6-трихлор-1,3,5-триазина, равно как и 4-бутиламино-2,2,6,6-тетраметилпиперидин (CAS регистрационный № [136504-96-6]); N-(2,2,6,6-тетраметил-4-пиперидил)-н-додецилсукцинимид, N-(1,2,2,6, 6-пентаметил-4-пиперидил)-н-додецилсукцинимид, 2-ундецил-7,7,9,9-тетраметил-1-окса-3,8-диаза-4-оксоспиро[4.5]декан, продукт взаимодействия 7,7,9,9-тетраметил-2-циклоундецил-1-окса-3, 8-диаза-4-оксоспиро[4.5]декана и эпихлоргидрина, 1,1-бис(1,2,2,6,6-пентаметил-4-пиперидилоксикарбонил)-2-(4-метоксифенил)этен, N,N′-бисформил-N,N′-бис(2,2,6, 6-тетраметил-4-пиперидил)гексаметилендиамин, диэфир 4-метоксиметиленмалоновой кислоты и 1,2,2,6,6-пентаметил-4-гидроксипиперидина, поли[метилпропил-3-окси-4-(2,2,6,6-тетраметил-4-пиперидил)]силоксан, продукт взаимодействия сополимера ангидрида малеиновой кислоты/α-олефина с 2,2,6,6-тетраметил-4-аминопиперидином или 1,2,2,6,6-пентаметил-4-аминопиперидином.
2.7. Оксамиды, например 4,4′-диоктилоксиоксанилид, 2,2′-диэтоксиоксанилид, 2,2′-диоктилокси-5,5′-дитрет-бутоксанилид, 2,2′-дидодецилокси-5,5′-дитрет-бутоксанилид, 2-этокси-2′-этилоксанилид, N,N′-бис(3-диметиламинопропил)оксамид, 2-этокси-5-трет-бутил-2′-этоксанилид и его смесь с 2-этокси-2′-этил-5,4′-дитрет-бутоксанилидом, смеси о- и п-метокси- и о- и п-этоксидизамещенных оксанилидов.
2.8. 2-(2-гидроксифенил)-1,3,5-триазины, например 2,4,6-трис(2-гидрокси-4-октилоксифенил)-1,3,5-триазин, 2-(2-гидрокси-4-октилоксифенил)-4,6-бис(2,4-диметилфенил)-1,3,5-триазин, 2-(2,4-дигидроксифенил)-4,6-бис(2,4-диметилфенил)-1,3,5-триазин, 2,4-бис(2-гидрокси-4-пропилоксифенил)-6-(2,4-диметилфенил)-1,3, 5-триазин, 2-(2-гидрокси-4-октилоксифенил)-4,6-бис(4-метилфенил)-1,3,5-триазин, 2-(2-гидрокси-4-додецилоксифенил)-4,6-бис(2,4-диметилфенил)-1,3,5-триазин, 2-(2-гидрокси-4-тридецилоксифенил)-4,6-бис(2, 4-диметилфенил)-1,3,5-триазин, 2-[2-гидрокси-4-(2-гидрокси-3-бутилоксипропилокси)фенил]-4,6-бис(2,4-диметилфенил)-1,3,5-триазин, 2-[2-гидрокси-4-(2-гидрокси-3-октилоксипропилокси)фенил]-4,6-бис(2, 4-диметил)фенил-1,3,5-триазин, 2-[4-(додецилокси/тридецилокси-2-гидроксипропокси)-2-гидроксифенил]-4,6-бис(2,4-диметилфенил)-1,3,5-триазины, 2-[2-гидрокси-4-(2-гидрокси-3-додецилоксипропокси)фенил]-4, 6-бис(2,4-диметилфенил)-1,3,5-триазин, 2-(2-гидрокси-4-гексилокси)фенил-4,6-дифенил-1,3,5-триазин, 2-(2-гидрокси-4-метоксифенил)-4,6-дифенил-1,3,5-триазин, 2,4, 6-трис[2-гидрокси-4-(3-бутокси-2-гидроксипропокси)фенил]-1,3,5-триазин, 2-(2-гидроксифенил)-4-(4-метоксифенил)-6-фенил-1,3,5-триазин, 2-{2-гидрокси-4-[3-(2-этилгексил-1-окси)-2-гидроксипропилокси]фенил}-4,6-бис(2,4-диметилфенил)-1,3,5-триазин.
3. Дезактиваторы металлов, например N,N′-дифенилоксамид, N-салицилал-N′-салицилоилгидразин, N,N′-бис(салицилоил)гидразин, N,N′-бис(3,5-дитрет-бутил-4-гидроксифенилпропионил)гидразин, 3-салицилоиламино-1,2,4-триазол, бис(бензилиденгидразид) щавелевой кислоты, оксанилид, дигидразид изофталевой кислоты, бисфенилгидразид себациновой кислоты, N,N′-диацетилдигидразид адипиновой кислоты, N,N′ -бис(салицилоилгидразид) щавелевой кислоты, N,N′-бис(салицилоилгидразид) тиопропионовой кислоты.
4. Фосфиты и фосфониты, например трифенилфосфит, дифенилалкилфосфиты, фенилдиалкилфосфиты, трис(нонилфенил)фосфит, трилаурилфосфит, триоктадецилфосфит, дистеарилпентаэритритилфосфит, трис(2,4-дитрет-бутилфенил)фосфит, диизодецилпентаэритритилдифосфит, бис(2, 4-дитрет-бутилфенил)пентаэритритилдифосфит, бис(2,6-дитрет-бутил-4-метилфенил)пентаэритритилдифосфит, бисизодецилоксипентаэритритилдифосфит, бис(2,4-дитрет-бутил-6-метилфенил)пентаэритритилдифосфит, бис(2,4,6-тритрет-бутилфенил)пентаэритритилдифосфит, тристеарилсорбитилтрифосфит, тетракис(2,4-дитрет-бутилфенил)-4,4′-дифенилендифосфонит, 6-изооктилокси-2,4,8,10-тетратрет-бутил-12Н-дибензо[d, g]-1,3,2-диоксафосфоцин, 6-фтор-2,4,8,10-тетратрет-бутил-12-метилдибензо[d,g]-1,3,2-диоксафосфоцин, бис(2,4-дитрет-бутил-6-метилфенил)метилфосфит, бис(2,4-дитрет-бутил-6-метилфенил)этилфосфит, 2, 2′,2′′-нитрил[триэтилтрис(3,3′,5,5′-тетратрет-бутил-1,1′-дифенил-2,2′-диил)фосфит], 2-этилгексил(3,3′,5,5′-тетратрет-бутил-1,1′ -дифенил-2,2′-диил)фосфит.
5. Гидроксиламины. например N,N-дибензилгидроксиламин, N,N-диэтилгидроксиламин, N,N-диоктилгидроксиламин, N,N-дилаурилгидроксиламин, N, N-дитетрадецилгидроксиламин, N,N-дигексадецилгидроксиламин, N,N-диоктадецилгидроксиламин, N-гексадецил-N-октадецилгидроксиламин, N-гептадецил-N-октадецилгидроксиламин, N,N-диалкилгидроксиламин, дериватизированный из аминов гидрированного таллового масла.
6. Нитроны, например N-бензил-α-фенилнитрон, N-этил-α-метилнитрон, N-октил-α-гептилнитрон, N-лаурил-α-ундецилнитрон, N-тетрадецил-α-тридецилнитрон, N-гексадецил-α-пентадецилнитрон, N-октадецил-α-гептадецилнитрон, N-гексадецил-α-гептадецилнитрон, N-октадецил-α-пентадецилнитрон, N-гептадецил-α-гептадецилнитрон, N-октадецил-α-гексадецилнитрон, нитроны, дериватизированные из N,N-диалкилгидроксиламинов, дериватизированных из аминов гидрированного таллового масла.
7. Тиосинергисты, например дилаурилтиодипропионат или дистеарилтиодипропионат.
8. Полиамидные стабилизаторы, например соли меди в сочетании с иодидами и/или соединениями фосфора и солями двухвалентного марганца.
9. Основные совместно используемые стабилизаторы, например меламин, поливинилпирролидинон, дициандиамид, триаллилцианурат, мочевиновые производные, гидразиновые производные, амины, полиамиды, полиуретаны, соли щелочных металлов и соли щелочно-земельных металлов высших жирных кислот, в частности стеарат кальция, стеарат цинка, бегенат магния, стеарат магния, рицинолеат натрия, пальмитат калия, катехолат сурьмы и катехолат цинка.
10. Зародыши кристаллизации, например неорганические вещества, такие, как тальк, оксиды металлов, такие, как диоксид титана и оксид магния, фосфаты, карбонаты и сульфаты, предпочтительно щелочно-земельных металлов; органические соединения, такие, как монокарбоновые и поликарбоновые кислоты и их соли, например 4-трет-бутилбензойная кислота, адипиновая кислота, дифенилуксусная кислота, сукцинат натрия и бензоат натрия; полимерные соединения, такие, как ионогенные сополимеры (иономеры).
11. Наполнители и армирующие наполнители, например карбонат кальция, силикаты, стекловолокно, полый стеклянный бисер, тальк, каолин, слюда, сульфат бария, оксиды и гидроксиды металлов, углеродная сажа, графит, древесная мука и мука или волокна других природных продуктов, синтетические волокна.
12. Другие добавки, например пластификаторы, смазки, эмульгаторы, пигменты, модификаторы реологических свойств, катализаторы, выравнивающие средства, оптические отбеливатели, антипирены, антистатики и газообразующие средства.
13. Бензофураноны и индолиноны. например те, которые представлены в US 4325863, US 4338244, US 5175312, US 5216052, US 5252643, DE-A 4316611, DE-A 4316622, DE-A 4316876, ЕР-А 0589839 или ЕР-А 0591102, или 3-[4-(2-ацетоксиэтокси)фенил]-5,7-дитрет-бутилбензофуран-2-он, 5,7-дитрет-бутил-3-[4-(2-стеароилоксиэтокси)фенил]бензофуран-2-он, 3,3′-бис[5, 7-дитрет-бутил-3-(4-[2-гидроксиэтокси]фенил)бензофуран-2-он], 5,7-дитрет-бутил-3-(4-этоксифенил)бензофуран-2-он, 3-(4-ацетокси-3,5-диметилфенил)-5,7-дитрет-бутилбензофуран-2-он, 3-(3, 5-диметил-4-пивалоилоксифенил)-5,7-дитрет-бутилбензофуран-2-он, 3-(3,4-диметилфенил)-5,7-дитрет-бутилбензофуран-2-он, 3-(2,3-диметилфенил)-5,7-дитрет-бутилбензофуран-2-он.
В конкретном варианте выполнения изобретения подвергаемый деструкции полимер получают с добавлением вышеописанных гидроксиламиновых сложных эфиров (I) совместно с выбранными антиоксидантами и технологическими стабилизаторами или их смесями. Примерами предпочтительных соединений являются: пентаэритритилтетракис(3-(3,5-дитрет-бутил-4-гидроксифенил)пропионат) (продукт IRGANOX® 1010), октадецил(3-(3,5-дитрет-бутил-4-гидроксифенил)пропионат) (продукт IRGANOX 1076), 3,3′,3′,5,5′,5′-гексатрет-бутил-α,α′,α′-(мезитилен-2,4, 6-триил)три-п-крезол (продукт IRGANOX 1330), диэтилбис(((3,5-бис(1,1-диметилэтил)-4-гидроксифенил)метил)фосфонат) кальция (продукт IRGANOX 1425), 1,3,5-трис(3,5-дитрет-бутил-4-гидроксибензил)-1,3, 5-триазин-2,4,6-(1Н,3Н,5Н)трион (продукт IRGANOX 3114);
трис(2,4-дитрет-бутилфенил)фосфит (продукт Irgafos® 168), трис(нонилфенил)фосфит, тетракис(2, 4-дитрет-бутилфенил)-[1,1-дифенил]-4,4′-диилбисфосфонит (продукт IRGANOX P-EPQ), а также фосфиты следующего строения:
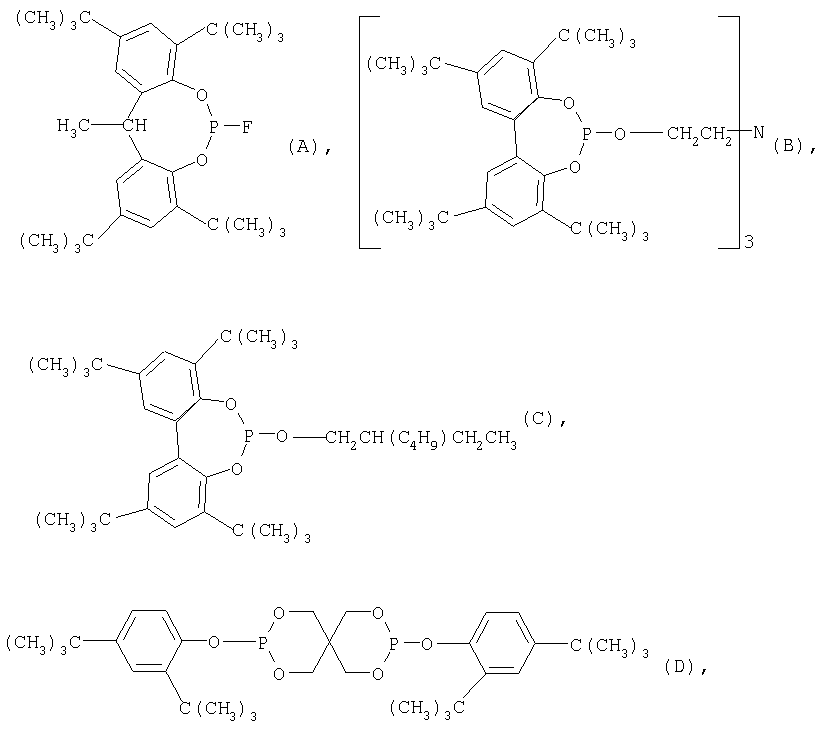
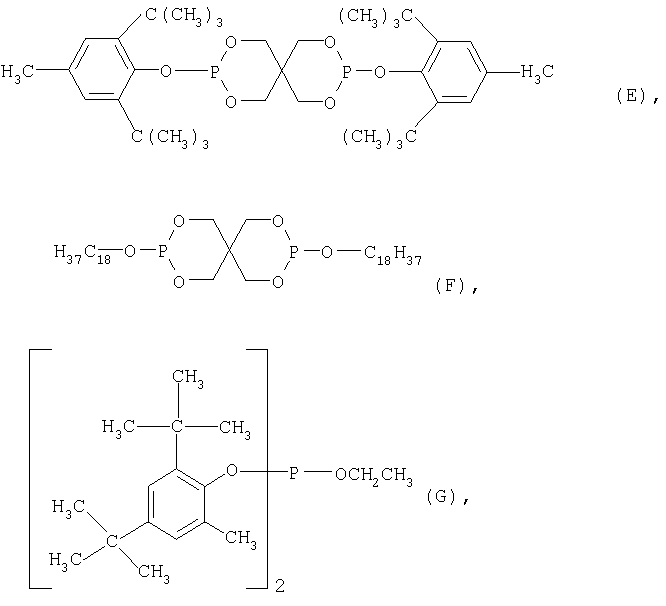
дидодецил-3,3′-тиодипропионат (продукт IRGANOX PS 800), диоктадецил-3,3′-тиодипропионат (продукт IRGANOX PS 802);
5,7-дитрет-бутил-3-(3,4-диметилфенил)-3Н-бензофуран-2-он (продукт IRGANOX® HP 136) и дистеарилгидроксиламин (продукт Irgastab® FS 042).
Другими добавками, которые можно упомянуть, являются антикислоты, такие, как стеарат кальция и стеарат цинка, гидроталькиты, лактат кальция и лактилат кальция фирмы Patco (торговое наименование Pationic).
В конкретном варианте в подвергаемые деструкции полимеры в дополнение к гидроксиламиновым сложным эфирам (I) можно добавлять другие источники свободных радикалов, например подходящее бисазосоединение, пероксид или гидропероксид.
Приемлемыми бисазосоединениями являются технически доступные продукты, например 2,2′-азобисизобутиронитрил, 2,2′-азобис(2-метилбутиронитрил), 2,2′-азобис(2,4-диметилвалеронитрил), 2, 2'-азобис(4-метокси-2,4-диметилвалеронитрил), 1,1′-азобис(1-циклогексанкарбонитрил), дигидрат 2,2′-азобис(изобутирамида), 2-фенилазо-2,4-диметил-4-метоксивалеронитрил, диметил-2,2′ -азобисизобутират, 2-(карбамоилазо)изобутиронитрил, 2,2′-азобис(2,4,4-триметилпентан), 2,2′- азобис(2-метилпропан), 2,2′-азобис(N,N′-диметиленизобутирамидин) в форме свободного основания или гидрохлорида, 2,2′-азобис(2-амидинопропан) в форме свободного основания или гидрохлорида, 2,2′-азобис{2-метил-N-[1,1-бис(гидроксиметил)этил]пропионамид} или 2, 2′-азобис{2-метил-N-[1,1-бис(гидроксиметил)-2-гидроксиэтил]пропионамид}.
Подходящими пероксидами и гидропероксидами являются технически доступные продукты, например пероксид ацетилциклогексансульфонила, диизопропилпероксидикарбонат, трет-амилпернеодеканоат, трет-бутилпернеодеканоат, трет-бутилперпивалат, трет-амилперпивалат, бис(2,4-дихлорбензоил)пероксид, пероксид диизононаноила, пероксид дидеканоила, пероксид диоктаноила, пероксид дилауроила, бис(2-метилбензоил)пероксид, пероксид дисукциноила, диацетилпероксид, дибензоилпероксид, пер-2-этилгексаноат трет-бутила, бис(4-хлорбензоил)пероксид, трет-бутилперизобутират, трет-бутилпермалеат, 1,1-бис(трет-бутилперокси)-3,5,5-триметилциклогексан, 1,1-бис(трет-бутилперокси)циклогексан, трет-бутилпероксиизопропилкарбонат, трет-бутилперизононаоат, 2,5-диметилгексан-2,5-дибензоат, трет-бутилперацетат, трет-амилпербензоат, трет-бутилпербензоат, 2,2-бис(трет-бутилперокси)бутан, 2, 2-бис(трет-бутилперокси)пропан, пероксид дикуменила, 2,5-диметилгексан-2,5-дитрет-бутилпероксид, 3-трет-бутилперокси-3-фенилфталид, пероксид дитрет-амила, α,α′ -бис(трет-бутилпероксиизопропил)бензол, 3,5-бис(трет-бутилперокси)-3,5-диметил-1,2-диоксолан, пероксид дитрет-бутила, пероксид 2,5-диметилгексин-2,5-дитрет-бутила, 3,3,6,6,9,9-гексаметил-1,2,4, 5-тетраоксациклононан, гидропероксид п-ментана, гидропероксид пинана, диизопропилбензолмоно-α-гидропероксид, гидропероксид кумола или гидропероксид трет-бутила.
Вышеупомянутые бисазосоединения, пероксиды и гидропероксиды добавляют в подвергаемые деструкции полимеры в количествах, которые меньше тех, в которых их обычно используют по отдельности в известных в данной области техники способах.
В другом предпочтительном варианте выполнения настоящего изобретения используют по меньшей мере 2 инициатора свободно-радикальной полимеризации, которые характеризуются разной температурой разложения, благодаря чему деструкция полимеров может протекать в 2 стадии. Этот метод называют также последовательной деструкцией.
Приемлемые композиции включают, например, инициаторы свободно-радикальной полимеризации по изобретению и вышеупомянутые пероксиды или сочетание NOR-соединений, описанных в WO 97/49737, и гидроксиламиновых сложных эфиров (I), описанных выше.
Существенное значение имеет то, что обе температуры разложения разнятся в достаточной мере для того, чтобы обусловить 2-стадийный процесс. Так, например, пероксид, температура разложения которого находится в интервале примерно от 189 до 220°С, можно сочетать с гидроксиламиновым сложным эфиром (I), температура разложения которого находится в интервале примерно от 240 до 280°С, или гидроксиламиновый сложный эфир (I), температура разложения которого находится в интервале примерно от 240 до 280°С, можно сочетать с NOR-соединением, описанным в WO 97/49737, температура разложения которого превышает 300°С.
Было установлено, что деструкцию целесообразно проводить в присутствии небольших количеств свободных нитроксильных радикалов. Обеспечивается более легко регулируемая деструкция полимера, что приводит к более постоянным характеристикам плавления. Подходящие нитроксильные радикалы известны и описаны в US 4581429 или ЕР-А 621878. Ациклические структуры представлены в WO 99/03894 и WO 00/07981. Более того, NO-производные пиперидинового типа представлены в WO 99/67298 и в описании к патенту Великобритании 2335190. Другие NO-производные гетероциклических соединений представлены в описании к патенту Великобритании 2342649.
При осуществлении предлагаемого способа также возможно, естественно, применение смесей источников свободных радикалов, которые характеризуются разными температурами разложения.
Предпочтительным вариантом выполнения изобретения является способ, в котором добавляют гидроксиламиновый сложный эфир (Ia), у которого
Ra обозначает ацильный радикал, выбранный из группы, включающей -С(=O)-С1-С19алкил, трифторацетил, бензоил, -С(=O)-O-С1-С6алкил, С1-С6алкилкарбамоил и фенилкарбамоил;
R1-R4 каждый обозначает С1-С6алкил;
R5 и R6 каждый независимо друг от друга обозначает водородный атом или С1-С6алкил;
Q обозначает двухвалентный радикал -(CR7R8)-, где каждый из R7 и R8обозначает водородный атом; а
Z1 обозначает двухвалентный радикал -(CR12R13)-, где независимо друг от друга один из радикалов R12 и R13 представляет собой водородный атом, а другой представляет собой этерифицированный с образованием простого или сложного эфира гидроксил, выбранный из ряда, включающего С1-С6алкокси, бензоилокси, -O-С(=O)-С1-С19алкил, трифторацетокси, С1-С6алкилкарбамоилокси и фенилкарбамоилокси.
В этом предпочтительном варианте каждый из R1-R4 обозначает С1 -С6алкил, предпочтительно метил или этил.
R5 и R6 имеют значения, указанные выше в разделе а).
Q обозначает двухвалентный радикал -(CR7R8)- с водородным атомом в качестве значения для R7 и R8.
Z1 обозначает двухвалентный радикал -(CR12R13 )-, где один из радикалов R12 и R13 представляет собой водородный атом, а другой представляет собой этерифицированный с образованием простого или сложного эфира гидроксил, выбранный из ряда, включающего С1-С6алкокси, например метокси, этокси или н-пропокси, бензоилокси, -O-С(=O)-С1-С19алкил, например трет-бутоксикарбонилокси, трифторацетокси, С1-С6алкилкарбамоилокси и фенилкарбамоилокси.
В основе этого предпочтительного варианта лежит способ применения гидроксиламиновых сложных эфиров (Ia), у которых Ra обозначает, в частности, ацильный радикал, выбранный из ряда, включающего -С(=O)-С1-С19алкил, например ацетил, пивалоил или стеароил, трифторацетил, бензоил, -С(=O)-O-С1-С6алкил, например трет-бутоксикарбонил, С1-С6алкилкарбамоил, например этилкарбамоил,и фенилкарбамоил.
В еще одном предпочтительном варианте осуществления предлагаемого способа предусмотрено применение соединений вышеописанной формулы IC, в которой n обозначает 1:

где Ra, R1′, R2′ и R3′ имеют значения, указанные в описании формулы IA, а G3 обозначает С2-С8алкилен, например этилен или 2,2-диметилпропилен, или 2,2-диэтилпропилен, или С4-С22ацилоксиалкилен, например 1-ацетокси-2,3-пропилен, 2-С2-С18алканоилоксиметил-2-этилпропилен, например 2-ацетоксиметил-2-этилпропилен или 2-пальмитоилоксиметил-2-этилпропилен. Подходящие соединения формулы IC′ отвечают следующим структурным формулам:
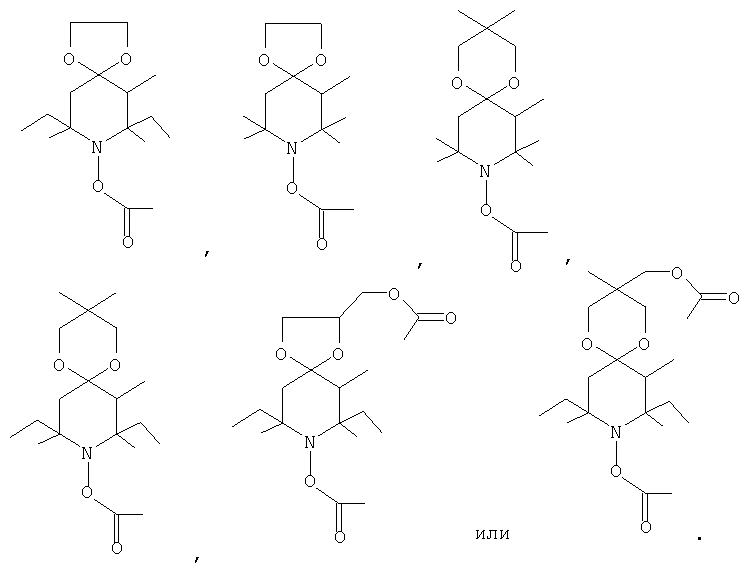
Особенно предпочтительный вариант заключается в способе уменьшения молекулярной массы полипропилена, пропиленовых сополимеров или полипропиленовых смесей, в котором в них добавляют по меньшей мере одно из вышеупомянутых новых соединений от а) до г) и смесь нагревают до температур ниже 280°С.
По изобретению далее предлагается способ достижения регулируемого увеличения молекулярной массы или сшивания полиэтиленов, например полиэтилена низкой плотности (ПЭНП), полиэтилена средней плотности (ПЭСП), линейного полиэтилена низкой плотности (ЛПЭНП), разветвленного полиэтилена низкой плотности (РПЭНП) или полиэтиленов, полученных с использованием катализаторов фирмы Phillips, или полиэтиленовых смесей с полипропиленом, пропиленовых сополимеров или полипропиленовых смесей как с применением вышеописанных новых соединений, так и с применением также известных гидроксиламиновых сложных эфиров (I), у которых гидроксильные группы этерифицируют вышеупомянутыми ацильными радикалами Ra.
Еще одно ценное свойство гидроксиламиновых сложных эфиров (I), которые могут быть использованы в технологии переработки, заключается в их приемлемости для сшивания полиэтилена. Полиолефиновые продукты высокомолекулярных сортов, которые требуются для изготовления труб и кабелей, синтезируют главным образом сшиванием с использованием пероксидов / см. Н.Domininghaus, Die Kunststoffe und ihre Etgenschaften, Springer-Verlag, Berlin, издание 5-е, 1998, глава 2.1.1, сс.156-159], например по способу Engel: экструзия с помощью поршневого экструдера; способу Sioplas: инициированная пероксидом привитая сополимеризация винилсиланов и последующее сшивание посредством воды. Если целевые параметры, например вязкость расплава, задают посредством стадии переработки полимера, то для успешной реакции существенное значение имеют регулируемая реакционная способность и разновидность действия вводимых добавок/систем добавок. В то время как вещества для улучшения технологических свойств, например полиэтиленовые воски, фторированные полимеры, металлические мыла, эфиры жирных кислот и т.д., и наполнители существенного влияния на молекулярную массу и, следовательно, на технологические свойства полимеров не оказывают, реакции сшивания с пероксидами, множество ненасыщенных олефинов или ненасыщенных полимеров обычно обуславливают технологические проблемы, например очень высокую вязкость расплава, желатинизацию и т.д. (см. изложенное выше). Более того, продукты взаимодействия с пероксидом и остатками пероксидов могут вызвать ухудшение долгосрочной стабильности полимеров. Также важную роль играют аспекты безопасности при переработке полимеров с добавлением пероксидов.
Таким образом, существует потребность в создании простой в обращении эффективной системы добавок, наличие которой позволяет регулировать сшивание, например задавание целевой вязкости расплава как меры молекулярной массы во время переработки полимеров, и применение которой разрешает проблемы, с которыми сопряжено использование пероксидов в качестве источников свободных радикалов.
Было установлено, что как вышеописанные новые соединения, так и известные гидроксиламиновые сложные эфиры (I), у которых гидроксильные группы этерифицируют указанными ацильными радикалами Ra, приемлемы для достижения регулируемого увеличения молекулярной массы/сшивания полиэтиленов, например полиэтилена низкой плотности (ПЭНП), полиэтилена средней плотности (ПЭСП), линейного полиэтилена низкой плотности (ЛПЭНП), разветвленного полиэтилена низкой плотности (РПЭНП), полиэтиленов, полученных с использованием катализаторов фирмы Phillips, или полиэтиленовых смесей.
В случае сополимеров и тройных сополимеров или сополимерных смесей большие количества этиленовых звеньев обуславливают поведение, аналогичное поведению полиэтилена, в то время как высокое содержание пропиленовых звеньев обуславливает поведение, аналогичное поведению полипропилена. Если вышеупомянутые сополимеры и тройные сополимеры или сополимерные смеси включают некоторые количества звеньев полиненасыщенных олефинов, то с повышением концентрации свободных двойных связей возможность сшивания увеличивается.
Степень сшивания полиэтилена зависит, во-первых, от природы полимера, а во-вторых, от условий переработки (температура) и концентрации используемой добавки. Следствием повышенной концентрации добавки является более высокая степень сшивания.
Способ достижения регулируемого увеличения молекулярной массы полиэтиленов характеризуется тем, что в полиэтилен или полиэтиленовую смесь, молекулярную массу которой необходимо увеличить, добавляют соединение I, как оно представлено выше, в частности соединение (Ia), где
Ra обозначает ацильный радикал, выбранный из группы, включающей -С(=O)-Н, -С(=O)-С1-С19алкил, -С(=O)-С2-С19алкенил, -С(=O)-С2-С4алкенил-С6-С10арил, -С(=O)-С6-С10арил, -С(=O)-O-С1-С6алкил, -С(=O)-O-С6-С10арил, -С(=O)-NH-С1-С6алкил, -С(=O)-NH-С6-С10арил, -С(=O)-N(С1-С6алкил)2, -Р(=O)- С1-С19алкил, -Р(=O)2-С1-С19алкил, -Р(=O)-С6-С10арил, -Р=O(-С1-С19алкил)2, -Р=O(-С1 -С10арил)2, -Р(=O)-O-С1-С6алкил, -Р(=O)-O-С6-С10арил, -P=O(-O-С1-С6алкил)2, -Р=O(-O-С6 -С10арил)2, -Р(-O-С1-С6алкил)2 и -Р(-O-С6-С10арил)2;
R1-R4 каждый обозначает С1-С6алкил;
R5 и R6 каждый независимо друг от друга обозначает водородный атом, С1-С6алкил или С6 -С10арил; или
R5 и R6 совместно обозначают атом кислорода;
Q обозначает прямую связь или двухвалентный радикал -(CR7R8)- или -(CR7R8-CR9R10)-, где
R7, R8, R9 и R10 каждый независимо друг от друга обозначает водородный атом или С1-С6алкил; а
Z1 обозначает атом кислорода или двухвалентный радикал -NR11- или -(CR12R13)-, где
R11 обозначает водородный атом, С1-С6алкил, С6-С10арил или ацильный радикал Ra, имеющий вышеупомянутые значения; или независимо друг от друга R12 и R13 каждый обозначает водородный атом или С1-С6алкил, или один из радикалов R12 и R12 представляет собой водородный атом или С1-С6алкил, а другой представляет собой С1-С6алкил, С1-С6алкокси, арилокси, ацилоксирадикал, выбранный из ряда, включающего -O-С(=O)-Н, -O-С(=O)-С1-С19алкил, -O-С(=O)-С6-С10арил, -О-С(=О)-О-С1-С6алкил, -O-С(=O)-O-С6-С10 арил, -O-С(=O)-NH-С1-С6алкил, -O-С(=O)-NH-С6-С10арил и -O-C(=O)-N(С1-С6алкил)2, С1-С6алкиламино-, ди-С1-С6алкиламино-, С6-С10ариламино-, ациламиновый радикал, выбранный из ряда, включающего -NH-C(=O)-H, -NH-С(=O)-С1-С19алкил, -NH-С(=O)-С6-С10арил, -NH-С(=O)-O-С1-С6алкил, -NH-С(=O)-O-С6-С10арил, -NH-C(=O)-NH-С1-С6алкил, -NH-С(=O)-NH-С6-С10арил и -NH-С(=O)-N(С1-С6алкил)2, диациламиновый радикал, выбранный из ряда, включающего -N[-C(=O)-С1-С19 алкил]2, -N[-С(=O)-С6-С10арил]2, -N[-C(=O)-С1-С6алкилен-С(=O)-], -N[-C(=O)-С2-С6алкенилен-C(=O)-] и фталимидный радикал, или N-ацил-N-С1-С6алкиламиновый радикал; или оба радикала R12 и R13 совместно образуют оксогруппу.
Добавление в этиленовый полимер гидроксиламиновых сложных эфиров (I), включая соединения с IA по IN, как они представлены выше, можно осуществлять во всех обычных смесительных устройствах, в которых полимер плавят и смешивают с добавками. Подходящими устройствами являются те, которые известны специалистам в данной области техники. Ими служат смесители, пластикаторы и экструдеры. В предпочтительном варианте предлагаемый способ осуществляют введением добавки во время переработки в экструдере.
Особенно предпочтительными перерабатывающими устройствами являются одночервячные экструдеры, двухчервячные экструдеры с вращением в одном направлении и с противовращением, экструдеры с планетарными системами шнеков, кольцевые экструдеры и шнековые месильные машины, снабженные по меньшей мере одной секцией для удаления газов, к которой может быть подключена система создания вакуума.
Подходящие экструдеры и пластикаторы описаны, например, помимо прочего, в вышеупомянутой работе Handbuch der Kunststoffextrusion, том 1, сс.3-7.
Если добавляют множество компонентов, их можно предварительно смешивать или добавлять индивидуально.
Полимеры подвергают воздействию повышенной температуры в течение периода времени, достаточного для того, чтобы вызвать необходимую деструкцию. В предпочтительном варианте осуществления способа по настоящему изобретению температурный интервал составляет от примерно 160 до 300°С. В особенно предпочтительном варианте осуществления способа температура находится в интервале от примерно 170 до 280°С, в частности примерно от 180 до 240°С.
Период времени, необходимый для увеличения молекулярной массы или сшивания, можно варьировать в зависимости от температуры, количества материала, молекулярную массу которого необходимо увеличить, и типа любого применяемого экструдера. Обычно он составляет от примерно 10 с до 20 мин, в частности от 20 с до 10 мин.
Вышеописанные гидроксиламиновые сложные эфиры (I) приемлемы для увеличения молекулярной массы разветвленных полиэтиленов и полиэтиленовых смесей во время компаундирования, когда они, подобно пероксидам, которые обычно используют в соответствии в известной технинологией, вызывают сшивание полимерных цепей.
В процессе увеличения молекулярной массы (в процессе сшивания) полиэтиленов гидроксиламиновые сложные эфиры (I) содержатся в концентрациях от примерно 0,01 до 10,0 мас.%, в частности от 0,1 до 5,0 мас.%, предпочтительно от 0,2 до 3,0 мас.%, а особенно предпочтительно от 0,1 до 2,0 мас.%, в пересчете на количество полимера, молекулярную массу которого необходимо увеличить.
Приемлемыми полимерами полиэтиленового типа являются, например, полиэтилен высокой плотности (ПЭВП), полиэтилен высокой плотности с высокой молекулярной массой (ПЭВП-ВММ), полиэтилен высокой плотности со сверхвысокой молекулярной массой (ПЭВП-СВММ), полиэтилен средней плотности (ПЭСП), полиэтилен низкой плотности (ПЭНП), линейный полиэтилен низкой плотности (ЛПЭНП), разветвленный полиэтилен низкой плотности (РПЭНП) и полиэтилены и этиленовые сополимеры, полученные посредством катализаторов фирмы "Филлипс", а также полиэтиленовые смеси. В этом случае этиленовые сополимеры могут включать различные количества сомономерных звеньев. Примерами, которые можно упомянуть, являются 1-олефины, такие, как пропен, 1-бутен, 1-пентен, 1-гексен, 1-гептен, 1-октен и изобутилен, стирол, циклоолефины, такие, как циклопентен, циклогексен и норборнен, и диены, такие, как бутадиен, изопрен, 1,4-гексадиен, циклопентадиен, дициклопентадиен, норборнадиен и этилиденнорборнен.
Полиэтиленовые смеси представляют собой смеси полиэтиленов с другими полиолефинами. Примерами являются смеси полипропилена (ПП), смеси с ПЭ различных типов, в частности с полиэтиленом высокой плотности (ПЭВП), полиэтиленом высокой плотности с высокой молекулярной массой (ПЭВП-ВММ), полиэтиленом высокой плотности со сверхвысокой молекулярной массой (ПЭВП-СВММ), полиэтиленом средней плотности (ПЭСП), полиэтиленом низкой плотности (ПЭНП), линейным полиэтиленом низкой плотности (ЛПЭНП), разветвленным полиэтиленом низкой плотности (РПЭНП), а преимущественно с этилен-пропилен-диеновыми тройными сополимерами (ЭПДМ), содержащими большие количества диеновых звеньев.
Введение в полимеры можно осуществлять, например, подмешиванием вышеописанных новых или известных гидроксиламиновых сложных эфиров (I) или их смесей и, если необходимо, других добавок с применением методов, которые для технологии переработки обычны.
По другому варианту их введение можно производить при температурах, которые еще не вызывают деструкции компаундов, используемых в соответствии с изобретением (латентный компаунд). В дальнейшем полимеры, приготовленные таким путем, можно нагревать во второй раз и подвергать воздействию повышенной температуры в течение периода времени, достаточного для целевого увеличения молекулярной массы (сшивания) полимера.
Предлагаемые соединения можно также добавлять в полимеры, молекулярную массу которых необходимо увеличить, в форме маточной смеси, в которой эти соединения содержатся, в частности, в концентрации от примерно 1 до 25 мас.%. Такая маточная смесь (концентрат) может быть приготовлена при температурах, которые еще не вызывают разложения соединений, используемых в соответствии с изобретением.
В конкретном варианте в полимер, молекулярную массу которого необходимо увеличить, можно вводить добавки и/или стабилизаторы, как они представлены выше применительно к способу деструкции полипропиленов.
В другом конкретном варианте в дополнение к вышеописанным гидроксиламиновым сложным эфирам (I) в полимеры, молекулярную массу которых необходимо увеличить, можно добавлять источник свободных радикалов, например бисазосоединения, пероксиды или гидропероксиды, как они представлены выше применительно к способу деструкции полипропиленов.
Упомянутые бисазосоединения, пероксиды или гидропероксиды добавляют в полимеры, молекулярную массу которых необходимо увеличить, в количествах, которые меньше обычных количеств, когда их используют самостоятельно в соответствии с методами, известными для данной области техники.
Вышеописанные новые соединения можно получать по методу, который известен. Получение этих соединений также составляет объект настоящего изобретения, его можно осуществлять, например, проведением реакции соответствующего гидроксиламина одной из формул:
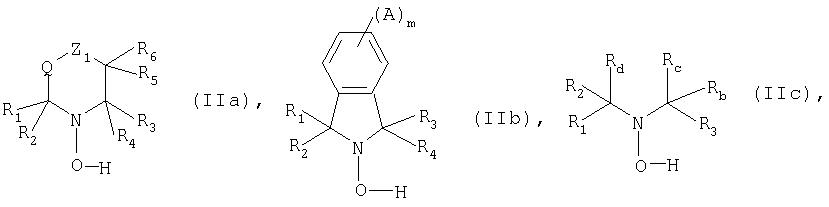
в условиях обычной реакции этерификации с кислотой Ra-H, которая вводит группу Ra и соответствует ацильному радикалу, выбранному, например, из ряда, включающего -С(=O)-Н, -С(=O)-С1-С19алкил, -С(=O)-С2-С19алкенил, -С(=O)-С2-С4алкенил-С6-С10арил, -С(=O)-С6-С10арил, -С(=O)-O-С1-С6алкил, -С(=O)-O-С6-С10арил, -С(=О)-NH-С1-С6алкил, -С(=O)-NH-С6-С10арил и -С(=O)- N(С1-С6алкил)2, или с ее реакционноспособным функциональным производным, например с галоидангидридом кислоты Ra-X, в частности с хлорангидридом кислоты, или ангидридом, в частности с (Ra)2O.
Соединения (Ia), у которых Ra обозначает ацильный радикал, выбранный из ряда, включающего -Р(=O)-С1-С19алкил, -Р(=O)-С6-С10арил, -Р(=O)2-С6-С10арил, -Р=O(-С1-С19алкил)2, -Р=O(-С6 -С10арил)2, -Р(=O)-O-С1-С6алкил, -Р(=O)-O-С6-С10арил, -Р=O(-O-С1-С6алкил)2, -Р=O(-O-С6 -С10арил)2, -Р(-O-С1-С6алкил)2 и -Р(-O-С6-С10арил)2, также могут быть получены этерификацией гидроксиламинов реакционноспособными функциональными производными, например галоидангидридами кислот, соответствующих фосфорсодержащих кислот.
Бициклические соединения Id) могут быть получены, например, реакцией гидроксиламина (IIa) с функциональным производным дикарбоновой кислоты (НООС)2Х, которое способно вводить группу

например с дигалоидангидридом (ХОС)2Х, в частности с оксалилхлоридом (X обозначает 0, прямую связь) или адипоилхлоридом (X обозначает 4).
Вышеописанные исходные материалы для получения новых соединений известны.
Получение известных гидроксиламиновых сложных эфиров (Ia), которые могут быть использованы в способах получения олигомера, соолигомера, полимера или сополимера свободно-радикальной полимеризацией описаны, например, в US 4590231, 5300647, 4831134, 5204473, 5004770, 5096950, 5021478, 5118736, 5021480, 5015683, 5021481, 5019613, 5021486, 5021483, 5145893, 5286865, 5359069, 4983737, 5047489, 5077340, 5021577, 5189086, 5015682, 5015678, 5051511, 5140081, 5204422, 5026750, 5185448, 5180829, 5262538, 5371125, 5216156, 5300544.
Описанная выше сущность изобретения проиллюстрирована следующими примерами.
Примеры
А) получение соединений
А1: N-трет-бутил-N-(1-трет-бутиламинокарбонил-1-метилэтил)гидроксиламиновый эфир уксусной кислоты (101)
5,2 мл (0,055 моля) уксусного ангидрида по каплям добавляют при одновременном охлаждении в раствор 11,5 г (0,05 моля) N-трет-бутил-N-(1-трет-бутиламинокарбонил-1-метилэтил)гидроксиламина, получение которого описано в примере А-2 WO 00/07891, и 0,5 г 4-диметиламинопиридина в 50 мл пиридина. Смесь перемешивают в течение последующих 18 ч при комнатной температуре, затем разбавляют 500 мл воды и экстрагируют 2 порциями по 50 мл трет-бутилметилового эфира. Органическую фазу промывают 5%-ной HCl и водой и сушат над MgSO4. В результате отгонки растворителя в роторном испарителе получают 25,3 г (выход: 93%) соединения 101, которое находится в форме бесцветной жидкости.
Рассч. для C14H28N2O3: 61.73% С, 10,36% Н, 10,28% N; обнаруж.: 61.65% С, 10,37% Н, 10,14% N.
А2: N-трет-бутил-N-(1-трет-бутиламинокарбонил-1-метилэтил)гидроксиламиновый эфир бензойной кислоты (102)
В результате повторения эксперимента примера A1 с использованием бензоилхлорида с достижением 80%-ного выхода получают соединение 102, которое выделяют в форме бесцветных кристаллов; температура плавления: 61-64°С (гексан).
1Н-ЯМР (CBCl3, 300 МГц): 1,27 s (трет-Bu), 1,29 s (Me), 1,39 s (трет-Bu), 1,49 s (Me), 7,45-8,08 m (5 ArH), 7,79 широкий s (NH).
A3: 2,2,5, 5-тетраметил-4-оксоимидазолидин-1-илацетат (103)
44,7 г (0,23 моля) 39%-ной перуксусной кислоты по каплям добавляют в суспензию 28,2 г (0,2 моля) 2,2,5,5-тетраметил-4-оксоимидазолидина [получен так, как описано T.Toda и др.: Bull.Chem.Soc.Japan 44, 3345 (1971)] в 200 мл этилацетата при одновременном охлаждении льдом. Суспензию перемешивают в течение последующих 20 ч при комнатной температуре и затем фильтруют. Фильтровальный пирог промывают небольшим количеством этилацетата и сушат. В результате в виде белого порошка получают 18,9 г 1-гидрокси-2,2,5, 5-тетраметил-4-оксоимидазолидина; температура плавления: 240-245°С; MS (EI): m/e=158 (M+).
С использованием этого гидроксиламинового соединения в эксперименте, который в других отношениях аналогичен получению соединения 101, с достижением 84%-ного выхода выделяют указанное в заглавии соединение 103, которое получают в форме бесцветных кристаллов; температура плавления: 188-190°С (дихлорметан/гексан).
Рассч. для C9H16N2O3: 53,99% С, 8,05% Н, 13,99% N; обнаруж.: 54,37% С, 7,90% Н, 13,90% N.
А4: 1,1,3,3-тетраметил-1,3-дигидроизоиндол-2-ил-2,4,6-триметилбензоат (104)
6,6 г (0,035 моля) 1,1,3,3-тетраметил-1,3-дигидроизоиндол-N-оксида гидрируют под атмосферным давлением до насыщения в 66 мл этанола над 0,12 г PtO2. Катализатор отфильтровывают, а растворитель выпаривают в роторном испарителе, после чего кристаллический остаток перекристаллизовывают из небольшого количества дихлорметана. В результате этого получают 5,2 г (выход: 78%) N-гидрокси-1,1,3,3-тетраметил-1,3-дигидроизоиндола, который выделяют в форме бесцветных кристаллов; температура плавления: 128-130°С.
Рассч. для C12H17NO: 75,35% С, 8,96% Н, 7,32% N; обнаруж.: 75,19% С, 8,95% Н, 7,23% N.
С использованием этого гидроксиламинового соединения и 2,4,6-триметилбензоилхлорида в эксперименте, который в другом отношении аналогичен эксперименту с получением соединения 101, с 92%-ным выходом получают соединение 104, которое выделяют в форме бесцветных кристаллов; температура плавления: 181-183°С (дихлорметан/метанол).
Рассч. для C22H27NO2: 78,30% С, 8,06% Н, 4,15% N; обнаруж.: 78,46% С, 8,12% H, 4,02% N.
А5: 1-ацетокси-2,2,6,6-тетраметилпиперидин-4-илбензоат (105)
С использованием 1-гидрокси-4-бензоилокси-2,2,6,6-тетраметилпиперидина [получен так, как описано в работе T.Kurumada и др., J.Polym. Sci., Polym.Chem.Ed. (1984), 22(1), 277-81] в эксперименте, который в других отношениях аналогичен эксперименту с получением соединения 101, с 90%-ным выходом получают соединение 105, которое выделяют в форме бесцветных кристаллов; температура плавления: 110-112°С (ацетонитрил).
Рассч. для C18H25NO4: 67,69% С, 7,89% Н, 4,39% N; обнаруж.: 67,61% С, 7,77% H, 4,38% N.
А6: 4-ацетокси-2,2,6, 6-тетраметилпиперидин-1-илацетат (106)
С использованием 1,4-дигидрокси-2,2,6,6-тетраметилпиперидина, полученного так, как описано в работе Paleos C.M. и др., J.Chem.Soc., Chem.Commun. (1977), (10), 345-6, в эксперименте, в другом отношении аналогичном получению соединения 101, с 40%-ным выходом получают соединение 106, которое выделяют в форме бесцветных кристаллов; температура плавления: 70-73°С (ацетонитрил).
1Н-ЯМР (300 МГц, CDCl3): 5,13-5,03 m (1H), 2,11 s (СН3), 2,04 s (СН3), 1,95-1,74 m(4H), 1,25 s (2×СН3), 1,11 s (2×СН3).
А7: 1-(2,2-диметилпропионилокси)-2,2,6,6-тетраметилпиперидин-4-илбензоат (107)
С использованием 1-гидрокси-4-бензоилокси-2,2,6,6-тетраметилпиперидина (получен так, как описано в работе Kurumada Т. и др. в упомянутом месте) и пивалоилхлорида в эксперименте, который в других отношениях аналогичен получению соединения 101, с 70%-ным выходом получают соединение 107, которое выделяют в форме бесцветных кристаллов; температура плавления: 107-110°С (гексан).
Рассч. для C21H31NO4: 69,78% С, 8,64% Н, 3,8% N; обнаруж.: 69,69% С, 8,54% Н, 3,86% N.
А8: 4-(2,2-диметилпропионилокси)-2,2,6,6-тетраметилпиперидин-1-ил-2, 2-диметилпропионат(108)
С использованием 1,4-дигидрокси-2,2,6,6-тетраметилпиперидина, полученного так, описано в работе Paleos C.M. и др. в упомянутом месте, и пивалоилхлорида в эксперименте, который в другом отношении аналогичен получению соединения 101, с 67%-ным выходом получают соединение 108, которое выделяют в форме бесцветных кристаллов; температура плавления: 43-46°С (пентан).
1Н-ЯМР (300 МГц, CDCl3): 5,09-5,01 m (1H), 1,92-1,74 m (4H), 1,28 s (трет-Bu), 1,26 s (2×СН3), 1,18s (трет-Bu), 1,08 s (2×СН3).
А9: 2,2,6,6-тетраметил-1-октадеканоилоксипиперидин-4-илбензоат (109)
С использованием 1-гидрокси-4-бензоилокси-2,2,6,6-тетраметилпиперидина, полученного так, как описано в работе Kurumada Т. и др. в упомянутом месте, и стеароилхлорида в эксперименте, который в другом отношении аналогичен получению соединения 101, с 60%-ным выходом получают соединение 109, которое выделяют в форме бесцветных кристаллов; температура плавления: 85-89°С (ацетонитрил).
Рассч. для C34H57NO4: 75,09% С, 10, 56% Н, 2,58% N; обнаруж.: 75,00% С, 10,22% Н, 2,57% N.
А10: 2,2,6,6-тетраметил-4-пропоксипиперидин-1-ил-2,2-диметилпропионат (110)
21,4 г (0,1 моля) 4-пропокси-2,2,6, 6-тетраметилпиперидин-N-оксида (описание получения см. в DE-A 4219459) гидрируют до насыщения под давлением 4 бара в 20 мл толуола с использованием 0,05 г платины (10%-ная на угле). Катализатор отфильтровывают и в бесцветный фильтрат в азотной атмосфере медленно, по каплям добавляют 13 г (0,108 моля) пивалоилхлорида. После ослабления слегка экзометрической реакции смесь перемешивают в течение последующего 1 ч при комнатной температуре и разбавляют 20 мл воды. Органическую фазу промывают 4%-ным раствором NaOH, сушат над MgSO4 и освобождают от толуола в роторном испарителе. В результате этого получают 13,5 г (выход: 45%) соединения 110, которое находится в форме бесцветного масла.
1Н-ЯМР (300 МГц, CDCl3): 3,63-3,54 m (1H), 3,38 t (СН3), 1,92-1,48 m (6H), 1,27 s (трет-Bu), 1,23 s (2×СН3), 0,93 s (2×СН3), 0,90 t (СН3).
А11: 1-бензоилокси-2,2,6, 6-тетраметилпиперидин-4-илбензоат (111)
С использованием 1-гидрокси-4-бензоилокси-2,2,6,6-тетраметилпиперидина, полученного так, как описано в работе Kurumada Т. и др. в упомянутом месте, и бензоилхлорида в эксперименте, который в другом отношении аналогичен эксперименту с получением соединения 101, с достижением 83%-ного выхода выделяют соединение 111, которое находится в форме бесцветных кристаллов; температура плавления: 138-140°С (толуол/гексан).
Рассч. для C23H27NO4: 72,42% С, 7,13% Н, 3,67% N; обнаруж.: 72,28% С, 7, 20% Н, 3,70% N.
А12: 2,2,6,6-тетраметил-4-пропоксипиперидин-1-илацетат (112)
Смесь 21,4 г (0,1 моля) 4-пропокси-2,2,6,6-тетраметилпиперидин-N-оксида (описание получения см. в DE-A 4219459) и 11 г (0,108 моля) уксусного ангидрида гидрируют до насыщения под давлением 4 бара над 0,15 г платины (10%-ная на угле). Катализатор отфильтровывают и фильтрат разбавляют 50 мл трет-бутилметилового эфира, промывают холодным 12%-ным раствором NaOH, 5%-ной HCl и, наконец, водой, сушат над MgSO4 и освобождают от растворителя в роторном испарителе. В результате этого получают 18,1 г (выход: 70%) соединения 112, которое находится в форме бесцветного масла.
1Н-ЯМР (300 МГц, CDCl3): 3,60-3,50 m (1H), 3,34 t (СН2), 2,05 s (СН3СО), 1,90-1,49 m (6H), 1,15 s (2×СН3), 1,05 s (2×СН3), 0,87 t (СН3).
А13: бис(4-бензоилокси-2,2,6, 6-тетраметилпиперидин-1-ил)гександикарбоксилат (113)
С использованием 1-гидрокси-4-бензоилокси-2,2,6,6-тетраметилпиперидина, полученного так, как описано в работе Kurumada Т. и др. в упомянутом месте, и адипоилхлорида в эксперименте, который в другом отношении аналогичен эксперименту с получением соединения 101, с 81%-ным выходом выделяют соединение 113, которое находится в форме бесцветных кристаллов; температура плавления: 130-135°С (дихлорметан/ацетонитрил).
Рассч. для C38H52N2O8: 68,65% С, 7,88% Н, 4,21% N; обнаруж.: 68,58% С, 8,07% Н, 4,34% N.
А14: бис(4-бензоилокси-2,2,6,6-тетраметилпиперидин-1-ил)оксалат (114)
С использованием 1-гидрокси-4-бензоилокси-2,2,6, 6-тетраметилпиперидина, полученного так, как описано в работе Kurumada Т. и др. в упомянутом месте, и оксалилхлорида в эксперименте, который в другом отношении аналогичен эксперименту с получением соединения 101, с 70%-ным выходом выделяют соединение 114, которое находится в форме бесцветных кристаллов; температура плавления: 211-215°С (дихлорметан/гексан).
Рассч. для C33H44N2O8: 67,09% С, 7,29% Н, 4,60% N; обнаруж.: 66,89% С, 7,22% Н, 4,56% N.
А15: 1-трет-бутоксикарбонилокси-2,2,6, 6-тетраметилпиперидин-4-илбензоат (115)
6,95 г (0,025 моля) 1-гидрокси-4-бензоилокси-2,2,6,6-тетраметилпиперидина, полученного так, описано в работе Т.Kurumada и др. в упомянутом месте, 0,15 г 4-диметиламинопиридина и 9,5 г (0,043 моля) дитрет-бутилдикарбоната в 30 мл ТГФ перемешивают при 45°С в течение 30 ч. Реакционную смесь выпаривают досуха в роторном испарителе. Хроматографией остатка на силикагеле с использованием гексана и этилацетата в соотношении 9:1 получают 6,2 г (выход: 66%) соединения 115, которое после перекристаллизации из дихлорметана/гексана плавится при 109-111°С.
Рассч. для C21H31NO5: 66,82% С, 8,28% Н, 3,71% N; обнаруж.: 66,83% С, 7,96% H, 3,65% N.
А16: 1-дифенилфосфиноилокси-2,2,6,6-тетраметилпиперидин-4-илбензоат (116)
С использованием 1-гидрокси-4-бензоилокси-2,2,6,6-тетраметилпиперидина, полученного так, как описано в работе Kurumada Т. и др. в упомянутом месте, и дифенилфосфинхлорида в эксперименте, который в других отношениях аналогичен эксперименту с получением соединения 101, с 84%-ным выходом выделяют соединение 116, которое находится в форме бесцветных кристаллов; температура плавления: 169-173°С (дихлорметан/гексан).
Рассч. для C28H32NO4P: 70,43% С, 6,75% Н, 2,93% N; обнаруж.: 70,25% С, 6,67% Н, 2,79% N.
А17: 1-этилкарбамоилокси-2,2,6,6-тетраметилпиперидин-4-илэтилкарбамат (117)
20 мл (0,26 моля) этилизоцианата в азотной атмосфере по каплям добавляют к 10,0 г (0,058 моля) 1,4-дигидрокси-2,2,6,6-тетраметилпиперидина, полученного так, как описано в работе Paleos С.М. и др. в упомянутом месте, в 100 мл 1,2-дихлорэтана. Смесь перемешивают при 70°С в течение 30 ч и затем выпаривают досуха в роторном испарителе. В результате перекристаллизации остатка из ксилола в форме бесцветных кристаллов получают 14,4 г (выход: 77%) соединения 117; температура плавления: 149-151°С.
Рассч. для C15H29N3O4: 57,12% С, 9,27% Н, 13,32% N; обнаруж.: 57,42% С, 9,28% Н, 13,02% N.
А18: 1-фенилкарбамоилокси-2,2,6,6-тетраметилпиперидин-4-илфенилкарбамат (118)
Соединение 118 получают с использованием фенилизоцианата в эксперименте, который аналогичен эксперименту с получением соединения 117, и выделяют с 64%-ным выходом в форме бесцветных кристаллов; температура плавления:188-190°С.
1Н-ЯМР (300 МГц, CDCl3): 8,7 широкий s (NH), 7,49-7,08 m (10 ArH), 6,63 широкий s (NH), 5,20-5,10 m (1H), 2,33-1,72 m (4H), 1,42 s (2×СН3), 1,27 s (2×СН3).
А19: 1-ацетокси-2,2-диэтил-6,6-диметилпиперидин-4-илацетат (119)
2,2-диэтил-6,6-диметил-4-гидроксипиперидин-N-оксид (описание получения см. в заявке на патент Германии 19949352.9) гидрируют аналогично примеру А10 с получением соответствующего гидроксиламина. Сырой гидроксиламин ацетилируют посредством уксусного ангидрида аналогично примеру А
1. Соединение 119 выделяют с 62%-ным выходом в форме желтоватого масла.
1Н-ЯМР (300 МГц, CDCl3): 5,10-5,0 m (1H), 2,05 s (СН3СО), 2,03 s (СН3 СО), 1,95-1,52 m (8Н), 1,28 s (СН3), 1,10 s (СН3), 0,98-0,83 m (2×СН3).
А20: 4-ацетокси-2,6-диэтил-2,3,6-триметилпиперидин-1-илацетат (120)
Соединение 120 получают из 2,6-диэтил-2,3,6-триметил-4-гидроксипиперидин-N-оксида аналогично примеру А19 в форме слегка желтоватого масла.
1Н-ЯМР (300 МГц, CDCl3): 5,40-4,85 m (1H), 2,23-0,8 m (28H).
А21: 4-ацетокси-2,6-диэтил-2,3,6-триметилпиперидин-1-ил-2,2-диметилпропионат (121)
2,6-диэтил-2,3, 6-триметил-4-гидроксипиперидин-N-оксид (описание получения см. в заявке на патент Германии 19949352.9) ацетилируют аналогично примеру А1 и превращают аналогично примеру А10 в соединение 121, которое находится в форме бесцветного масла.
1Н-ЯМР (300 МГц, CDCl3): 5,36-4,83 m (1H), 2,20-0,77 m (34H).
А22: 4-трет-бутил-2,2-диэтил-6, 6-диметил-3-оксопиперазин-1-илацетат (122)
4-трет-бутил-2,2-диэтил-6,6-диметилпиперазин-3-он-N-оксид (описание получения см. в заявке на патент Германии 19949352.9) восстанавливают до соответствующего гидроксиламина аналогично примеру А10 и превращают ацетилированием аналогично примеру 1 в маслянистое соединение 122.
1Н-ЯМР (300 МГц, CDCl3): 3, 24-3,15 m (2H), 2,04 s (СН3СО), 2,04-1,72 m (2×CH2), 1,40 s (трет-Bu), 1,19 s (СН3), 1,12 s (СН3), 0,99-0,91 m (2 СН3).
А23: 4-трет-бутил-2,2,6,6-тетраэтил-3-оксопиперазин-1-илацетат (123)
4-трет-бутил-2,2,6,6-тетраэтилпиперазин-3-он-N-оксид (описание получения см. в заявке на патент Германии 19949352.9) превращают аналогично примеру А22 в маслянистое соединение 123.
1Н-ЯМР (300 МГц, CDCl3): 3,21-3,16 m (2H), 2,05 s (СН3СО), 2,05-1,46 m (4×СН2), 1,43 s (трет-Bu), 1,00-0,87 m (4×СН3).
А24: 4-трет-бутил-2,2,6,6-тетраэтил-3-оксопиперазин-1-илбензоат (124)
Эксперимент примера А 23 повторяют с использованием бензоилхлорида, получая соединение 124, которое находится в форме бесцветных кристаллов; температура плавления: 91-93°С.
Рассч. для С23Н36Н2O3: 71,10% С, 9,34% Н, 7,21% N; обнаруж.: 71,12% С, 9,42% H, 7,18% N.
А25: 4-трет-бутил-2,2,6,6-тетраэтил-3-оксопиперазин-1-ил-2, 2-диметилпропионат (125)
Эксперимент примера А23 повторяют с использованием пивалоилхлорида, получая соединение 125, которое находится в форме бесцветных кристаллов; температура плавления: 58-60°С.
Рассч. для C21H40N2O3: 68,44% С, 10,94% Н, 7,60% N; обнаруж.: 68,29% С, 10,43% Н, 7,49% N.
А26: 2, 2,6,6-тетраметил-4-(2,2,2-трифторацетокси)пиперидин-1-илтрифторацетат (126)
Эксперимент примера А6 повторяют с использованием трифторуксусного ангидрида, получая соединение 126, которое находится в форме бесцветных кристаллов.
1Н-ЯМР (300 МГц, CDCl3): 5,34-5,24 m (1Н), 2,31-1,87 m (4Н), 1,33 s (2×СН3), 1,19 s (2× СН3).
А27: 1-трифторацетокси-4-трет-бутил-2,2-диэтил-6,6-диметилпиперазин-3-он (127)
Эксперимент примера А22 повторяют с использованием трифторуксусного ангидрида, получая соединение 127, которое находится в форме бесцветного масла.
1Н-ЯМР (300 МГц, CDCl3): 3,27-3,14 m (2H), 2,20-0,95 m (16H), 1,46 s (трет-Bu).
А28: 4-(N-ацетил-N-2,2-диметилпропиониламино)-2,2,6,6-тетраметилпиперидин-1-ил-2,2-диметилпропионат (128)
Раствор 21 г (0,098 моля) 1-ацетиламинотетраметилпиперидин-1-оксида (фирма Fluka) в 170 мл ТГФ при комнатной температуре и под давлением 3 бара гидрируют над 0,5 г платинового катализатора (5%-ный на угле) до прекращения абсорбции водорода. Катализатор отфильтровывают и фильтрат выпаривают в роторном испарителе. Бесцветный кристаллический остаток растворяют в 100 мл пиридина и смешивают с 13,7 мл (0,11 моля) пивалоилхлорида. После перемешивания при комнатной температуре в течение 1 ч смесь выливают в 250 мл смеси воды со льдом, образовавшийся осадок отфильтровывают под вакуумом и перекристаллизовывают из ацетонитрила. В результате этого в форме бесцветных кристаллов получают 4,6 г указанного в заглавии соединения (128); температура плавления: 169-173°С.
1Н-ЯМР (300 МГц, CDCl3): 4,04-3,96 m (1H), 2,32-2,24 m (2H), 2,16 s (СОСН3), 1,65-1,60 (m, 2H), 1,28 s (трет-Bu), 1,27 s (трет-Bu), 1,25 s (2×СН3), 1,20 s (2×СН3).
А29: 4-ацетиламино-2,2,6,6-тетраметилпиперидин-1-ил-2,2-диметилпропионат (129)
Водный фильтрат после выделения соединения 128 примера 28 экстрагируют 3 раза 100 мл дихлорметана. Экстракты промывают 8 раз 20 мл воды и выпаривают в роторном испарителе. Остаток растворяют в 20 мл дихлорметана, промывают 10 мл 10%-ного NaOH и вновь выпаривают. В результате перекристаллизации остатка из толуола/гексана получают 4,68 г указанного в заглавии соединения 129; температура плавления: 128-135°С.
1Н-ЯМР (300 МГц, CDClз ): 5,92 широкий s (NH), 4,29-4,18 m (1H), 1,96 s (СОСН3), 1,89-1,83 m (2H), 1,67-1,59 (m, 2Н), 1,28 s (трет-Bu), 1,27 s (2×СН3), 1,06 s (2×СН3).
А30: 4-ацетиламино-2,2,6,6-тетраметилпиперидин-1-илацетат (130)
Раствор 21,4 г (0,1 моля) 4-ацетиламинотетраметилпиперидин-1-оксида (фирма Fluka) и 0,1 г 4-диметиламинопиридина в 150 мл уксусного ангидрида при комнатной температуре и под давлением 3 бара гидрируют над 0,5 г платинового катализатора (5%-ный на угле) до прекращения абсорбции водорода. Катализатор отфильтровывают и фильтрат выпаривают в роторном испарителе. В результате перекристаллизации остатка из ацетонитрила в форме бесцветных кристаллов получают 8,85 г указанного в заглавии соединения 130; температура плавления: 129-32°С.
1Н-ЯМР (300 МГц, CDCl3): 5,66 широкий s (NH), 4,29-4,16 m (1H), 2,10 s (СОСН3), 1,96 s (СОСН3), 1,89-1,84 m (2H), 1,62-1,54 (m, 2H), 1,25 s (2×СН3), 1,08 s (2×СН3).
А31: бис[1-(2,2-диметилпропионилокси)-2,2,6, 6-тетраметилпиперидин-4-ил]декандиоат (131)
15,3 г (0,03 моля) бис(2,2,6,6-тетраметил-1-оксипиперидин-4-ил)себацата [получен так, как описано в Polym. Degrad. Stab. (1982), 4(1), 1-16] превращают аналогично примеру А28 в 16,8 г указанного в заглавии соединения 131; температура плавления: 93-97°С.
1Н-ЯМР (300 МГц, CDCl3): 5,12-5,03 m (2H), 2,29-1,92 m (4H), 1,91-1,57 (14Н), 1,32-1,23 (36Н), 1,08 s (12H).
А32: 4-(N-ацетил-N-н-бутиламино)-2,2,6,6-тетраметилпиперидин-1-ил-2,2-диметилпропионат (132)
26,95 г (0,1 моля) 4-(N-ацетил-N-н-бутиламино)-2,2,6,6-тетраметилпиперидин-1-оксида (получен так, как описано в WO 00/03965) превращают аналогично примеру А28 в 26 г указанного в заглавии соединения 132, которое выделяют в форме бесцветных кристаллов; температура плавления: 81-94°С.
Рассч. для C20H38N2O3: 67,75% С, 10,80% Н, 7,90% N; обнаруж. 67,74% С, 10,78% Н, 7,87% N.
А33: 2,6-диэтил-2,3,6-триметил-4-оксопиперидин-1-илацетат (133)
10,95 г (0,052 моля) 2,6-диэтил-2,3, 6-триметил-4-оксопиперидин-1-оксида (описание получения см. в DE-A 19909767) превращают аналогично примеру А30 в указанное в заглавии соединение (133), которое выделяют в форме бесцветного масла; выход: 11,9 г.
Рассч. для C14H25NO3: 65,85% С, 9,87% Н, 5,49% N; обнаруж. 65,71% С, 9,64% Н, 5,39% N.
А34: 2,2,6, 6-тетраметил-4-оксопиперидин-1-илацетат (134)
Указанное в заглавии соединение получают по методу, приведенному в J.Chem.Soc.Perkin Trans. 1, 9, 2243 (1991).
А35: 4-трет-бутил-2,2-диэтил-6,6-диметил-3-оксопиперазин-1-илфенилкарбамат (135)
4-трет-бутил-2,2-диэтил-6,6-диметилпиперазин-3-он-N-оксид (описание получения см. в заявке на патент Германии 19949352.9) восстанавливают до соответствующего гидроксиламина аналогично примеру А10 и с использованием фенилизоцианата аналогично примеру А18 превращают в соединение 135, которое выделяют в форме бесцветных кристаллов; температура плавления:160-163°С.
Рассч. для C21H33N3O3: 67,17% С, 8,86% Н, 11,19% N; обнаруж. 67,21% С, 8,84% Н, 11,06% N.
А36: 4-трет-бутил-2,2-диэтил-6,6-диметил-3-оксопиперазин-1-илдифенилацетат (136)
4-трет-бутил-2,2-диэтил-6,6-диметилпиперазин-3-он-N-оксид (описание получения см. в заявке на патент Германии 19949352.9) восстанавливают до соответствующего гидроксиламина аналогично примеру 10 и с использованием дифенилацетилхлорида аналогично примеру 25 превращают в соединение 136, которое выделяют в форме бесцветных кристаллов; температура плавления: примерно 109°С.
1Н-ЯМР (300 МГц, CDCl3): 7,38-7,26 m (10Н), 5,0 s (1H), 3,22-3,00 m (2H), 1,93-1,61 m (4Н), 1,40 s (9H), 1,12 s (3Н), 0,98 s (3Н), 0,97-0,81 m (6H).
А37: 2,6-диэтил-2,3,6-триметилпиперидин-1-илацетат (137)
2,6-диэтил-2, 3,6-триметилпиперидин-1-оксид (описание получения см. в US 4131599) аналогично примеру А30 превращают в соединение 137, которое выделяют в форме бесцветного масла.
1Н-ЯМР (300 МГц, CDCl3): 2,05 s (ЗН), 2,0-0,79 m (24H).
A38: 2,6-диэтил-2,3,6-триметилпиперидин-1-илстеарат (138)
2,6-диэтил-2,3,6-триметилпиперидин-1-оксид (описание получения см. в US 4131599) аналогично примеру А30 с использованием стеароилхлорида превращают в соединение 137, которое выделяют в форме бесцветного масла.
1Н-ЯМР (300 МГц, CDCl3): 2,29 t (2H), 1,81-0,78 m (57H).
A39: 3,3,8,8,10,10-гексаметил-1,5-диокса-9-азаспиро[5.5]ундец-9-илацетат (139)
3,3,8,8,10,10-гексаметил-1, 5-диокса-9-азаспиро[5.5]ундекан-9-оксид (способ получения см. в ЕР-А 574666) аналогично примеру А 30 превращают в соединение 139, которое выделяют в форме бесцветных кристаллов; температура плавления: 109-111°С.
1Н-ЯМР (300 МГц, CDCl3): 3,48 широкий s (4H), 2,26 d (2H), 2,1 s (3Н), 1,8 d (2H), 1,29 s (6H), 1,09 s (6H), 0,97 s (6H).
А40: 7, 9-диэтил-6,7,9-триметил-1,4-диокса-8-азаспиро[4.5]дец-8-илацетат (140)
7,9-диэтил-6,7,9-триметил-1,4-диокса-8-азаспиро[4.5]декан-8-оксид (описание получения см. в US 4105626) аналогично примеру А30 превращают в соединение 140, которое выделяют в форме бесцветного масла.
1Н-ЯМР (300 МГц, CDCl3): 4,09-3,76 m (4H), 2,25-0,79 m (22H), 2,04 s (3Н).
А41: 8-ацетокси-7,9-диэтил-6,7,9-триметил-1,4-диокса-8-азаспиро[4.5]дец-2-илметилацетат (141)
Раствор 10,25 г (0,035 моля) 7,9-диэтил-6,7,9-триметил-1, 4-диокса-8-азаспиро[4.5]дец-2-ил)метанол-8-оксида (способ получения см. в US 4105626) в азотной атмосфере перемешивают с раствором 20 г аскорбата натрия в 40 мл воды в течение 4 ч. Бесцветную органическую фазу отделяют и выпаривают в роторном испарителе. Полученное таким путем гидроксиламиновое производное аналогично примеру А1 с использованием уксусного ангидрида превращают в соединение 141, которое выделяют в форме бесцветного масла.
1Н-ЯМР (300 МГц, CDCl3): 4,39-3,21 m (5H), 2,16-0,83 m (28H)
А42: 8,10-диэтил-3,3,7,8, 10-пентаметил-1,5-диокса-9-азаспиро[5.5]ундец-9-илацетат (142)
8,10-диэтил-3,3,7,8,10-пентаметил-1,5-диокса-9-азаспиро[5.5]ундекан-9-оксид (способ получения см. в US 4105626) аналогично примеру А30 превращают в соединение 142, которое находится в форме бесцветного масла.
1Н-ЯМР (300 МГц, CDCl3): 3,74-2,58 m (4H), 2,04 s (3Н), 1,96-0,68 m (28H).
А43: 3-ацетоксиметил-3,8,10-триэтил-7,8,10-триметил-1,5-диокса-9-азаспиро[5.5]ундец-9-илацетат (143)
3,8,10-триэтил-7,8,10-триметил-1, 5-диокса-9-азаспиро[5.5]ундец-3-илметанол (способ получения см. в US 41058226) аналогично примеру А30 превращают в соединение 143, которое выделяют в форме бесцветного масла.
1Н-ЯМР (300 МГц, CDCl3): 4,37-2,58 m (6H), 2,04 s (3Н), 2,08-0,81 m (30Н).
А44: 9-ацетокси-3,8,10-триэтил-7,8,10-триметил-1, 5-диокса-9-азаспиро[5.5]ундец-3-илметилстеарат (144)
12 г (0,037 моля) 3,8,10-триэтил-7,8,10-триметил-1,5-диокса-9-азаспиро[5.5]ундец-3-илметанола (способ получения см. в US 4105626) растворяют в 40 мл пиридина и смешивают с 11,7 г (0,039 моля) стеароилхлорида. После перемешивания в течение 18 ч при комнатной температуре реакционную смесь разбавляют 200 мл воды и экстрагируют 2 раза, используя по 50 мл метилтрет-бутилового эфира. После отгонки растворителя образовавшийся стеароилнитроксид аналогично примеру А 30 превращают в соединение 144, которое выделяют в форме бесцветного масла (145).
1Н-ЯМР (300 МГц, CDCl3): 4,39-2,58 m (6Н), 2,32 t (2H), 2,04 s (3H), 1,91-0,80 m (62 Н).
А45: 1-ацетокси-2,2,6, 6-тетраметилпиперидин-4-илстеарат
2,2,6,6-тетраметилпиперидин-4-илстеарат-1-оксид (описание получения см. в WO 99/67298) аналогично примеру А30 превращают в соединение 145, которое выделяют в форме бесцветных кристаллов, температура плавления: 63-70°С.
1Н-ЯМР (300 МГц, CDCl3): 5,12-5,03 m (1H), 2,29-2,22 t (2H), 2,06 s (3H), 1,93-0,84 m (49H).
A46: 1-ацетокси-2,6-диэтил-2,3,6-триметилпиперидин-4-илстеарат (146)
2,6-диэтил-2,3,6-триметилпиперидин-4-илстеарат-1-оксид (описание получения см. в DE-A 19949352.9) аналогично примеру А30 превращают в соединение 146, которое находится в форме бесцветного масла.
Рассч. для C32H61NO4: 73,37% С, 11,74% Н, 2,67% N; обнаруж. 73,39% С, 11,58% H, 2,58% N.
A47: бис(1-ацетокси-2,2,6,6-тетраметилпиперидин-4-ил)декандиоат (147)
(2,2,6,6-тетраметилпиперидин-4-ил-1-оксид)диэфир декандиоата (получение см. в WO 99/05108) аналогично примеру А 30 превращают в соединение 147, которое выделяют в форме бесцветных кристаллов; температура плавления: 81-94°С.
Рассч. для C32H56N2O8: 64,40% С, 9,46% Н, 4,69% N; обнаруж. 64,18% С, 9,44% Н, 4,61% N.
А48: бис(1-ацетокси-2,2,6, 6-тетраметилпиперидин-4-ил)терефталат (148)
(2,2,6,6-тетраметилпиперидин-4-ил-1-оксид)диэфир терефталевой кислоты [описание получения см. в работе Z.Naturforsch., В: Chem.Sci. 55(7), 567-575 (2000)] аналогично примеру А30 превращают в соединение 148, которое выделяют в форме бесцветных кристаллов; температура плавления: 206-212°С.
Рассч. для C30 H44N2O8: 64,27% С, 7,91% Н, 5,00% N; обнаруж. 63,79% С, 7,93% Н, 4,87% N.
А49: 4-{[4,6-бис(1-ацетокси-2,2,6,6-тетраметилпиперидин-4-ил)бутиламино[1,3, 5]триазин-2-ил]бутиламино}-2,2,6,6-тетраметилпиперидин-1-илацетат (149)
18,5 мл перуксусной кислоты (40%-ная в уксусной кислоте) по каплям добавляют в раствор 12,85 г (0,018 моля) N, N′,N′′-трибутил-N,N′,N′′-трис(2,2,6,6-тетраметилпиперидин-4-ил)[1,3,5]триазин-2,4,6-триамина (описание получения см. в ЕР-А 107615) в 95 мл дихлорметана. Раствор перемешивают в течение 20 ч, промывают водой и 10%-ным раствором NaHCO3 и выпаривают. К остатку добавляют 25 мл тетрагидрофурана, 7,2 мл уксусного ангидрида и 2,8 г платинового катализатора (5%-ный на угле) и смесь гидрируют до насыщения под давлением водорода 4 бара. Катализатор отфильтровывают и фильтрат выпаривают в роторном испарителе. Остаток суспендируют в 30 мл ацетонитрила, отфильтровывают и сушат. В результате этого в форме бесцветного порошка получают 10,3 г соединения 149; температура плавления: 232-244°С.
1Н-ЯМР (300 МГц, CDCl3): 5,37-5,29 m (3Н), 3,32-3,29 m (6H), 2,08 s (9H), 1,96-1,87 t (6H), 1,61-1,49 m (18H), 1,28 s (18Н), 1,11 s (18H), 0,92-0,87 t (9H).
А50: полимер (150):
а) 2,4,6-трихлор-1,3,5-триазина
б) 4-{6-[1-(2,2-диметилпропионилокси)-2,2,6,6-тетраметилпиперидин-4-иламино]гексиламино}-2,2,6,6-тетраметилпиперидин-1-ил-2, 2-диметилпропионата
в) 4-бутиламино-2,2,6,6-тетраметилпиперидин-1-ил-2,2-диметилпропионата
г) дибутиламина.
25 г продукта CHIMASSORB® 2020 (производитель: фирма Ciba SC) аналогично примеру А49 с использованием пивалоилхлорида превращают в 19 г полимера 150, который получают в форме бесцветного порошка; температура плавления:140-160°С.
1Н-ЯМР (300 МГц, CDCl3): 5,06-4,25 m, 3,1-2,9 m, 1,95-0,58 m
А51: полимер(151) из
а) 2,4,6-трихлор-1,3, 5-триазина
б) 4-[6-(1-ацетокси-2,2,6,6-тетраметилпиперидин-4-иламино)гексиламино]-2,2,6,6-тетраметилпиперидин-1-илацетата
в) 4-бутиламино-2,2,6, 6-тетраметилпиперидин-1-илацетата
г) дибутиламина.
25 г продукта CHIMASSORB® 2020 (производитель: фирма Ciba SC) аналогично примеру А49 с использованием уксусного ангидрида превращают в 25,3 г полимера 151, который получают в форме бесцветного порошка; температура плавления: 154-164°С.
Элементный анализ: 64,48% С, 9,81% Н, 15, 19% N.
А52: полимер (152) из
а) 2,6-диэтил-2,3,6-триметилпиперидин-1,4-диола
б) терефталевой кислоты.
2,6-диэтил-2,3, 6-триметил-4-гидроксипиперидин-N-оксид (описание получения см. в заявке на патент Германии 19949352.9) аналогично примеру А10 гидрируют до соответствующего гидроксиламина. 10,7 г (0,05 моля) этого гидроксиламина растворяют в 100 мл пиридина и в этот раствор медленно, по каплям добавляют 10,15 г (0,05 моля) дихлорангидрида терефталевой кислоты. Смесь перемешивают в азотной атмосфере при 30°С в течение 20 ч. Добавляют 1,9 мл уксусного ангидрида и по прошествии 1 ч смесь разбавляют 500 мл воды. Образовавшийся осадок отфильтровывают под вакуумом, промывают водой и сушат. В результате этого получают 17,8 г полимера 152, который выделяют в форме бесцветного порошка; температура плавления: 190-210°С.
Элементный анализ: 65,17% С, 7,71% Н, 3,45% N.
А53: полимер (153) из
а) 2,6-диэтил-2,3,6-триметилпиперидин-1,4-диола
б) изофталевой кислоты.
Аналогично примеру А52 11,8 г (0,055 моля) 2, 6-диэтил-2,3,6-триметил-1,4-дигидроксипиперидина и 11,15 г (0,055 моля) дихлорангидрида изофталевой кислоты превращают в 19,55 г полимера 153, который получают в форме бесцветного порошка; температура плавления: 206-215°С.
1Н-ЯМР (300 МГц, CDCl3): 8,73 широкий s, 8,72 широкий s, 5,65-5,17 m, 2,59-0,64 m.
А54:полимер (154) из
а) 2,6-диэтил-2,3,6-триметилпиперидин-1,4-диола
б) изофталевой кислоты
в) терефталевой кислоты.
Аналогично примеру А49 11,8 г (0,055 моля) 2, 6-диэтил-2,3,6-триметил-1,4-дигидроксипиперидина, 5,57 г (0,0275 моля) дихлорангидрида терефталевой кислоты и 5,57 г (0,0275 моля) дихлорангидрида изофталевой кислоты превращают в 16,85 г полимера 154, который получают в форме бесцветного порошка; температура плавления: 212-218°С.
1Н-ЯМР (300 МГц, CDCl3): 8,74 широкий s, 8,28 широкий s, 8,16 широкий s, 7, 62 широкий s, 5,64-5,05 m, 2,68-0,74 m.
A55: полимер(155) из
а) 2,6-диэтил-2,3,6-триметилпиперидин-1,4-диола
б) адипиновой кислоты.
Аналогично примеру А 49 11,8 г (0,055 моля) 2,6-диэтил-2,3,6-триметил-1,4-дигидроксипиперидина и 10,08 г (0,055 моля) адипоилдихлорида превращают в 16,1 г полимера 155, который получают в форме бесцветного вязкого масла.
1Н-ЯМР (300 МГц, CDCl3): 5,29-4,80 m, 4,28-3,91 m, 2,55-0,77 m.
А-56: полимер (156) из
а) 2,6-диэтил-2, 3,6-триметилпиперидин-1,4-диола
б) адипиновой кислоты
в) терефталевой кислоты.
Аналогично примеру А49 11,8 г (0,055 моля) 2,6-диэтил-2,3,6-триметил-1, 4-дигидроксипиперидина, 5,57 г (0,0275 моля) дихлорангидрида терефталевой кислоты и 5,03 г (0,0275 моля) адипоилдихлорида превращают в 15,1 г полимера 156, который получают в форме бесцветного аморфного твердого вещества; температура плавления: 112-120°С.
1Н-ЯМР (300 МГц, CDCl3): 8,13 m, 5,66-4,88 m, 2,37-0,77 m.
А57: 4-ацетоксиимино-2,6-диэтил-2,3,6-триметилпиперидин-1-илацетат (157)
39,5 г (0,2 моля) 2,6-диэтил-2,3,6-триметил-4-оксопиперидина (описание получения см. в US 4131599) в 40 мл метанола выдерживают с 14,55 г 50%-ного водного раствора гидроксиламина при 50°С в течение 4 ч. Смесь выпаривают в роторном испарителе, остаток растворяют в 100 мл толуола и промывают 3 раза 50 мл воды. В дальнейшем добавляют 0,2 г 4-диметиламинопиридина и 20,8 мл (0,22 моля) уксусного ангидрида и смесь перемешивают при 30°С в течение 2 ч. Затем ее промывают водным раствором NaHCO3, сушат над сульфатом магния и выпаривают. В результате этого получают 34,95 г 2,6-диэтил-2,3,6-триметил-4-ацетоксииминопиперидина.
25,45 г (0,1 моля) этого соединения растворяют в 100 мл этилацетата и медленно, по каплям добавляют в 29,9 мл 40%-ной перуксусной кислоты (40%-ная в уксусной кислоте). После перемешивания в течение 21 ч при комнатной температуре смесь промывают водой и водным раствором NaHCO3, сушат над сульфатом магния и выпаривают. В результате этого получают 25,7 г 2,6-диэтил-2,3,6-триметил-4-ацетоксииминопиперидин-1-оксида, который аналогично примеру 30 превращают в соединение 157, которое получают в форме бесцветного масла.
CI-MS для C16H28N2O4 (312,41): обнаруж. MH+: 313.
А58: 4-ацетокси-2,2,6,6-тетраметилпиперидин-1-илстеарат (158)
2,2,6,6-тетраметилпиперидин-4-илацетат-1-оксид (описание получения см. в DE-A 4219459) аналогично примеру А10 восстанавливают до гидроксиламинового производного. В результате ацилирования стеарилхлоридом аналогично примеру А1 получают указанное в заглавии соединение, которое находится в форме бесцветных кристаллов; температура плавления: 55-58°С.
1Н-ЯМР (CDCl3, 300 МГц): 5,11-5,04 m (1H), 2,37-2,32 t (2H), 2,03 s (Me), 1,94-0,86 m (49H).
A59: 2,2,6,6-тетраметил-1-стеароилоксипиперидин-4-илстеарат (159)
2,2,6,6-тетраметилпиперидин-4-илстеарат-1-оксид (описание получения см. в WO 99/67298) аналогично примеру А69 превращают в соединение 159, которое получают в форме бесцветных кристаллов; температура плавления: 62-65°С.
1Н-ЯМР (CDCl3, 300 МГц): 5,09-5,05 m (1H), 2, 36-2,32 t (2H), 2,28-2,24 t (2H), 1,92-0,86 m (82H).
А60: 4-ацетокси-2,2,6,6-тетраметилпиперидин-1-ил-3-фенилакрилат (160)
2,2,6, 6-тетраметилпиперидин-4-илацетат-1-оксид (описание получения см. в DE-A 4219459) аналогично примеру 10 восстанавливают до гидроксиламинового производного. В результате ацилирования циннамоилхлоридом аналогично примеру А1 получают указанное в заглавии соединение, которое выделяют в форме бесцветных кристаллов; температура плавления: 130-132°С.
1Н-ЯМР (300 МГц, CDCl3): 7,79-7,74 d (1H), 7,58-7,55 m (2H), 7,44-7,40 m (3H), 6,51-6,46 d (1H), 5,17-5,07 m (1H), 2,03 s (Me), 1,98-1,77 m (4H), 1,31 s (2×Me), 1,5 s (2×Me).
A61: 4-ацетокси-2,2,6,6-тетраметилпиперидин-1-илада-мантан-1-карбоксилат (161)
Аналогично примеру 10 2,2,6,6-тетраметилпиперидин-4-илацетат-1-оксид (описание получения см. в DE-A 4219459) восстанавливают до гидроксиламинового производного. В результате ацилирования хлорангидридом адамантан-1-карбоновой кислоты аналогично примеру А1 получают указанное в заглавии соединение (161), которое выделяют в форме бесцветных кристаллов; температура плавления: 132-134°С.
1Н-ЯМР (300 МГц, CDCl3): 5,13-5,02 m (1H), 2,35-1,70 m (19H), 2,03 s (Me), l,26 s (2×Me), 1,06 s (2×Me).
A62: 1-ацетокси-2,2-диэтил-6,6-диметилпиперидин-4-илстеарат (162)
2,2-диэтил-6,6-диметил-4-гидроксипиперидин-N-оксид (описание получения см. в заявке на патент Германии 19949352.9) этерифицируют стеароилхлоридом аналогично примеру А1 и гидрируют до соответствующего гидроксиламина аналогично примеру А10. Сырой гидроксиламин аналогично примеру А1 ацетилированием превращают в указанное в заглавии соединение, которое выделяют в форме бесцветных кристаллов; температура плавления: 41-44°С.
1Н-ЯМР (300 МГц, CDCl3): 5,10-5,02 m (1H), 2,30-2,25 t (2H), 2,06 s (Me), 1,98-0,86 m (53H).
A63: бис(1-ацетокси-2,2,6,6-тетраметилпиперидин-4-ил)эфир 9, 10-динонилоктадекандикислоты (163)
Смесь, включающую 114 г (0,2 моля) 9,10-динонилоктадекандикислоты, 44 мл (0,4 моля) тионилхлорида и 0,1 мл ДМФ медленно нагревают до 65°С и перемешивают при этой температуре до замедления выделения газа (в течение 3-4 ч). Добавляют 300 мл толуола. Под пониженным давлением, составляющим 100 мбара, удаляют 100 мл толуола и избыток тионилхлорида. Получают 292,1 г коричневого раствора, который содержит 0,2 моля 9,10-динонилоктадекандиоилдихлорида.
4-гидрокси-2,2,6,6-тетраметилпиперидин-1-оксид в присутствии основного пиридина вышеупомянутым хлорангидридом кислоты превращают в диэфир. Затем гидратацией в соответствии с методом примера А10 этот диэфир превращают в гидроксиламин. Далее ацетилированием сырой гидроксиламин превращают в указанное в заглавии соединение, которое выделяют в форме желтоватой маслянистой жидкости.
1Н-ЯМР (CDCl3, 300 МГц): 5,12-5,04 m (2H), 2, 28-2,25 t (4H), 2,1 s (6H), 2,04-0,83 m (96H).
А64: бис(1-ацетокси-2,6-диэтил-2,3,6-триметилпиперидин-4-ил)эфир 9,10-динонилоктадекандикислоты (164)
Указанное в заглавии соединение получают аналогично примеру А 63 из 2,6-диэтил-4-гидрокси-2,3,6-триметилпиперидин-N-оксида и выделяют в форме желтоватой маслянистой жидкости.
1Н-ЯМР (CDCl3, 300 МГц): 5,32-4,91 m (2H), 2,32-0,83 m (118H).
Структурные формулы этих соединений представлены в приведенной ниже таблице 1.
Применение примеров
Б) Примеры полимеризации с использованием выбранных из таблицы 1 соединений
Материалы и методы
Незадолго до применения все растворители и мономеры в аргоновой атмосфере или под пониженным давлением перегоняют через колонку Вигре.
Перед полимеризацией все реакционные смеси освобождают от кислорода продувкой аргоном с применением технологии замораживания/оттаивания с последующей выдержкой в токе аргона.
До начала реакции полимеризации реагенты находятся в форме прозрачного гомогенного раствора.
После выпаривания непрореагировавшего мономера при 80°С и под остаточным давлением 0,27 мбара в течение 20 ч и удаления использованного инициатора взвешиванием остатка определяют превращение мономера.
Полимеры характеризуют ГПХ (гельпроникающей хроматографией) и/или MALDI-MC.
Для ГПХ применяют рабочий модельный двухпоршневой насос RHEOS 4000 фирмы FLUX INSTRUMENTS (представлена компанией Ercatech AG, Берн, Швейцария). Производительность такого насоса составляет 1 мл/мин. Хроматографию проводят на двух колонках с Plgel, 5-мкм, со смешанным С сорбентом фирмы POLYMER INSTRUMENTS, графство Шропшир, Великобритания, подключенных последовательно, при 40°С в ТГФ. Эти колонки калибруют с использованием полистирольных эталонов, значения Mn которых находятся в интервале от 200 до 2000000. Фракции определяют при 30°C с помощью рефрактометрического детектора (показатель преломления) ERC-7515А фирмы ERCATECH AG.
Определение MALDI-MC осуществляют с помощью линейной времяпролетной масс-спектрометрии (TOF MALDI-MC LDI-1700 фирмы Linear Scientific Inc., Рено, США). В качестве матрицы используют 2, 5-дигидроксибензойную кислоту, а длина волны лазерного излучателя составляет 33 нм.
Б1: полимеризация н-бутилакрилата с использованием соединения 101 при 145°С
319 мг (1,17 ммоля) соединения 101 и 10 г (78 ммолей) н-бутилакрилата загружают в 50-миллилитровую трехгорлую круглодонную колбу, снабженную термометром, холодильником и магнитной мешалкой, и смесь дегазируют. Прозрачный раствор в токе аргона нагревают до 145°С. Его перемешивают в течение последующего 1 ч при 145°С, охлаждают до 60°С и под высоким вакуумом выпаривают остаточный мономер. После превращения 4 г (40%) мономера получают прозрачную бесцветную вязкую жидкость. ГПХ: Mn составляет 70000, Mw равна 182000, PD=2,6.
Б2: полимеризация н-бутилакрилата с использованием соединения 101 при 120°С
Исходную смесь см. в примере Б1.
Прозрачный раствор в токе аргона нагревают до 120°С. Смесь перемешивают в течение последующих 2 ч при 120°С, охлаждают до 60°С и под высоким вакуумом выпаривают остаточный мономер. После превращения 5 г (50%) мономера получают прозрачную бесцветную вязкую жидкость. ГПХ: Mn составляет 91000, Mw равна 500500, PD=5,5.
Б3: полимеризация н-бутилакрилата с использованием соединения 102 при 145°С
391 мг (1,17 ммоля) соединения 102 и 10 г (78 ммолей) н-бутилакрилата загружают в 50-миллилитровую трехгорлую круглодонную колбу, снабженную термометром, холодильником и магнитной мешалкой, и смесь дегазируют. Прозрачный раствор в токе аргона нагревают до 145°С. Его перемешивают в течение последующих 2 ч при 145°С, охлаждают до 60°С и под высоким вакуумом выпаривают остаточный мономер. После превращения 5,9 г (59%) мономера получают прозрачную бесцветную вязкую жидкость. ГПХ: Mn составляет 184300, Mw равна 681900, PD=3,7.
Б4: полимеризация н-бутилакрилата с использованием соединения 123 при 130°С
382 мг (1,17 ммоля) соединения 123 и 10 г (78 ммолей) н-бутилакрилата загружают в 50-миллилитровую трехгорлую круглодонную колбу, снабженную термометром, холодильником и магнитной мешалкой, и смесь дегазируют. Прозрачный раствор в токе аргона нагревают до 130°С. Его перемешивают в течение последующих 5 ч при 130°С, охлаждают до 60°С и под высоким вакуумом выпаривают остаточный мономер. После превращения 4,0 г (40%) мономера получают прозрачную бесцветную вязкую жидкость. ГПХ: Mn составляет 41000, Mw равна 492000, PD=12,0.
Б5: полимеризация н-бутилакрилата с использованием соединения 124 при 110°С
455 мг (1,17 ммоля) соединения 124 и 10 г (78 ммолей) н-бутилакрилата загружают в 50-миллилитровую трехгорлую круглодонную колбу, снабженную термометром, холодильником и магнитной мешалкой, и смесь дегазируют. Прозрачный раствор в токе аргона нагревают до 110°С. Его перемешивают в течение последующих 2,5 ч при 110°С, охлаждают до 60°С и под высоким вакуумом выпаривают остаточный мономер. После превращения 4,5 г (45%) мономера получают прозрачную бесцветную вязкую жидкость. ГПХ: Mn составляет 160000, Mw равна 560000, PD=3,5.
Б6: полимеризация н-бутилакрилата с использованием соединения 125 при 100°С
431 мг (1,17 ммоля) соединения 125 и 10 г (78 ммолей) н-бутилакрилата загружают в 50-миллилитровую трехгорлую круглодонную колбу, снабженную термометром, холодильником и магнитной мешалкой, и смесь дегазируют. Прозрачный раствор в токе аргона нагревают до 100°С. Его перемешивают в течение последующих 3 ч при 100°С, охлаждают до 60°С и под высоким вакуумом выпаривают остаточный мономер. После превращения 8,0 г (80%) мономера получают прозрачную бесцветную вязкую жидкость. ГПХ: Mn составляет 7500, Mw равна 157500, PD=21,0.
Б7: полимеризация н-бутилакрилата с использованием соединения 152 при 145°С
Исходная смесь: 1,5 мольных% соединения 152 в н-бутилакрилате (масса)
Прозрачный раствор в аргоновой атмосфере нагревают до 145°С. Сразу же наблюдают высокоэкзотермическую реакцию. После превращения 68,5% мономера получают прозрачную бесцветную вязкую жидкость. ГПХ: Mn составляет 28525, PD=3,55.
Б7: полимеризация н-бутилакрилата с использованием соединения 152 при 100°С
Исходная смесь: 1,5 мольных% соединения 152 в н-бутилакрилате (масса)
Прозрачный раствор в аргоновой атмосфере нагревают до 100°С. После превращения 5% мономера в течение 5 ч получают прозрачную бесцветную вязкую жидкость. ГПХ: Mn составляет 3550, PD=1,5.
Б7: полимеризация н-бутилакрилата с использованием соединения 139 при 145°С
Исходная смесь: 1,5 мольных% соединения 152 в н-бутилакрилате (масса)
Прозрачный раствор в аргоновой атмосфере нагревают до 145°С. После превращения 32% мономера в течение 3 ч получают прозрачную бесцветную вязкую жидкость. ГПХ: Mn составляет 76830, PD=4,7.
В) регулируемая деструкция полипропилена посредством NOR соединений
Общий метод
Во всех случаях, если не указано иное, технический полипропилен (продукт PRofax® 6501, производитель: фирма Montell) экструдируют в двухчервячном экструдере ZSK 25 фирмы Werner & Pfleiderer при температуре Тмакс 270°С (зоны нагрева с 1 по 6) при производительности 4 кг/ч и скорости вращения шнеков 100 об/мин с введением базового количества стабилизатора и добавок, которые указаны в таблицах с 1 по 13, гранулированных в водяной бане. Вязкость расплава (СРР) определяют в соответствии с международным стандартом ISO 1133. Большое увеличение скорости истечения расплава указывает на существенную деструкцию цепей.
В указанных технологических условиях добавление NOR соединения приводит к возрастанию степени деструкции используемого ПП, что отражают повышенные значения СРР в сопоставлении с этим же показателем у исходного полимера (или в сравнительных примерах). В противоположность алкилированным гидроксиламинам при применении в такой же концентрации гидроксиламиновые сложные эфиры, используемые в соответствии с изобретением, вызывают значительно более существенную деструкцию полимера (более высокие значения СРР). Во всех экспериментах, если не указано иное, добавки готовят из испытываемого соединения и в каждом случае 0,1% продукта IRGANOX В 225 и 0,05%-ного стеарата кальция. Продукт IRGANOX В 225 представляет собой смесь продукта Irgafos® 168 и продукта IRGANOX 1010 в соотношении 1:1.
Известные в данной области техники соединения, использованные в сравнительных экспериментах, представлены в таблице 2:

NOR 1:

NOR 2:

NOR 3:

NOR 4:
Полимер: плотность составляет 0,79 г/см3; СРР230/2,16 равна 7,1 г/10 мин
Полимер: плотность составляет 0,79 г/см3; СРР230/2,16 равна 6,8 г/10 мин
Полимер: плотность составляет 0,79 г/см3; СРР230/2,16 равна 6,1 г/10 мин
Полимер: плотность составляет 0,79 г/см3; СРР230/2,16 равна 6,1 г/10 мин
Приготовление концентратов
Синтез концентратов с последующей деструкцией во время экструзии стадии аналогичны стадиям в общем методе (температуре в зоне 1: 35°С, зоне 2: 130°С, зоне 3: 170°С, зоне 4: 170°С, зоне 5: 170°С, зоне 6: 165°С; полипропилен Profax® 6501, фирма Montell). Обычный метод улучшения гомогенизации добавок состоит в добавлении минерального масла (вазелиновое масло).
Деструкция полимеров
Стадии экструзии аналогичны стадиям в общем методе (зоны нагрева с 1 по 6, Tмакс: 250°С; полипропилен Profax® 6501, фирма Montell).
Последующая деструкция полипропилена
Стадии экструзии аналогичны стадиям в общем методе. На первой стадии экструзии полимер экструдируют при 230°С (зоны нагрева с 1 по 6, Tмакс: 230°С) и гранулируют. В дальнейшем экструдат вновь экструдируют при 270°С (зоны нагрева с 1 по 6, Tмакс: 270°С; полипропилен Profax® 6501, фирма Montell).
Значения вязкости расплава после двух стадий экструзии представлены в таблице 9.
Последующая деструкция полипропилена
Стадии экструзии аналогичны стадиям в общем методе (зоны нагрева с 1 по 6, Tмакс: 250°С; полипропилен Profax® 6501, фирма Montell). Гидроксиламиновый сложный эфир добавляют в виде смеси в минеральном масле.
Регулируемая деструкция с использованием других NOR соединений
Стадии экструзии аналогичны стадиям в общем методе (зоны нагрева с 1 по 6, Tмакс: 250°С; полипропилен Profax® 6501, фирма Montell). Разные количества подмешиваемых добавок вследствие применения поправочного коэффициента, принимаемого во внимание с учетом разницы молекулярных масс.
Добавление солей металлов
Стадии экструзии аналогичны стадиям в общем методе (зоны нагрева с 1 по 6, Tмакс: 250°С; полипропилен Profax® 6501, фирма Montell). Добавление солей металлов приводит к улучшению значений СРР при пониженных температурах экструзии.
Добавление нитроксильных радикалов
Стадии экструзии аналогичны стадиям в общем методе (зоны нагрева с 1 по 6, Tмакс: 250°С; полипропилен Novolen® фирма Targor). Добавление солей металлов несколько снижает скорость деструкции и приводит к улучшению характеристик расплавов полимеров.
нитроксил А: бис(1-оксил-2,2,6, 6-тетраметилпиперидин-4-ил)декандиоат, продукт Prostab® 5415 (фирма Ciba SC)
Г) Регулируемое увеличение молекулярной массы полиэтилена
Общий метод
36 г полиэтилена (продукт Lupolen® 1812 Е, фирма Elenac GmbH) пластицируют в азотной атмосфере в течение 10 мин в смесителе Брабендера W50, в котором поддерживают температуру 220°С (скорость вращения: 40 об/мин). Вначале в смесительную камеру вместе с полиэтиленом вводят добавки. По прошествии периода реакции в течение 10 мин смешение прекращают, полимерную композицию из смесительной камеры извлекают и подвергают предварительному прессованию под нагрузкой примерно 50 кН в течение 1 мин при 220°С. После измельчения образца в соответствии с международным стандартом ISO 1133 определяют вязкость расплава (СРР).
В условиях переработки используемый полимер претерпевает уменьшение молекулярной массы (значение СРР больше, чем в случае исходного материала RY 653) (в примере Г1 добавки отсутствуют). В противоположность результатам этого сравнительного примера в эксперименте, который проводят в соответствии с настоящим изобретением (пример Г2), происходит увеличение молекулярной массы, которое выражается в уменьшении значения СРР.
Экструзия
Технический полиэтилен (Hostalen® GB7250, фирма Hoechst) экструдируют в двухчервячном экструдере ZSK 25 фирмы Werner & Pfleiderer при температуре Tмакс 270°С (зоны нагрева с 1 по 6), производительности 4 кг/ч и скорости вращения шнеков 100 об/мин с введением указанных добавок, гранулированных в водяной бане, и в соответствии с международным стандартом ISO 1133 определяют вязкость расплава (СРР). Уменьшение скорости истечения расплава указывает на возрастание длины цепей (увеличение молекулярной массы).
Вследствие добавления гидроксиламинового сложного эфира в создаваемых условиях переработки используемый ПЭВП претерпевает увеличение молекулярной массы, которое выражается в более низких значениях СРР в отличие от ее значений в сравнительном примере.
Реферат
Изобретение относится к области химии полимеров, а именно к применению гидроксиламиновых сложных эфиров для уменьшения молекулярной массы полипропилена, пропиленовых сополимеров или полипропиленовых смесей. При этом к пропиленовым полимерам, подвергаемым деструкции, добавляют, по меньшей мере, один гидроксиламиновый сложный эфир, выбранный из группы, включающей

где n обозначает 1, Ra обозначает ацильный радикал алифатической карбоновой кислоты, содержащей от 2 до 18 атомов углерода, R1′, R2 ′ и R3′ независимо друг от друга обозначают водородный атом или метил; a G означает ацил ацильного радикала алифатической карбоновой кислоты, содержащей от 1 до 18 атомов углерода, или ароматической карбоновой кислоты, содержащей от 7 до 18 атомов углерода;

где n обозначает 1, Ra обозначает ацильный радикал алифатической карбоновой кислоты, содержащей от 2 до 18 атомов углерода, R1′, R2′ и R3′ каждый независимо друг от друга означает водород или метил, G1 обозначает водородный атом, C2-C18алканоил, а G2 обозначает водородный атом, C1-C8алкил, ацил ацильного радикала алифатической карбоновой кислоты, содержащей от 1 до 18 атомов углерода;

где n обозначает 1, Ra обозначает ацильный радикал алифатической карбоновой кислоты, содержащей от 2 до 18 атомов углерода, R1′, R2′ и R3′ каждый независимо один от другого означает водород или метил, G3 имеет следующее значение C2-C8 алкилен, С4-С22ацилоксиалкилен или ацильный радикал алифатической карбоновой кислоты, содержащей от 1 до 18 атомов углерода, и смесь нагревают до температуры ниже чем 280° С. Добавление гидроксиламиновых сложных эфиров приводит к возрастанию степени деструкции используемого полипропиленового полимера, что отражают повышенные значения скорости истечения расплава в сопоставлении с этим же показателем у исходного полимера. 2 з.п. ф-лы, 15 табл.
Формула
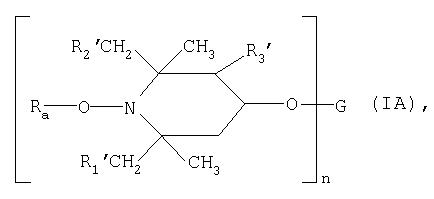

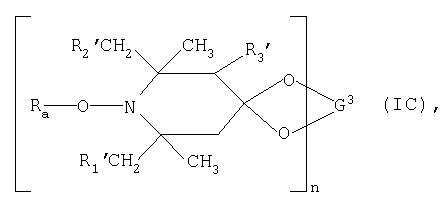
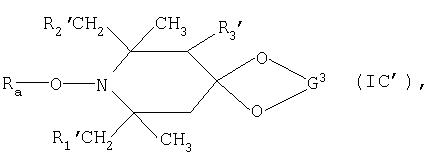

Документы, цитированные в отчёте о поиске
Способ и промежуточные продукты для получения простых гидроксиламиновых эфиров и их солей
Полипропилен с улучшенными свойствами и способ его получения











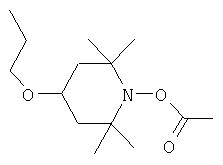





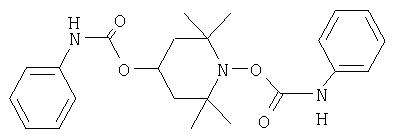






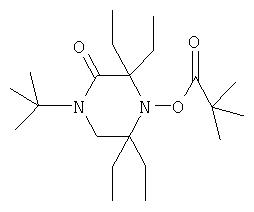
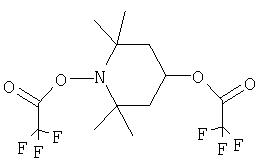
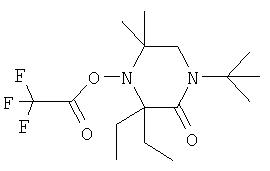


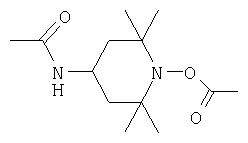
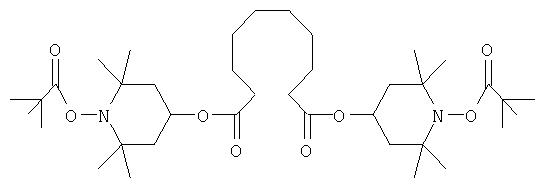

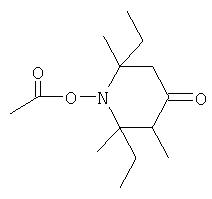
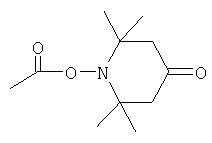
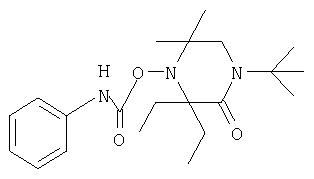
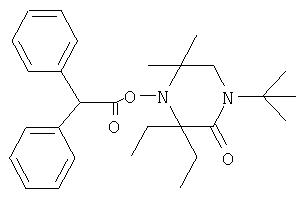






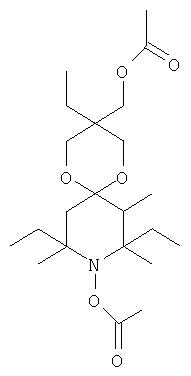
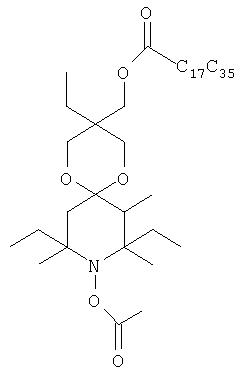




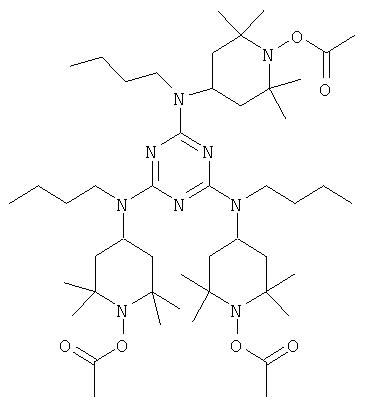









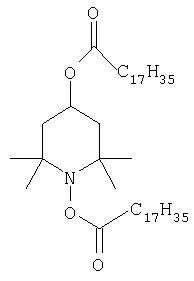

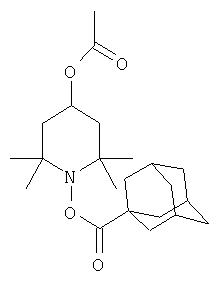
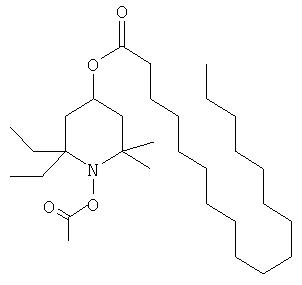
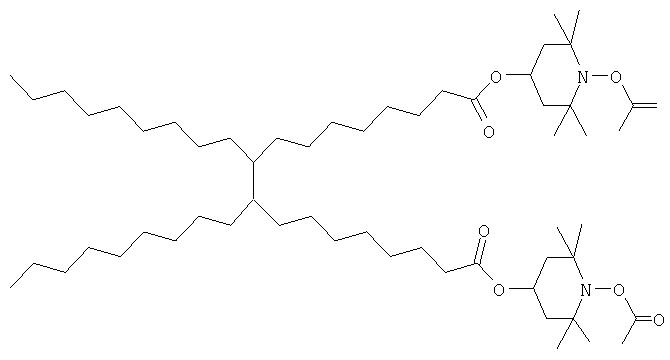
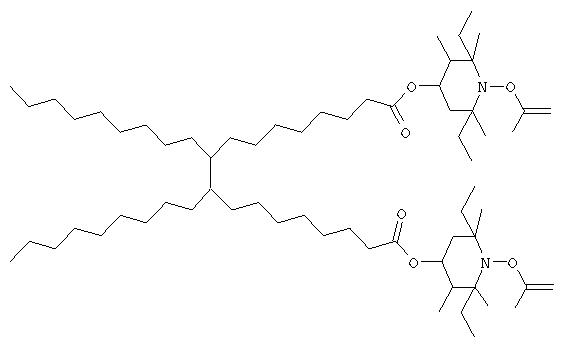

Комментарии