Корм для рыб - RU2060010C1
Код документа: RU2060010C1
Чертежи

Описание
Изобретение относится к корму
для рыб, содержащему измельченные пищевые компоненты и лекарственное средство [1]
Корм по изобретению в качестве лекарственного средства содержит соединение
следующей общей формулы (I):
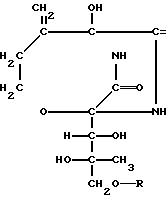
В последние годы достигнуты значительные успехи в борьбе (при разведении пресноводных и морских рыб) с сопутствующими вспышками различных заболеваний рыб. Для предотвращения и лечения определенных болезней рыб, например псевдотуберкулез у желтохвоста, часто применяют антибактериальные препараты типа ампициллина, оксолиновой кислоты и тому подобных. Однако обычное употребление этих антибактериальных препаратов представляет собой проблему, заключающуюся в том, что с увеличением частоты использования появлялись патогенные бактерии, устойчивые к этим антибактериальным препаратам.
Поэтому имеется насущная потребность в создании новых антибактериальных препаратов для предупреждения и лечения заболеваний у рыб, которые не обладали бы неблагоприятной невосприимчивостью традиционных лекарственных средство и являлись бы активными против такого рода невосприимчивых микроорганизмов.
Для решения этой проблемы заявители намеревались использовать бикозамицин (то же самое вещество, что и вещество WS-4545, которое вырабатывается некоторыми микроорганизмами рода streptomyces, публикация Японской патентной заявки N 29158, 1973), но нашли, что это вещество не обладало удовлетворительной усваиваемостью из кишечного тракта.
Между тем, некоторые сложные эфиры, синтезированные с целью улучшения поглощения бикозамицина после перорального введения (те же вещества, что и ацилированное вещество WS-4545, выкладка Японской патентной заявки N 39497, 1973), удовлетворяли этому требованию (Fhe Iournal of Antibiotics, т. XXY, N 10, с. 576-581), однако воздерживались от применения таких эфиров бикозамицина для рыб по следующей причине. Так, лекарственные препараты для рыб обычно вводят в виде включенных в состав сырого рыбного фарша, однако обычно полагают, что если эфир бикозамицина будет введен рыбе таким образом, особенно желтохвосту, то этот эфир будет гидролизоваться обратно до бикозамицина под действием эстеразы, находящейся в рыбном фарше, так что цель улучшения перорального поглощения лекарственного препарата не будет достигнута. (Действительно, когда известный эфир ампициллина, а именно бикампициллин, помещают в рыбный фарш перед употреблением, то он в фарше разлагается).
В данных условиях попробовали в порядке эксперимента ввести рыбам вышеуказанным способом эфир бикозамицина, соединение (I), и неожиданно нашли, что этот эфир практически не разлагался в рыбном фарше, однако хорошо поглощался кровью и сохранялся там с высокой концентрацией в течение длительного времени. За этим открытием последовала исследовательская работа, результаты которой изложены в данном изобретении.
Целью изобретения является преодоление вышеуказанной проблемы, и оно направлено на корм для рыб, предназначенный для предупреждения и лечения болезней у рыб и содержащий в качестве активного ингредиента соединение (I).
В соответствии с данным изобретением, используемое соединение (I), как сказано выше, представляет собой по существу известное соединение. Кроме того, бикозамицин, являющийся исходным веществом для этого соединения (I), известен в качестве антибиотика, вырабатываемого Streptomyces sapporonensis АТСС 21532, что описано в Японской публикации патентной заявки N 29158, 1973, на которую ссылались выше.
Упомянутый выше штамм продуцента.
Депозитарий: Американская коллекция типовых культур.
Адрес: Parklawn Drive 12301, Rockville, ellaryland, США.
Дата депонирования: апрель 21, 1970.
Депозитарный N: АТСС 21532.
Говоря о соединении(I), предпочтительные примеры указанной алканоильной группы включают ацетил, пропионил, бутирил, изобутирил, валерил, изовалерил, октаноил, пильмитоил и так далее; предпочтительными алкилами указанной низшей алкильной группы являются метил, этил, пропил и так далее; а предпочтительными галогенами являются хлор, бром и йод.
Ниже приведен неполный список типичных представителей соединения (I), которые могут быть использованы в данном изобретении.
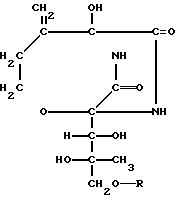
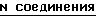
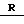
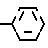
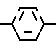
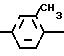
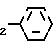
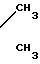
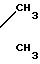
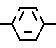
Рыбы и их заболевания, для которых применим корм по изобретению, включают среди прочих псевдотуберкулез (Pasteurella piscicida) желтохвоста и каранга, вибриоз (Vibrio anguillarum) желтохвоста, айю и морского карася, эдвардсиллез (Edwardsiella tarda) японского угря, плоской рыбы и морского карася и фурункулез (Aeromonas salmonicida) радужной форели.
Корм по изобретению может быть приготовлен переработкой соединения (I) в лекарственную форму типа порошка, пыли, микрогранул тонкого помола, гранул, гранул тонкого помола, таблеток, жидкости, пилюли или сиропа с твердым, полутвердым или жидким носителем или без носителя, и добавлением пищевых компонентов с получением рецептурного корма, содержащего соединение (I) или указанную лекарственную форму.
Носитель включает среди прочих сырой рыбный фарш (например, мелкоизрубленную скумбрию, сардину, кремериевые, макрелещуку, минтай, кальмар и так далее), рецептурный корм, основанный на рыбной муке, жмыхе сои, дрожжах, пшеничной муке, витаминах и так далее, и также общепринятые носители как лактоза, сахароза, глюкоза, крахмал, тальк, кислая глина и так далее.
Кроме того, могут быть добавлены в соответствующих количествах эмульгаторы, диспергирующие агенты, агенты желатинизации, связующие вещества и так далее.
Корма, содержащие соединение (I), можно применять для предупреждения заболеваний и лечения болезней у желтохвоста, каранга, айю, карпа, морского карася, японского угря, плоской рыбы, радужной форели и так далее. Например, для профилактики и лечения псевдотуберкулеза у желтохвоста наиболее предпочтительное лечебное воздействие, учитывая преимущество в стабильности соединения (I) в рыбном фарше, достигается добавлением соединения (I) в виде порошка или мелкозернистых гранул, предварительно смешанного с указанным носителем, к сырому рыбному фаршу или к смеси такого сырого рыбного фарша и рецептурного корма, и введением всей смеси или в том виде, как она есть, или предварительно в спрессованном виде в виде гранул или влажных гранул.
Дозировка и продолжительность кормления для лечения болезней у рыб зависит от вида и возраста рыб, температуры воды, тяжести заболевания и так далее. Например, для предупреждения и лечения псевдотуберкулеза у желтохвоста обычно может быть введено перорально от 1 до 50 мг в расчете на соединение (I) в день на 1 кг веса рыбы в течение 3-10 дней.
Корм, содержащий соединение (I), не проявляет неблагоприятную невосприимчивость традиционных лекарственных средств, активен против невосприимчивых штаммов микроорганизмов и устойчив в виде сырого рыбного фарша. Следовательно, когда корм в виде смеси с сырым рыбным фаршем вводят рыбам, то этот корм гарантирует с достаточной надежностью в крови рыб высокую концентрацию бикозамицина в течение длительного периода времени. Следующие испытательные примеры предназначены для иллюстрации эффективности этого изобретения.
Тест 1 (временная зависимость концентрации бикозамицина в крови желтохвоста).
Активное соединение смешивали с размельченным карангом и вводили желтохвосту свободно, доступным способом, в виде однократной дозы в 50 мг/кг. Через 6, 9, 12, 24, 36, 48 и 72 ч после введения из сердца брали кровь.
Затем определяли концентрацию бикозамицина в крови посредством биопробы, используя в качестве испытуемого микроорганизма Е.coli BS-10.
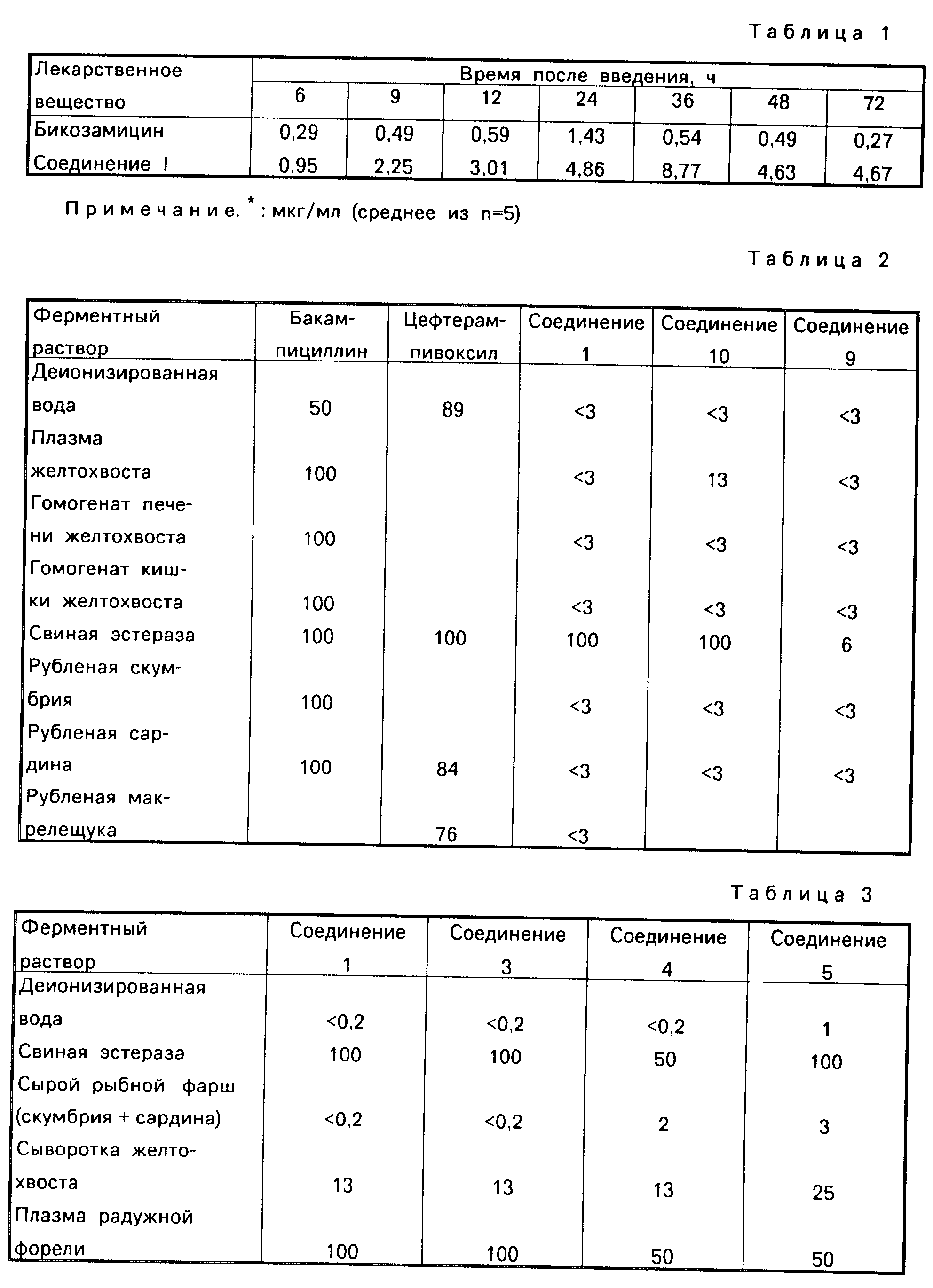
Результаты приведены в табл.1.
Тест 2 (стабильность в ферментных растворах 1).
Каждое испытуемое лекарственное средство растворяли в воде до конечной концентрации 2000 мкг/мл.
Затем к различным ферментным растворам (порции по 0,9 мл) добавляли растворы каждого лекарственного средства (порции по 0,1 мл).
Ферментные растворы готовили следующим образом.
Деионизированная вода: контроль на отсутствие фермента.
Плазма желтохвоста: в гепаринизированный шприц отбирали кровь из сердца желтохвоста, центрифугировали ее в течение 15 мин при 3000 об/мин и получали плазму.
Гомогенат печени желтохвоста: у живого выращенного желтохвоста брали печень, размельчали ее и гомогенизировали.
Гомогенат кишки желтохвоста: у живого выращенного желтохвоста брали кишку, размельчали ее и гомогенизировали.
Свиная эстераза: выпускаемую промышленностью свиную эстеразу (Sigma) разбавляли 50-кратным объемом воды.
Рубленая скумбрия: покупали свежую скумбрию, всю рыбу размельчали и пропускали через мясорубку. Рыбный фарш гомогенизировали с 2 объемами воды, центрифугировали в течение 15 мин при 3000 об/мин и использовали супернатант в качестве ферментного раствора.
Рубленая сардина: получали таким же образом, как и рубленую скумбрию.
Рубленая макрелещука: получали таким же образом, как и рубленую скумбрию.
Раствор лекарственного средства смешивали с ферментным раствором и проводили реакцию при 25оС в течение 2 ч.
Для того, чтобы погасить ферментативную реакцию, добавляли 1,0 мл метанола.
Реакционную смесь осторожно перемешивали и центрифугировали в течение 5 мин при 6400 об/мин. В супернатант погружали диск из бумаги и определяли концентрацию ампициллина, цефтерама (родственное соединение цефтерам пивоксила) или бикозамицина посредством биопробы, используя в качестве испытуемого штамма Е.сoli BS-10.
Результаты приведены в табл.2. Приведенные цифровые данные представляют собой скорости превращения бакампициллина в ампициллин, цефтерам пивоксила в его родственное соединение (Journal of. Japan Society of chemotherapy, т. 34, S-2, с. 44-60, 1986) и соединения этого изобретения в бикозамицин.
Тест 3 (стабильность в ферментных растворах 2).
Каждое испытуемое лекарственное средство растворяли в воде до конечной концентрации 1000 мкг/мл.
Затем к порциям по 0,36 мл различных ферментных растворов добавляли порции по 0,04 мл раствора каждого лекарственного средства.
Ферментные растворы готовили следующим образом.
Деионизированная вода: контроль отсутствия фермента.
Свиная эстераза: выпускаемую промышленностью свиную эстеразу (Sigma) разбавляли 50-кратным объемом воды.
Сырой рыбный фарш: покупали свежую скумбрию и сардину и равные доли соответствующих целых рыб размельчали и перемешивали. Эту смесь пропускали через мясорубку, гомогенизировали с 2 объемами воды и центрифугировали в течение 15 мин при 3000 об/мин. В качестве ферментного раствора использовали супернатант.
Сыворотка желтохвоста: в шприц отбирали кровь из сердца желтохвоста, выдерживали ее при комнатной температуре в течение 1 ч, а затем центрифугировали в течение 15 мин при 3000 об/мин и получали сыворотку.
Плазма радужной форели: в гепаринизированный шприц отбирали кровь из сердца радужной форели, центрифугировали ее в течение 15 мин при 3000 об/мин и получали плазму.
Раствор лекарственного средства смешивали с ферментным раствором и проводили реакцию при 30оС в течение 3 ч.
Для того, чтобы погасить ферментативную реакцию, добавляли 0,4 мл метанола.
После осторожного перемешивания реакционную смесь центрифугировали при 64000 об/мин в течение 5 мин. В супернатант погружали диск из бумаги и определяли концентрацию бикозамицина посредством биопробы, используя в качестве испытуемого штамма Е.coli BS-10.
Результаты приведены в табл.3. Приведенные цифровые данные представляют собой скорости превращения соединений этого изобретения в бикозамицин.
Тест 4 (сравнение с традиционными лекарственными препаратами).
Желтохвостов весом около 200 г каждый, которые имели развитый псевдотуберкулез на большом пространстве, разделили на 7 групп по 200 рыб и лечили по следующей схеме применения лекарственного средства. Группа I: контрольная группа, которой не давали лекарственные средства; группа II: ампициллин 20 мг/кг; группа III: оксолиновая кислота 30 мг/кг; группа IV: соединение I 20 мг/кг; группа V: соединение I 40 мг/кг; группа VI: соединение 2 20 мг/кг; группа VII: соединение 2 40 мг/кг. Был определен общий вес рыб в каждой группе. В каждой группе рыб не кормили в течение одного дня, а затем давали им один раз в день в течение 5 последовательных дней смесь рецептурного корма для желтохвоста и соответствующего лекарственного средства (10% в лактозе) в виде дополнительной смеси к размельченным кремериевым. Каждый день в утренние часы умерших рыб вытаскивали и регистрировали число погибших рыб. Кроме того, для подтверждения того, что смерть наступила вследствие псевдотуберкулеза, производили вскрытие всех умерших рыб.
Ежедневно, в утренние часы, измеряли температуру воды и записывали ее.
Результаты приведены в табл.4.
Тест 5 (сравнение с бикозамицином).
Желтохвостов весом около 200 г каждый, которые имели развитый псевдотуберкулез на большом пространстве, разделили на 4 группы по 300-320 рыб и лечили по следующей схеме применения лекарственного средства. Группа I: контрольная группа, которой не давали лекарственные средства; группа II: бикозамицин 20 мг/кг; группа III: соединение I 20 мг/кг; группа IV: соединение 2 20 мг/кг. Был определен общий вес рыб в каждой группе. Рыб в каждой группе не кормили в течение одного дня, а затем давали им один раз в день в течение 5 последовательных дней смесь рецептурного корма для желтохвоста и соответствующего лекарственного средства (10% в лактозе) в виде дополнительной смеси к размельченным кремериевым. Каждый день в утренние часы умерших рыб вытаскивали и регистрировали число погибших рыб. Кроме того, для подтверждения того, что смерть наступила вследствие псевдотуберкулеза, производили вскрытие всех умерших рыб.
Ежедневно в утренние часы измеряли температуру воды и записывали ее.
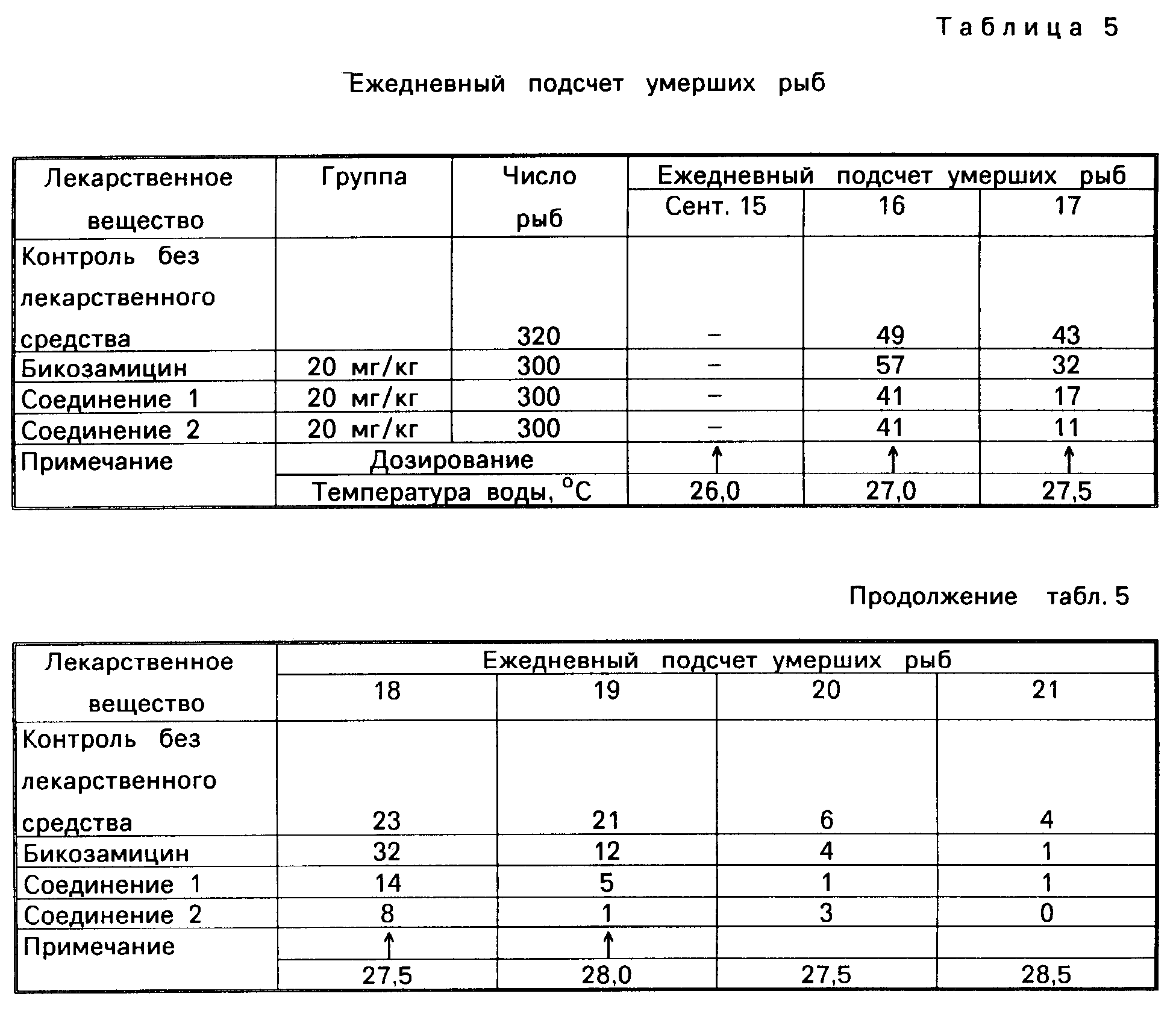
Результаты приведены в табл.5.
П р и м е р 1. Порошок получают, смешивая 6,7 мас.ч. соединения I (по эффективности соответствует 5 мас.ч. бикозамицина) с 93,3 мас.ч. лактозы.
Используя 100 г этого порошка в качестве единицы суточной дозы, кормят около 20000 желтохвостов (вес одного желтохвоста составлял около 50 г, а суммарный вес всех рыб 1 т) смесью, содержащей эту суточную дозу и 200 кг фарша из кремериевых, в течение 5 последовательных дней. Вышеуказанный режим питания достигает цели, заключающейся в предотвращении и лечении псевдотуберкулеза у желтохвостов.
П р и м е р 2. Порошок получают, смешивая 6,7 мас.ч. соединения I (по эффективности соответствует 5 мас.ч. бикозамицина) с 93,3 мас.ч. лактозы.
Около 15000 желтохвостов (вес одного желтохвоста около 200 г, а суммарный вес всех рыб 3 т) дают в течение 5 последовательных дней влажные гранулы (цилиндрические гранулы, полученные смешиванием фарша из сардин с порошкообразным рецептурным кормом на основе рыбной муки в соотношении 6:4 с последующим механическим гранулированием этой смеси), к которым добавлены 300 г вышеуказанного порошка. Этот режим питания достигает цели, заключающейся в предотвращении и лечении псевдотуберкулеза у желтохвостов.
Исходя из вышеуказанного, корм по изобретению может быть использован в качестве профилактического/терапевтического средства, в частности терапевтического средства для лечения болезней рыб и, таким образом, для увеличения добычи рыбы.
Реферат
Использование: в рыбоводстве в
качестве профилактического или терапевтического средства против болезней рыб. Корм для рыб включает измельченные пищевые компоненты и
лекарственное средство, в качестве которого в корм вводят
соединение следующей общей формулы
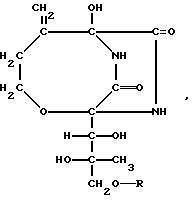
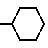
где R - алконоильная группа, бензоильная группа, возможно имеющая одну или более групп-заместителей, выбранных из группы, состоящей из низших алкилов и галогенатомов; фенилацетильная группа или циклогексанкарбонильная группа. Корм, содержащий соединение общей формулы, не проявляет неблагоприятную невосприимчивость традиционных лекарственных средств, активен против невосприимчивых штаммов микроорганизмов и устойчив в виде сырого рыбного фарша. Корм гарантирует в крови рыб высокую концентрацию бикозамицина в течение длительного периода времени. 5 табл.
Формула
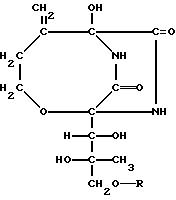
R алконоильная группа, бензоильная группа, возможно имеющая одну или более групп-заместителей, выбранных из группы, состоящей из низших алкилов и галоген-атомов, фенилацетильная группа или циклогексанкарбонильная группа.

Комментарии