Способ безметочного одномолекулярного секвенирования днк и устройство для его реализации - RU2679494C1
Код документа: RU2679494C1
Чертежи

























Описание
Область техники
Группа изобретений относится к области технологии определения нуклеотидной последовательности, или секвенирования, нуклеиновых кислот, а именно ДНК или РНК. Раскрываемое изобретение может найти применение при генетической диагностике различных заболеваний человека и животных, а также в других областях прикладной или научной деятельности.
Уровень техники
В течение последних двух десятилетий были разработаны многие новые методы высокопродуктивного секвенирования нуклеиновых кислот и некоторые из них в настоящее время широко используются в медицинских, сельскохозяйственных задачах, в вопросах безопасности, идентификации личности, в пищевых и биотехнологиях. Эти методы относятся к трем основным группам технологий: (1) секвенирование методами лигирования (например, метод секвенирования SOLiD, используемый Life Technologies / Thermo Fisher; метод секвенирования Combinatorial Probe-Anchor Ligation™ (cPAL™), используемый BGI/Complete Genomics); (2) секвенирование методами последовательного синтеза, включающее: (а) циклическое секвенирование, используемое как Illumina Inc., так и Qiagen Inc., (б) метод одномолекулярного виртуального терминирования в режиме реального времени, используемый Helicos BioSciences, (с) подход с поочередным однонуклеотидным присоединением, включая 454 пиросеквенирование с оптическим считыванием, используемый Roche Inc., и метод на основе ионно-чувствительного полевого транзистора с электронным считыванием, используемый Ion Torrent / ThermoFisher; (3) одномолекулярные методы секвенирования в режиме реального времени, позволяющие получать при прочтении длинные непрерывные последовательности нуклеиновых кислот (длинные риды) из одной реакции: (а) одномолекулярное секвенирование в реальном времени (SMRT), основанное на обнаружении нуклеотидов в волноводе размером меньше длины волны (ZMW) от Pacific Biosciences, которое использует нуклеотиды, меченые флуорофорами, и (б) безметочный метод секвенирования, использующий электронный способ считывания сигнала при прохождении фрагмента дезоксирибонуклеиновой кислоты (ДНК) через нанопору, используемый Oxford Nanopore Technologies. Первая (1) и вторая (2) группы технологий, упомянутые выше, в совокупности называются технологиями секвенирования второго поколения (SGS), а третья (3) группа - технологиями секвенирования третьего поколения (TGS).
Секвенирование с помощью методов лигирования (SOLiD и cPAL) использует дорогостоящие меченые флуорофором зонды, их скорость секвенирования, а также длина считывания ограничена внутренними свойствами ДНК-лигаз. Методы секвенирования путем синтеза от Illumina и Qiagen быстрее и дают считывание длиной до 300 пар оснований (п.о.) по сравнению с секвенированием методами лигирования, но также зависят от дорогостоящих флуоресцентно меченных молекул, терминаторных нуклеотидов. Полупроводниковое секвенирование от Ion Torrent / Thermo Fisher в настоящее время является единственным коммерчески доступным методом безметочного секвенирования, но он по-прежнему полагается на циклы добавления одиночных нуклеотидов, в отличие от одномолекулярного секвенирования в реальном времени (SMRT-метода), движимого высокопроизводительной ДНК-полимеразой. Последний метод является единственным быстрым коммерческим методом секвенирования с длинными ридами в режиме реального времени. Недостатками метода SMRT являются использование меченых нуклеотидов и громоздкой дорогой оптики, высокая частота ошибок, высокая чувствительность к переносимым примесям, введенным при построении библиотеки, и значительно меньшая пропускная способность по сравнению, например, с методами Illumina, SOLiD, Ion Torrent / Thermo Fisher и BGI / Complete Genomics. Эти недостатки метода SMRT приводят к высокой стоимости как инструмента, так и секвенируемой нуклеотидной последовательности.
Платформы секвенирования SGS, за исключением метода виртуального терминирования Helicos Biosciences, выполняют секвенирование кластеров (ансамблей клонированных амплифицированных с помощью ДНК-полимеразы молекул ДНК), тогда как технологии TGS непосредственно определяют нуклеотидную последовательность отдельных молекул. Кроме того, на платформах SGS используются технологии «промывка и сканирование» (например, Illumina) или «промывка и измерение» электрического сигнала (Ion Torrent), а платформы TGS - непрерывные технологии непрерывного последовательного управления, без необходимости останавливаться между шагами чтения. Секвенирование TGS происходит очень быстро, и скорость определяется скоростью синтеза полимеразы или скоростью перемещения ДНК через нанопору. Кроме того, технологии TGS не требуют предварительной амплификации ДНК (во время подготовки библиотеки или генерации кластеров), тем самым упрощая сложности, связанные с амплификацией (такие как возникновение ошибок и дискриминация фрагментов ДНК библиотеки с высоким содержанием GC и/или AT). Длинные непрерывные последовательности нуклеиновых кислот, полученные методами TGS (длинные риды), значительно помогают в фазировании геномов и, таким образом, уменьшают потребность в дополнительных методах для сборки генома.
Несмотря на то, что технологии TGS обеспечивают короткий временной цикл обработки, их основным недостатком в конкурентной борьбе по сравнению с технологиями SGS является высокая частота ошибок, более низкий выход данных для одной ячейки секвенирования и высокая стоимость для каждой секвенированной последовательности. Для расширения биомедицинских применений TGS необходимо минимизировать количество ошибок, увеличить производительность секвенирования, снизить стоимость. Настоящее описание представляет способы, устройства и их композиции для низкозатратного, высокопроизводительного, безметочного одномолекулярного секвенирования в реальном времени с электронным считыванием. Эти способы представляют собой новую технологию секвенирования нуклеиновых кислот и могут использоваться в различных биомедицинских, сельскохозяйственных и биологических целях.
Определения и термины
Для лучшего понимания настоящего изобретения ниже приведены некоторые термины, примененные в настоящем описании изобретения.
В описании данного изобретения слова «включает» и «включающий» интерпретируются как означающие «включает, помимо всего прочего». Указанные слова далее по тексту, за исключением специально оговариваемых случаев, не предназначены для того, чтобы их истолковывали как «состоит только из».
Под нуклеотидом в описании данного изобретения следует понимать, в зависимости от варианта реализации, как рибонуклеотиды, например, аденозинтрифосфат, гуанозинтрифосфат, цитидинтрифосфат и уридинтрифосфат, обозначаемые ATP, GTP, СТР, UTP), так и дезоксирибонуклеотиды, например, дезоксиаденозинтрифосфат, дезоксигуанозинтрифосфат, дезоксицитидинтрифосфат и дезокситимидинтрифосфат (dATP, dGTP, dCTP, dTTP). В предпочтительных вариантах изобретения используются нуклеотиды, не содержащие меток и модификаций.
Под реакционной смесью понимается водный раствор, содержащий все необходимые вещества для обеспечения выполнения реакции полимеризации одноцепочечных фрагментов ДНК, находящихся в составе комплекса «полимераза-фрагмент ДНК», иммобилизованного на поверхности сенсора ячейки матрицы микросхемы.
Под разделением зарядов, происходящим в результате встраивания полимеразой нуклеотида в растущую цепь нуклеиновой кислоты, следует понимать разделение одной пары зарядов (присоединение электрона к растущей цепи нуклеиновой кислоты и выделение иона водорода в раствор), которое объективно происходит всякий раз, когда происходит встраивание нуклеотида в полимеризуемый фрагмент ДНК или РНК.
Сенсором называется электронное устройство, одна или несколько электрических характеристик которого модулируются в результате образования одной пары несвязанных зарядов, происходящего в непосредственной близости от поверхности сенсора, в результате встраивания полимеразой нуклеотида в полимеризуемый фрагмент ДНК.
Ячейкой называется электронное устройство, включающее в себя сенсор и аналого-цифровую схему, которая в каждый дискретный интервал времени преобразует значение модулируемой характеристики сенсора в логический «0» или «1» в зависимости от ее величины.
Матрицей ячеек сенсоров называется упорядоченный массив из ячеек, организованный в виде строк и столбцов, как правило, в форме квадрата или прямоугольника, содержащей вертикальные и горизонтальные сдвиговые регистры, обеспечивающие вывод цифровых данных от каждой ячейки матрицы за ее границы, для последующей, например, компьютерной обработки.
Микросхемой матрицы ячеек сенсоров называется совокупность матрицы ячеек сенсоров и аналого-цифровой схемы, включающей в себя генератор тактовых импульсов, источник опорного напряжения, контроллер управления режимами работы ячеек, обеспечивающей функционирование ячеек и регистров матрицы и изготовленных в одном технологическом цикле.
Электродом смещения называется металлический проводник той или иной формы, например, в форме решетки, тем или иным способом закрепленный на крышке микросхемы (изготовленной из токонепроводящего материала), в рабочем состоянии находящийся в рабочем растворе, гальванически связанный с источником опорного напряжения микросхемы, обеспечивающий разницей потенциалов с электродом каждой ячейки матрицы наличие электрического поля в растворе, которое способствует скорейшему удалению иона водорода от места разделения пары зарядов при встраивании полимеразой нуклеотида в полимеризуемый фрагмент ДНК.
Циклограммой в настоящем изобретении названа последовательность дискретных интервалов времени, в которой логической единицей "1" обозначены те дискретные интервалы времени, в течении которых аналого-цифровой схемой ячейки были зарегистрированы факты разделения зарядов в результате встраивания полимеразой нуклеотидов, а логическими нулями "0" обозначены дискретные интервалы времени, когда таких фактов зарегистрировано не было. Дискретным интервалом времени назван период тактовых импульсов, обеспечивающих работу аналого-цифровой схемы ячейки.
Процессивность (англ. processivity) - это способность фермента осуществлять последовательность химических реакций, без высвобождения субстрата. В случае полимеразы процессивность - это среднее число нуклеотидов, добавляемое ферментом к растущей цепи за одно связывание с поверхностью матрицы микросхемы.
Если не определено отдельно, технические и научные термины в данной заявке имеют стандартные значения, общепринятые в научной и технической литературе.
Сущность изобретения
Задачей настоящего изобретения является создание быстрого, высокоточного и недорогого метода определения нуклеотидной последовательности, или секвенирования, нуклеиновых кислот. В настоящем изобретении указанная задача решается путем реализации нескольких технических решений. Реализуются совместно три основных положения, позволяющие обеспечить технический результат: (1) минимум манипуляций с реагентами и ДНК, которые участвуют в биохимической реакции; (2) регистрация электронным сенсором полезного сигнала о фактах разделения одной пары зарядов, которые происходят в результате встраивания полимеразой ДНК каждого нуклеотида в растущую цепь ДНК; (3) оригинальный алгоритм секвенирования, который позволяет разделить во времени процедуру формирования полезных сигналов и процедуру формирования целевой информации, как результат обработки полезных сигналов, - что позволяет отказаться от меток для нуклеотидов.
Указанная задача решается путем создания способа определения нуклеотидной последовательности молекулы нуклеиновой кислоты, включающего по меньшей мере следующие стадии:
(а) получение образца нуклеиновой кислоты, представляющего собой множество закольцованных фрагментов нуклеиновой кислоты; (б) иммобилизация на твердой поверхности комплексов, состоящих по меньшей мере из указанных закольцованных фрагментов нуклеиновой кислоты и полимеразы, имеющей сродство к нуклеиновой кислоте, где твердая поверхность представляет собой поверхность сенсора, а иммобилизация сохраняет функциональность полимеразы и обеспечивает нахождение полимеразы вблизи поверхности сенсора в течение всего процесса определения нуклеотидной последовательности; (в) обеспечение условий для функциональной активности указанной полимеразы, заключающейся в катализе присоединения нуклеотидов к растущей цепи нуклеиновой кислоты, где условия для функциональной активности полимеразы включают: добавление на поверхность сенсора смеси двух или более видов немеченых дезоксирибонуклеотидов, выбранных из группы, состоящей из дезоксиаденозинтрифосфата, дезоксигуанозинтрифосфата, дезоксицитидинтрифосфата и дезокситимидинтрифосфата, или добавление на поверхность сенсора смеси двух или более видов немеченых рибонуклеотидов, выбранных из группы, состоящей из аденозинтрифосфата, гуанозинтрифосфата, цитидинтрифосфата и уридинтрифосфата, при этом в указанной смеси нуклеотид одного вида присутствует в значительно меньшей концентрации, чем нуклеотиды других видов; (г) регистрация сенсором факта разделения зарядов, происходящего в результате встраивания полимеразой нуклеотида в растущую цепь нуклеиновой кислоты, и определение временных интервалов между каждым последующим зарегистрированным фактом разделения зарядов; (д) по меньшей мере однократное повторение стадий (в) и (г), при этом при каждом повторении вид нуклеотида, присутствующего в добавляемой смеси нуклеотидов в значительно меньшей концентрации по сравнению с другими видами, изменяется; (е) определение нуклеотидной последовательности указанной молекулы нуклеиновой кислоты, основанное на анализе определенных на стадиях (г) и (д) временных интервалов между каждым зарегистрированным фактом разделения зарядов, где разделения зарядов произошли в результате встраивания полимеразой указанных немеченых нуклеотидов в растущую цепь нуклеиновой кислоты.
Некоторые варианты изобретения включают в себя описанный выше способ, в котором указанные в (а) закольцованные фрагменты нуклеиновой кислоты имеют по меньшей мере один одноцепочечный участок (см. Фиг. 1А и 1Б); указанные в (б и в) комплексы, дополнительно включают секвенирующий праймер, имеющий нуклеотидную последовательность, комплементарную указанному одноцепочечному участку; и условия для функциональной активности полимеразы дополнительно включают условия, обеспечивающие образование дуплекса секвенирующего праймера с комплементарным участком указанного закольцованного одноцепочечного фрагмента дезоксирибонуклеиновой кислоты (см. Фиг. 1А и 1Б).
В некоторых вариантах изобретения указанные в (а) закольцованные фрагменты не имеют одноцепочечных участков способных образовать дуплекс с секвенирующим праймером (см. Фиг. 1В), поэтому указанные в (б и в) комплексы не включают секвенирующий праймер (см. Фиг. 1В); а синтез ДНК инициируется полимеразой с искусственно созданного свободного 3' конца в одной из цепей двухцепочечного закольцованного фрагмента.
Некоторые варианты изобретения включают в себя описанный выше способ, в котором нуклеиновой кислотой является ДНК; полимеразой, имеющей сродство к нуклеиновой кислоте, является ДНК полимераза, и нуклеотидами, добавляемыми на стадиях (в) и (д), являются дезоксиаденозинтрифосфат, дезоксигуанозинтрифосфат, дезоксицитидинтрифосфат или дезокситимидинтрифосфат. ДНК полимераза, пригодная для осуществления способа, включает по меньшей мере следующие ферменты: полимераза Phi29, большой фрагмент Bst ДНК полимеразы, полимераза VentR™, большой фрагмент Bsm ДНК полимеразы, Klenow фрагмент ДНК полимеразы I. Другие варианты изобретения включают в себя описанный выше способ, в котором полимеразой, имеющей сродство к нуклеиновой кислоте, является РНК полимераза; и нуклеотидами, добавляемыми на стадиях (в) и (д), являются аденозинтрифосфат, гуанозинтрифосфат, цитидинтрифосфат и/или уридинтрифосфат.
В некоторых предпочтительных вариантах изобретения в описанном выше способе на стадиях (в) и (д) происходит обеспечение четырех различных условий для функциональной активности полимеразы, а именно, добавление четырех различных смесей дезоксинуклеозидтрифосфатов на поверхность сенсора; при этом каждое из четырех различных условий для функциональной активности полимеразы присутствует непрерывно в течение интервала времени, достаточного для синтеза по меньшей мере одной копии закольцованного фрагмента ДНК, или по меньшей мере пяти копий закольцованного фрагмента ДНК. В этом случае анализ последовательности временных интервалов, используемый для определения нуклеотидной последовательности указанной молекулы нуклеиновой кислоты, включает по меньшей мере три этапа:
1) полученные последовательности временных интервалов между каждыми зарегистрированными фактами разделения зарядов, произошедшими в результате встраивания полимеразой немеченых нуклеотидов в растущую цепь нуклеиновой кислоты, преобразуют в форму последовательностей логических нулей и единиц, причем в каждой такой последовательности логической единицей обозначены факты встраивания нуклеотидов того вида, концентрация которого была известна и понижена в соответствующей этой последовательности реакционной смеси, а логическими нулями обозначены нуклеотиды видов, концентрация которых была нормальной в той же реакционной смеси;
2) формируют нуклеотидные последовательности фрагментов нуклеиновой кислоты из четырех последовательностей логических нулей и единиц, полученных после первого этапа преобразования данных для каждого фрагмента нуклеиновой кислоты;
3) нуклеотидные последовательности фрагментов нуклеиновых кислот преобразуют в определяемую нуклеотидную последовательность указанной молекулы нуклеиновой кислоты.
В других предпочтительных вариантах изобретения в описанном выше способе на стадиях (в) и (д) происходит одновременное использование четырех различных условий для функциональной активности полимеразы, включающее: (i) наличие четырех пространственно разнесенных матриц ячеек, содержащих указанные сенсоры; и (ii) параллельное добавление четырех различных смесей дезоксинуклеозидтрифосфатов на поверхность сенсоров, находящихся в четырех пространственно разнесенных матрицах ячеек сенсоров. В этом случае анализ последовательности временных интервалов, используемый для определения нуклеотидной последовательности указанной молекулы нуклеиновой кислоты, включает по меньшей мере четыре этапа:
1) полученные от сенсоров ячеек четырех матриц последовательности временных интервалов между каждыми зарегистрированными фактами разделения зарядов, произошедшими в результате встраивания полимеразой немеченых нуклеотидов в растущую цепь нуклеиновой кислоты, преобразуют в форму последовательностей логических нулей и единиц, причем логической единицей обозначены нуклеотиды того вида, концентрация которого была известна и понижена в реакционной смеси, а логическими нулями обозначены нуклеотиды видов, концентрация которых была нормальной в той же реакционной смеси над поверхностью той матрицы, от ячеек которой преобразуются выходные последовательности;
2) уменьшают количества последовательностей логических нулей и единиц до количества фрагментов, полученных после фрагментации исходной нуклеиновой кислоты, посредством операций сортировки, сравнения, выбора и усреднения одинаковых с определенной вероятностью последовательностей логических нулей и единиц, полученных от клонов одного фрагмента, иммобилизованных в составе комплексов на поверхности сенсоров ячеек одной матрицы, в одну последовательность логических нулей и единиц;
3) формируют нуклеотидные последовательности фрагментов нуклеиновой кислоты из четырех полученных последовательностей логических нулей и единиц,
4) нуклеотидные последовательности фрагментов нуклеиновых кислот преобразуют в определяемую нуклеотидную последовательность указанной молекулы нуклеиновой кислоты.
Указанная задача также решается путем создания устройства, реализующего тот или иной вариант способа одномолекулярного, безметочного секвенирования нуклеиновых кислот, описанный выше. Устройство для определения нуклеотидной последовательности молекулы нуклеиновой кислоты содержит: 1) по меньшей мере одну микросхему матрицы ячеек сенсоров, включающую матрицу с множеством ячеек сенсоров и аналого-цифровую схему; 2) микрофлюидное устройство для обеспечения подачи рабочих растворов к сенсорам ячеек матрицы микросхемы; 3) устройство обработки и отображения данных для управления режимами работы микрофлюидного устройства и микросхемы матрицы ячеек сенсоров для преобразования данных выходных последовательностей ячеек матрицы в нуклеотидную последовательность указанной молекулы нуклеиновой кислоты. В некоторых предпочтительных вариантах изобретения устройство характеризуется тем, что 1) каждая ячейка матрицы включает: сенсор, поверхность которого пригодна для иммобилизации полимеразного комплекса, регистрирующий факты разделения одной пары зарядов в водном растворе, происходящие в результате встраивания полимеразой каждого нуклеотида в полимеризуемый фрагмент ДНК комплекса, и формирующий сигналы, соответствующие зарегистрированным фактам разделения пар зарядов; аналого-цифровую схему ячейки для формирования выходных последовательностей дискретных интервалов времени соответствующих сигналам сенсора; и 2) аналого-цифровая схема микросхемы матрицы ячеек сенсоров включает: схему формирования токов, напряжений и тактовых частот, необходимых для работы аналого-цифровых схем ячеек матрицы; схему передачи выходных последовательностей ячеек матрицы в устройство обработки и отображения данных; схему дешифрирования данных, полученных от устройства обработки и отображения данных.
Твердая поверхность, пригодная для иммобилизации полимеразного комплекса, представляет собой поверхность сенсора, модифицированная для возможности иммобилизации полимеразного комплекса. Функциональные варианты модификации поверхности сенсора будут рассмотрены ниже. Аналого-цифровая схема микросхемы матрицы ячеек сенсоров выполнена с возможностью формирования токов, напряжений и тактовых частот, необходимых для работы аналого-цифровых схем ячеек матрицы, управления передачей выходных последовательностей ячеек матрицы в устройство обработки и отображения данных. Устройство также содержит микрофлюидное устройство для обеспечения подачи рабочих растворов к сенсорам ячеек матрицы микросхемы, устройство управления микрофлюидным устройством, микросхемой матрицы ячеек сенсоров, передачей данных от микросхемы к устройству обработки и отображения данных и устройство обработки и отображения данных для управления режимами работы микрофлюидного устройства, микросхемы матрицы ячеек сенсоров, для преобразования данных выходных последовательностей ячеек матрицы в нуклеотидную последовательность молекулы нуклеиновой кислоты.
Некоторые варианты изобретения подразумевают, что каждый дискретный интервал времени в выходных последовательностях обозначен логическими нулем или единицей, причем логической единицей обозначен тот интервал времени, в котором сенсором ячейки был зарегистрирован факт разделения пары зарядов в результате реакции.
В некоторых вариантах изобретения устройство дополнительно включает устройство поддержания температуры рабочего раствора над поверхностью матрицы микросхемы, управляемое устройством обработки и отображения данных.
В разных вариантах изобретения сенсор может быть выполнен в виде нанопроводного полевого транзистора, одноэлектронного транзистора, диода, полевого транзистора, или полупроводниковой структуры (электронной схемы) с S-образной или N-образной вольтамперной или передаточной характеристиками.
Некоторые варианты изобретения включают в себя последовательный способ секвенирования, при котором устройство секвенирования содержит только одну микросхему матрицы ячеек сенсоров, а реакционные смеси подаются поочередно на поверхность матрицы микросхемы. При этом устройство обработки и отображения данных преобразует данные выходных последовательностей от ячеек матрицы микросхемы в нуклеотидную последовательность молекулы нуклеиновой кислоты в три последовательных этапа.
На первом этапе данные выходных последовательностей, полученные от ячеек матрицы микросхемы последовательно преобразуются в форму последовательностей логических нулей и единиц, причем логической единицей обозначены факты встраивания нуклеотидов вида, концентрация которого была известна и понижена в соответствующей реакционной смеси, а логическими нулями обозначены нуклеотиды видов, концентрация которых была нормальной в той же смеси реакции; на втором этапе формируются нуклеотидные последовательности фрагментов нуклеиновой кислоты из четырех последовательностей логических нулей и единиц, полученных после первого этапа преобразования данных с одной и той же ячейки матрицы микросхемы; на третьем этапе нуклеотидные последовательности фрагментов нуклеиновых кислот могут быть преобразованы в нуклеотидные последовательности нуклеиновых кислот.
Некоторые варианты изобретения включают в себя параллельный способ секвенирования, при котором устройство секвенирования содержит четыре микросхемы матрицы ячеек сенсоров, а реакционные смеси подаются одновременно, асинхронно на поверхность матрицы каждой микросхемы. При этом устройство обработки и отображения преобразует данные выходных последовательностей, полученные ото всех ячеек всех матриц микросхем, в нуклеотидную последовательность молекулы нуклеиновой кислоты в четыре последовательных этапа.
На первом этапе данные выходных последовательностей, полученные от ячеек матриц четырех микросхем, преобразуются в форму последовательностей логических нулей и единиц, причем логической единицей обозначены нуклеотиды того вида, концентрация которого была известна и понижена в реакционной смеси, а логическими нулями обозначены нуклеотиды видов, концентрация которых была нормальной в той же реакционной смеси над поверхностью матрицы той микросхемы, от ячеек которой преобразуются выходные последовательности; на на втором этапе производится уменьшение количества последовательностей логических нулей и единиц до количества фрагментов, полученных после фрагментации исходной нуклеиновой кислоты, посредством операций сортировки, сравнения, выбора и усреднения одинаковых с определенной вероятностью последовательностей логических нулей и единиц, полученных от клонов одного фрагмента, иммобилизованных в составе комплексов на поверхности сенсоров ячеек матрицы одной микросхемы, - в одну последовательность логических нулей и единиц; на третьем этапе формируются нуклеотидные последовательности фрагментов нуклеиновой кислоты из четырех последовательностей логических нулей и единиц, взятых по одной от каждой из четырех микросхем; на четвертом этапе нуклеотидные последовательности фрагментов нуклеиновых кислот могут быть преобразованы в нуклеотидные последовательности нуклеиновых кислот.
Некоторые варианты изобретения включают в себя комбинированный способ секвенирования, при котором устройство секвенирования содержит две или три микросхемы матрицы ячеек сенсоров, и часть реакционных смесей подаются одновременно, асинхронно на поверхность матрицы каждой микросхемы, а оставшаяся часть реакционных смесей подается последовательно с первоначально поданной частью реакционных смесей.
В предпочтительных вариантах изобретения в реакционных смесях применяется пониженная концентрация нуклеотидов одного вида, против нормальной концентрации нуклеотидов трех других видов в реакционной смеси (суть способа секвенирования не изменится, если реакционная смесь содержит нуклеотиды одного вида, концентрация которых нормальна и нуклеотиды трех других видов, концентрация которых понижена; или, если реакционная смесь содержит нуклеотиды одного вида, концентрация которых повышена и нуклеотиды трех других видов, концентрация которых нормальна, и т.п.).
В предпочтительных вариантах изобретения для целей медицинской диагностики применяется последовательный способ секвенирования, как не требующий обязательной амплификации нуклеиновой кислоты, взятой для секвенирования.
При осуществлении изобретения достигаются следующие технические результаты:
- предложенное устройство одномолекулярного безметочного секвенирования обеспечивает повышение точности секвенирования нуклеиновых кислот по сравнению с существующими устройствами секвенирования за счет многократной полимеризации закольцованного фрагмента ДНК комплекса в одной и той же реакционной смеси, что обеспечивает возможность усреднения длительности интервалов времени перед встраиванием каждого нуклеотида в закольцованном фрагменте ДНК комплекса и повышает вероятность правильного определения мест расположения на фрагменте ДНК нуклеотидов вида, концентрация которого понижена в этой реакционной смеси;
- предложенное устройство одномолекулярного безметочного секвенирования обеспечивает повышенную производительность секвенирования за счет возможности использования способа секвенирования синтезом (SBS) с предельно возможным темпом полимеризации фрагмента ДНК (получение ресеквенированного генома человека менее чем за 12 часов);
- предложенное устройство одномолекулярного безметочного секвенирования обеспечивает более низкую стоимость устройства и результата секвенирования по сравнению с другими устройствами секвенирования (менее $1000 за ресеквенированный геном человека), за счет отсутствия дорогостоящих меток для нуклеотидов, низкого расхода реагентов, невысокой стоимости микросхемы матрицы ячеек сенсоров, изготовленной на основе промышленной полупроводниковой технологии.
Краткое описание чертежей
Прилагаемые чертежи, которые включены в состав настоящего описания и являются его частью, иллюстрируют варианты осуществления изобретения и совместно с вышеприведенным общим описанием изобретения и нижеприведенным подробным описанием вариантов осуществления служат для пояснения принципов настоящего изобретения.
На фиг. 1 представлено схематическое изображение вариантов закольцованных фрагментов ДНК и соответствующих сформированных комплексов этих фрагментов с полимеразой. (А) одноцепочечное кольцо ДНК; (Б) гантелеобразная кольцевая ДНК; (В) двухцепочечное кольцо ДНК, в котором одна цепь ковалентно замкнута, а вторая - нет.
На фиг. 2 изображена схема возможного варианта метода пробоподготовки.
На фиг. 3 представлено схематическое изображение последовательности шагов процедуры секвенирования в предпочтительных вариантах изобретения. (А) Последовательная процедура секвенирования: последовательное добавление четырех реакционных смесей нуклеозидтрифосфатов, причем каждая из смесей имеет один вид нуклеозидтрифосфатов, молекулы которого находятся в концентрации, ограничивающей темп синтеза; (Б) Параллельная процедура секвенирования: включающая предварительное разделение комплексов на четыре части, их иммобилизацию на поверхности сенсоров ячеек матриц четырех микросхем, с последующим асинхронным добавлением по одной из четырех различных реакционных смесей нуклеозидтрифосфатов на поверхности ячеек матрицы каждой из четырех микросхем.
На фиг. 4 схематически изображен вариант процедуры иммобилизации на поверхность сенсора единичного полимеразного комплекса, начало и остановка полимеризации закольцованного фрагмента нуклеиновой кислоты.
На фиг. 5А для одноматричного, последовательного устройства секвенирования представлены временные последовательности дискретных интервалов времени, сформированных схемой ячейки матрицы микросхемы в результате полимеризации одного и того же фрагмента ДНК в составе комплекса последовательно, в четырех реакционных смесях, в каждой из которых понижена концентрация нуклеотидов только одного вида, имя которого написано более мелким шрифтом около оси Y; логической единицей "1" отмечены интервалы времени, в которых сенсором ячейки были зарегистрированы факты разделения пары зарядов в результате реакции.
На фиг. 5Б представлена схема формирования результирующей нуклеотидной последовательности фрагмента из 4-х последовательностей, каждая из которых получена на предыдущем шаге обработки данных (см. фиг. 5А).
На фиг. 6А показано изображение, полученное на флюоресцентном микроскопе Zeiss Axiovert, продуктов реакции синтеза ДНК, полученных путем механизма «репликации катящегося кольца» Phi29 полимеразами, которые иммобилизованы в составе тройных комплексов на подготовленной поверхности покровного стекла; продукты реакции синтеза ДНК окрашены ДНК интеркаляторным красителем GelStar Stain. Продемонстрирована способность ДНК полимеразы Phi29, иммобилизованной на твердую поверхность, осуществлять синтез ДНК с кольцевой матрицы.
На фиг. 6Б показано изображение, полученное на флюоресцентном микроскопе Zeiss Axiovert, на котором видны немногочисленные продукты реакции синтеза ДНК, полученные только от тех тройных комплексов, которые неспецифически иммобилизовались на PEG-биотин поверхность покровного стекла.
На фиг. 7 показано распределение временных задержек для каждого вида нуклеотидов. По оси X - величина задержки в условных единицах времени, по оси Y - количество задержек определенных на оси X длительностей, полученных численными экспериментами. Представлена ситуация, когда концентрации каждого из видов нуклеотидов в реакционной смеси одинаковы.
На фиг. 8 показано распределение временных задержек для каждого вида нуклеотидов (по оси X - величина задержки в условных единицах времени, по оси Y - количество задержек определенных на оси X длительностей) при условии уменьшения в 100 раз концентрации нуклеотидов одного вида, - нуклеотидов вида А в реакционной смеси.
На фиг. 9А показано распределение среднего значения времени задержки для случая, когда концентрации каждого из видов нуклеотидов в растворе одинаковы (по оси X - номер задержки, по оси Y - среднее значение задержки в условных единицах времени, рассчитанное для текущего номера задержки).
На фиг. 9Б показано распределение среднего значения времени задержки для каждого вида нуклеотидов при условии уменьшения в 10 раз концентрации нуклеотидов одного вида, - нуклеотидов вида А в реакционной смеси (по оси X - номер задержки, по оси Y - среднее значение задержки в условных единицах времени, рассчитанное для текущего номера задержки).
На фиг. 10 представлена структурная схема микросхемы матрицы ячеек сенсоров в одном из вариантов изобретения. Числами римскими I, II, III, IV - обозначены секции матрицы ячеек сенсоров, каждая, например, размером 2000×2000 ячеек; числами 1, 2, 3, 4 в кружочках обозначены выходы горизонтальных сдвиговых регистров, выводящих цифровые данные из ячеек, расположенных, соответственно, в секциях I, II, III, IV. Числами в прямоугольных (квадратных) формах обозначены: 1 - ячейка сенсоров; 2 - вертикальный сдвиговый регистр переноса цифровых данных из ячеек сенсоров секции матрицы, расположенных в один ряд; 3 - USB интерфейс передачи данных между компьютером и микросхемой: 4 - горизонтальный сдвиговый регистр переноса цифровых данных из вертикальных сдвиговых регистров одной секции матрицы ячеек сенсоров; 5 - электрод смещения, потенциал на котором устанавливается источником напряжения, который регулируется контроллером; 6 - разъем между источником напряжения микросхемы и электродом смещения, который расположен на крышке микросхемы; 7 - контроллер управления режимами работы микросхемы; 8 - регулируемый генератор тактовой частоты, к которому извне микросхемы подсоединяется кварцевый резонатор; 9 - регулируемый источник вторичного питания.
На фиг. 11 изображена структурная схема четырехматричного устройства, реализующего один из вариантов одномолекулярного, безметочного способа секвенирования нуклеиновых кислот. Микросхема матрицы ячеек сенсоров с крышкой микрофлюидного устройства является основным компонентом устройства одномолекулярного секвенирования 12, микрофлюидное устройство включает в себя четыре бака малого объема 10 для размещения в них четырех водных растворов с реакционными смесями; три бака большого объема 11 для размещения в них, соответственно, буферного раствора, комплексов, например, «полимераза-фрагмент ДНК-праймер», отработанных растворов; насос 13 с электрическим приводом, для каждой микросхемы 12 устройства секвенирования; отсечные клапаны 14 с электрическим приводом, обеспечивающие возможность раздельной подачи буферного раствора, раствора с веществами для иммобилизации комплексов, раствора с реакционной смесью на поверхность матрицы микросхемы 12; электроды 15 для измерения проводимости раствора на выходном патрубке каждой крышки микросхемы 12; элемент Пельтье 16 (входящий в состав устройства поддержания температуры рабочего раствора) для каждой микросхемы 12 устройства секвенирования; микрофлюидное устройство и каждая микросхема 12 устройства секвенирования работают под управлением контроллера 17 и устройства обработки и отображения данных (компьютера) 18. Функции контроллера 17 могут быть реализованы внутри микросхемы 12.
На фиг. 12. изображена структурная схема сенсора ячейки матрицы с иммобилизованным на его поверхность тройным комплексом. Комплекс "полимераза-праймер-фрагмент ДНК", иммобилизованный на поверхности сенсора, обозначен числом 19, подложка из кремния p-типа в которой изготовлен сенсор, аналого-цифровая схема ячейки, матрица ячеек, аналого-цифровая схема микросхемы и т.д., обозначена числом 20, числом 21 обозначены слои изолирующего диэлектрика (например, диоксида кремния SiO2), числом 22 обозначен водный раствор реакционной смеси, обеспечивающая проведение реакции полимеризации фрагмента ДНК, числом 23 обозначен электрод смещения, пассивирующим изолирующим слоем 24 защищена от раствора вся поверхность ячейки за исключением поверхности сенсора.
На фиг. 13 изображена структурная схема сенсора ячейки матрицы, изготовленной по стандартной КМОП технологии, с иммобилизованным на его поверхность тройным комплексом. Комплекс "полимераза-праймер-фрагмент ДНК", иммобилизованный на поверхности сенсора, обозначен числом 25, подложка из кремния p-типа в которой изготовлен сенсор, аналого-цифровая схема ячейки, матрица ячеек, аналого-цифровая схема микросхемы и т.д., обозначена числом 26, числом 30 обозначены слои изолирующего диэлектрика (например, диоксида кремния SiO2), числом 28 обозначен водный раствор реакционной смеси, обеспечивающая проведение реакции полимеризации фрагмента ДНК, числом 29 обозначен электрод смещения, пассивирующим изолирующим слоем 27 защищена от раствора вся поверхность ячейки за исключением поверхности сенсора.
На фиг. 14 представлена структурная схема двух сенсоров ячейки матрицы: с иммобилизованным на подготовленную поверхность сенсора тройным полимеразным комплексом 31, и с поверхностью сенсора 37, защищенной от специфического связывания с комплексом, и аналого-цифровая структурная схемы ячейки. Числом 32 обозначена подложка из кремния p-типа, в которой изготовлен сенсор, аналого-цифровая схема ячейки, матрица ячеек, аналого-цифровая схема микросхемы и т.д., числом 36 обозначены слои изолирующего диэлектрика (например, диоксида кремния SiO2), числом 34 обозначен водный раствор реакционной смеси, обеспечивающий проведение реакции полимеризации фрагмента ДНК, числом 35 обозначен электрод смещения; пассивирующим изолирующим слоем 33 защищена от раствора вся поверхность ячейки за исключением поверхности двух сенсоров.
На фиг. 15 изображены структуры сенсора и аналого-цифровой схемы ячейки, использующей явление стохастического резонанса для регистрации сформированного сенсором сигнала от результата разделения пары зарядов в результате встраивания полимеразой нуклеотида в полимеризуемый фрагмент ДНК. Числом 38 показан комплекс "полимераза-праймер-фрагмент ДНК", иммобилизованный на поверхности сенсора, подложка из кремния p-типа в которой изготовлен сенсор, аналого-цифровая схема ячейки, матрица ячеек, аналого-цифровая схема микросхемы и т.д., обозначена числом 39, числом 40 обозначены слои изолирующего диэлектрика (например, диоксида кремния SiO2), числом 41 обозначен водный раствор реакционной смеси, обеспечивающая проведение реакции полимеризации фрагмента ДНК, числом 42 обозначен электрод смещения, пассивирующим изолирующим слоем 43 защищена от раствора вся поверхность ячейки за исключением поверхности сенсора. В Примере 5 приведено описание применения явления стохастического резонанса указанной схемой ячейки.
На Фиг. 16 представлена структурная схема нанопроводного транзистора с иммобилизованным тройным комплексом, которая состоит из планарной тонкопленочной металлической наноструктуры, нанесенной на слой диэлектрика 49, покрывающий подложку 45; тонкопленочная металлическая электродная наноструктура 46 (контакты к нанопроводу) совместно с металлическим каналом-нанопроводом 50 формируется на диэлектрической подложке методами фото- и электронной литографии с использованием фото- и электронного резиста, технологии травления экспонированной области и технологии напыления металла магнетронным или термическим способом. Управляющим электродом также может служить проводящий подслой (например, допированный кремний), находящийся под слоем диэлектрика 49. Для устранения контакта подводящих электродов с водным раствором в микрофлюдной ячейке они покрываются тонким слоем диэлектрика 51, наносимого через маску. Также числами 44, 47, 48 показаны, соответственно, иммобилизованный полимеразный комплекс, водный раствор реакционной смеси и электрод смещения.
На Фиг. 17 представлено распределение электрического потенциала для одной частицы, несущей единичный заряд.
На Фиг. 18 представлено распределение потенциала вдоль оси, соединяющей центр нанопровода с центром заряженной частицы, и нормировано на значение потенциала на поверхности нанопровода со стороны частицы, диаметр нанопровода 100 нм (по оси X - расстояние в метрах, по оси Y - a.u. (atomic units)).
На Фиг. 19 показано, как отдельные нанопроводные транзисторы могут быть размещены в интегральной структуре, представляющей собой чип с массивом нанопроводных транзисторов с адресной шиной, позволяющей осуществлять индивидуальное измерение на каждом нанотранзисторе.
На Фиг. 20 представлена фотография сформированного нанопроводного транзистора с утолщенным до 600 нм диэлектрическим слоем SiO2 под подводящими металлическими контактами и поверхностным изолирующим слоем SiO2 толщиной 200 нм; числом 52 обозначен нанопровод, 53 - контактные площадки, 54 - металлические проводники, 55 - слой диэлектрика, изолирующий проводники от водного раствора.
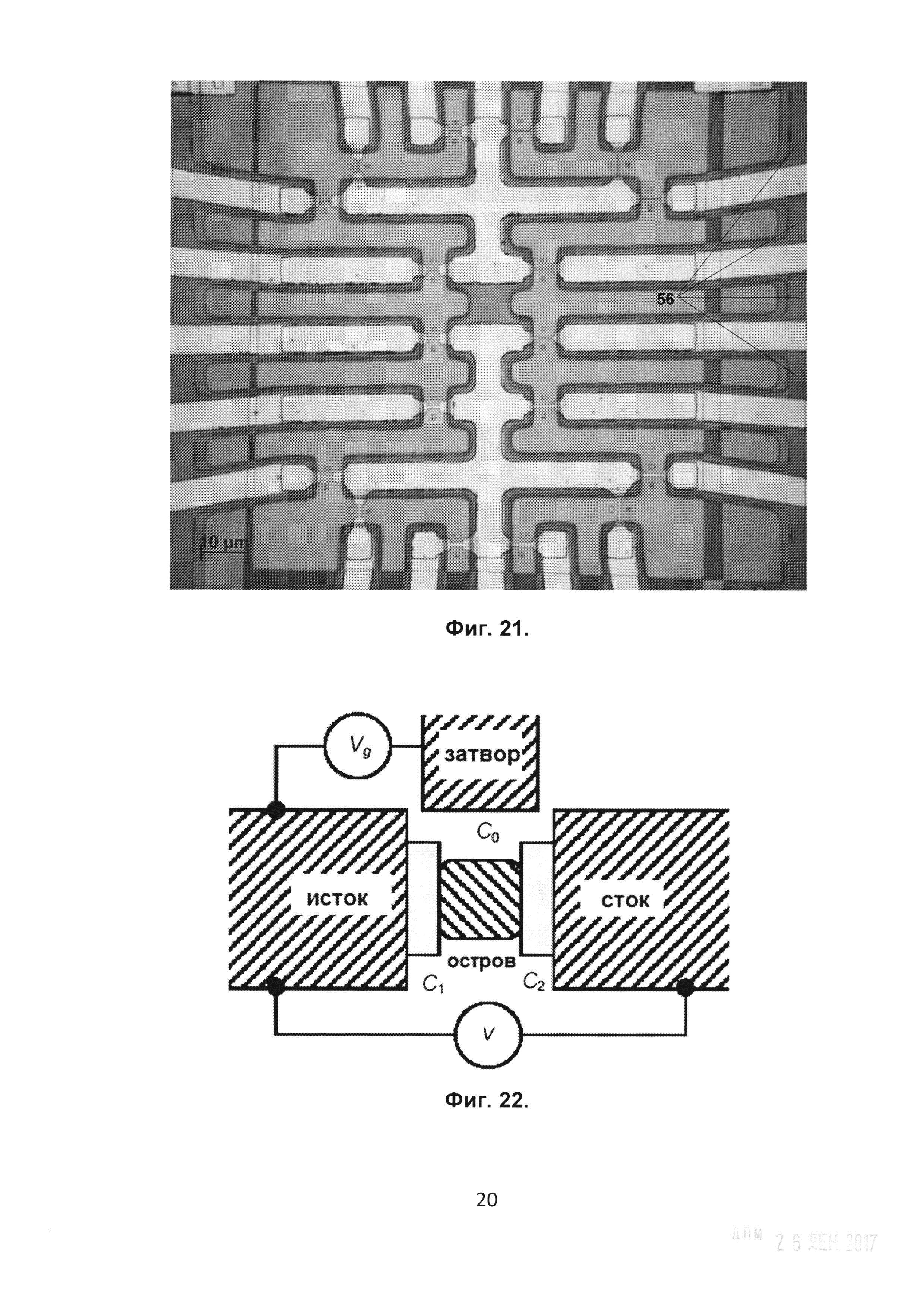
На Фиг. 21 представлена фотография вида окончательно сформированных структур нанопроводных транзисторов в центральной области чипа; числом 56 обозначен двойной слой диэлектрика под проводниками для исключения токов утечки.
На Фиг. 22 показана эквивалентная электрическая схема одноэлектронного транзистора.
На Фиг. 23 представлены: а - вольт-амперная характеристика транзистора (сплошная линия - состояние кулоновской блокады; пунктирная - полностью разблокированный транзистор); 6 - модуляционная характеристика одноэлектронного транзистора.
На Фиг. 24 представлена эквивалентная схема одноэлектронного транзистора-электрометра с источником измеряемого заряда Qx, имеющим собственную емкость Cs и емкость связи Cg.
На Фиг. 25 представлено схематическое изображение одномолекулярного транзистора с подвешенными электродами: М - молекула, осажденная в зазор и зафиксированная там при помощи SH-групп.
На Фиг. 26 показана фотография КНИ-структуры с висящими электродами над подложкой.
На Фиг. 27 представлена фотография наноструктуры одноэлектронного транзистора с нанозазором, полученным методом электронно-лучевой литографии.
На Фиг. 28 представлена фотография нанозазора, полученного методом электромиграции (электротреппинг).
На Фиг. 29 представлена фотография нанозазора, полученного методом ионно-лучевой литографии (FIB-технология).
На Фиг. 30 представлена фотография наноструктуры из 16 ячеек для транзисторов с нанозазорами.
На Фиг. 31 представлена фотография одной из 16 ячеек из транзистора с нанозазором (чертой указано расстояние 100 нм).
На Фиг. 32 представлена фотография центрального электрода-острова в структуре одноэлектронного транзистора из нанопровода, полученного применением FIB - технологии для формирования необходимой геометрии наноструктур.
На Фиг. 33 представлена фотография сформированного нанозазора для создания молекулярного одноэлектронного транзистора.
На Фиг. 34 представлена тестовая вольтамперная характеристика сформированного нанозазора; показывающая зависимость тока утечки через нанозазор от напряжения на нем (по оси X - величина напряжения, в вольтах, по оси Y - величина тока, в амперах); форма этой зависимости показывает, что нанозазор был сформирован.
Подробное раскрытие изобретения
Предлагаемый способ электронного одномолекулярного секвенирования нуклеиновых кислот основан на следующих закономерностях. Во-первых, основания одной цепи ДНК соединяются с основаниями другой цепи ДНК за счет водородных связей по строго определенным правилам Чаргаффа (например, нуклеотид А образует пару с Т, G образует пару с С), поэтому достаточно определить последовательность оснований в одной цепи для того, чтобы определить нуклеотидную последовательность секвенируемой ДНК. Определение имен оснований в последовательности одной цепи ДНК в ходе реакции полимеризации называется секвенированием путем синтеза (sequencing by synthesis, SBS) и применяется в настоящем способе секвенирования нуклеиновых кислот, ДНК или РНК. Во-вторых, в результате встраивания полимеразой каждого комплементарного нуклеотида в полимеризуемый фрагмент ДНК/РНК происходит разделение зарядов (Pourmand N., et al., Proc Natl Acad Sci USA, 2006 Apr 25; 103 (17): 6466-70): один электрон остается на полимеризуемом фрагменте ДНК/РНК, а один протон выделяется в водный раствор. В-третьих, сразу после разделения зарядов электрон и ион водорода индуцируют на поверхности электронного сенсора противозаряды одинаковой величины, но противоположного знака, которые компенсируют друг друга, но только на то время, пока ион водорода не удалится от места своего образования на некоторое расстояние в результате тепловой диффузии и действия электрического поля, сформированного зарядом электрода смещения ячейки. После чего на поверхности электронного сенсора остается некомпенсированный противозаряд, индуцированный электроном (Pourmand N., et al., Proc Natl Acad Sci USA, 2006 Apr 25; 103 (17): 6466-70), результат воздействия которого на электронный сенсор преобразуется последним в электрический сигнал и регистрируется последующей схемой усиления и обработки сигнала, как факт разделения зарядов (факт встраивания нуклеотида) и отмечается на выходной циклограмме логической единицей. В-четвертых, результаты регистрации фактов разделения зарядов будут иметь хорошую повторяемость, если разделение зарядов в ячейке матрицы происходят в одном и том же месте ячейки относительно сенсора этой ячейки, при одинаковых условиях реакции для каждого встраиваемого нуклеотида. В-пятых, если концентрация одного вида нуклеотидов в реакционной смеси изменена (понижена или повышена) и имя этого вида нуклеотидов известно, тогда усредненные (средние) интервалы времени перед встраиванием нуклеотидов именно этого вида будут иметь большую (при пониженной концентрации) или меньшую (при повышенной концентрации) длительность, по сравнению с усредненной (средней) длительностью интервалов времени перед встраиванием нуклеотидов трех других видов, которые имеют оптимальные концентрации в этой рабочей смеси для осуществления реакции полимеризации молекулы ДНК или РНК. Предпочтительным является вариант с меньшей концентрацией одного вида нуклеотида против нормальных концентраций трех других видов нуклеотидов в реакционной смеси, при этом темп встраивания нуклеотидов того вида, концентрация которого понижена, в среднем становится ниже, чем темп встраивания нуклеотидов других видов, концентрация которых нормальна.
В некоторых вариантах изобретения значительно меньшая концентрация одного из нуклеотидов достигается, когда его концентрация меньше, чем концентрация других нуклеотидов в 5-10 раз. В некоторых вариантах изобретения значительно меньшая концентрация одного из нуклеотидов достигается, когда его концентрация меньше, чем концентрация других нуклеотидов в 10-20 раз. В некоторых вариантах изобретения значительно меньшая концентрация одного из нуклеотидов достигается, когда его концентрация меньше, чем концентрация других нуклеотидов в 20-40 раз. В других вариантах изобретения значительно меньшая концентрация одного из нуклеотидов достигается, когда его концентрация меньше, чем концентрация других нуклеотидов в 40-100 раз. В-шестых, погрешность результатов измерений является случайной величиной при множестве результатов измерений одним и тем же средством измерений, и поэтому ее можно уменьшить путем усреднения результатов многократных измерений; усреднение N некоррелированных, статистически независимых результатов измерений (т.е. при отсутствии постоянных, например, искусственных помех (50-60 Гц и т.д.)) позволяет уменьшать случайную составляющую погрешности результата в √N раз до тех пор, пока она не станет настолько малой, что суммарная погрешность будет определяться систематической составляющей погрешности. В-седьмых, существуют ДНК-полимеразы, например фага Phi29, обладающие способностью вытеснять растущую цепь формирующейся ДНК, когда синтез, а значит и "чтение" ДНК, может производиться несколько раз по закольцованному фрагменту ДНК, аналогично «репликации по типу катящегося кольца" (РКК); применение такого вида ДНК полимераз позволяет увеличить точность секвенирования в несколько раз за счет усреднения информации о длительности интервалов времени перед фактами разделения зарядов (фактами встраивания нуклеотидов).
Предлагаемый метод одномолекулярного секвенирования нуклеиновых кислот возможно реализовать двумя основными способами: последовательным и параллельным, каждый из которых имеет свои преимущества. Для реализации каждого из способов ниже приведены примеры используемых устройств, которые приведены в целях раскрытия характеристик настоящего изобретения и их не следует рассматривать как каким-либо образом ограничивающие объем изобретения.
При последовательном способе одномолекулярного секвенирования применяется одна микросхема матрицы ячеек сенсоров, в которой на поверхность каждого сенсора иммобилизуют тройной комплекс «праймер-полимераза-матрица», после чего на поверхность матрицы последовательно подаются четыре вида реакционных смесей (каждая реакционная смесь подается один раз, очередность подачи реакционных смесей может быть любой), отличающихся тем, что в каждой реакционной смеси понижена концентрация только одного вида нуклеотидов против нормальной концентрации трех остальных видов нуклеотидов; длительность времени нахождения каждой реакционной смеси над сенсорами ячеек матрицы микросхемы зависит от темпа встраивания нуклеотидов ДНК полимеразой (нуклеотиды в секунду) и определяется временем, которое необходимо для ДНК/РНК полимеразы, чтобы "скопировать" закольцованный фрагмент нуклеиновой кислоты столько раз, сколько требуется для достижения заданной точности секвенирования. Исходя из факта, что конечное число синтезированных копий ограничено процессивностью полимеразы (например, средняя процессивность ДНК полимеразы Phi29 равна ~80,000 нуклеотидов), количество секвенированных копий обратно пропорционально длине в нуклеотидах одной копии закольцованной ДНК. Например, при длине копии матрицы в 1000 нуклеотидов можно прочитать матрицу максимум 80 раз, суммарно для всех четырех реакционных смесей; т.е. в каждой реакционной смеси может быть получена информация о синтезе 20 копий. При длине копии матрицы в 5000 нуклеотидов можно прочитать матрицу максимум 16 раз, суммарно для всех четырех реакционных смесей, т.е. в каждой реакционной смеси может быть получена информация о синтезе четырех копий каждой матрицы. В предпочтительных вариантах изобретения закольцованная матрица прочитывается столько раз в каждой реакционной смеси, сколько требуется для получения желаемой точности секвенирования фрагмента ДНК, например, так, как показано в Примере 9 ниже.
При параллельном способе секвенирования применяются четыре пространственно изолированные матрицы ячеек сенсоров, на поверхность каждого сенсора каждой матрицы иммобилизуют комплекс «праймер-матрица-полимераза», после чего на поверхность каждой из четырех матриц подают только одну из четырех реакционных смесей, отличающихся тем, что в каждой реакционной смеси понижена концентрация одного вида нуклеотидов против нормальной концентрации трех остальных видов нуклеотидов; "копируют" закольцованный фрагмент нуклеиновой кислоты в каждой ячейке каждой матрицы столько раз, сколько требуется для достижения заданной точности секвенирования; реакции полимеризации фрагментов ДНК в каждой ячейке каждой матрицы происходят асинхронно. Учитывая процессивность ДНК полимеразы Phi29, равную ~80,000 нуклеотидов, и факт, что эта процессивность является лимитирующим фактором в каждой из четырех изолированных матриц, получающих параллельно четыре реакционных смеси, а не в единственной матрице, как при последовательном способе секвенирования (см. выше), то максимальное количество копий, потенциально прочитанных полимеразой в каждой реакционной смеси будет в четыре раза больше, чем при последовательном способе секвенирования. Так, при длине копии матрицы в 1000 нуклеотидов, можно прочитать матрицу в каждой из четырех реакционных смесей максимум 80 раз, т.е. в каждой реакционной смеси может быть получено до 80-ти выходных последовательностей дискретных интервалов времени от каждой ячейки матрицы. При длине копии матрицы в 5000 нуклеотидов можно прочитать матрицу в каждой из четырех реакционных смесей 16 раз, т.е. точность секвенирования при параллельном способе секвенирования может быть значительно увеличена против последовательного способа секвенирования за счет точного определения нуклеотидной последовательности более длинных фрагментов ДНК. Но такое потенциально возможное увеличение точности достигается за счет увеличения в 4 раза количества микросхем матриц ячеек сенсоров, дополнительного количества реагентов, а значит и стоимости секвенирования.
Возможна реализация предлагаемого метода одномолекулярного секвенирования и комбинированным способом: последовательно-параллельным: две матрицы, на каждую последовательно подаются две реакционных смеси из четырех подготовленных, в каждой реакционной смеси понижена концентрация только одного вида нуклеотидов, в каждой реакционной смеси - своего вида. Но комбинированный способ не имеет преимуществ по предельным значениям технико-экономических характеристик ни перед последовательным способом, ни перед параллельным.
Принципиальным преимуществом последовательного способа секвенирования против параллельного способа является отсутствие необходимости в предварительной амплификации секвенируемой молекулы ДНК/РНК при конструировании библиотеки. Параллельный способ работает только тогда, если исходная ДНК была фрагментирована, а фрагменты клонально амплифицированы в процессе конструирования библиотеки (например, с помощью ПЦР), чтобы обеспечить попадание клонов каждого исходного фрагмента молекулы нуклеиновой кислоты на все четыре матрицы, в составе тройных комплексов. Также, при той же точности результата секвенирования, стоимость результата секвенирования последовательным способом заметно ниже. Последовательный способ секвенирования уступает параллельному только по производительности.
Определение имени вида каждого нуклеотида в анализируемой последовательности ДНК/РНК при последовательном способе секвенирования происходит в три этапа:
На первом этапе сенсором каждой ячейки матрицы производится регистрация фактов разделения зарядов в результате встраивания каждого нуклеотида в полимеризуемый фрагмент ДНК/РНК, иммобилизованный в составе комплекса на его поверхности. Зарегистрированные сенсором факты разделения зарядов преобразуются аналого-цифровой схемой ячейки сенсора в полезный сигнал в форме выходной последовательности дискретных интервалов времени, причем логической единицей "1" отмечены те интервалы времени, в которых сенсором ячейки были зарегистрированы факты разделения зарядов; выходные последовательности передаются в устройство обработки и отображения данных, например, компьютер. Для получения предельно точной информации о местах расположения на выходной последовательности дискретных интервалов времени нуклеотидов вида, концентрация которого понижена в реакционной смеси, выполняют несколько циклов секвенирования закольцованного фрагмента ДНК в каждой ячейке матрицы, одинаковое для каждой реакционной смеси количество циклов, и получают соответствующее число выходных последовательностей дискретных интервалов времени (вероятно, потребуются разные количества времени на полимеризацию одного и того же фрагмента ДНК в каждой из четырех реакционных смесей, но выходные последовательности дискретных интервалов времени поступают от ячеек матрицы в компьютер в реальном времени, поэтому компьютер отдаст команду на смену реакционной смеси или на промывку буферным раствором матрицы микросхемы только после того, как каждая из выходных последовательностей дискретных интервалов времени ячейки поступит в компьютер столько раз, сколько было задано пользователем перед началом процедуры секвенирования). Возможное количество циклов секвенирования в каждой реакционной смеси определяется в основном длиной секвенируемых фрагментов ДНК/РНК и процессивностью полимеразы.
На втором этапе статистически определяют короткие и длинные интервалы времени перед встраиванием нуклеотидов (сравнивают количество логических нулей "0" перед каждой логической единицей "1") для каждой выходной последовательности дискретных интервалов времени, полученных на первом этапе, и для каждой ячейки перезаписывают данные в виде четырех последовательностей логических единиц "1" и нулей "0" (по одной для каждой реакционной смеси) таким образом, что теперь логической единицей «1» обозначен каждый длинный интервал времени, соответствующий встраиванию нуклеотидов вида, концентрация которого была понижена в соответствующей реакционной смеси и известна, а логическим нулем «0» обозначаются короткие интервалы времени, соответствующие встраиванию нуклеотидов видов, концентрация которых была нормальна в этой же реакционной смеси.
Для каждой ячейки сопоставляют данные о местах расположения нуклеотидов известных видов на каждой из четырех последовательностей логических единиц «1» и нулей «0» друг с другом, и методом исключения, следуя правилу, что на одной позиции в нуклеотидной последовательности фрагмента ДНК может располагаться нуклеотид только одного вида, формируют результирующую нуклеотидную последовательность секвенируемого фрагмента ДНК.
На третьем этапе из нуклеотидных последовательностей фрагментов ДНК/РНК составляют нуклеотидную последовательность всей исходной ДНК/РНК с помощью компьютерной программы, реализующей, в зависимости от решаемой задачи, например, алгоритм RACA (Kim J., et al., Proc Natl Acad Sci USA, 2013 Jan 29; 110 (5): 1785-90) или алгоритм Ragout для референсной сборки (Kolmogorov М., et al., Bioinformatics, 2014 Jun 15; 30 (12): i302-9), или же алгоритмы для сборки de novo, например, алгоритмы основанные на графическом методе De Bruijn (Compeau Р., et al., Nature Biotechnology, 2011, 29 (11): 987-991) или любые другие подходящие алгоритмы.
Определение имени вида каждого нуклеотида в анализируемой последовательности ДНК/РНК при параллельном способе секвенирования производится в четыре этапа:
На первом этапе сенсором каждой ячейки каждой матрицы производится регистрация фактов разделения зарядов в результате встраивания каждого нуклеотида в полимеризуемый фрагмент ДНК/РНК, иммобилизованный в составе комплекса на его поверхности. Зарегистрированные сенсором факты разделения зарядов преобразуются аналого-цифровой схемой ячейки сенсора в полезный сигнал в форме выходной последовательности дискретных интервалов времени, обозначенных логическими единицами "1" и нулями "0", причем логической единицей "1" отмечены те интервалы времени, в которых сенсором ячейки были зарегистрированы факты разделения зарядов; выходные последовательности передаются в устройство обработки и отображения данных, например, компьютер. Для получения предельно точной информации о местах расположения на выходной последовательности дискретных интервалов времени нуклеотидов вида, концентрация которого понижена в реакционной смеси над конкретной матрицей, выполняют несколько циклов секвенирования закольцованного фрагмента ДНК в каждой ячейке каждой матрицы и получают соответствующее число выходных последовательностей дискретных интервалов времени. Возможное количество циклов секвенирования определяется в основном длиной секвенируемых фрагментов ДНК/РНК, процессивностью полимеразы и выполняется одинаковое количество раз в каждой ячейке каждой матрицы.
На втором этапе статистически определяют короткие и длинные интервалы времени перед встраиванием нуклеотидов (сравнивают количество логических нулей "0" перед каждой логической единицей "1") для каждой выходной последовательности дискретных интервалов времени, полученных на первом этапе, и для каждой ячейки каждой матрицы перезаписывают данные в виде одной последовательности логических единиц "1" и нулей "0" таким образом, что теперь логической единицей «1» обозначен каждый длинный интервал времени, соответствующий встраиванию нуклеотидов вида, концентрация которого была понижена в соответствующей реакционной смеси и известна, а логическим нулем «0» обозначаются короткие интервалы времени, соответствующие встраиванию нуклеотидов видов, концентрация которых была нормальна в этой же реакционной смеси.
Так как параллельный способ секвенирования предполагает амплификацию фрагментов, полученных после фрагментации нуклеиновой кислоты, то отдельно для каждой микросхемы матрицы ячеек сенсоров минимизируют количество последовательностей логических единиц "1" и нулей "0" посредством сортировки, сравнения, выбора, усреднения одинаковых с определенной вероятностью последовательностей логических единиц "1" и нулей "0" и преобразования их в одну последовательность логических единиц "1" и нулей "0".
На третьем этапе, посредством сортировки, сравнения и исключения - из четырех последовательностей логических единиц "1" и нулей "0", взятых от каждой из четырех микросхем матриц ячеек сенсоров, сопоставляя данные о местах расположения нуклеотидов известных видов на каждой из четырех последовательностей логических единиц «1» и нулей "0" друг с другом, и следуя правилу, что на одной позиции в нуклеотидной последовательности фрагмента ДНК может располагаться нуклеотид только одного вида, - формируют нуклеотидные последовательности фрагментов нуклеиновых кислот.
На четвертом этапе из нуклеотидных последовательностей фрагментов нуклеиновой кислоты составляют полную нуклеотидную последовательность исходной ДНК/РНК образца с помощью компьютерной программы, реализующей, в зависимости от решаемой задачи, например, алгоритм RACA (Kim J., et al., Proc Natl Acad Sci USA, 2013 Jan 29; 110 (5): 1785-90) или алгоритм Ragout для референсной сборки (Kolmogorov М., et al., Bioinformatics, 2014 Jun 15; 30 (12): i302-9), или же алгоритмы для сборки de novo, например, алгоритмы, основанные на графическом методе De Bruijn (Compeau Р., et al., Nature Biotechnology, 2011, 29 (11): 987-991) или любой другой подходящий алгоритм.
В предпочтительных вариантах изобретения регистрацию факта разделения зарядов при присоединении ДНК полимеразой очередного нуклеотида осуществляют измерением модуляции тока в канале полевого транзистора посредством индуцированного потенциала на поверхности сенсора (затвора полевого транзистора). В других вариантах изобретения факт разделения зарядов можно зарегистрировать путем измерения емкости или проводимости окружающего раствора. Регистрацию проводят с помощью электронного сенсора, расположенного на поверхности ячейки матрицы и изготовленного на основе наноразмерной полупроводниковой структуры, например, нанопроводного полевого транзистора, одноэлектронного транзистора, полевого транзистора, диода, или на основе структуры с S-образной или N-образной вольтамперной или передаточной характеристикой (например, диод специальной конструкции), используемой в составе схемы и реализующей эффект стохастического резонанса для улучшения отношения сигнал/шум.
Для воспроизводимой регистрации полезного сигнала необходимо, чтобы комплекс «полимераза-матрица ДНК» был иммобилизован на поверхности сенсора достаточно продолжительное время, большее, чем процессивное время ДНК полимеразы. Для этого используют сенсор с модифицированной поверхностью для иммобилизации полимеразного комплекса на поверхности. Аналого-цифровая электронная схема ячейки матрицы считывает сигналы сенсора, отмечает моменты их получения логической единицей "1" на формируемой выходной последовательности дискретных интервалов времени, и передает ее в компьютер в реальном времени. Так как имя вида нуклеотидов, концентрация которого понижена в реакционной смеси над матрицей, известно, то места расположения нуклеотидов этого вида в последовательности секвенируемой нуклеиновой кислоты определяются результатами анализа длительности интервалов времени перед полезными сигналами или между ними (логическими "1"), сформированными в ячейках этой матрицы.
Принципиально, что за счет иммобилизации комплекса "полимераза-матрица ДНК" в непосредственной близости от поверхности сенсора, каждый факт разделения пары зарядов при встраиваниях комплементарных нуклеотидов в полимеризуемый фрагмент нуклеиновой кислоты производится на минимальном, одинаковом (с определенной точностью) расстоянии от поверхности сенсора, тем самым обеспечивая эффективную регистрацию фактов разделения зарядов в ходе полимеризации фрагментов нуклеиновой кислоты, в том числе длинных фрагментов (тысячи пар нуклеотидов).
В сочетании с применением безметочного алгоритма секвенирования ДНК, становится возможным в каждой ячейке матрицы организовать процедуру регистрации результатов встраивания комплементарных нуклеотидов в растущую цепь фрагмента нуклеиновой кислоты, и, на основе информации о величине дискретных интервалов времени между зарегистрированными результатами встраивания нуклеотидов, установить имя вида каждого нуклеотида в последовательности исходного фрагмента нуклеиновой кислоты.
Использование изобретения позволит повысить производительность и точность процедуры секвенирования молекул нуклеиновой кислоты, в том числе для целей применения в медицинской диагностике.
В некоторых аспектах изобретение обеспечивает способ секвенирования нуклеиновых кислот, который относится к группе методов секвенирования по методу синтеза (SBS), и основан на обнаружении результатов включения полимеразой нуклеотидов в полимеризуемую нить нуклеиновой кислоты. В отличие от ряда современных способов коммерческого секвенирования этой группы, в способе по настоящему изобретению используют природные нуклеотиды и полимеразу, которая не имеет модификаций аминокислот необходимых для улучшения включения синтетических нуклеотидов с присоединенными флуорофорами или другими химическими модификациями. Основной принцип способа настоящего изобретения основан на обнаружении в реальном времени событий разделения пары зарядов, сопровождающих включение нуклеотидов молекулой одиночной полимеразы в растущую нить одиночных молекул нуклеиновой кислоты в комплексе «полимераза-матрица ДНК», иммобилизованном на поверхности сенсора. Обнаружение серий событий однократного разделения зарядов осуществляется чувствительным к изменению заряду электронным сенсором. В реакциях с четырьмя различными начальными условиями, каждое из которых определено одним из четырех видов нуклеотидов, находящимся в пониженной концентрации, регистрируются временные ряды событий разделения зарядов, показывающие временные задержки при включении нуклеотидов обедненного вида. Анализ полученных четырех временных рядов этих событий при реакции одного полимеразного комплекса приводит к определению нуклеотидной последовательности исследуемой молекулы нуклеиновой кислоты. Раскрытые здесь методы могут быть классифицированы как методы реального времени, одномолекулярные, электронные, асинхронные методы секвенирования.
В некоторых аспектах изобретение обеспечивает способ секвенирования нуклеиновых кислот, содержащий: обеспечение множества наносенсорных элементов (ячеек), размещенных в матрице, причем каждая ячейка содержит чувствительное к заряду устройство (наносенсор), усилитель и аналого-цифровой преобразователь сигнала, причем наносенсор содержит, например, исток, сток и затвор (наноразмерный транзистор); обеспечение образца, содержащего множество закольцованных молекул целевой нуклеиновой кислоты; обеспечение олигонуклеотидного праймера и условий отжига с образованием комплекса праймера-матрицы; контактирование праймер-матрицы с ферментом полимеразы с образованием тройного комплекса «полимераза-праймер-матрица ДНК»; обеспечение условий присоединения тройного комплекса к поверхности наносенсора, приводящих к образованию множества наносенсоров с иммобилизованными на их поверхности одиночными тройными комплексами; подвергая указанные тройные комплексы четырем реакциям полимеризации, каждую в реакционной смеси, содержащую все четыре дезоксинуклеозидтрифосфата (dATP, dTTP, dGTP, dCTP), (или нуклеозидтрифосфаты ATP, UTP, GTP, СТР), где каждая реакционная смесь имеет один дезоксинуклеозидтрифосфат (или нуклеозидтрифосфат), присутствующий в пониженной концентрации; обнаружение событий разделения пары зарядов, сопровождающих включение нуклеотида в полимеризуемый фрагмент одноцепочечной нуклеиновой кислоты; регистрация временных рядов фактов разделения пар зарядов и идентификацию длинных временных интервалов, предшествующих включению обедненных нуклеотидов для каждой из четырех реакционных смесей, и, таким образом, поиск положений каждого нуклеотида обедненного вида вдоль целевой молекулы нуклеиновой кислоты; сравнивая последовательности положений нуклеотидов обедненного вида для всех четырех реакционных смесей и определяя нуклеотидную последовательность целевой молекулы нуклеиновой кислоты.
В некоторых аспектах настоящее изобретение относится к способам секвенирования нуклеиновых кислот, включающим последовательное или параллельное проведение реакций полимеризаций с четырьмя реакционными смесями, каждая из которых имеет один обедненный нуклеотид из четырех, где, например, реакционная смесь 1 содержит низкую концентрацию нуклеотидов А, смесь 2 - G, смесь 3 - Т и смесь 4 - С; в котором кратность повторного синтеза нуклеиновой кислоты целевой последовательности рассчитана для каждой из четырех реакционных смесей таким образом, чтобы позволить полимеразе копировать количество целевых нуклеиновых кислот столько раз, чтобы достичь высокой (требуемой) точности секвенирования. В параллельном методе секвенирования используются четыре матрицы наносенсоров, и четыре реакционных смеси, которые одновременно могут добавляться к четырем матрицам.
В некоторых вариантах осуществления настоящее изобретение относится к электронному одномолекулярному секвенированию, включающему получение множества кольцевых молекул целевой нуклеиновой кислоты (библиотек), условий сборки тройного полимеразного комплекса и присоединения указанного комплекса к поверхности наносенсора, композиции реакционных смесей и условия репликации (или транскрипции) по типу «катящегося кольца».
Для реализации вышеуказанных способов согласно заявляемым вариантам осуществления используют устройство электронного одномолекулярного секвенирования, которое также является предметом настоящего изобретения. Устройство содержит микрофлюидное устройство, обеспечивающую подачу реагентов к сенсорам ячеек матрицы микросхемы; непосредственно саму микросхему матрицы ячеек сенсоров (по меньшей мере одну); устройство электронного управления: микрофлюидным устройством, микросхемой, обменом данными с устройство обработки и отображения данных (компьютером); компьютер со специальным программным обеспечением, которое регистрирует и хранит первичные сигналы, генерируемые сенсорами ячеек матрицы микросхемы, анализирует, обрабатывает эти данные и определяет нуклеотидные последовательности целевых нуклеиновых кислот из множества ее фрагментов.
Устройство обработки и отображения данных может выполняться на базе широкого спектра электронно-вычислительных устройство, например, персонального компьютера, ноутбука, серверного кластера и т.п. В общем случае указанное устройство содержит один или более процессоров, выполняющих основную вычислительную работу при реализации этапов способа и оперативную память (ОЗУ), предназначенную для оперативного хранения команд, исполняемых одним или более процессорами.
Ниже более подробно описывается процесс пробоподготовки по настоящему изобретению, включающий выделение нуклеиновых кислот, конструирование библиотеки, образование комплексов «полимераза-матрица ДНК» и их иммобилизация на поверхности сенсоров ячеек матрицы микросхемы.
Нуклеиновые кислоты, используемые в методах и системах секвенирования в вариантах изобретения, могут быть одноцепочечными и двухцепочечными, или же содержать участки одноцепочечных и двухцепочечных последовательностей. Например, нуклеиновые кислоты могут представлять собой геномную ДНК, митохондриальную ДНК, кДНК, мРНК, рибосомальную РНК, малую РНК, некодирующую РНК, малую ядерную РНК, малую ядрышковую РНК и Y РНК. В некоторых вариантах осуществления нуклеиновые кислоты экстрагируются и очищаются из образца или пробы. В некоторых вариантах осуществления РНК конвертируется в ДНК в процессе обратной транскрипции при участии обратной транскриптазы - специализированной ДНК полимеразы, способной синтезировать цепь ДНК используя РНК в качестве матрицы. Нуклеиновые кислоты (например, геномная ДНК), используемые в вариантах изобретения, могут быть изолированы/получены из любого интересующего организма. Такими организмами могут быть, например, животные (например, млекопитающие, включая человека и приматов), растения, грибы, или патогены, такие как бактерии или вирусы. В некоторых вариантах осуществления нуклеиновые кислоты (например, геномная ДНК или РНК) являются бактериальными или вирусными нуклеиновыми кислотами.
Нуклеиновые кислоты получают из образцов интересующих организмов. Неограничивающие примеры образцов включают клетки, жидкости организма (включая, но не ограничивая, кровь, мочу, сыворотку, лимфу, слюну, анальные и вагинальные выделения, пот и семенную жидкость), пробы из окружающей среды (например, образцы воды, почвы, воздуха, сельского хозяйства), образцы агентов биологического оружия, исследовательские образцы (например, продукты реакций амплификации нуклеиновых кислот, таких как ПЦР или реакции амплификации всего генома), очищенные образцы, такие как очищенная геномная ДНК, препараты РНК, и необработанные первичные образцы (бактерии, вирусы, и т.д.).
Методы получения нуклеиновых кислот (например, геномной ДНК) хорошо известны в данной области исследований (например, Sambrook et al., Molecular Cloning: A Laboratory Manual (1999)).
В некоторых вариантах осуществления нуклеиновые кислоты, используемые в данном предложении, представляют собой геномную ДНК. В некоторых вариантах осуществления нуклеиновые кислоты представляют собой часть генома (например, часть генома представляющую интерес для определенного/конкретного применения, например, выборка генов которые могут нести мутации в частной выборке популяции, например, пациентов имеющих рак). В некоторых вариантах осуществления нуклеиновые кислоты представляют собой экзомную ДНК, например, часть полного генома, обогащенную транскрибируемыми последовательностями ДНК. В некоторых вариантах осуществления нуклеиновые кислоты представляют собой часть или полный транскриптом, например, набор всех мРНК или транскриптов производимых клеткой или популяцией клеток.
В некоторых вариантах осуществления нуклеиновые кислоты (например, геномная ДНК) подвергаются фрагментированию. Может быть использован любой метод фрагментации. Например, в некоторых вариантах осуществления нуклеиновые кислоты фрагментируются механическим способом (например, ультразвуковым, акустическим, или небулизацией), химическими или энзиматическими методами (например, путем использования эндонуклеаз). Методы фрагментации нуклеиновых кислот хорошо известны в области данного изобретения (например, US 9127306 В2). В некоторых вариантах осуществления фрагментация производится ультразвуком (например, используя сфокусированный ультразвуковой облучатель фирмы Covaris, США). В других вариантах осуществления фрагментация производится путем обработки нуклеиновых кислот нуклеазами или их смесями (например, смесь нуклеаз Fragmentase, New England Biolabs, США). В некоторых вариантах осуществления размер фрагментированной нуклеиновой кислоты находится в интервале 50-200 пар оснований (п.о.). В некоторых вариантах осуществления размер фрагментированной нуклеиновой кислоты находится в интервале 100-500 п.о. В некоторых вариантах осуществления размер фрагментированной нуклеиновой кислоты находится в интервале 200-2000 п.о. В некоторых вариантах осуществления размер фрагментированной нуклеиновой кислоты находится в интервале 500-5000 п.о. В некоторых вариантах осуществления размер фрагментированной нуклеиновой кислоты находится в интервале 1000-10000 п.о. В некоторых вариантах осуществления размер фрагментированной ДНК находится в интервале 3000-20000 п.о. В некоторых вариантах осуществления размер фрагментированной ДНК находится в интервале 5000-40000 п.о.
В некоторых вариантах осуществления методы, описанные в данном разделе, представляют собой выделение/экстракцию нуклеиновых кислот из биологических образцов и их подготовку к секвенированию. Некоторые методы экстракции нуклеиновых кислот из образцов/проб различного происхождения используют лизирующие клетку ферменты, ультразвуковую обработку, высокое давление пресса, или комбинацию любых из этих методов. Во многих случаях после высвобождения нуклеиновых кислот из клетки они дополнительно очищаются от дебриса клеточной стенки, белков, и других компонентов с помощью коммерчески доступных методов включающих использование протеиназ, органических растворителей, технику обессоливания, спин-колонок, а также связывание нуклеиновых кислот с функционализированным матриксом, например, магнитными наночастицами. В некоторых случаях нуклеиновая кислота представляет собой бесклеточную свободную нуклеиновую кислоту (например, т.н. жидкостная биопсия) и не требует процесса экстракции из клетки.
Методы конструирования библиотек нуклеиновых кислот представленного изобретения имеют конечной целью создание кольцевой ДНК матрицы, которая служит субстратом для ДНК полимеразы в реакции «репликации по механизму катящегося кольца» (РКК) - предпочтительного способа ДНК синтеза используемого в представленном изобретении. Такая закольцованная ДНК матрица с неизвестной нуклеотидной последовательностью секвенируется с многократной повторяемостью методами, изложенными в данном изобретении для достижения высокой точности определения нуклеотидов в последовательности кольцевой матрицы.
В некоторых вариантах осуществления закольцованная матрица представляет собой полимер ДНК, а полимеразой служит РНК полимераза, например РНК полимераза бактериофага 17, и процесс секвенирования производится путем «транскрипции по механизму катящегося кольца» (Mohsen and Kool, Асе. Chem. Res., 2016, v. 49 (11): 2540-2550). В некоторых вариантах осуществления закольцованной матрицей для полимеразы служит ковалентно замкнутое полностью одноцепочечное кольцо ДНК (Фиг. 1А). Методы конструирования таких одноцепочечных матриц хорошо известны в области науки, к которой относится настоящее изобретение. Пример такого метода приведен в деталях на Фиг. 2.
В некоторых вариантах осуществления закольцованная матрица может быть в форме двухцепочечного ДНК кольца, имеющего «надрез» или «брешь» в одной цепи (Фиг. 1В). При этом образующийся 3' конец служит сайтом связывания ДНК полимеразы и начала синтеза ДНК. Такая матрица может быть получена в результате двух энзиматических реакций. Сначала производится лигирование двухцепочечного адаптера ДНК лигазой к концу двухцепочечного фрагмента ДНК образца. При этом может быть использовано как лигирование «тупых» концов, так и лигирование адаптера, имеющего выступающий 3' Т-конец с ДНК фрагментом, у которого на 3' концы добавлены нуклеотиды А. Затем окаймленный адаптерами двухцепочечный фрагмент ДНК напрямую закольцовывается с помощью ДНК лигазы, либо для закольцовывания добавляется дополнительный «адаптер-мостик» с концами совместимыми с концами уже пришитых адаптеров (например, используются комплементарные «липкие» концы).
В других вариантах осуществления матрица может топологически представлять собой закольцованно замкнутую частично двухцепочечную структуру вида «ДНК гантели». Такая структура позволяет определять последовательность сразу двух цепей ДНК двухцепочечной части «ДНК гантели» (Фиг. 1Б), смысловой и антисмысловой, при секвенировании путем механизма РКК. Методы конструирования таких ДНК гантелей хорошо известны в данной области техники (например, Travers K.J., et al., Nucleic Acids Research, 2010, Vol. 38, No. 15 e159).
В некоторых вариантах осуществления метод конструирования библиотек одноцепочечных закольцованных ДНК молекул состоит из нескольких последовательных шагов. Пример такого метода приведен на Фиг. 1 и состоит из следующих шагов: (а) фрагментирование ДНК полученной из образца для получения множества ДНК фрагментов; (б) селекция и отбор фрагментированной ДНК по размеру; (в) денатурация двухцепочечной фрагментированной ДНК нужного размера для получения одноцепочечной ДНК, где денатурация производится термическим или химическим воздействием; (г) репарирование 5'- и 3'-концов для восстановления 5'-фосфатных и 3'-гидроксильных групп; (д) лигирование 5' и 3' полуадаптеров к репарированным одноцепочечным фрагментам ДНК, получая таким образом множество одноцепочечных фрагментов ДНК, окаймленных по флангам верхними цепями полу адаптеров; (е) амплификация полученных лигированных молекул с помощью полимеразной цепной реакции (ПЦР), где прямой и обратный праймеры представляют собой олигонуклеотиды гомологичные последовательностям пришитых полуадаптеров; (ж) денатурация амплифицированных фрагментов ДНК для превращения их в одноцепочечную форму; (з) закольцовывание одноцепочечных фрагментов ДНК, состоящее из (1) отжига олигонуклеотида-«мостика» к концам одноцепочечных фрагментов, сближающее таким образом 5'- и 3'-концы последовательностей адаптеров и приводящее к образованию двухцепочечного никированного (содержащего «ник» - одноцепочечный разрыв ДНК) участка в закольцованном одноцепочечном фрагменте, и (2) лигирования с помощью ДНК лигазы упомянутого «ника» (одноцепочечного разрыва ДНК) приводящее к образованию ковалентно замкнутых закольцованных одноцепочечных ДНК молекул; (и) переваривание с помощью экзонуклеаз оставшихся (направленная деградация/разрушение) незакольцованных линейных фрагментов ДНК, а также олигонуклеотида-«мостика», как свободного в растворе, так и отожженного, приводящее к образованию библиотеки одноцепочечных кольцевых ДНК.
В некоторых вариантах осуществления фрагментация ДНК осуществляется с помощью разрыва ДНК воздействием ультразвуком (например, DNA Shearing for NGS: with the M220™ Focused-ultrasonicator™, Application Notes, www.covarisinc.com; Fisher et al., Genome Biology, 2011, 12:R1) В некоторых вариантах осуществления ДНК фрагментируется энзиматически, например, ферментом Fragmentase (New England Biolabs Inc., США) приводя к образованию фрагментов с 5'- и 3'-концами имеющими фосфатные и гидроксильные группы соответственно.
В некоторых вариантах осуществления после фрагментации ДНК производят селекцию получившихся фрагментов по размеру, чтобы сузить интервал разброса размеров фрагментов (диапазон вариабильности размеров фрагментов) и таким образом получить библиотеки с более однородными по размеру закольцованными фрагментами. В некоторых вариантах осуществления отбираются фрагменты нуклеиновой кислоты размером 200-400 п.о. В некоторых вариантах осуществления отбираются фрагменты нуклеиновой кислоты размером 400-1000 п.о. В некоторых вариантах осуществления отбираются фрагменты нуклеиновой кислоты размером 1000-2000 п.о. В некоторых вариантах осуществления отбираются фрагменты нуклеиновой кислоты размером 2000-4000 п.о. В некоторых вариантах осуществления отбираются фрагменты нуклеиновой кислоты размером 4000-6000 п.о. В некоторых вариантах осуществления отбираются фрагменты нуклеиновой кислоты размером 6000-10000. В некоторых вариантах осуществления отбираются фрагменты нуклеиновой кислоты размером 10000-20000. В некоторых вариантах осуществления отбираются фрагменты нуклеиновой кислоты размером 20000-40000.
В некоторых вариантах осуществления селекция фрагментов по размеру осуществляется методом Solid Phase Reversible Immobilisation (SPRI) разработанным в Whitehead Institute (DeAngelis M.M., et al., Nucleic Acids Res, 1995, 23: 4742-4743), который использует магнитные шарики, связывающиеся с ДНК, например, AMPureXP beads (Beckman Coulter, Inc. США). В некоторых вариантах осуществления селекция высокомолекулярных фрагментов ДНК (вплоть до 50 к.п.о.) по размеру проводится с помощью автоматического фракционирования ДНК, используя специальный инструмент, например, BluePippin (Sage Science, Inc., США).
Для конструирования библиотеки фрагментов нуклеиновой кислоты, подходящей для метода секвенирования, представленного в настоящем изобретении, множество ДНК фрагментов, образуемых в результате фрагментации, должны быть фланкированы адаптерами - частично или полностью двухцепочечными молекулами ДНК, получаемыми путем отжига двух олигонуклеотидов с известной последовательностью. Методы/способы прикрепления адаптеров к 5'- и 3'-концам ДНК фрагментов хорошо известны в области науки, к которой относится настоящее изобретение, и основаны на реакции лигирования ДНК с помощью фермента ДНК лигазы, например, ДНК лигазы фага 14 (New England Biolabs Inc., США).
В некоторых вариантах осуществления перед лигированием адаптеров двухцепочечные фрагменты ДНК, полученные с помощью ультразвуковой фрагментации, подвергаются реакциям репарации ДНК, чтобы восстановить 5' фосфатные и 3' гидроксильные концевые группы, и превратить 5' и 3' выступающие и/или рецессированные концы в тупые. Это достигается инкубацией фрагментированной ДНК с полинуклеотид-киназой фага 14, ДНК полимеразой фага 14, и иногда дополнительно с Кленов Фрагментом ДНК полимеразы I Е. coli.
В некоторых вариантах осуществления, когда ДНК фрагментируется энзиматически, например, ферментом Fragmentase (New England Biolabs Inc., США), нет необходимости проводить восстановление 5' и 3' концевых химических групп, так как энзиматический метод фрагментации сохраняет целостность 5' фосфатных и 3' гидроксильных групп в местах атаки ДНК используемыми нуклеазами. В некоторых вариантах осуществления, когда адаптеры пришиваются методом лигирования тупых концов, тем не менее, фрагментированная ультразвуком ДНК обрабатывается ДНК полимеразой фага 14 и иногда дополнительно Кленов Фрагментом ДНК полимеразы I, чтобы сделать концы тупыми перед лигированием двухцепочечных адаптеров по краям фрагментов.
В предпочтительных вариантах осуществления фрагментированную ДНК сначала денатурируют, а затем лигируют в одноцепочечной форме к адаптерам, как показано на Фиг. 1. В этом случае репарация концов ограничивается восстановлением 5' фосфатных и 3' гидроксильных групп, если ДНК была фрагментирована физическим способом, например, ультразвуком, и ее не требуется вообще, если ДНК была фрагментирована энзиматически. Далее за репарацией концов следует направленное пришивание 5' и 3' полу-адаптеров с помощью ДНК лигазы (например, ДНК лигазы фага 14 или ДНК лигазы фага Т7), приводящее к образованию двухцепочечных участков ДНК, имеющих «ник» в месте стыка фрагмента и адаптеров который «зашивается» ДНК лигазой.
В некоторых вариантах осуществления два адаптера (например, адаптер А и адаптер В) пришиваются к двухцепочечным фрагментам ДНК случайным ненаправленным способом - реакцией лигирования тупых концов, катализируемой ДНК лигазой, что приводит к образованию трех типов молекул: фланкированных адаптерами А (АА комбинация), адаптерами В (ВВ комбинация), и адаптером А и адаптером В (АВ комбинация). При таком способе используются адаптеры, не способные к лигированию между собой, т.е. не образующие гомо- и гетеродимеры. Отбор и обогащение библиотеки фрагментами ДНК, имеющими комбинацию АВ, производится с помощью ПЦР, использующей праймеры, гомологичные участкам адаптеров А и В (Drmanac R. et al., Science, 2010, v. 327 (5961): 78-81).
В некоторых вариантах осуществления к 3' концам двухцепочечных фрагментов ДНК сначала добавляется нуклеотид А с помощью Кленов (Klenow) Фрагмента мутантной ДНК полимеразы I, не имеющей 3'-->5' экзонуклеазной активности (3'-->5' ехо-), или Taq полимеразы. В этом случае используются адаптеры, представляющие собой два отожженных друг на друга олигонуклеотида, образующих двухцепочечные олигонуклеотиды с 5' фосфатными группами и выступающими Т нуклеотидами на 3' концах. В некоторых вариантах осуществления адаптер, имеющий выступающий нуклеотид Т на лигируемом конце, имеет частично двухцепочечную структуру, например, в форме Y-структуры, часто называемой «вилкой» (описано в US 6287825 В1; US 7741463 В2), или в форме "заколки-адаптера» (описано в US 7368265 В2).
В некоторых вариантах осуществления библиотека фрагментов ДНК с пришитыми адаптерами подвергается ПЦР амплификации, использующей прямой и обратный праймеры с фосфорилированными 5' концами, что позволяет ковалентно закольцевать такие молекулы с помощью ДНК лигазы на следующем этапе, этапе закольцовывания фрагментов. В некоторых вариантах осуществления ДНК фрагменты с прикрепленными адаптерами фосфорилируются полинуклеотид киназой и закольцовываются без предварительной ДНК амплификации.
В некоторых вариантах осуществления закольцовывание ДНК фрагментов с пришитыми адаптерами включает в себя следующие этапы: (а) денатурация амплифицированных с помощью ПЦР или не амплифицированных фрагментов ДНК, и (б) последующее внутри-молекулярное лигирование с использованием вспомогательного олигонуклеотида-«мостика», при котором денатурированные ДНК фрагменты отжигаются с олигонуклеотидом-«мостиком» в присутствии ДНК лигазы, например лигазы фага Т4, что приводит к образованию ковалентно замкнутых одноцепочечных кольцевых ДНК.
В некоторых вариантах осуществления, для обогащения библиотеки кольцевыми молекулами, незакольцевавшиеся линейные одноцепочечные фрагменты и избыток олигонуклеотида - «мостика» перевариваются (гидролизуются) в результате обработки лигированной смеси ДНК экзонуклеазами, например смесью Экзонуклазы I и Экзонуклеазы III Е. coli. Полученные таким образом кольца ДНК представляют собой библиотеку фрагментов ДНК из интересующего образца, готовую к процедуре секвенирования методом, описываемым в настоящем изобретении.
В некоторых вариантах осуществления вся библиотека ДНК из индивидуального образца, или же отдельные индивидуальные молекулы, составляющие библиотеку, метятся путем добавления баркодов [Kinde I., et al., Detection and quantification of rare mutations with massively parallel sequencing. Proc Natl Acad Sci USA. 2011; 108: 9530-35 и Kivioja T., et al. Counting absolute numbers of molecules using unique molecular identifiers. Nat Methods. 2012; 9: 72-4] к последовательности адаптеров, либо перед их лигированием с фрагментами ДНК образца, или в процессе ПЦР амплификации ДНК, когда баркоды являются частью последовательности ПЦР праймера(ов). Последовательности баркодов выбираются из последовательностей N-меров, где длина баркода N определяет размер конечного набора баркодов, отобранного по критерию близкой к 100% вероятности различить баркоды друг от друга. В некоторых вариантах осуществления используется один набор баркодов. В некоторых вариантах осуществления используется два или более наборов баркодов, что позволяет увеличить число меченых библиотек (или меченых индивидуальных молекул одной ДНК библиотеки) за счет возможности применить комбинаторную схему баркодирования (Фиг. 1). В некоторых вариантах осуществления баркодирование используется для мечения индивидуальных библиотек в целях их одновременного секвенирования после смешивания. Использование таких вариантов баркодирования в технологиях секвенирования называется мультиплексным секвенированием (Smith et al., Nucleic Acid Research, 2010, v. 38 (13), e142).
Метод секвенирования, представленный в настоящем изобретении, может быть классифицирован как одномолекулярный асинхронный электронный метод секвенирования в реальном времени. Он не требует множественных модификаций полимеразы, за исключением модификации для ее иммобилизации на поверхности сенсора. Метод секвенирования настоящего изобретения может использовать как ДНК, так и РНК полимеразы. В некоторых вариантах осуществления полимеразой может являться РНК полимераза, которая может быть выбрана из группы полимераз состоящей из РНК полимеразы фага Т7, РНК полимеразы фага Т3, РНК полимеразы фага SP6, и РНК полимеразы Е. coli. Эти полимеразы инициируют синтез РНК в специализированном участке двухцепочечной ДНК, называемом промотером. Транскрипция с закольцованной ДНК матрицы по механизму «транскрипции катящегося кольца» (ТКК) была продемонстрирована для РНК полимеразы фага Т7 (Mohsen and Kool, Асе. Chem. Res., 2016, v. 49 (11): 2540-2550).
В предпочтительных вариантах осуществления данного изобретения применяется ДНК полимераза. Однако такая полимераза должна соответствовать нескольким требованиям, чтобы сделать возможным секвенирование ДНК по методу, представленному в настоящем изобретении, а именно: (а) обладать сильной активностью вытеснения цепи и отсутствием 5'-3' флап-эндонуклеазной активности; (б) отсутствием 3'-5' зкзонуклеазной активности; (в) высокой процессивностью синтеза ДНК; (г) иметь возможность быть прикрепленной к поверхности сенсора способом, который бы не изменял ее функциональные свойства, такие как (а) и (в). В сравнении с методами секвенирования второго (например, Illumina) и третьего (например, Pacific Biosciences) поколения в представленном здесь методе отсутствует необходимость вводить мутационные изменения в аминокислотную последовательность полимеразы, чтобы она могла использовать для синтеза химически модифицированные нуклеотиды, так как полимераза, используемая в настоящем изобретении, имеет дело с природными не модифицированными нуклеотидами. Активность вытеснения цепи необходима полимеразе настоящего изобретения, чтобы быть способной проводить синтез ДНК, используя в качестве матрицы закольцованную ДНК, такую как одноцепочечные ДНК кольца или структуры типа «ДНК гантели». Такой тип синтеза ДНК, называемый «репликацией по механизму катящегося кольца» (РКК), копирует последовательность закольцованной матрицы множество раз, что приводит к образованию длинных конкатемерных одноцепочечных продуктов синтеза. Высокая процессивность синтеза ДНК необходима полимеразе для полимеризации десятков тысяч п.о. после единственного акта связывания с ДНК субстратом. Отсутствие 3'-5' зкзонуклеазной активности необходимо полимеразе для осуществления синтеза ДНК в 5'-3' направлении, без возможности удалять только что встроенный в цепь ДНК нуклеотид за счет экзонуклеазной коррекционной активности. Если же полимераза будет иметь такую коррекционную активность, она может иногда включать в растущую полинуклеотидную цепь один и тот же нуклеотид дважды и более раз, что приведет к двойной (тройной, и т.д.) регистрации сенсором включения этого нуклеотида, а значит, ошибке секвенирования. Многие из известных сегодня полимераз (Кленов Фрагмент ДНК полимеразы I, ДНК полимераза фага Phi29), и многие архейные ДНК полимеразы (например, Pfu полимераза) имеют такую экзонуклеазную активность, которая важна для высокой точности воспроизведения при естественном ДНК синтезе, так как позволяет проводить коррекцию случайного встраивания неправильных нуклеотидов, но является неприемлемой для секвенирования методом настоящего изобретения.
В предпочтительных вариантах осуществления используется мутантная 3'-5' ехо-полимераза, например, мутантная ДНК полимераза фага Phi29. Примером ДНК полимеразы фага Phi29 с отсутствием 3'-5' экзонуклеазной активности является ее производная полимераза с двойной мутацией, приводящей к замене двух аминокислот - D12A/D66A (Lagunavicius, A., et al., RNA, 2008; 14: 503-513). Другие мутации гена полимеразы фага Phi29 приводящие к заменам одиночных аминокислот, N62D и T15I, также значительно снижают 3'-5' экзонуклеазную активность (De Vega М, et al, EMBO J, 1996, 15: 1182-1192). Получены и другие одиночные и двойные мутантные варианты полимеразы фага Phi29 снижающие в 100-1000 раз 3'-5' экзонуклеазную активность полимеразы по сравнению с ферментом дикого типа, как, например, D12A, Е14А, D66A, и E14A/D66A (описаны в патенте US 5198543).
В некоторых вариантах осуществления ДНК полимераза для настоящего изобретения может быть выбрана из группы полимераз, включающих: ДНК полимеразу фага Phi29 (3'-5' ехо-), Большой Фрагмент Bst ДНК полимеразы, Bst 2.0 ДНК полимераза (полученная в результате in silico дизайна гомолога Большого Фрагмента ДНК полимеразы I из Bacillus stearothermophilus, New England Biolabs, США), Большой Фрагмент Bsm ДНК полимеразы (часть белка ДНК полимеразы из Bacillus smithii, Thermo Fisher Inc., США), VentR™ (3'-5' ехо-) ДНК полимераза, Кленов Фрагмент ДНК полимеразы I Е. coli, и большой фрагмент Bsu ДНК полимеразы.
В некоторых вариантах осуществления РРК инициируется на матрице, представляющей комплекс «ДНК праймер-ДНК кольцо» или «ДНК праймер-ДНК гантеля», полимеразой, обладающей сильной активностью вытеснения цепи ДНК, что является необходимым условием для высокопроцессивного механизма РКК. Термин "вытеснение цепи" описывает способность полимеразы вытеснять по пути синтеза нижележащую встречную цепь ДНК. ДНК полимераза фага Phi29 обладает самой сильной активностью вытеснения цепи ДНК среди известных полимераз и наиболее активна в пределах диапазона температур 20-37°C. Bsm ДНК полимераза не имеет 5'→3' и 3'→5' экзонуклеазных активностей, а Большой Фрагмент Bsm ДНК полимеразы имеет сильную активность вытеснения цепи и активен в широком диапазоне температур от 30°C до 63°C с оптимальной для синтеза температурой 60°C. Большой Фрагмент Bsu ДНК полимеразы имеет умеренную активность вытеснения цепи и работает в умеренном диапазоне температур, 20-37°C. Большой Фрагмент Bst ДНК полимеразы, с другой стороны, будучи ферментом, хорошо вытесняющим цепь, имеет высокую оптимальную температуру 65°C. Две другие полимеразы производства Nippon Gene Ltd. (Япония), Csa ДНК полимераза (оптимальная температура реакции 60-70°C) и 96-7 ДНК полимераза (оптимальная температура реакции 50-55°C), тоже обладают сильной активностью вытеснения цепи и используются в реакциях ДНК/РНК амплификации, таких как РКК или LAMP (Loop mediated isothermal amplification). Реакция РКК использует «катящееся кольцо», репликативную структуру, в которой только одна цепь кольцевого дуплекса ДНК используется как матрица для множества раундов репликации, и приводит к линейной амплификации ДНК в виде линейных одноцепочечных конкатемеров за счет повторного синтеза одной и той же цепи с кольцевой матрицы. «Катящееся кольцо» образуется тогда, когда синтез ДНК, инициированный на 3'-конце праймера, отожженного на одноцепочечном кольце (или 3'-конце «ника» - одноцепочечного разрыва в двухцепочечной ДНК, или 3'-конце «бреши» в ДНК), достигает 5-конца этого же отожженного на кольце праймера (в случае одноцепочечного ДНК кольца), или двухцепочечного участка ДНК «гантели», или 5' конца «ника» или «бреши». Затем ДНК полимераза начинает вытеснять вышележащий 5' конец и саму цепь ДНК, не служащую матрицей для синтеза новой ДНК. Таким образом, при РКК копируется только одна цепь ДНК. Элонгация синтезируемой цепи продолжается, и ДНК полимераза движется вокруг кольца, таким образом копируя последовательность ДНК кольцевой матрицы множество раз. Конечный продукт РКК представляет собой соединенное конец-в-конец (конкатенированное) большое число копий кольца в виде одноцепочечной ДНК. Конечная длина такой конкатенированной ДНК зависит от процессивности ДНК полимеразы. Так, РКК, катализируемая ДНК полимеразой фага Phi29, производит конкатемерные продукты размером >50 тыс. п.о. всего за 20-30 минут синтеза. Такие вновь синтезированные длинные линейные одноцепочечные молекулы спонтанно сворачиваются случайным образом в спирали размером в сотни нанометров и даже нескольких микрометров в длину.
В некоторых вариантах осуществления РКК инициируется на 3'-конце «ника» или «бреши» в полностью двухцепочечной кольцевой ДНК. В этом случае ДНК полимераза не копирует сначала всю одноцепочечную кольцевую матрицу (как в случае одноцепочечного кольца) или же одноцепочечную часть ДНК «гантели» прежде чем начать вытеснять выше лежащую цепь, а сразу (или через один или несколько нуклеотидов) начинает вытеснять 5' конец выше лежащего ДНК дуплекса.
В некоторых вариантах осуществления перед тем как полимераза помещается на поверхность, чтобы начать секвенирование по механизму РКК, осуществляется формирование комплексов «Полимераза-Праймер-ДНК Матрица». Это достигается путем двухступенчатого процесса: (а) отжиг-гибридизация олигонуклеотидных праймеров секвенирования с кольцами одноцепочечной ДНК (оцДНК) или одноцепочечными петлями ДНК «гантель» путем нагрева смеси до температуры >95°C с последующим медленным охлаждением до ~22-30°C приводящая к образованию бинарного комплекса «Праймер-ДНК Матрица»; (б) последующее добавление загрузочного буфера (буфер, способствующий связыванию полимеразы с поверхностью сенсора, т.е. «загрузке» полимеразы на поверхность) и ДНК полимеразы фага Phi29, приводящее к связыванию полимеразы с комплексом «Праймер-ДНК Матрица» и образование таким образом так называемого "замороженного" или "неактивного" (т.е. не функционирующего в данный момент, но готового к синтезу при наличии кофакторов) тройного комплекса «Полимераза-Праймер-ДНК Матрица». На этом этапе нуклеотиды и ионы магния отсутствуют в реакционной смеси, чтобы предотвратить инициацию ДНК синтеза. Далее перед началом инициации реакции секвенирования неактивные тройные комплексы загружаются в проточную ячейку, подаются на поверхность матрицы и иммобилизуются на поверхности сенсоров ячеек матрицы.
В некоторых вариантах осуществления комплексы для иммобилизации, содержащие ДНК матрицу, могут быть собраны в один этап добавлением загрузочного буфера и ДНК полимеразы, например, фага Phi29, непосредственно к двухцепочечным ДНК (дцДНК) кольцам, имеющим «ник» или «брешь» в одной из цепей ДНК (бинарный комплекс «Полимераза-ДНК Матрица»), так как праймер для начала секвенирования в этом случае не нужен. Как и в других вариантах осуществления, нуклеотиды и ионы магния отсутствуют в реакционной смеси, чтобы предотвратить инициацию ДНК синтеза. Далее перед началом инициации реакции секвенирования неактивные бинарные комплексы загружаются в проточную ячейку и иммобилизуются на поверхности матрицы сенсоров, представляющей собой чип секвенирования.
В некоторых вариантах осуществления перед загрузкой тройных комплексов в проточную ячейку и их иммобилизацией на поверхности сенсоров инициируется контролируемый, ограниченный по времени РКК синтез ДНК тройными комплексами в реакционной смеси, чтобы получить относительно громоздкие структуры, представляющие собой тройные комплексы, связанные с одноцепочечными продуктами ограниченного синтеза, свернутыми в спираль небольшого размера. Линейный размер такого комплекса должен примерно соответствовать длине стороны ячейки сенсора, что контролируется длительностью РКК по времени. Такая ограниченная контролируемая по времени РКК инициируется добавлением всех четырех нуклеотидов и ионов магния к сформированным тройным комплексам в растворе. После добавления кофакторов ДНК синтеза и инкубации при 25-30°C в течение времени, необходимого для получения продукта определенной длины, например, 2-5 минут, РКК реакция останавливается при помощи добавления в реакционную смесь хелатирующего ионы магния химического агента, например, этилендиаминтетрауксусной кислоты (ЭДТА). Сворачивание образованных конкатемерных РКК продуктов в случайную спираль, прикрепленную к исходной ДНК матрице и полимеразе, приводит к образованию компактных структур ДНК определенного диаметра. Длина продуктов РКК синтеза зависит линейно от времени реакции РКК, а их диаметр - не линейно. В некоторых аспектах свернутые конкатемерные частицы имеют диаметр поперечного сечения по крайней мере 5 нанометров, по крайней мере 5 нанометров, по крайней мере 10 нанометров, по крайней мере 20 нанометров, по крайней мере 30 нанометров, по крайней мере 40 нанометров, по крайней мере 50 нанометров, по крайней мере 100 нанометров, по крайней мере 500 нанометров, по крайней мере 800 нанометров, по крайней мере 1 микрометр, по крайней мере 2 микрометра и более.
Такие громоздкие структуры, состоящие из случайной спирали, прикрепленной к полимеразе и исходной ДНК матрице («Полимераза-ДНК Матрица-РКК Продукт»), могут быть использованы в методах настоящего изобретения, для того чтобы только один полимеразный комплекс мог связаться с поверхностью только одного сенсора за счет эффекта стерического препятствия (steric hindrance effect). Таким образом, исключается возможность связывание двух и более тройных комплексов с одним сенсором. Однако вероятность связывания более одного тройного комплекса с одним сенсором достаточно высока при использовании тройных комплексов, не подвергшихся ограниченной РКК, когда загрузка комплексов следует вероятностному распределению Пуассона (Poisson Distribution), так как ввиду малости своего размера по сравнению с площадью поверхности, события связывания тройного комплекса с поверхностью сенсора независимы друг от друга. Такой метод загрузки интермедиата реакции РКК, вместо нативных тройных комплексов, также позволяет обойти правило Пуассона и добиться почти 100% заполнения матрицы сенсоров единичными тройными комплексами. Загрузка же тройных комплексов, не подвергшихся ограниченному синтезу, следует распределению Пуассона и приводит в лучшем случае к ~40% заполненности сенсоров только одним иммобилизованным тройным комплексом.
В некоторых вариантах осуществления линейный размер комплексов «Полимераза-ДНК Матрица-РКК Продукт» примерно такой же, как поперечное сечение сенсора, и составляет по крайней мере 5-10 нанометров. В некоторых вариантах осуществления линейный размер комплексов «Полимераза-ДНК Матрица-Продукт РКК» составляет по крайней мере 10-20 нанометров (нм), или 20-50 нм, или 50-100 нм, или 100-1000 нм, или 1-2 микрометра.
Методы настоящего изобретения основаны на детекции единичных актов разделения заряда (образование одного протона и одного электрона) происходящих в активном центре фермента полимеразы при встраивании ею нуклеотида в растущую при синтезе цепь ДНК. Для того чтобы обнаружить такие единичные явления активный центр полимеразы в составе тройного комплекса должен быть расположен достаточно близко к поверхности сенсора. В некоторых случаях полимераза расположена на расстоянии примерно 100 нм от немодифицированной поверхности сенсора, примерно 80 нм от немодифицированной поверхности сенсора, примерно 60 нм от немодифицированной поверхности сенсора, примерно 50 нм от немодифицированной поверхности сенсора, примерно 20 нм от немодифицированной поверхности сенсора, примерно 15 нм от немодифицированной поверхности сенсора, примерно 10 нм от немодифицированной поверхности сенсора, примерно 5 нм от немодифицированной поверхности сенсора. В других случаях полимераза расположена на расстоянии меньше чем примерно 5 нм от немодифицированной поверхности сенсора: примерно 4 нм от немодифицированной поверхности сенсора, примерно 3 нм от немодифицированной поверхности сенсора, примерно 2 нм от немодифицированной поверхности сенсора, или примерно 1 нм от немодифицированной поверхности сенсора. Чтобы соответствовать этим требованиям, собранный заранее комплекс, «Полимераза-Праймер-ДНК Матрица» или «Полимераза-ДНК Матрица-РКК Продукт», должен быть привязан к поверхности сенсора за счет полимеразной части комплекса. Чтобы добиться этого, молекула полимеразы должна быть определенным способом (химически, или генетически, или биохимически) модифицирована так, чтобы создать участок связывания, который бы при взаимодействии с химической(ими) группой(ами), или лигандом(ами), или белком(ами), прикрепленными на поверхности сенсора, мог образовать химическую связь(и) достаточно крепкую, чтобы выдержать физические и химические условия среды, сопутствующие процессу секвенирования. В частности, определение потенциальных участков для модификации на поверхности ДНК полимеразы фага Phi29 значительно облегчается наличием известной трехмерной структуры белка (Berman A.J., et al., EMBO J. (2007) 26 p. 3494-3505). Очень важно, чтобы контролируемая модификация полимеразы была последовательно одинаковой для всех молекул полимеразы в комплексах. Тогда все молекулы полимеразы, привязанные к массиву сенсоров, будут ориентированы одинаково и будут иметь последовательно одинаковое расстояние от активного центра фермента до поверхности сенсора, а значит меньшую вариабельность в детектировании акта встраивания нуклеотида при секвенировании. Таким образом, и полимераза, и поверхность сенсора должны быть модифицированы так, чтобы полимеразная часть комплекса могла связаться с поверхностью сенсора на как можно более близком расстоянии, чтобы сенсор мог детектировать событие встраивания каждого нуклеотида.
Подходы и технологии иммобилизации можно условно разбить на три группы: физическая сорбция, биоафинное связывание и ковалентное связывание. Только два последних типа иммобилизации могут быть осуществлены в полностью контролируемом режиме в плане заданной трехмерной ориентации фермента относительно поверхности. Среди них ковалентная иммобилизация наиболее предпочтительна из-за ее специфичности, стабильности и быстроты.
В некоторых вариантах осуществления полимераза иммобилизуется на поверхности за счет биоафинного связывания. Например, полимераза модифицируется путем создания одной, двух и более биотиновых меток на поверхности белка. Такая биотиновая метка может представлять собой искусственный пептид AviTag, состоящий из 15 аминокислот (GLNDIFEAQKIEWHE) (Avidity LLC, США; см. http://www.avidity.com), который специфически узнается ферментом Биотин Лигазой (BirA) из Е. Coli, который биотинилирует аминокислоту лизин (K) в AviTag (Beckett D., et al., Protein Sci. 1999 Apr; 8 (4): 921-9; M. Fairhead and M. Howarth, Methods Mol Biol. 2015; 1266: 171-184). После идентификации места на поверхности полимеразы для встраивания AviTag производится модификация гена полимеразы, и AviTag становится интегральной частью фермента. Далее выделенный белок биотинилируется in vitro путем обработки Биотин-протеин лигазой (ЕС 6.3.4.15), которая активирует биотин с образованием биотинил 5' аденилата и переносит биотин на AviTag полимеразы. Avidity LLC (США) коммерциализировала также штаммы, например, AVB101, в которых можно при наращивании бактериальной массы индуцировать биотинилирование AviTag in vivo. Такая биотинилированная полимераза может быть селективно иммобилизованна на поверхности сенсора, несущего молекулу(ы) стрептавидина, белка имеющего сильную афинность к биотину. Формирующийся стрептавидин-биотин комплекс является самым сильным не ковалентным взаимодействием (Kd=10-15 М) из известных между белком и лигандом. Модификация поверхности сенсора осуществляется в несколько этапов. Если поверхность состоит из диоксида кремния (SiO2), она сначала покрывается биотин-ПЭГ-силаном (например, биотин-полиэтиленгликоль-триметоксисиланом от Laysan Bio., Inc., США) или смесью биотин-ПЭГ-силана и ПЭГ-силана (например, 2-[метокси(полиэтиленокси)6-9пропил]триметоксисилан, Мол. Вес 460-590 от Gelest, Inc.). В качестве альтернативы поверхность сенсора может быть модифицирована т.н. ZeroBkg «щеткой» биотин-ПЭГа (производится MicroSurfaces Inc. США). Следующим этапом такая пегилированная и биотинилированная поверхность обрабатывается тетрамерным белком стрептавидином, который связывается с одним или двумя биотинами на поверхности, образуя тем самым слой стрептавидина. После удаления несвязавшегося стрептавидина добавляются ДНК-полимеразные комплексы, несущие биотиновую группу в составе AviTag, которые связываются в свою очередь с оставшимися свободными валентностями на молекулах стрептавидина. В целом депозитирование биотин-ПЭГ-силана (или смеси биотин-ПЭГ-силана и мПЭГ-силана) с помощью техники ковалентного переноса из растворителя (solvent-based, covalent grafting technique) улучшает специфичность прикрепления биотинилированной полимеразы за счет отталкивания неспецифической адсорбции белков. Успешным примером использования AviTag технологии является удачная встройка двух биотиновых «ножек» в ДНК полимеразу, где привязанная к поверхности полимераза стала более процессивной (John G. K. Williams, et al, Nucleic Acids Research, 2008, Vol. 36, No. 18 e121).
В некоторых вариантах осуществления биоафинного связывания, когда поверхность сенсора покрыта золотом (Au) тоже может быть использована полимераза, модифицированная путем создания одной, двух и более биотиновых меток на поверхности белка. Биотин является витамином и представляет собой бициклическое кольцо и карбоксильную группу на боковой цепи валериановой кислоты. Эта карбоксильная группа биотина после модификации может стать биотинилирующим агентом. Такие функциализированные NHS-эфиром, гидразидом, или малеимидом биотины сохраняют интактным бициклическое кольцо, нужное для связывания с авидином (S. Luo и D.R. Walt. Anal. Chem. 61:1069 (1989); и R.N. Orth, Т.G. Clark и H.G. Craighead, Biomed. Microdevices, 2003, 5, 29). Биотины с этими функциональными группами могут быть нанесены непосредственно на поверхность золота, покрытую самособирающимся монослоем (ССМ) за счет реакции с аминами, тиолами, или другими подходящими реакционными группами на концах ССМ. Также молекулы биотина могут быть созданы на поверхности золота непосредственно путем образования ССМ рядом химических соединений на основе серы (S) содержащих биотиновые и гидроксильные группы (J. Spinke, et al., J. Chem. Phys., 1993, 99, 7012). Таким образом, полимераза иммобилизуется на поверхности золота за счет связывания с биотинами на ССМ через формирование «сэндвича» биотин-стрептавидин-биотин.
В некоторых вариантах осуществления для биоафинного связывания с поверхностью, содержащей диоксид кремния (SiO2), полимераза может быть модифицирована с помощью добавления поли-гистидиновой метки, например шести аминокислотных оснований гистидина, к N-концу или С-концу белка. При такой модификации [His]6-меченная полимераза иммобилизуется на поверхности сенсора через взаимодействие с хелатирующими ионами Cu2+ или Ni2+, прикрепленными к слою высокоплотного полиэтиленгликоля (ПЭГ), покрывающего SiO2 поверхность сенсора. Такая обработка сенсора, Ni-HTA-ПЭГ (Ni-нитрилотриацетатная кислота-ПЭГ) или Cu-НТА-ПЭГ (Cu-нитрилотриацетатная кислота-ПЭГ) (MicroSurfaces Inc., США), создает высокогидрофильную поверхность, препятствующую неспецифическому связыванию полимеразного комплекса с поверхностью.
В некоторых вариантах осуществления для биоафинного связывания с поверхностью, содержащей золото (Au), полимераза модифицирована с помощью добавления поли-гистидиновой метки, например шести аминокислотных оснований гистидинаб [His]6, к N- или С-концу белка. При такой модификации [His]6-меченная полимераза иммобилизуется на поверхности сенсора через взаимодействие с хелатирующими ионами Cu2+ или Ni2+, прикрепленными к самособирающемуся монослою (ССМ), имеющему НТА (нитрилотриацетатная кислота) группы. Такая модификация поверхности золота может быть получена, например, следующим способом в два этапа: сначала используя меркаптогексадеканоевую кислоту, формируется высокоупорядоченный слой с концевыми карбоксильными группами, а затем карбоксильная группа конденсируется с помощью производного нитрилотриацетатной кислоты содержащей аминогруппу для формирования пептидной связи. Плотность НТА групп контролируется условиями реакции (Thao Т. Le, et al., Phys. Chem. Chem. Phys., 2011, 13, 5271-5278). ССМ с НТА группами можно получить и другим способом, например, обработкой ССМ, собранного из 11-меркаптоундециламина гетеробифункциональным линкером N-сукцинимидил S-ацетилтиопропионатом (САТП), что приводит к образованию на поверхности ССМ концевых сульфгидрильных групп. Затем реакция малеимид-НТА молекул с сульфгидрильными группами приводит к образованию поверхности покрытой НТА-группами (Greta J. Wegner, et al., Anal. Chem., 2003, 75 (18), pp. 4740-4746). Можно также прикрепить НТА с концевыми аминогруппами к ССМ, несущему NHS-концевые группы, как описано в Vallina-Garcia R, et al., Biosens Bioelectron, 2007 Sep 30; 23 (2): 210-7. Еще можно использовать самособирающийся на Au-поверхности полимер, представляющий собой полиакриламид-ко-n-акрилоксисукцинимид кополимер, функционализированный тандемом активного эфира (NHS) сшитого с 3-(метилтио)пропиламином (МТП) и НТА. В результате получается гидрофильная пленка толщиной 2-5 нм несущая НТА-группы (Thompson LB, et al., Phys Chem Chem Phys. 2010 May 7; 12 (17): 4301-8).
В некоторых вариантах осуществления полимераза, несущая одну или больше сульфгидрильных (тиоловых) групп (-SH) на ее поверхности, иммобилизуется на поверхности сенсора, модифицированной малеимидной реактивной группой. Сульфгидрильные группы находятся в боковых цепях цистеина (Cys, С). Часто они являются частью вторичной или третичной структуры белка, и могут быть соединены через боковые цепи дисульфидными связями (-S-S-). Ковалентная связь между малеимидной группой и сульфгидрильной группой является одной из наиболее селективных и легких реакций в химии биоконъюгации. Большим преимуществом такой стратегии является то, что для ковалентной иммобилизации белка в общем случае не нужна пришивка специальных меток-«тэгов» и химических модификаций белка. Кроме того, тиольные группы могут быть использованы, чтобы направить реакцию связывания белка с поверхностью подальше от активных центров ферментов. Иммобилизация на поверхности проводится следующим образом: сначала создаются сульфгидрильные группа(ы) на поверхности белка путем восстановления дисульфидных связей, или после химической модификации первичных аминов путем введения SH-групп с помощью специфических реагентов. Затем эти сульфгидрильные группы ковалентно связываются с поверхностью, модифицированной (активированной) малеимидом. Хотя дисульфидные связи между двумя цистеинами в белках являются очень стабильными, они могут быть восстановлены редуцирующими агентами (R-SH) такими как дитиотрейтол (ДТП, 2-меркаптоэтанол, и т.д.
В некоторых вариантах осуществления для иммобилизации на активированной малеимидом поверхности могут быть использованы уже существующие в полимеразе сульфгидрильные группы, находящиеся на поверхности белка, или же новые цистеины могут быть созданы в заданных участка белка, лежащих на поверхности, основываясь на данных трехмерной структуры фермента. Для создания новых остатков Cys желательно заменять на них поверхностно лежащие серины (Ser) (полярная и изостеричная аминокислота) и аланины (Ala) (маленькая, гидрофобная аминокислота), так как такие замены меньше всего нарушают существующую структуру белка. При необходимости «зарытые» внутрь белка и не вовлеченные в дисульфидные связи Cys остатки могут быть элиминированы заменой на, например, Ser и Ala.
В некоторых вариантах осуществления для связывания полимеразы имеющей сульфгидрильные группы на поверхность сенсора, содержащую золото (Au), может использована химическая реакция, основанная на самособирающемся монослое (ССМ) алкантиолов, на концах которых расположены функциональные группы, такие как амин или карбоксильная группа. Атомы серы алкантиолов взаимодействуют с золотом, образуя крепкие стабильные связи, а цепи метиленов способствуют самосборке алкантиолового слоя за счет сил ванн-дер-Ваальса. Затем ССМ с концевым амином модифицируется с помощью амин-сульфгидрил кросслинкера ССМЦК (сульфосукцинимидил 4-(N-малеимидометил)циклогексан-1-карбоксилат), который содержит NHS-эфир и малеимидные рективные группы на противоположных концах. В результате получается активированный ССМ с концевыми малеимидными группами готовыми ковалентно связать фермент, имеющий доступную для связывания сульфгидрильную группу(ы).
В некоторых вариантах осуществления для связывания полимеразы, имеющей сульфгидрильные группы, на поверхность сенсора, содержащую диоксид кремния, используется линейный гетеробифункциональный ПЭГ реагент, имеющий малеимид и силан: МАЛ-ПЭГ-Силан, например сделанный CreativePEG Works Inc., США (Ogorzalek, TL, Examining the Behavior of Surface Tethered Enzymes, Diss. University of Michigan, 2015). Малеимид взаимодействует с сульфгидрильной группой, а силан - с гидроксилированной поверхностью диоксида кремния. ПЭГ подавляет неспецифическое связывание заряженных молекул, например, ДНК и белков, с поверхностью.
Ниже приведено более подробное описание вариантов устройства секвенирования, реализующих одномолекулярный способ секвенирования, которые также являются предметом настоящего изобретения.
Устройство содержит микросхему матрицы ячеек сенсоров, которая является основным компонентом устройства одномолекулярного секвенирования (секвенатор) во всех вариантах его конструктивного исполнения.
В каждой ячейке матрицы микросхемы организуют выполнение процедуры полимеризации одного одноцепочечного фрагмента нуклеиновой кислоты, в составе иммобилизованного на подготовленную поверхность сенсора ячейки комплекса «полимераза-матрица ДНК-праймер», результаты встраивания нуклеотидов полимеразой в ходе реакции полимеризации одноцепочечных фрагментов ДНК (далее - реакция) в каждой ячейке матрицы преобразуются в полезный сигнал сенсором ячейки и регистрируется аналого-цифровой схемой ячейки; реакции полимеризации фрагментов ДНК в ячейках матрицы происходят независимо друг от друга.
В зависимости от решаемой задачи секвенирования может быть:
- выбран темп встраивания нуклеотидов одновременно для всех ячеек матрицы, в широком диапазоне: от 1-го нуклеотида в секунду и менее, и до 50-60-ти нуклеотидов в секунду и более, посредством управления значениями таких параметров реакции, как температура, pH раствора, концентрация нуклеотидов в реакционной смеси, выбором варианта генной модификации той или иной полимеразы;
- выбрана микросхема матрицы с соответствующим количеством ячеек сенсоров (может содержать от менее чем 1048576 до 256000000 и более ячеек в матрице);
- выбран одноматричный или четырехматричный вариант конструкции секвенатора для применения последовательного или параллельного способа секвенирования, соответственно.
В некоторых вариантах осуществления темп встраивания нуклеотида составляет 0. 1-2 нуклеотида в секунду. В некоторых вариантах осуществления темп встраивания нуклеотида составляет 1-10 нуклеотидов в секунду. В некоторых вариантах осуществления темп встраивания нуклеотида составляет 10-50 нуклеотидов в секунду. В некоторых вариантах осуществления темп встраивания нуклеотида составляет 50-100 нуклеотидов в секунду.
Микросхема матрицы ячеек сенсоров может изготавливаться по стандартному полупроводниковому КМОП технологическому процессу или по индивидуальному технологическому процессу (в зависимости от того, какая конструкция сенсора применяется). Обеспечение доступа биоматериала к поверхности сенсора каждой ячейки матрицы реализуется набором стандартных технологических операций, предусмотренных технологическим процессом, и последующей обработкой этих поверхностей тем или иным способом, варианты которых описаны в разделе «Подходы и технологии иммобилизации…».
Например, микросхема матрицы ячеек сенсоров может как содержать все ниже перечисленные блоки, так и содержать только часть из них. Один из возможных вариантов структурной схемы микросхемы матрицы ячеек сенсоров показан на Фиг. 10.
1. Матрица ячеек сенсоров включает в себя:
1.1. Ячейки сенсоров, расположенные в рядах и столбцах матрицы, каждая из которых состоит из:
1.1.1. Электронного сенсора №1, формирующего полезный сигнал;
1.1.2. Электронного сенсора №2, формирующего фоновый сигнал;
1.1.3. Дифференциального зарядового усилителя, подключенного к сенсорам;
1.1.4. Усилителя сигнала (повторителя);
1.1.5. Триггера Шмитта (для исключения влияния шумов входного сигнала на выходной сигнал)
1.1.6. Делителя тактовой частоты, схемы тактирования триггера;
1.1.7. Тактируемого триггера (например, D триггер с выходом с тремя состояниями) для перезаписи сигнала с выхода триггера Шмитта на выход схемы ячейки;
1.2. Датчик температуры со схемой измерения и передачей данных в контроллер микросхемы.
1.3. Вертикальный сдвиговый регистр переноса данных от выхода схем ячеек - для каждого столбца ячеек матрицы.
1.4. Горизонтальный сдвиговый регистр переноса данных из вертикальных регистров на выход микросхемы.
2. Контроллер обмена данными с устройством обработки и отображения данных (компьютером) по интерфейсу USB, обеспечивающий вывод данных от каждой ячейки матрицы в компьютер, управляющий величинами опорных напряжений и частотой тактовых импульсов, необходимых для работы аналого-цифровых схем ячеек матрицы, управляющий температурой микросхемы и водного раствора над ее поверхностью (или только температурой водного раствора над поверхностью матрицы микросхемы).
3. Генератор тактовой частоты формирует сетку частот для работы аналого-цифровых схем ячеек матрицы и сдвиговых регистров переноса данных, управляемых контроллером.
4. Источник опорных напряжений обеспечивает необходимыми токами и напряжениями элементы аналого-цифровых схем ячеек матрицы, регистры переноса данных.
5. Электрод смещения и управляемый контроллером источник напряжения для него.
6. USB интерфейс передачи данных между компьютером и микросхемой.
Пример варианта структурной схемы четырехматричного устройства, реализующего одномолекулярный способ секвенирования, показан на Фиг. 11.
Микросхема матрицы ячеек сенсоров с крышкой микрофлюидного устройства 12 является основным компонентом устройства одномолекулярного секвенирования.
Неотъемлемой частью устройства секвенирования в любом из его вариантов конструктивного выполнения является микрофлюидное устройство, которое обеспечивает:
- подачу водных растворов на поверхность матриц микросхем с целью иммобилизации комплексов на поверхность сенсоров ячеек матрицы,
- подачу водных растворов реакционных смесей на поверхность матриц микросхем 12 с целью обеспечения проведения реакций в ячейках матриц,
- подачу буферного раствора на поверхность матриц микросхем 12 с целью подготовки этих поверхностей к процедурам иммобилизации комплексов и секвенирования,
- измерение проводимости раствора на выходе крышки микросхемы 12 с целью определения качества промывки буферным раствором поверхности матрицы микросхемы 12,
- регулирование температуры матрицы микросхемы 12 и водного раствора над ней посредством элемента Пельтье посредством контроллера микросхемы на основании показаний датчика температуры; значение температуры, которое необходимо поддерживать, передается контроллеру микросхемы устройством обработки и отображения данных (компьютером);
- слив растворов с поверхности матрицы микросхемы 12.
В состав микрофлюидного устройства (изображено на Фиг. 11) может входить:
- четыре бака малого объема для размещения в них четырех растворов 10 с реакционными смесями;
- один бак большого объема 11 для размещения в нем буферного раствора,
- один бак большого объема 11 для размещения в нем комплексов, например, «полимераза-фрагмент ДНК-праймер»,
- один бак большого объема 11 для размещения в нем раствора веществ, необходимых для подготовки поверхности матрицы микросхемы к иммобилизации комплексов на поверхности сенсоров ячеек матриц микросхемы,
- один бак большого объема 11 для слива растворов с поверхности матрицы микросхемы;
- крышка микросхемы матрицы ячеек сенсоров для одноматричного устройства секвенирования, и четыре крышки микросхемы матрицы ячеек сенсоров для 4-матричного устройства секвенирования, - для удержания растворов на поверхности матрицы микросхемы,
- насос 13 с электрическим приводом, для каждой микросхемы 12 устройства секвенирования;
- отсечные клапана 14 с электрическим приводом, обеспечивающие возможность раздельной подачи буферного раствора, раствора с веществами для иммобилизации комплексов, раствора с реакционной смесью на поверхность матрицы микросхемы 12;
- элемент Пельтье 16 (входящий в состав устройства поддержания температуры рабочего раствора) для каждой микросхемы 12 устройства секвенирования;
- датчик температуры полупроводникового типа, интегрированный в состав схемы микросхемы вместе со схемой формирования электрического сигнала, соответствующего показаниям датчика; датчик температуры может быть дискретным, полупроводникового или иного типа, интегрированным в крышку микросхемы матрицы ячеек сенсоров, со схемой формирования электрического сигнала, интегрированного в состав схемы микросхемы;
- электроды 15 для измерения проводимости раствора на выходном патрубке каждой крышки микросхемы 12.
Микрофлюидное устройство и каждая микросхема 12 матрицы ячеек сенсоров работают под управлением контроллера 17 и устройства обработки и отображения данных (компьютера) 18 устройства секвенирования, которые также являются неотъемлемой частью устройства секвенирования. Устройство обработки и отображения данных 18, включающее один или несколько процессоров, служит для приема, обработки и хранения данных о секвенируемых нуклеиновых кислотах, а также для управления всеми процедурами секвенирования. Как вариант, микрофлюидное устройство и микросхема могут работать под управлением контроллера микросхемы, соответствующие команды которому передаются устройством обработки и отображения данных (компьютером).
Средство хранения данных может представлять собой жесткий диск (HDD), твердотельный накопитель (SSD), флэш-память (NAND- flash, EEPROM, Secure Digital и т.п.), оптический диск (CD, DVD, Blue Ray), мини диск или их совокупность.
Несмотря на то, что изобретение описано со ссылкой на раскрываемые варианты воплощения, для специалистов в данной области должно быть очевидно, что конкретные подробно описанные эксперименты приведены лишь в целях иллюстрирования настоящего изобретения, и их не следует рассматривать как каким-либо образом ограничивающие объем изобретения. Должно быть понятно, что возможно осуществление различных модификаций без отступления.
Нижеследующие примеры работы устройства приведены в целях раскрытия характеристик настоящего изобретения и их не следует рассматривать как каким-либо образом ограничивающие объем изобретения, от сути настоящего изобретения.
Пример 1. Репликация катящегося кольца (РКК) тройным комплексом «Полимераза-Праймер-ДНК Матрица» происходит на твердой поверхности сенсора.
Чтобы сконструировать кольцевую одноцепочечную ДНК матрицу для синтеза ДНК полимеразой фага Phi29 в качестве матрицы для ПЦР использовали 10 нг олигонуклеотида Ультрамера длиной 177 нт (Integrated DNA Technologies Inc., США). Реакция проводилась в реакционной смеси в объеме 50 мкл содержащем 2х Q5 Polymerase смесь (New England Biolabs, Inc., США), матрицу, и 500 нМ прямого и обратного ПЦР праймеров.
Термоциклирование проводилось в следующих условиях: 98°C 30 сек; затем 30 циклов - 98°C 10 сек, 58°C 30 сек, 72°C 40 сек; далее 72°C 2 мин. По завершению ПЦР двухцепочечные продукты были очищены, используя набор для очистки ДНК и элюированы 50 мкл 50 мМ Трис pH 8.0.
2 пикомоля (пм) ПЦР продукта были смешаны со 100 пм олигонуклеотида-«мостика», денатурированы нагреванием 3 мин при 95°C с последующим кратким охлаждением 3 мин во льду, и закольцованы лигированием 1 час при 37°C в 1х ТА Буфере (33 мМ Трис-ацетат pH 7.5, 66 мМ калий ацетат, 10 мМ магний ацетат, и 0.5 мМ ДТТ) с добавлением 1 мМ АТФ, 2 Единиц/мкл 14 ДНК Лигазы (New England Biolabs, Inc., США). Для переваривания остатков не закольцованного ПЦР продукта и избытков олигонуклеотида-«мостика» к лигазной смеси были добавлены Экзонуклеаза I и Экзонуклеаза III (обе от Enzymatics, Inc., США) до конечной концентрации 0.7 Единиц/мкл и 1 Единиц/мкл соответственно, и реакция переваривания продолжалась 30 мин при 37°C. Реакция была остановлена добавлением ЭДТА до конечной концентрации 25 мМ.
Ковалентно замкнутые одноцепочечные кольца (оцКольца) были очищены из реакционной смеси, используя NucleoSpin® Gel и PCR Clean-Up Kit (Clontech, Takara Co., Япония).
В приводимом примере олигонуклеотид-«мостик» использовался также в качестве праймера для РКК, с которого инициировался синтез ДНК полимеразой фага Phi29. Для получения тройных комплексов «Полимераза-Праймер-ДНК Матрица» сначала 100 фемтомолей оцКолец были смешаны с олигонуклеотидом-«мостиком» (конечная концентрация 0.5 микроМоль) в буфере 10 мМ Трис pH 8.0/25 мМ NaCl/0.1 мМ ЭДТА, нагреты до 94°C на протяжении 3 мин, охлаждены до 52°C в течение 5 мин, и затем медленно охлаждены до 30°C. В результате этого были получены комплексы «Праймер-Матрица». Затем к комплексам был добавлен 10х Загрузочный Буфер до 1х конечной концентрации: 50 мМ Трис-HCl/10 мМ (NH4)2SO4/4 мМ ДТТ/0.05% Твин-80 pH 7.5. Затем к смеси была добавлена Ехо- (D66A) ДНК полимераза фага Phi29 несущая N-терминальную Биотин-метку, создавая 2-кратный избыток комплекса «Праймер-Матрица» по отношению к полимеразе. Смесь инкубировалась при 10°C в течение 15 мин для образования тройных комплексов. Метод прикрепления к полимеразе биотиновой метки хорошо известен в уровне техники (например, Beckett D., et al, Protein Sci., 1999 Apr; 8 (4): 921-9; Fairhead и Howarth, Methods Mol Biol., 2015, 1266: 171-184).
Тройные комплексы были помещены в проточную ячейку, сделанную из ПЭГилированного с помощью ПЭГ-силана (2-[methoxy(polyethyleneoxy) 6-9 propyl] trimethoxysilane, MPEOPS, MW=460-590, Gelest Inc., США) стеклянного слайда, тонкого покровного стекла, модифицированного ПЭГ-биотином (MicroSurfaces Inc., США), и чувствительного к давлению адгезивного материала толщиной 100 микрометров (PSA, 3М Inc., США), играющего роль спэйсера. Перед помещением тройных комплексов белок стрептавидин был иммобилизован на биотинилированном слое ПЭГ в результате добавления 20 мкл 0.1 мг/мл стрептавидина, растворенного в буфере, содержащем 10 мМ Трис-HCl/50 тмМ NaCl pH 8.0. После одноминутной инкубации избыток стрептавидина был удален из проточной ячейки ее промывкой 100 мкл того же буфера. После этого в ячейку были добавлены тройные комплексы и иммобилизованы на ПЭГ-Биотин-Стрептавидин поверхности в течение 15 мин при 10°C. В качестве контроля тройные комплексы были также помещены во вторую проточную ячейку, поверхность которой не была обработана стрептавидином. Не связавшиеся с поверхностью комплексы были удалены из проточных ячеек промыванием 200 мкл 1х Загрузочного Буфера. Затем, чтобы запустить РКК реакцию, в проточную ячейку был подан раствор 1х Загрузочного Буфера с добавкой 10 мМ MgCl2 (конечная концентрация) и 400 нМ dNTP (конечная концентрация каждого нуклеотида). РКК реакция продолжалась 20 мин при 30°C. Реакция была остановлена добавлением 25 мМ раствора ЭДТА pH 8.0.
Для того, чтобы визуализировать продукты реакции ДНК синтеза, выполненного Phi29 полимеразой на поверхности чипа, продукты реакции были окрашены ДНК интеркаляторным красителем GelStar Stain (Lonza Rockland Inc., Rockland, USA), разведенным 10000 раз в буфере: 10 мМ Трис-HCl/50 mM NaCl pH 8.0. Сразу после добавления красителя в проточную ячейку чип помещался на флюоресцентный микроскоп Zeiss Axiovert, освещался 480 нанометровым лазером, и окрашивание продуктов записывалось на цифровую камеру. Результаты этого эксперимента представлены на Фиг. 6А, и демонстрируют способность иммобилизованной на поверхности ДНК полимеразы Phi29 осуществлять синтез ДНК с кольцевой матрицы. Контрольный образец поверхности покровного стекла не пассивирован стрептавидином, а значит, не способен связывать тройной комплекс, что и приводит к отсутствию видимых продуктов синтеза ДНК полимеразой. Отдельные немногочисленные продукты, видимые на контрольной поверхности, возникают за счет слабого неспецифического связывания тройных комплексов с PEG-биотин поверхностью (см. Фиг. 6Б).
Пример 2. Полупроводниковый сенсор и схема ячейки матрицы, изготовленные по полупроводниковой КМОП технологии.
Примеры возможных конструкций ячейки сенсора представлены на Фиг. 12-14, 16, 17, в том числе со схемой, реализующей функцию стохастического резонанса, представленной на Фиг. 15.
Реакция полимеризации фрагмента ДНК полимеразой комплекса 19, 25, 31, 38, иммобилизованного на поверхности сенсора ячейки, в результате взаимодействия полимеразы с реагентами раствора реакционной смеси 22, 28, 34, 41, сопровождается разделением и локализацией отрицательного заряда (электрона) и свободного протона около активированного сегмента фрагмента ДНК. Таким образом, результатом реакции является генерация пары электрон - протон, с последующей локализацией электрона на активированном сегменте фрагмента ДНК и дрейфом протона в водном растворе реакционной смеси во внешнем электрическом поле ячейки по направлению к электроду смещения 23, 29, 35, 42, который подключен к источнику напряжения, управляемому контроллером микросхемы матрицы ячеек сенсоров. В процессе дрейфа протона происходит его экранировка отрицательными ионами раствора (например, ОН-) за характерное время тэп. Кроме того, локализованный электрон, находящийся в области диффузионного слоя, в течение некоторого характерного времени тээ также будет экранирован ионами раствора. Таким образом, на приемном электроде (т.е. в объеме затворной области канала транзистора считывающего заряд - далее считывающий электрод), с характерным временем дрейфа тd протона в рабочем растворе растет величина заряда, индуцированного суперпозицией полей от локализованного на активированном сегменте фрагмента ДНК отрицательного заряда и положительного заряда протона, дрейфующего от места разделения зарядов во внешнем поле в направлении электрода смещения, усугубленного развивающейся экранировкой протона ионами гидроксильных групп. Т.е. принципиально важным обстоятельством, обеспечивающим саму возможность появления индуцированного потенциала на считывающем электроде, является наличие электрического поля в водном растворе, которое увеличивает скорость дрейфа протона, что обеспечивает большую величину для характерного времени тэп полной экранировки протона отрицательными ионами раствора. Электрическое поле в водном растворе создается приложенным потенциалом к электроду смещения, который расположен, например, на внутренней стороне крышки микросхемы. Напряжение смещения задается управляемым источником напряжения (питания) относительно потенциала общего электрода (на Фигурах не показан). Источником напряжения смещения управляет контроллер микросхемы, имеющий обратную связь с аналого-цифровой схемой ячейки. После того как все подготовительные к секвенированию операции завершены, устройство обработки и отображения (компьютер) передает данные контроллеру микросхемы о том, что реакции полимеризации фрагментов ДНК, с большой долей вероятности, начались в ячейках. После декодирования этих данных контроллер микросхемы анализирует значения логических величин в последовательности временных интервалов с выхода аналого-цифровой схемы ячейки, последовательно, с временной задержкой, управляет увеличением напряжения с выхода источника напряжения (питания) смещения от нуля вольт до некоторой величины, которая обеспечивает регистрацию и формирование сигнала. Механизм индуцирования заряда на поверхности затвора полевого транзистора в ходе реакции полимеризации фрагмента ДНК и регистрации результата его образования описан, например, в работах Надара Пурманда (Pourmand N., et al., Proc Natl Acad Sci USA, 2006 Apr 25; 103 (17): 6466-70; Pourmand N., et al., A label-free CMOS DNA microarray based on charge sensing, in Proceedings of the IEEE Instrumentation and Measurement Technology Conference, Victoria, ВС, Canada, May 12-15, 2008).
Реакция полимеризации фрагмента ДНК в ячейке организована таким образом, что происходит в среднем несколько, например, пять встраиваний полимеразой комплементарных нуклеотидов в секунду. Каждое встраивание нуклеотида сопровождается разделением одной пары зарядов. Факт разделения каждой пары зарядов регистрируется и преобразуется сенсором ячейки в электрический сигнал, который сначала усиливается дифференциальным зарядовым усилителем, потом усилителем, с выхода которого поступает на компаратор с положительной обратной связью (триггер Шмитта); с выхода которого сигнал уже в цифровой форме фиксируется, например, D-триггером, установкой его выхода в состояние логической "1".
Функционально, индуцированный потенциал на затворе полевого транзистора модулирует амплитуду тока в канале транзистора, сток которого подключен к дифференциальному зарядовому усилителю; другой вход дифференциального усилителя подключен, например, к стоку полевого транзистора сенсора, транзистором которого формируют фоновый сигнал Фиг. 14. Выход дифференциального усилителя соединен со входом усилителя, назначение которого состоит в том, чтобы сформировать на своем выходе амплитуду напряжения полезного сигнала такой величины, которая достаточна для переключения триггера Шмитта, построенного на основе компаратора с положительной обратной связью, в состояние логической "1". Выход триггера Шмитта соединен со входом D-триггера, который тактируется схемой деления ячейки тактовой частотой генератора микросхемы, перезаписывая логические значения ("1" и "0") с выхода триггера Шмитта на выход D-триггера с частотой, превышающую частоту (темп) встраивания нуклеотидов в ходе реакции полимеризации, например, в четыре раза. В результате, на выходе аналого-цифровой схемы будут формироваться последовательности дискретных интервалов времени, аналогичные тем последовательностям, которые представлены на Фиг. 5А: логической единицей обозначаются интервалы времени, когда сенсором и аналого-цифровой схемой ячейки были, соответственно, зарегистрированы и сформированы сигналы о фактах разделения зарядов вблизи от считывающего электрода. Сопоставить зарегистрированные факты разделения пар зарядов с их причиной (встраиванием полимеразой комплементарного нуклеотида) помогает знание априори темпа встраивания полимеразой нуклеотидов трех видов, концентрация которых нормальна в водном растворе реакционной смеси. Сначала производится расчет значений параметров водного раствора реакционной смеси, таких как: pH, температура раствора, концентрации нуклеотидов всех видов, которые обеспечивают желаемый темп полимеризации фрагмента ДНК, а потом значения этих параметров устанавливаются для рабочих растворов перед началом секвенирования.
Напряженность электрического поля на границе раздела считывающий электрод - раствор определяется суперпозицией полей от упомянутых выше зарядов: локализованного на активном сегменте фрагмента ДНК отрицательного заряда величиной в один электрон, и положительного заряда дрейфующего протона, и может быть представлена выражением:

Здесь μp - подвижность протона в электролите, Е - напряженность суперпозиции полей в электролите близ считывающего электрода, t - текущее время, xm - расстояние от места локализации электрона на фрагменте ДНК до плоскости границы раздела электрод - раствор (х=0), ε - диэлектрическая проницаемость рабочего раствора, q - элементарный заряд, εо - диэлектрическая постоянная вакуума.
С течением времени поле на считывающем электроде стремится к максимальной величине, равной:

Для определения возможности полупроводниковым сенсором регистрировать результат разделения одной пары зарядов были выполнены соответствующие расчеты. Оценки параметров ячейки выполнялись для размеров считывающего электрода (затвора полевого транзистора) 30 нм × 100 нм, для водного раствора с pH=7,5 концентрации протонов и ионов (ОН-) взята равной ~ N(H+) ≈ N(OH-1) ≈ 3,3×10-10 моль/см3 (в 1 см-3 находится N(H+)=N(OH-1)≅2×1014 штук), т.е. расстояние между ними (ионами гидроксильных групп и протонами) в водном растворе ro=(Nиона)-1/3≈2×10-5 см = 0,2 мкм = 2×10-7 м; коэффициент диффузии протона в водном растворе принят равным Dp=9,3×10-5 см2/Вс, коэффициент диффузии иона гидроксильной группы принят равным DOH=5×10-5 см2/Вс; для коэффициента диэлектрической проницаемости водного раствора приняли значение равным 30.
Дрейфовые характеристики протонов и ионов (ОН-) в водном растворе (характерные времена экранирования этих зарядов) будут определяться минимальным электрическим полем E*=q/{[(Nиона)-1/3]2εoε4π. Характерное время экранирования указанных зарядов с концентрацией ионов Nионов в водном растворе оценивали как т*=[N(H+)]-1/3/(μиона⋅Е*), где r0=[N(H)+]-1/3=[N(OH)]-1/3 - среднее расстояние между взаимно одноименными и взаимно разноименными ионами гидроксильных групп (ОН-) и протонами (Н+); подвижности ионов гидроксильных групп (ОН-) и протонов (Н+) рассчитали и приняли равными: μр=3,54⋅10-7 м2/Вс, μОН-=1,075⋅10-7м2/Вс.
Оценили величину минимальной напряженности электрического поля Е* от дрейфующего протона, которое, взаимодействуя с отрицательными ионами раствора, будет определять время экранирования протона:
Е*=q/{[(Nиона)-1/3]2εоε4π=(1,6×10-19)/{[2×10-7]2×8,85×10-12×30×4×3, 14}=1,1×103 В/м.
Это минимальное поле (поле на максимальных расстояниях между протоном и гидроксильной группой), которое и будет определять время экранирования протона.
Для случая расположения активного сегмента фрагмента ДНК в диффузионной части (но вне приповерхностной части (слой Гельмгольца двойного слоя)) двойного слоя оценили время выхода потенциала считывающего электрода на насыщение, которое определяется скоростью дрейфа протона в диффузионной части двойного слоя:
тэ**>тр=rо/(μp⋅Е**)≈(2⋅10-7/3,54⋅10-7⋅5×103)≈2×10-4 с, где Е**≈5×103 В/м, - это оценка снизу; понятно, что оценка времени экранирования протона сверху будет на порядок меньше. Также понятно, что если время экранирования протона после его образования в результате разделения пары зарядов стремится к нулю, то ставится под вопрос сама возможность появления индуцированного потенциала на считывающем электроде.
Если принять расстояние от считывающего электрода до электрода смещения, находящегося под отрицательным потенциалом, например, 0,5 В, равным 1 мм, то средняя величина электрического поля в этом промежутке будет равно 5 В/см (или 500 В/м). Тогда время дрейфа протона во внешнем поле можно оценить как:
t2=(2xm)/(μpEвн)=2⋅10-8/(3,54⋅10-7⋅500)≈10-4 с
За это время протон уйдет от места разделения зарядов xm на расстояние:
L(тэр)=μp⋅Е*⋅тэр=3,54×10-7×500×10-4=1,8×10-8 м = 18 нм.
Таким образом, влияние электрического поля дрейфующего протона на процесс индуцирования заряда на считывающем электроде уменьшается с течением времени за счет дрейфа протона, а не за счет его экранирования подвижными ионами водного раствора (гидроксильными группами ОН-). Индуцированный заряд на емкости считывающего электрода преобразуется в потенциал, который модулирует ток в канале полевого транзистора, который, в свою очередь, можно считывать во внешнюю цепь посредством зарядочувствительного (электрометрического) усилителя.
Для считывающего электрода размером 30 нм × 100 нм, при расстоянии между местом локализации электрона на фрагменте ДНК после разделения зарядов и поверхностью считывающего электрода в 20 нм, и диэлектрической проницаемости водного раствора равной 30, для емкости считывающего электрода получаем величину Сэ=4×10-16 Ф. Заметим, что емкость хорошего зарядочувствительного (электрометрического) усилителя составляет величину Свх.≈1015 Ф. При указанных параметрах ячейки, с учетом возникающего емкостного делителя, величина индуцированного потенциала составит 4×104 В, а выходное напряжение электрометрического усилителя окажется равным 14,5×10-6 В. Заметим, что в водном растворе с большей ионной силой, для расположения места локализации электрона на фрагменте ДНК после разделения зарядов в диффузионной части двойного слоя, расстояние между этим местом и поверхностью считывающего электрода необходимо будет уменьшить, что приведет к большей величине индуцированного потенциала на емкости считывающего электрода чем 4×10-4 В.
Оценки электрических шумов при принятых значениях параметров ячейки и водного раствора реакционной смеси показали следующие величины:
ток дробового шума ~3,5×10-15 А,
напряжение теплового шума ~4,2 мкВ,
ток генерационно-рекомбинационного шума ~2,5⋅1017 А,
напряжение генерационно-рекомбинационного шума ~24 нВ.
Таким образом, результаты анализа и расчета величин электрофизических параметров физико-химических процессов сопровождающих процесс секвенирования фрагмента ДНК в ячейке подтверждают возможность регистрации результата разделения одной пары зарядов, которое сопровождает встраивание полимеразой нуклеотида в полимеризуемый фрагмент ДНК, предложена методика регистрации и ее схемная реализация.
Указанные размеры считывающего электрода (затвора транзистора), конструкции сенсора, ячейки, аналого-цифровую схему ячейки, матрицу ячеек, микросхему матрицы ячеек сенсоров в целом, - возможно реализовать средствами полупроводниковых промышленных технологий, например, применением технологии TSMC с технологическими нормами на длину затвора транзистора 28 нм и менее.
Пример 3. Наноразмерный сенсор на основе нанопроводного полевого транзистора.
Наноразмерный сенсор на основе нанопроводного полевого транзистора предназначен для регистрации результатов разделения пары зарядов около поверхности сенсора после каждого встраивания полимеразой нуклеотидов в полимеризуемый фрагмент ДНК. в составе иммобилизованного на поверхность нанопровода полимеразного комплекса 44.
Структурная схема нанопроводного транзистора с иммобилизованным тройным комплексом представлена на Фиг. 16, и состоит из планарной тонкопленочной металлической наноструктуры, нанесенной на слой диэлектрика 49, покрывающий подложку 45; тонкопленочная металлическая электродная наноструктура 46 (контакты к нанопроводу) совместно с металлическим каналом-нанопроводом 50 формируется на диэлектрической подложке методами фото- и электронной литографии с использованием фото- и электронного резиста, технологии травления экспонированной области и технологии напыления металла магнетронным или термическим способом. Управляющим электродом также может служить проводящий подслой (например, допированный кремний), находящийся под слоем диэлектрика 49. Для устранения контакта подводящих электродов с водным раствором в микрофлюдной ячейке они покрываются тонким слоем диэлектрика 51, наносимого через маску. Также числами 44, 47, 48 показаны, соответственно, иммобилизованный полимеразный комплекс, водный раствор реакционной смеси и электрод смещения.
Проводимость канала транзистора зависит от напряженности электрического поля, в котором находится нанопровод (НП). Локальные изменения поля достаточной величины также способны изменить проводимость нанопровода, что дает возможность регистрации с помощью такого устройства локального изменения заряда в области нанопровода, а также присоединения к (или отсоединении от) поверхности нанопровода малых заряженных частиц.
Нанопроводной транзистор может быть реализован на основе КНИ-технологии. КНИ-материал (кремний на изоляторе) представляет собой слой монокристаллического кремния, отделенный от кремниевой подложки слоем оксида кремния. В этом верхнем слое кремния и формируют наноструктуры различных конфигураций. С использованием КНИ-материала можно изготавливать подвешенные НП. Сначала литографическим методом в верхнем слое кремния формируется структура НП. Затем образец помещается в раствор плавиковой кислоты, в результате чего удалялся расположенный под НП слой SiO2. При этом широкие области кремния служат маской для травления SiO2, а тонкий провод оказывается подвешенным за счет «подтрава» под него, обусловленного изотропностью процесса травления SiO2.
Из-за большой площади подводящих электродов (несколько мм2) утечка тока через диэлектрический слой пластины КНИ становилась значительной (более 10 рА) и для ее блокировки производилось утолщение диэлектрического слоя двумя последовательными напылениями SiO2 толщиной по 200 нм на всю поверхность чипа, за исключением центральной области 80×80 мкм2 с наноструктурами (на Фиг. 20 и 21 видна граница дополнительного изолирующего слоя). В результате проведенного усовершенствования утечка с подложки на контактные площадки практически исчезала при приложенных напряжениях до 10 В.
После утолщения диэлектрического слоя методами фотолитографии и магнетронного напыления формировалась крупноразмерная часть структуры, содержащая подводящие Ti электроды толщиной 100-160 нм. В качестве затворного электрода полевого транзистора использовался нижний слой кремния (подложка).
На заключительном этапе изготовления для проведения измерений в жидкостной среде происходила изоляция всех открытых токопроводящих поверхностей структуры транзистора путем напыления слоя SiO2 толщиной 200 нм. Изоляционный слой покрывал Ti электроды и большую часть площади кремниевых контактных площадок, оставляя открытой канал-нанопровод транзистора. На Фиг. 21 показан вид окончательно сформированных структур нанопроводных транзисторов в центральной области чипа.
В зависимости от технологических требований геометрия НП в транзисторе может быть реализована в различных формах, например, в линейной или в V образной. Удельная проводимость полупроводникового канала p-типа определяется выражением:

где p - подвижность дырок. Чувствительность сенсора можно характеризовать безразмерным параметром

где pp - модуляция концентрации дырок, обусловленная изменением потенциала. Данный параметр соответствует объемному отношению между той частью нанопровода, где концентрация эффективно модулирована электрическим потенциалом, и остальным объемом. Видно, что он будет максимальным, когда длина экранирования Дебая в полупроводнике много больше радиуса нанопровода λD>>R. Данный параметр можно представить в явном виде:

где Δφ соответствует изменению потенциала в нанопроводе, которое описывается найденной функцией

На Фиг. 17 показано рассчитанное распределение электрического потенциала для случая одной частицы, несущей единичный заряд. На Фиг. 17а) показано распределение потенциала на плоскости z=φ(x, у) перпендикулярной оси нанопровода, с началом координат в центре нанопровода. Значения потенциала вблизи заряженной частицы не показаны, поскольку в этой области потенциал стремится к бесконечности. На Фиг. 17б) показан график эквипотенциальных линий; в центре замкнутых контуров находится заряженная частица; пунктирной линией показана граница нанопровода.
Профиль распределения потенциала вдоль оси, соединяющей центр нанопровода с центром частицы, представлен на Фиг. 18. Расчеты сделаны для следующих параметров: частица находится на расстоянии h=6 нм от нанопровода, радиус которого R=50 нм. Длина экранирования Дебая в электролите
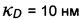
Распределение потенциала представлено вдоль оси, соединяющей центр нанопровода с центром заряженной частицы, и нормировано на значение потенциала на поверхности нанопровода со стороны частицы.
В случае детектирования отдельных заряженных объектов, поле единичного электрона проникает вглубь нанопровода и способно целиком «пережать» проводящий канал в силу малости поперечных размеров полупроводникового нанопровода, как показано на рисунке Figure 3d в статье [Salfi J., et al. Direct observation of single-charge-detection capability of nanowire field-effect transistors // Nature Nanotechnology. 2010. - Sep. Vol. 5, no. 10. P. 737-741]. Чувствительность сенсора в этом режиме может быть исключительно высока. В упомянутой статье показано, что в случае детектирования с помощью нанопровода единичных электронов, расположенных в зарядовых ловушках на поверхности специально приготовленного образца, зарядовая чувствительность достигает величины 4*10-5е/√Гц при криогенных температурах. При комнатных температурах в работе [Denis Е. Presnov, et al. A highly pH-sensitive nanowire field-effect transistor based on silicon on insulator / Beilstein J. Nanotechnol. 2013, 4, 330-335] была дана оценка предельной зарядовой чувствительности нанопроводного транзистора величиной 5*10-3e/√Гц.
Особенности конструкции устройства позволяют существенно упростить метод его изготовления, избегая трудоемких и сложных процессов легирования и отжига, необходимых для формирования омических контактов к кремниевым областям стока и истока транзистора. Возможности применяемого материала КНИ позволяют также сформировать подвешенный канал-нанопровод, частично удалив подслой SiO2, который является источником зарядовых флуктуаций, увеличивающих собственный шум транзистора. Транзистор с подвешенным каналом-нанопроводом будет обладать большей чувствительностью как за счет уменьшения собственного шума, так и за счет увеличения рабочей поверхности нанопровода.
Отдельные нанопроводные транзисторы могут быть размещены в интегральной структуре, представляющей собой чип с массивом нанопроводных транзисторов с адресной шиной, позволяющей осуществлять индивидуальное измерение на каждом нанотранзисторе, как это показано на Фиг. 19.
Пример 4. Наноразмерный сенсор на основе одноэлектронного транзистора предназначен для формирования сигнала от результата разделения пары зарядов в после встраивания полимеразой нуклеотида в полимеризуемый фрагмент ДНК.
Одноэлектронным транзистором называется электронная наноструктура, состоящая из двух сверхмалых последовательно соединенных туннельных переходов C1 и С2, между которыми расположен электрод (остров), соединенный с управляющим электродом (затвором) через емкость С0, как показано рисунке Фиг. 22.
Вольтамперная характеристика этого устройства, представленная на рисунке Фиг. 23, имеет характерную область кулоновской блокады (сплошная линия) при напряжениях

При напряжениях Vg на управляющем электроде, соответствующих C0Vg=Qg=е/2+ne туннелирование возможно при любых V и в этом случае вольтамперная характеристика транзистора не имеет блокадного участка (пунктирная линия). В связи с этим зависимость тока транзистора I (V=const) от величины поляризационного заряда Qg на центральном острове, получившая название модуляционной характеристики, имеет вид периодической функции с периодом по заряду в один электрон е, т.е. I(Q0+e)=I(Q0) (Рисунок 26). Процесс коррелированного туннелирования электронов при напряжениях порядка Voff и менее характерен тем, что электроны приходят и уходят с острова транзистора последовательно один за другим. По этой причине транзистор назван одноэлектронным.
Для того чтобы одноэлектронные эффекты были хорошо различимы на фоне тепловых и квантовых флуктуаций, характерная электростатическая (Кулоновская) энергия системы (e2/2CS) должна значительно превосходить характерную энергию тепловых (kT) и квантовых (~I, где = RC) флуктуаций, т.е. должны выполняться условия:

где Rq - квантовое сопротивление, R - туннельное сопротивление переходов.
Одноэлектронный транзистор характеризуется весьма высокой чувствительностью к изменению заряда на центральном острове. Даже небольшое изменение заряда острова dQ, которое может быть существенно меньше, чем заряд электрона е, приводит к заметному изменению dI тока транзистора (см. Рисунок 2б) и может быть зарегистрировано. Это свойство одноэлектронного транзистора позволяет использовать его как уникальный электрометр с субэлектронной чувствительностью.
Как следует из формулы (1), характерные размеры элементов одноэлектронных устройств, определяющие их емкость, напрямую влияют на рабочую температуру устройств. Оценивая по этой формуле характерные значения емкостей и размеров туннельных переходов, необходимых для нормальной работы одноэлектронных устройств при комнатной температуре Т=300 K, получаем емкость С=10-18-10-19 Ф, и, соответственно, размеры порядка нанометра. Такой транзистор можно создать, используя в качестве «острова» одноэлектронного транзистора одиночную молекулу. Это и является основой современной молекулярной одноэлектроники.
Минимальное значение уровня шума в одноэлектронном транзисторе, а следовательно, максимальная чувствительность, достигается при смещающем напряжении V, незначительно превышающем порог кулоновской блокады Voff. Кроме того, минимум шума является функцией величины измеряемого заряда Qx.
Помимо оптимизации параметров транзистора и режимов его работы, получены выражения для оценки максимальной чувствительности одноэлектронного транзистора при учете низкочастотных флуктуаций тока транзистора. В случаях, когда собственная емкость источника сигнала при нулевом напряжении Cs 0, измеряемый заряд Qx, показанные на рисунке эквивалентной схемы одноэлектронного транзистора Фиг. 24, оценка максимальной чувствительности одноэлектронного транзистора может быть представлена выражением:

где SI(0) - спектральная плотность флуктуаций туннельного тока на низких частотах. Величина измеряемого заряда определяется флуктуациями числа туннельных событий в каждом из переходов транзистора.
В случае классических шумов результат (2) упрощается когда собственная емкость источника заряда мала Cs0, а сопротивления и емкости его переходов одинаковы (С=С1=С2, R=R1=R2):

Соотношение (2) принимает простой вид и в случае большой емкости источника сигнала Cs, когда источник заряда удобнее


где R=min(R1,R2).
Как видно из формул (3) и (4), шумы транзистора уменьшаются с уменьшением температуры и сопротивления переходов, однако при Т=0 заметную роль начинают играть квантовые флуктуации, не описываемые формулой (2). Оценка абсолютного минимума квантового шума дает:

Существует по крайней мере два способа уменьшения квантового шума в одноэлектронном транзисторе. Один из способов - выбор рабочей точки транзистора, близкой к е/2, при V~Vt (где Vt - модулируемый порог кулоновской блокады), в этом случае вероятность сотуннелирования уменьшается при уменьшении Vt, поэтому вклад квантового шума минимален. Сотуннелированием называют квантовый процесс перехода электрона с одного внешнего электрода на другой через виртуальное промежуточное и энергетически невыгодное состояние заряженного острова транзистора). Второй способ - использование сильно несимметричного одноэлектронного транзистора (R1>>R2). Классический шум в транзисторе зависит преимущественно от меньшего из сопротивлений, т.о. увеличение второго сопротивления не существенно. Однако время сотуннелирования пропорционально 1/R1R2, и, соответственно, оно уменьшается при увеличении большего из сопротивлений. Отметим, что на одном из склонов модуляционной характеристики несимметричного транзистора увеличивается значение производной dI/dQg, что приводит к увеличению выходного сигнала:
Спектр шума одноэлектронного транзистора имеет ярко выраженную компоненту 1/f. Экспериментальные значения уровня шума транзисторов планарной геометрии составляют величину

Многочисленные эксперименты показали, что предельные характеристики одноэлектронных устройств определяются уровнем флуктуаций поляризационного фонового заряда, которые на низких частотах доминируют над их естественными компонентами.
В большинстве случаев избыточный шум в одноэлектронном транзисторе имеет зарядовую природу. Показано, что уровень выходного шума в одноэлектронном транзисторе зависит от положения рабочей точки (а именно от коэффициента преобразования dI/dQs), причем при максимуме производной выходной шум максимален. В то же время при пересчете в зарядовые единицы уровень шума оказывается примерно одинаковым для всех рабочих точек. Это указывает на то, что регистрируемый избыточный шум имеет зарядовую природу, т.е. выходной шум является реакцией транзистора на флуктуации зарядов в его непосредственном окружении.
Одно из проявлений шума фоновых зарядов - телеграфный шум тока со случайным переключением между 2, 3 и более уровнями с эквивалентной величиной скачков вплоть до 0.2 е. Телеграфный шум - вид шума, довольно часто проявляющийся в одноэлектронных структурах. Его наблюдение и изучение позволило сделать вывод, что природа избыточного шума связана с совокупным влиянием зарядовых двухуровневых флуктуаторов, в большом количестве распределенных в толще диэлектрика, окружающего остров транзистора и, по-видимому, связанных с несовершенством структуры этой среды.
Задача создания молекулярного транзистора разделяется на две подзадачи. Первая - создание электродов с нанозазором между ними, который бы позволил исследовать объекты нанометровых размеров. Вторая - помещение и закрепление одиночной молекулы между такими электродами.
Нанозазоры могут быть сформированы различными способами:
- метод "механически контролируемого разрыва нанопровода",
- "усовершенствованная" электронно-лучевая литография,
- электрохимические методы, такие как осаждение металла в область предварительно сформированного зазора или создание зазора путем травления:
- электромиграция,
- абляционная литография просвечивающим электронным микроскопом, ионно-лучевая литография,
- метод, в котором используется молекулярно-лучевая эпитаксия.
На Фиг. 25 представлено схематическое изображение одномолекулярного транзистора с подвешенными электродами: М - молекула, осажденная в зазор и зафиксированная там при помощи SH-групп.
На Фиг. 26 показана фотография КНИ-структуры с висящими электродами над подложкой.
На Фиг. 27 показана фотография наноструктуры одноэлектронного транзистора с нанозазором, полученным методом электронно-лучевой литографии.
На Фиг. 28 показана фотография нанозазора, полученного методом электромиграции (электротреппинг).
На Фиг. 29 показана фотография нанозазора, полученного методом ионно-лучевой литографии (FIB-технология).
На Фиг. 30 показана фотография изготовленной наноструктуры из 16 ячеек для транзисторов с нанозазорами.
На Фиг. 31 показана фотография одной из 16-ти ячеек на основе транзистора с нанозазором.
На Фиг. 32 показана фотография сформированного центрального электрода-острова в структуре одноэлектронного транзистора из нанопровода.
На Фиг. 33 представлена фотография сформированного нанозазора для создания молекулярного одноэлектронного транзистора.
На Фиг. 34 представлена вольт-амперная характеристика транзисторной структуры с нанозазором; форма тока утечки показывает, что нанозазор сформирован.
На сегодняшний день одноэлектронные транзисторы обладают максимальной зарядовой чувствительностью. Известны публикации с описанием схемы одноэлектронного транзистора для детектирования отдельных молекул, например, стрептавидина [Nakajima, A.; Kudo, Т.; Furuse, S. Biomolecule detection based on Si single-electron transistors for practical use. Appl. Phys. Lett. 2013, 103.].
Пример 5. Наноразмерный сенсор со схемой стохастического резонанса.
Опционально, для повышения отношения уровня сигнала к уровню шума в схему ячейки матрицы микросхемы может быть добавлена схема, реализующий режим стохастического резонанса, состоящая из полупроводникового элемента (или группы элементов), имеющего передаточную характеристику или вольт-амперную характеристику с областью бистабильности, включающую схему смещения (задание рабочей точки) по постоянному току, включающую источник (генератор) шума, включающую схему формирования выходного сигнала. Схема стохастического резонанса реализуется посредством подключения источника сигнала, а также схемы смещения (задания рабочей точки) по постоянному току, источника (генератора) шума ко входу полупроводникового элемента (устройства, или группы элементов), реализующего передаточную характеристику или вольт-амперную характеристику с областью бистабильности, и подключения выхода полупроводникового элемента (устройства, или группы элементов), реализующего передаточную характеристику или вольт-амперную характеристику с областью бистабильности, ко входу схемы ячейки, в которой формируется выходной цифровой сигнал.
Вариант реализации ячейки сенсора, использующей стохастический резонанс для обнаружения фактов разделения зарядов, показан на Фиг. 15. Схема ячейки содержит полевой транзистор сенсора, на затвор которого иммобилизуется молекула полимеразы, в составе комплекса 38, биполярный транзистор V1, а также источники напряжений U0 (напряжение смещения), Uпит (напряжение питания схемы сенсора) и UN (напряжение шума). Выходной сигнал снимается с контактов Uвых.
Полевой транзистор сенсора и биполярный транзистор V1 совместно образуют триггер Шмитта, реализующий S-образную передаточную характеристику Uвых=F(Uвx). Под Uвх здесь понимают разность потенциалов между общим проводом схемы и затвором полевого транзистора. S-образная передаточная характеристика в данной схеме образуется за счет наличия положительной обратной связи по напряжению, реализуемой посредством подачи усиливаемого сигнала со стока полевого транзистора (p+-сток на Фиг. 15) на базу биполярного транзистора V1 через цепь резистивного делителя R5-R4, и усиленного сигнала в цепь истока полевого транзистора (p+-исток на Фиг. 15) через общий резистор R3. Параметры схемы (тип и характеристики транзистора V1 и номиналы резисторов R1-R5) выбираются таким образом, чтобы обеспечить появление бистабильности на передаточной характеристике схемы [1]. При этом входной сигнал схемы Uвхопределяется как сумма сигнала шума UN и сигнала, т.е. потенциала, индуцированного на затворе полевого транзистора, как это описано в разделе "Подробное раскрытие изобретения". При совместном действии сигнала напряжения, индуцированного на затворе полевого транзистора и сигнала шума, под действием последнего изменяется (модулируется) вероятность нахождения схемы триггера Шмитта между двумя устойчивыми состояниями в пределах области бистабильности передаточной характеристики. Это приводит к появлению на выходе схемы (напряжение Uвых) импульсов напряжения в моменты времени, когда на затворе полевого транзистора сенсора индуцируется потенциал. Параметры (статистика распределения, дисперсия) сигнала шума UN задается таким образом, чтобы обеспечить описанный выше режим стохастического резонанса [2-5], т.е. чтобы в схеме происходило усиление отношения «сигнал-шум», что и проявляется в виде импульсов напряжения на выходе схемы. Таким образом, указанная схема сенсора, не обеспечивая усиление полезного сигнала по напряжению, в то же время усиливает отношение «сигнал-шум», что делает слабый полезный сигнал доступным для дальнейшей обработки.
В качестве источника шума может быть использовано любое устройство, формирующее напряжение шума UN с требуемыми характеристиками. В качестве примеров таких источников (но не ограничиваясь ими) могут быть рассмотрены всевозможные схемы на сдвиговых регистрах, в том числе с аналого-цифровым преобразованием на выходе, генераторы шума на тепловых или пробойных источниках (усиливаются тепловые шумы тока через сопротивление или шум тока пробоя обратно смещенного p-n-перехода, и т.п.).
Сигнал с выхода схемы на основе эффекта стохастического резонанса подается для последующего усиления, нормализации и преобразования в цифровую форму. На Фиг. 15 показано, как для этих целей сигнал Uвыхпоступает на интегратор (фильтр низкой частоты) Yi1, а далее - на нормирующий усилитель Yi2 и компаратор Yi3, с выхода которого сформированные импульсы поступают на D-триггер Yi4. С выхода D-триггера дискретизированный во времени цифровой сигнал DATA поступает на соответствующую шину данных матрицы микросхемы для дальнейшей передачи в компьютер. Приведенная схема сенсора на основе стохастического резонанса может быть использована аналогично для схемы на Фиг. 14, в двухканальном исполнении, что позволит вычитать из сигнала уровень фонового потенциала рабочей смеси.
Пример 6. Формирование первичных сигналов и их преобразование в нуклеотидную последовательность секвенируемого фрагмента ДНК.
На Фиг. 5 показаны основные стадии формирования и преобразования данных о нуклеотидной последовательности фрагмента ДНК следующего состава: AACGTCTTCAGGGCTAGCACCAT.
Аналого-цифровая схема ячейки формирует временную последовательность дискретных интервалов времени, каждый из которых обозначен логическими «1» единицей и "0" нулем, причем логической единицей «1» обозначены те интервалы времени, когда сенсором ячейки был зарегистрирован факт разделения одной пары зарядов, сопровождающий встраивание полимеразой нуклеотида в полимеризуемый фрагмент ДНК, и сформирован соответствующий сигнал. Если последовательно проводить полимеризацию указанного фрагмента ДНК в составе комплекса, иммобилизованного на поверхность сенсора ячейки, в четырех различных реакционных смесях, отличающихся тем, что в каждой из них понижена концентрация нуклеотидов только одного вида, и в каждой смеси вида отличного от других смесей, то схемой ячейки будут последовательно сформированы четыре временных последовательности, которые (четыре сверху) показаны на Фиг. 5А. Можно видеть, что на каждой временной последовательности количество дискретных интервалов времени, обозначенных логическим нулем "0", различно перед каждым интервалом, обозначенным логической единицей «1»; условно, можно говорить о коротких и длинных интервалах времени перед встраиванием нуклеотидов. Указанные временные последовательности в реальном времени (т.е. в процессе их формирования) передаются в компьютер, в котором специальное программное обеспечение считывает, суммирует, сравнивает, анализирует длительности интервалов времени перед встраиванием каждого нуклеотида, т.е. определяет количество дискретных интервалов времени, обозначенных логическим нулем "0", перед каждым интервалом времени, обозначенным логической единицей «1». Согласно алгоритму секвенирования, длинные (в среднем) интервалы времени наблюдаются перед встраиванием нуклеотидов вида, концентрация которого была понижена против нормальной концентрации нуклеотидов трех других видов в реакционной смеси. Т.к. на этапе пробоподготовки известно имя вида нуклеотидов, концентрация которого понижена для каждой реакционной смеси, то на первой стадии преобразования данных компьютерная программа преобразует каждую временную последовательность в последовательность логических единиц «1» и логических нулей "0"; причем теперь логической единицей «1» обозначен каждый длинный интервал времени, соответствующий встраиванию нуклеотидов вида, концентрация которого была понижена в соответствующей реакционной смеси и известна, а логическим нулем "0" обозначаются короткие интервалы времени, соответствующие встраиванию нуклеотидов видов, концентрация которых была нормальна в этой же реакционной смеси. Полученные таким образом последовательности логических единиц «1» и логических нулей "0" представлены на Фиг. 5Б. На следующей стадии преобразования данных, компьютерная программа сопоставляет данные о местах расположения нуклеотидов известных видов на каждой из четырех последовательностей логических единиц «1» и нулей "0" друг с другом, и методом исключения, следуя правилу, что на одной позиции в нуклеотидной последовательности фрагмента ДНК может располагаться нуклеотид только одного вида, - формирует результирующую нуклеотидную последовательность секвенируемого фрагмента ДНК: AACGTCTTCAGGGCTAGCACCAT.
Пример 7. Структурная схема микросхемы матрицы ячеек сенсоров.
Структурная схема микросхемы матрицы ячеек сенсоров представлена на Фиг. 10. Микросхема предназначена для применения в составе устройства, реализующего одномолекулярный способ секвенирования нуклеиновых кислот. Микросхема матрицы ячеек сенсоров может состоять, например, из 16000000 ячеек сенсоров, которые организованы в матрицу с количеством столбцов и строк 4000×4000, которая поделена на четыре секции; структурная схема микросхемы представлена на рисунке ниже. Числами римскими I, II, III, IV - обозначены секции матрицы ячеек сенсоров, каждая, например, размером 2000×2000 ячеек; числами 1, 2, 3, 4 в кружочках обозначены выходы горизонтальных сдвиговых регистров, выводящих цифровые данные из ячеек, расположенных, соответственно, в секциях I, II, III, IV. Числами в прямоугольных (квадратных) формах обозначены: 1 - ячейка сенсоров; 2 - вертикальный сдвиговый регистр переноса цифровых данных из ячеек сенсоров секции матрицы, расположенных в один ряд; 3 - USB интерфейс передачи данных между компьютером и микросхемой: 4 - горизонтальный сдвиговый регистр переноса цифровых данных из вертикальных сдвиговых регистров одной секции матрицы ячеек сенсоров; 5 - электрод смещения, потенциал на котором устанавливается источником напряжения, регулируемого контроллером; 6 - разъем между источником напряжения микросхемы и электродом смещения, который расположен на крышке микросхемы; 7 - контроллер управления режимами работы микросхемы; 8 - регулируемый генератор тактовой частоты, к которому извне микросхемы подсоединяется кварцевый резонатор; 9 - регулируемый источник вторичного питания.
Схема вывода информации из ячеек матрицы функционально организована аналогично схеме вывода информации в матрице ПЗС со строчным переносом заряда. Состояние выхода D-триггера цифровой схемы каждой ячейки, расположенной в столбце матрицы, перезаписывается в вертикальный сдвиговый регистр, предназначенный для переноса логических данных ("1" или "0") в горизонтальный сдвиговый регистр, из которого данные через USB интерфейс поступают в компьютер.
Контроллер микросхемы обеспечивает обмен данными с персональным компьютером по интерфейсу USB, обеспечивает анализ данных с каждого выходного регистра матрицы ячеек, на основании которого управляет частотой тактовых импульсов и величиной напряжения, обеспечивающих функционирование электрической схемы каждой ячейки матрицы. Через USB интерфейс схема матрицы ячеек сенсоров получает напряжение питания 5 В. Напряжение питания может подаваться на микросхему от автономного источника питания, например, от аккумуляторной батареи. На компьютере предустанавливается специальный драйвер, который обеспечивает согласование с персональным компьютером на уровне программного обеспечения работу контроллера микросхемы матрицы сенсора. Этот драйвер обеспечивает первичную настройку параметров микросхемы матрицы ячеек сенсоров, оперативное управление работой и обмен данными между микросхемой и компьютером. Ввиду высокой скорости передачи данных применяется интерфейс с высокой пропускной способностью, например, USB 2.0 (400 Мбит в секунду).
Пример 8. Численный эксперимент по определению качества временных задержек перед встраиванием нуклеотидов в реакции полимеризации ДНК в процессе секвенирования предложенным способом.
Численные эксперименты по определению временных задержек перед встраиванием нуклеотидов в ходе реакции полимеризации ДНК для различных соотношений концентраций нуклеотидов 4-х видов были выполнены на основе клеточного автомата [Марголус Н., Тоффоли Т. Машины клеточных автоматов: Пер. с англ. - М.: Мир, 1991. 280 с; Margolus, N., Physics-like models of computation, Physica D 10, 8195 (1984)] с применением разработанной кинетической модели диффузионного процесса в реакции полимеризации ДНК [Manturov А.О., Grigoryev A.V., DNA SEQUENCING BY SYNTHESIS BASED ON ELONGATION DELAY DETECTION, Progress in Biomedical Optics and Imaging - Proceedings of SPIE Optical Technologies in Biophysics and Medicine XVI; Laser Physics and Photonics XVI; and Computational Biophysics. 2014. С. 94481Т].
Задержка - это время, которое полимераза ожидает подхода комплементарного нуклеотида к сайту копирования перед его встраиванием в полимеризуемый фрагмент ДНК. Распределение задержек для нуклеотидов каждого вида представлено на Фиг. 7; по оси X отмечается величина задержки в условных единицах времени, по оси Y - количество задержек определенных на оси X длительностей, полученных численными экспериментами. Как видно из рисунка: большинство задержек равны нулю для случая, когда концентрации нуклеотидов каждого вида в реакционной смеси одинаковы. Если концентрация нуклеотидов одного вида в реакционной смеси будет уменьшена против нормальной концентрации нуклеотидов остальных видов, то численные эксперименты покажут распределение, представленное на Фиг. 8. Из этого распределения видно, что уменьшение концентрации нуклеотидов вида А уменьшает количество коротких по времени задержек для этих нуклеотидов и увеличивает количество длинных по времени задержек для нуклеотидов остальных видов. Среднее время задержки для нуклеотидов 4-х видов в ходе реакции полимеризации ДНК представлено на Фиг. 9. Время средней задержки рассчитывается методом скользящего окна в 50 тактов клеточного автомата. На графиках, по оси Y отложено рассчитанное среднее значение задержки в условных единицах для текущего номера задержки. На Фиг. 9А показаны результаты расчетов, когда концентрация нуклеотидов 4-х видов одинакова в реакционной смеси. На Фиг. 9Б представлены результаты расчетов, когда концентрация нуклеотидов вида А в 10 раз меньше нормальной концентрации нуклеотидов 3-х других видов; на этом графике видно, что задержки для нуклеотидов обедненного вида в среднем продолжительней, чем для нуклеотидов остальных видов. Расчеты выполнены для олигонуклеотида, нуклеотидная последовательность которого представлена ниже.
На Фиг. 9Б видно, что некоторое пороговое значение, например, число 15, будет однозначно разделять задержки по времени для нуклеотидов обедненного вида и для нуклеотидов не обедненных видов. Эффект, представленный на фиг. 9А и 9Б показывает средние времена задержек в каждой позиции нуклеотидной последовательности ДНК после серии К независимых экспериментов. Усредняя данные по К экспериментам при обеднении реакционной смеси нуклеотидами, например, вида А, можно точно определить позиции в нуклеотидной последовательности фрагмента ДНК, в которые были присоединены нуклеотиды вида А. Поочередно, обедняя нуклеотиды остальных видов, аналогичным образом определяются положения нуклеотидов остальных видов, в нуклеотидной последовательности того же фрагмента ДНК.
Перечень последовательностей, примененных в численных экспериментах:
SEQ ID NO: 1 - Олигонуклеотид-ультрамер использованный для получения одноцепочечной кольцевой ДНК (IDT Inc., США)

Пример 9. Численный эксперимент по реконструкции ДНК.
Алгоритм секвенирования основан на диффузионном механизме движения нуклеотидов к сайту сборки, где полимераза встраивает комплементарные нуклеотиды в полимеризуемый фрагмент нуклеиновой кислоты, и на гипотезе, что в среднем отношение длительности интервалов времени перед встраиванием нуклеотидов с пониженной концентрацией к длительности интервалов времени перед встраиванием нуклеотидов с нормальной концентрацией будет тем больше, чем будет больше разница в их концентрациях. Для проверки этой гипотезы была разработана математическая модель и проведены численные эксперименты, результаты которых подтвердили достоверность гипотезы.
Численные эксперименты по восстановлению нуклеотидной последовательности ДНК выполнены на базе двух программных модулей: модуля из Примера 8, который использовался для генерации величин временных задержек перед встраиванием каждого нуклеотида в ходе реакции полимеризации фрагмента ДНК и модуля, который восстанавливает исходную нуклеотидную последовательность фрагмента ДНК из данных величин временных задержек.
Модуль для восстановления исходной нуклеотидной последовательности ДНК обрабатывает статистически результаты от нескольких независимых экспериментов. В Таблицах 1, 2, 3 представлены статистически обработанные результаты от 2000 экспериментов по расчету точности восстановления закольцованных нуклеотидных последовательностей фрагментов ДНК в форме «гантель» (dumbbell): для матричных фрагментов ДНК длиной 1000, 2000, 3000 и 5000 нуклеотидов, соединенных "мостиком" длиной в 25 нуклеотидов с каждой стороны "гантели".
Предлагаемый алгоритм секвенирования не требует меток для нуклеотидов, т.к. полезной информацией является длительность интервала времени перед встраиванием каждого нуклеотида.
Алгоритм секвенирования является уникальным потому, что в отличии от большинства известных алгоритмов секвенирования, в нем разделены во времени процедура формирования полезного сигнала и процедура его идентификации, т.е. определение имени того вида нуклеотидов, которому этот сигнал соответствует. Именно благодаря этому свойству алгоритм позволяет выбирать ту точность результата секвенирования, которая требуется. При этом чем больше времени дается на процедуру секвенирования, тем более точный результат можно получить. В зависимости от решаемой задачи, на этапе пробоподготовке, можно сформировать условия, которые обеспечат желаемый по точности результат секвенирования.
Характеристики молекул, участвующих в процедуре секвенирования, накладывают свои ограничения на параметры результатов секвенирования, и можно дать им следующие оценки, при условии, что применяемая полимераза Phi29 имеет процессивность в 800000 нуклеотидов.
Результаты расчетов для отношения концентраций одного вида нуклеотидов к трем другим видам, как 1:10 показали, что точность секвенирования фрагмента ДНК составляет в среднем 86,9138% для фрагментов длиной 2000 нуклеотидов и эта точность практически не зависит от длины фрагмента, т.к. результат встраивания каждого нуклеотида не зависит от результатов встраивания других нуклеотидов в тот же полимеризуемый фрагмент нуклеиновой кислоты. Таблица 1 с результатами расчетов при отношении пониженной концентрации одного вида нуклеотидов к трем другим, как 1:10, со статистической обработкой двух тысяч численных экспериментов для фрагментов нуклеиновой кислоты в 2000 нуклеотидов, организованных в форме "гантели" (dumbbell), представлена ниже:

Таблица 2 с результатами расчетов при отношении пониженной концентрации одного вида нуклеотидов к трем другим, как 1:10, со статистической обработкой двух тысяч численных экспериментов для фрагментов нуклеиновой кислоты в 5000 нуклеотидов, организованных в форме "гантели" (dumbbell), представлена ниже:
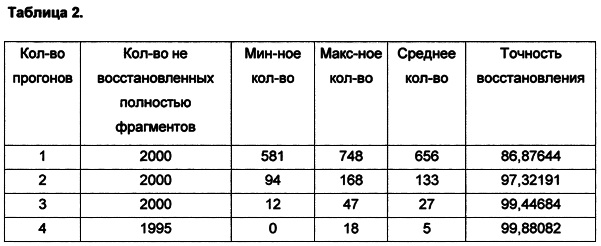

В первом столбце Таблиц 1 и 2 показано количество прогонов, т.е. циклов полной полимеризации фрагмента ДНК, во втором столбце показано количество экспериментов, в которых нуклеотидная последовательность не была восстановлена со 100% точностью. В третьем, четвертом и пятом столбцах показано количество нуклеотидов, соответственно, минимальное, максимальное и среднее, которые не были восстановлены в секвенируемых фрагментах ДНК. В шестом столбце показана, усредненная по 2000-м экспериментов, точность восстановления секвенируемых фрагментов ДНК.
Понятно, что если установить соотношение концентраций, например, 1:20, то увеличивается точность после одного прочтения, т.е. меняется время на точность. Соответствующие результаты расчетов, со статистической обработкой двух тысяч численных экспериментов для фрагментов нуклеиновой кислоты в 2000 нуклеотидов, организованных в форме "гантели" (dumbbell), показаны в Таблице 3 ниже:

Длина секвенируемого фрагмента зависит от процессивности полимеразы и выбранного устройства секвенирования: одно матричного или четырех матричного.
В первом случае, на поверхность ячеек матриц микросхемы, в ячейках которой, на сенсорах иммобилизованы комплексы "полимераза-фрагмент ДНК" поочередно подаются четыре реакционных смеси, отличающиеся тем, что в каждом из них понижена концентрация нуклеотидов только одного вида, и всякий раз - другого вида. В этом случае, т.к. одна и таже полимераза работает в одной и той же ячейке, но с 4-мя разными реакционными смесями, - в одной реакционной смеси она сможет встроить только 20000 нуклеотидов; в зависимости от желаемой точности секвенирования фрагмента ДНК можно выбрать, например, фрагмент ДНК длиной 5000 нуклеотидов, провести 4-е цикла его полимеризации и получить точность 99,88%; а можно взять фрагмент длиной 3000 нуклеотидов и получить точность 99,997% и т.д.
Во втором случае, указанные выше реакционные смеси подаются каждая на поверхность своей матрицы микросхемы, в ячейках которых, на сенсорах иммобилизованы комплексы с клонами исходных фрагментов ДНК; в этом случае одна и та же полимераза работает в одной и той же ячейке только с одной реакционной смесью и так же может встроить 80000 нуклеотидов. В этом случае можно секвенировать фрагменты ДНК длиной 10000 нуклеотидов и более, опять же, в зависимости от желаемой точности.
Используемая литература
1.

2. Kramers H.A. Brownian motion in a field of force and the diffusion model of chemical reactions. Physica v. 7(4), p. 284-304. - 1940.
3. Benzi R., Sutera A., Vulpiani A. The Mechanism of Stochastic Resonance. Journal of Physics A: Mathematical and General, 1981, 14: 453-457.
4. Fauve S., Heslot F. Stochastic resonance in a bistable system. Physics Lett. A 97 (1-2). - 1983. p. 5-7.
5. Gammaitoni L. et al. Stochastic resonance. Reviews of Modern Physics, Vol. 70, No. 1, Jan. 1998. p. 223-287.
Реферат
Группа изобретений относится к области биотехнологии. Предложен способ и устройство определения нуклеотидной последовательности молекулы нуклеиновой кислоты. Способ включает иммобилизацию на сенсоре закольцованных фрагментов нуклеиновой кислоты и полимеразы, добавление на поверхность сенсора смеси немеченых дезоксирибонуклеотидов или рибонуклеотидов, где нуклеотид одного вида присутствует в меньшей концентрации, регистрацию сенсором факта разделения зарядов и определение временных интервалов между каждым фактом, повторение стадий добавления, регистрации и определения, где при каждом повторении вид нуклеотида с меньшей концентрацией изменяется, а далее определение нуклеотидной последовательности на основе определенных временных интервалов. Устройство включает матрицу с множеством ячеек сенсоров и аналого-цифровую схему, микрофлюидное устройство, устройство обработки и отображения данных, микросхемы матрицы ячеек сенсоров. Изобретения обеспечивают повышение точности и производительности секвенирования. 2 н. и 19 з.п. ф-лы, 34 ил., 3 табл., 8 пр.

Комментарии