Обнаружение рекомбиназной полимеразной амплификации с применением зонда с двойным гаптеном - RU2020110056A
Код документа: RU2020110056A
Формула
1. Композиция для рекомбиназной полимеразной амплификации, содержащая:
объемообразующий агент;
олигонуклеотидный зонд с уходящей группой с двойным гаптеном; и
фермент-нуклеазу.
2. Композиция по п. 1, характеризующаяся тем, что указанный объемообразующий агент содержит полиэтиленгликоль (ПЭГ), поливиниловый спирт (ПВС), поливинилпирролидон (ПВП), фиколл или декстран.
3. Композиция по п. 1 или 2, характеризующаяся тем, что указанный объемообразующий агент имеет молекулярную массу по меньшей мере 1 кДа, по меньшей мере 2 кДа, по меньшей мере 3 кДа, по меньшей мере 4 кДа, по меньшей мере 5 кДа, по меньшей мере 6 кДа, по меньшей мере 8 кДа или по меньшей мере 10 кДа.
4. Композиция по пп. 1-3, характеризующаяся тем, что указанный объемообразующий агент присутствует в композиции в концентрации по меньшей мере 15% об./об., концентрации по меньшей мере 12% об./об., концентрации по меньшей мере 10% об./об, концентрации по меньшей мере 8% об./об., по меньшей мере 6% об./об., концентрации по меньшей мере 5% об./об., концентрации по меньшей мере 4% об./об. или концентрации по меньшей мере 3% об./об.
5. Композиция по пп. 1-4, характеризующаяся тем, что указанный объемообразующий агент имеет профиль вязкости при 20°С менее или равный 5 мПа/с, менее или равный 4 мПа/с, менее или равный 3 мПа/с, менее или равный 2 мПа/с или менее или равный 1 мПа/с.
6. Композиция по пп. 1-5, характеризующаяся тем, что указанный объемообразующий агент представляет собой ПЭГ, имеющий вязкость при 20°С меньше или равную 3 мПа/с.
7. Композиция по пп. 1-6, характеризующаяся тем, что указанный объемообразующий агент представляет собой ПЭГ, имеющий молекулярную массу 3 кДа, и при этом концентрация указанного ПЭГ составляет 6,5% об./об.
8. Композиция по п. 1, характеризующаяся тем, что указанный олигонуклеотидный зонд содержит нуклеотид dR-O-[C]n, у которого отсутствует основание, связывающий уходящую группу с олигонуклеотидом.
9. Композиция по п. 1, характеризующаяся тем, что указанная нуклеаза представляет собой формамидопиримидин-ДНК-гликозилазу.
10. Композиция по пп. 1-9, характеризующаяся тем, что указанный олигонуклеотидный зонд с двойным гаптеном, при расщеплении формамидопиримидин-ДНК-гликозилазой, когда олигонуклеотидный зонд гибридизован с комплементарной нуклеотидной последовательностью, высвобождает уходящую группу с двойным гаптеном.
11. Композиция по п. 1, характеризующаяся тем, что указанная уходящая группа с двойным гаптеном содержит две иммуногенные группы, имеющие различные эпитопы.
12. Композиция по п. 11, характеризующаяся тем, что указанные иммуногенные группы содержат флуоресцентную группу, фермент или его фрагмент, пептид или его фрагмент, биотин.
13. Композиция по п. 12, характеризующаяся тем, что указанные иммуногенные группы выбраны из группы, включающей биотин, флуоресцеин, дигоксигенин или динитрофенил.
14. Композиция по п. 1, характеризующаяся тем, что указанный олигонуклеотидный зонд расщепляется экзонуклеазой, и при этом указанный олигонуклеотид высвобождает указанную уходящую группу с двойным гаптеном при расщеплении.
15. Композиция по п. 14, характеризующаяся тем, что указанная экзонуклеаза представляет собой экзонуклеазу III.
16. Композиция по п. 14, характеризующаяся тем, что указанный олигонуклеотидный зонд имеет структуру 5’X(n)aL(n)bH(n)cB3', где n представляют собой нуклеотиды, a, b и c представляют собой целые числа, X представляет собой 5' гексил, H представляет собой остаток ТГФ, B представляет собой спейсер C3, и L представляет собой разветвленный модификатор, содержащий множество гаптенов.
17. Композиция по п. 16, характеризующаяся тем, что указанные гаптены выбраны из группы, состоящей из DNP, FAM и биотина.
18. Композиция по п. 16, характеризующаяся тем, что указанный олигонуклеотидный зонд содержит фосфотиоатную связь между гаптенами.
19. Композиция по п. 16, характеризующаяся тем, что указанный спейсер C3 представляет собой пропанол.
20. Композиция, содержащая:
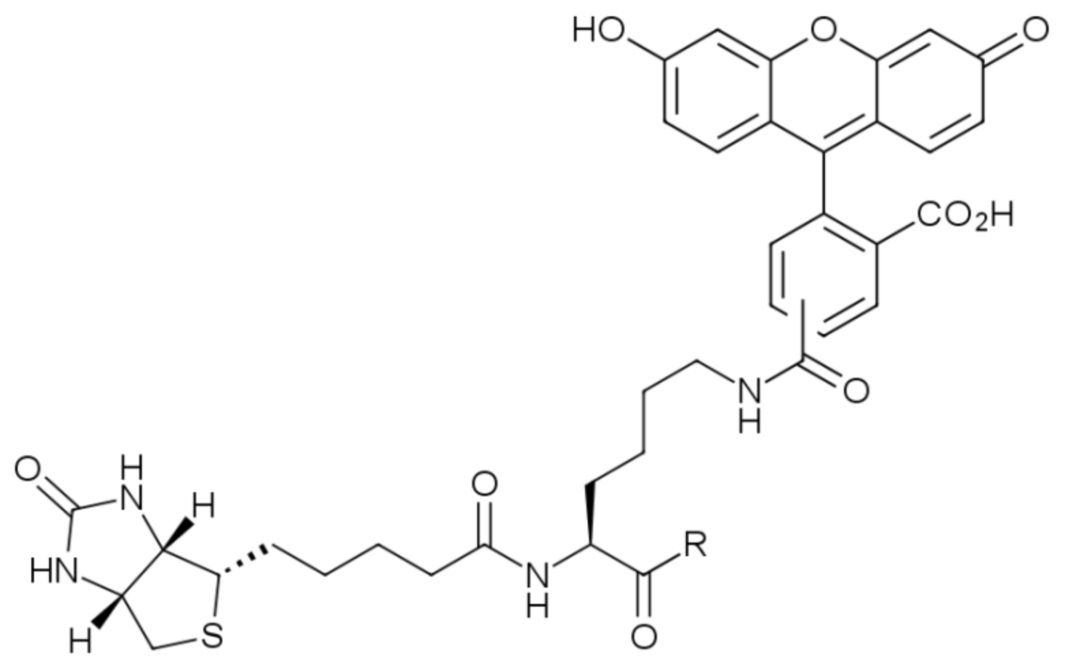
где R представляет собой OH или -NH(CH2)6OH.
21. Композиция, содержащая:

где R представляет собой OH или -NH(CH2)6OH.
22. Композиция, содержащая:
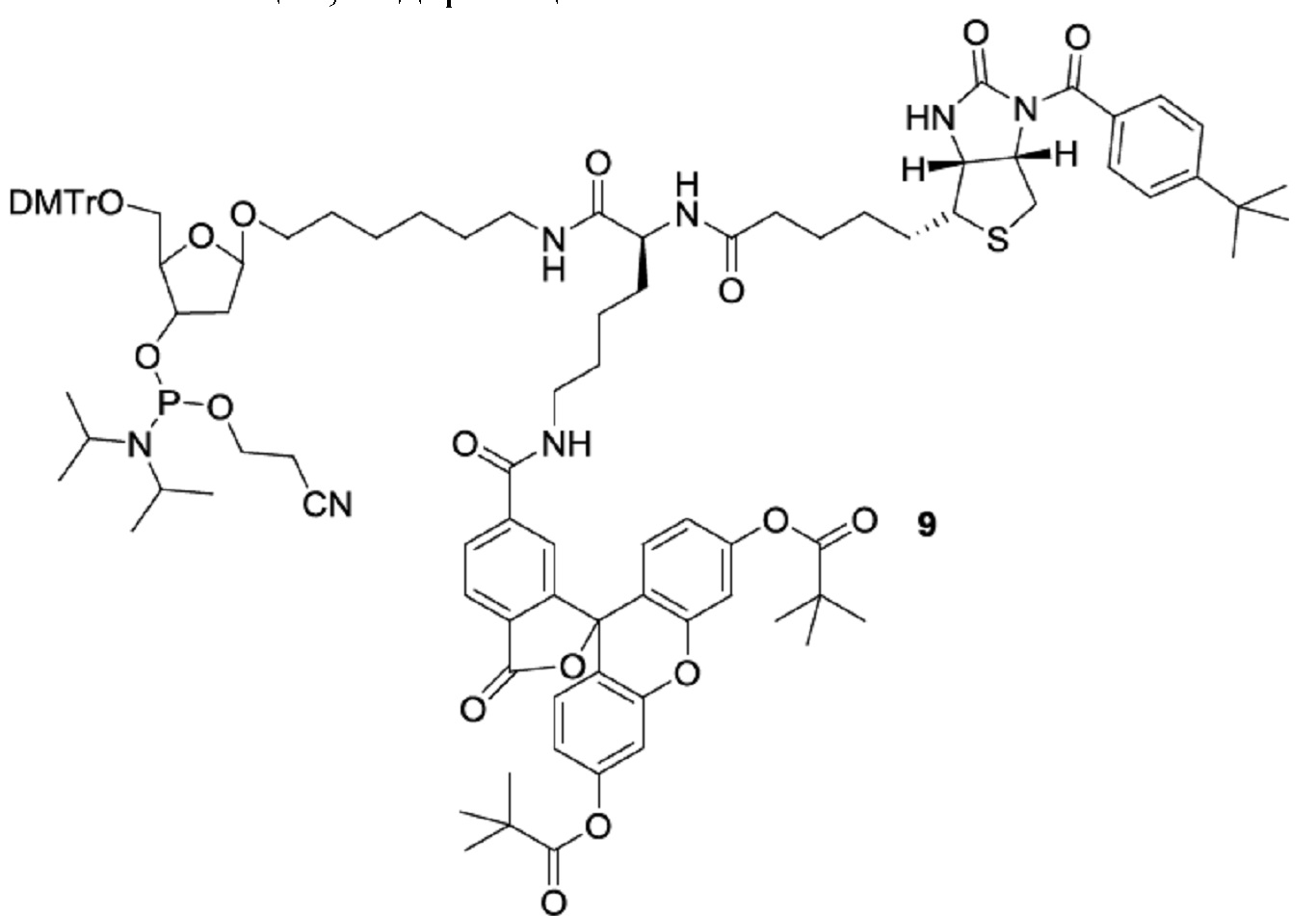
где DMTr представляет собой диметокситритил.
23. Композиция, содержащая:
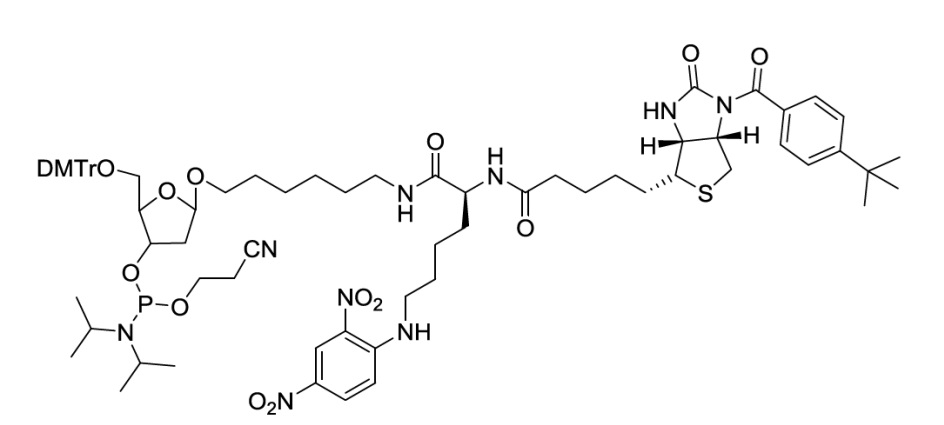
где DMTr представляет собой диметокситритил.
24. Композиция, содержащая:

где Гаптен 1 и Гаптен 2 представляют собой иммуногенные группы по пп. 22 или 23;
Z выбран из: (i) C1' лишенного азотистого основания рибозного или дезоксирибозного кольца в случае РНК- или ДНК-олигонуклеотида, соответственно; с бета-конфигурацией у аномерного атома углерода; (ii) фосфоамидитного соединения, сконфигурированного для присоединения в ДНК или РНК-олигонуклеотид; и при этом, если Z представляет собой фосфоамидит ДНК или РНК, реакционноспособные группы Гаптена 1 и Гаптена 2 могут быть необязательно защищены пивалоилом; трет-бутилбензоилом; ацилом; бензоилом; или изобутирилом;
R представляет собой водород или линейный или разветвленный C1-C6 алкил;
X1, X2 и X4 представляют собой соединяющие группы, которые могут независимо отсутствовать или могут представлять собой линейный или разветвленный C1-C12 алкил, который необязательно может быть прерван одной или более группами -O-, -C(=O)- или -NR-;
X3 представляет собой линейный или разветвленный C1-C6 алкил; и
Х5 представляет собой линейный или разветвленный С1-С12 алкил, который необязательно прерван одной или более группами -O-, -C(=O)- или -NR-.
25. Устройство, содержащее:
полоску с латеральным потоком, содержащую
зону нанесения образца;
зону реагентов после зоны нанесения образца, находящуюся в жидкостной связи с ней, при этом зона реагентов содержит высушенную композицию реагентов RPA для амплификации целевой нуклеиновой кислоты, связывающий агент, специфичный к амплифицированной продукту целевой нуклеиновой кислоты, и обнаруживаемую молекулу;
по меньшей мере одну тестовую зону после зоны реагентов, находящуюся в жидкостной связи с ней, при этом тестовая зона содержит иммобилизованную захватывающую молекулу, специфичную для амплифицированного продукта целевой нуклеиновой кислоты; и
контрольную зону после тестовой зоны.
26. Устройство по п. 25, характеризующееся тем, что указанная высушенная композиция реагентов RPA содержит объемообразующий агент, рекомбиназу, полимеразу, нуклеазу, зонд с двойным гаптеном и обнаруживаемую молекулу.
27. Устройство по п. 26, характеризующееся тем, что указанный зонд с двойным гаптеном содержит конъюгат биотина и карбоксифлуоресцеина (FAM) или биотина и динитрофенила (DNP).
28. Устройство по п. 25, характеризующееся тем, что указанная иммобилизованная захватывающая молекула, специфичная в отношении амплифицированной целевой нуклеиновой кислоты, выбрана из группы, состоящей из захватывающей молекулы против FAM или захватывающей молекулы против DNP.
29. Устройство по п. 28, характеризующееся тем, что указанная молекула против FAM или молекула против DNP независимо выбраны из группы, состоящей из поликлонального антитела, моноклонального антитела и функционального связывающего фрагмента такого антитела, включая FAB, ScFv, Fv или DAB.
30. Устройство по п. 25, характеризующееся тем, что указанная обнаруживаемая молекула выбрана из группы, состоящей из золя золота, золя серебра, золя латекса, целлюлозной наногранулы или углеродной наноструны и захватывающей молекулы против биотина.
31. Устройство по п. 25, характеризующееся тем, что указанная контрольная зона содержит зону связывания, которая свидетельствует о правильном функционировании полоски с латеральным потоком.
32. Устройство по п. 25, характеризующееся тем, что указанная контрольная зона содержит линию захвата антитела против мышиного белка.
33. Способ обнаружения продуктов амплификации, включающий:
приведение образца, предположительно содержащего целевую нуклеиновую кислоту, представляющую интерес, в контакт с реагентами RPA для амплификации целевой нуклеиновой кислоты, олигонуклеотидным зондом, содержащим последовательность нуклеиновой кислоты, комплементарную целевой нуклеиновой кислоте, и ковалентно связанную уходящую группу с двойным гаптеном, и нуклеазой;
амплификацию целевой нуклеиновой кислоты с получением продукта целевой нуклеиновой кислоты; и
обнаружение продукта целевой нуклеиновой кислоты путем обнаружения свободных фрагментов двойного гаптена, отщепленных от олигонуклеотидного зонда, гибридизованного с целевой нуклеиновой кислотой.
34. Способ по п. 33, характеризующийся тем, что указанные реагенты RPA расположены на зоне нанесения образца полоски с латеральным потоком.
35. Способ по п. 33, характеризующийся тем, что амплификацию нуклеиновой кислоты выполняют на полоске с латеральным потоком после контакта образца с реагентами RPA с образованием смеси для амплификации нуклеиновой кислоты.
36. Способ по п. 33, характеризующийся тем, что амплификацию нуклеиновой кислоты выполняют на полоске с латеральным потоком без разбавления или добавления другой жидкости к смеси RPA.
37. Способ по п. 33, характеризующийся тем, что указанный фрагмент двойного гаптена, отщепленный от олигонуклеотидного зонда, селективно захватывается в тестовой зоне на полоске с латеральным потоком, расположенной после зоны нанесения образца.
38. Способ по пп. 33-37, характеризующийся тем, что олигонуклеотидный зонд, содержащий ковалентно связанный двойной гаптен, не захватывается селективно в тестовой зоне на полоске с латеральным потоком.
39. Способ по любому из пп. 33-38, характеризующийся тем, что указанная полоска с латеральным потоком содержит тестовую зону и контрольную зону, причем указанная тестовая зона содержит член связывающейся пары для захвата двойного гаптена, отщепленного от олигонуклеотида, и указанная контрольная зона содержит член связывающейся пары для внутреннего контроля.
40. Способ по п. 39, характеризующийся тем, что указанная контрольная зона содержит антитело против мышиного белка или его фрагмент.
41. Способ по п. 39, характеризующийся тем, что указанная тестовая зона содержит захватывающую молекулу против DNP или захватывающую молекулу против FAM.
42. Способ по п. 40, характеризующийся тем, что указанная захватывающая молекула против FAM выбрана из группы, состоящей из моноклонального антитела, поликлонального антитела и функционального связывающего фрагмента такого антитела.
43. Способ по п. 42, характеризующийся тем, что указанная захватывающая молекула против DNP выбрана из группы, состоящей из моноклонального антитела, поликлонального антитела или функционального связывающего фрагмента такого антитела.
44. Способ по пп. 33-43, характеризующийся тем, что обнаружение продуктов амплификации включает захват уходящей группы с двойным гаптеном в тестовой зоне и мечение захваченной уходящей группы с двойным гаптеном с применением обнаруживаемой молекулы.
45. Способ по п. 44, характеризующийся тем, что указанная обнаруживаемая молекула выбрана из группы, состоящей из золя золота, золя серебра, золя латекса, целлюлозной наногранулы и углеродной наноструны.
46. Способ, включающий:
нанесение образца, предположительно содержащего целевую нуклеиновую кислоту, на полоску с латеральным потоком;
приведение образца в контакт со смесью реагентов RPA для амплификации целевой нуклеиновой кислоты, высушенной на зоне реагентов полоски с латеральным потоком; и
обнаружение продуктов амплификации, если они присутствуют, на тестовой зоне полоски с латеральным потоком.
47. Способ по п. 46, характеризующийся тем, что указанный образец, предположительно содержащий целевую нуклеиновую кислоту, вносят в зону нанесения полоски с латеральным потоком.
48. Способ по п. 47, характеризующийся тем, что указанная смесь реагентов RPA содержит объемообразующий агент, рекомбиназу, полимеразу, нуклеазу и олигонуклеотидный зонд с двойным гаптеном.
49. Способ по п. 48, характеризующийся тем, что указанный объемообразующий агент выбран из группы, состоящей из полиэтиленгликоля (ПЭГ), поливинилового спирта (ПВС), поливинилпирролидона (ПВП), фиколла и декстрана.
50. Способ по п. 48 или 49, характеризующийся тем, что указанный объемообразующий агент имеет молекулярную массу по меньшей мере 1 кДа, по меньшей мере 2 кДа, по меньшей мере 3 кДа, по меньшей мере 4 кДа, по меньшей мере 5 кДа, по меньшей мере 6 кДа, по меньшей мере 8 кДа или по меньшей мере 10 кДа.
51. Способ по п. 49 или 50, характеризующийся тем, что указанный объемообразующий агент присутствует в смеси в концентрации по меньшей мере 15% об./об., по меньшей мере 12% об./об., конечной концентрации по меньшей мере 10% об./об., по меньшей мере 8% об./об., по меньшей мере 6% об./об., по меньшей мере 5% об./об., по меньшей мере 4% об./об. или конечной концентрации по меньшей мере 3% об./об.
52. Способ по любому из пп. 46-51, характеризующийся тем, что указанный объемообразующий агент имеет профиль вязкости при 20°С менее или равный 5 мПа/с, менее или равный 4 мПа/с, менее или равный 3 мПа/с, менее или равный 2 мПа/с или менее или равный 1 мПа/с.
53. Способ по п. 46, характеризующийся тем, что указанный объемообразующий агент представляет собой ПЭГ и имеет вязкость при 20°С меньше или равную 3 мПа/с.
54. Способ по п. 46, характеризующийся тем, что указанный объемообразующий агент представляет собой ПЭГ с молекулярной массой 3 кДа, и при этом конечная концентрация ПЭГ составляет 6,5% об./об.
55. Способ по п. 48, характеризующийся тем, что обнаружение продуктов амплификации, если они присутствуют, включает обнаружение фрагмента двойного гаптена, отщепленного от олигонуклеотидного зонда, гибридизованного с продуктами амплификации.
56. Способ по п. 46, характеризующийся тем, что перед обнаружением продуктов амплификации не требуется разбавление смеси RPA.

Комментарии