Реассортантный штамм вируса гриппа rn2/66-human a(h7n2) для определения антител к нейраминидазе при гриппозной инфекции и вакцинации - RU2625024C1
Код документа: RU2625024C1
Чертежи

Описание
Изобретение относится к медицинской вирусологии и может быть использовано в здравоохранении для диагностических целей при гриппозной инфекции, а также для оценки иммуногенности при вакцинации гриппозными вакцинами.
Вирусы гриппа А подтипа H2N2 не циркулируют в человеческой популяции с 1968 года, поэтому большая часть населения, прежде всего лица старше 45 лет, не имеет иммунитета к их главному поверхностному антигену - гемагглютинину (НА) - и, соответственно, будет до определенной степени уязвимой в случае возвращения указанного подтипа вируса в циркуляцию. Современные эпидемические штаммы подтипа A(H3N2), имея значительные антигенные различия в гемагглютинине с вышедшими из циркуляции штаммами A(H2N2), представляют с ними один подтип нейраминидазы. Таким образом, наличие у контингента людей, прививаемых сезонной трехвалентной живой гриппозной вакциной (ЖГВ), или у лиц, перенесших естественную инфекцию, вызванную эпидемическим штаммом вируса гриппа A(H3N2), составляющей противогриппозного иммунного ответа, нацеленной на минорный поверхностный антиген вируса (N2), возможно, окажется решающим в снижении смертности и ограничении распространения пандемии на ее начальном этапе, пока не будет развернута массовая вакцинация населения штаммом с антигенно актуальным НА.
Одной из приоритетных задач всемирной организации здравоохранения является подготовка к пандемии гриппа A(H2N2), которая включает в себя оценку степени восприимчивости населения к потенциально пандемическому штамму вируса гриппа A(H2N2) и создание международных и государственных коллекций вакцинных штаммов с целью скорейшего начала производства пандемических вакцин и иммунизации населения в случае возвращения вирусов A(H2N2). Первый этап подготовки подразумевает исследование гетеросубтипического противогриппозного иммунитета, опосредованного антинейраминидазными антителами и другими факторами, отличными от антигемагглютинирующих антител. Второй этап включает всестороннюю, полную характеристику иммуногенности и защитной эффективности вакцинных препаратов потенциально пандемического подтипа, в том числе с применением методов выявления гуморального иммунного ответа к NA вируса гриппа.
Для определения антител к нейраминидазе вируса гриппа ранее применялись реассортантные штаммы на основе вируса гриппа А/лошадь/Прага/1/56(Н7N7) с нерелевантным для человека гемагглютинином, содержащие нейраминидазу эпидемических вирусов человека A(H1N1) и A(H3N2) [Вопр. вирусологии. - 1985. - №1. - стр. 35-39]. При этом использовалась реакция ингибирования элюирования вируса с эритроцитов, основанная на блокировании антителами ферментативной активности NA, что препятствовало разрушению агглютинации эритроцитов, вызванной НА вируса гриппа. Известен также реассортантный штамм RN1/09-swine A(H7N1), применяющийся для выявления антител к нейраминидазе пандемического штамма 2009 года подтипа A(H1N1) в твердофазной реакции ингибирования сиалидазной активности [Патент РФ 2428476, заявл. 21.06.2010, опубл. 10.09.2011, Бюл. №25].
Задачей, на решение которой направлено заявляемое изобретение, является подготовка диагностического реассортантного штамма вируса гриппа А для специфичного выявления в сыворотках крови антинейраминидазных антител к вышедшим из циркуляции в 1968 году, потенциально пандемическим вирусам гриппа подтипа A(H2N2) в твердофазной реакции ингибирования сиалидазной активности. Для этих целей использовали методы классической генетической реассортации в развивающихся куриных эмбрионах (РКЭ) вируса А/лошадь/Прага/1/56(Н7N7) и вакцинного штамма А/17/Калифорния/66/395(Н2N2), содержащего поверхностные антигены от вируса гриппа А/Калифорния/1/1966(Н2N2), выделенного на исходе последнего периода циркуляции штаммов A(H2N2). Для отбора клонов с нужными свойствами и составом генома проводили ряд селективных пассажей при пониженной до 25°С температуре в присутствии крысиной иммунной сыворотки к штамму А/Калифорния/1/1966(Н2N2), обедненной по содержанию анти-N2 антител.
Вакцинный штамм А/17/Калифорния/66/395(Н2N2), являющийся реассортантом на основе холодоадаптированного донора аттенуации А/Ленинград/134/17/57(Н2N2) с формулой генома 6:2, унаследовавшим 6 генов внутренних и неструктурных белков от донора аттенуации, а гены НА и NA - от вируса гриппа А/Калифорния/1/1966(Н2N2) [PloS one. - 2014. - Vol. 9.- №7. - е102339; PMID: 25058039], был получен из коллекции отдела вирусологии ФГБНУ «ИЭМ».
Вирус А/лошадь/Прага/1/1956(Н7N7) был предоставлен центром по контролю и предупреждению заболеваний США (Атланта, Джорджия).
Реассортант RN2/66-human A(H7N2) унаследовал ген NA от штамма А/Калифорния/1/1966(Н2N2). На фиг. 1 представлен пример анализа гена NA при помощи обратнотранскриптазной полимеразной цепной реакции (ОТ-ПЦР) с праймерами, специфичными для нейраминидазы только одного из родительских вирусов: подтипа N2 (дорожки со 2 по 4) или подтипа N7 (дорожки с 7 по 9). Дорожки на электрофорезном геле имеют следующее соответствие: 1 - ДНК-маркер (100 bp + 1.5 Kb, НПО «СибЭнзим»), 2 - ОТ-ПЦР с праймерами к N2 и РНК штамма А/лошадь/Прага/1/56 (H7N7), 3 - ОТ-ПЦР с праймерами к N2 и РНК штамма А/17/Калифорния/66/395(Н2N2), 4 - ОТ-ПЦР с праймерами к N2 и РНК штамма RN2/66-human A(H7N2), 5, 6 - ДНК-маркер (100 bp + 1.5 Kb, НПО «СибЭнзим»), 7 - ОТ-ПЦР с праймерами к N7 и РНК штамма А/лошадь/Прага/1/56 (H7N7), 8 - ОТ-ПЦР с праймерами к N7 и РНК штамма А/17/Калифорния/66/395(Н2N2), 9 - ОТ-ПЦР с праймерами к N7 и РНК штамма RN2/66-human A(H7N2). Наличие амплификации РНК реассортанта RN2/66-human A(H7N2) (4-я дорожка) с праймерами к N2 подобно родительскому штамму А/17/Калифорния/66/395(Н2N2) (3-я дорожка) и отсутствие ПЦР-продукта (9-я дорожка) при проведении полимеразной цепной реакции с праймерами, комплементарными участкам гена NA штамма А/лошадь/Прага/1/56(Н7N7), свидетельствуют об идентичности генов NA реассортанта RN2/66-human A(H7N2) и штамма А/Калифорния/1/1966(Н2N2).
ОТ-ПЦР-рестрикционный анализ шести генов негликозилированных белков [Journal of Virological Methods. - 1995. - №55. - P. 445-446] показал, что 5 сегментов РНК, кодирующих внутренние белки вируса (РВ2, РВ1, PA, NP, М), были унаследованы реассортантом от донора аттенуации А/Ленинград/134/17/57(Н2N2), а сегмент РНК, кодирующий неструктурные белки вируса (NS), - от вируса гриппа лошади А/лошадь/Прага/1/1956(Н71N7).
Идентичность гемагглютинина реассортанта соответствующему поверхностному гликопротеину родительского штамма А/лошадь/Прага/1/1956(Н7N7) подтверждена в реакции торможения гемагглютинации (РТГА) с крысиными антисыворотками.
Наличие нейраминидазы вируса гриппа потенциально пандемического подтипа A(H2N2) делает возможным применение указанного штамма для выявления гомологичных и перекрестно-реагирующих антинейраминидазных антител у лиц, перенесших инфекцию штаммами A(H2N2)/A(H3N2) или прошедших вакцинацию гриппозными вакцинами соответствующих подтипов. Поскольку представленный диагностический реассортантный штамм обладает антигенной специфичностью гемагглютинина нерелевантного для человека вируса А/лошадь/Прага/1/1956(Н71N7), его применение исключает искажение результатов серологических тестов, направленных на выявление антинейраминидазных антител, из-за присутствия в исследуемых образцах сывороток крови также антител к гемагглютинину современных эпидемических и предположительно пандемических штаммов.
Штамм депонирован в Государственной коллекции вирусов НИИ вирусологии им. Д.И. Ивановского ФГБУ «ФНИЦЭМ им. Н.Ф. Гамалеи» Минздрава России под № ГКВ 2771.
ХАРАКТЕРИСТИКА ПОЛУЧЕННОГО ШТАММА
Морфология штамма - полиморфная, типичная для вируса гриппа.
Инфекционная активность реассортантного штамма RN2/66-human A(H7N2) при репродукции в развивающихся куриных эмбрионах при 33°С в течение 48 часов - 8,5 lg ЭИД50/0,2 мл.
Гемагглютинирующая активность - 512 ГАЕ/50 мкл.
Паспорт на реассортантный штамм RN2/66-human A(H7N2) прилагается.
ПАСПОРТ ШТАММА
вируса гриппа RN2/66-human A(H7N2)
1. Название вируса, штамма (семейство, таксономическая и антигенная группа):
семейство Orthomyxoviridae, род Influenzavirus А, подтип H7N2, штамм RN2/66-human A(H7N2) [А/лошадь/Прага/1/1956(Н7)×А/Калифорния/1/1966(N2)].
2. Выделен (год, место выделения, от кого и из какого материала): штамм получен в октябре 2013 года методом классической генетической реассортации в развивающихся куриных эмбрионах. Характеристика родительских вирусов:
а) вирус гриппа лошади - А/лошадь/Прага/1/1956(Н7N7);
б) вакцинный штамм А/17/Калифорния/66/395(Н2N2), содержащий гены НА и NA эпидемического вируса гриппа А/Калифорния/1/1966(Н2N2), остальные 6 сегментов РНК донора аттенуации А/Ленинград/134/17/1957(H2N2).
3. Физико-химические свойства {криптограмма, размер, фильтрация, РНК, ДНК):
Морфология штамма - полиморфная, типичная для вируса гриппа.
4. Генетические признаки
Состав генома: НА от вируса гриппа лошади А/лошадь/Прага/1/1956(Н7N7); NA от эпидемического вируса гриппа А/Калифорния/1/1966(Н2N2); 5 сегментов РНК, кодирующих внутренние белки вируса (РВ2, РВ1, PA, NP, М), от донора аттенуации А/Ленинград/134/17/1957(H2N2); сегмент РНК, кодирующий неструктурные белки вируса (NS), от вируса гриппа лошади А/лошадь/Прага/1/1956(Н7N7).
5. Антигенные свойства
Антигенно идентичен гемагглютинину вируса А/лошадь/Прага/1/1956(Н7N7) по данным РТГА с крысиной антисывороткой.
6. Прочие свойства
Штамм RN2/66-human A(H7N2) обладает нерелевантным для человека гемагглютинином и предназначен для специфичного выявления в сыворотке крови антинейраминидазных антител.
7. Количество пассажей
7 в процессе реассортации; затем 2 накопительных пассажа в системе развивающихся куриных эмбрионов при температуре инкубации 33°С.
8. Оптимальный титр
Оптимальный титр достигается при культивирования штамма в 10-11 дневных развивающихся куриных эмбрионах при 33°С в течение 48 часов, при этом инфекционная активность штамма составляет 8,5 lg ЭИД50/0,2 мл, гемагглютинирующая активность с 0,5% взвесью куриных эритроцитов составляет 512 ГАЕ/50 мкл.
9. Режим высушивания
Вирус лиофилизирован 21 октября 2013 г. Объем материала в ампуле - 1,0 мл, стабилизатор - раствор 13% пептона.
10. Условия хранения
Вирус хранят в виде лиофилизированной суспензии при температуре не выше +4°С. Для восстановления инфекционных свойств необходимы 1-2 пассажа на куриных эмбрионах. Инфекционная активность штамма после лиофилизации - 8,3 ЭИД50/0,2 мл, гемагглютинирующая активность - 256 ГАЕ/50 мкл.
11. Патогенность для человека
Относится к микроорганизмам III группы патогенности.
12.Чувствительность к экспериментальной инфекции (животные, эмбрионы, членистоногие и клеточные культуры)

13. Авторы штамма
Смолоногина Т.А., к.б.н., с.н.с. отдела вирусологии ФГБНУ «ИЭМ»;
Дешева Ю.А., д.м.н., в.н.с. отдела вирусологии ФГБНУ «ИЭМ»;
Руденко Л.Г., проф., д.м.н., зав. отделом вирусологии ФГБНУ «ИЭМ».
Назначение полученного штамма - качественное и количественное определение антител к NA вирусов гриппа потенциально пандемического подтипа A(H2N2) в сыворотках крови.
1. Штамм может применяться для выявления уровня сывороточных антинейраминидазных антител среди населения при помощи твердофазной реакции ингибирования нейраминидазной активности (РИНА).
Методика такого выявления основана на определении титра антинейраминидазных ингибирующих антител, представляющего собой величину, обратную разведению тестируемой сыворотки, в котором наблюдается 50%-ое снижение сиалидазной активности NA диагностического штамма RN2/66-human A(H7N2). Сиалидазная активность NA определяется по отношению к высокомолекулярному натуральному субстрату (фетуин), сорбированному на полимерном носителе, с использованием специфически связывающего демаскированные полисахариды пероксидазно-меченного лектина.
У обследуемых волонтеров отбираются пробы венозной крови. Полученные после центрифугирования сыворотки крови хранятся при -20°С.
Пример выполнения эксперимента
Антитела к N2 в сыворотках крови добровольцев в возрасте 18-40 лет, обследованных осенью 2013 года, определяли при помощи твердофазной реакции ингибирования нейраминидазной активности и диагностического штамма RN2/66-human A(H7N2).
Распределение волонтеров по уровню сывороточных антинейраминидазных антител к штамму А/Калифорния/1/66(Н2N2) представлено на фиг. 2. У 11 из 36 обследованных добровольцев (30,5%) 1973-1995 годов рождения в твердофазной РИНА были выявлены антитела к NA штамма подтипа A(H2N2), вышедшего из циркуляции среди человеческой популяции еще в 1968 году, в тирах, превышающих значение 1:40. Среднегеометрический титр анти-NA антител для указанной группы из 11 серопозитивных лиц составил 1:88. В силу возраста волонтеров не представляется возможной их встреча непосредственно с эпидемическими вирусами рассматриваемого подтипа, что также подтверждается данными РТГА: ни один из участвовавших в исследовании добровольцев не был иммунен к НА штамма А/Калифорния/1/66(Н2N2). Можно предположить, что присутствие среди рассматриваемой возрастной группы фона сывороточных антинейраминидазных антител к штамму 1966 года выделения объясняется перекрестным реагированием анти-N2 иммуноглобулинов, сформировавшихся в результате контакта обследованных лиц с эпидемическими штаммами подтипа A(H3N2), пришедшими на смену вирусам A(H2N2) и представляющими с ними один и тот же подтип нейраминидазы.
2. Штамм может применяться для выявления антинейраминидазных антител в сыворотках крови волонтеров, иммунизированных ЖГВ, при помощи реакции ингибирования нейраминидазной активности.
Пример выполнения эксперимента
После характеристики исходного иммунологического статуса волонтерам в рамках клинических испытаний двукратно интраназально с интервалом 28 дней вводилось 7,9 lg ЭИД50/0,5 мл моновалентной ЖГВ на основе аттенуированного штамма потенциально пандемического подтипа А/17/Калифорния/66/395(Н2N2). Образцы сывороток крови вакцинированных лиц и волонтеров из группы плацебо отбирали на 28 день после первой и второй иммунизации, а также через 56 дней после второй прививки.
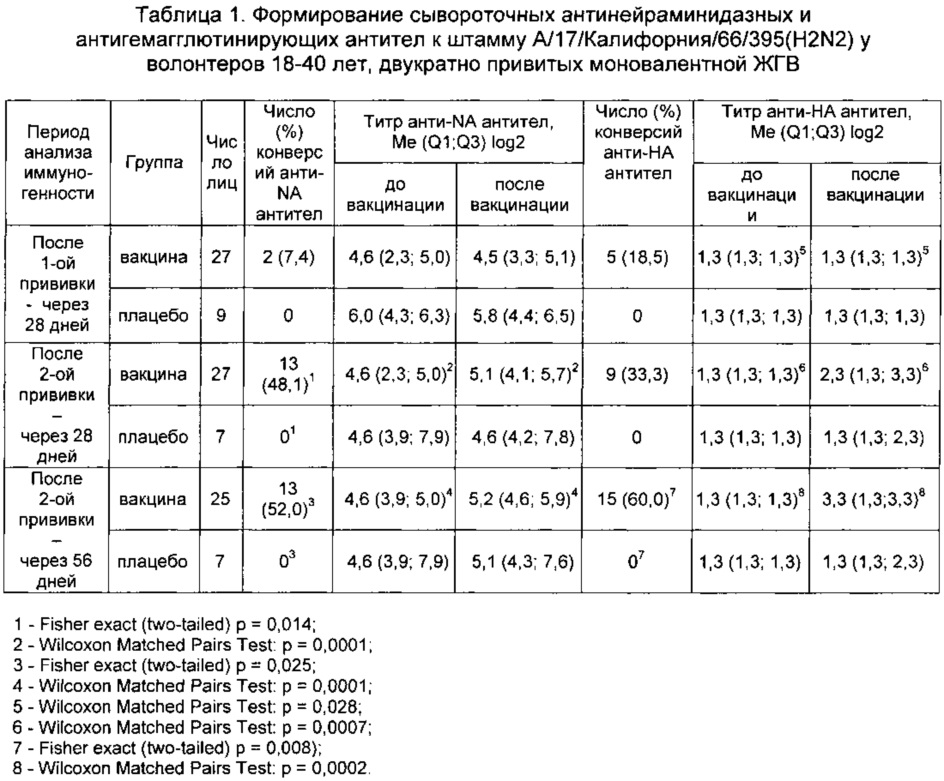
Согласно твердофазной РИНА и РТГА исходный иммунологический статус группы вакцинированных и получивших препарат плацебо волонтеров не различался (Mann-Whitney U Test, p>0,05). Статистически значимый прирост титров антинейраминидазных антител к вакцинному штамму был отмечен только на 28 и 56 день после двукратной иммунизации ЖГВ (см. таблицу 1). Статистически значимый прирост титров антигемагглютинирующих антител к вакцинному штамму наблюдался уже на 28 день после однократного введения ЖГВ, но для более выраженного иммунного ответа к НА аттенуированного штамма все же требовалась ревакцинация. В группе лиц, получивших препарат плацебо, изменения соответствующих серологических показателей отсутствовали.
Процент совпадения результатов РТГА и твердофазной РИНА в плане выявления / не выявления сероконверсий к поверхностным антигенам штамма А/17/Калифорния/66/395(Н2N2) в одних и тех же парах сывороток крови вакцинированных волонтеров был невысоким - 52,0-74,1%. У 14,8-28,0% привитых выявлялись достоверные приросты титров антител только к НА вакцинного штамма; 7,4-29,6% приходилось на долю лиц положительно ответивших выработкой антинейраминидазных, но не антигемагглютинирующих антител. Двусторонний вариант точного критерия Фишера не выявил связи между сероконверсиями антител к двум поверхностным гликопротеинам вируса у одних и тех же лиц (p>0,7).
Результаты экспериментов наглядно демонстрируют пригодность заявляемого реассортантного штамма для выявления антител к нейраминидазе N2 вируса гриппа, благодаря чему этот штамм может быть использован для диагностики, при изучении иммуногенности гриппозной вакцины, для анализа фоновых значений антинейраминидазных антител в человеческой популяции в целом.
Реферат
Изобретение относится к области биотехнологии, вирусологии и медицины. Диагностический штамм вируса гриппа RN2/66-human A(H7N2) получен путем скрещивания вируса гриппа лошади А/лошадь/Прага/1/1956(Н7N7) с холодоадаптированным вакцинным штаммом А/17/Калифорния/66/395(Н2N2) на основе донора аттенуации А/Ленинград/134/17/57(Н2N2). Штамм содержит нейраминидазу эпидемического вируса гриппа подтипа N2 А/Калифорния/1/1966 (H2N2) и гемагглютинин вируса гриппа А/лошадь/Прага/1/1956 (H7N7). Штамм RN2/66-human A(H7N2) активно размножается в развивающихся куриных эмбрионах при оптимальной температуре 33°С, что позволяет накапливать вирусный материал для последующей очистки и концентрации. Штамм RN2/66-human A(H7N2) может применяться в твердофазной реакции ингибирования нейраминидазной активности для анализа фоновых значений сывороточных антител к нейраминидазе N2 вируса гриппа в человеческой популяции и их изменения в результате инфекции/вакцинации. 2 ил., 1 табл., 2 пр.

Комментарии