Способ ультравысокопроизводительного скрининга клеток или микроорганизмов и средство для ультравысокопроизводительного скрининга клеток или микроорганизмов - RU2656216C1
Код документа: RU2656216C1
Чертежи







Описание
Изобретение относится к области биотехнологии и фармацевтики.
Современная биотехнология и фармацевтика являются крайне высокотехнологичными областями, чьи успехи тесно связаны с разработкой новых принципов поиска различных видов биологической активности. Возможности, которые открывает нам «пост-геномная» эра, позволяют выявлять новые мишени для поиска терапевтических агентов [1], а также осуществлять виртуальный скрининг потенциальных кандидатов лекарственных препаратов insilico [2].
Несмотря на колоссальные перспективы методов молекулярного моделирования, данный подход не является универсальным, т.к. ресурсы существующих в настоящее время суперкомпьютеров не позволяют рассчитывать взаимодействия биомолекул de novo и используют различные приближения, требующие наличия кристаллической структуры мишени, ее динамики, а также четкого понимания механизма ее действия [3]. Комбинаторные методы скрининга, основанные на эксперименте, напротив, не требуют никаких дополнительных данных для поиска новой биологической активности, так как базируются на предположении о том, что достаточно большая выборка различных вариантов за счет своего разнообразия уже содержит в себе искомую активность и задача исследователя состоит лишь в том, чтобы эффективно отобрать ее из общего пула вариантов [4].
Несмотря на уникальные возможности поиска биологической активности in silico denovo, подавляющее большинство современных препаратов получено на основе комбинации методов компьютерного моделирования и высокопроизводительного скрининга лекарственных кандидатов [5]. В настоящее время высокопроизводительный скрининг осуществляется на базе автоматизированных роботизированных станций [6], однако существует очевидная тенденция к переходу биотехнологических платформ на формат "лаборатории-на-чипе", основанный на современных успехах в области микрофлюидики [7]. Использование микрофлюидики приводит к миниатюризации оборудования, уменьшению расходов на реагенты и эксплуатацию. Происходит многократное увеличение производительности и осуществляется переход к ультравысокопроизводительному скринингу [8] за счет использования микрофлюидных капельных технологий. Несмотря на значительные успехи ряда мировых центров [8-13], в вопросах технологии формирования микрофлюидных потоков, систем отбора и идентификации активных клонов существует еще достаточное количество нерешенных проблем.
Изобретение относится к созданию универсальной ультравысокопроизводительной микрофлюидной платформы для скрининга различных типов биокаталитической и биологической активности клеток, белков.
В настоящее время существует множество разнообразных ультравысокопроизводительных подходов, позволяющих эффективно отбирать различные биомолекулы, обладающие высокоспецифичным и высокоаффинным связыванием с целевыми молекулами-мишенями: скрининг с использованием микросфер [14], рибосомный дисплей [15], фаговый дисплей [16, 17], бактериальный дисплей [18], дрожжевой дисплей [19], дисплей на клетках млекопитающих [20], SELEX [21]. В то же время разработка ультравысокопроизводительных методов, направленных на отбор химической или биологической активности, в отличие от связывания, зачастую сопряжена с большими трудностями. Прежде всего, данные методы не универсальны и в каждом отдельном случае имеют ряд серьезных недостатков, принципиально ограничивающих их применение. В частности, многие из них применимы лишь для скрининга активности, связанной с образованием ковалентной связи [22, 23]. Другие требуют вовлечения дополнительных молекулярно-биологических механизмов, таких как преимущество скорости роста или возникновение выживаемости в процессе селекции [24-26]. Некоторые методы используют специфические субстраты, образующие флуоресцентные продукты, заякоренные на клеточной стенке (или обладающие высокой гидрофобностью), в результате протекания биохимической реакции, катализируемой селектируемым ферментом [27, 28], что позволяет отбирать наиболее активные клетки по флуоресценции продукта с использованием флуоресцентно-активированного клеточного сортинга (FACS). Таким образом, для создания универсальной технологии отбора на активность в каплях в общем виде требуется решение двух принципиально важных задач:
1) детекции активности на уровне единичных капель;
2) возможности отбора единичных активных капель из смеси.
Наиболее простое решение этих задач было впервые продемонстрировано в работе [29]. В качестве аналитического сигнала для высокочувствительной детекции биокаталитической активности была использована флуоресценция, а отбор капель эмульсии производился при помощи стандартного клеточного сортера (FACS). При этом наиболее принципиальным усовершенствованием предыдущей технологии был переход от однократной эмульсии вода-в-масле к двойной эмульсии вода-в-масле-в-воде. Это позволяет непосредственно анализировать индивидуальную биокаталитическую активность изолированных генов.
Дальнейшее усовершенствование технологии эмульсионного скрининга связано с усовершенствованием самих компартментов - капель эмульсии. Дело в том, что изначально [30] стадии генерации как однократной, так и двойной эмульсии проводились с использованием гомогенизаторов. Несмотря на то, что использование гомогенизаторов позволяет быстро получать большие количества капель, данная технология имеет ряд принципиальных недостатков:
- стохастическая генерация капель эмульсии приводит к высокой полидисперсности;
- получаемая двойная эмульсия является мультикомпартментной (т.е. зачастую одна капля несет несколько изолированных капель);
- генерация эмульсии протекает в жестких условиях высокого сдвигового стресса.
Данные недостатки существенно снижают чувствительность данного метода скрининга (т.к. разные по размеру и гранулярности капли имеют разный объем и рассеяние, а следовательно, приводят к разным условиям протекания реакций внутри капель), значительно снижают максимальную производительность (т.к. доля капель целевого размера и гранулярности составляет 1-5%) и не позволяют заключать в капли различные биологические объекты, чувствительные к эмульсификации (клетки млекопитающих, многие виды микроорганизмов, а также многоклеточные организмы).
Решением перечисленных выше проблем является использование микрофлюидных технологий генерации эмульсии. Современные успехи в области микрофлюидики основаны на использовании микрофлюидных чипов - миниатюрных устройств, состоящих из каналов и текстур размером от нескольких десятков до нескольких микрометров [31], позволяющих реализовать концепцию "лаборатории-на-чипе".
Инкапсуляция живых клеток и микроорганизмов в индивидуальных каплях микрофлюидной эмульсии представляет большой интерес, так как открывает уникальные возможности для изучения уникальных свойств индивидуальных объектов среди их популяционного разнообразия. Успехи в этой области связаны с разработкой инертных органических жидкостей и биосовместимых эмульсификаторов. Наиболее простым решением этой проблемы является использование минерального масла и высокоэффективных биосовместимых эмульсификаторов на основе полисилоксанов (например, цетил полиэтиленгликоль/полипропиленгликоль-10/1 диметикон) [30, 32]. Данный подход был успешно применен для компартментализаци живых клеток факультативных анаэробов (бактерий Escherichia coli, Bacillus subtilis и дрожжей Saccharomyces cerevisiae), а также проведения бесклеточной in vitro транскрипции/трансляции. В то же время минеральное масло сильно ограничивает транспорт газов [33], что является принципиальным недостатком, ингибирующим рост микроорганизмов и затрудняющим его использование для инкапсуляции клеток млекопитающих и многочисленных видов аэробных бактерий.
Многочисленные фторуглеродные соединения - "фторуглеродные масла" (перфторуглеродные амины (FC-40, FC-70), перфторуглеводороды (перфтороктан, перфтордекалин), перфторпроизводные простых эфиров (HFE-7100, HFE-7500) и их смеси (FC-77)) представляют более удобную альтернативу минеральному маслу. Среди всех технических жидкостей, фторуглеродные масла обладают наиболее высокой газопроницаемостью, обеспечивающей эффективное дыхание клеток в каплях. Кроме того, они представляют собой "альтернативную фазу", т.е. обладают чрезвычайно низкой растворимостью в воде, углеводородах и жирах, что приводит к их инертности и биосовместимости. Имея плотность (1.6-1.9 г/см3), значительно превышающую плотность воды, фторуглеродные масла образуют двойную эмульсию, склонную к седиментации, что позволяет легко осуществлять ее сбор и реинжекцию. Стабилизация биосовместимых фторуглеродных микрофлюидных эмульсий может осуществляться с использованием неионных фторуглеродных поверхностно-активных веществ [34]. Получаемые в результате капли обладают высокой стабильностью и могут играть роль универсальных микрокомпартментов, обеспечивающих не только выживаемость, но и культивацию клеток дрожжей [34], а также линий клеток человека (причем как суспензионных Jurkat, так и адгезионных НЕK293Т) и, более того, рост, развитие и размножение в том числе и многоклеточных организмов, таких как С.elegans [35].
Использование возможностей направленной манипуляции над движением отдельно взятой капли в каналах чипа [36, 37] открыло принципиально новый взгляд на возможности микрофлюидики для ультравысокопроизводительного скрининга активности. В предыдущих работах отсутствовала стадия селекции, основанной непосредственно на анализе активности в индивидуальной капле. В то же время преимущество микрофлюидных технологий заключается в том числе и в возможности осуществлять полный цикл отбора улучшенной биокаталитической активности в чипе [8]. Использование микрофлюидной платформы для инкапсуляции индивидуальных дрожжевых клеток в каплях биосовместимой эмульсии, их инкубации и сортинга в чипе позволило проводить скрининг активности клеток с производительностью более 2000 событий в секунду.
Использование аналогичной микрофлюидной платформы для направленной эволюции арилсульфатазы Pseudomonas aeruginosa привело к 6 кратному увеличению ее каталитической активности по отношению к синтетическому флуорогенному фосфонату за один раунд отбора из библиотеки представительностью порядка 106 вариантов [9]. В данной работе, на основании индивидуальной активности клеточных лизатов единичных бактериальных клеток в каплях, проводился отбор наиболее активных вариантов с производительностью порядка 1000 событий в секунду. Процедура скрининга основана на экспрессии рекомбинантного фермента в клетках Е. coli, их последующего лизиса и повторной трансформации для проведения следующих раундов отбора. Таким образом, в отличие от предыдущей, данная платформа имеет ряд ограничений, лимитирующих ее практическое применение.
Известна заявка США №2016/0169788 на получение патента на изобретение в котором описан состав масляной фазы, использованной для генерации биосовместимой эмульсии, которая совпадает с масляной фазой, использованной в настоящей заявке. Однако в заявке США используется однократная эмульсия.
Перечень иллюстраций:
Рис. 1. Микрофлюидная платформа для ультравысокопроизводительного скрининга в каплях микрофлюидной двойной эмульсии.
Рис. 2. Генерация двойной микрофлюидной эмульсии методом последовательной эмульсификации в микрофлюидных чипах.
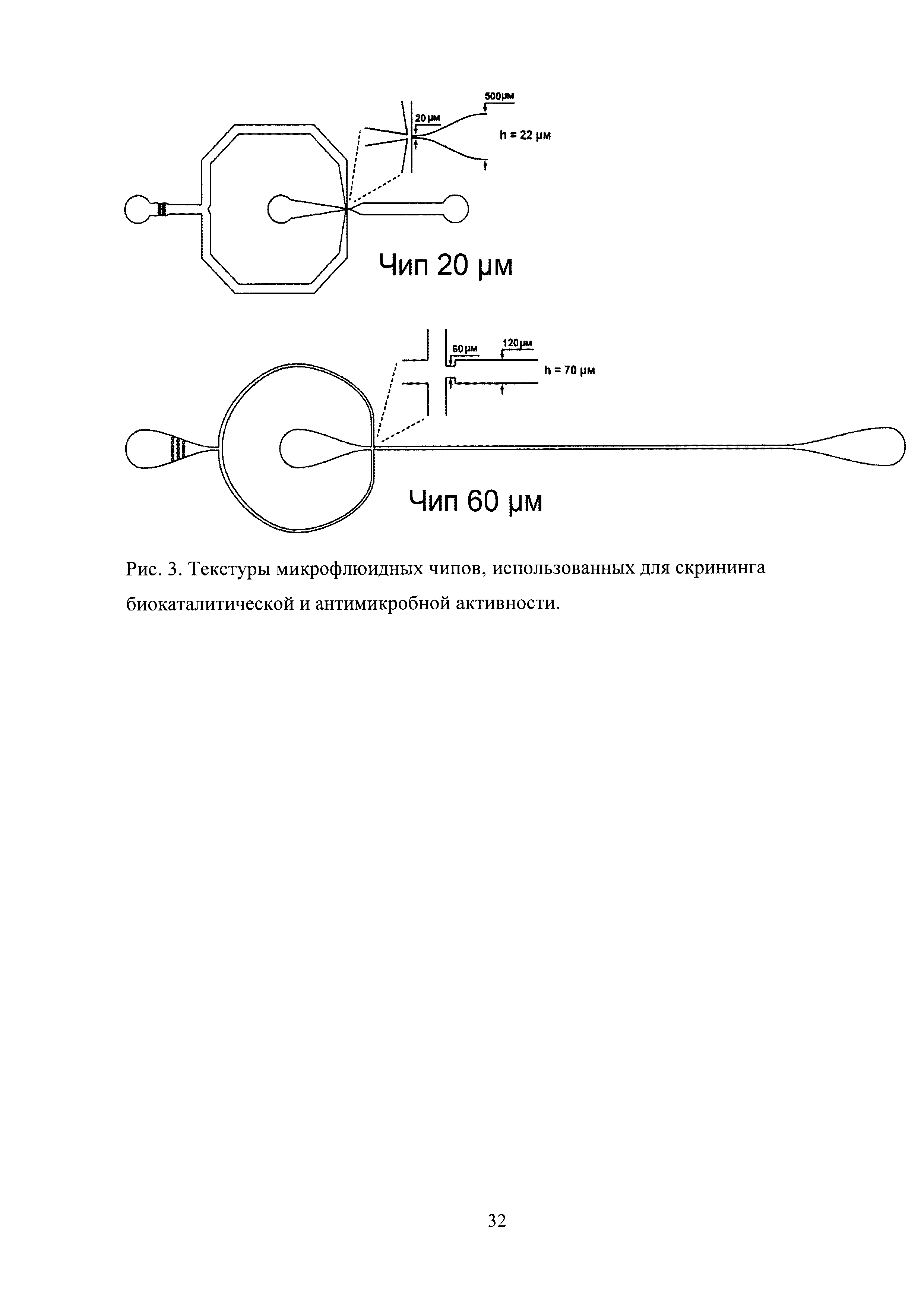
Рис. 3. Текстуры микрофлюидных чипов, использованных для скрининга биокаталитической и антимикробной активности.
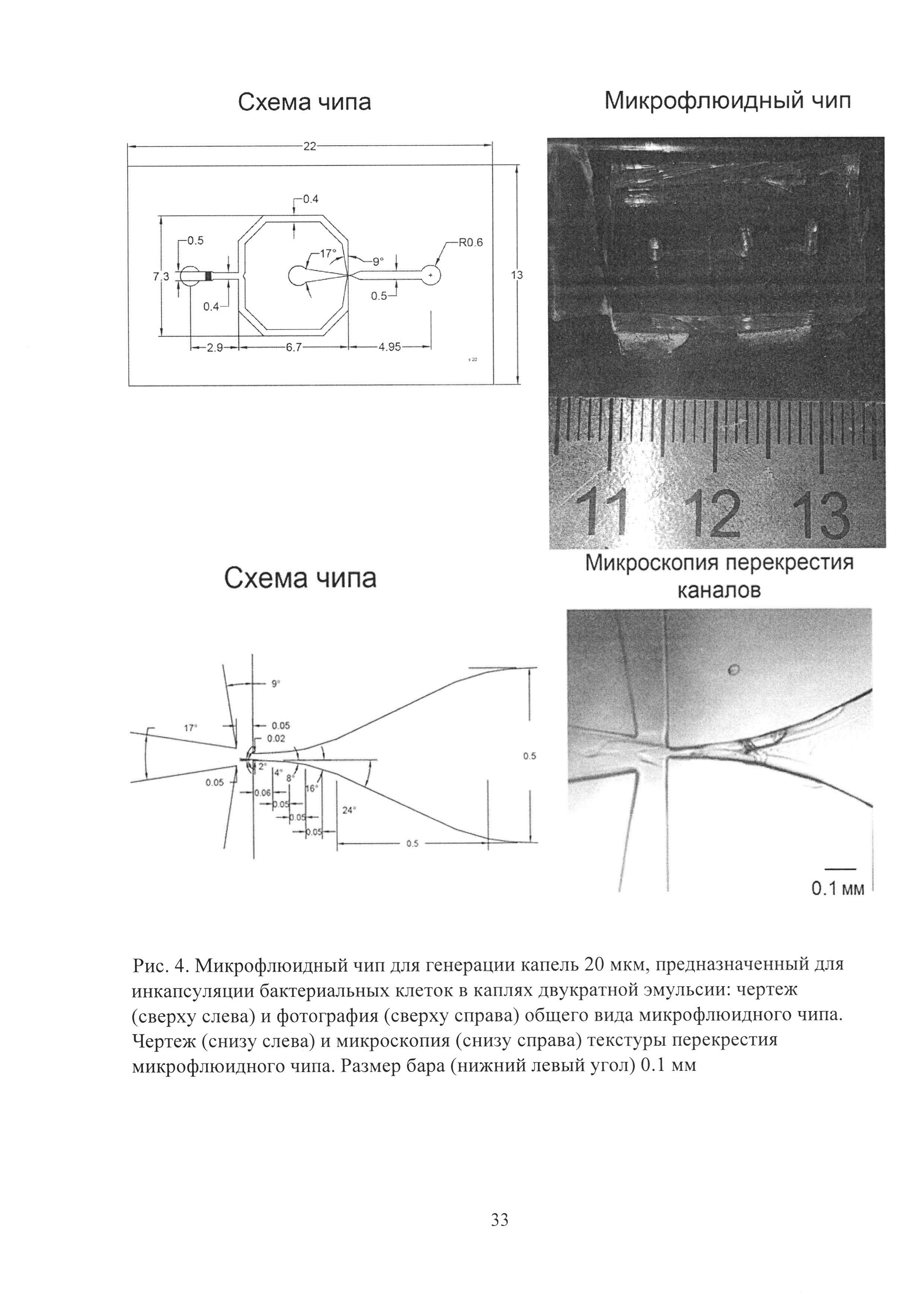
Рис. 4. Микрофлюидный чип для генерации капель 20 мкм, предназначенный для инкапсуляции бактериальных клеток в каплях двукратной эмульсии: чертеж (сверху слева) и фотография (сверху справа) общего вида микрофлюидного чипа. Чертеж (снизу слева) и микроскопия (снизу справа) текстуры перекрестия микрофлюидного чипа. Размер бара (нижний левый угол) 0.1 мм.
Рис. 5. Микрофлюидный чип для генерации капель 60 мкм, предназначенный для инкапсуляции бактериальных клеток в каплях двукратной эмульсии: чертеж (сверху слева) и фотография (сверху справа) общего вида микрофлюидного чипа. Чертеж (снизу слева) и микроскопия (снизу справа) текстуры перекрестия микрофлюидного чипа. Размер бара (нижний левый угол) 0.1 мм.
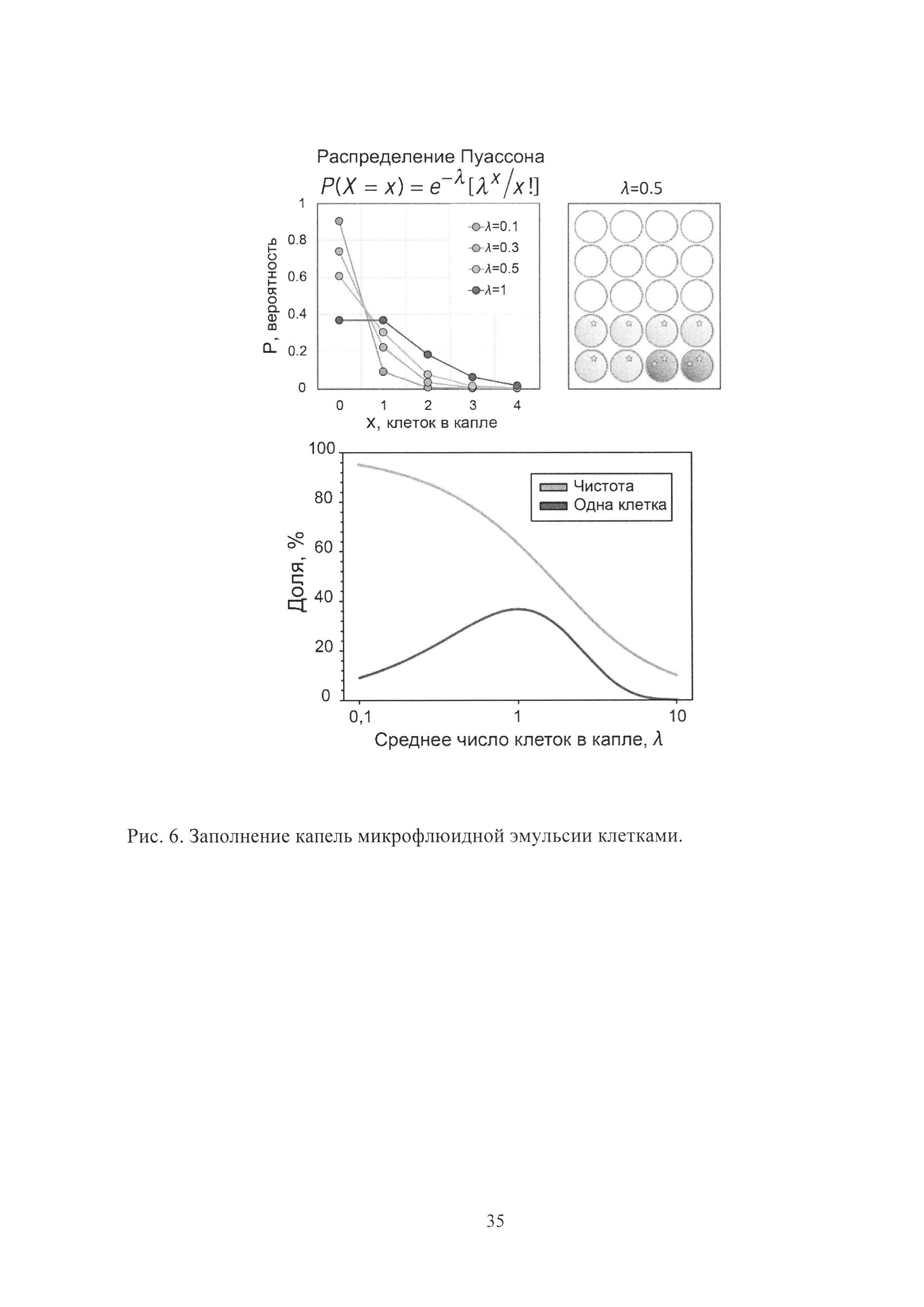
Рис. 6. Заполнение капель микрофлюидной эмульсии клетками.
Рис. 7. Дрожжевой дисплей биокатализаторов.
Рис. 8. Схемы и кинетические константы ферментативных реакций, использованных для скрининга биокатализаторов в каплях.
Рис. 9. Схема ультравысокопроизводительного скрининга биокатализаторов в каплях двойной эмульсии.
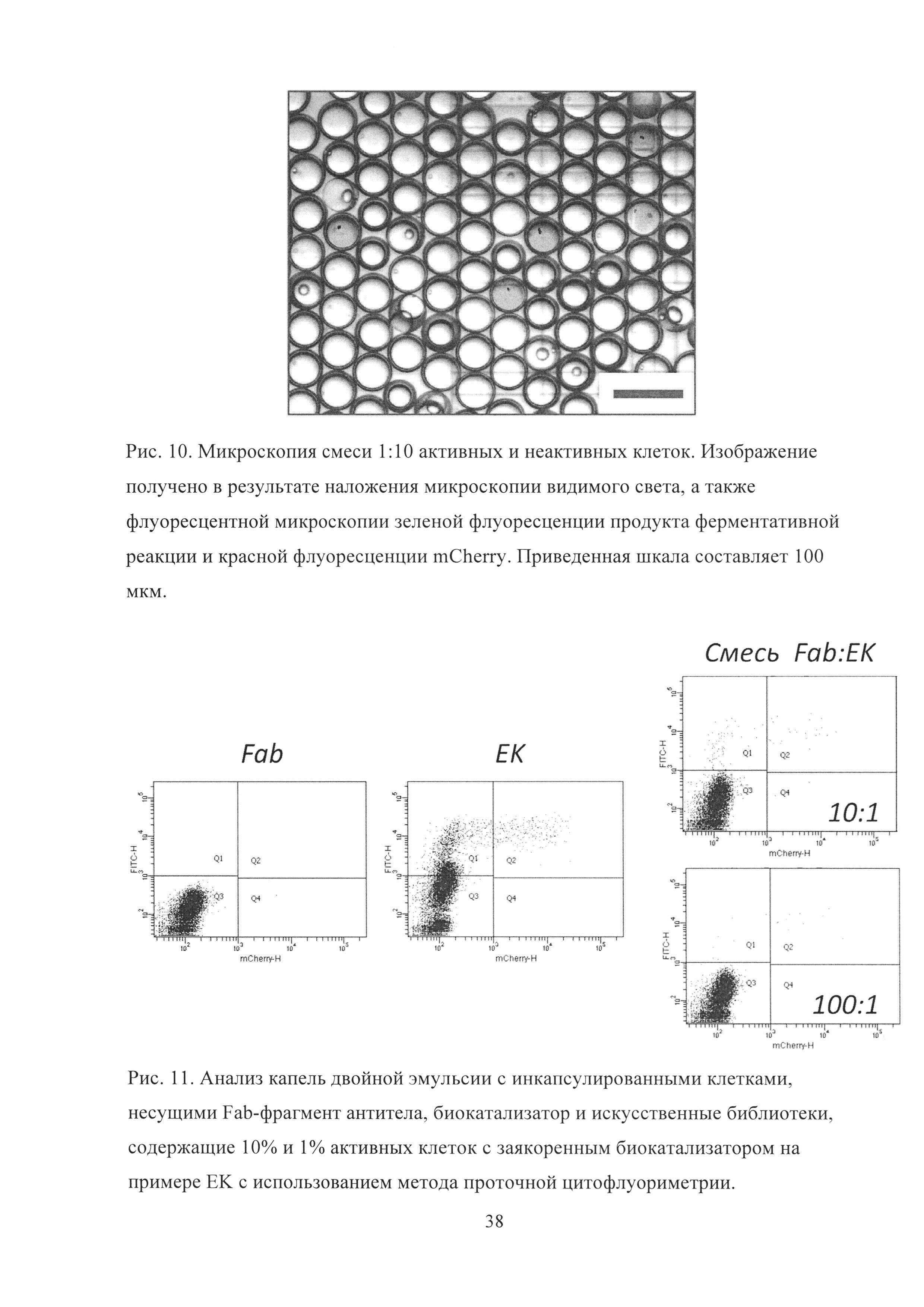
Рис. 10. Микроскопия смеси 1:10 активных и неактивных клеток. Изображение получено в результате наложения микроскопии видимого света, а также флуоресцентной микроскопии зеленой флуоресценции продукта ферментативной реакции и красной флуоресценции mCherry. Приведенная шкала составляет 100 мкм.
Рис. 11. Анализ капель двойной эмульсии с инкапсулированными клетками, несущими Fab-фрагмент антитела, биокатализатор и искусственные библиотеки, содержащие 10% и 1% активных клеток с заякоренным биокатализатором на примере ЕК с использованием метода проточной цитофлуориметрии.
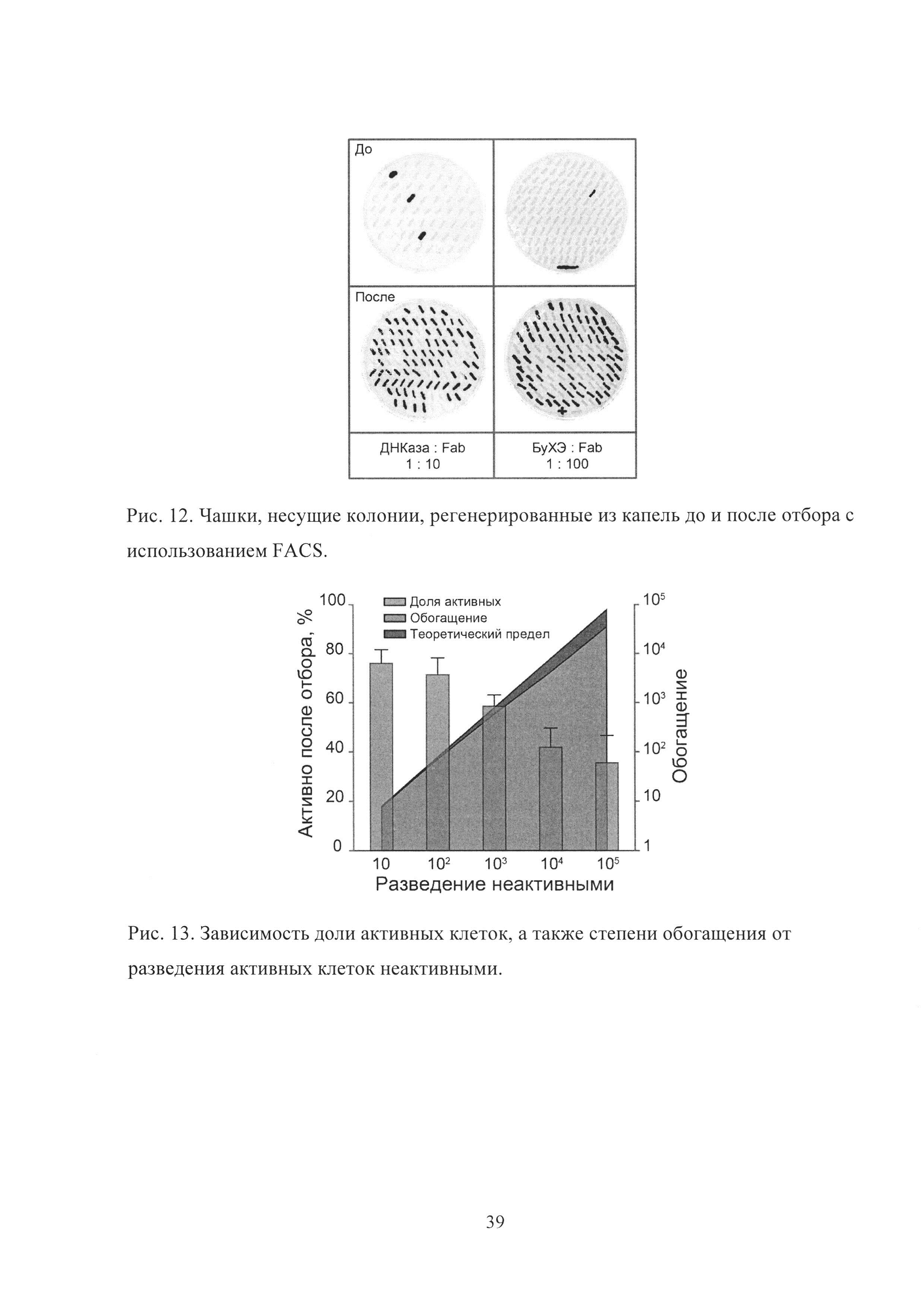
Рис. 12. Чашки, несущие колонии, регенерированные из капель до и после отбора с использованием FACS.
Рис. 13. Зависимость доли активных клеток, а также степени обогащения от разведения активных клеток неактивными.
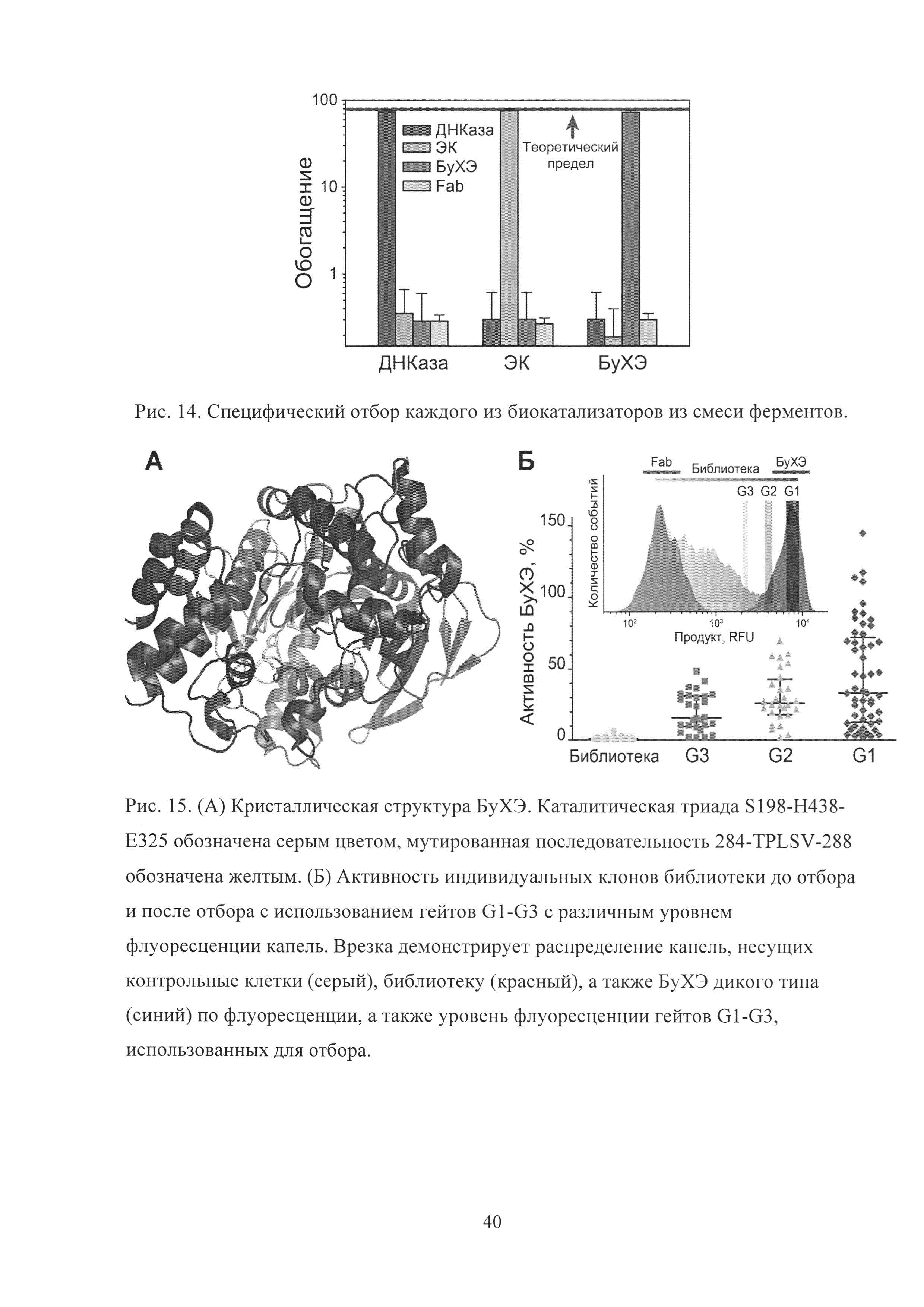
Рис. 14. Специфический отбор каждого из биокатализаторов из смеси ферментов.
Рис. 15. (А) Кристаллическая структура БуХЭ. Каталитическая триада S198-H438-Е325 обозначена серым цветом, мутированная последовательность 284-TPLSV-288 обозначена желтым. (Б) Активность индивидуальных клонов библиотеки до отбора и после отбора с использованием гейтов G1-G3 с различным уровнем флуоресценции капель. Врезка демонстрирует распределение капель, несущих контрольные клетки (серый), библиотеку (красный), а также БуХЭ дикого типа (синий) по флуоресценции, а также уровень флуоресценции гейтов G1-G3, использованных для отбора.
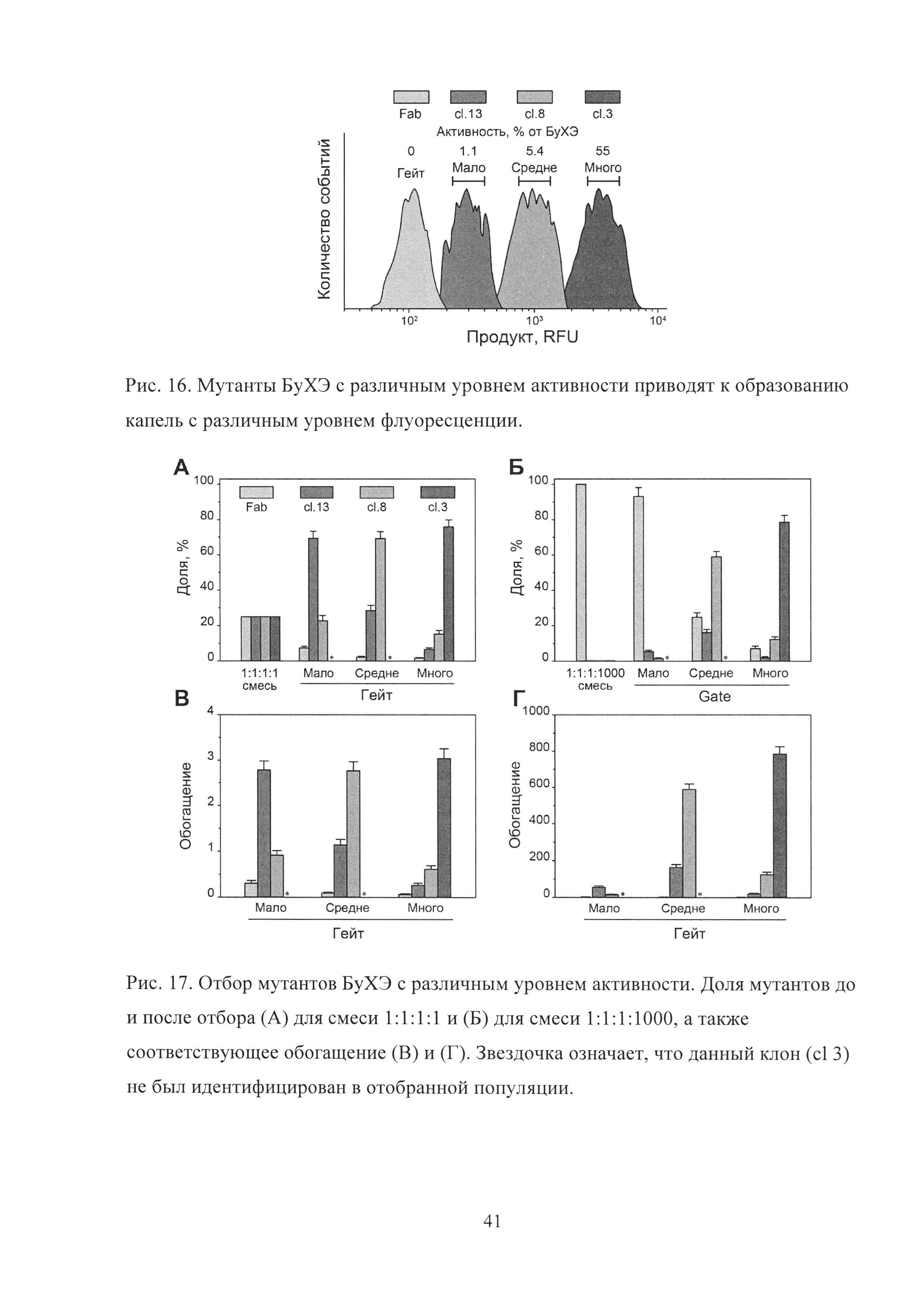
Рис. 16. Мутанты БуХЭ с различным уровнем активности приводят к образованию капель с различным уровнем флуоресценции.
Рис. 17. Отбор мутантов БуХЭ с различным уровнем активности. Доля мутантов до и после отбора (А) для смеси 1:1:1:1 и (Б) для смеси 1:1:1:1000, а также соответствующее обогащение (В) и (Г). Звездочка означает, что данный клон (cl 3) не был идентифицирован в отобранной популяции.
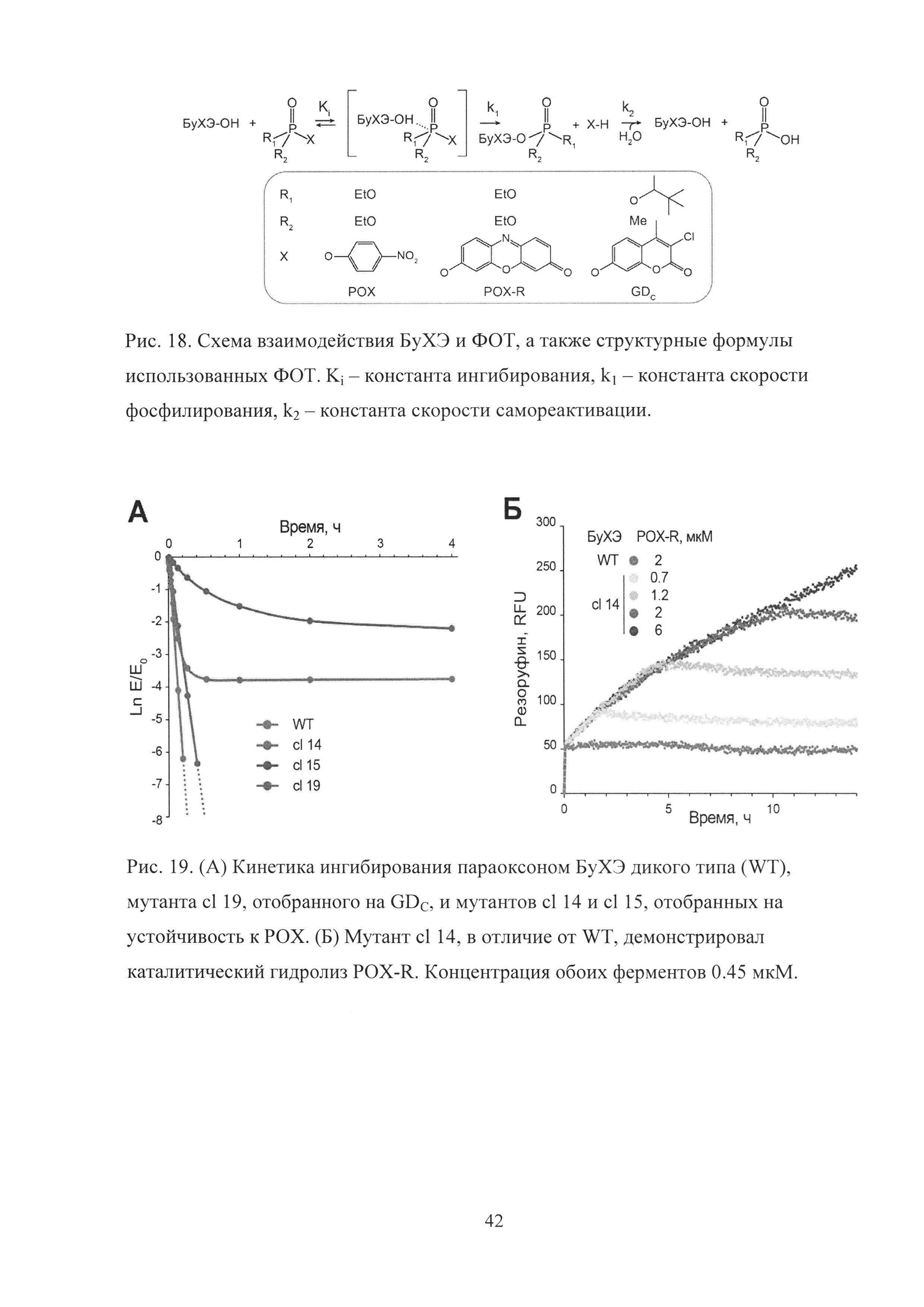
Рис. 18. Схема взаимодействия БуХЭ и ФОТ, а также структурные формулы использованных ФОТ. Кi - константа ингибирования, k1 - константа скорости фосфилирования, k2 - константа скорости самореактивации.
Рис. 19. (А) Кинетика ингибирования параоксоном БуХЭ дикого типа (WT), мутанта cl 19, отобранного на GDC, и мутантов cl 14 и cl 15, отобранных на устойчивость к РОХ. (Б) Мутант cl 14, в отличие от WT, демонстрировал каталитический гидролиз POX-R. Концентрация обоих ферментов 0.45 мкМ.
Рис. 20. (А) Схема скрининга попарных взаимодействий для отбора бактерий, ингибирующих рост S. aureus, в каплях биосовместимой двойной микрофлюидной эмульсии. (Б) Микроскопия капель, несущих смесь клеток S. aureus+S. venezuelae и S. aureus+E.coli. Изображения получены в результате микроскопии видимого света, флуоресцентной микроскопии зеленой флуоресценции S. aureus (жертва), красной флуоресценции S. venezuelae (эффектор слева) и дальне-красной флуоресценции Е. coli (эффектор справа), а также их общего наложения (перекрытие). Приведенная шкала составляет 100 мкм.
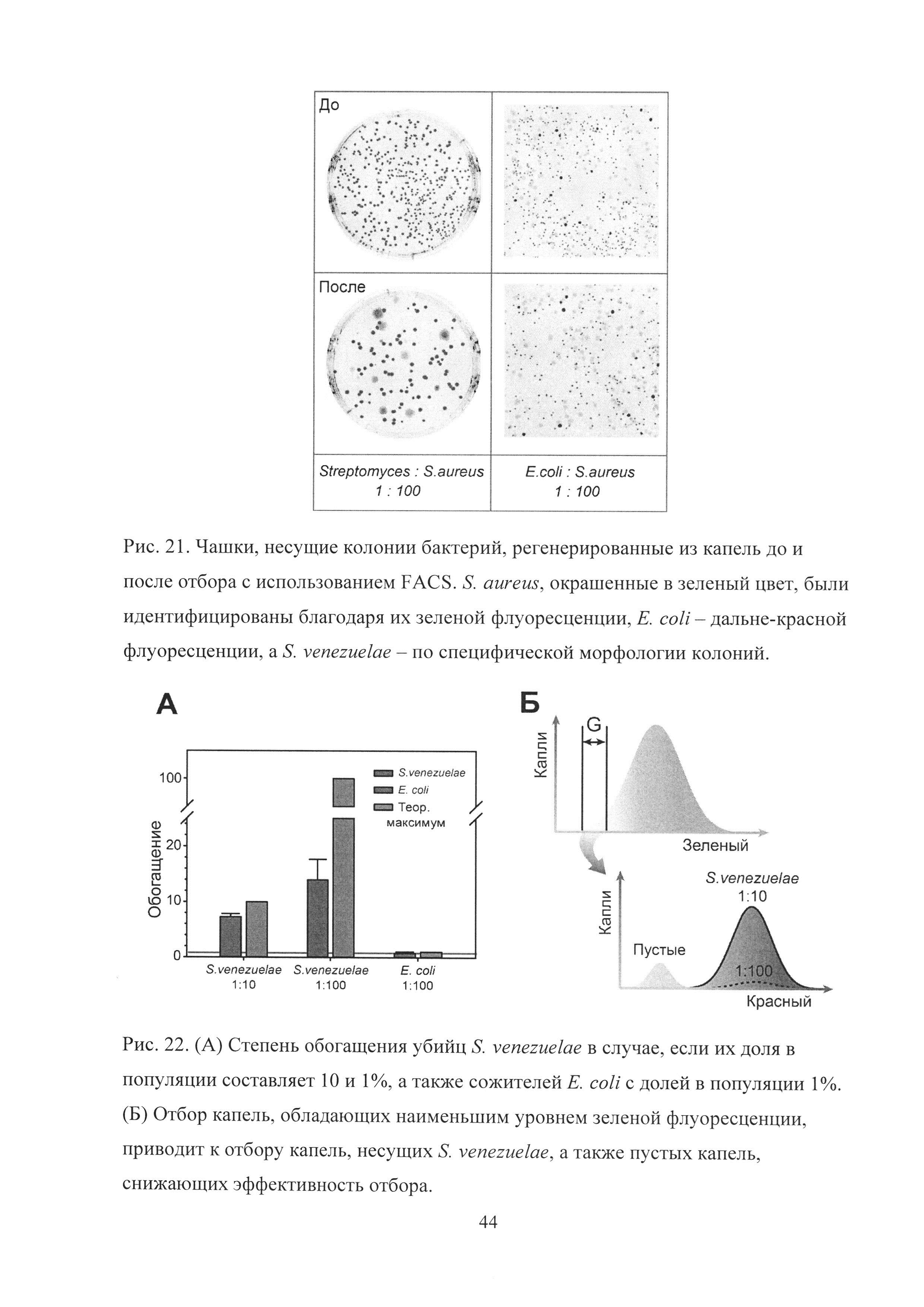
Рис. 21. Чашки, несущие колонии бактерий, регенерированные из капель до и после отбора с использованием FACS. S. aureus, окрашенные в зеленый цвет, были идентифицированы благодаря их зеленой флуоресценции, Е. coli - дальне-красной флуоресценции, a S. venezuelae - по специфической морфологии колоний.
Рис. 22. (А) Степень обогащения убийц S. venezuelae в случае, если их доля в популяции составляет 10 и 1%, а также сожителей Е. coli с долей в популяции 1%. (Б) Отбор капель, обладающих наименьшим уровнем зеленой флуоресценции, приводит к отбору капель, несущих S. venezuelae, а также пустых капель, снижающих эффективность отбора.
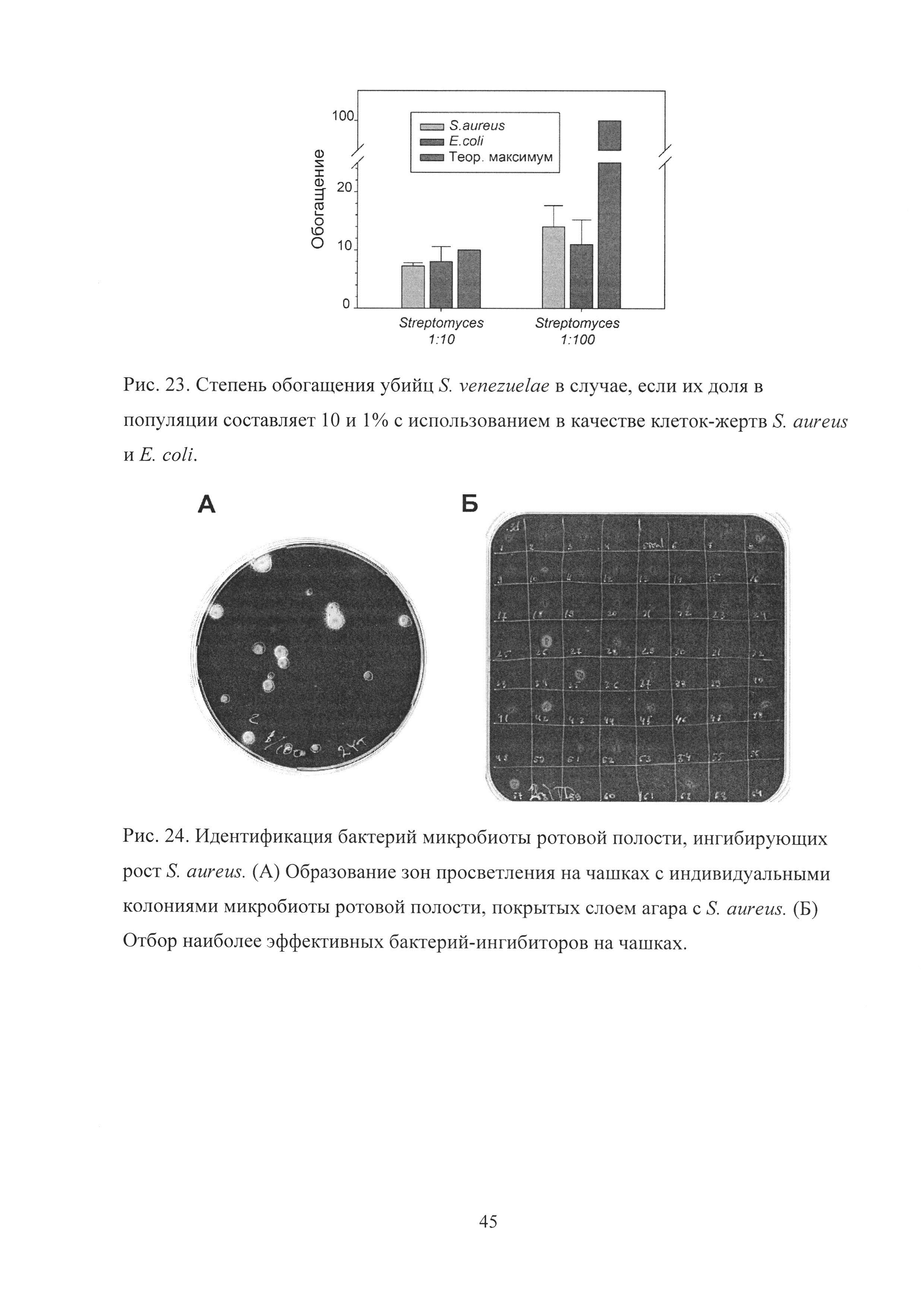
Рис. 23. Степень обогащения убийц S. venezuelae в случае, если их доля в популяции составляет 10 и 1% с использованием в качестве клеток-жертв S. aureus и Е. coli.
Рис. 24. Идентификация бактерий микробиоты ротовой полости, ингибирующих рост S. aureus. (А) Образование зон просветления на чашках с индивидуальными колониями микробиоты ротовой полости, покрытых слоем агара с S. aureus. (Б) Отбор наиболее эффективных бактерий-ингибиторов на чашках.
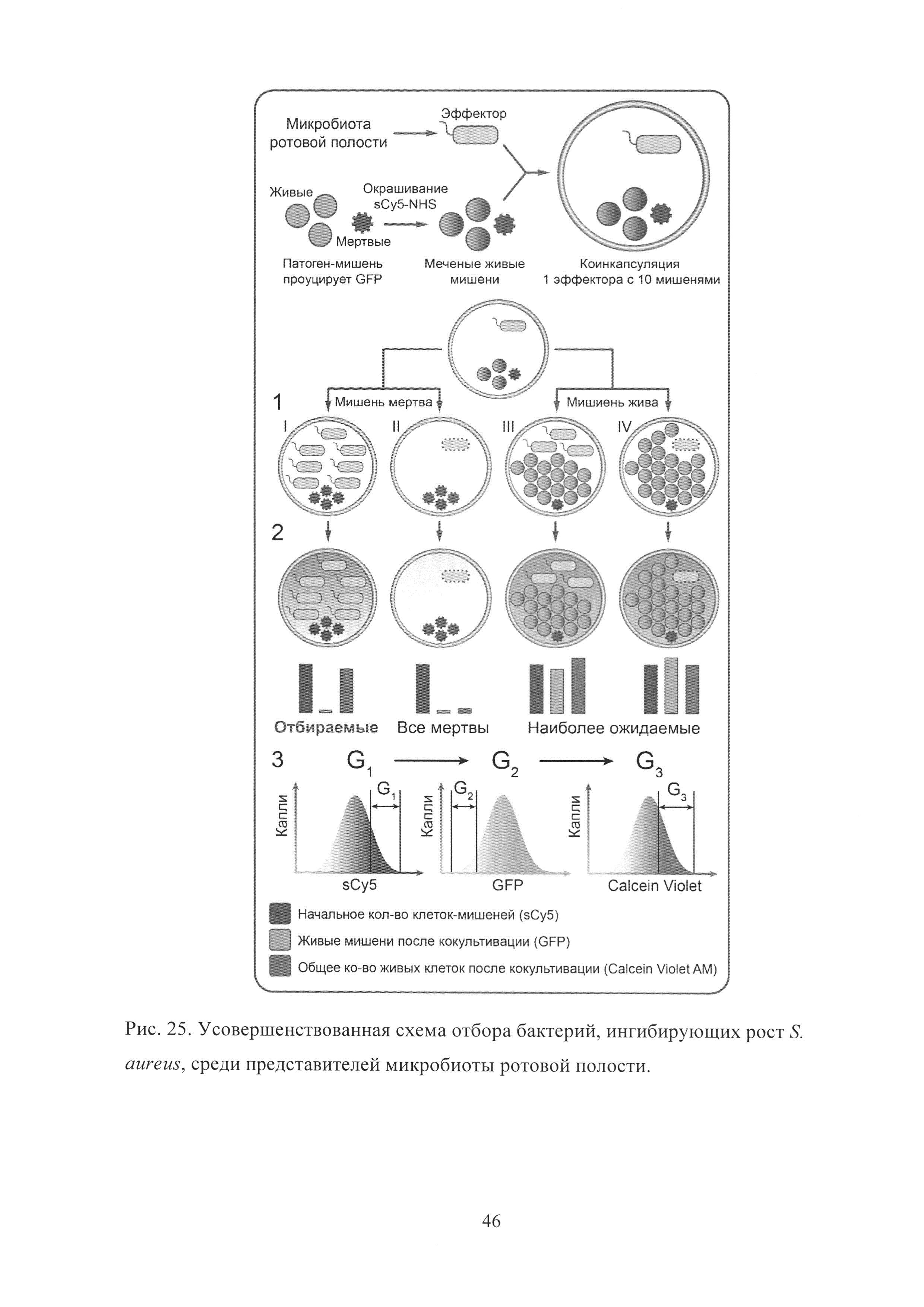
Рис. 25. Усовершенствованная схема отбора бактерий, ингибирующих рост S. aureus, среди представителей микробиоты ротовой полости.
Рис. 26. Предсказание родов бактерий, ингибирующих рост S. aureus, по результатам 16S рРНК секвенирования.
Рис. 27. Клоны стрептококков, отобранные с использованием микрофлюидной платформы (капли), демонстрировали значительно более эффективное ингибирование роста S. aureus, чем клоны, полученные с использованием платформы Ваксмана (чашки).
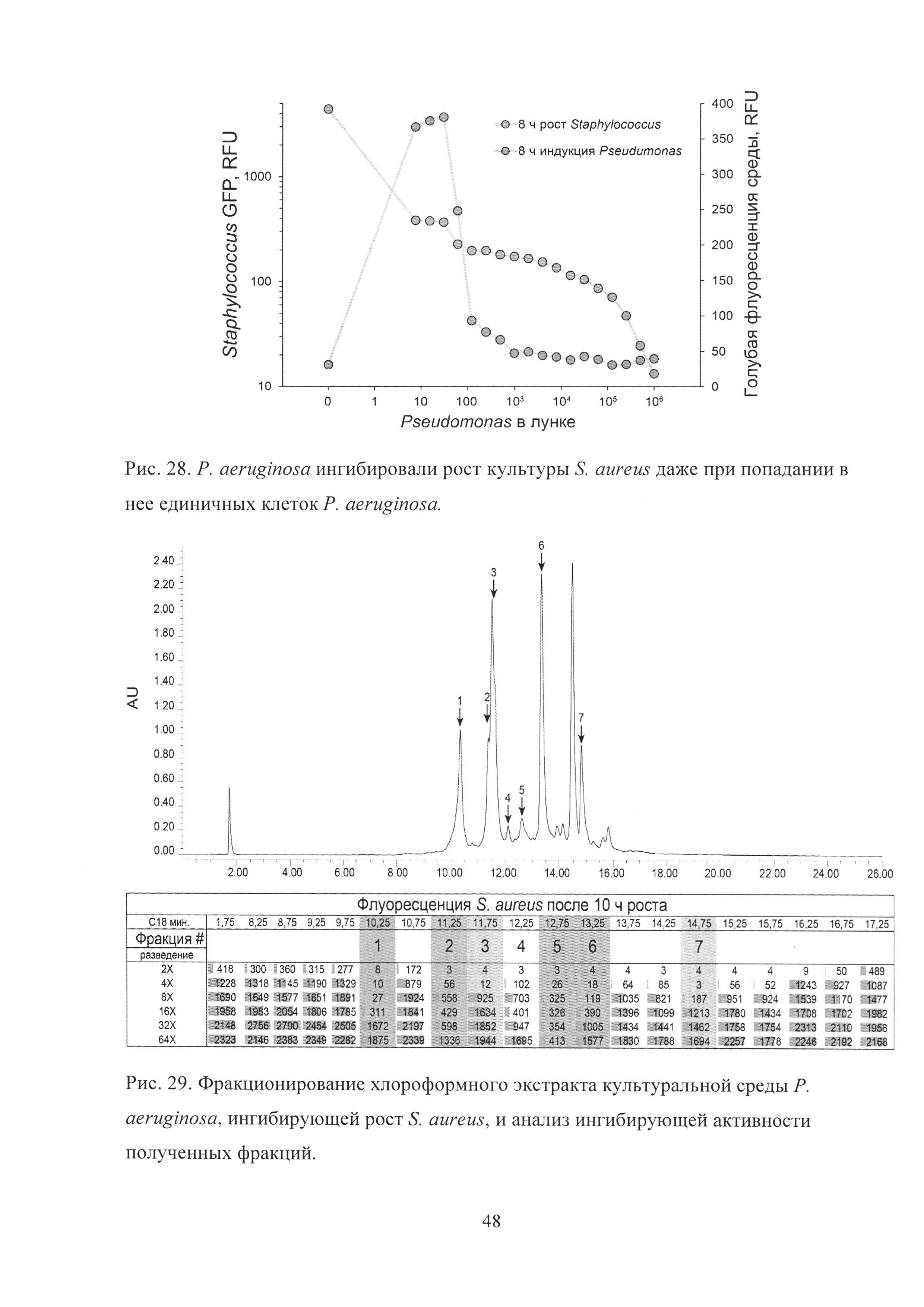
Рис. 28. P. aeruginosa ингибировали рост культуры S. aureus даже при попадании в нее единичных клеток P. aeruginosa.
Рис. 29. Фракционирование хлороформного экстракта культуральной среды Р. aeruginosa, ингибирующей рост S. aureus, и анализ ингибирующей активности полученных фракций.
Рис. 30. (А) Синергическое ингибирование роста S. aureus фракциями 1 и 6, полученными в результате фракционирования с использованием высокоэффективной обращенно-фазовой хроматографии. (Б) Основные действующие вещества фракций 1 и 6, идентифицированные с использованием масс-спектрометрии.
Подробное описание изобретения
Задачей изобретения является создание универсальной платформы для ультравысокопроизводительного скрининга с использованием принципа in vitro компартментализации в каплях двойной эмульсии. Для решения этой задачи был создан способ ультравысокопроизводительного скрининга биологических объектов, основанный на микрофлюидной генерации капель, что обеспечивает их монодисперсность. Монодисперсность эмульсии, в свою очередь, приводит к одинаковым концентрациям реагентов, а также одинаковым условиям проведения реакций в каплях, что позволяет многократно снизить соотношение «сигнал/шум» (signal/noise ratio) в процессе скрининга т.е. повысить чувствительность и специфичность отбора. Микрофлюидная генерация эмульсии позволяет обеспечить мягкие условия инкапсуляции, что позволяет, в свою очередь, использовать ее для живых клеток, а контролируемые условия генерации позволяют заключать в каплях эмульсии заданное количество клеток или других микроскопических биообъектов.
Для проведения скрининга в каплях микрофлюидной двойной эмульсии (Рис. 1) необходимо подобрать некий высоко специфический механизм, активируемый искомым фенотипом. Активированный механизм должен приводить к изменению флуоресценции, используемой в качестве аналитического сигнала. Микрофлюидная компартментализация библиотеки фенотипов вместе с механизмом в каплях биосовместимой двойной эмульсии вода-масло-вода приводит множеству индивидуальных микрокомпартментов, в которых может происходить активация механизма, приводящая к изменению флуоресценции. После этого фенотипы-активаторы подвергаются отбору с использованием флуоресцентно-активированного клеточного сортинга (FACS), после чего они могут быть проанализированы напрямую без культивации методом широкомасштабного секвенирования (что принципиально важно в случае некультивируемых и медленнорастущих микроорганизмов) или подвергнуты культивации. Культивируемые фенотипы-активаторы в последствии подвергаются генотипическому, фенотипическому, структурному и функциональному анализу.
Генерация двойной микрофлюидной эмульсии проводилась методом последовательной эмульсификации в микрофлюидных чипах (Рис. 2). Контроллер давления осуществлял подачу сжатого воздуха в 4 резервуара с жидкостями: водной фазой, несущей библиотеку фенотипов; водной фазой, несущей механизм; масляной фазой и внешней водной фазой. Давление сжатого воздуха вызывало течение жидкостей по тефлоновым трубочкам, ведущим в чип. Скорость течения жидкостей определялась контроллерами потока, соединенными петлей обратной связи с контроллером давления, таким образом, контроллер автоматически поддерживал заданную скорость потока за счет увеличения или уменьшения давления в резервуарах. Непосредственно перед входом в чип потоки водных фаз, несущих библиотеку фенотипов и механизм, соединялись и попадали в гидрофобизированный чип. В гидрофобном чипе поток объединенной внутренней водной фазы разбивался на отдельные капли в потоке масляной фазы, и полученная в результате однократная эмульсия вода/масло попадала в гидрофильный чип. В гидрофильном чипе поток эмульсии вода/масло разбивался на отдельные капли двойной эмульсии вода/масло/вода в потоке внешней водной фазы.
В качестве внутренней водной фазы могут быть использованы раствор фосфатносолевого буфера, трис-HCl, ионы двухвалентных металлов, ростовые среды. В качестве масляной фазы могут быть использованы минеральные масла с эмульсификатором 3% Abil ЕМ 180 или 2% Pico-Surf2 во фторуглеродном масле Novec7500. Внешняя водная фаза может содержать 50 мМ натрий или калий фосфатный буфер, 2%Pluronic и 0,1% Mowiol 23-88.
Поверхности каналов чипов должны иметь более высокую смачиваемость по отношению к дисперсионной среде, в противном случае генерация эмульсии нестабильна. Для химической модификации были использованы гидрофобизирующие реагенты (трихлороктадецилсилан или Aquapel), а для стабилизации гидрофильной поверхности был использован поливиниловый спирт. В качестве масляной фазы было использовано минеральное масло или фторуглеродное масло. Минеральное масло обладает высокой вязкостью, снижает транспорт газов и приводит к флотирующей эмульсии, что затрудняет его применение. В свою очередь фторуглеродные масла HFE-7500 и FC-40 обладали значительно меньшей вязкостью, что позволило использовать их для генерации двойной эмульсии диаметром 20 мкм. Высокая газопроницаемость фторуглеродных масел была использована для скрининга, совмещенного с культивацией, а высокая плотность приводила к образованию седиментирующей эмульсии, более удобной для отбора. Для того чтобы обеспечить биосовместимость эмульсии, были использованы высокомолекулярные поверхностно-активные вещества, обладающие чрезвычайно низкой способностью к межфазному транспорту: Abil ЕМ 180 для минерального масла, Pico-Surf 2 для фторуглеродного масла и Pluronic F-127 для внешней водной фазы. Разрушение отобранной после FACS эмульсии происходило за счет ее высыхания на чашке с питательной средой, что приводило к 90±20% выживаемости дрожжевых клеток.
Для микрофлюидной компартментализации были использованы микрофлюидные чипы из полидиметилсилоксана, полученные с использованием технологии мягкой литографии (Рис. 3). Использование двух чипов для однократной эмульсификации оказалось значительно технологичнее, чем одного чипа для генерации двойной эмульсии, ввиду их взаимозаменяемости и существенно более простой технологии химической модификации. Разбиение потока дисперсной фазы происходило в самом узком месте чипа, где встречались потоки несмешивающихся жидкостей. Использованные чипы имели размер каналов 20 мкм (Рис. 4) и 60 мкм (Рис. 5), что позволяло генерировать двойную микрофлюидную эмульсию диаметром 20-90 мкм. Уменьшение размеров каналов чипа приводит к увеличению производительности. Генерация микрофлюидной двойной эмульсии происходила с производительностью ≈25000 событий в секунду в чипе с размером каналов 20 мкм и ≈3000 событий в секунду в 60 мкм чипе.
Как уже упоминалось ранее, благодаря монодисперсности микрофлюидной эмульсии, заполнение ее капель дискретными объектами происходит в соответствии с распределением Пуассона (Рис. 6).
Таким образом, чем ниже степень заполнения λ, тем выше чистота отбора за счет снижения вероятности попадания двух и более клеток в одну каплю. В то же время при λ<0.3 доля заполненных капель стремительно падает, что снижает эффективность скрининга. Для λ=0.1 капли, несущие одну клетку, составляют 95.1% от общего числа заполненных капель, тем не менее 90.5% капель при этом остаются пустыми. Таким образом, для достижения компромисса между чистотой и эффективностью скрининга наиболее оптимальным является диапазон 0.3<λ<0.7. Для скрининга биокатализаторов была использована степень заполнения λ=0.5, что соответствует максимальной чистоте отбора 78.7%. С другой стороны, в том случае если требуется, чтобы все капли были заполнены (что было использовано для клеток S. aureus в случае отбора антибиотической активности), необходимо использовать λ>>1. Для λ=10, использованного для заполнения капель клетками S. aureus, доля пустых капель составляет <0.005%.
Скрининг биокаталитической активности в каплях микрофлюидной двойной эмульсии
Дрожжевой дисплей биокатализаторов и высокочувствительная детекция биокаталитической активности
Ранее для скрининга биокатализаторов в каплях за счет in vitro компартментализации использовались подходы, основанные на in vitro транскрипции/трансляции, лизисе индивидуальных бактериальных клеток в каплях, а также бактериальном и дрожжевом дисплее [8]. Из всех вышеупомянутых, дрожжевой дисплей представляет собой наиболее универсальный подход, так как позволяет обеспечить фолдинг сложных белков, образование правильных дисульфидных связей, а также обеспечить их гликозилирование, что было принципиально важно в случае рчБуХЭ, продукция которой в активном виде возможна исключительно в эукариотических клетках.
Для того, чтобы иметь возможность впоследствии легко идентифицировать клетки, обладающие активностью, мы использовали красный флуоресцентный белок-репортер mCherry, в то же время необходимо, чтобы количество mCherry и фермента коррелировали. Для этого их экспрессия проводилась с использованием одного промотора, а последовательности mCherry и фермента были разделены "самопроцессирующимся" F2A пептидом, обеспечивающим одновременную продукцию mCherry и фермента с использованием одного мРНК транскрипта за счет процесса "пропуска" (skipping) рибосомы. Таким образом, генетическая конструкция, использованная для дрожжевого дисплея биокатализаторов (Рис. 7А) содержала метанол-идуцибельный промотор алкогольоксидазы АОХ1, последовательность красного флуоресцентного белка-репортера mCherry, "самопроцессирующийся" F2A пептид, лидерный пептид человеческого сывороточного альбумина (ЧСА) для внеклеточного транспорта, фермент, эпитоп гемагглютинина (НА) для иммунофлуоресцентной детекции заякоренного фермента и последовательность SAG1, соединенную серин-глициновым линкером, обеспечивавшую заякоревание фермента на дрожжевой клетке.
Для демонстрации универсальности платформы были использованы три различных фермента демонстрирующие фосфодиэстеразную (дезоксирибонуклеаза I - ДНКаза), протеазную (энтеропептидаза - ЭК) и эстеразную (бутирилхолинэстераза - БуХЭ) активность (Рис. 7Б). Иммунофлуоресцентное окрашивание свидетельствовало о том, что все три фермента продуцировались в заякоренном виде (наблюдался ореол флуоресценции) на поверхности дрожжевых клеток. В то же время mCherry демонстрировал внутриклеточную локализацию (наблюдалась равномерная флуоресценция клеток). Дрожжи, продуцировавшие заякоренные ферменты, и контрольные дрожжи, продуцировавшие Fab-фрагмент антитела, были проанализированы на наличие биокаталитической активности с использованием соответствующих субстратов (реактива Эллмана в случае БуХЭ, Gly-(Аsp)4-Lys-нафтиламида в случае ЭК и FAM-AAAAAAACCCCCCCATATAGCGCGTTTTTTT-RTQ1 в случае ДНКазы) и было показано, что все биокатализаторы продуцировались в активном виде.
Для проведения скрининга в каплях необходимо, чтобы продукт ферментативной реакции обладал высокой гидрофильностью (что исключает его транспорт через слой масла во внешнюю водную фазу), а также спектром возбуждения/эмиссии флуоресценции, соответствующим возбуждающим лазерам и эмиссионным фильтрам клеточного сортера. Ввиду того, что дрожжи, несущие заякоренные ферменты, обладали красной флуоресценцией, для флуоресценции продукта был использован зеленый (530/30 нм) и голубой (450/50 нм) канал флуоресценции. Для трех ферментов были использованы разные флуорогенные субстраты (Рис. 8), действовавшие по принципу FRET-пары, нефлуоресцентного амида, и сопряженной реакции, в которой продукт классической реакции, катализируемой БуХЭ, вступал в реакцию с нефлуоресцентным субстратом с образованием флуоресцентного аддукта.
Ферменты обладали каталитической эффективностью по отношению к данным флуорогенным субстратам, различавшейся приблизительно в 100 раз. Для суспензии клеток, несущих заякоренный биокатализатор, соотношение скоростей ферментативного и самопроизвольного гидролиза составляло от 550 до 85, что через сутки инкубации приводило к соотношению сигнал/фон от 33 до 6.5 при проведении реакции в лунках 384 луночной плашки. Иммунофлуоресцентное окрашивание и цитофлуориметрия с использованием флуоресцентных шаров, несущих стандартное количество флуорофора, показали, что на поверхности одной дрожжевой клетки находится 7000±3000 молекул биокатализатора, что позволило оценить ферментативные константы заякоренных биокатализаторов. Эффективность отбора биокатализаторов из смеси активных и неактивных клеток.
Для оценки эффективности скрининга биокатализаторов были использованы искусственные смеси активных (продуцирующих заякоренный фермент и красный флуоресцентный белок-репортер mCherry) и неактивных (продуцирующих Fab-фрагмент антитела и не имеющих флуоресцентного репортера) дрожжевых клеток (Рис. 9).
Компартментализация смеси активных и неактивных клеток вместе с флуорогенным субстратом в каплях микрофлюидной двойной эмульсии приводила к образованию двух популяций с различным уровнем флуоресценции продукта. Отбор капель, обладавших наибольшим уровнем флуоресценции, с использованием FACS приводил к обогащению активными клетками. Микрофлюидная эмульсия обладала высокой монодисперсностью (Рис. 10), а накопление продукта реакции происходило исключительно в каплях, несущих активные дрожжевые клетки.
Для того, чтобы оценить эффективность отбора (степень обогащения) с использованием методики скрининга библиотек биокатализаторов методом проточной цитофлуориметриии с последующим сортингом (FACS) в эмульсионной системе вода-масло-вода для каждого биокатализатора был проведен модельный скрининг искусственных библиотек биокатализаторов. В одинаковых условиях производилась запаковка четырех образцов вместе с соответствующим флуорогенным субстратом: 1) дрожжи с заякоренным Fab-фрагментом антитела (капли в которых идет только фоновый уровень реакции), 2) дрожжи с заякоренным биокатализатором (капли в которых идет только каталитический гидролиз субстрата), 3) Смесь биокатализатор/Fab 1:10, 4) Смесь биокатализатор/Fab 1:100. После запаковки образец подвергался анализу и сортингу с использованием прибора BD FACSAria III (Рис. 11).
После протекания реакции в каплях с использованием FACS в режиме максимальной чистоты скрининга производился отбор популяции капель, обладавших высоким уровнем флуоресценции, с производительностью в диапазоне 10000-20000 событий в секунду. Отобранные капли высевались на чашки и через 2-3 дня наблюдалось образование дрожжевых колоний. Колонии, полученные из капель до и после отбора, перекалывались на чашки с метанолом, где происходила индукция экспрессии флуоресцентного репортера (Рис. 12). В результате наблюдалось эффективное обогащение каждого из биокатализаторов.
Для того чтобы определить, как эффективность скрининга зависит от соотношения активных и неактивных клеток, были проведены отборы биокатализаторов из смесей с различным соотношением активных и неактивных клеток в диапазоне 1:10-1:105 (Рис. 13).
Степень обогащения активных клеток из смеси с неактивными была близка к теоретическому пределу в случае разведений 1:10 и 1:100. Даже для разведения 1:105 наблюдалось более 35% активных клонов после одного раунда отбора, что всего в 2 раза меньше, чем теоретический максимум.
Таким образом, для клеток, обладающих биокаталитической активностью, была показана чрезвычайно высокая эффективность отбора из смеси активных и неактивных клеток с использованием лишь одного раунда скрининга. Селективность отбора биокатализаторов из смеси биокатализаторов с разной специфичностью или различным уровнем активности.
Для проведения скрининга биокатализаторов из смеси с различной субстратной специфичностью мы использовали "искусственную библиотеку активностей", представляющую собой смесь дрожжей, несущих по отдельности каждый из трех использованных ранее биокатализаторов, разведенную в 100 раз неактивными клетками. Таким образом, доля клеток каждого типа активности составляла менее 1% в смеси. "Библиотека активностей" была отобрана на каждый тип активности отдельно с использованием соответствующего флуорогенного субстрата (Рис. 14).
Каждый из типов биокаталитической активности был селективно отобран на заданную ферментативную активность с эффективностью, близкой к теоретическому максимуму, без обогащения клетками, несущими другой тип активности.
Для того чтобы изучить как эффективность и селективность отбора зависит от активности биокатализатора, была использована библиотека БуХЭ. Библиотека имела представительность порядка 3×105 вариантов и содержала 5 подряд идущих аминокислотных замен в последовательности БуХЭ дикого типа (WT) 284-TPLSV-288 ацил-связывающей петли, расположенной недалеко от активного центра фермента (Рис.15А). Введение аминокислотных замен существенно снизило активность клонов. Средняя активность библиотеки составляла менее 0.5% от активности БуХЭ дикого типа. Дрожжи, несущие заякоренные мутанты БуХЭ, были инкапсулированы вместе с флуорогенным субстратом в каплях микрофлюидной двойной эмульсии. Полученные в результате капли обладали различным уровнем флуоресценции и были отобраны с использованием трех гейтов G1-G3 с различным уровнем флуоресценции G1>G2>G3 (Рис. 15Б).
Анализ активности индивидуальных клонов, полученных до и после отбора, свидетельствует об эффективности отбора в случае использования каждого из трех гейтов. В то же время клоны, отобранные из капель с наибольшим уровнем флуоресценции, обладали наибольшим уровнем активности. Таким образом, было качественно показано, что разработанная платформа может быть использована для отбора биокатализаторов с разным уровнем одинаковой активности.
Для того чтобы количественно оценить эффективность отбора биокатализаторов с различным уровнем одинаковой активности, были использованы три клона с различным уровнем ферментативной активности, отобранных с помощью гейтов G1-G3. Сl 13, отобранный из G3, обладал незначительным уровнем активности (1.1% от БуХЭ дикого типа), демонстрировав приблизительно в 2 раза большую активность в 384 луночной плашке по сравнению с контрольными клетками. Сl 8 и cl 3 были отобраны из G2 и G1 соответственно и обладали 5.4 и 55% от активности БуХЭ дикого типа. Компартментализация cl 3, cl 8, cl 13 и контрольных клеток вместе с субстратом в каплях приводила к образованию четырех популяций с разным уровнем флуоресценции, соответствовавших разным уровням накопления продукта: сумного, cl 8 - средне, cl 13 - мало (Рис. 16).
Мутанты БуХЭ cl 3, cl 8 и cl 13, а также контрольные клетки (Fab) были смешаны друг с другом в равном соотношении и в соотношении 1:1:1:1000 и отобраны с использованием гейтов «Много», «Средне», «Мало» (Рис. 16), соответствовавших высокой, средней и низкой флуоресценции продукта. Для соотношения 1:1:1:1 мы наблюдали специфическое обогащение каждого из мутантов БуХЭ с эффективностью, близкой к теоретическому максимуму (Рис.17А, В). В то же время в случае соотношения 1:1:1:1000 обогащение cl 3, cl 8 также происходило с эффективностью, близкой к максимальной, в то время как эффективность обогащения cl 13 была приблизительно на порядок ниже (Рис. 17 Б, Г).
Таким образом, концентрация клеток, обладающих в 384 луночной плашке активностью в 2 раза выше, чем у контрольных клеток, должна быть не менее 0.1%, чтобы они могли быть отобраны за 1 раунд скрининга. В то же время в случае клеток, обладающих более чем в 5 раз большей активностью по сравнению с контролем, эффективный отбор за 1 раунд скрининга возможен даже в том случае, если их популяция составляет менее 0.1%. В случае высокоактивных ферментов ДНКазы, ЭК и БуХЭ дикого типа, доля активных клеток может составлять менее 0.001%. Следует также отметить, что отбор капель, обладающих средней и низкой флуоресценцией, приводит к высокоэффективному исключению высокоактивного cl 3, что может быть использовано для идентификации мутаций, приводящих к потере активности.
Создание новых биокатализаторов с заданной активностью с использованием способа ультравысокопроизводительного скрининга
Для отбора мутантов БуХЭ, устойчивых к действию ФОТ, была использована описанная ранее библиотека БуХЭ. Дрожжевые клетки, несущие мутанты БуХЭ, инкубировались с ФОТ параоксоном (РОХ) или кумариновым аналогом зомана (GDC) после чего отмывались от избытка ФОТ и подвергались скринингу на наличие остаточной активности БуХЭ. После 1 раунда скрининга были отобраны два мутанта, демонстрировавших устойчивость к ингибированию POX (cl 14 и cl 15), и шесть мутантов (5 копий мутанта cl 19 и одна cl 14) с повышенной устойчивостью к GDC. Для того чтобы определить, чем обусловлена наблюдаемая устойчивость, эти мутанты были секвенированы и были получены в чистом виде в клетках млекопитающих линии FreeStyle™ 293-F для проведения кинетических исследований.
Взаимодействие БуХЭ дикого типа и ФОТ (Рис. 18) приводит к быстрой (с высокой бимолекулярной константой скорости k1/Ki) и необратимой (k2≈0) инактивации БуХЭ за счет фосфилирования S198 в активном центре.
В отличие от БуХЭ дикого типа (WT), cl 14 и cl 15 демонстрировали наличие остаточной активности даже в случае продолжительного ингибирования РОХ (Рис. 19А). Более того, в отличие от WT, cl 14 и cl 15 демонстрировали каталитический гидролиз ФОТ, который был идентифицирован с использованием флуоресцентного аналога POX-R (Рис. 19Б). После быстрой стадии ковалентной модификации cl 14 и WT, приводящей к выделению стехиометрического количества резоруфина, WT остается полностью модифицированным в то время как cl 14 продолжает медленно реагировать с новыми молекулами POX-R, что в итоге приводит к полному гидролизу POX-R. Таким образом, мутанты cl 14 и cl 15 приобретали новую параоксоназную каталитическую активность за счет возникновения самореактивации (k2>0).
В отличие от cl 14, обладавшего высокой реакционноспособностью по отношению к РОХ, сопоставимой с WT, cl 15, также демонстрировавший каталитический гидролиз POX-R, обладал значительно более низкой скоростью взаимодействия с РОХ (Таблица 1).


Мутанты, отобранные на устойчивость к GDC, не обладали каталитическим гидролизом GDc, что, по-видимому, было связано с чрезвычайно быстрым старением аддуктов зомана (τ1/2<1 минуты) по сравнению с РОХ (t1/2=8.6 часов), наблюдаемым для WT чБуХЭ. В свою очередь возникновение повышенной устойчивости мутанта cl 19, отобранного на устойчивость к GDC, была связана с более чем 60 кратным снижением реакционноспособности по отношению к GDC.
Таким образом, в результате скрининга относительно небольшого разнообразия мутантов БуХЭ, за один раунд отбора из библиотеки представительностью порядка 3×105, были отобраны варианты фермента, демонстрировавшие значительно более высокую устойчивость по отношению к ингибированию ФОТ. Причем в случае РОХ были de novo созданы мутанты БуХЭ, обладающие новой каталитической активностью. В результате были получены новые каталитические антидоты на основе стехиометрического антидота БуХЭ. Скрининг антибактериальной активности в каплях микрофлюидной двойной эмульсии.
Создание модельной системы для изучения попарных взаимодействий микроорганизмов
Одним из наиболее привлекательных преимуществ разработанной платформы является ее биосовместимость, позволяющая осуществлять культивацию микроорганизмов в каплях микрофлюидной двойной эмульсии. Для изучения попарных межклеточных взаимодействий микроорганизмов в каплях была разработана простая модельная система, имитирующая взаимодействия между тремя различными видами бактерий, игравших роль "жертвы", "убийцы" и "сожителя" (Рис. 20А). Разработанная схема была использована для отбора бактерий-продуцентов антибиотиков, ингибировавших рост патогенных бактерий Staphylococcus aureus. Штамм S. aureus, конститутивно продуцирующий зеленый флуоресцентный белок-репортер, был использован в качестве "жертвы". Бактерии Streptomyces venezuelae, продуцирующие антибиотик хрорамфеникол и ингибировавшие рост S. aureus, были выбраны в качестве "убийцы". S. venezuelae продуцировали широкий спектр вторичных метаболитов, в том числе продигнины, обладавшие красной флуоресценцией, что было использовано для идентификации их наличия в каплях. В качестве нейтрального "сожителя", не ингибировавшего рост S. aureus, были использованы клетки Е. coli, продуцировавшие дальне-красный флуоресцентный белок-репортер Katushka2S.
Таким образом, в том случае, если в одну каплю попадали клетки S. aureus и S. venezuelae, S. venezuelae ингибировали рост S. aureus и заполняли собой весь объем капли, что приводило к образованию капли, обладавшей высоким уровнем красной и низким уровнем зеленой флуоресценции. В том случае, если в каплю попадали только клетки S. aureus, они делились неконтролируемо, что приводило к образованию капли с интенсивной зеленой флуоресценцией. Если же в каплю одновременно попадали клетки S. aureus и Е. coli обе бактерии делились, что приводило к каплям с высоким уровнем зеленой и дальне-красной флуоресценции. После кокультивации в каплях отбор капель с наименьшим уровнем зеленой флуоресценции приводил к обогащению S. venezuelae, а не Е. coli.
Ожидаемая картина наблюдалась в каплях (Рис. 20Б). В результате совместной коинкапсуляции клеток S. aureus+S. venezuelae капли, в которые попадали клетки S. venezuelae, обладали интенсивной красной флуоресценцией и в то же время не обладали зеленой флуоресценцией. Большинство капель, не обладавших красной флуоресценцией, обладали при этом интенсивной зеленой флуоресценцией. Напротив, в результате совместной коинкапсуляции клеток S. aureus+E. coli, капли, в которые попадали клетки Е. coli, обладали одновременно интенсивной дальне-красной и зеленой флуоресценцией.
Последующий высокопроизводительный отбор капель с наименьшим уровнем зеленой флуоресценции с использованием FACS приводил к обогащению S. venezuelae, но не приводил к обогащению Е. coli, что было идентифицировано в результате культивации отобранных капель и капель до отбора на чашках (Рис. 21).
В то же время, по сравнению с отбором биокатализаторов, осуществляемого по принципу позитивной селекции (отбора капель с наибольшим уровнем флуоресценции), негативный отбор наименее флуоресцентных капель приводил к значительно более низкой степени обогащения (Рис. 22А).
В случае позитивной селекции эффективный отбор активных клеток наблюдался даже при их доле в популяции 0.001%. В случае негативной селекции наблюдалось обогащение убийц, а не сожителей. В то же время отбор убийц с эффективностью, близкой к теоретическому максимуму, происходил лишь в случае, если их доля в популяции была больше 10%. В том случае, если доля S. venezuelae составляла менее 1%, эффективность обогащения стремительно падала. Наблюдаемое падение эффективности отбора связано с наличием популяции пустых капель, а также капель, в которых не происходило деления S. aureus из-за их перехода в состояние персистенции или гибели (Рис. 22Б).
Для того чтобы показать, что возможности данной платформы не ограничены использованием именно клеток S. aureus в качестве жертвы, были использованы клетки Е. coli. Используя Е. coli, чей рост также ингибировался S. venezuelae, было показано, что и в этом случае негативный отбор приводит к низкой эффективности обогащения S. venezuelae, если их доля в популяции составляет менее 1% (Рис. 23).
Полученные результаты свидетельствуют о том, что для проведения высокоэффективного скрининга, основанного на негативной селекции популяции клеток-эффекторов с долей менее 1%, необходимо наличие дополнительных флуоресцентных репортеров, основанных на позитивной селекции. Скрининг представителей микробиоты ротовой полости, ингибирующих рост S. aureus.
Несмотря на свою чрезвычайно высокую патогенность, S. aureus достаточно редко ассоциирован с дентоальвеолярными инфекциями, что позволяет сделать предположение о наличии неких неизвестных естественных эффекторов микробиоты ротовой полости, ингибирующих рост S. aureus. Использование классических бактериологических подходов скрининга на чашках (так называемой платформы Ваксмана) показало наличие в ротовой полости бактерий, ингибирующих рост S. aureus (Рис. 24А).
Отобранные клоны-ингибиторы демонстрировали разный размер зон просветления (Рис. 24Б). Клоны с наиболее яркими зонами наибольшего диаметра были использованы для дальнейшей работы.
В отличие от классической платформы Ваксмана, разработанная микрофлюидная платформа позволяет осуществлять скрининг значительно большего биологического разнообразия, что было использовано для отбора бактерий, ингибирующих рост S. aureus, среди представителей микробиоты ротовой полости. Для этого разработанная ранее схема скрининга попарных взаимодействий в каплях была модифицирована двумя дополнительными флуоресцентными сигналами-репортерами, позволяющими избежать проблемы, связанной с отбором пустых капель и капель с изначально низким количеством клеток S. aureus (Рис. 25).
Клетки микробиоты ротовой полости подвергались микрофлюидной компартментализации вместе с избытком клеток S. aureus, прижизненно меченых красным флуоресцентным красителем сульфоцианином5 (sCy5). Кокультивация S. aureus и эффекторов микробиоты приводила к четырем различным вариантам I-IV. I - эффектор ингибировал рост S. aureus и оставался живым в процессе кокультивации. II - эффектор и S. aureus погибали. III - эффектор и S. aureus сожительствовали в капле и не ингибировали рост друг друга. IV - S. aureus ингибировал рост эффектора. Для того чтобы различить эти варианты, был использован лейко-краситель Calcein Violet AM, представляющий собой нефлуоресцирующий гидрофобный ацетоксиметильный эфир, способный проникать через слой масла. В случае наличия в капле живых клеток, их эстеразы гидролизуют ацетоксиметильный эфир, что в свою очередь приводит к образованию высокогидрофильного продукта, обладающего интенсивной голубой флуоресценцией, неспособного к транспорту через гидрофобный слой масла. Таким образом, отбор популяции капель, обладающих высоким уровнем красной, низким уровнем зеленой и высоким уровнем голубой флуоресценции, приводит к отбору капель с высокой изначальной загрузкой клетками S. aureus, которые не делились в каплях, в то же время в каплях присутствовали другие живые клетки, отличные от S. aureus.
Так как различные виды бактерий обладают разной скоростью роста и могут ингибировать рост друг друга на чашках, отобранные капли напрямую подвергались 16S рРНК и полногеномному (WGA) широкомасштабному секвенированию с целью идентификации медленнорастущих и некультивируемых бактерий, ингибировавших рост S. aureus в каплях. Сравнение количества прочтений до и после отбора показало, что, как по результатам 16S рРНК (Рис. 26), так и полногеномного секвенирования, Propionibacterium acnes обладали наибольшим обогащением среди всех бактерий.
16S рРНК секвенирование позволило выявить две субпопуляции бактерий-ингибиторов, отобранных с различной эффективностью. Бактерии родов Propionibacterium, Stenotrophomonas, Sphingomonas, Pseudomonas, и Escherichia обладали наивысшим уровнем обогащения, в то время как Corynebacterium, Janthinobacterium, Serratia, Enterobacter и Streptococcus были также достоверно обогащены с более низкой степенью обогащения. Streptococcus представляли при этом популяцию наиболее распространенных ингибиторов S. aureus среди представителей микробиоты ротовой полости. Полногеномное секвенирование подтвердило чрезвычайно эффективное обогащение медленно растущих Propionibacterium acnes, также позволив идентифицировать некоторых бактерий-ингибиторов с точностью до вида. Группа Streptococcus mitis (S. pneumoniae, S. mitis, S. oralis и S. pseudopneumoniae), Prevotella dentalis (медленно растущий вид), Staphylococcus epidermidis (известный эффектор S. aureus) и Pseudomonas aeruginosa были значительно обогащены после отбора.
Отобранные капли подвергались культивации с целью идентификации культивируемых бактерий-ингибиторов S. aureus. Более 90% бактериальных колоний, отличных от S. aureus, регенерированных из капель на чашках, принадлежали роду Streptococcus и более 64% из них были классифицированы при помощи масс-спектрометрии как Streptococcus oralis. Отобранные клоны в процессе роста продуцировали в ростовую среду метаболиты, ингибировавшие рост S. aureus, причем Streptococcus oralis демонстрировали наибольшее ингибирующее разведение ростовой среды (вплоть до 16 кратного разведения). Анализ клонов-ингибиторов, полученных с использованием классического скрининга на чашках, и клонов, полученных в результате отбора с использованием капель, показал, что клоны, полученные с использованием капель, обладали значительно большим ингибирующим разведением ростовой среды, чем клоны, полученные с использованием чашек (Рис. 27).
Кокультивация разбавленной (<106 КОЕ/мл) культуры Streptococcus oralis и S. aureus, тем не менее, не приводила к ингибированию роста S. aureus, что, по-видимому, связано со значительно более быстрой кинетикой роста S. aureus. В то же время физиологическая значимость Streptococcus oralis может быть весьма высокой, и реальная картина может значительно отличаться от того, что наблюдалось при кокультивации в разбавленной культуре, так как слюна является значительно более бедной ростовой средой, а локальные концентрации стрептококков на поверхности десен значительно выше, чем те, что были использованы в жидкой культуре. Кроме того, на чашках наблюдалось эффективное ингибирование S. aureus, что также свидетельствует в пользу того, что стрептококки, в частности Streptococcus oralis, могут играть важную физиологическую роль защитного барьера, препятствующего колонизации S. aureus.
Исключительно с использованием микрофлюидной платформы был отобран штамм Pseudomonas aeruginosa, полностью ингибировавший рост S. aureus в культуре даже при попадании единичных клеток P. aeruginosa (Рис. 28). Условно патогенные P. aeruginosa не являются нормальным компонентом микрофлоры ротовой полости и могли присутствовать среди представителей микробиоты ротовой полости лишь в концентрации <0.005%, что делало их отбор с использованием классической платформы Ваксмана практически невозможным.
В отличие от S. oralis, P. aeruginosa продуцировали вторичные метаболиты, ингибирующие рост S. aureus, не конститутивно, а индуцибельно в процессе кокультивации со S. aureus, причем максимальный уровень индукции соответствовал минимальной концентрации P. aeruginosa в ростовой среде при кокультивации (Рис. 28) и коррелировал с голубой флуоресценцией пиовердина. В то же время ингибирование роста S. aureus происходило не за счет пиовердина, так как после экстракции хлороформом водная фаза (содержащая пиовердин) полностью теряла ингибирующую активность, а хлороформный экстракт, напротив, практически полностью приобретал ее.
Хлороформный экстракт ростовой среды P. aeruginosa, ингибировавшей рост S. aureus и полученной в результате кокультивации избытка S. aureus (108КОЕ/мл) и P. aeruginosa (≈1 КОЕ/мл), был фракционирован с использованием высокоэффективной обращенно-фазовой хроматографии (Рис. 29). P. aeruginosa продуцировали широкий спектр вторичных метаболитов, ингибировавших рост S. aureus.
Фракции 1 и 6 демонстрировали высокоэффективное синергическое ингибирование, приводившее к гибели S. aureus (Рис. 30А). Основными действующими веществами, идентифицированными с помощью масс-спектрометрии (Рис. 30Б), были пиоцианин и феназин-1-карбоновая кислота (фракция 1) и 2-гептил-4-гидроксихинолин N-оксид (фракция 6). Пиоцианин и феназин-1-карбоновая кислота являются ингибиторами каталазы, а также выступают в роли переносчиков электронов электрон-транспортной цепи, вызывая продукцию активных форм кислорода, в то время как 2-гептил-4-гидроксихинолин N-оксид вызывает ингибирование пути окисления гидрохинонов. Таким образом, P. aeruginosa контролируют рост S. aureus за счет использования синергических механизмов, направленных, в первую очередь, на индукцию окислительного стресса S. aureus, приводящего к остановке деления и гибели S. aureus.
Список использованной литературы:
1. Zhou Y., Zhu S., Cai С, Yuan P., Li C, et al. High-throughput screening of a CRISPR/Cas9 library for functional genomics in human cells. // Nature. - 2014. -Vol. 509, №7501. - P. 487-491.
2. Bleicher K.H., Bohm H.-J., Muller K., Alanine A.I. Hit and lead generation: beyond high-throughput screening. // Nat Rev Drug Discov. - 2003. - Vol. 2, №5. - P. 369-378.
3. Zheng F., Xue L., Hou S., Liu J., Zhan M., et al. A highly efficient cocaine-detoxifying enzyme obtained by computational design. // Nat Commun. - 2014. - Vol. 5. - P. 3457.
4. Arnold F.H. Combinatorial and computational challenges for biocatalyst design. // Nature.-2001. - Vol. 409, №6817. - P. 253-257.
5. Bajorath J. Integration of virtual and high-throughput screening. // Nat Rev Drug Discov. - 2002. - Vol. 1, №11. - P. 882-894.
6. Inglese J., Shamu C.E., Guy R.K. Reporting data from high-throughput screening of small-molecule libraries. // Nat Chem Biol. - 2007. - Vol.3, №8. - P. 438-441.
7. Sackmann E.K., Fulton A.L., Beebe D.J. The present and future role of microfluidics in biomedical research. // Nature. - 2014. - Vol.507, №7491. - P. 181-189.
8. Agresti J.J., Antipov E., Abate A.R., Ahn K., Rowat A.C., et al. Ultrahigh-throughput screening in drop-based microfluidics for directed evolution. // Proceedings of the National Academy of Sciences. - 2010. - Vol.107, №9. - P. 4004-4009.
9. Kintses В., Hein C, Mohamed MarkF., Fischlechner M., Courtois F., et al. Picoliter Cell Lysate Assays in Microfluidic Droplet Compartments for Directed Enzyme Evolution. // Chemistry & Biology. - 2012. - Vol.19, №8. - P. 1001-1009.
10. Fallah-Araghi A., Baret J.-C, Ryckelynck M., Griffiths A.D. A completely in vitro ultrahigh-throughput droplet-based microfluidic screening system for protein engineering and directed evolution. // Lab on a Chip. - 2012. - Vol. 12, №5. - P. 882-891.
11. Mazutis L., Gilbert J., Ung W.L., Weitz D.A., Griffiths A.D., et al. Single-cell analysis and sorting using droplet-based microfluidics. // Nat. Protocols. - 2013. - Vol. 8, №5. - P. 870-891.
12. Macosko Evan Z., Basu A., Satija R., Nemesh J., Shekhar K., et al. Highly Parallel Genome-wide Expression Profiling of Individual Cells Using Nanoliter Droplets. // Cell. - 2015. - Vol. 161, №5. - P. 1202-1214.
13. Colin P.-Y., Kintses В., Gielen F., Miton СМ., Fischer G., et al. Ultrahigh-throughput discovery of promiscuous enzymes by picodroplet functional metagenomics. // Nat Commun. - 2015. - Vol. 6. - P. 10008.
14. Lam K.S., Salmon S.E., Hersh E.M., Hruby V.J., Kazmierski W.M., et al. A new type of synthetic peptide library for identifying ligand-binding activity. // Nature. - 1991. - Vol. 354, №6348. - P. 82-84.
15. Zahnd C, Amstutz P., Pluckthun A. Ribosome display: selecting and evolving proteins in vitro that specifically bind to a target. // Nat Meth. - 2007. - Vol. 4, №3. - P. 269-279.
16. Bruin R.d., Spelt K., Mol J., Koes R., QuattrocchioFrancesca. Selection of high-affinity phage antibodies from phage display libraries. // Nat Biotech. - 1999. - Vol. 17, №4. - P. 397-399.
17. Lee C.M.Y., Iorno N., Sierra F., Christ D. Selection of human antibody fragments by phage display. // Nat. Protocols. - 2007. - Vol. 2, №11. - P. 3001-3008.
18. Rockberg J., Lofblom J., Hjelm В., Uhlen M., Stahl S. Epitope mapping of antibodies using bacterial surface display. // Nat Meth. - 2008. - Vol. 5, №12. - P. 1039-1045.
19. Boder E.T., Wittrup K.D. Yeast surface display for screening combinatorial polypeptide libraries. // Nat Biotech. - 1997. - Vol. 15, №6. - P. 553-557.
20. Li C.-Z., Liang Z.-K., Chen Z.-R., Lou H.-B., Zhou Y., et al. Identification of HBsAg-specific antibodies from a mammalian cell displayed full-length human antibody library of healthy immunized donor. // Cell Mol Immunol. - 2012. - Vol. 9, №2. - P. 184-190.
21. Tuerk C, Gold L. Systematic evolution of ligands by exponential enrichment: RNA ligands to bacteriophage T4 DNA polymerase. // Science. - 1990. - Vol. 249, №4968. - P. 505-510.
22. Seelig В. mRNA display for the selection and evolution of enzymes from in vitro-translated protein libraries. // Nat. Protocols. - 2011. - Vol. 6, №4. - P. 540-552.
23. Chen I., Dorr B.M., Liu D.R. A general strategy for the evolution of bond-forming enzymes using yeast display // Proceedings of the National Academy of Sciences. - 2011. - Vol. 108, №28. - P. 11399-11404.
24. Castle L.A., Siehl D.L., Gorton R., Patten P.A., Chen Y.H., et al. Discovery and Directed Evolution of a Glyphosate Tolerance Gene. // Science. - 2004. - Vol. 304, №5674. - P. 1151-1154.
25. Tsai P.-C, Fox N., Bigley A.N., Harvey S.P., Barondeau D.P., et al. Enzymes for the Homeland Defense: Optimizing Phosphotriesterase for the Hydrolysis of Organophosphate Nerve Agents. // Biochemistry. - 2012. - Vol. 51, №32. - P. 6463-6475.
26. Esvelt K.M., Carlson J.C., Liu D.R. A system for the continuous directed evolution of biomolecules // Nature. - 2011. - Vol. 472, №7344. - P. 499-503.
27. Yoo Т.Н., Pogson M., Iverson B.L., Georgiou G. Directed Evolution of Highly Selective Proteases by Using a Novel FACS-Based Screen that Capitalizes on the p53 Regulator MDM2. // ChemBioChem. - 2012. - Vol. 13, №5. - P. 649-653.
28. Chen C.-P., Hsieh Y.-T., Prijovich Z.M., Chuang H.-Y., Chen K.-C, et al. ECSTASY, an adjustable membrane-tethered/soluble protein expression system for the directed evolution of mammalian proteins. // Protein Engineering Design and Selection. - 2012. - Vol. 25, №7. - P. 367-375.
29. Bernath K., Hai M., Mastrobattista E., Griffiths A.D., Magdassi S., et al. In vitro compartmentalization by double emulsions: sorting and gene enrichment by fluorescence activated cell sorting. // Analytical Biochemistry. - 2004. - Vol. 325, №l. - P. 151-157.
30. Miller O.J., Bernath K., Agresti J.J., Amitai G., Kelly B.T., et al. Directed evolution by in vitro compartmentalization. // Nat Meth. - 2006. - Vol. 3, №7. - P. 561-570.
31. Mark D., Haeberle S., Roth G., von Stetten F., Zengerle R. Microfluidic lab-on-a-chip platforms: requirements, characteristics and applications. // Chemical Society Reviews. - 2010. - Vol. 39, №3. - P. 1153-1182.
32. Ghadessy F.J., Holliger P. A novel emulsion mixture for in vitro compartmentalization of transcription and translation in the rabbit reticulocyte system. // Protein Engineering Design and Selection. - 2004. - Vol. 17, №3. - P. 201-204.
33. Gruner P., Riechers В.,
34. Holtze C, Rowat A.C., Agresti J.J., Hutchison J.B., Angile F.E., et al. Biocompatible surfactants for water-in-fluorocarbon emulsions. // Lab on a Chip.- 2008. - Vol. 8, №10. - P. 1632-1639.
35. Clausell-Tormos J., Lieber D., Baret J.-C, El-Harrak A., Miller O.J., et al. Droplet-Based Microfluidic Platforms for the Encapsulation and Screening of Mammalian Cells and Multicellular Organisms. // Chemistry & Biology. - 2008. - Vol. 15, №5. - P. 427-437.
36. Ahn K., Kerbage C, Hunt T.P., Westervelt R.M., Link D.R., et al. Dielectrophoretic manipulation of drops for high-speed microfluidic sorting devices. // Applied Physics Letters. - 2006. - Vol. 88, №2. - P. 024104.
37. Baret J.-C, Miller O.J., Taly V., Ryckelynck M., El-Harrak A., et al. Fluorescence-activated droplet sorting (FADS): efficient microfluidic cell sorting based on enzymatic activity. // Lab on a Chip. - 2009. - Vol. 9, №13. - P. 1850-1858.
Реферат
Группа изобретений относится к области биохимии. Предложен способ ультравысокопроизводительного скрининга клеток или микроорганизмов, а также представляющее собой биосовместимую двойную эмульсию вода-масло-вода средство для ультравысокопроизводительного скрининга клеток или микроорганизмов. Способ включает микрофлюидную генерацию капель биосовместимой двойной эмульсии вода/масло/вода методом последовательной эмульсификации в микрофлюидных чипах, инкубирование указанной эмульсии до появления флуоресцентного сигнала, скринирование с использованием флуоресцентного клеточного сортера, отбор популяции капель с заданным уровнем флуоресценции и анализ с использованием секвенирования. Причём генерацию осуществляют с использованием водной фазы, несущей библиотеку клеток или микроорганизмов, водной фазы, несущей необходимые для детекции активности фенотипа флуорогенный субстрат или репортерную клеточную линию, масляной фазы и внешней водной фазы. Изобретения обеспечивают монодисперстность капель биосовместимой двойной эмульсии вода/масло/вода. 2 н. и 2 з.п. ф-лы, 30 ил., 1 табл.

Комментарии