Каталитическая композиция для сополимеризации окиси углерода с альфа-олефинами и способ получения сополимеров окиси углерода с альфа-олефинами - RU2060259C1
Код документа: RU2060259C1
Описание
Изобретение относится к каталитическим композициям, предназначенным для получения полимеров окиси углерода с одним или несколькими олефинненасыщенными соединениями.
Известно, что линейные полимеры окиси углерода с одним или несколькими олефинненасыщенными соединениями, в которых звенья окиси углерода, с одной стороны, и звенья олефинненасыщенных соединений, с другой стороны, расположены в чередующемся порядке, можно получить путем контактирования мономеров с каталитической композицией, содержащей металл группы VIII и бисфосфин общей формулы (R1)2 P-R-P( R1)2, в которой R1 представляет ароматическую гидрокарбонильную группу, а R двухвалентную мостиковую группу, содержащую три атома углерода в мостике, из которых центральный атом углерода образует часть -CH2-группы.
При получении вышеуказанного полимера важную роль играет как скорость полимеризации, так и средняя молекулярная масса образуемых полимеров. С одной стороны, желательно, чтобы при получении полимера достигалась наибольшая скорость реакции, а с другой стороны, с учетом их применения предпочтение отдается полимерам с более высокой средней молекулярной массой. На скорость реакции и среднюю молекулярную массу может оказывать влияние температура, применяемая в процессе полимеризации. Температура оказывает противоположное влияние на скорость полимеризации и среднюю молекулярную массу: повышение температуры реакции ведет к увеличению скорости реакции, а также к уменьшению средней молекулярной массы образующихся полимеров при условии, что другие условия реакции не изменяются. Это означает, что в зависимости от применения полимеров температуру реакции следует выбирать таким образом, чтобы получить полимеры с достаточно высокой средней молекулярной массой для данного применения при приемлемой скорости реакции, соответствующей этой температуре.
В известном исследовании вышеуказанных каталитических композиций было установлено, что их поведение в отношении зависимости между достигаемой скоростью реакции и средней молекулярной массой получаемых полимеров можно улучшить посредством замены бисфосфина общей формулы (R1)2 P-R-P(R1)2 бисфосфином общей формулы (R2)2 P-R-P (R2)2, в которой представляет арильную группу, содержащую по крайней мере один алкоксильный заместитель в ортоположении относительно атома фосфора, к которому присоединяется арильная группа.
В ходе последующего исследования указанных последними каталитических композиций было установлено, что их поведение в отношении зависимости между скоростью реакции и средней молекулярной массой получаемых полимеров можно еще более улучшить посредством замены бисфосфина общей формулы (R2 )2 P-R-P(R2)2 бисфосфином общей формулы (R2)2 P-R3 -P(R2)2, в которой R3 представляет двухвалентную мостиковую группу, содержащую три атома углерода в мостике, из которых центральный атом углерода образует часть -CHR4-группы, в которой R4 представляет одновалентный заместитель, включающий углерод, водород и вариантно кислород. Сравнение поведения первоначальных каталитических композиций, содержащих бисфосфин общей формулы (R2)2 P-R-P (R2 )2 с модифицированными каталитическими композициями, содержащими бисфосфин общей формулы (R2 )2 P-R3-P(R2)2, показывает, что при скорости реакции, равной для обеих композиций, с помощью модифицированных композиций можно получить полимеры с более высокой средней молекулярной массой. При использовании обеих композиций для получения полимеров с одинаковой средней молекулярной массой модифицированные композиции создают большую скорость реакции. Это вызывает удивление с учетом того, что замена бисфосфина общей формулы (R1)2 P-R-P(R1)2 бисфосфином общей формулы (R1)2 P-R3-P(R1)2 ведет к ухудшению зависимости между достигаемой скоростью реакции и средней молекулярной массой получаемых полимеров, как это было ранее установлено заявителем.
Каталитические композиции, содержащие металл группы VIII и бисфосфин общей формулы (R2)2 P-R3-P(R2)2, обладают существенной новизной. Поэтому изобретение относится к новым каталитическими композициями, содержащим металл группы VIII и бисфосфин общей формулы (R2)2 P-R3-P (R2)2, в которой R2 представляет арильную группу, включающую по крайней мере один алкоксильный заместитель в ортоположении относительно атома фосфора, к которому присоединяется арильная группа, а R3 представляет двухвалентную мостиковую группу, содержащую три атома углерода в мостике, из которых центральный атом углерода образует часть -CHR4-группы, в которой R4 является одновалентным заместителем, включающим углерод, водород и вариантно кислород. Изобретение относится к применению этих каталитических композиций для получения полимеров окиси углерода с одним или несколькими олефинненасыщенными соединениями.
Ряд бисфосфинов общей формулы (R2)2 P-R3-P(R2)2, которые могут использоваться в каталитических композициях по настоящему изобретению, также являются новыми соединениями. Предмет изобретения эти новые соединения и способ их получения. Один из дигалогенидов, получаемый в качестве промежуточного продукта во время получения новых бисфосфинов, также представляет новое соединение.
Металлы группы VIII представляют такие благородные металлы, как рутений, родий, палладий, осмий, иридий и платину, а также металл группы железа, такой как железо, кобальт и никель. Металл группы VIII, используемый в каталитических композициях по настоящему изобретению, предпочтительно выбирают из палладия, никеля и кобальта. В качестве металла группы VIII особое предпочтение отдается палладию. Включение металла группы VIII в каталитические композиции предпочтительно производится в форме соли карбоновой кислоты, а частности в форме ацетата. Помимо металла группы VIII и бисфосфина, каталитические композиции по настоящему изобретению также предпочтительно содержат анион кислоты с рКа менее 4, в частности анион кислоты с рКа менее 2. Примерами кислот с рКа менее 2 могут служить серная и перхлорная кислоты, сульфоновые кислоты, такие как метансульфоновая, трифторметансульфоновая и паратолуолсульфоновая кислоты, а также галогенкарбоновые кислоты, такие как трихлоруксусная, дифторуксусная и трифторуксусная кислоты. Предпочтение отдается сульфоновой кислоте, такой как паратолуолсульфоновая кислота или галогенкарбоновой кислоте, такой как трифторуксусная кислота. Анион может вводиться в каталитические композиции или в форме соединения, от которого он отщепляется, или в форме смеси соединений, из которой желаемый анион образует посредством реакции обменного разложения. Как правило, анион включается в каталитические композиции в форме кислоты. Этот анион также может вводиться в каталитическую композицию в форме соли металла основной группы или в форме соли неблагородного переходного металла, образуемой из указанной кислоты. В случае выбора аниона карбоновой кислоты его включение в каталитическую композицию может производиться в форме кислоты или в форме ее производного, такого как сложный алкиловый или ариловый эфир, амид, имид, ангидрид, сложный ортоэфир, лактон, лактам или алкилидендикарбоксилат. Указанный анион предпочтительно присутствует в каталитических композициях в количестве 1-100, в частности 2-50 моль на гат металла группы VIII. За исключением случаев применения в качестве отдельного компонента, анион кислоты с показателем кислотности (рКа) менее 4 также может присутствовать в каталитических композициях, например, в виде трифторацетата палладия или паратозилата палладия, представляющего соединение металла группы VIII.
Помимо металла группы VIII, бисфосфина и вариантно аниона кислоты с рКа менее 4 каталитические композиции по настоящему изобретению могут включать органический окислитель. В качестве примеров приемлемых оpганических окислителей можно привести 1,2= и 1,4=хиноны, алифатические нитриты, такие как бутилнитрит, и ароматические нитросоединения, такие как нитробезол и 2,4-динитротолуол. Предпочтение отдается 1,4-бензохинону и 1,4-нафтохинону. Органический окислитель предпочтительно используется в количестве 5-5000, в частности 10-1000 моль на гат металла группы VIII.
В каталитических композициях по настоящему изобретению бисфосфин предпочтительно присутствует в количестве 0,5-2 и в частности 0,75-1,5 моль на гат металла группы VIII. В бисфосфине группа R2 предпочтительно является фенильной группой, содержащей по крайней мере один метоксильный заместитель в ортоположении относительно атома фосфора, к которому присоединяется фенильная группа. Примерами таких групп R2 могут служить 2-метоксифенильная, 2,4-диметоксифенильная, 2, 6-диметоксифенильная и 2,4,6-триметоксифенильная группы. Предпочтение отдается бисфосфинам, у которых группа R2 представляет 2-метоксифенильную группу. Предпочтительными также являются бисфосфины, у которых мостиковая группа R3 представляет группу -CH2-CHR4-CH2-. В качестве приемлемых групп R4 может указать арильные группы, такие как фенильная группа, аралкильные группы, такие как бензильная группа, алкильные группы, такие как пропильная группа, аралкилоксигруппы, такие как бензилоксигруппа и 2,4, 6-триметилбензилоксигруппа, алкоксиалкоксильные группы, такие как этоксиметоксильная группа, и гидроксиалкильные группы, такие как 6-гидроксигексильная группа.
Бисфосфины общей формулы (R2)2 P-CH2-CHR4-CH2-P(R2)2, в которой R4 представляет арильную, аралкильную, алкильную, аралкилокси- или алкоксиалкоксильную группу, является новыми соединениями. Эти соединения можно получить в результате взаимодействия диарилфосфида щелочного металла общей формулы MP(R2 )2, в которой М представляет такой щелочной металл, как натрий, с дигалогенидом общей формулы CH2X-CHR4-CH2X, в которой Х представляет такой галоген, как хлор или бром. Диарилфосфиды щелочных металлов, необходимые для синтеза новых бисфосфинов, можно получить в результате взаимодействия в жидком аммиаке щелочного металла М с трифосфином общей формулы (R2)3 P. Способ получения дигалогенидов, необходимых для синтеза новых бисфосфинов, зависит от природы находящейся в нем группы R4. Если группа R4 представляет алкильную, арильную или аралкильную группу, то необходимые дигалогены можно получить путем превращения в результате восстановления, например, алюмогидридом лития диалкилмалонового эфира, включающего группу R4 в качестве заместителя у центрального атома углерода, в соответствующее дигидроксильное соединение и последующего превращения этого соединения посредством галогенирования, например, трибромидом фосфора или бромистоводородной кислотой в дигалогенид. Если группа R4 представляет аралкилоксигруппу, то необходимые дигалогениды можно получить в результате взаимодействия аралкилгалогенида с таким эпигалоидогидрином, как эпибромгидрин. Если группа R4 представляет алкоксиалкоксильную группу, то необходимые дигалогениды можно получить в результате взаимодействия галогеналкилалкилового эфира с таким эпигалоидогидридом, как эпихлоргидрин.
Новые бисфосфины по настоящему изобретению включают:
a)
2-фенил-1,
3-бис[бис(2-метоксифенил)фосфино]пропан;
b) 2-бензил-1,3-бис[бис(2-метоксифенил)фосфино]пропан;
с) 2-пропил-1,3-бис[бис(2-метоксифенил)фосфино]пропан;
d)
2-бензилокси-1,
3-бис[бис(2-метоксифенил)фосфино]пропан;
е) 2-(2,4,6-триметилбензилокси)-1,3-бис[бис(2-метоксифенил)-фосфино]пропан;
f) 2-этоксиметокси-1,
3-бис[бис(2-метоксифенил)фосфино]пропан.
Все эти соединения были получены в результате взаимодействия ди(2-метоксифенил)фосфида натрия, полученного при взаимодействии в жидком аммиаке натрия с трис(2-метоксифенил)фосфином, с одним из следующих галогенидов.
Для получения бисфосфина, указанного в п. а, использовали 2-фенил-1,3-дибромпропан, полученный из 2-фенилмалоновой кислоты посредством ее эстерификации этанолом, восстановления полученного таким образом 2-фенилдиэтилмалоната алюмогидридом лития в 2-фенил-1,3-дигидро- ксипропан и бромирования этого соединения трибромидом фосфора.
Для получения бисфосфина, указанного в п. b, использовали 2-бензил-1,3-дибромпропан, полученный из диэтилмалоната в результате его превращения с помощью бензилхлорида и метанолата натрия в 2-бензилдиэтилмалонат, восстановления этого соединения алюмогидридом лития в 2-бензил-1,3-дигидроксипропан с последующим бромированием бромистоводородной кислотой.
Для получения бисфосфина, указанного в п. с, использовали 2-пропил-1,3-дибромпропан, полученный из 2-пропилдиэтилмалоната путем восстановления этого соединения алюмогидридом лития в 2-пропил-1,3-дигидроксипропан с последующим бромированием бромистоводородной кислотой.
Для получения бисфосфина, указанного в п. d, использовали 2-бензилокси-1,3-дибромпропан, полученный в результате взаимодействия бензилбромида с эпибромгидрином.
Для получения бисфосфина, указанного в п. е, использовали 2-(2,4,6-триметилбензилокси)-1,3-дибромпропан, полученный из мезитилена в результате его превращения с помощью параформальдегида и бромистоводородной кислоты в бромметил-2,4,6-триметилбензол и взаимодействия этого соединения с эпибромгидрином. Соединение 2-(2,4,6-триметилбензилокси)-1, 3-дибромпропан является новым соединением.
Для получения бисфосфина, указанного в п. f, использовали 2-этоксиметокси-1,3-дихлорпропан, полученный в результате взаимодействия этилхлорметилового эфира с эпихлоргидрином.
Полимеризацию с использованием каталитических композиций по настоящему изобретению предпочтительно осуществляют путем контактирования мономеров с раствором каталитической композиции в разбавителе, в котором полимеры почти или совсем не растворяются. В качестве разбавителей пригодны низшие спирты, такие как метанол. При желании полимеризацию также можно производить в газовой фазе. Олеолефинненасыщенные соединения, которые могут полимеризоваться с окисью углерода при помощи каталитических композиций по настоящему изобретению, могут представлять соединения, состоящие исключительно из углерода и водорода, или соединения, содержащие помимо углерода и водорода один или несколько гетероатомов. Каталитические композиции по настоящему изобретению предпочтительно используют в процессе получения полимеров окиси углерода с одним или несколькими олефинненасыщенными углеводородами. Примерами приемлемых углеводородных мономеров являются этилен, пропилен, бутилен-1, гексен-1, октан-1, стирол, циклопентен, норборнен и дициклопентадиен. Каталитические композиции по настоящему изобретению особенно подходят для получения сополимеров окиси углерода с этиленом и для получения тройных сополимеров окиси углерода с этиленом и а-олефином, в частности пропиленом.
Количество каталитических композиций, используемых в процессе полимеризации, может изменяться в широких пределах. Количество катализатора определяется в пересчете на моль олефинненасыщенного соединения, подлежащего полимеризации, при содержании 10-7-10-3, в частности 10-6-10-4, гат металла группы VIII.
Получение полимеров предпочтительно производится при температуре 25-150оС и давлении 2-150 бар, в частности при температуре 30-130оС и давлении 5-100 бар. Молярное соотношение олефинненасыщенных соединений и окиси углерода в полимеризуемой смеси предпочтительно составляет от 10:1 до 1:10, в частности от 5:1 до 1:5. Полимеризация может осуществляться в периодическом или непрерывном режиме.
Чем больше средняя молекулярная масса настоящих полимером, тем выше будет их характеристическая вязкость. Для определения характеристической вязкости настоящих полимеров первые четыре раствора получают путем растворения полимера в четырех различных концентрациях в метакрезоле. С помощью вискозиметра для каждого раствора определяли вязкость при температуре 60оС по отношению к метакрезолу, находящемуся при температуре 60оС. Если То время истечения метакрезола, а Тр время истечения раствора полимера, то относительную вязкость ηrel получают из отношения ηrel=Tp/To. Характеристическую вязкость ηinh можно высчитать из ηrel по формуле ηinh=(In. ηrel) с концентрацией с полимера в граммах на 100 мл раствора.
Теперь можно определить характеристическую вязкость η в дл/г, построив график ηinh для каждого из четырех растворов полимеров в зависимости от соответствующей концентрации с последующей экстраполяцией к с=0.
Вместо термина "характеристическая вязкость" далее будет использоваться определение "предельное число вязкости", рекомендованное Международным союзом теоретической и прикладной химии.
П р и м е р 1. 2-бензилдиэтилмалонат получали следующим образом. 49,5 г (0,31 моль) диэтилмалоната добавляли к раствору 0,3 моль метанолата натрия в 200 мл безводного этанола с такой скоростью, что эта смесь умеренно кипела с обратным холодильником. Затем в течение 1 ч добавляли 37,98 г (0,30 моль) бензилхлорида, после чего эту смесь кипятили с обратным холодильником в течение 2 ч. После концентрирования смеси добавляли 100 мл воды. Неочищенный сложный эфир экстрагировали дважды, используя каждый раз 10 мл хлороформа, сушили над сульфатом магния и перегоняли. Выход 2-бензилдиэтилмалоната составил 50 г (66%).
П р и м е р 2.
2-фенилдиэтилмалонат получали путем эстерификации 2-фенилмалоновой кислоты в толуоле с помощью этанола в присутствии
каталитического количества серной кислоты. 2-фенилдиэтилмалонат очищали перегонкой.
Выход составил 90%
П р и м е р 3. 2-бензил-1,3-дигидроксипропан получали следующим образом. 25,07 г (0,1
моль) 2-бензилдиэтиламлоната, полученного в соответствии с примером 1, растворяли в
100 мл диэтилового эфира. Этот раствор добавляли к раствору 0,105 мл алюмогидрида лития в 105 мл диэтилового эфира
с такой скоростью, при которой достигалось умеренное кипение этой смеси с обратным
холодильником. После окончания добавления эту смесь кипятили с обратным холодильником еще в течение одного часа, а
затем добавляли 9,8 мл этилацетата. Образовавшееся белое твердое вещество отделяли,
растворяли в разбавленной серной кислоте, после чего раствор шесть раз экстрагировали 100 мл диэтилового эфира.
Органический раствор сушили над сульфатом магния, концентрировали и перегоняли. Выход
2-бензил-1,3-дигидироксипропана составил 11 г (66%).
П р и м е р 4. 2-фенил-1,3-дигидироксипропан
получали так же, как 2-бензил -1,3-дигидроксипропан в примере 3, но в качестве
исходного материала использовали 2-фенилдиэтилмалонат, полученный в соответствии с примером 2. Выход 2-фенил-1,
3-дигидироксипропана составил 59%
П р и м е р 5. 2-пропил-1,3-дигидроксипропан
получали так же, как 2-бензил-1,3-дигидроксипропан в примере 3, но в качестве исходного материала использовали
выпускаемый промышленностью 2-пропилдиэтилмалонат. Выход 2-пропил-1,3-дигидрокси- пропана
составил 50%
П р и м е р 6. 2-бензил-1,3-дибромпропан получали следующим образом. К смеси 25 г
48%-ного водного раствора бромистоводородной кислоты и 7,5 г концентрированной серной кислоты
добавляли 10 г (0,06 моль) 2-бензил-1,3-дигидроксипропана, полученного в соответствии с примером 3. После
добавления 6 г концентрированной серной кислоты эту смесь кипятили с обратным холодильником в
течение 3,5 ч. После охлаждения и добавления воды эту смесь трижды экстрагировали дихлорметаном.
Органический слой последовательно промывали водой, 5%-ным водным раствором бикарбоната натрия и снова
водой, сушили над сульфатом магния и перегоняли. Выход 2-бензил-1,3-дибромпропан составил 12 г
(68% ).
П р и м е р 7. 2-фенил-1,3-дибромпропан получали следующим образом. К охлажденной
льдом и перемешанной смеси 0,1 г пиридина и 0,065 моль 2-фенил-1,3-дигидро- ксипропана,
полученного в соответствии с примером 4, медленно добавляли 0,13 моль трибромида фосфора. Эту смесь перемешивали
при комнатной температуре в течение 5 дней, а затем нагревали 2 ч при температуре
100оС. Эту смесь выливали на лед и экстрагировали дихлорметаном. Органический слой последовательно
промывали водой, 10%-ным водным раствором бикарбоната натрия и снова водой, сушили над
сульфатом магния и перегоняли. Выход 2-фенил-1,3-дибромпропана составил 71%
П р и м е р 8. 2-пропил-1,
3-дибромпропан получали так же, как 2-бензил-1,3-дибромпропан в примере 6, но в качестве
исходного материала вместо 2-бензил-1,3-дигидроксипропана использовали 2-пропил-1,3-дигидроксипропан,
полученный в соответствии с примером 5. Выход 2-пропил-1,3-дибромпропана составил 62%
П
р и м е р 9. Бромметил-2,4,6-триметилбензол получали следующим образом. К смеси 12,0 г (0,10 моль)
мезитилена, 3,08 г (0,10 моль) параформальдегида и 50 мл 99,7%-ной ледяной уксусной кислоты быстро
добавляли 20 мл 31% -ного раствора бромистоводородной кислоты в уксусной кислоте. Эту смесь
выдерживали при температуре 45оС в течение 2 ч, а затем выливали в 100 мл воды. Твердый материал
отфильтровывали и промывали пентаном. Выход бромметил-2,4,6-триметилбензола составил 20,0
(94%).
П р и м е р 10. 2-бензилокси-1,3-дибромпропан получали следующим образом. Смесь 24,6 г
(0,18 моль) эпибромгидрина, 29 г (0,17 моль) бензилбромида и 20 мг хлористой ртути (II)
нагревали 8 ч при температуре 160оС. Реакционную смесь перегоняли при пониженном давлении. Выход
2-бензилокси-1,3-дибромпропана составил 57%
П р и м е р 11. 2-этоксиметокси-1,
3-дихлорпропан получали следующим образом. 0,1 моль только что перегнанного этилхлорметилового эфира медленно
добавляли к охлажденной льдом смеси 0,1 моль эпихлоргидрина и 10 мг хлористой ртути (II).
После выстаивания в течении 12 ч при комнатной температуре реакционную смесь перегоняли. Выход
2-этоксиметокси-1,3-ди- хлорпропана составил 96%
П р и м е р 12. 2-(2,4,6-триметилбензилокси)-1,
3-дибромпропан получали так же, как 2-бензилокси-1,3-дибромпропан в примере 10, но в качестве
исходного материала вместо бензилбромида использовали бромметил-2,4,6-триметилбензол, полученный в
соответствии с примером 9. Выход 2-(2,4,6-триметилбензилокси)-1,3-дибромпропана составил 90%
П р и м е р 13. 2-бензил-1,3-бис[бис(2-метоксифенил)фосфино]пропан получали следующим образом.
(Все стадии осуществляли в атмосфере аргона). К 125 мл сухого аммиака, который находился при
температуре -78оС, добавляли 0,4 г (17,5 ммоль) натрия, 3,1 г (8,75 ммоль)
трис-(2-метоксифенил)фосфина и 12,5 мл тетрагидрофурана, высушенного натрием. После перемешивания в течение 6 ч
при температуре -78оС добавляли 0,467 г (8,75 ммоль) хлористого аммония.
Через 30 мин добавляли 1,26 г (4,3 ммоль) 2-бензил-1,3-дибромпропана, полученного в соответствии с примером 6,
который был растворен в 50 мл тетрагидрофурана. После выпаривания аммиака реакционную
смесь очищали следующим образом (способ очистки 1). Растворитель удаляли при пониженном давлении. Оставшийся
твердый материал растворяли в 50 мл дихлорметана и промывали 50 мл 5%-ного водного раствора
хлористого аммония. Затем растворитель удаляли и добавляли 50 мл тетрагидрофурана. Этот раствор фильтровали,
концентрировали до 10 мл и добавляли 50 мл метанола, в результате чего происходило
осаждения бисфосфина. Выход 2-бензил 1,3-бис[бис(2-метоксифенил)фосфино]пропана составил 2,53 г (95%). При желании
реакционную смесь можно очистить следующим образом (способ очистки 2). К реакционной
смеси добавляли 50 мл диэтилового эфира и суспензию центрифугируют 5 мин при скорости 3300 об/мин. После
концентрирования раствора добавляют метанол, что вызывает осаждение бисфосфина.
П р и м е р 14. 2-фенил-1,3-бис[бис(2-метоксифенил)фосфино]пропан получали так же, как 2-бензил-1,
3-бис[бис(2-метоксифенил)фосфино]пропан в примере 13, за исключением того, что вместо 2-бензил- 1,
3-дибромпропана использовали 2-фенил-1,3-дибромпропан, полученный в соответствии с примером 7. Выход
2-фенил-1,3-бис [бис(2-метоксифенил)фосфино]пропана составил 90%
П р и м е р 15.
2-пропил-1,3-бис[бис(2-метоксифенил)фосфино]пропан получали так же, как 2-бензил-1,
3-бис[бис(2-метоксифенил)фосфино]пропан в примере 13, за исключением того, что вместо 2-бензил- 1,3-дибромпропана
использовали 2-пропил-1,3-дибромпропан, полученный в соответствии с примером 8. Выход
2-пропил-1,3-бис[бис(2-метоксифенил)фос- фино]пропана составил 90%
П р и м е р 16. 2-бензилокси-1,
3-бис[бис(2-метоксифенил)фосфино]пропан получали так же, как 2-бензил-1,
3-бис[бис(2-метоксифенил)фосфино]пропан в примере 13, за исключением того, что вместо 2-бензил-1,3-дибромпропана использовали
2-бензилокси-1,3-дибромпропан, полученный в соответствии с примером 10.
Выход 2-бензилокси-1,3-бис[бис(2-метоксифенил)фос-фино] пропана составил 91%
П р и м е р 17. 2-этоксиметокси-1,
3-бис[бис(2-метоксифенил)фосфино]пропан получали так же, как 2-бензил-1,
3-бис[бис(2-метоксифенил)фосфино]пропан в примере 13, за исключением того, что вместо 2-бензил-1,3-дибромпропана использовали
2-этоксиметокси-1,3-дихлорпропан, полу- ченный в соответствии с примером
11. Выход 2-этоксиметокси-1,3-бис[бис(2-метоксифенил)фосфино]пропана составил 20%
П р и м е р 18. 2-(2,4,
6-триметилбензилокси)-1,3-бис[бис(2-метоксифенил)фосфи- но]пропан получали также, как
2-бензил-1,3-бис[бис(2-метоксифенил)фосфино] про-пан в примере 13, за исключением того, что вместо 2-бензил-1,
3-дибромпропана использовали 2-(2,4,6-триметилбензилокси)-1,3-дибромпропан, полученный в
соответствии с примером 12. Выход 2-(2,4,6-триметилбензилокси)-1,3-бис[бис(2-меток-сифенил)фосфино]пропана
составил 60%
П р и м е р 19. Тройной сополимер окиси углерода, этилена и пропилена
получали следующим образом. В автоклав объемом 300 мл при перемешивании вводили раствор катализатора,
содержащий 135 мл метанола, 4 мл ацетона, 0,009 ммоль ацетата палладия, 0,19 ммоль
трифторуксусной кислоты и 0,01 ммоль 1,3-бис(дифенилфосфино)пропана. Воздух из автоклава удаляли путем закачивания в
него окиси углерода до достижения давления, равного 50 бар, с последующим
снижением давления, и эту процедуру повторяли дважды. После нагревания автоклава до 80оС в него закачивали окись
углерода под давление 25 бар, затем пропилен под давлением 10 бар и наконец
этилен под давлением 15 бар. Во время полимеризации давление в автоклаве поддерживали равным 52 бар путем закачивания в него
смеси окиси углерода и этилена с соотношением 1: 1. Через 3,1 ч
полимеризацию заканчивали посредством охлаждения до комнатной температуры и снижения давления. Тройной сополимер отфильтровывали,
промывали метанолом и сушили. Было получено 13 г тройного сополимера.
Скорость реакции составила 4,4 кг тройного сополимера / г палладия в час. Тройной сополимер имел предельное число вязкости (60),
равное 0,5 дл/г.
П р и м е р 20. Тройной сополимер окиси углерода, этилена и пропилена получали так же, как в примере 19, за исключением того, что: раствор катализатора содержал 0,01 ммоль 2-бензилокси-1,3-бис(дифенилфосфино)пропана вместо 1,3-бис (дифенилфосфино) пропана; температура реакции равнялась 85оС вместо 80оС; время реакции составило 2,7 ч вместо 3, 1 ч. Было получено 7,6 г тройного сополимера. Скорость реакции равнялась 3,0 кг тройного сополимера /г палладия в час. Тройной сополимер имел предельное число вязкости (60), равное 0,3 дл/г.
П р и м е р 21. Тройной сополимер окиси углерода, этилена и пропилена получали так же, как в примере 19, за исключением того, что: раствор катализатора содержал 0,01 ммоль 1, 3-биc[бис(2-метоксифенил)фосфино] пропана вместо 1, 3-бис(дифенилфосфино)пропана; температура реакции равнялась 85оС вместо 80оС; время реакции составило 2,9 ч вместо 3,1. Было получено 13,1 г тройного сополимера. Скорость реакции равнялась 4,6 кг тройного сополимера / г палладия в час. Тройной сополимер имел предельное число вязкости (60), равное 1,1 дл/г.
П р и м е р 22. Тройной сополимер окиси углерода, этилена и пропилена получали так же, как в примере 19, за исключением того, что: раствор катализатора содержал 0,01 ммоль 2-(2,4,6-триметилбензилокси)-1, 3-бис[бис(2-метоксифенил)фосфино] пропана, полученного в соответствии с примером 18, вместо 1,3-бис(дифенилфосфино)пропана; температура реакции равнялась 85оС вместо 80оС; время реакции составило 3,2 ч вместо 3, 1 ч. Было получено 16,6 г тройного сополимера. Скорость реакции равнялась 5,4 кг тройного сополимера / г палладия в час. Тройной сополимер имел предельное число вязкости (60), равное 2,2 дл/г.
П р и м е р 23. Тройной сополимер окиси углерода, этилена и пропилена получали так же, как в примере 19, за исключением того, что: раствор катализатора содержал 0,01 ммоль 2-бензил-1, 3-бис-[бис(2-метоксифенил)фосфино] пропана, полученного в соответствии с примером 13, вместо 1,3-бис(дифенилфосфино)пропана; температура реакции равнялась 85о С вместо 80оС; время реакции составило 3,4 ч вместо 3,1 ч. Было получено 19,5 г тройного сополимера. Скорость реакции равнялась 6,0 кг тройного сополимера / г палладия в час. Тройной сополимер имел предельное число вязкости (60), равное 1,8 дл/г.
П р и м е р 24. Тройной сополимер окиси углерода, этилена и пропилена получали так же, как в примере 19, за исключением того, что: раствор катализатора содержал 0,01 ммоль 2-бензилокси-1,3-бис[бис(2-метоксифенил)фосфино] пропана, полученного в соответствии с примером 16, вместо 1,3-бис(дифенилфосфино)пропана; температура реакции равнялось 85оС вместо 80оС; время реакции составило 2,5 ч вместо 3,1 ч. Было получено 20,8 г тройного сополимера. Скорость реакции равнялась 8,7 кг тройного сополимера / г палладия в час. Тройной сополимер имел предельное число вязкости (60), равное 1,4 дл/г.
П р и м е р 25. Тройной сополимер окиси углерода, этилена и пропилена получали так же, как в примере 19, за исключением того, что: раствор катализатора содержал 0,01 ммоль 2-пропил-1,3-бис[бис(2-метоксифенил)фосфино] пропана, полученного в соответствии с примером 15, вместо 1, 3-бис(дифенилфосфино)пропана; температура реакции равнялась 85оС вместо 80оС; время реакции составило 2,2 ч вместо 3,1 ч. Было получено 12,5 г тройного сополимера. Скорость реакции равнялась 5,8 кг тройного сополимера / г палладия в час. Тройной сополимер имел предельное число вязкости (60), равное 1,8 дл/г.
П р и м е р 26. Тройной сополимер окиси углерода, этилена и пропилена получали так же, как в примере 19, за исключением того, что: раствор катализатора содержал; 135 мл метанола, 2 мл ацетона, 0,0045 ммоль ацетата палладия, 0,09 ммоль трифторуксусной кислоты и 0,005 ммоль 2-(6-гидроксигексил)-1,3-бис[бис(2-метоксифенил)фосфино] пропана; температура реакции равнялась 85оС вместо 80оС; время реакции составило 5, 7 ч вместо 3,1 ч. Было получено 24,5 г тройного сополимера. Скорость реакции равнялась 9,0 кг тройного сополимера / г палладия в час. Тройной сополимер имел предельное число вязкости (60), равное 2,4 дл/г.
Из примеров 1-26 в соответствии с настоящим изобретением были выполнены примеры 12-18 и 22-26. Пример 12 относится к получению нового дигалогенида по настоящему изобретению, который использовали для получения нового бисфосфина в соответствии с примером 18. Примеры 13-18 относятся к получению новых бисфосфинов в соответствии с настоящим изобретением. Примеры 22-26 относятся к получению тройных сополимеров окиси углерода, этилена и пропилена с использованием новых каталитических композиций по настоящему изобретению. Примеры 1-11 и 19-21 выходят за пределы объема данного изобретения. Примеры 1-11 относятся к получению дигалогенидов общей формулы CH2X-CHR4-CН2X, которые использовали для получения новых бисфосфинов в соответствии с примерами 13-17. Примеры 19-21 относятся к получению тройных сополимеров окиси углерода, этилена и пропилена с использованием каталитических композиций, содержащих бисфосфины, которые не соответствуют общей формуле (R2 )2 P-R3 P(R2)2.
С помощью анализа13С-ЯМР было установлено, что тройные сополимеры окиси углерода, этилена и пропилена, полученные в соответствии с примерами 19-26 имели линейные цепи, в которых звенья окиси углерода, с одной стороны, и звенья этилена и пропилена, с другой стороны, располагались в чередующемся порядке. В полимерных цепях звенья этилена и пропилена располагались в произвольном порядке.
Благоприятное влияние на поведение полученных каталитических композиций в случае замены бисфосфина общей формулы (R1)2 P-R-P(R1)2бисфосфином общей формулы (R2)2 P-R-P(R2)2 становится очевидным в результате сравнения результатов, полученных в примерах 19 и 21 (более высокая скорость реакции при большей средней молекулярной масс).
Вредное влияние на
поведение каталитических
композиций в случае замены бисфосфина общей формулы (R1)2 P-R-P(R1)2 бисфосфином общей формулы (R1)2
P-R3-P(R1)2 становится очевидным при сравнении результатов, полученных в примерах 19 и 20 (более низкая скорость реакции наряду с меньшей средней молекулярной
массой).
Дальнейшее улучшение поведения каталитических композиций, которые могут быть получены в соответствии с настоящим изобретением, достигается в результате включения в них бисфосфина общей формулы (R2)2 P-R3-P (R2)2, что становится очевидным при сравнении результатов, полученных в примерах 22-26 с результатами, полученными в примере 21 (во всех случаях полимеры с большей средней молекулярной массой были получены при более высокой скорости реакции).
Реферат
Использование: для получения пластмасс. Сущность: проводят сополимеризацию олефинов с окисью углерода на каталитической композиции, состоящей из соли паладия и карбоновой кислоты, кислоты с РКа менее 4, бисфосфина и органического растворителя. Бисфосфин имеет формулу R2P-CH2-CH(R')-CH2-PR2, где R-2-алкоксифенил, R'-алкилгидроксиалкил, бензил, бензилокси или триалкилбензилокси. 2 с. п. ф-лы.
Формула
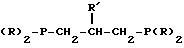
где R 2-алкоксифенил;
R′ алкил, гидроксиалкил, бензил, бензилокси или триалкилбензилокси.
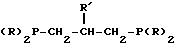
где R 2-алкоксифенил;
R′ алкил, гидроксиалкил, бензил, бензилокси или триалкилбензилокси.

Комментарии